Изобретение относится к области аналитической химии, а именно к способам разделения химических соединений методом хроматографии.
Заявляемый способ хроматографического анализа органических веществ относится к методам разделения смесей веществ и предназначен для их анализа. Для осуществления заявляемого способа использована плоскостная хроматография - вид жидкостной хроматографии. Плоскостная хроматография основана на распределении веществ на хроматографической пластине между двумя фазами - неподвижной (сорбентом), и подвижной (элюентом).
Метод плоскостной хроматографии относится к экспресс-методам (быстрым и простым). Он занимает особое место среди методов разделения благодаря простоте по технике выполнения методики и доступности оборудования, гибкости, широкой области применения. Используется для разделения и анализа неорганических и органических (полимеры, липиды, аминокислоты, ферменты, белки и др.) веществ. В настоящее время из известных видов хроматографии наблюдается широкое использование тонкослойной хроматографии за счет развития дальнейших процессов инструментализации и автоматизации метода.
Из патента РФ №2170421 на изобретение известен способ количественного определения химического состава вещества и энергий связи остовных электронов, включающий измерение линии фотоэлектронного спектра по меньшей мере одного элемента, разложение ее по известному набору элементарных составляющих, соответствующих различным химическим фазам, и известной последовательности энергий связи остовного электрона выбранного элемента в этих фазах, минимизацию функционала ошибок между измеренной линией спектра и суммарной расчетной огибающей набора элементарных составляющих с выбором их амплитуд и ширины в качестве свободных параметров и определение искомого состава по относительному вкладу этих составляющих в разлагаемую линию спектра с учетом стехиометрии химических фаз, отличающийся тем, что вышеупомянутые операции производят для каждой линии спектра двух или более выбранных элементов, дополнительно выбирая в качестве свободных параметров энергии связи элементов в химических фазах и, сравнивая полученные для всех линий спектра результаты между собой, варьируют свободными параметрами до совпадения результатов с учетом заданной ошибки.
Из патента РФ №2299432 на изобретение известен способ определения качественного состава органических веществ в объектах окружающей среды, включающий предварительное высушивание пробы материала, при этом пробу экстрагируют в стеклянной колонке на слое сульфата натрия двухкратно дихлорметаном, разделяют на фракции методом тонкослойной хроматографии в смеси гексана, четыреххлористого углерода, этилацетата и определение органических веществ проводят, сравнивая параметр, характеризующий положение хроматографической зоны вещества, Rf полученных фракций с Rf веществ, идентифицированных методом хроматомасспектрометрии.
Из патента РФ №2439552 на изобретение известен способ хроматографического анализа многокомпонентного вещества, при котором пробу вещества, характеризующегося фракционным составом, растворяют в вытеснителе, в котором растворимы все фракции пробы; раствор из смеси вытеснителя и растворенной в нем пробы помещают в/на неподвижную фазу, затем через смесь вытеснителя с пробой пропускают элюент, в качестве которого используют вещество, в котором нерастворима как минимум одна исследуемая фракция, затем проявившееся из смеси вытеснителя с пробой и в/на неподвижной фазе каждое вещество идентифицируют.
Способ по патенту №2439552 выбран в качестве наиболее близкого аналога (прототипа).
Все известные хроматографические способы анализа веществ не позволяют установить, является ли образованное из двух или более исходных веществ новое сложное вещество супрамолекулярным или не является таковым.
Вопрос о характере вновь полученного сложного вещества (является оно супрамолекулярным или нет) важен, поскольку предопределяет возможность область использования нового вещества. Супрамолекулярные вещества широко используются в медицине для получения лекарственных форм пролонгированного действия, в аромотерапии, для получения любых продуктов, обеспечивающих постепенное высвобождение активного вещества.
В 1978 г. Ж.М. Лен предложил первое определение супрамолекулярной химии: «подобно тому, как существует область молекулярной химии, основанной на ковалентных связях, существует и область, химии молекулярных ансамблей и межмолекулярных связей» (Жан-Мари Лен Супрамолекулярная химия: Концепции и перспективы/ Ж. - М. Мен; Пер. с англ. Новосибирск: Наука. Сиб. Предприятие РАН, 1998, стр. 7).
«Супрамолекулярные соединения - это группа молекулярных компонентов, индивидуальные свойства которых интегрированы в свойства целого ансамбля (ковалентного или нековалентного)» (стр. 263, Рамбиди Н.Г., Березкин А.В. «Физические и химические основы нанотехнологий», М, изд. «ФИЗМАТЛИТ», 2008).
Аналогичные сведения содержатся в источнике: Стид Джонатан В., Джерри Л. Этвуд «Супромолекулярная химия», пер. с англ.: в 2 т. – М., ИКЦ «Академкнига», 2007, Т1 - 2007, стр. 27.
Понятие супрамолекулярных комплексов (соединений) также дано в нижеприведенных источниках.
Супрамолекулярные соединения (комплексы), это особые химические системы, компоненты которых связаны между собой посредством межмолекулярных (нековалентных) взаимодействий (из патента РФ №2641111), посредством механических зацеплений молекул между собой, за счет водородного связывания, электростатического взаимодействия и др. Такие силы межмолекулярного взаимодействия в супрамолекулярных соединениях являются более слабыми, чем силы, основанные на ковалентных связях.
Известно также что супрамолекулярный комплекс (SMC), известный также как клатрат (из патента РФ №25690870) - соединение включения или комплекс «хозяин-гость», представляющий собой многокомпонентную систему атомов, ионов и/или молекул, которые скреплены по меньшей мере частично, посредством нековалентных взаимодействий, например, водородных связей, ван-дер-ваальсовых сил, π-π взаимодействий и/или электростатических эффектов. Эти разные силы притяжения значительно слабее ковалентного связывания и, следовательно, супрамолекулярные комплексы обычно гораздо менее стабильны, чем соединения, которые целиком связаны ковалентными связями. Например, SMC поддаются разрушению при повышенных температурах или при воздействии условий, разрушающих механизмы слабого связывания, которые скрепляют данные комплексы. Эти условия могут включать условия кислотного или щелочного гидролиза, гидролиз или сольватацию, например, полярным растворителем, который может разрывать водородную связь комплексов. Супрамолекулярная химия является направлением нанотехнологий (источник «Физические и химические основы нанотехнологий», Н.Г. Рамбиди, А.В. Березкин, Москва, изд. «Физматлит», 2008 г., стр. 263).
Техническая проблема, решаемая предлагаемым изобретением - создание способа, позволяющего устанавливать образуется или нет в результате взаимодействия двух заранее известных органических индивидуальных веществ супрамолекулярный комплекс (соединение) или нет.
Технический результат - расширение арсенала средств, позволяющих устанавливать характер соединения (супрамолекулярное или нет), обеспечение быстроты, точности, простоты и надежности способа хроматографического анализа, направленного на установление характера вновь образованного соединения (супрамолекулярное или нет).
Технический результат достигается за счет того, что в способе хроматографического анализа органических веществ, включающем тонкослойное хроматографирование смеси, образованной из двух исходных известных индивидуальных органических веществ, обладающих заранее известными характеристиками - эталонами, для анализа готовят пригодную для хроматографирования пробу в виде раствора из смеси исходных индивидуальных органических веществ, часть полученного раствора выдерживают в течение времени не менее 30 минут для возможного взаимодействия исходных индивидуальных веществ, на линию старта хроматографической пластины наносят первую пробу раствора, не подвергшегося выдержке, также на линию старта этой же или другой хроматографической пластины наносят вторую пробу раствора, подвергшегося выдержке, обе пробы помещают в элюент, согласно изобретению помещение обеих проб в элюент осуществляют до их высыхания на хроматографической пластине, сравнивают проявившиеся на пластине после хроматографирования пятна от первой и второй пробы, вывод об образовании супрамолекулярного соединения делают по наличию на пластине помимо проявившихся от второй пробы пятен исходных индивидуальных веществ дополнительного проявившегося пятна с характеристиками, отличными от эталонов, проявившихся на пластине от первой пробы, или по отклонению характеристики одного из проявившихся пятен от второй пробы от эталона соответствующего исходного индивидуального вещества, проявившегося от первой пробы.
В качестве растворителя смеси исходных индивидуальных органических веществ моет быть использован элюент.
Отличительной особенностью органических реакций от ионных неорганических является снижение скорости реакций. Поэтому, чтобы образовалось супрамолекулярное соединение нужно время. Первоначально при добавлении к органическому веществу растворителя происходит процесс растворения и только после процесса растворения может образоваться или не образоваться новое супрамолекулярное соединение, т.е. требуется выдержка полученного раствора. Время выдержки должно составлять не менее 30 минут, чем больше время выдержки, тем ярче проявившееся позднее дополнительное пятно или видоизменение одного из пятен.
Проба полученного раствора после выдержки наносится как обычно на линию старта хроматографической пластинки, но не сушится, чтобы не разрушить возможно образовавшееся супрамолекулярное соединение. Получаемая хроматограмма сравнивается с хроматограммой только что приготовленного раствора эталона без выдержки и без сушки пробы., т.е. в одинаковых условиях.
Если при взаимодействии исходных органических веществ в растворе образуется супрамолекулярное соединение, обнаружить его по результатам хроматографирования пробы, высушенной после ее нанесения на линию старта (как это бывает при стандартной тонкослойной хроматографии) невозможно, т.к. высушенная проба адсорбирует на силикагеле хроматографической пластины. При разбавлении такой пробы элюентом происходит полное разрушение супрамолекулярного соединения.
При пропускании элюента через невысушенную пробу, нанесенную на линию старта, обеспечивается «мягкое разделение» пробы, на пластине проявляются и исходные вещества и супрамолекулярное соединение.
Характеристиками пятен, которыми характеризуются исходные и вновь образованные вещества (соединения, комплексы) при хроматографии являются площадь пятна, высота перемещения пятна от линии старта, цвет пятна, коэффициент распределения Rf.
Проявившиеся на хроматографической пластине пятна анализируют методом спектроскопии, или ядерно-магнитного резонанса для определения количественных и качественных характеристик пятен.
Заявляемый способ относится к способам хроматографического анализа органических веществ и осуществляется с использованием хроматографической пластины.
Применение метода хроматографического анализа для выявления, является вновь образованное из известных исходных органических веществ соединение (комплекс) супрамолекулярным или нет, на первый взгляд является неочевидным, поскольку известно, что для выявления супрамолекулярных соединений по настоящее время используются как правило, физические методы исследования.
Из источника «Нанотехнология. Физико-химия нанокластеров, наноструктур и наноматериалов», И.П. Суздалев, Москва, изд. «КомКнига», 2006 г., стр. 40-114 известны следующие методы для изучения нанокластеров, наноструктур и наноматериалов: дифракционные методы; полевые методы; сканирующая зондовая микроскопия; рентгеновская спектроскопия и дифракция; электронная спектроскопия; оптическая и колебательная спектроскопия; гамма-резонансная спектроскопия; радиоспектроскопия (ядерный магнитный резонанс, электронный парамагнитный резонанс).
Из источника «Основы аналитической химии. Книга 1 «Общие вопросы. Методы разделения», под ред. Ю.А. Золотова, Москва, изд. «Высшая школа», 2004, стр. 263 известно, для каких целей используют методы хроматографического анализа:
«По цели хроматографирования выделяют аналитическую хроматографию (качественный и количественный анализ); препаративную хроматографию (для получения веществ в чистом виде, для концентрирования и выделения микропримесей); промышленную (производственную) хроматографию для автоматического управления процессом (при этом целевой продукт из колонки поступает в датчик). Хроматографию широко используют для исследования растворов, каталитических процессов, кинетики химических процессов и т.п.».
Таким образом, использование методов хроматографического анализа для выявления и идентификации супрамолекулярных комплексов в виде «ансамбля» молекулярного объединения нескольких исходных индивидуальных соединений из уровня техники не известно.
Неочевидность использования хроматографического анализа для выявления супрамолекулярного комплекса обусловлена также следующим.
Известно, что хроматография это физико-химический метод разделения веществ, основанный на распределении компонентов между фазами - неподвижной и подвижной. Неподвижной (стационарной) фазой обычно служит твердое вещество (его часто называют сорбентом) или пленка жидкости, нанесенная на твердое вещество. Подвижная фаза представляет собой жидкость или газ, протекающий через неподвижную фазу. В зависимости от сил взаимодействия исследуемого вещества с поверхностью сорбента компоненты исследуемого вещества вместе с подвижной фазой перемещаются вдоль неподвижной фазы с разной скоростью, характеризующей конкретное вещество. Таким образом, происходит разделение компонентов исследуемого вещества. Хроматографический метод позволяет разделять многокомпонентную смесь, идентифицировать компоненты и определять ее количественный состав.
Известно, что силы взаимодействия химических веществ с поверхностью сорбента (за счет адсорбции или по иному механизму), составляющие порядка 8-20 кДж/моль, (стр. 194, Пузаков «Общая химия. Биофизическая химия. Химия биогенных элементов», учебник для мед. Спец. Вузов, Ю.А. Ершов, В.А. Попков. А.С. Берлянд и др.; под ред. Ю.А. Ершова, М., изд. «Высшая школа», 1993). Клатраты по Кремеру в основном образованы за счет сил Ван дер-Ваальса менее 5 кДж/моль, сильнее, чем связи между молекулами в супрамолекулярных соединениях. Поэтому возможность выделения супрамолекулярного комплекса хроматографическим методом на первый взгляд кажется невозможной, в силу того, что такой супрамолекулярный комплекс при взаимодействии с сорбентом (твердой фазой) должен распадаться на исходные компоненты, т.е. при взаимодействии супрамолекулярного комплекса с твердой фазой оно должно разрушаться. Также, кажется очевидным, что супрамолекулярный комплекс может разрушиться от элюента - растворителя с последующим разделением элюентом в виде исходных компонентов.
Однако, опытным путем авторы доказали, что это не так. Авторы исходили из следующих знаний. Во-первых, чтобы не разрушить молекулярное соединение за счет адсорбции, использован прием не высушивания пробы. Во-вторых, при хроматографировании, элюент подается на пробу с нарастанием количества элюента во времени, т.е. через пробу проходит все новые и новые порции элюента, что способствует не мгновенному разрушению молекулярного соединения. Скорость и количество такого нарастания порций элюента не имеют принципиального значения, главное, чтобы количество элюента увеличивалось во времени.
Для разрушения супрамолекулярных структур нужны меньшие затраты энергии, благодаря чему их легко «разобрать» в случае необходимости. В связи с тем, что межмолекулярные взаимодействия в супрамолекулярных комплексах (соединениях) слабые, логично было предположить возможность их разрушения за счет и адсорбента и растворителя в процессе тонкослойного хроматографирования, когда не меняется ни температура, ни давление, но используется элюент (растворитель, подвижная фаза), меняется количество проходящего через вещество элюента; также на соединение влияет неподвижная фаза. При разложении одного супрамолекулярного комплекса должно появиться (как минимум) из одного соединения два дополнительных, т.е. исходных соединений, из которых образован супрамолекулярный комплекс. Этот способ разложения с одновременной идентификацией может явиться первоначальным экспресс анализом на наличие супрамолекулярных комплексов. Тем более, что можно менять и температуру проведения хроматографирования в тонком слое, имеются также приспособления для изменения давления. А далее, можно детально изучать структуру супрамолекулярного комплекса (соединения).
Известно, что супрамолекулярные комплексы (в том числе клатраты) образуются самопроизвольно (их образование энергетически выгодно), но легко разрушаются, даже простым увеличением количества растворителя, что согласуется с предположением авторов о возможном влиянии элюента. Природа супрамолекулярных взаимодействий описана в работе Дж. В. Стид, Дж., Л. Этвуд «Супрамолекулярная химия» в двух томах. Москва, ИКЦ «АКАДЕМКНИГА» 2007, т. 1, стр. 5-6: диполь - дипольные взаимодействия 5-50 кДж/моль; водородная связь 4-120 кДж/моль; катион - π - взаимодействие 5-80 кДж/моль; π-π - Стэкинг - взаимодействие 0-50 кДж/моль, силы Ван-дер-Ваальса. Величина физической адсорбции составляет 8-20 кДж/моль (стр. 194, Пузаков «Общая химия. Биофизическая химия. Химия биогенных элементов», учебник для мед. Спец. дер-Ваальса менее 5 кДж/моль. Клатраты по Кремеру в основном образованы за счет сил Ван Вузов, Ю.А. Ершов, В.А. Попков. А.С. Берлянд и др.; под ред. Ю.А. Ершова, М., изд. «Высшая школа», 1993). Следовательно, кроме разрушения элюентом, сорбция на пластинке вполне может являться причиной разрушения непрочных супрамолекулярных комплексов.
Сорбированная вода на неподвижном носителе (которую визуально не видно), по-видимому, снижает величину адсорбции и может помешать сорбенту разложить непрочный супрамолекулярный «ансамбль». «Вода является неподвижным растворителем и находится в порах носителя, например, крахмала, силикагеля»: источник А.П. Крешков «Основы аналитической химии. Качественный и количественный анализ», М, изд. «Химия», 1965 часть 1, стр. 142.
Авторы предположили, что высыхание исследуемой посредством метода тонкослойного хроматографирования пробы перед размещением пластины с пробой в элюент за счет физической адсорбции может разрушать непрочный супрамолекулярный комплекс, поэтому применили способ получения тонкослойной хроматограммы без высыхания пробы. Таким образом, прием отказа от сушки пробы перед хроматографией в заявляемом способе используется с целью сохранения «ансамбля» молекулярного соединения, в том числе с учетом того, что многие из супрамолекулярных комплексов существуют только в растворе, например, ряд клатратов, сольваты.
Для подтверждения своих предположений, авторы брали супрамолекулярный комплекс, образованный из заранее известных исходных индивидуальных веществ. При проведении хроматографирования такого супрамолекулярного комплекса (их было более 10) было установлено следующее. Каждое вещество разделялось по индивидуальным компонентам в соответствии с известными правилами и характеристиками.
После хроматографирования пробы, подвергнутой перед нанесением на линию старта дополнительной выдержке по времени, на хроматограмме проявлялось новое дополнительное пятно, не обусловленное индивидуальными исходными компонентами вещества. Этим проявленным позднее пятном являлось сам исходный супрамолекулярный комплекс. Соответствие этого позднее проявленного пятна исходному супрамолекулярному комплексу было подтверждено на основании анализа этого пятна одним из известных традиционных методов (в частности, ЯМР, спектроскопия).
Никаких иных пятен на хроматографической пластине позднее не проявлялось - проявились только исходные индивидуальные компоненты, а между ними исходное супрамолекулярное вещество.
Имела место другая ситуация, на основании которой делали вывод о том, что исследуемое вещество представляет собой супрамолекулярный комплекс.
После дополнительной выдержки времени на пластине проявлялось два пятна (по количеству исходных индивидуальных веществ), однако, одно из пятен имело характеристики (площадь, или расположение от линии старта), не соответствующие эталону исходного индивидуального вещества (при том, что другое проявившееся пятно имело характеристики (площадь, или расположение от линии старта), совпадающие с эталоном данного индивидуального вещества).
По результатам исследования такого проявившегося пятна с отличными от эталона характеристиками традиционными методами (ЯМР, спектроскопия) было установлено, что данное пятно представляет собой супрамолекулярный комплекс.
При проявлении на хроматографической пластине помимо двух пятен, идентифицирующих исходные индивидуальные вещества, третьего пятна, или при видоизменение одного из пятен до видимого состояния с характеристиками, отличными от характеристик соответствующего индивидуального вещества (при соответствии эталону характеристик другого проявившегося на пластине пятна) можно сделать вывод о том, что образованное из двух известных исходных индивидуальных веществ соединение, является супрамолекулярным комплексом.
Предлагаемый метод является простым, надежным, достоверным и, главное, очень быстрым. Способ позволяет осуществлять качественный и количественный анализ супрамолекулярных комплексов, в том числе при использовании дополнительных известных методов исследования супрамолекулярных комплексов.
Заявляемый способ осуществляли согласно следующим примерам.
Примеры осуществляли исходя из следующего: известно, что хинолин может образовывать супрамолекулярное соединение (Жан-мари Лен «Супрамолекулярная химия. Концепции и перспективы», Новосибирск. «Наука», Сибирское предприятие РАН, 1998, стр. 171).
Цель примеров определить, возможно ли с помощью тонкослойной хроматографии определить образование хинолином супрамолекулярного комплекса с толуолом или другим ароматическим веществом. Выбран хинолин, т.к. он не только может образовывать молекулярые соединения, но и хорошо виден на хроматограмме. На белой пластине после хроматографии через некоторое время (не менее 10 минут) появляется окрашивание за счет присутствия самого хинолина (слабое окисление на пластине). Исследовать другие (неокрашенные) вещества можно используя обычные известные способы хроматографии (реагенты для обнаружения соединений).
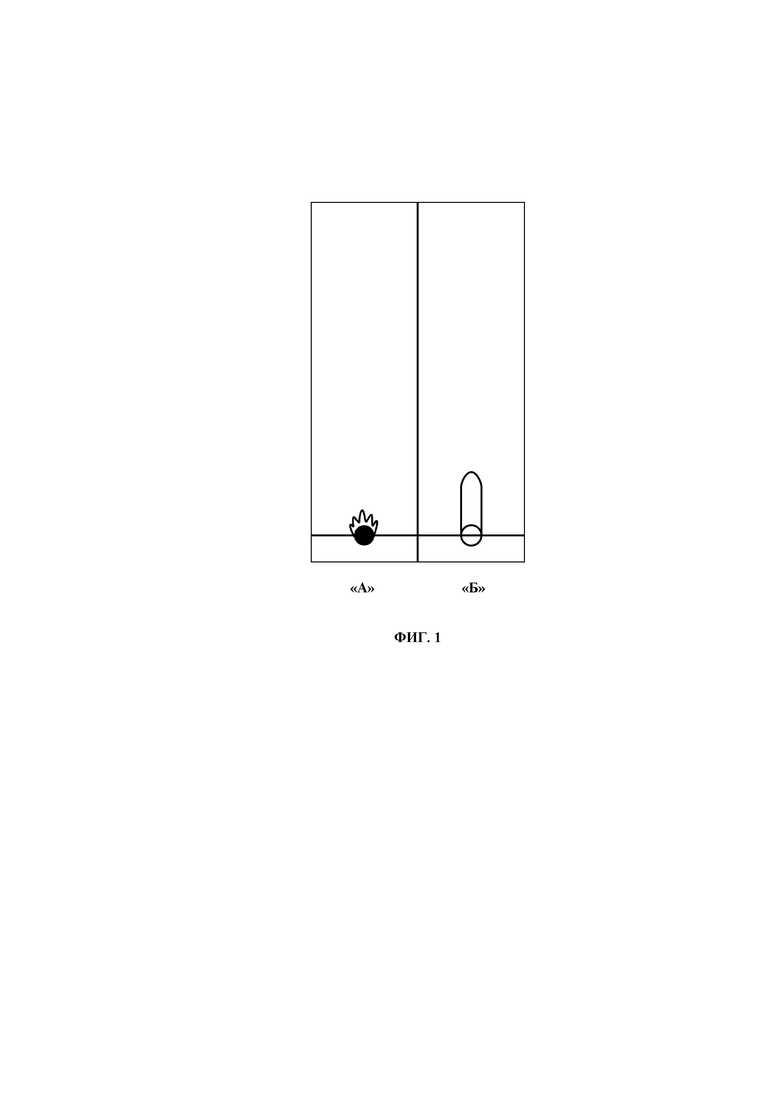
Пример 1. Тонкослойная хроматография чистого хинолина (фиг. 1, А, Б).
Брали хинолин C9H7N производства НТМК «чистый» в соответствии с ТУ-6-094326-86. Температурные пределы 235-238°С. В качестве элюента использовали толуол, С7Н8, ЧДА, ГОСТ 5789-78, изм. №1, 2. На линию старта пластинки наносится шприцом пятно хинолина (хинолин - жидкость), объем пробы 1-5 мкл. Визуально сразу же на пластинке видно «сырое» пятно хинолина на линии старта. Найти исходное пятно хинолина на белом фоне пластинки визуально сложно, поэтому после постановки капли на пластинку на линию старта сразу отмечают на стартовой линии карандашом диаметр исходного пятна. Сразу же, после маркировки пятна, осуществляют стадию сушки пробы - хинолина. Запах хинолина ощущается даже через сутки. После сушки пластинку ставят в закрытую емкость (банку и т.д.) с элюентом - толуолом на восходящую хроматографию. После хроматографирования (элюент дошел до линии финиша) пластинка вынимается. На хроматограмме (анализируемое вещество - хинолин, элюент - толуол) пятно хинолина не уходит со старта, фиг. 1А.
На фиг. 1Б показана хроматография того же хинолина, элюент толуол, но проба хинолина сразу же, после маркировки пятна, не подвергается сушке, и пластинку ставят в закрытую емкость (банку и т.д.) с элюентом - толуолом на хроматографию. После хроматографирования (элюент дошел до линии финиша) пластинка вынимается. На хроматограмме (анализируемое вещество - хинолин, элюент - толуол) хинолин дает длинный пик, не уходящий с линии старта, высота которого зависит от количества хинолина, что коррелируется с диаметром исходного пятна на линии старта (фиг. 1 «Б»). Вывод: хинолин вероятно не образует с толуолом (элюентом) нового соединения в этих условиях.
Используя хинолин, мы визуально видим картины хроматограммы. Если визуальное восприятие отсутствует, то в хроматографическом анализе пользуются набором реагентов для обнаружения пятен (Губен-Вейль. «Методы органической химии. Методы анализа», изд. «ХИМИЯ», Москва, 1967, стр. 883).
Пример 2. Брали хинолин, C9H7N, производства НТМК «чистый» согласно ТУ-6-094326-86. Температурные пределы 235-238°С. В качестве, как растворителя, так и элюента использован толуол С7Н8, ЧДА, ГОСТ 5789-78, изм. №1, 2.
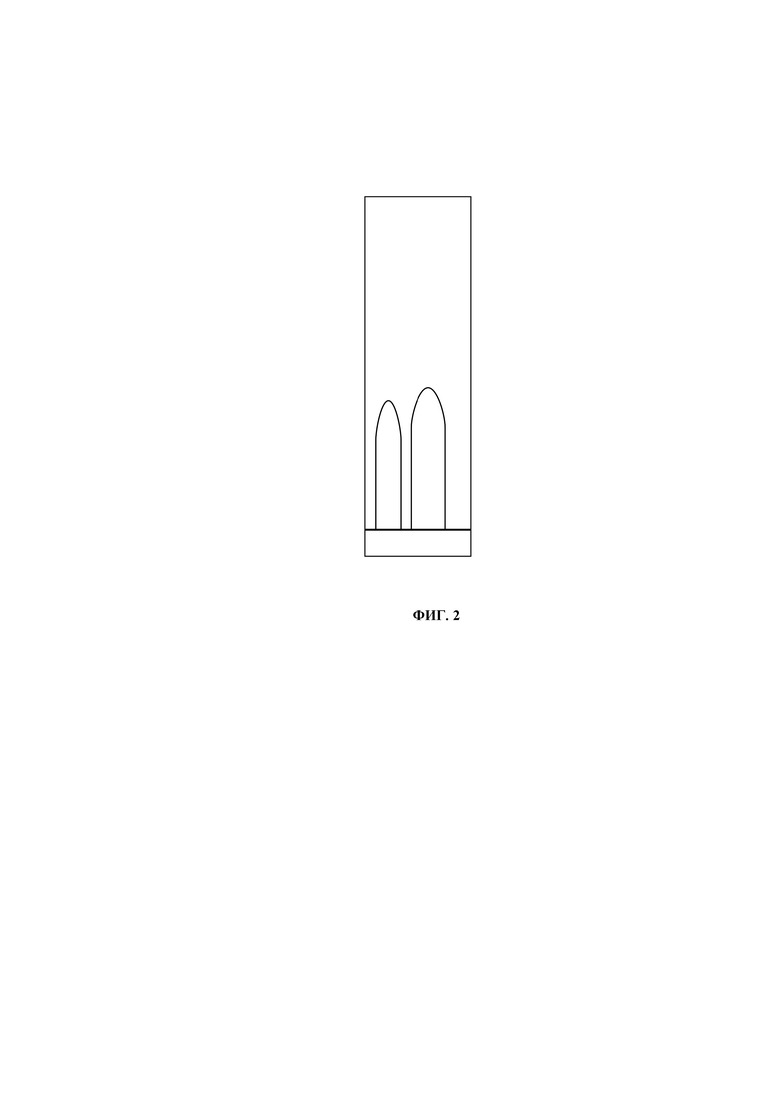
Готовим раствор для хроматографирования в пенициллиновом пузырьке: добавляем с помощью пипеток к 1 части хинолина 2 части толуола. Встряхнули вручную пузырек. Пробу из приготовленной смеси поставили сразу после приготовления смеси на хроматографическую пластинку и без сушки начали хроматографирование. Вид хроматограммы показан на фиг. 2. Констатируем получение язычка (пятна) хинолина. Однако, если оценить высоту язычка, то он оказывается выше, чем язычок, который получается из того же количества хинолина без использования растворителя.
В примере 2 хинолин контактировал с толуолом (элюентом) в течение получения хроматограммы, т.е. около 5 минут и при этом через пятно хинолина происходил постоянный поток нового элюента. Дополнительного вещества (пятна) не было обнаружено.
Пример 3. Брали хинолин, C9H7N, производства НТМК «чистый» согласно ТУ-6-094326-86. Температурные пределы 235-238°С. В качестве как растворителя, так и элюента использован толуол С7Н8, ЧДА, ГОСТ 5789-78, изм. №1, 2. Цель - определить возможное образование супрамолекулярного комплекса при смешивании хинолина с толуолом и необходимое время выдержки смеси.
В примере 3 значительно увеличили время контакта хинолина и толуола до начала хроматографирования.
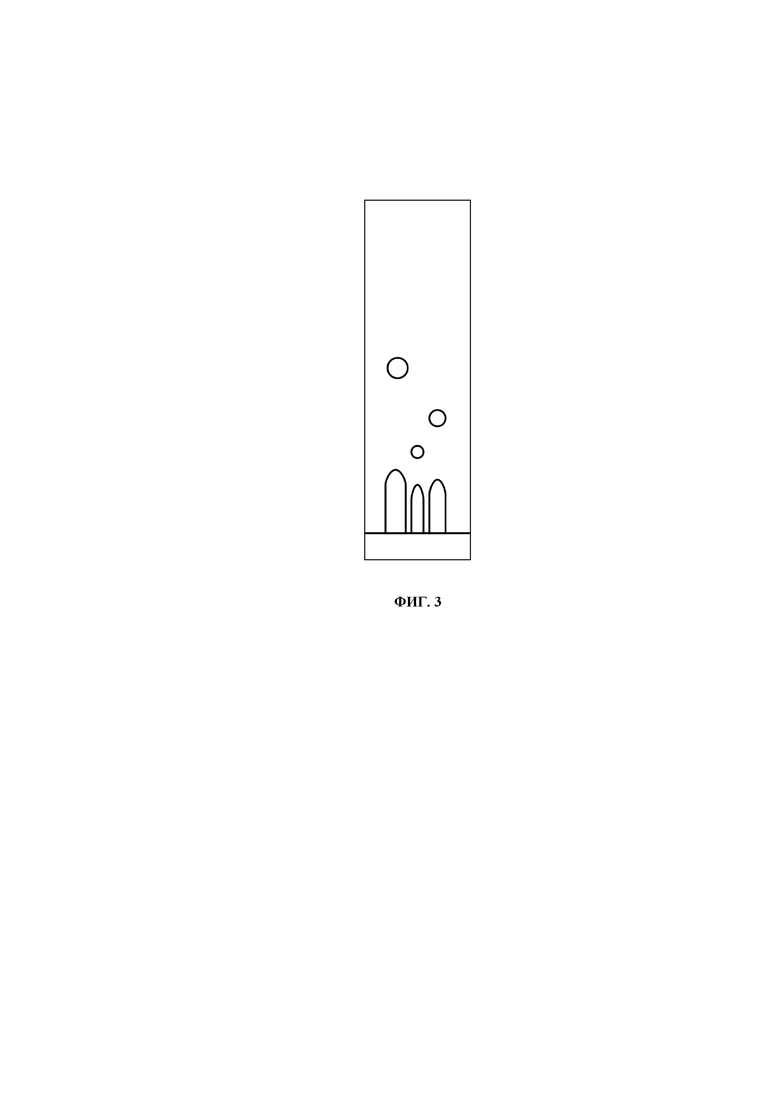
Готовим раствор для хроматографирования в пенициллиновом пузырьке: добавляем с помощью пипеток к 1 части хинолина 2 части толуола. Встряхнули вручную пузырек и его оставили на сутки. После этой выдержки пробу из приготовленной смеси поставили на хроматографическую пластинку и без сушки начали хроматографирование. Хроматограмма представлена на фиг. 3. На рисунке видны: хинолин, уходящий с линии старта в виде язычка, пятно нового соединения (адсорбционный механизм), а толуол не может дать пятна, т.к. в качестве элюента взят также толуол. Следовательно, подобраны условия для получения и анализа молекулярного соединения, образующегося из хинолина и толуола.
Пример 4. Тонкослойное хроматографирование хингидрона C6H4O2⋅C6H4(OH)2.
Цель - показать хроматографию известного (имеющегося в продаже) твердого супрамолекулярного комплекса, клатрата или молекулярного комплекса для описания продуктов ассоциации двух или большего числа молекул применяется также термин молекулярный комплекс (источник: Л. Эндрюс, Р. Кифер Молекулярные комплексы в органической химии, Из-во «МИР» 1967, стр. 11, 17-18, 71).
Чтобы доказать предположение о специфической тонкослойной хроматографии супрамолекулярного комплекса, был использован чистый хингидрон.
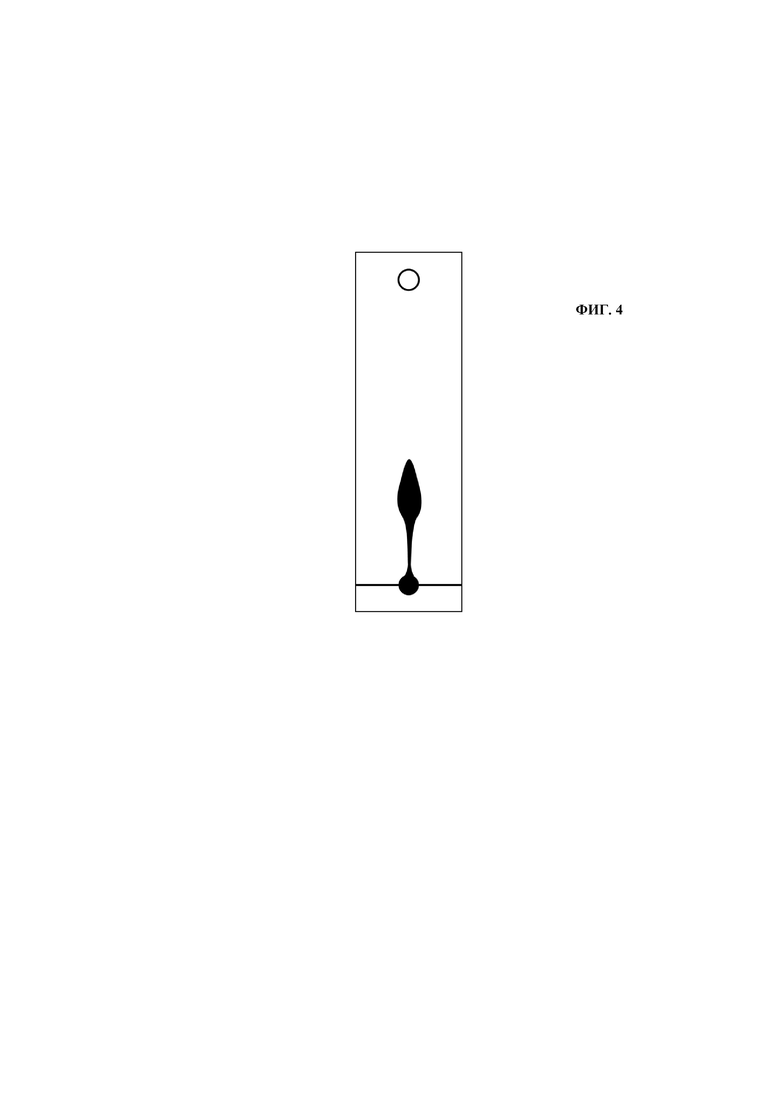
Результат примера 4 представлен на фиг. 4.
Известно (источник: Губен-Вейль«Методы органической химии», том 2 «Методы анализа», изд. «ХИМИЯ», Москва, 1967, стр. 474), что хиноны и гидрохиноны соединяются в растворах или в расплавах и образуют интенсивно окрашенные хингидроны, удобные для идентификации хинонов. Большинство хингидронов устойчиво только в кристаллическом состоянии, в растворе они сильно диссоциируют на составные части и ведут себя как смесь хинона и гидрохинона.
Способ получения хингидрона следующий. Приблизительно эквивалентные количества n-бензохинона С6Н4О2 (желтый цвет, Губен-Вейль «Методы органической химии», том 2 «Методы анализа», изд. «ХИМИЯ», Москва, 1967, стр. 472) и гидрохинона C6H4(ОН)2 (серо-белый цвет) растворяют в воде, оба раствора сливают вместе. Почти моментально кристаллизуются зеленые иглы хингидрона C6H4O2⋅C6H4(OH)2; которые отфильтровывают, промывают водой, сушат (Губен-Вейль «Методы органической химии», том 2 «Методы анализа», изд. «ХИМИЯ», Москва, 1967, стр. 474). Хингидрон применяют в физико-химических исследованиях при определении концентрации водородных ионов и окислительно-восстановительных потенциалов, поэтому это доступный реактив, имеющийся в продаже. Хингидрон, как индивидуальное супрамолекулярное (клатратное) соединение, растворяется в воде и в органических растворителях хуже, чем исходные хинон и гидрохинон (источник: И.С. Иоффе «Органическая химия», Ленинград, Госхимиздат, 1956. стр. 254). Была проведена тонкослойная хроматография этого супрамолекулярного соединения. Объект исследования хингидрон (использован купленный реактив). Тонкослойная хроматограмма представлена на фиг. 4. Визуально определено три пятна. Два исходных веществ и третье пятно гидрохинон.
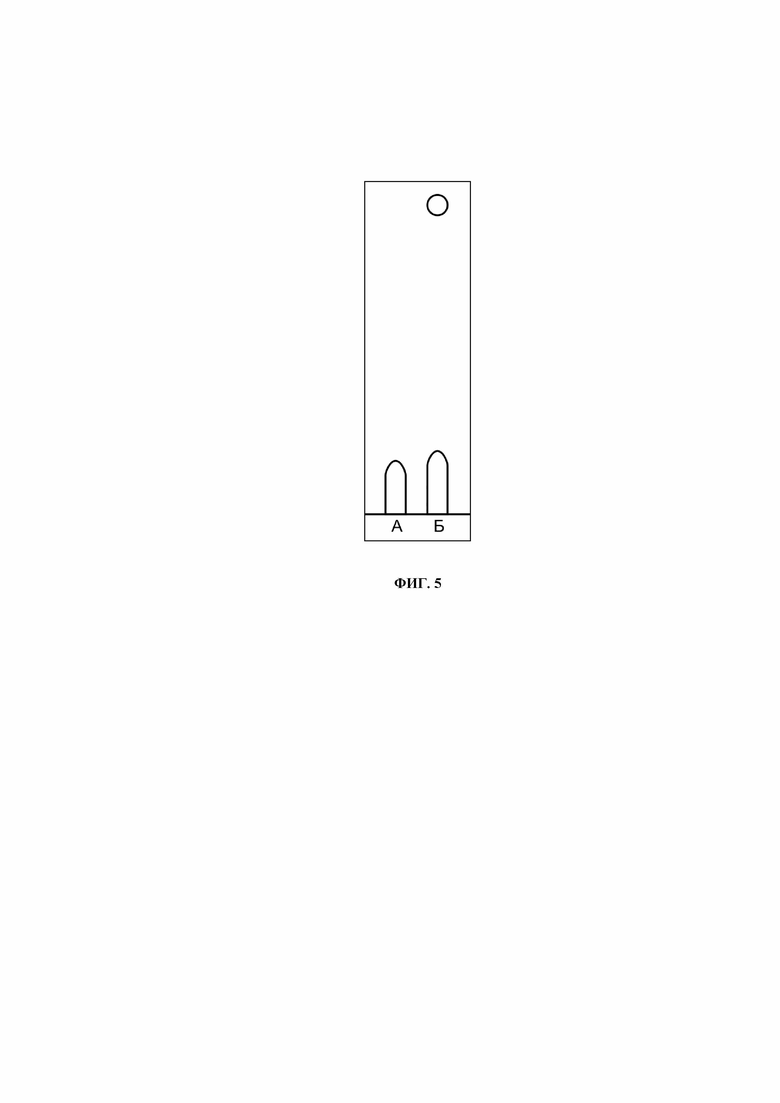
Пример 5. Хинолин в количестве 5 мл (как растворитель) и 0,08 г пирена хорошо смешали в пузырьке. Шприцом отобрали пробу смеси в количестве 5 мкл и поставили на пластину. Сушка пробы отсутствует. Элюент - толуол. Пирен, согласно своего коэффициента распределения (Rf), дал пятно вверху пластины. Также оказалось, что в смеси зона хинолина («язычок» со старта) увеличилась по высоте, что можно замерить линейкой, по сравнению с таким же количеством одного хинолина. Следовательно, на старте остается новое вещество и хинолин. Сделано около 10 хроматограмм, чтобы не ошибиться в наблюдении. Такие же показатели и у смеси хинолин-антрацен и т.д. Результат примера 5 представлен на фиг. 5.
По всем примерам не приводятся хроматограммы отдельно исходных веществ - эталонов, т.к. они образуются и анализируются для сравнения стандартным и известным образом.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА МНОГОКОМПОНЕНТНОГО ВЕЩЕСТВА | 2010 |
|
RU2439552C1 |
| СПОСОБ ХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА ОРГАНИЧЕСКИХ ВЕЩЕСТВ | 2012 |
|
RU2512252C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГРУППОВОГО ФРАКЦИОННОГО СОСТАВА КАМЕНОУГОЛЬНЫХ СМОЛ | 2012 |
|
RU2512620C1 |
| СПОСОБ ВЫДЕЛЕНИЯ МОНОСЛОЯ ВЕЩЕСТВА | 2012 |
|
RU2512630C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КАЧЕСТВА КАМЕННОУГОЛЬНЫХ ПРОДУКТОВ | 2012 |
|
RU2512627C1 |
| СПОСОБ ОБНАРУЖЕНИЯ И ИДЕНТИФИКАЦИИ ВЗРЫВЧАТЫХ ВЕЩЕСТВ | 2007 |
|
RU2336523C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ БЕНЗОКСАЗОЛОНА-2 И 6-ХЛОРБЕНЗОКСАЗОЛОНА-2 В ПРОИЗВОДСТВЕ ПЕСТИЦИДОВ, ОТНОСЯЩИХСЯ К ПРОИЗВОДНЫМ БЕНЗОКСАЗОЛОНА-2, ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИЕЙ | 1991 |
|
RU2018825C1 |
| СПОСОБ ПРОВЕДЕНИЯ ПРОТОЧНОЙ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ И УСТРОЙСТВО ДЛЯ ЕГО РЕАЛИЗАЦИИ | 2000 |
|
RU2216018C2 |
| Способ определения 4-нитроанилина и продуктов его хлорирования в смеси | 1986 |
|
SU1385068A1 |
| Способ оценки качества нефтяных моторных топлив по оперативно определяемому содержанию метиловых эфиров жирных кислот | 2024 |
|
RU2838147C1 |
Изобретение относится к области аналитической химии. Способ хроматографического анализа органических веществ включает тонкослойное хроматографирование смеси, образованной из двух исходных известных индивидуальных органических веществ, обладающих заранее известными характеристиками – эталонами, для анализа готовят пригодную для хроматографирования пробу в виде раствора из смеси исходных индивидуальных органических веществ, часть полученного раствора выдерживают в течение времени не менее 30 минут для возможного взаимодействия исходных индивидуальных веществ, на линию старта хроматографической пластины наносят первую пробу раствора, не подвергшегося выдержке, также на линию старта этой же или другой хроматографической пластины наносят вторую пробу раствора, подвергшегося выдержке, обе пробы помещают в элюент, помещение обеих проб в элюент осуществляют до их высыхания на хроматографической пластине, сравнивают проявившиеся на пластине после хроматографирования пятна от первой и второй пробы, вывод об образовании супрамолекулярного соединения делают по наличию на пластине помимо проявившихся от второй пробы пятен исходных индивидуальных веществ дополнительного проявившегося пятна с характеристиками, отличными от эталонов, проявившихся на пластине от первой пробы, или по отклонению характеристики одного из проявившихся пятен от второй пробы от эталона соответствующего исходного индивидуального вещества, проявившегося от первой пробы. Техническим результатом является расширение арсенала средств, позволяющих устанавливать характер соединения. 1 з.п. ф-лы, 5 ил.
1. Способ хроматографического анализа органических веществ, включающий тонкослойное хроматографирование смеси, образованной из двух исходных известных индивидуальных органических веществ, обладающих заранее известными характеристиками – эталонами, для анализа готовят пригодную для хроматографирования пробу в виде раствора из смеси исходных индивидуальных органических веществ, отличающийся тем, что часть полученного раствора выдерживают в течение времени не менее 30 минут для возможного взаимодействия исходных индивидуальных веществ, на линию старта хроматографической пластины наносят первую пробу раствора, не подвергшегося выдержке, также на линию старта этой же или другой хроматографической пластины наносят вторую пробу раствора, подвергшегося выдержке, обе пробы помещают в элюент, помещение обеих проб в элюент осуществляют до их высыхания на хроматографической пластине, сравнивают проявившиеся на пластине после хроматографирования пятна от первой и второй пробы, вывод об образовании супрамолекулярного соединения делают по наличию на пластине помимо проявившихся от второй пробы пятен исходных индивидуальных веществ дополнительного проявившегося пятна с характеристиками, отличными от эталонов, проявившихся на пластине от первой пробы, или по отклонению характеристики одного из проявившихся пятен от второй пробы от эталона соответствующего исходного индивидуального вещества, проявившегося от первой пробы.
2. Способ по п. 1, отличающийся тем, что в качестве растворителя смеси исходных индивидуальных органических веществ используют элюент.
| СПОСОБ ХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА МНОГОКОМПОНЕНТНОГО ВЕЩЕСТВА | 2010 |
|
RU2439552C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУПРАМОЛЕКУЛЯРНОГО ГИДРОГЕЛЯ | 2016 |
|
RU2641111C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КАЧЕСТВЕННОГО СОСТАВА ОРГАНИЧЕСКИХ ВЕЩЕСТВ В ОБЪЕКТАХ ОКРУЖАЮЩЕЙ СРЕДЫ | 2005 |
|
RU2299432C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ХИМИЧЕСКОГО СОСТАВА ВЕЩЕСТВА И ЭНЕРГИЙ СВЯЗИ ОСТОВНЫХ ЭЛЕКТРОНОВ | 2000 |
|
RU2170421C1 |
Авторы
Даты
2020-04-21—Публикация
2019-07-30—Подача