ПЕРЕКРЕСТНАЯ ССЫЛКА НА СВЯЗАННЫЕ ЗАЯВКИ
[0001] По настоящей заявке испрашивается приоритет патентной заявки США с серийным № 61/919347, зарегистрированной 20 декабря 2013 года, которая полностью включена в настоящий документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0002] Настоящее изобретение, в числе прочего, относится к способам, наборам и фармацевтическим композициям для лечения или смягчение действия злокачественной опухоли у индивидуума с применением (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF типа 1, такой как дабрафениб или его фармацевтически приемлемая соль, для лечения или смягчение действия злокачественной опухоли.
ВКЛЮЧЕНИЕ СПИСКА ПОСЛЕДОВАТЕЛЬНОСТЕЙ ПОСРЕДСТВОМ ССЫЛКИ
[0003] Настоящая заявка содержит ссылки на последовательности аминокислот и/или нуклеиновых кислот, которые поданы одновременно с ней в виде текстового файла со списком последовательностей "0375604.txt", размером файла 255 KB, датой создания 19 декабря 2014 года. Таким образом, указанный выше список последовательностей полностью включен посредством ссылки в соответствии с 37 C.F.R. 1.52(e)(5).
УРОВЕНЬ ТЕХНИКИ, ПРЕДШЕСТВУЮЩИЙ ИЗОБРЕТЕНИЮ
[0004] Ингибиторы лекарственных средств, которые нацелены на компоненты пути передачи сигнала митоген-активируемых протеинкиназ (MAPK), демонстрируют клиническую эффективность для ряда злокачественных опухолей, в частности, злокачественных опухолей, несущих мутации в протеинкиназе BRAF. Ингибиторы киназ RAF и MEK одобрены для применения в качестве единственного средства при метастатической меланоме с мутантной BRAF на поздней стадии, и комбинация дабрафениба и траметиниба в настоящее время проходит рассмотрение для этого показания в управлении по контролю за качеством пищевых продуктов и лекарственных средств (FDA). Отдельно или в комбинации, ингибиторы BRAF и MEK демонстрируют вариабельную активность при других злокачественных опухолях с возможной эффективностью при раке щитовидной железы и легких с мутантной BRAF, а также возможной маргинальной активностью при колоректальном раке с мутантной BRAF.
[0005] При применении ингибиторов BRAF и MEK наблюдают различные профили клинической эффективности. Степень и проявление исходной регрессии опухоли, а также длительность ответа перед прогрессированием заболевания уникальным образом варьируют в зависимости от каждого класса лекарственных средств при введении отдельно или при введении при любой из стратегий комбинирования с последовательным или одновременным введением. В настоящее время предпочтительным вмешательством при обусловленной мутантной BRAF меланоме, по-видимому, является одновременное комбинированное лечение дабрафенибом и траметинибом.
[0006] Как и для других лечебных средств направленного действия, на профили реакции заболевания на ингибиторы RAF и MEK по-видимому, влияет генетическая гетерогенность, существующая в злокачественных опухолях, при которых используют лекарственные средства. Например, показано, что при определенных генетических альтерациях, включая PTEN и другие изменения, которые активируют сигналы роста клеток, обусловленные PI3K, при обусловленной мутантной BRAF меланоме, подвергаемой лечению ингибитором RAF вемурафенибом, можно прогнозировать плохой исходный ответ и/или относительно быстрое прогрессирование. Подобным образом, в опухолях, которые прогрессируют после лечения лекарственными средствами против BRAF, MEK или комбинированными лекарственными средствами, по-видимому, возникают прямые мутации в локусах гена MEK. Несколько дополнительных примеров, основанных на мутациях амплификации и сплайсинга генов RAS и RAF, позволяют предположить, что когда онкогенная плейотропность сталкивается с селективным давлением лечения лекарственными средствами направленного действия, вырабатывается приобретенная устойчивость к лекарственным средствам.
[0007] Таким образом, новые средства направленного действия теоретически могли бы ингибировать различные узловые точки онкогенных метаболических путей, а также являться эффективными в комбинациях, увеличивая силу селективного давления, которое превзошло бы адаптивную способность различных злокачественных геномов. Настоящая заявка, в числе прочего, направлена на удовлетворении постребности в новых средствах направленного действия.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0008] Одним из вариантов осуществления настоящего изобретения является способ лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Этот способ включает введение индивидууму эффективного количества (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF типа 1 или его фармацевтически приемлемую соль, для лечения или смягчения действия злокачественной опухоли.
[0009] Другой вариант осуществления настоящего изобретения представляет собой способ лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Этот способ включает введение индивидууму эффективного количества (i) BVD-523 или его фармацевтически приемлемой соли, и (ii) второго средства против злокачественной опухоли, которое представляет собой дабрафениб или его фармацевтически приемлемую соль, для лечения или смягчения действия злокачественной опухоли.
[0010] Дополнительный вариант осуществления настоящего изобретения представляет собой способ уничтожения злокачественной клетки. Этот способ включает приведение злокачественной клетки в контакт с эффективным количеством (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF типа 1 или его фармацевтически приемлемую соль.
[0011] Дополнительный вариант осуществления настоящего изобретения представляет собой набор для лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Этот набор содержит эффективное количество (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF типа 1 или его фармацевтически приемлемую соль, упакованные вместе с инструкциями по их применению.
[0012] Дополнительный вариант осуществления настоящего изобретения представляет собой фармацевтическая композиция для лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Эта фармацевтическая композиция содержит фармацевтически приемлемый разбавитель или носитель и эффективное количество (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF типа 1 или его фармацевтически приемлемую соль, где введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно.
[0013] Другой вариант осуществления настоящего изобретения представляет собой способ лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Этот способ включает введение индивидууму эффективного количества (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF, выбранный из группы, состоящей из AAL881 (Novartis); AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BeiGene-283 (BeiGene), BIIB-024 (MLN 2480) (Sunesis & Takeda), ингибитора b-raf (Sareum), ингибитора киназы BRAF (Selexagen Therapeutics), миРНК 313 (tacaccagcaagctagatgca) и 253 (cctatcgttagagtcttcctg) BRAF (Liu et al., 2007), CTT239065 (Institute of Cancer Research), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), LErafAON (NeoPharm, Inc.), LBT613 (Novartis), LGX-818 (Novartis), пазопаниба (GlaxoSmithKline), PLX5568 (Plexxikon), RAF-265 (Novartis), RAF-365 (Novartis), регорафениба (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), TAK 632 (Takeda), TL-241 (Teligene), XL-281 (Exelixis), их фармацевтически приемлемых солей и их сочетаний, для лечения или смягчения действия злокачественной опухоли.
[0014] Дополнительный вариант осуществления настоящего изобретения представляет собой способ уничтожения злокачественной клетки. Этот способ включает приведение злокачественной клетки в контакт с эффективным количеством (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF, выбранный из группы, состоящей из AAL881 (Novartis); AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BeiGene-283 (BeiGene), BIIB-024 (MLN 2480) (Sunesis & Takeda), ингибитора b-raf (Sareum), ингибитора киназы BRAF (Selexagen Therapeutics), миРНК 313 (tacaccagcaagctagatgca) и 253 (cctatcgttagagtcttcctg) BRAF, CTT239065 (Institute of Cancer Research), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), LErafAON (NeoPharm, Inc.), LBT613 (Novartis), LGX-818 (Novartis), пазопаниба (GlaxoSmithKline), PLX5568 (Plexxikon), RAF-265 (Novartis), RAF-365 (Novartis), регорафениба (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), TAK 632 (Takeda), TL-241 (Teligene), XL-281 (Exelixis), их фармацевтически приемлемых солей и их сочетаний.
[0015] Дополнительный вариант осуществления настоящего изобретения представляет собой набор для лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Этот набор содержит эффективное количество (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF, выбранный из группы, состоящей из AAL881 (Novartis); AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BeiGene-283 (BeiGene), BIIB-024 (MLN 2480) (Sunesis & Takeda), ингибитора b-raf (Sareum), ингибитора киназы BRAF (Selexagen Therapeutics), миРНК 313 (tacaccagcaagctagatgca) и 253 (cctatcgttagagtcttcctg) BRAF, CTT239065 (Institute of Cancer Research), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), LErafAON (NeoPharm, Inc.), LBT613 (Novartis), LGX-818 (Novartis), пазопаниба (GlaxoSmithKline), PLX5568 (Plexxikon), RAF-265 (Novartis), RAF-365 (Novartis), регорафениба (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), TAK 632 (Takeda), TL-241 (Teligene), XL-281 (Exelixis), их фармацевтически приемлемых солей и их сочетаний, упакованных вместе с инструкциями по их применению.
[0016] Другой вариант осуществления настоящего изобретения представляет собой фармацевтическую композицию для лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Эта фармацевтическая композиция содержит фармацевтически приемлемый разбавитель или носитель и эффективное количество (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF, выбранный из группы, состоящей из AAL881 (Novartis); AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BeiGene-283 (BeiGene), BIIB-024 (MLN 2480) (Sunesis & Takeda), ингибитора b-raf (Sareum), ингибитора киназы BRAF (Selexagen Therapeutics), миРНК 313 (tacaccagcaagctagatgca) и 253 (cctatcgttagagtcttcctg) BRAF, CTT239065 (Institute of Cancer Research), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), LErafAON (NeoPharm, Inc.), LBT613 (Novartis), LGX-818 (Novartis), пазопаниба (GlaxoSmithKline), PLX5568 (Plexxikon), RAF-265 (Novartis), RAF-365 (Novartis), регорафениба (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), TAK 632 (Takeda), TL-241 (Teligene), XL-281 (Exelixis), их фармацевтически приемлемых солей и их сочетаний, где введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0017] Материалы патента или заявки содержат по меньшей мере один чертеж, выполненный в цвете. Копии этого патента или публикации патентной заявки с цветным чертежом(ами) предоставляются агентством при запросе и оплате необходимых отчислений.
[0018] На фиг. 1A-C представлен ход исследования с увеличением дозы на линии клеток злокачественной меланомы человека (клетки A375) в течение месяца 1. Различные лечебные средства (траметиниб (ингибитор MEK типа 2), дабрафениб (ингибитор BRAF) и BVD-523 (ингибитор ERK1/2)) являются такими, как обозначено.
[0019] На фиг. 2A-H представлены результаты анализа пролиферации, в котором отслеживаются изменения в чувствительности на увеличиваемые дозы средств(а) в течение месяца 1. Различные лечебные средства (траметиниб, дабрафениб, BVD-523 и паклитаксел) являются такими, как обозначено вверху диаграммы. Подпись справа от диаграммы демонстрирует различные типы клеток, получаемые при исследовании с увеличением дозы. Например, "дабрафениб" относится к клеткам, которые обрабатывали наибольшей дозой дабрафениба, начиная с месяца 1 исследования с увеличением дозы. Первичный относится к контрольным клеткам, которые не обрабатывали лекарственными средствами. Фиг. 2A-2C и 2G нормализованы на контроль, тогда как на фиг. 2D-2F и 2H представлены необработанные данные.
[0020] На фиг. 3A-3D представлен ход исследования с увеличением дозы в клетках A375 в течение месяца 2. Различные лекарственные средства (траметиниб, дабрафениб и BVD-523) являются такими, как обозначено.
[0021] На фиг. 4A-H представлены результаты анализа пролиферации, в котором отслеживаются изменения в чувствительности на увеличиваемые дозы средств(а) в течение месяца 2. Различные лечебные средства (траметиниб, дабрафениб, BVD-523 и паклитаксел) являются такими, как обозначено вверху диаграммы. Подпись справа от диаграммы демонстрирует различные типы клеток, получаемые при исследовании с увеличением дозы. Например, "дабрафениб" относится к клеткам, которые обрабатывали наибольшей дозой дабрафениба, начиная с месяца 2 исследования с увеличением дозы. Исходные относится к контрольным клеткам, которые не обрабатывали лекарственными средствами. Фиг. 4A-4C и 4G нормализованы на контроль, тогда как фиг. 4D-4F и 4H демонстрируют необработанные данные.
[0022] На фиг. 5A-H представлены данные только для исходной линии клеток и линии клеток BVD-523 с ФИГ. 4. Различные лечебные средства (траметиниб, дабрафениб, BVD-523 и паклитаксел) являются такими, как обозначено. Фиг. 5A-5C и 5G нормализованы на контроль, тогда как фиг. 5D-5F и 5H демонстрируют необработанные данные.
[0023] На фиг. 6A-D представлен ход исследования с увеличением дозы на линии злокачественных клеток человека (клетки A375) в течение месяца 3. Различные лечебные средства (траметиниб, дабрафениб, и BVD-523) являются такими, как обозначено.
[0024] Фиг. 7 представляет собой гистограмму, демонстрирующую результаты анализа пролиферации в применении к клеткам, выращиваемым в лунках с контролем DMSO, при анализе с увеличением дозы.
[0025] Фиг. 8A-D представляют собой группу линейных графиков, демонстрирующую анализы пролиферации в течение месяца 3 исследования. Различные лечебные средства (траметиниб, дабрафениб, BVD-523 и паклитаксел) являются такими, как обозначено вверху диаграммы. Подпись справа от диаграммы демонстрирует различные типы клеток, получаемых при исследовании с увеличением дозы. Например, "дабрафениб" относится к клеткам, которые обрабатывали наибольшей дозой дабрафениба, начиная с месяца 3 исследования с увеличением дозы. Исходные относится к контрольным клеткам, которые не обрабатывали лекарственными средствами.
[0026] На фиг. 9A-D представлены только данные для исходной линии клеток, линии клеток дабрафениба и линии клеток BVD-523 с ФИГ. 8.
[0027] Фиг. 10A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации траметиниба/дабрафениба в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 10B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации траметиниба/дабрафениба. Фиг. 1°C и 10D демонстрируют % жизнеспособности при обработке дабрафенибом и траметинибом в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 10E представлен % жизнеспособности при комбинированной обработке дабрафенибом и траметинибом относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0028] Фиг. 11A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации траметиниба/дабрафениба в клетках A375 с использованием анализа жизнеспособности клеток CellTiter-Glo. Фиг. 11B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации траметиниба/дабрафениба. Фиг. 11C и 11D демонстрируют % жизнеспособности при обработке дабрафенибом и траметинибом в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток CellTiter-Glo. На фиг. 11E представлен % жизнеспособности при комбинированной обработке дабрафенибом и траметинибом относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток CellTiter-Glo.
[0029] Фиг. 12A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации BVD-523/дабрафениба в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 12B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации BVD-523/дабрафениба. Фиг. 12C и 12D демонстрируют % жизнеспособности при обработке дабрафенибом и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 12E представлен % жизнеспособности при комбинированной обработке дабрафенибом и BVD-523 относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0030] Фиг. 13A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации BVD-523/дабрафениба в клетках A375 с использованием анализа жизнеспособности клеток CellTiter-Glo. Фиг. 13B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации BVD-523/дабрафениба. Фиг. 13C и 13D демонстрируют % жизнеспособности при обработке дабрафенибом и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток CellTiter-Glo. На фиг. 13E представлен % жизнеспособности при комбинированной обработке дабрафенибом и BVD-523 относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток CellTiter-Glo.
[0031] Фиг. 14A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации траметиниба/BVD-523 в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 14B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации траметиниба/BVD-523. Фиг. 14C и 14D демонстрируют % жизнеспособности при обработке BVD-523 и траметинибом в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 14E представлен % жизнеспособности при комбинированной обработке BVD-523 и траметинибом относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0032] Фиг. 15A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации траметиниба/BVD-523 в клетках A375 с использованием анализа жизнеспособности клеток CellTiter-Glo. Фиг. 15B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации траметиниба/BVD-523. Фиг. 15C и 15D демонстрируют % жизнеспособности при обработке BVD-523 и траметинибом в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток CellTiter-Glo. На фиг. 15E представлен % жизнеспособности при комбинированной обработке BVD-523 и траметинибом относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток CellTiter-Glo.
[0033] Фиг. 16A-D представляют собой группу изображений, демонстрирующих анализ вестерн-блоттинга передачи сигналов MAPK в клетках A375 через 4 часа обработки различными концентрациями (в нМ) BVD-523, дабрафениба (Даб) и траметиниба (Трам). На каждую дорожку, за исключением тех, где указано иначе, внесено всего по 40 мкг белка. В этом эксперименте собирали дублированные образцы. Фиг. 16A и 16B демонстрируют результаты, полученные на дублированных образцах. Подобным образом, на фиг. 16C и 16D также представлены результаты, полученные на дублированных образцах. На фиг. 16A и 16B у pRSK1 выявлен относительно слабый сигнал в клетках A375 по сравнению с другими маркерами. Тестировали другое антитело к pRSK1-S380 из Cell Signaling (кат. № 11989) тестировали, но детектируемого сигнала не получили (данные не показаны). На фиг. 16C и 16D pCRAF-338 давала минимальный сигнал.
[0034] Фиг. 17A-D представляют собой группу изображений, демонстрирующий анализ вестерн-блоттинга передачи сигналов MAPK в линии клеток колоректальной карциномы человека (клетки HCT116) через 4 часа после обработки различными концентрациями (в нМ) BVD-523, дабрафениба (Даб) и траметиниба (Трам). На каждую дорожку, за исключением тех, где указано иначе, внесено всего по 40 мкг белка. В этом эксперименте собирали дублированные образцы. Фиг. 17A и 17B демонстрируют результаты, полученные на дублированных образцах. Подобным образом, на фиг. 17C и 17D также представлены результаты, полученные на дублированных образцах. На фиг. 17A-17B, уровни pRSK1 в клетках HCT116 выглядят очень низкими, а на фиг. 17C и 17D, сигнал pCRAF-338 также был очень слабым.
[0035] Фиг. 18A-D представляют собой группу изображений, демонстрирующих анализ вестерн-блоттинга белков клеточного цикла и апоптоз в клетках меланомы A375 через 24 часа после обработки различными концентрациями (в нМ) BVD-523 ("BVD523"), траметиниба ("трам") и/или дабрафениба ("Даб"), как обозначено. На каждую дорожку, за исключением тех, где указано иначе, внесено всего по 50 мкг белка. В этом эксперименте собирали дублированные образцы. Фиг. 18A и 18B демонстрируют результаты, полученные на дублированных образцах. Подобным образом, на фиг. 18C и 18D также представлены результаты, полученные на дублированных образцах. На фиг. 18A и 18B не видно ни одной полосы размера, соответствующего расщепленной PARP (89 кДа).
[0036] Фиг. 19 представляет собой гистограмму, демонстрирующую жизнеспособность клеток A375 через 96 часов инкубации с различными количествами BVD-523 или BVD-523 в комбинации с 30 нМ AZ628 (ингибитор RAF) или 3 нМ дабрафенибом. Показатели по Блиссу представлены в желтых рамках.
[0037] Фиг. 20 представляет собой гистограмму, демонстрирующую каспазную активность в клетках A375 через 24 часа инкубации с различными количествами BVD-523 или BVD-523 в комбинации с 30 нМ AZ628 или 3 нМ дабрафенибом.
[0038] Фиг. 21 представляет собой гистограмму, демонстрирующую каспазную активность в клетках A375 через 48 часов инкубации с различными количествами BVD-523 или BVD-523 в комбинации с 30 нМ AZ628 или 3 нМ дабрафенибом.
[0039] Фиг. 22 представляет собой гистограмму, демонстрирующую жизнеспособность клеток HCT116 через 96 часов инкубации с различными количествами BVD-523 или BVD-523 в комбинации с 3 мкМ ABT-263. Показатели по Блиссу представлены в желтых рамках.
[0040] Фиг. 23 представляет собой гистограмму, демонстрирующую каспазную активность в клетках HCT116 через 24 часа инкубации с различными количествами BVD-523 или BVD-523 в комбинации с 3 мкМ ABT-263.
[0041] Фиг. 24 представляет собой гистограмму, демонстрирующую каспазную активность в клетках HCT116 через 48 часов инкубации с различными количествами BVD-523 или BVD-523 в комбинации с 3 мкМ ABT-263.
[0042] Фиг. 25 представляет собой блок-схему, демонстрирующую протокол увеличения дозы, используемый в настоящем документе.
[0043] На фиг. 26 представлены индивидуальные временные интервалы до конечных точек для мышей в исследовании.
[0044] На фиг. 27 представлен средний рост опухоли (фиг. 27A) и диаграмма Каплана-Мейера (фиг. 27B) для исследования.
[0045] На фиг. 28A-28D представлен средний рост опухоли в различных группах мышей, которым вводили комбинации дабрафениба/BVD-523, по сравнению с монотерапией.
[0046] На фиг. 29 представлен процент изменения средней массы тела, начиная с суток 1, в исследовании in vivo.
[0047] На фиг. 30 схематически представлены сигнальный путь митоген-активируемых протеинкиназ (MAPK).
[0048] Фиг. 31A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации AZ628/траметиниба в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 31B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации AZ628/траметиниба. Фиг. 31C и 31D демонстрируют % жизнеспособности при обработке AZ628 и траметинибом в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 31E представлен % жизнеспособности при комбинированной обработке AZ628/траметинибом относительно контролей, обработанных только DMSO, в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0049] Фиг. 32A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации AZ628/BVD-523 в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 32B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации AZ628/BVD-523. Фиг. 32C и 32D демонстрируют % жизнеспособности при обработке AZ628 и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 32E представлен % жизнеспособности при комбинированной обработке AZ628/BVD-523 относительно контролей, обработанных только DMSO, в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0050] Фиг. 33A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации сорафениба/траметиниба в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 33B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации сорафениба/траметиниба. Фиг. 33C и 33D демонстрируют % жизнеспособности при обработке сорафенибом и траметинибом в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 33E представлен % жизнеспособности при комбинированной обработке сорафенибом/траметинибом относительно контролей, обработанных только DMSO, в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0051] Фиг. 34A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации сорафениба/BVD-523 в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 34B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации сорафениба/BVD-523. Фиг. 34C и 34D демонстрируют % жизнеспособности при обработке сорафенибом и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 34E представлен % жизнеспособности при комбинированной обработке сорафенибом/BVD-523 относительно контролей, обработанных только DMSO, в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0052] Фиг. 35A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации дабрафениба/траметиниба в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 35B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации дабрафениба/траметиниба. Фиг. 35C и 35D демонстрируют % жизнеспособности при обработке дабрафенибом и траметинибом в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 35E представлен % жизнеспособности при комбинированной обработке дабрафенибом/траметинибом относительно контролей, обработанных только DMSO, в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0053] Фиг. 36A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации дабрафениба/BVD-523 в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 36B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации дабрафениба/BVD-523. Фиг. 36C и 36D демонстрируют % жизнеспособности при обработке дабрафенибом и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 36E представлен % жизнеспособности при комбинированной обработке дабрафенибом/BVD-523 относительно контролей, обработанных только DMSO, в клетках HCT116 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0054] Фиг. 37A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации AZ628/BVD-523 в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 37B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации AZ628/BVD-523. Фиг. 37C и 37D демонстрируют % жизнеспособности при обработке AZ628 и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 37E представлен % жизнеспособности при комбинированной обработке AZ628/BVD-523 относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0055] Фиг. 38A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации сорафениба/траметиниба в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 38B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации сорафениба/траметиниба. Фиг. 38C и 38D демонстрируют % жизнеспособности при обработке сорафенибом и траметинибом в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 38E представлен % жизнеспособности при комбинированной обработке сорафенибом/траметинибом относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0056] Фиг. 39A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации сорафениба/BVD-523 в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 39B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации сорафениба/BVD-523. Фиг. 39C и 39D демонстрируют % жизнеспособности при обработке сорафенибом и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 39E представлен % жизнеспособности при комбинированной обработке сорафенибом/BVD-523 относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0057] Фиг. 40A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации дабрафениба/траметиниба в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 40B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации дабрафениба/траметиниба. Фиг. 4°C и 40D демонстрируют % жизнеспособности при обработке дабрафенибом и траметинибом в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 40E представлен % жизнеспособности при комбинированной обработке дабрафенибом/траметинибом относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0058] Фиг. 41A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации дабрафениба/BVD-523 в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. Фиг. 41B представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации дабрафениба/BVD-523. Фиг. 41C и 41D демонстрируют % жизнеспособности при обработке дабрафенибом и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue. На фиг. 41E представлен % жизнеспособности при комбинированной обработке дабрафенибом/BVD-523 относительно контролей, обработанных только DMSO, в клетках A375 с использованием анализа жизнеспособности клеток с Alamar Blue.
[0059] На фиг. 42 представлены результаты анализов пролиферации с единственным средством в клетках A375 (фиг. 42A - ФИГ. 42F) и G-361 (фиг. 42G - ФИГ. 42L). Результаты пролиферации представлены для обработки дабрафенибом (фиг. 42A и ФИГ. 42G), вемурафенибом (фиг. 42B и ФИГ. 42H), TAK-632 (фиг. 42C и ФИГ. 42I), BVD-523 (фиг. 42D и ФИГ. 42J), SCH772984 (фиг. 42E и ФИГ. 42K) и паклитакселом (фиг. 42F и ФИГ. 42L).
[0060] Фиг. 43A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации дабрафениба/BVD-523 в клетках A375. Фиг. 43B представляет собой матрицу доз, демонстрирующую приращение по Леве для комбинации дабрафениба/BVD-523. Фиг. 43C представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации дабрафениба/BVD-523. Фиг. 43D и 43E, соответственно, демонстрируют % жизнеспособности при обработке дабрафенибом и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375.
[0061] Фиг. 44A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации дабрафениба/SCH772984 в клетках A375. Фиг. 43B представляет собой матрицу доз, демонстрирующую приращение по Леве для комбинации дабрафениба/SCH772984. Фиг. 43C представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации дабрафениба/SCH772984. Фиг. 43D и 43E, соответственно, демонстрируют % жизнеспособности при обработке дабрафенибом и SCH772984 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375.
[0062] Фиг. 45A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации вемурафениба/BVD-523 в клетках A375. Фиг. 45B представляет собой матрицу доз, демонстрирующую приращение по Леве для комбинации вемурафениба/BVD-523. Фиг. 45C представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации вемурафениба/BVD-523. Фиг. 45D и 45E, соответственно, демонстрируют % жизнеспособности при обработке вемурафенибом и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375.
[0063] Фиг. 46A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации вемурафениба/SCH772984 в клетках A375. Фиг. 46B представляет собой матрицу доз, демонстрирующую приращение по Леве для комбинации вемурафениба/SCH772984. Фиг. 46C представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации вемурафениба/SCH772984. Фиг. 46D и 46E, соответственно, демонстрируют % жизнеспособности при обработке вемурафенибом и SCH772984 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375.
[0064] Фиг. 47A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации TAK-632/BVD-523 в клетках A375. Фиг. 47B представляет собой матрицу доз, демонстрирующую приращение по Леве для комбинации TAK-632/BVD-523. Фиг. 47C представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации TAK-632/BVD-523. Фиг. 47D и 47E, соответственно, демонстрируют % жизнеспособности при обработке TAK-632 и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375.
[0065] Фиг. 48A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации TAK-632/SCH772984 в клетках A375. Фиг. 48B представляет собой матрицу доз, демонстрирующую приращение по Леве для комбинации TAK-632/SCH772984. Фиг. 48C представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации TAK-632/SCH772984. Фиг. 48D и 48E, соответственно, демонстрируют % жизнеспособности при обработке TAK-632 и SCH772984 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках A375.
[0066] Фиг. 49A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации дабрафениба/BVD-523 в клетках G-361. Фиг. 49B представляет собой матрицу доз, демонстрирующую приращение по Леве для комбинации дабрафениба/BVD-523. Фиг. 49C представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации дабрафениба/BVD-523. Фиг. 49D и 49E, соответственно, демонстрируют % жизнеспособности при обработке дабрафенибом и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках G-361.
[0067] Фиг. 50A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации дабрафениба/SCH772984 в клетках G-361. Фиг. 50B представляет собой матрицу доз, демонстрирующую приращение по Леве для комбинации дабрафениба/SCH772984. Фиг. 5°C представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации дабрафениба/SCH772984. Фиг. 50D и 50E, соответственно, демонстрируют % жизнеспособности при обработке дабрафенибом и SCH772984 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках G-361.
[0068] Фиг. 51A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации вемурафениба/BVD-523 в клетках G-361. Фиг. 51B представляет собой матрицу доз, демонстрирующую приращение по Леве для комбинации вемурафениба/BVD-523. Фиг. 51C представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации вемурафениба/BVD-523. Фиг. 51D и 51E, соответственно, демонстрируют % жизнеспособности при обработке вемурафенибом и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках G-361.
[0069] Фиг. 52A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации вемурафениба/SCH772984 в клетках G-361. Фиг. 52B представляет собой матрицу доз, демонстрирующую приращение по Леве для комбинации вемурафениба/SCH772984. Фиг. 52C представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации вемурафениба/SCH772984. Фиг. 52D и 52E, соответственно, демонстрируют % жизнеспособности при обработке вемурафенибом и SCH772984 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках G-361.
[0070] Фиг. 53A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации TAK-632/BVD-523 в клетках G-361. Фиг. 53B представляет собой матрицу доз, демонстрирующую приращение по Леве для комбинации TAK-632/BVD-523. Фиг. 53C представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации TAK-632/BVD-523. Фиг. 53D и 53E, соответственно, демонстрируют % жизнеспособности при обработке TAK-632 и BVD-523 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках G-361.
[0071] Фиг. 54A представляет собой матрицу доз, демонстрирующую % ингибирования комбинации TAK-632/SCH772984 в клетках G-361. Фиг. 54B представляет собой матрицу доз, демонстрирующую приращение по Леве для комбинации TAK-632/SCH772984. Фиг. 54C представляет собой матрицу доз, демонстрирующую приращение по Блиссу для комбинации TAK-632/SCH772984. Фиг. 54D и 54E, соответственно, демонстрируют % жизнеспособности при обработке TAK-632 и SCH772984 в качестве единственного средства относительно контролей, обработанных только DMSO, в клетках G-361.
[0072] На фиг. 55A представлены показатели синергии для тестируемых комбинаций в клетках A375 и G-361. На фиг. 55B представлена диаграмма значений, представленных на фиг. 55A.
[0073] На фиг. 56A представлены объемы по Леве для тестируемых комбинаций в клетках A375 и G-361. На фиг. 56B представлена диаграмма значений, представленных на фиг. 56A.
[0074] На фиг. 57A представлены объемы по Блиссу для тестируемых комбинаций в клетках A375 и G-361. На фиг. 57B представлена диаграмма значений, представленных на фиг. 57A.
[0075] На фиг. 58 представлены результаты для комбинации BVD-523 и SCH772984. На фиг. 58A представлена матрица доз, демонстрирующая ингибирование (%) для комбинации в клетках A375. ФИГ. 58B - ФИГ. 58C демонстрируют результаты анализов пролиферации с единственным средством для комбинации в 58A. На фиг. 58D представлено приращение по Леве для комбинации в 58A, и на фиг. 58E представлено приращение по Блиссу для комбинации в 58A.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0076] Один из вариантов осуществления настоящего изобретения представляет собой способ лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Этот способ включает введение индивидууму эффективного количества (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF типа 1 или его фармацевтически приемлемую соль, для лечения или смягчения действия злокачественной опухоли.
[0077] Как используют в настоящем документе, термины "лечить", "лечение", "лечебное средство" и их грамматические варианты означают обеспечение индивидуума протоколом, схемой лечения, способом или лекарственным средством, при которых у этого индивидуума, например, пациента, желательно получить физиологический ответ или результат. В частности, способы и композиции по настоящему изобретению можно использовать для замедления развития симптомов заболевания или задержки начала заболевания или патологического состояния, или остановки прогрессирования развития заболевания. Однако так как не каждый подвергаемый лечению индивидуум может отвечать на конкретные протокол лечения, схему лечения, способ или лекарственное средство, лечение не требует, чтобы желаемый физиологический ответ или результат достигался у каждого индивидуума или группы индивидуумов, например, группы пациентов. Таким образом, данные индивидуум или группа индивидуумов, например, группа пациентов, могут не отвечать или неадекватно отвечать на лечебное средство.
[0078] Как используют в настоящем документе, термины "улучшить состояние", "улучшение состояния" и их грамматические варианты означают снижение тяжести симптомов заболевания у индивидуума.
[0079] Как используют в настоящем документе, "индивидуум" представляет собой млекопитающее, предпочтительно, человека. В дополнение к людям, категории млекопитающих в объеме настоящего изобретения включают, например, сельскохозяйственных животных, домашних животных, лабораторных животных и т.д. Некоторые примеры сельскохозяйственных животных включают коров, свиней, лошадей, коз и т.д. Некоторые примеры домашних животных включают собак, кошек и т.д. Некоторые примеры лабораторных животных включают приматов, крыс, мышей, кроликов, морских свинок и т.д.
[0080] По настоящему изобретению BVD-523 представляет собой соединение формулы (I):
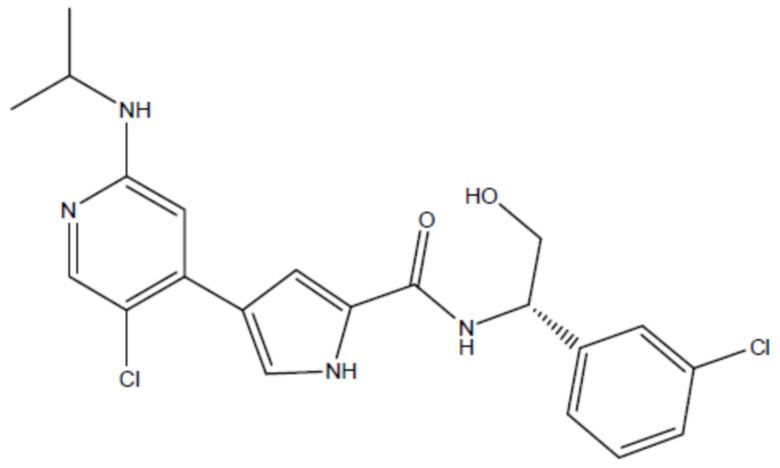
и его фармацевтически приемлемые соли. BVD-523 можно синтезировать способами, описанными, например, в патенте США № 7354939. Энантиомеры и рацемические смеси обоих энантиомеров BVD-523 также включены в объем настоящего изобретения. BVD-523 представляет собой ингибитор ERK1/2 с механизмом действия, который, по предположениям, является, например, уникальным и отличным от некоторых других ингибиторов ERK1/2, таких как SCH772984. Например, другие ингибиторы ERK1/2, такие как SCH772984, ингибируют аутофосфорилирование ERK (Morris et al., 2013), тога как BVD-523 допускает аутофосфорилирование ERK, при этом все еще ингибируя ERK (фиг. 18).
[0081] Как используют в настоящем документе, "ингибитор RAF" означает вещества, которые (i) непосредственно взаимодействуют с RAF, например, связываясь с RAF и (ii) снижают экспрессию или активность RAF. ингибиторы RAF можно классифицировать на два типа соответственно их способам связывания. Как используют в настоящем документе, ингибиторы RAF "типа 1" представляют собой ингибиторы, которые направлены к участкам связывания АТФ киназой в ее активной конформации. ингибиторы RAF "2 типа" представляют собой ингибиторы, которые преимущественно связываются с неактивной конформацией киназы. Неограничивающие примеры ингибиторов RAF типа 1 включают:
соединение 7 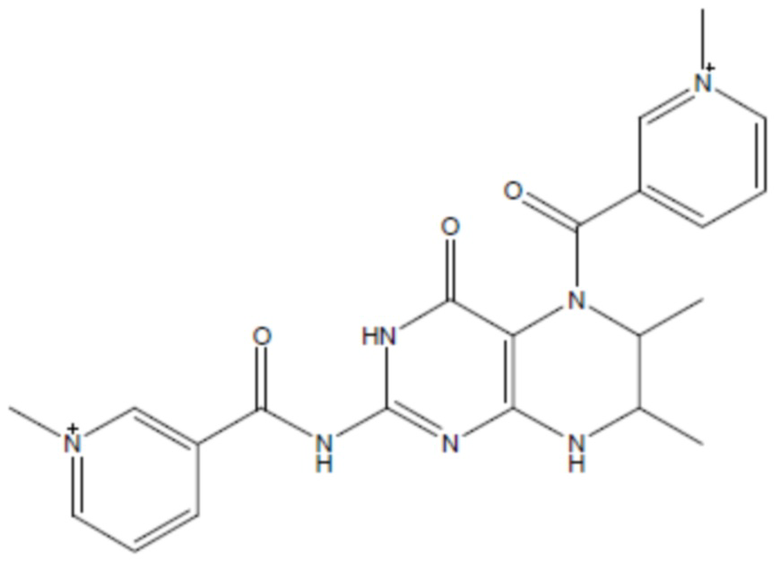 (Li et al., 2010),
(Li et al., 2010),
соединение 9 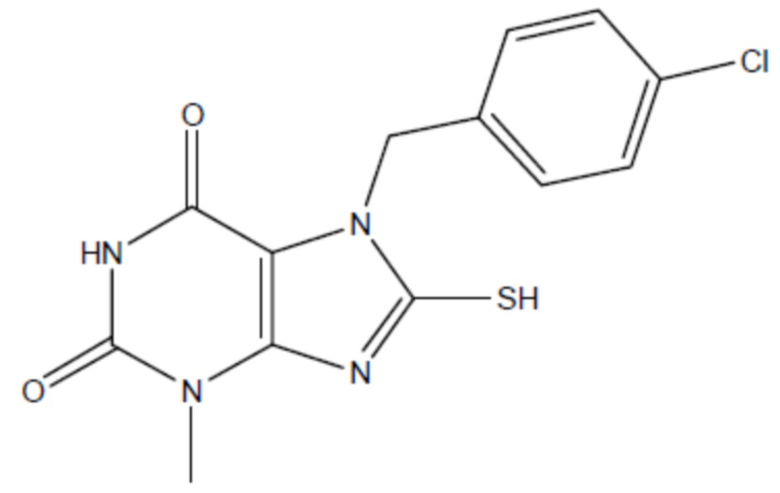 (там же.),
(там же.),
соединение 10 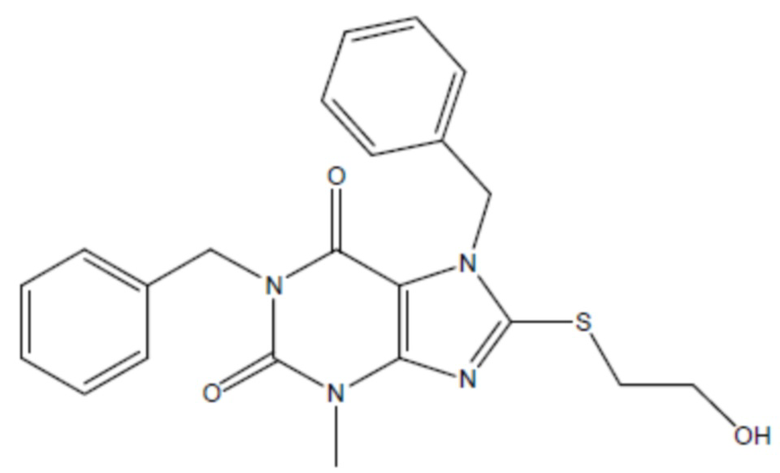 (там же),
(там же),
соединение 13 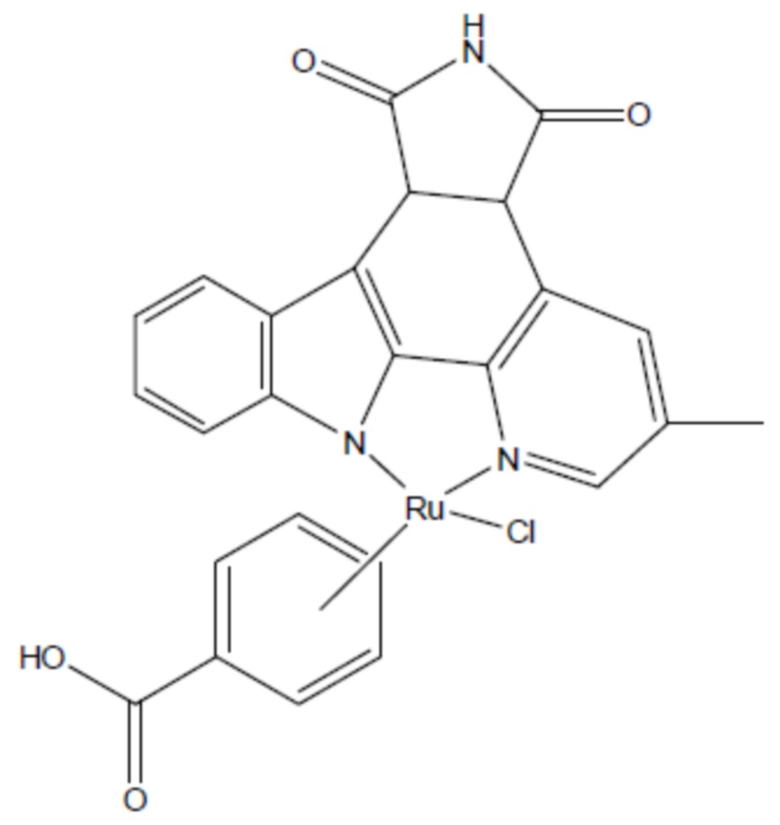 (там же),
(там же),
соединение 14 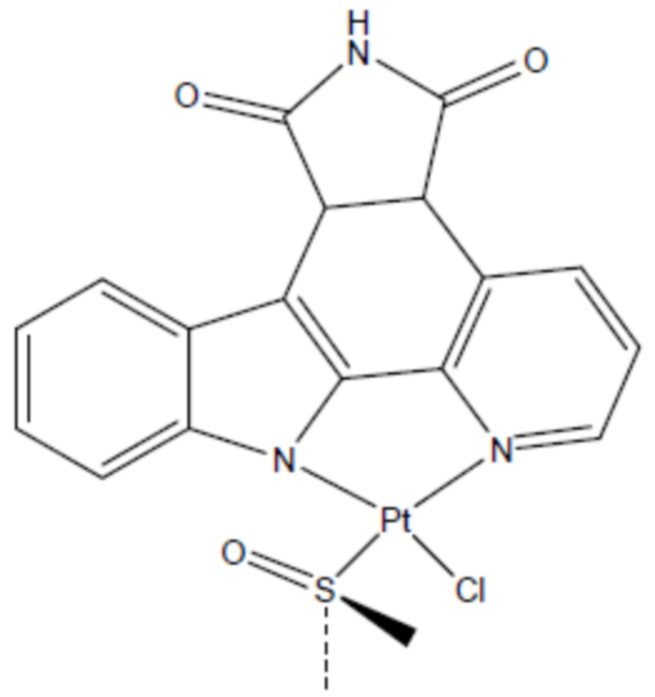 (там же), дабрафениб (GlaxoSmithKline), GDC-0879 (Genentech), L-779450 B-Raf (Merck), PLX3202 (Plexxikon), PLX4720 (Plexxikon), SB-590885 (GlaxoSmithKline), SB-699393 (GlaxoSmithKline), вемурафениб (Plexxikon), их фармацевтически приемлемые соли и их сочетания. Предпочтительно, ингибитор RAF типа 1 представляет собой дабрафениб или его фармацевтически приемлемую соль.
(там же), дабрафениб (GlaxoSmithKline), GDC-0879 (Genentech), L-779450 B-Raf (Merck), PLX3202 (Plexxikon), PLX4720 (Plexxikon), SB-590885 (GlaxoSmithKline), SB-699393 (GlaxoSmithKline), вемурафениб (Plexxikon), их фармацевтически приемлемые соли и их сочетания. Предпочтительно, ингибитор RAF типа 1 представляет собой дабрафениб или его фармацевтически приемлемую соль.
[0082] В одном из аспектов этого варианта осуществления индивидуум со злокачественной опухолью несет соматическую мутацию BRAF или устойчив к лечению ингибитором сигнального пути MAPK. Предпочтительно индивидуум устойчив к лечению ингибитором сигнального пути, не являющимся ERK MAPK.
[0083] Как используют в настоящем документе, "соматическая мутация" означает изменение, происходящее в любой клетке, не предопределенной стать половой клеткой. Мутация может представлять собой, например, замену, делецию, вставку или слияние. В таблице 1 ниже представлен обзор распределения мутаций BRAF, как представлено в базе данных центра Сэнгера.
Обзор распределения мутаций BRAF
[0084] Мутации BRAF выявляют приблизительно в 66% меланом (Davies et al., 2002; Brose et al., 2002; Hocket et al., 2007) и в относительно меньшем проценте других злокачественных опухолей, в 36% опухолей щитовидной железы и 10% рака толстого кишечника (Xu et al., 2003; Fransen et al., 2004). Наиболее преобладающая мутация BRAF происходит по аминокислоте 600 протеинкиназы дикого типа (SEQ ID NO:2) с заменой валина глутаминовой кислотой, что приводит к мутантной B-RafV600E, что составляет приблизительно 80% мутаций BRAF (Davies et al., 2002; Hocker et al., 2007). Киназный домен B-RafV600E обладает в 500 раз более высокой киназной активностью по сравнению с базальной активностью B-Raf дикого типа (Wan et al., 2004). Из других мутаций BRAF, идентифицированных при меланоме, частыми также являются V600K и V600D/R, и они составляют 16% и 3% от всех мутаций BRAF, соответственно (Long et al., 2011). Кроме меланомы, мутации BRAF часто возникают во многих других злокачественных опухолях, включая папиллярную карциному щитовидной железы, карциному яичника и колоректальную карциному. (Wellbrock et al., 2004). В одном из исследований, варианты сплайсинга BRAF (с вырезанием экзонов 14 и 15) выявлены в 5/24 (21%) линий клеток колоректального рака (Seth et al., 2009).
[0085] В таблице 2 ниже из базы данных центра Сэнгера представлено распределение и частота мутаций BRAF в опухолях человека.
[0086] В таблице 3 ниже продемонстрированы выбранные последовательности нуклеиновых кислот и аминокислот BRAF. Эти последовательности можно использовать в способах идентификации индивидуумов с мутантным генотипом BRAF (так, как в приведенных ниже способах).
[0087] Способы идентификации мутаций в нуклеиновых кислотах, таких как указанные выше гены BRAF, известны в данной области. Нуклеиновые кислоты можно получать из биологических образцов. По настоящему изобретению биологические образцы в качестве неограничивающих примеров включают кровь, плазму, мочу, кожу, слюну и биопсию. Биологические образцы получают у индивидуума стандартными способами и способами, известными в данной области.
[0088] Неограничивающие примеры способов идентификации мутаций включают анализы ПЦР, секвенирование, захват гибридов, захват в растворе, инвертируемые молекулярные зонды, флуоресцентная гибридизация in situ (FISH) и их сочетания.
[0089] В данной области известно множество способов секвенирования. Они в качестве неограничивающих примеров включают секвенирование по Сэнгеру (также обозначаемое как секвенирование с дидезоксинуклеотидами) и различные способы секвенирования посредством синтеза (SBS), как описано, например, в Metzker 2005, секвенирования посредством гибридизации, посредством лигирования (например, WO 2005021786), посредством разрушения (например, патенты США №№ 5622824 и 6140053) и секвенирование через нанопоры (которое коммерчески доступно в Oxford Nanopore Technologies, UK). В способах глубокого секвенирования данный нуклеотид в последовательности в процессе секвенирования считывается более одного раза. Способы глубокого секвенирования описаны например, в патентной публикации США № 20120264632 и международной патентной публикации № WO2012125848.
[0090] Способы детекции мутаций на основе ПЦР известны в данной области, и в них применяют ПЦР-амплификацию, когда для каждой последовательности-мишени в образце существует соответствующая пара уникальных, специфичных для этой последовательности праймеров. Например, способ полимеразной цепной реакции-полиморфизма длин рестрикционных фрагментов (ПЦР-ПДРФ) обеспечивает быструю детекцию мутаций после амплификации геномных последовательностей посредством ПЦР. Мутацию выявляют посредством расщепления специфическими рестрикционными эндонуклеазами и идентифицируют посредством электрофореза. См., например, Ota et al., 2007. Мутации также можно детектировать с применениям ПЦР с детекцией в реальном времени. См., например, публикацию международной заявки № WO2012046981.
[0091] Способы захвата гибридов известны в данной области и описаны, например, в патентной публикации США № 20130203632 и патентах США №№ 8389219 и 8288520. Эти способы основаны на селективной гибридизации геномных областей-мишеней со сконструированными исследователем олигонуклеотидами. Гибридизацию можно проводить с олигонуклеотидами, иммобилизованными на микропанели с высокой или низкой плотностью (захват на чипе), или она может представлять собой гибридизацию в жидкой фазе с олигонуклеотидами, модифицированными лигандом (например, биотином), который затем можно иммобилизовать на твердой поверхности, такой как гранула (захват в растворе).
[0092] Способы с инвертируемыми молекулярными зондами (MIP) известны в данной области и описаны, например, в Absalan et al., 2008. В таких способах используют молекулы MIP, которые представляют собой особые "замыкающиеся в кольцо" зонды (Nilsson et al., 1994) для генотипирования. Молекула MIP представляет собой линейный олигонуклеотид, который содержит особые области, универсальные последовательности, участки рестрикции и последовательность-метку (индекс) (16-22 п.н.). В таких способах гибридизуется MIP непосредственно вокруг исследуемого генетического маркера/SNP. В способе с MIP также можно использовать ряд наборов "замыкающихся в кольцо" зондов, которые гибридизуются с геномной ДНК параллельно (Hardenbol et al., 2003). В случае точного совпадения гомологичные геномные области подвергаются лигированию, проходя инверсию конфигурации (как свидетельствует название способа) и формируя циклическую молекулу. После первой рестрикции все молекулы амплифицируют с универсальными праймерами. Ампликоны снова рестрицируют с получением коротких фрагментов для гибридизации на микропанели. Полученные короткие фрагменты метят и посредством последовательности-метки гибридизуют с cTag (комплементарная цепь для индекса) на панели. После формирования дуплекса метка-cTag детектируют сигнал.
[0093] Как используют в настоящем документе, быть "устойчивым" к лечению ингибитором сигнального пути MAPK означает, что эффективность одного или нескольких ингибиторов сигнального пути MAPK при лечении злокачественной опухоли снижена.
[0094] Как используют в настоящем документе, "ингибитор сигнального пути митоген-активируемой протеинкиназы (MAPK)" представляют собой любое вещество, которое снижает активность, экспрессию или фосфорилирование белков в сигнальном пути MAPK, что приводит к уменьшению клеточного роста или увеличению гибели клеток.
[0095] Обзор каскадов MAPK млекопитающих представлен на фиг. 30. Подробности сигнальных путей MAPK рассмотрены, например, в Akinleye et al., 2013. В кратком изложении, в отношении модуля ERK1/2 на фиг. 30 (светло-фиолетовая рамка), сигнальный каскад MAPK 1/2 активируется связыванием лиганда с рецепторными тирозинкиназами (RTK). Активированные рецепторы рекрутируют и фосфорилируют адаптерные белки Grb2 и SOS, которые затем взаимодействуют с мембраносвязанной ГТФазой Ras и вызывают ее активацию. В своей активированной ГТФ-связанной форме, Ras рекрутирует и активирует киназы Raf (A-Raf, B-Raf и C-Raf/RaF-1). Активированные киназы Raf активируют MAPK 1/2 (MKK1/2), которые в свою очередь катализируют фосфорилирование треониновых и тирозиновых остатков в активируемой последовательности Thr-Glu-Tyr ERK1/2. В отношении модуля JNK/p38 (желтая рамка на фиг. 30), расположенные выше по каскаду киназы, MAP3K, такие как MEKK1/4, ASK1/2 и MLK1/2/3, активируют MAP2K3/6 (MKK3/6), MAP2K4 (MKK4) и MAP2K7 (MKK7). Эти MAP2K затем активируют протеинкиназы JNK, включая JNK1, JNK2 и JNK3, а также p38 α/β/γ/δ. Для осуществления их функций JNK активируют несколько факторов транскрипции, включая c-Jun, ATF-2, NF-ATc1, HSF-1 и STAT3. В отношении модуля ERK5 (синяя рамка на фиг. 30), киназы выше MAP2K5 (MKK5) представляют собой MEKK2 и MEKK3. Наиболее охарактеризованной расположенной ниже по каскаду целью MEK5 является ERK5, также известная как большая MAP-киназа 1 (BMK1) ввиду того, что ее размер вдвое превышает другие MAPK.
[0096] Неограничивающие примеры ингибиторов сигнального пути MAPK включают ингибиторы RAS, RAF ингибиторы, ингибиторы MEK, ингибиторы ERK1/2, их фармацевтически приемлемые соли и их сочетания.
[0097] Как используют в настоящем документе, a "ингибитор RAS" означает вещества, которые (i) непосредственно взаимодействуют с RAS, например, связываясь с RAS, и (ii) снижают экспрессию или активность RAS. Неограничивающие иллюстративные ингибиторы RAS в качестве неограничивающих примеров включают ингибиторы фарнезилтрансферазы (например, такие как типифарниб и лонафарниб), содержащие фарнезильную группу низкомолекулярные соединения (например, такие как салирасиб и TLN-4601), DCAI, как описано в Maurer (Maurer et al., 2012), Kobe0065 и Kobe2602, как описано в Shima (Shima et al., 2013), HBS 3 (Patgiri et al., 2011) и AIK-4 (Allinky).
[0098] Как используют в настоящем документе, "ингибитор RAF" означает вещества, которые (i) непосредственно взаимодействуют с RAF, например, связываясь с RAF, и (ii) снижают экспрессию или активность RAF, например, таких как A-RAF, B-RAF и C-RAF (Raf-1). Неограничивающие иллюстративные ингибиторы RAF включают:
соединение 7
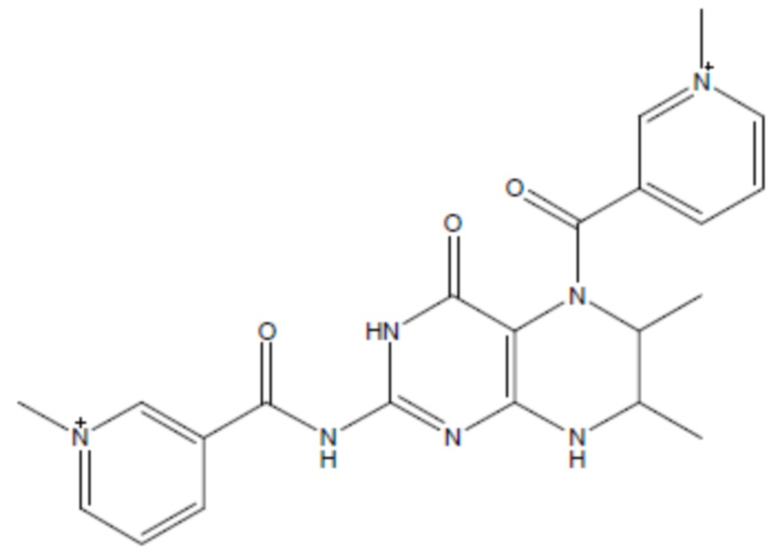 (Li et al., 2010),
(Li et al., 2010),
соединение 9
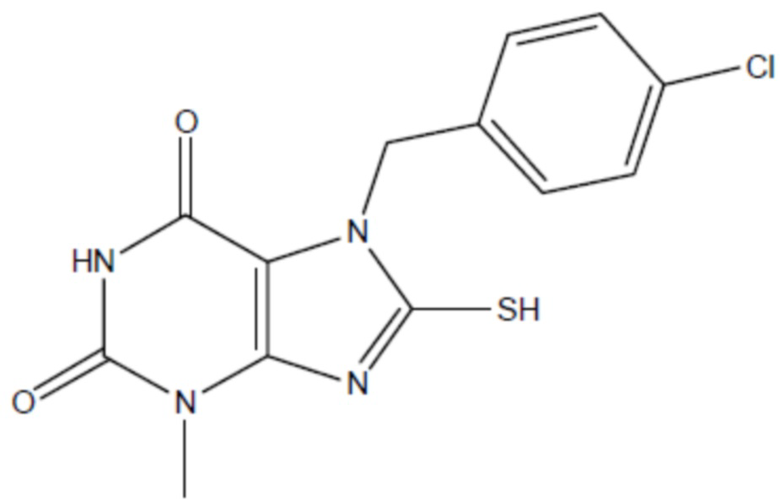 (там же),
(там же),
соединение 10
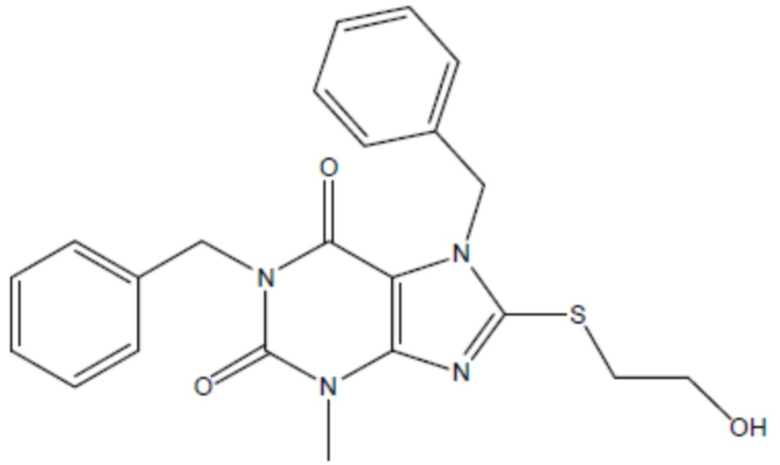 (там же),
(там же),
соединение 13
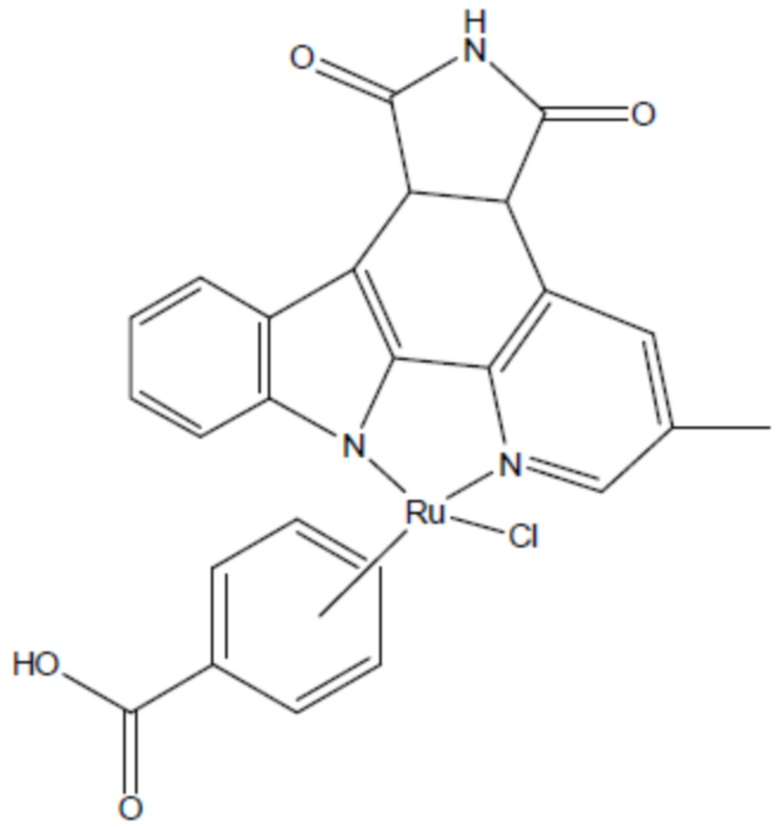 (там же),
(там же),
соединение 14
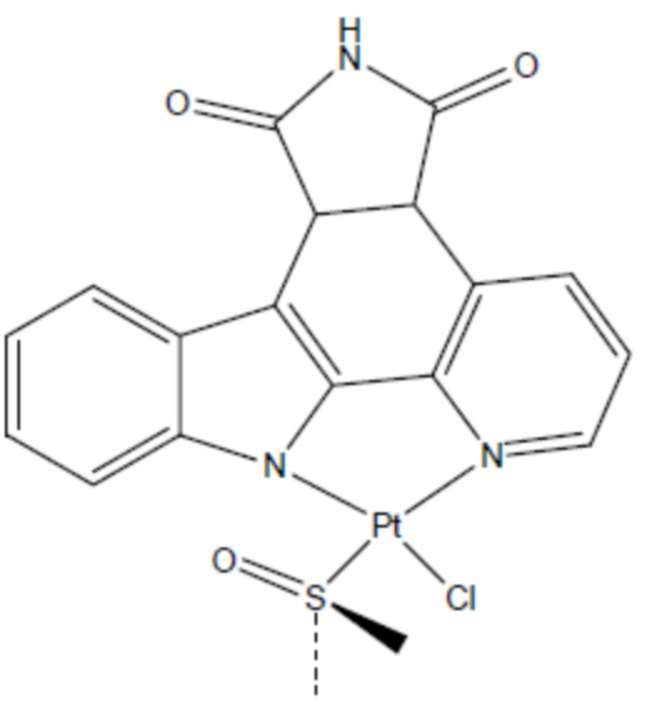 (там же),
(там же),
соединение 15
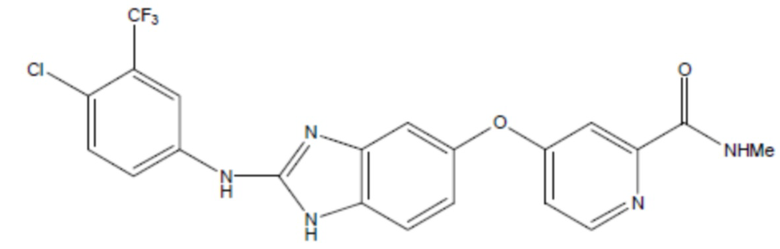 (там же),
(там же),
соединение 16
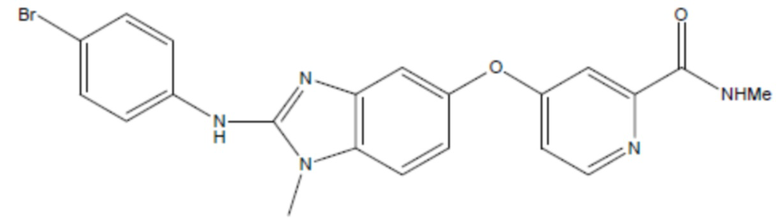 (там же),
(там же),
соединение 18
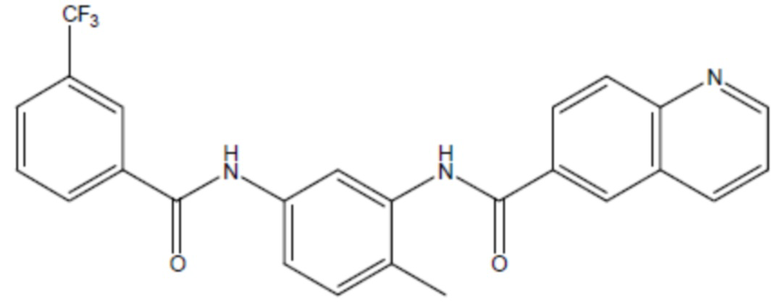 (там же),
(там же),
соединение 19
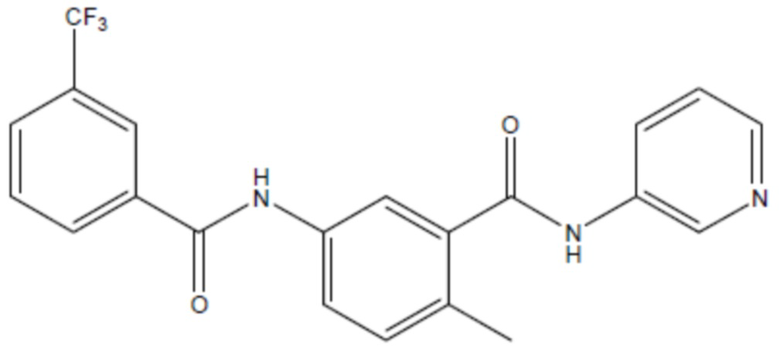 (там же),
(там же),
соединение 20
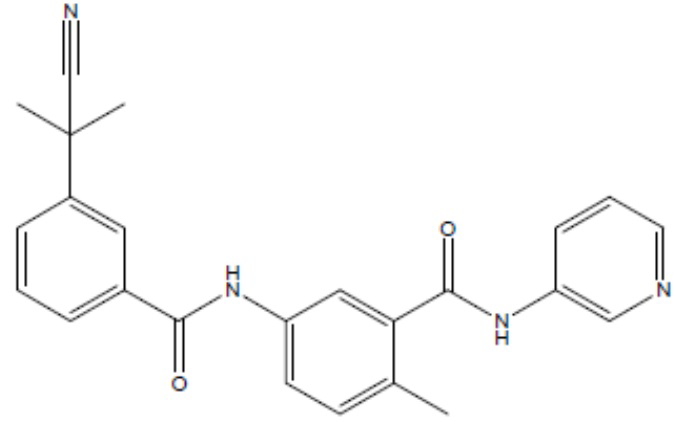 (там же),
(там же),
соединение 21
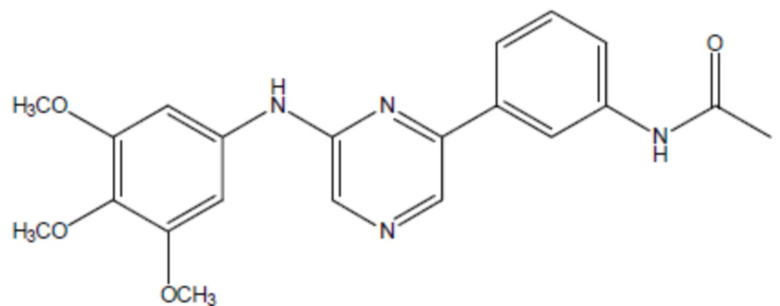 (там же),
(там же),
соединение 22
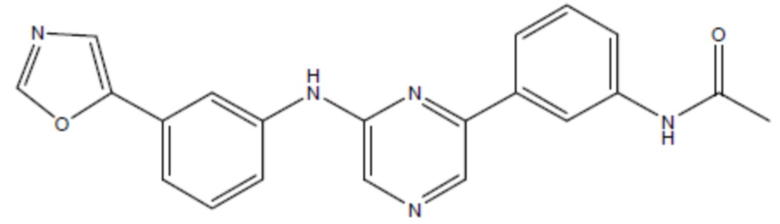 (там же),
(там же),
соединение 23
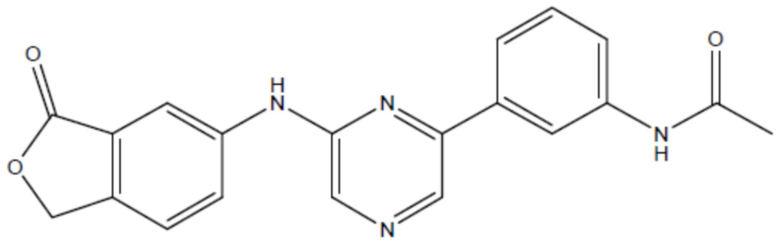 (там же),
(там же),
соединение 24
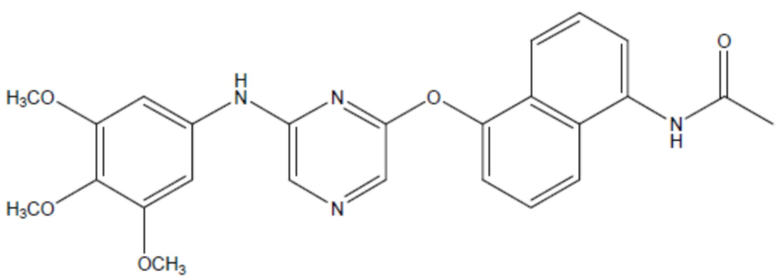 (там же),
(там же),
соединение 25
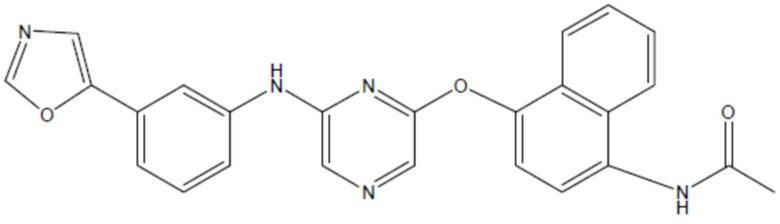 (там же),
(там же),
соединение 26
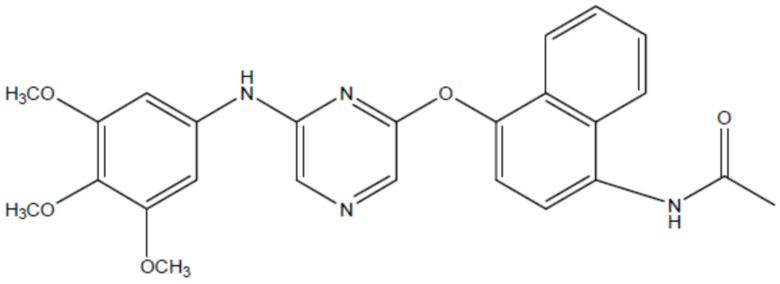 (там же),
(там же),
соединение 27
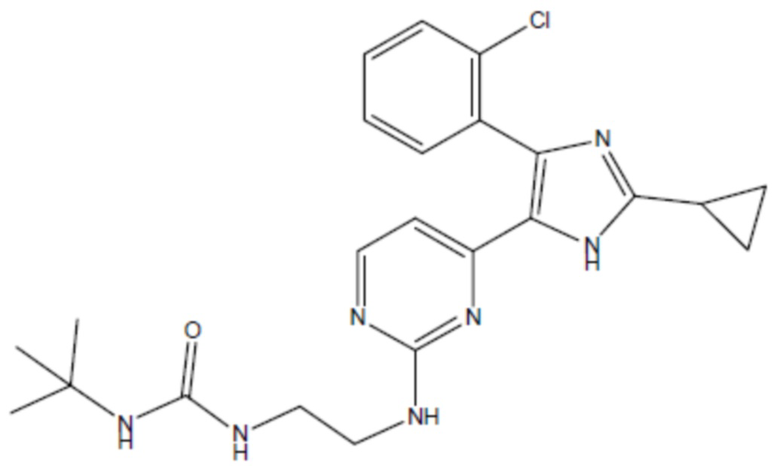 (там же),
(там же),
соединение 28
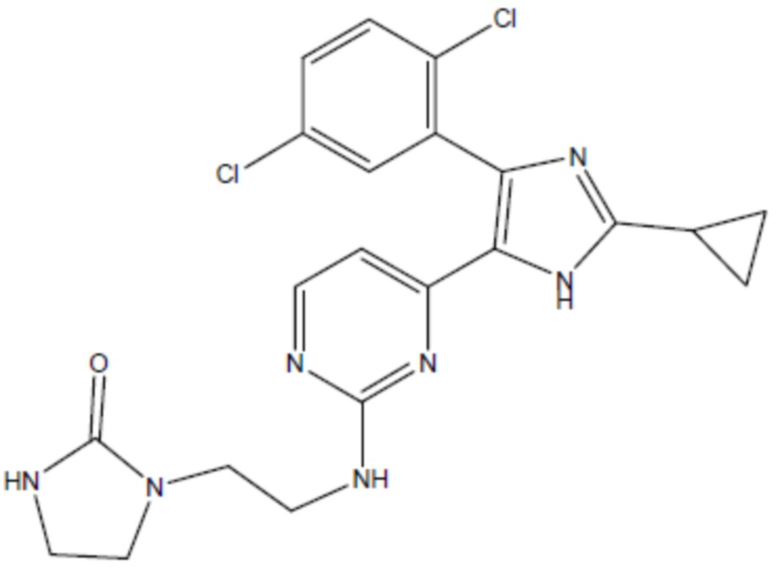 (там же),
(там же),
соединение 30
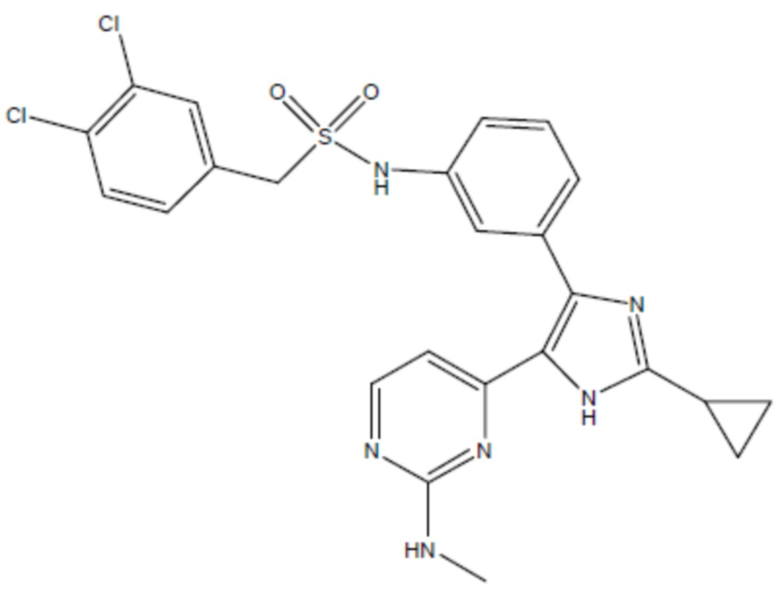 (там же),
(там же),
соединение 31
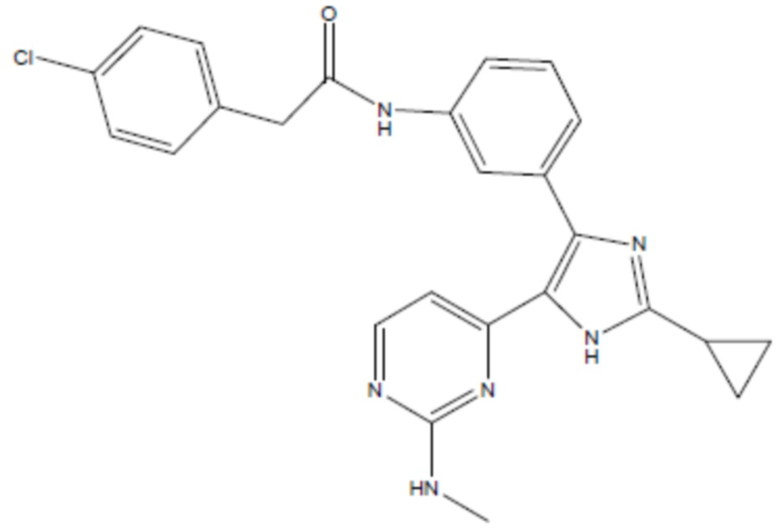 (там же),
(там же),
соединение 32
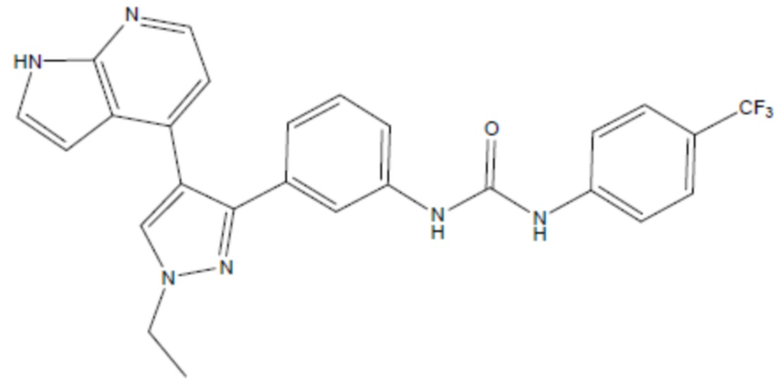 (там же),
(там же),
соединение 33
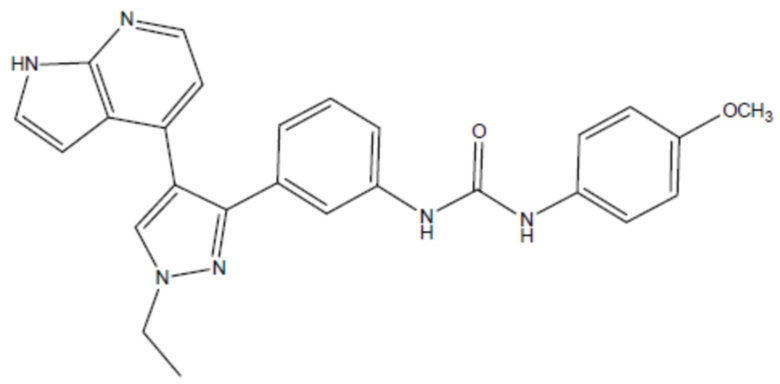 (там же),
(там же),
соединение 34
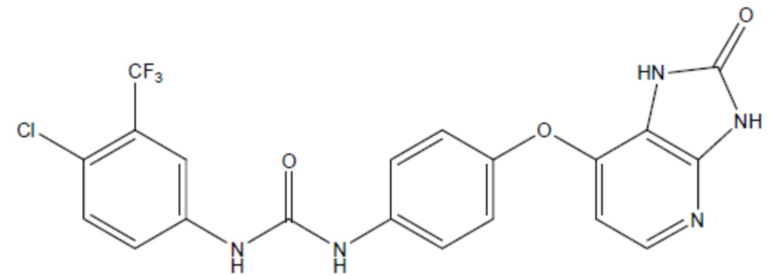 (там же),
(там же),
соединение 35
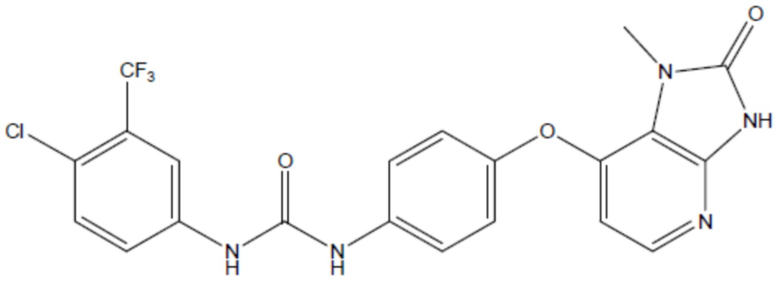 (там же),
(там же),
соединение 36
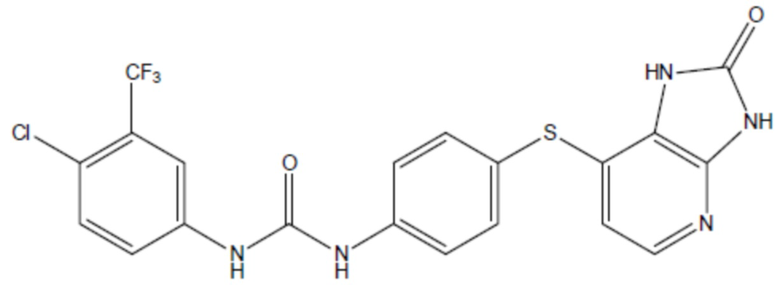 (там же),
(там же),
соединение 37
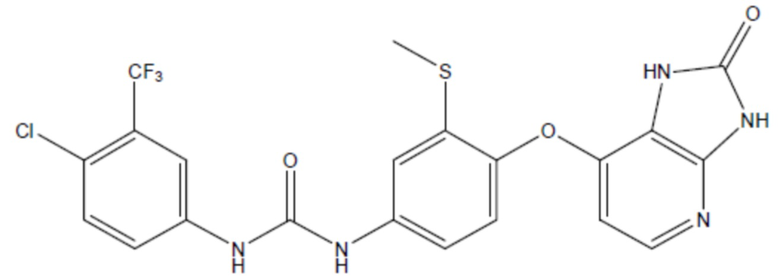 (там же),
(там же),
соединение 38
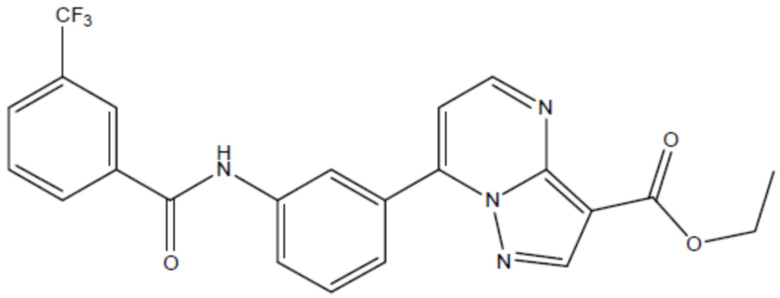 (там же),
(там же),
соединение 39
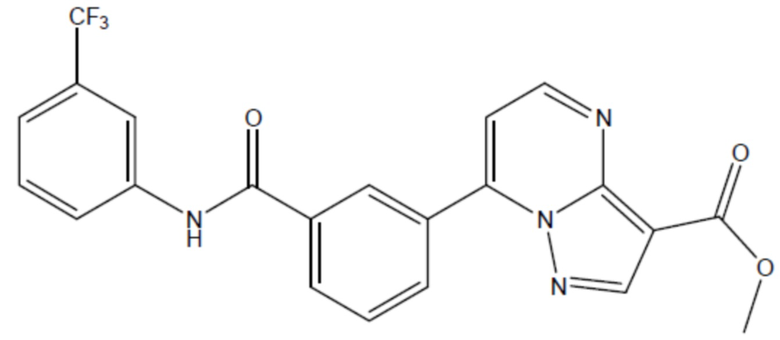 (там же),
(там же),
соединение 40
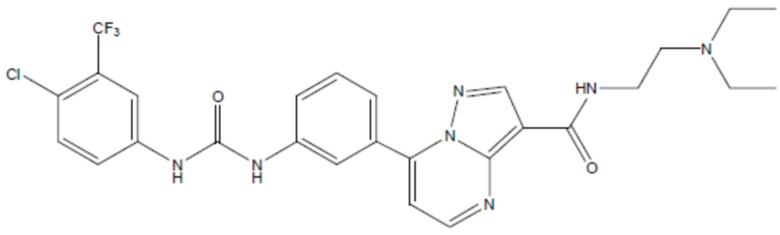 (там же),
(там же),
AAL881 (Novartis); AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BeiGene-283 (BeiGene), BIIB-024 (MLN 2480) (Sunesis & Takeda), ингибитор b-raf (Sareum), ингибитор киназы BRAF (Selexagen Therapeutics), миРНК 313 (tacaccagcaagctagatgca) и 523 (cctatcgttagagtcttcctg) BRAF (Liu et al., 2007), CTT239065 (Institute of Cancer Research), дабрафениб (GSK2118436), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GDC-0879 (Genentech), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), L779450 (Merck), LBT613 (Novartis), LErafAON (NeoPharm, Inc.), LGX-818 (Novartis), пазопаниб (GlaxoSmithKline), PLX3202 (Plexxikon), PLX4720 (Plexxikon), PLX5568 (Plexxikon), RAF-265 (Novartis), RAF-365 (Novartis), регорафениб (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), SB-590885 (GlaxoSmithKline), SB699393 (GlaxoSmithKline), сорафениб (Onyx Pharmaceuticals), TAK 632 (Takeda), TL-241 (Teligene), вемурафениб (RG7204 или PLX4032) (Daiichi Sankyo), XL-281 (Exelixis), ZM-336372 (AstraZeneca), их фармацевтически приемлемые соли и их сочетания.
[0099] Как используют в настоящем документе, "ингибитор MEK" означает вещества, которые (i) непосредственно взаимодействуют с MEK, например, связываясь с MEK и (ii) снижают экспрессию или активность MEK. Таким образом, ингибиторы, которые действуют выше MEK, такие как ингибиторы RAS и ингибиторы RAF, не являются ингибиторами MEF по настоящему изобретению. Неограничивающие примеры ингибиторов MEK включают токсин сибирской язвы, антрохинолол (Golden Biotechnology), ARRY-142886 (6-(4-бром-2-хлорфениламино)-7-фтор-3-метил-3H-бензоимидазол-5-карбоновую кислоту (2-гидроксиэтокси)амид) (Array BioPharma), ARRY-438162 (Array BioPharma), AS-1940477 (Astellas), AS-703988 (Merck KGaA), бентамапимод (Merck KGaA), BI-847325 (Boehringer Ingelheim), E-6201 (Eisai), GDC-0623 (Hoffmann-La Roche), GDC-0973 (кобиметиниб) (Hoffmann-La Roche), L783277 (Merck), часть фактора летальности токсина сибирской язвы, MEK162 (Array BioPharma), PD 098059 (2-(2'-амино-3'-метоксифенил)-оксанафталин-4-он) (Pfizer), PD 184352 (CI-1040) (Pfizer), PD-0325901 (Pfizer), пимасертиб (Santhera Pharmaceuticals), RDEA119 (Ardea Biosciences/Bayer), рефаметиниб (AstraZeneca), RG422 (Chugai Pharmaceutical Co.), RO092210 (Roche), RO4987655 (Hoffmann-La Roche), RO5126766 (Hoffmann-La Roche), селуметиниб (AZD6244) (AstraZeneca), SL327 (Sigma), TAK-733 (Takeda), траметиниб (Japan Tobacco), U0126 (1,4-диамино-2,3-дициано-1,4-бис(2-аминофенилтио)бутадиен) (Sigma), WX-554 (Wilex), полипептид YopJ (Mittal et al., 2010), их фармацевтически приемлемые соли и их сочетания.
[0100] Как используют в настоящем документе, "ингибитор ERK1/2" означает вещества, которые (i) непосредственно взаимодействуют с ERK1 и/или ERK2, например, связываясь с ERK1/2 и (ii) снижают экспрессию или активность протеинкиназ ERK1 и/или ERK2. Таким образом, ингибиторы, которые действуют выше ERK1/2, такие как ингибиторы MEK и ингибиторы RAF, не являются ингибиторами ERK1/2 по настоящему изобретению. Неограничивающие примеры ингибиторов ERK1/2 включают AEZS-131 (Aeterna Zentaris), AEZS-136 (Aeterna Zentaris), BVD-523, SCH-722984 (Merck & Co.), SCH-772984 (Merck & Co.), SCH-900353 (MK-8353) (Merck & Co.), их фармацевтически приемлемые соли и их сочетания.
[0101] В другом аспекте этого варианта осуществления способ дополнительно включает введение индивидууму по меньшей мере одного дополнительного терапевтического средства, эффективного для лечения или смягчения действия злокачественной опухоли. Дополнительное терапевтическое средство можно выбирать из группы, состоящей из антитела или его фрагмента, цитотоксического средства, токсина, радионуклида, иммуномодулятора, фотоактивного терапевтического средства, радиосенсибилизирующего средства, гормона, средства против ангиогенеза и их сочетаний.
[0102] Как используют в настоящем документе, "антитело" включает природные иммуноглобулины, а также неприродные иммуноглобулины, включая, например, одноцепочечные антитела, химерные антитела (например, гуманизированные антитела мыши) и гетероконъюгированные антитела (например, биспецифические антитела). Фрагменты антител включают фрагменты, которые связывают антигены (например, Fab', F(ab')2, Fab, Fv и rIgG). Также см., например, Pierce Catalog and Handbook, 1994-1995 (Pierce Chemical Co., Rockford, Ill.); Kuby, J., Immunology, 3rd Ed., W.H. Freeman & Co., New York (1998). Термин антитело также включает двухвалентные или биспецифические молекулы, диатела, триотела и тетратела. Кроме того, термин "антитело" включает поликлональные и моноклональные антитела.
[0103] Примеры терапевтических антител, которые можно использовать по настоящему изобретению включают ритуксимаб (ритуксан), цетуксимаб (эрбитукс), бевацизумаб (авастин) и ибритумомаб (зевалин).
[0104] Цитотоксические средства по настоящему изобретению включают повреждающие ДНК средства, антиметаболиты, средства против микротрубочек, антибиотические средства и т.д. Повреждающие ДНК средства включают алкилирующие средства, средства на основе платины, интеркаляторы и ингибиторы репликации ДНК. Неограничивающие примеры алкилирующих ДНК средств включают циклофосфамид, мехлоретамин, урамустин, мелфалан, хлорамбуцил, ифосфамид, кармустин, ломустин, стрептозоцин, бусульфан, темозоломид, их фармацевтически приемлемые соли, пролекарственные средства и сочетания. Неограничивающие примеры средств на основе платины включают цисплатин, карбоплатин, оксалиплатин, недаплатин, сатраплатин, тетранитрат триплатина, их фармацевтически приемлемые соли, пролекарственные средства и сочетания. Неограничивающие примеры интеркаляторов включают доксорубицин, даунорубицин, идарубицин, митоксантрон, их фармацевтически приемлемые соли, пролекарственные средства и сочетания. Неограничивающие примеры ингибиторов репликации ДНК включают иринотекан, топотекан, амсакрин, этопозид, фосфат этопозида, тенипозид, их фармацевтически приемлемые соли, пролекарственные средства и сочетания. Антиметаболиты включают антагонисты фолатов, такие как метотрексат и пеметрексед, антагонисты пуринов, такие как 6-меркаптопурин, дакарбазин и флударабин, и антагонисты пиримидинов, такие как 5-фторурацил, арабинозилцитозин, капецитабин, гемцитабин, децитабин, их фармацевтически приемлемые соли, пролекарственные средства и сочетания. Средства против микротрубочек в качестве неограничивающих примеров включают алкалоиды барвинка, паклитаксел (таксол®), доцетаксел (таксотер®) и иксабепилон (иксемпра®). Антибиотические средства в качестве неограничивающих примеров включают актиномицин, антрациклины, валрубицин, эпирубицин, блеомицин, пликамицин, митомицин, их фармацевтически приемлемые соли, пролекарственные средства и сочетания.
[0105] Цитотоксические средства по настоящему изобретению также включают ингибитор сигнального пути PI3K/Akt. Неограничивающие примеры ингибиторов сигнального пути PI3K/Akt включают A-674563 (CAS # 552325-73-2), AGL 2263, AMG-319 (Amgen, Thousand Oaks, CA), AS-041164 (5-бензо[1,3]диоксол-5-илметилентиазолидин-2,4-дион), AS-604850 (5-(2,2-дифтор-бензо[1,3]диоксол-5-илметилен)тиазолидин-2,4-дион), AS-605240 (5-хиноксилин-6-метилен-1,3-тиазолидин-2,4-дион), AT7867 (CAS # 857531-00-1), ряд бензимидазолов, Genentech (Roche Holdings Inc., South San Francisco, CA), BML-257 (CAS # 32387-96-5), CAL-120 (Gilead Sciences, Foster City, CA), CAL-129 (Gilead Sciences), CAL-130 (Gilead Sciences), CAL-253 (Gilead Sciences), CAL-263 (Gilead Sciences), CAS # 612847-09-3, CAS # 681281-88-9, CAS # 75747-14-7, CAS # 925681-41-0, CAS # 98510-80-6, CCT128930 (CAS # 885499-61-6), CH5132799 (CAS # 1007207-67-1), CHR-4432 (Chroma Therapeutics, Ltd., Abingdon, UK), FPA 124 (CAS # 902779-59-3), GS-1101 (CAL-101) (Gilead Sciences), GSK 690693 (CAS # 937174-76-0), H-89 (CAS # 127243-85-0), Honokiol, IC87114 (Gilead Science), IPI-145 (Intellikine Inc.), KAR-4139 (Karus Therapeutics, Chilworth, UK), KAR-4141 (Karus Therapeutics), KIN-1 (Karus Therapeutics), KT 5720 (CAS # 108068-98-0), Miltefosine, дигидрохлорид MK-2206 (CAS # 1032350-13-2), ML-9 (CAS # 105637-50-1), гидрохлорид налтриндола, OXY-111A (NormOxys Inc., Brighton, MA), перифосин, PHT-427 (CAS # 1191951-57-1), ингибитор киназы PI3 дельта, Merck KGaA (Merck & Co., Whitehouse Station, NJ), ингибиторы киназы PI3 дельта, Genentech (Roche Holdings Inc.), ингибиторы киназы PI3 дельта, Incozen (Incozen Therapeutics, Pvt. Ltd., Hydrabad, India), ингибиторы киназы PI3 дельта-2, Incozen (Incozen Therapeutics), ингибитор киназы PI3, Roche-4 (Roche Holdings Inc.), ингибиторы киназы PI3, Roche (Roche Holdings Inc.), ингибиторы киназы PI3, Roche-5 (Roche Holdings Inc.), ингибиторы PI3-альфа/дельта, Pathway Therapeutics (Pathway Therapeutics Ltd., South San Francisco, CA), ингибиторы PI3 дельта, Cellzome (Cellzome AG, Heidelberg, Germany), ингибиторы PI3 дельта, Intellikine (Intellikine Inc., La Jolla, CA), ингибиторы PI3 дельта, Pathway Therapeutics-1 (Pathway Therapeutics Ltd.), ингибиторы PI3 дельта, Pathway Therapeutics-2 (Pathway Therapeutics Ltd.), ингибиторы PI3 дельта/гамма, Cellzome (Cellzome AG), ингибиторы PI3 дельта/гамма, Cellzome (Cellzome AG), ингибиторы PI3 дельта/гамма, Intellikine (Intellikine Inc.), ингибиторы PI3 дельта/гамма, Intellikine (Intellikine Inc.), ингибиторы PI3 дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторы PI3 дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибитор PI3 гамма Evotec (Evotec), ингибитор PI3 гамма, Cellzome (Cellzome AG), ингибиторы PI3 гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторы PI3K дельта/гамма, Intellikine-1 (Intellikine Inc.), ингибиторы PI3K дельта/гамма, Intellikine-1 (Intellikine Inc.), пиктилисиб (Roche Holdings Inc.), PIK-90 (CAS # 677338-12-4), SC-103980 (Pfizer, New York, NY), SF-1126 (Semafore Pharmaceuticals, Indianapolis, IN), SH-5, SH-6, тетрагидрокуркумин, TG100-115 (Targegen Inc., San Diego, CA), трицирибин, X-339 (Xcovery, West Palm Beach, FL), XL-499 (Evotech, Hamburg, Germany), их фармацевтически приемлемые соли и их сочетания.
[0106] По настоящему изобретению термин "токсин" означает антигенное отравляющее вещество или яд растительного или животного происхождения. Примером является дифтерийный токсин или его части.
[0107] По настоящему изобретению термин "радионуклид" означает радиоактивное вещество, вводимое пациенту, например, внутривенно или перорально, после чего оно посредством нормального метаболизма пациента проникает в орган- или ткань-мишень, где оно производит локальное облучение в течение короткого периода времени. Примеры радионуклидов в качестве неограничивающих примеров включают I-125, At-211, Lu-177, Cu-67, I-131, Sm-153, Re-186, P-32, Re-188, In-114m и Y-90.
[0108] По настоящему изобретению термин "иммуномодулятор" означает вещество, которое изменяет иммунный ответ посредством повышения или снижения способности иммунной системы продуцировать антитела или сенсибилизировать клетки, которые распознают и реагируют с антигеном, который инициировал их продукцию. Иммуномодуляторы могут быть рекомбинантными, синтетическими или природными препаратами и включают цитокины, кортикостероиды, цитотоксические средства, тимозин и иммуноглобулины. Некоторые иммуномодуляторы присутствуют в организме в природе, и некоторые из них доступны в фармакологических препаратах. Примеры иммуномодуляторов в качестве неограничивающих примеров включают гранулоцитарный колониестимулирующий фактор (G-CSF), интерфероны, имиквимод и фракции клеточных мембран бактерий, IL-2, IL-7, IL-12, CCL3, CCL26, CXCL7 и синтетический цитозинфосфогуанозин (CpG).
[0109] По настоящему изобретению термин "фотоактивное терапевтическое средство" означает соединения и композиции, которые активируются при воздействии света. Определенные примеры фотоактивных терапевтических средств описаны, например, в патентной заявке США с серийным № 2011/0152230 A1, "Photoactive Metal Nitrosyls For Blood Pressure Regulation And Cancer Therapy".
[0110] По настоящему изобретению термин "радиосенсибилизирующее средство" означает соединение, которое делает опухолевые клетки более чувствительными к лучевой терапии. Примеры радиосенсибилизирующих средств включают мисонидазол, метронидазол, тирапазамин и транс-кроцетинат натрия.
[0111] По настоящему изобретению термин "гормон" означает вещество, высвобождаемое клетками в одном отделе организма, которое действует на клетки в другом отделе организма. Примеры гормонов в качестве неограничивающих примеров включают простагландины, лейкотриены, простациклин, тромбоксан, амилин, антимюллеров гормон, адипонектин, адренокортикотропный гормон, ангиотензиноген, ангиотензин, вазопрессин, атриопептин, натрийуретический пептид головного мозга, кальцитонин, холецистокинин, кортикотропин-высвобождающий гормон, энкефалин, эндотелин, эритропоэтин, фолликулостимулирующий гормон, галанин, гастрин, грелин, глюкагон, гонадотропин-высвобождающий гормон, гормон высвобождения гормона роста, хорионический гонадотропин человека, плацентарный лактоген человека, гормон роста, ингибин, инсулин, соматомедин, лептин, липотропин, лютеинизирующий гормон, меланоцит-стимулирующий гормон, мотилин, орексин, окситоцин, панкреатический полипептид, паратиреоидный гормон, пролактин, пролактин-высвобождающий гормон, релаксин, ренин, секретин, соматостатин, тромбопоэтин, стимулирующий щитовидную железу гормон, тестостерон, дегидроэпиандростерон, андростендион, дигидротестостерон, альдостерон, эстрадиол, эстрон, эстриол, кортизол, прогестерон, кальцитриол и кальцидиол.
[0112] Определенные соединения препятствуют активности определенных гормонов или останавливают продукцию определенных гормонов. Эти препятствующие гормонам соединения в качестве неограничивающих примеров включают тамоксифен (нолвадекс®), анастрозол (аримидекс®), летрозол (фемару®) и фулвестрант (фаслодекс®). Такие соединения также входят в понятие гормон по настоящему изобретению.
[0113] Как используют в настоящем документе, средство "против ангиогенеза" означает вещество, которое снижает или ингибирует рост новых кровеносных сосудов, например, такое как ингибитор фактора роста эндотелия сосудов (VEGF) и ингибитор миграции клеток эндотелия. Средства против ангиогенеза в качестве неограничивающих примеров включают 2-метоксиэстрадиол, ангиостатин, бевацизумаб, получаемый из хряща фактор ингибирования ангиогенеза, эндостатин, IFN-α, IL-12, итраконазол, линомид, тромбоцитарный фактор-4, пролактин, SU5416, сурамин, тасквинимод, текогалан, тетратиомолибдат, талидомид, тромбоспондин, тромбоспондин, TNP-470, зив-афлиберцепт, их фармацевтически приемлемые соли, пролекарственные средства и сочетания.
[0114] В дополнительном аспекте этого варианта осуществления введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно. Как используют в настоящем документе, "синергическое" означает большее, чем аддитивное. Синергическое действие можно определять посредством различных анализов, известных в данной области, включая в качестве неограничивающих примеров анализы, описываемые в настоящем документе, такие как анализ приращения по Блиссу.
[0115] Другой вариант осуществления настоящего изобретения представляет собой способ лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Этот способ включает введение индивидууму эффективного количества (i) BVD-523 или его фармацевтически приемлемой соли и (ii) второго средства против злокачественной опухоли, которое представляет собой дабрафениб или его фармацевтически приемлемую соль, для лечения или смягчения действия злокачественной опухоли.
[0116] Подходящие и предпочтительные индивидуумы являются такими, как описано в настоящем документе. В этом варианте осуществления способы можно использовать для лечения злокачественных опухолей, описанных выше, включая злокачественные опухоли с мутантным происхождением, определенные выше. Способы идентификации таких мутаций также являются такими, как указано выше.
[0117] В одном из аспектов этого варианта осуществления BVD-523 или его фармацевтически приемлемую соль вводят в форме фармацевтической композиции, дополнительно содержащей фармацевтически приемлемый носитель или разбавитель.
[0118] В дополнительном аспекте этого варианта осуществления дабрафениб или его фармацевтически приемлемую соль вводят в форме фармацевтической композиции, дополнительно содержащей фармацевтически приемлемый носитель или разбавитель.
[0119] В дополнительном аспекте этого варианта осуществления способ дополнительно включает введение по меньшей мере одного дополнительного терапевтического средства, предпочтительно ингибитора сигнального пути PI3K/Akt, как описано в настоящем документе.
[0120] В дополнительном аспекте этого варианта осуществления введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно.
[0121] Другой вариант осуществления настоящего изобретения представляет собой способ уничтожения злокачественной клетки. Этот способ включает приведение злокачественной клетки в контакт с эффективным количеством (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF типа 1 или его фармацевтически приемлемую соль.
[0122] Подходящие и предпочтительные ингибиторы RAF типа 1 являются такими, как описано в настоящем документе. В этом варианте осуществления уничтожение злокачественной клетки можно проводить у злокачественных клеток с различным мутантным происхождением и/или у клеток, которые характеризуются, как описано выше. Способы идентификации таких мутаций также являются такими, как указано выше.
[0123] В одном из аспектов этого варианта осуществления способы можно проводить in vitro или in vivo, и можно использовать для уничтожения злокачественных клеток, например, посредством цитолиза злокачественных клеток в клетках типов злокачественных опухолей, описываемых в настоящем документе.
[0124] В другом аспекте этого варианта осуществления злокачественная клетка представляет собой злокачественную клетку млекопитающего. Предпочтительно, злокачественную клетку млекопитающего получают у млекопитающего, выбранного из группы, состоящей из людей, приматов, сельскохозяйственных животных и домашних животных. Более предпочтительно, злокачественная клетка млекопитающего представляет собой злокачественную клетку человека.
[0125] В дополнительном аспекте этого варианта осуществления приведение злокачественной клетки в контакт с первым и вторым средствами против злокачественных опухолей обеспечивает синергическое действие по сравнению с приведением злокачественной клетки в контакт с любым из этих средств против злокачественных опухолей отдельно.
[0126] В другом аспекте этого варианта осуществления способ дополнительно включает приведение злокачественной клетки в контакт по меньшей мере с одним дополнительным терапевтическим средством, предпочтительно ингибитором сигнального пути PI3K/Akt, как описано в настоящем документе.
[0127] В дополнительном аспекте этого варианта осуществления приведение злокачественной клетки в контакт с первым и вторым средствами против злокачественных опухолей обеспечивает синергическое действие по сравнению с приведением злокачественной клетки в контакт с любым из этих средств против злокачественных опухолей отдельно. В этом варианте осуществления "приведение в контакт" означает приведение BVD-523 и ингибиторов RAF типа 1 и, необязательно, одного или нескольких дополнительных терапевтических средств в непосредственную близость со злокачественными клетками. Это можно проводить общепринятыми способами доставки лекарственных средств млекопитающим или в условиях in vitro, например, помещая BVD-523 и ингибиторы RAF типа 1 и, необязательно, другие терапевтические средства в среды для культивирования, в которых находятся злокачественные клетки.
[0128] Дополнительный вариант осуществления настоящего изобретения представляет собой набор для лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Этот набор содержит эффективное количество (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF типа 1 или его фармацевтически приемлемую соль, упакованные вместе с инструкциями по их применению.
[0129] Наборы также могут включать подходящие контейнеры для хранения, например, ампулы, флаконы, пробирки и т.д., для каждого средства против злокачественной опухоли по настоящему изобретению (которое может, например, находиться в форме фармацевтических композиций) и других реагентов, например, буферов, буферных солевых растворов и т.д., для применения при введении средства против злокачественных опухолей индивидуумам. Средства против злокачественных опухолей по изобретению и другие реагенты можно предоставлять в наборах в любой удобной форме, например, такой как в форме раствора или в форме порошка. Дополнительно наборы могут содержать упаковочный контейнер, необязательно с одним или несколькими отделениями для содержания фармацевтической композиции и других необязательных реагентов.
[0130] Подходящие и предпочтительные индивидуумы и ингибиторы RAF типа 1 являются такими, как описано в настоящем документе. В этом варианте осуществления набор можно использовать для лечения злокачественных опухолей, описанных выше, включая злокачественные опухоли с мутантным происхождением, определенные в настоящем документе. Способы идентификации таких мутаций являются такими, как указано выше.
[0131] В дополнительном аспекте этого варианта осуществления набор дополнительно содержит по меньшей мере одно дополнительное терапевтическое средство, предпочтительно ингибитор сигнального пути PI3K/Akt, как описано в настоящем документе.
[0132] В дополнительном аспекте этого варианта осуществления введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно.
[0133] Другой вариант осуществления настоящего изобретения представляет собой фармацевтическую композицию для лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Эта фармацевтическая композиция содержит фармацевтически приемлемый разбавитель или носитель и эффективное количество (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF типа 1 или его фармацевтически приемлемую соль, где введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно. Дополнительно эта фармацевтическая композиция может содержать фармацевтически приемлемый разбавитель или носитель.
[0134] Подходящие и предпочтительные индивидуумы и ингибиторы RAF типа 1 являются такими, как описано в настоящем документе. Фармацевтические композиции по изобретению можно использовать для лечения злокачественных опухолей, описанных выше, включая злокачественные опухоли с мутантным происхождением, определенные в настоящем документе. Способы идентификации таких мутаций также являются такими, как указано выше.
[0135] В дополнительном аспекте этого варианта осуществления фармацевтическая композиция дополнительно содержит по меньшей мере одно дополнительное терапевтическое средство, предпочтительно ингибитор сигнального пути PI3K/Akt, как описано в настоящем документе.
[0136] Другой вариант осуществления настоящего изобретения представляет собой способ лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Этот способ включает введение индивидууму эффективного количества (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF, выбранный из группы, состоящей из AAL881 (Novartis); AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BeiGene-283 (BeiGene), BIIB-024 (MLN 2480) (Sunesis & Takeda), ингибитора b-raf (Sareum), ингибитора киназы BRAF (Selexagen Therapeutics), миРНК 313 (tacaccagcaagctagatgca) и 253 (cctatcgttagagtcttcctg) BRAF, CTT239065 (Institute of Cancer Research), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), LErafAON (NeoPharm, Inc.), LBT613 (Novartis), LGX-818 (Novartis), пазопаниба (GlaxoSmithKline), PLX5568 (Plexxikon), RAF-265 (Novartis), RAF-365 (Novartis), регорафениба (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), TAK 632 (Takeda), TL-241 (Teligene), XL-281 (Exelixis), их фармацевтически приемлемых солей и их сочетаний, для лечения или смягчения действия злокачественной опухоли. Предпочтительно, второе средство против злокачественной опухоли представляет собой регорафениб или его фармацевтически приемлемую соль.
[0137] В этом варианте осуществления подходящие и предпочтительные индивидуумы являются такими, как описано в настоящем документе. В этом варианте осуществления способы можно использовать для лечения злокачественных опухолей, описанных выше, включая злокачественные опухоли с мутантным происхождением, определенные выше. Способы идентификации таких мутаций также являются такими, как указано выше.
[0138] В дополнительном аспекте этого варианта осуществления способ дополнительно включает введение по меньшей мере одного дополнительного терапевтического средства, предпочтительно ингибитора сигнального пути PI3K/Akt, как описано в настоящем документе.
[0139] В другом аспекте этого варианта осуществления введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно.
[0140] Дополнительный вариант осуществления настоящего изобретения представляет собой способ уничтожения злокачественной клетки. Этот способ включает приведение злокачественной клетки в контакт с эффективным количеством (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF, выбранный из группы, состоящей из AAL881 (Novartis); AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BeiGene-283 (BeiGene), BIIB-024 (MLN 2480) (Sunesis & Takeda), ингибитора b-raf (Sareum), ингибитора киназы BRAF (Selexagen Therapeutics), миРНК 313 (tacaccagcaagctagatgca) и 253 (cctatcgttagagtcttcctg) BRAF, CTT239065 (Institute of Cancer Research), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), LErafAON (NeoPharm, Inc.), LBT613 (Novartis), LGX-818 (Novartis), пазопаниба (GlaxoSmithKline), PLX5568 (Plexxikon), RAF-265 (Novartis), RAF-365 (Novartis), регорафениба (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), TAK 632 (Takeda), TL-241 (Teligene), XL-281 (Exelixis), их фармацевтически приемлемых солей и их сочетаний. Предпочтительно, второе средство против злокачественной опухоли представляет собой регорафениб или его фармацевтически приемлемую соль.
[0141] Подходящие и предпочтительные злокачественные клетки являются такими, как описано в настоящем документе. В этом варианте осуществления уничтожение злокачественных клеток можно проводить у злокачественных клеток с различным мутантных происхождением и/или у злокачественных клеток, характеризуемых так, как описано выше. Способы идентификации таких мутаций также являются такими, как указано выше.
[0142] Способы этого варианта осуществления, который можно проводить in vitro или in vivo, можно использовать для уничтожения злокачественных клеток, например, посредством цитолиза злокачественных клеток в клетках типов злокачественных опухолей, описываемых в настоящем документе.
[0143] В одном из аспектов этого варианта осуществления злокачественная клетка представляет собой злокачественную клетку млекопитающего. Предпочтительно, злокачественную клетку млекопитающего получают у млекопитающего, выбранного из группы, состоящей из людей, приматов, сельскохозяйственных животных и домашних животных. Более предпочтительно, злокачественная клетка млекопитающего представляет собой злокачественную клетку человека.
[0144] В другом аспекте этого варианта осуществления способ дополнительно включает введение по меньшей мере одного дополнительного терапевтического средства, предпочтительно ингибитора сигнального пути PI3K/Akt, как описано в настоящем документе.
[0145] В дополнительном аспекте этого варианта осуществления приведение злокачественной клетки в контакт с первым и вторым средствами против злокачественных опухолей обеспечивает синергическое действие по сравнению с приведением злокачественной клетки в контакт с любым из этих средств против злокачественных опухолей отдельно.
[0146] В этом варианте осуществления "приведение в контакт" означает приведение BVD-523 и ингибиторов RAF и, необязательно, одного или нескольких дополнительных терапевтических средств в непосредственную близость со злокачественными клетками. Это можно проводить общепринятыми способами доставки лекарственных средств млекопитающим или в условиях in vitro, например, помещая BVD-523 и ингибиторы RAF и, необязательно, другие терапевтические средства в среды для культивирования, в которых находятся злокачественные клетки.
[0147] Дополнительный вариант осуществления настоящего изобретения представляет собой набор для лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Этот набор содержит эффективное количество (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF, выбранный из группы, состоящей из AAL881 (Novartis); AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BeiGene-283 (BeiGene), BIIB-024 (MLN 2480) (Sunesis & Takeda), ингибитора b-raf (Sareum), ингибитора киназы BRAF (Selexagen Therapeutics), миРНК 313 (tacaccagcaagctagatgca) и 253 (cctatcgttagagtcttcctg) BRAF, CTT239065 (Institute of Cancer Research), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), LErafAON (NeoPharm, Inc.), LBT613 (Novartis), LGX-818 (Novartis), пазопаниба (GlaxoSmithKline), PLX5568 (Plexxikon), RAF-265 (Novartis), RAF-365 (Novartis), регорафениба (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), TAK 632 (Takeda), TL-241 (Teligene), XL-281 (Exelixis), их фармацевтически приемлемых солей и их сочетаний, упакованные вместе с инструкциями по их применению. Предпочтительно, второе средство против злокачественной опухоли представляет собой регорафениб или его фармацевтически приемлемую соль.
[0148] В этом варианте осуществления подходящие и предпочтительные индивидуумы являются такими, как описано в настоящем документе. В этом варианте осуществления набор можно использовать для лечения злокачественных опухолей, описанных выше, включая злокачественные опухоли с мутантным происхождением, определенные в настоящем документе. Способы идентификации таких мутаций являются такими, как указано выше.
[0149] В дополнительном аспекте этого варианта осуществления набор дополнительно содержит по меньшей мере одно дополнительное терапевтическое средство, предпочтительно ингибитор сигнального пути PI3K/Akt, как описано в настоящем документе.
[0150] В другом аспекте этого варианта осуществления введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно.
[0151] Другой вариант осуществления настоящего изобретения представляет собой фармацевтическую композицию для лечения или смягчения действия злокачественной опухоли у нуждающегося в этом индивидуума. Эта фармацевтическая композиция содержит фармацевтически приемлемый разбавитель или носитель и эффективное количество (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF, выбранный из группы, состоящей из AAL881 (Novartis); AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BeiGene-283 (BeiGene), BIIB-024 (MLN 2480) (Sunesis & Takeda), ингибитора b-raf (Sareum), ингибитора киназы BRAF (Selexagen Therapeutics), миРНК 313 (tacaccagcaagctagatgca) и 253 (cctatcgttagagtcttcctg) BRAF, CTT239065 (Institute of Cancer Research), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), LErafAON (NeoPharm, Inc.), LBT613 (Novartis), LGX-818 (Novartis), пазопаниба (GlaxoSmithKline), PLX5568 (Plexxikon), RAF-265 (Novartis), RAF-365 (Novartis), регорафениба (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), TAK 632 (Takeda), TL-241 (Teligene), XL-281 (Exelixis), их фармацевтически приемлемых солей и их сочетаний, где введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно.
[0152] В этом варианте осуществления подходящие и предпочтительные индивидуумы являются такими, как описано в настоящем документе. Фармацевтические композиции по изобретению можно использовать для лечения злокачественных опухолей, описанных выше, включая злокачественные опухоли с мутантным происхождением, определенные в настоящем документе. Способы идентификации таких мутаций также являются такими, как указано выше.
[0153] В дополнительном аспекте этого варианта осуществления фармацевтическая композиция дополнительно содержит по меньшей мере одно дополнительное терапевтическое средство, предпочтительно ингибитор сигнального пути PI3K/Akt, как описано в настоящем документе.
[0154] Фармацевтические композиции по настоящему изобретению могут находиться в стандартной дозированной форме, содержащей оба средства против злокачественной опухоли. В другом аспекте этого варианта осуществления первое средство против злокачественной опухоли находится в первой стандартной дозированной форме, а второе средство против злокачественной опухоли находится во второй стандартной дозированной форме, отдельной от первой.
[0155] Первое и второе средства против злокачественных опухолей можно вводить индивидууму, одновременно или в различные моменты времени по назначению лечащего врача. Если первое и второе средства против злокачественных опухолей вводят в различные моменты времени, например, посредством последовательного введения, первое средство против злокачественной опухоли можно вводить индивидууму перед вторым средством против злокачественной опухоли. Альтернативно, второе средство против злокачественной опухоли можно вводить индивидууму перед первым средством против злокачественной опухоли.
[0156] По настоящему изобретению "эффективное количество" или "терапевтически эффективное количество" средства против злокачественной опухоли по изобретению, включая содержащие его фармацевтические композиции, которые описаны в настоящем документе, представляет собой количество такого средства или композиции, которого при введении индивидууму достаточно для получения полезных или желаемых результатов, как описано в настоящем документе. Эффективные дозированные формы, способы введения и величины доз можно определять эмпирически, и получение таких определений известно специалистам в данной области. Специалистам в данной области понятно, что величина дозы варьирует в зависимости от маршрута введения, скорости выведения, длительности лечения, характеристик любых других вводимых лекарственных средств, возраста, размеров и вида млекопитающего, например, человека, и подобных факторов, хорошо известных в областях медицины и ветеринарной медицины. Как правило, подходящей дозой средства или композиции по изобретению является такое количество средства или композиции, которое представляет собой наименьшую дозу эффективную для обеспечения желаемого действия. Эффективную дозу средства или композиции по настоящему изобретению можно вводить в виде двух, трех, четырех, пяти, шести или более поддоз, вводимых раздельно с подходящими интервалами на протяжении суток.
[0157] Подходящим неограничивающим примером дозировки BVD-523, ингибитора RAF или другого средства против злокачественной опухоли по настоящему изобретению является приблизительно от 1 мг/кг до приблизительно 2400 мг/кг в сутки, например, приблизительно от 1 мг/кг до приблизительно 1200 мг/кг в сутки, от 75 мг/кг в сутки до приблизительно 300 мг/кг в сутки, включая приблизительно от 1 мг/кг до приблизительно 100 мг/кг в сутки. Другие типичные дозировки таких средств включают приблизительно 1 мг/кг, 5 мг/кг, 10 мг/кг, 15 мг/кг, 20 мг/кг, 25 мг/кг, 30 мг/кг, 35 мг/кг, 40 мг/кг, 45 мг/кг, 50 мг/кг, 60 мг/кг, 70 мг/кг, 75 мг/кг, 80 мг/кг, 90 мг/кг, 100 мг/кг, 125 мг/кг, 150 мг/кг, 175 мг/кг, 200 мг/кг, 250 мг/кг, 300 мг/кг, 400 мг/кг, 500 мг/кг, 600 мг/кг, 700 мг/кг, 800 мг/кг, 900 мг/кг, 1000 мг/кг, 1100 мг/кг, 1200 мг/кг, 1300 мг/кг, 1400 мг/кг, 1500 мг/кг, 1600 мг/кг, 1700 мг/кг, 1800 мг/кг, 1900 мг/кг, 2000 мг/кг, 2100 мг/кг, 2200 мг/кг, и 2300 мг/кг в сутки. Эффективную дозу BVD-523, ингибиторов RAF или других средств против злокачественных опухолей, описываемых в настоящем документе, можно вводить в виде двух, трех, четырех, пяти, шести или более поддоз, вводимых раздельно с подходящими интервалами на протяжении суток.
[0158] BVD-523, ингибиторы RAF или другие средства против злокачественных опухолей или содержащие их фармацевтические композиции по настоящему изобретению можно вводить любым желаемым и эффективным способом: для перорального введения, или в виде мази или капель для местного введения в глаза, или для парентерального или другого введения любым подходящим способом, таким как интраперитонеальное, подкожное, топическое, интрадермальное, ингаляция, внутрилегочное, ректальное, вагинальное, сублингвальное, внутримышечное, внутривенное, внутриартериальное, интратекальное или внутрилимфатическое. Кроме того, BVD-523, ингибиторы RAF или другие средства против злокачественных опухолей или содержащие их фармацевтические композиции по настоящему изобретению можно вводить в сочетании с другими лечебными средствами. При желании BVD-523, ингибиторы RAF или другие средства против злокачественных опухолей или содержащие их фармацевтические композиции можно инкапсулировать или иным образом защищать от желудочного или других секретов.
[0159] Фармацевтические композиции по изобретению содержат один или несколько активных ингредиентов, например, средств против злокачественных опухолей, в смеси с одним или несколькими фармацевтически приемлемыми разбавителями или носителями и, необязательно, с одним или несколькими другими соединениями, лекарственными средствами, ингредиентами и/или веществами. Вне зависимости от выбранного маршрута введения средства/соединения по настоящему изобретению формулируют в фармацевтически приемлемые дозированные формы общепринятыми способами, известными специалистам в данной области. См., например, Remington, The Science and Practice of Pharmacy (21st Edition, Lippincott Williams and Wilkins, Philadelphia, PA.).
[0160] Фармацевтически приемлемые разбавители или носители хорошо известны в данной области (см., например, Remington, The Science and Practice of Pharmacy (21st Edition, Lippincott Williams and Wilkins, Philadelphia, PA.) и The National Formulary (American Pharmaceutical Association, Washington, D.C.)) и включают сахара (например, лактозу, сахарозу, маннит и сорбит), крахмалы, препараты целлюлозы, фосфаты кальция (например, дифосфат кальция, трифосфат кальция и гидрофосфат кальция), цитрат натрия, воду, водные растворы (например, солевое раствор, инъекционный хлорид натрия, раствор Рингера, декстрозу для инъекций, декстрозу и хлорид натрия для инъекций инъекция, раствор Рингера с лактатом для инъекций), спирты (например, этиловый спирт, пропиловый спирт и бензиловый спирт), полиолы (например, глицерин, пропиленгликоль и полиэтиленгликоль), сложные органические эфиры (например, этилолеат и триглицериды), биоразлагаемые полимеры (например, полилактид-полигликолид, сложные поли(полиортоэфиры) и поли(ангидриды)), эластомерные матриксы, липосомы, микросферы, масла (например, кукурузное, зародышей пшеницы, оливковое, касторовое, кунжутное, хлопковое и арахисовое), масло какао, воска (например, воска для суппозиториев), парафины, соединения кремния, тальк, силикат и т.д. Каждый фармацевтически приемлемый разбавитель или носитель, используемый в фармацевтической композиции по изобретению, должен быть "приемлемым" в смысле совместимости с другими ингредиентами состава и отсутствия вреда индивидууму. Разбавители или носители, подходящие для выбранной дозированной формы и назначенного пути введения, хорошо известны в данной области, и специалист в данной области может определить приемлемые разбавители или носители для выбранных дозированной формы и способа введения.
[0161] Фармацевтическая композиции по изобретению необязательно может содержать дополнительные ингредиенты и/или вещества широко используемые в фармацевтических композициях. Эти ингредиенты и вещества хорошо известны в данной области и включают (1) наполнители или средства увеличения объема, такие как крахмалы, лактоза, сахароза, глюкоза, маннит и кремниевая кислота; (2) связывающие средства, такие как карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, гидроксипропилметилцеллюлоза, сахароза и гуммиарабик; (3) увлажнители, такие как глицерин; (4) дезинтегрирующие средства, такие как агар-агар, карбонат кальция, картофельный или тапиоковый крахмал, альгиновая кислота, определенные силикаты, крахмалгликолят натрия, сшитые карбоксиметилцеллюлоза натрия и карбонат натрия; (5) замедляющие растворение средства, такие как парафин; (6) ускорители всасывания, такие как четвертичные аммонийные соединения; (7) средства для смачивания, такие как цетиловый спирт и моностеарат глицерина; (8) абсорбенты, такие как каолин и бентонитовая глина; (9) смазочные средства, такие как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли и лаурилсульфат натрия; (10) суспендирующие средства, такие как этоксилированные изостеариловые спирты, полиоксиэтиленсорбит и сорбитановые сложные эфиры, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант; (11) буферные средства; (12) эксципиенты, такие как лактоза, молочные сахара, полиэтиленгликоли, животные и растительные жиры, масла, воска, парафины, масло какао, крахмалы, трагакант, производные целлюлозы, полиэтиленгликоль, соединения кремния, бентониты, кремниевая кислота, тальк, салицилат, оксид цинка, гидроксид алюминия, силикаты кальция и полиамидный порошок; (13) инертные разбавители, такие как вода или другие растворители; (14) консерванты; (15) поверхностно-активные средства; (16) диспергирующие средства; (17) средства, контролирующие высвобождение или замедляющие всасывание, такие как гидроксипропилметилцеллюлоза, другие полимерные матриксы, биоразлагаемые полимеры, липосомы, микросферы, моностеарат алюминия, желатин и воска; (18) средства, снижающие прозрачность; (19) адъюванты; (20) средства для смачивания; (21) эмульгирующие и суспендирующие средства; (22) солюбилизаторы и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, масла (в частности, хлопковое, арахисовое, кукурузное, проростков пшеницы, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофуриловый спирт, полиэтиленгликоли и сложные эфиры жирных кислот сорбитана; (23) пропелленты, такие как хлорфторуглеводороды и летучие незамещенные углеводороды, такие как бутан и пропан; (24) антиоксиданты; (25) средства обеспечения изотоничности состава с кровью назначенного реципиента, такие как сахара и хлорид натрия; (26) загустители; (27) покрытия, такие как лецитин; и (28) подсластители, вкусо-ароматические добавки, красители, отдушки и консерванты. Каждый такой ингредиент или вещество должны быть "приемлемыми" в смысле совместимости с другими ингредиентами состава и отсутствия вреда индивидууму. Ингредиенты и вещества, подходящие для выбранной дозированной формы и назначенного пути введения, хорошо известны в данной области, и специалист в данной области может определить приемлемые ингредиенты и вещества для выбранных дозированной формы и способа введения.
[0162] Фармацевтические композиции по настоящему изобретению, подходящие для перорального введение, могут находиться в форме капсул, крахмальных капсул, пилюль, таблеток, порошков, гранул, растворов или суспендирования в водной или неводной жидкости, жидкой эмульсии масло-в-воде или вода-в-масле, эликсире или сиропе, пастилки, болюсов, электуария или пасты. Эти составы можно получать известными в данной области способами, например, посредством общепринятых способов дражирования, смешивания, гранулирования или лиофилизации.
[0163] Твердые лекарственные формы для перорального введения (капсулы, таблетки, пилюли, драже, порошки, гранулы и т.п.) можно получать, например, смешивая активный ингредиент(ы) с одним или несколькими фармацевтически приемлемыми разбавителями или носителями и, необязательно, одним или несколькими наполнителями, увеличителями объема, связывающими средствами, увлажнителями, дезинтегрирующими средствами, средствами замедления растворения, ускорителями всасывания, средствами для смачивания, абсорбентами, смазочными средствами и/или красителями. Твердые композиции сходного типа можно использовать в качестве наполнителей в мягких и твердых наполняемых желатиновых капсулах с использованием подходящего эксципиента. Таблетки можно получать посредством прессования или формовки, необязательно с одним или несколькими дополнительными ингредиентами. Прессованные таблетки можно получать с использованием подходящего связывающего средства, смазочного средства, инертного разбавителя, консерванта, дезинтегранта, поверхностно активного или диспергирующего средства. Формованные таблетки можно получать посредством формования в подходящем устройстве. Таблетки и другие твердые дозированные формы, такие как драже, капсулы, пилюли и гранулы, необязательно могут быть шероховатыми или полученными с использованием покрытий и оболочек, таких как растворяющиеся в кишечнике покрытия и другие покрытия, хорошо известные в области формулирования фармацевтических средств. Также их можно формулировать так, чтобы обеспечивать замедленное или контролируемое высвобождение активного ингредиента. Их можно стерилизовать, например, посредством фильтрования через удерживающий бактерии фильтр. Также эти композиции необязательно могут содержать средства, снижающие прозрачность и могут представлять собой композиции, которые высвобождают активный ингредиент только, или предпочтительно, в определенном отделе желудочно-кишечного тракта, необязательно, в замедленном режиме. Также активный ингредиент может находиться в микроинкапсулированной форме.
[0164] Жидкие дозированные формы для перорального введения включают фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. Жидкие дозированные формы могут содержать подходящие инертные разбавители, широко используемые в данной области. Кроме инертных разбавителей пероральные композиции также могут содержать вспомогательные средства, такие как средства для смачивания, эмульгирующие и суспендирующие средства, подсластители, вкусо-ароматические добавки, красители, отдушки и консерванты. Суспензии могут содержать суспендирующие средства.
[0165] Фармацевтические композиции по настоящему изобретению для ректального или вагинального введения могут быть представлены в виде суппозиториев, которые можно получать, смешивая один или несколько активных ингредиентов с одним или несколькими подходящими нераздражающими разбавителями или носителями, которые являются твердыми при комнатной температуре, но жидкими при температуре тела и, таким образом, плавятся в полости прямой кишки или влагалища и высвобождают активное соединение. Фармацевтические композиции по настоящему изобретению, которые подходят для вагинального введения, также включают пессарии, тампоны, кремы, гели, пасты, пенные или спрейные составы, содержащие такие фармацевтически приемлемые разбавители или носители, для которых в данной области известно, что они являются приемлемыми.
[0166] Дозированные формы для топического или трансдермального введения включают порошки, спреи, мази, пасты, кремы, лосьоны, гели, растворы, пластыри, капли и ингаляторы. Активное средство(а)/соединение(я) можно смешивать в стерильных условиях с подходящим фармацевтически приемлемым разбавителем или носителем. Мази, пасты, кремы и гели могут содержать эксципиенты. Порошки и спреи могут содержать эксципиенты и пропелленты.
[0167] Фармацевтические композиции по настоящему изобретению, подходящие для парентерального введения, могут содержать одно или несколько средств/соединений в комбинации с одним или несколькими фармацевтически приемлемыми стерильными изотоническими водными или неводными растворами, дисперсиями, суспензиями или эмульсиями или со стерильными порошками, которые можно восстанавливать в стерильных инъецируемых растворах или дисперсиях непосредственно перед применением, которые могут содержать подходящие антиоксиданты, буферы, растворители, которые делают состав изотоническим с кровью назначенного реципиента, или суспендирующие средства или загустители. Должную текучесть можно поддерживать, например, с использованием материалов покрытий, поддерживая требуемый размер частиц в случае дисперсий, и используя поверхностно-активные вещества. Эти фармацевтические композиции также могут содержать подходящие вспомогательные средства, такие как средства для смачивания, эмульгаторы и диспергирующие средства. Желательным также может являться включение средств придания изотоничности. Кроме того, посредством включения средств, задерживающих всасывание, можно обеспечивать пролонгированное всасывание инъецируемой фармацевтической формы.
[0168] В некоторых случаях, для продления действия лекарственного средства (например, фармацевтического состава), желательно замедлить его всасывание после подкожной или внутримышечной инъекции. Это можно обеспечивать, используя жидкую суспензию кристаллического или аморфного материала с плохой растворимостью в воде.
[0169] Тогда скорость всасывания активного средства/лекарственного средства зависит от его скорости растворения, которая в свою очередь может зависеть от размеров кристаллов и формы кристаллов. Альтернативно, задержанное всасывание парентерально вводимого средства/лекарственного средства можно обеспечивать, растворяя или суспендируя активное средство/лекарственное средство в масляном носителе. Можно получать формы инъецируемых депо, формируя микроинкапсулированные матриксы активного ингредиента в биоразлагаемых полимерах. Скорость высвобождения активного ингредиента можно контролировать как функцию отношения активного ингредиента к полимеру и характера конкретного используемого полимера. Составы инъецируемых депо также получают, заключая лекарственное средство в липосомы или микроэмульсии, которые совместимы с тканями организма. Инъецируемые материалы можно стерилизовать, например, посредством фильтрации через удерживающий бактерии фильтр.
[0170] Составы можно предоставлять в однодозовых или многодозовых герметизированных контейнерах, например, ампулах и флаконах, и можно хранить в лиофилизированном состоянии, требующем только добавления непосредственно перед применением стерильного жидкого разбавителя или носителя, например, воды для инъекций. Получаемые для немедленной инъекции растворы и суспензии можно получать из стерильных порошков, гранул и таблеток описанных выше типов.
[0171] Настоящее изобретение относится к комбинациям, для которых показано, что они усиливают действие ингибиторов ERK. В настоящем документе заявители также продемонстрировали, что подобным образом синергичны комбинации различных ингибиторов ERK. Таким образом, предусмотрено, что действие комбинаций, описываемых в настоящем документе, можно дополнительно улучшать, используя один или несколько дополнительных ингибиторов ERK. Таким образом, определенные варианты осуществления настоящего изобретения включают один или несколько дополнительных ингибиторов ERK.
[0172] Для дальнейшей иллюстрации способов по настоящему изобретению предоставлены приводимые ниже примеры. Эти примеры являются исключительно иллюстративными и никоим образом не предназначены для ограничения объема изобретения.
ПРИМЕРЫ
Пример 1
МАТЕРИАЛЫ И МЕТОДЫ
[0173] Линии злокачественных клеток поддерживали в культуре клеток в условиях со стандартными средами и сыворотками. Для исследований с увеличением дозы клетки A375 разделяли, выращивали приблизительно до 40-60% конфлуэнтности, а затем обрабатывали исходной дозой указанного лекарственного средства. В таблице 4 представлен список обработок лекарственными средствами с увеличением дозы.
Список обработок с увеличением дозы
[0174] Увеличение дозы с единственным применяемым средством проводили на основе Little et al., 2011, и это описано на фиг. 25. Затем клеткам позволяли расти до 70-90% конфлуэнтности и разделяли. Коэффициенты разделения соблюдали настолько "нормальными" насколько возможно и обоснованно согласовывали с лечебными средствами (например, минимум 50% нормального коэффициента разделения родителей). Среду обновляли каждые 3-4 суток. Когда клетки снова достигали приблизительно 40-60% конфлуэнтности, дозу увеличивали. В случае, когда окно 40-60% пропускали, клетки снова разделяли и дозировали после того, как они достигали 40-60% конфлуэнтности. Среду снова обновляли каждые 3-4 суток. Процесс повторяли столько, сколько было необходимо (фиг. 25).
[0175] Для обработок одним средством начальные концентрации и увеличение доз проводили, начиная приблизительно от IC50, проводя увеличение с небольшими приращениями или осторожно для первых 4-5 доз, удваивая дозу, увеличивая с таким же приращением для следующих 4 доз, затем переходя на 1,5-кратное увеличение концентрации для последующих доз.
[0176] Для комбинированных обработок начальные концентрации и увеличение доз проводили, начиная с половины приблизительно IC50 каждого соединения (анализ комбинаций свидетельствовал о том, что это приводит приблизительно к интервалу ингибирования 40-70%), проводя увеличение в соответствии с анализом одного средства (т.е. проводя начальное удвоение, а затем увеличивая с тем же приращением в течение 4 доз, затем переходя на 1,5-кратное увеличение концентрации). В таблице 5 представлено проектируемое увеличение доз с использованием этих схем.
Проектируемое увеличение доз - месяц 1
[0177] Клональные популяции устойчивых клеток получали из популяций устойчивых клеток посредством лимитирующих разведений.
[0178] Для отслеживания изменении в чувствительности к увеличиваемым дозам средств(а) использовали анализы пролиферации через подходящие временные интервалы (например, каждый месяц, хотя выбор интервалов зависит от достаточных количеств доступных клеток). Для анализов пролиферации клетки высевали в 96-луночные планшеты в количестве 3000 клеток на лунку в среду DMEM, не содержащую лекарственного средства, содержащую 10% FBS, и позволяли прикрепляться в течение ночи с последующим добавлением соединений или контроля носителя. Соединения получали из исходных растворов в DMSO с получением диапазона конечных концентраций, как представлено на фиг. 2A-H. Конечная концентрация DMSO являлось постоянной, составляя 0,1%. Тестируемые соединения инкубировали с клетками в течение 96 часов при 37°C и 5% CO2 в увлажненной атмосфере. Затем добавляли 10% Alamar Blue (об./об.) и инкубировали в течение 4 часов и детектировали флуоресцентный продукт с использованием планшетного спектрофотометра FLUOstar BMG. Вычитали средние фоновые значения для сред, не содержащих тестируемых соединений, и данные анализировали с использованием 4-параметрического логистического уравнения в GraphPad Prism. В качестве положительного контроля использовали паклитаксел.
[0179] Анализы пролиферации в течение месяца 1 начинали на сутки 28 с использованием клеток, растущих в концентрациях каждого средства, указанных в таблице 6.
Исходные концентрации лекарственных средств, используемых в анализах пролиферации - месяц 1
[0180] Анализы пролиферации в течение месяца 2 начинали на сутки 56 с использованием клеток, растущих в концентрациях каждого средства, указанных в таблице 7.
Исходные концентрации лекарственных средств, используемых в анализах пролиферации - месяц 2
[0181] В конце месяца 3 периода увеличения дозы культуры поддерживали при наибольшей концентрации в течение 2 недель с последующим конечным циклом анализов пролиферации и потенциальным клонированием единичных клеток. Так как анализы пролиферации/клонирования единичных клеток требовали активно пролиферирующих клеток, для обработок, где клетки при наибольшей концентрации пролиферировали очень медленно или для которых только недавно поднимали дозу, также поддерживали запасную культуру при наименьшей концентрации (таблица 8). Для обработки BVD-523, где клетки по наблюдением почти полностью останавливали рост и при наибольшей концентрации (1,8 мкМ) выглядели особенно неустойчивыми, культуры в течение периода 2 недель поддерживали при наименьшей концентрации.
Подробности обработок при культивировании при фиксированной концентрации в течение 2 недель
[0182] В анализах пролиферации в течение месяца 3 использовали клетки, растущие в концентрациях каждого средства, указанных в таблице 9.
Исходные концентрации лекарственных средств, используемых в анализах пролиферации - месяц 3
[0183] Для исследований комбинаций клетки A375 (ATCC) высевали в трех повторениях в 96-луночные планшеты при плотности клеток 3000 клеток/лунку в DMEM, дополненную 10% FBS, и позволяли прикрепляться в течение ночи с последующим добавлением тестируемого соединения или контроля носителя. Комбинации тестировали с использованием матрицы доз 10×8 с конечной концентрацией DMSO 0,2%. Далее проводили анализирующий период инкубации в течение 96 час с последующим добавлением 10% Alamar Blue (об./об.) и 4 часами инкубации с последующим считыванием на флуоресцентном планшетном спектрофотометре. После считывания показателей Alamar Blue смесь среды/Alamar Blue удаляли и добавляли 100 мкл CellTiter-Glo/PBS (1:1) и планшеты обрабатывали по инструкциям производителя (Promega). Перед анализом данных вычитали средние фоновые значения для сред, не содержащих тестируемых соединений. Затем использовали аддитивную модель Блисса.
[0184] В кратком изложении, для комбинированного ингибирования теоретически рассчитывали значения парциального ингибирования с использованием уравнения Cbliss=A+B - (A×B), где A и B представляют собой парциальные ингибирования, получаемые отдельно для лекарственного средства A или отдельно для лекарственного средства B при указанных концентрациях. Cbliss представляет собой парциальное ингибирование, которое можно ожидать, если комбинация двух лекарственных средств была бы точно аддитивной. Значения Cbliss вычитают из экспериментально наблюдаемых значений парциального ингибирования с получением значения "приращения по Блиссу". Значения приращения по Блиссу, большие 0, указывают на синергию, тогда как значения, меньшие 0, указывают на антагонизм. Значения приращений по Блиссу графически изображают в виде тепловых карт ± SD.
[0185] Данные для единственных средств и комбинаций также представляют в виде кривых зависимостей "доза-эффект", получаемых в GraphPad Prism (изображаемых с использованием % жизнеспособности относительно контролей, обработанных только DMSO,).
[0186] Для сфокусированных исследований комбинаций анализы жизнеспособности с Alamar Blue проводили, как описано выше для исследований комбинаций. Кроме того, проводили анализы с каспазой-Glo 3/7. В кратком изложении, клетки HCT116 высевали в трех повторениях в 96-луночные белые планшеты при плотности клеток 5000 клеток/лунку в среду McCoy 5A с 10% FBS. Клетки A375 высевали при плотности 5000 клеток/лунку в среду DMEM с 10% FBS. Клеткам позволяли прикрепляться в течение ночи с последующим добавлением указанного количества тестируемого соединения или контроля носителя. Конечная концентрация DMSO составляла 0,2%, а в качестве положительного контроля добавляли 800 нМ стауроспорин. Использовали анализирующие периоды инкубации 24 и 48 часов. Затем добавляли каспазу-Glo® 3/7 50% (об./об.), планшеты перемешивали в течение 5 минут на круговой качалке и инкубировали в течение 1 часа при комнатной температуре с последующим считыванием на люминесцентном планшетном спектрофотометре. Перед анализом данных вычитали средние фоновые значения для сред, не содержащих тестируемых соединений.
Пример 2
Увеличение дозы и анализы пролиферации - месяц 1
Ход увеличения дозы - месяц 1
[0187] У клеток A375 проводили увеличение дозы с использованием BVD-523, дабрафениба и траметиниба в качестве единственных средств или в комбинации. В течение первого месяца дозы увеличивали с небольшими приращениями. За исключением заметного снижения скорости роста, клетки в основном хорошо переносили увеличение дозы и в течение месяца 2 дозы планировали увеличивать более агрессивно с использованием больших приращений. На фиг. 1A-C представлен ход исследований с увеличением дозы в течение месяца 1.
Результаты анализов пролиферации - месяц 1
[0188] Анализы пролиферации проводили для оценки ответа линий клеток, для которых проводили увеличение дозы, на обработку BVD-523, дабрафенибом и траметинибом по сравнению с исходной линией клеток.
[0189] На фиг. 2A-H представлены нормализованные и необработанные результаты анализов пролиферации, полученные во время исследований в течение месяца 1. Следует отметить, что различия в максимальных сигналах в контролях DMSO при различных обработках (фиг. 2D-F, 2H) свидетельствуют о различных скоростях роста при различных обработках. Эти различия в анализах пролиферации могут влиять на ответ линий на ингибиторы.
[0190] В таблице 10 представлены данные IC50, полученные в течение месяца 1 исследований.
Данные IC50 - месяц 1
[0191] Ранее существовали признаки того, что клетки, растущие в присутствии увеличиваемых доз дабрафениба или траметиниба, в качестве единственных средств или в комбинациях, в анализах пролиферации демонстрировали сниженные ответы на эти два средства.
[0192] На ранних этапах месяца 2 скорость роста клеток при обработке только дабрафенибом значительно возрастала относительно ранних этапов месяца 1. Это обеспечивало увеличенную скорость прогрессирования и свидетельствовало о том, что выявляли устойчивость.
Пример 3
Увеличение дозы и анализы пролиферации - месяц 2
Ход увеличения дозы - Месяц 2
[0193] На втором месяце исследований изучали переход большинства обработок на этап, когда дозы увеличивали с большим приращением (в 1,5 раза) по сравнению с исходной фазой небольшого увеличения. Увеличение дозы единственных средств дабрафениба и траметиниба было наибыстрейшим с клетками, растущими в концентрациях, эквивалентных 100×IC50 для исходных клеток (фиг. 3A,B). Увеличение дозы единственного средства BVD-523 по сравнению с дабрафенибом и траметинибом проходило медленнее (фиг. 3C). См. фиг. 3D для сравнения увеличения дозы единственных средств. Клетки с увеличиваемой дозой BVD-523 по сравнению с популяциями с увеличиваемыми дозами дабрафениба и траметиниба выглядели более "неустойчивыми" и наблюдали большее количество плавающих клеток.
[0194] Увеличение доз комбинированных средств проходило медленнее, чем обработки единственным средством. Комбинация BVD-523/траметиниб для предотвращения развития клеток была особенно эффективной.
Результаты анализа пролиферации - месяц 2
[0195] Анализы пролиферации у популяций клеток с увеличиваемыми дозами единственных средств дабрафениба и траметиниба выявили умеренные сдвиги кривых доза-ответ, что свидетельствует о том, что дополнительный период увеличения дозы мог быть благоприятным для дальнейшего обогащения устойчивыми клетками. Что интересно, при анализах пролиферации появились основания, позволяющие предполагать, что клетки, подвергаемые действию BVD-523, при отмене ингибитора росли хуже, возможно указывая на уровень привыкания.
[0196] На фиг. 4A-H представлены нормализованные и необработанные результаты анализов пролиферации, полученные в течение месяца 2 исследований. Следует отметить, что различия в максимальных сигналах в контролях DMSO при различных обработках (фиг. 4D-F, 4H) свидетельствуют о различных скоростях роста при различных обработках. Эти различия в анализах пролиферации могут влиять на ответ линий на ингибиторы.
[0197] На фиг. 5A-H представлены нормализованные и необработанные результаты анализов пролиферации, полученные в течение месяца 2 исследований, с фокусом только на данных об исходной линии и линии BVD-523.
[0198] В таблице 11 представлены данные IC50, полученные в течение месяца 2 исследований. Относительные IC50 определяли на основе подбора кривых по 4 параметрам в Prism.
Данные IC50 - месяц 2
Пример 4
Увеличение дозы и анализы пролиферации - месяц 3
Ход увеличения дозы - месяц 3
[0199] На фиг. 6A-C представлено увеличение дозы для единственных средств и комбинации средств для месяца 3 исследований. На фиг. 6D представлено сравнение увеличений дозы для единственных средств.
Результаты анализа пролиферации - месяц 3
[0200] На фиг. 7 представлена оценка роста в анализе пролиферации в лунках с контролем DMSO. На фиг. 8A-D представлены результаты, полученные в течение месяца 3 исследований. На фиг. 9A-D представлены результаты, полученные в течение месяца 3 исследований с фокусом на линиях клеток с единственными лечебными средствами.
[0201] В таблице 12 представлены данные IC50, полученные в течение месяца 3 исследований. Относительные IC50 определяли на основе подбора кривых по 4 параметрам в Prism. Значения IC50 не определяли в линии клеток, для которой увеличение дозы проводили с использованием траметиниба вследствие отсутствия роста при анализе (н.п.: не проводили).
Данные IC50 - месяц 3
Пример 5
Результаты исследований комбинаций
[0202] Как и ожидалось, клетки A375, которые несут мутацию BRAF (V600E), были чувствительны к дабрафенибу. Значения IC50 для единственных средств, рассчитанные с использованием Alamar Blue (фиг. 10, 12, 14), для дабрафениба и BVD-523 как правило, были немного меньше по сравнению со значениями, полученными с использованием CellTiter-Glo (фиг. 11, 13, 15). Опубликованные значения IC50 для дабрафениба и траметиниба в анализе CellTiter-Glo в течение 72 часов составляли 28±16 нМ и 5±3 нМ, соответственно (Greger et al., 2012; King et al., 2013) -результаты для единственных средств, приводимые в настоящем документе соответствуют этим значениям. Существовали определенные свидетельства об окне синергии при всех обработках. Отклонения между тремя повторениями были низкими, однако существовали определенные свидетельства пограничных эффектов, которые правдоподобно объясняют видимый усиленный рост, наблюдаемый при некоторых лечебных средствах по сравнению с контролем без лекарственного средства (например, в частности наблюдаемый при комбинации траметиниб/BVD-523). Это делает интерпретацию анализа по Блиссу более сложной, так как для некоторых лечебных средств он может приводить к ложному увеличению уровня синергии.
[0203] Анализы комбинаций повторяли для клеток A375. Кроме того, в контрольном анализе комбинаций использовали клетки HCT116. Результаты этих экспериментов представлены на фиг. 31-41. Активность единственных средств BVD-523, траметиниба и дабрафениба согласовывалась с активностью, описанной в предыдущих исследованиях.
[0204] Клетки HCT116 представляют собой клетки колоректального рака человека с мутациями в KRAS. Дабрафениб и траметиниб являлись антагонистами при рассматриваемых действенных концентрациях. В отличие от этого, траметиниб в широком диапазоне комбинаций с AZ628 и с высокими концентрациями сорафениба демонстрировал синергию. BVD-523 демонстрировал окно синергии и с AZ628, и с сорафенибом.
[0205] В клетках A375 траметиниб демонстрировал сегменты синергии при низких концентрациях дабрафениба и AZ628. BVD-523 демонстрировал окно синергии с низкими концентрациями сорафениба.
Пример 6
BVD-523 изменял маркеры активности и эффекторной функции MAPK-киназ
[0206] Для исследований вестерн-блоттингом клетки HCT116 (5×106) высевали в 10 см чашки в среду McCoy 5A с 10% FBS. Клетки A375 (2,5×106) высевали в 10 см чашки в среду DMEM с 10% FBS. Клеткам позволяли прикрепляться в течение ночи с последующим добавлением указанного количества тестируемого соединения (BVD-523) или контроля носителя. Клетки обрабатывали в течение 4 или 24 часов с последующим выделением цельноклеточных лизатов белков, как указано ниже. Клетки собирали посредством трипсинизации, осаждали и быстро замораживали. Лизаты получали с использованием буфера для RIPA (радиоиммунопреципитационный анализ), очищали посредством центрифугирования и количественно определяли посредством анализа с бицинхониновой кислотой (BCA). 20-50 мкг белка разрешали посредством электрофореза в SDS-PAGE, переносили на мембрану PVDF и исследовали с использованием антител, указанных в таблице 13 (для обработки в течение 4 часов) и в таблице 14 (для обработки в течение 24 часов) ниже.
Подробное описание антител
блокировки
Подробное описание антител
блокировки
[0207] На фиг. 16-18 представлены анализы вестерн-блоттингом клеток, обработанных BVD-523 в различных концентрациях, для следующего: 1) компоненты передачи сигналов MAPK в клетках A375 через 4 часа; 2) передача сигналов клеточного цикла и апоптоза в клетках A375 через 24 часа обработки различными количествами BVD-523 и 3) передача сигналов MAPK в клетках HCT-116, обработанных в течение 4 часов. Результаты демонстрируют, что кратковременная и длительная обработка BVD-523 мутантных по RAF и RAS злокачественных клеток in vitro действовала на фосфорилирование субстрата и цели эффекторов киназ ERK. Концентрации BVD-523, необходимые для индукции этих изменений, как правило, находятся в низком микромолярном диапазоне.
[0208] Изменения некоторых маркеров специфической активности заслуживают внимания. Во-первых, после обработки BVD-523 увеличивается относительное содержание медленно мигрирующих изоформ киназы ERK; можно наблюдать незначительные изменения при кратковременной обработке и увеличение после длительной обработки. Хотя это может указывать на увеличение ферментативно активных, фосфорилированных форм ERK, остается заслуживающим внимания, что после обработки BVD-523 несколько белков, являющихся мишенью прямого и непрямого регулирования ERK, остаются "в неактивном состоянии". Во-первых, у белков RSK1/2 выявляют сниженное фосфорилирование по остаткам, которые в отношении модификации белков строго зависят от ERK (T359/S363). Во-вторых, обработка BVD-523 индуцирует комплексные изменения в обратной фосфатазе MAPK, DUSP6: после кратковременной обработки снижены уровни медленно мигрирующих изоформ белков, при этом после длительной обработки BVD-523 значительно снижены уровни тотального белка. Оба этих результата согласуются со сниженной активностью киназ ERK, которые контролируют функцию DUSP6 посредством посттрансляционных и транскрипционных механизмов. В общем, несмотря на возрастание клеточных форм ERK, которые, как правило, считают активными, по-видимому вероятно, что после кратковременной или длительной обработки BVD-523 активность клеточных ферментов ERK полностью ингибирована.
[0209] В соответствии с этими наблюдениями после обработки BVD-523 изменены эффекторные гены, которым необходим сигнальный путь MAPK. Передача сигналов MAPK на посттрансляционном и транскрипционном уровне регулирует аппарат клеточного цикла G1/S, и уровни белка циклина D1 после длительной обработки BVD-523 значительно снижены. Подобным образом, экспрессия генов и относительное содержание белков эффекторов апоптоза часто требует интактной передачи сигналов MAPK, и после длительной обработки BVD-523 возрастают общие уровни Bim-EL. Однако, как указано выше, в исходных клетках A375 расщепление белка PARP и увеличение апоптоза не наблюдали; это позволяет предположить, что на трансляцию изменений в передаче сигнала зависимым от BVD-523/ERK эффекторам в определенные события, такие как гибель клеток и арест клеточного цикла, могут влиять дополнительные факторы.
[0210] В соответствии с клеточной активностью BVD-523, анализ маркеров позволяет предположить, что ингибирование ERK изменяет ряд событий молекулярной передачи сигналов в злокачественных клетках, делая их предрасположенными к сниженной клеточной пролиферации и жизнеспособности.
[0211] В итоге на фиг. 16-18 представлено, что BVD-523 ингибирует путь передачи сигналов MAPK и в этих условиях может быть более предпочтительным, чем ингибирование RAF или MEK.
[0212] В результате свойства BVD-523 могут делать его предпочтительным средством для применения в качестве ингибитора ERK по сравнению с другими средствами со сходной активностью. Известно, что ингибирующие киназу лекарственные средства демонстрируют уникальные и специфические взаимодействия с их ферментами-мишенями, и что эффективность лекарственных средств сильно зависит от способа прямого ингибирования, а также от предрасположенности к адаптивным изменениям, которые происходят после лечения. Например, ингибиторы киназ ABL, KIT, EGFR и ALK эффективны только когда узнаваемые ими мишени находятся в активных или неактивных конфигурациях. Подобным образом, некоторые из этих ингибиторов уникальным образом чувствительны к вторичным генетическим мутациям или посттрансляционным адаптивным изменениям белков-мишеней. Наконец, ингибиторы RAF демонстрируют дифференциальную активность в отношении киназ RAF, присутствующих в определенных белковых комплексах и/или в определенных субклеточных локализациях. В итоге, так как подобным образом известно, что киназы ERK существуют в различных, переменных и комплексных биохимических состояниях, по видимому, вероятно, что BVD-523 может взаимодействовать с этими мишенями и ингибировать их таким способом, который явно и очень предпочтителен по сравнению с другими средствами.
Пример 7
Анализ in vivo
Мыши
[0213] На сутки исследования 1 самки бестимусных голых мышей (Crl:NU(Ncr)-Foxn/nu, Charles River) находились в возрасте девяти недель с диапазоном массы тела (BW) от 17,5 до 26,2 грамм. Животных содержали в условиях неограниченной доступности воды (обратный осмос, 1 м.д. Cl) и питания NIH 31 Modified and Irradiated Lab Diet®, состоящего из 18,0% общего белка, 5,0% общего жира и 5,0% общих волокон. Мышей содержали на облучаемой подстилке Enrich-o'cobsTM Laboratory Animal Bedding в статических микроизоляторах с 12-часовым световым циклом при 20-22°C (68-72°F) и 40-60% влажности. В отношении содержания, ухода, хирургических процедур, кормления и регулирования жидкости и ветеринарной помощи выполнялись рекомендации руководства по содержанию и использованию лабораторных животных Guide for Care and Use of Laboratory Animals.
Имплантация и рост опухоли in vivo
[0214] Опухолевые ксенотрансплантаты вводили с использованием клеток меланомы человека A375 посредством серийной подкожной трансплантации бестимусным голым мышам. На сутки имплантации опухоли каждая тестируемая мышь получала 1 мм3 фрагмента A375, имплантированного подкожно в левый бок, и рост опухоли наблюдали в виде среднего размера, достигающего запланированного диапазона от 80 до 120 мм3. Опухоли измеряли в двух измерениях с использованием штангенциркуля, и объем рассчитывали по формуле:
Объем опухоли (мм3) =w2×l/2
где w=ширина и l=длина опухоли в мм. Массу опухоли можно рассчитать в предположении, что 1 мм3 объема опухоли эквивалентен 1 мг.
[0215] Через десять суток после имплантации опухоли, обозначаемых как сутки 1 исследования, животных сортировали по девяти группам (группы 1-9), где каждая состояла из пятнадцати мышей, и одной группе (группа 10), состоящей из десяти мыши. Индивидуальные объемы опухолей находились в диапазоне от 75 до 144 мм3 и средние групповые объемы опухолей составляли 110 или 111 мм3.
Терапевтические средства
[0216] BVD-523 и дабрафениб получали в виде сухих порошков и хранили при комнатной температуре с защитой от света.
[0217] Дозы BVD-523 получали, суспендируя требуемое количество порошка BVD-523 в 1% карбоксиметилцеллюлозе в деионизированной воде ("1% CMC"). Получали исходное разведение BVD-523 10 мг/мл и использовали для дозирования в группе 100 мг/кг BVD-523. Аликвоты исходного разведения разбавляли носителем до концентрации 5,0 мг/мл с получением дозы 50 мг/кг BVD-523 в объеме дозирования 10 мл/кг. Дозы BVD-523 хранили при 4°C с защитой от света в течение периода до одной недели.
[0218] Сухой порошок дабрафениба состоял из 84,5% активного соединения, которые определяли при получении доз. Дабрафениб формулировали в 1% CMC с концентрациями 11,834 и 5,917 мг/мл с получением дозировок 100 и 50 мг/кг активного соединения, соответственно, в объеме дозирования 10 мл/кг. Дозы дабрафениба хранили с защитой от света при 4°C в течение периода до одной недели.
[0219] Для дозирования контрольной группы использовали 1% носитель CMC ("носитель").
[0220] Дозы темозоломида (темодар (Temodar®), Schering Corporation, номер партии 2RSA013) получали, суспендируя содержимое требуемого количества 100 мг капсул темодара (Temodar®) в деионизированной воде в концентрации 15 мг/мл, что обеспечивало дозировку 150 мг/кг в объеме дозирования 10 мл/кг. Темозоломид хранили с защитой от света при 4°C в течение периода дозирования 5 суток.
Обработка
[0221] На сутки 1 исследования мышей сортировали по девяти группам (группа 1-9), где каждая состояла из пятнадцати мышей, и одной группе (группа 10), состоящей из десяти мышей, и начинали дозирование по плану обработки, приведенному в таблице 15 ниже. Каждую дозу вводили посредством перорального принудительного кормления (п/о) в объеме дозирования 10 мл/кг (0,2 мл на 20 грамм массы тела), в соответствии с массой тела каждого отдельного животного. Дозы носителя и дабрафениба были предназначены для введения раз в сутки до конца исследования (раз в сутки до конца), тогда как дозы BVD-523 были предназначены для введения дважды в сутки до конца исследования(дважды в сутки до конца). При дозировании дважды в сутки дозирование начинали в полдень на сутки 1 так, чтобы на первые сутки ввести одну дозу ("1 доза на первые сутки").
Схема протокола для исследования A375 in vivo
BVD-523
50
п/о
дважды в сутки до конца
BVD-523
100
п/о
дважды в сутки до конца
BVD-523
50
п/о
дважды в сутки до конца
BVD-523
100
п/о
дважды в сутки до конца
Носитель=1% карбоксиметилцеллюлоза (CMC) в DI воде
При дозировании дважды в сутки одну дозу вводили в полдень на первые сутки и одну дозу вводили утром на последние сутки.
[0222] Дозирования в группах с комбинациями в течение исследования модифицировали как описано ниже.
[0223] Группа 1 получала 1% носителя CMC и служила в качестве контрольной группы для расчета % TGD. Группа 10 получала темозоломид на уровне 150 мг/кг раз в сутки в течение пяти суток (раз в сутки × 5) и служила в качестве эталонной группы.
Обработка посредством монотерапии
[0224] Группы 6 и 7 получали 50 и 100 мг/кг дабрафениба, соответственно. Группы 8 и 9 получали 50 и 100 мг/кг BVD-523, соответственно.
Комбинированные обработки
[0225] Группы 2 и 3 получали комбинации 50 мг/кг дабрафениба с 50 или 100 мг/кг BVD-523, соответственно. Группы 4 и 5 получали комбинации 100 мг/кг дабрафениба с 50 или 100 мг/кг BVD-523, соответственно. Вследствие выраженного ответа на комбинированное лечение дозирование в группах 2-5 останавливали на сутки 20 для контроля повторного роста опухоли. Когда средний размер опухоли достигал 1000 мм3, дозирование в группе начинали снова. На сутки 42 ни в одной группе с комбинацией опухоли среднего размера 1000 мм3 не достигали. Дозирование начинали повторно для обеспечения получения образцов дозы в сыворотке и опухолей после завершения для фармакокинетических анализов. Начиная с суток 42, группы 2-5 получали дабрафениб раз в сутки в течение четырех суток и BVD-523 дважды в сутки в течение трех суток с последующей одной дозой BVD-523 утром на сутки 45. Конечные схемы дозирования приведены ниже в таблице 16.
Итоговые результаты в исследовании A375 in vivo
TGD
Низ-ший пре-дел
раз в сутки × 4
дважды в сутки × 3, затем раз в сутки × 1
раз в сутки × 4
дважды в сутки × 3, затем раз в сутки × 1
раз в сутки × 4
дважды в сутки × 3, затем раз в сутки × 1
раз в сутки × 4
дважды в сутки × 3, затем раз в сутки × 1
Конечная точка и анализ задержки роста опухоли (TGD)
[0226] Опухоли измеряли с использованием штангенциркуля дважды в неделю и каждое животное подвергали эвтаназии, когда его опухоль достигала предопределенной конечной точки с объемом опухоли 2000 мм3 или в последние сутки, в зависимости от того, что достигалось раньше. Животных, которых убирали из исследования вследствие достижения конечной точки по объему опухоли регистрировали как подвергнутых эвтаназии вследствие прогрессирования опухоли (TP) с датой эвтаназии. Время до конечной точки (TTE) для анализа рассчитывали для каждой мыши по следующему уравнению:
TTE=log0 (конечный объем) - b
m
где TTE выражена в сутках, конечный объем выражен в мм3, b представляет собой пересечение, и m представляет собой угол наклона прямой, получаемой посредством линейной регрессии лог-трансформированного набора данных о росте опухоли. Набор данных состоит из первого наблюдения, которое превосходило конечный объем, используемый в анализе, и трех последовательных наблюдений, которые непосредственно предшествовали достижению этого конечного объема. Расчетное TTE, как правило, являлось меньше, чем дата TP: сутки, на которые животного подвергали эвтаназии вследствие размера опухоли. Животным с опухолями, которые не достигали конечного объема, присваивали значение TTE, равное последним суткам исследования. Любых животных, классифицируемых как погибших вследствие NTR (не связанных с обработкой) причин вследствие случайности (NTRa) или вследствие неизвестных причин (NTRu), исключали из расчетов TTE (и всех последующих анализов). Животным, классифицируемым как погибшим по причине TR (связанной с обработкой) гибели или NTRm (не связанной с обработкой гибели вследствие метастазирования), присваивали значение TTE, равное суткам гибели.
[0227] Исход обработки оценивали на основании задержки роста опухоли (TGD), определяемой как увеличение медианного времени до конечной точки (TTE) в обрабатываемой группе по сравнению с контрольной группой:
TGD=T - C,
выражаемой в сутках или в виде процента от медианного TTE контрольной группы:
%TGD=T-C×100
C
где:
T=медианное TTE в обрабатываемой группе, и
C=медианное TTE в назначенной контрольной группе.
Критерии для ответов в виде регрессии
[0228] Эффективность обработки можно определять на основе частоты и размеров ответов в виде регрессии, наблюдаемых в течение исследования. Обработка может вызывать частичную регрессию (PR) или полную регрессию (CR) опухоли у животного. При ответе в виде PR объем опухоли составлял 50% или менее от ее объема на сутки 1 в течение трех последовательных измерений в течение исследования, и составлял 135 мм3 или более при одном или нескольких из этих трех измерений. При ответе в виде CR объем опухоли составлял менее 135 мм3 при трех последовательных измерениях в течение исследования. Животных с ответом в виде CR в конце исследования дополнительно классифицировали как выживших без опухоли (TFS). У животных контролировали ответы в виде регрессии.
Токсичность
[0229] Животных ежедневно взвешивали на сутки 1-5, затем дважды в неделю до завершения исследования. Мышей часто наблюдали на открытые признаки любых вредных связанных с обработкой (TR) побочных эффектов и при наличии клинические признаки регистрировали. Индивидуальную потерю массы тела контролировали в соответствии с протоколом, и любое животное, превзошедшее пределы приемлемой потери массы тела, подвергали эвтаназии. В соответствии с протоколом также контролировали потерю средней групповой массы тела. Дозирование прекращали, если любая группа превосходила приемлемые потери средней массы тела. Если средняя масса тела восстанавливалась, дозирование в этой группе возобновляли, но с меньшей дозой или со схемой дозирования с меньшей частотой.
[0230] Приемлемую токсичность для максимально переносимой дозы (MTD) определяли как потерю в течение исследования средней групповой массы тела менее 20% и не более 10% связанной с обработкой (TR) гибели. Гибель классифицировали как TR, если можно было отнести к связанным с обработкой побочным эффектам, о чем свидетельствовали клинические признаки и/или некроскопия, или также классифицировали как TR, если она происходила вследствие неизвестных причин в течение периода дозирования или в пределах 14 суток после последней дозы. Гибель классифицировали как не связанную с обработкой (NTR), если не было свидетельств того, что гибель связана с побочными эффектами после обработки. NTR гибель дополнительно характеризовали на основе причины гибели. Гибель классифицировали как NTRa, если она являлась результатом несчастного случая или ошибки человека. Гибель классифицировали как NTRm, если некроскопия свидетельствовала, что она могла быть результатом диссеминации опухоли посредством инвазии и/или метастазирования. Гибель классифицировали как NTRu, если причина гибели являлась неизвестной и не было доступно свидетельств гибели, связанной с побочными эффектами после обработки, метастазирования, несчастного случая или ошибки человека, хотя гибель вследствие побочных эффектов после обработки исключать было нельзя.
Получение образцов
[0231] При доступности пять мышей на группу подвергали эвтаназии посредством конечной сердечной пункции с анестезией диоксидом углерода через 3, 6 и 12 часов после конечной дозы, и собирали весь объем крови каждого животного. Отделяли сыворотку и хранили в замороженном состоянии при -80°C до транспортировки. Кроме того, опухоли этих мышей собирали и разделяли на две части. Одну часть быстро замораживали и хранили при -80°C. Другую часть фиксировали в течение 16-24 часов в 10% нейтральном буферизованном формалине, а затем переносили в 70% этанол. Для групп с мышами, у которых не детектировали опухоли, у трех мышей на группу собирали участок имплантата, включая всю толщину кожи и мышц.
Статистический и графический анализы
[0232] Для графических представлений и статистических анализов использовали Prism (GraphPad) для Windows 3.03.
[0233] Для анализа значимости различий значений TTE в двух группах использовали логранговый критерий, который оценивает общее выживание. Логранговый анализ включает данные всех животных в группе за исключением тех, у кого определили NTR гибель. Проводили двусторонние статистические анализы на уровне значимости p=0,05. Статистические тесты не корректировали на множественные сравнения. Prism представляет результаты тестирования как незначимые (н.з.) при p>0,05, значимые (помечаемые "*") при 0,01<p<0,05, очень значимые ("**") при 0,001<p<0,01 и экстремально значимые ("***") при p<0,001. Так как тесты на статистическую значимость не предоставляют оценки величины различий между группами, все уровни значимости в тексте данного описания описывали или как значимые, или как незначимые.
[0234] Для демонстрации значений TTE для отдельных мышей по группам строили диаграмму рассеяния. Средние групповые объемы опухолей наносили на диаграмму в виде функции от времени. Когда животных удаляли из исследования вследствие размера опухоли, вместе с данными, используемыми для расчета среднего объема в последующие моменты времени, включали конечный объем опухоли, зарегистрированный у животного. Величины ошибок (когда присутствуют) означают стандартную ошибку среднего (SEM). Диаграммы Каплана-Мейера демонстрируют процент животных в каждой группе, оставшихся в исследовании в зависимости от времени. В диаграммах Каплана-Мейера и логранговом критерии использовали одни и те же наборы данных TTE. Для каждой группы для каждых суток измерения массы тела рассчитывали процент изменений средней массы тела, начиная с суток 1, и наносили на график в виде функции от времени. Графики рост опухоли и массы тела исключали данные для NTR гибели, и их обрезали после удаления из исследования 50% доступных животных в группах.
Результаты
[0235] Группы в исследовании A375 in vivo обрабатывали в соответствии с модифицированным протоколом, как описано в таблице 15. Эксперимент заканчивали на сутки 45. В таблице 16 представлены результаты ответов на обработки для каждой группы. Фиг. 26 представляет собой диаграмму рассеяния, демонстрирующую индивидуальные TTE для каждой группы. Фиг. 27 представляет собой графики среднего роста опухоли (фиг. 27A) и выживания Каплана-Мейера (фиг. 27B) для каждой группы в исследовании. Фиг. 28A-D представляют собой графики среднего роста опухоли для четырех комбинации по сравнению с соответствующей им монотерапией. Фиг. 29 представляют собой графики процента изменений средней массы тела, начиная с суток 1, для каждой группы.
Эффективность - Рост клеток меланомы человека A375 у контрольных мышей (группа 1)
[0236] В группе 1 одна контрольная мышь погибла без некропсии на сутки 4, и гибель оценили как NTRu. Другие четырнадцать контрольных опухолей быстро и равномерно прогрессировали до конечной точки 2000 мм3 с медианным TTE 9,2 суток, составляя максимально возможную TGD 35,8 суток (389%) для 45-суточного исследования (таблица 15). На диаграмме рассеяния можно наблюдать кластер контрольных TTE (фиг. 26). График среднего роста опухоли для группы 1 иллюстрировал быстрый рост контрольной опухоли (фиг. 27A и фиг. 28A-D).
Эффективность - Ответ на дабрафениб в качестве монотерапии (группы 6 и 7)
[0237] Группы 6 и 7 получали дабрафениб в качестве монотерапии в концентрациях 50 и 100 мг/кг, соответственно, п/о, раз в сутки до конца. Медианные TTE для групп 6 и 7 составляли 16,1 и 28,5 суток, соответственно, что соответствует зависимым от дозы TGD 6,9 суток (75%) и 19,3 суток (210%) со значимым различием в выживаемости для каждой по сравнению с контролем (группа 1 по сравнению с 6 или 7, p<0,001). В группе со 100 мг/кг дабрафениба зарегистрирован один PR (таблица 16). Все опухоли в группе 6 достигали конечного объема опухоли 2000 мм3, тогда как в группе 7 конечной точки достигали 13/15 опухолей, и две на сутки 45 оставались с MTV 282 мм3 (таблица 16). Графики среднего роста опухоли для групп 6 и 7 иллюстрировали зависимые от дозы задержки, хотя опухоли в обеих группах в течение обработки прогрессировали (фиг. 27A).
Эффективность - Ответ на BVD-523 в качестве монотерапии (группы 8 и 9)
[0238] Группы 8 и 9 получали BVD-523 в качестве монотерапии в концентрации 50 и 100 мг/кг, соответственно, п/о дважды в сутки до конца. Медианные TTE для групп 8 и 9 составляли 8,6 и 18,5 суток, соответственно, что соответствовало отсутствию TGD для группы 50 мг/кг BVD-523 и TGD 9,3 суток (101%) для группы 100 мг/кг BVD-523 (таблица 16). Логранговые анализы детектировали значимое отличие в выживаемости по сравнению с контролями только для 100 мг/кг BVD-523 (группа 1 по сравнению с 8, p>0,05; группа 1 по сравнению с 9, p<0,001). В группе 8 наблюдали один CR, который, оставался TFS на сутки 45, тогда как в группе 9 наблюдали два CR/TFS, и все другие опухоли в этих двух группах достигали конечного объема опухоли 2000 мм3 (таблица 16). График среднего роста опухоли для группы 50 мг/кг BVD-523 был сравним с графиком среднего роста опухоли для контролей, тогда как группа 100 мг/кг BVD-523 продемонстрировала несущественную задержку у опухолей, которые прогрессировали в течение обработки (фиг. 27A).
Эффективность - Ответ на обработку комбинациями дабрафениба и BVD-523 (группы 2-5)
[0239] Группы 2 и 3 получали 50 мг/кг дабрафениба с 50 или 100 мг/кг BVD-523, соответственно, тогда как группы 4 и 5 получали 100 мг/кг дабрафениба с 50 или 100 мг/кг BVD-523, соответственно. Как указано в таблице 16, схемы обработки комбинациями модифицировали так, что дозирование заканчивалось после суток 20, а затем повторно начиналось на сутки 42 (таблица 16).
[0240] Каждая из медианных TTE для групп 2-5 составляла 45,0 суток, соответствуя максимально возможной TGD для исследования (35,8 суток, 389%) и значимому общему положительному действию на выживаемость по сравнению с контролями (группа 1 по сравнению с 2-5, p<0,001).
[0241] Пять опухолей в группе 2 достигали конечного объема 2000 мм3, тогда как в группах 3-5 опухолей, которые достигали конечного объема, не было. В группе 2 наблюдали три PR и восемь CR с семью мышами, которые оставались TFS на сутки 45 (таблица 16). В группе 3 выявлена одна гибель NTRu на сутки 31, а у остальных четырнадцати мышей наблюдали CR и они оставались TFS в конце исследования. В группе 4 выявлен один PR и четырнадцать CR, которые оставались TFS, тогда как в группе 5 наблюдали 100% TFS.
[0242] Средние массы опухолей в группах 2-5 на сутки 20, когда дозирование останавливали, не детектировали (фиг. 27A). Средний рост опухоли возобновлялся только в группе с наименьшей дозировкой комбинации (группа 2) и оставался недетектируемым до конца исследования в других трех группах с комбинациями (фиг. 27Al). График роста опухоли для каждой группы с комбинацией демонстрировал заметную активность по сравнению с соответствующей им монотерапией (фиг. 28A-D).
Эффективность - Ответ на обработку темозоломидом (группа 10)
[0243] Обработка эталонным темозоломидом приводила к медианному TTE 10,5 суток, что соответствует незначительному TGD (1,3 суток, 14%) с отсутствием регрессии (таблица 16). Логранговые анализы не детектировали значимого различия в выживаемости для группы с темозоломидом по сравнению с контролями (группа 1 по сравнению с 10, p=0,052). График среднего роста опухоли для этой группы демонстрировал незначительную задержку по сравнению с графиком для контрольной группы 1 (фиг. 27A).
Побочные эффекты
[0244] В таблице 16 предоставлена итоговая информация о максимальных потерях средней BW, TR и NTR гибели. Фиг. 29 представляет собой диаграммы процента изменений средней BW, начиная с суток 1, для каждой группы.
[0245] В исследовании не регистрировали TR гибели, но два случая гибели оценивали как NTRu (таблица 16). Одну гибель NTRu зарегистрировали в группе 1 на сутки 4, а вторую гибель NTRu зарегистрировали в группе 3 на сутки 31. Животное в группа 1 найдено мертвым без некропсии без предварительного клинического обследования, тогда как мышь в группе 3 непосредственно перед гибелью была истощенной, сутулой и сонной, и некропсия выявила массу белых узелков на печени, что означает, что возможной причиной гибели было метастатическое заболевание. В группах в исследовании потери средней BW были незначительными или их не наблюдали (таблица 16 и фиг. 29), и в группах с моно- и комбинированной обработкой BVD-523 и дабрафенибом не наблюдали заметных признаков связанных с обработкой побочных эффектов.
Общие результаты
[0246] В исследовании in vivo оценивали комбинации BVD-523 с дабрафенибом на эффективность в модели с ксенотрансплантатом меланомы человека A375 на голых мышах. BVD-523 вводили перорально в концентрациях 50 или 100 мг/кг со схемой дозирования дважды в сутки, а дабрафениб вводили перорально в концентрациях 50 или 100 мг/кг со схемой раз в сутки, отдельно и в комбинации. Вследствие выраженного ответа на комбинированное лечение дозирование в группах с комбинациями останавливали на сутки 20 для наблюдения за повторным ростом опухоли и повторно начинали на сутки 42 для сбора образцов в конце исследования на сутки 45.
[0247] Контрольные опухоли A375 быстро и равномерно прогрессировали до конечного объема опухоли. Медианные TTE для контролей составляли 9,2 суток, составляя максимально возможную TGD 35,8 суток (389%) для 45-суточного исследования. Узкий диапазон контрольных TTE, который отражал равномерный рост контрольных опухолей, обеспечивал возможность детекции логранговым критерием небольших различий между контрольными и обработанными мышами. Обработка эталонным темозоломидом приводила к незначительной TGD (1,3 суток, 14%) и отсутствию регрессий в соответствии с предыдущими результаты для темозоломида в этой модели опухоли.
[0248] Монотерапия 50 и 100 мг/кг дабрафениба приводила к зависимой от дозы эффективности с TGD 6,9 суток (75%) и 19,3 суток (210%), соответственно, и одним PR в группе со 100 мг/кг дабрафениба. Монотерапия 50 мг/кг BVD-523 была неактивна, не приводя к TGD и к значимому отличию в выживаемости от контролей (p>0,05). Единственное TFS в этой группе могло являться результатом обработки или спонтанного регресса. Монотерапия 100 мг/кг BVD-523 была незначительно активной, приводя к TGD 9,3 суток (101%), значимому отличию в выживаемости по сравнению с контролем (p<0,001) и двум TFS, которые могли являться результатом обработки или спонтанного регресса.
[0249] Каждая из четырех тестируемых в этом исследовании комбинаций дабрафениба с BVD-523 была высокоактивна, обеспечивая максимальную возможную TGD, заметные ответы в виде регрессии, и статистически значимо превосходили общую выживаемость по сравнению с соответствующей им монотерапией (p<0,001). Группа с комбинацией в наименьших дозах (группа 2) приводила к получению заметных 7/15 TFS. При трех комбинациях с наибольшими дозами (группы 3-5) достигли 43/44 выживших без опухоли в конце исследования, включая 15/15 TFS в группе с комбинацией в наибольших дозах (группа 5). Заслуживает внимание, что учитывая среднее время удвоения контрольных опухолей менее 3 суток, у 43/44 мышей в группах 3-5 в течение перерыва в дозировании в течение суток 21-42, что являлось периодом времени, соответствующим приблизительно 7 удвоениям опухоли, повторного роста опухоли не наблюдали. Эти результаты соответствуют лечебной или близкой к лечебной активности.
[0250] В итоге, каждый из дабрафениба и BVD-523 обеспечивал незначительную зависимую от дозы эффективность в виде монотерапии, но заметную активность в комбинации. Комбинации дабрафениба с BVD-523, тестируемые в этом исследовании, обеспечивали заметную выживаемость без опухоли, и превосходную эффективность по сравнению с любым из этих средств, вводимых отдельно.
[0251] Авторы демонстрируют, что ингибирование киназы ERK, проиллюстрированное на примере с использованием BVD-523, эффективно в комбинации с ингибитором RAF дабрафенибом в модели обусловленной мутантным BRAF меланомы. В клетках, комбинированная обработка BVD-523 и дабрафенибом индуцирует окна синергического ингибирования клеточной пролиферации. При совместном дозировании в модели с ксенотрансплантатом, комбинированное лечение вызывает заметный и длительный регресс опухоли по сравнению с терапией единственным средством.
[0252] Кроме того, когда клетки A375 индуцированы к проявлению приобретенной устойчивости к лекарственным средствам после длительного воздействия ингибиторов каскада MAPK, ингибирование ERK с использованием BVD-523 демонстрирует привлекательные свойства. В течение недели после обработки дабрафенибом или траметинибом, можно выделять клетки A375, которые быстро растут в концентрациях, более чем в 10 раз превосходящих соответствующие ингибирующие рост концентрации IC50 соединений. Через 2 месяца клетки, подвергаемые действию только BVD-523, росли плохо и могли переносить обработку только менее чем 10-кратным увеличением воздействия лекарственного средства более IC50. Подобным образом, клетки, обрабатываемые комбинацией BVD-523 и дабрафенибом, демонстрируют плохой рост, и их можно культивировать только при незначительно увеличенных уровнях дабрафениба в комбинации.
[0253] В заключение BVD-523 тестировали в модели меланомы с ксенотрансплантатам, происходящими из биопсий, получаемых у пациентов с выявленным прогрессированием заболевания после исходного ответа на вемурафениб. Представляет интерес, что в этой модели in vivo выявили приобретенную перекрестную устойчивость, продемонстрировав нечувствительность к дабрафенибу и траметинибу. Однако BVD-523 являлся эффективным в этой модели и индуцировал эффективный противоопухолевый ответ отдельно или в комбинации с дабрафенибом.
[0254] В целом эти результаты свидетельствуют, что комбинированная обработка ингибиторами ERK и RAF является эффективной в условиях обусловленной мутантным BRAF меланомы. BVD-523 обладает новым способом лекарственного действия и, возможно, демонстрирует увеличенную продолжительность действия в моделях, которые демонстрируют существенную чувствительность или приобретенную устойчивость к ингибиторам BRAF или MEK. Комбинация ингибиторов RAF и ERK для мутантных по BRAF злокачественных опухолей ингибирует онкогенный сигнальный путь в двух контрольных точках, что в свою очередь, по-видимому, создает труднопреодолимый барьер против разрушения и приобретенной устойчивости к лекарственным средствам.
[0255] Эти результаты указывают на то, что терапия комбинацией ингибиторами ERK и RAF может быть эффективна при ряде злокачественных опухолей, в частности опухолей, несущих онкогенные изменения в BRAF, включая меланому, рак щитовидной железы, легких и толстого кишечника.
Пример 8
Дополнительные исследования комбинаций
Анализ пролиферации при единственном средстве
[0256] Клетки высевали в 96-луночные планшеты с плотностями и условиями сред, указанными в таблице 17 и позволяли прикрепляться в течение ночи с последующим добавлением соединений или контрольных носителей. Соединения получали из исходных разведений в DMSO с получением желаемых конечных концентраций. Конечная концентрация DMSO являлась постоянной на уровне 0,1%. Тестируемые соединения инкубировали с клетки в течение 72 часов при 37°C, 5% CO2 в увлажненной атмосфере. Добавляли реагент CellTiter-Glo® (Promega, Madison, WI) по инструкциям производителя и люминесценцию детектировали с использованием планшетного спектрофотометра FLUOstar BMG (BMG Labtech, Ortenberg, Germany). Вычитали средние фоновые значения для сред, не содержащих тестируемых соединений, и данные анализировали с использованием 4-параметрического логистического уравнения в GraphPad Prism (GraphPad Software, La Jolla, CA).
Анализ пролиферации при комбинациях
[0257] Клетки высевали в трех повторениях в 96-луночные планшеты с плотностями и условиями сред, указанными в таблице 17 и позволяли прикрепляться в течение ночи с последующим добавлением соединений или контрольных носителей. Соединения получали из исходных разведений DMSO с получением желаемых конечных концентраций. Конечная концентрация DMSO являлась постоянной на уровне 0,2%. Комбинации тестировали с использованием матрицы доз 10×8. Тестируемые соединения инкубировали с клетками в течение 72 часов при 37°C, 5% CO2 в увлажненной атмосфере. Добавляли реагент CellTiter-Glo® (Promega, Madison, WI) по инструкциям производителя и люминесценцию детектировали с использованием планшетного спектрофотометра FLUOstar BMG (BMG Labtech, Ortenberg, Germany). Вычитали средние фоновые значения для сред, не содержащих тестируемых соединений, и данные анализировали
[0258] Для анализов комбинаций в формате 10×8 в матрице доз определяли комбинационные взаимодействия по моделям аддитивности Леве и независимости Блисса с использованием программного анализа комбинаций Chalice™ (Horizon Discovery Group, Cambridge, MA), как описано в руководстве пользователя (доступном по адресу chalice.horizondiscovery.com/chalice-portal/documentation/analyzer/home.jsp). Синергию определяют, комбинируя экспериментально наблюдаемый уровень ингибирования для каждой точки с комбинацией со значением, ожидаемым для аддитивности, которое получают на основе ответов на единственные средство по граням матрицы. Потенциальные синергические взаимодействия идентифицируют, посредством отображения рассчитанного избыточного ингибирования по сравнению с теоретически рассчитанным в качестве аддтитивного в матрице доз в виде тепловой карты, и выводя количественный "источник синергии" на основе модели Леве. Данные по единственным средствам, получаемые на основе анализа планшетов с комбинациями представляли в виде кривых зависимостей "доза-эффект", получаемых в GraphPad Prism (GraphPad Software, La Jolla, CA) (наносимых на график с использованием процента жизнеспособности относительно контролей, обработанных только DMSO).
Плотность посевов линий клеток и среды для выращивания
Результаты
[0259] Целью этого исследования являлась оценка действия комбинирования ингибиторов ERK с ингибиторами RAF типа 1. Один новый ингибитор ERK BVD-523 с двумя ингибиторами RAF типа I, дабрафенибом (GSK2118436) и вемурафенибом (PLX4032), и ингибитором типа II TAK-632, в двух линиях клеток меланомы с мутацией V600E BRAF, A375 и G-361. Также в комбинациях с дабрафенибом (GSK2118436) и вемурафенибом (PLX4032) тестировали второй ингибитор ERK (SCH772984) с отличающимся механизмом действия.
[0260] Сначала проводили анализы пролиферации с единственным средством для выбора подходящего диапазона концентраций для исследования комбинаций. Хотя обе линии клеток обладают сходным уровнем чувствительности к паклитакселу, клетки G-361 по-видимому в 4-6 раз мене чувствительны к ингибированию ERK и RAF по сравнению с клетками A375 (фиг. 42). Результаты для IC50 обобщены в таблице 18.
Значения IC50 единственных средств для тестируемых соединений
[0261] Комбинационные взаимодействия между двумя соединениями оценивали в матрице концентраций 8×10 с использованием моделей аддитивности Леве и независимости Блисса с использованием биоинформатического программного обеспечения Chalice™ (Horizon Discovery Group, Cambridge, MA). Chalice™ обеспечивает идентификацию потенциальных синергических взаимодействий отображая рассчитанное избыточное ингибирование по сравнению с теоретически рассчитанным в качестве аддитивного в матрице доз в виде тепловой карты, и выводя количественный "источник синергии" на основе модели Леве.
[0262] В клетках A375 (фиг. 43 - фиг. 48) анализ с использованием модели Леви показал, что комбинации с BVD-523 в основном являлись аддитивными. Результаты с использованием способа Блисса были сходными, хотя этот способ позволил предположить наличие области слабого антагонизма при высоких концентрациях для каждой из комбинаций. В отличие от этого, в клетках G-361 (фиг. 49 - фиг. 54), при том, что большинство взаимодействий в матрице доз также были аддитивными, обе модели в анализе также выявили небольшие области умеренной синергии при средних концентрациях. Подобные результаты получали со вторым ингибитором ERK (SCH772984) с отличающимся механизмом действия. Это поддерживает точку зрения, что синергия, наблюдаемая для G-361, вероятно специфически связана с ингибированием ERK, а не с побочными эффектами.
[0263] В итоге, эти результаты позволяют предположить, что взаимодействия между BVD-523 и ингибиторами RAF типа I и типа II в линиях клеток меланомы, несущих мутацию BRAF V600E, являются по меньшей мере аддитивными и, в некоторых случаях, синергическими.
[0264] Синергические взаимодействия оценивали двумя способами (фиг. 55 - фиг. 57). Избыточную активность по сравнению с теоретически рассчитанной, в случае если бы комбинация была аддитивной, можно рассчитывать с использованием простой объемной оценкой, которая рассчитывает объем между измеряемой и теоретически рассчитанной поверхностью ответа. Эта объемная оценка демонстрирует, является ли общий ответ на комбинацию синергическим (положительные значения), антагонистическим (отрицательные значения) или аддитивным (значения ~ 0). Кроме того, "источник синергии" представляет собой положительный благоприятствующий ингибированию объем, больший аддитивности по Леве. Это обеспечивает дополнительное упорядочивание, благоприятствующее комбинациям, синергия у которых происходит на высоких уровнях действия, игнорируя антагонистические части поверхности ответа.
Пример 9
Комбинационные взаимодействия между ингибиторами ERK
[0265] Мутантную по RAF линия клеток меланомы A375 культивировали в DMEM с 10% FBS и в трех повторениях высевали в 96-луночные планшеты с исходной плотностью 2000 клеток на лунку. Комбинационные взаимодействия между ингибиторами ERK BVD-523 и SCH772984 анализировали через 72 часа, как описано выше в примере 8. Жизнеспособность определяли с использованием реагента CellTiter-Glo® (Promega, Madison, WI) по инструкциям производителя, а люминесценцию детектировали с использованием планшетного спектрофотометра FLUOstar BMG (BMG Labtech, Ortenberg, Germany).
[0266] Визуализация тепловых карт с "избытком ингибирования" Леве и Блисса позволяли предполагать, что комбинация BVD-523 и SCH772984 была в основном аддитивной с окнами потенциальной синергии в диапазоне средних доз (фиг. 58).
[0267] В итоге, эти результаты позволяют предполагать, что взаимодействия между BVD-523 и SCH772984 являются по меньшей мере аддитивными, а в некоторых случаях синергическими.
Документы
AVRUCH, J.; et al. Ras activation of the Raf kinase: tyrosine kinase recruitment of the MAP kinase cascade. Recent Prog. Horm. Res., 2001, 127-155.
BROSE, et al. BRAF and RAS mutations in human lung cancer and melanoma. Cancer Res., 2002, 62, 6997-7000.
DAVIES et al., Mutations of the BRAF gene in human cancer. Nature, 2002, 417, 949-954.
FRANSEN et al., Mutation analysis of the BRAF, ARAF and RAF-1 genes in human colorectal adenocarcinomas. Carcinogenesis, 2004, 25, 527-533.
GARNETT, M.J.; et al. Wildtype and mutant B-RAF activate C-RAF through distinct mechanisms involving heterodimerization. Mol. Cell, 2005, 20, 963-969.
GREGER, James G., et al. "Combinations of BRAF, MEK, and PI3K/mTOR inhibitors overcome acquired resistance to the BRAF inhibitor GSK2118436 dabrafenib, mediated by NRAS or MEK mutations". Molecular cancer therapeutics 11.4 (2012): 909-920.
HOCKER et al., Ultraviolet radiation and melanoma: A systematic review and analysis of reported sequence variants. Hum. Mutat., 2007, 28, 578-588.
KING, Alastair J., et al. "Dabrafenib; preclinical characterization, increased efficacy when combined with trametinib, while BRAF/MEK tool combination reduced skin lesions". PloS one 8.7 (2013): e67583.
LI et al., Recent advances in the research and development of B-Raf Inhibitors. Current Medicinal Chemistry, 2010, 17:1618-1634.
LIU, Dingxie, et al. "BRAF V600E maintains proliferation, transformation, and tumorigenicity of BRAF-mutant papillary thyroid cancer cells". Journal of Clinical Endocrinology & Metabolism 92.6 (2007): 2264-2271.
LITTLE, A.S., et al., Amplification of the Driving Oncogene, KRAS or BRAF, Underpins Acquired Resistance to MEK1/2 Inhibitors in Colorectal Cancer Cells. Sci. Signal. 4, ra17 (2011).
LONG GV, Menzies AM, Nagrial AM, et al. Prognostic and Clinicopathologic Associations of Oncogenic BRAF in Metastatic Melanoma. J Clin Oncol. 2011
MANANDHAR SP, Hildebrandt ER, Schmidt WK. Small-molecule inhibitors of the Rce1p CaaX protease. J Biomol Screen. 2007;12(7):983-993.
MAURER, T, Garrenton, LS, Oh, A, Pitts, K, Anderson, DJ, Skelton, NJ, Fauber, BP, Pan, B, Malek, S, Stokoe, D, Ludlam, MJC, Bowman, KK, Wu, J, Giannetti, AM, Starovasnik, MA, Mellman, I, Jackson, PK, Rudolph, J, Wang, W, Fang, G. Small-molecule ligands bind to a distinct pocket in Ras and inhibit SOS-mediated nucleotide exchange activity. PNAS. 2012;109(14):5299-304.
MITTAL, Rohit et al. "The acetyltransferase activity of the bacterial toxin YopJ of Yersinia is activated by eukaryotic host cell inositol hexakisphosphate". Journal of Biological Chemistry 285.26 (2010): 19927-19934.
PATGIRI, A, Yadav, KK, Arora, PS, Bar-Sagi, D. An orthosteric inhibitor of the Ras-Sos interaction. Nat Chem Biol. 2011;7:585-587.
PORTER SB, Hildebrandt ER, Breevoort SR, Mokry DZ, Dore TM, Schmidt WK. Inhibition of the CaaX proteases Rce1p and Ste24p by peptidyl (acyloxy)methyl ketones. Biochim Biophys Acta.2007;1773(6):853-862.
RUSHWORTH, L.K.; et al. Regulation and role of Raf-1/B-Raf heterodimerization. Mol. Cell Biol., 2006, 26, 2262-2272.
SETH et al., Concomitant mutations and splice variants in KRAS and BRAF demonstrate complex perturbation of the Ras/Raf signalling pathway in advanced colorectal cancer, Gut 2009;58:1234-1241
SHIMA, F, Yoshikawa, Y, Ye, M, Araki, M, Matsumoto, S, Liao, J, Hu, L, Sugimoto, T, Ijiri, Y, Takeda, A, Nishiyama, Y, Sato, C, Muraoka, S, Tamura, A, Osoda, T, Tsuda, K-I, Miyakawa, T, Fukunishi, H, Shimada, J, Kumasaka, Yamamoto, M, Kataoka, T. In silico discovery of small-molecule Ras inhibitors that display antitumor activity by blocking the Ras-effector interaction. PNAS. 2013;110(20):8182-7.
WAN, et al., Mechanism of activation of the RAF-ERK signaling pathway by oncogenic mutations of B-RAF. Cell, 2004, 116, 855- 867.
WEBER, C.K.; et al. Active Ras induces heterodimerization of cRaf and BRaf. Cancer Res., 2001, 61, 3595-3598.
Wellbrock et al. The RAF proteins take centre stage. Nat. Rev. Mol. Cell Biol., 2004, 5, 875-885.
XU et al., High prevalence of BRAF gene mutation in papillary thyroid carcinomas and thyroid tumor cell lines. Cancer Res., 2003, 63, 4561-4567.
[0268] Все документы, цитируемые в этой заявке, таким образом, включены посредством ссылки так, как если бы они были полностью изложены в настоящем документе.
[0269] Хотя в настоящем документе описаны иллюстративные варианты осуществления настоящего изобретения, следует понимать, что изобретение не ограничено описанными вариантами, и что специалист в данной области может осуществлять другие различные изменения или модификации без отклонения от объема или сущности изобретения.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> SAHA, Saurabh
<120> ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ С ПРИМЕНЕНИЕМ КОМБИНАЦИЙ
ИНГИБИТОРОВ ERK И RAF
<130> C065272/0375604
<140> US61/919,347
<141> 2013-12-20
<160> 45
<170> PatentIn version 3.5
<210> 1
<211> 5898
<212> ДНК
<213> Homo sapiens
<400> 1
cgcctccctt ccccctcccc gcccgacagc ggccgctcgg gccccggctc tcggttataa 60
gatggcggcg ctgagcggtg gcggtggtgg cggcgcggag ccgggccagg ctctgttcaa 120
cggggacatg gagcccgagg ccggcgccgg cgccggcgcc gcggcctctt cggctgcgga 180
ccctgccatt ccggaggagg tgtggaatat caaacaaatg attaagttga cacaggaaca 240
tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa tatatctgga 300
ggcctatgaa gaatacacca gcaagctaga tgcactccaa caaagagaac aacagttatt 360
ggaatctctg gggaacggaa ctgatttttc tgtttctagc tctgcatcaa tggataccgt 420
tacatcttct tcctcttcta gcctttcagt gctaccttca tctctttcag tttttcaaaa 480
tcccacagat gtggcacgga gcaaccccaa gtcaccacaa aaacctatcg ttagagtctt 540
cctgcccaac aaacagagga cagtggtacc tgcaaggtgt ggagttacag tccgagacag 600
tctaaagaaa gcactgatga tgagaggtct aatcccagag tgctgtgctg tttacagaat 660
tcaggatgga gagaagaaac caattggttg ggacactgat atttcctggc ttactggaga 720
agaattgcat gtggaagtgt tggagaatgt tccacttaca acacacaact ttgtacgaaa 780
aacgtttttc accttagcat tttgtgactt ttgtcgaaag ctgcttttcc agggtttccg 840
ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaagttc cactgatgtg 900
tgttaattat gaccaacttg atttgctgtt tgtctccaag ttctttgaac accacccaat 960
accacaggaa gaggcgtcct tagcagagac tgccctaaca tctggatcat ccccttccgc 1020
acccgcctcg gactctattg ggccccaaat tctcaccagt ccgtctcctt caaaatccat 1080
tccaattcca cagcccttcc gaccagcaga tgaagatcat cgaaatcaat ttgggcaacg 1140
agaccgatcc tcatcagctc ccaatgtgca tataaacaca atagaacctg tcaatattga 1200
tgacttgatt agagaccaag gatttcgtgg tgatggagga tcaaccacag gtttgtctgc 1260
taccccccct gcctcattac ctggctcact aactaacgtg aaagccttac agaaatctcc 1320
aggacctcag cgagaaagga agtcatcttc atcctcagaa gacaggaatc gaatgaaaac 1380
acttggtaga cgggactcga gtgatgattg ggagattcct gatgggcaga ttacagtggg 1440
acaaagaatt ggatctggat catttggaac agtctacaag ggaaagtggc atggtgatgt 1500
ggcagtgaaa atgttgaatg tgacagcacc tacacctcag cagttacaag ccttcaaaaa 1560
tgaagtagga gtactcagga aaacacgaca tgtgaatatc ctactcttca tgggctattc 1620
cacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagct tgtatcacca 1680
tctccatatc attgagacca aatttgagat gatcaaactt atagatattg cacgacagac 1740
tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc tcaagagtaa 1800
taatatattt cttcatgaag acctcacagt aaaaataggt gattttggtc tagctacagt 1860
gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca ttttgtggat 1920
ggcaccagaa gtcatcagaa tgcaagataa aaatccatac agctttcagt cagatgtata 1980
tgcatttgga attgttctgt atgaattgat gactggacag ttaccttatt caaacatcaa 2040
caacagggac cagataattt ttatggtggg acgaggatac ctgtctccag atctcagtaa 2100
ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc tcaaaaagaa 2160
aagagatgag agaccactct ttccccaaat tctcgcctct attgagctgc tggcccgctc 2220
attgccaaaa attcaccgca gtgcatcaga accctccttg aatcgggctg gtttccaaac 2280
agaggatttt agtctatatg cttgtgcttc tccaaaaaca cccatccagg cagggggata 2340
tggtgcgttt cctgtccact gaaacaaatg agtgagagag ttcaggagag tagcaacaaa 2400
aggaaaataa atgaacatat gtttgcttat atgttaaatt gaataaaata ctctcttttt 2460
ttttaaggtg aaccaaagaa cacttgtgtg gttaaagact agatataatt tttccccaaa 2520
ctaaaattta tacttaacat tggattttta acatccaagg gttaaaatac atagacattg 2580
ctaaaaattg gcagagcctc ttctagaggc tttactttct gttccgggtt tgtatcattc 2640
acttggttat tttaagtagt aaacttcagt ttctcatgca acttttgttg ccagctatca 2700
catgtccact agggactcca gaagaagacc ctacctatgc ctgtgtttgc aggtgagaag 2760
ttggcagtcg gttagcctgg gttagataag gcaaactgaa cagatctaat ttaggaagtc 2820
agtagaattt aataattcta ttattattct taataatttt tctataacta tttcttttta 2880
taacaatttg gaaaatgtgg atgtctttta tttccttgaa gcaataaact aagtttcttt 2940
ttataaaaac gcctcccttc cccctccccg cccgacagcg gccgctcggg ccccggctct 3000
cggttataag atggcggcgc tgagcggtgg cggtggtggc ggcgcggagc cgggccaggc 3060
tctgttcaac ggggacatgg agcccgaggc cggcgccggc gccggcgccg cggcctcttc 3120
ggctgcggac cctgccattc cggaggaggt gtggaatatc aaacaaatga ttaagttgac 3180
acaggaacat atagaggccc tattggacaa atttggtggg gagcataatc caccatcaat 3240
atatctggag gcctatgaag aatacaccag caagctagat gcactccaac aaagagaaca 3300
acagttattg gaatctctgg ggaacggaac tgatttttct gtttctagct ctgcatcaat 3360
ggataccgtt acatcttctt cctcttctag cctttcagtg ctaccttcat ctctttcagt 3420
ttttcaaaat cccacagatg tggcacggag caaccccaag tcaccacaaa aacctatcgt 3480
tagagtcttc ctgcccaaca aacagaggac agtggtacct gcaaggtgtg gagttacagt 3540
ccgagacagt ctaaagaaag cactgatgat gagaggtcta atcccagagt gctgtgctgt 3600
ttacagaatt caggatggag agaagaaacc aattggttgg gacactgata tttcctggct 3660
tactggagaa gaattgcatg tggaagtgtt ggagaatgtt ccacttacaa cacacaactt 3720
tgtacgaaaa acgtttttca ccttagcatt ttgtgacttt tgtcgaaagc tgcttttcca 3780
gggtttccgc tgtcaaacat gtggttataa atttcaccag cgttgtagta cagaagttcc 3840
actgatgtgt gttaattatg accaacttga tttgctgttt gtctccaagt tctttgaaca 3900
ccacccaata ccacaggaag aggcgtcctt agcagagact gccctaacat ctggatcatc 3960
cccttccgca cccgcctcgg actctattgg gccccaaatt ctcaccagtc cgtctccttc 4020
aaaatccatt ccaattccac agcccttccg accagcagat gaagatcatc gaaatcaatt 4080
tgggcaacga gaccgatcct catcagctcc caatgtgcat ataaacacaa tagaacctgt 4140
caatattgat gacttgatta gagaccaagg atttcgtggt gatggaggat caaccacagg 4200
tttgtctgct accccccctg cctcattacc tggctcacta actaacgtga aagccttaca 4260
gaaatctcca ggacctcagc gagaaaggaa gtcatcttca tcctcagaag acaggaatcg 4320
aatgaaaaca cttggtagac gggactcgag tgatgattgg gagattcctg atgggcagat 4380
tacagtggga caaagaattg gatctggatc atttggaaca gtctacaagg gaaagtggca 4440
tggtgatgtg gcagtgaaaa tgttgaatgt gacagcacct acacctcagc agttacaagc 4500
cttcaaaaat gaagtaggag tactcaggaa aacacgacat gtgaatatcc tactcttcat 4560
gggctattcc acaaagccac aactggctat tgttacccag tggtgtgagg gctccagctt 4620
gtatcaccat ctccatatca ttgagaccaa atttgagatg atcaaactta tagatattgc 4680
acgacagact gcacagggca tggattactt acacgccaag tcaatcatcc acagagacct 4740
caagagtaat aatatatttc ttcatgaaga cctcacagta aaaataggtg attttggtct 4800
agctacagtg aaatctcgat ggagtgggtc ccatcagttt gaacagttgt ctggatccat 4860
tttgtggatg gcaccagaag tcatcagaat gcaagataaa aatccataca gctttcagtc 4920
agatgtatat gcatttggaa ttgttctgta tgaattgatg actggacagt taccttattc 4980
aaacatcaac aacagggacc agataatttt tatggtggga cgaggatacc tgtctccaga 5040
tctcagtaag gtacggagta actgtccaaa agccatgaag agattaatgg cagagtgcct 5100
caaaaagaaa agagatgaga gaccactctt tccccaaatt ctcgcctcta ttgagctgct 5160
ggcccgctca ttgccaaaaa ttcaccgcag tgcatcagaa ccctccttga atcgggctgg 5220
tttccaaaca gaggatttta gtctatatgc ttgtgcttct ccaaaaacac ccatccaggc 5280
agggggatat ggtgcgtttc ctgtccactg aaacaaatga gtgagagagt tcaggagagt 5340
agcaacaaaa ggaaaataaa tgaacatatg tttgcttata tgttaaattg aataaaatac 5400
tctctttttt tttaaggtga accaaagaac acttgtgtgg ttaaagacta gatataattt 5460
ttccccaaac taaaatttat acttaacatt ggatttttaa catccaaggg ttaaaataca 5520
tagacattgc taaaaattgg cagagcctct tctagaggct ttactttctg ttccgggttt 5580
gtatcattca cttggttatt ttaagtagta aacttcagtt tctcatgcaa cttttgttgc 5640
cagctatcac atgtccacta gggactccag aagaagaccc tacctatgcc tgtgtttgca 5700
ggtgagaagt tggcagtcgg ttagcctggg ttagataagg caaactgaac agatctaatt 5760
taggaagtca gtagaattta ataattctat tattattctt aataattttt ctataactat 5820
ttctttttat aacaatttgg aaaatgtgga tgtcttttat ttccttgaag caataaacta 5880
agtttctttt tataaaaa 5898
<210> 2
<211> 765
<212> PRT
<213> Homo sapiens
<400> 2
Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Ala Glu Pro Gly Gln Ala
1 5 10 15
Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala Gly Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Met Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ala
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Ala Leu Thr Ser Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Ala Ser Asp Ser Ile Gly Pro Gln Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Gly Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Thr Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr
660 665 670
Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met
675 680 685
Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro
690 695 700
Leu Phe Pro Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser Leu
705 710 715 720
Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala Gly
725 730 735
Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys Thr
740 745 750
Pro Ile Gln Ala Gly Gly Tyr Gly Ala Phe Pro Val His
755 760 765
<210> 3
<211> 3906
<212> ДНК
<213> Rattus norvegicus
<400> 3
atggcggcgc tgagtggcgg cggtggcagc agcagcggtg gcggtggcgg cggcggcggc 60
ggcggtggtg gcggcggcgg cggcggcgcc gaacagggac aggctctgtt caatggcgac 120
atggagccgg aggccggcgc tggcgccgcg gcctcttcgg ccgcggaccc ggccattcct 180
gaagaggtgt ggaatatcaa gcaaatgatt aagttgacac aggaacatat agaggcccta 240
ttggacaagt ttggtgggga gcataaccca ccgtcaatat acctggaggc ctatgaagag 300
tacaccagca agctagatgc ccttcagcag agagagcagc agctgttgga atccctggtt 360
tttcaaactc ccacagatgt atcacggaac aaccccaagt caccacagaa acctatcgtt 420
cgtgtcttcc tgcccaacaa acagaggaca gtggtgcccg caagatgtgg tgtaacggtc 480
cgagacagtc taaagaaagc actaatgatg aggggtctca tcccagagtg ctgtgctgtt 540
tacagaattc aggacggaga gaagaaacca attggctggg acactgacat ttcctggctt 600
actggagagg agctacatgt tgaagtacta gagaatgttc ctctgacaac ccacaacttc 660
gtacggaaaa cttttttcac cttagcattt tgtgactttt gccgaaagct gcttttccag 720
ggtttccgct gtcaaacatg tggttataag tttcaccagc gttgtagtac agaggttcca 780
ctgatgtgtg ttaattatga ccaacttgat ttgctgtttg tctccaagtt ctttgagcat 840
cacccagtac cacaggagga ggccttctca gcagagacta cccttccatc tggatgctct 900
tccgcacccc cctcagactc tattgggccc caaatcctca ccagtccatc tccttcaaaa 960
tccattccaa ttccacagcc cttccggcca gcagatgaag atcatcgcaa tcagtttggg 1020
caacgagacc gctcctcctc cgctcccaat gttcatataa acacaatcga acctgtcaat 1080
attgatgaaa aattcccaga agtggaatta caggatcaaa gggatttgat tagagaccag 1140
gggtttcgtg gggatggagc ccctttgaac cagctgatgc gctgtcttcg gaaataccaa 1200
tcccggactc ccagccccct cctccattct gtccccagtg aaatagtgtt tgattttgag 1260
cctggcccag tgttcagagg gtcaaccaca ggcttgtcgg ccaccccacc tgcctcatta 1320
cctggctcac tcactaacgt gaaagcctta cagaaatctc caggacctca gcgggaaagg 1380
aagtcctcct cctcctcctc ctccacggaa gacagaagtc ggatgaaaac acttggtaga 1440
agagattcaa gtgatgattg ggagattcct gatggacaga ttacagtggg acagagaatt 1500
ggatctgggt cctttggaac tgtctacaag ggaaagtggc atggcgacgt ggcagtgaaa 1560
atgctgaatg tgacagcacc cacacctcag cagttacagg ccttcaaaaa cgaagtcgga 1620
gtactcagga aaactcgaca tgtgaacatc ctccttttca tgggctattc tacaaagcca 1680
cagctggcta ttgttacaca gtggtgtgaa ggctccagct tatatcacca tctccacatc 1740
attgagacca aatttgagat gatcaaactt atagatattg cacggcagac tgcacagggc 1800
atggattact tacacgccaa gtcaatcatc cacagagacc tcaagagtaa taatatattt 1860
cttcatgaag acctcacggt aaaaataggt gactttggtt tagccacagt gaagtcccga 1920
tggagtgggt cccatcagtt tgaacagttg tctggatcta ttttgtggat ggcacccgaa 1980
gtaatcagaa tgcaagataa aaacccatat agctttcagt cagacgtgta tgcatttggg 2040
attgttctgt atgaactgat gactggtcag ctaccttatt caaacatcaa caacagggat 2100
cagataattt ttatggtggg acgaggatac ctatctccag atctcagtaa ggtacggagt 2160
aactgtccaa aagccatgaa gagattaatg gcagagtgcc tcaaaaagaa aagagacgag 2220
agaccactct ttccccaaat tctcgcctct attgagctgc tggcccgctc attgccaaaa 2280
attcaccgca gtgcatcaga accctccttg aatcgggctg gtttccaaac agaagatttt 2340
agtctgtatg cttgtgcttc tccaaaaaca cccatccaag cagggggata tggagaattt 2400
gcagccttca agtagccact ccatcatggc agcatctact ctttatttct taagtcttgt 2460
gttcatacaa tttgttaaca tcaaaacaca gttctgttcc tcaaattttt tttaaagata 2520
caaaattttc aatgcataag ctcgtgtgga acagaatgga atttcctatt caacaaaaga 2580
gggaagaatg ttttaggaac cagaattctc tgctgcccgt gtttcttctt caacacaaat 2640
atcatgtgca tacaactctg cccattccca agaagaaaga ggagagaccc cgaattctgc 2700
ccttttggtg gtcaggcatg atggaaagaa tttgctgctg cagcttggga aaaattgcta 2760
tggaaagtct gccagtcaac tttgcccttc taaccaccag atccatttgt ggctggtcat 2820
ctgatggggc gatttcaatc accaagcatc gttcttgcct gttgtgggat tatgtcgtgg 2880
agcactttcc ctatccacca ccgttaattt ccgagggatg gagtaaatgc agcataccct 2940
ttgtgtagca cctgtccagt cctcaaccaa tgctatcaca gtgaagctct ttaaatttaa 3000
gtggtgggtg agtgttgagg agagactgcc ttgggggcag agaaaagggg atgctgcatc 3060
ttcttcctca cctccagctc tctcacctcg ggttgccttg cacactgggc tccgcctaac 3120
cactcgggct gggcagtgct ggcacacatt gccgcctttt ctcattgggt ccagcaattg 3180
agcagagggt tgggggattg tttcctccac aatgtagcaa attctcagga aaatacagtc 3240
catatcttcc tctcagctct tccagtcacc aaatacttac gtggctcctt tgtccaggac 3300
ataaaacacc gtggacaaca cctaattaaa agcctacaaa actgcttact gacagttttg 3360
aatgtgagac atttgtgtaa tttaaatgta aggtacaggt cttaatttct tctattaagt 3420
ttcttctatt tttatttaaa cgaagaaaat aattttcagg tttaattgga ataaacgaat 3480
acttcccaaa agactatata ccctgaaaat tatatttttg ttaattgtaa acaactttta 3540
aaaaatggtt attatccttt tctctaccta aaattatggg aaatcttagc ataatgacaa 3600
ttatttatac tttttaaata aatggtactt gctggatcca cactaacatc tttgctaaca 3660
ttcccattgt ttcttccaac ttcactccta cactacatcc tccatcctct ttctagtctt 3720
ttatctataa tatgcaacct aaaataaaag tggtggtgtc tccattcatt cttcttcttc 3780
cttttttccc caagcctggt cttcaaaagg ttgggtaatt tagtagctga gttccctagg 3840
tagaaataga actattaggg acattggggt tgtaggaaag cgtgaggcct gtcaccagtt 3900
gttctt 3906
<210> 4
<211> 804
<212> PRT
<213> Rattus norvegicus
<400> 4
Met Ala Ala Leu Ser Gly Gly Gly Gly Ser Ser Ser Gly Gly Gly Gly
1 5 10 15
Gly Gly Gly Gly Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu Gln
20 25 30
Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala Gly
35 40 45
Ala Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp
50 55 60
Asn Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu
65 70 75 80
Leu Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu
85 90 95
Ala Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu
100 105 110
Gln Gln Leu Leu Glu Ser Leu Val Phe Gln Thr Pro Thr Asp Val Ser
115 120 125
Arg Asn Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
130 135 140
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
145 150 155 160
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
165 170 175
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
180 185 190
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
195 200 205
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
210 215 220
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
225 230 235 240
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
245 250 255
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
260 265 270
Phe Val Ser Lys Phe Phe Glu His His Pro Val Pro Gln Glu Glu Ala
275 280 285
Phe Ser Ala Glu Thr Thr Leu Pro Ser Gly Cys Ser Ser Ala Pro Pro
290 295 300
Ser Asp Ser Ile Gly Pro Gln Ile Leu Thr Ser Pro Ser Pro Ser Lys
305 310 315 320
Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His Arg
325 330 335
Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val His
340 345 350
Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Glu Lys Phe Pro Glu Val
355 360 365
Glu Leu Gln Asp Gln Arg Asp Leu Ile Arg Asp Gln Gly Phe Arg Gly
370 375 380
Asp Gly Ala Pro Leu Asn Gln Leu Met Arg Cys Leu Arg Lys Tyr Gln
385 390 395 400
Ser Arg Thr Pro Ser Pro Leu Leu His Ser Val Pro Ser Glu Ile Val
405 410 415
Phe Asp Phe Glu Pro Gly Pro Val Phe Arg Gly Ser Thr Thr Gly Leu
420 425 430
Ser Ala Thr Pro Pro Ala Ser Leu Pro Gly Ser Leu Thr Asn Val Lys
435 440 445
Ala Leu Gln Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser
450 455 460
Ser Ser Ser Ser Thr Glu Asp Arg Ser Arg Met Lys Thr Leu Gly Arg
465 470 475 480
Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp Gly Gln Ile Thr Val
485 490 495
Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys
500 505 510
Trp His Gly Asp Val Ala Val Lys Met Leu Asn Val Thr Ala Pro Thr
515 520 525
Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val Gly Val Leu Arg Lys
530 535 540
Thr Arg His Val Asn Ile Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro
545 550 555 560
Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly Ser Ser Leu Tyr His
565 570 575
His Leu His Ile Ile Glu Thr Lys Phe Glu Met Ile Lys Leu Ile Asp
580 585 590
Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr Leu His Ala Lys Ser
595 600 605
Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile Phe Leu His Glu Asp
610 615 620
Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala Thr Val Lys Ser Arg
625 630 635 640
Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp
645 650 655
Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe
660 665 670
Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu Tyr Glu Leu Met Thr
675 680 685
Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe
690 695 700
Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu Ser Lys Val Arg Ser
705 710 715 720
Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala Glu Cys Leu Lys Lys
725 730 735
Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Ile Leu Ala Ser Ile Glu
740 745 750
Leu Leu Ala Arg Ser Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro
755 760 765
Ser Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala
770 775 780
Cys Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly Gly Tyr Gly Glu Phe
785 790 795 800
Ala Ala Phe Lys
<210> 5
<211> 9728
<212> ДНК
<213> Mus musculus
<400> 5
ccctcaggct cggctgcgcc ggggccgccg gcgggttcca gaggtggcct ccgccccggc 60
cgctccgccc acgccccccg cgcctccgcg cccgcctccg cccgccctgc gcctcccttc 120
cccctccccg ccccgcggcg gccgctcggc ccggctcgcg cttcgaagat ggcggcgctg 180
agtggcggcg gtggcagcag cagcggtggc ggcggcggcg gtggcggcgg cggtggcggt 240
ggcgacggcg gcggcggcgc cgagcagggc caggctctgt tcaatggcga catggagccg 300
gaggccggcg ctggcgccgc ggcctcttcg gctgcggacc cggccattcc tgaagaggta 360
tggaatatca agcaaatgat taagttgaca caggaacata tagaggccct attggacaaa 420
tttggtggag agcataaccc accatcaata tacctggagg cctatgaaga gtacaccagc 480
aagctagatg cccttcagca aagagaacag cagcttttgg aatccctggt ttttcaaact 540
cccacagatg catcacggaa caaccccaag tcaccacaga aacctatcgt tagagtcttc 600
ctgcccaaca aacagaggac agtggtaccc gcaagatgtg gtgttacagt tcgagacagt 660
ctaaagaaag cactgatgat gagaggtctc atcccagaat gctgtgctgt ttacagaatt 720
caggatggag agaagaaacc aattggctgg gacacggaca tttcctggct tactggagag 780
gagttacatg ttgaagtact ggagaatgtc ccacttacaa cacacaactt tgtacggaaa 840
acttttttca ccttagcatt ttgtgacttt tgccgaaagc tgcttttcca gggtttccgt 900
tgtcaaacat gtggttataa atttcaccag cgttgtagta cagaggttcc actgatgtgt 960
gtaaattatg accaacttga tttgctgttt gtctccaagt tctttgagca tcacccagta 1020
ccacaggagg aggcctcctt cccagagact gcccttccat ctggatcctc ttccgcaccc 1080
ccctcagact ctactgggcc ccaaatcctc accagtccat ctccttcaaa atccattcca 1140
attccacagc ccttccgacc agcagatgaa gatcatcgca atcagtttgg gcaacgagac 1200
cggtcctcct cagctcccaa tgttcatata aacacaattg agcctgtgaa tatcgatgaa 1260
aaattcccag aagtggaatt acaggatcaa agggatttga ttagagacca ggggtttcgt 1320
ggtgatggag cccccttgaa ccaactgatg cgctgtcttc ggaaatacca atcccggact 1380
cccagccccc tcctccattc tgtccccagt gaaatagtgt ttgattttga gcctggccca 1440
gtgttcagag ggtcaaccac aggcttgtcc gccaccccgc ctgcctcatt acctggctca 1500
ctcactaacg tgaaagcctt acagaaatct ccaggtcctc agcgggaaag gaagtcatct 1560
tcttcctcat cctcggagga cagaagtcgg atgaaaacac ttggtagaag agattcaagt 1620
gatgactggg agattcctga tggacagatt acagtgggac agagaattgg atctgggtca 1680
tttggaactg tctacaaggg aaagtggcat ggtgatgtgg cagtgaaaat gttgaatgtg 1740
acagcaccca cacctcaaca gctacaggcc ttcaaaaatg aagtaggagt gctcaggaaa 1800
actcgacatg tgaatatcct ccttttcatg ggctattcta caaagccaca actggcaatt 1860
gttacacagt ggtgtgaggg ctccagctta tatcaccatc tccacatcat tgagaccaaa 1920
tttgagatga tcaaacttat agatattgct cggcagactg cacagggcat ggattactta 1980
cacgccaagt caatcatcca cagagacctc aagagtaata atatatttct tcatgaagac 2040
ctcacggtaa aaataggtga ctttggtcta gccacagtga aatctcggtg gagtgggtcc 2100
catcagtttg aacagttgtc tggatctatt ttgtggatgg caccagaagt aatcagaatg 2160
caagataaaa acccgtatag ctttcagtca gacgtgtatg cgtttgggat tgttctgtac 2220
gaactgatga ccggccagct accttattca aacatcaaca acagggatca gataattttt 2280
atggtgggac gaggatacct atctccagat ctcagtaagg tacggagtaa ctgtccaaaa 2340
gccatgaaga gattaatggc agagtgcctc aaaaagaaaa gagacgagag accactcttt 2400
ccccaaattc tcgcctccat tgagctgctg gcccgctcat tgccaaaaat tcaccgcagt 2460
gcatcagaac cttccttgaa tcgggctggt ttccaaacag aagattttag tctgtatgct 2520
tgtgcttctc cgaaaacacc catccaagca gggggatatg gagaatttgc agccttcaag 2580
tagccagtcc atcatggcag catctactct ttatttctta agtcttgtgt tcatacagtt 2640
tgttaacatc aaaacacagt tctgttcctc aaaaaatttt ttaaagatac aaaattttca 2700
atgcataagt tcatgtggaa cagaatggaa tttcctattc aacaaaagag ggaagaatgt 2760
tttaggaacc agaattctct gctgcccgtg tttcttcttc aacataacta tcacgtgcat 2820
acaagtctgc ccattcccaa gaagaaagag gagagaccct gaattctgcc cttttggtgg 2880
tcaggcatga tggaaagaat ttgctgctgc agcttgggaa aattgctatg gaaagtctgc 2940
cagtcgactt tgcccttcta accaccagat cagcctgtgg ctggtcatct gatggggcga 3000
tttccatcac caagcatcgt tcttgcctat tctgggatta tgttgtggag cactttccct 3060
gtccagcacc gttcatttct gagggatgga gtaaatgcag cattcccttg tgtagcgcct 3120
gttcagtcct cagcagctgc tgtcacagcg aagcttttta cagttaagtg gtgggggaga 3180
gttgaggaga gcctgcctcg gggcagagaa aagggggtgc tgcatcttct tcctcacctc 3240
cagctctctc acctcgggtt gccttgctca ctgggctccg cctaaccact caggctgctc 3300
agtgctggca cacattgcct tcttttctca ttgggtccag caattgagga gagggttggg 3360
ggattgtttc ctcctcaatg tagcaaattc tcaggaaaat acagtccata tcttcctctc 3420
agctcttcca gtcaccaaat acttacgtgg ctcctttgtc caggacataa aacaccgtgg 3480
acaacaccta attaaaagcc tacaaaactg cttactgaca gttttgaatg tgagacactt 3540
gtgtaattta aatgtaaggt acaggtttta atttctgagt ttcttctatt tttatttaaa 3600
agaagaaaat aattttcagt tttaattgga ataaatgagt acttcccaca agactatata 3660
ccctgaaaat tatatttttg ttaattgtaa acaactttta aagaataatt attatccttt 3720
tctctaccta aaaattatgg ggaatcttag cataatgaca attatttata ctttttaaat 3780
aaatggtact tgctggatcc acactaacat ctttgctaac aatcccattg tttcttccaa 3840
cttaactcct acactacatc ctacatcctc tttctagtct tttatctata atatgcaacc 3900
taaaataaac gtggtggcgt ctccattcat tctccctctt cctgttttcc ccaagcctgg 3960
tcttcaaaag gttgggtaat cggtccctga gctccctagc tggcaatgca actattaggg 4020
acattggagt tgcaggagag caggaagcct gtccccagct gttcttctag aaccctaaat 4080
cttatctttg cacagatcaa aagtatcacc tcgtcacagt tctccttagc ctttacttac 4140
aggtaatata aataaaaatc accatagtag taaagaaaac aactggatgg attgatgacc 4200
agtacctctc agagccagga atcttgaatc tccaggattt atacgtgcaa atttaaggag 4260
atgtacttag caacttcaag ccaagaactt ccaaaatact agcgaatcta aaataaaatg 4320
gaattttgag ttatttttaa agttcaaatt ataattgata ccactatgta tttaagccta 4380
ctcacagcaa gttagatgga ttttgctaaa ctcattgcca gactgtggtg gtggtggtgg 4440
tagtgtgcac ctttaatcca agcaactcag caatcagaat gaggtaaatc tctgtgaata 4500
caaggcctgc ctagtctgca gcgctagttc caggatagcc agggctacac acacaaaaac 4560
cctctctcaa aaaaaacaaa attaattagt tgataataaa aaataactaa agtatcatca 4620
aaggaaggcc tactggaagt tttatatatt cccagtaaat tgaaaaatat tctgaagtta 4680
ttaaccagtt agcaacaatg tgtttttaag tcttacataa acagagcaaa gtcttcaaat 4740
gtttcagagc tgagaagata attgtgcttg atatgaaaaa tagcctctcc atatgatgtg 4800
ccacattgaa aggcgtcatt acccttttaa atacttctta atgtggcttt gttcccttta 4860
cccaggatta gctagaaaga gctaggtagg cttcggccac agttgcacat ttcgggcctg 4920
ctgaagaatg ggagctttga aggctggcct tggtggagga gcccctcagt gctggagggt 4980
ggggcgtgta cgcagcatgg aagtggtcta gacagagtgc aaagggacag acttctttct 5040
cattttagta tagggtgatg tctcacttga aatgagaaag tagagttgat attaaacgaa 5100
gctgtgccca gaaaccaggc tcagggtatt gtgagatttt ctttttaaat agagaatata 5160
aaagatagaa ataaatattt aaaccttcct tcttattttc tatcaaatag atttttttta 5220
tcatttgcaa acaacataaa aaaaggtttc ttttgtgggg ttttctttcc ttcttttttt 5280
tttttttttt tttttaagac tgcagataat cttgttgagc tcctcggaaa atacaaggaa 5340
gtccgtgttt gtgcagagcg ctttatgagt aactgtatag acagtgtggc tgcttcactc 5400
atcccagagg gctgcagctg tcggcccatg aagtggctgc agtgcctcgt gagatctgct 5460
ttgttttgtt tggagtgaag tctttgaaag gtttgagtgc aactatatag gactgttttt 5520
aaataagtag tattcctcat gaactttctc attgttaagc tacaggaccc aaactctacc 5580
actaagatat tattaacctc aaaatgtagt ttatagaagg aatttgcaaa tagaatatcc 5640
agttcgtact tatatgcatc ttcaacaaag attctctgtg acttgttgga tttggttcct 5700
gaacagccca tttctgtatt tgaggttagg agggcataat gaggcatcct aaaagacaat 5760
ctgatataaa ctgtatgcta gatgtatgct ggtaggggag aaagcattct gtaaagacat 5820
gatttaagac ttcagctctg tcaaccagaa accttgtaaa tacttcctgt cttggtgcag 5880
ccccgcccct ttgatcacac gatgttgtct tgtgcttgtc agacactgtc agagctgctg 5940
ttcgtccctc tgcagatctc acctgtcccc actgcacacc cacctcctgc ctcttgcaga 6000
cctcagcatc tagctttagt tggaaacagt tcagggttca ggtgacttct taaaaaaaaa 6060
aaaaaaccct acctcctcag aatgaggtaa tgaatagtta tttatttaaa gtatgaagag 6120
tcaggagcgc tcgaacatga aggtgattta agatggttcc tttcgtgtgt attgtagctg 6180
agcacttgtt tttgtcctaa agggcattat acatttaagc agtgattctg tttaaagatg 6240
tttttcttta aaggtgtagc tcagagtatc tgttgttgga attggtgcca gagtctgctt 6300
aatagatttc agaatcctaa gcttaagtca gtcgcatgaa gttaagtagt tatggtaaca 6360
ctttgctagc catgatataa ttctactttt taggagtagg tttggcaaaa ctgtatgcct 6420
tcaaagtgag ttggccacag ctttgtcaca tgcacagata ctcatctgaa gagactgccc 6480
agctaagagg gcggaaggat accctttttt cctacgattc gcttctttgt ccacgttggc 6540
attgttagta ctagtttatc agcaccttga ccagcagatg tcaaccaata agctattttt 6600
aaaaccatag ccagagatgg agaggtcact gtgagtagaa acagcaggac gcttacagga 6660
gtgaaatggt gtagggaggc tctagaaaaa tatcttgaca atttgccaaa tgatcttact 6720
gtgccttcat gatgcaataa aaaagctaac attttagcag aaatcagtga tttacgaaga 6780
gagtggccag tctggtttaa ctcagctggg ataatatttt tagagtgcaa tttagactgc 6840
gaagataaat gcactaaaga gtttatagcc aattcacatt tgaaaaataa gaaaatggta 6900
aattttcagt gaaatatttt tttaaagcac ataatcccta gtgtagccag aaatatttac 6960
cacatagagc agctaggctg agatacagtc cagtgacatt tctagagaaa ccttttctac 7020
tcccacgggc tcctcaaagc atggaaattt tatacaaaat gtttgacatt ttaagatact 7080
gctgtagttt agttttgaaa tagtatgtgc tgagcagcaa tcatgtacta actcagagag 7140
agaaaacaac aacaaattgt gcatctgatt tgttttcaga gaaatgctgc caacttagat 7200
actgagttct cagagcttca agtgtaaact tgcctcccaa gtcctgtttg caaatgaagt 7260
tggctagtgc tactgactgc tccagcacat gatggaaggc agggggctgt ctctgaagtg 7320
tcttctataa agggacaata gaatagtgag agacctggtc agtgtgtgtc agctggacac 7380
tccatgctat gggacttgca tcttctgtcc tcaccatccc caagacattg tgctttcctc 7440
agttgtcctc tagctgtttc actcagacac caagatgaat tactgatgcc agaaggggcc 7500
aaaatggcca gtgtgttttg ggggttgtat cagttgactg gacaataact ttaatagttt 7560
cagatcattt atttttactt ccattttgac agacatttaa atggaaattt agtcctaact 7620
tttgtcattt gaaaggaaaa attaacagtt cctataagat acttttgagg tggaatctga 7680
catcctaatt ttttttcttt tcagtgggtt tgcagcgagg gtcttgtatg cactaggcaa 7740
gggttctacc actaagccac atttcccagg aaataaaatg ttaacagtta aaacatacac 7800
acaaatacac aaacacctta ttaccacttt agtaaagtga gagatgtgcg tcctttgtct 7860
cagtctccac gatttcagct gccccttgta tgaataactc agtctcgcta aactgtttac 7920
ttttatttac ctggtttgac tagttgcagc tatataacca gttgtgcatg aggacaacag 7980
ccagtgtgtt tgttttgttt ttggtttttt gtggtacatt ttttgtaaag aattctgtag 8040
attgaagtgc tctttgaaaa cagaactgag atatatttat tcttgttagc atcaaaaaac 8100
attttgtgca aatgatttgc ttttcctggc aggctgagta ccatatccag cgcccacaat 8160
tgcgggttcc catctaccat gtccacaggg gagacagacg ggaagcacat gaggggtgtg 8220
tttacagagt tgtaggagtt atgtagttct cttgttgcct tggaaatcac tgttgtttta 8280
agactgttga acccgtgtgt ttggctgggc tgtgagttac atgaagaaac tgcaaactag 8340
catatgcaga caaagctcac agactaggcg taaatggagg aaaatggacc aaaataaggc 8400
agggtgacac ataaaccttg ggcttcggag aaaactaagg gtggagatga actataatca 8460
cctgaataca atgtaagagt gcaataagtg tgcttattct aagctgtgaa cttcttttaa 8520
atcattcctt tctaatacat ttatgtatgt tccattgctg actaaaacca gctatgagaa 8580
catatgcctt tttattcatg ttaactacca gtttaagtgg ctaaccttaa tgtcttattt 8640
atcttcattt tgtattagtt tacataccag gtatgtgtgt gtgctgtact cttcttccct 8700
ttatttgaaa acacttttca ctgggtcatc tccttggcca ttccacaaca caactttggt 8760
ttggctttca atgtcacctt atttgatggc ctgtgtccca gtagcagaat ttatggtatt 8820
cccattgctg gctgctcttc cgaccctttg cttctacagc acttgtctct cctaagatag 8880
tcagaaacta actgatcagg ggatggactt caccattcat cgtgtctctt caattctatt 8940
aaatagacca ctcttgggct ttagaccagg aaaaaggaga cagctctagc catctaccaa 9000
gcctcaccct aaaaggtcac ccgtacttct tggtctgagg acaagtctcc actccagtaa 9060
gggagagggg aggaaatgct tcctgtttga aatgcagtga attcctatgg ctcctgtttc 9120
accacccgca cctatggcaa cccatataca ttcctcttgt ctgtaactgc caaaggttgg 9180
gtttatgtca cttcagttcc actcaagcat tgaaaaggtt ctcatggagt ctggggtgtg 9240
cccagtgaaa agatggggac tttttcatta tccacagacc tctctatacc tgctttgcaa 9300
aaattataat ggagtaacta tttttaaagc ttatttttca attcataaga aaaagacatt 9360
tattttcaat caaatggatg atgtctctta tcccttatcc ctcaatgttt gcttgaattt 9420
tgtttgttcc ctatacctac tccctaattc tttagttcct tcctgctcag gtcccttcat 9480
ttgtactttg gagtttttct catgtaaatt tgtataatgg aaaatattgt tcagtttgga 9540
tagaaagcat ggagaaataa ataaaaaaag atagctgaaa atcaaattga agaaatttat 9600
ttctgtgtaa agttatttaa aaactctgta ttatatttaa agaaaaaagc ccaacccccc 9660
aaaaagtgct atgtaattga tgtgaatatg cgaatactgc tataataaag attgactgca 9720
tggagaaa 9728
<210> 6
<211> 804
<212> PRT
<213> Mus musculus
<400> 6
Met Ala Ala Leu Ser Gly Gly Gly Gly Ser Ser Ser Gly Gly Gly Gly
1 5 10 15
Gly Gly Gly Gly Gly Gly Gly Gly Gly Asp Gly Gly Gly Gly Ala Glu
20 25 30
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
35 40 45
Gly Ala Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val
50 55 60
Trp Asn Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala
65 70 75 80
Leu Leu Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu
85 90 95
Glu Ala Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg
100 105 110
Glu Gln Gln Leu Leu Glu Ser Leu Val Phe Gln Thr Pro Thr Asp Ala
115 120 125
Ser Arg Asn Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe
130 135 140
Leu Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr
145 150 155 160
Val Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro
165 170 175
Glu Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile
180 185 190
Gly Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val
195 200 205
Glu Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys
210 215 220
Thr Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe
225 230 235 240
Gln Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys
245 250 255
Ser Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu
260 265 270
Leu Phe Val Ser Lys Phe Phe Glu His His Pro Val Pro Gln Glu Glu
275 280 285
Ala Ser Phe Pro Glu Thr Ala Leu Pro Ser Gly Ser Ser Ser Ala Pro
290 295 300
Pro Ser Asp Ser Thr Gly Pro Gln Ile Leu Thr Ser Pro Ser Pro Ser
305 310 315 320
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
325 330 335
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
340 345 350
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Glu Lys Phe Pro Glu
355 360 365
Val Glu Leu Gln Asp Gln Arg Asp Leu Ile Arg Asp Gln Gly Phe Arg
370 375 380
Gly Asp Gly Ala Pro Leu Asn Gln Leu Met Arg Cys Leu Arg Lys Tyr
385 390 395 400
Gln Ser Arg Thr Pro Ser Pro Leu Leu His Ser Val Pro Ser Glu Ile
405 410 415
Val Phe Asp Phe Glu Pro Gly Pro Val Phe Arg Gly Ser Thr Thr Gly
420 425 430
Leu Ser Ala Thr Pro Pro Ala Ser Leu Pro Gly Ser Leu Thr Asn Val
435 440 445
Lys Ala Leu Gln Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser
450 455 460
Ser Ser Ser Ser Ser Glu Asp Arg Ser Arg Met Lys Thr Leu Gly Arg
465 470 475 480
Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp Gly Gln Ile Thr Val
485 490 495
Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys
500 505 510
Trp His Gly Asp Val Ala Val Lys Met Leu Asn Val Thr Ala Pro Thr
515 520 525
Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val Gly Val Leu Arg Lys
530 535 540
Thr Arg His Val Asn Ile Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro
545 550 555 560
Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly Ser Ser Leu Tyr His
565 570 575
His Leu His Ile Ile Glu Thr Lys Phe Glu Met Ile Lys Leu Ile Asp
580 585 590
Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr Leu His Ala Lys Ser
595 600 605
Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile Phe Leu His Glu Asp
610 615 620
Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala Thr Val Lys Ser Arg
625 630 635 640
Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp
645 650 655
Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe
660 665 670
Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu Tyr Glu Leu Met Thr
675 680 685
Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe
690 695 700
Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu Ser Lys Val Arg Ser
705 710 715 720
Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala Glu Cys Leu Lys Lys
725 730 735
Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Ile Leu Ala Ser Ile Glu
740 745 750
Leu Leu Ala Arg Ser Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro
755 760 765
Ser Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala
770 775 780
Cys Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly Gly Tyr Gly Glu Phe
785 790 795 800
Ala Ala Phe Lys
<210> 7
<211> 2232
<212> ДНК
<213> Oryctolagus cuniculus
<400> 7
atggggaatg tgtggaatat caaacaaatg attaagttga cacaggagca tatagaggcc 60
ctattggaca aatttggtgg ggagcataat ccaccatcaa tatatctgga ggcctacgaa 120
gaatacacca gcaagctaga tgccctccaa caaagagaac agcagttatt ggaatcccta 180
gtttttcaaa atcccacaga tgtgtcacgg agcaacccca agtcaccaca aaaacctatt 240
gttagagtct tcctgcccaa caaacagagg acagtggtac ctgcaagatg tggagttacg 300
gttcgagaca gtctaaagaa agcgctgatg atgagaggtc tgatcccaga atgctgtgct 360
gtttacagaa ttcaggatgg agagaagaag ccaattggct gggacactga tatttcctgg 420
ctcactggag aagagctgca tgtggaagtg ttagagaatg tcccactcac cacacataac 480
tttgtacgga aaactttttt caccttagca ttttgtgact tctgtagaaa gctgcttttc 540
cagggtttcc gctgtcaaac atgtggctac aaatttcacc agcgttgtag tacggaagtt 600
ccactgatgt gtgttaatta tgaccaactt gatttgctgt ttgtctccaa gttctttgaa 660
caccacccag taccacagga ggaggcctcc ttagcagaga ctgccctcac atctgggtca 720
tcgccttccg cacctccctc agactctatt gggcaccaaa ttctcaccag tccgtcccct 780
tcaaaatcca ttccgattcc acagtccttc cgaccagcag atgaagatca tcgaaatcag 840
tttgggcaac gagaccggtc ttcatcagcg cctaatgttc acattaacac aatagaacct 900
gtcaatattg atgaaaaatt cccagaagtg gaattacagg atcaaaggga cttgattaga 960
gaccaagggt ttcgtggtga tggagcccct ttgaaccagc tgatgcgctg tcttcggaaa 1020
taccaatccc ggactcccag tcccctccta ccttctgtcc ccagtgacat agtgtttgat 1080
tttgagcctg gcccagtgtt cagaggatcg accacgggtt tgtctgccac tccccctgcc 1140
tcattacctg gctcactcac tagtgtgaaa gctgtacaga gatccccagg acctcagcga 1200
gagaggaagt cgtcttcctc ctcagaagac aggaatcgaa tgaaaactct tggtagacgg 1260
gattcaagtg atgattggga gattcctgat gggcagatca ccgtgggaca gagaattgga 1320
tctggatcat ttggaaccgt ctacaaggga aaatggcacg gtgatgtggc agtaaaaatg 1380
ttgaatgtga cagcacctac acctcagcag ttacaggcct tcaaaaatga agtaggagta 1440
ctcaggaaaa cacgacatgt gaatatccta cttttcatgg gctattccac aaagccacag 1500
ctggctattg ttacccagtg gtgtgagggc tccagtttat atcaccatct ccacatcatt 1560
gagaccaaat tcgagatgat caaacttata gatattgcac ggcagactgc acagggcatg 1620
gattacttac acgccaagtc aatcatccac agagacctca agagtaataa tatatttctt 1680
catgaagacc tcacagtaaa aataggtgat tttggtctag ccacagtgaa atctcgatgg 1740
agtgggtccc atcagtttga acaattgtct ggatccattt tgtggatggc accagaagta 1800
atcagaatgc aagacaaaaa cccatatagc tttcagtcag atgtatatgc atttgggatt 1860
gttctgtatg aattgatgac tgggcagtta ccttactcaa acatcaacaa cagggaccag 1920
atcattttta tggtgggacg tggctacctg tctccagacc tcagtaaggt acggagtaac 1980
tgtccgaaag ccatgaagag attaatggca gagtgcctca aaaagaaaag agatgagaga 2040
ccactctttc cccaaattct cgcctccatt gagctgctgg cccgctcatt gccaaaaatc 2100
caccgcagtg catcagaacc ctccttgaat cgggctggtt tccagacaga ggattttagt 2160
ctatatgctt gtgcttctcc aaaaacaccc atccaggcag ggggatatgg agaatttgca 2220
gccttcaagt ag 2232
<210> 8
<211> 743
<212> PRT
<213> Oryctolagus cuniculus
<400> 8
Met Gly Asn Val Trp Asn Ile Lys Gln Met Ile Lys Leu Thr Gln Glu
1 5 10 15
His Ile Glu Ala Leu Leu Asp Lys Phe Gly Gly Glu His Asn Pro Pro
20 25 30
Ser Ile Tyr Leu Glu Ala Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala
35 40 45
Leu Gln Gln Arg Glu Gln Gln Leu Leu Glu Ser Leu Val Phe Gln Asn
50 55 60
Pro Thr Asp Val Ser Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile
65 70 75 80
Val Arg Val Phe Leu Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg
85 90 95
Cys Gly Val Thr Val Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg
100 105 110
Gly Leu Ile Pro Glu Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu
115 120 125
Lys Lys Pro Ile Gly Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu
130 135 140
Glu Leu His Val Glu Val Leu Glu Asn Val Pro Leu Thr Thr His Asn
145 150 155 160
Phe Val Arg Lys Thr Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg
165 170 175
Lys Leu Leu Phe Gln Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe
180 185 190
His Gln Arg Cys Ser Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp
195 200 205
Gln Leu Asp Leu Leu Phe Val Ser Lys Phe Phe Glu His His Pro Val
210 215 220
Pro Gln Glu Glu Ala Ser Leu Ala Glu Thr Ala Leu Thr Ser Gly Ser
225 230 235 240
Ser Pro Ser Ala Pro Pro Ser Asp Ser Ile Gly His Gln Ile Leu Thr
245 250 255
Ser Pro Ser Pro Ser Lys Ser Ile Pro Ile Pro Gln Ser Phe Arg Pro
260 265 270
Ala Asp Glu Asp His Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser
275 280 285
Ser Ala Pro Asn Val His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp
290 295 300
Glu Lys Phe Pro Glu Val Glu Leu Gln Asp Gln Arg Asp Leu Ile Arg
305 310 315 320
Asp Gln Gly Phe Arg Gly Asp Gly Ala Pro Leu Asn Gln Leu Met Arg
325 330 335
Cys Leu Arg Lys Tyr Gln Ser Arg Thr Pro Ser Pro Leu Leu Pro Ser
340 345 350
Val Pro Ser Asp Ile Val Phe Asp Phe Glu Pro Gly Pro Val Phe Arg
355 360 365
Gly Ser Thr Thr Gly Leu Ser Ala Thr Pro Pro Ala Ser Leu Pro Gly
370 375 380
Ser Leu Thr Ser Val Lys Ala Val Gln Arg Ser Pro Gly Pro Gln Arg
385 390 395 400
Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn Arg Met Lys Thr
405 410 415
Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp Gly Gln
420 425 430
Ile Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr Val Tyr
435 440 445
Lys Gly Lys Trp His Gly Asp Val Ala Val Lys Met Leu Asn Val Thr
450 455 460
Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val Gly Val
465 470 475 480
Leu Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe Met Gly Tyr Ser
485 490 495
Thr Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly Ser Ser
500 505 510
Leu Tyr His His Leu His Ile Ile Glu Thr Lys Phe Glu Met Ile Lys
515 520 525
Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr Leu His
530 535 540
Ala Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile Phe Leu
545 550 555 560
His Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala Thr Val
565 570 575
Lys Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser Gly Ser
580 585 590
Ile Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys Asn Pro
595 600 605
Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu Tyr Glu
610 615 620
Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg Asp Gln
625 630 635 640
Ile Ile Phe Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu Ser Lys
645 650 655
Val Arg Ser Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala Glu Cys
660 665 670
Leu Lys Lys Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Ile Leu Ala
675 680 685
Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro Lys Ile His Arg Ser Ala
690 695 700
Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp Phe Ser
705 710 715 720
Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly Gly Tyr
725 730 735
Gly Glu Phe Ala Ala Phe Lys
740
<210> 9
<211> 2186
<212> ДНК
<213> Cavia porcellus
<400> 9
atggcggcgc tcagcggcgg cggtggcgcg gagcagggcc aggctctgtt caacggggac 60
atggagctcg aggccggcgc cggcgccgca gcctcttcgg ctgcagaccc tgccattccc 120
gaggaggtat ggaatatcaa acaaatgatt aagttgacgc aggaacacat agaggcccta 180
ttggacaaat ttggtggaga gcataatcca ccatcaatat acctggaggc ctatgaagaa 240
tacaccagca aactagatgc cctccaacaa agagaacagc agttactgga atccctcggg 300
aatggaactg atttttctgt ttctagctct gcatcactgg acaccgttac atcttcttct 360
tcttctagcc tttcagtact accttcatct ctttcagttt ttcaaaatcc tacagatgtg 420
tcacggagca accccaaatc accacaaaaa cctattgtta gagtcttcct gcccaacaaa 480
cagaggacag tggtacctgc aaggtgtgga gttacagtcc gagacagtct gaagaaagca 540
ctcatgatga gaggtcttat cccagagtgc tgtgctgtgt acagaattca ggatggagaa 600
aagaaaccaa ttggctggga cactgacatt tcctggctta ctggggaaga attacatgta 660
gaagtattgg agaatgttcc acttacaaca cacaattttg tatgtatctt tatatttttt 720
ttgctgtttg tctccaagtt ctttgaacac cacccaatac cacaggagga ggcttcctta 780
gcagagacca cccttacatc tggatcatcc ccttctgcac ccccctcaga gtccattggg 840
cccccaattc tcaccagccc atctccttca aaatccattc caattccaca gcctttccgg 900
ccaggagagg aagatcatcg aaatcaattt gggcagcgag accggtcctc atctgctccc 960
aatgtgcata taaacacaat agaacctgtc aatattgatg atttgattag agaccaaggg 1020
tttcgtagtg atggaggatc aactacaggt ttgtctgcca ccccacctgc ctcattacct 1080
ggctcactca ctaatgtgaa agccttacag aaatctccag gacctcagcg agaaaggaag 1140
tcatcttcat cctcagaaga cagaaatcga atgaaaacgc ttggtagacg ggactcaagt 1200
gatgattggg agattcctga tgggcagatt acagtgggac aaagaattgg atctgggtca 1260
tttggaacag tctacaaggg gaagtggcat ggtgacgtgg cagtgaaaat gttgaatgtg 1320
acagcaccca cacctcaaca gttacaggcc ttcaaaaatg aagtaggagt actcaggaaa 1380
acacgacatg tgaatatcct actcttcatg ggctattcca caaagccaca gctagctatt 1440
gttacccagt ggtgtgaggg ctccagctta taccaccatc tccacatcat cgagaccaaa 1500
tttgagatga tcaaacttat agatattgca cgacagactg cccagggcat ggattactta 1560
cacgccaagt caatcatcca cagagacctc aagagtaata atatatttct tcacgaagac 1620
ctcacggtta aaataggtga ttttggtcta gccacagtga aatctcgatg gagtgggtcc 1680
catcagtttg aacagttgtc tggatccatt ttgtggatgg caccagaagt aatcagaatg 1740
cgagataaaa acccatacag ttttcagtcc gatgtatatg catttgggat tgttctatat 1800
gaattgatga ctgggcagtt accctattca aatatcaaca acagggacca gataattttt 1860
atggtgggac gaggatatct atctccagat ctcagcaagg tacggagtaa ctgtccaaaa 1920
gccatgaaga ggttaatggc ggagtgcctc aaaaagaaaa gagatgagag accactcttt 1980
ccccaaattc tcgcctctat tgagctgctg gcccgctcat tgccaaaaat tcaccgcagt 2040
gcatcagaac cctccttgaa tcgggctggt ttccaaacag aggattttag tctctatgct 2100
tgtgcttctc caaaaacacc catccaggca gggggatatg gtgcgtttcc tgtccactga 2160
tgcaaattaa atgagtgaga aataaa 2186
<210> 10
<211> 719
<212> PRT
<213> Cavia porcellus
<400> 10
Met Ala Ala Leu Ser Gly Gly Gly Gly Ala Glu Gln Gly Gln Ala Leu
1 5 10 15
Phe Asn Gly Asp Met Glu Leu Glu Ala Gly Ala Gly Ala Ala Ala Ser
20 25 30
Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn Ile Lys Gln
35 40 45
Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu Asp Lys Phe
50 55 60
Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala Tyr Glu Glu
65 70 75 80
Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln Gln Leu Leu
85 90 95
Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser Ser Ala Ser
100 105 110
Leu Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser Val Leu Pro
115 120 125
Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser Arg Ser Asn
130 135 140
Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu Pro Asn Lys
145 150 155 160
Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val Arg Asp Ser
165 170 175
Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu Cys Cys Ala
180 185 190
Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly Trp Asp Thr
195 200 205
Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu Val Leu Glu
210 215 220
Asn Val Pro Leu Thr Thr His Asn Phe Val Cys Ile Phe Ile Phe Phe
225 230 235 240
Leu Leu Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu
245 250 255
Glu Ala Ser Leu Ala Glu Thr Thr Leu Thr Ser Gly Ser Ser Pro Ser
260 265 270
Ala Pro Pro Ser Glu Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser
275 280 285
Pro Ser Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Gly Glu Glu
290 295 300
Asp His Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro
305 310 315 320
Asn Val His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile
325 330 335
Arg Asp Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser
340 345 350
Ala Thr Pro Pro Ala Ser Leu Pro Gly Ser Leu Thr Asn Val Lys Ala
355 360 365
Leu Gln Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser
370 375 380
Ser Glu Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser
385 390 395 400
Asp Asp Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile
405 410 415
Gly Ser Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp
420 425 430
Val Ala Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu
435 440 445
Gln Ala Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val
450 455 460
Asn Ile Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile
465 470 475 480
Val Thr Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile
485 490 495
Ile Glu Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln
500 505 510
Thr Ala Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg
515 520 525
Asp Leu Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys
530 535 540
Ile Gly Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser
545 550 555 560
His Gln Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu
565 570 575
Val Ile Arg Met Arg Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val
580 585 590
Tyr Ala Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro
595 600 605
Tyr Ser Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg
610 615 620
Gly Tyr Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys
625 630 635 640
Ala Met Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu
645 650 655
Arg Pro Leu Phe Pro Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg
660 665 670
Ser Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg
675 680 685
Ala Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro
690 695 700
Lys Thr Pro Ile Gln Ala Gly Gly Tyr Gly Ala Phe Pro Val His
705 710 715
<210> 11
<211> 3229
<212> ДНК
<213> Canis lupus
<400> 11
gtaatgctgg attttcatgg aataagtttg acctgtgctg cagtggcctc cagcaaggta 60
cccgcaagat gtggagttac agtccgggac agtctaaaga aagctctgat gatgagaggt 120
ctaatcccag agtgctgtgc tgtttacaga attcaggatg gagagaagaa accgattggc 180
tgggacactg atatttcctg gctcactgga gaggaattgc atgtagaagt gttggaaaat 240
gttccgctta ccacacacaa ctttgtacgg aaaacttttt tcaccttagc attttgtgac 300
ttttgtcgaa agctgctttt ccagggtttt cgctgtcaaa catgtggtta taaatttcac 360
cagcgttgta gtacagaggt tccactgatg tgtgttaatt atgaccaact tgatttgctg 420
tttgtctcca agttctttga acaccaccca ataccacagg aggaggcctc catagcagag 480
actgccctta cgtctggatc atccccttct gctcccccct ccgattctcc tgggccccca 540
attctgacca gtccgtctcc ttcaaaatcc attccaattc cacagccttt ccgaccagca 600
gatgaagatc atcgaaatca gtttggacaa cgagaccggt cctcatcagc tccaaatgtg 660
catataaaca caatagaacc cgtcaacatt gatgacttga ttagagacca agggtttcgt 720
agtgatggag gatcaaccac aggtttgtct gccacccccc ctgcctcatt gcctggctca 780
ctcactaatg taaaagcatt acagaaatct ccaggacctc agcgggaaag aaaatcatct 840
tcatcctcag aagataggaa tcgaatgaaa acacttggta gacgggattc aagtgatgat 900
tgggagatac ctgatgggca gatcacagtg ggacagagaa ttggatccgg gtcatttggg 960
acagtctaca agggaaagtg gcatggtgac gtggcagtga aaatgttgaa tgtgacagca 1020
cccacacctc agcagttaca ggccttcaaa aatgaagtag gagtactcag gaaaactcga 1080
catgtgaata tcctactctt tatgggctat tcaacaaagc cccaactggc tattgttacc 1140
cagtggtgtg agggctccag cttatatcac catctccaca tcattgagac caaatttgag 1200
atgataaagc ttatagatat tgcacggcag actgcacagg gcatggatta cttacacgcc 1260
aagtcaatca tccacagaga cctcaagagt aataatattt ttcttcatga agacctcaca 1320
gtaaaaatag gtgattttgg tctagccaca gtgaaatctc gatggagtgg gtcccatcag 1380
tttgaacagt tgtctggatc cattttgtgg atggcaccag aagtgatccg aatgcaagac 1440
aaaaacccat atagcttcca gtcagatgta tacgcatttg ggattgttct atatgaattg 1500
atgacagggc agttacctta ttcaaacatc aacaacaggg accagataat ttttatggtg 1560
ggacgaggat atctttctcc agatctcagt aaggtacgga gtaactgtcc aaaagccatg 1620
aagagattga tggcagagtg cctaaaaaag aaaagagatg agaggccact ctttccccaa 1680
attctcgcct ctattgagct gctggcccgc tcattgccaa aaattcaccg cagtgcatca 1740
gaaccctcct tgaatcgggc tggcttccaa acagaggatt ttagtctcta tgcttgcgct 1800
tctccaaaaa cacccatcca ggcaggggga tacggagaat ttgcagcctt caagtagcca 1860
caccatcatg gcaacaacta ctcttatttc ttaagtcttg tgttcgtaca atttgttaac 1920
atcaaaacac agttctgttc ctcaaatctt tttttaaaga tacagaattt tcaatgcata 1980
agctggtgtg gaacagaatg gaatttccca tccaacaaaa gagggaagaa tgttttagga 2040
accagaattc tctgctgcca gtgtttcttc ttcaacacaa ataccacgtg catacaagtc 2100
tgcccactcc caggaaggaa gaggagagcc tgagttctga ccttttgatg gtcaggcatg 2160
atggaaagaa actgctgcta cagcttggga gattggctgt ggagagcctg cccgtcagct 2220
ctgcccttct aaccgccaga tgagtgtgtg gctggtcacc tgacagggca gctgcaatcg 2280
ccaagcatcg ttctctttcc tgtcctggga ttttgtcgtg gagctctttc cccctagtca 2340
ccaccggttc atttctgagg gatggaacaa aaatgcagca tggcctttct gtgtggtgca 2400
tgtccggtct ttgacaaatt tttatcaagt gaagctcttg tatttaaatg gagaatgaga 2460
ggcgaggggg ggggatcacg ttttggtgta ggggcaaagg gaatgctgca tctttttcct 2520
gacccactgg gtttctggcc tttgtttcct tgctcactga gggtgtctgc ctataaccac 2580
gcaggctgga aagtgctggc acacattgcc ttctcttctc actgggtcca gcaatgaaga 2640
caagtgttgg ggattttttt ttttgccctc cacaatgtag caagttctca ggaaaataca 2700
gttaatatct tcctcctaag ctcttccagt catcaagtac ttatgtggct actttgtcca 2760
gggcacaaaa tgccatggcg gtatccaatt aaaagcctac aaaactgctt gataacagtt 2820
ttgaatgtgt gagacattta tgtaatttaa atgtaaggta caagttttaa tttctgagtt 2880
tctctattat atttttatta aaaagaaaat aattttcaga tttaattgaa ttggaataaa 2940
ataatacttc ccaccagaat tatatatcct ggaaaattgt atttttgtta tataaacaac 3000
ttttaaagaa agatcattat ccttttctct acctaaatat ggggagtctt agcataatga 3060
cagatattta taatttttaa attaatggta cttgctggat ccacactaac atctttgcta 3120
atatctcatg ttttcctcca acttactcct acactacatc ctccatcctc tttccagtct 3180
tttatctaga atatgcaacc taaaataaaa atggtggtgt ctccattca 3229
<210> 12
<211> 617
<212> PRT
<213> Canis lupus
<400> 12
Met Leu Asp Phe His Gly Ile Ser Leu Thr Cys Ala Ala Val Ala Ser
1 5 10 15
Ser Lys Val Pro Ala Arg Cys Gly Val Thr Val Arg Asp Ser Leu Lys
20 25 30
Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu Cys Cys Ala Val Tyr
35 40 45
Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly Trp Asp Thr Asp Ile
50 55 60
Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu Val Leu Glu Asn Val
65 70 75 80
Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr Phe Phe Thr Leu Ala
85 90 95
Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln Gly Phe Arg Cys Gln
100 105 110
Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser Thr Glu Val Pro Leu
115 120 125
Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu Phe Val Ser Lys Phe
130 135 140
Phe Glu His His Pro Ile Pro Gln Glu Glu Ala Ser Ile Ala Glu Thr
145 150 155 160
Ala Leu Thr Ser Gly Ser Ser Pro Ser Ala Pro Pro Ser Asp Ser Pro
165 170 175
Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser Lys Ser Ile Pro Ile
180 185 190
Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His Arg Asn Gln Phe Gly
195 200 205
Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val His Ile Asn Thr Ile
210 215 220
Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp Gln Gly Phe Arg Ser
225 230 235 240
Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr Pro Pro Ala Ser Leu
245 250 255
Pro Gly Ser Leu Thr Asn Val Lys Ala Leu Gln Lys Ser Pro Gly Pro
260 265 270
Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn Arg Met
275 280 285
Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp
290 295 300
Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr
305 310 315 320
Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala Val Lys Met Leu Asn
325 330 335
Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val
340 345 350
Gly Val Leu Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe Met Gly
355 360 365
Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly
370 375 380
Ser Ser Leu Tyr His His Leu His Ile Ile Glu Thr Lys Phe Glu Met
385 390 395 400
Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr
405 410 415
Leu His Ala Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile
420 425 430
Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala
435 440 445
Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser
450 455 460
Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys
465 470 475 480
Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu
485 490 495
Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg
500 505 510
Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu
515 520 525
Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala
530 535 540
Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Ile
545 550 555 560
Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro Lys Ile His Arg
565 570 575
Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp
580 585 590
Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly
595 600 605
Gly Tyr Gly Glu Phe Ala Ala Phe Lys
610 615
<210> 13
<211> 1889
<212> ДНК
<213> Canis lupus
<400> 13
ggaatatcaa acaaatgatt aagttgacac aggaacatat agaagcccta ttggacaagt 60
ttggtgggga gcataatcca ccatcaatat atctggaggc ctatgaagaa tacaccagca 120
aactagatgc cctccaacag cgagaacaac agttattgga atccctgggg aatggaactg 180
atttttctgt ttctagctct gcatcaacgg acaccgttac atcttcttcc tcttctagcc 240
tttcagtgct accttcatct ctttcagttt ttcaaaatcc cacagatata tcacggagca 300
atcccaagtc accacaaaaa cctatcgtta gagtcttcct gcccaataaa cagaggacgg 360
tggtacccgc aagatgtgga gttacagtcc gggacagtct aaagaaagct ctgatgatga 420
gaggtctaat cccagagtgc tgtgctgttt acagaattca ggatggagag aagaaaccga 480
ttggctggga cactgatatt tcctggctca ctggagagga attgcatgta gaagtgttgg 540
aaaatgttcc gcttaccaca cacaactttg tacggaaaac ttttttcacc ttagcatttt 600
gtgacttttg tcgaaagctg cttttccagg gttttcgctg tcaaacatgt ggttataaat 660
ttcaccagcg ttgtagtaca gaggttccac tgatgtgtgt taattatgac caacttgatt 720
tgctgtttgt ctccaagttc tttgaacacc acccaatacc acaggaggag gcctccatag 780
cagagactgc ccttacgtct ggatcatccc cttctgctcc cccctccgat tctcctgggc 840
ccccaattct gaccagtccg tctccttcaa aatccattcc aattccacag cctttccgac 900
cagcagatga agatcatcga aatcagtttg gacaacgaga ccggtcctca tcagctccaa 960
atgtgcatat aaacacaata gaacccgtca acattgatga cttgattaga gaccaagggt 1020
ttcgtagtga tggaggatca accacaggtt tgtctgccac cccccctgcc tcattgcctg 1080
gctcactcac taatgtaaaa gcattacaga aatctccagg acctcagcgg gaaagaaaat 1140
catcttcatc ctcagaagat aggaatcgaa tgaaaacact tggtagacgg gattcaagtg 1200
atgattggga gatacctgat gggcagatca cagtgggaca gagaattgga tccgggtcat 1260
ttgggacagt ctacaaggga aagtggcatg gtgacgtggc agtgaaaatg ttgaatgtga 1320
cagcacccac acctcagcag ttacaggcct tcaaaaatga agtaggagta ctcaggaaaa 1380
ctcgacatgt gaatatccta ctctttatgg gctattcaac aaagccccaa ctggctattg 1440
ttacccagtg gtgtgagggc tccagcttat atcaccatct ccacatcatt gagaccaaat 1500
ttgagatgat aaagcttata gatattgcac ggcagactgc acagggcatg gattacttac 1560
acgccaagtc aatcatccac agagacctca agagtaataa tatttttctt catgaagacc 1620
tcacagtaaa aataggtgat tttggtctag ccacagtgaa atctcgatgg agtgggtccc 1680
atcagtttga acagttgtct ggatccattt tgtggatggc accagaagtg atccgaatgc 1740
aagacaaaaa cccatatagc ttccagtcag atgtatacgc atttgggatt gttctatatg 1800
aattgatgac agggcagtta ccttattcaa acatcaacaa cagggaccag ctcagatcat 1860
gatcacggtg tcatgagatc aagccccac 1889
<210> 14
<211> 615
<212> PRT
<213> Canis lupus
<400> 14
Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu Asp Lys Phe
1 5 10 15
Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala Tyr Glu Glu
20 25 30
Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln Gln Leu Leu
35 40 45
Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser Ser Ala Ser
50 55 60
Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser Val Leu Pro
65 70 75 80
Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Ile Ser Arg Ser Asn
85 90 95
Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu Pro Asn Lys
100 105 110
Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val Arg Asp Ser
115 120 125
Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu Cys Cys Ala
130 135 140
Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly Trp Asp Thr
145 150 155 160
Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu Val Leu Glu
165 170 175
Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr Phe Phe Thr
180 185 190
Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln Gly Phe Arg
195 200 205
Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser Thr Glu Val
210 215 220
Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu Phe Val Ser
225 230 235 240
Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala Ser Ile Ala
245 250 255
Glu Thr Ala Leu Thr Ser Gly Ser Ser Pro Ser Ala Pro Pro Ser Asp
260 265 270
Ser Pro Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser Lys Ser Ile
275 280 285
Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His Arg Asn Gln
290 295 300
Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val His Ile Asn
305 310 315 320
Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp Gln Gly Phe
325 330 335
Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr Pro Pro Ala
340 345 350
Ser Leu Pro Gly Ser Leu Thr Asn Val Lys Ala Leu Gln Lys Ser Pro
355 360 365
Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn
370 375 380
Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile
385 390 395 400
Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe
405 410 415
Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala Val Lys Met
420 425 430
Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn
435 440 445
Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe
450 455 460
Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys
465 470 475 480
Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu Thr Lys Phe
485 490 495
Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met
500 505 510
Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn
515 520 525
Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly
530 535 540
Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln
545 550 555 560
Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln
565 570 575
Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile
580 585 590
Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn
595 600 605
Asn Arg Asp Gln Leu Arg Ser
610 615
<210> 15
<211> 3521
<212> ДНК
<213> Felis catus
<220>
<221> misc_feature
<222> (630)..(649)
<223> n представляет собой a, c, g, или t
<400> 15
atgcctaacc tcagtctctg ccaccacggc caatttgctc atgtgcccac tgtgtcggca 60
ctgggatatt ttgtgatttg ccttggccat tgtccactgt ccttgacatt gcctgaagga 120
gaaccactga tgctaatgtt gaaggtgacc tttgcaggct ctccactact cataccaaag 180
atgcggcccc ctgataatcc cagagccact gtctgcacat gggcaaaaca ggctacattc 240
tgtgcagact ggggagaaag gttccaagaa cacagtgcca tagttttggg cagagagttt 300
caacacagca tagtgtctat ggcagtatct ggatttggcc gggggaagtg cccaagagga 360
gacagtcagg ctgtgtccta cggccaagga cctgcactta tttttgcatg cagtggttta 420
gcacagggaa gagaacgaag taggaaatcg gagccatgga aacggcagag cggaggaaac 480
gtgcacgcgc gagggtgggc acgaaaggaa agaaccctcc ccagaagact gcgcgagggc 540
gctcctagga ttacgtcacg caccccgcga aaactgaaat gtactgtgtg tggtctttta 600
attgaactat cttccttatg tgcacttaan nnnnnnnnnn nnnnnnnnng cggcggcggc 660
ggtggcgcgg agcagggcca ggctctgttc aacggggaca tggagcccga agccggcgcc 720
gcggcctctt cggctgcgga ccctgccatt cccgaggagg tgtggaatat caaacaaatg 780
attaagttga cacaggaaca tatagaggcc ctattggaca aatttggtgg ggagcataat 840
ccaccatcaa tatatctaga ggcctatgaa gaatacacca gcaagctaga tgccctccaa 900
cagagagaac aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc 960
tctgcatcaa cagacaccgt tacatcttcc tcctcttcta gcctttcagt gctaccttca 1020
tctctttcag tttttcaaaa ccccacagat gtgtcacgga gcaatcccaa gtcaccacag 1080
aaacctatcg ttagagtctt cctgcctaat aaacagagga cagtggtacc tgcaagatgt 1140
ggagttacag tccgggacag tctaaagaaa gctctgatga tgagaggtct aatccctgag 1200
tgctgtgctg tttacagaat tcaggatgga gagaagaaac caattggctg ggacactgat 1260
atctcctggc tcaccggaga ggaattgcat gtagaagtgt tggaaaatgt tccacttaca 1320
actcacaact ttgtatgtac ggaaaacgtt ttcaccttag cattttgtga cttttgtcga 1380
aagctgcttt tccaaggttt tcgctgtcaa acgtgtggtt ataaatttca ccagcgttgt 1440
agtacagagg ttccactgat gtgtgttaat tatgaccaac ttgatttgct gtttgtctcc 1500
aagttctttg aacaccaccc aataccacag gaggaggcct ccatagcaga gactgcccta 1560
acgtctggat cgtccccttc tgcccccccc tccgattcta ctgggcccca aattctcacc 1620
agtccgtctc cttcaaaatc cattccaatt ccacagcctt tccgaccagc agatgaagat 1680
catcgaaatc aatttggaca gcgagaccgg tcctcatcag ctccaaatgt gcatataaat 1740
acaatagaac ctgtcaatat tgatgacttg attagagacc aggggtttcg tagtgatgga 1800
ggatcaacca caggcttgtc tgccaccccc cctgcctcat tgccgggctc tctcactaat 1860
gtaaaagcat tacagaaatc tccagggcct cagcgggaaa ggaaatcttc ttcatcctca 1920
gaagatagga atcgaatgaa aacacttggt agaagggatt caagtgatga ttgggagatt 1980
cctgatgggc agatcacagt gggacagaga attggatccg ggtcatttgg gacagtctac 2040
aagggaaagt ggcatggtga tgtggcagtg aaaatgttga atgtgacagc acccacacct 2100
cagcagttac aggccttcaa aaatgaagta ggagtactca ggaaaactcg gcatgtgaac 2160
atcctgctct tcatgggcta ttcaacaaag ccccagctgg ctattgtcac ccagtggtgt 2220
gagggctcca gcttatacca ccatctccac atcatcgaga ccaaattcga gatgatcaag 2280
ctgatagata ttgctcggca gactgcgcag ggcatggatt acttacacgc caagtcaatc 2340
atccacagag acctcaagag taataatatt tttcttcacg aagacctcac agtaaaaata 2400
ggtgattttg gtctagccac agtgaaatct cgatggagtg ggtcccatca gtttgaacag 2460
ttgtctggat ccattttgtg gatggcacca gaagtaattc gaatgcaaga taaaaaccca 2520
tatagctttc agtcagatgt atatgcattt gggattgttc tatatgaatt gatgactgga 2580
cagttacctt attcaaacat caacaacagg gaccagataa tttttatggt gggacgagga 2640
tatctttctc cagatctcag taaggtacga agtaactgtc caaaagccat gaagagattg 2700
atggcagagt gcctaaaaaa gaaaagagat gagaggccac tgtttcccca aattcttgcc 2760
tctattgagc tgctggcccg ctcattgcca aaaattcacc gcagtgcatc agaaccctcc 2820
ttgaatcggg ctggcttcca gacagaggat tttagtctct atgcttgtgc ttctccaaaa 2880
acacccatcc aggcaggggg atatggtgcg tttcccgtcc actgagataa gttagatgag 2940
tgcgcgagtg cagggggccg gggccaagga ggtggaaatg tgcgtgcttc tgtactaagt 3000
tggatagcat cttctttttt aaaaaaagat gaaccaaaga atgtgtatgt ttttaaagac 3060
tagatataat tatttcctga tctaaaatgt atacttagct ttggattttc aatatccaag 3120
ggttttcaaa atgcacagac attgctgaac atttgcagta cctcttctgg aggctttact 3180
tcctgttaca aattggtttt gtttactggc ttatcctaat tattaaactt caattaaact 3240
tttctcctgc accttttgtt atgagctatc acatgtccct tagggactcg caagagcagt 3300
actgcccccg tgtacgggct tgcaggtaga aaggggatga cgggttttaa cacctgtgtg 3360
aggcaaggca gtccgaacag atctcattta ggaagccacg agagttgaat aagttatttt 3420
tattcttagt attttttctg taactacttt ttattataac ttggaaaata tggatgtcct 3480
ttatacacct tagcaataga ctgaatttct ttttataaat t 3521
<210> 16
<211> 974
<212> PRT
<213> Felis catus
<220>
<221> misc_feature
<222> (210)..(217)
<223> Xaa can be any naturally occurring amino acid
<400> 16
Met Pro Asn Leu Ser Leu Cys His His Gly Gln Phe Ala His Val Pro
1 5 10 15
Thr Val Ser Ala Leu Gly Tyr Phe Val Ile Cys Leu Gly His Cys Pro
20 25 30
Leu Ser Leu Thr Leu Pro Glu Gly Glu Pro Leu Met Leu Met Leu Lys
35 40 45
Val Thr Phe Ala Gly Ser Pro Leu Leu Ile Pro Lys Met Arg Pro Pro
50 55 60
Asp Asn Pro Arg Ala Thr Val Cys Thr Trp Ala Lys Gln Ala Thr Phe
65 70 75 80
Cys Ala Asp Trp Gly Glu Arg Phe Gln Glu His Ser Ala Ile Val Leu
85 90 95
Gly Arg Glu Phe Gln His Ser Ile Val Ser Met Ala Val Ser Gly Phe
100 105 110
Gly Arg Gly Lys Cys Pro Arg Gly Asp Ser Gln Ala Val Ser Tyr Gly
115 120 125
Gln Gly Pro Ala Leu Ile Phe Ala Cys Ser Gly Leu Ala Gln Gly Arg
130 135 140
Glu Arg Ser Arg Lys Ser Glu Pro Trp Lys Arg Gln Ser Gly Gly Asn
145 150 155 160
Val His Ala Arg Gly Trp Ala Arg Lys Glu Arg Thr Leu Pro Arg Arg
165 170 175
Leu Arg Glu Gly Ala Pro Arg Ile Thr Ser Arg Thr Pro Arg Lys Leu
180 185 190
Lys Cys Thr Val Cys Gly Leu Leu Ile Glu Leu Ser Ser Leu Cys Ala
195 200 205
Leu Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Gly Gly Gly Gly Gly Ala Glu
210 215 220
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
225 230 235 240
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
245 250 255
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
260 265 270
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
275 280 285
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
290 295 300
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
305 310 315 320
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
325 330 335
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
340 345 350
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
355 360 365
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
370 375 380
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
385 390 395 400
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
405 410 415
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
420 425 430
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Cys Thr Glu
435 440 445
Asn Val Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe
450 455 460
Gln Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys
465 470 475 480
Ser Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu
485 490 495
Leu Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu
500 505 510
Ala Ser Ile Ala Glu Thr Ala Leu Thr Ser Gly Ser Ser Pro Ser Ala
515 520 525
Pro Pro Ser Asp Ser Thr Gly Pro Gln Ile Leu Thr Ser Pro Ser Pro
530 535 540
Ser Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp
545 550 555 560
His Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn
565 570 575
Val His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg
580 585 590
Asp Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala
595 600 605
Thr Pro Pro Ala Ser Leu Pro Gly Ser Leu Thr Asn Val Lys Ala Leu
610 615 620
Gln Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser
625 630 635 640
Glu Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp
645 650 655
Asp Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly
660 665 670
Ser Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val
675 680 685
Ala Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln
690 695 700
Ala Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn
705 710 715 720
Ile Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val
725 730 735
Thr Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile
740 745 750
Glu Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr
755 760 765
Ala Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp
770 775 780
Leu Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile
785 790 795 800
Gly Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His
805 810 815
Gln Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val
820 825 830
Ile Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr
835 840 845
Ala Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr
850 855 860
Ser Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly
865 870 875 880
Tyr Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala
885 890 895
Met Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg
900 905 910
Pro Leu Phe Pro Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser
915 920 925
Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala
930 935 940
Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys
945 950 955 960
Thr Pro Ile Gln Ala Gly Gly Tyr Gly Ala Phe Pro Val His
965 970
<210> 17
<211> 3853
<212> ДНК
<213> Bos taurus
<400> 17
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc 60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc 120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg 180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg 240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt 300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga 360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa 420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac 480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa 540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag 600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg 660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag 720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg 780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc 840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact 900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc 960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc 1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac 1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat 1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt 1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt 1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg 1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag 1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc 1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc 1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga 1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc 1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg 1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca 1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt 1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg 1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc 1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc 1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca 2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt 2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt 2160
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag 2220
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc 2280
taaaaaagaa aagagatgaa agaccactct ttccccaaat tctcgcctct attgagctgc 2340
tggcccgctc attgccaaaa attcaccgca gtgcatcaga accctccttg aatcgggctg 2400
gcttccaaac agaggatttt agtctatatg cttgtgcttc tccaaaaaca cccattcagg 2460
cagggggata tggtacgttt cctgttcact gaaacaaacc gagtgagtga cagcatgtag 2520
gagggtaggg acaaaagaaa gtgaacaaat gtttgcttat atatttgtta aattgaatag 2580
gattttcttt ttctttaaag gtgaacaaga gaacatgtgt gtttttaaag tttggatata 2640
gttttcttcc cagtctaaaa cccatagtta gcattacatt ttcaacatcg aatttttttt 2700
taattcatag acattgctga aaatttataa taccttttcc agaggcttta cttcccattc 2760
caagtttgtt ttgtttactt ggttagtcta atcattaaac tttaaacttt ccccacctac 2820
cttttgctgt tagctatccc gcatccatta ggggctccaa gaacagcact gtctgcgtgt 2880
gtgtgttggc aggtgggaag ctgatggtaa gttaggctgt gttagtgaag gtaaactgac 2940
caggtctaat taggagtcac tagaattgaa taagcttatt tttattaata ttttttctta 3000
taactatttc tttttgtaat aatttagaaa atataattgt tctttattcc cttacagcag 3060
tataaattat tggtgcaggt aaccaaagat attactgagg agtggcatgt ttgacatgag 3120
tgacatggtt taactttgga tttttagtta atatttcttt atatattaag gatgtcttac 3180
acattataga agtcaaattt actgacaaag gtattgcctc ctcttcctcc ccaaaaacac 3240
agcaaaattc tctgggaact cgtagcattg ttggttttct tttggatgac tatggttgcc 3300
aaacaaccaa gtaattgatt ttttttaaat tattattgct ttagattata ctcacctctc 3360
atgatgcctg ttagcaatca cctttatcca tgtgtcttgt aaaatatctt tcctccttat 3420
attctttgcc caacaagagt ctacttgtta tgaatgagta ctattttctt tttttgattc 3480
cccagtataa ttagtatgtt tagtgctttc taggacttcc actttcttat gttaaaaaaa 3540
aaaacaaact aatgtggcag tcagtatatt cttactgtga atcagagtct ttactgggaa 3600
tcaaagtgaa agaagcagct gttctgactt cagagtcagc ctagggacca aaaccagcct 3660
cttaaataca ccttcattta ttcagtttgg atttgtgatg attttcatta tagctgacag 3720
ttcaaggtta ttcagtggca cacagatagc atctgcataa atgcctttct tcttgaaaat 3780
aaaggagaaa attgggaaga ctttacacca atagtttagt ctttaagtac cacagataac 3840
acacaccata aat 3853
<210> 18
<211> 764
<212> PRT
<213> Bos taurus
<400> 18
Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu Gln
1 5 10 15
Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala Ala
20 25 30
Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn Ile
35 40 45
Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu Asp
50 55 60
Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala Tyr
65 70 75 80
Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln Gln
85 90 95
Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser Ser
100 105 110
Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser Val
115 120 125
Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser Arg
130 135 140
Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu Pro
145 150 155 160
Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val Arg
165 170 175
Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu Cys
180 185 190
Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly Trp
195 200 205
Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu Val
210 215 220
Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr Phe
225 230 235 240
Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln Gly
245 250 255
Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser Thr
260 265 270
Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu Phe
275 280 285
Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala Ser
290 295 300
Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro Pro
305 310 315 320
Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser Lys
325 330 335
Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His Arg
340 345 350
Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val His
355 360 365
Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp Gln
370 375 380
Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr Pro
385 390 395 400
Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln Lys
405 410 415
Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp
420 425 430
Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp
435 440 445
Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser Gly
450 455 460
Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala Val
465 470 475 480
Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe
485 490 495
Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile Leu
500 505 510
Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr Gln
515 520 525
Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu Thr
530 535 540
Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln
545 550 555 560
Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu Lys
565 570 575
Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly Asp
580 585 590
Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln Phe
595 600 605
Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile Arg
610 615 620
Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe
625 630 635 640
Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn
645 650 655
Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr Leu
660 665 670
Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met Lys
675 680 685
Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro Leu
690 695 700
Phe Pro Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro
705 710 715 720
Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe
725 730 735
Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro
740 745 750
Ile Gln Ala Gly Gly Tyr Gly Thr Phe Pro Val His
755 760
<210> 19
<211> 4936
<212> ДНК
<213> Bos taurus
<400> 19
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc 60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc 120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg 180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg 240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt 300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga 360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa 420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac 480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa 540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag 600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg 660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag 720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg 780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc 840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact 900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc 960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc 1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac 1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat 1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt 1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt 1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg 1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag 1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc 1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc 1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga 1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc 1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg 1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca 1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt 1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg 1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc 1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc 1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca 2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt 2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt 2160
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag 2220
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc 2280
taaaaaagaa aagagatgaa agaccactct ttccccaagt aggaaagact ctcctaagca 2340
agagacaaaa ttcagaagtt atcagggaaa aagataagca gattctcgcc tctattgagc 2400
tgctggcccg ctcattgcca aaaattcacc gcagtgcatc agaaccctcc ttgaatcggg 2460
ctggcttcca aacagaggat tttagtctat atgcttgtgc ttctccaaaa acacccattc 2520
aggcaggggg atatgaagca gatttggctc ttacatcaaa taaaaataga gtagaagttg 2580
ggatttagag atttcctgac atgcaagaag gaataagcaa gaaaaaaagg tttgttttcc 2640
ccaaatcata tctattgtct tttacttcta ttttttctta aattttttgt gatttcagag 2700
acatgtagag ttttattgat acctaaacta tgagttcttt tttttttttt tttttcatta 2760
ttttgatttt tttggccaag aggcatatgg gatcttagct tgagaaagca acaattttct 2820
tgatgtcatt ttgggtgagg gcacatattg ctgtgaacag tgtggtgata gccaccaggg 2880
accaaactca cacccgctgc attgaaaggt gaagtcttaa acactggacc agcagagaaa 2940
ttcctactct atgagttctt tttgtcatcc cctccccgca ccctccaccc ccaacctaaa 3000
gtctgatgat gaaatcaaca actattccat tagaagcagt agattctggt agcatgatct 3060
ttagtttgtt agtaagattt tgtgctttgt ggggttgtgt cgttttaagg ctaatattta 3120
agtttgtcaa atagaatgct gttcagattg taaaaatgag taataaacat ctgaagtttt 3180
ttttaagtta tttttaacat ggtatataca gttgagctta gagtttatca ttttctgata 3240
ttctcttact tagtagatga attctagcca ttttttataa agatttctgt taagcaaatc 3300
ctgttttcac atgggcttcc tttaagggat tttagattct gctggatatg gtgactgctc 3360
ataagactgt tgaaaattac ttttaagatg tattagaata cttctgaaaa aaaatagcaa 3420
ccttaaaacc ataagcaaaa gtagtaaggg tgtttataca tttctagagt ccctgtttag 3480
gtaatagcct cctatgattg tactttaaat gttttgctct ccaaggtttt agtaacttgg 3540
ctttttttct aatcagtgcc aaactccccc agttttttta actttaaata tgaggtaata 3600
aatcttttac ccttccttga tcttttgact tataatacct tggtcagttg tttcttaaaa 3660
ggaatcctta aatggaaaga gacaatatca ctgtctgcag ttctgattag tagttttatt 3720
cagaatggaa aaacagatta ttcatttttg aaaattgttc aggggtatgt tcattgttag 3780
gaccttggac tttggagtca gtgcctagct atgcattcca ggtctgccat tttctggctg 3840
tgaaattttg gacaagttac ttaaccactt taaaccccag ctttaagaag taaattaacc 3900
ccagtaaatt aagaagtaat agcagccact tcgtagagtt gttatgaggc tcagatgcag 3960
tgcaaatgtg tataaagtat tcagggagtc acctggtata ctataataga cactagaata 4020
gttgccaata ttatcagcat acaatctgag gattctgtca gccaatcatt agcaatctgt 4080
tgtttgttgg gacatgccag tgttctccag ttgaaatcag tagcaatcta aaaatggata 4140
gattattcct catttaaata gtgtgttcat ataagtgatt gcttggatcc ttatcagaag 4200
ttgctgttac tgaaaaatga taaggctgac taaattgtga tagttgtcag ttactaacca 4260
actcccagaa atgaataaga ggaacctatc tctagttcct agtagaaggt atggacaaaa 4320
tagtaggtga aaaataatgt cttgaacccc caaattaagt aagctttaaa gagtacaata 4380
cctcaaaggg tctttgcggt ttaaaatttg tatgctgaga atgatgttca ttgacatgtg 4440
cctatatgta attttttgat agtttaaaag gtgaaatgaa ctacagatgg gagaggtctg 4500
aattttcttg ccttcagtca aatgtgtaat gtggacatat tatttgacct gtgaatttta 4560
tcttttaaaa aagattaatt cctgcttctt ccttcctaat agttgcatta taataatgaa 4620
aatgagttga taatttgggg ggaaagtatt ctacaaatca accttattat tttaccattg 4680
gtttctgaga aattttgttc atttgaaccg tttatagctt gattagaatc atagcatgta 4740
aaacccaact gagggattat ctgcagactt aatgtagtat tatgtaagtt gtcttctttc 4800
atttcgacct tttttgcttt tgttgttgct agatctgtag tatgtagcta gtcacctttc 4860
agcgaggttt cagcgaggct tttctgtgtc tctaggttat ttgagataac ttttttaaaa 4920
ttagctcttg tcctcc 4936
<210> 20
<211> 797
<212> PRT
<213> Bos taurus
<400> 20
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr
660 665 670
Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met
675 680 685
Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro
690 695 700
Leu Phe Pro Gln Val Gly Lys Thr Leu Leu Ser Lys Arg Gln Asn Ser
705 710 715 720
Glu Val Ile Arg Glu Lys Asp Lys Gln Ile Leu Ala Ser Ile Glu Leu
725 730 735
Leu Ala Arg Ser Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser
740 745 750
Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys
755 760 765
Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly Gly Tyr Glu Ala Asp Leu
770 775 780
Ala Leu Thr Ser Asn Lys Asn Arg Val Glu Val Gly Ile
785 790 795
<210> 21
<211> 4154
<212> ДНК
<213> Bos taurus
<400> 21
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc 60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc 120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg 180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg 240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt 300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga 360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa 420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac 480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa 540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag 600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg 660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag 720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg 780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc 840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact 900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc 960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc 1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac 1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat 1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt 1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt 1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg 1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag 1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc 1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc 1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga 1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc 1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg 1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca 1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt 1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg 1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc 1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc 1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca 2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt 2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt 2160
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag 2220
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc 2280
taaaaaagaa aagagatgaa agaccactct ttccccaagt aggaaagact ctcctaagca 2340
agagacaaaa ttcagaagtt atcagggaaa aagataagca gattctcgcc tctattgagc 2400
tgctggcccg ctcattgcca aaaattcacc gcagtgcatc agaaccctcc ttgaatcggg 2460
ctggcttcca aacagaggat tttagtctat atgcttgtgc ttctccaaaa acacccattc 2520
aggcaggggg atatggctga gcacattgtc catcacccac aagtggctgg ttctcatcgc 2580
agaatctacg tagggaatcg ggcgtgaaat tcacttaaga gatagagcag aggaagtgtt 2640
ctgtttacag gaatggagat gagagttatg agtaagttgc ttagtcagtt ggctttgttt 2700
tgaaaattat tgtgttatat ttgtgttaac ctacttgtgt tttgacagta tatgtcacat 2760
aggaagaaac ctcagactag cataataaca aagctcagac taggcacaga tgtacacaga 2820
atggaccaaa atgggatggg ggaaggtatg ggaataagtc taggggtagg gaaaaattga 2880
tgtgagggtg ggaaataaac tgtaattacc tgaaataaaa tgtaagagtg caataagtgt 2940
gctttttatt ctaagctgtg aatgggtttt ttaaaaaaag cattccttcc caatgcattt 3000
gcctatgttc catagctgat taaaaccagc tatataaaca tatgcctttt tattcatgtt 3060
aattaccaat ataaatggct aacctttacg tcttatttat cttcatgtta tgttagttta 3120
catacaggga tgtgtgtgtg tgtgtatgct ataaattttc cctccttcgt ttaaaaacgc 3180
gtttgttgga tcctctctgt ttccttaggc catgccacag ctcatagtct cagcttggcc 3240
ttcctgtcac ctgatctgaa ggactatcac agtgacgtag ctcgttcatt ggttgtacac 3300
actctaaccc ttttccttgc tcagcaatta ctgtgtcttc taaaacagga gtgtacaacc 3360
atgagattgc aattaattgt ttgacatatg tccctttgaa ttctatttat tagttatgat 3420
tgattgctct ttggtttgga ccaagaaaaa cgaaatccca cctccccacc ttttcactta 3480
tttcttactt tgaggacaat tctgtaagag agaggaaagg gaactccttc atgttttaac 3540
tgcagcaagt taatggccct ggtttacacc aaacattatg gtgattcaca ttcacattcc 3600
tctcctctct tgctgccaga ggtttgggtt ttgttcagtt ctgctcaagc actgaaaaag 3660
ttttcatgga gtctggagag tgcccagtga aaagatggtt tttaattgtc cacagacctt 3720
tctgttcctg ctttgcaaaa attacaaagg agtaactatt tttaaagctt atttttcaat 3780
tcataaaaaa gacatttatt ttcagtcaga tgatgtctcc ttgtccctta atcctcaatg 3840
tttgcttgaa tctttttttt ttttctgatt ttctcccatc cccacttctt gatacttctt 3900
gagttctctt tcctgctcag gtcctttcat ttgtactttg gagttttttc tcatgtaaat 3960
ttgtacaatg gaaaatattg ttcagtttgg atagaacgca tggagaatta aataaaaaag 4020
atagctgaaa ttcagattga aatttatttg tgtaaagtta tttaaaaact ctgtactata 4080
taaaaggcaa aaaaagttct atgtacttga tgtgaatatg cgaatactgc tataataaag 4140
attgactgca tgga 4154
<210> 22
<211> 781
<212> PRT
<213> Bos taurus
<400> 22
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr
660 665 670
Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met
675 680 685
Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro
690 695 700
Leu Phe Pro Gln Val Gly Lys Thr Leu Leu Ser Lys Arg Gln Asn Ser
705 710 715 720
Glu Val Ile Arg Glu Lys Asp Lys Gln Ile Leu Ala Ser Ile Glu Leu
725 730 735
Leu Ala Arg Ser Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser
740 745 750
Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys
755 760 765
Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly Gly Tyr Gly
770 775 780
<210> 23
<211> 7914
<212> ДНК
<213> Bos taurus
<400> 23
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc 60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc 120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg 180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg 240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt 300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga 360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa 420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac 480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa 540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag 600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg 660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag 720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg 780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc 840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact 900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc 960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc 1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac 1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat 1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt 1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt 1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg 1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag 1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc 1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc 1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga 1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc 1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg 1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca 1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt 1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg 1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc 1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc 1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca 2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt 2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt 2160
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag 2220
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc 2280
taaaaaagaa aagagatgaa agaccactct ttccccaaat tctcgcctct attgagctgc 2340
tggcccgctc attgccaaaa attcaccgca gtgcatcaga accctccttg aatcgggctg 2400
gcttccaaac agaggatttt agtctatatg cttgtgcttc tccaaaaaca cccattcagg 2460
cagggggata tggagaattt gcagccttca agtagccaca ccatcatgac agcatctact 2520
cttatttctt aagtcttgtg ttcgtacaat ttgttaacat caaaacacag ttctgttcct 2580
caactctttt taaagttaaa atttttcagt gcataagctg gtgtggaaca gaaggaaatt 2640
tcccatccaa caaaagaggg aagaatgttt taggaaccag aattctctgc tgccagtgtt 2700
tcttcttcaa cacaaatatc acaagtctgc ccactcccag gaagaaagag gagagaccct 2760
gagttctgac cttttgatgg tcaggcatga tggaaagaaa ctgctgctac agcttgggag 2820
atttgctctg ggaagtctgc cagtcaactt tgcccttcta accaccagat caatatgtgg 2880
ctgatcatct gatggggcag ttgcaatcac caagccttgt tctctttcct gttctgggat 2940
tgtgttgtgg aacccttttc cctagccacc accagttcat ttctgaggga tggaacaaaa 3000
atgcagcatg cccttcctgt gtggtgcatg ttcagtcctt gacaaatttt taccaaaatg 3060
aagctacttt atttaaaagg agggtgagag gtgaggaggt cactttgggt gtggcggaaa 3120
gggaatgctg catctttttc ctgggctgct ggggctctgg ccttggcttg ccagccggaa 3180
gcgctggcac gcatcgcctt cttttcccat tgggtccagc aatgaagacg agtgtttggg 3240
gttttttttt tctccaccat gtagcaagtt ctcaggaaaa tacaattgat atcttcctcc 3300
taagctcttc caatcagtca ccaagtactt atgtggttac tttgtccagg gcacaaaatg 3360
cctgtatcta attaaaagcc tacaaaactg cttgataaca gttttgaatg tgagacattt 3420
atgtaattta aatgtaaggt acaagtttta atttctgagt ttcttctatt atatttttat 3480
taaaaaaaga aaataatttt cagattgaat tggagtaaaa taatattact tcccactaga 3540
attatatatc ctggaaaatt gtatttttgt tacataagca gcttttaaag aaagatcatt 3600
acccttttct ctacataaat atatggggag tcttagccta atgacaaata tttataattt 3660
ttaaattaat ggtacttgct ggatccatac taacatcttt actaatacct cattgtttct 3720
tccaacttac tcctacacta catcctacat cttcttccta gtcttttatc tagaatatgc 3780
aacctcaaat aaaaatggtg gtgtcctcat tcattctcct ccttcctttt ttcccaagcc 3840
tgatcttcaa aaggttggtt aatttggcag ctgagttcct ccccaggcag agaatagacc 3900
aattttaggt gtattgggac tgagggagga tgtgtaaaga ttaacatcag taaagaaccg 3960
ctgtggagta attaagaact ttgttcttta taactggaga atataaccta accctaacat 4020
ccctcagcct ttactaaagt gtggcgtaaa tcacagtagt agcaaagaaa gtgactctgg 4080
atgtgttcct ggccagtacc tcccttatca tgaatgtaga ctctctcatc aagatttagg 4140
aatataaatc aaatcaaatg tgcccagcca agctatgtag taagggactt gaacaatatt 4200
aggcagaacc tataaaataa atcagggaat tagaaattat ttaaagtttt caaattgtaa 4260
attgccccgg tgtctttcag cctactgcca ttatttttgc tacaatacct acatttcaga 4320
ggagggccta ctgaaaattc catgcaagtg gaaaataatc ctcaagttat taatgagttt 4380
gaaaagcaat gagttcttaa gtctttgtga gtagagcaag atcctacaaa attcagaaat 4440
agtaaaaatg gattcatgct gatttgaaga gcatctgtgt gcataatata atgctgcatc 4500
tcttttaaaa gcagtctatt tttcttttta aatttgtccc catagatgct tttgaacatg 4560
aacatgctta tgttaccttt tccgaggttg ggaagagcca ggagctctca ggcagggccc 4620
cctccctcag ctgggcagga gctgctcagg aggagctagt tatagaggaa gcttagcgtt 4680
ggcattttca aaattcaagg tgataacgct ttcttcttcc tttctgtttt agaatagatt 4740
gctgtctgat ttgaaaaagg gaaatagatt tgatctcaaa tgaatctgtg cccagaagcc 4800
aggctcaggg tattcagaga tttgtatagt gccctcaaaa aataacaaaa ttttagcttt 4860
ccttttttct tcttttctcc atcaaattct tttttctcta gtttacaaat gacatggaaa 4920
aggaatttcc cctgagtttt gtatgccttt ttttttttgg cttagactat agataggcgt 4980
gttgagctcc taagaaaata caaggaggaa ctctttgttg tgcagagcac tttatgagta 5040
gtttgtgtgg ataatatgtg actgcttccc tgacgagctt gtgaggctgt acttatgtct 5100
ttcctgtaag gcagcttcag tgccttctgt agtgtatata aggaaagatt acgccttctg 5160
aaaaatctca gagcaaccat aagattattt taaaatatgt agtatgactg atggactttt 5220
tcatcattaa attagtctag catctaaact tttaccactg aaataatatt gaccaaaaag 5280
caatttataa aaggtatttg tgaatagaaa atacaatgtg atcatttgta cttatgtgca 5340
ccttaaaaga ggaattctgt ctagctgtca aattctggtt ccttaacatc cagtccttga 5400
ttgtgattga gatctggtag gacgtgctgg ggcacgctag cagataaaat cccgtatact 5460
ttaggataga tgttacattt atgtcagtgt tggcaaagag cattgtgtag taataaagaa 5520
ttcaagactt cagcaatgtc aacctgaaac tttgtaaata tttcctagat tgttatttga 5580
tgcagtcaca gctctttatc acacaatgtt gtctttccct catcaggcaa ttttagaact 5640
gctgcacacc cctcctcaga tctcacctgc ccctcctgta cattcacctc tccagccttg 5700
tgcacacctc atttagcttt agtttgaaac acattgcagg gttcaggtga cctcttcaaa 5760
aactacctcc tcagaatgag gtaatgaata gttatttatt ttaaaatatg aaaagtcagg 5820
agctctagaa tatgaagatg atctaagatt ttaactttta tgtatacttg ttgagcactc 5880
tccttttgtc ctaaagggca ttatacattt aagcagtaat actgaaaaat gtagctcaga 5940
gtaactgaat gttgttgaaa gtggtgccag aatctgtttt aggggtacgt atcagaatct 6000
taatcttaaa tcggttacat gaaattaaat agttaatggt aacacttgac taacagatat 6060
aattttaatt ttcggtaggc ttttagcaag acagtaagta catcttcata atgagttagc 6120
cacagcttca tcacatgcac agattttcct gttgagagac tgcccagtta agagggtaga 6180
atgatgaacc atttttcagg attctcttct ttgtccaaac tggcattgtg agtgctagaa 6240
tatcagcact ttcaaactag tgattccaac tattaggcta ttaaaaagca aaacaaacca 6300
aacaaaccat agccagacat gggaagttta ctatgagtat aaacagcaaa tagcttacag 6360
gtcatacatt gaaatggtgt aggtaaggcg ttagaaaaat accttgacaa tttgccaaat 6420
gatcttactg tgccttcatg atgcaataaa aaaaaaaaaa atttagcata aatcagtgat 6480
ttgtgaagag agcagccacc ctggtctaac tcagctgtgt taatattttt tagcgtgcaa 6540
tttagactgc aaagataaat gcactaaaga gtttatagcc aaaatcacat ttaaaaaatg 6600
agagaaaaca caggtaaatt ttcagtgaac aaaattattt ttttaaagta cataatccct 6660
agtatagtca gatatattta tcacatagag caaataggtt gaaatcacaa ttcagtgaca 6720
tttctagaga aactttttct actcccatag gttcttcaaa gcatggaact tttatataac 6780
agaaatgtgt gacggtcatt ttaaattgct gtagtttggg gctgaagtac tgtgtgctgg 6840
gcagcaatca catgtattaa ctagtgagaa aggagaaatt aagatatagg acagaatttg 6900
attttcttgt tcccagatta ctgctgccaa cctagacact gagtttccag aggctgaaac 6960
gtaaacttgc agctcagcaa ctgttttgca aagttagtgg gactgtcctg cttatgctgt 7020
tcaaaaatgc tctgagggcc aggtggggcc tccaggggct cctctctgag gggacatcag 7080
actagctaac gacctggcgg gcggatgtga accggacaca ctccatggtg tgcttcttgt 7140
atcggtccct cgccaccctc aagaaaggct tcagcgggtt ctctagacgt ctccactaag 7200
gtgtgttact aacagccatg ggttgttgag cacccgagga gtgcaatagc atctctgcat 7260
gattgtatat tggcccgaag agaatgaagt ggccagtgta ctcatgttcc atgttgctag 7320
ctctggtaaa ctgaaaatac tggtaagatt tttgttttat cagtacacta gagagtaagc 7380
tttgttttgt tgtttttaga taatgttttc acttccattt ggaaagacat ttaaattgag 7440
tttcagtcct aaattttgcc agtcatggta attagcagtt tctatcaggt atttttaagg 7500
tagaagagga tagaaacata agttctaaaa gcttaaggta accgtggttt attttaaaat 7560
gtttaggggt ggttagtctc tacctcaaaa aaagtgagtg aatcttttat ttcagcattc 7620
acaagttcgg ctgttgtttt tgtaatacat ttttttttta accttttgac ccccctttac 7680
ctaagtgtca atgtagtttt attaattact aagtcagttt cattaaaatg tttatttagc 7740
agttttgact aattgcaatg attaatatag ccagttgtgc atgaggacac agccagtgag 7800
tatatctggg ttttttttgt gatgcttttt ttcttaagac ttctgtagat ttatgaagta 7860
ctcattgaaa acaactaaaa tacgtttatt cgtgttaata tggaaaaaaa aaaa 7914
<210> 24
<211> 766
<212> PRT
<213> Bos taurus
<400> 24
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr
660 665 670
Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met
675 680 685
Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro
690 695 700
Leu Phe Pro Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser Leu
705 710 715 720
Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala Gly
725 730 735
Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys Thr
740 745 750
Pro Ile Gln Ala Gly Gly Tyr Gly Glu Phe Ala Ala Phe Lys
755 760 765
<210> 25
<211> 4670
<212> ДНК
<213> Bos taurus
<400> 25
ggtgtgtcat agtgcagcag attgaatgca gaagatatga aaattcagat gtcttctgtt 60
aaggtgtgga atatcaaaca aatgattaag ttgacacagg agcatataga ggccctattg 120
gacaaatttg gtggggagca taatccacca tcaatatatc tggaggccta tgaagaatac 180
accagcaagc tagatgccct ccaacaaaga gaacaacagt tattggaatc cctggggaat 240
ggaactgatt tttctgtttc tagctctgca tcaacggaca ccgttacatc ttcttcctct 300
tctagccttt cagtgctgcc ttcatctctt tcagtttttc aaaatcccac agatgtgtca 360
cggagcaacc ccaagtcacc acaaaaacct atcgttagag tcttcctgcc caataaacag 420
aggacagtgg tacctgcacg gtgtggagtc acagtccggg acagcctgaa gaaggcactg 480
atgatgagag gtctaatccc agagtgctgt gctgtttaca gaattcagga tggggagaag 540
aaaccaattg gctgggacac tgatatttcc tggcttactg gagaggagtt gcatgtagaa 600
gtgttggaga atgttccact tacaacacac aactttgtac ggaaaacttt tttcacctta 660
gcattttgtg acttctgtag aaagctgctt ttccagggat tccgctgtca aacatgtggt 720
tataaatttc accagcgttg tagtacagag gttccactga tgtgtgttaa ttatgaccaa 780
ctagatttgc tgtttgtctc caagttcttt gaacaccacc caataccaca ggaggaggcc 840
tccttagcag agactaccct tccatgtggc tcatcccctt ctgcaccccc ctccgattct 900
attgggcccc caattctcac cagtccatct ccttcaaaat ccattccaat tccacagcct 960
ttccgaccag cagatgaaga tcatcgaaat cagtttggac aacgagaccg gtcctcatca 1020
gctccaaatg tgcatataaa cacaatagaa cccgtcaata ttgatgactt gattagagac 1080
caagggtttc gtagtgatgg aggatcaacc acaggtttat ccgccacacc ccctgcctca 1140
ttacctggct cactctctaa tgtgaaagca ttgcagaaat ctccaggacc tcagcgagaa 1200
agaaagtcct cttcatcctc agaagacagg aatcgaatga aaacgcttgg tagacgggat 1260
tcaagtgacg attgggagat tcctgatgga cagatcacag tgggacaaag aattggatca 1320
gggtcatttg ggacagtcta caagggaaag tggcatggtg atgtggcagt gaaaatgttg 1380
aatgtgacag cacccacacc tcagcagtta caggccttca aaaatgaagt aggagtactc 1440
aggaaaacgc gacatgtgaa tatcctcctc ttcatgggtt attcaacaaa gccacaactg 1500
gctattgtta cccagtggtg tgagggctcc agtttatatc atcatctcca catcattgag 1560
accaaattcg agatgatcaa acttatagat attgcacggc agactgcaca gggcatggat 1620
tacttacacg ccaagtcaat catccacaga gacctcaaga gtaataatat ttttcttcat 1680
gaagacctca cagtaaaaat aggtgatttt ggtctagcca cagtgaaatc tcgatggagt 1740
gggtcccatc agtttgaaca gttgtctgga tccattttgt ggatggcacc agaagtaatc 1800
agaatgcaag ataaaaaccc atatagcttt cagtcagatg tatatgcatt tgggattgtt 1860
ctgtatgaat tgatgaccgg acagttacct tattcaaata tcaacaacag ggaccagata 1920
atttttatgg tgggacgagg atatctgtct ccagatctca gtaaggtacg gagtaactgt 1980
ccaaaagcca tgaagagatt aatggcagag tgcctaaaaa agaaaagaga tgaaagacca 2040
ctctttcccc aagtaggaaa gactctccta agcaagagac aaaattcaga agttatcagg 2100
gaaaaagata agcagattct cgcctctatt gagctgctgg cccgctcatt gccaaaaatt 2160
caccgcagtg catcagaacc ctccttgaat cgggctggct tccaaacaga ggattttagt 2220
ctatatgctt gtgcttctcc aaaaacaccc attcaggcag ggggatatga agcagatttg 2280
gctcttacat caaataaaaa tagagtagaa gttgggattt agagatttcc tgacatgcaa 2340
gaaggaataa gcaagaaaaa aaggtttgtt ttccccaaat catatctatt gtcttttact 2400
tctatttttt cttaaatttt ttgtgatttc agagacatgt agagttttat tgatacctaa 2460
actatgagtt cttttttttt tttttttttc attattttga tttttttggc caagaggcat 2520
atgggatctt agcttgagaa agcaacaatt ttcttgatgt cattttgggt gagggcacat 2580
attgctgtga acagtgtggt gatagccacc agggaccaaa ctcacacccg ctgcattgaa 2640
aggtgaagtc ttaaacactg gaccagcaga gaaattccta ctctatgagt tctttttgtc 2700
atcccctccc cgcaccctcc acccccaacc taaagtctga tgatgaaatc aacaactatt 2760
ccattagaag cagtagattc tggtagcatg atctttagtt tgttagtaag attttgtgct 2820
ttgtggggtt gtgtcgtttt aaggctaata tttaagtttg tcaaatagaa tgctgttcag 2880
attgtaaaaa tgagtaataa acatctgaag ttttttttaa gttattttta acatggtata 2940
tacagttgag cttagagttt atcattttct gatattctct tacttagtag atgaattcta 3000
gccatttttt ataaagattt ctgttaagca aatcctgttt tcacatgggc ttcctttaag 3060
ggattttaga ttctgctgga tatggtgact gctcataaga ctgttgaaaa ttacttttaa 3120
gatgtattag aatacttctg aaaaaaaata gcaaccttaa aaccataagc aaaagtagta 3180
agggtgttta tacatttcta gagtccctgt ttaggtaata gcctcctatg attgtacttt 3240
aaatgttttg ctctccaagg ttttagtaac ttggcttttt ttctaatcag tgccaaactc 3300
ccccagtttt tttaacttta aatatgaggt aataaatctt ttacccttcc ttgatctttt 3360
gacttataat accttggtca gttgtttctt aaaaggaatc cttaaatgga aagagacaat 3420
atcactgtct gcagttctga ttagtagttt tattcagaat ggaaaaacag attattcatt 3480
tttgaaaatt gttcaggggt atgttcattg ttaggacctt ggactttgga gtcagtgcct 3540
agctatgcat tccaggtctg ccattttctg gctgtgaaat tttggacaag ttacttaacc 3600
actttaaacc ccagctttaa gaagtaaatt aaccccagta aattaagaag taatagcagc 3660
cacttcgtag agttgttatg aggctcagat gcagtgcaaa tgtgtataaa gtattcaggg 3720
agtcacctgg tatactataa tagacactag aatagttgcc aatattatca gcatacaatc 3780
tgaggattct gtcagccaat cattagcaat ctgttgtttg ttgggacatg ccagtgttct 3840
ccagttgaaa tcagtagcaa tctaaaaatg gatagattat tcctcattta aatagtgtgt 3900
tcatataagt gattgcttgg atccttatca gaagttgctg ttactgaaaa atgataaggc 3960
tgactaaatt gtgatagttg tcagttacta accaactccc agaaatgaat aagaggaacc 4020
tatctctagt tcctagtaga aggtatggac aaaatagtag gtgaaaaata atgtcttgaa 4080
cccccaaatt aagtaagctt taaagagtac aatacctcaa agggtctttg cggtttaaaa 4140
tttgtatgct gagaatgatg ttcattgaca tgtgcctata tgtaattttt tgatagttta 4200
aaaggtgaaa tgaactacag atgggagagg tctgaatttt cttgccttca gtcaaatgtg 4260
taatgtggac atattatttg acctgtgaat tttatctttt aaaaaagatt aattcctgct 4320
tcttccttcc taatagttgc attataataa tgaaaatgag ttgataattt ggggggaaag 4380
tattctacaa atcaacctta ttattttacc attggtttct gagaaatttt gttcatttga 4440
accgtttata gcttgattag aatcatagca tgtaaaaccc aactgaggga ttatctgcag 4500
acttaatgta gtattatgta agttgtcttc tttcatttcg accttttttg cttttgttgt 4560
tgctagatct gtagtatgta gctagtcacc tttcagcgag gtttcagcga ggcttttctg 4620
tgtctctagg ttatttgaga taactttttt aaaattagct cttgtcctcc 4670
<210> 26
<211> 761
<212> PRT
<213> Bos taurus
<400> 26
Met Lys Ile Gln Met Ser Ser Val Lys Val Trp Asn Ile Lys Gln Met
1 5 10 15
Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu Asp Lys Phe Gly
20 25 30
Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala Tyr Glu Glu Tyr
35 40 45
Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln Gln Leu Leu Glu
50 55 60
Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser Ser Ala Ser Thr
65 70 75 80
Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser Val Leu Pro Ser
85 90 95
Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser Arg Ser Asn Pro
100 105 110
Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu Pro Asn Lys Gln
115 120 125
Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val Arg Asp Ser Leu
130 135 140
Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu Cys Cys Ala Val
145 150 155 160
Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly Trp Asp Thr Asp
165 170 175
Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu Val Leu Glu Asn
180 185 190
Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr Phe Phe Thr Leu
195 200 205
Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln Gly Phe Arg Cys
210 215 220
Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser Thr Glu Val Pro
225 230 235 240
Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu Phe Val Ser Lys
245 250 255
Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala Ser Leu Ala Glu
260 265 270
Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro Pro Ser Asp Ser
275 280 285
Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser Lys Ser Ile Pro
290 295 300
Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His Arg Asn Gln Phe
305 310 315 320
Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val His Ile Asn Thr
325 330 335
Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp Gln Gly Phe Arg
340 345 350
Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr Pro Pro Ala Ser
355 360 365
Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln Lys Ser Pro Gly
370 375 380
Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn Arg
385 390 395 400
Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro
405 410 415
Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly
420 425 430
Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala Val Lys Met Leu
435 440 445
Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu
450 455 460
Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe Met
465 470 475 480
Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys Glu
485 490 495
Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu Thr Lys Phe Glu
500 505 510
Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met Asp
515 520 525
Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn Asn
530 535 540
Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu
545 550 555 560
Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu
565 570 575
Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln Asp
580 585 590
Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile Val
595 600 605
Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn
610 615 620
Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr Leu Ser Pro Asp
625 630 635 640
Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met Lys Arg Leu Met
645 650 655
Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln
660 665 670
Val Gly Lys Thr Leu Leu Ser Lys Arg Gln Asn Ser Glu Val Ile Arg
675 680 685
Glu Lys Asp Lys Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser
690 695 700
Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala
705 710 715 720
Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys
725 730 735
Thr Pro Ile Gln Ala Gly Gly Tyr Glu Ala Asp Leu Ala Leu Thr Ser
740 745 750
Asn Lys Asn Arg Val Glu Val Gly Ile
755 760
<210> 27
<211> 4816
<212> ДНК
<213> Bos taurus
<400> 27
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc 60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc 120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg 180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg 240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt 300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga 360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa 420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac 480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa 540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag 600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg 660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag 720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg 780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc 840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact 900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc 960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc 1020
cactgatgtg tgttaattat gaccaactag agcccccaat tctcaccagt ccatctcctt 1080
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt 1140
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg 1200
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag 1260
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc 1320
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc 1380
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga 1440
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc 1500
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg 1560
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca 1620
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt 1680
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg 1740
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc 1800
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc 1860
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca 1920
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt 1980
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt 2040
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag 2100
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc 2160
taaaaaagaa aagagatgaa agaccactct ttccccaagt aggaaagact ctcctaagca 2220
agagacaaaa ttcagaagtt atcagggaaa aagataagca gattctcgcc tctattgagc 2280
tgctggcccg ctcattgcca aaaattcacc gcagtgcatc agaaccctcc ttgaatcggg 2340
ctggcttcca aacagaggat tttagtctat atgcttgtgc ttctccaaaa acacccattc 2400
aggcaggggg atatgaagca gatttggctc ttacatcaaa taaaaataga gtagaagttg 2460
ggatttagag atttcctgac atgcaagaag gaataagcaa gaaaaaaagg tttgttttcc 2520
ccaaatcata tctattgtct tttacttcta ttttttctta aattttttgt gatttcagag 2580
acatgtagag ttttattgat acctaaacta tgagttcttt tttttttttt tttttcatta 2640
ttttgatttt tttggccaag aggcatatgg gatcttagct tgagaaagca acaattttct 2700
tgatgtcatt ttgggtgagg gcacatattg ctgtgaacag tgtggtgata gccaccaggg 2760
accaaactca cacccgctgc attgaaaggt gaagtcttaa acactggacc agcagagaaa 2820
ttcctactct atgagttctt tttgtcatcc cctccccgca ccctccaccc ccaacctaaa 2880
gtctgatgat gaaatcaaca actattccat tagaagcagt agattctggt agcatgatct 2940
ttagtttgtt agtaagattt tgtgctttgt ggggttgtgt cgttttaagg ctaatattta 3000
agtttgtcaa atagaatgct gttcagattg taaaaatgag taataaacat ctgaagtttt 3060
ttttaagtta tttttaacat ggtatataca gttgagctta gagtttatca ttttctgata 3120
ttctcttact tagtagatga attctagcca ttttttataa agatttctgt taagcaaatc 3180
ctgttttcac atgggcttcc tttaagggat tttagattct gctggatatg gtgactgctc 3240
ataagactgt tgaaaattac ttttaagatg tattagaata cttctgaaaa aaaatagcaa 3300
ccttaaaacc ataagcaaaa gtagtaaggg tgtttataca tttctagagt ccctgtttag 3360
gtaatagcct cctatgattg tactttaaat gttttgctct ccaaggtttt agtaacttgg 3420
ctttttttct aatcagtgcc aaactccccc agttttttta actttaaata tgaggtaata 3480
aatcttttac ccttccttga tcttttgact tataatacct tggtcagttg tttcttaaaa 3540
ggaatcctta aatggaaaga gacaatatca ctgtctgcag ttctgattag tagttttatt 3600
cagaatggaa aaacagatta ttcatttttg aaaattgttc aggggtatgt tcattgttag 3660
gaccttggac tttggagtca gtgcctagct atgcattcca ggtctgccat tttctggctg 3720
tgaaattttg gacaagttac ttaaccactt taaaccccag ctttaagaag taaattaacc 3780
ccagtaaatt aagaagtaat agcagccact tcgtagagtt gttatgaggc tcagatgcag 3840
tgcaaatgtg tataaagtat tcagggagtc acctggtata ctataataga cactagaata 3900
gttgccaata ttatcagcat acaatctgag gattctgtca gccaatcatt agcaatctgt 3960
tgtttgttgg gacatgccag tgttctccag ttgaaatcag tagcaatcta aaaatggata 4020
gattattcct catttaaata gtgtgttcat ataagtgatt gcttggatcc ttatcagaag 4080
ttgctgttac tgaaaaatga taaggctgac taaattgtga tagttgtcag ttactaacca 4140
actcccagaa atgaataaga ggaacctatc tctagttcct agtagaaggt atggacaaaa 4200
tagtaggtga aaaataatgt cttgaacccc caaattaagt aagctttaaa gagtacaata 4260
cctcaaaggg tctttgcggt ttaaaatttg tatgctgaga atgatgttca ttgacatgtg 4320
cctatatgta attttttgat agtttaaaag gtgaaatgaa ctacagatgg gagaggtctg 4380
aattttcttg ccttcagtca aatgtgtaat gtggacatat tatttgacct gtgaatttta 4440
tcttttaaaa aagattaatt cctgcttctt ccttcctaat agttgcatta taataatgaa 4500
aatgagttga taatttgggg ggaaagtatt ctacaaatca accttattat tttaccattg 4560
gtttctgaga aattttgttc atttgaaccg tttatagctt gattagaatc atagcatgta 4620
aaacccaact gagggattat ctgcagactt aatgtagtat tatgtaagtt gtcttctttc 4680
atttcgacct tttttgcttt tgttgttgct agatctgtag tatgtagcta gtcacctttc 4740
agcgaggttt cagcgaggct tttctgtgtc tctaggttat ttgagataac ttttttaaaa 4800
ttagctcttg tcctcc 4816
<210> 28
<211> 757
<212> PRT
<213> Bos taurus
<400> 28
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Glu Pro Pro
275 280 285
Ile Leu Thr Ser Pro Ser Pro Ser Lys Ser Ile Pro Ile Pro Gln Pro
290 295 300
Phe Arg Pro Ala Asp Glu Asp His Arg Asn Gln Phe Gly Gln Arg Asp
305 310 315 320
Arg Ser Ser Ser Ala Pro Asn Val His Ile Asn Thr Ile Glu Pro Val
325 330 335
Asn Ile Asp Asp Leu Ile Arg Asp Gln Gly Phe Arg Ser Asp Gly Gly
340 345 350
Ser Thr Thr Gly Leu Ser Ala Thr Pro Pro Ala Ser Leu Pro Gly Ser
355 360 365
Leu Ser Asn Val Lys Ala Leu Gln Lys Ser Pro Gly Pro Gln Arg Glu
370 375 380
Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn Arg Met Lys Thr Leu
385 390 395 400
Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp Gly Gln Ile
405 410 415
Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr Val Tyr Lys
420 425 430
Gly Lys Trp His Gly Asp Val Ala Val Lys Met Leu Asn Val Thr Ala
435 440 445
Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val Gly Val Leu
450 455 460
Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe Met Gly Tyr Ser Thr
465 470 475 480
Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly Ser Ser Leu
485 490 495
Tyr His His Leu His Ile Ile Glu Thr Lys Phe Glu Met Ile Lys Leu
500 505 510
Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr Leu His Ala
515 520 525
Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile Phe Leu His
530 535 540
Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala Thr Val Lys
545 550 555 560
Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser Gly Ser Ile
565 570 575
Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys Asn Pro Tyr
580 585 590
Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu Tyr Glu Leu
595 600 605
Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg Asp Gln Ile
610 615 620
Ile Phe Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu Ser Lys Val
625 630 635 640
Arg Ser Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala Glu Cys Leu
645 650 655
Lys Lys Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Val Gly Lys Thr
660 665 670
Leu Leu Ser Lys Arg Gln Asn Ser Glu Val Ile Arg Glu Lys Asp Lys
675 680 685
Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro Lys Ile
690 695 700
His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe Gln Thr
705 710 715 720
Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro Ile Gln
725 730 735
Ala Gly Gly Tyr Glu Ala Asp Leu Ala Leu Thr Ser Asn Lys Asn Arg
740 745 750
Val Glu Val Gly Ile
755
<210> 29
<211> 2499
<212> ДНК
<213> Bos taurus
<400> 29
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc 60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc 120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg 180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg 240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt 300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga 360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa 420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac 480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa 540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag 600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg 660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag 720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg 780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc 840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact 900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc 960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc 1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac 1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat 1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt 1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt 1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg 1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag 1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc 1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc 1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga 1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc 1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg 1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca 1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt 1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg 1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc 1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc 1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca 2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt 2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt 2160
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag 2220
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc 2280
taaaaaagaa aagagatgaa agaccactct ttccccaagt aggaaagact ctcctaagca 2340
agagacaaaa ttcagaagtt atcagggaaa aagataagca ggaaaagtat gtttctttag 2400
tacattccag gcatttggga ttacagtaaa aacaatattc tcgcctctat tgagctgctg 2460
gcccgctcat tgccaaaaat tcaccgcagt gcatcagaa 2499
<210> 30
<211> 744
<212> PRT
<213> Bos taurus
<400> 30
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr
660 665 670
Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met
675 680 685
Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro
690 695 700
Leu Phe Pro Gln Val Gly Lys Thr Leu Leu Ser Lys Arg Gln Asn Ser
705 710 715 720
Glu Val Ile Arg Glu Lys Asp Lys Gln Glu Lys Tyr Val Ser Leu Val
725 730 735
His Ser Arg His Leu Gly Leu Gln
740
<210> 31
<211> 2404
<212> ДНК
<213> Bos taurus
<400> 31
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc 60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc 120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg 180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg 240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt 300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga 360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa 420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac 480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa 540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag 600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg 660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag 720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg 780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc 840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact 900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc 960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc 1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac 1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat 1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt 1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt 1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg 1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag 1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc 1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc 1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga 1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc 1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg 1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca 1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt 1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg 1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc 1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc 1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca 2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt 2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt 2160
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag 2220
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc 2280
taaaaaagaa aagagatgaa agaccactct ttccccaaga tctctcttcc caccatagac 2340
acaaaaattt cagatggcta caggtttaca tgtaaaaaac agaattataa caaatgattt 2400
ttat 2404
<210> 32
<211> 726
<212> PRT
<213> Bos taurus
<400> 32
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr
660 665 670
Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met
675 680 685
Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro
690 695 700
Leu Phe Pro Gln Asp Leu Ser Ser His His Arg His Lys Asn Phe Arg
705 710 715 720
Trp Leu Gln Val Tyr Met
725
<210> 33
<211> 2331
<212> ДНК
<213> Bos taurus
<400> 33
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc 60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc 120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg 180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg 240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt 300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga 360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa 420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac 480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa 540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag 600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg 660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag 720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg 780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc 840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact 900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc 960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc 1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac 1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat 1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt 1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt 1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg 1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag 1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc 1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc 1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga 1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc 1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg 1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca 1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt 1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg 1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc 1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc 1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca 2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt 2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt 2160
caaatatcaa caacagggac caggtgcttt gtcctccatg ggagtgtaat aaatgctgtg 2220
caagggctta cttcccatga gagaagtgag tgaccaacag aaggataatt tttatggtgg 2280
gacgaggata tctgtctcca gatctcagta aggtacggag taactgtcca a 2331
<210> 34
<211> 681
<212> PRT
<213> Bos taurus
<400> 34
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Val Leu Cys Pro Pro Trp Glu Cys Asn
660 665 670
Lys Cys Cys Ala Arg Ala Tyr Phe Pro
675 680
<210> 35
<211> 2319
<212> ДНК
<213> Bos taurus
<400> 35
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc 60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc 120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg 180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg 240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt 300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga 360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa 420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac 480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa 540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag 600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg 660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag 720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg 780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc 840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact 900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc 960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc 1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac 1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat 1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt 1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt 1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg 1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag 1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc 1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc 1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga 1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc 1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg 1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca 1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt 1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg 1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc 1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc 1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca 2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt 2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt 2160
caaatatcaa caacagggac caggtgcttt gtcctccatg ggagtgtaat aaatgctgtg 2220
caagggctta cttcccatga gagaagtgag tgaccaacag aaggtctgtg caaggaaaag 2280
agacaaagcc acggatcaga agcacatggc cataactga 2319
<210> 36
<211> 681
<212> PRT
<213> Bos taurus
<400> 36
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Val Leu Cys Pro Pro Trp Glu Cys Asn
660 665 670
Lys Cys Cys Ala Arg Ala Tyr Phe Pro
675 680
<210> 37
<211> 2661
<212> ДНК
<213> Bos taurus
<400> 37
tcagctgcgc cgggtctcac aagacggttc ccgaggtggc ccaggcgccg tcccaccgcc 60
gacgccgccc gggccgcccg ggccgtccct ccccgctgcc ccccgtcctc cgcctccgcc 120
tccccccgcc ctcagcctcc cttccccctc cccgcccagc agcggtcgct cgggcccggc 180
tctcggttat aagatggcgg cgctgagtgg cggcggcggc ggcggcggcg gtggcgcgga 240
gcagggccag gctctgttca acggggacat ggagcccgag gccggcgccg cggcctcttc 300
ggctgcggac cccgccattc ccgaggaggt gtggaatatc aaacaaatga ttaagttgac 360
acaggagcat atagaggccc tattggacaa atttggtggg gagcataatc caccatcaat 420
atatctggag gcctatgaag aatacaccag caagctagat gccctccaac aaagagaaca 480
acagttattg gaatccctgg ggaatggaac tgatttttct gtttctagct ctgcatcaac 540
ggacaccgtt acatcttctt cctcttctag cctttcagtg ctgccttcat ctctttcagt 600
ttttcaaaat cccacagatg tgtcacggag caaccccaag tcaccacaaa aacctatcgt 660
tagagtcttc ctgcccaata aacagaggac agtggtacct gcacggtgtg gagtcacagt 720
ccgggacagc ctgaagaagg cactgatgat gagaggtcta atcccagagt gctgtgctgt 780
ttacagaatt caggatgggg agaagaaacc aattggctgg gacactgata tttcctggct 840
tactggagag gagttgcatg tagaagtgtt ggagaatgtt ccacttacaa cacacaactt 900
tgtacggaaa acttttttca ccttagcatt ttgtgacttc tgtagaaagc tgcttttcca 960
gggattccgc tgtcaaacat gtggttataa atttcaccag cgttgtagta cagaggttcc 1020
actgatgtgt gttaattatg accaactaga tttgctgttt gtctccaagt tctttgaaca 1080
ccacccaata ccacaggagg aggcctcctt agcagagact acccttccat gtggctcatc 1140
cccttctgca cccccctccg attctattgg gcccccaatt ctcaccagtc catctccttc 1200
aaaatccatt ccaattccac agcctttccg accagcagat gaagatcatc gaaatcagtt 1260
tggacaacga gaccggtcct catcagctcc aaatgtgcat ataaacacaa tagaacccgt 1320
caatattgat gacttgatta gagaccaagg gtttcgtagt gatggaggat caaccacagg 1380
tttatccgcc acaccccctg cctcattacc tggctcactc tctaatgtga aagcattgca 1440
gaaatctcca ggacctcagc gagaaagaaa gtcctcttca tcctcagaag acaggaatcg 1500
aatgaaaacg cttggtagac gggattcaag tgacgattgg gagattcctg atggacagat 1560
cacagtggga caaagaattg gatcagggtc atttgggaca gtctacaagg gaaagtggca 1620
tggtgatgtg gcagtgaaaa tgttgaatgt gacagcaccc acacctcagc agttacaggc 1680
cttcaaaaat gaagtaggag tactcaggaa aacgcgacat gtgaatatcc tcctcttcat 1740
gggttattca acaaagccac aactggctat tgttacccag tggtgtgagg gctccagttt 1800
atatcatcat ctccacatca ttgagaccaa attcgagatg atcaaactta tagatattgc 1860
acggcagact gcacagggca tggattactt acacgccaag tcaatcatcc acagagacct 1920
caagagtaat aatatttttc ttcatgaaga cctcacagta aaaataggtg attttggtct 1980
agccacagtg aaatctcgat ggagtgggtc ccatcagttt gaacagttgt ctggatccat 2040
tttgtggatg gcaccagaag taatcagaat gcaagataaa aacccatata gctttcagtc 2100
agatgtatat gcatttggga ttgttctgta tgaattgatg accggacagt taccttattc 2160
aaatatcaac aacagggacc agtctgtgca aggaaaagag acaaagccac ggatcagaag 2220
cacatggcca taactgaaga ttttgtgaac tctcacaagg aaaaaatttg ctctttgaac 2280
aataagaagg aactcactaa aatgtaactg agaactgttc aacaggttga aagctgaaag 2340
atgccattgg aactgacaaa atgtttctta aacataaatg atgaaacagt gaaactacat 2400
aatatctcct ctggctgaaa cattcaagaa gtttaaaatg cttaagttaa aaataaaatc 2460
ctagtaaaca atggacttac tgtgcaacat agagaatatc ttacgataac ctgtaatgga 2520
aaagaatctg aaaaagaatg tatataactg aatcactttg ctgtaaacta gaatctgaca 2580
caacactgta aatcactaca cttttctgtt gcatgccaaa gattatttaa taacgtcatt 2640
aaaaaattat tttaataatt a 2661
<210> 38
<211> 679
<212> PRT
<213> Bos taurus
<400> 38
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Ser Val Gln Gly Lys Glu Thr Lys Pro
660 665 670
Arg Ile Arg Ser Thr Trp Pro
675
<210> 39
<211> 7434
<212> ДНК
<213> Bos taurus
<400> 39
acaccgttac atcttcttcc tcttctagcc tttcagtgct gccttcatct ctttcagttt 60
ttcaaaatcc cacagatgtg tcacggagca accccaagtc accacaaaaa cctatcgtta 120
gagtcttcct gcccaataaa cagaggacag tggtacctgc acggtgtgga gtcacagtcc 180
gggacagcct gaagaaggca ctgatgatga gaggtctaat cccagagtgc tgtgctgttt 240
acagaattca ggatggggag aagaaaccaa ttggctggga cactgatatt tcctggctta 300
ctggagagga gttgcatgta gaagtgttgg agaatgttcc acttacaaca cacaactttg 360
tacggaaaac ttttttcacc ttagcatttt gtgacttctg tagaaagctg cttttccagg 420
gattccgctg tcaaacatgt ggttataaat ttcaccagcg ttgtagtaca gaggttccac 480
tgatgtgtgt taattatgac caactagatt tgctgtttgt ctccaagttc tttgaacacc 540
acccaatacc acaggaggag gcctccttag cagagactac ccttccatgt ggctcatccc 600
cttctgcacc cccctccgat tctattgggc ccccaattct caccagtcca tctccttcaa 660
aatccattcc aattccacag cctttccgac cagcagatga agatcatcga aatcagtttg 720
gacaacgaga ccggtcctca tcagctccaa atgtgcatat aaacacaata gaacccgtca 780
atattgatga cttgattaga gaccaagggt ttcgtagtga tggaggatca accacaggtt 840
tatccgccac accccctgcc tcattacctg gctcactctc taatgtgaaa gcattgcaga 900
aatctccagg acctcagcga gaaagaaagt cctcttcatc ctcagaagac aggaatcgaa 960
tgaaaacgct tggtagacgg gattcaagtg acgattggga gattcctgat ggacagatca 1020
cagtgggaca aagaattgga tcagggtcat ttgggacagt ctacaaggga aagtggcatg 1080
gtgatgtggc agtgaaaatg ttgaatgtga cagcacccac acctcagcag ttacaggcct 1140
tcaaaaatga agtaggagta ctcaggaaaa cgcgacatgt gaatatcctc ctcttcatgg 1200
gttattcaac aaagccacaa ctggctattg ttacccagtg gtgtgagggc tccagtttat 1260
atcatcatct ccacatcatt gagaccaaat tcgagatgat caaacttata gatattgcac 1320
ggcagactgc acagggcatg gattacttac acgccaagtc aatcatccac agagacctca 1380
agagtaataa tatttttctt catgaagacc tcacagtaaa aataggtgat tttggtctag 1440
ccacagtgaa atctcgatgg agtgggtccc atcagtttga acagttgtct ggatccattt 1500
tgtggatggc accagaagta atcagaatgc aagataaaaa cccatatagc tttcagtcag 1560
atgtatatgc atttgggatt gttctgtatg aattgatgac cggacagtta ccttattcaa 1620
atatcaacaa cagggaccag ataattttta tggtgggacg aggatatctg tctccagatc 1680
tcagtaaggt acggagtaac tgtccaaaag ccatgaagag attaatggca gagtgcctaa 1740
aaaagaaaag agatgaaaga ccactctttc cccaagtagg aaagactctc ctaagcaaga 1800
gacaaaattc agaagttatc agggaaaaag ataagcagat tctcgcctct attgagctgc 1860
tggcccgctc attgccaaaa attcaccgca gtgcatcaga accctccttg aatcgggctg 1920
gcttccaaac agaggatttt agtctatatg cttgtgcttc tccaaaaaca cccattcagg 1980
cagggggata tggagaattt gcagccttca agtagccaca ccatcatgac agcatctact 2040
cttatttctt aagtcttgtg ttcgtacaat ttgttaacat caaaacacag ttctgttcct 2100
caactctttt taaagttaaa atttttcagt gcataagctg gtgtggaaca gaaggaaatt 2160
tcccatccaa caaaagaggg aagaatgttt taggaaccag aattctctgc tgccagtgtt 2220
tcttcttcaa cacaaatatc acaagtctgc ccactcccag gaagaaagag gagagaccct 2280
gagttctgac cttttgatgg tcaggcatga tggaaagaaa ctgctgctac agcttgggag 2340
atttgctctg ggaagtctgc cagtcaactt tgcccttcta accaccagat caatatgtgg 2400
ctgatcatct gatggggcag ttgcaatcac caagccttgt tctctttcct gttctgggat 2460
tgtgttgtgg aacccttttc cctagccacc accagttcat ttctgaggga tggaacaaaa 2520
atgcagcatg cccttcctgt gtggtgcatg ttcagtcctt gacaaatttt taccaaaatg 2580
aagctacttt atttaaaagg agggtgagag gtgaggaggt cactttgggt gtggcggaaa 2640
gggaatgctg catctttttc ctgggctgct ggggctctgg ccttggcttg ccagccggaa 2700
gcgctggcac gcatcgcctt cttttcccat tgggtccagc aatgaagacg agtgtttggg 2760
gttttttttt tctccaccat gtagcaagtt ctcaggaaaa tacaattgat atcttcctcc 2820
taagctcttc caatcagtca ccaagtactt atgtggttac tttgtccagg gcacaaaatg 2880
cctgtatcta attaaaagcc tacaaaactg cttgataaca gttttgaatg tgagacattt 2940
atgtaattta aatgtaaggt acaagtttta atttctgagt ttcttctatt atatttttat 3000
taaaaaaaga aaataatttt cagattgaat tggagtaaaa taatattact tcccactaga 3060
attatatatc ctggaaaatt gtatttttgt tacataagca gcttttaaag aaagatcatt 3120
acccttttct ctacataaat atatggggag tcttagccta atgacaaata tttataattt 3180
ttaaattaat ggtacttgct ggatccatac taacatcttt actaatacct cattgtttct 3240
tccaacttac tcctacacta catcctacat cttcttccta gtcttttatc tagaatatgc 3300
aacctcaaat aaaaatggtg gtgtcctcat tcattctcct ccttcctttt ttcccaagcc 3360
tgatcttcaa aaggttggtt aatttggcag ctgagttcct ccccaggcag agaatagacc 3420
aattttaggt gtattgggac tgagggagga tgtgtaaaga ttaacatcag taaagaaccg 3480
ctgtggagta attaagaact ttgttcttta taactggaga atataaccta accctaacat 3540
ccctcagcct ttactaaagt gtggcgtaaa tcacagtagt agcaaagaaa gtgactctgg 3600
atgtgttcct ggccagtacc tcccttatca tgaatgtaga ctctctcatc aagatttagg 3660
aatataaatc aaatcaaatg tgcccagcca agctatgtag taagggactt gaacaatatt 3720
aggcagaacc tataaaataa atcagggaat tagaaattat ttaaagtttt caaattgtaa 3780
attgccccgg tgtctttcag cctactgcca ttatttttgc tacaatacct acatttcaga 3840
ggagggccta ctgaaaattc catgcaagtg gaaaataatc ctcaagttat taatgagttt 3900
gaaaagcaat gagttcttaa gtctttgtga gtagagcaag atcctacaaa attcagaaat 3960
agtaaaaatg gattcatgct gatttgaaga gcatctgtgt gcataatata atgctgcatc 4020
tcttttaaaa gcagtctatt tttcttttta aatttgtccc catagatgct tttgaacatg 4080
aacatgctta tgttaccttt tccgaggttg ggaagagcca ggagctctca ggcagggccc 4140
cctccctcag ctgggcagga gctgctcagg aggagctagt tatagaggaa gcttagcgtt 4200
ggcattttca aaattcaagg tgataacgct ttcttcttcc tttctgtttt agaatagatt 4260
gctgtctgat ttgaaaaagg gaaatagatt tgatctcaaa tgaatctgtg cccagaagcc 4320
aggctcaggg tattcagaga tttgtatagt gccctcaaaa aataacaaaa ttttagcttt 4380
ccttttttct tcttttctcc atcaaattct tttttctcta gtttacaaat gacatggaaa 4440
aggaatttcc cctgagtttt gtatgccttt ttttttttgg cttagactat agataggcgt 4500
gttgagctcc taagaaaata caaggaggaa ctctttgttg tgcagagcac tttatgagta 4560
gtttgtgtgg ataatatgtg actgcttccc tgacgagctt gtgaggctgt acttatgtct 4620
ttcctgtaag gcagcttcag tgccttctgt agtgtatata aggaaagatt acgccttctg 4680
aaaaatctca gagcaaccat aagattattt taaaatatgt agtatgactg atggactttt 4740
tcatcattaa attagtctag catctaaact tttaccactg aaataatatt gaccaaaaag 4800
caatttataa aaggtatttg tgaatagaaa atacaatgtg atcatttgta cttatgtgca 4860
ccttaaaaga ggaattctgt ctagctgtca aattctggtt ccttaacatc cagtccttga 4920
ttgtgattga gatctggtag gacgtgctgg ggcacgctag cagataaaat cccgtatact 4980
ttaggataga tgttacattt atgtcagtgt tggcaaagag cattgtgtag taataaagaa 5040
ttcaagactt cagcaatgtc aacctgaaac tttgtaaata tttcctagat tgttatttga 5100
tgcagtcaca gctctttatc acacaatgtt gtctttccct catcaggcaa ttttagaact 5160
gctgcacacc cctcctcaga tctcacctgc ccctcctgta cattcacctc tccagccttg 5220
tgcacacctc atttagcttt agtttgaaac acattgcagg gttcaggtga cctcttcaaa 5280
aactacctcc tcagaatgag gtaatgaata gttatttatt ttaaaatatg aaaagtcagg 5340
agctctagaa tatgaagatg atctaagatt ttaactttta tgtatacttg ttgagcactc 5400
tccttttgtc ctaaagggca ttatacattt aagcagtaat actgaaaaat gtagctcaga 5460
gtaactgaat gttgttgaaa gtggtgccag aatctgtttt aggggtacgt atcagaatct 5520
taatcttaaa tcggttacat gaaattaaat agttaatggt aacacttgac taacagatat 5580
aattttaatt ttcggtaggc ttttagcaag acagtaagta catcttcata atgagttagc 5640
cacagcttca tcacatgcac agattttcct gttgagagac tgcccagtta agagggtaga 5700
atgatgaacc atttttcagg attctcttct ttgtccaaac tggcattgtg agtgctagaa 5760
tatcagcact ttcaaactag tgattccaac tattaggcta ttaaaaagca aaacaaacca 5820
aacaaaccat agccagacat gggaagttta ctatgagtat aaacagcaaa tagcttacag 5880
gtcatacatt gaaatggtgt aggtaaggcg ttagaaaaat accttgacaa tttgccaaat 5940
gatcttactg tgccttcatg atgcaataaa aaaaaaaaaa atttagcata aatcagtgat 6000
ttgtgaagag agcagccacc ctggtctaac tcagctgtgt taatattttt tagcgtgcaa 6060
tttagactgc aaagataaat gcactaaaga gtttatagcc aaaatcacat ttaaaaaatg 6120
agagaaaaca caggtaaatt ttcagtgaac aaaattattt ttttaaagta cataatccct 6180
agtatagtca gatatattta tcacatagag caaataggtt gaaatcacaa ttcagtgaca 6240
tttctagaga aactttttct actcccatag gttcttcaaa gcatggaact tttatataac 6300
agaaatgtgt gacggtcatt ttaaattgct gtagtttggg gctgaagtac tgtgtgctgg 6360
gcagcaatca catgtattaa ctagtgagaa aggagaaatt aagatatagg acagaatttg 6420
attttcttgt tcccagatta ctgctgccaa cctagacact gagtttccag aggctgaaac 6480
gtaaacttgc agctcagcaa ctgttttgca aagttagtgg gactgtcctg cttatgctgt 6540
tcaaaaatgc tctgagggcc aggtggggcc tccaggggct cctctctgag gggacatcag 6600
actagctaac gacctggcgg gcggatgtga accggacaca ctccatggtg tgcttcttgt 6660
atcggtccct cgccaccctc aagaaaggct tcagcgggtt ctctagacgt ctccactaag 6720
gtgtgttact aacagccatg ggttgttgag cacccgagga gtgcaatagc atctctgcat 6780
gattgtatat tggcccgaag agaatgaagt ggccagtgta ctcatgttcc atgttgctag 6840
ctctggtaaa ctgaaaatac tggtaagatt tttgttttat cagtacacta gagagtaagc 6900
tttgttttgt tgtttttaga taatgttttc acttccattt ggaaagacat ttaaattgag 6960
tttcagtcct aaattttgcc agtcatggta attagcagtt tctatcaggt atttttaagg 7020
tagaagagga tagaaacata agttctaaaa gcttaaggta accgtggttt attttaaaat 7080
gtttaggggt ggttagtctc tacctcaaaa aaagtgagtg aatcttttat ttcagcattc 7140
acaagttcgg ctgttgtttt tgtaatacat ttttttttta accttttgac ccccctttac 7200
ctaagtgtca atgtagtttt attaattact aagtcagttt cattaaaatg tttatttagc 7260
agttttgact aattgcaatg attaatatag ccagttgtgc atgaggacac agccagtgag 7320
tatatctggg ttttttttgt gatgcttttt ttcttaagac ttctgtagat ttatgaagta 7380
ctcattgaaa acaactaaaa tacgtttatt cgtgttaata tggaaaaaaa aaaa 7434
<210> 40
<211> 603
<212> PRT
<213> Bos taurus
<400> 40
Met Met Arg Gly Leu Ile Pro Glu Cys Cys Ala Val Tyr Arg Ile Gln
1 5 10 15
Asp Gly Glu Lys Lys Pro Ile Gly Trp Asp Thr Asp Ile Ser Trp Leu
20 25 30
Thr Gly Glu Glu Leu His Val Glu Val Leu Glu Asn Val Pro Leu Thr
35 40 45
Thr His Asn Phe Val Arg Lys Thr Phe Phe Thr Leu Ala Phe Cys Asp
50 55 60
Phe Cys Arg Lys Leu Leu Phe Gln Gly Phe Arg Cys Gln Thr Cys Gly
65 70 75 80
Tyr Lys Phe His Gln Arg Cys Ser Thr Glu Val Pro Leu Met Cys Val
85 90 95
Asn Tyr Asp Gln Leu Asp Leu Leu Phe Val Ser Lys Phe Phe Glu His
100 105 110
His Pro Ile Pro Gln Glu Glu Ala Ser Leu Ala Glu Thr Thr Leu Pro
115 120 125
Cys Gly Ser Ser Pro Ser Ala Pro Pro Ser Asp Ser Ile Gly Pro Pro
130 135 140
Ile Leu Thr Ser Pro Ser Pro Ser Lys Ser Ile Pro Ile Pro Gln Pro
145 150 155 160
Phe Arg Pro Ala Asp Glu Asp His Arg Asn Gln Phe Gly Gln Arg Asp
165 170 175
Arg Ser Ser Ser Ala Pro Asn Val His Ile Asn Thr Ile Glu Pro Val
180 185 190
Asn Ile Asp Asp Leu Ile Arg Asp Gln Gly Phe Arg Ser Asp Gly Gly
195 200 205
Ser Thr Thr Gly Leu Ser Ala Thr Pro Pro Ala Ser Leu Pro Gly Ser
210 215 220
Leu Ser Asn Val Lys Ala Leu Gln Lys Ser Pro Gly Pro Gln Arg Glu
225 230 235 240
Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn Arg Met Lys Thr Leu
245 250 255
Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp Gly Gln Ile
260 265 270
Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr Val Tyr Lys
275 280 285
Gly Lys Trp His Gly Asp Val Ala Val Lys Met Leu Asn Val Thr Ala
290 295 300
Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val Gly Val Leu
305 310 315 320
Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe Met Gly Tyr Ser Thr
325 330 335
Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly Ser Ser Leu
340 345 350
Tyr His His Leu His Ile Ile Glu Thr Lys Phe Glu Met Ile Lys Leu
355 360 365
Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr Leu His Ala
370 375 380
Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile Phe Leu His
385 390 395 400
Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala Thr Val Lys
405 410 415
Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser Gly Ser Ile
420 425 430
Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys Asn Pro Tyr
435 440 445
Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu Tyr Glu Leu
450 455 460
Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg Asp Gln Ile
465 470 475 480
Ile Phe Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu Ser Lys Val
485 490 495
Arg Ser Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala Glu Cys Leu
500 505 510
Lys Lys Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Val Gly Lys Thr
515 520 525
Leu Leu Ser Lys Arg Gln Asn Ser Glu Val Ile Arg Glu Lys Asp Lys
530 535 540
Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro Lys Ile
545 550 555 560
His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe Gln Thr
565 570 575
Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro Ile Gln
580 585 590
Ala Gly Gly Tyr Gly Glu Phe Ala Ala Phe Lys
595 600
<210> 41
<211> 2295
<212> ДНК
<213> Equus caballus
<220>
<221> misc_feature
<222> (79)..(79)
<223> n представляет собой a, c, g, или t
<400> 41
atgaagacgc tgagcggcgg cggcggcggc gcggagcagg gccaggctct gttcaacggg 60
gacatggaac ccggaggcnc cgcgccggcg cccgcggcct cgtcggccgc ggaccctgcc 120
attcccgagg aggtatggaa tatcaaacaa atgattaaat tgacacagga acatatagag 180
gccctattgg acaaatttgg tggggagcat aatccaccat caatatatct ggaggcctat 240
gaagaataca ccagcaagct agatgccctc caacaaagag aacaacagtt attggaatcc 300
ctggggaatg gaactgattt ttctgtttct agttctgcat caacggacac cgttacatct 360
tcttcctctt ctagcctttc agtgctacct tcatctcttt cagtttttca aaatcccaca 420
gatgtgtcac ggagcaaccc taagtcacca caaaaaccta tcgttagagt cttcctgccc 480
aacaaacaga ggacagtggt acctgcaagg tgtggcgtta cagtccggga cagtctaaag 540
aaagcactga tgatgagagg tctaatccca gagtgctgtg ctgtttacag aattcaggat 600
ggagagaaga aaccaattgg ctgggacact gatatttcct ggctcactgg agaggaattg 660
catgtagaag tgttggagaa tgttccactt acaacacaca actttgtacg gaaaactttt 720
ttcaccttag cattttgtga cttttgtcga aagctgcttt tccagggttt ccgctgtcaa 780
acatgtggtt ataaatttca ccagcgttgt agtacagagg ttccactgat gtgtgttaat 840
tatgaccaac ttgatttgct gtttgtctcc aagttctttg aacaccaccc agtatcacag 900
gaggaggcct ccttagcaga gactgccctt acatctggat catccccttc tgcacccccc 960
tccgattcca ttgggcccca aattctcacc agtccatctc cttcaaaatc cattccaatt 1020
ccacagcctt tccgaccagc agatgaagat catcgaaatc agtttggaca acgagaccgg 1080
tcctcatcag ctccaaatgt acatataaac acaatagaac ctgtcaatat tgatgacttg 1140
attagagacc aagggtttcg tagtgatgga ggatcaacca caggtttatc tgccaccccc 1200
cctgcctcat tacctggctc actcactaat gtgaaggcat tacagaaatc tccaggacct 1260
caacgggaaa ggaaatcatc ttcatcctca gaagacagga atcgaatgaa aactcttggt 1320
agacgggatt caagtgacga ttgggagatt cctgatgggc agatcacagt gggacaaaga 1380
attggatctg ggtcatttgg gacagtctac aagggaaagt ggcatggtga tgtggcagtg 1440
aaaatgttga atgtgacagc acccacacct cagcagttac aggccttcaa aaatgaagta 1500
ggagtactca ggaaaactcg acatgtgaat atcctactct tcatgggcta ttcaacaaag 1560
ccacaactgg ctattgttac ccagtggtgt gagggctcca gcttatatca ccatctccac 1620
atcattgaga ccaaatttga gatgatcaaa cttatagata ttgctcggca aactgcacag 1680
ggcatggatt acttacacgc caagtcaatc atccacagag acctcaagag taataatatt 1740
tttcttcatg aagacctcac agtaaaaata ggtgattttg gtctagccac agtgaaatct 1800
cgatggagtg ggtcccatca gtttgaacag ttgtctggat ccattttgtg gatggcacca 1860
gaagtaatca gaatgcaaga taaaaacccg tatagctttc aatcagatgt atatgccttt 1920
gggattgttc tgtatgaatt gatgactgga cagttacctt attcaaacat caacaacagg 1980
gaccagataa tttttatggt gggaagagga tatctatctc cagatctcag taaggtacgg 2040
agtaactgtc caaaagccat gaagagatta atggcagagt gcctaaaaaa gaaaagagac 2100
gagagaccac tcttccccca aattctcgcc tctattgagc tgctggcccg ctcattgcca 2160
aaaattcacc gcagtgcatc agagccctcc ttgaatcggg ctggcttcca gacagaggat 2220
tttagtctat atgcttgtgc ttctccgaaa acacccatcc aggcaggggg atatggtgcg 2280
tttcctgtcc actga 2295
<210> 42
<211> 764
<212> PRT
<213> Equus caballus
<220>
<221> misc_feature
<222> (27)..(27)
<223> Xaa can be any naturally occurring amino acid
<400> 42
Met Lys Thr Leu Ser Gly Gly Gly Gly Gly Ala Glu Gln Gly Gln Ala
1 5 10 15
Leu Phe Asn Gly Asp Met Glu Pro Gly Gly Xaa Ala Pro Ala Pro Ala
20 25 30
Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn Ile
35 40 45
Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu Asp
50 55 60
Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala Tyr
65 70 75 80
Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln Gln
85 90 95
Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser Ser
100 105 110
Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser Val
115 120 125
Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser Arg
130 135 140
Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu Pro
145 150 155 160
Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val Arg
165 170 175
Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu Cys
180 185 190
Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly Trp
195 200 205
Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu Val
210 215 220
Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr Phe
225 230 235 240
Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln Gly
245 250 255
Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser Thr
260 265 270
Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu Phe
275 280 285
Val Ser Lys Phe Phe Glu His His Pro Val Ser Gln Glu Glu Ala Ser
290 295 300
Leu Ala Glu Thr Ala Leu Thr Ser Gly Ser Ser Pro Ser Ala Pro Pro
305 310 315 320
Ser Asp Ser Ile Gly Pro Gln Ile Leu Thr Ser Pro Ser Pro Ser Lys
325 330 335
Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His Arg
340 345 350
Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val His
355 360 365
Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp Gln
370 375 380
Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr Pro
385 390 395 400
Pro Ala Ser Leu Pro Gly Ser Leu Thr Asn Val Lys Ala Leu Gln Lys
405 410 415
Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp
420 425 430
Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp
435 440 445
Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser Gly
450 455 460
Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala Val
465 470 475 480
Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe
485 490 495
Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile Leu
500 505 510
Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr Gln
515 520 525
Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu Thr
530 535 540
Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln
545 550 555 560
Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu Lys
565 570 575
Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly Asp
580 585 590
Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln Phe
595 600 605
Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile Arg
610 615 620
Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe
625 630 635 640
Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn
645 650 655
Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr Leu
660 665 670
Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met Lys
675 680 685
Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro Leu
690 695 700
Phe Pro Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro
705 710 715 720
Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe
725 730 735
Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro
740 745 750
Ile Gln Ala Gly Gly Tyr Gly Ala Phe Pro Val His
755 760
<210> 43
<211> 2678
<212> ДНК
<213> Gallus gallus
<400> 43
tccccctccc tcgccccagc gcttcgatcc aagatggcgg cgctgagcag cggcagcagc 60
gccgaggggg cctcgctctt caacggggac atggagcccg agccgccgcc gcccgtgctg 120
ggcgcctgct acgccgggag cggcggcggc gacccggcca tcccggagga ggtgtggaat 180
atcaaacaga tgattaaatt aacacaagaa catatagaag cgctgttaga caagtttgga 240
ggagagcata acccaccatc aatatattta gaggcctatg aggagtacac cagcaaacta 300
gatgctctac agcagagaga acagcagtta ttggaatcca tgggaaatgg aactgatttc 360
tctgtttcca gttcagcttc aacggacaca gttgcatcat cttcctcctc tagcctctct 420
gtagcacctt catccctttc agtttatcaa aatcctactg atatgtcgcg gaataaccct 480
aagtctccac agaagcctat tgttagagtc ttcctgccca acaagcaaag gactgtggtt 540
ccggcaagat gtggggtgac agtccgagac agcctgaaga aagctctgat gatgagaggt 600
cttattccag aatgctgtgc tgtttacaga atacaggatg gagagaagaa gccaattggc 660
tgggacactg acatttcctg gctaaccgga gaggagttac acgtggaggt cttggagaat 720
gtgccactca caacacacaa ttttgtacga aaaacattct tcacgttagc gttctgcgac 780
ttctgtcgaa agctgctttt ccagggattc cgatgccaga catgtggcta caaatttcac 840
cagcgctgta gcacagaagt gccactgatg tgtgttaact acgaccaact cgatttgctg 900
tttgtctcca agttctttga acatcacccc atatcgcagg aggagaccac cttaggagag 960
accaccccgg catcgggatc gtacccctca gtgcccccat cagattctgt tggaccacca 1020
attctcccta gtccttctcc ttcaaaatcc attccaatcc cacagccctt ccgaccagca 1080
gatgaagacc atcggaatca gtttgggcaa cgcgaccgat cctcttcagc tcccaatgtt 1140
cacatcaata caattgagcc agtcaatatt gatgacttga ttagagacca gggtgtacga 1200
ggagagggag cccctttgaa ccagctgatg cgctgtcttc ggaaatacca atcccggact 1260
cccagtcccc tccttcattc tgtccccagt gaaatagtgt ttgattttga gcctggccca 1320
gtgttcagag gttcaactgc aggtttgtct gcaacacctc ctgcatcttt gcctgggtca 1380
cttaccaatg tgaaagcatt acagaaatca ccaggccccc aacgggaaag gaaatcatcc 1440
tcatcctcag aagacagaaa taggatgaaa acccttggtc gacgagattc aagtgatgat 1500
tgggaaatac cagatgggca gatcacagtt ggacaaagga taggatctgg atcatttgga 1560
acagtctaca aaggaaagtg gcatggtgac gtggcagtga aaatgttgaa tgttacagca 1620
cccacacctc aacagttaca ggctttcaaa aatgaagtag gagtgctcag gaaaacacgg 1680
catgtgaata tcctactttt tatgggttat tcaacaaaac ctcagttggc tattgttaca 1740
cagtggtgtg aggggtccag cttatatcac catctgcaca taattgagac caagtttgaa 1800
atgatcaaac taattgatat tgcacgacag actgcacaag gcatggatta tttgcatgcc 1860
aagtcaatca tccacagaga cctcaagagt aataatattt ttcttcatga agacctcaca 1920
gtaaaaatag gtgacttcgg tctggctaca gtgaaatcac gatggagtgg atctcatcaa 1980
tttgaacagt tatctggatc aattctatgg atggcaccgg aagtgatcag gatgcaagac 2040
aaaaacccat atagctttca gtcagatgtg tatgcattcg ggattgtgct ttatgaactg 2100
atgactggac agttaccata ctcaaacatc aacaacaggg accagataat ttttatggtg 2160
ggacgaggat atctatctcc agacctcagt aaagtaagaa gtaactgtcc aaaagctatg 2220
aagagactaa tggcagaatg cttgaaaaag aaaagagatg agagacctct ttttccacag 2280
attcttgcct ccattgagct tctggcccgg tcgttgccaa aaattcaccg cagtgcatct 2340
gagccgtcac taaaccgggc tggcttccag accgaggatt tcagtctgta tgcttgtgct 2400
tctccaaaaa cgcccatcca agcaggggga tacggtgggt ttccagtaca ctgaaaagaa 2460
atgtgaaagc gtgtgcctgt ttgctcatgt gctggtgtgt tcctgtgtgt gcaacgcata 2520
cgtacgttct cagttcctac cagcgacttt ttaaggttta ctgagggaat gaagactcat 2580
ttcctaacat ggggcattga acgtcctgag cacaagtcag tgctggtaag gaatgtcttg 2640
ggaacagctg gcaagaagaa ttagaaggta cttaaagg 2678
<210> 44
<211> 806
<212> PRT
<213> Gallus gallus
<400> 44
Met Ala Ala Leu Ser Ser Gly Ser Ser Ala Glu Gly Ala Ser Leu Phe
1 5 10 15
Asn Gly Asp Met Glu Pro Glu Pro Pro Pro Pro Val Leu Gly Ala Cys
20 25 30
Tyr Ala Gly Ser Gly Gly Gly Asp Pro Ala Ile Pro Glu Glu Val Trp
35 40 45
Asn Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu
50 55 60
Leu Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu
65 70 75 80
Ala Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu
85 90 95
Gln Gln Leu Leu Glu Ser Met Gly Asn Gly Thr Asp Phe Ser Val Ser
100 105 110
Ser Ser Ala Ser Thr Asp Thr Val Ala Ser Ser Ser Ser Ser Ser Leu
115 120 125
Ser Val Ala Pro Ser Ser Leu Ser Val Tyr Gln Asn Pro Thr Asp Met
130 135 140
Ser Arg Asn Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe
145 150 155 160
Leu Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr
165 170 175
Val Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro
180 185 190
Glu Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile
195 200 205
Gly Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val
210 215 220
Glu Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys
225 230 235 240
Thr Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe
245 250 255
Gln Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys
260 265 270
Ser Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu
275 280 285
Leu Phe Val Ser Lys Phe Phe Glu His His Pro Ile Ser Gln Glu Glu
290 295 300
Thr Thr Leu Gly Glu Thr Thr Pro Ala Ser Gly Ser Tyr Pro Ser Val
305 310 315 320
Pro Pro Ser Asp Ser Val Gly Pro Pro Ile Leu Pro Ser Pro Ser Pro
325 330 335
Ser Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp
340 345 350
His Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn
355 360 365
Val His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg
370 375 380
Asp Gln Gly Val Arg Gly Glu Gly Ala Pro Leu Asn Gln Leu Met Arg
385 390 395 400
Cys Leu Arg Lys Tyr Gln Ser Arg Thr Pro Ser Pro Leu Leu His Ser
405 410 415
Val Pro Ser Glu Ile Val Phe Asp Phe Glu Pro Gly Pro Val Phe Arg
420 425 430
Gly Ser Thr Ala Gly Leu Ser Ala Thr Pro Pro Ala Ser Leu Pro Gly
435 440 445
Ser Leu Thr Asn Val Lys Ala Leu Gln Lys Ser Pro Gly Pro Gln Arg
450 455 460
Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn Arg Met Lys Thr
465 470 475 480
Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp Gly Gln
485 490 495
Ile Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr Val Tyr
500 505 510
Lys Gly Lys Trp His Gly Asp Val Ala Val Lys Met Leu Asn Val Thr
515 520 525
Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val Gly Val
530 535 540
Leu Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe Met Gly Tyr Ser
545 550 555 560
Thr Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly Ser Ser
565 570 575
Leu Tyr His His Leu His Ile Ile Glu Thr Lys Phe Glu Met Ile Lys
580 585 590
Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr Leu His
595 600 605
Ala Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile Phe Leu
610 615 620
His Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala Thr Val
625 630 635 640
Lys Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser Gly Ser
645 650 655
Ile Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys Asn Pro
660 665 670
Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu Tyr Glu
675 680 685
Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg Asp Gln
690 695 700
Ile Ile Phe Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu Ser Lys
705 710 715 720
Val Arg Ser Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala Glu Cys
725 730 735
Leu Lys Lys Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Ile Leu Ala
740 745 750
Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro Lys Ile His Arg Ser Ala
755 760 765
Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp Phe Ser
770 775 780
Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly Gly Tyr
785 790 795 800
Gly Gly Phe Pro Val His
805
<210> 45
<211> 2949
<212> ДНК
<213> Homo sapiens
<400> 45
cgcctccctt ccccctcccc gcccgacagc ggccgctcgg gccccggctc tcggttataa 60
gatggcggcg ctgagcggtg gcggtggtgg cggcgcggag ccgggccagg ctctgttcaa 120
cggggacatg gagcccgagg ccggcgccgg cgccggcgcc gcggcctctt cggctgcgga 180
ccctgccatt ccggaggagg tgtggaatat caaacaaatg attaagttga cacaggaaca 240
tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa tatatctgga 300
ggcctatgaa gaatacacca gcaagctaga tgcactccaa caaagagaac aacagttatt 360
ggaatctctg gggaacggaa ctgatttttc tgtttctagc tctgcatcaa tggataccgt 420
tacatcttct tcctcttcta gcctttcagt gctaccttca tctctttcag tttttcaaaa 480
tcccacagat gtggcacgga gcaaccccaa gtcaccacaa aaacctatcg ttagagtctt 540
cctgcccaac aaacagagga cagtggtacc tgcaaggtgt ggagttacag tccgagacag 600
tctaaagaaa gcactgatga tgagaggtct aatcccagag tgctgtgctg tttacagaat 660
tcaggatgga gagaagaaac caattggttg ggacactgat atttcctggc ttactggaga 720
agaattgcat gtggaagtgt tggagaatgt tccacttaca acacacaact ttgtacgaaa 780
aacgtttttc accttagcat tttgtgactt ttgtcgaaag ctgcttttcc agggtttccg 840
ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaagttc cactgatgtg 900
tgttaattat gaccaacttg atttgctgtt tgtctccaag ttctttgaac accacccaat 960
accacaggaa gaggcgtcct tagcagagac tgccctaaca tctggatcat ccccttccgc 1020
acccgcctcg gactctattg ggccccaaat tctcaccagt ccgtctcctt caaaatccat 1080
tccaattcca cagcccttcc gaccagcaga tgaagatcat cgaaatcaat ttgggcaacg 1140
agaccgatcc tcatcagctc ccaatgtgca tataaacaca atagaacctg tcaatattga 1200
tgacttgatt agagaccaag gatttcgtgg tgatggagga tcaaccacag gtttgtctgc 1260
taccccccct gcctcattac ctggctcact aactaacgtg aaagccttac agaaatctcc 1320
aggacctcag cgagaaagga agtcatcttc atcctcagaa gacaggaatc gaatgaaaac 1380
acttggtaga cgggactcga gtgatgattg ggagattcct gatgggcaga ttacagtggg 1440
acaaagaatt ggatctggat catttggaac agtctacaag ggaaagtggc atggtgatgt 1500
ggcagtgaaa atgttgaatg tgacagcacc tacacctcag cagttacaag ccttcaaaaa 1560
tgaagtagga gtactcagga aaacacgaca tgtgaatatc ctactcttca tgggctattc 1620
cacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagct tgtatcacca 1680
tctccatatc attgagacca aatttgagat gatcaaactt atagatattg cacgacagac 1740
tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc tcaagagtaa 1800
taatatattt cttcatgaag acctcacagt aaaaataggt gattttggtc tagctacaga 1860
gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca ttttgtggat 1920
ggcaccagaa gtcatcagaa tgcaagataa aaatccatac agctttcagt cagatgtata 1980
tgcatttgga attgttctgt atgaattgat gactggacag ttaccttatt caaacatcaa 2040
caacagggac cagataattt ttatggtggg acgaggatac ctgtctccag atctcagtaa 2100
ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc tcaaaaagaa 2160
aagagatgag agaccactct ttccccaaat tctcgcctct attgagctgc tggcccgctc 2220
attgccaaaa attcaccgca gtgcatcaga accctccttg aatcgggctg gtttccaaac 2280
agaggatttt agtctatatg cttgtgcttc tccaaaaaca cccatccagg cagggggata 2340
tggtgcgttt cctgtccact gaaacaaatg agtgagagag ttcaggagag tagcaacaaa 2400
aggaaaataa atgaacatat gtttgcttat atgttaaatt gaataaaata ctctcttttt 2460
ttttaaggtg aaccaaagaa cacttgtgtg gttaaagact agatataatt tttccccaaa 2520
ctaaaattta tacttaacat tggattttta acatccaagg gttaaaatac atagacattg 2580
ctaaaaattg gcagagcctc ttctagaggc tttactttct gttccgggtt tgtatcattc 2640
acttggttat tttaagtagt aaacttcagt ttctcatgca acttttgttg ccagctatca 2700
catgtccact agggactcca gaagaagacc ctacctatgc ctgtgtttgc aggtgagaag 2760
ttggcagtcg gttagcctgg gttagataag gcaaactgaa cagatctaat ttaggaagtc 2820
agtagaattt aataattcta ttattattct taataatttt tctataacta tttcttttta 2880
taacaatttg gaaaatgtgg atgtctttta tttccttgaa gcaataaact aagtttcttt 2940
ttataaaaa 2949
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ С АТИПИЧНЫМИ МУТАЦИЯМИ BRAF | 2018 |
|
RU2812706C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ИЛИ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2016 |
|
RU2718499C2 |
| Белки, связывающие NKG2D, CD16 и опухолеассоциированный антиген | 2018 |
|
RU2816716C2 |
| КЛЕТКА | 2014 |
|
RU2732236C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2019 |
|
RU2781542C2 |
| МУЛЬТИВАЛЕНТНЫЕ PD-L1-СВЯЗЫВАЮЩИЕ СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2020 |
|
RU2816646C2 |
| КЛЕТКА | 2014 |
|
RU2717984C2 |
| АДЕНОВИРУСЫ И СПОСОБЫ ПРИМЕНЕНИЯ АДЕНОВИРУСОВ | 2019 |
|
RU2782528C1 |
| ВВЕДЕНИЕ СКОНСТРУИРОВАННЫХ Т-КЛЕТОК ДЛЯ ЛЕЧЕНИЯ РАКА ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ | 2017 |
|
RU2757308C2 |
| ТЕРАПЕВТИЧЕСКИЕ СОЕДИНЕНИЯ И СПОСОБЫ | 2016 |
|
RU2770001C2 |
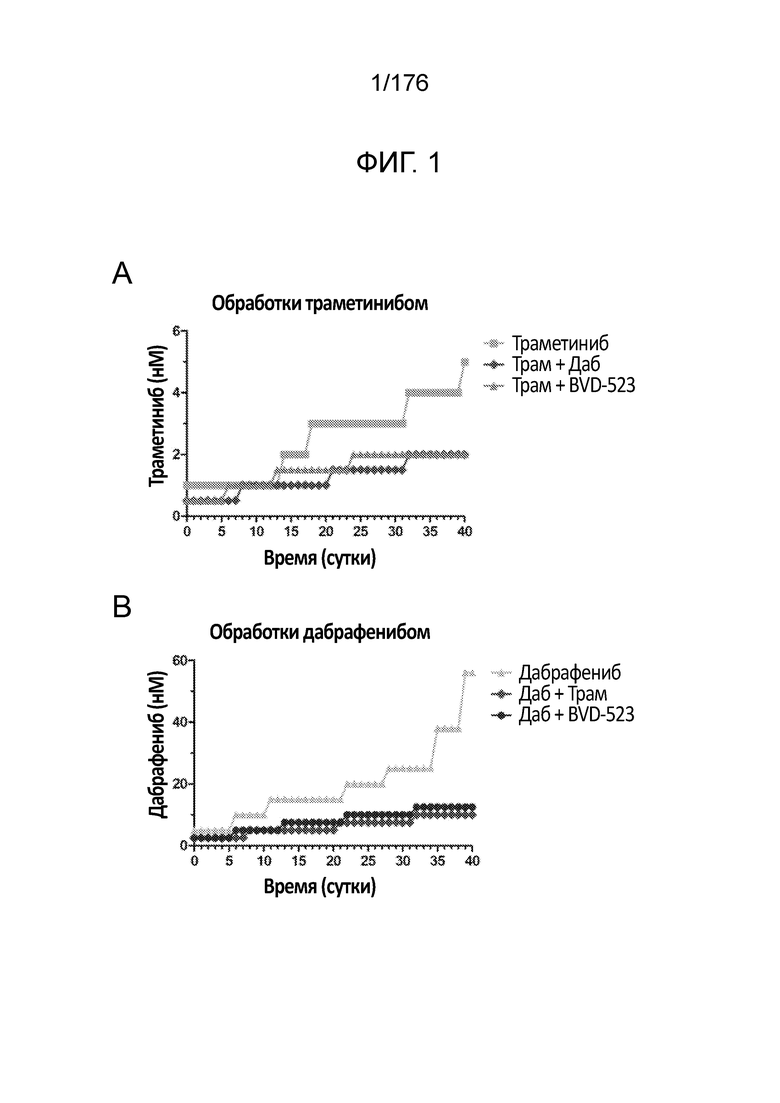
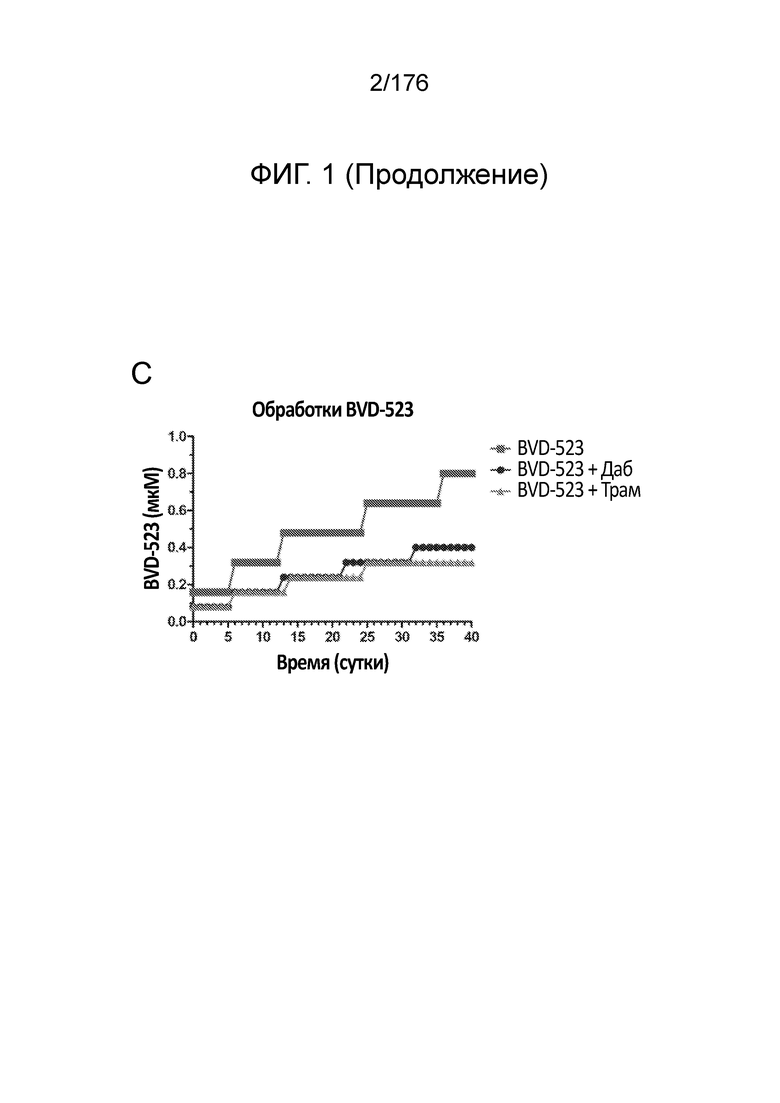
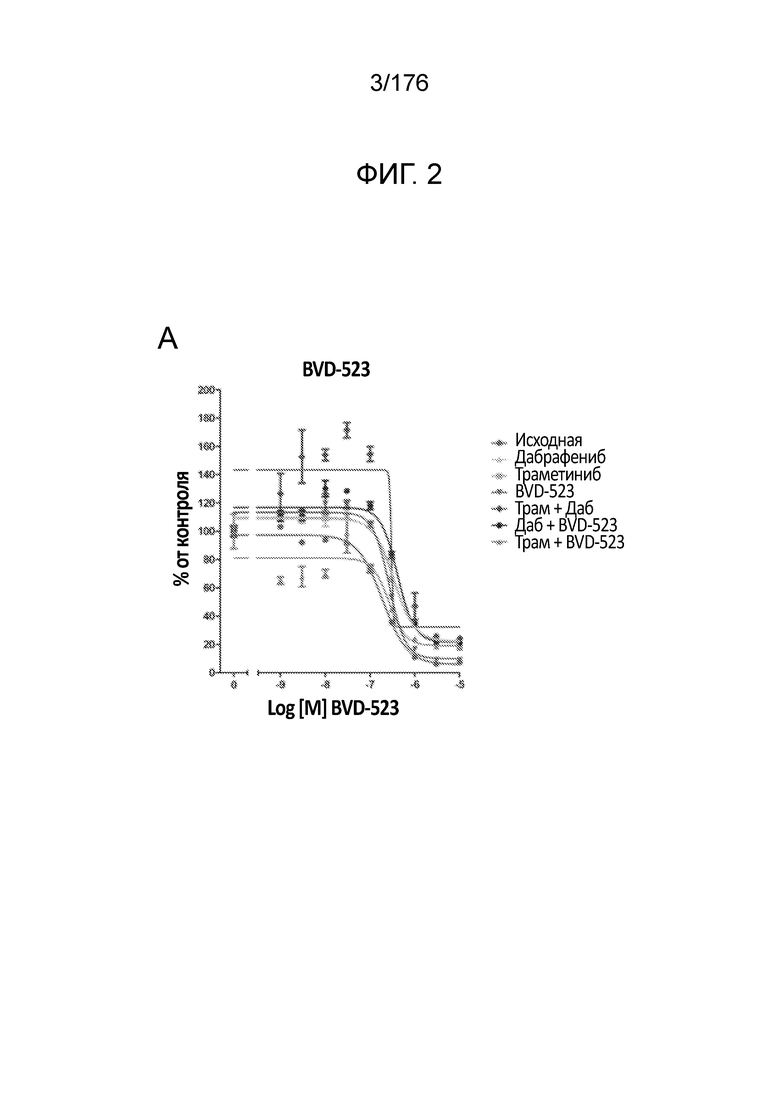
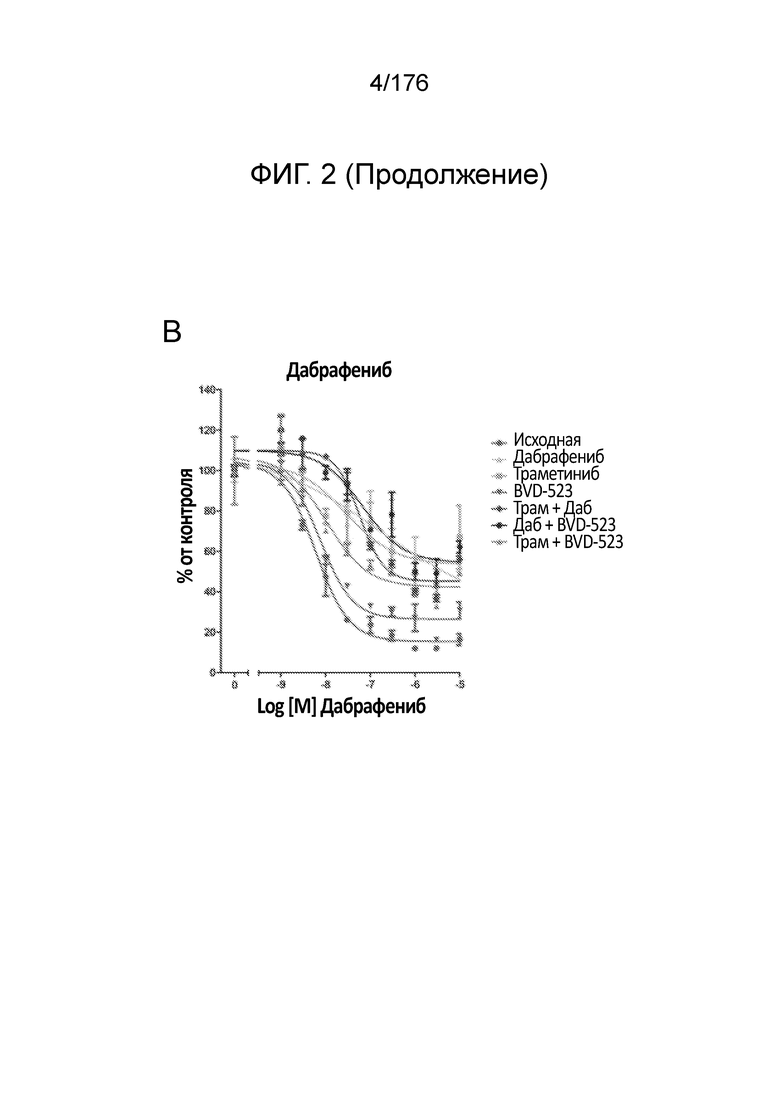
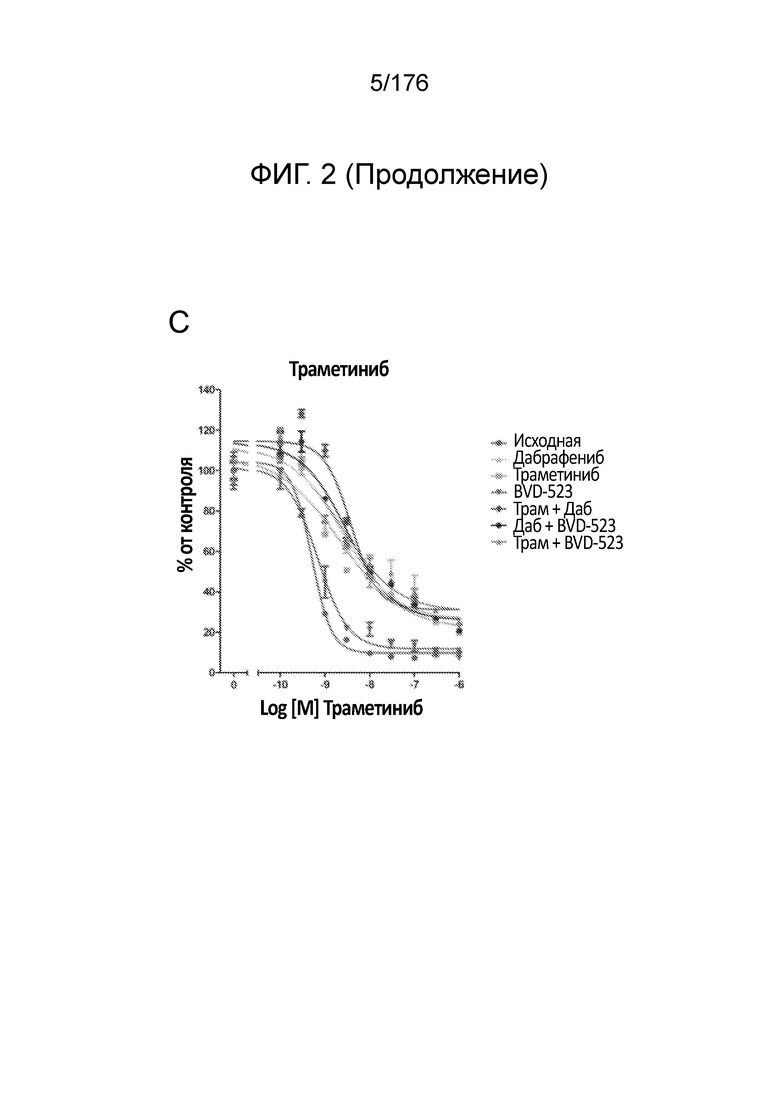
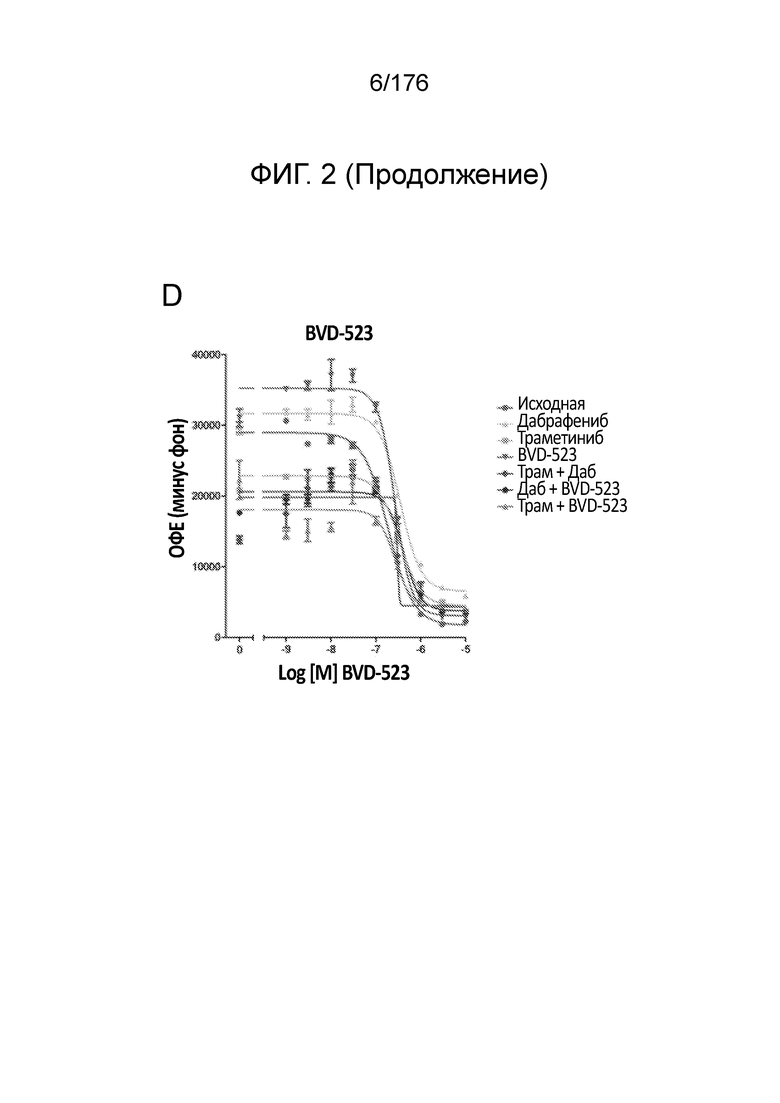
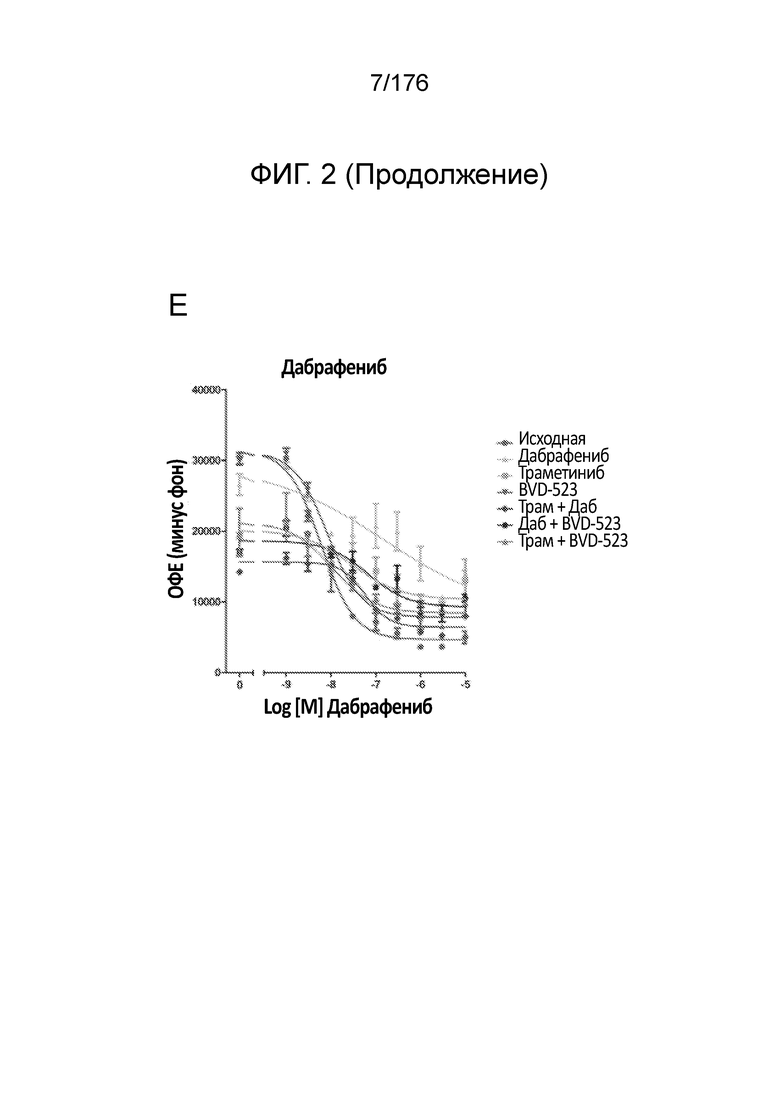
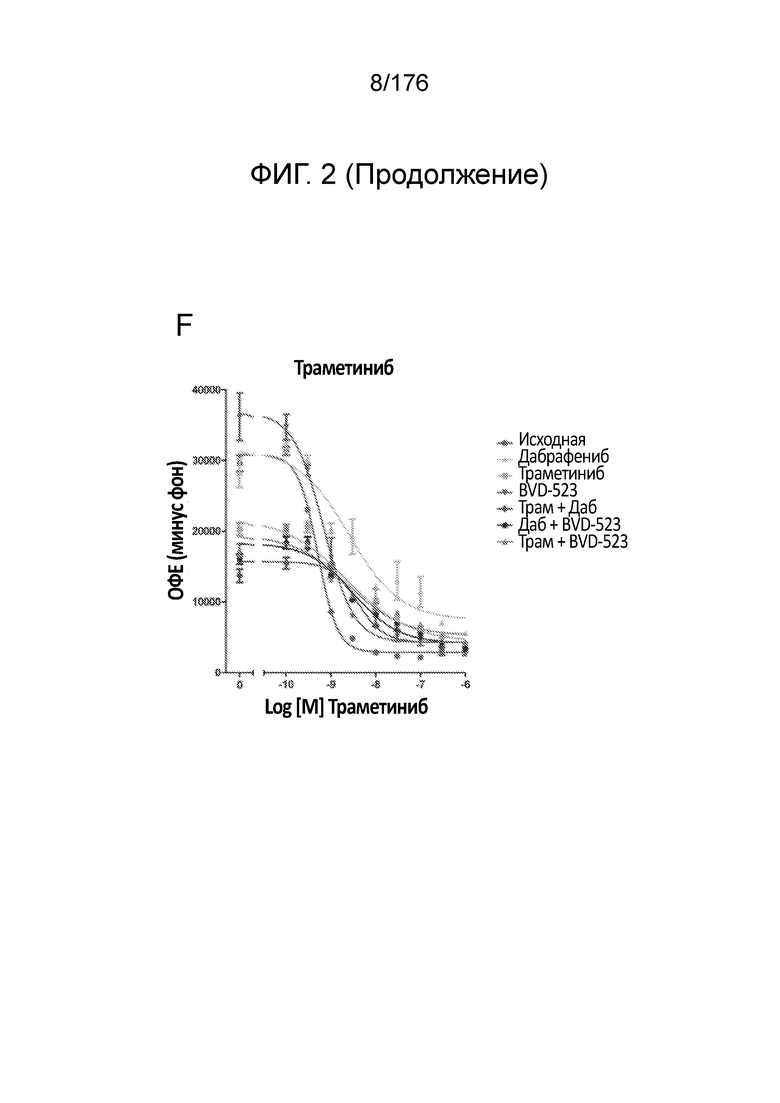
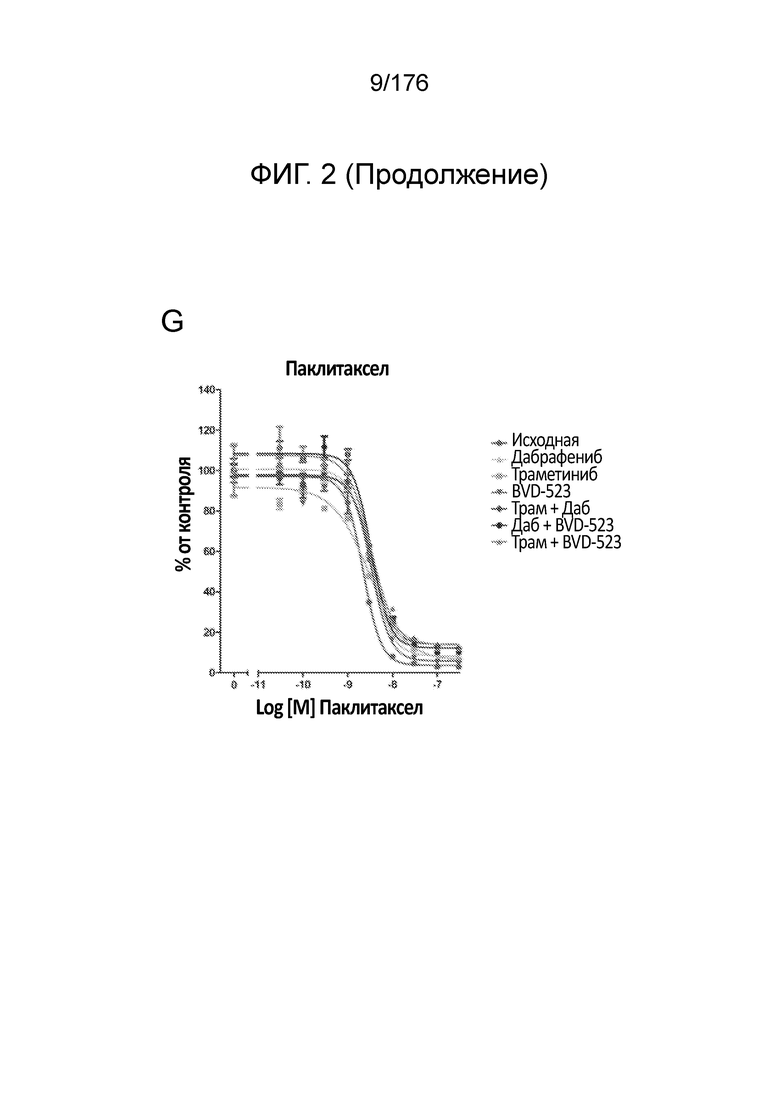
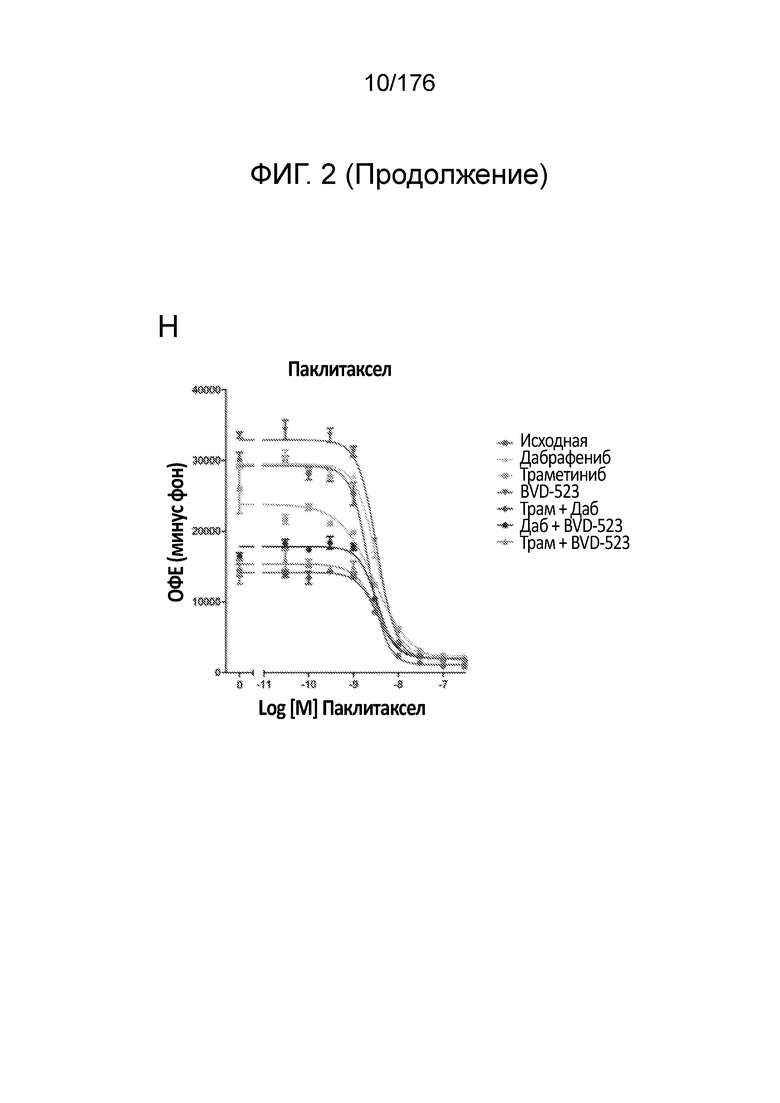
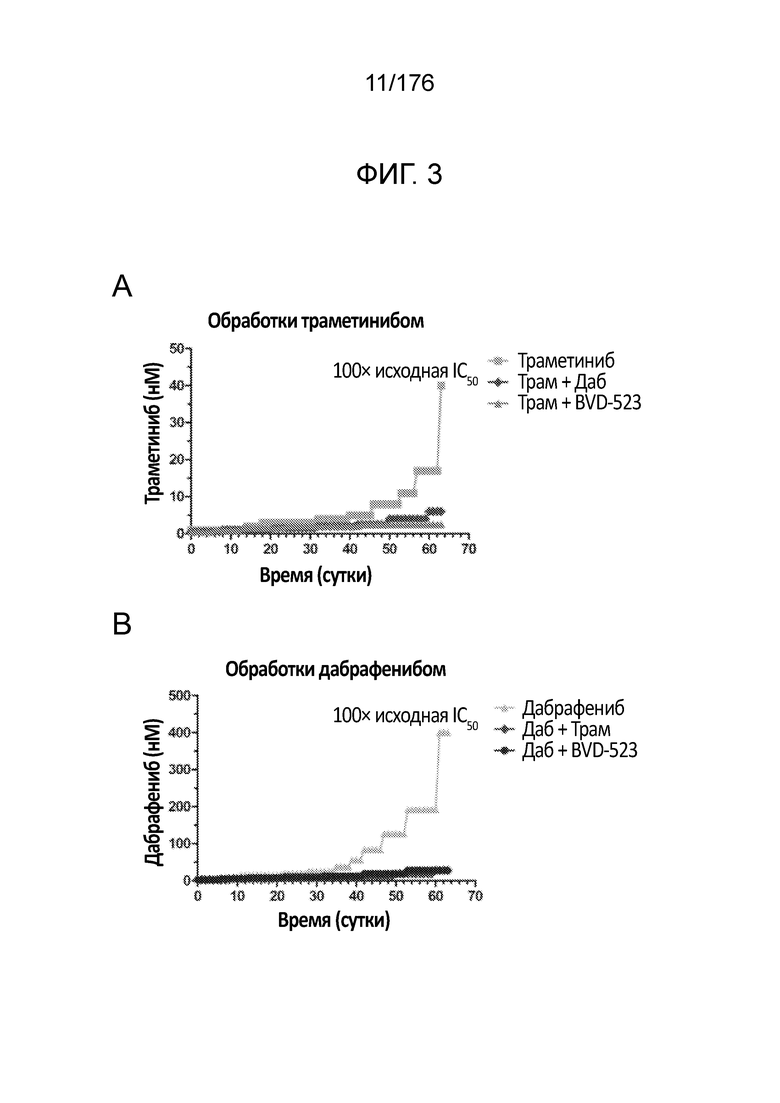
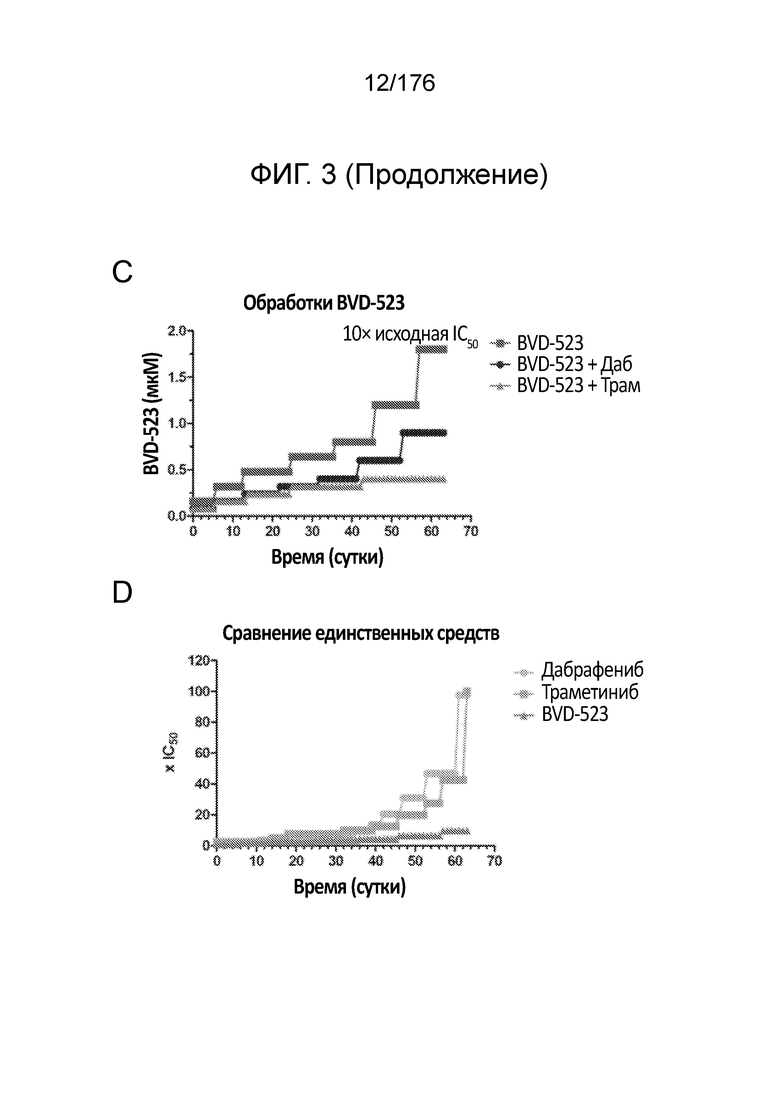
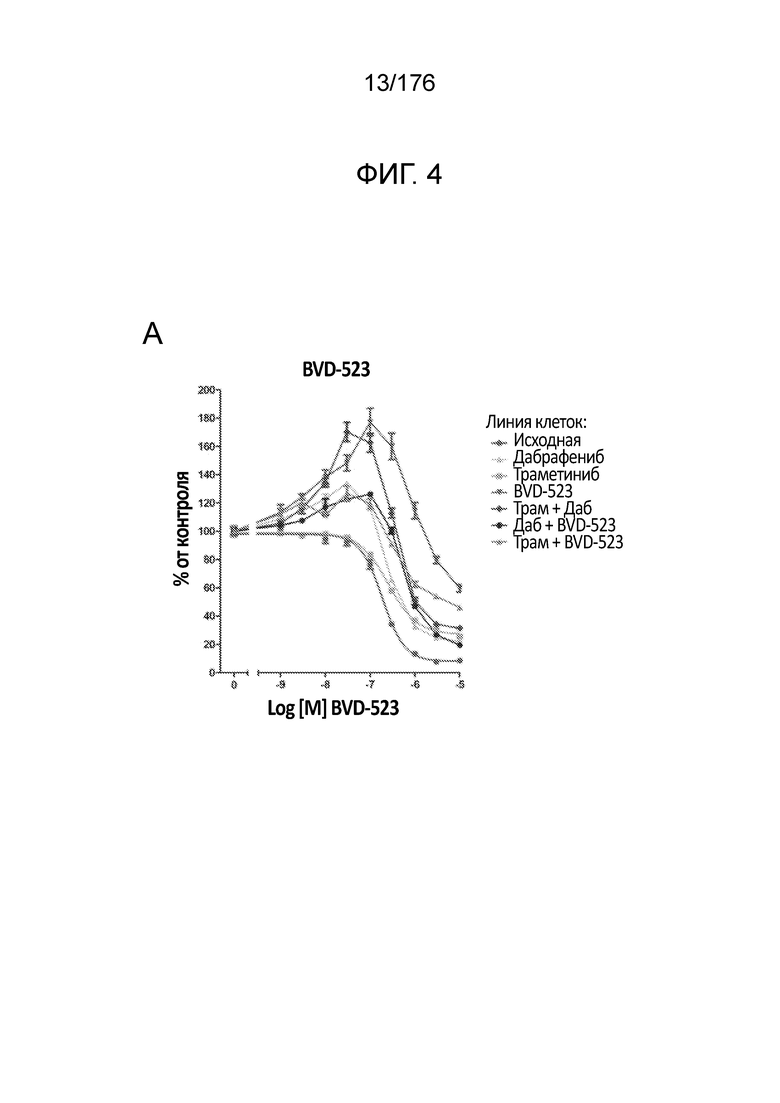
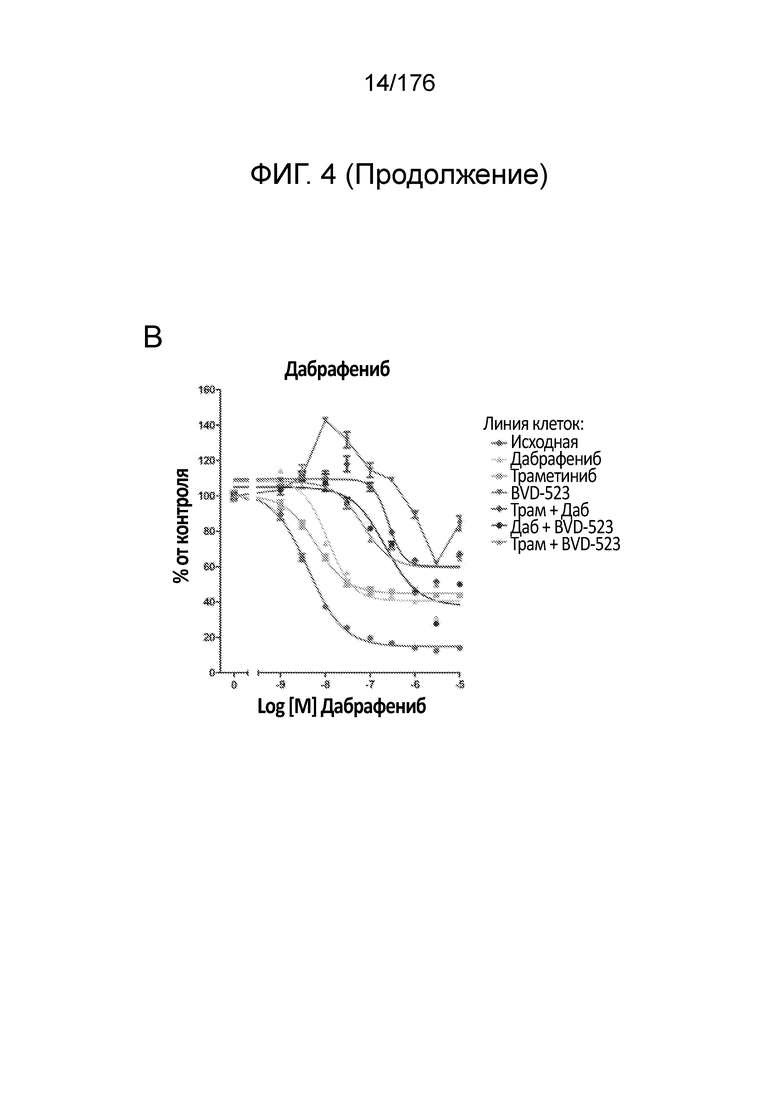
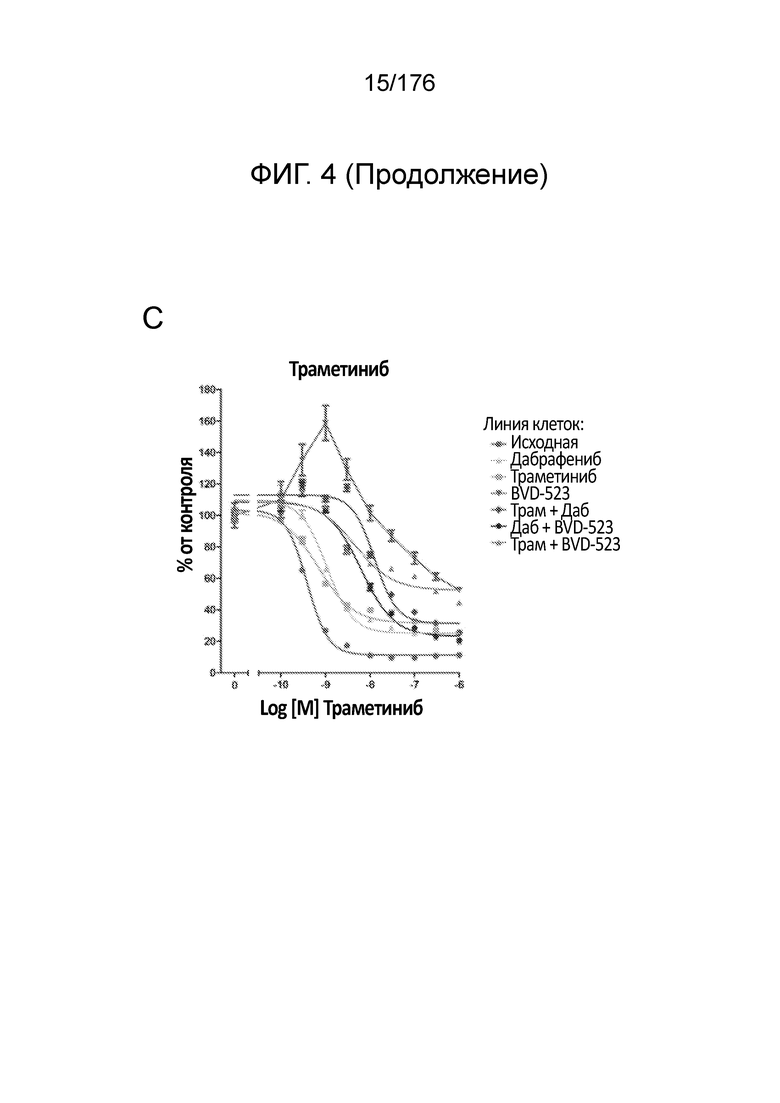
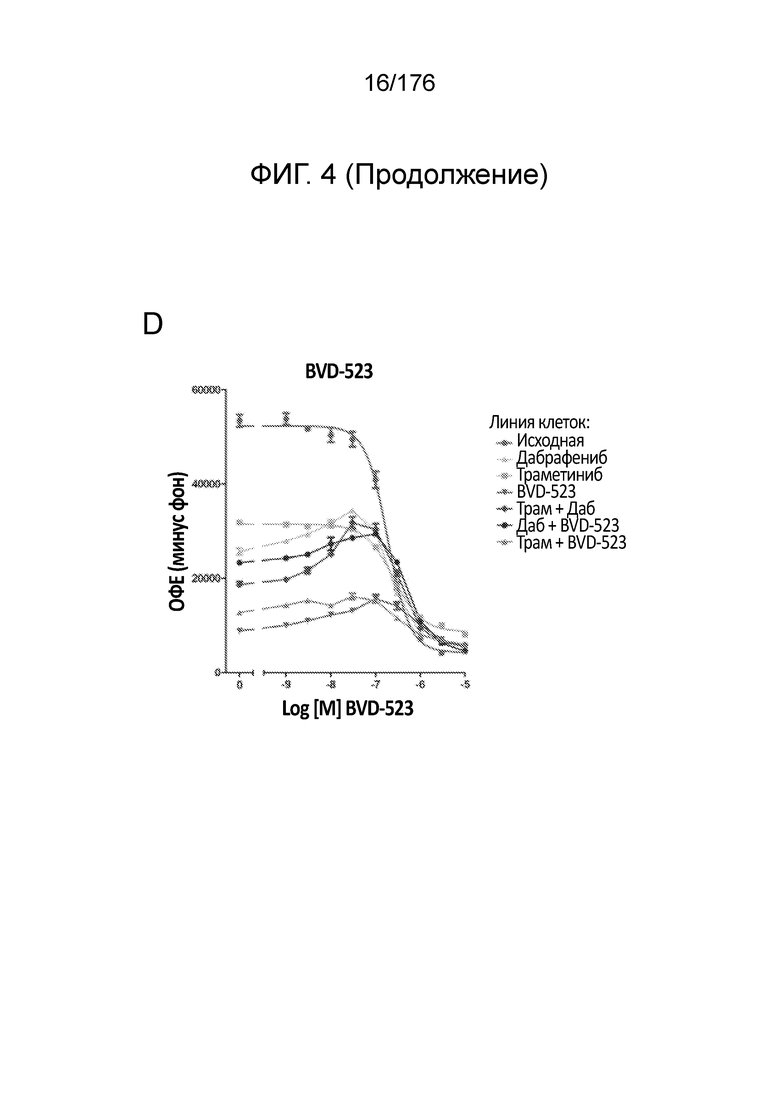
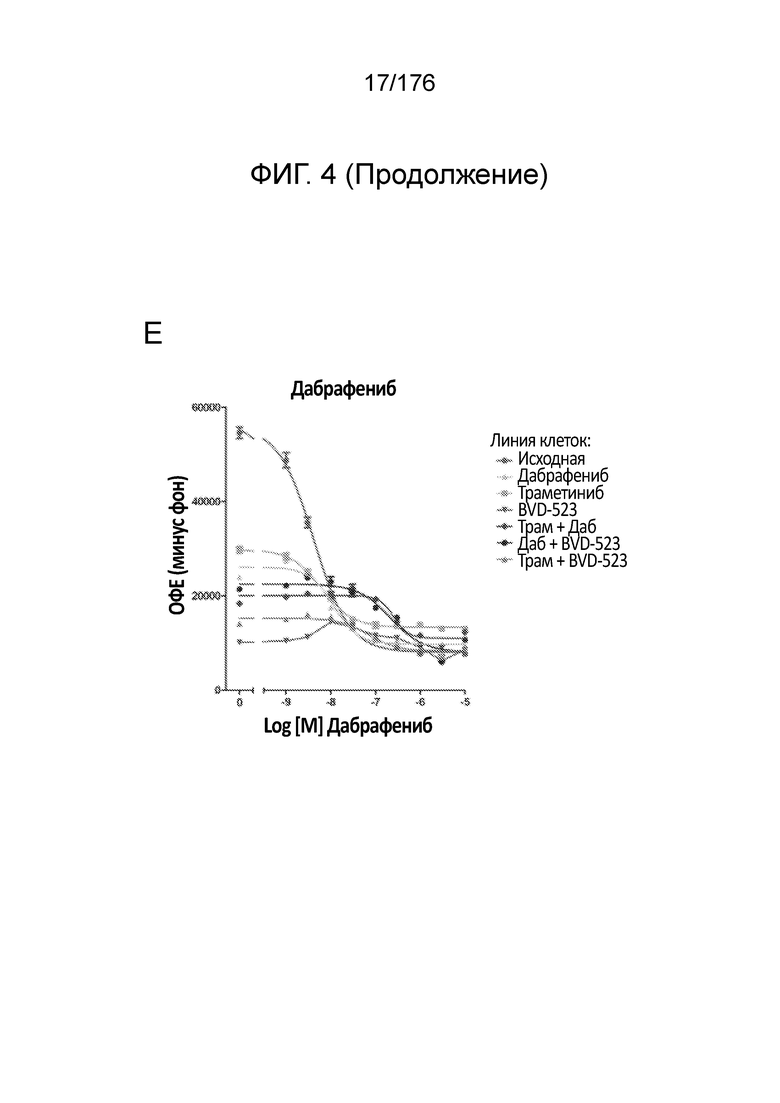
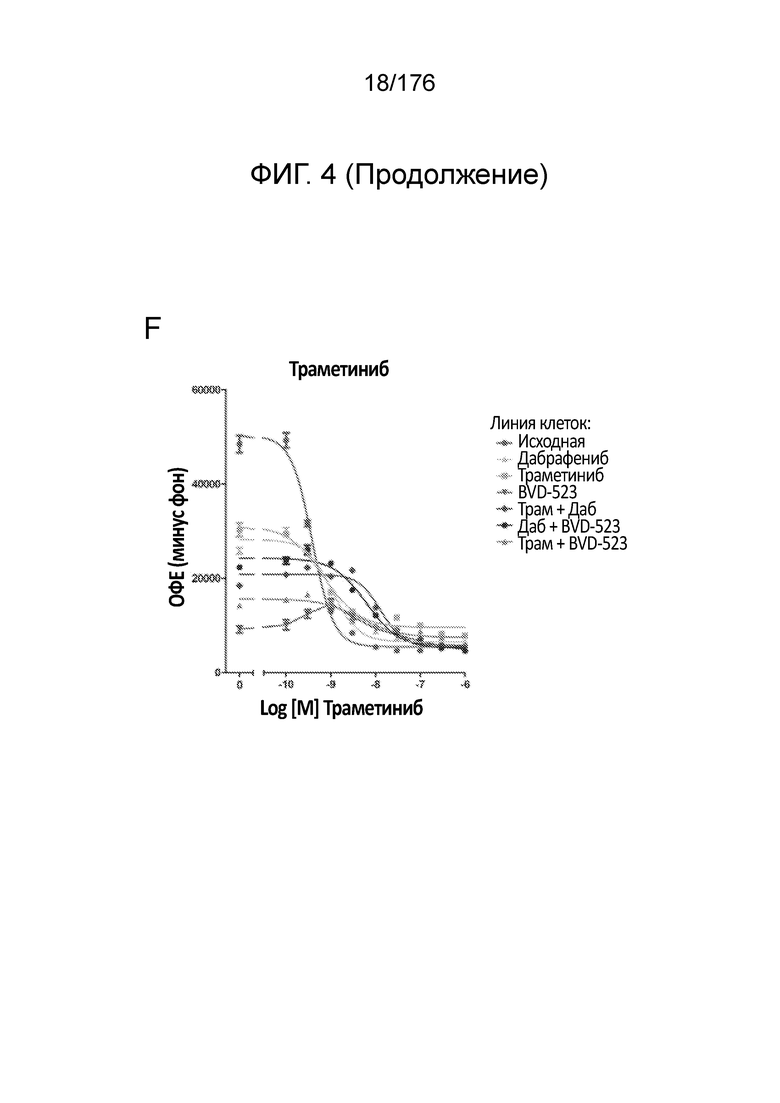
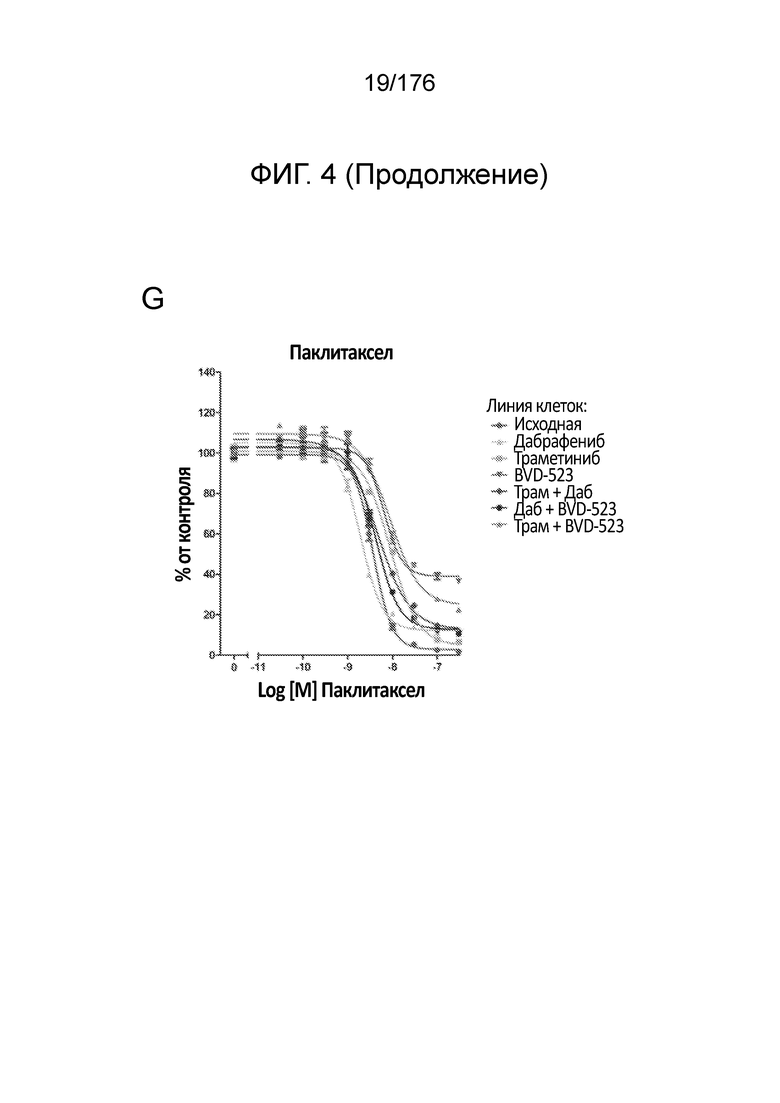
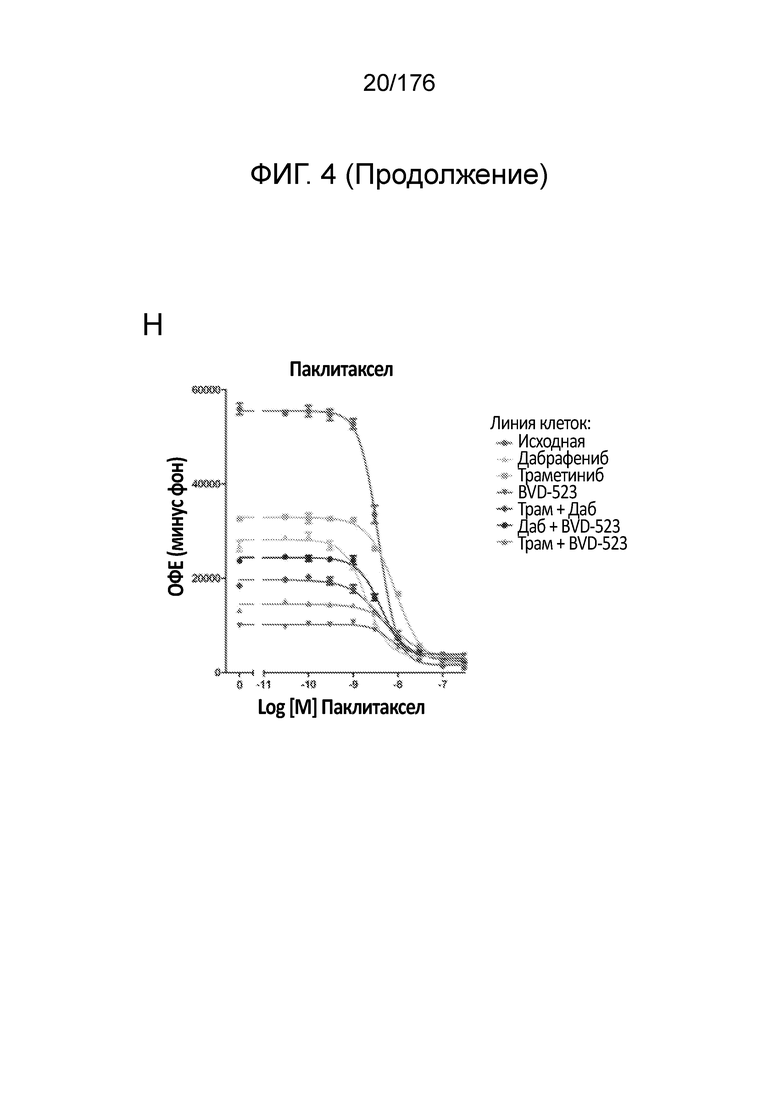
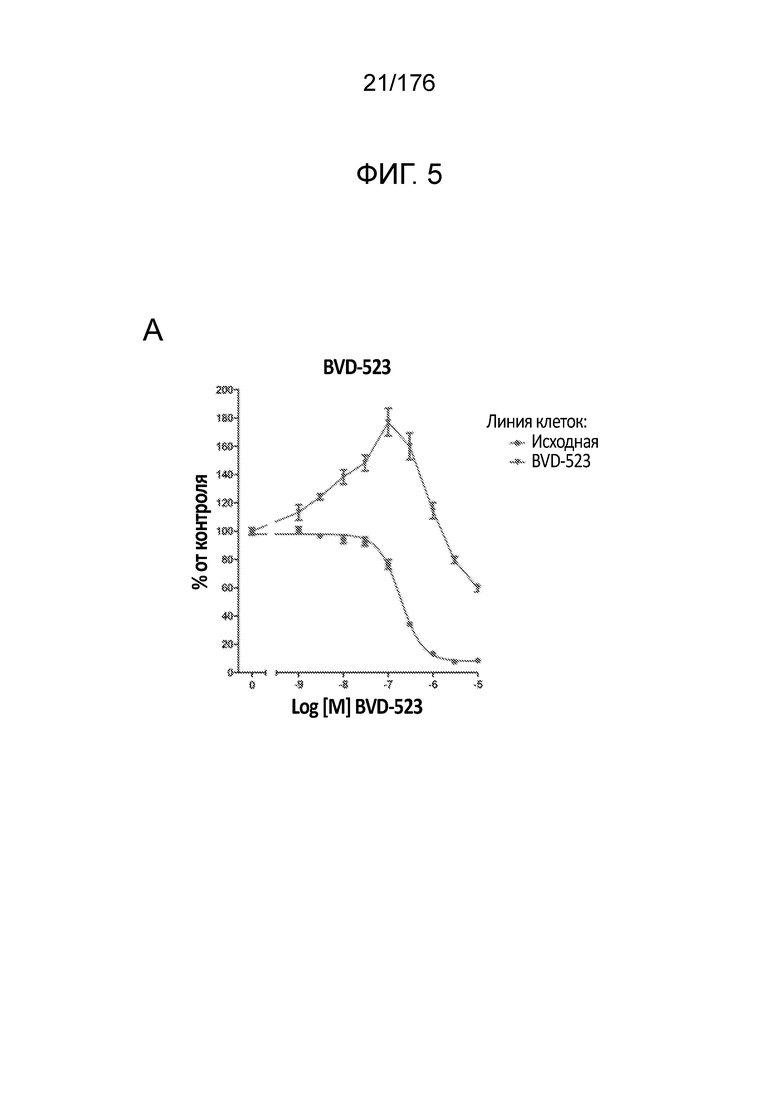
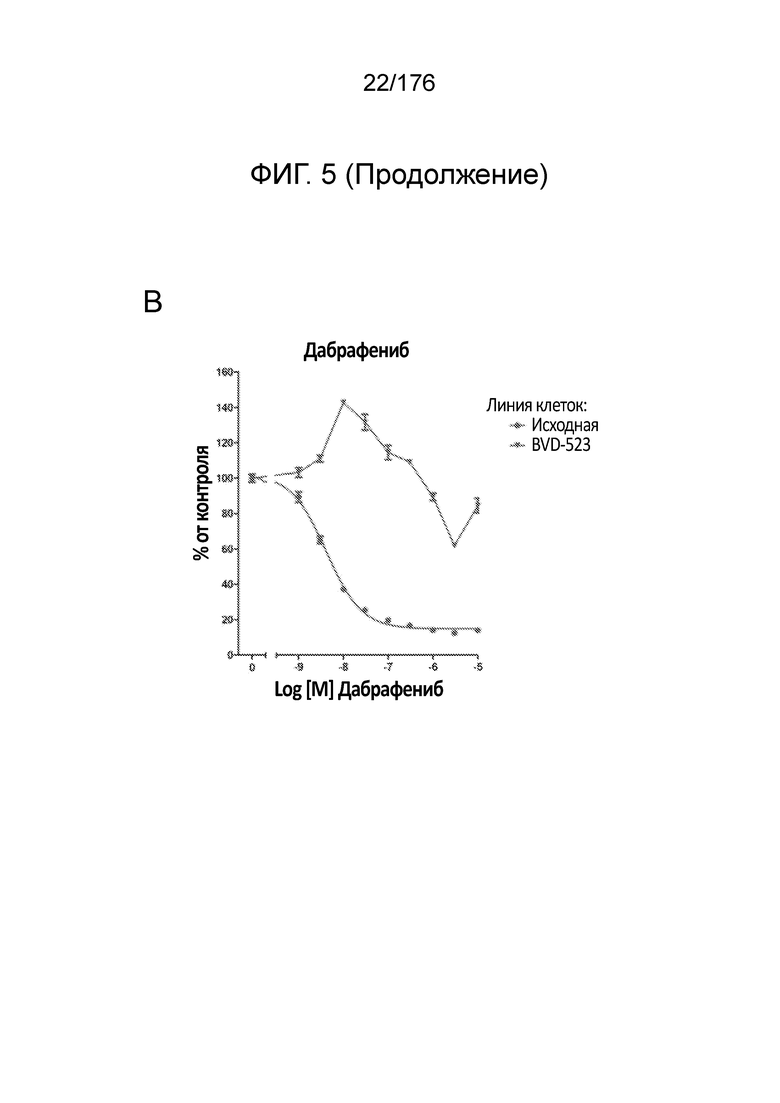
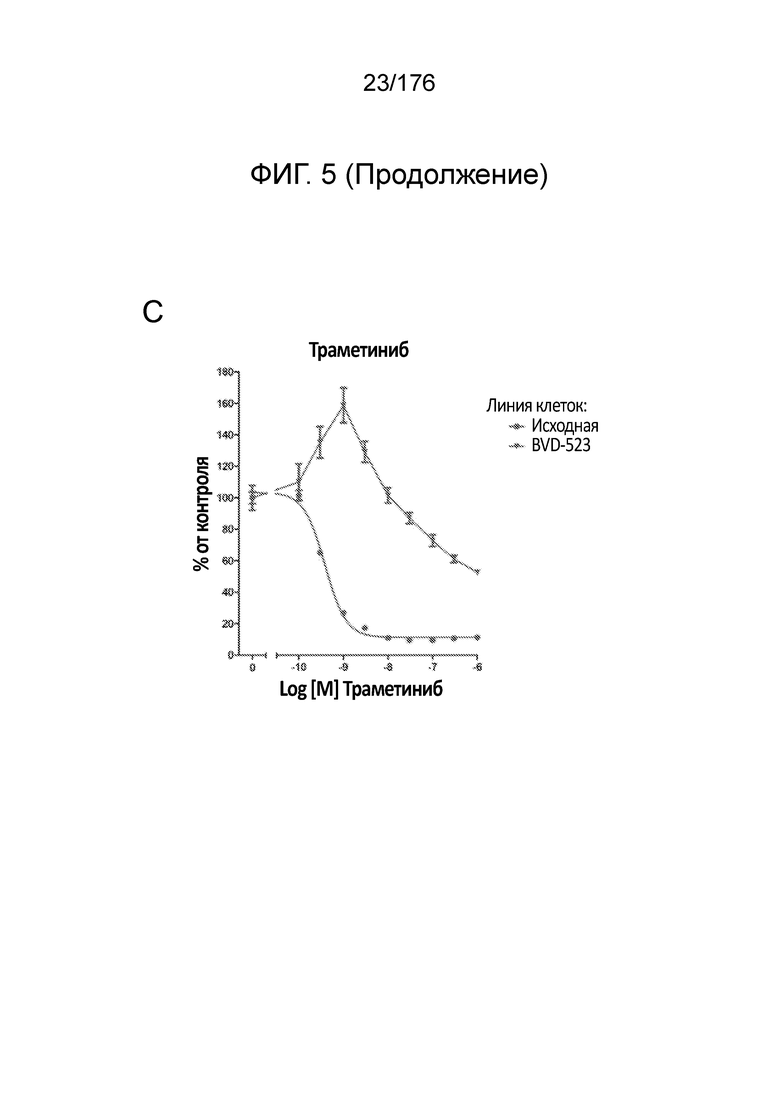
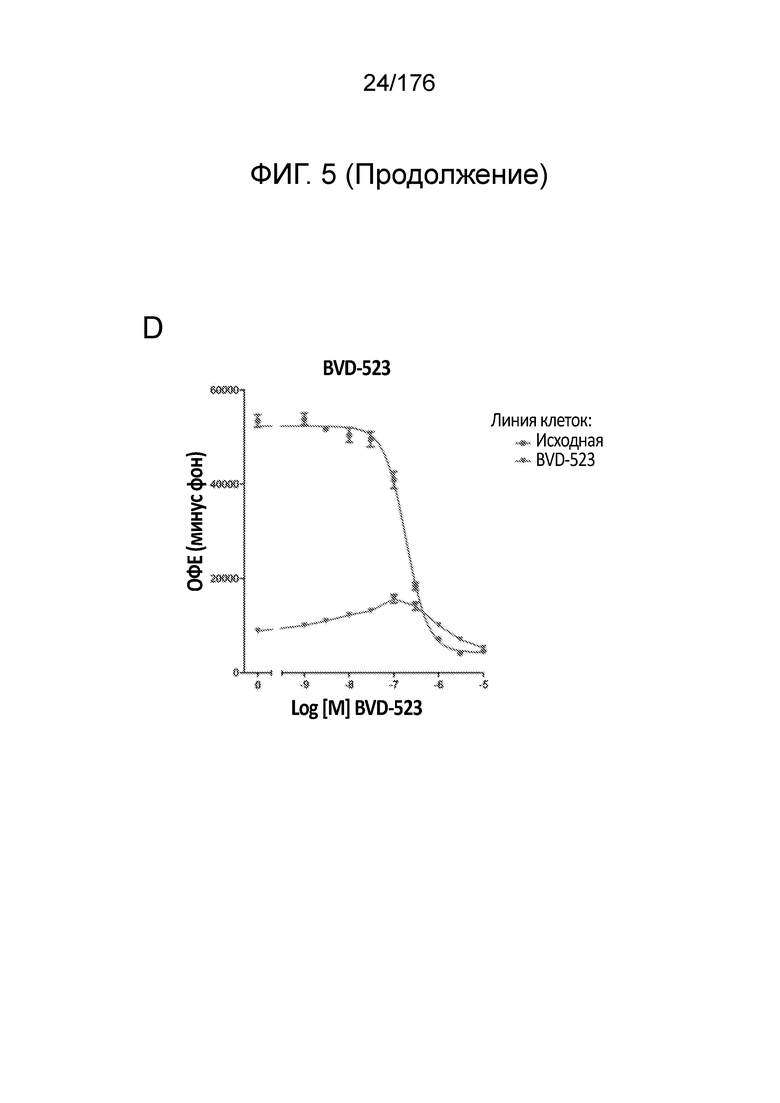
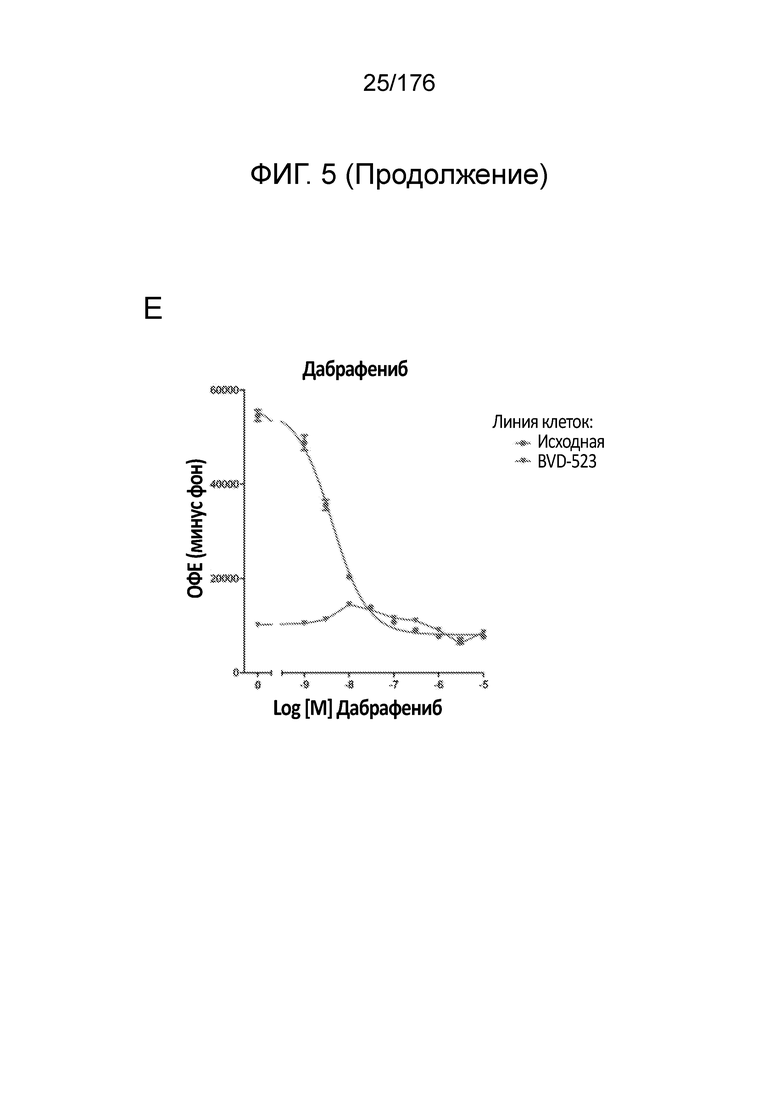
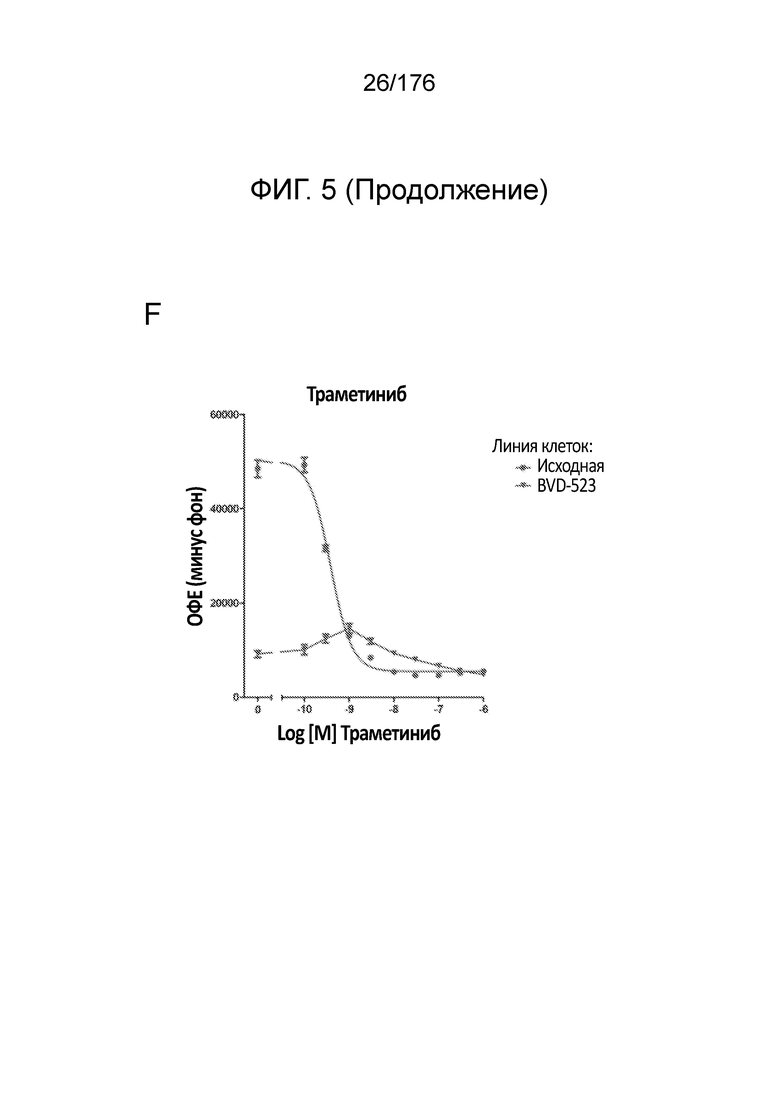
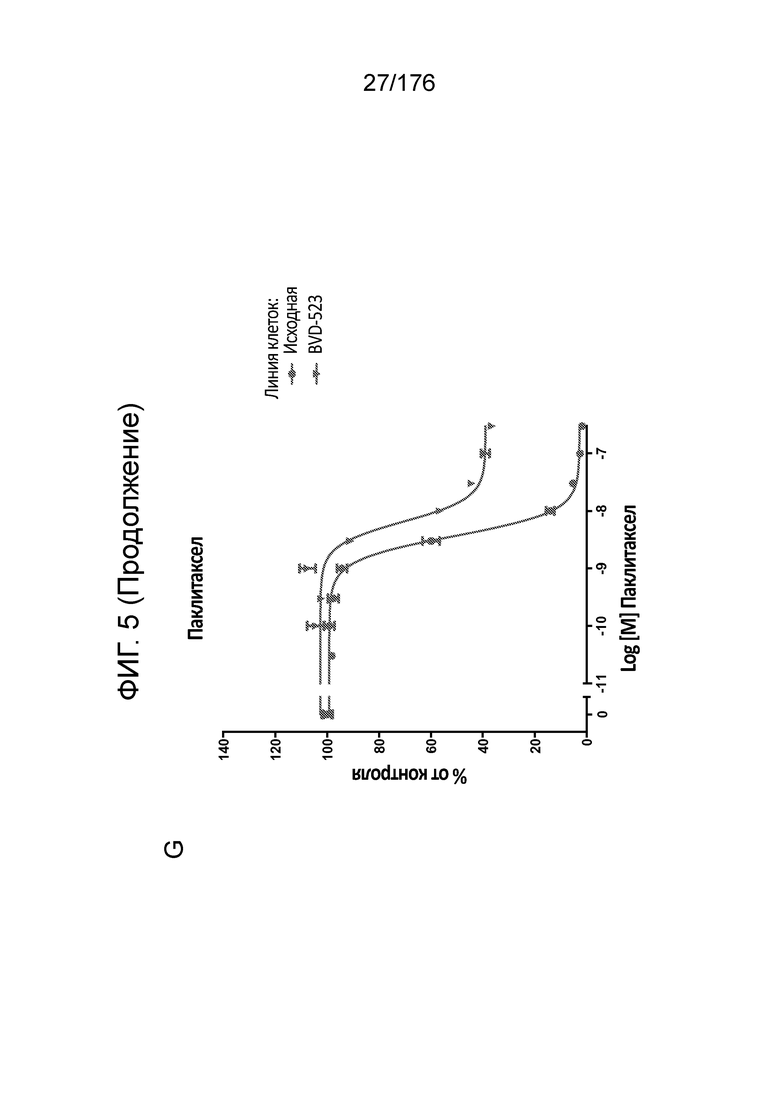
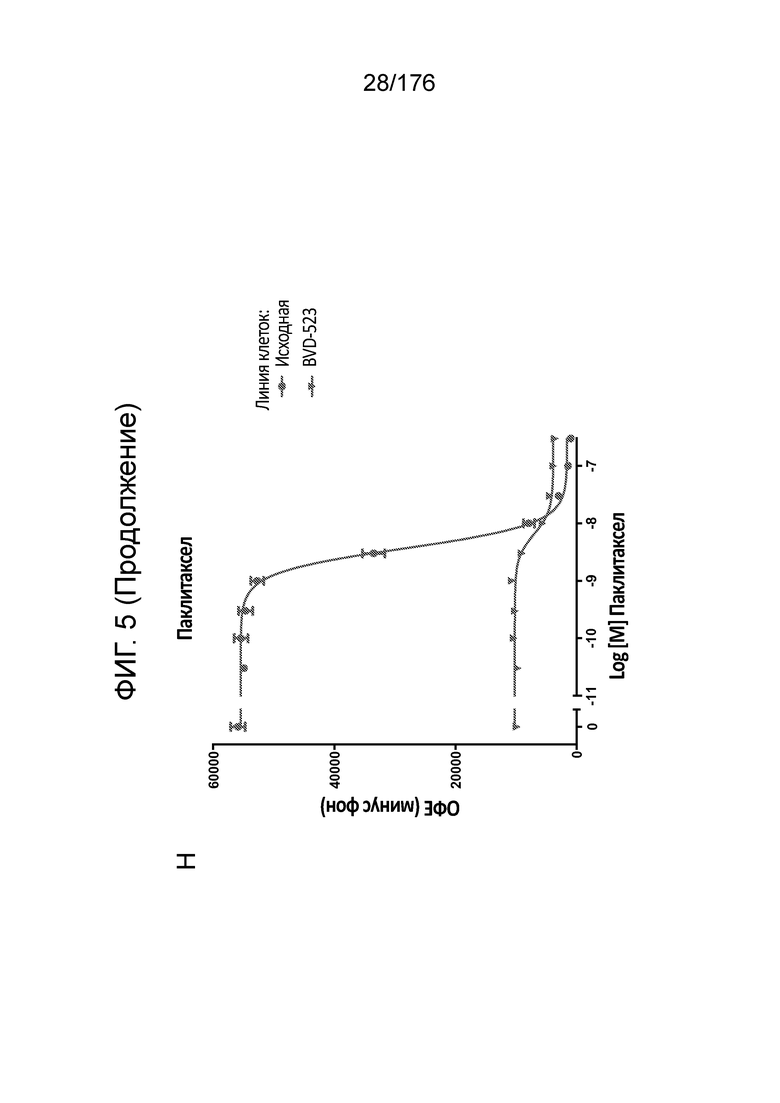
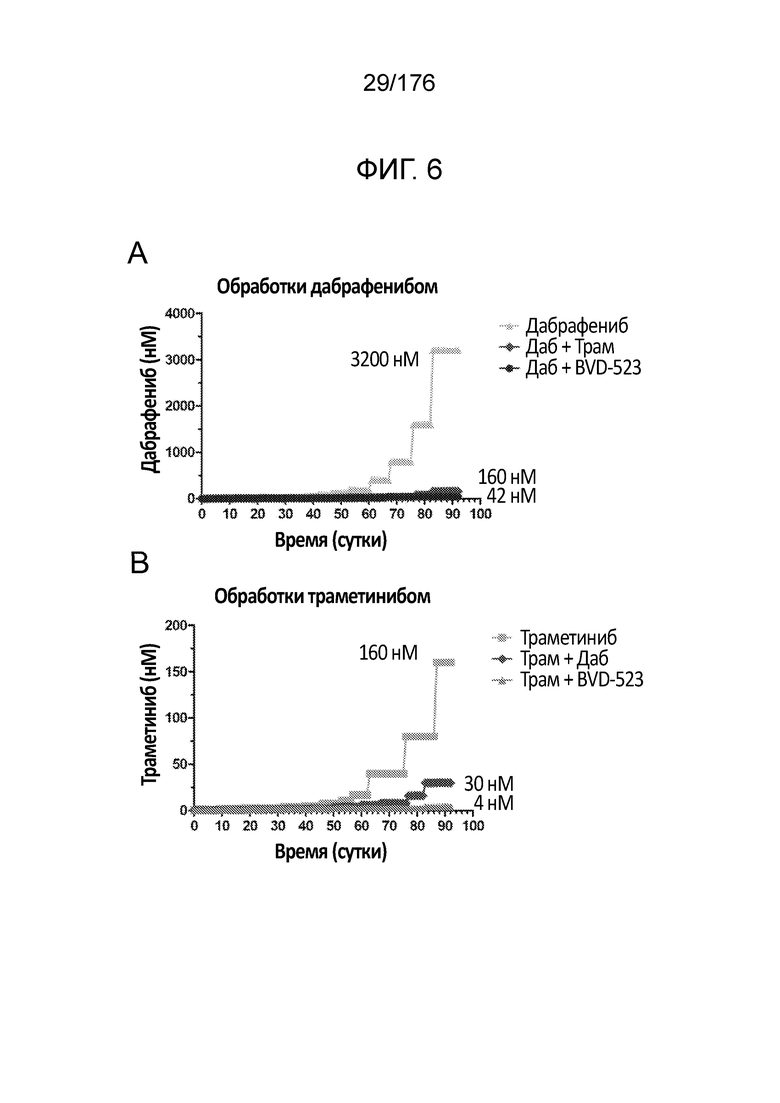
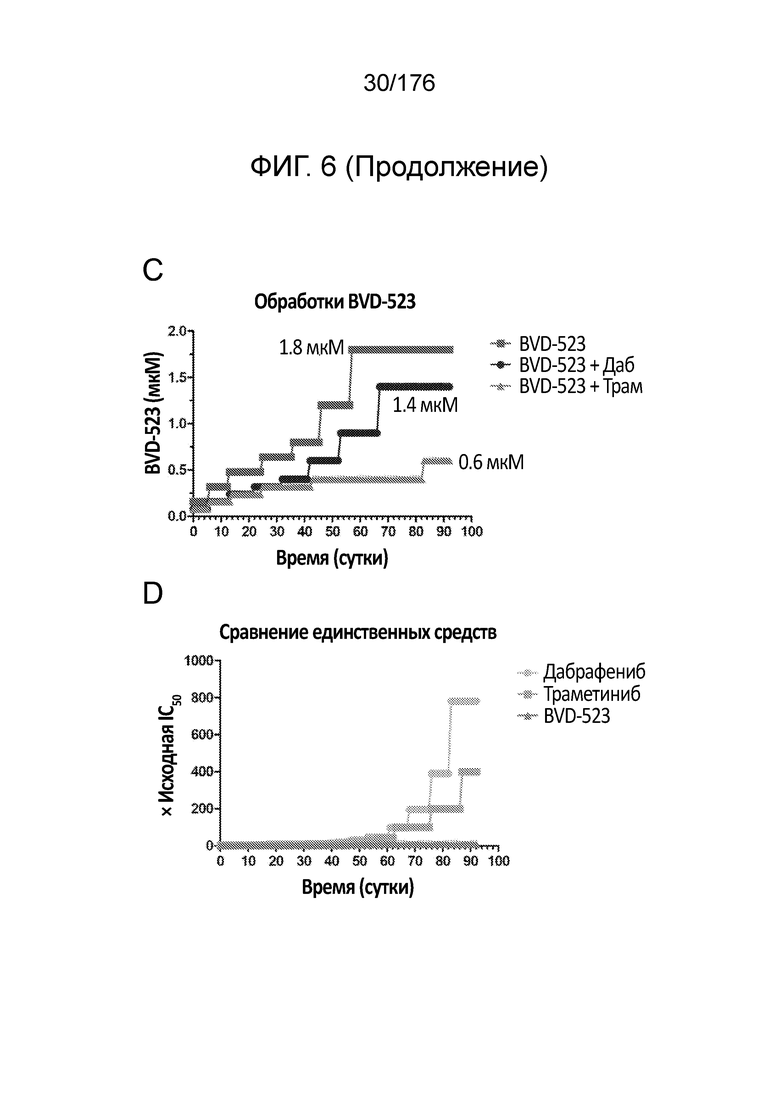
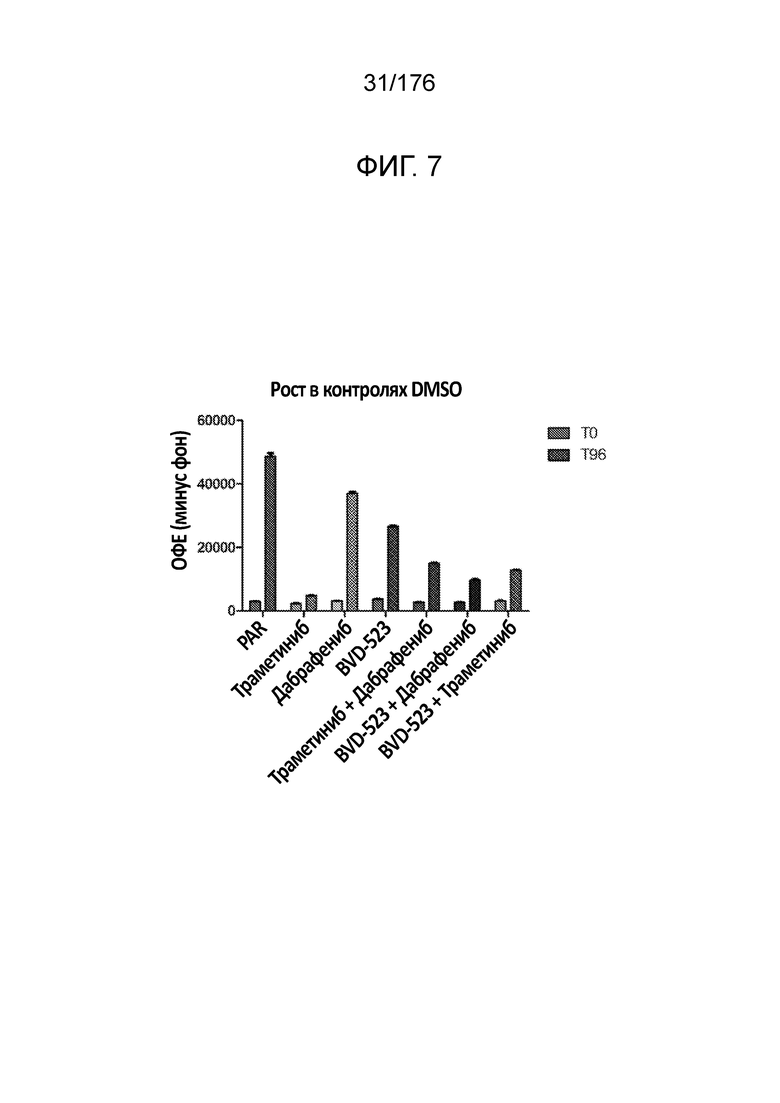
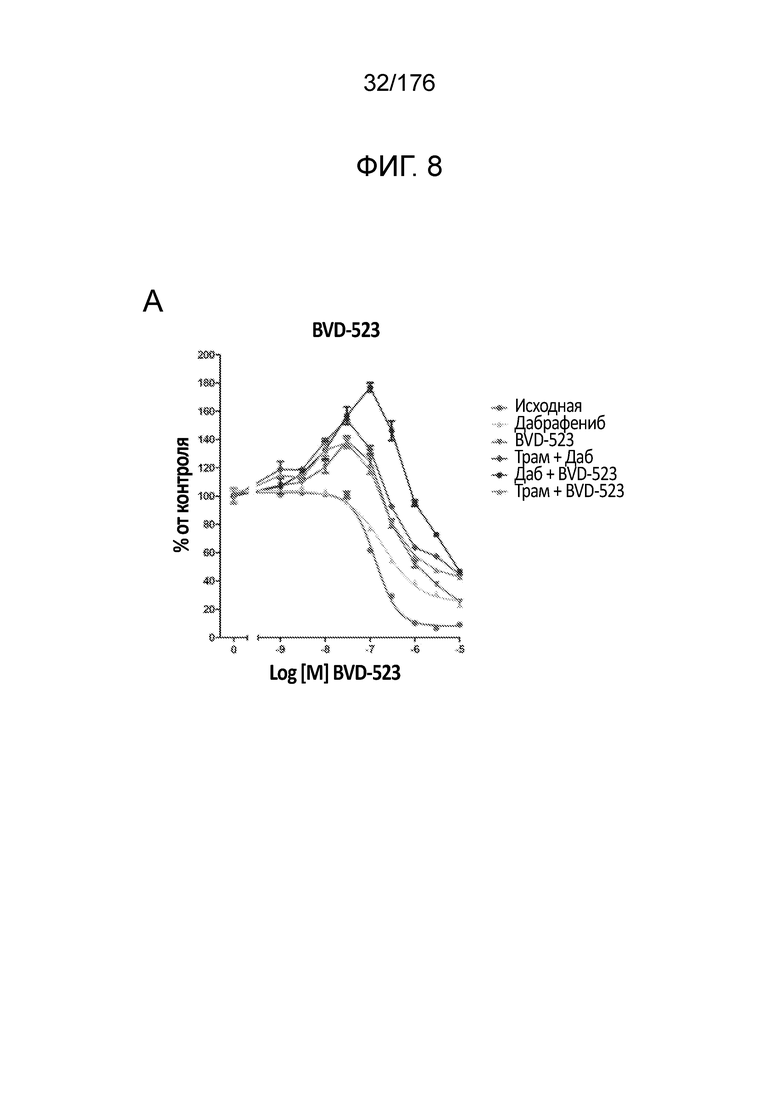
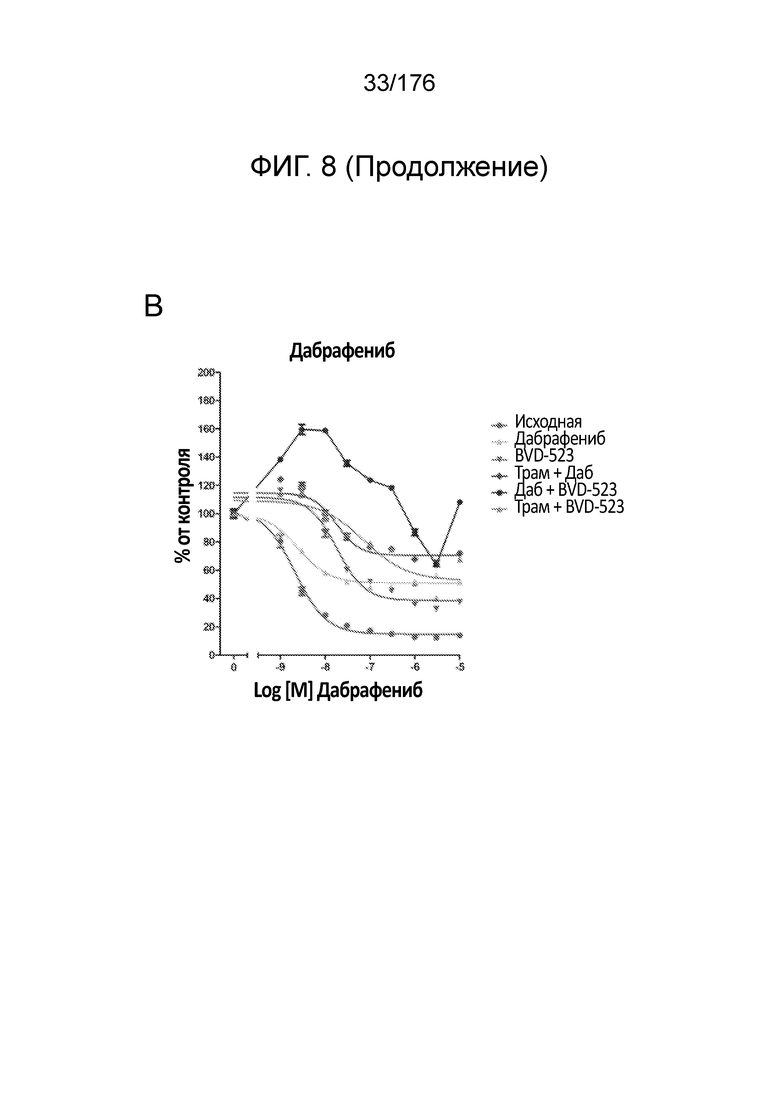
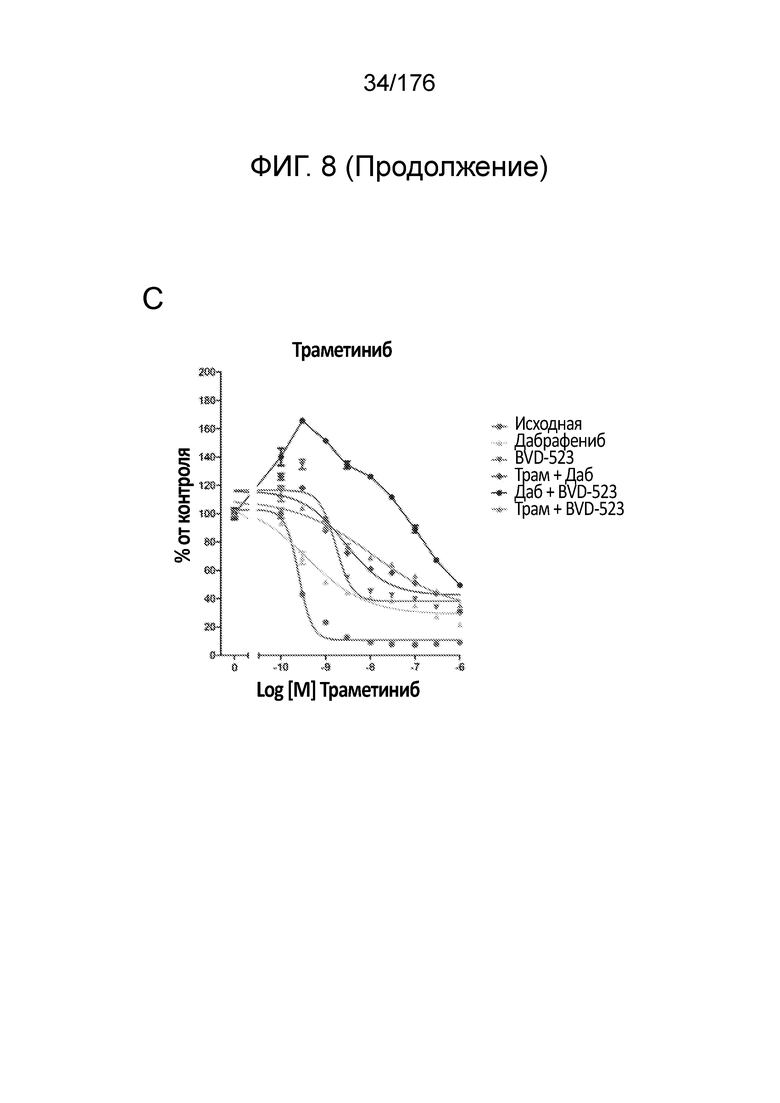
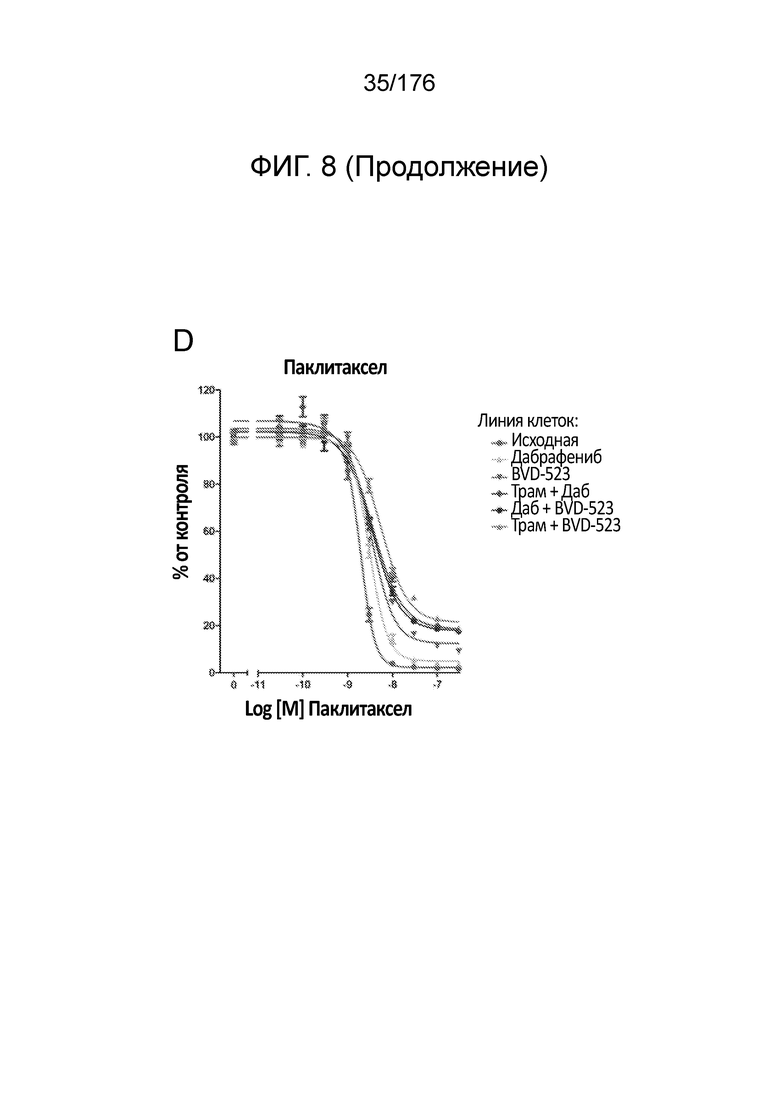
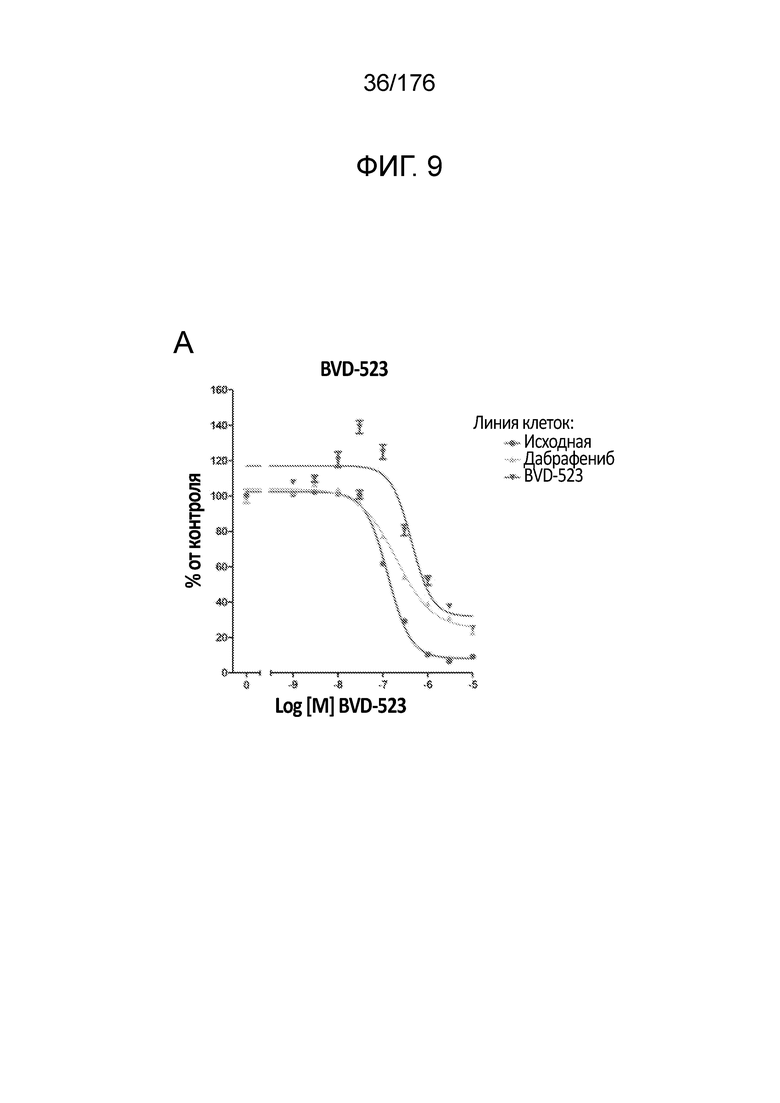
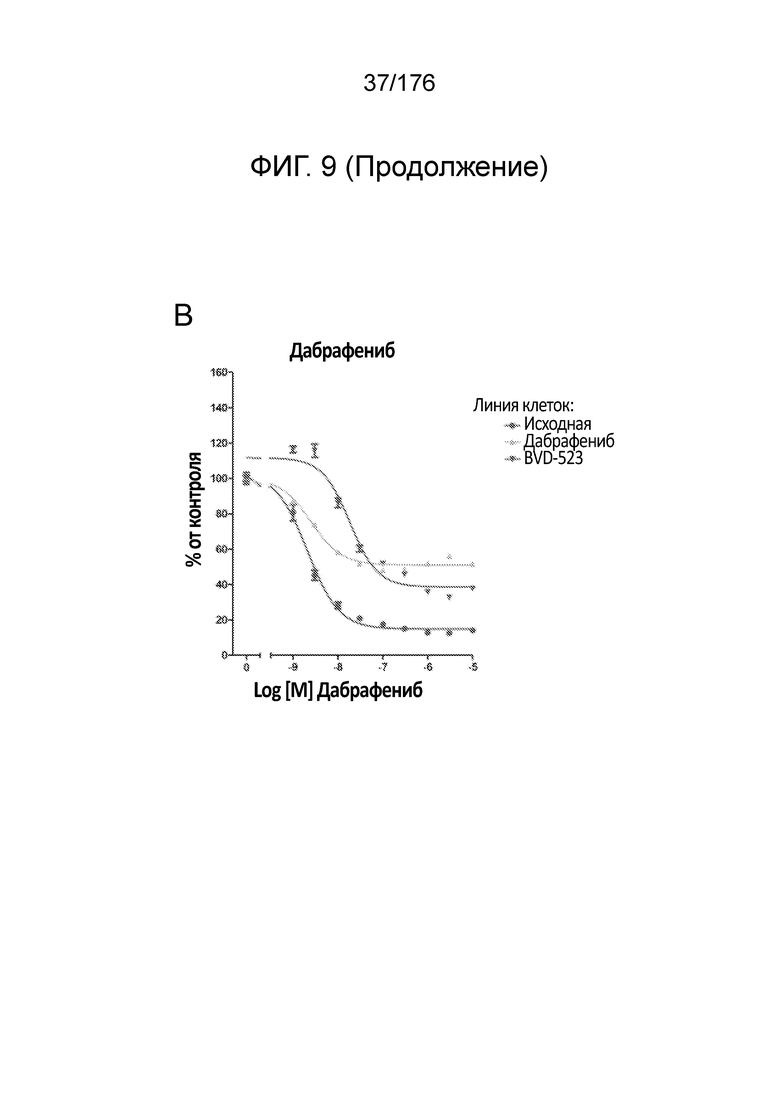
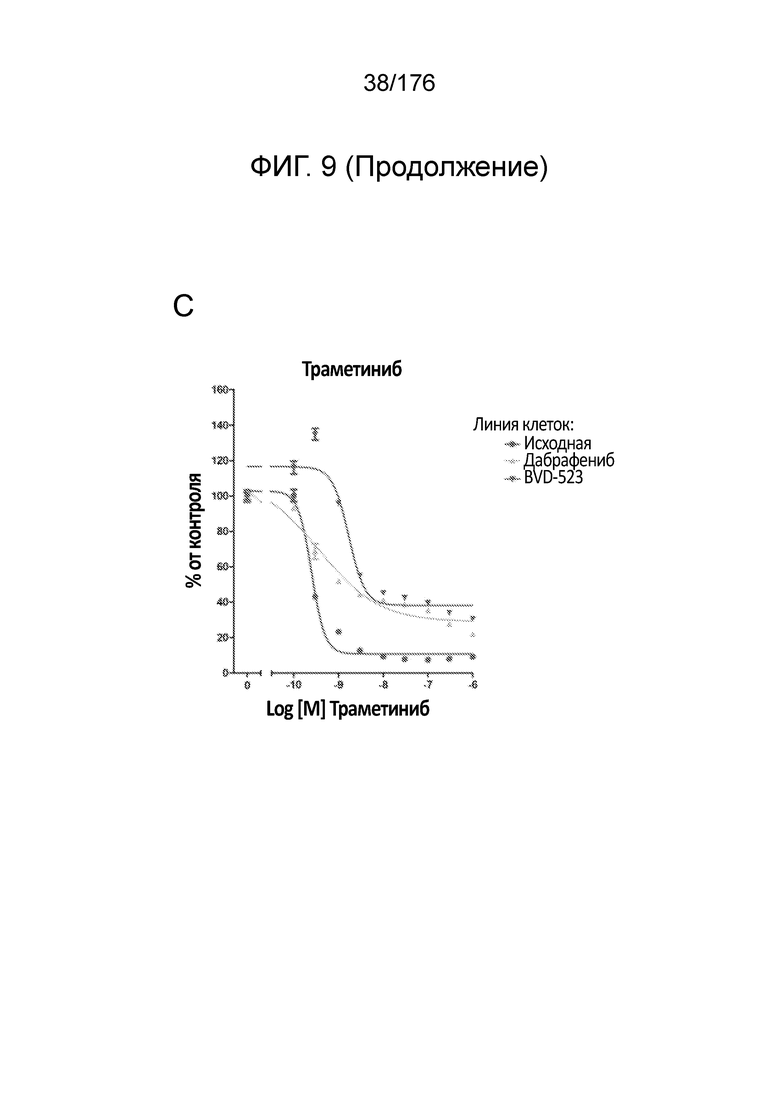
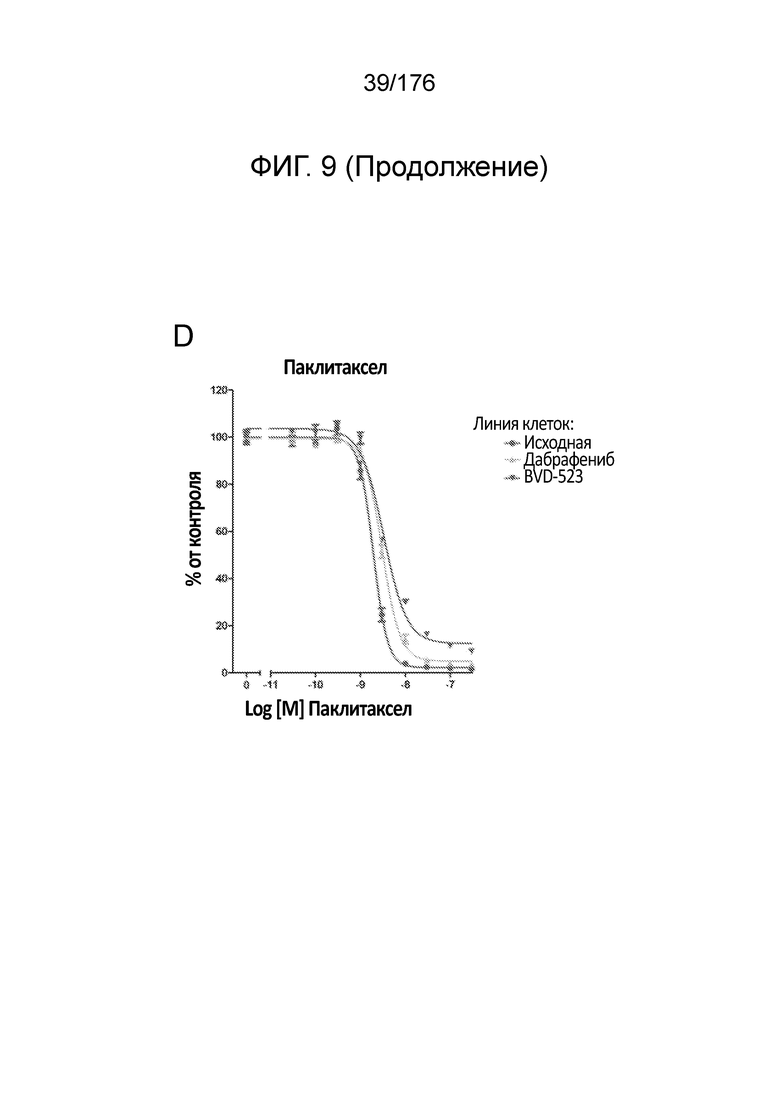
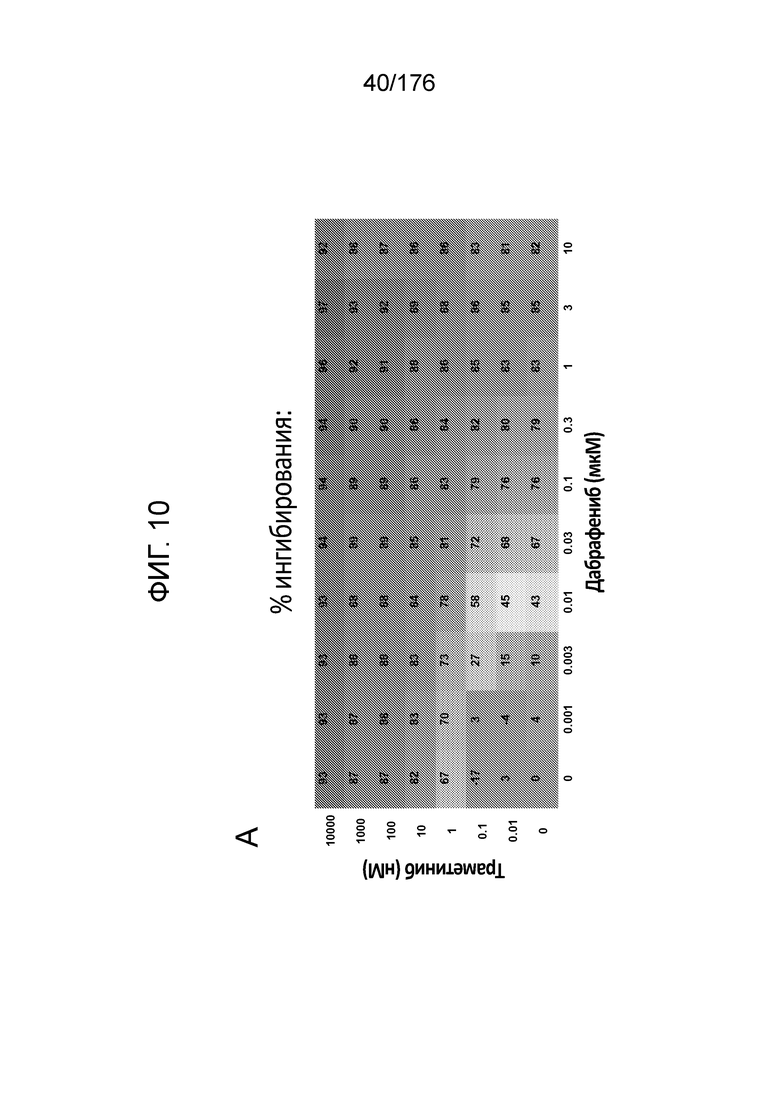
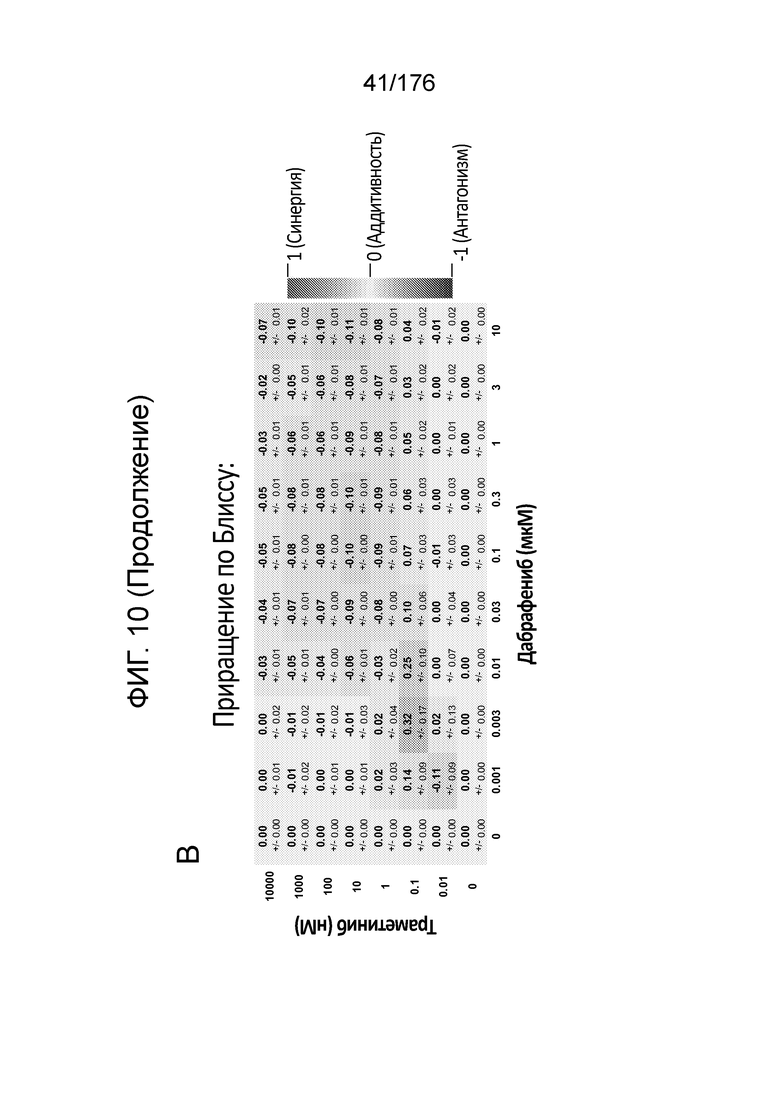
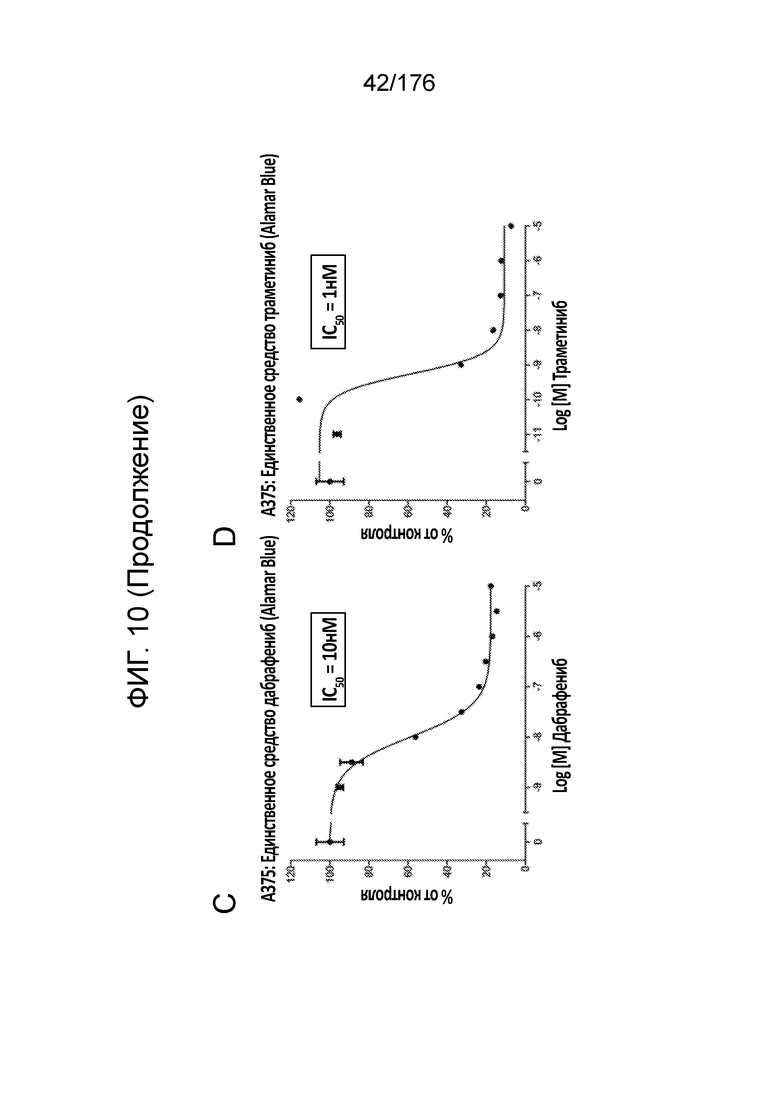
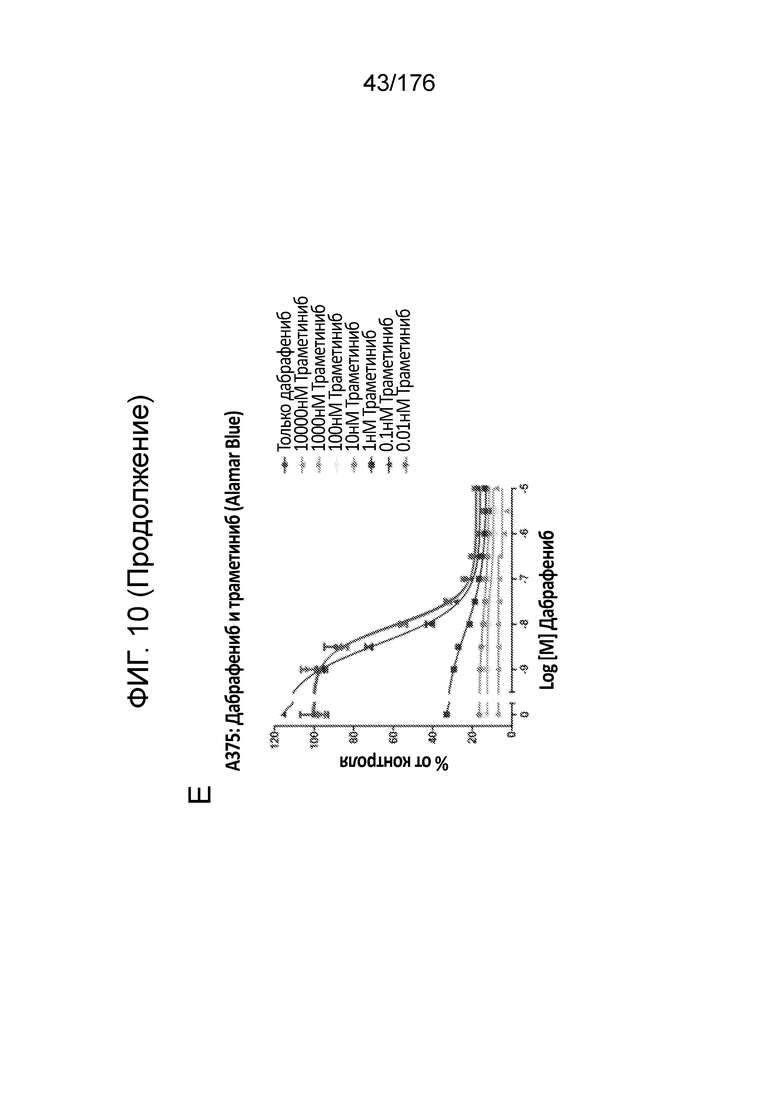
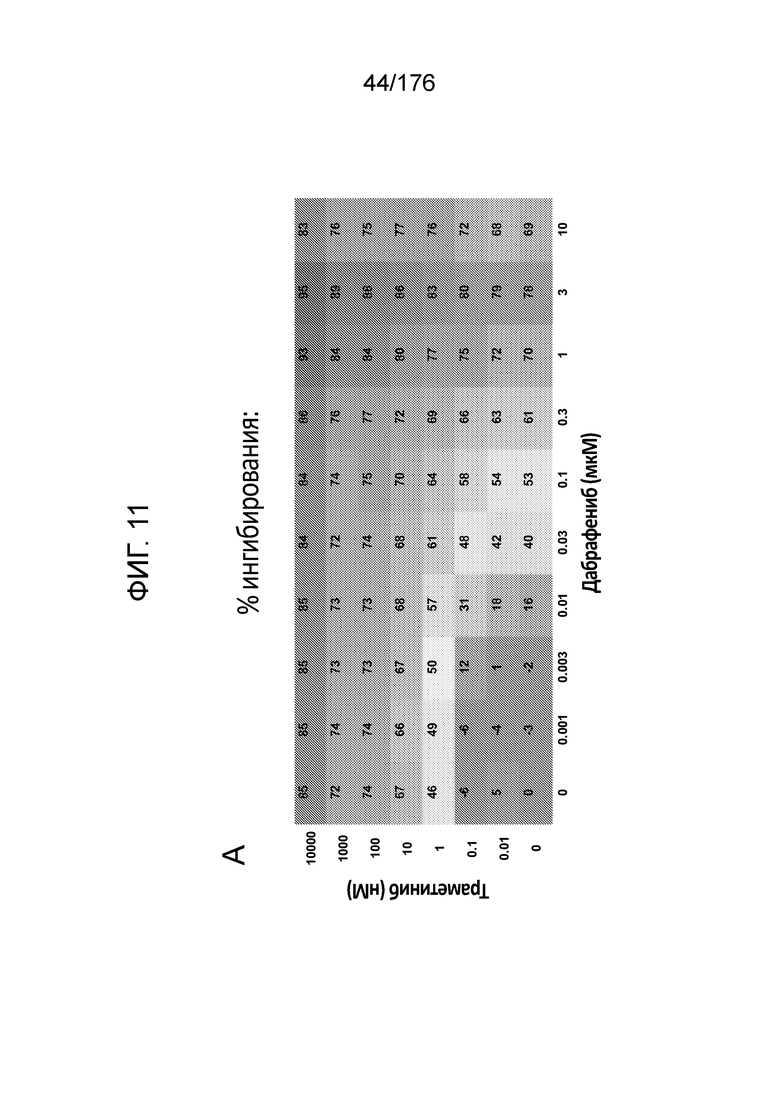
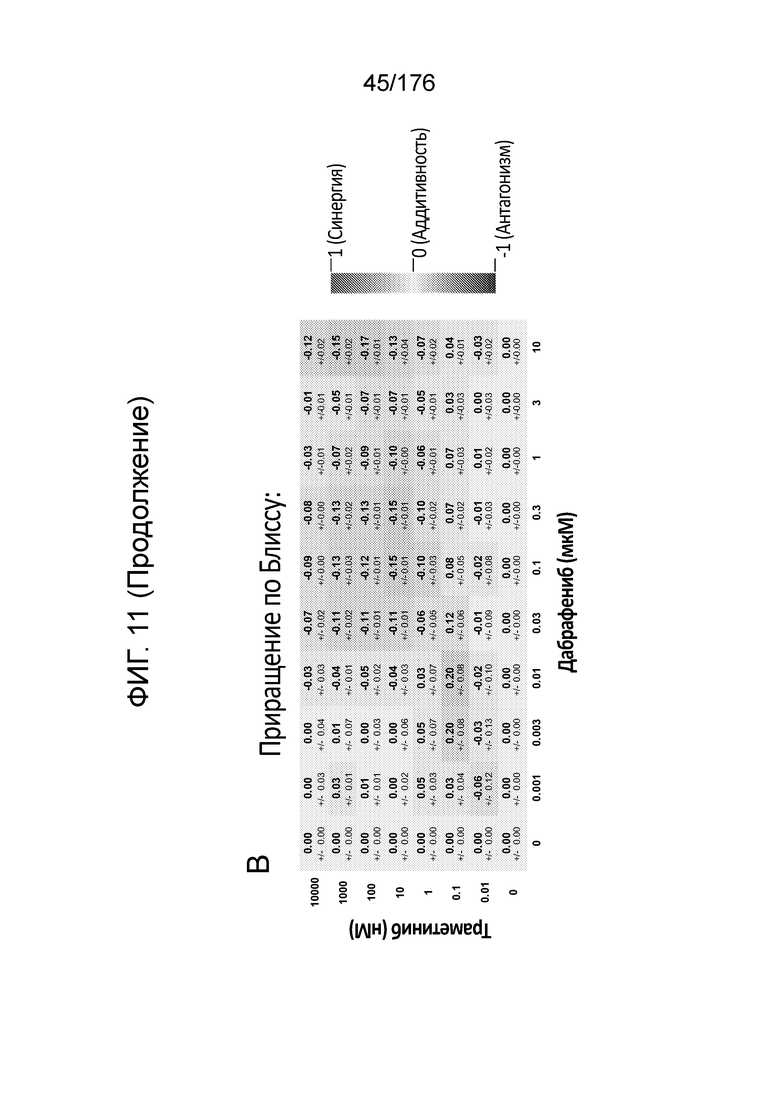
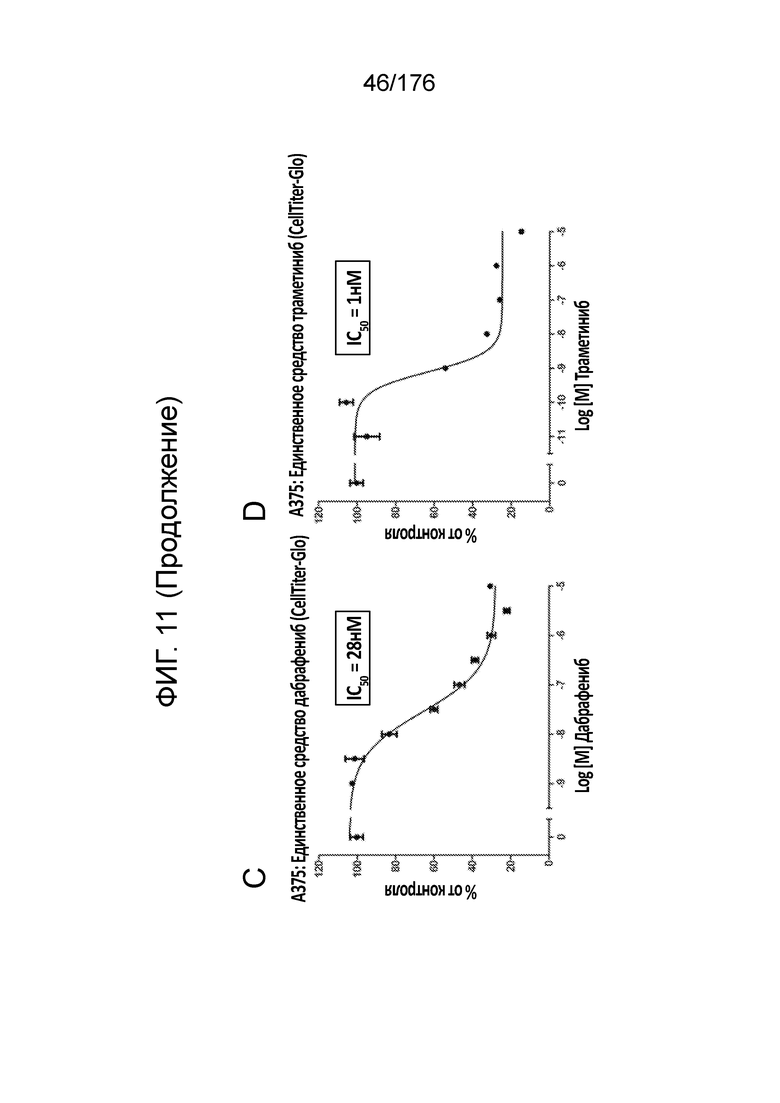
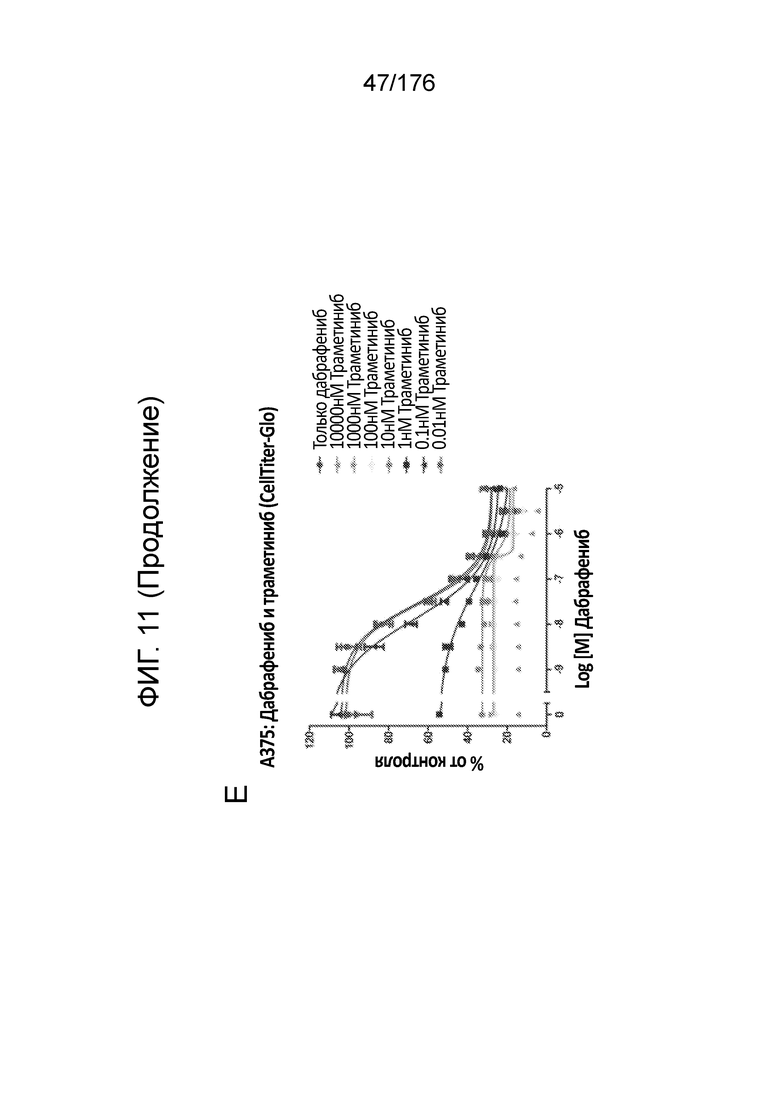
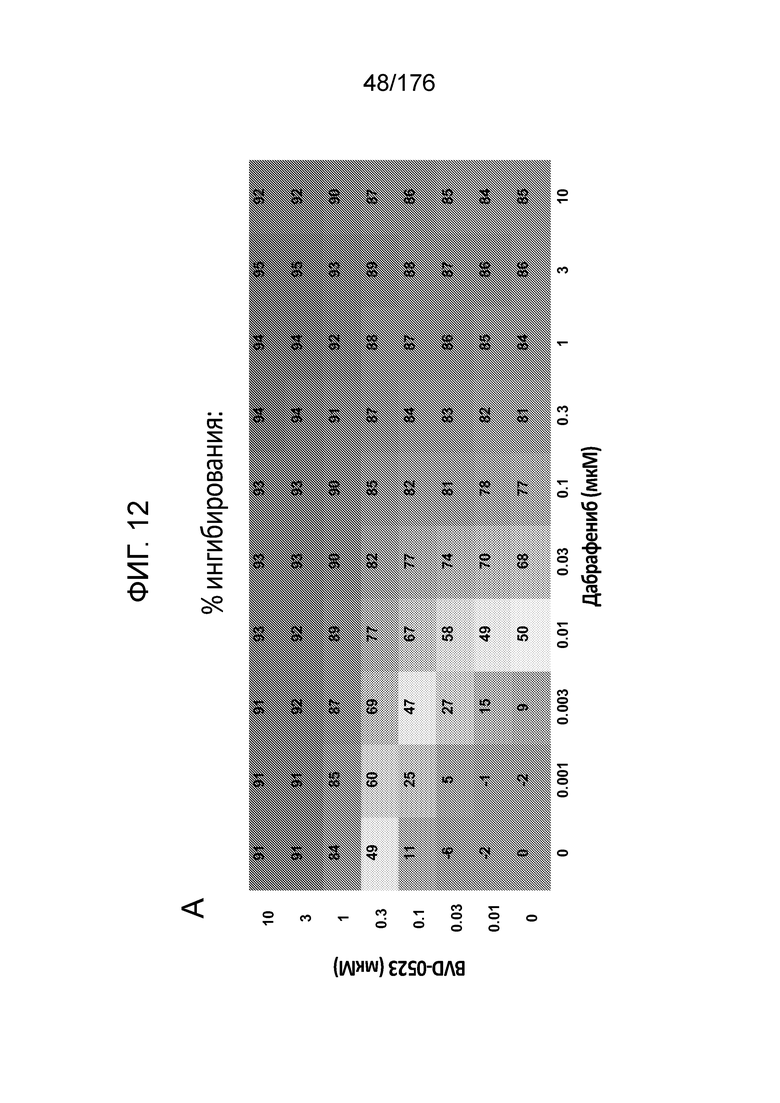
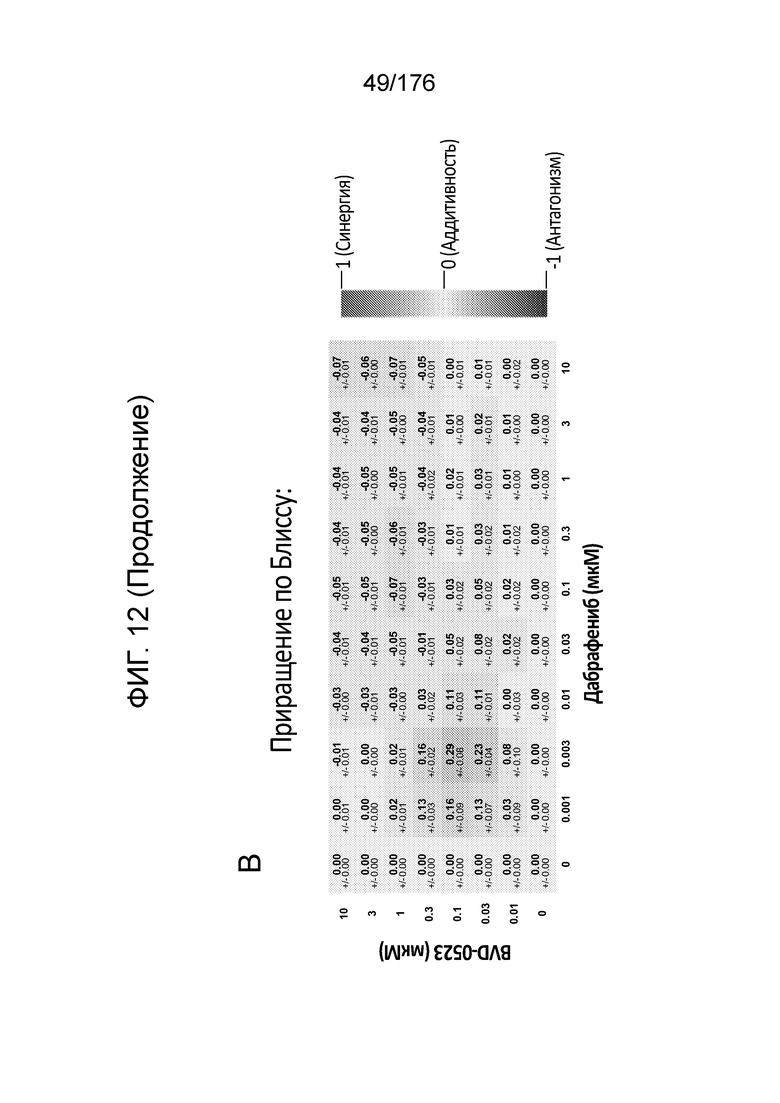
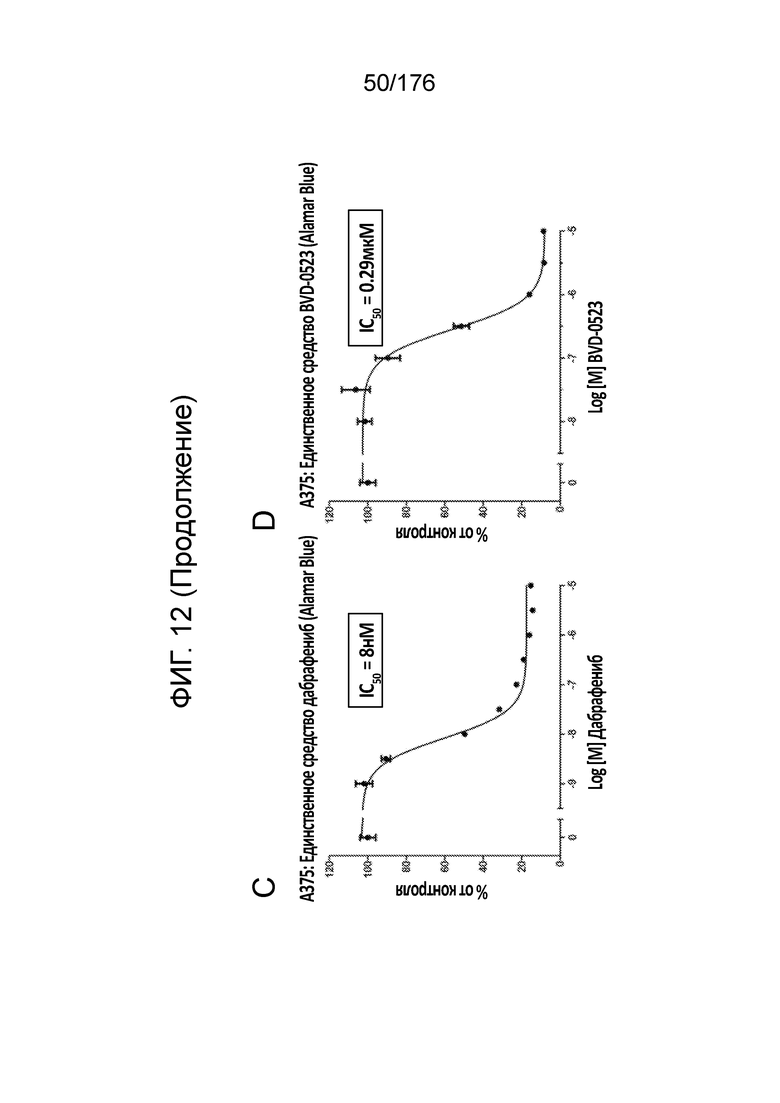
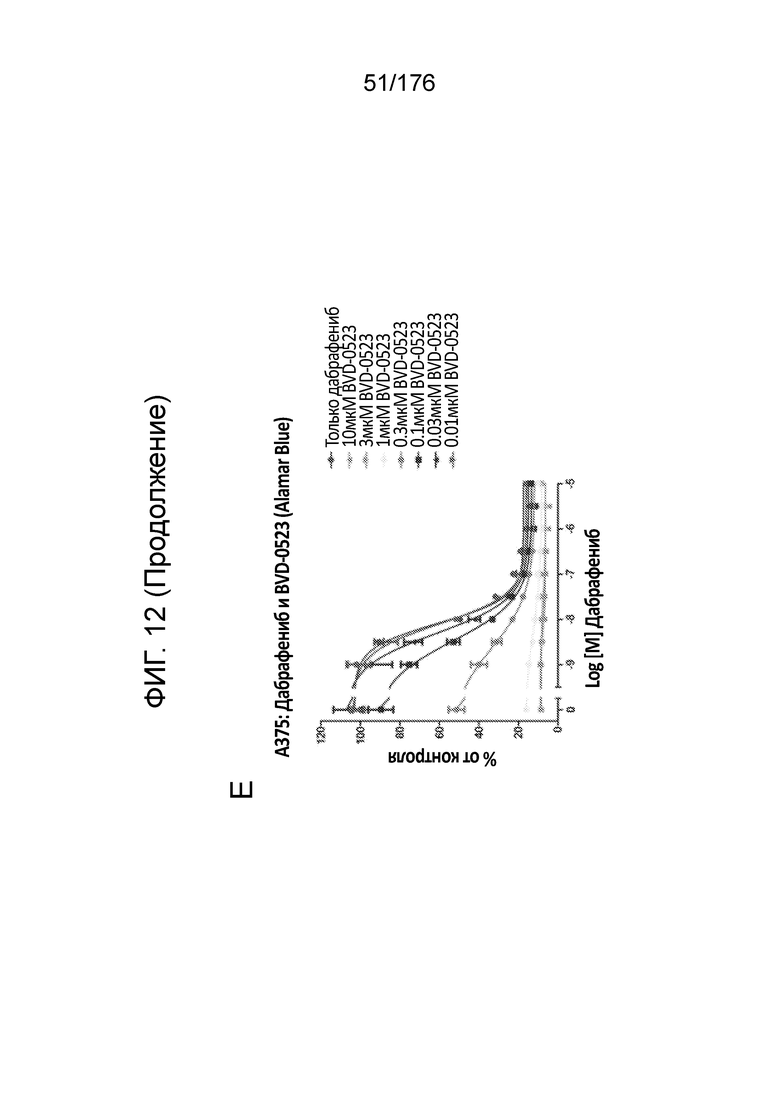
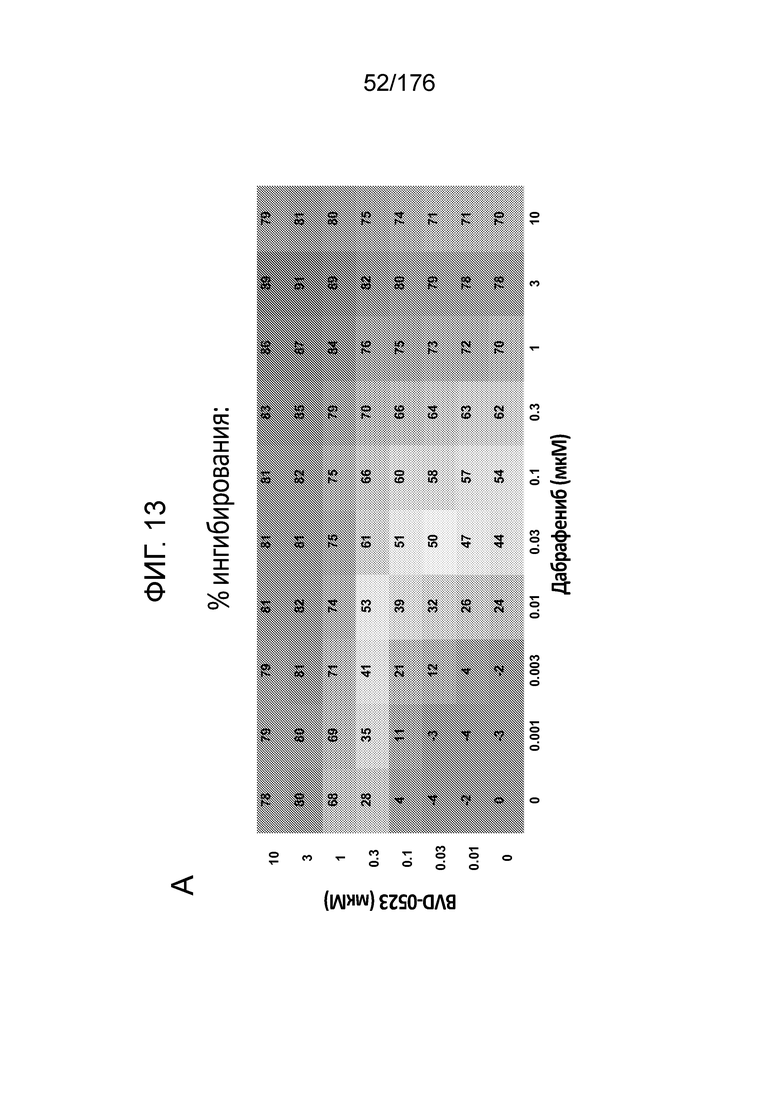
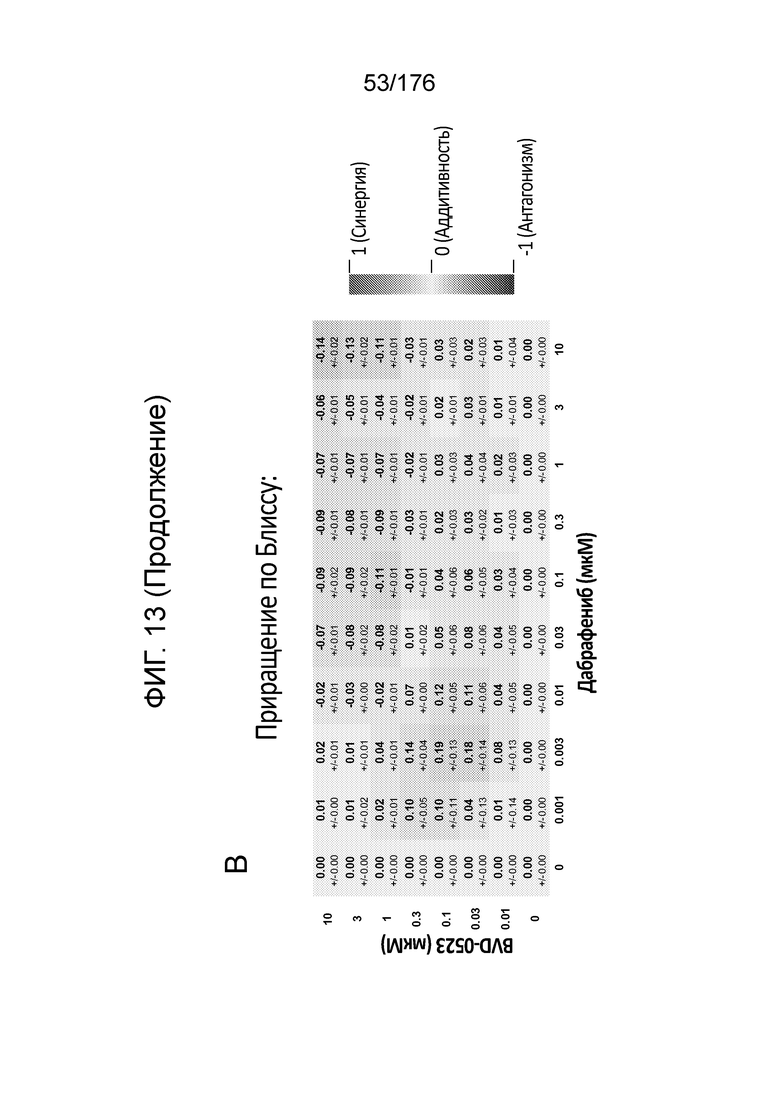
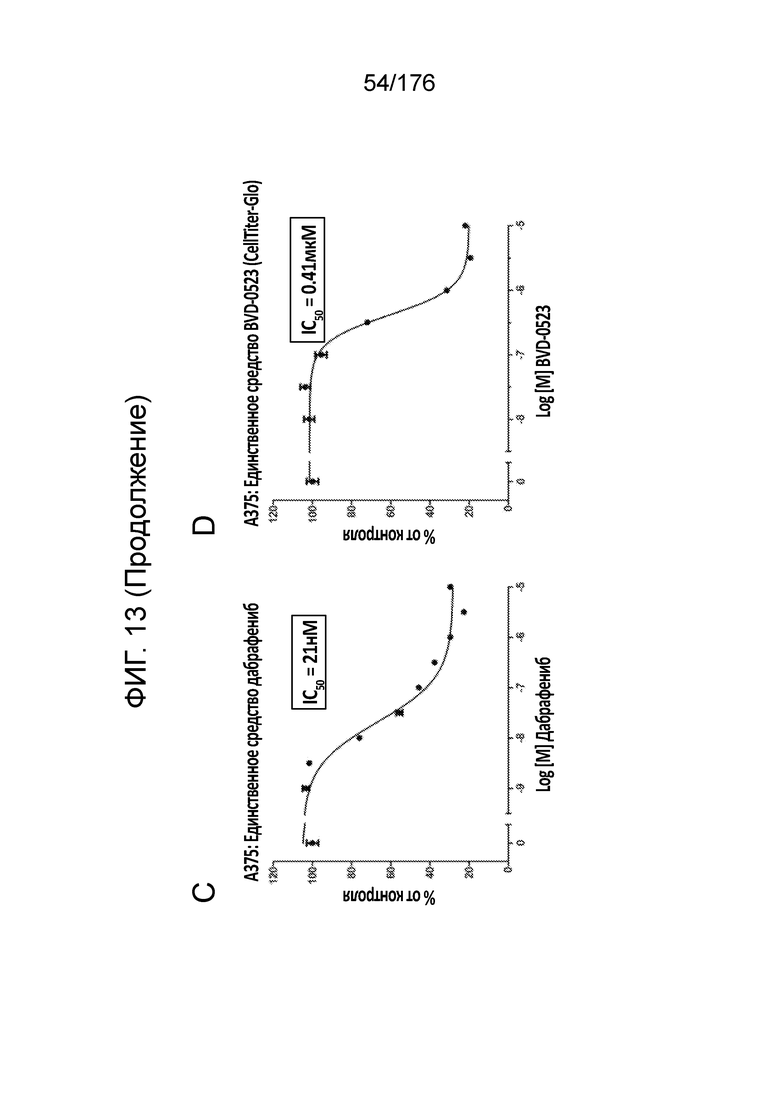
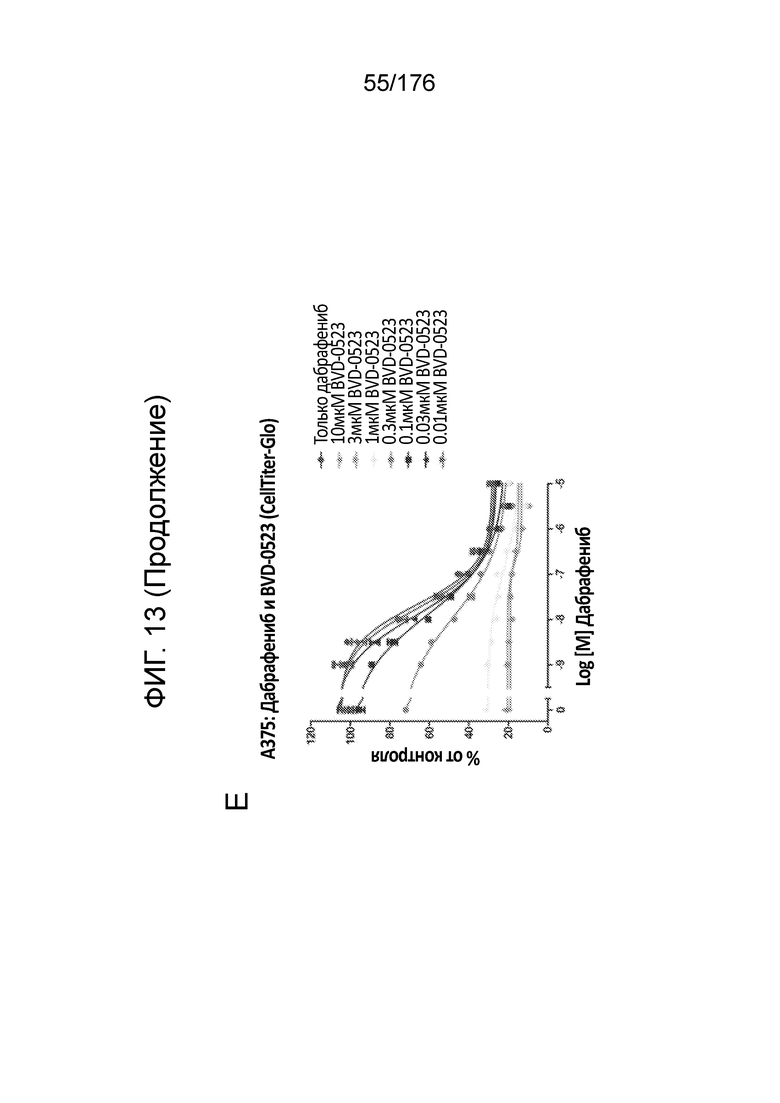
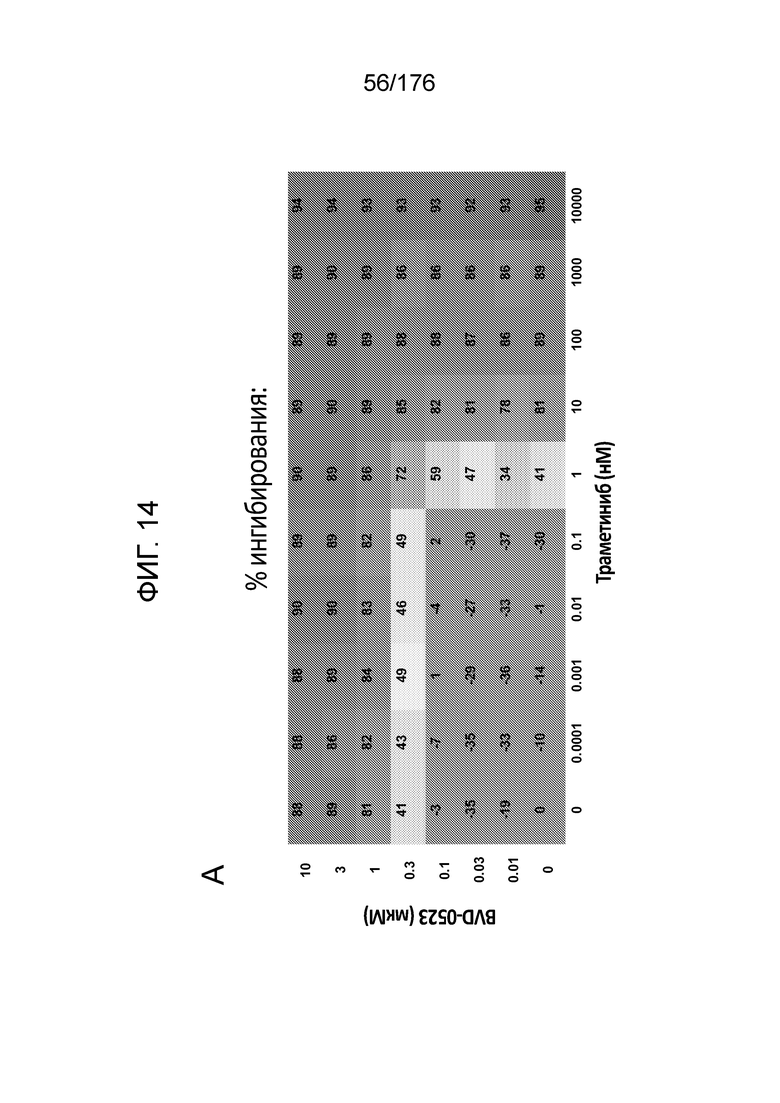
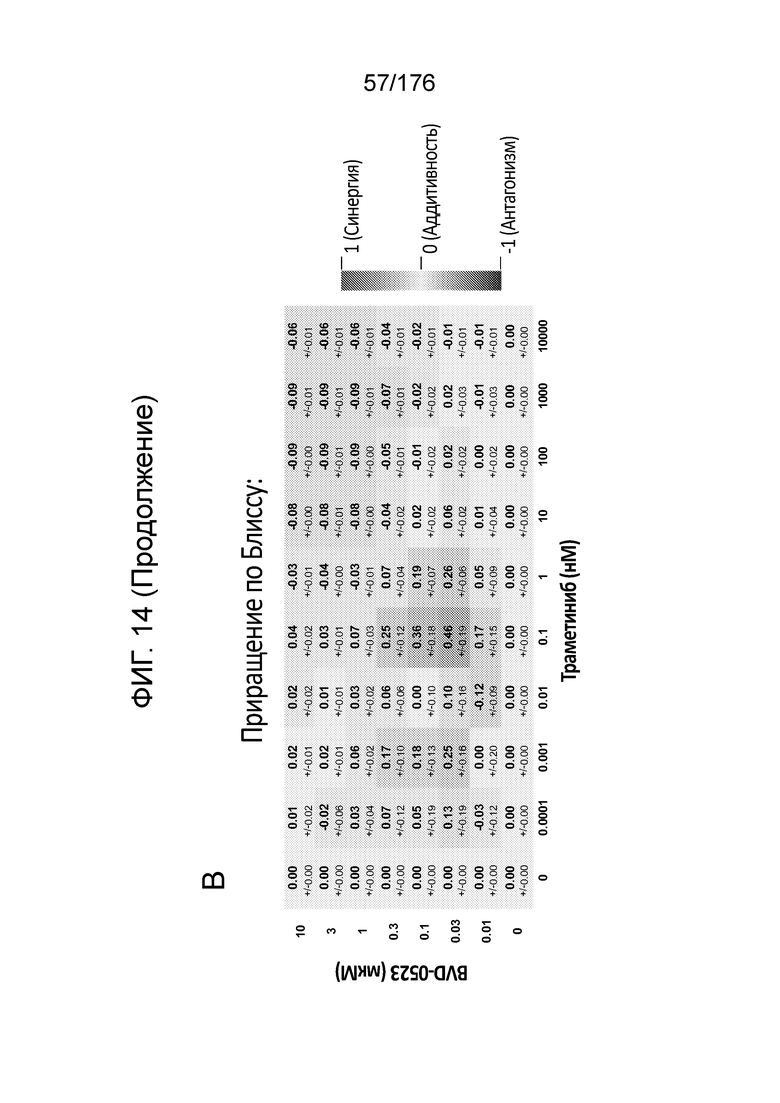
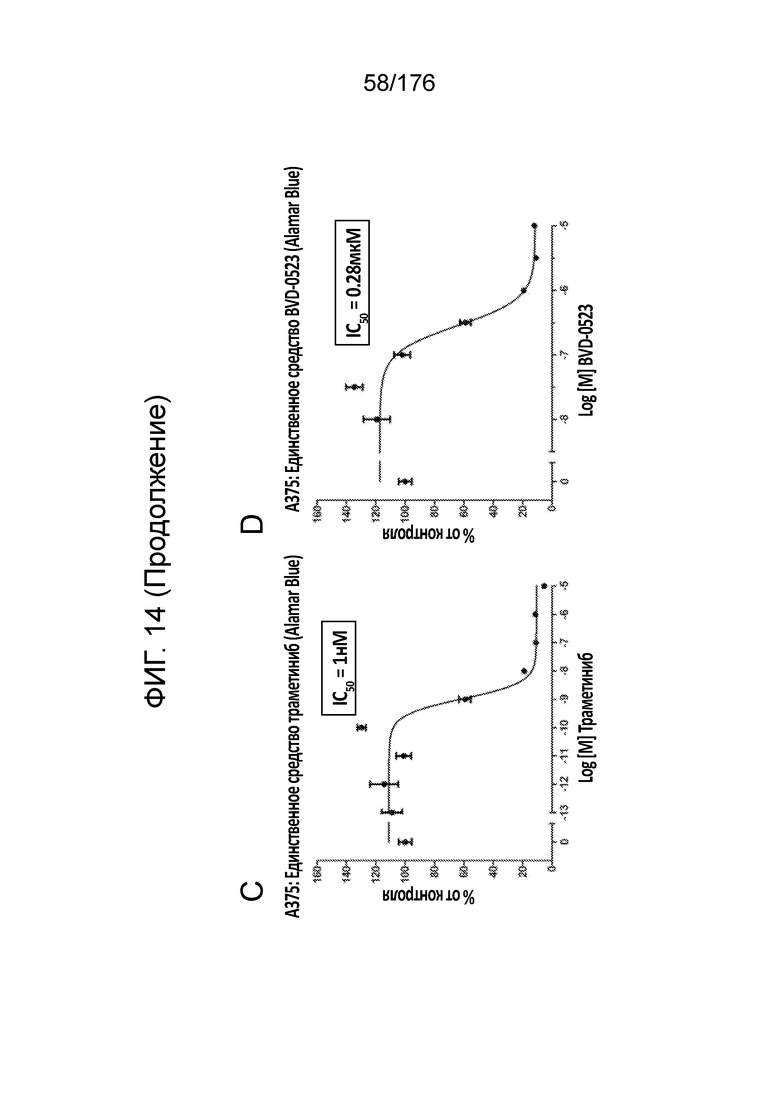
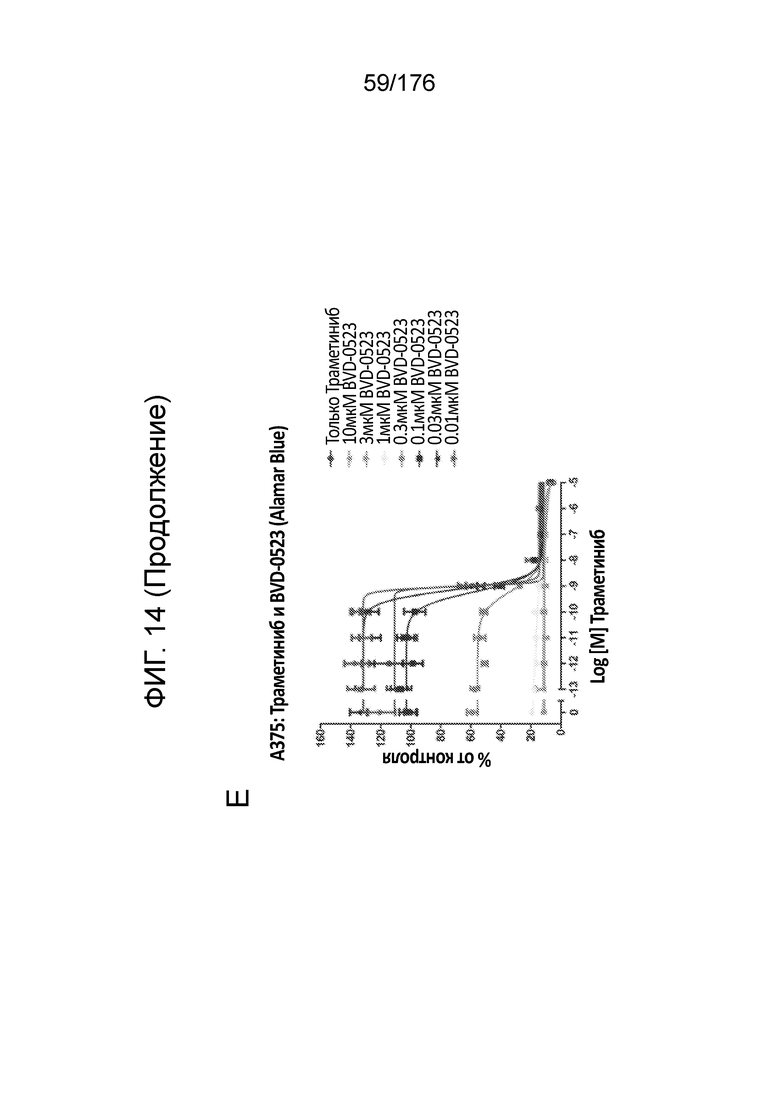
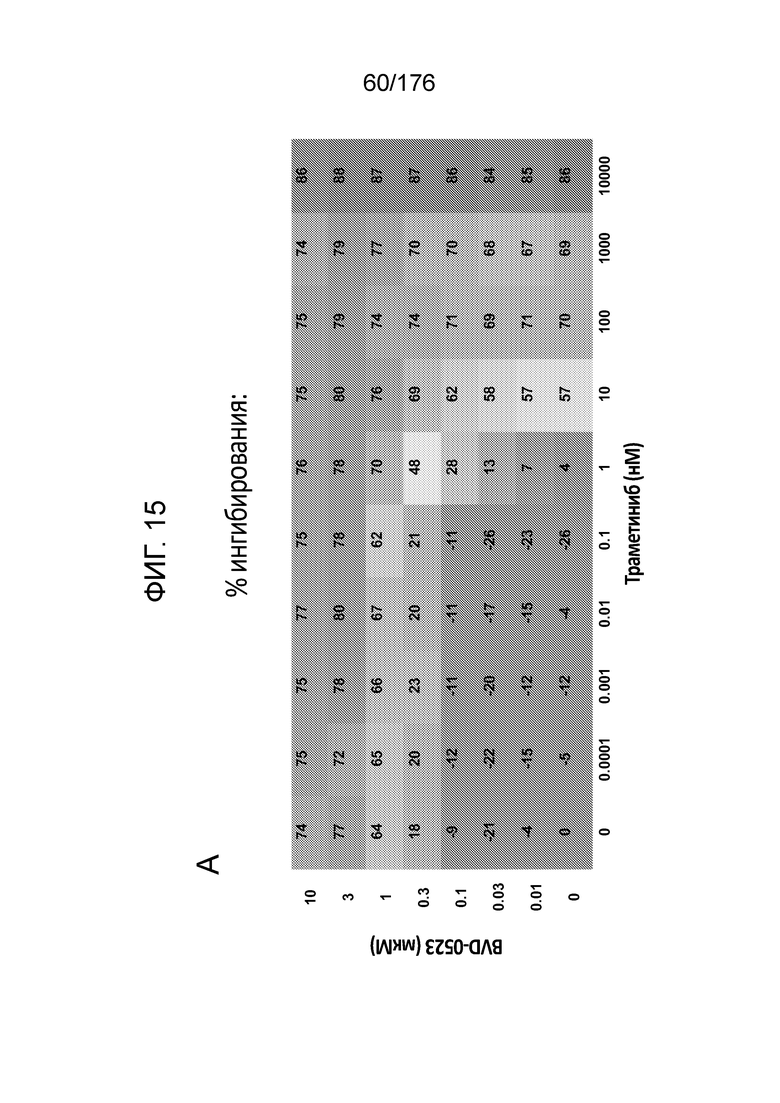
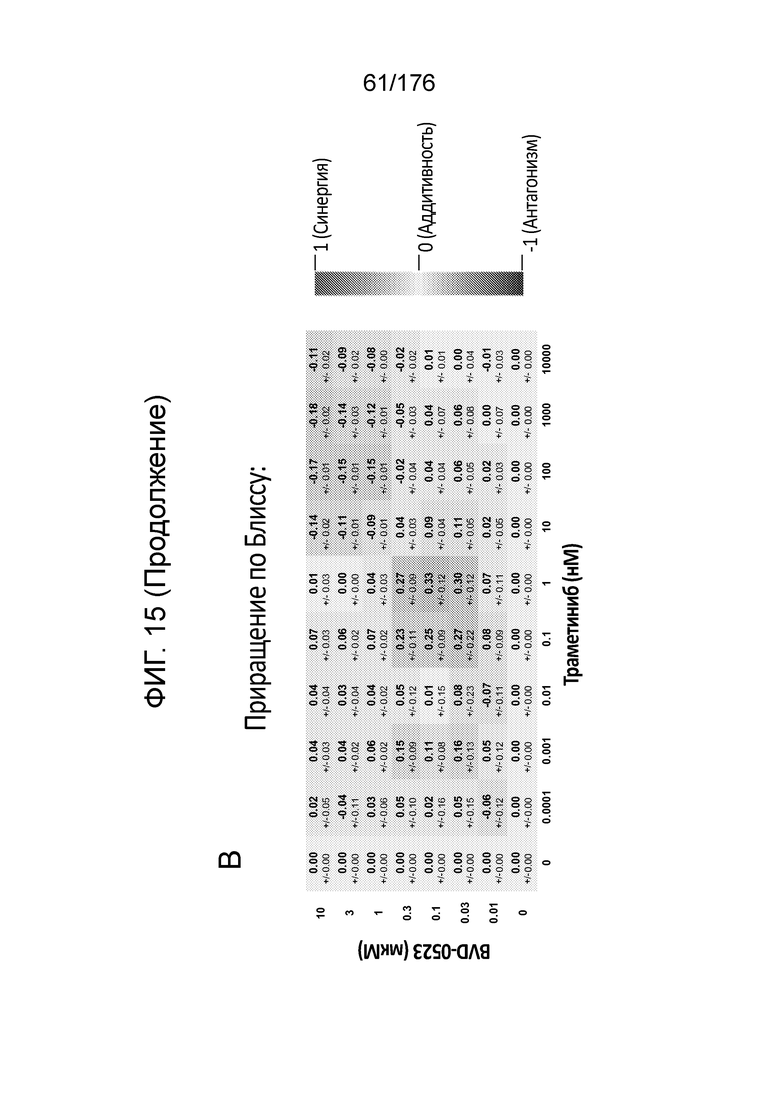
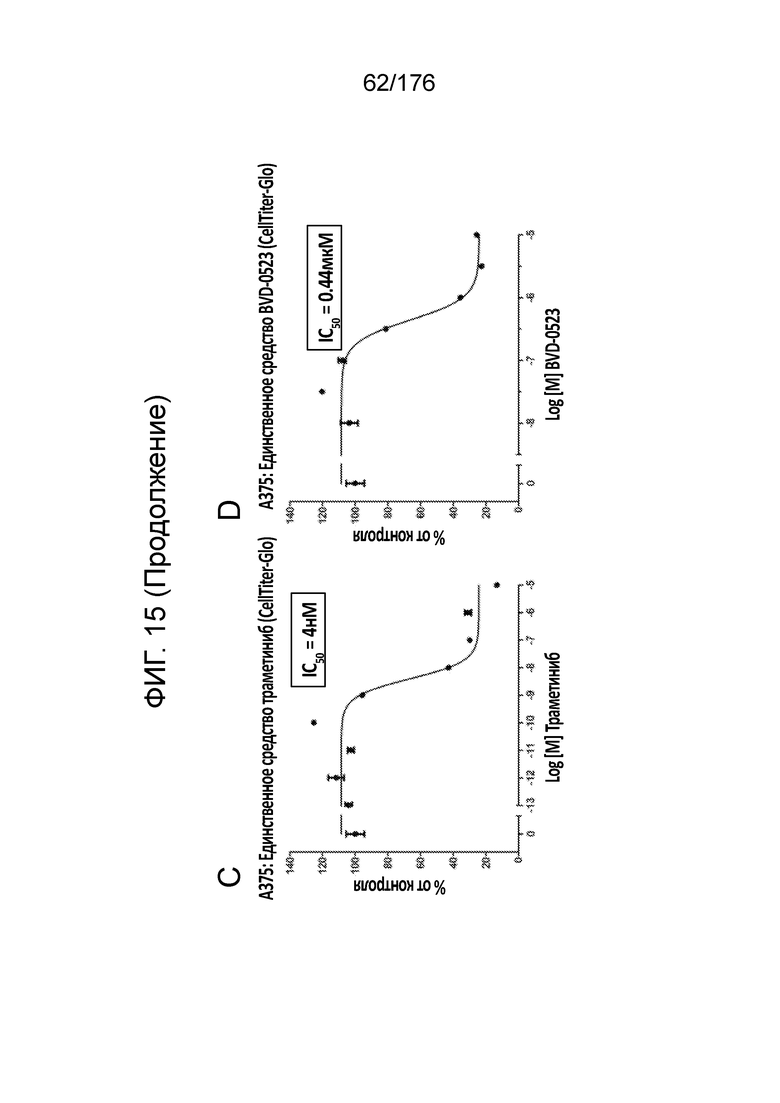
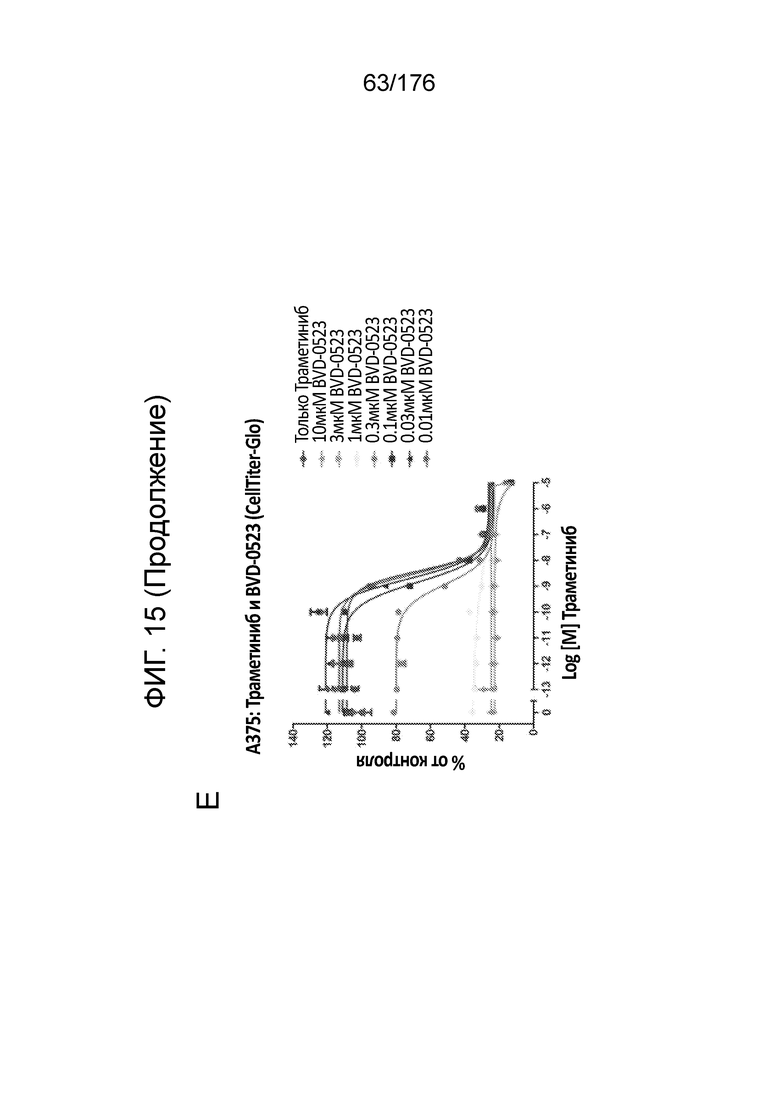
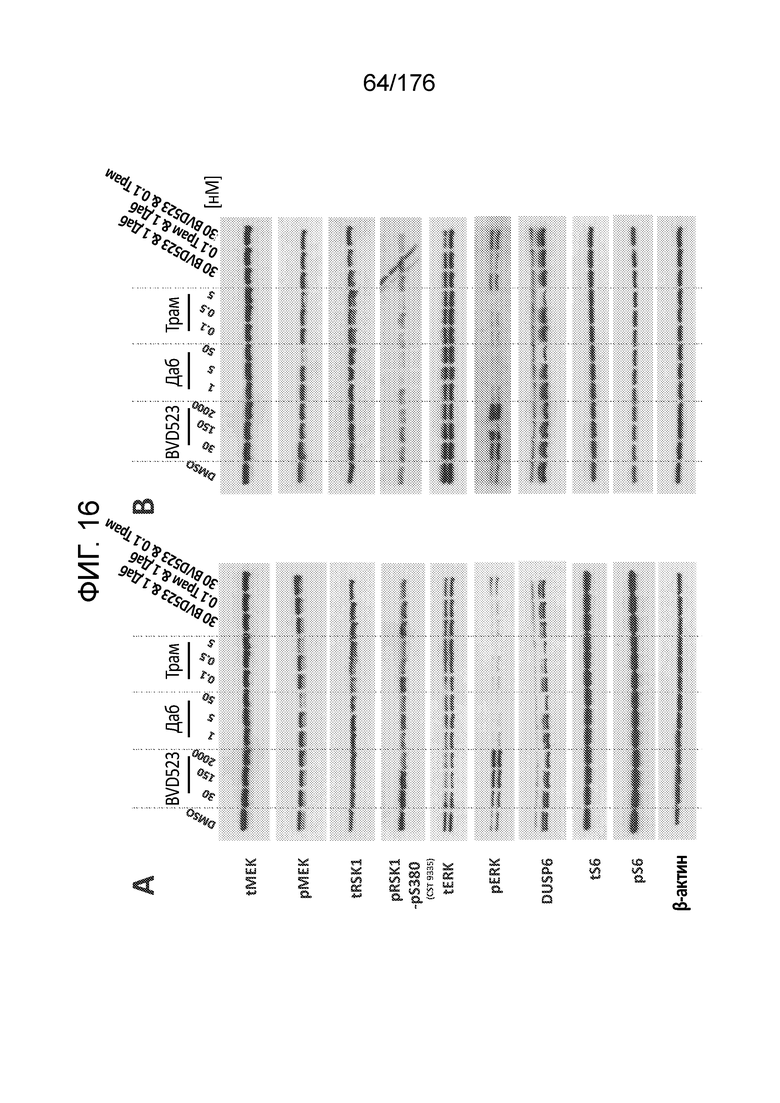
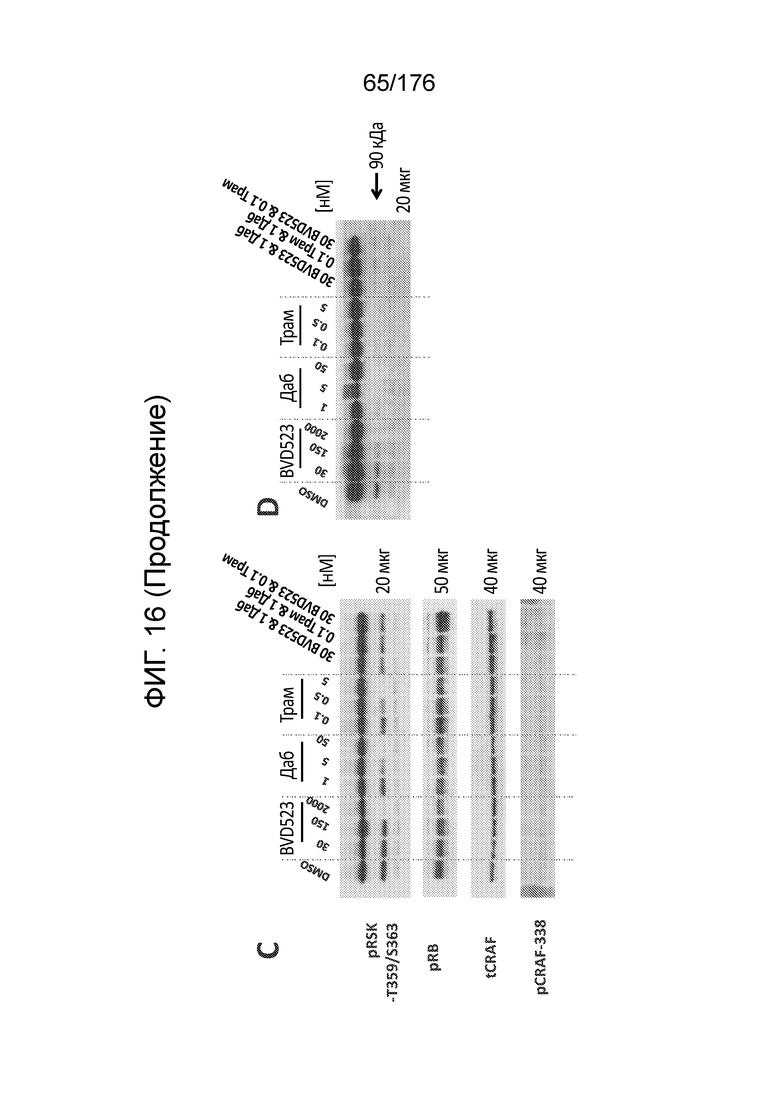
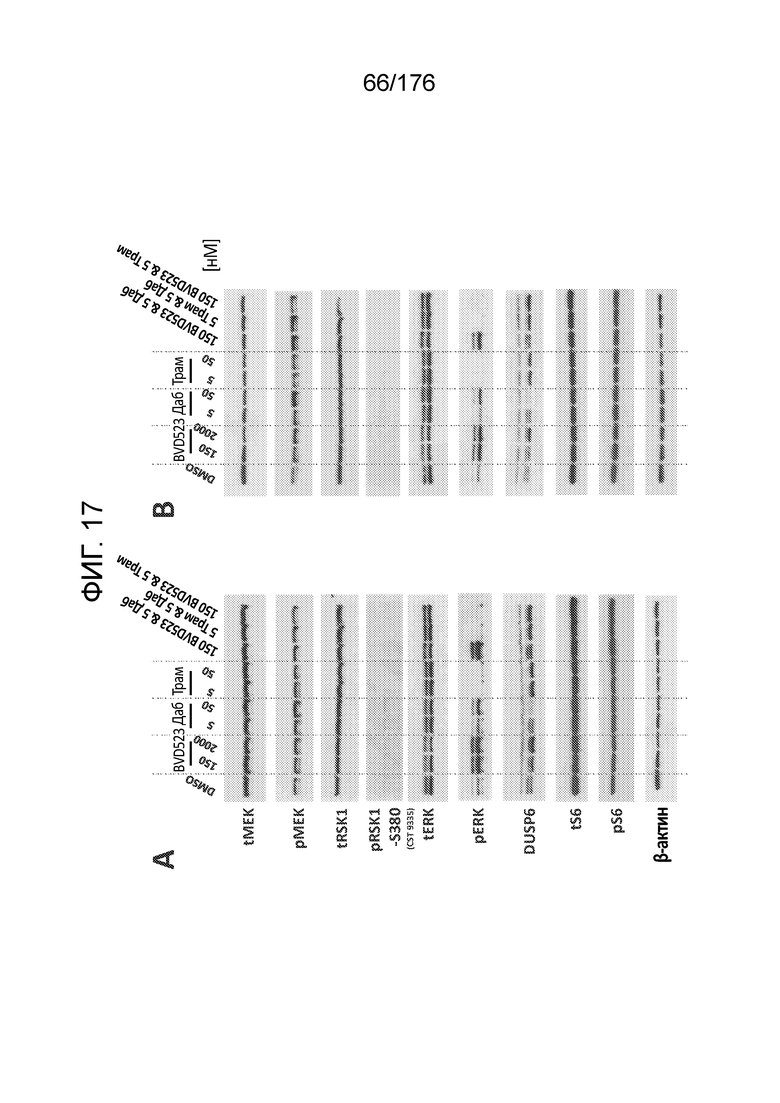
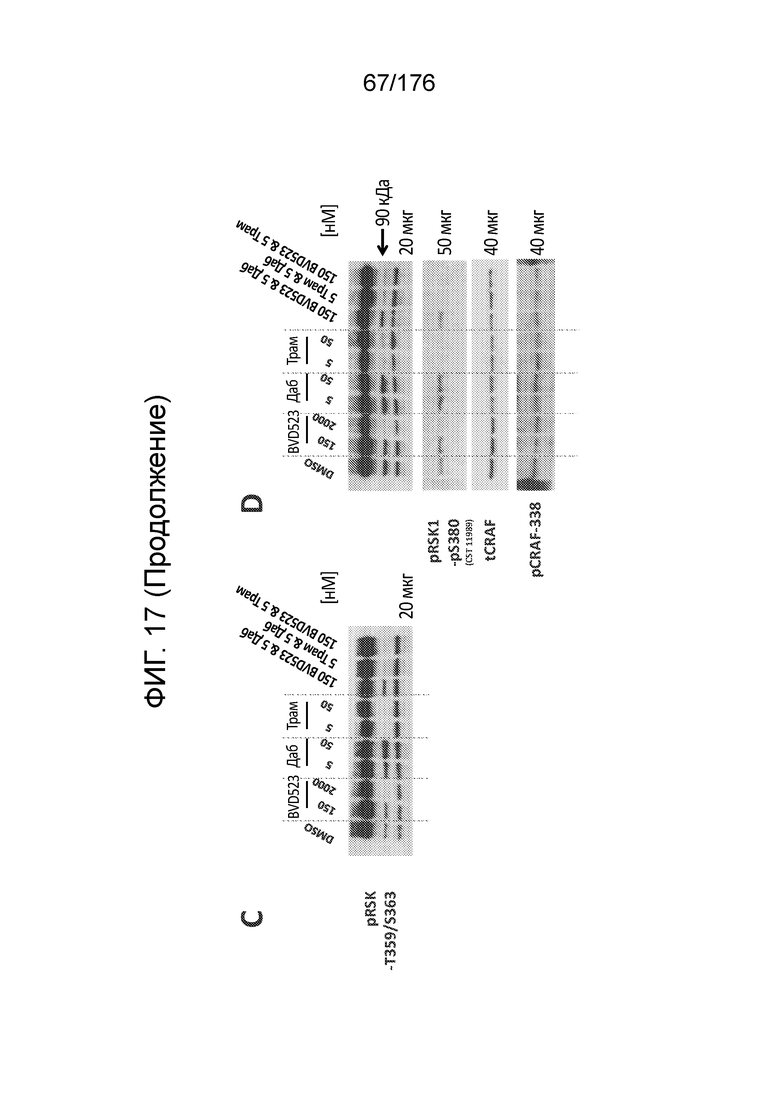

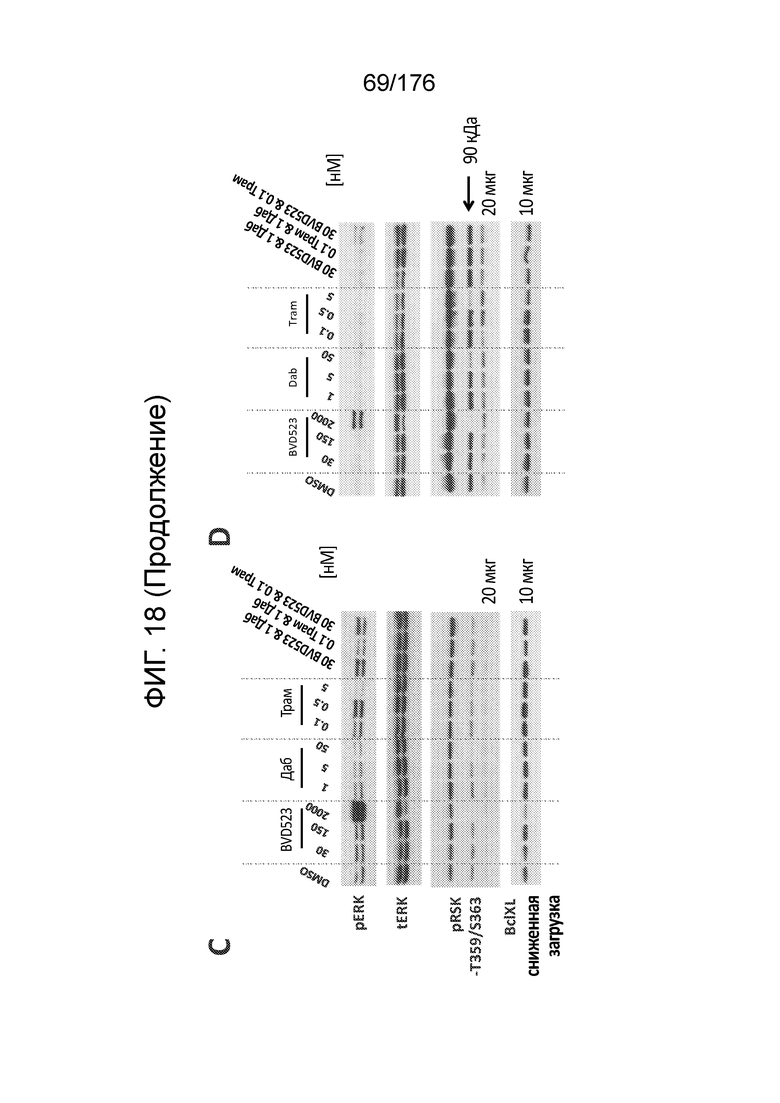
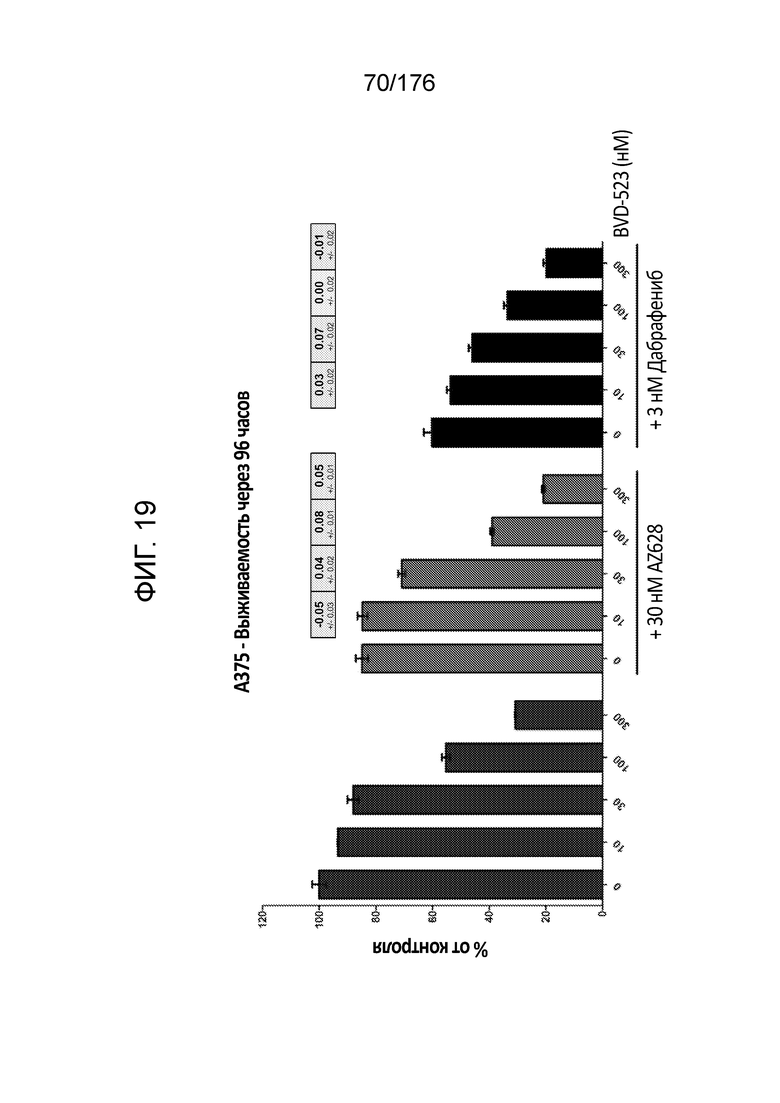
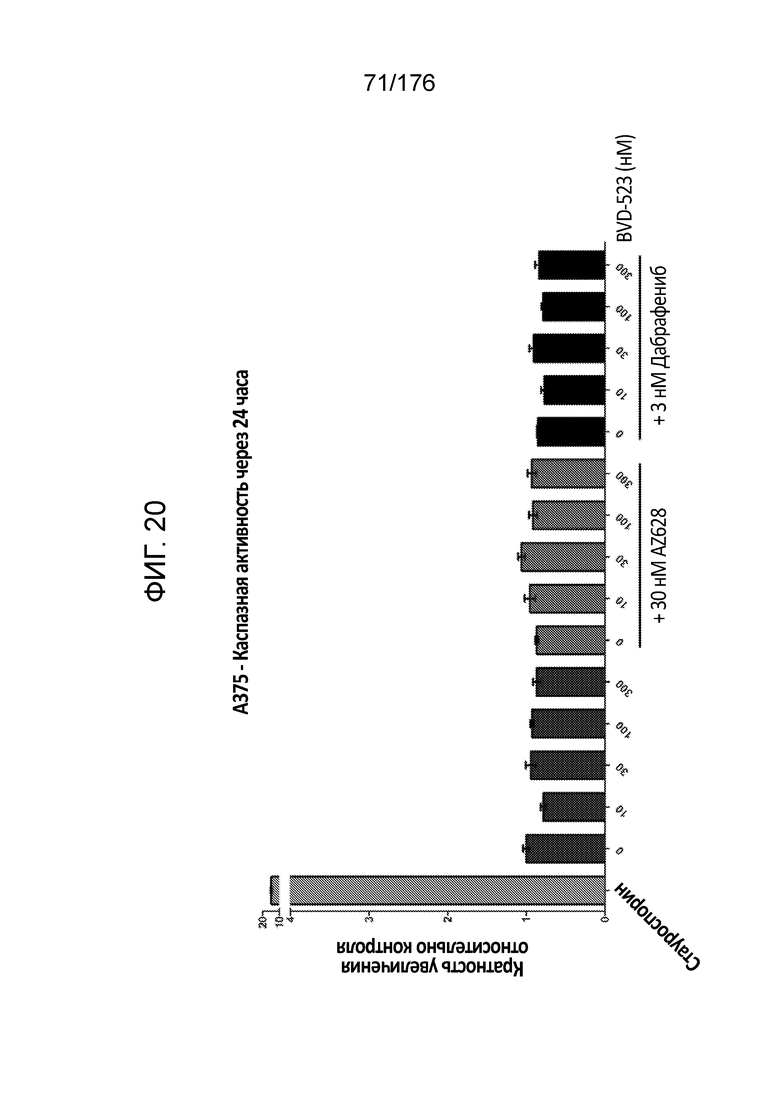
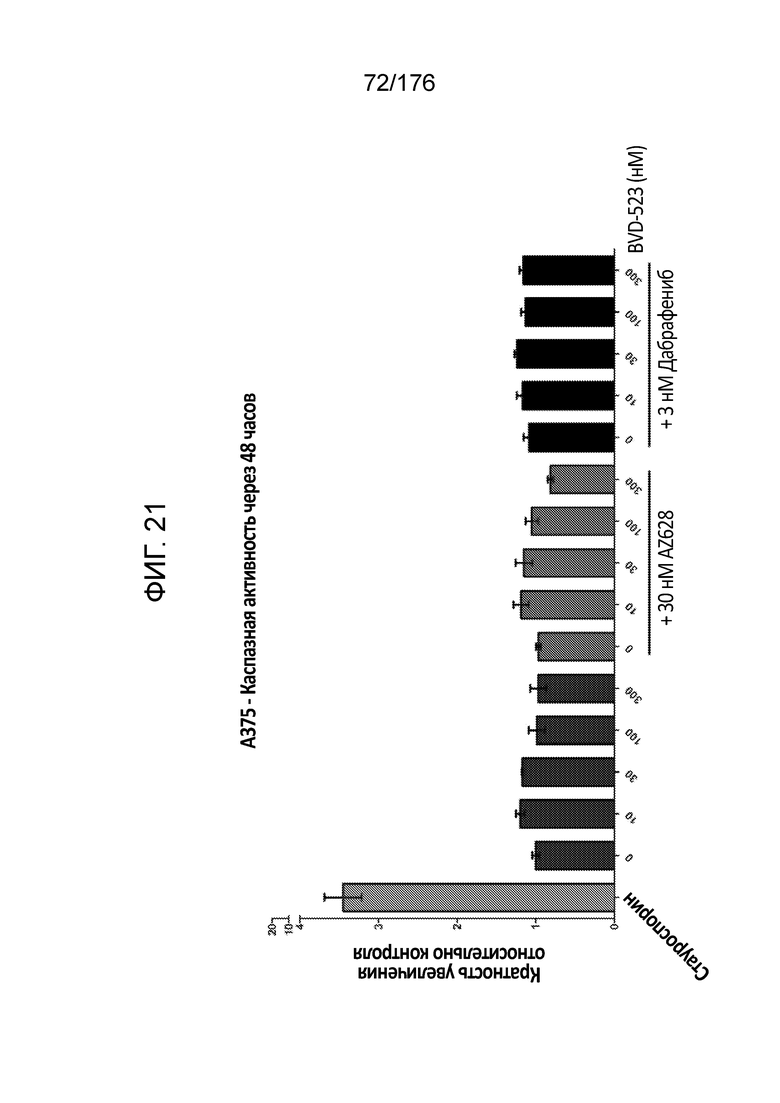
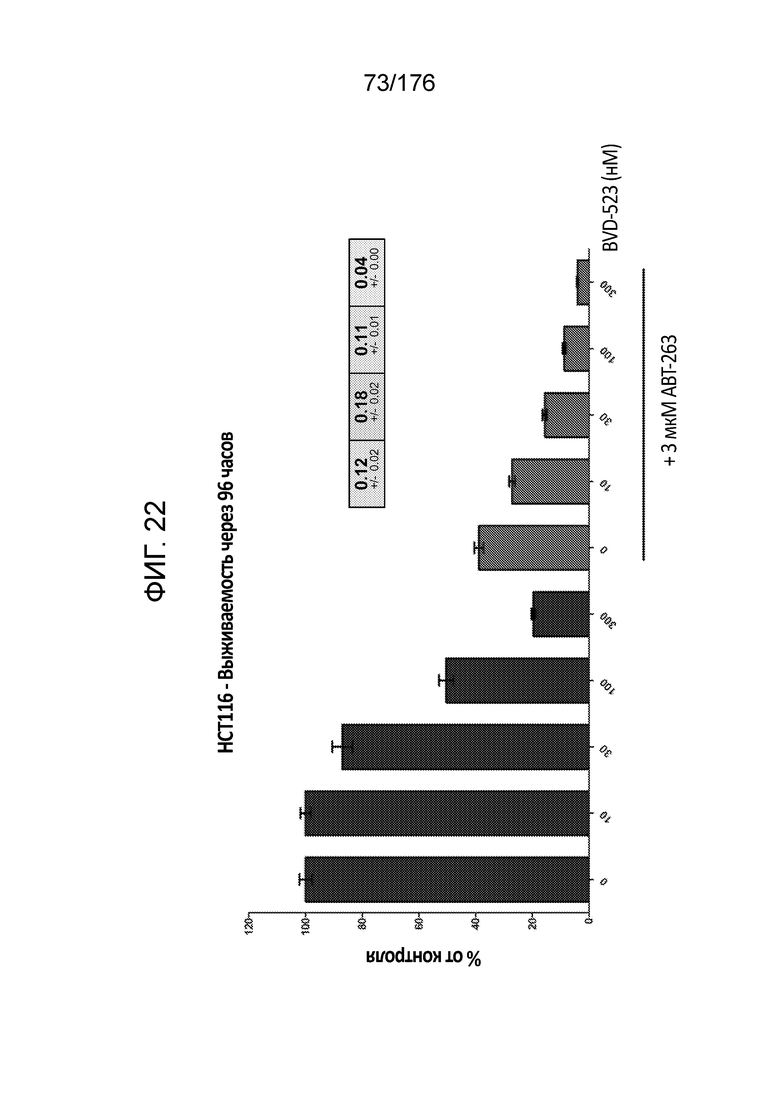
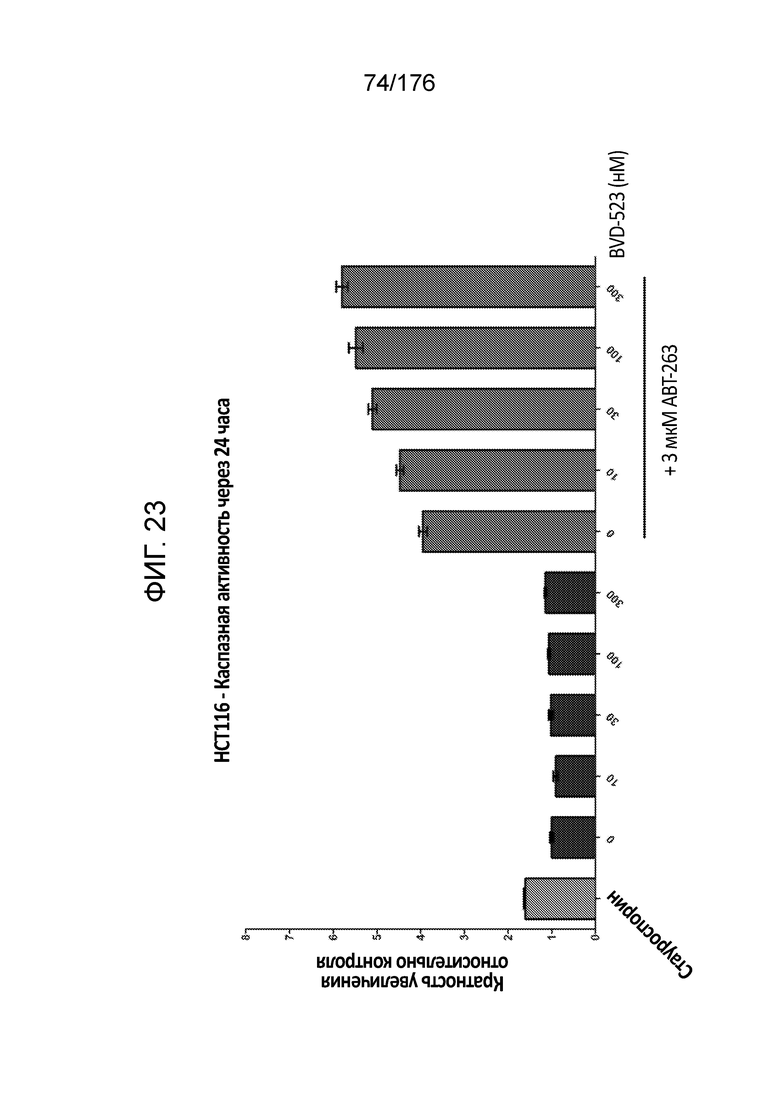
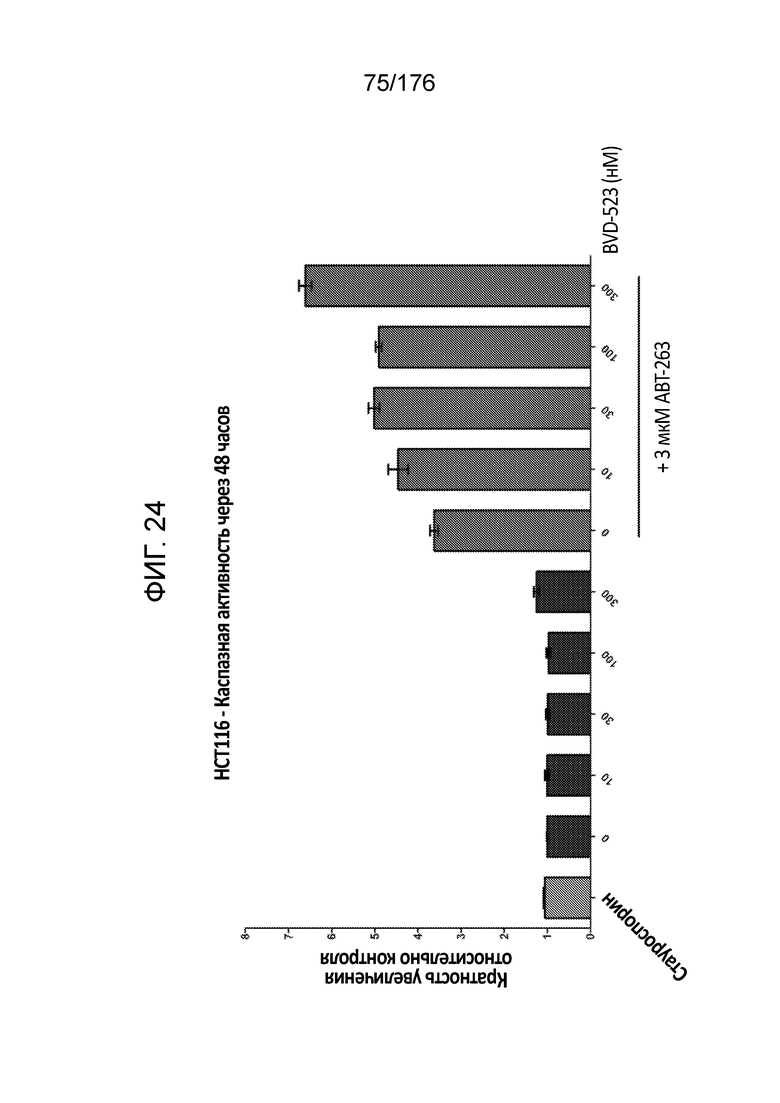
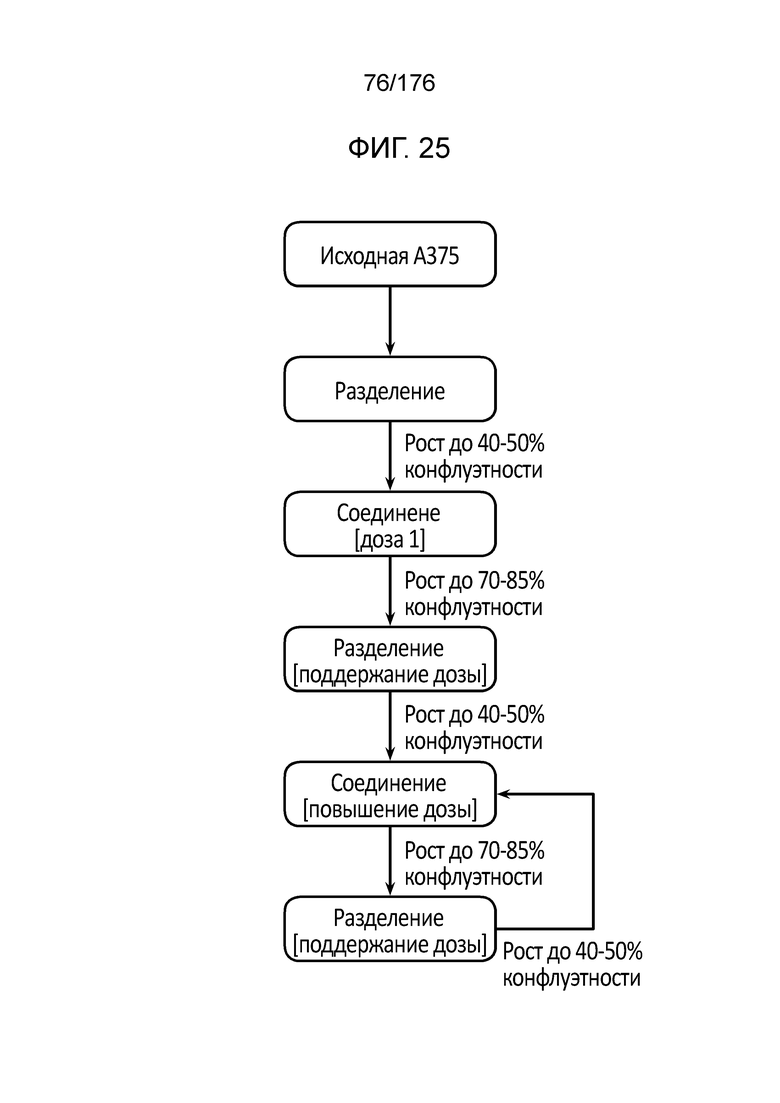
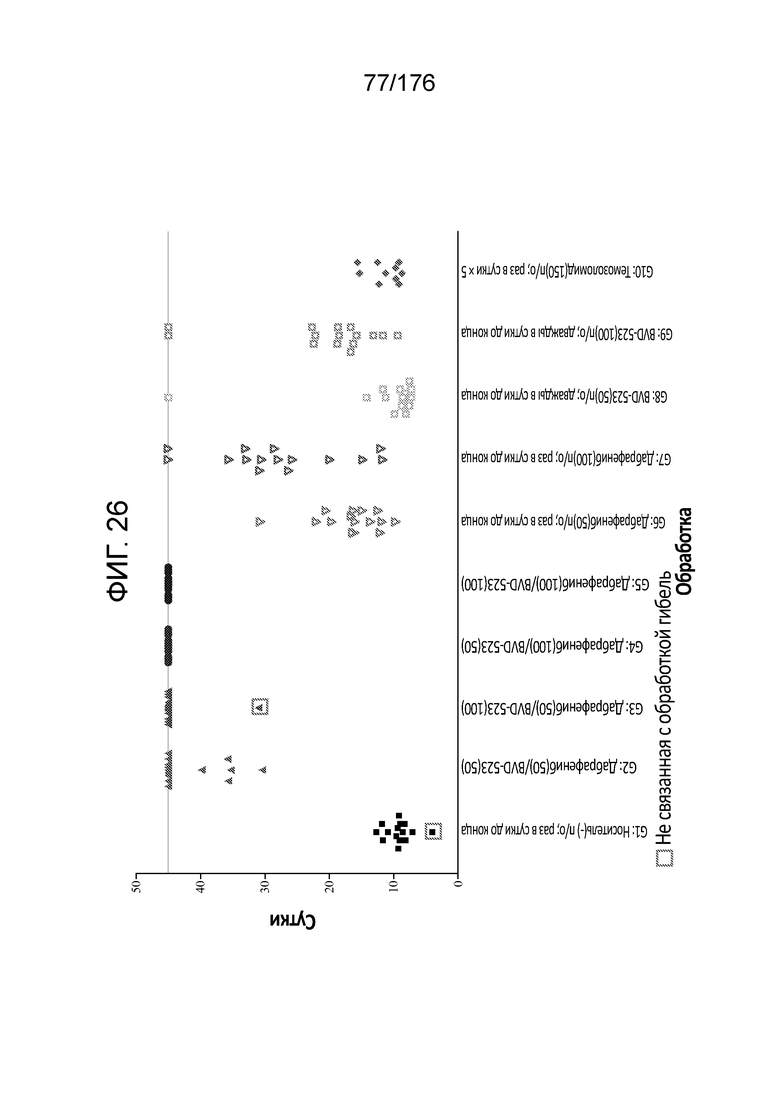
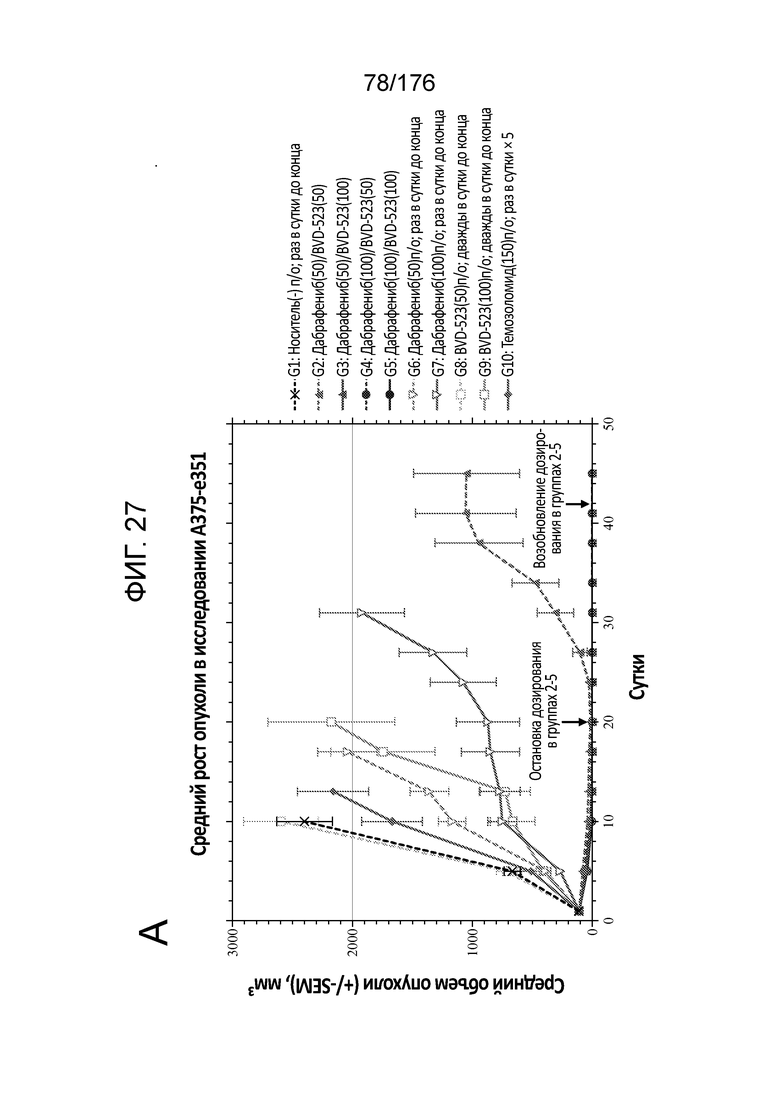
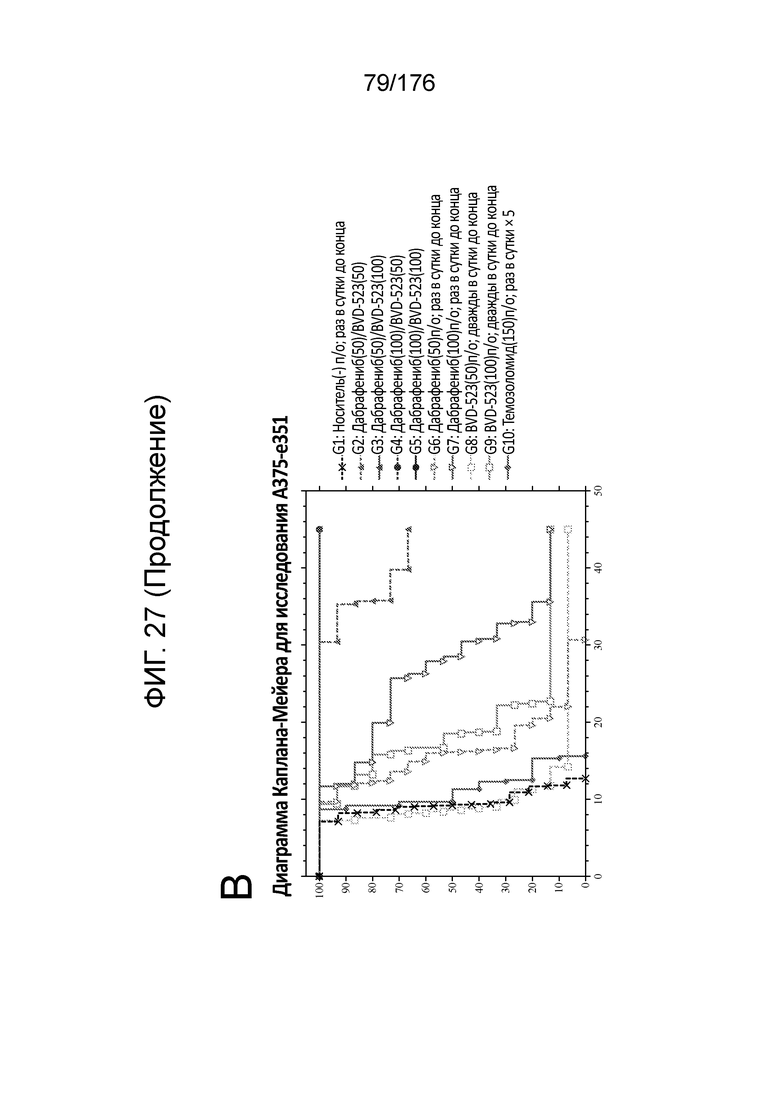
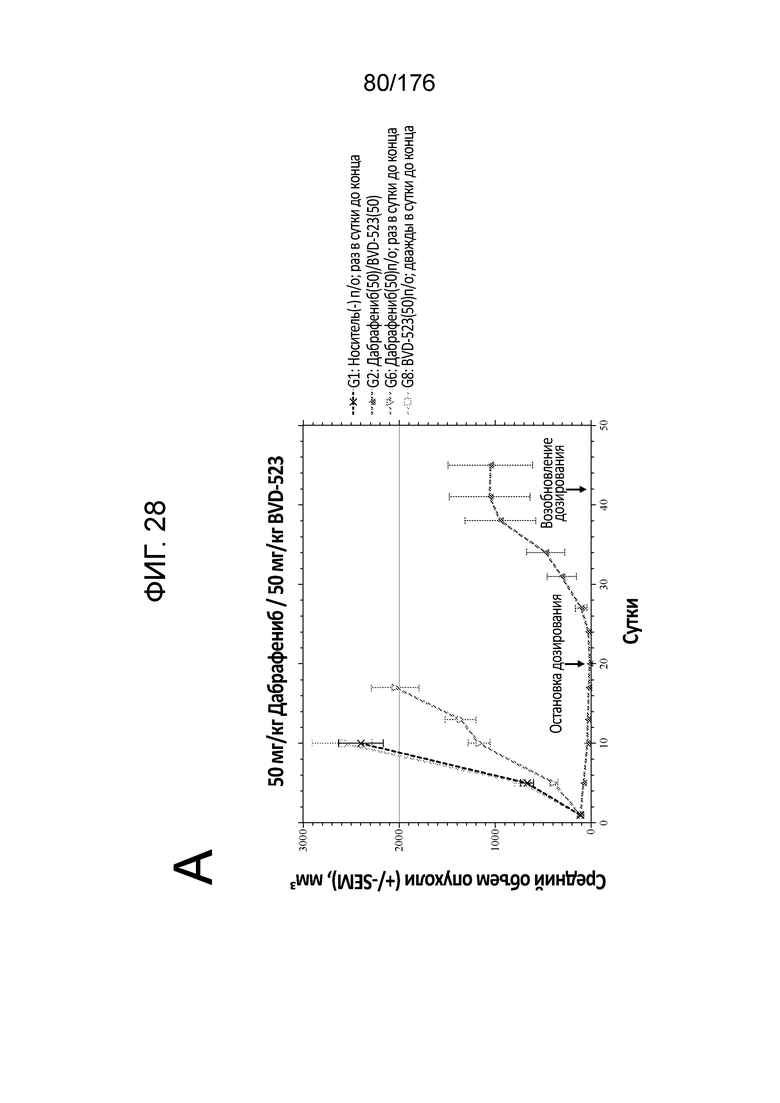
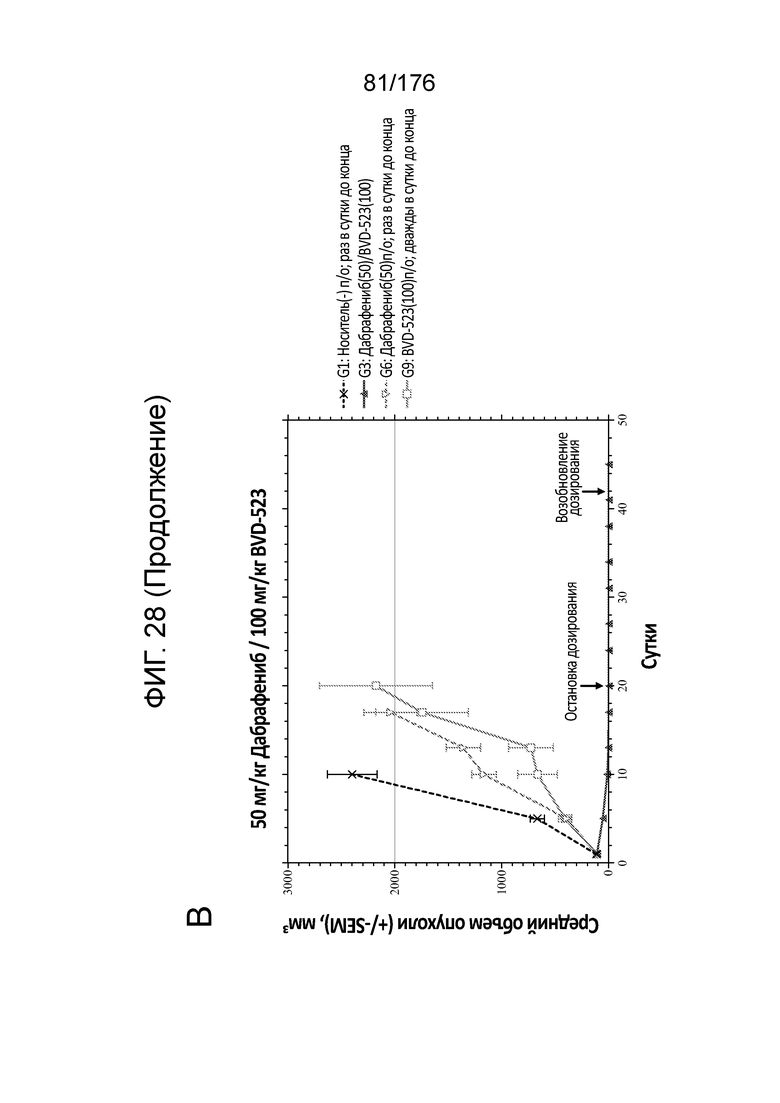
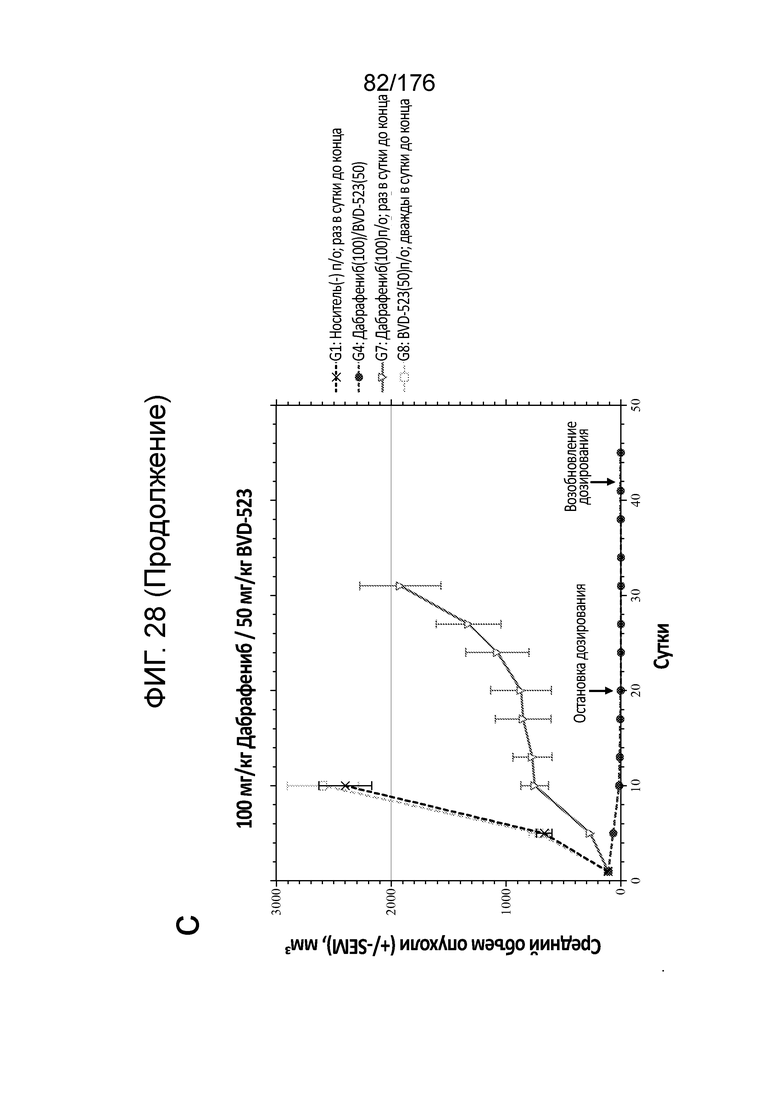
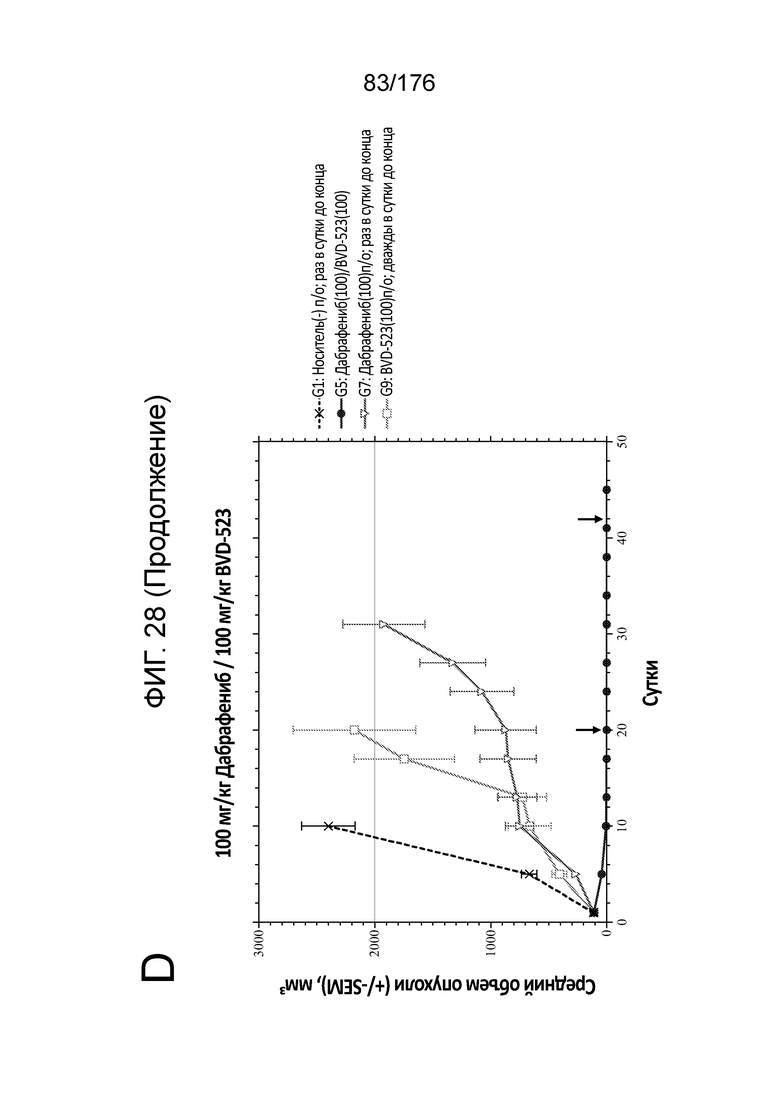
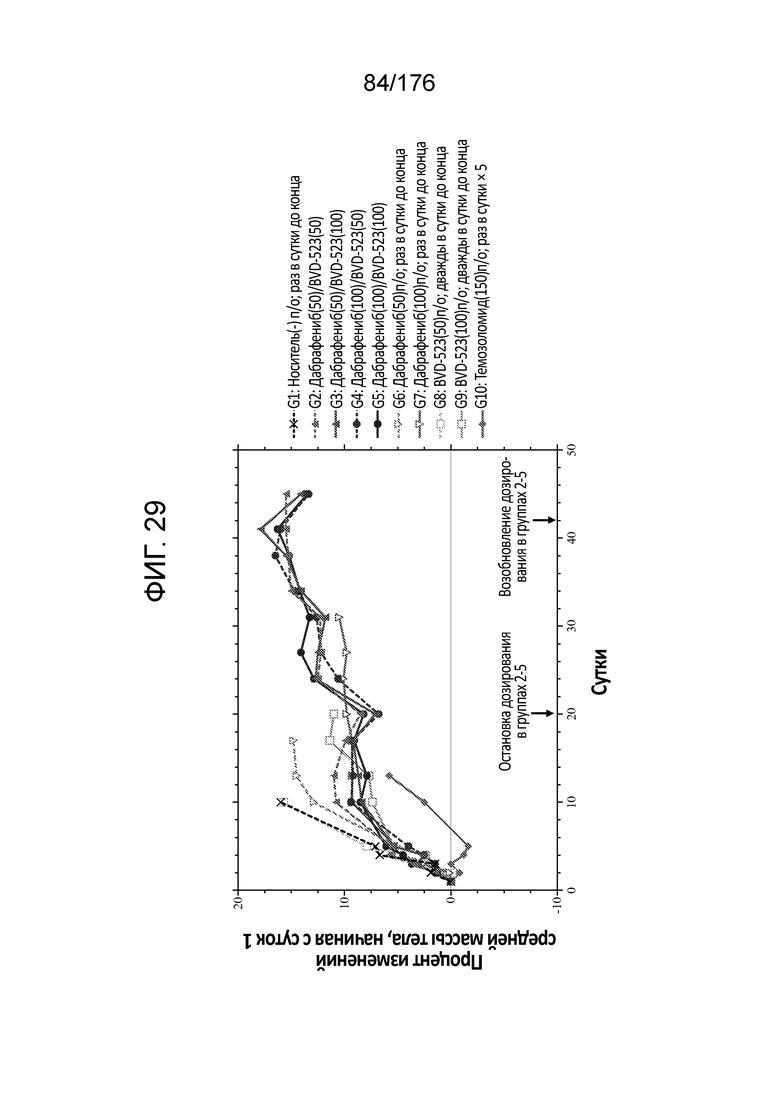
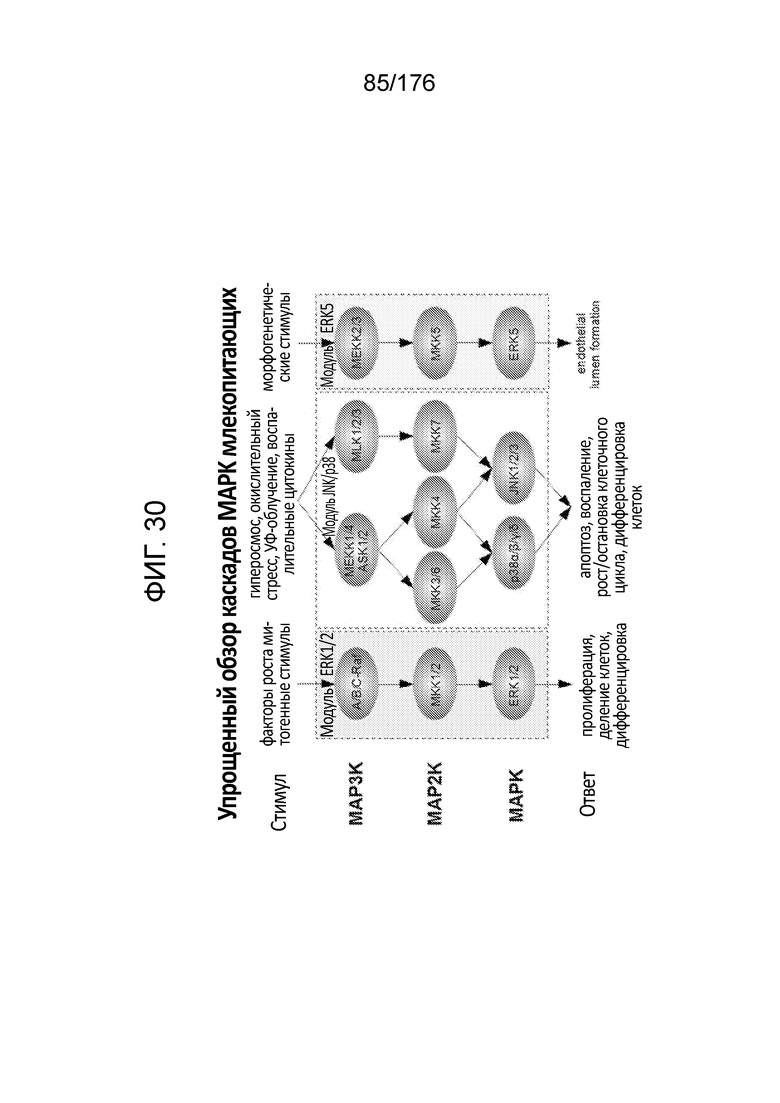
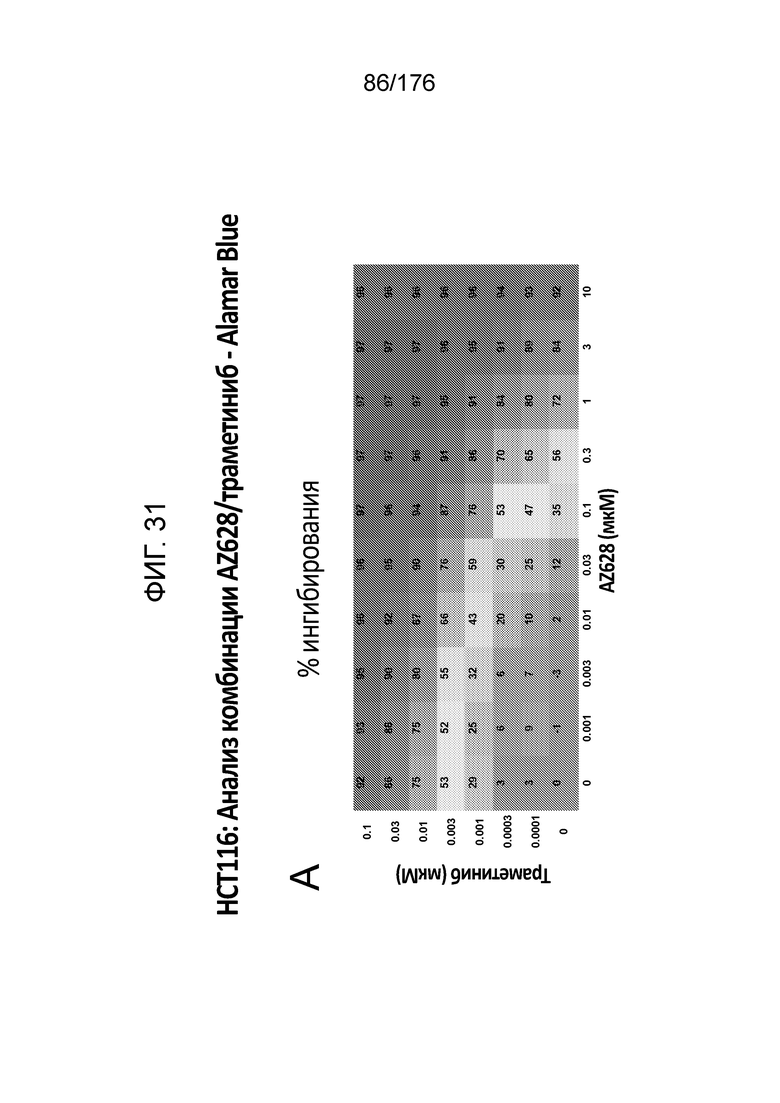
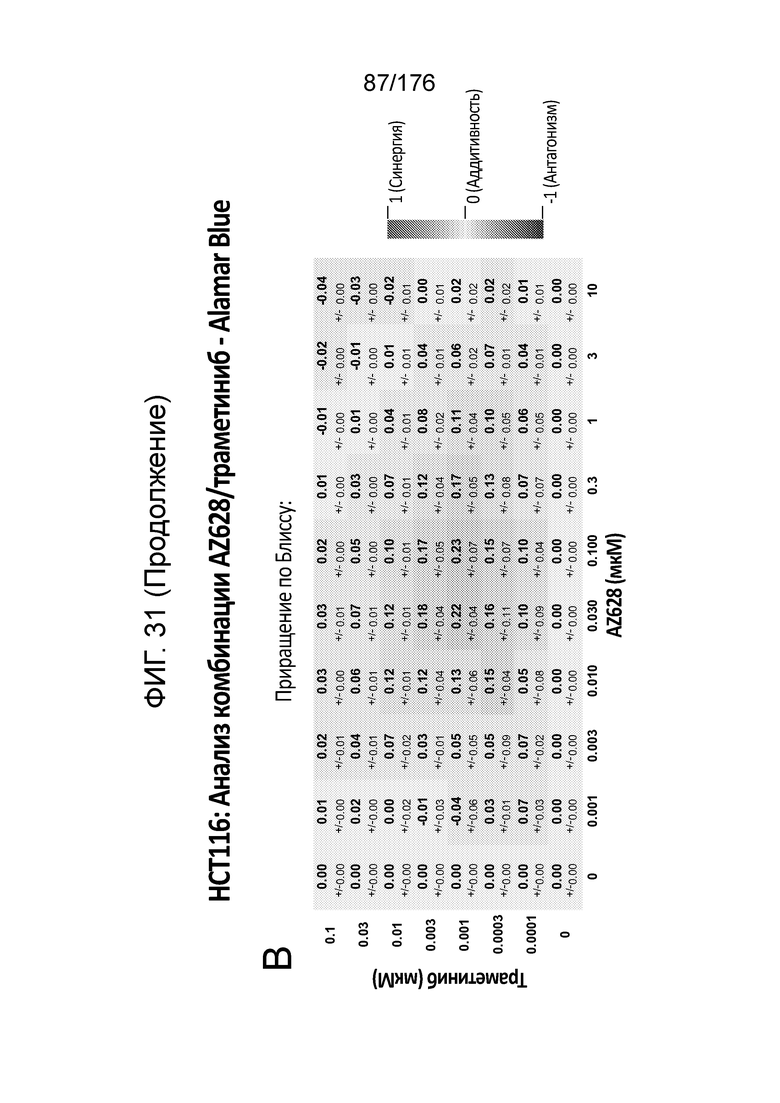
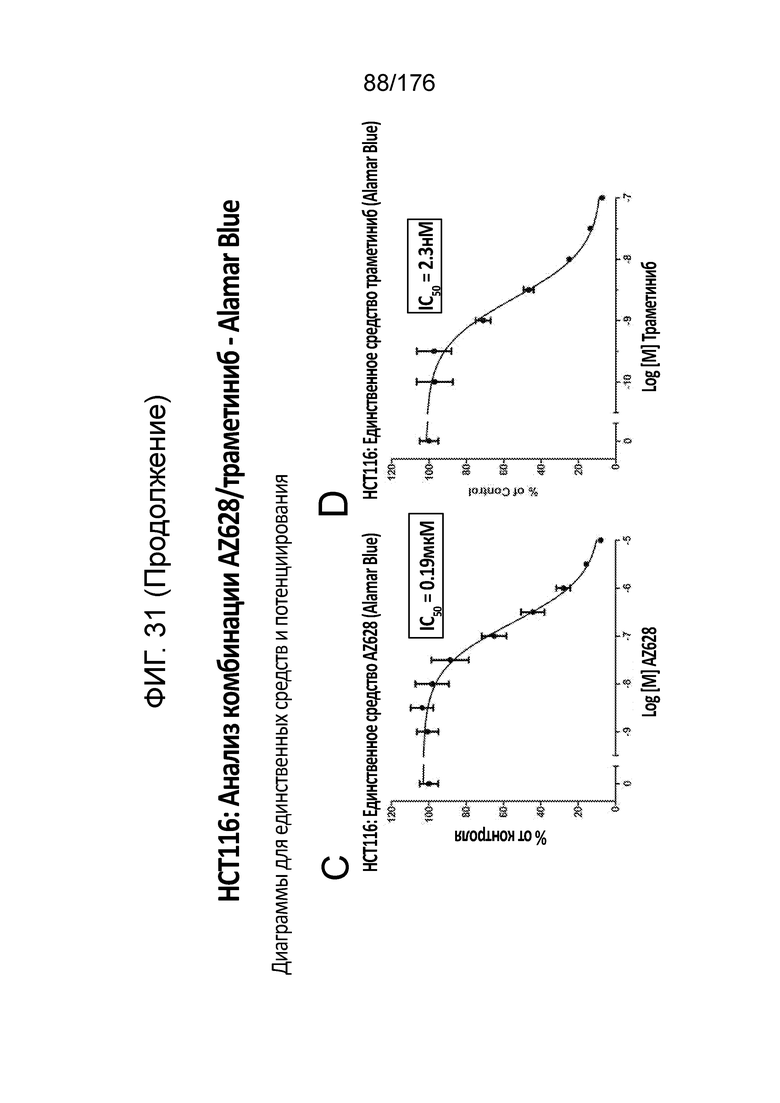
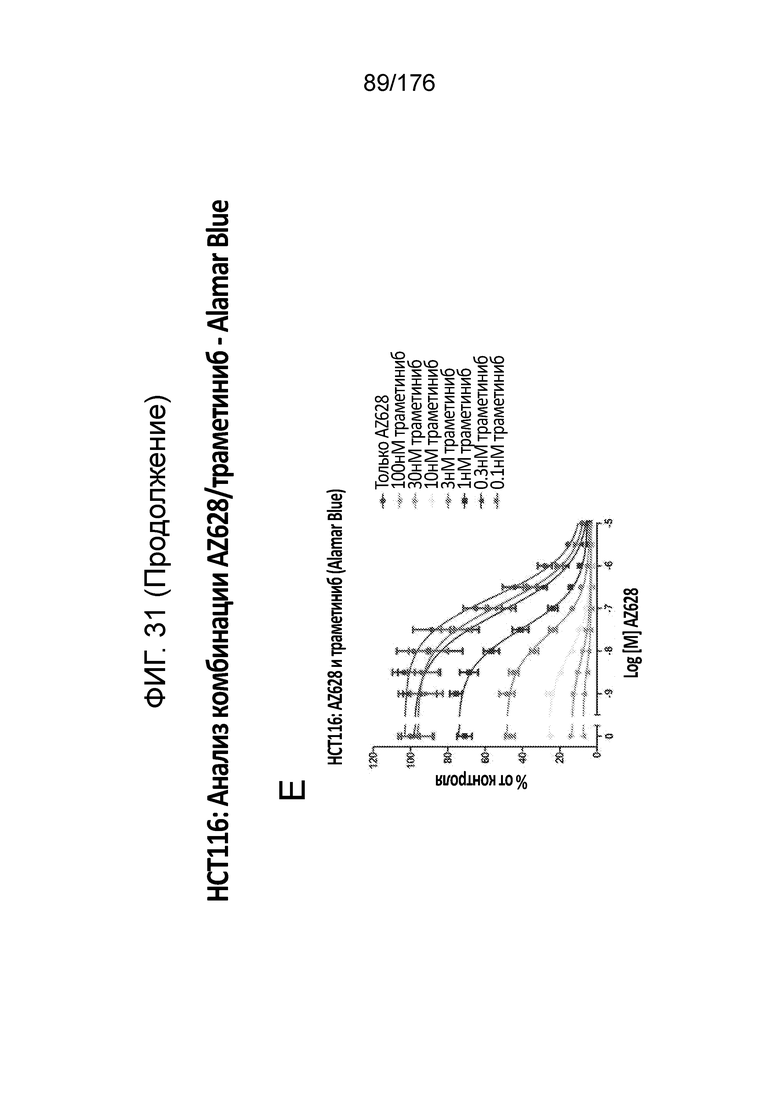
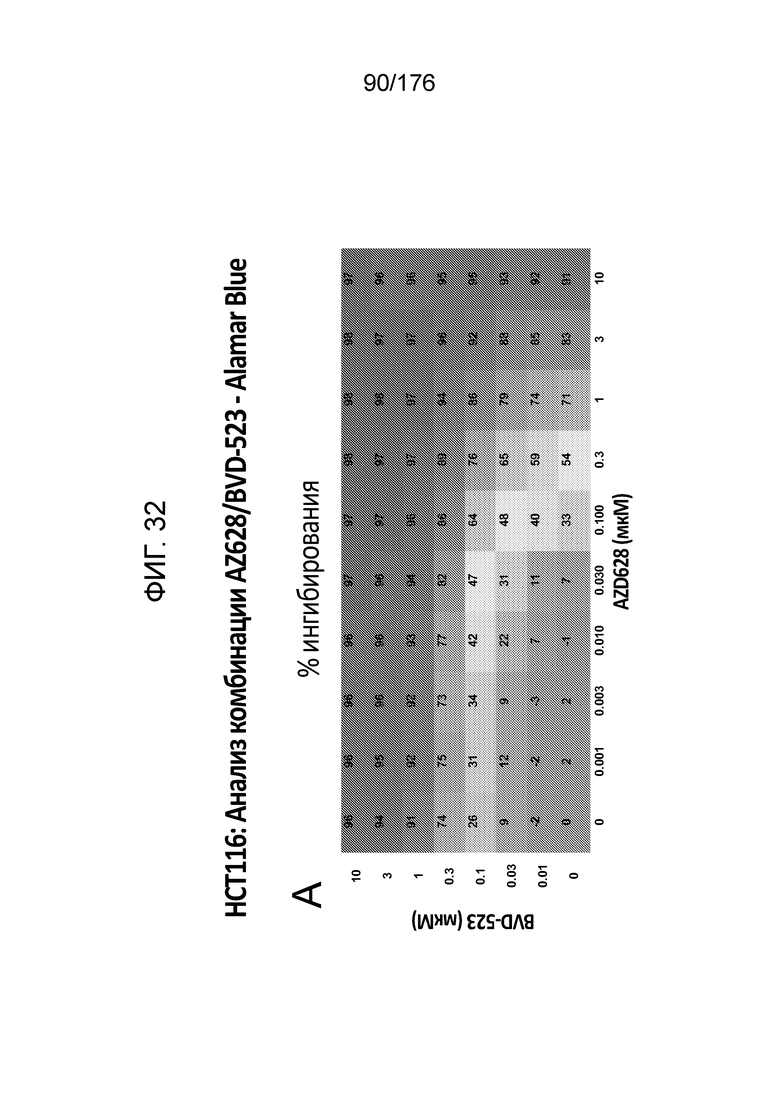

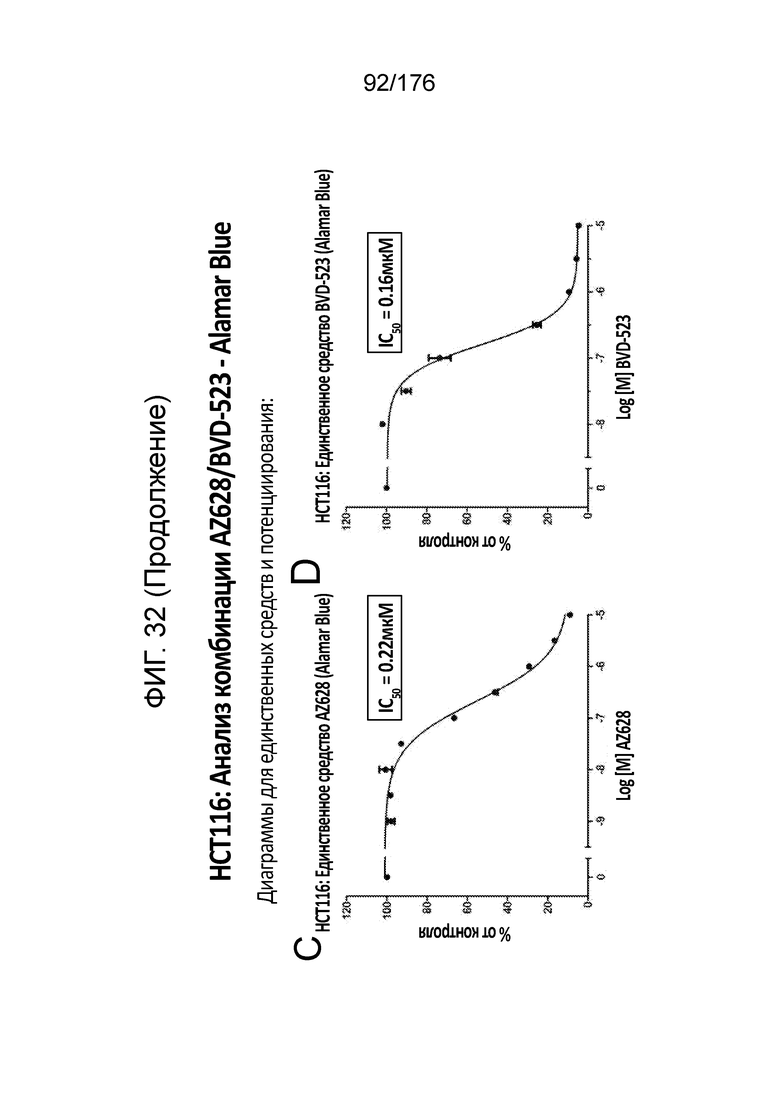
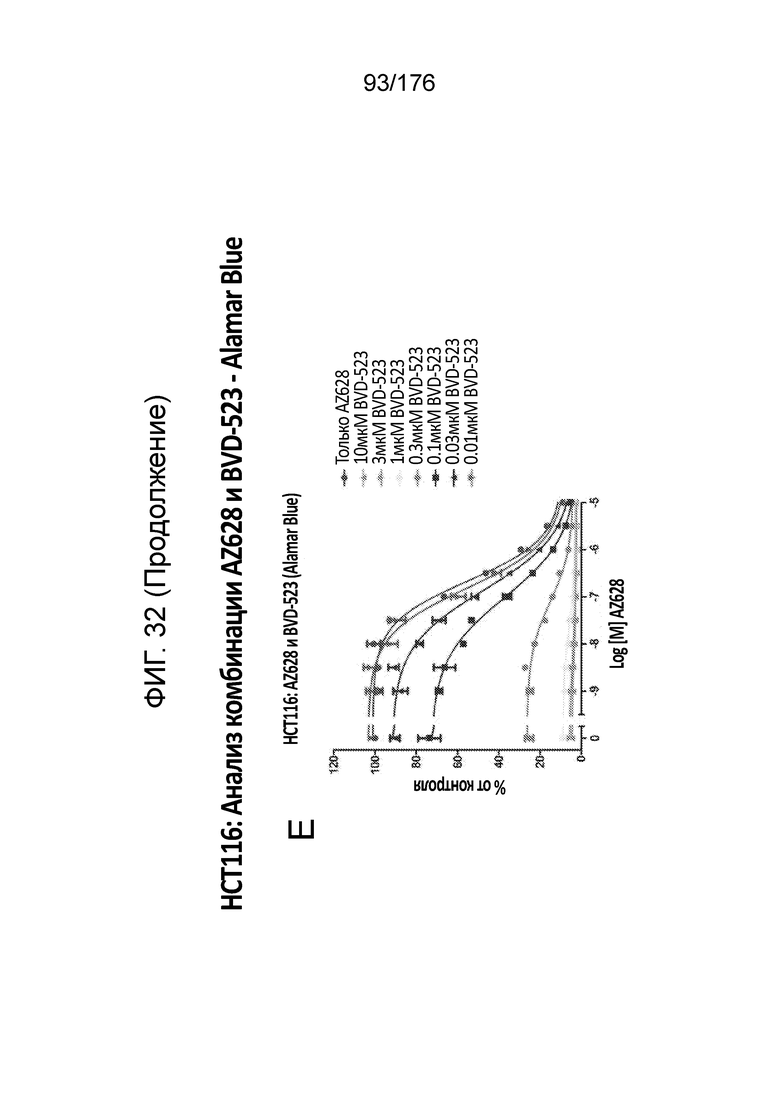
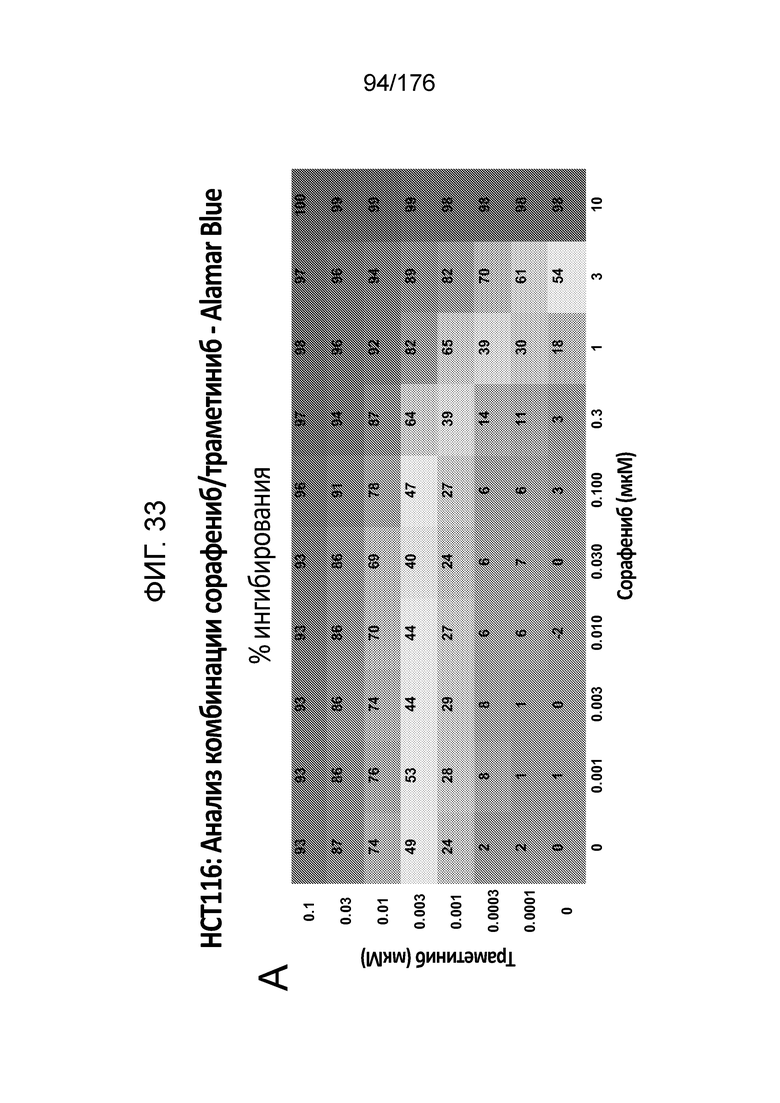

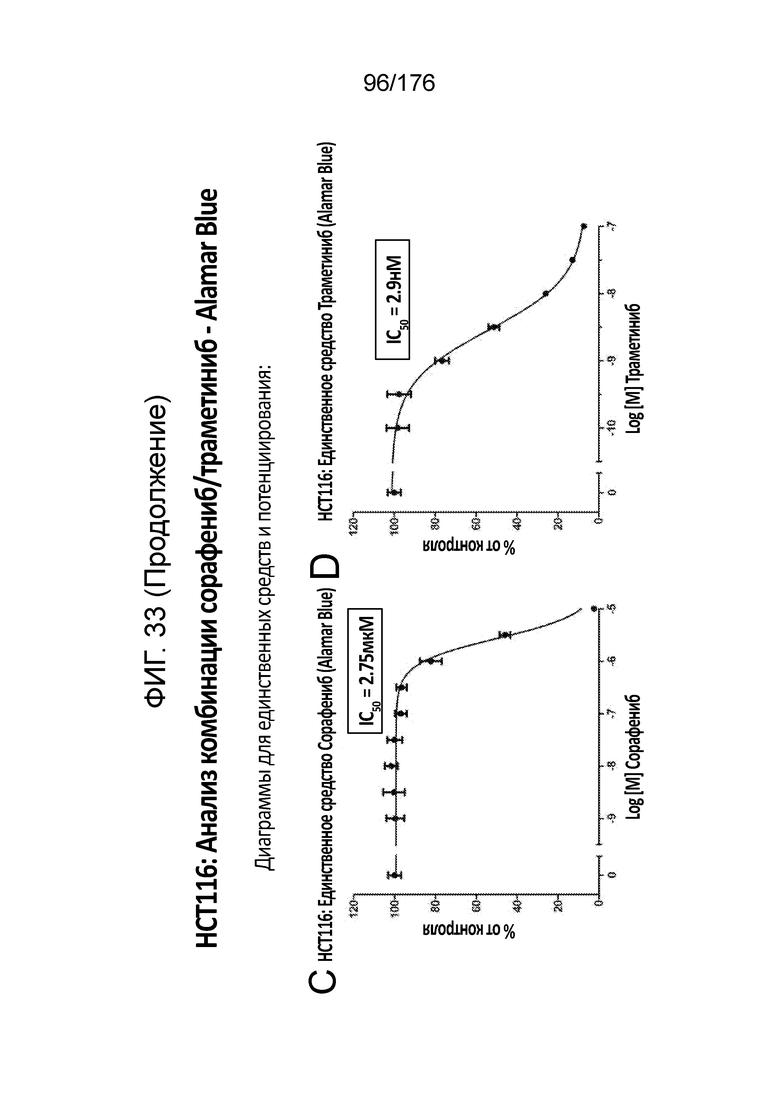
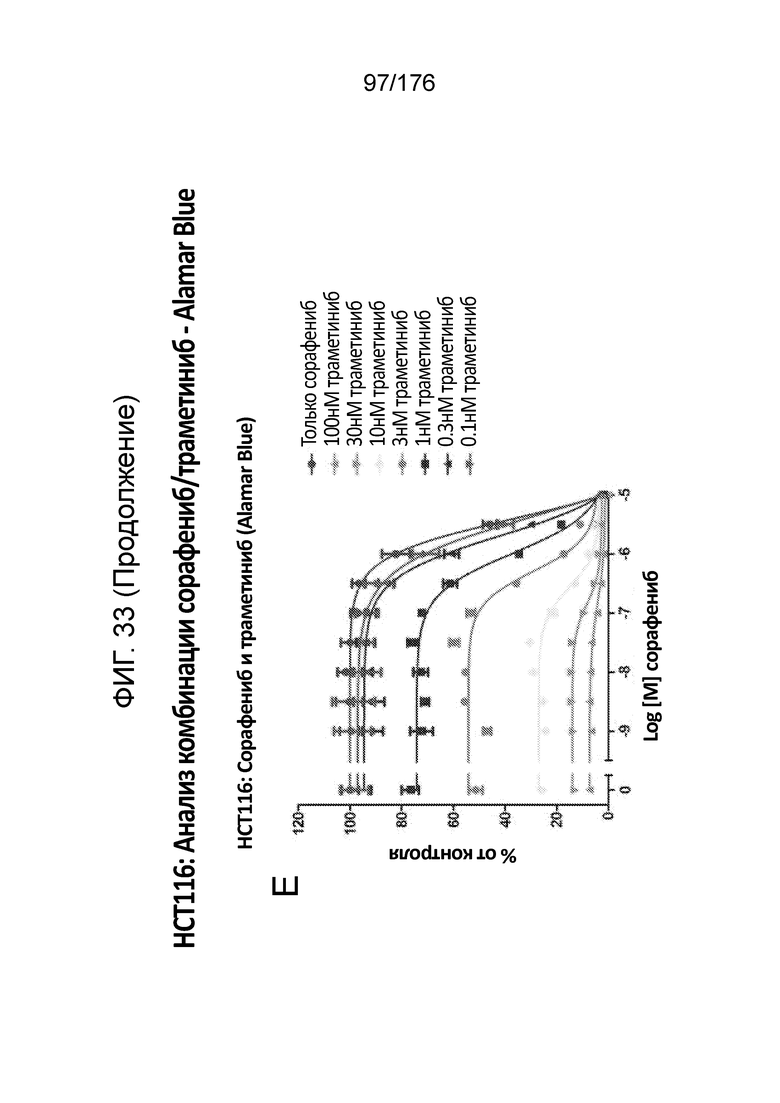
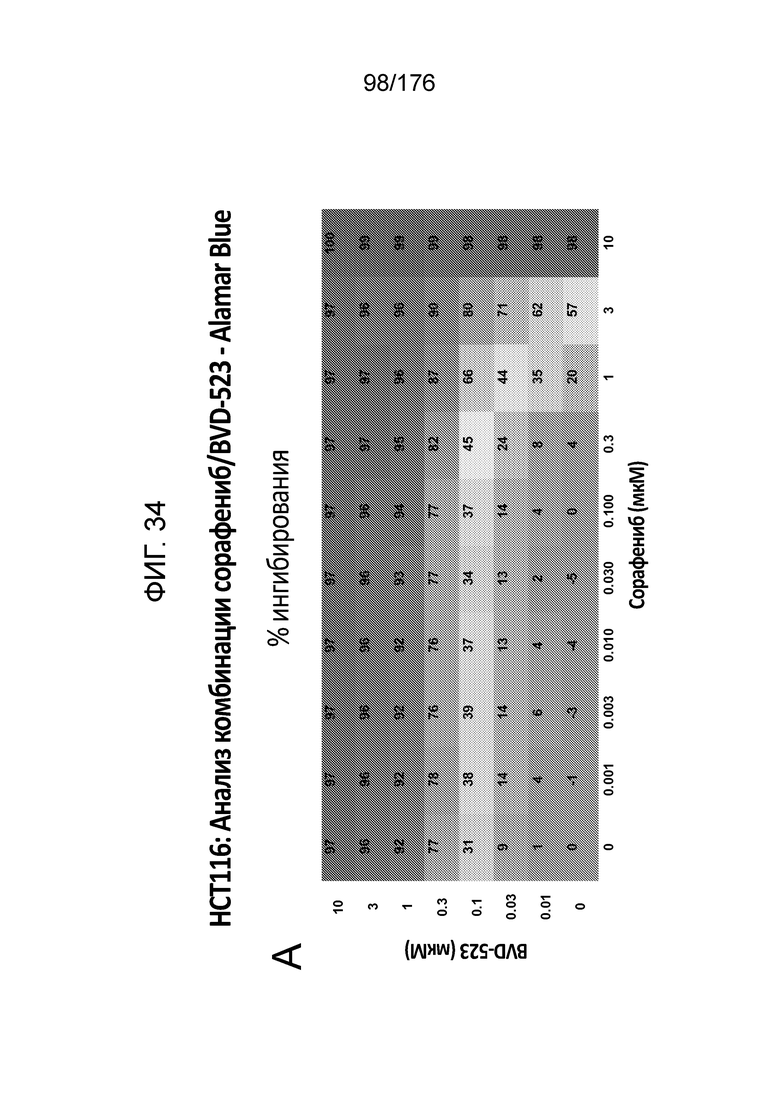

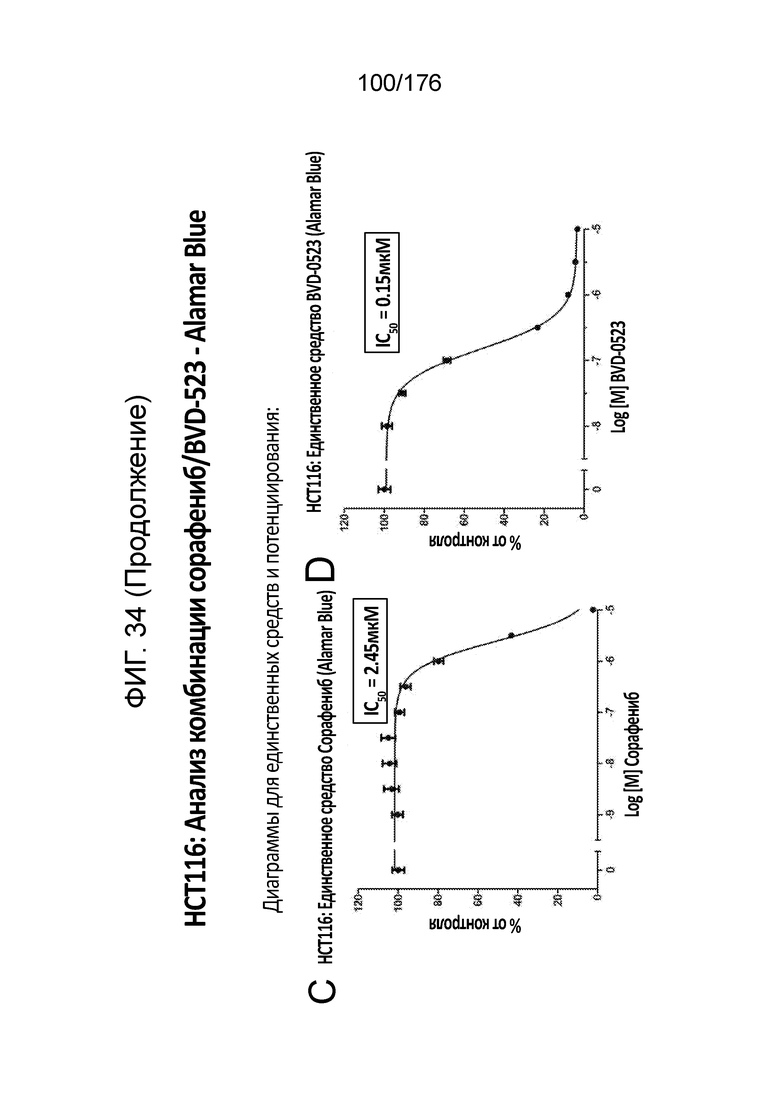
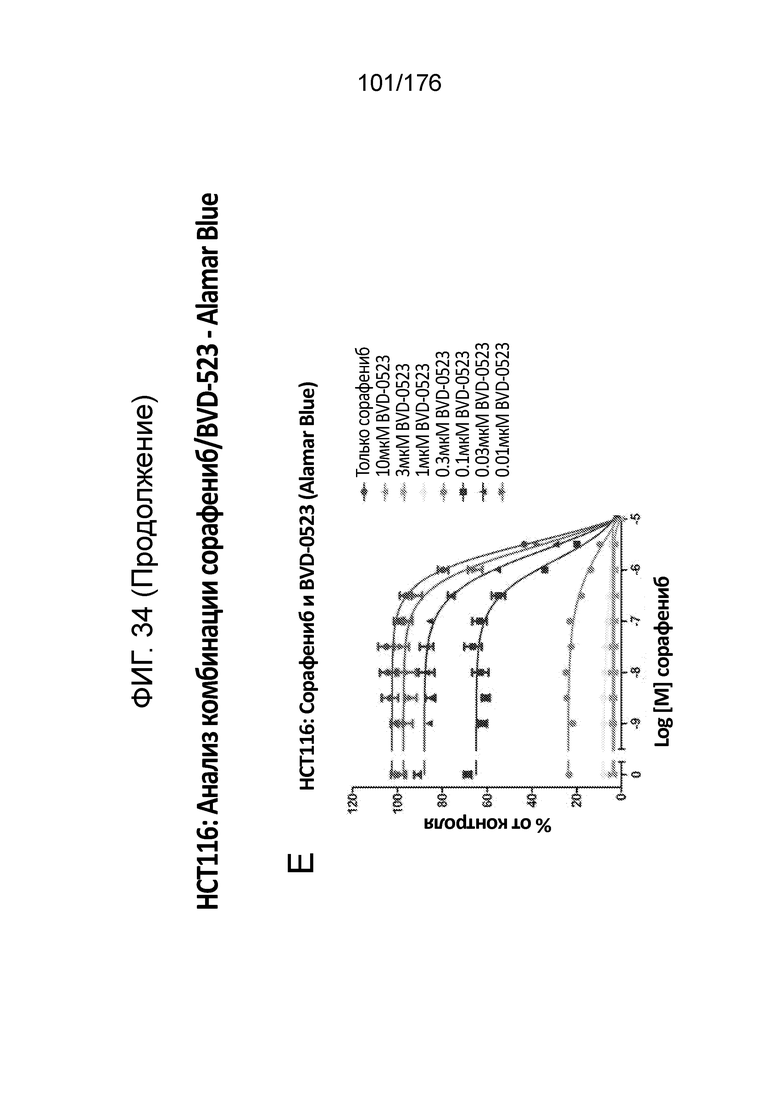
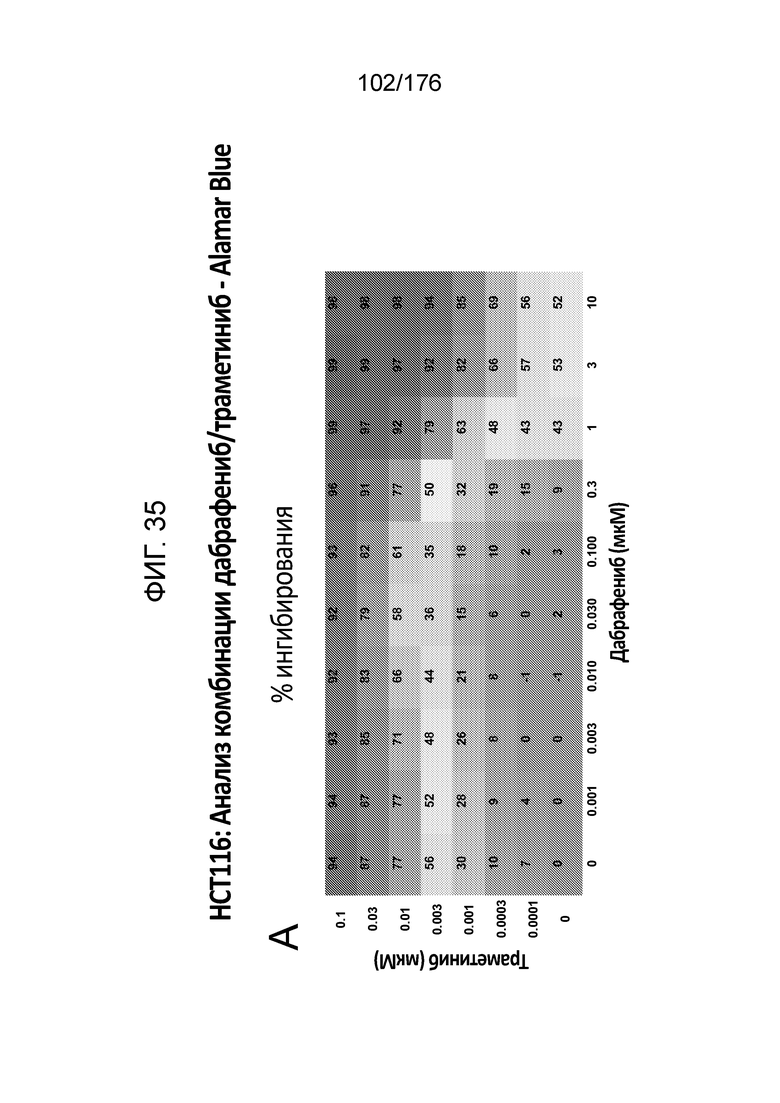

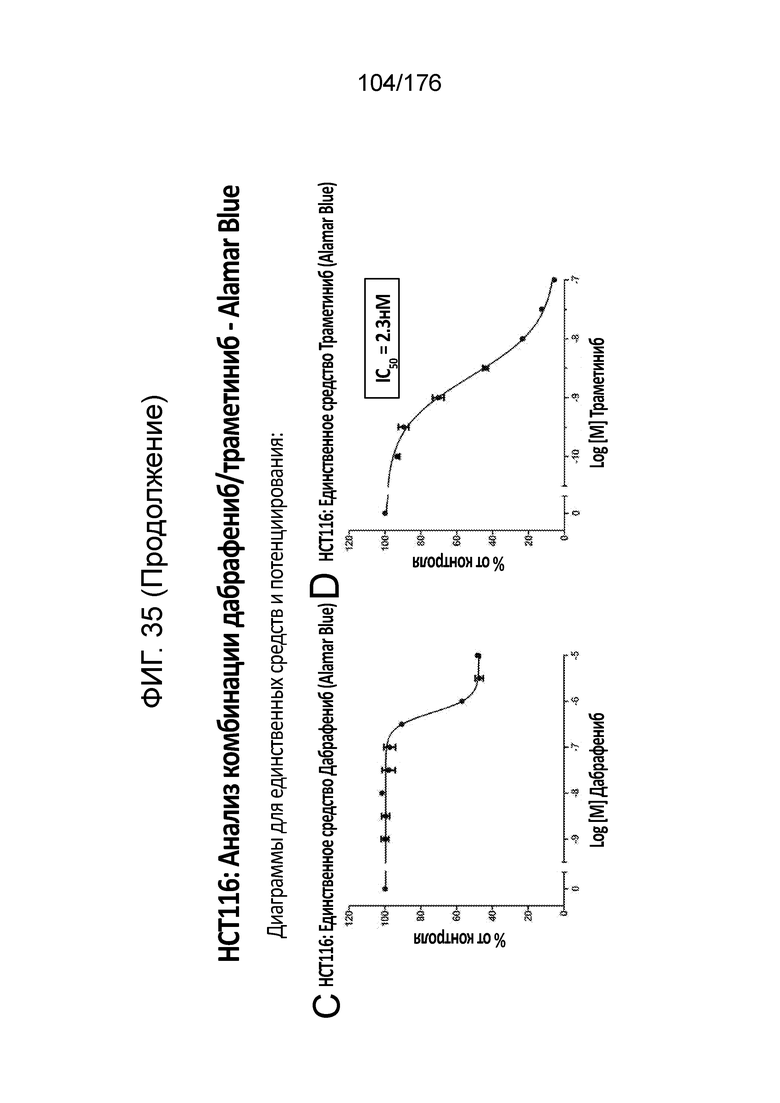
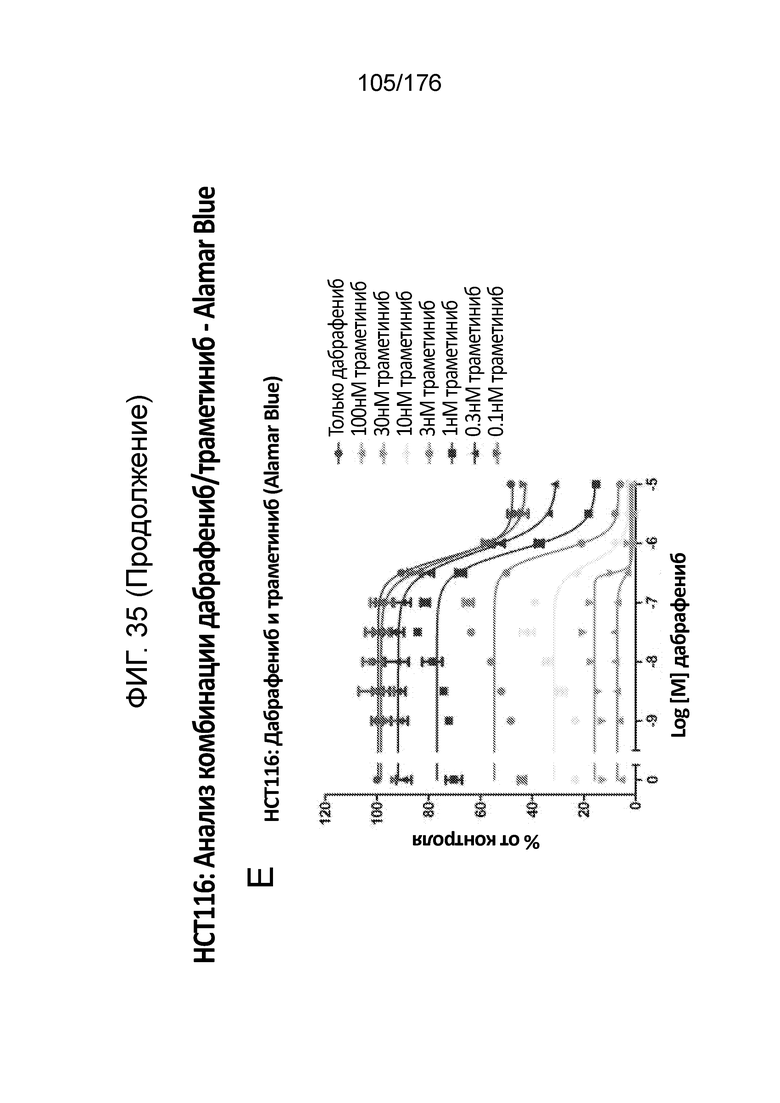
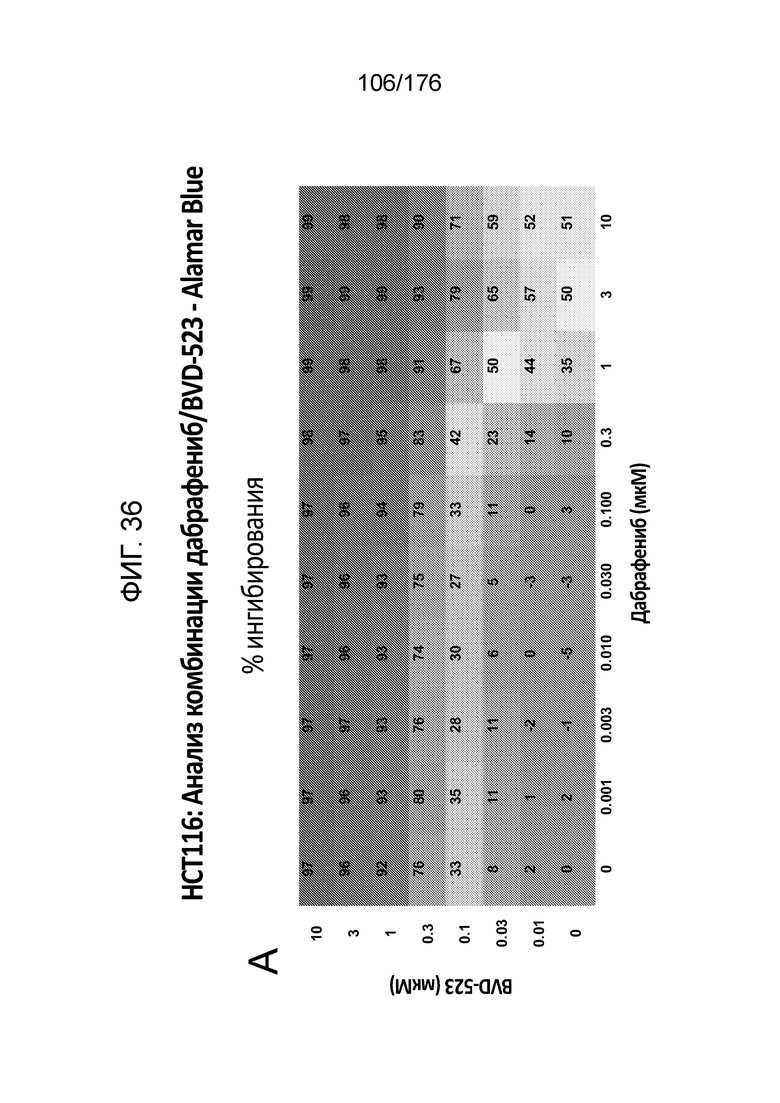

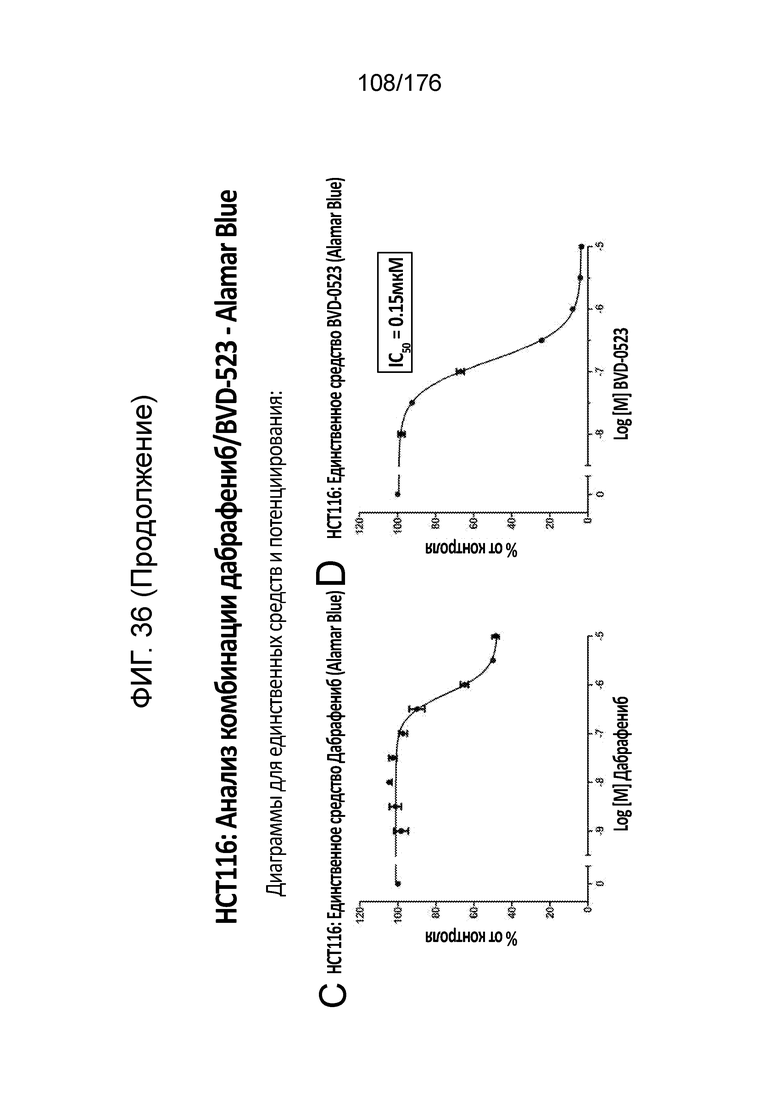
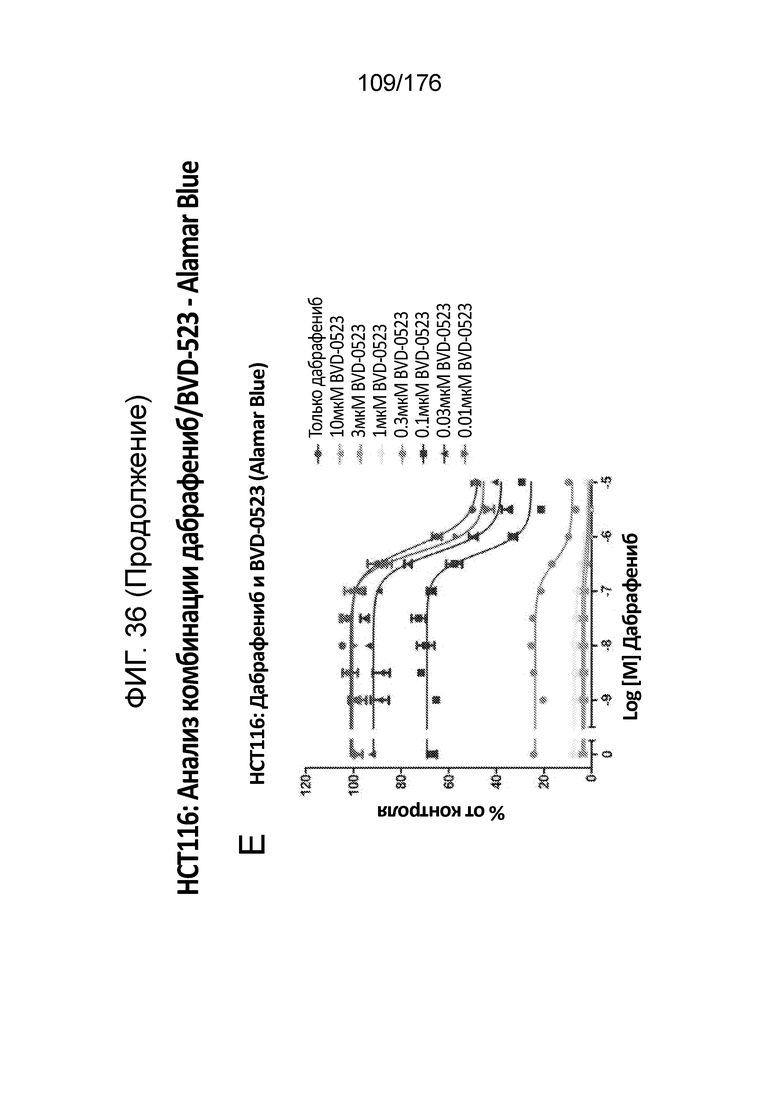
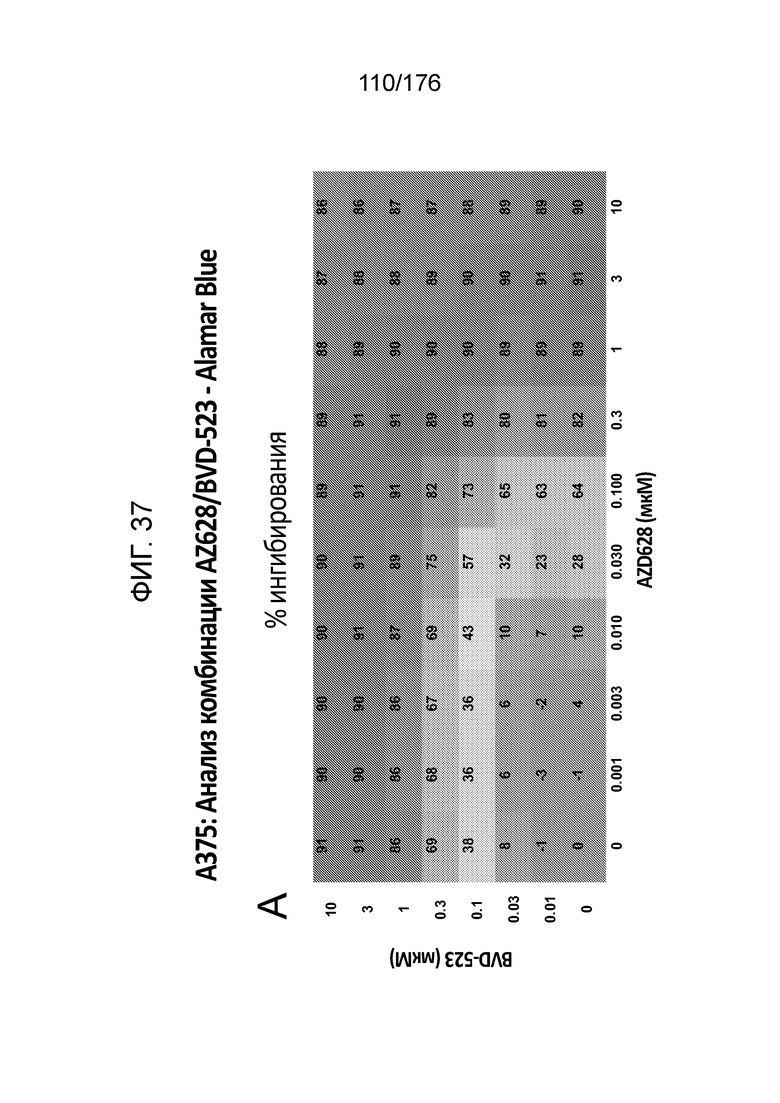
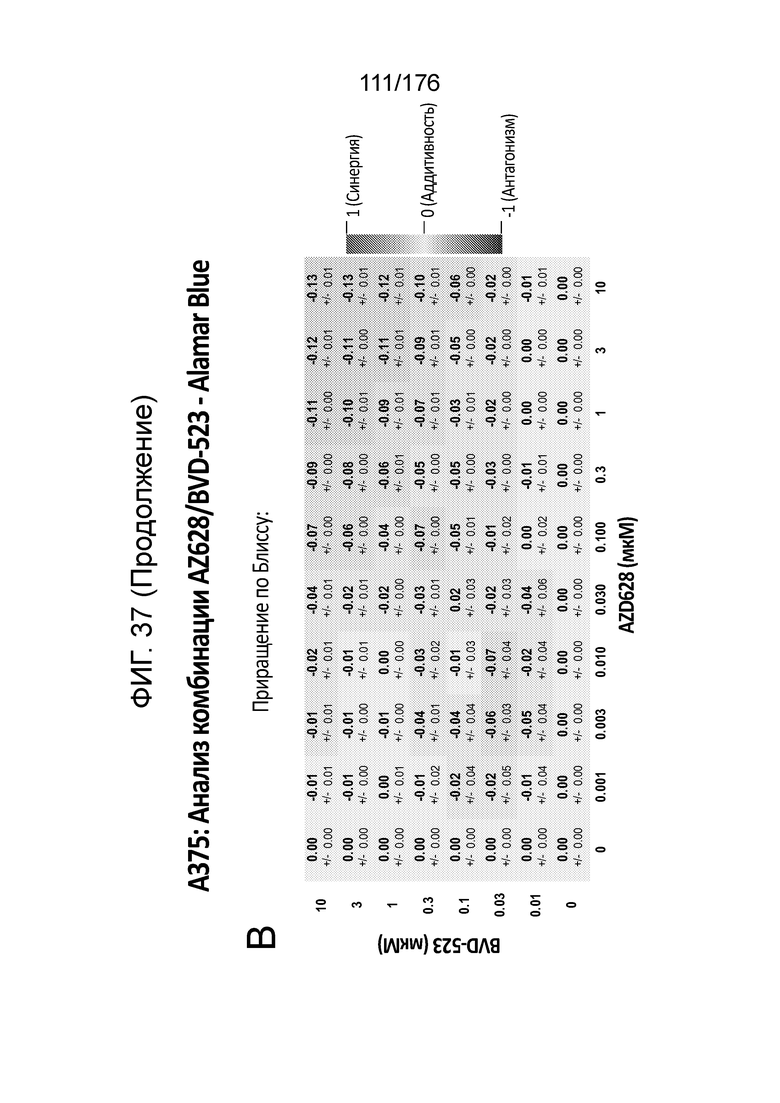
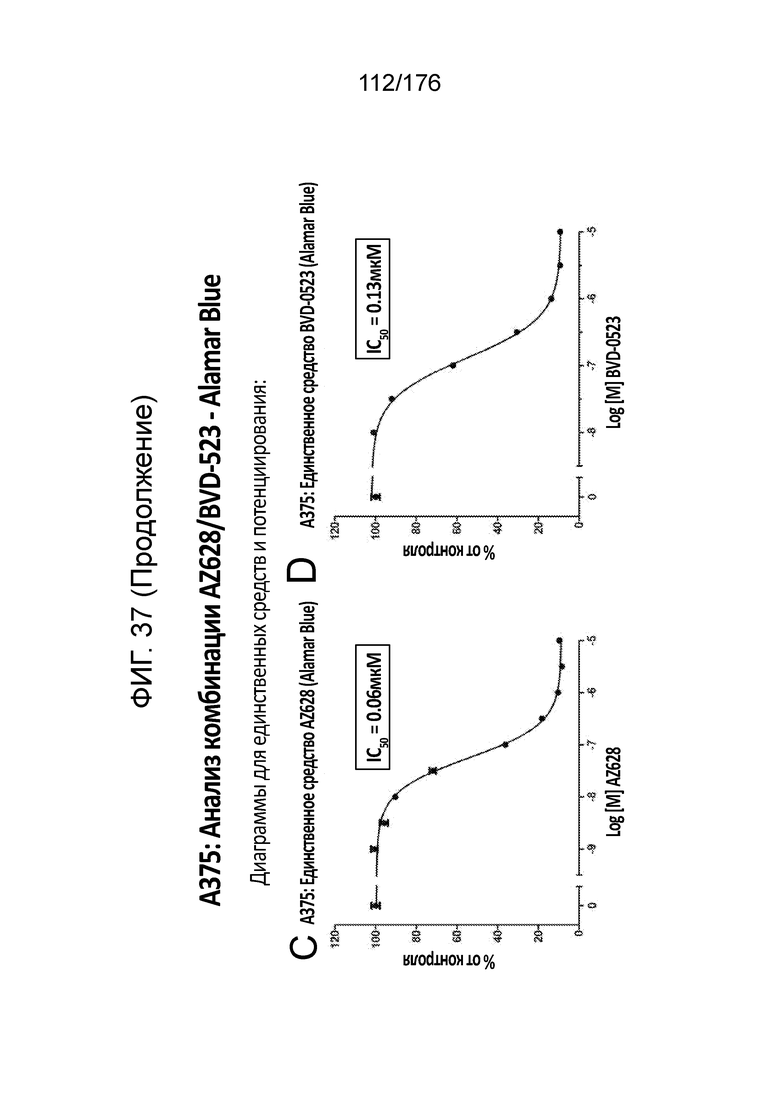
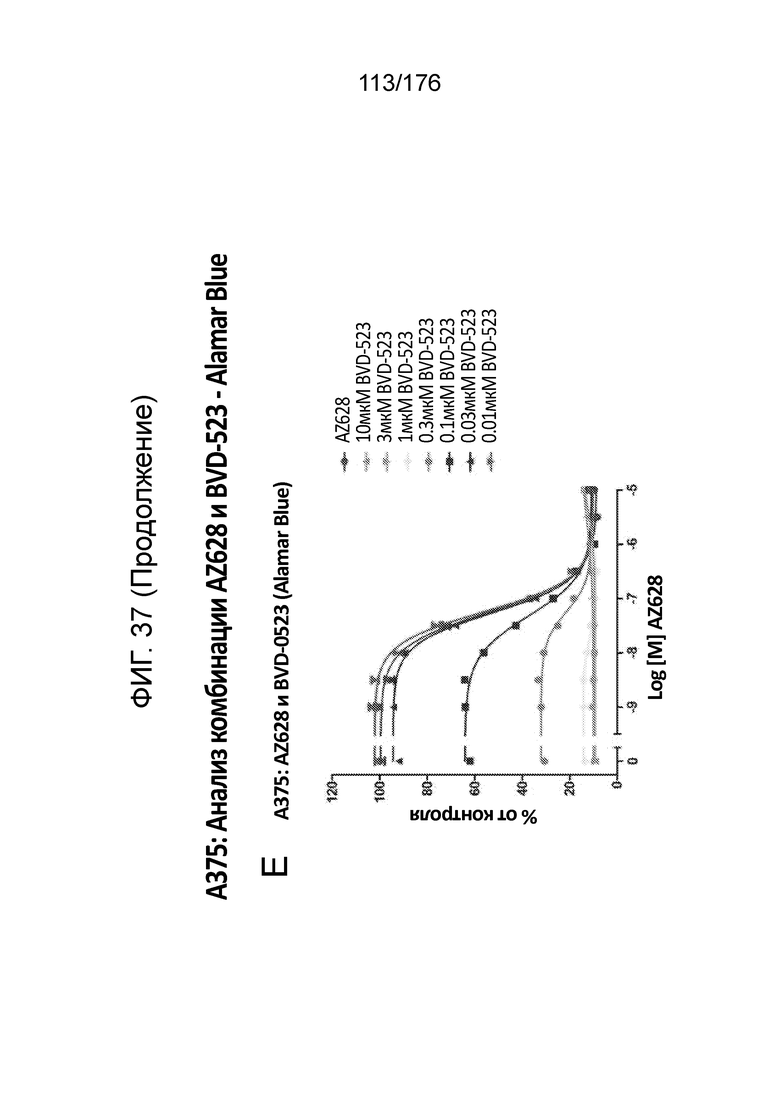
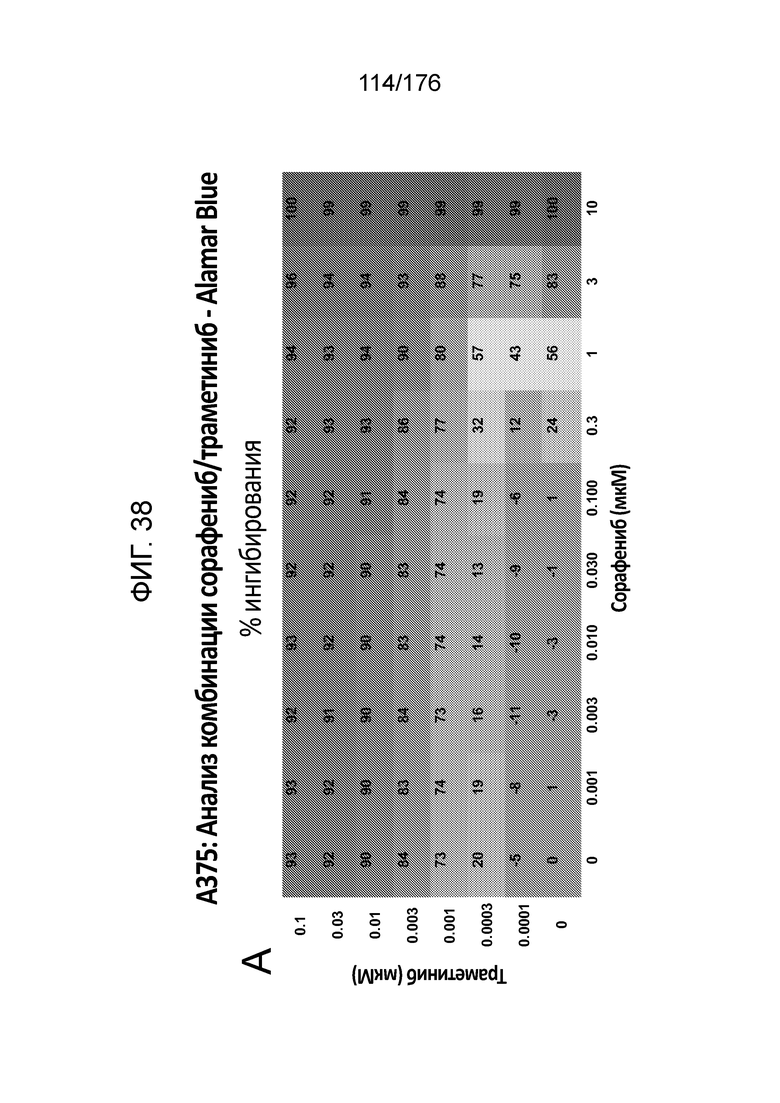
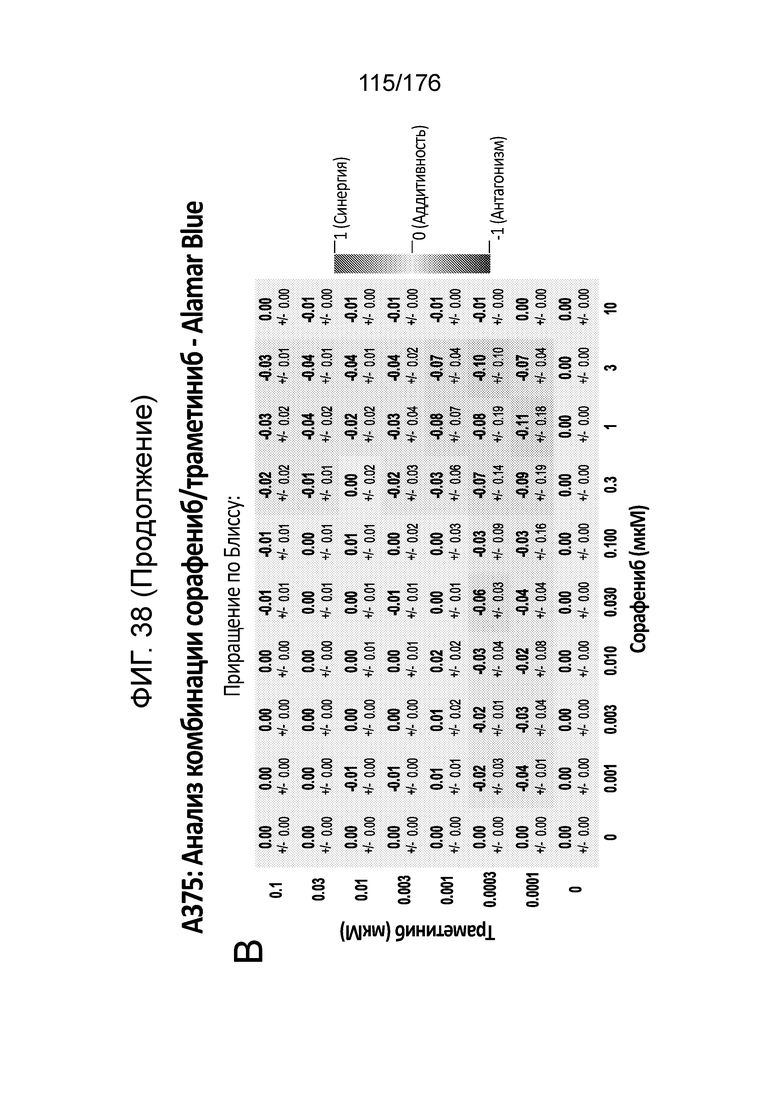
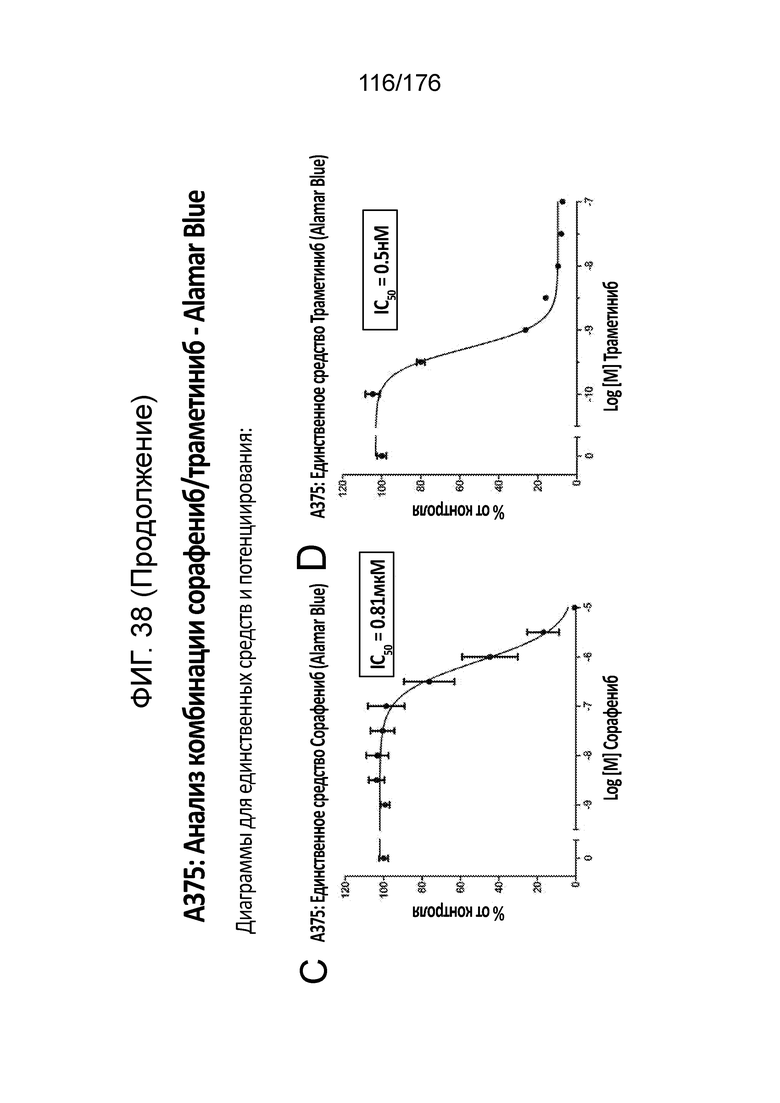
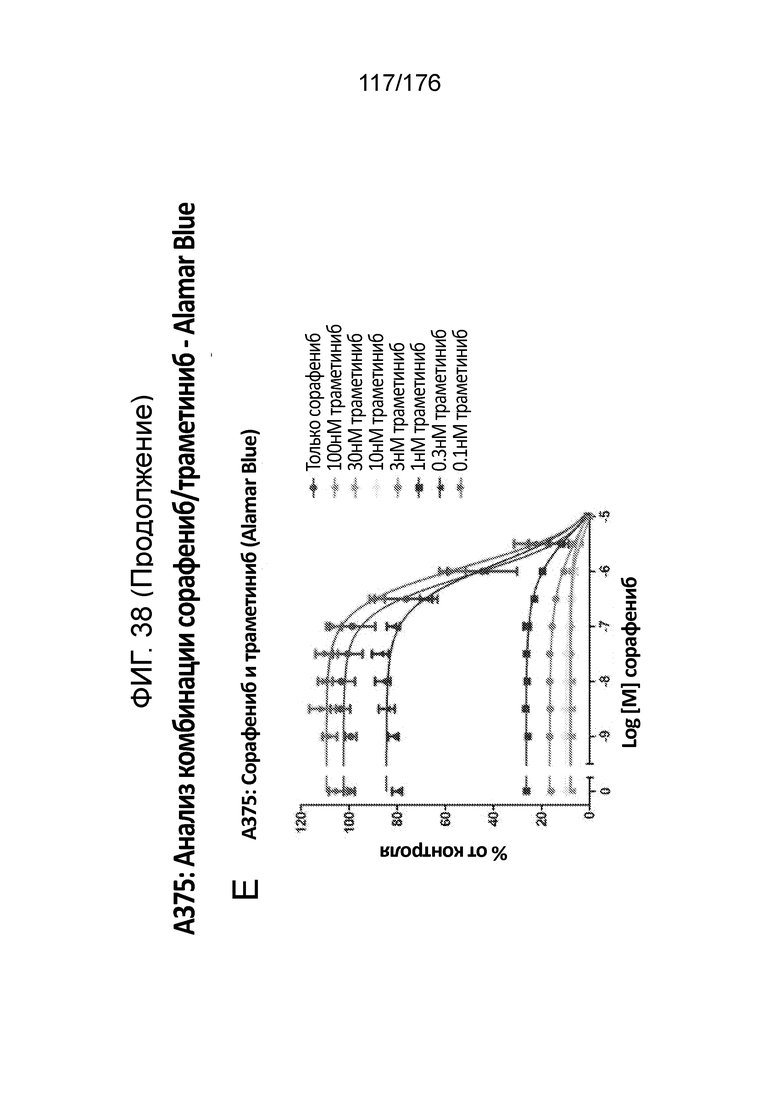
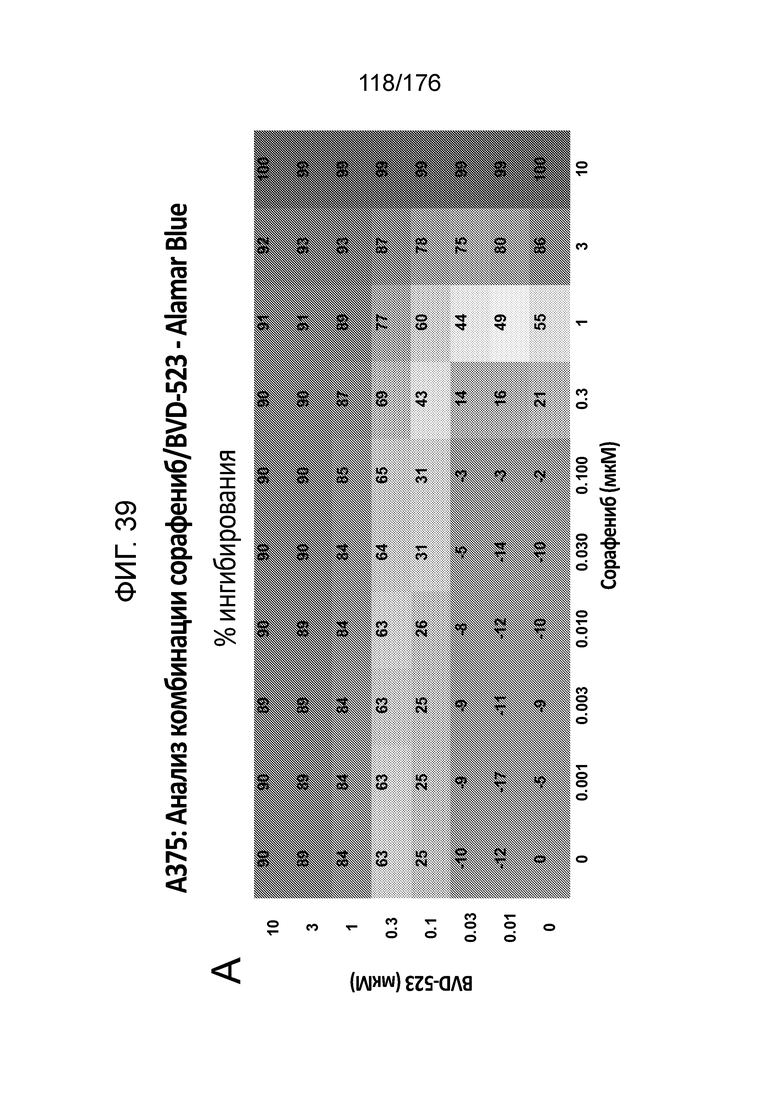
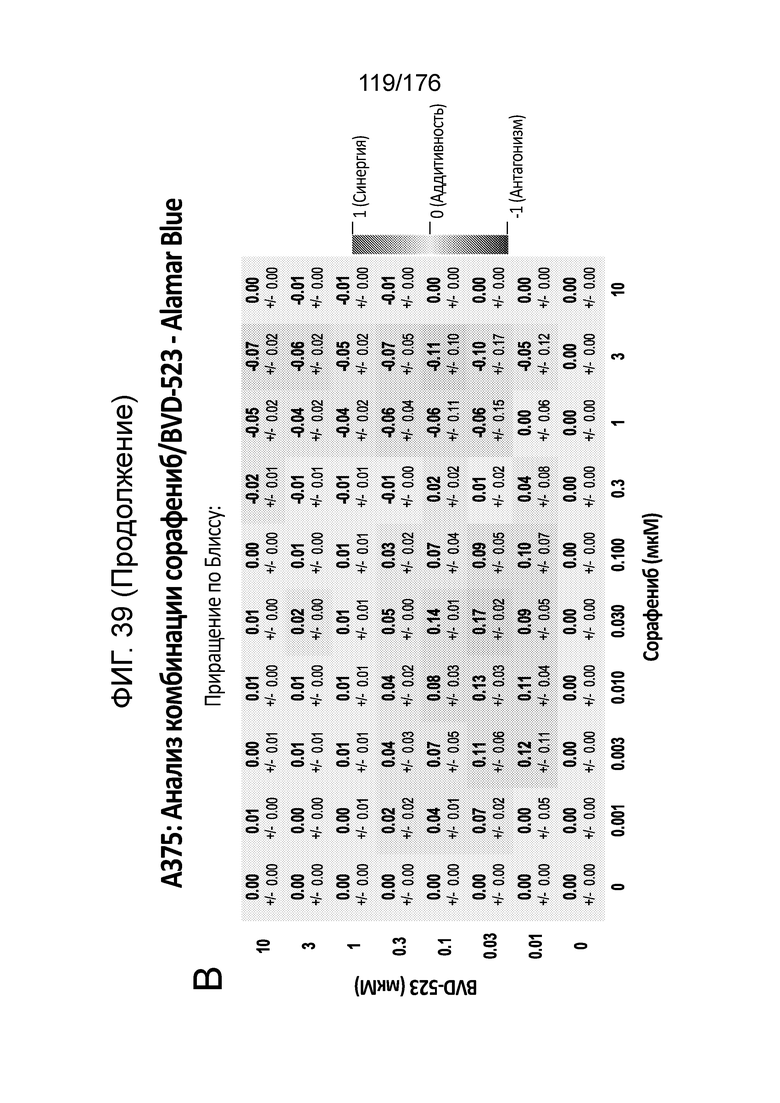
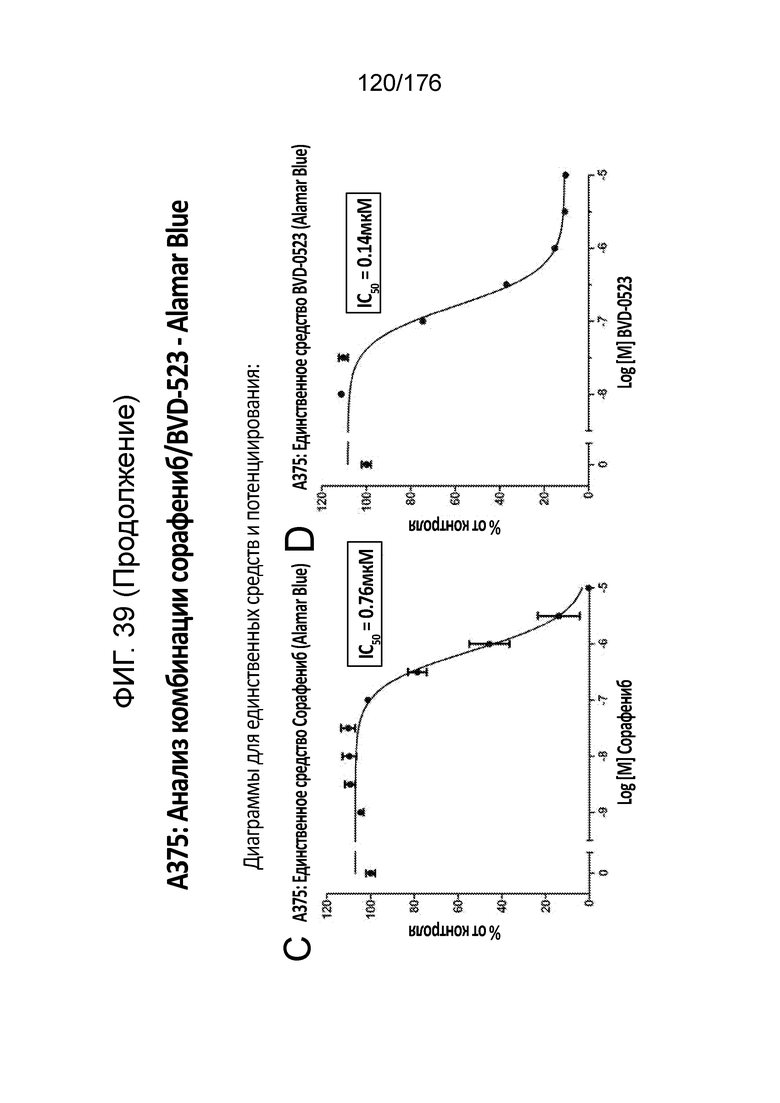
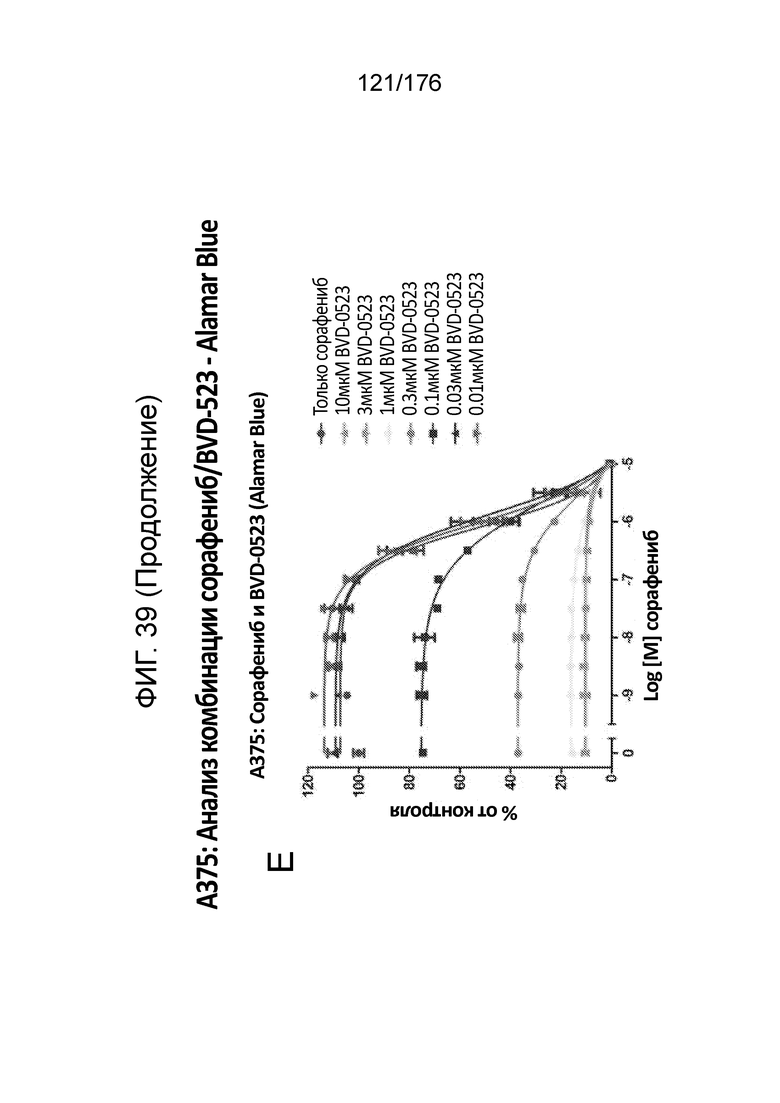
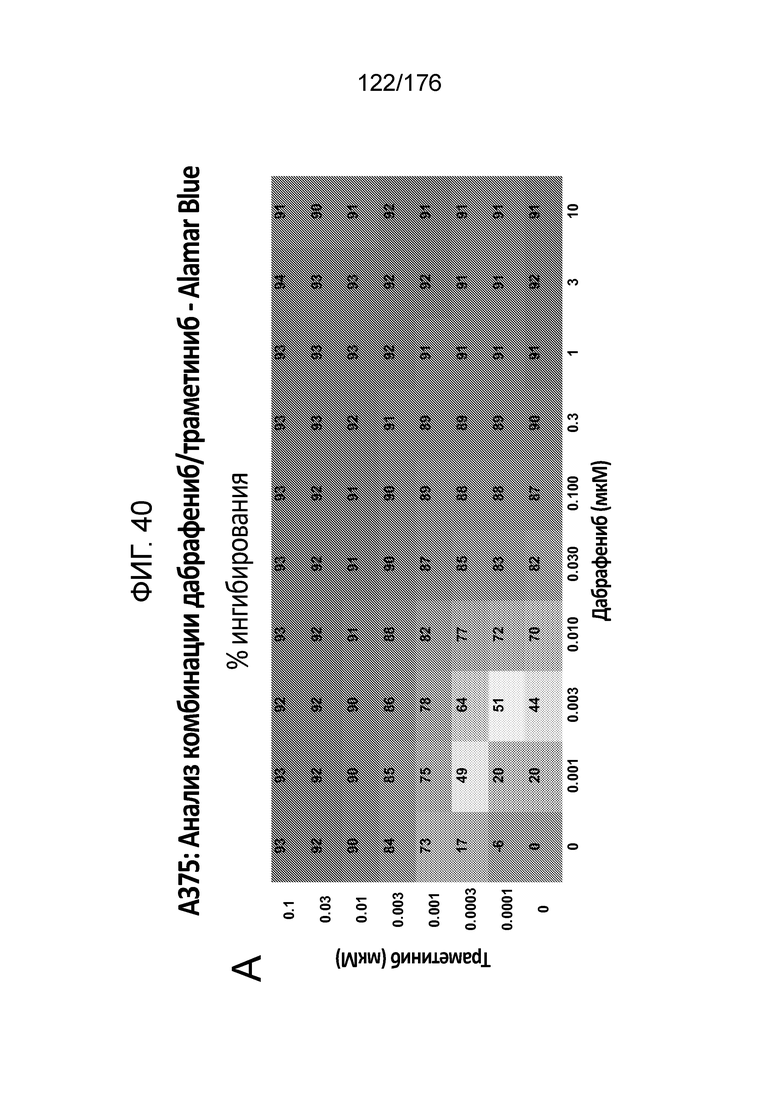

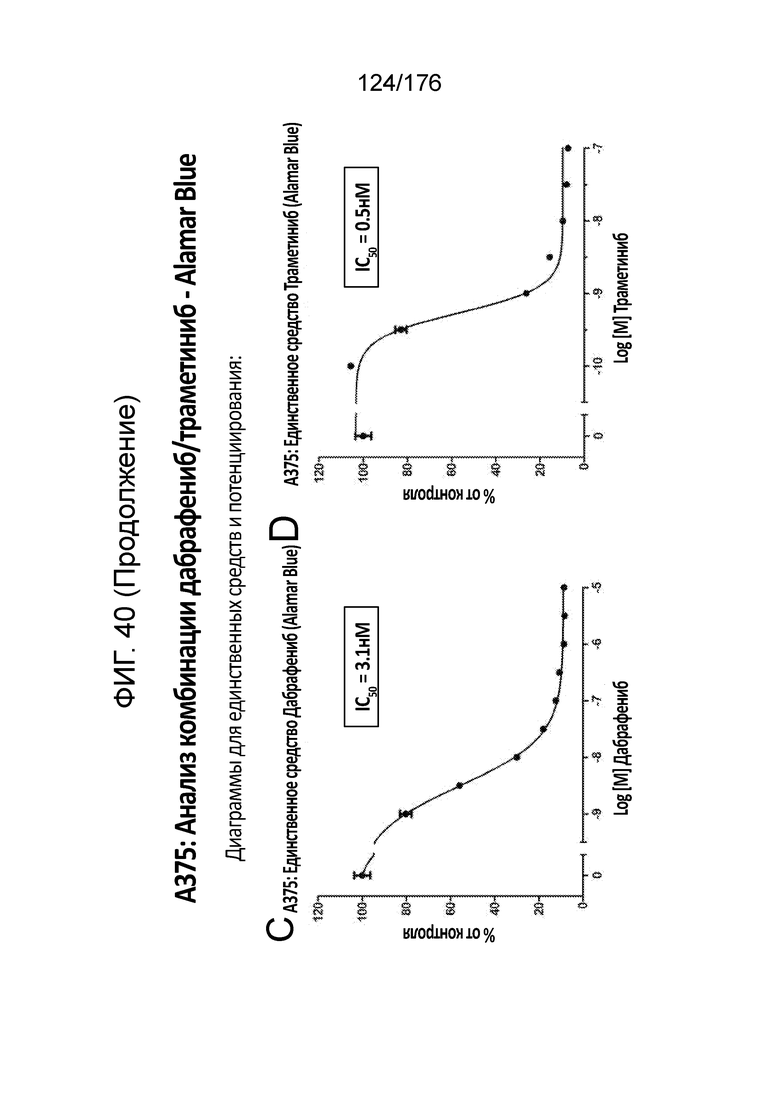
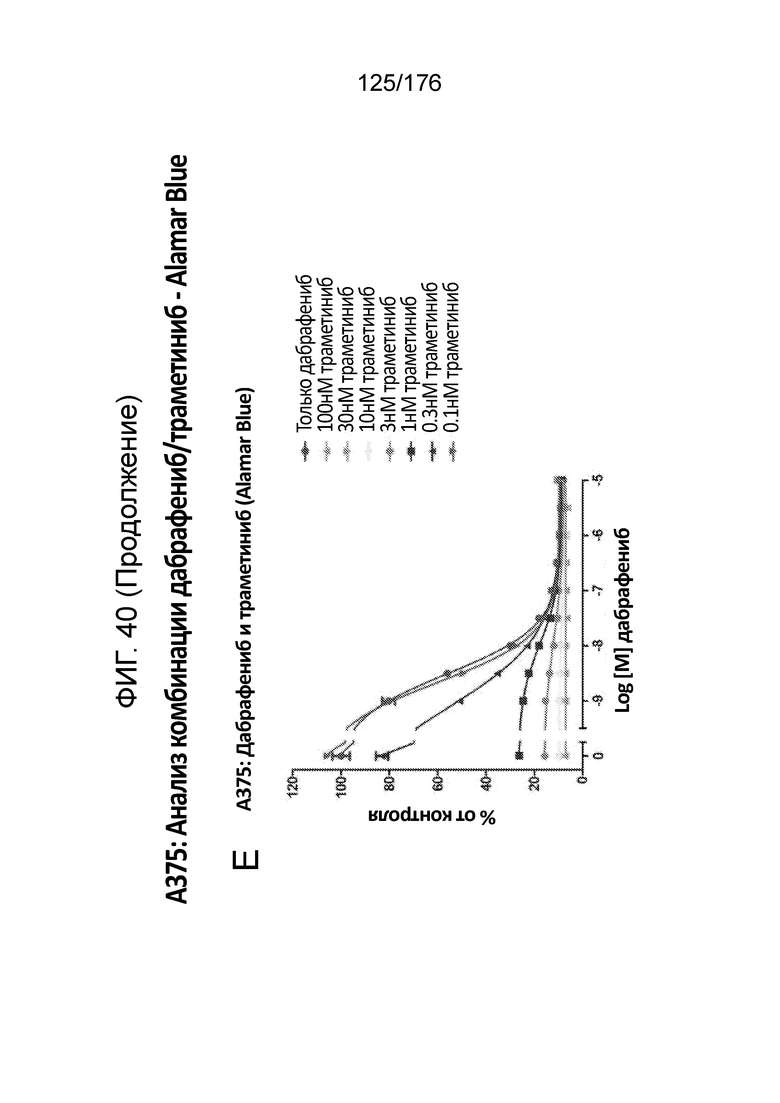
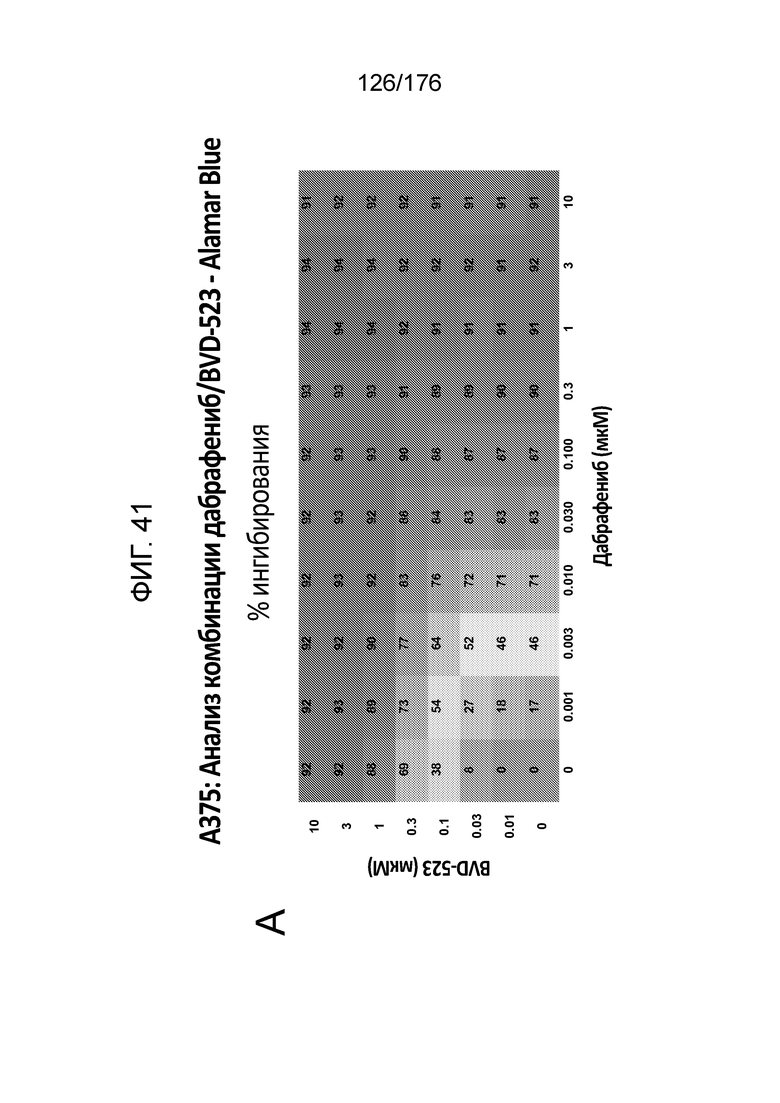
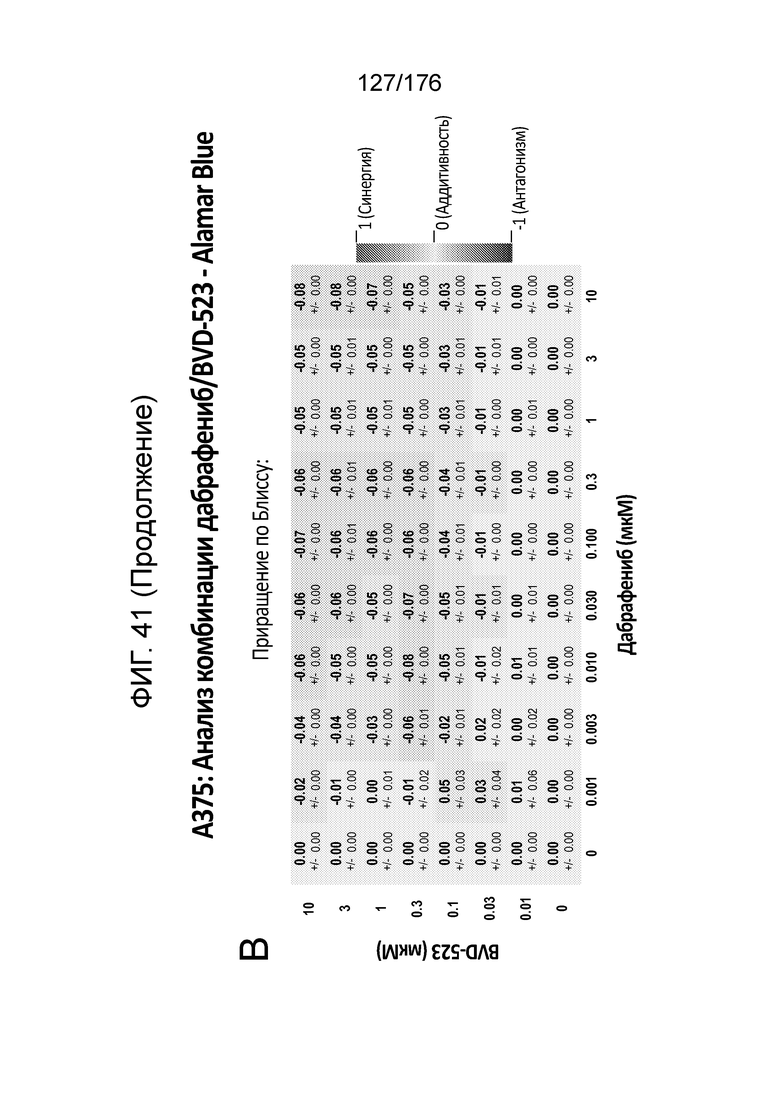
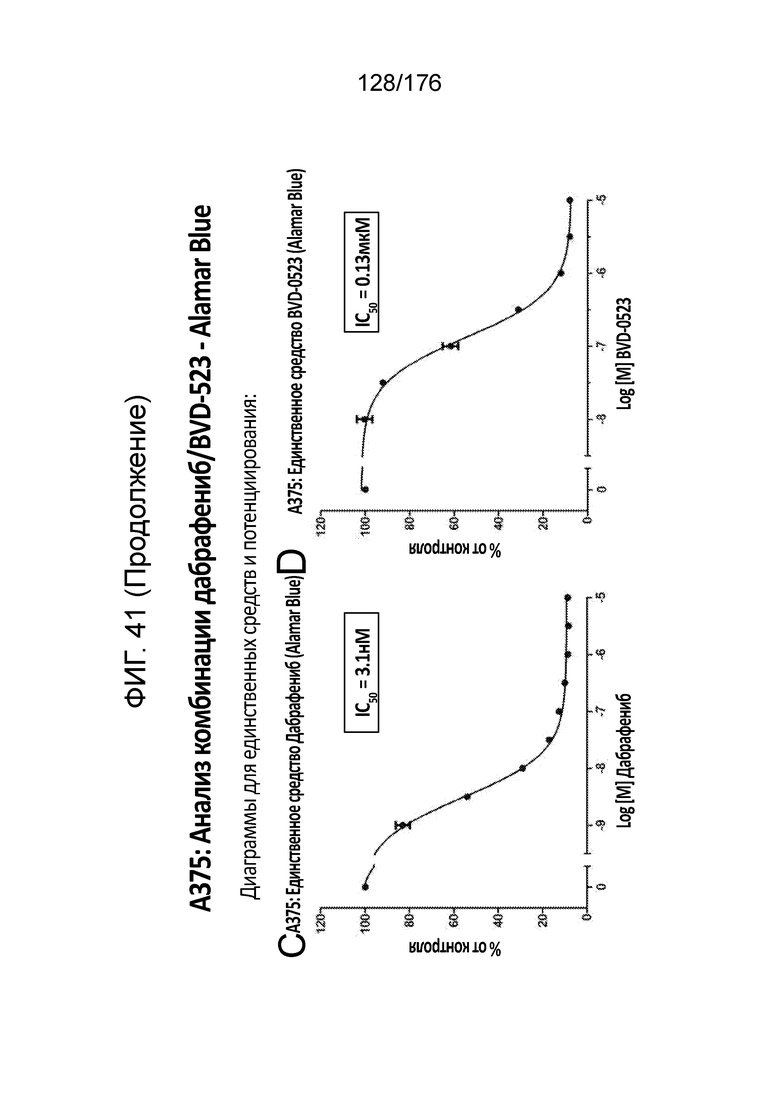
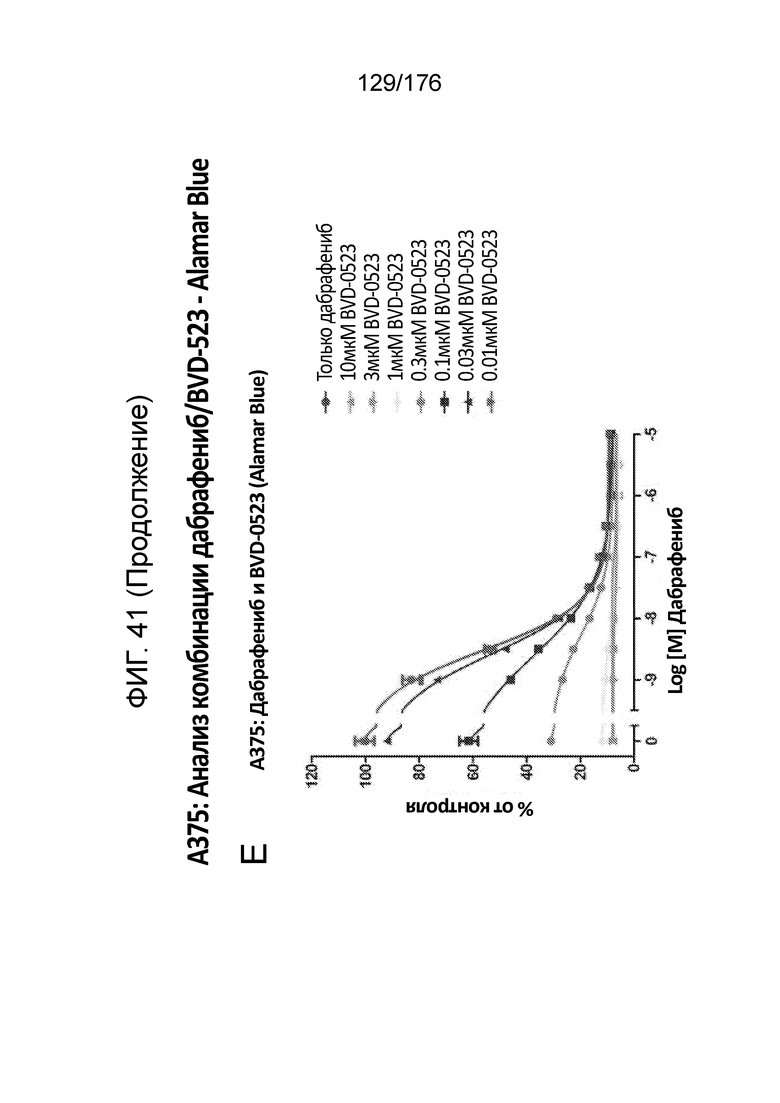
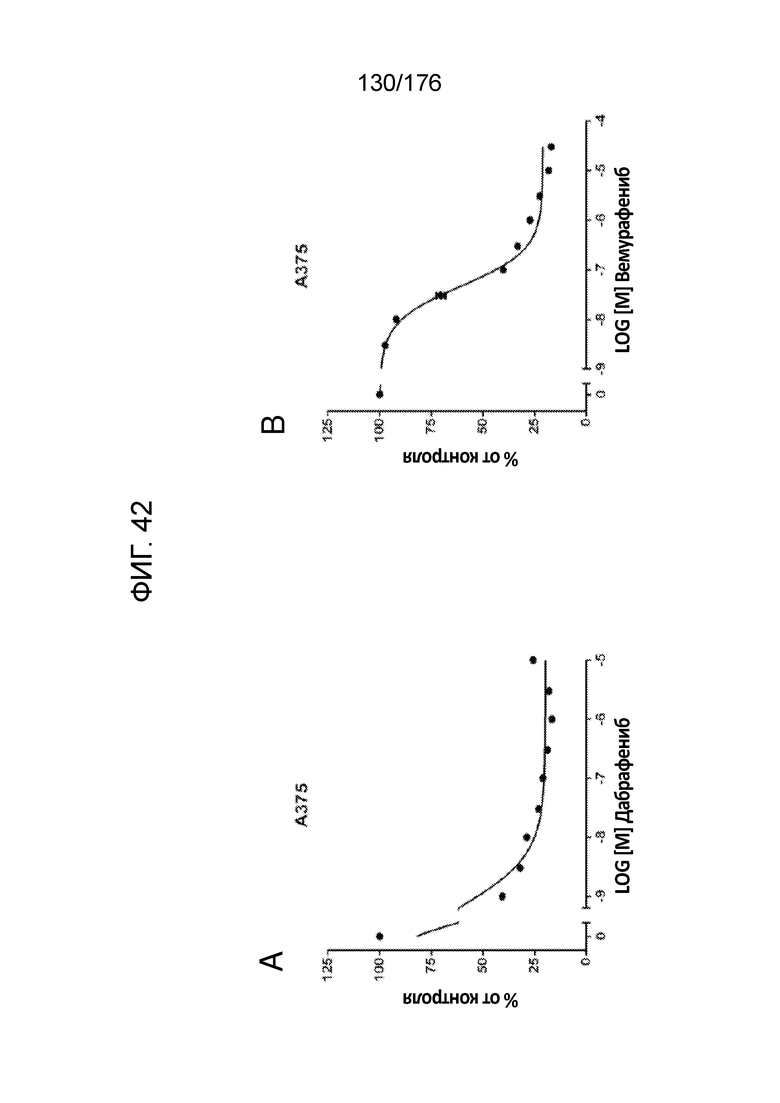
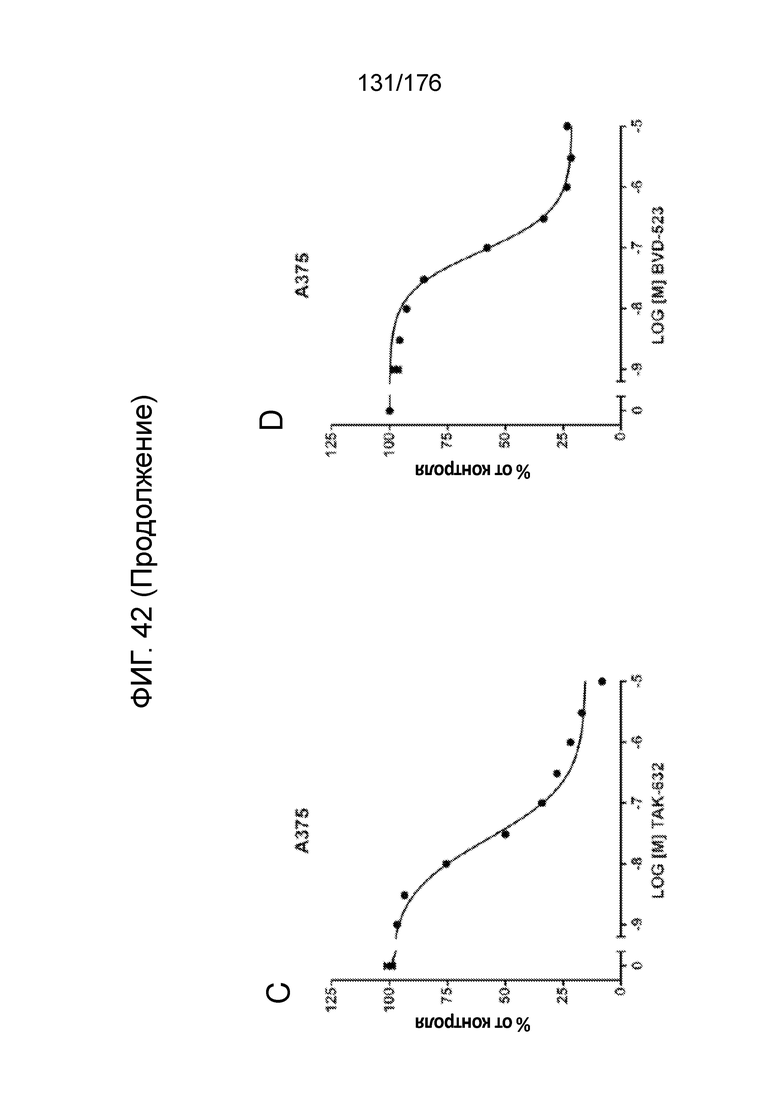
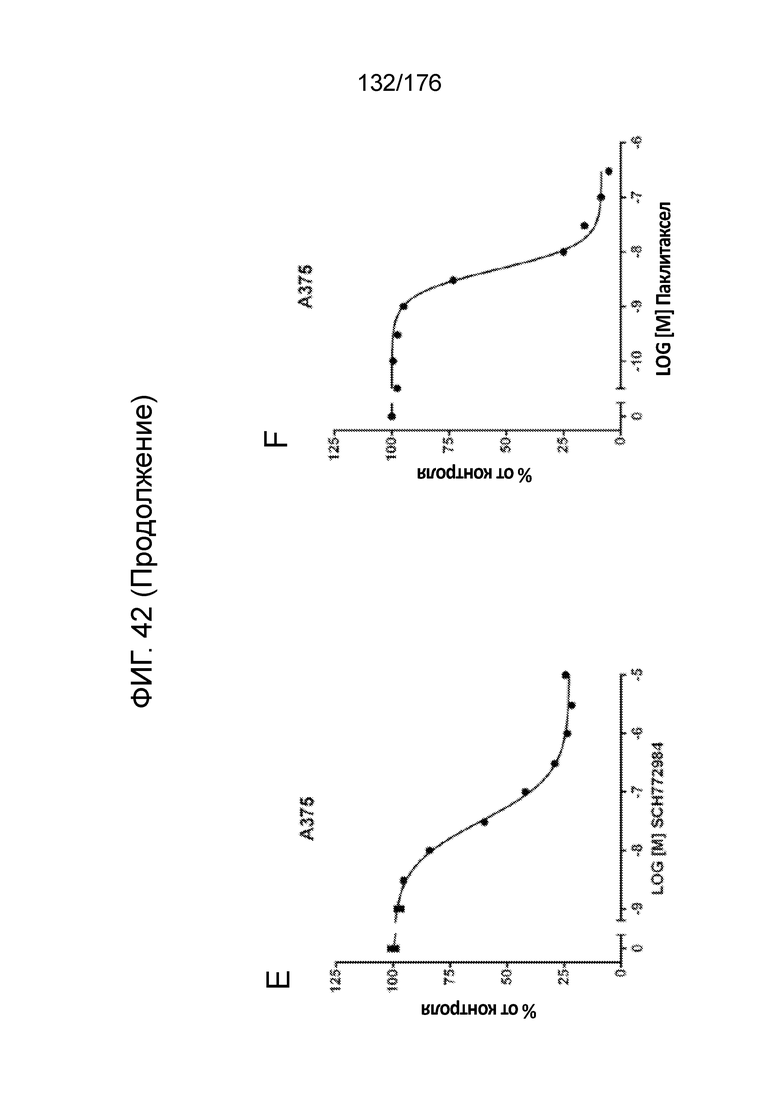
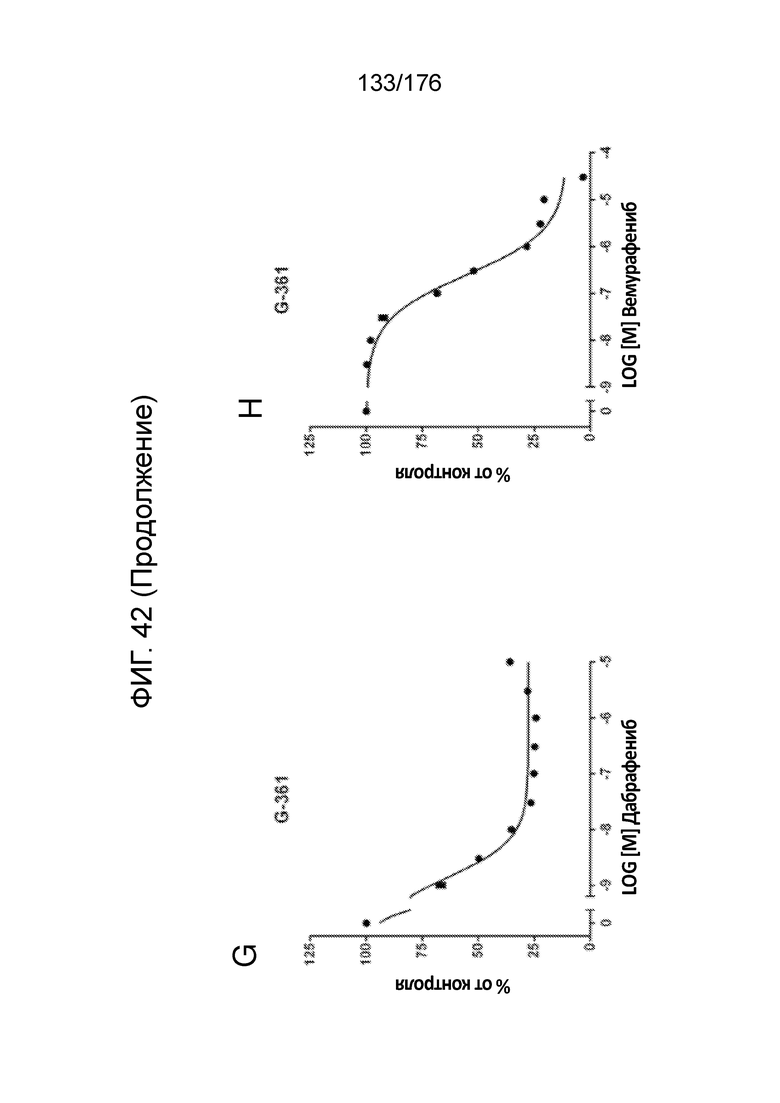
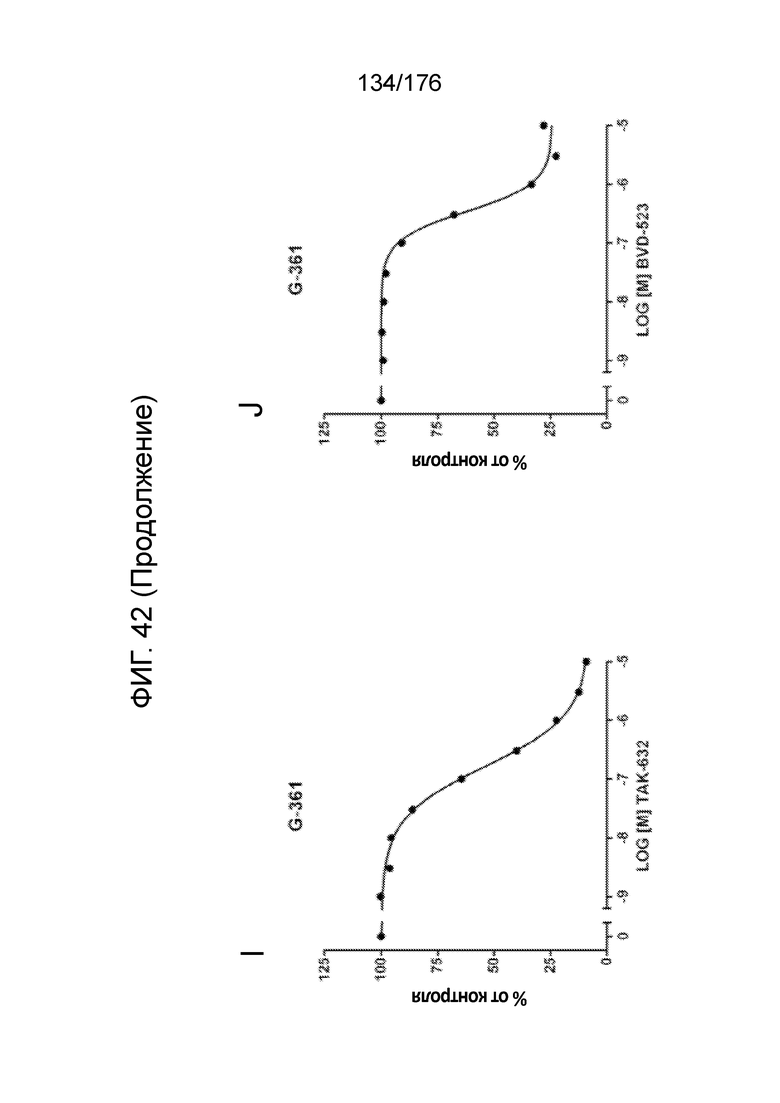
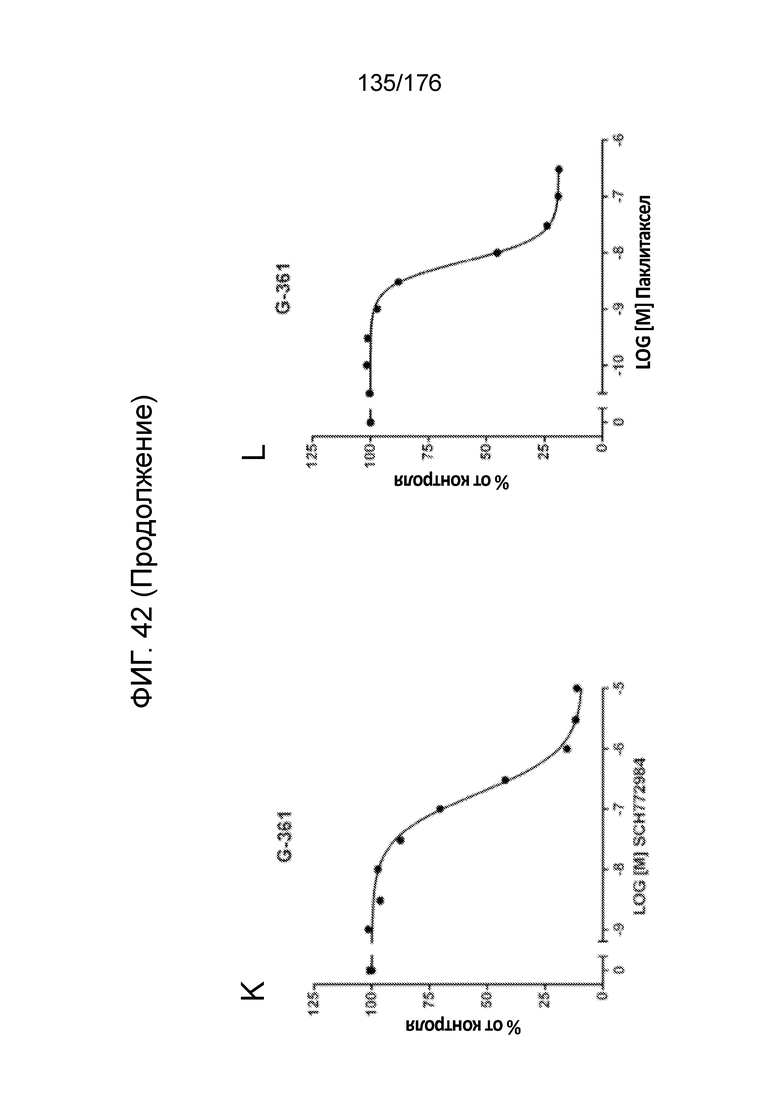
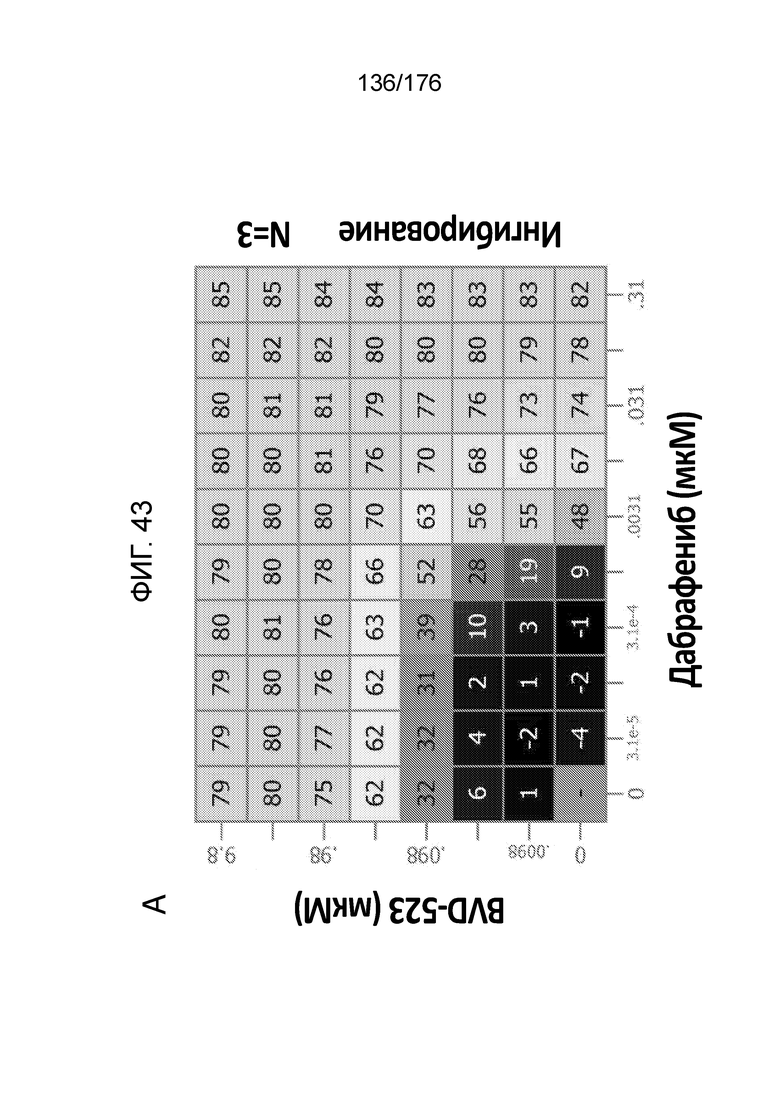
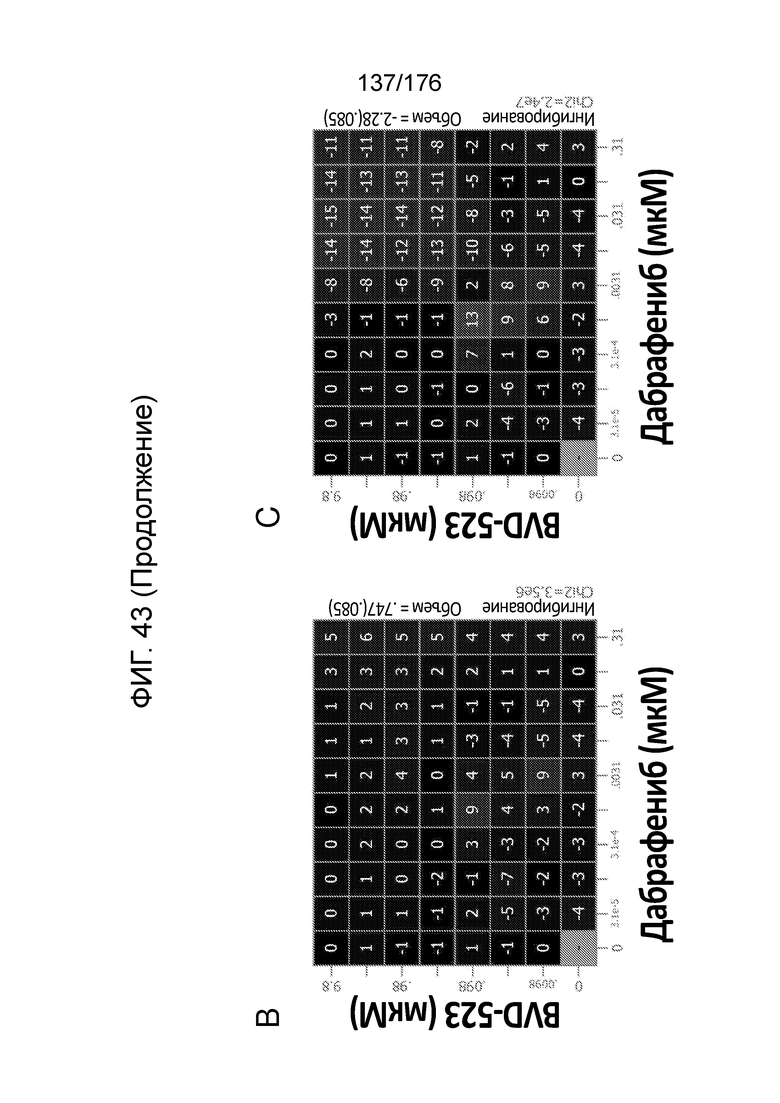
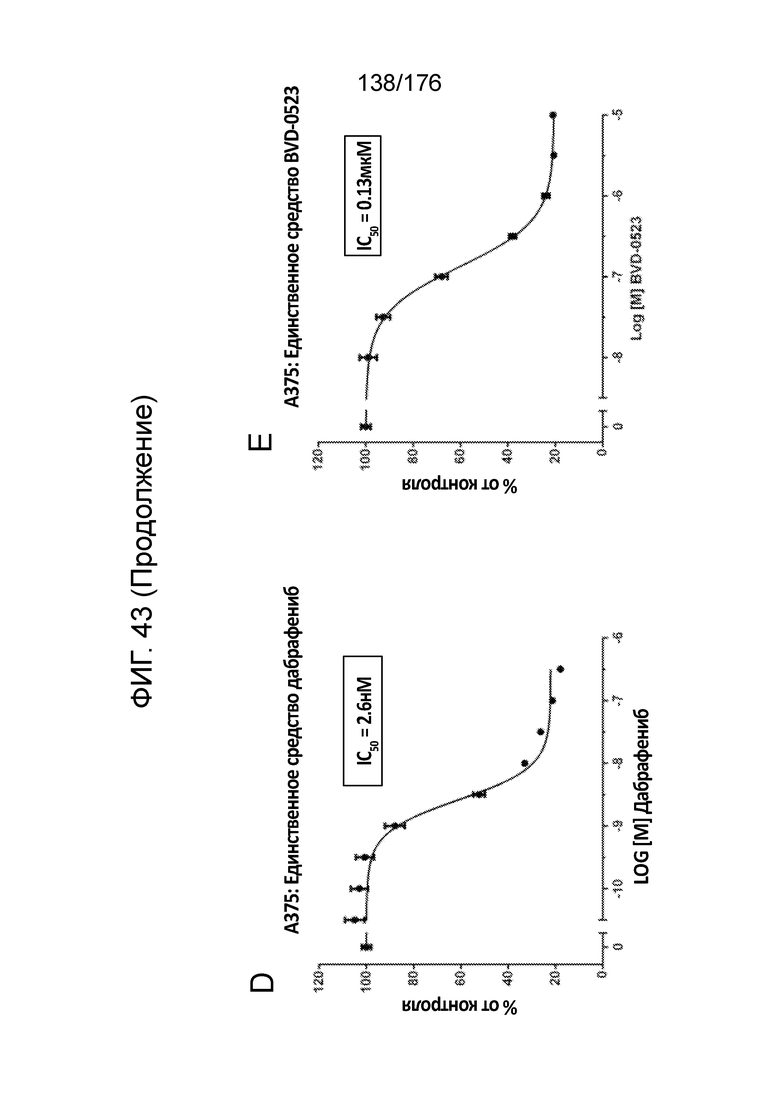
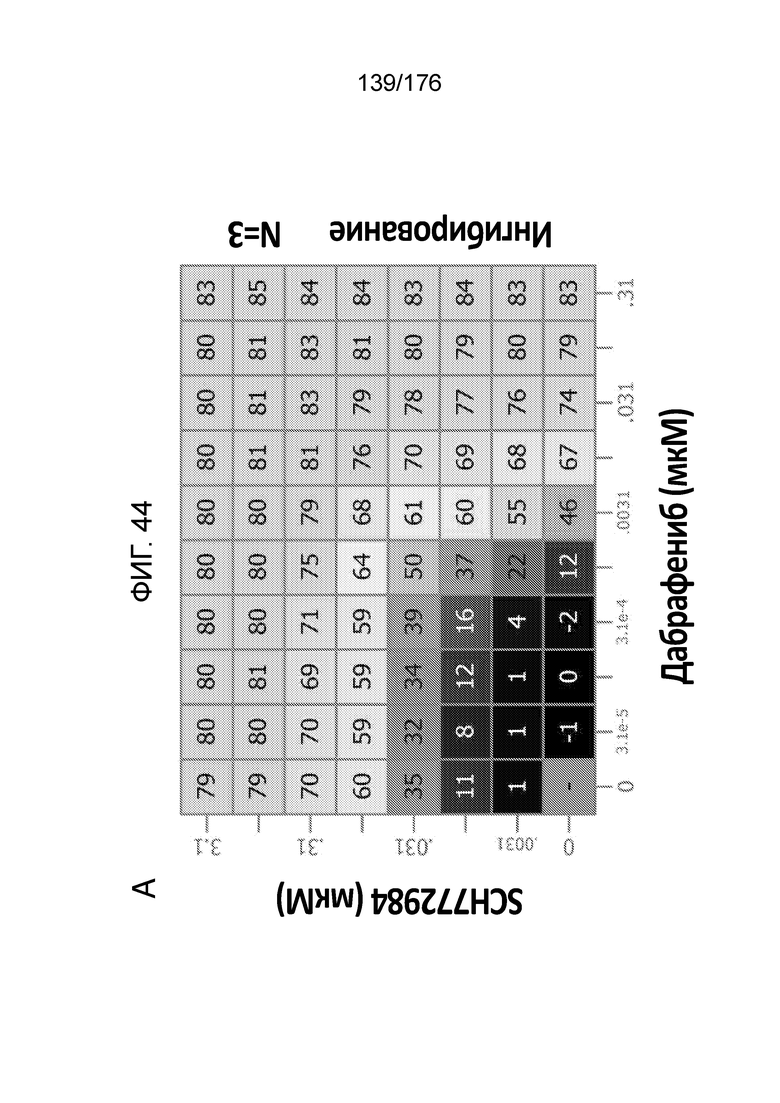
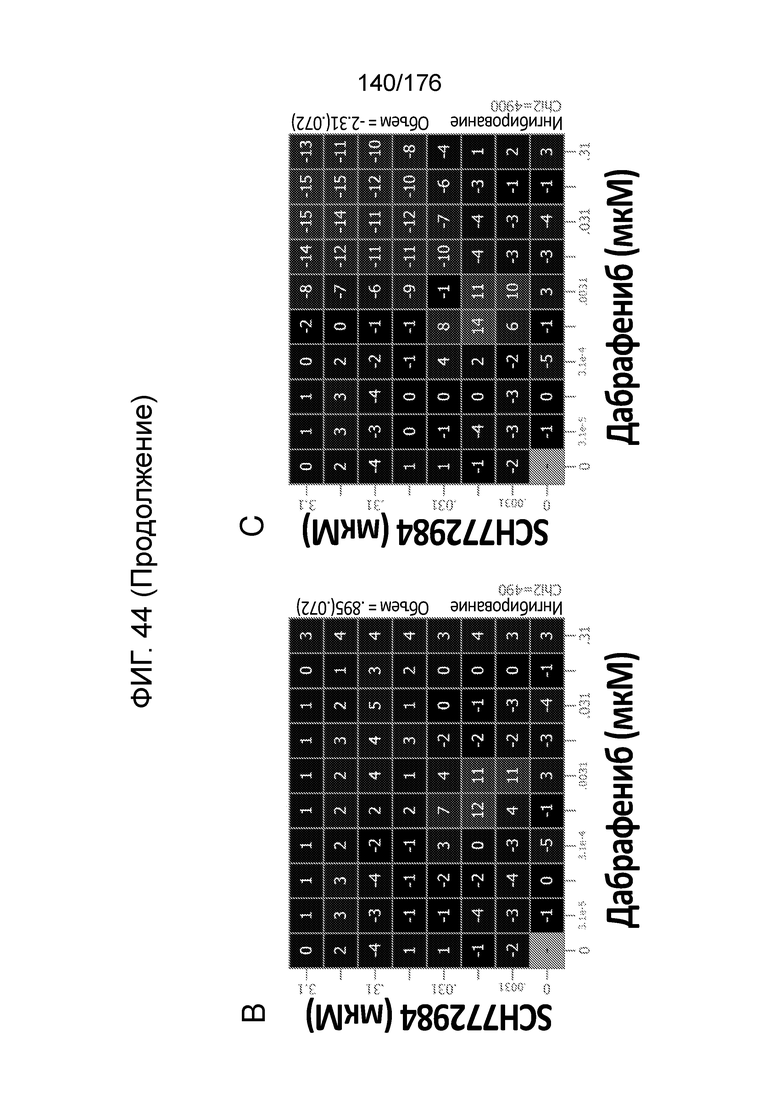
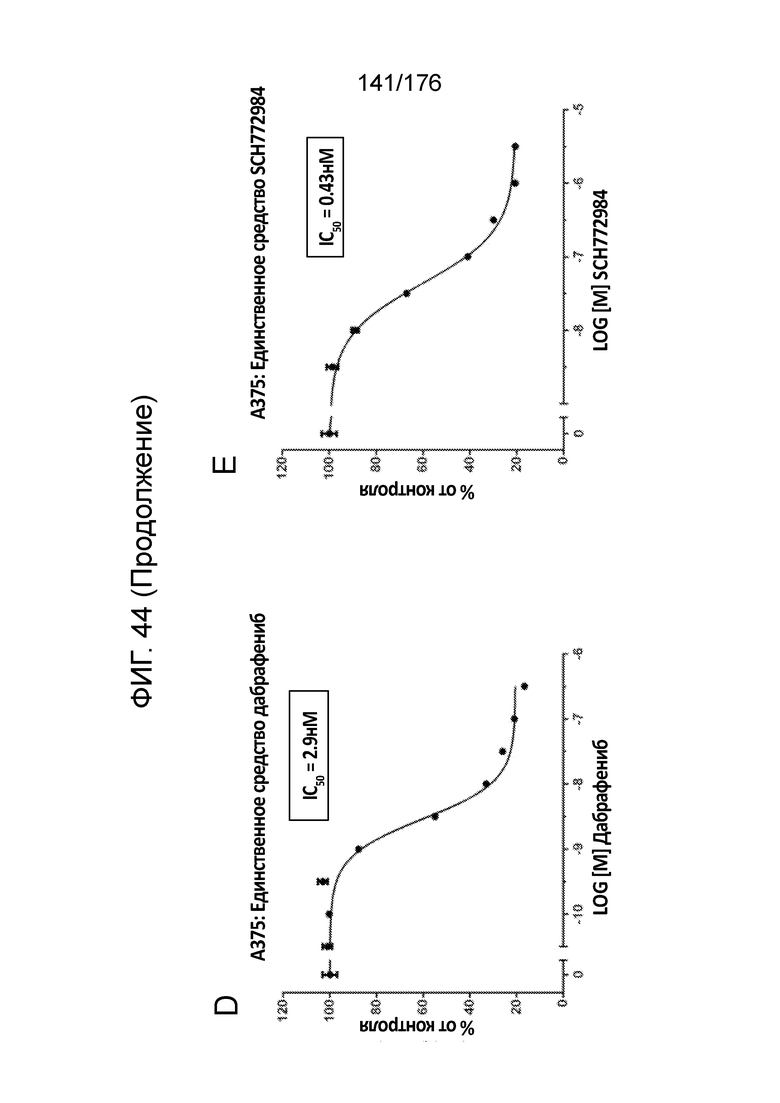

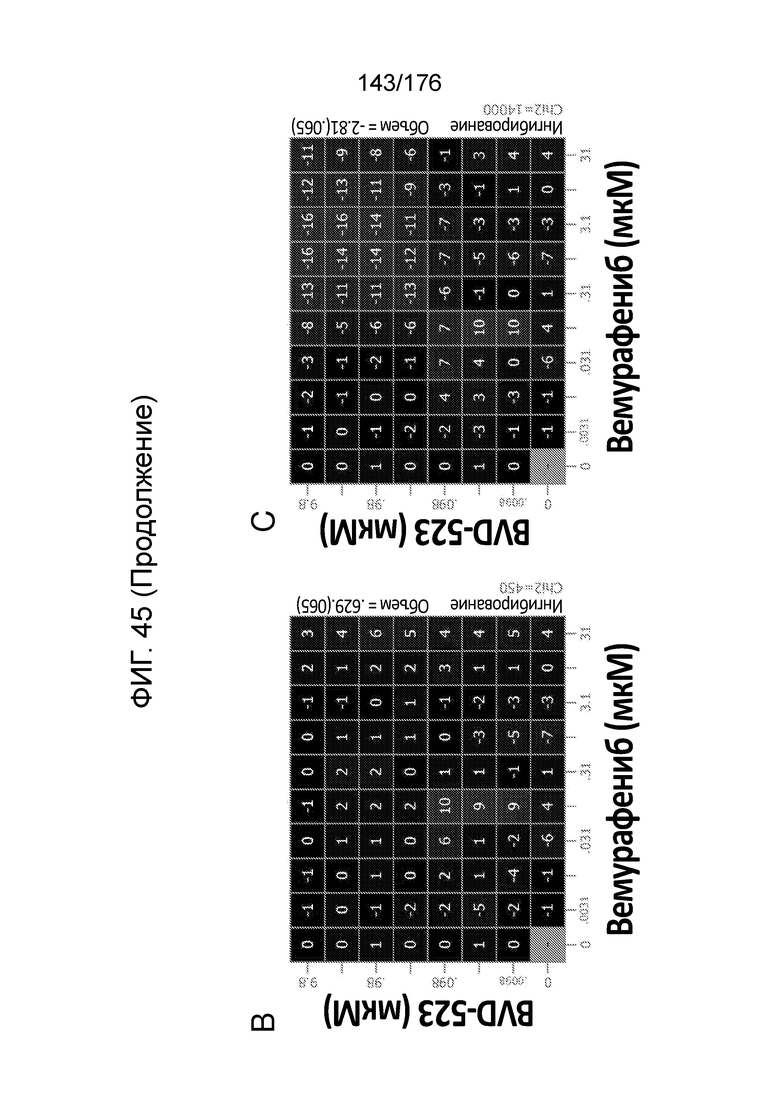
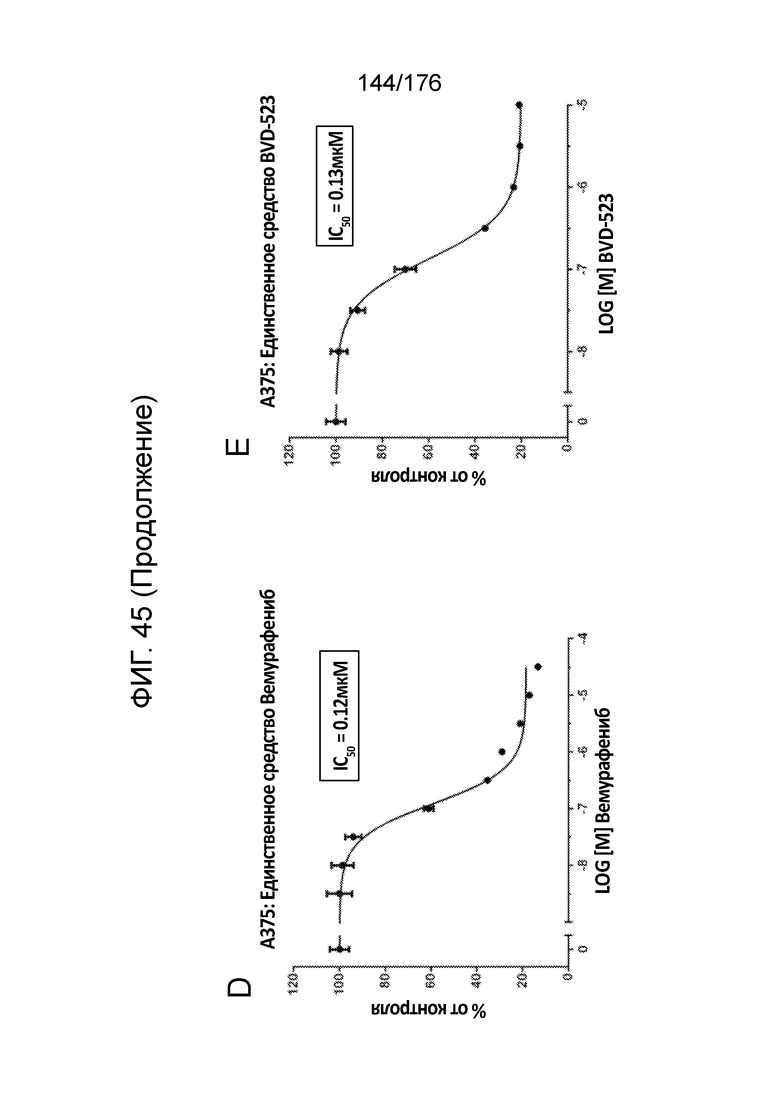
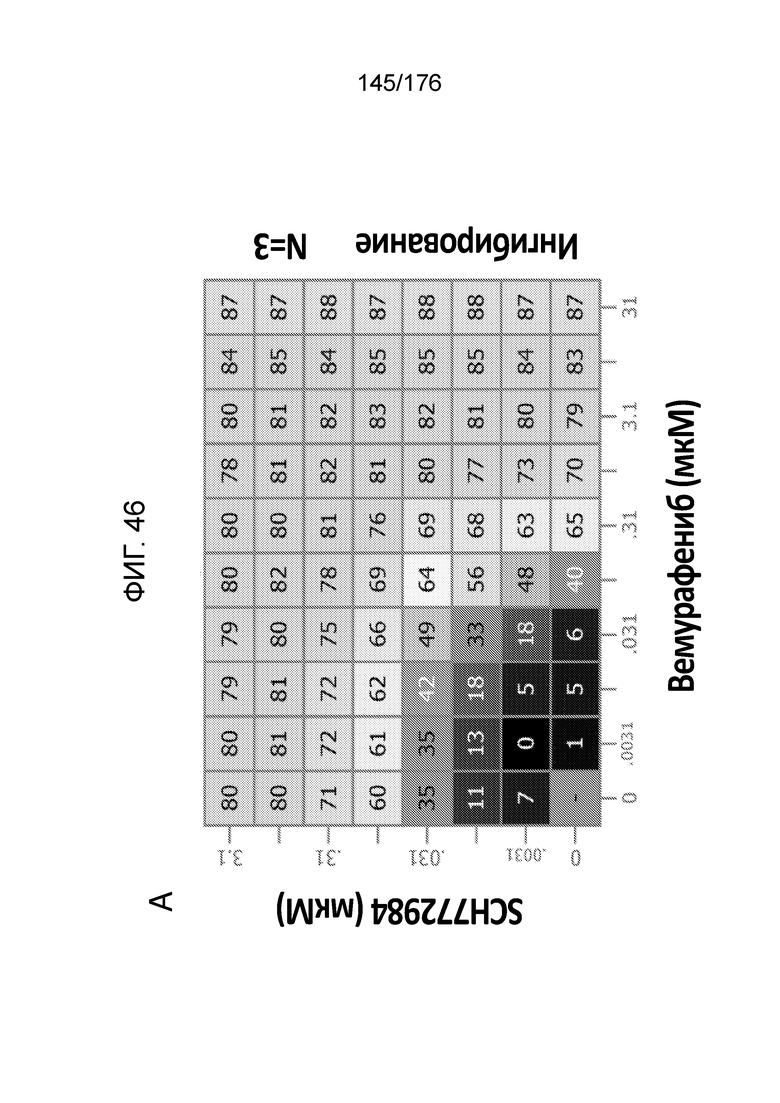

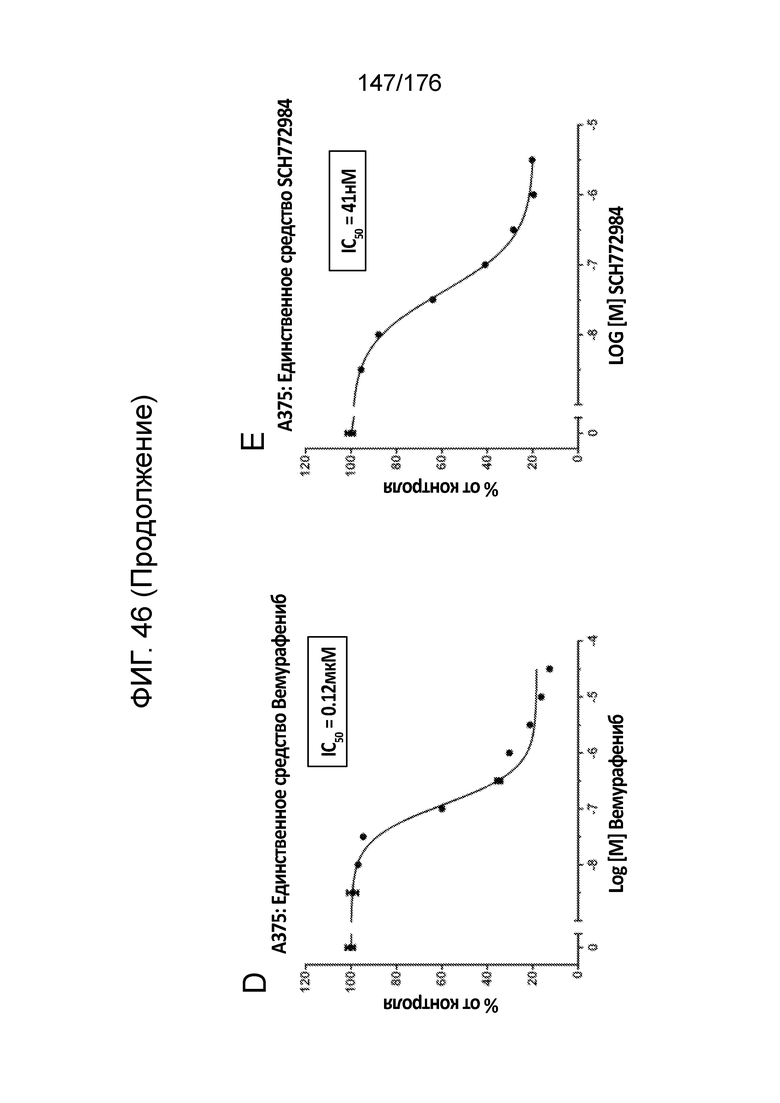
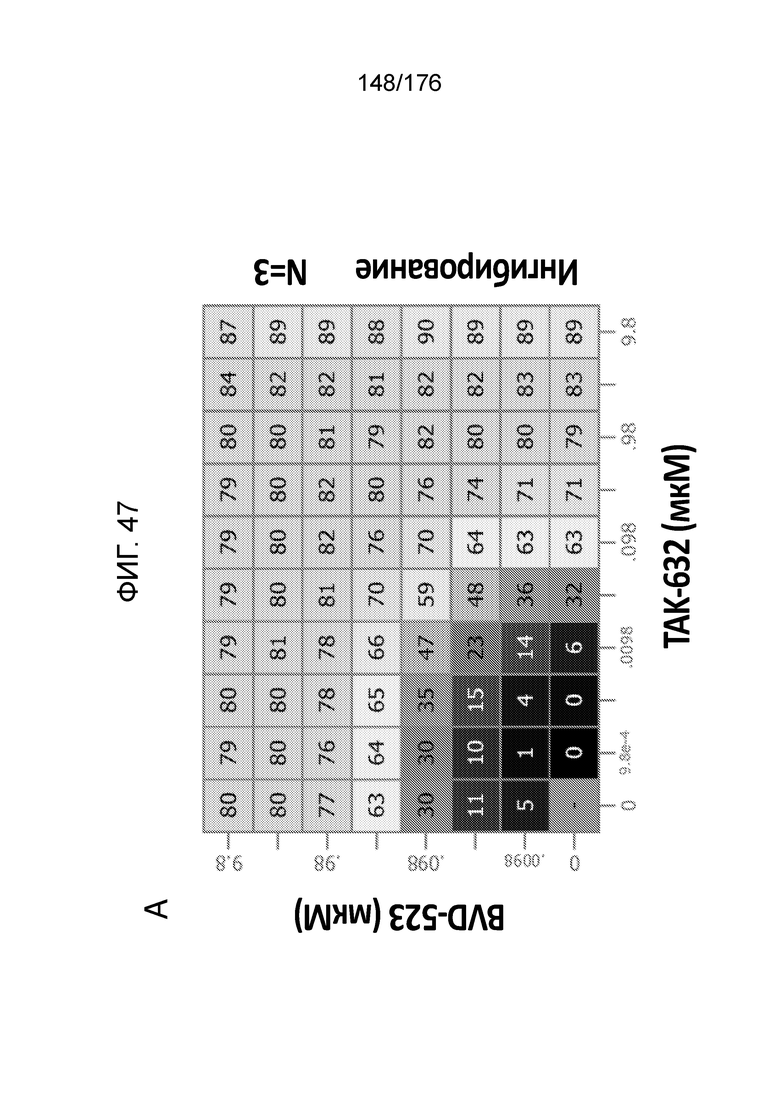
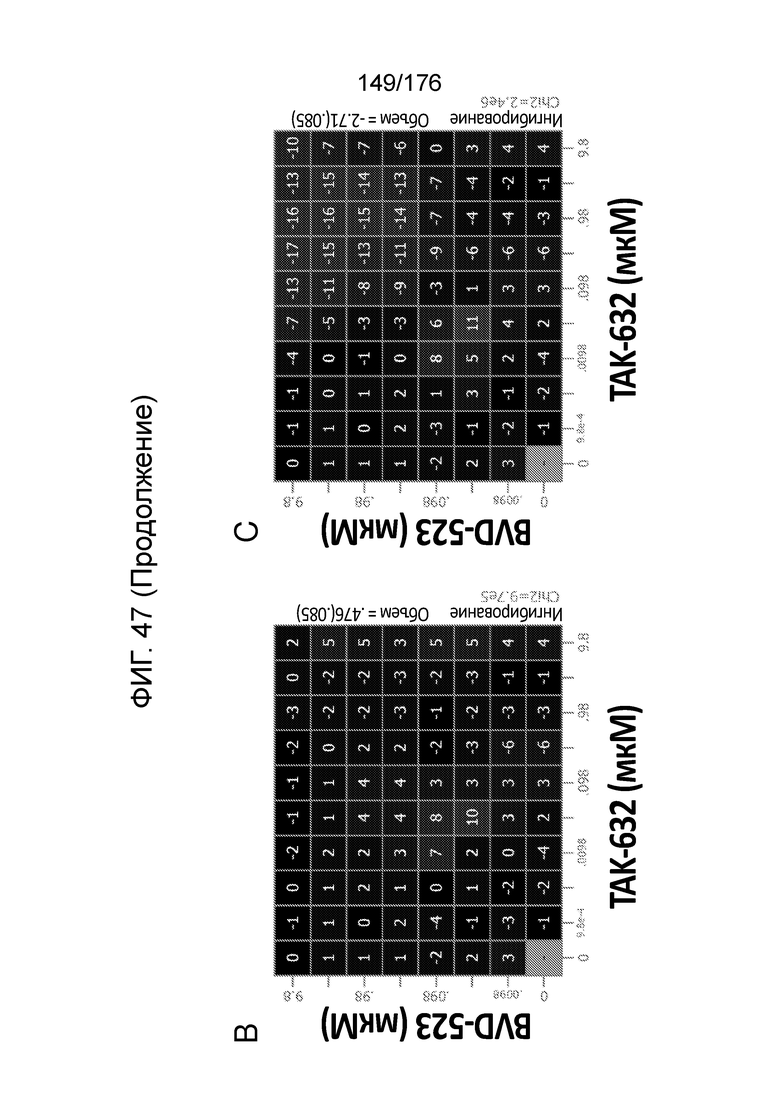
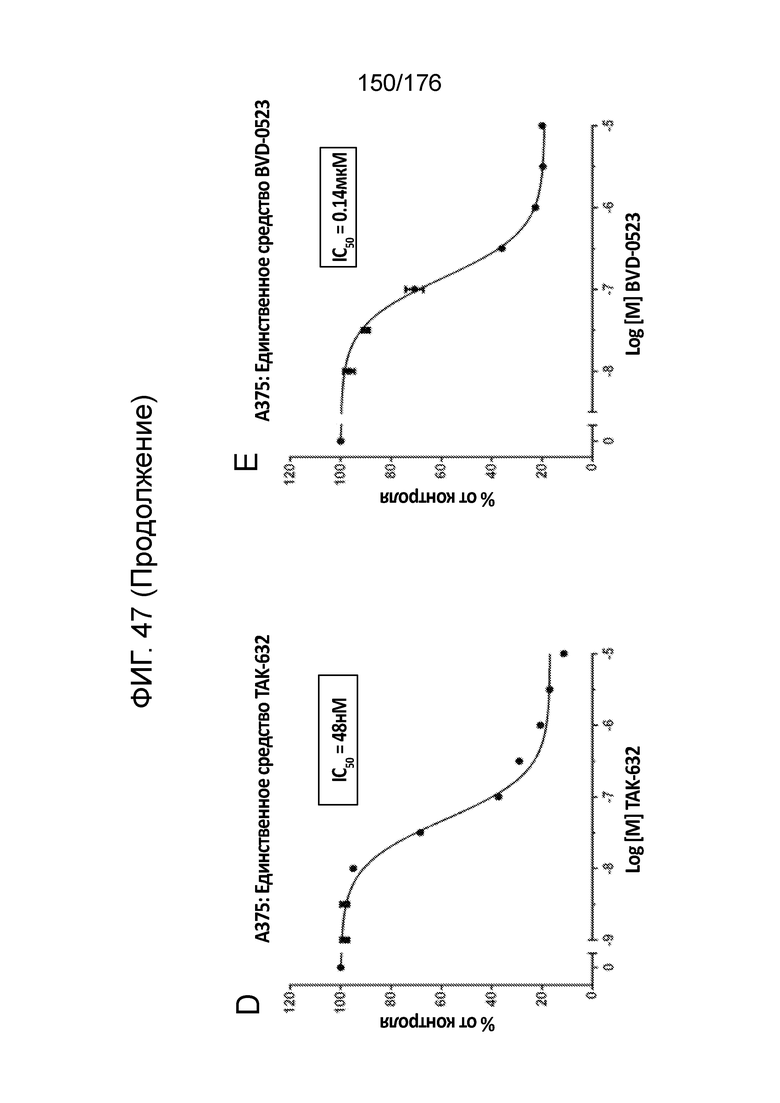
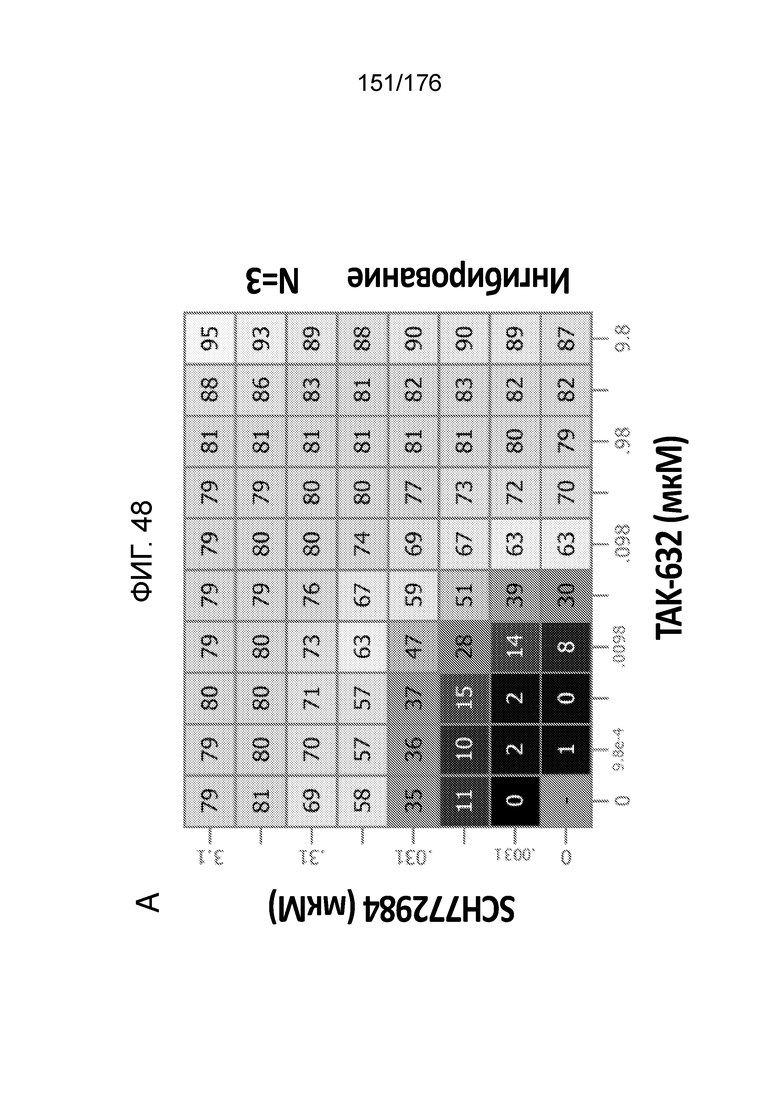
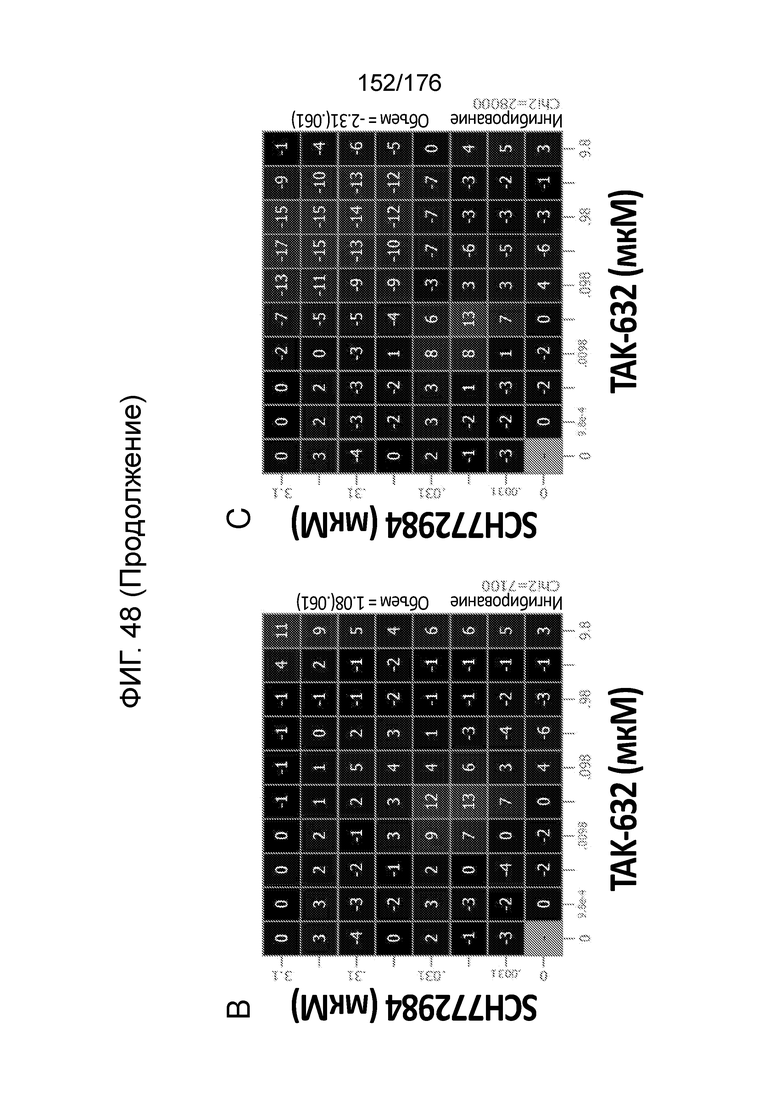
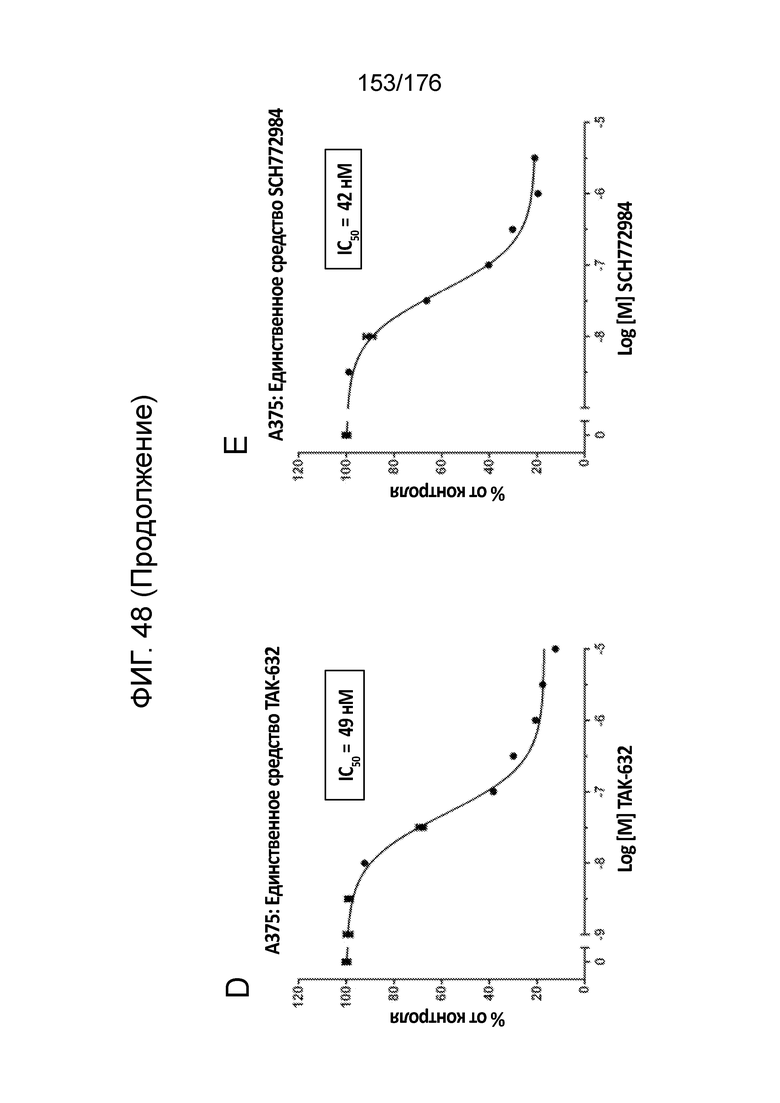
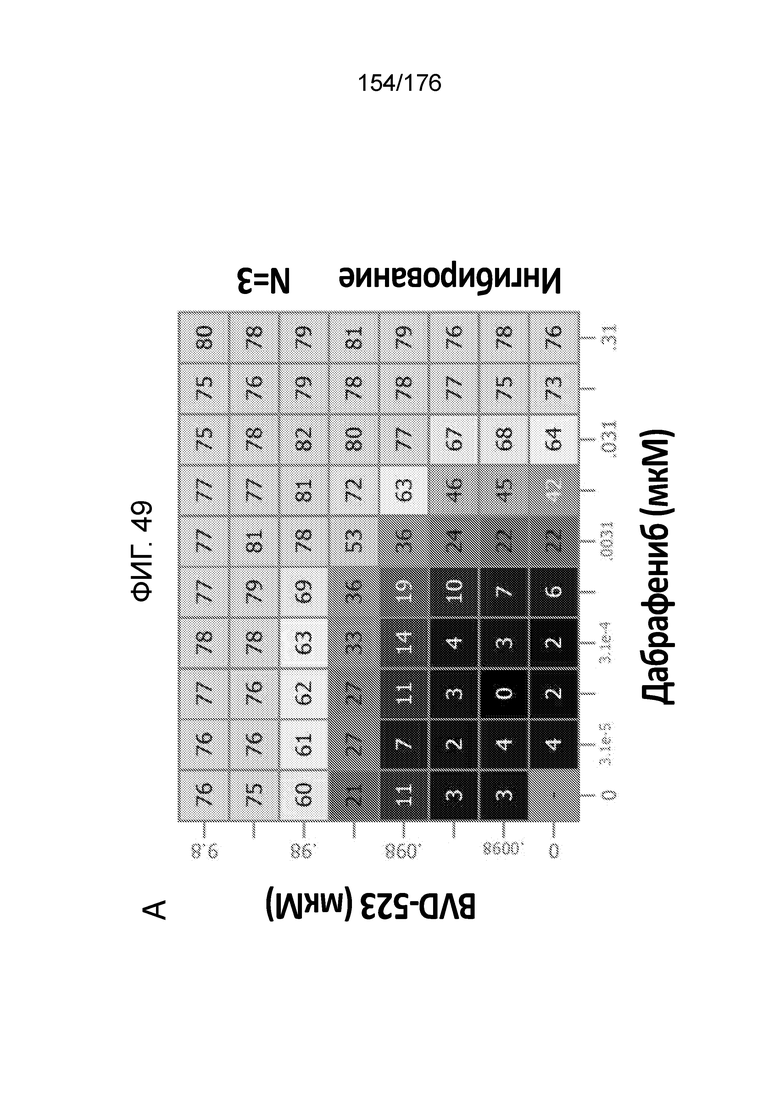

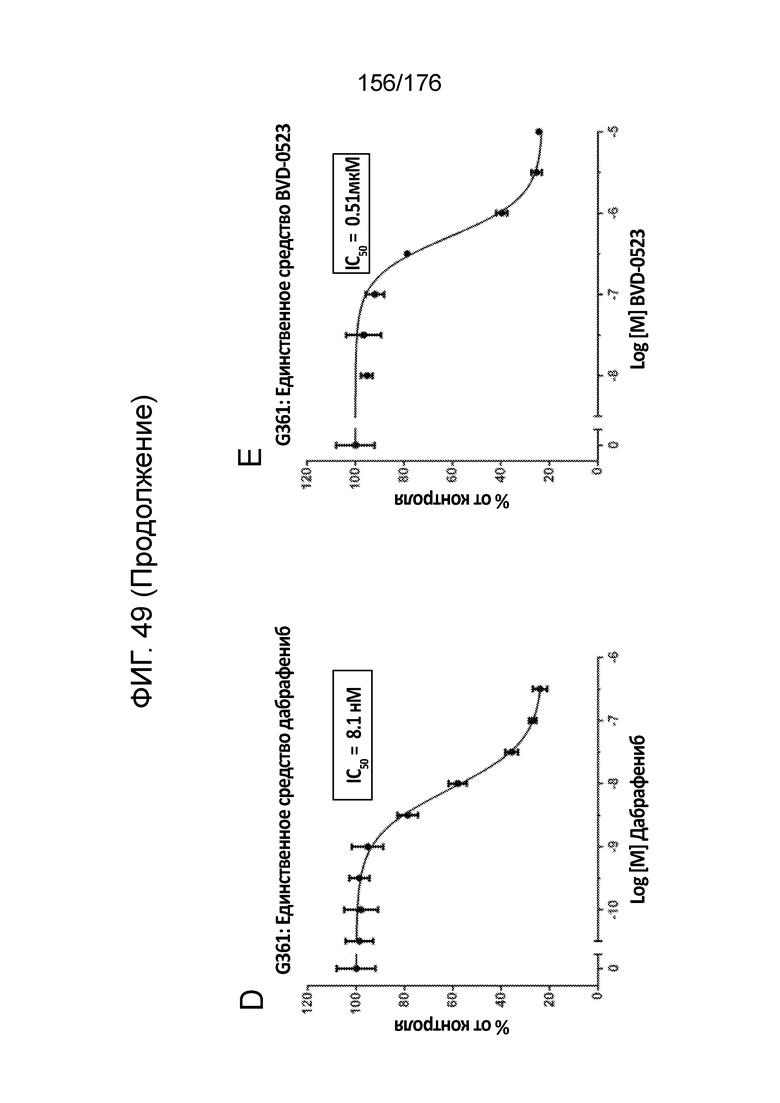
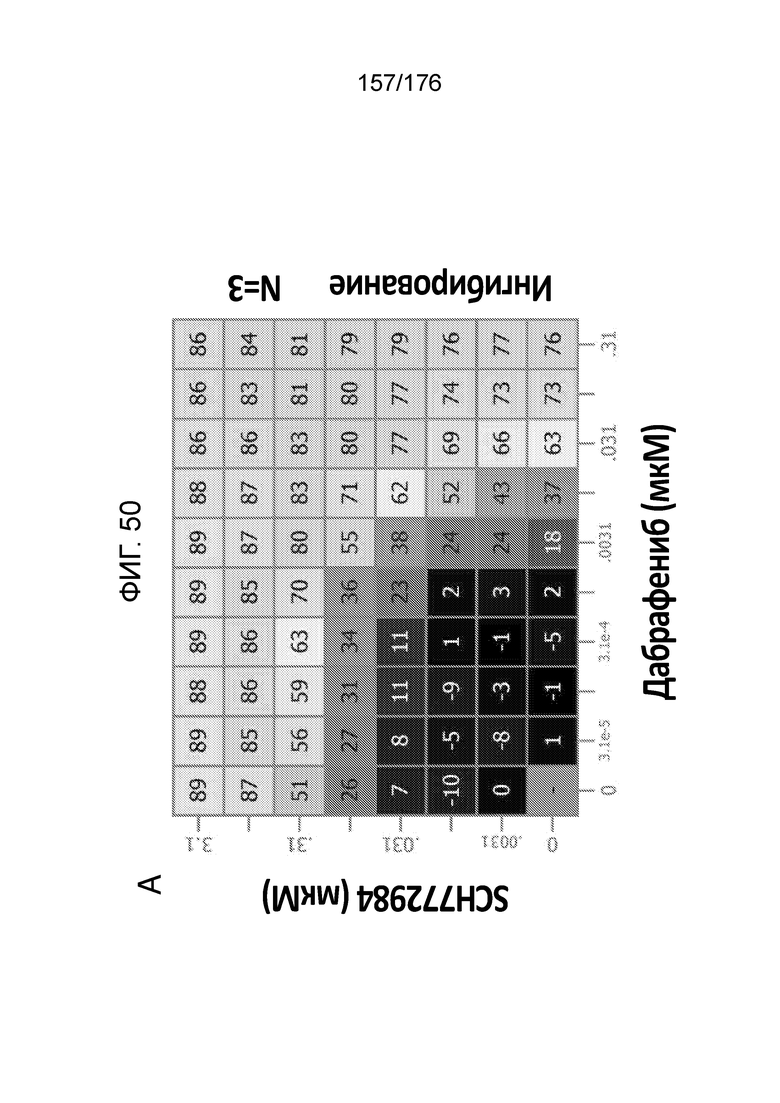

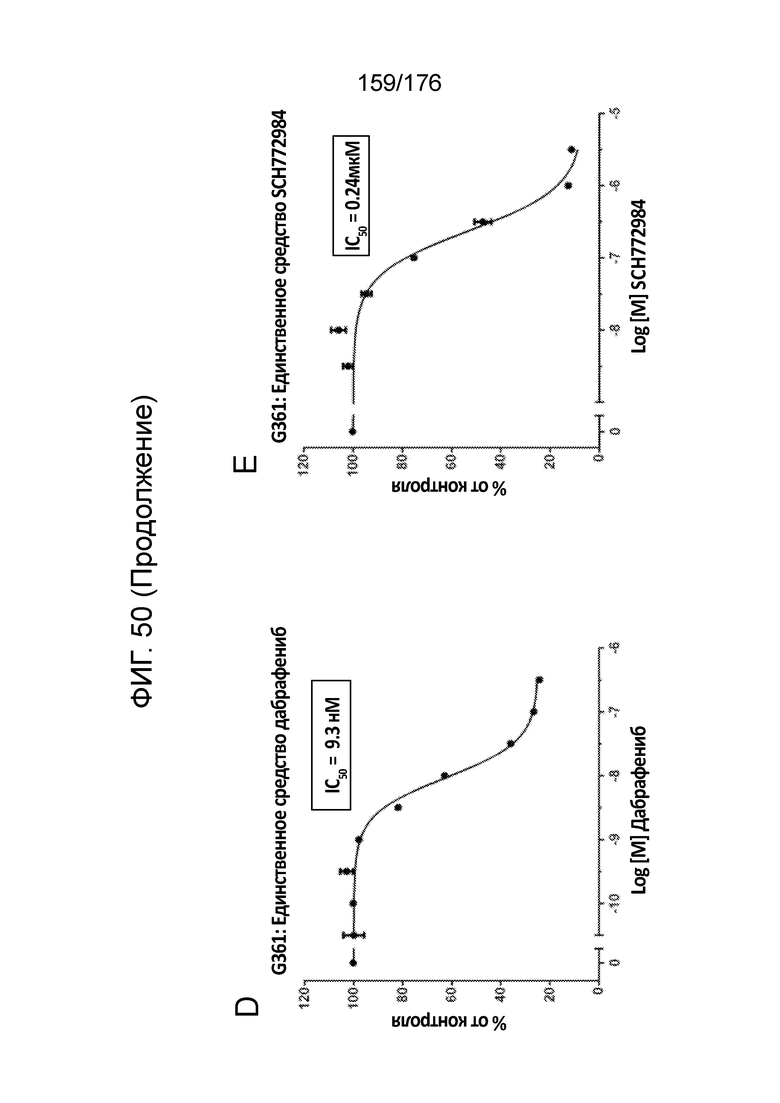

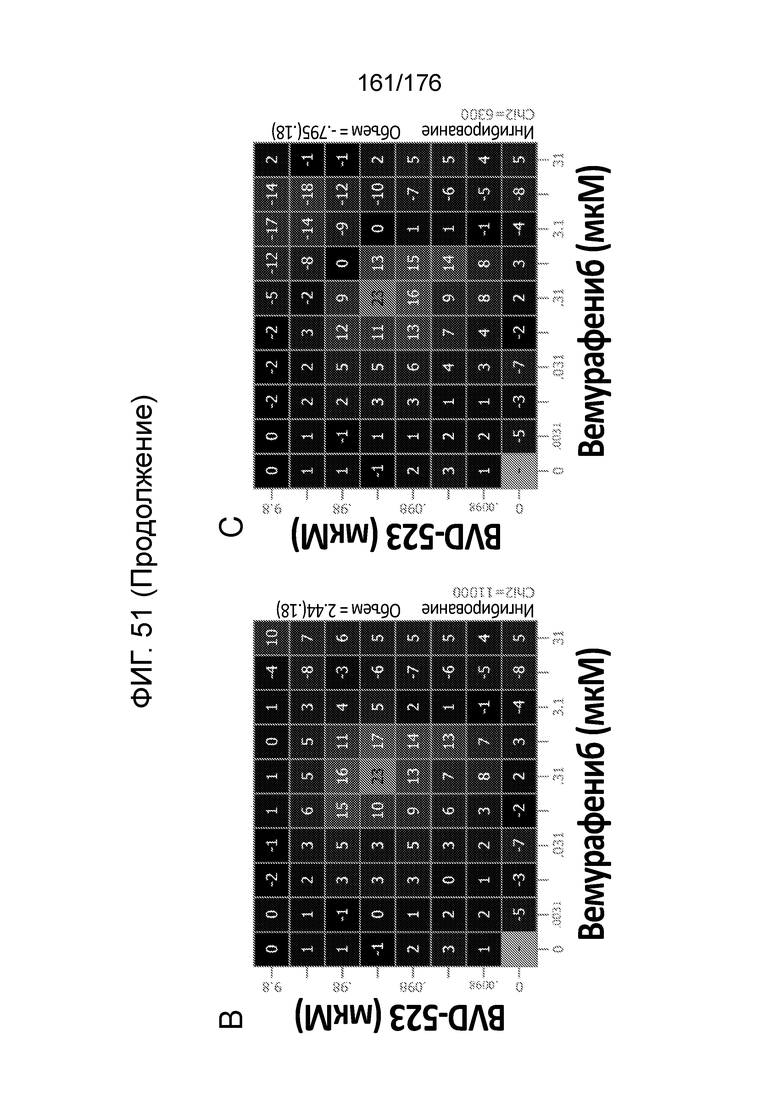
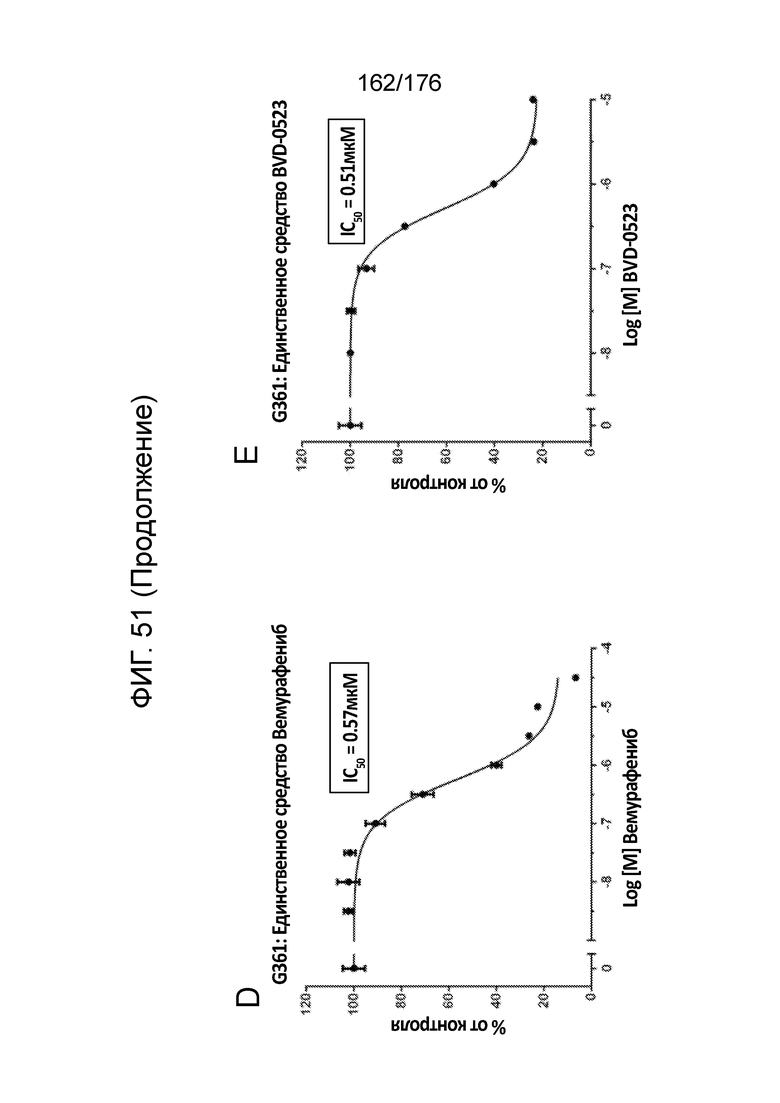
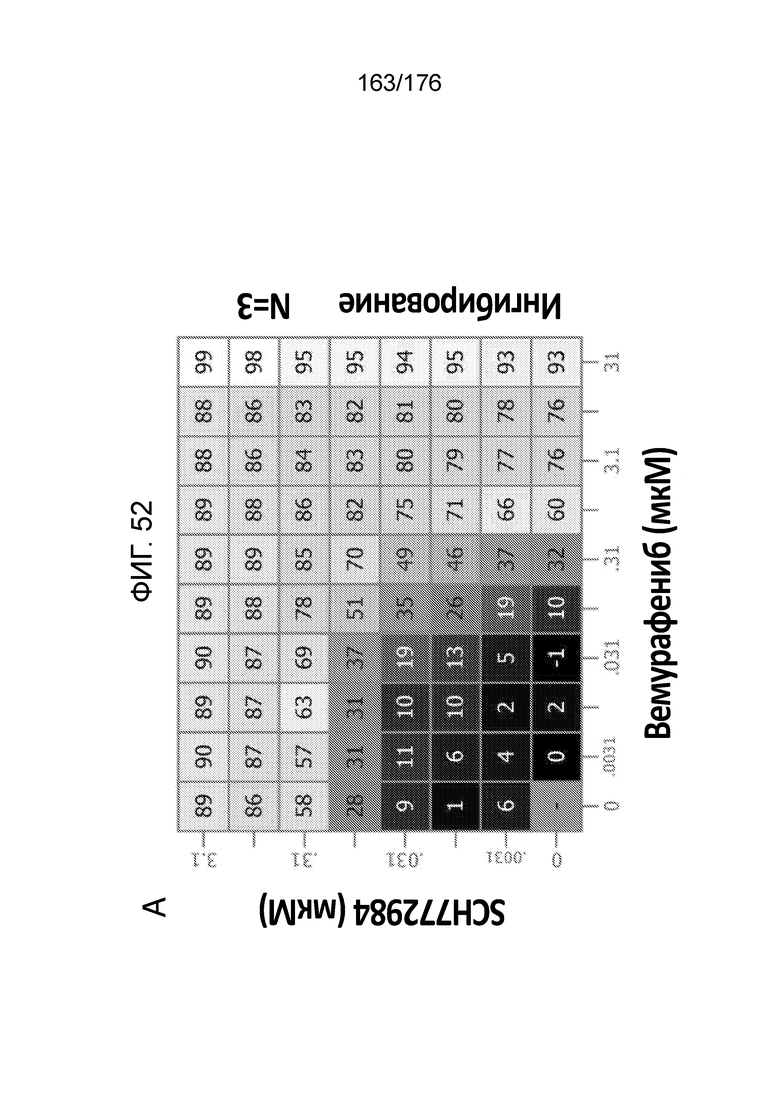

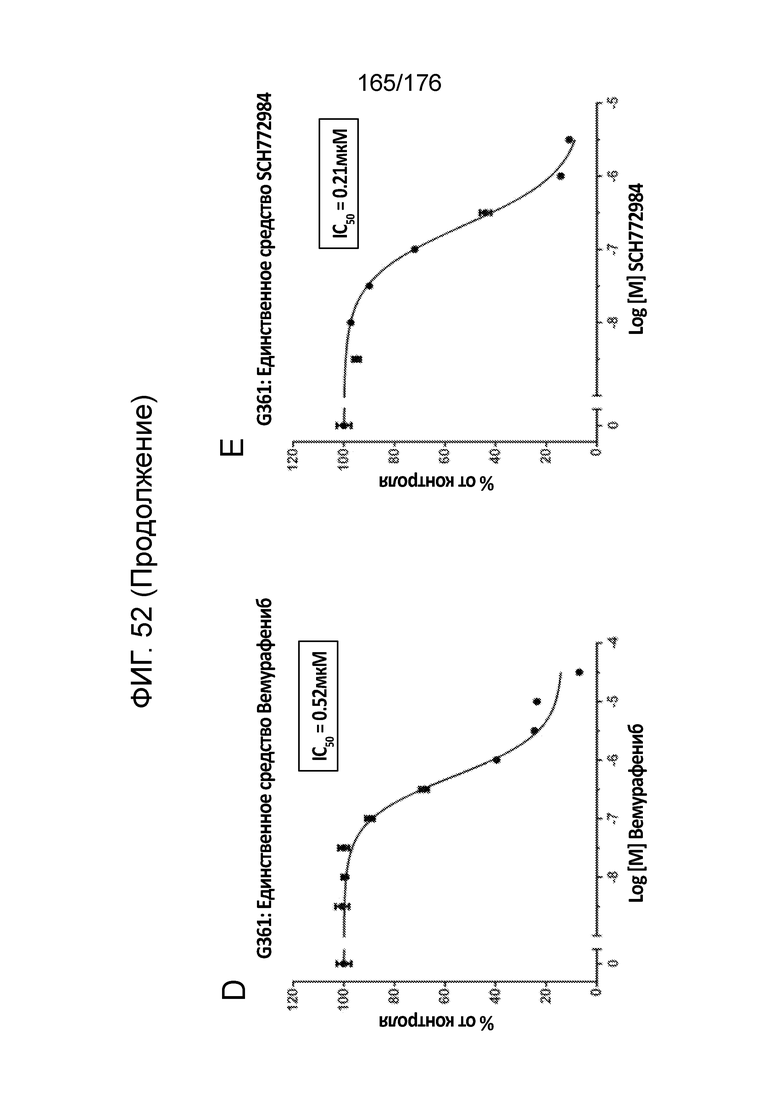
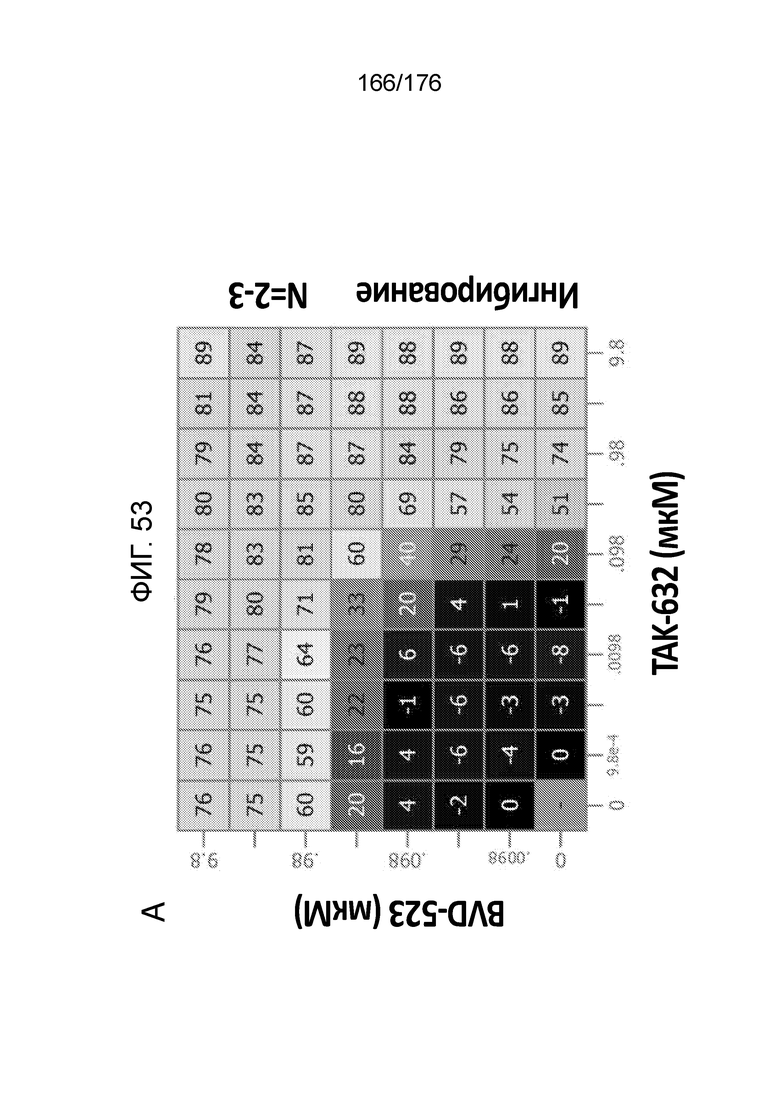
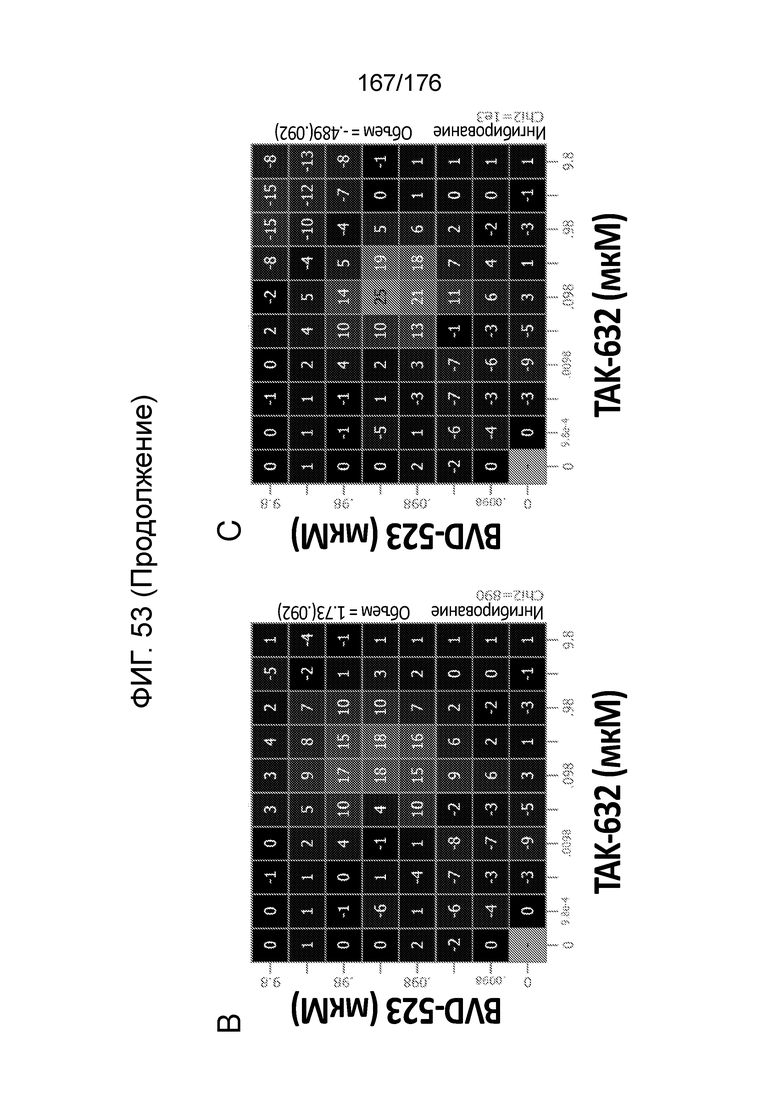
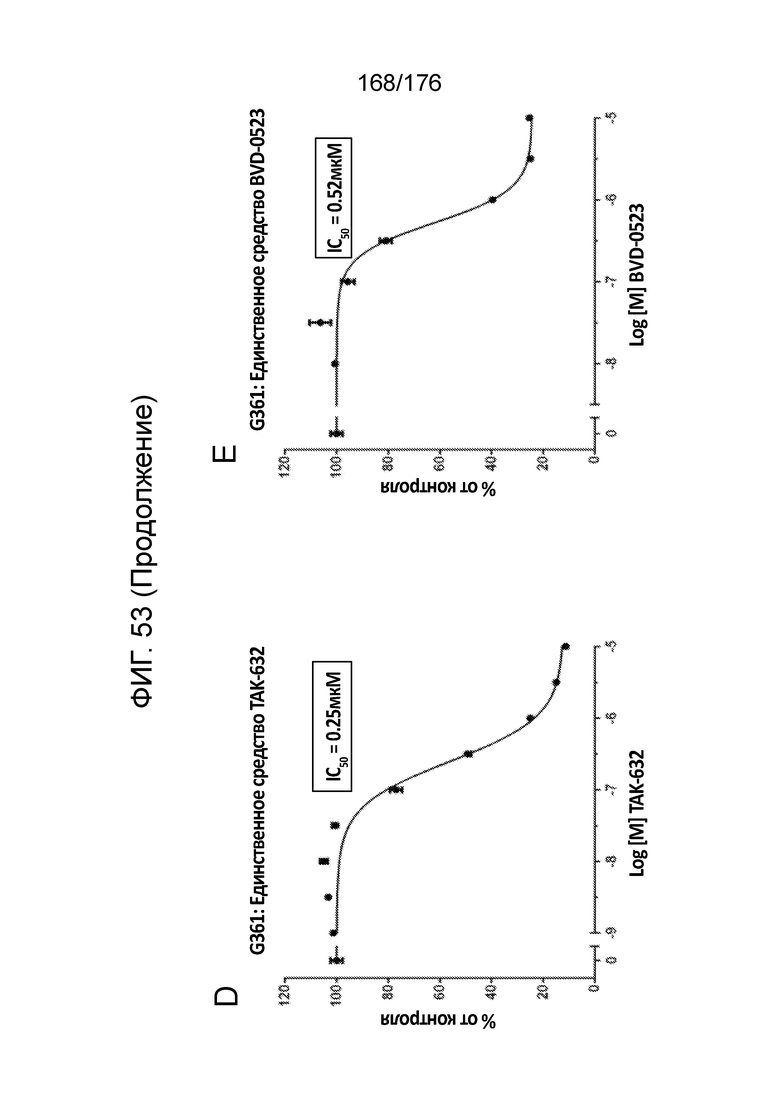
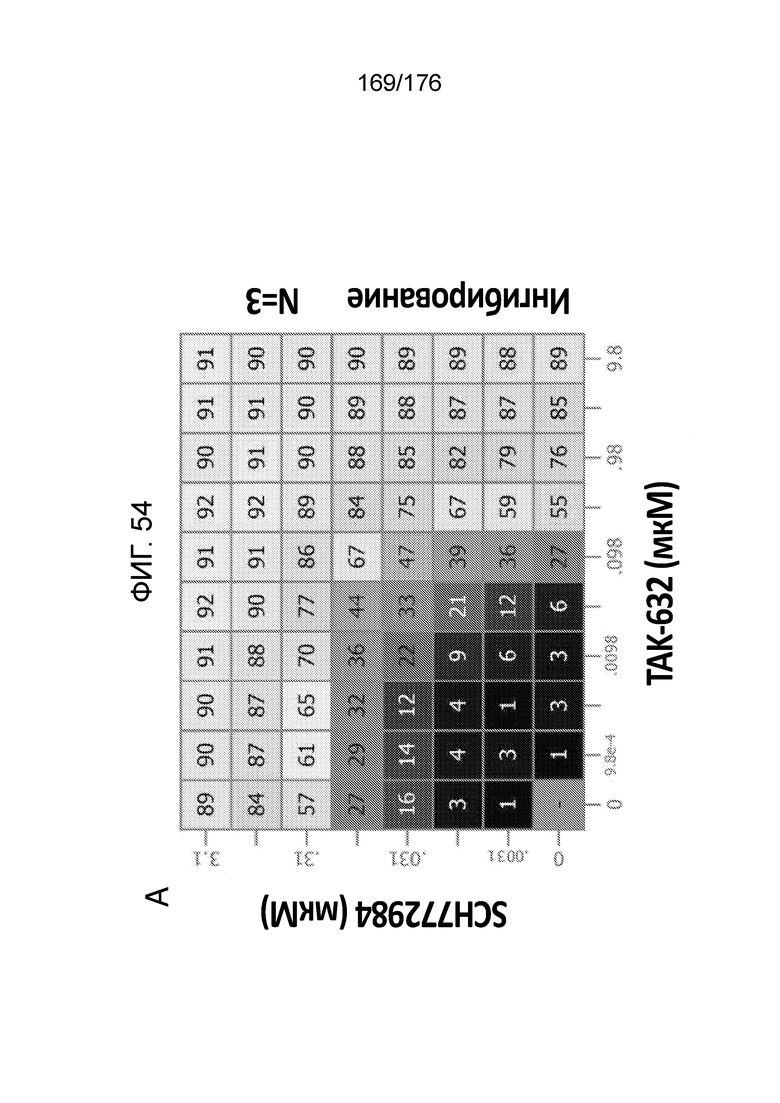
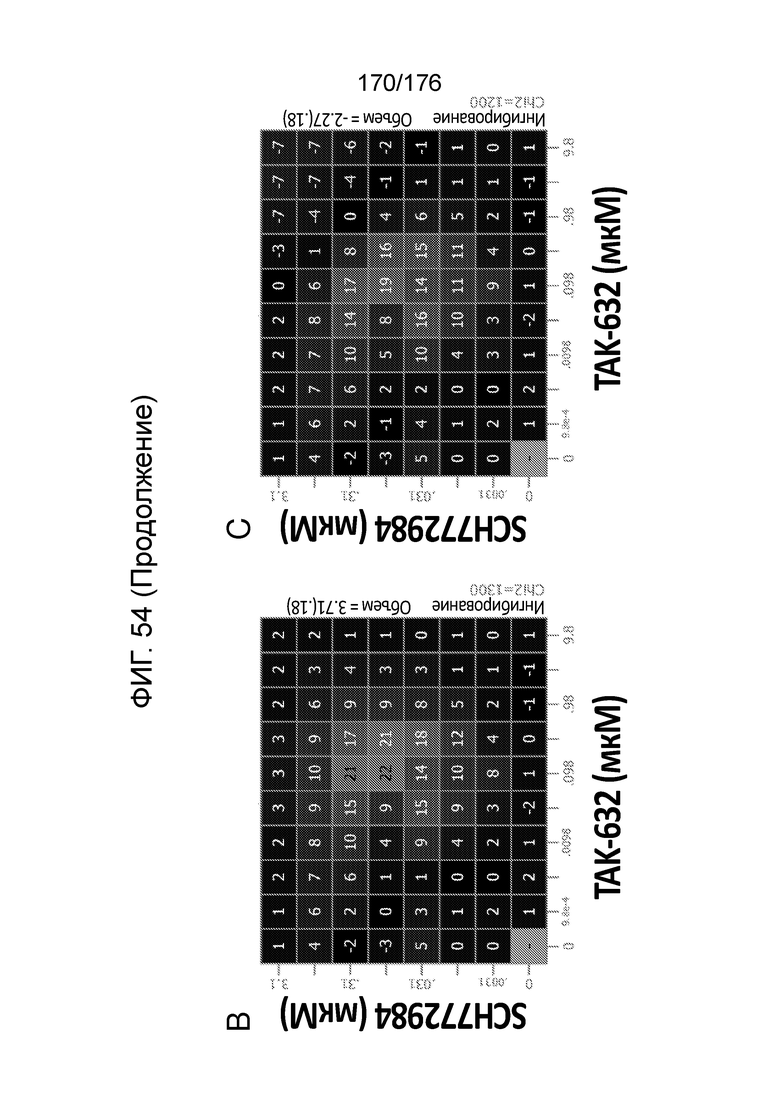
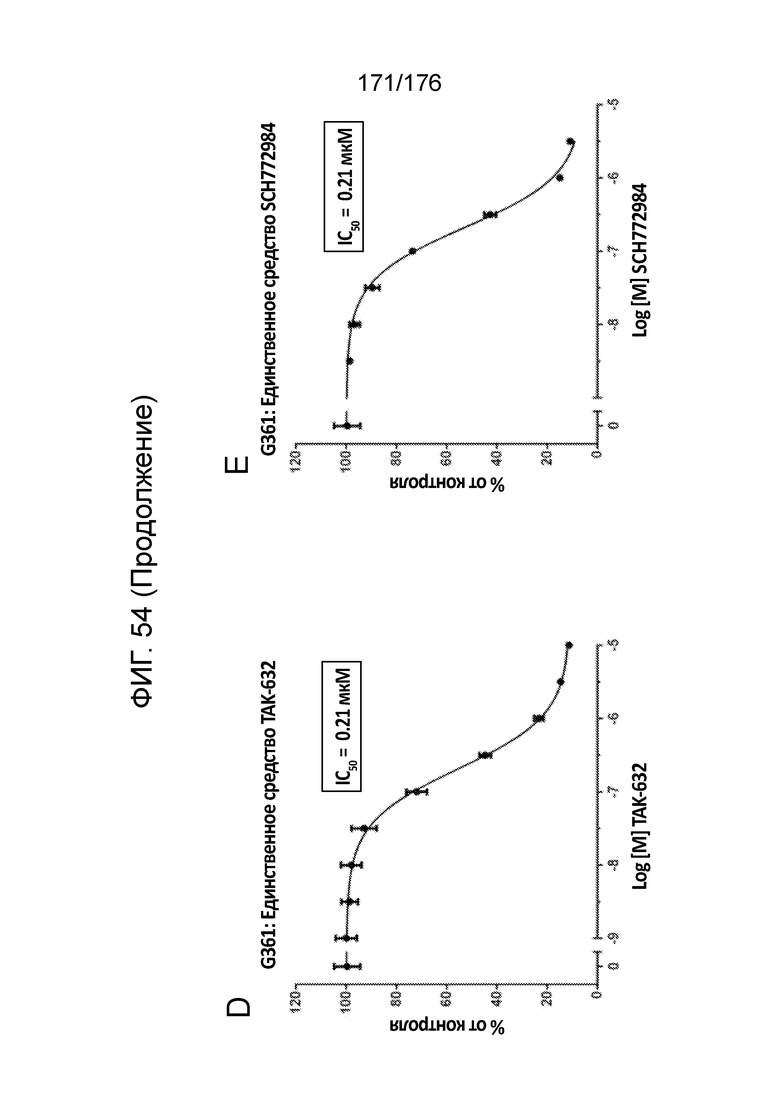
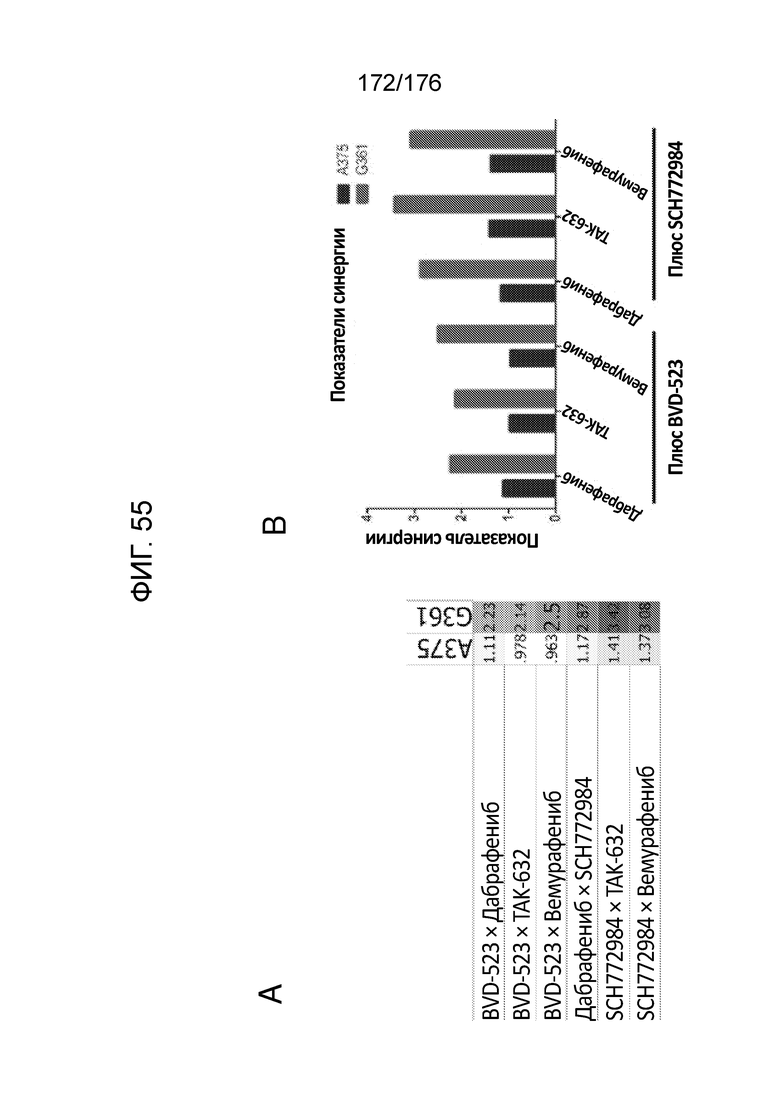
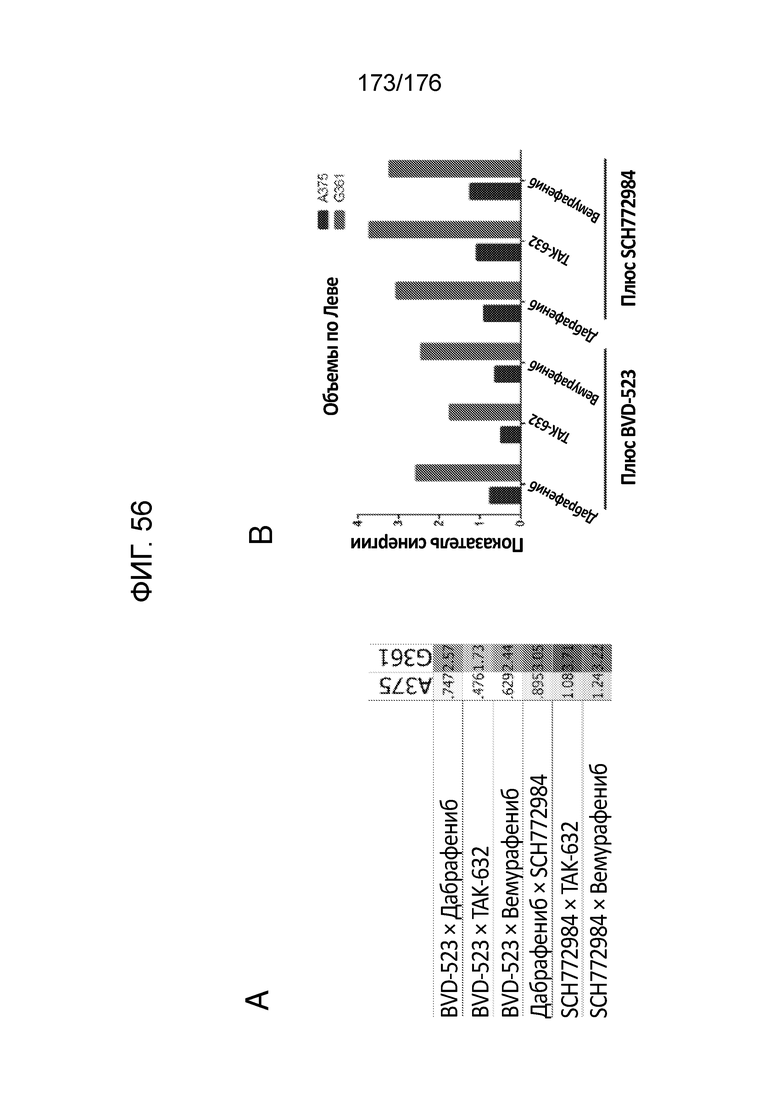
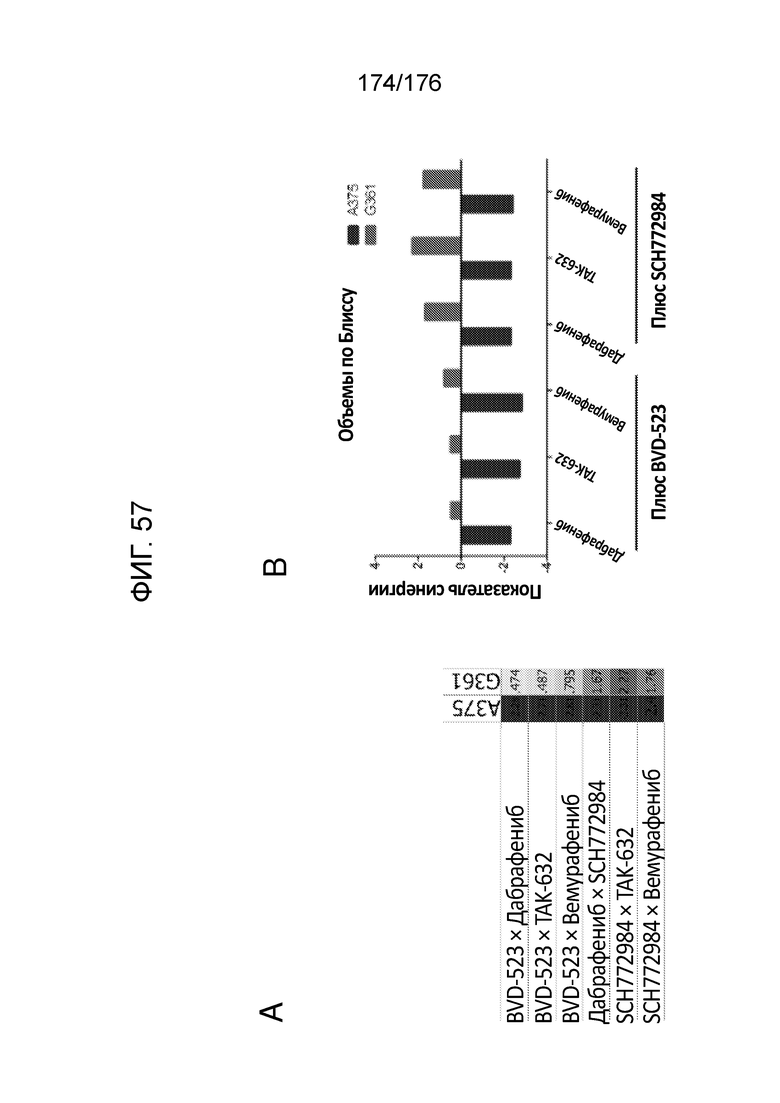
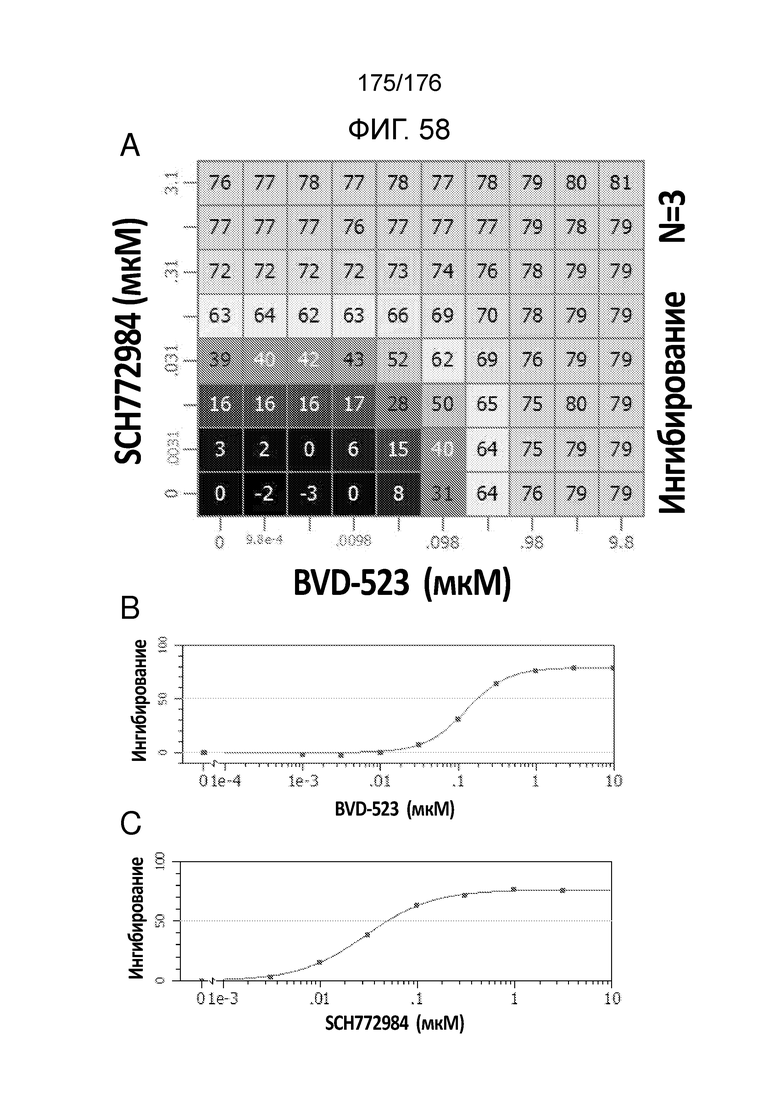
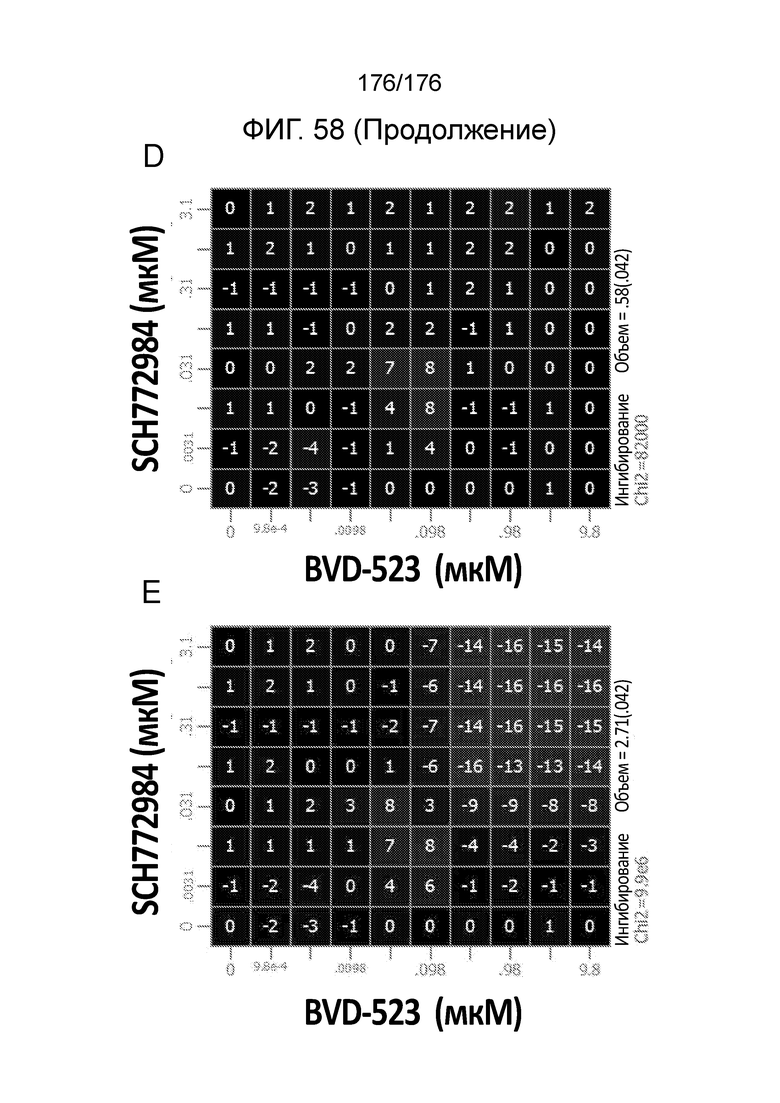
Группа изобретений относится к медицине и может быть использована для лечения злокачественной опухоли у нуждающегося в этом индивидуума. Для этого индивидууму вводят эффективное количество BVD-523 или его фармацевтически приемлемую соль и ингибитор RAF типа 1 или его фармацевтически приемлемую соль. При этом ингибитор RAF типа 1 выбран из группы, состоящей из дабрафениба, TAK 632, вемурафениба, их фармацевтически приемлемых солей. Введение указанных средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против опухолей отдельно. Также предложены способы, фармацевтические композиции и наборы для лечения опухоли. Группа изобретений обеспечивает лечение опухолей у индивидуума за счет синергического действия указанных средств. 8 н. и 47 з.п. ф-лы, 18 табл., 9 пр., 58 ил.
1. Способ лечения злокачественной опухоли у нуждающегося в этом индивидуума, включающий введение индивидууму эффективного количества (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF типа 1 или его фармацевтически приемлемую соль, для лечения злокачественной опухоли,
где ингибитор RAF типа 1 выбран из группы, состоящей из дабрафениба, TAK 632, вемурафениба, их фармацевтически приемлемых солей и их сочетаний, и
где введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно.
2. Способ по п. 1, где индивидуум представляет собой млекопитающее.
3. Способ по п. 2, где млекопитающее выбрано из группы, состоящей из людей, приматов, сельскохозяйственных животных и домашних животных.
4. Способ по п. 2, где млекопитающее представляет собой человека.
5. Способ по п. 1, где ингибитор RAF типа 1 представляет собой дабрафениб или его фармацевтически приемлемую соль.
6. Способ по п. 1, где индивидуум со злокачественной опухолью несет соматическую мутацию BRAF или устойчив к лечению ингибитором сигнального пути MAPK.
7. Способ по п. 1, дополнительно включающий введение по меньшей мере одного дополнительного терапевтического средства, выбранного из группы, состоящей из антитела или его фрагмента, цитотоксического средства, токсина, радионуклида, иммуномодулятора, фотоактивного терапевтического средства, радиосенсибилизирующего средства, гормона, средства против ангиогенеза и их сочетаний.
8. Способ по п. 7, где дополнительное терапевтическое средство представляет собой ингибитор сигнального пути PI3K/Akt.
9. Способ по п. 8, где ингибитор сигнального пути PI3K/Akt выбран из группы, состоящей из A-674563 (CAS # 552325-73-2), AGL 2263, AMG-319, AS-041164 (5-бензо[1,3]диоксол-5-илметилентиазолидин-2,4-диона), AS-604850 (5-(2,2-дифтор-бензо[1,3]диоксол-5-илметилен)тиазолидин-2,4-диона), AS-605240 (5-хиноксилин-6-метилен-1,3-тиазолидин-2,4-диона), AT7867 (CAS # 857531-00-1), ряда бензимидазолов, BML-257 (CAS # 32387-96-5), CAL-120, CAL-129, CAL-130, CAL-253, CAL-263, CAS # 612847-09-3, CAS # 681281-88-9, CAS # 75747-14-7, CAS # 925681-41-0, CAS # 98510-80-6, CCT128930 (CAS # 885499-61-6), CH5132799 (CAS # 1007207-67-1), CHR-4432, FPA 124 (CAS # 902779-59-3), GS-1101 (CAL-101), GSK 690693 (CAS # 937174-76-0), H-89 (CAS # 127243-85-0), Хонокиола, IC87114, IPI-145, KAR-4139, KAR-4141, KIN-1, KT 5720 (CAS # 108068-98-0), Милтефозина, дигидрохлорида MK-2206 (CAS # 1032350-13-2), ML-9 (CAS # 105637-50-1), гидрохлорида налтриндола, OXY-111A, перифосина, PHT-427 (CAS # 1191951-57-1), пиктилисиба, PIK-90 (CAS # 677338-12-4), SC-103980, SF-1126, SH-5, SH-6, тетрагидрокуркумина, TG100-115, трицирибина, X-339, XL-499, их фармацевтически приемлемых солей и их сочетаний.
10. Способ лечения злокачественной опухоли у нуждающегося в этом индивидуума, включающий введение индивидууму эффективного количества (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемой соли и (ii) второго средства против злокачественной опухоли, которое представляет собой дабрафениб или его фармацевтически приемлемую соль, для лечения злокачественной опухоли, где введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно.
11. Способ по п. 10, где индивидуум представляет собой млекопитающее.
12. Способ по п. 11, где млекопитающее выбрано из группы, состоящей из людей, приматов, сельскохозяйственных животных и домашних животных.
13. Способ по п. 11, где млекопитающее представляет собой человека.
14. Способ по п. 10, где BVD-523 или его фармацевтически приемлемую соль вводят в форме фармацевтической композиции, дополнительно содержащей фармацевтически приемлемый носитель или разбавитель.
15. Способ по п. 10, где дабрафениб или его фармацевтически приемлемую соль вводят в форме фармацевтической композиции, дополнительно содержащей фармацевтически приемлемый носитель или разбавитель.
16. Способ по п. 10, где индивидуум со злокачественной опухолью несет мутацию BRAF или устойчив к лечению ингибитором сигнального пути MAPK.
17. Способ по п. 10, дополнительно включающий введение по меньшей мере одного дополнительного терапевтического средства, выбранного из группы, состоящей из антитела или его фрагмента, цитотоксического средства, токсина, радионуклида, иммуномодулятора, фотоактивного терапевтического средства, радиосенсибилизирующего средства, гормона, средства против ангиогенеза и их сочетаний.
18. Способ по п. 17, где дополнительное терапевтическое средство представляет собой ингибитор сигнального пути PI3K/Akt.
19. Способ по п. 18, где ингибитор сигнального пути PI3K/Akt выбран из группы, состоящей из A-674563 (CAS # 552325-73-2), AGL 2263, AMG-319, AS-041164 (5-бензо[1,3]диоксол-5-илметилентиазолидин-2,4-диона), AS-604850 (5-(2,2-дифтор-бензо[1,3]диоксол-5-илметилен)тиазолидин-2,4-диона), AS-605240 (5-хиноксилин-6-метилен-1,3-тиазолидин-2,4-диона), AT7867 (CAS # 857531-00-1), ряда бензимидазолов, BML-257 (CAS # 32387-96-5), CAL-120, CAL-129, CAL-130, CAL-253, CAL-263, CAS # 612847-09-3, CAS # 681281-88-9, CAS # 75747-14-7, CAS # 925681-41-0, CAS # 98510-80-6, CCT128930 (CAS # 885499-61-6), CH5132799 (CAS # 1007207-67-1), CHR-4432, FPA 124 (CAS # 902779-59-3), GS-1101 (CAL-101), GSK 690693 (CAS # 937174-76-0), H-89 (CAS # 127243-85-0), Хонокиола, IC87114, IPI-145, KAR-4139, KAR-4141, KIN-1, KT 5720 (CAS # 108068-98-0), Милтефозина, дигидрохлорида MK-2206 (CAS # 1032350-13-2), ML-9 (CAS # 105637-50-1), гидрохлорида налтриндола, OXY-111A, перифосина, PHT-427 (CAS # 1191951-57-1), пиктилисиба, PIK-90 (CAS # 677338-12-4), SC-103980, SF-1126, SH-5, SH-6, тетрагидрокуркумина, TG100-115, трицирибина, X-339, XL-499, их фармацевтически приемлемых солей и их сочетаний.
20. Способ уничтожения злокачественной клетки, включающий приведение злокачественной клетки в контакт с эффективным количеством (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF типа 1 или его фармацевтически приемлемую соль,
где ингибитор RAF типа 1 выбран из группы, состоящей из дабрафениба, TAK 632, вемурафениба, их фармацевтически приемлемых солей и их сочетаний, и
где введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно.
21. Способ по п. 20, где злокачественная клетка представляет собой злокачественную клетку млекопитающего.
22. Способ по п. 21, где злокачественную клетку млекопитающего получают у млекопитающего, выбранного из группы, состоящей из людей, приматов, сельскохозяйственных животных и домашних животных.
23. Способ по п. 21, где злокачественная клетка млекопитающего представляет собой злокачественную клетку человека.
24. Способ по п. 20, где ингибитор RAF типа 1 представляет собой дабрафениб или его фармацевтически приемлемую соль.
25. Способ по п. 20, где индивидуум со злокачественной опухолью несет соматическую мутацию BRAF или устойчив к лечению ингибитором сигнального пути MAPK.
26. Способ по п. 20, дополнительно включающий введение по меньшей мере одного дополнительного терапевтического средства, выбранного из группы, состоящей из антитела или его фрагмента, цитотоксического средства, токсина, радионуклида, иммуномодулятора, фотоактивного терапевтического средства, радиосенсибилизирующего средства, гормона, средства против ангиогенеза и их сочетаний.
27. Способ по п. 26, где дополнительное терапевтическое средство представляет собой ингибитор сигнального пути PI3K/Akt.
28. Способ по п. 27, где ингибитор сигнального пути PI3K/Akt выбран из группы, состоящей из A-674563 (CAS # 552325-73-2), AGL 2263, AMG-319, AS-041164 (5-бензо[1,3]диоксол-5-илметилентиазолидин-2,4-диона), AS-604850 (5-(2,2-дифтор-бензо[1,3]диоксол-5-илметилен)тиазолидин-2,4-диона), AS-605240 (5-хиноксилин-6-метилен-1,3-тиазолидин-2,4-диона), AT7867 (CAS # 857531-00-1), ряда бензимидазолов, BML-257 (CAS # 32387-96-5), CAL-120, CAL-129, CAL-130, CAL-253, CAL-263, CAS # 612847-09-3, CAS # 681281-88-9, CAS # 75747-14-7, CAS # 925681-41-0, CAS # 98510-80-6, CCT128930 (CAS # 885499-61-6), CH5132799 (CAS # 1007207-67-1), CHR-4432, FPA 124 (CAS # 902779-59-3), GS-1101 (CAL-101), GSK 690693 (CAS # 937174-76-0), H-89 (CAS # 127243-85-0), Хонокиола, IC87114, IPI-145, KAR-4139, KAR-4141, KIN-1, KT 5720 (CAS # 108068-98-0), Милтефозина, дигидрохлорида MK-2206 (CAS # 1032350-13-2), ML-9 (CAS # 105637-50-1), гидрохлорида налтриндола, OXY-111A, перифосина, PHT-427 (CAS # 1191951-57-1), пиктилисиба, PIK-90 (CAS # 677338-12-4), SC-103980, SF-1126, SH-5, SH-6, тетрагидрокуркумина, TG100-115, трицирибина, X-339, XL-499, их фармацевтически приемлемых солей и их сочетаний.
29. Набор для лечения злокачественной опухоли у нуждающегося в этом индивидуума, содержащий эффективное количество (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF типа 1 или его фармацевтически приемлемую соль, упакованные вместе с инструкциями по их применению,
где ингибитор RAF типа 1 выбран из группы, состоящей из дабрафениба, TAK 632, вемурафениба, их фармацевтически приемлемых солей и их сочетаний, и
где введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно.
30. Набор по п. 29, где индивидуум представляет собой млекопитающее.
31. Набор по п. 30, где млекопитающее выбрано из группы, состоящей из людей, приматов, сельскохозяйственных животных и домашних животных.
32. Набор по п. 30, где млекопитающее представляет собой человека.
33. Набор по п. 29, где ингибитор RAF типа 1 представляет собой дабрафениб или его фармацевтически приемлемую соль.
34. Набор по п. 29, где индивидуум со злокачественной опухолью несет соматическую мутацию BRAF или устойчив к лечению ингибитором сигнального пути MAPK.
35. Набор по п. 29, дополнительно содержащий по меньшей мере одно дополнительное терапевтическое средство, выбранное из группы, состоящей из антитела или его фрагмента, цитотоксического средства, токсина, радионуклида, иммуномодулятора, фотоактивного терапевтического средства, радиосенсибилизирующего средства, гормона, средства против ангиогенеза и их сочетаний.
36. Набор по п. 35, где дополнительное терапевтическое средство представляет собой ингибитор сигнального пути PI3K/Akt.
37. Набор по п. 36, где ингибитор сигнального пути PI3K/Akt выбран из группы, состоящей из A-674563 (CAS # 552325-73-2), AGL 2263, AMG-319, AS-041164 (5-бензо[1,3]диоксол-5-илметилентиазолидин-2,4-диона), AS-604850 (5-(2,2-дифтор-бензо[1,3]диоксол-5-илметилен)тиазолидин-2,4-диона), AS-605240 (5-хиноксилин-6-метилен-1,3-тиазолидин-2,4-диона), AT7867 (CAS # 857531-00-1), ряда бензимидазолов, BML-257 (CAS # 32387-96-5), CAL-120, CAL-129, CAL-130, CAL-253, CAL-263, CAS # 612847-09-3, CAS # 681281-88-9, CAS # 75747-14-7, CAS # 925681-41-0, CAS # 98510-80-6, CCT128930 (CAS # 885499-61-6), CH5132799 (CAS # 1007207-67-1), CHR-4432, FPA 124 (CAS # 902779-59-3), GS-1101 (CAL-101), GSK 690693 (CAS # 937174-76-0), H-89 (CAS # 127243-85-0), Хонокиола, IC87114, IPI-145, KAR-4139, KAR-4141, KIN-1, KT 5720 (CAS # 108068-98-0), Милтефозина, дигидрохлорида MK-2206 (CAS # 1032350-13-2), ML-9 (CAS # 105637-50-1), гидрохлорида налтриндола, OXY-111A, перифосина, PHT-427 (CAS # 1191951-57-1), пиктилисиба, PIK-90 (CAS # 677338-12-4), SC-103980, SF-1126, SH-5, SH-6, тетрагидрокуркумина, TG100-115, трицирибина, X-339, XL-499, их фармацевтически приемлемых солей и их сочетаний.
38. Фармацевтическая композиция для лечения злокачественной опухоли у нуждающегося в этом индивидуума, где фармацевтическая композиция содержит фармацевтически приемлемый разбавитель или носитель и эффективное количество (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой ингибитор RAF типа 1 или его фармацевтически приемлемую соль, где ингибитор RAF типа 1 выбран из группы, состоящей из дабрафениба, TAK 632, вемурафениба, их фармацевтически приемлемых солей и их сочетаний, и где введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно.
39. Фармацевтическая композиция по п. 38, где индивидуум представляет собой млекопитающее.
40. Фармацевтическая композиция по п. 39, где млекопитающее выбрано из группы, состоящей из людей, приматов, сельскохозяйственных животных и домашних животных.
41. Фармацевтическая композиция по п. 39, где млекопитающее представляет собой человека.
42. Фармацевтическая композиция по п. 38, где ингибитор RAF типа 1 представляет собой дабрафениб или его фармацевтически приемлемую соль.
43. Фармацевтическая композиция по п. 38, где индивидуум со злокачественной опухолью несет соматическую мутацию BRAF или устойчив к лечению ингибитором сигнального пути MAPK.
44. Фармацевтическая композиция по п. 38, дополнительно содержащая по меньшей мере одно дополнительное терапевтическое средство, выбранное из группы, состоящей из антитела или его фрагмента, цитотоксического средства, токсина, радионуклида, иммуномодулятора, фотоактивного терапевтического средства, радиосенсибилизирующего средства, гормона, средства против ангиогенеза и их сочетаний.
45. Фармацевтическая композиция по п. 44, где дополнительное терапевтическое средство представляет собой ингибитор сигнального пути PI3K/Akt.
46. Фармацевтическая композиция по п. 45, где ингибитор сигнального пути PI3K/Akt выбран из группы, состоящей из A-674563 (CAS # 552325-73-2), AGL 2263, AMG-319, AS-041164 (5-бензо[1,3]диоксол-5-илметилентиазолидин-2,4-диона), AS-604850 (5-(2,2-дифтор-бензо[1,3]диоксол-5-илметилен)тиазолидин-2,4-диона), AS-605240 (5-хиноксилин-6-метилен-1,3-тиазолидин-2,4-диона), AT7867 (CAS # 857531-00-1), ряда бензимидазолов, BML-257 (CAS # 32387-96-5), CAL-120, CAL-129, CAL-130, CAL-253, CAL-263, CAS # 612847-09-3, CAS # 681281-88-9, CAS # 75747-14-7, CAS # 925681-41-0, CAS # 98510-80-6, CCT128930 (CAS # 885499-61-6), CH5132799 (CAS # 1007207-67-1), CHR-4432, FPA 124 (CAS # 902779-59-3), GS-1101 (CAL-101), GSK 690693 (CAS # 937174-76-0), H-89 (CAS # 127243-85-0), Хонокиола, IC87114, IPI-145, KAR-4139, KAR-4141, KIN-1, KT 5720 (CAS # 108068-98-0), Милтефозина, дигидрохлорида MK-2206 (CAS # 1032350-13-2), ML-9 (CAS # 105637-50-1), гидрохлорида налтриндола, OXY-111A, перифосина, PHT-427 (CAS # 1191951-57-1), пиктилисиба, PIK-90 (CAS # 677338-12-4), SC-103980, SF-1126, SH-5, SH-6, тетрагидрокуркумина, TG100-115, трицирибина, X-339, XL-499, их фармацевтически приемлемых солей и их сочетаний.
47. Фармацевтическая композиция по п. 38, которая находится в стандартной дозированной форме, содержащей оба средства против злокачественных опухолей.
48. Фармацевтическая композиция по п. 38, в которой первое средство против злокачественной опухоли находится в первой стандартной дозированной форме, а второе средство против злокачественной опухоли находится во второй стандартной дозированной форме, отдельно от первой.
49. Фармацевтическая композиция по п. 38, где первое и второе средства против злокачественных опухолей вводят индивидууму совместно.
50. Фармацевтическая композиция по п. 38, где первое и второе средства против злокачественных опухолей вводят индивидууму последовательно.
51. Фармацевтическая композиция по п. 50, где первое средство против злокачественной опухоли вводят индивидууму перед вторым средством против злокачественной опухоли.
52. Фармацевтическая композиция по п. 50, где второе средство против злокачественной опухоли вводят индивидууму перед первым средством против злокачественной опухоли.
53. Фармацевтическая композиция для лечения злокачественной опухоли у нуждающегося в этом индивидуума, где фармацевтическая композиция содержит фармацевтически приемлемый разбавитель или носитель и эффективное количество (i) первого средства против злокачественной опухоли, которое представляет собой BVD-523 или его фармацевтически приемлемую соль, и (ii) второго средства против злокачественной опухоли, которое представляет собой вемурафениб или его фармацевтически приемлемую соль, где введение первого и второго средств против злокачественных опухолей обеспечивает синергическое действие по сравнению с введением любого из этих средств против злокачественных опухолей отдельно.
54. Способ лечения злокачественной опухоли у нуждающегося в этом индивидуума, включающий введение индивидууму эффективного количества фармацевтической композиции по п. 53 для лечения злокачественной опухоли.
55. Набор для лечения злокачественной опухоли у нуждающегося в этом индивидуума, где набор содержит эффективное количество фармацевтической композиции по п. 53.
| US 7354939 B2, 08.04.2008 | |||
| US 20130296318 A1, 07.11.2013 | |||
| JIN F | |||
| et al., Exploration of N-(2-aminoethyl)piperidine-4-carboxamide as a potential scaffold for development of VEGFR-2, ERK-2 and Abl-1 multikinase inhibitor, Bioorg Med Chem | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| MORRIS E.J | |||
| et al., Discovery of a novel ERK inhibitor with activity in models | |||
Авторы
Даты
2020-06-03—Публикация
2014-12-19—Подача