ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящей заявке испрашивается приоритет по предварительной патентной заявке США № 62/506995, поданной 16 мая 2017 года, которая включена в настоящее описание в качестве ссылки в полном объеме.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[0002] Настоящее изобретение относится к способам, наборам и фармацевтическим композициям для лечения или смягчения эффектов злокачественной опухоли с атипичными генетическими мутациями с использованием одного или нескольких средств против злокачественной опухоли.
ВКЛЮЧЕНИЕ СПИСКА ПОСЛЕДОВАТЕЛЬНОСТЕЙ В КАЧЕСТВЕ ССЫЛКИ
[0003] Настоящая заявка содержит ссылки на аминокислотные последовательности и/или последовательности нуклеиновых кислот, которые были предоставлены с настоящим описанием в качестве текстового файла списка последовательностей "2391211.txt", размер файла 246 кБ, созданного 15 мая 2018 года. Вышеупомянутый список последовательностей включен в настоящее описание в качестве ссылки в полном объеме согласно 37 C.F.R. § 1.52(e)(5).
УРОВЕНЬ ТЕХНИКИ, К КОТОРОМУ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0004] Передача сигнала митоген-активируемой протеинкиназы (MAPK) или RAS/RAF/MEK/ERK ответственна за несколько клеточных каскадов передачи сигнала, вовлеченных в контроль пролиферации, дифференцировки и апоптоза. Обнаружено, что каскад клеточной передачи сигнала MAPK нарушается в злокачественных опухолях человека, часто вследствие активирующих мутаций генов KRAS, NRAS или BRAF. Были разработаны селективные ингибиторы BRAF, такие как вемурафениб и дабрафениб, для нацеливания на опухоли с мутациями BRAF. Например, вемурафениб одобрен для нерезектабельных или метастазирующих меланом с мутацией BRAF V600E, и детекция мутациии BRAF V600E стала стандартной манипуляцией для прогнозирования ответа на лечение вемурафенибом, дабрафенибом и траметинибом.
[0005] В то время как мутация V600E является наиболее распространенной мутацией BRAF, которая наблюдается во многих типах опухолей, в базе данных Catolog of Somatic Mutations in Cancer (COSMIC) было описано более 100 других мутаций в экзонах 11 и 15 гена BRAF. Клиническое значение мутаций BRAF не в кодоне V600 по большей части неизвестно.
[0006] Ввиду вышеуказанного, существует потребность в новых лекарственных средствах, которые нацелены на каскад MAPK в типах клеток, содержащих мутации BRAF, отличные от V600E. Настоящая заявка направлена на удовлетворение этих и других потребностей.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0007] В соответствии с одним аспектом настоящее изобретение относится к способу лечения или смягчения эффектов злокачественной опухоли у индивидуума, имеющей мутацию BRAF не V600E/K, причем способ включает введение индивидууму эффективного количества ингибитора ERK или его фармацевтически приемлемой соли.
[0008] В соответствии с некоторыми вариантами осуществления ингибитор ERK выбран из группы, состоящей из BVD-523, SCH-722984 (Merck & Co.), SCH-772984 (Merck & Co.), SCH-900353 (MK-8353) (Merck & Co.), LY3214996 (Lilly), AEZS-140 (Aeterna Zentaris), AEZS-131 (Aeterna Zentaris), AEZS-136 (Aeterna Zentaris), LTT-462 (Novartis), RG-7842 (Genentech), CC-90003 (Celgene), KIN-4050 (Kinentia) и их комбинаций.
[0009] Согласно некоторым вариантам осуществления ингибитор ERK представляет собой BVD-523.
[0010] Согласно некоторым вариантам осуществления мутация BRAF не V600E/K представляет собой активирующую киназу мутацию, нарушающую функцию киназы мутацию или мутацию с неизвестным действием на киназу, и их комбинации.
[0011] Согласно некоторым вариантам осуществления активирующая киназу мутация выбрана из группы, состоящей из R462I, I463S, G464E, G464R, G464V, G466A, G469A, N581S, E586K, F595L, L597Q, L597R, L597S, L597V, A598V, T599E, V600R, K601E, S602D, A728V и их комбинаций.
[0012] Согласно некоторым вариантам осуществления нарушающая функцию киназы мутация выбрана из группы, состоящей из G466E, G466R, G466V, Y472C, K483M, D594A, D594E, D594G, D594H, D594N, D594V, G596R, T599A, S602A и их комбинаций.
[0013] Согласно некоторым вариантам осуществления мутация с неизвестным действием на киназу выбрана из группы, состоящей из T440I, S467L, G469E, G469R, G469S, G469V, L584F, L588F, V600_K601delinsE, S605I, Q609L, E611Q и их комбинаций.
[0014] Согласно некоторым вариантам осуществления мутация BRAF не V600E/K выбрана из группы, состоящей из D594, G469, K601E, L597, дупликации T599, L485W, F247L, G466V, слияния BRAF, перестроения BRAF-AGAP3, варианта сплайсинга экзона 15 BRAF, и их комбинаций.
[0015] Согласно некоторым вариантам осуществления индивидуумом является млекопитающее.
[0016] Согласно некоторым вариантам осуществления млекопитающее выбрано из группы, состоящей из человека, приматов, сельскохозяйственных животных и домашних животных.
[0017] Согласно некоторым вариантам осуществления млекопитающее представляет собой человека.
[0018] Согласно некоторым вариантам осуществления злокачественная опухоль представляет собой солидную злокачественную или гематологическую злокачественную опухоль.
[0019] Согласно некоторым вариантам осуществления злокачественная опухоль выбрана из группы, состоящей из глиобластомы, меланомы, холангиокарциномы, мелкоклеточного рака легкого, рака ободочной и прямой кишки, рака предстательной железы, рака влагалища, ангиосаркомы, немелкоклеточного рака легкого, рака аппендикса, плоскоклеточного рака, карциномы протоков слюнной железы, аденокистозной карциномы, рака тонкого кишечника и рака желчного пузыря.
[0020] Согласно некоторым вариантам осуществления злокачественная опухоль выбрана из группы, состоящей из рака тонкого кишечника, немелкоклеточного рака легкого, рака желчного пузыря и плоскоклеточного рака.
[0021] Согласно некоторым вариантам осуществления способ дополнительно включает введение индивидууму по меньшей мере одного дополнительного лекарственного средства, выбранного из группы, состоящей из ингибитора MEK, ингибитора RAF, ингибитора HDAC и их комбинаций.
[0022] Согласно некоторым вариантам осуществления ингибитор MEK выбран из группы, состоящей из токсина сибирской язвы, антрохинолола (Golden Biotechnology), ARRY-142886 ((2-гидроксиэтокси)амид 6-(4-бром-2-хлор-фениламино)-7-фтор-3-метил-3H-бензоимидазол-5-карбоновой кислоты) (Array BioPharma), ARRY-438162 (Array BioPharma) биниметиниба (MEK162, ARRY-1662), AS-1940477 (Astellas), AS-703988 (Merck KGaA), бентамапимода (Merck KGaA), BI-847325 (Boehringer Ingelheim), E-6201 (Eisai), GDC-0623 (Hoffmann-La Roche), GDC-0973 (кобиметиниб) (Hoffmann-La Roche), L783277 (Merck), части токсина сибирской язвы, являющейся летальным фактором, MEK162 (Array BioPharma), PD 098059 (2-(2'-амино-3'-метоксфенил)оксанафталин-4-он) (Pfizer), PD 184352 (CI-1040) (Pfizer), PD-0325901 (Pfizer), PD318088 (Pfizer), PD334581 (Pfizer), 6-метокси-7-(3-морфолин-4-илпропокси)-4-(4-феноксифениламино)хинолин-3-карбонитрила, 4-[3-хлор-4-(1-метил-1H-имидазол-2-илсульфанил)фениламино]-6-метокси-7-(3-морфолин-4-илпропокси)хинолин-3-карбонитрила, пимасертиба (Santhera Pharmaceuticals), RDEA119 (Ardea Biosciences/Bayer), рефаметиниба (AstraZeneca), RG422 (Chugai Pharmaceutical Co.), R0092210 (Roche), R04987655 (Hoffmann-La Roche), R05126766 (Hoffmann-La Roche), селуметиниба (AZD6244) (AstraZeneca), SL327 (Sigma), TAK-733 (Takeda), траметиниба (Japan Tobacco), U0126 (1,4-диамино-2,3-дициано-1,4-бис(2-аминофенилтио)бутадиена) (Sigma), WX-554 (Wilex), полипептида YopJ (Mittal et al., 2010), их фармацевтически приемлемых солей и их комбинаций.
[0023] Согласно некоторым вариантам осуществления ингибитор RAF выбран из группы, состоящей из AAL881 (Novartis), AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BAY 43-9006 сорафениба, BeiGene-283 (BeiGene), BUB-024 (MLN 2480) (Sunesis & Takeda), ингибитора b-raf (Sareum), ингибитора киназы BRAF (Selexagen Therapeutics), миРНК против BRAF 313 (tacaccagcaagctagatgca) и 523 (cctatcgttagagtcttcctg) (Liu et al., 2007), CHIR-265 (Novartis), CTT239065 (Institute of Cancer Research), дабрафениба (GSK2118436), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GDC-0879 (Genentech), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), L779450 (Merck), LBT613 (Novartis), LXH254 (Novartis), LErafAON (NeoPharm, Inc.), LGX-818 (Novartis), пазопаниба (GlaxoSmithKline), PLX3202 (Plexxikon), PLX4720 (Plexxikon), PLX5568 (Plexxikon), PLX3603 (Daiichi Sankyo), PLX8394 (Daiichi Sankyo), RAF-265 (Novartis), RAF-365 (Novartis), REDX0535 (RedX Pharma Plc), регорафениба (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), SB-590885 (GlaxoSmithKline), SB699393 (GlaxoSmithKline), сорафениба (Onyx Pharmaceuticals), TAK 632 (Takeda), TL-241 (Teligene), вемурафениба (RG7204 или PLX4032) (Daiichi Sankyo), XL-281 (Exelixis), ZM-336372 (AstraZeneca), их фармацевтически приемлемых солей и их комбинаций.
[0024] Согласно некоторым вариантам осуществления ингибитор HDAC выбран из группы, состоящей из Абексиностата (PCI-24781), Гивиностата, Энтиностата, Вориностата, CI-994, CUDC-101, Энтиностата, BML-210, M344, NVP-LAQ824, Панобиностата, Прациносата (SB939), Моцетиностата, Ресминостата, Ромидепсина, Белиностата, их фармацевтически приемлемых солей и их комбинаций.
[0025] Согласно некоторым вариантам осуществления способ дополнительно включает введение индивидууму по меньшей мере одного дополнительного лекарственного средства, выбранного из группы, состоящей из антитела, фрагмента антитела, конъюгата антитела, цитотоксического средства, токсина, радионуклида, иммуномодулятора, фотоактивного лекарственного средства, радиосенсибилизирующего средства, гормона, антиангиогенного средства и их комбинаций.
[0026] Согласно некоторым вариантам осуществления антитело, его фрагмент или их конъюгат выбраны из группы, состоящей из ритуксимаба (Ритуксан), Брентуксимаба Ведотина (Адцетриз), Адотрастузумаба эмтансина (Кадсила), Цетуксимаба (Эрбитукс), бевацизумаба (Авастин), Ибритумомаба (Зевалин), ведолизумаба (Энтивио), Ипилимумаба (Ервой), Ниволумаба (Опдиво), пембролизумаба (Кейтруда), Алемтузумаба атезолизумаба (Тецентрик), авелумаба (Бавенцио), дурвалумаба (Имфинзи), B-701, Офатумумаба, Обинутузумаба (Газива), Панитумумаба, плозализумаба, BI-754091, OREG-103, COM-701, BI-754111 и их комбинаций.
[0027] Согласно некоторым вариантам осуществления цитотоксическое средство выбрано из группы, состоящей из циклофосфамида, мехлорэтамина, урамустина, мелфалана, хлорамбуцила, ифосфамида, кармустина, ломустина, стрептозоцина, бусульфана, темозоломида, цисплатина, карбоплатина, оксалиплатина, недаплатина, сатраплатина, триплатина тетранитрата, доксорубицина, даунорубицина, идарубицина, митоксантрона, метотрексата, пеметрекседа, 6-меркаптопурина, дакарбазина, флударабина, 5-фторурацила, арабинозилцитозина, капецитабина, гемцитабина, децитабина, алкалоидов барвинка, паклитаксела (Таксол), доцетаксела (Таксотер), иксабепилона (Икземпра), актиномицина, антрациклинов, валрубицина, эпирубицина, блеомицина, пликамицина, митомицина, их фармацевтически приемлемых солей, их пролекарств и комбинаций.
[0028] Согласно некоторым вариантам осуществления токсин представляет собой дифтерийный токсин или его части.
[0029] Согласно некоторым вариантам осуществления радионуклид выбран из группы, состоящей из I-125, At-211, Lu-177, Cu-67, I-131, Sm-153, Re-186, P-32, Re-188, In-114m, Y-90 и их комбинаций.
[0030] Согласно некоторым вариантам осуществления иммуномодулятор выбран из группы, состоящей из гранулоцитарного колониестимулирующего фактора (G-CSF), LAG-3, IMP-321, JCAR-014, ASLAN-002 (BMS-777607), интерферонов, имиквимода и клеточных мембранных фракций из бактерий, IL-2, IL-7, IL-12, CCL3, CCL26, CXCL7, синтетического цитозинфосфат-гуанозина (CpG), ингибиторов иммунной точки контроля и их комбинаций.
[0031] Согласно некоторым вариантам осуществления радиосенсибилизирующее средство выбрано из группы, состоящей из мизонидазола, метронидазола, тирапазамина, транс-кроцетината натрия и их комбинаций.
[0032] Согласно некоторым вариантам осуществления гормон выбран из группы, состоящей из простагландинов, лейкотриенов, простациклина, тромбоксана, амилина, антимюллерова гормона, адипонектина, адренокортикотропного гормона, ангиотензиногена, ангиотензина, вазопрессина, атриопептина, натрийуретического пептида головного мозга, кальцитонина, холицистокинина, кортикотропин-рилизинг гормона, энцефалина, эндотелина, эритропоэтина, фоликулостимулирующего гормона, галанина, гастрина, грелина, глюкагона, гонадотропин-рилизинг гормона, рилизинг-фактора гормона роста, хорионического гонадотропина человека, лактогена плаценты человека, гормона роста, ингибина, инсулина, соматомедина, лептина, липотропина, лютеинизирующего гормона, меланоцит-стимулирующего гормона, мотилина, орексина, окситоцина, панкреатического полипептида, паратиреоидного гормона, пролактина, пролактин-рилизинг гормона, релаксина, ренина, секретина, соматостатина, тромбопоэтина, тиреотропного гормона, тестостерона, дегидроэпиандростерона, андростендиона, дигидротестостерона, альдостерона, эстрадиола, эстрона, эстриола, кортизола, прогестерона, кальцитриола, кальцидиола, тамоксифена (Нолвадекс), анастрозола (Аримидекс), лектрозола (Фемара), фулвестранта (Фаслодекс) и их комбинаций.
[0033] Согласно некоторым вариантам осуществления антиангиогенное средство выбрано из группы, состоящей из 2-метоксиэстрадиола, ангиостатина, бевацизумаба, хрящевого ингибирующего ангиогенез фактора, эндостатина, IFN-альфа, IL-12, итраконазола, линомида, тромбоцитарного фактора-4, пролактина, SU5416, сурамина, тасквинимода, текогалана, тетратиомолибдата, талидомида, тромбоспондина, тромбоспондина, TNP-470, зив-афлиберцепта, их фармацевтически приемлемых солей, пролекарств и их комбинаций.
[0034] Согласно некоторым вариантам осуществления дополнительное лекарственное средство представляет собой ингибитор каскада PI3K/Akt.
[0035] Согласно некоторым вариантам осуществления ингибитор каскада PI3K/Akt выбран из группы, состоящей из A-674563 (CAS № 552325-73-2), AGL 2263, AMG-319 (Amgen, Thousand Oaks, CA), AS-041164 (5-бензо[1,3]диоксол-5-илметилентиазолидин-2,4-дион), AS-604850 (5-(2,2-дифтор-бензо[1,3]диоксол-5-илметилен)тиазолидин-2,4-дион), AS-605240 (5-хиноксилин-6-метилен-1,3-тиазолидин-2,4-дион), AT7867 (CAS № 857531-00-1), серии бензимидазолов, Genentech (Roche Holdings Inc., South San Francisco, CA), BML-257 (CAS № 32387-96-5), BVD-723, CAL-120 (Gilead Sciences, Foster City, CA), CAL-129 (Gilead Sciences), CAL-130 (Gilead Sciences), CAL-253 (Gilead Sciences), CAL-263 (Gilead Sciences), CAS № 612847-09-3, CAS № 681281-88-9, CAS № 75747-14-7, CAS № 925681-41-0, CAS № 98510-80-6, CCT128930 (CAS № 885499-61-6), CH5132799 (CAS № 1007207-67-1), CHR-4432 (Chroma Therapeutics, Ltd., Abingdon, UK), FPA 124 (CAS № 902779-59-3), GS-1101 (CAL-101) (Gilead Sciences), GSK 690693 (CAS № 937174-76-0), H-89 (CAS № 127243-85-0), Хонокиола, IC87114 (Gilead Science), IPI-145 (Intellikine Inc.), KAR-4139 (Karus Therapeutics, Chilworth, Великобритания), KAR-4141 (Karus Therapeutics), KIN-1 (Karus Therapeutics), KT 5720 (CAS № 108068-98-0), Милтефозина, MK-2206 дигидрохлорида (CAS № 1032350-13-2), ML-9 (CAS № 105637-50-1), Налтриндола гидрохлорида, OXY-111A (NormOxys Inc., Brighton, MA), перифозина, PHT-427 (CAS № 1191951-57-1), ингибитора PI3-киназы дельта, Merck KGaA (Merck & Co., Whitehouse Station, NJ), ингибиторов PI3-киназы дельта, Genentech (Roche Holdings Inc.), ингибиторов PI3-киназы дельта, Incozen (Incozen Therapeutics, Pvt. Ltd., Hydrabad, Индия), ингибиторов-2 PI3-киназы дельта, Инкозена (Incozen Therapeutics), ингибитора PI3-киназы, Roche-4 (Roche Holdings Inc.), ингибиторов PI3-киназы, Roche (Roche Holdings Inc.), ингибиторов PI3-киназы, Roche-5 (Roche Holdings Inc.), ингибиторов PI3-альфа/дельта, Pathway Therapeutics (Pathway Therapeutics Ltd., South San Francisco, CA), ингибиторов PI3-дельта, Cellzome (Cellzome AG, Heidelberg, Germany), ингибиторов PI3-дельта, Intellikine (Intellikine Inc., La Jolla, CA), ингибиторов PI3-дельта, Pathway Therapeutics-1 (Pathway Therapeutics Ltd.), ингибиторов PI3-дельта, Pathway Therapeutics-2 (Pathway Therapeutics Ltd.), ингибиторов PI3-дельта/гамма, Cellzome (Cellzome AG), ингибиторов PI3-дельта/гамма, Cellzome (Cellzome AG), ингибиторов PI3-дельта/гамма, Intellikine (Intellikine Inc.), ингибиторов PI3-дельта/гамма, Intellikine (Intellikine Inc.), ингибиторов PI3-дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторов PI3-дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибитора PI3-гамма Evotec (Evotec), ингибитора PI3-гамма, Cellzome (Cellzome AG), ингибиторов PI3-гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторов PI3K-дельта/гамма, Intellikine-1 (Intellikine Inc.), ингибиторов PI3K-дельта/гамма, Intellikine-1 (Intellikine Inc.), пиктилисиба (Roche Holdings Inc.), PIK-90 (CAS № 677338-12-4), SC-103980 (Pfizer, Нью-Йорк, NY), SF-1126 (Semafore Pharmaceuticals, Индианаполис, IN), SH-5, SH-6, тетрагидрокуркумина, TG100-115 (Targegen Inc., San Diego, CA), Трицирибина, X-339 (Xcovery, Уэст-Палм-Бич, FL), XL-499 (Evotech, Гамбург, Германия), их фармацевтически приемлемых солей и их комбинаций.
[0036] В соответствии с одним аспектом настоящее изобретение относится к способу лечения или смягчения эффектов злокачественной опухоли у индивидуума, включающему: (a) идентификацию индивидуума со злокачественной опухолью, имеющей мутацию BRAF не V600E/K; и (b) введение индивидууму эффективного количества ингибитора ERK или его фармацевтически приемлемой соли.
[0037] Согласно некоторым вариантам осуществления ингибитор ERK выбран из группы, состоящей из BVD-523, SCH-722984 (Merck & Co.), SCH-772984 (Merck & Co.), SCH-900353 (MK-8353) (Merck & Co.), LY3214996 (Lilly), AEZS-140 (Aeterna Zentaris), AEZS-131 (Aeterna Zentaris), AEZS-136 (Aeterna Zentaris), LTT-462 (Novartis), RG-7842 (Genentech), CC-90003 (Celgene), KIN-4050 (Kinentia) и их комбинаций.
[0038] Согласно некоторым вариантам осуществления ингибитор ERK представляет собой BVD-523.
[0039] Согласно некоторым вариантам осуществления мутация BRAF не V600E/K представляет собой активирующую киназу мутацию, нарушающую функцию киназы мутацию или мутацию с неизвестным действием на киназу, и их комбинации.
[0040] Согласно некоторым вариантам осуществления активирующая киназу мутация выбрана из группы, состоящей из R462I, I463S, G464E, G464R, G464V, G466A, G469A, N581S, E586K, F595L, L597Q, L597R, L597S, L597V, A598V, T599E, V600R, K601E, S602D, A728V и их комбинаций.
[0041] Согласно некоторым вариантам осуществления нарушающая функцию киназы мутация выбрана из группы, состоящей из G466E, G466R, G466V, Y472C, K483M, D594A, D594E, D594G, D594H, D594N, D594V, G596R, T599A, S602A и их комбинаций.
[0042] Согласно некоторым вариантам осуществления мутация с неизвестным действием на киназу выбрана из группы, состоящей из T440I, S467L, G469E, G469R, G469S, G469V, L584F, L588F, V600_K601delinsE, S605I, Q609L, E611Q и их комбинаций.
[0043] Согласно некоторым вариантам осуществления индивидуумом является млекопитающее.
[0044] Согласно некоторым вариантам осуществления млекопитающее выбрано из группы, состоящей из людей, приматов, сельскохозяйственных животных и домашних животных.
[0045] Согласно некоторым вариантам осуществления млекопитающее представляет собой человека.
[0046] Согласно некоторым вариантам осуществления злокачественная опухоль представляет собой солидную злокачественную опухоль или гематологическую злокачественную опухоль.
[0047] Согласно некоторым вариантам осуществления злокачественная опухоль выбрана из группы, состоящей из глиобластомы, меланомы, холангиокарциномы, мелкоклеточного рака легкого, рака ободочной и прямой кишки, рака предстательной железы, рака влагалища, ангиосаркомы, немелкоклеточного рака легкого, рака аппендикса, плоскоклеточного рака, карциномы протоков слюнных желез, аденокистозной карциномы, рака тонкого кишечника и рака желчного пузыря.
[0048] Согласно некоторым вариантам осуществления злокачественная опухоль выбрана из группы, состоящей из рака тонкого кишечника, немелкоклеточного рака легкого, рака желчного пузыря и плоскоклеточного рака.
[0049] Согласно некоторым вариантам осуществления способ дополнительно включает (i) получение биологического образца от индивидуума; и (ii) скрининг образца для определения того, имеет ли индивидуум мутацию BRAF не V600E/K.
[0050] Согласно некоторым вариантам осуществления способ дополнительно включает введение индивидууму по меньшей мере одного дополнительного лекарственного средства, выбранного из группы, состоящей из ингибитора MEK, ингибитора RAF, ингибитора HDAC и их комбинаций.
[0051] Согласно некоторым вариантам осуществления ингибитор MEK выбран из группы, состоящей из токсина сибирской язвы, антрохинонола (Golden Biotechnology), ARRY-142886 ((2-гидроксиэтокси)амид) 6-(4-бром-2-хлорфениламино)-7-фтор-3-метил-3H-бензоимидазол-5-карбоновой кислоты (Array BioPharma), ARRY-438162 (Array BioPharma) биниметиниба (MEK162, ARRY-1662), AS-1940477 (Astellas), AS-703988 (Merck KGaA), бентамапимода (Merck KGaA), BI-847325 (Boehringer Ingelheim), E-6201 (Eisai), GDC-0623 (Hoffmann-La Roche), GDC-0973 (кобиметиниб) (Hoffmann-La Roche), L783277 (Merck), части токсина сибирской язвы, являющейся летальным фактором, MEK162 (Array BioPharma), PD 098059 (2-(2'-амино-3'-метоксфенил)оксанафталин-4-он) (Pfizer), PD 184352 (CI-1040) (Pfizer), PD-0325901 (Pfizer), PD318088 (Pfizer), PD334581 (Pfizer), 6-метокси-7-(3-морфолин-4-илпропокси)-4-(4-феноксифениламино)хинолин-3-карбонитрила, 4-[3-хлор-4-(1-метил-1H-имидазол-2-илсульфанил)фениламино]-6-метокси-7-(3-морфолин-4-илпропокси)хинолин-3-карбонитрила, пимасертиба (Santhera Pharmaceuticals), RDEA119 (Ardea Biosciences/Bayer), рефаметиниба (AstraZeneca), RG422 (Chugai Pharmaceutical Co.), R0092210 (Roche), R04987655 (Hoffmann-La Roche), R05126766 (Hoffmann-La Roche), селуметиниба (AZD6244) (AstraZeneca), SL327 (Sigma), TAK-733 (Takeda), траметиниба (Japan Tobacco), U0126 (1,4-диамино-2,3-дициано-1,4-бис(2-аминофенилтио)бутадиена) (Sigma), WX-554 (Wilex), полипептида YopJ (Mittal et al., 2010), их фармацевтически приемлемых солей и их комбинаций.
[0052] Согласно некоторым вариантам осуществления ингибитор RAF выбран из группы, состоящей из AAL881 (Novartis), AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BAY 43-9006 сорафениба, BeiGene-283 (BeiGene), BUB-024 (MLN 2480) (Sunesis & Takeda), ингибитора b-raf (Sareum), ингибитора киназы BRAF (Selexagen Therapeutics), миРНК против BRAF 313 (tacaccagcaagctagatgca) и 523 (cctatcgttagagtcttcctg) (Liu et al., 2007), CHIR-265 (Novartis), CTT239065 (Institute of Cancer Research), дабрафениба (GSK2118436), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GDC-0879 (Genentech), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), L779450 (Merck), LBT613 (Novartis), LXH254 (Novartis), LErafAON (NeoPharm, Inc.), LGX-818 (Novartis), пазопаниба (GlaxoSmithKline), PLX3202 (Plexxikon), PLX4720 (Plexxikon), PLX5568 (Plexxikon), PLX3603 (Daiichi Sankyo), PLX8394 (Daiichi Sankyo), RAF-265 (Novartis), RAF-365 (Novartis), REDX0535 (RedX Pharma Plc), регорафениба (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), SB-590885 (GlaxoSmithKline), SB699393 (GlaxoSmithKline), сорафениба (Onyx Pharmaceuticals), TAK 632 (Takeda), TL-241 (Teligene), вемурафениба (RG7204 или PLX4032) (Daiichi Sankyo), XL-281 (Exelixis), ZM-336372 (AstraZeneca), их фармацевтически приемлемых солей и их комбинаций.
[0053] Согласно некоторым вариантам осуществления ингибитор HDAC выбран из группы, состоящей из Абексиностата (PCI-24781), Гивиностата, Энтиностата, Вориностата, CI-994, CUDC-101, Энтиностата, BML-210, M344, NVP-LAQ824, Панобиностата, Прациносата (SB939), Моцетиностата, Ресминостата, Ромидепсина, Белиностата, их фармацевтически приемлемых солей и их комбинаций.
[0054] Согласно некоторым вариантам осуществления способ дополнительно включает введение индивидууму по меньшей мере одного дополнительного лекарственного средства, выбранного из группы, состоящей из антитела, фрагмента антитела, конъюгата антитела, цитотоксического средства, токсина, радионуклида, иммуномодулятора, фотоактивного лекарственного средства, радиосенсибилизирующего средства, гормона, антиангиогенного средства и их комбинаций.
[0055] Согласно некоторым вариантам осуществления антитело, его фрагмент или их конъюгат выбраны из группы, состоящей из ритуксимаба (Ритуксан), Брентуксимаба Ведотина (Адцетриз), Адотрастузумаба эмтансина (Кадсила), Цетуксимаба (Эрбитукс), бевацизумаба (Авастин), Ибритумомаба (Зевалин), ведолизумаба (Энтивио), Ипилимумаба (Ервой), Ниволумаба (Опдиво), пембролизумаба (Кейтруда), Алемтузумаба атезолизумаба (Тецентрик), авелумаба (Бавенцио), дурвалумаба (Имфинзи), B-701, Офатумумаба, Обинутузумаба (Газива), Панитумумаба, плозализумаба, BI-754091, OREG-103, COM-701, BI-754111 и их комбинаций.
[0056] Согласно некоторым вариантам осуществления цитотоксическое средство выбрано из группы, состоящей из циклофосфамида, мехлорэтамина, урамустина, мелфалана, хлорамбуцила, ифосфамида, кармустина, ломустина, стрептозоцина, бусульфана, темозоломида, цисплатина, карбоплатина, оксалиплатина, недаплатина, сатраплатина, триплатина тетранитрата, доксорубицина, даунорубицина, идарубицина, митоксантрона, метотрексата, пеметрекседа, 6-меркаптопурина, дакарбазина, флударабина, 5-фторурацила, арабинозилцитозина, капецитабина, гемцитабина, децитабина, алкалоидов барвинка, паклитаксела (Таксол), доцетаксела (Таксотер), иксабепилона (Икземпра), актиномицина, антрациклинов, валрубицина, эпирубицина, блеомицина, пликамицина, митомицина, их фармацевтически приемлемых солей, их пролекарств и комбинаций.
[0057] Согласно некоторым вариантам осуществления токсин представляет собой дифтерийный токсин или его части.
[0058] Согласно некоторым вариантам осуществления радионуклид выбран из группы, состоящей из I-125, At-211, Lu-177, Cu-67, I-131, Sm-153, Re-186, P-32, Re-188, In-114m, Y-90 и их комбинаций.
[0059] Согласно некоторым вариантам осуществления иммуномодулятор выбран из группы, состоящей из гранулоцитарного колониестимулирующего фактора (G-CSF), LAG-3, IMP-321, JCAR-014, ASLAN-002 (BMS-777607), интерферонов, имиквимода и клеточных мембранных фракций из бактерий, IL-2, IL-7, IL-12, CCL3, CCL26, CXCL7, синтетического цитозинфосфат-гуанозина (CpG), ингибиторов иммунной точки контроля и их комбинаций.
[0060] Согласно некоторым вариантам осуществления радиосенсибилизирующее средство выбрано из группы, состоящей из мизонидазола, метронидазола, тирапазамина, транс-кроцетината натрия, и их комбинаций.
[0061] Согласно некоторым вариантам осуществления гормон выбран из группы, состоящей из простагландинов, лейкотриенов, простациклина, тромбоксана, амилина, антимюллерова гормона, адипонектина, адренокортикотропного гормона, ангиотензиногена, ангиотензина, вазопрессина, атриопептина, натрийуретического пептида головного мозга, кальцитонина, холицистокинина, кортикотропин-рилизинг гормона, энцефалина, эндотелина, эритропоэтина, фоликулостимулирующего гормона, галанина, гастрина, грелина, глюкагона, гонадотропин-рилизинг гормона, рилизинг-фактора гормона роста, хорионического гонадотропина человека, лактогена плаценты человека, гормона роста, ингибина, инсулина, соматомедина, лептина, липотропина, лютеинизирующего гормона, меланоцит-стимулирующего гормона, мотилина, орексина, окситоцина, панкреатического полипептида, паратиреоидного гормона, пролактина, пролактин-рилизинг гормона, релаксина, ренина, секретина, соматостатина, тромбопоэтина, тиреотропного гормона, тестостерона, дегидроэпиандростерона, андростендиона, дигидротестостерона, альдостерона, эстрадиола, эстрона, эстриола, кортизола, прогестерона, кальцитриола, кальцидиола, тамоксифена (Нолвадекс), анастрозола (Аримидекс), лектрозола (Фемара), фулвестранта (Фаслодекс) и их комбинаций.
[0062] Согласно некоторым вариантам осуществления антиангиогенное средство выбрано из группы, состоящей из 2-метоксиэстрадиола, ангиостатина, бевацизумаба, хрящевого ингибирующего ангиогенез фактора, эндостатина, IFN-альфа, IL-12, итраконазола, линомида, тромбоцитарного фактора-4, пролактина, SU5416, сурамина, тасквинимода, текогалана, тетратиомолибдата, талидомида, тромбоспондина, тромбоспондина, TNP-470, зив-афлиберцепта, их фармацевтически приемлемых солей, пролекарств и их комбинаций.
[0063] Согласно некоторым вариантам осуществления дополнительное лекарственное средство представляет собой ингибитор каскада PI3K/Akt.
[0064] Согласно некоторым вариантам осуществления ингибитор каскада PI3K/Akt выбран из группы, состоящей из A-674563 (CAS № 552325-73-2), AGL 2263, AMG-319 (Amgen, Thousand Oaks, CA), AS-041164 (5-бензо[1,3]диоксол-5-илметилентиазолидин-2,4-дион), AS-604850 (5-(2,2-дифтор-бензо[1,3]диоксол-5-илметилен)тиазолидин-2,4-дион), AS-605240 (5-хиноксилин-6-метилен-1,3-тиазолидин-2,4-дион), AT7867 (CAS № 857531-00-1), серии бензимидазолов, Genentech (Roche Holdings Inc., South San Francisco, CA), BML-257 (CAS № 32387-96-5), BVD-723, CAL-120 (Gilead Sciences, Foster City, CA), CAL-129 (Gilead Sciences), CAL-130 (Gilead Sciences), CAL-253 (Gilead Sciences), CAL-263 (Gilead Sciences), CAS № 612847-09-3, CAS № 681281-88-9, CAS № 75747-14-7, CAS № 925681-41-0, CAS № 98510-80-6, CCT128930 (CAS № 885499-61-6), CH5132799 (CAS № 1007207-67-1), CHR-4432 (Chroma Therapeutics, Ltd., Abingdon, UK), FPA 124 (CAS № 902779-59-3), GS-1101 (CAL-101) (Gilead Sciences), GSK 690693 (CAS № 937174-76-0), H-89 (CAS № 127243-85-0), Хонокиола, IC87114 (Gilead Science), IPI-145 (Intellikine Inc.), KAR-4139 (Karus Therapeutics, Chilworth, Великобритания), KAR-4141 (Karus Therapeutics), KIN-1 (Karus Therapeutics), KT 5720 (CAS № 108068-98-0), Милтефозина, MK-2206 дигидрохлорида (CAS № 1032350-13-2), ML-9 (CAS № 105637-50-1), Налтриндола гидрохлорида, OXY-111A (NormOxys Inc., Brighton, MA), перифозина, PHT-427 (CAS № 1191951-57-1), ингибитора PI3-киназы дельта, Merck KGaA (Merck & Co., Whitehouse Station, NJ), ингибиторов PI3-киназы дельта, Genentech (Roche Holdings Inc.), ингибиторов PI3-киназы дельта, Incozen (Incozen Therapeutics, Pvt. Ltd., Hydrabad, Индия), ингибиторов-2 PI3-киназы дельта, Инкозена (Incozen Therapeutics), ингибитора PI3-киназы, Roche-4 (Roche Holdings Inc.), ингибиторов PI3-киназы, Roche (Roche Holdings Inc.), ингибиторов PI3-киназы, Roche-5 (Roche Holdings Inc.), ингибиторов PI3-альфа/дельта, Pathway Therapeutics (Pathway Therapeutics Ltd., South San Francisco, CA), ингибиторов PI3-дельта, Cellzome (Cellzome AG, Heidelberg, Germany), ингибиторов PI3-дельта, Intellikine (Intellikine Inc., La Jolla, CA), ингибиторов PI3-дельта, Pathway Therapeutics-1 (Pathway Therapeutics Ltd.), ингибиторов PI3-дельта, Pathway Therapeutics-2 (Pathway Therapeutics Ltd.), ингибиторов PI3-дельта/гамма, Cellzome (Cellzome AG), ингибиторов PI3-дельта/гамма, Cellzome (Cellzome AG), ингибиторов PI3-дельта/гамма, Intellikine (Intellikine Inc.), ингибиторов PI3-дельта/гамма, Intellikine (Intellikine Inc.), ингибиторов PI3-дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторов PI3-дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибитора PI3-гамма Evotec (Evotec), ингибитора PI3-гамма, Cellzome (Cellzome AG), ингибиторов PI3-гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторов PI3K-дельта/гамма, Intellikine-1 (Intellikine Inc.), ингибиторов PI3K-дельта/гамма, Intellikine-1 (Intellikine Inc.), пиктилисиба (Roche Holdings Inc.), PIK-90 (CAS № 677338-12-4), SC-103980 (Pfizer, Нью-Йорк, NY), SF-1126 (Semafore Pharmaceuticals, Индианаполис, IN), SH-5, SH-6, тетрагидрокуркумина, TG100-115 (Targegen Inc., San Diego, CA), Трицирибина, X-339 (Xcovery, Уэст-Палм-Бич, FL), XL-499 (Evotech, Гамбург, Германия), их фармацевтически приемлемых солей и их комбинаций.
[0065] В соответствии с одним аспектом настоящее изобретение относится к способу идентификации индивидуума, имеющего злокачественную опухоль, для которого будет полезной терапия ингибитором ERK или его фармацевтически приемлемой солью, причем способ включает: (a) получение биологического образца от индивидуума; и (b) скрининг образца для определения того, имеет ли индивидуум мутацию BRAF не V600E/K, где наличие мутации BRAF не V600E/K подтверждает, что индивидууму будет полезна терапия ингибитором ERK или его фармацевтически приемлемой солью.
[0066] Согласно некоторым вариантам осуществления ингибитор ERK выбран из группы, состоящей из BVD-523, SCH-722984 (Merck & Co.), SCH-772984 (Merck & Co.), SCH-900353 (MK-8353) (Merck & Co.), LY3214996 (Lilly), AEZS-140 (Aeterna Zentaris), AEZS-131 (Aeterna Zentaris), AEZS-136 (Aeterna Zentaris), LTT-462 (Novartis), RG-7842 (Genentech), CC-90003 (Celgene), KIN-4050 (Kinentia) и их комбинаций.
[0067] Согласно некоторым вариантам осуществления ингибитор ERK представляет собой BVD-523.
[0068] Согласно некоторым вариантам осуществления мутация BRAF не V600E/K представляет собой активирующую киназу мутацию, нарушающую функцию киназы мутацию или мутацию с неизвестным действием на киназу, и их комбинации.
[0069] Согласно некоторым вариантам осуществления активирующая киназу мутация выбрана из группы, состоящей из R462I, I463S, G464E, G464R, G464V, G466A, G469A, N581S, E586K, F595L, L597Q, L597R, L597S, L597V, A598V, T599E, V600R, K601E, S602D, A728V и их комбинаций.
[0070] Согласно некоторым вариантам осуществления нарушающая функцию киназы мутация выбрана из группы, состоящей из G466E, G466R, G466V, Y472C, K483M, D594A, D594E, D594G, D594H, D594N, D594V, G596R, T599A, S602A и их комбинаций.
[0071] Согласно некоторым вариантам осуществления мутация с неизвестным действием на киназу выбрана из группы, состоящей из T440I, S467L, G469E, G469R, G469S, G469V, L584F, L588F, V600_K601delinsE, S605I, Q609L, E611Q, и их комбинаций.
[0072] Согласно некоторым вариантам осуществления индивидуумом является млекопитающее.
[0073] Согласно некоторым вариантам осуществления млекопитающее выбрано из группы, состоящей из человека, приматов, сельскохозяйственных животных и домашних животных.
[0074] Согласно некоторым вариантам осуществления млекопитающее представляет собой человека.
[0075] Согласно некоторым вариантам осуществления злокачественная опухоль представляет собой солидную злокачественную или гематологическую злокачественную опухоль.
[0076] Согласно некоторым вариантам осуществления злокачественная опухоль выбрана из группы, состоящей из глиобластомы, меланомы, холангиокарциномы, мелкоклеточного рака легкого, рака ободочной и прямой кишки, рака предстательной железы, рака влагалища, ангиосаркомы, немелкоклеточного рака легкого, рака аппендикса, плоскоклеточного рака, карциномы протоков слюнной железы, аденокистозной карциномы, рака тонкого кишечника и рака желчного пузыря.
[0077] Согласно некоторым вариантам осуществления злокачественная опухоль выбрана из группы, состоящей из рака тонкого кишечника, немелкоклеточного рака легкого, рака желчного пузыря и плоскоклеточного рака.
[0078] Согласно некоторым вариантам осуществления способ дополнительно включает введение ингибитора ERK или его фармацевтически приемлемой соли индивидууму, имеющему мутацию BRAF не V600E/K.
[0079] Согласно некоторым вариантам осуществления способ дополнительно включает введение индивидууму по меньшей мере одного дополнительного лекарственного средства, выбранного из группы, состоящей из ингибитора MEK, ингибитора RAF, ингибитора HDAC и их комбинаций.
[0080] Согласно некоторым вариантам осуществления ингибитор MEK выбран из группы, состоящей из токсина сибирской язвы, антрохинолола (Golden Biotechnology), ARRY-142886 ((2-гидроксиэтокси)амид 6-(4-бром-2-хлор-фениламино)-7-фтор-3-метил-3H-бензоимидазол-5-карбоновой кислоты) (Array BioPharma), ARRY-438162 (Array BioPharma) биниметиниба (MEK162, ARRY-1662), AS-1940477 (Astellas), AS-703988 (Merck KGaA), бентамапимода (Merck KGaA), BI-847325 (Boehringer Ingelheim), E-6201 (Eisai), GDC-0623 (Hoffmann-La Roche), GDC-0973 (кобиметиниб) (Hoffmann-La Roche), L783277 (Merck), части токсина сибирской язвы, являющейся летальным фактором, MEK162 (Array BioPharma), PD 098059 (2-(2'-амино-3'-метоксфенил)оксанафталин-4-он) (Pfizer), PD 184352 (CI-1040) (Pfizer), PD-0325901 (Pfizer), PD318088 (Pfizer), PD334581 (Pfizer), 6-метокси-7-(3-морфолин-4-илпропокси)-4-(4-феноксифениламино)хинолин-3-карбонитрила, 4-[3-хлор-4-(1-метил-1H-имидазол-2-илсульфанил)фениламино]-6-метокси-7-(3-морфолин-4-илпропокси)хинолин-3-карбонитрила, пимасертиба (Santhera Pharmaceuticals), RDEA119 (Ardea Biosciences/Bayer), рефаметиниба (AstraZeneca), RG422 (Chugai Pharmaceutical Co.), R0092210 (Roche), R04987655 (Hoffmann-La Roche), R05126766 (Hoffmann-La Roche), селуметиниба (AZD6244) (AstraZeneca), SL327 (Sigma), TAK-733 (Takeda), траметиниба (Japan Tobacco), U0126 (1,4-диамино-2,3-дициано-1,4-бис(2-аминофенилтио)бутадиена) (Sigma), WX-554 (Wilex), полипептида YopJ (Mittal et al., 2010), их фармацевтически приемлемых солей и их комбинаций.
[0081] Согласно некоторым вариантам осуществления ингибитор RAF выбран из группы, состоящей из AAL881 (Novartis), AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BAY 43-9006 сорафениба, BeiGene-283 (BeiGene), BUB-024 (MLN 2480) (Sunesis & Takeda), ингибитора b-raf (Sareum), ингибитора киназы BRAF (Selexagen Therapeutics), миРНК против BRAF 313 (tacaccagcaagctagatgca) и 523 (cctatcgttagagtcttcctg) (Liu et al., 2007), CHIR-265 (Novartis), CTT239065 (Institute of Cancer Research), дабрафениба (GSK2118436), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GDC-0879 (Genentech), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), L779450 (Merck), LBT613 (Novartis), LXH254 (Novartis), LErafAON (NeoPharm, Inc.), LGX-818 (Novartis), пазопаниба (GlaxoSmithKline), PLX3202 (Plexxikon), PLX4720 (Plexxikon), PLX5568 (Plexxikon), PLX3603 (Daiichi Sankyo), PLX8394 (Daiichi Sankyo), RAF-265 (Novartis), RAF-365 (Novartis), REDX0535 (RedX Pharma Plc), регорафениба (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), SB-590885 (GlaxoSmithKline), SB699393 (GlaxoSmithKline), сорафениба (Onyx Pharmaceuticals), TAK 632 (Takeda), TL-241 (Teligene), вемурафениба (RG7204 или PLX4032) (Daiichi Sankyo), XL-281 (Exelixis), ZM-336372 (AstraZeneca), их фармацевтически приемлемых солей и их комбинаций.
[0082] Согласно некоторым вариантам осуществления ингибитор HDAC выбран из группы, состоящей из Абексиностата (PCI-24781), Гивиностата, Энтиностата, Вориностата, CI-994, CUDC-101, Энтиностата, BML-210, M344, NVP-LAQ824, Панобиностата, Прациносата (SB939), Моцетиностата, Ресминостата, Ромидепсина, Белиностата, их фармацевтически приемлемых солей и их комбинаций.
[0083] Согласно некоторым вариантам осуществления способ дополнительно включает введение индивидууму, имеющему мутацию BRAF не V600E/K, по меньшей мере одного дополнительного лекарственного средства, выбранного из группы, состоящей из антитела, фрагмента антитела, конъюгата антитела, цитотоксического средства, токсина, радионуклида, иммуномодулятора, фотоактивного лекарственного средства, радиосенсибилизирующего средства, гормона, антиангиогенного средства и их комбинаций.
[0084] Согласно некоторым вариантам осуществления антитело, его фрагмент или их конъюгат выбраны из группы, состоящей из ритуксимаба (Ритуксан), Брентуксимаба Ведотина (Адцетриз), Адотрастузумаба эмтансина (Кадсила), Цетуксимаба (Эрбитукс), бевацизумаба (Авастин), Ибритумомаба (Зевалин), ведолизумаба (Энтивио), Ипилимумаба (Ервой), Ниволумаба (Опдиво), пембролизумаба (Кейтруда), Алемтузумаба атезолизумаба (Тецентрик), авелумаба (Бавенцио), дурвалумаба (Имфинзи), B-701, Офатумумаба, Обинутузумаба (Газива), Панитумумаба, плозализумаба, BI-754091, OREG-103, COM-701, BI-754111 и их комбинаций.
[0085] Согласно некоторым вариантам осуществления цитотоксическое средство выбрано из группы, состоящей из циклофосфамида, мехлорэтамина, урамустина, мелфалана, хлорамбуцила, ифосфамида, кармустина, ломустина, стрептозоцина, бусульфана, темозоломида, цисплатина, карбоплатина, оксалиплатина, недаплатина, сатраплатина, триплатина тетранитрата, доксорубицина, даунорубицина, идарубицина, митоксантрона, метотрексата, пеметрекседа, 6-меркаптопурина, дакарбазина, флударабина, 5-фторурацила, арабинозилцитозина, капецитабина, гемцитабина, децитабина, алкалоидов барвинка, паклитаксела (Таксол), доцетаксела (Таксотер), иксабепилона (Икземпра), актиномицина, антрациклинов, валрубицина, эпирубицина, блеомицина, пликамицина, митомицина, их фармацевтически приемлемых солей, их пролекарств и комбинаций.
[0086] Согласно некоторым вариантам осуществления токсин представляет собой дифтерийный токсин или его части.
[0087] Согласно некоторым вариантам осуществления радионуклид выбран из группы, состоящей из I-125, At-211, Lu-177, Cu-67, I-131, Sm-153, Re-186, P-32, Re-188, In-114m, Y-90 и их комбинаций.
[0088] Согласно некоторым вариантам осуществления иммуномодулятор выбран из группы, состоящей из гранулоцитарного колониестимулирующего фактора (G-CSF), LAG-3, IMP-321, JCAR-014, ASLAN-002 (BMS-777607), интерферонов, имиквимода и клеточных мембранных фракций из бактерий, IL-2, IL-7, IL-12, CCL3, CCL26, CXCL7, синтетического цитозинфосфат-гуанозина (CpG), ингибиторов иммунной точки контроля и их комбинаций.
[0089] Согласно некоторым вариантам осуществления радиосенсибилизирующее средство выбрано из группы, состоящей из мизонидазола, метронидазола, тирапазамина, транс-кроцетината натрия, и их комбинаций.
[0090] Согласно некоторым вариантам осуществления гормон выбран из группы, состоящей из простагландинов, лейкотриенов, простациклина, тромбоксана, амилина, антимюллерова гормона, адипонектина, адренокортикотропного гормона, ангиотензиногена, ангиотензина, вазопрессина, атриопептина, натрийуретического пептида головного мозга, кальцитонина, холицистокинина, кортикотропин-рилизинг гормона, энцефалина, эндотелина, эритропоэтина, фоликулостимулирующего гормона, галанина, гастрина, грелина, глюкагона, гонадотропин-рилизинг гормона, рилизинг-фактора гормона роста, хорионического гонадотропина человека, лактогена плаценты человека, гормона роста, ингибина, инсулина, соматомедина, лептина, липотропина, лютеинизирующего гормона, меланоцит-стимулирующего гормона, мотилина, орексина, окситоцина, панкреатического полипептида, паратиреоидного гормона, пролактина, пролактин-рилизинг гормона, релаксина, ренина, секретина, соматостатина, тромбопоэтина, тиреотропного гормона, тестостерона, дегидроэпиандростерона, андростендиона, дигидротестостерона, альдостерона, эстрадиола, эстрона, эстриола, кортизола, прогестерона, кальцитриола, кальцидиола, тамоксифена (Нолвадекс), анастрозола (Аримидекс), лектрозола (Фемара), фулвестранта (Фаслодекс) и их комбинаций.
[0091] Согласно некоторым вариантам осуществления антиангиогенное средство выбрано из группы, состоящей из 2-метоксиэстрадиола, ангиостатина, бевацизумаба, хрящевого ингибирующего ангиогенез фактора, эндостатина, IFN-альфа, IL-12, итраконазола, линомида, тромбоцитарного фактора-4, пролактина, SU5416, сурамина, тасквинимода, текогалана, тетратиомолибдата, талидомида, тромбоспондина, тромбоспондина, TNP-470, зив-афлиберцепта, их фармацевтически приемлемых солей, пролекарств и их комбинаций.
[0092] Согласно некоторым вариантам осуществления дополнительное лекарственное средство представляет собой ингибитор каскада PI3K/Akt.
[0093] Согласно некоторым вариантам осуществления ингибитор каскада PI3K/Akt выбран из группы, состоящей из A-674563 (CAS № 552325-73-2), AGL 2263, AMG-319 (Amgen, Thousand Oaks, CA), AS-041164 (5-бензо[1,3]диоксол-5-илметилентиазолидин-2,4-дион), AS-604850 (5-(2,2-дифтор-бензо[1,3]диоксол-5-илметилен)тиазолидин-2,4-дион), AS-605240 (5-хиноксилин-6-метилен-1,3-тиазолидин-2,4-дион), AT7867 (CAS № 857531-00-1), серии бензимидазолов, Genentech (Roche Holdings Inc., South San Francisco, CA), BML-257 (CAS № 32387-96-5), BVD-723, CAL-120 (Gilead Sciences, Foster City, CA), CAL-129 (Gilead Sciences), CAL-130 (Gilead Sciences), CAL-253 (Gilead Sciences), CAL-263 (Gilead Sciences), CAS № 612847-09-3, CAS № 681281-88-9, CAS № 75747-14-7, CAS № 925681-41-0, CAS № 98510-80-6, CCT128930 (CAS № 885499-61-6), CH5132799 (CAS № 1007207-67-1), CHR-4432 (Chroma Therapeutics, Ltd., Abingdon, UK), FPA 124 (CAS № 902779-59-3), GS-1101 (CAL-101) (Gilead Sciences), GSK 690693 (CAS № 937174-76-0), H-89 (CAS № 127243-85-0), Хонокиола, IC87114 (Gilead Science), IPI-145 (Intellikine Inc.), KAR-4139 (Karus Therapeutics, Chilworth, Великобритания), KAR-4141 (Karus Therapeutics), KIN-1 (Karus Therapeutics), KT 5720 (CAS № 108068-98-0), Милтефозина, MK-2206 дигидрохлорида (CAS № 1032350-13-2), ML-9 (CAS № 105637-50-1), Налтриндола гидрохлорида, OXY-111A (NormOxys Inc., Brighton, MA), перифозина, PHT-427 (CAS № 1191951-57-1), ингибитора PI3-киназы дельта, Merck KGaA (Merck & Co., Whitehouse Station, NJ), ингибиторов PI3-киназы дельта, Genentech (Roche Holdings Inc.), ингибиторов PI3-киназы дельта, Incozen (Incozen Therapeutics, Pvt. Ltd., Hydrabad, Индия), ингибиторов-2 PI3-киназы дельта, Инкозена (Incozen Therapeutics), ингибитора PI3-киназы, Roche-4 (Roche Holdings Inc.), ингибиторов PI3-киназы, Roche (Roche Holdings Inc.), ингибиторов PI3-киназы, Roche-5 (Roche Holdings Inc.), ингибиторов PI3-альфа/дельта, Pathway Therapeutics (Pathway Therapeutics Ltd., South San Francisco, CA), ингибиторов PI3-дельта, Cellzome (Cellzome AG, Heidelberg, Germany), ингибиторов PI3-дельта, Intellikine (Intellikine Inc., La Jolla, CA), ингибиторов PI3-дельта, Pathway Therapeutics-1 (Pathway Therapeutics Ltd.), ингибиторов PI3-дельта, Pathway Therapeutics-2 (Pathway Therapeutics Ltd.), ингибиторов PI3-дельта/гамма, Cellzome (Cellzome AG), ингибиторов PI3-дельта/гамма, Cellzome (Cellzome AG), ингибиторов PI3-дельта/гамма, Intellikine (Intellikine Inc.), ингибиторов PI3-дельта/гамма, Intellikine (Intellikine Inc.), ингибиторов PI3-дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторов PI3-дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибитора PI3-гамма Evotec (Evotec), ингибитора PI3-гамма, Cellzome (Cellzome AG), ингибиторов PI3-гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторов PI3K-дельта/гамма, Intellikine-1 (Intellikine Inc.), ингибиторов PI3K-дельта/гамма, Intellikine-1 (Intellikine Inc.), пиктилисиба (Roche Holdings Inc.), PIK-90 (CAS № 677338-12-4), SC-103980 (Pfizer, Нью-Йорк, NY), SF-1126 (Semafore Pharmaceuticals, Индианаполис, IN), SH-5, SH-6, тетрагидрокуркумина, TG100-115 (Targegen Inc., San Diego, CA), Трицирибина, X-339 (Xcovery, Уэст-Палм-Бич, FL), XL-499 (Evotech, Гамбург, Германия), их фармацевтически приемлемых солей и их комбинаций.
[0094] В соответствии с одним аспектом, настоящее изобретение относится к фармацевтической композиции для лечения или смягчения эффектов злокачественной опухоли у индивидуума, имеющей мутацию BRAF не V600E/K, причем композиция содержит фармацевтически приемлемый носитель или разбавитель и эффективное количество ингибитора ERK или его фармацевтически приемлемой соли.
[0095] Согласно некоторым вариантам осуществления ингибитор ERK выбран из группы, состоящей из BVD-523, SCH-722984 (Merck & Co.), SCH-772984 (Merck & Co.), SCH-900353 (MK-8353) (Merck & Co.), LY3214996 (Lilly), AEZS-140 (Aeterna Zentaris), AEZS-131 (Aeterna Zentaris), AEZS-136 (Aeterna Zentaris), LTT-462 (Novartis), RG-7842 (Genentech), CC-90003 (Celgene), KIN-4050 (Kinentia) и их комбинаций.
[0096] Согласно некоторым вариантам осуществления ингибитор ERK представляет собой BVD-523.
[0097] Согласно некоторым вариантам осуществления мутация BRAF не V600E/K представляет собой активирующую киназу мутацию, нарушающую функцию киназы мутацию или мутацию с неизвестным действием на киназу, и их комбинации.
[0098] Согласно некоторым вариантам осуществления активирующая киназу мутация выбрана из группы, состоящей из R462I, I463S, G464E, G464R, G464V, G466A, G469A, N581S, E586K, F595L, L597Q, L597R, L597S, L597V, A598V, T599E, V600R, K601E, S602D, A728V и их комбинаций.
[0099] Согласно некоторым вариантам осуществления нарушающая функцию киназы мутация выбрана из группы, состоящей из G466E, G466R, G466V, Y472C, K483M, D594A, D594E, D594G, D594H, D594N, D594V, G596R, T599A, S602A и их комбинаций.
[0100] Согласно некоторым вариантам осуществления мутация с неизвестным действием на киназу выбрана из группы, состоящей из T440I, S467L, G469E, G469R, G469S, G469V, L584F, L588F, V600_K601delinsE, S605I, Q609L, E611Q и их комбинаций.
[0101] Согласно некоторым вариантам осуществления индивидуумом является млекопитающее.
[0102] Согласно некоторым вариантам осуществления млекопитающее выбрано из группы, состоящей из людей, приматов, сельскохозяйственных животных и домашних животных.
[0103] Согласно некоторым вариантам осуществления млекопитающее представляет собой человека.
[0104] Согласно некоторым вариантам осуществления злокачественная опухоль представляет собой солидную злокачественную опухоль или гематологическую злокачественную опухоль.
[0105] Согласно некоторым вариантам осуществления злокачественная опухоль выбрана из группы, состоящей из глиобластомы, меланомы, холангиокарциномы, мелкоклеточного рака легкого, рака ободочной и прямой кишки, рака предстательной железы, рака влагалища, ангиосаркомы, немелкоклеточного рака легкого, рака аппендикса, плоскоклеточного рака, карциномы протоков слюнных желез, аденокистозной карциномы, рака тонкого кишечника и рака желчного пузыря.
[0106] Согласно некоторым вариантам осуществления злокачественная опухоль выбрана из группы, состоящей из рака тонкого кишечника, немелкоклеточного рака легкого, рака желчного пузыря и плоскоклеточного рака.
[0107] Согласно некоторым вариантам осуществления композицию вводят индивидууму перорально или путем инъекции.
[0108] Согласно некоторым вариантам осуществления композицию вводят индивидууму в качестве таблетки.
[0109] Согласно некоторым вариантам осуществления фармацевтическая композиция содержит по меньшей мере одно дополнительное лекарственное средство, выбранное из группы, состоящей из ингибитора MEK, ингибитора RAF, ингибитора HDAC и их комбинаций.
[0110] Согласно некоторым вариантам осуществления ингибитор MEK выбран из группы, состоящей из токсина сибирской язвы, антрохинонола (Golden Biotechnology), ARRY-142886 ((2-гидроксиэтокси)амид) 6-(4-бром-2-хлорфениламино)-7-фтор-3-метил-3H-бензоимидазол-5-карбоновой кислоты (Array BioPharma), ARRY-438162 (Array BioPharma) биниметиниба (MEK162, ARRY-1662), AS-1940477 (Astellas), AS-703988 (Merck KGaA), бентамапимода (Merck KGaA), BI-847325 (Boehringer Ingelheim), E-6201 (Eisai), GDC-0623 (Hoffmann-La Roche), GDC-0973 (кобиметиниб) (Hoffmann-La Roche), L783277 (Merck), части токсина сибирской язвы, являющейся летальным фактором, MEK162 (Array BioPharma), PD 098059 (2-(2'-амино-3'-метоксфенил)оксанафталин-4-он) (Pfizer), PD 184352 (CI-1040) (Pfizer), PD-0325901 (Pfizer), PD318088 (Pfizer), PD334581 (Pfizer), 6-метокси-7-(3-морфолин-4-илпропокси)-4-(4-феноксифениламино)хинолин-3-карбонитрила, 4-[3-хлор-4-(1-метил-1H-имидазол-2-илсульфанил)фениламино]-6-метокси-7-(3-морфолин-4-илпропокси)хинолин-3-карбонитрила, пимасертиба (Santhera Pharmaceuticals), RDEA119 (Ardea Biosciences/Bayer), рефаметиниба (AstraZeneca), RG422 (Chugai Pharmaceutical Co.), R0092210 (Roche), R04987655 (Hoffmann-La Roche), R05126766 (Hoffmann-La Roche), селуметиниба (AZD6244) (AstraZeneca), SL327 (Sigma), TAK-733 (Takeda), траметиниба (Japan Tobacco), U0126 (1,4-диамино-2,3-дициано-1,4-бис(2-аминофенилтио)бутадиена) (Sigma), WX-554 (Wilex), полипептида YopJ (Mittal et al., 2010), их фармацевтически приемлемых солей и их комбинаций.
[0111] Согласно некоторым вариантам осуществления ингибитор RAF выбран из группы, состоящей из AAL881 (Novartis), AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BAY 43-9006 сорафениба, BeiGene-283 (BeiGene), BUB-024 (MLN 2480) (Sunesis & Takeda), ингибитора b-raf (Sareum), ингибитора киназы BRAF (Selexagen Therapeutics), миРНК против BRAF 313 (tacaccagcaagctagatgca) и 523 (cctatcgttagagtcttcctg) (Liu et al., 2007), CHIR-265 (Novartis), CTT239065 (Institute of Cancer Research), дабрафениба (GSK2118436), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GDC-0879 (Genentech), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), L779450 (Merck), LBT613 (Novartis), LXH254 (Novartis), LErafAON (NeoPharm, Inc.), LGX-818 (Novartis), пазопаниба (GlaxoSmithKline), PLX3202 (Plexxikon), PLX4720 (Plexxikon), PLX5568 (Plexxikon), PLX3603 (Daiichi Sankyo), PLX8394 (Daiichi Sankyo), RAF-265 (Novartis), RAF-365 (Novartis), REDX0535 (RedX Pharma Plc), регорафениба (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), SB-590885 (GlaxoSmithKline), SB699393 (GlaxoSmithKline), сорафениба (Onyx Pharmaceuticals), TAK 632 (Takeda), TL-241 (Teligene), вемурафениба (RG7204 или PLX4032) (Daiichi Sankyo), XL-281 (Exelixis), ZM-336372 (AstraZeneca), их фармацевтически приемлемых солей и их комбинаций.
[0112] Согласно некоторым вариантам осуществления ингибитор HDAC выбран из группы, состоящей из Абексиностата (PCI-24781), Гивиностата, Энтиностата, Вориностата, CI-994, CUDC-101, Энтиностата, BML-210, M344, NVP-LAQ824, Панобиностата, Прациносата (SB939), Моцетиностата, Ресминостата, Ромидепсина, Белиностата, их фармацевтически приемлемых солей и их комбинаций.
[0113] Согласно некоторым вариантам осуществления способ дополнительно включает введение индивидууму по меньшей мере одного дополнительного лекарственного средства, выбранного из группы, состоящей из антитела, фрагмента антитела, конъюгата антитела, цитотоксического средства, токсина, радионуклида, иммуномодулятора, фотоактивного лекарственного средства, радиосенсибилизирующего средства, гормона, антиангиогенного средства и их комбинаций.
[0114] Согласно некоторым вариантам осуществления антитело, его фрагмент или их конъюгат выбраны из группы, состоящей из ритуксимаба (Ритуксан), Брентуксимаба Ведотина (Адцетриз), Адотрастузумаба эмтансина (Кадсила), Цетуксимаба (Эрбитукс), бевацизумаба (Авастин), Ибритумомаба (Зевалин), ведолизумаба (Энтивио), Ипилимумаба (Ервой), Ниволумаба (Опдиво), пембролизумаба (Кейтруда), Алемтузумаба атезолизумаба (Тецентрик), авелумаба (Бавенцио), дурвалумаба (Имфинзи), B-701, Офатумумаба, Обинутузумаба (Газива), Панитумумаба, плозализумаба, BI-754091, OREG-103, COM-701, BI-754111 и их комбинаций.
[0115] Согласно некоторым вариантам осуществления цитотоксическое средство выбрано из группы, состоящей из циклофосфамида, мехлорэтамина, урамустина, мелфалана, хлорамбуцила, ифосфамида, кармустина, ломустина, стрептозоцина, бусульфана, темозоломида, цисплатина, карбоплатина, оксалиплатина, недаплатина, сатраплатина, триплатина тетранитрата, доксорубицина, даунорубицина, идарубицина, митоксантрона, метотрексата, пеметрекседа, 6-меркаптопурина, дакарбазина, флударабина, 5-фторурацила, арабинозилцитозина, капецитабина, гемцитабина, децитабина, алкалоидов барвинка, паклитаксела (Таксол), доцетаксела (Таксотер), иксабепилона (Икземпра), актиномицина, антрациклинов, валрубицина, эпирубицина, блеомицина, пликамицина, митомицина, их фармацевтически приемлемых солей, их пролекарств и комбинаций.
[0116] Согласно некоторым вариантам осуществления токсин представляет собой дифтерийный токсин или его части.
[0117] Согласно некоторым вариантам осуществления радионуклид выбран из группы, состоящей из I-125, At-211, Lu-177, Cu-67, I-131, Sm-153, Re-186, P-32, Re-188, In-114m, Y-90 и их комбинаций.
[0118] Согласно некоторым вариантам осуществления иммуномодулятор выбран из группы, состоящей из гранулоцитарного колониестимулирующего фактора (G-CSF), LAG-3, IMP-321, JCAR-014, ASLAN-002 (BMS-777607), интерферонов, имиквимода и клеточных мембранных фракций из бактерий, IL-2, IL-7, IL-12, CCL3, CCL26, CXCL7, синтетического цитозинфосфат-гуанозина (CpG), ингибиторов иммунной точки контроля и их комбинаций.
[0119] Согласно некоторым вариантам осуществления радиосенсибилизирующее средство выбрано из группы, состоящей из мизонидазола, метронидазола, тирапазамина, транс-кроцетината натрия и их комбинаций.
[0120] Согласно некоторым вариантам осуществления гормон выбран из группы, состоящей из простагландинов, лейкотриенов, простациклина, тромбоксана, амилина, антимюллерова гормона, адипонектина, адренокортикотропного гормона, ангиотензиногена, ангиотензина, вазопрессина, атриопептина, натрийуретического пептида головного мозга, кальцитонина, холицистокинина, кортикотропин-рилизинг гормона, энцефалина, эндотелина, эритропоэтина, фоликулостимулирующего гормона, галанина, гастрина, грелина, глюкагона, гонадотропин-рилизинг гормона, рилизинг-фактора гормона роста, хорионического гонадотропина человека, лактогена плаценты человека, гормона роста, ингибина, инсулина, соматомедина, лептина, липотропина, лютеинизирующего гормона, меланоцит-стимулирующего гормона, мотилина, орексина, окситоцина, панкреатического полипептида, паратиреоидного гормона, пролактина, пролактин-рилизинг гормона, релаксина, ренина, секретина, соматостатина, тромбопоэтина, тиреотропного гормона, тестостерона, дегидроэпиандростерона, андростендиона, дигидротестостерона, альдостерона, эстрадиола, эстрона, эстриола, кортизола, прогестерона, кальцитриола, кальцидиола, тамоксифена (Нолвадекс), анастрозола (Аримидекс), лектрозола (Фемара), фулвестранта (Фаслодекс), и их комбинаций.
[0121] Согласно некоторым вариантам осуществления антиангиогенное средство выбрано из группы, состоящей из 2-метоксиэстрадиола, ангиостатина, бевацизумаба, хрящевого ингибирующего ангиогенез фактора, эндостатина, IFN-альфа, IL-12, итраконазола, линомида, тромбоцитарного фактора-4, пролактина, SU5416, сурамина, тасквинимода, текогалана, тетратиомолибдата, талидомида, тромбоспондина, тромбоспондина, TNP-470, зив-афлиберцепта, их фармацевтически приемлемых солей, пролекарств и их комбинаций.
[0122] Согласно некоторым вариантам осуществления дополнительное лекарственное средство представляет собой ингибитор каскада PI3K/Akt.
[0123] Согласно некоторым вариантам осуществления ингибитор каскада PI3K/Akt выбран из группы, состоящей из A-674563 (CAS № 552325-73-2), AGL 2263, AMG-319 (Amgen, Thousand Oaks, CA), AS-041164 (5-бензо[1,3]диоксол-5-илметилентиазолидин-2,4-дион), AS-604850 (5-(2,2-дифтор-бензо[1,3]диоксол-5-илметилен)тиазолидин-2,4-дион), AS-605240 (5-хиноксилин-6-метилен-1,3-тиазолидин-2,4-дион), AT7867 (CAS № 857531-00-1), серии бензимидазолов, Genentech (Roche Holdings Inc., South San Francisco, CA), BML-257 (CAS № 32387-96-5), BVD-723, CAL-120 (Gilead Sciences, Foster City, CA), CAL-129 (Gilead Sciences), CAL-130 (Gilead Sciences), CAL-253 (Gilead Sciences), CAL-263 (Gilead Sciences), CAS № 612847-09-3, CAS № 681281-88-9, CAS № 75747-14-7, CAS № 925681-41-0, CAS № 98510-80-6, CCT128930 (CAS № 885499-61-6), CH5132799 (CAS № 1007207-67-1), CHR-4432 (Chroma Therapeutics, Ltd., Abingdon, UK), FPA 124 (CAS № 902779-59-3), GS-1101 (CAL-101) (Gilead Sciences), GSK 690693 (CAS № 937174-76-0), H-89 (CAS № 127243-85-0), Хонокиола, IC87114 (Gilead Science), IPI-145 (Intellikine Inc.), KAR-4139 (Karus Therapeutics, Chilworth, Великобритания), KAR-4141 (Karus Therapeutics), KIN-1 (Karus Therapeutics), KT 5720 (CAS № 108068-98-0), Милтефозина, MK-2206 дигидрохлорида (CAS № 1032350-13-2), ML-9 (CAS № 105637-50-1), Налтриндола гидрохлорида, OXY-111A (NormOxys Inc., Brighton, MA), перифозина, PHT-427 (CAS № 1191951-57-1), ингибитора PI3-киназы дельта, Merck KGaA (Merck & Co., Whitehouse Station, NJ), ингибиторов PI3-киназы дельта, Genentech (Roche Holdings Inc.), ингибиторов PI3-киназы дельта, Incozen (Incozen Therapeutics, Pvt. Ltd., Hydrabad, Индия), ингибиторов-2 PI3-киназы дельта, Инкозена (Incozen Therapeutics), ингибитора PI3-киназы, Roche-4 (Roche Holdings Inc.), ингибиторов PI3-киназы, Roche (Roche Holdings Inc.), ингибиторов PI3-киназы, Roche-5 (Roche Holdings Inc.), ингибиторов PI3-альфа/дельта, Pathway Therapeutics (Pathway Therapeutics Ltd., South San Francisco, CA), ингибиторов PI3-дельта, Cellzome (Cellzome AG, Heidelberg, Germany), ингибиторов PI3-дельта, Intellikine (Intellikine Inc., La Jolla, CA), ингибиторов PI3-дельта, Pathway Therapeutics-1 (Pathway Therapeutics Ltd.), ингибиторов PI3-дельта, Pathway Therapeutics-2 (Pathway Therapeutics Ltd.), ингибиторов PI3-дельта/гамма, Cellzome (Cellzome AG), ингибиторов PI3-дельта/гамма, Cellzome (Cellzome AG), ингибиторов PI3-дельта/гамма, Intellikine (Intellikine Inc.), ингибиторов PI3-дельта/гамма, Intellikine (Intellikine Inc.), ингибиторов PI3-дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторов PI3-дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибитора PI3-гамма Evotec (Evotec), ингибитора PI3-гамма, Cellzome (Cellzome AG), ингибиторов PI3-гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторов PI3K-дельта/гамма, Intellikine-1 (Intellikine Inc.), ингибиторов PI3K-дельта/гамма, Intellikine-1 (Intellikine Inc.), пиктилисиба (Roche Holdings Inc.), PIK-90 (CAS № 677338-12-4), SC-103980 (Pfizer, Нью-Йорк, NY), SF-1126 (Semafore Pharmaceuticals, Индианаполис, IN), SH-5, SH-6, тетрагидрокуркумина, TG100-115 (Targegen Inc., San Diego, CA), Трицирибина, X-339 (Xcovery, Уэст-Палм-Бич, FL), XL-499 (Evotech, Гамбург, Германия), их фармацевтически приемлемых солей и их комбинаций.
[0124] Согласно некоторым вариантам осуществления фармацевтическая композиция находится в единичной дозированной форме, содержащей как ингибитор ERK, так и дополнительное лекарственное средство.
[0125] Согласно некоторым вариантам осуществления фармацевтическая композиция ингибитора ERK находится в первой единичной дозированной форме и дополнительное лекарственное средство находится во второй единичной дозированной форме, отдельной от первой.
[0126] Согласно некоторым вариантам осуществления ингибитор ERK и дополнительное лекарственное средство вводят индивидууму совместно.
[0127] Согласно некоторым вариантам осуществления ингибитор ERK и дополнительное лекарственное средство вводят индивидууму последовательно.
[0128] Согласно некоторым вариантам осуществления ингибитор ERK вводят индивидууму до или после введения дополнительного лекарственного средства.
[0129] В соответствии с одним аспектом настоящее изобретение относится к способу лечения или смягчения эффектов злокачественной опухоли, имеющей мутацию BRAF не V600E/K, причем способ включает введение индивидууму эффективного количества BVD-523 или его фармацевтически приемлемой соли.
[0130] В соответствии с одним аспектом, настоящее изобретение относится к способу лечения или смягчения эффектов злокачественной опухоли у индивидуума, включающему: (a) идентификацию индивидуума со злокачественной опухолью, имеющей мутацию BRAF не V600E/K; и (b) введение индивидууму эффективного количества BVD-523 или его фармацевтически приемлемой соли.
[0131] В соответствии с одним аспектом, настоящее изобретение относится к способу идентификации индивидуума, имеющего злокачественную опухоль, для которого была бы полезна терапия BVD-523 или его фармацевтически приемлемой солью, причем способ включает: (a) получение биологического образца от индивидуума; и (b) скрининг образца для определения того, имеет ли индивидуум мутацию BRAF не V600E/K, где присутствие мутации BRAF не V600E/K подтверждает, что индивидууму была бы полезной терапия BVD-523 или его фармацевтически приемлемой солью.
[0132] В соответствии с одним аспектом настоящее изобретение относится к фармацевтической композиции для лечения или смягчения эффектов злокачественной опухоли у индивидуума, имеющей мутацию BRAF не V600E/K, причем композиция содержит фармацевтически приемлемый носитель или разбавитель и эффективное количество BVD-523 или его фармацевтически приемлемой соли.
[0133] В соответствии с одним аспектом настоящее изобретение относится к набору для лечения или смягчения эффектов злокачественной опухоли у индивидуума, имеющей мутацию BRAF не V600E/K, причем набор содержит фармацевтическую композицию по любому из п.п.88, 103 и 107, упакованную вместе с инструкциями по применению.
[0134] Согласно некоторым вариантам осуществления ингибитор RAF выбран из группы, состоящей из эрлотиниба (Тарцева), гефитиниба (Иресса), иматиниба мезилата (Гливек), лапатиниба (Тайверб), сунитиниба малата (Сутент), их фармацевтически приемлемых солей и их комбинаций.
[0135] Согласно некоторым вариантам осуществления ингибитор RAF выбран из группы, состоящей из LXH254 (Novartis), PLX3603 (Daiichi Sankyo), PLX8394 (Daiichi Sankyo), REDX0535 (RedX Pharma Plc), их фармацевтически приемлемых солей и их комбинаций.
[0136] Согласно некоторым вариантам осуществления ингибитор HDAC выбран из группы, состоящей из Вориностата, Панобиностата, Ромидепсина, Белиностата, их фармацевтически приемлемых солей и их комбинаций.
[0137] Согласно некоторым вариантам осуществления антитело, его фрагмент или их конъюгат выбран из группы, состоящей из ритуксимаба (Ритуксан), Брентуксимаба Ведотина (Адцетриз), Адотрастузумаба эмтансина (Кадсила), Ипилимумаба (Ервой), Ниволумаба (Опдиво), пембролизумаба (Кейтруда), Алемтузумаба атезолизумаба (Тецентрик), дурвалумаба (Имфинзи), Офатумумаба, Обинутузумаба (Газива), Панитумумаба и их комбинаций.
[0138] Согласно некоторым вариантам осуществления ингибитор каскада PI3K/Akt представляет собой BVD-723.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0139] На фиг.1 представлена схема каскада митоген-активируемых протеинкиназ (MAPK).
[0140] На фиг.2 представлен ответ у пациентов, которым вводили BVD-523. Включены все пациенты с заболеванием, определенным в соответствии с RECIST v1.1, которым проводили введение одной дозы или более исследуемого лекарственного средства и более 1 оценки опухоли в ходе лечения. Ответ определяли в качестве изменения от исходного уровня суммы наибольших диаметров каждого очага повреждения, являющегося мишенью. Сплошной линией указано пороговое значение для частичного ответа в соответствии с RECIST v1.1. Сокращенные обозначения: GBM, глиобластома; NSCLC, немелкоклеточный рак легкого; CRC, рак ободочной и прямой кишки. Указана атипичная мутация BRAF, ассоциированная со злокачественной опухолью каждого пациента.
[0141] На фиг.3 представлена длительность лечения на графике "дорожек бассейна", распределенная по группам. Члены 1 группы представляют собой любых пациентов с любой мутацией BRAF в любом типе опухоли, отличном от рака ободочной и прямой кишки (CRC) и немелкоклеточной карциномы легких (NSCLC), и которых ранее лечили ингибитором каскада MAPK. Члены 2 группы представляют собой пациентов с любой мутацией BRAF в CRC, которых ранее не лечили ингибитором каскада MAPK. Члены 3 группы представляют собой пациентов, имеющих мутацию BRAF V600E/K, которые рефрактерны к ингибитору MAPK. Члены 6 группы представляют собой пациентов с любой мутацией BRAF, присутствующей в NSCLC. Как показано на фиг.3, включены все 28 пациентов, как показано горизонтальными столбиками, по одному для каждого индивидуума. Длительность лечения для каждого индивидуума в каждой группе проиллюстрирована сверху (наибольшая длительность лечения) вниз (наименьшая длительность лечения) по группам. По горизонтальной оси представлена длительность в сутках нахождения индивидуума в исследовании. На фиг.3 также представлен тип ответа, достигнутый каждым пациентом в соответствии с RECIST v1.1 (ромб=частичный ответ; круг=стабильное заболевание; вертикальный столбик=прогрессирующее заболевание; треугольник=оценка не проводилась).
[0142] На фиг.4 представлена длительность лечения на графике "дорожек бассейна" в соответствии с мутацией BRAF. Включены все 28 пациентов, у которых определены критерии ответа RECIST v1.1, плюс дополнительные пациенты, которых не оценивали посредством RECIST v1.1 (ромб=частичный ответ; круг=стабильное заболевание; вертикальный столбик=прогрессирующее заболевание; треугольник=оценка не проводилась).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0143] В соответствии с одним аспектом, настоящее изобретение относится к способу лечения или смягчения эффектов злокачественной опухоли у индивидуума, имеющей мутацию BRAF не V600E/K, включающему введение индивидууму эффективного количества ингибитора ERK или его фармацевтически приемлемой соли.
[0144] Как используют в рамках изобретения, термины "мутация BRAF V600E/K", относящиеся к злокачественной опухоли у индивидуума, и их грамматические варианты означают злокачественную клетку, которая содержит мутацию с несинонимической заменой в гене, кодирующем BRAF человека (SEQ ID NO:2), которая вызывает замену аминокислоты валина (V) в положении аминокислоты 600 BRAF на глутаминовую кислоту (E) или лизин (K). Как используют в рамках изобретения, термины "содержащий мутацию BRAF не V600E/K", относящиеся злокачественной опухоли у индивидуума, и его грамматические варианты означают, что злокачественная клетка содержит соматическую мутацию клетки, которая не является мутацией BRAF V600E/K. Как используют в рамках изобретения, все мутации BRAF основаны на последовательности дикого типа человека (SEQ ID NO: 2). Также в рамках настоящего описания предусматриваются их ортологи из других видов.
[0145] Как используют в рамках изобретения, термины "лечить", "лечащий", "лечение" и их грамматические варианты означают проведение у индивидуума протокола, режима, процесса или способа лечения, при которых желательно достигнуть физиологического ответа или исхода у этого индивидуума, например, пациента. В частности, способы и композиции по настоящему изобретению можно использовать для замедления развития симптомов заболевания или замедления возникновения заболевания или состояния, и остановки прогрессирования развития заболевания. Однако, поскольку каждый подвергаемый лечению индивидуум может не отвечать на конкретный протокол лечения, режим, процесс или способ лечения, лечение не требует, чтобы желаемый физиологический ответ или исход достигался у каждого индивидуума или в каждой популяции индивидуумов, например, популяции пациентов. Таким образом, данный индивидуум или популяция индивидуумов, например, популяция пациентов, может не отвечать или недостаточно отвечать на лечение.
[0146] Как используют в рамках изобретения, термины "смягчать", "смягчение" и их грамматические варианты означают снижение тяжести симптомов заболевания у индивидуума.
[0147] Как используют в рамках изобретения, "индивидуум" представляет собой млекопитающего, предпочтительно, человека. В дополнение к людям, категории млекопитающих, входящих в объем настоящего изобретения, включают, например, сельскохозяйственных животных, домашних животных, лабораторных животных и т.д. Некоторые примеры сельскохозяйственных животных включают коров, свиней, лошадей, коз и т.д. Некоторые примеры домашних животных включают собак, кошек, и т.д. Некоторые примеры лабораторных животных включают приматов, крыс, мышей, кроликов, морских свинок и т.д.
[0148] Как используют в рамках изобретения, термин "эффективное количество" или "терапевтически эффективное количество" соединения или композиции, описанных в настоящем описании, представляет собой количество такого соединения или композиции, которое является недостаточным для обеспечения полезных или желательных результатов, как описано в настоящем описании, при введении человеку. Эффективные дозированные формы, способы введения и дозировки можно определять эмпирически, и проведение таких определений входит в пределы квалификации в данной области. Специалистам в данной области понятно, что дозировка будет варьироваться в зависимости от пути введения, скорости экскреции, длительности лечения, типа каких-либо других вводимых лекарственных средств, возраста, размера и вида млекопитающего, например, пациента-человека, и подобных факторов, хорошо известных в области медицины и ветеринарной медицины. Как правило, подходящая доза соединения или композиции по изобретению будет представлять собой количество композиции, которое является наименьшей дозой, эффективной для обеспечения желаемого эффекта. Эффективную дозу соединения или композиции по настоящему изобретению можно вводить в качестве двух, трех, четырех, пяти, шести ил более субдоз, вводимых по отдельности с надлежащими интервалами на протяжении дня.
[0149] Согласно некоторым вариантам осуществления ингибитор ERK выбран из группы, состоящей из BVD-523, SCH-722984 (Merck & Co.), SCH-772984 (Merck & Co.), SCH-900353 (MK-8353) (Merck & Co.), LY3214996 (Lilly), AEZS-140 (Aeterna Zentaris), AEZS-131 (Aeterna Zentaris), AEZS-136 (Aeterna Zentaris), LTT-462 (Novartis), RG-7842 (Genentech), CC-90003 (Celgene), KIN-4050 (Kinentia) и их комбинаций. Согласно некоторым вариантам осуществления ингибитор ERK представляет собой BVD-523.
[0150] В рамках настоящего изобретения BVD-523 представляет собой соединение формулы (I):
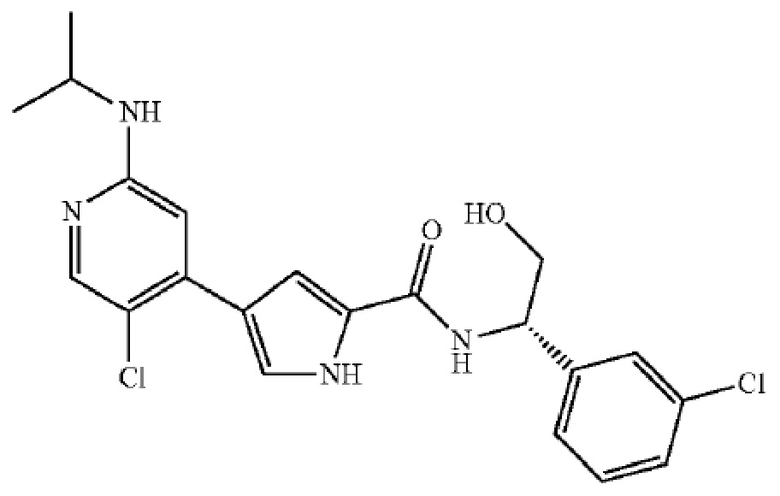
[0151] и его фармацевтически приемлемые соли. BVD-523 представляет собой высокоэффективный, селективный, обратимый, конкурирующий с ATP ингибитор ERK1/2. BVD-523 можно синтезировать способами, описанными, например, в патенте США № 7354939, который включен в настоящее описание в качестве ссылки. Также объем настоящего изобретения охватывает энантиомеры и рацемические смеси обоих энантиомеров BVD-523. BVD-523 представляет собой ингибитор ERK1/2 с механизмом действия, который, как полагают, является, например, уникальным и отличным от определенных других ингибиторов ERK1/2, таких как SCH772984. Например, другие ингибиторы ERK1/2, такие как SCH772984, ингибируют аутофосфорилирование ERK (Morris et al., 2013), в то время как BVD-523 позволяет аутофосфорилирование ERK, в то же время ингибируя ERK.
[0152] Согласно некоторым вариантам осуществления злокачественная опухоль индивидуума имеет соматическую мутацию в гене BRAF. Как используют в рамках изобретения, "соматическая мутация" означает изменение, происходящее в любой клетке, которая не призвана стать зародышевой клеткой. Мутация может представлять собой, например, замену, делецию, инсерцию или слияние. В таблице 1 ниже представлен обзор распределения мутаций BRAF, как показано в базе данных Sanger.
ТАБЛИЦА 1
[0153] Мутации BRAF встречаются приблизительно в 66% случаев меланомы (Davies et al., 2002; Brose et al., 2002; Hocket et al., 2007) и в относительно более низком проценте других злокачественных опухолей: в 36% опухолей щитовидной железы и в 10% случаев рака толстого кишечника (Xu et al., 2003; Fransen et al., 2004). Наиболее распространенная мутация BRAF возникает в положении аминокислоты 600 протеинкиназы дикого типа человека (SEQ ID NO: 2) посредством замещения валина на глутаминовую кислоту, что приводит к мутанту B-RafV600E, и она составляет приблизительно 80% мутаций BRAF (Davies et al., 2002; Hocker et al., 2007). Киназный домен B-RafV600E обладает в 500 раз более высокой киназной активностью по сравнению с базальной активностью B-Raf дикого типа (Wan et al., 2004). Среди других мутаций BRAF, идентифицированных при меланоме, также частыми являются V600K и V600D/R, и они составляют 16% и 3% всех мутаций BRAF, соответственно (Long et al., 2011). В дополнение к меланоме, мутации BRAF также являются частыми при многих других злокачественных опухолях, включая папиллярную карциному щитовидной железы, карциному яичника и карциному ободочной и прямой кишки. (Wellbrock et al., 2004). В одном исследовании варианты сплайсинга BRAF (с вырезанием путем сплайсинга экзонов 14 и 15) были найдены в 5/24 (21%) клеточных линий рака ободочной и прямой кишки (Seth et al., 2009).
[0154] В таблице 2 ниже из базы данных Sanger представлено распределение и частота мутаций BRAF в опухолях человека.
ТАБЛИЦА 2
[0155] В таблице 3 ниже представлены отдельные последовательности нуклеиновых кислот и аминокислотные последовательности BRAF. Эти последовательности можно использовать в способах идентификации индивидуумов с мутантным генотипом BRAF (как в способах, описанных ниже).
ТАБЛИЦА 3
[0156] Способы идентификации мутаций в нуклеиновых кислотах, таких как указанные выше гены BRAF, известны в данной области. Нуклеиновые кислоты можно получать из биологических образцов. В рамках настоящего изобретения биологические образцы включают, но не ограничиваются ими, кровь, плазму, мочу, кожу, слюну и биоптаты. Биологические образцы получают от индивидуума с использованием стандартных методик и способов, которые известны в данной области.
[0157] Неограничивающие примеры способов идентификации мутаций включают ПЦР, секвенирование, гибридную ловушку, улавливание в растворе, инвертируемый молекулярный зонд, анализы с использованием флуоресцентной гибридизации in situ (FISH) и их комбинации.
[0158] В данной области известны различные способы секвенирования. Они включают, но не ограничиваются ими, секвенирование по методу Сэнгера (также называемое дидезоксисеквенированием) и различные способы секвенирования посредством синтеза (SBS), как описано, например, в Metzker 2005, секвенирование посредством гибридизации, лигирования (например, WO 2005021786), деградации (например, патенты США № 5622824 и 6140053) и секвенирование с использованием нанопор (которое является коммерчески доступным от Oxford Nanopore Technologies, Великобритания). В способах глубинного секвенирования данный нуклеотид в последовательности считывается более одного раза в ходе секвенирования. Способы глубинного секвенирования описаны, например, в публикации патента США № 20120264632 и международной публикации патента № WO2012125848.
[0159] Способы на основе ПЦР для детекции мутаций известны в данной области и в них используется ПЦР-амплификация, где каждая последовательность-мишень в образце имеет соответствующую пару уникальных последовательность-специфических праймеров. Например, способ полимеразной цепной реакции с полиморфизмом длин рестрикционных фрагментов (ПЦР-RFLP) позволяет быструю детекцию мутаций после амплификации геномных последовательностей способом ПЦР. Мутацию обнаруживают путем расщепления специфическими эндонуклеазами рестрикции и идентифицируют путем электрофореза. См., например, Ota et al., 2007. Мутации также можно выявлять с использованием ПЦР с детекцией в реальном времени. См., например, публикацию международной заявки № WO2012046981.
[0160] Способы гибридной ловушки известны в данной области и описаны, например, в публикации патента США № 20130203632 и патентах США № 8389219 и 8288520. Эти способы основаны на селективной гибридизации геномных областей-мишеней со сконструированными пользователем олигонуклеотидами. Гибридизация может быть осуществлена с олигонуклеотидами, иммобилизованными на микрочипах высокой или низкой плотности (улавливание на чипе), или посредством гибридизации в фазе раствора с олигонуклеотидами, модифицированными лигандом (например, биотин), которые впоследствии могут быть иммобилизованы на твердой поверхности, такой как гранула (гибридизация в растворе).
[0161] Способы с инвертируемым молекулярным зондом (MIP) известны в данной области и описаны, например, в Absalan et al., 2008. В таких способах используются молекулы MIP, которые являются специализированными зондами типа "навесной замок" (Nilsson et al., 1994), для генотипирования. Молекула MIP представляет собой линейный олигонуклеотид, который содержит специфические области, универсальные последовательности, участки рестрикции и последовательность метки (маркерная) (16-22 п.н.). В таких способах MIP гибридизуется непосредственно в области представляющего интерес генетического маркера/SNP. В способе MIP также может использоваться ряд наборов зондов типа "навесной замок", которые гибридизуются с геномной ДНК параллельно (Hardenbol et al., 2003). В случае абсолютного соответствия, области геномной гомологии лигируются, претерпевая инверсию конфигурации (на что указывает название технологии) и создавая кольцевую молекулу. После первой рестрикции все молекулы амплифицируют с универсальными праймерами. Ампликоны рестрицируют вновь, обеспечивая короткие фрагменты для гибридизации на микрочипе. Полученные короткие фрагменты метят и через последовательность метки гибридизуют с cTag (комплементарная цепь для маркера) на чипе. После образования дуплекса Tag-cTag сигнал детектируется.
[0162] Согласно некоторым вариантам осуществления мутация BRAF не V600E/K представляет собой активирующую киназу мутацию, нарушающую функцию киназы мутацию или мутацию с неизвестным действием на киназу, и их комбинации. Как используют в рамках изобретения, термин "активирующая киназу мутация" и его грамматические варианты означает, что мутация вызывает повышение киназной активности мутантной киназы относительно киназы дикого типа. Как используют в рамках изобретения, термин "нарушающая функцию киназы мутация" и его грамматические варианты означает, что мутация вызывает снижение киназной активности мутантной киназы относительно киназы дикого типа. Как используют в рамках изобретения, термин "мутация с неизвестным действием на киназу" и его грамматические варианты означает, что активность мутантной киназы неизвестна или что активность мутантной киназы приблизительно эквивалентна киназной активности киназы дикого типа (см. Zheng, G., et al., Clinical detection and categorization of uncommon and concomitant mutations involving BRAF, BMC Cancer, (2015) 15:779, включенную в настоящее описание в качестве ссылки в полном объеме).
[0163] Согласно некоторым вариантам осуществления активирующая мутация BRAF-киназы выбрана из группы, состоящей из R462I, I463S, G464E, G464R, G464V, G466A, G469A, N581S, E586K, F595L, L597Q, L597R, L597S, L597V, A598V, T599E, V600R, K601E, S602D, A728V и их комбинаций. Согласно некоторым вариантам осуществления нарушающая функцию киназы мутация BRAF выбрана из группы, состоящей из G466E, G466R, G466V, Y472C, K483M, D594A, D594E, D594G, D594H, D594N, D594V, G596R, T599A, S602A и их комбинаций. Согласно некоторым вариантам осуществления мутация с неизвестным действием на киназу BRAF выбрана из группы, состоящей из T440I, S467L, G469E, G469R, G469S, G469V, L584F, L588F, V600_K601delinsE, S605I, Q609L, E611Q и их комбинаций. Как используют в рамках изобретения, все мутации BRAF основаны на последовательности дикого типа человека (SEQ ID NO: 2). Также в рамках настоящего описания предусматриваются их ортологи из других видов.
[0164] В рамках настоящего изобретения способ и композиция для лечения мутаций BRAF не V600E/K являются эффективными против болезненных состояний, которые имеют единичную мутацию и одну или несколько мутаций. Действительно, любые единичные мутации или любую комбинацию мутаций, описанную в настоящем описании (или указанную далее) можно лечить с использованием композиций или в соответствии со способами по настоящему изобретению (например, любую комбинацию мутаций не V600E/K или любую комбинацию мутации не V600E/K с мутацией V600E/K).
[0165] Согласно некоторым вариантам осуществления мутация BRAF не V600E/K выбрана из группы, состоящей из D594, G469, K601E, L597, дупликации T599, L485W, F247L, G466V, слияния BRAF, перестроения BRAF-AGAP3, варианта сплайсинга экзона 15 BRAF и их комбинаций.
[0166] Как используют в рамках изобретения, обозначение мутации с заменой аминокислоты включает следующий законченный формат: аминокислота дикого типа; положение; замещающая аминокислота (например, K601E). Как используют в рамках изобретения, обозначение аминокислотной замены также включает следующий открытый формат: аминокислота дикого типа; положение (например, G469). Как используют в рамках изобретения, открытое обозначение включает замены на любую аминокислоту. Например, мутация G469 относится к замене глицина в положении 469 любыми из аминокислот A, R, N, D, C, Q, E, H, I, L, K, M, F, P, S, T, W, Y, V. Также, как используют в рамках изобретения, закрытое обозначение включает замены на любую аминокислоту и предпочтительно на указанную замещающую аминокислоту. Например, мутация K601E относится к замене лизина в положении 601 на любую из аминокислот A, R, N, D, C, Q, E, G, H, I, L, M, F, P, S, T, W, Y, V, и более предпочтительно на аминокислоту E. Использование закрытого обозначения, как используют в рамках изобретения, не следует истолковывать как ограничивающее описание конкретной указанной аминокислотной заменой.
[0167] Согласно некоторым вариантам осуществления индивидуумом, имеющим злокачественную опухоль, имеющую мутацию BRAF не V600E/K, является млекопитающее. Согласно некоторым вариантам осуществления млекопитающее выбрано из группы, состоящей из людей, приматов, сельскохозяйственных животных и домашних животных. Согласно некоторым вариантам осуществления млекопитающим является человек.
[0168] В соответствии с некоторыми аспектами настоящее изобретение относится как к солидным, так и к гематологическим злокачественным опухолям. Неограничивающие примеры солидных злокачественных опухолей включают карциному надпочечников, рак анального канала, рак мочевого пузыря, рак кости (такой как остеосаркома), злокачественную опухоль головного мозга, рак молочной железы, карциноидную опухоль, карциному, рак шейки матки, рак толстого кишечника, рак эндометрия, рак пищевода, внепеченочный рак желчных протоков, семейство злокачественных опухолей Юинга, экстракраниальный рак из зародышевых клеток, рак глаза, рак желчного пузыря, рак желудка, опухоль зародышевых клеток, гестационную трофобластическую опухоль, рак головы и шеи, гипофарингеальный рак, карциному островковых клеток, рак почки, рак толстого кишечника, рак гортани, лейкоз, рак губ и полости рта, опухоль/рак печени, опухоль/рак легкого, лимфому, злокачественную мезотелиому, карциному из клеток Меркеля, фунгоидный микоз, миелодиспластический синдром, миелопролиферативные нарушения, назофарингеальный рак, нейробластому, рак полости рта, рак ротоглотки, остеосаркому, эпителиальный рак яичника, рак зародышевых клеток яичника, рак поджелудочной железы, рак околоносовых пазух и полости носа, рак паращитовидной железы, рак полового члена, рак гипофиза, новообразование из плазмацитов, рак предстательной железы, рабдомиосаркому, рак прямой кишки, почечно-клеточный рак, переходно-клеточный рак почечной лоханки и мочеточника, рак слюнных желез, синдром Сезари, злокачественные опухоли кожи (такие как Т-клеточная лимфома кожи, саркома Капоши, опухоль из тучных клеток и меланома), рак тонкого кишечника, саркому мягких тканей, рак желудка, рак яичка, тимому, рак щитовидной железы, рак уретры, рак тела матки, рак влагалища, рак вульвы и опухоль Вильмса.
[0169] Примеры гематологических злокачественных опухолей включают, но не ограничиваются ими, лейкозы, такие как взрослый/детский острый лимфобластный лейкоз, взрослый/детский острый миелоидный лейкоз, хронический лимфоцитарный лейкоз, хронический миелогенный лейкоз и волосатоклеточный лейкоз, лимфомы, такие как СПИД-связанная лимфома, Т-клеточная лимфома кожи, взрослая/детская лимфома Ходжкина, фунгоидный микоз, взрослая/детская неходжкинская лимфома, первичная лимфома центральной нервной системы, синдром Сезари, Т-клеточная лимфома кожи и макроглобулинемия Вальденстрема, а также другие пролиферативные нарушения, такие как хронические миелопролиферативные нарушения, гистиоцитоз из клеток Лангерганса, множественная миелома/новообразование из плазмацитов, миелодиспластические синдромы и миелодиспластические/миелопролиферативные новообразования.
[0170] Согласно некоторым вариантам осуществления злокачественная опухоль индивидуума выбрана из группы, состоящей из глиобластомы, меланомы, холангиокарциномы, мелкоклеточного рака легкого, рака ободочной и прямой кишки, рака предстательной железы, рака влагалища, ангиосаркомы, немелкоклеточного рака легкого, рака аппендикса, плоскоклеточного рака, карциномы протоков слюнных желез, аденокистозной карциномы, рака тонкого кишечника и рака желчного пузыря. Предпочтительно, злокачественная опухоль выбрана из группы, состоящей из рака тонкого кишечника, немелкоклеточного рака легкого, рак желчного пузыря и плоскоклеточного рака.
[0171] В соответствии с некоторыми аспектами, настоящее изобретение относится к введению индивидууму по меньшей мере одного дополнительного ингибитора каскада митоген-активируемой протеинкиназы (MAPK). Согласно некоторым вариантам осуществления по меньшей мере одно дополнительное лекарственное средство выбрано из группы, состоящей из ингибитора MEK, ингибитора RAF, ингибитора HDAC, ингибитора ERK и их комбинаций.
[0172] Как используют в рамках изобретения, "ингибитор каскада митоген-активируемой протеинкиназы (MAPK)" представляет собой любое вещество, которое модулирует, например, снижает, активность, экспрессию или фосфорилирование белков в каскаде MAPK, что приводит к снижению роста клеток или увеличению гибели клеток.
[0173] Обзор каскадов MAPK млекопитающих представлен на фиг.1. Детали каскадов MAPK рассмотрены, например, в Akinleye et al., 2013. В кратком изложении, что касается модуля ERK1/2 на фиг.1 (светло-фиолетовая рамка), каскад передачи сигнала MAPK 1/2 активируется лигандом, связывающимся с рецепторными тирозинкиназами (RTK). Активированные рецепторы привлекают и фосфорилируют адапторные белки Grb2 и SOS, которые затем взаимодействуют с мембрана-связанной GTP-азой Ras и вызывают ее активацию. В ее активированной GTP-связанной форме Ras привлекает и активирует Raf-киназы (A-Raf, B-Raf и C-Raf/RaF-1). Активированные Raf-киназы активируют MAPK 1/2 (MKK1/2), которая в свою очередь катализирует фосфорилирование остатков треонина и тирозина в активирующей последовательности Thr-Glu-Tyr ERK1/2. Что касается модуля JNK/p38 (желтая рамка на фиг.1), вышерасположенные киназы MAP3K, такие как MEKK1/4, ASK1/2 и MLK1/2/3, активируют MAP2K3/6 (MKK3/6), MAP2K4 (MKK4) и MAP2K7 (MKK7). Затем эти MAP2K активируют протеинкиназы JNK, включая JNK1, JNK2 и JNK3, а также p38 α/β/γ/Δ. Для выполнения своих функций JNK активируют несколько факторов транскрипции, включая c-Jun, ATF-2, NF-ATc1, HSF-1 и STAT3. Что касается модуля ERK5 (синяя рамка на фиг.1), киназы выше MAP2K5 (MKK5) представляют собой MEKK2 и MEKK3. Наиболее охарактеризованной нижерасположенной мишенью MEK5 является ERK5, также известная как большая MAP-киназа 1 (BMK1), поскольку ее размер в два раза превышает размер других MAPK.
[0174] Неограничивающие примеры ингибиторов каскада MAPK включают ингибиторы RAS, ингибиторы RAF, ингибиторы MEK, ингибиторы ERK1/2, их фармацевтически приемлемые соли и их комбинации.
[0175] Как используют в рамках изобретения, "ингибитор RAS" означает вещества, которые (i) прямо взаимодействуют с RAS, например, путем связывания с RAS, и (ii) снижают экспрессию или активность RAS. Неограничивающие иллюстративные ингибиторы RAS включают, но не ограничиваются ими, ингибиторы фарнезилтрансферазы (например, такие как типифарниб и лонафарниб), низкомолекулярные соединения, содержащие фарнезильную группу (например, такие как салирасиб и TLN-4601), DCAI, как описано Maurer (Maurer et al., 2012), Kobe0065 и Kobe2602, как описано Shima (Shima et al., 2013), HBS 3 (Patgiri et al., 2011) и AIK-4 (Allinky).
[0176] Как используют в рамках изобретения, "ингибитор RAF" означает вещества, которые (i) прямо взаимодействуют с RAF, например, путем связывания с RAF и (ii) снижают экспрессию или активность RAF, например, такие как A-RAF, B-RAF и C-RAF (Raf-1). Неограничивающие иллюстративные ингибиторы RAF включают:
Соединение 7  (Li et al.),
(Li et al.),
Соединение 9  (Там же),
(Там же),
Соединение 10  (Там же),
(Там же),
Соединение 13 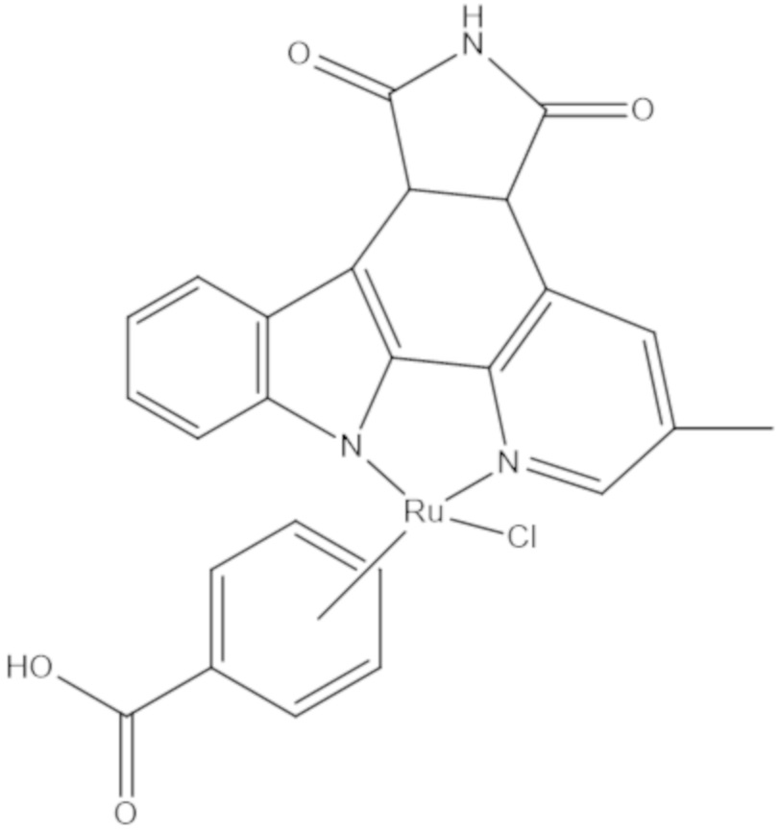 (Там же),
(Там же),
Соединение 14 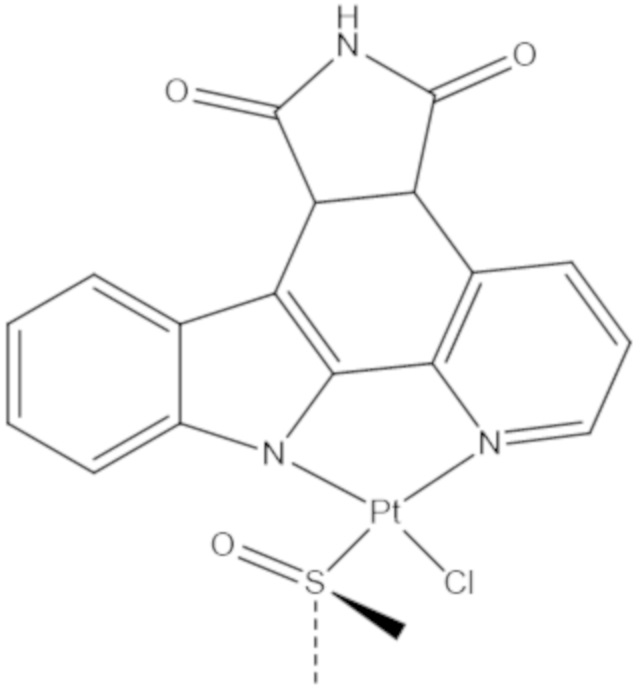 (Там же),
(Там же),
Соединение 15 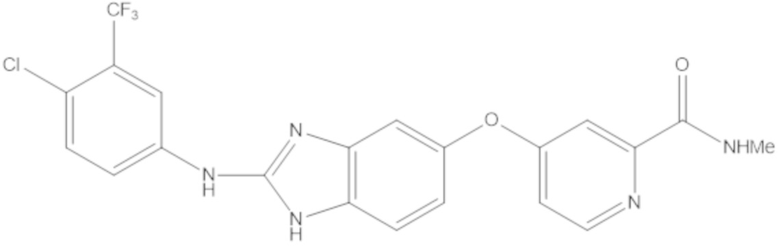 (Там же),
(Там же),
Соединение 16 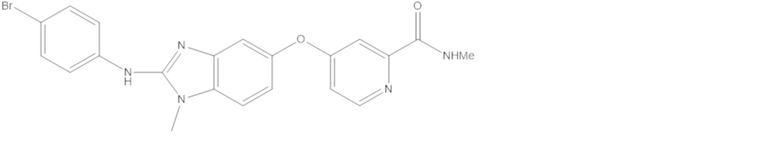 (Там же),
(Там же),
Соединение 18 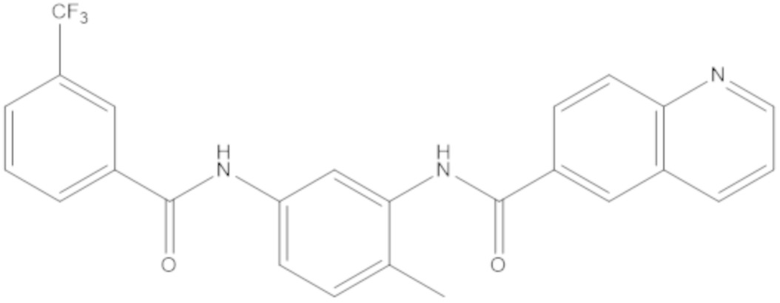 (Там же),
(Там же),
Соединение 19 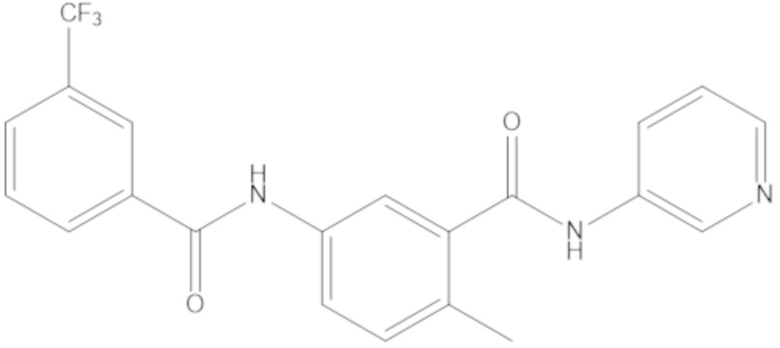 (Там же),
(Там же),
Соединение 20 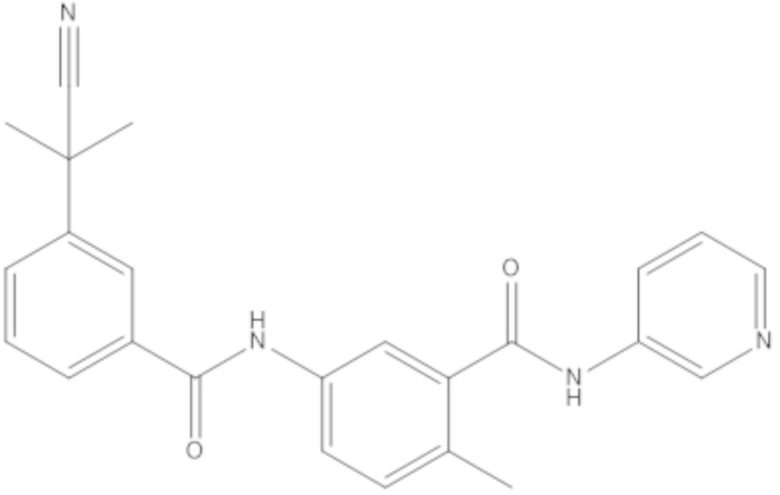 (Там же),
(Там же),
Соединение 21 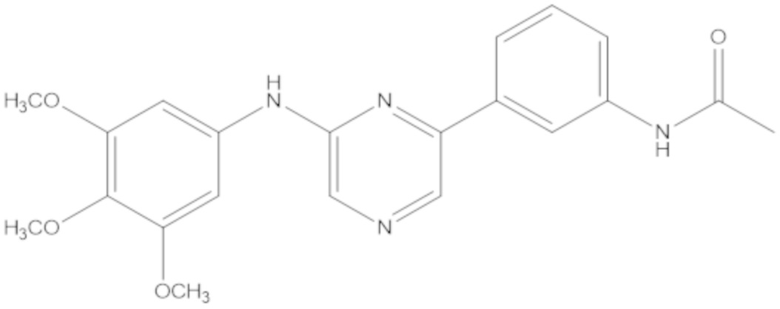 (Там же),
(Там же),
Соединение 22 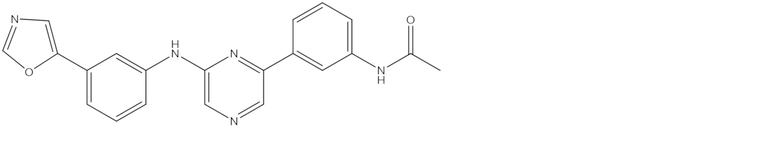 (Там же),
(Там же),
Соединение 23 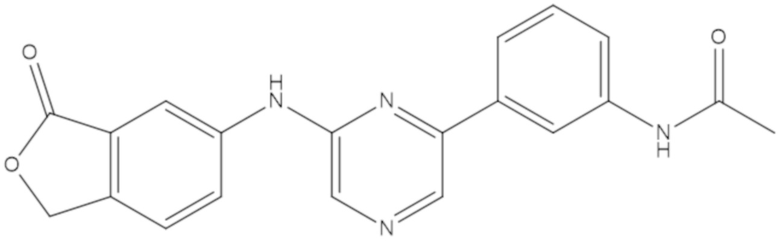 (Там же),
(Там же),
Соединение 24 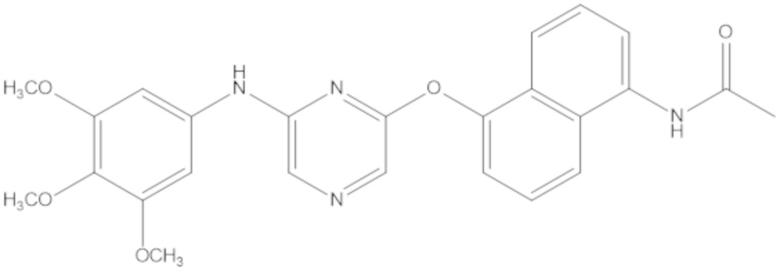 (Там же),
(Там же),
Соединение 25 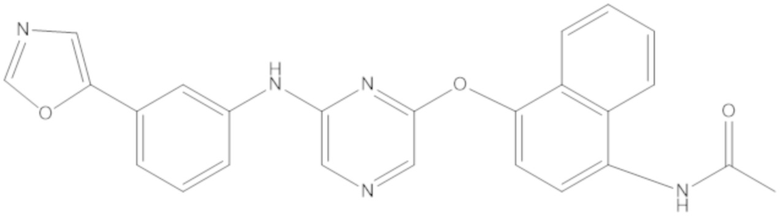 (Там же),
(Там же),
Соединение 26 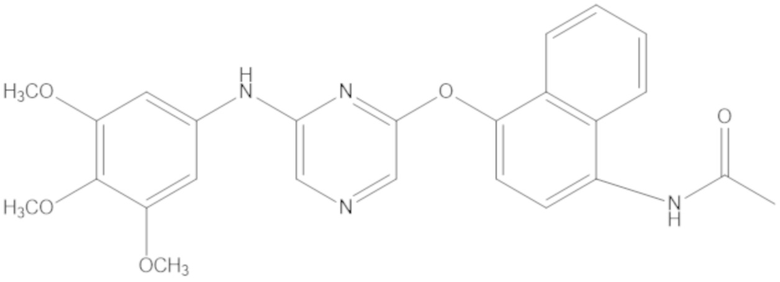 (Там же),
(Там же),
Соединение 27 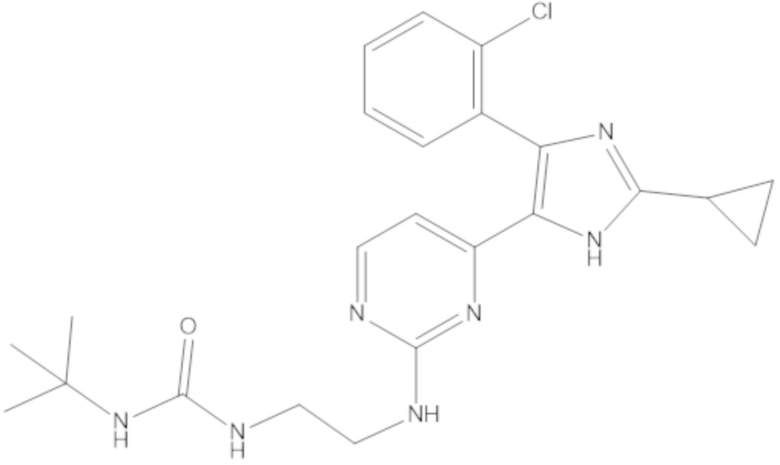 (Там же),
(Там же),
Соединение 28 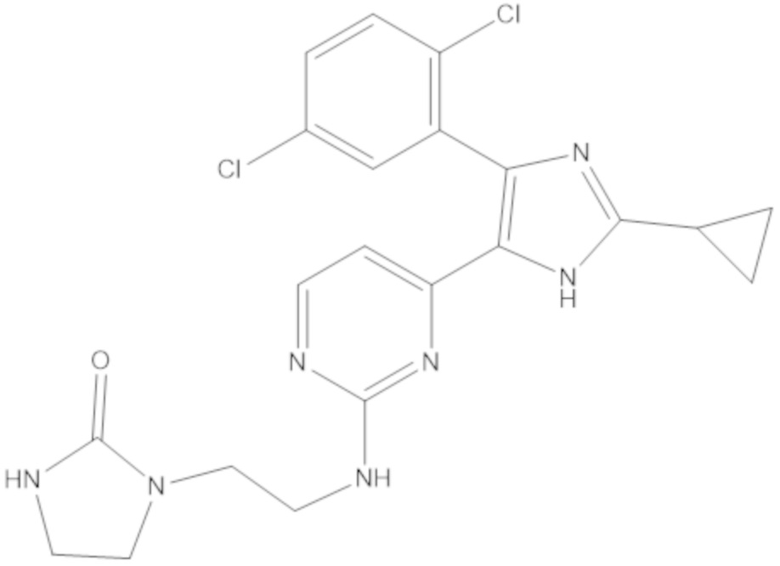 (Там же),
(Там же),
Соединение 30 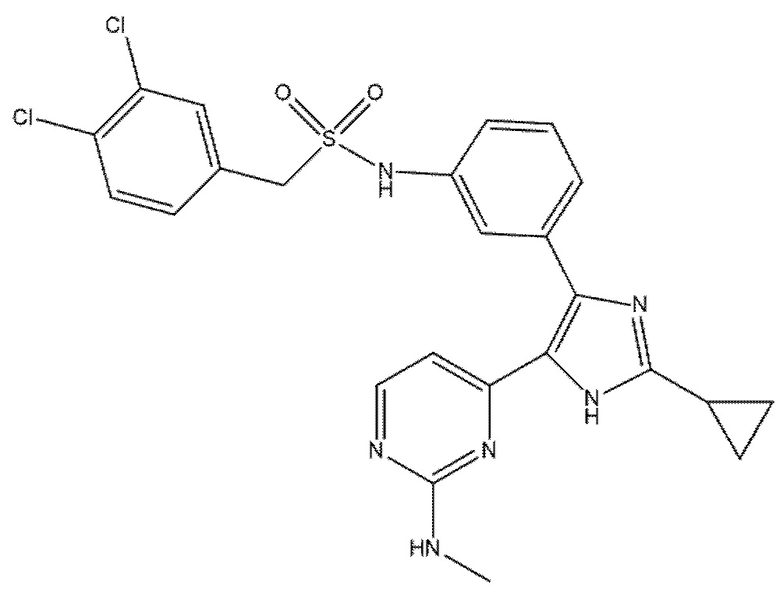 (Там же),
(Там же),
Соединение 31 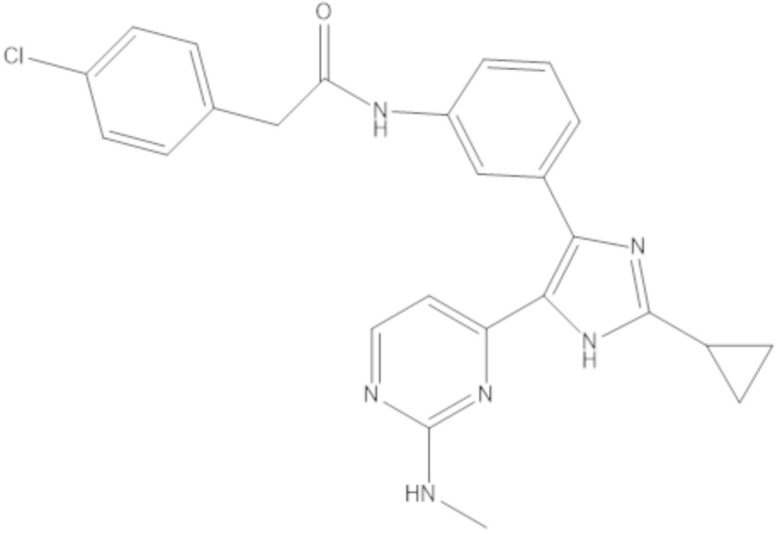 (Там же),
(Там же),
Соединение 32 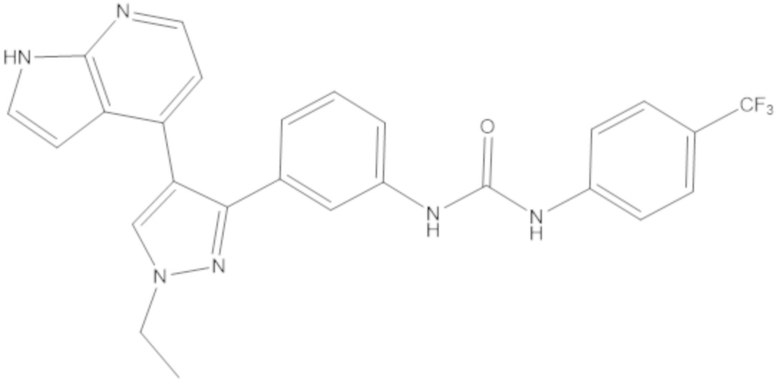 (Там же),
(Там же),
Соединение 33 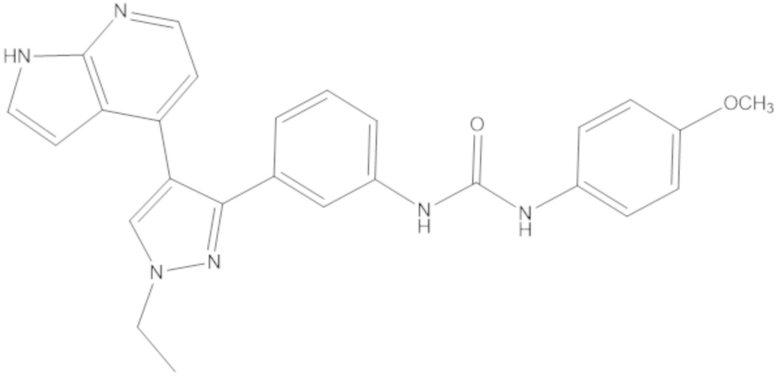 (Там же),
(Там же),
Соединение 34 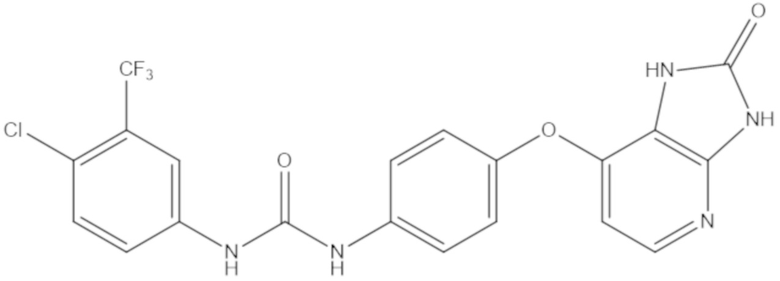 (Там же),
(Там же),
Соединение 35 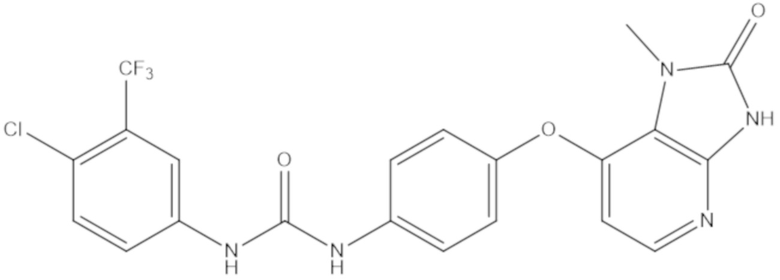 (Там же),
(Там же),
Соединение 36 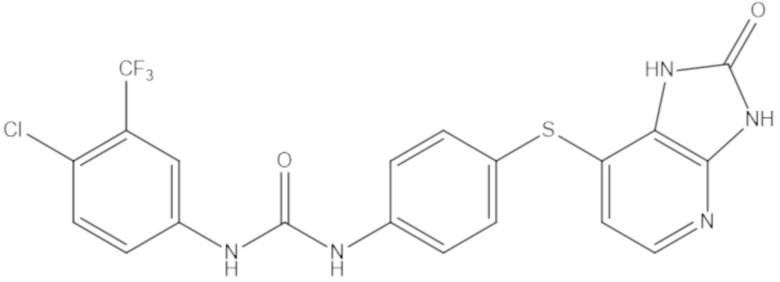 (Там же),
(Там же),
Соединение 37 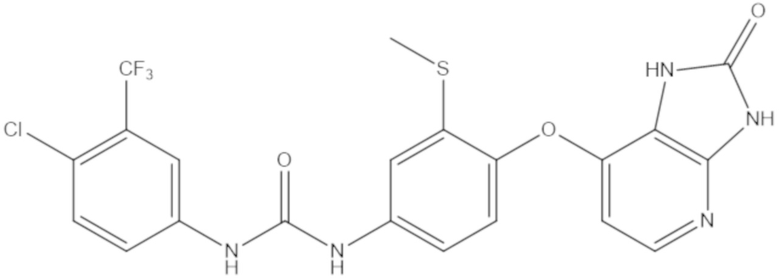 (Там же),
(Там же),
Соединение 38 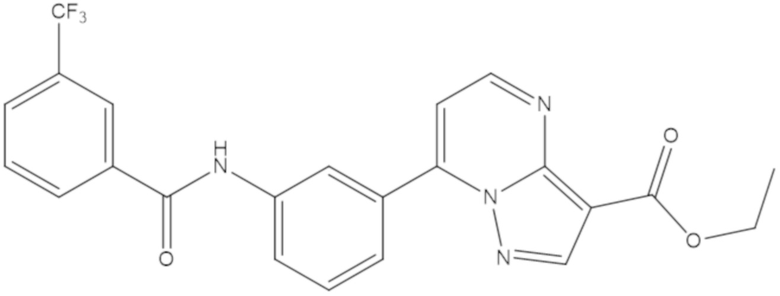 (Там же),
(Там же),
Соединение 39 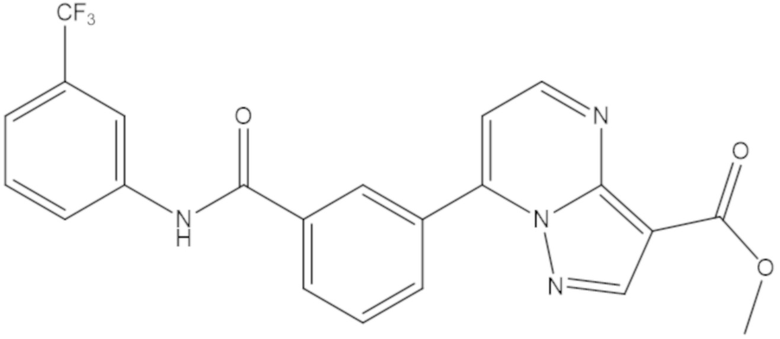 (Там же),
(Там же),
Соединение 40  (Там же),
(Там же),
[0177] AAL881 (Novartis); AB-024 (Ambit Biosciences), ARQ-736 (ArQule), ARQ-761 (ArQule), AZ628 (Axon Medchem BV), BAY 43-9006 сорафениб, BeiGene-283 (BeiGene), BUB-024 (MLN 2480) (Sunesis & Takeda), ингибитор b-raf (Sareum), ингибитор BRAF-киназы (Selexagen Therapeutics), миРНК BRAF 313 (tacaccagcaagctagatgca) и 523 (cctatcgttagagtcttcctg) (Liu et al., 2007), CHIR-265 (Novartis), CTT239065 (Institute of Cancer Research), дабрафениб (GSK2118436), DP-4978 (Deciphera Pharmaceuticals), HM-95573 (Hanmi), GDC-0879 (Genentech), GW-5074 (Sigma Aldrich), ISIS 5132 (Novartis), L779450 (Merck), LBT613 (Novartis), LXH254 (Novartis), LErafAON (NeoPharm, Inc.), LGX-818 (Novartis), пазопаниб (GlaxoSmithKline), PLX3202 (Plexxikon), PLX4720 (Plexxikon), PLX5568 (Plexxikon), PLX3603 (Daiichi Sankyo), PLX8394 (Daiichi Sankyo), RAF-265 (Novartis), RAF-365 (Novartis), REDX0535 (RedX Pharma Plc), регорафениб (Bayer Healthcare Pharmaceuticals, Inc.), RO 5126766 (Hoffmann-La Roche), SB-590885 (GlaxoSmithKline), SB699393 (GlaxoSmithKline), сорафениб (Onyx Pharmaceuticals), TAK 632 (Takeda), TL-241 (Teligene), вемурафениб (RG7204 или PLX4032) (Daiichi Sankyo), XL-281 (Exelixis), ZM-336372 (AstraZeneca), их фармацевтически приемлемые соли и их комбинации.
[0178] Согласно некоторым вариантам осуществления ингибиторы RAF включают общие ингибиторы, неограничивающие примеры которых включают эрлотиниб (Тарцева), гефитиниб (Иресса), иматиниб мезилат (Гливек), лапатиниб (Тайверб), сунитиниб малат (Сутент), их фармацевтически приемлемые соли и их комбинации.
[0179] Как используют в рамках изобретения, "ингибитор MEK" означает вещества, которые (i) прямо взаимодействуют с MEK, например, посредством связывания MEK, и (ii) снижают экспрессию или активность MEK. Таким образом, ингибиторы, которые действуют выше MEK, такие как ингибиторы RAS и ингибиторы RAF, не являются ингибиторами MEF в соответствии с настоящим изобретением. Неограничивающие примеры ингибиторов MEK включают токсин сибирской язвы, антрохинолол (Golden Biotechnology), ARRY-142886 ((2-гидроксиэтокси)амид 6-(4-бром-2-хлор-фениламино)-7-фтор-3-метил-3H-бензоимидазол-5-карбоновой кислоты) (Array BioPharma), ARRY-438162 (Array BioPharma) биниметиниба (MEK162, ARRY-1662), AS-1940477 (Astellas), AS-703988 (Merck KGaA), бентамапимод (Merck KGaA), BI-847325 (Boehringer Ingelheim), E-6201 (Eisai), GDC-0623 (Hoffmann-La Roche), GDC-0973 (кобиметиниб) (Hoffmann-La Roche), L783277 (Merck), часть токсина сибирской язвы, являющуюся летальным фактором, MEK162 (Array BioPharma), PD 098059 (2-(2'-амино-3'-метоксфенил)оксанафталин-4-он) (Pfizer), PD 184352 (CI-1040) (Pfizer), PD-0325901 (Pfizer), PD318088 (Pfizer), PD334581 (Pfizer), 6-метокси-7-(3-морфолин-4-илпропокси)-4-(4-феноксифениламино)хинолин-3-карбонитрил, 4-[3-хлор-4-(1-метил-1H-имидазол-2-илсульфанил)фениламино]-6-метокси-7-(3-морфолин-4-илпропокси)хинолин-3-карбонитрил, пимасертиб (Santhera Pharmaceuticals), RDEA119 (Ardea Biosciences/Bayer), рефаметиниб (AstraZeneca), RG422 (Chugai Pharmaceutical Co.), R0092210 (Roche), R04987655 (Hoffmann-La Roche), R05126766 (Hoffmann-La Roche), селуметиниб (AZD6244) (AstraZeneca), SL327 (Sigma), TAK-733 (Takeda), траметиниб (Japan Tobacco), U0126 (1,4-диамино-2,3-дициано-1,4-бис(2-аминофенилтио)бутадиен) (Sigma), WX-554 (Wilex), полипептид YopJ (Mittal et al., 2010), их фармацевтически приемлемую соль и их комбинацию.
[0180] Как используют в рамках изобретения, "ингибитор ERK1/2" означает вещества, которые (i) прямо взаимодействуют с ERK1 и/или ERK2, например, путем связывания с ERK1/2, и (ii) снижают экспрессию или активность протеинкиназ ERK1 и/или ERK2. Таким образом, ингибиторы, которые действуют выше ERK1/2, такие как ингибиторы MEK и ингибиторы RAF, не являются ингибиторами ERK1/2 в соответствии с настоящим изобретением. Неограничивающие примеры ингибитора ERK1/2 включают AEZS-131 (Aeterna Zentaris), AEZS-136 (Aeterna Zentaris), BVD-523, SCH-722984 (Merck & Co.), SCH-772984 (Merck & Co.), SCH-900353 (MK-8353) (Merck & Co.), LY3214996 (Lilly), их фармацевтически приемлемые соли и их комбинации.
[0181] Как используют в рамках изобретения, "ингибитор HDAC" означает вещества, которые (i) прямо взаимодействуют с деацетилазой гистонов (HDAC), например, путем связывания с HDAC, и (ii) снижают экспрессию или активность HDAC. Неограничивающие примеры ингибиторов HDAC включают Абексиностат (PCI-24781), Гивиностат, Энтиностат, Вориностат, CI-994, CUDC-101 Энтиностат, BML-210, M344, NVP-LAQ824, Панобиностат, Прациносат (SB939), Моцетиностат, Ресминостат, Ромидепсин, Белиностат, их фармацевтически приемлемые соли и их комбинации.
[0182] Согласно некоторым вариантам осуществления ингибитор HDAC выбран из группы, состоящей из Вориностата, Панобиностата, Ромидепсина, Белиностата, их фармацевтически приемлемых солей и их комбинаций.
[0183] В другом аспекте способ дополнительно включает введение индивидууму по меньшей мере одного дополнительного лекарственного средства, эффективного для лечения или смягчения эффектов злокачественной опухоли. Дополнительное лекарственное средство может быть выбрано из группы, состоящей из антитела, фрагмента антитела, конъюгата антитела, цитотоксического средства, токсина, радионуклида, иммуномодулятора, фотоактивного лекарственного средства, радиосенсибилизирующего средства, гормона, антиангиогенного средства и их комбинаций.
[0184] Как используют в рамках изобретения, "антитело" охватывает встречающиеся в природе иммуноглобулины, а также не встречающиеся в природе иммуноглобулины, включая, например, одноцепочечные антитела, химерные антитела (например, гуманизированные антитела мыши) и гетероконъъюгаты антител (например, биспецифические антитела). Фрагменты антител включают фрагменты, которые связывают антиген (например, Fab', F(ab')2, Fab, Fv и rIgG). Также см., например, Pierce Catalog and Handbook, 1994-1995 (Pierce Chemical Co., Rockford, Ill.); Kuby, J., Immunology, 3rd Ed., W.H.Freeman & Co., Нью-Йорк (1998). Термин "антитело" также включает двухвалентные или биспецифические молекулы, диантитела, триантитела и тетраантитела. Термин "антитело", кроме того, включает как поликлональные, так и моноклональные антитела.
[0185] Примеры терапевтических антител, которые можно использовать в рамках настоящего изобретения, включают ритуксимаб (Ритуксан), Брентуксимаб Ведотин (Адцетриз), Адотрастузумаб эмтансин (Кадсила), Цетуксимаб (Эрбитукс), бевацизумаб (Авастин), Ибритумомаб (Зевалин), ведолизумаб (Энтивио), Ипилимумаб (Ервой), Ниволумаб (Опдиво), пембролизумаб (Кейтруда), Алемтузумаб атезолизумаб (Тецентрик), авелумаб (Бавенцио), дурвалумаб (Имфинзи), B-701, Офатумумаб, Обинутузумаб (Газива), Панитумумаб, плозализумаб, BI-754091, OREG-103, COM-701, BI-754111 и их комбинации.
[0186] Согласно некоторым вариантам осуществления антитело, его фрагмент или их конъюгат выбран из группы, состоящей из ритуксимаба (Ритуксан), Брентуксимаба Ведотина (Адцетриз), Адотрастузумаба эмтансина (Кадсила), Ипилимумаба (Ервой), Ниволумаба (Опдиво), пембролизумаб (Кейтруда), Алемтузумаба атезолизумаба (Тецентрик), дурвалумаба (Имфинзи), Офатумумаба, Обинутузумаба (Газива), Панитумумаба и их комбинаций.
[0187] Цитотоксические средства в соответствии с настоящим изобретением включают повреждающие ДНК средства, антиметаболиты, средства, направленные против микротрубочек, антибиотики и т.д. Повреждающие ДНК средства включают алкилирующие средства, средства на основе платины, интеркалирующие средства и ингибиторы репликации ДНК. Неограничивающие примеры алкилирующих ДНК средств включают циклофосфамид, мехлорэтамин, урамустин, мелфалан, хлорамбуцил, ифосфамид, кармустин, ломустин, стрептозоцин, бусульфан, темозоломид, их фармацевтически приемлемые соли, их пролекарства и комбинации. Неограничивающие примеры средств на основе платины включают цисплатин, карбоплатин, оксалиплатин, недаплатин, сатраплатин, триплатина тетранитрат, их фармацевтически приемлемые соли, пролекарства и комбинации. Неограничивающие примеры интеркалирующих средств включают доксорубицин, даунорубицин, идарубицин, митоксантрон, их фармацевтически приемлемые соли, пролекарства и их комбинации. Неограничивающие примеры ингибиторов репликации ДНК включают иринотекан, топотекан, амсакрин, этопозид, этопозида фосфат, тенипозид, их фармацевтически приемлемые соли, пролекарства и комбинации. Антиметаболиты включают антагонисты фолатов, такие как метотрексат и преметрексед, антагонисты пуринов, такие как 6-меркаптопурин, дакарбазин и флударабин, и антагонисты пиримидинов, такие как 5-фторурацил, арабинозилцитозин, капецитабин, гемцитабин, децитабин, их фармацевтически приемлемые соли, пролекарства и их комбинации. Средства, направленные против микротрубочек, включают, но не ограничиваются ими, алкалоиды барвинка, паклитаксел (Таксол®), доцетаксел (Таксотер®) и иксабепилона (Икземпра®). Антибиотики включают, но не ограничиваются ими, актиномицин, антрациклины, валрубицин, эпирубицин, блеомицин, пликамицин, митомицин, их фармацевтически приемлемые соли, пролекарства и комбинации.
[0188] Согласно некоторым вариантам осуществления цитотоксическое средство выбрано из группы, состоящей из циклофосфамида, мехлорэтамина, урамустина, мелфалана, хлорамбуцила, ифосфамида, кармустина, ломустина, стрептозоцина, бусульфана, темозоломида, цисплатина, карбоплатина, оксалиплатина, недаплатина, сатраплатина, триплатина тетранитрата, доксорубицина, даунорубицина, идарубицина, митоксантрона, метотрексата, пеметрекседа, 6-меркаптопурина, дакарбазина, флударабина, 5-фторурацила, арабинозилцитозина, капецитабина, гемцитабина, децитабина, алкалоидов барвинка, паклитаксела (Таксол), доцетаксела (Таксотер), иксабепилона (Икземпра), актиномицина, антрациклинов, валрубицина, эпирубицина, блеомицина, пликамицина, митомицина, их фармацевтически приемлемых солей, пролекарств и комбинаций.
[0189] Цитотоксические средства в соответствии с настоящим изобретением также включают ингибитор каскада PI3K/Akt. Неограничивающие примеры ингибитора каскада PI3K/Akt включают A-674563 (CAS №552325-73-2), AGL 2263, AMG-319 (Amgen, Thousand Oaks, Calif.), AS-041164 (5-бензо[1,3]диоксол-5-илметилентиазолидин-2,4-дион), AS-604850 (5-(2,2-дифторбензо[1,3]диоксол-5-илметилен)тиазолидин-2,4-дион), AS-605240 (5-хиноксилин-6-метилен-1,3-тиазолидин-2,4-дион), AT7867 (CAS №857531-00-1), серию бензимидазолов, Genentech (Roche Holdings Inc., South San Francisco, Calif.), BML-257 (CAS №32387-96-5), BVD-723, CAL-120 (Gilead Sciences, Foster City, Calif.), CAL-129 (Gilead Sciences), CAL-130 (Gilead Sciences), CAL-253 (Gilead Sciences), CAL-263 (Gilead Sciences), CAS №612847-09-3, CAS №681281-88-9, CAS №75747-14-7, CAS №925681-41-0, CAS №98510-80-6, CCT128930 (CAS №885499-61-6), CH5132799 (CAS №1007207-67-1), CHR-4432 (Chroma Therapeutics, Ltd., Abingdon, UK), FPA 124 (CAS №902779-59-3), GS-1101 (CAL-101) (Gilead Sciences), GSK 690693 (CAS №937174-76-0), H-89 (CAS №127243-85-0), Хонокиол, IC87114 (Gilead Science), IPI-145 (Intellikine Inc.), KAR-4139 (Karus Therapeutics, Chilworth, Великобритания), KAR-4141 (Karus Theryubapeutics), KIN-1 (Karus Therapeutics), KT 5720 (CAS №108068-98-0), Милтефозин, MK-2206 дигидрохлорид (CAS №1032350-13-2), ML-9 (CAS №105637-50-1), Налтриндола гидрохлорид, OXY-111A (NormOxys Inc., Brighton, Mass.), перифозин, PHT-427 (CAS №1191951-57-1), ингибитор PI3-киназы дельта, Merck KGaA (Merck & Co., Whitehouse Station, N.J.), ингибиторы PI3-киназы дельта, Genentech (Roche Holdings Inc.), ингибиторы PI3-киназы дельта, Incozen (Incozen Therapeutics, Pvt. Ltd., Hydrabad, Индия), ингибиторы 2 PI3-киназы дельта, Incozen (Incozen Therapeutics), ингибитор PI3-киназы, Roche-4 (Roche Holdings Inc.), ингибиторы PI3-киназы, Roche (Roche Holdings Inc.), ингибиторы PI3-киназы, Roche-5 (Roche Holdings Inc.), ингибиторы PI3-альфа/дельта, Pathway Therapeutics (Pathway Therapeutics Ltd., South San Francisco, Calif.), ингибиторы PI3-дельта, Cellzome (Cellzome AG, Heidelberg, Germany), ингибиторы PI3-дельта, Intellikine (Intellikine Inc., La Jolla, Calif.), ингибиторы PI3-дельта, Pathway Therapeutics-1 (Pathway Therapeutics Ltd.), ингибиторы PI3-дельта, Pathway Therapeutics-2 (Pathway Therapeutics Ltd.), ингибиторы PI3-дельта/гамма, Cellzome (Cellzome AG), ингибиторы PI3-дельта/гамма, Cellzome (Cellzome AG), ингибиторы PI3-дельта/гамма, Intellikine (Intellikine Inc.), ингибиторы PI3-дельта/гамма, Intellikine (Intellikine Inc.), ингибиторы PI3-дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторы PI3-дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибитор PI3-гамма Evotec (Evotec) и ингибитор PI3-гамма, Cellzome (Cellzome AG), ингибиторы PI3-гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторы PI3K-дельта/гамма, Intellikine-1 (Intellikine Inc.), ингибиторы PI3-дельта/гамма, Intellikine-1 (Intellikine Inc.), пиктилисиб (Roche Holdings Inc.), PIK-90 (CAS №677338-12-4), SC-103980 (Pfizer, Нью-Йорк, N.Y.), SF-1126 (Semafore Pharmaceuticals, Индианаполис, Ind.), SH-5, SH-6, Тетрагидрокуркумин, TG100-115 (Targegen Inc., San Diego, Calif.), трицирибин, X-339 (Xcovery, Уэст-Палм-Бич, Fla.), XL-499 (Evotech, Гамбург, Германия), их фармацевтически приемлемые соли и их комбинации.
[0190] В рамках настоящего изобретения BVD-723 представляет собой соединение формулы (II):
[0191] и его фармацевтически приемлемые соли. BVD-723 представляет собой селективный ингибитор PI3Kγ. BVD-723 можно синтезировать способами, описанными, например, в публикации США № 2016/0214980, которая включена в настоящее описание в качестве ссылки в полном объеме. Также в объем настоящего изобретения входят энантиомеры и рацемические смеси обоих энантиомеров BVD-723.
[0192] В рамках настоящего изобретения термин "токсин" означает антигенное отравляющее вещество или яд растительного или животного происхождения. Примером является дифтерийный токсин или его части.
[0193] В рамках настоящего изобретения термин "радионуклид" означает радиоактивное вещество, вводимое пациенту, например, внутривенно или перорально, после чего оно проникает посредством нормального метаболизма пациента в орган-мишень или ткань-мишень, где оно обеспечивает локальную радиацию в течение короткого периода времени. Примеры радионуклидов включают, но не ограничиваются ими, I-125, At-211, Lu-177, Cu-67, I-131, Sm-153, Re-186, P-32, Re-188, In-114m и Y-90.
[0194] В рамках настоящего изобретения термин "иммуномодулятор" означает вещество, которое изменяет иммунный ответ путем усиления или снижения способности иммунной системы продуцировать антитела или сенсибилизированные клетки, которые распознают и реагируют с антигеном, который инициировал их продукцию. Иммуномодуляторы могут представлять собой рекомбинантные, синтетические или натуральные препараты и включают цитокины, кортикостероиды, цитотоксические средства, тимозин и иммуноглобулины. Некоторые иммуномодуляторы естественным образом присутствуют в организме и некоторые из них доступны в фармакологических препаратах. Примеры иммуномодуляторов включают, но не ограничиваются ими, гранулоцитарный колониестимулирующий фактор (G-CSF), LAG-3, IMP-321, JCAR-014, ASLAN-002 (BMS-777607), интерфероны, имиквимод и клеточные мембранные фракции из бактерий, IL-2, IL-7, IL-12, CCL3, CCL26, CXCL7, синтетический цитозинфосфат-гуанозин (CpG), ингибиторы иммунной точки контроля и их комбинации.
[0195] В рамках настоящего изобретения термин "фотоактивное лекарственное средство" означает соединения и композиции, которые становятся активными под действием света. Определенные примеры фотоактивных лекарственных средств описаны, например, в патентной заявка США с серийным номером № 2011/0152230 A1, "Photoactive Metal Nitrosyls For Blood Pressure Regulation And Cancer Therapy".
[0196] В рамках настоящего изобретения термин "радиосенсибилизирующее средство" означает соединение, которое делает опухолевые клетки более чувствительными к лучевой терапии. Примеры радиосенсибилизирующих средств включают мизонидазол, метронидазол, тирапазамин и транс-кроцетинат натрия, и их комбинацию.
[0197] В рамках настоящего изобретение термин "гормон" означает вещество, высвобождаемое клетками в одной части организма, которое влияет на клетки в другой части организма. Примеры гормонов включают, но не ограничиваются ими, простагландины, лейкотриены, простациклин, тромбоксан, амилин, антимюллеров гормон, адипонектин, адренокортикотропный гормон, ангиотензиноген, ангиотензин, вазопрессин, атриопептид, натрийуретический пептид головного мозга, кальцитонин, холицистокинин, кортикотропин-рилизинг гормон, энцефалин, эндотелин, эритропоэтин, фоликулостимулирующий гормон, галанин, гастрин, грелин, глюкагон, гонадотропин-рилизинг гормон, рилизинг-фактор гормона роста, хорионический гонадотропин человека, лактоген плаценты человека, гормон роста, ингибин, инсулин, соматомедин, лептин, липтропин, лютеинизирующий гормон, меланоцит-стимулирующий гормон, мотилин, орексин, окситоцин, панкреатический полипептид, паратиреоидный гормон, пролактин, пролактин-рилизинг гормон, релаксин, ренин, секретин, соматостатина, тромбопоэтин, тиреотропный гормон, тестостерон, дегидроэпиандростерон, андростендион, дигидротестостерон, альдостерон, эстрадиол, эстрон, эстриол, кортизол, прогестерон, кальцитриол и кальцидиол.
[0198] Некоторые соединения препятствуют активности определенных гормонов или останавливают продукцию определенных гормонов. Эти препятствующие гормонам соединения включают, но не ограничиваются ими, тамоксифен (Нолвадекс®), анастрозола (Аримидекс®), лектрозол (Фемара®) и фулвестрант (Фаслодекс®). Такие соединения также входят в значение термина "гормон" в рамках настоящего изобретения.
[0199] Как используют в рамках изобретения, "антиангиогенное" средство означает вещество, которое снижает или ингибирует рост новых кровеносных сосудов, например, такое как ингибитор сосудисто-эндотелиального фактора роста (VEGF) и ингибитор миграции эндотелиальных клеток. Антиангиогенные средства включают, но не ограничиваются ими, 2-метоксиэстрадиол, ангиостатин, бевацизумаб, хрящевой ингибирующий ангиогенез фактор, эндостатин, IFN-α, IL-12, итраконазол, линомид, тромбоцитарный фактор 4, пролактин, SU5416, сурамин, тасквинимод, текогалан, тетратиомолибдат, талидомид, тромбоспондин, тромбоспондин, TNP-470, зив-афлиберцепт, их фармацевтически приемлемые соли, пролекарства и комбинации.
[0200] В соответствии с одним аспектом настоящее изобретение относится к способу лечения или смягчения эффектов злокачественной опухоли у индивидуума, включающему (a) идентификацию индивидуума со злокачественной опухолью, имеющего мутацию BRAF не V600E/K; и (b) введение индивидууму эффективного количества ингибитора ERK или его фармацевтически приемлемой соли.
[0201] В соответствии с одним вариантом осуществления ингибитор ERK выбран из группы, состоящей из BVD-523, SCH-722984 (Merck & Co.), SCH-772984 (Merck & Co.), SCH-900353 (MK-8353) (Merck & Co.), LY3214996 (Lilly), AEZS-140 (Aeterna Zentaris), AEZS-131 (Aeterna Zentaris), AEZS-136 (Aeterna Zentaris), LTT-462 (Novartis), RG-7842 (Genentech), CC-90003 (Celgene), KIN-4050 (Kinentia) и их комбинаций. В соответствии с одним вариантом осуществления ингибитор ERK представляет собой BVD-523. В одном аспекте этого варианта осуществления BVD-523 или его фармацевтически приемлемую соль вводят в форме фармацевтической композиции, дополнительно содержащей фармацевтически приемлемый носитель или разбавитель.
[0202] В соответствии с одним аспектом настоящее изобретение относится к идентификации индивидуума со злокачественной опухолью, имеющего мутацию BRAF не V600E/K, включающей (i) получение биологического образца от индивидуума; и (ii) скрининг образца для определения того, имеет ли индивидуум мутацию BRAF не V600E/K.
[0203] Пригодными и предпочтительными индивидуумами являются индивидуумы, описанные в настоящем описании. В этом варианте осуществления способы можно использовать для лечения злокачественных опухолей, описанных выше, включая злокачественные опухоли с мутационным базисом, идентифицированным выше. Способы идентификации таких мутаций также являются такими, как описано выше.
[0204] В рамках настоящего изобретения биологические образцы включают, но не ограничиваются ими, кровь, плазму, мочу, кожу, слюну и биоптаты. Биологические образцы получают от индивидуума с использованием стандартных методик и способов, которые известны в данной области. Неограничивающие примеры способов идентификации мутаций включают ПЦР, секвенирование, гибридную ловушку, улавливание в растворе, инвертируемые молекулярные зонды, способы анализа с использованием флуоресцентной гибридизации in situ (FISH) и их комбинации.
[0205] В соответствии с одним вариантом осуществления способ дополнительно включает введение индивидууму по меньшей мере одного дополнительного лекарственного средства, выбранного из группы, состоящей из ингибитора MEK, ингибитора RAF, ингибитора HDAC и их комбинаций. Подходящими и предпочтительными индивидуумами являются индивидуумы, как описано в настоящем описании. В этом варианте осуществления способы можно использовать для лечения злокачественных опухолей, описанных выше, включая злокачественные опухоли с мутационным базисом, идентифицированным выше, с использованием одного или нескольких дополнительных лекарственных средств, описанных выше. Способы идентификации таких мутаций также являются такими, как указано выше.
[0206] В соответствии с одним аспектом настоящее изобретение относится к способу идентификации индивидуума, имеющего злокачественную опухоль, для которого была бы полезной терапия ингибитором ERK или его фармацевтически приемлемой солью, причем способ включает (a) получение биологического образца от индивидуума; и (b) скрининг образца для определения того, имеет ли индивидуум мутацию BRAF не V600E/K, где присутствие мутации BRAF не V600E/K подтверждает, что индивидууму была бы полезной терапия ингибитором ERK или его фармацевтически приемлемой солью. Согласно некоторым вариантам осуществления способ дополнительно включает введение индивидууму ингибитора ERK или его фармацевтически приемлемой соли. Согласно некоторым вариантам осуществления способ дополнительно включает введение индивидууму по меньшей мере одного дополнительного лекарственного средства. В этом варианте осуществления способ можно использовать для идентификации мутационного базиса, идентифицированного выше, в злокачественных опухолях, описанных выше. Способы идентификации таких мутаций также являются такими, как указано выше. В этом варианте осуществления ингибитор ERK, который был бы полезен идентифицированному пациенту, является таким, как описано выше. Дополнительные лекарственные средства являются такими, как описано выше. Подходящие и предпочтительные индивидуумы являются такими, как описано выше.
[0207] В соответствии с одним аспектом, настоящее изобретение относится к способу лечения или смягчения эффектов злокачественной опухоли у индивидуума, включающему (a) идентификацию индивидуума со злокачественной опухолью, имеющего мутацию BRAF не V600E/K; и (b) введение индивидууму эффективного количества BVD-523 или его фармацевтически приемлемой соли. В соответствии с одним аспектом настоящее изобретение относится к способу идентификации индивидуума, имеющего злокачественную опухоль, для которого была бы полезной терапия BVD-523 или его фармацевтически приемлемой солью, причем способ включает (a) получение биологического образца от индивидуума; и (b) скрининг образца для определения того, имеет ли индивидуум мутацию BRAF не V600E/K, где присутствие мутации BRAF не V600E/K подтверждает, что индивидууму была бы полезна терапия BVD-523 или его фармацевтически приемлемой солью. В этих вариантах осуществления способ можно использовать для идентификации мутационного базиса, идентифицированного выше, в злокачественных опухолях, описанных выше. Способы идентификации таких мутаций также указаны выше. Подходящими и предпочтительными индивидуумами являются индивидуумы, описанные выше.
[0208] Следующий аспект настоящего изобретения относится к набору для лечения или смягчения эффектов злокачественной опухоли у индивидуума, имеющей мутацию BRAF не V600E/K. Согласно некоторым вариантам осуществления набор содержит эффективное количество ингибитора ERK, как описано выше, и необязательно дополнительное лекарственное средство, как описано выше.
[0209] Наборы также могут включать подходящие контейнеры для хранения, например, ампулы, флаконы, пробирки и т.д., для каждого средства против злокачественной опухоли по настоящему изобретению (которое может быть, например, в форме фармацевтических композиций), и другие реагенты, например, буферы, сбалансированные солевые растворы и т.д., для применения для введения средств против злокачественной опухоли индивидуумам. Средства против злокачественной опухоли по изобретению и другие реагенты могут присутствовать в наборах в любой удобной форме, например, такой как форма раствора или порошка. Кроме того, наборы могут включать контейнер для упаковывания, необязательно имеющий одно или несколько отделений для содержания фармацевтической композиции и других необязательных реагентов.
[0210] В рамках настоящего изобретения "эффективное количество" или "терапевтически эффективное количество" средства против злокачественной опухоли по изобретению, включая фармацевтические композиции, содержащие его, которые описаны в настоящем описании, представляет собой количество такого средства или композиции, которое является достаточным для обеспечения благоприятных или желательных результатов, как описано в настоящем описании, при введении индивидууму. Эффективные дозированные формы, способы введения и дозировки можно определять эмпирически и проведение таких определений входит в пределы квалификации в данной области. Специалистам в данной области будет понятно, что дозировка будет варьироваться в зависимости от пути введения, скорости экскреции, длительности лечения, типа любых других вводимых лекарственных средств, возраста, размера и вида пациента-млекопитающего, например, пациента-человека, и подобных факторов, хорошо известны в области медицины и ветеринарной медицины. Как правило, подходящая доза средства или композиции по изобретению представляет собой количество средства или композиции, которое является наименьшей дозой, эффективной для обеспечения желаемого эффекта. Эффективную дозу средства или композиции по настоящему изобретению можно вводить в качестве двух, трех, четырех, пяти, шести или более субдоз, вводимых отдельно с соответствующими интервалами на протяжении дня.
[0211] Подходящий неограничивающий пример дозировки BVD-523, ингибитора RAF, ингибитора ERK или другого средства против злокачественной опухоли, описанного в настоящем описании, представляет собой от приблизительно 1 мг/кг до приблизительно 2400 мг/кг в сутки, как например, от приблизительно 1 мг/кг до приблизительно 1200 мг/кг в сутки, от 75 мг/кг в сутки до приблизительно 300 мг/кг в сутки, в том числе от приблизительно 1 мг/кг до приблизительно 100 мг/кг в сутки. Другие репрезентативные дозировки таких средств включают приблизительно 1 мг/кг, 5 мг/кг, 10 мг/кг, 15 мг/кг, 20 мг/кг, 25 мг/кг, 30 мг/кг, 35 мг/кг, 40 мг/кг, 45 мг/кг, 50 мг/кг, 60 мг/кг, 70 мг/кг, 75 мг/кг, 80 мг/кг, 90 мг/кг, 100 мг/кг, 125 мг/кг, 150 мг/кг, 175 мг/кг, 200 мг/кг, 250 мг/кг, 300 мг/кг, 400 мг/кг, 500 мг/кг, 600 мг/кг, 700 мг/кг, 800 мг/кг, 900 мг/кг, 1000 мг/кг, 1100 мг/кг, 1200 мг/кг, 1300 мг/кг, 1400 мг/кг, 1500 мг/кг, 1600 мг/кг, 1700 мг/кг, 1800 мг/кг, 1900 мг/кг, 2000 мг/кг, 2100 мг/кг, 2200 мг/кг и 2300 мг/кг в сутки. Эффективную дозу BVD-523, ингибиторов RAF, ингибиторов ERK или других средств против злокачественной опухоли, описанных в настоящем описании, можно вводить в качестве двух, трех, четырех, пяти, шести или более субдоз, вводимых по отдельности с соответствующими на протяжении дня.
[0212] BVD-523, ингибиторы RAF, ингибиторы ERK или другие лекарственные средства или фармацевтические композиции, содержащие их, по настоящему изобретению можно вводить любым желаемым или эффективным способом: путем перорального приема или в качестве мази или капель для локального введения в глаза, и путем парентерального или другого введения любым подходящим способом, таким как внутрибрюшинный, внутриопухолевый, подкожный, местный, внутрикожный, ингаляционный, внутрилегочный, ректальный, вагинальный, сублингвальный, внутримышечный, внутривенный, внутриартериальный, интратекальный или внутрилимфатический. Кроме того, BVD-523, ингибиторы RAF или другие лекарственные средства или фармацевтические композиции, содержащие их, по настоящему изобретению можно вводить совместно с другими способами лечения. При желании BVD-523, ингибиторы RAF или другие лекарственные средства или фармацевтические композиции, содержащие их, могут быть инкапсулированы или иным образом защищены против желудочных или иных секретов.
[0213] Фармацевтические композиции по изобретению содержат один или несколько активных ингредиентов, например, лекарственных средств, в смеси с одним или несколькими фармацевтически приемлемыми разбавителями или носителями и, необязательно, одним или несколькими другими соединениями, лекарственными средствами, ингредиентами и/или материалами. Независимо от выбранного пути введения средства/соединения по настоящему изобретению составляют в фармацевтически приемлемые дозированные формы общепринятыми способами, известными специалистам в данной области. См., например, Remington, The Science and Practice of Pharmacy (21st Edition, Lippincott Williams and Wilkins, Philadelphia, Pa.).
[0214] Фармацевтически приемлемые разбавители или носители хорошо известны в данной области (см., например, Remington, The Science and Practice of Pharmacy (21st Edition, Lippincott Williams and Wilkins, Philadelphia, Pa.) и The National Formulary (American Pharmaceutical Association, Washington, D.C.)) и включают сахара (например, лактоза, сахароза, маннит и сорбит), крахмалы, препараты целлюлозы, фосфаты кальция (например, дикальций фосфат, трикальций фосфат и гидрофосфат кальция), цитрат натрия, воду, водные растворы (например, физиологический раствор, хлорид натрия инъекционный, раствор Рингера инъекционный, раствор декстрозы инъекционный, раствор декстрозы и хлорида натрия инъекционный, лактатный раствор Рингера инъекционный), спирты (например, этиловый спирт, пропиловый спирт и бензиловый спирт), полиолы (например, глицерин, пропиленгликоль и полиэтиленгликоль), органические сложные эфиры (например, этилолеат и триглицериды), биодеградируемые полимеры (например, полилактид-полигликолид, сложные поли(ортоэфиры) и поли(ангидриды)), эластомерные матрицы, липосомы, микросферы, масла (например, кукурузное, масло из зародышей, оливковое, касторовое, кунжутное, хлопковое и арахисовое масло), масло какао, воски (например, воски суппозиториев), парафины, силиконы, тальк, силицилат и т.д. Каждый фармацевтически приемлемый разбавитель или носитель, используемый в фармацевтической композиции по изобретению, должен быть "приемлемым" с точки зрения совместимости с другими ингредиентами состава и не вредоносным для индивидуума. Разбавители или носители, пригодные для выбранной дозированной формы и предполагаемого пути введения, хорошо известны в данной области, и приемлемые разбавители или носители для выбранной дозированной формы и способа введения могут быть определены с использованием обычных навыков в данной области.
[0215] Фармацевтические композиции по изобретению необязательно могут содержать дополнительные ингредиенты и/или материалы, часто используемые в фармацевтических композициях. Эти ингредиенты и материалы хорошо известны в данной области и включают (1) наполнители или разбавители, такие как крахмалы, лактоза, сахароза, глюкоза, маннит и кремниевая кислота; (2) связующие вещества, такие как карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, гидроксипропилметилцеллюлоза, сахароза и гуммиарабик; (3) увлажнители, такие как глицерин; (4) разрыхлители, такие как агар-агар, карбонат кальция, картофельный или тапиоковый крахмал, альгиновая кислота, определенные силикаты, натрия крахмала гликолят, сшитая натрий карбоксиметилцеллюлоза и карбонат натрия; (5) замедляющие растворение средства, такие как парафин; (6) средства, ускоряющие всасывание, такие как четвертичные соединения аммония; (7) смачивающие вещества, такие как цетиловый спирт и глицеринмоностеарат; (8) поглотители, такие как каолин и бентонитовая глина; (9) смазывающие вещества, такие как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли и лаурилсульфат натрия; (10) суспендирующие вещества, такие как этоксилированные изостеариловые спирты, полиоксиэтилен сорбит и сложные эфиры сорбитана, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант; (11) буферные средства; (12) эксципиенты, такие как лактоза, молочные сахара, полиэтиленгликоли, животные и растительные жиры, масла, воски, парафины, масло какао, крахмалы, трагакант, производные целлюлозы, полиэтиленгликоль, силиконы, бентониты, кремниевая кислота, тальк, салицилат, оксид цинка, гидроксид алюминия, силикаты кальция и полиамидный порошок; (13) инертные разбавители, такие как вода или другие растворители; (14) консерванты; (15) поверхностно-активные вещества; (16) диспергирующие вещества; (17) средства контролируемого высвобождения или замедления всасывания, такие как гидроксипропилметилцеллюлоза, другие полимерные матрицы, биодеградируемые полимеры, липосомы, микросферы, моностеарат алюминия, желатин и воски; (18) замутнители; (19) адъюванты; (20) смачивающие вещества; (21) эмульгирующие и суспендирующие вещества; (22) солюбилизаторы и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, масла (в частности, хлопковое, арахисовое, кукурузное, из зародышей, оливковое, касторовое и кунжутное масло), глицерин, тетрагидрофуриловый спирт, полиэтиленгликоли и сложные эфиры жирных кислот и сорбитана; (23) пропелленты, такие как хлорфторуглеводороды и летучие незамещенные углеводороды, такие как бутан и пропан; (24) антиоксиданты; (25) средства, которые обеспечивают изотоничность состава с кровью предполагаемого реципиента, такие как сахара и хлорид натрия; (26) загустители; (27) материалы покрытия, такие как лецитин; и (28) подсластители, вкусовые добавки, красители, отдушки и консерванты. Каждый такое ингредиент или материал должен быть "приемлемым" с точки зрения совместимости с другими ингредиентами состава и не вредоносным для индивидуума. Ингредиенты и материалы, пригодные для выбранной дозированной формы и предполагаемого пути введения, хорошо известны в данной области, и приемлемые ингредиенты и материалы для выбранной дозированной формы и способа введения могут быть определены с использованием стандартных навыков в данной области.
[0216] Фармацевтические композиции по настоящему изобретению, пригодные для перорального введения, могут быть в форме капсул, крахмальных капсул, пилюль, таблеток, порошков, гранул, раствора или суспензии в водной или неводной жидкости, жидкой эмульсии типа "масло в воде" или "вода в масле", эликсира или сиропа, пастилки, болюса, электуария или пасты. Эти составы можно получать способами, известными в данной области, например, посредством общепринятых способов покрытия целиком, смешения, гранулирования или лиофилизации.
[0217] Твердые дозированные формы для перорального введения (капсулы, таблетки, пилюли, драже, порошки, гранулы и т.п.) можно получать, например, путем смешения активного ингредиента(ов) с одним или несколькими фармацевтически приемлемыми разбавителями или носителями и необязательно одним или несколькими наполнителями, разбавителями, связующими веществами, увлажнителями, разрыхлителями, замедляющими растворение средствами, средствами, ускоряющими всасывание, смачивающими веществами, поглотителями, смазывающими веществами и/или красителями. Твердые композиции сходного типа можно использовать в качестве наполнителей в мягких и твердых заполненных желатиновых капсулах с использованием подходящего эксципиента. Таблетка может быть получена путем прессования или формования, необязательно с одним или несколькими дополнительными ингредиентами. Прессованные таблетки можно получать с использованием подходящего связующего вещества, смазывающего вещества, инертного разбавителя, консерванта, разрыхлителя, поверхностно-активного вещества или диспергирующего вещества. Формованные таблетки можно получать путем формования в подходящем устройстве. Таблетки и другие твердые дозированные формы, такие как драже, капсулы, пилюли и гранулы, необязательно иметь борозду или могут быть изготовлены с покрытиями и оболочками, такими как кишечнорастворимые покрытия и другие покрытия, хорошо известные в области составления фармацевтических препаратов. Также их можно составлять так, чтобы обеспечить медленное или контролируемое высвобождение из них активного ингредиента. Их можно стерилизовать, например, путем фильтрации через удерживающий бактерии фильтр. Эти композиции также необязательно могут содержать замутнители, и они могут иметь такой состав, что они высвобождают активный ингредиент только или предпочтительно в определенной части желудочно-кишечного тракта, необязательно замедленным образом. Активный ингредиент также может быть в микроинкапсулированной форме.
[0218] Жидкие дозированные формы для перорального введения включают фармацевтически приемлемые эмульсии, микроэмульссии, растворы, суспензии, сиропы и эликсиры. Жидкие дозированные формы могут содержать подходящие инертные разбавители, часто используемые в данной области. Помимо инертных разбавителей, пероральные композиции также могут включать адъюванты, такие как смачивающие вещества, эмульгирующие и суспендирующие вещества, подсластители, вкусовые добавки, красители, отдушки и консерванты. Суспензии могут содержать суспендирующие вещества.
[0219] Фармацевтические композиции по настоящему изобретению для ректального или вагинального введения могут быть предоставлены в качестве суппозитория, который может быть получен путем смешения одного или нескольких активного ингредиента(ов) с одним или несколькими подходящими не вызывающими раздражения разбавителями или носителями, которые являются твердыми при комнатной температуре, но жидкими при температуре тела и, таким образом, плавятся в прямой кишке или вагинальной полости и высвобождают активное соединение. Фармацевтические композиции по настоящему изобретению, которые пригодны для вагинального введения, также включают пессарии, тампоны, кремы, гели, пасты, пены или составы спреев, содержащие такие фармацевтически приемлемые разбавители или носители, которые известны в данной области в качестве пригодных.
[0220] Дозированные формы для местного или трансдермального введения включают порошки, спреи, мази, пасты, кремы, лосьоны, гели, растворы, пластыри, капли и ингалируемые формы. Активное вещество(а)/соединение(я) можно смешивать в стерильных условиях с подходящим фармацевтически приемлемым разбавителем или носителем. Мази, пасты, кремы и гели могут содержать эксципиенты. Порошки и спреи могут содержать эксципиенты и пропелленты.
[0221] Фармацевтические композиции по настоящему изобретению, пригодные для парентерального введения, могут содержать одно или несколько средство(средств)/соединение(соединений) в комбинации с одним или несколькими фармацевтически приемлемыми обеспечивающими изотоничность водными или неводными растворами, дисперсиями, суспензиями или эмульсиями, или стерильными порошками, которые можно восстанавливать в стерильные инъекционные растворы или дисперсии непосредственно перед применением, которые могут содержать подходящие антиоксиданты, буферы, растворенные вещества, которые обеспечивают изотоничность состава с кровью предполагаемого реципиента или суспендирующие вещества или загустители. Надлежащую текучесть можно поддерживать, например, с использованием материалов покрытия, путем поддержания требуемого размера частиц в случае дисперсий и путем использования поверхностно-активных веществ. Эти фармацевтические композиции также могут содержать подходящие адъюванты, такие как смачивающие вещества, эмульгаторы и диспергирующие вещества. Также может быть желательным включение обеспечивающих изотоничность средств. Кроме того, пролонгированного всасывания инъекционной фармацевтической формы можно достигать путем включения веществ, которые замедляют всасывание.
[0222] В некоторых случаях для пролонгирования эффекта лекарственного средства (например, фармацевтического состава), желательно замедлять его всасывание после подкожной или внутримышечной инъекции. Это можно осуществлять с использованием жидкой суспензии кристаллического или аморфного материала, имеющего низкую растворимость в воде.
[0223] В результате скорость всасывания активного вещества/лекарственного средства зависит от скорости его растворения, которая в свою очередь может зависеть от размера кристаллов и кристаллической формы. Альтернативно замедленного всасывания парентерально вещества/лекарственного средства можно достигать путем растворения или суспендирования активного вещества/лекарственного средства в масляном носителе. Инъекционные депо-формы можно получать путем формирования матриксов активного ингредиента, микроинкапсулированных в биодеградируемые полимеры. В зависимости от соотношения активного ингредиента и полимера и природы используемого конкретного полимера можно контролировать скорость высвобождения активного ингредиента. Инъекционные депо-составы также получают путем заключения лекарственного средства в липосомы или микроэмульсии, которые совместимы с тканью организма. Инъекционные материалы можно стерилизовать, например, фильтрацией через удерживающие бактерии фильтры.
[0224] Составы могут быть предоставлены в закрытых контейнерах с единичной дозой или множеством доз, например, ампулах и флаконах, и их можно хранить в лиофилизированном состоянии, требующем только добавления стерильного жидкого разбавителя или носителя, например, водя для инъекций, непосредственно перед применением. Растворы и суспензии для приготовления непосредственно перед инъекцией можно получать из стерильных порошков, гранул и таблеток описанного выше типа.
[0225] Приведенные ниже примеры предоставлены для дальнейшей иллюстрации способов по настоящему изобретению. Эти примеры являются только иллюстративными и не предназначены для ограничения объема изобретения каким-либо образом.
ПРИМЕР 1
[0226] В приведенном ниже примере представлены результаты испытания BVD-523 фазы 1b для солидной опухоли. На водопадной диаграмме, представленной на фиг.2 предоставлена иллюстрация информации о пациентах-людях клинического испытания, демонстрирующая ответ каждого конкретного индивидуума на лечение BVD-523 при определении по % изменению опухолевой нагрузки. Пациентам, главным образом, вводили 600 мг два раза в сутки (BID), причем некоторым пациентам вводили сниженную дозу 300 мг-400 мг BID, если побочные эффекты не удавалось контролировать посредством другого паллиативного медикаментозного вмешательства.
[0227] Как показано на фиг.2, ответ опухоли на BVD-523 оценивали у 28 поддающихся оценке пациентов пациенты с использованием Response Evaluation Criteria in Solid Tumors version 1.1 (RECIST v1.1). Одному пациенту не проводилось оба сканирования очагов повреждения и, таким образом, его не оценивали. Горизонтальная ось, проходящая через график, служит в качестве исходного показателя для каждого пациента. Вертикальная ось является показателем максимального процентного изменения от исходного уровня; т.е. процентного роста или снижения опухолевой нагрузки в соответствии с радиологическим определением в соответствии с RECIST v1.1. Радиологическое определение включало сканирование с использованием компьютерной томографии (CT) и иногда магнитно-резонансную томографию (MRI).
[0228] Данные об опухолевой нагрузке, представленные на фиг.2, представлены от наихудшей величины (т.е. наибольшее прогрессирование опухолевой нагрузки) слева на графике до наилучшей величины (т.е. наибольшее уменьшение опухолевой нагрузки) справа на графике. Критерии ответа RECIST v1.1 для измеренных очагов повреждения описаны ранее (см. Eisenhauer, E.A., et al., New response evaluation criteria in solid tumours: Revised RECIST guideline (version 1.1), European J. of Cancer 45, 228-247 (2009), включенную в настоящее описание в качестве ссылки в полном объеме). Критерии ответа являются следующими:
[0229] Полный ответ (CR) - исчезновение всех очагов-мишеней;
[0230] Частичный ответ (PR) - по меньшей мере 30% снижение суммы диаметров очагов-мишеней при использовании в качестве эталона исходную сумму диаметров; как показано на фиг.2, 30% порог снижения для частичного ответа указан горизонтальной линией;
[0231] Прогрессирующее заболевание (PD) - по меньшей мере 20% увеличение суммы диаметров очагов-мишеней при использовании в качестве эталона наименьшей суммы в исследовании (это включает исходную сумму, если она является наименьшей в исследовании). В дополнение к относительному повышению на 20%, сумма также должна демонстрировать абсолютное увеличение по меньшей мере на 5 мм (примечание: появление одного или нескольких новых очагов также считается прогрессированием);
[0232] Стабильное заболевание (SD) - не достаточное уменьшение для определения как PR, ни достаточное увеличение для определения как PD при использовании в качестве эталона наименьшей суммы диаметров в испытании.
[0233] На фиг.2 также представлен тип злокачественной опухоли или орган, где определяли опухолевую нагрузку для каждого пациента, и тип атипичной мутации BRAF, идентифицированной в образце опухоли этого пациента. Из 28 представленных пациентов 13 опухолей пациентов содержали мутацию BRAF D594 (семь случаев D594G и шесть случаев D594N); опухоль 1 пациента содержала мутацию BRAF F247L; опухоль 1 пациента содержала слияние гена BRAF с геном ядерного фактора IC (NFIC) (т.е. мутация со слиянием BRAF-NFIC); опухоль 1 пациента содержала мутацию BRAF G466V; опухоли 5 пациентов содержали мутацию BRAF G469 (одна представляла собой G469V и четыре представляли собой G469A); опухоли 3 пациентов содержали мутацию BRAF K601E; опухоль 1 пациента содержала мутацию BRAF L485W; опухоли 3 пациентов содержали мутацию BRAF L597 (одна была не идентифицирована и две представляли собой L597Q), и опухоли 2 пациентов содержали дупликацию T599. Тип мутации BRAF указан в соответствии с цветовым кодом и типом злокачественной опухоли для каждого пациента (см. фиг.2).
[0234] Пять пациентов с PR имели от 35% до 100% снижения суммы очагов-мишеней от исходного уровня. Эти пациенты имели: опухоль желчного пузыря, содержащую мутацию L485W; плоскоклеточную опухоль головы/шеи, содержащую мутацию G469A; немелкоклеточную карциному легких, содержащую мутацию BRAF L597Q или дупликацию BRAF T599; и опухоль тонкого кишечника, содержащую мутацию BRAF G469A. 19 пациентов демонстрировали стабильное заболевание. Три пациента имели прогрессирующее заболевание при первой оценке (см. фиг.2). Таким образом, лечение BVD-523 неожиданно приводило к частичному ответу или стабильному заболеванию у 24 из 28 пациентов с атипичными мутациями BRAF (т.е. не V600E/K).
[0235] На фиг.3 представлена длительность лечения на графике "дорожек бассейна", распределенная по группам. Члены 1 группы представляют собой любых пациентов с любой мутацией BRAF в любом типе опухоли, отличном от рака ободочной и прямой кишки (CRC) и немелкоклеточной карциномы легких (NSCLC), и которых ранее лечили ингибитором каскада MAPK. Члены 2 группы представляют собой пациентов с любой мутацией BRAF в CRC, которых ранее не лечили ингибитором каскада MAPK. Члены 3 группы представляют собой пациентов, имеющих мутацию BRAF V600E/K, которые рефрактерны к ингибитору MAPK. Члены 6 группы представляют собой пациентов с любой мутацией BRAF, присутствующей в NSCLC. Как показано на фиг.3, включены все 28 пациентов, как показано горизонтальными столбиками, по одному для каждого индивидуума. Длительность лечения для каждого индивидуума в каждой группе проиллюстрирована сверху (наибольшая длительность лечения) вниз (наименьшая длительность лечения) по группам. По горизонтальной оси представлена длительность в сутках нахождения индивидуума в исследовании. На фиг.3 также представлен тип ответа, достигнутый каждым пациентом в соответствии с RECIST v1.1 (ромб=частичный ответ; круг=стабильное заболевание; вертикальный столбик=прогрессирующее заболевание; треугольник=оценка не проводилась).
[0236] На фиг.4 представлена длительность лечения на водопадной диаграмме в соответствии с мутацией BRAF. Включены все 28 пациентов, у которых определены критерии ответа RECIST v1.1, плюс дополнительные пациенты, которых не оценивали посредством RECIST v1.1 (ромб=частичный ответ; круг=стабильное заболевание; вертикальный столбик=прогрессирующее заболевание; треугольник=оценка не проводилась). Средняя длительность лечения BVD-523 перед прекращением лечения для опухолей, для опухолей, имеющих указанную мутацию BRAF, составляла: D594, 73,6 суток; G469, 208,14 суток; K601E, 50,25 суток; L597, 73,3 суток; T599 Dup, 63,5 суток. Для случаев одного пациента с конкретной мутацией BRAF длительность лечения составляла: L485W, 304 суток; F247L, 84 суток; G466V, 77 суток; слияние BRAF, 65 суток; перестройка BRAF-AGAP3, 43 суток; вариант сплайсинга 15 экзона BRAF. Посредством геномного скрининга пациентов со злокачественной опухолью в отношении мутации BRAF и лечения их перед полной охарактеризацией этих мутаций in vitro (в качестве пусковой мутации) показано, что BVD-523 является пригодным для изучения и разработки эффективных возможностей лечения для пациентов, имеющих мутации BRAF. Клиническая популяция пациентов и эффективность определяются главным образом не типом опухоли, а скорее мутационным статусом ферментов, таких как BRAF, выше активации киназы ERK 1/2.
[0237] В общем, в приведенных примерах предоставлены данные испытания BVD-523, нового ингибитора ERK, фазы 1b для солидной опухоли в качестве способа лечения для пациентов со злокачественными опухолями, имеющими атипичные мутации BRAF. Непрерывное введение BVD-523 два раза в сутки обеспечивало противвоопухолевые эффекты у нескольких пациентов и не ограничивалось каким-либо одним конкретным типом злокачественной опухоли или атипичной мутацией BRAF.
Документы
ABSALAN, Farnaz, Mostafa Ronaghi (2008). Molecular Inversion Probe Assay. Methods in Molecular Biology 396. Humana Press. pp. 315-330.
AHRONIAN LG, Sennott EM, Van Allen EM, Wagle N, Kwak EL, Faris JE, et al. Clinical acquired resistance to RAF inhibitor combinations in BRAF-mutant colorectal cancer through MAPK pathway alterations. Cancer Discov 2015;5:358-67.
ARCILA ME, Drilon A, Sylvester BE, Lovly CM, Borsu L, Reva B, et al. MAP2K1 (MEK1) mutations define a distinct subset of lung adenocarcinoma associated with smoking. Clin Cancer Res 2015;21:1935-43.
ARONOV AM, Baker C, Bemis GW, Cao J, Chen G, Ford PJ, et al. Flipped out: structure-guided design of selective pyrazolylpyrrole ERK inhibitors. J Med Chem 2007;50:1280-7.
ARONOV AM, Tang Q, Martinez-Botella G, Bemis GW, Cao J, Chen G, et al. Structure-guided design of potent and selective pyrimidylpyrrole inhibitors of extracellular signal-regulated kinase (ERK) using conformational control. J Med Chem 2009;52:6362-8.
ARRINGTON AK, Heinrich EL, Lee W, Duldulao M, Patel S, Sanchez J, et al. Prognostic and predictive roles of KRAS mutation in colorectal cancer. Int J Mol Sci 2012;13:12153-68.
CARGNELLO M, Roux PP. Activation and function of the MAPKs and their substrates, the MAPK-activated protein kinases. Microbiol Mol Biol Rev 2011;75:50-83.
CARLINO MS, Fung C, Shahheydari H, Todd JR, Boyd SC, Irvine M, et al. Preexisting MEK1P124 mutations diminish response to BRAF inhibitors in metastatic melanoma patients. Clin Cancer Res 2015;21:98-105.
CHAPMAN PB, Hauschild A, Robert C, Haanen JB, Ascierto P, Larkin J, et al. Improved survival with vemurafenib in melanoma with BRAF V600E mutation. N Engl J Med 2011;364:2507-16.
CORCORAN, R.B., et al. BRAF gene amplification can promote acquired resistance to MEK inhibitors in cancer cells harboring the BRAF V600E mutation. Sci Signal (2010);3(149): ra84.
DAI, B., et al. STAT3 mediates resistance to MEK inhibitor through microRNA miR-17. Cancer Res (2011);71:3658-3668.
DAVIES H, Bignell GR, Cox C, Stephens P, Edkins S, Clegg S, et al. Mutations of the BRAF gene in human cancer. Nature 2002;417:949-54.
DESCHENES-SIMARD X, Kottakis F, Meloche S, Ferbeyre G. ERKs in cancer: friends or foes? Cancer Res 2014;74:412-9.
DOBRZYCKA B, Terlikowski SJ, Kowalczuk O, Niklinska W, Chyczewski L, Kulikowski M. Mutations in the KRAS gene in ovarian tumors. Folia Histochem Cytobiol 2009;47:221-4.
EMERY, C.M., et al. MEK1 mutations confer resistance to MEK and B-RAF inhibition. PNAS (2009); 106(48):20411-6.
FEDOROV O, Niesen FH, Knapp S. Kinase inhibitor selectivity profiling using differential scanning fluorimetry. Methods Mol Biol 2012;795:109-18.
FERNÁNDEZ-MEDARDE A, Santos E. Ras in cancer and developmental diseases. Genes Cancer 2011;2:344-58.
FLAHERTY KT, Infante JR, Daud A, Gonzalez R, Kefford RF, Sosman J, et al. Combined BRAF and MEK inhibition in melanoma with BRAF V600 mutations. N Engl J Med 2012;367:1694-703.
GOETZ EM, Ghandi M, Treacy DJ, Wagle N, Garraway LA. ERK mutations confer resistance to mitogen-activated protein kinase pathway inhibitors. Cancer Res 2014;74:7079-89.
GOLLOB JA, Wilhelm S, Carter C, Kelley SL. Role of Raf kinase in cancer: therapeutic potential of targeting the Raf/MEK/ERK signal transduction pathway. Semin Oncol 2006;33:392-406.
GREGER, James G., et al. "Combinations of BRAF, MEK, and PI3K/mTOR inhibitors overcome acquired resistance to the BRAF inhibitor GSK2118436 dabrafenib, mediated by NRAS or MEK mutations." Molecular cancer therapeutics 11.4 (2012): 909-920.
GROENENDIJK FH, Bernards R. Drug resistance to targeted therapies: deja vu all over again. Mol Oncol 2014;8:1067-83.
HALL RD, Kudchadkar RR. BRAF mutations: signaling, epidemiology, and clinical experience in multiple malignancies. Cancer Control 2014;21:221-30.
HARDENBOL, P., et al. Multiplexed genotyping with sequence-tagged molecular inversion probes. Nat. Biotechnol. 2003, no.21 , p.673-678.
HATZIVASSILIOU, Georgia, et al. "RAF inhibitors prime wild-type RAF to activate the MAPK pathway and enhance growth." Nature 464.7287 (2010): 431-435.
HATZIVASSILIOU G, Liu B, O'Brien C, Spoerke JM, Hoeflich KP, Haverty PM, et al. ERK inhibition overcomes acquired resistance to MEK inhibitors. Mol Cancer Ther 2012;11:1143-54.
HAUSCHILD A, Grob J-J, Demidov LV, Jouary T, Gutzmer R, Millward M, et al. Dabrafenib in BRAF-mutated metastatic melanoma: a multicentre, open-label, phase 3 randomised controlled trial. Lancet 2012;380:358-65.
HAYES TK, Neel NF, Hu C, Gautam P, Chenard M, Long B, et al. Long-Term ERK Inhibition in KRAS-Mutant Pancreatic Cancer Is Associated with MYC Degradation and Senescence-like Growth Suppression. Cancer Cell 2016;29:75-89.
HEZEL AF, Noel MS, Allen JN, Abrams TA, Yurgelun M, Faris JE, et al. Phase II study of gemcitabine, oxaliplatin in combination with panitumumab in KRAS wild-type unresectable or metastatic biliary tract and gallbladder cancer. Br J Cancer 2014;111:430-6.
JHA S, Morris EJ, Hruza A, Mansueto MS, Schroeder G, Arbanas J, et al. Dissecting therapeutic resistance to ERK inhibition. Mol Cancer Ther 2016;15:548-59.
JOHANNESSEN, C.M., et al. COT/MAP3K8 drives resistance to RAF inhibition through MAP kinase pathway reactivation. Nature (2010);468(7326):968-972.
JOHNSON DB, Menzies AM, Zimmer L, Eroglu Z, Ye F, Zhao S, et al. Acquired BRAF inhibitor resistance: A multicenter meta-analysis of the spectrum and frequencies, clinical behaviour, and phenotypic associations of resistance mechanisms. Eur J Cancer 2015;51:2792-9.
KANDA M, Matthaei H, Wu J, Hong SM, Yu J, Borges M, et al. Presence of somatic Mutations in most early-stage pancreatic intraepithelial neoplasia. Gastroenterology 2012;142:730-733.
KHATTAK M, Fisher R, Turajlic S, Larkin J. Targeted therapy and immunotherapy in advanced melanoma: an evolving paradigm. Ther Adv Med Oncol 2013;5:105-18.
KING, Alastair J., et al. "Dabrafenib; preclinical characterization, increased efficacy when combined with trametinib, while BRAF/MEK tool combination reduced skin lesions." PloS one 8.7 (2013): e67583.
LARKIN J, Ascierto PA, Dréno B, Atkinson V, Liszkay G, Maio M, et al. Combined vemurafenib and cobimetinib in BRAF-mutated melanoma. N Engl J Med 2014;371:1867-76.
LITTLE, A.S., et al., Amplification of the Driving Oncogene, KRAS or BRAF, Underpins Acquired Resistance to MEK1/2 Inhibitors in Colorectal Cancer Cells. Sci. Signal. 4, ra17 (2011).
LIU, Dingxie, et al. "BRAF V600E maintains proliferation, transformation, and tumorigenicity of BRAF-mutant papillary thyroid cancer cells." Journal of Clinical Endocrinology & Metabolism 92.6 (2007): 2264-2271.
LIU B, Fu L, Zhang C, Zhang L, Zhang Y, Ouyang L, et al. Computational design, chemical synthesis, and biological evaluation of a novel ERK inhibitor (BL-EI001) with apoptosis-inducing mechanisms in breast cancer. Oncotarget 2015;6:6762-75.
LONG GV, Fung C, Menzies AM, Pupo GM, Carlino MS, Hyman J, et al. Increased MAPK reactivation in early resistance to dabrafenib/trametinib combination therapy of BRAF-mutant metastatic melanoma. Nat Commun 2014;5:5694.
LONG GV, Stroyakovskiy D, Gogas H, Levchenko E, de Braud F, Larkin J, et al. Dabrafenib and trametinib versus dabrafenib and placebo for Val600 BRAF-mutant melanoma: a multicentre, double-blind, phase 3 randomised controlled trial. Lancet 2015;386:444-51.
MANANDHAR SP, Hildebrandt ER, Schmidt WK. Small-molecule inhibitors of the Rce1p CaaX protease. J Biomol Screen. 2007;12(7):983-993.
MASSEY PR, Prasad V, Figg WD, Fojo T. Multiplying therapies and reducing toxicity in metastatic melanoma. Cancer Biol Ther 2015;16:1014-8.
MAURER, T, Garrenton, LS, Oh, A, Pitts, K, Anderson, DJ, Skelton, NJ, Fauber, BP, Pan, B, Malek, S, Stokoe, D, Ludlam, MJC, Bowman, KK, Wu, J, Giannetti, AM, Starovasnik, MA, Mellman, I, Jackson, PK, Rudolph, J, Wang, W, Fang, G. Small-molecule ligands bind to a distinct pocket in Ras and inhibit SOS-mediated nucleotide exchange activity. PNAS. 2012;109(14):5299-304.
MCARTHUR GA, Chapman PB, Robert C, Larkin J, Haanen JB, Dummer R, et al. Safety and efficacy of vemurafenib in BRAFv600E and BRAFv600K mutation-positive melanoma (BRIM-3): extended follow-up of a phase 3, randomised, open-label study. Lancet Oncol 2014;15:323-32.
MEKINIST [package insert]. Research Triangle Park, NC: GlaxoSmithKline; 2014.
METZKER, Emerging technologies in DNA sequencing Genome Res. 2005. 15: 1767-1776.
MITTAL, Rohit et al. "The acetyltransferase activity of the bacterial toxin YopJ of Yersinia is activated by eukaryotic host cell inositol hexakisphosphate." Journal of Biological Chemistry 285.26 (2010): 19927-19934.
MORRIS EJ, Jha S, Restaino CR, Dayananth P, Zhu H, Cooper A, et al. Discovery of a novel ERK inhibitor with activity in models of acquired resistance to BRAF and MEK inhibitors. Cancer Discov 2013;3:742-50.
NAZARIAN, R., et al. Melanomas acquire resistance to B-RAF (V600E) inhibition by RTK or N-RAS upregulation. Nature. 2010; 468(7326):973-977.
NIKOLAEV SI, Rimoldi D, Iseli C, Valsesia A, Robyr D, Gehrig C, et al. Exome sequencing identifies recurrent somatic MAP2K1 and MAP2K2 mutations in melanoma. Nat Genet 2012;44:133-9.
NILSSON, M., et al. Padlock probes: circularizing oligonucleotides for localized DNA detection. Science. 1994, no.265, p.2085-2088.
O'HARA AJ, Bell DW. The genomics and genetics of endometrial cancer. Adv Genomics Genet 2012;2012:33-47.
OJESINA AI, Lichtenstein L, Freeman SS, Pedamallu CS, Imaz-Rosshandler I, Pugh TJ, et al. Landscape of genomic alterations in cervical carcinomas. Nature 2014;506:371-5.
OTA et al., Single nucleotide polymorphism detection by polymerase chain reaction-restriction fragment length polymorphism. Nat Protoc. 2007;2(11):2857-64.
PARAISO KHT, Fedorenko IV, Cantini LP, Munko AC, Hall M, Sondak VK, et al. Recovery of phospho-ERK activity allows melanoma cells to escape from BRAF inhibitor therapy. Br J Cancer 2010;102:1724-30.
PATGIRI A, Yadav, KK, Arora, PS, Bar-Sagi, D. An orthosteric inhibitor of the Ras-Sos interaction. Nat Chem Biol. 2011;7:585-587.
PENNYCUICK A, Simpson T, Crawley D, Lal R, Santis G, Cane P, et al. Routine EGFR and KRAS mutation analysis using COLD-PCR in non-small cell lung cancer. Int J Clin Pract 2012;66:748-52.
PORTER SB, Hildebrandt ER, Breevoort SR, Mokry DZ, Dore TM, Schmidt WK. Inhibition of the CaaX proteases Rce1p and Ste24p by peptidyl (acyloxy)methyl ketones. Biochim Biophys Acta.2007;1773(6):853-862.
POULIKAKOS PI, Persaud Y, Janakiraman M, Kong X, Ng C, Moriceau G, et al. RAF inhibitor resistance is mediated by dimerization of aberrantly spliced BRAF(V600E). Nature 2011;480:387-90.
QUEIROLO P, Picasso V, Spagnolo F. Combined BRAF and MEK inhibition for the treatment of BRAF-mutated metastatic melanoma. Cancer Treat Rev 2015;41:519-26.
RASOLA A, Sciacovelli M, Chiara F, Pantic B, Brusilow WS, Bernardi P. Activation of mitochondrial ERK protects cancer cells from death through inhibition of the permeability transition. Proc Natl Acad Sci U S A 2010;107:726-31.
RIZOS H, Menzies AM, Pupo GM, Carlino MS, Fung C, Hyman J, et al. BRAF inhibitor resistance mechanisms in metastatic melanoma: spectrum and clinical impact. Clin Cancer Res 2014;20:1965-77.
ROBERT C, Karaszewska B, Schachter J, Rutkowski P, Mackiewicz A, Stroiakovski D, et al. Improved overall survival in melanoma with combined dabrafenib and trametinib. N Engl J Med 2015;372:30-9.
ROMEO Y, Zhang X, Roux PP. Regulation and function of the RSK family of protein kinases. Biochem J 2012;441:553-69.
RUDOLPH J, Xiao Y, Pardi A, Ahn NG. Slow inhibition and conformation selective properties of extracellular signal-regulated kinase 1 and 2 inhibitors. Biochemistry 2015;54:22-31.
SHAUL YD, Seger R. The MEK/ERK cascade: from signaling specificity to diverse functions. Biochim Biophys Acta 2007;1773:1213-26.
SHI H, Hugo W, Kong X, Hong A, Koya RC, Moriceau G, et al. Acquired resistance and clonal evolution in melanoma during BRAF inhibitor therapy. Cancer Discov 2014;4:80-93.
SHIMA, F, Yoshikawa, Y, Ye, M, Araki, M, Matsumoto, S, Liao, J, Hu, L, Sugimoto, T, Ijiri, Y, Takeda, A, Nishiyama, Y, Sato, C, Muraoka, S, Tamura, A, Osoda, T, Tsuda, K-I, Miyakawa, T, Fukunishi, H, Shimada, J, Kumasaka, Yamamoto, M, Kataoka, T. In silico discovery of small-molecule Ras inhibitors that display antitumor activity by blocking the Ras-effector interaction. PNAS. 2013;110(20):8182-7.
SCHUBBERT S, Shannon K, Bollag G. Hyperactive Ras in developmental disorders and cancer. Nat Rev Cancer 2007;7:295-308.
SUN C, Hobor S, Bertotti A, Zecchin D, Huang S, Galimi F, et al. Intrinsic resistance to MEK inhibition in KRAS mutant lung and colon cancer through transcriptional induction of ERBB3. Cell Rep 2014;7:86-93.
TAFLINAR [package insert]. Research Triangle Park, NC: GlaxoSmithKline; 2015.
TRUNZER K, Pavlick AC, Schuchter L, Gonzalez R, McArthur GA, Hutson TE, et al. Pharmacodynamic effects and mechanisms of resistance to vemurafenib in patients with metastatic melanoma. J Clin Oncol 2013;31:1767-74.
VILLANUEVA, J., et al. Acquired resistance to BRAF inhibitors mediated by a RAF kinase switch in melanoma can be overcome by cotargeting MEK and IGF-1R/PI3K. Cancer Cell. 2010;18:683-695.
WAGLE, N., et al. Dissecting therapeutic resistance to RAF inhibition in melanoma by tumor genomic profiling. Journal of Clinical Oncology 2011;29(22):3085-3096.
WAGLE N, Van Allen EM, Treacy DJ, Frederick DT, Cooper ZA, Taylor-Weiner A, et al. MAP kinase pathway alterations in BRAF-mutant melanoma patients with acquired resistance to combined RAF/MEK inhibition. Cancer Discov 2014;4:61-8.
Wainstein E, Seger R. The dynamic subcellular localization of ERK: mechanisms of translocation and role in various organelles. Curr Opin Cell Biol 2016;39:15-20.
WANG, H., et al. Identification of the MEK1(F129L) activating mutation as a potential mechanism of acquired resistance to MEK inhibition in human cancers carrying the B-RAF V600E mutation. Cancer Res (2011);71(16):5535-45.
YANG W, Soares J, Greninger P, Edelman EJ, Lightfoot H, Forbes S, et al. Genomics of Drug Sensitivity in Cancer (GDSC): a resource for therapeutic biomarker discovery in cancer cells. Nucleic Acids Res 2013;41:D955-D961.
YAO Z, Torres NM, Tao A, Gao Y, Luo L, Li Q, et al. BRAF Mutants Evade ERK-Dependent Feedback by Different Mechanisms that Determine Their Sensitivity to Pharmacologic Inhibition. Cancer Cell 2015;28:370-83.
YOHE S. Molecular genetic markers in acute myeloid leukemia. J Clin Med 2015;4:460-78.
ZELBORAF [package insert]. South San Francisco, CA: Genentech USA, Inc.; 2015.
Все документы, цитированные в настоящей заявке, включены в качестве ссылки в полном объеме.
Хотя в настоящем описании описаны иллюстративные варианты осуществления настоящего изобретения, следует понимать, что изобретение не ограничивается описанными вариантами осуществления и что различные другие изменения или модификации могут быть осуществлены специалистом в данной области без отклонения от объема и сущности изобретения.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ:
<110> Biomed Valley Discoveries, Inc.
<120> КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ С
АТИПИЧНЫМИ МУТАЦИЯМИ BRAF
<130> C065272/2391211
<140> US 62/506,995
<141> 2017-05-16
<160> 44
<210> 1
<211> 2949
<212> ДНК
<213> Homo sapiens
<400> 1
cgcctccctt ccccctcccc gcccgacagc ggccgctcgg gccccggctc tcggttataa
60
gatggcggcg ctgagcggtg gcggtggtgg cggcgcggag ccgggccagg ctctgttcaa
120
cggggacatg gagcccgagg ccggcgccgg cgccggcgcc gcggcctctt cggctgcgga
180
ccctgccatt ccggaggagg tgtggaatat caaacaaatg attaagttga cacaggaaca
240
tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa tatatctgga
300
ggcctatgaa gaatacacca gcaagctaga tgcactccaa caaagagaac aacagttatt
360
ggaatctctg gggaacggaa ctgatttttc tgtttctagc tctgcatcaa tggataccgt
420
tacatcttct tcctcttcta gcctttcagt gctaccttca tctctttcag tttttcaaaa
480
tcccacagat gtggcacgga gcaaccccaa gtcaccacaa aaacctatcg ttagagtctt
540
cctgcccaac aaacagagga cagtggtacc tgcaaggtgt ggagttacag tccgagacag
600
tctaaagaaa gcactgatga tgagaggtct aatcccagag tgctgtgctg tttacagaat
660
tcaggatgga gagaagaaac caattggttg ggacactgat atttcctggc ttactggaga
720
agaattgcat gtggaagtgt tggagaatgt tccacttaca acacacaact ttgtacgaaa
780
aacgtttttc accttagcat tttgtgactt ttgtcgaaag ctgcttttcc agggtttccg
840
ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaagttc cactgatgtg
900
tgttaattat gaccaacttg atttgctgtt tgtctccaag ttctttgaac accacccaat
960
accacaggaa gaggcgtcct tagcagagac tgccctaaca tctggatcat ccccttccgc
1020
acccgcctcg gactctattg ggccccaaat tctcaccagt ccgtctcctt caaaatccat
1080
tccaattcca cagcccttcc gaccagcaga tgaagatcat cgaaatcaat ttgggcaacg
1140
agaccgatcc tcatcagctc ccaatgtgca tataaacaca atagaacctg tcaatattga
1200
tgacttgatt agagaccaag gatttcgtgg tgatggagga tcaaccacag gtttgtctgc
1260
taccccccct gcctcattac ctggctcact aactaacgtg aaagccttac agaaatctcc
1320
aggacctcag cgagaaagga agtcatcttc atcctcagaa gacaggaatc gaatgaaaac
1380
acttggtaga cgggactcga gtgatgattg ggagattcct gatgggcaga ttacagtggg
1440
acaaagaatt ggatctggat catttggaac agtctacaag ggaaagtggc atggtgatgt
1500
ggcagtgaaa atgttgaatg tgacagcacc tacacctcag cagttacaag ccttcaaaaa
1560
tgaagtagga gtactcagga aaacacgaca tgtgaatatc ctactcttca tgggctattc
1620
cacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagct tgtatcacca
1680
tctccatatc attgagacca aatttgagat gatcaaactt atagatattg cacgacagac
1740
tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc tcaagagtaa
1800
taatatattt cttcatgaag acctcacagt aaaaataggt gattttggtc tagctacagt
1860
gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca ttttgtggat
1920
ggcaccagaa gtcatcagaa tgcaagataa aaatccatac agctttcagt cagatgtata
1980
tgcatttgga attgttctgt atgaattgat gactggacag ttaccttatt caaacatcaa
2040
caacagggac cagataattt ttatggtggg acgaggatac ctgtctccag atctcagtaa
2100
ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc tcaaaaagaa
2160
aagagatgag agaccactct ttccccaaat tctcgcctct attgagctgc tggcccgctc
2220
attgccaaaa attcaccgca gtgcatcaga accctccttg aatcgggctg gtttccaaac
2280
agaggatttt agtctatatg cttgtgcttc tccaaaaaca cccatccagg cagggggata
2340
tggtgcgttt cctgtccact gaaacaaatg agtgagagag ttcaggagag tagcaacaaa
2400
aggaaaataa atgaacatat gtttgcttat atgttaaatt gaataaaata ctctcttttt
2460
ttttaaggtg aaccaaagaa cacttgtgtg gttaaagact agatataatt tttccccaaa
2520
ctaaaattta tacttaacat tggattttta acatccaagg gttaaaatac atagacattg
2580
ctaaaaattg gcagagcctc ttctagaggc tttactttct gttccgggtt tgtatcattc
2640
acttggttat tttaagtagt aaacttcagt ttctcatgca acttttgttg ccagctatca
2700
catgtccact agggactcca gaagaagacc ctacctatgc ctgtgtttgc aggtgagaag
2760
ttggcagtcg gttagcctgg gttagataag gcaaactgaa cagatctaat ttaggaagtc
2820
agtagaattt aataattcta ttattattct taataatttt tctataacta tttcttttta
2880
taacaatttg gaaaatgtgg atgtctttta tttccttgaa gcaataaact aagtttcttt
2940
ttataaaaa
2949
<210> 2
<211> 766
<212> БЕЛОК
<213> Homo sapiens
<400> 2
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Ala Glu Pro Gly Gln
1 5 10 15
Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala Gly Ala Gly
20 25 30
Ala Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp
35 40 45
Asn Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu
50 55 60
Leu Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu
65 70 75 80
Ala Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu
85 90 95
Gln Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser
100 105 110
Ser Ser Ala Ser Met Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu
115 120 125
Ser Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val
130 135 140
Ala Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe
145 150 155 160
Leu Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr
165 170 175
Val Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro
180 185 190
Glu Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile
195 200 205
Gly Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val
210 215 220
Glu Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys
225 230 235 240
Thr Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe
245 250 255
Gln Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys
260 265 270
Ser Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu
275 280 285
Leu Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu
290 295 300
Ala Ser Leu Ala Glu Thr Ala Leu Thr Ser Gly Ser Ser Pro Ser Ala
305 310 315 320
Pro Ala Ser Asp Ser Ile Gly Pro Gln Ile Leu Thr Ser Pro Ser Pro
325 330 335
Ser Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp
340 345 350
His Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn
355 360 365
Val His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg
370 375 380
Asp Gln Gly Phe Arg Gly Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala
385 390 395 400
Thr Pro Pro Ala Ser Leu Pro Gly Ser Leu Thr Asn Val Lys Ala Leu
405 410 415
Gln Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser
420 425 430
Glu Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp
435 440 445
Asp Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly
450 455 460
Ser Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val
465 470 475 480
Ala Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln
485 490 495
Ala Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn
500 505 510
Ile Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val
515 520 525
Thr Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile
530 535 540
Glu Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr
545 550 555 560
Ala Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp
565 570 575
Leu Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile
580 585 590
Gly Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His
595 600 605
Gln Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val
610 615 620
Ile Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr
625 630 635 640
Ala Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr
645 650 655
Ser Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly
660 665 670
Tyr Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala
675 680 685
Met Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg
690 695 700
Pro Leu Phe Pro Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser
705 710 715 720
Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala
725 730 735
Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys
740 745 750
Thr Pro Ile Gln Ala Gly Gly Tyr Gly Ala Phe Pro Val His
755 760 765
<210> 3
<211> 3906
<212> ДНК
<213> Rattus norvegicus
<400> 3
atggcggcgc tgagtggcgg cggtggcagc agcagcggtg gcggtggcgg cggcggcggc
60
ggcggtggtg gcggcggcgg cggcggcgcc gaacagggac aggctctgtt caatggcgac
120
atggagccgg aggccggcgc tggcgccgcg gcctcttcgg ccgcggaccc ggccattcct
180
gaagaggtgt ggaatatcaa gcaaatgatt aagttgacac aggaacatat agaggcccta
240
ttggacaagt ttggtgggga gcataaccca ccgtcaatat acctggaggc ctatgaagag
300
tacaccagca agctagatgc ccttcagcag agagagcagc agctgttgga atccctggtt
360
tttcaaactc ccacagatgt atcacggaac aaccccaagt caccacagaa acctatcgtt
420
cgtgtcttcc tgcccaacaa acagaggaca gtggtgcccg caagatgtgg tgtaacggtc
480
cgagacagtc taaagaaagc actaatgatg aggggtctca tcccagagtg ctgtgctgtt
540
tacagaattc aggacggaga gaagaaacca attggctggg acactgacat ttcctggctt
600
actggagagg agctacatgt tgaagtacta gagaatgttc ctctgacaac ccacaacttc
660
gtacggaaaa cttttttcac cttagcattt tgtgactttt gccgaaagct gcttttccag
720
ggtttccgct gtcaaacatg tggttataag tttcaccagc gttgtagtac agaggttcca
780
ctgatgtgtg ttaattatga ccaacttgat ttgctgtttg tctccaagtt ctttgagcat
840
cacccagtac cacaggagga ggccttctca gcagagacta cccttccatc tggatgctct
900
tccgcacccc cctcagactc tattgggccc caaatcctca ccagtccatc tccttcaaaa
960
tccattccaa ttccacagcc cttccggcca gcagatgaag atcatcgcaa tcagtttggg
1020
caacgagacc gctcctcctc cgctcccaat gttcatataa acacaatcga acctgtcaat
1080
attgatgaaa aattcccaga agtggaatta caggatcaaa gggatttgat tagagaccag
1140
gggtttcgtg gggatggagc ccctttgaac cagctgatgc gctgtcttcg gaaataccaa
1200
tcccggactc ccagccccct cctccattct gtccccagtg aaatagtgtt tgattttgag
1260
cctggcccag tgttcagagg gtcaaccaca ggcttgtcgg ccaccccacc tgcctcatta
1320
cctggctcac tcactaacgt gaaagcctta cagaaatctc caggacctca gcgggaaagg
1380
aagtcctcct cctcctcctc ctccacggaa gacagaagtc ggatgaaaac acttggtaga
1440
agagattcaa gtgatgattg ggagattcct gatggacaga ttacagtggg acagagaatt
1500
ggatctgggt cctttggaac tgtctacaag ggaaagtggc atggcgacgt ggcagtgaaa
1560
atgctgaatg tgacagcacc cacacctcag cagttacagg ccttcaaaaa cgaagtcgga
1620
gtactcagga aaactcgaca tgtgaacatc ctccttttca tgggctattc tacaaagcca
1680
cagctggcta ttgttacaca gtggtgtgaa ggctccagct tatatcacca tctccacatc
1740
attgagacca aatttgagat gatcaaactt atagatattg cacggcagac tgcacagggc
1800
atggattact tacacgccaa gtcaatcatc cacagagacc tcaagagtaa taatatattt
1860
cttcatgaag acctcacggt aaaaataggt gactttggtt tagccacagt gaagtcccga
1920
tggagtgggt cccatcagtt tgaacagttg tctggatcta ttttgtggat ggcacccgaa
1980
gtaatcagaa tgcaagataa aaacccatat agctttcagt cagacgtgta tgcatttggg
2040
attgttctgt atgaactgat gactggtcag ctaccttatt caaacatcaa caacagggat
2100
cagataattt ttatggtggg acgaggatac ctatctccag atctcagtaa ggtacggagt
2160
aactgtccaa aagccatgaa gagattaatg gcagagtgcc tcaaaaagaa aagagacgag
2220
agaccactct ttccccaaat tctcgcctct attgagctgc tggcccgctc attgccaaaa
2280
attcaccgca gtgcatcaga accctccttg aatcgggctg gtttccaaac agaagatttt
2340
agtctgtatg cttgtgcttc tccaaaaaca cccatccaag cagggggata tggagaattt
2400
gcagccttca agtagccact ccatcatggc agcatctact ctttatttct taagtcttgt
2460
gttcatacaa tttgttaaca tcaaaacaca gttctgttcc tcaaattttt tttaaagata
2520
caaaattttc aatgcataag ctcgtgtgga acagaatgga atttcctatt caacaaaaga
2580
gggaagaatg ttttaggaac cagaattctc tgctgcccgt gtttcttctt caacacaaat
2640
atcatgtgca tacaactctg cccattccca agaagaaaga ggagagaccc cgaattctgc
2700
ccttttggtg gtcaggcatg atggaaagaa tttgctgctg cagcttggga aaaattgcta
2760
tggaaagtct gccagtcaac tttgcccttc taaccaccag atccatttgt ggctggtcat
2820
ctgatggggc gatttcaatc accaagcatc gttcttgcct gttgtgggat tatgtcgtgg
2880
agcactttcc ctatccacca ccgttaattt ccgagggatg gagtaaatgc agcataccct
2940
ttgtgtagca cctgtccagt cctcaaccaa tgctatcaca gtgaagctct ttaaatttaa
3000
gtggtgggtg agtgttgagg agagactgcc ttgggggcag agaaaagggg atgctgcatc
3060
ttcttcctca cctccagctc tctcacctcg ggttgccttg cacactgggc tccgcctaac
3120
cactcgggct gggcagtgct ggcacacatt gccgcctttt ctcattgggt ccagcaattg
3180
agcagagggt tgggggattg tttcctccac aatgtagcaa attctcagga aaatacagtc
3240
catatcttcc tctcagctct tccagtcacc aaatacttac gtggctcctt tgtccaggac
3300
ataaaacacc gtggacaaca cctaattaaa agcctacaaa actgcttact gacagttttg
3360
aatgtgagac atttgtgtaa tttaaatgta aggtacaggt cttaatttct tctattaagt
3420
ttcttctatt tttatttaaa cgaagaaaat aattttcagg tttaattgga ataaacgaat
3480
acttcccaaa agactatata ccctgaaaat tatatttttg ttaattgtaa acaactttta
3540
aaaaatggtt attatccttt tctctaccta aaattatggg aaatcttagc ataatgacaa
3600
ttatttatac tttttaaata aatggtactt gctggatcca cactaacatc tttgctaaca
3660
ttcccattgt ttcttccaac ttcactccta cactacatcc tccatcctct ttctagtctt
3720
ttatctataa tatgcaacct aaaataaaag tggtggtgtc tccattcatt cttcttcttc
3780
cttttttccc caagcctggt cttcaaaagg ttgggtaatt tagtagctga gttccctagg
3840
tagaaataga actattaggg acattggggt tgtaggaaag cgtgaggcct gtcaccagtt
3900
gttctt
3906
<210> 4
<211> 804
<212> БЕЛОК
<213> Rattus norvegicus
<400> 4
Met Ala Ala Leu Ser Gly Gly Gly Gly Ser Ser Ser Gly Gly Gly Gly
1 5 10 15
Gly Gly Gly Gly Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu Gln
20 25 30
Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala Gly
35 40 45
Ala Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp
50 55 60
Asn Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu
65 70 75 80
Leu Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu
85 90 95
Ala Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu
100 105 110
Gln Gln Leu Leu Glu Ser Leu Val Phe Gln Thr Pro Thr Asp Val Ser
115 120 125
Arg Asn Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
130 135 140
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
145 150 155 160
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
165 170 175
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
180 185 190
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
195 200 205
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
210 215 220
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
225 230 235 240
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
245 250 255
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
260 265 270
Phe Val Ser Lys Phe Phe Glu His His Pro Val Pro Gln Glu Glu Ala
275 280 285
Phe Ser Ala Glu Thr Thr Leu Pro Ser Gly Cys Ser Ser Ala Pro Pro
290 295 300
Ser Asp Ser Ile Gly Pro Gln Ile Leu Thr Ser Pro Ser Pro Ser Lys
305 310 315 320
Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His Arg
325 330 335
Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val His
340 345 350
Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Glu Lys Phe Pro Glu Val
355 360 365
Glu Leu Gln Asp Gln Arg Asp Leu Ile Arg Asp Gln Gly Phe Arg Gly
370 375 380
Asp Gly Ala Pro Leu Asn Gln Leu Met Arg Cys Leu Arg Lys Tyr Gln
385 390 395 400
Ser Arg Thr Pro Ser Pro Leu Leu His Ser Val Pro Ser Glu Ile Val
405 410 415
Phe Asp Phe Glu Pro Gly Pro Val Phe Arg Gly Ser Thr Thr Gly Leu
420 425 430
Ser Ala Thr Pro Pro Ala Ser Leu Pro Gly Ser Leu Thr Asn Val Lys
435 440 445
Ala Leu Gln Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser
450 455 460
Ser Ser Ser Ser Thr Glu Asp Arg Ser Arg Met Lys Thr Leu Gly Arg
465 470 475 480
Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp Gly Gln Ile Thr Val
485 490 495
Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys
500 505 510
Trp His Gly Asp Val Ala Val Lys Met Leu Asn Val Thr Ala Pro Thr
515 520 525
Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val Gly Val Leu Arg Lys
530 535 540
Thr Arg His Val Asn Ile Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro
545 550 555 560
Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly Ser Ser Leu Tyr His
565 570 575
His Leu His Ile Ile Glu Thr Lys Phe Glu Met Ile Lys Leu Ile Asp
580 585 590
Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr Leu His Ala Lys Ser
595 600 605
Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile Phe Leu His Glu Asp
610 615 620
Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala Thr Val Lys Ser Arg
625 630 635 640
Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp
645 650 655
Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe
660 665 670
Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu Tyr Glu Leu Met Thr
675 680 685
Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe
690 695 700
Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu Ser Lys Val Arg Ser
705 710 715 720
Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala Glu Cys Leu Lys Lys
725 730 735
Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Ile Leu Ala Ser Ile Glu
740 745 750
Leu Leu Ala Arg Ser Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro
755 760 765
Ser Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala
770 775 780
Cys Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly Gly Tyr Gly Glu Phe
785 790 795 800
Ala Ala Phe Lys
<210> 5
<211> 9728
<212> ДНК
<213> Mus musculus
<400> 5
ccctcaggct cggctgcgcc ggggccgccg gcgggttcca gaggtggcct ccgccccggc
60
cgctccgccc acgccccccg cgcctccgcg cccgcctccg cccgccctgc gcctcccttc
120
cccctccccg ccccgcggcg gccgctcggc ccggctcgcg cttcgaagat ggcggcgctg
180
agtggcggcg gtggcagcag cagcggtggc ggcggcggcg gtggcggcgg cggtggcggt
240
ggcgacggcg gcggcggcgc cgagcagggc caggctctgt tcaatggcga catggagccg
300
gaggccggcg ctggcgccgc ggcctcttcg gctgcggacc cggccattcc tgaagaggta
360
tggaatatca agcaaatgat taagttgaca caggaacata tagaggccct attggacaaa
420
tttggtggag agcataaccc accatcaata tacctggagg cctatgaaga gtacaccagc
480
aagctagatg cccttcagca aagagaacag cagcttttgg aatccctggt ttttcaaact
540
cccacagatg catcacggaa caaccccaag tcaccacaga aacctatcgt tagagtcttc
600
ctgcccaaca aacagaggac agtggtaccc gcaagatgtg gtgttacagt tcgagacagt
660
ctaaagaaag cactgatgat gagaggtctc atcccagaat gctgtgctgt ttacagaatt
720
caggatggag agaagaaacc aattggctgg gacacggaca tttcctggct tactggagag
780
gagttacatg ttgaagtact ggagaatgtc ccacttacaa cacacaactt tgtacggaaa
840
acttttttca ccttagcatt ttgtgacttt tgccgaaagc tgcttttcca gggtttccgt
900
tgtcaaacat gtggttataa atttcaccag cgttgtagta cagaggttcc actgatgtgt
960
gtaaattatg accaacttga tttgctgttt gtctccaagt tctttgagca tcacccagta
1020
ccacaggagg aggcctcctt cccagagact gcccttccat ctggatcctc ttccgcaccc
1080
ccctcagact ctactgggcc ccaaatcctc accagtccat ctccttcaaa atccattcca
1140
attccacagc ccttccgacc agcagatgaa gatcatcgca atcagtttgg gcaacgagac
1200
cggtcctcct cagctcccaa tgttcatata aacacaattg agcctgtgaa tatcgatgaa
1260
aaattcccag aagtggaatt acaggatcaa agggatttga ttagagacca ggggtttcgt
1320
ggtgatggag cccccttgaa ccaactgatg cgctgtcttc ggaaatacca atcccggact
1380
cccagccccc tcctccattc tgtccccagt gaaatagtgt ttgattttga gcctggccca
1440
gtgttcagag ggtcaaccac aggcttgtcc gccaccccgc ctgcctcatt acctggctca
1500
ctcactaacg tgaaagcctt acagaaatct ccaggtcctc agcgggaaag gaagtcatct
1560
tcttcctcat cctcggagga cagaagtcgg atgaaaacac ttggtagaag agattcaagt
1620
gatgactggg agattcctga tggacagatt acagtgggac agagaattgg atctgggtca
1680
tttggaactg tctacaaggg aaagtggcat ggtgatgtgg cagtgaaaat gttgaatgtg
1740
acagcaccca cacctcaaca gctacaggcc ttcaaaaatg aagtaggagt gctcaggaaa
1800
actcgacatg tgaatatcct ccttttcatg ggctattcta caaagccaca actggcaatt
1860
gttacacagt ggtgtgaggg ctccagctta tatcaccatc tccacatcat tgagaccaaa
1920
tttgagatga tcaaacttat agatattgct cggcagactg cacagggcat ggattactta
1980
cacgccaagt caatcatcca cagagacctc aagagtaata atatatttct tcatgaagac
2040
ctcacggtaa aaataggtga ctttggtcta gccacagtga aatctcggtg gagtgggtcc
2100
catcagtttg aacagttgtc tggatctatt ttgtggatgg caccagaagt aatcagaatg
2160
caagataaaa acccgtatag ctttcagtca gacgtgtatg cgtttgggat tgttctgtac
2220
gaactgatga ccggccagct accttattca aacatcaaca acagggatca gataattttt
2280
atggtgggac gaggatacct atctccagat ctcagtaagg tacggagtaa ctgtccaaaa
2340
gccatgaaga gattaatggc agagtgcctc aaaaagaaaa gagacgagag accactcttt
2400
ccccaaattc tcgcctccat tgagctgctg gcccgctcat tgccaaaaat tcaccgcagt
2460
gcatcagaac cttccttgaa tcgggctggt ttccaaacag aagattttag tctgtatgct
2520
tgtgcttctc cgaaaacacc catccaagca gggggatatg gagaatttgc agccttcaag
2580
tagccagtcc atcatggcag catctactct ttatttctta agtcttgtgt tcatacagtt
2640
tgttaacatc aaaacacagt tctgttcctc aaaaaatttt ttaaagatac aaaattttca
2700
atgcataagt tcatgtggaa cagaatggaa tttcctattc aacaaaagag ggaagaatgt
2760
tttaggaacc agaattctct gctgcccgtg tttcttcttc aacataacta tcacgtgcat
2820
acaagtctgc ccattcccaa gaagaaagag gagagaccct gaattctgcc cttttggtgg
2880
tcaggcatga tggaaagaat ttgctgctgc agcttgggaa aattgctatg gaaagtctgc
2940
cagtcgactt tgcccttcta accaccagat cagcctgtgg ctggtcatct gatggggcga
3000
tttccatcac caagcatcgt tcttgcctat tctgggatta tgttgtggag cactttccct
3060
gtccagcacc gttcatttct gagggatgga gtaaatgcag cattcccttg tgtagcgcct
3120
gttcagtcct cagcagctgc tgtcacagcg aagcttttta cagttaagtg gtgggggaga
3180
gttgaggaga gcctgcctcg gggcagagaa aagggggtgc tgcatcttct tcctcacctc
3240
cagctctctc acctcgggtt gccttgctca ctgggctccg cctaaccact caggctgctc
3300
agtgctggca cacattgcct tcttttctca ttgggtccag caattgagga gagggttggg
3360
ggattgtttc ctcctcaatg tagcaaattc tcaggaaaat acagtccata tcttcctctc
3420
agctcttcca gtcaccaaat acttacgtgg ctcctttgtc caggacataa aacaccgtgg
3480
acaacaccta attaaaagcc tacaaaactg cttactgaca gttttgaatg tgagacactt
3540
gtgtaattta aatgtaaggt acaggtttta atttctgagt ttcttctatt tttatttaaa
3600
agaagaaaat aattttcagt tttaattgga ataaatgagt acttcccaca agactatata
3660
ccctgaaaat tatatttttg ttaattgtaa acaactttta aagaataatt attatccttt
3720
tctctaccta aaaattatgg ggaatcttag cataatgaca attatttata ctttttaaat
3780
aaatggtact tgctggatcc acactaacat ctttgctaac aatcccattg tttcttccaa
3840
cttaactcct acactacatc ctacatcctc tttctagtct tttatctata atatgcaacc
3900
taaaataaac gtggtggcgt ctccattcat tctccctctt cctgttttcc ccaagcctgg
3960
tcttcaaaag gttgggtaat cggtccctga gctccctagc tggcaatgca actattaggg
4020
acattggagt tgcaggagag caggaagcct gtccccagct gttcttctag aaccctaaat
4080
cttatctttg cacagatcaa aagtatcacc tcgtcacagt tctccttagc ctttacttac
4140
aggtaatata aataaaaatc accatagtag taaagaaaac aactggatgg attgatgacc
4200
agtacctctc agagccagga atcttgaatc tccaggattt atacgtgcaa atttaaggag
4260
atgtacttag caacttcaag ccaagaactt ccaaaatact agcgaatcta aaataaaatg
4320
gaattttgag ttatttttaa agttcaaatt ataattgata ccactatgta tttaagccta
4380
ctcacagcaa gttagatgga ttttgctaaa ctcattgcca gactgtggtg gtggtggtgg
4440
tagtgtgcac ctttaatcca agcaactcag caatcagaat gaggtaaatc tctgtgaata
4500
caaggcctgc ctagtctgca gcgctagttc caggatagcc agggctacac acacaaaaac
4560
cctctctcaa aaaaaacaaa attaattagt tgataataaa aaataactaa agtatcatca
4620
aaggaaggcc tactggaagt tttatatatt cccagtaaat tgaaaaatat tctgaagtta
4680
ttaaccagtt agcaacaatg tgtttttaag tcttacataa acagagcaaa gtcttcaaat
4740
gtttcagagc tgagaagata attgtgcttg atatgaaaaa tagcctctcc atatgatgtg
4800
ccacattgaa aggcgtcatt acccttttaa atacttctta atgtggcttt gttcccttta
4860
cccaggatta gctagaaaga gctaggtagg cttcggccac agttgcacat ttcgggcctg
4920
ctgaagaatg ggagctttga aggctggcct tggtggagga gcccctcagt gctggagggt
4980
ggggcgtgta cgcagcatgg aagtggtcta gacagagtgc aaagggacag acttctttct
5040
cattttagta tagggtgatg tctcacttga aatgagaaag tagagttgat attaaacgaa
5100
gctgtgccca gaaaccaggc tcagggtatt gtgagatttt ctttttaaat agagaatata
5160
aaagatagaa ataaatattt aaaccttcct tcttattttc tatcaaatag atttttttta
5220
tcatttgcaa acaacataaa aaaaggtttc ttttgtgggg ttttctttcc ttcttttttt
5280
tttttttttt tttttaagac tgcagataat cttgttgagc tcctcggaaa atacaaggaa
5340
gtccgtgttt gtgcagagcg ctttatgagt aactgtatag acagtgtggc tgcttcactc
5400
atcccagagg gctgcagctg tcggcccatg aagtggctgc agtgcctcgt gagatctgct
5460
ttgttttgtt tggagtgaag tctttgaaag gtttgagtgc aactatatag gactgttttt
5520
aaataagtag tattcctcat gaactttctc attgttaagc tacaggaccc aaactctacc
5580
actaagatat tattaacctc aaaatgtagt ttatagaagg aatttgcaaa tagaatatcc
5640
agttcgtact tatatgcatc ttcaacaaag attctctgtg acttgttgga tttggttcct
5700
gaacagccca tttctgtatt tgaggttagg agggcataat gaggcatcct aaaagacaat
5760
ctgatataaa ctgtatgcta gatgtatgct ggtaggggag aaagcattct gtaaagacat
5820
gatttaagac ttcagctctg tcaaccagaa accttgtaaa tacttcctgt cttggtgcag
5880
ccccgcccct ttgatcacac gatgttgtct tgtgcttgtc agacactgtc agagctgctg
5940
ttcgtccctc tgcagatctc acctgtcccc actgcacacc cacctcctgc ctcttgcaga
6000
cctcagcatc tagctttagt tggaaacagt tcagggttca ggtgacttct taaaaaaaaa
6060
aaaaaaccct acctcctcag aatgaggtaa tgaatagtta tttatttaaa gtatgaagag
6120
tcaggagcgc tcgaacatga aggtgattta agatggttcc tttcgtgtgt attgtagctg
6180
agcacttgtt tttgtcctaa agggcattat acatttaagc agtgattctg tttaaagatg
6240
tttttcttta aaggtgtagc tcagagtatc tgttgttgga attggtgcca gagtctgctt
6300
aatagatttc agaatcctaa gcttaagtca gtcgcatgaa gttaagtagt tatggtaaca
6360
ctttgctagc catgatataa ttctactttt taggagtagg tttggcaaaa ctgtatgcct
6420
tcaaagtgag ttggccacag ctttgtcaca tgcacagata ctcatctgaa gagactgccc
6480
agctaagagg gcggaaggat accctttttt cctacgattc gcttctttgt ccacgttggc
6540
attgttagta ctagtttatc agcaccttga ccagcagatg tcaaccaata agctattttt
6600
aaaaccatag ccagagatgg agaggtcact gtgagtagaa acagcaggac gcttacagga
6660
gtgaaatggt gtagggaggc tctagaaaaa tatcttgaca atttgccaaa tgatcttact
6720
gtgccttcat gatgcaataa aaaagctaac attttagcag aaatcagtga tttacgaaga
6780
gagtggccag tctggtttaa ctcagctggg ataatatttt tagagtgcaa tttagactgc
6840
gaagataaat gcactaaaga gtttatagcc aattcacatt tgaaaaataa gaaaatggta
6900
aattttcagt gaaatatttt tttaaagcac ataatcccta gtgtagccag aaatatttac
6960
cacatagagc agctaggctg agatacagtc cagtgacatt tctagagaaa ccttttctac
7020
tcccacgggc tcctcaaagc atggaaattt tatacaaaat gtttgacatt ttaagatact
7080
gctgtagttt agttttgaaa tagtatgtgc tgagcagcaa tcatgtacta actcagagag
7140
agaaaacaac aacaaattgt gcatctgatt tgttttcaga gaaatgctgc caacttagat
7200
actgagttct cagagcttca agtgtaaact tgcctcccaa gtcctgtttg caaatgaagt
7260
tggctagtgc tactgactgc tccagcacat gatggaaggc agggggctgt ctctgaagtg
7320
tcttctataa agggacaata gaatagtgag agacctggtc agtgtgtgtc agctggacac
7380
tccatgctat gggacttgca tcttctgtcc tcaccatccc caagacattg tgctttcctc
7440
agttgtcctc tagctgtttc actcagacac caagatgaat tactgatgcc agaaggggcc
7500
aaaatggcca gtgtgttttg ggggttgtat cagttgactg gacaataact ttaatagttt
7560
cagatcattt atttttactt ccattttgac agacatttaa atggaaattt agtcctaact
7620
tttgtcattt gaaaggaaaa attaacagtt cctataagat acttttgagg tggaatctga
7680
catcctaatt ttttttcttt tcagtgggtt tgcagcgagg gtcttgtatg cactaggcaa
7740
gggttctacc actaagccac atttcccagg aaataaaatg ttaacagtta aaacatacac
7800
acaaatacac aaacacctta ttaccacttt agtaaagtga gagatgtgcg tcctttgtct
7860
cagtctccac gatttcagct gccccttgta tgaataactc agtctcgcta aactgtttac
7920
ttttatttac ctggtttgac tagttgcagc tatataacca gttgtgcatg aggacaacag
7980
ccagtgtgtt tgttttgttt ttggtttttt gtggtacatt ttttgtaaag aattctgtag
8040
attgaagtgc tctttgaaaa cagaactgag atatatttat tcttgttagc atcaaaaaac
8100
attttgtgca aatgatttgc ttttcctggc aggctgagta ccatatccag cgcccacaat
8160
tgcgggttcc catctaccat gtccacaggg gagacagacg ggaagcacat gaggggtgtg
8220
tttacagagt tgtaggagtt atgtagttct cttgttgcct tggaaatcac tgttgtttta
8280
agactgttga acccgtgtgt ttggctgggc tgtgagttac atgaagaaac tgcaaactag
8340
catatgcaga caaagctcac agactaggcg taaatggagg aaaatggacc aaaataaggc
8400
agggtgacac ataaaccttg ggcttcggag aaaactaagg gtggagatga actataatca
8460
cctgaataca atgtaagagt gcaataagtg tgcttattct aagctgtgaa cttcttttaa
8520
atcattcctt tctaatacat ttatgtatgt tccattgctg actaaaacca gctatgagaa
8580
catatgcctt tttattcatg ttaactacca gtttaagtgg ctaaccttaa tgtcttattt
8640
atcttcattt tgtattagtt tacataccag gtatgtgtgt gtgctgtact cttcttccct
8700
ttatttgaaa acacttttca ctgggtcatc tccttggcca ttccacaaca caactttggt
8760
ttggctttca atgtcacctt atttgatggc ctgtgtccca gtagcagaat ttatggtatt
8820
cccattgctg gctgctcttc cgaccctttg cttctacagc acttgtctct cctaagatag
8880
tcagaaacta actgatcagg ggatggactt caccattcat cgtgtctctt caattctatt
8940
aaatagacca ctcttgggct ttagaccagg aaaaaggaga cagctctagc catctaccaa
9000
gcctcaccct aaaaggtcac ccgtacttct tggtctgagg acaagtctcc actccagtaa
9060
gggagagggg aggaaatgct tcctgtttga aatgcagtga attcctatgg ctcctgtttc
9120
accacccgca cctatggcaa cccatataca ttcctcttgt ctgtaactgc caaaggttgg
9180
gtttatgtca cttcagttcc actcaagcat tgaaaaggtt ctcatggagt ctggggtgtg
9240
cccagtgaaa agatggggac tttttcatta tccacagacc tctctatacc tgctttgcaa
9300
aaattataat ggagtaacta tttttaaagc ttatttttca attcataaga aaaagacatt
9360
tattttcaat caaatggatg atgtctctta tcccttatcc ctcaatgttt gcttgaattt
9420
tgtttgttcc ctatacctac tccctaattc tttagttcct tcctgctcag gtcccttcat
9480
ttgtactttg gagtttttct catgtaaatt tgtataatgg aaaatattgt tcagtttgga
9540
tagaaagcat ggagaaataa ataaaaaaag atagctgaaa atcaaattga agaaatttat
9600
ttctgtgtaa agttatttaa aaactctgta ttatatttaa agaaaaaagc ccaacccccc
9660
aaaaagtgct atgtaattga tgtgaatatg cgaatactgc tataataaag attgactgca
9720
tggagaaa
9728
<210> 6
<211> 804
<212> БЕЛОК
<213> Mus musculus
<400> 6
Met Ala Ala Leu Ser Gly Gly Gly Gly Ser Ser Ser Gly Gly Gly Gly
1 5 10 15
Gly Gly Gly Gly Gly Gly Gly Gly Gly Asp Gly Gly Gly Gly Ala Glu
20 25 30
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
35 40 45
Gly Ala Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val
50 55 60
Trp Asn Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala
65 70 75 80
Leu Leu Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu
85 90 95
Glu Ala Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg
100 105 110
Glu Gln Gln Leu Leu Glu Ser Leu Val Phe Gln Thr Pro Thr Asp Ala
115 120 125
Ser Arg Asn Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe
130 135 140
Leu Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr
145 150 155 160
Val Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro
165 170 175
Glu Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile
180 185 190
Gly Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val
195 200 205
Glu Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys
210 215 220
Thr Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe
225 230 235 240
Gln Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys
245 250 255
Ser Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu
260 265 270
Leu Phe Val Ser Lys Phe Phe Glu His His Pro Val Pro Gln Glu Glu
275 280 285
Ala Ser Phe Pro Glu Thr Ala Leu Pro Ser Gly Ser Ser Ser Ala Pro
290 295 300
Pro Ser Asp Ser Thr Gly Pro Gln Ile Leu Thr Ser Pro Ser Pro Ser
305 310 315 320
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
325 330 335
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
340 345 350
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Glu Lys Phe Pro Glu
355 360 365
Val Glu Leu Gln Asp Gln Arg Asp Leu Ile Arg Asp Gln Gly Phe Arg
370 375 380
Gly Asp Gly Ala Pro Leu Asn Gln Leu Met Arg Cys Leu Arg Lys Tyr
385 390 395 400
Gln Ser Arg Thr Pro Ser Pro Leu Leu His Ser Val Pro Ser Glu Ile
405 410 415
Val Phe Asp Phe Glu Pro Gly Pro Val Phe Arg Gly Ser Thr Thr Gly
420 425 430
Leu Ser Ala Thr Pro Pro Ala Ser Leu Pro Gly Ser Leu Thr Asn Val
435 440 445
Lys Ala Leu Gln Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser
450 455 460
Ser Ser Ser Ser Ser Glu Asp Arg Ser Arg Met Lys Thr Leu Gly Arg
465 470 475 480
Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp Gly Gln Ile Thr Val
485 490 495
Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys
500 505 510
Trp His Gly Asp Val Ala Val Lys Met Leu Asn Val Thr Ala Pro Thr
515 520 525
Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val Gly Val Leu Arg Lys
530 535 540
Thr Arg His Val Asn Ile Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro
545 550 555 560
Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly Ser Ser Leu Tyr His
565 570 575
His Leu His Ile Ile Glu Thr Lys Phe Glu Met Ile Lys Leu Ile Asp
580 585 590
Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr Leu His Ala Lys Ser
595 600 605
Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile Phe Leu His Glu Asp
610 615 620
Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala Thr Val Lys Ser Arg
625 630 635 640
Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp
645 650 655
Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe
660 665 670
Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu Tyr Glu Leu Met Thr
675 680 685
Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe
690 695 700
Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu Ser Lys Val Arg Ser
705 710 715 720
Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala Glu Cys Leu Lys Lys
725 730 735
Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Ile Leu Ala Ser Ile Glu
740 745 750
Leu Leu Ala Arg Ser Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro
755 760 765
Ser Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala
770 775 780
Cys Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly Gly Tyr Gly Glu Phe
785 790 795 800
Ala Ala Phe Lys
<210> 7
<211> 2232
<212> ДНК
<213> Oryctolagus cuniculus
<400> 7
atggggaatg tgtggaatat caaacaaatg attaagttga cacaggagca tatagaggcc
60
ctattggaca aatttggtgg ggagcataat ccaccatcaa tatatctgga ggcctacgaa
120
gaatacacca gcaagctaga tgccctccaa caaagagaac agcagttatt ggaatcccta
180
gtttttcaaa atcccacaga tgtgtcacgg agcaacccca agtcaccaca aaaacctatt
240
gttagagtct tcctgcccaa caaacagagg acagtggtac ctgcaagatg tggagttacg
300
gttcgagaca gtctaaagaa agcgctgatg atgagaggtc tgatcccaga atgctgtgct
360
gtttacagaa ttcaggatgg agagaagaag ccaattggct gggacactga tatttcctgg
420
ctcactggag aagagctgca tgtggaagtg ttagagaatg tcccactcac cacacataac
480
tttgtacgga aaactttttt caccttagca ttttgtgact tctgtagaaa gctgcttttc
540
cagggtttcc gctgtcaaac atgtggctac aaatttcacc agcgttgtag tacggaagtt
600
ccactgatgt gtgttaatta tgaccaactt gatttgctgt ttgtctccaa gttctttgaa
660
caccacccag taccacagga ggaggcctcc ttagcagaga ctgccctcac atctgggtca
720
tcgccttccg cacctccctc agactctatt gggcaccaaa ttctcaccag tccgtcccct
780
tcaaaatcca ttccgattcc acagtccttc cgaccagcag atgaagatca tcgaaatcag
840
tttgggcaac gagaccggtc ttcatcagcg cctaatgttc acattaacac aatagaacct
900
gtcaatattg atgaaaaatt cccagaagtg gaattacagg atcaaaggga cttgattaga
960
gaccaagggt ttcgtggtga tggagcccct ttgaaccagc tgatgcgctg tcttcggaaa
1020
taccaatccc ggactcccag tcccctccta ccttctgtcc ccagtgacat agtgtttgat
1080
tttgagcctg gcccagtgtt cagaggatcg accacgggtt tgtctgccac tccccctgcc
1140
tcattacctg gctcactcac tagtgtgaaa gctgtacaga gatccccagg acctcagcga
1200
gagaggaagt cgtcttcctc ctcagaagac aggaatcgaa tgaaaactct tggtagacgg
1260
gattcaagtg atgattggga gattcctgat gggcagatca ccgtgggaca gagaattgga
1320
tctggatcat ttggaaccgt ctacaaggga aaatggcacg gtgatgtggc agtaaaaatg
1380
ttgaatgtga cagcacctac acctcagcag ttacaggcct tcaaaaatga agtaggagta
1440
ctcaggaaaa cacgacatgt gaatatccta cttttcatgg gctattccac aaagccacag
1500
ctggctattg ttacccagtg gtgtgagggc tccagtttat atcaccatct ccacatcatt
1560
gagaccaaat tcgagatgat caaacttata gatattgcac ggcagactgc acagggcatg
1620
gattacttac acgccaagtc aatcatccac agagacctca agagtaataa tatatttctt
1680
catgaagacc tcacagtaaa aataggtgat tttggtctag ccacagtgaa atctcgatgg
1740
agtgggtccc atcagtttga acaattgtct ggatccattt tgtggatggc accagaagta
1800
atcagaatgc aagacaaaaa cccatatagc tttcagtcag atgtatatgc atttgggatt
1860
gttctgtatg aattgatgac tgggcagtta ccttactcaa acatcaacaa cagggaccag
1920
atcattttta tggtgggacg tggctacctg tctccagacc tcagtaaggt acggagtaac
1980
tgtccgaaag ccatgaagag attaatggca gagtgcctca aaaagaaaag agatgagaga
2040
ccactctttc cccaaattct cgcctccatt gagctgctgg cccgctcatt gccaaaaatc
2100
caccgcagtg catcagaacc ctccttgaat cgggctggtt tccagacaga ggattttagt
2160
ctatatgctt gtgcttctcc aaaaacaccc atccaggcag ggggatatgg agaatttgca
2220
gccttcaagt ag
2232
<210> 8
<211> 743
<212> БЕЛОК
<213> Oryctolagus cuniculus
<400> 8
Met Gly Asn Val Trp Asn Ile Lys Gln Met Ile Lys Leu Thr Gln Glu
1 5 10 15
His Ile Glu Ala Leu Leu Asp Lys Phe Gly Gly Glu His Asn Pro Pro
20 25 30
Ser Ile Tyr Leu Glu Ala Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala
35 40 45
Leu Gln Gln Arg Glu Gln Gln Leu Leu Glu Ser Leu Val Phe Gln Asn
50 55 60
Pro Thr Asp Val Ser Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile
65 70 75 80
Val Arg Val Phe Leu Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg
85 90 95
Cys Gly Val Thr Val Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg
100 105 110
Gly Leu Ile Pro Glu Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu
115 120 125
Lys Lys Pro Ile Gly Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu
130 135 140
Glu Leu His Val Glu Val Leu Glu Asn Val Pro Leu Thr Thr His Asn
145 150 155 160
Phe Val Arg Lys Thr Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg
165 170 175
Lys Leu Leu Phe Gln Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe
180 185 190
His Gln Arg Cys Ser Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp
195 200 205
Gln Leu Asp Leu Leu Phe Val Ser Lys Phe Phe Glu His His Pro Val
210 215 220
Pro Gln Glu Glu Ala Ser Leu Ala Glu Thr Ala Leu Thr Ser Gly Ser
225 230 235 240
Ser Pro Ser Ala Pro Pro Ser Asp Ser Ile Gly His Gln Ile Leu Thr
245 250 255
Ser Pro Ser Pro Ser Lys Ser Ile Pro Ile Pro Gln Ser Phe Arg Pro
260 265 270
Ala Asp Glu Asp His Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser
275 280 285
Ser Ala Pro Asn Val His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp
290 295 300
Glu Lys Phe Pro Glu Val Glu Leu Gln Asp Gln Arg Asp Leu Ile Arg
305 310 315 320
Asp Gln Gly Phe Arg Gly Asp Gly Ala Pro Leu Asn Gln Leu Met Arg
325 330 335
Cys Leu Arg Lys Tyr Gln Ser Arg Thr Pro Ser Pro Leu Leu Pro Ser
340 345 350
Val Pro Ser Asp Ile Val Phe Asp Phe Glu Pro Gly Pro Val Phe Arg
355 360 365
Gly Ser Thr Thr Gly Leu Ser Ala Thr Pro Pro Ala Ser Leu Pro Gly
370 375 380
Ser Leu Thr Ser Val Lys Ala Val Gln Arg Ser Pro Gly Pro Gln Arg
385 390 395 400
Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn Arg Met Lys Thr
405 410 415
Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp Gly Gln
420 425 430
Ile Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr Val Tyr
435 440 445
Lys Gly Lys Trp His Gly Asp Val Ala Val Lys Met Leu Asn Val Thr
450 455 460
Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val Gly Val
465 470 475 480
Leu Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe Met Gly Tyr Ser
485 490 495
Thr Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly Ser Ser
500 505 510
Leu Tyr His His Leu His Ile Ile Glu Thr Lys Phe Glu Met Ile Lys
515 520 525
Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr Leu His
530 535 540
Ala Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile Phe Leu
545 550 555 560
His Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala Thr Val
565 570 575
Lys Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser Gly Ser
580 585 590
Ile Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys Asn Pro
595 600 605
Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu Tyr Glu
610 615 620
Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg Asp Gln
625 630 635 640
Ile Ile Phe Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu Ser Lys
645 650 655
Val Arg Ser Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala Glu Cys
660 665 670
Leu Lys Lys Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Ile Leu Ala
675 680 685
Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro Lys Ile His Arg Ser Ala
690 695 700
Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp Phe Ser
705 710 715 720
Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly Gly Tyr
725 730 735
Gly Glu Phe Ala Ala Phe Lys
740
<210> 9
<211> 2186
<212> ДНК
<213> Cavia porcellus
<400> 9
atggcggcgc tcagcggcgg cggtggcgcg gagcagggcc aggctctgtt caacggggac
60
atggagctcg aggccggcgc cggcgccgca gcctcttcgg ctgcagaccc tgccattccc
120
gaggaggtat ggaatatcaa acaaatgatt aagttgacgc aggaacacat agaggcccta
180
ttggacaaat ttggtggaga gcataatcca ccatcaatat acctggaggc ctatgaagaa
240
tacaccagca aactagatgc cctccaacaa agagaacagc agttactgga atccctcggg
300
aatggaactg atttttctgt ttctagctct gcatcactgg acaccgttac atcttcttct
360
tcttctagcc tttcagtact accttcatct ctttcagttt ttcaaaatcc tacagatgtg
420
tcacggagca accccaaatc accacaaaaa cctattgtta gagtcttcct gcccaacaaa
480
cagaggacag tggtacctgc aaggtgtgga gttacagtcc gagacagtct gaagaaagca
540
ctcatgatga gaggtcttat cccagagtgc tgtgctgtgt acagaattca ggatggagaa
600
aagaaaccaa ttggctggga cactgacatt tcctggctta ctggggaaga attacatgta
660
gaagtattgg agaatgttcc acttacaaca cacaattttg tatgtatctt tatatttttt
720
ttgctgtttg tctccaagtt ctttgaacac cacccaatac cacaggagga ggcttcctta
780
gcagagacca cccttacatc tggatcatcc ccttctgcac ccccctcaga gtccattggg
840
cccccaattc tcaccagccc atctccttca aaatccattc caattccaca gcctttccgg
900
ccaggagagg aagatcatcg aaatcaattt gggcagcgag accggtcctc atctgctccc
960
aatgtgcata taaacacaat agaacctgtc aatattgatg atttgattag agaccaaggg
1020
tttcgtagtg atggaggatc aactacaggt ttgtctgcca ccccacctgc ctcattacct
1080
ggctcactca ctaatgtgaa agccttacag aaatctccag gacctcagcg agaaaggaag
1140
tcatcttcat cctcagaaga cagaaatcga atgaaaacgc ttggtagacg ggactcaagt
1200
gatgattggg agattcctga tgggcagatt acagtgggac aaagaattgg atctgggtca
1260
tttggaacag tctacaaggg gaagtggcat ggtgacgtgg cagtgaaaat gttgaatgtg
1320
acagcaccca cacctcaaca gttacaggcc ttcaaaaatg aagtaggagt actcaggaaa
1380
acacgacatg tgaatatcct actcttcatg ggctattcca caaagccaca gctagctatt
1440
gttacccagt ggtgtgaggg ctccagctta taccaccatc tccacatcat cgagaccaaa
1500
tttgagatga tcaaacttat agatattgca cgacagactg cccagggcat ggattactta
1560
cacgccaagt caatcatcca cagagacctc aagagtaata atatatttct tcacgaagac
1620
ctcacggtta aaataggtga ttttggtcta gccacagtga aatctcgatg gagtgggtcc
1680
catcagtttg aacagttgtc tggatccatt ttgtggatgg caccagaagt aatcagaatg
1740
cgagataaaa acccatacag ttttcagtcc gatgtatatg catttgggat tgttctatat
1800
gaattgatga ctgggcagtt accctattca aatatcaaca acagggacca gataattttt
1860
atggtgggac gaggatatct atctccagat ctcagcaagg tacggagtaa ctgtccaaaa
1920
gccatgaaga ggttaatggc ggagtgcctc aaaaagaaaa gagatgagag accactcttt
1980
ccccaaattc tcgcctctat tgagctgctg gcccgctcat tgccaaaaat tcaccgcagt
2040
gcatcagaac cctccttgaa tcgggctggt ttccaaacag aggattttag tctctatgct
2100
tgtgcttctc caaaaacacc catccaggca gggggatatg gtgcgtttcc tgtccactga
2160
tgcaaattaa atgagtgaga aataaa
2186
<210> 10
<211> 719
<212> БЕЛОК
<213> Cavia porcellus
<400> 10
Met Ala Ala Leu Ser Gly Gly Gly Gly Ala Glu Gln Gly Gln Ala Leu
1 5 10 15
Phe Asn Gly Asp Met Glu Leu Glu Ala Gly Ala Gly Ala Ala Ala Ser
20 25 30
Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn Ile Lys Gln
35 40 45
Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu Asp Lys Phe
50 55 60
Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala Tyr Glu Glu
65 70 75 80
Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln Gln Leu Leu
85 90 95
Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser Ser Ala Ser
100 105 110
Leu Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser Val Leu Pro
115 120 125
Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser Arg Ser Asn
130 135 140
Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu Pro Asn Lys
145 150 155 160
Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val Arg Asp Ser
165 170 175
Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu Cys Cys Ala
180 185 190
Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly Trp Asp Thr
195 200 205
Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu Val Leu Glu
210 215 220
Asn Val Pro Leu Thr Thr His Asn Phe Val Cys Ile Phe Ile Phe Phe
225 230 235 240
Leu Leu Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu
245 250 255
Glu Ala Ser Leu Ala Glu Thr Thr Leu Thr Ser Gly Ser Ser Pro Ser
260 265 270
Ala Pro Pro Ser Glu Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser
275 280 285
Pro Ser Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Gly Glu Glu
290 295 300
Asp His Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro
305 310 315 320
Asn Val His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile
325 330 335
Arg Asp Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser
340 345 350
Ala Thr Pro Pro Ala Ser Leu Pro Gly Ser Leu Thr Asn Val Lys Ala
355 360 365
Leu Gln Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser
370 375 380
Ser Glu Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser
385 390 395 400
Asp Asp Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile
405 410 415
Gly Ser Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp
420 425 430
Val Ala Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu
435 440 445
Gln Ala Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val
450 455 460
Asn Ile Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile
465 470 475 480
Val Thr Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile
485 490 495
Ile Glu Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln
500 505 510
Thr Ala Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg
515 520 525
Asp Leu Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys
530 535 540
Ile Gly Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser
545 550 555 560
His Gln Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu
565 570 575
Val Ile Arg Met Arg Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val
580 585 590
Tyr Ala Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro
595 600 605
Tyr Ser Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg
610 615 620
Gly Tyr Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys
625 630 635 640
Ala Met Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu
645 650 655
Arg Pro Leu Phe Pro Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg
660 665 670
Ser Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg
675 680 685
Ala Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro
690 695 700
Lys Thr Pro Ile Gln Ala Gly Gly Tyr Gly Ala Phe Pro Val His
705 710 715
<210> 11
<211> 3229
<212> ДНК
<213> Canis familiaris
<400> 11
gtaatgctgg attttcatgg aataagtttg acctgtgctg cagtggcctc cagcaaggta
60
cccgcaagat gtggagttac agtccgggac agtctaaaga aagctctgat gatgagaggt
120
ctaatcccag agtgctgtgc tgtttacaga attcaggatg gagagaagaa accgattggc
180
tgggacactg atatttcctg gctcactgga gaggaattgc atgtagaagt gttggaaaat
240
gttccgctta ccacacacaa ctttgtacgg aaaacttttt tcaccttagc attttgtgac
300
ttttgtcgaa agctgctttt ccagggtttt cgctgtcaaa catgtggtta taaatttcac
360
cagcgttgta gtacagaggt tccactgatg tgtgttaatt atgaccaact tgatttgctg
420
tttgtctcca agttctttga acaccaccca ataccacagg aggaggcctc catagcagag
480
actgccctta cgtctggatc atccccttct gctcccccct ccgattctcc tgggccccca
540
attctgacca gtccgtctcc ttcaaaatcc attccaattc cacagccttt ccgaccagca
600
gatgaagatc atcgaaatca gtttggacaa cgagaccggt cctcatcagc tccaaatgtg
660
catataaaca caatagaacc cgtcaacatt gatgacttga ttagagacca agggtttcgt
720
agtgatggag gatcaaccac aggtttgtct gccacccccc ctgcctcatt gcctggctca
780
ctcactaatg taaaagcatt acagaaatct ccaggacctc agcgggaaag aaaatcatct
840
tcatcctcag aagataggaa tcgaatgaaa acacttggta gacgggattc aagtgatgat
900
tgggagatac ctgatgggca gatcacagtg ggacagagaa ttggatccgg gtcatttggg
960
acagtctaca agggaaagtg gcatggtgac gtggcagtga aaatgttgaa tgtgacagca
1020
cccacacctc agcagttaca ggccttcaaa aatgaagtag gagtactcag gaaaactcga
1080
catgtgaata tcctactctt tatgggctat tcaacaaagc cccaactggc tattgttacc
1140
cagtggtgtg agggctccag cttatatcac catctccaca tcattgagac caaatttgag
1200
atgataaagc ttatagatat tgcacggcag actgcacagg gcatggatta cttacacgcc
1260
aagtcaatca tccacagaga cctcaagagt aataatattt ttcttcatga agacctcaca
1320
gtaaaaatag gtgattttgg tctagccaca gtgaaatctc gatggagtgg gtcccatcag
1380
tttgaacagt tgtctggatc cattttgtgg atggcaccag aagtgatccg aatgcaagac
1440
aaaaacccat atagcttcca gtcagatgta tacgcatttg ggattgttct atatgaattg
1500
atgacagggc agttacctta ttcaaacatc aacaacaggg accagataat ttttatggtg
1560
ggacgaggat atctttctcc agatctcagt aaggtacgga gtaactgtcc aaaagccatg
1620
aagagattga tggcagagtg cctaaaaaag aaaagagatg agaggccact ctttccccaa
1680
attctcgcct ctattgagct gctggcccgc tcattgccaa aaattcaccg cagtgcatca
1740
gaaccctcct tgaatcgggc tggcttccaa acagaggatt ttagtctcta tgcttgcgct
1800
tctccaaaaa cacccatcca ggcaggggga tacggagaat ttgcagcctt caagtagcca
1860
caccatcatg gcaacaacta ctcttatttc ttaagtcttg tgttcgtaca atttgttaac
1920
atcaaaacac agttctgttc ctcaaatctt tttttaaaga tacagaattt tcaatgcata
1980
agctggtgtg gaacagaatg gaatttccca tccaacaaaa gagggaagaa tgttttagga
2040
accagaattc tctgctgcca gtgtttcttc ttcaacacaa ataccacgtg catacaagtc
2100
tgcccactcc caggaaggaa gaggagagcc tgagttctga ccttttgatg gtcaggcatg
2160
atggaaagaa actgctgcta cagcttggga gattggctgt ggagagcctg cccgtcagct
2220
ctgcccttct aaccgccaga tgagtgtgtg gctggtcacc tgacagggca gctgcaatcg
2280
ccaagcatcg ttctctttcc tgtcctggga ttttgtcgtg gagctctttc cccctagtca
2340
ccaccggttc atttctgagg gatggaacaa aaatgcagca tggcctttct gtgtggtgca
2400
tgtccggtct ttgacaaatt tttatcaagt gaagctcttg tatttaaatg gagaatgaga
2460
ggcgaggggg ggggatcacg ttttggtgta ggggcaaagg gaatgctgca tctttttcct
2520
gacccactgg gtttctggcc tttgtttcct tgctcactga gggtgtctgc ctataaccac
2580
gcaggctgga aagtgctggc acacattgcc ttctcttctc actgggtcca gcaatgaaga
2640
caagtgttgg ggattttttt ttttgccctc cacaatgtag caagttctca ggaaaataca
2700
gttaatatct tcctcctaag ctcttccagt catcaagtac ttatgtggct actttgtcca
2760
gggcacaaaa tgccatggcg gtatccaatt aaaagcctac aaaactgctt gataacagtt
2820
ttgaatgtgt gagacattta tgtaatttaa atgtaaggta caagttttaa tttctgagtt
2880
tctctattat atttttatta aaaagaaaat aattttcaga tttaattgaa ttggaataaa
2940
ataatacttc ccaccagaat tatatatcct ggaaaattgt atttttgtta tataaacaac
3000
ttttaaagaa agatcattat ccttttctct acctaaatat ggggagtctt agcataatga
3060
cagatattta taatttttaa attaatggta cttgctggat ccacactaac atctttgcta
3120
atatctcatg ttttcctcca acttactcct acactacatc ctccatcctc tttccagtct
3180
tttatctaga atatgcaacc taaaataaaa atggtggtgt ctccattca
3229
<210> 12
<211> 617
<212> БЕЛОК
<213> Canis familiaris
<400> 12
Met Leu Asp Phe His Gly Ile Ser Leu Thr Cys Ala Ala Val Ala Ser
1 5 10 15
Ser Lys Val Pro Ala Arg Cys Gly Val Thr Val Arg Asp Ser Leu Lys
20 25 30
Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu Cys Cys Ala Val Tyr
35 40 45
Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly Trp Asp Thr Asp Ile
50 55 60
Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu Val Leu Glu Asn Val
65 70 75 80
Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr Phe Phe Thr Leu Ala
85 90 95
Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln Gly Phe Arg Cys Gln
100 105 110
Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser Thr Glu Val Pro Leu
115 120 125
Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu Phe Val Ser Lys Phe
130 135 140
Phe Glu His His Pro Ile Pro Gln Glu Glu Ala Ser Ile Ala Glu Thr
145 150 155 160
Ala Leu Thr Ser Gly Ser Ser Pro Ser Ala Pro Pro Ser Asp Ser Pro
165 170 175
Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser Lys Ser Ile Pro Ile
180 185 190
Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His Arg Asn Gln Phe Gly
195 200 205
Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val His Ile Asn Thr Ile
210 215 220
Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp Gln Gly Phe Arg Ser
225 230 235 240
Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr Pro Pro Ala Ser Leu
245 250 255
Pro Gly Ser Leu Thr Asn Val Lys Ala Leu Gln Lys Ser Pro Gly Pro
260 265 270
Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn Arg Met
275 280 285
Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp
290 295 300
Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr
305 310 315 320
Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala Val Lys Met Leu Asn
325 330 335
Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val
340 345 350
Gly Val Leu Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe Met Gly
355 360 365
Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly
370 375 380
Ser Ser Leu Tyr His His Leu His Ile Ile Glu Thr Lys Phe Glu Met
385 390 395 400
Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr
405 410 415
Leu His Ala Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile
420 425 430
Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala
435 440 445
Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser
450 455 460
Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys
465 470 475 480
Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu
485 490 495
Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg
500 505 510
Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu
515 520 525
Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala
530 535 540
Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Ile
545 550 555 560
Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro Lys Ile His Arg
565 570 575
Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp
580 585 590
Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly
595 600 605
Gly Tyr Gly Glu Phe Ala Ala Phe Lys
610 615
<210> 13
<211> 1889
<212> ДНК
<213> Canis familiaris
<400> 13
ggaatatcaa acaaatgatt aagttgacac aggaacatat agaagcccta ttggacaagt
60
ttggtgggga gcataatcca ccatcaatat atctggaggc ctatgaagaa tacaccagca
120
aactagatgc cctccaacag cgagaacaac agttattgga atccctgggg aatggaactg
180
atttttctgt ttctagctct gcatcaacgg acaccgttac atcttcttcc tcttctagcc
240
tttcagtgct accttcatct ctttcagttt ttcaaaatcc cacagatata tcacggagca
300
atcccaagtc accacaaaaa cctatcgtta gagtcttcct gcccaataaa cagaggacgg
360
tggtacccgc aagatgtgga gttacagtcc gggacagtct aaagaaagct ctgatgatga
420
gaggtctaat cccagagtgc tgtgctgttt acagaattca ggatggagag aagaaaccga
480
ttggctggga cactgatatt tcctggctca ctggagagga attgcatgta gaagtgttgg
540
aaaatgttcc gcttaccaca cacaactttg tacggaaaac ttttttcacc ttagcatttt
600
gtgacttttg tcgaaagctg cttttccagg gttttcgctg tcaaacatgt ggttataaat
660
ttcaccagcg ttgtagtaca gaggttccac tgatgtgtgt taattatgac caacttgatt
720
tgctgtttgt ctccaagttc tttgaacacc acccaatacc acaggaggag gcctccatag
780
cagagactgc ccttacgtct ggatcatccc cttctgctcc cccctccgat tctcctgggc
840
ccccaattct gaccagtccg tctccttcaa aatccattcc aattccacag cctttccgac
900
cagcagatga agatcatcga aatcagtttg gacaacgaga ccggtcctca tcagctccaa
960
atgtgcatat aaacacaata gaacccgtca acattgatga cttgattaga gaccaagggt
1020
ttcgtagtga tggaggatca accacaggtt tgtctgccac cccccctgcc tcattgcctg
1080
gctcactcac taatgtaaaa gcattacaga aatctccagg acctcagcgg gaaagaaaat
1140
catcttcatc ctcagaagat aggaatcgaa tgaaaacact tggtagacgg gattcaagtg
1200
atgattggga gatacctgat gggcagatca cagtgggaca gagaattgga tccgggtcat
1260
ttgggacagt ctacaaggga aagtggcatg gtgacgtggc agtgaaaatg ttgaatgtga
1320
cagcacccac acctcagcag ttacaggcct tcaaaaatga agtaggagta ctcaggaaaa
1380
ctcgacatgt gaatatccta ctctttatgg gctattcaac aaagccccaa ctggctattg
1440
ttacccagtg gtgtgagggc tccagcttat atcaccatct ccacatcatt gagaccaaat
1500
ttgagatgat aaagcttata gatattgcac ggcagactgc acagggcatg gattacttac
1560
acgccaagtc aatcatccac agagacctca agagtaataa tatttttctt catgaagacc
1620
tcacagtaaa aataggtgat tttggtctag ccacagtgaa atctcgatgg agtgggtccc
1680
atcagtttga acagttgtct ggatccattt tgtggatggc accagaagtg atccgaatgc
1740
aagacaaaaa cccatatagc ttccagtcag atgtatacgc atttgggatt gttctatatg
1800
aattgatgac agggcagtta ccttattcaa acatcaacaa cagggaccag ctcagatcat
1860
gatcacggtg tcatgagatc aagccccac
1889
<210> 14
<211> 615
<212> БЕЛОК
<213> Canis familiaris
<400> 14
Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu Asp Lys Phe
1 5 10 15
Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala Tyr Glu Glu
20 25 30
Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln Gln Leu Leu
35 40 45
Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser Ser Ala Ser
50 55 60
Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser Val Leu Pro
65 70 75 80
Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Ile Ser Arg Ser Asn
85 90 95
Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu Pro Asn Lys
100 105 110
Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val Arg Asp Ser
115 120 125
Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu Cys Cys Ala
130 135 140
Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly Trp Asp Thr
145 150 155 160
Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu Val Leu Glu
165 170 175
Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr Phe Phe Thr
180 185 190
Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln Gly Phe Arg
195 200 205
Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser Thr Glu Val
210 215 220
Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu Phe Val Ser
225 230 235 240
Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala Ser Ile Ala
245 250 255
Glu Thr Ala Leu Thr Ser Gly Ser Ser Pro Ser Ala Pro Pro Ser Asp
260 265 270
Ser Pro Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser Lys Ser Ile
275 280 285
Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His Arg Asn Gln
290 295 300
Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val His Ile Asn
305 310 315 320
Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp Gln Gly Phe
325 330 335
Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr Pro Pro Ala
340 345 350
Ser Leu Pro Gly Ser Leu Thr Asn Val Lys Ala Leu Gln Lys Ser Pro
355 360 365
Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn
370 375 380
Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile
385 390 395 400
Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe
405 410 415
Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala Val Lys Met
420 425 430
Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn
435 440 445
Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe
450 455 460
Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys
465 470 475 480
Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu Thr Lys Phe
485 490 495
Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met
500 505 510
Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn
515 520 525
Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly
530 535 540
Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln
545 550 555 560
Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln
565 570 575
Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile
580 585 590
Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn
595 600 605
Asn Arg Asp Gln Leu Arg Ser
610 615
<210> 15
<211> 3521
<212> ДНК
<213> Felis catus
<220>
<221> дополнительный признак
<222> (630)..(649)
<223> n is a, c, g, or t
<400> 15
atgcctaacc tcagtctctg ccaccacggc caatttgctc atgtgcccac tgtgtcggca
60
ctgggatatt ttgtgatttg ccttggccat tgtccactgt ccttgacatt gcctgaagga
120
gaaccactga tgctaatgtt gaaggtgacc tttgcaggct ctccactact cataccaaag
180
atgcggcccc ctgataatcc cagagccact gtctgcacat gggcaaaaca ggctacattc
240
tgtgcagact ggggagaaag gttccaagaa cacagtgcca tagttttggg cagagagttt
300
caacacagca tagtgtctat ggcagtatct ggatttggcc gggggaagtg cccaagagga
360
gacagtcagg ctgtgtccta cggccaagga cctgcactta tttttgcatg cagtggttta
420
gcacagggaa gagaacgaag taggaaatcg gagccatgga aacggcagag cggaggaaac
480
gtgcacgcgc gagggtgggc acgaaaggaa agaaccctcc ccagaagact gcgcgagggc
540
gctcctagga ttacgtcacg caccccgcga aaactgaaat gtactgtgtg tggtctttta
600
attgaactat cttccttatg tgcacttaan nnnnnnnnnn nnnnnnnnng cggcggcggc
660
ggtggcgcgg agcagggcca ggctctgttc aacggggaca tggagcccga agccggcgcc
720
gcggcctctt cggctgcgga ccctgccatt cccgaggagg tgtggaatat caaacaaatg
780
attaagttga cacaggaaca tatagaggcc ctattggaca aatttggtgg ggagcataat
840
ccaccatcaa tatatctaga ggcctatgaa gaatacacca gcaagctaga tgccctccaa
900
cagagagaac aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc
960
tctgcatcaa cagacaccgt tacatcttcc tcctcttcta gcctttcagt gctaccttca
1020
tctctttcag tttttcaaaa ccccacagat gtgtcacgga gcaatcccaa gtcaccacag
1080
aaacctatcg ttagagtctt cctgcctaat aaacagagga cagtggtacc tgcaagatgt
1140
ggagttacag tccgggacag tctaaagaaa gctctgatga tgagaggtct aatccctgag
1200
tgctgtgctg tttacagaat tcaggatgga gagaagaaac caattggctg ggacactgat
1260
atctcctggc tcaccggaga ggaattgcat gtagaagtgt tggaaaatgt tccacttaca
1320
actcacaact ttgtatgtac ggaaaacgtt ttcaccttag cattttgtga cttttgtcga
1380
aagctgcttt tccaaggttt tcgctgtcaa acgtgtggtt ataaatttca ccagcgttgt
1440
agtacagagg ttccactgat gtgtgttaat tatgaccaac ttgatttgct gtttgtctcc
1500
aagttctttg aacaccaccc aataccacag gaggaggcct ccatagcaga gactgcccta
1560
acgtctggat cgtccccttc tgcccccccc tccgattcta ctgggcccca aattctcacc
1620
agtccgtctc cttcaaaatc cattccaatt ccacagcctt tccgaccagc agatgaagat
1680
catcgaaatc aatttggaca gcgagaccgg tcctcatcag ctccaaatgt gcatataaat
1740
acaatagaac ctgtcaatat tgatgacttg attagagacc aggggtttcg tagtgatgga
1800
ggatcaacca caggcttgtc tgccaccccc cctgcctcat tgccgggctc tctcactaat
1860
gtaaaagcat tacagaaatc tccagggcct cagcgggaaa ggaaatcttc ttcatcctca
1920
gaagatagga atcgaatgaa aacacttggt agaagggatt caagtgatga ttgggagatt
1980
cctgatgggc agatcacagt gggacagaga attggatccg ggtcatttgg gacagtctac
2040
aagggaaagt ggcatggtga tgtggcagtg aaaatgttga atgtgacagc acccacacct
2100
cagcagttac aggccttcaa aaatgaagta ggagtactca ggaaaactcg gcatgtgaac
2160
atcctgctct tcatgggcta ttcaacaaag ccccagctgg ctattgtcac ccagtggtgt
2220
gagggctcca gcttatacca ccatctccac atcatcgaga ccaaattcga gatgatcaag
2280
ctgatagata ttgctcggca gactgcgcag ggcatggatt acttacacgc caagtcaatc
2340
atccacagag acctcaagag taataatatt tttcttcacg aagacctcac agtaaaaata
2400
ggtgattttg gtctagccac agtgaaatct cgatggagtg ggtcccatca gtttgaacag
2460
ttgtctggat ccattttgtg gatggcacca gaagtaattc gaatgcaaga taaaaaccca
2520
tatagctttc agtcagatgt atatgcattt gggattgttc tatatgaatt gatgactgga
2580
cagttacctt attcaaacat caacaacagg gaccagataa tttttatggt gggacgagga
2640
tatctttctc cagatctcag taaggtacga agtaactgtc caaaagccat gaagagattg
2700
atggcagagt gcctaaaaaa gaaaagagat gagaggccac tgtttcccca aattcttgcc
2760
tctattgagc tgctggcccg ctcattgcca aaaattcacc gcagtgcatc agaaccctcc
2820
ttgaatcggg ctggcttcca gacagaggat tttagtctct atgcttgtgc ttctccaaaa
2880
acacccatcc aggcaggggg atatggtgcg tttcccgtcc actgagataa gttagatgag
2940
tgcgcgagtg cagggggccg gggccaagga ggtggaaatg tgcgtgcttc tgtactaagt
3000
tggatagcat cttctttttt aaaaaaagat gaaccaaaga atgtgtatgt ttttaaagac
3060
tagatataat tatttcctga tctaaaatgt atacttagct ttggattttc aatatccaag
3120
ggttttcaaa atgcacagac attgctgaac atttgcagta cctcttctgg aggctttact
3180
tcctgttaca aattggtttt gtttactggc ttatcctaat tattaaactt caattaaact
3240
tttctcctgc accttttgtt atgagctatc acatgtccct tagggactcg caagagcagt
3300
actgcccccg tgtacgggct tgcaggtaga aaggggatga cgggttttaa cacctgtgtg
3360
aggcaaggca gtccgaacag atctcattta ggaagccacg agagttgaat aagttatttt
3420
tattcttagt attttttctg taactacttt ttattataac ttggaaaata tggatgtcct
3480
ttatacacct tagcaataga ctgaatttct ttttataaat t
3521
<210> 16
<211> 974
<212> БЕЛОК
<213> Felis catus
<220>
<221> дополнительный признак
<222> (210)..(217)
<223> Xaa может представлять собой любую встречающуюся в природе
аминокислоту
<400> 16
Met Pro Asn Leu Ser Leu Cys His His Gly Gln Phe Ala His Val Pro
1 5 10 15
Thr Val Ser Ala Leu Gly Tyr Phe Val Ile Cys Leu Gly His Cys Pro
20 25 30
Leu Ser Leu Thr Leu Pro Glu Gly Glu Pro Leu Met Leu Met Leu Lys
35 40 45
Val Thr Phe Ala Gly Ser Pro Leu Leu Ile Pro Lys Met Arg Pro Pro
50 55 60
Asp Asn Pro Arg Ala Thr Val Cys Thr Trp Ala Lys Gln Ala Thr Phe
65 70 75 80
Cys Ala Asp Trp Gly Glu Arg Phe Gln Glu His Ser Ala Ile Val Leu
85 90 95
Gly Arg Glu Phe Gln His Ser Ile Val Ser Met Ala Val Ser Gly Phe
100 105 110
Gly Arg Gly Lys Cys Pro Arg Gly Asp Ser Gln Ala Val Ser Tyr Gly
115 120 125
Gln Gly Pro Ala Leu Ile Phe Ala Cys Ser Gly Leu Ala Gln Gly Arg
130 135 140
Glu Arg Ser Arg Lys Ser Glu Pro Trp Lys Arg Gln Ser Gly Gly Asn
145 150 155 160
Val His Ala Arg Gly Trp Ala Arg Lys Glu Arg Thr Leu Pro Arg Arg
165 170 175
Leu Arg Glu Gly Ala Pro Arg Ile Thr Ser Arg Thr Pro Arg Lys Leu
180 185 190
Lys Cys Thr Val Cys Gly Leu Leu Ile Glu Leu Ser Ser Leu Cys Ala
195 200 205
Leu Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Gly Gly Gly Gly Gly Ala Glu
210 215 220
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
225 230 235 240
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
245 250 255
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
260 265 270
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
275 280 285
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
290 295 300
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
305 310 315 320
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
325 330 335
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
340 345 350
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
355 360 365
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
370 375 380
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
385 390 395 400
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
405 410 415
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
420 425 430
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Cys Thr Glu
435 440 445
Asn Val Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe
450 455 460
Gln Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys
465 470 475 480
Ser Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu
485 490 495
Leu Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu
500 505 510
Ala Ser Ile Ala Glu Thr Ala Leu Thr Ser Gly Ser Ser Pro Ser Ala
515 520 525
Pro Pro Ser Asp Ser Thr Gly Pro Gln Ile Leu Thr Ser Pro Ser Pro
530 535 540
Ser Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp
545 550 555 560
His Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn
565 570 575
Val His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg
580 585 590
Asp Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala
595 600 605
Thr Pro Pro Ala Ser Leu Pro Gly Ser Leu Thr Asn Val Lys Ala Leu
610 615 620
Gln Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser
625 630 635 640
Glu Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp
645 650 655
Asp Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly
660 665 670
Ser Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val
675 680 685
Ala Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln
690 695 700
Ala Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn
705 710 715 720
Ile Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val
725 730 735
Thr Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile
740 745 750
Glu Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr
755 760 765
Ala Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp
770 775 780
Leu Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile
785 790 795 800
Gly Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His
805 810 815
Gln Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val
820 825 830
Ile Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr
835 840 845
Ala Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr
850 855 860
Ser Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly
865 870 875 880
Tyr Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala
885 890 895
Met Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg
900 905 910
Pro Leu Phe Pro Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser
915 920 925
Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala
930 935 940
Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys
945 950 955 960
Thr Pro Ile Gln Ala Gly Gly Tyr Gly Ala Phe Pro Val His
965 970
<210> 17
<211> 3853
<212> ДНК
<213> Bos taurus
<400> 17
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc
60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc
120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg
180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg
240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt
300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga
360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa
420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac
480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa
540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag
600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg
660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag
720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg
780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc
840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact
900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc
960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc
1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac
1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat
1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt
1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt
1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg
1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag
1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc
1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc
1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga
1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc
1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg
1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca
1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt
1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg
1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc
1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc
1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca
2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt
2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt
2160
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag
2220
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc
2280
taaaaaagaa aagagatgaa agaccactct ttccccaaat tctcgcctct attgagctgc
2340
tggcccgctc attgccaaaa attcaccgca gtgcatcaga accctccttg aatcgggctg
2400
gcttccaaac agaggatttt agtctatatg cttgtgcttc tccaaaaaca cccattcagg
2460
cagggggata tggtacgttt cctgttcact gaaacaaacc gagtgagtga cagcatgtag
2520
gagggtaggg acaaaagaaa gtgaacaaat gtttgcttat atatttgtta aattgaatag
2580
gattttcttt ttctttaaag gtgaacaaga gaacatgtgt gtttttaaag tttggatata
2640
gttttcttcc cagtctaaaa cccatagtta gcattacatt ttcaacatcg aatttttttt
2700
taattcatag acattgctga aaatttataa taccttttcc agaggcttta cttcccattc
2760
caagtttgtt ttgtttactt ggttagtcta atcattaaac tttaaacttt ccccacctac
2820
cttttgctgt tagctatccc gcatccatta ggggctccaa gaacagcact gtctgcgtgt
2880
gtgtgttggc aggtgggaag ctgatggtaa gttaggctgt gttagtgaag gtaaactgac
2940
caggtctaat taggagtcac tagaattgaa taagcttatt tttattaata ttttttctta
3000
taactatttc tttttgtaat aatttagaaa atataattgt tctttattcc cttacagcag
3060
tataaattat tggtgcaggt aaccaaagat attactgagg agtggcatgt ttgacatgag
3120
tgacatggtt taactttgga tttttagtta atatttcttt atatattaag gatgtcttac
3180
acattataga agtcaaattt actgacaaag gtattgcctc ctcttcctcc ccaaaaacac
3240
agcaaaattc tctgggaact cgtagcattg ttggttttct tttggatgac tatggttgcc
3300
aaacaaccaa gtaattgatt ttttttaaat tattattgct ttagattata ctcacctctc
3360
atgatgcctg ttagcaatca cctttatcca tgtgtcttgt aaaatatctt tcctccttat
3420
attctttgcc caacaagagt ctacttgtta tgaatgagta ctattttctt tttttgattc
3480
cccagtataa ttagtatgtt tagtgctttc taggacttcc actttcttat gttaaaaaaa
3540
aaaacaaact aatgtggcag tcagtatatt cttactgtga atcagagtct ttactgggaa
3600
tcaaagtgaa agaagcagct gttctgactt cagagtcagc ctagggacca aaaccagcct
3660
cttaaataca ccttcattta ttcagtttgg atttgtgatg attttcatta tagctgacag
3720
ttcaaggtta ttcagtggca cacagatagc atctgcataa atgcctttct tcttgaaaat
3780
aaaggagaaa attgggaaga ctttacacca atagtttagt ctttaagtac cacagataac
3840
acacaccata aat
3853
<210> 18
<211> 764
<212> БЕЛОК
<213> Bos taurus
<400> 18
Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu Gln
1 5 10 15
Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala Ala
20 25 30
Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn Ile
35 40 45
Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu Asp
50 55 60
Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala Tyr
65 70 75 80
Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln Gln
85 90 95
Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser Ser
100 105 110
Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser Val
115 120 125
Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser Arg
130 135 140
Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu Pro
145 150 155 160
Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val Arg
165 170 175
Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu Cys
180 185 190
Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly Trp
195 200 205
Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu Val
210 215 220
Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr Phe
225 230 235 240
Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln Gly
245 250 255
Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser Thr
260 265 270
Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu Phe
275 280 285
Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala Ser
290 295 300
Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro Pro
305 310 315 320
Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser Lys
325 330 335
Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His Arg
340 345 350
Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val His
355 360 365
Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp Gln
370 375 380
Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr Pro
385 390 395 400
Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln Lys
405 410 415
Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp
420 425 430
Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp
435 440 445
Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser Gly
450 455 460
Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala Val
465 470 475 480
Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe
485 490 495
Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile Leu
500 505 510
Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr Gln
515 520 525
Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu Thr
530 535 540
Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln
545 550 555 560
Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu Lys
565 570 575
Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly Asp
580 585 590
Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln Phe
595 600 605
Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile Arg
610 615 620
Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe
625 630 635 640
Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn
645 650 655
Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr Leu
660 665 670
Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met Lys
675 680 685
Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro Leu
690 695 700
Phe Pro Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro
705 710 715 720
Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe
725 730 735
Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro
740 745 750
Ile Gln Ala Gly Gly Tyr Gly Thr Phe Pro Val His
755 760
<210> 19
<211> 4936
<212> ДНК
<213> Bos taurus
<400> 19
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc
60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc
120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg
180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg
240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt
300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga
360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa
420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac
480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa
540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag
600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg
660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag
720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg
780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc
840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact
900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc
960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc
1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac
1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat
1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt
1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt
1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg
1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag
1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc
1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc
1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga
1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc
1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg
1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca
1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt
1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg
1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc
1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc
1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca
2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt
2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt
2160
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag
2220
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc
2280
taaaaaagaa aagagatgaa agaccactct ttccccaagt aggaaagact ctcctaagca
2340
agagacaaaa ttcagaagtt atcagggaaa aagataagca gattctcgcc tctattgagc
2400
tgctggcccg ctcattgcca aaaattcacc gcagtgcatc agaaccctcc ttgaatcggg
2460
ctggcttcca aacagaggat tttagtctat atgcttgtgc ttctccaaaa acacccattc
2520
aggcaggggg atatgaagca gatttggctc ttacatcaaa taaaaataga gtagaagttg
2580
ggatttagag atttcctgac atgcaagaag gaataagcaa gaaaaaaagg tttgttttcc
2640
ccaaatcata tctattgtct tttacttcta ttttttctta aattttttgt gatttcagag
2700
acatgtagag ttttattgat acctaaacta tgagttcttt tttttttttt tttttcatta
2760
ttttgatttt tttggccaag aggcatatgg gatcttagct tgagaaagca acaattttct
2820
tgatgtcatt ttgggtgagg gcacatattg ctgtgaacag tgtggtgata gccaccaggg
2880
accaaactca cacccgctgc attgaaaggt gaagtcttaa acactggacc agcagagaaa
2940
ttcctactct atgagttctt tttgtcatcc cctccccgca ccctccaccc ccaacctaaa
3000
gtctgatgat gaaatcaaca actattccat tagaagcagt agattctggt agcatgatct
3060
ttagtttgtt agtaagattt tgtgctttgt ggggttgtgt cgttttaagg ctaatattta
3120
agtttgtcaa atagaatgct gttcagattg taaaaatgag taataaacat ctgaagtttt
3180
ttttaagtta tttttaacat ggtatataca gttgagctta gagtttatca ttttctgata
3240
ttctcttact tagtagatga attctagcca ttttttataa agatttctgt taagcaaatc
3300
ctgttttcac atgggcttcc tttaagggat tttagattct gctggatatg gtgactgctc
3360
ataagactgt tgaaaattac ttttaagatg tattagaata cttctgaaaa aaaatagcaa
3420
ccttaaaacc ataagcaaaa gtagtaaggg tgtttataca tttctagagt ccctgtttag
3480
gtaatagcct cctatgattg tactttaaat gttttgctct ccaaggtttt agtaacttgg
3540
ctttttttct aatcagtgcc aaactccccc agttttttta actttaaata tgaggtaata
3600
aatcttttac ccttccttga tcttttgact tataatacct tggtcagttg tttcttaaaa
3660
ggaatcctta aatggaaaga gacaatatca ctgtctgcag ttctgattag tagttttatt
3720
cagaatggaa aaacagatta ttcatttttg aaaattgttc aggggtatgt tcattgttag
3780
gaccttggac tttggagtca gtgcctagct atgcattcca ggtctgccat tttctggctg
3840
tgaaattttg gacaagttac ttaaccactt taaaccccag ctttaagaag taaattaacc
3900
ccagtaaatt aagaagtaat agcagccact tcgtagagtt gttatgaggc tcagatgcag
3960
tgcaaatgtg tataaagtat tcagggagtc acctggtata ctataataga cactagaata
4020
gttgccaata ttatcagcat acaatctgag gattctgtca gccaatcatt agcaatctgt
4080
tgtttgttgg gacatgccag tgttctccag ttgaaatcag tagcaatcta aaaatggata
4140
gattattcct catttaaata gtgtgttcat ataagtgatt gcttggatcc ttatcagaag
4200
ttgctgttac tgaaaaatga taaggctgac taaattgtga tagttgtcag ttactaacca
4260
actcccagaa atgaataaga ggaacctatc tctagttcct agtagaaggt atggacaaaa
4320
tagtaggtga aaaataatgt cttgaacccc caaattaagt aagctttaaa gagtacaata
4380
cctcaaaggg tctttgcggt ttaaaatttg tatgctgaga atgatgttca ttgacatgtg
4440
cctatatgta attttttgat agtttaaaag gtgaaatgaa ctacagatgg gagaggtctg
4500
aattttcttg ccttcagtca aatgtgtaat gtggacatat tatttgacct gtgaatttta
4560
tcttttaaaa aagattaatt cctgcttctt ccttcctaat agttgcatta taataatgaa
4620
aatgagttga taatttgggg ggaaagtatt ctacaaatca accttattat tttaccattg
4680
gtttctgaga aattttgttc atttgaaccg tttatagctt gattagaatc atagcatgta
4740
aaacccaact gagggattat ctgcagactt aatgtagtat tatgtaagtt gtcttctttc
4800
atttcgacct tttttgcttt tgttgttgct agatctgtag tatgtagcta gtcacctttc
4860
agcgaggttt cagcgaggct tttctgtgtc tctaggttat ttgagataac ttttttaaaa
4920
ttagctcttg tcctcc
4936
<210> 20
<211> 797
<212> БЕЛОК
<213> Bos taurus
<400> 20
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr
660 665 670
Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met
675 680 685
Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro
690 695 700
Leu Phe Pro Gln Val Gly Lys Thr Leu Leu Ser Lys Arg Gln Asn Ser
705 710 715 720
Glu Val Ile Arg Glu Lys Asp Lys Gln Ile Leu Ala Ser Ile Glu Leu
725 730 735
Leu Ala Arg Ser Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser
740 745 750
Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys
755 760 765
Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly Gly Tyr Glu Ala Asp Leu
770 775 780
Ala Leu Thr Ser Asn Lys Asn Arg Val Glu Val Gly Ile
785 790 795
<210> 21
<211> 4154
<212> ДНК
<213> Bos taurus
<400> 21
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc
60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc
120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg
180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg
240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt
300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga
360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa
420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac
480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa
540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag
600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg
660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag
720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg
780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc
840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact
900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc
960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc
1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac
1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat
1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt
1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt
1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg
1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag
1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc
1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc
1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga
1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc
1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg
1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca
1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt
1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg
1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc
1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc
1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca
2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt
2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt
2160
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag
2220
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc
2280
taaaaaagaa aagagatgaa agaccactct ttccccaagt aggaaagact ctcctaagca
2340
agagacaaaa ttcagaagtt atcagggaaa aagataagca gattctcgcc tctattgagc
2400
tgctggcccg ctcattgcca aaaattcacc gcagtgcatc agaaccctcc ttgaatcggg
2460
ctggcttcca aacagaggat tttagtctat atgcttgtgc ttctccaaaa acacccattc
2520
aggcaggggg atatggctga gcacattgtc catcacccac aagtggctgg ttctcatcgc
2580
agaatctacg tagggaatcg ggcgtgaaat tcacttaaga gatagagcag aggaagtgtt
2640
ctgtttacag gaatggagat gagagttatg agtaagttgc ttagtcagtt ggctttgttt
2700
tgaaaattat tgtgttatat ttgtgttaac ctacttgtgt tttgacagta tatgtcacat
2760
aggaagaaac ctcagactag cataataaca aagctcagac taggcacaga tgtacacaga
2820
atggaccaaa atgggatggg ggaaggtatg ggaataagtc taggggtagg gaaaaattga
2880
tgtgagggtg ggaaataaac tgtaattacc tgaaataaaa tgtaagagtg caataagtgt
2940
gctttttatt ctaagctgtg aatgggtttt ttaaaaaaag cattccttcc caatgcattt
3000
gcctatgttc catagctgat taaaaccagc tatataaaca tatgcctttt tattcatgtt
3060
aattaccaat ataaatggct aacctttacg tcttatttat cttcatgtta tgttagttta
3120
catacaggga tgtgtgtgtg tgtgtatgct ataaattttc cctccttcgt ttaaaaacgc
3180
gtttgttgga tcctctctgt ttccttaggc catgccacag ctcatagtct cagcttggcc
3240
ttcctgtcac ctgatctgaa ggactatcac agtgacgtag ctcgttcatt ggttgtacac
3300
actctaaccc ttttccttgc tcagcaatta ctgtgtcttc taaaacagga gtgtacaacc
3360
atgagattgc aattaattgt ttgacatatg tccctttgaa ttctatttat tagttatgat
3420
tgattgctct ttggtttgga ccaagaaaaa cgaaatccca cctccccacc ttttcactta
3480
tttcttactt tgaggacaat tctgtaagag agaggaaagg gaactccttc atgttttaac
3540
tgcagcaagt taatggccct ggtttacacc aaacattatg gtgattcaca ttcacattcc
3600
tctcctctct tgctgccaga ggtttgggtt ttgttcagtt ctgctcaagc actgaaaaag
3660
ttttcatgga gtctggagag tgcccagtga aaagatggtt tttaattgtc cacagacctt
3720
tctgttcctg ctttgcaaaa attacaaagg agtaactatt tttaaagctt atttttcaat
3780
tcataaaaaa gacatttatt ttcagtcaga tgatgtctcc ttgtccctta atcctcaatg
3840
tttgcttgaa tctttttttt ttttctgatt ttctcccatc cccacttctt gatacttctt
3900
gagttctctt tcctgctcag gtcctttcat ttgtactttg gagttttttc tcatgtaaat
3960
ttgtacaatg gaaaatattg ttcagtttgg atagaacgca tggagaatta aataaaaaag
4020
atagctgaaa ttcagattga aatttatttg tgtaaagtta tttaaaaact ctgtactata
4080
taaaaggcaa aaaaagttct atgtacttga tgtgaatatg cgaatactgc tataataaag
4140
attgactgca tgga
4154
<210> 22
<211> 781
<212> БЕЛОК
<213> Bos taurus
<400> 22
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr
660 665 670
Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met
675 680 685
Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro
690 695 700
Leu Phe Pro Gln Val Gly Lys Thr Leu Leu Ser Lys Arg Gln Asn Ser
705 710 715 720
Glu Val Ile Arg Glu Lys Asp Lys Gln Ile Leu Ala Ser Ile Glu Leu
725 730 735
Leu Ala Arg Ser Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser
740 745 750
Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys
755 760 765
Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly Gly Tyr Gly
770 775 780
<210> 23
<211> 7914
<212> ДНК
<213> Bos taurus
<400> 23
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc
60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc
120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg
180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg
240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt
300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga
360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa
420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac
480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa
540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag
600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg
660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag
720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg
780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc
840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact
900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc
960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc
1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac
1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat
1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt
1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt
1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg
1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag
1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc
1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc
1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga
1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc
1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg
1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca
1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt
1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg
1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc
1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc
1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca
2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt
2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt
2160
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag
2220
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc
2280
taaaaaagaa aagagatgaa agaccactct ttccccaaat tctcgcctct attgagctgc
2340
tggcccgctc attgccaaaa attcaccgca gtgcatcaga accctccttg aatcgggctg
2400
gcttccaaac agaggatttt agtctatatg cttgtgcttc tccaaaaaca cccattcagg
2460
cagggggata tggagaattt gcagccttca agtagccaca ccatcatgac agcatctact
2520
cttatttctt aagtcttgtg ttcgtacaat ttgttaacat caaaacacag ttctgttcct
2580
caactctttt taaagttaaa atttttcagt gcataagctg gtgtggaaca gaaggaaatt
2640
tcccatccaa caaaagaggg aagaatgttt taggaaccag aattctctgc tgccagtgtt
2700
tcttcttcaa cacaaatatc acaagtctgc ccactcccag gaagaaagag gagagaccct
2760
gagttctgac cttttgatgg tcaggcatga tggaaagaaa ctgctgctac agcttgggag
2820
atttgctctg ggaagtctgc cagtcaactt tgcccttcta accaccagat caatatgtgg
2880
ctgatcatct gatggggcag ttgcaatcac caagccttgt tctctttcct gttctgggat
2940
tgtgttgtgg aacccttttc cctagccacc accagttcat ttctgaggga tggaacaaaa
3000
atgcagcatg cccttcctgt gtggtgcatg ttcagtcctt gacaaatttt taccaaaatg
3060
aagctacttt atttaaaagg agggtgagag gtgaggaggt cactttgggt gtggcggaaa
3120
gggaatgctg catctttttc ctgggctgct ggggctctgg ccttggcttg ccagccggaa
3180
gcgctggcac gcatcgcctt cttttcccat tgggtccagc aatgaagacg agtgtttggg
3240
gttttttttt tctccaccat gtagcaagtt ctcaggaaaa tacaattgat atcttcctcc
3300
taagctcttc caatcagtca ccaagtactt atgtggttac tttgtccagg gcacaaaatg
3360
cctgtatcta attaaaagcc tacaaaactg cttgataaca gttttgaatg tgagacattt
3420
atgtaattta aatgtaaggt acaagtttta atttctgagt ttcttctatt atatttttat
3480
taaaaaaaga aaataatttt cagattgaat tggagtaaaa taatattact tcccactaga
3540
attatatatc ctggaaaatt gtatttttgt tacataagca gcttttaaag aaagatcatt
3600
acccttttct ctacataaat atatggggag tcttagccta atgacaaata tttataattt
3660
ttaaattaat ggtacttgct ggatccatac taacatcttt actaatacct cattgtttct
3720
tccaacttac tcctacacta catcctacat cttcttccta gtcttttatc tagaatatgc
3780
aacctcaaat aaaaatggtg gtgtcctcat tcattctcct ccttcctttt ttcccaagcc
3840
tgatcttcaa aaggttggtt aatttggcag ctgagttcct ccccaggcag agaatagacc
3900
aattttaggt gtattgggac tgagggagga tgtgtaaaga ttaacatcag taaagaaccg
3960
ctgtggagta attaagaact ttgttcttta taactggaga atataaccta accctaacat
4020
ccctcagcct ttactaaagt gtggcgtaaa tcacagtagt agcaaagaaa gtgactctgg
4080
atgtgttcct ggccagtacc tcccttatca tgaatgtaga ctctctcatc aagatttagg
4140
aatataaatc aaatcaaatg tgcccagcca agctatgtag taagggactt gaacaatatt
4200
aggcagaacc tataaaataa atcagggaat tagaaattat ttaaagtttt caaattgtaa
4260
attgccccgg tgtctttcag cctactgcca ttatttttgc tacaatacct acatttcaga
4320
ggagggccta ctgaaaattc catgcaagtg gaaaataatc ctcaagttat taatgagttt
4380
gaaaagcaat gagttcttaa gtctttgtga gtagagcaag atcctacaaa attcagaaat
4440
agtaaaaatg gattcatgct gatttgaaga gcatctgtgt gcataatata atgctgcatc
4500
tcttttaaaa gcagtctatt tttcttttta aatttgtccc catagatgct tttgaacatg
4560
aacatgctta tgttaccttt tccgaggttg ggaagagcca ggagctctca ggcagggccc
4620
cctccctcag ctgggcagga gctgctcagg aggagctagt tatagaggaa gcttagcgtt
4680
ggcattttca aaattcaagg tgataacgct ttcttcttcc tttctgtttt agaatagatt
4740
gctgtctgat ttgaaaaagg gaaatagatt tgatctcaaa tgaatctgtg cccagaagcc
4800
aggctcaggg tattcagaga tttgtatagt gccctcaaaa aataacaaaa ttttagcttt
4860
ccttttttct tcttttctcc atcaaattct tttttctcta gtttacaaat gacatggaaa
4920
aggaatttcc cctgagtttt gtatgccttt ttttttttgg cttagactat agataggcgt
4980
gttgagctcc taagaaaata caaggaggaa ctctttgttg tgcagagcac tttatgagta
5040
gtttgtgtgg ataatatgtg actgcttccc tgacgagctt gtgaggctgt acttatgtct
5100
ttcctgtaag gcagcttcag tgccttctgt agtgtatata aggaaagatt acgccttctg
5160
aaaaatctca gagcaaccat aagattattt taaaatatgt agtatgactg atggactttt
5220
tcatcattaa attagtctag catctaaact tttaccactg aaataatatt gaccaaaaag
5280
caatttataa aaggtatttg tgaatagaaa atacaatgtg atcatttgta cttatgtgca
5340
ccttaaaaga ggaattctgt ctagctgtca aattctggtt ccttaacatc cagtccttga
5400
ttgtgattga gatctggtag gacgtgctgg ggcacgctag cagataaaat cccgtatact
5460
ttaggataga tgttacattt atgtcagtgt tggcaaagag cattgtgtag taataaagaa
5520
ttcaagactt cagcaatgtc aacctgaaac tttgtaaata tttcctagat tgttatttga
5580
tgcagtcaca gctctttatc acacaatgtt gtctttccct catcaggcaa ttttagaact
5640
gctgcacacc cctcctcaga tctcacctgc ccctcctgta cattcacctc tccagccttg
5700
tgcacacctc atttagcttt agtttgaaac acattgcagg gttcaggtga cctcttcaaa
5760
aactacctcc tcagaatgag gtaatgaata gttatttatt ttaaaatatg aaaagtcagg
5820
agctctagaa tatgaagatg atctaagatt ttaactttta tgtatacttg ttgagcactc
5880
tccttttgtc ctaaagggca ttatacattt aagcagtaat actgaaaaat gtagctcaga
5940
gtaactgaat gttgttgaaa gtggtgccag aatctgtttt aggggtacgt atcagaatct
6000
taatcttaaa tcggttacat gaaattaaat agttaatggt aacacttgac taacagatat
6060
aattttaatt ttcggtaggc ttttagcaag acagtaagta catcttcata atgagttagc
6120
cacagcttca tcacatgcac agattttcct gttgagagac tgcccagtta agagggtaga
6180
atgatgaacc atttttcagg attctcttct ttgtccaaac tggcattgtg agtgctagaa
6240
tatcagcact ttcaaactag tgattccaac tattaggcta ttaaaaagca aaacaaacca
6300
aacaaaccat agccagacat gggaagttta ctatgagtat aaacagcaaa tagcttacag
6360
gtcatacatt gaaatggtgt aggtaaggcg ttagaaaaat accttgacaa tttgccaaat
6420
gatcttactg tgccttcatg atgcaataaa aaaaaaaaaa atttagcata aatcagtgat
6480
ttgtgaagag agcagccacc ctggtctaac tcagctgtgt taatattttt tagcgtgcaa
6540
tttagactgc aaagataaat gcactaaaga gtttatagcc aaaatcacat ttaaaaaatg
6600
agagaaaaca caggtaaatt ttcagtgaac aaaattattt ttttaaagta cataatccct
6660
agtatagtca gatatattta tcacatagag caaataggtt gaaatcacaa ttcagtgaca
6720
tttctagaga aactttttct actcccatag gttcttcaaa gcatggaact tttatataac
6780
agaaatgtgt gacggtcatt ttaaattgct gtagtttggg gctgaagtac tgtgtgctgg
6840
gcagcaatca catgtattaa ctagtgagaa aggagaaatt aagatatagg acagaatttg
6900
attttcttgt tcccagatta ctgctgccaa cctagacact gagtttccag aggctgaaac
6960
gtaaacttgc agctcagcaa ctgttttgca aagttagtgg gactgtcctg cttatgctgt
7020
tcaaaaatgc tctgagggcc aggtggggcc tccaggggct cctctctgag gggacatcag
7080
actagctaac gacctggcgg gcggatgtga accggacaca ctccatggtg tgcttcttgt
7140
atcggtccct cgccaccctc aagaaaggct tcagcgggtt ctctagacgt ctccactaag
7200
gtgtgttact aacagccatg ggttgttgag cacccgagga gtgcaatagc atctctgcat
7260
gattgtatat tggcccgaag agaatgaagt ggccagtgta ctcatgttcc atgttgctag
7320
ctctggtaaa ctgaaaatac tggtaagatt tttgttttat cagtacacta gagagtaagc
7380
tttgttttgt tgtttttaga taatgttttc acttccattt ggaaagacat ttaaattgag
7440
tttcagtcct aaattttgcc agtcatggta attagcagtt tctatcaggt atttttaagg
7500
tagaagagga tagaaacata agttctaaaa gcttaaggta accgtggttt attttaaaat
7560
gtttaggggt ggttagtctc tacctcaaaa aaagtgagtg aatcttttat ttcagcattc
7620
acaagttcgg ctgttgtttt tgtaatacat ttttttttta accttttgac ccccctttac
7680
ctaagtgtca atgtagtttt attaattact aagtcagttt cattaaaatg tttatttagc
7740
agttttgact aattgcaatg attaatatag ccagttgtgc atgaggacac agccagtgag
7800
tatatctggg ttttttttgt gatgcttttt ttcttaagac ttctgtagat ttatgaagta
7860
ctcattgaaa acaactaaaa tacgtttatt cgtgttaata tggaaaaaaa aaaa
7914
<210> 24
<211> 766
<212> БЕЛОК
<213> Bos taurus
<400> 24
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr
660 665 670
Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met
675 680 685
Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro
690 695 700
Leu Phe Pro Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser Leu
705 710 715 720
Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala Gly
725 730 735
Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys Thr
740 745 750
Pro Ile Gln Ala Gly Gly Tyr Gly Glu Phe Ala Ala Phe Lys
755 760 765
<210> 25
<211> 4670
<212> ДНК
<213> Bos taurus
<400> 25
ggtgtgtcat agtgcagcag attgaatgca gaagatatga aaattcagat gtcttctgtt
60
aaggtgtgga atatcaaaca aatgattaag ttgacacagg agcatataga ggccctattg
120
gacaaatttg gtggggagca taatccacca tcaatatatc tggaggccta tgaagaatac
180
accagcaagc tagatgccct ccaacaaaga gaacaacagt tattggaatc cctggggaat
240
ggaactgatt tttctgtttc tagctctgca tcaacggaca ccgttacatc ttcttcctct
300
tctagccttt cagtgctgcc ttcatctctt tcagtttttc aaaatcccac agatgtgtca
360
cggagcaacc ccaagtcacc acaaaaacct atcgttagag tcttcctgcc caataaacag
420
aggacagtgg tacctgcacg gtgtggagtc acagtccggg acagcctgaa gaaggcactg
480
atgatgagag gtctaatccc agagtgctgt gctgtttaca gaattcagga tggggagaag
540
aaaccaattg gctgggacac tgatatttcc tggcttactg gagaggagtt gcatgtagaa
600
gtgttggaga atgttccact tacaacacac aactttgtac ggaaaacttt tttcacctta
660
gcattttgtg acttctgtag aaagctgctt ttccagggat tccgctgtca aacatgtggt
720
tataaatttc accagcgttg tagtacagag gttccactga tgtgtgttaa ttatgaccaa
780
ctagatttgc tgtttgtctc caagttcttt gaacaccacc caataccaca ggaggaggcc
840
tccttagcag agactaccct tccatgtggc tcatcccctt ctgcaccccc ctccgattct
900
attgggcccc caattctcac cagtccatct ccttcaaaat ccattccaat tccacagcct
960
ttccgaccag cagatgaaga tcatcgaaat cagtttggac aacgagaccg gtcctcatca
1020
gctccaaatg tgcatataaa cacaatagaa cccgtcaata ttgatgactt gattagagac
1080
caagggtttc gtagtgatgg aggatcaacc acaggtttat ccgccacacc ccctgcctca
1140
ttacctggct cactctctaa tgtgaaagca ttgcagaaat ctccaggacc tcagcgagaa
1200
agaaagtcct cttcatcctc agaagacagg aatcgaatga aaacgcttgg tagacgggat
1260
tcaagtgacg attgggagat tcctgatgga cagatcacag tgggacaaag aattggatca
1320
gggtcatttg ggacagtcta caagggaaag tggcatggtg atgtggcagt gaaaatgttg
1380
aatgtgacag cacccacacc tcagcagtta caggccttca aaaatgaagt aggagtactc
1440
aggaaaacgc gacatgtgaa tatcctcctc ttcatgggtt attcaacaaa gccacaactg
1500
gctattgtta cccagtggtg tgagggctcc agtttatatc atcatctcca catcattgag
1560
accaaattcg agatgatcaa acttatagat attgcacggc agactgcaca gggcatggat
1620
tacttacacg ccaagtcaat catccacaga gacctcaaga gtaataatat ttttcttcat
1680
gaagacctca cagtaaaaat aggtgatttt ggtctagcca cagtgaaatc tcgatggagt
1740
gggtcccatc agtttgaaca gttgtctgga tccattttgt ggatggcacc agaagtaatc
1800
agaatgcaag ataaaaaccc atatagcttt cagtcagatg tatatgcatt tgggattgtt
1860
ctgtatgaat tgatgaccgg acagttacct tattcaaata tcaacaacag ggaccagata
1920
atttttatgg tgggacgagg atatctgtct ccagatctca gtaaggtacg gagtaactgt
1980
ccaaaagcca tgaagagatt aatggcagag tgcctaaaaa agaaaagaga tgaaagacca
2040
ctctttcccc aagtaggaaa gactctccta agcaagagac aaaattcaga agttatcagg
2100
gaaaaagata agcagattct cgcctctatt gagctgctgg cccgctcatt gccaaaaatt
2160
caccgcagtg catcagaacc ctccttgaat cgggctggct tccaaacaga ggattttagt
2220
ctatatgctt gtgcttctcc aaaaacaccc attcaggcag ggggatatga agcagatttg
2280
gctcttacat caaataaaaa tagagtagaa gttgggattt agagatttcc tgacatgcaa
2340
gaaggaataa gcaagaaaaa aaggtttgtt ttccccaaat catatctatt gtcttttact
2400
tctatttttt cttaaatttt ttgtgatttc agagacatgt agagttttat tgatacctaa
2460
actatgagtt cttttttttt tttttttttc attattttga tttttttggc caagaggcat
2520
atgggatctt agcttgagaa agcaacaatt ttcttgatgt cattttgggt gagggcacat
2580
attgctgtga acagtgtggt gatagccacc agggaccaaa ctcacacccg ctgcattgaa
2640
aggtgaagtc ttaaacactg gaccagcaga gaaattccta ctctatgagt tctttttgtc
2700
atcccctccc cgcaccctcc acccccaacc taaagtctga tgatgaaatc aacaactatt
2760
ccattagaag cagtagattc tggtagcatg atctttagtt tgttagtaag attttgtgct
2820
ttgtggggtt gtgtcgtttt aaggctaata tttaagtttg tcaaatagaa tgctgttcag
2880
attgtaaaaa tgagtaataa acatctgaag ttttttttaa gttattttta acatggtata
2940
tacagttgag cttagagttt atcattttct gatattctct tacttagtag atgaattcta
3000
gccatttttt ataaagattt ctgttaagca aatcctgttt tcacatgggc ttcctttaag
3060
ggattttaga ttctgctgga tatggtgact gctcataaga ctgttgaaaa ttacttttaa
3120
gatgtattag aatacttctg aaaaaaaata gcaaccttaa aaccataagc aaaagtagta
3180
agggtgttta tacatttcta gagtccctgt ttaggtaata gcctcctatg attgtacttt
3240
aaatgttttg ctctccaagg ttttagtaac ttggcttttt ttctaatcag tgccaaactc
3300
ccccagtttt tttaacttta aatatgaggt aataaatctt ttacccttcc ttgatctttt
3360
gacttataat accttggtca gttgtttctt aaaaggaatc cttaaatgga aagagacaat
3420
atcactgtct gcagttctga ttagtagttt tattcagaat ggaaaaacag attattcatt
3480
tttgaaaatt gttcaggggt atgttcattg ttaggacctt ggactttgga gtcagtgcct
3540
agctatgcat tccaggtctg ccattttctg gctgtgaaat tttggacaag ttacttaacc
3600
actttaaacc ccagctttaa gaagtaaatt aaccccagta aattaagaag taatagcagc
3660
cacttcgtag agttgttatg aggctcagat gcagtgcaaa tgtgtataaa gtattcaggg
3720
agtcacctgg tatactataa tagacactag aatagttgcc aatattatca gcatacaatc
3780
tgaggattct gtcagccaat cattagcaat ctgttgtttg ttgggacatg ccagtgttct
3840
ccagttgaaa tcagtagcaa tctaaaaatg gatagattat tcctcattta aatagtgtgt
3900
tcatataagt gattgcttgg atccttatca gaagttgctg ttactgaaaa atgataaggc
3960
tgactaaatt gtgatagttg tcagttacta accaactccc agaaatgaat aagaggaacc
4020
tatctctagt tcctagtaga aggtatggac aaaatagtag gtgaaaaata atgtcttgaa
4080
cccccaaatt aagtaagctt taaagagtac aatacctcaa agggtctttg cggtttaaaa
4140
tttgtatgct gagaatgatg ttcattgaca tgtgcctata tgtaattttt tgatagttta
4200
aaaggtgaaa tgaactacag atgggagagg tctgaatttt cttgccttca gtcaaatgtg
4260
taatgtggac atattatttg acctgtgaat tttatctttt aaaaaagatt aattcctgct
4320
tcttccttcc taatagttgc attataataa tgaaaatgag ttgataattt ggggggaaag
4380
tattctacaa atcaacctta ttattttacc attggtttct gagaaatttt gttcatttga
4440
accgtttata gcttgattag aatcatagca tgtaaaaccc aactgaggga ttatctgcag
4500
acttaatgta gtattatgta agttgtcttc tttcatttcg accttttttg cttttgttgt
4560
tgctagatct gtagtatgta gctagtcacc tttcagcgag gtttcagcga ggcttttctg
4620
tgtctctagg ttatttgaga taactttttt aaaattagct cttgtcctcc
4670
<210> 26
<211> 761
<212> БЕЛОК
<213> Bos taurus
<400> 26
Met Lys Ile Gln Met Ser Ser Val Lys Val Trp Asn Ile Lys Gln Met
1 5 10 15
Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu Asp Lys Phe Gly
20 25 30
Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala Tyr Glu Glu Tyr
35 40 45
Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln Gln Leu Leu Glu
50 55 60
Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser Ser Ala Ser Thr
65 70 75 80
Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser Val Leu Pro Ser
85 90 95
Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser Arg Ser Asn Pro
100 105 110
Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu Pro Asn Lys Gln
115 120 125
Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val Arg Asp Ser Leu
130 135 140
Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu Cys Cys Ala Val
145 150 155 160
Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly Trp Asp Thr Asp
165 170 175
Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu Val Leu Glu Asn
180 185 190
Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr Phe Phe Thr Leu
195 200 205
Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln Gly Phe Arg Cys
210 215 220
Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser Thr Glu Val Pro
225 230 235 240
Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu Phe Val Ser Lys
245 250 255
Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala Ser Leu Ala Glu
260 265 270
Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro Pro Ser Asp Ser
275 280 285
Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser Lys Ser Ile Pro
290 295 300
Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His Arg Asn Gln Phe
305 310 315 320
Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val His Ile Asn Thr
325 330 335
Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp Gln Gly Phe Arg
340 345 350
Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr Pro Pro Ala Ser
355 360 365
Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln Lys Ser Pro Gly
370 375 380
Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn Arg
385 390 395 400
Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro
405 410 415
Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly
420 425 430
Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala Val Lys Met Leu
435 440 445
Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu
450 455 460
Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe Met
465 470 475 480
Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys Glu
485 490 495
Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu Thr Lys Phe Glu
500 505 510
Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met Asp
515 520 525
Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn Asn
530 535 540
Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu
545 550 555 560
Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu
565 570 575
Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln Asp
580 585 590
Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile Val
595 600 605
Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn
610 615 620
Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr Leu Ser Pro Asp
625 630 635 640
Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met Lys Arg Leu Met
645 650 655
Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln
660 665 670
Val Gly Lys Thr Leu Leu Ser Lys Arg Gln Asn Ser Glu Val Ile Arg
675 680 685
Glu Lys Asp Lys Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser
690 695 700
Leu Pro Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala
705 710 715 720
Gly Phe Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys
725 730 735
Thr Pro Ile Gln Ala Gly Gly Tyr Glu Ala Asp Leu Ala Leu Thr Ser
740 745 750
Asn Lys Asn Arg Val Glu Val Gly Ile
755 760
<210> 27
<211> 4816
<212> ДНК
<213> Bos taurus
<400> 27
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc
60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc
120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg
180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg
240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt
300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga
360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa
420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac
480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa
540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag
600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg
660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag
720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg
780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc
840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact
900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc
960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc
1020
cactgatgtg tgttaattat gaccaactag agcccccaat tctcaccagt ccatctcctt
1080
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt
1140
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg
1200
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag
1260
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc
1320
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc
1380
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga
1440
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc
1500
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg
1560
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca
1620
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt
1680
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg
1740
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc
1800
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc
1860
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca
1920
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt
1980
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt
2040
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag
2100
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc
2160
taaaaaagaa aagagatgaa agaccactct ttccccaagt aggaaagact ctcctaagca
2220
agagacaaaa ttcagaagtt atcagggaaa aagataagca gattctcgcc tctattgagc
2280
tgctggcccg ctcattgcca aaaattcacc gcagtgcatc agaaccctcc ttgaatcggg
2340
ctggcttcca aacagaggat tttagtctat atgcttgtgc ttctccaaaa acacccattc
2400
aggcaggggg atatgaagca gatttggctc ttacatcaaa taaaaataga gtagaagttg
2460
ggatttagag atttcctgac atgcaagaag gaataagcaa gaaaaaaagg tttgttttcc
2520
ccaaatcata tctattgtct tttacttcta ttttttctta aattttttgt gatttcagag
2580
acatgtagag ttttattgat acctaaacta tgagttcttt tttttttttt tttttcatta
2640
ttttgatttt tttggccaag aggcatatgg gatcttagct tgagaaagca acaattttct
2700
tgatgtcatt ttgggtgagg gcacatattg ctgtgaacag tgtggtgata gccaccaggg
2760
accaaactca cacccgctgc attgaaaggt gaagtcttaa acactggacc agcagagaaa
2820
ttcctactct atgagttctt tttgtcatcc cctccccgca ccctccaccc ccaacctaaa
2880
gtctgatgat gaaatcaaca actattccat tagaagcagt agattctggt agcatgatct
2940
ttagtttgtt agtaagattt tgtgctttgt ggggttgtgt cgttttaagg ctaatattta
3000
agtttgtcaa atagaatgct gttcagattg taaaaatgag taataaacat ctgaagtttt
3060
ttttaagtta tttttaacat ggtatataca gttgagctta gagtttatca ttttctgata
3120
ttctcttact tagtagatga attctagcca ttttttataa agatttctgt taagcaaatc
3180
ctgttttcac atgggcttcc tttaagggat tttagattct gctggatatg gtgactgctc
3240
ataagactgt tgaaaattac ttttaagatg tattagaata cttctgaaaa aaaatagcaa
3300
ccttaaaacc ataagcaaaa gtagtaaggg tgtttataca tttctagagt ccctgtttag
3360
gtaatagcct cctatgattg tactttaaat gttttgctct ccaaggtttt agtaacttgg
3420
ctttttttct aatcagtgcc aaactccccc agttttttta actttaaata tgaggtaata
3480
aatcttttac ccttccttga tcttttgact tataatacct tggtcagttg tttcttaaaa
3540
ggaatcctta aatggaaaga gacaatatca ctgtctgcag ttctgattag tagttttatt
3600
cagaatggaa aaacagatta ttcatttttg aaaattgttc aggggtatgt tcattgttag
3660
gaccttggac tttggagtca gtgcctagct atgcattcca ggtctgccat tttctggctg
3720
tgaaattttg gacaagttac ttaaccactt taaaccccag ctttaagaag taaattaacc
3780
ccagtaaatt aagaagtaat agcagccact tcgtagagtt gttatgaggc tcagatgcag
3840
tgcaaatgtg tataaagtat tcagggagtc acctggtata ctataataga cactagaata
3900
gttgccaata ttatcagcat acaatctgag gattctgtca gccaatcatt agcaatctgt
3960
tgtttgttgg gacatgccag tgttctccag ttgaaatcag tagcaatcta aaaatggata
4020
gattattcct catttaaata gtgtgttcat ataagtgatt gcttggatcc ttatcagaag
4080
ttgctgttac tgaaaaatga taaggctgac taaattgtga tagttgtcag ttactaacca
4140
actcccagaa atgaataaga ggaacctatc tctagttcct agtagaaggt atggacaaaa
4200
tagtaggtga aaaataatgt cttgaacccc caaattaagt aagctttaaa gagtacaata
4260
cctcaaaggg tctttgcggt ttaaaatttg tatgctgaga atgatgttca ttgacatgtg
4320
cctatatgta attttttgat agtttaaaag gtgaaatgaa ctacagatgg gagaggtctg
4380
aattttcttg ccttcagtca aatgtgtaat gtggacatat tatttgacct gtgaatttta
4440
tcttttaaaa aagattaatt cctgcttctt ccttcctaat agttgcatta taataatgaa
4500
aatgagttga taatttgggg ggaaagtatt ctacaaatca accttattat tttaccattg
4560
gtttctgaga aattttgttc atttgaaccg tttatagctt gattagaatc atagcatgta
4620
aaacccaact gagggattat ctgcagactt aatgtagtat tatgtaagtt gtcttctttc
4680
atttcgacct tttttgcttt tgttgttgct agatctgtag tatgtagcta gtcacctttc
4740
agcgaggttt cagcgaggct tttctgtgtc tctaggttat ttgagataac ttttttaaaa
4800
ttagctcttg tcctcc
4816
<210> 28
<211> 757
<212> БЕЛОК
<213> Bos taurus
<400> 28
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Glu Pro Pro
275 280 285
Ile Leu Thr Ser Pro Ser Pro Ser Lys Ser Ile Pro Ile Pro Gln Pro
290 295 300
Phe Arg Pro Ala Asp Glu Asp His Arg Asn Gln Phe Gly Gln Arg Asp
305 310 315 320
Arg Ser Ser Ser Ala Pro Asn Val His Ile Asn Thr Ile Glu Pro Val
325 330 335
Asn Ile Asp Asp Leu Ile Arg Asp Gln Gly Phe Arg Ser Asp Gly Gly
340 345 350
Ser Thr Thr Gly Leu Ser Ala Thr Pro Pro Ala Ser Leu Pro Gly Ser
355 360 365
Leu Ser Asn Val Lys Ala Leu Gln Lys Ser Pro Gly Pro Gln Arg Glu
370 375 380
Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn Arg Met Lys Thr Leu
385 390 395 400
Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp Gly Gln Ile
405 410 415
Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr Val Tyr Lys
420 425 430
Gly Lys Trp His Gly Asp Val Ala Val Lys Met Leu Asn Val Thr Ala
435 440 445
Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val Gly Val Leu
450 455 460
Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe Met Gly Tyr Ser Thr
465 470 475 480
Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly Ser Ser Leu
485 490 495
Tyr His His Leu His Ile Ile Glu Thr Lys Phe Glu Met Ile Lys Leu
500 505 510
Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr Leu His Ala
515 520 525
Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile Phe Leu His
530 535 540
Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala Thr Val Lys
545 550 555 560
Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser Gly Ser Ile
565 570 575
Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys Asn Pro Tyr
580 585 590
Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu Tyr Glu Leu
595 600 605
Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg Asp Gln Ile
610 615 620
Ile Phe Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu Ser Lys Val
625 630 635 640
Arg Ser Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala Glu Cys Leu
645 650 655
Lys Lys Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Val Gly Lys Thr
660 665 670
Leu Leu Ser Lys Arg Gln Asn Ser Glu Val Ile Arg Glu Lys Asp Lys
675 680 685
Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro Lys Ile
690 695 700
His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe Gln Thr
705 710 715 720
Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro Ile Gln
725 730 735
Ala Gly Gly Tyr Glu Ala Asp Leu Ala Leu Thr Ser Asn Lys Asn Arg
740 745 750
Val Glu Val Gly Ile
755
<210> 29
<211> 2499
<212> ДНК
<213> Bos taurus
<400> 29
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc
60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc
120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg
180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg
240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt
300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga
360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa
420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac
480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa
540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag
600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg
660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag
720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg
780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc
840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact
900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc
960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc
1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac
1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat
1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt
1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt
1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg
1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag
1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc
1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc
1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga
1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc
1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg
1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca
1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt
1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg
1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc
1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc
1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca
2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt
2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt
2160
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag
2220
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc
2280
taaaaaagaa aagagatgaa agaccactct ttccccaagt aggaaagact ctcctaagca
2340
agagacaaaa ttcagaagtt atcagggaaa aagataagca ggaaaagtat gtttctttag
2400
tacattccag gcatttggga ttacagtaaa aacaatattc tcgcctctat tgagctgctg
2460
gcccgctcat tgccaaaaat tcaccgcagt gcatcagaa
2499
<210> 30
<211> 744
<212> БЕЛОК
<213> Bos taurus
<400> 30
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr
660 665 670
Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met
675 680 685
Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro
690 695 700
Leu Phe Pro Gln Val Gly Lys Thr Leu Leu Ser Lys Arg Gln Asn Ser
705 710 715 720
Glu Val Ile Arg Glu Lys Asp Lys Gln Glu Lys Tyr Val Ser Leu Val
725 730 735
His Ser Arg His Leu Gly Leu Gln
740
<210> 31
<211> 2404
<212> ДНК
<213> Bos taurus
<400> 31
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc
60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc
120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg
180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg
240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt
300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga
360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa
420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac
480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa
540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag
600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg
660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag
720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg
780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc
840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact
900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc
960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc
1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac
1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat
1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt
1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt
1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg
1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag
1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc
1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc
1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga
1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc
1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg
1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca
1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt
1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg
1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc
1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc
1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca
2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt
2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt
2160
caaatatcaa caacagggac cagataattt ttatggtggg acgaggatat ctgtctccag
2220
atctcagtaa ggtacggagt aactgtccaa aagccatgaa gagattaatg gcagagtgcc
2280
taaaaaagaa aagagatgaa agaccactct ttccccaaga tctctcttcc caccatagac
2340
acaaaaattt cagatggcta caggtttaca tgtaaaaaac agaattataa caaatgattt
2400
ttat
2404
<210> 32
<211> 726
<212> БЕЛОК
<213> Bos taurus
<400> 32
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr
660 665 670
Leu Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met
675 680 685
Lys Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro
690 695 700
Leu Phe Pro Gln Asp Leu Ser Ser His His Arg His Lys Asn Phe Arg
705 710 715 720
Trp Leu Gln Val Tyr Met
725
<210> 33
<211> 2331
<212> ДНК
<213> Bos taurus
<400> 33
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc
60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc
120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg
180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg
240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt
300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga
360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa
420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac
480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa
540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag
600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg
660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag
720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg
780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc
840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact
900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc
960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc
1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac
1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat
1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt
1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt
1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg
1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag
1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc
1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc
1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga
1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc
1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg
1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca
1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt
1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg
1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc
1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc
1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca
2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt
2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt
2160
caaatatcaa caacagggac caggtgcttt gtcctccatg ggagtgtaat aaatgctgtg
2220
caagggctta cttcccatga gagaagtgag tgaccaacag aaggataatt tttatggtgg
2280
gacgaggata tctgtctcca gatctcagta aggtacggag taactgtcca a
2331
<210> 34
<211> 681
<212> БЕЛОК
<213> Bos taurus
<400> 34
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Val Leu Cys Pro Pro Trp Glu Cys Asn
660 665 670
Lys Cys Cys Ala Arg Ala Tyr Phe Pro
675 680
<210> 35
<211> 2319
<212> ДНК
<213> Bos taurus
<400> 35
ctcagctgcg ccgggtctca caagacggtt cccgaggtgg cccaggcgcc gtcccaccgc
60
cgacgccgcc cgggccgccc gggccgtccc tccccgctgc cccccgtcct ccgcctccgc
120
ctccccccgc cctcagcctc ccttccccct ccccgcccag cagcggtcgc tcgggcccgg
180
ctctcggtta taagatggcg gcgctgagtg gcggcggcgg cggcggcggc ggtggcgcgg
240
agcagggcca ggctctgttc aacggggaca tggagcccga ggccggcgcc gcggcctctt
300
cggctgcgga ccccgccatt cccgaggagg tgtggaatat caaacaaatg attaagttga
360
cacaggagca tatagaggcc ctattggaca aatttggtgg ggagcataat ccaccatcaa
420
tatatctgga ggcctatgaa gaatacacca gcaagctaga tgccctccaa caaagagaac
480
aacagttatt ggaatccctg gggaatggaa ctgatttttc tgtttctagc tctgcatcaa
540
cggacaccgt tacatcttct tcctcttcta gcctttcagt gctgccttca tctctttcag
600
tttttcaaaa tcccacagat gtgtcacgga gcaaccccaa gtcaccacaa aaacctatcg
660
ttagagtctt cctgcccaat aaacagagga cagtggtacc tgcacggtgt ggagtcacag
720
tccgggacag cctgaagaag gcactgatga tgagaggtct aatcccagag tgctgtgctg
780
tttacagaat tcaggatggg gagaagaaac caattggctg ggacactgat atttcctggc
840
ttactggaga ggagttgcat gtagaagtgt tggagaatgt tccacttaca acacacaact
900
ttgtacggaa aacttttttc accttagcat tttgtgactt ctgtagaaag ctgcttttcc
960
agggattccg ctgtcaaaca tgtggttata aatttcacca gcgttgtagt acagaggttc
1020
cactgatgtg tgttaattat gaccaactag atttgctgtt tgtctccaag ttctttgaac
1080
accacccaat accacaggag gaggcctcct tagcagagac tacccttcca tgtggctcat
1140
ccccttctgc acccccctcc gattctattg ggcccccaat tctcaccagt ccatctcctt
1200
caaaatccat tccaattcca cagcctttcc gaccagcaga tgaagatcat cgaaatcagt
1260
ttggacaacg agaccggtcc tcatcagctc caaatgtgca tataaacaca atagaacccg
1320
tcaatattga tgacttgatt agagaccaag ggtttcgtag tgatggagga tcaaccacag
1380
gtttatccgc cacaccccct gcctcattac ctggctcact ctctaatgtg aaagcattgc
1440
agaaatctcc aggacctcag cgagaaagaa agtcctcttc atcctcagaa gacaggaatc
1500
gaatgaaaac gcttggtaga cgggattcaa gtgacgattg ggagattcct gatggacaga
1560
tcacagtggg acaaagaatt ggatcagggt catttgggac agtctacaag ggaaagtggc
1620
atggtgatgt ggcagtgaaa atgttgaatg tgacagcacc cacacctcag cagttacagg
1680
ccttcaaaaa tgaagtagga gtactcagga aaacgcgaca tgtgaatatc ctcctcttca
1740
tgggttattc aacaaagcca caactggcta ttgttaccca gtggtgtgag ggctccagtt
1800
tatatcatca tctccacatc attgagacca aattcgagat gatcaaactt atagatattg
1860
cacggcagac tgcacagggc atggattact tacacgccaa gtcaatcatc cacagagacc
1920
tcaagagtaa taatattttt cttcatgaag acctcacagt aaaaataggt gattttggtc
1980
tagccacagt gaaatctcga tggagtgggt cccatcagtt tgaacagttg tctggatcca
2040
ttttgtggat ggcaccagaa gtaatcagaa tgcaagataa aaacccatat agctttcagt
2100
cagatgtata tgcatttggg attgttctgt atgaattgat gaccggacag ttaccttatt
2160
caaatatcaa caacagggac caggtgcttt gtcctccatg ggagtgtaat aaatgctgtg
2220
caagggctta cttcccatga gagaagtgag tgaccaacag aaggtctgtg caaggaaaag
2280
agacaaagcc acggatcaga agcacatggc cataactga
2319
<210> 36
<211> 681
<212> БЕЛОК
<213> Bos taurus
<400> 36
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Val Leu Cys Pro Pro Trp Glu Cys Asn
660 665 670
Lys Cys Cys Ala Arg Ala Tyr Phe Pro
675 680
<210> 37
<211> 2661
<212> ДНК
<213> Bos taurus
<400> 37
tcagctgcgc cgggtctcac aagacggttc ccgaggtggc ccaggcgccg tcccaccgcc
60
gacgccgccc gggccgcccg ggccgtccct ccccgctgcc ccccgtcctc cgcctccgcc
120
tccccccgcc ctcagcctcc cttccccctc cccgcccagc agcggtcgct cgggcccggc
180
tctcggttat aagatggcgg cgctgagtgg cggcggcggc ggcggcggcg gtggcgcgga
240
gcagggccag gctctgttca acggggacat ggagcccgag gccggcgccg cggcctcttc
300
ggctgcggac cccgccattc ccgaggaggt gtggaatatc aaacaaatga ttaagttgac
360
acaggagcat atagaggccc tattggacaa atttggtggg gagcataatc caccatcaat
420
atatctggag gcctatgaag aatacaccag caagctagat gccctccaac aaagagaaca
480
acagttattg gaatccctgg ggaatggaac tgatttttct gtttctagct ctgcatcaac
540
ggacaccgtt acatcttctt cctcttctag cctttcagtg ctgccttcat ctctttcagt
600
ttttcaaaat cccacagatg tgtcacggag caaccccaag tcaccacaaa aacctatcgt
660
tagagtcttc ctgcccaata aacagaggac agtggtacct gcacggtgtg gagtcacagt
720
ccgggacagc ctgaagaagg cactgatgat gagaggtcta atcccagagt gctgtgctgt
780
ttacagaatt caggatgggg agaagaaacc aattggctgg gacactgata tttcctggct
840
tactggagag gagttgcatg tagaagtgtt ggagaatgtt ccacttacaa cacacaactt
900
tgtacggaaa acttttttca ccttagcatt ttgtgacttc tgtagaaagc tgcttttcca
960
gggattccgc tgtcaaacat gtggttataa atttcaccag cgttgtagta cagaggttcc
1020
actgatgtgt gttaattatg accaactaga tttgctgttt gtctccaagt tctttgaaca
1080
ccacccaata ccacaggagg aggcctcctt agcagagact acccttccat gtggctcatc
1140
cccttctgca cccccctccg attctattgg gcccccaatt ctcaccagtc catctccttc
1200
aaaatccatt ccaattccac agcctttccg accagcagat gaagatcatc gaaatcagtt
1260
tggacaacga gaccggtcct catcagctcc aaatgtgcat ataaacacaa tagaacccgt
1320
caatattgat gacttgatta gagaccaagg gtttcgtagt gatggaggat caaccacagg
1380
tttatccgcc acaccccctg cctcattacc tggctcactc tctaatgtga aagcattgca
1440
gaaatctcca ggacctcagc gagaaagaaa gtcctcttca tcctcagaag acaggaatcg
1500
aatgaaaacg cttggtagac gggattcaag tgacgattgg gagattcctg atggacagat
1560
cacagtggga caaagaattg gatcagggtc atttgggaca gtctacaagg gaaagtggca
1620
tggtgatgtg gcagtgaaaa tgttgaatgt gacagcaccc acacctcagc agttacaggc
1680
cttcaaaaat gaagtaggag tactcaggaa aacgcgacat gtgaatatcc tcctcttcat
1740
gggttattca acaaagccac aactggctat tgttacccag tggtgtgagg gctccagttt
1800
atatcatcat ctccacatca ttgagaccaa attcgagatg atcaaactta tagatattgc
1860
acggcagact gcacagggca tggattactt acacgccaag tcaatcatcc acagagacct
1920
caagagtaat aatatttttc ttcatgaaga cctcacagta aaaataggtg attttggtct
1980
agccacagtg aaatctcgat ggagtgggtc ccatcagttt gaacagttgt ctggatccat
2040
tttgtggatg gcaccagaag taatcagaat gcaagataaa aacccatata gctttcagtc
2100
agatgtatat gcatttggga ttgttctgta tgaattgatg accggacagt taccttattc
2160
aaatatcaac aacagggacc agtctgtgca aggaaaagag acaaagccac ggatcagaag
2220
cacatggcca taactgaaga ttttgtgaac tctcacaagg aaaaaatttg ctctttgaac
2280
aataagaagg aactcactaa aatgtaactg agaactgttc aacaggttga aagctgaaag
2340
atgccattgg aactgacaaa atgtttctta aacataaatg atgaaacagt gaaactacat
2400
aatatctcct ctggctgaaa cattcaagaa gtttaaaatg cttaagttaa aaataaaatc
2460
ctagtaaaca atggacttac tgtgcaacat agagaatatc ttacgataac ctgtaatgga
2520
aaagaatctg aaaaagaatg tatataactg aatcactttg ctgtaaacta gaatctgaca
2580
caacactgta aatcactaca cttttctgtt gcatgccaaa gattatttaa taacgtcatt
2640
aaaaaattat tttaataatt a
2661
<210> 38
<211> 679
<212> БЕЛОК
<213> Bos taurus
<400> 38
Met Ala Ala Leu Ser Gly Gly Gly Gly Gly Gly Gly Gly Gly Ala Glu
1 5 10 15
Gln Gly Gln Ala Leu Phe Asn Gly Asp Met Glu Pro Glu Ala Gly Ala
20 25 30
Ala Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn
35 40 45
Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu
50 55 60
Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala
65 70 75 80
Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln
85 90 95
Gln Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser
100 105 110
Ser Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser
115 120 125
Val Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser
130 135 140
Arg Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu
145 150 155 160
Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val
165 170 175
Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu
180 185 190
Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly
195 200 205
Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu
210 215 220
Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr
225 230 235 240
Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln
245 250 255
Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser
260 265 270
Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu
275 280 285
Phe Val Ser Lys Phe Phe Glu His His Pro Ile Pro Gln Glu Glu Ala
290 295 300
Ser Leu Ala Glu Thr Thr Leu Pro Cys Gly Ser Ser Pro Ser Ala Pro
305 310 315 320
Pro Ser Asp Ser Ile Gly Pro Pro Ile Leu Thr Ser Pro Ser Pro Ser
325 330 335
Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His
340 345 350
Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val
355 360 365
His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp
370 375 380
Gln Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr
385 390 395 400
Pro Pro Ala Ser Leu Pro Gly Ser Leu Ser Asn Val Lys Ala Leu Gln
405 410 415
Lys Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu
420 425 430
Asp Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp
435 440 445
Trp Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser
450 455 460
Gly Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala
465 470 475 480
Val Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala
485 490 495
Phe Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile
500 505 510
Leu Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr
515 520 525
Gln Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu
530 535 540
Thr Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala
545 550 555 560
Gln Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu
565 570 575
Lys Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly
580 585 590
Asp Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln
595 600 605
Phe Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile
610 615 620
Arg Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala
625 630 635 640
Phe Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser
645 650 655
Asn Ile Asn Asn Arg Asp Gln Ser Val Gln Gly Lys Glu Thr Lys Pro
660 665 670
Arg Ile Arg Ser Thr Trp Pro
675
<210> 39
<211> 7434
<212> ДНК
<213> Bos taurus
<400> 39
acaccgttac atcttcttcc tcttctagcc tttcagtgct gccttcatct ctttcagttt
60
ttcaaaatcc cacagatgtg tcacggagca accccaagtc accacaaaaa cctatcgtta
120
gagtcttcct gcccaataaa cagaggacag tggtacctgc acggtgtgga gtcacagtcc
180
gggacagcct gaagaaggca ctgatgatga gaggtctaat cccagagtgc tgtgctgttt
240
acagaattca ggatggggag aagaaaccaa ttggctggga cactgatatt tcctggctta
300
ctggagagga gttgcatgta gaagtgttgg agaatgttcc acttacaaca cacaactttg
360
tacggaaaac ttttttcacc ttagcatttt gtgacttctg tagaaagctg cttttccagg
420
gattccgctg tcaaacatgt ggttataaat ttcaccagcg ttgtagtaca gaggttccac
480
tgatgtgtgt taattatgac caactagatt tgctgtttgt ctccaagttc tttgaacacc
540
acccaatacc acaggaggag gcctccttag cagagactac ccttccatgt ggctcatccc
600
cttctgcacc cccctccgat tctattgggc ccccaattct caccagtcca tctccttcaa
660
aatccattcc aattccacag cctttccgac cagcagatga agatcatcga aatcagtttg
720
gacaacgaga ccggtcctca tcagctccaa atgtgcatat aaacacaata gaacccgtca
780
atattgatga cttgattaga gaccaagggt ttcgtagtga tggaggatca accacaggtt
840
tatccgccac accccctgcc tcattacctg gctcactctc taatgtgaaa gcattgcaga
900
aatctccagg acctcagcga gaaagaaagt cctcttcatc ctcagaagac aggaatcgaa
960
tgaaaacgct tggtagacgg gattcaagtg acgattggga gattcctgat ggacagatca
1020
cagtgggaca aagaattgga tcagggtcat ttgggacagt ctacaaggga aagtggcatg
1080
gtgatgtggc agtgaaaatg ttgaatgtga cagcacccac acctcagcag ttacaggcct
1140
tcaaaaatga agtaggagta ctcaggaaaa cgcgacatgt gaatatcctc ctcttcatgg
1200
gttattcaac aaagccacaa ctggctattg ttacccagtg gtgtgagggc tccagtttat
1260
atcatcatct ccacatcatt gagaccaaat tcgagatgat caaacttata gatattgcac
1320
ggcagactgc acagggcatg gattacttac acgccaagtc aatcatccac agagacctca
1380
agagtaataa tatttttctt catgaagacc tcacagtaaa aataggtgat tttggtctag
1440
ccacagtgaa atctcgatgg agtgggtccc atcagtttga acagttgtct ggatccattt
1500
tgtggatggc accagaagta atcagaatgc aagataaaaa cccatatagc tttcagtcag
1560
atgtatatgc atttgggatt gttctgtatg aattgatgac cggacagtta ccttattcaa
1620
atatcaacaa cagggaccag ataattttta tggtgggacg aggatatctg tctccagatc
1680
tcagtaaggt acggagtaac tgtccaaaag ccatgaagag attaatggca gagtgcctaa
1740
aaaagaaaag agatgaaaga ccactctttc cccaagtagg aaagactctc ctaagcaaga
1800
gacaaaattc agaagttatc agggaaaaag ataagcagat tctcgcctct attgagctgc
1860
tggcccgctc attgccaaaa attcaccgca gtgcatcaga accctccttg aatcgggctg
1920
gcttccaaac agaggatttt agtctatatg cttgtgcttc tccaaaaaca cccattcagg
1980
cagggggata tggagaattt gcagccttca agtagccaca ccatcatgac agcatctact
2040
cttatttctt aagtcttgtg ttcgtacaat ttgttaacat caaaacacag ttctgttcct
2100
caactctttt taaagttaaa atttttcagt gcataagctg gtgtggaaca gaaggaaatt
2160
tcccatccaa caaaagaggg aagaatgttt taggaaccag aattctctgc tgccagtgtt
2220
tcttcttcaa cacaaatatc acaagtctgc ccactcccag gaagaaagag gagagaccct
2280
gagttctgac cttttgatgg tcaggcatga tggaaagaaa ctgctgctac agcttgggag
2340
atttgctctg ggaagtctgc cagtcaactt tgcccttcta accaccagat caatatgtgg
2400
ctgatcatct gatggggcag ttgcaatcac caagccttgt tctctttcct gttctgggat
2460
tgtgttgtgg aacccttttc cctagccacc accagttcat ttctgaggga tggaacaaaa
2520
atgcagcatg cccttcctgt gtggtgcatg ttcagtcctt gacaaatttt taccaaaatg
2580
aagctacttt atttaaaagg agggtgagag gtgaggaggt cactttgggt gtggcggaaa
2640
gggaatgctg catctttttc ctgggctgct ggggctctgg ccttggcttg ccagccggaa
2700
gcgctggcac gcatcgcctt cttttcccat tgggtccagc aatgaagacg agtgtttggg
2760
gttttttttt tctccaccat gtagcaagtt ctcaggaaaa tacaattgat atcttcctcc
2820
taagctcttc caatcagtca ccaagtactt atgtggttac tttgtccagg gcacaaaatg
2880
cctgtatcta attaaaagcc tacaaaactg cttgataaca gttttgaatg tgagacattt
2940
atgtaattta aatgtaaggt acaagtttta atttctgagt ttcttctatt atatttttat
3000
taaaaaaaga aaataatttt cagattgaat tggagtaaaa taatattact tcccactaga
3060
attatatatc ctggaaaatt gtatttttgt tacataagca gcttttaaag aaagatcatt
3120
acccttttct ctacataaat atatggggag tcttagccta atgacaaata tttataattt
3180
ttaaattaat ggtacttgct ggatccatac taacatcttt actaatacct cattgtttct
3240
tccaacttac tcctacacta catcctacat cttcttccta gtcttttatc tagaatatgc
3300
aacctcaaat aaaaatggtg gtgtcctcat tcattctcct ccttcctttt ttcccaagcc
3360
tgatcttcaa aaggttggtt aatttggcag ctgagttcct ccccaggcag agaatagacc
3420
aattttaggt gtattgggac tgagggagga tgtgtaaaga ttaacatcag taaagaaccg
3480
ctgtggagta attaagaact ttgttcttta taactggaga atataaccta accctaacat
3540
ccctcagcct ttactaaagt gtggcgtaaa tcacagtagt agcaaagaaa gtgactctgg
3600
atgtgttcct ggccagtacc tcccttatca tgaatgtaga ctctctcatc aagatttagg
3660
aatataaatc aaatcaaatg tgcccagcca agctatgtag taagggactt gaacaatatt
3720
aggcagaacc tataaaataa atcagggaat tagaaattat ttaaagtttt caaattgtaa
3780
attgccccgg tgtctttcag cctactgcca ttatttttgc tacaatacct acatttcaga
3840
ggagggccta ctgaaaattc catgcaagtg gaaaataatc ctcaagttat taatgagttt
3900
gaaaagcaat gagttcttaa gtctttgtga gtagagcaag atcctacaaa attcagaaat
3960
agtaaaaatg gattcatgct gatttgaaga gcatctgtgt gcataatata atgctgcatc
4020
tcttttaaaa gcagtctatt tttcttttta aatttgtccc catagatgct tttgaacatg
4080
aacatgctta tgttaccttt tccgaggttg ggaagagcca ggagctctca ggcagggccc
4140
cctccctcag ctgggcagga gctgctcagg aggagctagt tatagaggaa gcttagcgtt
4200
ggcattttca aaattcaagg tgataacgct ttcttcttcc tttctgtttt agaatagatt
4260
gctgtctgat ttgaaaaagg gaaatagatt tgatctcaaa tgaatctgtg cccagaagcc
4320
aggctcaggg tattcagaga tttgtatagt gccctcaaaa aataacaaaa ttttagcttt
4380
ccttttttct tcttttctcc atcaaattct tttttctcta gtttacaaat gacatggaaa
4440
aggaatttcc cctgagtttt gtatgccttt ttttttttgg cttagactat agataggcgt
4500
gttgagctcc taagaaaata caaggaggaa ctctttgttg tgcagagcac tttatgagta
4560
gtttgtgtgg ataatatgtg actgcttccc tgacgagctt gtgaggctgt acttatgtct
4620
ttcctgtaag gcagcttcag tgccttctgt agtgtatata aggaaagatt acgccttctg
4680
aaaaatctca gagcaaccat aagattattt taaaatatgt agtatgactg atggactttt
4740
tcatcattaa attagtctag catctaaact tttaccactg aaataatatt gaccaaaaag
4800
caatttataa aaggtatttg tgaatagaaa atacaatgtg atcatttgta cttatgtgca
4860
ccttaaaaga ggaattctgt ctagctgtca aattctggtt ccttaacatc cagtccttga
4920
ttgtgattga gatctggtag gacgtgctgg ggcacgctag cagataaaat cccgtatact
4980
ttaggataga tgttacattt atgtcagtgt tggcaaagag cattgtgtag taataaagaa
5040
ttcaagactt cagcaatgtc aacctgaaac tttgtaaata tttcctagat tgttatttga
5100
tgcagtcaca gctctttatc acacaatgtt gtctttccct catcaggcaa ttttagaact
5160
gctgcacacc cctcctcaga tctcacctgc ccctcctgta cattcacctc tccagccttg
5220
tgcacacctc atttagcttt agtttgaaac acattgcagg gttcaggtga cctcttcaaa
5280
aactacctcc tcagaatgag gtaatgaata gttatttatt ttaaaatatg aaaagtcagg
5340
agctctagaa tatgaagatg atctaagatt ttaactttta tgtatacttg ttgagcactc
5400
tccttttgtc ctaaagggca ttatacattt aagcagtaat actgaaaaat gtagctcaga
5460
gtaactgaat gttgttgaaa gtggtgccag aatctgtttt aggggtacgt atcagaatct
5520
taatcttaaa tcggttacat gaaattaaat agttaatggt aacacttgac taacagatat
5580
aattttaatt ttcggtaggc ttttagcaag acagtaagta catcttcata atgagttagc
5640
cacagcttca tcacatgcac agattttcct gttgagagac tgcccagtta agagggtaga
5700
atgatgaacc atttttcagg attctcttct ttgtccaaac tggcattgtg agtgctagaa
5760
tatcagcact ttcaaactag tgattccaac tattaggcta ttaaaaagca aaacaaacca
5820
aacaaaccat agccagacat gggaagttta ctatgagtat aaacagcaaa tagcttacag
5880
gtcatacatt gaaatggtgt aggtaaggcg ttagaaaaat accttgacaa tttgccaaat
5940
gatcttactg tgccttcatg atgcaataaa aaaaaaaaaa atttagcata aatcagtgat
6000
ttgtgaagag agcagccacc ctggtctaac tcagctgtgt taatattttt tagcgtgcaa
6060
tttagactgc aaagataaat gcactaaaga gtttatagcc aaaatcacat ttaaaaaatg
6120
agagaaaaca caggtaaatt ttcagtgaac aaaattattt ttttaaagta cataatccct
6180
agtatagtca gatatattta tcacatagag caaataggtt gaaatcacaa ttcagtgaca
6240
tttctagaga aactttttct actcccatag gttcttcaaa gcatggaact tttatataac
6300
agaaatgtgt gacggtcatt ttaaattgct gtagtttggg gctgaagtac tgtgtgctgg
6360
gcagcaatca catgtattaa ctagtgagaa aggagaaatt aagatatagg acagaatttg
6420
attttcttgt tcccagatta ctgctgccaa cctagacact gagtttccag aggctgaaac
6480
gtaaacttgc agctcagcaa ctgttttgca aagttagtgg gactgtcctg cttatgctgt
6540
tcaaaaatgc tctgagggcc aggtggggcc tccaggggct cctctctgag gggacatcag
6600
actagctaac gacctggcgg gcggatgtga accggacaca ctccatggtg tgcttcttgt
6660
atcggtccct cgccaccctc aagaaaggct tcagcgggtt ctctagacgt ctccactaag
6720
gtgtgttact aacagccatg ggttgttgag cacccgagga gtgcaatagc atctctgcat
6780
gattgtatat tggcccgaag agaatgaagt ggccagtgta ctcatgttcc atgttgctag
6840
ctctggtaaa ctgaaaatac tggtaagatt tttgttttat cagtacacta gagagtaagc
6900
tttgttttgt tgtttttaga taatgttttc acttccattt ggaaagacat ttaaattgag
6960
tttcagtcct aaattttgcc agtcatggta attagcagtt tctatcaggt atttttaagg
7020
tagaagagga tagaaacata agttctaaaa gcttaaggta accgtggttt attttaaaat
7080
gtttaggggt ggttagtctc tacctcaaaa aaagtgagtg aatcttttat ttcagcattc
7140
acaagttcgg ctgttgtttt tgtaatacat ttttttttta accttttgac ccccctttac
7200
ctaagtgtca atgtagtttt attaattact aagtcagttt cattaaaatg tttatttagc
7260
agttttgact aattgcaatg attaatatag ccagttgtgc atgaggacac agccagtgag
7320
tatatctggg ttttttttgt gatgcttttt ttcttaagac ttctgtagat ttatgaagta
7380
ctcattgaaa acaactaaaa tacgtttatt cgtgttaata tggaaaaaaa aaaa
7434
<210> 40
<211> 603
<212> БЕЛОК
<213> Bos taurus
<400> 40
Met Met Arg Gly Leu Ile Pro Glu Cys Cys Ala Val Tyr Arg Ile Gln
1 5 10 15
Asp Gly Glu Lys Lys Pro Ile Gly Trp Asp Thr Asp Ile Ser Trp Leu
20 25 30
Thr Gly Glu Glu Leu His Val Glu Val Leu Glu Asn Val Pro Leu Thr
35 40 45
Thr His Asn Phe Val Arg Lys Thr Phe Phe Thr Leu Ala Phe Cys Asp
50 55 60
Phe Cys Arg Lys Leu Leu Phe Gln Gly Phe Arg Cys Gln Thr Cys Gly
65 70 75 80
Tyr Lys Phe His Gln Arg Cys Ser Thr Glu Val Pro Leu Met Cys Val
85 90 95
Asn Tyr Asp Gln Leu Asp Leu Leu Phe Val Ser Lys Phe Phe Glu His
100 105 110
His Pro Ile Pro Gln Glu Glu Ala Ser Leu Ala Glu Thr Thr Leu Pro
115 120 125
Cys Gly Ser Ser Pro Ser Ala Pro Pro Ser Asp Ser Ile Gly Pro Pro
130 135 140
Ile Leu Thr Ser Pro Ser Pro Ser Lys Ser Ile Pro Ile Pro Gln Pro
145 150 155 160
Phe Arg Pro Ala Asp Glu Asp His Arg Asn Gln Phe Gly Gln Arg Asp
165 170 175
Arg Ser Ser Ser Ala Pro Asn Val His Ile Asn Thr Ile Glu Pro Val
180 185 190
Asn Ile Asp Asp Leu Ile Arg Asp Gln Gly Phe Arg Ser Asp Gly Gly
195 200 205
Ser Thr Thr Gly Leu Ser Ala Thr Pro Pro Ala Ser Leu Pro Gly Ser
210 215 220
Leu Ser Asn Val Lys Ala Leu Gln Lys Ser Pro Gly Pro Gln Arg Glu
225 230 235 240
Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn Arg Met Lys Thr Leu
245 250 255
Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp Gly Gln Ile
260 265 270
Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr Val Tyr Lys
275 280 285
Gly Lys Trp His Gly Asp Val Ala Val Lys Met Leu Asn Val Thr Ala
290 295 300
Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val Gly Val Leu
305 310 315 320
Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe Met Gly Tyr Ser Thr
325 330 335
Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly Ser Ser Leu
340 345 350
Tyr His His Leu His Ile Ile Glu Thr Lys Phe Glu Met Ile Lys Leu
355 360 365
Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr Leu His Ala
370 375 380
Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile Phe Leu His
385 390 395 400
Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala Thr Val Lys
405 410 415
Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser Gly Ser Ile
420 425 430
Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys Asn Pro Tyr
435 440 445
Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu Tyr Glu Leu
450 455 460
Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg Asp Gln Ile
465 470 475 480
Ile Phe Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu Ser Lys Val
485 490 495
Arg Ser Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala Glu Cys Leu
500 505 510
Lys Lys Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Val Gly Lys Thr
515 520 525
Leu Leu Ser Lys Arg Gln Asn Ser Glu Val Ile Arg Glu Lys Asp Lys
530 535 540
Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro Lys Ile
545 550 555 560
His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe Gln Thr
565 570 575
Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro Ile Gln
580 585 590
Ala Gly Gly Tyr Gly Glu Phe Ala Ala Phe Lys
595 600
<210> 41
<211> 2295
<212> ДНК
<213> Equus caballus
<220>
<221> дополнительный признак
<222> (79)..(79)
<223> n представляет собой a, c, g или t
<400> 41
atgaagacgc tgagcggcgg cggcggcggc gcggagcagg gccaggctct gttcaacggg
60
gacatggaac ccggaggcnc cgcgccggcg cccgcggcct cgtcggccgc ggaccctgcc
120
attcccgagg aggtatggaa tatcaaacaa atgattaaat tgacacagga acatatagag
180
gccctattgg acaaatttgg tggggagcat aatccaccat caatatatct ggaggcctat
240
gaagaataca ccagcaagct agatgccctc caacaaagag aacaacagtt attggaatcc
300
ctggggaatg gaactgattt ttctgtttct agttctgcat caacggacac cgttacatct
360
tcttcctctt ctagcctttc agtgctacct tcatctcttt cagtttttca aaatcccaca
420
gatgtgtcac ggagcaaccc taagtcacca caaaaaccta tcgttagagt cttcctgccc
480
aacaaacaga ggacagtggt acctgcaagg tgtggcgtta cagtccggga cagtctaaag
540
aaagcactga tgatgagagg tctaatccca gagtgctgtg ctgtttacag aattcaggat
600
ggagagaaga aaccaattgg ctgggacact gatatttcct ggctcactgg agaggaattg
660
catgtagaag tgttggagaa tgttccactt acaacacaca actttgtacg gaaaactttt
720
ttcaccttag cattttgtga cttttgtcga aagctgcttt tccagggttt ccgctgtcaa
780
acatgtggtt ataaatttca ccagcgttgt agtacagagg ttccactgat gtgtgttaat
840
tatgaccaac ttgatttgct gtttgtctcc aagttctttg aacaccaccc agtatcacag
900
gaggaggcct ccttagcaga gactgccctt acatctggat catccccttc tgcacccccc
960
tccgattcca ttgggcccca aattctcacc agtccatctc cttcaaaatc cattccaatt
1020
ccacagcctt tccgaccagc agatgaagat catcgaaatc agtttggaca acgagaccgg
1080
tcctcatcag ctccaaatgt acatataaac acaatagaac ctgtcaatat tgatgacttg
1140
attagagacc aagggtttcg tagtgatgga ggatcaacca caggtttatc tgccaccccc
1200
cctgcctcat tacctggctc actcactaat gtgaaggcat tacagaaatc tccaggacct
1260
caacgggaaa ggaaatcatc ttcatcctca gaagacagga atcgaatgaa aactcttggt
1320
agacgggatt caagtgacga ttgggagatt cctgatgggc agatcacagt gggacaaaga
1380
attggatctg ggtcatttgg gacagtctac aagggaaagt ggcatggtga tgtggcagtg
1440
aaaatgttga atgtgacagc acccacacct cagcagttac aggccttcaa aaatgaagta
1500
ggagtactca ggaaaactcg acatgtgaat atcctactct tcatgggcta ttcaacaaag
1560
ccacaactgg ctattgttac ccagtggtgt gagggctcca gcttatatca ccatctccac
1620
atcattgaga ccaaatttga gatgatcaaa cttatagata ttgctcggca aactgcacag
1680
ggcatggatt acttacacgc caagtcaatc atccacagag acctcaagag taataatatt
1740
tttcttcatg aagacctcac agtaaaaata ggtgattttg gtctagccac agtgaaatct
1800
cgatggagtg ggtcccatca gtttgaacag ttgtctggat ccattttgtg gatggcacca
1860
gaagtaatca gaatgcaaga taaaaacccg tatagctttc aatcagatgt atatgccttt
1920
gggattgttc tgtatgaatt gatgactgga cagttacctt attcaaacat caacaacagg
1980
gaccagataa tttttatggt gggaagagga tatctatctc cagatctcag taaggtacgg
2040
agtaactgtc caaaagccat gaagagatta atggcagagt gcctaaaaaa gaaaagagac
2100
gagagaccac tcttccccca aattctcgcc tctattgagc tgctggcccg ctcattgcca
2160
aaaattcacc gcagtgcatc agagccctcc ttgaatcggg ctggcttcca gacagaggat
2220
tttagtctat atgcttgtgc ttctccgaaa acacccatcc aggcaggggg atatggtgcg
2280
tttcctgtcc actga
2295
<210> 42
<211> 764
<212> БЕЛОК
<213> Equus caballus
<220>
<221> дополнительный признак
<222> (27)..(27)
<223> Xaa может представлять собой любую встречающуюся в природе
аминокислоту
<400> 42
Met Lys Thr Leu Ser Gly Gly Gly Gly Gly Ala Glu Gln Gly Gln Ala
1 5 10 15
Leu Phe Asn Gly Asp Met Glu Pro Gly Gly Xaa Ala Pro Ala Pro Ala
20 25 30
Ala Ser Ser Ala Ala Asp Pro Ala Ile Pro Glu Glu Val Trp Asn Ile
35 40 45
Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu Leu Asp
50 55 60
Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu Ala Tyr
65 70 75 80
Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu Gln Gln
85 90 95
Leu Leu Glu Ser Leu Gly Asn Gly Thr Asp Phe Ser Val Ser Ser Ser
100 105 110
Ala Ser Thr Asp Thr Val Thr Ser Ser Ser Ser Ser Ser Leu Ser Val
115 120 125
Leu Pro Ser Ser Leu Ser Val Phe Gln Asn Pro Thr Asp Val Ser Arg
130 135 140
Ser Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe Leu Pro
145 150 155 160
Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr Val Arg
165 170 175
Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro Glu Cys
180 185 190
Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile Gly Trp
195 200 205
Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val Glu Val
210 215 220
Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys Thr Phe
225 230 235 240
Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe Gln Gly
245 250 255
Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys Ser Thr
260 265 270
Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu Leu Phe
275 280 285
Val Ser Lys Phe Phe Glu His His Pro Val Ser Gln Glu Glu Ala Ser
290 295 300
Leu Ala Glu Thr Ala Leu Thr Ser Gly Ser Ser Pro Ser Ala Pro Pro
305 310 315 320
Ser Asp Ser Ile Gly Pro Gln Ile Leu Thr Ser Pro Ser Pro Ser Lys
325 330 335
Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp His Arg
340 345 350
Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn Val His
355 360 365
Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg Asp Gln
370 375 380
Gly Phe Arg Ser Asp Gly Gly Ser Thr Thr Gly Leu Ser Ala Thr Pro
385 390 395 400
Pro Ala Ser Leu Pro Gly Ser Leu Thr Asn Val Lys Ala Leu Gln Lys
405 410 415
Ser Pro Gly Pro Gln Arg Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp
420 425 430
Arg Asn Arg Met Lys Thr Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp
435 440 445
Glu Ile Pro Asp Gly Gln Ile Thr Val Gly Gln Arg Ile Gly Ser Gly
450 455 460
Ser Phe Gly Thr Val Tyr Lys Gly Lys Trp His Gly Asp Val Ala Val
465 470 475 480
Lys Met Leu Asn Val Thr Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe
485 490 495
Lys Asn Glu Val Gly Val Leu Arg Lys Thr Arg His Val Asn Ile Leu
500 505 510
Leu Phe Met Gly Tyr Ser Thr Lys Pro Gln Leu Ala Ile Val Thr Gln
515 520 525
Trp Cys Glu Gly Ser Ser Leu Tyr His His Leu His Ile Ile Glu Thr
530 535 540
Lys Phe Glu Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln
545 550 555 560
Gly Met Asp Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu Lys
565 570 575
Ser Asn Asn Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly Asp
580 585 590
Phe Gly Leu Ala Thr Val Lys Ser Arg Trp Ser Gly Ser His Gln Phe
595 600 605
Glu Gln Leu Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile Arg
610 615 620
Met Gln Asp Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe
625 630 635 640
Gly Ile Val Leu Tyr Glu Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn
645 650 655
Ile Asn Asn Arg Asp Gln Ile Ile Phe Met Val Gly Arg Gly Tyr Leu
660 665 670
Ser Pro Asp Leu Ser Lys Val Arg Ser Asn Cys Pro Lys Ala Met Lys
675 680 685
Arg Leu Met Ala Glu Cys Leu Lys Lys Lys Arg Asp Glu Arg Pro Leu
690 695 700
Phe Pro Gln Ile Leu Ala Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro
705 710 715 720
Lys Ile His Arg Ser Ala Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe
725 730 735
Gln Thr Glu Asp Phe Ser Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro
740 745 750
Ile Gln Ala Gly Gly Tyr Gly Ala Phe Pro Val His
755 760
<210> 43
<211> 2678
<212> ДНК
<213> Gallus gallus
<400> 43
tccccctccc tcgccccagc gcttcgatcc aagatggcgg cgctgagcag cggcagcagc
60
gccgaggggg cctcgctctt caacggggac atggagcccg agccgccgcc gcccgtgctg
120
ggcgcctgct acgccgggag cggcggcggc gacccggcca tcccggagga ggtgtggaat
180
atcaaacaga tgattaaatt aacacaagaa catatagaag cgctgttaga caagtttgga
240
ggagagcata acccaccatc aatatattta gaggcctatg aggagtacac cagcaaacta
300
gatgctctac agcagagaga acagcagtta ttggaatcca tgggaaatgg aactgatttc
360
tctgtttcca gttcagcttc aacggacaca gttgcatcat cttcctcctc tagcctctct
420
gtagcacctt catccctttc agtttatcaa aatcctactg atatgtcgcg gaataaccct
480
aagtctccac agaagcctat tgttagagtc ttcctgccca acaagcaaag gactgtggtt
540
ccggcaagat gtggggtgac agtccgagac agcctgaaga aagctctgat gatgagaggt
600
cttattccag aatgctgtgc tgtttacaga atacaggatg gagagaagaa gccaattggc
660
tgggacactg acatttcctg gctaaccgga gaggagttac acgtggaggt cttggagaat
720
gtgccactca caacacacaa ttttgtacga aaaacattct tcacgttagc gttctgcgac
780
ttctgtcgaa agctgctttt ccagggattc cgatgccaga catgtggcta caaatttcac
840
cagcgctgta gcacagaagt gccactgatg tgtgttaact acgaccaact cgatttgctg
900
tttgtctcca agttctttga acatcacccc atatcgcagg aggagaccac cttaggagag
960
accaccccgg catcgggatc gtacccctca gtgcccccat cagattctgt tggaccacca
1020
attctcccta gtccttctcc ttcaaaatcc attccaatcc cacagccctt ccgaccagca
1080
gatgaagacc atcggaatca gtttgggcaa cgcgaccgat cctcttcagc tcccaatgtt
1140
cacatcaata caattgagcc agtcaatatt gatgacttga ttagagacca gggtgtacga
1200
ggagagggag cccctttgaa ccagctgatg cgctgtcttc ggaaatacca atcccggact
1260
cccagtcccc tccttcattc tgtccccagt gaaatagtgt ttgattttga gcctggccca
1320
gtgttcagag gttcaactgc aggtttgtct gcaacacctc ctgcatcttt gcctgggtca
1380
cttaccaatg tgaaagcatt acagaaatca ccaggccccc aacgggaaag gaaatcatcc
1440
tcatcctcag aagacagaaa taggatgaaa acccttggtc gacgagattc aagtgatgat
1500
tgggaaatac cagatgggca gatcacagtt ggacaaagga taggatctgg atcatttgga
1560
acagtctaca aaggaaagtg gcatggtgac gtggcagtga aaatgttgaa tgttacagca
1620
cccacacctc aacagttaca ggctttcaaa aatgaagtag gagtgctcag gaaaacacgg
1680
catgtgaata tcctactttt tatgggttat tcaacaaaac ctcagttggc tattgttaca
1740
cagtggtgtg aggggtccag cttatatcac catctgcaca taattgagac caagtttgaa
1800
atgatcaaac taattgatat tgcacgacag actgcacaag gcatggatta tttgcatgcc
1860
aagtcaatca tccacagaga cctcaagagt aataatattt ttcttcatga agacctcaca
1920
gtaaaaatag gtgacttcgg tctggctaca gtgaaatcac gatggagtgg atctcatcaa
1980
tttgaacagt tatctggatc aattctatgg atggcaccgg aagtgatcag gatgcaagac
2040
aaaaacccat atagctttca gtcagatgtg tatgcattcg ggattgtgct ttatgaactg
2100
atgactggac agttaccata ctcaaacatc aacaacaggg accagataat ttttatggtg
2160
ggacgaggat atctatctcc agacctcagt aaagtaagaa gtaactgtcc aaaagctatg
2220
aagagactaa tggcagaatg cttgaaaaag aaaagagatg agagacctct ttttccacag
2280
attcttgcct ccattgagct tctggcccgg tcgttgccaa aaattcaccg cagtgcatct
2340
gagccgtcac taaaccgggc tggcttccag accgaggatt tcagtctgta tgcttgtgct
2400
tctccaaaaa cgcccatcca agcaggggga tacggtgggt ttccagtaca ctgaaaagaa
2460
atgtgaaagc gtgtgcctgt ttgctcatgt gctggtgtgt tcctgtgtgt gcaacgcata
2520
cgtacgttct cagttcctac cagcgacttt ttaaggttta ctgagggaat gaagactcat
2580
ttcctaacat ggggcattga acgtcctgag cacaagtcag tgctggtaag gaatgtcttg
2640
ggaacagctg gcaagaagaa ttagaaggta cttaaagg
2678
<210> 44
<211> 806
<212> БЕЛОК
<213> Gallus gallus
<400> 44
Met Ala Ala Leu Ser Ser Gly Ser Ser Ala Glu Gly Ala Ser Leu Phe
1 5 10 15
Asn Gly Asp Met Glu Pro Glu Pro Pro Pro Pro Val Leu Gly Ala Cys
20 25 30
Tyr Ala Gly Ser Gly Gly Gly Asp Pro Ala Ile Pro Glu Glu Val Trp
35 40 45
Asn Ile Lys Gln Met Ile Lys Leu Thr Gln Glu His Ile Glu Ala Leu
50 55 60
Leu Asp Lys Phe Gly Gly Glu His Asn Pro Pro Ser Ile Tyr Leu Glu
65 70 75 80
Ala Tyr Glu Glu Tyr Thr Ser Lys Leu Asp Ala Leu Gln Gln Arg Glu
85 90 95
Gln Gln Leu Leu Glu Ser Met Gly Asn Gly Thr Asp Phe Ser Val Ser
100 105 110
Ser Ser Ala Ser Thr Asp Thr Val Ala Ser Ser Ser Ser Ser Ser Leu
115 120 125
Ser Val Ala Pro Ser Ser Leu Ser Val Tyr Gln Asn Pro Thr Asp Met
130 135 140
Ser Arg Asn Asn Pro Lys Ser Pro Gln Lys Pro Ile Val Arg Val Phe
145 150 155 160
Leu Pro Asn Lys Gln Arg Thr Val Val Pro Ala Arg Cys Gly Val Thr
165 170 175
Val Arg Asp Ser Leu Lys Lys Ala Leu Met Met Arg Gly Leu Ile Pro
180 185 190
Glu Cys Cys Ala Val Tyr Arg Ile Gln Asp Gly Glu Lys Lys Pro Ile
195 200 205
Gly Trp Asp Thr Asp Ile Ser Trp Leu Thr Gly Glu Glu Leu His Val
210 215 220
Glu Val Leu Glu Asn Val Pro Leu Thr Thr His Asn Phe Val Arg Lys
225 230 235 240
Thr Phe Phe Thr Leu Ala Phe Cys Asp Phe Cys Arg Lys Leu Leu Phe
245 250 255
Gln Gly Phe Arg Cys Gln Thr Cys Gly Tyr Lys Phe His Gln Arg Cys
260 265 270
Ser Thr Glu Val Pro Leu Met Cys Val Asn Tyr Asp Gln Leu Asp Leu
275 280 285
Leu Phe Val Ser Lys Phe Phe Glu His His Pro Ile Ser Gln Glu Glu
290 295 300
Thr Thr Leu Gly Glu Thr Thr Pro Ala Ser Gly Ser Tyr Pro Ser Val
305 310 315 320
Pro Pro Ser Asp Ser Val Gly Pro Pro Ile Leu Pro Ser Pro Ser Pro
325 330 335
Ser Lys Ser Ile Pro Ile Pro Gln Pro Phe Arg Pro Ala Asp Glu Asp
340 345 350
His Arg Asn Gln Phe Gly Gln Arg Asp Arg Ser Ser Ser Ala Pro Asn
355 360 365
Val His Ile Asn Thr Ile Glu Pro Val Asn Ile Asp Asp Leu Ile Arg
370 375 380
Asp Gln Gly Val Arg Gly Glu Gly Ala Pro Leu Asn Gln Leu Met Arg
385 390 395 400
Cys Leu Arg Lys Tyr Gln Ser Arg Thr Pro Ser Pro Leu Leu His Ser
405 410 415
Val Pro Ser Glu Ile Val Phe Asp Phe Glu Pro Gly Pro Val Phe Arg
420 425 430
Gly Ser Thr Ala Gly Leu Ser Ala Thr Pro Pro Ala Ser Leu Pro Gly
435 440 445
Ser Leu Thr Asn Val Lys Ala Leu Gln Lys Ser Pro Gly Pro Gln Arg
450 455 460
Glu Arg Lys Ser Ser Ser Ser Ser Glu Asp Arg Asn Arg Met Lys Thr
465 470 475 480
Leu Gly Arg Arg Asp Ser Ser Asp Asp Trp Glu Ile Pro Asp Gly Gln
485 490 495
Ile Thr Val Gly Gln Arg Ile Gly Ser Gly Ser Phe Gly Thr Val Tyr
500 505 510
Lys Gly Lys Trp His Gly Asp Val Ala Val Lys Met Leu Asn Val Thr
515 520 525
Ala Pro Thr Pro Gln Gln Leu Gln Ala Phe Lys Asn Glu Val Gly Val
530 535 540
Leu Arg Lys Thr Arg His Val Asn Ile Leu Leu Phe Met Gly Tyr Ser
545 550 555 560
Thr Lys Pro Gln Leu Ala Ile Val Thr Gln Trp Cys Glu Gly Ser Ser
565 570 575
Leu Tyr His His Leu His Ile Ile Glu Thr Lys Phe Glu Met Ile Lys
580 585 590
Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met Asp Tyr Leu His
595 600 605
Ala Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn Asn Ile Phe Leu
610 615 620
His Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala Thr Val
625 630 635 640
Lys Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser Gly Ser
645 650 655
Ile Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln Asp Lys Asn Pro
660 665 670
Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile Val Leu Tyr Glu
675 680 685
Leu Met Thr Gly Gln Leu Pro Tyr Ser Asn Ile Asn Asn Arg Asp Gln
690 695 700
Ile Ile Phe Met Val Gly Arg Gly Tyr Leu Ser Pro Asp Leu Ser Lys
705 710 715 720
Val Arg Ser Asn Cys Pro Lys Ala Met Lys Arg Leu Met Ala Glu Cys
725 730 735
Leu Lys Lys Lys Arg Asp Glu Arg Pro Leu Phe Pro Gln Ile Leu Ala
740 745 750
Ser Ile Glu Leu Leu Ala Arg Ser Leu Pro Lys Ile His Arg Ser Ala
755 760 765
Ser Glu Pro Ser Leu Asn Arg Ala Gly Phe Gln Thr Glu Asp Phe Ser
770 775 780
Leu Tyr Ala Cys Ala Ser Pro Lys Thr Pro Ile Gln Ala Gly Gly Tyr
785 790 795 800
Gly Gly Phe Pro Val His
805
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ С ПРИМЕНЕНИЕМ КОМБИНАЦИЙ ИНГИБИТОРОВ ERK И RAF | 2014 |
|
RU2722784C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИФУНКЦИОНАЛЬНЫХ БЕЛКОВ И ИХ ПРОИЗВОДНЫХ | 2018 |
|
RU2795970C2 |
| АНТИ-PD-1 АНТИТЕЛА | 2019 |
|
RU2788095C2 |
| ВАРИАНТЫ FC-ОБЛАСТИ С МОДИФИЦИРОВАННОЙ СПОСОБНОСТЬЮ СВЯЗЫВАТЬСЯ С FCRN И С СОХРАНЕННОЙ СПОСОБНОСТЬЮ СВЯЗЫВАТЬСЯ С БЕЛКОМ А | 2015 |
|
RU2727639C2 |
| ВАРИАНТЫ FC-ОБЛАСТИ С МОДИФИЦИРОВАННЫМИ СПОСОБНОСТЯМИ СВЯЗЫВАТЬСЯ С FCRN | 2015 |
|
RU2730592C2 |
| МУЛЬТИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ БЕЛКИ С МУТАНТНЫМИ ДОМЕНАМИ FAB | 2019 |
|
RU2827657C2 |
| СПОСОБ ПРОДУЦИРОВАНИЯ АРЕНАВИРУСА, А ТАКЖЕ МУТАНТОВ АРЕНАВИРУСА С ПРОТИВООПУХОЛЕВЫМИ СВОЙСТВАМИ | 2019 |
|
RU2812046C2 |
| МУТАНТНЫЙ ПОЛИПЕПТИД ГИДРОКСИФЕНИЛПИРУВАТДИОКСИГЕНАЗА, КОДИРУЮЩИЙ ЕГО ГЕН И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2822892C1 |
| Новые варианты интерлейкина-2 для лечения рака | 2020 |
|
RU2833537C2 |
| PD1/CTLA4-СВЯЗЫВАЮЩИЕ ВЕЩЕСТВА | 2016 |
|
RU2755724C2 |
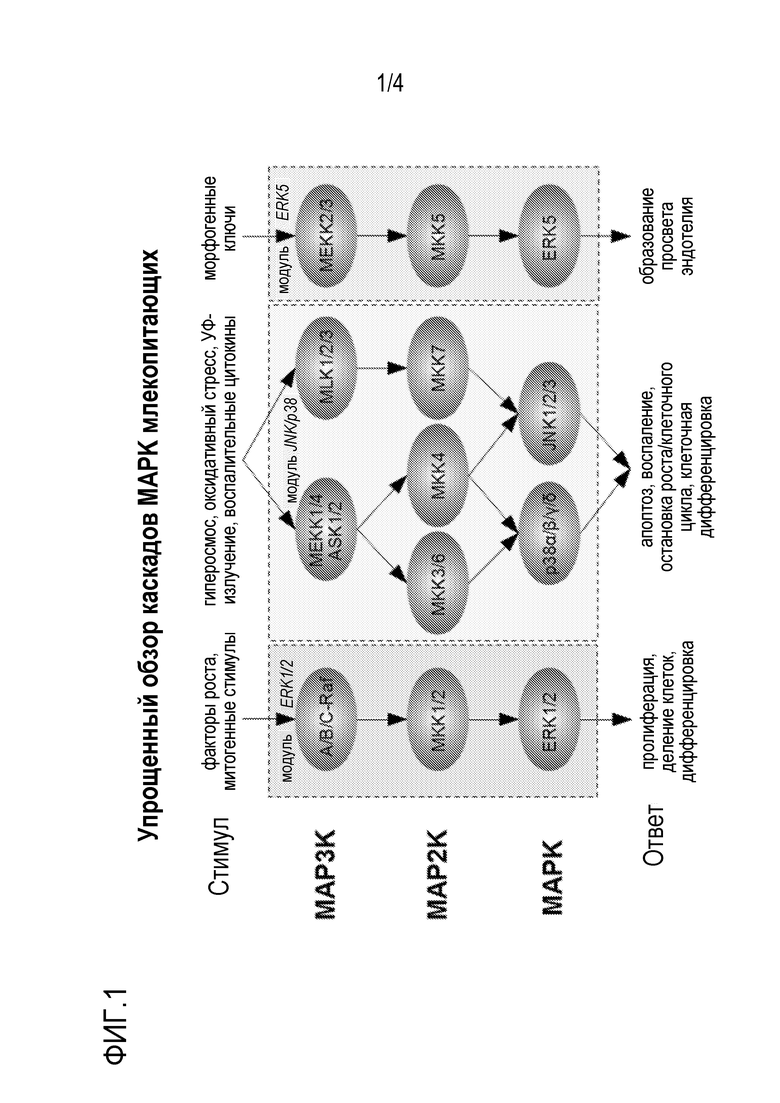
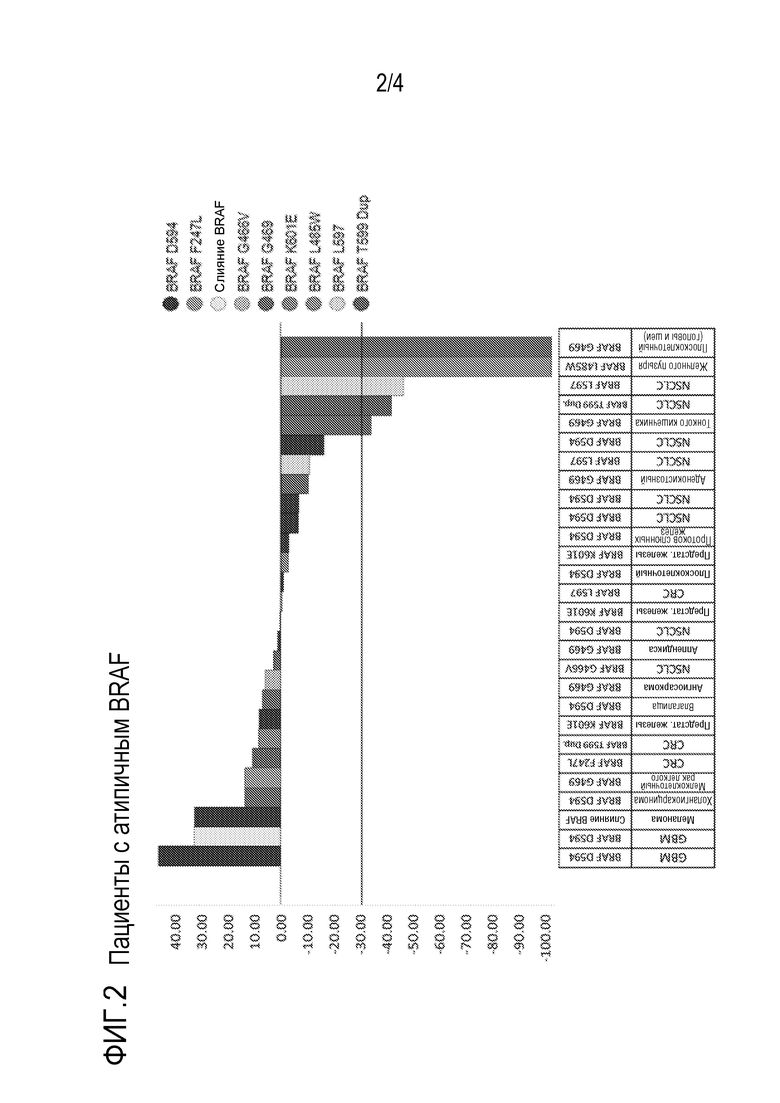
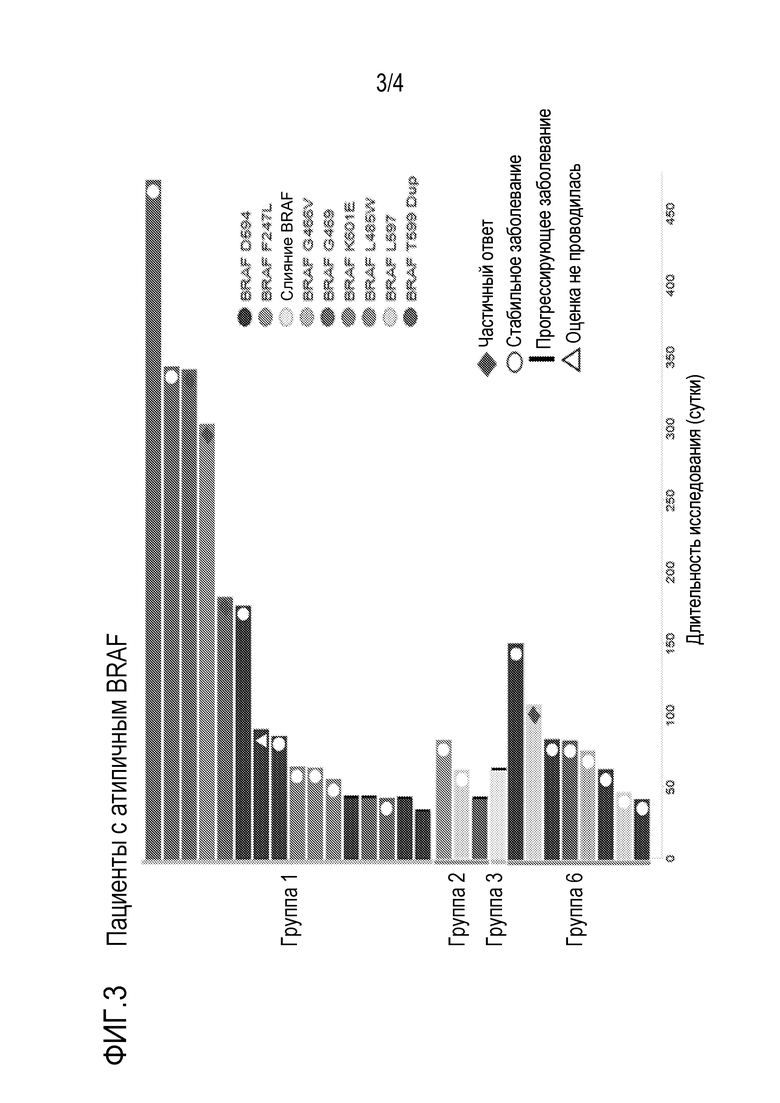
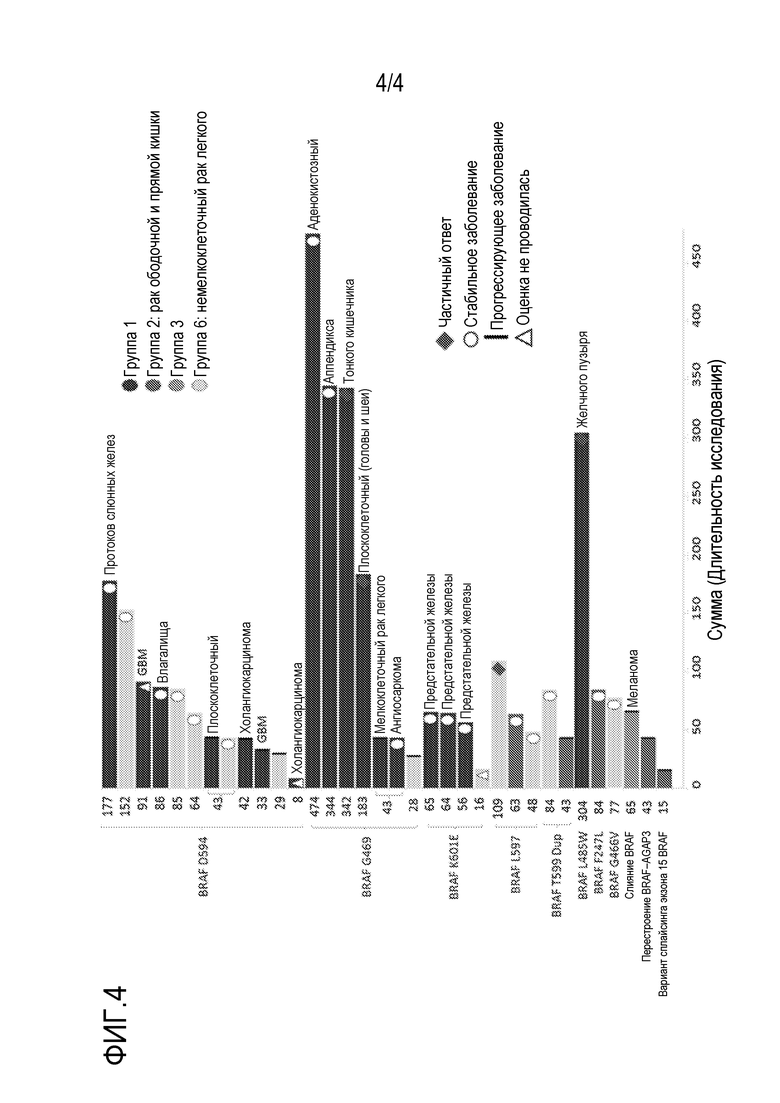
Настоящее изобретение относится к биотехнологии, в частности к способам, фармацевтическим композициям и наборам для лечения или смягчения эффектов злокачественной опухоли у индивидуума, которая имеет атипичную мутацию BRAF (т.е. мутацию BRAF не V600E/K), включающим ингибитор ERK. Также предусматриваются способы идентификации индивидуума, имеющего злокачественную опухоль с атипичной мутацией BRAF, для которого была бы полезной терапия, включающая ингибитор ERK. 5 н. и 63 з.п. ф-лы, 4 ил., 3 табл., 1 пр.
1. Способ лечения или смягчения эффектов злокачественной опухоли у индивидуума, имеющей мутацию BRAF не V600E/K, причем способ включает введение индивидууму эффективного количества ингибитора ERK или его фармацевтически приемлемой соли.
2. Способ по п.1, где ингибитор ERK выбран из группы, состоящей из BVD–523, SCH–722984 (Merck & Co.), SCH–772984 (Merck & Co.), SCH–900353 (MK–8353) (Merck & Co.), LY3214996 (Lilly), AEZS–140 (Aeterna Zentaris), AEZS–131 (Aeterna Zentaris), AEZS–136 (Aeterna Zentaris), LTT–462 (Novartis), RG–7842 (Genentech), CC–90003 (Celgene), KIN–4050 (Kinentia) и их комбинаций.
3. Способ по п.1, где ингибитор ERK представляет собой BVD–523.
4. Способ по п.1, где мутация BRAF не V600E/K представляет собой активирующую киназу мутацию, нарушающую функцию киназы мутацию или мутацию с неизвестным действием на киназу и их комбинации.
5. Способ по п.4, где активирующая киназу мутация выбрана из группы, состоящей из R462I, I463S, G464E, G464R, G464V, G466A, G469A, N581S, E586K, F595L, L597Q, L597R, L597S, L597V, A598V, T599E, V600R, K601E, S602D, A728V и их комбинаций.
6. Способ по п.4, где нарушающая функцию киназы мутация выбрана из группы, состоящей из G466E, G466R, G466V, Y472C, K483M, D594A, D594E, D594G, D594H, D594N, D594V, G596R, T599A, S602A и их комбинаций.
7. Способ по п.4, где мутация с неизвестным действием на киназу выбрана из группы, состоящей из T440I, S467L, G469E, G469R, G469S, G469V, L584F, L588F, V600_K601delinsE, S605I, Q609L, E611Q и их комбинаций.
8. Способ по п.1, где мутация BRAF не V600E/K выбрана из группы, состоящей из D594, G469, K601E, L597, дупликации T599, L485W, F247L, G466V, слияния BRAF, перестроения BRAF–AGAP3, варианта сплайсинга экзона 15 BRAF и их комбинаций.
9. Способ по п.1, где индивидуумом является млекопитающее.
10. Способ по п.9, где млекопитающее выбрано из группы, состоящей из человека, приматов, сельскохозяйственных животных и домашних животных.
11. Способ по п.9, где млекопитающее представляет собой человека.
12. Способ по п.1, где злокачественная опухоль представляет собой солидную злокачественную или гематологическую злокачественную опухоль.
13. Способ по п.1, злокачественная опухоль выбрана из группы, состоящей из глиобластомы, меланомы, холангиокарциномы, мелкоклеточного рака легкого, рака ободочной и прямой кишки, рака предстательной железы, рака влагалища, ангиосаркомы, немелкоклеточного рака легкого, рака аппендикса, плоскоклеточного рака, карциномы протоков слюнной железы, аденокистозной карциномы, рака тонкого кишечника и рака желчного пузыря.
14. Способ по п.13, где злокачественная опухоль выбрана из группы, состоящей из рака тонкого кишечника, немелкоклеточного рака легкого, рака желчного пузыря и плоскоклеточного рака.
15. Способ по п.1, дополнительно включающий введение индивидууму по меньшей мере одного дополнительного лекарственного средства, выбранного из группы, состоящей из ингибитора MEK, ингибитора HDAC и их комбинаций.
16. Способ по п.15, где ингибитор MEK выбран из группы, состоящей из токсина сибирской язвы, антрохинолола (Golden Biotechnology), ARRY–142886 ((2–гидроксиэтокси)амид 6–(4–бром–2–хлор–фениламино)–7–фтор–3–метил–3H–бензоимидазол–5–карбоновой кислоты) (Array BioPharma), ARRY–438162 (Array BioPharma) биниметиниба (MEK162, ARRY–1662), AS–1940477 (Astellas), AS–703988 (Merck KGaA), бентамапимода (Merck KGaA), BI–847325 (Boehringer Ingelheim), E–6201 (Eisai), GDC–0623 (Hoffmann–La Roche), GDC–0973 (кобиметиниб) (Hoffmann–La Roche), L783277 (Merck), части токсина сибирской язвы, являющейся летальным фактором, MEK162 (Array BioPharma), PD 098059 (2–(2'–амино–3'–метоксфенил)оксанафталин–4–он) (Pfizer), PD 184352 (CI–1040) (Pfizer), PD–0325901 (Pfizer), PD318088 (Pfizer), PD334581 (Pfizer), 6–метокси–7–(3–морфолин–4–илпропокси)–4–(4–феноксифениламино)хинолин–3–карбонитрила, 4–[3–хлор–4–(1–метил–1H–имидазол–2–илсульфанил)фениламино]–6–метокси–7–(3–морфолин–4–илпропокси)хинолин–3–карбонитрила, пимасертиба (Santhera Pharmaceuticals), RDEA119 (Ardea Biosciences/Bayer), рефаметиниба (AstraZeneca), RG422 (Chugai Pharmaceutical Co.), R0092210 (Roche), R04987655 (Hoffmann–La Roche), R05126766 (Hoffmann–La Roche), селуметиниба (AZD6244) (AstraZeneca), SL327 (Sigma), TAK–733 (Takeda), траметиниба (Japan Tobacco), U0126 (1,4–диамино–2,3–дициано–1,4–бис(2–аминофенилтио)бутадиена) (Sigma), WX–554 (Wilex), полипептида YopJ (Mittal et al., 2010), их фармацевтически приемлемых солей и их комбинаций.
17. Способ по п.15, где ингибитор HDAC выбран из группы, состоящей из Абексиностата (PCI–24781), Гивиностата, Энтиностата, Вориностата, CI–994, CUDC–101, Энтиностата, BML–210, M344, NVP–LAQ824, Панобиностата, Прациносата (SB939), Моцетиностата, Ресминостата, Ромидепсина, Белиностата, их фармацевтически приемлемых солей и их комбинаций.
18. Способ по п.1, дополнительно включающий введение индивидууму по меньшей мере одного дополнительного лекарственного средства, выбранного из группы, состоящей из антитела, фрагмента антитела, конъюгата антитела, цитотоксического средства, токсина, радионуклида, иммуномодулятора, фотоактивного лекарственного средства, радиосенсибилизирующего средства, гормона, антиангиогенного средства и их комбинаций.
19. Способ по п.18, где антитело, его фрагмент или их конъюгат выбраны из группы, состоящей из ритуксимаба (Ритуксан), Брентуксимаба Ведотина (Адцетриз), Адотрастузумаба эмтансина (Кадсила), Цетуксимаба (Эрбитукс), бевацизумаба (Авастин), Ибритумомаба (Зевалин), ведолизумаба (Энтивио), Ипилимумаба (Ервой), Ниволумаба (Опдиво), пембролизумаба (Кейтруда), Алемтузумаба атезолизумаба (Тецентрик), авелумаба (Бавенцио), дурвалумаба (Имфинзи), B–701, Офатумумаба, Обинутузумаба (Газива), Панитумумаба, плозализумаба, BI–754091, OREG–103, COM–701, BI–754111 и их комбинаций.
20. Способ по п.18, где цитотоксическое средство выбрано из группы, состоящей из циклофосфамида, мехлорэтамина, урамустина, мелфалана, хлорамбуцила, ифосфамида, кармустина, ломустина, стрептозоцина, бусульфана, темозоломида, цисплатина, карбоплатина, оксалиплатина, недаплатина, сатраплатина, триплатина тетранитрата, доксорубицина, даунорубицина, идарубицина, митоксантрона, метотрексата, пеметрекседа, 6–меркаптопурина, дакарбазина, флударабина, 5–фторурацила, арабинозилцитозина, капецитабина, гемцитабина, децитабина, алкалоидов барвинка, паклитаксела (Таксол), доцетаксела (Таксотер), иксабепилона (Икземпра), актиномицина, антрациклинов, валрубицина, эпирубицина, блеомицина, пликамицина, митомицина, их фармацевтически приемлемых солей, их пролекарств и комбинаций.
21. Способ по п.18, где токсин представляет собой дифтерийный токсин или его части.
22. Способ по п.18, где радионуклид выбран из группы, состоящей из I–125, At–211, Lu–177, Cu–67, I–131, Sm–153, Re–186, P–32, Re–188, In–114m, Y–90 и их комбинаций.
23. Способ по п.18, где иммуномодулятор выбран из группы, состоящей из гранулоцитарного колониестимулирующего фактора (G–CSF), LAG–3, IMP–321, JCAR–014, ASLAN–002 (BMS–777607), интерферонов, имиквимода и клеточных мембранных фракций из бактерий, IL–2, IL–7, IL–12, CCL3, CCL26, CXCL7, синтетического цитозинфосфат–гуанозина (CpG), ингибиторов иммунной точки контроля и их комбинаций.
24. Способ по п.18, где радиосенсибилизирующее средство выбрано из группы, состоящей из мизонидазола, метронидазола, тирапазамина, транс–кроцетината натрия и их комбинаций.
25. Способ по п.18, где гормон выбран из группы, состоящей из простагландинов, лейкотриенов, простациклина, тромбоксана, амилина, антимюллерова гормона, адипонектина, адренокортикотропного гормона, ангиотензиногена, ангиотензина, вазопрессина, атриопептина, натрийуретического пептида головного мозга, кальцитонина, холицистокинина, кортикотропин–рилизинг гормона, энцефалина, эндотелина, эритропоэтина, фоликулостимулирующего гормона, галанина, гастрина, грелина, глюкагона, гонадотропин–рилизинг гормона, рилизинг–фактора гормона роста, хорионического гонадотропина человека, лактогена плаценты человека, гормона роста, ингибина, инсулина, соматомедина, лептина, липотропина, лютеинизирующего гормона, меланоцит–стимулирующего гормона, мотилина, орексина, окситоцина, панкреатического полипептида, паратиреоидного гормона, пролактина, пролактин–рилизинг гормона, релаксина, ренина, секретина, соматостатина, тромбопоэтина, тиреотропного гормона, тестостерона, дегидроэпиандростерона, андростендиона, дигидротестостерона, альдостерона, эстрадиола, эстрона, эстриола, кортизола, прогестерона, кальцитриола, кальцидиола, тамоксифена (Нолвадекс), анастрозола (Аримидекс), лектрозола (Фемара), фулвестранта (Фаслодекс) и их комбинаций.
26. Способ по п.18, где антиангиогенное средство выбрано из группы, состоящей из 2–метоксиэстрадиола, ангиостатина, бевацизумаба, хрящевого ингибирующего ангиогенез фактора, эндостатина, IFN–альфа, IL–12, итраконазола, линомида, тромбоцитарного фактора–4, пролактина, SU5416, сурамина, тасквинимода, текогалана, тетратиомолибдата, талидомида, тромбоспондина, тромбоспондина, TNP–470, зив–афлиберцепта, их фармацевтически приемлемых солей, пролекарств и их комбинаций.
27. Способ по п.18, где дополнительное лекарственное средство представляет собой ингибитор каскада PI3K/Akt.
28. Способ по п.27, где ингибитор каскада PI3K/Akt выбран из группы, состоящей из A–674563 (CAS № 552325–73–2), AGL 2263, AMG–319 (Amgen, Thousand Oaks, CA), AS–041164 (5–бензо[1,3]диоксол–5–илметилентиазолидин–2,4–дион), AS–604850 (5–(2,2–дифтор–бензо[1,3]диоксол–5–илметилен)тиазолидин–2,4–дион), AS–605240 (5–хиноксилин–6–метилен–1,3–тиазолидин–2,4–дион), AT7867 (CAS № 857531–00–1), серии бензимидазолов, Genentech (Roche Holdings Inc., South San Francisco, CA), BML–257 (CAS № 32387–96–5), BVD–723, CAL–120 (Gilead Sciences, Foster City, CA), CAL–129 (Gilead Sciences), CAL–130 (Gilead Sciences), CAL–253 (Gilead Sciences), CAL–263 (Gilead Sciences), CAS № 612847–09–3, CAS № 681281–88–9, CAS № 75747–14–7, CAS № 925681–41–0, CAS № 98510–80–6, CCT128930 (CAS № 885499–61–6), CH5132799 (CAS № 1007207–67–1), CHR–4432 (Chroma Therapeutics, Ltd., Abingdon, UK), FPA 124 (CAS № 902779–59–3), GS–1101 (CAL–101) (Gilead Sciences), GSK 690693 (CAS № 937174–76–0), H–89 (CAS № 127243–85–0), Хонокиола, IC87114 (Gilead Science), IPI–145 (Intellikine Inc.), KAR–4139 (Karus Therapeutics, Chilworth, Великобритания), KAR–4141 (Karus Therapeutics), KIN–1 (Karus Therapeutics), KT 5720 (CAS № 108068–98–0), Милтефозина, MK–2206 дигидрохлорида (CAS № 1032350–13–2), ML–9 (CAS № 105637–50–1), Налтриндола гидрохлорида, OXY–111A (NormOxys Inc., Brighton, MA), перифозина, PHT–427 (CAS № 1191951–57–1), ингибитора PI3–киназы дельта, Merck KGaA (Merck & Co., Whitehouse Station, NJ), ингибиторов PI3–киназы дельта, Genentech (Roche Holdings Inc.), ингибиторов PI3–киназы дельта, Incozen (Incozen Therapeutics, Pvt. Ltd., Hydrabad, Индия), ингибиторов–2 PI3–киназы дельта, Инкозена (Incozen Therapeutics), ингибитора PI3–киназы, Roche–4 (Roche Holdings Inc.), ингибиторов PI3–киназы, Roche (Roche Holdings Inc.), ингибиторов PI3–киназы, Roche–5 (Roche Holdings Inc.), ингибиторов PI3–альфа/дельта, Pathway Therapeutics (Pathway Therapeutics Ltd., South San Francisco, CA), ингибиторов PI3–дельта, Cellzome (Cellzome AG, Heidelberg, Germany), ингибиторов PI3–дельта, Intellikine (Intellikine Inc., La Jolla, CA), ингибиторов PI3–дельта, Pathway Therapeutics–1 (Pathway Therapeutics Ltd.), ингибиторов PI3–дельта, Pathway Therapeutics–2 (Pathway Therapeutics Ltd.), ингибиторов PI3–дельта/гамма, Cellzome (Cellzome AG), ингибиторов PI3–дельта/гамма, Intellikine (Intellikine Inc.), ингибиторов PI3–дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибитора PI3–гамма Evotec (Evotec), ингибитора PI3–гамма, Cellzome (Cellzome AG), ингибиторов PI3–гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторов PI3K–дельта/гамма, Intellikine–1 (Intellikine Inc.), пиктилисиба (Roche Holdings Inc.), PIK–90 (CAS № 677338–12–4), SC–103980 (Pfizer, Нью–Йорк, NY), SF–1126 (Semafore Pharmaceuticals, Индианаполис, IN), SH–5, SH–6, тетрагидрокуркумина, TG100–115 (Targegen Inc., San Diego, CA), Трицирибина, X–339 (Xcovery, Уэст–Палм–Бич, FL), XL–499 (Evotech, Гамбург, Германия), их фармацевтически приемлемых солей и их комбинаций.
29. Фармацевтическая композиция для лечения или смягчения эффектов злокачественной опухоли у индивидуума, имеющей мутацию BRAF не V600E/K, причем композиция содержит фармацевтически приемлемый носитель или разбавитель и эффективное количество ингибитора ERK или его фармацевтически приемлемой соли.
30. Фармацевтическая композиция по п.29, где ингибитор ERK выбран из группы, состоящей из BVD–523, SCH–722984 (Merck & Co.), SCH–772984 (Merck & Co.), SCH–900353 (MK–8353) (Merck & Co.), LY3214996 (Lilly), AEZS–140 (Aeterna Zentaris), AEZS–131 (Aeterna Zentaris), AEZS–136 (Aeterna Zentaris), LTT–462 (Novartis), RG–7842 (Genentech), CC–90003 (Celgene), KIN–4050 (Kinentia) и их комбинаций.
31. Фармацевтическая композиция по п.29, где ингибитор ERK представляет собой BVD–523.
32. Фармацевтическая композиция по п.29, где мутация BRAF не V600E/K представляет собой активирующую киназу мутацию, нарушающую функцию киназы мутацию или мутацию с неизвестным действием на киназу и их комбинации.
33. Фармацевтическая композиция по п.32, где активирующая киназу мутация выбрана из группы, состоящей из R462I, I463S, G464E, G464R, G464V, G466A, G469A, N581S, E586K, F595L, L597Q, L597R, L597S, L597V, A598V, T599E, V600R, K601E, S602D, A728V и их комбинаций.
34. Фармацевтическая композиция по п.32, где нарушающая функцию киназы мутация выбрана из группы, состоящей из G466E, G466R, G466V, Y472C, K483M, D594A, D594E, D594G, D594H, D594N, D594V, G596R, T599A, S602A и их комбинаций.
35. Фармацевтическая композиция по п.32, где мутация с неизвестным действием на киназу выбрана из группы, состоящей из T440I, S467L, G469E, G469R, G469S, G469V, L584F, L588F, V600_K601delinsE, S605I, Q609L, E611Q и их комбинаций.
36. Фармацевтическая композиция по п.29, где индивидуумом является млекопитающее.
37. Фармацевтическая композиция по п.36, где млекопитающее выбрано из группы, состоящей из людей, приматов, сельскохозяйственных животных и домашних животных.
38. Фармацевтическая композиция по п.36, где млекопитающее представляет собой человека.
39. Фармацевтическая композиция по п.29, где злокачественная опухоль представляет собой солидную злокачественную опухоль или гематологическую злокачественную опухоль.
40. Фармацевтическая композиция по п.29, где злокачественная опухоль выбрана из группы, состоящей из глиобластомы, меланомы, холангиокарциномы, мелкоклеточного рака легкого, рака ободочной и прямой кишки, рака предстательной железы, рака влагалища, ангиосаркомы, немелкоклеточного рака легкого, рака аппендикса, плоскоклеточного рака, карциномы протоков слюнных желез, аденокистозной карциномы, рака тонкого кишечника и рака желчного пузыря.
41. Фармацевтическая композиция по п.40, где злокачественная опухоль выбрана из группы, состоящей из рака тонкого кишечника, немелкоклеточного рака легкого, рака желчного пузыря и плоскоклеточного рака.
42. Фармацевтическая композиция по п.29, где композицию вводят индивидууму перорально или путем инъекции.
43. Фармацевтическая композиция по п.29, где композицию вводят индивидууму в качестве таблетки.
44. Фармацевтическая композиция по п.29, дополнительно содержащая по меньшей мере одно дополнительное лекарственное средство, выбранное из группы, состоящей из ингибитора MEK, ингибитора HDAC и их комбинаций.
45. Фармацевтическая композиция по п.44, где ингибитор MEK выбран из группы, состоящей из токсина сибирской язвы, антрохинонола (Golden Biotechnology), ARRY–142886 ((2–гидроксиэтокси)амид) 6–(4–бром–2–хлорфениламино)–7–фтор–3–метил–3H–бензоимидазол–5–карбоновой кислоты (Array BioPharma), ARRY–438162 (Array BioPharma), биниметиниба (MEK162, ARRY–1662), AS–1940477 (Astellas), AS–703988 (Merck KGaA), бентамапимода (Merck KGaA), BI–847325 (Boehringer Ingelheim), E–6201 (Eisai), GDC–0623 (Hoffmann–La Roche), GDC–0973 (кобиметиниб) (Hoffmann–La Roche), L783277 (Merck), части токсина сибирской язвы, являющейся летальным фактором, MEK162 (Array BioPharma), PD 098059 (2–(2'–амино–3'–метоксфенил)оксанафталин–4–он) (Pfizer), PD 184352 (CI–1040) (Pfizer), PD–0325901 (Pfizer), PD318088 (Pfizer), PD334581 (Pfizer), 6–метокси–7–(3–морфолин–4–илпропокси)–4–(4–феноксифениламино)хинолин–3–карбонитрила, 4–[3–хлор–4–(1–метил–1H–имидазол–2–илсульфанил)фениламино]–6–метокси–7–(3–морфолин–4–илпропокси)хинолин–3–карбонитрила, пимасертиба (Santhera Pharmaceuticals), RDEA119 (Ardea Biosciences/Bayer), рефаметиниба (AstraZeneca), RG422 (Chugai Pharmaceutical Co.), R0092210 (Roche), R04987655 (Hoffmann–La Roche), R05126766 (Hoffmann–La Roche), селуметиниба (AZD6244) (AstraZeneca), SL327 (Sigma), TAK–733 (Takeda), траметиниба (Japan Tobacco), U0126 (1,4–диамино–2,3–дициано–1,4–бис(2–аминофенилтио)бутадиена) (Sigma), WX–554 (Wilex), полипептида YopJ (Mittal et al., 2010), их фармацевтически приемлемых солей и их комбинаций.
46. Фармацевтическая композиция по п.44, где ингибитор HDAC выбран из группы, состоящей из Абексиностата (PCI–24781), Гивиностата, Энтиностата, Вориностата, CI–994, CUDC–101, Энтиностата, BML–210, M344, NVP–LAQ824, Панобиностата, Прациносата (SB939), Моцетиностата, Ресминостата, Ромидепсина, Белиностата, их фармацевтически приемлемых солей и их комбинаций.
47. Фармацевтическая композиция по п.29, дополнительно содержащая по меньшей мере одно дополнительное лекарственное средство, выбранное из группы, состоящей из антитела, фрагмента антитела, конъюгата антитела, цитотоксического средства, токсина, радионуклида, иммуномодулятора, фотоактивного лекарственного средства, радиосенсибилизирующего средства, гормона, антиангиогенного средства и их комбинаций.
48. Фармацевтическая композиция по п.47, где антитело, его фрагмент или их конъюгат выбраны из группы, состоящей из ритуксимаба (Ритуксан), Брентуксимаба Ведотина (Адцетриз), Адотрастузумаба эмтансина (Кадсила), Цетуксимаба (Эрбитукс), бевацизумаба (Авастин), Ибритумомаба (Зевалин), ведолизумаба (Энтивио), Ипилимумаба (Ервой), Ниволумаба (Опдиво), пембролизумаба (Кейтруда), Алемтузумаба атезолизумаба (Тецентрик), авелумаба (Бавенцио), дурвалумаба (Имфинзи), B–701, Офатумумаба, Обинутузумаба (Газива), Панитумумаба, плозализумаба, BI–754091, OREG–103, COM–701, BI–754111 и их комбинаций.
49. Фармацевтическая композиция по п.47, где цитотоксическое средство выбрано из группы, состоящей из циклофосфамида, мехлорэтамина, урамустина, мелфалана, хлорамбуцила, ифосфамида, кармустина, ломустина, стрептозоцина, бусульфана, темозоломида, цисплатина, карбоплатина, оксалиплатина, недаплатина, сатраплатина, триплатина тетранитрата, доксорубицина, даунорубицина, идарубицина, митоксантрона, метотрексата, пеметрекседа, 6–меркаптопурина, дакарбазина, флударабина, 5–фторурацила, арабинозилцитозина, капецитабина, гемцитабина, децитабина, алкалоидов барвинка, паклитаксела (Таксол), доцетаксела (Таксотер), иксабепилона (Икземпра), актиномицина, антрациклинов, валрубицина, эпирубицина, блеомицина, пликамицина, митомицина, их фармацевтически приемлемых солей, их пролекарств и комбинаций.
50. Фармацевтическая композиция по п.47, где токсин представляет собой дифтерийный токсин или его части.
51. Фармацевтическая композиция по п.47, где радионуклид выбран из группы, состоящей из I–125, At–211, Lu–177, Cu–67, I–131, Sm–153, Re–186, P–32, Re–188, In–114m, Y–90 и их комбинаций.
52. Фармацевтическая композиция по п.47, где иммуномодулятор выбран из группы, состоящей из гранулоцитарного колониестимулирующего фактора (G–CSF), LAG–3, IMP–321, JCAR–014, ASLAN–002 (BMS–777607), интерферонов, имиквимода и клеточных мембранных фракций из бактерий, IL–2, IL–7, IL–12, CCL3, CCL26, CXCL7, синтетического цитозинфосфат–гуанозина (CpG), ингибиторов иммунной точки контроля и их комбинаций.
53. Фармацевтическая композиция по п.47, где радиосенсибилизирующее средство выбрано из группы, состоящей из мизонидазола, метронидазола, тирапазамина, транс–кроцетината натрия и их комбинаций.
54. Фармацевтическая композиция по п.47, где гормон выбран из группы, состоящей из простагландинов, лейкотриенов, простациклина, тромбоксана, амилина, антимюллерова гормона, адипонектина, адренокортикотропного гормона, ангиотензиногена, ангиотензина, вазопрессина, атриопептина, натрийуретического пептида головного мозга, кальцитонина, холицистокинина, кортикотропин–рилизинг гормона, энцефалина, эндотелина, эритропоэтина, фоликулостимулирующего гормона, галанина, гастрина, грелина, глюкагона, гонадотропин–рилизинг гормона, рилизинг–фактора гормона роста, хорионического гонадотропина человека, лактогена плаценты человека, гормона роста, ингибина, инсулина, соматомедина, лептина, липотропина, лютеинизирующего гормона, меланоцит–стимулирующего гормона, мотилина, орексина, окситоцина, панкреатического полипептида, паратиреоидного гормона, пролактина, пролактин–рилизинг гормона, релаксина, ренина, секретина, соматостатина, тромбопоэтина, тиреотропного гормона, тестостерона, дегидроэпиандростерона, андростендиона, дигидротестостерона, альдостерона, эстрадиола, эстрона, эстриола, кортизола, прогестерона, кальцитриола, кальцидиола, тамоксифена (Нолвадекс), анастрозола (Аримидекс), лектрозола (Фемара), фулвестранта (Фаслодекс) и их комбинаций.
55. Фармацевтическая композиция по п.47, где антиангиогенное средство выбрано из группы, состоящей из 2–метоксиэстрадиола, ангиостатина, бевацизумаба, хрящевого ингибирующего ангиогенез фактора, эндостатина, IFN–альфа, IL–12, итраконазола, линомида, тромбоцитарного фактора–4, пролактина, SU5416, сурамина, тасквинимода, текогалана, тетратиомолибдата, талидомида, тромбоспондина, тромбоспондина, TNP–470, зив–афлиберцепта, их фармацевтически приемлемых солей, пролекарств и их комбинаций.
56. Фармацевтическая композиция по п.47, где дополнительное лекарственное средство представляет собой ингибитор каскада PI3K/Akt.
57. Фармацевтическая композиция по п.56, где ингибитор каскада PI3K/Akt выбран из группы, состоящей из A–674563 (CAS № 552325–73–2), AGL 2263, AMG–319 (Amgen, Thousand Oaks, CA), AS–041164 (5–бензо[1,3]диоксол–5–илметилентиазолидин–2,4–дион), AS–604850 (5–(2,2–дифтор–бензо[1,3]диоксол–5–илметилен)тиазолидин–2,4–дион), AS–605240 (5–хиноксилин–6–метилен–1,3–тиазолидин–2,4–дион), AT7867 (CAS № 857531–00–1), серии бензимидазолов, Genentech (Roche Holdings Inc., South San Francisco, CA), BML–257 (CAS № 32387–96–5), BVD–723, CAL–120 (Gilead Sciences, Foster City, CA), CAL–129 (Gilead Sciences), CAL–130 (Gilead Sciences), CAL–253 (Gilead Sciences), CAL–263 (Gilead Sciences), CAS № 612847–09–3, CAS № 681281–88–9, CAS № 75747–14–7, CAS № 925681–41–0, CAS № 98510–80–6, CCT128930 (CAS № 885499–61–6), CH5132799 (CAS № 1007207–67–1), CHR–4432 (Chroma Therapeutics, Ltd., Abingdon, UK), FPA 124 (CAS № 902779–59–3), GS–1101 (CAL–101) (Gilead Sciences), GSK 690693 (CAS № 937174–76–0), H–89 (CAS № 127243–85–0), Хонокиола, IC87114 (Gilead Science), IPI–145 (Intellikine Inc.), KAR–4139 (Karus Therapeutics, Chilworth, Великобритания), KAR–4141 (Karus Therapeutics), KIN–1 (Karus Therapeutics), KT 5720 (CAS № 108068–98–0), Милтефозина, MK–2206 дигидрохлорида (CAS № 1032350–13–2), ML–9 (CAS № 105637–50–1), Налтриндола гидрохлорида, OXY–111A (NormOxys Inc., Brighton, MA), перифозина, PHT–427 (CAS № 1191951–57–1), ингибитора PI3–киназы дельта, Merck KGaA (Merck & Co., Whitehouse Station, NJ), ингибиторов PI3–киназы дельта, Genentech (Roche Holdings Inc.), ингибиторов PI3–киназы дельта, Incozen (Incozen Therapeutics, Pvt. Ltd., Hydrabad, Индия), ингибиторов–2 PI3–киназы дельта, Инкозена (Incozen Therapeutics), ингибитора PI3–киназы, Roche–4 (Roche Holdings Inc.), ингибиторов PI3–киназы, Roche (Roche Holdings Inc.), ингибиторов PI3–киназы, Roche–5 (Roche Holdings Inc.), ингибиторов PI3–альфа/дельта, Pathway Therapeutics (Pathway Therapeutics Ltd., South San Francisco, CA), ингибиторов PI3–дельта, Cellzome (Cellzome AG, Heidelberg, Germany), ингибиторов PI3–дельта, Intellikine (Intellikine Inc., La Jolla, CA), ингибиторов PI3–дельта, Pathway Therapeutics–1 (Pathway Therapeutics Ltd.), ингибиторов PI3–дельта, Pathway Therapeutics–2 (Pathway Therapeutics Ltd.), ингибиторов PI3–дельта/гамма, Cellzome (Cellzome AG), ингибиторов PI3–дельта/гамма, Intellikine (Intellikine Inc.), ингибиторов PI3–дельта/гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибитора PI3–гамма Evotec (Evotec), ингибитора PI3–гамма, Cellzome (Cellzome AG), ингибиторов PI3–гамма, Pathway Therapeutics (Pathway Therapeutics Ltd.), ингибиторов PI3K–дельта/гамма, Intellikine–1 (Intellikine Inc.), пиктилисиба (Roche Holdings Inc.), PIK–90 (CAS № 677338–12–4), SC–103980 (Pfizer, Нью–Йорк, NY), SF–1126 (Semafore Pharmaceuticals, Индианаполис, IN), SH–5, SH–6, тетрагидрокуркумина, TG100–115 (Targegen Inc., San Diego, CA), Трицирибина, X–339 (Xcovery, Уэст–Палм–Бич, FL), XL–499 (Evotech, Гамбург, Германия), их фармацевтически приемлемых солей и их комбинаций.
58. Фармацевтическая композиция по п.44 или 47, которая находится в единичной дозированной форме, содержащей как ингибитор ERK, так и дополнительное лекарственное средство.
59. Фармацевтическая композиция по п.44 или 47, в которой ингибитор ERK находится в первой единичной дозированной форме и дополнительное лекарственное средство находится во второй единичной дозированной форме, отдельной от первой.
60. Фармацевтическая композиция по п.44 или 47, где ингибитор ERK и дополнительное лекарственное средство вводят индивидууму совместно.
61. Фармацевтическая композиция по п.44 или 47, где ингибитор ERK и дополнительное лекарственное средство вводят индивидууму последовательно.
62. Фармацевтическая композиция по п.61, где ингибитор ERK вводят индивидууму до или после введения дополнительного лекарственного средства.
63. Способ лечения или смягчения эффектов злокачественной опухоли, имеющей мутацию BRAF не V600E/K, причем способ включает введение индивидууму эффективного количества BVD–523 или его фармацевтически приемлемой соли.
64. Фармацевтическая композиция для лечения или смягчения эффектов злокачественной опухоли у индивидуума, имеющей мутацию BRAF не V600E/K, причем композиция содержит фармацевтически приемлемый носитель или разбавитель и эффективное количество BVD–523 или его фармацевтически приемлемой соли.
65. Набор для лечения или смягчения эффектов злокачественной опухоли у индивидуума, имеющей мутацию BRAF не V600E/K, причем набор содержит фармацевтическую композицию по любому из пп.29, 44 и 47, упакованную вместе с инструкциями по ее применению.
66. Способ по п.15 или фармацевтическая композиция по п.44, где ингибитор HDAC выбран из группы, состоящей из Вориностата, Панобиностата, Ромидепсина, Белиностата, их фармацевтически приемлемых солей и их комбинаций.
67. Способ по п.18 или фармацевтическая композиция по п.47, где антитело, его фрагмент или их конъюгат выбран из группы, состоящей из ритуксимаба (Ритуксан), Брентуксимаба Ведотина (Адцетриз), Адотрастузумаба эмтансина (Кадсила), Ипилимумаба (Ервой), Ниволумаба (Опдиво), пембролизумаба (Кейтруда), Алемтузумаба атезолизумаба (Тецентрик), дурвалумаба (Имфинзи), Офатумумаба, Обинутузумаба (Газива), Панитумумаба и их комбинаций.
68. Способ по п.27 или фармацевтическая композиция по п.56, где ингибитор каскада PI3K/Akt представляет собой BVD–723.
| US 2016310476 A1, 2016.10.27 | |||
| US 2014045843 A1, 2014.02.13 | |||
| WO 2017007941 A2, 2017.01.12 | |||
| Семенов Д | |||
| Ю | |||
| и др | |||
| Динамометрическая втулка | 1921 |
|
SU600A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| - Т | |||
| Способ окисления боковых цепей ароматических углеводородов и их производных в кислоты и альдегиды | 1921 |
|
SU58A1 |
| - No | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| - С | |||
| ИСКРОУЛОВИТЕЛЬ ДЛЯ ПАРОВОЗОВ | 1923 |
|
SU649A1 |
Авторы
Даты
2024-02-01—Публикация
2018-05-15—Подача