Изобретение относится к области нефтепереработки, в частности, к приготовлению массивных (без носителей) катализаторов гидроочистки нефтяных фракций, обладающих высокой активностью и повышенной химической стабильностью.
Известны способы гидроочистки нефтяных топливных фракций с использованием нанесенных катализаторов, которые представляют собой сочетание металл-сульфидных (например, Co/Ni-Mo/W-S) активных компонентов, размещенных на пористых носителях различного состава (Al2O3/AlOOH/SiO2 и т.д.). Они широко используются в процессах нефтепереработки в России и на Западе. Однако процедуры их приготовления многостадийны, требуют длительных температурных воздействий, использования растворных технологий и токсичных реагентов осернения [Патент РФ 2472585; Патент РФ 2626396].
Предложены способы получения и использования массивных сульфидных катализаторов. Это катализаторы без носителя, содержащие в своем составе только активный компонент. Примером являются наноразмерные псевдогомогенные каталитические системы, которые способны изменять структуру нефтяных дисперсных систем, в том числе, и тяжелого нефтяного сырья. Их получают методом мицеллярного синтеза, который развивается на Западе уже более 20 лет, в том числе, последние 10 лет и в России [Wilcoxon J.P., Samara G.A. // Phys. Rev. В. 1995. V. 51. P. 7299-7302; Хаджиев C.H., Кадиев X.M., Кадиева М.Х. // Нефтехимия. 2014. Т.54. №5. С.327-351; Rane J.P., Pauchard V., Couzis A., Banerjee S. // Langmuir. 2013. V. 29. Is. 15. P. 4750-4759]. Недостаток - необходимость привлечения растворных технологий и поверхностно-активных веществ (ПАВ).
Известны также твердофазные способы получения массивных катализаторов, которые в большей мере отвечают современным требованиям «зеленой химии». Среди них предпочтение отдается подходам, основанным на твердофазном механохимическом сочетании порошков металлов микронных размеров (катализаторы типа Ренея), или солей-прекурсоров, например, гидроксо-карбоната никеля, парамолибдата или метавольфрамата аммония, или же высокотемпературного разложения тетратиомолибдата аммония и др. [Floresz M.I., Estrada-Guel I., Orneals С. et al. // Advances in technology of materials and materials processing journal. 2006. V.8. Is.2. P.140-145.; Патент РФ 2346742; Polyakov M., Indris S., Schwamborn S. et al. // Journal of Catalysis. 2008. V. 260. Is. 2. P. 236-244]. Недостатком является необходимость проведения стадии окисления-сульфидирования каталитических прекурсоров и использование органических или водных растворов.
Описаны прямые (в одну стадию) методы приготовления сульфидных катализаторов с использованием очищенного минерала молибденита, как размерного MOS2-каталитического прекурсора. Для измельчения крупнодисперсного MOS2 обычно используют планетарные мельницы. Процесс измельчения выполняют в среде органических растворителей, при относительно больших массах мелющих тел, в условиях высоких значений центробежного ускорения (g=300-500 м2/с), соответствующих преимущественному вкладу воздействия ударного характера на измельчаемые субстраты [Masato К., Kunio U., Yasunori К., Fumikazu I. // Applied Catalysis A: General. 2004. V.276. P. 241-249; Kuriki Y., Uchida K., Sekreta E. et al. // Fuel Process. Technol. 1999. V.59. Is. 2-3. P. 189-200]. Недостаток - использование органических растворителей и быстрое зауглероживание катализатора.
Наиболее близким по сути к излагаемому изобретению является прямой твердофазный способ получения катализатора гидропереработки нефтяных фракций на основе молибденита (Патент РФ №2612222), когда в качестве исходного реагента берут крупнодисперсный коммерческий порошок дисульфида молибдена (молибденита), допируют к нему в микроколичествах метанол (100 мкл); субстрат измельчают в условиях механоактивации (МА) в мельнице в течение 8 часов. Катализатор (прототип) обеспечивает конверсию дибензотиофена на высоком уровне, не ниже 99%, а содержание остаточной серы в гидродесульфуризатах не превышает 1-2 ррм. Недостатком катализатора по прототипу, как было установлено позже [Feduschak Т., Akimov А., Morozov М. et al. // Comptes Rendus Chimie. 2016. V. 19. Is. 10, P. 1315-1325; Федущак T.A., Уймин M.A., Акимов A.C. и др. // Химия в интересах устойчивого развития. 2016. Т. 24. №2. С. 209-215], является его химическая неустойчивость к воздействию компонентов окружающей среды, в частности, воздуха и влаги (табл. 1). Нежелательные последствия проявляются практически сразу после контакта МА-порошка с воздухом, и выражаются в образовании на его поверхности S-O-соединений кислотного характера, которые в водной фазе порошковых суспензий образуют серную кислоту (рН>2.1; рис. 1). С одной стороны, значение рН является своего рода реперным признаком высокой каталитической активности порошков данной серии, но в то же время, влечет за собой сложности, возникающие при их хранении как кислот-содержащих систем (при нарушении герметичности тары). Также могут возникать и определенные ограничения к дальнейшему использованию порошков, например, в качестве присадок к маслам. Кроме того, перед непосредственным использованием, катализатор по прототипу дополнительно нуждается в предварительном его выдерживании в реакторе (табл. 1) в газовой токсичной сероводородсодержащей среде [Fedushchak Т., Uimin М., Zhuravkov S. et al. // Proceedings of the International symposium on advances in hydro-processing of oil fractions ISAHOF-2017, Mexico City, Mexico, June 4-7. P. 69-70; Fedushchak Т., Uimin M., Zhuravkov S. et al. // Book of Abstracts of the V International conference "Fundamental Bases of Mechanochemical Technologies", Novosibirsk, June 25-28, 2018. P. 41].
Задачей предлагаемого изобретения является разработка способа получения массивного катализатора гидроочистки нефтяных фракций высокого уровня гидродесульфирующей способности в виде порошка с более высоким уровнем химической устойчивости при его хранении, пониженным образованием легко гидролизующихся кислотных соединений на поверхности и, соответственно, кислот в сопряженных органических и водных средах, который не требует предварительной обработки сероводородом перед его непосредственным использованием, и обеспечивает ультранизкое содержание серы (<10 ppm) в гидродесульфуризатах.
Технический результат заключается в упрощении технологии процесса; повышении экологического уровня его исполнения; повышении химической устойчивости полученного предлагаемым способом катализатора к деградации при взаимодействии с компонентами окружающей среды, на его поверхности в течение длительного времени не образуются сильно кислотные компоненты.
Несколько десятилетий назад в мировой науке наблюдался спонтанный рост заявок на изобретения, связанные с использованием криогенных технологий в процессах механохимического измельчения субстратов [US Patent 6923392; US Patent 3771729; Пягай P.H. Исследование влияния криовоздействия на реакционную способность твердых веществ. Дисс. канд. хим. наук. М.: МГУ, 1982. 201 с.]. Это обусловлено значительным повышением хрупкости измельчаемых веществ и материалов при низких температурах (<77 К), что позволяет превращать в порошок твердые тела, пластичные при комнатной температуре (резина, свинец), значительно уменьшать размер частиц при измельчении хрупких материалов и, в некоторых случаях, снижать затраты энергии на измельчение. Криопомол стал одним из эффективных способов получения и нанопорошков [Гусева А.Н. Методы получения наноразмерных материалов. Екатеринбург: УрГУ, 2007. 79 с.]. Такого рода подход ранее не был применен непосредственно к процессам приготовления катализаторов, в том числе, и к получению катализаторов на основе молибденита.
Предмет данного изобретения связан с получением катализатора гидроочистки посредством механохимического измельчения молибденита (как размерного прекурсора) в криогенных условиях.
Активность каталитических систем по изобретению оценивали, как и в прототипе, по содержанию остаточной серы в модельной реакции гидрогенолиза дибензотиофена (Soct, ДБТ, табл. 1; установка высокого давления AUTOCLAVE ENGENEERS). В литературных источниках дибензотиофен (ДБТ) традиционно используют как модельное соединение [Патент РФ 2473387], химическая структура которого соответствует наиболее устойчивым сернистым соединениям, присутствующим в нефтяных фракциях. Физико-химические анализы порошков и их суспензий выполнены с привлечением рентгено-фазового анализа (РФА; дифрактометр D8-Discovery, Bruker, Germany), рентгеновской фотоэлектронной спектроскопии (РФЭС; фотоэлектронный спектрометр SPECS с использованием AlKα излучения), седиментационного анализа (дисковая центрифуга DC24000; CPS Instruments, USA). Значения рН водных фаз порошковых суспензий измерены на рН-метре HANNA HI 2215. Анализ гидрогенизатов на содержание остаточной серы выполнен методом рентгенофлуоресцентного анализа (Спектроскан S).
ОБЩИЕ МЕТОДИКИ. Крио-катализатор готовят из крупнодисперсного коммерческого порошка дисульфида молибдена MOS2 (марка ДМИ-7) следующим образом. Порошок молибденита массой 3 г загружают в ступку вибромельницы объемом 110 мл с шестью шарами массой 200 г (все из стали ШХ-15), ступку вакуумируют и заполняют аргоном под давлением 1300 Торр. Затем ступку размещают в стальном сосуде Дьюара, который заполняется жидким азотом. При этом аргон в ступке конденсируется и становится жидким. Частота вибраций 16 Гц, амплитуда 1-2 мм. Через 8 часов мельницу выключают. После того, как температура в Дьюаре поднимается до комнатной, газ из ступки откачивают, ступку переносят в аргоновый бокс, где порошок герметично упаковывают. Для выполнения экспериментов с учетом химической деградации образцов, последние, перед помещением в реактор, выдерживают на воздухе (сроки пребывания на воздухе приведены в табл. 1, строка №5).
Далее сравнительную оценку каталитических свойств для крио-образцов и прототипа выполняют в аналогичных условиях. В качестве модельного S-содержащего соединения, используют раствор ДБТ в гексадекане, соответствующий по содержанию исходной серы Sисх=500 ppm.
Общие условия проведения экспериментов по определению гидродесульфирующей активности в модельной реакции для прототипа и примеров №1-4 по изобретению приведены в табл. 1. В реактор помещают катализатор в количестве 0,64 г и выдерживают его в газовой атмосфере водорода или водород+сероводород (H2/H2+H2S; строки №3 и №4 соответственно) при давлении 3,4 МПа в течение 6 ч при 340°С. Температурное выдерживание образцов в газовой атмосфере - это стадия предварительной подготовки катализатора или его «активирования»; оно выполняется либо только в водородной среде, либо еще в присутствии сероводорода. Затем давление в реакторе сбрасывают, добавляют раствор дибензотиофена (навеска 0,17 г) в гексадекане (80 мл) и закачивают водород (давление 3,0÷3,4 МПа; строка №1). Пробы гидрогенизатов отбирают после выхода установки на режим (перемешивание, 340°С) и последующего выдерживания в реакторе в течение 8 ч. Гидродесульфирующую способность катализатора оценивают по величине остаточной серы (Socт) в гидродесульфуризатах.
Примеры конкретного выполнения экспериментов.
ПРИМЕР 1 (табл. 1). Крио-катализатор №1 готовят в условиях, как описано в общих методиках. Затем этот образец выдерживают на воздухе в течение 60 минут (строка 5), и параллельно определяют для него значение рН и его гидродесульфирующую активность. Значение рН водной фазы порошковой суспензии для крио-катализатора №1 соответствует более слабой кислотности рН=4,0 (строка 6), чем для прототипа, когда рН=2,1 (строка 6).
Испытание активности крио-катализатора №1 (табл. 1). В реактор установки высокого давления помещают 0,64 г катализатора №1, который выдерживают в газовой атмосфере водорода (строка 3) при давлении 3,4 МПа, в течение 6 ч при 340°С. Затем сбрасывают давление и добавляют раствор дибензотиофена (навеска 0,17 г) в 80 мл гексадекана. Давление в реакторе устанавливают на уровне 3,0 МПа (строка 1), температура 340°С.
Важно, что для варианта активирования катализатора №1 путем выдерживания его в атмосфере Н2 (строка 3), в продуктах гидрогенолиза обнаруживается минимум серы (Socт=1 ppm; строка 3), в то время как по прототипу Socт=150 ppm.
После предварительного выдерживания катализатора №1 в реакторе в атмосфере H2+H2S, (строка 2) содержание остаточной серы (Socт, ppm) по сравнению с прототипом оказывается больше, и составляет 20 ppm (строка 2).
ПРИМЕР 2 (табл. 1). Крио-катализатор №2 готовят и испытывают на активность в условиях, как в примере 1, но только после предварительного хранения образца на воздухе в течение 30 дней (строка 5), значение рН водной фазы для суспензии криокатализатора №2 составляет 3,8 (строка 6), а давление в реакторе ниже, и составляет не 3,5 МПа, как по прототипу, а 3,1 МПа (строка 1).
Для варианта предварительного выдерживания (активирования) крио-катализатора №2 в атмосфере Н2 (строка 4), в продуктах гидрогенолиза обнаруживается минимум серы (Soct=1 ppm; строка 3), в то время как по прототипу Soct=150 ppm..
При этом глубина гидродесульфирующей способности после активирования катализатора в реакторе в атмосфере H2+H2S оказывается выражена более слабо (Socт=25 ppm; строка 2), чем по прототипу (Socт=1 ppm; строка 2).
ПРИМЕР 3 (табл. 1). Крио-катализатор №3 готовят и испытывают на гидродесульфирующую способность, как в примере 1, только после хранения образца на воздухе в течение 60 дней (строка 5). Значение рН водной фазы для его порошковой суспензии соответствует среднекислотному значению рН=3,5 (строка 6). Давление в реакторе при проведении модельной реакции составляет 3,3 МПа (строка 1).
После активирования катализатора №3 в атмосфере H2+H2S, остаточное содержание серы выше, чем по прототипу и составляет Socт=20 ppm (строка 2).
Для варианта выдерживания катализатора только в атмосфере Н2, в гидродесульфуризатах остается минимум по сере и Socт=2 ppm (строка 3), в то время как по прототипу Socт=150 ppm..
ПРИМЕР 4 (табл. 1). Крио-катализатор №4 готовят и испытывают на гидродесульфирующую способность, как в примере 1, но только после хранения образца на воздухе в течение 150 дней (строка 5). Значение рН водной фазы порошковой суспензии рН=3,2 (строка 6), давление в реакторе составляет 3,4 МПа (строка 1).
При температурном выдерживании катализатора №4 в реакторе в атмосфере H2+H2S, остаточное содержание серы выше, чем по прототипу и составляет Socт=20 ppm (строка 2).
Однако при активировании катализатора №4 без H2S, в атмосфере только лишь Н2, в гидродесульфуризатах вновь обнаруживается ультранизкое содержание серы (Socт=4 ppm; строка 3); в то время как по прототипу Socт=150 ppm.
Из данных табл. 1 следует, что кислотность водных растворов для крио-порошков по примерам №1-№4 (по тексту и табл. 1; строка 6), находившихся в контакте с воздухом от 60 минут до 150 суток, лежит в области 3,2≤рН≤4,0, что соответствует диапазону «средней» кислотности, но никак не «очень сильной», как для прототипа (рН=2,1; табл. 1; строка 6).
Следовательно, в соответствии с данными таблицы 1 для крио-катализаторов не требуется активирование в среде сероводорода, в отличие от прототипа (строка №4). Практически полное гидродесульфирование ДБТ происходит при более низких давлениях (строка №1), чем по прототипу. Кислотность водных растворов суспензий для крио-порошков (в сравнении с прототипом) ослабевает (строка №6). Три названных момента (табл. 1) представляют особый практический и теоретический интерес.
Первый из них связан с отсутствием необходимости предварительной обработки катализатора сероводородом по сравнению с прототипом. Следует отметить, что вопросу изучения раздельного и совместного влияния на гидрообессеривающую активность катализатора предварительной обработки водородом и сероводородом посвящено значительное количество работ. Использование многих видов катализаторов, и выполнение работ в различных условиях, в том числе, и с применением перечня разных реагентов, дало возможность накопить большой объем информации, которая не всегда согласуется, а порой даже носит противоречивый характер. Тем не менее все-таки можно заключить, что традиционным и «наилучшим приемом активации катализаторов гидрообессеривания является их предварительная обработка смесью сероводорода с водородом» [Берг Г.А., Хабибуллин С.Г. Каталитическое гидрооблагораживание нефтяных остатков. Ленинград: Химия, 1986. С. 98]. Тот факт, что катализатор по изобретению (крио-катализатор) перед использованием его в реакции не требует предварительной обработки токсичным, химически агрессивным сероводородом, в отличие от прототипа (табл. 1; строка 4) является преимуществом.
Второй момент также отражен в табл. 1 (строка 1). Из приведенных данных становится очевидным, что в присутствии катализатора по изобретению, появляется возможность проводить модельную реакцию при более низком давлении в реакторе.
Третий момент - на поверхности крио-порошков образуются поверхностные S-O - соединения, которые, в конечном итоге, обуславливают более слабую кислотность водных порошковых суспензий в сравнении с прототипом.
Таким образом, в соответствии с полученными экспериментальными данными (табл. 1), можно сформулировать обобщающие результаты.
Результат изобретения состоит в следующем:
• В условиях крио-измельчения образуется крио-катализатор, устойчивый к химическому воздействию окружающей среды (воздуха и влаги) в течение 5 месяцев, в то время как для порошка по прототипу химическая деградация поверхности начинается практически сразу (табл. 1; примеры №1-4).
• Способ по изобретению выгодно отличается в экологическом аспекте, он не требует предварительной обработки катализатора перед началом процесса токсичным и агрессивным сероводородом, в то время как катализатор по прототипу без обработки сероводородом характеризуется низкой активностью (табл. 1).
• Реакцию гидродесульфирования на крио-катализаторе можно проводить при более низком давлении внутри реактора на 0,1-0,5 МПа (что соответствует возможности понижения рабочего давления на 1-5 атм), чем по прототипу (табл. 1).
• Крио-катализатор обеспечивает конверсию дибензотиофена на уровне прототипа (не ниже 99%), содержание остаточной серы в гидрогенизатах не превышает 1-4 ррм, что характеризует его как объект с высокой гидродесульфирующей способностью (табл. 1)
Результат достигается за счет того, что:
• В условиях крио-механохимического измельчения молибденита на поверхности порошковых катализаторов формируется слой с иным химическим составом, нежели по прототипу.
• Поверхностные S-O-соединения в крио-катализаторах содержатся в значительно меньшем количестве (в 3,6 раз ниже; табл. 2; №3).
• В отличие от порошков по прототипу (табл. 2; рис. 1 и рис. 2), поверхностные соединения в крио-порошковых суспензиях характеризуются меньшей кислотообразующей способностью (рН≥3,2) и большей химической стабильностью, которая предохраняет нанопорошки от деградации в течение нескольких месяцев (табл. 1). При этом для прототипа характерна сильная кислотность (рН=2,1) [Бейтс Р. Определение рН. Теория и практика. Ленинград: Химия, 1972].
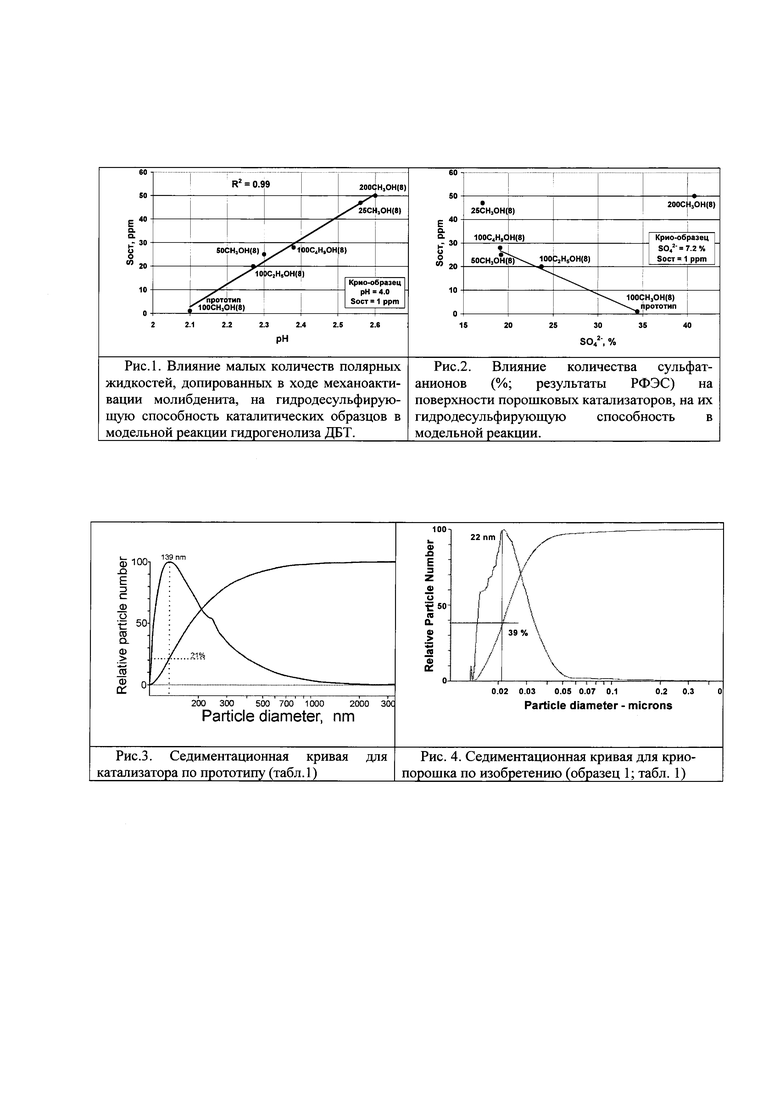
• Дисперсный состав порошка по изобретению представлен (рис. 4) ультра-мелкими фракциями. Это фракция размерного диапазона 12÷22 нм в количестве 39% и фракция дисперсностью 22÷55 нм в количестве 61% (рис. 4).
• Активные центры крио-порошка расположены на поверхности частиц. Предпосылкой утверждения является тот факт, что межплоскостные расстояния (D002, Ǻ) в нанокристаллитных пачках крио-катализатора в ходе криопомола остаются неизменными (табл. 3), и, следовательно, не могут служить рабочим пространством для протекания модельной реакции.
Ниже приводятся результаты физико-химических методов анализа порошковых катализаторов, как аргументы в пользу специфичности образцов по изобретению (табл. 2-3; рис. 1-4), полученные из данных РФЭ-спектров, седиментационного анализа (метод определения дисперсности), РФА (структурные особенности кристаллических нанокристаллитов), значений рН водных фаз порошковых суспензий (количественный индикатор поверхностных кислотных структур).
Как следует из данных табл. 2, для образца по Прототипу значение количественного соотношения поверхностных сульфат-сульфид-анионов в 3,6 раз больше (п. №3), чем для образца по Изобретению (п. №1-2). Для окисленных состояний молибдена (Мо6+/Мо4+) характерна аналогичная тенденция (п. №3; в 3,5 раз больше).
При этом обращают на себя внимание сравнительно близкие значения соотношений между S042-7S2- и Мо6+/Мо4+: 0,61 и 0,69 для образца по прототипу (п. №1), 0,17 и 0,20 для крио-образца (п. №2; табл. 2). Как следует из данных табл. 2, различия в условиях измельчения молибденита по изобретению, и по прототипу не отражаются на величине соотношений элементов S/Mo (неизменное значение 2,1).
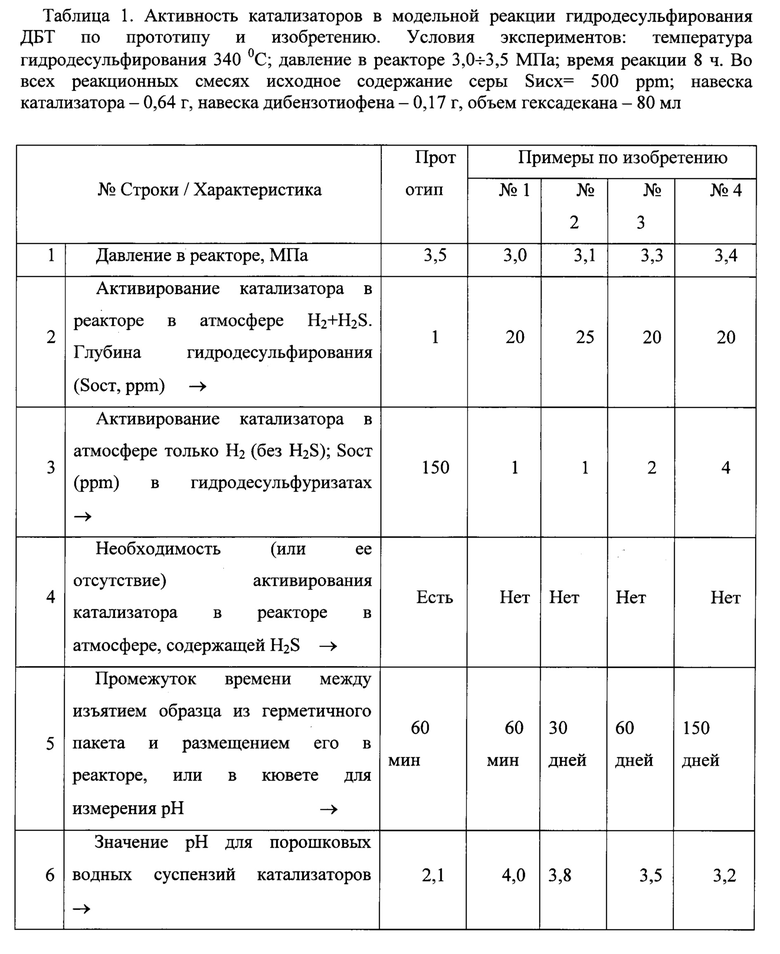
На рис. 1 представлены экспериментальные результаты, которые отражают характер влияния допированных микроколичеств низших спиртов (метанола, этанола, бутанола; 25÷200 мкл), на каталитическую активность получаемых образцов, приготовленных в условиях, аналогичных Прототипу, а также значения рН их водных суспензий.
Таким образом, присутствие малых количеств низших спиртов обуславливает сильно кислые значения рН для водных порошковых суспензий (рН=2,1÷2.6). При этом наименьшее значение остаточного содержания серы в продуктах модельной реакции (Socт=1 ppm; рис. 1; табл. 1) наблюдается для образца, полученного при МА молибденита (8 ч) в присутствии 100 мкл метанола (Прототип; табл. 1), имеющего на поверхности структуры кислотной природы (значение кислотности в сопряженной водной фазе рН=2,1; табл. 1). [Fedushchak Т., Uimin М., Zhuravkov S. et al. // Proceedings of the International symposium on advances in hydro-processing of oil fractions ISAHOF-2017, Mexico City, Mexico, June 4-7. P. 69-70; Fedushchak Т., Uimin M., Zhuravkov S. et al. // Book of Abstracts of the V International conference "Fundamental Bases of Mechanochemical Technologies", Novosibirsk, June 25-28, 2018. P. 41].
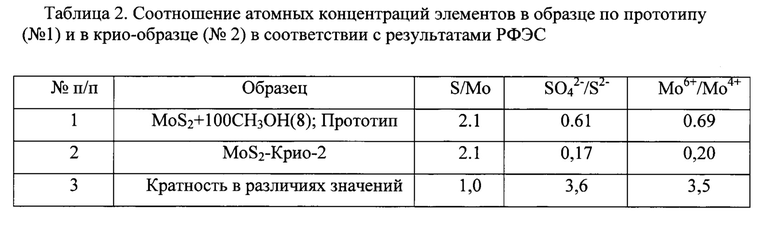
В то же время, линейный характер корреляции между концентрацией сульфат-анионов и гидродесульфирующей способностью (рис. 2), а также результаты качественной реакции (аналитический тест на присутствие сульфат-анионов в водном растворе - это качественная реакция водных маточников суспензий с раствором нитрата бария, которая сопровождается выпадением осадка сульфата бария), позволяют связать непосредственную причину столь сильно кислотных значений рН, с присутствием сульфат-анионов и, соответственно, образующейся серной кислоты в сопряженных водных фазах порошковых суспензий.
Следует отметить, что высокая протонная кислотность нежелательна, как для собственно катализаторов, так и для рабочих жидких сред, в которых происходят процессы гидродесульфирования. Так что высокая кислотность метанол-содержащих катализаторов мотивирует экспериментальный поиск дополнительных демпинговых приемов, с целью снижения уровня химической агрессивности порошковых катализаторов. Результаты поиска отражены на рис. 1-2 для крио-образцов, а их характеристики в табл. 3 и на рис. 3-4.
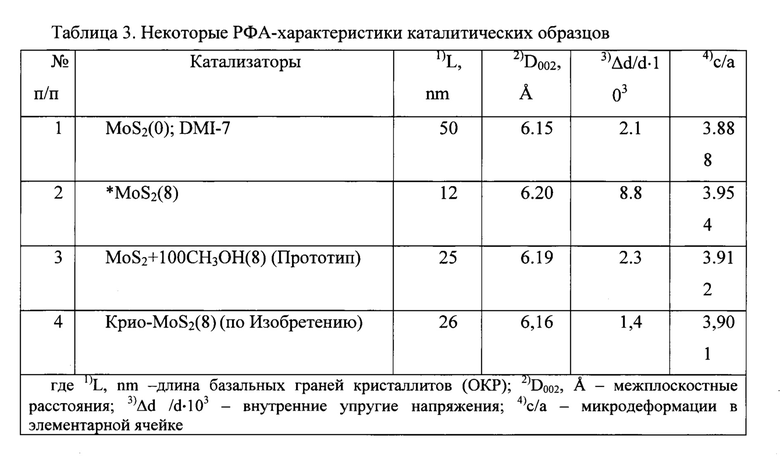
На рис. 3 и рис. 4 приведены результаты седиментационного анализа для порошков по прототипу и изобретению, которые характеризуют размер (дисперсность) сравниваемых катализаторов. На рис. 3 приведена асимметричная куполообразная седиментационная кривая для катализатора по прототипу с максимумом распределения частиц 139 нм. Фракция с размером частиц до 139 нм присутствует в количестве 21%. При этом 79% этого порошка приходится на частицы с дисперсностью сравнительно широкого размерного диапазона: от 139 нм до 1000 нм.
По сравнению с прототипом (рис. 3), для образца по изобретению (рис. 4) наблюдается большая симметрия и некоторое «сжатие» седиментационной кривой, а также зеркальная инверсия ее внешней формы, и смещение в область более высокой дисперсности, что согласуется с литературными данными для Fe-содержащих порошков [Степанов Е.Г., Котельников Г. Р. // Изв. вузов. Химия и хим. технол. 2003. Т. 46. №9. С. 26-31].
Таким образом, крио-частицы (рис. 4) MoS2 обладают более высокой дисперсностью. Их седиментационное распределение соответствует наноразмерным фракциям 10-22 нм (в количестве 39%). При этом 61% частиц относятся к размерному диапазону 23-55 нм. В соответствии с литературными данными, реакционная способность более мелких частиц порошков наноразмерного диспазона соответствует их большей активности как нанорегентов и нанокатализаторов [Сергеев Г.Б. // Ж. Рос. хим. об-ва им. Д.И. Менделеева. 2002. Т. XLVI. №5. С. 22-29].
В табл. 3 приведены некоторые структурные характеристики образцов, полученные методом рентгенофазового анализа (РФА). Отсюда следует, что после МА молибденита в течение 8 ч (образец №2, взят для сравнения; табл. 3) происходит явное уменьшение размеров базальных граней кристаллита (в 4,2 раза), некоторое увеличение межплоскостных расстояний (от 6,15 до 6,20 Ǻ), и четырехкратное возрастание внутренних упругих напряжений при возрастании микродеформаций в элементарной ячейке, что отражает высокий уровень дефектности порошка №2. Вместе с тем, для образцов №3 и №4 (прототип и образец по изобретению; табл. 3), кратность снижения длины базальных граней составляет всего ~2. Межплоскостные расстояния в пачечных нанокристаллитах в крио-MoS2 г(8) (по изобретению; D002=6,16 Ǻ) мало отличаются от аналогичной характеристики для исходного молибденита (№1; D002=6,15 Ǻ) и от прототипа (№3; D002=6,19 Ǻ; табл. 3). Однако уровень внутренних упругих напряжений для крио-образца оказывается в 1.5 раза ниже (№4; Δd/d⋅103=l,4), даже по сравнению с исходным образцом №1 (Δd/d⋅103=2,1) и образцом по прототипу (№3; Δd/d⋅103=2,3; табл. 3). В какой-то мере эти результаты согласуется с мнением авторов [Степанов Е.Г., Котельников Г.Р. // Изв. вузов. Химия и хим. технол. 2003. Т. 46. №9. С. 26-31] относительно «бездефектных» порошков, получаемых в условиях крио-помола на примере гематита. Значения, характеризующие уровень микродеформаций в элементарных ячейках (с/а) для прототипа и крио-образца различаются незначительно (образцы №3 и №4; с/а=3,912 и 3,901 соответственно).
Таким образом, показано, что в результате сочетания механического помола молибденита с криогенными условиями его исполнения, образуются наноразмерные порошки с иным химическим составом поверхности, с менее выраженной склонностью образовывать поверхностные соединения кислотного характера, с низкой концентрацией структурных дефектов, но при этом с высокой гидродесульфирующей способностью.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ГИДРОПЕРЕРАБОТКИ НЕФТЯНЫХ ФРАКЦИЙ | 2014 |
|
RU2612222C2 |
| СПОСОБ ГИДРООЧИСТКИ ДИЗЕЛЬНЫХ ФРАКЦИЙ | 2014 |
|
RU2596830C2 |
| КАТАЛИЗАТОР ГИДРООЧИСТКИ ДИЗЕЛЬНЫХ ФРАКЦИЙ | 2012 |
|
RU2496574C1 |
| Способ получения порошковой композиции на основе оксикарбидов алюминия | 2019 |
|
RU2690918C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОГО МАТЕРИАЛА НА ОСНОВЕ НИТРИДА КРЕМНИЯ | 2019 |
|
RU2736195C1 |
| СПОСОБ ПЕРЕРАБОТКИ ТЯЖЕЛОГО НЕФТЯНОГО СЫРЬЯ | 2016 |
|
RU2616300C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ N-(ФОСФОНОМЕТИЛ)-ГЛИЦИНА | 2018 |
|
RU2663905C1 |
| СПОСОБ ПЕРЕРАБОТКИ МАЗУТА И ТЯЖЕЛОГО НЕФТЯНОГО СЫРЬЯ В ДИСТИЛЛЯТНЫЕ ФРАКЦИИ | 2016 |
|
RU2624864C1 |
| Способ получения наноструктурированного материала для анодов металл-ионных аккумуляторов | 2020 |
|
RU2751131C1 |
| Способ формирования и состав противотурбулентной присадки | 2015 |
|
RU2607914C1 |
Предложен способ получения массивного катализатора гидропереработки нефтяных фракций на основе крупнодисперсного коммерческого порошка дисульфида молибдена, где крупнодисперсный коммерческий порошок дисульфида молибдена измельчают до размеров 12-55 нм в условиях механоактивации в среде жидкого аргона в течение 8 часов. Технический результат - упрощение технологии процесса; повышение экологического уровня его исполнения; повышение химической устойчивости полученного предлагаемым способом катализатора к деградации при взаимодействии с компонентами окружающей среды, на его поверхности в течение длительного времени, не образуя сильно кислотные компоненты. 4 пр., 3 табл., 4 ил.
Способ получения массивного катализатора гидропереработки нефтяных фракций на основе крупнодисперсного коммерческого порошка дисульфида молибдена, отличающийся тем, что крупнодисперсный коммерческий порошок дисульфида молибдена измельчают до размеров 12-55 нм в условиях механоактивации в среде жидкого аргона в течение 8 часов.
| АКИМОВ А.С., ДИССЕРТАЦИЯ НА СОИСКАНИЕ УЧЕНОЙ СТЕПЕНИ КАНДИДАТА ХИМИЧЕСКИХ НАУК: "ГИДРОДЕСУЛЬФИРОВАНИЕ СЕРНИСТЫХ СОЕДИНЕНИЙ ДИЗЕЛЬНЫХ ФРАКЦИЙ И МОДЕЛЬНЫХ СОЕДИНЕНИЙ В ПРИСУТСТВИИ МАССИВНЫХ СУЛЬФИДНЫХ КАТАЛИЗАТОРОВ", СТР | |||
| Аппарат для испытания прессованных хлебопекарных дрожжей | 1921 |
|
SU117A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Катализатор процесса облагораживания углеводородного сырья и способ его приготовления | 2017 |
|
RU2659076C1 |
| WO 2011036862 A1, 31.03.2011 | |||
| US 5244858 A1, 14.09.1993. | |||
Авторы
Даты
2020-06-23—Публикация
2019-06-03—Подача