Область техники, к которой относится изобретение
Настоящее изобретение относится к области биотехнологии. Изобретение, в частности, относится к пептиду, обладающему высокой аффинностью к белку PD-L1, и к его применению.
Предшествующий уровень техники
Опухоль является серьезным заболеванием, которое угрожает здоровью человека, и трудно осуществить его эффективное предотвращение. В настоящее время основные способы лечения опухолей включают лучевую терапию, химиотерапию и хирургическое лечение, но их терапевтический эффект неудовлетворителен, а 5-летняя выживаемость после операции является низкой. В настоящее время разработка эффективного лекарственного средства для лечения опухолей является актуальной темой в исследованиях рака. В последние годы терапия с использованием контрольных точек иммунитета, представленная анти-PD-1/PD-L1, была исследована как новый подход к лечению опухолей. Три препарата антител к PD-1/PD-L1 были одобрены Управлением по контролю продуктов питания и лекарственных средств США (FDA) для клинического применения. Хотя эти лекарства имеют определенные эффекты, у них есть недостатки, такие как низкая эффективность, побочные эффекты и нецелевое связывание. Поэтому необходимо разработать лекарство, которое будет эффективным, действующим в течение длительного времени и обладающим широким спектром терапевтических эффектов.
Изложение сущности изобретения
Целевой пептид по изобретению получали путем химического синтеза и очистки. Константу диссоциации между пептидом и белком PD-L1 определяли с помощью ELISA, и определяли блокирующий эффект пептида в отношении сигнального пути PD-1/PD-L1. Аффинность пептида к белку PD-L1, экспрессируемому на поверхности опухолевых клеток, определяли проточной цитометрией. Наконец, пептид применяли на модели опухоли мыши, и потенциальная ценность пептида при лечении опухоли была подтверждена изменениями размера опухоли и продолжительности выживания мышей.
Целью настоящего изобретения является обеспечение пептида, обладающего высокой аффинностью связывания с белком PD-L1, и применение пептида при лечении опухоли.
Настоящее изобретение относится к пептиду, обладающему высокой аффинностью к белку PD-L1 человека (обозначенному как PPLC), где пептид имеет аминокислотную последовательность, как указано в SEQ ID NO: 1. Пептид имеет следующие функциональные характеристики: (1) высокую аффинность к белку PD-L1 человека с константой диссоциации Kd 0,75 мкМ (значение Kd указывает концентрацию лиганда, когда половина рецепторов связана с лигандом, и чем меньше значение Kd, тем выше аффинность рецептора в отношении лиганда); (2) он может эффективно блокировать аффинность белка PD-1/PD-L1; (3) он может эффективно связываться с белком PD-L1, экспрессируемым на поверхности клетки; (4) инфузия пептида животным с опухолью позволяет эффективно ингибировать рост опухоли и увеличивать продолжительность выживания животных.
Настоящее изобретение также относится к гену, кодирующему пептид, обладающий высокой аффинностью к человеческому белку PD-L1 (состоящему из вырожденных кодонов соответствующих аминокислот), где ген имеет нуклеотидную последовательность, как указано в SEQ ID NO: 2.
Настоящее изобретение также обеспечивает биотехнологическими средствами серию пептидных последовательностей, имеющих ту же функцию, что и пептид, представленный SEQ ID NO: 1, где пептидные последовательности в основном включают SEQ ID NO: 3 и SEQ ID NO: 4.
Настоящее изобретение также относится к пептиду, содержащему аминокислотные последовательности пептидов, обладающих высокой аффинностью к белку PD-L1, как установлено в SEQ ID NO: 1, SEQ ID NO: 3 и SEQ ID NO: 4, где пептид представляет собой однократно или многократно повторяемую тандемную или разветвленную молекулярную последовательность пептидной природы, и молекулу, включающую эти последовательности как коровые (т.е. имеющую гомологию более 70%), где молекула имеет аминокислотную последовательность, установленную в SEQ ID NO: 5.
Настоящее изобретение также обеспечивает пептид, модифицированный биологической или химической группой, включающий пептид SEQ ID NO: 1, SEQ ID NO: 3 или SEQ ID NO: 4, обладающие высокой аффинностью к белку PD-L1, в виде коровой последовательности, а его C-концевая группа (N-концевая группа или группа боковой цепи) связана с антигеном или лекарственным средством, или модифицирована ПЭГ, или ковалентно модифицирована другими молекулярными группами.
Настоящее изобретение также относится к модифицированному пептиду, включающему вышеуказанный пептид, обладающий высокой аффинностью к белку PD-L1, который помечен флуорофором FITC, изотопом, хемилюминесцентной группой или ферментным реагентом, и модифицированный пептид можно использовать для детекции белка PD-L1.
Настоящее изобретение также относится к применению указанного выше пептида, обладающего высокой аффинностью к белку PD-L1, при получении антагониста белка PD-L1.
Настоящее изобретение также относится к применению указанного выше пептида, обладающего высокой аффинностью к белку PD-L1, для приготовления агента для детекции или для клинического анализа экспрессии белка PD-L1.
Настоящее изобретение также обеспечивает применение гена, имеющего нуклеотидную последовательность, как указано в SEQ ID NO: 2, при приготовлении антагониста белка PD-L1 или приготовлении агента для детекции с индикатором белка PD-L1.
Пептид по настоящему изобретению, имеющий аминокислотную последовательность из SEQ ID NO: 1, можно использовать в качестве лекарственного средства-антагониста белка PD-L1. Пептид обладает высокой аффинностью связывания с белком PD-L1, блокирует негативный регуляторный сигнальный путь PD-1/PD-L1 иммунитета человека и, таким образом, активирует иммунитет, инициирует цитотоксический эффект Т-клеток в отношении опухолей, и может использоваться в качестве потенциального препарата для таргетной терапии опухолей. Пептид по настоящему изобретению, имеющий аминокислотную последовательность SEQ ID NO: 3 или SEQ ID NO: 4, также можно использовать в качестве антагониста белка PD-L1. Эти пептиды также обладают высокой аффинностью связывания с белком PD-L1, блокируют аффинность PD-1/PD-L1 и инициируют иммунитет для уничтожения опухолевых клеток.
Анализ аффинности пептида PPLC к белку PD-L1.
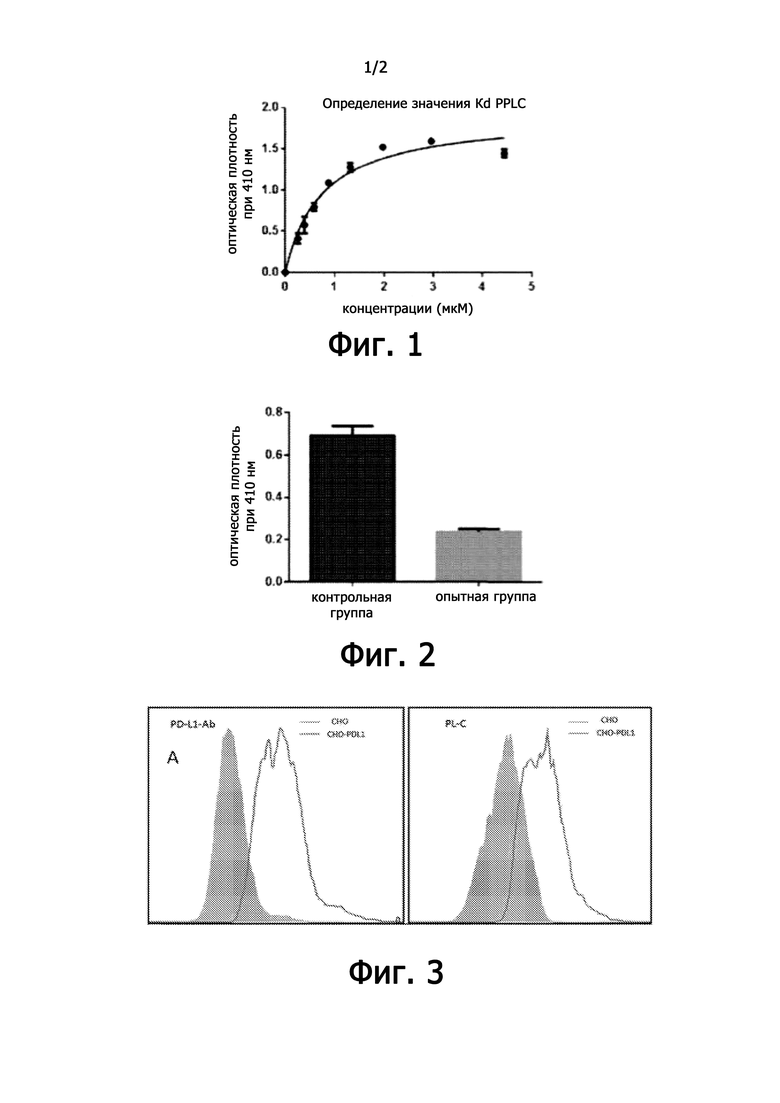
96-луночный планшет для ELISA покрывали 2 мкг/мл белка PD-L1 при 4°С в течение ночи. Различные концентрации пептида PPLC, меченного FITC, добавляли в каждую лунку и инкубировали в течение 1 часа. После инкубации добавляли конъюгированное с пероксидазой хрена анти-FITC антитело, инкубировали в течение 1 часа и затем добавляли окрашивающий раствор ABTS. Величину оптической плотности при 410 нм определяли с использованием ридера для микропланшетов M5, а GraphPad Prism 6 использовали для построения графиков и анализа. Результаты демонстрируют, что пептид PPLC обладает сильной аффинностью к белку PD-L1 с константой диссоциации Kd 0,75 мкМ (фиг. 1).
Анализ конкурентного связывания между пептидом PPLC и белком PD-1 - PD-L1.
96-луночный планшет для ELISA покрывали 2 мкг/мл белка PD-L1 при 4°С в течение ночи. Различные концентрации пептида PPLC и 1 мкг/мл белка PD-1 смешивали и инкубировали совместно. После инкубации в качестве первичного антитела добавляли кроличьи моноклональные антитела против человеческого PD-1, а затем в качестве вторичного антитела добавляли конъюгированное с пероксидазой хрена моноклональное антитело против IgG кроликов. После проявления окраски ABTS измеряли значение оптической плотности при 410 нм с использованием ридера для микропланшетов M5, а GraphPad Prism 6 использовали для построения графиков и анализа. Результаты демонстрируют, что пептид PPLC позволяет эффективно блокировать связывание PD-1/PD-L1 (фиг. 2).
Анализ связывания пептида PPLC с белком PD-L1, экспрессируемым на поверхности клетки.
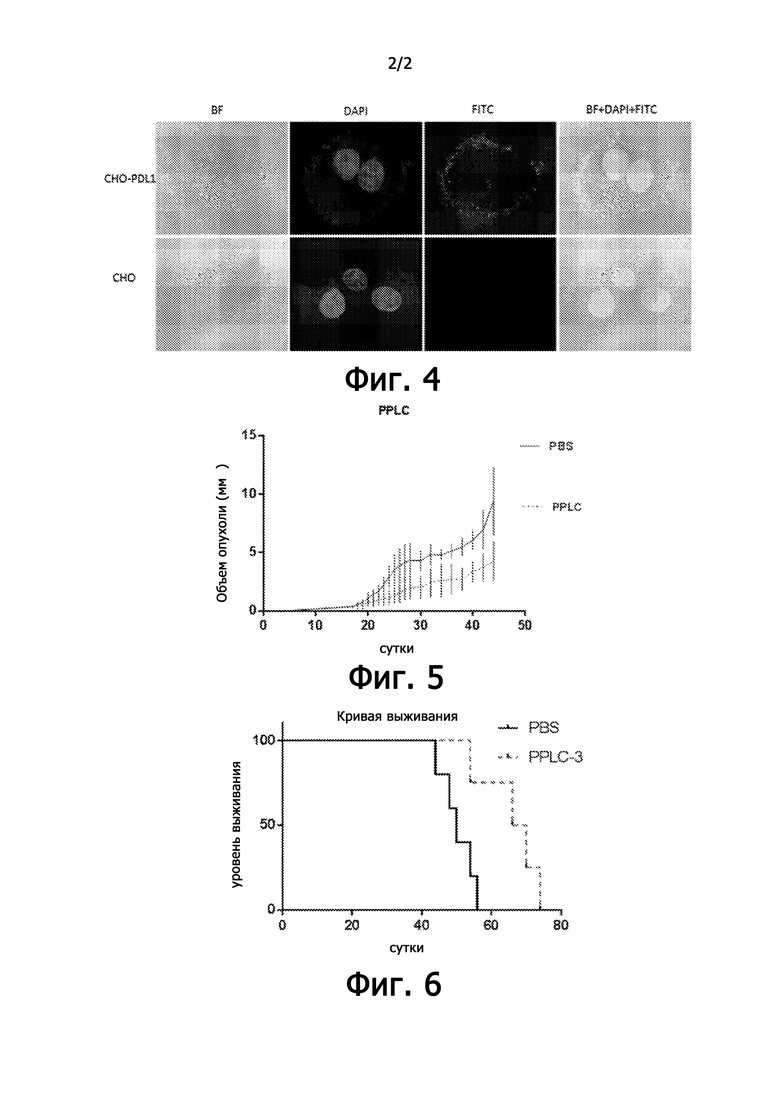
Рекомбинантную плазмиду, экспрессирующую рекомбинантный белок PD-L1 человека, трансфицировали в клеточную линию СНО и инкубировали в течение 36 часов. После инкубации добавляли моноклональное антитело анти-PD-L1 или пептид PPLC, меченный FITC, и инкубировали при 4°C в течение 30 минут. После инкубации проводили проточную цитометрию (фиг. 3). После трансфекции плазмиды клетки дополнительно культивировали в течение 36 часов, а затем добавляли пептид PPLC, меченный FITC, и инкубировали при 37°C в течение 30 минут. После инкубации проводили конфокальную флуоресцентную микроскопию (фиг. 4). Результаты демонстрируют, что пептид PPLC может эффективно связываться с белком PD-L1, экспрессируемым на клеточной поверхности (фиг. 3 и фиг. 4).
Влияние пептида PPLC на объем опухоли на животных моделях опухолей.
Экспериментальные животные были разделены на две группы: группа PBS (фосфатный буферный раствор) и группа PPLC. Опухоли вводили подкожно самкам мышей Balb/c в возрасте 6 недель. Спустя две недели, когда размер опухоли достигал 100 мм3, проводили медикаментозное лечение PPLC. Размер опухоли мыши измеряли ежедневно, и изменение регистрировали. Результаты показывают, что пептид PPLC позволяет значительно снизить скорость роста опухоли мыши (фиг. 5) и увеличить продолжительность выживания мышей (фиг. 6).
Можно видеть, что пептид, обеспеченный в настоящем изобретении, обладает высокой аффинностью к белку PD-L1 и может блокировать аффинность белка PD-1/ PD-L1 у человека. Таким образом, пептид может нарушать иммунную толерантность опухолей, активировать иммунитет, инициировать цитотоксический эффект Т-клеток в отношении опухолей и достигать цели лечения опухолей. Следовательно, пептид можно использовать в качестве лекарственного средства для таргетной терапии опухолей. Поскольку пептид PPLC обладает высокой аффинностью к белку PD-L1, его можно использовать для приготовления зонда для обнаружения белка PD-L1. Когда пептид PPLC мечен флуорофором FITC, изотопом, хемилюминесцентной группой или ферментным реагентом, его можно использовать для количественного, качественного определения, и определения расположения белка PD-L1 в различных биологических образцах и клетках.
Краткое описание чертежей
Фиг. 1 демонстрирует аффинность связывания пептида PPLC с белком PD-L1.
Фиг. 2 демонстрирует блокирование связывания PD-1/PD-L1 белка с помощью PPLC.
Фиг. 3 демонстрирует результаты проточной цитометрии. Левая панель показывает результаты обнаружения моноклонального антитела к PD-L1 (PD-L1-Ab), а правая панель показывает результаты обнаружения пептида PPLC. Серым цветом представлены клетки отрицательного контроля PD-L1, красные и синие линии представляют PDO-L1-позитивные CHO-PDL1-экспрессирующие клетки.
Фиг. 4 демонстрирует результаты флуоресцентного конфокального анализа. Верхняя правая панель демонстрирует результаты, полученные с помощью конфокальной микроскопии, показывающие, что FITC-меченный PPLC обладает высокой аффинностью к PD-L1, экспрессируемому на поверхности клеток CHO.
Фиг. 5 показывает, что пептид PPLC ингибирует рост опухоли у мышей.
Фиг. 6 показывает, что пептид PPLC увеличивает продолжительность выживания мыши.
Подробное описание вариантов осуществления
1. Получение и модификация пептидных последовательностей.
Необходимые пептиды, обладающие аффиностью к белку PD-L1 и блокирующие аффинность PD-1/PD-L1 белка, были искусственно синтезированы химическим способом.
2. Синтез и очистка пептида
Смолу Lys(Dde)-Wang замачивали в ДХМ в течение 10 минут, а затем ДХМ удаляли. В смолу добавляли 25% пиперидин (пиперидин/ ДМФА) с 3-кратным объемом, а затем пиперидин сливали после продувания азотом в течение 20 минут. ДМФ добавляли и продували в течение 1 мин. После 6 циклов ДМФА удаляли, и было обнаружено, что смола получала синюю окраску от нингидрина. Продукт является смолой H-Lys(Dde)-Wang. К смоле добавляли три эквивалента Fmoc-Val-OH, HATU, диизопропилэтиламин в ДМФА. После продувки азотом в течение 20 минут реакционный раствор ДМФА удаляли. Добавляли ДМФА, и продували азотом в течение 1 минуты перед удалением реагента. После 3 циклов смола была признана очищенной по реакции с нингидрином. Продукт представляет собой смолу Fmoc-Val-Lys(Dde)-Wang. Неочищенный продукт получали тем же способом. Очистку проводили на колонке Hanbang YCM C18 с использованием ацетонитрила и воды Milli-Q. Таким способом был получен пептид, имеющий высокую специфичность и высокую активность.
3. Аффинность пептида PPLC к белку PD-L1 и результаты экспериментов на животных
(1) Аффинность PPLC к белку PD-L1.
96-луночный планшет для ELISA покрывали 2 мкг/мл белка PD-L1 при 4°С в течение ночи. Различные концентрации пептида PPLC, меченного FITC, добавляли в каждую лунку и инкубировали в течение 1 часа. После инкубации добавляли конъюгированное с пероксидазой хрена анти-FITC антитело, инкубировали в течение 1 часа и затем добавляли окрашивающий раствор ABTS. Величину ОП при 410 нм измеряли с использованием ридера для микропланшетов M5, а GraphPad Prism 6 использовали для построения графиков и анализа. Результаты показывают, что пептид PPLC обладает высокой аффинностью связывания с белком PD-L1 с константой диссоциации Kd 0,75 мкМ.
(2) Анализ конкурентного связывания между пептидом PPLC и PD-1 - PD-L1 белком.
96-луночный планшет для ELISA покрывали 2 мкг/мл белка PD-L1 при 4°С в течение ночи. Различные концентрации пептида PPLC пептида и 1 мкг/мл белка PD-1 смешивали и инкубировали совместно. После инкубации в качестве первичного антитела добавляли кроличьи моноклональные антитела против человеческого PD-1, а затем в качестве вторичного антитела добавляли конъюгированное с пероксидазой хрена моноклональное антитело против IgG кроликов. После проявления цвета ABTS измеряли значение оптической плотности при 410 нм с использованием ридера для микропланшетов M5, а GraphPad Prism 6 использовали для построения графиков и анализа. Результаты показывают, что пептид PPLC может эффективно блокировать связывание PD-1/PD-L1.
(3) Анализ связывания пептида PPLC с белком PD-L1, экспрессируемым на клеточной поверхности.
Рекомбинантную плазмиду, экспрессирующую рекомбинантный белок PD-L1 человека, трансфицировали в клеточную линию СНО и инкубировали в течение 36 часов. После инкубации добавляли моноклональное антитело анти-PD-L1 или пептид PPLC, меченный FITC, и инкубировали при 4°C в течение 30 минут. После инкубации проводили проточную цитометрию. После трансфекции плазмиды клетки дополнительно культивировали в течение 36 часов, а затем добавляли пептид PPLC, меченный FITC, и инкубировали при 37°C в течение 30 минут. После инкубации проводили конфокальную флуоресцентную детекцию. Результаты показывают, что пептид PPLC может эффективно связываться с белком PD-L1, экспрессируемым на клеточной поверхности.
(4) Влияние пептида PPLC на объем опухоли на модели опухоли животного.
Экспериментальные животные были разделены на две группы: группа PBS (фосфатный буферный раствор) и группа PPLC. Опухоли вводили подкожно самкам мышей Balb/c. Спустя две недели, когда размер опухоли достигал 100 мм3, проводили медикаментозное лечение PPLC. Размер опухоли мыши измеряли ежедневно, и изменение регистрировали. Результаты демонстрируют, что пептид PPLC позволяет значительно снизить скорость роста опухоли мыши и увеличить продолжительность выживания мышей.
Как показано на фиг. 1-6, пептид PPLC обладает высокой аффинностью связывания с белком PD-L1 и может блокировать аффинность PD-1/PD-L1 белка на молекулярном уровне. Результаты на животных показали, что размер опухолей у мышей, получавших пептид PPLC, был значительно меньше, чем у контрольной группы. Вышеуказанные результаты показывают, что пептид PPLC может нарушать иммунную толерантность к опухоли, улучшать уничтожение опухолевых клеток Т-клетками и, таким образом, достигать цели лечения опухолей.
4. Промышленная применимость
Иммунотерапия опухолей - это новый метод лечения опухолей, разработанный в последние годы.
Терапия на основе блокады иммунной контрольной точки, представленной PD-1/PD-L1 белком, является важным компонентом иммунотерапии опухолей. В настоящее время некоторые препараты на основе антител к PD-1/PD-L1 были одобрены FDA и показали хорошие результаты в клиническом применении и при лечении таких заболеваний, как меланома. Однако, в то же время, терапия антителами также сталкивается со многими проблемами, такими как высокая иммуногенность, высокая стоимость, серьезные побочные эффекты и нецелевое связывание. Разработка противоопухолевого препарата с целевым эффектом и малой иммуногенностью является важным направлением развития иммунологии сегодня. Пептид, обладающий высокой аффинностью связывания с белком PD-L1, обеспеченный в настоящем документе, позволяет ингибировать связывание PD-1/PD-L1 белка, нарушать иммунную толерантность опухоли и значительно ингибировать рост опухолевых клеток. Таким образом, пептид по настоящему изобретению можно использовать в качестве потенциального лекарственного средства для таргетной терапии опухолей. Кроме того, модифицированный пептид PPLC можно использовать в качестве реагента для обнаружения экспрессии человеческого белка PD-L1.
--->
SEQUENCE LISTING <110> ZHU Naishuo
<120> PEPTIDE HAVING HIGH AFFINITY FOR PD-L1 PROTEIN AND USE THEREOF
<130> 001
<160> 5
<170> Patentln version 3.3
<210>
<211>
<212>
<213> 1
12
PRT
Artificial Sequence
<400> 1
Val Ser Val Ser His Phe Gln Lys Val Trp Val Val
1 5 10
<210>
<211>
<212>
<213> 2
45
DNA
Artificial Sequence
<400> 2
gtgagtgtgtcgcattttcagaaggtttgggttgtgggtggaggt 45
<210>
<211>
<212>
<213> 3
12
PRT
Artificial Sequence
<400> 3
His Glu Ser Trp Leu Pro Ala Tyr Val Leu Gly Ser
1 5 10
<210>
<211>
<212>
<213> 4
12
PRT
Artificial Sequence
<400> 4
His Thr Ser Trp Ile Leu Tyr Gly Glu Thr Gly Trp
1 5 10
<210>
<211>
<212>
<213> 5
40
PRT
Artificial Sequence
<400> 5
Val Ser Val Ser His Phe Gln Lys Val Trp Val Val Asp Met His Glu
Ser Trp Leu Pro Ala Tyr Val Leu Gly Ser Asp Met His Thr Ser Trp
20 25 30
Ile Leu Tyr Gly Glu Thr Gly Trp
35 40
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА К БЕЛКУ ПРОГРАММИРУЕМОЙ СМЕРТИ 1(PD-1) | 2016 |
|
RU2757316C2 |
| Антитело против PD-1 и его применение | 2017 |
|
RU2739610C1 |
| ГУМАНИЗИРОВАННОЕ АНТИТЕЛО ПРОТИВ PD-1 И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2803460C2 |
| НОВЫЕ АНТИ-PD-L1 АНТИТЕЛА | 2017 |
|
RU2776121C2 |
| НОВЫЕ АНТИ-PD-L1 АНТИТЕЛА | 2017 |
|
RU2744959C2 |
| НОВЫЕ АНТИ-PD-1 АНТИТЕЛА | 2016 |
|
RU2729830C2 |
| НОВЫЕ АНТИТЕЛА ПРОТИВ PD-L1 | 2016 |
|
RU2736151C2 |
| МУЛЬТИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2018 |
|
RU2837770C2 |
| НОВАЯ КОМБИНАЦИЯ ДЛЯ ПРИМЕНЕНИЯ ПРИ ЛЕЧЕНИИ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ | 2016 |
|
RU2742494C2 |
| СЛИТЫЙ БЕЛОК, СОДЕРЖАЩИЙ РЕЦЕПТОР TGF-БЕТА, И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2776204C1 |
Настоящее изобретение относится к области биотехнологии, конкретно к связывающим PD-L1 пептидам, и может быть использовано для получения антагониста белка PD-L1, для детекции или для клинического анализа экспрессии белка PD-L1. Изобретение обеспечивает получение пептида, способного связываться с человеческим PD-L1, с высокой аффинностью. 7 н.п. ф-лы, 6 ил.
1. Пептид, обладающий высокой аффинностью к человеческому белку PD-L1, характеризующийся аминокислотной последовательностью SEQ ID NO: 1, SEQ ID NO: 3 или SEQ ID NO: 4, или тандемный или разветвленный пептид с одним или несколькими повторами из SEQ ID NO: 1, SEQ ID NO: 3 или SEQ ID NO: 4, имеющий аминокислотную последовательность SEQ ID NO: 5.
2. Ген, кодирующий пептид, обладающий высокой аффинностью к человеческому белку PD-L1, по п. 1, где ген имеет нуклеотидную последовательность, как указано в SEQ ID NO: 2.
3. Пептид, модифицированный биологической или химической группой, включающий пептид, обладающий высокой аффинностью к человеческому белку PD-L1, по п. 1 в качестве коровой последовательности, и где его С-концевая группа, N-концевая группа или группа боковой цепи модифицирована ПЭГ или ковалентно модифицирована другими молекулярными группами.
4. Модифицированный пептид, включающий пептид, обладающий высокой аффинностью к человеческому белку PD-L1, по п. 1, который помечен флуорофором FITC, изотопом, хемилюминесцентной группой или ферментным реагентом, и где модифицированный пептид используется для детекции белка PD-L1.
5. Применение пептида, обладающего высокой аффинностью к человеческому белку PD-L1, по п. 1 для получения антагониста белка PD-L1.
6. Применение пептида, обладающего высокой аффинностью к человеческому белку PD-L1, по п. 1 для приготовления агента для детекции или для клинического анализа экспрессии белка PD-L1.
7. Применение гена, кодирующего пептид, обладающий высокой аффинностью к человеческому белку PD-L1, по п. 2 для получения антагониста белка PD-L1 или получения агента для детекции с индикатором белка PD-L1.
| CN 103936835 A, 23.07.2014 | |||
| WO 2016086021 А1, 02.06.2016 | |||
| EA 201490369 A1, 29.08.2014. |
Авторы
Даты
2020-07-07—Публикация
2018-01-25—Подача