Изобретение относится к биотехнологии, а именно к способу выявления кДНК вируса SARS-CoV-2 и может найти применение в медицине при лабораторной диагностике COVID-19. Вирус SARS-CoV-2 относится к группе коронавирусов и является возбудителем потенциально тяжелой острой респираторной инфекции COVID-19. Для лабораторной диагностики COVID-19 может быть использован иммунологический способ, основанный на выявлении антител к вирусу, описанный в статье [Li Z. et al. Development and Clinical Application of A Rapid IgM-IgG Combined Antibody Test for SARS-CoV-2 Infection Diagnosis // Journal of Medical Virology. - 2020.]. Способ обладает высокой специфичностью, но синтез антител в организме отстает от размножения вирусов, что часто не позволяет своевременно выявить заболевание. Другим надежным способом выявления вируса является способ секвенирования нового поколения (next generation sequencing, NGS), описанный в статье [Nasir J. A. et al. Rapid Design of a Bait Capture Platform for Culture-and Amplification-Free Next-Generation Sequencing of SARS-CoV-2. - 2020.]. Способ надежен, но приборы для его осуществления недостаточно распространены, что в условиях эпидемии делает его малоприменимым. Наиболее распространенным и удобным способом лабораторной диагностики COVID-19 является выявление кДНК вируса SARS-CoV-2 при помощи набора синтетических олигонуклеотидных праймеров и реакции ПЦР в реальном времени. Этот способ рекомендован центром по контролю и профилактике заболеваний США (CDC) и представлен на их сайте [https://www.cdc.gov/coronavirus/2019-ncov/lab/rt-pcr-detection-instructions.html]. Именно его мы выбрали в качестве прототипа.
Способ предусматривает, что предварительно из образца биоматериала выделена тотальная РНК одним из рекомендованных наборов реактивов. Затем, с помощью рекомендованных китов, осуществляется синтез первой цепи кДНК методом обратной транскрипции. Непосредственное выявление кДНК вируса SARS-CoV-2 проводят с использованием набора синтетических праймеров и флуоресцентных зондов в реакции ПЦР в реальном времени. Способ позволяет быстро, в течение часа-полутора получить результат. При осуществлении способа ставятся положительный и отрицательный контроли, что позволяет снизить вероятность получения ложноположительного и ложноотрицательного результатов.
Способ заключается в следующем. Используют набор синтетических олигонуклеотидных праймеров и зондов следующего состава, указанного в Табл. 1.
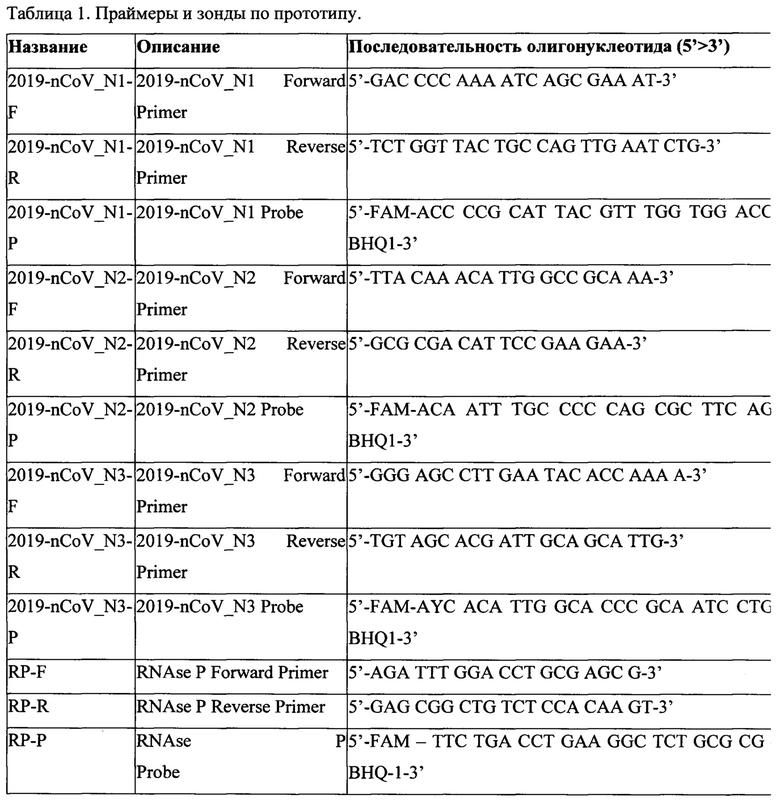
Праймеры гомологичны трем локусам гена N вируса SARS-CoV-2, а также гену рибонуклеазы человека. Меченые зонды служат для регистрации реакции TaqMan ПЦР в реальном времени. Ставят пробы, в число которых входят исследуемый образец, отрицательный контроль (без наличия ДНК), положительный контроль (содержащий кДНК вируса) с ожидаемым значением порогового цикла. С пробами проводят реакцию ПЦР в реальном времени. О наличии вируса SARS-CoV-2 в исследуемой пробе судят по следующим критериям. Кривая амплификации с праймерами на рибонуклеазу человека в исследуемой пробе и положительном контроле должна пересекать пороговую линию до 35-го цикла, все отрицательные контроли со всеми праймерами не должны пересекать пороговую линию, положительный контроль и исследуемая проба с праймерами на гены вируса должны пересекать пороговую линию на ожидаемом цикле.
Этот способ быстрый (до 2-х часов) и производителен. Однако, на наш взгляд, обладает рядом недостатков. Праймеры на целевую молекулы сконструированы на один ген. Из-за склонности вируса к мутированию это может угрожать надежности способа. Размеры ампликонов в прототипе 71 п.н., 66 п.н. и 71 п.н. Их размер не дает возможности различать их по подвижности во время электрофореза в 1-1,5% агарозном геле. Впрочем, метод ПЦР в реальном времени, для которого был осуществлен дизайн праймеров и не рассчитан на определения размеров ПЦР-продукта. Он предназначен для определения числа копий целевой молекулы. Но для цели качественного выявления вируса в биологическом материале использование прибора для проведения ПЦР в реальном времени нам представляется избыточным. Достаточно более распространенных и менее требовательных простых термоциклеров. В условиях пандемии это может стать важным для масштабных анализов при лечебных и карантинных мероприятиях.
Задача нашего изобретения - сделать способ более доступным и точным. Поставленная цель достигается тем, что мы предлагаем использовать синтетические олигонуклеотидные праймеры следующих последовательностей:
SEQ ID NO: 1-5' cagtctgtaccgtctgcgg 3',
SEQ ID NO: 2-5' cagtactagtgcctgtgccg 3'
SEQ ID NO: 3-5' ggtggaccctcagattcaactgg 3',
SEQ ID NO: 4-5' ttttaccgtcaccaccacgaa 3'
SEQ ID NO: 5-5' cgcattggcatggaagtcac 3',
SEQ ID NO: 6-5' tgtctctgcggtaaggcttg 3'.
Мы подобрали праймеры таким образом, чтобы реакция ПЦР могла быть осуществлена в простом термоциклере, а результат мог оценивается при проведении электрофоретического разделения ампликонов. Размер полученных ампликонов (158 п.н., 250 п.н. и 203 п.н.) дает четкие, хорошо различаемые по подвижности полосы на электрофореграмме, позволяет легко осуществлять фотодокументацию результатов. Размеры ампликонов позволяют надежно и специфично выявлять кДНК коронавируса SARS-CoV-2. Две пары праймеров (SEQ ID NO: 3 и SEQ ID NO: 4), (SEQ ID NO: 5 и SEQ ID NO: 6) отжигаются на гене N, а одна пара (SEQ ID NO: 1 и SEQ ID NO: 2) - на гене orf1ab. Для контроля на качество исследуемого материала мы используем праймеры к гену GAPDH человека (прямой - 5'-AGATCCCTCCAAAATCAAGTGG-3', обратный - 5'-GGCAGAGATGATGACCCTTTT-3'), с длиной ампликона 130 п.н. Этот ген обладает высокой экспрессией и часто используется для нормализации результатов по определению уровней транскрипции.
Заявленный способ реализуется следующим образом. Материалом исследования служит кДНК, полученная предварительно из биологического материала пациента путем выделения тотальной РНК и проведения реакции обратной транскрипции известными наборами реактивов. Олигонуклеотидные праймеры подобраны таким образом, чтобы отжиг мог быть осуществлен при 60°С, два ампликона синтезировались на гене N, а один -на гене orf1ab, длина ПЦР-продуктов находилась в диапазоне 150-250 п.н. В результате мы подобрали следующие олигонуклеотидные праймеры (Табл. 2).

Каждый исследуемый образец кДНК амплифицируют с каждой из трех пар праймеров. Кроме того, каждый образец амплифицируют с парой праймеров на ген GAPDH человека для того, чтобы убедиться в корректном выделении РНК из биологического материала и проведении реакции обратной транскрипции. Это позволит избежать ложноотрицательного результата. К каждой паре праймеров ставят отрицательный контроль, без матрицы, для исключения ложноположительных результатов за счет контаминации реактивов. После проведения ПЦР образцы наносят в 1,5% агарозный гель и проводят электрофорез в присутствии бромистого этидия. Позитивный результат выявления кДНК вируса SARS-CoV-2 следует, если амплификация исследуемого образца кДНК с парами праймеров (SEQ ID NO: 1 и SEQ ID NO: 2), (SEQ ID NO: 3 и SEQ ID NO: 4), (SEQ ID NO: 5 и SEQ ID NO: 6) приводит к синтезу ПЦР-продуктов длиной 158, 250 и 203 п.н. соответственно. При этом в пробах отрицательных контролей должны отсутствовать ПЦР-продукты этих размеров. Отрицательный результат выявления кДНК вируса SARS-CoV-2 следует, если амплификация исследуемого образца кДНК с парами праймеров (SEQ ID NO: 1 и SEQ ID NO: 2), (SEQ ID NO: 3 и SEQ ID NO: 4), (SEQ ID NO: 5 и SEQ ID NO: 6) не приводит к синтезу ПЦР-продуктов длиной 158, 250 и 203 п.н. соответственно. При этом в пробе с праймерами на ген GAPDH человека должен амплифицироваться ПЦР-продукт соответствующей длины.
Изобретение иллюстрируется следующими примерами конкретного выполнения способа.
Пример 1.
У больной П. из цельной крови была выделена тотальная РНК. После проведения реакции обратной транскрипции образец направлен для выявления кДНК вируса SARS-CoV-2. От момента завершения синтеза первой цепи кДНК до постановки реакции ПЦР образец хранили на льду.
Поставили полимеразную цепную реакцию в пробах следующего состава (Табл. 3).
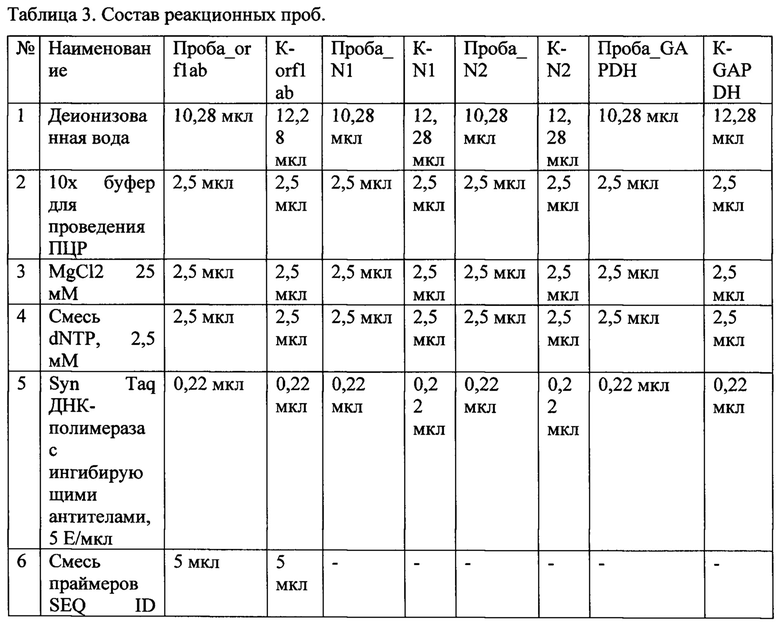
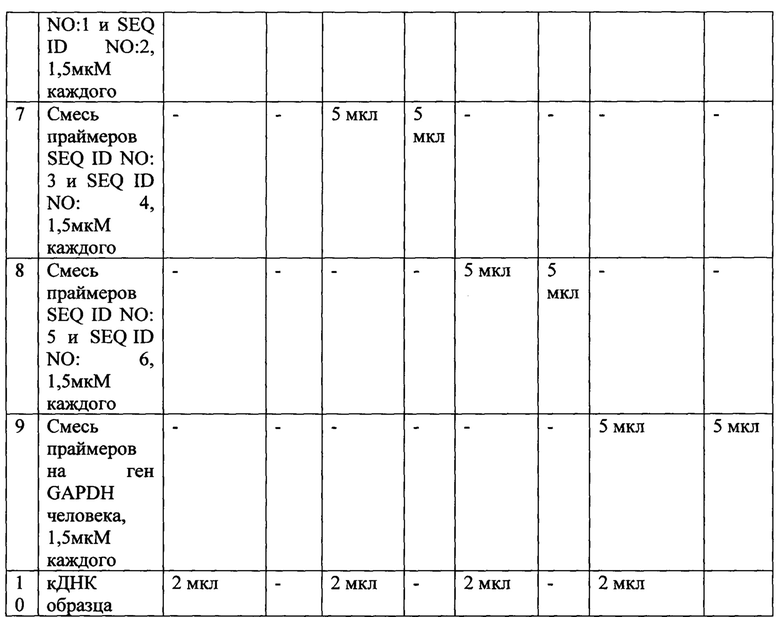
Режим амплификации: 95°С - 5 мин, (95°С - 10 сек, 60°С - 30 сек) х 40, 72°С - 10 мин. После амплификации образцы в объеме 5 мкл нанесли в лунки 1,5% агарозного геля с бромидом этидия и провели электрофорез. Схема нанесения образцов в лунки геля приведена в таблице 4.

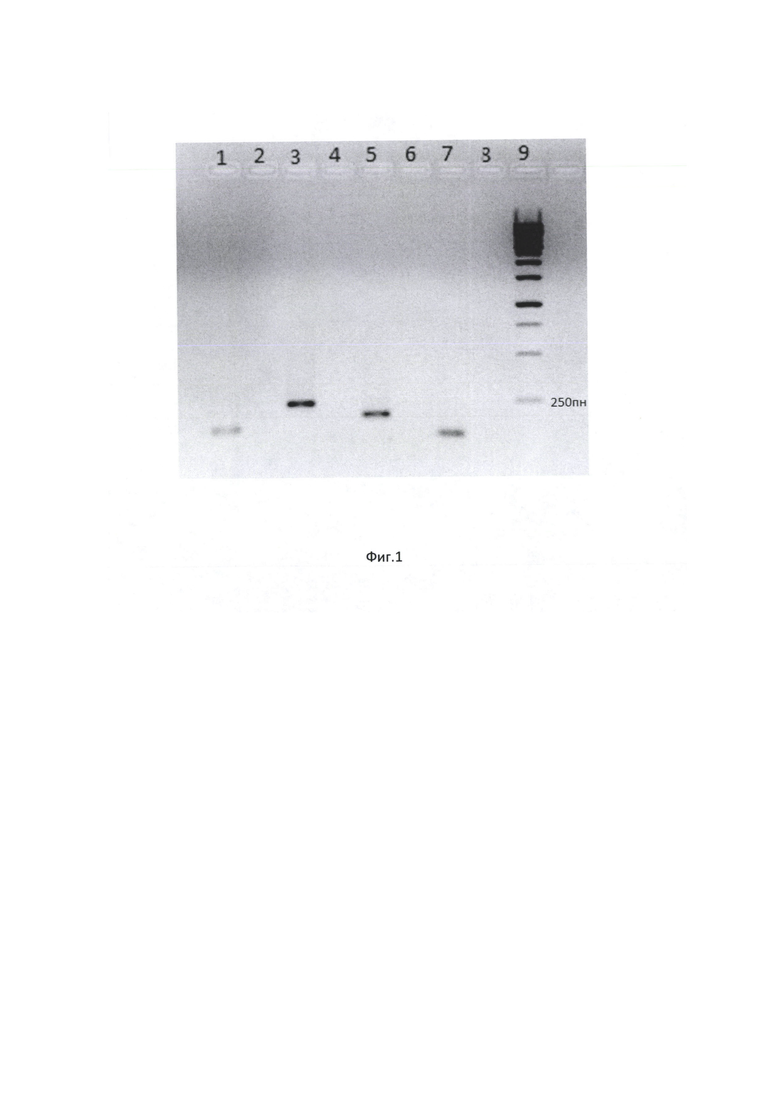
По окончании электрофореза гель поместили в трансиллюминатор и сфотографировали.
На электрофореграмме (Фиг. 1) мы наблюдали наличие ПЦР-продуктов соответствующих длин в лунках 1, 3, 5, 7. И одновременно отсутствие ПЦР-продуктов в лунках с отрицательным контролем - 2, 4, 6 и 8. На основании этого мы сделали вывод о наличии в организме П. коронавируса SARS-CoV-2. В дальнейшем на основании клинических и лабораторных показателей П. был поставлен диагноз COVID-19.
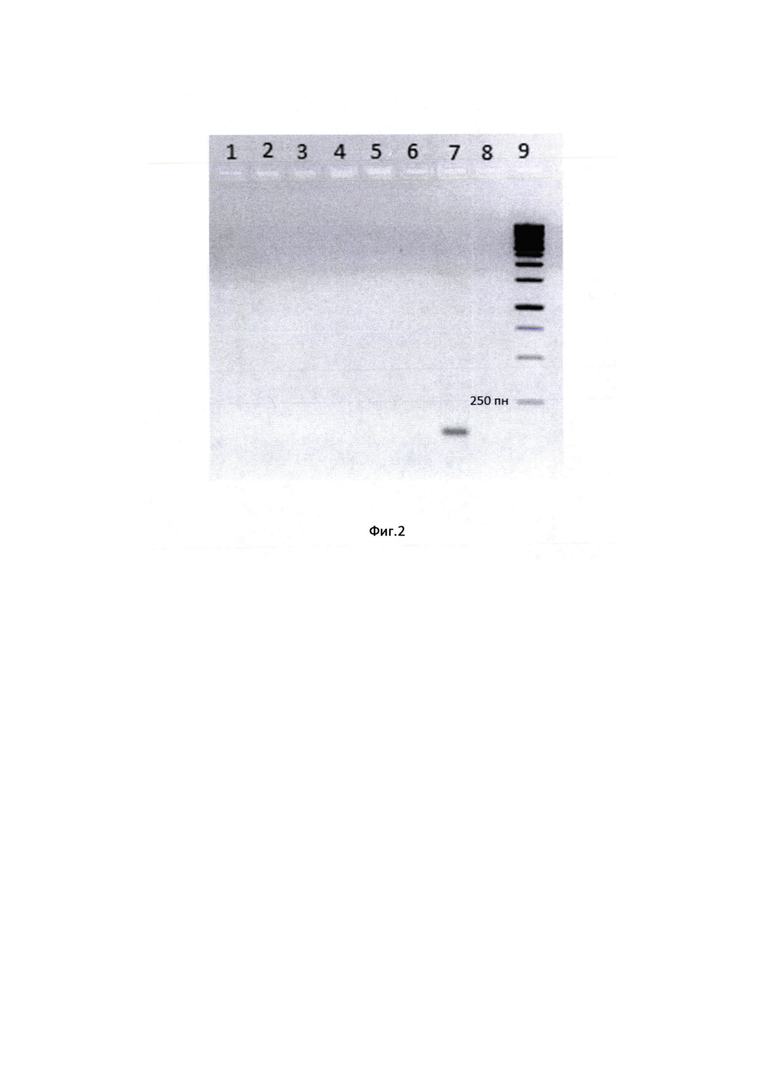
Пример 2. У пациента С. с симптомами ОРЗ и находящегося в карантине взят образец эпителия мазком из ротоглотки. Из биоматериала была выделена тотальная РНК. После проведения реакции обратной транскрипции образец направлен для выявления кДНК вируса SARS-CoV-2. Провели полимеразную цепную реакцию, электрофорез образцов и фотографирование геля, как описано в примере 1.
На электрофореграмме (Фиг. 2) мы не наблюдали амплификации фрагментов целевой молекулы. Тем не менее праймеры на ген GAPDH человека дали ПЦР-продукт соответствующей длины. Это значит, что процедуры выделения РНК из биоматериала и синтеза кДНК проведены корректно, но вируса SARS-CoV-2 в биоматериале не выявлено. Впоследствии С. был отпущен из карантина, у него на обнаружен COVID-19.
Таким образом, способ позволяет выявлять и идентифицировать наличие вируса SARS-CoV-2 в биологическом материале по наличию и длине ампликонов.
--->
Перечень последовательностей
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Набор олигонуклеотидов и способ мультиплексной полимеразной цепной реакции в режиме реального времени для выявления РНК SARS-CoV-2 | 2021 |
|
RU2752902C1 |
| Способ пробоподготовки образцов изолятов коронавируса SARS-CoV-2 и олигонуклеотидные праймеры для его реализации | 2021 |
|
RU2762759C1 |
| Набор для выявления коронавируса SARS-CoV-2 | 2021 |
|
RU2765497C1 |
| Тест-система и способ для выявления РНК коронавируса SARS-COV-2, вируса-возбудителя коронавирусного заболевания 2019 COVID-19, методом полимеразной цепной реакции в режиме реального времени (Варианты) | 2020 |
|
RU2731390C1 |
| Набор олигодезоксирибонуклетидных праймеров и флуоресцентно-меченого зонда для идентификации РНК коронавирусов человека SARS и 2019-nCoV методом ОТ-ПЦР с гибридизационно-флуоресцентной детекцией в режиме реального времени | 2020 |
|
RU2733665C1 |
| Олигонуклеотиды для определения мутации S:L452R SARS-CoV-2 | 2022 |
|
RU2795018C1 |
| НАБОР ПРАЙМЕРОВ ДЛЯ ОБНАРУЖЕНИЯ НУКЛЕИНОВЫХ КИСЛОТ, НАБОР ЗОНДОВ И НАБОР ДЛЯ ВЫЯВЛЕНИЯ НОВОГО ТИПА КОРОНАВИРУСА COVID-19 И СПОСОБ ЕГО ВЫЯВЛЕНИЯ | 2021 |
|
RU2772130C1 |
| Олигонуклеотиды для определения мутации S:N501Y SARS-CoV-2 | 2022 |
|
RU2791958C1 |
| НАБОР РЕАГЕНТОВ ДЛЯ ОБНАРУЖЕНИЯ РНК SARS-COV-2 МЕТОДОМ ПЕТЛЕВОЙ ИЗОТЕРМИЧЕСКОЙ АМПЛИФИКАЦИИ В РЕАЛЬНОМ ВРЕМЕНИ (КОВИГЕН-LAMP) | 2022 |
|
RU2779189C1 |
| Тест-система для выявления SARS-CoV-2, Influenza virus A, Influenza virus B методом одношаговой полимеразной цепной реакции с обратной транскрипцией | 2021 |
|
RU2761481C1 |
Изобретение относится к биотехнологии. Описан способ выявления кДНК вируса SARS-CoV-2. Использование специфичных праймеров позволяет выявлять генетический материал вируса SARS-CoV-2 в исследуемых образцах методом полимеразной цепной реакции (ПЦР). Одна пара праймеров подобрана к гену orf1ab. Их последовательности: SEQ ID NO: 1-5' cagtctgtaccgtctgcgg 3', SEQ ID NO: 2-5' cagtactagtgcctgtgccg 3'. Длина ампликона составляет 158 п.н. Две пары праймеров подобраны к гену N. Их последовательности и длина ампликонов: SEQ ID NO: 3-5' ggtggaccctcagattcaactgg 3', SEQ ID NO: 4-5' ttttaccgtcaccaccacgaa 3', длина ПЦР-продукта 250 п.н.; SEQ ID NO: 5-5' cgcattggcatggaagtcac 3', SEQ ID NO: 6-5' tgtctctgcggtaaggcttg 3', длина ПЦР-продукта 203 п.н. После проведения ПЦР продукты реакции разделяют в электрофорезе с маркером длины. По наличию и длине ампликонов способ позволяет выявлять и идентифицировать наличие вируса SARS-CoV-2 в биологическом материале. Изобретение может найти применение в медицине при лабораторной диагностике COVID-19. 2 ил., 4 табл., 2 пр.
Способ выявления кДНК коронавируса SARS-CoV-2 с помощью синтетических олигонуклеотидных праймеров в полимеразной цепной реакции, отличающийся тем, что праймеры имеют нуклеотидные последовательности:
SEQ ID NO: 1-5' cagtctgtaccgtctgcgg 3',
SEQ ID NO: 2-5' cagtactagtgcctgtgccg 3'
SEQ ID NO: 3-5' ggtggaccctcagattcaactgg 3',
SEQ ID NO: 4-5' ttttaccgtcaccaccacgaa 3'
SEQ ID NO: 5-5' cgcattggcatggaagtcac 3',
SEQ ID NO: 6-5' tgtctctgcggtaaggcttg 3',
и гомологичны консервативным участкам генов orf1ab и N, а в результате проведения ПЦР амплифицируются фрагменты, соответствующие размерам 158 п.н., 250 п.н. и 203 п.н.
| CN 105018644 B, 29.05.2018 | |||
| СПОСОБЫ ПРОГНОЗИРОВАНИЯ РИСКА ИНТЕРСТИЦИАЛЬНОЙ ПНЕВМОНИИ | 2014 |
|
RU2670148C2 |
| НАБОР ОЛИГОДЕЗОКСИРИБОНУКЛЕОТИДНЫХ ПРАЙМЕРОВ И ФЛУОРЕСЦЕНТНО-МЕЧЕННОГО ЗОНДА ДЛЯ ИДЕНТИФИКАЦИИ РНК КОРОНАВИРУСА ЧЕЛОВЕКА, АССОЦИИРОВАННОГО С ТЯЖЕЛЫМ ОСТРЫМ РЕСПИРАТОРНЫМ СИНДРОМОМ | 2012 |
|
RU2504585C1 |
Авторы
Даты
2020-07-17—Публикация
2020-04-24—Подача