Ссылка на перечень последовательностей
[0001] Настоящая заявка содержит перечень последовательностей, который был подан в электронном виде в формате ASCII, и этим включен посредством ссылки во всей своей полноте. Указанная ASCII-копия, созданная 16 июля 2014 года, носит название IL5R-605WO1_SL.txt и имеет размер 15940 байтов.
ПРЕДПОСЫЛКИ
[0002] Более 300 миллионов людей по всему миру болеют астмой. Несмотря на применение бронходилататоров длительного действия и ингаляционных кортикостероидов астма продолжает оставаться главным источником заболеваемости во всем мире. (Masoli M, et al. Allergy 59: 469-78(2004)).
[0003] Сообщалось, что после острого приступа астмы в 41-52% случаев через 12 недель происходил рецидив, несмотря на применение системных стероидов после выписки (Lederle F, et al. Arch Int Med 147:2201-03 (1987)). Ведение этих пациентов оказалось проблематичным вследствие либо тяжелого резистентного заболевания, либо отсутствия возможности и/или нежелания соблюдать требования в отношении фармакотерапии. В одном исследовании пациентов, поступивших в больницу, некоторые из которых имели почти смертельную астму, 50% пациентов не соблюдали требования в отношении приема системных кортикостероидов через 7 суток после выписки (Krishnan J, et al. AJRCCM 170: 1281-85 (2004)). Многие факторы могут способствовать несоблюдению предписанного режима, в том числе плохой доступ к медицинской помощи соответствующего качества (особенно во районах города с бедным населением), отсутствие должной образованности или понимания своего заболевания, нежелание признавать хроническую природу своего заболевания или отсутствие возможности получать лекарственные препараты.
[0004] На основании многих наборов данных делается вывод, что эозинофилы представляют собой главные клетки, которые вызывают воспаление дыхательных путей при астме (James A. Curr Opin Pulm Med 11(1):1-6 (2005)). Эозинофилия периферической крови (PB) является фактором риска для рецидива острой астмы (Janson C and Herala M. Resp Med 86(2):101-104 (1992)). Субъекты с эозинофилией периферической крови имеют в 7,4 раза больший (доверительный интервал, 2,8-19,7) риск умереть от астмы, чем субъекты без эозинофилии (Ulrik C and Fredericksen J. Chest 108:10-15 (1995)). Результаты вскрытия выявили 2 различных механизма патогенеза воспаления при смертельной астме (Restrepo R and Peters J. Curr Opin Pulm Med 14: 13-23 (2008)). Нейтрофильный инфильтрат более выражен у людей, которые умирают внезапно (приблизительно в течение 2 часов после появления симптомов), в то время как эозинофильный инфильтрат более распространен у людей, которые умирают от более продолжительных кризов астмы. У пациентов с быстрым появлением симптомов астмы, поступающих в отделение неотложной помощи, также может быть увеличено количество эозинофилов в мокроте и крови (Bellido-Casado J, et al. Arch Bronconeumol 46(11): 587-93 (2010)). Виды терапии, которые нацелены на эозинофилы, приводят к снижению числа и тяжести приступов астмы по сравнению с применением клинических рекомендаций (Green R, et al. Lancet 360:1715-21 (2002); Haldar P, et al. NEJM 360:973-84 (2009)).
[0005] Бенрализумаб (MEDI-563) представляет собой гуманизированное моноклональное антитело (mAb), которое связывается с альфа-цепью альфа-рецептора интерлейкина-5 (IL-5Rα), который экспрессируется на эозинофилах и базофилах. Он индуцирует апоптоз этих клеток посредством антителозависимой клеточной цитотоксичности. Однократная внутривенная (IV) доза бенрализумаба, которую вводили взрослым людям с легкой формой астмы, вызывала длительную эозинопению PB, вероятно, вследствие воздействий на клетки-предшественники эозинофилов/базофилов в костном мозге, которые экспрессируют мишень (Busse W, et al. JACI 125: 1237-1244 e2 (2010)). В дополнение, однократная доза бенрализумаба значительно снижала количество эозинофилов в крови у субъектов, которые поступали в отделение неотложной помощи с тяжелым приступом астмы, но не влияла на баллы согласно опроснику по контролю над астмой (ACQ), который предусматривает оценку симптомов астмы (WO 2013/066780).
[0006] ACQ представляет собой сообщаемый пациентом опросник, оценивающий симптомы астмы (ночное пробуждение, симптомы при пробуждении, ограничение активности, одышку, свистящее дыхание) и ежедневное применение бронходилататоров неотложной помощи и форсированный объем выдоха в одну секунду (FEV1). Juniper et al., Eur. Respir. J. 14:902-7 (1999) и Juniper et al., Chest 115:1265-70 (1999). Вопросы имеют одинаковую значимость, и им присваивают балл от 0 (полный контроль) до 6 (очень плохой контроль). Средний балл согласно ACQ представляет собой среднее значение ответов. Средние баллы ≤0,75 являются показателями хорошо контролируемой астмы; баллы от 0,75 до ≤1,5 являются показателями частично контролируемой астмы и балл >1,5 является показателем неконтролируемой астмы. Juniper et al., Respir. Med. 100:616-21 (2006). Индивидуальные изменения по меньшей мере на 0,5 считаются клинически значимыми. Juniper et al., Respir. Med. 99:553-8 (2005). ACQ-6 представляет собой сокращенную версию ACQ, которая оценивает симптомы астмы (ночное пробуждение, симптомы при пробуждении, ограничение активности, одышку, свистящее дыхание и применение агонистов β2 быстрого действия), исключая измерение FEV1 из оригинального балла согласно ACQ. Другие опросники, такие как опросник для оценки эффективности терапии астмы (ATAQ), тест по контролю над астмой (ACT), опросник оценки качества жизни у больных астмой (AQLQ), и дневники больного астмой также можно применять для оценки симптомов астмы.
[0007] Таким образом, с учетом большой неудовлетворенной потребности в нормализации симптомов астмы, например, измеряемых с применением ACQ, и того, что некоторые пациенты с астмой имеют эозинофильный компонент, исследовали влияние бенрализумаба на связанные с астмой опросники у взрослых субъектов.
КРАТКОЕ ОПИСАНИЕ
[0008] В данном документе предусмотрены способы нормализации балла согласно опроснику для оценки астмы у пациента с астмой. В определенных аспектах способ нормализации балла согласно опроснику для оценки астмы у пациента с астмой включает введение пациенту эффективного количества бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах опросник оценивает по меньшей мере один симптом, выбранный из группы, состоящей из ночного пробуждения, симптомов при пробуждении, ограничения активности, одышки, свистящего дыхания, применения лекарственного препарата неотложной помощи, частоты и тяжести симптомов в дневное время, частоты и тяжести симптомов в ночное время, уклонения от активности и ее ограничения, связанной с астмой тревоги и утомляемости. В определенных аспектах опросник оценивает ночное пробуждение, симптомы при пробуждении, ограничение активности, одышку, свистящее дыхание и применение лекарственного препарата неотложной помощи. В определенных аспектах опросник оценивает частоту симптомов в дневное время, тяжесть симптомов в дневное время и тяжесть в ночное время. В определенных аспектах опросник представляет собой опросник по контролю над астмой (ACQ). В определенных аспектах опросник для оценки астмы представляет собой опросник-6 по контролю над астмой (ACQ-6). В определенных аспектах опросник для оценки астмы представляет собой опросник оценки качества жизни у больных астмой (AQLQ).
[0009] В данном документе также предусмотрены способы лечения астмы. В определенных аспектах способ лечения астмы включает введение пациенту с астмой эффективного количества антитела к рецептору интерлейкина-5 (IL-5R), бенрализумаба, или его антигенсвязывающего фрагмента, где количество эозинофилов в крови пациента перед введением составляет по меньшей мере 300 клеток/мкл.
[0010] В определенных аспектах способ лечения астмы включает введение пациенту с астмой эффективного количества бенрализумаба или его антигенсвязывающего фрагмента, где форсированный объем выдоха в одну секунду (FEV1) у пациента перед введением составляет по меньшей мере 75% прогнозируемого значения.
[0011] В определенных аспектах способ лечения астмы включает введение пациенту с астмой по меньшей мере двух доз бенрализумаба или его антигенсвязывающего фрагмента.
[0012] В определенных аспектах способов, предусмотренных в данном документе, введение нормализует симптом астмы у пациента. В определенных аспектах симптом астмы выбран из группы, состоящей из ночного пробуждения, симптомов при пробуждении, ограничения активности, одышки, свистящего дыхания, применения лекарственного препарата неотложной помощи, частоты и тяжести симптомов в дневное время, частоты и тяжести симптомов в ночное время, уклонения от активности и ее ограничения, связанной с астмой тревоги и утомляемости.
[0013] В определенных аспектах способов, предусмотренных в данном документе, балл пациента согласно ACQ снижается. В определенных аспектах балл пациента согласно ACQ-6 снижается. В определенных аспектах бал согласно ACQ-6 пациента снижается не позднее 7 недель от первого введения. В определенных аспектах балл согласно ACQ-6 снижается по меньшей мере на 0,5. В определенных аспектах балл согласно ACQ-6 снижается по меньшей мере на 1. В определенных аспектах балл согласно ACQ-6 снижается по меньшей мере на 2.
[0014] В определенных аспектах способов, предусмотренных в данном документе, астма представляет собой эозинофильную астму. В определенных аспектах количество эозинофилов в крови пациента составляет по меньшей мере 300 клеток/мкл.
[0015] В определенных аспектах способов, предусмотренных в данном документе, форсированный объем выдоха в одну секунду (FEV1) у пациента перед введением составляет по меньшей мере 75% прогнозируемого значения. В определенных аспектах пациент применяет ингаляционные кортикостероиды (ICS) в высоких дозах. В определенных аспектах балл пациента согласно опроснику по контролю над астмой перед введением составляет по меньшей мере 1,5. В определенных аспектах пациент применяет агонисты β2 длительного действия (LABA). В определенных аспектах у пациента есть приступы в анамнезе. В определенных аспектах приступы в анамнезе включают по меньшей мере два приступа в год перед введением бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах приступы в анамнезе включают не более шести приступов в год перед введением бенрализумаба или его антигенсвязывающего фрагмента.
[0016] В определенных аспектах способов, предусмотренных в данном документе, пациенту вводят по меньшей мере две дозы бенрализумаба или его антигенсвязывающего фрагмента.
[0017] В определенных аспектах способов, предусмотренных в данном документе, бенрализумаб или его антигенсвязывающий фрагмент вводят из расчета от приблизительно 2 мг до приблизительно 100 мг на дозу. В определенных аспектах бенрализумаб или его антигенсвязывающий фрагмент вводят из расчета приблизительно 20 мг на дозу. В определенных аспектах бенрализумаб или его антигенсвязывающий фрагмент вводят из расчета приблизительно 30 мг на дозу. В определенных аспектах бенрализумаб или его антигенсвязывающий фрагмент вводят из расчета приблизительно 100 мг на дозу.
[0018] В определенных аспектах способов, предусмотренных в данном документе, бенрализумаб или его антигенсвязывающий фрагмент вводят от одного раза в четыре недели до одного раза в двенадцать недель. В определенных аспектах бенрализумаб или его антигенсвязывающий фрагмент вводят один раз в четыре недели. В определенных аспектах бенрализумаб или его антигенсвязывающий фрагмент вводят один раз в восемь недель. В определенных аспектах бенрализумаб или его антигенсвязывающий фрагмент вводят один раз в четыре недели на протяжении двенадцати недель, а затем один раз в восемь недель.
[0019] В определенных аспектах способов, предусмотренных в данном документе, бенрализумаб или его антигенсвязывающий фрагмент вводят парентерально. В определенных аспектах бенрализумаб или его антигенсвязывающий фрагмент вводят подкожно.
[0020] В определенных аспектах способов, предусмотренных в данном документе, бенрализумаб или его антигенсвязывающий фрагмент вводят в дополнение к терапии кортикостероидами.
[0021] В определенных аспектах способ нормализации балла согласно опроснику для оценки астмы у пациента с астмой включает введение пациенту с астмой 20-100 мг бенрализумаба или его антигенсвязывающего фрагмента, где количество эозинофилов в крови пациента перед введением составляет по меньшей мере 300 клеток/мкл. В определенных аспектах способ включает введение 20 мг бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах 20 мг бенрализумаба вводят один раз в четыре недели на протяжении двенадцати недель, а затем один раз в восемь недель. В определенных аспектах способ включает введение 30 мг бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах 30 мг бенрализумаба вводят один раз в четыре недели на протяжении восьми недель, а затем один раз в восемь недель. В определенных аспектах 30 мг бенрализумаба вводят один раз в четыре недели. В определенных аспектах способ включает введение 100 мг бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах 100 мг бенрализумаба вводят один раз в четыре недели на протяжении двенадцати недель, а затем один раз в восемь недель.
[0022] В определенных аспектах способ лечения астмы у пациента с астмой включает введение пациенту дозы, составляющей по меньшей мере 2 и менее 100 мг бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах способ включает введение 20 мг бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах способ включает введение 30 мг бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах способ включает введение дозы, составляющей по меньшей мере 20 и менее 100 мг бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах способ включает введение дозы, составляющей по меньшей мере 30 и менее 100 мг бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах способ снижает частоту приступов астмы. В определенных аспектах способ снижает годовую частоту приступов астмы. В определенных аспектах введение является подкожным.
[0023] В определенных аспектах предусмотренных способов введение бенрализумаба или его антигенсвязывающего фрагмента приводит к нормализации симптомов астмы, как показано на фиг. 2-10.
[0024] В определенных аспектах предусмотренных способов введение бенрализумаба или его антигенсвязывающего фрагмента приводит к нормализации симптомов астмы, как показано в примерах 1-2.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ/ФИГУР
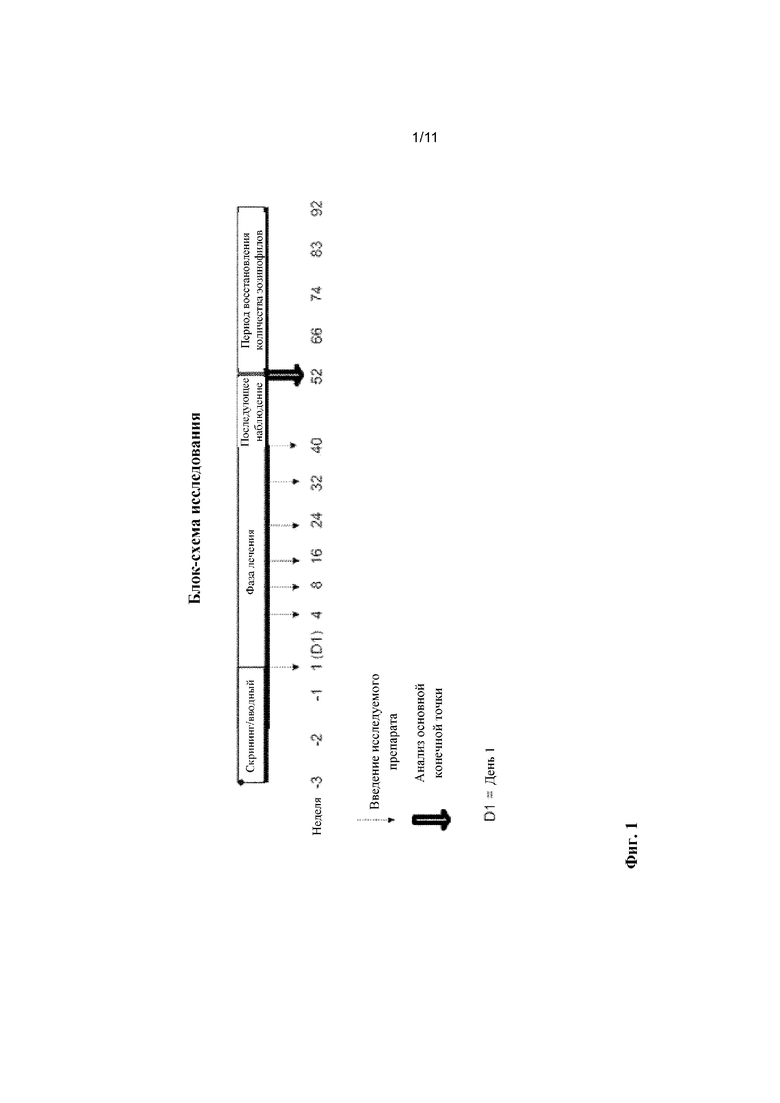
[0025] На фиг. 1 показана блок-схема исследования.
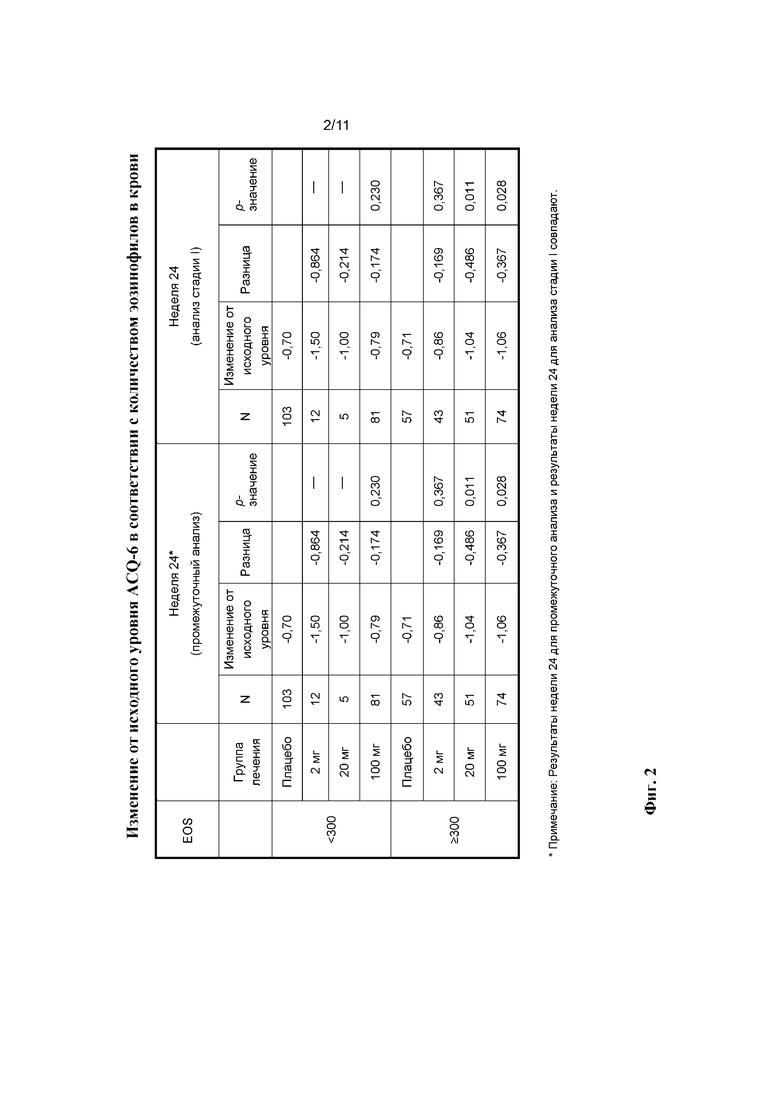
[0026] На фиг. 2 показано изменение от исходного уровня ACQ-6 на 24-неделе после начала лечения с помощью плацебо, 2 мг бенрализумаба, 20 мг бенрализумаба или 100 мг бенрализумаба у пациентов с показателем менее 300 эозинофилов/мкл и пациентов с показателем по меньшей мере 300 эозинофилов/мкл.
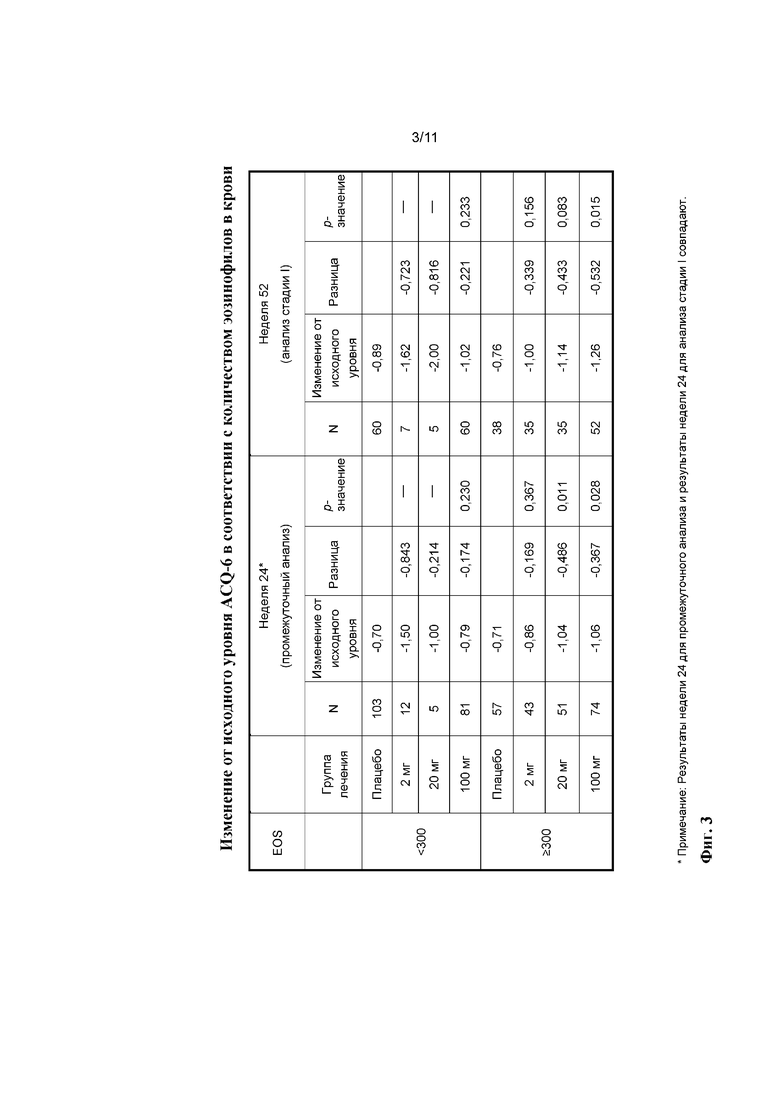
[0027] На фиг. 3 показано промежуточное (24 недели) изменение и изменение на стадии I (52 недели) от исходного уровня ACQ-6 после лечения с помощью плацебо, 2 мг бенрализумаба, 20 мг бенрализумаба или 100 мг бенрализумаба у пациентов с показателем менее 300 эозинофилов/мкл и пациентов с показателем по меньшей мере 300 эозинофилов/мкл.
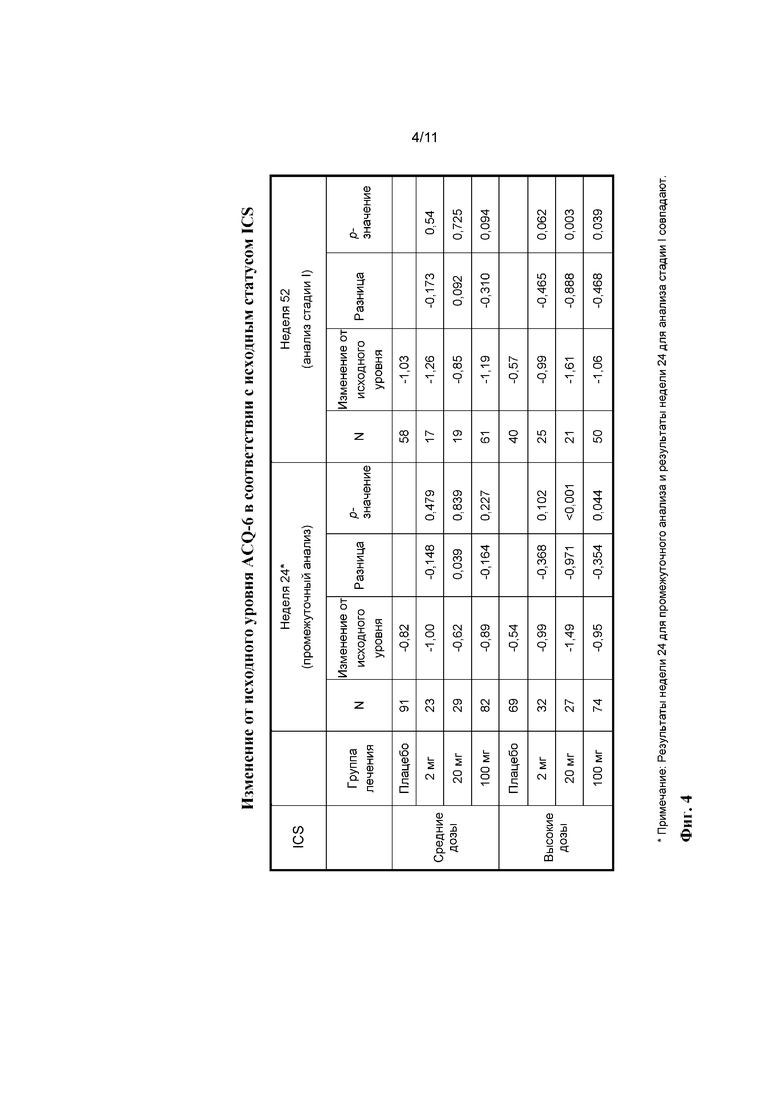
[0028] На фиг. 4 показано промежуточное (24 недели) изменение и изменение на стадии I (52 недели) от исходного уровня ACQ-6 после лечения с помощью плацебо, 2 мг бенрализумаба, 20 мг бенрализумаба или 100 мг бенрализумаба у пациентов со средним или высоким уровнем применения ингаляционных кортикостероидов (ICS).
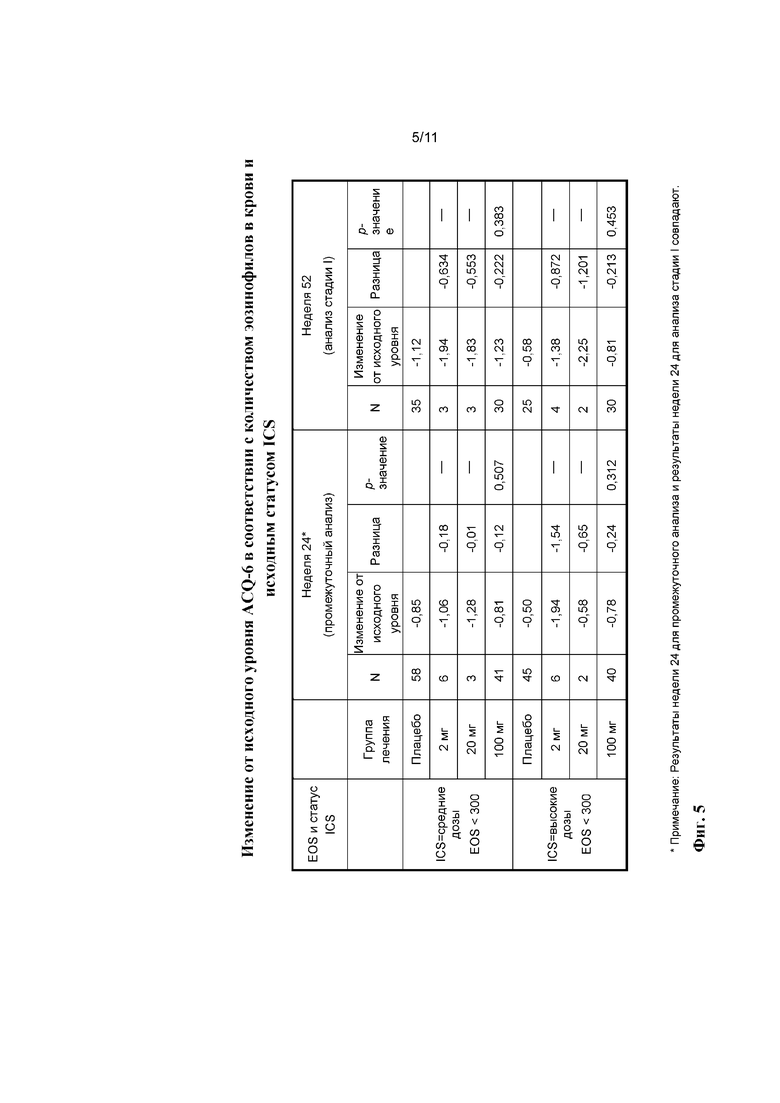
[0029] На фиг. 5 показано промежуточное (24 недели) изменение и изменение на стадии I (52 недели) от исходного уровня ACQ-6 после лечения с помощью плацебо, 2 мг бенрализумаба, 20 мг бенрализумаба или 100 мг бенрализумаба у пациентов с менее 300 эозинофилов/мкл и (i) средним уровнем применения ICS или (ii) высоким уровнем применения ICS.
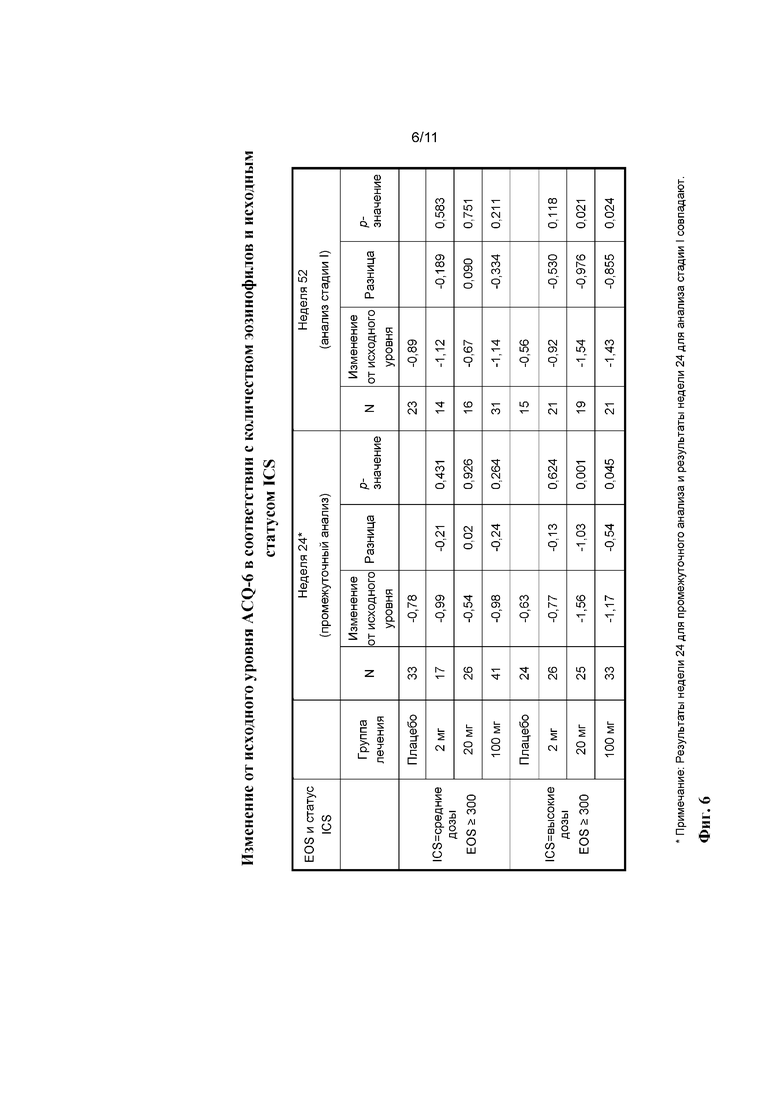
[0030] На фиг. 6 показано промежуточное (24 недели) изменение и изменение на стадии I (52 недели) от исходного уровня ACQ-6 после лечения с помощью плацебо, 2 мг бенрализумаба, 20 мг бенрализумаба или 100 мг бенрализумаба у пациентов с показателем по меньшей мере 300 эозинофилов/мкл и (i) средним уровнем применения ICS или (ii) высоким уровнем применения ICS.
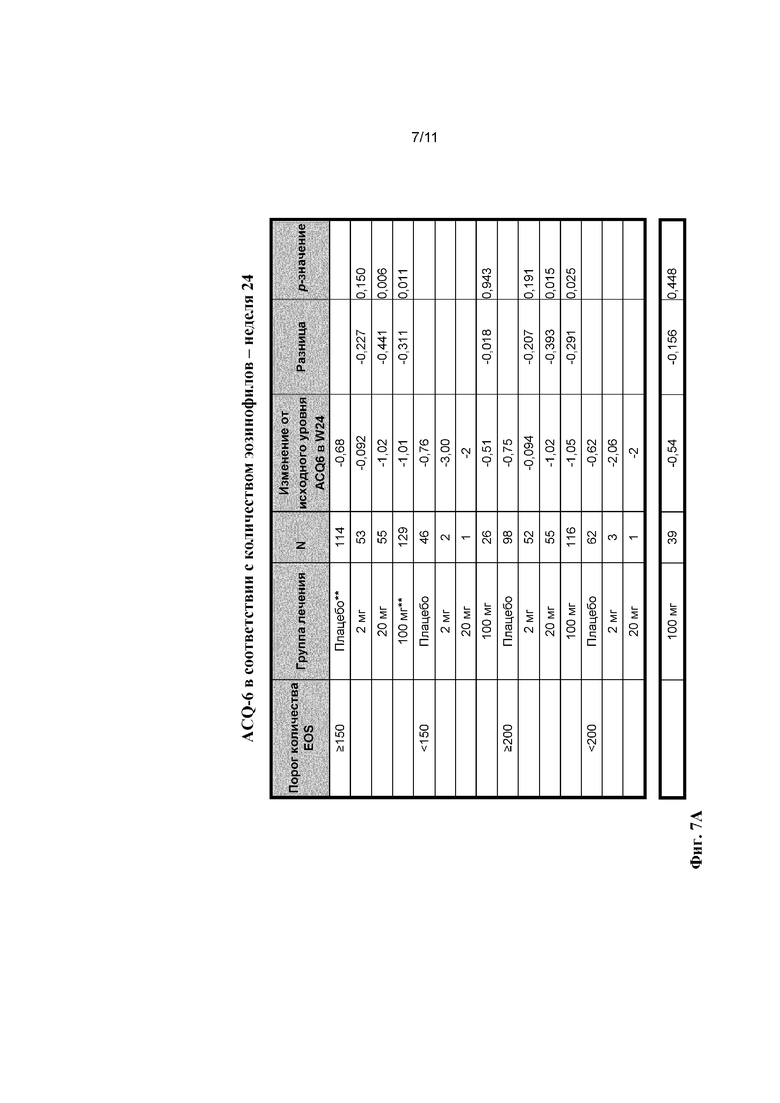
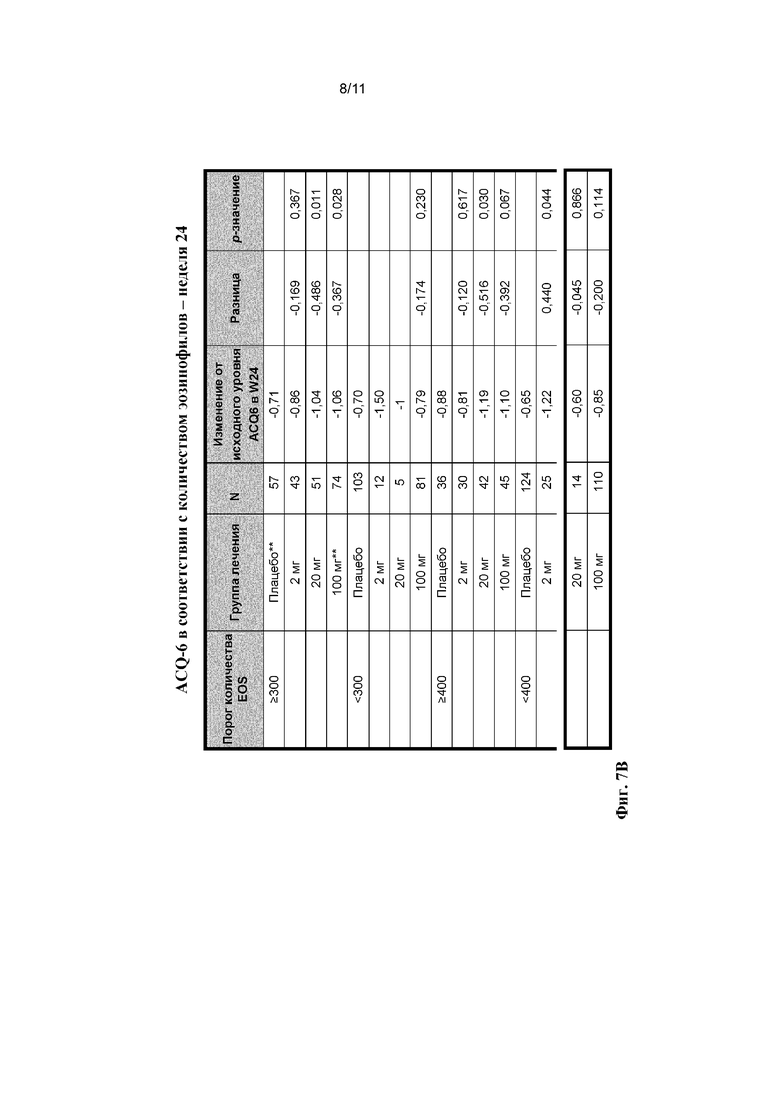
[0031] На фиг. 7A и 7B показаны изменения от исходного уровня согласно ACQ-6 у пациентов с различным количеством эозинофилов.
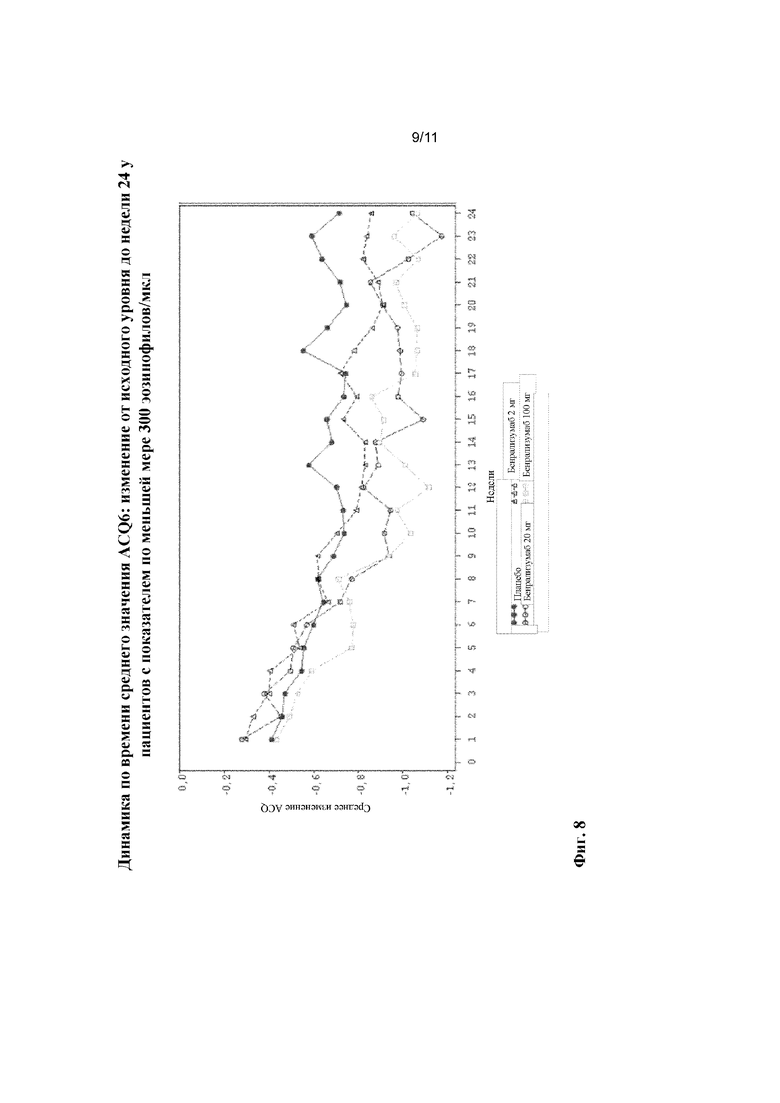
[0032] На фиг. 8 показано изменение среднего значения ACQ-6 в динамике по времени у пациентов с показателем по меньшей мере 300 эозинофилов/мкл.
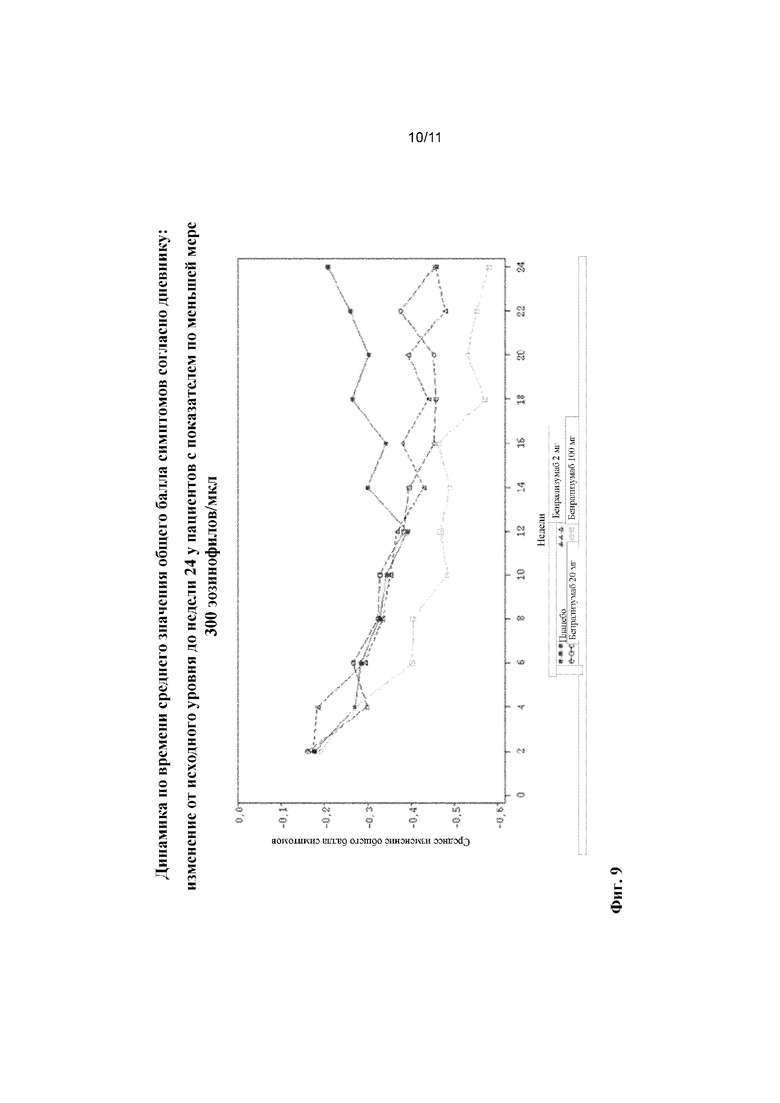
[0033] На фиг. 9 показано изменение среднего значения общего балла симптомов согласно дневнику в динамике по времени у пациентов с показателем по меньшей мере 300 эозинофилов/мкл.
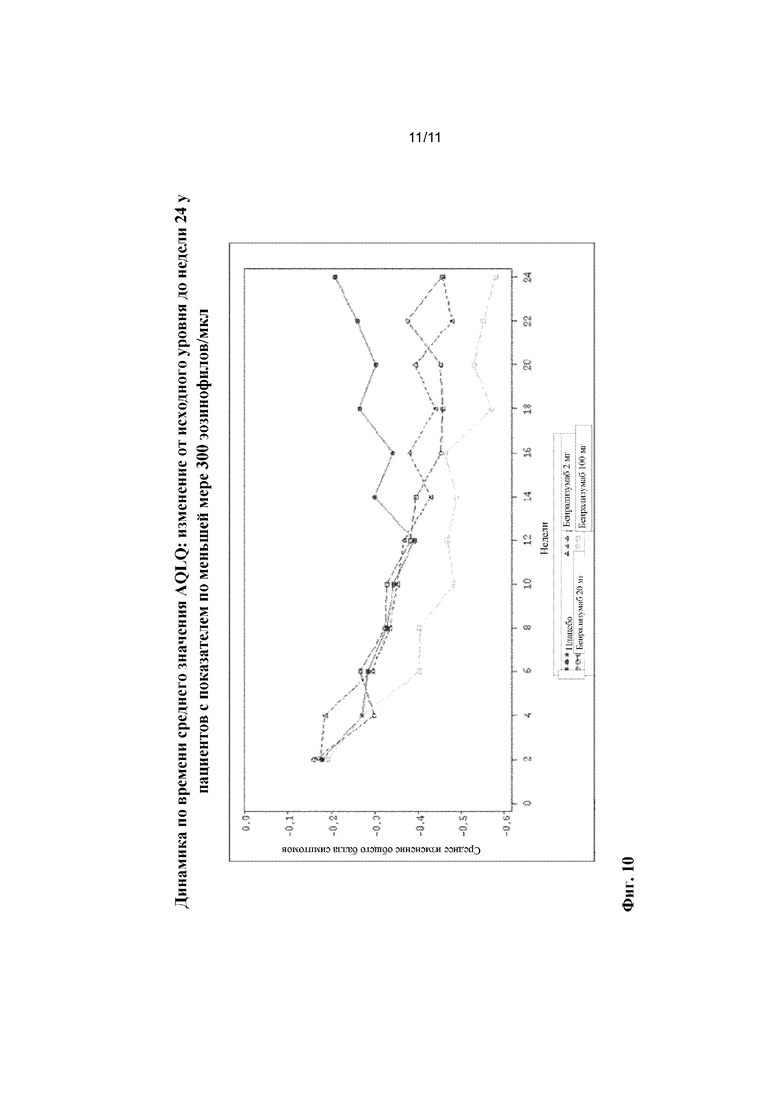
[0034] На фиг. 10 показано среднее значение изменения AQLQ у пациентов с показателем по меньшей мере 300 эозинофилов/мкл.
ПОДРОБНОЕ ОПИСАНИЕ
[0035] Следует отметить, что форма единственного числа объекта относится к одному или нескольким таким объектам; например, подразумевается, что "антитело к IL-5α" представляет собой одно или несколько антител к IL-5α. В связи с этим, формы единственного числа, выражения "один или несколько" и "по меньшей мере один" можно использовать в данном документе взаимозаменяемо.
[0036] В данном документе предусмотрены способы нормализации симптомов астмы, например, оцениваемых с применением опросника для оценки астмы, такого как опросник по контролю над астмой, (ACQ), ACQ-6, опросник для оценки эффективности терапии астмы (ATAQ), тест по контролю над астмой (ACT), опросник оценки качества жизни у больных астмой(AQLQ), или дневника симптомов астмы. Симптом может представлять собой, например, ночное пробуждение, симптомы при пробуждении, ограничение активности, одышку, свистящее дыхание и/или применение лекарственного препарата неотложной помощи (например, бронходилататор). Также симптом может представлять собой, например, частоту и тяжесть симптомов в дневное время, частоту и тяжесть симптомов в ночное время, уклонение от активности и ее ограничение, связанную с астмой тревогу, утомляемость и/или применение лекарственного препарата неотложной помощи. Симптомы также могут представлять собой, например, частоту симптомов в дневное время, тяжесть симптомов в дневное время и/или тяжесть симптомов в ночное время. Предусмотренные способы включают введение эффективного количества бенрализумаба или его антигенсвязывающего фрагмента.
[0037] Информацию, касающуюся бенрализумаба (или его фрагментов), для применения в способах, предусмотренных в данном документе, можно найти в публикации заявки на патент США № US 2010/0291073 A1, раскрытие которой включено в данный документ посредством ссылки во всей ее полноте. Бенрализумаб и его антигенсвязывающие фрагменты для применения в способах, предусмотренных в данном документе, содержат тяжелую цепь и легкую цепь или вариабельную область тяжелой цепи и вариабельную область легкой цепи. В дополнительном аспекте бенрализумаб или его антигенсвязывающий фрагмент для применения в способах, предусмотренных в данном документе, содержит любую из аминокислотных последовательностей с SEQ ID NO: 1-4. В конкретном аспекте бенрализумаб или его антигенсвязывающий фрагмент для применения в способах, предусмотренных в данном документе, содержит вариабельную область легкой цепи, содержащую аминокислотную последовательность с SEQ ID NO:1, и вариабельную область тяжелой цепи, содержащую аминокислотную последовательность с SEQ ID NO:3. В конкретном аспекте бенрализумаб или его антигенсвязывающий фрагмент для применения в способах, предусмотренных в данном документе, содержит легкую цепь, содержащую аминокислотную последовательность с SEQ ID NO: 2, и тяжелую цепь, содержащую аминокислотную последовательность с SEQ ID NO:4. В конкретном аспекте бенрализумаб или его антигенсвязывающий фрагмент для применения в способах, предусмотренных в данном документе, содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, где вариабельная область тяжелой цепи содержит определенные по Kabat последовательности CDR1, CDR2 и CDR3 с SEQ ID NO: 7-9, и где вариабельная область легкой цепи содержит определенные по Kabat последовательности CDR1, CDR2 и CDR3 с SEQ ID NO: 10-12. Специалисты в данной области с легкостью смогут распознать определенные по Chothia, определенные по Abm или другие CDR. В конкретном аспекте бенрализумаб или его антигенсвязывающий фрагмент для применения в способах, предусмотренных в данном документе, содержит последовательности CDR вариабельной области тяжелой цепи и вариабельной области легкой цепи антитела KM1259, раскрытые в U.S. 6018032, который включен в данный документ посредством ссылки во всей своей полноте.
[0038] В определенных аспектах пациенту, поступающему в кабинет врача или отделение неотложной помощи с астмой, вводят бенрализумаб или его антигенсвязывающий фрагмент. С учетом способности бенрализумаба снижать или сокращать количество эозинофилов на период до 12 недель или более (см. US 2010/0291073), бенрализумаб или его антигенсвязывающий фрагмент можно вводить только один раз или изредка, при этом это все еще будет приносить пользу пациенту за счет нормализации ACQ и/или ACQ-6. В дополнительных аспектах пациенту вводят дополнительные последующие дозы. Последующие дозы можно вводить с различными интервалами времени в зависимости от возраста, веса пациента, способности соблюдать указания врача, клинических анализов, количества эозинофилов (эозинофилов крови или мокроты), показателя катионного белка эозинофилов (ECP), показателя нейротоксина эозинофилов (EDN), показателя главного основного белка (MBP) и других факторов, в том числе мнения лечащего врача. Интервалы между дозами могут представлять собой через четыре недели, через пять недель, через 6 недель, через 8 недель, через 10 недель, через 12 недель или более продолжительные интервалы. В определенных аспектах интервалы между дозами могут представлять собой через 4 недели, через 8 недель или через 12 недель. В определенных аспектах пациенту с астмой вводят однократную дозу или первую дозу сразу после того, как пациент поступает с острым приступом, например, приступом легкой, умеренной или тяжелой степени. Например, однократную или первую дозу бенрализумаба или его антигенсвязывающего фрагмента можно вводить во время поступления в амбулаторию или больницу или, в случае приступов очень тяжелой степени, не позднее 1, 2, 3, 4, 5, 6, 7 или более суток, например, 7 суток от острого приступа, обеспечивая возможность стабилизации симптомов пациента перед введением бенрализумаба.
[0039] В некоторых вариантах осуществления пациенту вводят по меньшей мере две дозы бенрализумаба или его антигенсвязывающего фрагмента. В некоторых вариантах осуществления пациенту вводят по меньшей мере три дозы, по меньшей мере четыре дозы, по меньшей мере пять доз, по меньшей мере шесть доз или по меньшей мере семь доз. В некоторых вариантах осуществления бенрализумаб или его антигенсвязывающий фрагмент вводят в течение четырех недель, в течение восьми недель, в течение двенадцати недель, в течение двадцати четырех недель или в течение года.
[0040] Количество бенрализумаба или его антигенсвязывающего фрагмента, подлежащего введению пациенту, будет зависеть от различных параметров, таких как возраст, вес пациента, клинические анализы, количество эозинофилов (эозинофилы крови или мокроты), показатель катионного белка эозинофилов (ECP), показатель нейротоксина эозинофилов (EDN), показатель главного основного белка (MBP) и другие факторы, в том числе мнение лечащего врача. В определенных аспектах дозировка или интервал между дозировками не зависят от уровня эозинофилов в мокроте.
[0041] В определенных аспектах пациенту вводят одну или несколько доз бенрализумаба или его антигенсвязывающего фрагмента, где доза составляет от приблизительно 2 мг до приблизительно 100 мг, например, от приблизительно 20 мг до приблизительно 100 мг или от приблизительно 30 мг до приблизительно 100 мг. В определенных конкретных аспектах пациенту вводят одну или несколько доз бенрализумаба или его антигенсвязывающего фрагмента, где доза составляет приблизительно 20 мг, приблизительно 30 мг, приблизительно 40 мг, приблизительно 50 мг, приблизительно 60 мг, приблизительно 70 мг, приблизительно 80 мг, приблизительно 90 мг или приблизительно 100 мг. В некоторых вариантах осуществления доза составляет приблизительно 20 мг. В некоторых вариантах осуществления доза составляет приблизительно 30 мг. В некоторых вариантах осуществления доза составляет приблизительно 100 мг.
[0042] В определенных аспектах введение бенрализумаба или его антигенсвязывающего фрагмента согласно способам, предусмотренным в данном документе, осуществляют посредством парентерального введения. Например, бенрализумаб или его антигенсвязывающий фрагмент можно вводить путем внутривенной инфузии или путем подкожной инъекции.
[0043] В определенных аспектах бенрализумаб или его антигенсвязывающий фрагмент вводят согласно способам, предусмотренным в данном документе, в комбинации или в сочетании с дополнительными методами терапии астмы. Такие методы терапии включают без ограничения терапию ингаляционными кортикостероидами, лечение бронходилататорами длительного действия или кратковременного действия, подачу кислорода или другие стандартные методы терапии, описываемые, например, в руководстве NAEPP. В определенных аспектах применение способов, предусмотренных в данном документе, т.е. введение бенрализумаба или его антигенсвязывающего фрагмента пациенту с астмой с острыми приступами в анамнезе, служит в качестве вспомогательной терапии в ситуациях недостаточного соблюдения требований стандартных форм ведения астмы.
[0044] Способы, предусмотренные в данном документе, могут значительно снижать баллы согласно ACQ или ACQ-6 у больных астмой. Изменение в ACQ или ACQ-6 можно измерять в сравнении с ожидаемым ACQ или ACQ-6, основанным на большой популяции пациентов, на ACQ или ACQ-6, измеренном у контрольной популяции, или на индивидуальном ACQ или ACQ-6 пациента перед введением. В определенных аспектах популяция пациентов представляет собой пациентов, имевших ≥2 приступов, требующих введения пероральных системных кортикостероидов, за прошедший год. В определенных аспектах популяция пациентов представляет собой пациентов, имевших ≥2 приступов, требующих пульс-терапии системными кортикостероидами, за прошедший год, и ≤6 приступов, требующих пульс-терапии системными кортикостероидами, за прошедший год. В определенных аспектах популяция пациентов представляет собой пациентов, количество эозинофилов у которых составляет по меньшей мере 300 клеток/мкл.
[0045] В определенных аспектах применение способов, предусмотренных в данном документе, т.е. введение бенрализумаба или его антигенсвязывающего фрагмента нормализует баллы согласно ACQ или ACQ-6 в течение периода 24 недели после введения бенрализумаба или его антигенсвязывающего фрагмента по сравнению с исходным уровнем ACQ или ACQ-6 пациента. В определенных аспектах пациент может получать последующие дозы бенрализумаба или его антигенсвязывающего фрагмента с периодическими интервалами, например, через 4 недели, через 5 недель, через 6 недель, через 8 недель, через 12 недель или в соответствии с графиком, основанном на возрасте, весе пациента, способности соблюдать указания врача, клинических анализах, количестве эозинофилов (эозинофилов крови или мокроты), показателе катионного белка эозинофилов (ECP), показателе нейротоксина эозинофилов (EDN), показателе главного основного белка (MBP) и других факторах, в том числе мнении лечащего врача. Применение способов, предусмотренных в данном документе, может снижать баллы согласно ACQ или ACQ-6 по меньшей мере на 0,4, по меньшей мере на 0,5, по меньшей мере на 0,6, по меньшей мере на 0,7, по меньшей мере на 0,8, по меньшей мере на 0,9, по меньшей мере на 1,0, по меньшей мере на 1,1, по меньшей мере на 1,2, по меньшей мере на 1,3, по меньшей мере на 1,4, по меньшей мере на 1,5, по меньшей мере на 1,6, по меньшей мере на 1,7, по меньшей мере на 1,8, по меньшей мере на 1,9, по меньшей мере на 2,0, по меньшей мере на 2,1, по меньшей мере на 2,2, по меньшей мере на 2,3, по меньшей мере на 2,4, по меньшей мере на 2,5, по меньшей мере на 2,6, по меньшей мере на 2,7, по меньшей мере на 2,8, по меньшей мере на 2,9 или по меньшей мере на 3,0 в течение периода 24 недели.
[0046] В других аспектах применение способов, предусмотренных в данном документе, т.е. введение бенрализумаба или его антигенсвязывающего фрагмента пациенту с астмой, нормализует баллы согласно ACQ или ACQ-6 в течение периода 52 недели после введения бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах пациент может получать последующие дозы бенрализумаба или его антигенсвязывающего фрагмента с периодическими интервалами, например, через 4 недели, через 5 недель, через 6 недель, через 8 недель, через 12 недель или в соответствии с графиком, основанном на возрасте, весе пациента, способности соблюдать указания врача, клинических анализах, количестве эозинофилов (эозинофилов крови или мокроты), показателе катионного белка эозинофилов (ECP), показателе нейротоксина эозинофилов (EDN), показателе главного основного белка (MBP) и других факторах, в том числе мнении лечащего врача. В определенных аспектах интервал представляет собой через 4 недели, через 8 недель или через 12 недель. Применение способов, предусмотренных в данном документе, может снижать баллы согласно ACQ или ACQ-6 по меньшей мере на 0,4, по меньшей мере на 0,5, по меньшей мере на 0,6, по меньшей мере на 0,7, по меньшей мере на 0,8, по меньшей мере на 0,9, по меньшей мере на 1,0, по меньшей мере на 1,1, по меньшей мере на 1,2, по меньшей мере на 1,3, по меньшей мере на 1,4, по меньшей мере на 1,5, по меньшей мере на 1,6, по меньшей мере на 1,7, по меньшей мере на 1,8, по меньшей мере на 1,9, по меньшей мере на 2,0, по меньшей мере на 2,1, по меньшей мере на 2,2, по меньшей мере на 2,3, по меньшей мере на 2,4, по меньшей мере на 2,5, по меньшей мере на 2,6, по меньшей мере на 2,7, по меньшей мере на 2,8, по меньшей мере на 2,9 или по меньшей мере на 3,0.
[0047] В определенных аспектах применение способов, предусмотренных в данном документе, т.е. введение бенрализумаба или его антигенсвязывающего фрагмента, снижает баллы согласно ACQ или ACQ-6 не позднее 4 недель, не позднее 7 недель, не позднее 8 недель, не позднее 9 недель, не позднее 10 недель, не позднее 12 недель, не позднее 16 недель, не позднее 20 недель, не позднее 24 недель, не позднее 28 недель, не позднее 32 недель, не позднее 36 недель, не позднее 40 недель, не позднее 44 недель, не позднее 48 недель или не позднее 52 недель.
[0048] Способы, предусмотренные в данном документе, также могут в значительной степени нормализовать баллы в виде баллов согласно дневнику симптомов астмы, измеряющих частоту симптомов в дневное время, тяжесть симптомов в дневное время и тяжесть симптомов в ночное время. Изменение таких баллов симптомов согласно дневнику можно измерять в сравнении с ожидаемым баллом симптомов согласно дневнику, основанным на большой популяции пациентов, на балле симптомов согласно дневнику, измеренному в контрольной популяции, или на индивидуальном балле симптомов пациента согласно дневнику перед введением. В определенных аспектах популяция пациентов представляет собой пациентов, имевших ≥2 приступов, требующих введения пероральных системных кортикостероидов, за прошедший год. В определенных аспектах популяция пациентов представляет собой пациентов, имевших ≥2 приступов, требующих пульс-терапии системными кортикостероидами, за прошедший год, и ≤6 приступов, требующих пульс-терапии системными кортикостероидами, за прошедший год. В определенных аспектах популяция пациентов представляет собой пациентов, количество эозинофилов у которых составляет по меньшей мере 300 клеток/мкл.
[0049] В определенных аспектах применение способов, предусмотренных в данном документе, т.e. введение бенрализумаба или его антигенсвязывающего фрагмента, нормализует баллы симптомов согласно дневнику в течение периода 24 недели после введения бенрализумаба или его антигенсвязывающего фрагмента по сравнению с исходным уровнем баллом симптомов согласно дневнику пациента. В определенных аспектах пациент может получать последующие дозы бенрализумаба или его антигенсвязывающего фрагмента с периодическими интервалами, например, через 4 недели, через 5 недель, через 6 недель, через 8 недель, через 12 недель или в соответствии с графиком, основанном на возрасте, весе пациента, способности соблюдать указания врача, клинических анализах, количестве эозинофилов (эозинофилов крови или мокроты), показателе катионного белка эозинофилов (ECP), показателе нейротоксина эозинофилов (EDN), показателе главного основного белка (MBP) и других факторах, в том числе мнении лечащего врача. Применение способов, предусмотренных в данном документе, может снижать баллы симптомов согласно дневнику по меньшей мере на 0,5 в течение периода 24 недели.
[0050] В других аспектах применение способов, предусмотренных в данном документе, т.е. введение бенрализумаба или его антигенсвязывающего фрагмента пациенту с астмой, нормализует баллы симптомов согласно дневнику в течение периода 52 недели после введения бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах пациент может получать последующие дозы бенрализумаба или его антигенсвязывающего фрагмента с периодическими интервалами, например, через 4 недели, через 5 недель, через 6 недель, через 8 недель, через 12 недель или в соответствии с графиком, основанном на возрасте, весе пациента, способности соблюдать указания врача, клинических анализах, количестве эозинофилов (эозинофилов крови или мокроты), показателе катионного белка эозинофилов (ECP), показателе нейротоксина эозинофилов (EDN), показателе главного основного белка (MBP) и других факторах, в том числе мнении лечащего врача. В определенных аспектах интервал представляет собой через 4 недели, через 8 недель или через 12 недель. Применение способов, предусмотренных в данном документе, может снижать баллы симптомов согласно дневнику по меньшей мере на 0,5.
[0051] В определенных аспектах применение способов, предусмотренных в данном документе, т.e. введение бенрализумаба или его антигенсвязывающего фрагмента снижает баллы симптомов согласно дневнику не позднее 4 недель, 5 недель, не позднее 6 недель, не позднее 7 недель, не позднее 8 недель, не позднее 9 недель, не позднее 10 недель, не позднее 12 недель, не позднее 16 недель, не позднее 20 недель, не позднее 24 недель, не позднее 28 недель, не позднее 32 недель, не позднее 36 недель, не позднее 40 недель, не позднее 44 недель, не позднее 48 недель или не позднее 52 недель.
[0052] Способы, предусмотренные в данном документе, могут значительно повышать баллы согласно AQLQ у больных астмой. Изменение AQLQ можно измерять в сравнении с ожидаемым AQLQ, основанным на большой популяции пациентов, на AQLQ, измеренном в контрольной популяции, или на индивидуальном AQLQ пациента перед введением. В определенных аспектах популяция пациентов представляет собой пациентов, имевших ≥2 приступов, требующих введения пероральных системных кортикостероидов, за прошедший год. В определенных аспектах популяция пациентов представляет собой пациентов, имевших ≥2 приступов, требующих пульс-терапии системными кортикостероидами, за прошедший год, и ≤6 приступов, требующих пульс-терапии системными кортикостероидами, за прошедший год. В определенных аспектах популяция пациентов представляет собой пациентов, количество эозинофилов у которых составляет по меньшей мере 300 клеток/мкл.
[0053] В определенных аспектах применение способов, предусмотренных в данном документе, т.e. введение бенрализумаба или его антигенсвязывающего фрагмента, нормализует баллы согласно AQLQ в течение периода 24 недели после введения бенрализумаба или его антигенсвязывающего фрагмента по сравнению с исходным уровнем пациента согласно AQLQ. В определенных аспектах пациент может получать последующие дозы бенрализумаба или его антигенсвязывающего фрагмента с периодическими интервалами, например, через 4 недели, через 5 недель, через 6 недель, через 8 недель, через 12 недель или в соответствии с графиком, основанном на возрасте, весе пациента, способности соблюдать указания врача, клинических анализах, количестве эозинофилов (эозинофилов крови или мокроты), показателе катионного белка эозинофилов (ECP), показателе нейротоксина эозинофилов (EDN), показателе главного основного белка (MBP) и других факторах, в том числе мнении лечащего врача. Применение способов, предусмотренных в данном документе, может повышать баллы согласно AQLQ по меньшей мере на 0,5, по меньшей мере на 0,6, по меньшей мере на 0,7, по меньшей мере на 0,8, по меньшей мере на 0,9, по меньшей мере на 1,0, по меньшей мере на 1,1, по меньшей мере на 1,2 или по меньшей мере на 1,3 в течение периода 24 недели.
[0054] В других аспектах применение способов, предусмотренных в данном документе, т.е. введение бенрализумаба или его антигенсвязывающего фрагмента пациенту с астмой, нормализует баллы согласно AQLQ в течение периода 52 недели после введения бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах пациент может получать последующие дозы бенрализумаба или его антигенсвязывающего фрагмента с периодическими интервалами, например, через 4 недели, через 5 недель, через 6 недель, через 8 недель, через 12 недель или в соответствии с графиком, основанном на возрасте, весе пациента, способности соблюдать указания врача, клинических анализах, количестве эозинофилов (эозинофилов крови или мокроты), показателе катионного белка эозинофилов (ECP), показателе нейротоксина эозинофилов (EDN), показателе главного основного белка (MBP) и других факторах, в том числе мнении лечащего врача. В определенных аспектах интервал представляет собой через 4 недели, через 8 недель или через 12 недель. Применение способов, предусмотренных в данном документе, может повышать баллы согласно AQLQ по меньшей мере на 0,4, по меньшей мере на 0,5, по меньшей мере на 0,6, по меньшей мере на 0,7, по меньшей мере на 0,8, по меньшей мере на 0,9, по меньшей мере на 1,0, по меньшей мере на 1,1, по меньшей мере на 1,2 или по меньшей мере на 1,3.
[0055] В определенных аспектах применение способов, предусмотренных в данном документе, т.е. введение бенрализумаба или его антигенсвязывающего фрагмента повышает баллы согласно AQLQ не позднее 4 недель, не позднее 8 недель, не позднее 9 недель, не позднее 10 недель, не позднее 12 недель, не позднее 16 недель, не позднее 20 недель, не позднее 24 недель, не позднее 28 недель, не позднее 32 недель, не позднее 36 недель, не позднее 40 недель, не позднее 44 недель, не позднее 48 недель или не позднее 52 недель.
[0056] В определенных аспектах применение способов, предусмотренных в данном документе, т.е. введение бенрализумаба или его антигенсвязывающего фрагмента пациенту с астмой, нормализует балл согласно опроснику для оценки астмы (например, опроснику по контролю над астмой (ACQ)), снижает годовую частоту приступов и/или повышает форсированный объем выдоха в одну секунду (FEV1).
[0057] В определенных аспектах пациент является "эозинофил-положительным", что означает, что астма пациентов, вероятно, носит эозинофильный характер.
[0058] В определенных аспектах количество эозинофилов в крови пациента с астмой имеет конкретное значение, например, перед введением бенрализумаба или его антигенсвязывающего фрагмента. Количество эозинофилов в крови можно измерять, например, с применением общего анализа крови (CBC) с лейкоцитарной формулой.
[0059] В определенных аспектах количество эозинофилов в крови пациента с астмой перед введением бенрализумаба или его антигенсвязывающего фрагмента составляет по меньшей мере 300 клеток/мкл. В определенных аспектах количество эозинофилов в крови пациента с астмой перед введением бенрализумаба или его антигенсвязывающего фрагмента составляет по меньшей мере 350 клеток/мкл, по меньшей мере 400 клеток/мкл, по меньшей мере 450 клеток/мкл или по меньшей мере 500 клеток/мкл.
[0060] В определенных аспектах количество эозинофилов в крови пациента с астмой перед введением бенрализумаба или его антигенсвязывающего фрагмента составляет менее 300 клеток/мкл. В определенных аспектах количество эозинофилов в крови пациента с астмой перед введением бенрализумаба или его антигенсвязывающего фрагмента составляет по меньшей мере 100 клеток/мкл, по меньшей мере 150 клеток/мкл, по меньшей мере 180 клеток/мкл, по меньшей мере 200 клеток/мкл или по меньшей мере 250 клеток/мкл.
[0061] В определенных аспектах пациенту с астмой прописывали или он использовал среднюю дозу применения ингаляционных кортикостероидов (ICS) перед введением бенрализумаба или его антигенсвязывающего фрагмента. Средняя доза ICS может представлять собой дозу, составляющую по меньшей мере от 600 мкг до 1200 мкг будесонида ежедневно, или эквивалентную дозу другого ICS.
[0062] В определенных аспектах пациенту с астмой прописывали или он использовал высокую дозу применения ICS перед введением бенрализумаба или его антигенсвязывающего фрагмента. Высокая доза ICS может представлять собой дозу, составляющую по меньшей мере 1200 мкг будесонида ежедневно, или эквивалентную дозу другого ICS. Высокая доза ICS также может представлять собой дозу, составляющую от более 1200 мкг до 2000 мкг будесонида ежедневно, или эквивалентную дозу другого ICS.
[0063] В определенных аспектах пациенту с астмой прописывали или он использовал пероральные кортикостероиды перед введением бенрализумаба или его антигенсвязывающего фрагмента. В определенных аспектах введение бенрализумаба или его антигенсвязывающего фрагмента снижает применение пероральных кортикостероидов у пациента с астмой. В определенных аспектах введение снижает применение пероральных кортикостероидов у пациента с астмой по меньшей мере на 50%.
[0064] В определенных аспектах пациенту с астмой прописывали или он использовал бета-агонист длительного действия (LABA) перед введением бенрализумаба или его антигенсвязывающего фрагмента.
[0065] В определенных аспектах пациенту с астмой прописывали или он использовал как ICS, так и LABA перед введением бенрализумаба или его антигенсвязывающего фрагмента.
[0066] В определенных аспектах количество эозинофилов в крови пациента с астмой составляет по меньшей мере 300 клеток/мкл, и он применял высокую дозу ICS перед введением бенрализумаба или его антигенсвязывающего фрагмента.
[0067] В определенных аспектах балл согласно ACQ или ACQ-6 пациента с астмой перед введением бенрализумаба или его антигенсвязывающего фрагмента составляет по меньшей мере 1,5, по меньшей мере 2,0, по меньшей мере 2,5, по меньшей мере 3,0 или по меньшей мере 3,5. В определенных аспектах балл согласно ACQ или ACQ-6 пациента с астмой перед введением бенрализумаба или его антигенсвязывающего фрагмента составляет не более 3,2, не более 3,0, не более 2,9 или не более 2,8.
Примеры
ПРИМЕР 1: Пациенты и методы
(a) СУБЪЕКТЫ
[0068] В данном исследовании требовалось, чтобы субъекты имели возраст 18-75 лет и вес больше 45 кг и меньше или равный 150 кг (больше 100 фунтов, но меньше или равный 330 фунтов). Они также должны иметь диагноз астмы, установленный врачом, на протяжении минимум 12 месяцев перед скринингом, а также прописанное врачом ежедневное применение или ингаляционных кортикостероидов (ICS) в средних или высоких дозах и одновременно бета-агониста длительного действия (LABA) или любой комбинации из последовательного дозирования либо средней дозы, либо высокой дозы ICS/LABA в течение по меньшей мере 12 месяцев перед скринингом. Средние и высокие дозы ICS, как определено в данном исследовании, показаны в таблице 1 ниже.
Предполагаемые сравнительные ежедневные дозировки для ингаляционных кортикостероидов
40 или 80 мкг/впрыск
90, 180 или 200 мкг/ингаляция
80 или 160 мкг/ингаляция
250 мкг/впрыск
80 мкг/впрыск
HFA/MDI: 44, 110 или 220 мкг/впрыск
DPI: 50, 100 или 250 мкг/впрыск
>300-500 мкг
>500 мкг
200 мкг/ингаляция
75 мкг/впрыск
[0069] Доза других контролирующих астму лекарственных препаратов у субъектов должна была быть стабильной в течение по меньшей мере 30 дней перед скринингом. Субъекты также должны были иметь по меньшей мере 2, но не более 6, задокументированных приступов астмы в течение 12 месяцев перед скринингом, требовавших применения пульс-терапии системными кортикостероидами. Кроме того, форсированный объем выдоха в 1 секунду (FEV1) по утрам до приема бронходилататора субъектов должен был составлять по меньшей мере 40% и менее 90% от прогнозируемого во время периода скрининга/вводного периода (описано ниже). Субъекты также должны были удовлетворять одному из следующих критериев:
a) Доказательство обратимости обструкции дыхательных путей после применения бронходилататоров на ≥12% и ≥200 мл, задокументированное не позднее 36 месяцев перед рандомизацией, или доказательство положительного ответа [PC20 ≤8 мг/мл] на провокационную пробу с метахолином, задокументированное не позднее 36 месяцев перед рандомизацией; ИЛИ
b) Повышение FEV1 после применения бронходилататоров на ≥12% и ≥200 мл в визит скрининга на неделе -3; ИЛИ
c) Если a) и b) не соблюдались, а все остальные критерии включения/исключения соблюдались, субъекты с FEV1, составляющим ≥1,5 л и ≥60% от прогнозируемого значения в визит скрининга на неделе -2, могли подвергаться провокационной пробе с метахолином в визит скрининга на неделе -2 в центрах, где тестирование с применением метахолина было доступным. Если у субъекта достигался положительный ответ (PC20 ≤8 мг/мл), тогда данный критерий включения соблюдался.
[0070] Кроме того, балл согласно опроснику по контролю над астмой (ACQ) у субъекта должен был составлять по меньшей мере 1,5 по меньшей мере дважды во время периода скрининга/вводного периода.
[0071] Субъекты не могли принимать участие, если они имели стаж курения 10 пачко-лет или более, или курили не позднее 12 месяцев перед скринингом, или имели любое состояние (например, любое заболевание дыхательной системы с низким содержанием эозинофилов, отличное от астмы, хроническое обструктивное заболевание легких (COPD) или муковисцидоз), которое, по мнению исследователя или медицинского наблюдателя, будет мешать оценке. Субъекты также не могли принимать участие, если они получали пульс-терапию пероральными кортикостероидами или системные кортикостероиды быстрого действия не позднее 30 дней перед скринингом или во время периода скрининга/вводного периода.
(b) СХЕМА ИССЛЕДОВАНИЯ
[0072] Исследование представляло собой рандомизованное, двойное-слепое, плацебо-контролируемое, с подбором оптимальной дозировки, мультицентровое исследование фазы 2b (номер по ClinicalTrials.gov: NCT01238861), в котором несколько доз бенрализумаба подкожно вводили пациентам с астмой. Бенрализумаб вводили из расчета доз 2, 20 или 100 мг, и пациентов наблюдали в течение 1 года. Блок-схема исследования показана на фиг. 1.
[0073] 3-недельный период скрининга/вводный период предшествовал введению бенрализумаба или плацебо. Во время 3-недельного периода субъекты продолжали применение или того же самого комбинированного продукта ICS/LABA в средних или высоких дозах, как перед участием в исследовании (требовалось, чтобы дозы ICS/LABA были стабильными в течение 30 дней перед 3-недельным периодом скрининга/вводным периодом). Субъекты продолжали получать такую же дозу ICS/LABA на протяжении всего исследования.
[0074] Вводимая композиция бенрализумаба содержала бенрализумаб (50 мг/мл), 10 мМ гистидина, 10 мМ гистидин-HCl моногидрата, 9% (вес/объем) трегалозы дигидрата и 0,004% (вес/объем) полисорбата-20, pH 6. Вводимая композиция плацебо содержала 10 мМ гистидина, 10 мМ гистидина гидрохлорида моногидрата, 9% (вес/объем) трегалозы дигидрата и 0,02% (вес/объем) полисорбата-20, pH 6.
[0075] Субъекты получали две подкожные (SC) инъекции по 1 мл бенрализумаба или плацебо через четыре недели на протяжении первых 3 доз в недели 1 (день 1), 4 и 8, а затем через 8 недель впоследствии на протяжении последних 4 доз в недели 16, 24, 32 и 40. После недели 40 субъектов наблюдали в течение дополнительных 12 недель (до недели 52). День получения первой дозы бенрализумаба или плацебо считали днем 1.
[0076] ACQ-6 заполняли в каждый визит скрининга и еженедельно дома вплоть до визита в неделю 52. Центры проверяли соблюдение заполнения ACQ-6 субъектом в каждый визит вплоть до недели 52. В частности, ACQ-6 проводили в визит скрининга 1 (т.е. визит 1 в день -21), а затем заполняли ежедневно дома. ACQ-6 проверяли в визит скрининга 2 (т.е. визит 2 приблизительно в день -14), если имел место визит 2, и в визит скрининга 3 (т.е. визит 3 приблизительно в день -7). Соблюдение заполнения ACQ-6 дома проверяли в неделю 1 (день 1), неделю 4, неделю 8, неделю 12, неделю 16, неделю 24, неделю 40 и неделю 52. Субъектов просили вспомнить, как проходила их астма в течение предыдущей недели с помощью ответа на один вопрос по применению бронходилататоров и 5 вопросов о симптомах.
[0077] Изменение от исходного уровня (последняя действительная оценка перед первым введением исследуемого препарата в день 1) среднего значения ACQ-6 обобщали по обработке и визиту. Изменение от исходного уровня среднего значения ACQ-6 при различных визитах можно было анализировать с помощью ANCOVA с обработкой и исходными значениями в качестве возможных ковариат.
[0078] Субъекты также заполняли дневники симптомов астмы каждое утро дома. Эти дневники проверяли в каждый визит скрининга (за исключением первого визита скрининга) и ежедневно вплоть до недели 52. В этих дневниках субъектов просили вспомнить происходившие с ними случаи, связанные с частотой и тяжестью симптомов в дневное время и ночное время, уклонением от активности и ее ограничением, связанной с астмой тревогой и утомляемостью, а также применением лекарственного препарата неотложной помощи. Каждый симптом из частоты в дневное время, тяжести в дневное время и тяжести в ночное время оценивался субъектом от 0 (отсутствие симптомов) до 4 (наиболее частые/тяжелые симптомы). Общий балл симптомов рассчитывали как среднее значение этих 3 вопросов, касающихся симптомов.
[0079] Субъекты также заполняли опросник оценки качества жизни у больных астмой (стандартную версию). AQLQ[S] представляет собой опросник из 32 пунктов, который измеряет связанное со здоровьем качество жизни, испытываемое пациентами с астмой. Juniper et al., Chest. 115: 1265-70 (1999). AQLQ[S] заполняли в неделю -3 визита скрининга и день 1, а затем через 4 недели дома вплоть до визита недели 52. Соблюдение заполнения проверяли в некоторые визиты вплоть до визита недели 52. Опросник содержит 4 отдельные группы вопросов (симптомы, виды ограничения активности, эмоциональное состояние и воздействия окружающей среды). Субъектов просили вспомнить свое состояние в течение предыдущих 2 недель и выставить балл по каждому из 32 вопросов на основании шкалы из 7 баллов, в диапазоне от 7 (нарушение отсутствует) до 1 (тяжелое нарушение). Общий балл рассчитывали как среднее значение ответа на все вопросы. 4 индивидуальных баллов групп вопросов (симптомы, виды ограничения активности, эмоциональное состояние и воздействия окружающей среды) представляют собой средние значения ответов на вопросы в каждой из групп вопросов. Индивидуальную нормализацию как общего балла, так и индивидуальных баллов групп вопросов на 0,5 рассматривали как минимальное существенное изменение, при этом изменения балла на >1,5 рассматривали как большое значимое изменение. Juniper et al., J Clin Epidemiol. 47: 81-7 (1994).
(c) ОЦЕНКИ БЕЗОПАСНОСТИ
[0080] После введения плацебо или бенрализумаба отслеживали побочные явления. Другие оценки включали врачебное обследование, мониторинг показателей жизненно важных функций и лабораторные измерения.
ПРИМЕР 2: Результаты
(a) ВКЛЮЧЕНИЕ В ИССЛЕДОВАНИЕ И ИСХОДНЫЕ ХАРАКТЕРИСТИКИ
[0081] Исходные характеристики всех рандомизованных субъектов, которые получали любую дозу исследуемого препарата, представлены в таблице 2 ниже. Средняя доза ICS для популяций пациентов составляла 1100 эквивалентов будесонида в целом, 700 эквивалентов будесонида в группе, получающей среднюю дозу, и 1600 эквивалентов будесонида в группе, получающей высокую дозу.
Демографические данные относительно исходного уровня эозинофилов (EOS)
EOS <300
EOS < 300
EOS >=300
EOS >=300
[0082] Исходные характеристики рандомизованных субъектов, которые получали любую дозу исследуемого препарата и имели исходное количество эозинофилов по меньшей мере 300 клеток/мкл, показаны в таблице 3 ниже.
Демографические данные относительно ICS с исходным количеством EOS по меньшей мере 300 клеток/мкл
СРЕДНЯЯ ДОЗА ICS
СРЕДНЯЯ ДОЗА ICS
ВЫСОКАЯ ДОЗА ICS
ВЫСОКАЯ ДОЗА ICS
(b) ЭФФЕКТИВНОСТЬ
[0083] Эффекты введения бенрализумаба на ACQ-6 показаны на фиг. 2-8. Например, данные на фиг. 2 демонстрируют, что к неделе 24 у пациентов с количеством эозинофилов в крови, составляющим по меньшей мере 300 клеток/мкл, которые получали 2, 20 или 100 мг бенрализумаба, показано снижение баллов согласно ACQ-6. Аналогичные результаты также наблюдали в неделю 52 (фиг. 3). Данные на фиг. 4 демонстрируют, что баллы согласно ACQ-6 нормализовались у пациентов, получавших ICS либо в средних дозах, либо в высоких дозах, но нормализация была большей у пациентов, получавших ICS в высоких дозах. Данные на фиг. 5 сравнивают изменения баллов согласно ACQ-6 у пациентов с количеством эозинофилов в крови, составляющим менее 300 клеток/мкл, которые получали ICS в средних дозах, с изменениями у пациентов, получавших ICS в высоких дозах, и данные на фиг. 6 сравнивают изменения баллов согласно ACQ-6 у пациентов с количеством эозинофилов в крови, составляющим по меньшей мере 300 клеток/мкл, которые получали ICS в средних дозах, с изменениями у пациентов, получавших ICS в высоких дозах. Более подробное распределение согласно количеству эозинофилов представлено на фиг. 7. Как показано на фиг. 8, разницу в баллах согласно ACQ-6 между пациентами, получавшими бенрализумаб и плацебо, можно было наблюдать еще на неделе 7 у пациентов с количеством эозинофилов в крови, составляющим по меньшей мере 300 клеток/мкл.
[0084] Эффекты введения бенрализумаба на общие баллы симптомов в дневниках симптомов астмы показаны на фиг. 9. У пациентов с количеством эозинофилов в крови, составляющим по меньшей мере 300 клеток/мкл, которые получали 100 мг бенрализумаба, показаны снижения общих баллов симптомов согласно дневнику более чем на 0,5.
[0085] Эффекты введения бенрализумаба на баллы согласно AQLQ показаны на фиг. 10. У пациентов с количеством эозинофилов в крови, составляющим по меньшей мере 300 клеток/мкл, которые получали бенрализумаб, показаны повышения баллов согласно AQLQ более чем на 0,5 или 1,0.
(c) БЕЗОПАСНОСТЬ
[0086] Вызванные лечением побочные явления (TEAE) встречались у пациентов, которых лечили бенрализумабом, с частотой, которая приблизительно на 10 процентов превышала таковую у пациентов, которых лечили плацебо. Вызванные лечением серьезные побочные явления (TE-SAE) встречались с аналогичной частотой у пациентов, которых лечили бенрализумабом и плацебо. TEAE и TE-SAE не проявляли дозозависимость у пациентов, которых лечили бенрализумабом.
(d) АНТИТЕЛА К ЛЕКАРСТВЕННОМУ СРЕДСТВУ
[0087] Выработка антител к лекарственному средству (ADA), бенрализумабу, была обратно пропорциональна дозе, при этом самую большую долю ADA-положительных субъектов наблюдали в случае дозы, составляющей 2 мг (см. таблицу 4 ниже). Частота появления высоких титров ADA (≥400) составляла 12% и 9% у групп с дозой, составляющей 20 и 100 мг, соответственно. Высокие титры ADA были связаны со сниженной концентрацией бенрализумаба и варьирующими степенями восстановления количества эозинофилов, в случае присутствия. Фармакокинетическое/фармакодинамическое (PK/PD) влияние высоких титров ADA снижалось при воздействии более высоких доз лекарственного средства. Закономерности между TEAE и ADA не наблюдали.
Антитела в лекарственному средству в неделю 24
[0088] Основываясь как на PK, так и на иммунологических соображениях, новые пациенты будут получать дозу, составляющую 30 мг бенрализумаба. У некоторых пациентов дозу, составляющую 30 мг бенрализумаба, будут вводить через четыре недели. У некоторых пациентов дозу, составляющую 30 мг бенрализумаба, будут вводить один раз в четыре недели на протяжении трех доз, а затем один раз в восемь недель впоследствии.
(e) ОБСУЖДЕНИЕ
[0089] Данное исследование демонстрирует, что бенрализумаб нормализует симптомы астмы, измеряемые с применением ACQ-6. Нормализацию наблюдали в случае всех доз, но большая величина благоприятного эффекта была очевидной при дозах, составляющих 20 и 100 мг, по сравнению с дозой, составляющей 2 мг. Кроме того, баллы согласно ACQ-6 нормализовались в большей степени в случае ICS/LABA в высоких дозах, чем в случае ICS/LABA в средних дозах. Дневники симптомов астмы также сообщали о нормализации общих баллов симптомов, основанных на частоте симптомов в дневное время, тяжести симптомов в дневное время и тяжести симптомов в ночное время. Повышенные баллы согласно AQLQ у пациентов также указывают на нормализацию симптомов.
ПРИМЕР 3: Дополнительная оценка доз
[0090] Моделирование эффективности доз осуществляли для обнаружения дополнительных доз бенрализумаба, которые снижают годовую частоту приступов и являются безопасными и хорошо переносимыми. Моделирование показало, что доза, составляющая приблизительно 30 мг, является минимальной эффективной дозой, производящей 90% максимальный эффект лечения. Следовательно, пациенты с неконтролируемой астмой получали подкожные инъекции с 30 мг бенрализумаба или плацебо. Дозы в 30 мг вводили (i) через четыре недели или (ii) через четыре недели на протяжении восьми недель (3 дозы), а затем через восемь недель (т.е. через 8 недель, включая дополнительную дозу в неделю 4). Число приступов у пациентов, получавших 30 мг бенрализумаба, сравнивали с числом приступов у пациентов, получавших плацебо, чтобы продемонстрировать, что дозы, составляющие 30 мг бенрализумаба, снижали годовую частоту приступов. Кроме того, анализировали число приступов у пациентов с исходным количеством эозинофилов в крови, составляющим по меньшей мере 300 клеток/мкл, для демонстрации того, что дозы, составляющие 30 мг бенрализумаба, могут быть эффективны в снижении годовой частоты приступов у таких пациентов.
[0091] Специалисты в данной области техники признают или способны выявить с проведением всего лишь обычных экспериментов многие эквиваленты для конкретных аспектов настоящего раскрытия, описанных в данном документе. Подразумевается, что такие эквиваленты охвачены следующей формулой изобретения.
[0092] В данном документе цитируются различные публикации, раскрытия которых включены посредством ссылки во всей их полноте.
[0093] Хотя вышеизложенное изобретение было описано довольно подробно в качестве иллюстрации и примера для ясности понимания, очевидно, что можно вносить определенные изменения и модификации в пределах объема прилагаемой формулы изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
SEQ ID NO:1
>US20100291073_1 Последовательность 1 из патентного документа США 20100291073 Организм: Homo sapiens
DIQMTQSPSSLSASVGDRVTITCGTSEDIINYLNWYQQKPGKAPKLLIYHTSRLQSGVPSRFSGSGSGTDFTLTISSLQP
EDFATYYCQQGYTLPYTFGQGTKVEIK
SEQ ID NO:2
>US20100291073_2 Последовательность 2 патентного документа США 20100291073 Организм: Homo sapiens
DIQMTQSPSSLSASVGDRVTITCGTSEDIINYLNWYQQKPGKAPKLLIYHTSRLQSGVPSRFSGSGSGTDFTLTISSLQP
EDFATYYCQQGYTLPYTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQ
ESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO:3
>US20100291073_3 Последовательность 3 из патентного документа США 20100291073 Организм: Homo sapiens
EVQLVQSGAEVKKPGASVKVSCKASGYTFTSYVIHWVRQRPGQGLAWMGYINPYNDGTKYNERFKGKVTITSDRSTSTVY
MELSSLRSEDTAVYLCGREGIRYYGLLGDYWGQGTLVTVSS
SEQ ID NO:4
>US20100291073_4 Последовательность 4 из патентного документа США 20100291073 Организм: Homo sapiens
EVQLVQSGAEVKKPGASVKVSCKASGYTFTSYVIHWVRQRPGQGLAWMGYINPYNDGTKYNERFKGKVTITSDRSTSTVY
MELSSLRSEDTAVYLCGREGIRYYGLLGDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTV
SWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLG
GPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNG
KEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPP
VLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:5
>US20100291073_5 Последовательность 5 из патентного документа США 20100291073 Организм: Homo sapiens
DLLPDEKISLLPPVNFTIKVTGLAQVLLQWKPNPDQEQRNVNLEYQVKINAPKEDDYETRITESKCVTILHKGFSASVRT
ILQNDHSLLASSWASAELHAPPGSPGTSIVNLTCTTNTTEDNYSRLRSYQVSLHCTWLVGTDAPEDTQYFLYYRYGSWTE
ECQEYSKDTLGRNIACWFPRTFILSKGRDWLAVLVNGSSKHSAIRPFDQLFALHAIDQINPPLNVTAEIEGTRLSIQWEK
PVSAFPIHCFDYEVKIHNTRNGYLQIEKLMTNAFISIIDDLSKYDVQVRAAVSSMCREAGLWSEWSQPIYVGNDEHKPLR
EWFVIVIMATICFILLILSLICKICHLWIKLFPPIPAPKSNIKDLFVTTNYEKAGSSETEIEVICYIEKPGVETLEDSVF
SEQ ID NO:6
>US20100291073_6 Последовательность 6 из патентного документа США 20100291073 Организм: Mus musculus
DLLNHKKFLLLPPVNFTIKATGLAQVLLHWDPNPDQEQRHVDLEYHVKINAPQEDEYDTRKTESKCVTPLHEGFAASVRT
ILKSSHTTLASSWVSAELKAPPGSPGTSVTNLTCTTHTVVSSHTHLRPYQVSLRCTWLVGKDAPEDTQYFLYYRFGVLTE
KCQEYSRDALNRNTACWFPRTFINSKGFEQLAVHINGSSKRAAIKPFDQLFSPLAIDQVNPPRNVTVEIESNSLYIQWEK
PLSAFPDHCFNYELKIYNTKNGHIQKEKLIANKFISKIDDVSTYSIQVRAAVSSPCRMPGRWGEWSQPIYVGKERKSLVE
WHLIVLPTAACFVLLIFSLICRVCHLWTRLFPPVPAPKSNIKDLPVVTEYEKPSNETKIEVVHCVEEVGFEVMGNSTF
SEQ ID NO:7 - VH CDR1
SYVIH
SEQ ID NO:8 - VH CDR2
YINPYNDGTKYNERFKG
SEQ ID NO:9 - VH CDR3
EGIRYYGLLGDY
SEQ ID NO:10 - VL CDR1
GTSEDIINYLN
SEQ ID NO:11 - VL CDR2
HTSRLQS
SEQ ID NO:12 - VL CDR3
QQGYTLPYT
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> МЕДИММЬЮН, ЭлЭлСи
<120> СПОСОБЫ НОРМАЛИЗАЦИИ СИМПТОМОВ АСТМЫ С ПРИМЕНЕНИЕМ БЕНРАЛИЗУМАБА
<130> IL5R-605WO1
<140>
<141>
<150> 61/864950
<151> 2013-08-12
<160> 12
<170> PatentIn версия 3.5
<210> 1
<211> 107
<212> БЕЛОК
<213> Homo sapiens
<400> 1
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gly Thr Ser Glu Asp Ile Ile Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 2
<211> 214
<212> БЕЛОК
<213> Homo sapiens
<400> 2
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gly Thr Ser Glu Asp Ile Ile Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 3
<211> 121
<212> БЕЛОК
<213> Homo sapiens
<400> 3
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Val Ile His Trp Val Arg Gln Arg Pro Gly Gln Gly Leu Ala Trp Met
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Gly Thr Lys Tyr Asn Glu Arg Phe
50 55 60
Lys Gly Lys Val Thr Ile Thr Ser Asp Arg Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Leu Cys
85 90 95
Gly Arg Glu Gly Ile Arg Tyr Tyr Gly Leu Leu Gly Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 4
<211> 451
<212> БЕЛОК
<213> Homo sapiens
<400> 4
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Val Ile His Trp Val Arg Gln Arg Pro Gly Gln Gly Leu Ala Trp Met
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Gly Thr Lys Tyr Asn Glu Arg Phe
50 55 60
Lys Gly Lys Val Thr Ile Thr Ser Asp Arg Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Leu Cys
85 90 95
Gly Arg Glu Gly Ile Arg Tyr Tyr Gly Leu Leu Gly Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 5
<211> 400
<212> БЕЛОК
<213> Homo sapiens
<400> 5
Asp Leu Leu Pro Asp Glu Lys Ile Ser Leu Leu Pro Pro Val Asn Phe
1 5 10 15
Thr Ile Lys Val Thr Gly Leu Ala Gln Val Leu Leu Gln Trp Lys Pro
20 25 30
Asn Pro Asp Gln Glu Gln Arg Asn Val Asn Leu Glu Tyr Gln Val Lys
35 40 45
Ile Asn Ala Pro Lys Glu Asp Asp Tyr Glu Thr Arg Ile Thr Glu Ser
50 55 60
Lys Cys Val Thr Ile Leu His Lys Gly Phe Ser Ala Ser Val Arg Thr
65 70 75 80
Ile Leu Gln Asn Asp His Ser Leu Leu Ala Ser Ser Trp Ala Ser Ala
85 90 95
Glu Leu His Ala Pro Pro Gly Ser Pro Gly Thr Ser Ile Val Asn Leu
100 105 110
Thr Cys Thr Thr Asn Thr Thr Glu Asp Asn Tyr Ser Arg Leu Arg Ser
115 120 125
Tyr Gln Val Ser Leu His Cys Thr Trp Leu Val Gly Thr Asp Ala Pro
130 135 140
Glu Asp Thr Gln Tyr Phe Leu Tyr Tyr Arg Tyr Gly Ser Trp Thr Glu
145 150 155 160
Glu Cys Gln Glu Tyr Ser Lys Asp Thr Leu Gly Arg Asn Ile Ala Cys
165 170 175
Trp Phe Pro Arg Thr Phe Ile Leu Ser Lys Gly Arg Asp Trp Leu Ala
180 185 190
Val Leu Val Asn Gly Ser Ser Lys His Ser Ala Ile Arg Pro Phe Asp
195 200 205
Gln Leu Phe Ala Leu His Ala Ile Asp Gln Ile Asn Pro Pro Leu Asn
210 215 220
Val Thr Ala Glu Ile Glu Gly Thr Arg Leu Ser Ile Gln Trp Glu Lys
225 230 235 240
Pro Val Ser Ala Phe Pro Ile His Cys Phe Asp Tyr Glu Val Lys Ile
245 250 255
His Asn Thr Arg Asn Gly Tyr Leu Gln Ile Glu Lys Leu Met Thr Asn
260 265 270
Ala Phe Ile Ser Ile Ile Asp Asp Leu Ser Lys Tyr Asp Val Gln Val
275 280 285
Arg Ala Ala Val Ser Ser Met Cys Arg Glu Ala Gly Leu Trp Ser Glu
290 295 300
Trp Ser Gln Pro Ile Tyr Val Gly Asn Asp Glu His Lys Pro Leu Arg
305 310 315 320
Glu Trp Phe Val Ile Val Ile Met Ala Thr Ile Cys Phe Ile Leu Leu
325 330 335
Ile Leu Ser Leu Ile Cys Lys Ile Cys His Leu Trp Ile Lys Leu Phe
340 345 350
Pro Pro Ile Pro Ala Pro Lys Ser Asn Ile Lys Asp Leu Phe Val Thr
355 360 365
Thr Asn Tyr Glu Lys Ala Gly Ser Ser Glu Thr Glu Ile Glu Val Ile
370 375 380
Cys Tyr Ile Glu Lys Pro Gly Val Glu Thr Leu Glu Asp Ser Val Phe
385 390 395 400
<210> 6
<211> 398
<212> БЕЛОК
<213> Mus musculus
<400> 6
Asp Leu Leu Asn His Lys Lys Phe Leu Leu Leu Pro Pro Val Asn Phe
1 5 10 15
Thr Ile Lys Ala Thr Gly Leu Ala Gln Val Leu Leu His Trp Asp Pro
20 25 30
Asn Pro Asp Gln Glu Gln Arg His Val Asp Leu Glu Tyr His Val Lys
35 40 45
Ile Asn Ala Pro Gln Glu Asp Glu Tyr Asp Thr Arg Lys Thr Glu Ser
50 55 60
Lys Cys Val Thr Pro Leu His Glu Gly Phe Ala Ala Ser Val Arg Thr
65 70 75 80
Ile Leu Lys Ser Ser His Thr Thr Leu Ala Ser Ser Trp Val Ser Ala
85 90 95
Glu Leu Lys Ala Pro Pro Gly Ser Pro Gly Thr Ser Val Thr Asn Leu
100 105 110
Thr Cys Thr Thr His Thr Val Val Ser Ser His Thr His Leu Arg Pro
115 120 125
Tyr Gln Val Ser Leu Arg Cys Thr Trp Leu Val Gly Lys Asp Ala Pro
130 135 140
Glu Asp Thr Gln Tyr Phe Leu Tyr Tyr Arg Phe Gly Val Leu Thr Glu
145 150 155 160
Lys Cys Gln Glu Tyr Ser Arg Asp Ala Leu Asn Arg Asn Thr Ala Cys
165 170 175
Trp Phe Pro Arg Thr Phe Ile Asn Ser Lys Gly Phe Glu Gln Leu Ala
180 185 190
Val His Ile Asn Gly Ser Ser Lys Arg Ala Ala Ile Lys Pro Phe Asp
195 200 205
Gln Leu Phe Ser Pro Leu Ala Ile Asp Gln Val Asn Pro Pro Arg Asn
210 215 220
Val Thr Val Glu Ile Glu Ser Asn Ser Leu Tyr Ile Gln Trp Glu Lys
225 230 235 240
Pro Leu Ser Ala Phe Pro Asp His Cys Phe Asn Tyr Glu Leu Lys Ile
245 250 255
Tyr Asn Thr Lys Asn Gly His Ile Gln Lys Glu Lys Leu Ile Ala Asn
260 265 270
Lys Phe Ile Ser Lys Ile Asp Asp Val Ser Thr Tyr Ser Ile Gln Val
275 280 285
Arg Ala Ala Val Ser Ser Pro Cys Arg Met Pro Gly Arg Trp Gly Glu
290 295 300
Trp Ser Gln Pro Ile Tyr Val Gly Lys Glu Arg Lys Ser Leu Val Glu
305 310 315 320
Trp His Leu Ile Val Leu Pro Thr Ala Ala Cys Phe Val Leu Leu Ile
325 330 335
Phe Ser Leu Ile Cys Arg Val Cys His Leu Trp Thr Arg Leu Phe Pro
340 345 350
Pro Val Pro Ala Pro Lys Ser Asn Ile Lys Asp Leu Pro Val Val Thr
355 360 365
Glu Tyr Glu Lys Pro Ser Asn Glu Thr Lys Ile Glu Val Val His Cys
370 375 380
Val Glu Glu Val Gly Phe Glu Val Met Gly Asn Ser Thr Phe
385 390 395
<210> 7
<211> 5
<212> БЕЛОК
<213> Homo sapiens
<400> 7
Ser Tyr Val Ile His
1 5
<210> 8
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 8
Tyr Ile Asn Pro Tyr Asn Asp Gly Thr Lys Tyr Asn Glu Arg Phe Lys
1 5 10 15
Gly
<210> 9
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 9
Glu Gly Ile Arg Tyr Tyr Gly Leu Leu Gly Asp Tyr
1 5 10
<210> 10
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 10
Gly Thr Ser Glu Asp Ile Ile Asn Tyr Leu Asn
1 5 10
<210> 11
<211> 7
<212> БЕЛОК
<213> Homo sapiens
<400> 11
His Thr Ser Arg Leu Gln Ser
1 5
<210> 12
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 12
Gln Gln Gly Tyr Thr Leu Pro Tyr Thr
1 5
<---
Изобретение относится к медицине и может быть использовано для лечения астмы посредством нормализации балла согласно опроснику для оценки астмы у пациента. Для этого подкожно вводят пациенту бенрализумаб или его антигенсвязывающий фрагмент в дозе 30 мг один раз в четыре недели на протяжении двенадцати недель. Затем один раз в восемь недель. При этом количество эозинофилов в крови пациента составляет по меньшей мере 300 клеток/мкл. Опросник для оценки астмы выбран из группы, состоящей из опросника по контролю над астмой (ACQ), опросника-6 по контролю над астмой (ACQ-6) и опросника оценки качества жизни у больных астмой (AQLQ). Изобретение обеспечивает нормализацию балла согласно опроснику для оценки астмы у пациента с астмой. 10 з.п. ф-лы, 4 табл., 10 ил., 3 пр.
1. Способ лечения астмы посредством нормализации балла согласно опроснику для оценки астмы у пациента с астмой, включающий введение подкожно пациенту дозы 30 мг один раз в четыре недели на протяжении двенадцати недель, а затем один раз в восемь недель бенрализумаба или его антигенсвязывающего фрагмента, где количество эозинофилов в крови пациента составляет по меньшей мере 300 клеток/мкл, и где опросник для оценки астмы выбран из группы, состоящей из опросника по контролю над астмой (ACQ), опросника-6 по контролю над астмой (ACQ-6) и опросника оценки качества жизни у больных астмой (AQLQ).
2. Способ по п. 1, где опросник оценивает по меньшей мере один симптом, выбранный из группы, состоящей из ночного пробуждения, симптомов при пробуждении, ограничения активности, одышки, свистящего дыхания, применения лекарственного препарата неотложной помощи, частоты и тяжести симптомов в дневное время, частоты и тяжести симптомов в ночное время, уклонения от активности и ее ограничения, связанной с астмой тревоги и утомляемости.
3. Способ по п. 1, где балл пациента согласно ACQ снижается.
4. Способ по п. 1, где балл пациента согласно ACQ-6 снижается.
5. Способ по п. 1, где астма представляет собой эозинофильную астму.
6. Способ по п. 1, где балл пациента согласно ACQ-6 снижается после введения бенрализумаба или его антигенсвязывающего фрагмента.
7. Способ по п. 6, где балл согласно ACQ-6 снижается по меньшей мере на 0,5.
8. Способ по п. 1, где пациент применяет ингаляционные кортикостероиды (ICS) в высоких дозах.
9. Способ по п. 1, где пациент применяет агонисты β2 длительного действия (LABA).
10. Способ по п. 1, где у пациента есть приступы в анамнезе.
11. Способ по п. 1, где бенрализумаб или его антигенсвязывающий фрагмент вводят в дополнение к терапии кортикостероидами.
| US 2012156194 A1, 21.06.2012 | |||
| US 2012328606 A1, 27.12.2012 | |||
| JUNIPER EF | |||
| et al., Identifying 'well-controlled' and 'not well-controlled' asthma using the Asthma Control Questionnaire, Respir Med | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| АВДЕЕВ С.Н | |||
| Опросник ACQ - новый инструмент оценки контроля над бронхиальной астмой, Пульмонология, 2011, N 2, с.93-99. | |||
Авторы
Даты
2020-07-30—Публикация
2014-08-07—Подача