Данное изобретение относится к бактериальному штамму Lactobacillus plantarum Gos 42 (DSM 32131), и композициям, содержащим его, для применения в качестве пробиотика. Предложенный штамм в частности полезен в медицине, особенно при лечении и/или профилактике воспаления. Штамм и композиции, содержащие его, особенно полезны при лечении и/или предотвращении воспаления в полости рта, предпочтительно для лечения и/или профилактики гингивита и/или перидонтита.
В частности, штамм и композиции, содержащие его, могут быть применены в качестве противовоспалительных агентов для снижения или ингибирования высвобождения одного или более воспалительных факторов, выбранных из группы, состоящей из интерлейкина 1 (ИЛ-1), интерлейкина 6 (ИЛ-6), интерлейкина 8 (ИЛ-8), фактор некроза опухоли (ФНО), простагландина E2 (PGE2), изопростанов, матриксной металлопептидазы 9 (MMP9) и NF-κB (ядерного фактора «каппа-би»).
Предпочтительно штамм по изобретению представляет собой пробиотик, то есть микроганизм, который приносит выгоду при выращивании в конкретном микроокружении, например, ингибирование или предотвращение роста других организмов в пределах того же микроокружения. Примеры пробиотических микроорганизмов включают лактобактерии, которые могут колонизировать желудочно-кишечный тракт, по меньшей мере временно, для вытеснения или уничтожения патогенных организмов, а также для предоставления других преимуществ хозяину.
Используемый в данном документе термин «пробиотик» относится к микроорганизмам, которые образуют по меньшей мере часть транзиторной или эндогенной флоры и тем самым проявляют благоприятный профилактический и/или терапевтический эффект на организм-хозяин. Специалистам в данной области техники известно, что пробиотики являются клинически безопасными (то есть, непатогенными). В качестве примера, а не ограничения каким-либо конкретным механизмом, профилактический и/или терапевтический эффект бактерий, продуцирующих кислоту по данному изобретению, частично обусловлен конкурентным ингибированием роста патогенов из-за: (i) их превосходящей способности к колонизации; (ii) паразитизму нежелательных микроорганизмов; (iii) продуцированию кислоты (например, молочной, уксусной и других кислотных соединений) и/или других внеклеточных продуктов, обладающих антимикробной активностью; и (iv) различным их комбинациям. Следует отметить, что вышеупомянутые продукты и активности кислотообразующих бактерий по данному изобретению действуют синергически для получения полезного пробиотического эффекта, описанного в данном документе.
Под очищенным или изолированным препаратом бактериального штамма подразумевается, что препарат не содержит других бактериальных видов или штаммов в количестве, достаточном для вмешательства в репликацию препарата при определенной температуре. Очищенный или выделенный препарат бактериального штамма получают с использованием стандартных способов, например, нанесение покрытия при предельном разбавлении и выборе температуры.
Воспалительные состояния десен в первую очередь вызваны образованием зубного налета. Колонизирующие бактерии образуют биопленку на поверхности зубов с помощью присутствия пищевых остатков, а также компонентов слюны. Если на ранней стадии недостаточно очистить, зубные пленки на поверхности зубов приводят к осаждению зубного камня, который очень трудно удалить. Наличие повышенного количества бактерий на краю десны приводит к воспалению десны, известному как гингивит. У восприимчивых людей гингивит может прогрессировать до периодонтита, что может привести к потере зубов. В частности, липополисахариды (ЛПС), присутствующие в грамотрицательных бактериях, могут вызывать неспецифический иммунный ответ ЛПС-стимулированными макрофагами, которые высвобождают простагландин E2 (PEG2) и провоспалительные медиаторы, такие как интерлейкины и ФНО-α в пораженной ткани. Провоспалительные медиаторы индуцируют высвобождение дополнительных PGE2 и матриксных металлопротеиназ (MMP) из фибробластов, которые разрушают внеклеточный матрикс окружающей ткани. Это позволяет бактериям проникать глубже в ткань и способствовать воспалительному процессу независимо от внешнего слоя эпителия и корня зуба, что вызывает образование периодонтального кармана. Альвеолярная кость, поддерживающая зуб, резорбирует впереди продвигающихся бактерий и, заставляя зуб становиться неустойчивым и, если его не лечить, он выпадет.
Чтобы избежать прогрессирующего разрушения десен, воспалительные реакции в полости рта необходимо подавлять на ранних стадиях или в идеале предотвратить.
Для решения этой проблемы было поставлено много разных подходов, начиная от усовершенствованных методов механического удаления зубного налета с использованием продуктов для ухода за полостью рта с сильными антибактериальными свойствами.
Однако не все бактерии, присутствующие в ротовой полости, связаны с болезнью, и многие даже способствуют здоровью полости рта. Поэтому желательно установить баланс по отношению к здоровому составу микробиоты рта вместо неспецифического уничтожения резидентных бактерий.
Обычная микробиота ротовой полости очень сложна и включает более 700 бактериальных видов, а также археи, грибы, простейшие и вирусы. Было показано, что комменсалы нижней челюсти, такие как лактобактерии и бифидобактерии, оказывают благотворное влияние на здоровье кишечника, включая некоторые противовоспалительные свойства, при введении в качестве пробиотиков.
Пробиотическое действие бактерий в полости рта было подвергнуто некоторым исследованиям, но результаты сильно варьируют в зависимости от используемых видов и подходящих параметров для эффективного применения, которые трудно установить, поскольку действие может опираться на в значительной степени несвязанные эффекты.
Среди пробиотических воздействий общие антибактериальные эффекты против связанных с болезнью видов, уменьшение или предотвращение бактериальной адгезии к поверхности зубов, а также противовоспалительное действие обсуждались в литературе.
Однако мало известно о влиянии специфических пробиотических штаммов на воспалительные механизмы, в частности, в отношении подавления различных воспалительных медиаторов. Примечательно, что в обширных исследованиях, ведущих к данному изобретению, было обнаружено, что некоторые штаммы общепризнанных пробиотических бактерий могут также усиливать выделение провоспалительных факторов в определенных дозах. Следовательно, остается неудовлетворенная потребность в штаммах, которые проявляют желательный эффект на провоспалительные и противовоспалительные медиаторы воспаления.
Целью данного изобретения является создание бактериального штамма и композиций, содержащих его, которые могут быть применены в медицине, особенно при лечении и/или профилактике воспаления, например, в полости рта, в частности при лечении и/или профилактике гингивита и/или периодонтита.
Еще одной целью данного изобретения является создание бактериального штамма и композиций, содержащих его, которые способны снижать или ингибировать высвобождение одного или более воспалительных факторов, такого как интерлейкина 1 (ИЛ-1), интерлейкина 6 (ИЛ-6), интерлейкина 8 (ИЛ-8), фактор некроза опухоли (ФНО), простагландина E2 (PGE2), изопростанов, матриксной металлопептидазы 9 (MMP9) и NF-κB (ядерного фактора «каппа-би»).
Целью данного изобретения является обеспечение штамма Lactobacillus plantarum GOS 42, который был депонирован Probi AB из Sölvegatan 41, 22370 Лунд, Швеция в коллекцию микроорганизмов и культур клеток Leibniz Institute DSMZ-German, Inhoffenstr. 7 B, D-38124 Брауншвейг, в соответствии с требованиями Будапештского договора от 2 сентября 2015 года и получил номер доступа к депозиту DSM 32131 и композиции, содержащие его.
Штамм по изобретению был выделен из слюны здоровых людей-добровольцев и выбран из более чем 50 потенциальных пробиотических штаммов, включая штаммы Bacillus subtilis, Bifidobacterium animalis, Bifidobacterium bifidum, Bifdobacterium longum, Bifidobacterium breve, Bifidobacterium lactis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus LAFTI, Lactobacillus plantarum, Lactobacillus reuteri, Lactobacillus rhamnosus, Lactobacillus paracasei, Lactobacillus bulgaricus, Lactobacillus gasseri, Lactobacillus fermentum, Lactobacillus brevis, Lactobacillus cellobiosus, Lactobacillus salivarius, Streptococcus thermophilus и Lactococcus lactis.
При обширных скринингах бактериальный штамм в соответствии с изобретением был идентифицирован, чтобы проявлять отчетливую модулирующую активность, главным образом, ингибирующим способом против высвобождения определенных провоспалительных факторов, при этом в то же время не только или только незначительно усиливает высвобождение других провоспалительных факторов. Данное изобретение теперь позволяет оптимизировать использование пробиотического бактериального штамма для профилактики и/или лечения воспалительных состояний, особенно тех, которые происходят в полости рта, что было невозможно до этого.
Как объяснялось выше, колонизация слизистой оболочки полости рта бактериями, связанными с болезнями, и образование пятна могут перевернуть микробный баланс в полости рта в сторону накопления вредных микроорганизмов, что также называется дисбактериозом. Следовательно, микроорганизм, используемый для профилактики и/или лечения воспаления в полости рта в соответствии с изобретением, включает использование в профилактике и/или лечении заболеваний, связанных с пятном и пятнами, чтобы избежать дисбактериоза в ротовой полости путем балансирования флоры рта к здоровому состоянию.
В предпочтительном варианте осуществления данного изобретения описанный выше микроорганизм является аттенуированным или мертвым, предпочтительно термически инактивированным, в идеале путем инкубации в течение 2-8 минут при температуре от 70 до 100°C.
В исследованиях, описанных ниже, было продемонстрировано, что микроорганизм согласно изобретению может оказывать ингибирующее действие на высвобождение провоспалительных факторов даже в инактивированном состоянии. Поэтому также возможно использовать штамм, когда он является мертвым или термически инактивированным. Примечательно, что термически инактивированные штаммы могут проявлять ту же или даже слегка усиленную противовоспалительную активность по отношению к определенным факторам.
В одном аспекте данное изобретение относится к указанному выше микроорганизму для применения в качестве противовоспалительного средства, особенно для восстановления или ингибирования высвобождения одного или более воспалительных факторов, выбранных из группы, состоящей из интерлейкина 1 (ИЛ-1), интерлейкина 6 (ИЛ-6), интерлейкина 8 (ИЛ-8), фактор некроза опухоли (ФНО), простагландина E2 (PGE2), изопростанов, матриксной металлопептидазы 9 (MMP9) и NF-κB (ядерного фактора «каппа-би»).
В соответствии с другим аспектом данного изобретения фрагменты штамма микроорганизма, как определено в любом из аспектов, описанных выше, могут быть применены для лечения и/или профилактики воспаления, особенно в полости рта, и предпочтительно в лечении и/или профилактике гингивита и/или периодонтита.
Возможно, нет необходимости использовать целые клетки штамма по изобретению, поскольку смеси, содержащие только фрагменты (например, обломки деградированных клеток) микроорганизмов, являются достаточными для обеспечения эффектов изобретения.
В еще одном аспекте данное изобретение также относится к фармацевтической композиции, содержащей Lactobacillus plantarum GOS 42 или его фрагменты и фармацевтически приемлемый носитель, эксципиент и/или разбавитель. Общее количество микроорганизма или его фрагментов предпочтительно является достаточным для лечения и/или предотвращения воспаления, особенно в полости рта, предпочтительно для лечения и/или предотвращения гингивита и/или периодонтита. Предпочтительно общее количество микроорганизма или его фрагментов находится в диапазоне от 0,01 до 100%, более предпочтительно в диапазоне от 0,1 до 50%, наиболее предпочтительно в диапазоне от 1 до 10%, в каждом случае по отношению к общей массы композиции и/или где общее количество микроорганизма(ов) или его фрагментов находится в диапазоне от 1 × 103 до 1 × 1011 колониеобразующих единиц (КОЕ), более предпочтительно в диапазоне от 1 × 105 до 1 x 1010 КОЕ, и в идеале от 1 x 108 до 1 x 109 КОЕ.
В предпочтительном варианте осуществления микроорганизм (бактерии) согласно изобретению присутствует в композиции в концентрации, равной приблизительно 1 x 103 - 1 x 1014 колониеобразующих единиц (КОЕ) на грамм, предпочтительно приблизительно 1 x 105 - 1 x 1012 КОЕ/грамм, тогда как в других вариантах осуществления концентрации, равны приблизительно 1 x 109 - 1 x 1013 КОЕ/грамм, приблизительно 1 x 105 - 1 x 107 КОЕ/грамм или приблизительно 1 x 108 - 1 x 109 КОЕ/грамм. Тем не менее, будет понятно, что это самая общая КОЕ, а не концентрация, которая является наиболее важной.
В одном варианте бактерии по изобретению находятся в фармацевтически приемлемом носителе или пищевом продукте, пригодном для перорального введения млекопитающему, предпочтительно в виде порошкообразной пищевой добавки, гранулированной композиции или жидкой композиции. Млекопитающее предпочтительно представляет собой человека.
Специалисту известно, что пробиотический организм, используемый в композиции или продукте согласно изобретению, представляет собой биологический материал, активность которого может варьировать в зависимости от партии и зависит также от способа получения или обработки. Следовательно, подходящее количество может быть соответствующим образом отрегулировано в заданном диапазоне.
Кроме того, данное изобретение относится к композиции или продукту, как описано выше, для применения в медицине, предпочтительно при лечении и/или предотвращении воспаления, особенно в полости рта, и наиболее предпочтительно для применения при лечении и/или профилактике гингивита и/или периодонтита.
Композиция согласно изобретению может дополнительно содержать один или более компонентов, выбранных из группы, состоящей из носителей, эксципиентов или других активных ингредиентов, таких как, например, активные агенты из группы нестероидных противовоспалительных средств, антибиотики, стероиды, антитела против ФНО-альфа или других биотехнологически полученных активных агентов и/или веществ, а также анальгетики, декспантенол, преднизон, поливидон йодид, хлоргексидин-бис-D-глюконат, гексетидин, бензидамин HCl, лидокаин, бензокаин, макроголовый лауриловый эфир, бензокаин в сочетании с хлоридом цетидилпиридиния или макролиновым лауриловым эфиром в сочетании с гемодиализатом из крови теленка, свободным от белка, а также, например, наполнителей (например, целлюлоза, карбонат кальция), пластификаторы или вещества, улучшающие текучесть (например, тальк, стеарат магния), покрытия (например, поливинилацетат-фталат, гидроксилпропилметилцеллюлоза фталат), разрыхлители (например, крахмал, сшитый поливинилпирролидон), смягчитель (например, триэтилцитрат, дибутилфталат) вещества для гранулирования (лактоза, желатин), ретарданты (например, поли (мет) акриловой кислоты метил/этил/2-триметил сополимеризаты аминометилового эфира в дисперсии, винилацетат/сополимеризаты кротоновой кислоты), уплотнители (например, микрокристаллическая целлюлоза, лактоза), растворители, суспендирующие или диспергирующие агенты (например, вода, этанол), эмульгаторы (например, цетиловый спирт, лецитин), вещества для модификации реологических свойств (диоксид кремния, альгинат натрия), вещества для микробной стабилизации (например, хлорид бензалкония, сорбат калия), консерванты и антиоксиданты (например, DL-альфа-токоферол, аскорбиновая кислота) вещества для модификации pH (молочная кислота, лимонная кислота), вспенивающие агенты или инертные газы (например, фторированные хлорированные углеводороды, диоксид углерода), красители (оксид железа, оксид титана), основные ингредиенты для мази (например парафины, пчелиный воск) и другие, описанные в литературе (например, в Schmidt, Christin. Wirk- und Hilfsstoffe für Rezeptur, Defektur und Großherstellung. 1999; Wissenschaftliche Verlagsgesellschaft mbH Stuttgart oder Bauer, Frömming Führer. Lehrbuch der Pharmazeutischen Technologie. 8. Auflage, 2006. Wissenschaftliche Verlagsgesellschaft mbH Stuttgart).
Композиция или продукт в соответствии с данным изобретением также могут быть покрыты или инкапсулированы.
Инкапсулирование композиции в соответствии с изобретением может иметь то преимущество, что позволяет контролируемое высвобождение, например, при контакте с водой, или обеспечивать непрерывное высвобождение в течение длительного периода времени. Кроме того, композиция может быть защищена от деградации, что увеличивает срок годности продукта. Способы инкапсулирования активных ингредиентов хорошо известны в данной области техники, и имеется ряд материалов для инкапсуляции, а также способы их применения в композиции в соответствии с конкретными требованиями.
Кроме того, композиция или продукт в соответствии с изобретением могут быть в форме раствора, суспензии, эмульсии, таблеток, гранул, порошка или капсул.
Композиция или продукт в соответствии с изобретением могут быть выбраны из группы, состоящей из зубной пасты, зубного геля, зубного порошка, жидкости для чистки зубов, пены для чистки зубов, мытья полости рта, полоскания рта, спрея для рта, зубной нити, жевательной резинки и пастилки.
Такие композиции или продукты могут содержать абразивные системы (абразивные и/или полирующие компоненты) такие как силикаты, карбонат кальция, фосфат кальция, оксид алюминия и/или гидроксилапатит, поверхностно-активные вещества, такие как, например, лаурилсульфат натрия, лаурилсаркозинат натрия и/или кокамидопропилбетаин, увлажнители, такие как глицерин и/или сорбит, загустители, например, карбоксиметилцеллюлоза, полиэтиленгликоли, каррагинаны и/или Laponite®, подсластители, такие как сахарин, ароматизаторы и вкусовые добавки для устранения неприятных вкусовых впечатлений, вещества, модифицирующие вкус (например инозитолфосфат, нуклеотиды, например. гуанозинмонофосфат, аденозинмонофосфат или другие вещества, например. глутамат натрия или 2-феноксипропионовая кислота), охлаждающие агенты, такие как производные ментола (например, L-менталактат, L-ментилалкилкарбонат, ментоновые кетали), ицилин и производные ицилина, стабилизаторы и активные агенты, такие как фторид натрия, монофторфосфат натрия, дифторид олова, четвертичные аммониевые фториды, цитрат цинка, сульфат цинка, пирофосфат олова, дихлорид олова, смеси различных пирофосфатов, триклозан, хлорид цетилпиридиния, лактат алюминия, цитрат калия, нитрат калия, хлорид калия, хлорид стронция, перекись водорода, вещества-ароматизаторы, бикарбонат натрия и/или средства для коррекции запаха.
Жевательные резинки или жевательные резинки для ухода за полостью рта могут содержать основу жевательной резинки, содержащую эластомеры, например, поливинилацетат (PVA), полиэтилен, (низко или среднемолекулярный) полиизобутан (PIB), полибутадиен, изобутен/изопреновые сополимеры, поливинилэтиловый эфир (PVE), поливинилбутиловый эфир, виниловые эфиры и сополимеры виниловых эфиров, сополимеры стирола и бутадиена (SBR) или виниловые эластомеры, например, на основе винилацетата / виниллаурата, винилацетата / винилстеарата или этилена / винилацетата и смесей указанных эластомеров, например, примеры описаны EP 0 242325, US 4518615, US 5093136, US 5266336 US 5601858 или US 6986709. Кроме того, основы жевательной резинки могут содержать дополнительные ингредиенты, например, (минеральные) наполнители, т.е. карбонат кальция, диоксид титана, диоксид кремния, тальк, оксид алюминия, дикальцийфосфат, трикальцийфосфат, гидроксид магния и их смеси, пластификаторы (например, ланолин, стеариновая кислота, стеарат натрия, диацетат (диацетат глицерина), триацетин (триацетат глицерина ) и триацетат цитрат), эмульгаторы (например, фосфатиды, такие как лецитин, моно и диглицериды жирных кислот, например, моностеарат глицерина), антиоксиданты, воски (например, парафиновые воски, канделильные воски, карнаубские воски, микрокристаллические воски и полиэтиленовые воски), жиры или жирные масла (например, твердые (гидрированные) растительные или животные жиры) и моно, ди или триглицериды.
Краткое описание фигур:
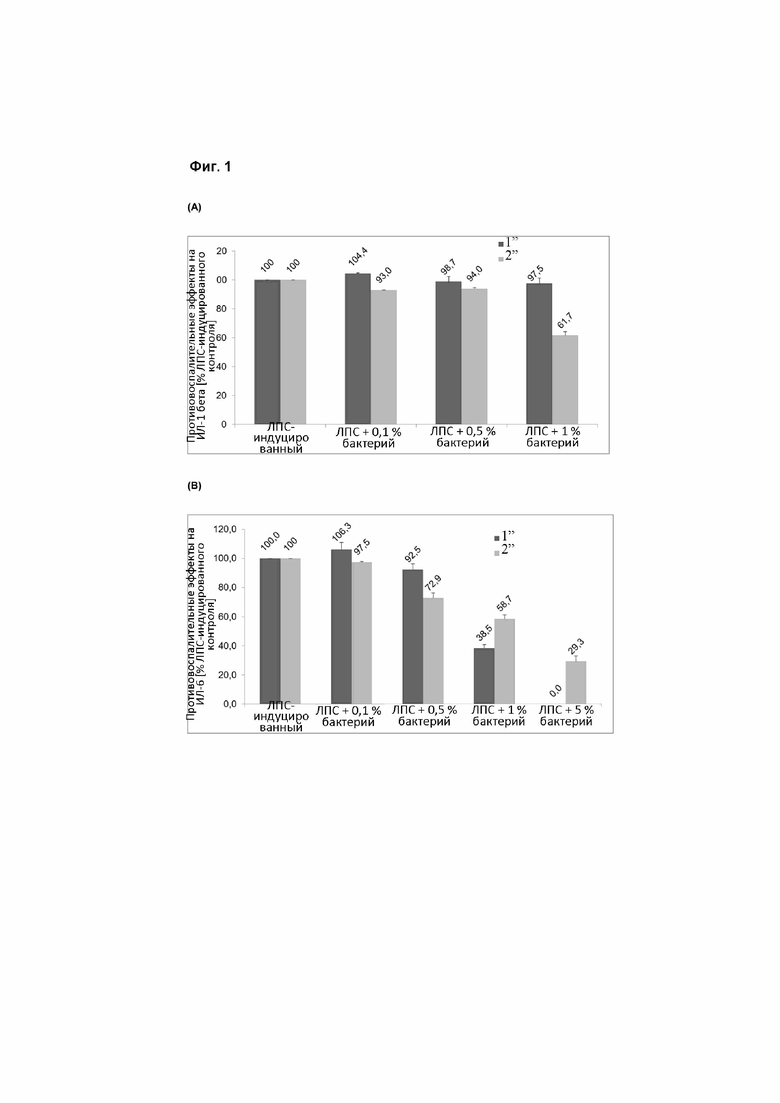
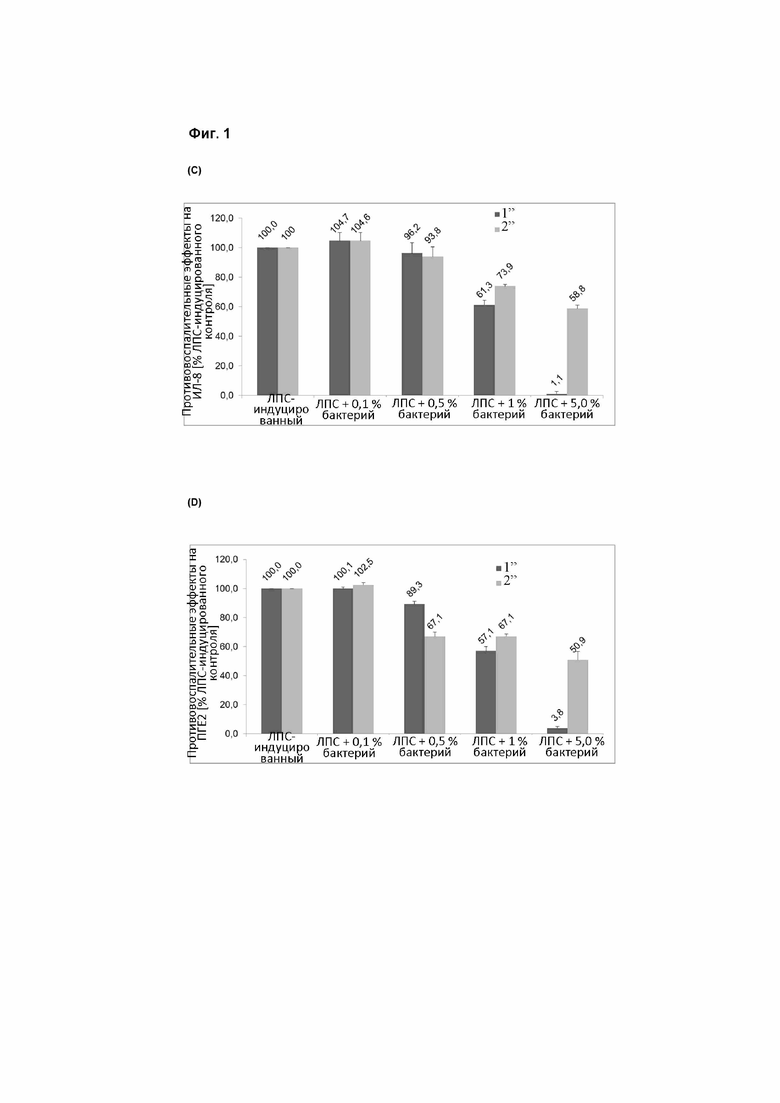
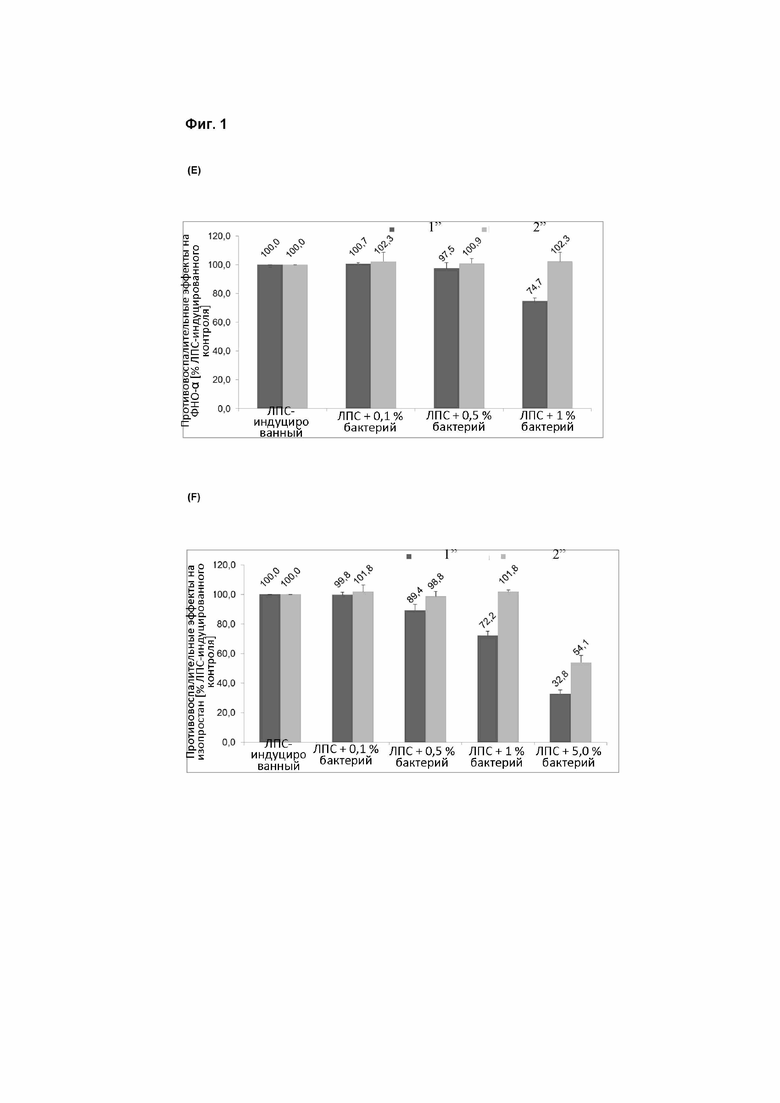
На фиг. 1 представлены противовоспалительные эффекты Lactobacillus plantarum GOS 42 (DSM 32131) в первичных моноцитах человека в отношении интерлейкина 1 бета (A), интерлейкина 6 (B), интерлейкина 8 (C), простагландина E2 (D), фактора некроза опухоли альфа (E) и изопростана (F). Левая колонка относится к необработанным клеткам, правая колонка - к аттенуированным клеткам.
На фиг. 2 представлены противовоспалительные эффекты Lactobacillus plantarum GOS 42 (DSM 32131) в аттенуированной форме в отношении интерлейкина в фибробластах десен человека. Левая колонка относится к интерлейкину 6, правая колонка к интерлейкину 8.
Следующие примеры добавлены для иллюстрации данного изобретения без ограничения его объема.
Пример 1: Культивирование и обработка пробиотических штаммов
Штамм по изобретению был выбран из более чем 50 потенциальных пробиотических штаммов, включая штаммы Bacillus subtilis, Bifidobacterium animalis, Bifidobacterium bifidum, Bifdobacterium longum, Bifidobacterium breve, Bifidobacterium lactis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus LAFTI, Lactobacillus plantarum, Lactobacillus reuteri, Lactobacillus rhamnosus, Lactobacillus paracasei, Lactobacillus bulgaricus, Lactobacillus gasseri, Lactobacillus fermentum, Lactobacillus brevis, Lactobacillus cellobiosus, Lactobacillus salivarius, Streptococcus thermophilus и Lactococcus lactis.
Для определения оптимальных условий роста и точек сбора, и определения колониеобразующих единиц (КОЕ) для пробиотических бактерий, подлежащих скринингу, были определены логарифмическая фаза и конец фазы роста.
Бактериальный рост
Замороженные (-80°C) исходные культуры пробиотиков размораживали в течение ночи при 4°С и 6 мл стерильного 9% раствора NaCl добавляли к 1,2 мл бактерий на следующее утро. Образцы центрифугировали (5 мин, 5000 об/мин), супернатант сливали, осадок промывали 8 мл 9% NaCl и снова центрифугировали в течение 5 мин при 5000 об/мин. Осадок затем ресуспендировали в 1,2 мл 9% NaCl и 1 мл образца добавляли к 50 мл 37 °C теплой среды (Бульон MRS, Carl Roth KG, Карлсруэ) и инкубировали при 37 °C. Инкубации проводили в 50 мл стерильной пробирке из полипропилена (Greiner), а пробы отбирали в разные моменты времени для оценки кривой роста.
Определение ОП
Для определения ОП, 500 мкл бактериальной суспензии удаляли и разбавляли в 1 мл Бульона MRS в 1,5 мл PS-кювете (Бренд). Определение ОП проводилось при 600 нм (ThermoScientific, Helios Epsilon). 1,5 мл Бульон MRS использовали в качестве прозрачного контроля.
Определение КОЕ
Для определения КОЕ бактерии разведенные (1:10000000, 1:50000000 и 1: 100000000), высевали на чашки с агаром MRS (MRS Agar, X924, Carl Roth) и инкубировали в течение 2 дней при 37 °C. Затем подсчитывали количество выросших колоний и вычисляли КОЕ.
Бактерии приблизились к логарифмической фазе с самого начала вплоть до 7-8 часов, когда они начали достигать фазы плато. Количество высеваемых бактерий не изменяет форму кривой. 5 часов были выбраны в качестве точки на самой крутой фазе выращивания для сбора бактерий в лог-фазе и 7 часов для сбора их в конце лог-фазы.
Пример 2: Стимуляция моноцитов человека пробиотиками
Стимуляцию культур клеток моноцитов штаммом пробиотиков определяли с использованием штаммов, полученных в виде порошка. Во-первых, были испытаны несколько форм применения, таких как использование выращенных бактерий (отобранных в логарифмическую фазу), супернатант выращиваемых бактериальных культур, непосредственное применение растворенного порошка и порошкового супернатанта. Согласно результатам, бактерии в конце логарифмической фазы испытывали это с двумя партиями замороженного штамма. Вместо использования супернатантов была проведена термическая инактивация этих двух штаммов и сравнивались инактивированные бактерии с активированными бактериями.
Измерение цитокинов; MMP-9 и PGE2 в первичных моноцитах человека
Первичные моноциты человека были выделены из лейкоцитарных пленок здоровых доноров крови человека. Клетки высевали в 24-луночные планшеты для экспериментов ИФА. Клетки инкубировали с ЛПС в течение 24 часов. Пробиотики (5 доз) добавляли за 30 мин до обработки ЛПС. Через 24 ч супернатанты удаляли, центрифугировали и исследовали на концентрации ИЛ-1 бета, ФНО-альфа, ИЛ-6, ИЛ-8, MMP-9, изопростана-8 и PGE2 в ИФА (PGE2, от AssayDesign, изопростана, от Cayman) или твердофазном ИФА (все цитокины, Immunotools, MMP-9, GE Healthcare) с использованием протокола производителя. Каждая доза была исследована 2-3 раза в двух лейкоцитарных пленках от двух разных доноров.
Во-первых, были испытаны различные типы пробиотических лиофилизированных порошковых препаратов для стимуляции моноцитов человека.
Пробиотики собирали и затем центрифугировали. Клетки растворяли в свежей среде и наносили на моноциты человека.
Затем моноциты инкубировали с пробиотиками в течение 30 минут, затем добавляли ЛПС и через 24 часа супернатант удаляли и использовали для определения воспалительных параметров.
Пример 3: Тестирование термически инактивированных штаммов
Проведение термической инактивации
Термическая инактивация была проведена для двух партий. В конце фазы бактериального роста удаляли аликвоту бактериальной суспензии, добавляли в свежую пробирку объемом 50 мл и инкубировали в течение 5 мин при 80°С на водяной бане. 5 минут при 80°C инактивировали бактерии и, таким образом, останавливали их рост.
Испытание термически инактивированных партий штамма обнаруживало, что эффекты на ИЛ-1 и ФНО не влияют на термическую обработку. Кроме того, термическая активация не оказывает или лишь незначительно влияет на ингибирование PGE2 обоими штаммами.
Пример 4: Скрининг пробиотиков на моноцитах человека и эффекты на активацию NF-kappaB
Различные штаммы пробиотиков подвергали скринингу в их активированной и аттенуированной (термически инактивированной форме) на ЛПС-индуцированных первичных моноцитах человека (определяли ИЛ-1 бета, ИЛ-6, ИЛ-8, ФНО альфа, PGE2, 8-изопростан и MMP-9).
Типичный противовоспалительный характер штамма согласно примерам 1-4 представлен на фиг. 1.
Эксперименты по тестированию эффектов на активацию NF-kappaB, индуцированную ФНО в фибробластах NIH-3T3, проводили в линии клеток фибробластов, которые содержали стабильно трансфицированный ген люциферазы с помощью NF-kappa-зависимого промотора. Клетки стимулировали ФНО в присутствии или отсутствии пробиотиков. Через 6 ч стимуляции клетки лизировали и активность люциферазы измеряли в люминометре.
Пример 5: Скрининг выбранных пробиотиков на фибробластах десен человека
Выбранный штамм по изобретению был применен к фибробластам десен человека. Культуры фибробластов поддерживали, как описано в протоколе изготовителя. Перед стимуляцией клетки высевали в 24-луночные планшеты для ИФА-экспериментов. Клетки инкубировали без (нестимулированный контроль) или с ИЛ-1 бета в течение 24 часов. Пробиотики (5 доз, в зависимости от результата скрининговых анализов) добавляют за 30 минут до лечения ИЛ-1. Через 24 ч супернатанты удаляли, центрифугировали и исследовали на концентрации ИЛ-6, ИЛ-8, изопростана и PGE2 в ИФА (PGE2, от AssayDesign, изопростан, от Cayman) или твердофазного ИФА (ИЛ-6, ИЛ-8, Immunotools), используя протокол производителя. Каждую дозу исследовали по меньшей мере 2-3 раза. Штаммы продемонстрировали некоторые ингибирующие ИЛ-6 эффекты.
Противовоспалительный характер штамма согласно примеру 5 представлен на фиг. 2.
Пример 6: Пробиотическая пастилка или таблетка
пробиотик
Optamint Peppermint (перечная мята)
р/с)
Способ изготовления:
- компоненты 1 и 6 сушат в вакуумной камерной сушилке при 50°С и макс. давлении 10 мбар в течение 16 часов
- все компоненты взвешивают точно
компоненты 1, 2, 3, 4 и 5 объединяют и тщательно перемешивают (блок А). Пробиотический материал наносят в лиофилизированной форме, имеющей активность, равную около 105 до 1012 колониеобразующих единиц (КОЕ) на грамм.
- блок А затем добавляют к компоненту 6 и тщательно перемешивают в течение 5 минут
- порошковую смесь прессуют в таблетки в таблетированном прессе EK0 (Korsch AG, Берлин) при заданном давлении 15-20 кН
целевые параметры:
- диаметр таблетки: 20 мм
- масса таблетки: 2,0 г
- хранение при комнатной температуре в герметичных алюминиевых пакетах. На 5 пастилок использовали для осушения 1 г осушителя (активируется 3 ч хранения при 105°С в вакуумной камерной сушилке)
Пример 7: Порошковое средство для чистки зубов
пробиотик
Optamint Peppermint (перечная мята)
р/с)
Способ изготовления:
- компоненты 7 сушат в вакуумной камерной сушилке при 50 °С и макс. давлении 10 мбар в течение 16 часов
- все компоненты взвешивают точно
- компоненты 1, 2, 3 и 4 объединяют и тщательно перемешивают вместе (блок А).
- компоненты 5 и 6, если необходимо, объединяют и тщательно перемешивают (блок B). Пробиотический материал наносят в лиофилизированной форме, имеющей активность, равную около 105 до 1012 колониеобразующих единиц (КОЕ) на грамм.
- блоки А и В затем объединяют и тщательно перемешивают вместе
- смесь добавляют к компоненту 7 и тщательно перемешивают в течение 5 минут
- порошковую смесь фасовали в порциях по 0,5 г, каждую хранили при комнатной температуре вместе с 1 г осушителя на порцию (активируется при хранении в течение 3 ч при 105 °С в вакуумной камерной сушилке) в герметичных алюминиевых пакетах
Пример 8: Порошковое средство для чистки зубов
Способ изготовления:
- компоненты 6, 9 и 10 сушат в вакуумной камерной сушилке при 50°С и макс. давлении 10 мбар в течение 16 часов
- все компоненты взвешивают точно
- компоненты 1, 2, 3, 4, 5 и 6 объединяют и тщательно перемешивают вместе (блок А).
- компоненты 7 и 8 объединяют и тщательно перемешивают вместе (блок А). Пробиотический материал наносят в лиофилизированной форме, имеющей активность, равную около 105 до 1012 колониеобразующих единиц (КОЕ) на грамм.
- блоки А и В затем объединяют и тщательно перемешивают вместе
- компоненты 9 и 10 объединяют и тщательно перемешивают вместе (блок C).
- две смеси (блок A/B и блок C) объединяют и тщательно перемешивают в течение 5 минут
- порошковую смесь прессуют в таблетки в прессе для таблеток EK0 (Korsch AG, Берлин) при заданном давлении 15-20 кН
целевые параметры
- диаметр таблетки: 9 мм
- масса таблетки: 0,3 г
- хранение при комнатной температуре в герметичных алюминиевых пакетах. На 3 таблетки использовали для осушения 1 г осушителя (активируется 3 ч хранения при 105°С в вакуумной камерной сушилке)
Пример 9: Жевательная резинка
р/с)
Способ изготовления:
- компоненты 2 сушат в вакуумной камерной сушилке при 50°С и макс. давлении 10 мбар в течение 16 часов
- все компоненты взвешивают точно
- компонент 1 нагревают до 45-59 °С в лабораторной смесителе с подогревом для жевательной резинки, перемешивают до получения гомогенной массы. Нагрев включен во время всего процесса смешивания
- компоненты 2,3 и 4 добавляют и перемешивают до тех пор, пока смесь не станет гомогенной, и порошок перестанет наблюдаться
- согласно формуле компонент 6 либо перерабатывается в компонент 5 (блок С), либо в компонент 7 (блок D). Пробиотический материал наносят в лиофилизированной форме, имеющей активность, равную около 105 до 1012 колониеобразующих единиц (КОЕ) на грамм. Компоненты смешивают до получения еще одной суспензии.
- Сначала блок С добавляют к массе жевательной резинки и снова замешивают до получения гомогенной массы.
- Наконец, блок D обрабатывают соответствующим образом. После добавления композицию необходимо замешивать до получения однородной массы жевательной резинки.
- массу вынимают из смесителя и формируется в мини-палочки с помощью тиснильного валика с использованием набора для тиснения «плитка»,
- хранение при комнатной температуре в герметичных алюминиевых пакетах. На 7 жевательных резинок использовали для осушения 1 г осушителя (активируется 3 ч хранения при 105°С в вакуумной камерной сушилке)
Пример 10: Пробиотические гранулы
мас.%
мас.%
мас.%
мас.%
Способ получения:
Получение хлористого кальция для осаждения альдегидных гранул:
- 2% раствор хлорида кальция производится из дистиллированной воды и хлорида кальция. Следует принять во внимание, что CaCl2 полностью растворяется.
Получение альгинатного раствора (вместо альгината также можно использовать пектин или геллановую камедь):
- в реакционный сосуд с мешалкой, который подходит для размера партии, заливают воду
- мешалку включают и при перемешивании на высоком уровне добавляют соответствующие количества альгината, гуммиарабика, пшеничного волокна и пробиотика, а также при необходимости, геллановую камедь
- смесь нагревают до 80°С при перемешивании и выдерживали при этой температуре в течение 5 минут - на этой стадии растворяют компоненты, образующие гель
- после этого нагревание отключают и раствор горячего геля дополнительно перемешивают в течение по меньшей мере 30 минут, пока он не будет свободным от комков
- впоследствии раствор охлаждают с помощью системы охлаждения до 39 – 43°C при перемешивании
- при необходимости в дополнительный сосуд помещают ароматизатор и краситель и тщательно перемешивают. В случае отсутствия ароматизатора краситель смешивают с глицерином
- когда дисперсию красителя смешивают гомогенно, ее добавляют в сосуд с раствором альгината. Смесительный сосуд промывают несколько раз приблиз. 10% от количества раствора альгината, используемого в воде и добавляемого к дисперсии
- дисперсию альгината дополнительно перемешивают в течение по меньшей мере 5 минут.
- Затем смесь перемешивают в течение по меньшей мере 15 минут с низкой скоростью для удаления потенциально присутствующего воздуха.
Титрование по каплям раствора альгината в раствор хлорида кальция для осаждения гранул:
- дисперсию альгината перемещают в плотно герметичный устойчивый к давлению реакционный сосуд, имеющий два выхода. На одном выходе подают сжатый воздух. Второй выход ведет к соплам капельницы через трубку.
- реакционный сосуд закаливают на нагревательной плите, так что раствор альгината достигает температуры приблиз. 45°C. Раствор слегка перемешивают с помощью магнитной мешалки.
- после приложения давления к реакционному сосуду раствор альгината прижимается к соплам, которые осциллируют осциллятором. При адаптации давления и частоты осциллятора можно изменить размер получаемых в результате капель на кончиках сопел.
- Капли раствора альгината, образующегося на кончиках его сопел, попадают в емкость для сбора в виде воронки, в которой циркулирует раствор хлорида кальция, приготовленный в начале.
- отвержденные альгинатные гранулы проходят через раствор хлорида кальция через воронку и собираются в сите, собранный раствор хлорида кальция откачивается обратно в воронку ниже капающего устройства и, таким образом, рециркулируется.
Гранулы сушат в сушильном шкафу Aeromatic при температуре приточного воздуха, равной 80°C до достижения температуры отводимого воздуха, равной 45°C.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОБИОТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЗДОРОВЬЯ ПОЛОСТИ РТА | 2011 |
|
RU2584610C2 |
| НОВЫЕ МОЛОЧНОКИСЛЫЕ БАКТЕРИИ И СОДЕРЖАЩИЕ ИХ СОСТАВЫ ПРОТИВ БАКТЕРИАЛЬНЫХ ПРОСТУДНЫХ ЗАБОЛЕВАНИЙ | 2012 |
|
RU2651466C2 |
| КОМПОЗИЦИИ LACTOBACILLUS PLANTARUM И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2773847C1 |
| Lactobacillus fermentum Ess-1, DSM17851, И ЕГО ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ КАНДИДОЗА И ИНФЕКЦИЙ МОЧЕВЫХ ПУТЕЙ | 2006 |
|
RU2413761C1 |
| Способ профилактики периимплантита на хирургическом этапе операции дентальной имплантации одиночных дефектов зубного ряда в области моляров и премоляров | 2023 |
|
RU2809168C1 |
| ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ Lactobacillus plantarum | 2018 |
|
RU2772025C2 |
| ПРОБИОТИЧЕСКОЕ СРЕДСТВО В ВИДЕ МАЗИ ДЛЯ ЛЕЧЕНИЯ СТОМАТОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2007 |
|
RU2352345C1 |
| МИКРООРГАНИЗМЫ МОЛОКА МЛЕКОПИТАЮЩЕГО, ИХ СОДЕРЖАЩИЕ КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ МАСТИТА | 2008 |
|
RU2446814C2 |
| ПРОБИОТИЧЕСКИЕ ШТАММЫ Lactobacillus (ВАРИАНТЫ) И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2316586C2 |
| КРАТКОВРЕМЕННАЯ ВЫСОКОТЕМПЕРАТУРНАЯ ОБРАБОТКА ДЛЯ МИКРОБНЫХ ПРЕПАРАТОВ С ПРОТИВОВОСПАЛИТЕЛЬНЫМИ СВОЙСТВАМИ | 2010 |
|
RU2542413C2 |

Группа изобретений относится к бактериальному штамму – L. plantarum GOS 42 (DSM 32131) и его применению в медицине. Раскрыт штамм микроорганизма Lactobacillus plantarum GOS 42 (DSM 32131) для лечения или профилактики воспаления. Также раскрыта композиция для лечения или профилактики воспаления. Группа изобретений обеспечивает уменьшение и/или ингибирование высвобождения одного или нескольких воспалительных факторов, выбранных из группы, состоящей из интерлейкина 1 (IL-1), интерлейкина 6 (IL-6), интерлейкина 8 (IL-8), фактора некроза опухоли (TNF), простагландина E2 (PGE2), изопростанов, матриксной металлопептидазы 9 (MMP9) и NF-κB. 2 н. и 13 з.п. ф-лы, 2 ил., 10 пр.
1. Штамм микроорганизма Lactobacillus plantarum GOS 42 (DSM 32131) для лечения или профилактики воспаления.
2. Штамм по п. 1, предназначенный для снижения и/или ингибирования высвобождения одного или нескольких воспалительных факторов, выбранных из группы, состоящей из интерлейкина 1 (IL-1), интерлейкина 6 (IL-6), интерлейкина 8 (IL-8), фактора некроза опухоли (TNF), простагландина E2 (PGE2), изопростанов, матриксной металлопептидазы 9 (MMP9) и NF-κB.
3. Композиция для лечения или профилактики воспаления, включающая микроорганизм по п. 1 вместе с носителем, эксципиентом и/или разбавителем.
4. Композиция по п. 3, в которой микроорганизм присутствует в виде вегетативных клеток и/или спор.
5. Композиция по п. 3 или 4, в которой микроорганизм ослаблен или мертв.
6. Композиция по любому из пп. 3-5, которая представляет собой фармацевтическую композицию.
7. Композиция по любому из пп. 3-6, в которой общее количество микроорганизма находится в диапазоне от 0,01%, более предпочтительно в диапазоне от 0,1 до 50%, наиболее предпочтительно в диапазоне от 1 до 10%. по отношению к общей массе композиции и/или где общее количество микроорганизма находится в диапазоне от 1×103 до 1×1011 колониеобразующих единиц (КОЕ), более предпочтительно в диапазоне от 1×105 до 1×1010 КОЕ.
8. Композиция по п. 7, в которой общее количество микроорганизма находится в диапазоне от 0,1 до 50% по отношению к общей массе композиции и/или общее количество микроорганизма находится в диапазоне от 1×105 до 1×1010 КОЕ.
9. Композиция по п. 8, в которой общее количество микроорганизма находится в диапазоне от 1 до 10% по отношению к общей массе композиции и/или где общее количество микроорганизма находится в диапазоне от 1×108 до 1×109 КОЕ.
10. Композиция по любому из пп. 3-9, которая изготовлена в форме раствора, суспензии, эмульсии, таблетки, гранулы, порошка или капсулы.
11. Композиция по любому из пп. 3-10, которая выбрана из группы, состоящей из зубной пасты, зубного геля, зубного порошка, жидкости для чистки зубов, пены для чистки зубов, ополаскивателя для полости рта, спрея для полости рта, зубной нити, жевательной резинки и пастилки.
12. Композиция по любому из пп. 10 или 11, которая изготовлена в форме таблетки с покрытием или пастилки с покрытием.
13. Композиция по любому из пп. 3-9, которая представляет собой компонент корма для животных.
14. Композиция по любому из пп. 3-9, которая представляет собой компонент напитка для животных.
15. Композиция по п. 3, предназначенная для уменьшения и/или ингибирования высвобождения одного или нескольких воспалительных факторов, выбранных из группы, состоящей из интерлейкина 1 (IL-1), интерлейкина 6 (IL-6), интерлейкина 8 (IL-8), фактора некроза опухоли (TNF), простагландина E2 (PGE2), изопростанов, матриксной металлопептидазы 9 (MMP9) и NF-κB.
| СПОСОБ ПРЕОБРАЗОВАНИЯ ВОДОРАСТВОРИМЫХ АКТИВНЫХ БЕЛКОВ В ГИДРОФОБНЫЕ АКТИВНЫЕ БЕЛКИ, ИХ ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ МОНОМОЛЕКУЛЯРНЫХ СЛОЕВ ОРИЕНТИРОВАННЫХ АКТИВНЫХ БЕЛКОВ И УСТРОЙСТВА, ВКЛЮЧАЮЩИЕ ВОДОРАСТВОРИМЫЕ АКТИВНЫЕ БЕЛКИ, ПРЕОБРАЗОВАННЫЕ В ГИДРОФОБНЫЕ АКТИВНЫЕ БЕЛКИ | 2006 |
|
RU2420580C2 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ВОСПАЛЕНИЯ В РОТОВОЙ ПОЛОСТИ ПОСЛЕ СТОМАТОЛОГИЧЕСКОЙ ХИРУРГИЧЕСКОЙ ОПЕРАЦИИ | 2012 |
|
RU2492851C1 |
| JP 2014000039 A, 09.01.2014 | |||
| WO 2014140080 A1, 18.09.2014. | |||
Авторы
Даты
2020-08-06—Публикация
2017-01-18—Подача