Изобретение относится к химии азолилэтиламидов общей формулы I:
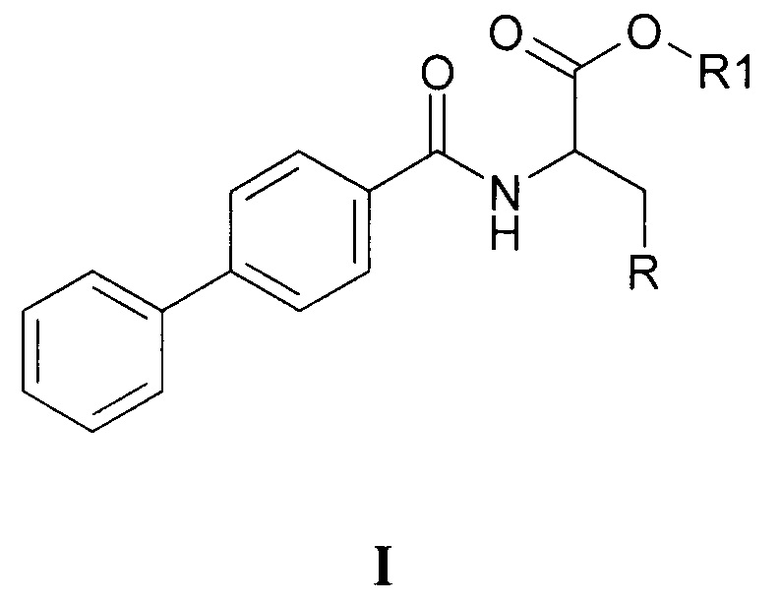
где R означает имидазольный или триазольный гетероциклический фрагмент, R1 означает алкильные группы нормального или разветвленного строения с числом атомов углерода от 1 до 4 и может найти применение в медицине.
В частности к способу получения соединения формулы I. Известен способ синтеза соединения формулы I. Он заключается в двухстадийном синтезе. Метиловый эфир L-серина превращают в метил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-гидроксипропаноат в результате амидирования эфира L-серина 4-бифенил карбоновой кислотой в присутствии 1,1 мольного избытка гидрохлорида 1-(3-диметиламинопропил)-3-этилкарбодиимида и гидроксибензотриазола. Полученный амид вводят во взаимодействие с 2 мольным избытком имидазола в присутствии 3 кратного мольного избытка 1,1'-карбонилдиимидазола. Выход заявленного соединения на последней стадии составляет 53,2% [Патент CN 104530038 А, 2014.12.10]; [Sun, В.; et al. Bioorg. Med. Chem. - 2015. - Vol. 23, Is. 20. - P. 6763-6773].
Основными недостатками этого метода получения соединения формулы I являются низкий выход целевого продукта и использование 1,1'-карбонилдиимидазола (DCC) для промышленного получения, которое приводит к увеличению затрат на хранение и транспортировку DCC.
Соединение формулы I является ингибитором одного из ферментов группы цитохрома Р450 (CYP26A1), отвечающего за превращение транс-ретиноевой кислоты в 4-гидрокси производное. Сама по себе трансретиноевая кислота способна регулировать клеточную дифференциацию и экспрессию генов и используется в антираковой терапии. В результате чего, соединения формулы I являются потенциальными препаратами для борьбы с лейкемией.
Задачей данного изобретения является разработка экономически доступного, альтернативного способа синтеза алкил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-азолил пропаноатов I с высоким выходом целевого продукта.
Поставленная задача решается способом получения (Схема 1) алкил 2-[([1,1-бифенил]-4-карбонил) амино]-3-гидроксипропаноата, который представляет собой трехстадийный процесс. Хлорангидрид 4-бифенил карбоновой кислоты конденсируют с гидрохлоридом алкил эфира L-серина в апротонном полярном растворителе, например ацетонитриле, пропионитриле, тетрагидрофуране в присутствии триэтиламина с получением алкил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-гидроксипропаноата. Полученный амид превращают в оксазолиновое производное в апротонном неоплярном растворителе, например хлористом метилене в присутствии 20-21 кратного мольного избытка тионилхлорида при 0-5°С. Далее алкил 2-([1,1'-бифенил]-4-ил)-4,5-дигидро-1,3-оксазол-4-карбоксилат раскрывают имидазолом или триазолом в присутствии 1-1,001 мол. % хлористого цинка при температуре 145-150°С без растворителя в расплаве в течение 20-30 ч с получением целевого алкил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-гидроксипропаноата I с 70-85% выходом на последней стадии.

Следующий пример предназначен для иллюстрации вариантов осуществления настоящего изобретения.
ЯМР 1H - спектры записаны на приборе «Bruker АМ300» (рабочая частота 300 МГц), сдвиги измерены относительно тетраметилсилана.
Получение гидрохлорида метилового эфира L-серина (1).
К суспензии 10 г (84 ммоль) L-серина в 150 мл метанола при 0°С по каплям добавляют 30 г (18 мл, 0,25 моль) тионилхлорида. Раствор кипятят в течение двух часов, после чего упаривают на роторном испарителе и получают гидрохлорид метилового эфира L-серина с выходом 98% и с т.пл.=112-113°С; 1Н ЯМР (400 МГц, CDCl3) δ м.д.: 3.63 (дд, J2=5.7, J3=4.4 Гц, 1Н), 3.71 (дд, J2=10.6 Гц, J3= 5.7 Гц, 1Н), 3.78 (с, 3Н), 3.80 (дд, J2=10.6, J3=4.5 Гц, 1Н).
Получение хлорангидрида 4-бифенил карбоновой кислоты (2).
10 г (50 ммоль) 4-Бифенил карбоновой кислоты растворяют в 18 г (11 мл, 150 ммоль) тионилхорида и кипятят в течение 3 часов, затем избыток тионилхлорида отгоняют и получают 10 г (98%) хлорангидрида 4-бифенил карбоновой кислоты в виде белых кристаллов с т.пл.=112-113°С; 1Н ЯМР (400 МГц, CDCl3) δ м.д.: 6.96-6.99 (м, 2Н), 7.28-7.32 (м, 1Н), 7.39-7.43 (м, 2Н), 7.51-7.56 (м, 4Н).
Пример 1. Метил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-гидрокси пропаноат (3).
5 г (30 ммоль) Метилового эфира гидрохлорида L-серина суспензируют в 100 мл сухого ацетонитрила, добавляют 9 г (12,5 мл, 90 ммоль) триэтиламина, смесь охлаждают до 0°С и по каплям добавляют 10 г (46 ммоль) хлорангидрида 4-бифенил карбоновой кислоты, поддерживая заданную температуру. После того как будет добавлен весь хлорангидрид, смесь кипятят в течение 5 часов. Смесь охлаждают до комнатной температуры и отфильтровывают осадок триэтиламина гидрохлорида. Маточный раствор упаривают, а остаток перекристаллизовывают из ацетонитрила. Получают 7,2 г (80%) метил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-гидрокси пропаноата в виде белых кристаллов с т.пл.=149-151°С.
Аналогично получены алкил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-гидрокси пропаноаты (таблица 1).

Пример 2. Метил 2-([1,1'-бифенил]-4-ил)-4,5-дигидро-1,3-оксазол-4-карбоксилат (7).
7,2 г (24 ммоль) Метил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-гидроксипропаноата растворяют в 100 мл хлористого метилена, охлаждают до 0°C, и прикапывают раствор 35 мл (57 г, 0,48 моль) тионилхлорида в 50 мл хлористого метилена. Смесь перемешивают при комнатной температуре 3 ч. И охлаждают при 0°С медленно прибавляют 150 мл 10% водного раствора карбоната натрия. Водный слой отделяют и экстрагируют хлористым метиленом (3×50 мл). Органический слой сушат над сульфатом магния, а затем упаривают на РПИ. Остаток перегоняют под вакуумом, собирая фракцию с т. кип. 163-164°С 0,2 Торр. Получают 4,7 г (70%) метил 2-([1,1'-бифенил]-4-ил)-4,5-дигидро-1,3-оксазол-4-карбоксилата в виде вязкого прозрачного масла.
Аналогично получены алкил 2-([1,1'-бифенил]-4-ил)-4,5-дигидро-1,3-оксазол-4-карбоксилаты (таблица 2).

Пример 3 Этил 2-([1,1'-бифенил]-4-ил)-4,5-дигидро-1,3-оксазол-4-карбоксилат (8). Аналогично примеру 2 получают этил 2-([1,1'-бифенил]-4-ил)-4,5-дигидро-1,3-оксазол-4-карбоксилат. Выход 72% (4.8 г).
Пример 4. Изопропил 2-([1,1'-бифенил]-4-ил)-4,5-дигидро-1,3-оксазол-4-карбоксилат (8).
Аналогично примеру 2 получают изопропил 2-([1,1'-бифенил]-4-ил)-4,5-дигидро-1,3-оксазол-4-карбоксилат. Выход 71%) (4.9 г).
Пример 5 Изобутил2-([1,1'-бифенил]-4-ил)-4,5-дигидро-1,3-оксазол-4-карбоксилат (8).
Аналогично примеру 2 получают изобутил 2-([1,1'-бифенил]-4-ил)-4,5-дигидро-1,3-оксазол-4-карбоксилат. Выход 69% (4.6 г).
Пример 6. Метил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-(1Н-имидазол-1-ил) пропаноат (11).
4,7 г (16 моль) Метил 2-([1,1'-бифенил]-4-ил)-4,5-дигидро-1,3-оксазол-4-карбоксилата загружают в стальную ампулу, добавляют 0,022 г (0,16 ммоль) хлорида цинка и 1,1 г (16 ммоль) имидазола. Смесь сплавляют на масляной бане в течение 30 часов, при температуре масляной бани 150°С. После охлаждения твердый остаток растворяют в метаноле, отфильтровывают осадок, фильтрат упаривают в вакууме водоструйного насоса. Добавляют ацетонитрил, остаток затирают, промывают на фильтре ацетонитрилом и получают 4,63 г (83%) вещества в виде белых кристаллов с т.пл. 133-134°С.
Аналогично получены алкил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-(азол-1-ил) пропаноаты (таблица 3).


Пример 7. Метил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-(1Н-имидазол-1-ил) пропаноат (11).
Аналогично примеру 6 получают метил 2-[([1,1'-бифенил]-4карбонил)амино]-3-(1Н-имидазол-1-ил) пропаноат, время взаимодействия 20 часов. Выход 70% (3.9 г).
Пример 8. Метил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-(1Н-имидазол-1-ил) пропаноат (11).
Аналогично примеру 6 получают метил 2-[([1,1'-бифенил]-4карбонил)амино]-3-(1Н-имидазол-1-ил) пропаноат, температура масляной бани 145С. Выход 71% (4.0 г).
Пример 9. Метил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-(1Н-триазол-1-ил) пропаноат (12).
Аналогично примеру 6 получают метил 2-[([1,1'-бифенил]-4карбонил)амино]-3-(1Н-триазол-1-ил) пропаноат. Выход 75% (4.16 г).
Пример 10. Этил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-(1Н-триазол-1-ил) пропаноат (12).
Аналогично примеру 6 получают этил 2-[([1,1'-бифенил]-4карбонил)амино]-3-(1Н-триазол-1-ил) пропаноат. Выход 82% (4.76 г).
Как видно из примеров, выход по целевому продукту выше по сравнению с прототипом. Представленный метод позволяет снизить затраты на сырье, поскольку не требует дорогостоящих реагентов, таких как 1,1'-карбонилдиимидазола, 1-(3-диметиламинопропил)-3-этилкарбодиимида и гидроксибензотриазола.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ СОЕДИНЕНИЯ И КОМПОЗИЦИИ ДЛЯ ИНГИБИРОВАНИЯ FASN | 2014 |
|
RU2737434C2 |
| ЦИКЛОАЛКИЛНИТРИЛПИРАЗОЛОПИРИДОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ЯНУС-КИНАЗЫ | 2014 |
|
RU2655380C2 |
| СОЕДИНЕНИЕ, ОБЛАДАЮЩЕЕ ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ KDM5, И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2021 |
|
RU2840256C1 |
| ЗАМЕЩЕННЫЕ ТИОФЕНКАРБОКСАМИДЫ И АНАЛОГИ В КАЧЕСТВЕ АНТИБАКТЕРИАЛЬНЫХ СРЕДСТВ | 2019 |
|
RU2797316C2 |
| ПРОИЗВОДНЫЕ ПЯТИЧЛЕННЫХ ГЕТЕРОЦИКЛОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2009 |
|
RU2530882C2 |
| ПРОИЗВОДНЫЕ ПЯТИЧЛЕННЫХ ГЕТЕРОЦИКЛОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2000 |
|
RU2380362C2 |
| ФЕНОКСИМЕТИЛЬНЫЕ ПРОИЗВОДНЫЕ | 2016 |
|
RU2746481C1 |
| ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ СЕЛЕКТИВНОГО ИНГИБИРОВАНИЯ СВЯЗЫВАНИЯ αβ ИНТЕГРИНА У МЛЕКОПИТАЮЩЕГО | 2000 |
|
RU2263109C2 |
| ЗАМЕЩЕННЫЕ ТИОФЕНКАРБОКСАМИДЫ И АНАЛОГИ В КАЧЕСТВЕ АНТИБАКТЕРИАЛЬНЫХ СРЕДСТВ | 2019 |
|
RU2797513C2 |
| БИАРИЛЬНЫЕ МОНОБАКТАМНЫЕ СОЕДИНЕНИЯ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2016 |
|
RU2746129C2 |
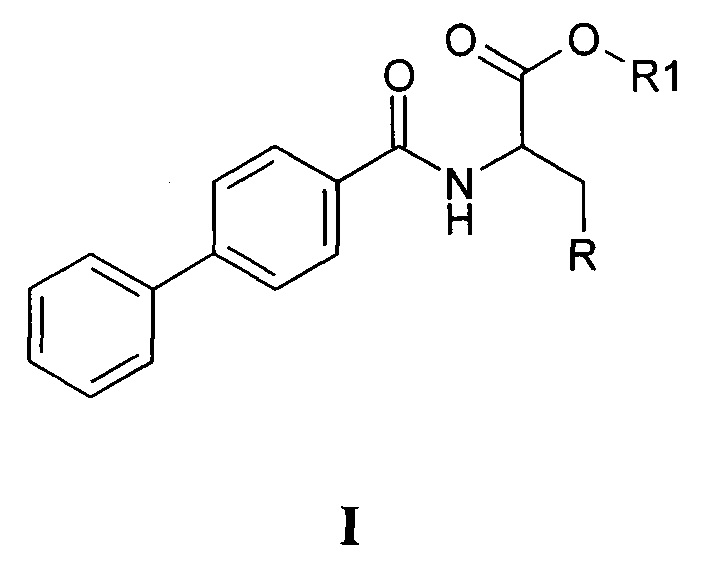
Изобретение относится к области органической химии, а именно к способу получения алкил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-(1Н-азол-1-ил) пропаноатов общей формулы I
 ,
,
где R означает имидазольный или триазольный гетероциклический фрагмент, R1 означает алкильные группы нормального или разветвленного строения с числом атомов углерода от 1 до 4. Способ, заключающийся в том, что хлорангидрид 4-бифенил карбоновой кислоты конденсируют с гидрохлоридом алкил эфира L-серина в апротонном полярном растворителе, ацетонитриле в присутствии триэтиламина с получением алкил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-гидроксипропаноата, полученный амид превращают в оксазолиновое производное в апротонном неполярном раствориителе в присутствии 20-21-кратного мольного избытка тионилхлорида при 0-5°С. Далее алкил 2-([1,1'-бифенил]-4-ил)-4,5-дигидро-1,3-оксазол-4-карбоксилат раскрывают имидазолом или триазолом в присутствии 1-1,001 мол.% хлористого цинка при температуре 145-150°С без растворителя в расплаве в течение 20-30 ч с получением целевого соединения формулы I. Технический результат: предложен новый способ получения алкил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-(1Н-азол-1-ил) пропаноата, имеющий более высокий выход продукта и являющийся более дешевым способом. 3 табл., 10 пр.
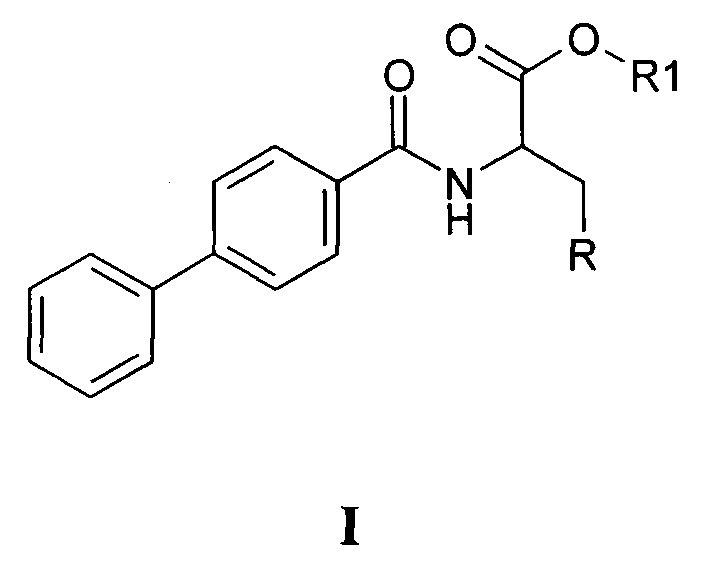
Способ получения алкил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-(1Н-азол-1-ил) пропаноатов общей формулы I
 ,
,
где R означает имидазольный или триазольный гетероциклический фрагмент, R1 означает алкильные группы нормального или разветвленного строения с числом атомов углерода от 1 до 4, заключающийся в том, что хлорангидрид 4-бифенил карбоновой кислоты конденсируют с гидрохлоридом алкил эфира L-серина в апротонном полярном растворителе, ацетонитриле в присутствии триэтиламина с получением алкил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-гидроксипропаноата, полученный амид превращают в оксазолиновое производное в апротонном неполярном раствориителе в присутствии 20-21-кратного мольного избытка тионилхлорида при 0-5°С, далее алкил 2-([1,1'-бифенил]-4-ил)-4,5-дигидро-1,3-оксазол-4-карбоксилат раскрывают имидазолом или триазолом в присутствии 1-1,001 мол.% хлористого цинка при температуре 145-150°С без растворителя в расплаве в течение 20-30 ч с получением целевого алкил 2-[([1,1'-бифенил]-4-карбонил)амино]-3-(1Н-азол-1-ил) пропаноата формулы I.
| CN 104530038 A, 22.04.2015 | |||
| ZHAO L | |||
| et al, Design, synthesis, and structure- activity relationship studies of L-amino alcohol derivatives as broad-spectrum antifungal agents, Europen Journal of Medicinal Chemistry, 05.2019, no.177, p.374-385 | |||
| ПРОИЗВОДНЫЕ АЗОЛОВ | 2012 |
|
RU2622639C2 |
Авторы
Даты
2020-08-24—Публикация
2019-12-27—Подача