Область техники
Настоящее изобретение относится к терапевтическому средству для лечения рака молочной железы, содержащему моноциклическое производное пиридина, характеризующееся ингибирующим действием по отношению к FGFR, или его фармакологически приемлемую соль. Настоящее изобретение, более конкретно, относится к терапевтическому средству для лечения рака молочной железы, содержащему 5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамид или его фармакологически приемлемую соль.
Уровень техники
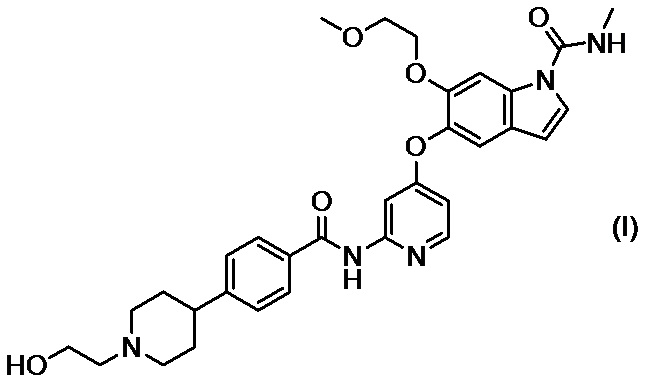
5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамид, представленный формулой (I), известен как ингибитор рецепторов фактора роста фибробластов (FGFR) 1, 2 и 3, и при этом имеются данные (патентный литературный источник 1), что это соединение оказывает ингибирующее действие на пролиферацию клеток при раке желудка, раке легких, раке мочевого пузыря и раке эндометрия.
Рак молочной железы подразделяют на группы в соответствии с наличием или отсутствием экспрессии эстрогенового рецептора, прогестеронового рецептора и HER2-рецептора. Могут быть предусмотрены как лекарственная терапия, соответствующая каждому типу, так и хирургическое удаление пораженного участка. К сожалению, даже при таком терапевтическом вмешательстве наблюдается снижение показателя 5-летней выживаемости в зависимости от стадии рака молочной железы. В случае рака молочной железы, относящегося к трижды негативному типу, при котором ни один из названных выше рецепторов не экспрессируется, в частности, введение противоракового лекарственного средства, такого как таксан, часто оказывает недостаточный эффект (непатентный литературный источник 1). Кроме того, имеются данные, что ингибитор FGFR является эффективным при лечении рака молочной железы (непатентный литературный источник 2).
Список использованной литературы
Патентная литература
Патентный литературный источник 1: публикация заявки на патент США № 2014-235614.
Непатентная литература
Непатентный литературный источник 1: Foulkes et al., "Triple-Negative Breast Cancer", The New England Journal of Medicine., 363, 1938-1948, 2010.
Непатентный литературный источник 2: Koziczak et al., "Blocking of FGFR signaling inhibits breast cancer cell proliferation through downregulation of D-type cyclins", Oncogene., 23, 3501-3508, 2004.
Краткое описание изобретения
Техническая задача
Целью настоящего изобретения является обеспечение нового терапевтического средства для лечения рака молочной железы.
Решение задачи
С учетом сложившихся обстоятельств, авторами настоящего изобретения проведено интенсивное исследование, в результате которого выявлено, что соединение, представленное формулой (I), оказывает выраженный терапевтический эффект против рака молочной железы. Вследствие этого было создано настоящее изобретение.
В частности, настоящее изобретение предусматривает следующие пункты [1] - [9].
[1] Терапевтическое средство для лечения рака молочной железы, содержащее соединение, представленное формулой (I):
 ,
,
или его фармакологически приемлемую соль.
[2] Применение соединения, представленного формулой (I), или его фармакологически приемлемой соли для лечения рака молочной железы.
[3] Соединение, представленное формулой (I), или его фармакологически приемлемая соль для применения в лечении рака молочной железы.
[4] Способ лечения рака молочной железы, включающий введение соединения, представленного формулой (I), или его фармакологически приемлемой соли нуждающемуся в этом пациенту.
[5] Композиция для лечения рака молочной железы, содержащая соединение, представленное формулой (I), или его фармакологически приемлемую соль.
[6] Композиция для лечения рака молочной железы, содержащая соединение, представленное формулой (I), или его фармакологически приемлемую соль и вспомогательное вещество.
[7] Терапевтическое средство, применение, соединение, способ или композиция согласно любому из изложенных выше пунктов, где рак молочной железы представляет собой местнораспространенный рак молочной железы, метастатический рак молочной железы или рецидивирующий рак молочной железы.
[8] Терапевтическое средство, применение, соединение, способ или композиция согласно любому из изложенных выше пунктов, где рак молочной железы экспрессирует FGFR.
[9] Терапевтическое средство, применение, соединение, способ или композиция согласно любому из изложенных выше пунктов, где FGFR представляет собой FGFR1, FGFR2 или FGFR3.
Полезные эффекты изобретения
Соединение, представленное формулой (I), может оказывать противораковое действие в отношении рака молочной железы с уменьшением объема опухоли.
Краткое описание графических материалов
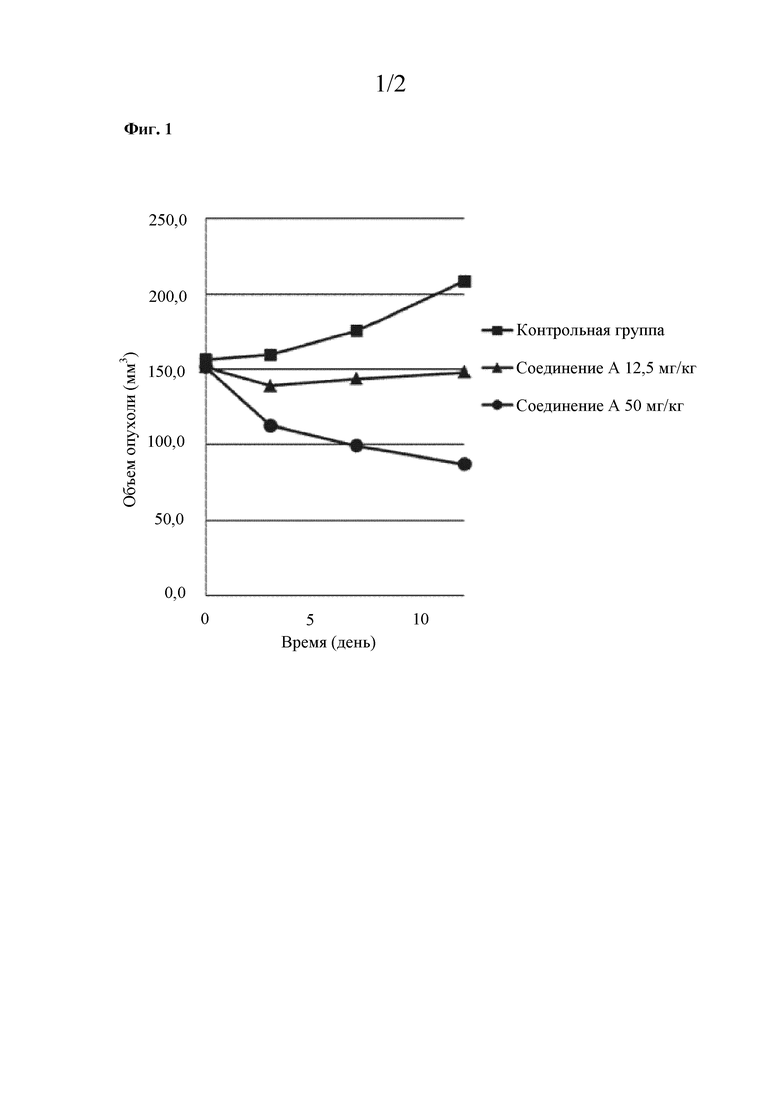
На фигуре 1 представлен график, демонстрирующий изменения объема опухоли в динамике по времени после начала введения лекарственного средства.
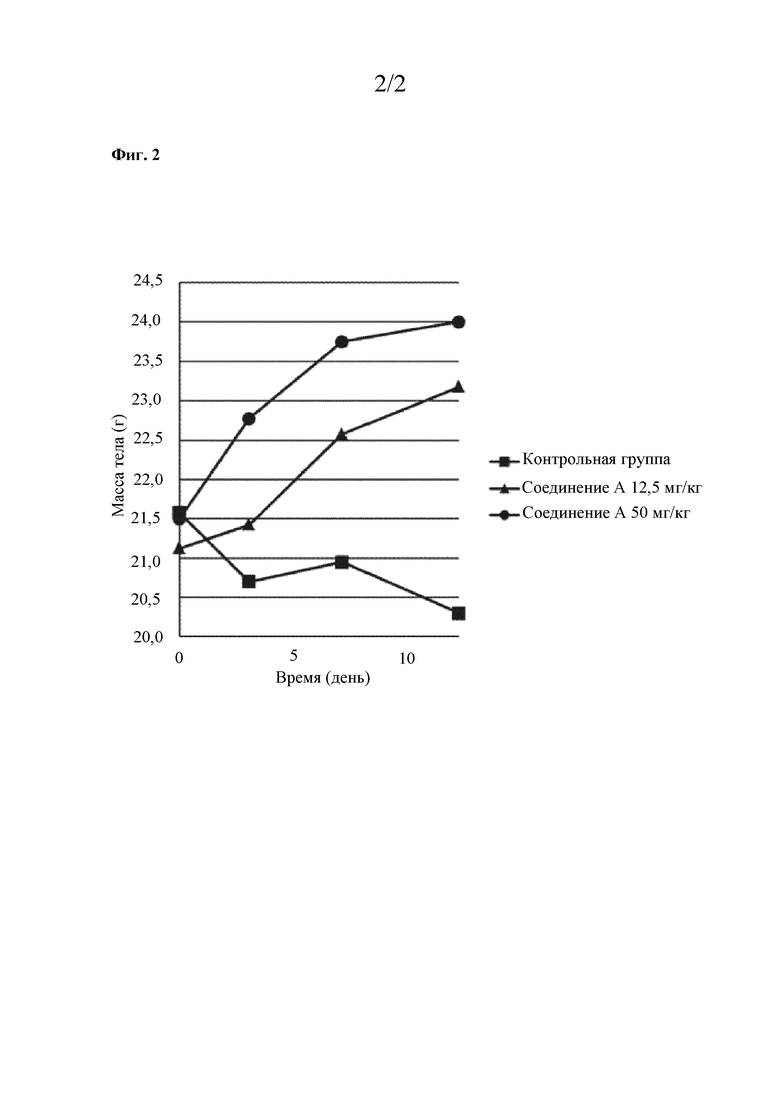
На фигуре 2 представлен график, демонстрирующий изменения массы тела в динамике по времени после начала введения лекарственного средства.
Описание вариантов осуществления
Соединение, представленное формулой (I), или его фармакологически приемлемая соль согласно настоящему изобретению могут быть получены посредством способа, описанного в патентном литературном источнике 1.
В данном контексте примеры фармакологически приемлемой соли включают соль неорганической кислоты, соль органической кислоты и соль кислой аминокислоты.
Предпочтительные примеры соли неорганической кислоты включают соли соляной кислоты, бромистоводородной кислоты, серной кислоты, азотной кислоты, фосфорной кислоты и т.п.
Предпочтительные примеры соли органической кислоты включают соли уксусной кислоты, янтарной кислоты, фумаровой кислоты, малеиновой кислоты, винной кислоты, лимонной кислоты, молочной кислоты, стеариновой кислоты, бензойной кислоты, метансульфоновой кислоты, этансульфоновой кислоты, п-толуолсульфоновой кислоты и т.п.
Предпочтительные примеры соли кислой аминокислоты включают соли аспарагиновой кислоты, глутаминовой кислоты и т.п.
Предпочтительная фармакологически приемлемая соль представляет собой сукцинат или малеат. Более предпочтительная соль представляет собой сукцинат. Особо предпочтительным является 1,5-сукцинат.
Терапевтическое средство для лечения рака молочной железы согласно настоящему изобретению может вводиться перорально в виде препарата в твердой форме, такого как таблетка, гранулы, мелкие частицы, порошок и капсула, или в виде жидкости, желе, сиропа и т.п. Также терапевтическое средство для лечения опухоли согласно настоящему изобретению может вводиться парентерально в виде инъекции, суппозитория, мази, компресса и т.п.
Терапевтическое средство для лечения рака молочной железы согласно настоящему изобретению может быть составлено согласно протоколу, описанному в Фармакопее Японии, 16-е издание.
Доза соединения, представленного формулой (I), или его фармакологически приемлемой соли, может быть подобрана надлежащим образом в зависимости от интенсивности симптома, возраста, пола, массы тела и различий в чувствительности пациента, пути введения, частоты дозирования, интервала дозирования, вида фармацевтического препарата и т.п. При пероральном введении соединения взрослому человеку (масса тела: 60 кг) суточная доза обычно составляет от 100 мкг до 10 г, предпочтительно от 500 мкг до 10 г и более предпочтительно от 1 мг до 5 г. Эта доза может вводиться, будучи разделенной на 1-3 раза в день.
В данном контексте рак молочной железы означает доброкачественную или злокачественную опухоль, развивающуюся в молочной железе (протоках и дольках молочной железы). Рак молочной железы включает местнораспространенный рак молочной железы, метастатический рак молочной железы и рецидивирующий рак молочной железы.
Примеры
Далее по тексту настоящее изобретение дополнительно подробно описано со ссылкой на примеры.
Пример получения 1
Получение 1,5-сукцинатной соли 5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамида (далее по тексту иногда называемой соединением A).
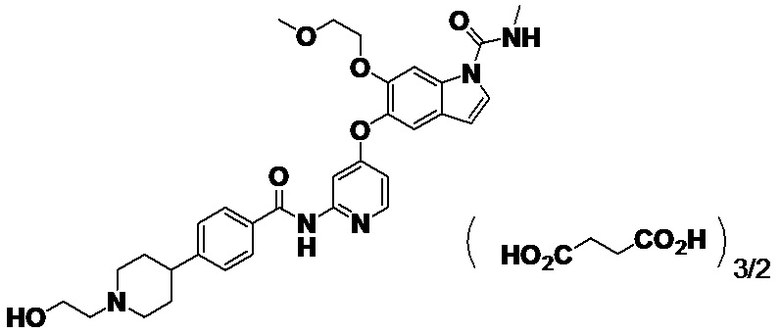
В лабораторную колбу отвешивали 2,93 г 5-({2-[({4-[1-(2-гидроксиэтил)пиперидин-4-ил]фенил}карбонил)амино]пиридин-4-ил}окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамида, добавляли 60 мл этанола, и смесь нагревали и перемешивали при 70°C на масляной бане до растворения. Добавляли янтарную кислоту (1,23 г), затем выключали масляную баню и постепенно охлаждали. Смесь перемешивали при комнатной температуре в течение 2 часов и дополнительно перемешивали при 5°C в течение 1 часа. Твердое вещество собирали посредством фильтрации с получением указанного в заголовке соединения (3,70 г).
Спектр 1H-ЯМР (600 МГц, CD3OD) δ (ppm): 1,96-2,10 (4H, m), 2,52 (6H, s), 2,93 (1H, m), 2,96 (3H, s), 3,01 (2H, m), 3,16 (2H, t, J=5,4 Гц), 3,22 (3H, s), 3,56 (2H, t, J=4,7 Гц), 3,61 (2H, m), 3,87 (2H, t, J=5,4 Гц), 4,14 (2H, t, J=4,6 Гц), 6,61 (1H, d, J=3,6 Гц), 6,68 (1H, dd, J=5,8, 2,3 Гц), 7,37 (1H, s), 7,42 (2H, d, J=8,3 Гц), 7,58 (1H, d, J=3,6 Гц), 7,73 (1H, d, J=2,2 Гц), 7,88 (2H, d, J=8,3 Гц), 8,08 (1H, s), 8,15 (1H, d, J=5,8 Гц).
Спектр 13C-ЯМР (100 МГц, твердая фаза) δ(ppm): 27,1, 28,3, 29,7, 34,8, 38,0, 41,3, 54,0, 57,3, 59,7, 60,9, 72,1, 72,5, 103,3, 104,2, 108,5, 116,9, 126,9, 128,6, 134,5, 136,7, 140,7, 149,4, 151,3, 155,1, 169,5, 170,1, 175,6, 179,9, 183,7.
Пример 1. Ингибирующее действие соединения A на рост клеточной линии рака молочной железы человека (MFM223).
Для оценки противоопухолевого эффекта при введении соединения A использовали группы по четыре бестимусные мыши (BALB/cAJcl-nu/nu, самки, CLEA Japan, Inc.).
Клеточную линию MFM223 (ECACC), полученную из рака молочной железы человека, подвергали подготовительной обработке. Клетки MFM223 суспендировали при концентрации 2 × 108 клеток/мл в HBSS (Wako Pure Chemical Industries, Ltd.). В полученную суспензию добавляли равный объем матрицы MatrigelTM (Becton, Dickinson and Company, Япония) и перемешивали смесь в достаточной мере. Затем 0,1 мл смеси подкожно трансплантировали в правый бок каждой бестимусной мыши (CAnN.Cg-Foxn1nu/CrlCrlj, самки, Charles River Laboratories International, Inc.). Во время кормления перорально вводили β-эстрадиол (Wako Pure Chemical Industries, Ltd.), полученный при конечной концентрации 2,5 мкг/мл в питьевой воде. Через 46 дней после трансплантации выполняли резекцию образовавшейся опухоли и ее разрезали на мелкие кусочки. К этому добавляли HBSS, содержащий коллагеназу I типа (SIGMA) в конечной концентрации 380 единиц/мл и дезоксирибонуклеазу I (SIGMA) в конечной концентрации 160 тыс. единиц/мл, и перемешивали смесь при 37°C. После пропускания смеси через 100-мкм клеточное сито (Falcon(зарегистрированный товарный знак)) и центрифугирования для сбора клеток, эти клетки культивировали в среде для культивирования EMEM, содержащей 10% бычьей сыворотки.
Клетки, полученные таким образом, суспендировали при концентрации 1,4 × 108 клеток/мл в среде для культивирования EMEM, содержащей 10% бычьей сыворотки (Wako Pure Chemical Industries, Ltd.). В полученную суспензию добавляли равный объем матрицы MatrigelTM (Becton, Dickinson and Company, Япония) и перемешивали полученную смесь в достаточной мере. Далее 0,1 мл смеси подкожно трансплантировали в правый бок каждой мыши и затем оценивали противоопухолевый эффект.
Через 20 дней после трансплантации для измерения значений длинного и короткого диаметров опухоли, представляющей интерес, использовали электронный цифровой штангенциркуль (DigimaticTM Caliper; Mitutoyo Corporation). Мышей разделяли на группы так, что каждая группа характеризовалась практически одинаковыми средними значениями объема опухоли. Необходимо отметить, что каждое значение объема опухоли рассчитывали с применением следующего уравнения:
объем опухоли (мм3)=длинный диаметр (мм) × короткий диаметр (мм) × короткий диаметр (мм)/2.
Соединение A, полученное как описано в примере получения 1, растворяли в очищенной воде с получением концентрации 0,625 мг/мл или 2,5 мг/мл.
Затем раствор перорально вводили мышам из каждой группы в дозе 20 мл/кг, т.е. 12,5 мг/кг или 50 мг/кг, один раз в день на протяжении 12 дней. В контрольной группе вводили очищенную воду при 20 мл/кг.
На 3, 7 и 12 день после начала введения измеряли объем опухоли у каждой мыши. Результаты показаны в таблице 1 и на фигуре 1. Кроме того, изменения массы тела в динамике по времени показаны в таблице 2 и на фигуре 2.
[Таблица 1]
Изменения объема опухоли в динамике по времени (мм3)
[Таблица 2]
Изменения массы тела в динамике по времени (г)
| название | год | авторы | номер документа |
|---|---|---|---|
| ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ПРОТИВ РАКА ЖЕЛЧНЫХ ПРОТОКОВ | 2016 |
|
RU2712222C2 |
| ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГЕПАТОЦЕЛЛЮЛЯРНОЙ КАРЦИНОМЫ | 2019 |
|
RU2777535C2 |
| СОЛЬ МОНОЦИКЛИЧЕСКОГО ПРОИЗВОДНОГО ПИРИДИНА И ЕЕ КРИСТАЛЛ | 2015 |
|
RU2658821C1 |
| МОНОЦИКЛИЧЕСКОЕ ПИРИДИНОВОЕ ПРОИЗВОДНОЕ | 2014 |
|
RU2645352C2 |
| N-(ФЕНИЛСУЛЬФОНИЛ) БЕНЗАМИДЫ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ BCL-2 | 2017 |
|
RU2744358C2 |
| N-(ФЕНИЛСУЛЬФОНИЛ) БЕНЗАМИДЫ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ BCL-2 | 2020 |
|
RU2831159C2 |
| N-(ФЕНИЛСУЛЬФОНИЛ) БЕНЗАМИДЫ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ BCL-2 | 2017 |
|
RU2722560C1 |
| ИНДАЗОЛЬНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ FGFR, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2015 |
|
RU2719428C2 |
| СОЕДИНЕНИЯ НА ОСНОВЕ ПИРАЗОЛОПИРИДИНОНА | 2018 |
|
RU2806625C2 |
| КОМБИНАЦИИ ИНГИБИТОРОВ FGFR4 И СЕКВЕСТРАНТОВ ЖЕЛЧНЫХ КИСЛОТ | 2017 |
|
RU2742033C2 |
Группа изобретений относится к области медицины и фармацевтики и может быть использована для лечения рака молочной железы. Для этого предложено применение 5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамида или его фармакологически приемлемой соли в качестве терапевтического средства для лечения рака молочной железы. Группа изобретений относится также к применению 5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамида или его фармакологически приемлемой соли для получения фармацевтической композиции для лечения рака молочной железы. Группа изобретений обеспечивает повышение эффективности лечения рака молочной железы за счет большей ингибирующей активности заявленного соединения в отношении клеток рака молочной железы. 2 н. и 4 з.п. ф-лы, 2 ил., 1 пр., 2 табл.
1. Применение 5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамида
или его фармакологически приемлемой соли в качестве терапевтического средства для лечения рака молочной железы.
2. Применение по п. 1, где соль представляет собой 1,5-сукцинат.
3. Применение 5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамида или его фармакологически приемлемой соли для получения фармацевтической композиции для лечения рака молочной железы.
4. Применение по п. 3, где соль представляет собой 1,5-сукцинат.
5. Применение по п. 1 или 2, где рак молочной железы представляет собой местнораспространенный рак молочной железы, метастатический рак молочной железы или рецидивирующий рак молочной железы.
6. Применение по п. 3 или 4, где рак молочной железы представляет собой местнораспространенный рак молочной железы, метастатический рак молочной железы или рецидивирующий рак молочной железы.
| US 20140235614 A1, 21.08.2014 | |||
| KOZICZAK M., HOLBRO T., HYNES N.E | |||
| Blocking of FGFR signaling inhibits breast cancer cell proliferation through downregulation of D-type cyclins", Oncogene, vol | |||
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| ТЕПЛОСИЛОВАЯ УСТАНОВКА ДЛЯ ТЕПЛОВОЗОВ | 1920 |
|
SU3501A1 |
| ANDRE F., BACHELOT T | |||
| ET AL | |||
| Ведущий наконечник для обсадной трубы, употребляемой при изготовлении бетонных свай в грунте | 1916 |
|
SU258A1 |
| Clinical | |||
Авторы
Даты
2020-08-24—Публикация
2016-12-15—Подача