Область техники
[0001] Настоящее изобретение относится к терапевтическому средству для лечения гепатоцеллюлярной карциномы, содержащему моноциклическое производное пиридина, характеризующееся ингибирующей активностью по отношению к рецептору фактора роста фибробластов (FGFR), или его фармакологически приемлемую соль. Более конкретно, настоящее изобретение относится к терапевтическому средству для лечения гепатоцеллюлярной карциномы, содержащему 5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамид или его фармакологически приемлемую соль.
Уровень техники
[0002]
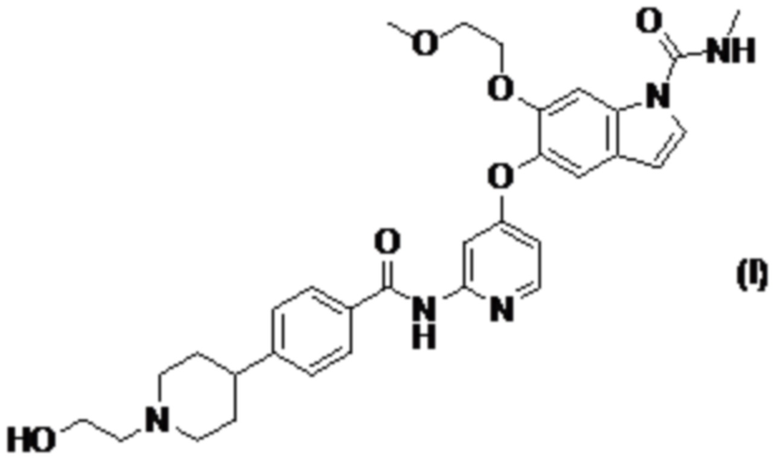
[0003] Сообщали, что 5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамид, представленный формулой (I), известен в качестве ингибитора FGFR1, FGFR2 или FGFR3 и характеризуется ингибирующей активностью по отношению к клеточной пролиферации при раке желудка, раке легкого, раке мочевого пузыря и раке эндометрия (патентный литературный источник 1). Сообщали, что приведенное выше соединение оказывает сильный терапевтический эффект по отношению к раку желчных протоков (патентный литературный источник 2) и раку молочной железы (патентный литературный источник 3). В качестве фармакологически приемлемой соли изложенного выше соединения известны сукцинат и малеат (патентный литературный источник 4).
[0004] Гепатоцеллюлярная карцинома развивается вследствие злокачественной трансформации клеток печени после хронического гепатита или цирроза печени. Примеры факторов, вызывающих развитие гепатоцеллюлярной карциномы, включают избыточное потребление алкоголя, избыток калорий в рационе, вирусную инфекцию и генетическую предрасположенность.
Примеры способов лечения гепатоцеллюлярной карциномы включают хирургическую резекцию, каутеризацию, эмболизацию печеночной артерии и терапию посредством инъекции этанола. Однако такие способы лечения имеют ограниченное применение в том случае, когда участок развития гепатоцеллюлярной карциномы является небольшим. В случае выявления множества раковых очагов или в случае распространения множества раковых очагов в других органах химиотерапию проводят посредством чреспеченочной артериальной инфузии или системного введения противоопухолевого средства. В качестве лекарственных средств, эффективных в лечении гепатоцеллюлярной карциномы, известны регорафениб, сорафениб (непатентные литературные источники 1 и 2) и т. п., но такие лекарственные средства часто вызывают побочные лекарственные реакции, такие как пневмония, гипертония и синдром "кисть-стопа", поэтому в будущем ожидается разработка нового лекарственного средства.
Список цитируемой литературы
Патентные литературные источники
[0005] Патентный литературный источник 1: US 2014-0235614 A
Патентный литературный источник 2: US 2018-0015079 A
Патентный литературный источник 3: публикация международной заявки № WO 2017/104739
Патентный литературный источник 4: US 2017-0217935 A
Непатентные литературные источники
[0006] Непатентный литературный источник 1: Kim K. et al., Regorafenib in advanced hepatocellular carcinoma (HCC): considerations for treatment, Cancer Chemotherapy and Pharmacology, 80, 945-954, 2017.
Непатентный литературный источник 2: Josep M. et al., Sorafenib in Advanced Hepatocellular Carcinoma, The New England Journal of Medicine, 359, 378-390, 2008.
Краткое описание изобретения
Техническая задача
[0007] Цель настоящего изобретения заключается в обеспечении нового терапевтического средства для лечения гепатоцеллюлярной карциномы.
Решение задачи
[0008] Принимая во внимания изложенные выше обстоятельства, в результате интенсивных исследований авторы настоящего изобретения выявили, что соединение, представленное формулой (I) выше, оказывает сильный терапевтический эффект по отношению к гепатоцеллюлярной карциноме, и таким образом реализовали настоящее изобретение.
[0009] В частности, в настоящем изобретение предусмотрено следующее [1] - [10]:
[1] терапевтическое средство для лечения гепатоцеллюлярной карциномы, содержащее соединение, представленное формулой (I), или его фармакологически приемлемую соль:
 .
.
[2] Применение соединения, представленного формулой (I), или его фармакологически приемлемой соли для лечения гепатоцеллюлярной карциномы.
[3] Соединение, представленное формулой (I), или его фармакологически приемлемая соль для лечения гепатоцеллюлярной карциномы.
[4] Способ лечения гепатоцеллюлярной карциномы, предусматривающий введение соединения, представленного формулой (I), или его фармакологически приемлемой соли нуждающемуся в этом пациенту.
[5] Композиция для лечения гепатоцеллюлярной карциномы, содержащая соединение, представленное формулой (I), или его фармакологически приемлемую соль.
[6] Композиция для лечения гепатоцеллюлярной карциномы, содержащая соединение, представленное формулой (I), или его фармакологически приемлемую соль и вспомогательное вещество.
[7] Терапевтическое средство, применение, соединение, способ или композиция, изложенные выше, где гепатоцеллюлярная карцинома является метастатической гепатоцеллюлярной карциномой или рецидивирующей гепатоцеллюлярной карциномой.
[8] Терапевтическое средство, применение, соединение, способ или композиция, изложенные выше, где при гепатоцеллюлярной карциноме экспрессируется FGFR.
[9] Терапевтическое средство, применение, соединение, способ или композиция, изложенные выше, где FGFR представляет собой FGFR1, FGFR2 или FGFR3.
[10] Терапевтическое средство, применение, соединение, способ или композиция, изложенные выше, где фармакологически приемлемая соль соединения, представленного формулой (I), представляет собой сесквисукцинат.
Полезные эффекты настоящего изобретения
[0010] Соединение, представленное формулой (I), может оказывать эффект, проявляющийся в уменьшении объема опухоли, по отношению к гепатоцеллюлярной карциноме.
Краткое описание графических материалов
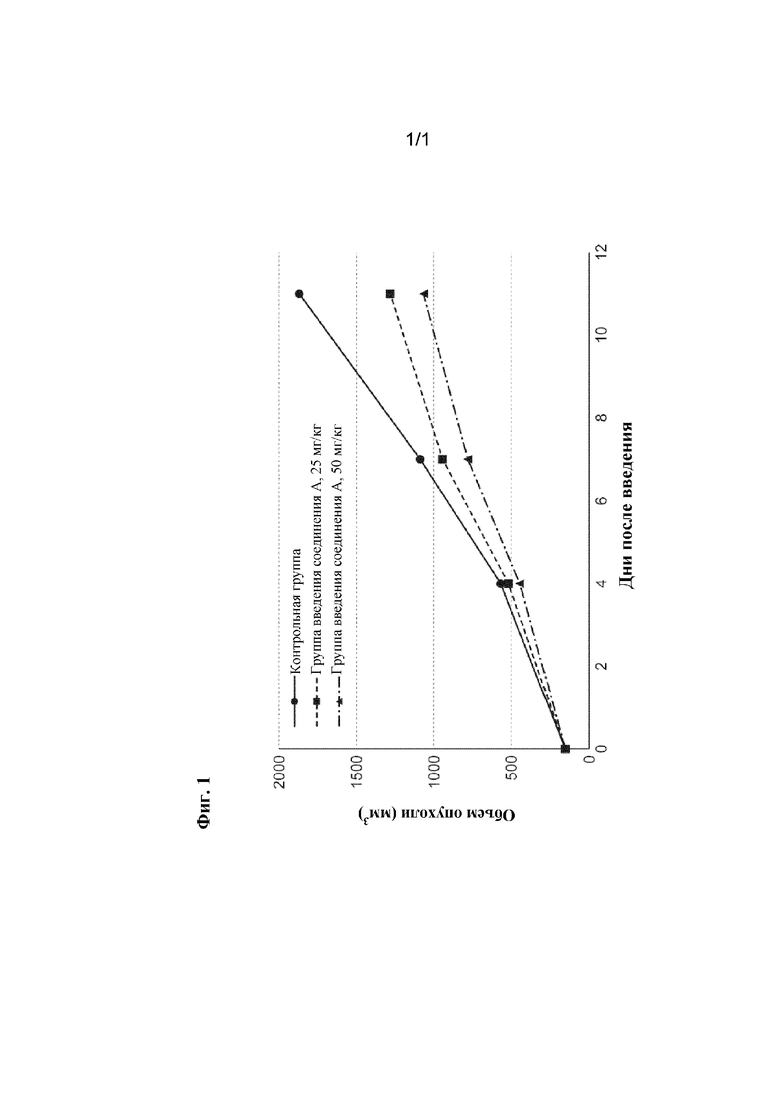
[0011] На фигуре 1 представлен график, показывающий результаты, полученные в примере 4. На оси ординат показан объем опухоли, а на оси абсцисс показаны дни после введения.
Описание вариантов осуществления
[0012] Соединение, представленное формулой (I), или его фармакологически приемлемую соль в соответствии с настоящим изобретением можно получить посредством способа, раскрытого в патентном литературном источнике 1.
[0013] В описании настоящего изобретения примеры фармакологически приемлемой соли включают соль неорганической кислоты, соль органической кислоты и соль кислой аминокислоты.
[0014] Предпочтительные примеры соли неорганической кислоты включают соли хлористоводородной кислоты, бромистоводородной кислоты, серной кислоты, азотной кислоты и фосфорной кислоты.
[0015] Предпочтительные примеры соли органической кислоты включают соли уксусной кислоты, янтарной кислоты, фумаровой кислоты, малеиновой кислоты, винной кислоты, лимонной кислоты, молочной кислоты, стеариновой кислоты, бензойной кислоты, метансульфоновой кислоты, этансульфоновой кислоты и п-толуолсульфоновой кислоты.
[0016] Предпочтительные примеры соли кислой аминокислоты включают соли аспарагиновой кислоты и глутаминовой кислоты.
[0017] Предпочтительная фармакологически приемлемая соль представляет собой сукцинат или малеат, но более предпочтительной солью является сукцинат. В частности, предпочтительно, чтобы соль была сесквисукцинатом.
[0018] Терапевтическое средство для лечения гепатоцеллюлярной карциномы в соответствии с настоящим изобретением можно вводить перорально в форме твердого препарата, такого как таблетка, гранулы, тонкодисперсные частицы, порошок или капсула, жидкости, желе, сиропа или т. п. Кроме того, терапевтическое средство для лечения гепатоцеллюлярной карциномы в соответствии с настоящим изобретением можно вводить парентерально в виде инъекции, суппозитория, мази, компресса или т. п.
[0019] Терапевтическое средство для лечения гепатоцеллюлярной карциномы в соответствии с настоящим изобретением может быть составлено посредством способа, описанного в семнадцатом издании Японской фармакопеи.
[0020] Дозу соединения, представленного формулой (I), или его фармакологически приемлемой соли можно соответствующим образом выбрать в зависимости от тяжести симптомов, возраста, пола, веса тела и различной чувствительности пациента, пути введения, времени введения, интервалов между введениями, типа фармацевтического препарата и т. п. Как правило, в случае перорального введения взрослому (вес тела: 60 кг) доза составляет от 100 мкг до 10 г, предпочтительно от 500 мкг до 10 г и, кроме того, еще более предпочтительно от 1 мг до 5 г в день. Данную дозу можно вводить 1-3 раздельными частями в день.
[0021] В настоящем описании гепатоцеллюлярная карцинома означает доброкачественную или злокачественную опухоль, развившуюся из клеток печени. Гепатоцеллюлярная карцинома включает метастатическую гепатоцеллюлярную карциному в ткани органа, отличного от печени, или рецидивирующую гепатоцеллюлярную карциному.
Примеры
[0022] Далее по тексту настоящее изобретение дополнительно подробно описано со ссылкой на примеры.
[0023] Пример получения 1
Посредством способа, раскрытого в описании из US 2017-0217935 A, получали сесквисукцинат 5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамида (далее в данном документе, называемый соединением A).
[0024] Пример 1. Показатель IC50 для соединения A по отношению к пролиферации клеточной линии гепатоцеллюлярной карциномы
В качестве клеточной линии гепатоцеллюлярной карциномы человека использовали SNU-398, Li-7, Hep3B2.1-7 и HuH-7. При этом SNU-398 и Hep3B2.1-7 получали из Американской коллекции типовых культур (ATCC), Li-7 получали из Центра клеточных ресурсов для биомедицинских исследований, Института исследования развития, старения и рака Университета Тохоку, и HuH-7 получали из банка клеток JCRB соответственно.
В случае каждой клеточной линии поддержание культуры проводили с использованием следующих сред.
(1) SNU-398 и Li-7
Среда RPMI-1640(Wako Pure Chemical Industries, Ltd.), содержащая 10% фетальной бычьей сыворотки (FBS) и пенициллин/стрептомицин.
(2) HuH-7
Среда DMEM с низким содержанием глюкозы (Wako Pure Chemical Industries, Ltd.), содержащая 10% FBS и пенициллин/стрептомицин.
(3) Hep3B2.1-7
Среда EMEM с низким содержанием глюкозы (Wako Pure Chemical Industries, Ltd.), содержащая 10% FBS и пенициллин/стрептомицин.
[0025] В каждую лунку 96-луночного черного планшета с прозрачным дном (Corning Incorporated, номер по каталогу: 3904) добавляли суспензию каждого вида клеток в количестве 80-90 мкл, которую готовили так, чтобы количество клеток составляло 0,75-1,25×104 клеток/мл, и затем клетки культивировали в течение ночи в инкубаторе с 5% CO2 (37°C). К полученным культивируемым клеткам добавляли соединение A, разведенное в каждой среде, содержащей 10% FBS, в количестве 10-20 мкл так, чтобы смесь была доведена до количества жидкости 100 мкл, а затем полученную смесь культивировали в течение 6 дней в инкубаторе с 5% CO2 (37°C).
[0026] Количество клеток в каждой лунке после культивирования рассчитывали путем измерения уровня внутриклеточного АТФ по интенсивности испускания с использованием CellTiter Glo-2.0 (Promega Corporation, номер по каталогу: G9243).
CellTiter Glo-2.0 добавляли в количестве 50 мкл в каждую лунку, и смесь смешивали в течение 10 минут с использованием перемешивающего устройства для планшетов. После этого обеспечивали прохождение реакции со смесью при комнатной температуре в течение 10 минут, и затем измеряли люминесценцию с помощью Multilabel Reader (ARVO X4, PerkinElmer, Inc.). Соотношение значений люминесценции в присутствии соединения A определяли исходя из того, что значение люминесценции в случае, когда соединение А не добавляли, принимали за 100%, а значение люминесценции в лунке, в которой отсутствовали клетки, принимали за 0%. Для тестируемого вещества рассчитывали концентрацию, требуемую для ингибирования пролиферации клеток на 50% (значение IC50). Результаты показаны в таблице 1.
[0027] [Таблица 1]
[0028] Пример 2. Противоопухолевая активность соединения A по отношению к клеточной линии гепатоцеллюлярной карциномы человека (HuH-7)
Пять голых мышей (CAnN.Cg-Foxn1nu/CrlCrlj, самок, CHARLES RIVER LABORATORIES JAPAN, INC.) использовали для каждой группы, и противоопухолевый эффект оценивали в том случае, когда вводили соединение A.
[0029] Клеточную линию гепатоцеллюлярной карциномы человека HuH-7 (полученной из банка клеток JCRB) суспендировали в среде DMEM (Wako Pure Chemical Industries, Ltd.), содержащей 10% бычьей сыворотки, так, чтобы концентрация клеток составила 8,0×107 клеток/мл. В суспензию добавляли матрицу MatrigelTM (Becton, Dickinson and Company, Япония) в объеме, равном объему суспензии, и полученную смесь перемешивали в достаточной степени. Смесь в количестве 0,1 мл подкожно трансплантировали в правый бок каждой мыши и оценивали противоопухолевый эффект у мыши.
[0030] Через 11 дней после трансплантации измеряли наиболее длинный диаметр и короткую ось опухоли с помощью электронного цифрового штангенциркуля (штангенциркулем DigimaticTM, Mitutoyo Corporation). Мышей разделяли на группы таким образом, что средние значения объемов опухолей в соответствующих группах были практически равными. Кроме того, объем опухоли рассчитывали в соответствии со следующим уравнением:
объем опухоли (мм3) = (наиболее длинный диаметр (мм)) × (короткая ось (мм)) × (короткая ось (мм))/2.
[0031] Соединение А растворяли в очищенной воде так, чтобы концентрация соединения А составила 2,5 мг/мл.
Соединение A вводили каждой из мышей в соответствующих группах в дозе 50 мг/кг один раз в день в течение 5 дней. После чего введение соединения A прекращали на 2 дня, а затем его вводили перорально в течение 3 дней. При этом объем, подлежащий введению, составлял 20 мл/кг, и контрольной группе вводили очищенную воду в том же объеме.
[0032] Измеренные значения объемов опухолей в контрольной группе и в группе введения соединения A показаны в таблице 2.
[0033] [Таблица 2]
[0034] Пример 3. Противоопухолевая активность соединения A по отношению к клеточной линии гепатоцеллюлярной карциномы человека (Hep3B2.1-7)
Пять голых мышей (CAnN.Cg-Foxn1nu/CrlCrlj, самок, CHARLES RIVER LABORATORIES JAPAN, INC.) использовали для каждой группы, и противоопухолевый эффект оценивали в том случае, когда вводили соединение A.
[0035] Клетки линии гепатоцеллюлярной карциномы человека Hep3B2.1-7 (полученной из ATCC) суспендировали в сбалансированном солевом растворе Хенка (HBSS) так, чтобы концентрация клеток составила 4×107 клеток/мл. В суспензию добавляли матрицу MatrigelTM (Becton, Dickinson and Company, Япония) в объеме, равном объему суспензии, и полученную смесь перемешивали в достаточной степени. Смесь в количестве 0,1 мл подкожно трансплантировали в правый бок каждой мыши и оценивали противоопухолевый эффект у мыши.
[0036] В день 19 после трансплантации измеряли наиболее длинный диаметр и короткую ось опухоли с помощью электронного цифрового штангенциркуля (штангенциркулем DigimaticTM, Mitutoyo Corporation). Мышей разделяли на группы таким образом, что средние значения объемов опухолей в соответствующих группах были по сути равными. Кроме того, объем опухоли рассчитывали в соответствии со следующим уравнением:
объем опухоли (мм3) = (наиболее длинный диаметр (мм)) × (короткая ось (мм)) × (короткая ось (мм))/2.
[0037] Соединение А растворяли в очищенной воде так, чтобы концентрация соединения А составила 5 мг/мл.
Соединение A вводили каждой из мышей в соответствующих группах в дозе 100 мг/кг один раз в день в течение 5 дней. После чего введение соединения A прекращали на 2 дня, а затем его вводили перорально в течение 4 дней. При этом объем, подлежащий введению, составлял 20 мл/кг, и контрольной группе вводили очищенную воду в том же объеме.
[0038] Измеренные значения объемов опухолей в контрольной группе и в группе введения соединения A показаны в таблице 3.
[0039] [Таблица 3]
[0040] Пример 4. Противоопухолевая активность соединения A по отношению к клеточной линии гепатоцеллюлярной карциномы человека (SNU-398)
Пять голых мышей (CAnN.Cg-Foxn1nu/CrlCrlj, самок, CHARLES RIVER LABORATORIES JAPAN, INC.) использовали для каждой группы, и противоопухолевый эффект оценивали в том случае, когда вводили соединение A.
[0041] Клетки линии гепатоцеллюлярной карциномы человека SNU-398 (полученной из ATCC) суспендировали в HBSS так, чтобы концентрация клеток составила 5×107 клеток/мл. В суспензию добавляли матрицу MatrigelTM (Becton, Dickinson and Company, Япония) в объеме, равном объему суспензии, и полученную смесь перемешивали в достаточной степени. Смесь в количестве 0,1 мл подкожно трансплантировали в правый бок каждой мыши и оценивали противоопухолевый эффект у мыши.
[0042] В день 9 после трансплантации измеряли наиболее длинный диаметр и короткую ось опухоли с помощью электронного цифрового штангенциркуля (штангенциркулем DigimaticTM, Mitutoyo Corporation). Мышей разделяли на группы таким образом, что средние значения объемов опухолей в соответствующих группах были практически равными. Кроме того, объем опухоли рассчитывали в соответствии со следующим уравнением:
объем опухоли (мм3) = (наиболее длинный диаметр (мм)) × (короткая ось (мм)) × (короткая ось (мм))/2.
[0043] Соединение А растворяли в очищенной воде так, чтобы концентрация соединения А составила 1,25 мг/кг или 2,5 мг/мл.
Соединение A вводили перорально каждой из мышей в соответствующих группах в дозе 25 мг/кг или 50 мг/кг один раз в день в течение 11 дней. При этом объем, подлежащий введению, составил 20 мл/кг. Контрольную группу не подвергали обработке.
[0044] Измеренные значения объемов опухолей в контрольной группе и в группе введения соединения A показаны в таблице 4 и на фигуре 1. Увеличение объема опухоли замедлялось дозозависимым образом за счет введения соединения A.
[0045] [Таблица 4]
| название | год | авторы | номер документа |
|---|---|---|---|
| ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2016 |
|
RU2730503C2 |
| ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ РАКА ЖЕЛЧЕВЫВОДЯЩИХ ПУТЕЙ | 2016 |
|
RU2728932C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ОПУХОЛИ | 2018 |
|
RU2750539C2 |
| ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ПРОТИВ РАКА ЖЕЛЧНЫХ ПРОТОКОВ | 2016 |
|
RU2712222C2 |
| ПРОТИВООПУХОЛЕВОЕ ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО | 2016 |
|
RU2718048C2 |
| Комбинированные терапии для лечения гепатоцеллюлярной карциномы | 2019 |
|
RU2787993C2 |
| МАКРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ И ЕГО ПРИМЕНЕНИЯ | 2018 |
|
RU2783238C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ИНГИБИТОРОМ EZH2 | 2018 |
|
RU2754131C1 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО И УСИЛИТЕЛЬ ПРОТИВООПУХОЛЕВОГО ДЕЙСТВИЯ | 2018 |
|
RU2783759C2 |
| КОМБИНАЦИЯ АНТАГОНИСТА PD-1, ИНГИБИТОРА ТИРОЗИНКИНАЗЫ VEGFR/FGFR/RET И ИНГИБИТОРА CBP/БЕТА-КАТЕНИНА ДЛЯ ЛЕЧЕНИЯ РАКА | 2020 |
|
RU2838452C1 |
Изобретение относится к применению 5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамида или его фармакологически приемлемой соли сесквицукцината в качестве терапевтического средства для лечения гепатоцеллюлярной карциномы. Технический результат: раскрыта возможность применения 5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамида для лечения гепатоцеллюлярной карциномы. 2 н. и 2 з.п. ф-лы, 4 табл., 4 пр. 1 ил.
1. Применение 5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамида или его фармакологически приемлемой соли:
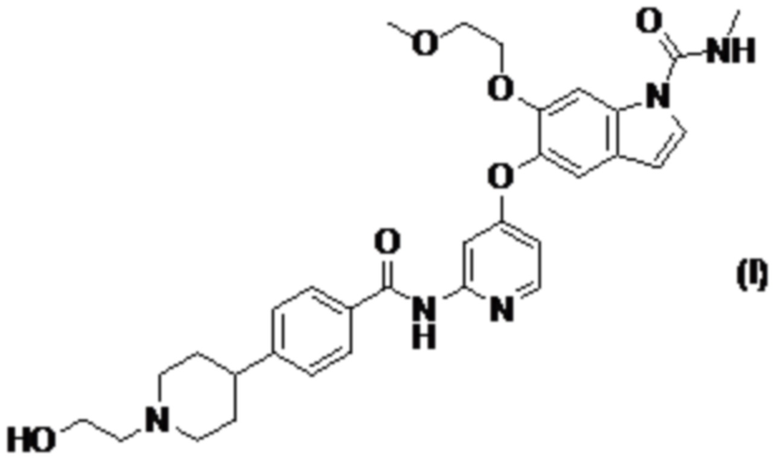
в качестве терапевтического средства для лечения гепатоцеллюлярной карциномы.
2. Применение по п. 1, где соль представляет собой сесквисукцинат.
3. Применение 5-((2-(4-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамид)пиридин-4-ил)окси)-6-(2-метоксиэтокси)-N-метил-1H-индол-1-карбоксамида или его фармакологически приемлемой соли для изготовления фармацевтической композиции для лечения гепатоцеллюлярной карциномы.
4. Применение по п. 3, где соль представляет собой сесквисукцинат.
| US 2017217935 A1, 03.08.2017 | |||
| WATANABE MIYANO ET AL | |||
| Телефонное устройство | 1926 |
|
SU7090A1 |
| MOLECULAR CANCER THERAPEUTICS, vol | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| TAO YU ET AL | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2022-08-08—Публикация
2019-03-26—Подача