Изобретение относится к области медицинской химии, а именно к новому 1,2,3-триазолсодержащему производному фузидовой кислоты формулы (1), представляющему собой (1-Бензил-1H-1,2,3-триазол-4-ил)метил (Z)-2-((3S,4S,8S,10S,11R,14S,16S)-16-ацетокси-3,11-дигидрокси-4,8,10,14-тетраме-тилгексадекагидро-17H-циклопента[a]фенантрен-17-илиден)-6-метилгепт-5-еноат, проявляющему антибактериальную активность в отношении Staphylococcus aureus (MRSA) и фунгицидную активность в отношении Cryptococcus neoformans.

Известны N,N'-(1,4-фенилен)бис(2-(4-R-1H-1, 2,3-триазол-1-ил)ацет-амид) в виде бис-1,2,3-триазола (2) и N,N'-(1,4-фенилен)бис(2-(4-(2-(4-R- 1H-1,2,3-триазол-1-ил)этил)-1H-1,2,3-триазол-1-ил)ацетамид) в виде тетракис-1,2,3-триазола (3), содержащие циклогексилметильный или циклопентильный заместители в молекуле, проявляющие антибактериальные и противогрибковые свойства (схема 1) [Y. Nural, S. Ozdemir, M. S. Yalcin, B. Demir, H. Atabey, Z. Seferoglu, A. Ece. New bis- and tetrakis-1,2,3-triazole derivatives: Synthesis, DNA cleavage, molecular docking, antimicrobial, antioxidant activity and acid dissociation constants. Bioorg. Med. Chem. Lett. 2022. 55. 128453].
Схема 1

Скрининг in vitro противомикробной активности данных соединений в отношении грамположительных (E. hirae, B. cereus, S. aureus) и грамотрицательных (P. aeruginosa, L. pneumophila subsp. pneumophiia, E. coli) микроорганизмов, а также двух грибковых культур C. albicans и C. tropicalis показал, что бис-1,2,3-триазольное производное (3) проявляло наибольшую антибактериальную активность в отношении штаммов E. coli и E. hirae со значениями МИК: 4 и 8 мкг/мл, соответственно. Активным в отношении бактерий E. hirae оказалось также соединение (4), проявлявшее также фунгицидное действие в отношении грибковой культуры C. tropicalis, показывая значение МИК 4 мкг/мл для обоих патогенов. Производное тетракис-1,2,3-триазола (5) обладало фунгицидным действием в отношении штаммов C. albicans и C. tropicalis (МИК 8 и 4 мкг/мл, соответственно).
Известны 1,2,3-триазольные производные бетулиновой (6-9) и олеаноловой (10-13) кислот, содержащие в триазольном кольце арилзамещенные фрагменты (схема 2).
Схема 2

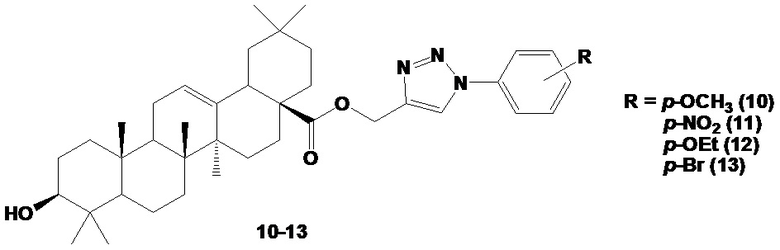
Изучение in vitro противоопухолевой активности соединений (6-13) показало, что коньюгаты бетулиновой кислоты (6-8) ингибировали рост раковых клеток более чем на 50%. Аналог бетулиновой кислоты (6), содержащий фторфенильный фрагмент, отмечен как лидер, продемонстрировавший умеренную цитотоксическую активность в отношении четырех клеточных линий рака человека (HL-60, Mia PaCa-2, PC-43, A549) с IC50 в диапазоне от 5 до 7 μМ [I. Khan, S.K. Guru, S.K. Rath, P.K Chinthakindi, B. Singh, S. Koul, S. Bhushan, P.L Sangwan. A novel triazole derivative of betulinic acid induces extrinsic and intrinsic apoptosis in human leukemia HL-60 Cells. Eur. J. Med. Chem. 2016. 108. 104-116]. Среди производных олеаноловой кислоты (10-13) соединение (11) с p-нирофенильным заместителем у триазольного фрагмента продемонстрировало лучшую ингибирующую активность в отношении клеток меланомы A372-S2 и фибросаркомы HT1080 с IC50 4.97 μМ и 3.51 μМ, соответственно [G. Wei, W. Luan, S. Wang, S. Cui, F. Li, Y. Liu, Y. Liu, M. Cheng. A Library of 1,2,3-triazole-substituted oleanolic acid derivatives as anticancer agents: design, synthesis, and biological evaluation. Org. Biomol. Chem. 2015. 13. 1507-1514]. Изучение антибактериальной активности не проводилось.
Известно 1,2,3-триазольное производное метилового эфира дигидрохинопимаровой кислоты (14), содержащее бензильный заместитель в триазольном кольце (схема 3).
Схема 3
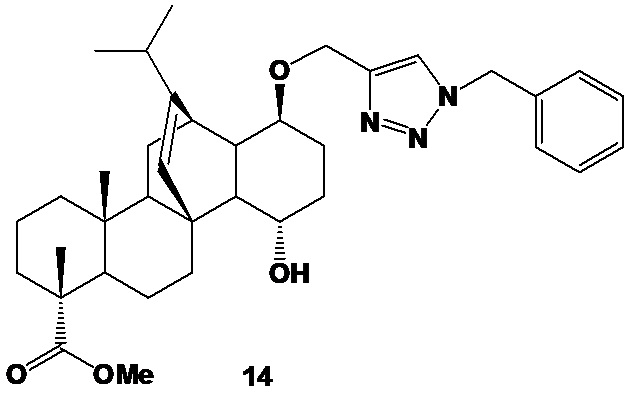
Изучение антибактериальнго действия in vitro в отношении грамположительных (S. aureus) и грамотрицательных (E. coli, K. Pneumoniae, A. baumannii, P. aeruginosa) микроорганизмов, а также двух грибковых культур (C. albicans, C. neoformans) показало, что полученное дитерпеновое производное (14) не проявляет противомикробное действие в отношении указанных патогенов [E.V. Tret'yakova, E.V. Salimova, L.V. Parfenova. Synthesis, modification, and biological activity of propargylated methyl dihydroquinopimarates. Nat. Prod. Res. 2022. 36(1). 79-86].
Таким образом, 1,2,3-триазолсодержащее производное фузидовой кислоты (1) и его противомикробная активность в литературе не описана.
Задачей предлагаемого изобретения является синтез и изучение противомикробной активности in vitro (1-бензил-1H-1,2,3-триазол-4-ил)метил (Z)-2-((3S,4S,8S,10S,11R,14S,16S)-16-ацетокси-3,11-дигидрокси-4,8,10,14-тетраме-тилгексадекагидро-17H-циклопента[a]фенантрен-17-илиден)-6-метилгепт-5-еноата (1) в отношении грамположительных и грамотрицательных микроорганизмов (S. aureus, E. coli, K. Pneumoniae, A. baumannii, P. aeruginosa), а также двух грибковых культур (C. albicans, C. neoformans) и оценка результатов в соответствии с системой скрининга противомикробных веществ, принятой в CO-ADD (http://www.co-add.org).
Заявленное соединение (1) было синтезировано с использованием катализируемого медью азид-алкинового циклоприсоединения (CuAAC) согласно методу, описанному в работе [E.V. Tret'yakova, E.V. Salimova, L.V. Parfenova. Synthesis, modification, and biological activity of propargylated methyl dihydroquinopimarates. Nat. Prod. Res. 2022. 36(1). 79-86]. На первой стадии смешивали эквимолярные количества бензилбромида, триэтиламина и азида натрия при комнатной температуре в хлористом метилене, в результате чего получали in situ бензилазид, который затем реагировал с пропаргиловым эфиром фузидовой кислоты (15) в присутствии CuI в качестве катализатора (схема 4). В результате реакции получали 1,2,3-триазольное производное фузидовой кислоты (1) с выходом 70%, которое представляло собой порошок белого цвета (т.пл. 108-110°С),  -2.7 (c 1.18, CHCl3). Структура соединения (1) установлена с помощью 1D и 2D спектроскопии ЯМР 1Н и 13С и масс-спектрометрии MALDI TOF/TOF.
-2.7 (c 1.18, CHCl3). Структура соединения (1) установлена с помощью 1D и 2D спектроскопии ЯМР 1Н и 13С и масс-спектрометрии MALDI TOF/TOF.
Схема 4
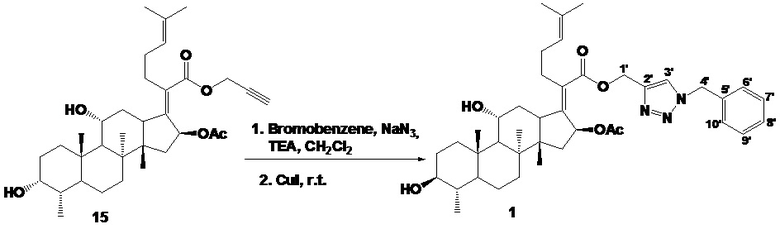
Сущность изобретения поясняется следующими примерами.
Пример 1. Смесь 1 ммоль (0,7 мл) триэтиламина, 1 ммоль (0,07 г) азида натрия и 1 ммоль (0,25 мл) бензилбромида в 5 мл CH2Cl2 интенсивно перемешивали в течение 30 мин при комнатной температуре. К смеси добавляли 0.5 ммоль (0.44 г) соединения (15) в 5 мл CH2Cl2 и 0.11 ммоль (0.02 г) иодида меди (I) и перемешивали 12 ч при комнатной температуре (контроль методом ТСХ). Реакционную смесь выливали в 50 мл воды, продукты экстрагировали хлороформом (2×50 мл), экстракт промывали водой до нейтральной рН, сушили CaCl2. Растворитель упаривали, осадок хроматографировали на колонке с силикагелем, элюируя смесью хлороформ : метанол 40:1. Выход соединения (1) 0.38 г (70%), порошок белого цвета. Т.пл. 108-110°С,  -2.7 (c 1.18, CHCl3).
-2.7 (c 1.18, CHCl3).
Спектральные характеристики (1-бензил-1H-1,2,3-триазол-4-ил)метил (Z)-2-((3S,4S,8S,10S,11R,14S,16S)-16-ацетокси-3,11-дигидрокси-4,8,10,14-тетраметилгексадекагидро-17H-циклопента[a]фенантрен-17-илиден)-6-метилгепт-5-еноата (1)1.
Спектр ЯМР 1Н (CDCl3), δ, м.д.: 0.89 с (3Н, Н18), 0.91 д (3Н, Н28, 3J 7.5 Гц), 0.96 с (3Н, Н19), 1.02-1.13 м (1Н, Н6), 1.07-1.15 м (1Н, Н7), 1.25 д (1Н, Н15, J 14.0 Гц), 1.35 с (1Н, Н30), 1.45-1.51 м (1Н, Н1), 1.49 с (3Н, Н27), 1.50-1.58 м (1Н, Н5), 1.50-1.66 м (1Н, Н6), 1.51-1.57 м (1Н, Н9), 1.61 с (3Н, Н26), 1.67-1.76 м (1Н, Н7), 1.69-1.76 м (1Н, Н2), 1.76-1.84 м (1Н, Н12), 1.78-1.87 м (1Н, Н2), 1.91 с (3Н, ОСОСН3), 1.91-1.97 м (1Н, Н23), 2.03-2.12 м (1Н, Н23), 2.06-2.15 м (1Н, Н4), 2.09-2.18 м (1Н, Н15), 2.11-2.19 м (1Н, Н1), 2.28 д (1Н, Н12, J 13.0 Гц), 2.34-2.53 м (2Н, Н22), 3.02 д (1Н, Н13, J 11.5 Гц), 3.70-3.75 м (1Н, Н3), 4.29-4.35 м (1Н, Н11), 5.02 т (1Н, Н24, J 7.0 Гц), 5.05 д (1Н, Н1', J 12.8 Гц), 5.22 д (1Н, Н1', J 12.8 Гц), 5.52 с (2Н, Н4'), 5.81 д (1Н, Н16, J 8.5 Гц), 7.25-7.31 м (1Н, Н8'), 7.27 д (2Н, Н6',10', J 6.0 Гц), 7.32-7.37 м (2Н, Н7',9'), 7.60 с (1Н, Н3'). Спектр ЯМР 13С (CDCl3), δ, м.д.: 15.99 (С28), 17.68 (С27), 17.77 (С18), 20.90 (С6), 20.96 (ОСОСН3), 23.09 (С19), 23.85 (С30), 25.69 (С26), 28.29 (С23), 28.93 (С22), 29.92 (С2), 30.09 (С1), 32.03 (С7), 35.14 (С4), 35.54 (С12), 36.45 (С5), 36.87 (С10), 38.99 (С15), 39.44 (С8), 44.11 (С13), 48.66 (С14), 49.28 (С9), 54.17 (С4'), 57.86 (С1'), 68.12 (С11), 71.36 (С3), 74.35 (С16), 122.97 (С24), 123.93 (С3'), 128.07 (С6', С10'), 128.76 (С8'), 129.11 (С7', С9'), 129.92 (С20), 132.52 (С25), 134.50 (С5'), 143.04 (С2'), 149.08 (С17), 169.80 (С21), 170.48 (ОСОСН3). Масс-спектр (MALDI TOF/TOF), m/z (Iотн., %): 710 (30.5) [М+Na]+, 726 (100) [M+K]+.
1Контроль реакции осуществляли методом ТСХ на пластинах Sorbfil (Сорбполимер, Краснодар, Россия), проявляли 10% раствором серной кислоты. Температура плавления определена на приборе РНМК 80/2617. Спектры ЯМР 1D (1Н, 13С) и 2D (COSY, NOESY, HSQC, HMBC) сняты на спектрометре Bruker Avance 500 (125.78 МГц для 13С и 500.17 МГц для 1Н) с использованием стандартных импульсных последовательностей фирмы Bruker, внутренний стандарт Me4Si, растворитель - CDCl3. Оптические углы измерены на поляриметре Perkin-Elmer 341. Масс-спектры MALDI TOF/TOF получены на спектрометре Bruker Autoflex TM III Smartbeam с использованием матрицы 3-(4-гидрокси-3,5-диметоксифенил)проп-2-еновой кислоты (синапиновая кислота).
Пример 2. Противомикробный скрининг соединения (1) проводили в CO-ADD (The Community for Antimicrobial Drug Discovery), финансируемым Wellcome Trust (Великобритания) и Университетом Квинсленда (Австралия), на пяти бактериальных штаммах: Escherichia coli (E. coli) ATCC 25922, Klebsiella pneumoniae (K. pneumoniae) ATCC 700603, Acinetobacter baumannii (A. baumannii) ATCC 19606, Pseudomonas aeruginosa (P. aeruginosa) ATCC 27853 и Staphylococcus aureus (S. aureus (MRSA)) ATCC 43300. Противогрибковую активность определяли на двух грибковых штаммах: Candida albicans (C. albicans) ATCC 90028 и Cryptococcus neoformans (C. neoformans) ATCC 208821.
Первичный скрининг противомикробной активности проводился путем тестов на ингибирование размножения клеток, используя образцы в одной (32 мкг/мл) концентрации. Аликвоту каждого образца в ДМСО помещали в 384-луночный планшет и обрабатывали соответствующей бактериальной культурой. Ингибирование роста бактерий определяли измерением поглощения при 600 нм (OD600) с использованием монохромного микропланшетного ридера Tecan M1000 Pro. Процент ингибирования роста рассчитывали для каждой лунки с использованием отрицательного контроля (только для среды) и положительного контроля (бактерии без ингибиторов) на той же пластинке. Все тесты продублированы. В случае если один или оба раза наблюдалось ингибирование роста ≥80%, соединение считалось активным.
При первичном скрининге было выявлено наличие противомикробной активности у (1-бензил-1H-1,2,3-триазол-4-ил)метил (Z)-2-((3S,4S,8S,10S,11R,14S,16S)-16-ацетокси-3,11-дигидрокси-4,8,10,14-тетраметилгексадекагидро-17H-циклопента[a]фенантрен-17-илиден)-6-метилгепт-5-еноата (1) в отношении культуры бактерий S. aureus (MRSA) и грибковой культуры C. neoformans (таблица 1).
цин
зол
1 S. aureus (MRSA); 2 E. coli; 3K. pneumonia; 4 P. aeruginosa; 5 A. baumannii;
6 C. albicans; 7 C. neoformans.
Для соединения (1) была определена минимальная ингибирующая концентрация в отношении вышеуказанных культур, а также изучена цитотоксическая активность (таблица 2).
0.25
32
32
0.25
32
32
*MIC (минимальная ингибирующая концентрация) - наименьшая концентрация, при которой было обнаружено полное ингибирование бактерий.
**СС50 - концентрация исследуемого вещества, при которой происходит гибель 50% клеточной линии эмбриональных почек человека HEK293.
Минимальную ингибирующую концентрацию (MIC; мкг/мл) определяли в соответствии с рекомендациями Института клинических и лабораторных стандартов (CLSI, https://clsi.org/), определяя самую низкую концентрацию, при которой было обнаружено полное ингибирование бактерий или грибов. Тесты проводились в двойном повторе. Максимальный процент ингибирования роста обозначался как Dmax. Соединения классифицировали как активные при MIC≤16 мкг/мл или MIC≤10 мкМ в любой реплике (n=2 на разных планшетах).
Цитотоксическое действие (Hk; СС50 (мкг/мл)) определяли на клеточной линии эмбриональных почек человека HEK293 путем определения концентрации, вызывающей гибель 50% клеток. Ингибирование роста клеток HEK293 определяли, измеряя флуоресценцию после добавления 5 мкл 25 мкг / мл резазурина (конечная концентрация 2.3 мкг/мл) и после инкубации в течение еще 3 ч при 37°C в 5% CO2. Интенсивность флуоресценции измеряли с использованием монохромного микропланшетного ридера Tecan M1000 Pro с использованием автоматического вычисления коэффициента усиления. Максимальный процент цитотоксичности обозначали как Dmax. Соединение считалось токсичным при CC50≤32 мкг / мл или CC50≤10 мкМ. Кроме того, образцы были отмечены как частичные цитотоксические, если Dmax≥50%, даже при CC50 выше максимальной тестируемой концентрации.
«Колистин» и «Ванкомицин» использованы в качестве положительных стандартов оценки бактериального ингибирования для грамотрицательных и грамположительных бактерий, соответственно. «Флуконазол» использован в качестве стандартного фунгицидного средства для C. albicans и C. neoformans. «Тамоксифен» использован в качестве положительного стандарта оценки цитотоксичности. Методики тестирования противомикробной, фунгицидной и цитотоксической активности in vitro соединений приведены на сайте http://www.co-add.org.
Анализ результатов противомикробного скрининга показал, что 1,2,3-триазолсодержащее производное фузидовой кислоты (1) в концентрации 0.25 мкг/мл проявляло высокую антибактериальную активность, ингибируя рост и размножение > 100% грамм-положительных бактерий Staphylococcus aureus (MRSA). Кроме того, соединение (1) также обладало умеренным фунгицидным действием в отношении штамма C. neoformans, ингибируя рост данной грибковой культуры на 54.9% в концентрации 32 мкг/мл, и проявляло низкую токсичность по отношению к клеточной линии НЕК293 при максимальной тестируемой концентрации 32 мкг/мл.
Таким образом, соединение (1) проявляет противомикробную активность в отношении патогенных микроорганизмов S. aureus (MRSA) и C. neoformans и обладает низкой токсичностью при максимально тестируемой концентрации.
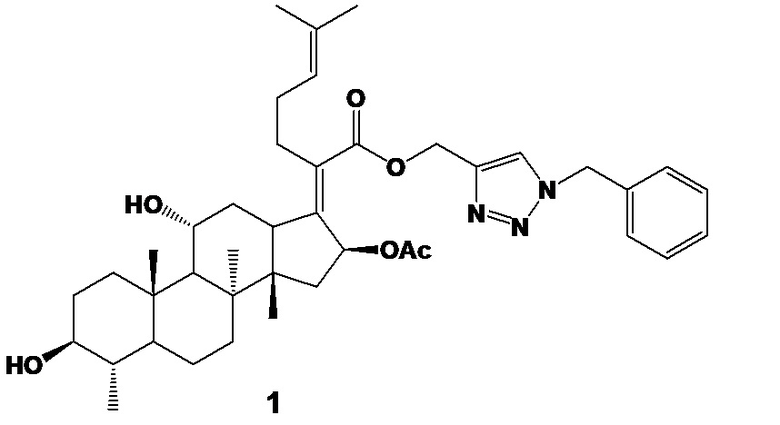
Изобретение относится к области медицинской химии, а именно к (1-Бензил-1H-1,2,3-триазол-4-ил)метил (Z)-2-((3S,4S,8S,10S,11R,14S,16S)-16-ацетокси-3,11-дигидрокси-4,8,10,14-тетраметилгексадекагидро-17H-циклопента[a]фенантрен-17-илиден)-6-метилгепт-5-еноату (1), который обладает противомикробной активностью. Изобретение относится также к применению указанного соединения в качестве средства с антимикробной активностью для борьбы с заболеваниями человека и животных, вызванными грамположительными бактериями Staphylococcus aureus (MRSA) и патогенными грибковыми культурами Cryptococcus neoformans. 2 н.п. ф-лы, 2 табл., 2 пр.
 .
.
1. (1-Бензил-1H-1,2,3-триазол-4-ил)метил (Z)-2-((3S,4S,8S,10S,11R,14S,16S)-16-ацетокси-3,11-дигидрокси-4,8,10,14-тетраметилгексадекагидро-17H-циклопента[a]фенантрен-17-илиден)-6-метилгепт-5-еноат (1)
 .
.
2. Применение 1,2,3-триазолсодержащего производного фузидовой кислоты по п. 1 в качестве средства с антимикробной активностью для борьбы с заболеваниями человека и животных, вызванными грамположительными бактериями Staphylococcus aureus (MRSA) и патогенными грибковыми культурами Cryptococcus neoformans.
| НОВЫЕ АМИНОПРОИЗВОДНЫЕ ФУЗИДОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2019 |
|
RU2735665C1 |
| N,N'-БИС(3-АМИНОПРОПИЛ)БУТАН-1,4-ДИАМИНОПРОИЗВОДНЫЕ ФУЗИДОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ ШИРОКИЙ СПЕКТР ПРОТИВОМИКРОБНОЙ АКТИВНОСТИ | 2019 |
|
RU2726196C1 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛА, ОБЛАДАЮЩИЕ ПРОТИВОГРИБКОВОЙ АКТИВНОСТЬЮ | 2000 |
|
RU2203280C2 |
| TW 201011004 A, 16.03.2010 | |||
| CN 104412985 A, 18.03.2015 | |||
| E.V | |||
| TRET'YAKOVA ET AL, Synthesis, modification, and biological activity of propargylated methyl dihydroquinopimarates, NAT | |||
| PROD | |||
| RES, 2022, 36(1), pp | |||
| Цилиндрический сушильный шкаф с двойными стенками | 0 |
|
SU79A1 |
| Y | |||
| NURAL ET AL, New bis- and | |||
Авторы
Даты
2022-11-23—Публикация
2022-07-13—Подача