Изобретение относится к области биотехнологии, генетической инженерии и медицины, в частности, к растворимому рекомбинантному слитому белку с пролонгированным периодом полувыведения из крови, обладающему свойством связывать ингибиторы ацетилхолинэстеразы.
Бутирилхолинэстераза (BChE, БХЭ, ЕС 3.1.1.8) является циркулирующим в крови гомологом ацетилхолинэстеразы (AChE, АХЭ, ЕС 3.1.1.7), фермента, ассоциированного с клеточными мембранами и ответственного за гидролиз нейротрансмиттера ацетилхолина в синаптической щели. БХЭ человека присутствует в крови в низких концентрациях 2-5 мг/л. При этом она обладает свойством связывать и инактивировать фосфорорганические отравляющие вещества и пестициды.
По структуре природная БХЭ представляет тетрамер из одинаковых гликозилированных субъединиц, соединенных вместе дополнительным пролин-богатым пептидом. Такая структура и большой молекулярный вес (примерно 340 кДа, вес не гликозилированной одной субъединицы 65 кДа) позволяют ей длительное время (десятки часов) циркулировать в крови и избегать выведения через почки (быстро выводятся из кровотока белки с молекулярным весом до 70 кДа).
Подсчитано, что для защиты взрослого человека от 2 ЛД50 токсических фосфорорганических соединений (ФОС) необходимы 200 мг чистого препарата человеческой БХЭ [Ashani Y; Pistinner S. Estimation of the upper limit of human butyrylcholinesterase dose required for protection against organophosphates toxicity: A mathematically based toxicokinetic model // Toxicol. Sci., 2004, 77:358-367]. В настоящее время БХЭ можно получать из коммерчески производимой фракции плазмы крови IV-4 Кона, из которой можно выделить 1,5 г белка на 80 кг фракции [Saxena A; Tipparaju P.; Luo С; Doctor BP. Pilot-scale production of human serum butyrylcholinesterase suitable for use as a bioscanvenger against nerve agent toxicity // Process Biochem., 2010, 45:1313-1318; Lockridge O; Schopfer LM; Winger G; Woods JH. Large scale purification of butyrylcholinesterase from human plasma suitable for injection into monkeys; a potential new therapeutic for protection against cocaine and nerve agent toxicity // J. Med. Chem. Biol. Radiol. Def., 2005, 3:nihms5095] с хорошими фармакокинетическими свойствами [Saxena A; Sun W; Luo С; Doctor BP. Human serum butyrylcholinesterase: In vitro and in vivo stability, pharmacokinetics, and safety in mice // Chem. Biol. Interact., 2005, 157-158, 199-203; Sun W; DoctorBP; Saxena A. Safety and pharmacokinetics of human serum butyrylcholinesterase in guinea pigs // Chem. Biol. Interact., 2005, 157-158, 428-429]. Тем не менее ежегодные запасы плазмы не позволяют производить достаточное количество БХЭ для удовлетворения потребностей в ней. Кроме того, ужесточаются требования к производству препаратов крови, в частности, очистке от контаминирующих патогенных вирусов, что приводит к увеличению этапов производства и существенному уменьшению выхода конечного продукта.
Получение рекомбинантной БХЭ в генно-модифицированных растениях [Geyer ВС; Kannan L; Garnaud РЕ; et al. Plant-derived human butyrylcholinesterase, but not an organophosphorous-compound hydrolyzing variant thereof, protects rodents against nerve agents // Proc. Natl. Acad. Sci. USA, 2010, 107: 20251-20256; Corbin JM, Hashimoto BI, Karuppanan K, et al. Semicontinuous Bioreactor Production of Recombinant Butyrylcholinesterase in Transgenic Rice Cell Suspension Cultures // Frontiers in Plant Science, 2016, 7:412] или трансгенных животных [Huang YJ; Huang Y; Baldassarre H; et al. Recombinant human butyrylcholinesterase from milk of transgenic animals to protect against organophosphate poisoning. Proc. Natl. Acad. Sci. USA, 2007, 104:13603-13608] позволяет производить большие количества белка, но выделенный белок до сих пор требует обработки после очистки [Pope С; Uchea С; Flynn N; et al. In vitro characterization of cationic copolymer-complexed recombinant human butyrylcholinesterase // Biochem. Pharmacol. 2015, 98:531-539], что повышает конечную стоимость. Единственным препаратом в мире, прошедшим первую фазу клинических испытаний, является рекомбинантная БХЭ человека, полученная из молока трансгенных коз с последующим после выделения белка его пегилированием, - Protexia®, (PharmAthene Canada, Inc., Канада), известная также из заявки на патент СА 2659809 А1. В настоящее время из-за нерентабельности производства и постепенного отказа от природного сырья из-за возможного содержания в нем эндогенных вирусов, препарат Protexia® не выпускается.
Имеются работы по получению рекомбинантной БХЭ в клетках насекомых и млекопитающих [Millard СВ, Lockridge О, Broomfield CA Design and expression of organophosphorous acid anhydride hydrolase activity in human butyrylcholinesterase // Biochemistry, 1995, 34:15925-15933; Altamirano CV and Lockridge O. Association of tetramers of human butyrylcholinesterase is mediated by conserved aromatic residues of the carboxy terminus // Chem. Biol. Interact., 1999, 119-120:53-60; Илюшин ДГ, Эртле ОМ, Бобик ТВ, и др. Рекомбинантная БХЭ человека как биологический антидот нового поколения: разработка эукариотической системы экспрессии // Acta Naturae, 2013, 1(16): 76-87], однако все они характеризуются крайне низким выходом: 5-25 мг на 1 литр в 1 неделю (приблизительные цифры) и что приводит к нерентабельности производства.
Наиболее рентабельным производством рекомбинантных белков в большом количестве с низкой стоимостью являются бактериальные системы, например, клетки Escherichia coli. Гетерологичная экспрессия генов в клетках грамотрицательных бактерий Е. coli является одним из наиболее эффективных и дешевых способов получения рекомбинантных белков ввиду хорошо изученной генетики данного микроорганизма, доступности удобных экспрессионных векторных систем и штаммов хозяина, простоты в использовании; низкой цены и высоких уровней экспрессии целевого гена, достигающих 40-45% от общего клеточного белка [Hannig G, Makrides S. Strategies for optimizing heterologous protein expression in Escherichia coli // Trends Biotechnol., 1998, 16(2):54-60; Baneyx F. Recombinant protein expression in Escherichia coli // Curr Opin Biotechnol., 1999, 10(5):411-421]. Однако, несмотря на большое количество достоинств E.coli, далеко не всегда можно рутинным способом получить высокий уровень экспрессии целевого гена в данной системе. Так, почти все попытки экспрессировать БХЭ в Е. coli были неуспешными и приводили к формированию в Е. coli телец включения, которые было невозможно рефолдировать (ренатурировать). Возможной причиной является наличие в структуре белка трех дисульфидных связей и девяти сайтов для гликозилирования, увеличивающих растворимость и стабильность белка. [Kolarich D; Weber A; Pabst М; et al. Glycoproteomic characterization of butyrylcholinesterase from human plasma // Proteomics, 2008, 8:254-263]. В 2016 г. Goldenzweig с соавторами опубликовали компьютерный алгоритм PROSS (Protein Repair One Stop Shop), который позволяет модифицировать последовательность эукариотического белка для увеличения его стабильности и растворимости при экспрессии в Е. coli [Goldenzweig A; Goldsmith М; Hill SE; et al. Automated structure- and sequence-based design of proteins for high bacterial expression and stability // Mol. Cell 2016, 63:337-346].
На основании этого алгоритма Brazzolotto в 2017 г. модифицировал последовательность БХЭ человека. Были экспрессированы в Е. coli 7 белков с разными мутациями в виде слитых белков с тиоредоксином, и модификация БХЭ, содержащая 48 мутаций, была самая активная, т.е. наиболее растворимая при экспрессии (Таблица 1) [Brazzolotto X, Igert A, Guillon V et al. Bacterial Expression of Human Butyrylcholinesterase as a Tool for Nerve Agent Bioscavengers Development // Molecules 2017, 22(11):1828].

Авторам удалось получить активную растворимую БХЭ, используя совокупность алгоритма PROSS, слияния белка с тиоредоксином и специализированных клеток, обеспечивающих правильный фолдинг белка. Однако слитый белок обладал молекулярным весом всего 74 кДа и, соответственно, коротким временем полувыведения из крови. Brazzolotto также использовал для увеличения растворимости технологию экспрессии рекомбинантных белков в виде слитых белков с тиоредоксином. Однако тиоредоксин является не самым эффективным белком, который обеспечивает увеличение растворимости белка партнера в слитом белке.
В 1993 году Маккой и его коллеги сообщили, что растворимость некоторых цитокинов и факторов роста млекопитающих может быть улучшена путем их слияния с высокорастворимым тиоредоксином белка E. coli. Однако они не рассматривали вопрос о том, могут ли другие высокорастворимые белки также функционировать как усилители растворимости. Капуст и Во в 1999 году сравнили растворимость 18 слитых белков, представляющих комбинации высокорастворимых белков с нерастворимыми. Оказалось, что мальтоза-связывающий белок Е. coli (МВР) чрезвычайно эффективно повышает растворимость его партнеров по слиянию [Waugh D.S. The remarkable solubility-enhancing power of Escherichia coli maltose-binding protein // Postepy Biochem., 2016, 62, 3:377-382]. Однако влияние МВР на растворимость БХЭ до сих пор не было исследовано
Таким образом, на сегодняшний день не существует эффективной и экономически выгодной системы экспрессии активной рекомбинантной БХЭ человека, обладающей увеличенным периодом полувыведения из крови.
Задачей, на решение которой направлено настоящее изобретение, являлось создание рекомбинантной растворимой при экспрессии в гетерологичном организме активной бутирилхолинэстеразы человека с увеличенным, не менее 20 часов, периодом полувыведения из крови.
Задача решалась получением рекомбинантного слитого белка, аминокислотная последовательность которого представлена в SEQ ID NO: 1. Слитый белок содержит полигистидиновую последовательность, последовательность мальтоза-связывающего белка (МВР) Е. coli, линкер и модифицированную последовательность БХЭ человека. Полигистидиновая последовательность служит для очистки слитого белка методом иммобилизованной металл-аффинной хроматографии. Последовательность МВР увеличивает растворимость слитого белка и, таким образом, обеспечивает увеличение выхода целевого белка, его правильную структуру и функции. Линкер между последовательностями БХЭ и МВР позволяет частям слитого белка должным образом независимо друг от друга формировать вторичную и третичную структуры.
Задача также решалась получением генетической конструкции, кодирующей слитый рекомбинантный белок по настоящему изобретению, оптимизированной для синтеза белка в системе бактериальных клеток Escherichia coli. Нуклеотидная последовательность генетической конструкции по настоящему изобретению представлена в SEQ ID NO: 2.
Также задача решалась созданием плазмидного экспрессионного вектора, кодирующего слитый рекомбинантный белок. Плазмидный экспрессионный вектор по настоящему изобретению представляет собой вектор рЕТ28а, содержащий генетическую конструкцию SEQ ID NO: 2, кодирующую слитый рекомбинантный белок по настоящему изобретению, которая введена в упомянутый вектор по сайтам рестрикции XhoI и NcoI. Карта полученного плазмидного экспрессионного вектора по настоящему изобретению приведена на Фиг. 2.
Также задача решалась созданием штамма Е. coli BL21[DE3] рЕТ28а-6his-MBP-BChE - продуцента слитого рекомбинантного белка по настоящему изобретению, посредством трансформации штамма Е. coli BL21[DE3] плазмидным экспрессионным вектором по настоящему изобретению.
Штамм-продуцент по настоящему изобретению позволяет получить активный растворимый слитый белок БХЭ человека и МВР Е. coli с выходом при неоптимизированном культивировании 5 мг белка из 1 г влажной биомассы, что в 267 раз больше, чем выход при выделении белка из фракции Кона, описанный ранее в патенте. При этом молекулярный вес слитого белка составляет ≈ 102 кДа, а время полувыведения из крови составляет 22,4 ч, что в несколько раз выше, чем у БХЭ, полученной в растениях или клетках линии СНО.
Изобретение иллюстрируется следующими графическими материалами:
На Фиг. 1. представлена аминокислотная последовательность рекомбинантного слитого белка, содержащего модифицированную БХЭ человека и МВР. Составные элементы белка (С-конец каждого элемента обозначен цифрой): * - полигистидиновая последовательность, окруженная гибкими мостиками (1-13 ак); ** - последовательность МВР из Е. coli (14-380 ак; *** - линкер (381-391 ак); **** - последовательность модифицированной БХЭ человека (392-920 ак).
На Фиг. 2. представлена карта плазмидного экспрессионного вектора pET28a-MBP-BChE, содержащего ген, кодирующий модифицированную БХЭ человека, слитую с МВР.
На Фиг. 3. представлена электрофореграмма лизатов клеток Е. coli в 10% ПААГ. 1 - маркер молекулярного веса Bio-Rad 1610377, 2 - контроль, 3 - 6his-BChE, 4 - 6his-MBP-BChE, 5 - контроль, 6 - 6his-BChE 37°С, 7 - 6his-BChE 20°C, 8 - 6his-MBP-BChE 37°C, 9 - 6his-MBP-BChE 20°C. Стрелками обозначены полосы, соответствующие рекомбинантным белкам.
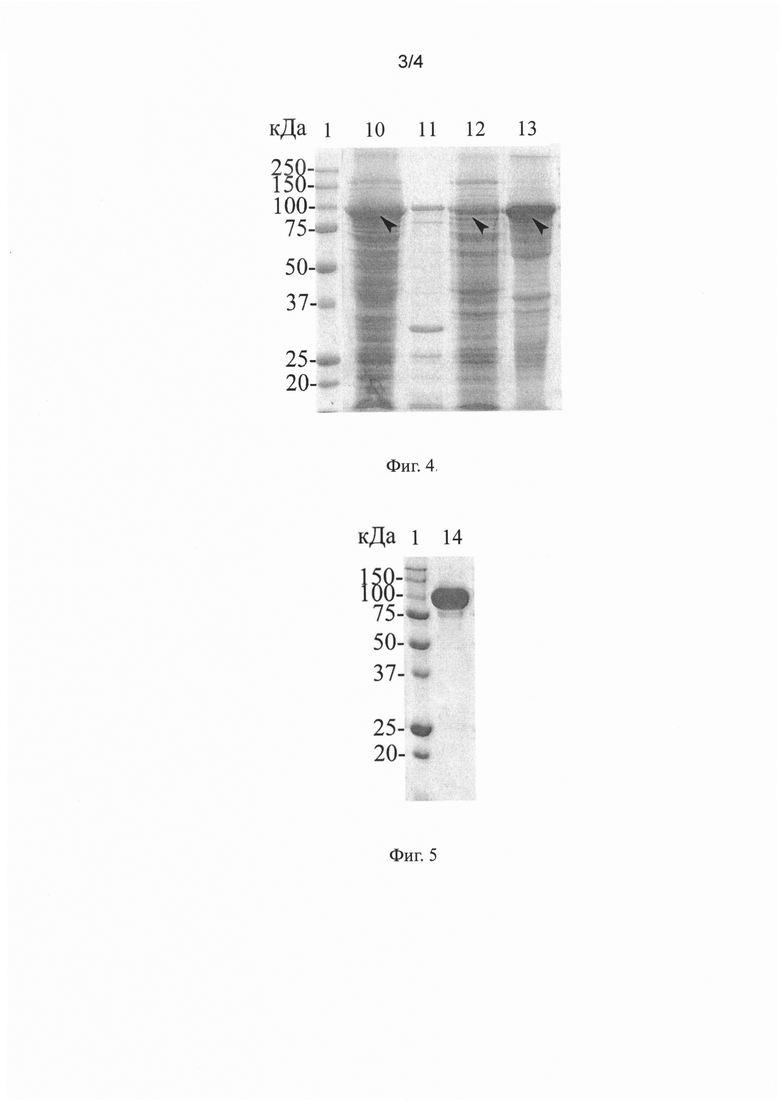
На Фиг. 4. представлена электрофореграмма рекомбинантных белков в 10% ПААГ. 1 - маркер молекулярного веса Precision Plus Protein™ Dual Xtra Prestained (Bio-Rad, кат №1610377), 10 - растворимая фракция 6his-MBP-BChE 20°C, 11 - нерастворимая фракция 6his-MBP-hBCHE 20°C, 12 - растворимая фракция 6his-MBP-BChE, 13 - нерастворимая фракция 6his-MBP-BChE. Стрелками обозначены полосы, соответствующие рекомбинантным белкам.
На Фиг. 5. представлена электрофореграмма образца очищенного белка 6his-MBP-BChE в 10% ПААГ. 1 - маркер молекулярного веса маркер молекулярного веса Precision Plus Protein™ Dual Xtra Prestained (Bio-Rad, кат №1610377), 14-20 мкг белка 6his-MBP-BChE.
На Фиг. 6. представлены результаты анализа ферментативной активности очищенного белка 6his-MBP-BChE по настоящему изобретению. А - белок 6his-MBP-BChE, В - стандартный образец БХЭ человека (рекомбинантная полноразмерная бутирилхолинэстераза человека, полученная в эукариотических клетках линии HEK293, Abeam, кат. №ab152070, Великобритания), *р<0,05.
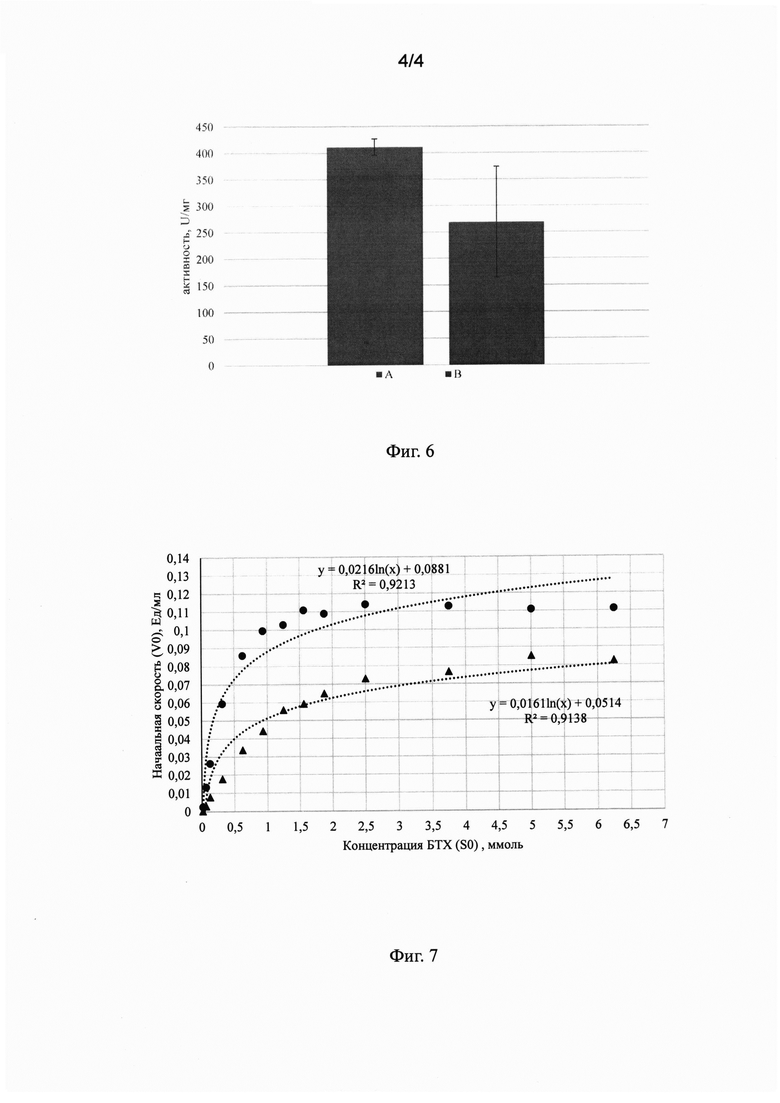
На Фиг. 7. представлены результаты определения константы ингибирования очищенного белка 6his-MBP-BChE по настоящему изобретению фосфорорганическим инсектицидом диизопропилфторфосфатом (ДФФ). График представляет собой зависимость концентрации субстрата (S0) в растворе от начальной скорости взаимодействия фермента с субстратом (V0). Средние значения приведены для четырехкратного измерения.  6his-MBP-BChE;
6his-MBP-BChE;  6his-MBP-BChE+ДФФ.
6his-MBP-BChE+ДФФ.
Пример 1. Дизайн белковой молекулы
Схема слитого белка представлена на Фиг. 1. Для получения растворимого активного белка БХЭ использовали последовательность фермента из статьи: Brazzolotto X, Igert A, Guillon V et al. Bacterial Expression of Human Butyrylcholinesterase as a Tool for Nerve Agent Bioscavengers Development // Molecules 2017, 22(11):1828; в качестве последовательности, улучшающей растворимость слитого белка, использовали последовательность МВР. Для обеспечения независимого фолдинга двух белков в слитом белке, между ними был помещен «мостик» - линкер из 11 аминокислот. С N-конца слитый белок содержит полигистидиновую последовательность для очистки методом иммобилизованной металл-аффинной хроматографии. Последовательность аминокислот слитого белка представлена в SEQ ID NO: 1.
Возможность слитого белка формировать трехмерную структуру была подтверждена с использованием компьютерного моделирования [http://zhanglab.ccmb.med.umich.edu/I-TASSER/output/S501955/, дата обращения 04.12.2019].
На основании аминокислотной последовательности с учетом кодонового предпочтения Е. coli была разработана нуклеотидная последовательность гена 6his-MBP-BChE (SEQ ID NO: 2).
Пример 2. Создание генетической конструкции
Последовательность гена по SEQ ID NO: 2, и кодирующую цепь, и антисмысловую, разбивали на олигонуклеотиды с использованием программы Gene2O1igo [Rouillard JM, Lee W, Truan G, et al. Gene2O1igo: oligonucleotide design for in vitro gene synthesis // Nucleic Acids Res., 2004;32:W176-W180]. Олигонуклеотиды подбирали таким образом, чтобы их концы перекрывались олигонуклеотидом комплементарной цепи.
Все олигонуклеотиды имели схожие термодинамические свойства (температура плавления, Tm, различалась на 3°С) для обеспечения равномерной гибридизации в процессе сборки и были очень специфически подобраны, чтобы избежать неправильной сборки.
Длина каждого олигонуклеотида составила около 50-100 п.н. Олигонуклеотиды синтезировали с использованием твердофазного синтеза.
ПЦР-сборку проводили в объеме 50 мкл, содержащем 200 мкМ каждого дНТФ, 0,1 мкМ каждого олигонуклеотида, 0,5 ед Taq ДНК-полимеразы (Promega) или 1 ед Pfu ДНК полимеразы (NEB) в буфере, содержащем 2,5 мМ MgCl2. Осуществляли ПЦР-сборку следующим образом: денатуририровали при 95°С в течение 2 мин с последующими 30 циклами при 95°С в течение 30 сек, 52°С в течение 30 сек и при 72°С в течение 1 мин, заканчивали инкубацию при 72°С течение 5 мин.
Лигазную цепную реакцию (LCR) проводили в конечном объеме 25 мкл, содержащем 0,1 мкМ каждого олигонуклеотида с использованием полинуклеотидкиназы Т4 (NEB) и 10 единиц Taq- ДНК-лигазы (NEB). LCR проводили следующим образом: 94°С в течение 2 мин, 40 циклов при 94°С в течение 30 сек, 51°С в течение 4 мин.
Полноразмерный продукт после LCR или сборки реакции ПЦР подвергали ПЦР-амплификации с использованием праймеров в 50 мкл реакционной смеси, содержащей 3 мкл смеси ПЦР-сборки или 5 мкл смеси LCR, 200 мкМ каждого дНТФ, 1 мкМ каждого праймера, 0,5 ед Taq ДНК-полимеразы (Promega) или 1 ед Pfu ДНК полимеразы (NEB) и буфер, содержащий 2,5 мМ MgCl2. ПЦР проводили следующим образом: денатурация при 95°С в течение 2 мин с последующими 30 циклами при 95°С в течение 30 сек, 55°С в течение 30 сек и 72°С в течение 1 мин, завершающая инкубация при 72°С в течение 5 мин.
Для каждого элемента гена произвели в общей сложности 21 гибридизацию олигонуклеотидов с блоками размером от 16 до 22 нуклеотидов и Tm от 62,5 до 69,6°С. Собранную последовательность клонировали в промежуточном плазмидном векторе pUC57 по сайту рестрикции EcoRV.
В результате была создана генетическая конструкция, которую в дальнейшем использовали для получения штаммов-продуцентов и наработки слитых рекомбинантных белков 6his-MBP-BChE, содержащих БХЭ человека и МВР (Фиг. 1, SEQ ID NO: 2). Для получения штамма-продуцента белка сравнения 6his-BChE использовалась аналогично полученная генетическая конструкция без последовательности МВР.
Пример 3. Создание плазмидного экспрессионного вектора Для получения плазмидного экспрессионного вектора полученную в Примере 2 генетическую конструкцию, содержащую ген рекомбинантной БХЭ с гистидиновым тэгом и МВР вставляли в плазмидную ДНК рЕТ28а по сайтам рестрикции XhoI и NcoI, после чего проводили его секвенирование. Карта полученного вектора pET28a-MBP-BChE приведена на Фиг. 2.
Пример 4. Получение штамма - продуцента рекомбинантной растворимой БХЭ человека.
Для получения штамма - продуцента растворимой рекомбинантной БХЭ человека проводили трансформацию компетентных клеток Е. coli штамма BL21[DE3] методом электропорации по стандартной методике. Вектор рЕТ28а, использованный в Примере 2, содержит промотор для Т7 РНК полимеразы, а используемый штамм содержит в геноме ген Т7 РНК полимеразы под контролем lacUV5 промотора, что позволяет индуцировать экспрессию рекомбинантного белка с помощью изопропил-β-D-1-тиогалактопиранозида ИПТГ или лактозы.
Используя данный штамм-продуцент, была показана экспрессия рекомбинантных белков 6his-BChE и 6his-MBP-BChE (Фиг. 3). Уровень экспрессии белка 6his-BChE очень низкий (около 1% от общих клеточных белков), однако хорошо видна полоса белка 6his-MBP-BChE (102 кДа, 15% от общих клеточных белков). Была проведена оптимизация культивирования по температуре. Понижение температуры культивирования до 20°С является одним из распространенных способов предотвращения образования телец включения благодаря тому, что при этом происходит медленное правильное сворачивание молекулы белка. Используя штамм-продуцент по настоящему изобретению, показали экспрессию рекомбинантных белков 6his-BChE и 6his-MBP-BChE при 20°С (Фиг. 3.). Уровень экспрессии белка 6his-BChE практически не определяется ни при 20°С, ни при 37°С и составляет всего около 1% от общих клеточных белков. При этом хорошо видна полоса белка 6his-MBP-BChE при 20°С (≈102 кДа). В качестве контроля использовали штамм-продуцент без индукции ИПТГ, полоса целевого белка отсутствует, что говорит об отсутствии неконтролируемой экспрессии гена. Таким образом использование МВР в составе слитого белка 6his-MBP-BChE позволило добиться уровня экспрессии (15%), достаточного для разработки технически и экономически обоснованной технологии получения рекомбинантного белка.
Пример 5. Проверка растворимости рекомбинантной растворимой БХЭ человека.
Обнаружение рекомбинантного слитого белка в растворимой фракции, полученной после осаждения разрушенных клеток Е. coli штамма-продуцента, косвенно говорит о правильной (нативной) конформации белка, при этом часто в клетках наблюдается образование телец включения - агломератов, которые содержат частично не свернутые рекомбинантные и клеточные белки.
Для определения состояния белка интереса в клетке использовали метод выделения белков при помощи ультразвуковой обработки на льду. Этот метод не приводит к денатурации белков при выделении и позволяет выделять белки в той форме, в которой они находятся в клетке, таким образом, можно определить растворимость рекомбинантного белка. Проводили разделение растворимой и нерастворимой фракций, полученных после разрушения клеток. На Фиг. 5. представлены результаты электрофореза образцов растворимой и нерастворимой фракций в штамме-продуценте, полученном в Примере 3. Как видно на рисунке белок 6his-MBP-BChE в клетках, культивируемых при 20°С, находится в цитоплазме, в растворимой фракции (дорожки 10-11), однако белок 6his-MBP-BChE в клетках, культивируемых при 37°С, находится, в основном, в нерастворимой фракции - в тельцах включения (дорожки 12-13).
Пример 6. Выделение и очистка рекомбинантной БХЭ человека.
Для первичной очистки рекомбинантного белка из клеточного лизата использовали стандартный метод высаливания сульфатом аммония (СА). Клетки лизировали при помощи ультразвуковой обработки на льду, в образец в лизирующем буфере добавили СА до 2,4 М, после чего проводили центрифугирование при 10000g. Полученный осадок растворяли и проводили анионообменную хроматографию на сорбенте Toyopearl GigaCap DEAE-650М (Tosoh), элюцию проводили градиентом хлорида натрия при рН буфера 8,0. Целевые фракции с анионообменной хроматографии дополнительно очищали с помощью иммобилизованной металл-аффинной хроматографии (ИМАХ) на сорбенте Ni2+ Sepharose™ High Performace (GE Healthcare), элюцию проводили градиентом имидазола при рН буфера 8.0. Целевые фракции диализовали и концентрировали методом диафильтрации, после чего тестировали на присутствие посторонних примесей (ГФ XIII, ОФС.1.2.1.0023.15). В результате был получен образец белка с чистотой более 95% (Фиг. 5).
Пример 7. Анализ ферментативной активности рекомбинантной БХЭ человека.
Была измерена ферментативная активность образца белка 6his-MBP-BChE, полученного в примере 6. Для измерения был использован набор Butyrylcholinesterase Assay Kit (ab241010, Abcam, Великобритания). В качестве контроля использовали стандартный образец БХЭ человека (рекомбинантная полноразмерная бутирилхолинэстераза человека, полученная в эукариотических клетках линии HEK293, ab152070, Abcam, Великобритания). Набор для анализа бутирилхолинэстеразы основан на способности бутирилхолинэстеразы гидролизовать субстрат и продуцировать тиохолин. Тиохолин взаимодействует с 5,5-дитиобисом (2-нитробензойной кислотой) (DTNB) и испускает желтый сигнал, который можно определить количественно при 412 нм. Было показано, что полученный препарат белка в пересчете на мг/мл имеет активность 411 U/мг достоверно большую (р<0,05), чем используемый стандартный образец. (Фиг. 6).
Пример 8. Определение времени полувыведения полученного препарата рекомбинантной БХЭ человека.
Было определено время полувыведения из крови у мышей линии BALB/c двух вариантов бутирилхолинэстеразы:
1. 6his-MBP-BChE - БХЭ слитая с 6his-MBP,
2. hBChE - БХЭ с отщепленной последовательностью 6his-MBP.
Для отщепления последовательности 6his-MBP использовали TEV протеазу, сайт для которой находится в линкере между бутирилхолинэстеразой и тэгом 6his-MBP. После отщепления проводили очистку от 6his-MBP с использованием ИМАХ.
В работе были использованы самки беспатогенных мышей линии BALB/c весом 20-22 г (НИИ «Питомник лабораторных животных» ФИБХ РАН, Пущино), которых содержали в условиях SPF-вивария, при 12-часовом цикле день/ночь. Животные получали стерильное питание и воду ad libitum. Каждая экспериментальная группа включала 10 животных.
БХЭ в количестве 100 U вводили животным внутрибрюшинно, после чего в различные временные точки отбирали 5 мкл крови из хвостовой вены для определения активности фермента в крови и времени его полувыведения  .
.
 для препарата БХЭ 6his-MBP-BChE составило 1344±160 мин,
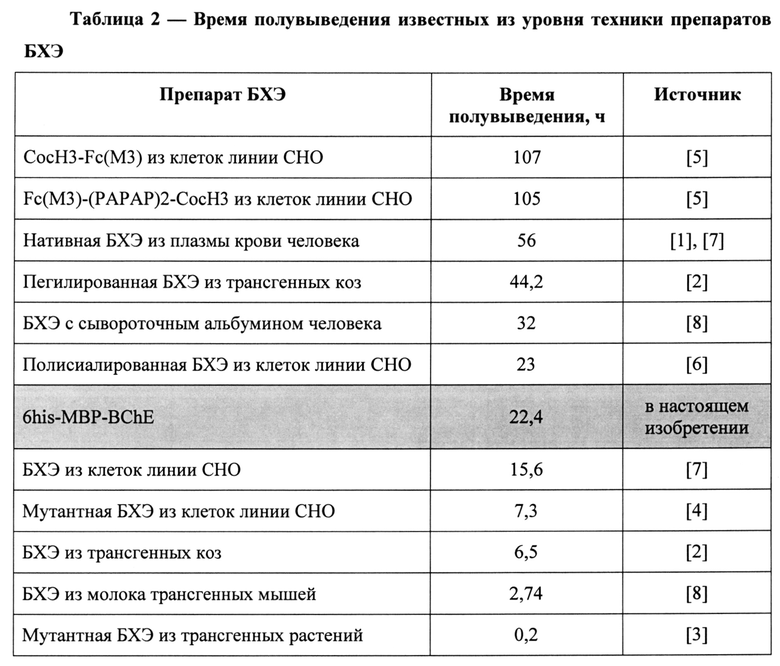
для препарата БХЭ 6his-MBP-BChE составило 1344±160 мин,  для бутирилхолинэстеразы с отщепленной последовательностью 6his-MBP составило 348±40 мин. Таким образом, рекомбинантный белок БХЭ слитый с последовательностью МВР характеризуется в 4 раза более длительным временем полу выведения из крови. Время полувыведения известных из уровня техники препаратов БХЭ для сравнения представлено в Таблице Таблица 2.
для бутирилхолинэстеразы с отщепленной последовательностью 6his-MBP составило 348±40 мин. Таким образом, рекомбинантный белок БХЭ слитый с последовательностью МВР характеризуется в 4 раза более длительным временем полу выведения из крови. Время полувыведения известных из уровня техники препаратов БХЭ для сравнения представлено в Таблице Таблица 2.
1. Lockridge О, Schopfer LM, Winger G, Woods JH. Large scale purification of butyrylcholinesterase from human plasma suitable for injection into monkeys; a potential new therapeutic for protection against cocaine and nerve agent toxicity // The Journal of Medical, Chemical, Biological, and Radiological Defense, 2005, 3: nihms5095.
2. Huang Y-J, Huang Y, Baldassarre H, et al. Recombinant human butyrylcholinesterase from milk of transgenic animals to protect against organophosphate poisoning // Proc Natl Acad Sci U S A, 2007, 104:13603-13608.
3. Wang G, Zhang T, Huang H, et al. Plant expression of cocaine hydrolase-Fc fusion protein for treatment of cocaine abuse // BMC biotechnology, 2016, 16:72.
4. Xue L, Hou S, Tong M, et al. Preparation and in vivo characterization of a cocaine hydrolase engineered from human butyrylcholinesterase for metabolizing cocaine // Biochem J, 2013, 453:447-454.
5. Chen X, Xue L, Hou S., et al. Long-acting cocaine hydrolase for addiction therapy // Proc Natl Acad Sci U S A, 2016, 113:422-427.
6. Ilyushin DG, Smirnov IV, Belogurov AA, et al. Chemical polysialylation of human recombinant butyrylcholinesterase delivers a long-acting bioscavenger for nerve agents in vivo // Proc Natl Acad Sci U S A., 2013; 110(4):1243-1248.
7. Duysen EG, Bartels CF, Lockridge O. Wild-type and A328W mutant human butyrylcholinesterase tetramers expressed in Chinese hamster ovary cells have a 16-hour half-life in the circulation and protect mice from cocaine toxicity // J Pharmacol Exp Ther., 2002, 302(2):751-758.
8. Huang YJ, Lundy PM, Lazaris A, et al. Substantially improved pharmacokinetics of recombinant human butyrylcholinesterase by fusion to human serum albumin // BMC Biotechnol., 2008, 8:50.
Пример 9. Определение константы ингибирования рекомбинантной растворимой БХЭ человека фосфорорганическим инсектицидом диизопропилфторфосфатом (ДФФ).
Была определена возможность полученной в настоящем изобретении рекомбинантной растворимой БХЭ человека служить антидотом при отравлениях фосфорорганическими соединениями. Для этого была определена константа ингибирования БХЭ фосфорорганическим инсектицидом ДФФ. Для определения использовался модифицированный метод Эллмана. В лунку 96-луночного планшета поочередно добавляли растворы 50 ммоль/л трис-HCl, 15 ммоль/л йодид S-бутирилтиохолина (БТХ), 3 ммоль/л 5,5'-дитиобис (2-нитробензойная кислоты (ДТНБ) в объеме 120, 25 и 30 мкл соответственно. Затем к содержимому лунки добавляли 25 мкл заранее разведенного раствора БХЭ,. Оптическую плотность измеряли при 405 нм с интервалом 30-60 с в течение 20 мин на спектрофотометре при 25°С. Раствор ДФФ в объеме 25 мкл вносили в реакционную смесь до внесения раствора БХЭ.
Для определения константы ингибирования предварительно определяли константу Михаэлиса (Km), зная начальные концентрации субстрата [S0] и начальные скорости ферментативных реакций V0, строили график их зависимости и вычисляли Km по значению концентрации субстрата, которому соответствует точка Vmax/2.
Начальную скорость ферментативной реакции вычисляли по наклону линейных участков, в графиках зависимости концентрации субстрата от времени.
Расчет константы ингибирования проводили с помощью формулы:

где Ki - константа ингибирования;
C0i - концентрация ингибитора;
Km - константа Михаэлиса;
Kmi - константа Михаэлиса в условиях ингибирования.
Были построены графики, характеризующие скорость ферментативной реакции БХЭ без и при добавлении ДФФ. (Фиг. 7).
Полученные графики были описаны уравнениями логарифмических функций, с помощью которых были рассчитаны значения константы Михаэлиса БХЭ, которая составила 3,0⋅10-4 моль, и константы ингибирования при добавлении ДФФ - 4,34⋅10-12 моль, в эквимолярных концентрациях, равных 0,1375⋅10-7 ммоль.
На примере взаимодействия с ДФФ БХЭ характеризуется высоким сродством к ингибиторам ацетилхолинэстеразы, что подтверждается низким значением константы ингибирования (4,34⋅10-12 моль). ДФФ в эквимолярных концентрациях при условии концентрации субстрата (БТХ) в среде до 0,1 ммоль ингибирует активность препарата БХЭ на 100%.
Пример 10. Исследование эффективности БХЭ для лечения отравлений диизопропилфторфосфатом (ДФФ).
Исследование проводили на самцах нелинейных мышей массой 35-40 г, полученных из питомника (ФГУП «ПЛЖ «Рапполово», Ленинградская обл.), которых содержали в условиях вивария, при 12-часовом цикле день/ночь. Животные получали стерильное питание и воду ad libitum. Формирование групп животных проводили по принципу аналогов, то есть отбирали особей одного пола, возраста, отличавшихся друг от друга массой тела не более чем на 10%. Каждая экспериментальная группа включала 10 животных.
Отравление ДФФ (Sigma Aldrich) моделировали путем его подкожного введения в дозе ЛД50 (3,0 мг/кг).
Препарат БХЭ вводили внутривенно в виде водного раствора через 1 мин после введения ДФФ в дозе 165 мг/кг.
Наблюдение за животными включало ежедневный клинический осмотр, оценку тяжести судорожного синдрома и регистрацию случаев гибели. Срок наблюдения составил 14 сут.
Выраженность судорожного синдрома оценивали по классификации Racine [Racine J.R. Modification of seizure activity by electrical stimulation: II. Motor seizure // Electroencephalography and Clinical Neurophysiology, 1972, 32(3):281-294]:
1 степень - непроизвольные движения рта и тризм;
2 степень - кивание головы, движение ушами, судороги в шейном отделе, тремор;
3 степень - клонус передних конечностей;
4 степень - вертикальные стойки;
5 степень - стойки и падения, отсутствие поступательного контроля, генерализованные судороги, выгибания тела.
В контрольной группе после введения ДФФ у 80% животных в течение 2,5 мин регистрировали последовательное развитие признаков отравления в виде снижения двигательной активности, замирания, тризма, тремора и судорожного синдрома. В дальнейшем у животных отмечали нарастание тяжести судорожного синдрома. Через 5-10 мин после введения ДФФ у большинства животных развивались генерализованные тонико-клоническими судороги 4-5 степени.
В группе, где после введения ДФФ выполняли лечебное введение БХЭ в дозе 165 мг/кг, отмечали увеличение лечебной активности препарата как по показателям, отражающим тяжесть судорожного синдрома, так и по количеству выживших животных, наблюдали более медленное развитие проявлений судорожного синдрома. Развитие тремора регистрировали через 5-8 мин, а развитие судорог 2 и 3 степени через 15 минут. Количество животных с судорогами 4 и 5 степени снижалось до 22% и 0%, соответственно.
Результаты оценки тяжести судорожного синдрома у животных в контрольной группе и после введения препарата БХЭ в различных дозах представлены в таблице 3.
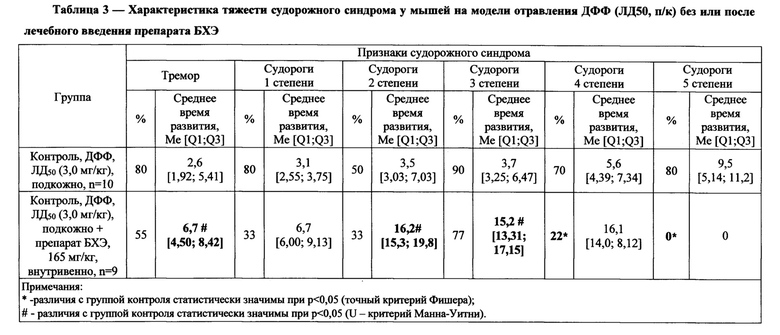
В течение первого часа наблюдения в контрольной группе регистрировали гибель 70% животных. При дальнейшем наблюдении случаев гибели животных в контрольной группе не фиксировали.
Общее количество погибших животных в группе, где после введения ДФФ выполняли лечебное введение БХЭ в дозе 165 мг/кг, через 30 мин составило 11%, через 3 ч - 22% и через 1 сут - 33%. Итоговое количество погибших животных на момент окончания срока наблюдения осталось на уровне 33%. Результаты оценки динамика гибели мышей приведены в таблице 4.
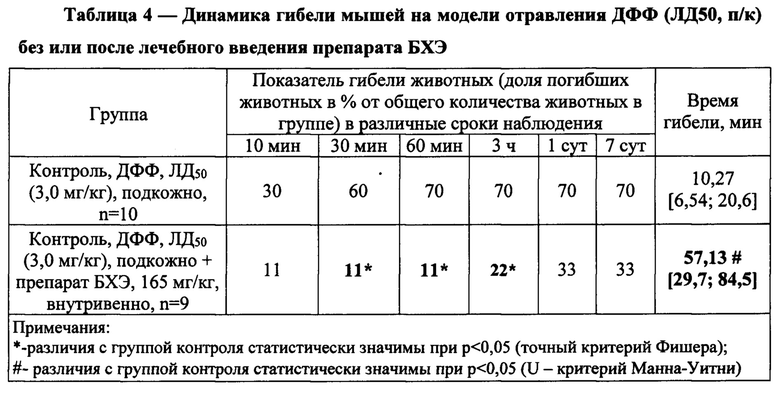
Таким образом, лечебное действие препарата БХЭ в дозе 165 мг/кг было подтверждено статически значимыми изменениями показателей, отражающих снижение тяжести судорожного синдрома, и количества погибших животных в первые 3 часа после введения ДФФ. О лечебной активности препарата в дозе 165 мг/кг также свидетельствовало статистически значимое увеличение показателя времени гибели до 57,13 мин.
Авторы и Заявитель просят рассмотреть материалы заявки на предмет выдачи патента на изобретение «Рекомбинантный слитый белок».
--->
Перечень последовательностей
<110> Аль-Шехадат Руслан Исмаилович, Максимяк Сергей Петрович
Al-Shekhadat Ruslan Ismailovich, Maksimyak Sergei Petrovich
<120> Рекомбинантный слитый белок
<130>
<160> 2
<210> 1
<211> 920
<212> белок
<213> Искусственная последовательность
<220>
<222> (1)…(920)
<223> Последовательность аминокислот рекомбинантного слитого белка, содержащего модифицированную бутирилхолинэстеразу и мальтоза-связывающий белок.
<400> 1
Met Gly Ser Ser His His His His His His Ser Ser Gly Met Lys Ile
1 5 10 15
Glu Glu Gly Lys Leu Val Ile Trp Ile Asn Gly Asp Lys Gly Tyr Asn
20 25 30
Gly Leu Ala Glu Val Gly Lys Lys Phe Glu Lys Asp Thr Gly Ile Lys
35 40 45
Val Thr Val Glu His Pro Asp Lys Leu Glu Glu Lys Phe Pro Gln Val
50 55 60
Ala Ala Thr Gly Asp Gly Pro Asp Ile Ile Phe Trp Ala His Asp Arg
65 70 75 80
Phe Gly Gly Tyr Ala Gln Ser Gly Leu Leu Ala Glu Ile Thr Pro Asp
85 90 95
Lys Ala Phe Gln Asp Lys Leu Tyr Pro Phe Thr Trp Asp Ala Val Arg
100 105 110
Tyr Asn Gly Lys Leu Ile Ala Tyr Pro Ile Ala Val Glu Ala Leu Ser
115 120 125
Leu Ile Tyr Asn Lys Asp Leu Leu Pro Asn Pro Pro Lys Thr Trp Glu
130 135 140
Glu Ile Pro Ala Leu Asp Lys Glu Leu Lys Ala Lys Gly Lys Ser Ala
145 150 155 160
Leu Met Phe Asn Leu Gln Glu Pro Tyr Phe Thr Trp Pro Leu Ile Ala
165 170 175
Ala Asp Gly Gly Tyr Ala Phe Lys Tyr Glu Asn Gly Lys Tyr Asp Ile
180 185 190
Lys Asp Val Gly Val Asp Asn Ala Gly Ala Lys Ala Gly Leu Thr Phe
195 200 205
Leu Val Asp Leu Ile Lys Asn Lys His Met Asn Ala Asp Thr Asp Tyr
210 215 220
Ser Ile Ala Glu Ala Ala Phe Asn Lys Gly Glu Thr Ala Met Thr Ile
225 230 235 240
Asn Gly Pro Trp Ala Trp Ser Asn Ile Asp Thr Ser Lys Val Asn Tyr
245 250 255
Gly Val Thr Val Leu Pro Thr Phe Lys Gly Gln Pro Ser Lys Pro Phe
260 265 270
Val Gly Val Leu Ser Ala Gly Ile Asn Ala Ala Ser Pro Asn Lys Glu
275 280 285
Leu Ala Lys Glu Phe Leu Glu Asn Tyr Leu Leu Thr Asp Glu Gly Leu
290 295 300
Glu Ala Val Asn Lys Asp Lys Pro Leu Gly Ala Val Ala Leu Lys Ser
305 310 315 320
Tyr Glu Glu Glu Leu Ala Lys Asp Pro Arg Ile Ala Ala Thr Met Glu
325 330 335
Asn Ala Gln Lys Gly Glu Ile Met Pro Asn Ile Pro Gln Met Ser Ala
340 345 350
Phe Trp Tyr Ala Val Arg Thr Ala Val Ile Asn Ala Ala Ser Gly Arg
355 360 365
Gln Thr Val Asp Glu Ala Leu Lys Asp Ala Gln Thr Asn Gly Ile Glu
370 375 380
Glu Asn Leu Tyr Phe Gln Gly Glu Asp Asp Ile Ile Ile Thr Thr Lys
385 390 395 400
Asn Gly Lys Val Arg Gly Met Asn Leu Thr Val Phe Gly Gly Thr Val
405 410 415
Thr Ala Phe Leu Gly Ile Pro Tyr Ala Gln Pro Pro Leu Gly Arg Leu
420 425 430
Arg Phe Lys Lys Pro Gln Pro Leu Thr Lys Trp Ser Gly Ile Trp Asn
435 440 445
Ala Thr Lys Tyr Ala Asn Ser Cys Met Gln Asn Ile Asp Thr Ser Phe
450 455 460
Pro Gly Phe His Gly Ser Glu Met Trp Asn Pro Asn Thr Asp Leu Ser
465 470 475 480
Glu Asp Cys Leu Tyr Leu Asn Val Trp Ile Pro Ala Pro Lys Pro Lys
485 490 495
Asn Ala Thr Val Met Val Trp Ile Tyr Gly Gly Gly Phe Gln Thr Gly
500 505 510
Thr Ser Ser Leu Pro Val Tyr Asp Gly Lys Phe Leu Ala Arg Val Glu
515 520 525
Arg Val Ile Val Val Ser Met Asn Tyr Arg Val Gly Ala Leu Gly Phe
530 535 540
Leu Ala Leu Pro Gly Asn Pro Glu Ala Pro Gly Asn Met Gly Leu Phe
545 550 555 560
Asp Gln Gln Leu Ala Leu Lys Trp Val Gln Asp Asn Ile Ala Ala Phe
565 570 575
Gly Gly Asp Pro Asn Arg Val Thr Leu Phe Gly Glu Ser Ala Gly Ala
580 585 590
Thr Arg Ala Ile Leu Gln Ser Gly Ser Ala Asn Ala Pro Trp Ala Val
610 615 620
Ala Ser Val Ser Leu His Leu Leu Ser Pro Gly Ser His Pro Leu Phe
595 600 605
Met Ser Pro Glu Glu Ala Arg Asn Arg Thr Leu Asn Leu Ala Lys Leu
625 630 635 640
Leu Gly Cys Ser Arg Glu Asn Glu Thr Glu Ile Ile Lys Cys Leu Arg
645 650 655
Asn Lys Asp Pro Gln Glu Ile Leu Asp Asn Glu Ala Phe Val Val Pro
660 665 670
Tyr Ser Thr Pro Leu Ser Val Asn Phe Gly Pro Thr Val Asp Gly Asp
675 680 685
Phe Leu Thr Asp Met Pro Asp Thr Leu Leu Glu Leu Gly Gln Phe Lys
690 695 700
Lys Thr Gln Ile Leu Val Gly Val Asn Lys Asp Glu Gly Thr Ala Phe
705 710 715 720
Leu Val Tyr Gly Ala Pro Gly Phe Ser Lys Asp Asn Asp Ser Ile Ile
725 730 735
Thr Arg Lys Glu Phe Gln Glu Gly Leu Lys Val Phe Phe Pro Asn Val
740 745 750
Ser Glu Phe Gly Lys Glu Ser Ile Leu Phe His Tyr Thr Asp Trp Glu
755 760 765
Asp Glu Asp Arg Pro Glu Asn Tyr Arg Asp Ala Leu Ala Glu Val Val
770 775 780
Gly Asp Tyr Phe Phe Ile Cys Pro Ala Leu Glu Phe Ala Lys Lys Tyr
785 790 795 800
Ala Glu His Gly Asn Asn Ala Tyr Phe Tyr Tyr Phe Glu His Arg Ser
805 810 815
Ser Lys Leu Pro Trp Pro Glu Trp Met Gly Val Met His Gly Tyr Glu
820 825 830
Ile Glu Phe Val Phe Gly Leu Pro Leu Glu Arg Arg Leu Asn Tyr Thr
835 840 845
Lys Glu Glu Glu Ile Leu Ser Arg Glu Ile Met Arg Arg Trp Ala Asn
850 855 860
Phe Ala Lys Tyr Gly Asn Pro Asn Glu Thr Gln Asn Asn Ser Thr Gln
865 870 875 880
Trp Pro Val Phe Lys Pro Thr Glu Gln Lys Tyr Leu Thr Leu Asn Thr
885 890 895
Glu Ser Ser Arg Ile Met Thr Lys Leu Arg Ala Gln His Cys Arg Phe
900 905 910
Trp Asn Ser Phe Phe Pro Lys Val
915 920
<210> 2
<211> 2760
<212> ДНК
<213> Искусственная последовательность
<220>
<222> (1)…(2760)
<223> Последовательность нуклеотидов ДНК, кодирующей рекомбинантный слитый белок, содержащий модифицированную бутирилхолинэстеразу и мальтоза-связывающий белок.
<400> 2
ATG GGC AGC AGC CAC CAC CAC CAC CAT CAT AGC AGC GGC ATG AAA ATC 48
Met Gly Ser Ser His His His His His His Ser Ser Gly Met Lys Ile
1 5 10 15
GAA GAA GGT AAA CTG GTA ATC TGG ATT AAC GGC GAT AAA GGC TAT AAC 96
Glu Glu Gly Lys Leu Val Ile Trp Ile Asn Gly Asp Lys Gly Tyr Asn
20 25 30
GGT CTC GCT GAA GTC GGT AAG AAA TTC GAG AAA GAT ACC GGA ATT AAA 144
Gly Leu Ala Glu Val Gly Lys Lys Phe Glu Lys Asp Thr Gly Ile Lys
35 40 45
GTC ACC GTT GAG CAT CCG GAT AAA CTG GAA GAG AAA TTC CCA CAG GTT 192
Val Thr Val Glu His Pro Asp Lys Leu Glu Glu Lys Phe Pro Gln Val
50 55 60
GCG GCA ACT GGC GAT GGC CCT GAC ATT ATC TTC TGG GCA CAC GAC CGC 240
Ala Ala Thr Gly Asp Gly Pro Asp Ile Ile Phe Trp Ala His Asp Arg
65 70 75 80
TTT GGT GGC TAC GCT CAA TCT GGC CTG TTG GCT GAA ATC ACC CCG GAC 288
Phe Gly Gly Tyr Ala Gln Ser Gly Leu Leu Ala Glu Ile Thr Pro Asp
85 90 95
AAA GCG TTC CAG GAC AAG CTG TAT CCG TTT ACC TGG GAT GCC GTA CGT 336
Lys Ala Phe Gln Asp Lys Leu Tyr Pro Phe Thr Trp Asp Ala Val Arg
100 105 110
TAC AAC GGC AAG CTG ATT GCT TAC CCG ATC GCT GTT GAA GCG TTA TCG 384
Tyr Asn Gly Lys Leu Ile Ala Tyr Pro Ile Ala Val Glu Ala Leu Ser
115 120 125
CTG ATT TAT AAC AAA GAT CTG CTG CCG AAC CCG CCA AAA ACC TGG GAA 432
Leu Ile Tyr Asn Lys Asp Leu Leu Pro Asn Pro Pro Lys Thr Trp Glu
130 135 140
GAG ATC CCG GCG CTG GAT AAA GAA CTG AAA GCG AAA GGT AAG AGC GCG 480
Glu Ile Pro Ala Leu Asp Lys Glu Leu Lys Ala Lys Gly Lys Ser Ala
145 150 155 160
CTG ATG TTC AAC CTG CAA GAA CCG TAC TTC ACC TGG CCG CTG ATT GCT 528
Leu Met Phe Asn Leu Gln Glu Pro Tyr Phe Thr Trp Pro Leu Ile Ala
165 170 175
GCT GAC GGG GGT TAT GCG TTC AAG TAT GAA AAC GGC AAG TAC GAC ATT 576
Ala Asp Gly Gly Tyr Ala Phe Lys Tyr Glu Asn Gly Lys Tyr Asp Ile
180 185 190
AAA GAC GTG GGC GTG GAT AAC GCT GGC GCG AAA GCG GGT CTG ACC TTC 624
Lys Asp Val Gly Val Asp Asn Ala Gly Ala Lys Ala Gly Leu Thr Phe
195 200 205
CTG GTT GAC CTG ATT AAA AAC AAA CAC ATG AAT GCA GAC ACC GAT TAC 672
Leu Val Asp Leu Ile Lys Asn Lys His Met Asn Ala Asp Thr Asp Tyr
210 215 220
TCC ATC GCA GAA GCT GCC TTT AAT AAA GGC GAA ACA GCG ATG ACC ATC 720
Ser Ile Ala Glu Ala Ala Phe Asn Lys Gly Glu Thr Ala Met Thr Ile
225 230 235 240
AAC GGC CCG TGG GCA TGG TCC AAC ATC GAC ACC AGC AAA GTG AAT TAT 768
Asn Gly Pro Trp Ala Trp Ser Asn Ile Asp Thr Ser Lys Val Asn Tyr
245 250 255
GGT GTA ACG GTA CTG CCG ACC TTC AAG GGT CAA CCA TCC AAA CCG TTC 816
Gly Val Thr Val Leu Pro Thr Phe Lys Gly Gln Pro Ser Lys Pro Phe
260 265 270
GTT GGC GTG CTG AGC GCA GGT ATT AAC GCC GCC AGT CCG AAC AAA GAG 864
Val Gly Val Leu Ser Ala Gly Ile Asn Ala Ala Ser Pro Asn Lys Glu
275 280 285
CTG GCA AAA GAG TTC CTC GAA AAC TAT CTG CTG ACT GAT GAA GGT CTG 912
Leu Ala Lys Glu Phe Leu Glu Asn Tyr Leu Leu Thr Asp Glu Gly Leu
290 295 300
GAA GCG GTT AAT AAA GAC AAA CCG CTG GGT GCC GTA GCG CTG AAG TCT 960
Glu Ala Val Asn Lys Asp Lys Pro Leu Gly Ala Val Ala Leu Lys Ser
305 310 315 320
TAC GAG GAA GAG TTG GCG AAA GAT CCA CGT ATT GCC GCC ACT ATG GAA 1008
Tyr Glu Glu Glu Leu Ala Lys Asp Pro Arg Ile Ala Ala Thr Met Glu
325 330 335
AAC GCC CAG AAA GGT GAA ATC ATG CCG AAC ATC CCG CAG ATG TCC GCT 1056
Asn Ala Gln Lys Gly Glu Ile Met Pro Asn Ile Pro Gln Met Ser Ala
340 345 350
TTC TGG TAT GCC GTG CGT ACT GCG GTG ATC AAC GCC GCC AGC GGT CGT 1104
Phe Trp Tyr Ala Val Arg Thr Ala Val Ile Asn Ala Ala Ser Gly Arg
355 360 365
CAG ACT GTC GAT GAA GCC CTG AAA GAC GCG CAG ACT AAT GGG ATC GAG 1152
Gln Thr Val Asp Glu Ala Leu Lys Asp Ala Gln Thr Asn Gly Ile Glu
370 375 380
GAA AAT CTA TAC TTC CAA GGA GAA GAT GAC ATT ATC ATC ACC ACC AAA 1200
Glu Asn Leu Tyr Phe Gln Gly Glu Asp Asp Ile Ile Ile Thr Thr Lys
385 390 395 400
AAT GGT AAA GTG CGT GGT ATG AAT CTG ACC GTG TTT GGT GGC ACC GTT 1248
Asn Gly Lys Val Arg Gly Met Asn Leu Thr Val Phe Gly Gly Thr Val
405 410 415
ACC GCA TTT CTG GGT ATT CCG TAT GCA CAG CCT CCG CTG GGT CGT CTG 1296
Thr Ala Phe Leu Gly Ile Pro Tyr Ala Gln Pro Pro Leu Gly Arg Leu
420 425 430
CGT TTC AAA AAA CCG CAG CCG CTG ACC AAA TGG TCA GGT ATT TGG AAT 1344
Arg Phe Lys Lys Pro Gln Pro Leu Thr Lys Trp Ser Gly Ile Trp Asn
435 440 445
GCA ACC AAA TAT GCC AAT AGC TGT ATG CAG AAT ATC GAT ACC AGC TTT 1392
Ala Thr Lys Tyr Ala Asn Ser Cys Met Gln Asn Ile Asp Thr Ser Phe
450 455 460
CCG GGT TTT CAT GGT AGC GAA ATG TGG AAT CCG AAT ACC GAT CTG AGC 1440
Pro Gly Phe His Gly Ser Glu Met Trp Asn Pro Asn Thr Asp Leu Ser
465 470 475 480
GAA GAT TGT CTG TAT CTG AAT GTT TGG ATT CCG GCA CCG AAA CCG AAA 1488
Glu Asp Cys Leu Tyr Leu Asn Val Trp Ile Pro Ala Pro Lys Pro Lys
485 490 495
AAT GCA ACC GTT ATG GTT TGG ATT TAT GGT GGT GGT TTT CAG ACC GGC 1536
Asn Ala Thr Val Met Val Trp Ile Tyr Gly Gly Gly Phe Gln Thr Gly
500 505 510
ACC AGC AGC CTG CCG GTT TAT GAT GGT AAA TTT CTG GCA CGT GTT GAA 1584
Thr Ser Ser Leu Pro Val Tyr Asp Gly Lys Phe Leu Ala Arg Val Glu
515 520 525
CGT GTT ATT GTG GTG AGC ATG AAT TAT CGT GTT GGT GCA CTG GGT TTT 1632
Arg Val Ile Val Val Ser Met Asn Tyr Arg Val Gly Ala Leu Gly Phe
530 535 540
CTG GCC CTG CCT GGT AAT CCG GAA GCA CCG GGT AAT ATG GGT CTG TTT 1680
Leu Ala Leu Pro Gly Asn Pro Glu Ala Pro Gly Asn Met Gly Leu Phe
545 550 555 560
GAT CAG CAG CTG GCA CTG AAA TGG GTT CAA GAT AAC ATT GCA GCA TTT 1728
Asp Gln Gln Leu Ala Leu Lys Trp Val Gln Asp Asn Ile Ala Ala Phe
565 570 575
GGT GGC GAT CCG AAT CGT GTT ACC CTG TTT GGT GAA AGT GCC GGT GCA 1776
Gly Gly Asp Pro Asn Arg Val Thr Leu Phe Gly Glu Ser Ala Gly Ala
580 585 590
GCA AGC GTT AGC CTG CAT CTG CTG AGT CCG GGT AGC CAT CCG CTG TTT 1824
Ala Ser Val Ser Leu His Leu Leu Ser Pro Gly Ser His Pro Leu Phe
595 600 605
ACC CGT GCA ATT CTG CAG AGC GGT AGC GCA AAT GCA CCG TGG GCA GTT 1872
Thr Arg Ala Ile Leu Gln Ser Gly Ser Ala Asn Ala Pro Trp Ala Val
610 615 620
ATG AGT CCG GAA GAA GCA CGT AAT CGT ACC CTG AAT CTG GCA AAA CTG 1920
Met Ser Pro Glu Glu Ala Arg Asn Arg Thr Leu Asn Leu Ala Lys Leu
625 630 635 640
CTG GGT TGT AGC CGT GAA AAT GAA ACC GAG ATT ATC AAA TGC CTG CGC 1968
Leu Gly Cys Ser Arg Glu Asn Glu Thr Glu Ile Ile Lys Cys Leu Arg
645 650 655
AAT AAA GAT CCG CAA GAA ATT CTG GAT AAT GAA GCC TTT GTT GTG CCG 2016
Asn Lys Asp Pro Gln Glu Ile Leu Asp Asn Glu Ala Phe Val Val Pro
660 665 670
TAT AGC ACA CCG CTG AGC GTT AAT TTT GGT CCG ACC GTT GAT GGT GAT 2064
Tyr Ser Thr Pro Leu Ser Val Asn Phe Gly Pro Thr Val Asp Gly Asp
675 680 685
TTT CTG ACC GAT ATG CCG GAT ACA CTG CTG GAA CTG GGT CAG TTC AAA 2112
Phe Leu Thr Asp Met Pro Asp Thr Leu Leu Glu Leu Gly Gln Phe Lys
690 695 700
AAA ACC CAG ATT CTG GTT GGC GTG AAT AAA GAT GAA GGC ACC GCC TTT 2160
Lys Thr Gln Ile Leu Val Gly Val Asn Lys Asp Glu Gly Thr Ala Phe
705 710 715 720
CTG GTT TAT GGC GCA CCG GGT TTT AGC AAA GAT AAC GAT AGC ATT ATT 2208
Leu Val Tyr Gly Ala Pro Gly Phe Ser Lys Asp Asn Asp Ser Ile Ile
725 730 735
ACC CGC AAA GAA TTT CAA GAG GGC CTG AAA GTT TTT TTT CCG AAC GTT 2256
Thr Arg Lys Glu Phe Gln Glu Gly Leu Lys Val Phe Phe Pro Asn Val
740 745 750
AGC GAA TTT GGC AAA GAA AGC ATC CTG TTT CAT TAT ACC GAT TGG GAA 2304
Ser Glu Phe Gly Lys Glu Ser Ile Leu Phe His Tyr Thr Asp Trp Glu
755 760 765
GAT GAA GAT CGT CCG GAA AAC TAT CGT GAT GCA CTG GCC GAA GTT GTT 2352
Asp Glu Asp Arg Pro Glu Asn Tyr Arg Asp Ala Leu Ala Glu Val Val
770 775 780
GGT GAT TAT TTC TTT ATT TGT CCG GCA CTG GAA TTT GCC AAA AAA TAC 2400
Gly Asp Tyr Phe Phe Ile Cys Pro Ala Leu Glu Phe Ala Lys Lys Tyr
785 790 795 800
GCA GAA CAT GGC AAC AAC GCC TAC TTC TAT TAT TTC GAA CAT CGT AGC 2448
Ala Glu His Gly Asn Asn Ala Tyr Phe Tyr Tyr Phe Glu His Arg Ser
805 810 815
AGC AAA CTG CCG TGG CCT GAA TGG ATG GGT GTT ATG CAT GGT TAT GAA 2496
Ser Lys Leu Pro Trp Pro Glu Trp Met Gly Val Met His Gly Tyr Glu
820 825 830
ATC GAA TTT GTT TTT GGT CTG CCG CTG GAA CGT CGT CTG AAT TAT ACC 2544
Ile Glu Phe Val Phe Gly Leu Pro Leu Glu Arg Arg Leu Asn Tyr Thr
835 840 845
AAA GAA GAA GAA ATC CTG AGT CGC GAA ATT ATG CGT CGT TGG GCA AAT 2592
Lys Glu Glu Glu Ile Leu Ser Arg Glu Ile Met Arg Arg Trp Ala Asn
850 855 860
TTT GCG AAA TAT GGT AAC CCG AAT GAA ACC CAG AAT AAT AGC ACC CAG 2640
Phe Ala Lys Tyr Gly Asn Pro Asn Glu Thr Gln Asn Asn Ser Thr Gln
865 870 875 880
TGG CCT GTT TTT AAA CCG ACC GAA CAG AAA TAT CTG ACC CTG AAT ACC 2688
Trp Pro Val Phe Lys Pro Thr Glu Gln Lys Tyr Leu Thr Leu Asn Thr
885 890 895
GAA AGC AGC CGT ATT ATG ACC AAA CTG CGT GCA CAG CAT TGT CGT TTT 2736
Glu Ser Ser Arg Ile Met Thr Lys Leu Arg Ala Gln His Cys Arg Phe
900 905 910
TGG AAT AGC TTT TTC CCG AAG GTG TAA 2763
Trp Asn Ser Phe Phe Pro Lys Val
915 920
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Последовательность нуклеотидов, кодирующая β-N-ацетилгексозаминидазу Aggregatibacter actinomycetemcomitans, и генетические конструкции, её содержащие | 2021 |
|
RU2789544C1 |
| Вакцина против герпеса | 2019 |
|
RU2731073C1 |
| Антитела против белка р17 ВИЧ-1 субтипа А | 2019 |
|
RU2727673C1 |
| СПОСОБ УВЕЛИЧЕНИЯ ФОТОСИНТЕТИЧЕСКОЙ ФИКСАЦИИ УГЛЕРОДА С ИСПОЛЬЗОВАНИЕМ БЕЛКА СЛИЯНИЯ ИЗ МНОГИХ СУБЪЕДИНИЦ ГЛИКОЛАТДЕГИДРОГЕНАЗЫ | 2011 |
|
RU2651501C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ БИОЛОГИЧЕСКОГО ПОЛУЧЕНИЯ ЛАКТАТА ИЗ С1-СОЕДИНЕНИЙ С ПРИМЕНЕНИЕМ ТРАНСФОРМАНТОВ ЛАКТАТ ДЕГИДРОГЕНАЗЫ | 2014 |
|
RU2710714C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРЕДОТВРАЩЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2016 |
|
RU2714205C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2019 |
|
RU2781542C2 |
| ШТАММ КЛЕТОК CHO-SE-9/4 - ПРОДУЦЕНТ ХИМЕРНОГО АНТИТЕЛА ПРОТИВ ЭРИТРОПОЭТИНА ЧЕЛОВЕКА И ХИМЕРНОЕ АНТИТЕЛО, ПРОДУЦИРУЕМОЕ ДАННЫМ ШТАММОМ | 2019 |
|
RU2717038C1 |
| БИОСЕНСОРНАЯ СИСТЕМА ДЛЯ БЫСТРОГО ОБНАРУЖЕНИЯ ОПРЕДЕЛЯЕМЫХ КОМПОНЕНТОВ | 2016 |
|
RU2717658C2 |
| МАТЕРИАЛЫ И МЕТОДЫ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ЛЕЧЕНИЯ РЕСПИРАТОРНЫХ ЗАБОЛЕВАНИЙ У СОБАК | 2020 |
|
RU2811752C2 |


Изобретение относится к биотехнологии, в частности к растворимому рекомбинантному слитому белку, обладающему свойством связывать ингибиторы ацетилхолинэстеразы. Представлен рекомбинантный слитый белок, содержащий полигистидиновую последовательность, последовательность мальтоза-связывающего белка (MBP) Е. coli, линкер и модифицированную последовательность БХЭ человека. Также представлена генетическая конструкция, кодирующая заявленный слитый белок, плазмидный экспрессионный вектор и штамм - продуцент слитого белка. Группа изобретений позволяет получить растворимый слитый белок с выходом 5 мг на 1 гр. влажной биомассы бактериальной культуры и с временем полувыведения из кровотока 22,4 часа. Слитый белок может быть использован в качестве антидота против различных ингибиторов холинэстераз. 4 н.п. ф-лы, 7 ил., 4 табл., 10 пр.
1. Рекомбинантный слитый белок, аминокислотная последовательность которого представлена в SEQ ID NO: 1, способный связывать ингибиторы ацетилхолинэстеразы.
2. Последовательность ДНК, кодирующая белок по п. 1, нуклеотидная последовательность которой представлена в SEQ ID NO: 2.
3. Плазмидный экспрессионный вектор, представляющий собой вектор рЕТ28а, в который по сайтам рестрикции XhoI и NcoI введена последовательность по п. 2.
4. Штамм - продуцент белка по п. 1, представляющий собой штамм Escherichia coli BL21[DE3], трансформированный вектором по п. 3.
| СПОСОБ ПОЛУЧЕНИЯ ХИМИЧЕСКИ ПОЛИСИАЛИРОВАННОЙ РЕКОМБИНАНТНОЙ БУТИРИЛХОЛИНЭСТЕРАЗЫ ЧЕЛОВЕКА | 2012 |
|
RU2645458C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pFUSE-MARX-29-PRAD-F2A/BChE-14, СОДЕРЖАЩАЯ ГЕН МОДИФИЦИРОВАННОЙ БУТИРИЛХОЛИНЭСТЕРАЗЫ ЧЕЛОВЕКА, ПРЕДНАЗНАЧЕННАЯ ДЛЯ ЭКСПРЕССИИ ГЕНА БУТИРИЛХОЛИНЭСТЕРАЗЫ В КЛЕТКАХ МЛЕКОПИТАЮЩИХ ДЛЯ ТЕРАПИИ ОТРАВЛЕНИЙ ФОСФОРОРГАНИЧЕСКИМИ ТОКСИНАМИ | 2016 |
|
RU2688729C1 |
Авторы
Даты
2020-09-22—Публикация
2019-12-26—Подача