ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение раскрывает полинуклеотидные последовательности нового варианта никотин-N-деметилазы (NND3) растений рода Nicotiana и их варианты, гомологи и фрагменты. Также раскрыты полипептидные последовательности и их варианты, гомологи и фрагменты. Также раскрыта модификация экспрессии этого гена или активности белка, кодируемого этим геном, для модулирования уровней одного или более специфичных для табака нитрозаминов (TSNA) в клетке растения или в растении.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Специфичные для табака нитрозамины (TSNA) образуются главным образом во время сушки и переработки табачных листьев. Сушка табака представляет собой процесс физических и биохимических изменений, которые определяют аромат и вкус каждой разновидности табака. Считается, что количество TSNA в сушеном табачном листе зависит от накопления нитритов, которые накапливаются при гибели растительной клетки и образуются во время сушки при восстановлении нитратов в близких к анаэробным (дефицит кислорода) условиях окружающей среды. Восстановление нитратов до нитритов, как полагают, происходит под действием бактерий на поверхности листа в анаэробных условиях, и это восстановление особенно выражено при определенных условиях. После того, как образуются нитриты, эти соединения, как полагают, соединяются с различными алкалоидами табака, в том числе пиридин-содержащими соединениями, с образованием нитрозаминов.
Четыре основных TSNA, то есть те, которые, как правило, обнаруживаются в самых высоких концентрациях, представляют собой N-нитрозоникотин (NNN), 4-(метилнитрозамино)-1-(3-пиридил)-1-бутанон (NNK), N-нитрозоанабазин (NAB) и N-нитрозоанатабин (NAT). Второстепенные соединения, то есть те, которые, как правило, обнаруживаются в значительно более низких уровнях, чем основные TSNA, включают в себя 4-(метилнитрозамино)-4-(3-пиридил)бутаналь (NNA), 4-(метилнитрозамино)-1-(3-пиридил)-1-бутанол (NNAL), 4-(метилнитрозамино)-4-(3-пиридил)-1-бутанол (изо-NNAL) и 4-(метилнитрозамино)-4-(3-пиридил)-1-масляную кислоту (изо-NNAC). Сообщалось, что по меньшей мере NNN и NNK являются канцерогенными при использовании на животных в лабораторных исследованиях.
Основной биохимический механизм образования NNN представляет собой N-нитрозирование норникотина, алкалоида, продуцируемого посредством N-деметилирования никотина с помощью фермента никотин-N-деметилазы. Несмотря на то, что норникотин, как правило, представляет <5% от общего содержания алкалоидов в культивируемом табаке, уровни норникотина могут существенно повышаться посредством механизма, называемого «превращением», при котором растения, накапливающие никотин в качестве их основного алкалоида, дают начало потомству, которое метаболизирует большую часть (до 95%) никотина листа в норникотин. В объектах, которые были генетически трансформированы (называемые «трансформантами»), N-деметилирование никотина в норникотин происходит главным образом в ходе старения и сушки. Поддержание низких уровней норникотина является желательным в связи с его хорошо изученной ролью в качестве предшественника NNN, а также в связи с тем, что норникотин сам по себе может отвечать за нежелательные воздействия на здоровье. В публикации Dickerson and Janda (2002) Proc. Natl. Acad. Sci. USA 99, 15084-15088 продемонстрировано, что норникотин может индуцировать аномальное гликирование белков, а также показано, что в плазме крови курильщиков увеличивается накопление модифицированных белков. Кроме того, в этом же обзоре представлены данные о том, что норникотин может взаимодействовать, с образованием ковалентной связи, с широко используемыми стероидными лекарственными средствами, такими как преднизон, потенциально изменяя как эффективность, так и токсичность этих лекарственных средств. В WO 98/58555 описывается обработка табачных листьев перед дымовой сушкой или в ходе нее с помощью микроволновой обработки для снижения количества TSNA. В патенте США №5810020 описывается способ удаления TSNA из табака путем приведения табачного материала в контакт с улавливающим поглотителем, где улавливающий поглотитель содержит выбранный комплекс переходного металла, который легко нитрозируется с образованием нитрозильного комплекса с небольшим кинетическим или термодинамическим барьером. В патенте США №6202649 описывается способ существенного предотвращения образования TSNA путем, среди прочего, сушки табака в контролируемой среде, имеющей достаточный воздушный поток, чтобы существенно предотвратить анаэробные условия в непосредственной близости от табачного листа. Контролируемую среду обеспечивают путем управления одним или несколькими параметрами сушки, такими как воздушный поток, влажность и температура. Однако способы, подобные этим, могут добавить значительную стоимость и время к производству табака и, следовательно, с меньшей вероятностью будут приняты в табачной промышленности. Таким образом, остается потребность в эффективном и относительно недорогом способе снижения количества TSNA.
Молекулярные способы снижения уровней TSNA в растениях весьма желательны, поскольку они не требуют дорогих и зачастую сложных способов для достижения сниженных уровней TSNA. Один из таких молекулярных подходов раскрыт в WO 2011/088180. В WO 2011/088180 раскрыты композиции и способы ингибирования экспрессии или функции полипептидов специфической для корня никотин-деметилазы (CYP82E10), принимающей участие в метаболическом превращении никотина в норникотин в корнях растений табака. Никотин-деметилаза относится к семейству цитохром Р450-зависимых монооксигеназ (CYP). Были описаны другие гены никотин-деметилазы, в том числе CYP82E4 и CYP82E5, которые принимают участие в превращении никотина в норникотин, и они описаны в WO 2006091194, WO 2008070274 и WO 2009064771. Нокаут CYP82E4, CYP82E5 и CYP82E10 способен снижать превращение никотина в норникотин с 3,2% до 1,1% в табаке Burley (см. WO 2011088180 А1).
Существует постоянная потребность в данной области в дополнительном снижении уровней норникотина в растениях табака для дополнительного снижения уровней метаболитов норникотина (например, TSNA - таких как NNN), которые образуются в ходе сушки. Настоящее изобретение направлено на удовлетворение этой потребности.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения идентифицировали еще один ген, относящийся к семейству никотин-N-деметилаз (NND) Nicotiana tabacum, который в данном документе называется NND3. Хотя полипептидная последовательность NND3 демонстрирует 94% идентичность последовательности с известной полипептидной последовательностью CYP82E4 и 91% идентичность последовательности с известной полипептидной последовательностью CYP82E5 и CYP82E10, профиль экспрессии NND3y N. tabacum на удивление отличается при сравнении с CYP82E4, CYP82E5 и CYP82E10. Как показано на фигуре 1, хотя каждый CYP82E4, CYP82E5, CYP82E10 и NND3 демонстрируют экспрессию в цветах и корнях, NND3 не экспрессируется на выявляемых уровнях в листьях, тогда как CYP82E4 характеризуется экспрессией исключительно в стареющих листьях, а CYP82E5 и CYP82E10 демонстрируют экспрессию во всех исследуемых типах листьев. Полинуклеотид, кодирующий последовательность NND3, кодирует функциональную никотин-N-деметилазу. Указанный ген изложен под SEQ ID NO: 1, и полинуклеотид, кодирующий последовательность, изложен под SEQ ID NO: 2. Полипептидная последовательность изложена под SEQ ID NO: 3. За счет снижения уровня экспрессии этого гена в растениях табака может наблюдаться сниженное превращение никотина в норникотин. Это может приводить в результате к снижению уровней норникотина и метаболитов норникотина, таких как NNN, которые образуются в ходе сушки. Это может приводить в результате к снижению уровней NNN в дыме от сушеного табачного материала. Настоящее изобретение, таким образом, является пригодным для модулирования (например, снижения) уровней норникотина и/или уровней TSNA в растениях, например, по меньшей мере NNN. В частности, настоящее изобретение может быть особенно применимым в комбинации с другими способами, с помощью которых можно снизить уровни норникотина и/или TSNA, таких как NNN. Таким образом, в некоторых вариантах осуществления может быть желательно снизить уровень экспрессии NND3, а также одного или более других генов никотин-деметилазы в растении табака. Ожидается, что такая комбинация будет дополнительно снижать превращение никотина в норникотин, что дополнительно будет снижать уровни метаболитов, образующихся в табаке в ходе сушки и при курении сушеного материала. Табачные изделия, полученные из растений табака, описанных в данном документе, могут найти применение в способах для снижения канцерогенного потенциала табачных изделий и снижения воздействия на человека канцерогенных нитрозаминов. Рассматривается одна или более мутаций в гене, кодирующем NND3, где мутации приводят к сниженной экспрессии или функции NND3. Растения табака дополнительно могут содержать одну или более мутаций в гене, кодирующем никотин-деметилазу CYP82E4, и/или одну или более мутаций в гене, кодирующем никотин-деметилазу CYP82E5, и/или одну или более мутаций в гене, кодирующем никотин-деметилазу CYP82E4, где мутации в этих генах приводят в результате к сниженной экспрессии или функции никотин-деметилазы CYP82E4, и/или CYP82E5, и/или CYP82E10.
АСПЕКТЫ И ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Аспекты и варианты осуществления настоящего изобретения изложены в прилагаемой формуле изобретения.
В первом аспекте описана мутантная, не встречающаяся в природе или трансгенная клетка растения табака, содержащая: (i) полинуклеотид, содержащий последовательность, кодирующую функциональную никотин-N-деметилазу, состоящий из нее или, по сути, состоящий из нее, и характеризующийся по меньшей мере 95% идентичностью последовательности с SEQ ID NO: 3; (ii) полипептид, кодируемый полинуклеотидом, изложенным в (i); (iii) полипептид, содержащий последовательность, кодирующую никотин-N-деметилазу, состоящий из нее или, по сути, состоящий из нее, и характеризующийся по меньшей мере 95% идентичностью последовательности с SEQ ID NO: 3; или (iv) конструкцию, вектор или вектор экспрессии, содержащий выделенный полинуклеотид, изложенный в (i), и где экспрессия или активность указанной никотин-деметилазы снижена по сравнению с контрольной клеткой растения табака, в которой экспрессия или активность указанной никотин-деметилазы не была снижена.
В одном варианте осуществления клетка растения табака характеризуется одной или более мутациями, снижающими экспрессию или активность указанной никотин-деметилазы.
В одном варианте осуществления мутантная, не встречающаяся в природе или трансгенная клетка растения табака дополнительно характеризуется одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4, где предпочтительно указанная никотин-деметилаза CYP82E4 выбрана из группы, включающей SEQ ID NO: 12-16 или комбинацию двух или более из них, где предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E4 и происходит в положении, выбранном из группы, включающей аминокислотные остатки 329, 364, 376, 382 и 458 в SEQ ID NO: 5 иликомбинацию двух или более из них, где предпочтительно указанная мутация выбрана из группы, включающей: а) замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 5; b) замену на аспарагин остатка лизина в положении 364 SEQ ID NO: 5; с) замену на метионин остатка валина в положении 376 SEQ ID NO: 5; d) замену на серии остатка пролина в положении 382 SEQ ID NO: 5; d) замену на серии остатка пролина в положении 458 SEQ ID NO: 5 и е) любую комбинацию двух или более из них.
В одном варианте осуществления мутантная, не встречающаяся в природе или трансгенная клетка растения табака дополнительно характеризуется одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5, где предпочтительно указанная никотин-деметилаза CYP82E5 выбрана из SEQ ID NO: 24 или 25 или их комбинации, где предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E5 и происходит по аминокислотным остаткам 422 или 449 в SEQ ID NO: 17 или их комбинации, где предпочтительно указанная мутация выбрана из группы, включающей: а) замену на стоп-кодон остатка триптофана в положении 422 SEQ ID NO: 17; b) замену на лейцин остатка пролина в положении 449 SEQ ID NO: 17 и с) их комбинацию.
В одном варианте осуществления мутантная, не встречающаяся в природе или трансгенная клетка растения табака дополнительно характеризуется одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10, где предпочтительно указанная никотин-деметилаза CYP82E10 выбрана из группы, включающей SEQ ID NO: 32-35 или комбинацию двух или более из них, где предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E10 и происходит в положении, выбранном из группы, включающей аминокислотные остатки 79, 107, 382, 419 в SEQ ID NO: 26 или комбинацию двух или более из них, где предпочтительно указанная мутация выбрана из группы, включающей: а) замену на серии остатка глицина в положении 79 SEQ ID NO: 26; b) замену на серии остатка пролина в положении 107 SEQ ID NO: 26; с) замену на серии остатка пролина в положении 382 SEQ ID NO: 26; d) замену на серии остатка пролина в положении 419 SEQ ID NO: 26и е) любую их комбинацию.
В одном варианте осуществления мутантная, не встречающаяся в природе или трансгенная клетка растения табака дополнительно характеризуется: (i) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4, где предпочтительно указанная никотин-деметилаза CYP82E4 выбрана из группы, включающей SEQ ID NO: 12-16 или комбинацию двух или более из них, где предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E4 и происходит в положении, выбранном из группы, включающей аминокислотные остатки 329, 364, 376, 382 и 458 в SEQ ID NO: 5 или комбинацию двух или более из них, где предпочтительно указанная мутация выбрана из группы, включающей: а) замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 5; b) замену на аспарагин остатка лизина в положении 364 SEQ ID NO: 5; с) замену на метионин остатка валина в положении 376 SEQ ID NO: 5; d) замену на серии остатка пролина в положении 382 SEQ ID NO: 5; d) замену на серии остатка пролина в положении 458 SEQ ID NO: 5 и е) любую комбинацию двух или более из них; и (ii) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5, где предпочтительно указанная никотин-деметилаза CYP82E5 выбрана из SEQ ID NO: 24 или 25 или их комбинации, где предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E5 и происходит по аминокислотным остаткам 422 или 449 в SEQ ID NO: 17 или их комбинации, где предпочтительно указанная мутация выбрана из группы, включающей: а) замену на стоп-кодон остатка триптофана в положении 422 SEQ ID NO: 17; b) замену на лейцин остатка пролина в положении 449 SEQ ID NO: 17 и с) их комбинацию; и (iii) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10, где предпочтительно указанная никотин-деметилаза CYP82E10 выбрана из группы, включающей SEQ ID NO: 32-35 или комбинацию двух или более из них, где предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E10 и происходит в положении, выбранном из группы, включающей аминокислотные остатки 79, 107, 382, 419 в SEQ ID NO: 26 или комбинацию двух или более из них, где предпочтительно указанная мутация выбрана из группы, включающей: а) замену на серии остатка глицина в положении 79 SEQ ID NO: 26; b) замену на серии остатка пролина в положении 107 SEQ ID NO: 26; с) замену на серии остатка пролина в положении 382 SEQ ID NO: 26; d) замену на серии остатка пролина в положении 419 SEQ ID NO: 26и е) любую их комбинацию.
В одном варианте осуществления мутантная, не встречающаяся в природе или трансгенная клетка растения табака дополнительно характеризуется (i) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E4, одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E5, и одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E10, где указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop), указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop), и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 33 (G79S); или(п) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E4, одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E5, и одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E10, где указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop), указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop), и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 34 (P107S); или (iii) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E4, одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E5, и одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E10, где указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop), указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop), и указанные никотин-деметилазы CYP82E10 содержат последовательность, изложенную под SEQ ID NO: 35 (P382S); или (iv) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E4, одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E5, и одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E10, где указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop), указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop), и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 32 (P419S).
В одном варианте осуществления указанная(указанные) мутация(указанные) представляет(представляют) собой мутацию в гомозиготной форме.
В одном варианте осуществления указанная клетка растения или растение, содержащее указанную растительную клетку, характеризуется превращением никотина в норникотин, составляющим менее приблизительно 1,0%, менее приблизительно 0,9%, менее приблизительно 0,8%, менее приблизительно 0,7%, менее приблизительно 0,6%, менее приблизительно 0,5%, менее приблизительно 0,4%, менее приблизительно 0,3%, менее приблизительно 0,2% или менее приблизительно 0,1%. % превращения рассчитывают с помощью уравнения [%норникотина/(%норникотина + %никотина)]×100.
В одном варианте осуществления указанная клетка растенияили растение, содержащее указанную растительную клетку, содержит менее приблизительно 0,04%, менее приблизительно 0,03%, менее приблизительно 0,02% или менее приблизительно 0,01% норникотина из расчета на сухой вес.
В дополнительном аспекте описано мутантное, не встречающееся в природе или трансгенное растение, содержащее растительную клетку, описанную в данном документе.
В дополнительном аспекте описан растительный материал, включающий биомассу, семя, стебли или листья растений, описанных в данном документе. Предпочтительно NND3 экспрессируется в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и корнях растительного материала. Предпочтительно NND3 экспрессируется исключительно или главным образом в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и корнях растительного материала.
В дополнительном аспекте описано табачное изделие, содержащее клетку растения, растение или растительный материал, описанные в данном документе.
В дополнительном аспекте описан способ получения растения табака со сниженными уровнями норникотина и/или NNN, причем указанный способ предусматривает стадии: (а) обеспечения растения, содержащего (i) полинуклеотид, содержащий последовательность, кодирующую (функциональную) никотин-N-деметилазу, состоящий из нее или, по сути, состоящий из нее, и характеризующийся по меньшей мере 95% идентичностью последовательности с SEQ ID NO: 2; (b) введения одной или более мутаций в указанный полинуклеотид указанного растения табака с целью создания мутантного растения табака; (с) необязательно сушки растительного материала табака и (d) измерения уровня норникотина и/или NNN в мутантном растении табака, где уменьшение уровня норникотина и/или NNN в мутантном растении табака по сравнению с контрольным растением табака свидетельствует о том, что уровни норникотина и/или NNN в указанном мутантном растении были снижены. Также рассматривается использование фрагментов последовательностей, описанных в данном документе. Например, фрагменты можно использовать в качестве конструкций для РНК-интерфенции с целью модулирования экспрессии.
В одном варианте осуществления растение табака из стадии (b) представляет собой мутантное растение табака, где предпочтительно указанное мутантное растение табака характеризуется одной или более мутациями в одном или более дополнительных генах никотин-N-деметилазы.
В одном варианте осуществления указанное мутантное растение табака характеризуется одной или более дополнительными мутациями в генах, состоящих из группы CYP82E4, CYP82E5 или CYP82E10 или комбинации двух или более из них.
В одном варианте осуществления растение табака из стадии (b) представляет собой мутантное растение табака, которое характеризуется сниженными уровнями норникотина по сравнению с контрольным растением табака.
В одном варианте осуществления указанное растение табака имеет одну или более мутаций в CYP82E4, CYP82E5 или CYP82E10 или комбинации двух или более из них.
В дополнительном аспекте описан способ идентификации одной или более мутаций растения табака, коррелирующих с низкими уровнями норникотина и/или NNN, где указанный способ предусматривает стадии: (а) идентификации растения табака с низкими уровнями норникотина и/или NNN по сравнению с контрольным растением табака; (b) получения образца нуклеиновой кислоты из растения табака, идентифицированного на стадии (а); (с) осуществления скрининга образца нуклеиновой кислоты из стадии (b) в отношении наличия одной или более мутаций в последовательности под SEQ ID NO: 2, отсутствующих у контрольного растения; (d) необязательного сравнения одной или более мутаций, идентифицированных на стадии (с), с известными мутациями, которые обуславливают снижение уровней норникотина и/или NNN в растении табака; и (е) идентификации таких одной или более мутаций, коррелирующих с низкими уровнями норникотина и/или NNN.
В дополнительном аспекте описан способ получения сушеного растительного материала, предпочтительно сушеных листьев, со сниженными в них уровнями норникотина и/или по меньшей мере NNN, предусматривающий стадии: (а) обеспечения по меньшей мере части растения или растительного материала, описанного в данном документе; (b) необязательно сбора растительного материала из него; и (с) сушки растительного материала в течение периода времени, достаточного для уменьшения в нем уровней норникотина и/или по меньшей мере NNN.
В дополнительном аспекте описано растение табака, характеризующееся одной или более мутациями в гене, кодирующем никотин-деметилазу NND3, одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E10, одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E4, и одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E5, где необязательно указанная никотин-деметилаза CYP82E10 характеризуется мутацией в положении 382 SEQ ID NO: SEQ ID NO: 26, указанная никотин-деметилаза CYP82E4 характеризуется мутацией в положении 329 SEQ ID NO: 5 и указанная никотин-деметилаза CYP82E5 характеризуется мутацией в положении 422 SEQ ID NO: 17, где предпочтительно каждая из указанных мутаций представляет собой мутацию в гомозиготной форме.
В дополнительном аспекте описано растение табака, характеризующееся одной или более мутациями в гене NND3, обуславливающих ингибирование активности никотин-деметилазы в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и в корнях, одной или более мутациями в гене CYP82E10, обуславливающих ингибирование активности никотин-деметилазы в корнях и/или листья, одной или более мутациями в гене CYP82E4v2, обуславливающих ингибирование активности никотин-деметилазы в стареющих листьях, и одной или более мутациями в гене CYP83E5v2, обуславливающих ингибирование активности никотин-деметилазы в корнях и/или листья.
В дополнительном аспекте описана выделенная полинуклеотидная последовательность, содержащая последовательность, кодирующую никотин-N-деметилазу NND3, состоящая из нее или, по сути, состоящая из нее, и имеющая последовательностью под SEQ ID NO: 2 или по меньшей мере 95% идентичность последовательности с SEQ ID NO: 2, где предпочтительно указанный выделенный полинуклеотид представляет собой синтетический полинуклеотид или кДНК.
В дополнительном аспекте описан выделенный полипептид, кодируемый полинуклеотидом, описанным в данном документе.
В дополнительном аспекте описан выделенный полипептид, содержащий последовательность, кодирующую никотин-N-деметилазу NND3, состоящий из нее или, по сути, состоящий из нее, и имеющий последовательность SEQ ID NO: 3 или по меньшей мере 95% идентичность последовательности с SEQ ID NO: 3, где предпочтительно указанный выделенный полипептид представляет собой синтетический полипептид. Также рассматриваются фрагменты полипептида, что описано в данном документе.
В дополнительном аспекте описана конструкция, вектор или вектор экспрессии, содержащий выделенный полинуклеотид, описанный в данном документе.
В дополнительном аспекте описана мутация в гене, кодирующем никотин-деметилазу NND3, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы NND3.
В дополнительном аспекте описан способ снижения уровня норникотина, или снижения скорости превращения никотина в норникотин, или снижения уровня по меньшей мере NNN в клетке растения табака, предусматривающий стадии: (а) снижения экспрессии или активности: (i) полинуклеотида, содержащего последовательность, кодирующую функциональную никотин-N-деметилазу, состоящего из нее или, по сути, состоящего из нее, и характеризующегося по меньшей мере 95% идентичностью последовательности с SEQ ID NO: 2; (ii) полипептида, кодируемого полинуклеотидом, изложенным в (i); (iii) полипептида, содержащего последовательность, кодирующую никотин-N-деметилазу, состоящего из нее или, по сути, состоящего из нее, и характеризующегося по меньшей мере 95% идентичностью последовательности с SEQ ID NO: 3; (b) измерения содержания по меньшей мере норникотина и/или NNN в растительной клетке, полученной на стадии (а); и (с) идентификации клетки растения, в которой содержание по меньшей мере норникотина и/или NNN изменено по сравнению с контрольным растением, в которой экспрессия или активность полинуклеотида или полипептида, изложенных в (а), не была подвергнута модулированию.
В дополнительном аспекте представлен способ снижения канцерогенного потенциала табачного изделия, где указанный способ предусматривает получение указанного табачного изделия из растения табака или его потомства, как описано в данном документе.
В дополнительном аспекте представлен способ уменьшения уровня норникотина, или снижения скорости превращения никотина в норникотин, или снижения уровня по меньшей мере NNN в растении табака, где указанный способ предусматривает введение в геном указанного растения одной или более мутаций в пределах по меньшей мере одного аллеля гена никотин-деметилазы NND3, где указанная мутация обуславливает снижение уровня экспрессии указанного гена никотин-деметилазы.
В одном варианте осуществления NND3 экспрессируется в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и в корнях.
В одном варианте осуществления NND3 экспрессируется исключительно или главным образом в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и в корнях.
Каждый из вариантов осуществления, рассматриваемых выше, раскрыт в виде вариантов осуществления каждого из аспектов настоящего изобретения. Также рассматриваются комбинации одного или более вариантов осуществления.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На фигуре 1 показаны относительные уровни экспрессии NND3 и родственных генов функциональной CYP82E в разных тканях растений. Столбцы показывают среднее ± SD трех биологических повторов, взятых из трех выращенных в теплице зрелых растений N. tabacum сорта TN90.
На фигуре 2 показаны относительные уровни экспрессии NND3 (А) и уровни превращения никотина в норникотин (В), измеряемые в листьях отдельных зрелых растений То, трансформированных последовательностью, кодирующей NND3, под контролем сильного конститутивного промотора в TN90 сур82е4/сур82е5/сур82е10 со сверхнизким уровнем превращения в качестве фона.
На фигуре 3 показаны относительные уровни экспрессии NND3 и родственных генов функциональной CYP82E в листьях N. tabacum сорта Stella в разные моменты времени сушки. Образцы отбирали из пулов нескольких листьев. Два пула анализировали в виде биологических повторов, (а) повтора 1 и (b) повтора 2. Столбцы показывают среднее ± SD трех технических повторов.
ОПРЕДЕЛЕНИЯ
Техническим терминам и выражениям, используемым в пределах объема данной заявки, следует придавать значение, которое обычно применяется к ним в данной области биологии растений и молекулярной биологии. Все нижеследующие определения терминов применяют ко всему содержанию данной заявки. Слово «содержащий» не исключает другие элементы или стадии, а формы единственного числа не исключают множественное. Одна стадия может выполнять функции нескольких признаков, изложенных в формуле изобретения. Термины «приблизительно», «главным образом» и «примерно» в контексте данного цифрового значения или диапазона относятся к значению или диапазону, который находится в пределах 20%, в пределах 10%, или в пределах 5%, 4%, 3%, 2% или 1% от заданного значения или диапазона.
Термин «выделенный» относится к любому объекту, который взят из его естественной среды, но этот термин не подразумевает какой-либо степени очистки.
«Вектор экспрессии» представляет собой средство доставки нуклеиновой кислоты, которое содержит комбинацию компонентов нуклеиновой кислоты для обеспечения экспрессии нуклеиновой кислоты. Подходящие векторы экспрессии включают в себя эписомы, способные к внехромосомной репликации, такие как кольцевые плазмиды из двухнитевой нуклеиновой кислоты; линеаризованные плазмиды из двухнитевой нуклеиновой кислоты и другие функционально эквивалентные векторы экспрессии любого происхождения. Вектор экспрессии содержит по меньшей мере промотор, расположенный выше по цепи и функционально связанный с нуклеиновой кислотой, конструкции нуклеиновых кислот или конъюгат нуклеиновых кислот, как определено ниже.
Термин «конструкция» относится к двухнитевому фрагменту рекомбинантной нуклеиновой кислоты, содержащему один или несколько полинуклеотидов. Конструкция содержит «матричную цепь», основания которой спарены с комплементарной «смысловой или кодирующей цепью». Данная конструкция может быть встроена в вектор в двух возможных ориентациях, либо в той же (или смысловой) ориентации, или в обратной (или антисмысловой) ориентации по отношению к ориентации промотора, расположенного в векторе, таком как вектор экспрессии.
«Вектор» относится к средству доставки нуклеиновой кислоты, которое содержит комбинацию компонентов нуклеиновой кислоты для обеспечения переноса нуклеиновой кислоты, конструкций нуклеиновых кислот и конъюгатов нуклеиновых кислот и тому подобного. Подходящие векторы включают в себя эписомы, способные к внехромосомной репликации, такие как кольцевые плазмиды из двухнитевой нуклеиновой кислоты; линеаризованные плазмиды из двухнитевой нуклеиновой кислоты и другие векторы любого происхождения.
«Промотор» относится к элементу/последовательности нуклеиновой кислоты, как правило расположенной выше по цепи и функционально связанной с фрагментом двухнитевой ДНК. Промоторы могут быть получены целиком из областей вблизи нативного представляющего интерес гена, или могут состоять из разных элементов, полученных из различных нативных промоторов или сегментов синтетической ДНК.
Термины «гомология, идентичность или сходство» относятся к степени сходства последовательностей между двумя полипептидами или между двумя молекулами нуклеиновых кислот, сравниваемых путем выравнивания последовательностей. Степень гомологии между двумя отдельными сравниваемыми последовательностями нуклеиновых кислот является функцией количества идентичных или совпадающих нуклеотидов в сопоставимых положениях. Процент идентичности может быть определен путем визуального осмотра и математических расчетов. В качестве альтернативы, процент идентичности двух последовательностей нуклеиновых кислот можно определить путем сравнения информации о последовательностях с использованием компьютерной программы, такой как ClustalW, BLAST, FASTA или Smith-Waterman.
«Вариант» означает в значительной степени аналогичную последовательность. Вариант может обладать аналогичной функцией или в значительной степени аналогичной функцией относительно последовательности дикого типа. В случае никотин-деметилазы аналогичная функция составляет по меньшей мере приблизительно 50%, 60%, 70%, 80% или 90% от функции фермента дикого типа, состоящей в превращении никотина в норникотин при тех же условиях. В случае никотин-деметилазы в значительной степени аналогичная функция составляет по меньшей мере приблизительно 90%, 95%, 96%, 97%, 98% или 99% от функции фермента дикого типа, состоящей в превращении никотина в норникотин при тех же условиях. Например, последовательность, кодирующая NND3 дикого типа, изложена под SEQ ID NO: 2. Варианты могут иметь одну или более благоприятных мутаций, которые приводят в результате к образованию фермента, характеризующегося сниженным уровнем никотин-деметилазной активности по сравнению с полипептидом дикого типа. Варианты могут иметь одну или более благоприятных мутаций, которые приводят в результате к нокауту их никотин-деметилазной активности (то есть 100% ингибированию, и таким образом, образованию нефункционального полипептида). Иллюстративные варианты CYP82E10 дикого типа включают CYP82E10 P419S, который имеет благоприятную мутацию, которая приводит в результате к образованию фермента, обладающего всего приблизительно 25% активностью от никотин-деметилазной активности полипептида CYP82E10 дикого типа. Варианты CYP82E10 G79S, CYP82E10 P107S и CYP82E10 P382S имеют благоприятные мутации, которые приводят в результате к нокауту их никотин-деметилазной активности (то есть 100% ингибированию, и таким образом, образованию нефункционального полипептида). Иллюстративные варианты CYP82E4 дикого типа включают CYP82E4 V376M, который имеет благоприятную мутацию, приводящую в результате к образованию фермента, обладающего всего приблизительно 50% активностью от никотин-деметилазной активности полипептида CYP82E4 дикого типа. Варианты CYP82E4 W329Stop, CYP82E4 K364N, CYP82E4 P382S и CYP82E4 P458S имеют благоприятные мутации, которые приводят в результате к нокауту их никотин-деметилазной активности (то есть 100% ингибированию, и таким образом, образованию нефункционального полипептида). Иллюстративные варианты CYP82E5 дикого типа включают CYP82E5 P449L, который имеет благоприятную мутацию, приводящую в результате к ингибированию его никотин-деметилазной активности, а вариант CYP82E5 W22Stop имеет благоприятную мутацию, которая приводят к нокауту его никотин-деметилазной активности (то есть, 100% ингибированию, и таким образом, образованию нефункционального полипептида). Комбинации этих вариантов описаны в данном документе.
Термин «растение» относится к любому растению или части растения на любой стадии его жизненного цикла или развития, а также к его потомству. В одном варианте осуществления растение представляет собой «растение табака», которое относится к растению, принадлежащему к роду Nicotiana. Предпочтительные виды растения табака описаны в данном документе.
«Части растения» включают клетки растения, протопласты растений, тканевые культуры растительных клеток, из которых можно регенерировать целое растение, каллюсы растений, корневища растений и клетки растений, которые являются интактными в растениях или частях растений, таких как зародыши, пыльца, пыльники, семяпочки, семена, листья, цветки, стебли, ветви, плод, корни, кончики корней и т.п. Потомство, варианты и мутанты регенерированных растений также включены в объем настоящего раскрытия при условии, что они содержат введенные полинуклеотиды, описанные в данном документе.
«Клетка растения» относится к структурной и физиологической единице растения. Клетка растения может находиться в виде протопласта без клеточной стенки, выделенной отдельной клетки или культивируемой клетки или может быть представлена как часть более высокоорганизованной единицы, такой как, без ограничения, растительная ткань, орган растения или целое растение.
Термин «растительный материал» относится к любой твердой, жидкой или газообразной композиции, или их комбинации, получаемой из растения, включая биомассу, листья, стебли, корни, цветки или части цветка, плоды, пыльцу, яйцеклетки, зиготы, семена, черенки, секреты, экстракты, клеточные или тканевые культуры, или любые другие части или продукты растения. В одном варианте осуществления растительный материал содержит или состоит из биомассы, стеблей, семян или листьев. В другом варианте осуществления растительный материал содержит или состоит из листьев.
Термин «разновидность» относится к популяции растений, которые разделяют постоянные характеристики, отделяющие их от других растений того же вида. Имея один или несколько отличительных признаков, разновидность дополнительно характеризуется очень небольшим общим варьированием между особями в пределах этой разновидности. Разновидность часто продается на коммерческой основе.
Термин «линия» или «селекционная линия», используемый в данном документе, обозначает группу растений, которые используют при селекции растений. Линия отличается от разновидности, поскольку демонстрирует небольшую вариабельность между особями по одному или нескольким представляющим интерес признакам, хотя может присутствовать некоторая вариабельность между особями по другим признакам.
Термин «модулирование» может относиться к снижению, ингибированию, повышению или иному влиянию на экспрессию или активность полипептида. Этот термин может также относиться к снижению, ингибированию, повышению или иному влиянию на активность гена, кодирующего полипептид, которое может включать в себя, помимо прочего, модулирование транскрипционной активности.
Термин «снижение» или «сниженный», используемый в данном документе, относится к снижению от приблизительно 10% до приблизительно 99%, или снижению, составляющему по меньшей мере 10%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98%, по меньшей мере 99%, или по меньшей мере 100% или более от количества или активности, такой как, помимо прочего, полипептидная активность, транскрипционная активность и экспрессия белка.
Термин «ингибировать» или «ингибированный», используемый в данном документе, относится к снижению от приблизительно 98% до приблизительно 100%, или снижению, составляющему по меньшей мере 98%, по меньшей мере 99%, но в особенности 100% от количества или активности, такой как, помимо прочего, полипептидная активность, транскрипционная активность и экспрессия белка.
Термин «повышение» или «повышенный», используемый в данном документе, относится к повышению от приблизительно 5% до приблизительно 99%, или увеличению, составляющему по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98%, по меньшей мере 99%, или по меньшей мере 100% или более от количества или активности, такой как, помимо прочего, полипептидная активность, транскрипционная активность и экспрессия белка.
Термин «контроль» в контексте контрольного растения означает растение или растительную клетку, в которой не была модифицирована экспрессия или активность фермента (например, повышена или снижена), и поэтому он может обеспечить возможность сравнения с растением, в котором была модифицирована экспрессия или активность фермента. Контрольное растение может содержать пустой вектор. Контрольное растение или растительная клетка может соответствовать растению дикого типа или растительной клетке дикого типа. Например, контрольное растение или клетка растения может иметь тот же генотип, что и исходный материал для генетического изменения, результатом которого является исследуемое растение. Во всех таких случаях исследуемое растение и контрольное растение культивируют и собирают с использованием аналогичных протоколов для целей сравнения. Изменения в уровнях, соотношениях, активности или распределении в отношении генов или полипептидов, описанных в данном документе, или изменения в фенотипе растения табака, в частности, сниженное накопление норникотина и его канцерогенного метаболита, NNN, можно измерять путем сравнения исследуемого растения с контрольным растением, где исследуемое растение и контрольное растение культивировали и/или собирали с использованием аналогичных протоколов. Контрольное растение может обеспечивать эталонную точку для измерения изменений в фенотипе исследуемого растения. Показатель изменений в фенотипе можно измерять в любой момент времени для растения, в том числе, во время развития растения, старения или после сушки. Показатель изменений в фенотипе можно измерять для растений, выращенных в любых условиях, в том числе для растений, выращенных в камере для выращивания, теплице или на поле. Показатель изменений в фенотипе можно измерять путем определения скорости превращения никотина в норникотин. Степень превращения можно измерять путем деления процентного содержания норникотина или его метаболита (в виде процентного содержания от общего веса ткани) на сумму процентного содержания никотина и норникотина или его метаболита (в виде процентных содержаний от общего веса ткани) и умножения результата на 100. Изменения в фенотипе можно измерять путем измерения содержания TSNA, например, по меньшей мере содержания NNN, с помощью способов, хорошо известных в данной области.
ПОДРОБНОЕ ОПИСАНИЕ
В одном варианте осуществления предложен выделенный полинуклеотид, содержащий полинуклеотидную последовательность, состоящий из нее или, по сути, состоящий из нее, характеризующегося по меньшей мере 95% идентичностью последовательности с любой из последовательностей, описанных в данном документе, включая любой из полинуклеотидов, показанный в перечне последовательностей. Предпочтительно выделенный полинуклеотид содержит, состоит или состоит главным образом из последовательности, характеризующейся по меньшей мере 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности с ним.
В другом варианте осуществления предложен выделенный полинуклеотид, содержащий полинуклеотидную последовательность, состоящий из нее или, по сути, состоящей из нее, характеризующийся по меньшей мере 95% идентичностью последовательности с SEQ ID NO: 2. Предпочтительно выделенный полинуклеотид содержит последовательность, состоит из нее или, по сути, состоит из нее, характеризующуюся по меньшей мере приблизительно 95% 96%, 97%, 98%, 99%, 99,1%, 99,2%, 99,3%, 99,4%, 99,5%, 99,6%, 99,7%, 99,8%, 99,9% или 100% идентичностью последовательности с SEQ ID NO: 2.
В другом варианте осуществления предложен полинуклеотид, содержащий, полинуклеотид, состоящий из него или, по сути, состоящий из него, со значительной степенью гомологии (то есть, сходством последовательности) или значительной степенью идентичности с SEQ ID NO: 2.
В другом варианте осуществления предложены варианты полинуклеотида, характеризующиеся по меньшей мере приблизительно 95%, 95% 96%, 97%, 98%, 99%, 99,1%, 99,2%, 99,3%, 99,4%, 99,5%, 99,6%, 99,7%, 99,8% или 99,9% идентичностью последовательностей с последовательностью SEQ ID NO: 2.
В другом варианте осуществления предусмотрены фрагменты SEQ ID NO: 2 со значительной степенью гомологии (то есть, сходством последовательности) или значительной степенью идентичности, характеризующиеся по меньшей мере приблизительно 95% 96%, 97%, 98%, 99%, 99,1%, 99,2%, 99,3%, 99,4%, 99,5%, 99,6%, 99,7%, 99,8%, 99,9% или 100% идентичностью последовательностей с соответствующими фрагментами в SEQ ID NO: 2.
Предпочтительно фрагменты характеризуются указанной идентичностью последовательности в пределах отрезка по меньшей мере из 15 смежных нуклеотидов под SEQ ID NO: 1. В определенных вариантах осуществления идентичность последовательности распространяется по меньшей мере на 20, 25, 30, 35, 40, 45, 50 или больше смежных нуклеотидов.
В другом варианте осуществления предложены полинуклеотиды, имеющие достаточную или значительную степень идентичности или сходства с SEQ ID NO: 2, кодирующей полипептид, который выполняет функцию никотин-N-деметилазы. Предпочтительно полинуклеотид(полинуклеотиды), описанный(описанные) в данном документе, кодирует(кодируют) белок с никотин-N-деметилазной активностью, характеризующийся по меньшей мере приблизительно 50%, 60%, 70%, 80%, 90% 95%, 96%, 97%, 98%, 99% или 100% или большей активностью белка, изложенного под SEQ ID NO: 3. Чтобы определить, является ли полипептид функциональной никотин-деметилазой, его кДНК можно клонировать в вектор экспрессии и трансформировать в дрожжевой штамм, такой как штамм W(R). Штамм W(R) представляет собой линию дрожжевых клеток, сконструированную для сверхэкспрессии НАДФ-зависимой цитохром Р450-редуктазы дрожжей, фермента, который служит в качестве прямого донора электронов для Р450; эта система усиливает выявление чужеродной ферментативной активности Р450, экспрессируемого в клетках дрожжей (Pompon et al., (1995) Methods Enzymol. 272: 51-64). Анализы никотин-деметилазы можно проводить путем инкубирования препаратов микросомальных мембран дрожжей [14С]-никотином и разделения продуктов с помощью тонкослойной хроматографии, как описано в публикации Siminszky et al. (2005) Proc. Natl. Acad Sci. USA 102: 14919-14924.
Полинуклеотид, описанный в данном документе, может включать в себя полимер нуклеотидов, который может быть немодифицированной или модифицированной дезоксирибонуклеиновой кислотой (ДНК) или рибонуклеиновой кислотой (РНК). Соответственно, полинуклеотид может быть, без ограничения, геномной ДНК, комплементарной ДНК (кДНК), иРНК или антисмысловой РНК или их фрагментом(фрагментами). Кроме того, полинуклеотид может быть однонитевой или двухнитевой ДНК, ДНК, которая является смесью однонитевых и двухнитевых участков, гибридной молекулой, содержащей ДНК и РНК, или гибридной молекулой со смесью однонитевых и двухнитевых участков или их фрагментом(фрагментами). Кроме того, полинуклеотид может быть составлен из трехнитевых участков, содержащих ДНК, РНК или обе, или их фрагмент(ы). Полинуклеотид может содержать одно или несколько модифицированных оснований, таких как фосфоротиоаты, и может представлять собой пептидную нуклеиновую кислоту. Как правило, полинуклеотиды могут быть собраны из выделенных или клонированных фрагментов кДНК, геномной ДНК, олигонуклеотидов или отдельных нуклеотидов, или комбинации вышеперечисленного. Хотя полинуклеотидные последовательности, описанные в данном документе, представлены в виде последовательностей ДНК, последовательности включают в себя их соответствующие последовательности РНК и их комплементарные (например, полностью комплементарные) последовательности ДНК или РНК, в том числе, их обратно комплементарные цепи.
Полинуклеотид, описанный в данном документе, обычно содержит фосфодиэфирные связи, хотя в некоторых случаях включены полинуклеотидные аналоги, которые могут иметь альтернативные остовы, содержащие, например, фосфороамидатные, фосфоротиоатные, фосфородитиоатные или О-метилфосфороамидитные связи; и пептидные полинуклеотидные остовы и связи. Другие аналоги полинуклеотидов включают в себя полинуклеотиды с положительно заряженными каркасами, неионными каркасами и безрибозными каркасами. Модификации рибозофосфатного остова можно делать по целому ряду причин, например, для повышения стабильности и периода полужизни таких молекул в физиологических средах или в качестве зондов на биочипе. Можно получать смеси природных полинуклеотидов и аналогов; в качестве альтернативы, можно получать смеси разных полинуклеотидных аналогов и смеси природных полинуклеотидов и аналогов.
Известно множество полинуклеотидных аналогов, включая, например, фосфороамидатные, фосфоротиоатные, фосфородитиоатные или О-метилфосфороамидитные связи и пептидные полинуклеотидные каркасы и связи. Другие аналоги полинуклеотидов включают в себя полинуклеотиды с положительно заряженными каркасами, неионными каркасами и безрибозными каркасами. Полинуклеотиды, содержащие один или несколько карбоциклических сахаров, также включены.
Другие аналоги включают в себя пептидные полинуклеотиды, которые представляют собой пептидные полинуклеотидные аналоги. Эти остовы являются главным образом неионными в нейтральных условиях в отличие от высокозаряженного фосфодиэфирного каркаса встречающихся в природе полинуклеотидов. Это может давать преимущества. Во-первых, пептидный полинуклеотидный остов может характеризоваться улучшенной кинетикой гибридизации. Пептидные полинуклеотиды характеризуются более значительными изменениями температуры плавления для несоответствующих по сравнению с идеально совпадающими парами оснований. ДНК и РНК, как правило, проявляют понижения температуры плавления на 2-4 С из-за внутреннего несовпадения. В случае неионного пептидного полинуклеотидного каркаса падение составляет ближе к 7-9°С. Подобным образом, из-за их неионной природы, гибридизация оснований, присоединенных к этим каркасам, является относительно нечувствительной к концентрации солей. Кроме того, пептидные полинуклеотиды могут не разрушаться или разрушаться в меньшей степени клеточными ферментами, и, таким образом, могут быть более стабильными.
Среди применений раскрытых полинуклеотидов и их фрагментов находится применение фрагментов в качестве зондов в анализах с гибридизацией нуклеиновых кислот или праймеров для применения в анализах с амплификацией нуклеиновых кислот. Такие фрагменты обычно содержат по меньшей мере приблизительно 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 или более смежных нуклеотидов из последовательности ДНК. В других вариантах осуществления фрагмент ДНК содержит по меньшей мере приблизительно 10, 15, 20, 30, 40, 50 или 60 или более смежных нуклеотидов из последовательности ДНК. Таким образом, в одном аспекте также предусмотрен способ выявления полинуклеотида, кодирующего белок с никотин-N-деметилазной активностью или кодирующего фермент никотин-N-деметилазу, предусматривающий использование зондов или праймеров, или того и другого.
Основные параметры, влияющие на выбор условий гибридизации, и руководство для разработки подходящих условий описаны в Sambrook J., Е.F. Fritsch и Т. Maniatis (1989, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y.). Используя данные о генетическом коде в комбинации с аминокислотными последовательностями, описанными в данном документе, можно получить наборы вырожденных олигонуклеотидов. Такие олигонуклеотиды применимы в качестве праймеров, например, в полимеразных цепных реакциях (ПЦР), с помощью которых выделяют и амплифицируют фрагменты ДНК. В определенных вариантах осуществления вырожденные праймеры можно использовать в качестве зондов для генетических библиотек. Такие библиотеки будут включать в себя, помимо прочего, библиотеки кДНК, геномные библиотеки и даже электронные библиотеки меток экспрессируемых последовательностей или ДНК. Гомологичные последовательности, идентифицированные этим способом, будут затем использованы в качестве зондов для идентификации гомологов последовательностей, указанных в данном документе.
Кроме того, потенциал использования имеют полинуклеотиды и олигонуклеотиды (например, праймеры или зонды), которые гибридизируются в условиях пониженной жесткости, как правило, в условиях средней жесткости, и обычно, в условиях высокой жесткости с полинуклеотидом(полинуклеотидами), описанным(описанными) в данном документе. Основные параметры, влияющие на выбор условий гибридизации, и руководство для разработки подходящих условий изложены в Sambrook J., Е. F. Fritsch и Т. Maniatis (1989, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y.) и могут быть легко определены обычными специалистами в данной области на основе, например, длины или композиции оснований полинуклеотида. Один из путей достижения умеренно жестких условий включает в себя использование раствора для предварительного отмывания, содержащего 5х стандартный цитрат натрия, 0,5% додецилсульфата натрия, 1,0 мМ этилендиаминтетрауксусной кислоты (рН 8,0), гибридизационного буфера с приблизительно 50% формамида, 6х стандартного цитрата натрия и температуры гибридизации в приблизительно 55°С (или других подобных гибридизационных растворов, таких как содержащих приблизительно 50% формамида с температурой гибридизации около 42°С) и условий отмывания с приблизительно 60°С в 0,5х стандартного цитрата натрия, 0,1% додецилсульфата натрия. Как правило, условия высокой жесткости определяются как условия гибридизации, как описано выше, но с отмыванием при примерно 68 С, 0,2х стандартным цитратом натрия, 0,1% додецилсульфатом натрия. SSPE (1x SSPE представляет собой 0,15 М хлорида натрия, 10 мМ фосфата натрия, 1,25 мМ этилендиаминтетрауксусной кислоты, рН 7,4) можно заменить стандартным цитратом натрия (1х стандартный цитрат натрия представляет собой 0,15 М хлорида натрия и 15 мМ цитрата натрия) в гибридизационных буферах и отмывочных буферах; отмывания выполняют в течение 15 минут после завершения гибридизации. Следует понимать, что температуру отмывания и концентрацию солей для отмывания можно скорректировать по мере необходимости для достижения требуемой степени жесткости с применением основных принципов, которые регулируют реакции гибридизации и стабильность двойной спирали, как это известно специалистам в данной области и дополнительно описано ниже (см., например, Sambrook, J., Е. F. Fritsch и Т. Maniatis (1989, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y.). При гибридизации полинуклеотида с целевым полинуклеотидом с неизвестной последовательностью длина гибрида предполагается такой, как у гибридизируемого полинуклеотида. Когда гибридизируют полинуклеотиды с известными последовательностями, длина гибрида может быть определена путем выравнивания последовательностей полинуклеотидов и идентификации участка или участков с оптимальной комплементарностью последовательности. Температура гибридизации для гибридов, которые предположительно составят менее чем 50 пар оснований в длину, должна быть на 5-10 С меньше, чем температура плавления гибрида, где температуру плавления определяют в соответствии со следующими уравнениями. Для гибридов, длина которых составляет менее 18 пар оснований, температура плавления (°С) = 2(количество оснований А+Т)+4(количество оснований G+C). Для гибридов, длина которых составляет более 18 пар оснований, температура плавления (°С)=81,5+16,6(log10 [Na+])+0,41(% G+C)-(600/N), где N - количество оснований в гибриде и [Na+] - концентрация ионов натрия в буфере для гибридизации ([Na+] для 1х стандартного цитрата натрия =0,165М). Как правило, каждый такой гибридизируемый полинуклеотид имеет длину, которая составляет по меньшей мере 25% (обычно, по меньшей мере 50%, 60% или 70%, и наиболее часто, по меньшей мере 80%) от длины полинуклеотида, с которым он гибридизируется, и характеризуется по меньшей мере 60% идентичностью последовательности (например, по меньшей мере 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100%) с полинуклеотидом, с которым он гибридизируется.
Как будет понятно специалисту в данной области, линейная ДНК имеет две возможные ориентации: направление 5'-3' и направление 3'-5'. Например, если эталонная последовательность расположена в направлении 5'-3', и если вторая последовательность расположена в направлении 5'-3' в той же полинуклеотидной молекуле/цепи, то эталонная последовательность и вторая последовательность ориентированы в одном направлении или имеют одинаковую ориентацию. Как правило, последовательность промотора и представляющий интерес ген, находящийся под контролем данного промотора, расположены в одинаковой ориентации. Однако если по отношению к эталонной последовательности, расположенной в направлении 5'-3', вторая последовательность расположена в направлении 3'-5' в той же полинуклеотидной молекуле/цепи, тогда эталонная последовательность и вторая последовательность ориентированы в антисмысловом направлении или имеют антисмысловую ориентацию. Две последовательности, имеющие антисмысловые ориентации по отношению друг к другу, могут быть альтернативно описаны как имеющие одинаковую ориентацию, если эталонная последовательность (направление 5'-3') и обратно комплементарная последовательность эталонной последовательности (эталонной последовательности, расположенной в 5'-3') расположены в пределах одной полинуклеотидной молекулы/цепи. Последовательности, изложенные в данном документе, показаны в направлении 5'-3'.
Рекомбинантные конструкции, предложенные в данном документе, могут быть использованы для трансформации растений или клеток растений для модулирования уровней экспрессии и/или активности белка. Рекомбинантная полинуклеотидная конструкция может содержать полинуклеотид, кодирующий один или более полинуклеотидов, описанных в данном документе, функционально связанных с регуляторным участком, подходящим для экспрессии полипептида в растении или растительной клетке. Таким образом, полинуклеотид может содержать кодирующую последовательность, которая кодирует полипептид, описанный в данном документе. Растения или клетки растений, в которых модулируют уровни экспрессии и/или активности белка, могут включать в себя мутантные, не встречающиеся в природе, трансгенные, созданные человеком или полученные с помощью методик генной инженерии растения или клетки растений. Соответственно, трансгенное растение или клетка растения содержит геном, который был изменен путем устойчивой интеграции рекомбинантной ДНК. Рекомбинантная ДНК включает в себя ДНК, которая была получена с помощью методик генной инженерии и сконструирована вне клетки, и включает в себя ДНК, содержащую встречающуюся в природе ДНК, или кДНК, или синтетическую ДНК. Трансгенное растение может включать в себя растение, регенерированное из первоначально трансформированной клетки растения, и потомство трансгенных растений от более поздних поколений, или гибриды трансформированного растения. Соответственно, трансгенная модификация изменяет экспрессию или активность полинуклеотида или полипептида, описанного в данном документе, по сравнению с контрольным растением.
Полипептид, кодируемый рекомбинантным полинуклеотидом, может быть нативным полипептидом, или может быть гетерологичным по отношению к клетке. В некоторых случаях рекомбинантная конструкция содержит полинуклеотид, который модулирует экспрессию, функционально связанный с регуляторным участком. Примеры подходящих регуляторных участков описаны в данном документе.
Также предусмотрены векторы, содержащие рекомбинантные полинуклеотидные конструкции, такие как описанные в данном документе. Подходящие основы для векторов включают в себя, например, те, которые обычно используют в данной области, такие как плазмиды, вирусы, искусственные хромосомы, искусственные хромосомы бактерий, искусственные хромосомы дрожжей или искусственные хромосомы бактериофагов. Подходящие векторы экспрессии включают в себя, без ограничения, плазмиды и вирусные векторы, полученные из, например, бактериофага, бакуловирусов и ретровирусов. Многочисленные векторы и системы экспрессии являются коммерчески доступными. Векторы могут включать в себя, например, точки начала репликации, участки связывания с ядерным матриксом или маркеры. Маркерный ген может обеспечивать селектируемый фенотип растительной клетке. Например, маркер может придавать биоцидную устойчивость, такую как устойчивость к антибиотику (например, к канамицину, G418, блеомицину или гигромицину), или к гербициду (например, к глифосату, хлорсульфурону или фосфинотрицину). Кроме того, вектор экспрессии может включать в себя последовательность метки, предназначенную для облегчения манипуляций или выявления (например, очистки или локализации) экспрессированного полипептида. Последовательности меток, такие как последовательности люциферазы, бета-глюкуронидазы, зеленого флуоресцентного белка, глутатион S-трансферазы, полигистидина, с-myc или гемагглютинина, как правило, экспрессируются в виде слияния с кодируемым полипептидом. Такие метки могут быть вставлены в любом месте в пределах полипептида, в том числе на карбоксильном или амино-конце.
Растение или растительную клетку можно трансформировать путем интегрирования рекомбинантного полинуклеотида в ее геном с получением стабильной трансформации. Растение или растительная клетка, описанная в данном документе, может быть стабильно трансформированной. Стабильно трансформированные клетки, как правило, сохраняют введенный полинуклеотид с каждым клеточным делением. Растение или клетку растения также можно временно трансформировать таким образом, что рекомбинантный полинуклеотид не интегрируется в их геном. Временно трансформированные клетки, как правило, теряют весь введенный рекомбинантный полинуклеотид или некоторую его часть с каждым клеточным делением, так что введенный рекомбинантный полинуклеотид нельзя выявить в дочерних клетках после достаточного числа клеточных делений. Предпочтительно NND3 экспрессируется в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и в корнях растения. Предпочтительно NND3 экспрессируется исключительно или главным образом в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и в корнях растения. Также рассматривается использование редактирования генома.
Существует ряд способов, доступных в данной области для трансформации клетки растения, каждый из которых охвачен в данном документе, в том числе, биолистика, методы с применением генной пушки, Agrobacterium-опосредованная трансформация, опосредованная вирусным вектором трансформация и электропорация. Система Agrobacterium для интеграции чужеродной ДНК в хромосомы растений была тщательно изучена, модифицирована и использована для генной инженерии растений. Молекулы оголенной рекомбинантной ДНК, содержащие последовательности ДНК, соответствующие исследуемому очищенному белку табака, функционально связанные в смысловой или антисмысловой ориентации с регуляторными последовательностями, соединяют с соответствующими последовательностями Т-ДНК с помощью обычных способов. Их вводят в протопласты табака при помощи методики с полиэтиленгликолем или методики электропорации, каждая из которых является стандартной. В качестве альтернативы, такие векторы, содержащие молекулы рекомбинантной ДНК, кодирующие исследуемый очищенный белок табака, вводят в живые клетки Agrobacterium, которые затем переносят ДНК в клетки растения табака. Трансформацию с помощью оголенной ДНК без сопутствующих векторных последовательностей Т-ДНК можно выполнять посредством слияния протопластов табака с ДНК-содержащими липосомами или посредством электропорации. Оголенную ДНК, не дополненную векторными последовательностями Т-ДНК, также можно использовать для трансформации клеток табака с помощью инертных, высокоскоростных микрочастиц.
Если клетку или культивируемую ткань используют в качестве реципиентной ткани для трансформации, растения можно регенерировать из трансформированных культур, при желании, с помощью методов, известных специалистам в данной области.
Выбор регуляторных участков, которые будут включены в рекомбинантную конструкцию, зависит от нескольких факторов, в том числе без ограничения от эффективности, селективности, индуцибельности, желаемого уровня экспрессии и клеточной или тканевой предпочтительности экспрессии. Обычным делом для специалиста в данной области является модулирование экспрессии кодирующей последовательности путем соответствующего выбора и размещения регуляторных участков по отношению к кодирующей последовательности. Транскрипцию полинуклеотида можно модулировать подобным образом. Некоторые подходящие регуляторные участки инициируют транскрипцию исключительно или преимущественно в определенных типах клеток. Способы идентификации и установления характеристик регуляторных участков в геномной ДНК растений хорошо известны в данной области.
Подходящие промоторы включают в себя тканеспецифичные промоторы, распознаваемые тканеспецифичными факторами, присутствующими в разных тканях или типах клеток (например, специфичные для корня промоторы, специфичные для побега промоторы, специфичные для ксилемы промоторы), или присутствующими на различных стадиях развития, или присутствующими в ответ на разные условия окружающей среды. Подходящие промоторы включают в себя конститутивные промоторы, которые могут быть активированы в большинстве типов клеток, не требуя специфических индукторов. Примеры подходящих промоторов для управления получением полипептидов при RNAi включают в себя промотор 35S вируса мозаики цветной капусты (CaMV/35S), SSU, OCS, lib4, usp, STLS1, В33, nos или промоторы гена убиквитина или гена фазеолина. Специалисты в данной области могут создавать множество вариантов рекомбинантных промоторов.
Тканеспецифичные промоторы представляют собой элементы управления транскрипцией, которые активны только в определенных клетках или тканях в определенное время в ходе развития растений, например, в вегетативных тканях или репродуктивных тканях. Тканеспецифичная экспрессия может быть преимущественной, например, когда экспрессия полинуклеотидов в определенных тканях является предпочтительной. Примеры тканеспецифичных промоторов, связанных с развитием, включают в себя промоторы, которые могут инициировать транскрипцию только (или в основном только) в определенных тканях, таких как вегетативные ткани, например, корни или листья, или репродуктивные ткани, такие как плоды, семяпочки, семена, пыльца, тычинки, цветки или любая эмбриональная ткань. Промоторы, специфичные для репродуктивных тканей, могут быть, например, специфичными для пыльника, специфичными для семяпочки, специфичными для зародыша, специфичными для эндосперма, специфичными для интегумента, специфичными для семян и кожуры семян, специфичными для пыльцы, специфичными для лепестка, специфичными для чашелистика или их комбинациями.
Подходящие специфичные для листа промоторы включают в себя промотор гена пируватортофосфатдикиназы (PPDK) из С4-растения (кукурузы), промотор cab-mlCa+2 из кукурузы, промотор родственных myb генов из Arabidopsis thaliana (Atmyb5), промоторы рибулозобифосфаткарбоксилазы (RBCS) (например, генов томата RBCS 1, RBCS2 и RBCS3A, экспрессируемые в листьях и выращенных на свету саженцах, RBCS1 и RBCS2, экспрессируемые в развивающихся плодах томата, или промотор гена рибулозобифосфаткарбоксилазы, экспрессируемый на высоких уровнях почти исключительно в мезофильных клетках листовых пластинок и листовых пазух).
Подходящие специфичные для стареющих тканей промоторы включают в себя промотор из томата, активный во время созревания плодов, старения и опадения листьев, промотор гена, кодирующего цистеиновую протеазу кукурузы, промотор гена 82Е4 и промотор гена SAG. Можно использовать подходящие специфичные для пыльника промоторы. Можно выбрать подходящие предпочтительные для корней промоторы, известные специалистам в данной области. Подходящие предпочтительные для семян промоторы включают в себя как специфичные для семян промоторы (промоторы, активные в процессе развития семян, такие как промоторы запасаемых белков семян), так и промоторы прорастающих семян (промоторы, активные во время прорастания семян). Такие предпочтительные для семян промоторы включают в себя без ограничения промотор гена Cim1 (цитокинин-индуцированный сигнал); cZ19B1 (19 кДа зеин кукурузы); milps (миоинозитол-1-фосфатсинтаза); mZE40-2, также известный как Zm-40; nuclc и celA (целлюлозосинтаза). Промотор гена гамма-зеина представляет собой специфичный для эндосперма промотор. Промотор гена Glob-1 представляет собой специфичный для зародыша промотор. Для двудольных растений, специфичные для семян промоторы включают в себя без ограничения промотор гена бета-фазеолина фасоли, гена напина, гена β-конглицинина, гена лектина сои, гена круциферина и им подобные. Для однодольных растений специфичные для семян промоторы включают в себя без ограничения промотор гена 15 кДа зеина кукурузы, промотор гена 22 кДа зеина, промотор гена 27 кДа зеина, промотор гена g-зеина, промотор гена 27 кДа гамма-зеина (такой как промотор gzw64A, см. номер доступа S78780 в Genbank), промотор гена waxy, промотор гена shrunken 1, промотор гена shrunken 2, промотор гена глобулина 1 (см. номер доступа L22344 в Genbank), промотор гена Itp2, промотор гена cim1, промоторы генов end1 и end2 кукурузы, промотор гена nuc1, промотор гена Zm40, промотор гена eep1 и еер2; промотор гена lec1, промотор гена тиоредоксина Н; промотор гена mlip15, промотор гена PCNA2 и промотор гена shrunken-2.
Примеры индуцибельных промоторов включают в себя промоторы, реагирующие на воздействие патогенов, анаэробные условия, повышенную температуру, свет, засуху, низкую температуру или высокую концентрацию солей. Патоген-индуцибельные промоторы включают в себя промоторы связанных с патогенезом белков (белки PR), которые индуцируются после инфицирования патогеном (например, белки PR, белки SAR, бета-1,3-глюканаза, хитиназа).
В дополнение к промоторам растений можно получать другие подходящие промоторы бактериального происхождения (например,, промотор гена октопинсинтазы, промотор гена нопалинсинтазы и другие промоторы, полученные из Ti плазмид), или их можно получать из вирусных промоторов (например, промоторы 35S и 19S РНК вируса мозаики цветной капусты (CaMV), конститутивные промоторы вируса табачной мозаики, промоторы 19S и 35S вируса мозаики цветной капусты (CaMV) или промотор 35S вируса мозаики норичника).
В другом аспекте предложен выделенный полипептид, содержащий полипептидную последовательность, состоящий из нее или, по сути, состоящий из нее, характеризующуюся по меньшей мере 95% идентичностью последовательности с любой из полипептидных последовательностей, описанных в данном документе, включая любые полипептиды, приведенные в перечне последовательностей. Соответственно, выделенный полинуклеотид содержит последовательность, состоит или, по сути, состоит из нее, которая характеризуется по меньшей мере 95%, 96%, 97%, 98%, 99%, 99,1%, 99,2%, 99,3%, 99,4%, 99,5%, 99,6%, 99,7%, 99,8%, 99,9% или 100% идентичностью последовательности с ним. В одном варианте осуществления предусмотрен полипетид, кодируемый SEQ ID NO: 3.
В другом варианте осуществления предложен выделенный полипептид, содержащий последовательность, состоящий из нее или, по сути, состоящий из нее, которая характеризуется по меньшей мере 95% 96%, 97%, 98%, 99%, 99,1%, 99,2%, 99,3%, 99,4%, 99,5%, 99,6%, 99,7%, 99,8%, 99,9% или 100% идентичностью последовательности под SEQ ID NO: 3.
В другом варианте осуществления предложен вариант полипептида, содержащий аминокислотную последовательность, состоящий или, по сути, состоящий из нее, которая кодируется вариантом полинуклеотида, характеризующимся по меньшей мере приблизительно 95%, 96%, 97%, 98%, 99%, 99,1%, 99,2%, 99,3%, 99,4%, 99,5%, 99,6%, 99,7%, 99,8% или 99,9% идентичностью последовательности под SEQ ID NO: 3.
В другом варианте осуществления предложены фрагменты полипептида под SEQ ID NO: 3 или фрагменты под SEQ ID NO: 3, которые характеризуются по меньшей мере приблизительно 95% 96%, 97%, 98%, 99%, 99,1%, 99,2%, 99,3%, 99,4%, 99,5%, 99,6%, 99,7%, 99,8%, 99,9% или 100% идентичностью последовательности с соответствующими фрагментами из SEQ ID NO: 3.
Фрагменты из SEQ ID NO: 3, длина которых составляет, например, по меньшей мере 15 аминокислот, содержат 15 смежных аминокислот из SEQ ID NO: 3. Кроме того, длина фрагментов может составлять 20, 25, 30, 35, 40 или больше аминокислот, вплоть до всех 517 аминокислот в длину, и содержат соответствующее число смежных аминокислот из SEQ ID NO: 3.
Предпочтительные фрагменты включают в себя фрагменты, охватывающие аминокислоты 1-15, 330-345, 420-450 и 480-510 из SEQ ID NO: 3.
Полипептид может содержать последовательности, имеющие достаточную или значительную степень идентичности или сходства с SEQ ID NO: 3 для функционирования в качестве никотин-N-деметилазы. Данные фрагменты полипептида(полипептидов), как правило, сохраняют некоторую или всю активность последовательности полной длины.
Как рассматривается в данном документе, полипептиды также включают в себя мутантов, полученных путем введения любого типа альтераций (например, вставки, делеции или замены аминокислот, изменения уровней гликозилирования, изменения, которые влияют на рефолдинг или изомеризацию, трехмерные структуры или состояния самоассоциации), которые могут быть намеренно сконструированы или легко выделены при условии, что они по прежнему сохраняют некоторую или всю свою функциональность или активность в качестве никотин-N-деметилазы. Предпочтительно функционирование или активность в качестве никотин-N-деметилазы модулируют, снижают или подавляют. Предпочтительно функционирование или активность в качестве никотин-N-деметилазы подавляют до такой степени, что никотин-N-деметилазная активность не выявляется.
Также раскрыт полипептид, кодируемый SEQ ID NO: 3, который характеризуется 100% идентичностью последовательности, или полипептид, содержащий последовательность, состоящий из нее или, по сути, состоящий из нее, которая изложена под SEQ ID NO: 3, характеризующийся 100% идентичностью последовательности с ним.
Полипептиды включают в себя варианты, полученные путем введения любого типа альтераций (например, вставки, делеции или замены аминокислот, изменения уровней гликозилирования, изменения, которые влияют на рефолдинг или изомеризацию, трехмерные структуры или состояния самоассоциации), которые могут быть намеренно сконструированы или легко выделены. Вариант может иметь альтерации, которые производят молчащее изменение и приводят в результате к образованию функционально эквивалентного белка. Намеренные аминокислотные замены можно осуществлять, исходя из сходства полярности, заряда, растворимости, гидрофобности, гидрофильности и амфипатической природы остатков при условии, что вторичная активность в отношении связывания вещества сохраняется. Например, отрицательно заряженные аминокислоты включают в себя аспарагиновую кислоту и глутаминовую кислоту, положительно заряженные аминокислоты включают в себя лизин и аргинин, и аминокислоты с незаряженными полярными концевыми группами с подобными значениями гидрофильности включают в себя лейцин, изолейцин, валин, глицин, аланин, аспарагин, глутамин, серии, треонин, фенилаланин и тирозин. Консервативные замены можно осуществлять, например, в соответствии с приведенной ниже таблицей. Аминокислоты в одном и том же блоке во втором столбце и предпочтительно в одной и той же строке в третьем столбце можно заменять одна на другую:

Полипептид может быть зрелым белком или незрелым белком, или белком, полученным из незрелого белка. Полипептиды могут быть в линейной форме или циклизированы с использованием известных способов. Полипептиды, как правило, содержат по меньшей мере 10, по меньшей мере 20, по меньшей мере 30, или по меньшей мере 40 смежных аминокислот.
Раскрываются растение или клетка растения табака, характеризующиеся мутацией в гене, кодирующем NND3, как описано в данном документе, где указанная мутация приводит в результате к сниженной экспрессии или подавлению функции указанной NND3. Экспрессию или функцию мутанта(мутантов) NND3 можно подавлять. Экспрессия или функция мутанта(мутантов) NND3 может не выявляться. Помимо одной или более мутаций в NND3, мутантные растения или клетки растений могут характеризоваться одной или более дополнительными мутациями в одном или более других генах или полипептидах. В определенных вариантах осуществления помимо одной или более мутаций в NND3, мутанты могут характеризоваться одной или более дополнительными мутациями в одном или более других генах или полипептидах, таких как один или более других генов или полипептидов никотин-деметилазы. Предпочтительно NND3 экспрессируется в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и в корнях мутантного растения. Предпочтительно NND3 экспрессируется исключительно или главным образом в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и в корнях мутантного растения.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4. Предпочтительно указанная никотин-деметилаза CYP82E4 выбрана из последовательности, изложенной под SEQ ID NO: 6-16, или комбинации двух или более из них. Предпочтительно указанная мутация, приводит в результате к модификации указанной никотин-деметилазы CYP82E4, происходящей в положении, выбранном из группы,включающей аминокислотные остатки 38, 171, 201, 169, 459, 427, 329, 364, 376, 382 и 458 под SEQ ID NO: 5 или комбинацию двух или более из них. Предпочтительно указанная мутация выбрана из группы, включающей: а) замену на лейцин остатка пролина в положении 38 SEQ ID NO: 5; b) замену на аспарагин остатка аспарагиновой кислоты в положении 171 SEQ ID NO: 5; с) замену на лизин остатка глутаминовой кислоты в положении 201 SEQ ID NO: 5; d) замену на глутамин остатка аргинина в положении 169 SEQ ID NO: 5; е) замену на аргинин остатка глицина в положении 459 SEQ ID NO: 5; f) замену на изолейцин остатка треонина в положении 427 SEQ ID NO: 5; g) замену на метионин остатка валина в положении 376 SEQ ID NO: 5; h) замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 5; i) замену на аспарагин остатка лизина в положении 364 SEQ ID NO: 5; j) замену на серии остатка пролина в положении 382 SEQ ID NO: 5; k) замену на серии остатка пролина в положении 458 SEQ ID NO: 5; или l) комбинацию двух или более из них.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5. Предпочтительно указанная никотин-деметилаза CYP82E5 выбрана из последовательности, изложенной под SEQ ID NO: 18-25 или комбинации двух или более из них. Предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E5, происходящей в положении, выбранном из группы, включающей аминокислотные остатки 72, 143, 174, 224, 235, 410, 422 или 449 в SEQ ID NO: 17 или комбинацию двух или более из них. Предпочтительно указанная мутация выбрана из группы, включающей: а) замену на лейцин остатка пролина в положении 72 SEQ ID NO: 17; b) замену на фенилаланин остатка лейцина в положении 143 SEQ ID NO: 17; с) замену на лейцин остатка серина в положении 174 SEQ ID NO: 17; d) замену на изолейцин остатка метионина в положении 224 SEQ ID NO: 17; е) замену на серии остатка пролина в положении 235 SEQ ID NO: 17; f) замену на изолейцин остатка треонина в положении 427 SEQ ID NO: 17; g) замену на метионин остатка валина в положении 376 SEQ ID NO: 17; h) замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 17; i) замену на валин остатка аланина в положении 410 SEQ ID NO: 17; j) замену на стоп-кодон остатка триптофана в положении 422 SEQ ID NO: 17; k) замену на лейцин остатка пролина в положении 449 SEQ ID NO: 17 или l) комбинацию двух или более из них.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10. Предпочтительно указанная никотин-деметилаза CYP82E4 выбрана из последовательности, изложенной под SEQ ID NO: 27-35 или комбинации двух или более из них. Предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E10, происходящей в положении, выбранном из группы, включающей аминокислотные остатки 148, 172, 344, 410, 417, 419, 79, 107 или 382 SEQ в ID NO: 26 или комбинацию двух или более из них. Предпочтительно указанная мутация выбрана из группы, включающей: а) замену на фенилаланин остатка лейцина в положении 148 SEQ ID NO: 26; b) замену на аргинин остатка глицина в положении 172 SEQ ID NO: 26; с) замену на треонин остатка аланина в положении 344 SEQ ID NO: 26; d) замену на треонин остатка аланина в положении 410 SEQ ID NO: 26; е) замену на гистидин остатка аргинина в положении 417 SEQ ID NO: 26; f) замену на серии остатка пролина в положении 419 SEQ ID NO: 26; g) замену на серии остатка глицина в положении 79 SEQ ID NO: 26; h) замену на серии остатка пролина в положении 107 SEQ ID NO: 26; i) замену на серии остатка пролина в положении 382 SEQ ID NO: 26 или j) комбинацию двух или более из них.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4. Предпочтительно указанная никотин-деметилаза CYP82E4 выбрана из последовательности, изложенной под SEQ ID NO: 13-16 или комбинации двух или более из них. Предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E4, происходящей в положении, выбранном из группы, включающей аминокислотные остатки 329, 365, 382 или 458 в SEQ ID NO: 5 или комбинацию двух или более из них. Предпочтительно указанная мутация выбрана из группы, включающей: а) замену на стоп-кодон остатка триптофана в положении 329; b) замену на аспарагин остатка лизина в положении 364; с) замену на метионин остатка валина в положении 376;d) замену на серии остатка пролина в положении 382;е) замену на серии остатка пролина в положении 458 и f) любую их комбинацию. Предпочтительно растение или клетка растения табака дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4. Предпочтительно указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop). Предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E4, происходящей по аминокислотному остатку 329 SEQ ID NO: 5. Предпочтительно указанная мутация представляет собой замену на стоп-кодон остатка триптофана в положении 329.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5. Предпочтительно указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 или 25 или комбинации двух или более из них. Предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E5, происходящей в положении, выбранном из группы, включающей аминокислотные остатки 422 и 449, где указанная нумерация соответствует SEQ ID NO: 12. Предпочтительно указанная мутация выбрана из группы, включающей: а) замену на стоп-кодон остатка триптофана в положении 422; b) замену на лейцин остатка пролина в положении 449 и с) любую их комбинацию.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5. Предпочтительно указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop). Предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E5, происходящей по аминокислотному остатку 422, где указанная нумерация соответствует SEQ ID NO: 17. Предпочтительно указанная мутация представляет собой замену на стоп-кодон остатка триптофана в положении 422.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10. Предпочтительно указанная никотин-деметилаза CYP82E10 выбрана из группы, включающей SEQ ID NO: 32-35 или комбинацию двух или более из них. Предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E10, происходящей в положении, выбранном из группы, включающей аминокислотные остатки 79, 107, 382, 419 и любую их комбинацию, где указанная нумерация соответствует SEQ ID NO: 26. Предпочтительно указанная мутация выбрана из группы, включающей: а) замену на серии остатка глицина в положении 79; b) замену на серии остатка пролина в положении 107; с) замену на серии остатка пролина в положении 382; d) замену на серии остатка пролина в положении 419 и е) любую их комбинацию.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10. Предпочтительно указанная никотин-деметилаза CYP82E10 выбрана из группы, включающей SEQ ID NO: 32-34 или комбинацию двух или более из них. Предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E10, происходящей в положении, выбранном из группы, включающей аминокислотные остатки 79, 107, 382 и любую их комбинацию, где указанная нумерация соответствует SEQ ID NO: 26. Предпочтительно указанная мутация выбрана из группы, включающей: а) замену на серии остатка глицина в положении 79; b) замену на серии остатка пролина в положении 107; с) замену на серии остатка пролина в положении 382 и d) любую их комбинацию.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется раскрытыми выше одной или более мутациями в гене никотин-деметилазы CYP82E4 и в гене никотин-деметилазы CYP82E5. Предпочтительно указанные растение или клетка растения табака дополнительно характеризуются описанными выше одной или более мутациями в гене никотин-деметилазы CYP82E4 и в гене никотин-деметилазы CYP82E10. Предпочтительно указанные растение или клетка растения табака дополнительно характеризуются описанными выше одной или более мутациями в гене никотин-деметилазы CYP82E5 и в гене никотин-деметилазы CYP82E10. Предпочтительно указанные растение или клетка растения табака дополнительно характеризуются описанными выше одной или более мутациями в гене никотин-деметилазы CYP82E4, и в гене никотин-деметилазы CYP82E5, и в гене никотин-деметилазы CYP82E10.
Предпочтительно указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop), указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop), и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 33 (G79S).
Предпочтительно указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop), указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop), и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 34 (P107S).
Предпочтительно указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop), указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop), и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 35 (P382S).
Предпочтительно указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop), указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop), и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 32 (P419S).
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и происходит по аминокислотному остатку 329 SEQ ID NO: 25, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и происходит по аминокислотному остатку 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и происходит по аминокислотному остатку 419 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и происходит по аминокислотному остатку 329 SEQ ID NO: 25, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и происходит по аминокислотному остатку 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и происходит по аминокислотному остатку 79 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и происходит по аминокислотному остатку 329 SEQ ID NO: 25, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и происходит по аминокислотному остатку 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и происходит по аминокислотному остатку 107 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и происходит по аминокислотному остатку 329 SEQ ID NO: 25, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и происходит по аминокислотному остатку 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и происходит по аминокислотному остатку 382 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и представляет собой замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 5, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и представляет собой замену на стоп-кодон остатка триптофана в положении 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и представляет собой замену на серии остатка глицина в положении 79 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и представляет собой замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 5, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и представляет собой замену на стоп-кодон остатка триптофана в положении 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, при этом указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и представляет собой замену на серии остатка пролина в положении 107 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и представляет собой замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 5, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и представляет собой замену на стоп-кодон остатка триптофана в положении 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, при этом указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и представляет собой замену на серии остатка пролина в положении 382 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гомозиготной форме в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и происходит по аминокислотному остатку 329 SEQ ID NO: 25, и характеризуется мутацией в гомозиготной форме в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и происходит по аминокислотному остатку 422 SEQ ID NO: 17, и характеризуется мутацией в гомозиготной форме в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и происходит по аминокислотному остатку 419 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гомозиготной форме в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и представляет собой замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 5, и характеризуется мутацией в гомозиготной форме в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и представляет собой замену на стоп-кодон остатка триптофана в положении 422 SEQ ID NO: 17, и характеризуется мутацией в гомозиготной форме в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и представляет собой замену на серии остатка пролина в положении 382 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4. Предпочтительно указанная никотин-деметилаза CYP82E4 выбрана из последовательности, изложенной под SEQ ID NO: 12-16 или комбинации двух или более из них. Предпочтительно указанная мутация, приводящая в результате к модификации указанной никотин-деметилазы CYP82E4, происходит в положении, выбранном из группы, включающей аминокислотные остатки 329, 364, 376, 382 и 458 SEQ ID NO: 5. Предпочтительно указанная мутация выбрана из группы, включающей: а) замену на стоп-кодон остатка триптофана в положении 329; b) замену на аспарагин остатка лизина в положении 364; с) замену на метионин остатка валина в положении 376; d) замену на серии остатка пролина в положении 382; е) замену на серии остатка пролина в положении 458 и f) любую их комбинацию. Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4. Предпочтительно указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop). Предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E4, происходящей по аминокислотному остатку 329 SEQ ID NO: 5. Предпочтительно указанная мутация представляет собой замену на стоп-кодон остатка триптофана в положении 329.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5. Предпочтительно указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 или 25 или комбинации двух или более из них. Предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E5, происходящей в положении, выбранном из группы, включающей аминокислотные остатки 422 и 449, где указанная нумерация соответствует SEQ ID NO: 12. Предпочтительно указанная мутация выбрана из группы, включающей: а) замену на стоп-кодон остатка триптофана в положении 422; b) замену на лейцин остатка пролина в положении 449 и с) любую их комбинацию.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5. Предпочтительно указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop). Предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E5, происходящей по аминокислотному остатку 422, где указанная нумерация соответствует SEQ ID NO: 17. Предпочтительно указанная мутация представляет собой замену на стоп-кодон остатка триптофана в положении 422.
Предпочтительно растение или растительная клетка табака с мутантной NND3 характеризуется дополнительной мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10. Предпочтительно указанная никотин-деметилаза CYP82E10 выбрана из группы, включающей SEQ ID NO: 32-35 или комбинацию двух или более из них. Предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E10, происходящей в положении, выбранном из группы, включающей аминокислотные остатки 79, 107, 382, 419 и любую их комбинацию, где указанная нумерация соответствует SEQ ID NO: 26. Предпочтительно указанная мутация выбрана из группы, включающей: а) замену на серии остатка глицина в положении 79; b) замену на серии остатка пролина в положении 107; с) замену на серии остатка пролина в положении 382; d) замену на серии остатка пролина в положении 419 и е) любую их комбинацию.
Предпочтительно растение или растительная клетка табака с мутантной NND3 характеризуется дополнительной мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10. Предпочтительно указанная никотин-деметилаза CYP82E10 выбрана из группы, включающей SEQ ID NO: 32-34 или комбинацию двух или более из них. Предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E10, происходящей в положении, выбранном из группы, включающей аминокислотные остатки 79, 107, 382 и любую их комбинацию, где указанная нумерация соответствует SEQ ID NO: 26. Предпочтительно указанная мутация выбрана из группы, включающей: а) замену на серии остатка глицина в положении 79; b) замену на серии остатка пролина в положении 107; с) замену на серии остатка пролина в положении 382 и d) любую их комбинацию.
Предпочтительно растение или растительная клетка табака с мутантной NND3 дополнительно характеризуются описанными выше одной или более мутациями в гене никотин-деметилазы CYP82E4 и в гене никотин-деметилазы CYP82E5. Предпочтительно указанные растение или клетка растения табака дополнительно характеризуются описанными выше одной или более мутациями в гене никотин-деметилазы CYP82E4 и в гене никотин-деметилазы CYP82E10. Предпочтительно указанные растение или клетка растения табака дополнительно характеризуются описанными выше одной или более мутациями в гене никотин-деметилазы CYP82E5 и в гене никотин-деметилазы CYP82E10. Предпочтительно указанные растение или клетка растения табака дополнительно характеризуются описанными выше одной или более мутациями в гене никотин-деметилазы CYP82E4, и в гене никотин-деметилазы CYP82E5, и в гене никотин-деметилазы CYP82E10.
Предпочтительно указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop), указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop), и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 33 (G79S).
Предпочтительно указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop), указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop), и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 34 (P107S).
Предпочтительно указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop), указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop), и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 35 (P382S).
Предпочтительно указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13 (W329Stop), указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24 (W422Stop), и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 32 (P419S).
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и происходит по аминокислотному остатку 329 SEQ ID NO: 25, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и происходит по аминокислотному остатку 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и происходит по аминокислотному остатку 419 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и происходит по аминокислотному остатку 329 SEQ ID NO: 25, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и происходит по аминокислотному остатку 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и происходит по аминокислотному остатку 79 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и происходит по аминокислотному остатку 329 SEQ ID NO: 25, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и происходит по аминокислотному остатку 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и происходит по аминокислотному остатку 107 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и происходит по аминокислотному остатку 329 SEQ ID NO: 25, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и происходит по аминокислотному остатку 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и происходит по аминокислотному остатку 382 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и представляет собой замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 5, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и представляет собой замену на стоп-кодон остатка триптофана в положении 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и представляет собой замену на серии остатка глицина в положении 79 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и представляет собой замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 5, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы С YP82E5 и представляет собой замену на стоп-кодон остатка триптофана в положении 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, при этом указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и представляет собой замену на серии остатка пролина в положении 107 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и представляет собой замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 5, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и представляет собой замену на стоп-кодон остатка триптофана в положении 422 SEQ ID NO: 17, и характеризуется мутацией в гене, кодирующем никотин-деметилазу CYP82E10, при этом указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и представляет собой замену на серии остатка пролина в положении 382 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гомозиготной форме в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и происходит по аминокислотному остатку 329 SEQ ID NO: 25, и характеризуется мутацией в гомозиготной форме в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и происходит по аминокислотному остатку 422 SEQ ID NO: 17, и характеризуется мутацией в гомозиготной форме в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и происходит по аминокислотному остатку 419 SEQ ID NO: 26.
Предпочтительно растение или клетка растения табака с мутантной NND3 дополнительно характеризуется мутацией в гомозиготной форме в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4 и представляет собой замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 5, и характеризуется мутацией в гомозиготной форме в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5 и представляет собой замену на стоп-кодон остатка триптофана в положении 422 SEQ ID NO: 17, и характеризуется мутацией в гомозиготной форме в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10 и представляет собой замену на серии остатка пролина в положении 382 SEQ ID NO: 26.
Предпочтительно растение, клетка растения, растительный материал или (сушеное) табачное изделие и им подобные., полученные или которые можно получить в соответствии с настоящим раскрытием, характеризуются превращением никотина в норникотин, составляющим менее приблизительно 1,0%, менее приблизительно 0,9%, менее приблизительно 0,8%, менее приблизительно 0,7%, менее приблизительно 0,6%, менее приблизительно 0,5%, менее приблизительно 0,4%, менее приблизительно 0,3%, менее приблизительно 0,2% или менее приблизительно 0,1%. % превращения рассчитывают с помощью уравнения [%норникотина/(%норникотина + %никотина)]×100.
Предпочтительно растение, клетка растения, растительный материал или (сушеное) табачное изделие и им подобные, полученные, или которые можно получить в соответствии с настоящим раскрытием, содержат менее приблизительно 0,04%, менее приблизительно 0,03%, менее приблизительно 0,02% или менее приблизительно 0,01% норникотина из расчета на сухой вес.
Указанные растение или клетка растения табака с мутантной NND3 могут быть гетерозиготными или гомозиготными по мутации(мутациям). Указанные растение или клетка растения табака с мутантной NND3 могут быть гетерозиготными по меньшей мере по одной мутации и гомозиготными по меньшей мере по одной отличающейся мутации.
Также предусмотрен способ снижения уровня норникотина или снижения скорости превращения никотина в норникотин или снижения уровня по меньшей мере NNN в (сушеном) растении табака или в (сушеном) растительном материале табака, где указанный способ предусматривает введение в геном указанного растения одной или более мутаций, которые снижают экспрессию по меньшей мере гена никотин-деметилазы, где указанный по меньшей мере один ген никотин-деметилазы кодирует NND3. Предпочтительно помимо мутации(мутаций) в NND3, одну или более мутаций также можно вводить по меньшей мере в один аллель по меньшей мере одного, двух или трех или более дополнительных генов никотин-деметилазы, при этом указанные гены выбраны из группы, включающей CYP82E4, CYP82E5 и CYP82E10 или комбинацию двух или более из них, как раскрыто выше.
Также предложен способ идентификации растения табака с низкими уровнями норникотина или низкими уровнями по меньшей мере NNN, при этом указанный способ предусматривает скрининг образца нуклеиновой кислоты из представляющего интерес растения табака на наличие одной или более мутаций в SEQ ID NO: 1 или 2, и необязательно сопоставление идентифицированной(идентифицированных) мутации(мутаций) с мутацией(мутациями), которая(которые), как известно, модулируют уровни норникотина или по меньшей мере NNN. Предпочтительно указанный способ дополнительно включает скрининг указанного образца нуклеиновой кислоты или другого образца нуклеиновой кислоты из указанного представляющего интерес растения табака на наличие мутации в SEQ ID NO: 5, наличие мутации в SEQ ID NO: 12 или наличие мутации в SEQ ID NO: 19, и необязательно сопоставление идентифицированной(идентифицированных) мутации(мутаций) с мутацией(мутациями), которая(которые), как известно, модулируют уровни норникотина или по меньшей мере NNN.
Также раскрыты растение или клетка растения табака, гетерозиготные или гомозиготные по мутациям в гене, кодирующем NND3, в гене, кодирующем никотин-деметилазу CYP82E10, в гене, кодирующем никотин-деметилазу CYP82E4, и в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции никотин-деметилаз NND3, CYP82E10, CYP82E4 и CYP82E5.
Также описаны растение или клетка растения табака, характеризующиеся одной или более мутациями в гетерозиготной или гомозиготной форме в гене NND3 или полипептиде, состоящие из них или, по сути, состоящие из них, как описано в данном документе, которые снижают активность никотин-деметилазы в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и в корнях, одной или более мутациями в гетерозиготной или гомозиготной форме в гене CYP82E10 или полипептиде, которые снижают активность никотин-деметилазы в корнях, одной или более мутациями в гетерозиготной или гомозиготной форме в гене CYP82E4 или полипептиде, которые снижают активность никотин-деметилазы в стареющих листьях, и одной или более мутациями в гене CYP83E5 или полипептиде, которые снижают активность никотин-деметилазы в зеленых листьях.
Для комбинирования мутаций в одном растении можно использовать ряд подходов, в том числе половое скрещивание. Растение с одной или более благоприятными мутациями в гетерозиготной или гомозиготной форме в NND3, которые снижают активность никотин-деметилазы, можно скрещивать с растением с одной или более благоприятными мутациями в гетерозиготной или гомозиготной форме в одном или более генах CYP82E4, CYP82E5 и CYP82E10, которые снижают активность никотин-деметилазы. В одном варианте осуществления скрещивания проводят с целью введения одной или более благоприятных мутаций в гетерозиготной или гомозиготной форме в NND3 и CYP82E10, или NND3 и CYP82E4, или NND3 и CYP82E5 в пределах одного и того же растения. Таким образом, растение с одной или более благоприятными мутациями в гетерозиготной или гомозиготной форме в NND3, которые снижают активность никотин-деметилаз в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и в корнях, скрещивают с растением с одной или более благоприятными мутациями в гетерозиготной или гомозиготной форме в CYP82E10, которые снижают активность никотин-деметилаз в корнях, или скрещивают с растением с одной или более благоприятными мутациями в гетерозиготной или гомозиготной формев CYP82E4, которые снижают активность никотин-деметилазы в стареющих листьях, или скрещивают с растением с одной или более благоприятными мутациями в гетерозиготной или гомозиготной форме в гене CYP83E5, которые снижают активность никотин-деметилазы в зеленых листьях. В другом варианте осуществления скрещивания проводят с целью введения одной или более благоприятных мутаций в гетерозиготной или гомозиготной форме в NND3, CYP82E10 и CYP82E4 в пределах одного и того же растения. Таким образом, растение с одной или более благоприятными мутациями в гетерозиготной или гомозиготной форме в NND3, которые снижают активность никотин-деметилаз в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и в корнях, скрещивают с растением с одной или более благоприятными мутациями в гетерозиготной или гомозиготной форме в CYP82E10, которые снижают активность никотин-деметилаз в корнях, и скрещивают с растением с одной или более благоприятными мутациями в гетерозиготной или гомозиготной формеформе в CYP82E4, которые снижают активность никотин-деметилазы в стареющих листьях. В другом варианте осуществления скрещивания проводят с целью введения одной или более благоприятных мутаций в гетерозиготной или гомозиготной форме в NND3, CYP82E10 и CYP82E5 в пределах одного и того же растения. Таким образом, растение с одной или более благоприятными мутациями в гетерозиготной или гомозиготной форме в NND3, которые снижают активность никотин-деметилаз вцветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и в корнях, скрещивают с растением с одной или более благоприятными мутациями в гетерозиготной или гомозиготной форме в CYP82E10, которые снижают активность никотин-деметилаз в корнях, и скрещивают с растением с одной или более благоприятными мутациями в гетерозиготной или гомозиготной формев CYP83E5, которые снижают активность никотин-деметилазы в зеленых листьях. В другом варианте осуществления скрещивания проводят с целью введения одной или более благоприятных мутаций в гетерозиготной или гомозиготной форме в NND3, CYP82E4 и CYP82E5 в пределах одного и того же растения. Таким образом, растение с одной или более благоприятными мутациями в гетерозиготной или гомозиготной форме в NND3, которые снижают активность никотин-деметилаз в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и в корнях, скрещивают с растением с одной или более благоприятными мутациями в гетерозиготной или гомозиготной формев CYP82E4, которые снижают активность никотин-деметилазы в стареющих листьях, и скрещивают с растением с одной или более благоприятными мутациями в гетерозиготной или гомозиготной формев CYP83E5, которые снижают активность никотин-деметилазы в зеленых листьях. В другом варианте осуществления скрещивания проводят с целью введения одной или более благоприятных мутаций в гетерозиготной или гомозиготной формев NND3, CYP82E4, CYP82E5 и CYP82E10 в пределах одного и того же растения. Таким образом, растение с одной или более благоприятными гетерозиготными или гомозиготными мутациями в NND3, которые снижают активность никотин-деметилаз в цветках (например, незрелом цветке, зрелом цветке, незрелой коробочке, сухой коробочке) и в корнях, скрещивают с растением с одной или более благоприятными мутациями в гетерозиготной или гомозиготной формев CYP82E10, которые снижают активность никотин-деметилаз в корнях, одной или более благоприятными мутациями в гетерозиготной или гомозиготной формев CYP82E4, которые снижают активность никотин-деметилазы в стареющих листьях, и одной или более благоприятнымимутациями в гетерозиготной или гомозиготной формев CYP83E5, которые снижают активность никотин-деметилазы в зеленых листьях. Путем введения одной или более благоприятных мутаций в ген(гены) никотин-деметилаз, таких как описанные в данном документе благоприятные мутации, можно получать растение со сниженным или незначительным или не выявляемым превращением никотина в норникотин или его метаболит, или растение со сниженным или незначительным, или не выявляемым уровнем NNN.
Активность одного или более полипептидов никотин-деметилазы по отношению к превращению никотина в норникотин или его метаболит в растении табака снижается или подавляется в соответствии с настоящим раскрытием, если активность по отношению к превращению статистически ниже, чем активность по отношению к превращению того же(тех же) полипептида(полипептидов) никотин-деметилазы в растении табака, которое не было модифицировано с целью подавления активности по отношению к превращению этого полипептида никотин-деметилазы, и которое культивировали и собирали с использованием аналогичных протоколов. Активность полипептида никотин-деметилазы по отношению к превращению никотина в норникотин в растении табака считается устраненной, если ее невозможно выявить с помощью аналитических способов, описанных в данном документе. Способы определения активности полипептида никотин-деметилазы по отношению к превращению никотина в норникотин в растении табака описаны в данном документе.
В некоторых вариантах осуществления благоприятную(благоприятные) мутацию(мутации) вводят в растение табака или клетку растения с использованием подхода с мутагенезом, и введенную мутацию идентифицируют или подвергают отбору с использованием способов, известных специалисту в данной области, таких как блоттинг Саузерна, секвенирование ДНК, ПЦР-анализ или фенотипический анализ. Мутации, которые влияют на экспрессию генов, или которые нарушают функцию кодируемого белка, можно определять с использованием способов, хорошо известных в данной области. Мутации по типу вставки в экзон гена, как правило, приводят к образованию нефункциональных мутантов. Мутации по консервативным остаткам могут быть особенно эффективными в отношении подавления метаболической функции кодируемого белка.
Также раскрыты способы получения мутантных полинуклеотидов и полипептидов. Любое представляющее интерес растение, в том числе клетку растения или растительный материал, можно генетически модифицировать различными способами, с помощью которых, как известно, индуцируется мутагенез, в том числе сайт-направленный мутагенез, олигонуклеотид-направленный мутагенез, индуцированный химическими соединениями мутагенез, индуцированный ионизирующим излучением мутагенез, мутагенез с использованием модифицированных оснований, мутагенез с использованием содержащей разрывы двухспиральной ДНК, мутагенез с двухнитевыми разрывами, мутагенез с использованием штаммов хозяев с нарушенной репарацией, мутагенез посредством синтеза полного гена, шаффлинг ДНК и другие эквивалентные способы.
Также раскрыты фрагменты полинуклеотидов NND3 и полипептидов, кодируемых при этом. Фрагменты полинуклеотида могут кодировать фрагменты белка, которые сохраняют биологическую активность нативного белка и, следовательно, участвуют в метаболическом превращении никотина в норникотин. В качестве альтернативы, фрагменты полинуклеотида, применимые в качестве зондов для гибридизации или ПЦР-праймеров, как правило, не кодируют фрагмент белка, сохраняющий биологическую активность. Кроме того, фрагменты раскрытых нуклеотидных последовательностей включают в себя такие фрагменты, которые могут быть собраны в рекомбинантные конструкции, как описано в данном документе. Фрагменты полинуклеотидной последовательности могут находиться в диапазоне по меньшей мере от приблизительно 25 нуклеотидов, приблизительно 50 нуклеотидов, приблизительно 75 нуклеотидов, приблизительно 100 нуклеотидов, приблизительно 150 нуклеотидов, приблизительно 200 нуклеотидов, приблизительно 250 нуклеотидов, приблизительно 300 нуклеотидов, приблизительно 400 нуклеотидов, приблизительно 500 нуклеотидов, приблизительно 600 нуклеотидов, приблизительно 700 нуклеотидов, приблизительно 800 нуклеотидов, приблизительно 900 нуклеотидов, приблизительно 1000 нуклеотидов, приблизительно 1100 нуклеотидов, приблизительно 1200 нуклеотидов, приблизительно 1300 нуклеотидов или приблизительно 1400 нуклеотидов и до полноразмерного полинуклеотида, кодирующего полипептиды, описанные в данном документе. Фрагменты полипептидной последовательности могут находиться в диапазоне по меньшей мере от приблизительно 25 аминокислот, приблизительно 50 аминокислот, приблизительно 75 аминокислот, приблизительно 100 аминокислот приблизительно 150 аминокислот, приблизительно 200 аминокислот, приблизительно 250 аминокислот, приблизительно 300 аминокислот, приблизительно 400 аминокислот, приблизительно 500 аминокислот и до полноразмерного полипептида, описанного в данном документе.
Мутантные варианты полипептида можно использовать для создания мутантных, не встречающихся в природе или трансгенных растений (например, мутантных, не встречающихся в природе, трансгенных, созданных человеком или полученных при помощи методик генной инженерии) или растительных клеток, содержащих один или более мутантных вариантов полипептида. Предпочтительно мутантные варианты полипептида сохраняют активность немутантного полипептида. Активность мутантного варианта полипептида может быть выше, ниже или приблизительно такой же, как немутантного полипептида.
Мутации в нуклеотидных последовательностях и полипептидах, описанных в данном документе, могут включать в себя внесенные человеком мутации или синтетические мутации, или мутации, созданные при помощи генной инженерии. Мутации в нуклеотидных последовательностях и полипептидах, описанных в данном документе, могут быть мутациями, которые получены или которые можно получить посредством способа, который включает в себя стадию манипуляции in vitro или in vivo. Мутации в нуклеотидных последовательностях и полипептидах, описанных в данном документе, могут быть мутациями, которые получены или которые можно получить посредством способа, который включает в себя вмешательство человека. В качестве примера, способ может включать в себя мутагенез с использованием экзогенно добавляемых химических соединений, таких как мутагенные, тератогенные или канцерогенныеорганические соединения, например этилметансульфонат (EMS), которые осуществляют случайные мутации в генетическом материале. В качестве дополнительного примера способ может включать в себя один или несколько этапов генной инженерии, таких как один или несколько этапов генной инженерии, которые описаны в данном документе, или их комбинации. В качестве дополнительного примера способ может включать в себя одну или несколько стадий скрещивания растений.
Полипептид можно получить путем культивирования трансформированных или рекомбинантных клеток-хозяев в условиях культивирования, подходящих для экспрессии полипептида. Полученный экспрессированный полипептид затем можно очистить из такой культуры с помощью известных способов очистки. Очистка полипептида может включать в себя использование аффинной колонки, содержащей средства, которые связываются с полипептидом; одну или несколько стадий с использованием колонки с такими аффинными смолами; одну или несколько стадий с участием хроматографии с гидрофобным взаимодействием или иммуноаффинную хроматографию. В качестве альтернативы, полипептид может быть экспрессирован в форме, которая будет облегчать очистку. Например, он может быть экспрессирован в виде полипептида слияния, например, с мальтозосвязывающим полипептидом, глутатион-5-трансферазой, his-тагом или тиоредоксином. Наборы для экспрессии и очистки полипептидов слияния являются коммерчески доступными. Полипептид можно метить эпитопом и затем очистить с использованием специфического антитела к такому эпитопу. Одна или несколько стадий жидкостной хроматографии, такой как обращенно-фазовая высокоэффективная жидкостная хроматография, можно использовать для дополнительной очистки полипептида. Некоторые или все из вышеуказанных стадий очистки в различных комбинациях можно использовать для получения практически гомогенного рекомбинантного полипептида. Очищенный таким образом полипептид может быть практически свободным от других полипептидов и определен в данном документе как «практически очищенный полипептид»; такие очищенные полипептиды включают полипептиды, фрагменты, варианты и т.п. Экспрессию, выделение и очистку полипептидов и фрагментов можно выполнять при помощи любой подходящей методики, в том числе, помимо прочего, способами, описанными в данном документе.
Кроме того, можно использовать аффинную колонку, например, с моноклональным антителом, созданным против полипептидов, для аффинной очистки экспрессированных полипептидов. Эти полипептиды можно удалять из аффинной колонки с помощью общепринятых методик, например, в элюирующем буфере с высоким содержанием солей с последующим диализом в буфере с низким содержанием солей для использования, или посредством изменения рН или других компонентов в зависимости от используемой аффинной матрицы, или путем конкурентного удаления с помощью естественного субстрата аффинного фрагмента.
Описаны выделенные или практически очищенные полинуклеотиды или композиции белков. «Выделенный» или «очищенный» полинуклеотид или белок, или его биологически активная часть, по сути, или в основном не содержит компоненты, которые обычно дополняют полинуклеотид или белок или взаимодействуют с ним, обнаруживаемые в его естественном окружении. Таким образом, выделенный или очищенный полинуклеотид или белок практически не содержит другой клеточный материал или культуральную среду при получении с помощью рекомбинантных методик, или практически не содержит предшественников химических соединений или других химических соединений при получении путем химического синтеза. В оптимальном случае «выделенный» полинуклеотид не содержит последовательности (оптимально кодирующие белок последовательности), которые в естественных условиях фланкируют полинуклеотид (например, последовательности, расположенные на 5'- и 3'-концах полинуклеотида) в геномной ДНК организма, из которого получен полинуклеотид. Например, в различных вариантах осуществления выделенный полинуклеотид может содержать менее приблизительно 5 т.п.о., 4 т.п.о., 3 т.п.о., 2 т.п.о., 1 т.п.о., 0.5 т.п.о., или 0,1 т.п.о. нуклеотидной последовательности, которая в естественных условиях фланкирует полинуклеотид в геномной ДНК клетки, из которой получен полинуклеотид. Белок, который практически не содержит клеточный материал, включает препараты белка, характеризующегося содержанием контаминирующего белка, составляющим менее приблизительно 30%, 20%, 10%, 5% или 1% (из расчета на сухой вес).
Полипептид можно также получать с помощью известных общепринятых методик химического синтеза. Способы конструирования полипептидов или их фрагментов способами синтеза известны специалистам в данной области. Синтетически сконструированные полипептидные последовательности благодаря общим первичным, вторичным или третичным структурным, или конформационным характеристикам с нативными полипептидами могут обладать общими с ними биологическими свойствами, включая биологическую активность.
Термин «не встречающийся в природе», используемый в данном документе, описывает объект (например, полинуклеотид, генетическую мутацию, полипептид, растение, клетку растения и растительный материал), который не образован естественным путем или не существует в природе. Такие не встречающиеся в природе объекты или искусственные объекты можно создать, синтезировать, произвести, модифицировать, подвергнуть вмешательству или манипуляции способами, описанными в данном документе, или которые известны в данной области. Такие не встречающиеся в природе объекты или искусственные объекты можно создать, синтезировать, произвести, модифицировать, подвергнуть вмешательству или манипуляции человеком. Таким образом, в качестве примера, не встречающееся в природе растение, не встречающуюся в природе клетку растения или не встречающийся в природе растительный материал можно создать с использованием традиционных методик селекции растений, таких как обратное скрещивание, или с помощью технологий манипуляции с генами, например, с использованием антисмысловой РНК, интерферирующей РНК, мегануклеазы и им подобных. В качестве дополнительного примера, не встречающееся в природе растение, не встречающуюся в природе растительную клетку или не встречающийся в природе растительный материал можно создать с использованием интрогрессии или путем переноса одной или нескольких генетических мутаций (например, одного или нескольких полиморфизмов) от первого растения или растительной клетки ко второму растению или растительной клетке (которые сами по себе могут быть встречающимися в природе), таким образом, что полученное растение, растительная клетка или растительный материал или их потомство содержит генетическую структуру (например, геном, хромосому или ее сегмент), которая не образована естественным путем, или которая не существует в природе. Полученное растение, клетка растения или растительный материал, таким образом, являются искусственными или не встречающимися в природе. Соответственно, искусственные или не встречающиеся в природе растение или клетку растения можно создать путем модификации генетической последовательности в первом встречающемся в природе растении или клетке растения, даже если полученная генетическая последовательность встречается в природе во втором растении или клетке растения, которая содержит другой генетический фон из первого растения или растительной клетки. В определенных вариантах осуществления мутация не является встречающейся в природе мутацией, которая существует в природе в нуклеотидной последовательности или полипептиде, таких как ген или белок.
Различия в генетическом фоне можно обнаружить по фенотипическим различиям или с помощью методик молекулярной биологии, известных в данной области, таких как секвенирование нуклеиновых кислот, определение наличия или отсутствия генетических маркеров (например, маркеров микросателлитной РНК).
Также предусмотрены антитела, которые являются иммунореактивными по отношению к полипептидам, описанным в данном документе. Полипептиды, фрагменты, варианты, полипептиды слияния и им подобные, изложенные в данном документе, можно использовать в качестве «иммуногенов» в получении антител, иммунореактивных по отношению к ним. Такие антитела могут специфически связываться с полипептидом через антигенсвязывающие сайты антитела. Специфически связывающимися антителами являются такие антитела, которые будут специфически распознавать полипептид, гомологи и варианты и связываться с ними, а не с другими молекулами. В одном варианте осуществления антитела являются специфичными для полипептидов, имеющих аминокислотную последовательность, изложенную в данном документе, и не взаимодействуют перекрестно с другими полипептидами.
Более конкретно, полипептиды, фрагмент, варианты, полипептиды слияния и им подобные содержат антигенные детерминанты или эпитопы, которые вызывают образование антител. Данные антигенные детерминанты или эпитопы могут быть линейными или конформационными (прерывистыми). Линейные эпитопы состоят из одного отрезка аминокислот полипептида, тогда как конформационные или прерывистые эпитопы состоят из аминокислотных частей из различных участков полипептидной цепи, которые были приведены в непосредственную близость при сворачивании полипептида. Эпитопы можно идентифицировать любыми способами, известными в данной области. Кроме того, эпитопы из полипептидов можно использовать в качестве реагентов для исследования, в анализах и для очистки специфически связывающихся антител из веществ, таких как поликлональные сыворотки или супернатанты из культивируемых гибридом. Такие эпитопы или их варианты можно получать с использованием методик, известных в данной области, например, путем твердофазного синтеза, химического или ферментативного расщепления полипептида, или с помощью технологии рекомбинантной ДНК.
Как поликлональные, так и моноклональные антитела к полипептидам можно получать с помощью общепринятых методик. Клеточные линии гибридом, которые продуцируют моноклональные антитела, специфичные для полипептидов, также рассматриваются в данном документе. Такие гибридомы можно получать и идентифицировать с помощью общеизвестных методик. Для получения антител различных животных-хозяев можно иммунизировать путем введения полипептида, его фрагмента, варианта или мутантов. К примеру, такие животные-хозяева могут включать, помимо прочего, кроликов, мышей и крыс. Различные адъюванты можно использовать для повышения иммунологического ответа. В зависимости от вида хозяина такие адъюванты включают, помимо прочего, адъюванты Фрейнда (полные и неполные), минеральные гели, такие как гидроксид алюминия, поверхностно-активные вещества, такие как лизолецитин, плюрониловые полиолы, полианионы, пептиды, масляные эмульсии, гемоцианин лимфы улитки, динитрофенол и потенциально пригодные адъюванты человека, такие как BCG (бацилла Кальметта-Герена) и Corynebacterium parvum. Моноклональные антитела можно выделять с помощью общепринятых методик. Такие моноклональные антитела могут быть иммуноглобулинами любого класса, в том числе IgG, IgM, IgE, IgA, IgD, и любого их подкласса.
Антитела можно также использовать в анализах для выявления присутствия полипетидов или фрагментов либо in vitro, либо in vivo. Антитела можно также использовать для очистки полипептидов или фрагментов с помощью иммуноаффинной хроматографии.
Помимо полученных с помощью мутагенеза, композиции, которые могут модулировать экспрессию или активность одного или более полинуклеотидов или полипептидов, выбранных из группы, включающей NND3, CYP82E4, CYP82E5 или CYP82E10 или комбинацию двух, трех или четырех из них (например, комбинацию NND3, CYP82E4, CYP82E5 и CYP82E10), включают ограничения специфичные для последовательности полинуклеотиды, которые могут нарушать транскрипцию одного или более эндогенного гена(генов); специфичные для последовательности полинуклеотиды, которые могут нарушать трансляцию транскриптов РНК (например, двухнитевые РНК, миРНК, рибозимы); специфичные для последовательности полипептиды, которые могут нарушать стабильность одного или нескольких белков; специфичные для последовательности полинуклеотиды, которые могут нарушать ферментативную активность одного или более белков или активность в отношении связывания одного или более белков с соответствующими субстратами или регуляторными белками; антитела, которые характеризуются специфичностью в отношении одного или более белков; низкомолекулярные соединения, которые могут нарушать стабильность одного или более белков или ферментативную активность одного или более белков или активность в отношении связывания одного или более белков; белки «цинковые пальцы», которые связывают один или несколько полинуклеотидов; и мегануклеазы, которые обладают активностью по отношению к одному или более полинуклеотидам. Технологии редактирования гена, генетические технологии редактирования и технологии редактирование генома хорошо известны в данной области.
Один из способов редактирования гена предусматривает использование подобных активатору транскрипции эффекторных нуклеаз (TALEN), вызывающих двухнитевые разрывы, на которые клетка может отвечать с привлечением механизмов репарации. Негомологичное соединение концов повторно сцепляет ДНК с обеих сторон двухнитевого разрыва, где имеет место незначительное, или вовсе отсутствуете перекрывание последовательности для комплементарного связывания. Этот механизм репарации индуцирует ошибки в геноме посредством вставки или делеции, либо хромосомной перестройки. Любые такие ошибки могут сделать генные продукты, закодированные в этом месте, не функциональными. Другой способ редактирования гена предусматривает использование бактериальной системы CRISPR/Cas. Бактерии и архебактерии характеризуются хромосомными элементами, называемыми короткими палиндромными повторами, регулярно расположенными группами (CRISPR), которые являются частью адаптивной иммунной системы, защищающей от проникновения вирусной и плазмидной ДНК. В системах CRISPR II типа, CRISPR РНК (crRNA) функционирует с трансактивирующей crRNA (tracrRNA) и CRISPR-ассоциированными (Cas) белками с внесением двухнитевых разрывов в целевую ДНК. Целевое расщепление с помощью Cas9 требует спаривания оснований crRNA и tracrRNA, а также спаривания оснований crRNA и целевой ДНК. Целевое распознавание облегчается при наличии короткого мотива, называемого прилегающим к протоспейсеру мотивом (РАМ), который соответствует последовательности NGG. Данную систему можно использовать для редактирования генома. Cas9 обычно программируется двойной РНК, состоящей из crRNA и tracrRNA. Тем не менее, коровые компоненты этих РНК могут быть объединены в единую гибридную «направляющую РНК» для нацеливания Cas9. Использование некодирующей направляющей РНК с нацеливанием ДНК для сайт-специфического расщепления обещает быть значительно более простым, чем существующие технологии, такие как TALEN. Использование стратегии CRISPR/Cas с перенацеливанием нуклеазного комплекса требует только введения новой последовательности РНК и нет необходимости в переконструировании специфичности факторов транскрипции белка.
Антисмысловая технология представляет собой другой известный способ, который можно использовать для модулирования экспрессии полипептида. Полинуклеотид гена, который подлежит репрессии, клонируют и функционально связывают с регуляторным участком и последовательностью терминации транскрипции, так что антисмысловая нить РНК транскрибируется. Затем рекомбинантной конструкцией трансформируют клетку растения и получают антисмысловую нить РНК. Полинуклеотид не обязательно является полной последовательностью гена, который подлежит репрессии, но, как правило, будет практически комплементарным по меньшей мере части смысловой нити гена, который должен быть репрессирован.
Полинуклеотид может быть транскрибирован в рибозим или каталитическую РНК, которая влияет на экспрессию иРНК. Рибозимы можно сконструировать для специфического спаривания практически с любой целевой РНК и расщепления фосфодиэфирного остова в определенном месте, тем самым функционально инактивируя целевую РНК. Гетерологичные полинуклеотиды могут кодировать рибозимы, сконструированные для расщепления конкретных транскриптов иРНК, предотвращая таким образом экспрессию полипептида. Рибозимы типа hammerhead являются применимыми для разрушения конкретных иРНК, хотя можно использовать различные рибозимы, которые расщепляют иРНК в последовательностях сайт-специфического распознавания. Рибозимы типа hammerhead расщепляют иРНК в местах, определяемых фланкирующими участками, которые формируют комплементарные пары оснований с целевой иРНК. Единственным требованием является то, что целевая РНК должна содержать нуклеотидную последовательность 5'-UG-3'. Конструирование и получение рибозимов типа hammerhead известно в данной области. Последовательности рибозимов типа hammerhead можно встроить в стабильную РНК, такую как транспортная РНК (тРНК) для повышения эффективности расщепления in vivo.
В одном варианте осуществления специфичный к последовательности полинуклеотид, который может нарушать трансляцию транскрипта(транскриптов) РНК, представляет собой интерферирующую РНК. РНК-интерференция или РНК-сайленсинг представляет собой эволюционно консервативный процесс, в котором конкретные иРНК могут быть нацелены для ферментативной деградации. Двухнитевую РНК (двухнитевая РНК) вводят в клетку или получают в клетке (например, двухнитевой РНК-вирус или полинуклеотиды интерферирующей РНК) для инициации пути интерферирующей РНК. Двухнитевую РНК можно преобразовывать в несколько двойных спиралей малых интерферирующих РНК 21-24 п.о. в длину с помощью РНКазы III, которая представляет собой специфичную для двухнитевой РНК эндонуклеазу. Малые интерферирующие РНК можно затем распознать РНК-индуцированными комплексами сайленсинга, которые способствуют раскручиванию малых интерферирующих РНК с помощью АТФ-зависимого процесса. Раскрученная антисмысловая нить малой интерферирующей РНК направляет активированные РНК-индуцированные комплексы сайленсинга к нацеленной иРНК, содержащей последовательность, комплементарную антисмысловой нити малой интерферирующей РНК. Нацеленная иРНК и антисмысловая нить могут образовывать А-форму спирали, и большую бороздку А-формы спирали можно распознать активированными РНК-индуцированными комплексами сайленсинга. Целевую иРНК можно расщепить с помощью активированных РНК-индуцированных комплексов сайленсинга в одном сайте, определенном сайтом связывания 5'-конца цепи малой интерферирующей РНК. Активированные РНК-индуцированные комплексы сайленсинга могут повторно использоваться для катализа еще одного события расщепления.
Векторы экспрессии интерферирующей РНК могут содержать конструкции интерферирующей РНК, кодирующие полинуклеотиды интерферирующей РНК, которые проявляют активностью в отношении РНК-интерференции путем снижения уровня экспрессии иРНК, пре-иРНК или родственных вариантов РНК. Векторы экспрессии могут содержать промотор, расположенный выше по цепи и функционально связанный с конструкцией интерферирующей РНК, как дополнительно описано в данном документе. Векторы экспрессии интерферирующей РНК могут содержать подходящий минимальный коровый промотор, представляющую интерес конструкцию интерферирующей РНК, расположенный выше по цепи (5') регуляторный участок, расположенный ниже по цепи (3') регуляторный участок, в том числе сигналы терминации транскрипции и полиаденилирования, и другие последовательности, известные специалистам в данной области, такие как различные селективные маркеры.
Полинуклеотиды можно получить в различных формах, в том числе в виде двухнитевых структур (то есть, двухнитевая молекула РНК, содержащая антисмысловую нить и комплементарную ей смысловую нить), двухнитевых шпилькообразных структур или однонитевых структур (то есть, молекула ssRNA, содержащая только антисмысловую нить). Структуры могут содержать вторичную структуру в виде двойной спирали, асимметричной двойной спирали, шпильки или асимметричной шпильки, имеющую самокомплементарную смысловую и антисмысловую нити. Двухнитевую интерферирующую РНК можно превратить ферментативным путем в двухнитевые малые интерферирующие РНК. Одну из нитей двойной спирали малой интерферирующей РНК можно отжечь с комплементарной последовательностью в целевой иРНК и родственных вариантах РНК. Двойные спирали малой интерферирующей РНК/иРНК распознаются РНК-индуцированными комплексами сайленсинга, которые могут расщеплять РНК в нескольких сайтах зависимым от последовательности образом, приводя в результате к разрушению целевой иРНК и родственных вариантов РНК.
Молекулы двухнитевой РНК могут включать в себя молекулы малой интерферирующей РНК, собранные из одного олигонуклеотида в структуре стебель-петля, где самокомплементарные смысловой и антисмысловой участки молекулы малой интерферирующей РНК соединены с помощью основанного на полинуклеотидах или не основанного на полинуклеотидах линкера(линкеров), а также кольцевую однонитевую РНК с двумя или более петлевыми структурами и стеблем, содержащую самокомплементарные смысловую и антисмысловую нити, где кольцевую РНК можно процессировать либо in vivo, либо in vitro с образованием активной молекулы малой интерферирующей РНК, способной опосредовать интерференции РНК.
Также предполагается использование молекул малой РНК, образующей шпильки. Они содержат специфичную антисмысловую последовательность в дополнение к обратно комплементарной (смысловой) последовательности, как правило, отделенной спейсером или последовательностью петли. Расщепление спейсера или петли обеспечивает молекулу однонитевой РНК и ее обратно комплементарную нить, так что их можно отжечь с образованием двухнитевой молекулы РНК (необязательно, с дополнительными стадиями обработки, которые могут привести в результате к добавлению или удалению одного, двух, трех или более нуклеотидов 3'-конца или 5'-конца одной или обеих нитей). Спейсер может иметь достаточную длину для обеспечения возможности комплементарного связывания антисмысловой и смысловой последовательностей и образования двухнитевой структуры (или стебля) до расщепления спейсера (и, необязательно, последующих стадий обработки, которые могут привести в результате к добавлению или удалению одного, двух, трех, четырех или более нуклеотидов с 3'-конца или с 5'-конца одной или обеих нитей). Спейсерная последовательность представляет собой, как правило, неродственную нуклеотидную последовательность, которая находится между двух комплементарных участков нуклеотидной последовательности, которая при комплементарном связывании в двухнитевой полинуклеотид содержит малую шпилечную РНК. Спейсерная последовательность обычно содержит от приблизительно 3 до приблизительно 100 нуклеотидов.
Любой представляющий интерес полинуклеотид РНК можно получить путем подбора подходящей композиции последовательности, размера петли и длины стебля для получения двойной спирали шпильки. Подходящий диапазон для конструирования длины стебля двойной спирали шпильки включает в себя длину стебля по меньшей мере в приблизительно 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 нуклеотидов, например, приблизительно 14-30 нуклеотидов, приблизительно 30-50 нуклеотидов, приблизительно 50-100 нуклеотидов, приблизительно 100-150 нуклеотидов, приблизительно 150-200 нуклеотидов, приблизительно 200-300 нуклеотидов, приблизительно 300-400 нуклеотидов, приблизительно 400-500 нуклеотидов, приблизительно 500-600 нуклеотидов и приблизительно 600-700 нуклеотидов. Подходящий диапазон для конструирования длины петли двойной спирали шпильки включает в себя длину петли в приблизительно 4-25 нуклеотидов, приблизительно 25-50 нуклеотидов или длиннее, если длина стебля двойной спирали шпильки является значительной. В определенных вариантах осуществления молекула двухнитевой РНК или ssRNA составляет от приблизительно 15 до приблизительно 40 нуклеотидов в длину. В другом варианте осуществления молекула малой интерферирующей РНК представляет собой молекулу двухнитевой РНК или ssRNA от приблизительно 15 до приблизительно 35 нуклеотидов в длину. В другом варианте осуществления молекула малой интерферирующей РНК представляет собой молекулу двухнитевой РНК или ssRNA от приблизительно 17 до приблизительно 30 нуклеотидов в длину. В другом варианте осуществления молекула малой интерферирующей РНК представляет собой молекулу двухнитевой РНК или ssRNA от приблизительно 19 до приблизительно 25 нуклеотидов в длину. В другом варианте осуществления молекула малой интерферирующей РНК представляет собой молекулу двухнитевой РНК или ssRNA от приблизительно 21 до приблизительно 24 нуклеотидов в длину. В определенных вариантах осуществления структуры в виде шпильки с участками двойной спирали длиннее, чем 21 нуклеотид, могут способствовать эффективному сайленсингу, управляемому малой интерферирующей РНК, вне зависимости от последовательности и длины петли. Иллюстративная последовательность для РНК-интерференции изложена под SEQ ID NO: 4.
Целевая последовательность иРНК составляет, как правило, от приблизительно 14 до приблизительно 50 нуклеотидов в длину. Целевую иРНК можно, таким образом, проверить на наличие участков от приблизительно 14 до приблизительно 50 нуклеотидов в длину, которые предпочтительно соответствуют одному или более из следующих критериев для целевой последовательности: соотношение A+T/G+C составляет от приблизительно 2:1 до приблизительно 1:2; динуклеотид АА или динуклеотид СА на 5'-конце целевой последовательности; последовательность из по меньшей мере 10 смежных нуклеотидов, уникальных для целевой иРНК (то есть, последовательность отсутствует в других последовательностях иРНК из этого же растения); и нет «полос» из более чем трех смежных гуаниновых (G) нуклеотидов или более чем трех смежных цитозиновых (С) нуклеотидов. Данные критерии можно оценивать с помощью различных методик, известных в данной области, например, компьютерные программы, такие как BLAST, можно использовать для поиска по общедоступным базам данных, чтобы определить, является ли выбранная целевая последовательность уникальной для целевой иРНК. В качестве альтернативы, можно выбрать целевую последовательность (и сконструировать последовательность малой интерферирующей РНК) с помощью коммерчески доступного компьютерного программного обеспечения (например, OligoEngine, Target Finder и Design Tool для малых интерферирующих РНК, которые являются коммерчески доступными).
В одном варианте осуществления выбраны целевые последовательности иРНК, которые составляют от приблизительно 14 до приблизительно 30 нуклеотидов в длину и соответствуют одному или более критериям, указанным выше. В другом варианте осуществления выбраны целевые последовательности, которые составляют от приблизительно 16 до приблизительно 30 нуклеотидов в длину и соответствуют одному или нескольким критериям, указанным выше. В дополнительном варианте осуществления выбраны целевые последовательности, которые составляют от приблизительно 19 до приблизительно 30 нуклеотидов в длину и соответствуют одному или нескольким критериям, указанным выше. В другом варианте осуществления выбраны целевые последовательности, которые составляют от приблизительно 19 до приблизительно 25 нуклеотидов в длину и соответствуют одному или нескольким критериям, указанным выше.
В иллюстративном варианте осуществления молекулы малой интерферирующей РНК содержат специфическую антисмысловую последовательность, которая комплементарна по меньшей мере 12, 13,14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более смежным нуклеотидам из любой из описанных в данном документе полинуклеотидных последовательностей.
Специфическая антисмысловая последовательность, содержащаяся в молекуле малой интерферирующей РНК, может быть идентичной или практически идентичной комплементарной цепи целевой последовательности. В одном варианте осуществления специфическая антисмысловая последовательность, содержащаяся в молекуле малой интерферирующей РНК, является по меньшей мере приблизительно на 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичной комплементарной цепи последовательности целевой иРНК. Способы определения идентичности последовательности известны в данной области, и ее можно определить, например, с помощью программы BLASTN программного обеспечения Computer Group (GCG) Университета штата Висконсин, или предоставленной на веб-сайте NCBI.
Специфическая антисмысловая последовательность молекул малой интерферирующей РНК может проявлять изменчивость в отношении различий (например, нуклеотидной замены, в том числе, транзиции или трансверсии) по одному, двум, трем, четырем или более нуклеотидам последовательности целевой иРНК. Если такие нуклеотидные замены находятся в антисмысловой цепи молекулы двухнитевой РНК, то комплементарный нуклеотид в смысловой цепи, с которым замещенный нуклеотид, как правило, должен образовывать водородные связи при спаривании оснований, может быть или может не быть соответственно замещенным. Молекулы двухнитевой РНК, в которых одна или более нуклеотидных замен происходят в смысловой последовательности, но не в антисмысловой нити, также рассмариваются. Если антисмысловая последовательность молекулы малой интерферирующей РНК содержит одно или несколько несовпадений между нуклеотидной последовательностью малой интерферирующей РНК и целевой нуклеотидной последовательностью, как описано выше, эти несоответствия могут быть обнаружены на 3'-конце, 5'-конце, или в центральной части антисмысловой последовательности.
В другом варианте осуществления молекулы малой интерферирующей РНК содержат специфическую антисмысловую последовательность, которая способна селективно гибридизироваться в жестких условиях с частью встречающегося в природе целевого гена или целевой иРНК. Как известно специалистам в данной области, вариации жесткости условий гибридизации могут быть достигнуты путем изменения времени, температуры или концентрации растворов, используемых для стадий гибридизации и отмывания. Подходящие условия могут также частично зависеть от конкретных используемых нуклеотидных последовательностей, например, последовательности целевой иРНК или гена.
Одним из способов индукции сайленсинга двухнитевой РНК в растениях является трансформация генной конструкцией, производящей РНК, образующую шпильки (см. Smith et al. (2000) Nature, 407, 319-320). Такие конструкции содержат инвертированные участки последовательности целевого гена, отделенные соответствующим спейсером. Вставка функционального интронного участка растения в качестве спейсерного фрагмента дополнительно повышает эффективность индукции сайленсинга гена в связи с выработкой РНК, образующей шпильки, сплайсированной с интроном (Wesley et al. (2001) Plant J., 27, 581-590). Предпочтительно длина стебля составляет от приблизительно 50 нуклеотидов до приблизительно 1 тысячи нуклеотидов в длину. Способы получения РНК, образующей шпильки, сплайсированной с интроном, хорошо описаны в данной области (см., например, Bioscience, Biotechnology, and Biochemistry (2008) 72, 2, 615-617).
Молекулы интерферирующей РНК, имеющие двуспиральную или двухнитевую структуру, например, двухнитевая РНК или малая РНК, образующая шпильки, могут иметь тупые концы, или могут иметь липкие 3'- или 5'-концы. Используемый в данном документе термин «липкий конец» относится к неспаренному нуклеотиду или нуклеотидам, которые выступают из двухспиральной структуры, если 3'-конец одной нити РНК выходит за пределы 5'-конца другой нити (липкий 3'-конец), или наоборот (липкий 5'-конец). Нуклеотиды, представляющие собой липкие концы, могут быть рибонуклеотидами, дезоксирибонуклеотидами или их модифицированными версиями. В одном варианте осуществления по меньшей мере одна нить молекулы интерферирующей РНК имеет липкий 3'-конец от приблизительно 1 до приблизительно 6 нуклеотидов в длину. В других вариантах осуществления липкий 3'-конец составляет от приблизительно 1 до приблизительно 5 нуклеотидов, от приблизительно 1 до приблизительно 3 нуклеотидов и от приблизительно 2 до приблизительно 4 нуклеотидов в длину.
Если молекула интерферирующей РНК содержит липкий 3'-конец на одном конце молекулы, другой конец может быть с тупым концом, или также иметь липкий конец (5' или 3'). Если молекула интерферирующей РНК содержит липкий конец с обоих концов молекулы, длина липких концов может быть одинаковой или разной. В одном варианте осуществления молекула интерферирующей РНК содержит липкие 3'-концы от приблизительно 1 до приблизительно 3 нуклеотидов в длину на обоих концах молекулы. В дополнительном варианте осуществления молекула интерферирующей РНК представляет собой двухнитевую РНК, имеющую липкий 3'-конец из 2 нуклеотидов с обоих концов молекулы. В еще одном варианте осуществления нуклеотиды, представляющие собой липкий конец интерферирующей РНК, являются динуклеотидами ТТ или динуклеотидами UU.
При определении процентной идентичности молекулы интерферирующей РНК, содержащей один или более липких концов, с последовательностью целевой иРНК, липкий конец(концы) может учитываться или не учитываться. Например, нуклеотиды с липкого 3'-конца и до 2 нуклеотидов с 5'- или 3'-конца двойной цепи могут быть модифицированы без существенной потери активности молекулы малой интерферирующей РНК.
Молекулы интерферирующей РНК могут содержать одну или несколько 5' или 3'-кэп-структур. Молекула интерферирующей РНК может содержать кэп-структуру на 3'-конце смысловой цепи, антисмысловой цепи или как смысловой, так и антисмысловой цепей; или на 5'-конце смысловой цепи, антисмысловой цепи или как смысловой, так и антисмысловой цепей молекулы интерферирующей РНК. В качестве альтернативы, молекула интерферирующей РНК может содержать кэп-структуру как на 3'-конце, так и на 5'-конце молекулы интерферирующей РНК. Термин «кэп-структура» относится к химической модификации, включенной с любого конца олигонуклеотида, которая защищает молекулу от разрушения эндонуклеазами и может также облегчать доставку или локализацию внутри клетки.
Другой модификацией, применяемой к молекулам интерферирующей РНК, является химическое связывание с молекулой интерферирующей РНК одного или более фрагментов или конъюгатов, которые повышают активность, клеточное распределение, клеточный захват, биодоступность или стабильность молекулы интерферирующей РНК. Полинуклеотиды можно синтезировать или модифицировать с помощью способов, общепринятых в данной области. Химические модификации могут включать без ограничения 2'-модификации, введение неприродных оснований, ковалентное присоединение лиганда и замещение фосфатных связей тиофосфатными связями. В данном варианте осуществления целостность двухспиральной структуры усиливают с помощью по меньшей мере одной и, как правило, двух химических связей. Химическое связывание может обеспечиваться с помощью любого из множества хорошо известных методик, например, путем введения ковалентных, ионных или водородных связей; гидрофобных взаимодействий, Ван-дер-Ваальсовых или стекинговых взаимодействий; посредством координации ионами металлов или благодаря использованию аналогов пуринов.
Нуклеотиды одной или обеих из двух одинарных цепей можно модифицировать для модулирования активации клеточных ферментов, таких как, например, без ограничения определенные нуклеазы. Методики для снижения или ингибирования активации клеточных ферментов известны в данной области и включают без ограничения 2'-аминомодификации, 2'-фтормодификации, 2'-алкилмодификации, модификации незаряженного каркаса, морфолиновые модификации, 2'-O-метилмодификации и фосфорамидат. Таким образом, по меньшей мере одну 2'-гидроксильную группу нуклеотидов двухнитевой РНК замещают химической группой. Также, по меньшей мере один нуклеотид можно модифицировать с образованием закрытого нуклеотида. Такой закрытый нуклеотид содержит метиленовый или этиленовый мостик, который соединяет 2'-кислород рибозы с 4'-углеродом рибозы. Введение закрытого нуклеотида в олигонуклеотид улучшает аффиность к комплементарным последовательностям и повышает температуру плавления на несколько градусов.
Можно конъюгировать лиганды с молекулой интерферирующей РНК, например, для повышения в отношении нее клеточной абсорбции. В определенных вариантах осуществления гидрофобный лиганд конъюгируют с молекулой для облегчения прямого проникновения через клеточную мембрану. Данные подходы использованы для облегчения проникновения в клетку антисмысловых олигонуклеотидов. В определенных случаях конъюгация катионного лиганда с олигонуклеотидами часто приводит к улучшенной устойчивости к нуклеазам. Типичные примеры катионных лигандов включают пропиламмоний и диметилпропиламоний. Антисмысловые олигонуклеотиды могут сохранять свою высокую аффинность связывания с иРНК, когда катионный лиганд распределен по всему олигонуклеотиду.
Молекулы и полинуклеотиды, описанные в данном документе, можно получить с помощью хорошо известных методик твердофазного синтеза. Любые другие средства для такого синтеза, известные в данной области, можно использовать дополнительно или в качестве альтернативы.
Различные варианты осуществления направлены на векторы экспрессии, содержащие один или более полинуклеотидов или одну или более конструкций интерферирующей РНК, которые содержат один или несколько полинуклеотидов, описанных в данном документе. Иллюстративная конструкция интерферирующей РНК показана в SEQ ID NO: 4.
Различные варианты осуществления направлены на векторы экспрессии, содержащие один или более полинуклеотидов или одну или более конструкций интерферирующей РНК, описанных в данном документе.
Различные варианты осуществления направлены на векторы экспрессии, содержащие один или более полинуклеотидов или одну или более конструкций интерферирующей РНК, кодирующих один или более полинуклеотидов интерферирующей РНК, описанных в данном документе, которые способны к самоотжигу с образованием структуры в виде шпильки, в которых конструкция содержит (а) один или более полинуклеотидов, описанных в данном документе; (b) вторую последовательность, кодирующую спейсерный элемент, который образует петлю структуры в виде шпильки; и (с) третью последовательность, содержащую обратно комплементарную последовательность первой последовательности, расположенную в той же ориентации, что и первая последовательность, где вторая последовательность расположена между первой последовательностью и третьей последовательностью, и третья последовательность функционально связана с первой последовательностью и третьей последовательностью.
Раскрытые последовательности можно использовать для конструирования различных полинуклеотидов, которые не образуют структуры в виде шпильки. Например, двухнитевая РНК может быть образована посредством (1) транскрибирования первой цепи ДНК путем функционального связывания с первым промотором и (2) транскрибирования обратно комплементарной последовательности фрагмента ДНК первой цепи путем функционального связывания со вторым промотором. Каждую цепь полинуклеотида можно транскрибировать из одного вектора экспрессии, или из разных векторов экспрессии. Двойную спираль РНК, обладающую активностью в отношении РНК-интерференции, можно ферментативно превратить в малые интерферирующие РНК для модулирования уровней РНК.
Таким образом, различные варианты осуществления направлены на векторы экспрессии, содержащие один или более полинуклеотидов или конструкций интерферирующей РНК, описанных в данном документе, кодирующих полинуклеотиды интерферирующей РНК, способные к самоотжигу, в которых конструкция содержит (а) один или более полинуклеотидов, описанных в данном документе; и (b) вторую последовательность, содержащую комплементарную (например, обратно комплементарную) последовательность первой последовательности, расположенную в той же ориентации, что и первая последовательность.
Предусмотрены различные композиции и способы для модулирования уровней эндогенной экспрессии одного или нескольких полипептидов, описанных в данном документе (или любой их комбинации, описанной в данном документе) путем стимулирования косупрессии экспрессии гена. Явление косупрессии возникает как результат введения множества копий трансгена в растительную клетку-хозяина. Интеграция множества копий трансгена может приводить к модулированию экспрессии трансгена и нацеленного эндогенного гена. Степень косупрессии зависит от степени идентичности последовательности между трансгеном и нацеленным эндогенным геном. Сайленсинг как эндогенного гена, так и трансгена может происходить из-за обширного метилирования подавляемых локусов (то есть, эндогенного промотора и эндогенного представляющего интерес гена), что может нарушать транскрипцию. В качестве альтернативы, в некоторых случаях косупрессия эндогенного гена и трансгена может происходить посредством пост-транскрипционного сайленсинга гена, при котором транскрипты могут быть получены, но повышенные уровни разрушения препятствуют накоплению транскриптов. Механизм косупрессии посредством пост-транскрипционного сайленсинга генов, как полагают, напоминает РНК-интерференцию в том, что РНК, по-видимому, важна как инициатор и мишень в этих процессах, и может быть опосредован, по меньшей мере частично, тем же молекулярным механизмом, возможно, через РНК-направляемое разрушение иРНК.
Косупрессия нуклеиновых кислот может быть достигнута путем введения множества копий нуклеиновой кислоты или ее фрагментов в качестве трансгенов в геном представляющего интерес растения. Растение-хозяин можно трансформировать вектором экспрессии, содержащим промотор, функционально связанный с такой нуклеиновой кислотой или ее фрагментами. Различные варианты осуществления направлены на векторы экспрессии для стимулирования косупрессии эндогенных генов, содержащих промотор, функционально связанный с полинуклеотидом.
Различные варианты осуществления направлены на способы модулирования уровня экспрессии одного или более полинуклеотида(полинуклеотидов), описанного(описанных) в данном документе (или любой их комбинации, как описано в данном документе) путем введения множества копий полинуклеотида (полинуклеотидов) в геном растения (табака), включающие: трансформацию растительной клетки-хозяина вектором экспрессии, который содержит промотор, функционально связанный с полинуклеотидом.
Различные композиции и способы предусмотрены для модулирования уровня экспрессии эндогенного гена путем модулирования трансляции иРНК. Клетку растения-хозяина (табака) можно трансформировать вектором экспрессии, содержащим: промотор, функционально связанный с полинуклеотидом, расположенным в антисмысловой ориентации по отношению к промотору для обеспечения возможности экспрессии полинуклеотидов РНК, имеющих последовательность, комплементарную части иРНК.
Различные векторы экспрессии для модулирования трансляции иРНК могут содержать: промотор, функционально связанный с полинуклеотидом, в антисмысловой ориентации по отношению к промотору. Длина полинуклеотидов антисмысловой РНК может варьировать и составлять от приблизительно 15-20 нуклеотидов, приблизительно 20-30 нуклеотидов, приблизительно 30-50 нуклеотидов, приблизительно 50-75 нуклеотидов, приблизительно 75-100 нуклеотидов, приблизительно 100-150 нуклеотидов, приблизительно 150-200 нуклеотидов и приблизительно 200-300 нуклеотидов.
Также на гены можно целенаправленно воздействовать для инактивации путем введения транспозонов (например, IS-элементов) в геномы представляющих интерес растений. Данные мобильные генетические элементы можно ввести с помощью полового перекрестного опыления и мутантов со вставками можно проверить в отношении потери активности белка. Разрушенный ген родительского растения можно ввести в другие растения путем скрещивания родительского растения с растением, не подвергнутым индуцированному транспозоном мутагенезу, например, путем полового перекрестного опыления. Можно использовать любые стандартные методики селекции, известные специалистам в данной области. В одном варианте осуществления один или более генов можно инактивировать путем вставки одного или более транспозонов. Мутации могут привести к гомозиготному разрушению одного или более генов, к гетерозиготному разрушению одного или более генов, или к комбинации гомозиготных и гетерозиготных разрушений, если разрушен более чем один ген. Подходящие мобильные элементы включают в себя ретротранспозоны, ретропозоны и SINE-подобные элементы. Такие способы известны специалистам в данной области.
В качестве альтернативы, на гены можно целенаправленно воздействовать для инактивации путем введения рибозимов, полученных из ряда малых кольцевых РНК, которые способны к саморасщеплению и репликации в растениях. Данные РНК могут реплицироваться либо самостоятельно (РНК вироида), либо с участием вируса-помощника (сателлитные РНК). Примеры подходящих РНК включают полученные из вироида солнечной пятнистости авокадо и сателлитные РНК, полученные из вируса кольцевой пятнистости табака, вируса временной полосатости люцерны, вируса бархатной пятнистости табака, вируса пятнистости Solanum nodiflorum и вируса пятнистости клевера подземного. Различные специфичные к целевой РНК рибозимы известны специалистам в данной области.
Как обсуждалось в данном документе, экспрессию одного или более полипептидов можно модулировать нетрансгенными способами, как например, путем создания одной или более мутаций в одном или более генах, как обсуждалось в данном документе. Способы, с помощью которых вводят случайную мутацию в генную последовательность, могут включать химический мутагенез, мутагенез с помощью EMS и радиационный мутагенез. Способы, с помощью которых вводят одну или более целенаправленно воздействующих мутаций в клетку, включают без ограничения технологию редактирования генома, в частности, мутагенез, опосредованный нуклеазой с мотивом цинкового пальца, TILLING (целенаправленные индуцированные локальные повреждения в геноме), гомологичную рекомбинацию, олигонуклеотид-направленный мутагенез и мутагенез, опосредованный мегануклеазой. В одном варианте осуществления используют TILLING. Он представляет собой технологию, которую можно использовать для создания и/или идентификации полинуклеотидов, кодирующих полипептиды с модифицированной экспрессией и/или активностью. TILLING также допускает отбор растений, несущих такие мутации. В TILLING комбинируют мутагенез высокой плотности со способами высокопроизводительного скрининга. Способы для проведения TILLING хорошо известны в данной области (см. McCallum et al., (2000) Nat Biotechnol 18:455-457 и Stemple (2004) Nat Rev Genet 5(2): 145-50).
Некоторые неограничивающие примеры мутаций представляют собой делеции, вставки и миссенс-мутации по меньшей мере одного нуклеотида, однонуклеотидные полиморфизмы и простую повторяющуюся последовательность. После внесения мутации можно провести скрининг для идентификации мутаций, которые создают ранние стоп-кодоны или другим образом нефункциональные гены. После внесения мутации можно провести скрининг для идентификации мутаций, которые создают функциональные гены, способные экспрессироваться на повышенных уровнях. Скрининг мутантов можно выполнить путем секвенирования, или с использованием одного или нескольких зондов или праймеров, специфичных для данного гена или белка. Можно также создать в полинуклеотидах конкретные мутации, которые приводят в результате к модулированию экспрессии гена, модулированию стабильности иРНК или модулированию стабильности белка. Такие растения названы в данном документе как «не встречающиеся в природе» или «мутантные» растения. Как правило, мутантные или не встречающиеся в природе растения будут включать в себя по меньшей мере часть чужеродной или синтетической или созданной человеком нуклеиновой кислоты (например, ДНК или РНК), которая не представлена в растении до проведения с ним манипуляций. Чужеродная нуклеиновая кислота может быть одним нуклеотидом, двумя или более нуклеотидами, двумя или более смежными нуклеотидами или двумя или более несмежными нуклеотидами, например, по меньшей мере 10, 20, 30, 40, 50,100, 200, 300, 400, 500, 600, 700, 800, 900, 1000, 1100, 1200, 1300, 1400 или 1500 более смежными или несмежными нуклеотидами.
Мутантные или не встречающиеся в природе растения или растительные клетки могут иметь любую комбинацию одной или более мутаций в одном или более генах, которая приводит в результате к модулированию уровней белка. Например, мутантные или не встречающиеся в природе растения или клетки растения могут иметь одну мутацию в одном гене; несколько мутаций в одном гене; одну мутацию в двух или более, или трех или более, или четырех или более генах; или несколько мутаций в двух или более, или трех или более, или четырех или более генах. Примеры таких мутаций описаны в данном документе. В качестве дополнительного примера, мутантные или не встречающиеся в природе растения или растительные клетки могут иметь одну или более мутаций в конкретной части гена(генов), например, в участке гена, который кодирует активный сайт белка или его часть. В качестве дополнительного примера, мутантные или не встречающиеся в природе растения или растительные клетки могут иметь одну или более мутаций в участке вне одного или более гена(генов), например, в области выше по цепи или ниже по цепи гена, который он регулирует, при условии, что они модулируют активность или экспрессию гена(генов). Элементы, расположенные выше по цепи, могут включать в себя промоторы, энхансеры или транскрипционные факторы. Некоторые элементы, такие как энхансеры, могут располагаться выше по цепи или ниже по цепи гена, который они регулируют. Элемент(элементы) - не обязательно расположен(расположены) рядом с геном, который он(они) регулирует(регулируют), поскольку некоторые элементы, как было обнаружено, расположены на протяжении несколько тысяч пар оснований выше по цепи или ниже по цепи гена, который они регулируют. Мутантные или не встречающиеся в природе растения или клетки растения могут иметь одну или более мутаций, расположенных в первых 100 нуклеотидах гена(генов), в первых 200 нуклеотидах гена(генов), в первых 300 нуклеотидах гена(генов), в первых 400 нуклеотидах гена(генов), в первых 500 нуклеотидах гена(генов), в первых 600 нуклеотидах гена(генов), в первых 700 нуклеотидах гена(генов), в первых 800 нуклеотидах гена(генов), в первых 900 нуклеотидах гена(генов), в первой 1000 нуклеотидов гена(генов), в первых 1100 нуклеотидах гена(генов), в первых 1200 нуклеотидах гена(генов), в первых 1300 нуклеотидах гена(генов), в первых 1400 нуклеотидах гена(генов) или в первых 1500 нуклеотидах гена(генов). Мутантные или не встречающиеся в природе растения или клетки растения могут иметь одну или более мутаций, расположенных в первом, втором, третьем, четвертом, пятом, шестом, седьмом, восьмом, девятом, десятом, одиннадцатом, двенадцатом, тринадцатом, четырнадцатом или пятнадцатом наборе из 100 нуклеотидов гена(генов) или их комбинации. Раскрыты мутантные или не встречающиеся в природе растения или клетки растения (например, мутантные, не встречающиеся в природе или трансгенные растения или растительные клетки и им подобные, как описано в данном документе), содержащие варианты мутантного полипептида.
В одном варианте осуществления семена растений подвергают мутагенезу и затем выращивают из них мутантные растения первого поколения. Затем растениям первого поколения дают самоопылиться и из семян от растений первого поколения выращивают растения второго поколения, которые затем проверяют на наличие мутаций в их локусах. Не смотря на то, что подвергнутый мутации растительный материал можно проверить на наличие мутаций, преимуществом скрининга растений второго поколения является то, что все соматические мутации соответствуют мутациям в зародышевых линиях. Специалисту в данной области будет понятно, что различный растительный материал, в том числе без ограничения семена, пыльцу, растительные ткани или растительные клетки, можно подвергнуть мутагенезу для создания мутантных растений. Однако тип растительного материала, подвергнутого мутагенезу, может иметь значение, когда нуклеиновую кислоту растения проверяют на наличие мутаций. Например, когда пыльцу подвергают мутагенезу до опыления не подвергнутого мутагенезу растения, из семян, полученных при этом опылении, выращивают растения первого поколения. Каждая клетка растений первого поколения будет содержать мутации, созданные в пыльце; таким образом, эти растения первого поколения можно затем проверить на наличие мутаций вместо того, чтобы ждать появления второго поколения.
Мутагены, которые создают главным образом точечные мутации и короткие делеции, вставки, трансверсии и/или транзиции, включая химические мутагены и облучение, можно использовать для создания мутаций. Мутагены включают без ограничения этилметансульфонат, метилметансульфонат, N-этил-N-нитрозомочевину, триэтилмеламин, N-метил-N-нитрозомочевину, прокарбазин, хлорамбуцил, циклофосфамид, диэтилсульфат, мономер акриламида, мельфалан, азотистый иприт, винкристин, диметилнитрозамин, N-метил-N'-нитро-нитрозогуанидин, нитрозогуанидин, 2-аминопурин, 7,12-диметил-бенз(а)антрацен, этиленоксид, гексаметилфосфорамид, бисульфан, диэпоксиалканы (диэпоксиоктан, диэпоксибутан и т.п.), 2-метокси-6-хлор-9[3-(этил-2-хлорэтил)аминопропиламино]акридина дигидрохлорид и формальдегид.
Спонтанные мутации в локусе, которые могут не быть непосредственно вызванными мутагеном, также рассматриваются, при условии, что они приводят в результате к желаемому фенотипу. Подходящие мутагенные средства могут также включать в себя, например, ионизирующее излучение, например, рентгеновское излучение, гамма-излучение, излучение быстрых нейтронов и ультрафиолетовое излучение. Любой способ получения нуклеиновой кислоты растения, известный специалистам в данной области, можно использовать для получения нуклеиновой кислоты растения для скрининга мутаций.
Полученную нуклеиновую кислоту из отдельных растений, клеток растения или растительного материала можно необязательно объединить для того, чтобы ускорить скрининг в отношении мутаций в популяции растений, происходящих из подвергнутых мутагенезу растительных тканей, клеток или материала. Можно проверить одно или более следующих поколений растений, клеток растения или растительного материала. Размер необязательно объединенной группы зависит от чувствительности используемого способа скрининга.
После того, как образцы нуклеиновых кислот необязательно объединили, их можно подвергнуть методикам полинуклеотид-специфичной амплификации, таким как полимеразная цепная реакция. Любой один или более праймеров или зондов, специфичных для гена или последовательностей, непосредственно примыкающих к гену, можно использовать для амплификации последовательностей в необязательно объединенном образце нуклеиновых кислот. Предпочтительно один или более праймеров или зондов конструируют для амплификации участков локуса, в которых с наибольшей вероятностью возникают полезные мутации. Наиболее предпочтительно праймер конструируют для выявления мутаций в участках полинуклеотида. Дополнительно, предпочтительным для праймера(праймеров) и зонда(зондов) было бы избегать известных полиморфных сайтов для облегчения скрининга точечных мутаций. Для облегчения выявления продуктов амплификации один или более праймеров или зондов можно метить с использованием любого общепринятого способа введения метки. Праймер(праймеры) или зонд(зонды) можно сконструировать на основе последовательностей, описанных в данном документе, с помощью способов, которые хорошо известны в данной области.
Для облегчения выявления продуктов амплификации праймер(праймеры) или зонд(зонды) можно пометить с использованием любого общепринятого способа внесения метки. Их можно сконструировать на основе последовательностей, описанных в данном документе, с помощью способов, которые хорошо известны в данной области. Полиморфизмы можно идентафицировать с помощью средств, известных в данной области, и некоторых из описанных в литературе.
В дополнительном аспекте предусмотрен способ получения мутантного растения. Способ включает получение по меньшей мере одной клетки растения, содержащей ген, кодирующий функциональный полинуклеотид, описанный в данном документе (или любую из комбинацию, описанную в данном документе). Далее, эту по меньшей мере одну клетку растения обрабатывают в условиях, эффективных для модулирования активности полинуклеотида(полинуклеотидов), описанного(описанных) в данном документе. По меньшей мере одну мутантную клетку растения затем размножают в мутантное растение, где мутантное растение имеет модулированный уровень описанного полипептида(полипептидов) (или любой их комбинации, описанной в данном документе) по сравнению с уровнем у контрольного растения. В одном варианте осуществления данного способа получения мутантного растения стадия обработки включает подвергание по меньшей мере одной клетки воздействию химического мутагенного средства, как описано выше, и в условиях, эффективных для получения по меньшей мере одной мутантной клетки растения. В другом варианте осуществления данного способа стадия обработки включает подвергание по меньшей мере одной клетки воздействию источника ионизирующего излучения в условиях, эффективных для получения по меньшей мере одной мутантной клетки растения. Термин «мутантное растение» включает мутантные растения, в которых генотип модифицирован по сравнению с контрольным растением, предпочтительно с помощью средств, отличных от генной инженерии и генетической модификации.
В определенных вариантах осуществления мутантное растение, мутантная клетка растения или мутантный растительный материал может содержать одну или более мутаций, которые встречаются в природе в другом растении, клетке растения или растительном материале и обеспечивают желаемый признак. Эту мутацию можно ввести (например, путем интрогрессии) в другое растение, клетку растения или растительный материал (например, растение, клетку растения или растительный материал с отличным генетическим фоном относительно растения, из которого происходит мутация) для обеспечения у них признака. Таким образом, в качестве примера, мутацию, которая встречается в природе в первом растении, можно ввести во второе растение, например, второе растение с отличающимся генетическим фоном относительно первого растения. Специалист в данной области, таким образом, может осуществлять поиск и идентифицировать растение, несущее в естественных условиях в своем геноме один или более мутантных аллелей генов, описанных в данном документе, которые обеспечивают желаемый признак. Мутантный аллель(аллели), который(которые) встречается(встречаются) в природе, можно перенести во второе растение различными способами, включая селекцию, обратное скрещивание и интрогрессию с получением линий, разновидностей или гибридов, которые имеют одну или более мутаций в генах, описанных в данном документе. Растения, демонстрирующие желаемый признак, можно отобрать из пула мутантных растений. Предпочтительно отбор осуществляют с использованием данных о нуклеотидных последовательностях, описанных в данном документе. Следовательно, можно осуществлять отбор по генетическому признаку по сравнению с контролем. Такой скрининговый подход может включать применение общепринятых методик амплификации и/или гибридизации нуклеиновых кислот, как обсуждается в данном документе. Таким образом, дополнительный аспект настоящего изобретения относится к способу идентификации мутантного растения, который включает стадии: (а) получения образца, содержащего нуклеиновую кислоту из растения; и (b) определения последовательности нуклеиновых кислот полинуклеотида, где различие в последовательности полинуклеотида по сравнению с полинуклеотидной последовательностью контрольного растения свидетельствует о том, что указанное растение является мутантным растением. В другом аспекте предусмотрен способ идентификации мутантного растения, которое накапливает сниженные уровни норникотина и/или по меньшей мере NNN по сравнению с контрольным растением, предусматривающий стадии: (а) получения образца из растения, подлежащего скринингу; (b) определения того, содержит ли указанный образец одну или более мутаций в одном или более полинуклеотидах, описанных в данном документе; и (с) определения содержания по меньшей мере норникотина и/или NNN в указанном растении. Предпочтительно содержание по меньшей мере NNN определяют в зеленых листьях или в дыме.
В другом аспекте предложен способ получения мутантного растения, которое имеет сниженные уровни норникотина и/или по меньшей мере NNN по сравнению с контрольным растением, предусматривающий стадии: (а) получения образца из первого растения; (b) определения того, содержит ли указанный образец одну или более мутаций в одном или болееполинуклеотидах, описанных в данном документе, которые приводят в результате к сниженным уровням норникотина и/или по меньшей мере NNN; и (с) переноса одной или более мутаций во второе растение. Предпочтительно содержание по меньшей мере NNN определяют в зеленых листьях или в дыме. Мутацию(мутации) можно перенести во второе растение с помощью различных способов, которые известны в данной области, например, с помощью генной инженерии, манипуляции с генами, интрогрессии, селекции растений, обратного скрещивания и им подобных. В одном варианте осуществления первое растение является встречающимся в природе растением. В одном варианте осуществления второе растение имеет отличающийся генетический фон относительно первого растения.
В другом аспекте предложен способ получения мутантного растения, которое имеет сниженные уровни норникотина и/или по меньшей мере NNN по сравнению с контрольным растением, предусматривающий стадии: (а) получения образца из первого растения; (b) определения того, содержит ли указанный образец одну или более мутаций в одном или более полинуклеотидах, описанных в данном документе, которые приводят в результате к сниженным уровням норникотина и/или по меньшей мере NNN; и (с) интрогрессии одной или более мутаций во второе растение. Предпочтительно содержание по меньшей мере NNN определяют в зеленых листьях или в дыме. В одном варианте осуществления стадия интрогрессии включает в себя селекцию растений, необязательно включая обратное скрещивание и им подобные. В одном варианте осуществления первое растение является встречающимся в природе растением. В одном варианте осуществления второе растение имеет отличающийся генетический фон относительно первого растения. В одном варианте осуществления первое растение не является сортом или элитным сортом. В одном варианте осуществления второе растение представляет собой сорт или элитный сорт. Дополнительный аспект относится к мутантному растению (включая мутантное растение сорта или элитного сорта), полученному или получаемому с помощью способов, описанных в данном документе. В определенных вариантах осуществления «мутантные растения» могут иметь одну или более мутаций, локализованных только в конкретном участке растения, например, в последовательности одного или более полинуклеотида(полинуклеотидов), описанного(описанных) в данном документе. Согласно данному варианту осуществления остальная геномная последовательность мутантного растения будет такой же или практически такой же, как у растения до мутагенеза.
В определенных вариантах осуществления мутантные растения могут иметь одну или более мутаций, локализованных в более чем одном участке растения, например, в последовательности одного или более полинуклеотидов, описанных в данном документе, и в одном или более дополнительных участках генома. Согласно данному варианту осуществления остальная геномная последовательность мутантного растения не будет такой же или не будет практически такой же, как у растения до мутагенеза. В определенных вариантах осуществления мутантные растения могут не иметь одну или более мутаций в одном или более, двух или более, трех или более, четырех или более или пяти или более экзонах полинуклеотида(полинуклеотидов), описанного(описанных) в данном документе; или могут не иметь одну или более мутаций в одном или более, двух или более, трех или более, четырех или более или пяти или более нитронах полинуклеотида(полинуклеотидов), описанного(оипсанных) в данном документе; или могут не иметь одну или более мутаций в промоторе полинуклеотида(полинуклеотидов), описанного(описанных) в данном документе; или могут не иметь одну или более мутаций в 3'-нетранслируемом участке полинуклеотида(полинуклеотидов), описанного(описанных) в данном документе; или могут не иметь одну или более мутаций в 5'-нетранслируемом участке полинуклеотида(полинуклеотидов), описанного(описанных) в данном документе; или могут не иметь одну или более мутаций в кодирующем участке полинуклеотида(полинуклеотидов), описанного(описанных) в данном документе; или могут не иметь одну или более мутаций в некодирующем участке полинуклеотида(полинуклеотидов), описанного(описанного) в данном документе; или любую комбинацию двух или более, трех или более, четырех или более, пяти или более, или шести или более из их частей.
В следующем аспекте предложен способ идентификации растения, клетки растения или растительного материала, содержащих мутацию в гене, кодирующем полинуклеотид, описанный в данном документе, предусматривающий: (а) подвергание растения, клетки растения или растительного материала мутагенезу; (b) получение образца нуклеиновой кислоты из указанного растения, клетки растения или растительного материала или их потомков; и (с) определение последовательности нуклеиновых кислот гена, кодирующего полинуклеотид, описанный в данном документе, или его вариантов или фрагментов, где различие в указанной последовательности свидетельствует об одной или более мутациях в ней.
Белки «цинковые пальцы» можно использовать для модулирования экспрессии или активности одного или нескольких полинуклеотидов, описанных в данном документе. В различных вариантах осуществления последовательность геномной ДНК, содержащую часть или всю кодирующую последовательность полинуклеотида, модифицируют путем мутагенеза, опосредованного нуклеазой с мотивом цинкового пальца. В последовательности геномной ДНК осуществляют поиск уникального сайта связывания белка «цинковый палец». В качестве альтернативы, в последовательности геномной ДНК осуществляют поиск двух уникальных сайтов для связывания белка «цинковый палец», где оба сайта находятся на противоположных цепях и близко друг к другу, например, на расстоянии 1, 2, 3, 4, 5, 6 или более пар оснований друг от друга. Соответственно, предложены белки «цинковые пальцы», которые связываются с полинуклеотидами.
Белок «цинковый палец» можно сконструировать для распознавания выбранного целевого сайта в гене. Белок «цинковый палец» может содержать любую комбинацию мотивов, полученных из природных ДНК-связывающих доменов цинкового пальца и неприродных ДНК-связывающих доменов цинкового пальца путем усечения или расширения или способа сайт-направленного мутагенеза в сочетании со способом отбора, таким как без ограничения отбор с помощью фагового дисплея, отбор с помощью бактериальной дигибридной системы или отбор с помощью бактериальной одногибридной системы. Термин «неприродный ДНК-связывающий домен цинкового пальца» относится к ДНК-связывающему домену цинкового пальца, который связывает последовательность из трех пар оснований в целевой нуклеиновой кислоте и который не происходит из клетки или организма, содержащего нуклеиновую кислоту, которая подлежит модификации. Способы конструирования белка «цинковый палец», который связывает специфические нуклеиновые последовательности, являющиеся уникальными для целевого гена, известны в данной области.
Нуклеазу с мотивом цинкового пальца можно сконструировать путем создания слияния первого полинуклеотида, кодирующего белок «цинковый палец», который связывается с полинуклеотидом, и второго полинуклеотида, кодирующего неспецифическую эндонуклеазу, такую как без ограничения эндонуклеаза типа IIS. Белок слияния между белком «цинковый палец» и нуклеазой может содержать спейсер, состоящий из двух пар оснований или, в качестве альтернативы, спейсер, состоящий из трех, четырех, пяти, шести, семи или более пар оснований. В различных вариантах осуществления нуклеаза цинкового пальца вносит двухнитевой разрыв в регуляторный участок, кодирующий участок или некодирующий участок последовательности геномной ДНК полинуклеотида и приводит к снижениюуровня экспрессии полинуклеотида или снижениюактивности белка, кодируемого им. Расщепление с помощью нуклеаз с мотивом цинкового пальца часто приводит в результате к делеции ДНК в сайте расщепления с последующей репарацией ДНК путем соединения негомологичных концов.
В других вариантах осуществления белок «цинковый палец» можно выбирать для связывания с регуляторной последовательностью полинуклеотида. Более конкретно, регуляторная последовательность может содержать сайт инициации транскрипции, стартовый кодон, участок экзона, границу раздела экзон-интрон, терминатор или стоп-кодон. Соответственно, настоящее изобретение предлагает мутантное, не встречающееся в природе или трансгенное растение или клетку растения, полученные с помощью мутагенеза, опосредованного нуклеазой с мотивом цинкового пальца, вблизи от полинуклеотида или в одном или более полинуклеотидах, описанных в данном документе, и способы создания такого растения или клетки растения с помощью мутагенеза, опосредованного нуклеазой с мотивом цинкового пальца. Способы доставки белка «цинковый палец» и нуклеазы с мотивом цинкового пальца в растение табака подобны описанным ниже для доставки мегануклеазы.
В другом аспекте описаны способы получения мутантных, не встречающихся в природе или трансгенных или другим образом генетически модифицированных растений с использованием мегануклеаз, таких как I-CreI. Встречающиеся в природе мегануклеазы, а также рекомбинантные мегануклеазы можно использовать для того, чтобы специфически вызывать двухнитевой разрыв в одном сайте или в относительно небольшом числе сайтов в геномной ДНК растения с разрушением одного или более полинуклеотидов, описанных в данном документе. Мегануклеаза может быть сконструированной мегануклеазой с измененными свойствами распознавания ДНК. Белки мегануклеаз можно доставлять в клетки растения с помощью ряда различных механизмов, известных в данной области.
Настоящее изобретение охватывает использование мегануклеаз для инактивации полинуклеотида(полинуклеотидов), описанного(описанных) в данном документе (или любой их комбинации, описанной в данном документе), в клетке растения или в растении. В частности, настоящее изобретение предусматривает способ инактивации полинуклеотида в растении с помощью мегануклеазы, предусматривающий: (а) обеспечение клетки растения, содержащей полинуклеотид, описанный в данном документе; (b) введение мегануклеазы или конструкции, кодирующей мегануклеазу, в указанную клетку растения и (с) предоставление возможности мегануклеазе в значительной степени инактивировать полинуклеотид(полинуклеотид).
Мегануклеазы можно использовать для расщепления сайтов распознавания мегануклеазы в кодирующих участках полинуклеотида. Такое расщепление часто приводит в результате к делеции ДНК в сайте распознавания мегануклеазы с последующей репарацией мутагенной ДНК путем соединения негомологичных концов. Такие мутации в кодирующей последовательности гена являются, как правило, достаточными для инактивации гена. Этот способ модификации клетки растения включает, во-первых, доставку кассеты экспрессии мегануклеазы в клетку растения с помощью подходящего способа трансформации. Для достижения максимальной эффективности желательно связать кассету экспрессии мегануклеазы с селектируемым маркером и отобрать успешно трансформированные клетки в присутствии селективного средства. Этот подход приведет к интеграции кассеты экспрессии мегануклеазы в геном, что, однако, может быть нежелательным, если растение, скорее всего, потребует официального разрешения. В таких случаях кассету экспрессии мегануклеазы (и связанный селектируемый маркерный ген) можно выделить из последующих поколений растения с использованием традиционных методик селекции. В качестве альтернативы, клетки растения можно изначально трансформировать кассетой экспрессии мегануклеазы без селектируемого маркера и можно вырастить на средах без селективного средства. В таких условиях часть обработанных клеток приобретет кассету экспрессии мегануклеазы и будет экспрессировать сконструированную мегануклеазу временно без интеграции кассеты экспрессии мегануклеазы в геном. Поскольку это не приводит к эффективности трансформации, последняя процедура трансформации требует скрининга большего количества обработанных клеток для получения желаемой модификации генома. Описанный выше подход можно также применить для модификации растительной клетки при использовании белка «цинковый палец» или нуклеазы с мотивом цинкового пальца.
После доставки кассеты экспрессии мегануклеазы клетки растения выращивают, изначально, в условиях, которые являются типичными для конкретной процедуры трансформации, которую использовали. Это может означать, что трансформированные клетки растут на средах при температуре ниже 26 С, зачастую в темноте. Такие стандартные условия можно использовать в течение периода времени, предпочтительно 1-4 дней, чтобы дать растительной клетке восстановиться после процесса трансформации. В любой момент после этого начального периода восстановления температуру роста можно повысить для стимулирования активности сконструированной мегануклеазы в отношении расщепления и мутирования сайта распознавания мегануклеазы.
Для определенных применений может быть желательным точное удаление полинуклеотидаиз генома растения. Такие применения возможны с использованием пары сконструированных мегануклеаз, каждая из которых расщепляет сайт распознавания мегануклеазы по обе стороны от предполагаемой делеции. Также можно использовать эффекторные нуклеазы TAL (TALEN), которые способны распознавать и связываться с геном и вносить двухнитевой разрыв в геном. Таким образом, в другом аспекте предлагаются способы получения мутантных, не встречающихся в природе или трансгенных или другим образом генетически модифицированных растений, описанных в данном документе, с помощью эффекторных нуклеаз TAL.
Растения, подходящие для использования в отношении генетической модификации, включают без ограничения однодольные и двудольные растения и системы клеток растений, в том числе виды из одного из следующих семейств: Acanthaceae, Alliaceae, Alstroemeriaceae, Amaryllidaceae, Apocynaceae, Arecaceae, Asteraceae, Berberidaceae, Bixaceae, Brassicaceae, Bromeliaceae, Cannabaceae, Caryophyllaceae, Cephalotaxaceae, Chenopodiaceae, Colchicaceae, Cucurbitaceae, Dioscoreaceae, Ephedraceae, Erythroxylaceae, Euphorbiaceae, Fabaceae, Lamiaceae, Linaceae, Lycopodiaceae, Malvaceae, Melanthiaceae, Musaceae, Myrtaceae, Nyssaceae, Papaveraceae, Pinaceae, Plantaginaceae, Poaceae, Rosaceae, Rubiaceae, Salicaceae, Sapindaceae, Solanaceae, Taxaceae, Theaceae или Vitaceae.
Подходящие виды могут включать представителей рода Abelmoschus, Abies, Acer, Agrostis, Allium, Alstroemeria, Ananas, Andrographis, Andropogon, Artemisia, Arundo, Atropa, Berberis, Beta, Bixa, Brassica, Calendula, Camellia, Camptotheca, Cannabis, Capsicum, Carthamus, Catharanthus, Cephalotaxus, Chrysanthemum, Cinchona, Citrullus, Coffea, Colchicum, Coleus, Cucumis, Cucurbita, Cynodon, Datura, Dianthus, Digitalis, Dioscorea, Elaeis, Ephedra, Erianthus, Erythroxylum, Eucalyptus, Festuca, Fragaria, Galanthus, Glycine, Gossypium, Helianthus, Hevea, Hordeum, Hyoscyamus, Jatropha, Lactuca, Linum, Lolium, Lupinus, Lycopersicon, Lycopodium, Manihot, Medicago, Mentha, Miscanthus, Musa, Nicotiana, Oryza, Panicum, Papaver, Parthenium, Pennisetum, Petunia, Phalaris, Phleum, Pinus, Poa, Poinsettia, Populus, Rauwolfia, Ricinus, Rosa, Saccharum, Salix, Sanguinaria, Scopolia, Secale, Solanum, Sorghum, Spartina, Spinacea, Tanacetum, Taxus, Theobroma, Triticosecale, Triticum, Uniola, Veratrum, Vinca, Vitis и Zea.
Подходящие виды могут включать Panicum spp., Sorghum spp., Miscanthus spp., Saccharum spp., Erianthus spp., Populus spp., Andropogon gerardii (бородач), Pennisetum purpureum (слоновая трава), Phalaris arundinacea (двукисточник тростниковидный), Cynodon dactylon (свинорой пальчатый), Festuca arundinacea (овсяница тростниковая), Spartina pectinata (спартина гребешковая), Medicago sativa (люцерна), Arundo donax (арундо тростниковый), Secale cereale (рожь), Salix spp. (ива), Eucalyptus spp.(эвкалипт), Triticosecale (тритикале), бамбук, Helianthus annuus (подсолнечник), Carthamus tinctorius (сафлор), Jatropha curcas (ятрофа), Ricinus communis (клещевина), Elaeis guineensis (масличная пальма), Linum usitatissimum (лен), Brassica juncea, Beta vulgaris (сахарная свекла), Manihot esculenta (маниок), Lycopersicon esculentum (томат), Lactuca sativa (латук), Musyclise alca (банан), Solanum tuberosum (картофель), Brassica oleracea (брокколи, цветная капуста, брюссельская капуста), Camellia sinensis (чай), Fragaria ananassa (земляника), Theobroma cacao (какао), Coffe ycliseca (кофе), Vitis vinifera (виноград), Ananas comosus (ананас), Capsicum annum (горький и сладкий перец), Allium сера (лук), Cucumis melo (дыня), Cucumis sativus (огурец), Cucurbita maxima (тыква гигантская), Cucurbita moschata (тыква мускатная), Spinacea oleracea (шпинат), Citrullus lanatus (арбуз), Abelmoschus esculentus (бамия), Solanum melongena (баклажан), Rosa spp. (роза), Dianthus caryophyllus (гвоздика), Petunia spp. (петуния), Poinsettiapulcherrima (пуансеттия), Lupinus albus (люпин), Uniola paniculata (овес), полевица (Agrostis spp.), Populus tremuloides (тополь осинообразный), Pinus spp. (сосна), Abies spp.(пихта), Acer spp. (клен), Hordeum vulgare (ячмень), Poa pratensis (мятлик), Lolium spp. (плевел) и Phleum pratense (тимофеевка), Panicum virgatum (просо), Sorghu8lyclise8lor (сорго, суданская трава), Miscanthus giganteus (мискантус), Saccharum sp.(сахарный тростник), Populus balsamifera (тополь), Zea mays (кукуруза), Glycine max (соя), Brassica napus (канола), Triticum aestivum (пшеница), Gossypium hirsutum (хлопок), Oryza sativa (рис), Helianthus annuus (подсолнечник), Medicago sativa (люцерна), Beta vulgaris (сахарная свекла) или Pennisetum glaucum (просо жемчужное).
Различные варианты осуществления направлены на мутантный табак, не встречающийся в природе табак или трансгенные растения табака, модифицированные для модулирования уровней экспрессии гена, в результате чего получают растение или клетку растения, например, растение табака или клетку растения, в которых уровень экспрессии полипептида модулируют в тканях растения, представляющего интерес, по сравнению с контрольным растением. Раскрытые композиции и способы можно применять для любого вида рода Nicotiana, в том числе N. rustica и N. tabacum (например, LA В21, LN KY171, TI 1406, Basma, Galpao, Perique, Beinhart 1000-1 и Petico). Другие виды включают N. acaulis, N. acuminata, N. africana, N. alata, N. ameghinoi, N. amplexicaulis, N. arentsii, N. attenuata, N. azambujae, N. benavidesii, N. benthamiana, N. bigelovii, N. bonariensis, N. cavicola, N. clevelandii, N. cordifolia, N. corymbosa, N. debneyi, N. excelsior, N. forgetiana, N. fragrans, N. glauca, N. glutinosa, N. goodspeedii, N. gossei, N. hybrid, N. ingulba, N. kawakamii, N. knightiana, N. langsdorffii, N. linearis, N. longiflora, N. maritima, N. megalosiphon, N. miersii, N. noctiflora, N. nudicaulis, N. obtusifolia, N. occidentalis, N. occidentalis subsp.hesperis, N. otophora, N. paniculata, N. pauciflora, N. petunioides, N. plumbaginifolia, N. quadrivalvis, N. raimondii, N. repanda, N. rosulata, N. rosulata subsp.ingulba, N. rotundifolia, N. setchellii, N. simulans, N. solanifolia, N. spegazzinii, N. stocktonii, N. suaveolens, N. sylvestris, N. thyrsiflora, N. tomentosa, N. tomentosiformis, N. trigonophylla, N. umbratica, N. undulata, N. velutina, N. wigandioides u N. x sanderae.
Использование сортов табака и элитных сортов табака также рассматривается в данном документе. Трансгенное, не встречающееся в природе или мутантное растение, следовательно, может быть разновидностью табака или элитным сортом табака, который содержит один или более трансгенов или одну или более генетических мутаций или их комбинацию. Генетическая мутация(мутации) (например, один или более полиморфизмов) могут представлять собой мутации, которые не существуют в природе в отдельной разновидности табака или сорте табака (например, элитном сорте табака), или может представлять собой генетическую мутацию(мутации), которая(которые) существует(существуют) в природе при условии, что мутация не существует в природе в отдельной разновидности табака или сорте табака (например, в элитном сорте табака).
Особенно применимые разновидности Nicotiana tabacum включают табак типа Burley, темного типа, типа дымовой сушки и восточного типа. Неограничивающими примерами разновидностей или сортов являются: BD 64, СС 101, СС 200, СС 27, СС 301, СС 400, СС 500, СС 600, СС 700, СС 800, СС 900, Coker 176, Coker 319, Coker 371 Gold, Coker 48, CD 263, DF911, DT 538 LC Galpao tobacco, GL 26H, GL 350, GL 600, GL 737, GL 939, GL 973, HB 04P, HB 04P LC, HB3307PLC, гибрид 403LC, гибрид 404LC, гибрид 501 LC, К 149, К 326, К 346, К 358, К394, К 399, К 730, KDH 959, КТ 200, KT204LC, KY10, KY14, KY 160, KY 17, KY 171, KY 907, KY907LC, KY14xL8 LC, Little Crittenden, McNair 373, McNair 944, msKY 14xL8, Narrow Leaf Madole, Narrow Leaf Madole LC, NBH 98, N-126, N-777LC, N-7371LC, NC 100, NC 102, NC 2000, NC 291, NC 297, NC 299, NC 3, NC 4, NC 5, NC 6, NC7, NC 606, NC 71, NC 72, NC 810, NC BH 129, NC 2002, Neal Smith Madole, OXFORD 207, PD 7302 LC, PD 7309 LC, PD 7312 LC, табак 'Perique', PVH03, PVH09, PVH19, PVH50, PVH51, R 610, R 630, R 7-11, R 7-12, RG 17, RG 81, RG H51, RGH 4, RGH 51, RS 1410, Speight 168, Speight 172, Speight 179, Speight 210, Speight 220, Speight 225, Speight 227, Speight 234, Speight G-28, Speight G-70, Speight H-6, Speight H20, Speight NF3, TI 1406, TI 1269, TN 86, TN86LC, TN 90, TN 97, TN97LC, TN D94, TN D950, TR (Tom Rosson) Madole, VA 309, VA359, AA 37-1, B13P, Xanthi (Mitchell-Мог), Bel-W3, 79-615, Samsun Holmes NN, KTRDC номер 2 гибрид 49, Burley 21, KY8959, KY9, MD 609, PG01, PG04, PO1, PO2, РО3, RG11, RG 8, VA509, AS44, Banket A1, Basma Drama B84/31, Basma I Zichna ZP4/B, Basma Xanthi BX 2A, Batek, Besuki Jember, С104, Coker 347, Criollo Misionero, Delcrest, Djebel 81, DVH 405, Galpao Comum, HB04P, Hicks Broadleaf, Kabakulak Elassona, Kutsage E1, LA BU 21, NC 2326, NC 297, PVH 2110, Red Russian, Samsun, Saplak, Simmaba, Talgar 28, Wislica, Yayaldag, Prilep HC-72, Prilep P23, Prilep PB 156/1, Prilep P12-2/1, Yaka JK-48, Yaka JB 125/3, TI-1068, KDH-960, TI-1070, TW136, Basma, TKF 4028, L8, TKF 2002, GR141, Basma xanthi, GR149, GR153, Petit Havana. Также предполагаются подразновидности вышеуказанного с низким уровнем превращения никотина в норникотин, даже если они специально не указаны в данном документе.
Варианты осуществления также направлены на композиции и способы получения мутантных растений, не встречающихся в природе растений, гибридных растений и трансгенных растений, которые были модифицированы для модулирования экспрессии или активности полинуклеотида(полинуклеотидов), описанного(описанных) в данном документе (или любой их комбинации, как описано в данном документе). Преимущественно, полученные мутантные растения, не встречающиеся в природе растения, гибридные растения или трансгенные растения могут быть подобными или практически такими же по общему внешнему виду по сравнению с контрольными растениями. Различные фенотипические характеристики, такие как степень зрелости, количество листьев на растении, высоту стебля, угол врастания листьев, размер листа (ширина и длина), расстояние междоузлия и соотношение листовая пластина-главная жилка можно оценить путем полевых наблюдений.
Один аспект относится к семенам мутантного растения, не встречающегося в природе растения, гибридного растения или трансгенного растения, описанного в данном документе. Предпочтительно, семена представляют собой семена табака. Следующий аспект относится к пыльце или семяпочке мутантного растения, не встречающегося в природе растения, гибридного растения или трансгенного растения, описанного в данном документе. Кроме того, предусмотрено мутантное растение, не встречающееся в природе растение, гибридное растение или трансгенное растение, описанное в данном документе, которое дополнительно содержит нуклеиновую кислоту, обеспечивающую мужскую стерильность.
Также предусмотрена тканевая культура регенерируемых клеток мутантного растения, не встречающегося в природе растения, гибридного растения или трансгенного растения или его части, как описано в данном документе, при этом из культуры регенерируются растения, способные экспрессировать все морфологические и физиологические родительские характеристики. Регенерируемые клетки включают без ограничения клетки из листьев, пыльцы, зародышей, семядолей, гипокотилей, корней, кончиков корней, пыльников, цветков и их части, семяпочек, побегов, стеблей, черешков, сердцевины и семенных коробочек или каллюса или протопластов, полученных из них.
Еще один дополнительный аспект относится к сушеному растительному материалу, такому как сушеный лист или сушеный табак, полученному или получаемому из мутантного, не встречающегося в природе или трансгенного растения или клетки, где экспрессия одного или более полинуклеотидов, описанных в данном документе, или активность белка, кодируемого ими, снижена и где снижено превращение никотина в норникотин, что приводит в результате к снижению уровней NNN.
Предпочтительно внешний вид указанного растения (например, листа) является практически таким же, как у контрольного растения. Предпочтительно растение представляет собой растение табака.
Варианты осуществления также направлены на композиции и способы получения мутантных, не встречающихся в природе или трансгенных растений или растительных клеток, которые были модифицированы для модулирования экспрессии или активности одного или более полинуклеотидов или полипептидов, описанных в данном документе, которые могут в результате дать растения или части растения (например, листья, такие как зеленые листья или сушеные листья, или табак) или клетки растения с модулированными уровнями норникотина и/или по меньшей мере NNN.
Мутантные, не встречающиеся в природе или трансгенные растения, полученные в соответствии со способами, описанными в данном документе, по внешнему виду могут быть подобными контрольным растениям или практически такими же. В одном варианте осуществления вес листьев у мутантного, не встречающегося в природе или трансгенного растения является практически таким же, как у контрольного растения. В одном варианте осуществления количество листьев у мутантного, не встречающегося в природе или трансгенного растения является практически таким же, как у контрольного растения. В одном варианте осуществления вес листьев и количество листьев у мутантного, не встречающегося в природе или трансгенного растения является практически таким же, как у контрольного растения. В одном варианте осуществления высота стебля у мутантных, не встречающихся в природе или трансгенных растений является практически такой же, как у контрольных растений через, например, один, два или три или более месяцев после пересадки в поле или через 10, 20, 30 или 36 или более дней после обрезания верхушек. Например, высота стебля у мутантных, не встречающихся в природе или трансгенных растений не меньше, чем высота стебля у контрольных растений. В другом варианте осуществления содержание хлорофилла у мутантных, не встречающихся в природе или трансгенных растений является практически таким же, как у контрольных растений. В другом варианте осуществления высота стебля у мутантных, не встречающихся в природе или трансгенных растений является практически такой же, как у контрольных растений, и содержание хлорофилла у мутантных, не встречающихся в природе или трансгенных растений является практически таким же, как у контрольных растений. В других вариантах осуществления размер или форма или количество или окраска листьев у мутантных, не встречающихся в природе или трансгенных растений является практически такой же, как у контрольных растений. Предпочтительно растение представляет собой растение табака.
В другом аспекте предложен способ модулирования (например, снижение) количества норникотина и/или NNN по меньшей мере в части растения (например, в листьях, таких как сушеные листья, или в табаке), предусматривающий стадии: (i) модулирования (например, снижения) экспрессии или активности одного или более полипептидов, описанных в данном документе (или любой их комбинации, как описано в данном документе), где предпочтительно полипептид(полипептиды) кодируется(кодируются) соответствующей полинуклеотидной последовательностью, описанной в данном документе; (ii) измерения содержания норникотина и/или NNN по меньшей мере в части (например, в листьях, таких как сушеные листья, или в табаке, или в дыме) мутантного, не встречающегося в природе или трансгенного растения, полученного на стадии (i); и (iii) идентификации мутантного, не встречающегося в природе или трансгенного растения, в котором содержание норникотина и/или NNN было модулировано (например, снижено) по сравнению с контрольным растением. Предпочтительно внешний вид указанного мутантного, не встречающегося в природе или трансгенного растения является практически таким же, как у контрольного растения. Предпочтительно растение представляет собой растение табака.
В другом аспекте предложен способ модулирования (например, снижения) количества норникотина и/или NNN по меньшей мере в части сушеного растительного материала, такого как сушеный лист, предусматривающий стадии: (i) модулирования (например, снижение) экспрессии или активности одного или более полипептидов (или любой их комбинации, описанной в данном документе), где предпочтительно полипептид(полипептиды) кодируется(кодируются) соответствующей полинуклеотидной последовательностью, описанной в данном документе; (ii) сбора растительного материала, такого как один или более листьев, и сушки в течение определенного периода времени; (iii) измерения содержания норникотина и/или NNN по меньшей мере в части сушеного растительного материала, полученного на стадии (ii); и (iv) идентификации сушеного растительного материала, в котором содержание норникотина и/или NNN было модулировано (например, снижено) по сравнению с контрольным растением.
Повышение уровня экспрессии по сравнению с контролем может составлять от приблизительно 5% до приблизительно 100%, или повышение может составлять по меньшей мере 10%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или 100% или больше, как например, 200% или 300% или больше, которое включает в себя повышение транскрипционной активности или уровня экспрессии полинуклеотида или уровня экспрессии полипептида или их комбинации.
Повышение активности по сравнению с контролем может составлять от приблизительно 5% до приблизительно 100%, или повышение может составлять по меньшей мере 10%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или 100% или больше, как например, 200% или 300% или больше.
Снижение уровня экспрессии по сравнению с контролем может составлять от приблизительно 5% до приблизительно 100%, или снижение может составлять по меньшей мере 10%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или 100%, которое включает в себя снижение транскрипционной активности или уровня экспрессии полинуклеотида или уровня экспрессии полипептида или их комбинации.
Снижение активности по сравнению с контролем может составлять от приблизительно 5% до приблизительно 100%, или снижение может составлять по меньшей мере 10%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или 100%.
Полинуклеотиды и рекомбинантные конструкции, описанные в данном документе, можно использовать для модулирования экспрессии ферментов, описанных в данном документе, в видах растений, представляющих интерес, предпочтительно в табаке.
Ряд способов на основе полинуклеотидов можно использовать для повышения уровня экспрессии генов в растениях и клетках растений. В качестве примера, можно получать конструкцию, вектор или вектор экспрессии, совместимые с подлежащем трансформированию растением, которое содержит представляющий интерес ген вместе с расположенным выше промотором, способным к сверхэкспрессии гена в растении и клетке растения. Иллюстративные промоторы описаны в данном документе. После трансформации и при росте в подходящих условиях промотор может управлять экспрессией с целью модулирования (например, снижения) уровней данного фермента в растении или в конкретной его ткани. В одном иллюстративном варианте осуществления создают вектор, несущий один или более полинуклеотидов, описанных в данном документе (или любую их комбинацию, как описано в данном документе), для сверхэкспрессии гена в растении или клетке растения. Вектор несет подходящий промотор, такой как промотор 35S вируса мозаики цветной капусты CaMV, выше по цепи трансгена, управляющего его конститутивной экспрессией во всех тканях растения. Вектор также несет ген устойчивости к антибиотику с целью обеспечения возможности отбора трансформированных каллюсов и клеточных линий.
Различные варианты осуществления, таким образом, направлены на способы модулирования (например, снижения) уровня экспрессии одного или более полинуклеотидов, описанных в данном документе (или любую их комбинацию, как описано в данном документе), путем интеграции множества копий полинуклеотида в геном растения, предусматривающие: трансформацию клетки растения-хозяина вектором экспрессии, который содержит промотор, функционально связанный с одним или более полинуклеотидами, описанными в данном документе. Полипептид, кодируемый рекомбинантным полинуклеотидом, может быть нативным полипептидом, или может быть гетерологичным по отношению к клетке.
Растение табака, несущее мутантный аллель одного или более полинуклеотидов, описанных в данном документе (или любую их комбинацию, как описано в данном документе) можно использовать в программе селекции растений для создания применимых линий, разновидностей и гибридов. В частности, мутантный аллель интрогрессируют в коммерчески важные разновидности, описанные выше. Таким образом, предложены способы селекции растений, которые предусматривают скрещивание мутантного растения, не встречающегося в природе растения или трансгенного растения, как описано в данном документе, с растением, содержащим отличающиеся генетические особенности. Способ может дополнительно предусматривать скрещивание потомства растения с другим растением и, необязательно, повторное скрещивание до тех пор, пока не будет получено потомство с желаемыми генетическими признаками или генетическим фоном. Одной из целей, для которой подходят такие способы селекции, является введение желаемого генетического признака в другие разновидности, селекционные линии, гибриды или сорта, особенно те, которые представляют коммерческий интерес. Другой целью является облегчение накопления генетических модификаций различных генов в отдельных разновидностях, линиях, гибридах или сортах растений. Предполагаются внутривидовые, а также межвидовые скрещивания. Растения потомки, которые возникают в результате таких скрещиваний, также названные селекционными линиями, являются примерами не встречающихся в природе растений по настоящему изобретению.
В одном варианте осуществления предложен способ получения не встречающегося в природе растения табака, предусматривающий: (а) скрещивание мутантного или трансгенного растения табака со вторым растением табака с получением семян-потомков табака; (b) выращивание семян-потомков табака в условиях роста растений с получением не встречающегося в природе растения табака. Способ может дополнительно включать: (с) скрещивание предыдущего поколения не встречающегося в природе растения табака с самим собою или с другим растением табака с получением семян-потомков табака; (d) выращивание семян-потомков табака из стадии (с) в условиях роста растений с получением дополнительных не встречающихся в природе растений табака; и (е) повторение стадий скрещивания и выращивания (с) и (d) много раз с созданием дополнительных поколений не встречающихся в природе растений табака. Способ может необязательно предусматривать перед стадией (а) стадию получения родительского растения, которое содержит охарактеризованные генетические особенности и которое не идентично мутантному или трансгенному растению. В некоторых вариантах осуществления, в зависимости от программы селекции, стадии скрещивания и выращивания повторяют от 0 до 2 раз, от 0 до 3 раз, от 0 до 4 раз, 0 до 5 раз, от 0 до 6 раз, от 0 до 7 раз, от 0 до 8 раз, от 0 до 9 раз или от 0 до 10 раз для создания поколения не встречающихся в природе растений табака. Обратное скрещивание является примером такого способа, в котором потомков скрещивают с одним из его родителей или с другим растением, генетически подобным его родителю, для получения потомка-растения в следующем поколении, которое имеет генетические особенности, более близкие к одному из родителей. Методики селекции растений, в частности селекции растений табака, хорошо известны и могут быть использованы в способах по настоящему изобретению. В настоящем изобретении дополнительно предложены не встречающиеся в природе растения табака, полученные с помощью этих способов. Определенные варианты осуществления исключают стадию селекции растения.
В некоторых вариантах осуществления способов, описанных в данном документе, линии, полученные в результате селекции и скрининга вариантных генов, оценивают в поле с использованием стандартных полевых процедур. Включены контрольные генотипы, в том числе исходных не подвергнутых мутагенезу родителей, и места посадки растений расположены в поле согласно рандомизированному полноблочному плану или согласно другому соответствующему планированию поля. Для табака используют стандартные агрономические методики, например, табак собирают, взвешивают и отбирают образцы для химического и другого общепринятого тестирования до и во время сушки. Статистический анализ данных выполняют для подтверждения сходства выбранных линий с родительской линией. Цитогенетические анализы выбранных растений необязательно выполняют для подтверждения взаимосвязей набора хромосом и конъюгации хромосом.
ДНК-фингерпринтинг, однонуклеотидный полиморфизм, микросателлитные маркеры или подобные технологии можно использовать в программе селекции с выбором с помощью маркера (MAS) для переноса или разведения мутантных аллелей гена в других растениях табака, как описано в данном документе. Например, селекционер может создать расщепляющиеся популяции при гибридизации генотипа, содержащего мутантный аллель, с требуемым с точки зрения агрономии генотипом. Растения из F2 или обратно скрещенных поколений можно подвергнуть скринингу с использованием маркера, полученного из геномной последовательности или ее фрагмента, с использованием одной из методик, перечисленных в данном документе. Растения, идентифицированные как обладающие мутантным аллелем, можно подвергнуть обратному скрещиванию или самоопылению для создания второй популяции, подлежащей скринингу. В зависимости от предполагаемого способа наследования или используемой технологии MAS может быть необходимым самоопыление для выбранных растений перед каждым циклом обратного скрещивания для облегчения обнаружения необходимых отдельных растений. Обратное скрещивание или другую процедуру селекции можно повторять до тех пор, пока необходимый фенотип рекуррентного родителя не восстановится.
Согласно настоящему раскрытию в программе селекции успешные скрещивания дают растения F1, которые являются фертильными. Выбранные растения F1 можно скрещивать с одним из родителей, и растения первого поколения обратного скрещивания можно самоопылить с получением популяции, которую снова подвергают скринингу на экспрессию вариантного гена (например, нулевой версии гена). Процесс обратного скрещивания, самоопыления и скрининга повторяют, например, по меньшей мере 4 раза до тех пор, пока при окончательном скрининге не получат растение, которое является фертильным и в достаточной степени подобным рекуррентному родителю. Это растение, при необходимости, самоопыляют и затем потомство снова подвергают скринингу, чтобы подтвердить, что растение демонстрирует экспрессию вариантного гена. В некоторых вариантах осуществления популяцию растений в поколении F2 подвергают скринингу на наличие экспрессии вариантного гена, например, растение, которое не экспрессирует полипептид из-за отсутствия гена, идентифицируют согласно стандартным способам, например, с помощью методики ПЦР с использованием праймеров, созданных на основе информации о последовательности нуклеотидов для полинуклеотида(полинуклеотидов), описанного в данном документе (или любой их комбинации, описанной в данном документе).
Разновидности гибридного табака можно получить путем предотвращения самоопыления женских родительских растений (то есть, семена родителей) первой разновидности, позволяя пыльце с мужских родительских растений второй разновидности оплодотворить женские родительские растения, и позволяя образовать гибридные F1 семена на женских растениях. Самоопыление женских растений можно предотвратить путем кастрации цветков на ранней стадии развития цветка. В качестве альтернативы, образование пыльцы на женских родительских растениях можно предотвратить, используя какую-либо форму мужской стерильности. Например, мужскую стерильность можно получить с помощью цитоплазматической мужской стерильности (CMS) или трансгенной мужской стерильности, где трансген продавляет микроспорогенез и/или образование пыльцы, или вызывает самонесовместимость. Женские родительские растения, содержащие CMS, являются особенно применимы. В вариантах осуществления, в которых женские родительские растения имеют CMS, пыльцу собирают с мужских фертильных растений и наносят вручную на рыльца женских родительских растений с CMS и собирают полученные семена F1.
Разновидности и линии, описанные в данном документе, можно использовать для образования простых гибридов F1 табака. В таких вариантах осуществления растения родительских разновидностей можно выращивать практически в виде однородно соединенных популяциях для облегчения естественного перекрестного опыления с мужских родительских растений на женские родительские растения. Семена F1, образовавшиеся на женских родительских растениях, выборочно собирают с помощью обычных средств. Можно также вырастить две разновидности родительского растения в массе и собрать смесь гибридных F1 семян, образовавшихся на женской особи, и семян, образовавшихся на мужской особи в результате самоопыления. В качестве альтернативы, можно осуществить трехлинейное скрещивание, где простой гибрид F1 используют в качестве женской особи и скрещивают с другой мужской особью. В качестве другой альтернативы, можно создать гибриды двойного скрещивания, где потомство F1 двух разных простых гибридов скрещивают само с собой.
Популяцию мутантных, не встречающихся в природе или трансгенных растений можно подвергнуть скринингу или отбору в отношении тех представителей популяции, которые имеют требуемый признак или фенотип. Например, популяцию потомства линии с одной трансформацией можно подвергнуть скринингу на те растения, которые имеют требуемый уровень экспрессии или активности полипептида(полипептидов), кодируемого(кодируемых) с ее помощью. Физические и биохимические способы можно использовать для выявления уровней экспрессии или активности. Они включают анализ по Саузерну или ПЦР-амплификацию для обнаружения полинуклеотида; нозерн-блоттинг, защиту от РНКазы S1, удлинение праймера, или ПЦР-амплификацию в реальном времени для обнаружения РНК-транскриптов; ферментативные анализы для обнаружения ферментативной или рибозимной активности полипептидов и полинуклеотидов; и гель-электрофорез белков, вестерн-блоттинг, иммунопреципитацию и иммуноферментные анализы для обнаружения полипептидов. Другие методики, такие как гибридизация in situ, ферментативное окрашивание и иммуноокрашивание и ферментативный анализ также можно использовать для обнаружения присутствия, или экспрессии, или активности полипептидов или полинуклеотидов.
В данном документе описаны мутантные, не встречающиеся в природе или трансгенные растительные клетки и растения, содержащие один или более рекомбинантных полинуклеотидов, одну или более полинуклеотидных конструкций, одну или более двухнитевых РНК, один или более конъюгатов или один или более векторов/векторов экспрессии.
Без ограничения, растения, описанные в данном документе, можно модифицировать для других целей либо до того, либо после того, как экспрессия или активность была модулирована в соответствии с настоящим изобретением. Одна или более следующих генетических модификаций могут присутствовать в мутантных, не встречающихся в природе или трансгенных растениях. В одном варианте осуществления один или более генов, которые принимают участие в превращении промежуточных азотистых продуктов метаболизма, модифицируют с получением в результате растений или частей растений (таких как листья или табак), которые в высушенном состоянии дают более низкие уровни по меньшей мере одного специфичного для табака нитрозамина, чем контрольные растения или их части. Неограничивающие примеры генов, которые можно модифицировать, включают, как описано в данном документе, гены, кодирующие никотин-деметилазу, такие как CYP82E4, CYP82E5 и CYP82E10, которые принимают участие в превращении никотина в норникотин и описаны в WO 2006091194, WO 2008070274, WO 2009064771 и PCT/US2011/021088, и как подробно описано в данном документе. В другом варианте осуществления один или более генов, которые принимают участие в поглощении тяжелых металлов или транспорте тяжелых металлов, модифицируют с получением в результате растений или частей растений (таких как листья), имеющих более низкое содержание тяжелых металлов, чем у контрольных растений или их частей без модификации(модификаций). Неограничивающие примеры включают гены семейства белков, ассоциированных с множественной лекарственной устойчивостью, семейства посредников катионной диффузии (CDF), семейства Zrt-, Irt-подобных белков (ZIP), семейства катионообменников (САХ), семейства транспортеров меди (СОРТ), семейства АТФаз тяжелых металлов Р-типа (например, НМА, как описано в WO 2009074325), семейства гомологов белков, ассоциированных с естественной устойчивостью макрофагов (NRAMP) и семейства транспортеров АТФ-связывающей кассеты (ABC) (например, MRP, описанных в WO 2012/028309, которые участвуют в транспорте тяжелых металлов, таких как кадмий. Термин тяжелый металл, используемый в данном документе, включает в себя переходные металлы. Примеры других модификаций включают выносливость в отношении гербицидов, например, глифосат является активным ингредиентом многих гербицидов широкого спектра действия. Устойчивые к глифосату трансгенные растения были разработаны путем переноса гена aroA (глифосат EPSP-синтетаза из Salmonella typhimurium и E.coli). Устойчивые к сульфонилмочевине растения были получены путем трансформации мутантного гена ALS (ацетолактатсинтетаза) из Arabidopsis. Белок ОВ фотосистемы II из мутантного Amaranthus hybridus был перенесен в растения с получением атразин-устойчивых трансгенных растений; и бромоксинил-устойчивые трансгенные растения были получены путем встраивания гена bxn бактерии Klebsiella pneumoniae. Другие примеры модификаций приводят в результате к получению растений, которые устойчивы к насекомым. Токсин Bacillus thuringiensis (Bt) может обеспечить эффективный путьзадержки появления Bt-устойчивых вредителей, как недавно показанона брокколи, где пирамидальные cry1Ac и cry1C гены Bt контролировали капустную моль, устойчивую к любому отдельному белку, и существенно задерживалиразвитие устойчивых насекомых. Другая иллюстративная модификация приводит к получению растений, которые устойчивы к заболеваниям, вызванным патогенами (например, вирусами, бактериями, грибами). Были сконструированы растения, экспрессирующие ген Ха21 (устойчивость к бактериальному некрозу) с растениями, экспрессирующими одновременно ген слияния Bt и ген хитиназы (устойчивость к желтому стеблевому пилильщику и устойчивость к шипоуске злаковой). Другая иллюстративная модификация приводит к измененной репродуктивной способности, такой как мужская стерильность. Другая иллюстративная модификация приводит в результате к получению растений, которые выносливы в отношении абиотического стресса (например, засухе, изменению температуры, засоленности), и выносливые трансгенные растения были получены путем переноса фермента ацилглицерол-фосфат-ацилтрансферазы из Arabidopsis; генов, кодирующих маннитол-дегидрогеназу и сорбитол-дегидрогеназу, которые принимают участие в синтезе маннита и сорбита, улучшают устойчивость к засухе. Другие иллюстративные модификации могут приводить в результате к получению растений с улучшенным накоплением белков и масел, растений с повышенной эффективностью фотосинтеза, растений с длительным сроком хранения, растений с повышенным содержанием углеводов и растений, устойчивых к грибам; растений, кодирующих фермент, участвующий в биосинтезе алкалоидов. Также рассматриваются трансгенные растения, в которых экспрессия S-аденозил-L-метионин (SAM) и/или цистатионин-гамма-синтазы (CGS) была модулирована.
Один или более таких признаков можно интрогрессировать в мутантные, не встречающиеся в природе или трансгенные растения табака из другого сорта табака или можно непосредственно трансформировать в него. Интрогрессию признака(признаков) в мутантные, не встречающиеся в природе или трансгенные растения табака по настоящему изобретению можно достичь при помощи любого способа селекции растений, известным в данной области, например, селекцией по потомству, обратным скрещиванием, двойной гаплоидной селекцией и им подобными (см. Wernsman, Е.A, and Rufty, R.С. 1987. Chapter Seventeen. Tobacco. Pages 669-698 в: Cultivar Development. Crop Species. Fehr (ed.), MacMillan Publishing Co, Inc., New York, N.Y. 761 pp.). Методики на основе молекулярной биологии, описанные выше, в частности, RFLP и микросателлитные маркеры, можно использовать при таком обратном скрещивании для выявления потомства с высокой степенью генетической идентичности с рекуррентным родителем. Это позволяет ускорить производство разновидностей табака, имеющих по меньшей мере 90%, предпочтительно по меньшей мере 95%, более предпочтительно по меньшей мере 99% генетической идентичности с рекуррентным родителем, еще более предпочтительно, генетически идентичных с рекуррентным родителем и дополнительно содержащих признак(и), интрогрессированный от донорского родителя. Такое определение генетической идентичности можно проводить на основе молекулярных маркеров, известных в данной области.
Последнее поколение обратного скрещивания можно подвергнуть самоопылению с получением потомков чистого разведения для подлежащей переносу нуклеиновой кислоты(нуклеиновых кислот). Полученные растения обычно имеют практически все морфологические и физиологические характеристики мутантных, не встречающихся в природе или трансгенных растений табака по настоящему изобретению в дополнение к перенесенному(перенесенным) признаку(признакам) (например, один или более признаков одного гена). Точный протокол обратного скрещивания будет зависеть от изменяемого признака для определения соответствующего протокола испытаний. Хотя способы обратного скрещивания упрощаются, если переносимый признак представляет собой доминантный аллель, рецессивный аллель также можно переносить. В данном случае может быть необходимым применить тест потомства с определением успешности переноса желаемого признака.
Различные варианты осуществления предусматривают мутантные растения, не встречающиеся в природе растения или трансгенные растения, а также биомассу, в которой уровень экспрессии полинуклеотида (или любой их комбинации, как описано в данном документе) модулируют для модулирования в них содержания норникотина или по меньшей мере NNN.
Части таких растений, в частности растений табака, и более конкретно, листовую пластинку и среднюю жилку растений табака, можно включить в изготовление или использовать в изготовлении различных продуктов потребления, включая без ограничения материалы, образующие аэрозоль, устройства, образующие аэрозоль, курительные изделия, изделия для курения, бездымные продукты и табачные изделия. Примеры материалов, образующих аэрозоль, включают без ограничения табачные композиции, табачные изделия, табачный экстракт, резаный табак, резаный наполнитель, сушеный табак, взорванный табак, гомогенизированный табак, восстановленный табак и трубочный табак. Курительные изделия и изделия для курения являются, как правило, устройствами, образующими аэрозоль. Примеры курительных изделий и изделий для курения включают без ограничения сигареты, сигариллы и сигары. Примеры бездымных продуктов включают в себя жевательный табак и нюхательный табак. В определенных устройствах, образующих аэрозоль, вместо сгорания, табачная композиция или другой материал, образующий аэрозоль, нагревают с помощью одного или более электрических нагревательных элементов с получением аэрозоля. В другом типе нагреваемого устройства, образующего аэрозоль, аэрозоль получают путем перемещения тепла от горючего топливного элемента или источника тепла к физически отделенному материалу, образующему аэрозоль, который может быть расположен внутри, вокруг или ниже по потоку относительно источника тепла. Бездымные табачные изделия и различные табак-содержащие материалы, образующие аэрозоль, могут содержать табак в любом виде, в том числе в виде высушенных частиц, кусков, гранул, порошков или суспензии, нанесенной на, смешанной с, окруженной или иным образом комбинированной с другими ингредиентами в любом формате, таком как хлопья, пленки, таблетки, пены или шарики. Используемый в данном документе термин «дым» используют для описания типа аэрозоля, который получен с помощью курительных изделий, таких как сигареты, или при сжигании материала, образующего аэрозоль.
В одном варианте осуществления предложен сушеный растительный материал из мутантных, трансгенных и не встречающихся в природе растений табака, описанных в данном документе. Способы сушки зеленых табачных листьев известны специалистам в данной области и включают без ограничения воздушную сушку, огневую сушку, дымовую сушку и вяление. Способ сушки зеленых табачных листьев зависит от типа собранного табака. Например, табак Virginia дымовой сушки (светлый), как правило, высушивают дымовой сушкой, Burley и некоторые темные разновидности обычно высушивают воздушной сушкой, а трубочный табак, жевательный табак и нюхательный табак обычно высушивают огневой сушкой.
В другом варианте осуществления описаны табачные изделия, в том числе табаксодержащие материалы, образующие аэрозоль, содержащие растительный материал, такой как листья, предпочтительно, сушеные листья, из мутантных растений табака, трансгенных растений табака или не встречающихся в природе растений табака, описанных в данном документе. Табачные изделия, описанные в данном документе, могут быть смешанными табачными изделиями, которые могут дополнительно содержать немодифицированный табак.
Количество норникотина в этих изделиях для курения и бездымных продуктах и их аэрозолях может быть по меньшей мере на приблизительно 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% и 100% ниже, например, на приблизительно 200% или 300% ниже, по сравнению с продуктами потребления, полученными из немутантных, не встречающихся в природе или нетрансгенных аналогов.
Количество NNN в этих изделиях для курения и бездымных продуктах и их аэрозолях может быть по меньшей мере на приблизительно 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% и 100% ниже, например, на приблизительно 200% или 300% ниже, по сравнению с продуктами потребления, полученными из немутантных, не встречающихся в природе или нетрансгенных аналогов.
Количество никотина в этих изделиях для курения и бездымных продуктах и их аэрозолях может быть по меньшей мере на приблизительно 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% и 100% ниже, например, на приблизительно 200% или 300% ниже, по сравнению с продуктами потребления, полученными из немутантных, не встречающихся в природе или нетрансгенных аналогов. Количество никотина в этих изделиях для курения и бездымных продуктах и их аэрозолях может быть приблизительно таким же по сравнению с продуктами потребления, полученными из немутантных, не встречающихся в природе или нетрансгенных аналогов.
Количество общих TSNA в этих изделиях для курения и бездымных продуктах и их аэрозолях может быть по меньшей мере на приблизительно 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% и 100% ниже, например, на приблизительно 200% или 300% ниже, по сравнению с продуктами потребления, полученными из немутантных, невстречающихся в природе или нетрансгенных аналогов.
Мутантные, не встречающиеся в природе или трансгенные растения могут иметь другие виды использования, например, в сельском хозяйстве. Например, мутантные, не встречающиеся в природе или трансгенные растения, описанные в данном документе, можно использовать для изготовления корма для животных и продуктов питания для человека.
В настоящем изобретении также предложены способы получения семян, предусматривающие выращивание мутантного растения, не встречающегося в природе растения или трансгенного растения, описанных в данном документе, и сбор семян культивируемых растений. Семена растений, описанных в данном документе, можно кондиционировать и упаковать в упаковочный материал с помощью средств, известных в данной области, с получением промышленного изделия. Упаковочный материал, такой как бумага или ткань, хорошо известен в данной области. Упаковка семян может иметь этикетку, например, метку или этикетку, прикрепленную к упаковочному материалу, этикетку, напечатанную на упаковке, которая описывает происхождение содержащихся в ней семян.
Композиции, способы и наборы для генотипирования растений для идентификации, отбора или селекции могут включать в себя средства для обнаружения присутствия полинуклеотида (или любой их комбинации, как описано в данном документе) в образце полинуклеотида. Соответственно, описана композиция, содержащая один или более праймеров для специфической амплификации по меньшей мере части одного или более полинуклеотидов и, необязательно, один или более зондов и, необязательно, один или более реагентов для проведения амплификации или обнаружения.
Соответственно, раскрыты ген-специфичные олигонуклеотидные праймеры или зонды, содержащие приблизительно 10 или более смежных нуклеотидов, соответствующих полинуклеотиду(полинуклеотидам), описанному в данном документе. Указанные праймеры или зонды могут содержать или состоять из приблизительно 15, 20, 25, 30, 40, 45 или 50 или больше смежных нуклеотидов, которые гибридизируются (например, специфически гибридизируются) с полинуклеотидом(полинуклеотидами), описанным в данном документе. В некоторых вариантах осуществления праймеры или зонды могут содержать или состоять из приблизительно 10-50 смежных нуклеотидов, приблизительно 10-40 смежных нуклеотидов, приблизительно 10-30 смежных нуклеотидов или приблизительно 15-30 смежных нуклеотидов, которые можно использовать в зависимых от последовательности способах идентификации гена (например, Саузерн-гибридизация) или выделения (например, гибридизация in situ бактериальных колоний или бляшек бактериофага) или обнаружения гена (например, в виде одного или более амплифицирующих праймеров при амплификации и обнаружении нуклеиновой кислоты). Один или более специфических праймеров или зондов можно спроектировать и использовать для амплификации и обнаружения части или всего полинуклеотида(полинуклеотидов). В качестве конкретного примера, два праймера можно использовать в протоколе полимеразной цепной реакции для амплификации фрагмента нуклеиновой кислоты, кодирующего нуклеиновую кислоту, такую как ДНК или РНК. Полимеразную цепную реакцию можно также проводить с использованием одного праймера, который получен из последовательности нуклеиновой кислоты, и второго праймера, который гибридизируется с последовательностью выше по цепи или ниже по цепи последовательности нуклеиновой кислоты, такой как последовательность промотора, 3'-конец предшественника иРНК или последовательность, полученная из вектора. Примеры термических и изотермических методик, применимых для амплификации полинуклеотидов in vitro, хорошо известны в данной области. Образец может происходить или его можно получить из растения, клетки растения или растительного материала или табачного изделия, изготовленного из растения, клетки растения или растительного материала, как описано в данном документе.
В следующем аспекте предложен способ обнаружения полинуклеотида(полинуклеотидов), описанного в данном документе (или любой их комбинации, описанной в данном документе) в образце, предусматривающий стадии: (а) получения образца, содержащего, или предположительно содержащего полинуклеотид; (b) приведения указанного образца в контакт с одним или более праймерами или одним или более зондами для специфического выявления по меньшей мере части полинуклеотида(полинуклеотидов) и (с) обнаружения присутствия продукта амплификации, где присутствие продукта амплификации свидетельствует о присутствии полинуклеотида(полинуклеотидов) в образце. В следующем аспекте также предложено использование одного или более праймеров или зондов для специфического обнаружения по меньшей мере части полинуклеотида(полинуклеотидов). Также предложены наборы для обнаружения по меньшей мере части полинуклеотида(полинуклеотидов), которые содержат один или более праймеров или зондов для специфического обнаружения по меньшей мере части полинуклеотида(полинуклеотидов). Набор может содержать реагенты для амплификации полинуклеотида, например реагенты для ПНР или реагенты для технологии обнаружения с использованием гибридизационного зонда, такой как Саузерн-блоттинг, нозерн-блоттинг, гибридизация in situ или микрочип. Набор может содержать реагенты для технологии обнаружения связывания антител, такой как вестерн-блоттинг, ELISA, SELDI-масс-спектрометрия или тест-полоски. Набор может содержать реагенты для секвенирования ДНК. Набор может содержать реагенты и инструкции для определения содержания по меньшей мере NNN, и/или содержания никотина, и/или общего содержания TSNA, и/или содержания норникотина. Предпочтительно набор содержит реагенты и инструкции для определения содержания по меньшей мере NNN, и/или содержания никотина, и/или общего содержания TSNA, и/или содержания норникотина в растительном материале, сушеном растительном материале или в сушеных листьях.
В некоторых вариантах осуществления набор может содержать инструкции для одного или более описанных способов. Описанные наборы могут быть применимы для определения генетической идентичности, филогенетических исследований, генотипирования, гаплотипирования, анализа родословной или селекции растений, в частности, с количественной оценкой кодоминантных признаков.
В настоящем изобретении также предложен способ генотипирования растения, клетки растения или растительного материала, содержащих полинуклеотид, описанный в данном документе. Генотипирование обеспечивает средства различения гомологов пары хромосом и может быть использовано для различения сегрегантов в популяции растений. Молекулярные способы с использованием маркеров можно применять для филогенетических исследований, характеризующих генетические связи между разновидностями сельскохозяйственных культур, выявления гибридов или соматических гибридов, локализации хромосомных сегментов, влияющих на моногенные признаки, клонирования на основе генетических карт и изучения количественного наследования. В определенном способе генотипирования может использоваться любое количество аналитических методик с молекулярным маркером, включая полиморфизмы длины амлифицированного фрагмента (AFLP). AFLP являются продуктом аллельных различий между фрагментами амплификации, вызванных изменчивостью нуклеотидной последовательности. Таким образом, настоящее изобретение дополнительно предлагает средства для отслеживания сегрегации одного или более генов или нуклеиновых кислот, а также хромосомных последовательностей, генетически связанных с этими генами или нуклеиновыми кислотами, с использованием таких методик, как анализ AFLP.
В одном варианте осуществления также предложен сушеный растительный материал из мутантных, трансгенных и не встречающихся в природе растений, описанных в данном документе. Например, способы сушки табачных листьев известны специалистам в данной области и включают без ограничения воздушную сушку, огневую сушку, дымовую сушку и вяление. Способ сушки зеленых табачных листьев зависит от типа собранного табака. Например, табак Virginia дымовой сушки (светлый), как правило, высушивают дымовой сушкой, Burley и некоторые темные разновидности обычно высушивают воздушной сушкой, а трубочный табак, жевательный табак и нюхательный табак обычно высушивают огневой сушкой.
В другом варианте осуществления описаны табачные изделия, в том числе табачные изделия, содержащие растительный материал, такой как листья, соответственно, сушеный растительный материал, такой как сушеные листья, из мутантных, трансгенных и не встречающихся в природе растений, описанных в данном документе, или которые получены по способам, описанным в данном документе. Табачные изделия, описанные в данном документе, могут дополнительно содержать немодифицированный табак.
В другом варианте осуществления описаны табачные изделия, содержащие растительный материал, предпочтительно листья, такие как сушеные листья, из мутантных, трансгенных и не встречающихся в природе растений, описанных в данном документе. Например, растительный материал можно добавить к внутренней или наружной части табачного изделия, так что при сжигании высвобождается желаемый аромат. Табачное изделие в соответствии с этим вариантом осуществления может даже представлять собой немодифицированный табак или модифицированный табак. Табачное изделие в соответствии с этим вариантом осуществления может быть получено из мутантного, трансгенного или не встречающегося в природе растения, которое имеет модификации в одном или более генах, отличающихся от генов, раскрытых в данном документе.
Настоящее изобретение дополнительно описано в Примерах ниже, которые представлены для более подробного описания настоящего изобретения. Эти примеры, в которых изложен предпочтительный режим, предполагаемый в настоящее время для осуществления настоящего изобретения, предназначены для иллюстрации, а не для ограничения настоящего изобретения.
ПРИМЕРЫ
Пример 1
Анализ уровня экспрессии NND3
Для определения функции NND3 и его роли в превращении никотина анализировали экспрессию NND3. С этой целью различные ткани выращенного в теплице N. tabacum разн. TN90 собирали и анализировали с помощью количественной ПЦР.
Выделение РНК осуществляли с использованием набора RNeasy Mini kit (Qiagen) в соответствии с инструкциями производителя. Образцы РНК разбавляли водой с получением 1 мкг РНК в конечном объеме 10 мкл. Затем осуществляли расщепление ДНКазой с использованием ДНКазы без РНКаз RQ1 (Promega). Реакцию с ДНКазой останавливали с использованием стоп-реагента ДНКазы RQ1 (Promega). Сразу после этого осуществляли реакцию с обратной транскриптазой (RT) для превращения РНК в комплементарную ДНК (кДНК). Для реакций с RT использовали обратную транскриптазу M-MLV, РНКазу Н Minus, Point Mutant (Promega) в комбинации с праймерами олиго(dT)15.
Количественную ПЦР в реальном времени осуществляли с использованием Stratagene Мх3005Р и соответствующего программного обеспечения. Для каждой мишени конструировали различные пары праймеров в соответствии с рекомендациями руководства по эксплуатации для Мх3005Р. Пары праймеров тестировали в отношении образования димеров праймеров и их характеристик в ходе qPCR. Их эффективность тестировали с использованием стандартного раствора с пятикратным разведением кДНК. ПЦР-продукты секвенировали с целью проверки специфичности амплификации праймеров с их целевой последовательностью. Поскольку различные гены CYP82E близки по последовательностям, конструирование праймера является сложным, и выбранные праймеры не всегда демонстрируют оптимальную эффективность.
Различия в эффективности означают, что экспериментальные значения qPCR являются ген-специфическими и не отображают абсолютное значение экспрессии. Следовательно, сравнение значений экспрессии применимо для каждого гена между различными тканями, но не между генами. Используемые пары праймеров и их эффективность перечислены в таблице 1. Использовали смесь ABsolute Blue QPCR SYBR Green low ROX Mix (Thermo Scientific) с концентрацией праймеров 300 нМ. В ходе qPCR использовали температуру денатурации 95°С, вначале в течение 15 минут, а затем в течение 15 секунд для каждого цикла, 15 секунд при 60°С для отжига и 25 секунд при 72°С для элонгации для 50 циклов. Каждый образец анализировали в трех повторах. Кроме того, использовали три биологические повтора. Экспрессию гена actin9 (ген «домашнего хозяйства») использовали для всех образцов в качестве нормализующей.
Результаты показаны на фигуре 1, и они подтверждают экспрессию CYP82E5 и CYP82E10 в зеленых листьях. Эти гены также экспрессируются на высоком уровне во всех других тканях, которые тестировали. Они демонстрируют схожий или очень схожий паттерн экспрессии. В то время как каждый из CYP82E4 и NND3 характеризуется экспрессией в цветках и корнях, NND3 не экспрессируется на выявляемом уровне в листьях, тогда как CYP82E4 характеризуется экспрессией исключительно в стареющих листьях. Для установления специфичности праймеров продукты ПЦР очищали и секвенировали. Низкий уровень сигнала наблюдали для NND3 в корнях, содержащих продукты NND3 и CYP82E4, тогда как продукты из материала цветков содержали только NND3.
Пример 2
Подтверждение того, что NND3 кодирует функциональную никотинде-метилазу
Хотя предсказанная последовательность белка представляет высокий уровень гомологии с известными деметилазами, такими как CYP82E4, CYP82E5 и CYP82E10, ее функции не могут быть определены гомологией, поскольку было показано, что в семействе цитохрома Р450 отличие в несколько аминокислот является достаточным для изменения или уменьшения субстратной специфичности.
Функции NND3 подтверждали по сверхэкспрессии в табаке. Для этой цели конструкцию для сверхэкспрессии разрабатывали с последовательностью, кодирующей NND3 (SEQ ID NO: 1), для конститутивной экспрессии под контролем промотора MMV в растениях burley со сверхнизким уровнем превращения в качестве фона, не содержащих гены функциональных CYP82E4, CYP82E5 и CYP82E10.
Создавали двадцать независимых трансгенных линий. Первичные трансформанты (Т0) переносили на грунт, и листья зрелых растений анализировали в отношении экспрессии NND3 с использованием праймеров NND3_F6 и NND3_R7 (фигура 2А), а также в отношении уровней никотина и норникотина (фигура 2В). Анализировали пять контрольных линий, для которых столбец и погрешность представляют собой среднее значение и стандартное отклонение.
Анализ экспрессии проводили в трех технических повторах. Столбцы и погрешности обозначают среднее значение и стандартное отклонение в повторах (рассчитанные с помощью программного обеспечения MxPro software, Stratagene).
Данные по экспрессии подтверждают, что NND3 не экспрессируются в зеленых листьях TN90, поскольку сигнал не может быть выявлен. Уровни экспрессии NND3, измеренные в различных растениях Т0, следовательно, были выражены относительно растения NND3#3, которое было выбрано случайным образом. У различных растений наблюдали значимую вариацию в экспрессии. Такой результат ожидали при изучении экспрессии трансгена в популяции Т0, поскольку каждое растение является результатом независимого события трансформации. Как результат, уровни экспрессии могут значительно варьировать от растения к растению, в зависимости как от количества копий трансгена, так и надлежащей вставки трансгена.
Некоторые образцы листа анализировали в рамках одного измерения в отношении никотина и норникотина.
Содержание никотина и норникотина в образцах анализировали с помощью HILIC-UPLC-UV/MS. Норникотин количественно определяли с помощью MS-детектирования (поз. ESI; режим MRM; внутренний стандарт: норникотин-d4); для никотина использовали UV-детектирование при 260 нм. Уровень превращения рассчитывали как [норникотин]/([норникотин]+[никотин])×100.
Шесть трансгенных линий, которые показали наивысший уровень экспрессии NND3 (№10, №3, №16, №15, №17 и №20), характеризовались повышенным уровнем превращения никотина. Уровень превращения никотина составлял 0,5% в растениях TN90 сур82е4/сур82е5/сур82е10, и повышался до четырехкратного в линиях MMV:NND3 с высокой экспрессией. Стабильно низкий уровень превращения, неотличимый от уровня в контрольном растении, наблюдали в растениях, демонстрирующих наиболее низкий уровень экспрессии трансгена.
Эти данные четко демонстрируют, что новый идентифицированный ген NND3 кодирует функциональную никотин-N-деметилазу.
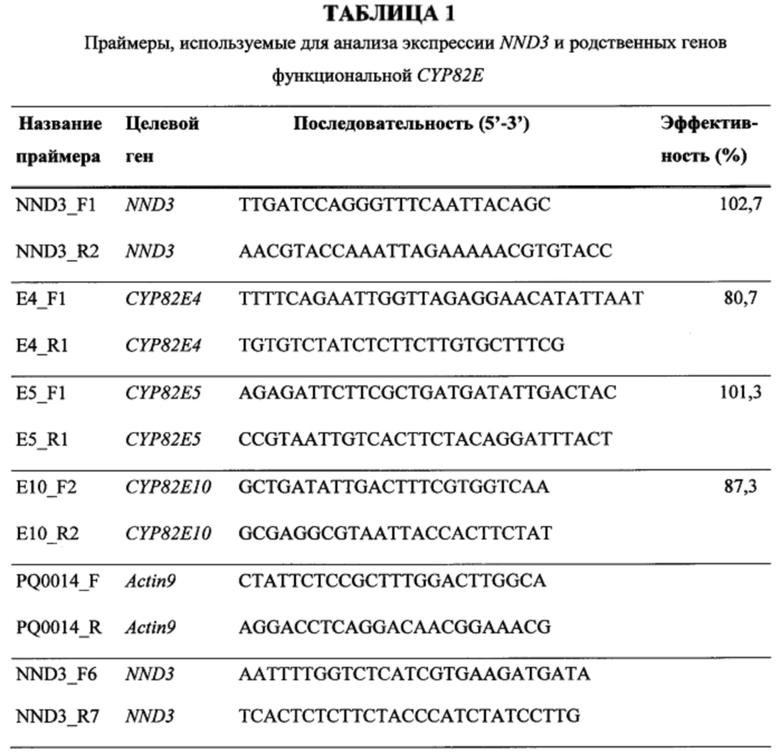
Пример 3
Подтверждение того, что сайленсинг NND3 приводит к снижению превращения никотина
Разработанная конструкция для сайленсинга предназначена для конститутивной экспрессии под контролем промотора MMV в растениях burley со сверхнизким уровнем превращения в качестве фона, не содержащих гены функциональных CYP82E4, CYP82E5 и CYP82E10. В случае конструкции для сайленсинга использовали последовательность из 100 п. о. в прямом и обратном направлении, отделенную интронной последовательностью (SEQ ID NO: 4.) Результаты указывают на то, что сайленсинг NND3 в цветках приводит к снижению превращения никотина, демонстрируя, что фермент NND3 является не только функциональным, но также оказывает влияние на превращение никотина в растении.
Пример 4
Относительные уровни экспрессии NND3 в листьях N. tabacum разн. Stella в разные моменты времени сушки
Анализировали относительные уровни экспрессии NND3 и родственных генов функциональной CYP82E в листьях N. tabacum разн. Stella в разные моменты времени сушки. Образцы отбирали в виде «зеленых» листьев (верхнее положение стебля) и в виде «зрелых» листьев (нижнее положение стебля) во время сбора. Листья переносили в амбар для воздушной сушки и образец отбирали вначале сушки («0 ч.»), и затем снова через 12 часов («12 ч»), 24 часа («24 ч») и 48 часов («48 ч»). Образцы отбирали из пулов нескольких листьев. Два пула анализировали в виде биологических повторов, повтора 1 (фигура 3а) и 2 (фигура 3b). Результаты показаны на фиг. 3. Столбцы показывают среднее ± SD трех технических повторов. Уровни экспрессии различных генов CYP82E можно рассматривать только независимо, но не путем прямого сравнения, что обусловлено различными показателями эффективности ПЦР. CYP82E5 и CYP82E10 экспрессировались в одинаковой степени во всех образцах листьев. Экспрессия CYP82E4 активировалась в стареющих листьях и повышалась в условиях сушки. NND3 не экспрессировалась в листьях во всех условиях анализа.
Любая публикация, цитированная или описанная в данном документе, предоставляет соответствующую информацию, раскрытую до даты подачи настоящей заявки. Заявления, сделанные в данном документе, не должны быть истолкованы как допускающие, что авторы настоящего изобретения не имеют право датировать более ранним числом такие раскрытия. Все публикации, упомянутые в вышеприведенном описании, включены в данный документ с помощью ссылки. Различные модификации и варианты настоящего изобретения будут очевидны специалистам в данной области без отступления от объема и сути настоящего изобретения. Несмотря на то, что настоящее изобретение было описано в связи с конкретными предпочтительными вариантами осуществления, следует понимать, что настоящее изобретение, как заявлено, не должно быть неправомерно ограничено такими конкретными вариантами осуществления. В действительности различные модификации описанных способов осуществления изобретения, которые очевидны специалистам в клеточной, молекулярной биологии и биологии растений или в смежных областях, предназначены находиться в пределах объема прилагаемой формулы изобретения.
ПОСЛЕДОВАТЕЛЬНОСТИ
SEQ ID NO: 1 (полинуклеотидная последовательность гена TN90 NND3-T N. tabacum. Интрон показан строчными буквами, кодирующая последовательность подчеркнута. Старт- и стоп-кодоны выделены серым цветом)

SEQ ID NO: 2 (полинуклеотид, кодирующий последовательность NND3, использовали в конструкции для сверхэкспрессии под контролем промотора MMV)

SEQ ID NO: 3 (полипептидная последовательность белка NND3 N. tabacum TN90)

SEQ ID NO: 4 (полинуклеотидная последовательность конструкции для РНК-интерференции с использованием уникальной последовательности NND3 из 100 п. о. в прямом и обратном направлении, отделенной интронной последовательностью, обнаруженной в гене IPMS2. Интронная последовательность указана строчными буквами)

SEQ ID NO: 5 (последовательность белка никотин-деметилазы CYP82E4)



SEQ ID NO: 6 (последовательность белка P38L, варианта никотин-деметилазы CYP82E4)


SEQ ID NO: 7 (последовательность белка D171N, варианта никотин-деметилазы CYP82E4)



SEQ ID NO: 8 (последовательность белка E201K, варианта никотин-деметилазы CYP82E4)


SEQ ID NO: 9 (последовательность белка R169Q, варианта никотин-деметилазы CYP82E4)


SEQ ID NO: 10 (последовательность белка G459R, варианта никотин-деметилазы CYP82E4)


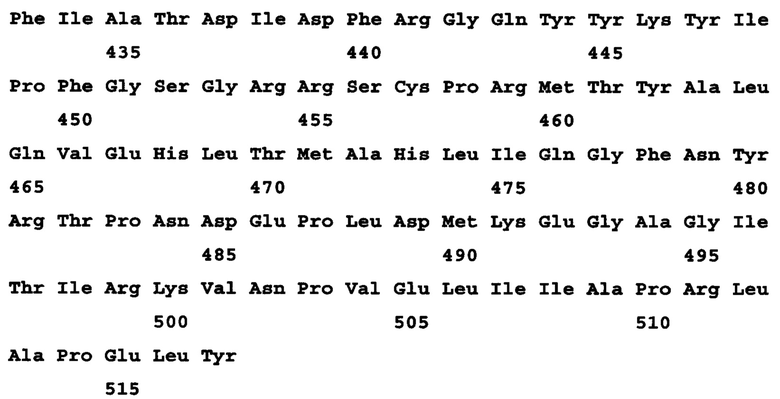
SEQ ID NO: 11 (последовательность белка T427I, варианта никотин-деметилазы CYP82E4)


SEQ ID NO: 12 (последовательность белка V376M, варианта никотин-деметилазы CYP82E4)


SEQ ID NO: 13 (последовательность белка W329Stop, варианта никотин-деметилазы CYP82E4)


SEQ ID NO: 14 (последовательность белка K364N, варианта никотин-деметилазы CYP82E4)



SEQ ID NO: 15 (последовательность белка P382S, варианта никотин-деметилазы CYP82E4)

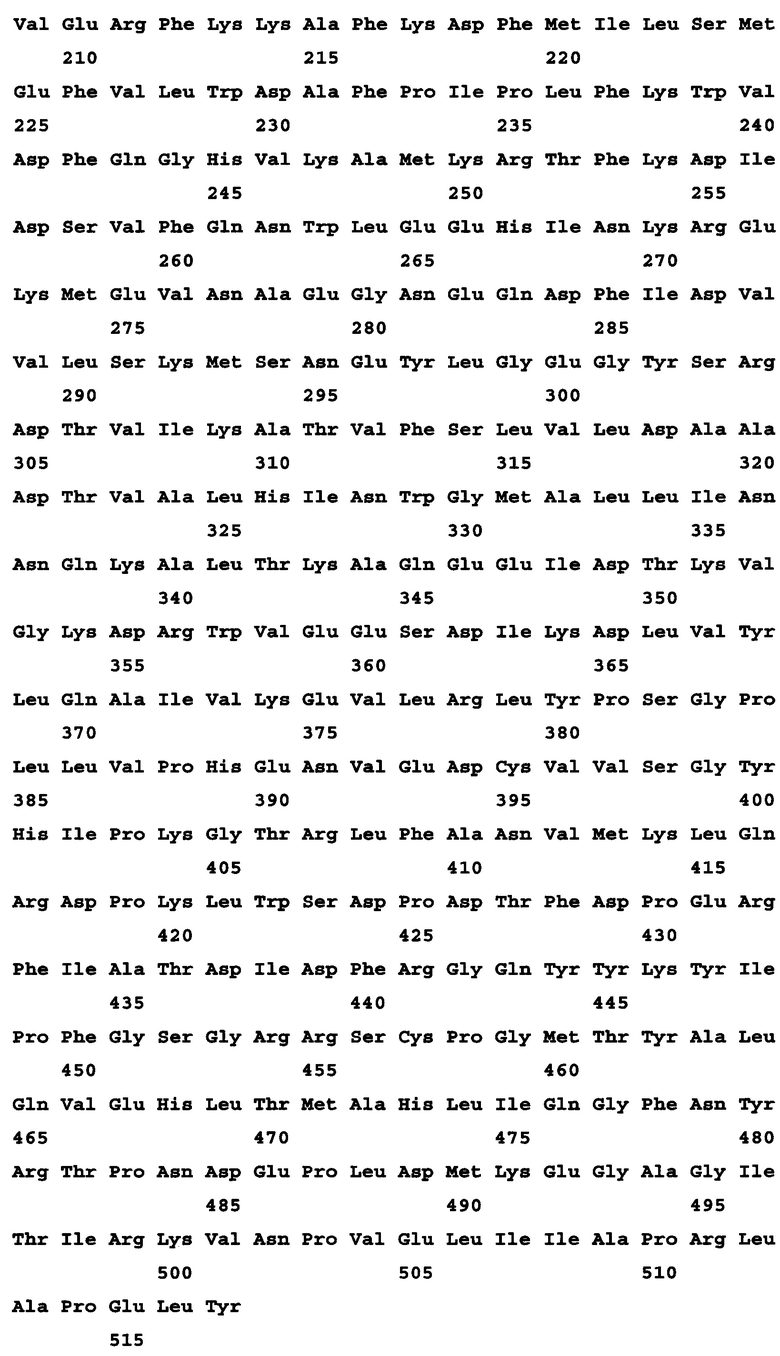
SEQ ID NO: 16 (последовательность белка P458S, варианта никотин-деметилазы CYP82E4)


SEQ ID NO: 17 (последовательность белка никотин-деметилазы CYP82E5)



SEQ ID NO: 18 (последовательность белка P72L, варианта никотин-деметилазы CYP82E5)


SEQ ID NO: 19 (последовательность белка L143F, варианта никотин-деметилазы CYP82E5)
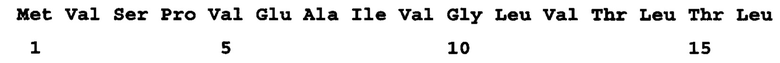


SEQ ID NO: 20 (последовательность белка S174L, варианта никотин-деметилазы CYP82E5)



SEQ ID NO: 21 (последовательность белка M224I, варианта никотин-деметилазы CYP82E5)

SEQ ID NO: 22 (последовательность белка P235S, варианта никотин-деметилазы CYP82E5)



SEQ ID NO: 23 (последовательность белка A410V, варианта никотин-деметилазы CYP82E5)


SEQ ID NO: 24 (последовательность белка W422Stop, варианта никотин-деметилазы CYP82E5)


SEQ ID NO: 25 (последовательность белка P449L, варианта никотин-деметилазы CYP82E5)


SEQ ID NO: 26 (последовательность белка никотин-деметилазы CYP82E10)


SEQ ID NO: 27 (последовательность белка L148F, варианта никотин-деметилазы CYP82E10)



SEQ ID NO: 28 (последовательность белка G172R, варианта никотин-деметилазы CYP82E10)


SEQ ID NO: 29 (последовательность белка A344T, варианта никотин-деметилазы CYP82E10)


SEQ ID NO: 30 (последовательность белка A410T, варианта никотин-деметилазы CYP82E10)



SEQ ID NO: 31 (последовательность белка R417H, варианта никотин-деметилазы CYP82E10)

SEQ ID NO: 32 (последовательность белка P419S, варианта никотин-деметилазы CYP82E10)



SEQ ID NO: 33 (последовательность белка G79S, варианта никотин-деметилазы CYP82E10)


SEQ ID NO: 34 (последовательность белка P107S, варианта никотин-деметилазы CYP82E10)


SEQ ID NO: 35 (последовательность белка P382S, варианта никотин-деметилазы CYP82E10)



--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Филип Моррис Продактс С.А.
<120> Снижение превращения никотина в норникотин в растениях
<130> P4362PC00
<150> EP 14167598.3
<151> 2014-05-08
<150> EP 14001645.2
<151> 2014-05-09
<160> 47
<170> PatentIn версии 3.3
<210> 1
<211> 2088
<212> ДНК
<213> Nicotiana tabacum
<400> 1
atggtttttc ccatagaagc cattgtagga ctagtaacct tcacatttct cttctacttc 60
ctatggacaa aaaaatctca aaaaccttca aaacccttac caccgaaaat ccccggagga 120
tggccggtaa ttggccatct tttccacttc aatgacgacg gcaacgaccg tccattagct 180
cgaaaactcg gagacttagc tgacaaatac ggccccgttt tcacttttcg gctaggcctt 240
ccccttgtgt tagttgtaag cagttacgaa gctataaaag actgtttctc tacaaatgat 300
gccattttct ctaatcgtcc agcttttctt tacggcgaat accttggcta caataatgcc 360
atgctatttt tggcaaatta cggaccttac tggcgaaaaa atcgtaaatt agttattcag 420
gaagttctct cagctagtcg tctcaaaaaa ttcaaacacg tgagattcgc cagaattcaa 480
acgagcatta agaatttata cactcgaatt gatagaaatt cgagtacgat aaatttaact 540
gattggttag aagaattgaa ttttggtctc atcgtgaaga tgatagctgg gaaaaattat 600
gaatccggta aaggagatga acaagtggag agatttaaga aagcgtttaa ggattttatg 660
attatatcaa tggagtttgt gttatgggat gcatttccaa ttccattatt taaatgggtg 720
gattttcaag ggcatgttaa ggctatgaaa aggacattta aggatataga ttctgttttt 780
cagaattggt tagaggaaca tattaacaaa agagaaaaaa tggaggttaa tgcagaaggg 840
aatgaacaag atttcattga tgtggtgctt tcaaaaatga gtaatgaata tcttggtgaa 900
ggttactctc gtgatactgt cataaaagca acagtttttg taagttcatc tgtcactccc 960
gaattctgct tgaatgcaga caccgagttg cctttttatt agactatcta aatattaagg 1020
atgattatat atagcaaaaa tatagtagga tttctcgggc tttgggatag aagaatattc 1080
atcattatat aacttttgat ggtaaaagat gagatctaac ctcttataat tgcccaacca 1140
cgttgatata tagaacaaaa cctttttact cccattgagc ataacgaaaa tgaaagcaaa 1200
gggacttctt ctctttttta ggaaaaaaat ctttgattgc ttgttgaata tacattcatg 1260
tttttctttt tctatttcta ataataatgg tgcttgaatc aggttgcgtg cctcgtgact 1320
tttgagaaaa aaaaacaaat tcattagtat aatgaggtgt gcatacttga caactactat 1380
actaactaga acaaggttcg gcagataatg acgctaacct acttttatat tgaattatca 1440
tttgtattta actgtattct attttgtcca cagagtttgg tcttggatgc tgcggacaca 1500
gttgctcttc acataaattg gggtatggca ttactgatca acaatcaaaa tgccttgaag 1560
aaagcacaag aagagataga cacaaaagtt ggcaaggata gatgggtaga agagagtgat 1620
attaaggatt tggtgtacct ccaagctatt gttaaagaag tgttacgatt atatccaccg 1680
ggacctttgt tagtaccaca tgaaaatata gaggattgtg ttgttagtgg atattacatt 1740
tctaaaggga ctagactatt cgcaaatgtt atgaaactgc agcgcgatcc taaactctgg 1800
ccaaatcctg ataatttcga tccagagaga tttgtcgctg caggtattga ctttcgtggt 1860
cagcattatg agtatatccc gtttggttct ggaagacgat cttgtccggg gatgacttat 1920
gcattgcaag tggaacactt aacaatggca catttgatcc agggtttcaa ttacagcact 1980
ccaaatgacg agcccttgga tatgaaggaa ggtgcaggta taactatacg taaggtaaat 2040
cccgtggaag tgataattat gcctcgcctg gcacctgagc tttattaa 2088
<210> 2
<211> 1554
<212> ДНК
<213> Nicotiana tabacum
<400> 2
atggtttttc ccatagaagc cattgtagga ctagtaacct tcacatttct cttctacttc 60
ctatggacaa aaaaatctca aaaaccttca aaacccttac caccgaaaat ccccggagga 120
tggccggtaa ttggccatct tttccacttc aatgacgacg gcaacgaccg tccattagct 180
cgaaaactcg gagacttagc tgacaaatac ggccccgttt tcacttttcg gctaggcctt 240
ccccttgtgt tagttgtaag cagttacgaa gctataaaag actgtttctc tacaaatgat 300
gccattttct ctaatcgtcc agcttttctt tacggcgaat accttggcta caataatgcc 360
atgctatttt tggcaaatta cggaccttac tggcgaaaaa atcgtaaatt agttattcag 420
gaagttctct cagctagtcg tctcaaaaaa ttcaaacacg tgagattcgc cagaattcaa 480
acgagcatta agaatttata cactcgaatt gatagaaatt cgagtacgat aaatttaact 540
gattggttag aagaattgaa ttttggtctc atcgtgaaga tgatagctgg gaaaaattat 600
gaatccggta aaggagatga acaagtggag agatttaaga aagcgtttaa ggattttatg 660
attatatcaa tggagtttgt gttatgggat gcatttccaa ttccattatt taaatgggtg 720
gattttcaag ggcatgttaa ggctatgaaa aggacattta aggatataga ttctgttttt 780
cagaattggt tagaggaaca tattaacaaa agagaaaaaa tggaggttaa tgcagaaggg 840
aatgaacaag atttcattga tgtggtgctt tcaaaaatga gtaatgaata tcttggtgaa 900
ggttactctc gtgatactgt cataaaagca acagttttta gtttggtctt ggatgctgcg 960
gacacagttg ctcttcacat aaattggggt atggcattac tgatcaacaa tcaaaatgcc 1020
ttgaagaaag cacaagaaga gatagacaca aaagttggca aggatagatg ggtagaagag 1080
agtgatatta aggatttggt gtacctccaa gctattgtta aagaagtgtt acgattatat 1140
ccaccgggac ctttgttagt accacatgaa aatatagagg attgtgttgt tagtggatat 1200
tacatttcta aagggactag actattcgca aatgttatga aactgcagcg cgatcctaaa 1260
ctctggccaa atcctgataa tttcgatcca gagagatttg tcgctgcagg tattgacttt 1320
cgtggtcagc attatgagta tatcccgttt ggttctggaa gacgatcttg tccggggatg 1380
acttatgcat tgcaagtgga acacttaaca atggcacatt tgatccaggg tttcaattac 1440
agcactccaa atgacgagcc cttggatatg aaggaaggtg caggtataac tatacgtaag 1500
gtaaatcccg tggaagtgat aattatgcct cgcctggcac ctgagcttta ttaa 1554
<210> 3
<211> 517
<212> БЕЛОК
<213> Nicotiana tabacum
<400> 3
Met Val Phe Pro Ile Glu Ala Ile Val Gly Leu Val Thr Phe Thr Phe
1 5 10 15
Leu Phe Tyr Phe Leu Trp Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
His Phe Asn Asp Asp Gly Asn Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Ile Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Ala Asn Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Lys Lys Phe Lys His Val Arg Phe Ala Arg Ile Gln
145 150 155 160
Thr Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Arg Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Lys Lys Ala Phe Lys Asp Phe Met Ile Ile Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Ile Asn Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Gly Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Ile Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln Asn Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Thr Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Ile Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
Tyr Ile Ser Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Pro Asn Pro Asp Asn Phe Asp Pro Glu Arg
420 425 430
Phe Val Ala Ala Gly Ile Asp Phe Arg Gly Gln His Tyr Glu Tyr Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Val Glu His Leu Thr Met Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Ser Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Ile
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Val Ile Ile Met Pro Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 4
<211> 469
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: полинуклеотидная последовательность для РНК-интерференции с использованием уникальной последовательности NND3 из 100 п.о., отделенной интронной последовательностью, обнаруженной в гене IPMS2
<400> 4
gcgatcctaa actctggcca aatcctgata atttcgatcc agagagattt gtcgctgcag 60
gtattgactt tcgtggtcag cattatgagt atatcccgtt tggtaacctt taatgtttaa 120
ccgttcacat ttctaatatt tacttatttg taacatgtcg tcacgtgtta gtttcattct 180
ttttatgaac caaacatgca tgcaaagata tttttagata tttggacggc gagtgagatt 240
tgaaactagg accgtttgcc tgatacaata ttaaaatatg taaccatttt atgtacaagt 300
ttaaactgtt gatagtagca tattttttac ttttatttaa gtatactata ttccaacagg 360
taagttaaca acgggatata ctcataatgc tgaccacgaa agtcaatacc tgcagcgaca 420
aatctctctg gatcgaaatt atcaggattt ggccagagtt taggatcgc 469
<210> 5
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка никотин-деметилазы CYP82E4
<400> 5
Met Leu Ser Pro Ile Glu Ala Ile Val Gly Leu Val Thr Phe Thr Phe
1 5 10 15
Leu Phe Phe Phe Leu Trp Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
His Phe Asn Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Asp Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Ala Asn Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Phe Lys His Val Arg Phe Ala Arg Ile Gln
145 150 155 160
Ala Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Lys Lys Ala Phe Lys Asp Phe Met Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Ile Asn Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Gly Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Ile Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln Lys Ala Leu Thr Lys Ala Gln Glu Glu Ile Asp Thr Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asp Pro Asp Thr Phe Asp Pro Glu Arg
420 425 430
Phe Ile Ala Thr Asp Ile Asp Phe Arg Gly Gln Tyr Tyr Lys Tyr Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Arg Met Thr Tyr Ala Leu
450 455 460
Gln Val Glu His Leu Thr Met Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Arg Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Ile
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Leu Ile Ile Ala Pro Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 6
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка P38L варианта никотин-деметилазы CYP82E4
<400> 6
Met Leu Ser Pro Ile Glu Ala Ile Val Gly Leu Val Thr Phe Thr Phe
1 5 10 15
Leu Phe Phe Phe Leu Trp Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Leu Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
His Phe Asn Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Asp Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Ala Asn Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Phe Lys His Val Arg Phe Ala Arg Ile Gln
145 150 155 160
Ala Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Lys Lys Ala Phe Lys Asp Phe Met Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Ile Asn Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Gly Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Ile Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln Lys Ala Leu Thr Lys Ala Gln Glu Glu Ile Asp Thr Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asp Pro Asp Thr Phe Asp Pro Glu Arg
420 425 430
Phe Ile Ala Thr Asp Ile Asp Phe Arg Gly Gln Tyr Tyr Lys Tyr Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Val Glu His Leu Thr Met Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Arg Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Ile
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Leu Ile Ile Ala Pro Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 7
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка D171N варианта никотин-деметилазы CYP82E4
<400> 7
Met Leu Ser Pro Ile Glu Ala Ile Val Gly Leu Val Thr Phe Thr Phe
1 5 10 15
Leu Phe Phe Phe Leu Trp Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
His Phe Asn Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Asp Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Ala Asn Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Phe Lys His Val Arg Phe Ala Arg Ile Gln
145 150 155 160
Ala Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asn Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Lys Lys Ala Phe Lys Asp Phe Met Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Ile Asn Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Gly Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Ile Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln Lys Ala Leu Thr Lys Ala Gln Glu Glu Ile Asp Thr Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asp Pro Asp Thr Phe Asp Pro Glu Arg
420 425 430
Phe Ile Ala Thr Asp Ile Asp Phe Arg Gly Gln Tyr Tyr Lys Tyr Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Val Glu His Leu Thr Met Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Arg Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Ile
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Leu Ile Ile Ala Pro Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 8
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка E210K варианта никотин-деметилазы CYP82E4
<400> 8
Met Leu Ser Pro Ile Glu Ala Ile Val Gly Leu Val Thr Phe Thr Phe
1 5 10 15
Leu Phe Phe Phe Leu Trp Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
His Phe Asn Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Asp Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Ala Asn Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Phe Lys His Val Arg Phe Ala Arg Ile Gln
145 150 155 160
Ala Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Lys Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Lys Lys Ala Phe Lys Asp Phe Met Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Ile Asn Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Gly Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Ile Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln Lys Ala Leu Thr Lys Ala Gln Glu Glu Ile Asp Thr Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asp Pro Asp Thr Phe Asp Pro Glu Arg
420 425 430
Phe Ile Ala Thr Asp Ile Asp Phe Arg Gly Gln Tyr Tyr Lys Tyr Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Val Glu His Leu Thr Met Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Arg Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Ile
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Leu Ile Ile Ala Pro Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 9
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка R169Q варианта никотин-деметилазы CYP82E4
<400> 9
Met Leu Ser Pro Ile Glu Ala Ile Val Gly Leu Val Thr Phe Thr Phe
1 5 10 15
Leu Phe Phe Phe Leu Trp Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
His Phe Asn Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Asp Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Ala Asn Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Phe Lys His Val Arg Phe Ala Arg Ile Gln
145 150 155 160
Ala Ser Ile Lys Asn Leu Tyr Thr Gln Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Lys Lys Ala Phe Lys Asp Phe Met Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Ile Asn Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Gly Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Ile Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln Lys Ala Leu Thr Lys Ala Gln Glu Glu Ile Asp Thr Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asp Pro Asp Thr Phe Asp Pro Glu Arg
420 425 430
Phe Ile Ala Thr Asp Ile Asp Phe Arg Gly Gln Tyr Tyr Lys Tyr Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Val Glu His Leu Thr Met Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Arg Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Ile
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Leu Ile Ile Ala Pro Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 10
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка G459R варианта никотин-деметилазы CYP82E4
<400> 10
Met Leu Ser Pro Ile Glu Ala Ile Val Gly Leu Val Thr Phe Thr Phe
1 5 10 15
Leu Phe Phe Phe Leu Trp Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
His Phe Asn Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Asp Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Ala Asn Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Phe Lys His Val Arg Phe Ala Arg Ile Gln
145 150 155 160
Ala Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Lys Lys Ala Phe Lys Asp Phe Met Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Ile Asn Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Gly Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Ile Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln Lys Ala Leu Thr Lys Ala Gln Glu Glu Ile Asp Thr Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asp Pro Asp Thr Phe Asp Pro Glu Arg
420 425 430
Phe Ile Ala Thr Asp Ile Asp Phe Arg Gly Gln Tyr Tyr Lys Tyr Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Arg Met Thr Tyr Ala Leu
450 455 460
Gln Val Glu His Leu Thr Met Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Arg Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Ile
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Leu Ile Ile Ala Pro Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 11
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка T427I варианта никотин-деметилазы CYP82E4
<400> 11
Met Leu Ser Pro Ile Glu Ala Ile Val Gly Leu Val Thr Phe Thr Phe
1 5 10 15
Leu Phe Phe Phe Leu Trp Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
His Phe Asn Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Asp Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Ala Asn Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Phe Lys His Val Arg Phe Ala Arg Ile Gln
145 150 155 160
Ala Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Lys Lys Ala Phe Lys Asp Phe Met Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Ile Asn Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Gly Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Ile Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln Lys Ala Leu Thr Lys Ala Gln Glu Glu Ile Asp Thr Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asp Pro Asp Ile Phe Asp Pro Glu Arg
420 425 430
Phe Ile Ala Thr Asp Ile Asp Phe Arg Gly Gln Tyr Tyr Lys Tyr Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Val Glu His Leu Thr Met Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Arg Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Ile
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Leu Ile Ile Ala Pro Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 12
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка V376M варианта никотин-деметилазы CYP82E4
<400> 12
Met Leu Ser Pro Ile Glu Ala Ile Val Gly Leu Val Thr Phe Thr Phe
1 5 10 15
Leu Phe Phe Phe Leu Trp Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
His Phe Asn Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Asp Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Ala Asn Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Phe Lys His Val Arg Phe Ala Arg Ile Gln
145 150 155 160
Ala Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Lys Lys Ala Phe Lys Asp Phe Met Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Ile Asn Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Gly Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Ile Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln Lys Ala Leu Thr Lys Ala Gln Glu Glu Ile Asp Thr Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Met Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asp Pro Asp Thr Phe Asp Pro Glu Arg
420 425 430
Phe Ile Ala Thr Asp Ile Asp Phe Arg Gly Gln Tyr Tyr Lys Tyr Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Val Glu His Leu Thr Met Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Arg Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Ile
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Leu Ile Ile Ala Pro Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 13
<211> 328
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка W329Stop варианта никотин-деметилазы CYP82E4
<400> 13
Met Leu Ser Pro Ile Glu Ala Ile Val Gly Leu Val Thr Phe Thr Phe
1 5 10 15
Leu Phe Phe Phe Leu Trp Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
His Phe Asn Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Asp Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Ala Asn Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Phe Lys His Val Arg Phe Ala Arg Ile Gln
145 150 155 160
Ala Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Lys Lys Ala Phe Lys Asp Phe Met Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Ile Asn Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Gly Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Ile Asn
325
<210> 14
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка K364N варианта никотин-деметилазы CYP82E4
<400> 14
Met Leu Ser Pro Ile Glu Ala Ile Val Gly Leu Val Thr Phe Thr Phe
1 5 10 15
Leu Phe Phe Phe Leu Trp Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
His Phe Asn Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Asp Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Ala Asn Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Phe Lys His Val Arg Phe Ala Arg Ile Gln
145 150 155 160
Ala Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Lys Lys Ala Phe Lys Asp Phe Met Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Ile Asn Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Gly Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Ile Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln Lys Ala Leu Thr Lys Ala Gln Glu Glu Ile Asp Thr Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Asn Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asp Pro Asp Thr Phe Asp Pro Glu Arg
420 425 430
Phe Ile Ala Thr Asp Ile Asp Phe Arg Gly Gln Tyr Tyr Lys Tyr Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Val Glu His Leu Thr Met Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Arg Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Ile
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Leu Ile Ile Ala Pro Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 15
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка P382S варианта никотин-деметилазы CYP82E4
<400> 15
Met Leu Ser Pro Ile Glu Ala Ile Val Gly Leu Val Thr Phe Thr Phe
1 5 10 15
Leu Phe Phe Phe Leu Trp Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
His Phe Asn Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Asp Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Ala Asn Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Phe Lys His Val Arg Phe Ala Arg Ile Gln
145 150 155 160
Ala Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Lys Lys Ala Phe Lys Asp Phe Met Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Ile Asn Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Gly Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Ile Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln Lys Ala Leu Thr Lys Ala Gln Glu Glu Ile Asp Thr Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Ser Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asp Pro Asp Thr Phe Asp Pro Glu Arg
420 425 430
Phe Ile Ala Thr Asp Ile Asp Phe Arg Gly Gln Tyr Tyr Lys Tyr Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Val Glu His Leu Thr Met Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Arg Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Ile
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Leu Ile Ile Ala Pro Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 16
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка P458S варианта никотин-деметилазы CYP82E4
<400> 16
Met Leu Ser Pro Ile Glu Ala Ile Val Gly Leu Val Thr Phe Thr Phe
1 5 10 15
Leu Phe Phe Phe Leu Trp Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
His Phe Asn Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Asp Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Ala Asn Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Phe Lys His Val Arg Phe Ala Arg Ile Gln
145 150 155 160
Ala Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Lys Lys Ala Phe Lys Asp Phe Met Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Ile Asn Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Gly Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Ile Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln Lys Ala Leu Thr Lys Ala Gln Glu Glu Ile Asp Thr Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asp Pro Asp Thr Phe Asp Pro Glu Arg
420 425 430
Phe Ile Ala Thr Asp Ile Asp Phe Arg Gly Gln Tyr Tyr Lys Tyr Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Ser Gly Met Thr Tyr Ala Leu
450 455 460
Gln Val Glu His Leu Thr Met Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Arg Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Ile
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Leu Ile Ile Ala Pro Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 17
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка никотин-деметилазы CYP82E5
<400> 17
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Leu Trp Pro Lys Lys Phe Gln Ile Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Ser Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Lys Ile Gln
145 150 155 160
Thr Ser Ile Lys Ser Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Gln Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Glu Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Asp Asp Ile Asp Tyr Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Ala Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Val Thr Ile Thr Ala Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 18
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка P72L варианта никотин-деметилазы CYP82E5
<400> 18
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Leu Trp Pro Lys Lys Phe Gln Ile Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Leu Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Ser Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Lys Ile Gln
145 150 155 160
Thr Ser Ile Lys Ser Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Gln Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Glu Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Asp Asp Ile Asp Tyr Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Ala Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Val Thr Ile Thr Ala Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 19
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка L143F варианта никотин-деметилазы CYP82E5
<400> 19
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Leu Trp Pro Lys Lys Phe Gln Ile Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Ser Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Phe Ser
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Lys Ile Gln
145 150 155 160
Thr Ser Ile Lys Ser Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Gln Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Glu Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Asp Asp Ile Asp Tyr Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Ala Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Val Thr Ile Thr Ala Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 20
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка S174L варианта никотин-деметилазы CYP82E5
<400> 20
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Leu Trp Pro Lys Lys Phe Gln Ile Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Ser Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Lys Ile Gln
145 150 155 160
Thr Ser Ile Lys Ser Leu Tyr Thr Arg Ile Asp Gly Asn Leu Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Gln Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Glu Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Asp Asp Ile Asp Tyr Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Ala Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Val Thr Ile Thr Ala Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 21
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка M224I варианта никотин-деметилазы CYP82E5
<400> 21
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Leu Trp Pro Lys Lys Phe Gln Ile Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Ser Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Lys Ile Gln
145 150 155 160
Thr Ser Ile Lys Ser Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Ile
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Gln Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Glu Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Asp Asp Ile Asp Tyr Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Ala Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Val Thr Ile Thr Ala Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 22
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка P235S варианта никотин-деметилазы CYP82E5
<400> 22
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Leu Trp Pro Lys Lys Phe Gln Ile Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Ser Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Lys Ile Gln
145 150 155 160
Thr Ser Ile Lys Ser Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Ser Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Gln Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Glu Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Asp Asp Ile Asp Tyr Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Ala Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Val Thr Ile Thr Ala Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 23
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка A410V варианта никотин-деметилазы CYP82E5
<400> 23
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Leu Trp Pro Lys Lys Phe Gln Ile Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Ser Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Lys Ile Gln
145 150 155 160
Thr Ser Ile Lys Ser Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Gln Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Glu Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Val Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Asp Asp Ile Asp Tyr Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Ala Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Val Thr Ile Thr Ala Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 24
<211> 421
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка W422Stop варианта никотин-деметилазы CYP82E5
<400> 24
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Leu Trp Pro Lys Lys Phe Gln Ile Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Ser Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Lys Ile Gln
145 150 155 160
Thr Ser Ile Lys Ser Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Gln Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Glu Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu
420
<210> 25
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка P449L варианта никотин-деметилазы CYP82E5
<400> 25
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Leu Trp Pro Lys Lys Phe Gln Ile Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Gly Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Val Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Ser Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Ser
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Lys Ile Gln
145 150 155 160
Thr Ser Ile Lys Ser Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Arg Glu
260 265 270
Lys Met Glu Val Asn Ala Gln Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Glu Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Ala Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Asp Asp Ile Asp Tyr Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Leu Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Leu
450 455 460
Gln Ala Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Val Glu Val Thr Ile Thr Ala Arg Leu
500 505 510
Ala Pro Glu Leu Tyr
515
<210> 26
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка никотин-деметилазы CYP82E10
<400> 26
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Ile Arg Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Ser Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Ile Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Cys
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Glu Ile Gln
145 150 155 160
Thr Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Lys Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Thr Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Ala Asp Ile Asp Phe Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Met
450 455 460
Gln Val Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Ile Glu Val Val Ile Thr Pro Arg Leu
500 505 510
Thr Pro Glu Leu Tyr
515
<210> 27
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка L148F варианта никотин-деметилазы CYP82E10
<400> 27
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Ile Arg Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Ser Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Ile Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Cys
130 135 140
Ala Ser Arg Phe Glu Lys Leu Lys His Val Arg Phe Gly Glu Ile Gln
145 150 155 160
Thr Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Lys Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Thr Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Ala Asp Ile Asp Phe Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Met
450 455 460
Gln Val Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Ile Glu Val Val Ile Thr Pro Arg Leu
500 505 510
Thr Pro Glu Leu Tyr
515
<210> 28
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка G172R варианта никотин-деметилазы CYP82E10
<400> 28
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Ile Arg Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Ser Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Ile Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Cys
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Glu Ile Gln
145 150 155 160
Thr Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Arg Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Lys Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Thr Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Ala Asp Ile Asp Phe Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Met
450 455 460
Gln Val Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Ile Glu Val Val Ile Thr Pro Arg Leu
500 505 510
Thr Pro Glu Leu Tyr
515
<210> 29
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка A344T варианта никотин-деметилазы CYP82E10
<400> 29
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Ile Arg Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Ser Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Ile Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Cys
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Glu Ile Gln
145 150 155 160
Thr Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Lys Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Thr Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Thr Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Ala Asp Ile Asp Phe Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Met
450 455 460
Gln Val Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Ile Glu Val Val Ile Thr Pro Arg Leu
500 505 510
Thr Pro Glu Leu Tyr
515
<210> 30
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка A410T варианта никотин-деметилазы CYP82E10
<400> 30
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Ile Arg Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Ser Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Ile Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Cys
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Glu Ile Gln
145 150 155 160
Thr Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Lys Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Thr Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Thr Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Ala Asp Ile Asp Phe Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Met
450 455 460
Gln Val Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Ile Glu Val Val Ile Thr Pro Arg Leu
500 505 510
Thr Pro Glu Leu Tyr
515
<210> 31
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка R417H варианта никотин-деметилазы CYP82E10
<400> 31
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Ile Arg Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Ser Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Ile Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Cys
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Glu Ile Gln
145 150 155 160
Thr Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Lys Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Thr Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
His Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Ala Asp Ile Asp Phe Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Met
450 455 460
Gln Val Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Ile Glu Val Val Ile Thr Pro Arg Leu
500 505 510
Thr Pro Glu Leu Tyr
515
<210> 32
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка P419S варианта никотин-деметилазы CYP82E10
<400> 32
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Ile Arg Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Ser Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Ile Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Cys
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Glu Ile Gln
145 150 155 160
Thr Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Lys Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Thr Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Ser Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Ala Asp Ile Asp Phe Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Met
450 455 460
Gln Val Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Ile Glu Val Val Ile Thr Pro Arg Leu
500 505 510
Thr Pro Glu Leu Tyr
515
<210> 33
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка G79S варианта никотин-деметилазы CYP82E10
<400> 33
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Ile Arg Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Ser Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Ser Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Ile Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Cys
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Glu Ile Gln
145 150 155 160
Thr Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Lys Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Thr Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Ala Asp Ile Asp Phe Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Met
450 455 460
Gln Val Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Ile Glu Val Val Ile Thr Pro Arg Leu
500 505 510
Thr Pro Glu Leu Tyr
515
<210> 34
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка P107S варианта никотин-деметилазы CYP82E10
<400> 34
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Ile Arg Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Ser Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Ile Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Ser Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Cys
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Glu Ile Gln
145 150 155 160
Thr Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Lys Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Thr Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Pro Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Ala Asp Ile Asp Phe Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Met
450 455 460
Gln Val Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Ile Glu Val Val Ile Thr Pro Arg Leu
500 505 510
Thr Pro Glu Leu Tyr
515
<210> 35
<211> 517
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность: последовательность белка P382S варианта никотин-деметилазы CYP82E10
<400> 35
Met Val Ser Pro Val Glu Ala Ile Val Gly Leu Val Thr Leu Thr Leu
1 5 10 15
Leu Phe Tyr Phe Ile Arg Thr Lys Lys Ser Gln Lys Pro Ser Lys Pro
20 25 30
Leu Pro Pro Lys Ile Pro Gly Gly Trp Pro Val Ile Gly His Leu Phe
35 40 45
Tyr Phe Asp Asp Asp Ser Asp Asp Arg Pro Leu Ala Arg Lys Leu Gly
50 55 60
Asp Leu Ala Asp Lys Tyr Gly Pro Val Phe Thr Phe Arg Leu Gly Leu
65 70 75 80
Pro Leu Val Leu Val Val Ser Ser Tyr Glu Ala Ile Lys Asp Cys Phe
85 90 95
Ser Thr Asn Asp Ala Ile Phe Ser Asn Arg Pro Ala Phe Leu Tyr Gly
100 105 110
Glu Tyr Leu Gly Tyr Asn Asn Ala Met Leu Phe Leu Thr Lys Tyr Gly
115 120 125
Pro Tyr Trp Arg Lys Asn Arg Lys Leu Val Ile Gln Glu Val Leu Cys
130 135 140
Ala Ser Arg Leu Glu Lys Leu Lys His Val Arg Phe Gly Glu Ile Gln
145 150 155 160
Thr Ser Ile Lys Asn Leu Tyr Thr Arg Ile Asp Gly Asn Ser Ser Thr
165 170 175
Ile Asn Leu Thr Asp Trp Leu Glu Glu Leu Asn Phe Gly Leu Ile Val
180 185 190
Lys Met Ile Ala Gly Lys Asn Tyr Glu Ser Gly Lys Gly Asp Glu Gln
195 200 205
Val Glu Arg Phe Arg Lys Ala Phe Lys Asp Phe Ile Ile Leu Ser Met
210 215 220
Glu Phe Val Leu Trp Asp Ala Phe Pro Ile Pro Leu Phe Lys Trp Val
225 230 235 240
Asp Phe Gln Gly His Val Lys Ala Met Lys Arg Thr Phe Lys Asp Ile
245 250 255
Asp Ser Val Phe Gln Asn Trp Leu Glu Glu His Val Lys Lys Lys Glu
260 265 270
Lys Met Glu Val Asn Ala Glu Gly Asn Glu Gln Asp Phe Ile Asp Val
275 280 285
Val Leu Ser Lys Met Ser Asn Glu Tyr Leu Asp Glu Gly Tyr Ser Arg
290 295 300
Asp Thr Val Ile Lys Ala Thr Val Phe Ser Leu Val Leu Asp Ala Ala
305 310 315 320
Asp Thr Val Ala Leu His Met Asn Trp Gly Met Ala Leu Leu Ile Asn
325 330 335
Asn Gln His Ala Leu Lys Lys Ala Gln Glu Glu Ile Asp Lys Lys Val
340 345 350
Gly Lys Asp Arg Trp Val Glu Glu Ser Asp Ile Lys Asp Leu Val Tyr
355 360 365
Leu Gln Thr Ile Val Lys Glu Val Leu Arg Leu Tyr Pro Ser Gly Pro
370 375 380
Leu Leu Val Pro His Glu Asn Val Glu Asp Cys Val Val Ser Gly Tyr
385 390 395 400
His Ile Pro Lys Gly Thr Arg Leu Phe Ala Asn Val Met Lys Leu Gln
405 410 415
Arg Asp Pro Lys Leu Trp Ser Asn Pro Asp Lys Phe Asp Pro Glu Arg
420 425 430
Phe Phe Ala Ala Asp Ile Asp Phe Arg Gly Gln His Tyr Glu Phe Ile
435 440 445
Pro Phe Gly Ser Gly Arg Arg Ser Cys Pro Gly Met Thr Tyr Ala Met
450 455 460
Gln Val Glu His Leu Thr Ile Ala His Leu Ile Gln Gly Phe Asn Tyr
465 470 475 480
Lys Thr Pro Asn Asp Glu Pro Leu Asp Met Lys Glu Gly Ala Gly Leu
485 490 495
Thr Ile Arg Lys Val Asn Pro Ile Glu Val Val Ile Thr Pro Arg Leu
500 505 510
Thr Pro Glu Leu Tyr
515
<210> 36
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер NND3_F1
<400> 36
ttgatccagg gtttcaatta cagc 24
<210> 37
<211> 28
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер NND3_R2
<400> 37
aacgtaccaa attagaaaaa cgtgtacc 28
<210> 38
<211> 31
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер E4_F1
<400> 38
ttttcagaat tggttagagg aacatattaa t 31
<210> 39
<211> 26
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер E4_R1
<400> 39
tgtgtctatc tcttcttgtg ctttcg 26
<210> 40
<211> 29
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер E5_F1
<400> 40
agagattctt cgctgatgat attgactac 29
<210> 41
<211> 29
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер E5_R1
<400> 41
ccgtaattgt cacttctaca ggatttact 29
<210> 42
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер E10_F2
<400> 42
gctgatattg actttcgtgg tcaa 24
<210> 43
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер E10_R2
<400> 43
gcgaggcgta attaccactt ctat 24
<210> 44
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер PQ0014_F
<400> 44
ctattctccg ctttggactt ggca 24
<210> 45
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер PQ0014_R
<400> 45
aggacctcag gacaacggaa acg 23
<210> 46
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер NND3_F6
<400> 46
aattttggtc tcatcgtgaa gatgata 27
<210> 47
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер NND3_R7
<400> 47
tcactctctt ctacccatct atccttg 27
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| УМЕНЬШЕНИЕ СОДЕРЖАНИЯ ТАБАК-СПЕЦИФИЧНЫХ НИТРОЗАМИНОВ ПОСРЕДСТВОМ ИЗМЕНЕНИЯ ПУТИ АССИМИЛЯЦИИ НИТРАТОВ | 2015 |
|
RU2721799C2 |
| МОДУЛИРОВАНИЕ СОДЕРЖАНИЯ САХАРОВ И АМИНОКИСЛОТ В РАСТЕНИИ (SULTR3) | 2020 |
|
RU2826107C1 |
| ГЕНЫ ПРОТЕАЗ ТАБАКА | 2015 |
|
RU2756102C2 |
| МОДУЛИРОВАНИЕ СОДЕРЖАНИЯ РЕДУЦИРУЮЩИХ САХАРОВ В РАСТЕНИИ | 2019 |
|
RU2801948C2 |
| МУТАНТНЫЙ ПОЛИПЕПТИД ГИДРОКСИФЕНИЛПИРУВАТДИОКСИГЕНАЗА, КОДИРУЮЩИЙ ЕГО ГЕН И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2822892C1 |
| СПОСОБ ПРИМЕНЕНИЯ ВОССТАНОВЛЕНИЯ ДЛЯ ПОЛУЧЕНИЯ (S)-НИКОТИНА | 2022 |
|
RU2833281C2 |
| МУТАНТЫ ГЕМАГГЛЮТИНИНА ВИРУСА ГРИППА | 2019 |
|
RU2801708C2 |
| МУТАНТЫ ГЕМАГГЛЮТИНИНА ВИРУСА ГРИППА | 2019 |
|
RU2809237C2 |
| ВОССТАНОВЛЕНИЕ ФЕРТИЛЬНОСТИ У РАСТЕНИЙ | 2019 |
|
RU2831789C2 |
| МУЛЬТИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ БЕЛКИ С МУТАНТНЫМИ ДОМЕНАМИ FAB | 2019 |
|
RU2827657C2 |
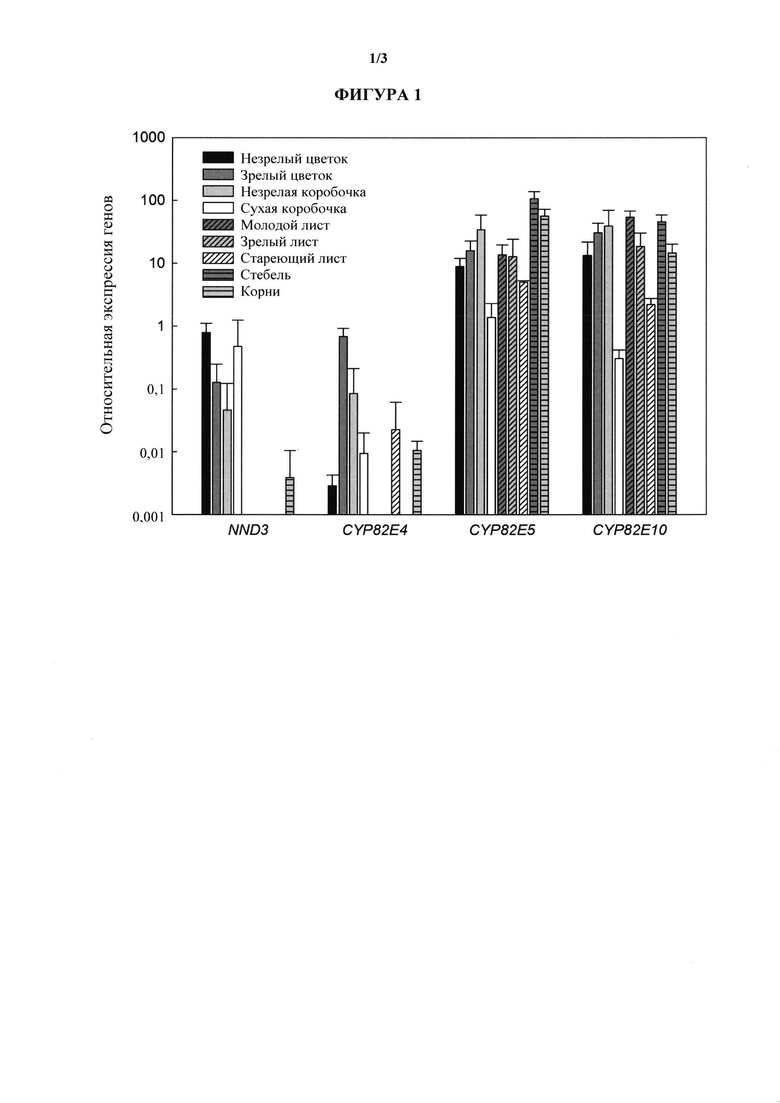
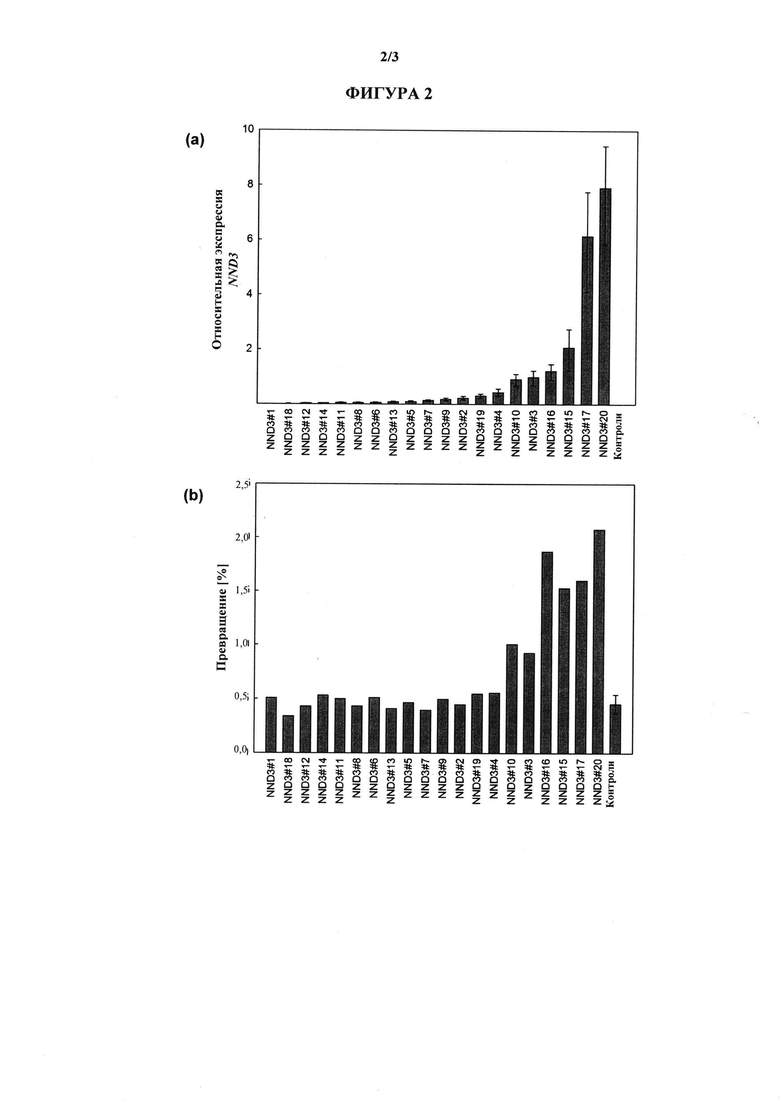
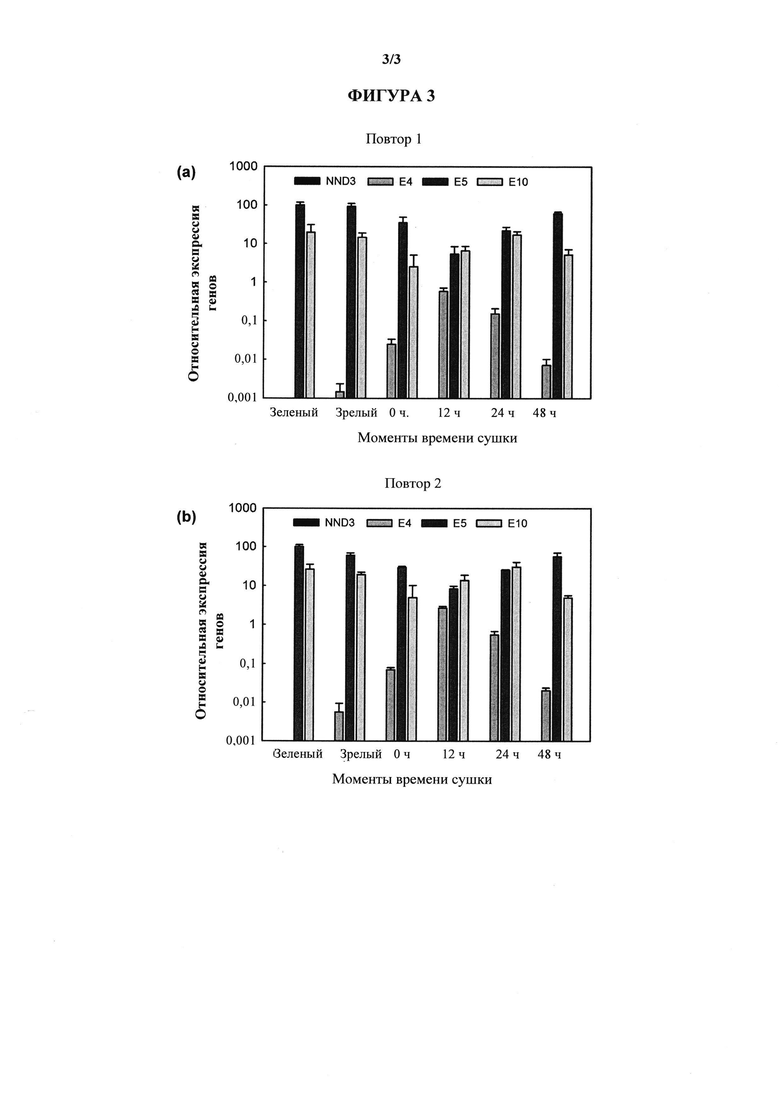
Изобретение относится к области биохимии, в частности к мутантной клетке растения табака, имеющей сниженный уровень норникотина по сравнению с клеткой растения табака дикого типа, а также к растению табака, растительному материалу и табачной композиции, содержащей вышеуказанную клетку. Также раскрыты способ снижения уровня норникотина в растении табака, способ снижения уровня N-нитрозоникотина (NNN) в растении табака, а также способ снижения уровней норникотина и N-нитрозоникотина (NNN) в растении табака. Изобретение также относится к способу получения сушеного растительного материала, предпочтительно сушеных листьев или цветков со сниженными в них уровнями по меньшей мере N-нитрозоникотина (NNN) по сравнению с сушенным растительным материалом на основе растения дикого типа. Изобретение позволяет эффективно снижать уровни норникотина в растении табака. 8 н. и 10 з.п. ф-лы, 3 ил., 1 табл., 4 пр.
1. Мутантная клетка растения табака, имеющая сниженный уровень норникотина по сравнению с клеткой растения табака дикого типа, где указанная клетка растения табака содержит:
(i) полинуклеотид, содержащий последовательность, кодирующую функциональную никотин-N-деметилазу, состоящий из нее или по сути состоящий из нее и имеющий последовательность, представленную SEQ ID NO: 2;
(ii) полипептид, кодируемый полинуклеотидом, изложенным в (i); или
(iii) полипептид, содержащий последовательность с активностью никотин-N-деметилазы, состоящий из нее или по сути состоящий из нее и имеющий последовательность, представленную SEQ ID NO: 3;
и где экспрессия или активность указанной никотин-деметилазы снижена по сравнению с клеткой растения табака дикого типа, в которой экспрессия или активность указанной никотин-деметилазы не была снижена.
2. Мутантная клетка растения табака по п. 1, где указанная клетка растения табака характеризуется одной или более мутациями, которые снижают экспрессию или активность указанной никотин-деметилазы.
3. Мутантная клетка растения табака по п. 1 или 2, которая характеризуется одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4, где предпочтительно указанная никотин-деметилаза CYP82E4 выбрана из группы, включающей SEQ ID NO: 12-16 или комбинацию двух или более из них, где предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E4 и происходит в положении, выбранном из группы, включающей аминокислотные остатки 329, 364, 376, 382 и 458 в SEQ ID NO: 5 или комбинацию двух или более из них, где предпочтительно указанная мутация выбрана из группы, включающей: а) замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 5; b) замену на аспарагин остатка лизина в положении 364 SEQ ID NO: 5; с) замену на метионин остатка валина в положении 376 SEQ ID NO: 5; d) замену на серин остатка пролина в положении 382 SEQ ID NO: 5; e) замену на серин остатка пролина в положении 458 SEQ ID NO: 5 и f) любую комбинацию двух или более из них.
4. Мутантная клетка растения табака по п. 1 или 3, которая характеризуется одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5, где предпочтительно указанная никотин-деметилаза CYP82E5 выбрана из SEQ ID NO: 24 или 25 или их комбинации, где предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E5 и происходит по аминокислотным остаткам 422 или 449 в SEQ ID NO: 17 или их комбинации, где предпочтительно указанная мутация выбрана из группы, включающей: а) замену на стоп-кодон остатка триптофана в положении 422 SEQ ID NO: 17; b) замену на лейцин остатка пролина в положении 449 SEQ ID NO: 17 и с) их комбинацию.
5. Мутантная клетка растения табака по п. 1 или 4, которая характеризуется одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10, где предпочтительно указанная никотин-деметилаза CYP82E10 выбрана из группы, включающей SEQ ID NO: 32-35 или комбинацию двух или более из них, где предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E10 и происходит в положении, выбранном из группы, включающей аминокислотные остатки 79, 107, 382, 419 в SEQ ID NO: 26 или комбинацию двух или более из них, где предпочтительно указанная мутация выбрана из группы, включающей: а) замену на серин остатка глицина в положении 79 SEQ ID NO: 26; b) замену на серин остатка пролина в положении 107 SEQ ID NO: 26; с) замену на серин остатка пролина в положении 382 SEQ ID NO: 26; d) замену на серин остатка пролина в положении 419 SEQ ID NO: 26 и е) любую их комбинацию.
6. Мутантная клетка растения табака по п. 1 или 2, которая дополнительно характеризуется:
(i) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E4, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E4, где предпочтительно указанная никотин-деметилаза CYP82E4 выбрана из группы, включающей SEQ ID NO: 12-16 или комбинацию двух или более из них, где предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E4 и происходит в положении, выбранном из группы, включающей аминокислотные остатки 329, 364, 376, 382 и 458 в SEQ ID NO: 5 или комбинацию двух или более из них, где предпочтительно указанная мутация выбрана из группы, включающей: а) замену на стоп-кодон остатка триптофана в положении 329 SEQ ID NO: 5; b) замену на аспарагин остатка лизина в положении 364 SEQ ID NO: 5; с) замену на метионин остатка валина в положении 376 SEQ ID NO: 5; d) замену на серин остатка пролина в положении 382 SEQ ID NO: 5; e) замену на серин остатка пролина в положении 458 SEQ ID NO: 5 и f) любую комбинацию двух или более из них; и
(ii) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E5, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E5, где предпочтительно указанная никотин-деметилаза CYP82E5 выбрана из SEQ ID NO: 24 или 25 или их комбинации, где предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E5 и происходит по аминокислотным остаткам 422 или 449 в SEQ ID NO: 17 или их комбинации, где предпочтительно указанная мутация выбрана из группы, включающей: а) замену на стоп-кодон остатка триптофана в положении 422 SEQ ID NO: 17; b) замену на лейцин остатка пролина в положении 449 SEQ ID NO: 17 и с) их комбинацию; и
(iii) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E10, где указанная мутация приводит в результате к сниженной экспрессии или функции указанной никотин-деметилазы CYP82E10, где предпочтительно указанная никотин-деметилаза CYP82E10 выбрана из группы, включающей SEQ ID NO: 32-35 или комбинацию двух или более из них, где предпочтительно указанная мутация приводит в результате к модификации указанной никотин-деметилазы CYP82E10 и происходит в положении, выбранном из группы, включающей аминокислотные остатки 79, 107, 382, 419 в SEQ ID NO: 26 или комбинацию двух или более из них, где предпочтительно указанная мутация выбрана из группы, включающей: а) замену на серин остатка глицина в положении 79 SEQ ID NO: 26; b) замену на серин остатка пролина в положении 107 SEQ ID NO: 26; с) замену на серин остатка пролина в положении 382 SEQ ID NO: 26; d) замену на серин остатка пролина в положении 419 SEQ ID NO: 26 и е) любую их комбинацию.
7. Мутантная клетка растения табака по п. 1 или 2, которая дополнительно характеризуется:
(i) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E4, одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E5, и одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E10, где указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13, указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24, и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 33; или
(ii) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E4, одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E5, и одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E10, где указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13, указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24, и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 34; или
(iii) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E4, одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E5, и одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E10, где указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13, указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24, и указанные никотин-деметилазы CYP82E10 содержат последовательность, изложенную под SEQ ID NO: 35;
(iv) одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E4, одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E5, и одной или более мутациями в гене, кодирующем никотин-деметилазу CYP82E10, где указанная никотин-деметилаза CYP82E4 содержит последовательность, изложенную под SEQ ID NO: 13, указанная никотин-деметилаза CYP82E5 содержит последовательность, изложенную под SEQ ID NO: 24, и указанная никотин-деметилаза CYP82E10 содержит последовательность, изложенную под SEQ ID NO: 32.
8. Мутантная клетка растения табака по любому из пп. 2-7, где указанная(указанные) мутация(мутации) представляет(представляют) собой мутацию в гетерозиготной или гомозиготной форме.
9. Мутантная клетка растения табака по любому из пп. 1-8, где указанная клетка растения характеризуется показателем превращения никотина в норникотин, составляющим менее 1%.
10. Мутантное растение табака, имеющее сниженный уровень норникотина по сравнению с растением табака дикого типа, где указанное мутантное растение табака содержит мутантную клетку растения табака по любому из пп. 1-9.
11. Растительный материал, включающий биомассу, цветки или корни, имеющие сниженный уровень норникотина по сравнению с клеткой растения табака дикого типа, где указанный растительный материал содержит мутантную клетку растения табака по любому из пп. 1-9.
12. Табачная композиция, содержащая мутантную клетку растения по любому из пп. 1-9, по меньшей мере часть мутантного растения по п. 10 или растительный материал по п. 11, где указанная табачная композиция имеет сниженное канцерогенное действие по сравнению с табачной композицией, содержащей клетку растения табака дикого типа, по меньшей мере часть растения табака дикого типа или материал растения дикого типа.
13. Способ снижения уровня норникотина в растении табака, причем указанный способ предусматривает стадии:
(a) обеспечения растения табака, содержащего полинуклеотид, содержащий последовательность, кодирующую функциональную никотин-N-деметилазу, состоящий из нее или по сути состоящий из нее и имеющий последовательность, представленную SEQ ID NO: 2;
(b) введения одной или более мутаций в указанный полинуклеотид указанного растения табака для создания мутантного растения табака;
(c) необязательно сушки мутантного растения табака и
(d) измерения уровня норникотина в мутантном растении табака, где уменьшение уровня норникотина в мутантном растении табака по сравнению с растением табака дикого типа свидетельствует о том, что уровень норникотина в указанном мутантном растении табака был снижен.
14. Способ снижения уровня N-нитрозоникотина (NNN) в растении табака, причем указанный способ предусматривает стадии:
(a) обеспечения растения табака, содержащего полинуклеотид, содержащий последовательность, кодирующую функциональную никотин-N-деметилазу, состоящий из нее или по сути состоящий из нее и имеющий последовательность, представленную SEQ ID NO: 2;
(b) введения одной или более мутаций в указанный полинуклеотид указанного растения табака для создания мутантного растения табака;
(c) сушки мутантного растения табака и
(d) измерения уровня NNN в мутантном растении табака, где уменьшение уровня NNN в мутантном растении табака по сравнению с растением табака дикого типа свидетельствует о том, что уровень NNN в указанном мутантном растении табака был снижен.
15. Способ снижения уровней норникотина и N-нитрозоникотина (NNN) в растении табака, причем указанный способ предусматривает стадии:
(a) обеспечения растения табака, содержащего полинуклеотид, содержащий последовательность, кодирующую функциональную никотин-N-деметилазу, состоящий из нее или по сути состоящий из нее и имеющий последовательность, представленную SEQ ID NO: 2;
(b) введения одной или более мутаций в указанный полинуклеотид указанного растения табака для создания мутантного растения табака;
(c) сушки мутантного растения табака и
(d) измерения уровней норникотина и NNN в мутантном растении табака, где уменьшение уровней норникотина и NNN в мутантном растении табака по сравнению с растением табака дикого типа свидетельствует о том, что уровни норникотина и NNN в указанном мутантном растении табака были снижены.
16. Способ по любому из пп. 13-15, где растение табака из стадии (b) представляет собой мутантное растение табака, где предпочтительно указанное мутантное растение табака характеризуется одной или более мутациями в одном или более дополнительных генах никотин-N-деметилазы.
17. Способ по п. 16, где указанное мутантное растение табака характеризуется одной или более дополнительными мутациями в генах, включающих группу CYP82E4, CYP82E5 или CYP82E10 или комбинацию двух или более из них.
18. Способ получения сушеного растительного материала, предпочтительно сушеных листьев или цветков со сниженными в них уровнями по меньшей мере N-нитрозоникотина (NNN) по сравнению с сушенным растительным материалом на основе растения дикого типа, предусматривающий стадии:
(a) обеспечения мутантного растения по п. 10 или растительного материала по п. 11;
(b) необязательно сбора с него растительного материала и
(c) сушки мутантного растения табака со стадии (а) или растительного материала со стадии (а) или (b) в течение некоторого периода времени с тем, чтобы уровни по меньшей мере NNN были ниже, чем в сушеном растительном материале на основе растения дикого типа.
| US 2008202541 A1, 28.08.2008 | |||
| US 2009205072 A1, 13.08.2009 | |||
| LARS OSTERGAARD et al | |||
| Establishing gene function by mutagenesis in Arabidopsis thaliana, The Plant Journal, 2004, Vol | |||
| Машина для изготовления проволочных гвоздей | 1922 |
|
SU39A1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРАНСГЕННЫХ РАСТЕНИЙ ТАБАКА С ПОВЫШЕННЫМ СОДЕРЖАНИЕМ ПРОЛИНА | 2006 |
|
RU2324737C1 |
Авторы
Даты
2020-10-07—Публикация
2015-05-07—Подача