Изобретение относится к медицинской вирусологии и может быть использовано в здравоохранении для профилактики заболеваемости гриппом среди взрослых и детей с помощью живой гриппозной интраназальной вакцины из штамма А/17/Брисбен/2018/3610 (H3N2) вируса гриппа А, семейства Orthomyxoviridae, рода Influenzavirus А.
В марте 2019 ВОЗ Всемирная организация здравоохранения (ВОЗ) дала рекомендации о замене H3N2 компонента в составе противогриппозных вакцин для Северного полушария на 2018-2019 гг.эпидемический сезон на вирусы гриппа, подобные А/Канзас/14/2017 (H3N2) [WHO. Recommended composition of influenza virus vaccines for use in the 2019-2020 northern hemisphere influenza season. 21 March 2018. https://www.who.int/influenza/vaccines/virus/recommendations/2019_20_north/en/].
Выбранный для подготовки гриппозных вакцин штамм А/Брисбен/34/2018 (H3N2) является антигенно родственным рекомендованному ВОЗ вирусу гриппа А/Канзас/14/2017 (H3N2). Штамм А/Брисбен/34/2018 и подготовленный на его основе вакцинный штамм А/17/Брисбен/2018/3610 (H3N2) характеризуются яично-адаптационными заменами в гемагглютинине G186V, S219Y. Рекомендованный ВОЗ штамм А/Канзас/14/2017 характеризуется аминокислотными остатками G186 и S219, при этом при адаптации к размножению в развивающихся куриных эмбрионах данный штамм приобрел аминокислотные замены в гемагглютинине D190N и N246T, что привело к снижению его репликационной активности в развивающихся куриных эмбрионах. По данным [Parker L, Wharton SA, Martin SR, Cross K, Lin Y, Liu Y, Feizi T, Daniels RS, McCauley JW. Effects of egg-adaptation on receptor-binding and antigenic properties of recent influenza A (H3N2) vaccine viruses. J Gen Virol. 2016 Jun; 97(6):1333-1344. doi: 10.1099/jgv.0.000457. Epub 2016 Mar 14. PMID: 26974849; PMCID: PMC5394856.] сочетание аминокислотных остатков 186V с 219Y в случае вирусов, реплицирующихся в куриных эмбрионах, позволяет улучшить ростовые характеристики без влияния на антигенные свойства штаммов. [Wu, N. С., Lv, Н., Thompson, A. J., Wu, D. С., Ng, W. W., Kadam, R. U., … & Paulson, J. C. (2019). Preventing an antigenically disruptive mutation in egg-based H3N2 seasonal influenza vaccines by mutational incompatibility. Cell host & microbe.] было показано, что А/Канзас/14/2017-подобные вакцинные штаммы с оптимальными ростовыми показателями характеризуются аминокислотными остатками 186V, 190D, 219Y и 246N. В связи с этим, получение вакцинного штамма на основе А/Брисбен/34/2018 (H3N2) (А/Канзас/14/2017-подобный) для подготовки вакцин для профилактики гриппа в северном полушарии в эпидемический сезон 2019-2020 позволило получить штамм, антигенно соответствующий актуальному эпидемическому вирусу, с оптимальными ростовыми характеристиками в развивающихся куриных эмбрионах.
В результате появления в циркуляции нового эпидемического штамма вируса гриппа А/Канзас/14/2017 (H3N2), известный вакцинный штамм А/17/Сингапур/2016/3571 (H3N2) - прототип [Ларионова Н.В., Баженова Е.А., Крутикова Е. В., Матюшенко В.А., Киселева И. В., Руденко Л.Г. Вакцинный штамм вируса гриппа А/17/Сингапур/2016/3571 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей. Патент РФ №2683500 от 28.03.2019 - Опубл. БИ 2019. - №10] - утратил антигенную актуальность и вследствие этого не может вызвать защитную реакцию во время эпидемии, вызванной А/Канзас/14/2017-подобными штаммами вируса гриппа.
Задачей, на решение которой направлено заявляемое изобретение, является получение антигенно актуального вакцинного штамма для взрослых и для детей на основе холодоадаптированного донора аттенуации А/Ленинград/134/17/57 (H2N2) и нового эпидемического А/Канзас/14/2017-подобного вируса А/Брисбен/34/2018 (H3N2).
Применяемые в настоящее время штаммы для живых гриппозных вакцин получают методом генетической реассортации эпидемически актуальных вирусов с холодоадаптированными, безвредными для человека штаммами - донорами аттенуации [Александрова Г.И. Применение метода генетической рекомбинации для получения вакцинных штаммов вируса гриппа // Вопр. Вирусол - 1977 - №4, - С. 387-395.].
Донор аттенуации А/Ленинград/134/17/57 (H2N2) - холодоадаптированный (са) и температурочувствительный (ts) штамм вируса гриппа - разрешен для получения живых интраназальных вакцин для взрослых и детей [Александрова Г.И. Новое в эпидемиологии и профилактике вирусных инфекций. Л., 1968. - С. 66-83].
Цель реассортации - получить штамм с вакцинной формулой генома 6:2 - два гена, кодирующих поверхностные белки вируса гриппа гемагглютинин (НА) и нейраминидазу (NA), наследуются от антигенно актуального циркулирующего эпидемического штамма, а шесть генов, кодирующих внутренние и неструктурные белки (РВ2, РВ1, PA, NP, М, NS) - от донора аттенуации.
Получение вакцинного штамма. Вакцинный штамм А/17/Брисбен/2018/3610 (H3N2) получен методом генетической реассортации эпидемического вируса А/Брисбен/34/2018 с донором аттенуации А/Ленинград/134/17/57 (H2N2) путем одновременного инфицирования развивающихся куриных эмбрионов (РКЭ) смесью родительских вирусов в эквивалентных инфекционных дозах, с последующей селекцией при пониженной до 26°С температуре инкубации в присутствии кроличьей антисыворотки к донору аттенуации. Клоны дополнительно очищены тремя последовательными клонированием методом предельных разведений в присутствии антисыворотки к донору при пониженной (26°С) и оптимальной (32°С) температурах инкубации. Выбранный чистый клон проверен по фенотипическим характеристикам (ts- и са-фенотип) и по формуле генома на соответствие вакцинному штамму.
Антигенная характеристика вакцинного штамма.
Изучение антигенных свойств вакцинного штамма А/17/Брисбен/2018/3610 (H3N2) показало, что:
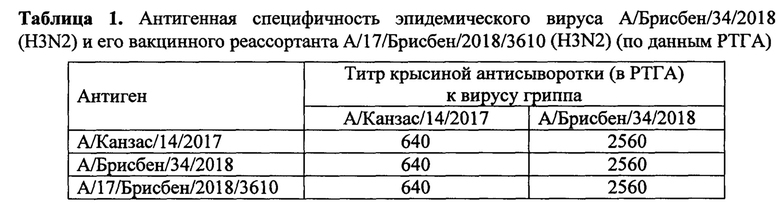
- ответственный за антигенную специфичность поверхностный белок вакцинного штамма - гемагглютинин (НА) - в РТГА с гомологичной сывороткой антигенно идентичен эпидемическому вирусу А/Брисбен/34/2018 (H3N2), поскольку показатели взаимодействия реассортанта А/17/Брисбен/2018/3610 (H3N2) и родительского штамма А/Брисбен/34/2018 (H3N2) с крысиной антисывороткой, полученной к вирусу А/Брисбен/34/2018 (H3N2), полностью совпадали (табл. 1). Кроме того, перекрестная постановка РТГА с вирусами А/Канзас/14/2017 (H3N2) и А/Брисбен/34/2018 (H3N2) в качестве антигенов с соответствующими гипериммунными крысиными сыворотками подтвердила близкое антигенное родство этих вирусов (табл. 1).
- второй ответственный за антигенную специфичность поверхностный белок вакцинного штамма - нейраминидаза (NA) - проверен методом частичного и полногеномного секвенирования, подтвердившими его идентичность эпидемическому родительскому вирусу вирусу А/Брисбен/34/2018 (H3N2).
Для анализа состава генома полученных реассортантов использовали метод пиросеквенирования ДНК копий генов [Степанова Е.А., Крутикова Е.В., Киселева И.В., Руденко Л.Г. Разработка протокола пиросеквенирования для анализа происхождения генов реассортантов при подготовке штаммов живой гриппозной вакцины.// «Молекулярная генетика, микробиология и вирусология» - №2. - 2018. - с. 101-107] с использованием комплекта высокоспецифичных олигонуклеотидов, разработанных в программе PSQ Assay Design для анализа генома современных штаммов подтипа H3N2 и донора аттенуации А/Ленинград/134/17/57 (H2N2).
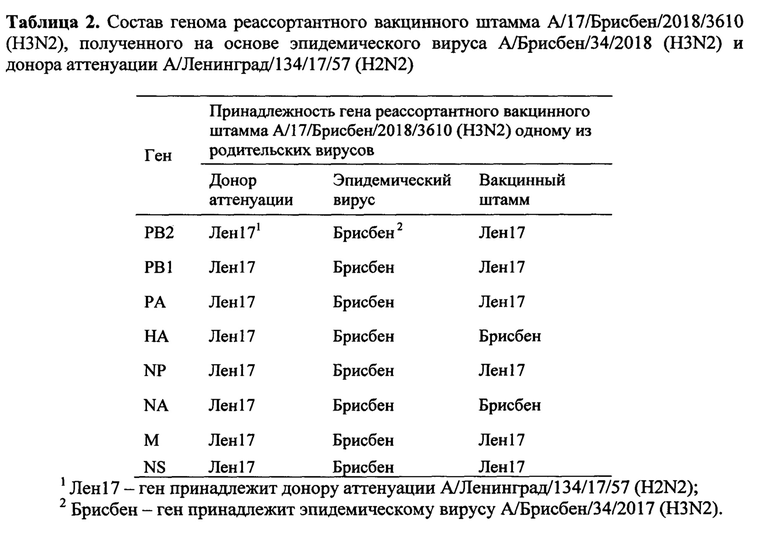
Результаты анализа всех генов вакцинного штамма А/17/Брисбен/2018/3610 (H3N2) представлены в табл. 2. Установлено, что формула генома вакцинного штамма А/17/Брисбен/2018/3610 (H3N2) - 6:2, что соответствует требованиям, предъявляемым к штаммам живой гриппозной вакцины: гены, кодирующие поверхностные белки гемагглютинин (НА) и нейраминидазу (NA) принадлежат эпидемическому родительскому вирусу А/Брисбен/34/2018 (H3N2), гены, кодирующие внутренние белки (РВ2, РВ1, РА, NP, М, NS), унаследованы от донора аттенуации А/Ленинград/134/17/57 (H2N2).
Данные, полученные при отборе вакцинного кандидата, были подтверждены полным секвенированием его генома и показали, что вакцинный штамм А/17/Брисбен/2018/3610 (H3N2) унаследовал все 6 генов, кодирующих внутренние и неструктурные белки, от донора аттенуации А/Ленинград/134/17/57 (H2N2) (табл. 2).
Генетическую стабильность кодирующих мутаций вакцинного штамма А/17/Брисбен/2018/3610 (H3N2) изучали сравнением сохранности кодирующих мутаций до и после пятикратного пассирования вакцинного штамма, подготовленного на основе донора аттенуации А/Ленинград/134/17/57, в куриных эмбрионах с использованием метода пиросеквенирования. Для данного анализа были разработаны специфические праймеры, позволяющие оценивать наличие данных мутаций с использованием пиросеквенатора PyroMark Q24. Праймеры разработаны с использованием компьютерной программы PSQ Assay Design.
Пример пирограммы, полученной для фрагмента гена РА, содержащего аттенуирующую мутацию в позиции 1045 у донора аттенуации А/Ленинград/134/17/57 (H2N2), приведен на фиг. 1, где а - вирус А/Ленинград/134/57 (H2N2), б - донор аттенуации А/Ленинград/134/17/57 (H2N2). в - вакцинный штамм А/17/Брисбен/2018/3610 (H3N2).
В результате пиросеквенирования вируса А/Ленинград/134/57 (H2N2) - эпидемического предшественника донора аттенуации, не обладающего аттенуирующей мутацией, пики в третьей (А) и четвертой (С) позициях одинаковой высоты (фиг. 1 а). Наличие аттенуирующей мутации С→А характеризуется пиком двукратной высоты в позиции А и отсутствием пика в позиции С, что можно увидеть на пирограмме, полученной для донора аттенуации А/Ленинград/134/17/57 (H2N2) (фиг. 1 б, черными стрелками отмечены пики/отсутствие пиков, свидетельствующие о наличии мутации), а также на пирограмме, полученной для гена РА вакцинного штамма А/17/Брисбен/2018/3610 (H3N2) (фиг. 1 в).
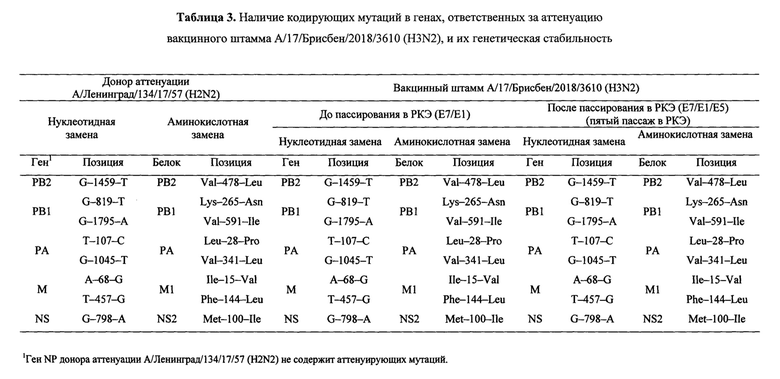
В таблице 3 приведены результаты пиросеквенирования всех участков генов вакцинного штамма А/17/Брисбен/2018/3610 (H3N2), содержащих аттенуирующие мутации, соответствующие донору аттенуации А/Ленинград/134/17/57 (H2N2), до и после пятикратного пассирования в развивающихся куриных эмбрионах. Все кодирующие нуклеотидные замены, охарактеризованные для донора аттенуации А/Ленинград/134/17/57 (H2N2) как ответственные за его аттенуацию (табл.3), присутствуют во внутренних генах реассортантного штамма А/17/Брисбен/2018/3610 (H3N2).
Таким образом, анализ генома вакцинного штамма А/17/Брисбен/2018/3610 (H3N2) показал генетическую стабильность его аттенуирующих мутаций.
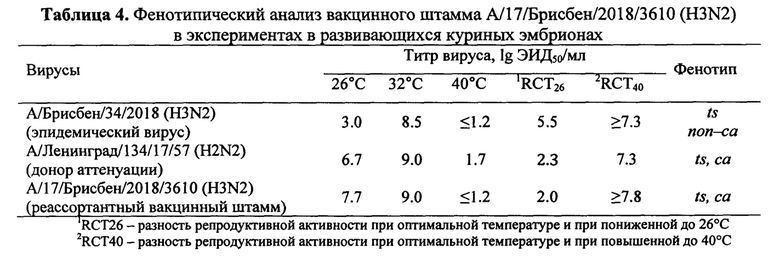
Оценку фенотипических свойств вакцинного штамма А/17/Брисбен/2018/3610 (H3N2), проводили путем его параллельного титрования в РКЭ при разных температурах. Вакцинный штамм А/17/Брисбен/2018/3610 (H3N2), в развивающихся куриных эмбрионах обладает выраженным температурочувствительным и холодоадаптированным фенотипом, идентичным фенотипу донора аттенуации А/Ленинград/134/17/57 (H2N2). Установлено, что вакцинный вирус является температурочувствительным (ts фенотип) - его инфекционная активность при температуре 40°С составила ≤ 1.2 log10 ЭИД50/мл, и холодоадаптированным (са фенотип) - инфекционная активность при пониженной до 26°С температуре инкубации достигала 7.7 log10 ЭИД50/мл, что свидетельствует о его безвредности для человека, поскольку по этим показателям он идентичен донору аттенуации А/Ленинград/134/17/57 (H2N2). Результаты фенотипического анализа представлены в таблице 4.
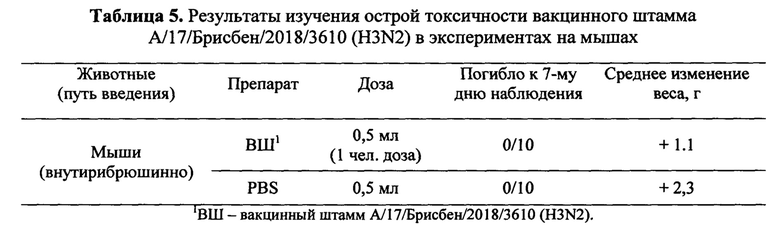
Безвредность для мышей. Доклинические исследования острой токсичности вакцинного штамма А/17/Брисбен/2018/3610 (H3N2) проводили на белых беспородных мышах в соответствии с Руководством по проведению доклинических исследований лекарственных средств (Иммунобиологические лекарственные препараты; Часть вторая. - М.: Гриф и К, 2012, 536 с) и с «Правилами надлежащей лабораторной практики» [Приказ МЗ РФ №199н от 01.04.2016. https://rg.ru/2016/09/02/minzdrav-prikaz199-site-dok.html]
Мышам вводили однократно внутрибрюшинно одну человеческую дозу, соответствующую 0.5 мл вакцинного вируса в дозе 7.0 lg ЭИД50/мл. Животным контрольной группы вводили внутрибрюшинно физиологический раствор. Ежедневно в течение всего исследования (7 дней) проводили контроль общего состояния каждого животного. Данные физиологического исследования (подвижность, поведенческие реакции, кинетика массы тела) показали, что внутрибрюшинное введение вакцинного штамма не вызывало гибели экспериментальных животных (табл. 5) и не приводило к изменению их внешнего вида, поведения, не отражалось на потреблении ими пищи и воды, что свидетельствует о безвредности вакцинного препарата.
Заключение
В результате проведенных доклинических исследований установлено, что заявляемый вакцинный штамм живой гриппозной вакцины А/17/Брисбен/2018/3610 (H3N2) характеризуется сочетанием полезных признаков, необходимых вакцинному штамму: антигенной специфичностью актуального эпидемического вируса А/Брисбен/34/2018 (H3N2), структурой генома 6:2, оптимальной для реассортантных вакцинных штаммов, а также характерной для донора аттенуации температурочувствительностью и холодоадаптированностью и безвредностью для лабораторных животных, что коррелирует с аттенуацией для человека. Образец паспорта на вакцинный штамм прилагается.
Таким образом, вакцинный штамм А/17/Брисбен/2018/3610 (H3N2) по основным биологическим свойствам, изученным в доклинических экспериментах in vitro и in vivo, соответствует требованиям, предъявляемым к вакцинным штаммам Фармакопейной статьей (ФСП: Р N003224/01-270313) на Ультравак®, вакцину гриппозную аллантоисную живую для интраназального применения для взрослых и для детей.
Полученный штамм А/17/Брисбен/2018/3610 (H3N2) депонирован 12.07.2019 года в Государственную коллекцию вирусов Института вирусологии им. Д.И. Ивановского ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России под №2932.
ХАРАКТЕРИСТИКА ШТАММА
Инфекционная активность штамма А/17/Брисбен/2018/3610 (H3N2) при репродукции в развивающихся куриных эмбрионах при 32°С в течение 48 часов - 9.0 log10 ЭИД50/мл. Гемагглютинирующая активность - 1:1024. Штамм проявляет генетическую стабильность фенотипических признаков после 5 пассажей на куриных эмбрионах (при использовании больших заражающих доз). Полезным свойством вакцинного штамма вируса гриппа А/17/Брисбен/2018/3610 (H3N2) является его пригодность для наработки живой гриппозной вакцины для профилактики гриппа как у взрослых, так и у детей с трехлетнего возраста.

| название | год | авторы | номер документа |
|---|---|---|---|
| Вакцинный штамм вируса гриппа А/17/БРИСБЕН/2017/7178 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2711101C1 |
| Вакцинный штамм вируса гриппа А/17/КАНЗАС/2017/631 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2732610C1 |
| Реассортантный штамм вируса гриппа А/17/Ньюкасл/2018/22 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2022 |
|
RU2783887C1 |
| Реассортантный штамм вируса гриппа А/17/Гонконг/2019/2573 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2022 |
|
RU2783894C1 |
| Вакцинный штамм вируса гриппа А/17/Швейцария/2017/51 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2715674C1 |
| Реассортантный штамм вируса гриппа А/17/Виктория/2019/276 (H1N1) pdm09 для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2022 |
|
RU2783878C1 |
| Реассортантный вакцинный штамм вируса гриппа А/17/Тасмания/2020/151 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2023 |
|
RU2825672C1 |
| Реассортантный штамм вируса гриппа А/17/Гуандун-Маонань/2019/211 (H1N1)pdm09 для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2022 |
|
RU2793387C1 |
| Реассортантный вакцинный штамм вируса гриппа А/17/Дарвин/2021/410 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2023 |
|
RU2825673C1 |
| Реассортантный вакцинный штамм вируса гриппа А/17/Мичиган/2020/484 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2023 |
|
RU2825583C1 |

Изобретение относится к области биотехнологии. Изобретение представляет штамм вируса гриппа А/17/Брисбен/2018/3610 (H3N2), депонированный в Государственную коллекцию вирусов Института вирусологии им. Д.И. Ивановского ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России под №2932, для производства живой гриппозной интраназальной вакцины для взрослых и для детей. Изобретение используется для профилактики заболеваемости гриппом среди взрослых и детей с помощью живой гриппозной интраназальной вакцины из штамма вируса гриппа А/17/Брисбен/2018/3610 (H3N2). 1 ил., 5 табл.
Штамм вируса гриппа А/17/Брисбен/2018/3610 (H3N2), депонированный в Государственную коллекцию вирусов Института вирусологии им. Д.И. Ивановского ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России под №2932, для производства живой гриппозной интраназальной вакцины для взрослых и для детей.
| ВАКЦИННЫЙ ШТАММ ВИРУСА ГРИППА А/17/СИНГАПУР/2016/3571 (H3N2) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2018 |
|
RU2683500C1 |
| ВАКЦИННЫЙ ШТАММ ВИРУСА ГРИППА А/17/БРИСБЕН/07/1 (H3N2) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2010 |
|
RU2416640C1 |
| PARKER L, et al., Effects of egg-adaptation on receptor-binding and antigenic properties of recent influenza A (H3N2) vaccine viruses | |||
| J Gen Virol | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
Авторы
Даты
2020-10-26—Публикация
2019-12-17—Подача