ПЕРЕКРЕСТНАЯ ССЫЛКА
По настоящей заявке испрашивается приоритет к предварительной заявке США № 62/764,817, поданной 16 августа 2018 и предварительной заявке на патент США № 62/810,112, поданной 25 февраля 2019, обе которые включены в настоящий документ в качестве ссылки полностью.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит список последовательностей, который представлен в электронном виде в формате ASCII и включен в настоящий документ в качестве ссылки полностью. Указанная копия ASCII создана 6 сентября 2019, названа 50401-726.601_SL.txt и имеет размер 419311 байтов.
УРОВЕНЬ ТЕХНИКИ
Т-клеточные рецепторы (TCR) являются членами суперсемейства иммуноглобулинов и обычно состоят из двух субъединиц, а именно α- и β-субъединиц. Они обладают одним N-концевым иммуноглобулиновым (Ig)-вариабельным (V) доменом, одним Ig-константным (C) доменом, трансмембранной/клеточномембранной спиральной областью и коротким цитоплазматическим концевым сегментом на C-конце. Вариабельные домены как α-цепи, так и β-цепи TCR имеют три гипервариабельных или определяющих комплементарность области (CDR), тогда как вариабельная область β-цепи имеет дополнительную область гипервариабельности (HV4), которая обычно не контактирует с антигеном и поэтому не считается CDR.
CDR3 является основным CDR, ответственным за распознавание процессированного антигена, хотя также было показано, что CDR1 альфа-цепи взаимодействует с N-концевой частью антигенного пептида, тогда как CDR1 бета-цепи взаимодействует с C-концевой частью пептида. Считается, что CDR2 распознает MHC. Константный домен домена TCR состоит из коротких соединительных последовательностей, в которых цистеиновый остаток образует дисульфидные связи, которые образуют связь между двумя цепями. Аффинность TCR к определенному антигену делает их ценными для нескольких терапевтических подходов. Например, онкологических пациентов, таких как пациенты с меланомой, можно эффективно лечить с помощью адоптивной иммунотерапии, поскольку TCR чрезвычайно чувствительны к своему антигену и могут направлять иммунные ответы на опухолевые клетки, экспрессирующие их когнатный антиген. Следовательно, существует потребность в TCR против комплексов пептидов-MHC для разработки новых эффективных терапевтических агентов.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящая заявка основана на разработке TCR против комплексов пептид-МНС и эффективного терапевтического агента, содержащего TCR. В настоящем документе представлены молекулы выделенной нуклеиновой кислоты, кодирующие TCR против комплексов пептид-МНС, T клетки, экспрессирующие TCR против комплексов пептид-МНС и фармацевтические композиции для применения в лечении заболеваний.
В настоящем документе представлена рекомбинантная нуклеиновая кислота, кодирующая Т-клеточный рецептор (TCR), содержащий конструкт бета цепи TCR, содержащий определяющую комплементарность область 3 (CDR3), имеющую аминокислотную последовательность, представленную SEQ ID NO: 52. В некоторых вариантах осуществления, конструкт Т-клеточного рецептора (TCR) дополнительно содержит определяющую комплементарность область 1 (CDR1) и определяющую комплементарность область 2 (CDR2), где CDR1 имеет аминокислотную последовательность, представленную SEQ ID NO: 50; и CDR2 имеет аминокислотную последовательность, представленную SEQ ID NO: 51. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность аминокислотной последовательности, представленной SEQ ID NO: 58. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 90% идентичность аминокислотной последовательности, представленной SEQ ID NO: 58. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 95%, 96%, 97%, 98% или 99% идентичность аминокислотной последовательности, представленной SEQ ID NO: 58. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, аминокислотную последовательность, представленную SEQ ID NO: 58. В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота, кодирующая Т-клеточный рецептор (TCR) по любому из вышепредставленных вариантов осуществления, дополнительно содержит конструкт альфа цепи TCR, имеющий CDR1, CDR2 и CDR3, где CDR1 имеет аминокислотную последовательность, представленную SEQ ID NO: 47; CDR2 имеет аминокислотную последовательность, представленную SEQ ID NO: 48; и CDR имеет аминокислотную последовательность, представленную SEQ ID NO: 49. В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота по любому из вышепредставленных вариантов осуществления содержит: (a) последовательность, имеющую, по меньшей мере, 80% идентичность последовательности SEQ ID NOs: 56 или 57, дополнительно содержащую последовательность, кодирующую, по меньшей мере, SEQ ID NO: 52; и (b) последовательность, имеющую, по меньшей мере, 80% идентичность последовательности SEQ ID NOs: 53 или 54, дополнительно содержащую последовательность, кодирующую, по меньшей мере, SEQ ID NO: 49. В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота, кодирующая Т-клеточный рецептор (TCR) по любому из вышепредставленных вариантов осуществления, содержит Конструкт альфа цепи TCR, который содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность аминокислотной последовательности, представленной SEQ ID NO: 55. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 90% идентичность аминокислотной последовательности, представленной SEQ ID NO: 55. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 95%, 96%, 97%, 98% или 99% идентичность аминокислотной последовательности, представленной SEQ ID NO: 55. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, аминокислотную последовательность, представленную SEQ ID NO: 55. В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота, кодирующая описанный выше TCR, содержит: (a) бета цепь, имеющую аминокислотную последовательность, представленную SEQ ID NO: 60, или аминокислотную последовательность, которая на, по меньшей мере, 80% идентична SEQ ID NO: 60; и (b) альфа цепь, имеющую аминокислотную последовательность, представленную SEQ ID NO: 59, или аминокислотную последовательность, которая на, по меньшей мере, 80% идентична SEQ ID NO: 59. В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота, кодирующая TCR по любому из вышепредставленных вариантов осуществления, связывается с эпитопом от RAS человека, содержащего мутацию G12V.
В настоящем документе представлена рекомбинантная нуклеиновая кислота, кодирующая TCR, содержащая конструкт бета цепи TCR и конструкт альфа цепи TCR, где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую аминокислотную последовательность, выбранную из SEQ ID NO: 537 и 563. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит CDR3, имеющий аминокислотную последовательность SEQ ID NO: 537. В некоторых вариантах осуществления, конструкт бета цепи TCR, содержащий CDR3, имеющую аминокислотную последовательность SEQ ID NO: 537, содержит вариабельную область, имеющую, по меньшей мере, 80%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичность аминокислотной последовательности, представленной SEQ ID NO: 541. В некоторых вариантах осуществления, конструкт бета цепи TCR имеет идентичность аминокислотной последовательности, представленной SEQ ID NO: 541. В некоторых вариантах осуществления, TCR, содержащий CDR3 бета цепи TCR, имеющую аминокислотную последовательность SEQ ID NO: 537, дополнительно конструкт альфа цепи TCR, который содержит вариабельную область, имеющую, по меньшей мере, 80%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичность аминокислотной последовательности, представленной SEQ ID NO: 539 или SEQ ID NO: 552. В некоторых вариантах осуществления, конструкт альфа цепи TCR имеет идентичность аминокислотной последовательности, представленной SEQ ID NO: 539. В некоторых вариантах осуществления, конструкт альфа цепи TCR имеет идентичность аминокислотной последовательности, представленной SEQ ID NO: 552. В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота, описанная выше, кодирует TCR, содержащий бета цепь, имеющую аминокислотную последовательность, представленную SEQ ID NO: 543, или последовательность, которая на, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 543; и альфа цепь, имеющую аминокислотную последовательность, представленную SEQ ID NO: 542, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 542. В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота, описанная выше, кодирует TCR, содержащую бета цепь, имеющую аминокислотную последовательность, представленную SEQ ID NO: 543, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 543; и альфа цепь, имеющую аминокислотную последовательность, представленную SEQ ID NO: 555, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 555. В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота, описанная выше, кодирует TCR, содержащий вариабельный домен бета цепи, имеющий аминокислотную последовательность, представленную SEQ ID NO: 541, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 541; и вариабельный домен альфа цепи, имеющий аминокислотную последовательность, представленную SEQ ID NO: 539, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 539. В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота, описанная выше, кодирует TCR, содержащий вариабельный домен бета цепи, имеющий аминокислотную последовательность, представленную SEQ ID NO: 541, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 541; и вариабельный домен альфа цепи, имеющий аминокислотную последовательность, представленную SEQ ID NO: 552, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 552.
В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота, кодирующая TCR, содержащий конструкт бета цепи TCR и конструкт альфа цепи TCR, конструкт бета цепи TCR, Конструкт бета цепи TCR, содержит CDR3, имеющий аминокислотную последовательность SEQ ID NO: 563. В некоторых вариантах осуществления конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичность аминокислотной последовательности, представленной SEQ ID NO: 567. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичность аминокислотной последовательности, представленной SEQ ID NO: 565. В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота, описанная выше, кодирует TCR, содержащий бета цепь, имеющую аминокислотную последовательность, представленную SEQ ID NO: 569, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 569; и вариабельный домен альфа цепи, имеющий аминокислотную последовательность, представленную SEQ ID NO: 568, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 568. В настоящем документе описан вектор, содержащий рекомбинантную нуклеиновую кислоту по любому из вариантов осуществления, описанных выше. Также в настоящем документе описана клетка, содержащая рекомбинантную нуклеиновую кислоту по любому из вариантов осуществления, описанных выше или вектор, такой как описан выше.
В настоящем документе представлена рекомбинантная нуклеиновая кислота, кодирующая конструкт TCR, содержащий: (a) конструкт бета цепи TCR, и (b) конструкт альфа цепи TCR; где TCR распознает и связывается с эпитопом из RAS человека, содержащего точечную мутацию G12V или G12C, где эпитопом является МНС-белковый комплекс человека, где MHC-белком человека является HLA антиген, кодированный HLA A03:01 аллелью. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит CDR3, имеющую аминокислотную последовательность, представленную SEQ ID NO: 68. В некоторых вариантах осуществления, конструкт бета цепи TCR дополнительно содержит определяющую комплементарность область 1 (CDR1) и определяющую комплементарность область 2 (CDR2), где CDR1 имеет аминокислотную последовательность, представленную SEQ ID NO: 66; и CDR2 имеет аминокислотную последовательность, представленную SEQ ID NO: 67. В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота, кодирующая Т-клеточный рецептор (TCR), описанный в этом параграфе, дополнительно содержит конструкт альфа цепи TCR, имеющий CDR1, CDR2 и CDR3, где CDR1 имеет аминокислотную последовательность, представленную SEQ ID NO: 63; CDR2 имеет аминокислотную последовательность, представленную SEQ ID NO: 64; и CDR имеет аминокислотную последовательность, представленную SEQ ID NO: 65. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80%, или, по меньшей мере, 90%, 95%, 96%, 97%, 98%, или 99% идентичность аминокислотной последовательности, представленной SEQ ID NO: 74. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, аминокислотную последовательность, представленную SEQ ID NO: 74. В некоторых вариантах осуществления, Т-клеточный рецептор (TCR) содержит конструкт альфа цепи TCR, где конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80%, или, по меньшей мере, 90%, 95%, 96%, 97%, 98% или 99% идентичность аминокислотной последовательности, представленной SEQ ID NO: 71. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, аминокислотную последовательность, представленную SEQ ID NO: 71. В некоторых вариантах осуществления, TCR содержит конструкт бета цепи, имеющий аминокислотную последовательность, представленную SEQ ID NO: 76, или последовательность, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 76; и конструкт альфа цепи, имеющий аминокислотную последовательность, представленную SEQ ID NO: 75, или последовательность, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 75. В настоящем документе представлен вектор, содержащий рекомбинантную нуклеиновую кислоту по любому из вариантов осуществления, описанных в этом параграфе. Также в настоящем документе представлена клетка, содержащая любую из рекомбинантных нуклеиновых кислот по любому из вариантов осуществления, описанных в этом параграфе, или вектор, описанный в этом параграфе.
В некоторых вариантах осуществления, TCR, который распознает и связывается с эпитопом RAS человека, содержащим точечную мутацию G12V, в комплексе с HLA антигеном, кодированным HLA A03:01 аллелью, содержит конструкт бета цепи TCR, содержащий CDR3, имеющий аминокислотную последовательность, представленную SEQ ID NO: 84. В некоторых вариантах осуществления, конструкт бета цепи TCR дополнительно содержит определяющую комплементарность область 1 (CDR1) и определяющую комплементарность область 2 (CDR2), где CDR1 имеет аминокислотную последовательность, представленную SEQ ID NO: 82; и CDR2 имеет аминокислотную последовательность, представленную SEQ ID NO: 83. В некоторых вариантах осуществления, TCR дополнительно содержит конструкт TCR альфа, имеющий CDR1, CDR2, и CDR3, где CDR1 имеет аминокислотную последовательность, представленную SEQ ID NO: 79; CDR2 имеет аминокислотную последовательность, представленную SEQ ID NO: 80; и CDR3 имеет аминокислотную последовательность, представленную SEQ ID NO: 81. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80%, или, по меньшей мере, 90%, 95%, 96%, 97%, 98% или 99% идентичность аминокислотной последовательности, представленной SEQ ID NO: 90. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, аминокислотную последовательность, представленную SEQ ID NO: 90. В некоторых вариантах осуществления, TCR, описанный выше, дополнительно содержит конструкт альфа цепи TCR, который содержит вариабельную область, имеющую, по меньшей мере, 80%, или, по меньшей мере, 90%, 95%, 96%, 97%, 98% или 99% идентичность аминокислотной последовательности, представленной SEQ ID NO: 87. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, аминокислотную последовательность, представленную SEQ ID NO: 71. В некоторых вариантах осуществления, TCR содержит конструкт бета цепи, имеющий аминокислотную последовательность SEQ ID NO: 92, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 92; и конструкт альфа цепи, имеющий аминокислотную последовательность SEQ ID NO: 91, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 91. В настоящем документе представлен вектор, содержащий рекомбинантную нуклеиновую кислоту по любому из вариантов осуществления, описанных в этом параграфе, и клетку, содержащую любую из рекомбинантных нуклеиновых кислот по любому из вариантов осуществления, описанных здесь.
В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота по варианту осуществления, описанному в предыдущем параграфе, TCR, который распознает и связывается с эпитопом из RAS человека, содержащим точечную мутацию G12V или G12C в комплексе с HLA антигеном, кодированным HLA A03:01 аллелью, содержит конструкт бета цепи TCR, содержащий CDR3, имеющую аминокислотную последовательность, представленную SEQ ID NO: 388. В некоторых вариантах осуществления, конструкт бета цепи TCR дополнительно содержит определяющую комплементарность область 1 (CDR1) и определяющую комплементарность область 2 (CDR2), где CDR1 имеет аминокислотную последовательность, представленную SEQ ID NO: 386; и CDR2 имеет аминокислотную последовательность, представленную SEQ ID NO: 387. В некоторых вариантах осуществления, TCR дополнительно содержит конструкт TCR альфа, имеющий CDR1, CDR2 и CDR3, где CDR1 имеет аминокислотную последовательность, представленную SEQ ID NO: 383; CDR2 имеет аминокислотную последовательность, представленную SEQ ID NO: 384; и CDR3 имеет аминокислотную последовательность, представленную SEQ ID NO: 385. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80%, или, по меньшей мере, 90%, 95%, 96%, 97%, 98% или 99% идентичность аминокислотной последовательности, представленной SEQ ID NO: 394. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, аминокислотную последовательность, представленную SEQ ID NO: 394. В некоторых вариантах осуществления, TCR, описаны выше, дополнительно содержит конструкт альфа цепи TCR, который содержит вариабельную область, имеющую, по меньшей мере, 80%, или, по меньшей мере, 90%, 95%, 96%, 97%, 98% или 99% идентичность аминокислотной последовательности, представленной SEQ ID NO: 391. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, аминокислотную последовательность, представленную SEQ ID NO: 391. В некоторых вариантах осуществления, TCR содержит конструкт бета цепи, имеющий аминокислотную последовательность SEQ ID NO: 396, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 396; и конструкт альфа цепи, имеющий аминокислотную последовательность SEQ ID NO: 395, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 395. В настоящем документе представлен вектор, содержащий рекомбинантную нуклеиновую кислоту по любому из вариантов осуществления, описанных в этом параграфе, и клетку, содержащую любую из рекомбинантных нуклеиновых кислот по любому из вариантов осуществления, описанных в настоящем документе.
В некоторых вариантах осуществления, рекомбинантная нуклеиновая кислота по варианту осуществления, описанному в предыдущем параграфе, TCR, который распознает и связывается с эпитопом из RAS человека, содержащим точечную мутацию G12C в комплексе с HLA антигеном, кодированным HLA A03:01 аллелью, содержит конструкт бета цепи TCR, содержащий CDR3, имеющий аминокислотную последовательность, представленную SEQ ID NO: 100. В некоторых вариантах осуществления, конструкт бета цепи TCR дополнительно содержит определяющую комплементарность область 1 (CDR1) и определяющую комплементарность область 2 (CDR2), где CDR1 имеет аминокислотную последовательность, представленную SEQ ID NO: 98; и CDR2 имеет аминокислотную последовательность, представленную SEQ ID NO: 99. В некоторых вариантах осуществления, TCR дополнительно содержит конструкт TCR альфа, имеющий CDR1, CDR2 и CDR3, где CDR1 имеет аминокислотную последовательность, представленную SEQ ID NO: 95; CDR2 имеет аминокислотную последовательность, представленную SEQ ID NO: 96; и CDR3 имеет аминокислотную последовательность, представленную SEQ ID NO: 97. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80%, или, по меньшей мере, 90%, 95%, 96%, 97%, 98% или 99% идентичность аминокислотной последовательности, представленной SEQ ID NO: 106. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую аминокислотную последовательность, представленную SEQ ID NO: 106. В некоторых вариантах осуществления, TCR, описанный выше, дополнительно содержит конструкт альфа цепи TCR, который содержит вариабельную область, имеющую, по меньшей мере, 80%, или, по меньшей мере, 90%, 95%, 96%, 97%, 98% или 99% идентичность аминокислотной последовательности, представленной SEQ ID NO: 103. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, аминокислотную последовательность, представленную SEQ ID NO: 103. В некоторых вариантах осуществления, TCR содержит конструкт бета цепи, имеющий аминокислотную последовательность SEQ ID NO: 108, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 108; и конструкт альфа цепи, имеющий аминокислотную последовательность SEQ ID NO: 107, или последовательность, которая имеет, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 107. В настоящем документе представлен вектор, содержащий рекомбинантную нуклеиновую кислоту по любому из вариантов осуществления, описанных в этом параграфе, и клетку, содержащую любую из рекомбинантных нуклеиновых кислот по любому из вариантов осуществления, описанных в настоящем документе.
В некоторых вариантах осуществления, эпитоп имеет длину 8-25 аминокислот. В некоторых вариантах осуществления, эпитоп содержит мутацию, которая отличается от дикого типа эпитопа, по меньшей мере, одной аминокислотой. В некоторых вариантах осуществления, эпитоп связывается с MHC человека с большей аффинностью, чем соответствующий эпитоп дикого типа. В некоторых вариантах осуществления, эпитоп связывается с МНС человека с KD или IC50 менее чем 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ. В некоторых вариантах осуществления, мутация не присутствует в не раковых клетках субъекта. В некоторых вариантах осуществления, TCR связывается с MHC-пептидным комплексом с KD или IC50 менее чем 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ. В некоторых вариантах осуществления, нуклеиновая кислот функционально связана с промотором. В некоторых вариантах осуществления, клеткой является CD4+ T клетка. В некоторых вариантах осуществления, клеткой является CD8+ T клетка. В некоторых вариантах осуществления, клетку выделяют у субъекта, имеющего мутацию RAS.
В настоящем документе представлена фармацевтическая композиция, содержащая: (a) нуклеиновую кислоту по любому из вариантов осуществления, описанных выше; или вектор по любому из вариантов осуществления, описанных выше; или клетку по любому из вариантов осуществления, описанных выше; и (b) фармацевтически приемлемый эксципиент или разбавитель. В некоторых вариантах осуществления, фармацевтическая композиция дополнительно содержит иммуномодулирующий агент или адъювант. В некоторых вариантах осуществления, адъювантом является поли I:C. В некоторых вариантах осуществления, фармацевтическая композиция по любому из вариантов осуществления, описанных выше, предназначена для применения в лечении иммунного заболевания или рака.
В настоящем документе представлен способ лечения субъекта, имеющего заболевание или состояние, включающий введение субъекту фармацевтической композиции по любому из вариантов осуществления, описанных выше. В некоторых вариантах осуществления, способ лечения субъекта с раком включает введение субъекту фармацевтической композиции по любому из вариантов осуществления, описанных выше.
Также в настоящем документе представлен способ идентификации субъекта с раком как кандидата для терапии, где способ включает определение субъекта как субъекта, который экспрессирует белок, кодированный HLA-A03:01 аллелью или HLA-A11:01 аллелью, где терапевтическим агентом является фармацевтическая композиция, выбранная из любого из вариантов осуществления, описанного выше.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из RAS в комплексе с МНС человека, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 84% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 3, 18, 33, 49, 65, 81, 97, 113, 241, 257, 273, 289, 305, 321, 337, 353, 369, 385, 401, 417 и 433, и/или где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 84% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 6, 21, 36, 52, 68, 84, 100, 116, 244, 260, 276, 292, 308, 324, 340, 356, 372, 388, 404, 420 и 436.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из RAS в комплексе с МНС человека, где эпитоп из RAS содержит область, имеющую, по меньшей мере, 70% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 15, 30, 45, 46, 61, 62, 77, 78, 93, 94, 109, 110, 125, 126, 219-222, 253, 254, 269, 270, 285, 286, 301, 302, 317, 318, 333, 334, 349, 350, 365, 366, 381,382, 397, 398, 413, 414, 429, 430, 445 и 446.
В настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR; где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека, кодированным HLA-A03:01 аллелью. В некоторых вариантах осуществления, конструкт альфа цепи содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 71, 87, 103, 295, 311, 327, 343, 359 и 391, где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека, кодированным HLA-A03:01 аллелью. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 74, 90, 106, 298, 314, 330, 346, 362 и 394, где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека, кодированным HLA-A03:01 аллелью.
В некоторых вариантах осуществления, конструкт альфа цепи TCR, как описано выше, содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 63, 79, 95, 287, 303, 319, 335, 351 и 383. В некоторых вариантах осуществления, конструкт бета цепи TCR, как описано выше, содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 66, 82, 98, 290, 306, 322, 338, 354 и 386. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 64, 80, 96, 288, 304, 320, 336, 352 и 384. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2),имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 67, 83, 99, 291, 307, 323, 339, 355 и 387. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 65, 81, 97, 289, 305, 321, 337, 353 и 385. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 68, 84, 100, 292, 308, 324, 340, 356 и 388.
В настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR; где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека кодированным HLA-A02:01 аллелью. В некоторых вариантах осуществления, конструкт альфа цепи содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 9 и 24, где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека кодированным HLA-A02:01 аллелью. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 12 и 27, где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека, кодированным HLA-A02:01 аллелью.
В некоторых вариантах осуществления, конструкт альфа цепи TCR, как описано выше, содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 1 и 16. В некоторых вариантах осуществления, конструкт бета цепи TCR, как описано выше, содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 4 и 19. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 2 и 17. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 5 и 20. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 3 и 18. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 6 и 21.
В настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR; где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека, кодированным HLA-A11:01 аллелью. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 39, 55, 122, 247, 263, 279, 375, 407 и 423, где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека кодированным HLA-A11:01 аллелью. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 42, 58, 125, 250, 266, 282, 378, 413 и 426, где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека, кодированным HLA-A11:01 аллелью.
В некоторых вариантах осуществления, конструкт альфа цепи TCR как описано выше, содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 31, 47, 111, 239, 255, 271, 367, 399 и 415. В некоторых вариантах осуществления, конструкт бета цепи TCR, как описано выше, содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 34, 50, 114, 242, 258, 274, 370, 402 и 418. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 32, 48, 112, 240, 256, 272, 368, 400 и 416. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 35, 51, 115, 243, 259, 275, 371, 403 и 419. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 33, 49, 113, 241, 257, 273, 369, 401, 417 и 433. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 36, 52, 116, 244, 260, 276, 372, 404 и 420. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 9; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 12. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 1, CDR2 с SEQ ID NO: 2, и CDR3 с SEQ ID NO: 3; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 4, CDR2 с SEQ ID NO: 5 и CDR3 с SEQ ID NO: 6. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 13, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 13. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 14 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 14. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 24; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 27. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 16, CDR2 с SEQ ID NO: 17, и CDR3 с SEQ ID NO: 18; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 19, CDR2 с SEQ ID NO: 20, и CDR3 с SEQ ID NO: 21. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 28, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 28. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 29 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 29. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 39; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 42. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 31, CDR2 с SEQ ID NO: 32, и CDR3 с SEQ ID NO: 33; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 34, CDR2 с SEQ ID NO: 35, и CDR3 с SEQ ID NO: 36. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 43, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 43. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 44 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 44. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 55; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 58. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 47, CDR2 с SEQ ID NO: 48, и CDR3 с SEQ ID NO: 49; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 50, CDR2 с SEQ ID NO: 51, и CDR3 с SEQ ID NO: 52. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 71; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 74. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 63, CDR2 с SEQ ID NO: 64 и CDR3 с SEQ ID NO: 65; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 66, CDR2 с SEQ ID NO: 67, и CDR3 с SEQ ID NO: 68. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 75, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 75. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 76 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 76. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 87; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 90. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 79, CDR2 с SEQ ID NO: 80, и CDR3 с SEQ ID NO: 81; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 82, CDR2 с SEQ ID NO: 83, и CDR3 с SEQ ID NO: 84. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 91, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 91. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 92 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 92. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 103; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 106. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 95, CDR2 с SEQ ID NO: 96, и CDR3 с SEQ ID NO: 97; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 98, CDR2 с SEQ ID NO: 99, и CDR3 с SEQ ID NO: 100. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 107, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 107. В некоторых вариантах осуществления, TCR содержит бета, цепь имеющую последовательность SEQ ID NO: 108 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 108. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 119; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 122. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 111, CDR2 с SEQ ID NO: 112, и CDR3 с SEQ ID NO: 113; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 114, CDR2 с SEQ ID NO: 115, и CDR3 с SEQ ID NO: 116. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 123, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 123. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 124 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 124. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 247; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 250. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 239, CDR2 с SEQ ID NO: 240 и CDR3 с SEQ ID NO: 241; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 242, CDR2 с SEQ ID NO: 243 и CDR3 с SEQ ID NO: 244. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 251, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 251. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 252 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 252. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 263; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 266. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 255, CDR2 с SEQ ID NO: 256, и CDR3 с SEQ ID NO: 257; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 258, CDR2 с SEQ ID NO: 259, и CDR3 с SEQ ID NO: 260. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 267, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 267. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 268 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 268. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 279; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 282. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 271, CDR2 с SEQ ID NO: 272, и CDR3 с SEQ ID NO: 273; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 274, CDR2 с SEQ ID NO: 275, и CDR3 с SEQ ID NO: 276. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 283, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 283. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 284 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 284. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 295; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 298. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 287, CDR2 с SEQ ID NO: 288, и CDR3 с SEQ ID NO: 289; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 290, CDR2 с SEQ ID NO: 291, и CDR3 с SEQ ID NO: 292. В некоторых вариантах осуществления, TCR содержит альфа цепь имеющую последовательность SEQ ID NO: 299, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 299. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 300 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 300. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 311; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 314. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 303, CDR2 с SEQ ID NO: 304, и CDR3 с SEQ ID NO: 305; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 306, CDR2 с SEQ ID NO: 307, и CDR3 с SEQ ID NO: 308. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 315, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 315. В некоторых вариантах осуществления, TCR содержит бета цепь имеющую последовательность SEQ ID NO: 316 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 316. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 327; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 330. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 319, CDR2 с SEQ ID NO: 320, и CDR3 с SEQ ID NO: 321; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 322, CDR2 с SEQ ID NO: 323, и CDR3 с SEQ ID NO: 324. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 331, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 331. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 332 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 332. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 343; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 346. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 335, CDR2 с SEQ ID NO: 336, и CDR3 с SEQ ID NO: 337; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 338, CDR2 с SEQ ID NO: 339, и CDR3 с SEQ ID NO: 340. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 347, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 347. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 348 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 348. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 359; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 362. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 351, CDR2 с SEQ ID NO: 352, и CDR3 с SEQ ID NO: 353; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 354, CDR2 с SEQ ID NO: 355, и CDR3 с SEQ ID NO: 356. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 363, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 363. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 364 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 364. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 375; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 378. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 367, CDR2 с SEQ ID NO: 368, и CDR3 с SEQ ID NO: 369; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 370, CDR2 с SEQ ID NO: 371, и CDR3 с SEQ ID NO: 372. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 379, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 379. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 380 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 380. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 391; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 394. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 383, CDR2 с SEQ ID NO: 384, и CDR3 с SEQ ID NO: 385; конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 386, CDR2 с SEQ ID NO: 387, и CDR3 с SEQ ID NO: 388. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 395, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 395. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 396 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 396. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 407; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 410. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 399, CDR2 с SEQ ID NO: 400, и CDR3 с SEQ ID NO: 401; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 402, CDR2 с SEQ ID NO: 403, и CDR3 с SEQ ID NO: 404. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 411, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 411. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 412 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 412. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 423; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 426. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 415, CDR2 с SEQ ID NO: 416, и CDR3 с SEQ ID NO: 417; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 418, CDR2 с SEQ ID NO: 419, и CDR3 с SEQ ID NO: 420. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 427, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 427. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 428 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 428. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 391; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 394.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из TMPRSS2:ERG в комплексе с МНС человека, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую последовательность SEQ ID NO: 144 и SEQ ID NO: 147, или последовательность, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 144 и SEQ ID NO: 147. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 154, или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 154. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 155 или последовательность, которая имеет, по меньшей мере, 80% идентичность с SEQ ID NO: 155.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из TMPRSS2:ERG в комплексе с МНС человека, где эпитоп из TMPRSS2:ERG содержит область, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 156.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 150. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 153. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую последовательность SEQ ID NO: 142 или последовательность, имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 142, и последовательность SEQ ID NO: 145 или последовательность, имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 145, соответственно. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 143 или SEQ ID NO: 146, соответственно. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, последовательность SEQ ID NO: 150 или, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 150; и конструкт бета цепи TCR содержит вариабельную область, имеющую последовательность SEQ ID NO: 153 или, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 153. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 142, CDR2 с SEQ ID NO: 143, и CDR3 с SEQ ID NO: 144; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 145, CDR2 с SEQ ID NO: 146, и CDR3 с SEQ ID NO: 147.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из GATA3 в комплексе с МНС человека, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 129, 132, 191, 194, 206 и 209.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), способный специфически связываться с мутантом GATA3 пептида в комплексе с белком, кодированным HLA аллелью, у субъекта с раком, где TCR содержит конструкт альфа цепи TCR и/или конструкт бета цепи TCR.
В настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, где TCR специфически связывается с мутантом GATA3 пептида в комплексе с HLA-A02:01, HLA-B07:02 или HLA-B08:01 белком; содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NOs: 129, 132, 191, 194, 206 или 209; и/или специфически связывается с мутантом GATA3 пептида, содержащего область, имеющую последовательность или имеющую последовательность с, по меньшей мере, 70% идентичностью последовательности SEQ ID NO: 141, 203 или 218.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из GATA3 в комплексе с МНС человека, где эпитоп из GATA3 содержит область, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 141, 203 или 218.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, последовательность SEQ ID NO: 135, 197 или 212; или последовательность с, по меньшей мере, 80% идентичностью последовательности с SEQ ID NO: 135, 197 или 212. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, последовательность SEQ ID NO: 138, 200 или 215; или последовательность, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 138, 200 или 215. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую аминокислотную последовательность, или имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 127, 130, 189, 192, 204 и 207. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую аминокислотную последовательность, или имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 128, 131, 190, 193, 205 и 208. В некоторых вариантах осуществления, связывающая GATA3 TCR альфа цепь содержит вариабельную область, имеющую, последовательность SEQ ID NO: 135, или последовательность, имеющую, по меньшей мере, 80% идентичность с SEQ ID NO: 135; и бета цепь содержит вариабельную область, имеющую последовательность SEQ ID NO: 138, или последовательность, имеющую, по меньшей мере, 80% идентичность с SEQ ID NO: 138. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 127, CDR2 с SEQ ID NO: 128 и CDR3 с SEQ ID NO: 129; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 130, CDR2 с SEQ ID NO: 131 и CDR3 с SEQ ID NO: 132. В некоторых вариантах осуществления, TCR имеет альфа цепь, имеющую последовательность SEQ ID NO: 139, или последовательность, имеющую, по меньшей мере, 80% идентичность с SEQ ID NO: 139. В некоторых вариантах осуществления, TCR имеет бета цепь, имеющую последовательность SEQ ID NO: 140, или последовательность, имеющую, по меньшей мере, 80% идентичность с SEQ ID NO: 140. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, аминокислотную последовательность, или имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 197; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 200. В некоторых вариантах осуществления TCR альфа цепь имеет последовательность SEQ ID NO: 201 или последовательность, имеющую, по меньшей мере, 80% идентичность с SEQ ID NO: 201. В некоторых вариантах осуществления TCR бета цепь имеет последовательность SEQ ID NO: 202 или последовательность, имеющую, по меньшей мере, 80% идентичность с SEQ ID NO: 202. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 189, CDR2 с SEQ ID NO: 190, и CDR3 с SEQ ID NO: 191; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 192, CDR2 с SEQ ID NO: 193, и CDR3 с SEQ ID NO: 194. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 212; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 215. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 204, CDR2 с SEQ ID NO: 205, и CDR3 с SEQ ID NO: 206; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 207, CDR2 с SEQ ID NO: 208, и CDR3 с SEQ ID NO: 209. В некоторых вариантах осуществления, TCR содержит альфа цепь, имеющую последовательность SEQ ID NO: 216 или последовательность, имеющую, по меньшей мере, 80% идентичность с SEQ ID NO: 216. В некоторых вариантах осуществления, TCR содержит бета цепь, имеющую последовательность SEQ ID NO: 217 или последовательность, имеющую, по меньшей мере, 80% идентичность с SEQ ID NO: 217.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из BTK в комплексе с МНС человека, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 161 и SEQ ID NO: 176, или где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 164 и SEQ ID NO: 179.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), способный специфически связываться с мутантом BTK пептида в комплексе с белком, кодированным HLA аллелью субъекта с раком, где TCR содержит конструкт альфа цепи TCR и/или конструкт бета цепи TCR.
В настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеинов кислот кодирует Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, где TCR специфически связывается с мутантом BTK пептида в комплексе с HLA-A02:01 белком; содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 161, 164, 176, или 179; и/или специфически связывается с мутантом BTK пептида, содержащим область с, по меньшей мере, 70% идентичностью последовательности SEQ ID NO: 173 или 188.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из BTK в комплексе с МНС человека, где эпитоп из BTK содержит область, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 173 или 188.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 167 или 182. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 170 или 185. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 159, 162, 174 и 177. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 160, 163, 175 и 178. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 167 или 182; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 170 или 185. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 159 или 174, CDR2 с SEQ ID NO: 160 или 175, и CDR3 с SEQ ID NO: 161 или 176; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 162 или 177, CDR2 с SEQ ID NO: 163 или 178, и CDR3 с SEQ ID NO: 164 или 179.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из EGFR в комплексе с МНС человека, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 449, SEQ ID NO: 466, SEQ ID NO: 483, SEQ ID NO: 500 и SEQ ID NO: 517, или где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 452, SEQ ID NO: 469, SEQ ID NO: 486, SEQ ID NO: 503 и SEQ ID NO: 520.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), способный специфически связываться с мутантом EGFR пептида в комплексе с белком, кодированным HLA аллелью субъекта с раком, где TCR содержит конструкт альфа цепи TCR и/или конструкт бета цепи TCR.
В настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеинов кислот кодирует Т-клеточный рецептор, (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, где TCR специфически связывается с мутантом EGFR пептида в комплексе с HLA-A02:01 белком; содержит определяющую комплементарность область 3 (CDR3), имеющую последовательность, или последовательность, имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 449, 466, 483, 500, 517, 452, 469, 486, 503, или 520; и/или специфически связывается с мутантом EGFR пептида, содержащего область, имеющую последовательность, или имеющую последовательность с, по меньшей мере, 70% идентичностью последовательности с SEQ ID NO: 461, 462, 463, 478, 479, 480, 495, 496, 497, 512, 513, 514, 529, 530 или 531.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из EGFR в комплексе с МНС человека, где эпитоп из EGFR содержит область, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 461, 462, 463, 478, 479, 480, 495, 496, 497, 512, 513, 514, 529, 530 или 531.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, последовательность, или последовательность, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 449, 466, 483, 500 или 517. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, последовательность, или последовательность, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 452, 469, 486, 503 или 520. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую последовательность, или последовательность, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 447, 464, 481, 498, 515, 450, 467, 484, 501 и 518. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую последовательность, или последовательность, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 448, 465, 482, 499, 516, 451, 468, 485, 502 и 519. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, последовательность, или последовательность, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 455, 472, 489, 506, или 523; и конструкт бета цепи TCR содержит вариабельную область, имеющую, последовательность, или последовательность, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 458, 475, 492, 509 или 526. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 447, 464, 481, 498 или 515, CDR2 с SEQ ID NO: 448, 465, 482, 499 или 516, и CDR3 с SEQ ID NO: 449, 466, 483, 500 или 517; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 450, 467, 484, 501 или 518, CDR2 с SEQ ID NO: 451, 468, 485, 502, или 519, и CDR3 с SEQ ID NO: 452, 469, 486, 503, или 520.
В некоторых вариантах осуществления, эпитоп содержит мутацию, выбранную из группы, состоящей из точечной мутации, мутации сайта сплайсинга, мутацию «сдвига рамки», мутацию сквозного прохождения, мутацию резистентности, мутацию слияния гена и любую их комбинацию. В некоторых вариантах осуществления, МНС человека кодирован либо HLA-A02:01 аллелью, либо HLA-A03:01 аллелью, либо HLA-A11:01 аллелью. В некоторых вариантах осуществления, RAS эпитоп содержит точечную мутацию. В некоторых вариантах осуществления, точечной мутацией является G12V мутация. В некоторых вариантах осуществления, точечной мутацией является G12C мутация. В некоторых вариантах осуществления, точечной мутацией является G12D мутация. В некоторых вариантах осуществления, МНС человека кодирован HLA-A02:01 аллелью. В некоторых вариантах осуществления, TMPRSS2:ERG эпитоп содержит мутацию слияния гена. В некоторых вариантах осуществления, МНС человека кодирован HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью. В некоторых вариантах осуществления, эпитоп содержит мутацию «сдвига рамки». В некоторых вариантах осуществления, МНС человека кодирован HLA-A02:01 аллелью. В некоторых вариантах осуществления, BTK эпитоп содержит точечную мутацию. В некоторых вариантах осуществления, точечной мутацией является C481S мутация. В некоторых вариантах осуществления, МНС человека кодирован HLA-A02:01 аллелью. В некоторых вариантах осуществления, EGFR эпитоп содержит точечную мутацию. В некоторых вариантах осуществления, точечной мутацией является T790M.
В некоторых вариантах осуществления, эпитоп имеет длину, по меньшей мере, 8 аминокислот. В некоторых вариантах осуществления, эпитоп имеет длину, по меньшей мере, 16 аминокислот. В некоторых вариантах осуществления, эпитоп имеет длину 8-25 аминокислот. В некоторых вариантах осуществления, эпитоп имеет длину 8-12 аминокислот. В некоторых вариантах осуществления, эпитоп имеет длину 16-25 аминокислот. В некоторых вариантах осуществления, эпитоп имеет длину 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 аминокислот.
В некоторых вариантах осуществления, эпитоп связывается с МНС человека с большей аффинностью, чем у эпитопа дикого типа. В некоторых вариантах осуществления, эпитоп связывается с МНС человека с KD или IC50 менее чем 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ.
В некоторых вариантах осуществления, мутация не присутствует в не раковых клетках субъекта. В некоторых вариантах осуществления, эпитоп кодирован геном или экспрессирует ген раковых клеток субъекта.
В некоторых вариантах осуществления, TCR связывается с MHC-пептидным комплексом с KD или IC50 менее чем 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ.
В некоторых вариантах осуществления, нуклеиновая кислота функционально связана с промотором.
В настоящем документе представлен вектор, содержащий нуклеиновую кислоту, описанную в настоящем документе. В некоторых вариантах осуществления, вектором является самоамплифицирующийся РНК репликон, плазмид, фаг, транспозон, космида, вирус или вирион. В некоторых вариантах осуществления, вектором является вирусный вектор. В некоторых вариантах осуществления, вектор получен из ретровируса, лентивируса, аденовируса, аденоассоциированного вируса, вируса герпеса, вируса оспы, альфа-вируса, вируса осповакцины, вируса гепатита B, папилломавируса человека или их псевдотипа. В некоторых вариантах осуществления, вектором является не вирусный вектор. В некоторых вариантах осуществления не вирусным вектором является наночастица, катионный липид, катионный полимер, металлический нанополимер, наностержень, липосома, мицелла, микропузырек, проникающий в клетки пептид или липосфера.
В настоящем документе представлен белок, кодированный нуклеиновой кислотой по любому из разделов, описанных выше.
В настоящем документе представлена клетка-хозяин, содержащая нуклеиновую кислоту, описанную выше, или белок, описанный выше. В некоторых вариантах осуществления, клеткой-хозяином является CD4+ T клетка. В некоторых вариантах осуществления, клеткой-хозяином является CD8+ T клетка. В некоторых вариантах осуществления, клеткой-хозяином является аутологичная клетка. В некоторых вариантах осуществления, клеткой-хозяином является аллогенная клетка. В некоторых вариантах осуществления, клеткой-хозяином является естественный киллер, В клетка или иммортализованная линия клеток. В некоторых вариантах осуществления, клеткой-хозяином является клетка человека.
В настоящем документе представлена фармацевтическая композиция, содержащая нуклеиновую кислоту, описанную выше, вектор, описанный выше, белок, описанный выше или клетку-хозяина, описанную выше; и фармацевтически приемлемый эксципиент или разбавитель. В некоторых вариантах осуществления, фармацевтическая композиция дополнительно содержит иммуномодулирующий агент или адъювант. В некоторых вариантах осуществления, иммуномодулирующим агентом в фармацевтической композиции является цитокин. В некоторых вариантах осуществления, адъювантом в фармацевтической композиции является поли I:C. В некоторых вариантах осуществления, фармацевтическая композиция предназначена для применения в лечении иммунного заболевания или рака.
В настоящем документе представлено применение фармацевтической композиции, описанной выше, для лечения иммунного заболевания или рака.
В настоящем документе представлен вектор, описанный в настоящем документе, белок, описанный в настоящем документе, или клетка-хозяин, описанная в настоящем документе, для производства лекарственного средства для лечения иммунного заболевания или рака. В некоторых вариантах осуществления, лекарственным средством является адоптивная T-клеточная терапия или TCR-генная терапия.
В настоящем документе представлен способ лечения субъекта с заболеванием или состоянием, включающий введение субъекту фармацевтической композиции, раскрытой в настоящем документе.
В настоящем документе представлен способ лечения субъекта с раком, включающий введение субъекту фармацевтической композиции, раскрытой в настоящем документе.
В настоящем документе представлен способ лечения субъекта с раком, включающий введение субъекту фармацевтической композиции; где субъект идентифицирован как экспрессирующий или экспрессирует белок, кодированный HLA-A02:01 аллелью, HLA-B07:02, HLA-B08:01, HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01 аллелью генома субъекта.
В настоящем документе представлен способ лечения субъекта с раком, включающий введение TCR или T клетки, экспрессирующей TCR, субъекту, где TCR специфически связывается с мутантом RAS пептида в комплексе с белком, кодированным HLA-A02:01, HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01; где субъект идентифицирован как экспрессирующий или экспрессирует белок, кодированный HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01 аллелью, где субъект экспрессирует HLA аллель.
В настоящем документе представлен способ лечения субъекта с раком, включающий введение субъекту фармацевтической композиции, описанной в настоящем документе; где TCR связывается с мутантным RAS пептидом, содержащим мутацию на G12 в комплексе с HLA-A02:01. HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01; где субъект идентифицирован как экспрессирующий белок, кодированный HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01 аллелью.
В настоящем документе представлен способ лечения субъекта с раком, включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR), специфический к мутанту GATA3 пептида в комплексе с HLA белком; где мутант GATA3 пептида содержит, по меньшей мере, одну мутантную аминокислоту и фрагмент, по меньшей мере, из 8 непрерывных аминокислот мутанта GATA3 белка, возникающий при мутации в GATA3 гене раковой клетки; где мутант GATA3 пептида связывается с белком, кодированным HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью.
В настоящем документе представлен способ лечения субъекта с раком, включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR), специфический для мутанта GATA3 пептида в комплексе с HLA белком; где мутант GATA3 пептида содержат одну или более мутантных GATA3 аминокислот, кодированных GATA3 neoORF последовательностью, где мутант GATA3 пептида связывается с белком, кодированным HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью.
В настоящем документе представлен способ лечения субъекта с раком, включающий введение TCR или T клетки, экспрессирующей TCR, субъекту; где TCR специфически связывается с мутантом GATA3 пептида в комплексе с белком, кодированным HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью; где субъект идентифицирован как экспрессирующий или экспрессирует белок, кодированный HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью.
В настоящем документе представлен способ лечения субъекта с раком, включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR), специфический к мутанту TMPRSS2:ERG пептида в комплексе с HLA белком; где мутант TMPRSS2:ERG пептида содержит, по меньшей мере, одну мутантную аминокислоту и является фрагментом TMPRSS2:ERG мутации слияния гена; где мутант TMPRSS2:ERG пептида связывается с белком, кодированным HLA-A02:01 аллелью.
В настоящем документе представлен способ лечения субъекта с раком, включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR), специфический к мутанту BTK пептида в комплексе с HLA белком; где мутант BTK пептида содержит, по меньшей мере, одну мутантную аминокислоту; где мутант BTK пептида связывается с белком, кодированным HLA-A02:01 аллелью.
В настоящем документе представлен способ лечения субъекта с раком, включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR), специфический к мутанту BTK пептида в комплексе с HLA белком; где мутант BTK пептида содержит мутацию резистентности или точечную мутацию; где мутант BTK пептид связывается с белком, кодированным HLA-A02:01 аллелью.
В настоящем документе представлен способ лечения субъекта с раком, включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR), специфический к мутанту BTK пептида в комплексе с HLA белком; где мутант BTK пептида содержит C481S мутацию; где мутант BTK пептида связывается с белком, кодированным HLA-A02:01 аллелью.
В настоящем документе представлен способ лечения субъекта с раком, включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR) или T клетку, экспрессирующую TCR, субъекту, где TCR специфически связывается с мутантом EGFR пептида в комплексе с белком, кодированным HLA-A02:01; где мутант EGFR пептида содержит мутацию резистентности или точечную мутацию, где субъект идентифицирован как экспрессирующий или экспрессирует белок, кодированный HLA-A02:01 аллелью. В некоторых вариантах осуществления, мутант EGFR пептида содержит T790M мутацию.
В настоящем документе представлен способ профилактики резистентности к противораковой терапии, где способ включает введение субъекту, нуждающемуся в этом, фармацевтической композиции, описанной в настоящем документе.
В настоящем документе представлен способ вызова иммунного ответа, где способ включает введение субъекту, нуждающемуся в этом, фармацевтической композиции, описанной в настоящем документе.
В настоящем документе представлен способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как субъекта, который экспрессирует белок, кодированный HLA-A02:01 аллелью, HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01 аллелью, где терапевтическим агентом является фармацевтическая композиция, описанная в настоящем документе.
В настоящем документе представлен способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как субъекта, который экспрессирует белок, кодированный HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR), специфический к мутанту GATA3 пептида в комплексе с HLA белком; где мутант GATA3 пептида содержит, по меньшей мере, одну мутантную аминокислоту и является фрагментом, по меньшей мере, из 8 непрерывных аминокислот мутанта GATA3 белка, возникающего при мутации в GATA3 гене раковой клетки; где мутант GATA3 пептида связывается с белком, кодированным HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью.
В настоящем документе представлен способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как субъекта, который экспрессирует белок, кодированный HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR), специфический к мутанту RAS пептида, содержащему мутацию на G12 в комплексе с HLA белком; где мутант RAS пептида связывается с белком, кодированным HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01 аллелью.
В настоящем документе представлен способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как субъекта, который экспрессирует белок, кодированный HLA-A02:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR), специфический к мутанту TMPRSS2:ERG пептида в комплексе с HLA белком; где мутант TMPRSS2:ERG пептида содержит, по меньшей мере, одну мутантную аминокислоту и является фрагментом TMPRSS2:ERG мутации слияния гена; где мутант TMPRSS2:ERG пептида связывается с белком, кодированным HLA-A02:01 аллелью.
В настоящем документе представлен способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как субъекта, который экспрессирует белок, кодированный HLA-A02:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR), специфический к мутанту BTK пептида в комплексе с HLA белком; где мутант BTK пептида содержит, по меньшей мере, одну мутантную аминокислоту; где мутант BTK пептида связывается с белком, кодированным HLA-A02:01 аллелью.
В настоящем документе представлен способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как субъекта, который экспрессирует белок, кодированный HLA-A02:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR), специфический к мутанту BTK пептида в комплексе с HLA белком; где мутант BTK пептида содержит мутация резистентности или точечную мутацию; где мутант BTK пептида связывается с белком, кодированным HLA-A02:01 аллелью.
В настоящем документе представлен способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как субъекта, который экспрессирует белок, кодированный HLA-A02:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR), специфический к мутанту BTK пептида в комплексе с HLA белком; где мутант BTK пептида содержит C481S мутацию; где мутант BTK пептида связывается с белком, кодированным HLA-A02:01 аллелью.
В настоящем документе представлен способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как субъекта, который экспрессирует белок, кодированный HLA-A02:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR), специфический к мутанту EGFR пептида в комплексе с HLA белком; где мутант EGFR пептида содержит, по меньшей мере, одну мутантную аминокислоту T790M; где мутант EGFR пептида связывается с белком, кодированным HLA-A02:01 аллелью.
В некоторых вариантах осуществления, рак выбран из группы, состоящей из рака груди, рака легких, немелкоклеточного рака легких, рака поджелудочной железы, колоректального рака, рака матки, меланомы, рака яичников, рака простаты, рака эндометрия, хронического лимфоцитарного лейкоза (CLL) и рака печени. В некоторых вариантах осуществления, субъект имеет рак груди, устойчивый к антиэстрогеновой терапии, рак груди MSI, метастатический рак груди, Her2-трицательный рак груди, Her2-положительный рак груди, ER-отрицательный рак груди, ER-положительный рак груди, рецидивирующий рак груди, метастатический рак груди или любую их комбинацию. В некоторых вариантах осуществления, рак груди экспрессирует рецептор эстрогена с мутацией.
В некоторых вариантах осуществления, субъекта имеет рак груди, устойчивый к терапии антиэстрогенами. В некоторых вариантах осуществления, рак груди экспрессирует рецептор эстрогена с мутацией. В некоторых вариантах осуществления, субъект имеет CLL, устойчивый к терапии ибрутинибом. В некоторых вариантах осуществления, CLL экспрессирует тирозинкиназу Брутона (BTK) с мутацией, такой как мутация C481S. В некоторых вариантах осуществления, субъект имеет рак легкого, резистентный к ингибитору тирозинкиназы. В некоторых вариантах осуществления, рак легкого экспрессирует рецептор эпидермального фактора роста (EGFR) с мутацией, такой как мутация T790M, L792F или C797S.
В некоторых вариантах осуществления, иммунный ответ вызывается у субъекта. В некоторых вариантах осуществления, иммунным ответом является гуморальный ответ. В некоторых вариантах осуществления, иммунным ответом является ответ цитотоксической T клетки.
В некоторых вариантах осуществления, способ дополнительно включает введение, по меньшей мере, одного дополнительного терапевтического агента или средства. В некоторых вариантах осуществления, по меньшей мере, одним дополнительным терапевтическим агентом или средством является хирургия, ингибитор контрольной точки, антитело или его фрагмент, химиотерапевтический агент, облучение, вакцина, малая молекула, Т клетка, вектор и APC, полинуклеотид, онколитический вирус или любая их комбинация. В некоторых вариантах осуществления, по меньшей мере, одним дополнительным терапевтическим агентом является анти-PD-1 агент и анти-PD-L1 агент, анти-CTLA-4 агент или анти-CD40 агент. В некоторых вариантах осуществления, дополнительный терапевтический агент вводят до, одновременно с или после введения фармацевтической композиции, описанной в настоящем документе.
В некоторых вариантах осуществления, введение включает подкожное или внутривенное введение.
В некоторых вариантах осуществления, субъектом является субъект, который имеет прогрессирование заболевания после эндокринной терапии в комбинации с ингибитором CDK 4/6.
В настоящем документе представлен способ включающий: идентификацию неоантиген-специфических Т клеток из образца, содержащего популяцию T клеток; идентификацию одного или более пептидов комплекса пептид-МНС, который представлен антигенпрезентирующими клетками (APC); идентификацию вариабельной последовательности Т-клеточного рецептора (TCR) из неоантиген-специфических Т-клеток; экспрессию рекомбинантного TCR, содержащего вариабельную последовательность TCR, идентифицированную в TCR клетке; и проведение функционального анализа, где функциональный анализ включает контакт TCR клетки с комплексом пептид-МНС, содержащим пептид из одного или более идентифицированных пептидов.
В некоторых вариантах осуществления, способ включает получение образца, содержащего популяцию клеток, содержащих неоантиген-специфические Т-клетки. В некоторых вариантах осуществления, получение образца включает получение образца Т-клеток от здорового субъекта или от субъекта, больного раком. В некоторых вариантах осуществления, образец Т-клеток берут у здорового донора. В некоторых вариантах осуществления, образец Т-клеток представляет собой образец мононуклеарных клеток периферической крови (PBMC).
В некоторых вариантах осуществления, идентификация неоантиген-специфических Т-клеток включает контакт популяции Т-клеток с, по меньшей мере, одним мультимерным комплексом пептид-МНС, содержащим неоантигенный пептид. В некоторых вариантах осуществления, идентификация неоантиген-специфических Т-клеток включает контакт популяции Т клеток с комплексом пептид-МНС, содержащим неоантигенный пептид. В некоторых вариантах осуществления, идентификация неоантиген-специфических Т-клеток включает контакт популяции Т клеток с APC, содержащими комплекс пептид-МНС. В некоторых вариантах осуществления, идентификация неоантиген-специфических Т-клеток дополнительно содержит выделение Т клеток из популяции Т клеток, специфичных к комплексу пептид-МНС. В некоторых вариантах осуществления, идентификация неоантиген-специфических Т-клеток дополнительно содержит идентификацию или прогнозирование Т клеток из популяции Т клеток, специфических к комплексу пептид-МНС на основе TCR клональности. В некоторых вариантах осуществления, идентификацию вариабельной последовательности TCR из неоантиген-специфических Т-клеток проводят до идентификации неоантиген-специфических Т-клеток. В некоторых вариантах осуществления, идентификация вариабельной последовательности TCR из неоантиген-специфических Т-клеток содержит секвенирование ДНК, РНК или их амплифицированных продуктов из одной или более неоантиген-специфических Т-клеток, которые кодируют вариабельную последовательность. В некоторых вариантах осуществления, идентификация вариабельной последовательности TCR из неоантиген-специфических Т-клеток содержит секвенирование ДНК, РНК или их амплифицированных продуктов из одной неоантиген-специфической Т клетки, которая кодирует вариабельную последовательность. В некоторых вариантах осуществления, идентификация вариабельной последовательности TCR из неоантиген-специфических Т-клеток содержит секвенирование штрихкодированной ДНК или штрихкодированной РНК, или их амплифицированных продуктов, из одной или более неоантиген-специфических Т-клеток, которые кодируют вариабельную последовательность. В некоторых вариантах осуществления, идентификация вариабельной последовательности TCR из неоантиген-специфических Т-клеток включает спаривание TCR-альфа цепи с TCR-бета цепью.
В некоторых вариантах осуществления, экспрессия рекомбинантного TCR включает экспрессию вариабельной последовательности, идентифицированной из полинуклеотида, содержащего последовательность, кодирующую идентифицированную вариабельную последовательность. В некоторых вариантах осуществления, полинуклеотидом является вектор. В некоторых вариантах осуществления, вектором является вирусный вектор. В некоторых вариантах осуществления, вирусным вектором является лентивирусный вектор. В некоторых вариантах осуществления, экспрессия рекомбинантного TCR включает трансдукцию или трансфекцию полинуклеотида в клетки. В некоторых вариантах осуществления, клетками являются линия Т-клеток или PMBC здорового донора.
В некоторых вариантах осуществления, идентификация одного или более пептидов комплекса пептид-МНС, которые представлены АРС, включает экспрессию одного или более пептидов в клетках. В некоторых вариантах осуществления, идентификация одного или более пептидов комплекса пептид-МНС, которые представлены АРС, включает загрузку одного или более пептидов в MHC клеток. В некоторых вариантах осуществления, идентификация одного или более пептидов комплекса пептид-МНС, которые представлены АРС, включает элюирование или выделение пептида одного или более пептидов из комплекса пептид-MHC. В некоторых вариантах осуществления, идентификация одного или более пептидов комплекса пептид-МНС, которые представлены АРС, включает проведение масс спектрометрии на пептиде из одного или более пептидов, которые выделены или элюированы из комплекса пептид-МНС. В некоторых вариантах осуществления, проведение функционального анализа включает определение экспрессии одного или более клеточных маркеров. В некоторых вариантах осуществления, один или более клеточных маркеров содержат TNF-α, IFN-γ, LAMP-1, 4-1BB, IL-2, IL-17A, Гранзим B, PD-1, CD25, CD69, TIM3, LAG3, CTLA-4, CD62L, CD45RA, CD45RO, FoxP3 или любое их сочетание.
ВКЛЮЧЕНИЕ В КАЧЕСТВЕ ССЫЛКИ
Все публикации, патенты и заявки на патенты, упомянутые в данном описании, включены сюда в качестве ссылки в той же степени, как если бы каждая отдельная публикация, патент или заявка на патент были специально и индивидуально указаны для включения в качестве ссылки.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Новые признаки изобретения подробно изложены в прилагаемой формуле изобретения. Лучшее понимание признаков и преимуществ настоящего изобретения будет получено при обращении к нижеследующему подробному описанию, в котором излагаются иллюстративные варианты осуществления, в которых используются принципы изобретения, и прилагаемым чертежам, в которых:
На ФИГ. 1 изображен технологический процесс идентификации и анализа антиген-специфических TCR. PBMC от здоровых доноров могут быть стимулированы антигеном, представляющим интерес, после чего антиген-специфические T клетки могут быть идентифицированы с мультимерами пептид-MHC (слева). Антиген-специфические T клетки могут быть выделены, и TCR могут быть секвенированы и проанализированы (слева от середины). TCR могут быть синтезированы и экспрессированы в клеточной линии или PBMC, и специфичность может быть снова подтверждена мультимером пептид-MHC (справа от середины). Линия TCR-экспрессирующих клеток или PBMC затем могут быть совместно культивированы с линиями антигенэкспрессирующих клеток для подтверждения функциональности TCR (справа).
На ФИГ. 2 представлен пример схемы размножения антигенспецифических CD8+ T клеток. PBMC могут быть стимулированы антигеном, представляющим интерес, и цитокинами. После размножения антигенспецифические CD8+ T клетки могут быть идентифицированы с мультимерами пептид-MHC.
На ФИГ. 3A представлен пример схемы конструктов рекомбинантного TCR и создания вектора для экспрессии конструктов TCR в клетках.
На ФИГ. 3B представлен пример схемы вирусного вектора, кодирующего рекомбинантные TCR для трансдукции или трансфекции в клетки.
На ФИГ. 4A изображен пример анализа проточной цитометрией размножения специфических к RAS антигену CD8+ T клеток в ответ на стимуляцию RAS пептидом.
На ФИГ. 4B изображен пример анализа проточной цитометрией специфических к RAS антигену клеток Jurkat после сортировки верхних 10% положительных к мультимеру клеток, экспрессирующих рекомбинантный TCR после пуромицинового выбора.
На ФИГ. 5 изображен пример анализа проточной цитометрией размножения специфических к RAS-пептид-HLA-A11:01 комплексу CD8+ T клеток в ответ на стимуляцию RAS G12V пептидом (слева), размножения специфических к RAS-пептид-HLA-A11:01 комплексу CD8+ T клеток в ответ на стимуляцию RAS G12C пептидом (середина) и размножения специфических к RAS-пептид-HLA-A11:01 комплексу CD8+ T клеток в ответ на стимуляцию RAS G12D пептидом (справа).
На ФИГ. 6A изображен пример анализа проточной цитометрией размножения специфических к RAS-пептид-HLA-A11:01 комплексу CD8+ T клеток в ответ на стимуляцию G12V или G12C мутантами RAS пептидов (слева), анализ распространенности клона TCR после секвенирования TCR из объединенных вариантов (середина) и подтверждение специфичности мутанта в сравнении с диким типом первых 2 извлеченных клонов после экспрессии рекомбинантного TCR в клетках Jurkat (справа).
На ФИГ.6B изображены экспериментальные результаты TCR функциональных анализов для оценки специфичности (слева) и авидности (справа) трех RAS TCR (RAS TCR-3, RAS TCR-4, RAS TCR-11). Графики показывают продуцирование IL-2 после совместного культивирования RAS TCR-трансдуцированных клеток Jurkat с клетками A375, экспрессирующими HLA-A11:01, загруженными либо RAS дикого типа или RAS-мутантного пептида (слева) или повышение количеств RAS-мутантного пептида (справа).
На ФИГ. 7A изображены экспериментальные результаты функционального анализа авидности TCR (пептидного титрования). График показывает продуцирование IL-2 после культивирования RAS TCR-трансдуцированных клеток Jurkat с клетками A375, экспрессирующими HLA-A11:01 загруженные повышающимися количествами RAS дикого типа или RAS мутантного пептида.
На ФИГ. 7B изображен пример графика, показывающего продуцирование IL-2 после совместного культивирования RAS TCR-4-трансдуцированных клеток Jurkat с клетками A375, модифицированными для экспрессии только HLA-A11:01, модифицированными для экспрессии HLA-A11:01 и KRAS G12V мутации, или модифицированными для экспрессии HLA-A11:01 и нерелевантной мутацией.
На ФИГ. 8A изображен пример графика, показывающего секрецию IFNγ из RAS TCR-4-трансдуцированных PBMC после совместного культивирования с природной RAS G12V мутантной линией SW620 клеток рака толстой кишки без обработки, с экспрессией HLA-A11:01 плюс добавленный RAS G12V и с экспрессией только HLA-A11:01.
На ФИГ. 8B изображен пример графика, показывающего активацию Каспазы-3 после совместного культивирования с RAS TCR-трансдуцированными PBMC в природной RAS G12V мутантной линии SW620 клеток рака толстой кишки без обработки, с экспрессией HLA-A11:01 плюс добавление RAS G12V пептида и с экспрессией только HLA-A11:01.
На ФИГ. 8C изображены экспериментальные результаты анализа цитотоксичности, в котором PBMC, трансдуцированные с нерелевантным TCR (слева) или RAS TCR-4 (справа), совместно культивированы с SW620 опухолевыми клетками-мишенями, экспрессирующими HLA-A11:01 и GFP при повышающемся диапазоне соотношений PBMC к мишеням. Графики изображают рост клеток-мишеней в течение 72 часов по данным GFP сигнала (верх) и гибель клеток-мишеней по данным подачи сигнала Аннексина V (низ), показывающий, что RAS TCR-трансдуцированные PBMC эффективно уничтожают клетки-мишени.
На ФИГ. 8D изображены экспериментальные результаты анализа цитотоксичности, в котором PBMC, трансдуцированные с нерелевантным TCR (слева) или RAS TCR-4 (справа) совместно культивируют с SNG-M опухолевыми клетками-мишенями при повышающемся диапазоне соотношений PBMC к мишеням. Графики изображают гибель клеток-мишеней по данным подачи сигнала Annexin V в течение 72 часов показывают, что RAS TCR-трансдуцированные PBMC уничтожают клетки-мишени.
На ФИГ. 8E изображает экспериментальные результаты скрининга безопасности RAS TCR-4. Слева представлен график, показывающий продуцирование IL-2 после совместного культивирования клеток Jurkat, трансдуцированных RAS TCR, с клетками A375, экспрессирующими HLA-A11:01, загруженными когнатными эпитопами RAS G12V или пептидами, в которых одно положение когнатного эпитопа изменено на аланин. В середине представлен график, показывающий продуцирование IL-2 после совместного культивирования клеток Jurkat, трансдуцированных RAS TCR, с клетками A375, экспрессирующими HLA-A11:01, загруженными эпитопами или пептидами RAS G12V, идентифицированными из начального скрининга безопасности. Справа представлен график, показывающий продуцирование IL-2 после совместного культивирования клеток Jurkat, трансдуцированных RAS TCR, с клетками A375, экспрессирующими HLA-A11:01, трансдуцированными Перилипином 4 и нагруженными пептидом RAS G12V или пептидом Перилипином 4 или без пептида (справа).
На ФИГ. 8F изображен технологический процесс, используемый для идентификации RAS TCR-26 и RAS TCR-27. Вверху слева представлен анализ проточной цитометрией размножения специфичных к комплексу RAS-пептид-HLA-A11:01 CD8+ Т-клеток в ответ на стимуляцию RAS G12V пептидом. Вверху справа показано измерение роста клеток-мишеней A375, экспрессирующих HLA-A11:01 и GFP, в течение 54 часов после совместного культивирования с размноженными CD8+ Т-клетками. В этом эксперименте Т-клетки, размноженные в присутствии пептидов, инкубируют с клетками A375, которые были загружены указанными количествами пептидов. Внизу слева показана специфическая цитотоксичность, рассчитанная через 48 часов сравнения клеток-мишеней, загруженных возрастающими количествами мутантного RAS-пептида, нормализованного к контролю, с пептидом дикого типа. Внизу справа показаны относительное распространение CDR3 областей TCR альфа и TCR бета после секвенирования одной клетки TCR в мультимер-положительных клетках. В левой части круговой диаграммы на ФИГ. 8F описаны "CAVKGGGSGTYKYIF" как SEQ ID NO: 603, "CAVGNNQGGKLIF" как SEQ ID NO: 604, "CAGPNTNAGKSTF" как SEQ ID NO: 605, "CAASIADGQKLLF" как SEQ ID NO: 606, "CAYIDAGNQFYF" как SEQ ID NO: 607, "CAVRGDSGGGADGLTF" как SEQ ID NO: 608, "CAVDIIGGKSTF" как SEQ ID NO: 609 и "CAANAGGTSYGKLTF" как SEQ ID NO: 610. В правой части круговой диаграммы на ФИГ. 8F описаны "CASSFFPTSTGRTDTQYF" как SEQ ID NO: 611, "CASSGPGPRGFNEQFF" как SEQ ID NO: 612, "CASSLGQDTEAFF" как SEQ ID NO: 613, "CASSESGSGEKLFF" как SEQ ID NO: 614, "CASITPRDEQFF" как SEQ ID NO: 615 и "CASSEWGSTGELFF" как SEQ ID NO: 616.
На ФИГ. 8G изображен технологический процесс, используемый для идентификации RAS TCR-28. Вверху слева представлен анализ проточной цитометрией размножения специфичных к комплексу RAS-пептид-HLA-A11:01 CD8+ Т клеток в ответ на стимуляцию RAS G12V пептидом. Вверху справа показано измерение роста клеток-мишеней A375, экспрессирующих HLA-A11:01 и GFP и загруженных различными количествами пептида, через 54 часа после совместного культивирования с размноженными CD8+ Т клетками. Данные показывают хорошую обратную корреляцию роста клеток с дозой пептида, что демонстрирует специфичность TCR к пептиду. Внизу слева показана специфическая цитотоксичность, рассчитанная через 48 часов сравнения клеток-мишеней, загруженных возрастающими количествами мутантного RAS-пептида, нормализованного к контролю с пептидом дикого типа. Внизу справа показаны относительные содержания CDR3 областей TCR альфа и TCR бета после секвенирования одной клетки TCR в мультимер-положительных клетках. В левой части круговой диаграммы, на ФИГ. 8G описаны "CAMREGRGAGNNRKLIW" как SEQ ID NO: 617, "CALSEAGLGGGKLIF" как SEQ ID NO: 618 и "CAASAVGQEYGNKLVF" как SEQ ID NO: 619. В правой части круговой диаграммы на ФИГ. 8G описаны "CASSQDRLAGDYEQYF" как SEQ ID NO: 620 и "CASSEYTMGTQYF" как SEQ ID NO: 621.
На ФИГ. 9 изображен пример анализа проточной цитометрией размножения специфических к RAS-пептид-HLA-A03:01 комплексу CD8+ T клеток в ответ на стимуляцию RAS G12V пептидом (слева) и специфических к RAS-пептид-HLA-A03:01 комплексу CD8+ T клеток в ответ на стимуляцию RAS G12C пептидом (справа).
На ФИГ. 10A изображен технологический процесс идентификации антигенспецифического TCR и анализ образца, изображенного на ФИГ. 9.
На ФИГ. 10B изображен технологический процесс идентификации антигенспецифического TCR образца, изображенного на ФИГ. 9.
На ФИГ. 10C изображены экспериментальные результаты анализы TCR функциональной авидности (пептидное титрование). Слева изображен график, показывающий продуцирование IL-2 после совместного культивирования RAS TCR-5-трансдуцированных клеток Jurkat с A375 клетками, экспрессирующими HLA-A03:01, загруженную повышающимися количествами RAS дикого типа или RAS мутантного пептида. Справа изображен график, показывающий продуцирование IL-2 после совместного культивирования RAS TCR-6-трансдуцированных клеток Jurkat с клетками A375, экспрессирующими HLA-A03:01, загруженными повышающимися количествами RAS дикого типа или RAS мутантного пептида.
На ФИГ. 10D изображены экспериментальные результаты анализа цитотоксичности, в котором PBMC, трансдуцированные с нерелевантным TCR (слева), RAS TCR-5 (середина) или RAS TCR-6 (справа) совместно культивируют с A375 опухолевыми клетками-мишенями, экспрессирующими HLA-A03:01 и GFP при повышающемся диапазоне соотношений PBMC к мишеням. Графики роста клеток-мишеней в течение 72 часов по данным GFP сигнала показывают, что RAS TCR-трансдуцированные PBMC эффективно уничтожают клетки-мишени.
На ФИГ. 10E изображены экспериментальные результаты анализа цитотоксичности, в котором PBMC, трансдуцированные с нерелевантным TCR, RAS TCR-5 или RAS TCR-6 совместно культивируют с NCI-H441 опухолевыми клетками-мишенями. Повышенный сигнал Аннексина V в клетках-мишенях в течение 48 часов показывают, что RAS TCR способны распознавать и уничтожать опухолевые клетки-мишени.
На ФИГ. 10F изображены экспериментальные результаты скрининга безопасности RAS TCR-5 (верх) и RAS TCR-6 (низ). Графики показывают продуцирование IL-2 после совместного культивирования RAS TCR-трансдуцированных клеток Jurkat с клетками A375, экспрессирующими HLA-A11:01, загруженными когнатным RAS G12V эпитопом или пептидами, в которых одно положение когнатного эпитопа изменено на аланин.
На ФИГ. 11 изображен пример технологического процесса для идентификации и анализа GATA3 антигенспецифического TCR. Слева изображен пример анализа проточной цитометрией размножения специфических к GATA3-пептид-HLA-A02:01 комплексу CD8+ T клеток в ответ на стимуляцию GATA3 мутантным пептидом.
На ФИГ. 12A изображены результаты анализа функциональной авидности TCR (пептидное титрование). График показывает продуцирование IL-2 после совместного культивирования GATA3 TCR-1-трансдуыироыанных T клеток с клетками, загруженными или трансдуцированными с повышающимися количествами GATA3 мутантного пептида.
На ФИГ. 12B изображен график, показывающий продуцирование IL-2 после совместного культивирования GATA3 TCR-трансдуцированных клеток Jurkat с клетками, загруженными нерелевантным пептидом или мутантным GATA3 пептидом, и клетками, трансдуцированными нерелевантным вектором или вектором, кодирующим GATA3 neoORF мутацию.
На ФИГ. 12C изображен график, показывающий положительную регуляцию продуцирования IFNγ в 2 образцах клеток, экспрессирующих контрольный пептид или GATA3 мутантный пептид.
На ФИГ. 12D изображен график, показывающий долю CD8 и CD107a положительных клеток в 2 образцах клеток, экспрессирующих контрольный пептид или GATA3 мутантный пептид.
На ФИГ. 12E изображен график, показывающий долю живых каспаза 3-положительных клеток в 2 образцах клеток, экспрессирующих контрольный пептид или GATA3 мутантный пептид.
На ФИГ. 13 изображен пример технологического процесса для идентификации и анализа TMPRSS2:ERG антигенспецифического TCR. Слева изображен пример анализа проточной цитометрией размножения специфических к TMPRSS2:ERG-пептид-HLA-A02:01 комплексу CD8+ T клеток в ответ на стимуляцию TMPRSS2:ERG мутантным пептидом.
На ФИГ. 14 изображен пример графика, показывающего продуцирование IL-2 после совместного культивирования TMPRSS2:ERG TCR-1-трансдуцированных клеток Jurkat с клетками 293T, без обработки, загруженными нерелевантным пептидом или загруженными TMPRSS2:ERG пептидом.
На ФИГ. 15 изображен пример технологического процесса для идентификации и анализа BTK антигенспецифического TCR. Слева изображен пример анализа проточной цитометрией размножения специфических к BTK-пептид-HLA-A02:01 комплексу CD8+ T клеток в ответ на стимуляцию BTK мутантным пептидом.
На ФИГ. 16A изображен пример анализа проточной цитометрией размножения специфических к EGFR-пептид-HLA-A02:01 комплексу CD8+ T клеток в ответ на стимуляцию EGFR T790M пептидом. Каждый график на ФИГ. 16A представляет образец размножения типовых Т клеток (лунка) с EGFR T790M пептидом. TCR из клеток секвенируют.
На ФИГ. 16B изображен пример анализа проточной цитометрией размножения специфических к EGFR-пептид-HLA-A02:01 комплексу CD8+ T клеток в ответ на стимуляцию EGFR T790M пептидом TCR которого предстоит севенировать. Каждый график на ФИГ. 16В представляет образец размножения типовых Т клеток (лунка) в ответ на EGFR T790M пептид.
ПОДРОБНОЕ ОПИСАНИЕ
Термин «примерно» или «приблизительно» означает в пределах допустимого диапазона ошибок для конкретного значения, как определено специалистом в данной области техники, который будет частично зависеть от того, как значение измеряется или определяется, т.е. от ограничений системы измерения. Например, «примерно» может означать в пределах 1 или более 1 стандартного отклонения в соответствии с практикой в данной области техники. Альтернативно, «примерно» может означать диапазон до 20%, до 10%, до 5% или до 1% от заданного значения. Альтернативно, особенно в отношении биологических систем или процессов, термин может означать в пределах порядка величины, предпочтительно в пределах 5-кратного и более предпочтительно 2-кратного значения. Если конкретные значения описаны в заявке и формуле изобретения, если не указано иное, термин «примерно» означает в пределах допустимого диапазона ошибок для конкретного значения.
Если не указано иное, все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понимается специалистом в области, к которой относится это описание. Хотя любые методы и материалы, аналогичные или эквивалентные тем, которые описаны в настоящем документе, также могут быть использованы на практике или при тестировании настоящего описания, описаны предпочтительные методы и материалы. Подробности одного или более конкретных вариантов осуществления изложены в описании ниже.
I. Определения
Если не указано иное, термин «TCR» должен пониматься как охватывающий полные TCR, а также их антигенсвязывающие части или антигенсвязывающие фрагменты (также называемые MHC-пептид связывающие фрагменты). В некоторых вариантах осуществления, TCR является интактным или полноразмерным TCR. В некоторых вариантах осуществления, TCR является антигенсвязывающей частью, которая меньше чем полноразмерный TCR, но которая связывается с определенной антигенной пептидной связью с (т.е. в контексте) молекулы MHC, т.е., MHC-пептидным комплексом. В некоторых случаях, антигенсвязывающая часть или фрагмент TCR может содержать только часть структурных доменов полноразмерного или интактного TCR, но также способен связывать эпитоп (например, MHC-пептидный комплекс), с которым связывается полный TCR. В некоторых случаях, антигенсвязывающая часть или фрагмент TCR содержит вариабельные домены TCR, такие как вариабельная α цепь и вариабельная β цепь TCR, достаточные для формирования сайта связывания с определенным MHC-пептидным комплексом, так, что обычно каждая цепь включает три определяющие комплементарность области. Включены полипептиды или белки, имеющие домен связывания, который является антигенсвязывающим доменом или является гомологичным антигенсвязывающему домену. TCR с определяющими комплементарность областями (CDR) и другие гуманизированные TCR (включая модификации CDR и модификации каркасной области) также охватываются этими терминами. Необходимо отметить, что хотя ссылка может быть сделана только на иммуноглобулиновые цепи (например, тяжелые цепи и легкие цепи), описанное изобретение может применяться, например, парам цепей Т-клеточного рецептора (TCRα и TCRβ цепей и TCRγ и TCRδ цепей) и не ограничено иммуноглобулинами.
Термины «определяющая комплементарность область» и «CDR», являющиеся синонимами «гипервариабельной области» или «HVR», известны в данной области техники и относятся к не непрерывным последовательностям аминокислот в TCR вариабельных областях, которые придают специфичность и/или аффинность связывания MHC-пептидному комплексу. В общем, имеется три CDR в каждой альфа цепи вариабельной области (CDR-H1, CDR-H2, CDR-H3) и три CDR в каждой бета цепи вариабельной области (CDR-L1, CDR-L2, CDR-L3). «Каркасные области» и «FR» известны в данной области техники как относящиеся к не CDR частям вариабельных областей альфа и бета цепей. В общем, имеется четыре FR в каждой полноразмерной вариабельной области альфа цепи (FR-H1, FR-H2, FR-H3 и FR-H4) и четыре FR в каждой полноразмерной вариабельной области бета цепи (FR-L1, FR-L2, FR-L3 и FR-L4).
Термин «вариабельная область» или «вариабельный домен» относятся к домену TCR альфа, бета, гамма или дельта цепи, который вовлечен в связывание TCR с антиген-MHC комплексами. Вариабельные домены альфа цепи и бета цепи (Vα и Vβ, соответственно) и гамма цепи и дельта цепи (Vγ и Vδ, соответственно) природного TCR обычно имеют похожие структуры, где каждый домен содержит четыре консервативных каркасных области (FR) и три CDR. Отдельного Vα или Vβ домена, или Vγ или Vδ домена, может быть достаточно для придания специфичности связывания с комплексом пептид-МНС.
Также в настоящем документе представлены TCR фрагменты, включая антигенсвязывающие фрагменты. В некоторых вариантах осуществления, TCR является его антигенсвязывающей частью, такой как вариант полноразмерного TCR, не содержащего его трансмембранные и/или цитоплазматические области, которая может быть названа полностью растворимым TCR. В некоторых вариантах осуществления, TCR является димерный TCR (dTCR). В некоторых вариантах осуществления, TCR является одноцепочечный (scTCR), такой как scTCR, имеющий структуру, описанную в патентных публикациях PCT №№ WO2003/020763, WO2004/033685 или WO2011/044186. В определенных вариантах осуществления, TCR является одноцепочечный TCR фрагмент, содержащий вариабельную область альфа цепи, связанную с вариабельной областью бета цепи, такой как scTv. В некоторых вариантах осуществления, scTv также называют scFv. Одноцепочечный Tv или scTv в некоторых аспектах относится к TCR фрагментам, которые содержат вариабельные домены альфа или гамма цепи (Vα или Vγ) и вариабельные домены бета или дельта цепи (Vβ или Vδ) TCR, где эти домены присутствуют в одной полипептидной цепи. В общем, Tv полипептид дополнительно содержит полипептидный линкер между Vα и Vβ доменами или Vγ и Vδ доменами, которые позволяют scTv формировать желаемую структуру для связывания антигена. В некоторых аспектах диатело относится к TCR фрагментам с двумя антигенсвязывающими сайтами, где фрагменты содержат Vα, соединенную с Vβ в одной полипептидной цепи (Vα-Vβ) или Vγ, соединенную с Vδ в одной полипептидной цепи (Vγ-Vδ). При применении линкера, который слишком короткий для того, чтобы позволить спаривание между двумя доменами на одной цепи, домены вынуждены спариваться с комплементарными доменами другой цепи и создавать два антигенсвязывающих сайта. Типовые диатела более подробно описаны в, например, EP404097 и WO93111161. В некоторых аспектах, Fv относится к TCR фрагменту, который содержит полное распознавание комплекса пептид-МНС и сайт связывания комплекса пептид-МНС. Эта область состоит из димера одной TCRα цепи и одной TCRβ цепи или одной TCRγ цепи и одной TCRδ цепи в тесной, не ковалентной связи. Именно в этой конфигурации три CDR каждого вариабельнго домена взаимодействуют с определением сайта связывания комплекса пептид-МНС на поверхности Vα-Vβ димера или Vγ-Vδ димера. Вместе, комбинация одной или более CDR из каждой из Vα-Vβ цепей или Vγ-Vδ цепей придает комплексу пептид-МНС специфичность связывания с TCR. Например, должно быть понятно, что, например, CDRα3 и CDRβ3 или CDRγ3 и CDRδ3 могут быть достаточными для придания антигенсвязывающей специфичности TCR при переносе на Vα и Vβ цепи или Vγ-Vδ цепи реципиента, выбранного TCR или его антигенсвязывающим фрагментом, и эта комбинация CDR может быть тестирована на связывание, сродство и т.д. Кроме того, хотя два домена Tv фрагмента (Vα и Vβ или Vγ и Vδ ) кодированы отдельными генами, они могут быть соединены с применением рекомбинатнных способов синтетическим линкером, который позволяет им существовать в виде одной белковой цепи, в которой области Vα и Vβ или Vγ и Vδ цепи спариваются с образованием одновалентных молекул (известных как одноцепочечный Tv (scTv). Такие scTv также охватываются связывающей частью комплекса пептид-МНС TCR.
«Биспецифический TCR» относится в некоторых аспектах к TCR, которые показывают специфичность к двум разным комплексам пептид-МНС или двум разным типам комплексов пептид-МНС. Применяемые здесь термины специфически включают, без ограничений, TCR, которые демонстрируют специфичность связывания с целевым комплексом пептид-МНС и с другим комплексом пептид-МНС, который способствует доставке в конкретную ткань. Также, мультиспецифические TCR имеют две или более специфичностей связывания. Линейный TCR относится, в некоторых аспектах, к паре тандемных Fd сегментов (например, Vα-Cα1-Vα-Cα1), которые образуют пару антигенсвязывающих областей. Линейные TCR могут быть биспецифическими или моноспецифическими.
«Антигенсвязывающий домен» относится в некоторых аспектах к одному или более фрагментам TCR, которые сохраняют способность специфически связываться с комплексом пептид-МНС. Неограничивающие примеры TCR фрагментов включенные в такие термины включают, но не ограничены ими, (i) Tab фрагмент, одновалентный фрагмент, состоящий из Vβ, Vα, Cβ и Cα доменов; (ii) T(ab’)2 фрагмент, двухвалентный фрагмент, содержащий два Tab фрагмента, связанных дисульфидным мостиком в шарнирной области; (iii) Td фрагмент, состоящий из Vα и Cα1 доменов; (iv) Tv фрагмент, содержащий Vβ и Vα домены одного плеча TCR, включая scTvs, (v) dAb фрагмент (Ward et al., (1989) Nature 341:544 546), который содержит Vα домен; и (vi) выделенную CDR. В это определение включены TCR с одной альфа цепью или одной бета цепью.
В представленные TCR включены гуманизированные и человеческие TCR. «Гуманизированным» TCR является TCR, в котором все или по существу все CDR аминокислотные остатки получены из CDR не человека, и все или по существу все FR аминокислотные остатки получены из FR человека. Гуманизированный TCR необязательно может включать, по меньшей мере, часть константной области TCR, полученную из TCR человека. «Гуманизированная форма» TCR не человека относится к варианту TCR не человека, который имеет, прошел гуманизацию, обычно для снижения иммуногенности у людей, при этом сохраняя специфичность и аффинность исходного TCR не человека. В некоторых вариантах осуществления, некоторые FR остатки в гуманизированном TCR замещены соответствующими остатками из TCR не человека (например, TCR, из которого получены CDR остатки), например, для восстановления или улучшения специфичности и аффинности TCR. «TCR человека» является TCR с аминокислотной последовательностью, соответствующей таковой TCR, продуцированного человеком или клеткой человека, или отличным от человека источником, применяющим репертуары TCR человека или другие последовательности, кодирующие TCR человека, включая библиотеки TCR человека. Термин исключает гуманизированные формы не человеческих TCR, содержащие связывающие области не человеческого комплекса пептид-МНС, такие, как те, в которых все или по существу все CDR являются не человеческими. TCR человека могут быть получены введением иммуногена трансгенному животному, которое имеет, было модифицировано для продуцирования интактных TCR человека или интактных TCR с вариабельными областями человека в ответ на провокацию антигеном. Такие животные обычно содержат все или часть локусов TCR человека, которые замещают локусы эндогенного TCR, или которые присутствуют экстрахромосомно или интегрированы произвольно в хромосомы животного. У таких трансгенных животных, локусы эндогенного TCR обычно инактивированы. TCR человека также могут быть получены из библиотек TCR человека, включая фаговый дисплей и бесклеточные библиотеки, содержащие последовательности, кодирующие TCR, полученные из репертуара человека.
Термин «раковый неоантиген» или «неоантиген» или «неоэпитоп» может относиться к антигенам, которые не кодированы в нормальном не мутированном геноме хозяина. Неоантиген может относиться к антигену, включающему одну или более модификаций аминокислоты по сравнению с исходным антигеном. Например, неоантигеном может быть опухолеассоциированный неоантиген, где термин «опухолеассоциированный неоантиген» может включать пептид или белок, включающий модификации аминокислот из-за опухолеспецифических мутаций. В некоторых случаях, неоантиген представляет либо онкогенные вирусные белки, либо аномальные белки, которые возникают как следствие соматических мутаций. Например, неоантиген может возникать в результате нарушения клеточных механизмов за счет активности вирусных белков. Другим примером может быть воздействие канцерогенного соединения, которое в некоторых случаях может привести к соматической мутации. Эта соматическая мутация в конечном итоге может привести к образованию опухоли/рака. Неоантиген может быть классом опухолевых антигенов, которые возникают в результате опухолеспецифических изменений белков. Неоантигены охватывают, но не ограничены ими, опухолевые антигены, которые возникают, например, в результате замещения в белковой последовательности, мутации «сдвига рамки», слияния полипептида, делеции в рамке считывания, вставки и экспрессии эндогенного ретровирусного полипептида. Неоэпитопом может быть эпитоп, которого нет в эталоне, таком как здоровая клетка, например, не злокачественная клетка или клетка зародышевой линии, но который обнаруживается в больной клетке, например, раковой клетке. Сюда включены ситуации, когда соответствующий эпитоп обнаруживается в нормальной здоровой клетке или клетке зародышевой линии, но из-за одной или более мутаций в больной клетке, например, в раковой клетке, последовательность эпитопа изменяется, что дает неоэпитоп.
«Эпитоп» в некоторых аспектах относится к части антигена или другой макромолекулы, способной образовывать связывающее взаимодействие со связывающим карманом вариабельной области TCR. В некоторых аспектах, эпитоп относится к части комплекса пептид-МНС, способной образовывать связывающее взаимодействие со связывающим карманом вариабельной области TCR. Такие связывающие взаимодействия могут проявляться как межмолекулярный контакт с одним или более аминокислотными остатками одной или более CDR. Связывание комплекса пептид-МНС может включать, например, CDR3, пару CDR3 или, в некоторых случаях, взаимодействия вплоть до всех шести CDR Vα и Vβ цепей или Vγ или Vδ цепей. Эпитопом может быть линейная пептидная последовательность (т.е. «непрерывная») или он может состоять из не непрерывных аминокислотных последовательностей (т.е. «конформационных» или «прерывистых»). TCR может распознавать одну или более аминокислотных последовательностей. Поэтому эпитоп может определять более одной отдельной аминокислотной последовательности. В некоторых аспектах, TCR может распознавать одну или более аминокислотных последовательностей или эпитопов в контексте MHC. Эпитопы, распознаваемые TCR, могут быть определены методами пептидного картирования и анализа последовательности, хорошо известными специалистам в данной области. Связывающие взаимодействия проявляются как межмолекулярные контакты с одним или более аминокислотными остатками CDR. Эпитоп может относиться к антигенной детерминанте в молекуле, такой как антиген, т.е. к части или фрагменту молекулы, которая распознается иммунной системой, например, которая распознается Т клеткой, в частности при представлении в контексте молекул MHC. Эпитоп белка, такого как опухолевый антиген, может включать непрерывную или прерывистую часть белка и может иметь от 5 до 100, от 5 до 50, от 8 до 30 или от 10 до 25 аминокислот в длину, например, эпитоп может быть 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 аминокислот в длину.
Термин «связывание» относится к прямой связи между двумя молекулами, например, из-за ковалентных, электростатических, гидрофобных и ионных и/или водородных взаимодействий в физиологических условиях, и включает такие взаимодействия, как солевые мостики и водные мостики, а также любые другие общепринятые средства связывания.
В некоторых вариантах осуществления, ссылка на TCR со «специфическим связыванием» относится к ситуации, в которой TCR не будет демонстрировать какого-либо значительного связывания с молекулами, отличными от комплекса пептид-МНС, содержащего эпитоп, распознаваемый TCR. Термин также применим, когда, например, антигенсвязывающий домен является специфическим для определенного эпитопа, который переносится множеством комплексов пептид-МНС, и в этом случае выбранный TCR или его фрагмент связывания или комплекса пептид-МНС, несущий домен связывания комплекса пептид-МНС, сможет связываться с различными комплексами пептид-МНС, несущими эпитоп. Термин «преимущественно связывает» или «специфически связывает» означает, что TCR или их фрагменты связываются с эпитопом с большей аффинностью, чем они связывают неродственные аминокислотные последовательности, и, если они перекрестно реагируют с другими полипептидами, содержащими эпитоп, не являются токсичными на уровнях в котором они составлены для использования человеком. В одном аспекте, такая аффинность в, по меньшей мере, 1-раз больше, по меньшей мере, 2-раза больше, по меньшей мере, 3-раза больше, по меньшей мере, 4-раза больше, по меньшей мере, 5-раз больше, по меньшей мере, 6-раз больше, по меньшей мере, 7-раз больше, по меньшей мере, 8-раз больше, по меньшей мере, 9-раз больше, 10-раз больше, по меньшей мере, 20-раз больше, по меньшей мере, 30-раз больше, по меньшей мере, 40-раз больше, по меньшей мере, 50-раз больше, по меньшей мере, 60-раз больше, по меньшей мере, 70-раз больше, по меньшей мере, 80-раз больше, по меньшей мере, 90-раз больше, по меньшей мере, 100-раз больше, или, по меньшей мере, 1000-раз больше, чем аффинность TCR или его фрагмент к неродственным аминокислотным последовательностям.
Термин «аффинность» относится к мере силы связывания между двумя членами связывающей пары (например, пептидом, связывающим человеческий лейкоцитарный антиген (HLA) и HLA I или II класса, или комплексом пептид-HLA и Т-клеточным рецептором (TCR)). Аффинность моет быть выражена как константа равновесия обратимого связывания двух агентов и может быть выражена как KD, KA, Koff или Kon. KD относится к константе диссоциации между двумя членами связывающей пары и имеет единицы молярности. KA относится к константе аффинности между двумя членами связывающей пары и является обратной константе диссоциации. Аффинность может быть определена экспериментально, например, поверхностным плазмонным резонансом (SPR) с применением коммерчески доступных единиц Biacore SPR. Koff относится к константе скорости диссоциации двух членов связывающей пары (например, константе скорости диссоциации HLA-связывающего пептида и HLA I или II класса, или комплекса пептид-HLA и TCR). Kon относится к константе скорости ассоциации двух членов связывающей пары (например, константе скорости ассоциации HLA-связывающего пептида и HLA I или II класса, или комплекса пептид-HLA и TCR). Аффинность связывания белка с лигандом, такая как аффинность TCR к эпитопу может составлять, например, от примерно 100 наномолей (нМ) до примерно 0,1 нМ, от примерно 100 нМ до примерно 1 пикомолей (пМ), или от примерно 100 нМ до примерно 1 фемтомоля (фМ). Термин «авидность» относится к резистентности комплекса двух или более агентов к диссоциации после разведения.
В настоящем описании, результаты «данных связывания» могут быть выражены как «IC50». Аффинность также может быть выражена как ингибирующая концентрация 50 (IC50) или концентрация, при которой 50% первого члена связывающей пары (например, пептида) замещена. Также, ln(IC50) относится к натуральному логарифму IC50. Например, IC50 может быть концентрацией тестируемого пептида в анализе связывания, при которой наблюдается 50% ингибирование связывания меченого эталонного пептида. Принимая во внимание условия, в которых проводят анализ (например, ограничивая концентрации HLA белка и/или концентрации меченого эталонного пептида), эти значения могут быть приблизительными значениями KD. Анализы для определения связывания хорошо известны в данной области техники и описаны подробно, например, в публикациях PCT WO 94/20127 и WO 94/03205 и других публикациях, таких как Sidney et al., Current Protocols in Immunology 18.3.1 (1998); Sidney, et al., J. Immunol. 154:247 (1995); и Sette, et al., Mol. Immunol. 31:813 (1994). Альтернативно, связывание может быть выражено относительно связывания эталонным стандартным пептидом. Связывание также может быть определено с применением других аналитических систем, включая такие, в которых применяют: живые клетки (например, Ceppellini et al., Nature 339:392 (1989); Christnick et al., Nature 352:67 (1991); Busch et al., Int. Immunol. 2:443 (1990); Hill et al., J. Immunol. 147:189 (1991); del Guercio et al., J. Immunol. 154:685 (1995)), бесклеточные системы с применением лизатов после обработки детергентом (например, Cerundolo et al., J. Immunol. 21:2069 (1991)), иммобилизованные очищенные MHC (например, Hill et al., J. Immunol. 152, 2890 (1994); Marshall et al., J. Immunol. 152:4946 (1994)), системы ELISA (например, Reay et al., EMBO J. 11:2829 (1992)), поверхностный плазмонный резонанс (например, Khilko et al., J. Biol. Chem. 268:15425 (1993)); тердофазные анализы с большой плотностью потока (Hammer et al., J. Exp. Med. 180:2353 (1994)) и измерения стабилизации или сборки MHC I класса (например, Ljunggren et al., Nature 346:476 (1990); Schumacher et al., Cell 62:563 (1990); Townsend et al., Cell 62:285 (1990); Parker et al., J. Immunol. 149:1896 (1992)).
Термины «главный комплекс гистосовместимости» и аббревиатура «MHC» могут включать молекулы MHC I класса и MHC II класса и относится к комплексу генов, которые возникают у всех млекопитающих. Белки или молекулы MHC могут быть важны для передачи сигналов между лимфоцитами и антигенпрезентирующими клетками или больными клетками в иммунных реакциях, где белки или молекулы MHC связывают пептиды и представляют их для распознавания Т-клеточными рецепторами. Белки, кодированные MHC, могут экспрессироваться на поверхности клеток, и отображать как собственные антигены (пептидные фрагменты из самой клетки), так и чужеродные антигены (например, фрагменты инвазивных микроорганизмов) в Т клетке. Область MHC можно разделить на три подгруппы: класс I, класс II и класс III. Белки MHC класса I могут содержать α-цепь и β2-микроглобулин (не часть MHC, кодируемого хромосомой 15). Они могут представлять фрагменты антигена цитотоксическим Т клеткам. Белки MHC класса II могут содержать α- и β-цепи и могут представлять фрагменты антигена Т хелперам. Область MHC класса III может кодировать другие иммунные компоненты, такие как компоненты комплемента и цитокины. MHC может быть как полигенным (существует несколько генов MHC класса I и MHC класса II), так и полиморфным (существует множество аллелей каждого гена).
Термин «гаплотип» может относиться к аллелям человеческого лейкоцитарного антигена (HLA), обнаруженным на одной хромосоме, и к кодируемым им белкам. Гаплотип может также относиться к аллели, присутствующей в любом одном локусе в MHC. Каждый класс MHC представлен несколькими локусами: например, HLA-A (человеческий лейкоцитарный антиген-A), HLA-B, HLA-C, HLA-E, HLA-F, HLA-G, HLA-H, HLA-J, HLA-K, HLA-L, HLA-P и HLA-V для класса I и HLA-DRA, HLA-DRB1-9, HLA-DQA1, HLA-DQB1, HLA-DPA1, HLA-DPB1, HLA-DPB2, HLA-DMA, HLA-DMB, HLA-DOA и HLA-DOB для класса II. Термины «HLA аллель» и «MHC аллель» применяют здесь взаимозаменяемо.
Термины «полинуклеотид», «нуклеотид», «нуклеотидная последовательность», «нуклеиновая кислота» и «олигонуклеотид» применяют взаимозаменяемо. Они могут относиться к полимерной форме нуклеотидов любой длины, либо дезоксирибонуклеотидам, либо рибонуклеотидам или их аналогам. Полинуклеотиды могут иметь любую трехмерную структуру и могут выполнять любую функцию, известную или неизвестную. Ниже представлены неограничивающие примеры полинуклеотидов: кодирующие или некодирующие области гена или фрагмент гена, локусы (локус), определенные из анализа связывания, экзоны, интроны, информационная РНК (иРНК), транспортная РНК (тРНК), рибосомная РНК (рРНК), короткая интерферирующая РНК (siРНК), короткая шпилечная РНК (shРНК), микро-РНК (miРНК), рибозимы, кДНК, рекомбинантные полинуклеотиды, разветвленные полинуклеотиды, плазмиды, векторы, изолированная ДНК любой последовательности, изолированная РНК любой последовательности, зонды нуклеиновой кислоты и праймеры. Полинуклеотид может содержать один или более модифицированных нуклеотидов, таких как метилированные нуклеотиды и аналоги нуклеотидов. Если присутствуют, модификации нуклеотидной структуры могут быть внесены до или после сборки полимера. Полинуклеотиды могут включать нестандартные нуклеотиды, такие как аналоги нуклеотидов или модифицированные нуклеотиды. В некоторых вариантах осуществления нестандартные нуклеотиды могут стабилизировать образование гибрида. В некоторых вариантах осуществления, нестандартные нуклеотиды могут дестабилизировать образование гибрида. В некоторых вариантах осуществления, нестандартные нуклеотиды могут повышать специфичность гибридизации. В некоторых вариантах осуществления, нестандартные нуклеотиды могут снижать специфичность гибридизации. Примеры модификаций нестандартных нуклеотидов включают 2 'O-Me, 2' O-аллил, 2 'O-пропаргил, 2' O-алкил, 2 'фтор, 2' арабино, 2 'ксило, 2' фторарабино, фосфоротиоат, фосфородитиоат фосфороамидаты, 2 'амино, 5-алкилзамещенный пиримидин, 3' дезоксигуанозин, 5-галогензамещенный пиримидин, алкилзамещенный пурин, галогензамещенный пурин, бициклические нуклеотиды, 2'MOE, молекулы PNA, молекулы LNA, LNA-подобные молекулы, диаминопурин, S2T, 5-фторурацил, 5-бромурацил, 5-хлороурацил, 5-йодурацил, гипоксантин, ксантин, 4-ацетилцитозин, 5-(карбоксигидроксилметил)урацил, 5-карбоксиметиламинометил-2-тиуридин, 5-карбоксиметиламинометилурацил, дигидроурацил, бета-D-галактозилкеозин, инозин, N6-изопентениладенин, 1-метилгуанин, 1-метилинозин, 2,2-диметилгуанин, 2-метиладенин, 2-метилгуанин, 3-метилцитозин, 5-метилцитозин, N6-аденин, 7-метилгуанин, 5-метиламинометилурацил, 5-метоксиаминометил-2-тиоурацил, бета-D-маннозилкеозин, 5'-метоксикарбоксиметилурацил, 5-метоксиурацил, 2-метилтио-D46-изопентениладенин, урацил-5-оксиуксусная кислота (v), вибутоксозин, псевдурацил, кеозин, 2-тиоцитозин, 5-метил-2-тиоурацил, 2-тиоурацил, 4-тиоурацил, 5-метилурацил, метиловый эфир урацил-5-оксиуксусной кислоты, урацил-5-оксиуксусная кислота (v), 5-метил-2-тиоурацил, 3-(3-амино-3-N-2-карбоксипропил)урацил, (acp3)w, 2,6-диаминопурин и их производные. Последовательность нуклеотидов может быть прервана не нуклеотидными компонентами. Полинуклеотид может быть дополнительно модифицирован после полимеризации, например, путем конъюгации с метящим компонентом.
«Комплементарность» может относиться к способности нуклеиновой кислоты образовывать водородную связь(и) с другой последовательностью нуклеиновой кислоты либо традиционным методом Уотсона-Крика или другими нетрадиционными типами. Процент комплементарности может указывать на долю остатков в молекуле нуклеиновой кислоты, которые могут образовывать водородные связи (например, спаривание оснований Уотсона-Крика) со второй последовательностью нуклеиновой кислоты (например, 5, 6, 7, 8, 9, 10 из 10, имеющие 50%, 60%, 70%, 80%, 90% и 100% комплементарности, соответственно). «Совершенно комплементарный» может означать, что все непрерывные остатки последовательности нуклеиновой кислоты будут связаны водородом с таким же количеством непрерывных остатков во второй последовательности нуклеиновой кислоты. «По существу комплементарный» относится к степени комплементарности, которая составляет, по меньшей мере, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% или 100% в области 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 35, 40, 45, 50 или более нуклеотидов, или могут относиться к двум нуклеиновым кислотам, которые гибридизуются в жестких условиях. Идентичность последовательности, например, для целей оценки доли комплементарности, может быть измерена подходящим алгоритмом выравнивания, включающим, но не ограниченным ими, алгоритм Нидлмана-Вунша (например, установка совмещения EMBOSS Needle от www.ebi.ac.uk/Tools/psa/emboss_needle/nucleotide.html, необязательно с уставками по умолчанию), алгоритм BLAST (см., например, инструмент для выравнивания BLAST от blast.ncbi.nlm.nih.gov/Blast.cgi, необязательно с уставками по умолчанию), или алгоритм Смита-Уотермана. Оптимальное выравнивание может быть оценено с применением любых подходящих параметров выбранного алгоритма, включая параметры по умолчанию.
Термины «полипептид» и «белок» применяют взаимозаменяемо и они относятся к полимеру аминокислотных остатков и не ограничены минимальной длиной. Например, полипептид может содержать, по меньшей мере, примерно 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 30, 40, 50, 60, 70, 80, 90, 100, 200, 300, 400, 500, 600, 700, 800, 900, или 1000 пептидов или аминокислот. Примеры полипептидов включают, но не ограничены ими, аминокислотные цепи, белки, пептиды, гормоны, полипептидные сахариды, липиды, гликолипиды, фосфолипиды, антитела, ферменты, киназы, рецепторы, факторы транскрипции и лиганды. Полипептиды, включая предоставленные TCR и цепи TCR и другие пептиды, например линкеры и связывающие пептиды, могут включать аминокислотные остатки, включая природные и/или не природные аминокислотные остатки. Термины также включают пост-экспрессионные модификации полипептида, например, гликозилирование, сиалилирование, ацетилирование, фосфорилирование и подобные. В некоторых аспектах полипептиды могут содержать модификации по отношению к нативной или природной последовательности, пока белок поддерживает желаемую активность. Эти модификации могут быть преднамеренными, например, сайт-направленный мутагенез, или могут быть случайными, например, мутация хозяев, которые продуцируют белки, или ошибок из-за амплификации ПЦР.
Используемые здесь двадцать обычных аминокислот и их аббревиатуры, известные специалисту в данной области техники, соответствуют общепринятому использованию. Стереоизомеры (например, D-аминоаминокислота) двадцати обычных аминокислот, не природные аминокислоты, такие как α-, α-дизамещенные аминокислоты, N-алкильные аминокислоты, молочная кислота и другие нестандартные аминокислоты, также могут быть подходящими компонентами для полипептидов по настоящему изобретению. Примеры нестандартных аминокислот включают: 4-гидроксипролин, γ-карбоксиглутамат, ε-N, N,N-триметиллизин, ε-N-ацетиллизин, O-фосфосерин, N-ацетилсерин, N-формилметионин, 3-метилгистидин, 5-гидроксилизин, σ-N-метиларгинин и другие аналогичные аминокислоты и иминокислоты (например, 4-гидроксипролин). В используемом здесь условном обозначении полипептида левым направлением является амино-концевое направление, и правым направлением является карбокси-концевое направление, в соответствии со стандартным использованием и соглашением. Долей (%) идентичности в отношении полипептидной последовательности (или последовательности нуклеиновой кислоты) является доля аминокислотных остатков (или нуклеотидов в случае последовательности нуклеиновой кислоты) в кандидатной последовательности, которые идентичны аминокислотным остаткам (или нуклеотидам) в эталонной полипептидной последовательности (или последовательности нуклеиновой кислоты) после выравнивания последовательностей и введения гэпов, если необходимо, для достижения максимальной доли идентичности последовательности и без учета каких-либо консервативных замещений как части идентичности последовательности. Выравнивание для определения процента идентичности аминокислотных последовательностей может быть достигнуто различными способами, которые известны специалистам в данной области, например, с использованием общедоступного компьютерного программного обеспечения, такого как программное обеспечение BLAST, BLAST-2, ALIGN или Megalign (DNASTAR). Специалисты в данной области могут определить подходящие параметры для выравнивания последовательностей, включая любые алгоритмы, необходимые для достижения максимального выравнивания по всей длине сравниваемых последовательностей. Однако для целей настоящего описания значения доли идентичности аминокислотной последовательности генерируют с использованием компьютерной программы сравнения последовательностей ALIGN-2. Компьютерная программа сравнения последовательности ALIGN-2 была разработана Genentech, Inc., а исходный код был помещен вместе с пользовательской документацией в U.S. Copyright Office, Washington D.C., 20559, где он зарегистрирован под U.S. Copyright Registration No. TXU510087. Программа ALIGN-2 является общедоступной от Genentech, Inc., South San Francisco, Calif., или могут быть скомпилированы из исходного кода. Программа ALIGN-2 может быть скомпилирована для применения на операционной системе UNIX, включая цифровую UNIX V4.0D. Все параметры сравнения последовательностей установлены программой ALIGN-2 и не варьируются. В ситуациях, где ALIGN-2 применяют для сравнения аминокислотных последовательностей, % идентичности аминокислотных последовательностей данной аминокислотной последовательности A к, с или против данной аминокислотной последовательности B (которая альтернативно может быть перефразирована как данная аминокислотная последовательность A, которая имеет, или содержит определенный % идентичности аминокислотной последовательности к, с или против данной аминокислотной последовательности B) рассчитывают следующим образом: 100 умножить на X/Y, где X равно количеству аминокислотных остатков, оцененных как идентично совпадающие по программе выравнивания последовательностей ALIGN-2 в выравнивании A и B по программе, и где Y является общим количеством аминокислотных остатков в B. Следует понимать, что там, где длина аминокислотной последовательности A не равна длине аминокислотной последовательности B, % идентичности аминокислотных последовательностей A и B не будет равен % идентичности аминокислотных последовательностей B и A. Если специально не указано иное, все % значения идентичности аминокислотных последовательностей, используемые здесь, получены, как описано в предыдущем абзаце, с использованием компьютерной программы ALIGN-2.
«Последовательность зародышевой линии» относится к генетической последовательности из гаплоидных гамет и тех диплоидных клеток, из которых они сформированы. ДНК зародышевой линии содержит несколько генных сегментов, которые кодируют одну TCRα или TCRβ цепь или одну TCRγ или TCRδ цепь. Эти генные сегменты переносятся в зародышевых клетках, но не могут быть транскрибированы и транслированы, пока не будут преобразованы в функциональные гены. Во время дифференциации Т клеток в костном мозге, эти генные сегменты случайным образом перетасовываются динамической генетической системой, способной генерировать более 108 специфичностей.
Ингибирование, «лечение» и «лечить» используются взаимозаменяемо и относятся, например, к остановке развития симптомов, продлению выживаемости, частичному или полному ослаблению симптомов и частичному или полному устранению состояния, заболевания или расстройства, связанного с избыточными уровнями белка или коррелирующего с активностью белка. Например, лечение рака включает, но не ограничено ими, остановку развития, частичное или полное устранение злокачественного новообразования или опухоли. Лечение или частичное устранение включает, например, уменьшение роста или размера опухоли и/или объема опухоли примерно в 2 раза, примерно в 3 раза, примерно в 4 раза, примерно в 5 раз, примерно в 10 раз, примерно в 20 раз, примерно в 50 раз или любая промежуточная кратность. Точно так же лечение или частичное устранение может включать процентное уменьшение роста или размера опухоли и/или объема примерно на 1%, 2%, 3%, 4%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или любое процентное уменьшение между ними. Профилактика относится к профилактике, предотвращению появления симптомов, предотвращению прогрессирования заболевания или расстройства, связанного с избыточными уровнями белка или коррелирующего с активностью белка.
«Субъект», «индивидуум», «хозяин» или «пациент» относится к живым организмам, таким как млекопитающие. Примеры субъектов и хозяев включают, но не ограничены ими, лошадей, коров, верблюдов, овец, свиней, коз, собак, кошек, кроликов, морских свинок, крыс, мышей (например, гуманизированных мышей), песчанок, нечеловеческих приматов (например, макаков), людей и подобных, не млекопитающих, в том числе, например, позвоночных животных, не являющихся млекопитающими, таких как птицы (например, куры или утки), рыбы (например, акулы) или лягушки (например, Xenopus) и не млекопитающих беспозвоночных, а также их трансгенные виды.
«Набор» относится к системе доставки материалов или реагентов для выполнения способа, раскрытого в настоящем документе. В некоторых вариантах осуществления, наборы включают системы, которые позволяют хранить, транспортировать или доставлять реагенты (например, зонды, ферменты и т.д. в подходящих контейнерах) и/или вспомогательные материалы (например, буферы, письменные инструкции по проведению анализа и т.д.) из одного места в другое. Например, наборы включают один или более вкладок (например, коробок), содержащих соответствующие реагенты и/или вспомогательные материалы. Такое содержимое может быть доставлено предполагаемому реципиенту вместе или по отдельности. Например, первый контейнер может содержать фермент для использования в анализе, тогда как второй контейнер содержит множество праймеров. Упаковка относится к физической структуре, в которой находятся компоненты набора. Упаковочный материал может обеспечивать стерильность компонентов и может быть изготовлен из материала, обычно используемого для таких целей (например, бумаги, гофрированного волокна, стекла, пластика, фольги, ампул и т.д.). Этикетка или вкладыш в упаковку могут включать соответствующие письменные инструкции. Поэтому наборы могут дополнительно включать этикетки или инструкции по использованию компонентов набора в любом способе изобретения. Набор может включать соединение в упаковке или дозаторе вместе с инструкциями по введению соединения в способе, описанном в настоящем документе.
Термин «мутация резистентности» относится к мутации гена, которая позволяет гену или клетке-хозяину, содержащей этот ген, стать резистентной к лечению лекарственным средством. Например, мутация BTK C481S является мутацией резистентности, которая может придавать резистентность к ибрутинибу.
II. Обзор
В настоящем раскрытии представлены Т-клеточные рецепторы (TCR) против неоантигенов, молекулы выделенной нуклеиновой кислоты, кодирующие TCR против неоантигенов, Т-клетки, экспрессирующие указанные TCR, и фармацевтические композиции для применения в лечении заболеваний, включающих злокачественные клетки, экспрессирующие указанные неоантигены.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из RAS в комплексе с МНС человека, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 84% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 3, 18, 33, 49, 65, 81, 97 и 113, и/или где конструкт бета цепи TCR содержит определяющую комплементарность области 3 (CDR3), имеющую, по меньшей мере, 84% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 6, 21, 36, 52, 68, 84, 100 и 116.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из RAS в комплексе с МНС человека, где эпитоп из RAS содержит область, имеющую, по меньшей мере, 70% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 15, 30, 45, 46, 61, 62, 77, 78, 93, 94, 109, 110, 125, 126 и 219-222.
В настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека кодированным HLA-A03:01 аллелью.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 9, 24, 39, 55, 71, 87, 103 и 119. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 12, 27, 42, 58, 74, 90, 106 и 122. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 1, 16, 31, 47, 63, 79, 95 и 111. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 4, 19, 34, 50, 66, 82, 98 и 114. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 2, 17, 32, 48, 64, 80, 96 и 112. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 5, 20, 35, 51, 67, 83, 99 и 115. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 9; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 12. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 1, CDR2 с SEQ ID NO: 2 и CDR3 с SEQ ID NO: 3; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 4, CDR2 с SEQ ID NO: 5 и CDR3 с SEQ ID NO: 6. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 24; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 27. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 16, CDR2 с SEQ ID NO: 17 и CDR3 с SEQ ID NO: 18; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 19, CDR2 с SEQ ID NO: 20 и CDR3 с SEQ ID NO: 21. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 39; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 42. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 31, CDR2 с SEQ ID NO: 32 и CDR3 с SEQ ID NO: 33; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 34, CDR2 с SEQ ID NO: 35 и CDR3 с SEQ ID NO: 36. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 55; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 58. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 47, CDR2 с SEQ ID NO: 48 и CDR3 с SEQ ID NO: 49; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 50, CDR2 с SEQ ID NO: 51 и CDR3 с SEQ ID NO: 52.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из TMPRSS2:ERG в комплексе с МНС человека, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 144 и SEQ ID NO: 147.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из TMPRSS2:ERG в комплексе с МНС человека, где эпитоп из TMPRSS2:ERG содержит область, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 156.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 150. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 153. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 142 или SEQ ID NO: 145. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 143 или SEQ ID NO: 146. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 150; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 153. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 142, CDR2 с SEQ ID NO: 143 и CDR3 с SEQ ID NO: 144; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 145, CDR2 с SEQ ID NO: 146 и CDR3 с SEQ ID NO: 147.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из GATA3 в комплексе с МНС человека, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 129 и SEQ ID NO: 132.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR) способный специфически связываться с мутантом GATA3 пептид в комплексе с белком, кодированным HLA аллелью субъекта с раком, где TCR содержит конструкт альфа цепи TCR и/или конструкт бета цепи TCR.
В настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, где TCR специфически связывается с мутантом GATA3 пептида в комплексе с HLA-A02:01 белком; содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 129 или SEQ ID NO: 132; и/или специфически связывается с мутантом GATA3 пептида, содержащим область с, по меньшей мере, 70% идентичностью последовательности с SEQ ID NO: 141.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из GATA3 в комплексе с МНС человека, где эпитоп из GATA3 содержит область, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 141.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 135. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 138. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 127 и SEQ ID NO: 130. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 128 и SEQ ID NO:131. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 135; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 138. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 127, CDR2 с SEQ ID NO: 128 и CDR3 с SEQ ID NO: 129; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 130, CDR2 с SEQ ID NO: 131 и CDR3 с SEQ ID NO: 132.
В другом аспекте, в настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из BTK в комплексе с МНС человека, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 161 и SEQ ID NO: 176, или где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 164 и SEQ ID NO: 179. В другом аспекте, в настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), способный специфически связываться с мутантом BTK пептида в комплексе с белком, кодированным HLA аллелью субъекта с раком, где TCR содержит конструкт альфа цепи TCR и/или конструкт бета цепи TCR. В другом аспекте, в настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, где TCR специфически связывается с мутантом BTK пептида в комплексе с HLA-A02:01 белком; содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 161, 164, 176 или 179; и/или специфически связывается с мутантом BTK пептида, содержащим область с, по меньшей мере, 70% идентичностью последовательности с SEQ ID NO: 173 или 188. В другом аспекте, в настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из BTK в комплексе с МНС человека, где эпитоп из BTK содержит область, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 173 или 188. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 167 или 182. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 170 или 185. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 159, 162, 174 и 177. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 160, 163, 175 и 178. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 167 или 182; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 170 или 185. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 159 или 174, CDR2 с SEQ ID NO: 160 или 175 и CDR3 с SEQ ID NO: 161 или 176; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 162 или 177, CDR2 с SEQ ID NO: 163 или 178 и CDR3 с SEQ ID NO: 164 или 179.
В еще одном аспекте, в настоящем описании представлена клетка-хозяин, содержащая нуклеиновую кислоту, кодирующую TCR против неоантигена, представленного в настоящем документе, вектор, содержащий последовательность нуклеиновой кислоты или белок, кодируемый нуклеиновой кислотой, представленной в настоящем документе. В некоторых вариантах осуществления, клеткой-хозяином является CD4+ Т-клетка. В некоторых вариантах осуществления, клеткой-хозяином является CD8+ Т-клетка. Клеткой-хозяином может быть естественный киллер (NK) или В клетка. Клетка-хозяин может быть линией иммортализованных клеток.
В еще одном аспекте, в настоящем описании представлены фармацевтические композиции, содержащие нуклеиновую кислоту, кодирующую TCR против неоантигена, представленного в настоящем документе, клетка-хозяин, содержащая нуклеиновую кислоту, кодирующую TCR против неоантигена, представленного в настоящем документе, вектор, содержащий последовательность нуклеиновых кислот, или белок, кодированный нуклеиновой кислотой, представленный в настоящем документе. В некоторых вариантах осуществления, в настоящем документе также представлен способ применения фармацевтических композиций, описанных в настоящем документе.
Также в настоящем документе в дополнительном аспекте представлен способ лечения субъекта, страдающего заболеванием или состоянием, включающий введение субъекту фармацевтической композиции, раскрытой в настоящем документе. В некоторых вариантах осуществления, субъект имеет рак.
III. Т-клеточные рецепторы (TCR)
Способность T клеток распознавать антигены, ассоциированные с разными видами рака или инфекционными организмами, предоставляется их TCR, которые состоят из обеих альфа (α) цепи и бета (β) цепи или гамма (γ) и дельта (δ) цепи. Белки, которые составляют эти цепи, кодированы ДНК, которая применяет уникальный механизм для генерирования значительного разнообразия TCR. Этот мультисубъединичный рецептор иммунного распознавания связывается с комплексом CD3 и связывает пептиды, представленные белками MHC I и II класса на поверхности антигенпрезентирующих клеток (APC). Связывание TCR с антигенным пептидом на APC является центральным событием в активации T клеток, которое происходит в иммунологическом синапсе в точке контакта между T клеткой и APC.
Каждый TCR содержит переменные определяющие комплементарность области (CDR), а также каркасные области (FR) и константную область. Аминокислотная последовательность петель третьей определяющей комплементарность области (CDR3) вариабельных доменов α- и β цепей в значительной степени определяет разнообразие последовательностей αβ Т клеток, возникающее в результате рекомбинации между вариабельным (Vβ), дополнительным (Dβ) и соединяющим (Jβ) сегментами гена в локусе β цепи и между аналогичными Vα и Jα сегментами гена в локусе α цепи, соответственно. Существование множества таких сегментов гена в локусах TCR α и β цепи позволяет значительное количество разных кодируемых CDR3 последовательностей. Независимое добавление и делеция нуклеотидов на Vβ-Dβ, Dβ-Jβ и Vα-Jα соединениях во время процесса перегруппировки TCR гена дополнительно повышает разнообразие CDR3 последовательностей. В связи с этим, иммунокомпетенция отражается в многообразии TCR. γδ TCR отличается от αβ TCR в том, что кодирует рецептор, который близко взаимодействует с врожденной иммунной системой. TCRγδ экспрессируется на ранней стадии развития, имеет специализированное анатомическое распределение, имеет уникальный патоген и низкомолекулярные специфичности и имеет широкий спектр врожденных и адаптивных клеточных взаимодействий. На ранней стадии онтогенеза, так как ограниченные подмножества TCRγδ клеток заселяют различные ткани в предродовом периоде, устанавливается смещенный шаблон экспрессии TCRγ V и J сегмента.
TCR представленной в настоящем документе мишени могут быть сконструированными TCR, например, химерными антигенными рецепторами (CAR). CAR могут быть составлены из трех областей: эктодомен, трансмембранный домен и эндодомен.
Эктодоменом может быть область рецептора, которая обрабатывается внеклеточной жидкостью и может состоять из антигенраспознающей области. В некоторых вариантах осуществления, эктодомен дополнительно содержит и спейсер. В некоторых вариантах осуществления, эктодомен дополнительно содержит и сигнальный пептид. Сигнальный пептид может направлять растущий белок в эндоплазматический ретикулюм. Сигнальным белком в CAR может быть одноцепочечный вариабельный фрагмент (scFv). Слитым белком может быть белок, который образуется слиянием двух или более генов, которые изначально кодируют разные белки, но когда они транслируются в клетке, трансляция продуцирует один или более полипептидов с функциональными свойствами, полученными для каждого из исходных генов. ScFv представляет собой химерный белок, состоящий из домена легкой цепи и вариабельного домена тяжелой цепи, соединенных с коротким линкерным пептидом. Линкер может содержать гидрофильные остатки с удлинениями глициновых и/или сериновых остатков. Линкер может содержать удлинения глутаматных и лизиновых остатков, которые могут улучшать растворимость.
Трансмембранный домен может быть гидрофобным доменом, охватывающим мембрану. В некоторых вариантах осуществления, трансмембранный домен содержит альфа-спиральный домен. Трансмембранный домен может быть функциональным для стабильности рецептора в целом. В некоторых вариантах осуществления, трансмембранный домен содержит трансмембранный домен из наиболее проксимального к мембране компонента эндодомена. В некоторых вариантах осуществления, трансмембранный домен содержит трансмембранный домен CD3-zeta. В некоторых вариантах осуществления, трансмембранный домен позволяет включать искусственный TCR в нативный комплекс TCR. В некоторых вариантах осуществления, трансмембранный домен содержит CD28 трансмембранный домен.
Эндодоменом может быть функциональная внутриклеточная часть рецептора, такая как TCR или CAR. После распознавания антигеном кластер рецепторов и сигнал могут передаваться в клетку. В некоторых вариантах осуществления, эндодомен содержит внутриклеточный домен CD3-дзета. В некоторых вариантах осуществления, эндодомен содержит, по меньшей мере, один ITAM. В некоторых вариантах осуществления, эндодомен содержит, по меньшей мере, 3 или, по меньшей мере, 3 ITAM. В некоторых вариантах осуществления, эндодомен содержит CD28 внутриклеточный домен. В некоторых вариантах осуществления, эндодомен содержит OX40 внутриклеточный домен. В некоторых вариантах осуществления, эндодомен содержит химерный внутриклеточный домен. Например, эндодомен может содержать CD28 внутриклеточный домен, OX40 внутриклеточный домен и CD3-дзета внутриклеточный домен.
IV. T клетки
Т клетки принадлежат к группе белых кровяных клеток, известных как лимфоциты, и играют центральную роль в клеточном иммунитете. Т клетки включают CD4+ Т клетки (хелперные Т клетки) и CD8+ Т клетки (цитотоксические Т клетки). CD4+ Т клетки могут помогать другим белым клеткам крови в иммунологических процессах, включая созревание В клеток и активацию цитотоксических Т клеток и макрофагов. CD4+ Т клетки активируются, когда они презентированы пептидными антигенами молекулами MHC II класса, экспрессируемыми на поверхности антигенпрезентирующих клеток (APC). После активации Т клетки могут быстро делиться и секретировать цитокины, которые регулируют активный иммунный ответ. CD8+ Т клетки могут разрушать инфицированные вирусом клетки и опухолевые клетки, а также могут вовлечены в отторжение трансплантата. CD8+ Т клетки могут распознавать свои мишени путем связывания с антигеном, ассоциированным с MHC I класса, который присутствует на поверхности почти каждой клетки тела. Большинство Т клеток имеют Т клеточный рецептор (TCR). Способность Т клеток распознавать антигены, ассоциированные с различными видами рака или инфекционными организмами, обеспечивается их TCR, который состоит из обеих альфа (α) цепи и из бета (β) цепи или гамма (γ) и дельта (δ) цепи. Белки, составляющие эти цепи, кодированы ДНК, которая использует уникальный механизм для создания разнообразия TCR. Этот мультисубъединичный рецептор иммунного распознавания может связываться с комплексом CD3 и связывать пептиды, презентированные белками MHC I и II класса на поверхности антигенпрезентирующих клеток (APC). Первым сигналом активации Т клеток может быть связывание Т клеточного рецептора с коротким пептидом, презентированным MHC на другой клетке. Это гарантирует, что активируется только Т клетка со специфическим для данного пептида TCR. Клеткой-партнером обычно является антигенпрезентирующая клетка, такая как профессиональная антигенпрезентирующая клетка, обычно дендритная клетка в случае интактных ответов, хотя B-клетки и макрофаги могут быть важными APC. Связывание TCR с антигенным пептидом на APC может быть центральным событием в активации T клеток, которая происходит в иммунологическом синапсе в точке контакта между T клеткой и APC.
Т-клетки могут быть получены способами, известными в данной области техники. Т клетки могут быть препаратом обогащенных Т клеток, препаратом истощенных APC клеток или по существу очищенным препаратом Т клеток. Т клетки могут представлять собой смешанную популяцию Т клеток или очищенную субпопуляцию Т клеток. Т клетки могут быть обогащенным препаратом Т клеток, содержащим количество или долю Т клеток, увеличенное по сравнению с изолированной популяцией Т клеток.
Т клетки или подмножество Т клеток может быть получено из различных лимфоидных тканей. Т клетки могут быть получены из ряда источников, включая мононуклеарные клетки периферической крови (PBMC), костный мозг, тимус, биопсию ткани, опухоль, ткань лимфатических узлов, кишечной лимфоидной ткани, лимфоидной ткани слизистых оболочек, ткани селезенки, лимфоидной ткани и опухолей. Термин «лимфоциты периферической крови» (PBL) и его грамматические эквиваленты в настоящем документе могут относиться к лимфоцитам, которые циркулируют в крови (например, периферической крови). Лимфоциты периферической крови могут относиться к лимфоцитам, не локализованным в органах. Лимфоциты периферической крови могут включать Т клетки, NK клетки, В клетки или любые их комбинации.
Способ может включать выделение Т клеток от субъекта. Способ может включать получение Т клеток, выделенных из субъекта. Т-клетки могут быть получены из линий Т клеток. Т клетки могут быть получены из аутологичных источников. Т клетки могут быть получены из аллогенных источников. Т клетки также могут быть получены из ксеногенного источника, например, от мыши, крысы, приматов, не относящихся к человеку, и свиней.
Т клетки могут быть препаратом клеток с истощенными APC. Т клетки могут по существу не содержать APC. Например, Т клетки могут включать Т клетки, отделенные более чем от 75% APC. В типовом варианте осуществления, мононуклеарные клетки периферической крови (PBMC) могут быть получены из крови, например, в гепаринизированных флаконах. РВМС могут быть отделены от красных клеток крови центрифугированием, РВМС восстановлены с поверхности раздела фаз. Восстановленные PBMC необязательно могут быть промыты (например, ФРФБ).
Очистка T клеток может быть проведена, например, положительным или отрицательным отбором, включающим, но не ограниченным ими, применение антител, направленных на молекулы CD2, CD3, CD4, CD5, CD8, CD14, CD19 и/или MHC II класса. Специфическое подмножество T клеток, таких как CD28+, CD4+, CD8+, CD45RA+ и/или CD45RO+ T клетки, может быть выделено методами положительного или отрицательного выбора. Например, CD3+, CD28+ T клетки могут быть положительно выбраны с применением CD3/CD28 конъюгированных магнитных шариков. В одном аспекте настоящего изобретения, обогащение популяции T клеток отрицательным выбором может производиться с комбинацией антител, направленной на поверхностные маркеры уникальные для отрицательно выбранных клеток.
Например, образец T клетки может содержать клетки из кровотока субъекта, и могут быть получены аферезом или лейкоферезом. Образец T клетки может содержать лимфоциты, включая T клетки, моноциты, гранулоциты, B клетки, другие ядросодержащие белые клетки крови, красные клетки крови и/или тромбоциты. Нежелательные компоненты образца T клетки могут быть удалены и, и оставшиеся T клетки могут быть суспендированы в культуральной среде. Например, клетки могут быть промыты для удаления фракции плазмы. Например, T клетки могут быть выделены из лимфоцитов периферической крови лизированием красных клеток крови и центрифугированием через градиент PERCOLL™.
В некоторых вариантах осуществления, T клетка содержит, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из RAS в комплексе с МНС человека. В некоторых вариантах осуществления, T клетка содержит, по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из TMPRSS2:ERG в комплексе с МНС человека. В некоторых вариантах осуществления, Т клетка содержит, по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из GATA3 в комплексе с МНС человека. В некоторых вариантах осуществления, клетка-хозяин содержит, по меньшей мере, один TCR, раскрытый в настоящем документе, где клеткой-хозяином является CD4+ T клетка. В некоторых вариантах осуществления, клеткой-хозяином является CD8+ T клетка. В некоторых вариантах осуществления, клеткой-хозяином является аутологичная клетка. В некоторых вариантах осуществления, клеткой-хозяином является аллогенная клетка. В некоторых вариантах осуществления, клеткой-хозяином является клетка человека. В некоторых других случаях, клеткой-хозяином может быть естественный киллер (NK), B клетка или иммортализованная линия клеток.
В некоторых вариантах осуществления, T клетки могут быть получены положительным отбором и/или отрицательным отбором. При положительном отборе, аффинный агент (такой как антитело, фрагмент антитела и аптамер) может применяться для связывания поверхностноклеточного маркера, экспрессированного на популяции клеток, например, CD3 для T клеток. С помощью аффинного агент, T клетки могут быть помечены. Меченые T клетки затем могут быть обогащены с применением разных способов, которые хорошо известны в данной области техники. Неограничивающие примеры этих способов включают сортировку флуоресцентно-активированных клеток (FACS) и клеточным разделением на основе (пара)магнитных частиц (например, с применением набора для разделения клеток MACS от Miltenyi Biotec).
При отрицательном отборе, аффинные агенты могут быть использованы для связывания поверхностноклеточных маркеров, экспрессируемых на клетках крови, отличных от желаемой популяции. Например, при попытке выделить Т клетки, коктейль аффинных агентов может быть использован для мечения В клеток, NK клеток, моноцитов, тромбоцитов, дендритных клеток, гранулоцитов и эритроцитов. Затем меченые клетки могут быть истощены, оставляя Т клетки обогащенными. Примеры способов истощения меченых клеток включают FACS и клеточным разделением на основе (пара)магнитных частиц.
Помимо выделения на основе мечения, могут использоваться особые условия роста для стимулирования роста одной конкретной популяции клеток. Например, особые условия роста можно получить с помощью специальных цитокинов или факторов роста. В другом примере, в культуральной среде, содержащей фитогемагглютинин (PHA), IL-2 и/или IL-15, Т клетки могут преимущественно пролиферировать.
В некоторых ситуациях, нефункциональные маркеры могут использоваться для выделения Т клеток, поскольку связывание функциональных маркеров, такое как связывание CD3 анти-CD3-антителом (отдельно или конъюгированным с магнитными частицами), может запускать нежелательные сигнальные события на Т клетках. Следовательно, смесь антител против CD14, CD15, CD16, CD19, CD34, CD36, CD56, CD123 и CD235a (гликофорин A) может быть использована для выделения Т клеток.
Подробный протокол может быть найден в опубликованной литературе (например, см. Lefort et al., J Vis Exp. 2010; (40): 2017), которая включена сюда в качестве ссылки. Наборы для выделения Т клеток могут быть получены от, например, STEMCELL Technologies, Thermofisher and Miltenyi Biotec.
T клеткой, описанной в настоящем документе, может быть аллогенная T клетка.
В некоторых вариантах осуществления, Т-клеткой может быть генетически модифицированная клетка, содержащая в своем геноме модифицированный ген альфа цепи Т клеточного рецептора человека (TCR) и/или модифицированный ген бета цепи TCR человека, где клетка имеет пониженную поверхностноклеточную экспрессию эндогенного TCR.
Нуклеазы, редактирующие ген, могут быть использованы для разрушения компонентов TCR. Альфа цепь TCR (TCRα) кодируется одним геном TRAC и соединяется с бета цепью TCR (TCRβ), кодированной двумя генами TCRB. Поскольку TCR димер α/β может продуцировать полностью функционирующий комплекс TCR, нарушение функции TCRα и/или TCRβ может снизить (даже устранить) экспрессию эндогенного TCR.
Для разрушения эндогенных генов TCRα или TCRβ могут использоваться различные методы. Например, существует четыре класса редактирующих гены белков, которые имеют общий способ действия при связывании определенной пользователем последовательности ДНК и опосредовании двухцепочечного разрыва ДНК (DSB). Цинк-пальцевые нуклеазы (ZFN) представляют собой гетеродимерные массивы, которые совместно локализуются в целевом сайте ДНК. ZFN включают отдельные пальцевые субъединицы, которые связывают ДНК и связаны с доменом нуклеазы Fokl, который расщепляет ДНК. Нуклеаза на основе эффектора, подобного активатора транскрипции (TALEN) включают повторяющиеся единицы, которые связывают ДНК посредством гипервариабельных двух аминокислотных последовательностей (повторных вариабельных диостатков; RVD) которые управляют распознаванием ДНК основания. Подобно ZFN, TALEN действует как димерные белки, которые конденсированы с доменом эндонуклеазы Fokl для создания DSB. Мегануклеазы (MN) являются мономерными белками с врожденной нуклеазной активностью, которые получены из бактериальных хоуминг-эндонуклеаз и сконструированы для уникального сайта-мишени. Платформа на основе кластеризованных регулярных промежуточных коротких палиндромных повторов (CRISPR) и ассоциированной Cas9 нуклеазы вовлекает транскрипт малой направляющей РНК (gРНК), который контактирует с ДНК последовательность-мишень через спаривание основание Уотсона-Крика, которые расщепляют ДНК.
В некоторых вариантах осуществления, введение редактирующей геном нуклеазы в T клетку включает введение в T клетку полинуклеотида, который кодирует редактирующую геном нуклеазу.
В некоторых вариантах осуществления, введение редактирующей геном нуклеазы в T клетку включает введение в T клетку Cas9 полипептида. В некоторых вариантах осуществления, редактирующая геном нуклеаза включает TALEN нуклеазу, CRISPR/Cas9 нуклеазу или a megaTAL нуклеазу.
В некоторых вариантах осуществления, CRISPR/Cas9 нуклеазу получают либо из Streptococcus pyogenes, либо из Staphylococcus aureus. В некоторых из этих вариантов осуществления, CRISPR/Cas9 нуклеаза включает резистентную к нуклеазе gРНК такую как, например, по меньшей мере, одно 2'-OMe-фосфоротиоат-модифицированное основание, по меньшей мере, одно 2'-O-метил-модифицированное основание или, по меньшей мере, одно 2'-O-метил 3' thioPACE модифицированное основание.
В некоторых вариантах осуществления, TALEN нуклеазой или megaTAL нуклеазой является кодированная РНК, которая имеет экзогенный сигнал полиаденилирования.
В некоторых вариантах осуществления, способ, описанный в настоящем документе, может дополнительно включать культивирование T клетки в условиях, эффективных для размножения популяции геном-модифицированных T клеток.
В некоторых вариантах осуществления, нарушение экспрессии TCRα и/или TCRβ дополнительно нарушает сборку TCRα и TCRβ. В некоторых вариантах, нарушение экспрессии TCRα дополнительно нарушает образование комплекса между TCR и CD3. В некоторых вариантах осуществления, нарушение экспрессии TCRα включает дальнейшее нарушение сборки TCRα и TCRβ.
В некоторых вариантах осуществления, генетически модифицированная Т-клетка содержит нарушенную альфа цепь и/или бета цепь TCR и инактивированный ген, кодирующий белок иммунной контрольной точки, такой как PD1 и CTLA-4. Это может быть сделано путем инактивации гена с использованием специфических TALE-нуклеаз, направленных против TCRальфа или TCRбета в сочетании с инактивацией генов, кодирующих белок иммунных контрольных точек, такой как PD1 и CTLA-4.
В некоторых вариантах осуществления, генетическая модификация основана на инактивации одного гена или двух генов, выбранных из группы, состоящей из PD1, CTLA-4, LAG3, Tim3, BTLA, BY55, TIGIT, B7H5, LAIR1, SIGLEC10, 2B4, TCR альфа и TCR бета. В некоторых вариантах осуществления, генетическая модификация основана на инактивации двух генов, выбранных из группы, состоящей из PD1 и TCR альфа, PD1 и TCR бета, CTLA-4 и TCR альфа, CTLA-4 и TCR бета, LAG 3 и TCR альфа, LAG 3 и TCR бета, Tim3 и TCR альфа, Tim3 и TCR бета, BTLA и TCR альфа, BTLA и TCR бета, BY55 и TCR альфа, BY55 и TCR бета, TIGIT и TCR альфа, TIGIT и TCR бета, B7H5 и TCR альфа, B7H5 и TCR бета, LAIRl и TCR альфа, LAIR1 и TCR бета, SIGLEC10 и TCR альфа, SIGLEC10 и TCR бета, 2B4 и TCR альфа, 2B4 и TCR бета. В некоторых вариантах осуществления, генетическая модификация основана на инактивации более чем двух генов. Генетическая модификация может проводиться ex-vivo.
V. TCR, специфические к RAS комплекса пептид-МНС
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из RAS в комплексе с МНС человека, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 84% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 3, 18, 33, 49, 65, 81, 97, 113, 241, 257, 273, 289, 305, 321, 337, 353, 369, 385, 401, 417 и 433, и/или где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 84% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 6, 21, 36, 52, 68, 84, 100, 116, 244, 260, 276, 292, 308, 324, 340, 356, 372, 388, 404, 420 и 436.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из RAS в комплексе с МНС человека, где эпитоп из RAS содержит область, имеющую, по меньшей мере, 70% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 15, 30, 45, 46, 61, 62, 77, 78, 93, 94, 109, 110, 125, 126, 219-222, 253, 254, 269, 270, 285, 286, 301, 302, 317, 318, 333, 334, 349, 350, 365, 366, 381,382, 397, 398, 413, 414, 429, 430, 445 и 446.
В настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR; где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека кодированным HLA-A03:01 аллелью. В некоторых вариантах осуществления, конструкт альфа цепи содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 71, 87, 103, 295, 311, 327, 343, 359 и 391, где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека кодированным HLA-A03:01 аллелью. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 74, 90, 106, 298, 314, 330, 346, 362 и 394, где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека, кодированным HLA-A03:01 аллелью.
В некоторых вариантах осуществления, конструкт альфа цепи TCR, как описано выше, содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 63, 79, 95, 287, 303, 319, 335, 351 и 383. В некоторых вариантах осуществления, конструкт бета цепи TCR как описано выше, содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 66, 82, 98, 290, 306, 322, 338, 354 и 386. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 64, 80, 96, 288, 304, 320, 336, 352 и 384. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 67, 83, 99, 291, 307, 323, 339, 355 и 387. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 65, 81, 97, 289, 305, 321, 337, 353 и 385. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 68, 84, 100, 292, 308, 324, 340, 356 и 388.
В настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеинов кислот кодирует, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR; где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека кодированным HLA-A02:01 аллелью. В некоторых вариантах осуществления, конструкт альфа цепи содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 9 и 24, где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека кодированным HLA-A02:01 аллелью. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 12 и 27, где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека кодированным HLA-A02:01 аллелью.
В некоторых вариантах осуществления, конструкт альфа цепи TCR как описано выше, содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 1 и 16. В некоторых вариантах осуществления, конструкт бета цепи TCR как описано выше, содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 4 и 19. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 2 и 17.В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 5 и 20.В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 3 и 18.В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 6 и 21.
В настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует, по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR; где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека кодированным HLA-A11:01 аллелью. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 39, 55, 122, 247, 263, 279, 375, 407, 423 и 439, где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека кодированным HLA-A11:01 аллелью. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 42, 58, 125, 250, 266, 282, 378, 413, 426 и 442, где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека кодированным HLA-A11:01 аллелью.
В некоторых вариантах осуществления, конструкт альфа цепи TCR как описано выше, содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 31,47, 111, 239, 255, 271, 367, 399, 415 и 431. В некоторых вариантах осуществления, конструкт бета цепи TCR как описано выше, содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 34, 50, 114, 242, 258, 274, 370, 402, 418 и 434. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 32, 48, 112, 240, 256, 272, 368, 400, 416 и 432. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 35, 51, 115, 243, 259, 275, 371, 403, 419 и 435. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 33, 49, 113, 241, 257, 273, 369, 401, 417 и 433. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 36, 52, 116, 228, 244, 260, 276, 372, 404, 420 и 434. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 9; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 12. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 1, CDR2 с SEQ ID NO: 2 и CDR3 с SEQ ID NO: 3; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 4, CDR2 с SEQ ID NO: 5 и CDR3 с SEQ ID NO: 6. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 24; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 27. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 16, CDR2 с SEQ ID NO: 17, и CDR3 с SEQ ID NO: 18; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 19, CDR2 с SEQ ID NO: 20, и CDR3 с SEQ ID NO: 21. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 39; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 42. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 31, CDR2 с SEQ ID NO: 32, и CDR3 с SEQ ID NO: 33; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 34, CDR2 с SEQ ID NO: 35, и CDR3 с SEQ ID NO: 36. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 55; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 58. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 47, CDR2 с SEQ ID NO: 48, и CDR3 с SEQ ID NO: 49; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 50, CDR2 с SEQ ID NO: 51, и CDR3 с SEQ ID NO: 52. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 71; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 74. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 63, CDR2 с SEQ ID NO: 64 и CDR3 с SEQ ID NO: 65; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 66, CDR2 с SEQ ID NO: 67, и CDR3 с SEQ ID NO: 68. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 87; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 90. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 79, CDR2 с SEQ ID NO: 80, и CDR3 с SEQ ID NO: 81; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 82, CDR2 с SEQ ID NO: 83, и CDR3 с SEQ ID NO: 84. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 103; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 106. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 95, CDR2 с SEQ ID NO: 96, и CDR3 с SEQ ID NO: 97; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 98, CDR2 с SEQ ID NO: 99 и CDR3 с SEQ ID NO: 100. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 119; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 122. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 111, CDR2 с SEQ ID NO: 112 и CDR3 с SEQ ID NO: 113; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 114, CDR2 с SEQ ID NO: 115 и CDR3 с SEQ ID NO: 116. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 263; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 266. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 255, CDR2 с SEQ ID NO: 256 и CDR3 с SEQ ID NO: 257; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 258, CDR2 с SEQ ID NO: 259 и CDR3 с SEQ ID NO: 260. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 279; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 282. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 271, CDR2 с SEQ ID NO: 272 и CDR3 с SEQ ID NO: 273; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 274, CDR2 с SEQ ID NO: 275 и CDR3 с SEQ ID NO: 276. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 295; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 298. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 287, CDR2 с SEQ ID NO: 288 и CDR3 с SEQ ID NO: 289; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 290, CDR2 с SEQ ID NO: 291 и CDR3 с SEQ ID NO: 292. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 311; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 314. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 303, CDR2 с SEQ ID NO: 304 и CDR3 с SEQ ID NO: 305; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 306, CDR2 с SEQ ID NO: 307 и CDR3 с SEQ ID NO: 308. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 327; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 330. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 319, CDR2 с SEQ ID NO: 320 и CDR3 с SEQ ID NO: 321; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 322, CDR2 с SEQ ID NO: 323 и CDR3 с SEQ ID NO: 324. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 343; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 346. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 335, CDR2 с SEQ ID NO: 336 и CDR3 с SEQ ID NO: 337; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 338, CDR2 с SEQ ID NO: 339 и CDR3 с SEQ ID NO: 340. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 343; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 346. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 351, CDR2 с SEQ ID NO: 352 и CDR3 с SEQ ID NO: 353; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 354, CDR2 с SEQ ID NO: 355 и CDR3 с SEQ ID NO: 356. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 343; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 346. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 367, CDR2 с SEQ ID NO: 368 и CDR3 с SEQ ID NO: 369; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 370, CDR2 с SEQ ID NO: 371 и CDR3 с SEQ ID NO: 372. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 391; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 394. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 383, CDR2 с SEQ ID NO: 384 и CDR3 с SEQ ID NO: 385; конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 386, CDR2 с SEQ ID NO: 387 и CDR3 с SEQ ID NO: 388. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 391; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 394. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 399, CDR2 с SEQ ID NO: 400 и CDR3 с SEQ ID NO: 401; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 402, CDR2 с SEQ ID NO: 403 и CDR3 с SEQ ID NO: 404. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 423; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 426. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 415, CDR2 с SEQ ID NO: 416 и CDR3 с SEQ ID NO: 417; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 418, CDR2 с SEQ ID NO: 419 и CDR3 с SEQ ID NO: 420. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 391; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 394. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 431, CDR2 с SEQ ID NO: 432 и CDR3 с SEQ ID NO: 433; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 434, CDR2 с SEQ ID NO: 435 и CDR3 с SEQ ID NO: 426.
В разных вариантах осуществления, последовательность нуклеиновых кислот, кодирующая TCR является кодон-оптимизированной.
Мутации в любом из трех ras генов, H-ras, K-ras и N-ras, является одним из наиболее частых событий в онкогенезе человека. Было найдено, что примерно 30% всех опухолей человека несут, по меньшей мере, одну мутацию в любом из канонических ras генов. Ras мутации очевидны в, например, аденокарциноме желчевыводящих путей, переходно-клеточной карциноме мочевого пузыря, карциноме молочной железы, аденокарциноме шейки матки, аденокарциноме толстой кишки, аденоме толстой кишки, нейробластоме (вегетативные ганглии), остром миелоидном лейкозе, хроническом миелоидном лейкозе, хроническом миеломоноцитарном лейкозе, ювенильном миеломоноцитарном лейкозе, остром лимфобластном лейкозе, лимфоме Буркитта, лимфоме Ходжкина, миеломе клеток плазмы, печеночно-клеточной карциноме, крупноклеточной карциноме, немелкоклеточной карциноме, протоковой карциноме, эндокринной опухоли, аденокарциноме простаты, базальноклеточной карциноме, плоскоклеточной карциноме, злокачественной меланоме, ангиосаркоме, лейомиосаркоме, липосаркоме, рабдомиосаркоме, миксоме, злокачественной фиброзной гистиоцитоме, плеоморфной саркоме, герминоме, семиноме, анапластической карциноме, фолликулярной карциноме, папиллярной карциноме и карциноме из клеток Гуртле. Ras мутации обнаруживаются при раке, поражающем многие ткани и органы тела, например, легкие, печень, грудь, мочевой пузырь, толстую кишку, шейку матки, поджелудочную железу, предстательную железу, желудок, щитовидную железу, яички, мягкие ткани, кожу и кровь.
В разных вариантах осуществления, TCR связывается с MHC:RAS пептидным комплексом, где RAS пептид содержит G12V мутацию. В разных вариантах осуществления, TCR связывается с MHC:RAS пептидным комплексом, где RAS пептид содержит G12C мутацию. В разных вариантах осуществления, TCR связывается с MHC:RAS пептидным комплексом, где RAS пептид содержит G12D мутацию. В разных вариантах осуществления, TCR связывается с MHC:RAS пептидным комплексом, где RAS пептид содержит мутацию на Q61. В разных вариантах осуществления, TCR связывается с MHC:RAS пептидным комплексом, где RAS пептид содержит последовательность VVGAVGVGK (SEQ ID NO: 45), VVVGAVGVGK (SEQ ID NO: 46), VVGADGVGK (SEQ ID NO: 301), VVVGADGVGK (SEQ ID NO: 302), VVGACGVGK (SEQ ID NO: 109), VVVGACGVGK (SEQ ID NO: 110), KLVVVGACGV (SEQ ID NO: 15), LVVVGACGV (SEQ ID NO: 30), KLVVVGADGV (SEQ ID NO: 219), LVVVGADGV (SEQ ID NO: 220), KLVVVGAVGV (SEQ ID NO: 221) или LVVVGAVGV (SEQ ID NO: 222).
В разных вариантах осуществления, TCR связывается с MHC:RAS пептидным комплексом, где МНС человека кодирован HLA-A02:01 аллелью. В разных вариантах осуществления, TCR связывается с MHC:RAS пептидным комплексом, где МНС человека кодирован HLA-A03:01 аллелью. В разных вариантах осуществления, TCR связывается с MHC:RAS пептидным комплексом, где МНС человека кодирован HLA-A11:01 аллелью.
В разных вариантах осуществления, TCR связывается с MHC:RAS пептидным комплексом, где МНС человека кодирован HLA-A02:01 аллелью, и где RAS пептид содержит последовательность VVGAVGVGK (SEQ ID NO: 45), VVVGAVGVGK (SEQ ID NO: 46), VVGADGVGK (SEQ ID NO: 301), VVVGADGVGK (SEQ ID NO: 302), VVGACGVGK (SEQ ID NO: 109), VVVGACGVGK (SEQ ID NO: 110), KLVVVGACGV (SEQ ID NO: 15), LVVVGACGV (SEQ ID NO: 30), KLVVVGADGV (SEQ ID NO: 219), LVVVGADGV (SEQ ID NO: 220), KLVVVGAVGV (SEQ ID NO: 221) или LVVVGAVGV (SEQ ID NO: 222). В разных вариантах осуществления, TCR связывается с MHC:RAS пептидным комплексом, где МНС человека кодирован HLA-A03:01 аллелью, и где RAS пептид содержит последовательность VVGAVGVGK (SEQ ID NO: 45), VVVGAVGVGK (SEQ ID NO: 46), VVGADGVGK (SEQ ID NO: 301), VVVGADGVGK (SEQ ID NO: 302), VVGACGVGK (SEQ ID NO: 109), VVVGACGVGK (SEQ ID NO: 110), KLVVVGACGV (SEQ ID NO: 15), LVVVGACGV (SEQ ID NO: 30), KLVVVGADGV (SEQ ID NO: 219), LVVVGADGV (SEQ ID NO: 220), KLVVVGAVGV (SEQ ID NO: 221) или LVVVGAVGV (SEQ ID NO: 222). В разных вариантах осуществления, TCR связывается с MHC:RAS пептидным комплексом, где МНС человека кодирован HLA-A11:01 аллелью, и где RAS пептид содержит последовательность VVGAVGVGK (SEQ ID NO: 45), VVVGAVGVGK (SEQ ID NO: 46), VVGADGVGK (SEQ ID NO: 301), VVVGADGVGK (SEQ ID NO: 302), VVGACGVGK (SEQ ID NO: 109), VVVGACGVGK (SEQ ID NO: 110), KLVVVGACGV (SEQ ID NO: 15), LVVVGACGV (SEQ ID NO: 30), KLVVVGADGV (SEQ ID NO: 219), LVVVGADGV (SEQ ID NO: 220), KLVVVGAVGV (SEQ ID NO: 221) или LVVVGAVGV (SEQ ID NO: 222).
В некоторых вариантах осуществления, один TCR, описанный в настоящем документе, демонстрирует специфическую аффинность связывания с эпитопным пептидом, содержащим точечную мутацию, найденную при раке, где эпитопный пептид находится в комплексе с MHC, кодированным определенной аллелью; и, дополнительно, TCR может демонстрировать разную аффинность связывания с другим эпитопным пептидом, содержащим разные точечные мутации одного и того же белка, где эпитопный пептид находится в комплексе с MHC, кодированным определенной аллелью, но не демонстрирует аффинность связывания с пептидом ДТ, который не содержит какую-либо мутацию.
VI. TCR специфические к TMPRSS2:ERG комплексам пептид-МНС
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из TMPRSS2:ERG в комплексе с МНС человека, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 144 и SEQ ID NO: 147.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из TMPRSS2:ERG в комплексе с МНС человека, где эпитоп из TMPRSS2:ERG содержит область, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 156.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 150. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 153. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 142 или SEQ ID NO: 145. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 143 или SEQ ID NO: 146. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 150; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 153. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 142, CDR2 с SEQ ID NO: 143 и CDR3 с SEQ ID NO: 144; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 145, CDR2 с SEQ ID NO: 146 и CDR3 с SEQ ID NO: 147.
В некоторых вариантах осуществления, TCR содержит конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из TMPRSS2:ERG в комплексе с МНС человека, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% идентичность последовательности с SEQ ID NO: 144 или 147.
В некоторых вариантах осуществления, TCR содержит конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из TMPRSS2:ERG в комплексе с МНС человека, где эпитоп из TMPRSS2:ERG содержит область, имеющую, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% идентичность последовательности с SEQ ID NO: 156.
В некоторых вариантах осуществления, конструкт альфа цепи TCR и или конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% идентичность последовательности с SEQ ID NO: 150 или 153.
В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% идентичность последовательности с SEQ ID NO: 142 или 145.
В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 143 или 146.
В некоторых вариантах осуществления, нуклеиновая кислота, кодирующая конструкт альфа цепи TCR и/или TCR бета цепь содержит последовательность нуклеиновой кислоты с, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% идентичностью последовательности с любой из SEQ ID NOs: 148, 149, 151 и 152. В разных вариантах осуществления, последовательность нуклеиновой кислоты, кодирующая TCR, является кодон-оптимизированной.
В разных вариантах осуществления, TCR связывается с MHC:TMPRSS2::ERG пептидным комплексом, где TMPRSS2::ERG пептид содержит мутацию слияния гена. В разных вариантах осуществления, TCR связывается с MHC:TMPRSS2::ERG пептидным комплексом, где TMPRSS2::ERG пептид содержит мутацию слияния гена, содержащую, по меньшей мере, две последовательных аминокислоты где, по меньшей мере, две последовательных аминокислоты содержат, по меньшей мере, одну аминокислоту TMPRSS2 и, по меньшей мере, одну аминокислоту ERG. В разных вариантах осуществления, TCR связывается с MHC:TMPRSS2::ERG пептидным комплексом, где TMPRSS2::ERG пептид содержит последовательность ALNSEALSV (SEQ ID NO: 156).
В разных вариантах осуществления, МНС человека кодирован HLA-A02:01 аллелью. В разных вариантах осуществления, TCR связывается с MHC:TMPRSS2::ERG пептидным комплексом, где МНС человека кодирован HLA-A02:01 аллелью.
В разных вариантах осуществления, МНС человека кодирован HLA-A02:01 аллелью. В разных вариантах осуществления, TCR связывается с MHC:TMPRSS2::ERG пептид комплексом, где МНС человека кодирован HLA-A02:01 аллелью, где TMPRSS2::ERG пептид содержит последовательность ALNSEALSV (SEQ ID NO: 156).
VII. TCR специфические к GATA3 комплексам пептид-МНС
В некоторых других вариантах осуществления, TCR содержит конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из GATA3 в комплексе с МНС человека, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% идентичность последовательности с SEQ ID NO: 129, 132, 191, 194, 206 или 209.
В некоторых вариантах осуществления, TCR содержит конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из GATA3 в комплексе с МНС человека, где эпитоп из GATA3 содержит область, имеющую, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% идентичность последовательности с SEQ ID NO: 141, 203 или 218.
В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% идентичность последовательности с SEQ ID NO: 135, 138, 197, 200, 212 или 215.
В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% идентичность последовательности с SEQ ID NO: 127, 130, 189, 192, 204 или 207.
В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% идентичность последовательности с SEQ ID NO: 128, 131, 190, 193, 205 или 208.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из GATA3 в комплексе с МНС человека, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 129, 132, 191, 194, 206 или 209.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR) способный специфически связываться с мутантом GATA3 пептида в комплексе с белком, кодированным HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью субъекта с раком, где TCR содержит конструкт альфа цепи TCR и/или конструкт бета цепи TCR.
В настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, где TCR специфически связывается с мутантом GATA3 пептида в комплексе с HLA-A02:01, HLA-B07:02 или HLA-B08:01 белком; содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 129, 132, 191, 194, 206 или 209; и/или специфически связывается с мутантом GATA3 пептида, содержащим область с, по меньшей мере, 70% идентичностью последовательности с SEQ ID NO: 141, 203 или 218.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из GATA3 в комплексе с МНС человека, где эпитоп из GATA3 содержит область, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 141, 203 или 218.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 135, 197 или 212. В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 138, 200 или 215. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 127, 130, 189, 192, 204 и 207. В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 128, 131, 190, 193, 205 и 208.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 135; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 138. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 197; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 200. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 212; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 215.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 127, CDR2 с SEQ ID NO: 128 и CDR3 с SEQ ID NO: 129; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 130, CDR2 с SEQ ID NO: 131 и CDR3 с SEQ ID NO: 132. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 189, CDR2 с SEQ ID NO: 190 и CDR3 с SEQ ID NO: 191; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 192, CDR2 с SEQ ID NO: 193 и CDR3 с SEQ ID NO: 194. В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 204, CDR2 с SEQ ID NO: 205 и CDR3 с SEQ ID NO: 206; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 207, CDR2 с SEQ ID NO: 208 и CDR3 с SEQ ID NO: 209.
В некоторых вариантах осуществления, нуклеиновая кислота, кодирующая конструкт альфа цепи TCR и/или бета цепи TCR, содержит последовательность нуклеиновой кислоты с, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% идентичностью последовательности с любой из SEQ ID NOs: 133, 134, 136 или 137. В некоторых вариантах осуществления, нуклеиновая кислота, кодирующая конструкт альфа цепи TCR и/или бета цепи TCR, содержит последовательность нуклеиновой кислоты с, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% идентичностью последовательности с любой из SEQ ID NOs: 195, 196, 198 или 199. В некоторых вариантах осуществления, нуклеиновая кислота, кодирующая конструкт альфа цепи TCR и/или бета цепи TCR, содержит последовательность нуклеиновой кислоты с, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 98% идентичность последовательности с любой из SEQ ID NOs: 210, 211, 213 или 214.
В разных вариантах осуществления, последовательность нуклеиновой кислоты, кодирующая TCR, является кодон-оптимизированной.
В разных вариантах осуществления, TCR связывается с MHC:GATA3 пептидным комплексом, где GATA пептид содержит, по меньшей мере, одну аминокислоту, кодированную GATA3 neoORF последовательностью. В разных вариантах осуществления, TCR связывается с MHC:GATA3 пептидным комплексом, где GATA пептид содержит, по меньшей мере, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 аминокислот, кодированных GATA3 neoORF последовательностью. В разных вариантах осуществления, TCR связывается с MHC:GATA3 пептидным комплексом, где GATA пептид содержит, по меньшей мере, одну аминокислоту, кодированную GATA3 neoORF последовательностью и, по меньшей мере, одну аминокислоту, кодированную GATA3 последовательностью дикого типа. В разных вариантах осуществления, TCR связывается с MHC:GATA3 пептидным комплексом, где GATA пептид содержит, по меньшей мере, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 аминокислот, кодированных GATA3 neoORF последовательностью и, по меньшей мере, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 аминокислот, кодированных GATA3 последовательностью дикого типа. В разных вариантах осуществления, TCR связывается с MHC:GATA3 пептидным комплексом, где GATA пептид содержит, по меньшей мере, одну аминокислоту, кодированную GATA3 neoORF последовательностью и, по меньшей мере, одну аминокислоту, не кодированную GATA3 neoORF последовательностью. В разных вариантах осуществления, TCR связывается с MHC:GATA3 пептидным комплексом, где GATA пептид содержит, по меньшей мере, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 аминокислот, кодированных GATA3 neoORF последовательность и, по меньшей мере, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 аминокислот, не кодированных GATA3 neoORF последовательностью. В разных вариантах осуществления, TCR связывается с MHC:GATA3 пептидным комплексом, где каждой аминокислотой GATA пептида является аминокислота, кодированная GATA3 neoORF последовательностью. В разных вариантах осуществления, TCR связывается с MHC:GATA3 пептидным комплексом, где GATA3 пептид содержит последовательность MLTGPPARV (SEQ ID NO: 141), KPKRDGYMF (SEQ ID NO: 203) или ESKIMFATL (SEQ ID NO: 218).
В разных вариантах осуществления, МНС человека кодирован HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью. В разных вариантах осуществления, TCR связывается с MHC:GATA3 пептидным комплексом, где МНС человека кодирован HLA-A02:01 аллелью. В разных вариантах осуществления, TCR связывается с MHC:GATA3 пептидным комплексом, где МНС человека кодирован HLA-B07:02 аллелью. В разных вариантах осуществления, TCR связывается с MHC:GATA3 пептидным комплексом, где МНС человека кодирован HLA-B08:01 аллелью.
В разных вариантах осуществления, TCR связывается с MHC:GATA3 пептидным комплексом, где МНС человека кодирован HLA-B08:01 аллелью и где GATA3 пептид содержит последовательность MLTGPPARV (SEQ ID NO: 141), KPKRDGYMF (SEQ ID NO: 203) или ESKIMFATL (SEQ ID NO: 218).
VIII. TCR специфические к BTK комплексам пептид-МНС
BTK ген может кодировать белок тирозинкиназы Брутона (BTK), который может иметь отношение к развитию и созреванию B клеток. Белок BTK может передавать химические сигналы, которые учат B клетки созревать и продуцировать антитела.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из BTK в комплексе с МНС человека, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 161 и SEQ ID NO: 176, или где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 164 и SEQ ID NO: 179.
Также, в настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует Т клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, где TCR специфически связывается с мутантом BTK пептида в комплексе с HLA-A02:01 белком; содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 161, 164, 176 или 179; и/или специфически связывается с мутантом BTK пептида, содержащим область с, по меньшей мере, 70% идентичностью последовательности с SEQ ID NO: 173 или 188.
Также в настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из BTK в комплексе с МНС человека, где эпитоп из BTK содержит область, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 173 или 188.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 167 или 182.
В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 170 или 185.
В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 159, 162, 174 и 177.
В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 160, 163, 175 и 178.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 167 или 182; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 170 или 185.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 159 или 174, CDR2 с SEQ ID NO: 160 или 175 и CDR3 с SEQ ID NO: 161 или 176; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 162 или 177, CDR2 с SEQ ID NO: 163 или 178 и CDR3 с SEQ ID NO: 164 или 179.
В некоторых вариантах осуществления, эпитоп содержит точечную мутацию. В некоторых вариантах осуществления, точечной мутацией является C481S мутация.
В разных вариантах осуществления, последовательность нуклеиновой кислоты, кодирующая TCR, является кодон-оптимизированной.
В разных вариантах осуществления, TCR связывается с MHC:BTK пептидным комплексом, где BTK пептид содержит точечную мутацию. В разных вариантах осуществления, TCR связывается с MHC:BTK пептидным комплексом, где BTK пептид содержит C481S точечную мутацию. В разных вариантах осуществления, TCR связывается с MHC:BTK пептидным комплексом, где BTK пептид содержит последовательность SLLNYLREM (SEQ ID NO: 173).
В некоторых вариантах осуществления, МНС человека кодирована HLA-A02:01 аллелью. В разных вариантах осуществления, МНС человека кодирована HLA-A02:01 аллелью. В разных вариантах осуществления, TCR связывается с MHC:BTK пептидным комплексом, где МНС человека кодирован HLA-A02:01 аллелью.
В разных вариантах осуществления, TCR связывается с MHC:BTK пептидным комплексом, где МНС человека кодирован HLA-A02:01 аллелью и где BTK пептид содержит последовательность SLLNYLREM (SEQ ID NO: 173).
IX. TCR специфические к EGFR комплексам пептид-МНС
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из EGFR в комплексе с МНС человека, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 449, SEQ ID NO: 466, SEQ ID NO: 483, SEQ ID NO: 500 и SEQ ID NO: 517, или где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 452, SEQ ID NO: 469, SEQ ID NO: 486, SEQ ID NO: 503 и SEQ ID NO: 520.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), способный специфически связываться с мутантом EGFR пептида в комплексе с белком, кодированным HLA аллелью субъекта с раком, где TCR содержит конструкт альфа цепи TCR и/или конструкт бета цепи TCR.
В настоящем документе представлена выделенная нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, где TCR специфически связывается с мутантом EGFR пептида в комплексе с HLA-A02:01 белком; содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с SEQ ID NO: 449, 466, 483, 500, 517, 452, 469, 486, 503, или 520; и/или специфически связывается с мутантом EGFR пептида, содержащим область с, по меньшей мере, 70% идентичностью последовательности с SEQ ID NO: 461, 462, 463, 478, 479, 480, 495, 496, 497, 512, 513, 514, 529, 530 или 531.
В настоящем документе представлена нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, способный специфически связываться с эпитопом из EGFR в комплексе с МНС человека, где эпитоп из EGFR содержит область, имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 461, 462, 463, 478, 479, 480, 495, 496, 497, 512, 513, 514, 529, 530 или 531.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 449, 466, 483, 500 или 517.
В некоторых вариантах осуществления, конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 452, 469, 486, 503 или 520.
В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 447, 464, 481, 498, 515, 450, 467, 484, 501 и 518.
В некоторых вариантах осуществления, конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 448, 465, 482, 499, 516, 451, 468, 485, 502 и 519.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 455, 472, 489, 506, или 523; и конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 458, 475, 492, 509 или 526.
В некоторых вариантах осуществления, конструкт альфа цепи TCR содержит CDR1 с SEQ ID NO: 447, 464, 481, 498 или 515, CDR2 с SEQ ID NO: 448, 465, 482, 499 или 516 и CDR3 с SEQ ID NO: 449, 466, 483, 500 или 517; и конструкт бета цепи TCR содержит CDR1 с SEQ ID NO: 450, 467, 484, 501 или 518, CDR2 с SEQ ID NO: 451, 468, 485, 502, или 519 и CDR3 с SEQ ID NO: 452, 469, 486, 503, или 520.
В некоторых вариантах осуществления, эпитоп содержит точечную мутацию. В некоторых вариантах осуществления, точечной мутацией является T790M мутация. В некоторых вариантах осуществления, МНС человека кодирован HLA-A02:01 аллелью.
В разных вариантах осуществления, последовательность нуклеиновой кислоты, кодирующая TCR, является кодон-оптимизированной.
В разных вариантах осуществления, TCR связывается с MHC:EGFR пептидным комплексом, где EGFR пептид содержит точечную мутацию. В разных вариантах осуществления, TCR связывается с MHC:EGFR пептидным комплексом, где EGFR пептид содержит T790M точечную мутацию. В разных вариантах осуществления, TCR связывается с MHC:EGFR пептидным комплексом, где EGFR пептид содержит последовательность QLIMQLMPF (SEQ ID NO: 461), LIMQLMPFGC (SEQ ID NO: 462) или MQLMPFGCLL (SEQ ID NO: 463).
В разных вариантах осуществления, МНС человека кодирован HLA-A02:01 аллелью. В разных вариантах осуществления, TCR связывается с MHC:EGFR пептидным комплексом, где МНС человека кодирован HLA-A02:01 аллелью.
В разных вариантах осуществления, TCR связывается с MHC:EGFR пептидным комплексом, где МНС человека кодирован HLA-A02:01 аллелью и где EGFR пептид содержит последовательность QLIMQLMPF (SEQ ID NO: 461), LIMQLMPFGC (SEQ ID NO: 462) или MQLMPFGCLL (SEQ ID NO: 463).
Доставка нуклеиновой кислоты или вектора
Нуклеиновые кислоты, кодирующие TCR или векторы, содержащие такие нуклеиновые кислоты могут быть доставлены в клетки-хозяева для осуществления экспрессии.
Такие термины, как «перенос», «введение» или «трансфекция» используются здесь взаимозаменяемо и относятся к введению нуклеиновых кислот, в частности экзогенных или гетерологичных нуклеиновых кислот, в клетку.
Клетки могут быть трансфицированы любыми носителями, с которыми может быть связана нуклеиновая кислота, например, путем образования комплексов с нуклеиновыми кислотами или образования везикул, в которые нуклеиновая кислота заключена или инкапсулирована, что приводит к повышению стабильности нуклеиновой кислоты по сравнению с голой нуклеиновой кислотой. Носители, применяемые согласно настоящему описанию, включают, например, жиросодержащие носители, такие как катионные липиды, липосомы, в частности катионные липосомы и мицеллы, и наночастицы. Катионные липиды могут образовывать комплексы с отрицательно заряженной нуклеиновой кислотой. В соответствии с настоящим описанием можно использовать любой катионный липид.
В разных вариантах осуществления, нуклеиновая кислота, кодирующая TCR в настоящем документе, функционально связана с промотором. Кроме того, в настоящем описании представлен, вектор, например, плазмида, челночный вектор, фагмид, космида, вектор экспрессии, ретровирусный вектор, аденовирусный вектор или частица и/или вектор для использования в генной терапии, который содержит одну или более нуклеиновых кислот, как описано выше. «Вектором» является молекула нуклеиновой кислоты, которая способна транспортировать другую нуклеиновую кислоту. Вектор содержит вставку нуклеиновой кислоты, которая кодирует полипептид или белок, желаемый для экспрессии в клетке, такой как клетка-хозяин. Для целей настоящего описания, вставкой может быть нуклеиновая кислота, кодирующая TCR; альфа цепь или бета цепь TCR или обе. Термин, «включение» последовательности нуклеиновой кислоты в вектор, может означать получение подходящего вектора экспрессии со вставкой, содержащей указанную последовательность нуклеиновой кислоты. «Вектором экспрессии» является вектор, который может управлять экспрессией белка, кодированного одним или более генами, переносимыми вектором, когда он присутствует в соответствующей среде. «Ретровирусами» являются вирусы, имеющие геном РНК. «Гаммаретровирус» относится к роду семейства retroviridae. Типовые гаммаретровирусы включают, но не ограничены ими, вирус стволовых клеток мыши, вирус лейкоза мышей, вирус лейкоза кошек, вирус саркомы кошек и вирусы ретикулоэндотелиоза птиц. «Лентивирус» относится к роду ретровирусов, которые способны инфицировать делящиеся и неделящиеся клетки. Несколько примеров лентивирусов включают ВИЧ (вирус иммунодефицита человека: включая ВИЧ 1 типа и ВИЧ 2 типа); вирус инфекционной анемии лошадей; вирус иммунодефицита кошек (FIV); вирус иммунодефицита крупного рогатого скота (BIV); и вирус иммунодефицита обезьян (SIV). Вектор, кодирующий основной вирус, также известен как «вирусный вектор». Существует большое количество доступных вирусных векторов, которые подходят для использования с изобретением, включая такие, которые идентифицированы для применения в генной терапии человека, например, описанные Pfeifer and Verma (Pfeifer, A. and I. M. Verma. 2001. Ann. Rev. Genomics Hum. Genet. 2:177-211). Подходящие вирусные векторы включают векторы на основе РНК вирусов, такие как векторы, полученные из ретровируса, например, векторы, полученные из вируса мышиного лейкоза Молони (MLV), и включают большее количество векторов, полученных из комплексных ретровирусов, например, векторы, полученные из лентивируса. К этой категории относятся векторы, полученные из ВИЧ-1. Другие примеры включают лентивирусные векторы, полученные из ВИЧ-2, FIV, вируса инфекционной анемии лошадей, SIV и вируса маэди/висна. Способы использования ретровирусных и лентивирусных вирусных векторов и упаковки клеток для трансдукции клеток-мишеней млекопитающих вирусными частицами, содержащими трансгены TCR, хорошо известны в данной области и были описаны ранее, например, в патенте США № 8,119,772; Walchli et al., 2011, PLoS One 6:327930; Zhao et al., J. Immunol., 2005, 174:4415-4423; Engels et al., 2003, Hum. Gene Ther. 14:1155-68; Frecha et al., 2010, Mol. Ther. 18:1748-57; Verhoeyen et al., 2009, Methods Mol. Biol. 506:97-114. Ретровирусные и лентивирусные векторные конструкты и системы экспрессии также коммерчески доступны. В некоторых вариантах осуществления, вирусный вектор используют для введения не эндогенной последовательности нуклеиновой кислоты, кодирующей TCRα цепь, специфичную для пептидного антигена, в гемопоэтические клетки-предшественники. Вирусным вектором может быть ретровирусный вектор или лентивирусный вектор. Вирусный вектор может также включать последовательность нуклеиновой кислоты, кодирующую маркер для трансдукции. Маркеры трансдукции для вирусных векторов известны в данной области и включают маркеры отбора, которые могут придавать резистентность к лекарственным средствам, или определяемые маркеры, такие как флуоресцентные маркеры или поверхностноклеточные белки, которые могут быть обнаружены такими способами, как проточная цитометрия. Если геном вирусного вектора содержит более одной последовательности нуклеиновой кислоты, предназначенной для экспрессии в клетке-хозяине, в виде отдельных транскриптов, вирусный вектор может также содержать дополнительную последовательность между двумя (или более) транскриптами, обеспечивающую бицистронную или мультицистронную экспрессию. Примеры таких последовательностей, используемых в вирусных векторах, включают внутренние участки посадки рибосомы (IRES), сайты расщепления фурином, вирусные 2A пептиды. Для доставки полинуклеотидов также могут быть использованы другие векторы, включая ДНК вирусные векторы, включая, например, векторы на основе аденовирусов и векторы на основе аденоассоциированных вирусов (AAV); векторы, полученные из вирусов простого герпеса (HSV), включая векторы ампликонов, HSV с дефектом репликации и ослабленный HSV (Krisky et al., 1998, Gene Ther. 5: 1517-30). Другие векторы включают векторы, полученные из бакуловирусов и альфа-вирусов (Jolly D J. 1999. Emerging viral vectors. pp 209-40 in Friedmann T. ed. 1999. The development of human gene therapy. New York: Cold Spring Harbor Lab).
Вектор может включать последовательности нуклеиновых кислот, которые позволяют нуклеиновым кислотам реплицироваться в клетке-хозяине, например, точку начала репликации. Вектор также может включать один или более селективных маркерных генов и другие генетические элементы, известные специалистам в данной области. Вектором предпочтительно является вектор экспрессии, который включает нуклеиновую кислоту по настоящему изобретению, функционально связанную с последовательностями, обеспечивающими экспрессию указанной нуклеиновой кислоты.
В некоторых вариантах осуществления, в настоящем документе представлен вектор, содержащий нуклеиновую кислоту, кодирующую TCR, описанную в настоящем документе. В некоторых вариантах осуществления, вектором является самоамплифицирующийся РНК репликон, плазмида, фаг, транспозон, космида, вирус или вирион. В некоторых вариантах осуществления вектором является вирусный вектор. В некоторых вариантах осуществления вектор получен из ретровируса, лентивируса, аденовируса, аденоассоциированного вируса, вируса герпеса, вируса оспы, вируса альфа, вируса осповакцины, вируса гепатита B, папилломавируса человека или их псевдотипа. В некоторых вариантах осуществления, вектором является не вирусный вектор. В некоторых вариантах осуществления не вирусным вектором является наночастица, катионный липид, катионный полимер, металлический нанополимер, наностержень, липосома, мицелла, микропузырек, проникающий пептид или липосфера.
В настоящем документе представлены конструкты, например, конструкты нуклеиновой кислоты, которые кодируют альфа цепь и бета цепь TCR для экспрессии в клетке. В некоторых вариантах осуществления, конструкты содержат один или более полинуклеотидов, кодирующих альфа цепь TCR и бета цепь TCR. В некоторых вариантах осуществления, полинуклеотиды включены в подходящий вектор. В некоторых вариантах осуществления, полинуклеотиды, кодирующие альфа цепь и бета цепь, включены в один и тот же вектор. В некоторых вариантах осуществления, полинуклеотиды, кодирующие альфа цепь и бета цепь, включены в разные векторы, и оба вектора доставляются для экспрессии в одной клетке.
В некоторых вариантах осуществления, клетка может быть трансдуцирована или трансфицирована нуклеиновой кислотой, кодирующей TCR, где клетка способна экспрессировать TCR, и клетка используется в качестве терапевтического агента. В некоторых вариантах осуществления, клетка получена от субъекта или хозяина, где субъект или хозяин является человеком. В некоторых вариантах осуществления, субъект или хозяин содержат клетку, имеющую мутацию в эпитопе, и экспрессируемый в клетке TCR способен специфически связываться с эпитопом, имеющим мутацию. В некоторых вариантах осуществления, клеткой является лимфоцит. В некоторых вариантах осуществления, Т лимфоцит. В некоторых вариантах осуществления, клеткой является клетка-предшественник лимфоцитов. В некоторых вариантах осуществления, клеткой является клетка-предшественник Т лимфоцитов. В некоторых вариантах осуществления, клеткой является клетка-потомок Т-лимфоцита. В некоторых вариантах осуществления, клеткой является тимоцит.
В некоторых вариантах осуществления, T клетками являются зрелые T клетки. В некоторых вариантах осуществления, T клетками являются антиген интатктные T клетки. Клетка-хозяин может быть культивирована ex vivo в течение 1, 2, 3, 4, 5 или более дней для отслеживания и восстановления после трансфекции или трансдукции полинуклеотидом(амии), кодирующим TCR.
Х. Неоантигены
TCR, раскрытые в настоящем документе, специфичны для иммуногенных неоантигенов. В некоторых вариантах осуществления, неоантигенный пептид получен из RAS. В некоторых вариантах осуществления, неоантигенный пептид получен из GATA3. В некоторых вариантах осуществления, неоантиген пептид получен из BTK. В некоторых вариантах осуществления, неоантиген пептид получен из TMPRSS2: ERG. В некоторых вариантах осуществления, один или более неоантигенных пептидов загружаются в APC, где APC, нагруженные пептидом, затем используются для стимуляции Т клеток с целью продуцирования антигенспецифических Т клеток. В некоторых вариантах осуществления, APC, используемые для загрузки пептида, являются дендритные клетки. Иммуногенные последовательности неоантигена могут быть идентифицированы любым подходящим способом, известным в данной области.
В разных вариантах осуществления, неоантиген содержит эпитоп. Как у животных, так и у людей, мутированные эпитопы могут быть потенциально эффективными в вызове иммунного ответа или активации Т клеток. В некоторых вариантах осуществления, эпитоп содержит мутацию. В некоторых вариантах осуществления, мутация выбрана из группы, состоящей из точечной мутации, мутации сайта сплайсинга, мутации «сдвига рамки», мутации сквозного прохождения, мутации слияния генов и любой их комбинации.
В некоторых вариантах осуществления, эпитоп имеет длину, по меньшей мере, 8 аминокислот. В некоторых вариантах осуществления, эпитоп имеет длину, по меньшей мере, 16 аминокислот. В некоторых вариантах осуществления, эпитоп имеет длину 8-25 аминокислот. В некоторых вариантах осуществления, эпитоп имеет длину 8-12 аминокислот. В некоторых вариантах осуществления, эпитоп имеет длину 16-25 аминокислот. В некоторых вариантах осуществления, эпитоп имеет длину 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 аминокислот.
В определенных вариантах осуществления, неоантиген или его эпитоп может содержать, но не ограничен ими, примерно 5, примерно 6, примерно 7, примерно 8, примерно 9, примерно 10, примерно 11, примерно 12, примерно 13, примерно 14, примерно 15, примерно 16, примерно 17, примерно 18, примерно 19, примерно 20, примерно 21, примерно 22, примерно 23, примерно 24, примерно 25, примерно 26, примерно 27, примерно 28, примерно 29, примерно 30, примерно 31, примерно 32, примерно 33, примерно 34, примерно 35, примерно 36, примерно 37, примерно 38, примерно 39, примерно 40, примерно 41, примерно 42, примерно 43, примерно 44, примерно 45, примерно 46, примерно 47, примерно 48, примерно 49, примерно 50, примерно 60, примерно 70, примерно 80, примерно 90, примерно 100, примерно 110, примерно 120 или больше аминокислотных остатков, и любой интервал, выводимый из них. В конкретных вариантах, неоантиген или его эпитоп равен или составляет менее чем 100 аминокислот.
В некоторых вариантах осуществления, неоантиген или его эпитоп для MHC I класса имеет длину 13 остатков или меньше, и обычно состоит примерно из 8-11 остатков, в частности 9 или 10 остатков. В некоторых вариантах осуществления, неоантиген или его эпитоп для MHC II класса имеет длину 9-24 остатка.
В некоторых вариантах осуществления, неоантигены связывают HLA белок (например, HLA I класса или HLA II класса). В конкретных вариантах осуществления, неоантигены связывают HLA белок с большей аффинностью, чем соответствующий пептид дикого типа. В конкретных вариантах осуществления, неоантигенный пептид или полипептид имеет IC50, по меньшей мере, менее чем 5000 нМ, по меньшей мере, менее чем 500 нМ, по меньшей мере, менее чем 100 нМ, по меньшей мере, менее чем 50 нМ или менее.
В некоторых вариантах осуществления, эпитоп связывается с МНС человека с большей аффинностью, чем у эпитопа дикого типа. В некоторых вариантах осуществления, эпитоп связывается с МНС человека с KD или IC50 менее чем 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ. В некоторых вариантах осуществления, эпитоп содержит мутацию, где мутация не присутствует в не раковых клетках субъекта. В некоторых вариантах осуществления, эпитоп кодирован геном или экспрессирует ген раковых клеток субъекта. В некоторых вариантах осуществления, TCR связывается с HLA-пептидным комплексом с KD или IC50 менее чем 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ.
В некоторых вариантах осуществления, неоантигенный пептид может иметь от примерно 8 до примерно 50 аминокислотных остатков в длину, или от примерно 8 до примерно 30, от примерно 8 до примерно 20, от примерно 8 до примерно 18, от примерно 8 до примерно 15, или от примерно 8 до примерно 12 аминокислотных остатков в длину. В некоторых вариантах осуществления, неоантигенный пептид может иметь от примерно 8 до примерно 500 аминокислотных остатков в длину, или от примерно 8 до примерно 450, от примерно 8 до примерно 400, от примерно 8 до примерно 350, от примерно 8 до примерно 300, от примерно 8 до примерно 250, от примерно 8 до примерно 200, от примерно 8 до примерно 150, от примерно 8 до примерно 100, от примерно 8 до примерно 50, или от примерно 8 до примерно 30 аминокислотных остатков в длину.
В некоторых вариантах осуществления, неоантигенный пептид может иметь, по меньшей мере, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, или более аминокислотных остатков в длину. В некоторых вариантах осуществления, неоантигенный пептид может иметь, по меньшей мере, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 55, 60, 70, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500 или более аминокислотных остатков в длину. В некоторых вариантах осуществления, неоантигенный пептид может иметь не более 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50 или менее аминокислотных остатков в длину. В некоторых вариантах осуществления, неоантигенный пептид может иметь не более 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 55, 60, 70, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500 или менее аминокислотных остатков в длину.
В некоторых вариантах осуществления, неоантигенный пептид имеет общую длину, по меньшей мере, 8, по меньшей мере, 9, по меньшей мере, 10, по меньшей мере, 11, по меньшей мере, 12, по меньшей мере, 13, по меньшей мере, 14, по меньшей мере, 15, по меньшей мере, 16, по меньшей мере, 17, по меньшей мере, 18, по меньшей мере, 19, по меньшей мере, 20, по меньшей мере, 21, по меньшей мере, 22, по меньшей мере, 23, по меньшей мере, 24, по меньшей мере, 25, по меньшей мере, 26, по меньшей мере, 27, по меньшей мере, 28, по меньшей мере, 29, по меньшей мере, 30, по меньшей мере, 40, по меньшей мере, 50, по меньшей мере, 60, по меньшей мере, 70, по меньшей мере, 80, по меньшей мере, 90, по меньшей мере, 100, по меньшей мере, 150, по меньшей мере, 200, по меньшей мере, 250, по меньшей мере, 300, по меньшей мере, 350, по меньшей мере, 400, по меньшей мере, 450, или, по меньшей мере, 500 аминокислот.
В некоторых вариантах осуществления, неоантигенный пептид имеет общую длину не более 8, не более 9, не более 10, не более 11, не более 12, не более 13, не более 14, не более 15, не более 16, не более 17, не более 18, не более 19, не более 20, не более 21, не более 22, не более 23, не более 24, не более 25, не более 26, не более 27, не более 28, не более 29, не более 30, не более 40, не более 50, не более 60, не более 70, не более 80, не более 90, не более 100, не более 150, не более 200, не более 250, не более 300, не более 350, не более 400, не более 450, или не более 500 аминокислот.
В некоторых вариантах осуществления, неоантигенный пептид может иметь значение pI от примерно 0,5 до примерно 12, от примерно 2 до примерно 10, или от примерно 4 до примерно 8. В некоторых вариантах осуществления, неоантигенный пептид может иметь значение pI, по меньшей мере, 4,5, 5, 5,5, 6, 6,5, 7, 7,5 или более. В некоторых вариантах осуществления, неоантигенный пептид может иметь значение pI не более 4,5, 5, 5,5, 6, 6,5, 7, 7,5 или менее.
В некоторых вариантах осуществления, неоантигенный пептид может иметь HLA аффинность связывания от примерно 1пМ до примерно 1мМ, от примерно 100пМ до примерно 500мкМ, от примерно 500пМ до примерно 10мкМ, от примерно 1нМ до примерно 1мкМ, или от примерно 10нМ до примерно 1мкМ. В некоторых вариантах осуществления, неоантигенный пептид может иметь HLA аффинность связывания, по меньшей мере, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 700, 800, 900 мкМ или более. В некоторых вариантах осуществления, неоантигенный пептид может иметь HLA аффинность связывания не более 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 700, 800, 900 мкМ.
В некоторых вариантах осуществления неоантиген, описанный в настоящем документе, может содержать носители, такие как те, которые хорошо известны в данной области, например, тиреоглобулин, альбумины, такие как сывороточный альбумин человека, столбнячный токсин, полиаминокислотные остатки, такие как поли L-лизин, поли L-глутаминовая кислота, белки вируса гриппа, сердцевинный белок вируса гепатита В и подобные.
В некоторых вариантах осуществления, неоантигенный пептид, описанный в настоящем документе, может быть модифицирован ацилированием концевого NH2, например, алканоилом (C1-C20), или тиогликолилацетилированием, амидированием концевого карбоксила, например аммиаком, метиламином и т.д. В некоторых вариантах осуществления, эти модификации могут предоставлять сайты для связывания с носителем или другой молекулой.
В некоторых вариантах осуществления, неоантигенный пептид, описанный в настоящем документе, может содержать модификации, такие как, но не ограничиваясь ими, гликозилирование, окисление боковой цепи, биотинилирование, фосфорилирование, добавление поверхностно-активного вещества, например жира, или может быть химически модифицирован, например, ацетилированием, и т.д. Более того, связи в пептиде могут быть иными, чем связи пептида, например, ковалентными связями, сложноэфирными или эфирными связями, дисульфидными связями, водородными связями, ионными связями и т.д.
В некоторых вариантах осуществления неоантигенный пептид, описанный в настоящем документе, может содержать замещения для модификации физических свойств (например, стабильности или растворимости) полученного пептида. Например, неоантигенные пептиды могут быть модифицированы замещением цистеина (C) на α-аминомасляную кислоту («B»). Благодаря своей химической природе, цистеин имеет склонность образовывать дисульфидный мостик и в достаточной степени изменять пептид структурно, чтобы уменьшить связывающую способность. Замещение C α-аминомасляной кислотой не только облегчает эту проблему, но и в некоторых случаях фактически улучшает способность связывания и перекрестного связывания. Замещение цистеина α-аминомасляной кислотой может происходить на любом остатке неоантигенного пептида, например, в якорных или не якорных положениях эпитопа или аналога в пептиде или на других положениях пептида.
В некоторых вариантах осуществления, неоантигенный пептид, описанный в настоящем документе, может содержать миметики аминокислоты или не природные аминокислотные остатки, например D- или L-нафтилаланин; D- или L-фенилглицин; D- или L-2-тиенеилаланин; D- или L-1, -2, 3- или 4-пиренеилаланин; D- или L-3 тиенеилаланин; D- или L-(2-пиридинил)-аланин; D- или L-(3-пиридинил)-аланин; D- или L-(2-пиразинил)-аланин; D- или L-(4-изопропил)-фенилглицин; D-(трифторметил)-фенилглицин; D-(трифторметил)-фенилаланин; D-.ро.-фторфенилаланин; D- или L-.ро.-бифенил-фенилаланин; D- или L-.ро.-метоксибифенилфенилаланин; D- или L-2-индол(аллил)аланины; и D- или L-алкилаланины, где алкильная группа может быть замещенным или незамещенным метилом, этилом, пропилом, гексилом, бутилом, пентилом, изопропилом, изобутилом, втор-изотилом, изопентилом или не кислыми аминокислотными остатками. Ароматические кольца не природной аминокислоты включают, например, тиазолил, тиофенил, пиразолил, бензимидазолил, нафтил, фуранил, пирролил и пиридил ароматические кольца. Особенно полезны модифицированные пептиды, содержащие различные миметики аминокислот или не природные аминокислотные остатки, поскольку они имеют тенденцию проявлять повышенную стабильность in vivo. Такие пептиды также могут обладать улучшенными свойствами при хранении или улучшенными производственными свойствами.
Стабильность пептида может оцениваться множеством путей. Например, пептидазы и разные биологические среды, такие как плазма человека и сыворотка, применяют для тестирования стабильности. См., например, Verhoef, et al., Eur. J. Drug Metab. Pharmacokinetics 11:291 (1986). Период полужизни пептидов, описанных в настоящем документе, удобно определять с помощью анализа в 25% сыворотки крови человека (об./об.). Протокол является следующим: объединенную сыворотка человека (тип AB, не инактивированная нагреванием) разрушают центрифугированием перед использованием. Затем сыворотку разводят до 25% RPMI-1640 или другой подходящей средой для культивирования тканей. Через заранее определенные интервалы времени небольшое количество реакционного раствора удаляют и добавляют либо 6% водную трихлоруксусную кислоту (TCA), либо этанол. Мутный реакционный образец охлаждают (4°C) в течение 15 минут, а затем центрифугируют для пеллетирования осажденных белков сыворотки. Затем присутствие пептидов определяют ВЭЖХ с обращенной фазой с использованием условий хроматографии, специфичных для стабильности.
В некоторых вариантах осуществления, неоантигенный пептид, описанный в настоящем документе, может быть получен синтетически, с помощью технологии рекомбинантной ДНК или химического синтеза, или может быть выделен из природных источников, таких как нативные опухоли или патогенные организмы. Эпитопы могут быть синтезированы индивидуально или прямо или косвенно объединены в пептид. Хотя неоантигенный пептид, описанный в настоящем документе, будет по существу свободен от других встречающихся в природе белков клетки-хозяина и их фрагментов, в некоторых вариантах осуществления, пептид может быть синтетически конъюгирован для присоединения к нативным фрагментам или частицам.
В некоторых вариантах осуществления, неоантигенный пептид, описанный в настоящем документе, может быть получен множеством способов. В некоторых вариантах осуществления, пептиды могут быть синтезированы в растворе или на твердом носителе в соответствии с общепринятыми методами. Различные автоматические синтезаторы коммерчески доступны и могут применяться в соответствии с известными протоколами. (См., например, Stewart & Young, SOLID PHASE PEPTIDE SYNTHESIS, 2D. ED., Pierce Chemical Co., 1984). Также, отдельные пептиды могут быть объединены с применением химического лигирования с получением больших пептидов, которые все еще находятся в рамках изобретения.
Альтернативно, можно использовать технологию рекомбинантной ДНК, где нуклеотидная последовательность, кодирующая пептид, вставленная в вектор экспрессии, трансформируется или трансфицируется в подходящую клетку-хозяин и культивируется в условиях, подходящих для экспрессии. Эти методики общеизвестны в данной области и описаны в общих чертах в Sambrook et al., MOLECULAR CLONING, A LABORATORY MANUAL, Cold Spring Harbor Press, Cold Spring Harbor, N.Y. (1989). Таким образом, рекомбинантные пептиды, которые содержат или состоят из одного или более эпитопов, описанных в настоящем документе, могут применяться для презентирования соответствующего Т клеточного эпитопа.
XI. Фармацевтические композиции
Фармацевтические композиции могут быть составлены с использованием одного или более физиологически приемлемых носителей, включая эксципиенты и вспомогательные вещества, которые облегчают переработку активных агентов в препараты, которые можно использовать в фармацевтике. Правильный состав может зависеть от выбранного пути введения. Любые из хорошо известных методик, носителей и эксципиентов могут быть использованы как подходящие и, как известно в данной области техники.
В некоторых случаях, фармацевтическую композицию составляют в виде терапевтического средства на клеточной основе, например, терапевтического средства на основе Т клеток. В некоторых вариантах осуществления, фармацевтическая композиция содержит терапию на основе пептидов, терапию на основе нуклеиновой кислоты, терапию на основе антител и/или терапию на основе клеток. В некоторых вариантах осуществления, фармацевтическая композиция содержит терапевтическое средство на основе пептидов или терапевтическое средство на основе нуклеиновой кислоты, в котором нуклеиновая кислота кодирует полипептиды. Композиция может содержать Т клетки, специфические для двух или более иммуногенных антигенов или неоантигенных пептидов. В некоторых вариантах осуществления, терапевтическое средство, специфическое для Т клеток, может быть дополнено одной или более дополнительными терапиями.
В некоторых вариантах осуществления, в настоящем документе раскрыта фармацевтическая композиция, содержащая: нуклеиновую кислоту, кодирующую TCR, таргетирующий неоантиген, вектор, содержащий нуклеиновую кислоту, белок, кодированный нуклеиновой кислотой или клетку-хозяина, содержащую нуклеиновую кислоту, белок или вектор; и фармацевтически приемлемый эксципиент или разбавитель. В некоторых вариантах осуществления, фармацевтическая композиция дополнительно содержит иммуномодулирующий агент или адъювант. В некоторых вариантах осуществления, иммуномодулирующим агентом является цитокин. В некоторых вариантах осуществления, адъювантом является поли I:C.
Также в настоящем документе представлено применение фармацевтических композиций в лечении иммунного заболевания или рака.
Фармацевтические композиции могут включать, помимо активного ингредиента, фармацевтически приемлемый эксципиент, носитель, буфер, стабилизатор или другие материалы, хорошо известные специалистам в данной области. Такие материалы должны быть нетоксичными и не должны влиять на эффективность активного ингредиента. Точная природа носителя или другого материала будет зависеть от пути введения. Приемлемые носители, эксципиенты или стабилизаторы включают такие, которые нетоксичны для реципиентов в используемых дозировках и концентрациях, и включают буферы, такие как фосфат, цитрат и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты (такие как хлорид октадецилдиметилбензиламмония; хлорид гексаметония; хлорид бензалкония, хлорид бензетония; фенол, бутиловый или бензиловый спирт; алкилпарабены, такие как метил или пропилпарабен; катехол; резорцин; циклогексанол; 3-пентанол; и м-крезол); низкомолекулярные (менее чем примерно 10 остатков) полипептиды; белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатирующие агенты, такие как ЭДТК; сахара, такие как сахароза, маннит, трегалоза или сорбит; солеобразующие противоионы, такие как натрий; металлические комплексы (например, Zn-протеиновые комплексы); и/или неионные поверхностно-активные вещества, такие как TWEEN®, PLURONICS® или полиэтиленгликоль(ПЭГ).
Приемлемые носители являются физиологически приемлемыми для пациента, которому их вводят, и сохраняют терапевтические свойства соединений, с/в которых он вводится. Приемлемые носители и их составы в общем описаны в, например, Remington’s Pharmaceutical Sciences (18th ed. A. Gennaro, Mack Publishing Co., Easton, PA 1990). Одним из примеров носителя является физиологический раствор. Фармацевтически приемлемым носителем является фармацевтически приемлемый материал, композиция или носитель, такой как жидкий или твердый наполнитель, разбавитель, эксципиент, растворитель или инкапсулирующий материал, участвующие в переносе или транспортировке рассматриваемых соединений из места введения одного органа или части тела в другой орган или часть тела или в in vitro аналитическую систему. Приемлемые носители совместимы с другими ингредиентами состава и не причиняют вреда субъекту, которому они вводятся. Приемлемый носитель также не должен изменять специфическую активность других ингредиентов.
В одном аспекте, в настоящем документе представлены фармацевтически приемлемые или физиологически приемлемые композиции, включающие растворители (водные или не водные), растворы, эмульсии, дисперсионные среды, покрытия, изотонические и усиливающие или замедляющие абсорбцию агенты, совместимые с фармацевтическим введением. Следовательно, фармацевтические композиции или фармацевтические составы относятся к композиции, подходящей для фармацевтического применения у субъекта. Композиции могут быть составлены таким образом, чтобы они были совместимы с конкретным путем введения (т.е. системным или местным). Таким образом, композиции включают носители, разбавители или эксципиенты, подходящие для введения различными путями.
В некоторых вариантах осуществления, фармацевтическая композиция может дополнительно содержать приемлемую добавку для улучшения стабильности композиции. Приемлемые добавки не могут изменять специфическую активность активного агента, например, иммунных клеток. Примеры приемлемых добавок включают, но не ограничены ими, сахар, такой как маннит, сорбит, глюкоза, ксилит, трегалоза, сорбоза, сахароза, галактоза, декстран, декстроза, фруктоза, лактоза и их смеси. Приемлемые добавки можно комбинировать с приемлемыми носителями и/или эксципиентами, такими как декстроза. Альтернативно, примеры приемлемых добавок включают, но не ограничены ими, поверхностно-активное вещество, такое как полисорбат 20 или полисорбат 80, для повышения стабильности пептида и уменьшения желирования раствора. Поверхностно-активное вещество может быть добавлено в композицию в количестве от 0,01% до 5% раствора. Добавление таких приемлемых добавок увеличивает стабильность и период полужизни композиции при хранении.
В некоторых вариантах осуществления фармацевтическая композиция содержит терапевтический агент, которым является T клетка, экспрессирующая один или более полинуклеотидов, кодирующих Т-клеточный рецептор. В некоторых вариантах осуществления, фармацевтическая композиция содержит физиологически приемлемый носитель, подходящий для суспензии клеток.
Фармацевтическая композиция может вводиться, например, путем инъекции. Фармацевтические композиции для инъекций включают водные растворы (если они водорастворимы) или дисперсии и стерильные порошки для немедленного приготовления стерильных растворов или дисперсий для инъекций. Для внутривенного введения, подходящие носители включают физиологический раствор, бактериостатическую воду или физиологический раствор с фосфатным буфером (ФРФБ). Носителем может быть растворитель или дисперсионная среда, содержащая, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль и подобные) и их подходящие смеси. Текучесть можно поддерживать, например, путем использования покрытия, такого как лецитин, путем поддержания необходимого размера частиц в случае дисперсии и использования поверхностно-активных веществ. Антибактериальные и противогрибковые агенты включают, например, парабены, хлорбутанол, фенол, аскорбиновую кислоту и тимеросал. В композицию могут быть включены изотонические агенты, например, сахара, многоатомные спирты, такие как маннит, сорбит, и хлорид натрия. Полученные растворы могут быть упакованы для использования как есть или лиофилизированы; лиофилизированный препарат может быть позже объединен со стерильным раствором до введения. Для внутривенного введения, инъекции или инъекции в место поражения активный ингредиент будет в форме парентерально приемлемого водного раствора, который не содержит пирогены и имеет подходящий pH, изотоничность и стабильность. Специалисты в данной области техники могут приготовить подходящие растворы с использованием, например, изотонических носителей, таких как инъекция хлорида натрия, инъекция Рингера, инъекция лактата Рингера. При необходимости могут быть включены консерванты, стабилизаторы, буферы, антиоксиданты и/или другие добавки. Стерильные растворы для инъекций могут быть приготовлены путем включения активного ингредиента в необходимом количестве в подходящий растворитель с одним или комбинацией ингредиентов, перечисленных выше, по необходимости, с последующей стерилизацией фильтрованием. Обычно дисперсии готовят путем включения активного ингредиента в стерильный носитель, который содержит основную дисперсионную среду и другие необходимые ингредиенты из перечисленных выше. В случае стерильных порошков для приготовления стерильных растворов для инъекций, предпочтительными способами приготовления могут быть вакуумная сушка и сублимационная сушка, которые дают порошок активного ингредиента плюс любого дополнительного желаемого ингредиента, из его раствора, предварительно стерилизованного фильтрованием.
Фармацевтические композиции могут быть удобно введены внутривенно, например, инъекцией стандартной дозы. Для инъекции активный ингредиент может быть в форме парентерально приемлемого водного раствора, который по существу не содержит пирогены и имеет подходящий pH, изотоничность и стабильность. Можно приготовить подходящие растворы, используя, например, изотонические носители, такие как инъекция хлорида натрия, инъекция Рингера, инъекция лактата Рингера. При необходимости могут быть включены консерванты, стабилизаторы, буферы, антиоксиданты и/или другие добавки. Кроме того, композиции можно вводить путем через аэрозоль.
Когда фармацевтические композиции рассматриваются для использования в лекарственных средствах или любом из способов, представленных в настоящем документе, предполагается, что композиция может по существу не содержать пирогены, так что композиция не будет вызывать воспалительную реакцию или небезопасную аллергическую реакцию при введении пациенту-человеку. Тестирование композиций на пирогены и приготовление композиций, по существу, не содержащих пирогены, хорошо известны специалисту в данной области техники и могут быть выполнены с использованием коммерчески доступных наборов.
Приемлемые носители могут содержать соединение, которое стабилизирует, увеличивает или задерживает абсорбцию, или увеличивает или задерживает клиренс. Такие соединения включают, например, углеводы, такие как глюкоза, сахароза или декстраны; низкомолекулярные белки; композиции, уменьшающие клиренс или гидролиз пептидов; или эксципиенты или другие стабилизаторы и/или буферы. К агентам, замедляющим всасывание, относятся, например, моностеарат алюминия и желатин. Детергенты также могут быть использованы для стабилизации или увеличения или уменьшения абсорбции фармацевтических композиций, включая липосомные носители. Для защиты от переваривания соединение можно объединить в комплекс с композицией, чтобы сделать его устойчивым к кислотному и ферментативному гидролизу, или соединение можно объединить в подходящем устойчивом носителе, таком как липосома. Средства защиты соединений от переваривания известны в данной области техники (например, Fix (1996) Pharm Res. 13:1760 1764; Samanen (1996) J. Pharm. Pharmacol. 48:119 135; и патент США № 5,391,377).
Фармацевтические композиции могут вводиться способом, совместимым с дозированной формой и в терапевтически эффективном количестве. Вводимое количество зависит от субъекта, которого лечат, способности иммунной системы субъекта использовать активный ингредиент и желаемой степени связывающей способности. Точные количества активного ингредиента, необходимые для введения, зависят от мнения практикующего врача и индивидуальны для каждого индивидуума. Подходящие схемы для начального введения и повторных инъекций также варьируются, но характеризуются начальным введением с последующими повторными дозами с интервалом в один или более часов с последующей инъекцией или другим введением. Альтернативно, рассматриваются непрерывные внутривенные инфузии, достаточные для поддержания концентраций в крови.
В некоторых вариантах осуществления, настоящее описание направлено на иммуногенную композицию, например, фармацевтическую композицию, способную вызывать неоантигенспецифический ответ (например, гуморальный или клеточно-опосредованный иммунный ответ). В некоторых вариантах осуществления, иммуногенная композиция содержит неоантигенные терапевтические средства (например, пептиды, полинуклеотиды, TCR, CAR, клетки, содержащие TCR или CAR, дендритные клетки, содержащие полипептид, дендритные клетки, содержащие полинуклеотид, антитело и т.д.), описанные в настоящем документе, соответствующие специфическому для опухоли антигену или неоантигену.
В некоторых вариантах осуществления, антиген, полипептиды или полинуклеотиды могут быть представлены в виде антигенпрезентирующих клеток (например, дендритных клеток), содержащих такие полипептиды или полинуклеотиды. В других вариантах осуществления, такие антигенпрезентирующие клетки применяют для стимуляции Т клеток для использования у пациентов. В некоторых вариантах осуществления, антигенпрезентирующими клетками являются дендритные клетки. В родственных вариантах осуществления, дендритными клетками являются аутологичные дендритные клетки, в которые вводят неоантиген, пептид или нуклеиновая кислота. Неоантигенным пептидом может быть любой подходящий пептид, который вызывает соответствующий Т клеточный ответ. В некоторых вариантах осуществления, Т клеткой является CTL. В некоторых вариантах осуществления, Т клеткой является HTL. Таким образом, один вариант осуществления настоящего раскрытия представляет иммуногенную композицию, содержащую, по меньшей мере, одну антигенпрезентирующую клетку (например, дендритную клетку), в которую введен или загружен один или более неоантигенных полипептидов или полинуклеотидов, описанных в настоящем документе. В некоторых вариантах осуществления, такие APC являются аутологичными (например, аутологичные дендритные клетки). Альтернативно, мононуклеарные клетки периферической крови (PBMC), выделенные у пациента, могут быть загружены неоантигенными пептидами или полинуклеотидами ex vivo. В родственных вариантах осуществления, такие APC или PBMC вводят инъекцией обратно пациенту. Полинуклеотидом может быть любой подходящий полинуклеотид, который способен трансдуцировать дендритную клетку, что приводит к презентированию неоантигенного пептида и вызову иммунитета. В некоторых вариантах осуществления, такие антигенпрезентирующие клетки (APC) (например, дендритные клетки) или мононуклеарные клетки периферической крови (PBMC) используют для стимуляции Т клетки (например, аутологичной Т клетки или аллогенной Т клетки). В родственных вариантах осуществления, Т клеткой является CTL. В других родственных вариантах осуществления, Т клеткой является HTL. В некоторых вариантах осуществления, Т клетками являются CD8+ Т клетки. В некоторых вариантах осуществления, Т клетками являются CD4+ Т клетки. Затем пациенту инъецируют такие Т клетки. В некоторых вариантах осуществления, пациенту инъецируют CTL. В некоторых вариантах осуществления пациенту инъецируют HTL. В некоторых вариантах осуществления, пациенту инъецируют как CTL, так и HTL. Введение любого из терапевтических средств можно проводить одновременно или последовательно и в любом порядке.
В некоторых вариантах осуществления, фармацевтические композиции (например, иммуногенные композиции), описанные в настоящем документе для терапевтического лечения, могут быть составлены для парентерального, местного, назального, перорального или локального введения. В некоторых вариантах осуществления, фармацевтические композиции, описанные в настоящем документе, вводят парентерально, например, внутривенно, подкожно, внутрикожно или внутримышечно. В некоторых вариантах осуществления, композицию можно вводить внутриопухолево. Композиции можно вводить в место хирургического иссечения, чтобы вызвать местный иммунный ответ на опухоль. В некоторых вариантах осуществления, в настоящем документе описаны композиции для парентерального введения, которые содержат раствор неоантигенных пептидов и иммуногенные композиции, растворенные или суспендированные в приемлемом носителе, например водном носителе. Можно использовать различные водные носители, например, воду, забуференную воду, 0,9% физиологический раствор, 0,3% глицин, гиалуроновую кислоту и подобные. Эти композиции можно стерилизовать обычными, хорошо известными способами стерилизации или можно стерилизовать фильтрованием. Полученные водные растворы могут быть упакованы для использования как есть или лиофилизированы, при этом лиофилизированный препарат перед введением объединяют со стерильным раствором. Композиции могут содержать фармацевтически приемлемые вспомогательные вещества, необходимые для приближения физиологических условий, такие как регулирующие pH и буферные агенты, регулирующие тоничность агенты, смачивающие агенты и подобные, например, ацетат натрия, лактат натрия, хлорид натрия, хлорид калия, хлорид кальция, монолаурат сорбитана, олеат триэтаноламина и т.д.
Способность адъюванта усиливать иммунный ответ на антиген обычно проявляется в значительном усилении иммуноопосредованной реакции или уменьшении симптомов заболевания. Например, повышение гуморального иммунитета может проявляться значительным увеличением титра антител, повышенных к антигену, и повышение активности Т клеток может проявляться в увеличении пролиферации клеток, или клеточной цитотоксичности, или секреции цитокина. Адъювант также может изменять иммунный ответ, например, изменяя преимущественно гуморальный ответ или ответ Т хелпера 2 на преимущественно клеточный ответ или ответ Т хелпера 1.
Подходящие адъюванты известны в данной области техники (см. WO 2015/095811) и включают, но не ограничены ими, поли(I:C), поли-ICLC, агонист STING, 1018 ISS, соли алюминия, Ампливакс, AS15, BCG, CP-870,893, CpG7909, CyaA, dSLIM, GM-CSF, IC30, IC31, Имиквимод, ImuFact IMP321, IS Patch, ISS, ISCOMATRIX, JuvImmune, LipoVac, MF59, монофосфориллипид A, Монтанид IMS 1312, Монтанид ISA 206, Монтанид ISA 50V, Монтанид ISA-51, OK-432, OM-174, OM-197-MP-EC, ONTAK, векторная система PepTel®, PLG микрочастицы, резиквимод, SRL172, виросомы и другие вирусоподобные частицы, YF-17D, VEGF ловушку, R848, β-глюкан, Pam3Cys, Pam3CSK4, Aquila’s QS21 стимулон (Aquila Biotech, Worcester, Mass., USA), который получают из сапонина, микобактериальные экстракты и синтетические миметики стенки бактериальных клеток, и другие подходящие адъюванты, такие как Ribi’s Detox. Quil или Superfos. Некоторые иммунологические адъюванты (например, MF59), специфические для дендритных клеток и их получения, были описаны (Dupuis M, et al., Cell Immunol. 1998; 186(1):18-27; Allison A C; Dev Biol Stand. 1998; 92:3-11) (Mosca et al. Frontiers in Bioscience, 2007; 12:4050-4060) (Gamvrellis et al. Immunol & Cell Biol. 2004; 82: 506-516). Также могут применяться цитокины. Для влияния на миграцию дендритных клеток, некоторые цитокины непосредственно связаны с лимфоидными тканями (например, TNF-α), усиливая созревание дендритных клеток в эффективные антигенпрезентирующие клетки для T-лимфоцитов (например, GM-CSF, PGE1, PGE2, IL-1, IL-1β, IL-4, IL-6 и CD40L) (патент США № 5,849,589, включенный в настоящий документ в качестве ссылки полностью) и действуя как иммуноадъюванты (например, IL-12) (Gabrilovich D I, et al., J Immunother Emphasis Tumor Immunol. 1996 (6):414-418).
Сообщалось также, что CpG иммуностимулирующие олигонуклеотиды усиливают действие адъювантов в терапевтических условиях. Не будучи связанными теорией, CpG олигонуклеотиды действуют через активацию врожденной (неадаптивной) иммунной системы через Toll-подобные рецепторы (TLR), в основном TLR9. Активация TLR9, запускаемая CpG, усиливает антигенспецифические гуморальные и клеточные ответы на широкий спектр антигенов, включая пептидные или белковые антигены, живые или убитые вирусы, иммуногенные фармацевтические композиции из дендритных клеток, аутологичные клеточные иммуногенные фармацевтические композиции и конъюгаты полисахаридов как в профилактических, так и в терапевтических иммуногенных фармацевтических композициях. Важно отметить, что это усиливает созревание и дифференциацию дендритных клеток, что приводит к усиленной активации TH1 клеток и сильному образованию цитотоксических Т-лимфоцитов (CTL), даже в отсутствие помощи CD4+ Т-клеток. Сдвиг TH1, вызванный стимуляцией TLR9, сохраняется даже в присутствии адъювантов, таких как квасцы или неполный адъювант Фрейнда (IFA), которые обычно способствуют сдвигу TH2. CpG олигонуклеотиды демонстрируют даже большую адъювантную активность при составлении или совместном введении с другими адъювантами или в таких составах, как микрочастицы, наночастицы, липидные эмульсии или аналогичные составы, которые особенно полезны для индукции сильного ответа, когда антиген относительно слаб. Они также могут ускорять иммунный ответ и позволяют снизить дозы антигена при сопоставимых ответах антител на иммуногенные фармацевтические композиции в полной дозе без CpG в некоторых экспериментах (Arthur M. Krieg, Nature Reviews, Drug Discovery, 5, June 2006, 471-484). В патенте США В US 6,406,705 описано комбинированное использование CpG олигонуклеотидов, адъювантов на основе не нуклеиновых кислот и антигена для вызова антигенспецифического иммунного ответа. Коммерчески доступным антагонистом CpG TLR9 является dSLIM (двойной иммуномодулятор «петля на стебле») от Mologen (Berlin, DE), который является компонентом фармацевтической композиции, описанной в настоящем документе. Также можно использовать другие связывающие TLR молекулы, такие как РНК связывающие TLR7, TLR8 и/или TLR9.
Другие примеры полезных адъювантов включают, но не ограничены ими, химически модифицированные CpGs (например, CpR, Idera), Поли(I:C) (например, полиI:CI2U), полиIC:LC, не-CpG бактериальная ДНК или РНК, ssRNA40 для TLR8, а также иммуноактивные малые молекулы и антитела, такие как циклофосфамид, сунитиниб, бевацизумаб, селебрекс, NCX-4016, силденафил, тадалафил, варденафил, сорафениб, XL-999, CP-547632, пазопаниб, ZD2171, AZD2171, ипилимумаб, тремелимумаб и SC58175, которые могут действовать терапевтически и/или как адъювант. Количества и концентрации адъювантов и добавок, применимые в контексте настоящего изобретения, могут быть легко определены квалифицированным специалистом без излишнего экспериментирования. Дополнительные адъюванты включают колониестимулирующие факторы, такие как гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF, сарграмостим).
В некоторых вариантах осуществления, иммуногенная композиция по настоящему описанию может содержать более одного различных адъювантов. Кроме того, изобретение охватывает фармацевтическую композицию, содержащую любое адъювантное вещество, включая любое из вышеперечисленных или их комбинации. В некоторых вариантах осуществления, иммуногенная композиция содержит неоантигенные терапевтические агенты (например, пептиды, полинуклеотиды, TCR, CAR, клетки, содержащие TCR или CAR, дендритные клетки, содержащие полипептид, дендритные клетки, содержащие полинуклеотид, антитело и т.д.), и адъювант может быть введен отдельно в любой подходящей последовательности.
Липидизация может быть классифицирована на несколько разных типов, таких как N-миристоилирование, пальмитоилирование, присоединение GPI-якоря, пренилирование и несколько дополнительных типов модификаций. N-миристоилированием является ковалентное присоединение миристата, C14 насыщенной кислоты, к глициновому остатку. Пальмитоилированием является тиоэфирная связь жирных кислот с длинной цепью (C16) с цистеиновыми остатками. Добавление GPI-якоря представляет собой связь гликозил-фосфатидилинозита (GPI) через амидную связь. Пренилированием является тиоэфирная связь изопреноидного липида (например, фарнезил (C-15), геранилгеранил (C-20)) с цистеиновыми остатками. Дополнительные типы модификаций могут включать присоединение S-диацилглицерина атомом серы цистеинов, конъюгацию O-октаноила через сериновые или треониновые остатки, конъюгацию S-археола с цистеиновыми остатками и присоединение холестерина.
Жирные кислоты для образования липидированных пептидов могут включать C2-C30 насыщенные, мононенасыщенные или полиненасыщенные жирные ацильные группы. Типовые жирные кислоты могут включать пальмитоильную, миристоильную, стеароильную и деканоильную группы. В некоторых случаях, липидную группу, которая имеет свойство адъюванта, присоединяют к полипептиду, представляющему интерес, для вызова или усиления иммуногенности в отсутствие внешнего адъюванта. Липидированный пептид или липопептид можно назвать самоадъювантным липопептидом. Любая из жирных кислот, описанных выше и в другом месте в настоящем документе, может вызывать или усиливать иммуногенность полипептида, представляющего интерес. Жирная кислота, которая может вызывать или повышать иммуногенность, может включать пальмитоильные, миристоильные, стеароильные, лауроильные, октаноильные и деканоильные группы.
Полипептиды, такие как голые пептиды или липидированные пептиды, могут быть включены в липосомы. Иногда липидированные пептиды могут быть включены в липосомы. Например, жировая часть липидированного пептида может спонтанно интегрироваться в жировой бислой липосомы. Таким образом, липопептид может быть презентирован на «поверхности» липосомы.
Липосомы также могут быть использованы для доставки нуклеиновых кислот в клетку. Нуклеиновая кислота, представляющая интерес, содержит одну или более последовательностей, кодирующих Т-клеточный рецептор. Липосомы могут применяться для доставки ДНК или РНК. Липосомы могут применяться для доставки нуклеиновой кислоты, включенной в вектор. Нуклеиновая кислота может иметь длину от 50 до 200000 нуклеотидов, от 100 до 500000 нуклеотидов или от 20 до 500000 нуклеотидов. Типовые липосомы, подходящие для включения в составы, включают, но не ограничены ими, многослойные везикулы (MLV), олиголамеллярные везикулы (OLV), однослойные везикулы (УФ), маленькие однослойные везикулы (SUV), однослойные везикулы среднего размера (MUV), большие однослойные везикулы (LUV), гигантские однослойные везикулы (GUV), мультивезикулярные везикулы (MVV), одно- или олиголамеллярные везикулы, полученные способом обращенно-фазового выпаривания (REV), многослойные везикулы, полученные методом обращенно-фазового испарения (MLV-REV), стабильные плюриламеллярные везикулы (SPLV), замороженные и размороженные MLV (FATMLV), везикулы, полученные методами экструзии (VET), везикулы, полученные методом French Press (FPV), везикулы, полученные путем слияния (FUV), везикулы дегидратации-регидратации (DRV) и бабблсомы (BSV).
В зависимости от способа получения, липосомы могут быть однослойными или многослойными и могут различаться по размеру в диапазоне диаметров от примерно 0,02 мкм до примерно 10 мкм. Липосомы могут адсорбировать многие типы клеток и затем высвобождать включенный агент (например, пептид, описанный в настоящем документе). В некоторых случаях, липосомы сливаются с клеткой-мишенью, в результате чего содержимое липосомы затем попадает в клетку-мишень. Липосома может быть подвергнута эндоцитозу фагоцитарными клетками. За эндоцитозом может следовать внутрилизосомная деградация липосомных липидов и высвобождение инкапсулированных агентов.
Представленные в настоящем документе липосомы также могут содержать жиры-носители. В некоторых вариантах осуществления, жирами-носителями могут быть фосфолипиды. Жиры-носители, способные образовывать липосомы, включают, но не ограничены ими, дипальмитоилфосфатидилхолин (DPPC), фосфатидилхолин (PC; лецитин), фосфатидную кислоту (PA), фосфатидилглицерин (PG), фосфатидилэтаноламин (PE), фосфатидилсерин (PS). Другие подходящие фосфолипиды дополнительно включают дистеароилфосфатидилхолин (DSPC), димиристоилфосфатидилхолин (DMPC), дипальмитоилфосфатидилглицерин (DPPG), дстеароилфосфатидилглицерин (DSPG), димиристоилфосфатидилглицерин (DMPG), дипальмитоилфосфатидную кислоту (DPPA); димиристоилфосфатидную кислоту (DMPA), дстеароилфосфатидную кислоту (DSPA), дипальмитоилфосфатидилсерин (DPPS), димиристоилфосфатидилсерин (DMPS), дстеароилфосфатидилсерин (DSPS), дипальмитоилфосфатидилэтаноламин (DPPE), димиристоилфосфатидилэтаноламин (DMPE), дстеароилфосфатидилэтаноламин (DSPE) и подобные, или их комбинации. В некоторых вариантах осуществления, липосомы дополнительно содержат стерин (например, холестерин), который модулирует образование липосомы. Жирами-носителями могут быть любые не фосфатные полярные жиры.
Фармацевтическая композиция может быть инкапсулирована в липосомы с использованием хорошо известной технологии. Биоразлагаемые микросферы также можно использовать в качестве носителей для фармацевтических композиций по настоящему изобретению.
Фармацевтические композиции могут вводиться в липосомах или микросферах (или микрочастицах). Способы приготовления липосом и микросфер для введения пациенту хорошо известны специалистам в данной области техники. По существу, материал растворяют в водном растворе, добавляют соответствующие фосфолипиды и жиры вместе с поверхностно-активными веществами, при необходимости, и материал диализируют или обрабатывают ультразвуком, при необходимости.
Микросферы, образованные из полимеров или белков, хорошо известны специалистам в данной области техники и могут быть адаптированы для прохождения через желудочно-кишечный тракт непосредственно в кровоток. Альтернативно, соединение может быть включено, и микросферы или композит микросфер имплантированы для медленного высвобождения в течение периода времени от дней до месяцев.
Субъекту также могут быть введены клеточные иммуногенные фармацевтические композиции. Например, иммуногенные фармацевтические композиции на основе антигенпрезентирующих клеток (APC) могут быть составлены с использованием любых хорошо известных методик, носителей и эксципиентов, если они подходят и как понятно в данной области. APC включают моноциты, клетки, происходящие из моноцитов, макрофаги и дендритные клетки. Иногда иммуногенной фармацевтической композицией на основе APC может быть иммуногенная фармацевтическая композиция на основе дендритных клеток.
Иммуногенная фармацевтическая композиция на основе дендритных клеток может быть получена любыми способами, хорошо известными в данной области техники. В некоторых случаях, иммуногенные фармацевтические композиции на основе дендритных клеток могут быть получены способом ex vivo или in vivo. Способ ex vivo может включать использование аутологичных DC, ex vivo загруженных полипептидами, описанными в настоящем документе, для активации или загрузки DC перед введением пациенту. Способ in vivo может включать таргетирование специфических рецепторов DC с использованием антител, связанных с полипептидами, описанными в настоящем документе. Иммуногенные фармацевтические композиции на основе DC могут дополнительно содержать активаторы DC, такие как агонисты TLR3, TLR-7-8 и CD40. Иммуногенные фармацевтические композиции на основе DC может дополнительно содержать адъюванты и фармацевтически приемлемый носитель.
Адъювант может быть использован для усиления иммунного ответа (гуморального и/или клеточного), вызываемого у пациента, получающего иммуногенную фармацевтическую композицию. Иногда адъюванты могут вызывать ответ Th1 типа. В других случаях, адъюванты могут вызывать ответ Th2 типа. Ответ Th1 типа может характеризоваться продуцированием цитокинов, таких как IFN-γ, в отличие от ответа Th2 типа, который может характеризоваться продуцированием цитокинов, таких как IL-4, IL-5 и IL-10.
В некоторых аспектах, адъюванты на основе липидов, такие как MPLA и MDP, могут использоваться с иммуногенными фармацевтическими композициями, раскрытыми в настоящем документе. Монофосфориллипид А (MPLA), например, является адъювантом, который вызывает повышенное презентирование липосомного антигена специфическим Т лимфоцитам. Кроме того, мурамилдипептид (MDP) также можно использовать в качестве подходящего адъюванта в сочетании с иммуногенными фармацевтическими препаратами, описанными в настоящем документе.
Адъювант также может содержать стимулирующие молекулы, такие как цитокины. Неограничивающие примеры цитокинов включают: CCL20, α-интерферон (IFNα), β-интерферон (IFNβ), γ-интерферон (IFNγ), фактор роста тромбоцитов (PDGF), TNFα, GM-CSF, эпидермальный фактор роста (EGF), кожный хемокин, привлекающий T клетку (CTACK), эпителиальный хемокин, экспрессированный тимусом (TECK), эпителиальный хемокин, ассоциированный со слизистой (MEC), IL-12, IL-15, IL-28, MHC, CD80, CD86, IL-1, IL-2, IL-4, IL-5, IL-6, IL-10, IL-18, MCP-1, MIP-la, MIP-1-, IL-8, L- селектин, P-селектин, E-селектин, CD34, GlyCAM-1, MadCAM-1, LFA-1, VLA-1, Mac-1, pl50.95, PECAM, ICAM-1, ICAM-2, ICAM-3, CD2, LFA-3, M-CSF, G-CSF, мутантные формы IL-18, CD40, CD40L, фактор роста сосудов, фактор роста фибробластов, IL-7, фактор роста нервов, фактор роста сосудистого эндотелия, Fas, TNF рецептор, Fit, Apo-1, p55, WSL-1, DR3, TRAMP, Apo-3, AIR, LARD, NGRF, DR4, DRS, KILLER, TRAIL-R2, TRICK2, DR6, Каспаза ICE, Fos, c-jun, Sp-1, Ap-1, Ap-2, p38, p65Rel, MyD88, IRAK, TRAF6, IκB, не активный NIK, SAP K, SAP-I, JNK, гены ответа интерферона, NFκB, Bax, TRAIL, TRAILrec, TRAILrecDRC5, TRAIL-R3, TRAIL-R4, RANK, RANK LIGAND, Ox40, Ox40 LIGAND, NKG2D, MICA, MICB, NKG2A, NKG2B, NKG2C, NKG2E, NKG2F, TAPI и TAP2.
Дополнительные адъюванты включают: MCP-1, MIP-la, MIP-lp, IL-8, RANTES, L-селектин, P-селектин, E-селектин, CD34, GlyCAM-1, MadCAM-1, LFA-1, VLA-1, Mac-1, pl50.95, PECAM, ICAM-1, ICAM-2, ICAM-3, CD2, LFA-3, M-CSF, G-CSF, IL-4, мутантные формы IL-18, CD40, CD40L, фактор роста сосудов, фактор роста фибробластов, IL-7, IL-22, фактор роста нервов, фактор роста сосудистого эндотелия, Fas, TNF рецептор, Fit, Apo-1, p55, WSL-1, DR3, TRAMP, Apo-3, AIR, LARD, NGRF, DR4, DR5, KILLER, TRAIL-R2, TRICK2, DR6, Каспаза ICE, Fos, c-jun, Sp-1, Ap-1, Ap-2, p38, p65Rel, MyD88, IRAK, TRAF6, IκB, не активный NIK, SAP K, SAP-1, JNK, гены ответа интерферона, NFκB, Bax, TRAIL, TRAILrec, TRAILrecDRC5, TRAIL-R3, TRAIL-R4, RANK, RANK LIGAND, Ox40, Ox40 LIGAND, NKG2D, MICA, MICB, NKG2A, NKG2B, NKG2C, NKG2E, NKG2F, TAP1, TAP2 и их функциональные фрагменты.
В некоторых аспектах адъювантом может быть модулятор Toll-подобного рецептора. Примеры модуляторов Toll-подобных рецепторов включают агонисты TLR9 и не ограничиваются низкомолекулярными модуляторами Toll -подобных рецепторов, такими как Имиквимод. Иногда адъювант выбирают из бактериальных анатоксинов, блок-полимеров полиоксипропилена-полиоксиэтилена, солей алюминия, липосом, CpG полимеров, эмульсий масло-в-воде или их комбинаций. Иногда адъювантом является эмульсия масло-в-воде. Эмульсия масло в воде может включать, по меньшей мере, одно масло и, по меньшей мере, одно поверхностно-активное вещество, при этом масло(а) и поверхностно-активное вещество(а) являются биоразлагаемыми (метаболизируемыми) и биосовместимыми. Капли масла в эмульсии могут иметь диаметр менее 5 мкм и даже субмикронный диаметр, причем эти небольшие размеры достигаются с помощью микрофлюидизатора для получения стабильных эмульсий. Капли размером менее 220 нм можно подвергать стерилизации на фильтре.
В некоторых случаях иммуногенная фармацевтическая композиция может включать носители и эксципиенты (включая, но не ограничиваясь ими, буферы, углеводы, маннит, белки, полипептиды или аминокислоты, такие как глицин, антиоксиданты, бактериостатики, хелатирующие агенты, суспендирующие агенты, загустители и/или консерванты), воду, масла, включая масла нефтяного, животного, растительного или синтетического происхождения, такие как арахисовое масло, соевое масло, минеральное масло, кунжутное масло и подобные, солевые растворы, водные растворы декстрозы и глицерина, ароматизаторы, красители и другие приемлемые добавки, адъюванты или связующие агенты, другие фармацевтически приемлемые вспомогательные вещества, необходимые для приближения к физиологическим условиям, такие как pH буферные агенты, агенты, регулирующие тоничность, эмульгирующие агенты, смачивающие агенты и подобные. Примеры эксципиентов включают крахмал, глюкозу, лактозу, сахарозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, моностеарат глицерина, тальк, хлорид натрия, сухое обезжиренное молоко, глицерин, пропилен, гликоль, воду, этанол и подобные. В других случаях, фармацевтический препарат по существу не содержит консерванты. В других случаях, фармацевтический препарат может содержать, по меньшей мере, один консервант. Следует понимать, что, хотя любой подходящий носитель, известный специалистам в данной области техники, можно использовать для введения фармацевтических препаратов, описанных в настоящем документе, тип носителя будет варьироваться в зависимости от способа введения.
Иммуногенная фармацевтическая композиция может включать консерванты, такие как тиомерсал или 2-феноксиэтанол. В некоторых случаях, иммуногенная фармацевтическая композиция по существу не содержит (например, <10 мкг/мл) ртутного материала, например, не содержит тиомерсал. Сукцинат α-токоферола может использоваться как альтернатива ртутным соединениям.
Для контроля тоничности в иммуногенную фармацевтическую композицию может быть включена физиологическая соль, такая как соль натрия. Другие соли могут включать хлорид калия, дигидрофосфат калия, динатрийфосфат и/или хлорид магния и подобные.
Иммуногенная фармацевтическая композиция может иметь осмоляльность от 200 мОсм/кг до 400 мОсм/кг, от 240-360 мОсм/кг, или в диапазоне 290-310 мОсм/кг.
Иммуногенная фармацевтическая композиция может содержать один или более буферов, таких как Tris буфер; боратный буфер; сукцинатный буфер; гистидиновый буфер (в частности, с адъювантом на основе гидроксида алюминия); или цитратный буфер. Буферы в некоторых случаях включены в диапазоне 5-20 или 10-50 мМ.
pH иммуногенной фармацевтической композиции может составлять от примерно 5,0 до примерно 8,5, от примерно 6,0 до примерно 8,0, от примерно 6,5 до примерно 7,5 или от примерно 7,0 до примерно 7,8.
Иммуногенная фармацевтическая композиция может быть стерильной. Иммуногенная фармацевтическая композиция может быть апирогенной, например содержать <1 ЕЭ (единица эндотоксина, стандартная мера) на дозу и может содержать <0,1 ЭЕ на дозу. Композиция может не содержать глютен.
Иммуногенная фармацевтическая композиция может включать детергент, например поверхностно-активное вещество на основе сложного эфира полиоксиэтиленсорбитана (известное как «Tweens») или октоксинол (такой как октоксинол-9 (Triton X-100) или т-октилфеноксиполиэтоксиэтанол). Детергент может присутствовать только в следовых количествах. Иммуногенная фармацевтическая композиция может включать в себя менее 1 мг/мл каждого из октоксинола-10 и полисорбата 80. Другими остаточными компонентами в следовых количествах могут быть антибиотики (например, неомицин, канамицин, полимиксин B).
Иммуногенная фармацевтическая композиция может быть составлена в виде стерильного раствора или суспензии в подходящих носителях, хорошо известных в данной области техники. Фармацевтические композиции можно стерилизовать обычными, хорошо известными способами стерилизации или можно стерилизовать фильтрованием. Полученные водные растворы могут быть упакованы для использования как есть или лиофилизированы, при этом лиофилизированный препарат перед введением объединяют со стерильным раствором.
Фармацевтические композиции, содержащие, например, активный агент, такой как иммунные клетки, раскрытые в настоящем документе, в комбинации с одним или более адъювантами, могут быть составлены так, чтобы они имели определенные молярные отношения. Например, могут быть использованы молярные отношения от примерно 99:1 до примерно 1:99 активного агента, такого как иммунная клетка, описанная в настоящем документе, в комбинации с одним или более адъювантами. В некоторых случаях, интервал молярных отношений активного агента, такого как иммунная клетка, описанная в настоящем документе, в комбинации с одним или более адъювантами, могут быть выбраны от примерно 80:20 до примерно 20:80; от примерно 75:25 до примерно 25:75, от примерно 70:30 до примерно 30:70, от примерно 66:33 до примерно 33:66, от примерно 60:40 до примерно 40:60; от примерно 50:50; до примерно 90:10 до примерно 10:90. Молярное отношение активного агента, такого как иммунная клетка, описанная в настоящем документе, в комбинации с одним или более адъювантами, может быть примерно 1:9, и в некоторых случаях, может быть примерно 1:1. Активный агент, такой как иммунная клетка, описанная в настоящем документе, в комбинации с одним или более адъювантами, может быть составлен вместе, в одной и той же дозированной единице, например, в одном флаконе, суппозитории, таблетке, капсуле, аэрозольном спрее; или каждый агент, форма и/или соединение могут быть составлены в виде отдельных единиц, например, двух флаконов, суппозиториев, таблеток, двух капсул, таблетки и флакона, аэрозольного спрея и подобного.
В некоторых случаях, иммуногенная фармацевтическая композиция может вводиться с дополнительным агентом. Выбор дополнительного агента может, по меньшей мере, частично зависеть от состояния, которое лечат. Дополнительный агент может включать, например, ингибитор иммунной контрольной точки, такой как анти-PD1, анти-CTLA4, анти-PD-L1, анти-CD40 или анти-TIM3 агент (например, анти-PD1, анти-CTLA4, анти-PD-L1, анти-CD40, или анти-TIM3 антитело; или любые агенты, оказывающие терапевтическое действие на патогенную инфекцию (например, вирусную инфекцию), включая, например, лекарственные средства, используемые для лечения воспалительных состояний, такие как НПВП, например, ибупрофен, напроксен, ацетаминофен, кетопрофен или аспирин. Например, ингибитором иммунной контрольной точки может быть антагонист PD-1/PD-L1, выбранный из группы, состоящей из: ниволумаба (ONO-4538/BMS-936558, MDX1 106, OPDIVO), пембролизумаба (MK-3475, KEYTRUDA), пидилизумаба (CT-011) и MPDL328OA (ROCHE). В качестве другого примера, составы могут дополнительно содержать одну или более добавок, таких как витамин C, E или другие антиоксиданты.
Фармацевтическая композиция, содержащая активный агент, такой как иммунная клетка, описанная в настоящем документе, в комбинации с одним или более адъювантами, может быть составлена обычным способом с использованием одного или более физиологически приемлемых носителей, содержащих эксципиенты, разбавители и/или вспомогательные вещества, например, которые облегчают переработку активных агентов в препараты, которые могут быть введены. Правильный состав может зависеть, по меньшей мере, частично, от выбранного пути введения. Агент(ы), описанный в настоящем документе, может быть доставлен пациенту с использованием ряда путей или способов введения, включая пероральный, трансбуккальный, местный, ректальный, трансдермальный, чрескожный, подкожный, внутривенный и внутримышечный, а также ингаляцией.
Активные агенты могут быть составлены для парентерального введения (например, инъекцией, например, болюсной инъекцией или непрерывной инфузией) и могут быть представлены в стандартной дозированной форме в ампулах, шприц-ручках, инфузиях небольшого объема или в многодозовых контейнерах с добавлением консерванта. Композиции могут принимать такие формы, как суспензии, растворы или эмульсии в масляных или водных носителях, например растворы в водном полиэтиленгликоле.
Для инъекционных составов, носитель может быть выбран из тех, которые известны в данной области как подходящие, включая водные растворы или масляные суспензии или эмульсии с кунжутным маслом, кукурузным маслом, хлопковым маслом или арахисовым маслом, а также эликсиры, маннит, декстрозу или стерильный водный раствор и аналогичные фармацевтические носители. Состав также может содержать биосовместимые, биоразлагаемые полимерные композиции, такие как поли(молочная-с-гликолевой)кислота. Эти материалы могут быть сделаны в виде микросфер или наносфер, загружены лекарственным средством и дополнительно покрыты или дериватизированы для обеспечения превосходных характеристик замедленного высвобождения. Носители, подходящие для окологлазной или внутриглазной инъекции, включают, например, суспензии терапевтического агента в воде для инъекций, липосомы и носители, подходящие для липофильных веществ. Другие носители для окологлазной или внутриглазной инъекции хорошо известны в данной области.
В некоторых случаях, фармацевтическая композиция составлена в соответствии с обычными методами в виде фармацевтической композиции, адаптированной для внутривенного введения человеку. Обычно, композиции для внутривенного введения представляют собой растворы в стерильном изотоническом водном буфере. При необходимости, композиция также может включать солюбилизирующий агент и местный анестетик, такой как лидокаин, для облегчения боли в месте инъекции. Обычно, ингредиенты поставляются либо по отдельности, либо смешанные вместе в стандартной дозированной форме, например, в виде сухого лиофилизированного порошка или безводного концентрата в герметично закрытом контейнере, таком как ампула или саше, с указанием количества активного агента. Если композицию следует вводить инфузией, она может быть предоставлена вместе с бутылкой для инфузии, содержащей стерильную воду или физиологический раствор для фармацевтического применения. Если композицию вводят инъекцией, может быть предоставлена ампула стерильной воды для инъекций или физиологического раствора, чтобы ингредиенты можно было смешать перед введением.
Если введение осуществляется инъекцией, активный агент может быть составлен в виде водных растворов, в частности, в физиологически совместимых буферах, таких как раствор Хенкса, раствор Рингера или физиологический солевой буфер. Раствор может содержать составные агенты, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты. В другом варианте, фармацевтическая композиция не содержит адъювант или какое-либо другое вещество, добавленное для усиления иммунного ответа.
В дополнение к составам, описанным ранее, активные агенты также могут быть составлены в виде депо препаратов. Такие составы длительного действия могут быть введены имплантацией или чрескожной доставкой (например, подкожно или внутримышечно), внутримышечной инъекцией или с применением трансдермального пластыря. Таким образом, например, агенты могут быть составлены с подходящими полимерными или гидрофобными материалами (например, в виде эмульсии в приемлемом масле) или ионообменными смолами или в виде умеренно растворимых производных, например, в виде умеренно растворимой соли.
В некоторых случаях, фармацевтические композиции, содержащие один или более агентов, оказывают местное и региональное действие при местном введении или инъекции в определенные места инфекции или рядом с ними. Прямое местное введение, например, вязкой жидкости, раствора, суспензии, растворов на основе диметилсульфоксида (ДМСО), липосомальных составов, геля, желе, крема, лосьона, мази, суппозитория, пены или аэрозольного спрея, можно применять для местного введения, чтобы получить, например, местный и/или региональный эффект. Фармацевтически подходящие носители для такого состава включают, например, низшие алифатические спирты, полигликоли (например, глицерин или полиэтиленгликоль), сложные эфиры жирных кислот, масла, жиры, силиконы и тому подобные. Такие препараты также могут включать консерванты (например, сложные эфиры п-гидроксибензойной кислоты) и/или антиоксиданты (например, аскорбиновую кислоту и токоферол). См. также Dermatological Formulations: Percutaneous absorption, Barry (Ed.), Marcel Dekker Incl, 1983. В другом варианте осуществления, составы для локального/местного применения, содержащие транспортер, носитель или ингибитор ионных каналов, используют для лечения вирусных инфекций эпидермиса или слизистых оболочек.
Фармацевтические композиции могут содержать адъюванты, такие как гидрофильные или липофильные гелеобразующие агенты, гидрофильные или липофильные активные агенты, консерванты, антиоксиданты, растворители, ароматизаторы, наполнители, солнцезащитные агенты, поглотители запаха и красители. Количества этих различных адъювантов такие, которые обычно используют в рассматриваемых областях, и, например, составляют от примерно 0,01% до примерно 20% от общей массы композиции. В зависимости от их природы, эти адъюванты могут быть введены в жировую фазу, в водную фазу и/или в жировые везикулы.
XII. Способы лечения
В настоящем документе представлены способы использования любой из нуклеиновых кислот, описанных выше, вектора, содержащего любую из последовательностей нуклеиновых кислот, описанного выше, белка, кодирующего нуклеиновую кислоту, описанного выше, или клетки-хозяина, описанной выше, для производства лекарственного средства для лечения иммунного заболевания или рака.
Также в настоящем документе представлены способы лечения субъекта с заболеванием, расстройством или состоянием. Способ лечения может включать введение фармацевтической композиции, раскрытой в настоящем документе субъекту с заболеванием, расстройством или состоянием. В настоящем описании представлены способы лечения, включающие иммуногенную терапию. Представлены способы лечения заболевания (такого как рак или вирусная инфекция). Способ может включать введение субъекту эффективного количества фармацевтической композиции, содержащей специфические к иммуногенному антигену T клетки. В некоторых вариантах осуществления, антиген содержит опухолевый антиген.
В некоторых вариантах осуществления, способ лечения субъекта с заболеванием или состоянием включает введение субъекту фармацевтической композиции, раскрытой в настоящем документе. В некоторых вариантах осуществления, способом является способ предотвращения резистентности к противораковой терапии, где способ включает введение субъекту, нуждающемуся в этом, фармацевтической композиции, раскрытой в настоящем документе. В некоторых вариантах осуществления, способом является способ вызова иммунного ответа, где способ включает введение субъекту, нуждающемуся в этом, фармацевтической композиции, раскрытой в настоящем документе. В некоторых вариантах осуществления, иммунным ответом является гуморальный ответ. В некоторых вариантах осуществления, иммунным ответом является ответ цитотоксических Т клеток.
В некоторых вариантах осуществления, субъекта имеет рак, где рак выбран из группы, состоящей из меланомы, рака яичников, рака легких, рака простаты, рака груди, колоректального рака, рака эндометрия и хронического лимфоцитарного лейкоза (CLL).
В некоторых вариантах осуществления, субъект имеет рак груди, резистентный к антиэстрогенной терапии. В некоторых вариантах осуществления, рак груди экспрессирует рецептор эстрогена с мутацией. В некоторых вариантах осуществления, субъект имеет CLL, резистентный к терапии ибрутинибом. В некоторых вариантах осуществления, CLL экспрессирует тирозинкиназу Брутона с мутацией, такой как C481S мутация. В некоторых вариантах осуществления, субъект имеет рак легких, резистентный к ингибитору тирозинкиназы. В некоторых вариантах осуществления, рак легких экспрессирует рецептор эпидермального фактора роста (EGFR) с мутацией, такой как T790M, L792F или C797S мутация.
В некоторых вариантах осуществления, способ включает введение, по меньшей мере, одного дополнительного терапевтического агента или средства. В некоторых вариантах осуществления, по меньшей мере, одним дополнительным терапевтическим агентом или средством является хирургическое вмешательство, ингибитор контрольной иммунной точки, антитело или его фрагмент, химиотерапевтический агент, облучение, вакцина, малая молекула, Т клетка, вектор и APC, полинуклеотид, онколитический вирус или любая их комбинация. В некоторых вариантах осуществления, по меньшей мере, одним дополнительным терапевтическим агентом является анти-PD-1 агент и анти-PD-L1 агент, анти-CTLA-4 агент или анти-CD40 агент. В некоторых вариантах осуществления, дополнительный терапевтический агент вводят до, одновременно или после введения фармацевтической композиции, раскрытой в настоящем документе.
В некоторых других аспектах, в настоящем документе представлено использование фармацевтической композиции для производства лекарственного средства для использования в терапии. В некоторых вариантах осуществления, способ лечения включает введение субъекту эффективного количества Т-клеток, специфически распознающих иммуногенный неоантигенный пептид. В некоторых вариантах осуществления, способ лечения включает введение субъекту эффективного количества TCR, который специфически распознает иммуногенный неоантигенный пептид, такой как TCR, экспрессируемый в Т клетке.
В некоторых вариантах осуществления, рак выбран из группы, состоящей из карциномы, лимфомы, бластомы, саркомы, лейкоза, плоскоклеточного рака, рака легких (включая мелкоклеточный рак легкого, немелкоклеточный рак легкого, аденокарциному легкого и плоскоклеточную карциному легкого), рака брюшины, печеночно-клеточного рака, рака ЖКТ или желудка (включая рак желудочно-кишечного тракта), рака поджелудочной железы, глиобластомы, рака шейки матки, рака яичников, рака печени, рака мочевого пузыря, гепатомы, рака груди, рака толстой кишки, меланомы, рака эндометрия или матки, рака слюнной железы, рака почек или почек, рака печени, рака простаты, рака вульвы, рака щитовидной железы, рака печени, рака головы и шеи, колоректального рака, рака прямой кишки, саркомы мягких тканей, саркомы Капоши, В-клеточной лимфомы (включая низкой степени/фолликулярную неходжкинскую лимфому (NHL), малую лимфоцитарную (SL) NHL, средней степени/фолликулярную NHL, диффузную NHL средней степени, иммунобластную NHL высокой степени, лимфобластную NHL высокой степени, мелкоклеточную NHL с нерассеченными ядрами высокой степени, NHL с генерализованной лимфаденопатией, мантийноклеточную лимфому, лимфому, связанная со СПИД и макроглобулинемию Вальденстрема), хронического лимфоцитарного лейкоза (CLL), острого лимфобластного лейкоза (ALL), миеломы, волосатоклеточного лейкоза, хронического миелобластного лейкоза и посттрансплантационного лимфопролиферативного расстройства (PTLD), аномальной пролиферации сосудов, связанной с факоматозом, отеком, синдромом Мейгса, и их комбинаций.
Способы согласно настоящему описанию можно использовать для лечения любого типа рака, известного в данной области техники. Неограничивающие примеры виды рака, подлежащего лечению способами настоящего раскрытия, могут включать меланому (например, метастатическую злокачественную меланому), рак почек (например, светлоклеточную карциному), рак простаты (например, гормонорезистентную аденокарциному простаты), аденокарциному поджелудочной железы, рак груди, рак толстой кишки, рак легких (например, немелкоклеточный рак легких), рак пищевода, плоскоклеточный рак головы и шеи, рак печени, рак яичников, рак шейки матки, рак щитовидной железы, глиобластому, глиому, лейкоз, лимфому и другие злокачественные новообразования.
Кроме того, в настоящем документе представлено заболевание или состояние, включающее не поддающиеся лечению или рецидивирующие злокачественные новообразования, рост которых может быть подавлен с использованием способов лечения по настоящему описанию. В некоторых вариантах осуществления, рак, подлежащий лечению способами лечения по настоящему описанию, выбран из группы, состоящей из карциномы, плоскоклеточной карциномы, аденокарциномы, саркомы, рака эндометрия, рака груди, рака яичников, рака шейки матки, рака маточной трубы, первичного рака брюшины, рака толстой кишки, колоректального рака, плоскоклеточного рака аногенитальной области, меланомы, почечно-клеточной карциномы, рака легких, немелкоклеточного рака легкого, плоскоклеточного рака легкого, рака желудка, рака мочевого пузыря, рака желчного пузыря, рака печени, рака щитовидной железы, рака гортани, рака слюнных желез, рака пищевода, рака головы и шеи, глиобластомы, глиомы, плоскоклеточной карицномы головы и шеи, рака простаты, рака поджелудочной железы, мезотелиомы, саркомы, гематологического рака, лейкоза, лимфомы, невромы и их комбинаций. В некоторых вариантах осуществления, рак, подлежащий лечению способами настоящего описания, включает, например, карциному, плоскоклеточную карциному (например, цервикального канала, века, конъюнктивы, влагалища, легкого, полости рта, кожи, мочевого пузыря, языка, гортани и пищевода) и аденокарциному (например, простаты, тонкого кишечника, эндометрия, цервикального канала, толстого кишечника, легкого, поджелудочной железы, пищевода, прямой кишки, матки, желудка, молочной железы и яичника). В некоторых вариантах осуществления, рак, подлежащий лечению способами настоящего описания, дополнительно включает саркому (например, миогенную саркому), лейкоз, неврому, меланому и лимфому. В некоторых вариантах осуществления, раком, подлежащим лечению способами настоящего описания, является рак груди. В некоторых вариантах осуществления, раком, подлежащим лечению способами настоящего описания, является трижды отрицательный рак груди (TNBC). В некоторых вариантах осуществления, раком, подлежащим лечению способами настоящего описания, является рак яичников. В некоторых вариантах осуществления, раком, подлежащим лечению способами настоящего описания, является колоректальный рак.
В некоторых вариантах осуществления, пациент или популяция пациентов, подлежащих лечению фармацевтической композицией настоящего описания, имеют солидную опухоль. В некоторых вариантах осуществления, солидной опухолью является меланома, почечно-клеточная карцинома, рак легких, рак мочевого пузыря, рак груди, рак шейки матки, рак толстой кишки, рак желчного пузыря, рак гортани, рак печени, рак щитовидной железы, рак желудка, рак слюнной железы, рак простаты, рак поджелудочной железы или карцинома из клеток Меркеля. В некоторых вариантах осуществления, пациент или популяция пациентов, подлежащих лечению фармацевтической композицией настоящего описания, имеют гематологический рак. В некоторых вариантах осуществления, пациент имеет гематологический рак, такой как диффузная В-крупноклеточная лимфома («DLBCL»), лимфома Ходжкина («HL»), неходжкинская лимфома («NHL»), фолликулярная лимфома («FL»), острый миелоидный лейкоз («AML») или множественная миелома («MM»). В некоторых вариантах осуществления, пациент или популяция пациентов, подлежащих лечению, имеют рак, выбранный из группы, состоящей из рака яичников, рака легкого и меланомы.
Конкретные примеры рака, который может быть предотвращен и/или лечен в соответствии с настоящим описанием, включают, но не ограничены ими, следующие: рак почек, рак почки, мультиформная глиобластома, метастатический рак груди; рак груди; саркома груди; нейрофиброма; нейрофиброматоз; детские опухоли; нейробластома; злокачественная меланома; карциномы эпидермиса; лейкозы, такие как, но не ограниченные ими, острый лейкоз, острый лимфоцитарный лейкоз, острые миелоцитарные лейкозы, такие как миелобластный, промиелоцитарный, миеломоноцитарный, моноцитарный, эритролейкозный лейкоз и миелодиспластический синдром, хронические лейкозы, такие как, но не ограниченные ими, хронический миелоцитарный (гранулоцитарный) лейкоз, хронический лимфоцитарный лейкоз, волосатоклеточный лейкоз; истинная полицитемия; лимфомы, такие как, но не ограниченные ими, болезнь Ходжкина, неходжкинская болезнь; множественные миеломы, такие как вялотекущая множественная миелома, несекреторная миелома, остеосклеротическая миелома, лейкоз клеток плазмы, солитарная плазмоцитома и экстрамедуллярная плазмоцитома; макроглобулинемия Вальденстрема; моноклональная гаммопатия неясного значения; доброкачественная моноклональная гаммопатия; болезнь тяжелой цепи; рак костей и саркомы соединительной ткани, такие как, но не ограниченные ими, саркома костей, миеломная болезнь костей, множественная миелома, остеосаркома костей, вызванная холестеатомой, костная болезнь Педжета, остеосаркома, хондросаркома, саркома Юинга, злокачественная гигантоклеточная опухоль, фибросаркома костей, хордома, паростальная саркома, саркомы мягких тканей, ангиосаркома (гемангиосаркома), фибросаркома, саркома Капоши, лейомиосаркома, липосаркома, лимфангиосаркома, неврилеммома, рабдомиосаркома и синовиальная саркома; опухоли головного мозга, такие как, но не ограниченные ими, глиома, астроцитома, глиома ствола головного мозга, эпендимома, олигодендроглиома, неглиальная опухоль, неврилеммома слухового нерва, краниофарингиома, медуллобластома, менингиома, пинеоцитома, пинеобластома и первичная лимфома головного мозга; рак груди, такие как, но не ограниченные ими, аденокарцинома, дольковая (мелкоклеточная) карцинома, внутрипротоковая карцинома, медуллярный рак груди, муцинозный рак груди, трубочковый рак груди, папиллярный рак груди, болезнь Педжета (включая ювенильную болезнь Педжета) и воспалительный рак груди; рак надпочечников, такой как, но не ограниченный ими, феохромоцитома и адренокортикальная карцинома; рак щитовидной железы, такой как, но не ограниченный ими, папиллярный или фолликулярный рак щитовидной железы, медуллярный рак щитовидной железы и анапластический рак щитовидной железы; рак поджелудочной железы, такой как, но не ограниченный ими, инсулинома, гастринома, глюкагонома, випома, соматостатин-секретирующая опухоль и карциноидная опухоль или опухоль островковых клеток; рак гипофиза, такой как, но не ограниченный ими, болезнь Кушинга, пролактин-секретирующая опухоль, акромегалия и не сахарный диабет; рак глаз, такой как, но не ограниченный ими, меланома глаза, такая как меланома радужной оболочки, меланома хориоидеи и меланома ресничного тела и ретинобластома; рак влагалища, такой как плоскоклеточный рак, аденокарцинома и меланома; рак вульвы, такой как плоскоклеточный рак, меланома, аденокарцинома, базальноклеточный рак, саркома и болезнь Педжета; рак шейки матки, такой как, но не ограниченный ими, плоскоклеточная карцинома и аденокарцинома; рак матки, такой как, но не ограниченный ими, карцинома эндометрия и саркома матки; рак яичников, такой как, но не ограниченный ими, эпителиальная карцинома яичников, пограничная опухоль, опухоль половых клеток и стромальная опухоль; рак шейки матки; рак пищевода, такой как, но не ограниченный ими, плоскоклеточный рак, аденокарцинома, адено-кистозная карцинома, мукоэпидермоидная карцинома, аденосквамозная карцинома, саркома, меланома, плазмоцитома, веррукозная карцинома и овсяноклеточная (мелкоклеточная) карцинома; рак желудка, такой как, но не ограниченный ими, аденокарцинома, грибовидный (полипоидный), язвенный, поверхностный распространяющийся, диффузно распространяющийся, злокачественная лимфома, липосаркома, фибросаркома и карциносаркома; рак толстой кишки; колоректальный рак, колоректальный рак с мутацией KRAS; карцинома толстой кишки; рак прямой кишки; рак печени, такой как, но не ограниченный ими, печеночно-клеточная карцинома и гепатобластома, рак желчного пузыря, такой как аденокарцинома; холангиокарциномы, такие как, но не ограниченные ими, папиллярные, узелковые и диффузные; рак легкого, такой как немелкоклеточный рак легкого с мутацией KRAS, немелкоклеточный рак легкого, плоскоклеточная карцинома (эпидермоидная карцинома), аденокарцинома, крупноклеточная карцинома и мелкоклеточный рак легкого; карцинома легких; рак яичек, такой как, но не ограниченный ими, зародышевые опухоли, семинома, анапластическая, классическая (типичная), сперматоцитарная, несеминома, эмбриональная карцинома, карцинома тератомы, хориокарцинома (опухоль желточного мешка), рак простаты, такой как, но не ограниченный ими, андроген-независимый рак простаты, андроген-зависимый рак простаты, аденокарцинома, лейомиосаркома и рабдомиосаркома; рак пениса; рак ротовой полости, такой как, но не ограничиваясь ими, плоскоклеточная карцинома; базальный рак; рак слюнных желез, такой как, но не ограниченный ими, аденокарцинома, мукоэпидермоидная карцинома и аденоидно-кистозная карцинома; рак глотки, такой как, но не ограниченный ими, плоскоклеточный рак и веррукозный рак; рак кожи, такой как, но не ограниченный ими, базальноклеточная карцинома, плоскоклеточная карцинома и меланома, поверхностная распространяющаяся меланома, узелковая меланома, лентиго злокачественная меланома, акраллентигинозная меланома; рак почек, такой как, но не ограниченный ими, почечно-клеточный рак, аденокарцинома, гипернефрома, фибросаркома, переходно-клеточный рак (рак почечной лоханки и/или матки); рак почек; опухоль Вильмса; рак мочевого пузыря, такой как, но не ограниченный ими, переходно-клеточную карциному, плоскоклеточный рак, аденокарциному, карциносаркому. Кроме того, раки включают миксосаркому, остеогенную саркому, эндотелиосаркому, лимфангиоэндотелиосаркому, мезотелиому, синовиому, гемангиобластому, эпителиальную карциному, цистаденокарциному, бронхогенную карциному, карциному потовых желез, карциному сальных желез, папиллярную карциному и папиллярные аденокарциномы.
Раки включают, но не ограничены ими, В-клеточный рак, например, множественную миелому, макроглобулинемию Вальденстрема, болезни тяжелой цепи, такие как, например, болезнь альфа цепи, болезнь гамма цепи и болезнь мю цепи, доброкачественную моноклональную гаммопатию и иммуноцитарный амилоидоз, меланомы, рак груди, рак легких, рак бронхов, колоректальный рак, рак простаты (например, метастатический, гормонорезистентный рак простаты), рак поджелудочной железы, рак желудка, рак яичников, рак мочевого пузыря, рак мозга или центральной нервной системы, рак периферической нервной системы, рак пищевода, рак шейки матки, рак матки или эндометрия, рак полости рта или глотки, рак печени, рак почки, рак яичек, рак желчных путей, рак тонкой кишки или аппендикса, рак слюнных желез, рак щитовидной железы, рак надпочечников, остеосаркому, хондросаркому, рак гематологических тканей и подобные. Другие неограничивающие примеры типов рака, применимых к способам, охватываемым настоящим описанием, включают саркомы и карциномы человека, например, фибросаркому, миксосаркому, липосаркому, хондросаркому, остеогенную саркому, хордому, ангиосаркому, эндотелиосаркому, лимфангиосаркому, лимфангиоэндотелиосаркому, синовиому, мезотелиому, опухоль Юинга, лейомиосаркому, рабдомиосаркому, рак толстой кишки, рак прямой кишки, рак груди, рак яичников, плоскоклеточную карциному, базальноклеточную карциному, аденокарциному, карциному потовых желез, карциному сальных желез, папиллярную карциному, папиллярную аденокарциному, цистаденокарциному, медуллярную карциному, бронхогенную карциному, почечно-клеточную карциному, гепатому, карциному желчных протоков, рак печени, хориокарциному, семиному, эмбриональную карциному, опухоль Вильмса, рак шейки матки, рак костей, опухоль мозга, рак яичек, карциному легких, мелкоклеточную карциному легких, карциному мочевого пузыря, эпителиальную карциному, глиому, астроцитому, медуллобластому, краниофарингиому, эпендимому, пинеалому, гемангиобластому, неврилеммому слухового нерва, олигодендроглиому, менингиому, меланому, нейробластому, ретинобластому; лейкозы, например, острый лимфоцитарный лейкоз и острый миелоцитарный лейкоз (миелобластный, промиелоцитарный, миеломоноцитарный, моноцитарный и эритролейкоз); хронический лейкоз (хронический миелоцитарный (гранулоцитарный) лейкоз и хронический лимфоцитарный лейкоз); и истинную полицитемию, лимфому (болезнь Ходжкина и неходжкинскую болезнь), множественную миелому, макроглобулинемию Вальденстрема и болезнь тяжелой цепи. В некоторых вариантах осуществления рак, фенотип которого определяется способом настоящего описания, представляет собой эпителиальный рак, такой как, но не ограниченный ими, рак мочевого пузыря, рак груди, рак шейки матки, рак толстой кишки, гинекологические раки, рак почек, рак гортани, рак легких, рак полости рта, рак головы и шеи, рак яичников, рак поджелудочной железы, рак простаты или рак кожи. В других вариантах осуществления, раком является рак груди, рак простаты, рак легких или рак толстой кишки. В других вариантах осуществления, эпителиальным раком является немелкоклеточный рак легкого, не папиллярная почечно-клеточная карцинома, карцинома шейки матки, карцинома яичников (например, серозная карцинома яичников) или карцинома молочной железы. Эпителиальный рак можно охарактеризовать различными другими способами, включая, помимо прочего, серозный, эндометриоидный, муцинозный, светлоклеточный, бреннеровский или недифференцированный. В некоторых вариантах осуществления, настоящее описание используют для лечения, диагностики и/или прогнозирования лимфомы или ее подтипов, включая, но не ограничиваясь ими, мантийноклеточную лимфому. Лимфопролиферативные расстройства также считаются пролиферативными заболеваниями.
В некоторых вариантах осуществления, субъект имеет рак груди, резистентный к антиэстрогенной терапии, MSI рак груди, метастатический рак груди, Her2 отрицательный рак груди, Her2 положительный рак груди, ER отрицательный рак груди, ER положительный рак груди или любая их комбинация.
В некоторых вариантах осуществления, рак груди экспрессирует рецептор эстрогена с мутацией.
В некоторых вариантах осуществления, раком является рецидивирующий или метастатический рак. В некоторых вариантах осуществления, раком, подлежащим лечению способами настоящего описания, является трижды отрицательный рак груди (TNBC).
Фармацевтические компании в настоящем документе представлены отдельно или в комбинации с обычными терапевтическими схемами, такими как хирургия, облучение, химиотерапия и/или трансплантация костного мозга (аутологическая, сингенная, аллогенная или неродственная).
В некоторых вариантах осуществления, по меньшей мере, один или более химиотерапевтических агентов могут быть введены в дополнение к фармацевтической композиции, включающей иммуногенную терапию. В некоторых вариантах осуществления, один или более химиотерапевтических агентов могут принадлежать к разным классам химиотерапевтических агентов.
При практическом применении способов лечения или применения, представленных в настоящем документе, терапевтически эффективные количества фармацевтических композиций могут вводиться субъекту, страдающему заболеванием или состоянием. Терапевтически эффективное количество может широко варьироваться в зависимости от тяжести заболевания, возраста и относительного состояния здоровья субъекта, эффективности используемых соединений и других факторов.
Субъектами могут быть, например, млекопитающие, люди, беременные женщины, пожилые люди, взрослые, подростки, дети-подростки, дети, малыши, младенцы, новорожденные или новорожденные в возрасте до 1 месяца. Субъектом может быть пациент. В некоторых случаях, субъектом может быть человек. В некоторых случаях, субъектом может быть ребенок (т.е. молодой человек, не достигший возраста полового созревания). В некоторых случаях субъектом может быть младенец. В некоторых случаях субъектом, может быть ребенок, находящийся на искусственном вскармливании. В некоторых случаях, субъектом может быть человек, участвующий в клиническом исследовании. В некоторых случаях, субъектом может быть лабораторное животное, например, млекопитающее или грызун. В некоторых случаях, субъектом может быть мышь. В некоторых случаях, субъект может страдать ожирением или избыточным весом.
В некоторых вариантах осуществления, субъекта ранее лечили одним или более различными способами лечения рака. В некоторых вариантах осуществления, субъекта ранее лечили одним или более из следующих способов: радиационная терапия, химиотерапия или иммунотерапия. В некоторых вариантах осуществления, субъект получал одну, две, три, четыре или пять линий предшествующей терапии. В некоторых вариантах осуществления, предшествующей терапией является цитотоксическая терапия.
В некоторых вариантах осуществления, заболеванием или состоянием, которое можно лечить с помощью способов по настоящему документу, является аномальный рост клеток. В некоторых вариантах осуществления, заболеванием или состоянием, которое можно лечить с помощью способов по настоящему документу, является рак. В некоторых вариантах осуществления, раком является злокачественный рак. В некоторых вариантах осуществления, раком является доброкачественный рак. В некоторых вариантах осуществления, раком является инвазивный рак. В некоторых вариантах осуществления, раком является солидная опухоль. В некоторых вариантах осуществления, раком является гемобластоз.
Способы согласно настоящему описанию можно использовать для лечения любого типа рака, известного в данной области. Неограничивающие примеры виды рака, подлежащего лечению способами настоящего описания, включают меланому (например, метастатическую злокачественную меланому), рак почек (например, светлоклеточную карциному), рак простаты (например, гормонорезистентную аденокарциному простаты), аденокарциному поджелудочной железы, рак груди, рак толстой кишки, рак легких (например, немелкоклеточный рак легких), рак пищевода, плоскоклеточную карциному головы и шеи, рак печени, рак яичников, рак шейки матки, рак щитовидной железы, глиобластому, глиому, лейкоз, лимфому и другие злокачественные новообразования.
Кроме того, в настоящем документе представлено заболевание или состояние, включающее не поддающиеся лечению или рецидивирующие злокачественные новообразования, рост которых может быть подавлен с использованием способов лечения по настоящему раскрытию. В некоторых вариантах осуществления, рак, подлежащий лечению способами настоящего описания, выбран из группы, состоящей из карциномы, плоскоклеточной карциномы, аденокарциномы, саркомы, рака эндометрия, рака груди, рака яичников, рака шейки матки, рака маточной трубы, первичного рака брюшины, рака толстой кишки, колоректального рака, плоскоклеточного рака аногенитальной области, меланомы, почечно-клеточной карциномы, рака легких, немелкоклеточного рака легкого, плоскоклеточного рака легкого, рака желудка, рака мочевого пузыря, рака желчного пузыря, рака печени, рака щитовидной железы, рака гортани, рака слюнных желез, рака пищевода, рака головы и шеи, глиобластомы, глиомы, плоскоклеточной карциномы головы и шеи, рака простаты, рака поджелудочной железы, саркомы, гематологического рака, лейкоза, лимфомы, невромы и их комбинаций. В некоторых вариантах осуществления, рак, подлежащий лечению способами настоящего описания, включает, например, карциному, плоскоклеточный рак (например, цервикального канала, века, конъюнктивы, влагалища, легкого, полости рта, кожи, мочевого пузыря, языка, гортани и пищевода) и аденокарциному (например, простаты, тонкого кишечника, эндометрия, цервикального канала, толстого кишечника, легкого, поджелудочной железы, пищевода, прямой кишки, матки, желудка, груди и яичника). В некоторых вариантах осуществления, рак, подлежащий лечению способами настоящего описания, дополнительно включает саркому (например, миогенную саркому), лейкоз, неврому, меланому и лимфому. В некоторых вариантах осуществления, раком, подлежащим лечению способами настоящего описания, является рак груди. В некоторых вариантах осуществления, раком, подлежащим лечению способами настоящего описания, является трижды отрицательный рак груди (TNBC). В некоторых вариантах осуществления, раком, подлежащим лечению способами настоящего описания, является рак яичников. В некоторых вариантах осуществления, раком, подлежащим лечению способами настоящего описания, является колоректальный рак.
В некоторых вариантах осуществления пациент или популяция пациентов, получающих лечение фармацевтической композицией по настоящему изобретению, имеют солидную опухоль. В некоторых вариантах осуществления, солидной опухолью является меланому, почечно-клеточная карцинома, рак легких, рак мочевого пузыря, рак груди, рак шейки матки, рак толстой кишки, рак желчного пузыря, рак гортани, рак печени, рак щитовидной железы, рак желудка, рак слюнной железы, рак простаты, рак поджелудочной железы или карцинома из клеток Меркеля. В некоторых вариантах осуществления, пациент или популяция пациентов, подлежащих лечению фармацевтической композицией настоящего описания, имеют гематологический рак. В некоторых вариантах осуществления, пациент имеет гематологический рак, такой как диффузная В-крупноклеточная лимфома («DLBCL»), лимфома Ходжкина («HL»), неходжкинская лимфома («NHL»), фолликулярная лимфома («FL»), острый миелоидный лекоз («AML») или множественная миелома («MM»). В некоторых вариантах осуществления, пациент или популяция пациентов, подлежащих лечению, имеют рак, выбранный из группы, состоящей из рака яичников, рака легкого и меланомы.
Конкретные примеры рака, который может быть предотвращен и/или лечен в соответствии с настоящим описанием, включают, но не ограничены ими, следующие: рак почек, рак почки, мультиформная глиобластома, метастатический рак груди; рак груди; саркома груди; нейрофиброма; нейрофиброматоз; детские опухоли; нейробластома; злокачественная меланома; карциномы эпидермиса; лейкозы, такие как, но не ограниченные ими, острый лейкоз, острый лимфоцитарный лейкоз, острые миелоцитарные лейкозы, такие как миелобластный, промиелоцитарный, миеломоноцитарный, моноцитарный, эритролейкозный лейкоз и миелодиспластический синдром, хронические лейкозы, такие как, но не ограниченные ими, хронический миелоцитарный (гранулоцитарный) лейкоз, хронический лимфоцитарный лейкоз, волосатоклеточный лейкоз; истинная полицитемия; лимфомы, такие как, но не ограниченные ими, болезнь Ходжкина, неходжкинская болезнь; множественные миеломы, такие как вялотекущая множественная миелома, несекреторная миелома, остеосклеротическая миелома, лейкоз клеток плазмы, солитарная плазмоцитома и экстрамедуллярная плазмоцитома; макроглобулинемия Вальденстрема; моноклональная гаммопатия неясного значения; доброкачественная моноклональная гаммопатия; болезнь тяжелой цепи; рак костей и саркомы соединительной ткани, такие как, но не ограниченные ими, саркома костей, миеломная болезнь костей, множественная миелома, остеосаркома костей, вызванная холестеатомой, костная болезнь Педжета, остеосаркома, хондросаркома, саркома Юинга, злокачественная гигантоклеточная опухоль, фибросаркома костей, хордома, паростальная саркома, саркомы мягких тканей, ангиосаркома (гемангиосаркома), фибросаркома, саркома Капоши, лейомиосаркома, липосаркома, лимфангиосаркома, неврилеммома, рабдомиосаркома и синовиальная саркома; опухоли головного мозга, такие как, но не ограниченные ими, глиома, астроцитома, глиома ствола головного мозга, эпендимома, олигодендроглиома, неглиальная опухоль, неврилеммома слухового нерва, краниофарингиома, медуллобластома, менингиома, пинеоцитома, пинеобластома и первичная лимфома головного мозга; рак груди, такие как, но не ограниченные ими, аденокарцинома, дольковая (мелкоклеточная) карцинома, внутрипротоковая карцинома, медуллярный рак груди, муцинозный рак груди, трубочковый рак груди, папиллярный рак груди, болезнь Педжета (включая ювенильную болезнь Педжета) и воспалительный рак груди; рак надпочечников, такой как, но не ограниченный ими, феохромоцитома и адренокортикальная карцинома; рак щитовидной железы, такой как, но не ограниченный ими, папиллярный или фолликулярный рак щитовидной железы, медуллярный рак щитовидной железы и анапластический рак щитовидной железы; рак поджелудочной железы, такой как, но не ограниченный ими, инсулинома, гастринома, глюкагонома, випома, соматостатин-секретирующая опухоль и карциноидная опухоль или опухоль островковых клеток; рак гипофиза, такой как, но не ограниченный ими, болезнь Кушинга, пролактин-секретирующая опухоль, акромегалия и не сахарный диабет; рак глаз, такой как, но не ограниченный ими, меланома глаза, такая как меланома радужной оболочки, меланома хориоидеи и меланома ресничного тела и ретинобластома; рак влагалища, такой как плоскоклеточный рак, аденокарцинома и меланома; рак вульвы, такой как плоскоклеточный рак, меланома, аденокарцинома, базальноклеточный рак, саркома и болезнь Педжета; рак шейки матки, такой как, но не ограниченный ими, плоскоклеточная карцинома и аденокарцинома; рак матки, такой как, но не ограниченный ими, карцинома эндометрия и саркома матки; рак яичников, такой как, но не ограниченный ими, эпителиальная карцинома яичников, пограничная опухоль, опухоль половых клеток и стромальная опухоль; рак шейки матки; рак пищевода, такой как, но не ограниченный ими, плоскоклеточный рак, аденокарцинома, адено-кистозная карцинома, мукоэпидермоидная карцинома, аденосквамозная карцинома, саркома, меланома, плазмоцитома, веррукозная карцинома и овсяноклеточная (мелкоклеточная) карцинома; рак желудка, такой как, но не ограниченный ими, аденокарцинома, грибовидный (полипоидный), язвенный, поверхностный распространяющийся, диффузно распространяющийся, злокачественная лимфома, липосаркома, фибросаркома и карциносаркома; рак толстой кишки; колоректальный рак, колоректальный рак с мутацией KRAS; карцинома толстой кишки; рак прямой кишки; рак печени, такой как, но не ограниченный ими, печеночно-клеточная карцинома и гепатобластома, рак желчного пузыря, такой как аденокарцинома; холангиокарциномы, такие как, но не ограниченные ими, папиллярные, узелковые и диффузные; рак легкого, такой как немелкоклеточный рак легкого с мутацией KRAS, немелкоклеточный рак легкого, плоскоклеточная карцинома (эпидермоидная карцинома), аденокарцинома, крупноклеточная карцинома и мелкоклеточный рак легкого; карцинома легких; рак яичек, такой как, но не ограниченный ими, зародышевые опухоли, семинома, анапластическая, классическая (типичная), сперматоцитарная, несеминома, эмбриональная карцинома, карцинома тератомы, хориокарцинома (опухоль желточного мешка), рак простаты, такой как, но не ограниченный ими, андроген-независимый рак простаты, андроген-зависимый рак простаты, аденокарцинома, лейомиосаркома и рабдомиосаркома; рак пениса; рак ротовой полости, такой как, но не ограничиваясь ими, плоскоклеточная карцинома; базальный рак; рак слюнных желез, такой как, но не ограниченный ими, аденокарцинома, мукоэпидермоидная карцинома и аденоидно-кистозная карцинома; рак глотки, такой как, но не ограниченный ими, плоскоклеточный рак и веррукозный рак; рак кожи, такой как, но не ограниченный ими, базальноклеточная карцинома, плоскоклеточная карцинома и меланома, поверхностная распространяющаяся меланома, узелковая меланома, лентиго злокачественная меланома, акраллентигинозная меланома; рак почек, такой как, но не ограниченный ими, почечно-клеточный рак, аденокарцинома, гипернефрома, фибросаркома, переходно-клеточный рак (рак почечной лоханки и/или матки); рак почек; опухоль Вильмса; рак мочевого пузыря, такой как, но не ограниченный ими, переходно-клеточную карциному, плоскоклеточный рак, аденокарциному, карциносаркому. Кроме того, раки включают миксосаркому, остеогенную саркому, эндотелиосаркому, лимфангиоэндотелиосаркому, мезотелиому, синовиому, гемангиобластому, эпителиальную карциному, цистаденокарциному, бронхогенную карциному, карциному потовых желез, карциному сальных желез, папиллярную карциному и папиллярные аденокарциномы.
В некоторых вариантах осуществления, у пациента с мутацией в RAS гене лечат рак введением фармацевтической композиции, содержащей TCR, который распознает RAS мутантный эпитоп в комплексе с MHC белком, кодированным HLA аллелью субъекта, где TCR имеет вариабельную область альфа цепи TCR и вариабельную область бета цепи TCR, имеющую аминокислотную последовательность, раскрытую в настоящем документе. В некоторых вариантах осуществления, фармацевтическая композиция содержит последовательность нуклеиновой кислоты, кодирующую TCR. В некоторых вариантах осуществления, нуклеиновой кислотой является ДНК или РНК. В некоторых вариантах осуществления, нуклеиновой кислотой информационная РНК, кодирующая TCR, имеющий вариабельную область альфа цепи TCR и вариабельную область бета цепи TCR, имеющую аминокислотную последовательность, раскрытую в настоящем документе. В некоторых вариантах осуществления, фармацевтическая композиция содержит вектор, который содержит последовательность нуклеиновой кислоты, кодирующую TCR, и способен направлять экспрессию TCR, где TCR распознает RAS мутантный эпитоп в комплексе с MHC белком, кодированным HLA аллелью субъекта, и где TCR имеет вариабельную область альфа цепи TCR и вариабельную область бета цепи TCR, имеющую аминокислотную последовательность, раскрытую в настоящем документе. В некоторых вариантах осуществления, фармацевтическая композиция содержит клетку, которая содержит последовательность нуклеиновой кислоты, кодирующую TCR, который распознает RAS мутантный эпитоп в комплексе с MHC белком, кодированным HLA аллелью субъекта, и где TCR имеет вариабельную область альфа цепи TCR и вариабельную область бета цепи TCR, имеющую аминокислотную последовательность, раскрытую в настоящем документе. В некоторых вариантах осуществления, субъекту, имеющему рак, вводят фармацевтическую композицию, содержащую TCR, который распознает RAS мутантный эпитоп в комплексе с MHC белком, кодированным HLA аллелью субъекта, и где TCR имеет вариабельную область альфа цепи TCR и вариабельную область бета цепи TCR, имеющую аминокислотную последовательность, раскрытую в настоящем документе, где рак выбран из аденокарциномы желчных путей, переходно-клеточной карциномы мочевого пузыря, карциномы груди, аденокарциномы шейки матки, аденокарциномы толстой кишки, аденомы толстой кишки, нейробластомы (вегетативных ганглиев), острого миелоидного лейкоза, хронического миелоидного лейкоза, хронического миеломоноцитарного лейкоза, острого лимфобластного лейкоза, лимфомы Буркитта, лимфомы Ходжкина, миеломы клеток плазмы, печеночно-клеточной карциномы, крупноклеточной карциномы, немелкоклеточной карциномы, протоковой карциномы, эндокринной опухоли, аденокарциномы простаты, базальноклеточной карциномы, плоскоклеточной карциномы, злокачественной меланомы, ангиосаркомы, лейомиосаркомы, липосаркомы, рабдомиосаркомы, миксомы, злокачественной фиброзной гистиоцитомы, плеоморфной саркомы, герминомы, семиномы, анапластической карциномы, фолликулярной карциномы, папиллярной карциномы и карциномы из клеток Гуртла.
В некоторых вариантах осуществления, субъекта с мутацией в гене GATA3 лечат от рака введением фармацевтической композиции, содержащей TCR, который распознает мутантный эпитоп GATA3 в комплексе с белком MHC, кодируемым HLA аллелью, где TCR имеет вариабельную область альфа цепи TCR и вариабельную область бета цепи TCR, имеющую аминокислотную последовательность, раскрытую в настоящем документе. В некоторых вариантах осуществления, субъекта с мутацией в гене GATA3 лечат от рака груди.
В некоторых вариантах осуществления, субъекта с мутацией в гене EGFR лечат от рака введением фармацевтической композиции, содержащей TCR, который распознает мутантный эпитоп EGFR в комплексе с белком MHC, кодируемым HLA аллелью, где TCR имеет вариабельную область альфа цепи TCR и вариабельную область бета цепи TCR, имеющую аминокислотную последовательность, раскрытую в настоящем документе. В некоторых вариантах осуществления, субъекта с мутацией в гене TMPRSS2:ERG лечат от рака введением фармацевтической композиции, содержащей TCR, который распознает мутантный эпитоп TMPRSS2:ERG в комплексе с белком MHC, кодируемым HLA аллелью, где TCR имеет вариабельную область альфа цепи TCR и вариабельную область бета цепи TCR, имеющую аминокислотную последовательность, раскрытую в настоящем документе.
В некоторых вариантах осуществления, субъекта с мутацией в гене BTK лечат от рака введением фармацевтической композиции, содержащей TCR, который распознает мутантный эпитоп BTKmutant эпитоп в комплексе с белком MHC, кодируемым HLA аллелью, где TCR имеет вариабельную область альфа цепи TCR и вариабельную область бета цепи TCR, имеющую аминокислотную последовательность, раскрытую в настоящем документе.
Хотя предпочтительные варианты осуществления настоящего изобретения были показаны и описаны в настоящем документе, специалистам в данной области техники будет очевидно, что такие варианты осуществления представлены только в качестве примера. Многочисленные вариации, изменения и замещения теперь будут очевидны специалистам в данной области без отклонения от изобретения. Следует понимать, что различные альтернативы вариантам осуществления изобретения, описанным в настоящем документе, могут быть использованы при практической реализации изобретения. Подразумевается, что нижеследующая формула изобретения определяет объем изобретения и что способы и структуры в рамках этой формулы изобретения и их эквиваленты охвачены ею.
ПРИМЕРЫ
Пример 1: Технологический процесс идентификации и валидации антигенспецифической T клетки
В этом примере описан типовой технологический процесс создания и применения антигенного пептида, специфического к TCR. На ФИГ. 1 показано графическое изображение технологического процесса. На ФИГ. 2 подробно показан типовая хронология технологического процесса, начиная с получения и культивирования PBMC от субъекта, затем PBMC стабилизируют в течение ночи в культуре и инкубируют в присутствии пептидов и цитокинов; полученные из моноцитов и DC антигенпрезентирующие клетки (APC) помогают индуцировать T клетки в ответ на пептидные антигены, презентированные APC; от 10 дней до 2 недель, антигенспецифические T клетки размножают и сортируют по специфичности к антигену и активации (например, экспрессия CD8+ маркера показывает на создание цитотоксических T лимфоцитов). Активированные, реагирующие на антиген T клетки содержат антигенспецифические TCR.
Коротко, мутированные пептиды, содержащие мутантные эпитопы-мишени (мутантные TMPRSS2:ERG, RAS, BTK и GATA3 пептиды) синтезируют с применением пептидного синтезатора. Синтезированные пептиды применяют для загрузки APC для стимуляции T клеток из образца мононуклеарных клеток периферической крови здорового донора (PBMC). PBMC от пациентов, имеющих неоантигены, представляющие интерес, также могут применяться для получения неоантиген-специфической Т-клетки. После инкубации с пептидом, загруженным APC, популяции T клеток анализируют проточной цитометрией. Антигенспецифические T клетки выделяют с применением проточной цитометрии (ФИГ. 1, 2, 4A, 5, 6, 8F, 8G, 9, 10A, 10B, 11, 13, 15, 16A и 16B). Секвенирование одноклеточных TCR проводят для выделенных антигенспецифических T клеток с применением системы 10x Genomics Single Cell V(D)J для профилирования последовательностей выделенных антигенспецифических TCR. Прочтение секвенирования анализируют с применением аналитического конвейера Cell Ranger™, и кандидатные последовательности TCR выбирают для дальнейшего анализа и функциональных анализов (ФИГ. 1, 6A, 10A, 10B, 11, 13, 15 и 16A и 16B).
Для анализа функциональности TCR, векторы или иРНК, кодирующие TMPRSS2:ERG, RAS, BTK или GATA3 пептиды, содержащие целевые мутантные эпитопы, трансдуцируют в HEK293T или A375 клетки для продуцирования клеточных линий, экспрессирующих антиген. Клетки Jurkat, TCRβ дефицитные клетки Jurkat или PBMC от здоровых доноров трансдуцируют нуклеиновыми кислотами (ФИГ. 3A), кодирующими кандидатные TCR в лентивирусном векторе. Типовой вектор показан на ФИГ. 3B. ФИГ. 4B, 6A и 6B, 10C-10F, 11 и 13 показывают функциональные анализы для клеток, трансдуцированных TCR-экспрессирующим вектором. Клеточные линии, экспрессирующие TMPRSS2:ERG, RAS, BTK и GATA3 антиген, совместно культивируют с клетками Jurkat, трансдуцированными TCR, TCRβ дефицитныеми клетками Jurkat или PBMC от здоровых доноров для анализов распознавания антигена для анализа функциональности кандидатных TCR (Фиг. 7A-7B, 8A-8E, 10A-10F, 12B и 14).
Пример 2: Получение антигенспецифических T клеток
In vitro индукцию T клетки применяют для размножения антигенспецифических T клеток. PBMC от здорового донора-человека высевают в каждую лунку 24-луночного планшета в среде AIM V (Invitrogen). Мутантные пептиды (TMPRSS2:ERG, RAS, BTK или GATA3), TNF-α, IL-1β,PGE1 и IL-7 добавляют в лунки после 24 часов инкубирования. Культуральную среду меняют каждые 2 дня на свежую среду. Антигенспецифические T клетки оценивают и выделяют в дни 10-20 (ФИГ. 2).
Пример 3: Окрашивание и сортировка HLA-мультимера
Неоантигенспецифические T клетки определяют объединением окрашивания HLA-мультимера 2 разными флуорохром-конъюгированными рекомбинантными HLA (HLA-A02.01, HLA-A03.01 или HLA-A11.01) мультимерами с неоантигенпептидами. Анти-CD8, анти-CD4, анти-CD19, анти-CD16, анти-CD14, анти-CD56 и антитела и краситель Live/Dead IR (Invitrogen) применяют для окрашивании поверхности клеток. CD8+ T клетки идентифицируют как CD8+CD4-CD19-CD16-CD14-CD56-IR- (Фиг. 1, 2, 4A, 5, 6A, 8F, 8G, 9, 10A, 10B, 11, 13, 15, 16A и 16B). Для сортировки, вплоть до 5×106 клеток инкубируют с 1-20 мкг мультимером в 100 мкл ФРФБ+0,5% сыворотки человека. Антитела и краситель Live/Dead IR применяют для окрашивания клеток в течение дополнительных 30 мин. После окрашивания, клетки промывают дважды и разводят в ФРФБ+0,5% сыворотки человека. Отрицательные к красителю Live/Dead IR клетки гейтируют, и CD8+/мультимер+ T клетки сортируют на клеточном сортере FACSAria (BD Biosciences).
Пример 4: Глубокое секвенирование антигенспецифических TCR
Антигенспецифические T клетки сортируют в смеси ФРФБ и 2% ФБС (Hyclone Defined) и набор 10x Genomics V(D)J применяют для генетического штрихкодирования РНК из отдельных T клеток. Библиотеки РНК получают согласно протоколам производителя. Полученные библиотеки секвенируют с применением платформы ILLUMINA’s MiSeq. Аналитическую программу 10x Genomics затем применяют для анализа данных секвенирования с получением спаренных TCR альфа и бета последовательностей. Доминантные клоны идентифицируют на основе частоты клеток с общим TCR альфа и/или TCR бета (Фиг. 1, 6, 8F, 8G, 10A, 10B, 11, 13, 15 и 16A).
Пример 5: Синтез и клонирование антигенспецифического TCR гена
ФИГ. 3A представлена графическая диаграмма дизайна типового вектора, включающего конструкт TCR альфа цепи и TCR бета цепи; где конструкты TCR альфа- и бета- цепи содержат последовательности нуклеиновых кислот, кодирующие вариабельную (V), разнообразную ((D), только в конструкте бета цепи), соединяющую (J) и константную (C) область для каждой из TCR альфа (α) цепи и TCR бета (β) цепи, как показано на диаграмме, в векторе с активирующим регуляторным элементом, содержащим элементы, необходимые для экспрессии включенной последовательности нуклеиновой кислоты, включая, например, промотор (пример EF1a область, как показано на диаграмме), дополнительно включающем F2A и P2A протеолитические сайты расщепления и последовательность, кодирующую для резистентности к пуромицину (Puro) для пуромицин-опосредованной выбора. Лентивирусные векторы конструируют из pCDH-EF1-T2A-Puro (SBI system bioscience). Антигенспецифические TCR лентивирусные векторы создают вставкой TCR бета вариабельной области, затем TCR бета константной области мыши, сайта расщепления фурином, SGSG (SEQ ID NO: 601) линкера, F2A сайта, TCR альфа вариабельной области, TCR альфа константной области, T2A сайта и гена резистентности к пуромицину (Фиг. 3A и 3B).
Пример 6: Трансфекция и трансдукция
Лентивирус, кодирующий антигенспецифические TCR, получают временной трансфекцией 293T клеток. Клетки высевают на 10 см планшет в количестве 7×106 клеток за 16 часов до трансфекции 7 мкг лентивирусного вектора, 7 мкг смеси пакующих плазмид (pPAX и pMD2.G), 28 мкл Fugene (Promega) и 1 мл Opti-MEM (Gibco). Культуральную среду меняют через день после трансфекции. Через 72 после трансфекции супернатант собирают с 10-кратной концентрацией.
Клетки Jurkat или PBMC трансдуцируют концентрированным лентивирусом, кодирующим TCR последовательности. Клетки Jurkat промывают и ресуспендируют в RPMI-1640, содержащей полибрен и 10% ФБС. 5×105 CD8-Jurkat клетки в 100 мкл среды высевают в лунку в 96-луночный планшет и добавляют 25 мкл концентрированного лентивируса. Клетки центрифугируют при 2400 оборотов в минуту (об./мин.) в течение 1 часа и инкубируют в инкубаторе CO2. Клетки затем трансдуцируют снова свежей средой с полибреном и ФБС и 25 мкл концентрированного лентивируса. Среду меняют на RPMI-1640, содержащую 10% ФБС и Pen/Strep через 24 часа после второй трансдукции. Обработку пуромицином (1 мег/мл) начинают на 4 день после трансдукции.
Пример 7: Связывание TCR трансдуцированных Jurkat с HLA-пептидом
Для оценки трансдукции TCR, трансдуцированные клетки Jurkat окрашивают флуорохром-конъюгированным мультимером (HLA-неоантигеном), анти-CD8 антителом, константной областью анти-mTCR антитела и красителем Live/Dead IR. Клетки, положительные к mTCR и мультимеру измеряют проточной цитометрией (Фиг. 4B, 6A, 6B, 10A-10F, 11 и 13).
Пример 8: Загрузка пептидом клеток-мишеней
Для экзогенной пептидной загрузки, 1×106 T2, 293T или A375 клетки инкубируют при 37°C и 5% CO2 в течение 2 ч с 10 пг/мл β2-микроглобулина человека (Calbiochem) и титрующими количествами, варьирующимися от 1×10−5 M до 1×10−12 M RAS или GATA3 пептидов, T2 клетки загружают 10−5 M GIL пептидом гриппа (матричным белком гриппа 58-66 GILGFVTL (SEQ ID NO: 602), Metabion), служащим в качестве контроля. После промывания, загруженные пептидом T2 клетки применяют в анализах выделения IL-2 (Фиг. 6B, 7, 8, 12E и 14).
Пример 9: Неоантиген экспрессирующие клетки-мишени
Для эндогенных антигенэкспрессирующих клеток-мишеней, 1×106 HEK293 или A375 клетки трансдуцируют лентивирусными векторами, кодирующими TMPRSS2::ERG, BTK, GATA3 или KRAS мутированные пептиды. Трансдуцированные клетки-мишени выбирают пуромицином (1 мкг/мл) в культуральной среде (DMEM с 10% ФБС).
Пример 10: Анализ выделения IL-2
Для исследования специфичности, клоны T клетки (2,5×105 клеток в 50 мкл) могут быть инкубированы с HEK293T, HLA-A03.01 трансдуцированными A375 или HLA-A11.01 трансдуцированными A375 клеточными линиями (5×104 клеток в 50 мкл) и TMPRSS2::ERG, BTK, GATA3 или KRAS мутированными пептидными неоантигенами. Следующие фигуры демонстрируют результаты анализа выделения IL2 в случае соответствующих TCR, как изображено на фигурах: Фиг. 6B, 7A, 7B, 8E, 10C, 12A, 12B и 14). Супернатанты культур собирают через 24 ч совместного культивирования и оценивают концентрацию IL-2 стандартным MSD с применением V-PLEX Human IL-2 анализов (Meso Scale Discovery).
Пример 11: Анализ выделения IFN- γ
Для исследования специфичности, клоны T клетки (2×103 клеток в 100 мкл) инкубируют с клеточными линиями, экспрессирующими TMPRSS2::ERG, BTK, GATA3 или KRAS мутированные пептидные неоантигены. Супернатанты культур собирают через 24 ч совместного культивирования и оценивают стандартным ELISA с применением набора OptEIA™ Human IFN-γ (BD Biosciences Pharmingen).
Пример 12: Анализ цитотоксичности
Цитотоксическая активность клонов T клетки может быть проанализирована в стандартном 4 ч анализе выделения 51-хрома. Коротко, 1×106 клеток-мишеней могут быть мечены 100 мкКи Na251CrO4 (ICN Biochemicals) в течение 1-1,5 ч. 51Cr-меченые клетки-мишени могут быть культивированы с T клетками в RPMI 1640 с 12% ФТС. Для определения функциональной авидности 1×104 T клетки могут быть добавлены к 1×103 загруженным пептидом T2 клеткам, загруженным тированными количествами TMPRSS2::ERG, BTK, GATA3 или KRAS мутированных пептидных неоантигенов, с получением постоянного E:T 10:1.
После 4 ч совместного культивирования при 37°C, 50 мкл супернатанта собирают и измеряют радиоактивность на гамма счетчике. Долю специфического лизиса рассчитывают как: 100×(экспериментальное выделение - спонтанное выделение)/(максимальное выделение - спонтанное выделение). Спонтанное выделение может оцениваться через инкубирование клеток-мишеней в отсутствии эффекторных клеток. Для расчета доли относительного лизиса, максимальная доля специфического лизиса может быть установлено как эталонное значение 100%, и соответствующие значения могут быть рассчитаны в соответствии с этим эталоном. Для определения полумаксимального лизиса, долю относительного лизиса наносят на график к концентрации пептида. Концентрацию пептида, при которой кривая пересекает 50% относительный лизис, принимают как значение полумаксимального лизиса.
Пример 13: Анализ уничтожения клеток
RAS-неоантигенспецифический рекомбинантный TCR трансдуцируют в PBMC и анализируют его способность уничтожать линию раковых клеток (Фиг. 8A, 8B). Уничтоженные рекомбинантные клетки, экспрессирующие TCR, показали более чем на 30% большую гибель линий раковых клеток по сравнению с контролем. Модифицированный рекомбинантный TCR (rTCR) с константными областями мыши экспрессируют из промотора SFFV, и получают 30% выход неоантигенспецифической трансдукции TCR в PBMC от здорового донора. В качестве клетки-мишени используют линию клеток SW620, которая естественным образом экспрессирует мутацию KRAS G12V. HLA-A11: 01 вводят в клеточную линию SW620 с помощью лентивирусных трансдукций. РВМС, трансдуцированные rTCR, культивируют совместно с двумя разными клеточными линиями SW620 с экспрессией или без экспрессии HLA-A11:01 в течение 6 часов. Затем собирают супернатант и клетки для анализа секреции цитокина и апоптоза.
Через 6 часов совместного культивирования, значительно более высокие уровни IFNγ, IL-2 и TNFα определяют в группах HLA-A11:01 трансдуцированных клеточных линий SW620 (клеточная линия Rasmut+HLA-A11:01) по сравнению с не трансдуцированными SW620 (клеточная линия Rasmut). Это показывает, что rTCR PBMC могут специфически распознавать RAS пептид, содержащий G12V мутацию на HLA-A11:01 клеточной линии, близкой к реальной модели опухоли. Также, значительно большую долю клеток, положительных к Каспазе-3 (маркер апоптоза) наблюдают в HLA-A11:01 трансдуцированных SW620 клеточных линиях по сравнению с контролем. Таким образом, rTCR трансдуцированные PBMC не только секретируют цитокин (IFNγ, IL-2 и TNFα), но также специфически функционально уничтожают клетки-мишени.
В некоторых примерах, цитотоксическую активность оценивают через совместное культивирование Т клеток, экспрессирующих TCR, специфичный для мутантного RAS пептида на конкретном HLA, с мутантными трансдуцированными RAS пептидом злокачественными клетками-мишенями, экспрессирующими соответствующий HLA, и через определение относительного роста клеток-мишеней, вместе со специфическим определением апоптотического маркера Аннексина V в раковых клетках-мишенях (Фиг. 8C, 8D, 10D, 10E). Раковые клетки-мишени сконструированы так, чтобы экспрессировать мутантный пептид вместе с правильной MHC-I аллелью. Ложно-трансдуцированные клетки-мишени (т.е. не экспрессирующие мутантный пептид) используют в качестве отрицательного контроля. Клетки также трансдуцируют для стабильной экспрессии GFP, что позволяет отслеживать рост клеток-мишеней. PBMC от здоровых доноров, используемые в качестве эффекторных клеток, трансдуцируют для экспрессии TCR, специфичного для мутантного RAS пептида. Ложно-трансдуцированные клетки используют в качестве отрицательного контроля. Клетки-мишени культивируют совместно с разным количеством эффекторных клеток в течение 72 часов в среде, содержащей реагент для обнаружения аннексина V. Сигнал GFP и сигнал Аннексина-V измеряют с течением времени с помощью аппарата IncuCyte S3. Сигнал Аннексина V, исходящий от эффекторных клеток, фильтруют методом разделения по размеру. Рост и гибель клеток-мишеней выражается как площадь GFP и Аннексина-V (мм2) с течением времени, соответственно. ФИГ. 8C демонстрирует высокую степень обратной корреляции уровней TCR, определенных соотношением TCR/CD8+:мишень, с ростом клеток-мишеней (верхняя панель). Точно так же, более высокие уровни TCR коррелируют с более высокими Аннексин V-положительными клетками-мишенями, что указывает на большее количество апоптотических клеток-мишеней. Это указывает на высокую степень специфичности и эффективности разрушения клеток-мишеней с помощью RAS TCR4.
В некоторых примерах, цитотоксическую активность оценивают перед клонированием TCR. Т-клетки, индуцированные против мутантного пептида RAS на конкретном HLA, совместно культивируют с мутантными раковыми клетками-мишенями, экспрессирующими соответствующий HLA, нагруженный различными концентрациями мутантных пептидов RAS (Фиг. 8F, 8G). Специфически измеряют относительный рост и апоптотический маркер Аннексин V в раковых клетках-мишенях. Клетки-мишени также трансдуцируют для стабильной экспрессии GFP, что позволяет отслеживать рост клеток-мишеней. Сигнал GFP и сигнал Аннексина-V измеряют с течением времени с помощью устройства IncuCyte S3. Сигнал Аннексина V, исходящий от эффекторных клеток, отфильтровывают методом разделения по размеру. Рост и гибель клеток-мишеней выражается как площадь GFP и Аннексина-V (мм2) с течением времени, соответственно. Для Т-клеток, демонстрирующих цитотоксичность при низких концентрациях пептида по сравнению с отсутствием пептида и/или пептидом дикого типа, можно быть проведено секвенирование TCR, как указано выше. Что касается данных, показанных в экспериментах, представленных на ФИГ. 8F и 8G (цифры в правом верхнем углу), цитотоксичность Т-клеток показала хорошую дозовую чувствительность к пептидам, о чем свидетельствуют более низкие GFP-экспрессирующие клетки с более высокой дозой пептидов в течение указанного времени. Обратная корреляция показывает, что с более высокими количествами пептидов для стимуляции TCR на Т клетках наблюдается более сильное подавление роста клеток-мишеней, что продемонстрировано более низкими GFP-положительными клетками. Это демонстрирует, что Т-клетки проявляют высокую TCR специфичность и эффективность при ограничении прогрессии клеток-мишеней.
Пример 14: Суммарная информация по разработанным рекомбинантным TCR
Этот пример предоставляет подробную информацию о разработанных TCR. В таблице 1 представлено общее описание TCR, описанных в настоящем документе, а в таблице 2 приведены описания конкретных аминокислот и кодирующих последовательностей.
G12C
TCR-1
Хотя предпочтительные варианты осуществления настоящего изобретения были показаны и описаны в настоящем документе, специалистам в данной области техники будет очевидно, что такие варианты осуществления представлены только в качестве примера. Многочисленные вариации, изменения и замещения теперь будут очевидны специалистам в данной области без отклонения от изобретения. Следует понимать, что различные альтернативы вариантам осуществления изобретения, описанным в настоящем документе, могут быть использованы при практической реализации изобретения. Подразумевается, что нижеследующая формула изобретения определяет объем изобретения и что способы и структуры в рамках этой формулы изобретения и их эквиваленты охвачены ею.
Таблица 2. ПОСЛЕДОВАТЕЛЬНОСТИ
ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
Следующие варианты рассматриваются в настоящем описании:
1. Нуклеиновая кислота, кодирующая по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из RAS в комплексе с МНС человека, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 84% идентичность последовательности с или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 3, 18, 33, 49, 65, 81, 97, 113, 241, 257, 273, 289, 305, 321, 337, 353, 369, 385, 401, 417, 534, 547 и 560 и/или где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 84% идентичность последовательности с или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 6, 21, 36, 52, 68, 84, 100, 116, 244, 260, 276, 292, 308, 324, 340, 356, 372, 388, 404, 420, 537, 550 и 563.
2. Нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из RAS в комплексе с МНС человека, где эпитоп из RAS содержит область, имеющую по меньшей мере, 70% идентичность последовательности с или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 15, 30, 45, 46, 61, 62, 77, 78, 93, 94, 109, 110, 125, 126, 219-222, 253, 254, 269, 270, 285, 286, 301, 302, 317, 318, 333, 334, 349, 350, 365, 366, 381, 382, 397, 398, 413, 414, 429, 430, 544, 557 и 600.
3. Нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий
a. конструкт альфа цепи TCR и/или
b. конструкт бета цепи TCR
где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека кодированным HLA-A03:01 аллелью.
4. Нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий
a. конструкт альфа цепи TCR и/или
b. конструкт бета цепи TCR
где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека, кодированным HLA-A02:01 аллелью.
5. Нуклеиновая кислота или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует, по меньшей мере, один Т-клеточный рецептор (TCR), содержащий
a. конструкт альфа цепи TCR и/или
b. конструкт бета цепи TCR
где TCR специфически связывается с эпитопом из RAS в комплексе с МНС человека, кодированным HLA-A11:01 аллелью.
6. Нуклеинов кислот по варианту осуществления в параграфе 3, где конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80%, или по меньшей мере, 90%, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 71, 87, 103, 295, 311, 327, 343, 359 и 391.
7. Нуклеинов кислот по варианту осуществления в параграфе 4, где конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80%, или, по меньшей мере, 90%, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 9 и 24.
8. Нуклеинов кислот по варианту осуществления в параграфе 5, где конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80%, или, по меньшей мере, 90%, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs:39, 55, 119, 247, 263, 279, 375, 407, 423, 539, 552 и 565.
9. Нуклеинов кислот по варианту осуществления в параграфе 3, где конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80%, или, по меньшей мере, 90%, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 74, 90, 106, 298, 314, 330, 346, 362 и 394.
10. Нуклеинов кислот по варианту осуществления 4, где конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80%, или, по меньшей мере, 90%, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 12 и 27.
11. Нуклеиновую кислоту по варианту осуществления 5, где конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80%, или, по меньшей мере, 90%, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 42, 58, 122, 250, 266, 282, 378, 410, 426, 541, 554 и 567.
12. Нуклеиновая кислота по вариантам осуществления по любому из вариантов осуществления в параграфах 1-3 и 6, где конструкт альфа цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 63, 79, 95, 287, 303, 319, 335, 351 и 383.
13. Нуклеиновая кислота по вариантам осуществления по любому из вариантов осуществления в параграфах 1-3 и 6, где конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 66, 82, 98, 290, 306, 322, 338, 354 и 386.
14. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-2, 4 и 7, где конструкт альфа цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 1 и 16.
15. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-2, 4 и 10, где конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 4 и 19.
16. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-2, 5 и 8, где конструкт альфа цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 31, 47, 111, 239, 255, 271, 367, 399, 415, 532, 545 и 558.
17. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-2, 5 и 11, где конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 34, 50, 114, 242, 258, 274, 370, 402, 418, 53, 548 и 561.
18. Нуклеиновая кислота по вариантам осуществления по любому из вариантов осуществления в параграфах 1-3, 6 и 12, где конструкт альфа цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 64, 80, 96, 288, 304, 320, 336, 352 и 384.
19. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-3, 6 и 13, где конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 67, 83, 99, 291, 307, 323, 339, 355 и 387.
20. Нуклеиновая кислота по вариантам осуществления по любому из вариантов осуществления в параграфах 1-2, 4, 7 и 14, где конструкт альфа цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 2 и 17.
21. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-2, 4, 10 и 15, где конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 5 и 20.
22. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-2, 5, 8 и 16, где конструкт альфа цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 32, 48, 112, 240, 256, 272, 368, 400, 416, 533, 546 и 559.
23. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-2, 5, 11 и 17, где конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 35, 51, 115, 243, 259, 275, 371, 403, 419, 536, 549 и 562.
24. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-3, 6, 12 и 18, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 65, 81, 97, 289, 305, 321, 337, 353 и 385.
25. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-3, 6, 13 и 19, где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 68, 84, 100, 292, 308, 324, 340, 356 и 388.
26. Нуклеиновая кислота по вариантам осуществления по любому из вариантов осуществления 1-2, 4, 7 14 и 20, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 3 и 18.
27. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-2, 4, 10, 15 и 21, где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 6 и 21.
28. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-2, 5, 8, 16 и 22, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs:33, 49, 113, 241, 257, 273, 369, 401, 417, 534, 547 и 560.
29. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-2, 5, 11, 17 и 23, где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs:36, 52, 116, 244, 260, 276, 372, 404, 420, 537, 550 и 563.
30.Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 9; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 12.
31. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 или 30, где
a. конструкт альфа цепи TCR содержит
i. CDR1 с SEQ ID NO: 1,
ii. CDR2 с SEQ ID NO: 2, и
iii. CDR3 с SEQ ID NO: 3; и
b. конструкт бета цепи TCR содержит
i. CDR1 с SEQ ID NO: 4,
ii. CDR2 с SEQ ID NO: 5, и
iii. CDR3 с SEQ ID NO: 6.
32. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 24; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 27.
33. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 32, где
a. конструкт альфа цепи TCR содержит
i. CDR1 с SEQ ID NO: 16,
ii. CDR2 с SEQ ID NO: 17, и
iii. CDR3 с SEQ ID NO: 18; и
b. конструкт бета цепи TCR содержит
i. CDR1 с SEQ ID NO: 19,
ii. CDR2 с SEQ ID NO: 20, и
iii. CDR3 с SEQ ID NO: 21.
34. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 39; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 42.
35. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 34, где
a. конструкт альфа цепи TCR содержит
i. CDR1 с SEQ ID NO: 31,
ii. CDR2 с SEQ ID NO: 32, и
iii. CDR3 с SEQ ID NO: 33; и
b. конструкт бета цепи TCR содержит
i. CDR1 с SEQ ID NO: 34,
ii. CDR2 с SEQ ID NO: 35, и
iii. CDR3 с SEQ ID NO: 36.
36. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 55; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 58.
37. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 36, где
a. конструкт альфа цепи TCR содержит
i. CDR1 с SEQ ID NO: 47,
ii. CDR2 с SEQ ID NO: 48, и
iii. CDR3 с SEQ ID NO: 49; и
b. конструкт бета цепи TCR содержит
i. CDR1 с SEQ ID NO: 50,
ii. CDR2 с SEQ ID NO: 51, и
iii. CDR3 с SEQ ID NO: 52.
38. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 71; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 74.
39. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 38, где
a. конструкт альфа цепи TCR содержит
i. CDR1 с SEQ ID NO: 63,
ii. CDR2 с SEQ ID NO: 64, и
iii. CDR3 с SEQ ID NO: 65; и
b. конструкт бета цепи TCR содержит
i. CDR1 с SEQ ID NO: 66,
ii. CDR2 с SEQ ID NO: 67, и
iii. CDR3 с SEQ ID NO: 68.
40. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 87; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 90.
41. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 40, где
a. конструкт альфа цепи TCR содержит
i. CDR1 с SEQ ID NO: 79,
ii. CDR2 с SEQ ID NO: 80, и
iii. CDR3 с SEQ ID NO: 81; и
b. конструкт бета цепи TCR содержит
i. CDR1 с SEQ ID NO: 82,
ii. CDR2 с SEQ ID NO: 83, и
iii. CDR3 с SEQ ID NO: 84.
42. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 103; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 106.
43. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 42, где
a. конструкт альфа цепи TCR содержит
i. CDR1 с SEQ ID NO: 95,
ii. CDR2 с SEQ ID NO: 96, и
iii. CDR3 с SEQ ID NO: 97; и
b. конструкт бета цепи TCR содержит
i. CDR1 с SEQ ID NO: 98,
ii. CDR2 с SEQ ID NO: 99, и
iii. CDR3 с SEQ ID NO: 100.
44. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 119; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 122.
45. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 44, где
a. конструкт альфа цепи TCR содержит
i. CDR1 с SEQ ID NO: 111,
ii CDR2 с SEQ ID NO: 112, и
iii CDR3 с SEQ ID NO: 113; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 114,
ii CDR2 с SEQ ID NO: 115, и
iii CDR3 с SEQ ID NO: 116.
46. Нуклеиновая кислота по любому из вариантов осуществления 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 247; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 250.
47. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 46, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 239,
ii CDR2 с SEQ ID NO: 240, и
iii CDR3 с SEQ ID NO: 241; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 242,
ii CDR2 с SEQ ID NO: 243, и
iii CDR3 с SEQ ID NO: 244.
48. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 263; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 266.
49. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 48, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 255,
ii CDR2 с SEQ ID NO: 256, и
iii CDR3 с SEQ ID NO: 257; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 258,
ii CDR2 с SEQ ID NO: 259, и
iii CDR3 с SEQ ID NO: 260.
50. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 279; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 282.
51. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 50, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 271,
ii CDR2 с SEQ ID NO: 272, и
iii CDR3 с SEQ ID NO: 273; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 274,
ii CDR2 с SEQ ID NO: 275, и
iii CDR3 с SEQ ID NO: 276.
52. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 295; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с S или 100% идентичность последовательности с EQ ID NO: 298.
53. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 52, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 287,
ii CDR2 с SEQ ID NO: 288, и
iii CDR3 с SEQ ID NO: 289; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 290,
ii CDR2 с SEQ ID NO: 291, и
iii CDR3 с SEQ ID NO: 292.
54. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 311; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 314.
55. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 54, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 303,
ii CDR2 с SEQ ID NO: 304, и
iii CDR3 с SEQ ID NO: 305; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 306,
ii CDR2 с SEQ ID NO: 307, и
iii CDR3 с SEQ ID NO: 308.
56. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 327; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 330.
57. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 56, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 319,
ii CDR2 с SEQ ID NO: 320, и
iii CDR3 с SEQ ID NO: 321; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 322,
ii CDR2 с SEQ ID NO: 323, и
iii CDR3 с SEQ ID NO: 324.
58. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 343; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 346.
59. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 58, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 335,
ii CDR2 с SEQ ID NO: 336, и
iii CDR3 с SEQ ID NO: 337; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 338,
ii CDR2 с SEQ ID NO: 339, и
iii CDR3 с SEQ ID NO: 340.
60. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 359; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 361.
61. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 60, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 351,
ii CDR2 с SEQ ID NO: 352, и
iii CDR3 с SEQ ID NO: 353; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 354,
ii CDR2 с SEQ ID NO: 355, и
iii CDR3 с SEQ ID NO: 356.
62. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 375; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 378.
63. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 62, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 367,
ii CDR2 с SEQ ID NO: 368, и
iii CDR3 с SEQ ID NO: 369; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 370,
ii CDR2 с SEQ ID NO: 371, и
iii CDR3 с SEQ ID NO: 372.
64. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 391; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 394.
65. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 64, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 383,
ii CDR2 с SEQ ID NO: 384, и
iii CDR3 с SEQ ID NO: 385; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 386,
ii CDR2 с SEQ ID NO: 387, и
iii CDR3 с SEQ ID NO: 388.
66. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 407; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 410.
67. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 66, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 399,
ii CDR2 с SEQ ID NO: 400, и
iii CDR3 с SEQ ID NO: 401; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 402,
ii CDR2 с SEQ ID NO: 403, и
iii CDR3 с SEQ ID NO: 404.
68. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 423; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 426.
69. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 68, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 415,
ii CDR2 с SEQ ID NO: 416, и
iii CDR3 с SEQ ID NO: 417; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 418,
ii CDR2 с SEQ ID NO: 419, и
iii CDR3 с SEQ ID NO: 420.
70. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 542; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 543.
71. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 70, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 532,
ii CDR2 с SEQ ID NO: 533, и
iii CDR3 с SEQ ID NO: 534; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 535,
ii CDR2 с SEQ ID NO: 536, и
iii CDR3 с SEQ ID NO: 537.
72. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 555; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 556.
73. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 72, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 545,
ii CDR2 с SEQ ID NO: 546, и
iii CDR3 с SEQ ID NO: 547; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 548,
ii CDR2 с SEQ ID NO: 549, и
iii CDR3 с SEQ ID NO: 550.
74. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 568; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 569.
75. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-5 и 74, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 558,
ii CDR2 с SEQ ID NO: 559, и
iii CDR3 с SEQ ID NO: 560; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 561,
ii CDR2 с SEQ ID NO: 562, и
iii CDR3 с SEQ ID NO: 563.
76. Нуклеиновая кислота, кодирующая по меньшей мере, один Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из TMPRSS2:ERG в комплексе с МНС человека, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 144 и SEQ ID NO: 147.
77. Нуклеиновая кислота, кодирующая по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из TMPRSS2:ERG в комплексе с МНС человека, где эпитоп из TMPRSS2:ERG содержит область, имеющую по меньшей мере, 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 156.
78. Нуклеиновая кислота по варианту осуществления в параграфе 76 или 77, где конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 150.
79. Нуклеиновая кислота по варианту осуществления в параграфе 76 или 77, где конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 153.
80. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 76-80, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 142 или SEQ ID NO: 145 соответственно.
81. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 76-80, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 143 или SEQ ID NO: 146.
82. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 76-81, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 150; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 153.
83. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 76-82, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 142,
ii CDR2 с SEQ ID NO: 143, и
iii CDR3 с SEQ ID NO: 144; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 145,
ii CDR2 с SEQ ID NO: 146, и
iii CDR3 с SEQ ID NO: 147.
84. Нуклеиновая кислота, кодирующая по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из GATA3 в комплексе с МНС человека, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 129, 132, 191, 194, 206 и 209.
85. Нуклеиновая кислота, кодирующая по меньшей мере, один Т-клеточный рецептор (TCR) способный специфически связываться с мутантом GATA3 пептида в комплексе с белком, кодированным HLA аллелью субъекта с раком, где TCR содержит
a. конструкт альфа цепи TCR и/или
b. конструкт бета цепи TCR.
86. Рекомбинантная нуклеиновая кислота, или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует, Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, где TCR
a. специфически связывается с мутантом GATA3 пептида в комплексе с HLA-A02:01, HLA-B07:02 или HLA-B08:01 белком;
b. содержит альфа цепь определяющей комплементарность области 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NOs: 129, 132, 191, 194, 206 или 209; и/или
c. специфически связывается с мутантом GATA3 пептида, содержащим область с, по меньшей мере, 70% идентичностью последовательности с, или 100% идентичность последовательности с SEQ ID NO: 141, 203 или 218.
87. Нуклеиновая кислота, кодирующая по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из GATA3 в комплексе с МНС человека, где эпитоп из GATA3 содержит область, имеющую по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 141, 203 или 218.
88. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 84-87, где конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 135, 197 или 212.
89. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 84-87, где конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 138, 200 или 215.
90. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 84-87, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 127, 130, 189, 192, 204 и 207.
91. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 84-87, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 128, 131, 190, 193, 205 и 208.
92. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 84-87, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 135; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 138.
93. Нуклеиновая кислота по варианту осуществления в параграфе 86, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 127,
ii CDR2 с SEQ ID NO: 128, и
iii CDR3 с SEQ ID NO: 129; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 130,
ii CDR2 с SEQ ID NO: 131, и
iii CDR3 с SEQ ID NO: 132.
94. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 84-87, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 197; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 200.
95. Нуклеиновая кислота по варианту осуществления в параграфе 94, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 189,
ii CDR2 с SEQ ID NO: 190, и
iii CDR3 с SEQ ID NO: 191; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 192,
ii CDR2 с SEQ ID NO: 193, и
iii CDR3 с SEQ ID NO: 194.
96. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 78-85, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 212; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 215.
97. Нуклеиновая кислота по варианту осуществления в параграфе 90, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 204,
ii CDR2 с SEQ ID NO: 205, и
iii CDR3 с SEQ ID NO: 206; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 207,
ii CDR2 с SEQ ID NO: 208, и
iii CDR3 с SEQ ID NO: 209.
98. Нуклеиновая кислота, кодирующая по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из BTK в комплексе с МНС человека, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 161 и SEQ ID NO: 176, или где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 164 и SEQ ID NO: 179.
99. Нуклеиновая кислота, кодирующая по меньшей мере, один Т-клеточный рецептор (TCR) способный специфически связываться с мутантом BTK пептида в комплексе с белком, кодированным HLA аллелью субъекта с раком, где TCR содержит
(a) конструкт альфа цепи TCR и/или
(b) конструкт бета цепи TCR.
100. Рекомбинантная нуклеиновая кислота, или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, где TCR
a. специфически связывается с мутантом BTK пептида в комплексе с HLA-A02:01 белком;
b. содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 161, 164, 176, или 179; и/или
c. специфически связывается с мутантом BTK пептида, содержащим область с, по меньшей мере, 70% идентичностью последовательности с, или 100% идентичностью последовательности с SEQ ID NO: 173 или 188.
101. Нуклеиновая кислота, кодирующая по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из BTK в комплексе с МНС человека, где эпитоп из BTK содержит область, имеющую по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 173 или 188.
102. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 98-101, где конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 167 или 182.
103. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 98-102, где конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 170 или 185.
104. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 98-103, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 159, 162, 174 и 177.
105. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 98-104, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 160, 163, 175 и 178.
106. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 98-105, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 167 или 182; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 170 или 185.
107. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 98-106, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 159 или 174,
ii CDR2 с SEQ ID NO: 160 или 175, и
iii CDR3 с SEQ ID NO: 161 или 176; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 162 или 177,
ii CDR2 с SEQ ID NO: 163 или 178, и
iii CDR3 с SEQ ID NO: 164 или 179.
108. Нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из EGFR в комплексе с МНС человека, где конструкт альфа цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 449, SEQ ID NO: 466, SEQ ID NO: 483, SEQ ID NO: 500 и SEQ ID NO: 517, или где конструкт бета цепи TCR содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NO: 452, SEQ ID NO: 469, SEQ ID NO: 486, SEQ ID NO: 503 и SEQ ID NO: 520.
109. Нуклеиновая кислота, кодирующая по меньшей мере, один Т-клеточный рецептор (TCR), способный специфически связываться с мутантом EGFR пептида в комплексе с белком, кодированным HLA аллелью субъекта с раком, где TCR содержит
a. конструкт альфа цепи TCR и/или
b. конструкт бета цепи TCR.
110. Рекомбинантная нуклеиновая кислота, или клетка, содержащая рекомбинантную нуклеиновую кислоту, где нуклеиновая кислота кодирует Т-клеточный рецептор (TCR), содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR, где TCR
a. специфически связывается с мутантом EGFR пептида в комплексе с HLA-A02:01 белком;
b. содержит определяющую комплементарность область 3 (CDR3), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 449, 466, 483, 500, 517, 452, 469, 486, 503, или 520; и/или
c. специфически связывается с мутантом EGFR пептида, содержащим область с, по меньшей мере, 70% идентичностью последовательности с, или 100% идентичностью последовательности с SEQ ID NO: 461, 462, 463, 478, 479, 480, 495, 496, 497, 512, 513, 514, 529, 530 или 531.
111. Нуклеиновая кислота, кодирующая, по меньшей мере, один Т-клеточный рецептор (TCR) содержащий конструкт альфа цепи TCR и/или конструкт бета цепи TCR способный специфически связываться с эпитопом из EGFR в комплексе с МНС человека, где эпитоп из EGFR содержит область, имеющую по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 461, 462, 463, 478, 479, 480, 495, 496, 497, 512, 513, 514, 529, 530 или 531.
112. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 108-111, где конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 455, 472, 489, 506 или 526.
113. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 108-112, где конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 458, 475, 492, 509, или 526.
114. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 108-113, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 1 (CDR1), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 447, 464, 481, 498, 515, 450, 467, 484, 501 и 518.
115. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 108-114, где конструкт альфа цепи TCR и/или конструкт бета цепи TCR содержит определяющую комплементарность область 2 (CDR2), имеющую, по меньшей мере, 90% идентичность последовательности с, или 100% идентичность последовательности с аминокислотной последовательностью, выбранной из SEQ ID NOs: 448, 465, 482, 499, 516, 451, 468, 485, 502 и 519.
116. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 108-115, где
a. конструкт альфа цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с, или 100% идентичность последовательности с SEQ ID NO: 455, 472, 489, 506, или 523; и
b. конструкт бета цепи TCR содержит вариабельную область, имеющую, по меньшей мере, 80% идентичность последовательности с SEQ ID NO: 458, 475, 492, 509 или 526.
117. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 108-116, где
a. конструкт альфа цепи TCR содержит
i CDR1 с SEQ ID NO: 447, 464, 481, 498 или 515,
ii CDR2 с SEQ ID NO: 448, 465, 482, 499 или 516, и
iii CDR3 с SEQ ID NO: 449, 466, 483, 500 или 517; и
b. конструкт бета цепи TCR содержит
i CDR1 с SEQ ID NO: 450, 467, 484, 501 или 518,
ii CDR2 с SEQ ID NO: 451, 468, 485, 502, или 519, и
iii CDR3 с SEQ ID NO: 452, 469, 486, 503, или 520.
118. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-117, где эпитоп содержит мутацию, выбранную из группы, состоящей из точечной мутации, мутации сайта сплайсинга, мутации «сдвига рамки», мутации сквозного прохождения, мутации резистентности, мутации слияния генов и любого их сочетания.
119. Нуклеиновая кислота по любому из вариантов осуществления 1-69, где МНС человека кодирован или HLA-A02:01 аллелью, или HLA-A03:01 аллелью или HLA-A11:01 аллелью.
120. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-69, где эпитоп содержит точечную мутацию.
121. Нуклеиновая кислота по варианту осуществления в параграфе 120, где точечной мутацией является G12V мутация.
122. Нуклеиновая кислота по варианту осуществления в параграфе 120, где точечной мутацией является G12C мутация.
123. Нуклеиновая кислота по варианту осуществления в параграфе 120, где точечной мутацией является G12D мутация.
124. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 76-83, где МНС человека кодирован HLA-A02:01 аллелью.
125. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 76-83 и 124, где эпитоп содержит мутацию слияния гена.
126. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 84-97, где МНС человека кодирован HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью.
127. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 84-97 и 126, где эпитоп содержит мутацию «сдвига рамки».
128. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 98-107, где МНС человека кодирован HLA-A02:01 аллелью.
129. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 98-107 и 128, где эпитоп содержит точечную мутацию.
130. Нуклеиновая кислота по варианту осуществления в параграфе 129, где точечной мутацией является C481S мутация.
131. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 108-117, где МНС человека кодирован HLA-A02:01 аллелью.
132. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 108-117, где эпитоп содержит точечную мутацию.
133. Нуклеиновая кислота по варианту осуществления в параграфе 132, где точечной мутацией является T790M.
134. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-130, где эпитоп имеет длину, по меньшей мере, 8 аминокислот.
135. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-134, где эпитоп имеет длину, по меньшей мере, 16 аминокислот.
136. Нуклеиновая кислота по любому из вариантов осуществления 1-135, где эпитоп имеет длину 8-25 аминокислот.
137. Нуклеиновая кислота по любому из вариантов осуществления 1-136, где эпитоп имеет длину 8-12 аминокислот.
138. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-136, где эпитоп имеет длину 16-25 аминокислот.
139. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-136, где эпитоп имеет длину 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, или 25 аминокислот.
140. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-139, где эпитоп связывается с МНС человека с большей аффинностью, чем у эпитопа дикого типа.
141. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-140, где эпитоп связывается с МНС человека с KD или IC50 менее чем 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ.
142. Нуклеиновая кислота по любому из вариантов осуществления 108-141, где мутация не присутствует в не раковых клетках субъекта.
143. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-142, где эпитоп кодирован геном или экспрессирует ген раковых клеток субъекта.
144. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-143, где TCR связывается с MHC-пептидным комплексом с KD или IC50 менее чем 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ.
145. Нуклеиновая кислота по любому из вариантов осуществления в параграфах 1-144, где нуклеиновая кислота функционально связана с промотором.
146. Вектор, содержащий нуклеиновую кислоту по любому из вариантов осуществления в параграфах 1-145.
147. Вектор по варианту осуществления в параграфе 146, где вектором является самоамплифицирующийся РНК репликон, плазмида, фаг, транспозон, космида, вирус или вирион.
148. Вектор по варианту осуществления в параграфах 146 или 147, где вектором является вирусный вектор.
149. Вектор по варианту осуществления в параграфе 148, где вектор получают от ретровируса, лентивируса, аденовируса, аденоассоциированного вируса, вируса герпеса, вируса оспы, вируса альфа, вируса осповакцины, вируса гепатита В, папилломавируса человека или их псевдотипа.
150. Вектор по варианту осуществления в параграфах 146 или 147, где вектором является не вирусный вектор.
151. Вектор по варианту осуществления в параграфе 150, где не вирусным вектором является наночастица, катионный липид, катионный полимер, металлический нанополимер, наностержень, липосома, мицелла, микропузырек, проникающий в клетки пептид или липосфера.
152. Белок, кодированный нуклеиновой кислотой по любому из вариантов осуществления в параграфах 1-145.
153. Клетка, содержащая нуклеиновую кислоту по любому из вариантов осуществления в параграфах 1-149, вектор по любому из вариантов осуществления 144-149, или белок по варианту осуществления 146.
154. Клетка по варианту осуществления 153, где клеткой является CD4+ T клетка.
155. Клетка по варианту осуществления 153, где клеткой является CD8+ T клетка.
156. Клетка по варианту осуществления 153, где клеткой является аутологичная клетка.
157. Клетка по варианту осуществления 153, где клеткой является аллогенная клетка.
158. Клетка по варианту осуществления 153, где клеткой является естественный киллер, B клетка или иммортализованная линия клеток.
159. Клетка по любому из вариантов осуществления в параграфах 153-156, где клеткой является клетка человека.
160. Фармацевтическая композиция, содержащая нуклеиновую кислоту по любому из вариантов осуществления в параграфах 1-143, вектор по любому из вариантов осуществления в параграфах 146-151, белок по варианту осуществления в параграфе 152, или клетку по любому из вариантов осуществления в параграфах 153-159; и фармацевтически приемлемый эксципиент или разбавитель.
161. Фармацевтическая композиция по варианту осуществления в параграфах 160, дополнительно содержащая иммуномодулирующий агент или адъювант.
162. Фармацевтическая композиция по варианту осуществления в параграфе 161, где иммуномодулирующим агентом является цитокин.
163. Фармацевтическая композиция по любому из вариантов осуществления в параграфах 160-162, где адъювантом является поли I:C.
164. Фармацевтическая композиция по любому из вариантов осуществления в параграфах 160-163, для применения в лечении иммунного заболевания или рака.
165. Применение фармацевтической композиции по любому из вариантов осуществления в параграфах 160-164, для лечения иммунного заболевания или рака.
166. Применение нуклеиновой кислоты по любому из вариантов осуществления в параграфах 1-145, вектора по любому из вариантов осуществления в параграфах 146-151, белка по варианту осуществления в параграфе 152, или клетки по любому из вариантов осуществления 153-159, для производства лекарственного средства для лечения иммунного заболевания или рака.
167. Применение по варианту осуществления в параграфе 166, где лекарственным средством является адоптивная T-клеточная терапия или TCR-генная терапия.
168. Способ лечения субъекта с заболеванием или состоянием, включающий введение субъекту фармацевтической композиции по любому из вариантов осуществления в параграфах 160-164.
169. Способ лечения субъекта с раком, включающий введение субъекту фармацевтической композиции по любому из вариантов осуществления в параграфах 160-164.
170. Способ лечения субъекта с раком включающий введение субъекту фармацевтической композиции по любому из вариантов осуществления в параграфах 160-164; где субъект идентифицирован как экспрессирующий или экспрессирует белок, кодированный HLA-A02:01 аллелью, HLA-B07:02, HLA-B08:01, HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01 аллелью генома субъекта.
171. Способ лечения субъекта с раком включающий введение TCR или T клетку, экспрессирующую TCR, субъекту, где TCR специфически связывается с мутантом RAS пептида в комплексе с белком, кодированным HLA-A02:01, HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01; где субъект идентифицирован как экспрессирующий или экспрессирует белок, кодированный HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01 аллелью, где субъект экспрессирует HLA аллель.
172. Способ лечения субъекта с раком, включающий введение субъекту фармацевтической композиции по любому из вариантов осуществления в параграфах 154-158; где TCR связывается с мутантом RAS пептида, содержащим мутацию на G12 в комплексе с HLA-A02:01. HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01; где субъект идентифицирован как экспрессирующий белок, кодированный HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01 аллелью.
173. Способ лечения субъекта с раком включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR), специфический к мутанту GATA3 пептида в комплексе с HLA белком; где мутант GATA3 пептида содержит, по меньшей мере, одну мутантную аминокислоту и является фрагментом из, по меньшей мере, 8 непрерывных аминокислот мутантного GATA3 белка, возникающего из мутации в GATA3 гене раковой клетки; где мутант GATA3 пептида связывается с белком кодированным HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью.
174. Способ лечения субъекта с раком включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR), специфический к мутанту GATA3 пептида в комплексе с HLA белком; где мутант GATA3 пептида содержит одну или более мутантных GATA3 аминокислот, кодированных GATA3 neoORF последовательностью, где мутант GATA3 пептида связывается с белком кодированным HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью.
175. Способ лечения субъекта с раком включающий введение TCR или T клетки, экспрессирующей TCR, субъекту; где TCR специфически связывается с мутантом GATA3 пептида в комплексе с белком, кодированным HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью; где субъект идентифицирован как экспрессирующий или экспрессирует белок, кодированный HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью.
176. Способ лечения субъекта с раком включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR), специфический к мутанту TMPRSS2:ERG пептида в комплексе с HLA белком; где мутант TMPRSS2:ERG пептида содержит, по меньшей мере, одну мутантную аминокислоту и является фрагментом TMPRSS2:ERG мутации слияния гена; где мутант TMPRSS2:ERG пептида связывается с белком кодированным HLA-A02:01 аллелью.
177. Способ лечения субъекта с раком включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR), специфический к мутанту BTK пептида в комплексе с HLA белком; где мутант BTK пептида содержит, по меньшей мере, одну мутантную аминокислоту; где мутант BTK пептида связывается с белком кодированным HLA-A02:01 аллелью.
178. Способ лечения субъекта с раком включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR), специфический к мутанту BTK пептида в комплексе с HLA белком; где мутант BTK пептида содержит мутацию резистентности или точечную мутацию; где мутант BTK пептида связывается с белком кодированным HLA-A02:01 аллелью.
179. Способ лечения субъекта с раком включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR), специфический к мутанту BTK пептида в комплексе с HLA белком; где мутант BTK пептида содержит C481S мутацию; где мутант BTK пептида связывается с белком кодированным HLA-A02:01 аллелью.
180. Способ лечения субъекта с раком включающий введение субъекту композиции, содержащей Т-клеточный рецептор (TCR) или T клетку, экспрессирующую TCR, субъекту, где TCR специфически связывается с мутантом EGFR пептида в комплексе с белком, кодированным HLA-A02:01; где мутант EGFR пептида содержит мутацию резистентности или точечную мутацию, где субъект идентифицирован как экспрессирующий или экспрессирует белок, кодированный HLA-A02:01 аллелью.
181. Способ по варианту осуществления в параграфе 178, где мутант EGFR пептида содержит T790M мутацию.
182. Способ профилактики резистентности к противораковой терапии, где способ включает введение субъекту, нуждающемуся в этом, фармацевтической композиции по любому из вариантов осуществления в параграфе 160-164.
183. Способ вызова иммунного ответа, где способ включает введение субъекту, нуждающемуся в этом, фармацевтической композиции по любому из вариантов осуществления в параграфах 160-164.
184. Способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как субъекта, который экспрессирует белок, кодированный HLA-A02:01 аллелью, HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01 аллелью, где терапевтическим агентом является фармацевтическая композиция по любому из вариантов осуществления в параграфах 160-164.
185. Способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как экспрессирующего белок, кодированный HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR) специфический к мутанту GATA3 пептида в комплексе с HLA белком; где мутант GATA3 пептид содержит, по меньшей мере, одну мутантную аминокислоту и является фрагментом из, по меньшей мере, 8 непрерывных аминокислот мутанта GATA3 белка, возникающего из мутации в GATA3 гене раковой клетки; где мутант GATA3 пептида связывается с белком кодированным HLA-A02:01, HLA-B07:02 или HLA-B08:01 аллелью.
186. Способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как экспрессирующего белок, кодированный HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR) специфический к мутанту RAS пептида, содержащему мутацию в G12, в комплексе с HLA белком; где мутант RAS пептида связывается с белком, кодированным HLA-A03:01 аллелью, HLA-A11:01 аллелью, HLA-A03:02 аллелью, HLA-A30:01 аллелью, HLA-A31:01 аллелью, HLA-A33:01 аллелью, HLA-A33:03 аллелью, HLA-A68:01 аллелью или HLA-A74:01 аллелью.
187. Способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как экспрессирующего белок, кодированный HLA-A02:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR), специфический к мутанту TMPRSS2:ERG пептида в комплексе с HLA белком; где мутант TMPRSS2:ERG пептида содержит, по меньшей мере, одну мутантную аминокислоту и является фрагментом TMPRSS2:ERG мутации слияния гена; где мутант TMPRSS2:ERG пептида связывается с белком кодированным HLA-A02:01 аллелью.
188. Способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как экспрессирующего белок, кодированный HLA-A02:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR), специфический к мутанту BTK пептида в комплексе с HLA белком; где мутант BTK пептида содержит, по меньшей мере, одну мутантную аминокислоту; где мутант BTK пептида связывается с белком, кодированным HLA-A02:01 аллелью.
189. Способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как экспрессирующего белок, кодированный HLA-A02:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR) специфический к мутанту BTK пептида в комплексе с HLA белком; где мутант BTK пептида содержит мутацию резистентности или точечную мутацию; где мутант BTK пептида связывается с белком, кодированным HLA-A02:01 аллелью.
190. Способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как экспрессирующего белок, кодированный HLA-A02:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR) специфический к мутанту BTK пептида в комплексе с HLA белком; где мутант BTK пептида содержит C481S мутацию; где мутант BTK пептид связывается с белком, кодированным HLA-A02:01 аллелью.
191. Способ идентификации субъекта с раком как кандидата для терапии, где способ включает идентификацию субъекта как экспрессирующего белок, кодированный HLA-A02:01 аллелью, где терапевтический агент содержит Т-клеточный рецептор (TCR) специфический к мутанту EGFR пептида в комплексе с HLA белком; где мутант EGFR пептида содержит, по меньшей мере, одну мутантную аминокислоту T790M; где мутант EGFR пептида связывается с белком кодированным HLA-A02:01 аллелью.
192. Способ по любому из вариантов осуществления в параграфах 162-185, где рак выбран из группы, состоящей из рака груди, рака легкого, немелкоклеточного рака легкого, рака поджелудочной железы, колоректального рака, рака матки, меланомы, рака яичников, рака простаты, рака эндометрия, хронического лимфоцитарного лейкоза (CLL) и рака печени.
193. Способ по любому из вариантов осуществления в параграфах 162-185, где субъект имеет рак груди, резистентный к антиэстрогенной терапии, MSI рак груди, метастатический рак груди, Her2 отрицательный рак груди, Her2 положительный рак груди, ER отрицательный рак груди, ER положительный рак груди, рецидивирующий рак груди, метастатический рак груди, или любую их комбинацию.
194. Способ по варианту 193, где рак груди экспрессирует рецептор эстрогена с мутацией.
195. Способ по любому из вариантов осуществления в параграфах 169-191, где субъект имеет рак груди, резистентный к антиэстрогенной терапии.
196. Способ по варианту осуществления в параграфе 195, где рак груди экспрессирует рецептор эстрогена с мутацией.
197. Способ по любому из вариантов осуществления в параграфах 169-196, где субъект имеет CLL, резистентный к терапиии ибрутинибом.
198. Способ по варианту осуществления в параграфе 197, где CLL экспрессирует тирозинкиназу Брутона (BTK) с мутацией, такой как C481S мутация.
199. Способ по любому из вариантов осуществления в параграфе 169-197, где субъект имеет рак легких, резистентный к ингибитору тирозинкиназы.
200. Способ по варианту осуществления в параграфах 199, где рак легких экспрессирует рецептор фактора роста эпидермиса (EGFR) с мутацией, такой как T790M, L792F, или C797S мутацией.
201. Способ по любому из вариантов осуществления в параграфах 169-200, дополнительно включающий введение, по меньшей мере, одного дополнительного терапевтического агента или метода.
202. Способ по любому из вариантов осуществления в параграфах 168-200, где иммунный ответ вызывается у субъекта.
203. Способ по варианту осуществления в параграфе 200, где иммунным ответом является гуморальный ответ.
204. Способ по варианту осуществления в параграфе 200, где иммунным ответом является ответ цитотоксической T клетки.
205. Способ по любому из вариантов осуществления в параграфах 168-204, дополнительно включающий введение, по меньшей мере, одного дополнительного терапевтического агента или метода.
206. Способ по варианту осуществления в параграфах 205, где, по меньшей мере, одним дополнительным терапевтическим агентом или методом является хирургия, ингибитор иммунной контрольной точки, антитело или его фрагмент, химиотерапевтический агент, облучение, вакцина, малая молекула, Т-клетка, вектор и APC, полинуклеотид, онколитический вирус или любая их комбинация .
207. Способ по варианту осуществления в параграфе 206, где, по меньшей мере, одним дополнительным терапевтическим агентом является анти-PD-1 агент и анти-PD-L1 агент, анти-CTLA-4 агент или анти-CD40 агент.
208. Способ по варианту осуществления в параграфе 206 или 207, где дополнительный терапевтический агент вводят до, одновременно с или после введения фармацевтической композиции по любому из вариантов осуществления 160-164.
209. Способ по любому из вариантов осуществления в параграфах 169-183, или любому из вариантов осуществления в параграфах 201-208, где введение включает подкожное или внутривенное введение.
210. Способ по любому из вариантов осуществления в параграфах 169-209, где субъектом является субъект, который имеет, имел прогрессирование после эндокринной терапии в комбинации с ингибитором CDK 4/6.
211. Способ, включающий:
a. идентификацию неоантигенспецифических Т-клеток из образца, содержащего популяцию T клеток;
b. идентификацию одного или более пептидов комплекса пептид-МНС, который презентирован антигенпрезентирующей клеткой (APC);
c. идентификацию вариабельной последовательности Т-клеточного рецептора (TCR) из неоантигенспецифической Т-клетки;
d. экспрессирование рекомбинантного TCR, содержащего вариабельные последовательности TCR, идентифицированные в TCR клетке; и
e. проведение функционального анализа, где функциональный анализ включает контакт TCR клетки с комплексом пептид-МНС, содержащим пептид из одного или более идентифицированных пептидов.
212. Способ по варианту осуществления в параграфе 211, где способ включает получение образца, содержащего популяцию клеток, содержащих неоантиген-специфические Т-клетки.
213. Способ по варианту осуществления в параграфе 212, где получение образца включает получение образца T клеток от здорового субъекта или от субъекта с раком.
214. Способ по варианту осуществления в параграфе 213, где образец T клетки получен от здорового донора.
215. Способ по варианту осуществления в параграфе 213 или 214, где образец T клетки является образцом мононуклеарной клетки периферической крови (PBMC).
216. Способ по любому из вариантов осуществления в параграфах 211-215, где идентификация неоантиген-специфических Т-клеток содержит контакт популяции T клеток с, по меньшей мере, одним пептид-MHC мультимерным комплексом, содержащим неоантигенный пептид.
217. Способ по любому из вариантов осуществления в параграфах 205-209, где идентификация неоантиген-специфических Т-клеток включает контакт популяции T клеток с комплексом пептид-МНС, содержащим неоантигенный пептид.
218. Способ по варианту осуществления в параграфе 211, где идентификация неоантиген-специфических Т-клеток включает контакт популяции T клеток с APC, содержащими комплекс пептид-МНС.
219. Способ по любому из вариантов осуществления в параграфах 216-218, где идентификация неоантиген-специфических Т-клеток дополнительно включает выделение T клеток из популяции T клеток, специфических к комплексу пептид-МНС.
220. Способ по любому из вариантов осуществления 216-218, где идентификация неоантиген-специфических Т-клеток дополнительно включает идентификацию или прогнозирование T клеток из популяции T клеток, специфических к комплексу пептид-МНС, на основе TCR клональности.
221. Способ по варианту осуществления в параграфах 220, где идентификацию вариабельной последовательности TCR из неоантиген-специфических Т-клеток проводят до идентификации неоантиген-специфических Т-клеток.
222. Способ по любому из вариантов осуществления в параграфах 211-221, где идентификация вариабельной последовательности TCR из неоантиген-специфических Т-клеток включает секвенирование ДНК, РНК или их амплифицированных продуктов из одной или более неоантиген-специфических Т-клеток, которые кодируют вариабельную последовательность.
223. Способ по любому из вариантов осуществления в параграфах 211-222, где идентификация вариабельной последовательности TCR из неоантиген-специфических Т-клеток включает секвенирование ДНК, РНК или их амплифицированных продуктов из одной неоантиген-специфической Т-клетки, которые кодируют вариабельную последовательность.
224. Способ по любому из вариантов осуществления в параграфах 215-223, где идентификация вариабельной последовательности TCR из неоантиген-специфических Т-клеток включает секвенирование штрихкодированной ДНК, штрихкодированной РНК или их амплифицированных продуктов из одной или более неоантиген-специфических Т-клеток, которые кодируют вариабельную последовательность.
225. Способ по любому из вариантов осуществления в параграфах 221-224, где идентификация вариабельной последовательности TCR из неоантиген-специфических Т-клеток включает спаривание TCR-альфа цепи с TCR-бета цепью.
226. Способ по любому из вариантов осуществления в параграфах 211-225, где экспрессирование рекомбинантного TCR включает экспрессирование вариабельной последовательности, идентифицированной из полинуклеотида, содержащего последовательность, кодирующую идентифицированную вариабельную последовательность.
227. Способ по варианту осуществления в параграфе 226, где полинуклеотидом является вектор.
228. Способ по варианту осуществления в параграфе 227, где вектором является вирусный вектор.
229. Способ по варианту осуществления в параграфе 228, где вирусным вектором является лентивирусный вектор.
230. Способ по любому из вариантов осуществления в параграфах 226-229, где экспрессирование рекомбинантного TCR включает трансдукцию или трансфекцию полинуклеотида в клетки.
231. Способ по варианту осуществления в параграфе 230, где клетками являются T клеточная линия или PMBC здорового донора.
232. Способ по любому из вариантов осуществления в параграфах 211-231, где идентификация одного или более пептидов комплекса пептид-МНС, которые представлены АРС, включает экспрессирование одного или более пептидов в клетках.
233. Способ по любому из вариантов осуществления в параграфах 211-231, где идентификация одного или более пептидов комплекса пептид-МНС, которые представлены АРС, включает загрузку одного или более пептидов в MHC клеток.
234. Способ по любому из вариантов осуществления в параграфах 211-233, где идентификация одного или более пептидов комплекса пептид-МНС, которые представлены АРС, включает элюирование и выделение пептида из одного или более пептидов из комплекса пептид-MHC.
235. Способ по любому из вариантов осуществления в параграфах 211-234, где идентификация одного или более пептидов комплекса пептид-МНС, которые представлены АРС, включает проведение масс спектрометрии на пептиде из одного или более пептидов, которые выделены или элюированы из комплекса пептид-МНС.
236. Способ по любому из вариантов осуществления в параграфах 211-235, где проведение функционального анализа включает определение экспрессии одного или более клеточных маркеров.
237. Способ по варианту осуществления в параграфе 236, один или более клеточных маркеров содержат TNF-α, IFN-γ, LAMP-1, 4-1BB, IL-2, IL-17A, Гранзим B, PD-1, CD25, CD69, TIM3, LAG3, CTLA-4, CD62L, CD45RA, CD45RO, FoxP3 или любую из комбинацию.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> NEON THERAPEUTICS, INC.
<120> КОНСТРУКТЫ T-КЛЕТОЧНОГО РЕЦЕПТОРА И ИХ ПРИМЕНЕНИЕ
<130> 50401-726.601
<140> PCT/US2019/046876
<141> 2019-08-16
<150> 62/810,112
<151> 2019-02-25
<150> 62/764,817
<151> 2018-08-16
<160> 621
<170> PatentIn version 3.5
<210> 1
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 1
Ser Ile Phe Asn Thr
1 5
<210> 2
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 2
Leu Tyr Lys Ala Gly Glu Leu
1 5
<210> 3
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 3
Cys Ala Gly Arg Asn Phe Gly Asn Glu Lys Leu Thr Phe
1 5 10
<210> 4
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 4
Asp Phe Gln Ala Thr Thr
1 5
<210> 5
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 5
Ser Asn Glu Gly Ser Lys Ala
1 5
<210> 6
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 6
Ser Ala Arg Asp Arg Gly Leu Val Ser Leu Pro Ser Val Glu Ala Phe
1 5 10 15
Phe
<210> 7
<211> 387
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 7
atgctccttg aacatttatt aataatcttg tggatgcagc tgacatgggt cagtggtcaa
60
cagctgaatc agagtcctca atctatgttt atccaggaag gagaagatgt ctccatgaac
120
tgcacttctt caagcatatt taacacctgg ctatggtaca agcaggaccc tggggaaggt
180
cctgtcctct tgatagcctt atataaggct ggtgaattga cctcaaatgg aagactgact
240
gctcagtttg gtataaccag aaaggacagc ttcctgaata tctcagcatc catacctagt
300
gatgtaggca tctacttctg tgctgggaga aactttggaa atgagaaatt aacctttggg
360
actggaacaa gactcaccat cataccc
387
<210> 8
<211> 387
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 8
atgctccttg aacatttatt aataatcttg tggatgcagc tgacatgggt cagtggtcaa
60
cagctgaatc agagtcctca atctatgttt atccaggaag gagaagatgt ctccatgaac
120
tgcacttctt caagcatatt taacacctgg ctatggtaca agcaggaccc tggggaaggt
180
cctgtcctct tgatagcctt atataaggct ggtgaattga cctcaaatgg aagactgact
240
gctcagtttg gtataaccag aaaggacagc ttcctgaata tctcagcatc catacctagt
300
gatgtaggca tctacttctg tgctgggaga aactttggaa atgagaaatt aacctttggg
360
actggaacaa gactcaccat cataccc
387
<210> 9
<211> 129
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 9
Met Leu Leu Glu His Leu Leu Ile Ile Leu Trp Met Gln Leu Thr Trp
1 5 10 15
Val Ser Gly Gln Gln Leu Asn Gln Ser Pro Gln Ser Met Phe Ile Gln
20 25 30
Glu Gly Glu Asp Val Ser Met Asn Cys Thr Ser Ser Ser Ile Phe Asn
35 40 45
Thr Trp Leu Trp Tyr Lys Gln Asp Pro Gly Glu Gly Pro Val Leu Leu
50 55 60
Ile Ala Leu Tyr Lys Ala Gly Glu Leu Thr Ser Asn Gly Arg Leu Thr
65 70 75 80
Ala Gln Phe Gly Ile Thr Arg Lys Asp Ser Phe Leu Asn Ile Ser Ala
85 90 95
Ser Ile Pro Ser Asp Val Gly Ile Tyr Phe Cys Ala Gly Arg Asn Phe
100 105 110
Gly Asn Glu Lys Leu Thr Phe Gly Thr Gly Thr Arg Leu Thr Ile Ile
115 120 125
Pro
<210> 10
<211> 405
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 10
atgctgctgc ttctgctgct tctggggcca ggctccgggc ttggtgctgt cgtctctcaa
60
catccgagca gggttatctg taagagtgga acctctgtga agatcgagtg ccgttccctg
120
gactttcagg ccacaactat gttttggtat cgtcagttcc cgaaacagag tctcatgctg
180
atggcaactt ccaatgaggg ctccaaggcc acatacgagc aaggcgtcga gaaggacaag
240
tttctcatca accatgcaag cctgaccttg tccactctga cagtgaccag tgcccatcct
300
gaagacagca gcttctacat ctgcagtgct cgcgacaggg ggcttgtatc gttgccgtcg
360
gtagaagctt tctttggaca aggcaccaga ctcacagttg tactg
405
<210> 11
<211> 405
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 11
atgctgctgc ttctgctgct tctggggcca ggctccgggc ttggtgctgt cgtctctcaa
60
catccgagca gggttatctg taagagtgga acctctgtga agatcgagtg ccgttccctg
120
gactttcagg ccacaactat gttttggtat cgtcagttcc cgaaacagag tctcatgctg
180
atggcaactt ccaatgaggg ctccaaggcc acatacgagc aaggcgtcga gaaggacaag
240
tttctcatca accatgcaag cctgaccttg tccactctga cagtgaccag tgcccatcct
300
gaagacagca gcttctacat ctgcagtgct cgcgacaggg ggcttgtatc gttgccgtcg
360
gtagaagctt tctttggaca aggcaccaga ctcacagttg tactg
405
<210> 12
<211> 134
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 12
Met Leu Leu Leu Leu Leu Leu Leu Gly Pro Gly Ser Gly Leu Gly Ala
1 5 10 15
Val Val Ser Gln His Pro Ser Arg Val Ile Cys Lys Ser Gly Thr Ser
20 25 30
Val Lys Ile Glu Cys Arg Ser Leu Asp Phe Gln Ala Thr Thr Met Phe
35 40 45
Trp Tyr Arg Gln Phe Pro Lys Gln Ser Leu Met Leu Met Ala Thr Ser
50 55 60
Asn Glu Gly Ser Lys Ala Thr Tyr Glu Gln Gly Val Glu Lys Asp Lys
65 70 75 80
Phe Leu Ile Asn His Ala Ser Leu Thr Leu Ser Thr Leu Thr Val Thr
85 90 95
Ser Ala His Pro Glu Asp Ser Ser Phe Tyr Ile Cys Ser Ala Arg Asp
100 105 110
Arg Gly Leu Val Ser Leu Pro Ser Val Glu Ala Phe Phe Gly Gln Gly
115 120 125
Thr Arg Leu Thr Val Val
130
<210> 13
<211> 270
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 13
Met Leu Leu Glu His Leu Leu Ile Ile Leu Trp Met Gln Leu Thr Trp
1 5 10 15
Val Ser Gly Gln Gln Leu Asn Gln Ser Pro Gln Ser Met Phe Ile Gln
20 25 30
Glu Gly Glu Asp Val Ser Met Asn Cys Thr Ser Ser Ser Ile Phe Asn
35 40 45
Thr Trp Leu Trp Tyr Lys Gln Asp Pro Gly Glu Gly Pro Val Leu Leu
50 55 60
Ile Ala Leu Tyr Lys Ala Gly Glu Leu Thr Ser Asn Gly Arg Leu Thr
65 70 75 80
Ala Gln Phe Gly Ile Thr Arg Lys Asp Ser Phe Leu Asn Ile Ser Ala
85 90 95
Ser Ile Pro Ser Asp Val Gly Ile Tyr Phe Cys Ala Gly Arg Asn Phe
100 105 110
Gly Asn Glu Lys Leu Thr Phe Gly Thr Gly Thr Arg Leu Thr Ile Ile
115 120 125
Pro Asp Ile Gln Asn Pro Asp Pro Ala Val Tyr Gln Leu Arg Asp Ser
130 135 140
Lys Ser Ser Asp Lys Ser Val Cys Leu Phe Thr Asp Phe Asp Ser Gln
145 150 155 160
Thr Asn Val Ser Gln Ser Lys Asp Ser Asp Val Tyr Ile Thr Asp Lys
165 170 175
Thr Val Leu Asp Met Arg Ser Met Asp Phe Lys Ser Asn Ser Ala Val
180 185 190
Ala Trp Ser Asn Lys Ser Asp Phe Ala Cys Ala Asn Ala Phe Asn Asn
195 200 205
Ser Ile Ile Pro Glu Asp Thr Phe Phe Pro Ser Pro Glu Ser Ser Cys
210 215 220
Asp Val Lys Leu Val Glu Lys Ser Phe Glu Thr Asp Thr Asn Leu Asn
225 230 235 240
Phe Gln Asn Leu Ser Val Ile Gly Phe Arg Ile Leu Leu Leu Lys Val
245 250 255
Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265 270
<210> 14
<211> 312
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 14
Met Leu Leu Leu Leu Leu Leu Leu Gly Pro Gly Ser Gly Leu Gly Ala
1 5 10 15
Val Val Ser Gln His Pro Ser Arg Val Ile Cys Lys Ser Gly Thr Ser
20 25 30
Val Lys Ile Glu Cys Arg Ser Leu Asp Phe Gln Ala Thr Thr Met Phe
35 40 45
Trp Tyr Arg Gln Phe Pro Lys Gln Ser Leu Met Leu Met Ala Thr Ser
50 55 60
Asn Glu Gly Ser Lys Ala Thr Tyr Glu Gln Gly Val Glu Lys Asp Lys
65 70 75 80
Phe Leu Ile Asn His Ala Ser Leu Thr Leu Ser Thr Leu Thr Val Thr
85 90 95
Ser Ala His Pro Glu Asp Ser Ser Phe Tyr Ile Cys Ser Ala Arg Asp
100 105 110
Arg Gly Leu Val Ser Leu Pro Ser Val Glu Ala Phe Phe Gly Gln Gly
115 120 125
Thr Arg Leu Thr Val Val Leu Glu Asp Leu Asn Lys Val Phe Pro Pro
130 135 140
Glu Val Ala Val Phe Glu Pro Ser Glu Ala Glu Ile Ser His Thr Gln
145 150 155 160
Lys Ala Thr Leu Val Cys Leu Ala Thr Gly Phe Phe Pro Asp His Val
165 170 175
Glu Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser
180 185 190
Thr Asp Pro Gln Pro Leu Lys Glu Gln Pro Ala Leu Asn Asp Ser Arg
195 200 205
Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser Ala Thr Phe Trp Gln Asn
210 215 220
Pro Arg Asn His Phe Arg Cys Gln Val Gln Phe Tyr Gly Leu Ser Glu
225 230 235 240
Asn Asp Glu Trp Thr Gln Asp Arg Ala Lys Pro Val Thr Gln Ile Val
245 250 255
Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys Gly Phe Thr Ser Val Ser
260 265 270
Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu
275 280 285
Gly Lys Ala Thr Leu Tyr Ala Val Leu Val Ser Ala Leu Val Leu Met
290 295 300
Ala Met Val Lys Arg Lys Asp Phe
305 310
<210> 15
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 15
Lys Leu Val Val Val Gly Ala Cys Gly Val
1 5 10
<210> 16
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 16
Val Ser Gly Asn Pro Tyr
1 5
<210> 17
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 17
Tyr Ile Thr Gly Asp Asn Leu Val
1 5
<210> 18
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 18
Cys Ala Val Arg Asp Gln Ser Gly Ala Asn Asn Leu Phe Phe
1 5 10
<210> 19
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 19
Ser Glu His Asn Arg
1 5
<210> 20
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 20
Phe Gln Asn Glu Ala Gln
1 5
<210> 21
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 21
Ala Ser Tyr Leu Ser Gly Ser Ile Tyr Asn Glu Gln Phe Phe
1 5 10
<210> 22
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 22
atggcctctg cacccatctc gatgcttgcg atgctcttca cattgagtgg gctgagagct
60
cagtcagtgg ctcagccgga agatcaggtc aacgttgctg aagggaatcc tctgactgtg
120
aaatgcacct attcagtctc tggaaaccct tatctttttt ggtatgttca ataccccaac
180
cgaggcctcc agttccttct gaaatacatc acaggggata acctggttaa aggcagctat
240
ggctttgaag ctgaatttaa caagagccaa acctccttcc acctgaagaa accatctgcc
300
cttgtgagcg actccgcttt gtacttctgt gctgtgagag accaaagtgg ggcaaacaac
360
ctcttctttg ggactggaac gagactcacc gttattccc
399
<210> 23
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 23
atggcttctg cgcctatatc aatgcttgcc atgctgttta cactgtccgg tctgagggct
60
caaagcgtgg cccaacctga ggatcaggtg aatgtagcgg agggcaatcc gttgacagtt
120
aagtgtacat actccgtatc aggcaatccg tacttgtttt ggtatgtgca gtaccccaat
180
cgggggcttc aattcttgct gaagtacatt acaggcgata atctggtaaa aggtagttat
240
ggttttgagg ccgaattcaa caaatcacaa acatcatttc atcttaaaaa gccaagcgca
300
cttgtcagtg actcagcgct ttatttctgt gcagtcagag accaatcagg ggcaaataat
360
ctgttctttg ggacagggac tagattgact gttataccc
399
<210> 24
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 24
Met Ala Ser Ala Pro Ile Ser Met Leu Ala Met Leu Phe Thr Leu Ser
1 5 10 15
Gly Leu Arg Ala Gln Ser Val Ala Gln Pro Glu Asp Gln Val Asn Val
20 25 30
Ala Glu Gly Asn Pro Leu Thr Val Lys Cys Thr Tyr Ser Val Ser Gly
35 40 45
Asn Pro Tyr Leu Phe Trp Tyr Val Gln Tyr Pro Asn Arg Gly Leu Gln
50 55 60
Phe Leu Leu Lys Tyr Ile Thr Gly Asp Asn Leu Val Lys Gly Ser Tyr
65 70 75 80
Gly Phe Glu Ala Glu Phe Asn Lys Ser Gln Thr Ser Phe His Leu Lys
85 90 95
Lys Pro Ser Ala Leu Val Ser Asp Ser Ala Leu Tyr Phe Cys Ala Val
100 105 110
Arg Asp Gln Ser Gly Ala Asn Asn Leu Phe Phe Gly Thr Gly Thr Arg
115 120 125
Leu Thr Val Ile Pro
130
<210> 25
<211> 402
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 25
atgggcacca gcctcctctg ctggatggcc ctgtgtctcc tgggggcaga tcacgcagat
60
actggagtct cccaggaccc cagacacaag atcacaaaga ggggacagaa tgtaactttc
120
aggtgtgatc caatttctga acacaaccgc ctttattggt accgacagac cctggggcag
180
ggcccagagt ttctgactta cttccagaat gaagctcaac tagaaaaatc aaggctgctc
240
agtgatcggt tctctgcaga gaggcctaag ggatctttct ccaccttgga gatccagcgc
300
acagagcagg gggactcggc catgtatctc tgtgccagct acctgagcgg ttccatttac
360
aatgagcagt tcttcgggcc agggacacgg ctcaccgtgc ta
402
<210> 26
<211> 402
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 26
atgggcacta gcctcttgtg ttggatggca ctttgccttc ttggcgcgga tcacgccgat
60
acaggcgtct cccaagatcc cagacataaa atcacaaaac ggggccagaa cgttaccttt
120
cgctgcgatc cgatatcaga gcataatcga ctgtattggt ataggcaaac tctcgggcaa
180
gggcctgagt tcctcactta tttccaaaat gaggcgcaac tggaaaagag ccggttgttg
240
agtgataggt tttccgcaga gcgacccaag gggagcttct caacactgga gatacaaagg
300
accgaacaag gtgattccgc aatgtatctc tgtgctagtt atttgagcgg ctccatatat
360
aacgaacagt ttttcggacc gggcactcgc ctgaccgtac ta
402
<210> 27
<211> 134
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 27
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Tyr Leu Ser Gly Ser Ile Tyr Asn Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu
130
<210> 28
<211> 274
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 28
Met Ala Ser Ala Pro Ile Ser Met Leu Ala Met Leu Phe Thr Leu Ser
1 5 10 15
Gly Leu Arg Ala Gln Ser Val Ala Gln Pro Glu Asp Gln Val Asn Val
20 25 30
Ala Glu Gly Asn Pro Leu Thr Val Lys Cys Thr Tyr Ser Val Ser Gly
35 40 45
Asn Pro Tyr Leu Phe Trp Tyr Val Gln Tyr Pro Asn Arg Gly Leu Gln
50 55 60
Phe Leu Leu Lys Tyr Ile Thr Gly Asp Asn Leu Val Lys Gly Ser Tyr
65 70 75 80
Gly Phe Glu Ala Glu Phe Asn Lys Ser Gln Thr Ser Phe His Leu Lys
85 90 95
Lys Pro Ser Ala Leu Val Ser Asp Ser Ala Leu Tyr Phe Cys Ala Val
100 105 110
Arg Asp Gln Ser Gly Ala Asn Asn Leu Phe Phe Gly Thr Gly Thr Arg
115 120 125
Leu Thr Val Ile Pro Asp Ile Gln Asn Pro Asp Pro Ala Val Tyr Gln
130 135 140
Leu Arg Asp Ser Lys Ser Ser Asp Lys Ser Val Cys Leu Phe Thr Asp
145 150 155 160
Phe Asp Ser Gln Thr Asn Val Ser Gln Ser Lys Asp Ser Asp Val Tyr
165 170 175
Ile Thr Asp Lys Thr Val Leu Asp Met Arg Ser Met Asp Phe Lys Ser
180 185 190
Asn Ser Ala Val Ala Trp Ser Asn Lys Ser Asp Phe Ala Cys Ala Asn
195 200 205
Ala Phe Asn Asn Ser Ile Ile Pro Glu Asp Thr Phe Phe Pro Ser Pro
210 215 220
Glu Ser Ser Cys Asp Val Lys Leu Val Glu Lys Ser Phe Glu Thr Asp
225 230 235 240
Thr Asn Leu Asn Phe Gln Asn Leu Ser Val Ile Gly Phe Arg Ile Leu
245 250 255
Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp
260 265 270
Ser Ser
<210> 29
<211> 311
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 29
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Tyr Leu Ser Gly Ser Ile Tyr Asn Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu Glu Asp Leu Asn Lys Val Phe Pro Pro Glu
130 135 140
Val Ala Val Phe Glu Pro Ser Glu Ala Glu Ile Ser His Thr Gln Lys
145 150 155 160
Ala Thr Leu Val Cys Leu Ala Thr Gly Phe Phe Pro Asp His Val Glu
165 170 175
Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr
180 185 190
Asp Pro Gln Pro Leu Lys Glu Gln Pro Ala Leu Asn Asp Ser Arg Tyr
195 200 205
Cys Leu Ser Ser Arg Leu Arg Val Ser Ala Thr Phe Trp Gln Asn Pro
210 215 220
Arg Asn His Phe Arg Cys Gln Val Gln Phe Tyr Gly Leu Ser Glu Asn
225 230 235 240
Asp Glu Trp Thr Gln Asp Arg Ala Lys Pro Val Thr Gln Ile Val Ser
245 250 255
Ala Glu Ala Trp Gly Arg Ala Asp Cys Gly Phe Thr Ser Val Ser Tyr
260 265 270
Gln Gln Gly Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly
275 280 285
Lys Ala Thr Leu Tyr Ala Val Leu Val Ser Ala Leu Val Leu Met Ala
290 295 300
Met Val Lys Arg Lys Asp Phe
305 310
<210> 30
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 30
Leu Val Val Val Gly Ala Cys Gly Val
1 5
<210> 31
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 31
Asn Ser Met Phe Asp Tyr
1 5
<210> 32
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 32
Ile Ser Ser Ile Lys Asp Lys
1 5
<210> 33
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 33
Ala Ala Ser Gly Gly Gly Gly Ala Asp Gly Leu Thr
1 5 10
<210> 34
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 34
Met Asn His Asn Tyr
1 5
<210> 35
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 35
Ser Val Gly Ala Gly Ile
1 5
<210> 36
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 36
Ala Ser Ser Tyr Ser Thr Glu Arg Gly Thr Ile Tyr
1 5 10
<210> 37
<211> 417
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 37
atggccatgc tcctgggggc atcagtgctg attctgtggc ttcagccaga ctgggtaaac
60
agtcaacaga agaatgatga ccagcaagtt aagcaaaatt caccatccct gagcgtccag
120
gaaggaagaa tttctattct gaactgtgac tatactaaca gcatgtttga ttatttccta
180
tggtacaaaa aataccctgc tgaaggtcct acattcctga tatctataag ttccattaag
240
gataaaaatg aagatggaag attcactgtc ttcttaaaca aaagtgccaa gcacctctct
300
ctgcacattg tgccctccca gcctggagac tctgcagtgt acttctgtgc agcaagcggg
360
ggaggaggtg ctgacggact cacctttggc aaagggactc atctaatcat ccagccc
417
<210> 38
<211> 417
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 38
atggccatgc tgctgggcgc cagcgtgctg attttatggc tgcagcccga ctgggtgaac
60
agccagcaga agaacgacga ccagcaagtg aagcagaact ccccttcttt aagcgtgcaa
120
gaaggtcgta tcagcatttt aaactgcgac tacaccaaca gcatgttcga ctacttttta
180
tggtacaaga agtaccccgc cgagggcccc acctttttaa tcagcatcag cagcatcaag
240
gacaagaacg aggacggtcg tttcaccgtg tttttaaaca agagcgccaa gcatttatct
300
ttacacatcg tgccctccca gcccggtgat agcgccgtgt acttctgcgc cgccagcgga
360
ggaggaggcg ccgatggact gaccttcggc aagggcaccc atttaatcat ccagccc
417
<210> 39
<211> 139
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 39
Met Ala Met Leu Leu Gly Ala Ser Val Leu Ile Leu Trp Leu Gln Pro
1 5 10 15
Asp Trp Val Asn Ser Gln Gln Lys Asn Asp Asp Gln Gln Val Lys Gln
20 25 30
Asn Ser Pro Ser Leu Ser Val Gln Glu Gly Arg Ile Ser Ile Leu Asn
35 40 45
Cys Asp Tyr Thr Asn Ser Met Phe Asp Tyr Phe Leu Trp Tyr Lys Lys
50 55 60
Tyr Pro Ala Glu Gly Pro Thr Phe Leu Ile Ser Ile Ser Ser Ile Lys
65 70 75 80
Asp Lys Asn Glu Asp Gly Arg Phe Thr Val Phe Leu Asn Lys Ser Ala
85 90 95
Lys His Leu Ser Leu His Ile Val Pro Ser Gln Pro Gly Asp Ser Ala
100 105 110
Val Tyr Phe Cys Ala Ala Ser Gly Gly Gly Gly Ala Asp Gly Leu Thr
115 120 125
Phe Gly Lys Gly Thr His Leu Ile Ile Gln Pro
130 135
<210> 40
<211> 486
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 40
atgaggtctc agaatgactt ccttgagagt cctgttcccc tttcatcaat gcacagatac
60
agaagacccc tccgtcctgg agcacctgcc atgagcatca gcctcctgtg ctgtgcagcc
120
tttcctctcc tgtgggcagg tccagtgaat gctggtgtca ctcagacccc aaaattccgc
180
atcctgaaga taggacagag catgacactg cagtgtaccc aggatatgaa ccataactac
240
atgtactggt atcgacaaga cccaggcatg gggctgaagc tgatttatta ttcagttggt
300
gctggtatca ctgataaagg agaagtcccg aatggctaca acgtctccag atcaaccaca
360
gaggatttcc cgctcaggct ggagttggct gctccctccc agacatctgt gtacttctgt
420
gccagcagtt actcgacgga acgcgggacc atatattttg gagagggaag ttggctcact
480
gttgta
486
<210> 41
<211> 486
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 41
atgaggagcc agaacgactt tttagagagc cccgtgcctc tgagcagcat gcataggtat
60
aggaggcctc tgagacccgg tgcccccgct atgagcatct ctttactgtg ctgtgctgcc
120
tttcctttac tgtgggctgg ccccgttaac gctggcgtga cccagacccc caagtttagg
180
attttaaaga tcggccagtc catgacttta cagtgcaccc aagatatgaa ccacaactac
240
atgtactggt atcgtcaaga tcccggcatg ggtttaaagc tgatttacta cagcgtggga
300
gccggcatca ccgacaaggg cgaggtgccc aacggctaca atgtgtctcg tagcaccacc
360
gaggacttcc ctctgagact ggagctggcc gcccctagcc agacaagcgt gtacttctgc
420
gcctcctcct acagcaccga gaggggcacc atctacttcg gcgagggcag ctggctgacc
480
gtggtg
486
<210> 42
<211> 162
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 42
Met Arg Ser Gln Asn Asp Phe Leu Glu Ser Pro Val Pro Leu Ser Ser
1 5 10 15
Met His Arg Tyr Arg Arg Pro Leu Arg Pro Gly Ala Pro Ala Met Ser
20 25 30
Ile Ser Leu Leu Cys Cys Ala Ala Phe Pro Leu Leu Trp Ala Gly Pro
35 40 45
Val Asn Ala Gly Val Thr Gln Thr Pro Lys Phe Arg Ile Leu Lys Ile
50 55 60
Gly Gln Ser Met Thr Leu Gln Cys Thr Gln Asp Met Asn His Asn Tyr
65 70 75 80
Met Tyr Trp Tyr Arg Gln Asp Pro Gly Met Gly Leu Lys Leu Ile Tyr
85 90 95
Tyr Ser Val Gly Ala Gly Ile Thr Asp Lys Gly Glu Val Pro Asn Gly
100 105 110
Tyr Asn Val Ser Arg Ser Thr Thr Glu Asp Phe Pro Leu Arg Leu Glu
115 120 125
Leu Ala Ala Pro Ser Gln Thr Ser Val Tyr Phe Cys Ala Ser Ser Tyr
130 135 140
Ser Thr Glu Arg Gly Thr Ile Tyr Phe Gly Glu Gly Ser Trp Leu Thr
145 150 155 160
Val Val
<210> 43
<211> 280
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 43
Met Ala Met Leu Leu Gly Ala Ser Val Leu Ile Leu Trp Leu Gln Pro
1 5 10 15
Asp Trp Val Asn Ser Gln Gln Lys Asn Asp Asp Gln Gln Val Lys Gln
20 25 30
Asn Ser Pro Ser Leu Ser Val Gln Glu Gly Arg Ile Ser Ile Leu Asn
35 40 45
Cys Asp Tyr Thr Asn Ser Met Phe Asp Tyr Phe Leu Trp Tyr Lys Lys
50 55 60
Tyr Pro Ala Glu Gly Pro Thr Phe Leu Ile Ser Ile Ser Ser Ile Lys
65 70 75 80
Asp Lys Asn Glu Asp Gly Arg Phe Thr Val Phe Leu Asn Lys Ser Ala
85 90 95
Lys His Leu Ser Leu His Ile Val Pro Ser Gln Pro Gly Asp Ser Ala
100 105 110
Val Tyr Phe Cys Ala Ala Ser Gly Gly Gly Gly Ala Asp Gly Leu Thr
115 120 125
Phe Gly Lys Gly Thr His Leu Ile Ile Gln Pro Asp Ile Gln Asn Pro
130 135 140
Asp Pro Ala Val Tyr Gln Leu Arg Asp Ser Lys Ser Ser Asp Lys Ser
145 150 155 160
Val Cys Leu Phe Thr Asp Phe Asp Ser Gln Thr Asn Val Ser Gln Ser
165 170 175
Lys Asp Ser Asp Val Tyr Ile Thr Asp Lys Thr Val Leu Asp Met Arg
180 185 190
Ser Met Asp Phe Lys Ser Asn Ser Ala Val Ala Trp Ser Asn Lys Ser
195 200 205
Asp Phe Ala Cys Ala Asn Ala Phe Asn Asn Ser Ile Ile Pro Glu Asp
210 215 220
Thr Phe Phe Pro Ser Pro Glu Ser Ser Cys Asp Val Lys Leu Val Glu
225 230 235 240
Lys Ser Phe Glu Thr Asp Thr Asn Leu Asn Phe Gln Asn Leu Ser Val
245 250 255
Ile Gly Phe Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu
260 265 270
Met Thr Leu Arg Leu Trp Ser Ser
275 280
<210> 44
<211> 339
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 44
Met Arg Ser Gln Asn Asp Phe Leu Glu Ser Pro Val Pro Leu Ser Ser
1 5 10 15
Met His Arg Tyr Arg Arg Pro Leu Arg Pro Gly Ala Pro Ala Met Ser
20 25 30
Ile Ser Leu Leu Cys Cys Ala Ala Phe Pro Leu Leu Trp Ala Gly Pro
35 40 45
Val Asn Ala Gly Val Thr Gln Thr Pro Lys Phe Arg Ile Leu Lys Ile
50 55 60
Gly Gln Ser Met Thr Leu Gln Cys Thr Gln Asp Met Asn His Asn Tyr
65 70 75 80
Met Tyr Trp Tyr Arg Gln Asp Pro Gly Met Gly Leu Lys Leu Ile Tyr
85 90 95
Tyr Ser Val Gly Ala Gly Ile Thr Asp Lys Gly Glu Val Pro Asn Gly
100 105 110
Tyr Asn Val Ser Arg Ser Thr Thr Glu Asp Phe Pro Leu Arg Leu Glu
115 120 125
Leu Ala Ala Pro Ser Gln Thr Ser Val Tyr Phe Cys Ala Ser Ser Tyr
130 135 140
Ser Thr Glu Arg Gly Thr Ile Tyr Phe Gly Glu Gly Ser Trp Leu Thr
145 150 155 160
Val Val Glu Asp Leu Asn Lys Val Phe Pro Pro Glu Val Ala Val Phe
165 170 175
Glu Pro Ser Glu Ala Glu Ile Ser His Thr Gln Lys Ala Thr Leu Val
180 185 190
Cys Leu Ala Thr Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp
195 200 205
Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln Pro
210 215 220
Leu Lys Glu Gln Pro Ala Leu Asn Asp Ser Arg Tyr Cys Leu Ser Ser
225 230 235 240
Arg Leu Arg Val Ser Ala Thr Phe Trp Gln Asn Pro Arg Asn His Phe
245 250 255
Arg Cys Gln Val Gln Phe Tyr Gly Leu Ser Glu Asn Asp Glu Trp Thr
260 265 270
Gln Asp Arg Ala Lys Pro Val Thr Gln Ile Val Ser Ala Glu Ala Trp
275 280 285
Gly Arg Ala Asp Cys Gly Phe Thr Ser Val Ser Tyr Gln Gln Gly Val
290 295 300
Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu
305 310 315 320
Tyr Ala Val Leu Val Ser Ala Leu Val Leu Met Ala Met Val Lys Arg
325 330 335
Lys Asp Phe
<210> 45
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 45
Val Val Gly Ala Val Gly Val Gly Lys
1 5
<210> 46
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 46
Val Val Val Gly Ala Val Gly Val Gly Lys
1 5 10
<210> 47
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 47
Thr Ser Ile Asn Asn
1 5
<210> 48
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 48
Ile Arg Ser Asn Glu Arg Glu
1 5
<210> 49
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 49
Ala Thr Asp Arg Gln Ser Ser Gly Asp Lys Leu Thr
1 5 10
<210> 50
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 50
Ser Gly His Ala Thr
1 5
<210> 51
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 51
Phe Gln Asn Asn Gly Val
1 5
<210> 52
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 52
Ala Ser Ser Leu Ala Asp Ile Tyr Glu Gln Tyr
1 5 10
<210> 53
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 53
atggaaactc tcctgggagt gtctttggtg attctatggc ttcaactggc tagggtgaac
60
agtcaacagg gagaagagga tcctcaggcc ttgagcatcc aggagggtga aaatgccacc
120
atgaactgca gttacaaaac tagtataaac aatttacagt ggtatagaca aaattcaggt
180
agaggccttg tccacctaat tttaatacgt tcaaatgaaa gagagaaaca cagtggaaga
240
ttaagagtca cgcttgacac ttccaagaaa agcagttcct tgttgatcac ggcttcccgg
300
gcagcagaca ctgcttctta cttctgtgct acggaccgtc aaagcagcgg agacaagctg
360
acttttggga ccgggactcg tttagcagtt aggccc
396
<210> 54
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 54
atggagactt tactgggcgt gtctttagtg attttatggc tgcagctggc tcgtgtgaat
60
agccagcaag gtgaagagga cccccaagct ttaagcatcc aagaaggcga gaacgccacc
120
atgaactgct cctacaagac cagcatcaac aatttacagt ggtatcgtca gaacagcggt
180
cgtggtttag tgcatttaat tttaattcgt agcaacgaga gggagaagca cagcggtcgt
240
ctgagggtga ctttagacac cagcaagaag agcagctctt tactgatcac agcctctagg
300
gccgctgaca ccgctagcta cttctgcgcc accgacagac agagcagcgg cgacaagctg
360
accttcggca ccggcacaag actggccgtg agaccc
396
<210> 55
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 55
Met Glu Thr Leu Leu Gly Val Ser Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ala Arg Val Asn Ser Gln Gln Gly Glu Glu Asp Pro Gln Ala Leu Ser
20 25 30
Ile Gln Glu Gly Glu Asn Ala Thr Met Asn Cys Ser Tyr Lys Thr Ser
35 40 45
Ile Asn Asn Leu Gln Trp Tyr Arg Gln Asn Ser Gly Arg Gly Leu Val
50 55 60
His Leu Ile Leu Ile Arg Ser Asn Glu Arg Glu Lys His Ser Gly Arg
65 70 75 80
Leu Arg Val Thr Leu Asp Thr Ser Lys Lys Ser Ser Ser Leu Leu Ile
85 90 95
Thr Ala Ser Arg Ala Ala Asp Thr Ala Ser Tyr Phe Cys Ala Thr Asp
100 105 110
Arg Gln Ser Ser Gly Asp Lys Leu Thr Phe Gly Thr Gly Thr Arg Leu
115 120 125
Ala Val Arg Pro
130
<210> 56
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 56
atgggcacca ggctcctctg ctgggcggcc ctctgtctcc tgggagcaga actcacagaa
60
gctggagttg cccagtctcc cagatataag attatagaga aaaggcagag tgtggctttt
120
tggtgcaatc ctatatctgg ccatgctacc ctttactggt accagcagat cctgggacag
180
ggcccaaagc ttctgattca gtttcagaat aacggtgtag tggatgattc acagttgcct
240
aaggatcgat tttctgcaga gaggctcaaa ggagtagact ccactctcaa gatccagcct
300
gcaaagcttg aggactcggc cgtgtatctc tgtgccagca gcttagccga catctacgag
360
cagtacttcg ggccgggcac caggctcacg gtcaca
396
<210> 57
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 57
atgggcacca gactgctgtg ctgggccgct ctgtgtctgc tgggcgctga gctgacagaa
60
gctggcgtgg cccagagccc tcgttacaag atcatcgaga agaggcagag cgtggccttc
120
tggtgcaacc ccatcagcgg ccacgccact ttatactggt accagcagat tttaggccaa
180
ggtcccaagc tgctgatcca gttccagaac aacggcgtgg tggacgacag ccagctgccc
240
aaggatcgtt tcagcgccga gaggctgaag ggcgtggaca gcactttaaa aatccagccc
300
gctaagctgg aggacagcgc cgtgtattta tgcgctagct ctttagccga catctacgag
360
cagtacttcg gccccggcac tcgtctgacc gtgacc
396
<210> 58
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 58
Met Gly Thr Arg Leu Leu Cys Trp Ala Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Glu Leu Thr Glu Ala Gly Val Ala Gln Ser Pro Arg Tyr Lys Ile Ile
20 25 30
Glu Lys Arg Gln Ser Val Ala Phe Trp Cys Asn Pro Ile Ser Gly His
35 40 45
Ala Thr Leu Tyr Trp Tyr Gln Gln Ile Leu Gly Gln Gly Pro Lys Leu
50 55 60
Leu Ile Gln Phe Gln Asn Asn Gly Val Val Asp Asp Ser Gln Leu Pro
65 70 75 80
Lys Asp Arg Phe Ser Ala Glu Arg Leu Lys Gly Val Asp Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ala Lys Leu Glu Asp Ser Ala Val Tyr Leu Cys Ala
100 105 110
Ser Ser Leu Ala Asp Ile Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Thr
130
<210> 59
<211> 273
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 59
Met Glu Thr Leu Leu Gly Val Ser Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ala Arg Val Asn Ser Gln Gln Gly Glu Glu Asp Pro Gln Ala Leu Ser
20 25 30
Ile Gln Glu Gly Glu Asn Ala Thr Met Asn Cys Ser Tyr Lys Thr Ser
35 40 45
Ile Asn Asn Leu Gln Trp Tyr Arg Gln Asn Ser Gly Arg Gly Leu Val
50 55 60
His Leu Ile Leu Ile Arg Ser Asn Glu Arg Glu Lys His Ser Gly Arg
65 70 75 80
Leu Arg Val Thr Leu Asp Thr Ser Lys Lys Ser Ser Ser Leu Leu Ile
85 90 95
Thr Ala Ser Arg Ala Ala Asp Thr Ala Ser Tyr Phe Cys Ala Thr Asp
100 105 110
Arg Gln Ser Ser Gly Asp Lys Leu Thr Phe Gly Thr Gly Thr Arg Leu
115 120 125
Ala Val Arg Pro Asp Ile Gln Asn Pro Asp Pro Ala Val Tyr Gln Leu
130 135 140
Arg Asp Ser Lys Ser Ser Asp Lys Ser Val Cys Leu Phe Thr Asp Phe
145 150 155 160
Asp Ser Gln Thr Asn Val Ser Gln Ser Lys Asp Ser Asp Val Tyr Ile
165 170 175
Thr Asp Lys Thr Val Leu Asp Met Arg Ser Met Asp Phe Lys Ser Asn
180 185 190
Ser Ala Val Ala Trp Ser Asn Lys Ser Asp Phe Ala Cys Ala Asn Ala
195 200 205
Phe Asn Asn Ser Ile Ile Pro Glu Asp Thr Phe Phe Pro Ser Pro Glu
210 215 220
Ser Ser Cys Asp Val Lys Leu Val Glu Lys Ser Phe Glu Thr Asp Thr
225 230 235 240
Asn Leu Asn Phe Gln Asn Leu Ser Val Ile Gly Phe Arg Ile Leu Leu
245 250 255
Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser
260 265 270
Ser
<210> 60
<211> 309
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 60
Met Gly Thr Arg Leu Leu Cys Trp Ala Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Glu Leu Thr Glu Ala Gly Val Ala Gln Ser Pro Arg Tyr Lys Ile Ile
20 25 30
Glu Lys Arg Gln Ser Val Ala Phe Trp Cys Asn Pro Ile Ser Gly His
35 40 45
Ala Thr Leu Tyr Trp Tyr Gln Gln Ile Leu Gly Gln Gly Pro Lys Leu
50 55 60
Leu Ile Gln Phe Gln Asn Asn Gly Val Val Asp Asp Ser Gln Leu Pro
65 70 75 80
Lys Asp Arg Phe Ser Ala Glu Arg Leu Lys Gly Val Asp Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ala Lys Leu Glu Asp Ser Ala Val Tyr Leu Cys Ala
100 105 110
Ser Ser Leu Ala Asp Ile Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Thr Glu Asp Leu Asn Lys Val Phe Pro Pro Glu Val Ala
130 135 140
Val Phe Glu Pro Ser Glu Ala Glu Ile Ser His Thr Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Thr Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro
180 185 190
Gln Pro Leu Lys Glu Gln Pro Ala Leu Asn Asp Ser Arg Tyr Cys Leu
195 200 205
Ser Ser Arg Leu Arg Val Ser Ala Thr Phe Trp Gln Asn Pro Arg Asn
210 215 220
His Phe Arg Cys Gln Val Gln Phe Tyr Gly Leu Ser Glu Asn Asp Glu
225 230 235 240
Trp Thr Gln Asp Arg Ala Lys Pro Val Thr Gln Ile Val Ser Ala Glu
245 250 255
Ala Trp Gly Arg Ala Asp Cys Gly Phe Thr Ser Val Ser Tyr Gln Gln
260 265 270
Gly Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala
275 280 285
Thr Leu Tyr Ala Val Leu Val Ser Ala Leu Val Leu Met Ala Met Val
290 295 300
Lys Arg Lys Asp Phe
305
<210> 61
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 61
Val Val Gly Ala Val Gly Val Gly Lys
1 5
<210> 62
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 62
Val Val Val Gly Ala Val Gly Val Gly Lys
1 5 10
<210> 63
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 63
Thr Ser Gly Phe Asn Gly
1 5
<210> 64
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 64
Asn Val Leu Asp Gly Leu
1 5
<210> 65
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 65
Cys Ala Pro Gly Asp Asn Phe Asn Lys Phe Tyr Phe
1 5 10
<210> 66
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 66
Ser Gly His Arg Ser
1 5
<210> 67
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 67
Tyr Phe Ser Glu Thr Gln
1 5
<210> 68
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 68
Cys Ala Ser Ser Ala Arg Asn Asp Glu Ala Phe Phe
1 5 10
<210> 69
<211> 378
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 69
atgtggggag ttttccttct ttatgtttcc atgaagatgg gaggcactac aggacaaaac
60
attgaccagc ccactgagat gacagctacg gaaggtgcca ttgtccagat caactgcacg
120
taccagacat ctgggttcaa cgggctgttc tggtaccagc aacatgctgg cgaagcaccc
180
acatttctgt cttacaatgt tctggatggt ttggaggaga aaggtcgttt ttcttcattc
240
cttagtcggt ctaaagggta cagttacctc cttttgaagg agctccagat gaaagactct
300
gcctcttacc tctgtgctcc cggggacaac ttcaacaaat tttactttgg atctgggacc
360
aaactcaatg taaaacca
378
<210> 70
<211> 378
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 70
atgtggggcg tgtttctgct gtacgtgtcc atgaagatgg gcggcaccac aggccagaac
60
atcgaccagc caaccgagat gaccgccaca gagggcgcca tcgtgcagat caactgcacc
120
taccagacat ctggcttcaa tggcctgttt tggtatcagc agcacgcagg agaggcaccc
180
acattcctga gctataatgt gctggatggc ctggaggaga agggcaggtt ctcctctttt
240
ctgtctcgca gcaagggcta ctcctatctg ctgctgaagg agctgcagat gaaggactcc
300
gcctcttacc tgtgcgcccc tggcgataac tttaataagt tctatttcgg ctctggcacc
360
aagctgaatg tgaagcca
378
<210> 71
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 71
Met Trp Gly Val Phe Leu Leu Tyr Val Ser Met Lys Met Gly Gly Thr
1 5 10 15
Thr Gly Gln Asn Ile Asp Gln Pro Thr Glu Met Thr Ala Thr Glu Gly
20 25 30
Ala Ile Val Gln Ile Asn Cys Thr Tyr Gln Thr Ser Gly Phe Asn Gly
35 40 45
Leu Phe Trp Tyr Gln Gln His Ala Gly Glu Ala Pro Thr Phe Leu Ser
50 55 60
Tyr Asn Val Leu Asp Gly Leu Glu Glu Lys Gly Arg Phe Ser Ser Phe
65 70 75 80
Leu Ser Arg Ser Lys Gly Tyr Ser Tyr Leu Leu Leu Lys Glu Leu Gln
85 90 95
Met Lys Asp Ser Ala Ser Tyr Leu Cys Ala Pro Gly Asp Asn Phe Asn
100 105 110
Lys Phe Tyr Phe Gly Ser Gly Thr Lys Leu Asn Val Lys Pro
115 120 125
<210> 72
<211> 390
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 72
atgggctcca ggctgctctg ttgggtgctg ctttgtctcc tgggagcagg cccagtaaag
60
gctggagtca ctcaaactcc aagatatctg atcaaaacga gaggacagca agtgacactg
120
agctgctccc ctatctctgg gcataggagt gtatcctggt accaacagac cccaggacag
180
ggccttcagt tcctctttga atacttcagt gagacacaga gaaacaaagg aaacttccct
240
ggtcgattct cagggcgcca gttctctaac tctcgctctg agatgaatgt gagcaccttg
300
gagctggggg actcggccct ttatctttgc gccagcagcg cgagaaatga tgaagctttc
360
tttggacaag gcaccagact cacagttgta
390
<210> 73
<211> 390
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 73
atgggcagcc ggctgctgtg ctgggtgctg ctgtgcctgc tgggagcagg accagtgaag
60
gcaggcgtga cccagacacc tcggtacctg atcaagacca gaggccagca ggtgacactg
120
agctgctccc caatctccgg ccacagatct gtgagctggt accagcagac cccaggacag
180
ggactgcagt tcctgtttga gtatttctcc gagacacaga ggaacaaggg caatttccct
240
ggccggtttt ctggcagaca gttttccaac tctcgcagcg agatgaatgt gagcaccctg
300
gagctgggcg actccgccct gtacctgtgc gccagctccg ccaggaacga tgaggccttc
360
tttggccagg gcacccggct gacagtggtg
390
<210> 74
<211> 130
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 74
Met Gly Ser Arg Leu Leu Cys Trp Val Leu Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Val Lys Ala Gly Val Thr Gln Thr Pro Arg Tyr Leu Ile Lys
20 25 30
Thr Arg Gly Gln Gln Val Thr Leu Ser Cys Ser Pro Ile Ser Gly His
35 40 45
Arg Ser Val Ser Trp Tyr Gln Gln Thr Pro Gly Gln Gly Leu Gln Phe
50 55 60
Leu Phe Glu Tyr Phe Ser Glu Thr Gln Arg Asn Lys Gly Asn Phe Pro
65 70 75 80
Gly Arg Phe Ser Gly Arg Gln Phe Ser Asn Ser Arg Ser Glu Met Asn
85 90 95
Val Ser Thr Leu Glu Leu Gly Asp Ser Ala Leu Tyr Leu Cys Ala Ser
100 105 110
Ser Ala Arg Asn Asp Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr
115 120 125
Val Val
130
<210> 75
<211> 267
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 75
Met Trp Gly Val Phe Leu Leu Tyr Val Ser Met Lys Met Gly Gly Thr
1 5 10 15
Thr Gly Gln Asn Ile Asp Gln Pro Thr Glu Met Thr Ala Thr Glu Gly
20 25 30
Ala Ile Val Gln Ile Asn Cys Thr Tyr Gln Thr Ser Gly Phe Asn Gly
35 40 45
Leu Phe Trp Tyr Gln Gln His Ala Gly Glu Ala Pro Thr Phe Leu Ser
50 55 60
Tyr Asn Val Leu Asp Gly Leu Glu Glu Lys Gly Arg Phe Ser Ser Phe
65 70 75 80
Leu Ser Arg Ser Lys Gly Tyr Ser Tyr Leu Leu Leu Lys Glu Leu Gln
85 90 95
Met Lys Asp Ser Ala Ser Tyr Leu Cys Ala Pro Gly Asp Asn Phe Asn
100 105 110
Lys Phe Tyr Phe Gly Ser Gly Thr Lys Leu Asn Val Lys Pro Asp Ile
115 120 125
Gln Asn Pro Asp Pro Ala Val Tyr Gln Leu Arg Asp Ser Lys Ser Ser
130 135 140
Asp Lys Ser Val Cys Leu Phe Thr Asp Phe Asp Ser Gln Thr Asn Val
145 150 155 160
Ser Gln Ser Lys Asp Ser Asp Val Tyr Ile Thr Asp Lys Thr Val Leu
165 170 175
Asp Met Arg Ser Met Asp Phe Lys Ser Asn Ser Ala Val Ala Trp Ser
180 185 190
Asn Lys Ser Asp Phe Ala Cys Ala Asn Ala Phe Asn Asn Ser Ile Ile
195 200 205
Pro Glu Asp Thr Phe Phe Pro Ser Pro Glu Ser Ser Cys Asp Val Lys
210 215 220
Leu Val Glu Lys Ser Phe Glu Thr Asp Thr Asn Leu Asn Phe Gln Asn
225 230 235 240
Leu Ser Val Ile Gly Phe Arg Ile Leu Leu Leu Lys Val Ala Gly Phe
245 250 255
Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 76
<211> 307
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 76
Met Gly Ser Arg Leu Leu Cys Trp Val Leu Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Val Lys Ala Gly Val Thr Gln Thr Pro Arg Tyr Leu Ile Lys
20 25 30
Thr Arg Gly Gln Gln Val Thr Leu Ser Cys Ser Pro Ile Ser Gly His
35 40 45
Arg Ser Val Ser Trp Tyr Gln Gln Thr Pro Gly Gln Gly Leu Gln Phe
50 55 60
Leu Phe Glu Tyr Phe Ser Glu Thr Gln Arg Asn Lys Gly Asn Phe Pro
65 70 75 80
Gly Arg Phe Ser Gly Arg Gln Phe Ser Asn Ser Arg Ser Glu Met Asn
85 90 95
Val Ser Thr Leu Glu Leu Gly Asp Ser Ala Leu Tyr Leu Cys Ala Ser
100 105 110
Ser Ala Arg Asn Asp Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr
115 120 125
Val Val Glu Asp Leu Asn Lys Val Phe Pro Pro Glu Val Ala Val Phe
130 135 140
Glu Pro Ser Glu Ala Glu Ile Ser His Thr Gln Lys Ala Thr Leu Val
145 150 155 160
Cys Leu Ala Thr Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp
165 170 175
Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln Pro
180 185 190
Leu Lys Glu Gln Pro Ala Leu Asn Asp Ser Arg Tyr Cys Leu Ser Ser
195 200 205
Arg Leu Arg Val Ser Ala Thr Phe Trp Gln Asn Pro Arg Asn His Phe
210 215 220
Arg Cys Gln Val Gln Phe Tyr Gly Leu Ser Glu Asn Asp Glu Trp Thr
225 230 235 240
Gln Asp Arg Ala Lys Pro Val Thr Gln Ile Val Ser Ala Glu Ala Trp
245 250 255
Gly Arg Ala Asp Cys Gly Phe Thr Ser Val Ser Tyr Gln Gln Gly Val
260 265 270
Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu
275 280 285
Tyr Ala Val Leu Val Ser Ala Leu Val Leu Met Ala Met Val Lys Arg
290 295 300
Lys Asp Phe
305
<210> 77
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 77
Val Val Gly Ala Val Gly Val Gly Lys
1 5
<210> 78
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 78
Val Val Val Gly Ala Val Gly Val Gly Lys
1 5 10
<210> 79
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 79
Asp Arg Gly Ser Gln Ser
1 5
<210> 80
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 80
Ile Tyr Ser Asn Gly Asp
1 5
<210> 81
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 81
Cys Ala Val Lys Ser Arg Ala Gly Ser Tyr Gln Leu Thr Phe
1 5 10
<210> 82
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 82
Ser Gly His Asn Ser
1 5
<210> 83
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 83
Phe Asn Asn Asn Val Pro
1 5
<210> 84
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 84
Cys Ala Ser Ser Leu Gly Asp Ser Glu Gln Tyr Phe
1 5 10
<210> 85
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 85
atgaaatcct tgagagtttt actagtgatc ctgtggcttc agttgagctg ggtttggagc
60
caacagaagg aggtggagca gaattctgga cccctcagtg ttccagaggg agccattgcc
120
tctctcaact gcacttacag tgaccgaggt tcccagtcct tcttctggta cagacaatat
180
tctgggaaaa gccctgagtt gataatgttc atatactcca atggtgacaa agaagatgga
240
aggtttacag cacagctcaa taaagccagc cagtatgttt ctctgctcat cagagactcc
300
cagcccagtg attcagccac ctacctctgt gccgtgaagt caagggctgg gagttaccaa
360
ctcactttcg ggaaggggac caaactctcg gtcatacca
399
<210> 86
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 86
atgaagagcc tgcgggtgct gctggtcatc ctgtggctgc agctgtcctg ggtgtggtct
60
cagcagaagg aggtggagca gaatagcgga ccactgtccg tgccagaggg agccatcgcc
120
tccctgaact gcacatactc tgacaggggc tcccagtctt tcttttggta ccgccagtat
180
agcggcaagt cccccgagct gatcatgttc atctactcta atggcgacaa ggaggatggc
240
aggtttaccg cccagctgaa caaggcctct cagtatgtga gcctgctgat ccgcgacagc
300
cagcctagcg attccgccac atacctgtgc gcagtgaagt cccgggcagg ctcttatcag
360
ctgacctttg gcaagggcac aaagctgagc gtgatccca
399
<210> 87
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 87
Met Lys Ser Leu Arg Val Leu Leu Val Ile Leu Trp Leu Gln Leu Ser
1 5 10 15
Trp Val Trp Ser Gln Gln Lys Glu Val Glu Gln Asn Ser Gly Pro Leu
20 25 30
Ser Val Pro Glu Gly Ala Ile Ala Ser Leu Asn Cys Thr Tyr Ser Asp
35 40 45
Arg Gly Ser Gln Ser Phe Phe Trp Tyr Arg Gln Tyr Ser Gly Lys Ser
50 55 60
Pro Glu Leu Ile Met Phe Ile Tyr Ser Asn Gly Asp Lys Glu Asp Gly
65 70 75 80
Arg Phe Thr Ala Gln Leu Asn Lys Ala Ser Gln Tyr Val Ser Leu Leu
85 90 95
Ile Arg Asp Ser Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala Val
100 105 110
Lys Ser Arg Ala Gly Ser Tyr Gln Leu Thr Phe Gly Lys Gly Thr Lys
115 120 125
Leu Ser Val Ile Pro
130
<210> 88
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 88
atggactcct ggaccttctg ctgtgtgtcc ctttgcatcc tggtagcgaa gcatacagat
60
gctggagtta tccagtcacc ccgccatgag gtgacagaga tgggacaaga agtgactctg
120
agatgtaaac caatttcagg ccacaactcc cttttctggt acagacagac catgatgcgg
180
ggactggagt tgctcattta ctttaacaac aacgttccga tagatgattc agggatgccc
240
gaggatcgat tctcagctaa gatgcctaat gcatcattct ccactctgaa gatccagccc
300
tcagaaccca gggactcagc tgtgtacttc tgtgccagca gtctcgggga cagcgagcag
360
tacttcgggc cgggcaccag gctcacggtc aca
393
<210> 89
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 89
atggacagct ggaccttctg ctgcgtgagc ctgtgcatcc tggtggccaa gcacacagat
60
gcaggcgtga tccagtcccc aaggcacgag gtgaccgaga tgggacagga ggtgacactg
120
aggtgtaagc ctatctctgg ccacaatagc ctgttctggt acaggcagac catgatgcgc
180
ggcctggagc tgctgatcta cttcaacaat aacgtgccta tcgacgattc cggcatgcca
240
gaggacagat tctctgccaa gatgcccaac gcctcctttt ctacactgaa gatccagcca
300
agcgagccta gggactccgc cgtgtacttc tgcgccagct ccctgggcga tagcgagcag
360
tattttggcc ctggcacccg gctgaccgtg aca
393
<210> 90
<211> 131
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 90
Met Asp Ser Trp Thr Phe Cys Cys Val Ser Leu Cys Ile Leu Val Ala
1 5 10 15
Lys His Thr Asp Ala Gly Val Ile Gln Ser Pro Arg His Glu Val Thr
20 25 30
Glu Met Gly Gln Glu Val Thr Leu Arg Cys Lys Pro Ile Ser Gly His
35 40 45
Asn Ser Leu Phe Trp Tyr Arg Gln Thr Met Met Arg Gly Leu Glu Leu
50 55 60
Leu Ile Tyr Phe Asn Asn Asn Val Pro Ile Asp Asp Ser Gly Met Pro
65 70 75 80
Glu Asp Arg Phe Ser Ala Lys Met Pro Asn Ala Ser Phe Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ser Glu Pro Arg Asp Ser Ala Val Tyr Phe Cys Ala
100 105 110
Ser Ser Leu Gly Asp Ser Glu Gln Tyr Phe Gly Pro Gly Thr Arg Leu
115 120 125
Thr Val Thr
130
<210> 91
<211> 274
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 91
Met Lys Ser Leu Arg Val Leu Leu Val Ile Leu Trp Leu Gln Leu Ser
1 5 10 15
Trp Val Trp Ser Gln Gln Lys Glu Val Glu Gln Asn Ser Gly Pro Leu
20 25 30
Ser Val Pro Glu Gly Ala Ile Ala Ser Leu Asn Cys Thr Tyr Ser Asp
35 40 45
Arg Gly Ser Gln Ser Phe Phe Trp Tyr Arg Gln Tyr Ser Gly Lys Ser
50 55 60
Pro Glu Leu Ile Met Phe Ile Tyr Ser Asn Gly Asp Lys Glu Asp Gly
65 70 75 80
Arg Phe Thr Ala Gln Leu Asn Lys Ala Ser Gln Tyr Val Ser Leu Leu
85 90 95
Ile Arg Asp Ser Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala Val
100 105 110
Lys Ser Arg Ala Gly Ser Tyr Gln Leu Thr Phe Gly Lys Gly Thr Lys
115 120 125
Leu Ser Val Ile Pro Asp Ile Gln Asn Pro Asp Pro Ala Val Tyr Gln
130 135 140
Leu Arg Asp Ser Lys Ser Ser Asp Lys Ser Val Cys Leu Phe Thr Asp
145 150 155 160
Phe Asp Ser Gln Thr Asn Val Ser Gln Ser Lys Asp Ser Asp Val Tyr
165 170 175
Ile Thr Asp Lys Thr Val Leu Asp Met Arg Ser Met Asp Phe Lys Ser
180 185 190
Asn Ser Ala Val Ala Trp Ser Asn Lys Ser Asp Phe Ala Cys Ala Asn
195 200 205
Ala Phe Asn Asn Ser Ile Ile Pro Glu Asp Thr Phe Phe Pro Ser Pro
210 215 220
Glu Ser Ser Cys Asp Val Lys Leu Val Glu Lys Ser Phe Glu Thr Asp
225 230 235 240
Thr Asn Leu Asn Phe Gln Asn Leu Ser Val Ile Gly Phe Arg Ile Leu
245 250 255
Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp
260 265 270
Ser Ser
<210> 92
<211> 308
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 92
Met Asp Ser Trp Thr Phe Cys Cys Val Ser Leu Cys Ile Leu Val Ala
1 5 10 15
Lys His Thr Asp Ala Gly Val Ile Gln Ser Pro Arg His Glu Val Thr
20 25 30
Glu Met Gly Gln Glu Val Thr Leu Arg Cys Lys Pro Ile Ser Gly His
35 40 45
Asn Ser Leu Phe Trp Tyr Arg Gln Thr Met Met Arg Gly Leu Glu Leu
50 55 60
Leu Ile Tyr Phe Asn Asn Asn Val Pro Ile Asp Asp Ser Gly Met Pro
65 70 75 80
Glu Asp Arg Phe Ser Ala Lys Met Pro Asn Ala Ser Phe Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ser Glu Pro Arg Asp Ser Ala Val Tyr Phe Cys Ala
100 105 110
Ser Ser Leu Gly Asp Ser Glu Gln Tyr Phe Gly Pro Gly Thr Arg Leu
115 120 125
Thr Val Thr Glu Asp Leu Asn Lys Val Phe Pro Pro Glu Val Ala Val
130 135 140
Phe Glu Pro Ser Glu Ala Glu Ile Ser His Thr Gln Lys Ala Thr Leu
145 150 155 160
Val Cys Leu Ala Thr Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp
165 170 175
Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln
180 185 190
Pro Leu Lys Glu Gln Pro Ala Leu Asn Asp Ser Arg Tyr Cys Leu Ser
195 200 205
Ser Arg Leu Arg Val Ser Ala Thr Phe Trp Gln Asn Pro Arg Asn His
210 215 220
Phe Arg Cys Gln Val Gln Phe Tyr Gly Leu Ser Glu Asn Asp Glu Trp
225 230 235 240
Thr Gln Asp Arg Ala Lys Pro Val Thr Gln Ile Val Ser Ala Glu Ala
245 250 255
Trp Gly Arg Ala Asp Cys Gly Phe Thr Ser Val Ser Tyr Gln Gln Gly
260 265 270
Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr
275 280 285
Leu Tyr Ala Val Leu Val Ser Ala Leu Val Leu Met Ala Met Val Lys
290 295 300
Arg Lys Asp Phe
305
<210> 93
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 93
Val Val Gly Ala Val Gly Val Gly Lys
1 5
<210> 94
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 94
Val Val Val Gly Ala Val Gly Val Gly Lys
1 5 10
<210> 95
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 95
Ser Ser Tyr Ser Pro Ser
1 5
<210> 96
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 96
Tyr Thr Ser Ala Ala Thr Leu Val
1 5
<210> 97
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 97
Cys Val Val Ser Gly Gly Gly Ser Ser Asn Thr Gly Lys Leu Ile Phe
1 5 10 15
<210> 98
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 98
Ser Gly His Ala Thr
1 5
<210> 99
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 99
Phe Gln Asn Asn Gly Val
1 5
<210> 100
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 100
Cys Ala Ser Ser Gln Arg Ser Asn Thr Gly Glu Leu Phe Phe
1 5 10
<210> 101
<211> 405
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 101
atgctcctgc tgctcgtccc agtgctcgag gtgattttta ctctgggagg aaccagagcc
60
cagtcggtga cccagcttga cagccacgtc tctgtctctg aaggaacccc ggtgctgctg
120
aggtgcaact actcatcttc ttattcacca tctctcttct ggtatgtgca acaccccaac
180
aaaggactcc agcttctcct gaagtacaca tcagcggcca ccctggttaa aggcatcaac
240
ggttttgagg ctgaatttaa gaagagtgaa acctccttcc acctgacgaa accctcagcc
300
catatgagcg acgcggctga gtacttctgt gttgtgagtg ggggaggctc tagcaacaca
360
ggcaaactaa tctttgggca agggacaact ttacaagtaa aacca
405
<210> 102
<211> 405
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 102
atgctgctgc tgctggtgcc cgtgctggaa gtgatcttca ccctgggagg aacaagggca
60
cagagcgtga cccagctgga ctcccacgtg tccgtgtctg agggcacacc cgtgctgctg
120
agatgcaact actcctctag ctatagcccc tccctgttct ggtacgtgca gcaccctaat
180
aagggcctgc agctgctgct gaagtatacc tccgccgcca cactggtgaa gggcatcaac
240
ggcttcgagg ccgagtttaa gaagagcgag acctccttcc acctgacaaa gccttctgcc
300
cacatgagcg atgccgccga gtacttttgc gtggtgagcg gcggcggctc ctctaatacc
360
ggcaagctga tcttcggcca gggcaccaca ctgcaggtga agcca
405
<210> 103
<211> 135
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 103
Met Leu Leu Leu Leu Val Pro Val Leu Glu Val Ile Phe Thr Leu Gly
1 5 10 15
Gly Thr Arg Ala Gln Ser Val Thr Gln Leu Asp Ser His Val Ser Val
20 25 30
Ser Glu Gly Thr Pro Val Leu Leu Arg Cys Asn Tyr Ser Ser Ser Tyr
35 40 45
Ser Pro Ser Leu Phe Trp Tyr Val Gln His Pro Asn Lys Gly Leu Gln
50 55 60
Leu Leu Leu Lys Tyr Thr Ser Ala Ala Thr Leu Val Lys Gly Ile Asn
65 70 75 80
Gly Phe Glu Ala Glu Phe Lys Lys Ser Glu Thr Ser Phe His Leu Thr
85 90 95
Lys Pro Ser Ala His Met Ser Asp Ala Ala Glu Tyr Phe Cys Val Val
100 105 110
Ser Gly Gly Gly Ser Ser Asn Thr Gly Lys Leu Ile Phe Gly Gln Gly
115 120 125
Thr Thr Leu Gln Val Lys Pro
130 135
<210> 104
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 104
atgggcacca ggctcctctg ctgggcggcc ctctgtctcc tgggagcaga actcacagaa
60
gctggagttg cccagtctcc cagatataag attatagaga aaaggcagag tgtggctttt
120
tggtgcaatc ctatatctgg ccatgctacc ctttactggt accagcagat cctgggacag
180
ggcccaaagc ttctgattca gtttcagaat aacggtgtag tggatgattc acagttgcct
240
aaggatcgat tttctgcaga gaggctcaaa ggagtagact ccactctcaa gatccaacct
300
gcaaagcttg aggactcggc cgtgtatctc tgtgccagca gccagaggtc gaacaccggg
360
gagctgtttt ttggagaagg ctctaggctg accgtactg
399
<210> 105
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 105
atgggcaccc ggctgctgtg ctgggccgcc ctgtgcctgc tgggagcaga gctgacagag
60
gcaggagtgg cccagtcccc acggtacaag atcatcgaga agagacagtc cgtggccttt
120
tggtgcaacc ccatctctgg ccacgccacc ctgtactggt atcagcagat cctgggccag
180
ggccctaagc tgctgatcca gttccagaac aatggcgtgg tggacgattc tcagctgcca
240
aaggacaggt ttagcgccga gcgcctgaag ggcgtggata gcaccctgaa gatccagcct
300
gccaagctgg aggacagcgc cgtgtatctg tgcgccagct cccagcggtc caatacaggc
360
gagctgttct ttggcgaggg ctctaggctg accgtgctg
399
<210> 106
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 106
Met Gly Thr Arg Leu Leu Cys Trp Ala Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Glu Leu Thr Glu Ala Gly Val Ala Gln Ser Pro Arg Tyr Lys Ile Ile
20 25 30
Glu Lys Arg Gln Ser Val Ala Phe Trp Cys Asn Pro Ile Ser Gly His
35 40 45
Ala Thr Leu Tyr Trp Tyr Gln Gln Ile Leu Gly Gln Gly Pro Lys Leu
50 55 60
Leu Ile Gln Phe Gln Asn Asn Gly Val Val Asp Asp Ser Gln Leu Pro
65 70 75 80
Lys Asp Arg Phe Ser Ala Glu Arg Leu Lys Gly Val Asp Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ala Lys Leu Glu Asp Ser Ala Val Tyr Leu Cys Ala
100 105 110
Ser Ser Gln Arg Ser Asn Thr Gly Glu Leu Phe Phe Gly Glu Gly Ser
115 120 125
Arg Leu Thr Val Leu
130
<210> 107
<211> 276
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 107
Met Leu Leu Leu Leu Val Pro Val Leu Glu Val Ile Phe Thr Leu Gly
1 5 10 15
Gly Thr Arg Ala Gln Ser Val Thr Gln Leu Asp Ser His Val Ser Val
20 25 30
Ser Glu Gly Thr Pro Val Leu Leu Arg Cys Asn Tyr Ser Ser Ser Tyr
35 40 45
Ser Pro Ser Leu Phe Trp Tyr Val Gln His Pro Asn Lys Gly Leu Gln
50 55 60
Leu Leu Leu Lys Tyr Thr Ser Ala Ala Thr Leu Val Lys Gly Ile Asn
65 70 75 80
Gly Phe Glu Ala Glu Phe Lys Lys Ser Glu Thr Ser Phe His Leu Thr
85 90 95
Lys Pro Ser Ala His Met Ser Asp Ala Ala Glu Tyr Phe Cys Val Val
100 105 110
Ser Gly Gly Gly Ser Ser Asn Thr Gly Lys Leu Ile Phe Gly Gln Gly
115 120 125
Thr Thr Leu Gln Val Lys Pro Asp Ile Gln Asn Pro Asp Pro Ala Val
130 135 140
Tyr Gln Leu Arg Asp Ser Lys Ser Ser Asp Lys Ser Val Cys Leu Phe
145 150 155 160
Thr Asp Phe Asp Ser Gln Thr Asn Val Ser Gln Ser Lys Asp Ser Asp
165 170 175
Val Tyr Ile Thr Asp Lys Thr Val Leu Asp Met Arg Ser Met Asp Phe
180 185 190
Lys Ser Asn Ser Ala Val Ala Trp Ser Asn Lys Ser Asp Phe Ala Cys
195 200 205
Ala Asn Ala Phe Asn Asn Ser Ile Ile Pro Glu Asp Thr Phe Phe Pro
210 215 220
Ser Pro Glu Ser Ser Cys Asp Val Lys Leu Val Glu Lys Ser Phe Glu
225 230 235 240
Thr Asp Thr Asn Leu Asn Phe Gln Asn Leu Ser Val Ile Gly Phe Arg
245 250 255
Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg
260 265 270
Leu Trp Ser Ser
275
<210> 108
<211> 310
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 108
Met Gly Thr Arg Leu Leu Cys Trp Ala Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Glu Leu Thr Glu Ala Gly Val Ala Gln Ser Pro Arg Tyr Lys Ile Ile
20 25 30
Glu Lys Arg Gln Ser Val Ala Phe Trp Cys Asn Pro Ile Ser Gly His
35 40 45
Ala Thr Leu Tyr Trp Tyr Gln Gln Ile Leu Gly Gln Gly Pro Lys Leu
50 55 60
Leu Ile Gln Phe Gln Asn Asn Gly Val Val Asp Asp Ser Gln Leu Pro
65 70 75 80
Lys Asp Arg Phe Ser Ala Glu Arg Leu Lys Gly Val Asp Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ala Lys Leu Glu Asp Ser Ala Val Tyr Leu Cys Ala
100 105 110
Ser Ser Gln Arg Ser Asn Thr Gly Glu Leu Phe Phe Gly Glu Gly Ser
115 120 125
Arg Leu Thr Val Leu Glu Asp Leu Asn Lys Val Phe Pro Pro Glu Val
130 135 140
Ala Val Phe Glu Pro Ser Glu Ala Glu Ile Ser His Thr Gln Lys Ala
145 150 155 160
Thr Leu Val Cys Leu Ala Thr Gly Phe Phe Pro Asp His Val Glu Leu
165 170 175
Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp
180 185 190
Pro Gln Pro Leu Lys Glu Gln Pro Ala Leu Asn Asp Ser Arg Tyr Cys
195 200 205
Leu Ser Ser Arg Leu Arg Val Ser Ala Thr Phe Trp Gln Asn Pro Arg
210 215 220
Asn His Phe Arg Cys Gln Val Gln Phe Tyr Gly Leu Ser Glu Asn Asp
225 230 235 240
Glu Trp Thr Gln Asp Arg Ala Lys Pro Val Thr Gln Ile Val Ser Ala
245 250 255
Glu Ala Trp Gly Arg Ala Asp Cys Gly Phe Thr Ser Val Ser Tyr Gln
260 265 270
Gln Gly Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys
275 280 285
Ala Thr Leu Tyr Ala Val Leu Val Ser Ala Leu Val Leu Met Ala Met
290 295 300
Val Lys Arg Lys Asp Phe
305 310
<210> 109
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 109
Val Val Gly Ala Cys Gly Val Gly Lys
1 5
<210> 110
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 110
Val Val Val Gly Ala Cys Gly Val Gly Lys
1 5 10
<210> 111
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 111
Thr Ser Ile Asn Asn
1 5
<210> 112
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 112
Ile Arg Ser Asn Glu Arg Glu
1 5
<210> 113
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 113
Cys Ala Thr Asp Ala Gly Gly Gly Ala Asp Gly Leu Thr Phe
1 5 10
<210> 114
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 114
Ser Gly Asp Leu Ser
1 5
<210> 115
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 115
Tyr Tyr Asn Gly Glu Glu
1 5
<210> 116
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 116
Cys Ala Ser Gly Gly Arg Asp Ser Thr Asp Thr Gln Tyr Phe
1 5 10
<210> 117
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 117
atggaaactc tcctgggagt gtctttggtg attctatggc ttcaactggc tagggtgaac
60
agtcaacagg gagaagagga tcctcaggcc ttgagcatcc aggagggtga aaatgccacc
120
atgaactgca gttacaaaac tagtataaac aatttacagt ggtatagaca aaattcaggt
180
agaggccttg tccacctaat tttaatacgt tcaaatgaaa gagagaaaca cagtggaaga
240
ttaagagtca cgcttgacac ttccaagaaa agcagttcct tgttgatcac ggcttcccgg
300
gcagcagaca ctgcttctta cttctgtgct acggacgccg gaggaggtgc tgacggactc
360
acctttggca aagggactca tctaatcatc cagccc
396
<210> 118
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 118
atggagacac tgctgggcgt gtccctggtc atcctgtggc tgcagctggc cagggtgaac
60
agccagcagg gagaggagga cccccaggcc ctgtctatcc aggagggcga gaacgccacc
120
atgaattgct cttacaagac aagcatcaac aatctgcagt ggtatagaca gaactccggc
180
aggggcctgg tgcacctgat cctgatccgc tccaatgagc gggagaagca ctctggccgg
240
ctgagagtga ccctggatac atctaagaag tcctctagcc tgctgatcac cgccagccgg
300
gcagcagaca cagcctccta cttttgtgcc accgatgccg ggggcggagc agacggactg
360
acattcggga aggggactca cctgattatc cagcca
396
<210> 119
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 119
Met Glu Thr Leu Leu Gly Val Ser Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ala Arg Val Asn Ser Gln Gln Gly Glu Glu Asp Pro Gln Ala Leu Ser
20 25 30
Ile Gln Glu Gly Glu Asn Ala Thr Met Asn Cys Ser Tyr Lys Thr Ser
35 40 45
Ile Asn Asn Leu Gln Trp Tyr Arg Gln Asn Ser Gly Arg Gly Leu Val
50 55 60
His Leu Ile Leu Ile Arg Ser Asn Glu Arg Glu Lys His Ser Gly Arg
65 70 75 80
Leu Arg Val Thr Leu Asp Thr Ser Lys Lys Ser Ser Ser Leu Leu Ile
85 90 95
Thr Ala Ser Arg Ala Ala Asp Thr Ala Ser Tyr Phe Cys Ala Thr Asp
100 105 110
Ala Gly Gly Gly Ala Asp Gly Leu Thr Phe Gly Lys Gly Thr His Leu
115 120 125
Ile Ile Gln Pro
130
<210> 120
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 120
atgggcttca ggctcctctg ctgtgtggcc ttttgtctcc tgggagcagg cccagtggat
60
tctggagtca cacaaacccc aaagcacctg atcacagcaa ctggacagcg agtgacgctg
120
agatgctccc ctaggtctgg agacctctct gtgtactggt accaacagag cctggaccag
180
ggcctccagt tcctcattca gtattataat ggagaagaga gagcaaaagg aaacattctt
240
gaacgattct ccgcacaaca gttccctgac ttgcactctg aactaaacct gagctctctg
300
gagctggggg actcagcttt gtatttctgt gccagcgggg gacgggattc cacagatacg
360
cagtattttg gcccaggcac ccggctgaca gtgctc
396
<210> 121
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 121
atgggctttc ggctgctgtg ctgcgtggct ttttgcctgc tgggggctgg gcctgtggat
60
agcggggtca ctcagacacc taaacatctg atcaccgcaa caggacagag ggtgaccctg
120
aggtgctctc ctcggagcgg cgacctgagc gtgtactggt atcagcagag cctggatcag
180
ggcctgcagt tcctgatcca gtactataac ggcgaggagc gcgccaaggg caatatcctg
240
gagcggttct ctgcccagca gtttccagac ctgcacagcg agctgaacct gagctccctg
300
gagctgggcg atagcgccct gtacttctgc gcctccggcg gcagagactc taccgataca
360
cagtattttg gccccggcac cagactgaca gtgctg
396
<210> 122
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 122
Met Gly Phe Arg Leu Leu Cys Cys Val Ala Phe Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Val Asp Ser Gly Val Thr Gln Thr Pro Lys His Leu Ile Thr
20 25 30
Ala Thr Gly Gln Arg Val Thr Leu Arg Cys Ser Pro Arg Ser Gly Asp
35 40 45
Leu Ser Val Tyr Trp Tyr Gln Gln Ser Leu Asp Gln Gly Leu Gln Phe
50 55 60
Leu Ile Gln Tyr Tyr Asn Gly Glu Glu Arg Ala Lys Gly Asn Ile Leu
65 70 75 80
Glu Arg Phe Ser Ala Gln Gln Phe Pro Asp Leu His Ser Glu Leu Asn
85 90 95
Leu Ser Ser Leu Glu Leu Gly Asp Ser Ala Leu Tyr Phe Cys Ala Ser
100 105 110
Gly Gly Arg Asp Ser Thr Asp Thr Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Leu
130
<210> 123
<211> 273
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 123
Met Glu Thr Leu Leu Gly Val Ser Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ala Arg Val Asn Ser Gln Gln Gly Glu Glu Asp Pro Gln Ala Leu Ser
20 25 30
Ile Gln Glu Gly Glu Asn Ala Thr Met Asn Cys Ser Tyr Lys Thr Ser
35 40 45
Ile Asn Asn Leu Gln Trp Tyr Arg Gln Asn Ser Gly Arg Gly Leu Val
50 55 60
His Leu Ile Leu Ile Arg Ser Asn Glu Arg Glu Lys His Ser Gly Arg
65 70 75 80
Leu Arg Val Thr Leu Asp Thr Ser Lys Lys Ser Ser Ser Leu Leu Ile
85 90 95
Thr Ala Ser Arg Ala Ala Asp Thr Ala Ser Tyr Phe Cys Ala Thr Asp
100 105 110
Ala Gly Gly Gly Ala Asp Gly Leu Thr Phe Gly Lys Gly Thr His Leu
115 120 125
Ile Ile Gln Pro Asp Ile Gln Asn Pro Asp Pro Ala Val Tyr Gln Leu
130 135 140
Arg Asp Ser Lys Ser Ser Asp Lys Ser Val Cys Leu Phe Thr Asp Phe
145 150 155 160
Asp Ser Gln Thr Asn Val Ser Gln Ser Lys Asp Ser Asp Val Tyr Ile
165 170 175
Thr Asp Lys Thr Val Leu Asp Met Arg Ser Met Asp Phe Lys Ser Asn
180 185 190
Ser Ala Val Ala Trp Ser Asn Lys Ser Asp Phe Ala Cys Ala Asn Ala
195 200 205
Phe Asn Asn Ser Ile Ile Pro Glu Asp Thr Phe Phe Pro Ser Pro Glu
210 215 220
Ser Ser Cys Asp Val Lys Leu Val Glu Lys Ser Phe Glu Thr Asp Thr
225 230 235 240
Asn Leu Asn Phe Gln Asn Leu Ser Val Ile Gly Phe Arg Ile Leu Leu
245 250 255
Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser
260 265 270
Ser
<210> 124
<211> 309
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 124
Met Gly Phe Arg Leu Leu Cys Cys Val Ala Phe Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Val Asp Ser Gly Val Thr Gln Thr Pro Lys His Leu Ile Thr
20 25 30
Ala Thr Gly Gln Arg Val Thr Leu Arg Cys Ser Pro Arg Ser Gly Asp
35 40 45
Leu Ser Val Tyr Trp Tyr Gln Gln Ser Leu Asp Gln Gly Leu Gln Phe
50 55 60
Leu Ile Gln Tyr Tyr Asn Gly Glu Glu Arg Ala Lys Gly Asn Ile Leu
65 70 75 80
Glu Arg Phe Ser Ala Gln Gln Phe Pro Asp Leu His Ser Glu Leu Asn
85 90 95
Leu Ser Ser Leu Glu Leu Gly Asp Ser Ala Leu Tyr Phe Cys Ala Ser
100 105 110
Gly Gly Arg Asp Ser Thr Asp Thr Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Leu Glu Asp Leu Asn Lys Val Phe Pro Pro Glu Val Ala
130 135 140
Val Phe Glu Pro Ser Glu Ala Glu Ile Ser His Thr Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Thr Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro
180 185 190
Gln Pro Leu Lys Glu Gln Pro Ala Leu Asn Asp Ser Arg Tyr Cys Leu
195 200 205
Ser Ser Arg Leu Arg Val Ser Ala Thr Phe Trp Gln Asn Pro Arg Asn
210 215 220
His Phe Arg Cys Gln Val Gln Phe Tyr Gly Leu Ser Glu Asn Asp Glu
225 230 235 240
Trp Thr Gln Asp Arg Ala Lys Pro Val Thr Gln Ile Val Ser Ala Glu
245 250 255
Ala Trp Gly Arg Ala Asp Cys Gly Phe Thr Ser Val Ser Tyr Gln Gln
260 265 270
Gly Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala
275 280 285
Thr Leu Tyr Ala Val Leu Val Ser Ala Leu Val Leu Met Ala Met Val
290 295 300
Lys Arg Lys Asp Phe
305
<210> 125
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 125
Val Val Gly Ala Val Gly Val Gly Lys
1 5
<210> 126
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 126
Val Val Val Gly Ala Val Gly Val Gly Lys
1 5 10
<210> 127
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 127
Asn Tyr Ser Pro Ala Tyr
1 5
<210> 128
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 128
Ile Arg Glu Asn Glu Lys Glu
1 5
<210> 129
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 129
Ala Leu Asp Ile Tyr Gly Asn Asn Arg Leu Ala
1 5 10
<210> 130
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 130
Met Asp His Glu Asn
1 5
<210> 131
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 131
Ser Tyr Asp Val Lys Met
1 5
<210> 132
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 132
Ala Ser Ser Leu Asp Phe Val Leu Ala Gly Ser Tyr Ser Tyr Asn Glu
1 5 10 15
Gln Phe
<210> 133
<211> 453
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 133
atggcttttt ggctgagaag gctgggtcta catttcaggc cacatttggg gagacgaatg
60
gagtcattcc tgggaggtgt tttgctgatt ttgtggcttc aagtggactg ggtgaagagc
120
caaaagatag aacagaattc cgaggccctg aacattcagg agggtaaaac ggccaccctg
180
acctgcaact atacaaacta ttctccagca tacttacagt ggtaccgaca agatccagga
240
agaggccctg ttttcttgct actcatacgt gaaaatgaga aagaaaaaag gaaagaaaga
300
ctgaaggtca cctttgatac cacccttaaa cagagtttgt ttcatatcac agcctcccag
360
cctgcagact cagctaccta cctctgtgct ctagacattt atgggaacaa cagactcgct
420
tttgggaagg ggaaccaagt ggtggtcata cca
453
<210> 134
<211> 453
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 134
atggccttct ggctgaggag actgggttta cacttcagac cccatttagg cagaagaatg
60
gagagctttt taggcggcgt gctgctgatt ttatggctgc aagttgactg ggtgaagagc
120
cagaagatcg agcagaacag cgaggcttta aacattcaag aaggcaagac agccacttta
180
acttgtaact ataccaacta ctcccccgct tatttacagt ggtacagaca agatcccggc
240
agaggccccg tgtttttact gctgattcgt gagaacgaga aggagaagag gaaggagaga
300
ctgaaggtga ccttcgacac cactttaaag cagtctttat tccacatcac cgccagccag
360
cccgctgata gcgccaccta tttatgcgct ttagacatct acggcaacaa tcgtctggcc
420
ttcggcaagg gcaaccaagt tgtggtgatc ccc
453
<210> 135
<211> 151
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 135
Met Ala Phe Trp Leu Arg Arg Leu Gly Leu His Phe Arg Pro His Leu
1 5 10 15
Gly Arg Arg Met Glu Ser Phe Leu Gly Gly Val Leu Leu Ile Leu Trp
20 25 30
Leu Gln Val Asp Trp Val Lys Ser Gln Lys Ile Glu Gln Asn Ser Glu
35 40 45
Ala Leu Asn Ile Gln Glu Gly Lys Thr Ala Thr Leu Thr Cys Asn Tyr
50 55 60
Thr Asn Tyr Ser Pro Ala Tyr Leu Gln Trp Tyr Arg Gln Asp Pro Gly
65 70 75 80
Arg Gly Pro Val Phe Leu Leu Leu Ile Arg Glu Asn Glu Lys Glu Lys
85 90 95
Arg Lys Glu Arg Leu Lys Val Thr Phe Asp Thr Thr Leu Lys Gln Ser
100 105 110
Leu Phe His Ile Thr Ala Ser Gln Pro Ala Asp Ser Ala Thr Tyr Leu
115 120 125
Cys Ala Leu Asp Ile Tyr Gly Asn Asn Arg Leu Ala Phe Gly Lys Gly
130 135 140
Asn Gln Val Val Val Ile Pro
145 150
<210> 136
<211> 414
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 136
atgggaatca ggctcctctg tcgtgtggcc ttttgtttcc tggctgtagg cctcgtagat
60
gtgaaagtaa cccagagctc gagatatcta gtcaaaagga cgggagagaa agtttttctg
120
gaatgtgtcc aggatatgga ccatgaaaat atgttctggt atcgacaaga cccaggtctg
180
gggctacggc tgatctattt ctcatatgat gttaaaatga aagaaaaagg agatattcct
240
gaggggtaca gtgtctctag agagaagaag gagcgcttct ccctgattct ggagtccgcc
300
agcaccaacc agacatctat gtacctctgt gccagcagtt tagattttgt gctagcgggg
360
tcctactcct acaatgagca gttcttcggg ccagggacac ggctcaccgt gcta
414
<210> 137
<211> 414
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 137
atgggcattc gtctgctgtg tcgtgtggcc ttctgctttt tagccgtggg tttagtggac
60
gtgaaggtga cccagtcctc tcgttattta gtgaagagga ccggcgagaa ggtgttttta
120
gaatgcgtgc aagatatgga ccacgagaac atgttctggt acagacaaga tcccggactg
180
ggtttaaggc tgatctactt cagctacgac gtgaagatga aggagaaggg cgacatcccc
240
gagggctact ccgtgtctcg tgagaagaag gagaggttct ctttaatttt agagtccgcc
300
agcaccaacc agaccagcat gtatttatgc gccagctctt tagactttgt gctggccggc
360
agctacagct acaacgagca gttcttcggc cccggcacca gactgaccgt gctg
414
<210> 138
<211> 138
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 138
Met Gly Ile Arg Leu Leu Cys Arg Val Ala Phe Cys Phe Leu Ala Val
1 5 10 15
Gly Leu Val Asp Val Lys Val Thr Gln Ser Ser Arg Tyr Leu Val Lys
20 25 30
Arg Thr Gly Glu Lys Val Phe Leu Glu Cys Val Gln Asp Met Asp His
35 40 45
Glu Asn Met Phe Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Leu
50 55 60
Ile Tyr Phe Ser Tyr Asp Val Lys Met Lys Glu Lys Gly Asp Ile Pro
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Arg Phe Ser Leu Ile
85 90 95
Leu Glu Ser Ala Ser Thr Asn Gln Thr Ser Met Tyr Leu Cys Ala Ser
100 105 110
Ser Leu Asp Phe Val Leu Ala Gly Ser Tyr Ser Tyr Asn Glu Gln Phe
115 120 125
Phe Gly Pro Gly Thr Arg Leu Thr Val Leu
130 135
<210> 139
<211> 292
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 139
Met Ala Phe Trp Leu Arg Arg Leu Gly Leu His Phe Arg Pro His Leu
1 5 10 15
Gly Arg Arg Met Glu Ser Phe Leu Gly Gly Val Leu Leu Ile Leu Trp
20 25 30
Leu Gln Val Asp Trp Val Lys Ser Gln Lys Ile Glu Gln Asn Ser Glu
35 40 45
Ala Leu Asn Ile Gln Glu Gly Lys Thr Ala Thr Leu Thr Cys Asn Tyr
50 55 60
Thr Asn Tyr Ser Pro Ala Tyr Leu Gln Trp Tyr Arg Gln Asp Pro Gly
65 70 75 80
Arg Gly Pro Val Phe Leu Leu Leu Ile Arg Glu Asn Glu Lys Glu Lys
85 90 95
Arg Lys Glu Arg Leu Lys Val Thr Phe Asp Thr Thr Leu Lys Gln Ser
100 105 110
Leu Phe His Ile Thr Ala Ser Gln Pro Ala Asp Ser Ala Thr Tyr Leu
115 120 125
Cys Ala Leu Asp Ile Tyr Gly Asn Asn Arg Leu Ala Phe Gly Lys Gly
130 135 140
Asn Gln Val Val Val Ile Pro Asp Ile Gln Asn Pro Asp Pro Ala Val
145 150 155 160
Tyr Gln Leu Arg Asp Ser Lys Ser Ser Asp Lys Ser Val Cys Leu Phe
165 170 175
Thr Asp Phe Asp Ser Gln Thr Asn Val Ser Gln Ser Lys Asp Ser Asp
180 185 190
Val Tyr Ile Thr Asp Lys Thr Val Leu Asp Met Arg Ser Met Asp Phe
195 200 205
Lys Ser Asn Ser Ala Val Ala Trp Ser Asn Lys Ser Asp Phe Ala Cys
210 215 220
Ala Asn Ala Phe Asn Asn Ser Ile Ile Pro Glu Asp Thr Phe Phe Pro
225 230 235 240
Ser Pro Glu Ser Ser Cys Asp Val Lys Leu Val Glu Lys Ser Phe Glu
245 250 255
Thr Asp Thr Asn Leu Asn Phe Gln Asn Leu Ser Val Ile Gly Phe Arg
260 265 270
Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg
275 280 285
Leu Trp Ser Ser
290
<210> 140
<211> 315
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 140
Met Gly Ile Arg Leu Leu Cys Arg Val Ala Phe Cys Phe Leu Ala Val
1 5 10 15
Gly Leu Val Asp Val Lys Val Thr Gln Ser Ser Arg Tyr Leu Val Lys
20 25 30
Arg Thr Gly Glu Lys Val Phe Leu Glu Cys Val Gln Asp Met Asp His
35 40 45
Glu Asn Met Phe Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Leu
50 55 60
Ile Tyr Phe Ser Tyr Asp Val Lys Met Lys Glu Lys Gly Asp Ile Pro
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Arg Phe Ser Leu Ile
85 90 95
Leu Glu Ser Ala Ser Thr Asn Gln Thr Ser Met Tyr Leu Cys Ala Ser
100 105 110
Ser Leu Asp Phe Val Leu Ala Gly Ser Tyr Ser Tyr Asn Glu Gln Phe
115 120 125
Phe Gly Pro Gly Thr Arg Leu Thr Val Leu Glu Asp Leu Asn Lys Val
130 135 140
Phe Pro Pro Glu Val Ala Val Phe Glu Pro Ser Glu Ala Glu Ile Ser
145 150 155 160
His Thr Gln Lys Ala Thr Leu Val Cys Leu Ala Thr Gly Phe Phe Pro
165 170 175
Asp His Val Glu Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser
180 185 190
Gly Val Ser Thr Asp Pro Gln Pro Leu Lys Glu Gln Pro Ala Leu Asn
195 200 205
Asp Ser Arg Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser Ala Thr Phe
210 215 220
Trp Gln Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln Phe Tyr Gly
225 230 235 240
Leu Ser Glu Asn Asp Glu Trp Thr Gln Asp Arg Ala Lys Pro Val Thr
245 250 255
Gln Ile Val Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys Gly Phe Thr
260 265 270
Ser Val Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile Leu Tyr Glu
275 280 285
Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val Ser Ala Leu
290 295 300
Val Leu Met Ala Met Val Lys Arg Lys Asp Phe
305 310 315
<210> 141
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 141
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 142
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 142
Thr Arg Asp Thr Thr Tyr Tyr
1 5
<210> 143
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 143
Arg Asn Ser Phe Asp Glu Gln Asn
1 5
<210> 144
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 144
Ala Leu Ser Glu Ala Arg Val Phe Asn Gly Ala Asn Ser Lys Leu Thr
1 5 10 15
<210> 145
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 145
Ser Gly His Asp Asn
1 5
<210> 146
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 146
Phe Val Lys Glu Ser Lys
1 5
<210> 147
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 147
Ala Ser Ser Gln Ala Asp Ser Pro Leu His
1 5 10
<210> 148
<211> 417
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 148
atgctgactg ccagcctgtt gagggcagtc atagcctcca tctgtgttgt atccagcatg
60
gctcagaagg taactcaagc gcagactgaa atttctgtgg tggagaagga ggatgtgacc
120
ttggactgtg tgtatgaaac ccgtgatact acttattact tattctggta caagcaacca
180
ccaagtggag aattggtttt ccttattcgt cggaactctt ttgatgagca aaatgaaata
240
agtggtcggt attcttggaa cttccagaaa tccaccagtt ccttcaactt caccatcaca
300
gcctcacaag tcgtggactc agcagtatac ttctgtgctc tgagtgaggc ccgcgttttc
360
aatggagcca atagtaagct gacatttgga aaaggaataa ctctgagtgt tagacca
417
<210> 149
<211> 417
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 149
atgctgaccg ccagcctgct gagggctgtg atcgccagca tctgcgtcgt gtccagcatg
60
gctcaaaagg tcacacaggc ccagacagag atctccgtcg tcgagaaaga ggacgtgacc
120
ctcgactgcg tgtatgagac cagggacacc acatactacc tgttttggta caagcagccc
180
cccagcggag agctcgtgtt tctgatcaga aggaacagct ttgatgaaca gaatgagatc
240
tccggcaggt actcctggaa cttccagaag agcacctcca gcttcaactt cacaattaca
300
gcttcccagg tggtggatag cgccgtgtat ttctgcgctc tcagcgaggc cagggtgttc
360
aacggcgcca attccaaact gaccttcggc aaaggcatca cactgtccgt gagaccc
417
<210> 150
<211> 139
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 150
Met Leu Thr Ala Ser Leu Leu Arg Ala Val Ile Ala Ser Ile Cys Val
1 5 10 15
Val Ser Ser Met Ala Gln Lys Val Thr Gln Ala Gln Thr Glu Ile Ser
20 25 30
Val Val Glu Lys Glu Asp Val Thr Leu Asp Cys Val Tyr Glu Thr Arg
35 40 45
Asp Thr Thr Tyr Tyr Leu Phe Trp Tyr Lys Gln Pro Pro Ser Gly Glu
50 55 60
Leu Val Phe Leu Ile Arg Arg Asn Ser Phe Asp Glu Gln Asn Glu Ile
65 70 75 80
Ser Gly Arg Tyr Ser Trp Asn Phe Gln Lys Ser Thr Ser Ser Phe Asn
85 90 95
Phe Thr Ile Thr Ala Ser Gln Val Val Asp Ser Ala Val Tyr Phe Cys
100 105 110
Ala Leu Ser Glu Ala Arg Val Phe Asn Gly Ala Asn Ser Lys Leu Thr
115 120 125
Phe Gly Lys Gly Ile Thr Leu Ser Val Arg Pro
130 135
<210> 151
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 151
atggtttcca ggcttctcag tttagtgtcc ctttgtctcc tgggagcaaa gcacatagaa
60
gctggagtta ctcagttccc cagccacagc gtaatagaga agggccagac tgtgactctg
120
agatgtgacc caatttctgg acatgataat ctttattggt atcgacgtgt tatgggaaaa
180
gaaataaaat ttctgttaca ttttgtgaaa gagtctaaac aggatgaatc cggtatgccc
240
aacaatcgat tcttagctga aaggactgga gggacgtatt ctactctgaa ggtgcagcct
300
gcagaactgg aggattctgg agtttatttc tgtgccagca gccaagcgga ttcacccctc
360
cactttggga atgggaccag gctcactgtg aca
393
<210> 152
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 152
atggtctcca ggctgctctc cctcgtgagc ctgtgtctcc tgggagccaa gcacattgag
60
gccggcgtga cccaattccc cagccacagc gtgattgaga agggacagac cgtcaccctg
120
aggtgtgatc ctatcagcgg ccacgacaac ctctactggt ataggagagt catgggcaag
180
gaaattaaat ttctgctgca tttcgtgaaa gagtccaaac aggacgaaag cggcatgccc
240
aataataggt tcctcgccga gaggaccggc ggcacatatt ccaccctgaa ggtccagccc
300
gctgagctcg aagactccgg cgtctatttc tgtgcctcca gccaggctga ctcccctctc
360
catttcggaa acggcaccag gctcaccgtg acc
393
<210> 153
<211> 131
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 153
Met Val Ser Arg Leu Leu Ser Leu Val Ser Leu Cys Leu Leu Gly Ala
1 5 10 15
Lys His Ile Glu Ala Gly Val Thr Gln Phe Pro Ser His Ser Val Ile
20 25 30
Glu Lys Gly Gln Thr Val Thr Leu Arg Cys Asp Pro Ile Ser Gly His
35 40 45
Asp Asn Leu Tyr Trp Tyr Arg Arg Val Met Gly Lys Glu Ile Lys Phe
50 55 60
Leu Leu His Phe Val Lys Glu Ser Lys Gln Asp Glu Ser Gly Met Pro
65 70 75 80
Asn Asn Arg Phe Leu Ala Glu Arg Thr Gly Gly Thr Tyr Ser Thr Leu
85 90 95
Lys Val Gln Pro Ala Glu Leu Glu Asp Ser Gly Val Tyr Phe Cys Ala
100 105 110
Ser Ser Gln Ala Asp Ser Pro Leu His Phe Gly Asn Gly Thr Arg Leu
115 120 125
Thr Val Thr
130
<210> 154
<211> 280
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 154
Met Leu Thr Ala Ser Leu Leu Arg Ala Val Ile Ala Ser Ile Cys Val
1 5 10 15
Val Ser Ser Met Ala Gln Lys Val Thr Gln Ala Gln Thr Glu Ile Ser
20 25 30
Val Val Glu Lys Glu Asp Val Thr Leu Asp Cys Val Tyr Glu Thr Arg
35 40 45
Asp Thr Thr Tyr Tyr Leu Phe Trp Tyr Lys Gln Pro Pro Ser Gly Glu
50 55 60
Leu Val Phe Leu Ile Arg Arg Asn Ser Phe Asp Glu Gln Asn Glu Ile
65 70 75 80
Ser Gly Arg Tyr Ser Trp Asn Phe Gln Lys Ser Thr Ser Ser Phe Asn
85 90 95
Phe Thr Ile Thr Ala Ser Gln Val Val Asp Ser Ala Val Tyr Phe Cys
100 105 110
Ala Leu Ser Glu Ala Arg Val Phe Asn Gly Ala Asn Ser Lys Leu Thr
115 120 125
Phe Gly Lys Gly Ile Thr Leu Ser Val Arg Pro Asp Ile Gln Asn Pro
130 135 140
Asp Pro Ala Val Tyr Gln Leu Arg Asp Ser Lys Ser Ser Asp Lys Ser
145 150 155 160
Val Cys Leu Phe Thr Asp Phe Asp Ser Gln Thr Asn Val Ser Gln Ser
165 170 175
Lys Asp Ser Asp Val Tyr Ile Thr Asp Lys Thr Val Leu Asp Met Arg
180 185 190
Ser Met Asp Phe Lys Ser Asn Ser Ala Val Ala Trp Ser Asn Lys Ser
195 200 205
Asp Phe Ala Cys Ala Asn Ala Phe Asn Asn Ser Ile Ile Pro Glu Asp
210 215 220
Thr Phe Phe Pro Ser Pro Glu Ser Ser Cys Asp Val Lys Leu Val Glu
225 230 235 240
Lys Ser Phe Glu Thr Asp Thr Asn Leu Asn Phe Gln Asn Leu Ser Val
245 250 255
Ile Gly Phe Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu
260 265 270
Met Thr Leu Arg Leu Trp Ser Ser
275 280
<210> 155
<211> 308
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 155
Met Val Ser Arg Leu Leu Ser Leu Val Ser Leu Cys Leu Leu Gly Ala
1 5 10 15
Lys His Ile Glu Ala Gly Val Thr Gln Phe Pro Ser His Ser Val Ile
20 25 30
Glu Lys Gly Gln Thr Val Thr Leu Arg Cys Asp Pro Ile Ser Gly His
35 40 45
Asp Asn Leu Tyr Trp Tyr Arg Arg Val Met Gly Lys Glu Ile Lys Phe
50 55 60
Leu Leu His Phe Val Lys Glu Ser Lys Gln Asp Glu Ser Gly Met Pro
65 70 75 80
Asn Asn Arg Phe Leu Ala Glu Arg Thr Gly Gly Thr Tyr Ser Thr Leu
85 90 95
Lys Val Gln Pro Ala Glu Leu Glu Asp Ser Gly Val Tyr Phe Cys Ala
100 105 110
Ser Ser Gln Ala Asp Ser Pro Leu His Phe Gly Asn Gly Thr Arg Leu
115 120 125
Thr Val Thr Glu Asp Leu Asn Lys Val Phe Pro Pro Glu Val Ala Val
130 135 140
Phe Glu Pro Ser Glu Ala Glu Ile Ser His Thr Gln Lys Ala Thr Leu
145 150 155 160
Val Cys Leu Ala Thr Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp
165 170 175
Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln
180 185 190
Pro Leu Lys Glu Gln Pro Ala Leu Asn Asp Ser Arg Tyr Cys Leu Ser
195 200 205
Ser Arg Leu Arg Val Ser Ala Thr Phe Trp Gln Asn Pro Arg Asn His
210 215 220
Phe Arg Cys Gln Val Gln Phe Tyr Gly Leu Ser Glu Asn Asp Glu Trp
225 230 235 240
Thr Gln Asp Arg Ala Lys Pro Val Thr Gln Ile Val Ser Ala Glu Ala
245 250 255
Trp Gly Arg Ala Asp Cys Gly Phe Thr Ser Val Ser Tyr Gln Gln Gly
260 265 270
Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr
275 280 285
Leu Tyr Ala Val Leu Val Ser Ala Leu Val Leu Met Ala Met Val Lys
290 295 300
Arg Lys Asp Phe
305
<210> 156
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 156
Ala Leu Asn Ser Glu Ala Leu Ser Val
1 5
<210> 157
<211> 201
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 157
Met Arg Arg Leu Ser Ala Ala Arg Arg Ala Gly Thr Ser Cys Ala Asn
1 5 10 15
Cys Gln Thr Thr Thr Thr Thr Leu Trp Arg Arg Asn Ala Asn Gly Asp
20 25 30
Pro Val Cys Asn Ala Cys Gly Leu Tyr Tyr Lys Leu His Asn Ile Asn
35 40 45
Arg Pro Leu Thr Met Lys Lys Glu Gly Ile Gln Thr Arg Asn Arg Lys
50 55 60
Met Ser Ser Lys Ser Lys Lys Cys Lys Lys Val His Asp Ser Leu Glu
65 70 75 80
Asp Phe Pro Lys Asn Ser Ser Phe Pro Gly Arg Pro Leu Gln Thr His
85 90 95
Val Leu Pro Glu Pro His Leu Ala Leu Gln Pro Leu Gln Pro His Ala
100 105 110
Asp His Ala His Ala Asp Ala Pro Ala Ile Gln Pro Val Leu Trp Thr
115 120 125
Thr Pro Pro Leu Gln His Gly His Arg His Gly Leu Glu Pro Cys Ser
130 135 140
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
145 150 155 160
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
165 170 175
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
180 185 190
Ser Leu Trp Cys Leu Cys Ser Asn His
195 200
<210> 158
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 158
Pro Gly Arg Pro Leu Gln Thr His Val Leu Pro Glu Pro His Leu Ala
1 5 10 15
Leu Gln Pro Leu Gln Pro His Ala Asp His Ala His Ala Asp Ala Pro
20 25 30
Ala Ile Gln Pro Val Leu Trp Thr Thr Pro Pro Leu Gln His Gly His
35 40 45
Arg His Gly Leu Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg
50 55 60
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
65 70 75 80
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
85 90 95
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
100 105 110
His
<210> 159
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 159
Asp Arg Gly Ser Gln Ser
1 5
<210> 160
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 160
Ile Tyr Ser Asn Gly Asp
1 5
<210> 161
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 161
Ala Val Asn Asp Tyr Gly Gly Ser Gln Gly Asn Leu Ile Phe
1 5 10
<210> 162
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 162
Ser Glu His Asn Arg
1 5
<210> 163
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 163
Phe Gln Asn Glu Ala Gln
1 5
<210> 164
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 164
Ala Ser Ser Phe Gly Pro Asp Glu Lys Leu Phe Phe
1 5 10
<210> 165
<211> 405
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 165
atgatgaaat ccttgagagt tttactagtg atcctgtggc ttcagttgag ctgggtttgg
60
agccaacaga aggaggtgga gcagaattct ggacccctca gtgttccaga gggagccatt
120
gcctctctca actgcactta cagtgaccga ggttcccagt ccttcttctg gtacagacaa
180
tattctggga aaagccctga gttgataatg ttcatatact ccaatggtga caaagaagat
240
ggaaggttta cagcacagct caataaagcc agccagtatg tttctctgct catcagagac
300
tcccagccca gtgattcagc cacctacctc tgtgccgtga acgattatgg aggaagccaa
360
ggaaatctca tctttggaaa aggcactaaa ctctctgtta aacca
405
<210> 166
<211> 405
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 166
atgatgaaga gcctgcgggt gctgctggtc atcctgtggc tgcagctgtc ttgggtgtgg
60
agccagcaga aggaggtgga gcagaactcc ggaccactgt ctgtgcctga gggagccatc
120
gccagcctga attgcaccta ctccgacaga ggctcccagt ctttcttttg gtacaggcag
180
tatagcggca agtcccccga gctgatcatg ttcatctact ccaacggcga caaggaggat
240
ggccgcttta cagcccagct gaataaggcc agccagtacg tgagcctgct gatccgggac
300
tctcagccaa gcgattccgc cacctacctg tgcgccgtga acgattatgg cggcagccag
360
ggcaatctga tctttggcaa gggcacaaag ctgtccgtga agccc
405
<210> 167
<211> 135
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 167
Met Met Lys Ser Leu Arg Val Leu Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ser Trp Val Trp Ser Gln Gln Lys Glu Val Glu Gln Asn Ser Gly Pro
20 25 30
Leu Ser Val Pro Glu Gly Ala Ile Ala Ser Leu Asn Cys Thr Tyr Ser
35 40 45
Asp Arg Gly Ser Gln Ser Phe Phe Trp Tyr Arg Gln Tyr Ser Gly Lys
50 55 60
Ser Pro Glu Leu Ile Met Phe Ile Tyr Ser Asn Gly Asp Lys Glu Asp
65 70 75 80
Gly Arg Phe Thr Ala Gln Leu Asn Lys Ala Ser Gln Tyr Val Ser Leu
85 90 95
Leu Ile Arg Asp Ser Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala
100 105 110
Val Asn Asp Tyr Gly Gly Ser Gln Gly Asn Leu Ile Phe Gly Lys Gly
115 120 125
Thr Lys Leu Ser Val Lys Pro
130 135
<210> 168
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 168
atgggcacca gcctcctctg ctggatggcc ctgtgtctcc tgggggcaga tcacgcagat
60
actggagtct cccagaaccc cagacacaag atcacaaaga ggggacagaa tgtaactttc
120
aggtgtgatc caatttctga acacaaccgc ctttattggt accgacagac cctggggcag
180
ggcccagagt ttctgactta cttccagaat gaagctcaac tagaaaaatc aaggctgctc
240
agtgatcggt tctctgcaga gaggcctaag ggatctttct ccaccttgga gatccagcgc
300
acagagcagg gggactcggc catgtatctc tgtgccagca gcttcggacc tgatgaaaaa
360
ctgttttttg gcagtggaac ccagctctct gtcttg
396
<210> 169
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 169
atgggcacct ctctgctgtg ctggatggca ctgtgcctgc tgggagcaga ccacgcagat
60
acaggcgtga gccagaaccc acgccacaag atcaccaagc ggggccagaa tgtgacattc
120
agatgcgacc ccatcagcga gcacaacagg ctgtactggt ataggcagac cctgggacag
180
ggaccagagt tcctgacata ctttcagaat gaggcccagc tggagaagtc tcggctgctg
240
agcgatagat tctccgccga gaggcctaag ggctcctttt ctaccctgga gatccagagg
300
acagagcagg gcgactccgc catgtatctg tgcgccagct ccttcggccc tgatgagaag
360
ctgttctttg gctctggcac ccagctgagc gtgctg
396
<210> 170
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 170
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asn Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Phe Gly Pro Asp Glu Lys Leu Phe Phe Gly Ser Gly Thr Gln
115 120 125
Leu Ser Val Leu
130
<210> 171
<211> 276
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 171
Met Met Lys Ser Leu Arg Val Leu Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ser Trp Val Trp Ser Gln Gln Lys Glu Val Glu Gln Asn Ser Gly Pro
20 25 30
Leu Ser Val Pro Glu Gly Ala Ile Ala Ser Leu Asn Cys Thr Tyr Ser
35 40 45
Asp Arg Gly Ser Gln Ser Phe Phe Trp Tyr Arg Gln Tyr Ser Gly Lys
50 55 60
Ser Pro Glu Leu Ile Met Phe Ile Tyr Ser Asn Gly Asp Lys Glu Asp
65 70 75 80
Gly Arg Phe Thr Ala Gln Leu Asn Lys Ala Ser Gln Tyr Val Ser Leu
85 90 95
Leu Ile Arg Asp Ser Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala
100 105 110
Val Asn Asp Tyr Gly Gly Ser Gln Gly Asn Leu Ile Phe Gly Lys Gly
115 120 125
Thr Lys Leu Ser Val Lys Pro Asp Ile Gln Asn Pro Asp Pro Ala Val
130 135 140
Tyr Gln Leu Arg Asp Ser Lys Ser Ser Asp Lys Ser Val Cys Leu Phe
145 150 155 160
Thr Asp Phe Asp Ser Gln Thr Asn Val Ser Gln Ser Lys Asp Ser Asp
165 170 175
Val Tyr Ile Thr Asp Lys Thr Val Leu Asp Met Arg Ser Met Asp Phe
180 185 190
Lys Ser Asn Ser Ala Val Ala Trp Ser Asn Lys Ser Asp Phe Ala Cys
195 200 205
Ala Asn Ala Phe Asn Asn Ser Ile Ile Pro Glu Asp Thr Phe Phe Pro
210 215 220
Ser Pro Glu Ser Ser Cys Asp Val Lys Leu Val Glu Lys Ser Phe Glu
225 230 235 240
Thr Asp Thr Asn Leu Asn Phe Gln Asn Leu Ser Val Ile Gly Phe Arg
245 250 255
Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg
260 265 270
Leu Trp Ser Ser
275
<210> 172
<211> 309
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 172
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asn Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Phe Gly Pro Asp Glu Lys Leu Phe Phe Gly Ser Gly Thr Gln
115 120 125
Leu Ser Val Leu Glu Asp Leu Asn Lys Val Phe Pro Pro Glu Val Ala
130 135 140
Val Phe Glu Pro Ser Glu Ala Glu Ile Ser His Thr Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Thr Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro
180 185 190
Gln Pro Leu Lys Glu Gln Pro Ala Leu Asn Asp Ser Arg Tyr Cys Leu
195 200 205
Ser Ser Arg Leu Arg Val Ser Ala Thr Phe Trp Gln Asn Pro Arg Asn
210 215 220
His Phe Arg Cys Gln Val Gln Phe Tyr Gly Leu Ser Glu Asn Asp Glu
225 230 235 240
Trp Thr Gln Asp Arg Ala Lys Pro Val Thr Gln Ile Val Ser Ala Glu
245 250 255
Ala Trp Gly Arg Ala Asp Cys Gly Phe Thr Ser Val Ser Tyr Gln Gln
260 265 270
Gly Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala
275 280 285
Thr Leu Tyr Ala Val Leu Val Ser Ala Leu Val Leu Met Ala Met Val
290 295 300
Lys Arg Lys Asp Phe
305
<210> 173
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 173
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 174
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 174
Asp Arg Gly Ser Gln Ser
1 5
<210> 175
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 175
Ile Tyr Ser Asn Gly Asp
1 5
<210> 176
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 176
Ala Val Asn Glu Gly Asp Ser Ser Tyr Lys Leu Ile
1 5 10
<210> 177
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 177
Ser Gly Asp Leu Ser
1 5
<210> 178
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 178
Tyr Tyr Asn Gly Glu Glu
1 5
<210> 179
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 179
Ala Ser Ser Pro Gly Ala Asn Glu Lys Leu Phe
1 5 10
<210> 180
<211> 402
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 180
atgatgaaat ccttgagagt tttactagtg atcctgtggc ttcagttgag ctgggtttgg
60
agccaacaga aggaggtgga gcagaattct ggacccctca gtgttccaga gggagccatt
120
gcctctctca actgcactta cagtgaccga ggttcccagt ccttcttctg gtacagacaa
180
tattctggga aaagccctga gttgataatg ttcatatact ccaatggtga caaagaagat
240
ggaaggttta cagcacagct caataaagcc agccagtatg tttctctgct catcagagac
300
tcccagccca gtgattcagc cacctacctc tgtgccgtga acgaggggga tagcagctat
360
aaattgatct tcgggagtgg gaccagactg ctggtcaggc ct
402
<210> 181
<211> 402
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 181
atgatgaaga gcctgcgggt gctgctggtc atcctgtggc tgcagctgag ctgggtgtgg
60
tcccagcaga aggaggtgga gcagaactct ggaccactga gcgtgcctga gggagccatc
120
gcctccctga attgcaccta ctctgacaga ggcagccagt ccttcttttg gtacaggcag
180
tattccggca agtctcccga gctgatcatg ttcatctaca gcaacggcga caaggaggat
240
ggccgcttta cagcccagct gaataaggcc tcccagtacg tgagcctgct gatccgggac
300
tctcagccat ctgatagcgc cacctacctg tgcgccgtga acgagggcga tagctcctat
360
aagctgatct ttggcagcgg cacaagactg ctggtgaggc cc
402
<210> 182
<211> 134
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 182
Met Met Lys Ser Leu Arg Val Leu Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ser Trp Val Trp Ser Gln Gln Lys Glu Val Glu Gln Asn Ser Gly Pro
20 25 30
Leu Ser Val Pro Glu Gly Ala Ile Ala Ser Leu Asn Cys Thr Tyr Ser
35 40 45
Asp Arg Gly Ser Gln Ser Phe Phe Trp Tyr Arg Gln Tyr Ser Gly Lys
50 55 60
Ser Pro Glu Leu Ile Met Phe Ile Tyr Ser Asn Gly Asp Lys Glu Asp
65 70 75 80
Gly Arg Phe Thr Ala Gln Leu Asn Lys Ala Ser Gln Tyr Val Ser Leu
85 90 95
Leu Ile Arg Asp Ser Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala
100 105 110
Val Asn Glu Gly Asp Ser Ser Tyr Lys Leu Ile Phe Gly Ser Gly Thr
115 120 125
Arg Leu Leu Val Arg Pro
130
<210> 183
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 183
atgggcttca ggctcctctg ctgtgtggcc ttttgtctcc tgggagcagg cccagtggat
60
tctggagtca cacaaacccc aaagcacctg atcacagcaa ctggacagcg agtgacgctg
120
agatgctccc ctaggtctgg agacctctct gtgtactggt accaacagag cctggaccag
180
ggcctccagt tcctcattca gtattataat ggagaagaga gagcaaaagg aaacattctt
240
gaacgattct ccgcacaaca gttccctgac ttgcactctg aactaaacct gagctctctg
300
gagctggggg actcagcttt gtatttctgt gccagcagcc cgggggctaa tgaaaaactg
360
ttttttggca gtggaaccca gctctctgtc ttg
393
<210> 184
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 184
atgggcttcc ggctgctgtg ctgcgtggca ttttgcctgc tgggagcagg accagtggac
60
tccggcgtga cccagacacc caagcacctg atcaccgcaa caggacagag ggtgaccctg
120
agatgttccc ctaggtctgg cgacctgagc gtgtactggt atcagcagtc cctggatcag
180
ggcctgcagt tcctgatcca gtactataac ggcgaggagc gcgccaaggg caatatcctg
240
gagcggttct ccgcccagca gtttcccgac ctgcactctg agctgaacct gagctccctg
300
gagctgggcg atagcgccct gtacttctgc gcctctagcc ctggcgccaa tgagaagctg
360
ttctttggca gcggcaccca gctgtccgtg ctg
393
<210> 185
<211> 131
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 185
Met Gly Phe Arg Leu Leu Cys Cys Val Ala Phe Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Val Asp Ser Gly Val Thr Gln Thr Pro Lys His Leu Ile Thr
20 25 30
Ala Thr Gly Gln Arg Val Thr Leu Arg Cys Ser Pro Arg Ser Gly Asp
35 40 45
Leu Ser Val Tyr Trp Tyr Gln Gln Ser Leu Asp Gln Gly Leu Gln Phe
50 55 60
Leu Ile Gln Tyr Tyr Asn Gly Glu Glu Arg Ala Lys Gly Asn Ile Leu
65 70 75 80
Glu Arg Phe Ser Ala Gln Gln Phe Pro Asp Leu His Ser Glu Leu Asn
85 90 95
Leu Ser Ser Leu Glu Leu Gly Asp Ser Ala Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Pro Gly Ala Asn Glu Lys Leu Phe Phe Gly Ser Gly Thr Gln Leu
115 120 125
Ser Val Leu
130
<210> 186
<211> 275
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 186
Met Met Lys Ser Leu Arg Val Leu Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ser Trp Val Trp Ser Gln Gln Lys Glu Val Glu Gln Asn Ser Gly Pro
20 25 30
Leu Ser Val Pro Glu Gly Ala Ile Ala Ser Leu Asn Cys Thr Tyr Ser
35 40 45
Asp Arg Gly Ser Gln Ser Phe Phe Trp Tyr Arg Gln Tyr Ser Gly Lys
50 55 60
Ser Pro Glu Leu Ile Met Phe Ile Tyr Ser Asn Gly Asp Lys Glu Asp
65 70 75 80
Gly Arg Phe Thr Ala Gln Leu Asn Lys Ala Ser Gln Tyr Val Ser Leu
85 90 95
Leu Ile Arg Asp Ser Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala
100 105 110
Val Asn Glu Gly Asp Ser Ser Tyr Lys Leu Ile Phe Gly Ser Gly Thr
115 120 125
Arg Leu Leu Val Arg Pro Asp Ile Gln Asn Pro Asp Pro Ala Val Tyr
130 135 140
Gln Leu Arg Asp Ser Lys Ser Ser Asp Lys Ser Val Cys Leu Phe Thr
145 150 155 160
Asp Phe Asp Ser Gln Thr Asn Val Ser Gln Ser Lys Asp Ser Asp Val
165 170 175
Tyr Ile Thr Asp Lys Thr Val Leu Asp Met Arg Ser Met Asp Phe Lys
180 185 190
Ser Asn Ser Ala Val Ala Trp Ser Asn Lys Ser Asp Phe Ala Cys Ala
195 200 205
Asn Ala Phe Asn Asn Ser Ile Ile Pro Glu Asp Thr Phe Phe Pro Ser
210 215 220
Pro Glu Ser Ser Cys Asp Val Lys Leu Val Glu Lys Ser Phe Glu Thr
225 230 235 240
Asp Thr Asn Leu Asn Phe Gln Asn Leu Ser Val Ile Gly Phe Arg Ile
245 250 255
Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu
260 265 270
Trp Ser Ser
275
<210> 187
<211> 308
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 187
Met Gly Phe Arg Leu Leu Cys Cys Val Ala Phe Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Val Asp Ser Gly Val Thr Gln Thr Pro Lys His Leu Ile Thr
20 25 30
Ala Thr Gly Gln Arg Val Thr Leu Arg Cys Ser Pro Arg Ser Gly Asp
35 40 45
Leu Ser Val Tyr Trp Tyr Gln Gln Ser Leu Asp Gln Gly Leu Gln Phe
50 55 60
Leu Ile Gln Tyr Tyr Asn Gly Glu Glu Arg Ala Lys Gly Asn Ile Leu
65 70 75 80
Glu Arg Phe Ser Ala Gln Gln Phe Pro Asp Leu His Ser Glu Leu Asn
85 90 95
Leu Ser Ser Leu Glu Leu Gly Asp Ser Ala Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Pro Gly Ala Asn Glu Lys Leu Phe Phe Gly Ser Gly Thr Gln Leu
115 120 125
Ser Val Leu Glu Asp Leu Asn Lys Val Phe Pro Pro Glu Val Ala Val
130 135 140
Phe Glu Pro Ser Glu Ala Glu Ile Ser His Thr Gln Lys Ala Thr Leu
145 150 155 160
Val Cys Leu Ala Thr Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp
165 170 175
Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln
180 185 190
Pro Leu Lys Glu Gln Pro Ala Leu Asn Asp Ser Arg Tyr Cys Leu Ser
195 200 205
Ser Arg Leu Arg Val Ser Ala Thr Phe Trp Gln Asn Pro Arg Asn His
210 215 220
Phe Arg Cys Gln Val Gln Phe Tyr Gly Leu Ser Glu Asn Asp Glu Trp
225 230 235 240
Thr Gln Asp Arg Ala Lys Pro Val Thr Gln Ile Val Ser Ala Glu Ala
245 250 255
Trp Gly Arg Ala Asp Cys Gly Phe Thr Ser Val Ser Tyr Gln Gln Gly
260 265 270
Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr
275 280 285
Leu Tyr Ala Val Leu Val Ser Ala Leu Val Leu Met Ala Met Val Lys
290 295 300
Arg Lys Asp Phe
305
<210> 188
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 188
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 189
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 189
Asn Ser Met Phe Asp Tyr
1 5
<210> 190
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 190
Ile Ser Ser Ile Lys Asp Lys
1 5
<210> 191
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 191
Ala Ala Ser Ala Ser Asn Asn Asp Met Arg
1 5 10
<210> 192
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 192
Ser Glu His Asn Arg
1 5
<210> 193
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 193
Phe Gln Asn Glu Ala Gln
1 5
<210> 194
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 194
Ala Ser Ser Gln Ser Gly Gln Gly Pro Tyr Glu Gln Tyr
1 5 10
<210> 195
<211> 411
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 195
atggccatgc tcctgggggc atcagtgctg attctgtggc ttcagccaga ctgggtaaac
60
agtcaacaga agaatgatga ccagcaagtt aagcaaaatt caccatccct gagcgtccag
120
gaaggaagaa tttctattct gaactgtgac tatactaaca gcatgtttga ttatttccta
180
tggtacaaaa aataccctgc tgaaggtcct acattcctga tatctataag ttccattaag
240
gataaaaatg aagatggaag attcactgtc ttcttaaaca aaagtgccaa gcacctctct
300
ctgcacattg tgccctccca gcctggagac tctgcagtgt acttctgtgc agcaagcgcg
360
tcaaacaatg acatgcgctt tggagcaggg accagactga cagtaaaacc a
411
<210> 196
<211> 411
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 196
atggcaatgc tgctgggagc ctctgtgctg atcctgtggc tgcagccaga ttgggtgaac
60
tcccagcaga agaatgacga tcagcaggtg aagcagaata gcccctccct gtctgtgcag
120
gagggcagaa tcagcatcct gaactgcgac tacaccaatt ccatgttcga ttattttctg
180
tggtacaaga agtatccagc cgagggcccc acctttctga tcagcatctc ctctatcaag
240
gacaagaacg aggatggcag gttcacagtg tttctgaata agtctgccaa gcacctgagc
300
ctgcacatcg tgccatccca gcctggcgac tctgccgtgt acttctgtgc cgccagcgcc
360
tccaacaatg atatgagatt tggcgccggc accaggctga cagtgaagcc c
411
<210> 197
<211> 137
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 197
Met Ala Met Leu Leu Gly Ala Ser Val Leu Ile Leu Trp Leu Gln Pro
1 5 10 15
Asp Trp Val Asn Ser Gln Gln Lys Asn Asp Asp Gln Gln Val Lys Gln
20 25 30
Asn Ser Pro Ser Leu Ser Val Gln Glu Gly Arg Ile Ser Ile Leu Asn
35 40 45
Cys Asp Tyr Thr Asn Ser Met Phe Asp Tyr Phe Leu Trp Tyr Lys Lys
50 55 60
Tyr Pro Ala Glu Gly Pro Thr Phe Leu Ile Ser Ile Ser Ser Ile Lys
65 70 75 80
Asp Lys Asn Glu Asp Gly Arg Phe Thr Val Phe Leu Asn Lys Ser Ala
85 90 95
Lys His Leu Ser Leu His Ile Val Pro Ser Gln Pro Gly Asp Ser Ala
100 105 110
Val Tyr Phe Cys Ala Ala Ser Ala Ser Asn Asn Asp Met Arg Phe Gly
115 120 125
Ala Gly Thr Arg Leu Thr Val Lys Pro
130 135
<210> 198
<211> 405
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 198
atgggcacca gcctcctctg ctggatggcc ctgtgtctcc tgggggcaga tcacgcagat
60
actggagtct cccaggaccc cagacacaag atcacaaaga ggggacagaa tgtaactttc
120
aggtgtgatc caatttctga acacaaccgc ctttattggt accgacagac cctggggcag
180
ggcccagagt ttctgactta cttccagaat gaagctcaac tagaaaaatc aaggctgctc
240
agtgatcggt tctctgcaga gaggcctaag ggatctttct ccaccttgga gatccagcgc
300
acagagcagg gggactcggc catgtatctc tgtgccagca gccaatcggg acaggggccc
360
tacgagcagt acttcgggcc gggcaccagg ctcacggtca cagag
405
<210> 199
<211> 405
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 199
atgggcacct ctctgctgtg ctggatggca ctgtgcctgc tgggagcaga ccacgcagat
60
acaggcgtga gccaggaccc ccgccacaag atcaccaagc ggggccagaa cgtgacattc
120
agatgcgatc ctatctccga gcacaatagg ctgtactggt ataggcagac cctgggacag
180
ggaccagagt tcctgacata ctttcagaac gaggcccagc tggagaagag ccggctgctg
240
tccgacagat tctctgccga gaggcctaag ggcagctttt ccaccctgga gatccagagg
300
acagagcagg gcgattctgc catgtatctg tgcgccagct cccagagcgg acagggacct
360
tacgagcagt atttcggacc aggaaccagg ctgaccgtga cagag
405
<210> 200
<211> 135
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 200
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Gln Ser Gly Gln Gly Pro Tyr Glu Gln Tyr Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Thr Glu
130 135
<210> 201
<211> 278
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 201
Met Ala Met Leu Leu Gly Ala Ser Val Leu Ile Leu Trp Leu Gln Pro
1 5 10 15
Asp Trp Val Asn Ser Gln Gln Lys Asn Asp Asp Gln Gln Val Lys Gln
20 25 30
Asn Ser Pro Ser Leu Ser Val Gln Glu Gly Arg Ile Ser Ile Leu Asn
35 40 45
Cys Asp Tyr Thr Asn Ser Met Phe Asp Tyr Phe Leu Trp Tyr Lys Lys
50 55 60
Tyr Pro Ala Glu Gly Pro Thr Phe Leu Ile Ser Ile Ser Ser Ile Lys
65 70 75 80
Asp Lys Asn Glu Asp Gly Arg Phe Thr Val Phe Leu Asn Lys Ser Ala
85 90 95
Lys His Leu Ser Leu His Ile Val Pro Ser Gln Pro Gly Asp Ser Ala
100 105 110
Val Tyr Phe Cys Ala Ala Ser Ala Ser Asn Asn Asp Met Arg Phe Gly
115 120 125
Ala Gly Thr Arg Leu Thr Val Lys Pro Asp Ile Gln Asn Pro Asp Pro
130 135 140
Ala Val Tyr Gln Leu Arg Asp Ser Lys Ser Ser Asp Lys Ser Val Cys
145 150 155 160
Leu Phe Thr Asp Phe Asp Ser Gln Thr Asn Val Ser Gln Ser Lys Asp
165 170 175
Ser Asp Val Tyr Ile Thr Asp Lys Thr Val Leu Asp Met Arg Ser Met
180 185 190
Asp Phe Lys Ser Asn Ser Ala Val Ala Trp Ser Asn Lys Ser Asp Phe
195 200 205
Ala Cys Ala Asn Ala Phe Asn Asn Ser Ile Ile Pro Glu Asp Thr Phe
210 215 220
Phe Pro Ser Pro Glu Ser Ser Cys Asp Val Lys Leu Val Glu Lys Ser
225 230 235 240
Phe Glu Thr Asp Thr Asn Leu Asn Phe Gln Asn Leu Ser Val Ile Gly
245 250 255
Phe Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr
260 265 270
Leu Arg Leu Trp Ser Ser
275
<210> 202
<211> 312
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 202
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Gln Ser Gly Gln Gly Pro Tyr Glu Gln Tyr Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Thr Glu Glu Asp Leu Asn Lys Val Phe Pro Pro
130 135 140
Glu Val Ala Val Phe Glu Pro Ser Glu Ala Glu Ile Ser His Thr Gln
145 150 155 160
Lys Ala Thr Leu Val Cys Leu Ala Thr Gly Phe Phe Pro Asp His Val
165 170 175
Glu Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser
180 185 190
Thr Asp Pro Gln Pro Leu Lys Glu Gln Pro Ala Leu Asn Asp Ser Arg
195 200 205
Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser Ala Thr Phe Trp Gln Asn
210 215 220
Pro Arg Asn His Phe Arg Cys Gln Val Gln Phe Tyr Gly Leu Ser Glu
225 230 235 240
Asn Asp Glu Trp Thr Gln Asp Arg Ala Lys Pro Val Thr Gln Ile Val
245 250 255
Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys Gly Phe Thr Ser Val Ser
260 265 270
Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu
275 280 285
Gly Lys Ala Thr Leu Tyr Ala Val Leu Val Ser Ala Leu Val Leu Met
290 295 300
Ala Met Val Lys Arg Lys Asp Phe
305 310
<210> 203
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 203
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 204
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 204
Tyr Gly Gly Thr Val Asn
1 5
<210> 205
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 205
Tyr Phe Ser Gly Asp Pro Leu Val
1 5
<210> 206
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 206
Ala Val Ile Ser Val Thr Gly Asn Asn Arg Lys Leu Ile
1 5 10
<210> 207
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 207
Leu Asn His Asp Ala
1 5
<210> 208
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 208
Ser Gln Ile Val Asn Asp
1 5
<210> 209
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 209
Ala Ser Ser Arg Thr Ala Met Asn Thr Glu Ala Phe
1 5 10
<210> 210
<211> 402
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 210
atgctcctgt tgctcatacc agtgctgggg atgatttttg ccctgagaga tgccagagcc
60
cagtctgtga gccagcataa ccaccacgta attctctctg aagcagcctc actggagttg
120
ggatgcaact attcctatgg tggaactgtt aatctcttct ggtatgtcca gtaccctggt
180
caacaccttc agcttctcct caagtacttt tcaggggatc cactggttaa aggcatcaag
240
ggctttgagg ctgaatttat aaagagtaaa ttctccttta atctgaggaa accctctgtg
300
cagtggagtg acacagctga gtacttctgt gccgtgatct ccgtgactgg caacaaccgt
360
aagctgattt ggggattggg aacaagcctg gcagtaaatc cg
402
<210> 211
<211> 402
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 211
atgctgctgc tgctgatccc tgtgctgggc atgatctttg cactgaggga cgcaagagca
60
cagtccgtgt ctcagcacaa ccaccacgtg atcctgagcg aggcagcctc cctggagctg
120
ggctgcaact actcttatgg cggcacagtg aatctgttct ggtacgtgca gtatccaggc
180
cagcacctgc agctgctgct gaagtacttt agcggcgacc ccctggtgaa gggcatcaag
240
ggcttcgagg ccgagtttat caagtccaag ttctctttta acctgcggaa gccatctgtg
300
cagtggagcg ataccgccga gtatttctgt gccgtgatca gcgtgacagg caacaataga
360
aagctgatct ggggactggg cacctccctg gccgtgaatc cc
402
<210> 212
<211> 134
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 212
Met Leu Leu Leu Leu Ile Pro Val Leu Gly Met Ile Phe Ala Leu Arg
1 5 10 15
Asp Ala Arg Ala Gln Ser Val Ser Gln His Asn His His Val Ile Leu
20 25 30
Ser Glu Ala Ala Ser Leu Glu Leu Gly Cys Asn Tyr Ser Tyr Gly Gly
35 40 45
Thr Val Asn Leu Phe Trp Tyr Val Gln Tyr Pro Gly Gln His Leu Gln
50 55 60
Leu Leu Leu Lys Tyr Phe Ser Gly Asp Pro Leu Val Lys Gly Ile Lys
65 70 75 80
Gly Phe Glu Ala Glu Phe Ile Lys Ser Lys Phe Ser Phe Asn Leu Arg
85 90 95
Lys Pro Ser Val Gln Trp Ser Asp Thr Ala Glu Tyr Phe Cys Ala Val
100 105 110
Ile Ser Val Thr Gly Asn Asn Arg Lys Leu Ile Trp Gly Leu Gly Thr
115 120 125
Ser Leu Ala Val Asn Pro
130
<210> 213
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 213
atgagcaacc aggtgctctg ctgtgtggtc ctttgtctcc tgggagcaaa caccgtggat
60
ggtggaatca ctcagtcccc gaagtacctg ttcagaaagg aaggacagaa tgtgaccctg
120
agttgtgaac agaatttgaa ccacgatgcc atgtactggt accgacagga cccagggcaa
180
gggctgagat tgatctacta ctcacagata gtaaatgact ttcagaaagg agatatagct
240
gaagggtaca gcgtctctcg ggagaagaag gaatcctttc ctctcactgt gacatcggcc
300
caaaagaacc cgacagcttt ctatctctgt gccagtagtc ggactgcaat gaacactgaa
360
gctttctttg gacaaggcac cagactcaca gttgta
396
<210> 214
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 214
atgtccaacc aggtgctgtg ctgcgtggtg ctgtgcctgc tgggagcaaa taccgtggac
60
ggaggcatca cacagtcccc caagtacctg ttcaggaagg agggccagaa cgtgaccctg
120
tcttgtgagc agaacctgaa tcacgacgcc atgtactggt ataggcagga ccccggacag
180
ggactgagac tgatctacta tagccagatc gtgaatgact ttcagaaggg cgacatcgcc
240
gagggctact ccgtgtctag ggagaagaag gagagcttcc ccctgaccgt gacatccgcc
300
cagaagaacc ctacagcctt ttatctgtgc gccagctccc gcaccgccat gaatacagag
360
gccttctttg gccagggcac caggctgaca gtggtg
396
<210> 215
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 215
Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Ser Arg Thr Ala Met Asn Thr Glu Ala Phe Phe Gly Gln Gly Thr Arg
115 120 125
Leu Thr Val Val
130
<210> 216
<211> 275
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 216
Met Leu Leu Leu Leu Ile Pro Val Leu Gly Met Ile Phe Ala Leu Arg
1 5 10 15
Asp Ala Arg Ala Gln Ser Val Ser Gln His Asn His His Val Ile Leu
20 25 30
Ser Glu Ala Ala Ser Leu Glu Leu Gly Cys Asn Tyr Ser Tyr Gly Gly
35 40 45
Thr Val Asn Leu Phe Trp Tyr Val Gln Tyr Pro Gly Gln His Leu Gln
50 55 60
Leu Leu Leu Lys Tyr Phe Ser Gly Asp Pro Leu Val Lys Gly Ile Lys
65 70 75 80
Gly Phe Glu Ala Glu Phe Ile Lys Ser Lys Phe Ser Phe Asn Leu Arg
85 90 95
Lys Pro Ser Val Gln Trp Ser Asp Thr Ala Glu Tyr Phe Cys Ala Val
100 105 110
Ile Ser Val Thr Gly Asn Asn Arg Lys Leu Ile Trp Gly Leu Gly Thr
115 120 125
Ser Leu Ala Val Asn Pro Asp Ile Gln Asn Pro Asp Pro Ala Val Tyr
130 135 140
Gln Leu Arg Asp Ser Lys Ser Ser Asp Lys Ser Val Cys Leu Phe Thr
145 150 155 160
Asp Phe Asp Ser Gln Thr Asn Val Ser Gln Ser Lys Asp Ser Asp Val
165 170 175
Tyr Ile Thr Asp Lys Thr Val Leu Asp Met Arg Ser Met Asp Phe Lys
180 185 190
Ser Asn Ser Ala Val Ala Trp Ser Asn Lys Ser Asp Phe Ala Cys Ala
195 200 205
Asn Ala Phe Asn Asn Ser Ile Ile Pro Glu Asp Thr Phe Phe Pro Ser
210 215 220
Pro Glu Ser Ser Cys Asp Val Lys Leu Val Glu Lys Ser Phe Glu Thr
225 230 235 240
Asp Thr Asn Leu Asn Phe Gln Asn Leu Ser Val Ile Gly Phe Arg Ile
245 250 255
Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu
260 265 270
Trp Ser Ser
275
<210> 217
<211> 309
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 217
Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Ser Arg Thr Ala Met Asn Thr Glu Ala Phe Phe Gly Gln Gly Thr Arg
115 120 125
Leu Thr Val Val Glu Asp Leu Asn Lys Val Phe Pro Pro Glu Val Ala
130 135 140
Val Phe Glu Pro Ser Glu Ala Glu Ile Ser His Thr Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Thr Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro
180 185 190
Gln Pro Leu Lys Glu Gln Pro Ala Leu Asn Asp Ser Arg Tyr Cys Leu
195 200 205
Ser Ser Arg Leu Arg Val Ser Ala Thr Phe Trp Gln Asn Pro Arg Asn
210 215 220
His Phe Arg Cys Gln Val Gln Phe Tyr Gly Leu Ser Glu Asn Asp Glu
225 230 235 240
Trp Thr Gln Asp Arg Ala Lys Pro Val Thr Gln Ile Val Ser Ala Glu
245 250 255
Ala Trp Gly Arg Ala Asp Cys Gly Phe Thr Ser Val Ser Tyr Gln Gln
260 265 270
Gly Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala
275 280 285
Thr Leu Tyr Ala Val Leu Val Ser Ala Leu Val Leu Met Ala Met Val
290 295 300
Lys Arg Lys Asp Phe
305
<210> 218
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 218
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 219
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 219
Lys Leu Val Val Val Gly Ala Asp Gly Val
1 5 10
<210> 220
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 220
Leu Val Val Val Gly Ala Asp Gly Val
1 5
<210> 221
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 221
Lys Leu Val Val Val Gly Ala Val Gly Val
1 5 10
<210> 222
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 222
Leu Val Val Val Gly Ala Val Gly Val
1 5
<210> 223
<400> 223
000
<210> 224
<400> 224
000
<210> 225
<400> 225
000
<210> 226
<400> 226
000
<210> 227
<400> 227
000
<210> 228
<400> 228
000
<210> 229
<400> 229
000
<210> 230
<400> 230
000
<210> 231
<400> 231
000
<210> 232
<400> 232
000
<210> 233
<400> 233
000
<210> 234
<400> 234
000
<210> 235
<400> 235
000
<210> 236
<400> 236
000
<210> 237
<400> 237
000
<210> 238
<400> 238
000
<210> 239
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 239
Ser Val Phe Ser Ser
1 5
<210> 240
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 240
Val Val Thr Gly Gly Glu Val
1 5
<210> 241
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 241
Ala Gly Gly Pro Asn Thr Gly Asn Gln Phe Tyr
1 5 10
<210> 242
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 242
Ser Gly His Asn Thr
1 5
<210> 243
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 243
Tyr Tyr Arg Glu Glu Glu
1 5
<210> 244
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 244
Ala Ser Ser Thr Ser Phe Trp Glu Val Asn Thr Glu Ala Phe
1 5 10
<210> 245
<211> 390
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 245
atggtcctga aattctccgt gtccattctt tggattcagt tggcatgggt gagcacccag
60
ctgctggagc agagccctca gtttctaagc atccaagagg gagaaaatct cactgtgtac
120
tgcaactcct caagtgtttt ttccagctta caatggtaca gacaggagcc tggggaaggt
180
cctgtcctcc tggtgacagt agttacgggt ggagaagtga agaagctgaa gagactaacc
240
tttcagtttg gtgatgcaag aaaggacagt tctctccaca tcactgcggc ccagcctggt
300
gatacaggcc tctacctctg tgcaggaggg ccgaacaccg gtaaccagtt ctattttggg
360
acagggacaa gtttgacggt cattccaaat
390
<210> 246
<211> 390
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 246
atggtgctga agttttccgt gtctatcctg tggattcagc tggcctgggt gtctacccag
60
ctgctggagc agagccccca gttcctgtcc atccaggagg gcgagaacct gacagtgtac
120
tgcaattcta gctccgtgtt ttctagcctg cagtggtata ggcaggagcc aggagaggga
180
cccgtgctgc tggtgaccgt ggtgacaggc ggcgaggtga agaagctgaa gagactgacc
240
ttccagtttg gcgacgccag gaaggattcc tctctgcaca tcaccgcagc acagcctggc
300
gatacaggac tgtacctgtg cgcaggagga ccaaacaccg gcaatcagtt ctattttggc
360
accggcacat ccctgacagt gatccctaat
390
<210> 247
<211> 130
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 247
Met Val Leu Lys Phe Ser Val Ser Ile Leu Trp Ile Gln Leu Ala Trp
1 5 10 15
Val Ser Thr Gln Leu Leu Glu Gln Ser Pro Gln Phe Leu Ser Ile Gln
20 25 30
Glu Gly Glu Asn Leu Thr Val Tyr Cys Asn Ser Ser Ser Val Phe Ser
35 40 45
Ser Leu Gln Trp Tyr Arg Gln Glu Pro Gly Glu Gly Pro Val Leu Leu
50 55 60
Val Thr Val Val Thr Gly Gly Glu Val Lys Lys Leu Lys Arg Leu Thr
65 70 75 80
Phe Gln Phe Gly Asp Ala Arg Lys Asp Ser Ser Leu His Ile Thr Ala
85 90 95
Ala Gln Pro Gly Asp Thr Gly Leu Tyr Leu Cys Ala Gly Gly Pro Asn
100 105 110
Thr Gly Asn Gln Phe Tyr Phe Gly Thr Gly Thr Ser Leu Thr Val Ile
115 120 125
Pro Asn
130
<210> 248
<211> 402
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 248
atgggccctg ggctcctctg ctgggtgctg ctttgtctcc tgggagcagg ctcagtggag
60
actggagtca cccaaagtcc cacacacctg atcaaaacga gaggacagca agtgactctg
120
agatgctctt ctcagtctgg gcacaacact gtgtcctggt accaacaggc cctgggtcag
180
gggccccagt ttatctttca gtattatagg gaggaagaga atggcagagg aaacttccct
240
cctagattct caggtctcca gttccctaat tatagctctg agctgaatgt gaacgccttg
300
gagctggacg actcggccct gtatctctgt gccagcagca catctttttg ggaggtgaac
360
actgaagctt tctttggaca aggcaccaga ctcacagttg ta
402
<210> 249
<211> 402
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 249
atgggaccag gactgctgtg ctgggtgctg ctgtgcctgc tgggagcagg ctccgtggag
60
accggcgtga cacagtctcc cacccacctg atcaagacaa gaggccagca ggtgaccctg
120
aggtgcagct cccagtctgg ccacaacaca gtgagctggt accagcaggc cctgggacag
180
ggacctcagt tcatctttca gtactatagg gaggaggaga acggccgcgg caatttcccc
240
cctcggttta gcggcctgca gttcccaaac tactctagcg agctgaacgt gaatgccctg
300
gagctggacg atagcgccct gtatctgtgc gcctcctcta cctccttttg ggaagtgaat
360
acagaggcct tctttggcca gggcacccgc ctgacagtgg tg
402
<210> 250
<211> 134
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 250
Met Gly Pro Gly Leu Leu Cys Trp Val Leu Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Ser Val Glu Thr Gly Val Thr Gln Ser Pro Thr His Leu Ile Lys
20 25 30
Thr Arg Gly Gln Gln Val Thr Leu Arg Cys Ser Ser Gln Ser Gly His
35 40 45
Asn Thr Val Ser Trp Tyr Gln Gln Ala Leu Gly Gln Gly Pro Gln Phe
50 55 60
Ile Phe Gln Tyr Tyr Arg Glu Glu Glu Asn Gly Arg Gly Asn Phe Pro
65 70 75 80
Pro Arg Phe Ser Gly Leu Gln Phe Pro Asn Tyr Ser Ser Glu Leu Asn
85 90 95
Val Asn Ala Leu Glu Leu Asp Asp Ser Ala Leu Tyr Leu Cys Ala Ser
100 105 110
Ser Thr Ser Phe Trp Glu Val Asn Thr Glu Ala Phe Phe Gly Gln Gly
115 120 125
Thr Arg Leu Thr Val Val
130
<210> 251
<211> 267
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 251
Met Val Leu Lys Phe Ser Val Ser Ile Leu Trp Ile Gln Leu Ala Trp
1 5 10 15
Val Ser Thr Gln Leu Leu Glu Gln Ser Pro Gln Phe Leu Ser Ile Gln
20 25 30
Glu Gly Glu Asn Leu Thr Val Tyr Cys Asn Ser Ser Ser Val Phe Ser
35 40 45
Ser Leu Gln Trp Tyr Arg Gln Glu Pro Gly Glu Gly Pro Val Leu Leu
50 55 60
Val Thr Val Val Thr Gly Gly Glu Val Lys Lys Leu Lys Arg Leu Thr
65 70 75 80
Phe Gln Phe Gly Asp Ala Arg Lys Asp Ser Ser Leu His Ile Thr Ala
85 90 95
Ala Gln Pro Gly Asp Thr Gly Leu Tyr Leu Cys Ala Gly Gly Pro Asn
100 105 110
Thr Gly Asn Gln Phe Tyr Phe Gly Thr Gly Thr Ser Leu Thr Val Ile
115 120 125
Pro Asn Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp
130 135 140
Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser
145 150 155 160
Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp
165 170 175
Lys Thr Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala
180 185 190
Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys
195 200 205
Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr
210 215 220
Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn
225 230 235 240
Leu Ser Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe
245 250 255
Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 252
<211> 307
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 252
Met Gly Pro Gly Leu Leu Cys Trp Val Leu Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Ser Val Glu Thr Gly Val Thr Gln Ser Pro Thr His Leu Ile Lys
20 25 30
Thr Arg Gly Gln Gln Val Thr Leu Arg Cys Ser Ser Gln Ser Gly His
35 40 45
Asn Thr Val Ser Trp Tyr Gln Gln Ala Leu Gly Gln Gly Pro Gln Phe
50 55 60
Ile Phe Gln Tyr Tyr Arg Glu Glu Glu Asn Gly Arg Gly Asn Phe Pro
65 70 75 80
Pro Arg Phe Ser Gly Leu Gln Phe Pro Asn Tyr Ser Ser Glu Leu Asn
85 90 95
Val Asn Ala Leu Glu Leu Asp Asp Ser Ala Leu Tyr Leu Cys Ala Ser
100 105 110
Ser Thr Ser Phe Trp Glu Val Asn Thr Glu Ala Phe Phe Gly Gln Gly
115 120 125
Thr Arg Leu Thr Val Val Lys Asp Leu Arg Asn Val Thr Pro Pro Lys
130 135 140
Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys
145 150 155 160
Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu
165 170 175
Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr
180 185 190
Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser
195 200 205
Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe
210 215 220
Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro
225 230 235 240
Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp
245 250 255
Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val
260 265 270
Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu
275 280 285
Tyr Ala Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys
290 295 300
Lys Asn Ser
305
<210> 253
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 253
Val Val Gly Ala Cys Gly Val Gly Lys
1 5
<210> 254
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 254
Val Val Val Gly Ala Cys Gly Val Gly Lys
1 5 10
<210> 255
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 255
Thr Ser Gly Phe Asn Gly
1 5
<210> 256
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 256
Asn Val Leu Asp Gly Leu
1 5
<210> 257
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 257
Ala Val Arg Glu Glu Val Leu Tyr Asn Gln Gly Gly Lys Leu Ile
1 5 10 15
<210> 258
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 258
Leu Asn His Asp Ala
1 5
<210> 259
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 259
Ser Gln Ile Val Asn Asp
1 5
<210> 260
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 260
Ala Ser Ser Lys Arg Gly Trp Pro Tyr Glu Gln Tyr
1 5 10
<210> 261
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 261
atgtggggag ttttccttct ttatgtttcc atgaagatgg gaggcactac aggacaaaac
60
attgaccagc ccactgagat gacagctacg gaaggtgcca ttgtccagat caactgcacg
120
taccagacat ctgggttcaa cgggctgttc tggtaccagc aacatgctgg cgaagcaccc
180
acatttctgt cttacaatgt tctggatggt ttggaggaga aaggtcgttt ttcttcattc
240
cttagtcggt ctaaagggta cagttacctc cttttgaagg agctccagat gaaagactct
300
gcctcttacc tctgtgctgt gagagaggag gtcctttata accagggagg aaagcttatc
360
ttcggacagg gaacggagtt atctgtgaaa ccc
393
<210> 262
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 262
atgtggggcg tgtttctgct gtacgtgagc atgaagatgg gcggcaccac aggccagaac
60
atcgaccagc caaccgagat gaccgccaca gagggcgcca tcgtgcagat caactgcacc
120
taccagacaa gcggcttcaa tggcctgttt tggtatcagc agcacgcagg agaggcaccc
180
acattcctgt cctataatgt gctggacggc ctggaggaga agggcaggtt ctcctctttt
240
ctgagccgct ccaagggcta ctcctatctg ctgctgaagg agctgcagat gaaggattct
300
gccagctacc tgtgcgccgt gcgggaggag gtgctgtata atcagggcgg caagctgatc
360
tttggccagg gcaccgagct gagcgtgaag cct
393
<210> 263
<211> 131
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 263
Met Trp Gly Val Phe Leu Leu Tyr Val Ser Met Lys Met Gly Gly Thr
1 5 10 15
Thr Gly Gln Asn Ile Asp Gln Pro Thr Glu Met Thr Ala Thr Glu Gly
20 25 30
Ala Ile Val Gln Ile Asn Cys Thr Tyr Gln Thr Ser Gly Phe Asn Gly
35 40 45
Leu Phe Trp Tyr Gln Gln His Ala Gly Glu Ala Pro Thr Phe Leu Ser
50 55 60
Tyr Asn Val Leu Asp Gly Leu Glu Glu Lys Gly Arg Phe Ser Ser Phe
65 70 75 80
Leu Ser Arg Ser Lys Gly Tyr Ser Tyr Leu Leu Leu Lys Glu Leu Gln
85 90 95
Met Lys Asp Ser Ala Ser Tyr Leu Cys Ala Val Arg Glu Glu Val Leu
100 105 110
Tyr Asn Gln Gly Gly Lys Leu Ile Phe Gly Gln Gly Thr Glu Leu Ser
115 120 125
Val Lys Pro
130
<210> 264
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 264
atgagcaacc aggtgctctg ctgtgtggtc ctttgtctcc tgggagcaaa caccgtggat
60
ggtggaatca ctcagtcccc gaagtacctg ttcagaaagg aaggacagaa tgtgaccctg
120
agttgtgaac agaatttgaa ccacgatgcc atgtactggt accgacagga cccagggcaa
180
gggctgagat tgatctacta ctcacagata gtaaatgact ttcagaaagg agatatagct
240
gaagggtaca gcgtctctcg ggagaagaag gaatcctttc ctctcactgt gacatcggcc
300
caaaagaacc cgacagcttt ctatctctgt gccagtagta aaaggggatg gccctacgag
360
cagtacttcg ggccgggcac caggctcacg gtcaca
396
<210> 265
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 265
atgtccaacc aggtgctgtg ctgcgtggtg ctgtgcctgc tgggagcaaa taccgtggac
60
ggaggcatca cacagtcccc caagtacctg ttccggaagg agggccagaa cgtgaccctg
120
tcttgtgagc agaacctgaa tcacgacgcc atgtactggt ataggcagga ccccggacag
180
ggactgagac tgatctacta tagccagatc gtgaacgact ttcagaaggg cgacatcgcc
240
gagggctaca gcgtgtcccg ggagaagaag gagtccttcc cactgaccgt gacatctgcc
300
cagaagaatc ccaccgcctt ttatctgtgc gccagctcca agagaggctg gccctacgag
360
cagtatttcg gccctggcac caggctgacc gtgaca
396
<210> 266
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 266
Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Ser Lys Arg Gly Trp Pro Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Thr
130
<210> 267
<211> 268
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 267
Met Trp Gly Val Phe Leu Leu Tyr Val Ser Met Lys Met Gly Gly Thr
1 5 10 15
Thr Gly Gln Asn Ile Asp Gln Pro Thr Glu Met Thr Ala Thr Glu Gly
20 25 30
Ala Ile Val Gln Ile Asn Cys Thr Tyr Gln Thr Ser Gly Phe Asn Gly
35 40 45
Leu Phe Trp Tyr Gln Gln His Ala Gly Glu Ala Pro Thr Phe Leu Ser
50 55 60
Tyr Asn Val Leu Asp Gly Leu Glu Glu Lys Gly Arg Phe Ser Ser Phe
65 70 75 80
Leu Ser Arg Ser Lys Gly Tyr Ser Tyr Leu Leu Leu Lys Glu Leu Gln
85 90 95
Met Lys Asp Ser Ala Ser Tyr Leu Cys Ala Val Arg Glu Glu Val Leu
100 105 110
Tyr Asn Gln Gly Gly Lys Leu Ile Phe Gly Gln Gly Thr Glu Leu Ser
115 120 125
Val Lys Pro Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys
130 135 140
Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp
145 150 155 160
Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr
165 170 175
Asp Lys Thr Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly
180 185 190
Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe
195 200 205
Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala
210 215 220
Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln
225 230 235 240
Asn Leu Ser Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val Ala Gly
245 250 255
Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 268
<211> 305
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 268
Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Ser Lys Arg Gly Trp Pro Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Thr Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys Asn
290 295 300
Ser
305
<210> 269
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 269
Val Val Gly Ala Cys Gly Val Gly Lys
1 5
<210> 270
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 270
Val Val Val Gly Ala Cys Gly Val Gly Lys
1 5 10
<210> 271
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 271
Thr Ser Ile Asn Asn
1 5
<210> 272
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 272
Ile Arg Ser Asn Glu Arg Glu
1 5
<210> 273
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 273
Ala Thr Asp Arg Gln Ser Ser Gly Asp Lys Leu Thr
1 5 10
<210> 274
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 274
Ser Gly His Ala Thr
1 5
<210> 275
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 275
Phe Gln Asn Asn Gly Val
1 5
<210> 276
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 276
Ala Ser Ser Leu Ala Asp Ile Tyr Glu Gln Tyr
1 5 10
<210> 277
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 277
atggaaactc tcctgggagt gtctttggtg attctatggc ttcaactggc tagggtgaac
60
agtcaacagg gagaagagga tcctcaggcc ttgagcatcc aggagggtga aaatgccacc
120
atgaactgca gttacaaaac tagtataaac aatttacagt ggtatagaca aaattcaggt
180
agaggccttg tccacctaat tttaatacgt tcaaatgaaa gagagaaaca cagtggaaga
240
ttaagagtca cgcttgacac ttccaagaaa agcagttcct tgttgatcac ggcttcccgg
300
gcagcagaca ctgcttctta cttctgtgct acggaccgtc aaagcagcgg agacaagctg
360
acttttggga ccgggactcg tttagcagtt aggccc
396
<210> 278
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 278
atggagaccc tgctgggcgt gtccctggtc atcctgtggc tgcagctggc cagggtgaac
60
agccagcagg gagaggagga cccccaggcc ctgagcatcc aggagggcga gaacgccacc
120
atgaattgct cttacaagac aagcatcaac aatctgcagt ggtataggca gaactccggc
180
cgcggactgg tgcacctgat cctgatccgg agcaatgaga gagagaagca ctccggccgg
240
ctgagagtga ccctggacac atctaagaag tcctctagcc tgctgatcac cgcctctcgg
300
gcagcagata cagccagcta cttctgtgcc accgacagac agtcctctgg cgataagctg
360
acctttggca ccggcacaag gctggccgtg cgcccc
396
<210> 279
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 279
Met Glu Thr Leu Leu Gly Val Ser Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ala Arg Val Asn Ser Gln Gln Gly Glu Glu Asp Pro Gln Ala Leu Ser
20 25 30
Ile Gln Glu Gly Glu Asn Ala Thr Met Asn Cys Ser Tyr Lys Thr Ser
35 40 45
Ile Asn Asn Leu Gln Trp Tyr Arg Gln Asn Ser Gly Arg Gly Leu Val
50 55 60
His Leu Ile Leu Ile Arg Ser Asn Glu Arg Glu Lys His Ser Gly Arg
65 70 75 80
Leu Arg Val Thr Leu Asp Thr Ser Lys Lys Ser Ser Ser Leu Leu Ile
85 90 95
Thr Ala Ser Arg Ala Ala Asp Thr Ala Ser Tyr Phe Cys Ala Thr Asp
100 105 110
Arg Gln Ser Ser Gly Asp Lys Leu Thr Phe Gly Thr Gly Thr Arg Leu
115 120 125
Ala Val Arg Pro
130
<210> 280
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 280
atgggcacca ggctcctctg ctgggcggcc ctctgtctcc tgggagcaga actcacagaa
60
gctggagttg cccagtctcc cagatataag attatagaga aaaggcagag tgtggctttt
120
tggtgcaatc ctatatctgg ccatgctacc ctttactggt accagcagat cctgggacag
180
ggcccaaagc ttctgattca gtttcagaat aacggtgtag tggatgattc acagttgcct
240
aaggatcgat tttctgcaga gaggctcaaa ggagtagact ccactctcaa gatccagcct
300
gcaaagcttg aggactcggc cgtgtatctc tgtgccagca gcttagccga catctacgag
360
cagtacttcg ggccgggcac caggctcacg gtcaca
396
<210> 281
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 281
atgggaacaa ggctgctgtg ctgggccgcc ctgtgcctgc tgggagcaga gctgaccgag
60
gccggcgtgg cccagagccc ccggtacaag atcatcgaga agagacagag cgtggccttc
120
tggtgcaacc ctatctccgg ccacgccaca ctgtactggt atcagcagat cctgggccag
180
ggcccaaagc tgctgatcca gttccagaac aatggcgtgg tggacgattc ccagctgccc
240
aaggaccggt tttctgccga gagactgaag ggcgtggatt ccaccctgaa gatccagccc
300
gccaagctgg aggactctgc cgtgtatctg tgcgccagct ccctggccga catctacgag
360
cagtatttcg gccctggcac aaggctgacc gtgaca
396
<210> 282
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 282
Met Gly Thr Arg Leu Leu Cys Trp Ala Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Glu Leu Thr Glu Ala Gly Val Ala Gln Ser Pro Arg Tyr Lys Ile Ile
20 25 30
Glu Lys Arg Gln Ser Val Ala Phe Trp Cys Asn Pro Ile Ser Gly His
35 40 45
Ala Thr Leu Tyr Trp Tyr Gln Gln Ile Leu Gly Gln Gly Pro Lys Leu
50 55 60
Leu Ile Gln Phe Gln Asn Asn Gly Val Val Asp Asp Ser Gln Leu Pro
65 70 75 80
Lys Asp Arg Phe Ser Ala Glu Arg Leu Lys Gly Val Asp Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ala Lys Leu Glu Asp Ser Ala Val Tyr Leu Cys Ala
100 105 110
Ser Ser Leu Ala Asp Ile Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Thr
130
<210> 283
<211> 269
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 283
Met Glu Thr Leu Leu Gly Val Ser Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ala Arg Val Asn Ser Gln Gln Gly Glu Glu Asp Pro Gln Ala Leu Ser
20 25 30
Ile Gln Glu Gly Glu Asn Ala Thr Met Asn Cys Ser Tyr Lys Thr Ser
35 40 45
Ile Asn Asn Leu Gln Trp Tyr Arg Gln Asn Ser Gly Arg Gly Leu Val
50 55 60
His Leu Ile Leu Ile Arg Ser Asn Glu Arg Glu Lys His Ser Gly Arg
65 70 75 80
Leu Arg Val Thr Leu Asp Thr Ser Lys Lys Ser Ser Ser Leu Leu Ile
85 90 95
Thr Ala Ser Arg Ala Ala Asp Thr Ala Ser Tyr Phe Cys Ala Thr Asp
100 105 110
Arg Gln Ser Ser Gly Asp Lys Leu Thr Phe Gly Thr Gly Thr Arg Leu
115 120 125
Ala Val Arg Pro Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu
130 135 140
Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe
145 150 155 160
Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile
165 170 175
Thr Asp Lys Thr Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn
180 185 190
Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile
195 200 205
Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp
210 215 220
Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe
225 230 235 240
Gln Asn Leu Ser Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val Ala
245 250 255
Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 284
<211> 305
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 284
Met Gly Thr Arg Leu Leu Cys Trp Ala Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Glu Leu Thr Glu Ala Gly Val Ala Gln Ser Pro Arg Tyr Lys Ile Ile
20 25 30
Glu Lys Arg Gln Ser Val Ala Phe Trp Cys Asn Pro Ile Ser Gly His
35 40 45
Ala Thr Leu Tyr Trp Tyr Gln Gln Ile Leu Gly Gln Gly Pro Lys Leu
50 55 60
Leu Ile Gln Phe Gln Asn Asn Gly Val Val Asp Asp Ser Gln Leu Pro
65 70 75 80
Lys Asp Arg Phe Ser Ala Glu Arg Leu Lys Gly Val Asp Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ala Lys Leu Glu Asp Ser Ala Val Tyr Leu Cys Ala
100 105 110
Ser Ser Leu Ala Asp Ile Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Thr Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys Asn
290 295 300
Ser
305
<210> 285
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 285
Val Val Gly Ala Cys Gly Val Gly Lys
1 5
<210> 286
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 286
Val Val Val Gly Ala Cys Gly Val Gly Lys
1 5 10
<210> 287
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 287
Thr Ser Glu Ser Asp Tyr Tyr
1 5
<210> 288
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 288
Gln Glu Ala Tyr Lys Gln Gln Asn
1 5
<210> 289
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 289
Ala Leu Tyr Ile Tyr Gly Gly Ser Gln Gly Asn Leu Ile
1 5 10
<210> 290
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 290
Ser Glu His Asn Arg
1 5
<210> 291
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 291
Phe Gln Asn Glu Ala Gln
1 5
<210> 292
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 292
Ala Ser Ser Ser Thr Asp Arg Ile Glu Ala Phe
1 5 10
<210> 293
<211> 408
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 293
atggcatgcc ctggcttcct gtgggcactt gtgatctcca cctgtcttga atttagcatg
60
gctcagacag tcactcagtc tcaaccagag atgtctgtgc aggaggcaga gaccgtgacc
120
ctgagctgca catatgacac cagtgagagt gattattatt tattctggta caagcagcct
180
cccagcaggc agatgattct cgttattcgc caagaagctt ataagcaaca gaatgcaaca
240
gagaatcgtt tctctgtgaa cttccagaaa gcagccaaat ccttcagtct caagatctca
300
gactcacagc tgggggatgc cgcgatgtat ttctgtgctc tctatattta tggaggaagc
360
caaggaaatc tcatctttgg aaaaggcact aaactctctg ttaaacca
408
<210> 294
<211> 408
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 294
atggcatgcc caggcttcct gtgggcactg gtcatcagca catgtctgga gttttctatg
60
gcccagaccg tgacacagtc tcagcctgag atgagcgtgc aggaggccga gaccgtgaca
120
ctgagctgca cctacgacac atctgagagc gattactatc tgttctggta taagcagcca
180
ccctccagac agatgatcct ggtcatcagg caggaggcct acaagcagca gaacgccacc
240
gagaatcggt tctccgtgaa ctttcagaag gccgccaagt ccttttctct gaagatcagc
300
gactcccagc tgggcgatgc cgccatgtat ttctgtgccc tgtacatcta tggcggctct
360
cagggcaatc tgatctttgg caagggcacc aagctgagcg tgaagcct
408
<210> 295
<211> 136
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 295
Met Ala Cys Pro Gly Phe Leu Trp Ala Leu Val Ile Ser Thr Cys Leu
1 5 10 15
Glu Phe Ser Met Ala Gln Thr Val Thr Gln Ser Gln Pro Glu Met Ser
20 25 30
Val Gln Glu Ala Glu Thr Val Thr Leu Ser Cys Thr Tyr Asp Thr Ser
35 40 45
Glu Ser Asp Tyr Tyr Leu Phe Trp Tyr Lys Gln Pro Pro Ser Arg Gln
50 55 60
Met Ile Leu Val Ile Arg Gln Glu Ala Tyr Lys Gln Gln Asn Ala Thr
65 70 75 80
Glu Asn Arg Phe Ser Val Asn Phe Gln Lys Ala Ala Lys Ser Phe Ser
85 90 95
Leu Lys Ile Ser Asp Ser Gln Leu Gly Asp Ala Ala Met Tyr Phe Cys
100 105 110
Ala Leu Tyr Ile Tyr Gly Gly Ser Gln Gly Asn Leu Ile Phe Gly Lys
115 120 125
Gly Thr Lys Leu Ser Val Lys Pro
130 135
<210> 296
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 296
atgggcacca gcctcctctg ctggatggcc ctgtgtctcc tgggggcaga tcacgcagat
60
actggagtct cccaggaccc cagacacaag atcacaaaga ggggacagaa tgtaactttc
120
aggtgtgatc caatttctga acacaaccgc ctttattggt accgacagac cctggggcag
180
ggcccagagt ttctgactta cttccagaat gaagctcaac tagaaaaatc aaggctgctc
240
agtgatcggt tctctgcaga gaggcctaag ggatctttct ccaccttgga gatccagcgc
300
acagagcagg gggactcggc catgtatctc tgtgccagca gctccaccga caggattgaa
360
gctttctttg gacaaggcac cagactcaca gttgta
396
<210> 297
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 297
atgggcacct ccctgctgtg ctggatggca ctgtgcctgc tgggagcaga ccacgcagat
60
acaggcgtgt ctcaggaccc acgccacaag atcaccaagc ggggccagaa cgtgacattc
120
agatgcgatc ccatctccga gcacaatagg ctgtactggt ataggcagac cctgggacag
180
ggaccagagt tcctgacata ctttcagaac gaggcccagc tggagaagag ccggctgctg
240
tccgacagat tctctgccga gaggcccaag ggctctttta gcaccctgga gatccagaga
300
acagagcagg gcgacagcgc catgtatctg tgcgccagct cctctaccga taggatcgag
360
gccttctttg gccagggcac ccgcctgaca gtggtg
396
<210> 298
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 298
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Ser Thr Asp Arg Ile Glu Ala Phe Phe Gly Gln Gly Thr Arg
115 120 125
Leu Thr Val Val
130
<210> 299
<211> 273
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 299
Met Ala Cys Pro Gly Phe Leu Trp Ala Leu Val Ile Ser Thr Cys Leu
1 5 10 15
Glu Phe Ser Met Ala Gln Thr Val Thr Gln Ser Gln Pro Glu Met Ser
20 25 30
Val Gln Glu Ala Glu Thr Val Thr Leu Ser Cys Thr Tyr Asp Thr Ser
35 40 45
Glu Ser Asp Tyr Tyr Leu Phe Trp Tyr Lys Gln Pro Pro Ser Arg Gln
50 55 60
Met Ile Leu Val Ile Arg Gln Glu Ala Tyr Lys Gln Gln Asn Ala Thr
65 70 75 80
Glu Asn Arg Phe Ser Val Asn Phe Gln Lys Ala Ala Lys Ser Phe Ser
85 90 95
Leu Lys Ile Ser Asp Ser Gln Leu Gly Asp Ala Ala Met Tyr Phe Cys
100 105 110
Ala Leu Tyr Ile Tyr Gly Gly Ser Gln Gly Asn Leu Ile Phe Gly Lys
115 120 125
Gly Thr Lys Leu Ser Val Lys Pro Asp Ile Gln Asn Pro Glu Pro Ala
130 135 140
Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu
145 150 155 160
Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser
165 170 175
Gly Thr Phe Ile Thr Asp Lys Thr Val Leu Asp Met Lys Ala Met Asp
180 185 190
Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr
195 200 205
Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp
210 215 220
Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met
225 230 235 240
Asn Leu Asn Phe Gln Asn Leu Ser Val Met Gly Leu Arg Ile Leu Leu
245 250 255
Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser
260 265 270
Ser
<210> 300
<211> 305
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 300
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Ser Thr Asp Arg Ile Glu Ala Phe Phe Gly Gln Gly Thr Arg
115 120 125
Leu Thr Val Val Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys Asn
290 295 300
Ser
305
<210> 301
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 301
Val Val Gly Ala Asp Gly Val Gly Lys
1 5
<210> 302
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 302
Val Val Val Gly Ala Asp Gly Val Gly Lys
1 5 10
<210> 303
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 303
Val Ser Asn Ala Tyr Asn
1 5
<210> 304
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 304
Gly Ser Lys Pro
1
<210> 305
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 305
Ala Thr Tyr Asn Phe Asn Lys Phe Tyr
1 5
<210> 306
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 306
Ser Gly His Thr Ser
1 5
<210> 307
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 307
Tyr Asp Glu Gly Glu Glu
1 5
<210> 308
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 308
Ala Ser Thr Thr Phe Lys Thr Gly Arg Ala Ile Glu Lys Leu Phe
1 5 10 15
<210> 309
<211> 387
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 309
atggctttgc agagcactct gggggcggtg tggctagggc ttctcctcaa ctctctctgg
60
aaggttgcag aaagcaagga ccaagtgttt cagccttcca cagtggcatc ttcagaggga
120
gctgtggtgg aaatcttctg taatcactct gtgtccaatg cttacaactt cttctggtac
180
cttcacttcc cgggatgtgc accaagactc cttgttaaag gctcaaagcc ttctcagcag
240
ggacgataca acatgaccta tgaacggttc tcttcatcgc tgctcatcct ccaggtgcgg
300
gaggcagatg ctgctgttta ctactgtgct acgtacaact tcaacaaatt ttactttgga
360
tctgggacca aactcaatgt aaaacca
387
<210> 310
<211> 387
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 310
atggccctgc agtctacact gggagccgtg tggctgggac tgctgctgaa ctctctgtgg
60
aaggtggccg agagcaagga ccaggtgttc cagcctagca ccgtggcctc ctctgaggga
120
gcagtggtgg agatcttttg caatcactcc gtgtctaacg cctacaattt cttttggtat
180
ctgcactttc caggatgtgc accaaggctg ctggtgaagg gcagcaagcc atcccagcag
240
ggccggtaca acatgaccta tgagagattc agctcctctc tgctgatcct gcaggtgaga
300
gaggccgatg ccgccgtgta ctattgtgcc acctacaact ttaataagtt ctattttggc
360
tccggcacaa agctgaatgt gaagcct
387
<210> 311
<211> 129
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 311
Met Ala Leu Gln Ser Thr Leu Gly Ala Val Trp Leu Gly Leu Leu Leu
1 5 10 15
Asn Ser Leu Trp Lys Val Ala Glu Ser Lys Asp Gln Val Phe Gln Pro
20 25 30
Ser Thr Val Ala Ser Ser Glu Gly Ala Val Val Glu Ile Phe Cys Asn
35 40 45
His Ser Val Ser Asn Ala Tyr Asn Phe Phe Trp Tyr Leu His Phe Pro
50 55 60
Gly Cys Ala Pro Arg Leu Leu Val Lys Gly Ser Lys Pro Ser Gln Gln
65 70 75 80
Gly Arg Tyr Asn Met Thr Tyr Glu Arg Phe Ser Ser Ser Leu Leu Ile
85 90 95
Leu Gln Val Arg Glu Ala Asp Ala Ala Val Tyr Tyr Cys Ala Thr Tyr
100 105 110
Asn Phe Asn Lys Phe Tyr Phe Gly Ser Gly Thr Lys Leu Asn Val Lys
115 120 125
Pro
<210> 312
<211> 405
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 312
atgggaccca ggctcctctt ctgggcactg ctttgtctcc tcggaacagg cccagtggag
60
gctggagtca cacaaagtcc cacacacctg atcaaaacga gaggacagca agcgactctg
120
agatgctctc ctatctctgg gcacaccagt gtgtactggt accaacaggc cctgggtctg
180
ggcctccagt tcctcctttg gtatgacgag ggtgaagaga gaaacagagg aaacttccct
240
cctagatttt caggtcgcca gttccctaat tatagctctg agctgaatgt gaacgccttg
300
gagctggagg actcggccct gtatctctgt gccagcacca cttttaagac gggacgggca
360
attgaaaaac tgttttttgg cagtggaacc cagctctctg tcttg
405
<210> 313
<211> 405
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 313
atgggaccaa ggctgctgtt ctgggcactg ctgtgcctgc tgggaaccgg acctgtggag
60
gccggcgtga cccagtctcc aacacacctg atcaagacca ggggacagca ggccacactg
120
aggtgtagcc ccatctccgg ccacacaagc gtgtactggt atcagcaggc cctgggactg
180
ggactgcagt tcctgctgtg gtacgacgag ggcgaggaga ggaaccgcgg caatttccca
240
cctcggttca gcggccggca gtttcccaac tacagctccg agctgaacgt gaatgccctg
300
gagctggagg acagcgccct gtatctgtgc gcctccacca cattcaagac cggcagggcc
360
atcgagaagc tgttctttgg ctctggcacc cagctgagcg tgctg
405
<210> 314
<211> 135
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 314
Met Gly Pro Arg Leu Leu Phe Trp Ala Leu Leu Cys Leu Leu Gly Thr
1 5 10 15
Gly Pro Val Glu Ala Gly Val Thr Gln Ser Pro Thr His Leu Ile Lys
20 25 30
Thr Arg Gly Gln Gln Ala Thr Leu Arg Cys Ser Pro Ile Ser Gly His
35 40 45
Thr Ser Val Tyr Trp Tyr Gln Gln Ala Leu Gly Leu Gly Leu Gln Phe
50 55 60
Leu Leu Trp Tyr Asp Glu Gly Glu Glu Arg Asn Arg Gly Asn Phe Pro
65 70 75 80
Pro Arg Phe Ser Gly Arg Gln Phe Pro Asn Tyr Ser Ser Glu Leu Asn
85 90 95
Val Asn Ala Leu Glu Leu Glu Asp Ser Ala Leu Tyr Leu Cys Ala Ser
100 105 110
Thr Thr Phe Lys Thr Gly Arg Ala Ile Glu Lys Leu Phe Phe Gly Ser
115 120 125
Gly Thr Gln Leu Ser Val Leu
130 135
<210> 315
<211> 266
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 315
Met Ala Leu Gln Ser Thr Leu Gly Ala Val Trp Leu Gly Leu Leu Leu
1 5 10 15
Asn Ser Leu Trp Lys Val Ala Glu Ser Lys Asp Gln Val Phe Gln Pro
20 25 30
Ser Thr Val Ala Ser Ser Glu Gly Ala Val Val Glu Ile Phe Cys Asn
35 40 45
His Ser Val Ser Asn Ala Tyr Asn Phe Phe Trp Tyr Leu His Phe Pro
50 55 60
Gly Cys Ala Pro Arg Leu Leu Val Lys Gly Ser Lys Pro Ser Gln Gln
65 70 75 80
Gly Arg Tyr Asn Met Thr Tyr Glu Arg Phe Ser Ser Ser Leu Leu Ile
85 90 95
Leu Gln Val Arg Glu Ala Asp Ala Ala Val Tyr Tyr Cys Ala Thr Tyr
100 105 110
Asn Phe Asn Lys Phe Tyr Phe Gly Ser Gly Thr Lys Leu Asn Val Lys
115 120 125
Pro Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro
130 135 140
Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln
145 150 155 160
Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys
165 170 175
Thr Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile
180 185 190
Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu
195 200 205
Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu
210 215 220
Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu
225 230 235 240
Ser Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn
245 250 255
Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 316
<211> 308
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 316
Met Gly Pro Arg Leu Leu Phe Trp Ala Leu Leu Cys Leu Leu Gly Thr
1 5 10 15
Gly Pro Val Glu Ala Gly Val Thr Gln Ser Pro Thr His Leu Ile Lys
20 25 30
Thr Arg Gly Gln Gln Ala Thr Leu Arg Cys Ser Pro Ile Ser Gly His
35 40 45
Thr Ser Val Tyr Trp Tyr Gln Gln Ala Leu Gly Leu Gly Leu Gln Phe
50 55 60
Leu Leu Trp Tyr Asp Glu Gly Glu Glu Arg Asn Arg Gly Asn Phe Pro
65 70 75 80
Pro Arg Phe Ser Gly Arg Gln Phe Pro Asn Tyr Ser Ser Glu Leu Asn
85 90 95
Val Asn Ala Leu Glu Leu Glu Asp Ser Ala Leu Tyr Leu Cys Ala Ser
100 105 110
Thr Thr Phe Lys Thr Gly Arg Ala Ile Glu Lys Leu Phe Phe Gly Ser
115 120 125
Gly Thr Gln Leu Ser Val Leu Lys Asp Leu Arg Asn Val Thr Pro Pro
130 135 140
Lys Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln
145 150 155 160
Lys Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val
165 170 175
Glu Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser
180 185 190
Thr Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser
195 200 205
Ser Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His
210 215 220
Phe Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp
225 230 235 240
Pro Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala
245 250 255
Trp Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly
260 265 270
Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr
275 280 285
Leu Tyr Ala Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys
290 295 300
Lys Lys Asn Ser
305
<210> 317
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 317
Val Val Gly Ala Asp Gly Val Gly Lys
1 5
<210> 318
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 318
Val Val Val Gly Ala Asp Gly Val Gly Lys
1 5 10
<210> 319
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 319
Thr Ser Gly Phe Asn Gly
1 5
<210> 320
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 320
Asn Val Leu Asp Gly Leu
1 5
<210> 321
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 321
Ala Val Arg Asp Arg Gly Gly Ser Tyr Ile Pro Thr
1 5 10
<210> 322
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 322
Met Asn His Glu Tyr
1 5
<210> 323
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 323
Ser Met Asn Val Glu Val
1 5
<210> 324
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 324
Ala Ser Ser Ser Arg Gly His Ser Gly Thr Glu Ala Phe
1 5 10
<210> 325
<211> 384
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 325
atgtggggag ttttccttct ttatgtttcc atgaagatgg gaggcactac aggacaaaac
60
attgaccagc ccactgagat gacagctacg gaaggtgcca ttgtccagat caactgcacg
120
taccagacat ctgggttcaa cgggctgttc tggtaccagc aacatgctgg cgaagcaccc
180
acatttctgt cttacaatgt tctggatggt ttggaggaga aaggtcgttt ttcttcattc
240
cttagtcggt ctaaagggta cagttacctc cttttgaagg agctccagat gaaagactct
300
gcctcttacc tctgtgctgt gagagatcga ggaggaagct acatacctac atttggaaga
360
ggaaccagcc ttattgttca tccg
384
<210> 326
<211> 384
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 326
atgtggggcg tgtttctgct gtacgtgtct atgaagatgg gcggcaccac aggccagaac
60
atcgaccagc ctaccgagat gaccgccaca gagggcgcca tcgtgcagat caactgcacc
120
taccagacat ctggcttcaa tggcctgttt tggtatcagc agcacgccgg cgaggcccca
180
acattcctgt cctataatgt gctggatggc ctggaggaga agggcaggtt ctctagcttt
240
ctgtcccgct ctaagggcta cagctatctg ctgctgaagg agctgcagat gaaggacagc
300
gcctcctacc tgtgcgccgt gcgggataga ggaggctcct atatccctac ctttggccgg
360
ggcacatctc tgatcgtgca ccca
384
<210> 327
<211> 128
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 327
Met Trp Gly Val Phe Leu Leu Tyr Val Ser Met Lys Met Gly Gly Thr
1 5 10 15
Thr Gly Gln Asn Ile Asp Gln Pro Thr Glu Met Thr Ala Thr Glu Gly
20 25 30
Ala Ile Val Gln Ile Asn Cys Thr Tyr Gln Thr Ser Gly Phe Asn Gly
35 40 45
Leu Phe Trp Tyr Gln Gln His Ala Gly Glu Ala Pro Thr Phe Leu Ser
50 55 60
Tyr Asn Val Leu Asp Gly Leu Glu Glu Lys Gly Arg Phe Ser Ser Phe
65 70 75 80
Leu Ser Arg Ser Lys Gly Tyr Ser Tyr Leu Leu Leu Lys Glu Leu Gln
85 90 95
Met Lys Asp Ser Ala Ser Tyr Leu Cys Ala Val Arg Asp Arg Gly Gly
100 105 110
Ser Tyr Ile Pro Thr Phe Gly Arg Gly Thr Ser Leu Ile Val His Pro
115 120 125
<210> 328
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 328
atgggccccc agctccttgg ctatgtggtc ctttgccttc taggagcagg ccccctggaa
60
gcccaagtga cccagaaccc aagatacctc atcacagtga ctggaaagaa gttaacagtg
120
acttgttctc agaatatgaa ccatgagtat atgtcctggt atcgacaaga cccagggctg
180
ggcttaaggc agatctacta ttcaatgaat gttgaggtga ctgataaggg agatgttcct
240
gaagggtaca aagtctctcg aaaagagaag aggaatttcc ccctgatcct ggagtcgccc
300
agccccaacc agacctctct gtacttctgt gccagcagtt ccagggggca ttcgggcact
360
gaagctttct ttggacaagg caccagactc acagttgta
399
<210> 329
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 329
atgggaccac agctgctggg atacgtggtg ctgtgcctgc tgggagcagg accactggag
60
gcacaggtga cccagaaccc acggtatctg atcaccgtga caggcaagaa gctgaccgtg
120
acatgttctc agaacatgaa tcacgagtac atgagctggt ataggcagga ccctggactg
180
ggactgagac agatctacta tagcatgaat gtggaggtga ccgacaaggg cgatgtgccc
240
gagggctaca aggtgtccag gaaggagaag cgcaacttcc ctctgatcct ggagtcccca
300
tctcccaatc agaccagcct gtatttttgc gccagctcct ctaggggaca ctccggaaca
360
gaggccttct ttggccaggg caccaggctg acagtggtg
399
<210> 330
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 330
Met Gly Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Ser Arg Gly His Ser Gly Thr Glu Ala Phe Phe Gly Gln Gly Thr
115 120 125
Arg Leu Thr Val Val
130
<210> 331
<211> 265
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 331
Met Trp Gly Val Phe Leu Leu Tyr Val Ser Met Lys Met Gly Gly Thr
1 5 10 15
Thr Gly Gln Asn Ile Asp Gln Pro Thr Glu Met Thr Ala Thr Glu Gly
20 25 30
Ala Ile Val Gln Ile Asn Cys Thr Tyr Gln Thr Ser Gly Phe Asn Gly
35 40 45
Leu Phe Trp Tyr Gln Gln His Ala Gly Glu Ala Pro Thr Phe Leu Ser
50 55 60
Tyr Asn Val Leu Asp Gly Leu Glu Glu Lys Gly Arg Phe Ser Ser Phe
65 70 75 80
Leu Ser Arg Ser Lys Gly Tyr Ser Tyr Leu Leu Leu Lys Glu Leu Gln
85 90 95
Met Lys Asp Ser Ala Ser Tyr Leu Cys Ala Val Arg Asp Arg Gly Gly
100 105 110
Ser Tyr Ile Pro Thr Phe Gly Arg Gly Thr Ser Leu Ile Val His Pro
115 120 125
Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg
130 135 140
Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile
145 150 155 160
Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Thr
165 170 175
Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala
180 185 190
Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr
195 200 205
Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr
210 215 220
Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Ser
225 230 235 240
Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu
245 250 255
Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 332
<211> 306
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 332
Met Gly Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Ser Arg Gly His Ser Gly Thr Glu Ala Phe Phe Gly Gln Gly Thr
115 120 125
Arg Leu Thr Val Val Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val
130 135 140
Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala
145 150 155 160
Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu
165 170 175
Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp
180 185 190
Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg
195 200 205
Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg
210 215 220
Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu
225 230 235 240
Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly
245 250 255
Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu
260 265 270
Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr
275 280 285
Ala Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys
290 295 300
Asn Ser
305
<210> 333
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 333
Val Val Gly Ala Asp Gly Val Gly Lys
1 5
<210> 334
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 334
Val Val Val Gly Ala Asp Gly Val Gly Lys
1 5 10
<210> 335
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 335
Thr Ser Ile Asn Asn
1 5
<210> 336
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 336
Ile Arg Ser Asn Glu Arg Glu
1 5
<210> 337
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 337
Ala Gly Leu Tyr Ser Ser Ala Ser Lys Ile Ile
1 5 10
<210> 338
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 338
Met Asn His Glu Tyr
1 5
<210> 339
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 339
Ser Met Asn Val Glu Val
1 5
<210> 340
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 340
Ala Ser Ser Ser Arg Gly His Ser Gly Thr Glu Ala Phe
1 5 10
<210> 341
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 341
atggaaactc tcctgggagt gtctttggtg attctatggc ttcaactggc tagggtgaac
60
agtcaacagg gagaagagga tcctcaggcc ttgagcatcc aggagggtga aaatgccacc
120
atgaactgca gttacaaaac tagtataaac aatttacagt ggtatagaca aaattcaggt
180
agaggccttg tccacctaat tttaatacgt tcaaatgaaa gagagaaaca cagtggaaga
240
ttaagagtca cgcttgacac ttccaagaaa agcagttcct tgttgatcac ggcttcccgg
300
gcagcagaca ctgcttctta cttctgtgct gggctgtaca gcagtgcttc caagataatc
360
tttggatcag ggaccagact cagcatccgg cca
393
<210> 342
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 342
atggagacac tgctgggcgt gtccctggtc atcctgtggc tgcagctggc cagagtgaac
60
agccagcagg gagaggagga ccctcaggcc ctgagcatcc aggagggcga gaacgccacc
120
atgaattgct cttacaagac aagcatcaac aatctgcagt ggtataggca gaactccggc
180
cgcggactgg tgcacctgat cctgatcagg tctaatgagc gcgagaagca cagcggccgg
240
ctgagagtga ccctggacac aagcaagaag tctagctccc tgctgatcac cgcctccaga
300
gcagcagata cagcctctta cttctgtgcc ggcctgtatt ctagcgcctc caagatcatc
360
tttggcagcg gcacccggct gtccatcaga ccc
393
<210> 343
<211> 131
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 343
Met Glu Thr Leu Leu Gly Val Ser Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ala Arg Val Asn Ser Gln Gln Gly Glu Glu Asp Pro Gln Ala Leu Ser
20 25 30
Ile Gln Glu Gly Glu Asn Ala Thr Met Asn Cys Ser Tyr Lys Thr Ser
35 40 45
Ile Asn Asn Leu Gln Trp Tyr Arg Gln Asn Ser Gly Arg Gly Leu Val
50 55 60
His Leu Ile Leu Ile Arg Ser Asn Glu Arg Glu Lys His Ser Gly Arg
65 70 75 80
Leu Arg Val Thr Leu Asp Thr Ser Lys Lys Ser Ser Ser Leu Leu Ile
85 90 95
Thr Ala Ser Arg Ala Ala Asp Thr Ala Ser Tyr Phe Cys Ala Gly Leu
100 105 110
Tyr Ser Ser Ala Ser Lys Ile Ile Phe Gly Ser Gly Thr Arg Leu Ser
115 120 125
Ile Arg Pro
130
<210> 344
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 344
atgggccccc agctccttgg ctatgtggtc ctttgccttc taggagcagg ccccctggaa
60
gcccaagtga cccagaaccc aagatacctc atcacagtga ctggaaagaa gttaacagtg
120
acttgttctc agaatatgaa ccatgagtat atgtcctggt atcgacaaga cccagggctg
180
ggcttaaggc agatctacta ttcaatgaat gttgaggtga ctgataaggg agatgttcct
240
gaagggtaca aagtctctcg aaaagagaag aggaatttcc ccctgatcct ggagtcgccc
300
agccccaacc agacctctct gtacttctgt gccagcagtt ccagggggca ttcgggcact
360
gaagctttct ttggacaagg caccagactc acagttgta
399
<210> 345
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 345
atgggcccac agctgctggg ctacgtggtg ctgtgcctgc tgggagcagg accactggag
60
gcacaggtga cccagaaccc caggtatctg atcaccgtga caggcaagaa gctgaccgtg
120
acatgtagcc agaacatgaa tcacgagtac atgtcctggt ataggcagga ccccggactg
180
ggactgagac agatctacta ttccatgaat gtggaggtga ccgacaaggg cgatgtgcct
240
gagggctaca aggtgtctag gaaggagaag cgcaacttcc cactgatcct ggagtcccca
300
tctcccaatc agacctccct gtatttttgc gccagctcct ctaggggcca ctctggcaca
360
gaggccttct ttggccaggg caccaggctg acagtggtg
399
<210> 346
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 346
Met Gly Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Ser Arg Gly His Ser Gly Thr Glu Ala Phe Phe Gly Gln Gly Thr
115 120 125
Arg Leu Thr Val Val
130
<210> 347
<211> 268
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 347
Met Glu Thr Leu Leu Gly Val Ser Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ala Arg Val Asn Ser Gln Gln Gly Glu Glu Asp Pro Gln Ala Leu Ser
20 25 30
Ile Gln Glu Gly Glu Asn Ala Thr Met Asn Cys Ser Tyr Lys Thr Ser
35 40 45
Ile Asn Asn Leu Gln Trp Tyr Arg Gln Asn Ser Gly Arg Gly Leu Val
50 55 60
His Leu Ile Leu Ile Arg Ser Asn Glu Arg Glu Lys His Ser Gly Arg
65 70 75 80
Leu Arg Val Thr Leu Asp Thr Ser Lys Lys Ser Ser Ser Leu Leu Ile
85 90 95
Thr Ala Ser Arg Ala Ala Asp Thr Ala Ser Tyr Phe Cys Ala Gly Leu
100 105 110
Tyr Ser Ser Ala Ser Lys Ile Ile Phe Gly Ser Gly Thr Arg Leu Ser
115 120 125
Ile Arg Pro Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys
130 135 140
Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp
145 150 155 160
Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr
165 170 175
Asp Lys Thr Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly
180 185 190
Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe
195 200 205
Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala
210 215 220
Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln
225 230 235 240
Asn Leu Ser Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val Ala Gly
245 250 255
Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 348
<211> 306
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 348
Met Gly Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Ser Arg Gly His Ser Gly Thr Glu Ala Phe Phe Gly Gln Gly Thr
115 120 125
Arg Leu Thr Val Val Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val
130 135 140
Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala
145 150 155 160
Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu
165 170 175
Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp
180 185 190
Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg
195 200 205
Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg
210 215 220
Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu
225 230 235 240
Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly
245 250 255
Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu
260 265 270
Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr
275 280 285
Ala Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys
290 295 300
Asn Ser
305
<210> 349
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 349
Val Val Gly Ala Asp Gly Val Gly Lys
1 5
<210> 350
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 350
Val Val Val Gly Ala Asp Gly Val Gly Lys
1 5 10
<210> 351
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 351
Asn Ile Ala Thr Asn Asp Tyr
1 5
<210> 352
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 352
Gly Tyr Lys Thr Lys
1 5
<210> 353
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 353
Leu Ala Asn Thr Gly Gly Phe Lys Thr Ile
1 5 10
<210> 354
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 354
Ser Gly His Val Ser
1 5
<210> 355
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 355
Phe Gln Asn Glu Ala Gln
1 5
<210> 356
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 356
Ala Thr Tyr Lys Val Gly Asp Glu Gln Phe
1 5 10
<210> 357
<211> 378
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 357
atgaggcaag tggcgagagt gatcgtgttc ctgaccctga gtactttgag ccttgctaag
60
accacccagc ccatctccat ggactcatat gaaggacaag aagtgaacat aacctgtagc
120
cacaacaaca ttgctacaaa tgattatatc acgtggtacc aacagtttcc cagccaagga
180
ccacgattta ttattcaagg atacaagaca aaagttacaa acgaagtggc ctccctgttt
240
atccctgccg acagaaagtc cagcactctg agcctgcccc gggtttccct gagcgacact
300
gctgtgtact actgcctcgc taatactgga ggcttcaaaa ctatctttgg agcaggaaca
360
agactatttg ttaaagca
378
<210> 358
<211> 378
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 358
atgaggcagg tggcacgcgt gatcgtgttt ctgaccctga gcacactgtc cctggccaag
60
accacacagc ctatctctat ggacagctac gagggccagg aggtgaacat cacctgctct
120
cacaacaata tcgccaccaa tgattacatc acatggtatc agcagttccc cagccagggc
180
cctcggttta tcatccaggg ctataagacc aaggtgacaa acgaggtggc cagcctgttc
240
atccctgccg acaggaagtc tagcaccctg tccctgccac gcgtgagcct gtccgataca
300
gccgtgtact attgtctggc caataccggc ggcttcaaga caatctttgg cgccggcacc
360
agactgtttg tgaaggcc
378
<210> 359
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 359
Met Arg Gln Val Ala Arg Val Ile Val Phe Leu Thr Leu Ser Thr Leu
1 5 10 15
Ser Leu Ala Lys Thr Thr Gln Pro Ile Ser Met Asp Ser Tyr Glu Gly
20 25 30
Gln Glu Val Asn Ile Thr Cys Ser His Asn Asn Ile Ala Thr Asn Asp
35 40 45
Tyr Ile Thr Trp Tyr Gln Gln Phe Pro Ser Gln Gly Pro Arg Phe Ile
50 55 60
Ile Gln Gly Tyr Lys Thr Lys Val Thr Asn Glu Val Ala Ser Leu Phe
65 70 75 80
Ile Pro Ala Asp Arg Lys Ser Ser Thr Leu Ser Leu Pro Arg Val Ser
85 90 95
Leu Ser Asp Thr Ala Val Tyr Tyr Cys Leu Ala Asn Thr Gly Gly Phe
100 105 110
Lys Thr Ile Phe Gly Ala Gly Thr Arg Leu Phe Val Lys Ala
115 120 125
<210> 360
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 360
atgggcacca ggctcctctg ctgggtggtc ctgggtttcc tagggacaga tcacacaggt
60
gctggagtct cccagtcccc taggtacaaa gtcgcaaaga gaggacagga tgtagctctc
120
aggtgtgatc caatttcggg tcatgtatcc cttttttggt accaacaggc cctggggcag
180
gggccagagt ttctgactta tttccagaat gaagctcaac tagacaaatc ggggctgccc
240
agtgatcgct tctttgcaga aaggcctgag ggatccgtct ccactctgaa gatccagcgc
300
acacagcagg aggactccgc cgtgtatctc tgtgccacct ataaggtcgg ggatgagcag
360
ttcttcgggc cagggacacg gctcaccgtg cta
393
<210> 361
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 361
atgggaacca ggctgctgtg ctgggtggtg ctgggcttcc tgggaaccga ccacacagga
60
gcaggcgtgt cccagtctcc aaggtacaag gtggcaaaga ggggacagga cgtggccctg
120
agatgtgatc ctatctccgg ccacgtgtct ctgttttggt accagcaggc cctgggacag
180
ggacctgagt tcctgaccta ttttcagaac gaggcacagc tggacaagag cggactgcca
240
tccgatcggt tctttgcaga gagaccagag ggcagcgtgt ccaccctgaa gatccagagg
300
acacagcagg aggactccgc cgtgtacctg tgcgccacat ataaagtggg cgatgagcag
360
ttctttggcc caggcacccg gctgacagtg ctg
393
<210> 362
<211> 131
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 362
Met Gly Thr Arg Leu Leu Cys Trp Val Val Leu Gly Phe Leu Gly Thr
1 5 10 15
Asp His Thr Gly Ala Gly Val Ser Gln Ser Pro Arg Tyr Lys Val Ala
20 25 30
Lys Arg Gly Gln Asp Val Ala Leu Arg Cys Asp Pro Ile Ser Gly His
35 40 45
Val Ser Leu Phe Trp Tyr Gln Gln Ala Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Asp Lys Ser Gly Leu Pro
65 70 75 80
Ser Asp Arg Phe Phe Ala Glu Arg Pro Glu Gly Ser Val Ser Thr Leu
85 90 95
Lys Ile Gln Arg Thr Gln Gln Glu Asp Ser Ala Val Tyr Leu Cys Ala
100 105 110
Thr Tyr Lys Val Gly Asp Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu
115 120 125
Thr Val Leu
130
<210> 363
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 363
Met Arg Gln Val Ala Arg Val Ile Val Phe Leu Thr Leu Ser Thr Leu
1 5 10 15
Ser Leu Ala Lys Thr Thr Gln Pro Ile Ser Met Asp Ser Tyr Glu Gly
20 25 30
Gln Glu Val Asn Ile Thr Cys Ser His Asn Asn Ile Ala Thr Asn Asp
35 40 45
Tyr Ile Thr Trp Tyr Gln Gln Phe Pro Ser Gln Gly Pro Arg Phe Ile
50 55 60
Ile Gln Gly Tyr Lys Thr Lys Val Thr Asn Glu Val Ala Ser Leu Phe
65 70 75 80
Ile Pro Ala Asp Arg Lys Ser Ser Thr Leu Ser Leu Pro Arg Val Ser
85 90 95
Leu Ser Asp Thr Ala Val Tyr Tyr Cys Leu Ala Asn Thr Gly Gly Phe
100 105 110
Lys Thr Ile Phe Gly Ala Gly Thr Arg Leu Phe Val Lys Ala Asp Ile
115 120 125
Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln
130 135 140
Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val
145 150 155 160
Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Thr Val Leu
165 170 175
Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser
180 185 190
Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala
195 200 205
Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys
210 215 220
Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Ser Val Met
225 230 235 240
Gly Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met
245 250 255
Thr Leu Arg Leu Trp Ser Ser
260
<210> 364
<211> 304
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 364
Met Gly Thr Arg Leu Leu Cys Trp Val Val Leu Gly Phe Leu Gly Thr
1 5 10 15
Asp His Thr Gly Ala Gly Val Ser Gln Ser Pro Arg Tyr Lys Val Ala
20 25 30
Lys Arg Gly Gln Asp Val Ala Leu Arg Cys Asp Pro Ile Ser Gly His
35 40 45
Val Ser Leu Phe Trp Tyr Gln Gln Ala Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Asp Lys Ser Gly Leu Pro
65 70 75 80
Ser Asp Arg Phe Phe Ala Glu Arg Pro Glu Gly Ser Val Ser Thr Leu
85 90 95
Lys Ile Gln Arg Thr Gln Gln Glu Asp Ser Ala Val Tyr Leu Cys Ala
100 105 110
Thr Tyr Lys Val Gly Asp Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu
115 120 125
Thr Val Leu Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu
130 135 140
Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu
145 150 155 160
Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp
165 170 175
Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln
180 185 190
Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg
195 200 205
Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln
210 215 220
Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser
225 230 235 240
Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala
245 250 255
Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu Ser Ala
260 265 270
Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val
275 280 285
Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys Asn Ser
290 295 300
<210> 365
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 365
Val Val Gly Ala Asp Gly Val Gly Lys
1 5
<210> 366
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 366
Val Val Val Gly Ala Asp Gly Val Gly Lys
1 5 10
<210> 367
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 367
Asp Ser Ala Ser Asn Tyr
1 5
<210> 368
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 368
Ile Arg Ser Asn Val Gly Glu
1 5
<210> 369
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 369
Ala Glu Thr Gly Phe Gln Lys Leu Val
1 5
<210> 370
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 370
Met Asp His Glu Asn
1 5
<210> 371
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 371
Ser Tyr Asp Val Lys Met
1 5
<210> 372
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 372
Ala Ser Ser Asp Trp Leu Ala Gly Ala Lys Asp Glu Gln Tyr
1 5 10
<210> 373
<211> 387
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 373
atgacatcca ttcgagctgt atttatattc ctgtggctgc agctggactt ggtgaatgga
60
gagaatgtgg agcagcatcc ttcaaccctg agtgtccagg agggagacag cgctgttatc
120
aagtgtactt attcagacag tgcctcaaac tacttccctt ggtataagca agaacttgga
180
aaaagacctc agcttattat agacattcgt tcaaatgtgg gcgaaaagaa agaccaacga
240
attgctgtta cattgaacaa gacagccaaa catttctccc tgcacatcac agagacccaa
300
cctgaagact cggctgtcta cttctgtgca gaaacaggct ttcagaaact tgtatttgga
360
actggcaccc gacttctggt cagtcca
387
<210> 374
<211> 387
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 374
atgacatcta tccgcgccgt gttcatcttt ctgtggctgc agctggacct ggtgaacggc
60
gagaatgtgg agcagcaccc aagcaccctg tccgtgcagg agggcgacag cgccgtgatc
120
aagtgcacat actctgatag cgcctccaac tactttccct ggtataagca ggagctgggc
180
aagcggcctc agctgatcat cgacatcaga tccaacgtgg gcgagaagaa ggatcagcgg
240
atcgccgtga ccctgaataa gacagccaag cacttcagcc tgcacatcac cgagacacag
300
cccgaggatt ccgccgtgta tttttgtgcc gagaccggct tccagaagct ggtgtttggc
360
accggcacaa gactgctggt gtcccct
387
<210> 375
<211> 129
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 375
Met Thr Ser Ile Arg Ala Val Phe Ile Phe Leu Trp Leu Gln Leu Asp
1 5 10 15
Leu Val Asn Gly Glu Asn Val Glu Gln His Pro Ser Thr Leu Ser Val
20 25 30
Gln Glu Gly Asp Ser Ala Val Ile Lys Cys Thr Tyr Ser Asp Ser Ala
35 40 45
Ser Asn Tyr Phe Pro Trp Tyr Lys Gln Glu Leu Gly Lys Arg Pro Gln
50 55 60
Leu Ile Ile Asp Ile Arg Ser Asn Val Gly Glu Lys Lys Asp Gln Arg
65 70 75 80
Ile Ala Val Thr Leu Asn Lys Thr Ala Lys His Phe Ser Leu His Ile
85 90 95
Thr Glu Thr Gln Pro Glu Asp Ser Ala Val Tyr Phe Cys Ala Glu Thr
100 105 110
Gly Phe Gln Lys Leu Val Phe Gly Thr Gly Thr Arg Leu Leu Val Ser
115 120 125
Pro
<210> 376
<211> 402
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 376
atgggaatca ggctcctctg tcgtgtggcc ttttgtttcc tggctgtagg cctcgtagat
60
gtgaaagtaa cccagagctc gagatatcta gtcaaaagga cgggagagaa agtttttctg
120
gaatgtgtcc aggatatgga ccatgaaaat atgttctggt atcgacaaga cccaggtctg
180
gggctacggc tgatctattt ctcatatgat gttaaaatga aagaaaaagg agatattcct
240
gaggggtaca gtgtctctag agagaagaag gagcgcttct ccctgattct ggagtccgcc
300
agcaccaacc agacatctat gtacctctgt gccagcagtg actggctagc gggagcgaag
360
gacgagcagt acttcgggcc gggcaccagg ctcacggtca ca
402
<210> 377
<211> 402
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 377
atgggcatcc ggctgctgtg cagagtggcc ttctgttttc tggccgtggg cctggtggac
60
gtgaaggtga cccagagctc ccggtacctg gtgaagagaa caggcgagaa ggtgttcctg
120
gagtgcgtgc aggacatgga tcacgagaac atgttttggt ataggcagga ccccggactg
180
ggactgagac tgatctactt cagctatgac gtgaagatga aggagaaggg cgacatccca
240
gagggctaca gcgtgtccag ggagaagaag gagcggttca gcctgatcct ggagtctgcc
300
agcaccaatc agacaagcat gtacctgtgc gcctctagcg actggctggc cggagcaaag
360
gatgagcagt atttcggccc aggcaccagg ctgaccgtga ca
402
<210> 378
<211> 134
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 378
Met Gly Ile Arg Leu Leu Cys Arg Val Ala Phe Cys Phe Leu Ala Val
1 5 10 15
Gly Leu Val Asp Val Lys Val Thr Gln Ser Ser Arg Tyr Leu Val Lys
20 25 30
Arg Thr Gly Glu Lys Val Phe Leu Glu Cys Val Gln Asp Met Asp His
35 40 45
Glu Asn Met Phe Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Leu
50 55 60
Ile Tyr Phe Ser Tyr Asp Val Lys Met Lys Glu Lys Gly Asp Ile Pro
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Arg Phe Ser Leu Ile
85 90 95
Leu Glu Ser Ala Ser Thr Asn Gln Thr Ser Met Tyr Leu Cys Ala Ser
100 105 110
Ser Asp Trp Leu Ala Gly Ala Lys Asp Glu Gln Tyr Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Thr
130
<210> 379
<211> 266
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 379
Met Thr Ser Ile Arg Ala Val Phe Ile Phe Leu Trp Leu Gln Leu Asp
1 5 10 15
Leu Val Asn Gly Glu Asn Val Glu Gln His Pro Ser Thr Leu Ser Val
20 25 30
Gln Glu Gly Asp Ser Ala Val Ile Lys Cys Thr Tyr Ser Asp Ser Ala
35 40 45
Ser Asn Tyr Phe Pro Trp Tyr Lys Gln Glu Leu Gly Lys Arg Pro Gln
50 55 60
Leu Ile Ile Asp Ile Arg Ser Asn Val Gly Glu Lys Lys Asp Gln Arg
65 70 75 80
Ile Ala Val Thr Leu Asn Lys Thr Ala Lys His Phe Ser Leu His Ile
85 90 95
Thr Glu Thr Gln Pro Glu Asp Ser Ala Val Tyr Phe Cys Ala Glu Thr
100 105 110
Gly Phe Gln Lys Leu Val Phe Gly Thr Gly Thr Arg Leu Leu Val Ser
115 120 125
Pro Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro
130 135 140
Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln
145 150 155 160
Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys
165 170 175
Thr Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile
180 185 190
Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu
195 200 205
Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu
210 215 220
Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu
225 230 235 240
Ser Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn
245 250 255
Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 380
<211> 307
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 380
Met Gly Ile Arg Leu Leu Cys Arg Val Ala Phe Cys Phe Leu Ala Val
1 5 10 15
Gly Leu Val Asp Val Lys Val Thr Gln Ser Ser Arg Tyr Leu Val Lys
20 25 30
Arg Thr Gly Glu Lys Val Phe Leu Glu Cys Val Gln Asp Met Asp His
35 40 45
Glu Asn Met Phe Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Leu
50 55 60
Ile Tyr Phe Ser Tyr Asp Val Lys Met Lys Glu Lys Gly Asp Ile Pro
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Arg Phe Ser Leu Ile
85 90 95
Leu Glu Ser Ala Ser Thr Asn Gln Thr Ser Met Tyr Leu Cys Ala Ser
100 105 110
Ser Asp Trp Leu Ala Gly Ala Lys Asp Glu Gln Tyr Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Thr Lys Asp Leu Arg Asn Val Thr Pro Pro Lys
130 135 140
Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys
145 150 155 160
Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu
165 170 175
Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr
180 185 190
Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser
195 200 205
Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe
210 215 220
Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro
225 230 235 240
Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp
245 250 255
Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val
260 265 270
Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu
275 280 285
Tyr Ala Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys
290 295 300
Lys Asn Ser
305
<210> 381
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 381
Val Val Gly Ala Asp Gly Val Gly Lys
1 5
<210> 382
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 382
Val Val Val Gly Ala Asp Gly Val Gly Lys
1 5 10
<210> 383
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 383
Thr Ser Ile Asn Asn
1 5
<210> 384
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 384
Ile Arg Ser Asn Glu Arg Glu
1 5
<210> 385
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 385
Ala Thr Asp Pro Leu Asp Tyr Lys Leu Ser
1 5 10
<210> 386
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 386
Met Asn His Glu Tyr
1 5
<210> 387
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 387
Ser Met Asn Val Glu Val
1 5
<210> 388
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 388
Ala Ser Ser Leu Val Ala Ser Asn Glu Gln Phe
1 5 10
<210> 389
<211> 390
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 389
atggaaactc tcctgggagt gtctttggtg attctatggc ttcaactggc tagggtgaac
60
agtcaacagg gagaagagga tcctcaggcc ttgagcatcc aggagggtga aaatgccacc
120
atgaactgca gttacaaaac tagtataaac aatttacagt ggtatagaca aaattcaggt
180
agaggccttg tccacctaat tttaatacgt tcaaatgaaa gagagaaaca cagtggaaga
240
ttaagagtca cgcttgacac ttccaagaaa agcagttcct tgttgatcac ggcttcccgg
300
gcagcagaca ctgcttctta cttctgtgct acggacccct tagactacaa gctcagcttt
360
ggagccggaa ccacagtaac tgtaagagca
390
<210> 390
<211> 390
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 390
atggagaccc tgctgggcgt gtctctggtc atcctgtggc tgcagctggc cagagtgaac
60
tctcagcagg gagaggagga ccctcaggcc ctgagcatcc aggagggcga gaacgccacc
120
atgaattgct cttacaagac aagcatcaac aatctgcagt ggtatcggca gaactccggc
180
agaggcctgg tgcacctgat cctgatcagg agcaatgagc gcgagaagca ctccggccgg
240
ctgagagtga ccctggacac atctaagaag tcctctagcc tgctgatcac cgcctctagg
300
gcagcagata cagccagcta cttctgtgcc accgacccac tggattataa gctgtccttt
360
ggcgccggca ccacagtgac cgtgcgcgcc
390
<210> 391
<211> 130
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 391
Met Glu Thr Leu Leu Gly Val Ser Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ala Arg Val Asn Ser Gln Gln Gly Glu Glu Asp Pro Gln Ala Leu Ser
20 25 30
Ile Gln Glu Gly Glu Asn Ala Thr Met Asn Cys Ser Tyr Lys Thr Ser
35 40 45
Ile Asn Asn Leu Gln Trp Tyr Arg Gln Asn Ser Gly Arg Gly Leu Val
50 55 60
His Leu Ile Leu Ile Arg Ser Asn Glu Arg Glu Lys His Ser Gly Arg
65 70 75 80
Leu Arg Val Thr Leu Asp Thr Ser Lys Lys Ser Ser Ser Leu Leu Ile
85 90 95
Thr Ala Ser Arg Ala Ala Asp Thr Ala Ser Tyr Phe Cys Ala Thr Asp
100 105 110
Pro Leu Asp Tyr Lys Leu Ser Phe Gly Ala Gly Thr Thr Val Thr Val
115 120 125
Arg Ala
130
<210> 392
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 392
atgggccccc agctccttgg ctatgtggtc ctttgccttc taggagcagg ccccctggaa
60
gcccaagtga cccagaaccc aagatacctc atcacagtga ctggaaagaa gttaacagtg
120
acttgttctc agaatatgaa ccatgagtat atgtcctggt atcgacaaga cccagggctg
180
ggcttaaggc agatctacta ttcaatgaat gttgaggtga ctgataaggg agatgttcct
240
gaagggtaca aagtctctcg aaaagagaag aggaatttcc ccctgatcct ggagtcgccc
300
agccccaacc agacctctct gtacttctgt gccagcagtt tggtggctag caatgagcag
360
ttcttcgggc cagggacacg gctcaccgtg cta
393
<210> 393
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 393
atgggcccac agctgctggg ctacgtggtg ctgtgcctgc tgggagcagg accactggag
60
gcacaggtga cccagaatcc ccggtatctg atcaccgtga caggcaagaa gctgaccgtg
120
acatgttccc agaacatgaa tcacgagtac atgtcttggt ataggcagga ccccggactg
180
ggactgaggc agatctacta ttctatgaac gtggaggtga cagacaaggg cgatgtgcct
240
gagggctaca aggtgagcag gaaggagaag cgcaacttcc cactgatcct ggagtcccca
300
tctcccaatc agaccagcct gtatttttgc gccagctccc tggtggcctc caacgagcag
360
ttctttggcc ctggcacccg gctgacagtg ctg
393
<210> 394
<211> 131
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 394
Met Gly Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Leu Val Ala Ser Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu
115 120 125
Thr Val Leu
130
<210> 395
<211> 267
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 395
Met Glu Thr Leu Leu Gly Val Ser Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ala Arg Val Asn Ser Gln Gln Gly Glu Glu Asp Pro Gln Ala Leu Ser
20 25 30
Ile Gln Glu Gly Glu Asn Ala Thr Met Asn Cys Ser Tyr Lys Thr Ser
35 40 45
Ile Asn Asn Leu Gln Trp Tyr Arg Gln Asn Ser Gly Arg Gly Leu Val
50 55 60
His Leu Ile Leu Ile Arg Ser Asn Glu Arg Glu Lys His Ser Gly Arg
65 70 75 80
Leu Arg Val Thr Leu Asp Thr Ser Lys Lys Ser Ser Ser Leu Leu Ile
85 90 95
Thr Ala Ser Arg Ala Ala Asp Thr Ala Ser Tyr Phe Cys Ala Thr Asp
100 105 110
Pro Leu Asp Tyr Lys Leu Ser Phe Gly Ala Gly Thr Thr Val Thr Val
115 120 125
Arg Ala Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp
130 135 140
Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser
145 150 155 160
Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp
165 170 175
Lys Thr Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala
180 185 190
Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys
195 200 205
Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr
210 215 220
Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn
225 230 235 240
Leu Ser Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe
245 250 255
Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 396
<211> 304
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 396
Met Gly Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Leu Val Ala Ser Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu
115 120 125
Thr Val Leu Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu
130 135 140
Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu
145 150 155 160
Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp
165 170 175
Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln
180 185 190
Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg
195 200 205
Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln
210 215 220
Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser
225 230 235 240
Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala
245 250 255
Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu Ser Ala
260 265 270
Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val
275 280 285
Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys Asn Ser
290 295 300
<210> 397
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 397
Val Val Gly Ala Val Gly Val Gly Lys
1 5
<210> 398
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 398
Val Val Val Gly Ala Val Gly Val Gly Lys
1 5 10
<210> 399
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 399
Thr Ser Glu Ser Asp Tyr Tyr
1 5
<210> 400
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 400
Gln Glu Ala Tyr Lys Gln Gln Asn
1 5
<210> 401
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 401
Ala Cys Gln Gly Gly Ser Glu Lys Leu Val
1 5 10
<210> 402
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 402
Ser Gly His Asn Thr
1 5
<210> 403
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 403
Tyr Tyr Arg Glu Glu Glu
1 5
<210> 404
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 404
Ala Ser Ser Leu Gly Leu Leu Leu Tyr Asn Glu Gln Phe
1 5 10
<210> 405
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 405
atggcatgcc ctggcttcct gtgggcactt gtgatctcca cctgtcttga atttagcatg
60
gctcagacag tcactcagtc tcaaccagag atgtctgtgc aggaggcaga gaccgtgacc
120
ctgagctgca catatgacac cagtgagagt gattattatt tattctggta caagcagcct
180
cccagcaggc agatgattct cgttattcgc caagaagctt ataagcaaca gaatgcaaca
240
gagaatcgtt tctctgtgaa cttccagaaa gcagccaaat ccttcagtct caagatctca
300
gactcacagc tgggggatgc cgcgatgtat ttctgtgctt gtcagggcgg atctgaaaag
360
ctggtctttg gaaagggaac gaaactgaca gtaaaccca
399
<210> 406
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 406
atggcatgcc caggcttcct gtgggcactg gtcatcagca cctgtctgga gttttctatg
60
gcccagaccg tgacacagag ccagccagag atgtccgtgc aggaggcaga gaccgtgaca
120
ctgtcctgta cctacgacac aagcgagtcc gattactatc tgttctggta taagcagcct
180
ccatctcgcc agatgatcct ggtcatccgg caggaggcct acaagcagca gaacgccacc
240
gagaatcggt tctctgtgaa ttttcagaag gccgccaagt cttttagcct gaagatctcc
300
gactctcagc tgggcgatgc cgccatgtat ttctgcgcat gtcagggagg cagcgagaag
360
ctggtgtttg gcaagggcac caagctgaca gtgaaccct
399
<210> 407
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 407
Met Ala Cys Pro Gly Phe Leu Trp Ala Leu Val Ile Ser Thr Cys Leu
1 5 10 15
Glu Phe Ser Met Ala Gln Thr Val Thr Gln Ser Gln Pro Glu Met Ser
20 25 30
Val Gln Glu Ala Glu Thr Val Thr Leu Ser Cys Thr Tyr Asp Thr Ser
35 40 45
Glu Ser Asp Tyr Tyr Leu Phe Trp Tyr Lys Gln Pro Pro Ser Arg Gln
50 55 60
Met Ile Leu Val Ile Arg Gln Glu Ala Tyr Lys Gln Gln Asn Ala Thr
65 70 75 80
Glu Asn Arg Phe Ser Val Asn Phe Gln Lys Ala Ala Lys Ser Phe Ser
85 90 95
Leu Lys Ile Ser Asp Ser Gln Leu Gly Asp Ala Ala Met Tyr Phe Cys
100 105 110
Ala Cys Gln Gly Gly Ser Glu Lys Leu Val Phe Gly Lys Gly Thr Lys
115 120 125
Leu Thr Val Asn Pro
130
<210> 408
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 408
atgggccctg ggctcctctg ctgggtgctg ctttgtctcc tgggagcagg ctcagtggag
60
actggagtca cccaaagtcc cacacacctg atcaaaacga gaggacagca agtgactctg
120
agatgctctt ctcagtctgg gcacaacact gtgtcctggt accaacaggc cctgggtcag
180
gggccccagt ttatctttca gtattatagg gaggaagaga atggcagagg aaacttccct
240
cctagattct caggtctcca gttccctaat tatagctctg agctgaatgt gaacgccttg
300
gagctggacg actcggccct gtatctctgt gccagcagct tgggactcct cctctacaat
360
gagcagttct tcgggccagg gacacggctc accgtgcta
399
<210> 409
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 409
atgggaccag gactgctgtg ctgggtgctg ctgtgcctgc tgggagcagg cagcgtggag
60
accggcgtga cacagtcccc tacccacctg atcaagacaa gaggccagca ggtgaccctg
120
aggtgcagct cccagtctgg ccacaataca gtgagctggt accagcaggc cctgggacag
180
ggacctcagt tcatctttca gtactatagg gaggaggaga acggccgcgg caatttcccc
240
cctcggttta gcggcctgca gttcccaaac tattctagcg agctgaacgt gaatgccctg
300
gagctggacg attccgccct gtacctgtgc gcctcctctc tgggcctgct gctgtataac
360
gagcagttct ttggccccgg caccagactg acagtgctg
399
<210> 410
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 410
Met Gly Pro Gly Leu Leu Cys Trp Val Leu Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Ser Val Glu Thr Gly Val Thr Gln Ser Pro Thr His Leu Ile Lys
20 25 30
Thr Arg Gly Gln Gln Val Thr Leu Arg Cys Ser Ser Gln Ser Gly His
35 40 45
Asn Thr Val Ser Trp Tyr Gln Gln Ala Leu Gly Gln Gly Pro Gln Phe
50 55 60
Ile Phe Gln Tyr Tyr Arg Glu Glu Glu Asn Gly Arg Gly Asn Phe Pro
65 70 75 80
Pro Arg Phe Ser Gly Leu Gln Phe Pro Asn Tyr Ser Ser Glu Leu Asn
85 90 95
Val Asn Ala Leu Glu Leu Asp Asp Ser Ala Leu Tyr Leu Cys Ala Ser
100 105 110
Ser Leu Gly Leu Leu Leu Tyr Asn Glu Gln Phe Phe Gly Pro Gly Thr
115 120 125
Arg Leu Thr Val Leu
130
<210> 411
<211> 270
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 411
Met Ala Cys Pro Gly Phe Leu Trp Ala Leu Val Ile Ser Thr Cys Leu
1 5 10 15
Glu Phe Ser Met Ala Gln Thr Val Thr Gln Ser Gln Pro Glu Met Ser
20 25 30
Val Gln Glu Ala Glu Thr Val Thr Leu Ser Cys Thr Tyr Asp Thr Ser
35 40 45
Glu Ser Asp Tyr Tyr Leu Phe Trp Tyr Lys Gln Pro Pro Ser Arg Gln
50 55 60
Met Ile Leu Val Ile Arg Gln Glu Ala Tyr Lys Gln Gln Asn Ala Thr
65 70 75 80
Glu Asn Arg Phe Ser Val Asn Phe Gln Lys Ala Ala Lys Ser Phe Ser
85 90 95
Leu Lys Ile Ser Asp Ser Gln Leu Gly Asp Ala Ala Met Tyr Phe Cys
100 105 110
Ala Cys Gln Gly Gly Ser Glu Lys Leu Val Phe Gly Lys Gly Thr Lys
115 120 125
Leu Thr Val Asn Pro Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln
130 135 140
Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp
145 150 155 160
Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe
165 170 175
Ile Thr Asp Lys Thr Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser
180 185 190
Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp
195 200 205
Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys
210 215 220
Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn
225 230 235 240
Phe Gln Asn Leu Ser Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val
245 250 255
Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265 270
<210> 412
<211> 306
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 412
Met Gly Pro Gly Leu Leu Cys Trp Val Leu Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Ser Val Glu Thr Gly Val Thr Gln Ser Pro Thr His Leu Ile Lys
20 25 30
Thr Arg Gly Gln Gln Val Thr Leu Arg Cys Ser Ser Gln Ser Gly His
35 40 45
Asn Thr Val Ser Trp Tyr Gln Gln Ala Leu Gly Gln Gly Pro Gln Phe
50 55 60
Ile Phe Gln Tyr Tyr Arg Glu Glu Glu Asn Gly Arg Gly Asn Phe Pro
65 70 75 80
Pro Arg Phe Ser Gly Leu Gln Phe Pro Asn Tyr Ser Ser Glu Leu Asn
85 90 95
Val Asn Ala Leu Glu Leu Asp Asp Ser Ala Leu Tyr Leu Cys Ala Ser
100 105 110
Ser Leu Gly Leu Leu Leu Tyr Asn Glu Gln Phe Phe Gly Pro Gly Thr
115 120 125
Arg Leu Thr Val Leu Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val
130 135 140
Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala
145 150 155 160
Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu
165 170 175
Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp
180 185 190
Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg
195 200 205
Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg
210 215 220
Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu
225 230 235 240
Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly
245 250 255
Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu
260 265 270
Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr
275 280 285
Ala Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys
290 295 300
Asn Ser
305
<210> 413
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 413
Val Val Gly Ala Val Gly Val Gly Lys
1 5
<210> 414
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 414
Val Val Val Gly Ala Val Gly Val Gly Lys
1 5 10
<210> 415
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 415
Thr Ser Ile Asn Asn
1 5
<210> 416
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 416
Ile Arg Ser Asn Glu Arg Glu
1 5
<210> 417
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 417
Ala Thr Asp Ala Gln Thr Gly Ala Asn Asn Leu Phe
1 5 10
<210> 418
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 418
Ser Gly His Ala Thr
1 5
<210> 419
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 419
Phe Gln Asn Asn Gly Val
1 5
<210> 420
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 420
Ala Ser Ser Leu Gly Asp Ser Tyr Glu Gln Tyr Phe
1 5 10
<210> 421
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 421
atggaaactc tcctgggagt gtctttggtg attctatggc ttcaactggc tagggtgaac
60
agtcaacagg gagaagagga tcctcaggcc ttgagcatcc aggagggtga aaatgccacc
120
atgaactgca gttacaaaac tagtataaac aatttacagt ggtatagaca aaattcaggt
180
agaggccttg tccacctaat tttaatacgt tcaaatgaaa gagagaaaca cagtggaaga
240
ttaagagtca cgcttgacac ttccaagaaa agcagttcct tgttgatcac ggcttcccgg
300
gcagcagaca ctgcttctta cttctgtgct acggacgctc aaactggggc aaacaacctc
360
ttctttggga ctggaacgag actcaccgtt attccc
396
<210> 422
<211> 396
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 422
atggagacac tgctgggcgt gtctctggtc atcctgtggc tgcagctggc cagagtgaat
60
agccagcagg gagaggagga cccccaggcc ctgtccatcc aggagggcga gaacgccacc
120
atgaattgca gctacaagac atccatcaac aatctgcagt ggtatcggca gaactctggc
180
agaggcctgg tgcacctgat cctgatccgg tccaatgaga gagagaagca ctctggccgg
240
ctgagagtga ccctggatac atccaagaag tcctctagcc tgctgatcac cgccagccgg
300
gcagcagaca cagcctccta tttttgtgcc accgatgccc agacaggcgc caacaatctg
360
ttctttggca ccggcacaag actgaccgtg atccct
396
<210> 423
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 423
Met Glu Thr Leu Leu Gly Val Ser Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ala Arg Val Asn Ser Gln Gln Gly Glu Glu Asp Pro Gln Ala Leu Ser
20 25 30
Ile Gln Glu Gly Glu Asn Ala Thr Met Asn Cys Ser Tyr Lys Thr Ser
35 40 45
Ile Asn Asn Leu Gln Trp Tyr Arg Gln Asn Ser Gly Arg Gly Leu Val
50 55 60
His Leu Ile Leu Ile Arg Ser Asn Glu Arg Glu Lys His Ser Gly Arg
65 70 75 80
Leu Arg Val Thr Leu Asp Thr Ser Lys Lys Ser Ser Ser Leu Leu Ile
85 90 95
Thr Ala Ser Arg Ala Ala Asp Thr Ala Ser Tyr Phe Cys Ala Thr Asp
100 105 110
Ala Gln Thr Gly Ala Asn Asn Leu Phe Phe Gly Thr Gly Thr Arg Leu
115 120 125
Thr Val Ile Pro
130
<210> 424
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 424
atgggcacca ggctcctctg ctgggcggcc ctctgtctcc tgggagcaga actcacagaa
60
gctggagttg cccagtctcc cagatataag attatagaga aaaggcagag tgtggctttt
120
tggtgcaatc ctatatctgg ccatgctacc ctttactggt accagcagat cctgggacag
180
ggcccaaagc ttctgattca gtttcagaat aacggtgtag tggatgattc acagttgcct
240
aaggatcgat tttctgcaga gaggctcaaa ggagtagact ccactctcaa gatccagcct
300
gcaaagcttg aggactcggc cgtgtatctc tgtgccagca gctta
345
<210> 425
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 425
atgggcacca ggctgctgtg ctgggccgcc ctgtgcctgc tgggagcaga gctgacagag
60
gcaggagtgg cccagagccc caggtacaag atcatcgaga agcgccagtc cgtggccttc
120
tggtgcaacc ctatctctgg ccacgccacc ctgtactggt atcagcagat cctgggccag
180
ggcccaaagc tgctgatcca gttccagaac aatggcgtgg tggacgattc tcagctgccc
240
aaggacaggt ttagcgccga gcgcctgaag ggcgtggatt ctaccctgaa gatccagcca
300
gcaaagctgg aggacagcgc cgtgtacctg tgcgccagct ccctg
345
<210> 426
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 426
Met Gly Thr Arg Leu Leu Cys Trp Ala Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Glu Leu Thr Glu Ala Gly Val Ala Gln Ser Pro Arg Tyr Lys Ile Ile
20 25 30
Glu Lys Arg Gln Ser Val Ala Phe Trp Cys Asn Pro Ile Ser Gly His
35 40 45
Ala Thr Leu Tyr Trp Tyr Gln Gln Ile Leu Gly Gln Gly Pro Lys Leu
50 55 60
Leu Ile Gln Phe Gln Asn Asn Gly Val Val Asp Asp Ser Gln Leu Pro
65 70 75 80
Lys Asp Arg Phe Ser Ala Glu Arg Leu Lys Gly Val Asp Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ala Lys Leu Glu Asp Ser Ala Val Tyr Leu Cys Ala
100 105 110
Ser Ser Leu
115
<210> 427
<211> 269
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 427
Met Glu Thr Leu Leu Gly Val Ser Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ala Arg Val Asn Ser Gln Gln Gly Glu Glu Asp Pro Gln Ala Leu Ser
20 25 30
Ile Gln Glu Gly Glu Asn Ala Thr Met Asn Cys Ser Tyr Lys Thr Ser
35 40 45
Ile Asn Asn Leu Gln Trp Tyr Arg Gln Asn Ser Gly Arg Gly Leu Val
50 55 60
His Leu Ile Leu Ile Arg Ser Asn Glu Arg Glu Lys His Ser Gly Arg
65 70 75 80
Leu Arg Val Thr Leu Asp Thr Ser Lys Lys Ser Ser Ser Leu Leu Ile
85 90 95
Thr Ala Ser Arg Ala Ala Asp Thr Ala Ser Tyr Phe Cys Ala Thr Asp
100 105 110
Ala Gln Thr Gly Ala Asn Asn Leu Phe Phe Gly Thr Gly Thr Arg Leu
115 120 125
Thr Val Ile Pro Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu
130 135 140
Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe
145 150 155 160
Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile
165 170 175
Thr Asp Lys Thr Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn
180 185 190
Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile
195 200 205
Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp
210 215 220
Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe
225 230 235 240
Gln Asn Leu Ser Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val Ala
245 250 255
Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 428
<211> 288
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 428
Met Gly Thr Arg Leu Leu Cys Trp Ala Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Glu Leu Thr Glu Ala Gly Val Ala Gln Ser Pro Arg Tyr Lys Ile Ile
20 25 30
Glu Lys Arg Gln Ser Val Ala Phe Trp Cys Asn Pro Ile Ser Gly His
35 40 45
Ala Thr Leu Tyr Trp Tyr Gln Gln Ile Leu Gly Gln Gly Pro Lys Leu
50 55 60
Leu Ile Gln Phe Gln Asn Asn Gly Val Val Asp Asp Ser Gln Leu Pro
65 70 75 80
Lys Asp Arg Phe Ser Ala Glu Arg Leu Lys Gly Val Asp Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ala Lys Leu Glu Asp Ser Ala Val Tyr Leu Cys Ala
100 105 110
Ser Ser Leu Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu
115 120 125
Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu
130 135 140
Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp
145 150 155 160
Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln
165 170 175
Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg
180 185 190
Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln
195 200 205
Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser
210 215 220
Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala
225 230 235 240
Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu Ser Ala
245 250 255
Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val
260 265 270
Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys Asn Ser
275 280 285
<210> 429
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 429
Val Val Gly Ala Val Gly Val Gly Lys
1 5
<210> 430
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 430
Val Val Val Gly Ala Val Gly Val Gly Lys
1 5 10
<210> 431
<400> 431
000
<210> 432
<400> 432
000
<210> 433
<400> 433
000
<210> 434
<400> 434
000
<210> 435
<400> 435
000
<210> 436
<400> 436
000
<210> 437
<400> 437
000
<210> 438
<400> 438
000
<210> 439
<400> 439
000
<210> 440
<400> 440
000
<210> 441
<400> 441
000
<210> 442
<400> 442
000
<210> 443
<400> 443
000
<210> 444
<400> 444
000
<210> 445
<400> 445
000
<210> 446
<400> 446
000
<210> 447
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 447
Thr Arg Asp Thr Thr Tyr Tyr
1 5
<210> 448
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 448
Arg Asn Ser Phe Asp Glu Gln Asn
1 5
<210> 449
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 449
Ala Leu Lys Gly Ala Asn Thr Gly Phe Gln Lys Leu Val
1 5 10
<210> 450
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 450
Ser Gly His Asp Tyr
1 5
<210> 451
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 451
Phe Asn Asn Asn Val Pro
1 5
<210> 452
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 452
Ala Ser Gly Gly Gly Leu Gly Leu Phe Glu Thr Gln Tyr
1 5 10
<210> 453
<211> 408
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 453
atgctgactg ccagcctgtt gagggcagtc atagcctcca tctgtgttgt atccagcatg
60
gctcagaagg taactcaagc gcagactgaa atttctgtgg tggagaagga ggatgtgacc
120
ttggactgtg tgtatgaaac ccgtgatact acttattact tattctggta caagcaacca
180
ccaagtggag aattggtttt ccttattcgt cggaactctt ttgatgagca aaatgaaata
240
agtggtcggt attcttggaa cttccagaaa tccaccagtt ccttcaactt caccatcaca
300
gcctcacaag tcgtggactc agcagtatac ttctgtgctc tgaaaggggc gaacacaggc
360
tttcagaaac ttgtatttgg aactggcacc cgacttctgg tcagtcca
408
<210> 454
<211> 408
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 454
atgctgacag cctccctgct gagggccgtg atcgcctcta tctgcgtggt gtctagcatg
60
gcccagaagg tgacccaggc ccagacagag atcagcgtgg tggagaagga ggacgtgacc
120
ctggattgcg tgtacgagac acgggacacc acatactatc tgttttggta taagcagcca
180
cccagcggcg agctggtgtt cctgatcagg cgcaattcct ttgatgagca gaacgagatc
240
tccggcagat actcttggaa tttccagaag tccacctcct ctttcaactt taccatcaca
300
gcctcccagg tggtggactc tgccgtgtat ttttgtgccc tgaagggcgc caacacaggc
360
ttccagaagc tggtgtttgg caccggcaca agactgctgg tgagccct
408
<210> 455
<211> 136
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 455
Met Leu Thr Ala Ser Leu Leu Arg Ala Val Ile Ala Ser Ile Cys Val
1 5 10 15
Val Ser Ser Met Ala Gln Lys Val Thr Gln Ala Gln Thr Glu Ile Ser
20 25 30
Val Val Glu Lys Glu Asp Val Thr Leu Asp Cys Val Tyr Glu Thr Arg
35 40 45
Asp Thr Thr Tyr Tyr Leu Phe Trp Tyr Lys Gln Pro Pro Ser Gly Glu
50 55 60
Leu Val Phe Leu Ile Arg Arg Asn Ser Phe Asp Glu Gln Asn Glu Ile
65 70 75 80
Ser Gly Arg Tyr Ser Trp Asn Phe Gln Lys Ser Thr Ser Ser Phe Asn
85 90 95
Phe Thr Ile Thr Ala Ser Gln Val Val Asp Ser Ala Val Tyr Phe Cys
100 105 110
Ala Leu Lys Gly Ala Asn Thr Gly Phe Gln Lys Leu Val Phe Gly Thr
115 120 125
Gly Thr Arg Leu Leu Val Ser Pro
130 135
<210> 456
<211> 402
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 456
atggactcct ggaccctctg ctgtgtgtcc ctttgcatcc tggtagcaaa gcacacagat
60
gctggagtta tccagtcacc ccggcacgag gtgacagaga tgggacaaga agtgactctg
120
agatgtaaac caatttcagg acacgactac cttttctggt acagacagac catgatgcgg
180
ggactggagt tgctcattta ctttaacaac aacgttccga tagatgattc agggatgccc
240
gaggatcgat tctcagctaa gatgcctaat gcatcattct ccactctgaa gatccagccc
300
tcagaaccca gggactcagc tgtgtacttc tgtgccagcg gagggggact aggtctattt
360
gagacccagt acttcgggcc aggcacgcgg ctcctggtgc tc
402
<210> 457
<211> 402
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 457
atggacagct ggaccctgtg ctgcgtgagc ctgtgcatcc tggtggccaa gcacacagat
60
gcaggcgtga tccagtcccc aaggcacgag gtgaccgaga tgggacagga ggtgacactg
120
aggtgtaagc ctatctctgg ccacgactac ctgttctggt atcggcagac catgatgaga
180
ggcctggagc tgctgatcta ctttaacaat aacgtgccta tcgacgattc tggcatgcca
240
gaggacaggt tcagcgccaa gatgcctaat gccagctttt ccaccctgaa gatccagcca
300
agcgagccaa gggattccgc cgtgtacttc tgcgcctccg gaggaggact gggactgttc
360
gagacccagt attttggccc aggcacaagg ctgctggtgc tg
402
<210> 458
<211> 134
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 458
Met Asp Ser Trp Thr Leu Cys Cys Val Ser Leu Cys Ile Leu Val Ala
1 5 10 15
Lys His Thr Asp Ala Gly Val Ile Gln Ser Pro Arg His Glu Val Thr
20 25 30
Glu Met Gly Gln Glu Val Thr Leu Arg Cys Lys Pro Ile Ser Gly His
35 40 45
Asp Tyr Leu Phe Trp Tyr Arg Gln Thr Met Met Arg Gly Leu Glu Leu
50 55 60
Leu Ile Tyr Phe Asn Asn Asn Val Pro Ile Asp Asp Ser Gly Met Pro
65 70 75 80
Glu Asp Arg Phe Ser Ala Lys Met Pro Asn Ala Ser Phe Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ser Glu Pro Arg Asp Ser Ala Val Tyr Phe Cys Ala
100 105 110
Ser Gly Gly Gly Leu Gly Leu Phe Glu Thr Gln Tyr Phe Gly Pro Gly
115 120 125
Thr Arg Leu Leu Val Leu
130
<210> 459
<211> 273
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 459
Met Leu Thr Ala Ser Leu Leu Arg Ala Val Ile Ala Ser Ile Cys Val
1 5 10 15
Val Ser Ser Met Ala Gln Lys Val Thr Gln Ala Gln Thr Glu Ile Ser
20 25 30
Val Val Glu Lys Glu Asp Val Thr Leu Asp Cys Val Tyr Glu Thr Arg
35 40 45
Asp Thr Thr Tyr Tyr Leu Phe Trp Tyr Lys Gln Pro Pro Ser Gly Glu
50 55 60
Leu Val Phe Leu Ile Arg Arg Asn Ser Phe Asp Glu Gln Asn Glu Ile
65 70 75 80
Ser Gly Arg Tyr Ser Trp Asn Phe Gln Lys Ser Thr Ser Ser Phe Asn
85 90 95
Phe Thr Ile Thr Ala Ser Gln Val Val Asp Ser Ala Val Tyr Phe Cys
100 105 110
Ala Leu Lys Gly Ala Asn Thr Gly Phe Gln Lys Leu Val Phe Gly Thr
115 120 125
Gly Thr Arg Leu Leu Val Ser Pro Asp Ile Gln Asn Pro Glu Pro Ala
130 135 140
Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu
145 150 155 160
Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser
165 170 175
Gly Thr Phe Ile Thr Asp Lys Thr Val Leu Asp Met Lys Ala Met Asp
180 185 190
Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr
195 200 205
Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp
210 215 220
Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met
225 230 235 240
Asn Leu Asn Phe Gln Asn Leu Ser Val Met Gly Leu Arg Ile Leu Leu
245 250 255
Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser
260 265 270
Ser
<210> 460
<211> 307
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 460
Met Asp Ser Trp Thr Leu Cys Cys Val Ser Leu Cys Ile Leu Val Ala
1 5 10 15
Lys His Thr Asp Ala Gly Val Ile Gln Ser Pro Arg His Glu Val Thr
20 25 30
Glu Met Gly Gln Glu Val Thr Leu Arg Cys Lys Pro Ile Ser Gly His
35 40 45
Asp Tyr Leu Phe Trp Tyr Arg Gln Thr Met Met Arg Gly Leu Glu Leu
50 55 60
Leu Ile Tyr Phe Asn Asn Asn Val Pro Ile Asp Asp Ser Gly Met Pro
65 70 75 80
Glu Asp Arg Phe Ser Ala Lys Met Pro Asn Ala Ser Phe Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ser Glu Pro Arg Asp Ser Ala Val Tyr Phe Cys Ala
100 105 110
Ser Gly Gly Gly Leu Gly Leu Phe Glu Thr Gln Tyr Phe Gly Pro Gly
115 120 125
Thr Arg Leu Leu Val Leu Lys Asp Leu Arg Asn Val Thr Pro Pro Lys
130 135 140
Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys
145 150 155 160
Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu
165 170 175
Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr
180 185 190
Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser
195 200 205
Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe
210 215 220
Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro
225 230 235 240
Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp
245 250 255
Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val
260 265 270
Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu
275 280 285
Tyr Ala Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys
290 295 300
Lys Asn Ser
305
<210> 461
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 461
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 462
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 462
Leu Ile Met Gln Leu Met Pro Phe Gly Cys
1 5 10
<210> 463
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 463
Met Gln Leu Met Pro Phe Gly Cys Leu Leu
1 5 10
<210> 464
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 464
Asp Ser Ser Ser Thr Tyr
1 5
<210> 465
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 465
Ile Phe Ser Asn Met Asp Met
1 5
<210> 466
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 466
Ala Glu Trp Ala Asn Thr Asp Lys Leu Ile
1 5 10
<210> 467
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 467
Asp Phe Gln Ala Thr Thr
1 5
<210> 468
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 468
Ser Asn Glu Gly Ser Lys Ala
1 5
<210> 469
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 469
Ser Ala Arg Arg Arg Glu Gly Glu Ile Glu Gln Tyr
1 5 10
<210> 470
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 470
atgaagacat ttgctggatt ttcgttcctg tttttgtggc tgcagctgga ctgtatgagt
60
agaggagagg atgtggagca gagtcttttc ctgagtgtcc gagagggaga cagctccgtt
120
ataaactgca cttacacaga cagctcctcc acctacttat actggtataa gcaagaacct
180
ggagcaggtc tccagttgct gacgtatatt ttttcaaata tggacatgaa acaagaccaa
240
agactcactg ttctattgaa taaaaaggat aaacatctgt ctctgcgcat tgcagacacc
300
cagactgggg actcagctat ctacttctgt gcagagtggg ctaacaccga caagctcatc
360
tttgggactg ggaccagatt acaagtcttt cca
393
<210> 471
<211> 393
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 471
atgaagacct tcgccggctt ctcctttctg ttcctgtggc tgcagctgga ctgcatgagc
60
cggggagagg atgtggagca gtccctgttc ctgtctgtga gggagggcga ctcctctgtg
120
atcaactgta catataccga tagctcctct acctacctgt attggtacaa gcaggagcca
180
ggagcaggac tgcagctgct gacatacatc tttagcaaca tggacatgaa gcaggatcag
240
cgcctgaccg tgctgctgaa taagaaggac aagcacctgt ctctgcggat cgccgacaca
300
cagaccggcg atagcgccat ctacttctgt gccgagtggg ccaataccga taagctgatc
360
tttggcacag gcacccggct gcaggtgttc cct
393
<210> 472
<211> 131
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 472
Met Lys Thr Phe Ala Gly Phe Ser Phe Leu Phe Leu Trp Leu Gln Leu
1 5 10 15
Asp Cys Met Ser Arg Gly Glu Asp Val Glu Gln Ser Leu Phe Leu Ser
20 25 30
Val Arg Glu Gly Asp Ser Ser Val Ile Asn Cys Thr Tyr Thr Asp Ser
35 40 45
Ser Ser Thr Tyr Leu Tyr Trp Tyr Lys Gln Glu Pro Gly Ala Gly Leu
50 55 60
Gln Leu Leu Thr Tyr Ile Phe Ser Asn Met Asp Met Lys Gln Asp Gln
65 70 75 80
Arg Leu Thr Val Leu Leu Asn Lys Lys Asp Lys His Leu Ser Leu Arg
85 90 95
Ile Ala Asp Thr Gln Thr Gly Asp Ser Ala Ile Tyr Phe Cys Ala Glu
100 105 110
Trp Ala Asn Thr Asp Lys Leu Ile Phe Gly Thr Gly Thr Arg Leu Gln
115 120 125
Val Phe Pro
130
<210> 473
<211> 390
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 473
atgctgctgc ttctgctgct tctggggcca ggctccgggc ttggtgctgt cgtctctcaa
60
catccgagct gggttatctg taagagtgga acctctgtga agatcgagtg ccgttccctg
120
gactttcagg ccacaactat gttttggtat cgtcagttcc cgaaacagag tctcatgctg
180
atggcaactt ccaatgaggg ctccaaggcc acatacgagc aaggcgtcga gaaggacaag
240
tttctcatca accatgcaag cctgaccttg tccactctga cagtgaccag tgcccatcct
300
gaagacagca gcttctacat ctgcagtgct agaaggcggg agggggagat cgagcagtac
360
ttcgggccgg gcaccaggct cacggtcaca
390
<210> 474
<211> 390
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 474
atgttattac tgctgctgct gctgggacca ggctccggac tgggagccgt ggtgtcccag
60
cacccttctt gggtcatctg caagtccggc acatctgtga agatcgagtg tcgctctctg
120
gactttcagg ccaccacaat gttttggtat cggcagttcc ccaagcagag cctgatgctg
180
atggccacaa gcaacgaggg ctccaaggcc acctacgagc agggcgtgga gaaggacaag
240
ttcctgatca atcacgcctc tctgaccctg agcaccctga cagtgacctc cgcccaccct
300
gaggatagct ccttttatat ctgctctgcc cggagaaggg agggcgagat cgagcagtac
360
ttcggcccag gcacaagact gacagtgacc
390
<210> 475
<211> 130
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 475
Met Leu Leu Leu Leu Leu Leu Leu Gly Pro Gly Ser Gly Leu Gly Ala
1 5 10 15
Val Val Ser Gln His Pro Ser Trp Val Ile Cys Lys Ser Gly Thr Ser
20 25 30
Val Lys Ile Glu Cys Arg Ser Leu Asp Phe Gln Ala Thr Thr Met Phe
35 40 45
Trp Tyr Arg Gln Phe Pro Lys Gln Ser Leu Met Leu Met Ala Thr Ser
50 55 60
Asn Glu Gly Ser Lys Ala Thr Tyr Glu Gln Gly Val Glu Lys Asp Lys
65 70 75 80
Phe Leu Ile Asn His Ala Ser Leu Thr Leu Ser Thr Leu Thr Val Thr
85 90 95
Ser Ala His Pro Glu Asp Ser Ser Phe Tyr Ile Cys Ser Ala Arg Arg
100 105 110
Arg Glu Gly Glu Ile Glu Gln Tyr Phe Gly Pro Gly Thr Arg Leu Thr
115 120 125
Val Thr
130
<210> 476
<211> 268
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 476
Met Lys Thr Phe Ala Gly Phe Ser Phe Leu Phe Leu Trp Leu Gln Leu
1 5 10 15
Asp Cys Met Ser Arg Gly Glu Asp Val Glu Gln Ser Leu Phe Leu Ser
20 25 30
Val Arg Glu Gly Asp Ser Ser Val Ile Asn Cys Thr Tyr Thr Asp Ser
35 40 45
Ser Ser Thr Tyr Leu Tyr Trp Tyr Lys Gln Glu Pro Gly Ala Gly Leu
50 55 60
Gln Leu Leu Thr Tyr Ile Phe Ser Asn Met Asp Met Lys Gln Asp Gln
65 70 75 80
Arg Leu Thr Val Leu Leu Asn Lys Lys Asp Lys His Leu Ser Leu Arg
85 90 95
Ile Ala Asp Thr Gln Thr Gly Asp Ser Ala Ile Tyr Phe Cys Ala Glu
100 105 110
Trp Ala Asn Thr Asp Lys Leu Ile Phe Gly Thr Gly Thr Arg Leu Gln
115 120 125
Val Phe Pro Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys
130 135 140
Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp
145 150 155 160
Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr
165 170 175
Asp Lys Thr Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly
180 185 190
Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe
195 200 205
Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala
210 215 220
Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln
225 230 235 240
Asn Leu Ser Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val Ala Gly
245 250 255
Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 477
<211> 303
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 477
Met Leu Leu Leu Leu Leu Leu Leu Gly Pro Gly Ser Gly Leu Gly Ala
1 5 10 15
Val Val Ser Gln His Pro Ser Trp Val Ile Cys Lys Ser Gly Thr Ser
20 25 30
Val Lys Ile Glu Cys Arg Ser Leu Asp Phe Gln Ala Thr Thr Met Phe
35 40 45
Trp Tyr Arg Gln Phe Pro Lys Gln Ser Leu Met Leu Met Ala Thr Ser
50 55 60
Asn Glu Gly Ser Lys Ala Thr Tyr Glu Gln Gly Val Glu Lys Asp Lys
65 70 75 80
Phe Leu Ile Asn His Ala Ser Leu Thr Leu Ser Thr Leu Thr Val Thr
85 90 95
Ser Ala His Pro Glu Asp Ser Ser Phe Tyr Ile Cys Ser Ala Arg Arg
100 105 110
Arg Glu Gly Glu Ile Glu Gln Tyr Phe Gly Pro Gly Thr Arg Leu Thr
115 120 125
Val Thr Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe
130 135 140
Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val
145 150 155 160
Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp
165 170 175
Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln Ala
180 185 190
Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val
195 200 205
Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val
210 215 220
Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro
225 230 235 240
Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp
245 250 255
Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu Ser Ala Thr
260 265 270
Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu
275 280 285
Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys Asn Ser
290 295 300
<210> 478
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 478
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 479
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 479
Leu Ile Met Gln Leu Met Pro Phe Gly Cys
1 5 10
<210> 480
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 480
Met Gln Leu Met Pro Phe Gly Cys Leu Leu
1 5 10
<210> 481
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 481
Thr Arg Asp Thr Thr Tyr Tyr
1 5
<210> 482
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 482
Arg Asn Ser Phe Asp Glu Gln Asn
1 5
<210> 483
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 483
Ala Leu Thr Pro Phe Pro Asn Ala Gly Gly Thr Ser Tyr Gly Lys Leu
1 5 10 15
Thr
<210> 484
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 484
Ser Gly His Asn Ser
1 5
<210> 485
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 485
Phe Asn Asn Asn Val Pro
1 5
<210> 486
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 486
Ala Ser Ser Leu Ala Tyr Leu Thr Gly Arg Val Glu Ala Phe
1 5 10
<210> 487
<211> 420
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 487
atgctgactg ccagcctgtt gagggcagtc atagcctcca tctgtgttgt atccagcatg
60
gctcagaagg taactcaagc gcagactgaa atttctgtgg tggagaagga ggatgtgacc
120
ttggactgtg tgtatgaaac ccgtgatact acttattact tattctggta caagcaacca
180
ccaagtggag aattggtttt ccttattcgt cggaactctt ttgatgagca aaatgaaata
240
agtggtcggt attcttggaa cttccagaaa tccaccagtt ccttcaactt caccatcaca
300
gcctcacaag tcgtggactc agcagtatac ttctgtgctc tgactccctt ccccaatgct
360
ggtggtacta gctatggaaa gctgacattt ggacaaggga ccatcttgac tgtccatcca
420
<210> 488
<211> 420
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 488
atgctgacag cctctctgct gagggccgtg atcgccagca tctgcgtggt gtcctctatg
60
gcccagaagg tgacccaggc ccagacagag atcagcgtgg tggagaagga ggacgtgacc
120
ctggattgcg tgtacgagac acgggacacc acatactatc tgttctggta taagcagcca
180
ccctccggcg agctggtgtt cctgatcagg cgcaattctt ttgatgagca gaacgagatc
240
tctggcagat acagctggaa ttttcagaag tctaccagct ccttcaactt taccatcaca
300
gcctctcagg tggtggatag cgccgtgtac ttctgtgccc tgacaccatt tcccaatgcc
360
ggcggcacca gctatggcaa gctgacattc ggccagggca ccatcctgac agtgcaccct
420
<210> 489
<211> 140
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 489
Met Leu Thr Ala Ser Leu Leu Arg Ala Val Ile Ala Ser Ile Cys Val
1 5 10 15
Val Ser Ser Met Ala Gln Lys Val Thr Gln Ala Gln Thr Glu Ile Ser
20 25 30
Val Val Glu Lys Glu Asp Val Thr Leu Asp Cys Val Tyr Glu Thr Arg
35 40 45
Asp Thr Thr Tyr Tyr Leu Phe Trp Tyr Lys Gln Pro Pro Ser Gly Glu
50 55 60
Leu Val Phe Leu Ile Arg Arg Asn Ser Phe Asp Glu Gln Asn Glu Ile
65 70 75 80
Ser Gly Arg Tyr Ser Trp Asn Phe Gln Lys Ser Thr Ser Ser Phe Asn
85 90 95
Phe Thr Ile Thr Ala Ser Gln Val Val Asp Ser Ala Val Tyr Phe Cys
100 105 110
Ala Leu Thr Pro Phe Pro Asn Ala Gly Gly Thr Ser Tyr Gly Lys Leu
115 120 125
Thr Phe Gly Gln Gly Thr Ile Leu Thr Val His Pro
130 135 140
<210> 490
<211> 405
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 490
atggactcct ggaccttctg ctgtgtgtcc ctttgcatcc tggtagcgaa gcatacagat
60
gctggagtta tccagtcacc ccgccatgag gtgacagaga tgggacaaga agtgactctg
120
agatgtaaac caatttcagg ccacaactcc cttttctggt acagacagac catgatgcgg
180
ggactggagt tgctcattta ctttaacaac aacgttccga tagatgattc agggatgccc
240
gaggatcgat tctcagctaa gatgcctaat gcatcattct ccactctgaa gatccagccc
300
tcagaaccca gggactcagc tgtgtacttc tgtgccagca gtttagccta cctgacaggg
360
agggttgaag ctttctttgg acaaggcacc agactcacag ttgta
405
<210> 491
<211> 405
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 491
atggactcct ggaccttctg ctgcgtgagc ctgtgcatcc tggtggccaa gcacacagat
60
gcaggcgtga tccagtcccc aaggcacgag gtgaccgaga tgggacagga ggtgacactg
120
aggtgtaagc ccatcagcgg ccacaattcc ctgttctggt accggcagac catgatgaga
180
ggcctggagc tgctgatcta cttcaacaat aacgtgccca tcgacgatag cggcatgcct
240
gaggaccggt tctccgccaa gatgcccaac gcctctttta gcaccctgaa gatccagcct
300
tccgagccaa gggattctgc cgtgtacttc tgcgccagct ccctggccta tctgaccgga
360
agggtggagg ccttctttgg acagggcacc aggctgacag tggtg
405
<210> 492
<211> 135
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 492
Met Asp Ser Trp Thr Phe Cys Cys Val Ser Leu Cys Ile Leu Val Ala
1 5 10 15
Lys His Thr Asp Ala Gly Val Ile Gln Ser Pro Arg His Glu Val Thr
20 25 30
Glu Met Gly Gln Glu Val Thr Leu Arg Cys Lys Pro Ile Ser Gly His
35 40 45
Asn Ser Leu Phe Trp Tyr Arg Gln Thr Met Met Arg Gly Leu Glu Leu
50 55 60
Leu Ile Tyr Phe Asn Asn Asn Val Pro Ile Asp Asp Ser Gly Met Pro
65 70 75 80
Glu Asp Arg Phe Ser Ala Lys Met Pro Asn Ala Ser Phe Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ser Glu Pro Arg Asp Ser Ala Val Tyr Phe Cys Ala
100 105 110
Ser Ser Leu Ala Tyr Leu Thr Gly Arg Val Glu Ala Phe Phe Gly Gln
115 120 125
Gly Thr Arg Leu Thr Val Val
130 135
<210> 493
<211> 277
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 493
Met Leu Thr Ala Ser Leu Leu Arg Ala Val Ile Ala Ser Ile Cys Val
1 5 10 15
Val Ser Ser Met Ala Gln Lys Val Thr Gln Ala Gln Thr Glu Ile Ser
20 25 30
Val Val Glu Lys Glu Asp Val Thr Leu Asp Cys Val Tyr Glu Thr Arg
35 40 45
Asp Thr Thr Tyr Tyr Leu Phe Trp Tyr Lys Gln Pro Pro Ser Gly Glu
50 55 60
Leu Val Phe Leu Ile Arg Arg Asn Ser Phe Asp Glu Gln Asn Glu Ile
65 70 75 80
Ser Gly Arg Tyr Ser Trp Asn Phe Gln Lys Ser Thr Ser Ser Phe Asn
85 90 95
Phe Thr Ile Thr Ala Ser Gln Val Val Asp Ser Ala Val Tyr Phe Cys
100 105 110
Ala Leu Thr Pro Phe Pro Asn Ala Gly Gly Thr Ser Tyr Gly Lys Leu
115 120 125
Thr Phe Gly Gln Gly Thr Ile Leu Thr Val His Pro Asp Ile Gln Asn
130 135 140
Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser
145 150 155 160
Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys
165 170 175
Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Thr Val Leu Asp Met
180 185 190
Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln
195 200 205
Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr
210 215 220
Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe
225 230 235 240
Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Ser Val Met Gly Leu
245 250 255
Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu
260 265 270
Arg Leu Trp Ser Ser
275
<210> 494
<211> 308
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 494
Met Asp Ser Trp Thr Phe Cys Cys Val Ser Leu Cys Ile Leu Val Ala
1 5 10 15
Lys His Thr Asp Ala Gly Val Ile Gln Ser Pro Arg His Glu Val Thr
20 25 30
Glu Met Gly Gln Glu Val Thr Leu Arg Cys Lys Pro Ile Ser Gly His
35 40 45
Asn Ser Leu Phe Trp Tyr Arg Gln Thr Met Met Arg Gly Leu Glu Leu
50 55 60
Leu Ile Tyr Phe Asn Asn Asn Val Pro Ile Asp Asp Ser Gly Met Pro
65 70 75 80
Glu Asp Arg Phe Ser Ala Lys Met Pro Asn Ala Ser Phe Ser Thr Leu
85 90 95
Lys Ile Gln Pro Ser Glu Pro Arg Asp Ser Ala Val Tyr Phe Cys Ala
100 105 110
Ser Ser Leu Ala Tyr Leu Thr Gly Arg Val Glu Ala Phe Phe Gly Gln
115 120 125
Gly Thr Arg Leu Thr Val Val Lys Asp Leu Arg Asn Val Thr Pro Pro
130 135 140
Lys Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln
145 150 155 160
Lys Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val
165 170 175
Glu Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser
180 185 190
Thr Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser
195 200 205
Ser Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His
210 215 220
Phe Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp
225 230 235 240
Pro Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala
245 250 255
Trp Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly
260 265 270
Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr
275 280 285
Leu Tyr Ala Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys
290 295 300
Lys Lys Asn Ser
305
<210> 495
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 495
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 496
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 496
Leu Ile Met Gln Leu Met Pro Phe Gly Cys
1 5 10
<210> 497
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 497
Met Gln Leu Met Pro Phe Gly Cys Leu Leu
1 5 10
<210> 498
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 498
Thr Arg Asp Thr Thr Tyr Tyr
1 5
<210> 499
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 499
Arg Asn Ser Phe Asp Glu Gln Asn
1 5
<210> 500
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 500
Ala Leu Ile Arg Gly Ser Tyr Gln Leu Ile
1 5 10
<210> 501
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 501
Asp Phe Gln Ala Thr Thr
1 5
<210> 502
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 502
Ser Asn Glu Gly Ser Lys Ala
1 5
<210> 503
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 503
Ser Ala Gln Gly Ser Ser Gly Arg Ile Glu Gln Phe
1 5 10
<210> 504
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 504
atgctgactg ccagcctgtt gagggcagtc atagcctcca tctgtgttgt atccagcatg
60
gctcagaagg taactcaagc gcagactgaa atttctgtgg tggagaagga ggatgtgacc
120
ttggactgtg tgtatgaaac ccgtgatact acttattact tattctggta caagcaacca
180
ccaagtggag aattggtttt ccttattcgt cggaactctt ttgatgagca aaatgaaata
240
agtggtcggt attcttggaa cttccagaaa tccaccagtt ccttcaactt caccatcaca
300
gcctcacaag tcgtggactc agcagtatac ttctgtgctc tgattcgagg gagctatcag
360
ttaatctggg gcgctgggac caagctaatt ataaagcca
399
<210> 505
<211> 399
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 505
atgctgaccg cctctctgct gagggccgtg atcgccagca tctgcgtggt gagctccatg
60
gcccagaagg tgacacaggc ccagaccgag atcagcgtgg tggagaagga ggacgtgaca
120
ctggattgcg tgtacgagac ccgcgacacc acatactatc tgttttggta taagcagcca
180
ccctccggcg agctggtgtt cctgatcagg cgcaactctt ttgatgagca gaatgagatc
240
tctggccggt acagctggaa cttccagaag agcacatcta gcttcaactt caccatcacc
300
gccagccagg tggtggactc cgccgtgtac ttttgtgccc tgatcagagg ctcctatcag
360
ctgatctggg gcgccggcac caagctgatc atcaagccc
399
<210> 506
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 506
Met Leu Thr Ala Ser Leu Leu Arg Ala Val Ile Ala Ser Ile Cys Val
1 5 10 15
Val Ser Ser Met Ala Gln Lys Val Thr Gln Ala Gln Thr Glu Ile Ser
20 25 30
Val Val Glu Lys Glu Asp Val Thr Leu Asp Cys Val Tyr Glu Thr Arg
35 40 45
Asp Thr Thr Tyr Tyr Leu Phe Trp Tyr Lys Gln Pro Pro Ser Gly Glu
50 55 60
Leu Val Phe Leu Ile Arg Arg Asn Ser Phe Asp Glu Gln Asn Glu Ile
65 70 75 80
Ser Gly Arg Tyr Ser Trp Asn Phe Gln Lys Ser Thr Ser Ser Phe Asn
85 90 95
Phe Thr Ile Thr Ala Ser Gln Val Val Asp Ser Ala Val Tyr Phe Cys
100 105 110
Ala Leu Ile Arg Gly Ser Tyr Gln Leu Ile Trp Gly Ala Gly Thr Lys
115 120 125
Leu Ile Ile Lys Pro
130
<210> 507
<211> 390
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 507
atgctgctgc ttctgctgct tctggggcca ggctccgggc ttggtgctgt cgtctctcaa
60
catccgagca gggttatctg taagagtgga acctctgtga agatcgagtg ccgttccctg
120
gactttcagg ccacaactat gttttggtat cgtcagttcc cgaaacagag tctcatgctg
180
atggcaactt ccaatgaggg ctccaaggcc acatacgagc aaggcgtcga gaaggacaag
240
tttctcatca accatgcaag cctgaccttg tccactctga cagtgaccag tgcccatcct
300
gaagacagca gcttctacat ctgcagcgcc caggggagta gcgggaggat tgagcagttc
360
ttcgggccag ggacacggct caccgtgcta
390
<210> 508
<211> 390
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 508
atgttattac tgctgctgct gctgggacca ggctccggac tgggagcagt ggtgtctcag
60
cacccaagca gagtgatctg caagtctggc accagcgtga agatcgagtg taggtccctg
120
gacttccagg ccaccacaat gttctggtac cgccagtttc caaagcagtc tctgatgctg
180
atggccacat ccaacgaggg ctctaaggcc acctatgagc agggcgtgga gaaggacaag
240
ttcctgatca atcacgccag cctgaccctg tccaccctga cagtgaccag cgcccaccca
300
gaggatagct ccttttacat ctgctccgcc cagggctcta gcggccggat cgagcagttc
360
tttggccctg gcacacggct gaccgtgctg
390
<210> 509
<211> 130
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 509
Met Leu Leu Leu Leu Leu Leu Leu Gly Pro Gly Ser Gly Leu Gly Ala
1 5 10 15
Val Val Ser Gln His Pro Ser Arg Val Ile Cys Lys Ser Gly Thr Ser
20 25 30
Val Lys Ile Glu Cys Arg Ser Leu Asp Phe Gln Ala Thr Thr Met Phe
35 40 45
Trp Tyr Arg Gln Phe Pro Lys Gln Ser Leu Met Leu Met Ala Thr Ser
50 55 60
Asn Glu Gly Ser Lys Ala Thr Tyr Glu Gln Gly Val Glu Lys Asp Lys
65 70 75 80
Phe Leu Ile Asn His Ala Ser Leu Thr Leu Ser Thr Leu Thr Val Thr
85 90 95
Ser Ala His Pro Glu Asp Ser Ser Phe Tyr Ile Cys Ser Ala Gln Gly
100 105 110
Ser Ser Gly Arg Ile Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu Thr
115 120 125
Val Leu
130
<210> 510
<211> 270
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 510
Met Leu Thr Ala Ser Leu Leu Arg Ala Val Ile Ala Ser Ile Cys Val
1 5 10 15
Val Ser Ser Met Ala Gln Lys Val Thr Gln Ala Gln Thr Glu Ile Ser
20 25 30
Val Val Glu Lys Glu Asp Val Thr Leu Asp Cys Val Tyr Glu Thr Arg
35 40 45
Asp Thr Thr Tyr Tyr Leu Phe Trp Tyr Lys Gln Pro Pro Ser Gly Glu
50 55 60
Leu Val Phe Leu Ile Arg Arg Asn Ser Phe Asp Glu Gln Asn Glu Ile
65 70 75 80
Ser Gly Arg Tyr Ser Trp Asn Phe Gln Lys Ser Thr Ser Ser Phe Asn
85 90 95
Phe Thr Ile Thr Ala Ser Gln Val Val Asp Ser Ala Val Tyr Phe Cys
100 105 110
Ala Leu Ile Arg Gly Ser Tyr Gln Leu Ile Trp Gly Ala Gly Thr Lys
115 120 125
Leu Ile Ile Lys Pro Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln
130 135 140
Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp
145 150 155 160
Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe
165 170 175
Ile Thr Asp Lys Thr Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser
180 185 190
Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp
195 200 205
Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys
210 215 220
Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn
225 230 235 240
Phe Gln Asn Leu Ser Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val
245 250 255
Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265 270
<210> 511
<211> 303
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 511
Met Leu Leu Leu Leu Leu Leu Leu Gly Pro Gly Ser Gly Leu Gly Ala
1 5 10 15
Val Val Ser Gln His Pro Ser Arg Val Ile Cys Lys Ser Gly Thr Ser
20 25 30
Val Lys Ile Glu Cys Arg Ser Leu Asp Phe Gln Ala Thr Thr Met Phe
35 40 45
Trp Tyr Arg Gln Phe Pro Lys Gln Ser Leu Met Leu Met Ala Thr Ser
50 55 60
Asn Glu Gly Ser Lys Ala Thr Tyr Glu Gln Gly Val Glu Lys Asp Lys
65 70 75 80
Phe Leu Ile Asn His Ala Ser Leu Thr Leu Ser Thr Leu Thr Val Thr
85 90 95
Ser Ala His Pro Glu Asp Ser Ser Phe Tyr Ile Cys Ser Ala Gln Gly
100 105 110
Ser Ser Gly Arg Ile Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu Thr
115 120 125
Val Leu Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe
130 135 140
Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val
145 150 155 160
Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp
165 170 175
Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln Ala
180 185 190
Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val
195 200 205
Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val
210 215 220
Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro
225 230 235 240
Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp
245 250 255
Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu Ser Ala Thr
260 265 270
Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu
275 280 285
Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys Asn Ser
290 295 300
<210> 512
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 512
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 513
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 513
Leu Ile Met Gln Leu Met Pro Phe Gly Cys
1 5 10
<210> 514
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 514
Met Gln Leu Met Pro Phe Gly Cys Leu Leu
1 5 10
<210> 515
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 515
Asp Ser Val Asn Asn
1 5
<210> 516
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 516
Ile Pro Ser Gly Thr
1 5
<210> 517
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 517
Ala Val Met Asp Ser Ser Tyr Lys Leu Ile
1 5 10
<210> 518
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 518
Asp Phe Gln Ala Thr Thr
1 5
<210> 519
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 519
Ser Asn Glu Gly Ser Lys Ala
1 5
<210> 520
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 520
Ser Ala Leu Pro Gly Phe Ser Tyr Glu Gln Tyr
1 5 10
<210> 521
<211> 384
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 521
atgaagagga tattgggagc tctgctgggg ctcttgagtg cccaggtttg ctgtgtgaga
60
ggaatacaag tggagcagag tcctccagac ctgattctcc aggagggagc caattccacg
120
ctgcggtgca atttttctga ctctgtgaac aatttgcagt ggtttcatca aaacccttgg
180
ggacagctca tcaacctgtt ttacattccc tcagggacaa aacagaatgg aagattaagc
240
gccacgactg tcgctacgga acgctacagc ttattgtaca tttcctcttc ccagaccaca
300
gactcaggcg tttatttctg tgctgtgatg gatagcagct ataaattgat cttcgggagt
360
gggaccagac tgctggtcag gcct
384
<210> 522
<211> 384
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 522
atgaagagaa tcctgggcgc cctgctggga ctgctgtccg cccaggtgtg ctgcgtgcgg
60
ggcatccagg tggagcagag cccaccagac ctgatcctgc aggagggagc caactccacc
120
ctgagatgca atttctccga ttctgtgaac aatctgcagt ggtttcacca gaacccttgg
180
ggccagctga tcaatctgtt ttacatccca tccggcacaa agcagaacgg caggctgtct
240
gccaccacag tggccaccga gcggtactct ctgctgtata tctcctctag ccagaccaca
300
gacagcggcg tgtacttctg tgccgtgatg gattcctctt ataagctgat ctttggcagc
360
ggcaccaggc tgctggtgcg ccct
384
<210> 523
<211> 128
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 523
Met Lys Arg Ile Leu Gly Ala Leu Leu Gly Leu Leu Ser Ala Gln Val
1 5 10 15
Cys Cys Val Arg Gly Ile Gln Val Glu Gln Ser Pro Pro Asp Leu Ile
20 25 30
Leu Gln Glu Gly Ala Asn Ser Thr Leu Arg Cys Asn Phe Ser Asp Ser
35 40 45
Val Asn Asn Leu Gln Trp Phe His Gln Asn Pro Trp Gly Gln Leu Ile
50 55 60
Asn Leu Phe Tyr Ile Pro Ser Gly Thr Lys Gln Asn Gly Arg Leu Ser
65 70 75 80
Ala Thr Thr Val Ala Thr Glu Arg Tyr Ser Leu Leu Tyr Ile Ser Ser
85 90 95
Ser Gln Thr Thr Asp Ser Gly Val Tyr Phe Cys Ala Val Met Asp Ser
100 105 110
Ser Tyr Lys Leu Ile Phe Gly Ser Gly Thr Arg Leu Leu Val Arg Pro
115 120 125
<210> 524
<211> 387
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 524
atgctgctgc ttctgctgct tctggggcca ggctccgggc ttggtgctgt cgtctctcaa
60
catccgagct gggttatctg taagagtgga acctctgtga agatcgagtg ccgttccctg
120
gactttcagg ccacaactat gttttggtat cgtcagttcc cgaaacagag tctcatgctg
180
atggcaactt ccaatgaggg ctccaaggcc acatacgagc aaggcgtcga gaaggacaag
240
tttctcatca accatgcaag cctgaccttg tccactctga cagtgaccag tgcccatcct
300
gaagacagca gcttctacat ctgcagtgct ctgcccggat tctcctacga gcagtacttc
360
gggccgggca ccaggctcac ggtcaca
387
<210> 525
<211> 387
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 525
atgttattac tgctgctgct gctgggacca ggcagcggac tgggagcagt ggtgagccag
60
cacccttcct gggtcatctg caagagcggc acatccgtga agatcgagtg tcggtctctg
120
gacttccagg ccaccacaat gttctggtac agacagtttc ctaagcagtc cctgatgctg
180
atggccacat ctaacgaggg cagcaaggcc acctatgagc agggcgtgga gaaggacaag
240
ttcctgatca atcacgcctc cctgaccctg tctaccctga cagtgacctc cgcccaccca
300
gaggatagct ccttttacat ctgctctgcc ctgccaggct tcagctacga gcagtatttt
360
ggccccggca cacggctgac agtgacc
387
<210> 526
<211> 129
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 526
Met Leu Leu Leu Leu Leu Leu Leu Gly Pro Gly Ser Gly Leu Gly Ala
1 5 10 15
Val Val Ser Gln His Pro Ser Trp Val Ile Cys Lys Ser Gly Thr Ser
20 25 30
Val Lys Ile Glu Cys Arg Ser Leu Asp Phe Gln Ala Thr Thr Met Phe
35 40 45
Trp Tyr Arg Gln Phe Pro Lys Gln Ser Leu Met Leu Met Ala Thr Ser
50 55 60
Asn Glu Gly Ser Lys Ala Thr Tyr Glu Gln Gly Val Glu Lys Asp Lys
65 70 75 80
Phe Leu Ile Asn His Ala Ser Leu Thr Leu Ser Thr Leu Thr Val Thr
85 90 95
Ser Ala His Pro Glu Asp Ser Ser Phe Tyr Ile Cys Ser Ala Leu Pro
100 105 110
Gly Phe Ser Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg Leu Thr Val
115 120 125
Thr
<210> 527
<211> 265
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 527
Met Lys Arg Ile Leu Gly Ala Leu Leu Gly Leu Leu Ser Ala Gln Val
1 5 10 15
Cys Cys Val Arg Gly Ile Gln Val Glu Gln Ser Pro Pro Asp Leu Ile
20 25 30
Leu Gln Glu Gly Ala Asn Ser Thr Leu Arg Cys Asn Phe Ser Asp Ser
35 40 45
Val Asn Asn Leu Gln Trp Phe His Gln Asn Pro Trp Gly Gln Leu Ile
50 55 60
Asn Leu Phe Tyr Ile Pro Ser Gly Thr Lys Gln Asn Gly Arg Leu Ser
65 70 75 80
Ala Thr Thr Val Ala Thr Glu Arg Tyr Ser Leu Leu Tyr Ile Ser Ser
85 90 95
Ser Gln Thr Thr Asp Ser Gly Val Tyr Phe Cys Ala Val Met Asp Ser
100 105 110
Ser Tyr Lys Leu Ile Phe Gly Ser Gly Thr Arg Leu Leu Val Arg Pro
115 120 125
Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg
130 135 140
Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile
145 150 155 160
Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Thr
165 170 175
Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala
180 185 190
Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr
195 200 205
Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr
210 215 220
Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Ser
225 230 235 240
Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu
245 250 255
Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 528
<211> 302
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 528
Met Leu Leu Leu Leu Leu Leu Leu Gly Pro Gly Ser Gly Leu Gly Ala
1 5 10 15
Val Val Ser Gln His Pro Ser Trp Val Ile Cys Lys Ser Gly Thr Ser
20 25 30
Val Lys Ile Glu Cys Arg Ser Leu Asp Phe Gln Ala Thr Thr Met Phe
35 40 45
Trp Tyr Arg Gln Phe Pro Lys Gln Ser Leu Met Leu Met Ala Thr Ser
50 55 60
Asn Glu Gly Ser Lys Ala Thr Tyr Glu Gln Gly Val Glu Lys Asp Lys
65 70 75 80
Phe Leu Ile Asn His Ala Ser Leu Thr Leu Ser Thr Leu Thr Val Thr
85 90 95
Ser Ala His Pro Glu Asp Ser Ser Phe Tyr Ile Cys Ser Ala Leu Pro
100 105 110
Gly Phe Ser Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg Leu Thr Val
115 120 125
Thr Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
130 135 140
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
145 150 155 160
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
165 170 175
Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln Ala Tyr
180 185 190
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
195 200 205
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
210 215 220
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
225 230 235 240
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
245 250 255
Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu Ser Ala Thr Ile
260 265 270
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
275 280 285
Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys Asn Ser
290 295 300
<210> 529
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 529
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 530
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 530
Leu Ile Met Gln Leu Met Pro Phe Gly Cys
1 5 10
<210> 531
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 531
Met Gln Leu Met Pro Phe Gly Cys Leu Leu
1 5 10
<210> 532
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 532
Asn Ser Met Phe Asp Tyr
1 5
<210> 533
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 533
Ile Ser Ser Ile Lys Asp Lys
1 5
<210> 534
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 534
Ala Ala Asn Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr
1 5 10
<210> 535
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 535
Ser Asn His Leu Tyr
1 5
<210> 536
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 536
Phe Tyr Asn Asn Glu Ile
1 5
<210> 537
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 537
Ala Ser Ser Glu Trp Gly Ser Thr Gly Glu Leu Phe
1 5 10
<210> 538
<211> 421
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 538
atggccatgc tcctgggggc atcagtgctg attctgtggc ttcagccaga ctgggtaaac
60
agtcaacaga agaatgatga ccagcaagtt aagcaaaatt caccatccct gagcgtccag
120
gaaggaagaa tttctattct gaactgtgac tatactaaca gcatgtttga ttatttccta
180
tggtacaaaa aataccctgc tgaaggtcct acattcctga tatctataag ttccattaag
240
gataaaaatg aagatggaag attcactgtc ttcttaaaca aaagtgccaa gcacctctct
300
ctgcacattg tgccctccca gcctggagac tctgcagtgt acttctgtgc agcaaatgct
360
ggtggtacta gctatggaaa gctgacattt ggacaaggga ccatcttgac tgtccatcca
420
a
421
<210> 539
<211> 140
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 539
Met Ala Met Leu Leu Gly Ala Ser Val Leu Ile Leu Trp Leu Gln Pro
1 5 10 15
Asp Trp Val Asn Ser Gln Gln Lys Asn Asp Asp Gln Gln Val Lys Gln
20 25 30
Asn Ser Pro Ser Leu Ser Val Gln Glu Gly Arg Ile Ser Ile Leu Asn
35 40 45
Cys Asp Tyr Thr Asn Ser Met Phe Asp Tyr Phe Leu Trp Tyr Lys Lys
50 55 60
Tyr Pro Ala Glu Gly Pro Thr Phe Leu Ile Ser Ile Ser Ser Ile Lys
65 70 75 80
Asp Lys Asn Glu Asp Gly Arg Phe Thr Val Phe Leu Asn Lys Ser Ala
85 90 95
Lys His Leu Ser Leu His Ile Val Pro Ser Gln Pro Gly Asp Ser Ala
100 105 110
Val Tyr Phe Cys Ala Ala Asn Ala Gly Gly Thr Ser Tyr Gly Lys Leu
115 120 125
Thr Phe Gly Gln Gly Thr Ile Leu Thr Val His Pro
130 135 140
<210> 540
<211> 400
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 540
atggatacct ggctcgtatg ctgggcaatt tttagtctct tgaaagcagg actcacagaa
60
cctgaagtca cccagactcc cagccatcag gtcacacaga tgggacagga agtgatcttg
120
cgctgtgtcc ccatctctaa tcacttatac ttctattggt acagacaaat cttggggcag
180
aaagtcgagt ttctggtttc cttttataat aatgaaatct cagagaagtc tgaaatattc
240
gatgatcaat tctcagttga aaggcctgat ggatcaaatt tcactctgaa gatccggtcc
300
acaaagctgg aggactcagc catgtacttc tgtgccagca gtgaatgggg aagcaccggg
360
gagctgtttt ttggagaagg ctctaggctg accgtactgg
400
<210> 541
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 541
Met Asp Thr Trp Leu Val Cys Trp Ala Ile Phe Ser Leu Leu Lys Ala
1 5 10 15
Gly Leu Thr Glu Pro Glu Val Thr Gln Thr Pro Ser His Gln Val Thr
20 25 30
Gln Met Gly Gln Glu Val Ile Leu Arg Cys Val Pro Ile Ser Asn His
35 40 45
Leu Tyr Phe Tyr Trp Tyr Arg Gln Ile Leu Gly Gln Lys Val Glu Phe
50 55 60
Leu Val Ser Phe Tyr Asn Asn Glu Ile Ser Glu Lys Ser Glu Ile Phe
65 70 75 80
Asp Asp Gln Phe Ser Val Glu Arg Pro Asp Gly Ser Asn Phe Thr Leu
85 90 95
Lys Ile Arg Ser Thr Lys Leu Glu Asp Ser Ala Met Tyr Phe Cys Ala
100 105 110
Ser Ser Glu Trp Gly Ser Thr Gly Glu Leu Phe Phe Gly Glu Gly Ser
115 120 125
Arg Leu Thr Val Leu
130
<210> 542
<211> 277
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 542
Met Ala Met Leu Leu Gly Ala Ser Val Leu Ile Leu Trp Leu Gln Pro
1 5 10 15
Asp Trp Val Asn Ser Gln Gln Lys Asn Asp Asp Gln Gln Val Lys Gln
20 25 30
Asn Ser Pro Ser Leu Ser Val Gln Glu Gly Arg Ile Ser Ile Leu Asn
35 40 45
Cys Asp Tyr Thr Asn Ser Met Phe Asp Tyr Phe Leu Trp Tyr Lys Lys
50 55 60
Tyr Pro Ala Glu Gly Pro Thr Phe Leu Ile Ser Ile Ser Ser Ile Lys
65 70 75 80
Asp Lys Asn Glu Asp Gly Arg Phe Thr Val Phe Leu Asn Lys Ser Ala
85 90 95
Lys His Leu Ser Leu His Ile Val Pro Ser Gln Pro Gly Asp Ser Ala
100 105 110
Val Tyr Phe Cys Ala Ala Asn Ala Gly Gly Thr Ser Tyr Gly Lys Leu
115 120 125
Thr Phe Gly Gln Gly Thr Ile Leu Thr Val His Pro Asp Ile Gln Asn
130 135 140
Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser
145 150 155 160
Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys
165 170 175
Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Thr Val Leu Asp Met
180 185 190
Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln
195 200 205
Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr
210 215 220
Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe
225 230 235 240
Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Ser Val Met Gly Leu
245 250 255
Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu
260 265 270
Arg Leu Trp Ser Ser
275
<210> 543
<211> 306
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 543
Met Asp Thr Trp Leu Val Cys Trp Ala Ile Phe Ser Leu Leu Lys Ala
1 5 10 15
Gly Leu Thr Glu Pro Glu Val Thr Gln Thr Pro Ser His Gln Val Thr
20 25 30
Gln Met Gly Gln Glu Val Ile Leu Arg Cys Val Pro Ile Ser Asn His
35 40 45
Leu Tyr Phe Tyr Trp Tyr Arg Gln Ile Leu Gly Gln Lys Val Glu Phe
50 55 60
Leu Val Ser Phe Tyr Asn Asn Glu Ile Ser Glu Lys Ser Glu Ile Phe
65 70 75 80
Asp Asp Gln Phe Ser Val Glu Arg Pro Asp Gly Ser Asn Phe Thr Leu
85 90 95
Lys Ile Arg Ser Thr Lys Leu Glu Asp Ser Ala Met Tyr Phe Cys Ala
100 105 110
Ser Ser Glu Trp Gly Ser Thr Gly Glu Leu Phe Phe Gly Glu Gly Ser
115 120 125
Arg Leu Thr Val Leu Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val
130 135 140
Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala
145 150 155 160
Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu
165 170 175
Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp
180 185 190
Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg
195 200 205
Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg
210 215 220
Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu
225 230 235 240
Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly
245 250 255
Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu
260 265 270
Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr
275 280 285
Ala Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys
290 295 300
Asn Ser
305
<210> 544
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 544
Val Val Gly Ala Val Gly Val Gly Lys
1 5
<210> 545
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 545
Thr Thr Ser Asp Arg
1 5
<210> 546
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 546
Leu Leu Ser Asn Gly Ala Val
1 5
<210> 547
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 547
Ala Val Asp Ile Ile Gly Gly Lys Ser Thr
1 5 10
<210> 548
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 548
Ser Asn His Leu Tyr
1 5
<210> 549
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 549
Phe Tyr Asn Asn Glu Ile
1 5
<210> 550
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 550
Ala Ser Ser Glu Trp Gly Ser Thr Gly Glu Leu Phe
1 5 10
<210> 551
<211> 385
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 551
atgaagaagc tactagcaat gattctgtgg cttcaactag accggttaag tggagagctg
60
aaagtggaac aaaaccctct gttcctgagc atgcaggagg gaaaaaacta taccatctac
120
tgcaattatt caaccacttc agacagactg tattggtaca ggcaggatcc tgggaaaagt
180
ctggaatctc tgtttgtgtt gctatcaaat ggagcagtga agcaggaggg acgattaatg
240
gcctcacttg ataccaaagc ccgtctcagc accctccaca tcacagctgc cgtgcatgac
300
ctctctgcca cctacttctg tgccgtggac atcatcggag gcaaatcaac ctttggggat
360
gggactacgc tcactgtgaa gccaa
385
<210> 552
<211> 128
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 552
Met Lys Lys Leu Leu Ala Met Ile Leu Trp Leu Gln Leu Asp Arg Leu
1 5 10 15
Ser Gly Glu Leu Lys Val Glu Gln Asn Pro Leu Phe Leu Ser Met Gln
20 25 30
Glu Gly Lys Asn Tyr Thr Ile Tyr Cys Asn Tyr Ser Thr Thr Ser Asp
35 40 45
Arg Leu Tyr Trp Tyr Arg Gln Asp Pro Gly Lys Ser Leu Glu Ser Leu
50 55 60
Phe Val Leu Leu Ser Asn Gly Ala Val Lys Gln Glu Gly Arg Leu Met
65 70 75 80
Ala Ser Leu Asp Thr Lys Ala Arg Leu Ser Thr Leu His Ile Thr Ala
85 90 95
Ala Val His Asp Leu Ser Ala Thr Tyr Phe Cys Ala Val Asp Ile Ile
100 105 110
Gly Gly Lys Ser Thr Phe Gly Asp Gly Thr Thr Leu Thr Val Lys Pro
115 120 125
<210> 553
<211> 400
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 553
atggatacct ggctcgtatg ctgggcaatt tttagtctct tgaaagcagg actcacagaa
60
cctgaagtca cccagactcc cagccatcag gtcacacaga tgggacagga agtgatcttg
120
cgctgtgtcc ccatctctaa tcacttatac ttctattggt acagacaaat cttggggcag
180
aaagtcgagt ttctggtttc cttttataat aatgaaatct cagagaagtc tgaaatattc
240
gatgatcaat tctcagttga aaggcctgat ggatcaaatt tcactctgaa gatccggtcc
300
acaaagctgg aggactcagc catgtacttc tgtgccagca gtgaatgggg aagcaccggg
360
gagctgtttt ttggagaagg ctctaggctg accgtactgg
400
<210> 554
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 554
Met Asp Thr Trp Leu Val Cys Trp Ala Ile Phe Ser Leu Leu Lys Ala
1 5 10 15
Gly Leu Thr Glu Pro Glu Val Thr Gln Thr Pro Ser His Gln Val Thr
20 25 30
Gln Met Gly Gln Glu Val Ile Leu Arg Cys Val Pro Ile Ser Asn His
35 40 45
Leu Tyr Phe Tyr Trp Tyr Arg Gln Ile Leu Gly Gln Lys Val Glu Phe
50 55 60
Leu Val Ser Phe Tyr Asn Asn Glu Ile Ser Glu Lys Ser Glu Ile Phe
65 70 75 80
Asp Asp Gln Phe Ser Val Glu Arg Pro Asp Gly Ser Asn Phe Thr Leu
85 90 95
Lys Ile Arg Ser Thr Lys Leu Glu Asp Ser Ala Met Tyr Phe Cys Ala
100 105 110
Ser Ser Glu Trp Gly Ser Thr Gly Glu Leu Phe Phe Gly Glu Gly Ser
115 120 125
Arg Leu Thr Val Leu
130
<210> 555
<211> 265
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 555
Met Lys Lys Leu Leu Ala Met Ile Leu Trp Leu Gln Leu Asp Arg Leu
1 5 10 15
Ser Gly Glu Leu Lys Val Glu Gln Asn Pro Leu Phe Leu Ser Met Gln
20 25 30
Glu Gly Lys Asn Tyr Thr Ile Tyr Cys Asn Tyr Ser Thr Thr Ser Asp
35 40 45
Arg Leu Tyr Trp Tyr Arg Gln Asp Pro Gly Lys Ser Leu Glu Ser Leu
50 55 60
Phe Val Leu Leu Ser Asn Gly Ala Val Lys Gln Glu Gly Arg Leu Met
65 70 75 80
Ala Ser Leu Asp Thr Lys Ala Arg Leu Ser Thr Leu His Ile Thr Ala
85 90 95
Ala Val His Asp Leu Ser Ala Thr Tyr Phe Cys Ala Val Asp Ile Ile
100 105 110
Gly Gly Lys Ser Thr Phe Gly Asp Gly Thr Thr Leu Thr Val Lys Pro
115 120 125
Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg
130 135 140
Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile
145 150 155 160
Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Thr
165 170 175
Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala
180 185 190
Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr
195 200 205
Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr
210 215 220
Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Ser
225 230 235 240
Val Met Gly Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu
245 250 255
Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 556
<211> 306
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 556
Met Asp Thr Trp Leu Val Cys Trp Ala Ile Phe Ser Leu Leu Lys Ala
1 5 10 15
Gly Leu Thr Glu Pro Glu Val Thr Gln Thr Pro Ser His Gln Val Thr
20 25 30
Gln Met Gly Gln Glu Val Ile Leu Arg Cys Val Pro Ile Ser Asn His
35 40 45
Leu Tyr Phe Tyr Trp Tyr Arg Gln Ile Leu Gly Gln Lys Val Glu Phe
50 55 60
Leu Val Ser Phe Tyr Asn Asn Glu Ile Ser Glu Lys Ser Glu Ile Phe
65 70 75 80
Asp Asp Gln Phe Ser Val Glu Arg Pro Asp Gly Ser Asn Phe Thr Leu
85 90 95
Lys Ile Arg Ser Thr Lys Leu Glu Asp Ser Ala Met Tyr Phe Cys Ala
100 105 110
Ser Ser Glu Trp Gly Ser Thr Gly Glu Leu Phe Phe Gly Glu Gly Ser
115 120 125
Arg Leu Thr Val Leu Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val
130 135 140
Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala
145 150 155 160
Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu
165 170 175
Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp
180 185 190
Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg
195 200 205
Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg
210 215 220
Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu
225 230 235 240
Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly
245 250 255
Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu
260 265 270
Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr
275 280 285
Ala Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys
290 295 300
Asn Ser
305
<210> 557
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 557
Val Val Gly Ala Val Gly Val Gly Lys
1 5
<210> 558
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 558
Asn Ser Met Phe Asp Tyr
1 5
<210> 559
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 559
Ile Ser Ser Ile Lys Asp Lys
1 5
<210> 560
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 560
Ala Ala Ser Ala Val Gly Gln Glu Tyr Gly Asn Lys Leu Val
1 5 10
<210> 561
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 561
Ser Glu His Asn Arg
1 5
<210> 562
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 562
Phe Gln Asn Glu Ala Gln
1 5
<210> 563
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 563
Ala Ser Ser Glu Tyr Thr Met Gly Thr Gln Tyr
1 5 10
<210> 564
<211> 424
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 564
atggccatgc tcctgggggc atcagtgctg attctgtggc ttcagccaga ctgggtaaac
60
agtcaacaga agaatgatga ccagcaagtt aagcaaaatt caccatccct gagcgtccag
120
gaaggaagaa tttctattct gaactgtgac tatactaaca gcatgtttga ttatttccta
180
tggtacaaaa aataccctgc tgaaggtcct acattcctga tatctataag ttccattaag
240
gataaaaatg aagatggaag attcactgtc ttcttaaaca aaagtgccaa gcacctctct
300
ctgcacattg tgccctccca gcctggagac tctgcagtgt acttctgtgc agcaagcgca
360
gtaggtcagg aatatggaaa caagctggtc tttggcgcag gaaccattct gagagtcaag
420
tcct
424
<210> 565
<211> 141
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 565
Met Ala Met Leu Leu Gly Ala Ser Val Leu Ile Leu Trp Leu Gln Pro
1 5 10 15
Asp Trp Val Asn Ser Gln Gln Lys Asn Asp Asp Gln Gln Val Lys Gln
20 25 30
Asn Ser Pro Ser Leu Ser Val Gln Glu Gly Arg Ile Ser Ile Leu Asn
35 40 45
Cys Asp Tyr Thr Asn Ser Met Phe Asp Tyr Phe Leu Trp Tyr Lys Lys
50 55 60
Tyr Pro Ala Glu Gly Pro Thr Phe Leu Ile Ser Ile Ser Ser Ile Lys
65 70 75 80
Asp Lys Asn Glu Asp Gly Arg Phe Thr Val Phe Leu Asn Lys Ser Ala
85 90 95
Lys His Leu Ser Leu His Ile Val Pro Ser Gln Pro Gly Asp Ser Ala
100 105 110
Val Tyr Phe Cys Ala Ala Ser Ala Val Gly Gln Glu Tyr Gly Asn Lys
115 120 125
Leu Val Phe Gly Ala Gly Thr Ile Leu Arg Val Lys Ser
130 135 140
<210> 566
<211> 397
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 566
atgggcacca gcctcctctg ctggatggcc ctgtgtctcc tgggggcaga tcacgcagat
60
actggagtct cccagaaccc cagacacaag atcacaaaga ggggacagaa tgtaactttc
120
aggtgtgatc caatttctga acacaaccgc ctttattggt accgacagac cctggggcag
180
ggcccagagt ttctgactta cttccagaat gaagctcaac tagaaaaatc aaggctgctc
240
agtgatcggt tctctgcaga gaggcctaag ggatctttct ccaccttgga gatccagcgc
300
acagagcagg gggactcggc catgtatctc tgtgccagca gtgaatatac tatggggacc
360
cagtacttcg ggccaggcac gcggctcctg gtgctcg
397
<210> 567
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 567
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asn Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Glu Tyr Thr Met Gly Thr Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Leu Val Leu
130
<210> 568
<211> 278
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 568
Met Ala Met Leu Leu Gly Ala Ser Val Leu Ile Leu Trp Leu Gln Pro
1 5 10 15
Asp Trp Val Asn Ser Gln Gln Lys Asn Asp Asp Gln Gln Val Lys Gln
20 25 30
Asn Ser Pro Ser Leu Ser Val Gln Glu Gly Arg Ile Ser Ile Leu Asn
35 40 45
Cys Asp Tyr Thr Asn Ser Met Phe Asp Tyr Phe Leu Trp Tyr Lys Lys
50 55 60
Tyr Pro Ala Glu Gly Pro Thr Phe Leu Ile Ser Ile Ser Ser Ile Lys
65 70 75 80
Asp Lys Asn Glu Asp Gly Arg Phe Thr Val Phe Leu Asn Lys Ser Ala
85 90 95
Lys His Leu Ser Leu His Ile Val Pro Ser Gln Pro Gly Asp Ser Ala
100 105 110
Val Tyr Phe Cys Ala Ala Ser Ala Val Gly Gln Glu Tyr Gly Asn Lys
115 120 125
Leu Val Phe Gly Ala Gly Thr Ile Leu Arg Val Lys Ser Asp Ile Gln
130 135 140
Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp
145 150 155 160
Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro
165 170 175
Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Thr Val Leu Asp
180 185 190
Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn
195 200 205
Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr
210 215 220
Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser
225 230 235 240
Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Ser Val Met Gly
245 250 255
Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr
260 265 270
Leu Arg Leu Trp Ser Ser
275
<210> 569
<211> 305
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 569
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asn Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Glu Tyr Thr Met Gly Thr Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Leu Val Leu Lys Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr His Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Gly Leu Val Leu Met Ala Met Val Lys Lys Lys Asn
290 295 300
Ser
305
<210> 570
<400> 570
000
<210> 571
<400> 571
000
<210> 572
<400> 572
000
<210> 573
<400> 573
000
<210> 574
<400> 574
000
<210> 575
<400> 575
000
<210> 576
<400> 576
000
<210> 577
<400> 577
000
<210> 578
<400> 578
000
<210> 579
<400> 579
000
<210> 580
<400> 580
000
<210> 581
<400> 581
000
<210> 582
<400> 582
000
<210> 583
<400> 583
000
<210> 584
<400> 584
000
<210> 585
<400> 585
000
<210> 586
<400> 586
000
<210> 587
<400> 587
000
<210> 588
<400> 588
000
<210> 589
<400> 589
000
<210> 590
<400> 590
000
<210> 591
<400> 591
000
<210> 592
<400> 592
000
<210> 593
<400> 593
000
<210> 594
<400> 594
000
<210> 595
<400> 595
000
<210> 596
<400> 596
000
<210> 597
<400> 597
000
<210> 598
<400> 598
000
<210> 599
<400> 599
000
<210> 600
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 600
Val Val Gly Ala Val Gly Val Gly Lys
1 5
<210> 601
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 601
Ser Gly Ser Gly
1
<210> 602
<211> 8
<212> БЕЛОК
<213> Вирус гриппа
<400> 602
Gly Ile Leu Gly Phe Val Thr Leu
1 5
<210> 603
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 603
Cys Ala Val Lys Gly Gly Gly Ser Gly Thr Tyr Lys Tyr Ile Phe
1 5 10 15
<210> 604
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 604
Cys Ala Val Gly Asn Asn Gln Gly Gly Lys Leu Ile Phe
1 5 10
<210> 605
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 605
Cys Ala Gly Pro Asn Thr Asn Ala Gly Lys Ser Thr Phe
1 5 10
<210> 606
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 606
Cys Ala Ala Ser Ile Ala Asp Gly Gln Lys Leu Leu Phe
1 5 10
<210> 607
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 607
Cys Ala Tyr Ile Asp Ala Gly Asn Gln Phe Tyr Phe
1 5 10
<210> 608
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 608
Cys Ala Val Arg Gly Asp Ser Gly Gly Gly Ala Asp Gly Leu Thr Phe
1 5 10 15
<210> 609
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 609
Cys Ala Val Asp Ile Ile Gly Gly Lys Ser Thr Phe
1 5 10
<210> 610
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 610
Cys Ala Ala Asn Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr Phe
1 5 10 15
<210> 611
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 611
Cys Ala Ser Ser Phe Phe Pro Thr Ser Thr Gly Arg Thr Asp Thr Gln
1 5 10 15
Tyr Phe
<210> 612
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 612
Cys Ala Ser Ser Gly Pro Gly Pro Arg Gly Phe Asn Glu Gln Phe Phe
1 5 10 15
<210> 613
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 613
Cys Ala Ser Ser Leu Gly Gln Asp Thr Glu Ala Phe Phe
1 5 10
<210> 614
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 614
Cys Ala Ser Ser Glu Ser Gly Ser Gly Glu Lys Leu Phe Phe
1 5 10
<210> 615
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 615
Cys Ala Ser Ile Thr Pro Arg Asp Glu Gln Phe Phe
1 5 10
<210> 616
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 616
Cys Ala Ser Ser Glu Trp Gly Ser Thr Gly Glu Leu Phe Phe
1 5 10
<210> 617
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 617
Cys Ala Met Arg Glu Gly Arg Gly Ala Gly Asn Asn Arg Lys Leu Ile
1 5 10 15
Trp
<210> 618
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 618
Cys Ala Leu Ser Glu Ala Gly Leu Gly Gly Gly Lys Leu Ile Phe
1 5 10 15
<210> 619
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 619
Cys Ala Ala Ser Ala Val Gly Gln Glu Tyr Gly Asn Lys Leu Val Phe
1 5 10 15
<210> 620
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 620
Cys Ala Ser Ser Gln Asp Arg Leu Ala Gly Asp Tyr Glu Gln Tyr Phe
1 5 10 15
<210> 621
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 621
Cys Ala Ser Ser Glu Tyr Thr Met Gly Thr Gln Tyr Phe
1 5 10
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| T-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ, РАСПОЗНАЮЩИЕ МУТАЦИЮ R175H ИЛИ Y220C В P53 | 2020 |
|
RU2830061C2 |
| Т-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ | 2017 |
|
RU2775623C2 |
| Т-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ, СПЕЦИФИЧНЫЕ В ОТНОШЕНИИ КОМПЛЕКСА ОПУХОЛЕВЫЙ АНТИГЕН NY-ESO-1/HLA-A*02 | 2016 |
|
RU2775394C2 |
| СПЕЦИФИЧНЫЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2020 |
|
RU2825837C2 |
| ВЫСОКОАФФИННЫЙ Т-КЛЕТОЧНЫЙ РЕЦЕПТОР ДЛЯ РАСПОЗНАВАНИЯ АНТИГЕНА AFP | 2019 |
|
RU2836365C2 |
| HPV-СПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2018 |
|
RU2804664C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛИВАЮЩИЕСЯ НА ВАРИАНТ III РЕЦЕПТОРА ЭПИДЕРМАЛЬНОГО ФАКТОРА РОСТА | 2017 |
|
RU2751662C2 |
| АНТИТЕЛА ПРОТИВ ТАУ-БЕЛКА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2732122C2 |
| НЕОАНТИГЕНЫ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2813924C2 |
| Т-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ | 2018 |
|
RU2762255C2 |
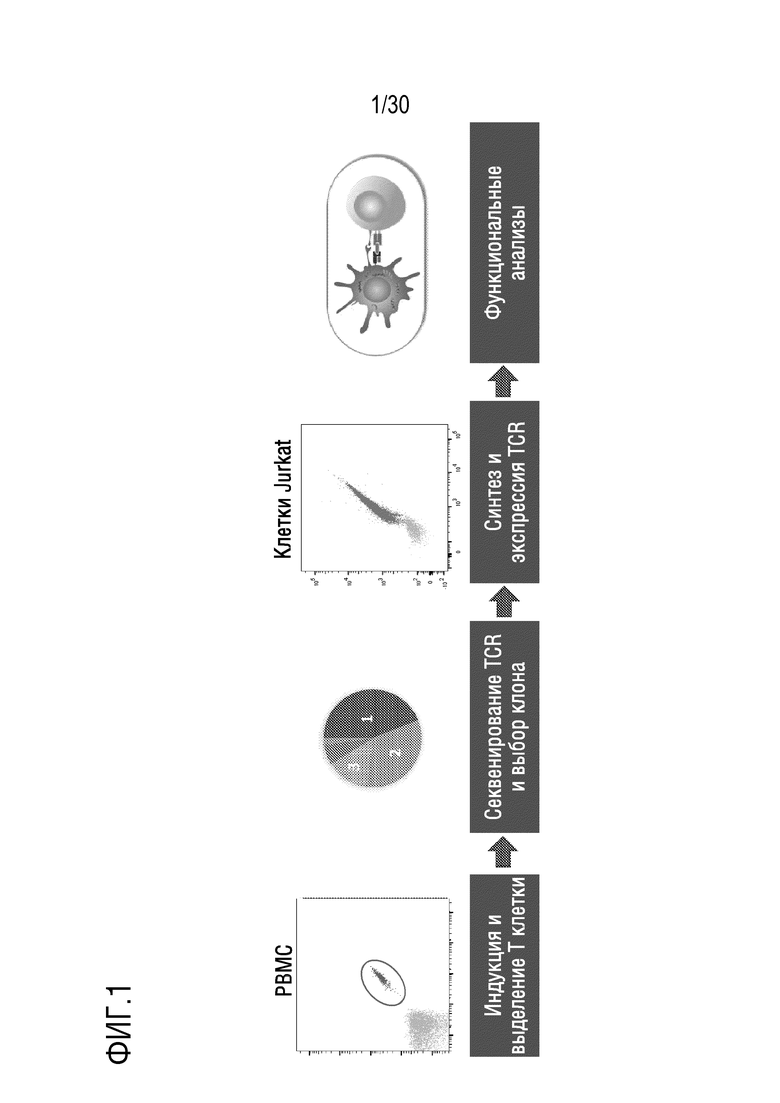
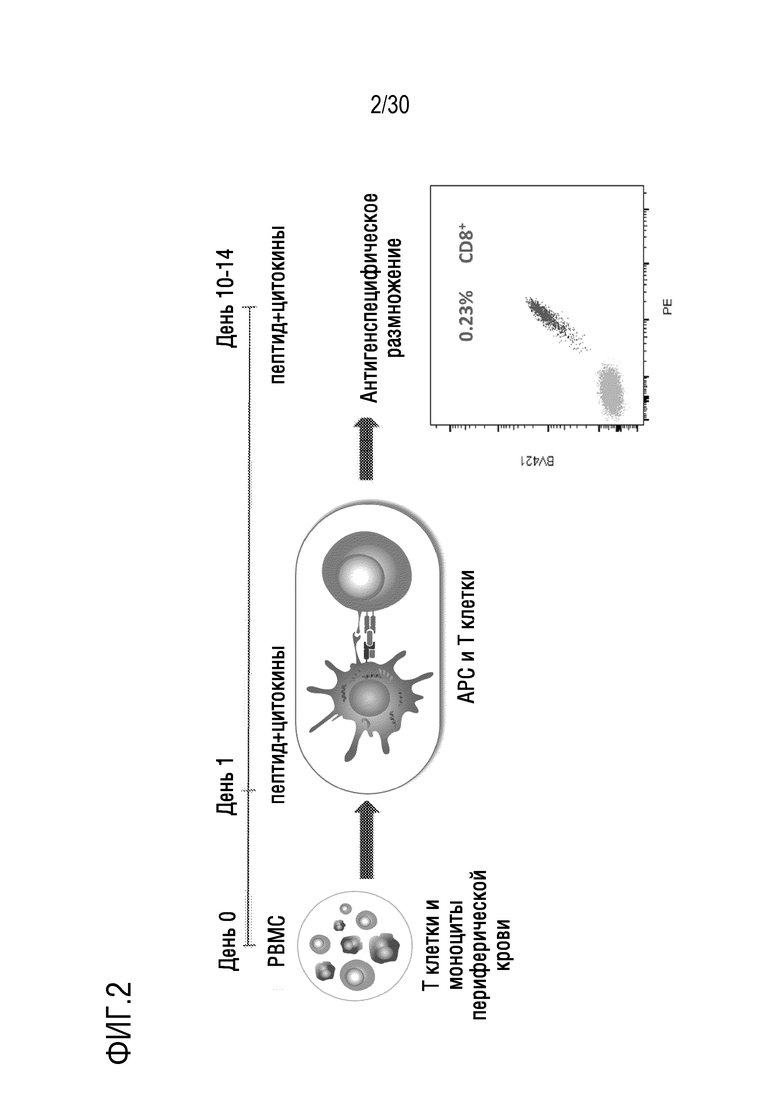
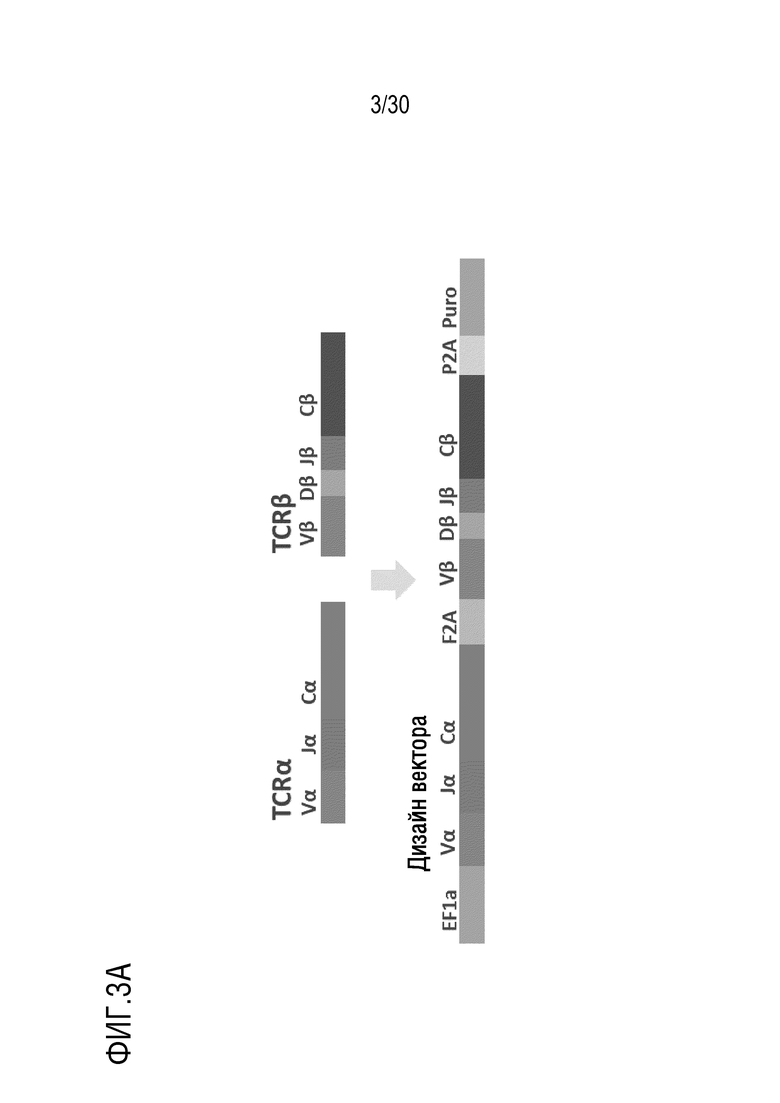
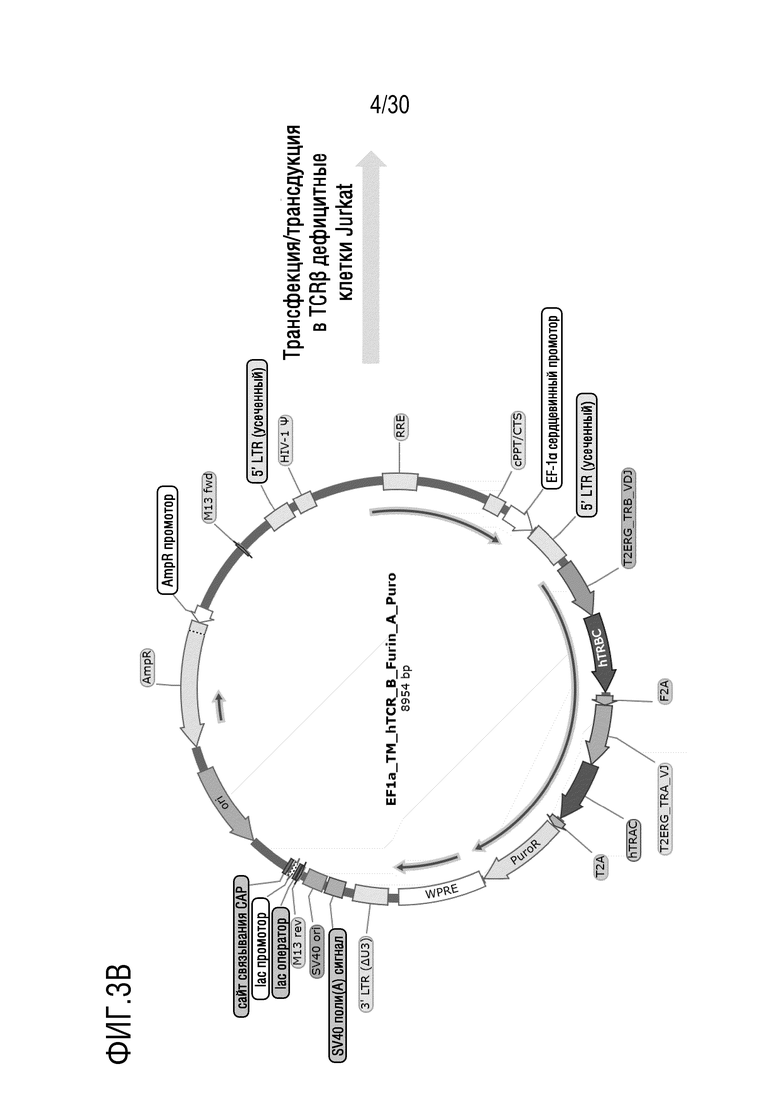
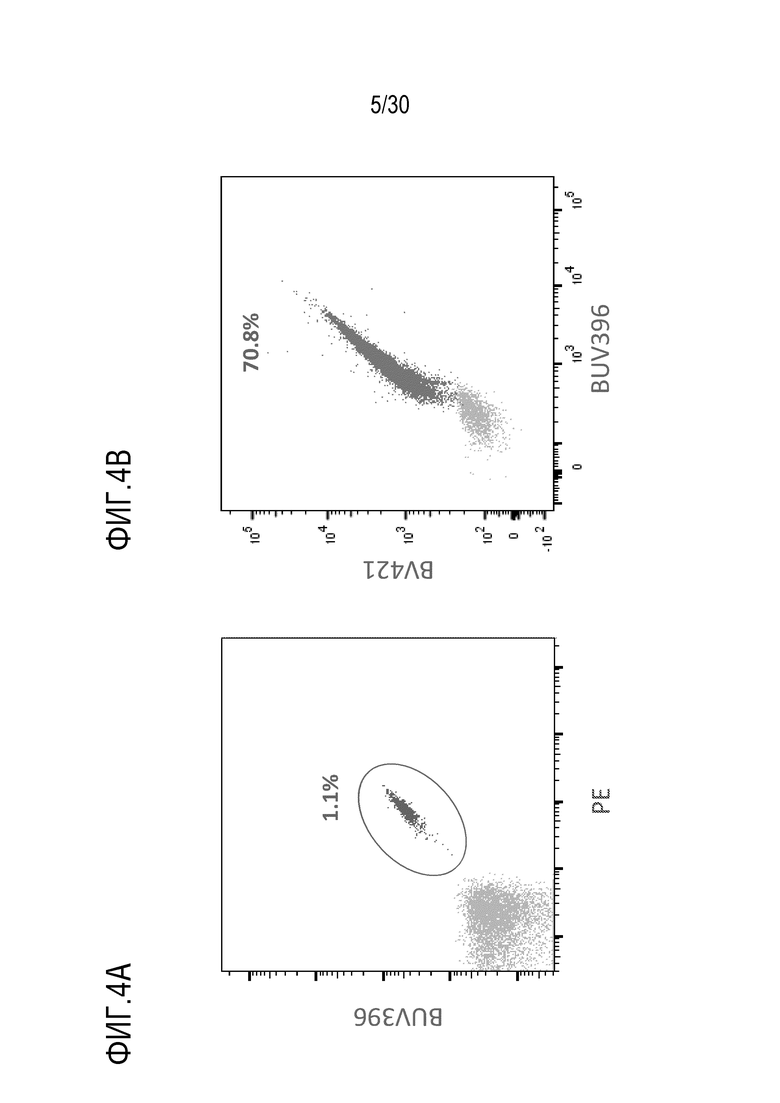
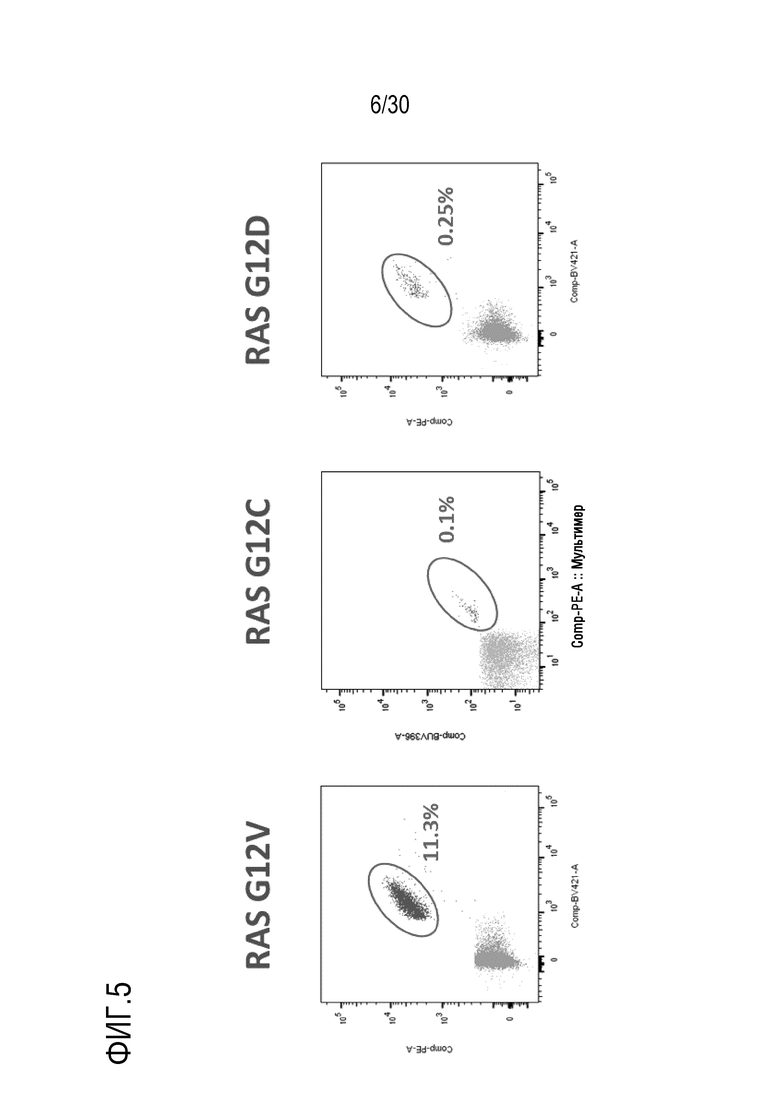
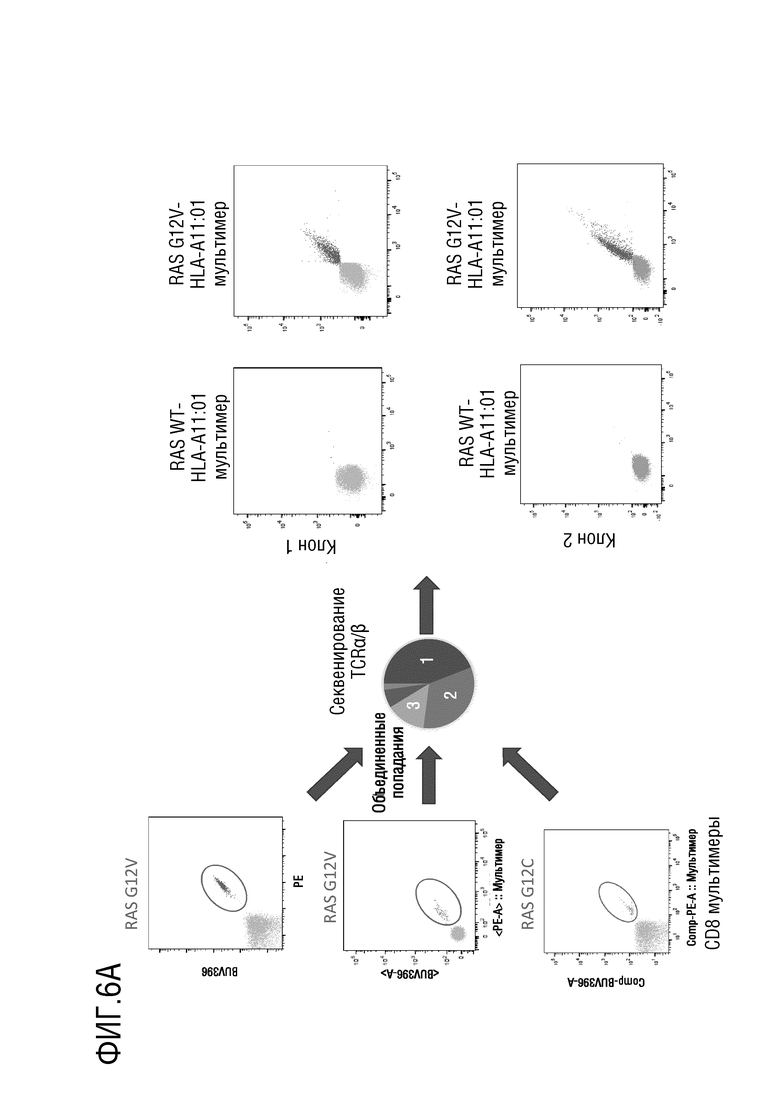
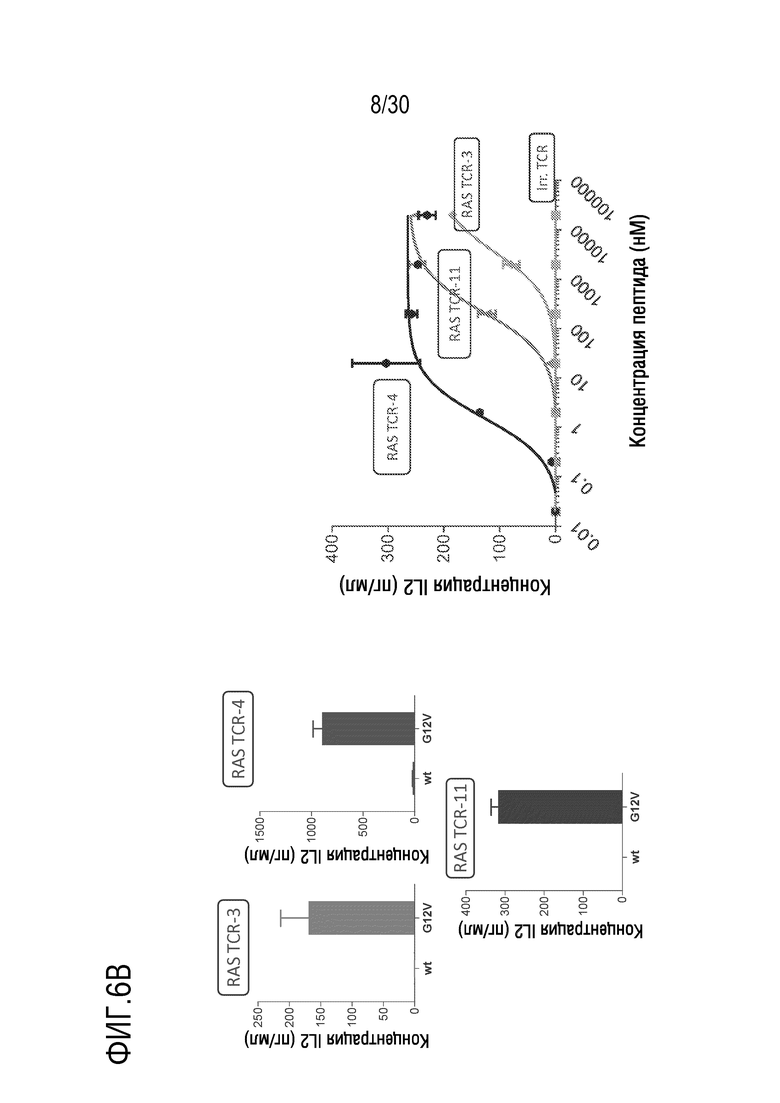
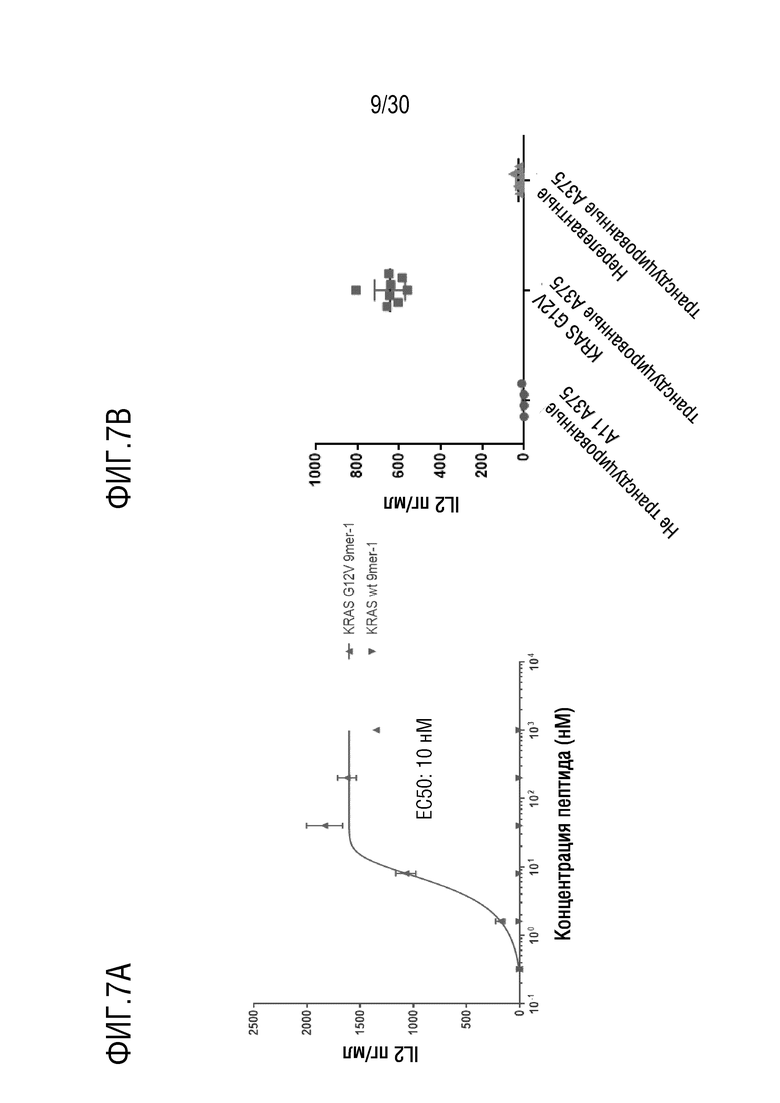
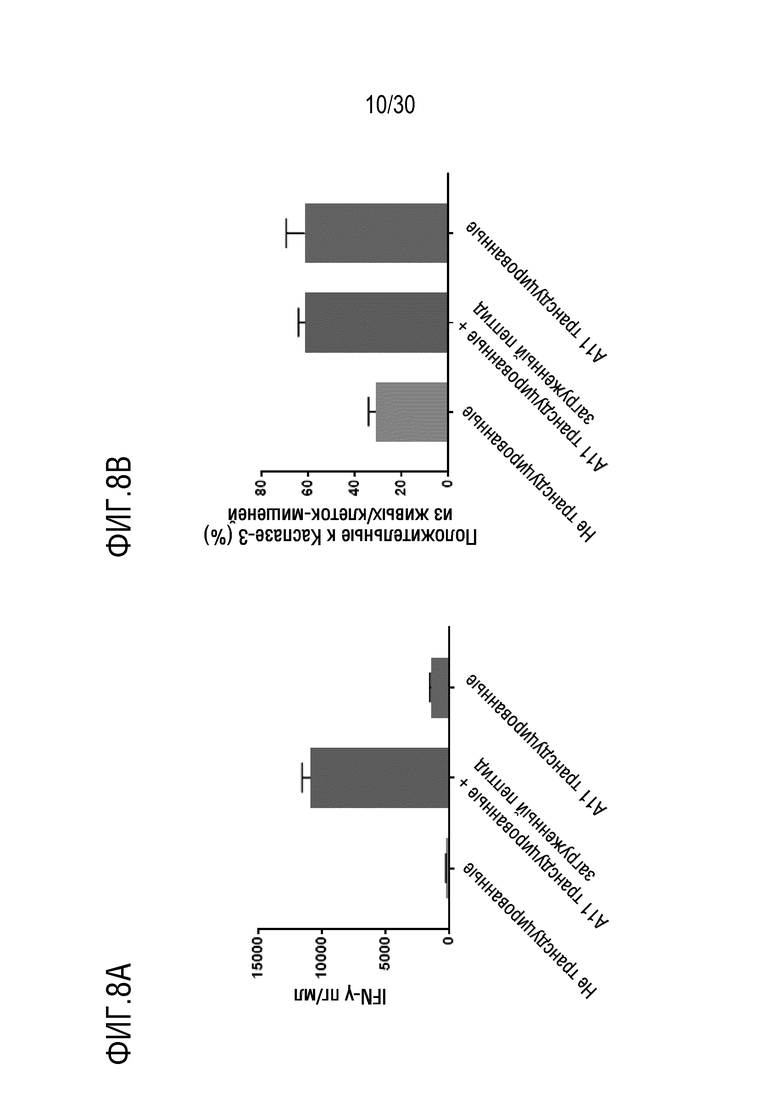

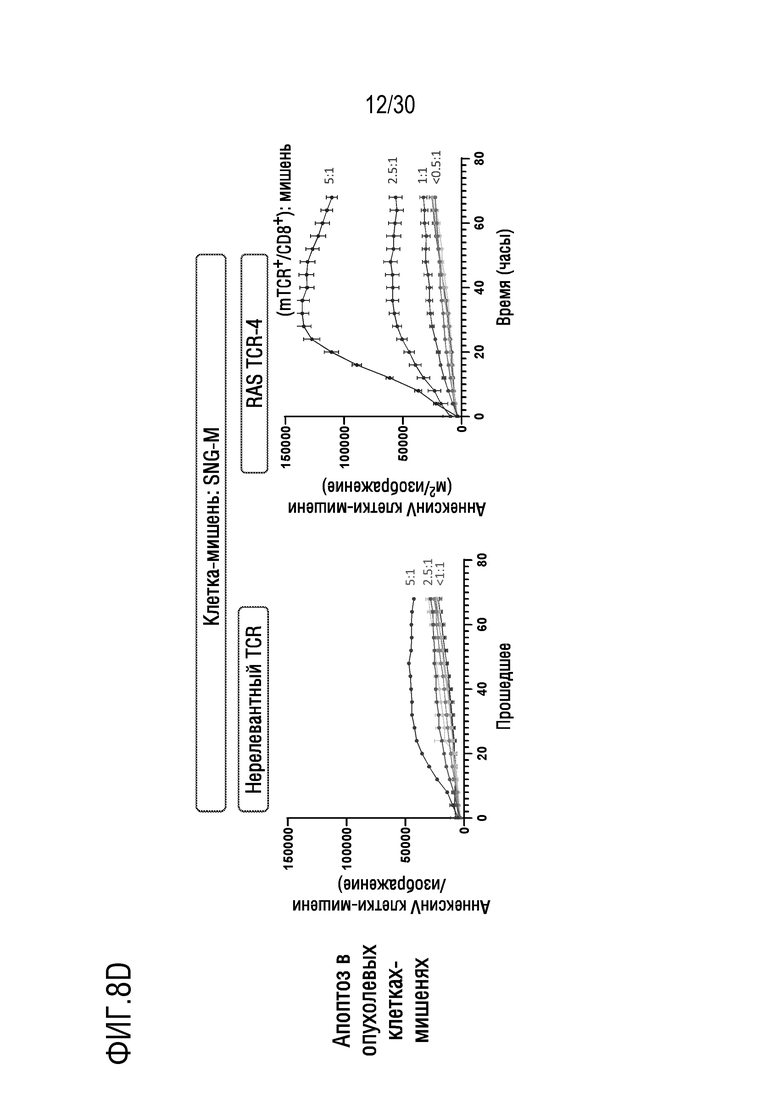

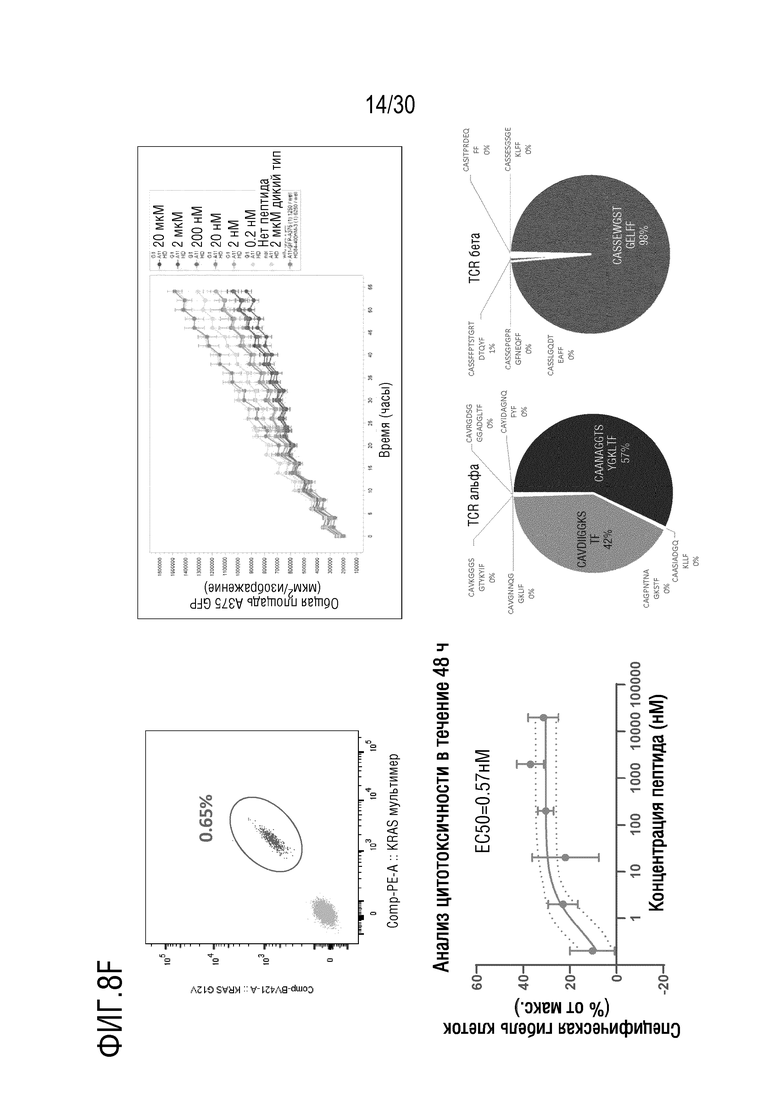
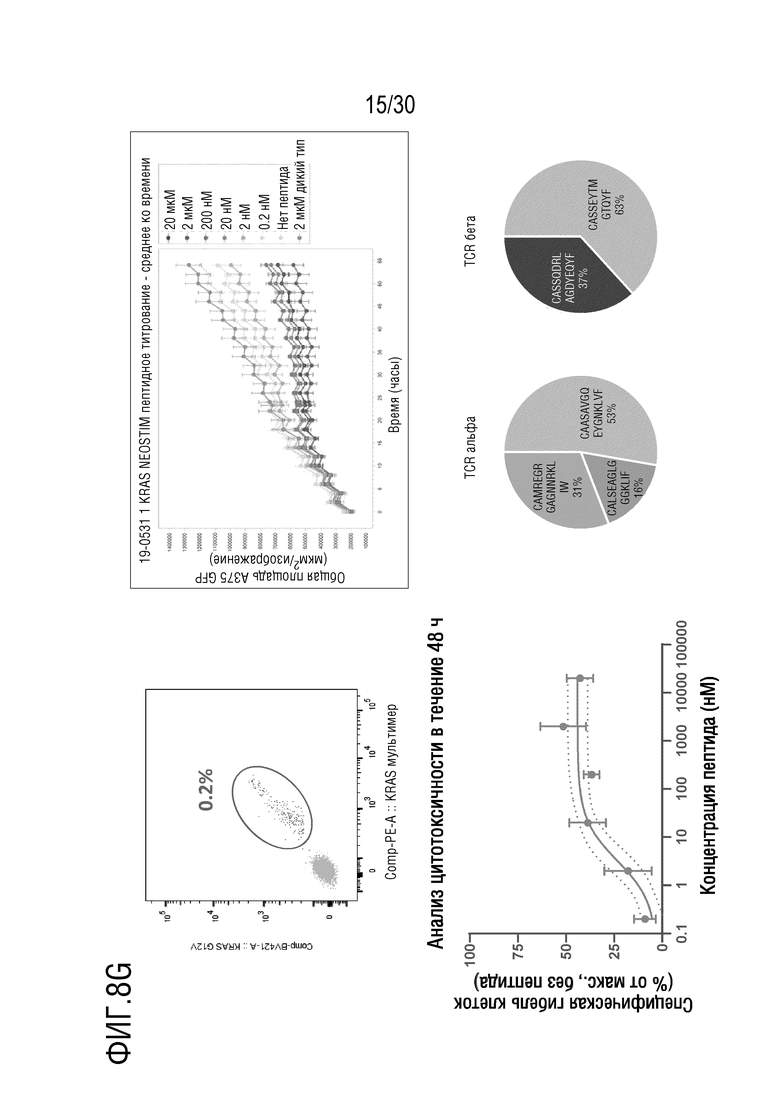
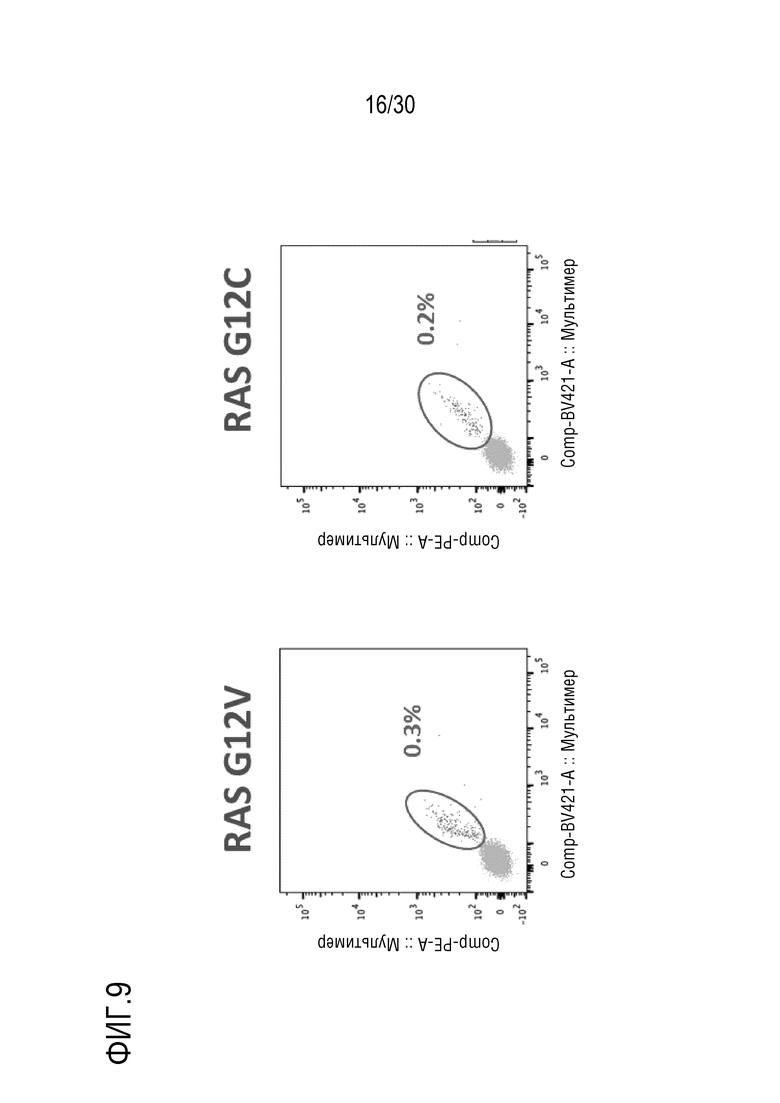
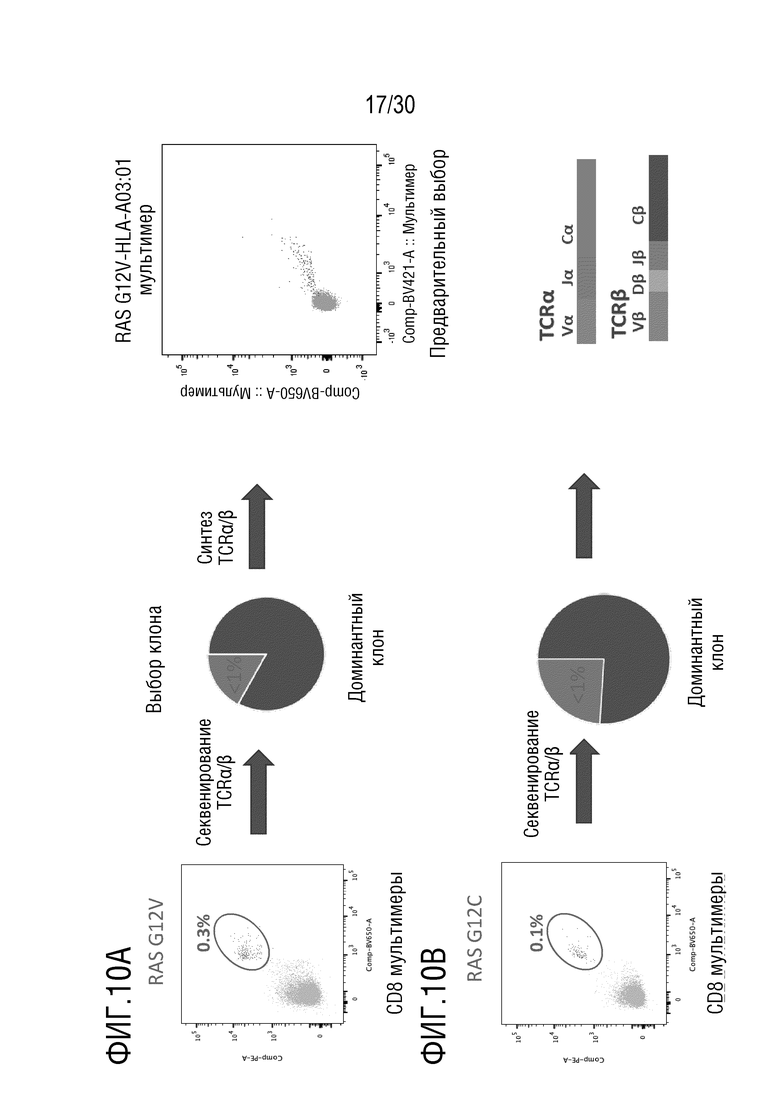
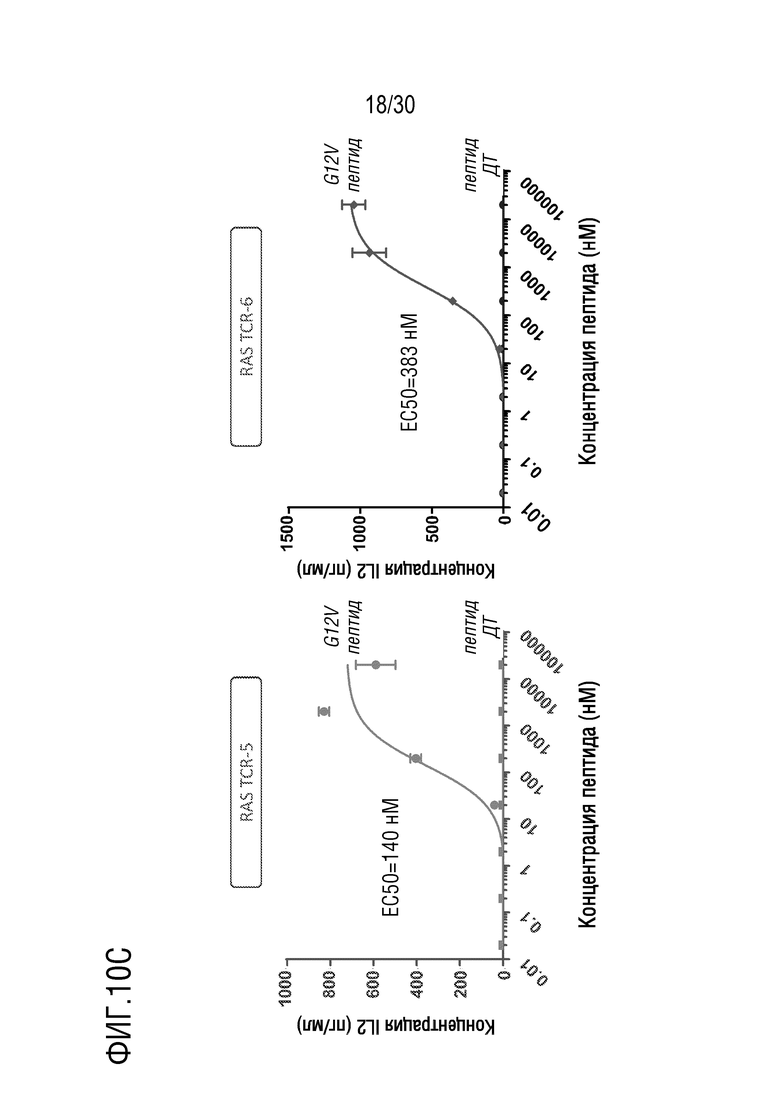
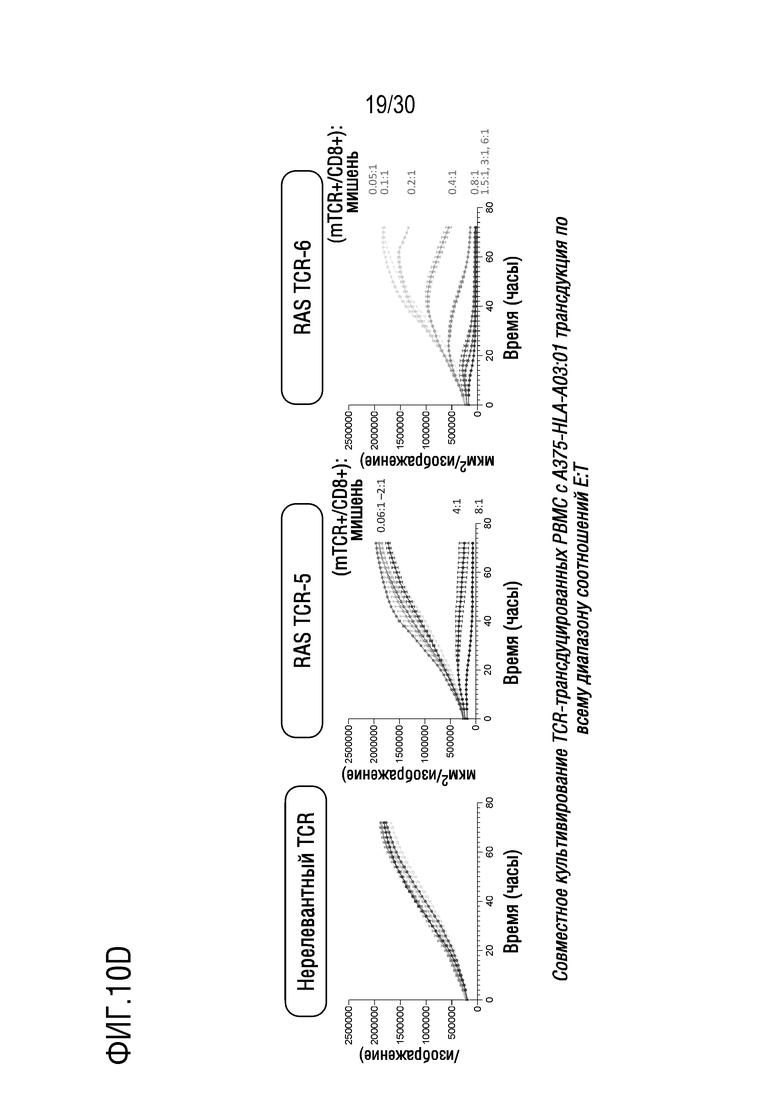
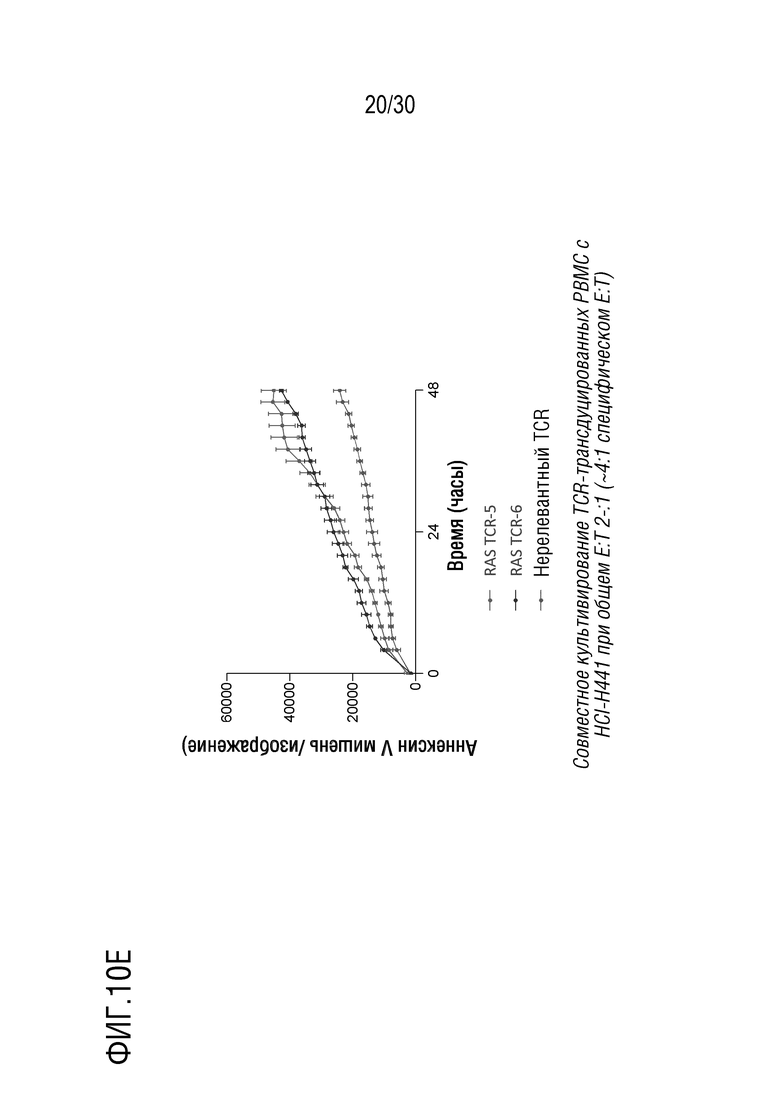
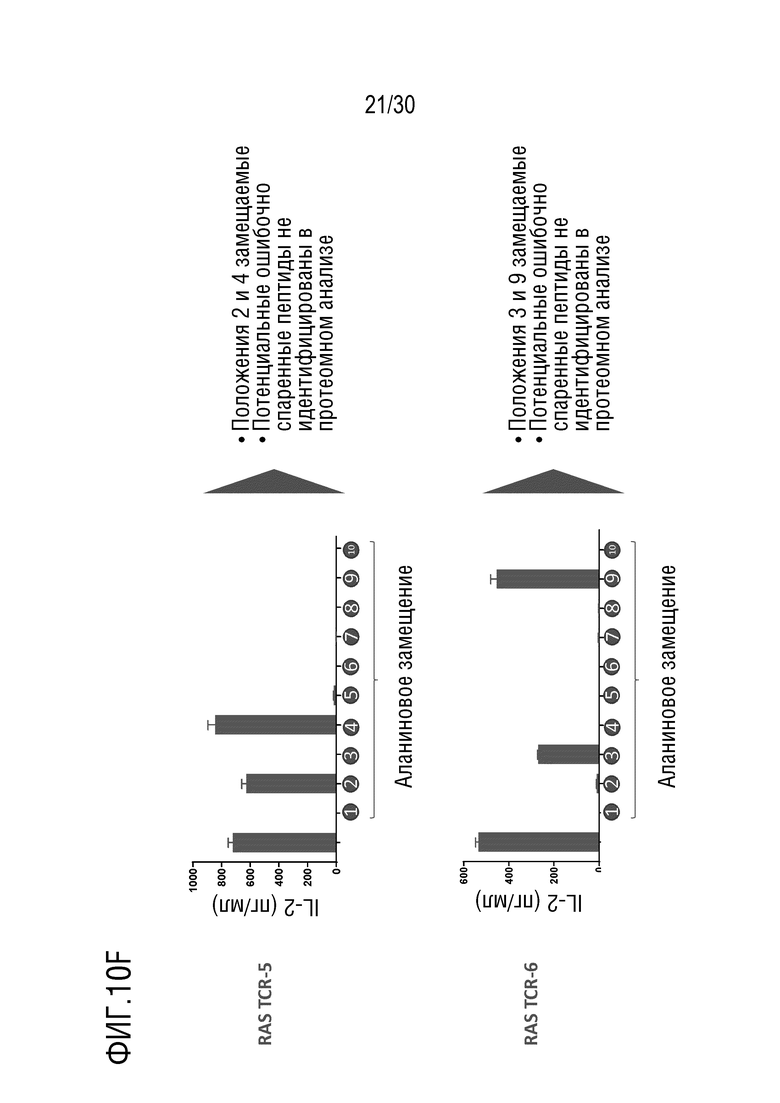
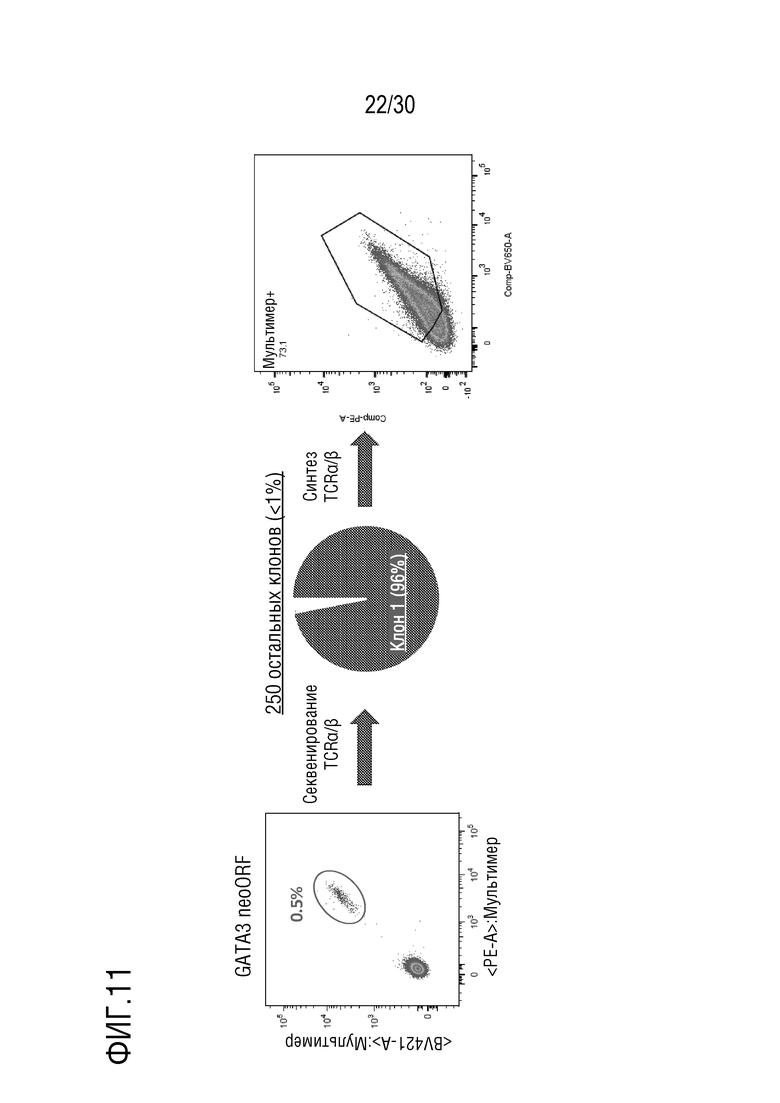
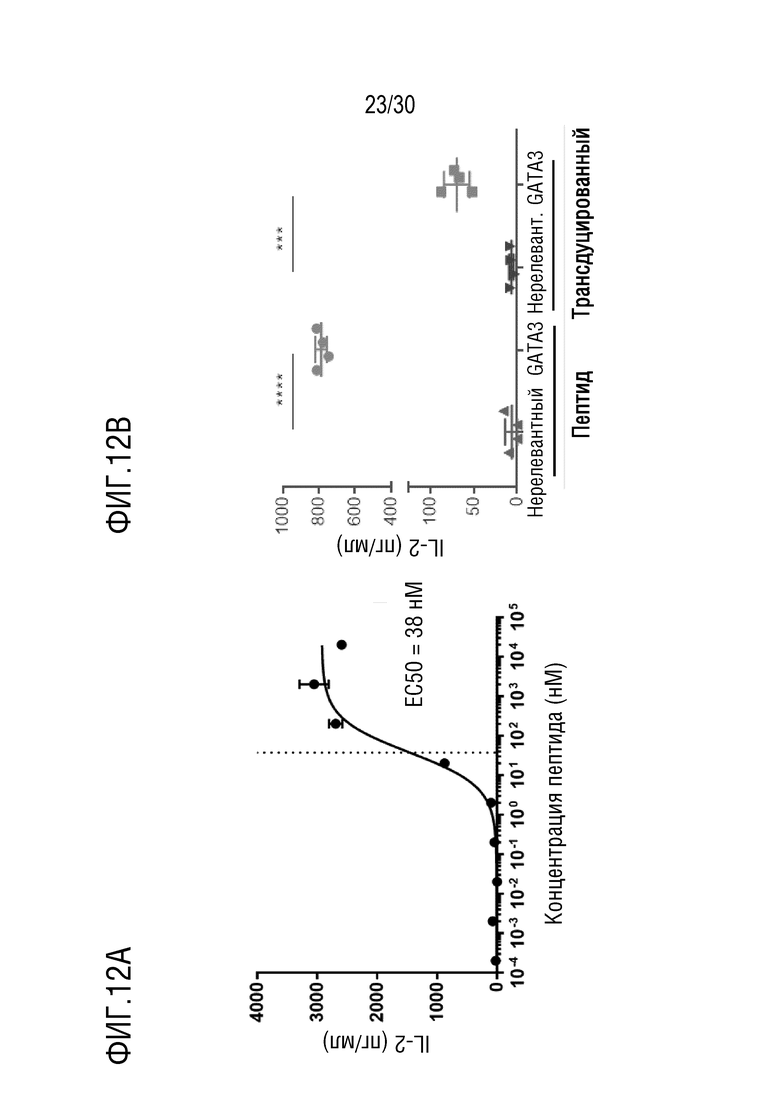
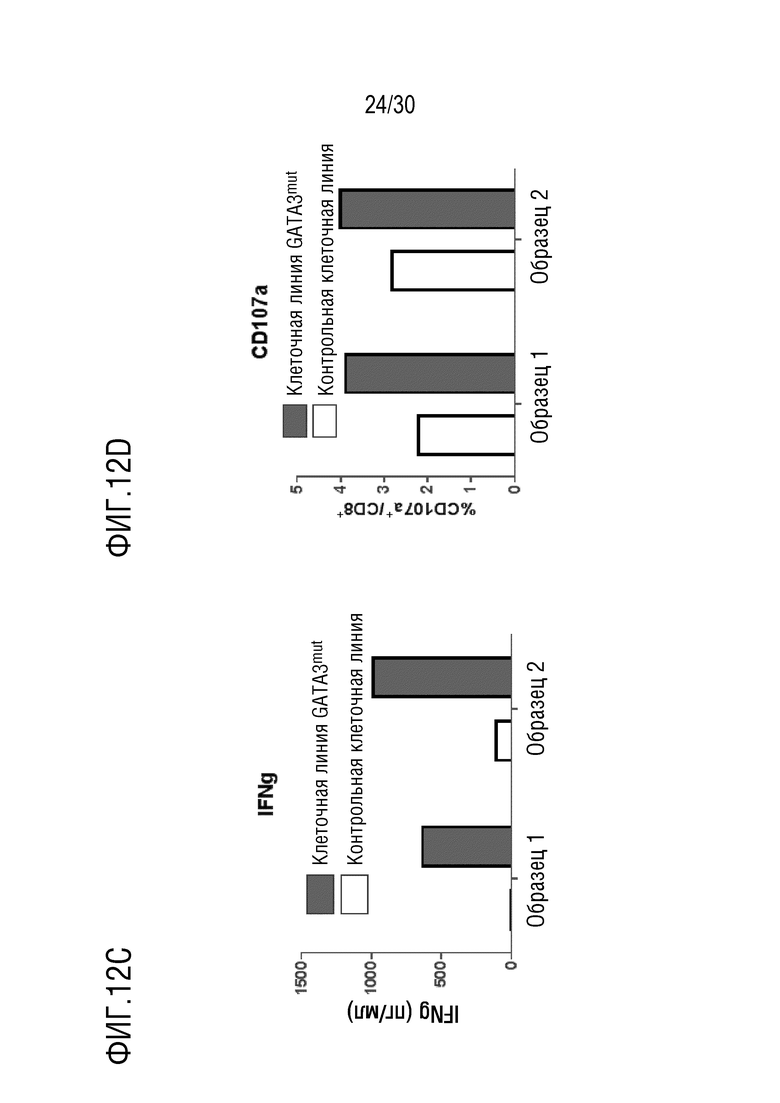
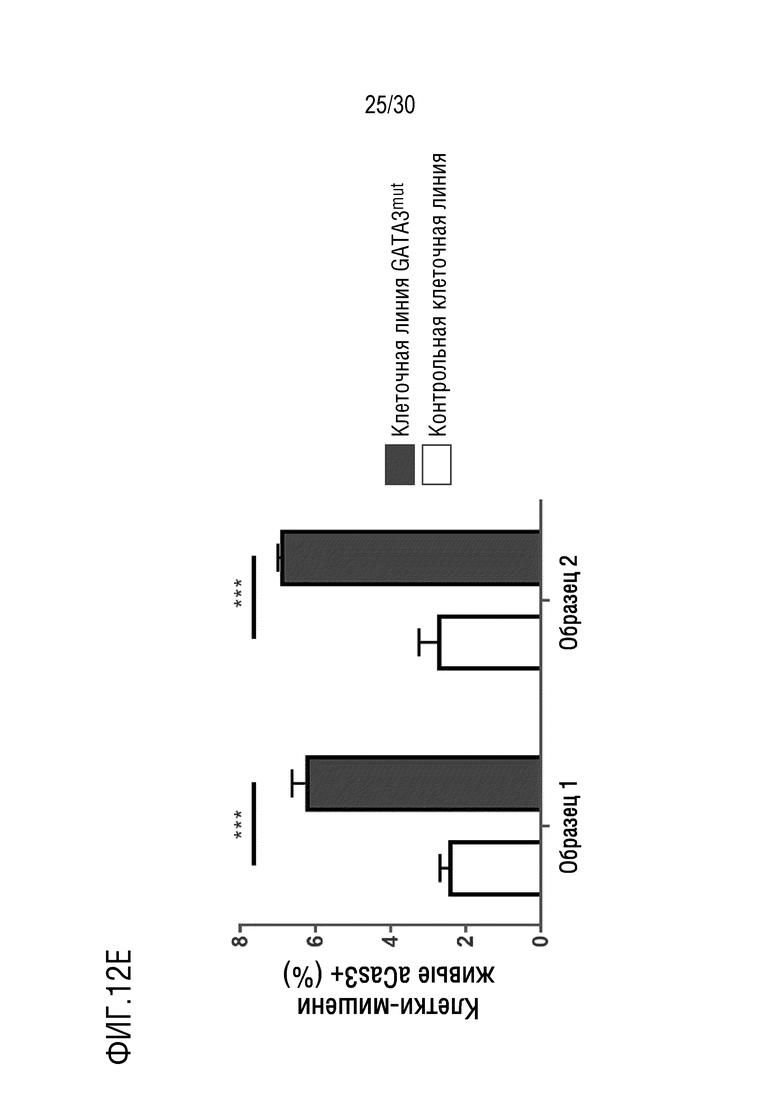

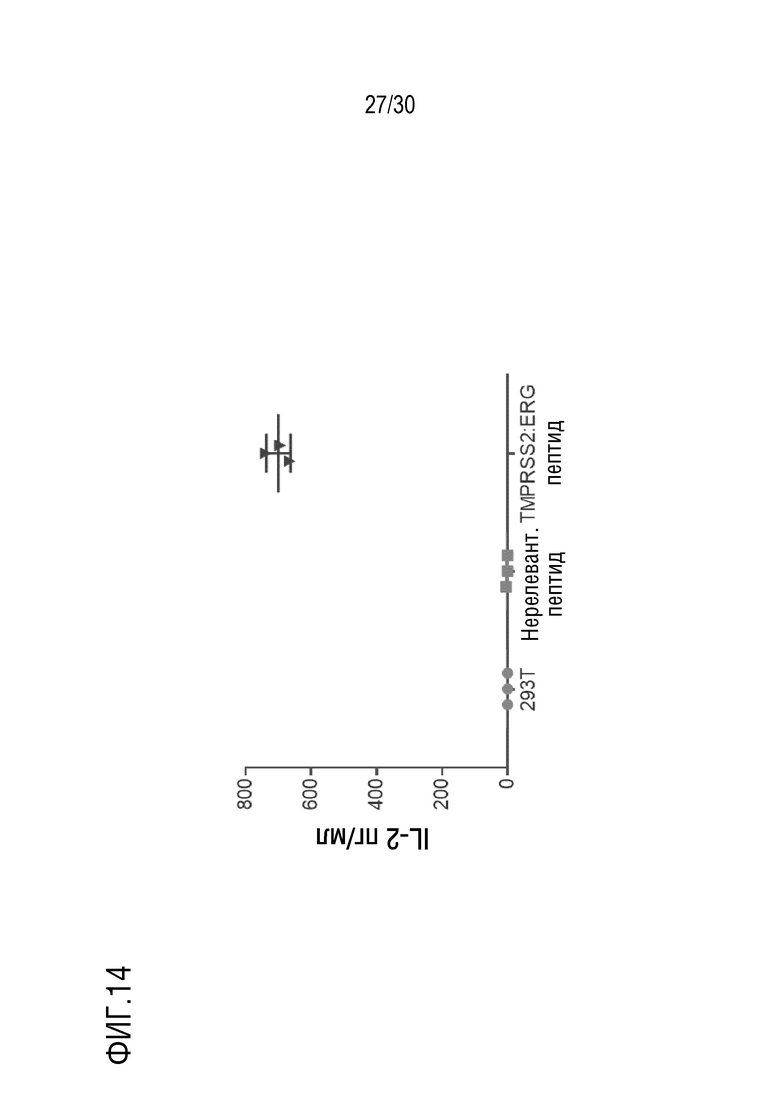
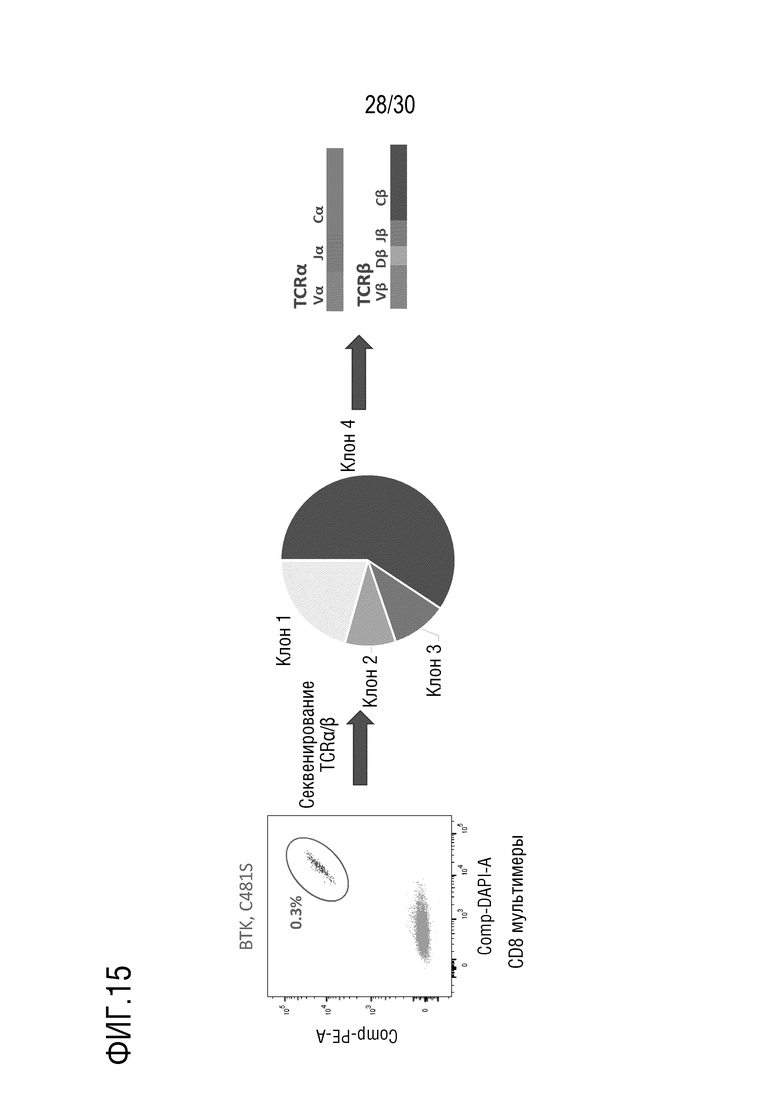
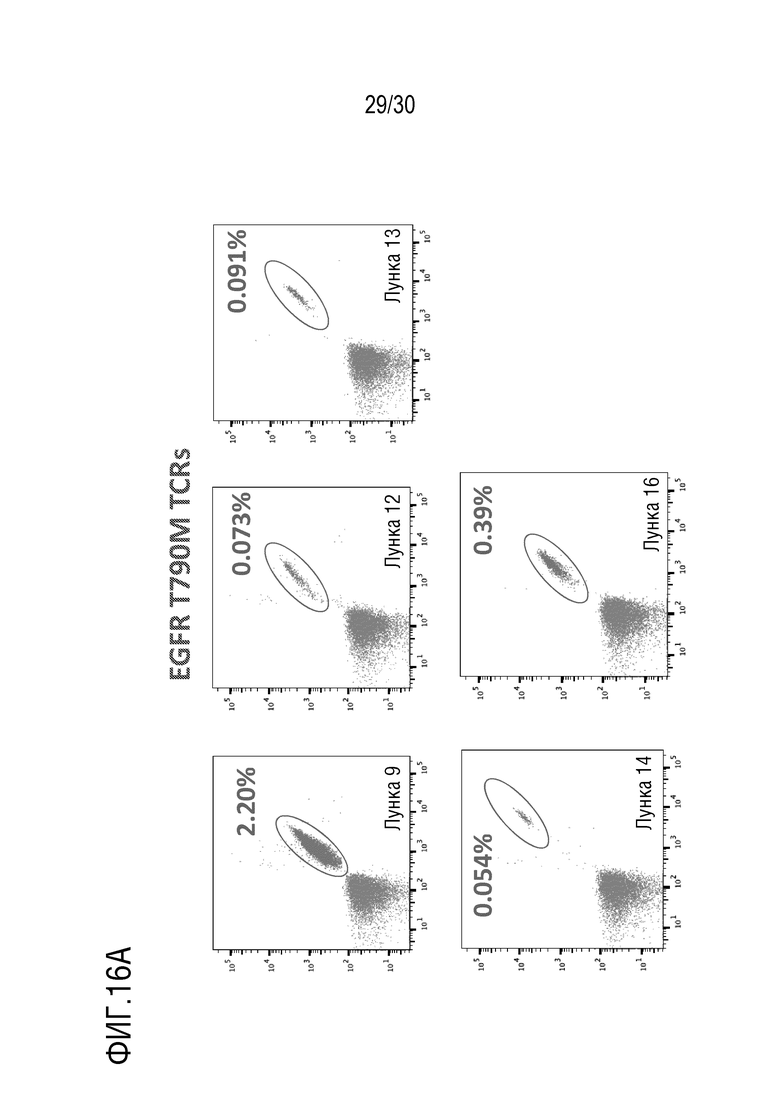
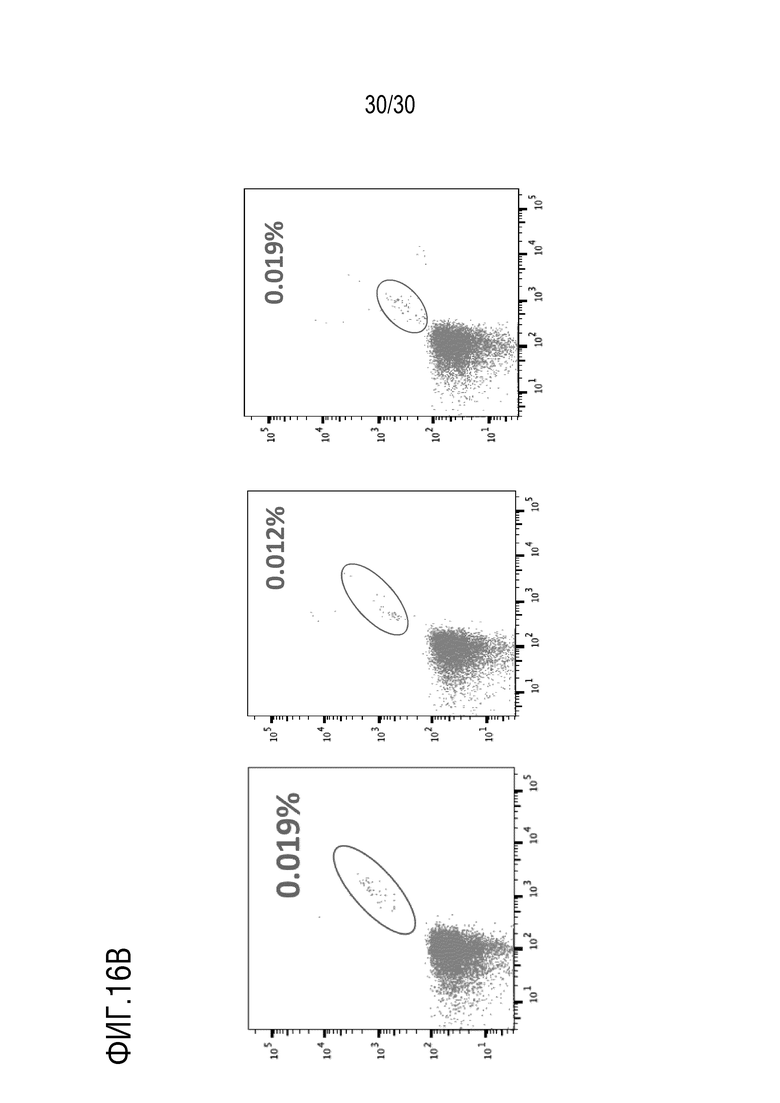
Группа изобретений относится к иммунологии. Предложены молекула выделенной нуклеиновой кислоты, кодирующая Т-клеточный рецептор (TCR) против комплексов пептид-МНС, T-клетки, экспрессирующие TCR, и фармацевтические композиции. Рекомбинантная нуклеиновая кислота кодирует TCR, содержащий (a) конструкцию бета-цепи, содержащую CDR1-3 с аминокислотными последовательностями SEQ ID NO: 50-52, и (b) конструкцию альфа-цепи TCR, содержащую CDR1-3 с аминокислотными последовательностями SEQ ID NO: 47-49. Рекомбинантная нуклеиновая кислота и содержащие ее Т-клетки пригодны для лечения заболевания или состояния, связанного с мутацией G12V RAS. Изобретения обеспечивают высокую степень специфичности и эффективности разрушения клеток-мишеней с мутацией G12V RAS. 5 н. и 24 з.п. ф-лы, 16 ил., 14 пр.
1. Рекомбинантная нуклеиновая кислота, кодирующая Т-клеточный рецептор (TCR), содержащий
(a) конструкцию бета-цепи TCR, содержащую:
(i) определяющую комплементарность область 1 (CDR1) с аминокислотной последовательностью SEQ ID NO: 50,
(ii) определяющую комплементарность область 2 (CDR2) c аминокислотной последовательностью SEQ ID NO: 51 и
(iii) определяющую комплементарность область 3 (CDR3) с аминокислотной последовательностью SEQ ID NO: 52; и
(b) конструкцию альфа-цепи TCR, содержащую:
(i) CDR1 c аминокислотной последовательностью SEQ ID NO: 47,
(ii) CDR2 c аминокислотной последовательностью SEQ ID NO: 48 и
(iii) CDR3 c аминокислотной последовательностью SEQ ID NO: 49.
2. Рекомбинантная нуклеиновая кислота по п.1, где конструкция бета-цепи TCR содержит вариабельную область с аминокислотной последовательностью, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO: 58.
3. Рекомбинантная нуклеиновая кислота по п.1 или 2, где конструкция бета-цепи TCR содержит вариабельную область, которая по меньшей мере на 90% идентична аминокислотной последовательности SEQ ID NO: 58.
4. Рекомбинантная нуклеиновая кислота по любому из предшествующих пунктов, где конструкция бета-цепи TCR содержит вариабельную область, которая по меньшей мере на 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности SEQ ID NO: 58.
5. Рекомбинантная нуклеиновая кислота по любому из предшествующих пунктов, где конструкция бета-цепи TCR содержит вариабельную область с аминокислотной последовательностью SEQ ID NO: 58.
6. Рекомбинантная нуклеиновая кислота по любому из предшествующих пунктов, содержащая:
(a) последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 56 или 57, где последовательность содержит последовательность, кодирующую по меньшей мере SEQ ID NO: 52, и
(b) последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 53 или 54, где последовательность содержит последовательность, кодирующую по меньшей мере SEQ ID NO: 49.
7. Рекомбинантная нуклеиновая кислота по любому из предшествующих пунктов, где конструкция альфа-цепи TCR содержит вариабельную область, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO: 55.
8. Рекомбинантная нуклеиновая кислота по любому из предшествующих пунктов, где конструкция альфа-цепи TCR содержит вариабельную область, которая по меньшей мере на 90% идентична аминокислотной последовательности SEQ ID NO: 55.
9. Рекомбинантная нуклеиновая кислота по любому из предшествующих пунктов, где конструкция альфа-цепи TCR содержит вариабельную область, которая по меньшей мере на 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности SEQ ID NO: 55.
10. Рекомбинантная нуклеиновая кислота по любому из предшествующих пунктов, где конструкция альфа-цепи TCR содержит вариабельную область с аминокислотной последовательностью SEQ ID NO: 55.
11. Рекомбинантная нуклеиновая кислота по п.1, где TCR содержит:
(a) бета-цепь с аминокислотной последовательностью SEQ ID NO: 60 или с аминокислотной последовательностью, которая по меньшей мере на 80% идентична SEQ ID NO: 60, и
(b) альфа-цепь с аминокислотной последовательностью SEQ ID NO: 59 или с аминокислотной последовательностью, которая по меньшей мере на 80% идентична SEQ ID NO: 59.
12. Рекомбинантная нуклеиновая кислота по любому из предшествующих пунктов, где TCR связывается с комплексом МНС-пептид, содержащим эпитоп из RAS человека, содержащий мутацию G12V и МНС, кодируемым аллелью HLA-A11:01.
13. Рекомбинантная нуклеиновая кислота по любому из предшествующих пунктов, где рекомбинантная нуклеиновая кислота представляет собой вектор.
14. Рекомбинантная нуклеиновая кислота по п.12 или 13, где TCR связывается с комплексом MHC-пептид с KD или IC50, меньшим чем 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ.
15. Рекомбинантная нуклеиновая кислота по п.14, где эпитоп имеет длину от 8 до 25 аминокислот.
16. Рекомбинантная нуклеиновая кислота по любому из предшествующих пунктов, где нуклеиновая кислота функционально связана с промотором.
17. Т-клетка, экспрессирующая Т-клеточный рецептор (TCR), содержащая рекомбинантную нуклеиновую кислоту по любому из предшествующих пунктов, где TCR содержит
(a) конструкцию бета-цепи TCR, содержащую:
(i) определяющую комплементарность область 1 (CDR1) с аминокислотной последовательностью SEQ ID NO: 50,
(ii) определяющую комплементарность область 2 (CDR2) c аминокислотной последовательностью SEQ ID NO: 51 и
(iii) определяющую комплементарность область 3 (CDR3) с аминокислотной последовательностью SEQ ID NO: 52; и
(b) конструкцию альфа-цепи TCR, содержащую:
(i) CDR1 c аминокислотной последовательностью SEQ ID NO: 47,
(ii) CDR2 c аминокислотной последовательностью SEQ ID NO: 48 и
(iii) CDR3 c аминокислотной последовательностью SEQ ID NO: 49.
18. Т-клетка по п.17, где Т-клеткой является CD4+ T клетка.
19. Т-клетка по п.17, где Т-клеткой является CD8+ T клетка.
20. Т-клетка по п.17, где Т-клетка выделена у индивида с мутацией G12V RAS.
21. Фармацевтическая композиция для лечения заболевания или состояния, связанного с мутацией G12V RAS, содержащая:
(a) рекомбинантную нуклеиновую кислоту по любому из пп.1-16 или Т-клетку по любому из пп.17-20 и
(b) фармацевтически приемлемый эксципиент или разбавитель.
22. Фармацевтическая композиция по п.21, дополнительно содержащая иммуномодулирующий агент или адъювант.
23. Фармацевтическая композиция по п.22, где адъювантом является поли I:C.
24. Фармацевтическая композиция по любому из пп.21-23, где заболевание или состояние, связанное с мутацией G12V RAS, представляет собой рак, связанный с мутацией G12V RAS.
25. Применение рекомбинантной нуклеиновой кислоты по любому из пп.1-16 или Т-клетки по любому из пп.17-20 для лечения заболевания или состояния, связанного с мутацией G12V RAS.
26. Применение по п.25, где заболевание или состояние, связанное с мутацией G12V RAS, представляет собой рак, связанный с мутацией G12V RAS.
27. Способ лечения индивида с заболеванием или состоянием, связанным с мутацией G12V RAS, включающий введение индивиду рекомбинантной нуклеиновой кислоты по любому из пп.1-16 или Т-клетки по любому из пп.17-20.
28. Способ по п.27, где заболевание или состояние, связанное с мутацией G12V RAS, представляет собой рак, связанный с мутацией G12V RAS.
29. Способ по п.28, где рак представляет собой рак, выбранный из группы, состоящей из аденокарциномы желчных путей, переходно-клеточной карциномы мочевого пузыря, рака груди, аденокарциномы шейки матки, аденокарциномы толстой кишки, аденомы толстой кишки, нейробластомы (вегетативных ганглиев), острого миелоидного лейкоза, хронического миелоидного лейкоза, хронического миеломоноцитарного лейкоза, ювенильного миеломоноцитарного лейкоза, острого лимфобластного лейкоза, лимфомы Буркитта, лимфомы Ходжкина, миеломы клеток плазмы, печеночно-клеточной карциномы, крупноклеточной карциномы, немелкоклеточной карциномы, протоковой карциномы, эндокринной опухоли, аденокарциномы простаты, базальноклеточной карциномы, плоскоклеточной карциномы, злокачественной меланомы, ангиосаркомы, лейомиосаркомы, липосаркомы, рабдомиосаркомы, миксомы, злокачественной фиброзной гистиоцитомы, плеоморфной саркомы, герминомы, семиномы, анапластической карциномы, фолликулярной карциномы, папиллярной карциномы и карциномы из клеток Гуртла.
| LI H | |||
| M | |||
| ET AL | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ получения целлюлозы из стеблей хлопчатника | 1912 |
|
SU505A1 |
| WO 2017044661 A1, 16.03.2017 | |||
| GJERTSEN, M | |||
| K., et al | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
Авторы
Даты
2022-12-15—Публикация
2019-08-16—Подача