Область настоящего изобретения
Настоящее изобретение относится к анализу для идентификации бактерии, способной связываться с тяжелыми металлами, такими как золото и/или серебро. Настоящее изобретение относится также к способу выделения или обогащения тяжелого металла, такого как золото и/или серебро, например, из руды (такой как минеральная руда). Кроме того, настоящее изобретение относится к применению бактерии для выделения или обогащения тяжелого металла, такого как серебро и/или золото.
Предпосылки создания настоящего изобретения
В последние десятилетия отмечается непрерывное истощение высокопроцентных минеральных ресурсов и одновременно все возрастающий спрос на драгоценные металлы. Спрос на золото никогда не прекращается. В то же время значительно возрастает настороженность в отношении охраны окружающей среды, связанная с современными технологиями добычи.
Золото (Au): является одним из самых редких элементов на земле. В морской воде, которая представляет собой самый крупный источник золота, его концентрация составляет лишь 0,01 мг/м3, в то время как было найдено, что его содержание в верхнем слое земной коры в среднем составляет 1-2 г/т. В этой части окружающей среды золото в основном находится в виде чистого металла (Au0), электрона (Ag/Au), золотосодержащих минералов и малых включений, которые были найдены в больших объемах материалов, обычно породы. Более того, золото было найдено (в большинстве случаев в ассоциации с кварцем) в виде теллурида (AuTe2) и селенида (AuSe2) или в виде включений в кристаллической решетке минералов, таких как пирит и арсенопирит (невидимое золото). В настоящее время объем добычи золота при промышленной разработке составляет от 0,5 до 13,7 г золота/тонну породы, при этом наблюдается все возрастающая тенденция к разработке низкопроцентных руд в связи с ограничением эксплуатации богатых руд.
Серебро (Ag): является примерно в 20 раз более распространенным металлом, чем золото. Основное количество добываемого в промышленном масштабе серебра отлагается в виде самородного серебра. Часто встречаются также сульфидные минералы, (Ag2S, акантит) и AgCl (кераргирит). Было обнаружено, что аналогично золоту, серебряные минералы часто присутствуют в виде включений в матрице диоксида кремния (кварц) с размером частиц от нано- до микрометрового интервала.
Ряд живых микроорганизмов, но также нежизнеспособных инактивированных клеток способны связывать ионы металлов. В первом случае связывание металла может происходить за счет адсорбции на поверхности клетки или за счет активного накопления ионов металла внутри клеток. В последнем случае предполагается, то есть в случае нежизнеспособных инактивированных клеток - этот случай часто называют биосорбцией - связывание с ионом металла происходит исключительно за счет поверхностной адсорбции. Емкость биосорбции как основная характеристика биомассы определяется присутствием хелатирующих групп (например, карбоксильные, амидные, гидроксильные, фосфатные и тиольные группы), которые содержатся в углеводах, липидах и белках, экспонированных на поверхности клеток. Как было описано, металлы могут накапливаться в биомассе в количестве вплоть до 50% в расчете на сухую массу клеток (Vieira и Volesky "Biosorption: a solution to pollution?" Int Microbiol 3(1): 17-24 (2000)). В патенте США 5055402 описан способ удаления ионов металла из водного раствора с использованием матрицы, полученной из металл-связывающих микроорганизмов, которые иммобилизовали и инактивировали при нагревании при температуре 300-500°С. В патенте ЕР 0432935 В1 описана адсорбция растворимых металл-цианидных комплексов также из водного раствора с использованием биомассы.
По традиции драгоценные металлы, такие как золото и/или серебро, извлекают россыпной добычей (осадочная порода) или разработкой руды с использованием гравитационных и пирометаллургических методов. В связи с истощением металлоносных руд все в большей степени используют гидрометаллургические технологии для извлечения драгоценных источников из низкопроцентных источников. Методы для извлечения драгоценных металлов, прежде всего золота, являются трудоемкими и требуют применение высокопроизводительных машин, а также опасных и не разлагаемых химических реагентов. В настоящее время примерно 90% общих промышленных процессов для извлечения драгоценных металлов основаны на методах цианирования, так как цианид является одним из очень немногих веществ, которые способны растворять золото. Чтобы обеспечить доступ цианидным ионам или другим соединениям к большой части металла, включенного в содержащую его руду. Руду обычно измельчают до частиц малого размера. Однако стандартный метод отделения драгоценных металлов с использованием выщелачивания цианидом является проблематичным в связи с охраной окружающей среды, а также с сохранением здоровья людей. Следовательно, существует необходимость в разработке экологически благоприятных способов.
В заявке WO 2009/130006 описана операция для извлечения металлов, особенно драгоценных металлов, или их соединений из частиц материала, такого как минеральные руды, с использованием биомассы определенного типа. Биомасса связывается с металлом или соединением металла за счет связывания с клеточными компонентами организма. После отделения биомассы от несвязавшегося материала частиц металл или соединение указанного металла можно отделить от биомассы. Однако выявление биомассы или другого пригодного для этой цели материала является непростой задачей.
В отличие от предшествующего уровня техники одна цель настоящего изобретения заключалась в разработке методологии идентификации материала, способного связываться с тяжелым металлом, таким как золото и/или серебро. Другая цель настоящего изобретения заключалась в разработке способа выделения тяжелого металла, такого как золото и/или серебро, из материала, содержащего тяжелый металл, такой как золото и/или серебро.
Краткое описание сущности настоящего изобретения
Соответственно в настоящем изобретении в том числе предлагаются следующие объекты:
1. Способ выделения или обогащения тяжелого металла, такого как золото и/или серебро, присутствующего в жидкой среде, включающий
стадию инкубации жидкой среды, содержащей тяжелый металл, и биомассу, включающую бактерию, способную связывать тяжелый металл,
стадию отделения биомассы, содержащей связанный тяжелый металл, из жидкой среды, полученной на предыдущей стадии, и
стадию выделения тяжелого металла из биомассы, отделенной на предыдущей стадии.
2. Способ по п. 1, где указанная бактерия принадлежит к роду Pseudochrobactrum или Stenotrophomonas.
3. Способ по п. 1, где указанную бактерию выбирают из следующих видов: Pseudochrobactrum asaccharolyticum, Bacillus subtilis, Bacillus pumilus, Pseudomonas fluorescens, Stenotrophomonas maltophilia, Bacillus cereu и Pseudomonas aeruginosa или из их комбинаций.
4. Способ по любому из пунктов 1-3, где указанную бактерию выбирают из следующих видов: Pseudochrobactrum asaccharolyticum (DSM-25619), подвид Bacillus subtilis (DSM-10), Bacillus pumilus (DSM-27), Pseudomonas fluorescens (DSM-50090), Stenotrophomonas maltophilia (DSM-50170), Bacillus cereus (DSM-31) и Pseudomonas aeruginosa (DSM-50071).
5. Способ по любому из пунктов 1-4, где указанная биомасса представляет собой живую биомассу и/или убитую биомассу.
6. Способ по п. 5, где указанная биомасса представляет собой убитую биомассу.
7. Способ по любому из пунктов 1-6, где стадия инкубации включает перемешивание жидкой среды, содержащей тяжелый металл и биомассу, для формирования пленки или пены, содержащей биомассу, которая включает связанный тяжелый металл, а стадия отделения включает удаление пленки или пены из жидкой среды.
8. Способ по любому из пунктов 1-7, где стадию инкубации проводят в реакторе, включающем перемешивающее устройство для перемешивания жидкой среды.
9. Способ по любому из пунктов 1-8, где указанный тяжелый металл выбирают из рутения, родия, палладия, серебра, осмия, иридия, платины, золота и/или редкоземельных металлов, предпочтительно тяжелый металл представляет собой серебро и/или золото.
10. Способ по любому из пунктов 1-9, где указанный тяжелый металл, присутствующий в указанной жидкой среде, находится в элементной форме или в форме соединения указанного тяжелого металла.
11. Способ по любому из пунктов 1-10, где указанный тяжелый металл связан с биомассой в форме частиц.
12. Способ по любому из пунктов 1-11, где указанная жидкая среда представляет собой суспензию, содержащую материал в виде частиц, который содержит тяжелый металл.
13. Способ по п. 12, где указанный материал в виде частиц содержит тяжелый металл в количестве не более 10000 мас. част./млн, предпочтительно не более 1000 мас. част./млн, более предпочтительно не более 100 мас. част./млн, даже более предпочтительно не более 10 мас. част./млн, даже более предпочтительно не более 1 мас. част./млн, и еще более предпочтительно не более 0,1 мас. част./млн.
14. Способ по п. 12 или п. 13, где указанный материал в виде частиц представляет собой минеральную руду, такую как сульфидная или оксидная минеральная руда.
15. Способ по любому из пунктов 12-14, где размер частиц указанного материала в виде частиц составляет не более 400 мкм, предпочтительно не более 300 мкм, более предпочтительно не более 200 мкм или даже не более 100 мкм, по данным измерения ситовым методом.
16. Способ по любому из пунктов 1-15, где стадии инкубации предшествует стадии биоокисления или стадия инкубации включает стадию биоокисления указанной минеральной руды в виде материала частиц, чтобы обеспечить высвобождение серебра или золота из указанной минеральной руды или чтобы повысить доступность биомассы к серебру или железу, присутствующих в минеральной руде.
17. Способ по любому из пунктов 12-15, где указанная суспензия на стадии отделения содержит сухую массу клеток указанной биомассы в количестве от 0,01 до 20 мас. % в расчете на массу руды, содержащейся в суспензии.
18. Способ по п. 17, где указанная суспензия содержит сухую массу клеток указанной биомассы в количестве от 0,05 до 0,5 мас. % в расчете на массу руды, содержащейся в суспензии.
19. Способ выделения или обогащения тяжелого металла, присутствующего в суспензии, содержащей частицы минеральной руды, содержащей тяжелый металл, и указанный способ включает
стадию инкубации суспензии, содержащей (i) частицы минеральной руды, содержащей тяжелый металл, и (ii) биомассу, включающую бактерию, способную связывать тяжелый металл,
стадию отделения биомассы, содержащей связанный тяжелый металл, из суспензии, полученной на предыдущей стадии, и
стадию выделения тяжелого металла из биомассы, отделенной на предыдущей стадии.
20. Способ по любому из пунктов 12-19, где указанная суспензия на стадии отделения содержит минеральную руду в количестве от 1 до 60 мас. % в расчете на общую массу суспензии, предпочтительно от 1 до 50 мас. % в расчете на общую массу суспензии.
21. Способ по любому из пунктов 12-20, где указанная суспензия на стадии отделения содержит минеральную руду в количестве от 10 до 40 мас. % в расчете на общую массу суспензии, предпочтительно от 10 до 25 мас. % в расчете на общую массу суспензии.
22. Применение бактерии, выбранной из следующих родов: Pseudochrobactrum и Stenotrophomona, или выбранной из группы видов, состоящей из Pseudochrobactrum asaccharolyticum, Bacillus subtilis, Bacillus pumilus, Pseudomonas fluorescens, Stenotrophomonas maltophilia, Bacillus cereu и Pseudomonas aeruginosa, для выделения или обогащения тяжелого металла, предпочтительно элементного золота и/или серебра.
23. Анализ для идентификации бактерии, способной связываться с элементным тяжелым металлом, таким как золото и/или серебро, включающий следующие стадии:
культивирование исследуемой бактерии в пригодной первой культуральной среде,
погружение по крайней мере части поверхности исследуемого инструмента в первую культуральную среду в течение второго предварительно определенного периода времени, при этом на указанной части поверхности соответственно нанесено покрытие из элементного тяжелого металла,
удаление указанного исследуемого инструмента из указанной первой культуральной среды и необязательно промывка исследуемого инструмента,
контактирование второй культуральной среды с покрытой элементным тяжелым металлом частью поверхности указанного исследуемого, удаленного на предыдущей стадии инструмента, и
идентификация исследуемой бактерии, способной связывать элементарный тяжелый металл из среды роста исследуемой бактерии в указанной второй культуральной среде.
24. Анализ по п. 23, где указанный контейнер является частью многолуночного планшета и указанный исследуемый инструмент представляет собой штифт на крышке многолуночного планшета, при этом на указанном штифте нанесено покрытие из элементного тяжелого металла, предпочтительно из серебра или золота, по крайней мере на верхней части штифта, причем указанный штифт располагает в направлении вниз от крышки в указанный контейнер и таким образом верхняя часть штифта погружается в первую культуральную среду на стадии (ii).
25. Анализ по п. 23 или п. 24, где указанная вторая культуральная среда, которая может представлять собой слой агара, содержит предпочтительно растворимую соль тяжелого металла, предпочтительно необязательно растворимую соль золота и/или серебра, соответственно, для выбора исследуемой бактерии, способной расти в присутствии указанной соли тяжелого металла, предпочтительно соли золота и/или серебра.
Авторами настоящего изобретения был найден способ идентификации бактерии, способной связываться с тяжелым металлом, таким как золото и/или серебро, предпочтительно в неионной форме. Способ можно осуществлять в многолуночном формате и, следовательно, указанный способ позволяет параллельно анализировать множество бактериальных штаммов. Способ позволяет комбинировать два критерия отбора, а именно, связывание бактерии с поверхностями, на которые нанесено покрытие тяжелого металла, такого как золото и/или серебро, и селекция в среде, содержащей соединение металла. Соответственно, можно идентифицировать с высокой эффективностью бактериальные штаммы, способные связываться с тяжелым металлом, таким как золото и/или серебро. Биомассу бактерии, идентифицированной анализом по настоящему изобретению или другими средствами, можно использовать для выделения тяжелого металла, такого как золото и/или серебро, из жидкой среды, содержащей тяжелый металл, такой как золото и/или серебро, соответственно.
Краткое описание фигур
Фиг. 1. Крышки для 96-луночных микропланшетов со штифтами. Слева направо: без покрытия, с покрытием из серебра, с покрытием из золота, нанесенным зуботехническим методом, с покрытием из золота, нанесенным методом напыления в вакууме.
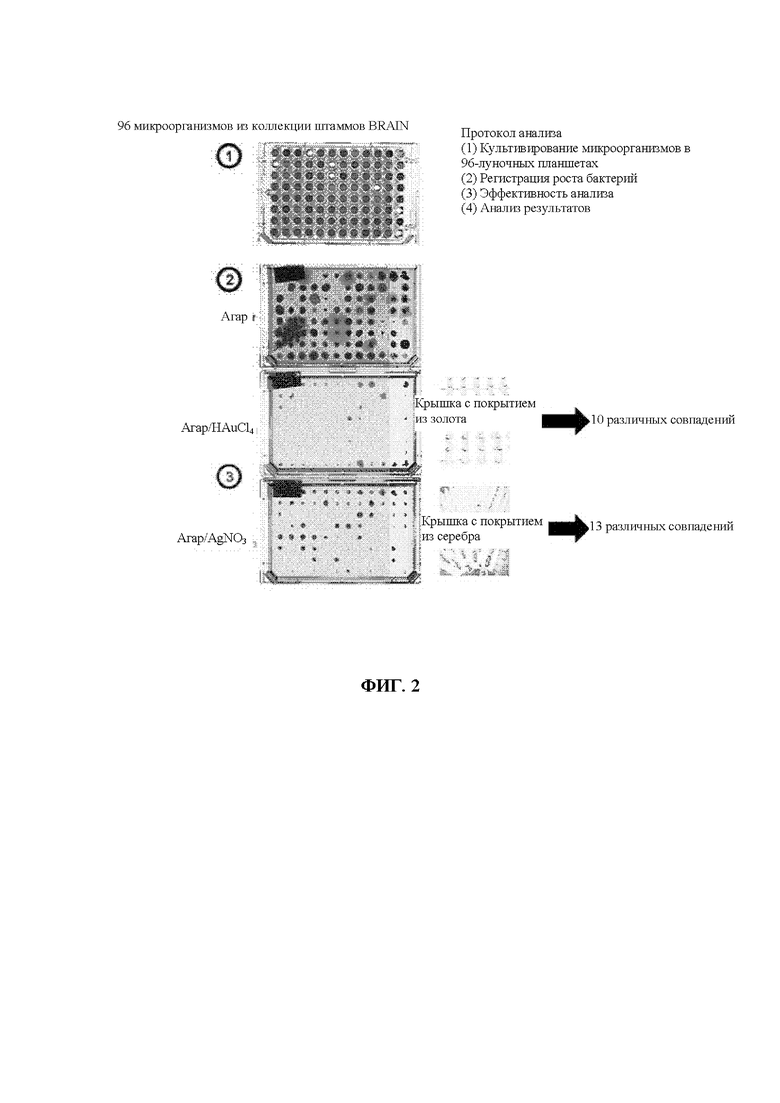
Фиг. 2. Анализ микроорганизмов из фирменной коллекции штаммов (Bioarchive of BRAIN AG) с использованием покрытых серебром и золотом штифтов и последующая селекция на среде агара, содержащей 200 мкМ AgNO3 или 400 мкМ HAuCl4, соответственно.
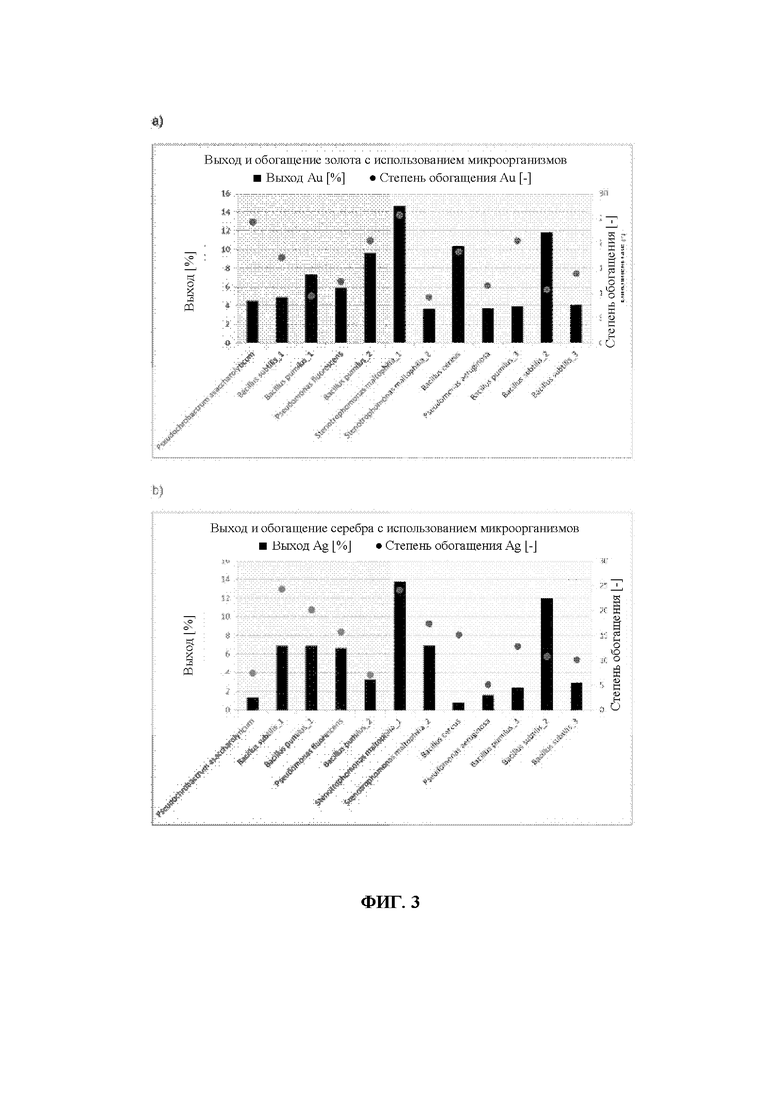
Фиг. 3: Селекция наилучших кандидатов. 12 микроорганизмов было выбрано из 168 по их устойчивости к ионам золота и серебра и их эффективности в процессе биологического разделения (BSP). Организмы 1-4 и 6 (слева направо) были выбраны для дальнейшего масштабирования процесса. Выход [%] ([мкг] AuK/([мкг] AuE)*100; K = концентрат (флотат); Е = общая масса руды; степень обогащения [-]: ([мкг] AuK/[г] K)/([мкг] AuE/[г] Е); K = концентрат (флотат); Е = общая руда; а) анализ золота, б) анализ серебра.
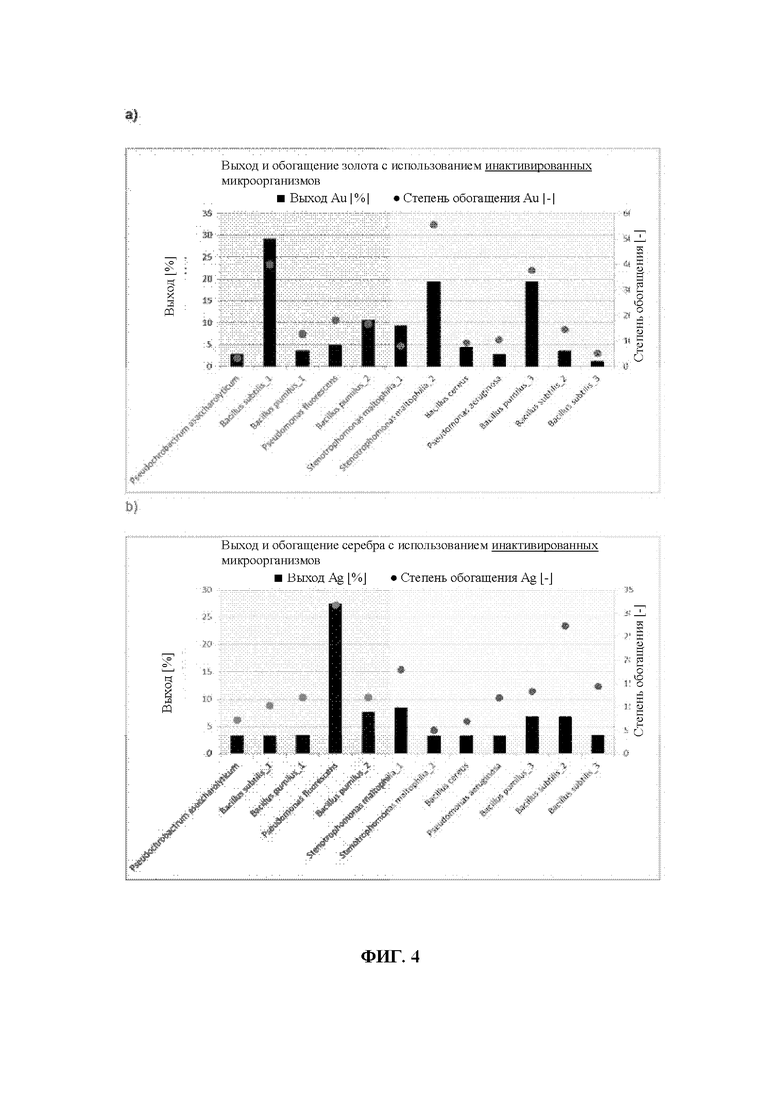
Фиг. 4: Инактивированная биомасса 12 выбранных микроорганизмов и их эффективность в процессе биологического разделения (BSP). Инактивированную биомассу получали при стерилизации (121°С, 20 мин, 1 бар). Выход [%] ([мкг] AuK/([мкг] AuE)*100; K = концентрат (флотат); Е = общая руда; степень обогащения [-]: ([мкг] AuK/[г] K)/([мкг] AuE/[г] Е); K = концентрат (флотат); Е = общая руда; а) анализ золота, б) аналтз серебра.
Подробное описание настоящего изобретения
В ходе анализа для идентификации бактерии, способной связываться с элементным тяжелым металлом, таким как золото и/или серебро, исследуемую бактерию сначала культивируют в культуральной среде, пригодной для исследуемой бактерии. Анализ можно также использовать для идентификации микроорганизмов, отличающихся от бактерий, таких как археи или грибы. Стадию культивирования можно проводить в пригодном контейнере, тип которого особенно не ограничивается и для культивирования бактерий можно использовать любой контейнер, изготовленный из стекла или пластика. Размер контейнера также не ограничивается. Однако предпочтительно проводить анализ с использованием малых объемов культуральной среды от 0,2 до 100 мл, предпочтительно от 0,3 до 20 мл, более предпочтительно от 0,5 до 10 мл и даже более предпочтительно от 1 до 3 мл. Контейнер может представлять собой лунку культурального планшета. В одном варианте осуществления настоящего изобретения проводят анализ множества исследуемых бактерий параллельно и/или для одной из той же бактерии параллельно в различных условиях или в различных культуральных средах. Для таких целей можно использовать многолуночные планшеты.
Культуральная среда или культуральные среды, предназначенные для применения, зависят от типа бактерий, которые необходимо культивировать. Известны культуральные среды, пригодные для культивирования множества бактерий и других микроорганизмов. Среда, пригодная для культивирования множества бактерий представляет собой среду Луриа-Бертани. Можно выбрать время культивирования, которое обеспечивает состояние бактерии в фазе роста, пригодной для связывания с тяжелым металлом, таким как золото и/или серебро. Состояние роста, пригодное для связывания с тяжелым металлом, таким как золото и/или серебро, может представлять собой экспоненциальную фазу роста. Однако можно исследовать также другие фазы роста, такие как стационарная фаза роста. Таким образом, способ можно также использовать в качестве анализа для выявления пригодных условий для связывания элементного тяжелого металла, такого как золото и/или серебро, с бактерией или другим микроорганизмом. Условия, которые необходимо исследовать, могут включать фазу роста, культуральную среду, температуру, буферное вещество, рН, плотность клеток и т.п.
На стадии (i) исследуемую бактерию культивируют для достижения пригодной плотности клеток исследуемых бактерий, необходимой для следующей стадии. Время культивирования может быть очень коротким, например, несколько минут, если исследуемая бактерия добавлена в контейнер уже при плотности клеток, пригодной для следующих стадий. В другом варианте время культивирования может составлять несколько часов, если бактерию высеивали в низкой концентрации в первой культуральной среде, помещенной в контейнер.
На стадии (ii) анализа по крайней мере часть поверхности исследуемого инструмента контактирует с исследуемой бактерией в культуральной среде. Исследуемый инструмент имеет часть поверхности, на которую нанесено покрытие из элементного тяжелого металла, такого как элементное золото и/или элементное серебро, или нанесено покрытие, содержащее элементный тяжелый металл, такой как золото и/или серебро. Исследуемая бактерия, которая характеризуется способностью связываться с элементным тяжелым металлом, таким как элементное золото и/или элементное серебро, будет связываться с покрытием, содержащим золото и/или серебро, на указанной части поверхности исследуемого инструмента. Существуют несколько способов нанесения покрытия из элементного тяжелого металла, такого как золото и/или серебро, на часть поверхности или на весь исследуемый инструмент. Один способ представляет собой электроосаждение тяжелого металла, такого как золото и/или серебро, соединений тяжелого металла (например, золота и/или серебра) в водном растворе (электронапыление), причем этот способ в основном известен в предшествующем уровне техники для обработки поверхностей. Другой применимый способ представляет собой химическое парофазное осаждение (CVD).
Исследуемый инструмент может иметь удлиненную форму и часть поверхности с покрытием на одном из его концов, что позволяет просто погружать по крайней мере часть его поверхности с покрытием в первую культуральную среду. Исследуемый инструмент можно прикрепить к крышке контейнера конецом, противоположным к тому концу, где расположена часть поверхности с покрытием. Таким способом исследуемый инструмент можно погрузить в культуральную среду, когда крышка закрывает часть или всю верхнюю часть отверстия контейнера. На стадии (i) крышку контейнера, присутствующую при культивировании на стадии (i), можно отсоединить от контейнера и заменить на комплект, включающий исследуемый инструмент с крышкой, чтобы часть поверхности с покрытием была погружена в первую культуральную среду. В другом варианте всю стадию культивирования (i) можно проводить при погружении исследуемого инструмента в культуральную среду, например, закрывая контейнер комплектом, включающим крышку и исследуемый инструмент в ходе стадии (i). В последнем случае крышка может не полностью закрывать верхнюю часть отверстия контейнера, чтобы обеспечить обмен воздуха с культуральной средой в контейнере. В вариантах осуществления настоящего изобретения, когда проводят множество анализов параллельно, например, в культуральных планшетах, крышки всех лунок могут включать исследуемый инструмент для погружения в культуральную среду лунок. В этом случае исследуемый инструмент может представлять собой штырь на каждой крышке многолуночного планшента, при этом на штыри нанесено покрытие из элементного серебра или золота, по крайней мере на верхнюю часть штыря. Штыри можно опускать по направлению вниз от крышки в контейнер или лунку, и таким образом штырь погружается в первую культуральную среду.
Для обеспечения воспроизводительности исследуемый инструмент следует погружать таким образом, чтобы его часть поверхности с покрытием была погружена в первую культуральную среду в течение предварительно определенного периода времени. Этот период должен быть достаточным для обеспечения специфического прикрепления исследуемых бактерий, которые могут связываться с элементным тяжелым металлом, таким как золото и/или серебро. Предварительно определенный период времени может составлять по крайней мере 10 с, но предпочтительно по крайней мере 1 мин, более предпочтительно по крайней мере 30 мин. Верхней предел периода времени особо не ограничивается, но через период более 48 ч не следует ожидать, что будет наблюдаться дополнительное или более эффективное специфическое прикрепление исследуемых бактерий к части поверхности с покрытием.
После завершения предварительно определенного периода времени или любого другого времени, который считается приемлемым для пользователя, исследуемый инструмент удаляют из культуральной среды. Предпочтительно поверхность с покрытием или весь исследуемый инструмент с покрытием ополаскивают или промывают для удаления неспецифически связанных или слабо связанных исследуемых бактерий от исследуемого инструмента. Для промывки можно использовать раствор для промывки, который может представлять собой стерильный водный буферный раствор или стерильную культуральную среду, совместимые с исследуемыми бактериями.
Затем исследуемый инструмент или по крайней мере часть поверхности с покрытием контактирует со второй культуральной средой для высеивания любой исследуемой бактерии во вторую культуральную среду при ее прикреплении к части поверхности исследуемого инструмента. Перед контактированием с исследуемым инструментом вторая культуральная среда должна быть стерильной. Второй культуральной средой может являться та же самая культуральная среда или отличаться от культуральной среды, использованной на стадии (i). В одном варианте осуществления настоящего изобретения вторая культуральная среда представляет собой твердую или полутвердую культуральную среду, такую как чашка с агаром. Если на стадии (i) используют многолуночный планшет, то на этой стадии можно использовать многолуночный планшет одинакового размера, одинаковой формы и лунками аналогичного формата для обеспечения автоматизации всего анализа.
Вторая культуральная среда предпочтительно может содержать водо-растворимое соединение тяжелого металла, такого как золото и/или серебро, для селекции исследуемой бактерии, способной расти в присутствии указанного растворимого соединения тяжелого металла, такого как золото и/или серебро, соответственно. В основном соединение тяжелого металла во второй культуральной среде представляет собой или содержит соединение того же тяжелого металла, который содержится в покрытии исследуемого инструмента. Такая конфигурация позволяет проводить вторую стадию селекции для идентификации бактерии, способной связываться с элементным тяжелым металлом, таким как золото и/или серебро. Однако можно также использовать, дополнительно или в альтернативном варианте, соединение тяжелого металла во второй культуральной среде, отличающегося от металла, который содержится в покрытии исследуемого инструмента. В качестве тяжелого металла, такого как золото и/или серебро, можно использовать предпочтительно водо-растворимую соль тяжелого металла, такого как золото и/или серебро. Концентрацию соединения или соли тяжелого металла, такого как золото и/или серебро, в указанной культуральной среде можно определять соответствующим образом, как описано в разделе Примеры. Пример растворимого соединения золота включает HAuCl4. Пример растворимого соединения серебра включает AgNO3. Растворимое соединение золота можно использовать в концентрации от 50 мкМ до 1 мМ, предпочтительно от 100 до 700 мкМ, более предпочтительно от 250 до 600 мкМ. Растворимое соединение серебра можна использовать в концентрации от 20 мкМ до 1 мМ, предпочтительно от 50 до 600 мкМ, более предпочтительно от 150 до 500 мкМ.
Исследуемую бактерию, способную связываться с тяжелым металлом, таким как золото и/или серебро, можно идентифицировать в ходе роста исследуемой бактерии в указанной второй культуральной среде. Вторую культуральную среду можно обследовать или анализировать по росту бактерий через предварительно определенное время культивирования, которое может составлять от 5 до 48 ч, предпочтительно от 10 до 20 ч. Такую идентификацию можно проводить с использованием коммерческих ридеров или с использованием фотографий второй культуральной среды.
Бактериальные штаммы, способные связывать элементное золото и/или серебро и идентифицируемые описанным выше способом анализа, выбирают из следующих рода и вида: Pseudochrobactrum, предпочтительно Pseudochrobactrum asaccharolyticum, Bacillus subtilis, Bacillus pumilus, Pseudomonas fluorescens, Stenotrophomonas, предпочтительно Stenotrophomonas maltophilia, Bacillus cereu и Pseudomonas aeruginosa. Конкретные примеры таких бактериальных штаммов включают: Pseudochrobactrum asaccharolyticum (DSM-25619), подвид Bacillus subtilis (DSM-10), Bacillus pumilus (DSM-27), Pseudomonas fluorescens (DSM-50090), Stenotrophomonas maltophilia (DSM-50170), Bacillus cereus (DSM-31) и Pseudomonas aeruginosa (DSM-50071). Номера DSM означают номера депонирования в немецкой коллекции микроорганизмов и клеточных культур (Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH). В другом варианте бактерию выбирают из Pseudochrobactrum, предпочтительно Pseudochrobactrum asaccharolyticum, Pseudomonas fluorescens, Stenotrophomonas, предпочтительно Stenotrophomonas maltophilia, и Pseudomonas aeruginosa.
Бактериальные штаммы, идентифицируемые или идентифицированные способом анализа по настоящему изобретению, прежде всего перечисленные выше, можно использовать в виде биомассы в процессе выделения или обогащения тяжелого металла, такого как золото и/или серебро. Биомасса может содержать бактерии, выбранные из родов, видов или штаммов, перечисленных выше. Биомасса может включать комбинацию двух или более бактерий, например, два или более бактериальных штаммов или бактериальных родов. Биомасса может включать комбинацию трех или более бактерий, например, три или более бактериальных штаммов или бактериальных родов.
Способ выделения или обогащения тяжелого металла, такого как золото и/или серебро, в основном проводят в жидкой среде. Биомасса связывается с тяжелым металлом, таким как золото и/или серебро, за счет связывания с клеточными компонентами бактерии. После отделения биомассы от несвязанного материала, тяжелый металл, такой как золото и/или серебро, можно выделить из биомассы. Согласно настоящему изобретению из материала, который содержит только малые количества тяжелого металла, такого как золото и/или серебро, можно выделить тяжелый металл, такой как золото и/или серебро, без применения опасных методов, таких как выщелачивание цианидом и/или обработка амальгамой. Материал, из которого выделяют и/или обогащают тяжелый металл, может содержать тяжелый металл в количестве не более 10000 мас. част./млн, предпочтительно не более 1000 мас. част./млн, более предпочтительно не более 100 мас. част./млн, даже более предпочтительно не более 10 мас. част./млн, даже более предпочтительно не более 1 мас. част./млн, и еще более предпочтительно не более 0,1 мас. част./млн. Способ по настоящему изобретению обеспечивает экологически безвредный доступ к тяжелому металлу, такому как золото и/или серебро, который требует низких энергозатрат и исключает загрязнение окружающей среды.
Биомасса по настоящему изобретению может включать живую биомассу, то есть биомасса может содержать жизнеспособные бактерии. Однако неожиданно было установлено, что можно также использовать убитую биомассу, то есть конкретную биомассу, которая содержит убитые бактерии. Таким образом, в предпочтительном варианте используют биомассу, которая содержит по крайней мере 70% убитой биомассы, прежде всего по крайней мере 70% убитых бактериальных клеток, предпочтительно по крайней мере 80 или 90% убитой биомассы, прежде всего по крайней мере 80 или 90% убитых бактериальных клеток, более предпочтительно по крайней мере 95 или по крайней мере 99% убитой биомассы, прежде всего по крайней мере 95 или по крайней мере 99% убитых бактериальных клеток. В одном варианте используют биомассу, которая включает по крайней мере 99,9% убитой биомассы, прежде всего по крайней мере 99,9% убитых бактериальных клеток.
В случае живой биомассы, дополнительно могут присутствовать убитые бактериальные клетки. Если используют живую биомассу или бактерии, жидкая среда, которую используют в способе выделения или обогащения тяжелого металла, такого как золото и/или серебро, предпочтительно содержит пригодные питательные вещества для поддержания роста и выживания бактерий в жидкой среде. Присутствие последних не обязательно, если используют мертвую биомассу. Мертвую биомассу можно получить из живой биомассы бактерий, выбранных из родов, видов или штаммов, перечисленных выше. Мертвая биомасса характеризуется неспособностью к пролиферации и/или неспособностью поддерживать метаболические функции. Мертвая биомасса может содержать менее 10% жизнеспособных бактериальных клеток, предпочтительно менее 5% жизнеспособных бактериальных клеток, более предпочтительно менее 1%, даже более предпочтительно менее 0,01% жизнеспособных бактериальных клеток, рассчитанные с учетом числа клеток в расчете на общее число клеток в образце биомассы. Мертвую биомассу можно получить при культивировании живой биомассы, содержащей бактерии в водной среде, до достижения пригодной высокой плотности клеток. Бактериальные клетки можно отделить от жидкой среды, например, при осаждении, прежде всего при центрифугировании, или другим методом, таким как фильтрование, при этом получают влажную биомассу. Отделенную влажную биомассу затем можно инактивировать и получить мертвую биомассу. Инактивацию можно проводить, например, при приложении к биомассе нагревания и/или при высокого давления, с использованием процессов, известных в данной области техники, таких как пастеризация или автоклавирование. Влажную биомассу можно высушивать при снижении содержания растворителя. Высушивание можно проводить при высокой температуре и/или в вакууме. На стадии высушивания в основном погибает большинство бактериальных клеток, при этом получают мертвую биомассу. Согласно предпочтительному способу получения мертвой биомассы, живые бактериальные клетки или влажную биомассу можно стерилизовать при повышенной температуре необязательно с дополнительным приложением давления. Стерилизацию можно проводить при температуре от 60°С до 140°С, предпочтительно от 70°С до 130°С, более предпочтительно от 80°С до 121°С. Продолжительность стерилизации можно выбирать в зависимости от используемой температуры, причем можно использовать более продолжительные периоды стерилизации, если температура находится в нижнем пределе указанных выше интервалов. В основном, стерилизацию проводят в течение от 5 мин до 3 ч, предпочтительно от 10 мин до 60 мин. В одном варианте температура составляет от 60°С до 90°С, а продолжительность составляет от 1 ч до 3 ч. В другом варианте температура составляет от 90°С до 130°С, а продолжительность от 10 мин до 30 мин. В дополнительном необязательном варианте давление может составлять от 0,5 до 5 бар, предпочтительно от 1 до 3 бар (выше давления окружающей среды). Конкретные примеры условий, используемых для стерилизации или инактивации бактериальных клеток, включают: 121°С в течение 20 мин, 1 бар и 80°С в течение 1 ч. Мертвую биомассу можно хранить до применения в способе по настоящему изобретению.
Для проведения способа выделения или обогащения тяжелого металла, такого как золото и/или серебро, мертвую или живую биомассу бактерии, для которой известно, что она способна специфически адсорбировать тяжелый металл, такой как золото и/или серебро, инкубируют, предпочтительно перемешивают, в жидкой среде, содержащей тяжелый металл, такой как золото и/или серебро. Тяжелый металл, такой как золото и/или серебро, содержащийся в жидкой среде, можно получить из любого материала, содержащего тяжелый металл, такой как золото и/или серебро, такой как элементный тяжелый металл (такой как элементные золото и/или серебро), или соединения тяжелого металла (такие как соединения золота и/или серебра), прежде всего минеральная руда. В одном варианте тяжелый металл, такой как золото и/или серебро, который необходимо выделить или обогатить, присутствует в твердом материале, из которого можно выделить или обогатить твердый металл, такой как золото и/или серебро. Твердый материал, такой как минеральная руда, содержащая тяжелый металл, такой как золото и/или серебро, предпочтительно дробят, измельчают или превращают в порошок для получения материала частиц перед его погружением в жидкую среду, и его можно предварительно обрабатывать с использованием методов, пригодных для ускорения высвобождения металла, таких как биоокисление или инкубация с микроорганизмами, которые продуцируют вызывающие коррозию метаболиты. Жидкая среда может представлять собой суспензию твердого материала, который формирует твердую фазу в жидкой фазе жидкой среды.
Стадию инкубации способа можно проводить в реакторе непрерывного действия, реакторе с перемешиванием или в открытом водоеме, который используют на установках по очистке сточных вод. В таких условиях можно контролировать параметры, которые являются важными для роста микроорганизмов (рН, температура, питательные вещества), и следовательно, бактерии можно поддерживать в стабильном состоянии в пространстве и времени. В основном, жидкую среду перемешивают на стадии инкубации, а затем обрабатывают на стадии отделения. В одном варианте можно использовать процедуру флотации, в ходе которой жидкую среду перемешивают таким образом, что в верхней части жидкой среды образуется пленка или пена, содержащая биомассу, которая содержит связанный тяжелый металл, такой как золото и/или серебро. Пленку или пену можно удалить из верхней части жидкой среды, и из пленки или пены можно выделить тяжелый металл, такой как золото и/или серебро. В другом варианте в жидкой среде можно создать градиент плотности, чтобы отделить биомассу в слое жидкой среды, и слой, содержащий биомассу, можно отделить от жидкой среды, например, отсасыванием. В еще одном варианте биомассу можно осадить в жидкой среде, и слой, содержащий осажденную биомассу, можно отделить из жидкой среды при удалении супернатанта.
Согласно способу по настоящему изобретению, эффект очень высокой концентрации в основном можно обеспечить при связывании с биомассой тяжелого металла, такого как золото и/или серебро, из низкосортного материала. Таким образом, масса биомассы, отделенной из жидкой среды и содержащей связанный тяжелый металл, будет значительно ниже, чем масса содержащего тяжелый металл материала, использованного в самом начале способа. Этот концентрационный эффект позволяет транспортировать биомассу, отделенную из жидкой среды, необязательно в высушенном состоянии, на большие расстояния, когда транспортировка исходного, содержащего тяжелый металл материала является экономически не выгодным. Таким образом настоящее изобретение позволяет отделить участок, где проводят стадии инкубации и разделения, от участка, где проводят стадию выделения.
Согласно настоящему изобретению тяжелый металл может представлять собой тяжелый металл в свободной, элементной форме (неионной или минеральной) или соединение, такое как соль или соли тяжелого металла. Тяжелый металл можно выбирать из рутения, родия, палладия, серебра, осмия, иридия, платины, золота и редкоземельных элементов (РЗЭ). РЗЭ можно выбрать из лантана, церия, празеодима, неодима, прометия, самария, европия, скандия, иттрия, гадолиния, тербия, диспрозия, голмия, эрбия, тулия, иттербия и лютетия. В предпочтительном варианте тяжелый металл представляет собой золото и/или серебро.
Металл в элементной форме характеризуется связями между атомами металла и состоянием окисления 0. Если тяжелый металл, такой как золото и/или серебро, выделенный или обогащенный способом по изобретению, находится в элементной форме, он может образовывать частицы в нанометровом диапазоне, такие как металлические кластеры. Нанометровые частицы тяжелого металла, такого как золото и/или серебро, и их кластеры могут характеризоваться лигандами, которые занимают свободные валентности атомов металла, расположенных на поверхности нанометровых металлических частиц или кластеров. Кластеры элементного тяжелого металла, такого как золото и/или серебро, могут включать от 2 до 1000 атомов металла. В одном варианте, кластеры могут включать от 3 до 500 атомов металла. В другом варианте кластеры могут включать от 5 до 400 или от 20 до 300 атомов металла. В основном размер нанометровых частиц составляет <500 нм, в одном варианте <100 нм, в другом варианте <50 нм, в еще одном варианте <10 нм. Металл в элементной форме обычно является не растворятся в водной среде. Однако нанометровый элементный тяжелый металл, такой как золото и/или серебро, или его кластеры можно диспергировать или они могут диспергироваться в водной среде, например, в форме коллоида.
В соединениях тяжелого металла, такого как золото и/или серебро, атомы металла могут находиться в окисленном состоянии 0 или могут быть окислены. Соединения металла могут содержать атомы металла в различном окисленном состоянии, равном 2 или более. Соединение тяжелого металла, такого как золото и/или серебро, может представлять собой соль тяжелого металла, такого как золото и/или серебро. Соединение тяжелого металла, такого как золото и/или серебро, может растворяться или не растворяться в водном растворе. В одном варианте соединение тяжелого металла, такого как золото и/или серебро, является в основном нерастворимым в воде при рН 7,0 и 25°С. В основном нерастворимое соединение означает, что в 1 л чистой воды растворяется менее 10 мг указанного соединения при рН 7,0 и 25°С. Если указанное соединение является нерастворимым или в основном нерастворимым в воде при рН 7,0 и 25°С, то соединение тяжелого металла, такого как золото и/или серебро, присутствующее в материале, таком как минеральная руда, можно получить в тонкодисперсном виде или оно является диспергируемым в воде, например, в форме коллоида.
Согласно способу по настоящему изобретению тяжелый металл, такой как золото и/или серебро, принимает участие в химической реакции, например, при связывании с указанной биомассой или при отделении от указанной биомассы. Таким образом, металл, выделенный на стадии выделения, может находиться в химической форме, отличающейся от химической формы на начальном этапе способа по настоящему изобретению. В настоящее изобретение включены процессы, в ходе которых происходит изменение химического состояния металла, предназначенного для выделения. Тяжелый металл, такой как золото и/или серебро, который предназначен для выделения, может содержать металл в двух или более различных химических состояниях или его соединения.
Материал, содержащий тяжелый металл, такой как золото и/или серебро, предназначенный для выделения, может представлять собой любой материал, такой как минеральная руда. В основном материал представляет собой частицы. Материал может содержать большие количества силикатов или кварца. Минеральная руда может представлять собой материал выборки пустой породы, полученный в процессе выделения необходимого компонента, отличающегося от металла по настоящему изобретению, из минеральной руды. Материал может, например, представлять собой сульфидный минеральный материал, такой как пирит, или содержать его. В одном варианте осуществления настоящего изобретения тяжелый металл, такой как золото и/или серебро, прежде всего, элементное золото и/или серебро, по настоящему изобретению может быть тонко распределенным в материале, таком как элементный металл, включенный в кристаллическую решетку минерала, такого как пирит. Такой исключительно тонко распределенный или диспергированный элементный металл в основном называют «невидимым металлом», а если металлом является золото, то его называют «невидимым золотом».
На стадии инкубации способа по настоящему изобретению водную смесь готовят с использованием материала, содержащего тяжелый металл, такой как золото и/или серебро, и биомассы по настоящему изобретению. Частицы материала, такие как частицы минеральной руды, которую предполагается использовать, должны быть тонко измельченными. Для этой цели перед стадией инкубации необходимо проводить стадию измельчения. Размер частиц материала может составлять по данным ситового анализа не более 5 мм. В другом варианте размер частиц материала может составлять не более 1 мм, не более 400 мкм или не более 100 мкм по данным ситового анализа. В другом варианте при просеивании измельченного материала можно получить частицы размером менее 100 мкм, менее 50 мкм или менее 10 мкм. Выход способа по настоящему изобретению тем выше, чем меньше размер частиц материала, использованного на стадии инкубации.
Стадию инкубации обычно проводят в реакторах, например, используемых при обработке сточных вод. Реактор предпочтительно содержит систему перемешивания для перемешивания водной смеси. Можно использовать реактор с перемешиванием и реактор периодического или непрерывного действия. Реактор может быть снабжен устройствами для измерения и контроля параметров, таких как температура, рН, содержание питательных веществ и т.п. Такие устройства известны в данной области техники. Жидкая среда или смесь, полученная на стадии инкубации, в основном представляет собой водную среду или смесь. Жидкая среда или смесь содержит биомассу, а также тяжелый металл, такой как золото и/или серебро, предназначенный для выделения или обогащения. Жидкую среду можно использовать для контроля условий связывания с биомассой тяжелого металла, такого как золото и/или серебро, таких как температура, концентрация биомассы и материала, содержащего тяжелый металл, такой как золото и/или серебро, рН, ионная сила и т.п. Жидкая среда или смесь могут дополнительно включать питательные вещества, необходимые для роста биомассы, если использованная биомасса включает или содержит жизнеспособные бактериальные клетки, необходимые для выделения или обогащения тяжелого металла, такого как золото и/или серебро. Пригодные условия роста и требования к питательным веществам для используемой биомассы известны в предшествующем уровне техники в области микробиологии. Пригодные условия роста также предоставляются коллекциями микроорганизмов, такими как американская коллекция клеточных культур (АТТС) или немецкая коллекция микроорганизмов и клеточных культур (Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, DSMZ), где можно получить пригодные бактериальные штаммы. Кроме того водная среда или смесь содержит биомассу, использованную для связывания золота и/или серебра, которые предполагается выделить. Обычно биомассу добавляют в реактор в количестве, которое обеспечивает дальнейший рост биомассы. Для этой цели одну или более прекультур можно выращивать в отдельных реакторах, чтобы поддерживать достаточно высокие количества биомассы в водной суспензии, которую предполагается использовать. В другом варианте для выделения или обогащения тяжелого металла, такого как золото и/или серебро, используют мертвую биомассу, как описано выше. В этом случае мертвую биомассу добавляют в жидкую среду или смесь.
Количество или концентрация биомассы в жидкой среде или смеси особо не ограничены. Однако если присутствует слишком малое количество биомассы, то биомасса будет связывать не все количество тяжелого металла, такого как золото и/или серебро, доступного для связывания. Если используется большее количество биомассы, чем количество, необходимое для связывания доступного тяжелого металла, такого как золото и/или серебро, то такие условия являются экономически невыгодными, к тому же могут возникнуть трудности при перемешивании из-за высокой вязкости биомассы. Пригодное количество биомассы для использования в крупномасштабном варианте можно определить с помощью ряда низкомасштабных экспериментов, в ходе которых количество или концентрацию биомассы для данного содержащего тяжелый металл, такой как золото и/или серебро, материала определяют при измерении количества тяжелого металла, такого как золото и/или серебро, соответственно, который может быть связан биомассой или остается в материале, исходно содержащем тяжелый металл, такой как золото и/или серебро.
Содержание материала в виде частиц (такого как минеральная руда) в водной среде или смеси на стадии инкубации может составлять, например, от 1 кг до 500 кг частиц в 1 м3 водной среды. В другом варианте указанное содержание может составлять от 5 кг до 100 кг в 1 м3 водной смеси. Аналогичным образом, как описано выше в отношении количества или концентрации биомассы, которую предполагается использовать, пригодное количество материала частиц можно определять экспериментально в ходе низкомасштабных экспериментов перед проведением крупномасштабных процессов.
На стадии инкубации способа по настоящему изобретению водную среду инкубируют, чтобы обеспечить связывание тяжелого металла, такого как золото и/или серебро, с биомассой. Продолжительность инкубации зависит от скорости связывания. В основном продолжительность инкубации составляет от 0,5 ч до 96 ч, предпочтительно от 0,5 ч до 48 ч, более предпочтительно от 1 ч до 48 ч, еще более предпочтительно от 1 ч до 24 ч и наиболее предпочтительно от 3 ч до 24 ч. Температура инкубации в основном зависит от типа использованной биомассы. Контроль температуры можно использовать для контроля роста указанной биомассы. В ходе инкубации регистрируют параметры жидкой среды или смеси, такие как рН, содержание питательных веществ, температура и т.п., и при необходимости для поддержания требуемых условий инкубации.
На стадии инкубации жидкую среду предпочтительно перемешивают с использованием мешалки и тщательно перемешивают для формирования пленки или пены, содержащей биомассу в верхней части среды. Однако нет необходимости перемешивать среду в ходе всего периода инкубации. Необязательно для поддержания формирования пленки или пены на поверхности жидкой среды в реактор подают газ, такой как воздух.
После стадии инкубации можно проводить стадию разделения. После стадии инкубации оставшийся материал частиц можно осадить и удалить. Затем, если сформировалась пленка или пена, содержащая биомассу со связанным тяжелым металлом, таким как золото и/или серебро, пленку или пену можно удалить из верхней части указанной жидкой среды. В другом варианте биомассу со связанным тяжелым металлом, таким как золото и/или серебро, отделяют другими методами, такими как седиментация. Отделенную биомассу можно в зависимости от следующей стадии высушивать для упрощения условий хранения и/или транспортировки биомассы перед проведением стадии выделения. Жидкая среда (такая как суспензия) на стадии разделения может содержать сухую клеточную массу биомассы в количестве от 0,01 до 20 мас. % в расчете на массу руды, содержащейся в жидкой среде (или суспензии). Предпочтительно жидкая среда (или суспензия) содержит сухую массу указанной биомассы в количестве от 0,05 до 5 мас. %, предпочтительно от 0,05 до 0,5 мас. % (w/w), в расчете на массу руды, содержащейся в жидкой среде или суспензии, соответственно. На стадии разделения жидкая среда, такая как суспензия, может содержать руду в количестве от 1 до 50 мас. %, предпочтительно от 10 до 25 мас. % в расчете на общую массу жидкой среды (или суспензии).
На стадии выделения, так называемого процесса биологического разделения (BSP), из указанной биомассы выделяют тяжелый металл, такой как золото и/или серебро, связанный с биомассой. Тяжелый металл, такой как золото и/или серебро, можно, например, десорбировать из биомассы в жидкой фазе с использованием кислотных или щелочных условий. В другом варианте биомассу можно сжигать для разрушения и удаления органического материала указанной биомассы. Металл можно очищать из остатка и/или золы биомассы.
Способ по настоящему изобретению можно комбинировать со стадиями способа для выделения металлов из металлических руд, известными в предшествующем уровне техники. Чтобы ускорить доступ биомассы, используемой в настоящем изобретении, к частицам или соединениям тяжелых металлов, присутствующим в материале частиц, можно использовать известную стадию биоокисления в комбинации с настоящим изобретением. Например, если указанный материал частиц представляет собой сульфидную руду, такую как пирит, можно использовать сульфид-окисляющие бактерии, такие как ацидофильные бактерии (Acidithiobacilli), по крайней мере для частичной деградации сульфидного минерала. Такие стадии биоокисления или биовыщелачивания описаны в статье (Rawlings and Johnson "The microbiology of biomining: development and optimization of mineral-oxidizing microbial consortia." Microbiology 153: 315-324 (2007)). Такую обработку можно проводить перед стадией инкубации по настоящему изобретению или одновременно с этой стадией при добавлении биоокисляющего организма в водный раствор на стадии (i). Примеры организмов для биоокисления или биовыщелачивания включают А. ferrooxidans, A. thiooxidans, Leptospirillum ferrooxidans, Т. organoparus, Thermothrix thiopara, Sulfolobus acidocaldarius и S. brierleyi. Можно также использовать способ, описанный в заявке US 2007/107550, для предварительной обработки рекальцитрантных руд, при этом стадию гидрометаллургической обработки заменяют на способ по настоящему изобретению.
Примеры
Пример 1
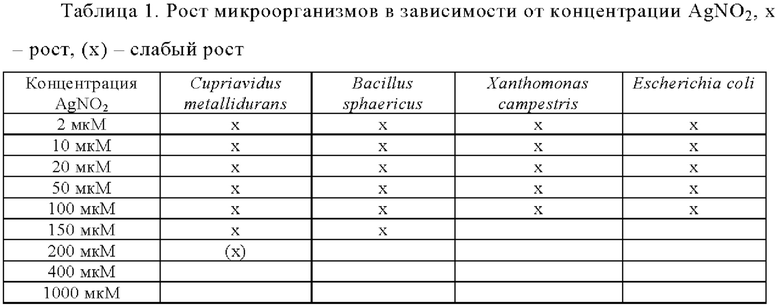
Анализ на устойчивость
Рост нескольких микроорганизмов (например, Escherichia coli, Xanthomonas campestris, Cupriavidus metallidurans и Bacillus sphaericus) регистрировали в присутствии крышек со штифтами с покрытием. Бактерии Escherichia coli и Xanthomonas campestris служили в качестве отрицательных контролей в отношении связывания с металлом, a Cupriavidus metallidurans в качестве положительного контроля. Кроме того, Bacillus sphaericus были использованы в качестве положительного контроля для связывания с серебром. Ранее авторами настоящего изобретения было выявлено связывание золотых частиц или покрытых золотом поверхностей с бактериями Bacillus sphaericus. Бактерии Cupriavidus metallidurans являются грамотрицательными палочковидными бактериями, которые обладают способностью связываться с золотом, как описано в литературе (Reith et al., 2006). Название рода metallidurans означает устойчивость этих бактерий к тяжелым металлам, а их способность выживать в присутствии золота и серебра была изучена ранее (Reith F, Rogers SL, McPhail DC и Webb D. "Biomineralization of gold: biofilms on bacterioform gold." Science 313(5784): 233-236 (2006); Reith F, Etschmann B, Grosse C, Moors H, Benotmane MA, Monsieurs P, Grass G, Doonan C, Vogt S, Lai B, Martinez-Criado G, George GN, Nies DH, Mergeay M, Pring A, Southam G and Brugger J. "Mechanisms of gold biomineralization in the bacterium Cupriavidus metallidurans." Proc Natl Acad Sci 106(42): 17757-17762 (2009); Ledrich ML1, Stemmler S, Laval-Gilly P, Foucaud L, and Falla J "Precipitation of silver-thiosulfate complex and immobilization of silver by Cupriavidus metallidurans CH34." Biometals 18(6): 643-650 (2005)).
Для исследования переносимой концентрации серебра и золота, микроорганизмы культивировали в жидкой среде и высеивали полосами на чашки с агаром с различной концентрацией AgNO3 или 400 HAuCl4, соответственно. Результаты представлены в табл. 1 и табл. 2.
Для оценки результатов анализа на устойчивость микроорганизмы культивировали, переносили в микропланшеты и инкубировали с течение 3 ч при 28°С со штифтами с покрытием из металла и без покрытия, соответственно. После инкубации крышки промывали солевым раствором и затем вдавливали в чашки с агаром, содержащим металл (среда Луриа-Бертани), культивировали в течение ночи при 28°С, и таким образом проводили тестирование микроорганизмов в ходе первой и второй стадии селекции. Для селекции на чашках с агаром, на конечном этапе среду дополняли 200 мкМ AgNO3 или 400 мкм HAuCl4, соответственно.
Пример 2
Анализ связывания
Для оценки способности связывания микробов с золотом и серебром использовали систему анализа, который проводили в 96-луночных микропланшетах для осуществления крупномасштабного скрининга. Для этого анализа использовали 96-луночные полистирольные микропланшеты MicroWell™ и полистирольные крышки Nunc-Immuno™ TSP (Transferable Solid Phase, переносимая твердая фаза). Крышки снабжены 96 штифтами, которые погружаются в лунки микропланшета, чтобы обеспечить прикрепление микроорганизмов. Крышки со штифтами изготовлены из различных поверхностных материалов, таких как MaxiSorp™ (высокая аффинность к соединениям с гидрофильными и гидрофобными участками) или PolySorp™ (высокая аффинность к гидрофобным соединениям). На крышки нанесено покрытие либо из серебра либо из золота с использованием гальванической обработки и зуботехнических методов, или покрытие из золота, нанесенное напрямую методом напыления в вакууме (фиг. 1). Было установлено, что поверхность MaxiSorp™ является наиболее пригодной для нанесения покрытия из серебра и золота, и что покрытие из золота является механически стабильным, то есть не наблюдается эрозии или разрушения после повторного использования в 96-луночных планшетах, содержащих культуральную среду.
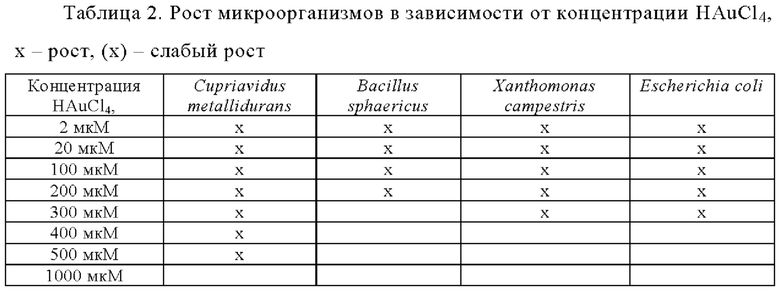
Для открытия новых микроорганизмов, устойчивых к серебру и золоту, был разработан анализ с использованием микроорганизмов из собственной коллекции штаммов фирмы BRAIN, указанных в табл. 2. Для этого анализа проводили вторую селекцию в присутствии концентраций 200 мкМ AgNO2 и 400 мкМ HAuCl4, соответственно.
Анализ проводили следующим образом. Сначала микроорганизмы культивировали в течение от 1 до 2 суток в 750 мл среды в 96-луночных планшетах с глубокими лункам при 300 об./мин и 28°С. 100 мкл каждой из культур переносили в два микропланшета, каждый из которых снабжен штифтами с покрытием из серебра или золота, соответственно. Затем планшеты инкубировали в течение 3 ч при 28°С и при 450 об./мин с последующей промывкой солевым раствором и удалением жидкости при постукивании на стерильной целлюлозной бумаге. Культуры вдавливали в агар, содержащий 200 мкМ AgNO3 и 400 мкМ HAuCl4, соответственно, и инкубировали при 28°С в течение от 4 до 6 суток (фиг. 2).
Пример 3
Процесс биологического разделения (BSP)
В экспериментах по разделению использовали 168 металлофильных микроорганизмов, идентифицированных по данным анализа на устойчивость и анализа связывания, и эксперименты проводили по следующей методике. Микроорганизмы высеивали полосами на чашки с агаром непосредственно после оттаивания (флаконы для хранения хранили при -80°С) и чашки культивировали при 28°С в течение ночи. Культуры высеивали в жидкую среду Луриа-Бертани и культивировали при 28°С в течение ночи. Затем прекультуры разделяли на части и высеивали в свежую среду. Одну из культур индуцировали при добавлении 20 мкМ AgNO3 или 40 мкМ HAuCl4, соответственно. Другую культуру выращивали в тех же условиях без обработки ионом металла. Обе культуры инкубировали при 28°С в течение ночи. Клетки осаждали при центрифугировании при 4500 об./мин в течение 10 мин, ресуспендировали в 0,9% NaCl и определяли оптическую плотность при 578 нм. И наконец, клетки разбавляли до OD5 в 20 мл с использованием 0,9% NaCl.
Содержащую серебро или золото руду просеивали и 0,5 г руды смешивали с 20 мл клеточной суспензии, полученной из 168 микроорганизмов, отобранных по положительным результатам скрининга, в стеклянном стакане объемом 25 мл. В стакан помещали крестообразный мешальник для магнитной мешалки, стакан закрывали пленкой Парафильм и смесь руды и клеточной суспензией перемешивали при 100 об./мин в течение 16 ч на магнитной мешалке. После инкубации с перемешиванием смесь выдерживали в течение 3 ч при температуре окружающей среды без перемешивания. Результаты биологического разделения BSP регистрировали с помощью фотографий и пленку, состоящую из биомассы со связанным металлом на ее поверхности, удаляли для последующего анализа содержания золота и серебра методом масс-спектрометрии с индуктивно связанной плазмой (ICP-MS). Отбирали 12 бактериальных видов, которые связывают наибольшее количество золота и серебра. Извлечение и степень обогащения для этих 12 не-индуцированных микроорганизмов представлены на фиг. 3а и 3б. Величины извлечения в %, указанные на первичной вертикальной оси, определяли по следующей формуле:
([мкг] AuK/[мкг] AuE)*100; K = Концентрат (Флотат); Е = Общая масса руды.
Степень обогащения [-], указанную на вторичной вертикальной оси, определяли по следующей формуле:
([мкг] AuK/[г] K)/([мкг] AuE/[г] Е); K = Концентрат (Флотат); Е = Общая масса руды.
Биологическое разделение проводили также с использованием инактивированной биомассы. Для этого использовали аналогичные условия, как описано выше. Вместо жизнеспособных микроорганизмов использовали инактивированную биомассу, которую инактивировали при 121°С в течение 20 мин при давлении 1 бар. Извлечение и степень обогащения золота и серебра для 12 не-индуцированных микроорганизмов представлены на фиг. 4а и 4б. Неожиданно было установлено, что для некоторых организмов извлечение золота и серебра значительно выше при использовании мертвой биомассы по сравнению с жизнеспособной биомассой.
Пример 4
Рабочие параметры для обогащения драгоценных металлов из руды
Получение биомассы и определение сухой массы клеток
Биомассу получали при ферментации в условиях культивирования, как описано выше. Бактериальные клетки собирали и определяли сухую массу клеток (СМК). Биомассу осаждали в культуральной среде при центрифугировании при 4500 об./мин в течение 10 мин, промывали 0,9% NaCl и высушивали на стеклоткани при 125°С.
Обогащение драгоценных металлов
Было установлено, что для обогащения ценных металлов Au и Ag в нерастворимой элементной форме согласно способу по настоящему изобретению соотношение биомассы к руде должно составлять оптимальную величину в интервале от 0,01 до 20%, более предпочтительно 0,05% до 0,5% (СМК/масса руды). В табл. 3 указаны микроорганизмы, в наибольшей степени пригодные для обогащения серебра и золота из различных руд в качестве источника.
Была также доказана целесообразность использования комбинаций микроорганизмов. Было установлено, что для обогащения золота более эффективные результаты обеспечивает комбинация В. subtilis (MO1) и Р. fluorescens (MO2) при соотношении биомассы MO1 к биомассе MO2, например, 80:20, 70:30, 30:70 или 20:80 по сравнению с применением биомассы, содержащей единственный микроорганизм. Можно использовать комбинации различных бактерий с MO1 и MO2, включающие более двух или более трех различных бактерий. Можно использовать биомассу, включающую смесь бактериальных видов при том же соотношении СМК/масса руды, что и для биомассы, включающей единственные виды.
При обработке руд, включающих 0,3-5 част./млн (мкг/г или г/т) элементного золота, способом, описанным в данном контексте, факторы обогащения (кратность) составляют от 30 до 98.

| название | год | авторы | номер документа |
|---|---|---|---|
| БИОЛОГИЧЕСКАЯ ОБРАБОТКА РУДЫ ДЛЯ ВЫДЕЛЕНИЯ ТЯЖЕЛЫХ МЕТАЛЛОВ | 2016 |
|
RU2716725C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИИ, СОДЕРЖАЩЕЙ КОЛЛОИДНОЕ НАНОСЕРЕБРО ИЛИ НАНОЗОЛОТО (ВАРИАНТЫ) | 2007 |
|
RU2460797C2 |
| ШТАММ БАКТЕРИЙ BACILLUS MEGATERIUM, МОБИЛИЗУЮЩИЙ ФОСФОР И КРЕМНИЙ ИЗ ОБЪЕКТОВ ЛИТОСФЕРЫ И УСТОЙЧИВЫЙ К ПОЛИГЕКСАМЕТИЛЕНГУАНИДИНУ | 2006 |
|
RU2327737C2 |
| СПОСОБ БИОТРАНСФОРМАЦИИ КОЛХИКОНОВОГО СОЕДИНЕНИЯ В СООТВЕТСТВУЮЩЕЕ 3-0-ГЛИКОЗИЛЬНОЕ ПРОИЗВОДНОЕ | 1998 |
|
RU2218409C2 |
| СПОСОБ ПЕРЕРАБОТКИ УПОРНЫХ ЗОЛОТО-МЫШЬЯКОВЫХ РУД И КОНЦЕНТРАТОВ | 2003 |
|
RU2234544C1 |
| СПОСОБ ПЕРЕРАБОТКИ ПЕРВИЧНЫХ ЗОЛОТОСУЛЬФИДНЫХ РУД | 2004 |
|
RU2256712C1 |
| СПОСОБ БИОТРАНСФОРМАЦИИ СОЕДИНЕНИЙ КОЛХИЦИНОИДОВ В СООТВЕТСТВУЮЩИЕ 3-ГЛИКОЗИЛПРОИЗВОДНЫЕ | 1997 |
|
RU2196826C2 |
| ШТАММ БАКТЕРИЙ ACIDITHIOBACILLUS FERROOXIDANS ИБ1 ДЛЯ БИОВЫЩЕЛАЧИВАНИЯ МЕДИ ИЗ ОТХОДОВ ОБОГАЩЕНИЯ СУЛЬФИДНЫХ РУД | 2007 |
|
RU2340668C1 |
| СПОСОБ ПЕРЕРАБОТКИ УПОРНЫХ ПИРРОТИН-АРСЕНОПИРИТ-ПИРИТ-БЕРТЬЕРИТ-СТИБНИТОВЫХ ЗОЛОТОСОДЕРЖАЩИХ РУД (ВАРИАНТЫ) | 2023 |
|
RU2807003C1 |
| ШТАММ БАКТЕРИЙ ACIDITHIOBACILLUS FERROOXIDANS ДЛЯ БИОВЫЩЕЛАЧИВАНИЯ МЕДИ ИЗ ОТХОДОВ ОБОГАЩЕНИЯ СУЛЬФИДНЫХ РУД | 2007 |
|
RU2349641C1 |

Изобретение относится к биологической обработке руды для выделения или обогащения. Способ идентификации бактерии, способной связываться с тяжелым металлом в виде золота, серебра, рутения, родия, палладия, осмия, иридия, платины и/или редкоземельного металла, включает культивирование исследуемой бактерии в контейнере с пригодной первой культуральной средой в течение первого периода времени, с обеспечением пригодной плотности ее клеток. Часть поверхности исследуемого инструмента, на который нанесено покрытие из тяжелого металла, погружают в первую среду в течение второго периода времени, достаточного для обеспечения прикрепления исследуемой бактерии к погруженной поверхности упомянутого инструмента. После чего удаляют исследуемый инструмент из контейнера с первой культуральной средой. Проводят контактирование поверхности упомянутого инструмента со второй культуральной средой, содержащей указанный металл, для высевания упомянутой бактерии во вторую культуральную среду при ее прикреплении к поверхности упомянутого инструмента. Проводят идентификации упомянутой исследуемой бактерии из среды роста исследуемой бактерии в указанной второй культуральной среде. Способ позволяет повысить кратность обогащения руды. 2 з.п. ф-лы, 4 ил., 3 табл., 4 пр.
1. Способ идентификации бактерии, способной связываться с тяжелым металлом в виде золота, серебра, рутения, родия, палладия, осмия, иридия, платины, и/или редкоземельного металла, включающий следующие стадии:
(i) культивирование исследуемой бактерии, способной связываться с тяжелым металлом, в контейнере с пригодной первой культуральной средой в течение первого периода времени, с обеспечением пригодной плотности ее клеток,
(ii) погружение по крайней мере части поверхности исследуемого инструмента, на который нанесено покрытие из указанного тяжелого металла, в первую культуральную среду в течение второго предварительно определенного периода времени, достаточного для обеспечения прикрепления исследуемой бактерии к погруженной поверхности исследуемого инструмента,
(iii) удаление указанного исследуемого инструмента из контейнера с указанной первой культуральной средой,
(iv) контактирование поверхности исследуемого инструмента со второй культуральной средой, содержащей указанный тяжелый металл, для высеивания бактерии, способной связываться с тяжелым металлом, во вторую культуральную среду при ее прикреплении к поверхности исследуемого инструмента,
(v) идентификация исследуемой бактерии, способной связываться с тяжелым металлом, из роста исследуемой бактерии в указанной второй культуральной среде.
2. Способ по п. 1, в котором указанный контейнер является частью многолуночного планшета и указанный исследуемый инструмент представляет собой штифт на нижней части крышки многолуночного планшета, при этом на по меньшей мере верхней части указанного штифта нанесено покрытие из указанного тяжелого металла, при этом верхнюю часть штифта погружают в первую культуральную среду на стадии (ii) и/или в указанную вторую культуральную среду, которой является слой агара, содержащую соль указанного тяжелого металла, для выбора исследуемой бактерии, способной расти в присутствии указанной соли тяжелого металла.
3. Способ по п. 1, в котором на стадии (iii) после удаления исследуемого инструмента из контейнера с первой культуральной средой проводят промывку исследуемого инструмента.
| Бумажная бутылка | 1932 |
|
SU42935A1 |
| US 5162105 A1, 10.11.1991 | |||
| CN 103205381 A, 17.07.2013 | |||
| СПОСОБ ПЕРЕРАБОТКИ СУЛЬФИДНЫХ МИНЕРАЛЬНЫХ ПРОДУКТОВ С ПРИМЕНЕНИЕМ БАКТЕРИЙ ДЛЯ ИЗВЛЕЧЕНИЯ МЕТАЛЛОВ | 2009 |
|
RU2418870C2 |
| СПОСОБ КУЛЬТИВИРОВАНИЯ THIOBACILLUS FERROOXIDANS И СПОСОБ ИЗВЛЕЧЕНИЯ НЕ МЕНЕЕ ОДНОГО МЕТАЛЛА ИЗ ТРУДНООБОГАТИМОЙ РУДЫ | 1992 |
|
RU2099412C1 |
Авторы
Даты
2021-01-14—Публикация
2016-03-30—Подача