ОПИСАНИЕ
Предшествующий уровень техники настоящего изобретения
[0001] Акне представляет собой кожное заболевание, характеризующееся наличием участков черных угрей, белых угрей, прыщей, жирной кожи и, зачастую, рубцов. Розацеа представляет собой кожное заболевание, характеризующееся наличием красных пятен на лице, расширенных малых и поверхностных кровеносных сосудов на коже лица, папул, пустул и припухлости. Акне и розацеа страдают индивидуумы всех возрастов. Лечение и того и другого состояния с помощью перорального введения дииндолилметана в некоторых случаях приводит к низкой эффективности.
Перекрестные ссылки на родственные заявки
[0002] Настоящая заявка испрашивает приоритет согласно предварительной заявке на патент США №62/395234, поданной 15 сентября 2016 года, которая включена в настоящий документ посредством ссылки во всей своей полноте.
Краткое раскрытие настоящего изобретения
[0003] Один вариант осуществления относится к способу лечения акне у нуждающегося в этом субъекта, предусматривающему введение субъекту композиции, содержащей замещенный или незамещенный дииндолилметан, где композицию вводят посредством сублингвального или буккального пути. Согласно некоторым вариантам осуществления композиция дополнительно содержит замещенный или незамещенный компонент на основе ретиноевой кислоты. Согласно некоторым вариантам осуществления предусмотрен способ согласно пункту 2, где компонент на основе ретиноевой кислоты представляет собой витамин А. Согласно некоторым вариантам осуществления композиция дополнительно содержит пальмитат витамина А. Согласно некоторым вариантам осуществления введение композиции посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с Cmax замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с AUC замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с Tmax замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления композицию вводят в лекарственной форме, которая распадается при помещении в сублингвальное или буккальное пространство. Согласно некоторым вариантам осуществления по меньшей мере один параметр, выбранный из биодоступности, Cmax, AUC, Tmax, процентной доли композиции, выводимой P-gp, процентной доли композиции, поглощаемой ОАТР, и процентной доли композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6, измеряют после введения однократной дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана. Согласно некоторым вариантам осуществления однократной дозе, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана, предшествует ежесуточное введение по меньшей мере 15 мг замещенного или незамещенного дииндолилметана в течение по меньшей мере 14 дней. Согласно некоторым вариантам осуществления Cmax замещенного или незамещенного дииндолилметана в плазме крови является более высокой, с кратностью от приблизительно 1 раза до приблизительно 50 раз, по сравнению с Cmax замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути, где Cmax сравниваемой композиции измеряют после введения однократной дозы, содержащей по меньшей мере 15 мг сравниваемой композиции, которой предшествует ежесуточное введение по меньшей мере 15 мг сравниваемой композиции в течение по меньшей мере 14 дней.
[0004] Другой вариант осуществления относится к способу лечения розацеа у нуждающегося в этом субъекта, предусматривающему введение субъекту композиции, содержащей замещенный или незамещенный дииндолилметан, где композицию вводят посредством сублингвального или буккального пути. Согласно некоторым вариантам осуществления композиция дополнительно содержит замещенный или незамещенный компонент на основе ретиноевой кислоты. Согласно некоторым вариантам осуществления компонент на основе ретиноевой кислоты представляет собой витамин А. Согласно некоторым вариантам осуществления композиция дополнительно содержит пальмитат витамина А. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с Cmax замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с AUC замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с Tmax замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления композицию вводят в лекарственной форме, которая распадается при помещении в сублингвальное или буккальное пространство. Согласно некоторым вариантам осуществления по меньшей мере один параметр, выбранный из биодоступности, Cmax, AUC, Tmax, процентной доли композиции, выводимой P-gp, процентной доли композиции, поглощаемой ОАТР, и процентной доли композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6, измеряют после введения однократной дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана. Согласно некоторым вариантам осуществления однократной дозе, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана, предшествует ежесуточное введение по меньшей мере 15 мг замещенного или незамещенного дииндолилметана в течение по меньшей мере 14 дней. Согласно некоторым вариантам осуществления Cmax замещенного или незамещенного дииндолилметана в плазме крови является более высокой, с кратностью от приблизительно 1 раза до приблизительно 50 раз, по сравнению с Cmax замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути, где Cmax сравниваемой композиции измеряют после введения однократной дозы, содержащей по меньшей мере 15 мг сравниваемой композиции, которой предшествует ежесуточное введение по меньшей мере 15 мг сравниваемой композиции в течение по меньшей мере 14 дней.
[0005] Согласно одному варианту осуществления в настоящем документе предусмотрен способ лечения акне у нуждающегося в этом субъекта, предусматривающий введение субъекту композиции, содержащей замещенный или незамещенный дииндолилметан, где композицию вводят посредством сублингвального или буккального пути. Согласно некоторым вариантам осуществления композиция дополнительно содержит замещенный или незамещенный компонент на основе ретиноевой кислоты. Согласно некоторым вариантам осуществления компонент на основе ретиноевой кислоты представляет собой витамин А.
[0006] Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 1 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 2 раза по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 3 раза по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 4 раза по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 5 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 10 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 20 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 30 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 40 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 50 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 60 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 70 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 80 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 100 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 200 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 300 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 400 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 500 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 600 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 700 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 800 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 900 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 1000 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления биодоступность замещенного или незамещенного дииндолилметана измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0007] Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 2 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 3 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 4 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 5 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 10 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 20 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 30 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 40 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 50 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 60 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 70 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 80 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 90 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 100 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 200 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 300 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 400 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 500 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 600 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 700 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 800 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 900 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 1000 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления Cmax замещенного или незамещенного дииндолилметана в плазме крови измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0008] Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 2 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 3 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 4 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 5 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 6 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 7 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 8 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 9 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 10 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 20 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 30 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 40 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 50 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 60 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 70 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 80 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 90 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 100 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 200 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 300 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 400 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 500 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 600 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 700 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 800 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 900 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 1000 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления AUC замещенного или незамещенного дииндолилметана в плазме крови измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0009] Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 1 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 2 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 3 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 4 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 5 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 10 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 20 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 30 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 40 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 50 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 60 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 70 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 80 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 90 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 100 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 200 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 300 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 400 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 500 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 600 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 700 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 800 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 900 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 1000 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления Tmax замещенного или незамещенного дииндолилметана в плазме крови измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0010] Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,1% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,2% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,3% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,4% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,5% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 1% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 2% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 3% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 4% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 5% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 6% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 7% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 8% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 9% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 10% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 20% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 30% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 40% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 50% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, и процентная доля сравниваемой композиции, выводимой P-gp после перорального введения, рассчитаны исходя из дозы введения, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,1% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,2% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буквальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,3% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,4% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,5% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,6% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,7% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,8% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,9% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 1% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 2% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 3% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 4% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 5% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 6% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 7% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 8% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 9% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 10% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 20% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 30% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 40% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 50% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, и процентная доля сравниваемой композиции, поглощаемой ОАТР после перорального введения, рассчитаны исходя из дозы введения, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,1% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,2% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,3% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,4% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,5% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,6% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,7% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,8% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,9% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 1% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 2% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 3% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 4% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 5% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 6% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 7% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 8% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 9% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 10% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 20% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 30% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 40% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, и процентная доля сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, рассчитаны исходя из дозы введения, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана. Согласно некоторым вариантам осуществления композицию вводят в лекарственной форме, которая распадается при помещении в сублингвальное или буккальное пространство.
[0011] Согласно одному варианту осуществления в настоящем документе предусмотрен способ лечения розацеа у нуждающегося в этом субъекта, предусматривающий введение субъекту композиции, содержащей замещенный или незамещенный дииндолилметан, где композицию вводят посредством сублингвального или буккального пути. Согласно некоторым вариантам осуществления композиция дополнительно содержит замещенный или незамещенный компонент на основе ретиноевой кислоты. Согласно некоторым вариантам осуществления компонент на основе ретиноевой кислоты представляет собой витамин А.
[0012] Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 1 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 2 раза по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 3 раза по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 4 раза по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 5 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 10 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 20 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 30 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 40 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 50 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 60 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 70 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 80 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 100 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 200 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 300 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 400 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 500 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 600 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 700 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 800 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 900 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 1000 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления биодоступность замещенного или незамещенного дииндолилметана измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0013] Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 2 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 3 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 4 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 5 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 10 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 20 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 30 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 40 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 50 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 60 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 70 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 80 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 90 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 100 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 200 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 300 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 400 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 500 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 600 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 700 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 800 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 900 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 1000 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления Cmax замещенного или незамещенного дииндолилметана в плазме крови измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0014] Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 2 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 3 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 4 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 5 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 6 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 7 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 8 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 9 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 10 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 20 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 30 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 40 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 50 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 60 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 70 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 80 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 90 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 100 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 200 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 300 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 400 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 500 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 600 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 700 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 800 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 900 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 1000 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления AUC замещенного или незамещенного дииндолилметана в плазме крови измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0015] Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 1 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 2 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 3 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 4 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 5 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 10 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 20 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 30 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 40 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 50 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 60 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 70 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 80 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 90 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 100 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 200 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 300 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 400 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 500 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 600 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 700 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 800 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 900 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 1000 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления Tmax замещенного или незамещенного дииндолилметана в плазме крови измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, выводимой Р-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,1% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,2% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,3% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,4% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,5% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 1% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 2% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 3% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 4% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 5% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 6% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 7% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 8% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буквальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 9% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 10% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 20% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 30% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 40% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 50% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, и процентная доля сравниваемой композиции, выводимой P-gp после перорального введения, рассчитаны исходя из дозы введения, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0016] Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,1% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,2% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,3% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,4% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,5% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,6% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,7% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,8% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 0,9% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 1% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 2% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 3% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 4% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 5% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 6% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 7% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 8% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 9% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 10% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 20% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 30% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 40% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет 50% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, и процентная доля сравниваемой композиции, поглощаемой ОАТР после перорального введения, рассчитаны исходя из дозы введения, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0017] Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,1% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,2% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,3% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,4% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,5% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,6% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,7% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,8% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,9% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 1% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 2% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 3% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 4% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 5% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 6% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 7% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 8% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 9% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 10% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 20% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 30% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 40% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, и процентная доля сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, рассчитаны исходя из дозы введения, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана. Согласно некоторым вариантам осуществления композицию вводят в лекарственной форме, которая распадается при помещении в сублингвальное или буккальное пространство.
Включение посредством ссылки
[0018] Все публикации, патенты и заявки на патенты, упомянутые в настоящем описании, включены в настоящий документ посредством ссылки в той же степени, как если бы каждая отдельная публикация, патент или заявка на патент были конкретно и индивидуально указаны для включения посредством ссылки.
Краткое описание чертежей
[0019] На фиг. 1 представлена концентрация DIM в плазме крови после перорального или сублингвального введения состава на основе DIM. С помощью верхней светло-серой линии показана концентрация в плазме крови после сублингвального введения, а с помощью нижней темно-серой линии показано то же самое после перорального введения.
[0020] На фиг. 2 представлена концентрация DIM в плазме крови после перорального или сублингвального введения однократной дозы состава на основе DIM, причем однократной дозе предшествовало введение многократных доз для перорального или сублингвального введения. С помощью верхней светло-серой линии показана концентрация в плазме крови после сублингвального введения, а с помощью нижней темно-серой линии показано то же самое после перорального введения.
Подробное описание настоящего раскрытия
[0021] Хотя в настоящем документе были показаны и описаны предпочтительные варианты осуществления настоящего раскрытия, для специалистов в данной области будет очевидно, что такие варианты осуществления приведены исключительно в качестве примера. Многочисленные вариации, изменения и замены будут приходить на ум специалистам в данной области без отступления от настоящего раскрытия. Следует понимать, что можно использовать различные альтернативы описанным в настоящем документе вариантам осуществления настоящего раскрытия. Подразумевается, что нижеследующая формула изобретения определяет объем настоящего раскрытия, и что способы и структуры в пределах объема этой формулы изобретения и их эквиваленты также охватываются ею.
[0022] Если не указано иное, все применяемые в настоящем документе технические и научные термины имеют те же значения, которые обычно понятны специалисту в данной области, к которой относится описанное в настоящем документе настоящее раскрытие. Все публикации, патенты и заявки на патенты, упомянутые в настоящем описании, включены в настоящий документ посредством ссылки в той же степени, как если бы каждая отдельная публикация, патент или заявка на патент были конкретно и индивидуально указаны для включения посредством ссылки.
[0023] Применяемые в настоящем документе заголовки разделов предназначены только для организационных целей и не должны истолковываться как ограничивающие описанный заявляемый объект. Все документы или части документов, цитируемые в настоящей заявке, включая без ограничения патенты, заявки на патент, статьи, книги, руководства и научные трактаты, явным образом включены в настоящий документ посредством ссылки во всей своей полноте для любой цели.
DIM
[0024] Дииндолилметан (DIM) представляет собой природное соединение, образующееся в ходе аутолитического распада глюкобрассицина, присутствующего в пищевых растениях рода Brassica, включая брокколи, кочанную капусту, брюссельскую капусту, цветную капусту и кудрявую капусту. Для аутолитического распада глюкобрассицина требуется каталитическая реакция фермента мирозиназы, который является эндогенным по отношению к таким растениям и высвобождается при разрушении клеточной стенки. Соединение обычно получают путем химического синтеза, однако согласно некоторым вариантам осуществления его также получают природным способом из экстрактов перечисленных выше овощных культур рода Brassica, в частности, из спаржевой капусты или из семян брокколи.
[0025] Таким образом, замещенный или незамещенный DIM согласно некоторым вариантам осуществления является синтетическим или согласно некоторым вариантам осуществления представляет собой природный продукт, полученный из растения рода Brassica, как обсуждалось выше.
Акне
[0026] Акне представляет собой хроническое воспалительное заболевание пилосебацейного комплекса, обусловленное андроген-индуцированным усиленным образованием кожного сала, измененной кератинизацией, воспалением и бактериальной колонизацией волосяных фолликулов на лице, шее, грудной клетке и спине Propionibacterium acnes. Первичное патологическое проявление акне представляет собой комедон и включает обыкновенные угри, угри новорожденных, угри раннего детского возраста и «помадные» угри. Заболевание акне характеризуется большим разнообразием клинических поражений. Хотя преобладать может один тип поражения (обычно комедон), тщательное наблюдение обычно позволяет выявить наличие нескольких типов поражений (комедоны, пустулы, папулы и/или нодулы). Поражения могут быть либо невоспалительными, либо, более типично, воспалительными. Помимо поражений у пациентов могут наблюдаться, как результат поражений, шрамы различного размера. Полностью развившийся открытый комедон (т.е. пробка из высохшего кожного сала в поре кожи) обычно не является участком воспалительных изменений, если только он не поврежден пациентом. Развивающийся микрокомедон и закрытый комедон являются основными участками развития воспалительных поражений. Поскольку кожа всегда подвергается самовосстановлению, слои клеток будут вырастать из эпидермиса (образуя придаточные структуры) с целью инкапсуляции воспалительной реакции. Эта инкапсуляция зачастую является неполной, и обычно происходит дальнейший разрыв поражения, что приводит к образованию многоканальных участков, которые видны как множественные постакне.
[0027] Существуют главным образом четыре фактора, которые, как полагают, способствуют появлению акне: (1) усиленное образование кожного сала; (2) образование комедонов, при котором фолликулярная воронка подвергается гиперкорнификации, гиперкератинизации и пониженной десквамации; (3) колонизация фолликула анаэробной пропионовокислой бактерией, главным образом P. acnes; и (4) воспалительная реакция организма-хозяина. Эти четыре фактора взаимосвязаны друг с другом. Кожное сало является комедогенным и само по себе вызывает воспаление. Пропионовокислая бактерия обладает высокой липолитической активностью и обуславливает выделение свободных жирных кислот из липидов кожного сала. Было показано, что свободные жирные кислоты вызывают выраженное воспаление. Микроорганизмы также продуцируют другие внеклеточные ферменты, такие как протеазы и гиалуронидазы, и хемотаксические факторы, которые могут иметь важное значение при воспалительном процессе. Другие факторы, такие как диета, также предполагались, однако они не доказаны. Рубцевание на лице вследствие акне затрагивает вплоть до 20% подростков. Акне может сохраняться во взрослом возрасте, что негативно влияет на самооценку. Заболевание настолько распространено среди молодых людей в период полового созревания, что его часто называют физиологическим. Несмотря на то, что у большинства людей акне перестает появляться к 25 годам, некоторые люди, большинство из которых женщины, переносят заболевание и во взрослой жизни. Такое «акне у взрослых» отличается от подросткового акне по локализации, а также тем что оно склонно к более выраженным воспалительным процессам с меньшим количеством комедонов.
[0028] В целом, в настоящее время существует четыре основных принципа, определяющих лечение акне: (i) коррекция измененной схемы кератинизации в фолликулах; (ii) снижение активности сальных желез; (iii) уменьшение популяции бактерий фолликулов (особенно P. acnes) и ингибирование продукции внеклеточных вызывающих воспаление продуктов посредством ингибирования таких микроорганизмов; и (iv) обеспечение противовоспалительного эффекта.
Розацеа
[0029] Розацеа представляет собой хроническое воспалительное состояние кожи лица, затрагивающее кровеносные сосуды и пилосебацейные комплексы. Розацеа чаще встречается у лиц северо- и западноевропейского происхождения со светлым цветом лица, но может поражать кожу любого цвета. Хотя симптомы могут то усиливаться, то ослабевать на протяжении короткого периода времени, розацеа со временем может прогрессировать. Пациенты при обследовании обычно жалуются на приливы жара и покраснение и чувствительную кожу, и их кожа может быть особенно раздражена местными препаратами. Розацеа имеет ряд причин возникновения; однако, они могут быть не замечены пациентом.
[0030] Розацеа представляет собой хроническое и прогрессирующее нарушение со стороны сосудов кожи, в основном поражающее скуловые и носовые области лица. Розацеа характеризуется наличием приливов жара, покраснения, папул, пустул, телеангиэктазии, отечности лица, поражений глаза и, в ее наиболее запущенной и тяжелой форме, гиперплазии ткани и сальных желез, что приводит к развитию ринофимы. Ринофима, разрастание багрового цвета кончика носа с гиперваскуляризацией и модулярностью, представляет собой аномальное прогрессирование розацеа неизвестной причины. Поражения глаза являются распространенными, включая конъюнктивит в легкой форме, жжение и ощущение песка в глазах. Блефарит, наиболее распространенное глазное проявление, является неязвенным состоянием краев век. Розацеа чаще всего встречается в возрасте от 30 до 60 лет и может наблюдаться у женщин, испытывающих гормональные изменения, связанные с менопаузой. Женщины страдают чаще, чем мужчины; однако наиболее тяжелые случаи наблюдаются у мужчин.
Способы лечения акне или розацеа путем сублингвального или буккального введения DIM
[0031] Согласно некоторым вариантам осуществления в настоящем документе предусмотрены способы лечения акне или розацеа у нуждающегося в этом субъекта, предусматривающие введение субъекту композиции, содержащей замещенный или незамещенный дииндолилметан, где композицию вводят посредством сублингвального или буккального пути. Согласно некоторым вариантам осуществления композиция, содержащая замещенный или незамещенный дииндолилметан, дополнительно содержит замещенный или незамещенный компонент на основе ретиноевой кислоты.
[0032] Согласно некоторым вариантам осуществления сублингвальная или буккальная доставка обеспечивает растворение замещенного или незамещенного дииндолилметана в непосредственной близости от места размещения продукта, а затем лекарственное средство проникает непосредственно в кровоток, за счет чего обеспечивается повышение биодоступности замещенного или незамещенного дииндолилметана и быстрое проявление его фармакологического действия.
[0033] Согласно некоторым вариантам осуществления повышение биодоступности замещенного или незамещенного дииндолилметана после доставки посредством сублингвального или буккального пути соотносится к биодоступности после введения посредством перорального пути, при такой же доставляемой дозе, для той же композиции. Согласно некоторым вариантам осуществления повышение биодоступности замещенного или незамещенного дииндолилметана после доставки посредством сублингвального или буккального пути соотносится к биодоступности после введения посредством перорального пути, при такой же доставляемой дозе, для сравниваемой композиции.
[0034] Согласно некоторым вариантам осуществления введение композиции, содержащей замещенный или незамещенный дииндолилметан, посредством сублингвального или буккального пути позволяет «обойти» желудочный сок, кислую среду и ферменты, присутствующие в желудочно-кишечном тракте. Согласно некоторым вариантам осуществления повышенная биодоступность замещенного или незамещенного дииндолилметана в результате сублингвального или буккального введения приписывается обходу желудочного сока, кислой среды и ферментов, присутствующих в желудочно-кишечном тракте. Согласно некоторым вариантам осуществления введение замещенного или незамещенного дииндолилметана посредством сублингвального или буккального пути позволяет «обойти» печень, которая является целевым органом для метаболизма лекарственного средства при пероральном введении. Согласно некоторым вариантам осуществления повышенная биодоступность замещенного или незамещенного дииндолилметана в результате сублингвального или буккального введения приписывается обходу пресистемного метаболизма в печени. Согласно некоторым вариантам осуществления богато васкуляризированная слизистая оболочка между щекой и десной, куда помещают буккальные составы, или под языком, куда помещают сублингвальные составы, является идеальной и подходящей локализацией для абсорбции замещенного или незамещенного дииндолилметана.
Повышение биодоступности DIM в результате сублингвального или буккального введения
[0035] Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 500 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 100 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 20 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 10 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0036] Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 1 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 2 раза по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 3 раза по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 4 раза по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 5 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 10 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 20 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 30 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 40 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 50 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 60 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 70 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 80 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 100 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 200 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 300 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 400 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 500 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 600 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 700 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 800 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 900 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 1000 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 100 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
Улучшенные фармакокинетические параметры после введения DIM посредством сублингвального или буккального пути
[0037] Биодоступность включает следующие иллюстративные фармакокинетические факторы: скорость (или интервал времени после введения) достижения минимальной эффективной концентрации (МЕС) лекарственного средства в сыворотке крови, максимальная концентрация лекарственного средства в сыворотке крови (Cmax), скорость (или интервал времени после введения) достижения максимальной концентрации лекарственного средства в сыворотке крови (Tmax) и площадь под кривой зависимости концентрации лекарственного средства в сыворотке крови от времени выше линии, соответствующей минимальной эффективной концентрации лекарственного средства в сыворотке крови (AUC). Согласно некоторым вариантам осуществления способы лечения акне или розацеа путем введения замещенного или незамещенного дииндолилметана посредством сублингвального или буккального пути, как описано в настоящем документе, обеспечивают улучшение в отношении одного или нескольких упоминаемых выше факторов.
Повышенная Cmax
[0038] Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 500 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 100 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 20 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 10 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0039] Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 1 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 2 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 3 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 4 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 5 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 6 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 7 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 8 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 9 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 10 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 20 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 30 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 40 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 50 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 60 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 70 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 80 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 90 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 100 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 200 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 300 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 400 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 500 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 600 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 700 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 800 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 800 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 900 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 1000 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
Повышенная AUC
[0040] Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 500 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 100 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 20 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 10 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0041] Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 1 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 2 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 3 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 4 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 5 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 6 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 7 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 8 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 9 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 10 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 20 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 30 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 40 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 50 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 60 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 70 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 80 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 90 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 100 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 200 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 300 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 400 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 500 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 600 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 700 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 800 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 800 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 900 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 1000 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
Сниженная Tmax
[0042] Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается с кратностью от приблизительно 1 раза до приблизительно 500 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается с кратностью от приблизительно 1 раза до приблизительно 100 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается с кратностью от приблизительно 1 раза до приблизительно 20 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается с кратностью от приблизительно 1 раза до приблизительно 10 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0043] Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 1 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 2 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 3 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 4 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 5 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 6 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 7 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 8 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 9 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 10 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 20 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 30 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 40 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 50 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 60 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 70 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 80 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 100 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 200 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 300 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 400 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 500 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 600 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 700 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 800 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 900 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе. Согласно некоторым вариантам осуществления после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 1000 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
Способы введения DIM для предотвращения выведения и/или поглощения мембранными транспортерами
[0044] Известно, что мембранные транспортеры являются основными определяющими факторами профилей фармакокинетики, безопасности и эффективности лекарственных средств. В частности, в пределах генома человека аннотировано более 400 мембранных транспортеров, в двух основных суперсемействах, АТФ-связывающая кассета (ABC) и транспортер растворенных веществ (SLC). Известно, что транспортеры in vivo играют роль в распределении лекарственного средства, терапевтической эффективности и развитии нежелательных реакции на лекарственное средство. Роль транспортеров in vivo продемонстрирована у нескольких видов животных, включая нокаутных мышей, и на примере генетических вариантов вследствие мутаций с потерей функции у людей. Эти исследования предоставили существенную информацию об in vivo роли многих ABC- и SLC-транспортеров. Результаты клинических исследований фармакокинетических взаимодействий лекарственных средств (DDI) позволили предположить, что транспортеры при абсорбции и выведении лекарственных средств зачастую функционируют вместе с ферментами, метаболизирующими лекарственные средства (DME).
P-gP
[0045] Р-гликопротеин (P-gp), 170-кДа член суперсемейства АТФ-связывающего кассетного транспортера (АВСВ1), является мембранным белком-транспортер, который, как известно, опосредует АТФ-зависимый экспорт лекарственных средств из клеток. Интестинальное выведение лекарственных средств P-gp является общепризнанным как основной фактор низкой или переменной пероральной абсорбции некоторых лекарственных средств. Было показано, что он экспрессируется на люминальной мембране клеток тонкого кишечника и в пределах гематоэнцефалического барьера и на апикальных мембранах экскреторных клеток, таких как гепатоциты и клетки эпителия проксимального канальца почки. В последние годы возник большой интерес к потенциальной роли P-gp, который, за счет его функции откачивания лекарственных средств из эпителиальных клеток обратно в просвет кишечника, предположительно ограничивает пероральную биодоступность широкого спектра лекарственных средств. Было показано, что некоторые лекарственные средства характеризуются низкой биодоступностью вследствие P-gp-опосредованного выведения, имеющего место в тонком кишечнике.
[0046] Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли этой же композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 0,1% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 0,2% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком Р-gp после сублингвального или буккального введения, составляет приблизительно 0,3% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 0,4% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 0,5% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 1% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 2% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 3% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 4% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 5% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 6% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 7% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 8% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 9% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 10% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 20% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 30% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 40% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, выводимой интестинальным белком P-gp после сублингвального или буккального введения, составляет приблизительно 50% процентной доли сравниваемой композиции, выводимой интестинальным белком P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0047] Согласно некоторым вариантам осуществления процентные доли содержащей замещенный или незамещенный дииндолилметан композиции для сублингвального или буккального введения, выводимой интестинальным белком P-gp, рассчитывают с применением анализа двунаправленного транспорта. Согласно некоторым вариантам осуществления процентные доли содержащей замещенный или незамещенный дииндолилметан сравниваемой композиции для перорального введения, выводимой интестинальным белком P-gp, рассчитывают с применением анализа двунаправленного транспорта. Согласно некоторым вариантам осуществления анализ транспорта представляет собой анализ двунаправленной проницаемости с использованием MDR1-MDCK. Согласно некоторым вариантам осуществления суммарное отношение потоков рассчитывают по результатам анализа двунаправленной проницаемости с использованием MDR1-MDCK.
[0048] Согласно некоторым вариантам осуществления процентные доли сублингвальной или буккальной композиции и сравниваемой пероральной композиции, выводимых P-gp, пропорциональны суммарному отношению потоков. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции меньше суммарного отношения потоков сравниваемой пероральной композиции с кратностью от приблизительно 2 раз до приблизительно 20 раз. Согласно некоторым вариантам осуществления суммарное отношение потоков представляет собой отношение транспорта композиции от базолатерального в апикальном направлении к транспорту от апикального в базолатеральном направлении, или, другими словами, отношение измеряемых выведения к поглощению. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции меньше суммарного отношения потоков сравниваемой пероральной композиции с кратностью от приблизительно 2 раз до приблизительно 20 раз. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции меньше суммарного отношения потоков сравниваемой пероральной композиции с кратностью от приблизительно 2 раз до приблизительно 15 раз. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции меньше суммарного отношения потоков сравниваемой пероральной композиции с кратностью от приблизительно 2 раз до приблизительно 10 раз. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции меньше суммарного отношения потоков сравниваемой пероральной композиции с кратностью от приблизительно 2 раз до приблизительно 5 раз. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 2 раза меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 3 раза меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 4 раза меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 5 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 6 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 7 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 8 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 9 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 10 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 11 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 12 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 13 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 14 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 15 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 16 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 17 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 18 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 19 раз меньше суммарного отношения потоков сравниваемой пероральной композиции. Согласно некоторым вариантам осуществления суммарное отношение потоков для сублингвальной или буккальной композиции в приблизительно 20 раз меньше суммарного отношения потоков сравниваемой пероральной композиции.
ОАТР
[0049] Полипептиды, транспортирующие органические анионы (ОАТР), составляют семейство поглощающих транспортеров, экспрессируемых в ряде тканей, важных в контексте фармакокинетики. Из 11 ОАТР-транспортеров человека ОАТР1В1, ОАТР1В3 и ОАТР2В1 экспрессируются на синусоидальной мембране гепатоцитов, и было показано, что они способствуют поглощению в печени лекарственных средств, являющихся их субстратами. ОАТР1А2 экспрессируется на люминальной мембране энтероцитов тонкого кишечника и в пределах гематоэнцефалического барьера, вероятно опосредуя транспорт лекарственных средств в пределах этих участков. Некоторые применяемые в клинической практике лекарственные средства были идентифицированы как субстраты ОАТР-транспортеров (например, многие статины являются субстратами ОАТР1В1). Некоторые лекарственные средства могут ингибировать ОАТР-транспортеры (например, циклоспорин), обуславливая фармакокинетические взаимодействия лекарственных средств.
[0050] Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли той же композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 0,1% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 0,2% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 0,3% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 0,4% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 0,5% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 1% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 2% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 3% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 4% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 5% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 6% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 7% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 8% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 9% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 10% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 20% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 30% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 40% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, поглощаемой в энтероцит или клетку печени ОАТР после сублингвального или буккального введения, составляет приблизительно 50% процентной доли сравниваемой композиции, поглощаемой в энтероцит или клетку печени ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
Способы предотвращения метаболизации CYP450 путем сублингвального или буккального введения DIM
CYP450
[0051] Цитохромы Р450 (CYP450) представляют собой суперсемейство гемопротеинов. Они представляют собой конечные оксидазы системы оксидаз смешанной функции. Суперсемейство генов системы цитохрома Р450 состоит по меньшей мере из 207 генов, которые были названы исходя из эволюционного родства цитохромов Р450. Было показано, что три семейства генов системы цитохрома Р450 (CYP1, CYP2 и CYP3) ответственны за метаболизм некоторых лекарственных средств. По меньшей мере 15 цитохромов Р450 были в разной степени охарактеризованы в печени человека. Печень содержит множество изоформ цитохрома Р450, и в ней могут подвергаться биотрансформации самые различные вещества. Энтероциты, выстилающие просвет кишечника, также характеризуются значительной активностью цитохрома Р450, и эта активность обусловлена преимущественно одним семейством изоферментов, 3А, и наиболее важными изоформами в метаболизме лекарственных средств. Иллюстративные цитохромы Р450, которые, как известно, метаболизируют лекарственные средства в печени, включают CYP3A4, CYP1A2 и CYP2B6.
Сниженная степень метаболизации ферментами семейства CYP450
[0052] Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой ферментом CYP450 после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли той же композиции, метаболизируемой ферментом CYP450 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой ферментом CYP450 после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой ферментом CYP450 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0053] Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли той же композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 0,1% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 0,2% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 0,3% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 0,4% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 0,5% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 1% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 2% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 3% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 4% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 5% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 6% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 7% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 8% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 9% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 10% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 20% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 30% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 40% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе. Согласно некоторым вариантам осуществления процентная доля содержащей замещенный или незамещенный дииндолилметан композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после сублингвального или буккального введения, составляет приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой по меньшей мере одним из CYP3A4, CYP1A2 и CYPB26 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
Композиция на основе DIM, составы, пути введения и доставляемая доза
[0054] Согласно некоторым вариантам осуществления описанные в настоящем документе композиции содержат замещенный или незамещенный дииндолилметан. Согласно некоторым вариантам осуществления описанные в настоящем документе композиции содержат замещенный или незамещенный дииндолилметан, который был модифицирован с целью улучшения биодоступности. Согласно некоторым вариантам осуществления замещенный или незамещенный дииндолилметан, который был модифицирован с целью улучшения биодоступности, представляет собой дииндолилметан Bioresponse (BR-DIM). Согласно некоторым вариантам осуществления описанная в настоящем документе композиция содержит замещенный или незамещенный дииндолилметан, который не был модифицирован с целью улучшения биодоступности. Согласно некоторым вариантам осуществления замещенный или незамещенный дииндолилметан, который не был модифицирован с целью улучшения биодоступности, не является BR-DIM. Согласно некоторым вариантам осуществления описанные в настоящем документе композиции дополнительно содержат замещенный или незамещенный компонент на основе ретиноевой кислоты.
[0055] Согласно некоторым вариантам осуществления компонент на основе ретиноевой кислоты представляет собой любое соединение, известное в данной области, которое подходит для сублингвального или буккального, перорального или местного введения. Например, согласно некоторым вариантам осуществления оно выбрано из замещенного или незамещенного ретиноида первого поколения, замещенного или незамещенного ретиноида второго поколения и замещенного или незамещенного ретиноида третьего поколения. Согласно некоторым вариантам осуществления ретиноид представляет собой замещенный или незамещенный ретиноид первого поколения. Согласно некоторым вариантам осуществления замещенный или незамещенный ретиноид первого поколения выбран из замещенного или незамещенного ретинола, замещенного или незамещенного ретиналя, замещенного или незамещенного третиноина (например, ретиноевой кислоты или ретина А), замещенного или незамещенного изотретиноина (например, Accutane™) и замещенного или незамещенного алитретиноина. Согласно некоторым вариантам осуществления ретиноид представляет собой витамин А. Согласно некоторым вариантам осуществления ретиноид представляет собой замещенный или незамещенный ретиноид второго поколения, выбранный из замещенного или незамещенного этретината и замещенного или незамещенного ацитретина. Согласно некоторым вариантам осуществления ретиноид представляет собой замещенный или незамещенный ретиноид третьего поколения, выбранный из замещенного или незамещенного тазаротена, замещенного или незамещенного бексаротена и замещенного или незамещенного адапалена.
[0056] Согласно некоторым вариантам осуществления описанная в настоящем документе композиция содержит дииндолилметан формулы 1:
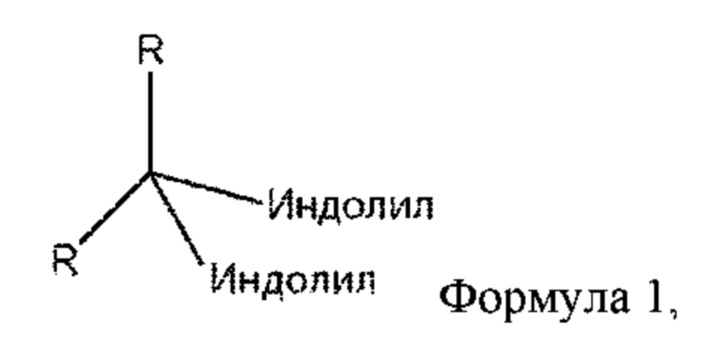
где R-группы независимо выбраны из атомов водорода и углеводородов С1-С6 в качестве заместителей; и где индолильные группы независимо выбраны из индол-3-ильных и индол-2-ильных групп; и где индолильные группы являются незамещенными или замещены одним или несколькими углеводородами С1-С6 в качестве заместителей.
[0057] Согласно некоторым вариантам осуществления описанная в настоящем документе композиция содержит незамещенный 3,3'-дииндолилметан. Согласно некоторым вариантам осуществления описанная в настоящем документе композиция содержит незамещенный 3,3'-дииндолилметан и соединение витамина А (например, пальмитат витамина А).
[0058] Согласно некоторым вариантам осуществления описанная в настоящем документе композиция содержит BR-DIM. Согласно некоторым вариантам осуществления описанная в настоящем документе композиция содержит BR-DIM и соединение витамина А (например, пальмитат витамина А).
[0059] Согласно некоторым вариантам осуществления композицию, содержащую замещенный или незамещенный дииндолилметан, вводят при доставляемой дозе, которая является достаточно низкой для предотвращения токсичности, с сохранением при этом требуемого фармацевтического эффекта. Согласно некоторым вариантам осуществления доставляемая доза композиции варьируется в зависимости от того, является ли она природным или синтетическим продуктом. Согласно некоторым вариантам осуществления доставляемую дозу композиции, содержащей замещенный или незамещенный дииндолилметан, определяют в зависимости от того, был ли или не был дииндолилметан модифицирован с целью улучшения биодоступности. Согласно некоторым вариантам осуществления доставляемая доза для композиции, содержащей BR-DIM, меньше доставляемой дозы для композиции, содержащей замещенный или незамещенный дииндолилметан, который не был модифицирован с целью улучшения биодоступности.
[0060] Согласно некоторым вариантам осуществления доставляемая доза составляет от приблизительно 10 мг до приблизительно 20 мг, от приблизительно 15 мг до приблизительно 25 мг, от приблизительно 20 мг до приблизительно 30 мг, от приблизительно 25 мг до приблизительно 35 мг, от приблизительно 30 мг до приблизительно 40 мг, от приблизительно 35 мг до приблизительно 45 мг, от приблизительно 40 мг до приблизительно 50 мг, от приблизительно 45 мг до приблизительно 55 мг, от приблизительно 50 мг до приблизительно 100 мг, от приблизительно 55 мг до приблизительно 150 мг, от приблизительно 60 мг до приблизительно 200 мг, от приблизительно 65 мг до приблизительно 250 мг, от приблизительно 70 мг до приблизительно 300 мг, от приблизительно 75 мг до приблизительно 350 мг, от приблизительно 80 мг до приблизительно 400 мг, от приблизительно 85 мг до приблизительно 450 мг, от приблизительно 90 мг до приблизительно 500 мг, от приблизительно 95 мг до приблизительно 550 мг, от приблизительно 100 мг до приблизительно 600 мг, от приблизительно 110 мг до приблизительно 700 мг, от приблизительно 120 мг до приблизительно 800 мг, от приблизительно 130 мг до приблизительно 900 мг, от приблизительно 140 мг до приблизительно 1000 мг, от приблизительно 150 мг до приблизительно 1100 мг, от приблизительно 200 мг до приблизительно 1200 мг, от приблизительно 250 мг до приблизительно 1300 мг, от приблизительно 300 мг до приблизительно 1400 мг или от приблизительно 350 мг до приблизительно 1500 мг.
[0061] Согласно некоторым вариантам осуществления доставляемая доза составляет по меньшей мере 15 мг, по меньшей мере 20 мг, по меньшей мере 30 мг, по меньшей мере 40 мг, по меньшей мере 55 мг, по меньшей мере 65 мг, по меньшей мере 75 мг, по меньшей мере 90 мг, по меньшей мере 100 мг, по меньшей мере 110 мг, по меньшей мере 120 мг, по меньшей мере 130 мг, по меньшей мере 140 мг или по меньшей мере 150 мг.
[0062] Согласно некоторым вариантам осуществления доставляемая доза описанных в настоящем документе композиций предусматривает суточную дозу замещенного или незамещенного дииндолилметана от приблизительно 10 мг до приблизительно 20 мг, от приблизительно 15 мг до приблизительно 25 мг, от приблизительно 20 мг до приблизительно 30 мг, от приблизительно 25 мг до приблизительно 35 мг, от приблизительно 30 мг до приблизительно 40 мг, от приблизительно 35 мг до приблизительно 45 мг, от приблизительно 40 мг до приблизительно 50 мг, от приблизительно 45 мг до приблизительно 55 мг, от приблизительно 50 мг до приблизительно 100 мг, от приблизительно 55 мг до приблизительно 150 мг, от приблизительно 60 мг до приблизительно 200 мг, от приблизительно 65 мг до приблизительно 250 мг, от приблизительно 70 мг до приблизительно 300 мг, от приблизительно 75 мг до приблизительно 350 мг, от приблизительно 80 мг до приблизительно 400 мг, от приблизительно 85 мг до приблизительно 450 мг, от приблизительно 90 мг до приблизительно 500 мг, от приблизительно 95 мг до приблизительно 550 мг, от приблизительно 100 мг до приблизительно 600 мг, от приблизительно 110 мг до приблизительно 700 мг, от приблизительно 120 мг до приблизительно 800 мг, от приблизительно 130 мг до приблизительно 900 мг, от приблизительно 140 мг до приблизительно 1000 мг, от приблизительно 150 мг до приблизительно 1100 мг, от приблизительно 200 мг до приблизительно 1200 мг, от приблизительно 250 мг до приблизительно 1300 мг, от приблизительно 300 мг до приблизительно 1400 мг или от приблизительно 350 мг до приблизительно 1500 мг.
[0063] Согласно некоторым вариантам осуществления доставляемая доза описанных в настоящем документе композиций предусматривает суточную дозу замещенного или незамещенного дииндолилметана, которая составляет по меньшей мере 20 мг, по меньшей мере 30 мг, по меньшей мере 40 мг, по меньшей мере 55 мг, по меньшей мере 65 мг, по меньшей мере 75 мг, по меньшей мере 90 мг, по меньшей мере 100 мг, по меньшей мере 110 мг, по меньшей мере 120 мг, по меньшей мере 130 мг, по меньшей мере 140 мг или по меньшей мере 150 мг.
[0064] Согласно некоторым вариантам осуществления композицию, содержащую замещенный или незамещенный дииндолилметан, вводят в любой из вышеупомянутых доз, включая, при необходимости, более высокие дозы. Согласно некоторым вариантам осуществления композицию, содержащую замещенный или незамещенный дииндолилметан, который был модифицирован с целью улучшения биодоступности, вводят в любой из вышеупомянутых доз, включая, при необходимости, более высокие дозы. Согласно некоторым вариантам осуществления замещенный или незамещенный дииндолилметан, который был модифицирован с целью улучшения биодоступности, представляет собой BR-DIM.
[0065] Согласно некоторым вариантам осуществления композиция, содержащая замещенный или незамещенный дииндолилметан, представляет собой состав, который вводят посредством сублингвального или буккального пути. Термин «состав, который вводят посредством сублингвального или буккального пути» в контексте настоящего документа относится к составу для доставки лекарственного средства, где активное соединение предусматривает абсорбцию через одну или несколько мембран в пределах буккального пространства, включая слизистую оболочку щеки, часть десны, расположенную на буккальной стороне зубов, слизистую оболочку языка, подъязычную мембрану и мягкое небо. Термин охватывает все подходящие твердые и мягкие лекарственные формы, включая троше, сублингвальные таблетки, буккальные таблетки (т.е. препарат, который может быть помещен под язык), шипучие таблетки, леденцы, капсулы, пленки, спреи и гели (например, гели на основе хитозана, мукоадгезивные гели). Термин «буккальный» используется в его самом широком смысле для обозначения ротовой полости в целом. Согласно некоторым вариантам осуществления предусматривающая состав композиция, которую вводят посредством сублингвального или буккального пути, также подходит для введения посредством перорального пути.
[0066] Согласно некоторым вариантам осуществления сравниваемая композиция, содержащая замещенный или незамещенный дииндолилметан, представляет собой состав, который вводят посредством перорального пути. Согласно некоторым вариантам осуществления состав, который вводят посредством перорального пути, находится в форме таблетки, капсулы, геля, крема или мази. Согласно некоторым вариантам осуществления предусматривающая состав сравниваемая композиция, которую вводят посредством перорального пути, также подходит для введения посредством сублингвального или буккального пути.
[0067] Согласно некоторым вариантам осуществления доставляемая доза композиции, содержащей замещенный или незамещенный дииндолилметан, зависит от пути введения.
[0068] Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 10 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 15 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 20 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 25 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 30 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 35 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 40 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 45 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 50 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 55 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 65 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 70 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 75 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 80 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 85 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 90 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 95 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 100 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 110 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 120 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 130 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 140 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет по меньшей мере 150 мг.
[0069] Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 10 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 15 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 20 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 25 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 30 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 35 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 40 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 45 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 50 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 55 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 65 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 70 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 75 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 80 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 85 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 90 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 95 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 100 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 110 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 120 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 130 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 140 мг. Согласно некоторым вариантам осуществления доставляемая доза для сублингвального или буккального введения составляет приблизительно 150 мг.
[0070] Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 10 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 15 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 20 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 25 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 30 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 35 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 40 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 45 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 50 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 55 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 65 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 70 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 75 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 80 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 85 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 90 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 95 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 100 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 110 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 120 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 130 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 140 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет по меньшей мере 150 мг.
[0071] Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 10 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 15 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 20 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 25 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 30 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 35 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 40 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 45 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 50 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 55 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 65 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 70 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 75 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 80 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 85 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 90 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 95 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 100 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 110 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 120 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 130 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 140 мг. Согласно некоторым вариантам осуществления доставляемая доза для перорального введения составляет приблизительно 150 мг.
[0072] Согласно некоторым вариантам осуществления доставляемые дозы для введения посредством сублингвального или буккального пути и посредством перорального пути являются одинаковыми. Согласно некоторым вариантам осуществления доставляемая доза для введения посредством сублингвального или буккального пути меньше доставляемой дозы для введения посредством перорального пути.
[0073] Согласно некоторым вариантам осуществления описанные в настоящем документе композиции содержат замещенный или незамещенный дииндолилметан в дозе, которая является частью суточной дозы, такой как половина суточной дозы или четверть суточной дозы, и, таким образом, присутствует в виде половины или четверти любой из указанных выше доз. Согласно таким вариантам осуществления каждая часть дозы принимается отдельно по времени для распределения дозы на протяжении дня.
[0074] Согласно некоторым вариантам осуществления описанные в настоящем документе композиции дополнительно содержат замещенный или незамещенный компонент на основе ретиноевой кислоты. Согласно некоторым вариантам осуществления компонент на основе ретиноевой кислоты вводят в дозе, которая является достаточно низкой для предотвращения токсичности, с сохранением при этом требуемого фармацевтического эффекта. Согласно некоторым вариантам осуществления доставляемая доза компонента на основе ретиноевой кислоты зависит от его биодоступности. Согласно некоторым вариантам осуществления биодоступность замещенного или незамещенного компонента на основе ретиноевой кислоты варьируется в зависимости от того, является ли он природным или синтетическим продуктом. Согласно некоторым вариантам осуществления биодоступность замещенного или незамещенного компонента на основе ретиноевой кислоты может различаться в зависимости от того, был ли он модифицирован с целью улучшения его биодоступности. Согласно некоторым вариантам осуществления доставляемые дозы описанных в настоящем документе композиций предусматривают суточную дозу замещенного или незамещенного компонента на основе ретиноевой кислоты от приблизительно 0,05 мг до приблизительно 3 мг, от приблизительно 0,1 до приблизительно 1 мг, от приблизительно 0,1 до приблизительно 5 мг, от приблизительно 1 мг до приблизительно 15 мг, от приблизительно 10 мг до приблизительно 45 мг, от приблизительно 25 мг до приблизительно 100 мг, от приблизительно 75 мг до приблизительно 200 мг, от приблизительно 150 мг до приблизительно 250 мг. Согласно некоторым вариантам осуществления доставляемые дозы описанных в настоящем документе композиций предусматривают суточную дозу замещенного или незамещенного компонента на основе ретиноевой кислоты, которая составляет по меньшей мере 0,05 мг, по меньшей мере 0,1 мг, по меньшей мере 0,2 мг, по меньшей мере 0,4 мг, по меньшей мере 0,5 мг, по меньшей мере 0,6 мг, по меньшей мере 0,7 мг, по меньшей мере 0,8 мг, по меньшей мере 0,9 мг, по меньшей мере 1 мг, по меньшей мере 5 мг или по меньшей мере 10 мг. Согласно некоторым вариантам осуществления доставляемые дозы описанных в настоящем документе композиций предусматривают суточную дозу замещенного или незамещенного компонента на основе ретиноевой кислоты, которая составляет приблизительно 0,05 мг, приблизительно 0,1 мг, приблизительно 0,2 мг, приблизительно 0,4 мг, приблизительно 0,5 мг, приблизительно 0,6 мг, приблизительно 0,7 мг, приблизительно 0,8 мг, приблизительно 0,9 мг, приблизительно 1 мг, приблизительно 5 мг или приблизительно 10 мг. Согласно некоторым вариантам осуществления доставляемые дозы описанных в настоящем документе композиций предусматривают суточную дозу замещенного или незамещенного компонента на основе ретиноевой кислоты, которая составляет до 15 мг, до 10 мг, до 9 мг, до 8 мг, до 7 мг, до 6 мг, до 5 мг, до 2,5 мг, до 2 мг, до 1 мг или до 0,5 мг.
[0075] Согласно некоторым вариантам осуществления суточная дозировка композиции, содержащей замещенный или незамещенный дииндолилметан и необязательно замещенный или незамещенный компонент на основе ретиноевой кислоты, предусмотрена в виде одной или нескольких разовых доз. Согласно некоторым вариантам осуществления суточная дозировка композиции, содержащей замещенный или незамещенный дииндолилметан и необязательно замещенный или незамещенный компонент на основе ретиноевой кислоты, предусмотрена в виде 2-4 разовых доз. Согласно таким вариантам осуществления две или более разовых доз принимаются на протяжении однодневного курса, как, например, одна разовая доза утром и одна разовая доза вечером, или четыре разовых дозы, распределенных равномерно на протяжении дня, или две разовых дозы одновременно два раза в сутки.
Способы получения
[0076] Согласно некоторым вариантам осуществления предусмотрены способы получения описанных в настоящем документе композиций для применения в описанных в настоящем документе способах лечения акне или розацеа. Согласно некоторым вариантам осуществления с применением описанных в настоящем документе способов получают композицию, подходящую для сублингвального или буккального введения. Согласно некоторым вариантам осуществления с применением описанных в настоящем документе способов получают сравниваемую композицию, подходящую для перорального введения. Согласно некоторым вариантам осуществления с применением описанных в настоящем документе способов получают композицию, подходящую как для сублингвального или буккального, так и для перорального введения.
[0077] Согласно некоторым вариантам осуществления используют любые известные в данной области способы смешивания или перемешивания различных компонентов композиции. Согласно некоторым вариантам осуществления используемые способы представляют собой способы смешивания и/или перемешивания порошков. Согласно некоторым вариантам осуществления способ предусматривает перемешивание замещенного или незамещенного дииндолилметана с одним или несколькими фармацевтически приемлемыми вспомогательными веществами и/или добавками и необязательно с замещенным или незамещенным компонентом на основе ретиноевой кислоты с получением композиции. Согласно некоторым вариантам осуществления каждый из замещенного или незамещенного дииндолилметана и замещенного или незамещенного компонента на основе ретиноевой кислоты, отдельно друг от друга, перемешивают с одним или несколькими фармацевтически приемлемыми вспомогательными веществами и/или добавками перед перемешиванием вместе с получением композиции. Согласно некоторым вариантам осуществления замещенный или незамещенный дииндолилметан, замещенный или незамещенный компонент на основе ретиноевой кислоты и/или фармацевтически приемлемые вспомогательные вещества в ходе процесса перемешивания последовательно добавляют к смеси.
[0078] Согласно некоторым вариантам осуществления выбор фармацевтически приемлемых вспомогательных веществ и способа смешивания модифицированы с целью преодоления каких-либо связанных с композицией проблем в отношении перемешивания, текучести и наполнения или проблем с продавливанием. Согласно некоторым вариантам осуществления композиция, содержащая замещенный или незамещенный дииндолилметан, предусмотрена в микроинкапсулированной форме, так что частицы порошка имеют склонность к комкованию между собой. Согласно некоторым вариантам осуществления композицию, содержащую первый компонент, предусматривающий замещенный или незамещенный дииндолилметан, смешивают с применением способа, который модифицирован для предотвращения образования точек скопления с повышенными концентрациями активных ингредиентов. Согласно некоторым вариантам осуществления композицию, содержащую замещенный или незамещенный дииндолилметан и необязательно замещенный или незамещенный компонент на основе ретиноевой кислоты, смешивают с применением способа, который включает короткое время обработки/смешивания с целью защиты композиции от света и воздуха, в случае когда композиция является гигроскопичной и светочувствительной. Согласно некоторым вариантам осуществления композицию, содержащую замещенный или незамещенный дииндолилметан и необязательно замещенный или незамещенный компонент на основе ретиноевой кислоты, получают в форме порошка, и в процессе хранения порошок защищен как от света, так и от воздуха.
[0079] Согласно некоторым вариантам осуществления одно или несколько из микрокристаллической целлюлозы, силиката магния, трикальцийфосфата и стеарата магния (традиционное смазывающее вещество) используют при получении описанных в настоящем документе композиций в качестве фармацевтически приемлемых добавок и вспомогательных веществ для улучшения характеристик текучести и/или лубрикации. Согласно некоторым вариантам осуществления при необходимости используют другие фармацевтически приемлемые добавки и вспомогательные вещества, известные в данной области. Согласно некоторым вариантам осуществления композиция содержит 50,0-65,0% по весу трикальцийфосфата. Согласно некоторым вариантам осуществления композиция содержит 55,0-60,0% по весу или 57,0-59,0% по весу трикальцийфосфата. Согласно некоторым вариантам осуществления композиция приблизительно 58% по весу трикальцийфосфата. Согласно некоторым вариантам осуществления композиция приблизительно 58,3% по весу трикальцийфосфата.
[0080] Согласно некоторым вариантам осуществления правильное смешивание всех ингредиентов является желательным для достижения однородного наполнения капсул описанными в настоящем документе композициями. Согласно некоторым вариантам осуществления правильное смешивание всех ингредиентов является желательным для достижения однородного наполнения капсул описанными в настоящем документе композициями. Согласно некоторым вариантам осуществления для успешного перемешивания высокоэффективным является V-образный блендер. Согласно некоторым вариантам осуществления для процесса перемешивания применяют сосуд из нержавеющей стали марки минимум 316. Согласно некоторым вариантам осуществления просеивание осуществляют в одном или нескольких из начала, середины и конца процесса перемешивания. Согласно некоторым вариантам осуществления исследования по смешиванию для подтверждения однородности смешивания выполняют с целью проверки способа и состава с применением известных в данной области способов и методик.
[0081] Согласно одному иллюстративному варианту осуществления сублингвальный или буккальный состав содержит: 50-75 мг BR-DIM; 200 мкг пальмитата витамина А в качестве эквивалентов ретинола (366,4 мкг ретинилпальмитата) (это эквивалентно 2,666 мг 250000 МЕ/г пальмитата витамина A (BASF); 100-175 мг трикальцийфосфата; 10-20 мг микрокристаллической целлюлозы; 5-10 мг витамина С (аскорбиновой кислоты); 5-10 мг пирогенного диоксида кремния (или тонкодисперсного осажденного диоксида кремния); 3-6 мг стеарата магния.
[0082] Согласно одному иллюстративному варианту осуществления пероральный состав содержит: 50-75 мг BR-DIM; 200 мкг пальмитата витамина А в качестве эквивалентов ретинола (366,4 мкг ретинилпальмитата) (это эквивалентно 2,666 мг 250000 МЕ/г пальмитата витамина A (BASF); 100-175 мг трикальцийфосфата; 10-20 мг микрокристаллической целлюлозы; 5-10 мг витамина С (аскорбиновой кислоты); 5-10 мг пирогенного диоксида кремния (или тонкодисперсного осажденного диоксида кремния); 3-6 мг стеарата магния.
Некоторые определения
[0083] Если не указано иное, все применяемые в настоящем документе технические и научные термины имеют те же значения, которые обычно понятны специалисту в данной области, к которой относится заявляемый объект. В том случае, когда имеются несколько определений для представленных в настоящем документе терминов, преимущественную силу имеют таковые данного раздела.
[0084] Следует понимать, что предшествующее общее описание и следующее подробное описание являются исключительно иллюстративными и пояснительными и не ограничивают какой-либо заявляемый объект. В настоящей заявке применение формы единственного числа включает форму множественного числа, если специально не указано иное. Следует отметить, что в контексте настоящего описания и прилагаемой формулы изобретения формы единственного числа включают формы множественного числа определяемого объекта, если контекстом явно не указано иное. Также следует отметить, что применение «или» означает «и/или», если не указано иное. Кроме того, применение термина «включая», а также других форм, таких как «включают», «включает» и «включенный», не является ограничивающим.
[0085] В контексте настоящего документа термин «приблизительно» применяют синонимично с термином «примерно». Для иллюстрации, применение термина «приблизительно» в отношении определенной терапевтически эффективной фармацевтической дозы указывает на то, что значения, немного выходящие за пределы указанных значений, например, плюс или минус 0,1%-10%, также являются эффективными и безопасными.
[0086] Термин «пациент», «субъект» или «индивидуум» применяют взаимозаменяемо. В контексте настоящего документа указанные термины относятся к индивидуумам, страдающим от нарушения и т.п., и охватывают млекопитающих и отличных от млекопитающих животных. Ни один из терминов не предусматривает необходимость того, чтобы индивидуум был под присмотром и/или наблюдением медицинского работника. Млекопитающие представляют собой любого представителя класса Млекопитающие, включая без ограничения людей, отличных от человека приматов, таких как шимпанзе и другие виды человекообразных обезьян и обезьянообразных; сельскохозяйственных животных, таких как крупный рогатый скот, лошади, овца, козы, свиньи; домашних животных, таких как кролики, собаки и кошки; лабораторных животных, включая грызунов, таких как крысы, мыши и морские свинки и т.д. Примеры отличных от млекопитающих животных включают без ограничения птиц, рыбу и т.д. Согласно некоторым вариантам осуществления способов и композиций, предусмотренных в настоящем документе, индивидуум представляет собой млекопитающее. Согласно предпочтительным вариантам осуществления индивидуум представляет собой человека.
[0087] Термины «лечить», «осуществление лечения» или «лечение» и другие грамматические эквиваленты в контексте настоящего документа включают ослабление, смягчение или облегчение заболевания или состояния или одного или нескольких их симптомов, предупреждение появления дополнительных симптомов, облегчение или предупреждение лежащих в основе метаболических причин появления симптомов, ингибирование заболевания или состояния, например, приостановку развития заболевания или состояния, ослабление тяжести заболевания или состояния, содействие регрессии заболевания или состояния, ослабление тяжести состояния, причиной которого является заболевание или состояние, или прекращение проявления симптомов заболевания или состояния, и подразумевается, что они включают профилактику. Термины дополнительно включают достижение терапевтической пользы и/или профилактической пользы. Под терапевтической пользой понимают устранение или облегчение подлежащего лечению первичного нарушения. Также терапевтическая польза достигается за счет устранения или облегчения одного или нескольких из физиологических симптомов, ассоциированных с первичным нарушением, так что у индивидуума наблюдается улучшение, несмотря на то, что индивидуум все еще страдает от первичного нарушения. В случае профилактической пользы композиции вводят индивидууму с риском развития конкретного заболевания или индивидууму, сообщающему об одном или нескольких из физиологических симптомов заболевания, даже если диагноз этого заболевания не был поставлен.
[0088] Термины «вводить», «осуществление введения», «введение» и т.п. в контексте настоящего документа относятся к способам, которые можно применять для обеспечения возможности доставки соединений или композиций в требуемый участок биологического действия. Такие способы включают без ограничения сублингвальные или буккальные пути, пероральные пути, интрадуоденальные пути, парентеральную инъекцию (включая внутривенную, подкожную, внутрибрюшинную, внутримышечную, внутрисосудистую инъекцию или инфузию), местное и ректальное введение. Специалисты в данной области знакомы с методиками введения, которые можно использовать для соединений и описанных в настоящем документе способов.
[0089] Термин «приемлемый» в контексте настоящего документа в отношении состава, композиции или ингредиента означает отсутствие постоянного негативного воздействия на общее состояние здоровья подлежащего лечению индивидуума.
[0090] Термин «фармацевтически приемлемый» в контексте настоящего документа относится к материалу, такому как носитель или разбавитель, который не нейтрализует биологическую активность или свойства описанных в настоящем документе соединений и является относительно нетоксичным, т.е. материал можно вводить индивидууму без стимуляции нежелательных биологических эффектов или без негативного взаимодействия с какими-либо из компонентов композиции, в которой он содержится.
[0091] Термин «DIM» в контексте настоящего документа относится к замещенному или незамещенному соединению дииндолилметана.
[0092] Термин «BR-DIM» или «DIM BioResponse» в контексте настоящего документа относится к незамещенному DIM, предоставляемому BioResponse LLC.
[0093] Термин «максимальная концентрация» или Сmax в контексте настоящего документа относится к Сmax, которая относится к максимальной (или пиковой) концентрации в сыворотке крови, которой достигает замещенный или незамещенный дииндолилметан в плазме крови после того, как он был введен, и перед введением второй дозы.
[0094] Термин «время достижения максимальной концентрации» или Тmax в контексте настоящего документа относится к моменту времени, при котором наблюдают Сmax.
[0095] Термин «площадь под кривой» или AUC или AUC0-inf в контексте настоящего документа относится к площади под кривой, также известной как определенный интеграл, на графике зависимости концентрации лекарственного средства в плазме крови от времени.
[0096] Термин «разовая доза» в контексте настоящего документа относится к количеству замещенного или незамещенного дииндолилметана, содержащемуся в одной дискретной фармацевтической лекарственной форме. Примеры фармацевтической лекарственной формы, которая содержит разовую дозу, включают без ограничения таблетку, капсулу, буккальную таблетку, сублингвальную таблетку, таблетку, распадающуюся в полости рта, шипучую таблетку, леденец, пастилку, троше, жидкий раствор или суспензию, порошок или жидкие или твердые кристаллы, которыми наполнена отдельная таблетка или капсула, крем, гель, мазь, лосьон.
Примеры
[0097] Следующие конкретные неограничивающие примеры должны рассматриваться лишь как иллюстративные, и они не ограничивают объем настоящего раскрытия. Без дополнительного уточнения, полагают, что специалист в данной области сможет, опираясь на описание в настоящем документе, использовать настоящее раскрытие в его наиболее полном объеме.
Пример 1. Эффект пути введения в отношении профиля PK DIM в плазме крови.
[0098] Целью этого исследования является определение фармакокинетического (PK) профиля состава на основе дииндолилметана (DEVI) в плазме крови после однократных и многократных доз DEVI, введенных либо посредством сублингвального пути, либо посредством перорального пути. Состав на основе DEVI для этого исследования синтезируют и готовят с применением любого из описанных выше способов.
[0099] Участники исследования будут распределены в (а) группу 1: DIM вводят посредством перорального пути, и (b) группу 2: DIM вводят посредством сублингвального или буккального пути.
[0100] Часть 1: фармакокинетические параметры состава на основе DIM в плазме крови после однократной пероральной дозы 75 мг.
[0101] Участникам исследования групп 1 и 2 будут вводить, перорально и посредством сублингвального или буккального пути соответственно, однократную дозу 90 мг состава на основе DIM. Образцы крови будут брать у участников исследования на исходном уровне и через 0,5, 1,0, 1,5, 2, 3, 4, 6, 8, 9 ч после введения дозы состава на основе DIM в день 1.
[0102] Часть 2: фармакокинетический профиль DIM после введения дозы два раза в сутки в течение 4 недель.
[0103] Во второй части исследования участникам исследования групп 1 и 2 будут вводить, перорально и посредством сублингвального или буккального пути соответственно, в дни 1-28, однократную дозу 45 мг состава на основе DIM дважды в сутки (т.е. каждый участник исследования будет получать в общей сложности 90 мг DFM в сутки). Образцы крови будут взяты по завершению лечения в соответствии со схемой, описанной для части 1.
[0104] Для каждой части исследования фармакокинетические параметры, включая без ограничения максимальную концентрацию (Сmax), время достижения Сmax (Тmax), биологический период полувыведения (t½) и площадь под кривой концентрация-время (AUC0-inf), будут рассчитывать для всех субъектов, которые завершили соответствующую часть исследования. Предполагается, что однокамерная модель скорости выведения будет соответствовать данным.
Пример 2. Эффект сублингвального или буккального состава на основе DIM в отношении активности определенных ферментов CYP450 печени.
[0105] Целью этого исследования является определение подверженности сублингвального или буккального состава на основе DIM метаболизации определенными ферментами CYP-450 печени. Исследование осуществляют в соответствии со способами, описанными в Chu et al. (2009, Drug Metab Dispos 37; 1339-1354).
[0106] Иллюстративный протокол включает следующие стадии:
• Свежие или высеваемые замороженные гепатоциты высевают либо в виде монослоя, либо в виде многослойной культуры, с 1-2 дневным восстановительным периодом после высевания.
• Гепатоциты в трех повторностях обрабатывают различными концентрациями сублингвального или буккального состава на основе DIM и положительными контролями в течение 2-3 дней (с заменой среды с тестируемыми соединениями каждые 24 ч) в среде, содержащей ITS (инсулин-трансферрин-селен), дексаметазон и пенициллин-стрептомицин в качестве добавок к среде.
• Иллюстративные положительные контроли включают без ограничения омепразол (25-50 мкМ), фенобарбитал (1000 мкМ) и рифампицин (10 мкМ) для CYP1A2, 2В6 и 3А4 соответственно в концентрациях, о которых известно, что они вызывают максимальный индукционный ответ.
• Эффект сублингвального или буккального состава на основе DIM в отношении индуцирования ферментов CYP печени рассчитывают с помощью эмпирического подхода, как, например, путем определения процентной доли изменения в сравнении с положительным контролем, или с помощью математического подхода или подхода на основе определения корреляции с применением терапевтической концентрации Сmax лекарственного средства в равновесном состоянии в качестве эталона для сравнения.
• Эксперимент по индукции гепатоцитов считается соответствующим требованиям, если положительные контроли CYP1A2, CYP2B6 и CYP3A4 проявляют ≥2-кратную каталитическую активность контроля носителем CYP и ≥6-кратный уровень мРНК контроля носителем.
Пример 3. Выведение сублингвального или буккального состава на основе DIM и перорального состава на основе DIM P-gp.
[0107] Целью этого исследования является оценка подверженности сублингвального или буккального состава на основе DIM выведению белком-транспортером (например, P-gp). Исследование осуществляют с применением анализа двунаправленного транспорта, например, анализа проницаемости с использованием MDR1-MDCK Cyprotex™.
[0108] Первый эксперимент осуществляют путем высевания клеток MDR1-MDCK (которые представляют собой клетки почки собаки Майдин-Дэрби (MDCK, Madin Darby canine kidney), трансфицированные геном MDR1, геном, кодирующим эффлюксный белок, Р-гликопротеин (P-gp)) на планшет Multiscreen™ (Millipore, Массачусетс, США) с получением конфлюентного монослоя за 4 дня перед проведением эксперимента. В день 4 тестируемый сублингвальный или буккальный состав на основе DIM добавляют на апикальную сторону (донор) мембраны и отслеживают транспорт соединения от апикального компартмента к базолатеральному (акцептор) компартменту (А-В) через монослой в течение промежутка времени 60 мин. Затем тестируемый сублингвальный или буккальный состав на основе DIM добавляют на базолатеральную (донор) сторону мембраны и отслеживают транспорт от базолатерального компартмента к апикальному (акцептор) компартменту (В-А) в течение промежутка времени 60 мин. Согласно некоторым вариантам осуществления накопленное количество сублингвального или буккального состава на основе DIM, со временем появляющееся в АР-компартменте, dQ/dt, будет применяться для расчета эффективной проницаемости (Рарр) с применением следующего уравнения: Рарр=dQ/dt × 1/(А × Со), где А представляет собой площадь фильтра и СО представляет собой исходную концентрацию сублингвального или буккального состава на основе DIM в компартменте-доноре. Рарр рассчитывают как для транспорта от апикальной к базолатеральной (РаррA-B) стороне, так и для транспорта от базолатеральной к апикальной (РаррB-A) стороне. Согласно некоторым вариантам осуществления суммарное отношение потоков рассчитывают путем деления РаррB-A на РаррA-B.
[0109] Второй эксперимент осуществляют с применением того же протокола, описанного выше для первого эксперимента, с использованием перорального состава на основе DIM. Суммарное отношение потоков во втором эксперименте сравнивают с таковым в первом эксперименте.
Пример 4. Улучшенная эффективность лечения розацеа путем сублингвального или буккального введения DIM.
[0110] Целью этого исследования является определение эффективности состава на основе дииндолилметана (DIM) в лечении розацеа после 4-недельного лечения DIM, введенного либо посредством сублингвального пути, либо посредством перорального пути. Состав на основе DIM для этого исследования синтезируют и готовят с применением любого из описанных выше способов.
[0111] Участники исследования будут распределены в (а) группу 1: DIM вводят посредством перорального пути, и (b) группу 2: DIM вводят посредством сублингвального или буккального пути.
[0112] Участникам исследования групп 1 и 2 будут вводить, перорально и посредством сублингвального или буккального пути соответственно, в дни 1-28, однократную дозу 45 мг состава на основе DIM дважды в сутки (т.е. каждый участник исследования будет получать в общей сложности 90 мг DIM в сутки). После завершения исследования от участников потребуется самостоятельно сообщить о некоторых характеристиках кожи, связанных с розацеа, например, покраснение, приливы жара, сухость, красные бугорки, отек.
Пример 5. Улучшенная эффективность лечения акне путем сублингвального или буккального введения DIM.
[0113] Целью этого исследования является определение эффективности состава на основе дииндолилметана (DIM) в лечении акне после 4-недельного лечения DIM, введенного либо посредством сублингвального пути, либо посредством перорального пути. Состав на основе DIM для этого исследования синтезируют и готовят с применением любого из описанных выше способов.
[0114] Участники исследования будут распределены в (а) группу 1: DIM вводят посредством перорального пути, и (b) группу 2: DIM вводят посредством сублингвального или буккального пути.
[0115] Участникам исследования групп 1 и 2 будут вводить, перорально и посредством сублингвального или буккального пути соответственно, в дни 1-28, однократную дозу 45 мг состава на основе DIM дважды в сутки. После завершения исследования будут оценены биофизические характеристики кожи участников исследования, связанные с акне, включая без ограничения кожное сало и уровни гидратации рогового слоя, значения трансэпидермальной потери влаги, рН, покраснение и параметры роста волос, такие как общее число, плотность и доля волос в фазе роста.
Пример 6. Эффект пути введения в отношении профиля PK DIM + витамин А в плазме крови.
[0116] Речь пойдет о рандомизированном, открытом, перекрестном исследовании фазы 1 с двумя последовательностями с участием здоровых участников исследования для определения фармакокинетических параметров дииндолилметана (DIM) после однократных и многократных доз перорального и сублингвального состава DIM + витамин А. Составы для этого исследования синтезируют и готовят с применением любого из описанных выше способов.
[0117] Это рандомизированное испытание I фазы преследует две основные цели:
• Определение сравниваемого PK-профиля DIM в плазме крови после однократной пероральной дозы 90 мг DIM по сравнению с однократной сублингвальной дозой 90 мг DIM. Оба состава будут содержать в общей сложности 800 мкг эквивалентов активности ретинола (RAE) или RE витамина А.
• Оценка сравниваемого PK-профиля DIM в плазме крови после суточного введения 90 мг, принимаемых в виде 2 капсул, введенных b.i.d., и дозы 90 мг сублингвальной формы DIM, принимаемой в виде 1 пастилки b.i.d. в течение 14 дней. Оба состава будут содержать в общей сложности 800 мкг RE.
ДИЗАЙН ИССЛЕДОВАНИЯ
[0118] Речь пойдет об открытом, рандомизированном, перекрестном исследовании с двумя последовательностями. Набор участников будет продолжаться до тех пор, пока 10 лиц мужского пола и 10 лиц женского пола не завершат обе части оценки PK исследования.
[0119] Завершивший исследование участник определяется как участник исследования, который получил как однократные, так и многократные дозы пероральных и сублингвальных составов, и который завершил все требуемые процедуры оценок. Участники исследования будут проходить период вымывания от 1 до 3 недель после завершения одной части и перед началом следующей.
[0120] Все участники исследования завершат два лечения: Часть 1, введение однократных (а) и многократных (b) пероральных доз, и Часть 2, введение однократных (а) и многократных (b) сублингвальных доз. Каждое лечение будет сопровождаться периодом вымывания по меньшей мере 7 дней. Участники исследования будут рандомизированы в соответствии с тем, какую последовательность лечения они получают. Все участники исследования будут выбраны случайным образом для первичного набора либо в часть 1, либо в часть 2 исследования, то есть для начала либо с перорального состава 1 (часть 1), либо с сублингвального состава 1 (часть 2); все участники исследования будут проходить набор в обе части исследования.
СХЕМА ПРИМЕНЕНИЯ
[0121] Часть 1а. Все участники исследования в первый день, после ночного голодания (по меньшей мере 8 часов), будут получать однократную пероральную дозу (4 капсулы) 90 мг DIM+800 мкг эквивалентов ретинола (RE), пероральный состав 1. В пределах 24-часового периода будут собраны образцы крови (0, (перед введением дозы), 0,5, 1, 1,5, 2, 3, 4, 6, 9, 12 и 24 ч) и мочи (0, (перед введением дозы), 0-4, 4-8 и 12-24 ч) в течение этого 24-часового периода. Уровни DIM, определяемые с применением утвержденного анализа, будут определены в плазме крови с целью определения PK-профиля DIM; уровни DIM в образцах мочи также будут определены.
[0122] Часть 1b. По истечении минимум 7-дневного периода вымывания пероральный состав 1 будет приниматься ежесуточно утром в виде двух капсул b.i.d. после ночного голодания (по меньшей мере 8 часов) и перед ночным сном (после голодания в течение по меньшей мере 3 часов) в течение 13 дней (эта доза является эквивалентной однократной пероральной дозе, используемой в части 1а). В день 14 участники исследования будут получать их последнюю дозу утром после ночного голодания. После этого будет проведен забор крови и сбор мочи, как описано в части 1а. На следующий день (день 15) после последней дозы (утром дня 14) у участников исследования один раз будут брать кровь (образец крови к 24 часу), и они должны будут предоставить 12-24-часовой образец мочи. Будут оценивать PK-профиль DIM в равновесном состоянии в плазме крови; также будут определять уровни DIM в образцах мочи.
[0123] Промежуток времени между периодами лечения частей 1 и 2 будет составлять минимум 7 дней.
[0124] Часть 2а. Однократную дозу (2 пастилки) сублингвального состава Сублингвальный Состав 1, содержащего одинаковые концентрации DIM и RE, как и для пероральной дозы (Пероральный Состав 1), будут давать после ночного голодания в течение по меньшей мере 8 часов, после чего будут брать и оценивать образцы крови и мочи за 24-часовой период, как описано в части 1а.
[0125] Часть 2b. По истечении минимум 7-дневного периода вымывания сублингвальный состав 1 будет приниматься ежесуточно в виде двух введений (одна пастилка b.i.d) утром после ночного голодания (по меньшей мере 8 часов) и перед ночным сном (после голодания в течение по меньшей мере 3 часов) в течение 13 дней. Суточная доза будет эквивалентной однократной дозе, используемой в части 2а. В день 14 участники исследования будут получать их утреннюю дозу после ночного голодания (по меньшей мере 8 часов). После этого будет проведен забор крови и сбор мочи, как описано в части 1а. На следующий день (день 15) после последней дозы (утром дня 14) у участников исследования один раз будут брать кровь (образец крови к 24 часу) и они предоставят 12-24-часовой образец мочи. Будут оценивать PK-профиль DIM в равновесном состоянии в плазме крови. Также будут определять уровни DIM в образцах мочи.
[0126] Кроме того, для каждого периода лечения образцы мочи будут предоставлены в день 1 перед первой дозой и в день 14 для оценки уровней котинина в моче и DIM, полученного из рациона. Также до набора и перед началом каждой фазы исследования будут проводить оценку с использованием алкометра на алкоголь. После завершения интервенционного исследования участники исследования с текущими нежелательными эффектами (АЕ) будут находиться под наблюдением в течение по меньшей мере 1 недели для регистрации каких-либо наблюдаемых АЕ или до момента устранения АЕ, по мере клинической целесообразности по мнению врача-исследователя.
[0127] Участники заполнят 3-дневный дневник питания в начале и конце части В для обеих частей 1 и 2.
ВЫБОР УЧАСТНИКОВ ИССЛЕДОВАНИЯ
[0128] А. Критерии включения
1. Здоровые лица мужского и женского пола в возрасте 18-35 лет на момент скрининга.
2. Некурящий, что подтверждено в анализе мочи на котинин, и не потреблявший продукты с содержанием никотина (или продукты, заменяющие никотин) в течение предшествующих 6 месяцев до скрининга.
3. Гемоглобин: лица мужского пола: 130-180 г/л; лица женского пола: 115-165 г/л.
4. Количество лейкоцитов: 4,0-11,0×109/л.
5. Креатинин: лица мужского пола 64-104 мкмоль/л; лица женского пола 49-90 мкмоль/л.
6. eGFR >60 мл/мин/1,73 м2.
7. Альбумин 35-50 г/л.
8. Билирубин в пределах верхней границы нормального диапазона (ULN).
9. AST и ALT в пределах верхней границы нормального диапазона (ULN).
10. Щелочная фосфатаза 30-130 МЕ/л.
11. Индекс массы тела >20 и <25.
12. Отсутствие серьезных, острых, нестабильных, хронических или рецидивирующих патологических состояний.
13. Соглашение на воздержание от употребления овощей семейства Крестоцветные в пределах 2 недель до и после и в ходе периода исследования, что подтверждается в анализе мочи на наличие DIM или I3С (индол-3-карбинол). Овощи семейства Крестоцветные включают брокколи, кочанную капусту (включая капустный салат), цветную капусту, бок-чой, брюссельскую капусту, капусту листовую, кудрявую капусту, кольраби, салатную горчицу, брюкву, кормовую репу и жеруху обыкновенную.
14. Участники исследования должны воздерживаться от употребления грейпфрута или грейпфрутового сока в течение двух недель до включения в исследование и на протяжении всего исследования. Другие пищевые добавки должны быть исключены на время исследования.
15. Отсутствие серьезных форм аллергии на лекарственные средства или другие формы непереносимости или аллергии, что определяет исследователь (сезонная аллергия в легкой форме допускается).
16. Отсутствие хронических состояний, включая головные боли, дисфорию, синдром хронической усталости, головокружение, размытое зрение, бессонницу, ринорею, тошноту, рвоту, боль в животе, диарею, запор, климактерические приливы/ночную потливость или клинически значимый предменструальный синдром.
17. Отсутствие необходимости в постоянном лечении лекарственными средствами.
18. Отсутствие употребления алкоголя в пределах 48 часов предусмотренных исследованием визитов.
19. Отсутствие предшествующей химиотерапии.
20. Отсутствие приема сопутствующих регулярных лекарственных препаратов или каких-либо недавних изменений в отношении лекарственных препаратов или дозировки лекарственных препаратов или гормонов, кроме гормональной контрацепции.
21. Отсутствие приема сопутствующих пищевых добавок или витаминов.
22. Если участники исследования пьют кофе, их ежедневное употребление не должно превышать 500 мг кофеина в сутки. Если этот критерий удовлетворяется, то требуется, чтобы питейные привычки (число или крепость кофейных напитков) не менялись в течение 2 недель до и в ходе исследования.
23. Если в исследование зачислен участник женского пола, принимающий комбинированный оральный контрацептив, ожидается, что как доза, так и состав этого контрацептива останутся постоянными (оральные контрацептивы или имплантаты на основе только прогестогена не допускаются).
24. Доступен для посещения, визитов в ходе всего исследования.
[0129] В. Критерии исключения
1. Участники исследования, которые сообщают о получении какого-либо исследуемого лекарственного средства в течение 3 месяцев до начала исследования.
2. Участники исследования, которые сообщают о каком-либо наличии или присутствии в анамнезе клинически значимого нарушения, включающего заболевание сердечно-сосудистой системы, респираторной системы, почек, желудочно-кишечного тракта, иммунной системы, заболевание крови, заболевание эндокринной или нервной системы (систем) или психическое заболевание, как определено врачом(-ами)-исследователем(-ями).
3. Участники исследования, значения клинико-лабораторных исследований у которых выходят за пределы приемлемого диапазона нормы (верхняя граница нормального диапазона (ULN)).
4. Участники исследования, у которых наблюдается реакция на поверхностный антиген вируса гепатита В, наличие антитела к вирусу гепатита С или антитела к ВИЧ.
5. Участники исследования женского пока, которые являются беременными, зачали ребенка и являются лактирующими, или которые обладают репродуктивным потенциалом, и которые не дают согласие на использование или продление использования стандартных способов контрацепции в ходе всего исследования.
6. Участники исследования, которые сообщают о случаях в истории болезни аллергического(-их) ответа(-ов) на какой-либо из ингредиентов в тестируемых составах или его компоненты.
7. Участники исследования, которые сообщают о применении каких-либо системных рецептурных лекарственных препаратов за 14 дней до введения дозы, которые были исключены (комбинированные оральные контрацептивы, гиполипидемические и антигипертензивные лекарственные препараты допускаются).
8. Участники исследования, которые сообщают о применении какого-либо из безрецептурных (ОТС) лекарственных препаратов (за исключением низких доз аспирина и парацетамола) за 3 дня до введения дозы.
9. Участники исследования, которые сообщают о клинически значимой болезни в течение 4 недель до введения дозы или о любом состоянии, которое, по мнению исследователя, негативно влияет на возможность участника исследования соответствовать требованиям протокола или завершить исследование.
10. Участники исследования, которые сообщают о случаях в истории болезни наркотической или алкогольной зависимости или злоупотребления в течение прошлого года.
11. Участники исследования, у которых наблюдается положительный результат пробы на алкоголь в выдыхаемом воздухе.
12. Участники исследования, у которых наблюдается положительный результат в тесте на употребление наркотиков.
13. Участники исследования, которые сообщают о сдаче более 150 мл крови в течение 28 дней до введения дозы. Всем участникам исследования будет рекомендовано не сдавать кровь в течение четырех недель после завершения исследования.
14. Участники исследования, которые сообщают о сдаче плазмы крови (например, плазмаферез) в пределах 14 дней до введения дозы. Всем участникам исследования будет рекомендовано не сдавать плазму крови в течение четырех недель после завершения исследования.
15. Участники исследования, которые сообщают о чрезмерных желудочно-кишечных расстройствах (например, диарея, запор, тошнота, рвота).
16. Любое состояние, которое, по мнению исследователя, негативно влияет на возможность участника исследования соответствовать требованиям протокола или завершить исследование.
ФАРМАКОКИНЕТИЧЕСКИЙ АНАЛИЗ
[0130] Соответствующий пакет обработки PK-данных (например, WinNonlin, ex. Pharsight) будут использовать с целью получения полного PK-профиля DIM в плазме крови на протяжении периода исследования. Переменные, которые будут определять, представляют собой первичные и производные PK-параметры: Cmax, Tmax, kelim, t1/2, AUC0-t, AUC0-inf. Относительная биодоступность: FСУБЛИНГВАЛЬНО/FПЕРОРАЛЬНО (Fсл/Fпeр) будет определено из отношения: (АUСсл/АUСпер)*(Дозапер/Дозасл). Значения будут определять для каждой лекарственной формы после введения однократной (конец дня 1) и многократных доз (конец дня 15), и соответствующие сравнительные оценки будут выполнять для двух лекарственных форм.
Пример 7. Сублингвальное введение обеспечивает повышение максимальной концентрации в плазме крови (Cmax) и биодоступности (AUC) DIM в плазме крови.
[0131] Целью этого исследования являлось определение фармакокинетического (PK) профиля состава на основе дииндолилметана (DIM) в плазме крови после однократных и многократных доз DIM, введенных либо посредством сублингвального пути, либо посредством перорального пути. Состав на основе DIM для этого исследования представлял собой иллюстративный состав, синтезированный и приготовленный с применением описанных выше способов.
[0132] Участники исследования были распределены в (а) группу 1: DIM вводили посредством перорального пути, и (b) группу 2: DIM вводили посредством сублингвального пути.
[0133] Результаты. Фармакокинетические параметры состава на основе DIM в плазме крови после однократной пероральной или сублингвальной дозы.
[0134] Участники исследования были разделены на две группы, и им вводили, перорально и сублингвально соответственно, однократную дозу 90 мг состава на основе DIM в форме 4 капсул. Эти участники исследования ранее не подвергались воздействию DIM, и, следовательно, являются субъектами, которые не получали лечение. Наблюдали, что средняя Cmax в случае сублингвального введения составляла 38 нг/мл, тогда как в случае пероральной дозы она составляла приблизительно 15 нг/мл, как показано на Фиг. 1. Таким образом, Cmax в случае сублингвального введения DIM была в приблизительно 2,5 раза, или на приблизительно 40% выше, чем в случае перорального введения. Биодоступность DIM выводили из значений AUC после однократной дозы 90 мг, сублингвально или перорально, у субъектов, которые не получали лечение. Как можно видеть из графика на фиг. 1, AUC у субъектов, которые не получали лечение, была в приблизительно 2 раза выше после сублингвального введения, по сравнению с пероральным введением.
[0135] Результаты. Фармакокинетический профиль однократной дозы DIM, пероральной или сублингвальной, после ежесуточного введения дозы в течение 14 дней.
[0136] Участники исследования были разделены на две группы. В одной группе вводили суточную пероральную дозу 90 мг DIM в дни 1-14, а в другой группе вводили суточную сублингвальную дозу 90 мг DIM в дни 1-14. Дозы DIM 90 мг вводили как 45 мг утром (2 капсулы) и 45 мг вечером (2 капсулы). В день 15 однократную пероральную дозу 45 мг DIM вводили группе с пероральным введением и однократную сублингвальную дозу 45 мг DIM вводили группе с сублингвальным введением, с последующим сбором крови и других биологических образцов, таких как моча, для фармакокинетических анализов. Фармакокинетические параметры измеряли последовательно. Было обнаружено, что после введения однократной сублингвальной дозы 45 мг DIM субъектам, подвергавшимся воздействию DIM, т.е. спустя 14 дней ежесуточного введения сублингвальной дозы, среднее значение Cmax составляло приблизительно 9 нг/мл. Также было обнаружено, что после введения однократной пероральной дозы 45 мг DIM субъектам, подвергавшимся воздействию DIM, спустя 14 дней ежесуточного введения пероральной дозы, среднее значение Cmax DIM составляло приблизительно 6 нг/мл. Результаты представлены на графике, показанном на фиг. 2.
[0137] Краткое изложение результатов статистических анализов для значений Cmax и AUC после однократных доз представлено в таблицах 1 и 2. Было обнаружено, что пиковая концентрация в плазме крови DIM является более высокой после введения как однократных, так и многократных доз для сублингвального пути, по сравнению с пероральным.
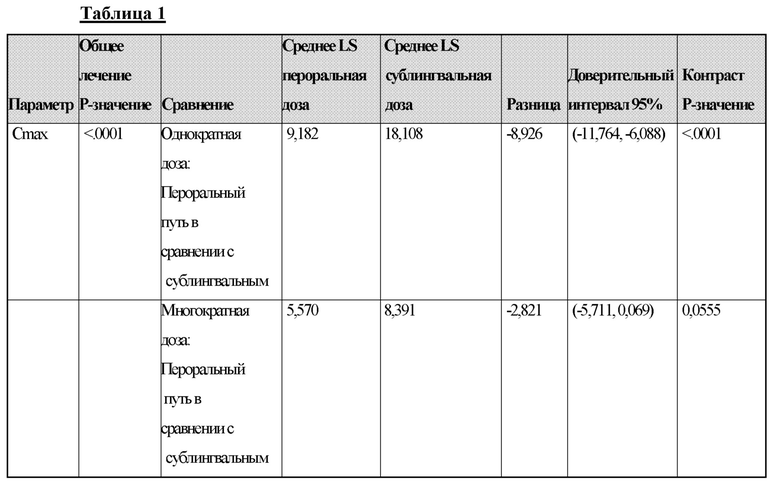
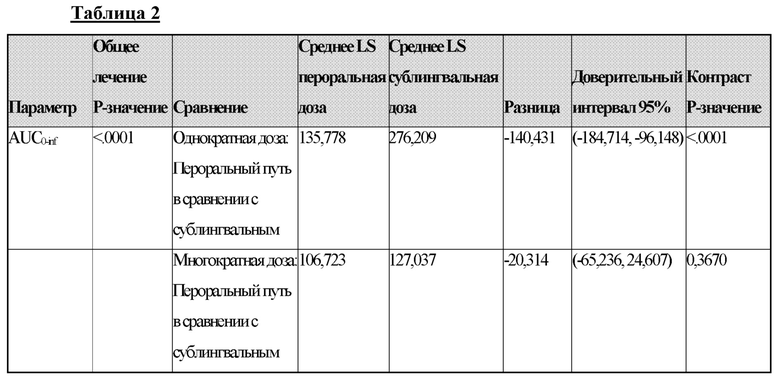
Определенные варианты осуществления
[0138] Вариант осуществления 1 относится к способу лечения акне у нуждающегося в этом субъекта, предусматривающему введение субъекту композиции, содержащей замещенный или незамещенный дииндолилметан, где композицию вводят посредством сублингвального или буккального пути.
[0139] Вариант осуществления 2 относится к способу согласно варианту осуществления 1, где композиция дополнительно содержит замещенный или незамещенный компонент на основе ретиноевой кислоты.
[0140] Вариант осуществления 3 относится к способу согласно варианту осуществления 2, где компонент на основе ретиноевой кислоты представляет собой витамин А.
[0141] Вариант осуществления 4 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0142] Вариант осуществления 5 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 1 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0143] Вариант осуществления 6 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 2 раза по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0144] Вариант осуществления 7 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 3 раза по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0145] Вариант осуществления 8 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 4 раза по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0146] Вариант осуществления 9 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 5 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0147] Вариант осуществления 10 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 10 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0148] Вариант осуществления 11 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 20 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0149] Вариант осуществления 12 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 30 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0150] Вариант осуществления 13 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 40 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0151] Вариант осуществления 14 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 50 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0152] Вариант осуществления 15 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 60 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0153] Вариант осуществления 16 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 70 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0154] Вариант осуществления 17 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 80 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0155] Вариант осуществления 18 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 100 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0156] Вариант осуществления 19 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 200 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0157] Вариант осуществления 20 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 300 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0158] Вариант осуществления 21 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 400 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0159] Вариант осуществления 22 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 500 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0160] Вариант осуществления 23 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 600 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0161] Вариант осуществления 24 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 700 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0162] Вариант осуществления 25 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 800 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0163] Вариант осуществления 26 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 900 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0164] Вариант осуществления 27 относится к способу согласно любому из вариантов осуществления 1-3, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 1000 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0165] Вариант осуществления 28 относится к способу согласно любому из вариантов осуществления 4-27, где биодоступность замещенного или незамещенного дииндолилметана измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0166] Вариант осуществления 29 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0167] Вариант осуществления 30 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 2 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0168] Вариант осуществления 31 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 3 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0169] Вариант осуществления 32 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 4 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0170] Вариант осуществления 33 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 5 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0171] Вариант осуществления 34 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 10 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0172] Вариант осуществления 35 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 20 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0173] Вариант осуществления 36 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 30 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0174] Вариант осуществления 37 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 40 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0175] Вариант осуществления 38 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 50 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0176] Вариант осуществления 39 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 60 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0177] Вариант осуществления 40 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 70 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0178] Вариант осуществления 41 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 80 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0179] Вариант осуществления 42 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 90 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0180] Вариант осуществления 43 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 100 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0181] Вариант осуществления 44 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 200 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0182] Вариант осуществления 45 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 300 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0183] Вариант осуществления 46 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 400 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0184] Вариант осуществления 47 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 500 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0185] Вариант осуществления 48 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 600 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0186] Вариант осуществления 49 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 700 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0187] Вариант осуществления 50 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 800 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0188] Вариант осуществления 51 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 900 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0189] Вариант осуществления 52 относится к способу согласно любому из вариантов осуществления 1-28, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 1000 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0190] Вариант осуществления 53 относится к способу согласно любому из вариантов осуществления 29-52, где Cmax замещенного или незамещенного дииндолилметана в плазме крови измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0191] Вариант осуществления 54 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0192] Вариант осуществления 55 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 2 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0193] Вариант осуществления 56 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 3 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0194] Вариант осуществления 57 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 4 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0195] Вариант осуществления 58 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 5 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0196] Вариант осуществления 59 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 6 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0197] Вариант осуществления 60 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 7 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0198] Вариант осуществления 61 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 8 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0199] Вариант осуществления 62 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 9 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0200] Вариант осуществления 63 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 10 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0201] Вариант осуществления 64 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 20 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0202] Вариант осуществления 65 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 30 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0203] Вариант осуществления 66 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 40 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0204] Вариант осуществления 67 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 50 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0205] Вариант осуществления 68 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 60 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0206] Вариант осуществления 69 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 70 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0207] Вариант осуществления 70 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 80 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0208] Вариант осуществления 71 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 90 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0209] Вариант осуществления 72 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 100 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0210] Вариант осуществления 73 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 200 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0211] Вариант осуществления 74 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 300 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0212] Вариант осуществления 75 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 400 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0213] Вариант осуществления 76 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 500 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0214] Вариант осуществления 77 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 600 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0215] Вариант осуществления 78 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 700 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0216] Вариант осуществления 79 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 800 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0217] Вариант осуществления 80 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 900 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0218] Вариант осуществления 81 относится к способу согласно любому из вариантов осуществления 1-53, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 1000 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0219] Вариант осуществления 82 относится к способу согласно любому из вариантов осуществления 54-81, где AUC замещенного или незамещенного дииндолилметана в плазме крови измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0220] Вариант осуществления 83 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0221] Вариант осуществления 84 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 1 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0222] Вариант осуществления 85 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 2 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0223] Вариант осуществления 86 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 3 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0224] Вариант осуществления 87 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 4 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0225] Вариант осуществления 88 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 5 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0226] Вариант осуществления 89 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 10 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0227] Вариант осуществления 90 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 20 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0228] Вариант осуществления 91 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 30 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0229] Вариант осуществления 92 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 40 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0230] Вариант осуществления 93 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 50 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0231] Вариант осуществления 94 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 60 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0232] Вариант осуществления 95 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 70 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0233] Вариант осуществления 96 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 80 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0234] Вариант осуществления 97 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 90 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0235] Вариант осуществления 98 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 100 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0236] Вариант осуществления 99 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 200 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0237] Вариант осуществления 100 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 300 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0238] Вариант осуществления 101 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 400 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0239] Вариант осуществления 102 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 500 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0240] Вариант осуществления 103 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 600 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0241] Вариант осуществления 104 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 700 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0242] Вариант осуществления 105 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 800 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0243] Вариант осуществления 106 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 900 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0244] Вариант осуществления 107 относится к способу согласно любому из вариантов осуществления 1-82, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 1000 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0245] Вариант осуществления 108 относится к способу согласно любому из вариантов осуществления 83-107, где Tmax замещенного или незамещенного дииндолилметана в плазме крови измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0246] Вариант осуществления 109 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0247] Вариант осуществления 110 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,1% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0248] Вариант осуществления 111 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,2% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0249] Вариант осуществления 112 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,3% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0250] Вариант осуществления 113 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,4% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0251] Вариант осуществления 114 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,5% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0252] Вариант осуществления 115 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 1% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0253] Вариант осуществления 116 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 2% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0254] Вариант осуществления 117 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 3% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0255] Вариант осуществления 118 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 4% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0256] Вариант осуществления 119 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 5% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0257] Вариант осуществления 120 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 6% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0258] Вариант осуществления 121 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 7% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0259] Вариант осуществления 122 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 8% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0260] Вариант осуществления 123 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 9% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0261] Вариант осуществления 124 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 10% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0262] Вариант осуществления 125 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 20% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0263] Вариант осуществления 126 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 30% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0264] Вариант осуществления 127 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 40% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0265] Вариант осуществления 128 относится к способу согласно любому из вариантов осуществления 1-108, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 50% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0266] Вариант осуществления 129 относится к способу согласно любому из вариантов осуществления 109-128, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, и процентная доля сравниваемой композиции, выводимой P-gp после перорального введения, рассчитаны исходя из дозы введения, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0267] Вариант осуществления 130 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0268] Вариант осуществления 131 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,1% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0269] Вариант осуществления 132 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,2% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0270] Вариант осуществления 133 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,3% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0271] Вариант осуществления 134 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,4% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0272] Вариант осуществления 135 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,5% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0273] Вариант осуществления 136 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,6% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0274] Вариант осуществления 137 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,7% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0275] Вариант осуществления 138 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,8% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0276] Вариант осуществления 139 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,9% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0277] Вариант осуществления 140 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 1% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0278] Вариант осуществления 141 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 2% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0279] Вариант осуществления 142 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 3% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0280] Вариант осуществления 143 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 4% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0281] Вариант осуществления 144 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 5% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0282] Вариант осуществления 145 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 6% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0283] Вариант осуществления 146 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 7% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0284] Вариант осуществления 147 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 8% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0285] Вариант осуществления 148 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 9% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0286] Вариант осуществления 149 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 10% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0287] Вариант осуществления 150 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 20% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0288] Вариант осуществления 151 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 30% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0289] Вариант осуществления 152 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 40% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0290] Вариант осуществления 153 относится к способу согласно любому из вариантов осуществления 1-129, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 50% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0291] Вариант осуществления 154 относится к способу согласно любому из вариантов осуществления 130-153, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, и процентная доля сравниваемой композиции, поглощаемой ОАТР после перорального введения, рассчитаны исходя из дозы введения, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0292] Вариант осуществления 155 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0293] Вариант осуществления 156 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,1% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0294] Вариант осуществления 157 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,2% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0295] Вариант осуществления 158 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,3% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0296] Вариант осуществления 159 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,4% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0297] Вариант осуществления 160 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,5% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0298] Вариант осуществления 161 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,6% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0299] Вариант осуществления 162 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,7% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0300] Вариант осуществления 163 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,8% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0301] Вариант осуществления 164 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,9% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0302] Вариант осуществления 165 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 1% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0303] Вариант осуществления 166 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 2% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0304] Вариант осуществления 167 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 3% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0305] Вариант осуществления 168 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 4% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0306] Вариант осуществления 169 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 5% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0307] Вариант осуществления 170 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 6% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0308] Вариант осуществления 171 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 7% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0309] Вариант осуществления 172 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 8% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0310] Вариант осуществления 173 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 9% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0311] Вариант осуществления 174 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 10% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0312] Вариант осуществления 175 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 20% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0313] Вариант осуществления 176 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 30% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0314] Вариант осуществления 177 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 40% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0315] Вариант осуществления 178 относится к способу согласно любому из вариантов осуществления 1-154, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0316] Вариант осуществления 179 относится к способу согласно любому из вариантов осуществления 155-178, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, и процентная доля сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, рассчитаны исходя из дозы введения, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0317] Вариант осуществления 180 относится к способу согласно любому из вариантов осуществления 1-179, где композицию вводят в лекарственной форме, которая распадается при помещении в сублингвальное или буккальное пространство.
[0318] Вариант осуществления 181 относится к способу лечения розацеа у нуждающегося в этом субъекта, предусматривающему введение субъекту композиции, содержащей замещенный или незамещенный дииндолилметан, где композицию вводят посредством сублингвального или буккального пути.
[0319] Вариант осуществления 182 относится к способу согласно пункту 181, где композиция дополнительно содержит замещенный или незамещенный компонент на основе ретиноевой кислоты.
[0320] Вариант осуществления 183 относится к способу согласно пункту 182, где компонент на основе ретиноевой кислоты представляет собой витамин А.
[0321] Вариант осуществления 184 относится к способу согласно любому из вариантов осуществления 181-183, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0322] Вариант осуществления 185 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 1 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0323] Вариант осуществления 186 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 2 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0324] Вариант осуществления 187 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 3 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0325] Вариант осуществления 188 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 4 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0326] Вариант осуществления 189 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 5 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0327] Вариант осуществления 190 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 10 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0328] Вариант осуществления 191 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 20 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0329] Вариант осуществления 192 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 30 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0330] Вариант осуществления 193 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 40 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0331] Вариант осуществления 194 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 50 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0332] Вариант осуществления 195 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 60 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0333] Вариант осуществления 196 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 70 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0334] Вариант осуществления 197 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 80 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0335] Вариант осуществления 198 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 100 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0336] Вариант осуществления 199 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 200 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0337] Вариант осуществления 200 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 300 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0338] Вариант осуществления 201 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 400 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0339] Вариант осуществления 202 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 500 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0340] Вариант осуществления 203 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 600 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0341] Вариант осуществления 204 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 700 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0342] Вариант осуществления 205 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 800 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0343] Вариант осуществления 206 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 900 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0344] Вариант осуществления 207 относится к способу согласно любому из вариантов осуществления 181-184, где введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана в приблизительно 1000 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
[0345] Вариант осуществления 208 относится к способу согласно любому из вариантов осуществления 185-207, где биодоступность замещенного или незамещенного дииндолилметана измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0346] Вариант осуществления 209 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0347] Вариант осуществления 210 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 2 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0348] Вариант осуществления 211 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 3 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0349] Вариант осуществления 212 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 4 раза по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0350] Вариант осуществления 213 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 5 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0351] Вариант осуществления 214 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 10 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0352] Вариант осуществления 215 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 20 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0353] Вариант осуществления 216 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 30 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0354] Вариант осуществления 217 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 40 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0355] Вариант осуществления 218 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 50 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0356] Вариант осуществления 219 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 60 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0357] Вариант осуществления 220 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 70 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0358] Вариант осуществления 221 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 80 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0359] Вариант осуществления 222 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 90 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0360] Вариант осуществления 223 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 100 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0361] Вариант осуществления 224 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буквального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 200 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0362] Вариант осуществления 225 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 300 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0363] Вариант осуществления 226 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 400 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0364] Вариант осуществления 227 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 500 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0365] Вариант осуществления 228 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 600 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0366] Вариант осуществления 229 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 700 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0367] Вариант осуществления 230 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 800 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0368] Вариант осуществления 231 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 900 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0369] Вариант осуществления 232 относится к способу согласно любому из вариантов осуществления 181-208, где после введения композиции посредством сублингвального или буккального пути Cmax замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 1000 раз по сравнению с Cmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0370] Вариант осуществления 233 относится к способу согласно любому из вариантов осуществления 209-232, где Cmax замещенного или незамещенного дииндолилметана в плазме крови измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0371] Вариант осуществления 234 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0372] Вариант осуществления 235 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 2 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0373] Вариант осуществления 236 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 3 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0374] Вариант осуществления 237 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 4 раза по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0375] Вариант осуществления 238 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 5 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0376] Вариант осуществления 239 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 6 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0377] Вариант осуществления 240 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 7 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0378] Вариант осуществления 241 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 8 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0379] Вариант осуществления 242 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 9 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0380] Вариант осуществления 243 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 10 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0381] Вариант осуществления 244 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 20 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0382] Вариант осуществления 245 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 30 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0383] Вариант осуществления 246 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 40 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0384] Вариант осуществления 247 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 50 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0385] Вариант осуществления 248 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 60 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0386] Вариант осуществления 249 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 70 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0387] Вариант осуществления 250 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 80 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0388] Вариант осуществления 251 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 90 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0389] Вариант осуществления 252 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 100 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0390] Вариант осуществления 253 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буквального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 200 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0391] Вариант осуществления 254 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 300 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0392] Вариант осуществления 255 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 400 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0393] Вариант осуществления 256 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 500 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0394] Вариант осуществления 257 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 600 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0395] Вариант осуществления 258 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 700 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0396] Вариант осуществления 259 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 800 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0397] Вариант осуществления 260 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 900 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0398] Вариант осуществления 261 относится к способу согласно любому из вариантов осуществления 181-233, где после введения композиции посредством сублингвального или буккального пути AUC замещенного или незамещенного дииндолилметана в плазме крови повышается в приблизительно 1000 раз по сравнению с AUC после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0399] Вариант осуществления 262 относится к способу согласно любому из вариантов осуществления 234-261, где AUC замещенного или незамещенного дииндолилметана в плазме крови измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0400] Вариант осуществления 263 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается с кратностью от приблизительно 1 раза до приблизительно 1000 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0401] Вариант осуществления 264 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 1 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0402] Вариант осуществления 265 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 2 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0403] Вариант осуществления 266 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 3 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0404] Вариант осуществления 267 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 4 раза по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0405] Вариант осуществления 268 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 5 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0406] Вариант осуществления 269 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 10 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0407] Вариант осуществления 270 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 20 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0408] Вариант осуществления 271 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 30 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0409] Вариант осуществления 272 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 40 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0410] Вариант осуществления 273 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 50 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0411] Вариант осуществления 274 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 60 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0412] Вариант осуществления 275 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 70 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0413] Вариант осуществления 276 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 80 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0414] Вариант осуществления 277 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 90 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0415] Вариант осуществления 278 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 100 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0416] Вариант осуществления 279 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 200 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0417] Вариант осуществления 280 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 300 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0418] Вариант осуществления 281 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 400 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0419] Вариант осуществления 282 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буквального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 500 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0420] Вариант осуществления 283 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 600 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0421] Вариант осуществления 284 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 700 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0422] Вариант осуществления 285 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 800 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0423] Вариант осуществления 286 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 900 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0424] Вариант осуществления 287 относится к способу согласно любому из вариантов осуществления 181-262, где после введения композиции посредством сублингвального или буккального пути Tmax замещенного или незамещенного дииндолилметана в плазме крови снижается в приблизительно 1000 раз по сравнению с Tmax после введения сравниваемой композиции посредством перорального пути при такой же доставляемой дозе.
[0425] Вариант осуществления 288 относится к способу согласно любому из вариантов осуществления 263-287, где Tmax замещенного или незамещенного дииндолилметана в плазме крови измеряют после введения дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0426] Вариант осуществления 289 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0427] Вариант осуществления 290 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,1% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0428] Вариант осуществления 291 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,2% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0429] Вариант осуществления 292 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,3% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0430] Вариант осуществления 293 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,4% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0431] Вариант осуществления 294 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 0,5% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0432] Вариант осуществления 295 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 1% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0433] Вариант осуществления 296 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 2% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0434] Вариант осуществления 297 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 3% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0435] Вариант осуществления 298 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 4% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0436] Вариант осуществления 299 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 5% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буквальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0437] Вариант осуществления 300 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 6% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0438] Вариант осуществления 301 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 7% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0439] Вариант осуществления 302 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 8% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0440] Вариант осуществления 303 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 9% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0441] Вариант осуществления 304 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 10% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0442] Вариант осуществления 305 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 20% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0443] Вариант осуществления 306 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 30% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0444] Вариант осуществления 307 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 40% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0445] Вариант осуществления 308 относится к способу согласно любому из вариантов осуществления 181-288, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет приблизительно 50% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0446] Вариант осуществления 309 относится к способу согласно любому из вариантов осуществления 289-308, где процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, и процентная доля сравниваемой композиции, выводимой P-gp после перорального введения, рассчитаны исходя из дозы введения, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0447] Вариант осуществления 310 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0448] Вариант осуществления 311 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буквального введения, составляет приблизительно 0,1% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0449] Вариант осуществления 312 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,2% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0450] Вариант осуществления 313 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,3% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0451] Вариант осуществления 314 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,4% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0452] Вариант осуществления 315 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,5% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0453] Вариант осуществления 316 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,6% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0454] Вариант осуществления 317 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,7% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0455] Вариант осуществления 318 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,8% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0456] Вариант осуществления 319 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 0,9% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0457] Вариант осуществления 320 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 1% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0458] Вариант осуществления 321 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 2% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0459] Вариант осуществления 322 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 3% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буквальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0460] Вариант осуществления 323 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 4% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0461] Вариант осуществления 324 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 5% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0462] Вариант осуществления 325 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 6% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0463] Вариант осуществления 326 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 7% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0464] Вариант осуществления 327 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 8% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0465] Вариант осуществления 328 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 9% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0466] Вариант осуществления 329 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 10% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0467] Вариант осуществления 330 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 20% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0468] Вариант осуществления 331 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 30% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0469] Вариант осуществления 332 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 40% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0470] Вариант осуществления 333 относится к способу согласно любому из вариантов осуществления 181-309, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет приблизительно 50% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0471] Вариант осуществления 334 относится к способу согласно любому из вариантов осуществления 310-333, где процентная доля композиции, поглощаемой ОАТР после сублингвального или буквального введения, и процентная доля сравниваемой композиции, поглощаемой ОАТР после перорального введения, рассчитаны исходя из дозы введения, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0472] Вариант осуществления 335 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0473] Вариант осуществления 336 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,1% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0474] Вариант осуществления 337 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,2% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0475] Вариант осуществления 338 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,3% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0476] Вариант осуществления 339 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,4% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0477] Вариант осуществления 340 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,5% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0478] Вариант осуществления 341 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,6% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0479] Вариант осуществления 342 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,7% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0480] Вариант осуществления 343 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,8% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0481] Вариант осуществления 344 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 0,9% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0482] Вариант осуществления 345 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 1% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0483] Вариант осуществления 346 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 2% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0484] Вариант осуществления 347 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 3% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0485] Вариант осуществления 348 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 4% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0486] Вариант осуществления 349 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 5% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0487] Вариант осуществления 350 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 6% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0488] Вариант осуществления 351 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 7% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0489] Вариант осуществления 352 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 8% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0490] Вариант осуществления 353 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 9% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0491] Вариант осуществления 354 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 10% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0492] Вариант осуществления 355 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 20% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0493] Вариант осуществления 356 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 30% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0494] Вариант осуществления 357 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 40% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0495] Вариант осуществления 358 относится к способу согласно любому из вариантов осуществления 181-334, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
[0496] Вариант осуществления 359 относится к способу согласно любому из вариантов осуществления 335-358, где процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, и процентная доля сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, рассчитаны исходя из дозы введения, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
[0497] Вариант осуществления 360 относится к способу согласно любому из вариантов осуществления 181-359, где композицию вводят в лекарственной форме, которая распадается при помещении в сублингвальное или буккальное пространство.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ КОЖНЫХ ЗАБОЛЕВАНИЙ | 2018 |
|
RU2775974C2 |
| НОВЫЕ КОМПОЗИЦИИ И СПОСОБЫ | 2018 |
|
RU2767410C2 |
| КОМПОЗИЦИИ ДЛЯ ВВЕДЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2009 |
|
RU2554814C2 |
| КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ДИИНДОЛИЛМЕТАН И РЕТИНОИД ДЛЯ ЛЕЧЕНИЯ КОЖНОЙ ПАТОЛОГИИ | 2012 |
|
RU2619851C2 |
| СОСТАВ ДЛЯ ИНГИБИРОВАНИЯ ОБРАЗОВАНИЯ АГОНИСТОВ 5-HT2B И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2017 |
|
RU2746000C2 |
| ТРАНСДЕРМАЛЬНАЯ СИСТЕМА ДОСТАВКИ ДОНЕПЕЗИЛА | 2017 |
|
RU2779471C2 |
| СПОСОБЫ ЛЕЧЕНИЯ БОЛЕЗНИ ГОШЕ | 2018 |
|
RU2781242C2 |
| ПРОИЗВОДНЫЕ ЭФИРОВ ФОСФОНОВЫХ КИСЛОТ И СПОСОБЫ ИХ СИНТЕЗА | 2011 |
|
RU2581045C2 |
| КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ДИИНДОЛИЛМЕТАН И РЕТИНОИД ДЛЯ ЛЕЧЕНИЯ КОЖНОЙ ПАТОЛОГИИ | 2012 |
|
RU2779195C2 |
| ОРОМУКОЗНЫЕ НАНОВОЛОКОННЫЕ НОСИТЕЛИ ДЛЯ ТЕРАПЕВТИЧЕСКОГО ЛЕЧЕНИЯ | 2017 |
|
RU2751508C2 |
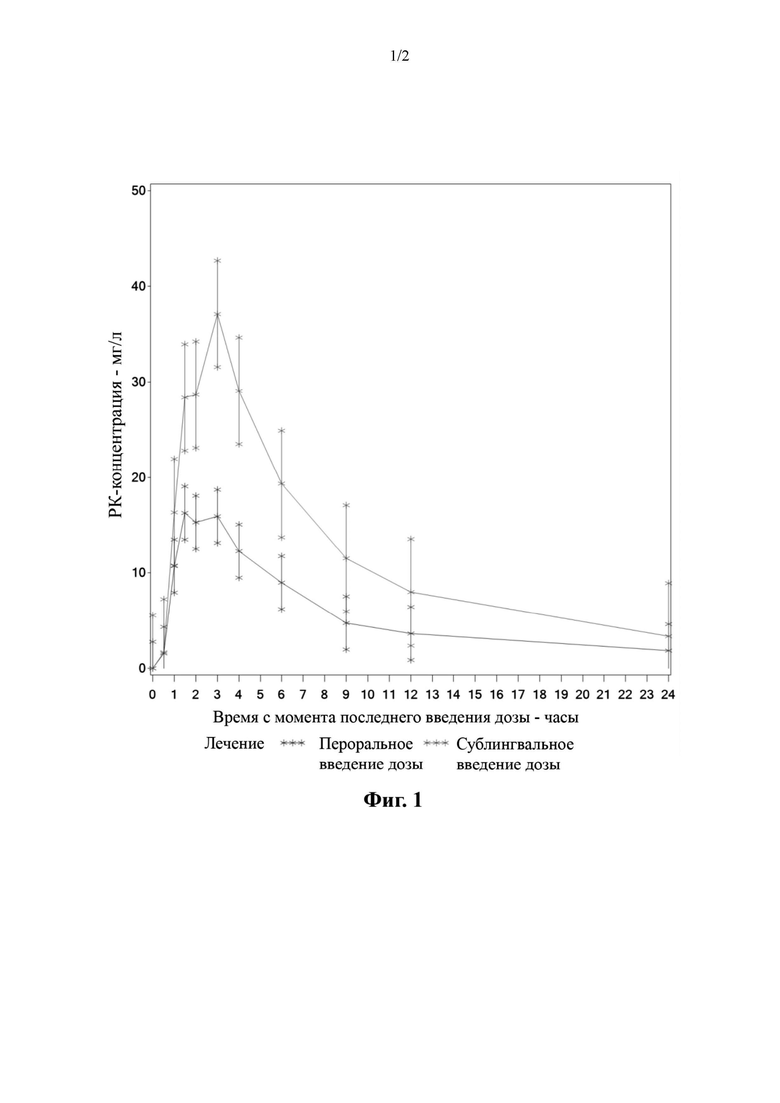
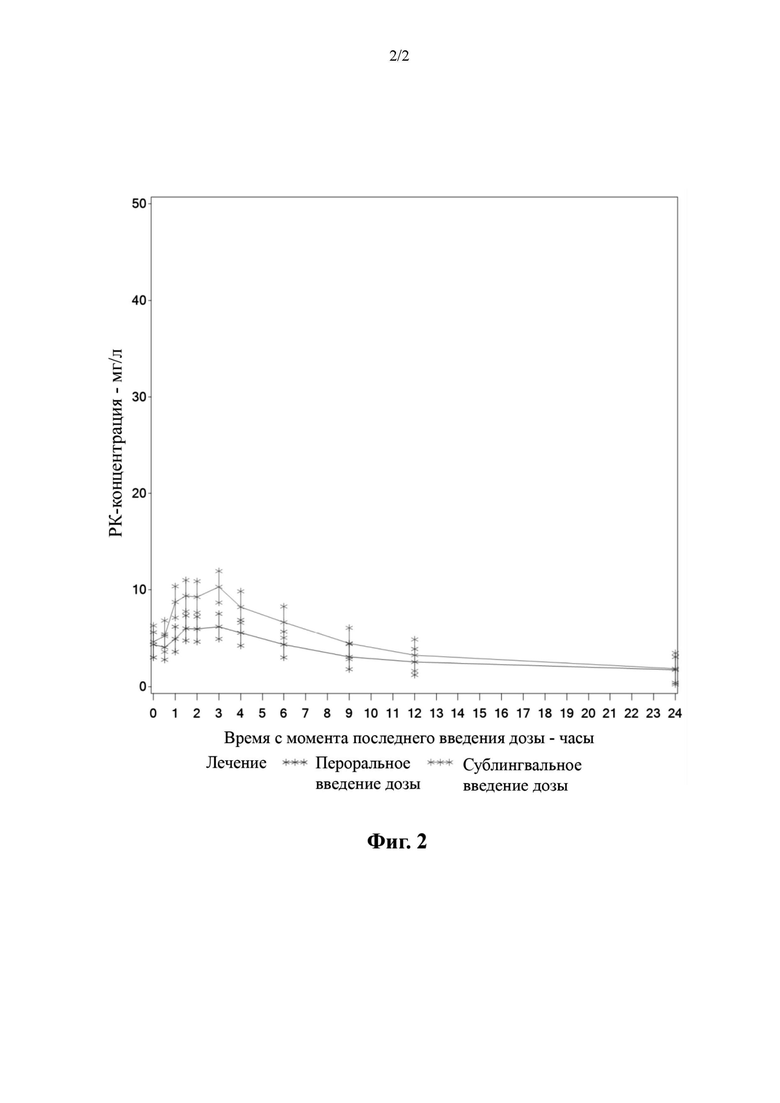
Группа изобретения относится к лечению кожных заболеваний. Способ лечения акне у субъекта, нуждающегося в этом, включает введение субъекту композиции, содержащей замещенный или незамещенный дииндолилметан, где композицию вводят посредством сублингвального или буккального пути. Также раскрыт способ лечения розацеа у субъекта, нуждающегося в этом. Группа изобретений обеспечивает улучшение биодоступности и фармакокинетических параметров замещенного или незамещенного дииндолилметана после сублингвального или буккального введения в сравнении с пероральным введением. 2 н. и 28 з.п. ф-лы, 2 табл., 7 пр., 2 ил.
1. Способ лечения акне у субъекта, нуждающегося в этом, включающий введение субъекту композиции, содержащей замещенный или незамещенный дииндолилметан, где композицию вводят посредством сублингвального или буккального пути.
2. Способ по п. 1, в котором композиция дополнительно содержит замещенный или незамещенный компонент на основе ретиноевой кислоты.
3. Способ по п. 2, в котором компонент на основе ретиноевой кислоты представляет собой витамин А.
4. Способ по п. 1, в котором композиция дополнительно содержит пальмитат витамина А.
5. Способ по п. 1, в котором введение композиции посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
6. Способ по п. 1, в котором после введения композиции посредством сублингвального или буккального пути происходит повышение Cmax замещенного или незамещенного дииндолилметана в плазме крови с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с Cmax замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
7. Способ по п. 1, в котором после введения композиции посредством сублингвального или буккального пути происходит повышение AUC замещенного или незамещенного дииндолилметана в плазме крови с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с AUC замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
8. Способ по п. 1, в котором после введения композиции посредством сублингвального или буккального пути происходит снижение Tmax замещенного или незамещенного дииндолилметана в плазме крови с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с Tmax замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
9. Способ по п. 1, в котором процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
10. Способ по п. 1, в котором процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
11. Способ по п. 1, в котором процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
12. Способ по п. 1, в котором композицию вводят в лекарственной форме, которая распадается при помещении в сублингвальное или буккальное пространство.
13. Способ по п. 1, в котором по меньшей мере один параметр, выбранный из биодоступности, Cmax, AUC, Tmax, процентной доли композиции, выводимой P-gp, процентной доли композиции, поглощаемой ОАТР, и процентной доли композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6, измеряют после введения однократной дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
14. Способ по п. 13, в котором однократной дозе, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана, предшествует ежесуточное введение по меньшей мере 15 мг замещенного или незамещенного дииндолилметана в течение по меньшей мере 14 дней.
15. Способ по п. 14, в котором Cmax замещенного или незамещенного дииндолилметана в плазме крови является более высокой, с кратностью от приблизительно 1 раза до приблизительно 50 раз, по сравнению с Cmax замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути, где Cmax сравниваемой композиции измеряют после введения однократной дозы, содержащей по меньшей мере 15 мг сравниваемой композиции, которой предшествует ежесуточное введение по меньшей мере 15 мг сравниваемой композиции в течение по меньшей мере 14 дней.
16. Способ лечения розацеа у субъекта, нуждающегося в этом, включающий введение субъекту композиции, содержащей замещенный или незамещенный дииндолилметан, где композицию вводят посредством сублингвального или буккального пути.
17. Способ по п. 16, в котором композиция дополнительно содержит замещенный или незамещенный компонент на основе ретиноевой кислоты.
18. Способ по п. 17, в котором компонент на основе ретиноевой кислоты представляет собой витамин А.
19. Способ по п. 16, в котором композиция дополнительно содержит пальмитат витамина А.
20. Способ по п. 16, в котором введение посредством сублингвального или буккального пути обеспечивает повышение биодоступности замещенного или незамещенного дииндолилметана с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с биодоступностью замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
21. Способ по п. 16, в котором после введения композиции посредством сублингвального или буккального пути происходит повышение Сmах замещенного или незамещенного дииндолилметана в плазме крови с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с Cmax замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
22. Способ по п. 16, в котором после введения композиции посредством сублингвального или буккального пути происходит повышение AUC замещенного или незамещенного дииндолилметана в плазме крови с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с AUC замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
23. Способ по п. 16, в котором после введения композиции посредством сублингвального или буккального пути происходит снижение Tmax замещенного или незамещенного дииндолилметана в плазме крови с кратностью от приблизительно 1 раза до приблизительно 50 раз по сравнению с Tmax замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути при такой же доставляемой дозе.
24. Способ по п. 16, в котором процентная доля композиции, выводимой P-gp после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, выводимой P-gp после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
25. Способ по п. 16, в котором процентная доля композиции, поглощаемой ОАТР после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, поглощаемой ОАТР после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
26. Способ по п. 16, в котором процентная доля композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после сублингвального или буккального введения, составляет от приблизительно 0,1% до приблизительно 50% процентной доли сравниваемой композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6 после перорального введения, где сублингвальные или буккальные и пероральные введения осуществляют при одинаковой доставляемой дозе.
27. Способ по п. 16, в котором композицию вводят в лекарственной форме, которая распадается при помещении в сублингвальное или буккальное пространство.
28. Способ по п. 16, в котором по меньшей мере один параметр, выбранный из биодоступности, Cmax, AUC, Tmax, процентной доли композиции, выводимой P-gp, процентной доли композиции, поглощаемой ОАТР, и процентной доли композиции, метаболизируемой CYP3A4, CYP1A2 или CYP2B6, измеряют после введения однократной дозы, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана.
29. Способ по п. 28, в котором однократной дозе, содержащей по меньшей мере 15 мг замещенного или незамещенного дииндолилметана, предшествует ежесуточное введение по меньшей мере 15 мг замещенного или незамещенного дииндолилметана в течение по меньшей мере 14 дней.
30. Способ по п. 29, в котором Cmax замещенного или незамещенного дииндолилметана в плазме крови является более высокой, с кратностью от приблизительно 1 раза до приблизительно 50 раз, по сравнению с Cmax замещенного или незамещенного дииндолилметана сравниваемой композиции, вводимой посредством перорального пути, где Cmax сравниваемой композиции измеряют после введения однократной дозы, содержащей по меньшей мере 15 мг сравниваемой композиции, которой предшествует ежесуточное введение по меньшей мере 15 мг сравниваемой композиции в течение по меньшей мере 14 дней.
| WO 2012130698 A1, 04.10.2012 | |||
| WO 2016012523 A1, 28.01.2016 | |||
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ПЕРОРАЛЬНОЙ ДОСТАВКИ ДИИНДОЛИЛМЕТАНА (DIM) И СПОСОБЫ ПРИМЕНЕНИЯ ЭТИХ КОМПОЗИЦИЙ | 2009 |
|
RU2409363C9 |
| DE 102013104441 A1, 16.10.2014. | |||
Авторы
Даты
2021-01-27—Публикация
2017-09-15—Подача