ПРАВА ПРАВИТЕЛЬСТВА
Настоящее изобретение было сделано при поддержке правительства в рамках МН063663, присуждаемой Национальным институтом здоровья. Правительство имеет определенные права на данное изобретение.
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет согласно §119 (е) Свода законов США на основании предварительной заявки на патент №61/971862, поданной 28 марта 2014 г., полное описание которой включено в настоящий документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Изобретение, описанное в настоящем документе, относится к соединениям, а также композициям, способам и их применению для лечения нейродегенеративных заболеваний и расстройств. В частности, настоящее изобретение, описанное в настоящем документе, относится к модуляторам рецептора вазопрессина, а также композициям, способам и их применению для лечения нейропсихиатрических аспектов нейродегенеративных заболеваний, таких как болезнь Хантингтона, болезнь Паркинсона и болезнь Альцгеймера.
УРОВЕНЬ ТЕХНИКИ И СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Нейродегенеративные расстройства (ND) и заболевания часто имеют общий нейродегенеративный компонент, который приводит как к двигательным нарушениям, таким как гемибаллизм, атаксия, гиперкинез, паркинсонизмы, атетоз, хорея, дискинезия и тому подобное, так и к нейропсихиатрическим симптомам. В частности, болезнь Хантингтона (HD), болезнь Паркинсона (PD), болезнь Альцгеймера (AD), каждая представлена совокупностью симптомов. Например, каждая из HD, PD и/или AD может иметь симптомы, в том числе двигательные нарушения или дисфункции, а также нейропсихиатрические расстройства, такие как агрессия, раздражительность и гнев. Хотя некоторые двигательные нарушения, такие как хорея, можно лечить с помощью лекарственных средств, одобренных для некоторых нейродегенеративных заболеваний, таких как HD и PD, нейропсихиатрические аспекты нейродегенеративных заболеваний не излечиваются, так как традиционные лекарства не оказались эффективными. При отсутствии лечения такие нейропсихиатрические симптомы могут привести к широкому диапазону сложных сопутствующих и часто не связанных последствий. Соответственно, в настоящее время существует потребность в соединениях, композициях и способах лечения нейропсихиатрических аспектов нейродегенеративных расстройств и заболеваний.
HD представляет собой наследственное заболевание, которое возникает в результате умножения тринуклеотида повтора (CAG, цитозин/аденин/гуанин), который кодирует полиглутаминовый путь в белке хантингтина. Как правило, она возникает в возрасте от 35 до 44 лет, но может начаться гораздо раньше или позже. Симптомы включают снижение поведенческих, когнитивных и двигательных функций. Психические симптомы, включая раздражительность и агрессию, являются общими у пациентов с HD и являются одними из самых неблагоприятных аспектов болезни. Для 40%-70% пациентов с HD раздражительность и агрессия негативно влияют на повседневную жизнь и часто приводят к институционализации (van Duijn et al., Psychopathology in verified Huntington's disease gene carriers. J Neuropsychiatry Clin Neurosci. 19:441-8 (2007)). Несмотря на частое возникновение и тяжелые последствия раздражительности и агрессивного поведения при HD, указанные симптомы получили мало внимания. Различные инструменты оценки были использованы для оценки раздражительности при HD, включая нейропсихиатрический опросник (NPI), Единую оценочную шкалу болезни Хантингтона, шкалу раздражительности (Чаттерджи) и оценку проблем поведения болезни Хантингтона (PBA-HD). Тем не менее, слепые клинические исследования болезни Хантингтона и долгосрочные исследование лекарственной терапии с отслеживанием для нейропсихиатрических аспектов HD, таких как раздражительность и агрессия, не проводились.
Кроме того, сообщалось, что имеющиеся в настоящее время лекарственные средства, которые были эффективными для лечения агрессии, раздражительности и гнева и/или депрессии и тревоги при других заболеваниях, таких как большое депрессивное расстройство и генерализованное тревожное расстройство, либо не работают, либо только кратковременно эффективны для лечения нейропсихиатрических симптомов HD, PD и/или AD. Например, сообщалось, что лечение антидепрессантом венлаксафином XR у пациентов с HD улучшило депрессивные симптомы, но привело к повышенной раздражительности. Аналогично, у пациентов с AD лечение антипсихотическим рисперидоном только кратковременно снизило агрессивность и было неэффективно после 12 недель. Аналогично, арипипразол обеспечил также только кратковременные эффекты. Кроме того, последнее правительственное руководство предостерегало против использования антипсихотических препаратов у пожилых пациентов для лечения слабоумия в связи с наблюдением серьезных побочных эффектов, а также общими рисками для здоровья, связанными с указанными лекарственными средствами, включая экстрапирамидные симптомы, ускоренное снижение когнитивных функций, инсульт и смерть. Таким образом, указанные лекарственные средства не считаются хорошим выбором для клинического применения при лечении нейродегенеративных заболеваний, и особенно рекомендуется их использование только для краткосрочного лечения (см. Ballard & Corbett, CNS Drugs 24(9):729-739 (2010)).
Данные неудачи терапии также свидетельствуют о том, что характер нейропсихиатрических симптомов у HD, AD и PD отличен. Иными словами можно сказать, что раздражительность, гнев, агрессия, депрессия и беспокойство при HD, AD и PD не такие, как казалось те же поведенческие показатели при других заболеваниях, таких как параноидная шизофрения, эпилепсия, большое депрессивное расстройство и тому подобное, которые можно эффективно лечить с помощью лекарственных средств, доступных в настоящее время. Не будучи связанными теорией, полагают, что в данном случае внешние проявления нейропсихиатрических аспектов, связанных с HD, PD и/или AD, таких как агрессия, раздражительность и гнев, имеют другую исходную причину. Таким образом, агрессия, раздражительность, и гнев, и депрессия, и тревога, возникающие у пациентов, страдающих HD, PD и/или AD, являются отдельным расстройством или дисфункцией, и не имеют отношения к агрессии, раздражительности, гневу при других заболеваниях. Дополнительное подтверждение данного вывода вытекает из сообщений, о том что, например, раздражительность можно наблюдать в ряде заболеваний и расстройств, однако все же исходная причина или дисфункция, которая проявляется в виде раздражительности, может быть различной в каждом конкретном случае. Примеры таких расстройств включают дефицит МОА-А, черепно-мозговую травму, инсульт, умственную отсталость, большое депрессивное расстройство, биполярное расстройство и тому подобное, каждое из которых проявляется в раздражительности или агрессивном поведении. В частности, сообщалось, что избыточная передача сигнала через рецептор вазопрессина V1b отвечает за различные нейропсихиатрические симптомы, вызывая связанные со стрессом расстройства, тревогу, депрессию, дисфункцию памяти, агрессивность и социальное поведение (см.,  "Vasopressin V1a and V1b receptor modulators: a patent review (2012-2014)" Expert Opinion Ther. Patents (2015). Поэтому, не будучи связанными теорией, также полагают, что в данном случае, сообщаемые неудачи терапии могут возникнуть в результате нацеливания на неправильные причины, лежащие в основе нейропсихиатрических симптомов, характерных для HD, AD и/или PD. Лечение нейропсихиатрических симптомов HD/AD/PD, таких как агрессия, раздражительность, гнев, депрессия и тревога, представляет неудовлетворенную медицинскую потребность.
"Vasopressin V1a and V1b receptor modulators: a patent review (2012-2014)" Expert Opinion Ther. Patents (2015). Поэтому, не будучи связанными теорией, также полагают, что в данном случае, сообщаемые неудачи терапии могут возникнуть в результате нацеливания на неправильные причины, лежащие в основе нейропсихиатрических симптомов, характерных для HD, AD и/или PD. Лечение нейропсихиатрических симптомов HD/AD/PD, таких как агрессия, раздражительность, гнев, депрессия и тревога, представляет неудовлетворенную медицинскую потребность.
Было неожиданно обнаружено в настоящем изобретении, что изменение передачи сигнала вазопрессина в центральной нервной системе (ЦНС) эффективно для лечения нейропсихиатрических аспектов, иногда называемых поведенческими и психологическими симптомами деменции (BPSD), при нейро дегенеративных расстройствах и заболеваниях, в том числе, но не ограничиваясь ими, HD, AD и/или PD. В частности, было неожиданно обнаружено в настоящем изобретении, что нейродегенеративные расстройства и заболевания, в том числе, но не ограничиваясь ими, HD, AD и/или PD, и, в частности, их нейропсихиатрические аспекты, можно лечить путем введения антагонистов вазопрессина, которые обеспечивают достижение терапевтически эффективных концентраций в ЦНС. Кроме того, было неожиданно обнаружено в настоящем изобретении, что соединения и композиции, описанные в настоящем документе, показывают эффекты в ЦНС после перорального введения и модулируют специфические контуры мозга, вовлеченные в реакции на стимулы, которые приводят к раздражительности и агрессии, а также другим нейропсихиатрическим аспектам ND у пациентов с HD, AD и PD.
Интересно отметить, что нет никаких доказательств того, что повышенные уровни аргинина вазопрессина (AVP) присутствуют в ЦНС у больных с HD, PD и/или AD. Кроме того, повышенный уровень экспрессии рецептора аргинина-вазопрессина (AVPR) в ЦНС не наблюдаются у пациентов с HD, PD и/или AD. Учитывая, что нейродегенерация является одной из отличительных черт HD, PD и AD, можно было бы ожидать патологию, которая включает разрушение или нарушение тканей в головном мозге, которые контролируют исполнительные функции. Например, нейропсихиатрические симптомы, характерные для HD, PD и AD, могут возникнуть в результате разрушения тканей мозга, которые отвечают за управление исполнительными функциями. Однако в настоящем изобретении было обнаружено обратное в отношении уровней экспрессии AVPR, уровни экспрессии которых были аналогичны уровням экспрессии у пациентов, не страдающих от HD, PD или AD. Таким образом, с патофизиологической точки зрения, животных-хозяев, страдающих от HD, PD и/или AD, нельзя отличить от обычных когорт на этом основании. Тем не менее, хотя и не будучи связанными какой-либо теорией, в настоящем изобретении полагают, что нейропсихиатрические аспекты нейродегенеративных расстройств и заболеваний, таких как HD, PD и/или AD могут быть результатом зависимой от среды избыточной сигнализации вазопрессина или увеличения сигнализации вазопрессина, а не из-за повышенных уровней AVP или чрезмерной экспрессии AVPR по сравнению со здоровыми индивидуумами. Вместо этого, в настоящем изобретении полагают, нейропсихиатрические аспекты заболеваний, таких как HD, PD и/или AD, обусловлены зависимой от состояния гиперчувствительностью AVP в ЦНС. Соответственно, по-видимому, в ином случае нормальные уровни AVP тем не менее вызывают чрезмерную сигнализацию вазопрессина у животных-хозяев с HD, PD и/или AD. Не будучи связанными теорией, в настоящем изобретении также полагают, что эффективность соединений, композиций и способов, описанных в настоящем документе, обусловлена по меньшей мере частично модуляцией, коррекцией или даже предотвращением чрезмерной сигнализации вазопрессина, даже в отсутствие избыточных концентраций AVP или экспрессии AVP в ЦНС. Кроме того, хотя и не будучи связанными какой-либо теорией, в настоящем изобретении полагают, что чрезмерная сигнализация вазопрессина, которая возникает вследствие гиперчувствительности AVP, приводит к дисфункции или потери функции исполнительного управления. Указанные дисфункция или потеря функции приводит к потере способности адекватно контролировать ситуационно зависимое ненадлежащее поведение, такое как агрессия, раздражительность и гнев, и/или сделать ситуационно зависимые соответствующие решения, особенно в условиях стресса или тревоги.
Данные неожиданные обнаружения и изобретение, описанное в данном описании, относятся к лечению того, что в ином случае могло бы считаться нормальной сигнализацией вазопрессина, где в больном организме животного-хозяина другие ингибирующие или корректирующие системы являются неэффективными или не могут корректировать зависящую от среды чрезмерную сигнализацию вазопрессина. Таким образом, введение соединений или композиций, описанных в настоящем документе, уменьшает передачу сигнала вазопрессина до уровня ниже, чем в ином случае будет считаться нормальным, в результате чего дизрегуляция систем передачи сигнала, в том числе и тех, которые контролируют исполнительные функции, возвращаются в равновесие.
В одном иллюстративном варианте реализации настоящего изобретения селективные антагонисты вазопрессина V1a, и композиции, и способы применения таких антагонистов вазопрессина, описаны в настоящем документе. В другом иллюстративном варианте реализации селективные антагонисты вазопрессина V1a, и композиции, и способы применения таких антагонистов вазопрессина, которые получены с возможностью достижения или способные генерировать концентрации в ЦНС по меньшей мере примерно 100 нМ при введении в организм животного-хозяина, описаны в настоящем документе. В другом иллюстративном варианте реализации селективные антагонисты вазопрессина V1a, и композиции, и способы применения таких антагонистов вазопрессина, которые получены с возможностью достижения или способные генерировать концентрации в ЦНС по меньшей мере примерно 10 нМ или по меньшей мере примерно 1 нМ при введении в организм животного-хозяина, описаны в настоящем документе. В другом иллюстративном варианте реализации селективные антагонисты вазопрессина V1a, и композиции, и способы применения таких антагонистов вазопрессина, которые получены с возможностью достижения или способные генерировать концентрации в ЦНС по меньшей мере приблизительно 100 пМ, по меньшей мере, примерно 10 пМ или по меньшей мере примерно 1 пМ при введении в организм животного-хозяина, описаны в настоящем документе.
Следует понимать, что в настоящем документе нейропсихиатрические аспекты нейродегенеративных заболеваний, таких как HD, PD и/или AD могут присутствовать до хореи или других двигательных нарушений. Соответственно, если поставлен диагноз раннего прогрессирования заболевания, соединения, композиции и способы, описанные в настоящем документе, могут также быть эффективными для задержки начала двигательных нарушений и других более поздних симптомов или аспектов нейродегенеративных заболеваний. Кроме того, в настоящем документе описаны соединения, композиции и способы профилактического лечения нейродегенеративных заболеваний, таких как HD, PD и/или AD, например, профилактического лечения двигательных нарушений и дисфункций и других более поздних симптомов.
В настоящем изобретении было обнаружено, что нейродегенеративных расстройств и заболевания, таких как HD, PD и AD, и в частности, их нейропсихиатрические аспекты, можно лечить с помощью селективных антагонистов вазопрессина V1a. Согласно одному из вариантов реализации антагонисты рецептора вазопрессина имеют формулу
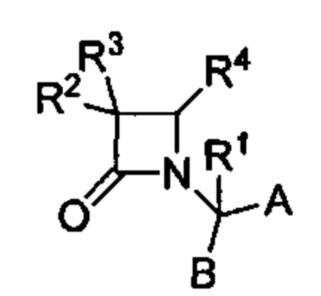
и их фармацевтически приемлемые соли; где
А представляет собой карбоновую кислоту, сложный эфир или амид;
В представляет собой карбоновую кислоту, сложный эфир или амид; или В представляет собой спирт или тиол или его производное;
R1 представляет собой водород или C1-С6 алкил;
R2 представляет собой водород, алкил, алкенил, алкинил, алкокси, алкилтио, галоген, галогеналкил, циано, формил, алкилкарбонил или заместитель, выбранный из группы, состоящей из -CO2R8, -CONR8R8', и -NR8(COR9); где каждый R8 и R8' независимо выбран из водорода, алкила, циклоалкила, необязательно замещенного арила или необязательно замещенного арилалкила; или R8 и R8' взяты вместе с присоединенным атомом азота с образованием гетероциклильной группы; и где R9 выбран из водорода, алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила, необязательно замещенного гетероарилалкила и R8R8'N-(C1-C4 алкил);
R3 представляет собой амино, амидо, ациламидо или уреидогруппу, которая необязательно замещена; или R3 представляет собой азотсодержащую гетероциклильную группу, присоединенную по атому азота; и
R4 представляет собой алкил, алкенил, алкинил, циклоалкил, циклоалкенил, алкилкарбонил, необязательно замещенный арил, необязательно замещенный арилалкил, необязательно замещенный арилгалогеналкил, необязательно замещений арилалкоксиалкил, необязательно замещенньш арилалкенил, необязательно замещенный арилгалогеналкенил или необязательно замещенный арилалкинил.
Согласно другому варианту реализации фармацевтические композиции, содержащие одно или более соединений, также описаны в настоящем документе. В одном аспекте композиции включают терапевтически эффективное количество одного или более соединений для лечения животного-хозяина с нейродегенеративным заболеванием. Следует понимать, что композиции могут включать другие компоненты и/или ингредиенты, включая, но не ограничиваясь ими, другие терапевтически активные соединения, и/или один или более носителей, разбавителей, вспомогательных веществ и тому подобное, и их комбинации. Согласно другому варианту реализации способы применения соединений и фармацевтических композиций для лечения животных-хозяев с нейродегенеративным заболеванием, также описаны в настоящем документе. В одном аспекте способы включают стадию введения одного или более соединений и/или композиций, описанных в данном документе, животному-хозяину. В другом аспекте способы включают введение терапевтически эффективного количества одного или более соединений и/или композиций, описанных в настоящем документе, для лечения нейродегенеративного заболевания животных-хозяев. Согласно другому варианту реализации применение соединений и композиций для получения лекарственного средства для лечения животных-хозяев с нейродегенеративным заболеванием также описано в настоящем документе. В одном из аспектов, лекарственные средства включают терапевтически эффективное количество одного или более соединений и/или композиций, описанных в настоящем документе.
Следует понимать в настоящем изобретении, что соединения, описанные в настоящем документе, можно применять отдельно или в комбинации с другими соединениями, подходящими для лечения нейродегенеративных заболеваний, в том числе соединениями, которые могут быть терапевтически эффективными в соответствии с теми же или другими принципами действия. Кроме того, следует понимать в настоящем изобретении, что соединения, описанные в настоящем документе, можно применять в комбинации с другими соединениями, которые вводят для лечения других симптомов нейродегенеративных заболеваний, такими как соединения, которые вводят для лечения хореи или иных двигательных нарушений и т.п.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фигуре 1 показано структурное изображение высокого расширения уменьшения BOLD-сигнала в височно-теменной доле коры (поля Бродмана 39).
На фигуре 2 показано структурное изображение высокого расширения уменьшения BOLD-сигнала в передней поясной коре и медиальной префронтальной коре.
На фигуре 3 показан снимок головного мозга для миндалины, коры, гиппокампа, таламуса и для необработанного контроля в рамках парадигмы теста стресса резидент + интрудер.
На фигуре 4 показан снимок головного мозга для миндалины, коры, гиппокампа, таламуса для животных, предварительно обработанных SRX251 в рамках парадигмы теста стресса резидент + интрудер.
На фигуре 5 показано сравнение обработки носителем, хлордиазэпоксидом (CDP) и обработки SRX246 в тесте социального взаимодействия.
На фигуре 6А, фигуре 6В и фигуре 6С показано время, которое исследуемые животные тратили на свету, время, которое исследуемые животные тратили в темноте, и количесво входов свет-темнота в тесте с челночной камерой со светом и темнотой.
ПОДРОБНОЕ ОПИСАНИЕ
В настоящем документе описано применение одного или более антагонистов рецептора вазопрессина V1a в качестве терапевтического подхода для лечения нейродегенеративных заболеваний. Соединения, описанные в настоящем документе, могут иметь потенциал для значительного улучшения жизни людей, страдающих от нейродегенеративных заболеваний, таких как AD, PD и HD. Тяжелое протекание и смертность, связанные с нейродегенеративными заболеваниями, такими как AD, PD и HD, проявляются не только из-за двигательных нарушений и дисфункции, которые сопровождают нейродегенеративные заболевания, но и вследствие нейропсихиатрических расстройств, таких, как неконтролируемая или несоответствующая агрессия, гнев, раздражительность, и связанные с ними симптомы.
Несколько иллюстративных вариантов реализации настоящего изобретения описаны с помощью следующих иллюстративных пунктов:
Способ лечения нейродегенеративного заболевания или расстройства, такого как HD, AD или PD, у животного-хозяина, включающий стадию введения композиции, содержащей один или более селективных антагонистов рецептора вазопрессина V1a животному-хозяину.
Способ лечения нейропсихиатрических аспектов нейродегенеративного заболевания или расстройства, такого как HD, AD или PD, у животного-хозяина, включающий стадию введения композиции, содержащей один или более селективных антагонистов рецептора вазопрессина V1a животному-хозяину.
Способ по любому из предыдущих пунктов, где нейропсихиатрические аспекты включают агрессию.
Способ по любому из предыдущих пунктов, где нейропсихиатрические аспекты включают раздражительность.
Способ по любому из предыдущих пунктов, где нейропсихиатрические аспекты включают гнев.
Способ по любому из предыдущих пунктов, где способ приводит к улучшению показателей в следующем: вопросник девиантного поведения (англ. Aberrant Behavior Checklist, ABCi), опросник Коген-Мансфилд для возбуждения (CMAI), оценку проблем поведения болезни, которая форма (англ. Problem Behaviors Assessment, РВА-) и/или шкала раздражительности (IS).
Способ по любому из предыдущих пунктов, где один или более антагонистов выбраны из соединений формулы:
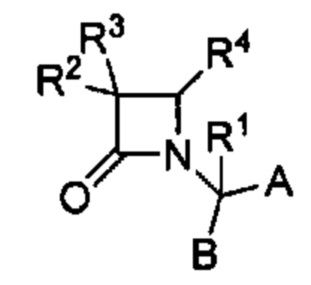
и их фармацевтически приемлемые соли, где
А представляет собой карбоновую кислоту, сложный эфир или амид;
В представляет собой карбоновую кислоту, сложный эфир или амид; или В представляет собой спирт или тиол или его производное;
R1 представляет собой водород или C1-С6 алкил;
R2 представляет собой водород, алкил, алкенил, алкинил, алкокси, алкилтио, галоген, галогеналкил, циано, формил, алкилкарбонил или заместитель, выбранный из группы, состоящей из -CO2R8, -CONR8R8', и -NR8(COR9); где каждый R8 и R8' независимо выбран из водорода, алкила, циклоалкила, необязательно замещенного арила или необязательно замещенного арилалкила; или R8 и R8' взяты вместе с присоединенным атомом азота с образованием гетероциклильной группы; и где R9 выбран из водорода, алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила, необязательно замещенного гетероарилалкила и R8R8'N-(C1-C4 алкил);
R3 представляет собой амино, амидо, ациламидо или уреидогруппу, которая необязательно замещена; или R3 представляет собой азотсодержащую гетероциклильную группу, присоединенную по атому азота; и
R4 представляет собой алкил, алкенил, алкинил, циклоалкил, циклоалкенил, алкилкарбонил, необязательно замещенный арил, необязательно замещенный арилалкил, необязательно замещенный арилгалогеналкил, необязательно замещенный арилалкоксиалкил, необязательно замещенный арилалкенил, необязательно замещенный арилгалогеналкенил или необязательно замещенный арилалкинил.
Способ по любому из предыдущих пунктов, где один или более антагонистов выбраны из соединений формулы:
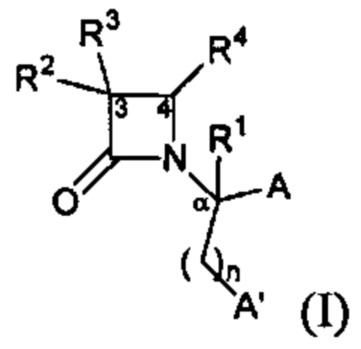
и их фармацевтически приемлемые соли, где
каждый А и А' независимо выбран из -СО2Н или его сложноэфирного или амидного производного;
n представляет собой целое число, выбранное из от 0 до примерно 3;
R1 представляет собой водород или C1-С6 алкил;
R2 представляет собой водород, алкил, алкенил, алкинил, алкокси, алкилтио, галоген, галогеналкил, циано, формил, алкилкарбонил или заместитель, выбранный из группы, состоящей из -CO2R8, -CONR8R8', и -NR8(COR9); где каждый R8 и R8' независимо выбран из водорода, алкила, циклоалкила, необязательно замещенного арила или необязательно замещенного арилалкила; или R8 и R8' взяты вместе с присоединенным атомом азота с образованием гетероцикл; и где R9 выбран из водорода, алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила, необязательно замещенного гетероарилалкила и R8R8N-(C1-C4 алкил);
R3 представляет собой амино, амидо, ациламидо, или уреидогруппу, которая необязательно замещена; или R3 представляет собой азотсодержащую гетероциклильную группу, присоединенную по атому азота; и
R4 представляет собой алкил, алкенил, алкинил, циклоалкил, циклоалкенил, алкилкарбонил, необязательно замещенный арил, необязательно замещенный арилалкил, необязательно замещенный арилгалогеналкил, необязательно замещенный арилалкоксиалкил, необязательно замещенный арилалкенил, необязательно замещенный арилгалогеналкенил или необязательно замещенный арилалкинил.
Способ по любому из предыдущих пунктов, где один или более антагонистов выбраны из соединений формулы:
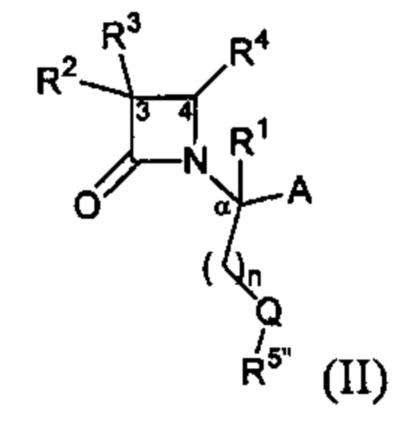
и их фармацевтически приемлемые соли, где
А представляет собой -СО2Н или его сложноэфирное или амидное производное;
Q представляет собой кислород; или Q представляет собой серу или дисульфид или его окисленное производное;
n представляет собой целое число от 1 до 3;
R1, R2, R3 и R4 являются такими, как определено в формуле I; и
R5” выбран из водорода, алкила, циклоалкила, алкоксиалкила, необязательно замещенного арилалкила, необязательно замещенного гетероциклила или необязательно замещенного гетероциклилалкила и необязательно замещенного аминоалкила.
Способ по любому из предыдущих пунктов, где А представляет собой -CO2R5; где R5 выбран из водорода, алкила, циклоалкила, алкоксиалкила, необязательно замещенного арилалкила, гетероциклила, гетероциклил(C1-С4 алкил), и R6R7N-(C2-C4 алкил).
Способ по любому из предыдущих пунктов, где А представляет собой монозамещенную амидогруппу, дизамещенную амидогруппу или необязательно замещенный азотсодержащий гетероциклиламидо.
Способ по любому из предыдущих пунктов, где гетероциклил независимо выбран из тетрагидрофурила, морфолинила, пирролидинила, пиперидинила, пиперазинила, гомопиперазинила или хинуклидинила; где указанный морфолинил, пирролидинил, пиперидинил, пиперазинил, гомопиперазинил или хинуклидинил необязательно N-замещен С1-С4 алкилом или необязательно замещенным арил(С1-С4 алкилом). Следует понимать, что в каждом случае различных вариантов реализации, описанных в настоящем документе, гетероциклил выбран независимо в каждом случае.
Способ по любому из предыдущих пунктов, где R6 независимо выбран из водорода или алкила; и R7 выбран независимо в каждом случае из алкила, циклоалкила, необязательно замещенного арила или необязательно замещенного арилалкила. Способ по любому из предыдущих пунктов, где R6 и R7 взяты вместе с присоединенным атомом азота с образованием необязательно замещенного гетероцикла, такого как пирролидинил, пиперидинил, морфолинил, пиперазинил, и гомопиперазинил; где указанный пиперазинил или гомопиперазинил также необязательно N-замещен R13; где R13 выбран независимо в каждом случае из водорода, алкила, циклоалкила, алкоксикарбонила, необязательно замещенного арилоксикарбонила, необязательно замещенного арилалкила и необязательно замещенного арилоила. Также следует понимать в каждом случае различных вариантов реализации, описанных в настоящем документе, каждый R6 и R7 выбран независимо в каждом случае.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид. Способ по любому из предыдущих пунктов, где оба А и А' представляют собой амиды. Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид вторичного амина, также называемый в данном документе как вторичный амид. Способ по любому из предыдущих пунктов, где оба А и А' представляют собой вторичные амиды. Следует понимать, что вторичные амиды включают амиды циклических аминов, присоединенных по азоту.
Способ по любому из предыдущих пунктов, где А представляют собой амид. Способ по любому из предыдущих пунктов, где А представляют собой амид вторичного амина, также называемый в данном документе как вторичный амид.
Способ по любому из предыдущих пунктов, где антагонисты представляют собой сложные диэфиры, сложные эфиры кислот или дикислоты, включая их фармацевтически приемлемые соли, где каждый из А и А' выбран независимо. Способ по любому из предыдущих пунктов, где антагонисты представляют собой сложные эфиры-амиды, где один из А и А' представляет собой сложный эфир, и другой представляет собой амид. Способ по любому из предыдущих пунктов, где антагонисты представляют собой диамиды, где каждый из А и А' независимо выбран из монозамещенной амидогруппы, дизамещенной амидогруппы и необязательно замещенного азотсодержащего гетероциклиламидо.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой независимо выбранную монозамещенную амидогруппу формулы C(O)NHX-, где X выбран из алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, гетероциклила, гетероциклил-(С1-С4 алкил), R6R7N- и R6R7N-(C2-C4 алкил), где каждый гетероциклил выбран независимо.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой независимо выбранную дизамещенную амидогруппу формулы C(O)NR14X-, где R14 выбран из гидрокси, алкила, алкоксикарбонила и бензила; и X выбран из алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, гетероциклила, гетероциклил-(С1-С4 алкил), R6R7N-, и R6R7N-(С2-С4 алкил), где каждый гетероциклил выбран независимо.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид независимо выбранного необязательно замещенного азотсодержащего гетероцикла, присоединенного по азоту. Иллюстративные азотсодержащие гетероциклы включают, но не ограничиваются ими, пирролидинил, пиперидинил, пиперазинил, гомопиперазинил, триазолидинил, триазинил, оксазолидинил, изоксазолидинил, тиазолидинил, изотиазолидинил, 1,2-оксазинил, 1,3-оксазинил, морфолинил, оксадиазолидинил и тиадиазолидинил; каждый из которых необязательно замещен. Такие необязательные замещения включают группы R10, R12, R6R7N-, и R6R7N-(C1-G4 алкил), как определено в настоящем документе.
Способ по любому из предыдущих пунктов, где А и/или А' выбран независимо из пирролидинонила, пиперидинонила, 2-(пирролидин-1-илметил)пирролидин-1-ила или 1,2,3,4-тетрагидроизохинолин-2-ила, каждый из которых необязательно замещен, и присоединен по азоту.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой независимо выбранный амид необязательно замещенного пиперидинила присоединенного по азоту. Иллюстративные необязательные замещения включают гидрокси, алкил, циклоалкил, алкокси, алкоксикарбонил, гидроксиалкилоксиалкил, включая (гидрокси(С2-С4 алкилокси))-(С2-С4 алкил), R6R7N-, R6R7N-алкил, включая R6R7N-(C1-C4 алкил), дифенилметил, необязательно замещенный арил, необязательно замещенный арил(С1-С4 алкил) и пиперидин-1-ил(С1-С4 алкил).
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой независимо выбранный пиперидинил, замещенный по положению 4 и присоединенный по азоту.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой независимо выбранный амид необязательно замещенного пиперазинила, присоединенного по азоту. Иллюстративные необязательные замещения включают гидрокси, алкил, циклоалкил, алкокси, алкоксикарбонил, гидроксиалкилоксиалкил, включая (гидрокси(С2-С4 алкилокси))-(С2-С4 алкил), R6R7N-, R6R7N-алкил, включая R6R7N-(C1-C4 алкил), дифенилметил, необязательно замещенный арил, необязательно замещенный арил(С1-С4 алкил) и пиперидин- 1-ил(С1-С4 алкил). Способ по любому из предыдущих пунктов, где А и/или А' представляют собой независимо выбранный пиперазинил, замещенный по положению 4 и присоединенный по азоту.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой независимо выбранный амид необязательно замещенного гомопиперазинила, присоединенного по азоту. Иллюстративные необязательные замещения включают гидрокси, алкил, циклоалкил, алкокси, алкоксикарбонил, гидроксиалкилоксиалкил, включая (гидрокси(С2-С4 алкилокси))-(С2-С4 алкил), R6R7N-, R6R7N-алкил, включая R6R7N-(C1-C4 алкил), дифенилметил, необязательно замещенный арил, необязательно замещенный арил(С1-С4 алкил) и пиперидин-1-ил(С1-С4 алкил). Способ по любому из предыдущих пунктов, где А и/или А' представляют собой независимо выбранный гомопиперазинил замещенный по положению 4 и присоединенный по азоту. Способ по любому из предыдущих пунктов, где А и/или А' представляют собой независимо выбранный гомопиперазинил, замещенный по положению 4 алкилом, арилом, арил(С1-С4 алкил), и присоединенный по азоту.
Способ по любому из предыдущих пунктов, где А' представляет собой монозамещенную амидогруппу, дизамещенную амидогруппу или необязательно замещенный азотсодержащий гетероциклиламидо. Способ по любому из предыдущих пунктов, где А' представляет собой -CO2R5; где R5' выбран из водорода, алкила, циклоалкила, алкоксиалкила, необязательно замещенного арилалкила, гетероциклила, гетероциклил(С1-С4 алкил) и R6R7N-(C2-C4 алкил); где гетероциклил в каждом случае независимо выбран из тетрагидрофурила, морфолинила, пирролидинила, пиперидинила, пиперазинила, гомопиперазинила или хинуклидинила; где указанный морфолинил, пирролидинил, пиперидинил, пиперазинил, гомопиперазинил или хинуклидинил необязательно N-замещен С1-С4 алкилом или необязательно замещенным арил(С1-С4 алкилом). Способ по любому из предыдущих пунктов, где R5' представляет собой необязательно замещенный гетероциклилалкил или необязательно замещенный аминоалкил, включая R6R7N-(C2-C4 алкил).
Способ по любому из предыдущих пунктов, где А имеет формулу
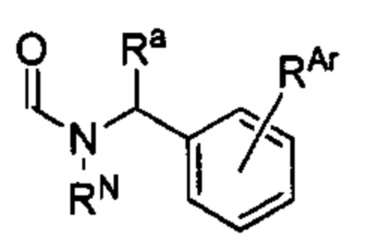
где RN представляет собой водород или необязательно замещенный алкил, или группу, образующую пролекарство амида; Ra представляет собой водород или необязательно замещенный алкил; и RAr представляет собой водород или один или более арильных заместителей, таких как, но не ограничиваясь ими, галоген, гидрокси, необязательно замещенный алкил, необязательно замещенный алкокси, нитро и т.п. Способ по любому из предыдущих пунктов, где по меньшей мере один из RN, Ra и RAr не представляет собой водород. Способ по любому из предыдущих пунктов, где по меньшей мере один из RN и Ra не представляет собой водород. Согласно другому варианту реализации А имеет формулу
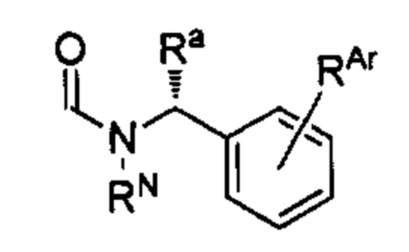
где RN, Ra и RAr являются такими, как определено в настоящем документе.
Способ по любому из предыдущих пунктов, где А выбран из монозамещенной амидогруппы, дизамещенной амидогруппы и необязательно замещенного азотсодержащего гетероциклиламидо. Способ по любому из предыдущих пунктов, где А представляют собой амид необязательно замещенного 1-тетрагидронафтиламина.
Способ по любому из предыдущих пунктов, где А и/или А' представляет собой монозамещенную амидогруппу формулы C(O)NHX, где X выбран из алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, гетероциклила, гетероциклил-(C1-С4 алкил), R6R7N-, и R6R7N-(С2-С4 алкил), где каждый гетероциклил выбран независимо.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой дизамещенную амидогруппу формулы C(O)NR14X, где R14 выбран из гидрокси, алкила, алкоксикарбонила и бензила; и X выбран из алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, гетероциклила, гетероциклил-(C1-С4 алкил), R6R7N-, и R6R7N-(C2-C4 алкил), где каждый гетероциклил выбран независимо.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид необязательно замещенного азотсодержащего гетероцикла, присоединенного по азоту. Иллюстративные азотсодержащие гетероциклы включают, но не ограничиваются ими, пирролидинил, пиперидинил, пиперазинил, гомопиперазинил, триазолидинил, триазинил, оксазолидинил, изоксазолидинил, тиазолидинил, изотиазолидинил, 1,2-оксазинил, 1,3-оксазинил, морфолинил, оксадиазолидинил и тиадиазолидинил; каждый из которых необязательно замещен. Такие необязательные замещения включают группы R10, R12, R6R7N-, и R6R7N-(C1-C4 алкил), как определено в настоящем документе. Способ по любому из предыдущих пунктов, где А представляет собой пирролидинонил, пиперидинонил, 2-(пирролидин-1-илметил)пирролидин-1-ил, или 1,2,3,4-тетрагидроизохинолин-2-ил, каждый из которых необязательно замещен, и присоединен по азоту.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид необязательно замещенного пиперидинила, присоединенного по азоту. Иллюстративные необязательные замещения включают гидрокси, алкил, циклоалкил, алкокси, алкоксикарбонил, гидроксиалкилоксиалкил, включая (гидрокси(С2-С4 алкилокси))-(С2-С4 алкил), R6R7N-, R6R7N-алкил, включая R6R7N-(C1-C4 алкил), дифенилметил, необязательно замещенный арил, необязательно замещенный арил(С1-С4 алкил) и пиперидин-1-ил(С1-С4 алкил). Способ по любому из предыдущих пунктов, где А и/или А' представляет собой пиперидинил, замещенный по положению 4 и присоединенный по азоту.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид необязательно замещенного пиперазинила, присоединенного по азоту. Иллюстративные необязательные замещения включают гидрокси, алкил, циклоалкил, алкокси, алкоксикарбонил, гидроксиалкилоксиалкил, включая (гидрокси(С2-С4 алкилокси))-(С2-С4 алкил), R6R7N-, R6R7N-алкил, включая R6R7N-(C1-C4 алкил), дифенилметил, необязательно замещенный арил, необязательно замещенный арил(С1-С4 алкил), и пиперидин-1-ил(С1-С4 алкил). Способ по любому из предыдущих пунктов, где А и/или А' представляет собой пиперазинил, замещенный по положению 4 и присоединенный по азоту.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид необязательно замещенного гомопиперазинила, присоединенного по азоту. Иллюстративные необязательные замещения включают гидрокси, алкил, циклоалкил, алкокси, алкоксикарбонил, гидроксиалкилоксиалкил, включая (гидрокси(С2-С4 алкилокси))-(С2-С4 алкил), R6R7N-, R6R7N-алкил, включая R6R7N-(C1-C4 алкил), дифенилметил, необязательно замещенный арил, необязательно замещенный арил(С1-С4 алкил) и пиперидин-1-ил(С1-С4 алкил). Способ по любому из предыдущих пунктов, где А и/или А' представляет собой гомопиперазинил, замещенный по положению 4 и присоединенный по азоту. Способ по любому из предыдущих пунктов, где А и/или А' представляет собой гомопиперазинил, замещенный по положению 4 алкилом, арилом, арил(С1-С4 алкил), и присоединенный по азоту.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид гетероцикла, присоединенного по азоту, где гетероцикл замещен гетероциклилом, гетероциклилалкилом, циклоалкилом, циклоалкилалкилом, арилом арил алкил ом.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид необязательно замещенного бензила, необязательно замещенного 1-нафтилметила или необязательно замещенного 2-нафтилметиламина. Необязательные замещения включают, но не ограничиваются ими, 2,3-дихлор, 2,5-дихлор, 2,5-диметокси, 2-трифторметил, 2-фтор-3-трифторметил, 2-фтор-5-трифторметил, 2-метил, 2-метокси, 3,4-дихлор, 3,5-дитрифторметил, 3,5-дихлор, 3,5-диметил, 3,5-дифтор, 3,5-диметокси, 3-бром, 3-трифторметил, 3-хлор-4-фтор, 3-хлор, 3-фтор-5-трифторметил, 3-фтор, 3-метил, 3-нитро, 3-трифторметокси, 3-метокси, 3-фенил, 4-трифторметил, 4-хлор-3-трифторметил, 4-фтор-3-трифторметил, 4-метил и т.п.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид необязательно замещенного бензила-метиламина. Согласно другому варианту реализации А в формуле (I) или (II) представляет собой амид необязательно замещенного бензил-Н-бутиламина, включая н-бутил и трет-бутил. Способ по любому из предыдущих пунктов, где А представляют собой амид необязательно замещенного бензил-N-бензиламина. Необязательные замещения включают, но не ограничиваются ими, 2,3-дихлор, 3,5-дихлор, 3-бром, 3-трифторметил, 3-хлор, 3-метил и т.п.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид необязательно замещенного 1-фенилэтила, 2-фенилэтила, 2-фенилпропила или 1-фенилбензиламина. Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид необязательно замещенного 1-фенилэтила, 2-фенилэтила, 2-фенилпропила, 1-фенилбензиламин-N-метиламина. Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид необязательно замещенного 2-фенил-β-аланина, или его производного, 1-фенилпропаноламина и т.п. Необязательные замещения включают, но не ограничиваются ими, 3-трифторметокси, 3-метокси, 3,5-диметокси, 2-метил и т.п.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид необязательно замещенного 1-фенилциклопропила, 1-фенилциклопентила, или 1-фенилциклогексиламина. Необязательные замещения включают, но не ограничиваются ими, 3-фтор, 4-метокси, 4-метил, 4-хлор, 2-фтор и т.п.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид необязательно замещенного гетероарилметиламина, включая, но не ограничиваясь ими, 2-фурил, 2-тиенил, 2-пиридил, 3-пиридил, 4-пиридил и т.п. Необязательные замещения включают, но не ограничиваются ими, 5-метил, 3-хлор, 2-метил и т.п.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид частично замещенного бициклического арила, включая, но не ограничиваясь ими, 1-, 2-, 4-, и 5-инданиламин, 1- и 2-тетрагидронафтиламин, индолинил, тетрагидрохинолинил, тетрагидроизохинолинил и т.п., каждый из которых необязательно замещен.
Способ по любому из предыдущих пунктов, где А и/или А' представляют собой амид замещенного пиперидина или пиперазина. Заместители на пиперидине или пиперазине включают гетероциклил, гетероциклилалкил, необязательно замещенный арил и необязательно замещенный арилалкил. Иллюстративные пиперидины и пиперазины включают формулы:
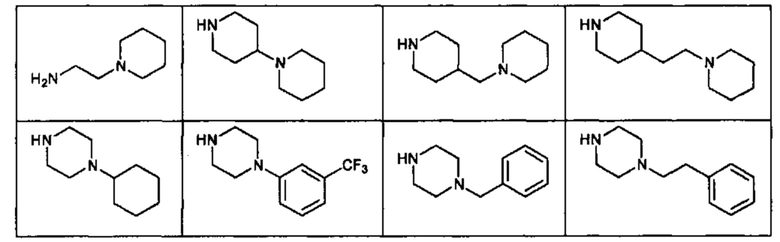
Способ по любому из предыдущих пунктов, где А' представляет собой амид замещенного гетероцикла, присоединенного по азоту. Заместители включают алкил, циклоалкил, циклоалкилалкил, гетероциклил, гетероциклилалкил, арил и арилалкил. Способ по любому из предыдущих пунктов, где А' представляет собой амид гетероцикла, присоединенного по азоту замещенного алкилом, циклоалкилом, циклоалкилалкилом, гетероциклилом или гетероциклилалкилом.
Способ по любому из предыдущих пунктов, где А' представляют собой амид необязательно замещенного арилгетероциклиламина, арилалкилгетероциклиламина, гетероциклилалкиламина или гетероарилалкиламина. Способ по любому из предыдущих пунктов, где А' представляет собой амид пиперидин-1-илпиперидина или пиперидин-1-илалкилпиперидина. Согласно другому варианту реализации алкил представляет собой С1-С2-алкил.
Способ по любому из предыдущих пунктов, где Q представляет собой кислород или серу. Способ по любому из предыдущих пунктов, где R" представляет собой необязательно замещенный арилалкил. Способ по любому из предыдущих пунктов, где А представляют собой амид замещенного пиперидина или пиперазина.
Способ по любому из предыдущих пунктов, где n представляет собой 1 или 2. Способ по любому из предыдущих пунктов, где n представляет собой 1.
Способ по любому из предыдущих пунктов, где R2 представляет собой водород, алкил, алкокси, алкилтио, циано, формил, алкилкарбонил или заместитель, выбранный из группы, состоящей из -CO2R8 и -CONR8R8, где каждый R8 и R8' независимо выбран из водорода и алкила. Способ по любому из предыдущих пунктов, где R2 представляет собой водород или алкил. Способ по любому из предыдущих пунктов, где R2 представляет собой водород.
Способ по любому из предыдущих пунктов, где R1 представляет собой водород. Способ по любому из предыдущих пунктов, где R1 представляет собой метил. Способ по любому из предыдущих пунктов, где оба R1 и R2 представляют собой водород.
Способ по любому из предыдущих пунктов, где R3 имеет формулы:
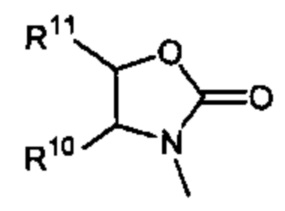
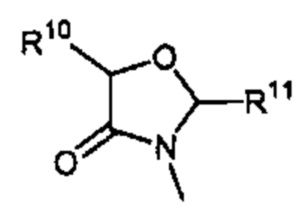
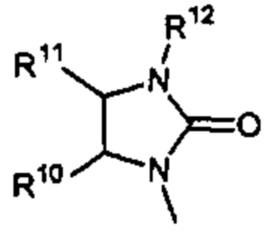
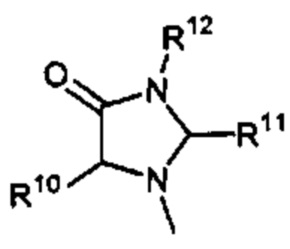
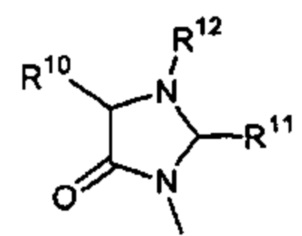
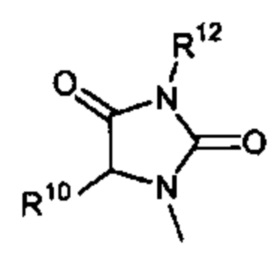
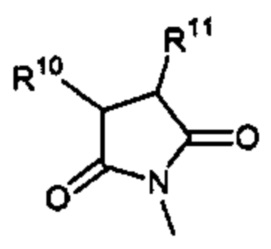
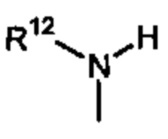
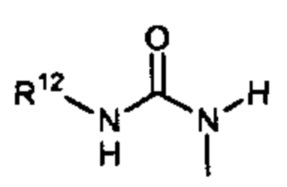
где каждый R10 и R11 независимо выбран из водорода, необязательно замещенного алкила, необязательно замещенного циклоалкила, алкоксикарбонила, алкилкарбонилокси, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного арилалкилокси, необязательно замещенного арилалкилкарбонилокси, дифенилметокси, трифенилметокси и т.п.; и R12 выбран из водорода, алкила, циклоалкила, алкоксикарбонила, необязательно замещенного арилоксикарбонила, необязательно замещенного арилалкила, необязательно замещенного арилоила и т.п.
Способ по любому из предыдущих пунктов, где R3 имеет формулы:
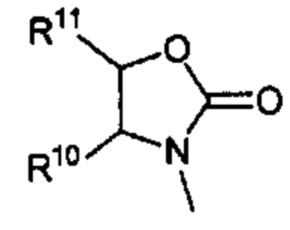
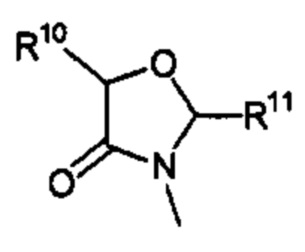
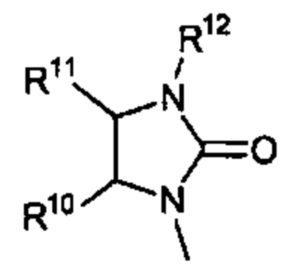
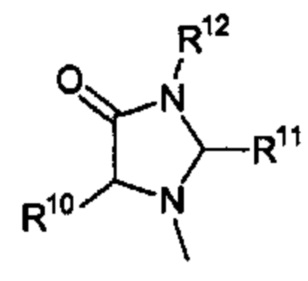
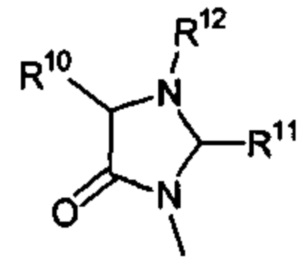
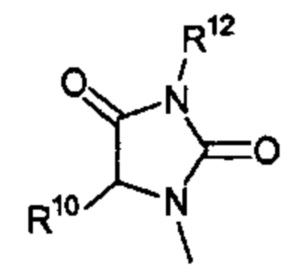
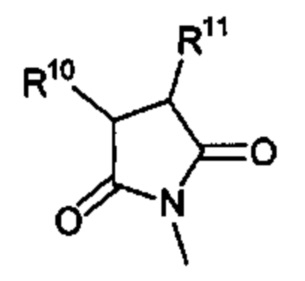
где R10, R11, и R12 являются такими, как определено в настоящем документе.
Способ по любому из предыдущих пунктов, где R3 имеет формулы:
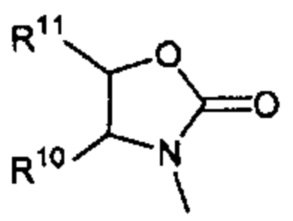
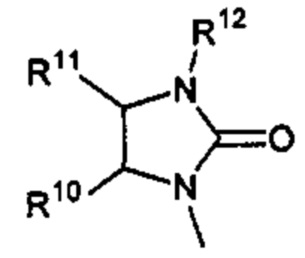
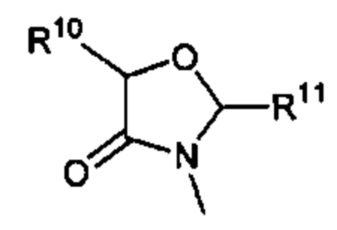
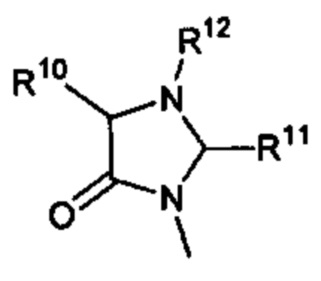
где R10, R11, и R12 являются такими, как определено в настоящем документе.
Способ по любому из предыдущих пунктов, где R3 имеет формулу:
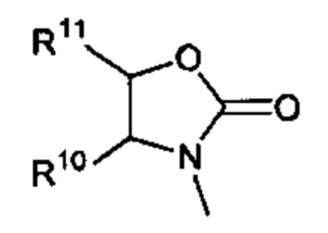
где R10 и R11 являются такими, как определено в настоящем документе.
Способ по любому из предыдущих пунктов, где R4 имеет формулы:
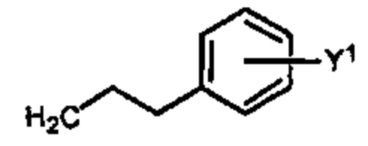
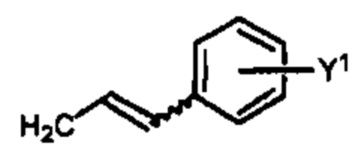
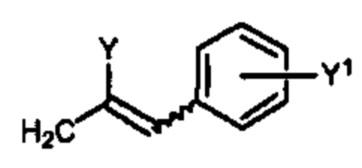
где Y представляет собой электроноакцепторную группу, такую как галоген, и представляет собой водород или один или более арильных заместителей, таких как, но не ограничиваясь ими, галоген, гидрокси, амино, нитро, необязательно замещенный алкил, необязательно замещенный алкокси и т.п. Следует понимать, что двойная связь в формулах может быть полностью или по существу полностью (Е), полностью или по существу полностью (Z), или их смесью. Способ по любому из предыдущих пунктов, где двойная связь в формулах является полностью или по существу полностью (Е). Способ по любому из предыдущих пунктов, где R4 имеет формулу:
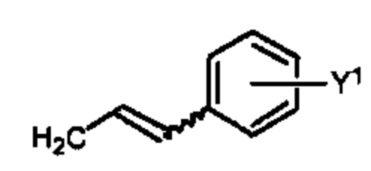
где Y1 является таким, как определено в настоящем документе. Согласно другому варианту реализации Y1 не представляет собой водород.
Способ по любому из предыдущих пунктов, где n представляет собой 1, стереохимия α-углерода представляет собой (S) или (R), или представляет собой эпимерную смесь. Способ по любому из предыдущих пунктов, где n представляет собой 1, стереохимия α-углерода представляет собой (R). Способ по любому из предыдущих пунктов, где n представляет собой 2, стереохимия α-углерода представляет собой (S). Способ по любому из предыдущих пунктов, где n представляет собой 1 и Q представляет собой кислород, стереохимия α-углерода представляет собой (R). Способ по любому из предыдущих пунктов, где n представляет собой 1 и Q представляет собой серу, стереохимия α-углерода представляет собой (S). Следует понимать, что соединения формул (I) и (II) являются хиральными по α-углероду, за исключением когда А=А' и n=0.
Способ по любому из предыдущих пунктов, где R5” представляет собой необязательно замещенный арил(С2-С4 алкил). Способ по любому из предыдущих пунктов, где R5” представляет собой необязательно замещенный арил(С1-С2 алкил). Способ по любому из предыдущих пунктов, где R5” представляет собой необязательно замещенный бензил. Способ по любому из предыдущих пунктов, где R5” представляет собой необязательно замещенный алкил.
Способ по любому из предыдущих пунктов, где по меньшей мере одно соединение представляет собой SRX228 (Пример 233).
Способ по любому из предыдущих пунктов, где по меньшей мере одно соединение представляет собой SRX246 (Пример 224).
Способ по любому из предыдущих пунктов, где по меньшей мере одно соединение представляет собой SRX251 (Пример 225).
Способ по любому из предыдущих пунктов, где по меньшей мере одно соединение представляет собой SRX296 (Пример 232Е).
Способ по любому из предыдущих пунктов, где по меньшей мере одно соединение представляет собой SRX576 (Пример 266).
Способ по любому из предыдущих пунктов, где стадия введения включает общую суточную дозу от примерно 160 до примерно 700 мг в общей сложности одного или более соединений по любому из предшествующих пунктов, в отдельной или разделенной форме.
Способ по любому из предыдущих пунктов, где стадия введения включает общую суточную дозу от примерно 160 до примерно 500 мг в общей сложности одного или более соединений по любому из предшествующих пунктов, в отдельной или разделенной форме.
Способ по любому из предыдущих пунктов, где стадия введения включает общую суточную дозу от примерно 160 до примерно 400 мг в общей сложности одного или более соединений по любому из предшествующих пунктов, в отдельной или разделенной форме.
Способ по любому из предыдущих пунктов, где стадия введения включает общую суточную дозу от примерно 160 до примерно 320 мг в общей сложности одного или более соединений по любому из предшествующих пунктов, в отдельной или разделенной форме.
Способ по любому из предыдущих пунктов, где стадия введения включает общую суточную дозу от примерно 160 до примерно 240 мг в общей сложности одного или более соединений по любому из предшествующих пунктов, в отдельной или разделенной форме.
Способ по любому из предыдущих пунктов, где стадия введения включает протокол введения один раз в сутки.
Способ по любому из предыдущих пунктов, где стадия введения включает протокол введения два раза в сутки.
Способ по любому из предыдущих пунктов, где стадия введения включает протокол дозирования с замедленным высвобождением.
Фармацевтическая композиция, выполненная с возможностью или подходящая для лечения нейродегенеративного заболевания или расстройства, такого как HD, AD или PD, у животного-хозяина, причем композиция содержит одно или более соединений по любому из предшествующих пунктов и, необязательно, один или более носителей, разбавителей или адьювантов, или их комбинации.
Единичная доза или единичная лекарственная форма, выполненная с возможностью или подходящая для лечения нейродегенеративного заболевания или расстройства, такого как HD, AD или PD, у животного-хозяина, причем композиция содержит одно или более соединений по любому из предшествующих пунктов и, необязательно, один или более носителей, разбавителей или адьювантов, или их комбинации.
Единичная доза или единичная лекарственная форма по любому из предшествующих пунктов, содержащая от примерно 80 до примерно 350 мг в общей сложности одного или более соединений по любому из предшествующих пунктов, в отдельной или разделенной форме.
Единичная доза или единичная лекарственная форма по любому из предшествующих пунктов, содержащая от примерно 80 до примерно 250 мг в общей сложности одного или более соединений по любому из предшествующих пунктов, в отдельной или разделенной форме.
Единичная доза или единичная лекарственная форма по любому из предшествующих пунктов, содержащая от примерно 80 до примерно 200 мг в общей сложности одного или более соединений по любому из предшествующих пунктов, в отдельной или разделенной форме.
Единичная доза или единичная лекарственная форма по любому из предшествующих пунктов, содержащая от примерно 80 до примерно 160 мг в общей сложности одного или более соединений по любому из предшествующих пунктов, в отдельной или разделенной форме.
Единичная доза или единичная лекарственная форма по любому из предшествующих пунктов, содержащая от примерно 80 до примерно 120 мг в общей сложности одного или более соединений по любому из предшествующих пунктов, в отдельной или разделенной форме.
Единичная доза или единичная лекарственная форма по любому из предшествующих пунктов, выполненная с возможностью перорального введения.
Единичная доза или единичная лекарственная форма по любому из предшествующих пунктов, выполненная с возможностью замедленного высвобождения.
Следует понимать, что каждый из предшествующих пунктов и в каждом описанном в настоящем документе варианте реализации (I), различные виды, подвиды и
представители каждого из A, A', Y, Y1, n, R1, R2, R3, R4, R5 и т.п., могут быть объединены без ограничения, и следовательно каждый такой дополнительный вариант реализации настоящего изобретения, таким образом, описывается комбинацией. Также следует понимать каждый из предшествующих пунктов и в каждом описанном в настоящем документе варианте реализации (II), различные виды, подвиды и представители каждого из A, Q, Y, Y1, n, R1, R2, R3, R4, R5, R5” и т.п. Могут быть объединены без ограничения, и следовательно каждый такой дополнительный вариант реализации настоящего изобретения, таким образом, описывается комбинацией. Например, способ по любому из предыдущих пунктов, где соединения формулы (I) описываются как
(a) А имеет формулу
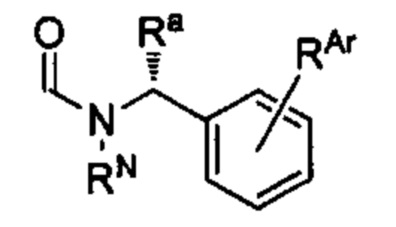
где RN, Ra, и RAr являются такими, как определено в настоящем документе; и n представляет собой 1;
(b) n представляет собой 1, и R1 представляет собой водород;
(c) А имеет формулу
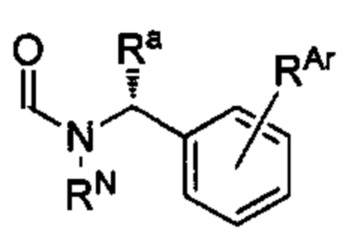
где RN, Ra, и RAr являются такими, как определено в настоящем документе; n представляет собой 1; и R1 представляет собой водород;
(d) оба R1 и R3 представляют собой водород;
(e) оба R1 и R2 представляют собой водород; и R3 имеет формулу
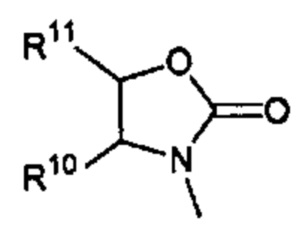
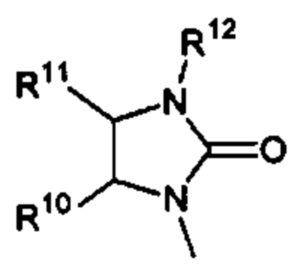
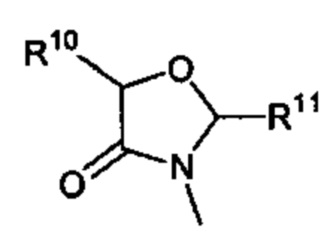
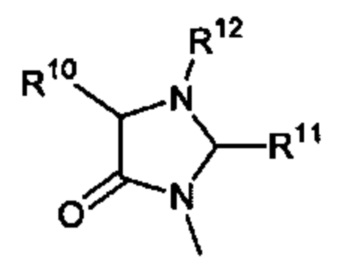
где R10, R11, и R12 являются такими, как определено в настоящем документе;
(f) А имеет формулу
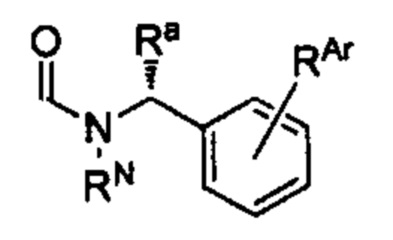
где RN, Ra, и RAr являются такими, как определено в настоящем документе; n представляет собой 1; оба R1 и R2 представляют собой водород; и R3 имеет формулу
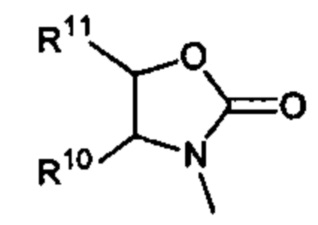
где R10 и R11 являются такими, как определено в настоящем документе;
(g) А имеет формулу
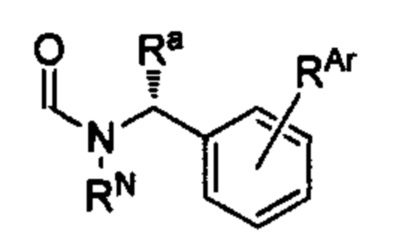
где RN, Ra, и RAr являются такими, как определено в настоящем документе; n представляет собой 1; оба R1 и R2 представляют собой водород; и А' имеет формулу
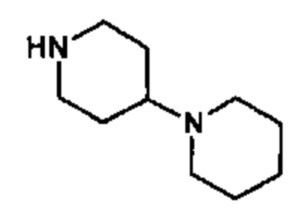 или
или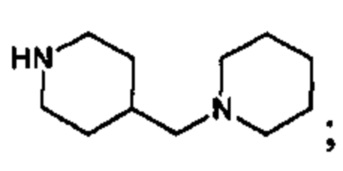
и тому подобное.
Следует понимать, что в иллюстративных пунктах и вариантах реализации, описанных в настоящем документе, А и/или А' могут включать хиральный центр, каждый из оптически чистых энантиомеров может быть включен в соединения, описанные в настоящем документе; альтернативно, может быть использована рацемическая форма. Например, один или оба следующих может быть включен в соединения, описанные в настоящем документе (R)-1-(3-метоксифенил)этиламин, (R)-1-(3-трифторметилфенил)этиламин, (R)-1,2,3,4-тетрагидро-1-нафтиламин, (R)-1-инданиламин, (R)-α,N-диметилбензиламин, (R)-α-метилбензиламин, (S)-1-(3-метоксифенил)этиламин, (S)-1-(3-трифторметилфенил)этиламин, (S)-1,2,3,4-тетрагидро-1-нафтиламин, (S)-1-инданиламин и (S)-α-метилбензиламин и т.п.
Не будучи связанными теорией, полагают, что в данном документе AVP и родственные пептиды представляют собой семейство химических сигналов у позвоночных и выполняют важную роль в контроле социального поведения и эмоций. AVP синтезируется в нейронах в гипоталамусе всех млекопитающих. Он освобождается из нервных окончаний в медиальное возвышение и переносится в гипофиз, где он усиливает высвобождение адренокортикотропного гормона (АСТН) и, в конечном счете, уровень гормонов стресса в кровотоке посредством воздействия на рецепторы AVP гипофиза. От нервных окончаний в гипофизе AVP также поступает в общий кровоток, где он действует на сердце и кровеносные сосуды с изменением работы сердца и почек с уменьшением объема мочи. Нейроны и нервные волокна AVP также встречаются по всей лимбической системе головного мозга. AVP проявляет свое физиологическое и поведенческое действие путем связывания со специфическими рецепторами, сопряженными с G-белком (GPCR), в центральной нервной системе и некоторых периферических тканях/сайтах. Были идентифицированы три различных подвида рецепторов AVP - V1a, V1b и V2. V1a является преобладающим рецептором AVP, находящимся в лимбической системе и коре головного мозга, рецептор V1b находится в лимбической системе и гипофизе, хотя он менее распространен, чем V1a. Рецептор V2 локализуется в почках, где он опосредует антидиуретический эффект вазопрессина. В настоящем изобретении полагают, что V2 не экспрессируется в нервной системе взрослых животных или людей.
Согласно другому варианту реализации соединения, описанные в настоящем документе, селективно активны в отношении рецептора AVP V1a. Согласно другому варианту реализации соединения, описанные в настоящем документе, селективно активны в отношении рецептора AVP V1a, и менее активны, существенно менее активны, и/или не активны в отношении других рецепторов AVP, таких как подвиды рецепторов AVP V1b и/или V2. Согласно другому варианту реализации соединения, описанные в настоящем документе, в 10-раз селективнее в отношении рецептора V1a по сравнению с рецептором V1b и/или V2. Согласно другому варианту реализации соединения, описанные в настоящем документе, в 100-раз селективнее в отношении V1a рецептор по сравнению с рецептором V1b и/или V2. Согласно другому варианту реализации соединения, описанные в настоящем документе, в 1000-раз селективнее в отношении V1a рецептор по сравнению с рецептором V1b и/или V2. Согласно другому варианту реализации соединения, описанные в настоящем документе, в 10000-раз селективнее в отношении V1a рецептор по сравнению с рецептором V1b и/или V2.
Согласно другому варианту реализации соединения, описанные в настоящем документе, проходят гематоэнцефалический барьер (ВВВ) и показывают высокую проницаемость ЦНС. Согласно другому варианту реализации соединения, описанные в настоящем документе, демонстрируют эффективные уровни дозировки в головном мозге для лечения нейродегенеративных расстройств. Согласно другому варианту реализации соединения, описанные в настоящем документе, демонстрируют уровни в плазме на уровне или сверх уровней, которые необходимы для клинической эффективности для лечения нейродегенеративных расстройств. Согласно другому варианту реализации соединения, описанные в настоящем документе, демонстрируют фармакокинетику, согласующуюся с дозированием дважды в сутки (b.i.d.). Согласно другому варианту реализации соединения, описанные в настоящем документе, демонстрируют фармакокинетику, согласующуюся с дозированием один раз в сутки (q.d). В настоящем изобретении следует понимать, что оба режима дозирования b.i.d. и q.d. могут быть важными компонентами в улучшении соблюдения пациентом режима лечения, что приводит к общему повышению клинической эффективности. Согласно другому варианту реализации соединения, описанные в настоящем документе, метаболически стабильны в желудке и крови. Согласно другому варианту реализации соединения, описанные в настоящем документе, демонстрируют сердечно-сосудистые профили безопасности как in vivo, так и in vitro в соответствии с лечением нейродегенеративных расстройств. Согласно другому варианту реализации соединения, описанные в настоящем документе, демонстрируют дыхательную безопасность in vivo.
Согласно другому варианту реализации соединения, описанные в настоящем документе, и фармацевтические композиции и лекарственные средства, содержащие их, демонстрируют высокие уровни в плазме крови и высокие уровни в мозгу, включая пероральное введение. Согласно другому варианту реализации соединения, описанные в настоящем документе, и фармацевтические композиции и лекарственные средства, содержащие их, способен проникать через гематоэнцефалический барьер (ВВВ), включая пероральное введение. Согласно другому варианту реализации соединения, описанные в настоящем документе, и фармацевтические композиции и лекарственные средства, содержащие их, проявляют высокую биологическую доступность в ЦНС и высокое сродство без существенного или конкурентного связывания с другими заданными GPCR, или другими заданными рецепторами, включая, но не ограничиваясь ими, рецепторы, связанные с нейротрансмиттерами, стероидные рецепторы, ионные каналы, рецепторы вторичных мессенджеров, рецепторы простагландина, рецепторы фактор роста и рецепторы гормонов, другие пептидные рецепторы головного мозга и желудочно-кишечного тракта, другие ферменты и т.п. В одном аспекте, соединения, описанные в настоящем документе, и фармацевтические композиции и лекарственные средства, содержащие их, неактивны или по существу неактивны при 100 нМ в отношении стандартной панели из 64 рецепторов, включая 35 GPCR (панель Novascreen), включая рецепторы, связанные с нейротрансмиттерами, стероидные рецепторы, ионные каналы, рецепторы вторичных мессенджеров, рецепторы простагландина, рецепторы фактор роста, рецепторы гормонов, пептиды мозга/желудка (не включая вазопрессин 1), и ферменты.
Согласно другому варианту реализации соединения, описанные в настоящем документе, и фармацевтические композиции и лекарственные средства, содержащие их, имеют специфические поведенческие эффекты, которые являются контекстно-зависимыми (см., например, Ferris & Potegal Physiology и Behavior, 44:235-239 (1988)). Например, согласно другому варианту реализации соединения, описанные в настоящем документе, и фармацевтические композиции и лекарственные средства, содержащие их эффективны в модулировании нейропсихиатрических расстройств, но малоэффективны или не влияют на сексуальное поведение.
В каждом из предшествующих пунктов и каждом из вариантов реализации, описанном в настоящем документе, следует понимать, что формулы включают и представляют собой не только все фармацевтически приемлемые соли соединений, но и включают любой и все гидраты и/или сольваты соединений формул. Следует понимать, что некоторые функциональные группы, такие как гидрокси, амино и подобные группы образуют комплексы и/или координационные соединения с водой и/или различными растворителями, в различных физических формах соединений. Соответственно, следует понимать, что приведенные выше формулы являются описанием таких гидратов и/или сольватов, в том числе фармацевтически приемлемых сольватов.
В каждом из пунктов и каждом из вариантов реализации, описанном в настоящем документе, также следует понимать, что формулы включают и представляют собой каждый возможный изомер, такой как стереоизомеры и геометрические изомеры, как оба по-отдельности, так и в любой или всех возможных смесях. В каждом из предшествующих и каждом из следующих вариантов реализации, также следует понимать, что формулы включают и представляют собой любую и все кристаллические формы, частично кристаллические формы, а также некристаллические и/или аморфные формы соединений.
В настоящем документе термин «сольваты» относится к соединениям, описанным в настоящем документе, образующим комплекс с молекулой растворителя. Следует понимать, что соединения, описанные в настоящем документе, могут образовывать такие комплексы с растворителями простым смешиванием соединений с растворителем или путем растворения соединений в растворителе. Следует понимать, что когда соединения используются в качестве фармацевтических средств, такие растворители являются фармацевтически приемлемыми растворителями. Также следует понимать, что когда соединения используются в качестве фармацевтических средств, относительное количество растворителя, который образует сольват, должно быть меньше, чем установлено требованиями в отношении таких фармацевтических применений, например, меньше, чем указано в руководстве Международной конференции по гармонизации (ICH). Следует понимать, что сольваты могут быть отделены от избыточного растворителя выпариванием, осаждением и/или кристаллизацией. Согласно некоторым вариантам реализации сольваты являются аморфными, и согласно другим вариантам реализации сольваты являются кристаллическими.
Соединения, описанные в настоящем документе, могут содержать один или более хиральных центров, или в противном случае могут существовать в виде нескольких стереоизомеров. Следует понимать, что согласно одному из вариантов реализации изобретение, описанное в настоящем документе, не ограничивается требованием к какой либо конкретной стереохимии, и что соединения и композиции, способы, применения, а также лекарственные средства, которые их включают, могут быть оптически чистыми, или, могут представлять собой любую из разнообразных смесей стереоизомеров, включая рацемические и другие смеси энантиомеров, другие смесей диастереомеров, и тому подобное. Также следует понимать, что такие смеси стереоизомеров могут включать одну стереохимическую конфигурацию на одном или более хиральных центре, при этом включая смеси стереохимической конфигурации на одном или более других хиральных центрах.
Аналогичным образом, соединения, описанные в настоящем документе, могут включать геометрические центры, такие как цис, транс, Е и Z двойных связи. Следует понимать, что в другом варианте реализации изобретение, описанное в настоящем документе, не ограничивается требованием к какому-либо конкретному геометрическому изомеру, и что соединения и композиции, способы, применения, а также лекарственные средства, которые их включают, могут быть чистыми, или могут представлять собой любую из разнообразных смесей геометрических изомеров. Также следует понимать, что такие смеси геометрических изомеров, могут включают одну конфигурацию в одной или более двойных связей, при этом включая смесь геометрии в одной или более других двойных связях.
В настоящем документе термин «алкил» включает цепь атомов углерода, которая необязательно разветвлена. В настоящем документе термины «алкенил» и «алкинил», каждый включают цепь атомов углерода, которая необязательно разветвлена, и включают по меньшей мере одну двойную связь или тройную связь, соответственно. Следует понимать, что алкинил может также включать одну или более двойных связей. Следует также понимать, что согласно некоторым вариантам реализации алкил преимущественно ограничен по длине, включая С1-С24, С1-С12, C1-C8, C1-С6, и С1-С4 и С2-С24, С2-С12, С2-С8, С2-С6, и С2-С4 и т.п. Иллюстративно, такая частная ограниченная по длине алкильная группа, включая C1-C8, C1-С6, и С1-С4, и С2-С8, С2-С6 и С2-С4 и т.п. может называться низшим алкилом. Следует также понимать, что согласно некоторым вариантам реализации каждый алкенил и/или алкинил может быть преимущественно ограничен по длине, включая С2-С24, С2-С12, С2-С8, С2-С6, и С2-С4, и С3-С24, С3-С12, С3-С8, С3-С6, и С3-С4 и т.п. Иллюстративно, такие частные ограниченные по длине алкенильные и/или алкинильные группы, включая С2-С8, С2-С6, и С2-С4, и С3-С8, С3-С6, и С3-С4 и т.п. могут называться низшим алкенилом и/или алкинилом. В настоящем документе следует понимать, что более короткие алкильные, алкенильные, и/или алкинильные группы могут добавить меньше липофильности соединению и соответственно будет иметь различное фармакокинетическое поведение. Согласно вариантам реализации изобретения, описанного в настоящем документе, следует понимать, в каждом случае, что упоминание алкила относится к алкилу, как определено в настоящем документе, и необязательно низшему алкилу. Согласно вариантам реализации изобретения, описанного в настоящем документе, следует понимать, в каждом случае, что упоминание алкенила относится к алкенилу, как определено в настоящем документе, и необязательно низшему алкенилу. Согласно вариантам реализации изобретения, описанного в настоящем документе, следует понимать, в каждом случае, что упоминание алкинила относится к алкинилу, как определено в настоящем документе, и необязательно низшему алкинилу. Иллюстративные алкильные, алкенил, и алкинил группы представляют собой, но не ограничиваются ими, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил, 2-пентил, 3-пентил, неопентил, гексил, гептил, октил и т.п., и соответствующие группы содержащих одну или более двойных и/или тройных связей, или их комбинацию.
В настоящем документе термин «алкилен» включает двухвалентную цепь атомов углерода, которая необязательно разветвлена. В настоящем документе термин «алкенилен» и «алкинилен» включает двухвалентную цепь атомов углерода, которая необязательно разветвлена, и включает по меньшей мере одну двойную связь или тройную связь, соответственно. Следует понимать, что алкинилен может также включать одну или более двойных связей. Следует также понимать, что согласно некоторым вариантам реализации алкилен преимущественно ограничен по длине, включая С1-С24, С1-С12, C1-C8, C1-С6, и С1-С4, и С2-С24, С2-С12, С2-С8, С2-С6, и С2-С4 и т.п. Иллюстративно, такие частные ограниченные по длине алкиленовые группы, включая C1-C8, C1-С6, и С1-С4, и С2-С8, С2-С6, и С2-С4 и т.п. могут называться низшим алкиленом. Следует также понимать, что согласно некоторым вариантам реализации каждый алкенилен и/или алкинилен может быть ограничен по длине, включая С2-С24, С2-С12, С2-С8, С2-С6, и С2-С4, и С3-С24, С3-С12, С3-С8, С3-С6, и С3-С4 и т.п. Иллюстративно, такие частные ограниченные по длине алкениленовые и/или алкиниленовые группы, включая С2-С8, С2-С6, и С2-С4, и С3-С8, С3-С6, и С3-С4 и т.п. могут называться низшим алкениленом и/или алкиниленом. В настоящем документе следует понимать, что более короткие алкиленовые, алкениленовые и/или алкиниленовые группы могут добавлять меньше липофильности соединению и соответственно будут иметь различное фармакокинетическое поведение. Согласно вариантам реализации изобретения, описанного в настоящем документе, следует понимать, в каждом случае, что упоминание алкилена, алкенилена и алкинилена относится к алкилену, алкенилену и алкинилену, как определено в настоящем документе, и необязательно низшему алкилену, алкенилену и алкинилену. Иллюстративные алкильные группы представляют собой, но не ограничиваются ими, метилен, этилен, н-пропилен, изопропилен, н-бутилен, изобутилен, втор-бутилен, пентилен, 1,2-пентилен, 1,3-пентилен, гексилен, гептилен, октален и т.п.
В настоящем документе термин «циклоалкил» включает цепь атомов углерода, которая необязательно разветвлена, где по меньшей мере часть цепи является циклической. Следует понимать, что циклоалкилалкил представляет собой подгруппу циклоалкила. Следует понимать, что циклоалкил может быть полициклическим. Иллюстративные циклоалкилы включают, но не ограничиваются ими, циклопропил, циклопентил, циклогексил, 2-метилциклопропил, циклопентилэт-2-ил, адамантил и т.п. В настоящем документе термин «циклоалкенил» включает цепь атомов углерода, которая необязательно разветвлена, и включает по меньшей мере одну двойную связь, где по меньшей мере часть цепи является циклической. Следует понимать, что одна или более двойных связей может быть в циклической части циклоалкенила и/или нециклической части циклоалкенил. Следует понимать, что каждый циклоалкенилалкил и циклоалкилалкенил представляет собой подгруппу циклоалкенила. Следует понимать, что циклоалкил может быть полициклическим. Иллюстративные циклоалкенилы включают, но не ограничиваются ими, циклопентенил, циклогексилэтен-2-ил, циклогептенилпропенил и т.п. Следует также понимать, что цепеобразующий циклоалкил и/или циклоалкенил преимущественно ограничен по длине, включая С3-С24, С3-С12, С3-С8, С3-С6 и С5-С6. В настоящем документе следует понимать, что более короткие алкильные и/или алкенильные цепеобразующие циклоалкилы и/или циклоалкенилы, соответственно, могут добавлять меньше липофильности соединению и соответственно будут иметь различное фармакокинетическое поведение.
В настоящем документе термин «гетероалкил» включает цепь атомов, которая включает как углерод, так и по меньшей мере один гетероатом, и он необязательно разветвлен. Иллюстративные гетероатомы включают азот, кислород и серу. В некоторых вариантах иллюстративные гетероатомы также включают фосфор и селен. В настоящем документе термин «циклогетероалкил», включая гетероциклил и гетероцикл, включает цепь атомов, которая включает как углерод, так и по меньшей мере один гетероатом, например, гетероалкил, и необязательно разветвлена, где по меньшей мере часть цепи является циклической. Иллюстративные гетероатомы включают азот, кислород и серу. В некоторых вариантах иллюстративные гетероатомы также включают фосфор и селен. Иллюстративные циклогетероалкил включают, но не ограничиваются ими, тетрагидрофурил, пирролидинил, тетрагидропиранил, пиперидинил, морфолинил, пиперазинил, гомопиперазинил, хинуклидинил и т.п.
В настоящем документе термин «арил» включает моноциклические и полициклические ароматические карбоциклические группы, каждая из которых может быть необязательно замещена. Иллюстративные ароматические карбоциклические группы, описанные в настоящем документе, включают, но не ограничиваются ими, фенил, нафтил и т.п. В настоящем документе термин «гетероарил» включает ароматические гетероциклические группы, каждая из которых может быть необязательно замещена. Иллюстративные ароматические гетероциклические группы включают, но не ограничиваются ими, пиридинил, пиримидинил, пиразинил, триазинил, тетразинил, хинолинил, хиназолинил, хиноксалинил, тиенил, пиразолил, имидазолил, оксазолил, тиазолил, изоксазолил, изотиазолил, оксадиазолил, тиадиазолил, триазолил, бензимидазолил, бензоксазолил, бензтиазолил, бензизоксазолил, бензизотиазолил и т.п.
В настоящем документе термин «амино» включает группу NH2, алкиламино, и диалкиламино, где две алкильные группы в диалкиламино могут быть одинаковыми или различными, т.е. алкилалкиламино. Иллюстративно, амино включает метиламино, этиламино, диметиламино, метилэтиламино и т.п. Кроме того, следует понимать, что когда амино модифицирует или модифицирован другим термином, например как аминоалкил или ациламино, указанные выше варианты данного термина амино включены в объем настоящего изобретения. Иллюстративно, аминоалкил включает H2N-алкил, метиламиноалкил, этиламиноалкил, диметиламиноалкил, метилэтиламиноалкил и т.п. Иллюстративно, ациламино включает ацилметиламино, ацилэтиламино и т.п.
В настоящем документе термин «амино и его производные» включает аминогруппы, описанные в настоящем документе, и алкиламино, алкениламино, алкиниламино, гетероалкиламино, гетероалкениламино, гетероалкиниламино, циклоалкиламино, циклоалкениламино, циклогетероалкиламино, циклогетероалкениламино, ариламино, арилалкиламино, арилалкениламино, арилалкиниламино, гетероариламино, гетероарилалкиламино, гетероарилалкениламино, гетероарилалкиниламино, ациламино и т.п., каждый из которых необязательно замещен. Термин «производное амино» также включает мочевину, карбамат и т.п.
В настоящем документе термин «гидрокси и его производные» включает ОН и алкилокси, алкенилокси, алкинилокси, гетероалкилокси, гетероалкенилокси, гетероалкинилокси, циклоалкилокси, циклоалкенилокси, циклогетероалкилокси, циклогетероалкенилокси, арилокси, арилалкилокси, арилалкенилокси, арилалкинилокси, гетероарилокси, гетероарилалкилокси, гетероарилалкенилокси, гетероарилалкинилокси, ацилокси и т.п., каждый из которых необязательно замещен. Термин «производное гидрокси» также включает карбамат и т.п.
В настоящем документе термин «тио и его производные» включает SH и алкилтио, алкенилтио, алкинилтио, гетероалкилтио, гетероалкенилтио, гетероалкинилтио, циклоалкилтио, циклоалкенилтио, циклогетероалкилтио, циклогетероалкенилтио, арилтио, арилалкилтио, арилалкенилтио, арилалкинилтио, гетероарилтио, гетероарилалкилтио, гетероарилалкенилтио, гетероарилалкинилтио, ацилтио и т.п., каждый из которых необязательно замещен. Термин «производное тио» также включает тиокарбамат и т.п.
В настоящем документе термин «ацил» включает формил и алкилкарбонил, алкенилкарбонил, алкинилкарбонил, гетероалкилкарбонил, гетероалкенилкарбонил, гетероалкинилкарбонил, циклоалкилкарбонил, циклоалкенилкарбонил, циклогетероалкилкарбонил, циклогетероалкенилкарбонил, арилкарбонил, арилалкилкарбонил, арилалкенилкарбонил, арилалкинилкарбонил, гетероарилкарбонил, гетероарилалкилкарбонил, гетероарилалкенилкарбонил, гетероарилалкинилкарбонил, ацилкарбонил и т.п., каждый из которых необязательно замещен.
В настоящем документе термин «карбонил и его производные» включает группу С(О), C(S), C(NH) и замещенные его аминопроизводные.
В настоящем документе термин «карбоновая кислота и ее производные» включает группу СО2Н и ее соли и сложные эфиры и амиды, и CN.
В настоящем документе термин «сульфиновая кислота или ее производное» включает SO2H и ее соли, и сложные эфиры и амиды.
В настоящем документе термин «сульфоновая кислота или ее производное» включает SO3H и ее соли, и сложные эфиры и амиды.
В настоящем документе термин «сульфонил» включает алкилсульфонил, алкенилсульфонил, алкинилсульфонил, гетероалкилсульфонил, гетероалкенилсульфонил, гетероалкинилсульфонил, циклоалкилсульфонил, циклоалкенилсульфонил, циклогетероалкилсульфонил, циклогетероалкенилсульфонил, арилсульфонил, арилалкилсульфонил, арилалкенилсульфонил, арилалкинилсульфонил, гетероарилсульфонил, гетероарилалкилсульфонил, гетероарилалкенилсульфонил, гетероарилалкинилсульфонил, ацилсульфонил и т.п., каждый из которых необязательно замещен.
В настоящем документе термин «гидроксиламино и его производные» включает NHOH и алкилоксилNН алкенилоксилNН алкинилоксилNН гетероалкилоксилNH гетероалкенилоксилNН гетероалкинилоксилNН циклоалкилоксилNН циклоалкенилоксилNН циклогетероалкилоксилNН циклогетероалкенилоксилNН арилоксилNН арилалкилоксилNН арилалкенилоксилNН арилалкинилоксилNH гетероарилоксилNН гетероарилалкилоксилNН гетероарилалкенилоксилNН гетероарилалкинилоксилNН ацилокси и т.п., каждый из которых необязательно замещен.
В настоящем документе термин «гидразино и его производные» включает алкилNHNH, алкенилNHNH, алкинилNHNH, гетероалкилNНNН, гетероалкенилNНNН, гетероалкинилNНNН, циклоалкилNНNН, циклоалкенилNНNН, циклогетероалкилNНNН, циклогетероалкенилNНNН, арилNHNH, арилалкилNНNН, арилалкенилNНNН, арилалкинилNНNН, гетероарилNНNН, гетероарилалкилNНNН, гетероарилалкенилNНNН, гетероарилалкинилNНNН, ацилNНNН и т.п., каждый из которых необязательно замещен.
Термин «необязательно замещенный» в настоящем документе включает замену атомов водорода другими функциональными группами на радикале, которые является необязательно замещенным. Такие другие функциональные группы иллюстративно включают, но не ограничиваются ими, амино, гидроксил, галоген, тиол, алкил, галогеналкил, гетероалкил, арил, арилалкил, арилгетероалкил, гетероарил, гетероарилалкил, гетероарилгетероалкил, нитро, сульфоновые кислоты и их производные, карбоновые кислоты и их производные и т.п. Иллюстративно, любой из амино, гидроксила, тиола, алкила, галогеналкила, гетероалкила, арила, арилалкила, арилгетероалкила, гетероарила, гетероарилалкила, гетероарилгетероалкила и/или сульфоновой кислоты необязательно замещен.
В настоящем документе термины «необязательно замещенный арил» и «необязательно замещенный гетероарил» включают замену атомов водорода другими функциональными группами на ариле или гетероариле, который является необязательно замещенным. Такие другие функциональные группы иллюстративно включают, но не ограничиваются ими, амино, гидрокси, галоген, тио, алкил, галогеналкил, гетероалкил, арил, арилалкил, арилгетероалкил, гетероарил, гетероарилалкил, гетероарилгетероалкил, нитро, сульфоновые кислоты и их производные, карбоновые кислоты и их производные и т.п. Иллюстративно, любой из амино, гидрокси, тио, алкила, галогеналкила, гетероалкила, арила, арилалкила, арилгетероалкила, гетероарила, гетероарилалкила, гетероарилгетероалкила и/или сульфоновой кислоты необязательно замещен.
Иллюстративные заместители включают, но не ограничиваются ими, радикал -(CH2)xZX, где х представляет собой целое число от 0-6 и Zx выбран из галогена, гидрокси, алканоилокси, включая C1-С6 алканоилокси, необязательно замещенный ароилокси, алкил, включая C1-С6 алкил, алкокси, включая C1-С6 алкокси, циклоалкил, включая С3-C8 циклоалкил, циклоалкокси, включая С3-C8 циклоалкокси, алкенил, включая С2-С6 алкенил, алкинил, включая С2-С6 алкинил, галогеналкил, включая C1-C6 галогеналкил, галогеналкокси, включая C1-C6 галогеналкокси, галогенциклоалкил, включая С3-C8 галогенциклоалкил, галогенциклоалкокси, включая С3-C8 галогенциклоалкокси, амино, C1-С6 алкиламино, (C1-С6 алкил)(С1-С6 алкил)амино, алкилкарбониламино, N-(C1-C6 алкил)алкилкарбониламино, аминоалкил, C1-C6 алкиламиноалкил, (C1-С6 алкил)(С1-С6 алкил)аминоалкил, алкилкарбониламиноалкил, N-(C1-C6 алкил)алкилкарбониламиноалкил, циано и нитро; или ZX выбран из -CO2R4 и -CONR5R6, где каждый R4, R5, и R6 выбран независимо в каждом случае из водорода, C1-С6 алкила, арил-C1-С6 алкила и гетероарил-С1-С6 алкила.
Термин «пролекарство» в настоящем документе в целом относится к любому соединению, которое при введении в биологическую систему генерирует биологически активное соединение в результате одного или более из спонтанной химической реакции(-й), ферментативной химической реакции(-й) и/или метаболический химической реакции(-й), или их комбинации. In vivo, на пролекарство обычно воздействует фермент (например, эстеразы, фосфатазы, амидазы и т.п.), простая биологическая химия или другой процесс in vivo, с высвобождением или регенерацией более фармакологически активного лекарственного средства. Данная активация может происходить под действием эндогенного фермента хозяина или неэндогенного фермента, который вводят хозяину перед, после или во время введения пролекарства. Дополнительные подробности использования пролекарств описаны в патенте США. №5627165. Следует понимать, что пролекарство предпочтительно преобразуется в оригинальное лекарственное средство, как только достигаются цели, такие как направленная доставка, безопасности, стабильность и тому подобное, с последующим быстрым выведением высвободившихся остатков группы, образующей пролекарство.
Пролекарства можно получать из соединений, описанных в настоящем документе, путем присоединения группы, которая полностью расщепляется in vivo до одной или более функциональной группы, присутствующей на соединении, такой как -ОН-, -SH, -СО2Н, -NR2. Иллюстративные пролекарства включают, но не ограничиваются ими, карбоксилатные сложные эфиры, где группа представляет собой алкил, арил, арилалкил, гетероарил, гетероарилалкил, ацилоксиалкил, алкоксикарбонилоксиалкил, а также сложные эфиры гидроксила, тиола и аминов, где присоединенная группа представляет собой ацильную группу, алкоксикарбонил, аминокарбонил, фосфат или сульфат. Иллюстративные сложные эфиры, также называемые как активные сложные эфиры, включают, но не ограничиваются ими, 1-инданил, N-оксисукцинимид; ацилоксиалкильные группы, такие как ацетоксиметил, пивалоилоксиметил, β-ацетоксиэтил, β-пивалоилоксиэтил, 1-(циклогексилкарбонилокси)проп-1-ил, (1-аминоэтил)карбонилоксиметил и т.п.; алкоксикарбонилоксиалкильные группы, такие как этоксикарбонилоксиметил, α-этоксикарбонилоксиэтил, β-этоксикарбонилоксиэтил и т.п.; диалкиламиноалкильные группы, включая ди-низшие алкиламиноалкильные группы, такие как диметиламинометил, диметиламиноэтил, диэтиламинометил, диэтиламиноэтил и т.п.; 2-(алкоксикарбонил)-2-алкенильные группы, такие как 2-(изобутоксикарбонил) пент-2-енил, 2-(этоксикарбонил)бут-2-енил и т.п.; и лактоновые группы, такие как фталидил, диметоксифталидил и т.п.
Дополнительные иллюстративные пролекарства содержат химический фрагмент, такой как амидная или фосфорная группа, действующие с увеличением растворимости и/или стабильности соединений, описанных в настоящем документе. Дополнительные иллюстративные пролекарства для аминогрупп включают, но не ограничиваются ими, (С3-С20)алканоил; галоген-(С3-С20)алканоил; (С3-С20)алкеноил; (С4-С7)циклоалканоил; (С3-С6)-циклоалкил(С2-С16)алканоил; необязательно замещенного ароил, такой как незамещенный ароил или ароил, замещенный 1-3 заместителями, выбранными из группы, состоящей из галогена, циано, трифторметансульфанилокси, (C1-С3)алкила и (С1-С3)алкокси, каждый из которых необязательно дополнительно замещен одним или более из 1-3 атомов галогена; необязательно замещенного арил(С2-С16)алканоила и необязательно замещенного гетероарил(С2-С16)алканоила, например арильный или гетероарильный радикал является незамещенным или замещенным 1-3 заместителями, выбранными из группы, состоящей из галогена, (С1-С3)алкила и (C1-С3)алкокси, каждый из которых необязательно дополнительно замещен 1-3 атомами галогена; и необязательно замещенного гетероарилалканоила, имеющего от одного до трех гетероатомов, выбранных из О, S и N в гетероарильном фрагменте и 2-10 атомов углерода в алканоильном фрагменте, например гетероарильный радикал является незамещенным или замещенным 1-3 заместителями, выбранными из группы, состоящей из галогена, циано, трифторметансульфанилокси, (С1-С3)алкила и (С1-С3)алкокси, каждый из которых необязательно дополнительно замещен 1-3 атомами галогена. Показанные группы являются иллюстративными, а не исчерпывающими, и могут быть получены традиционными способами.
Следует понимать, что сами пролекарства могут не обладать существенной биологической активностью, но вместо того подвергаться одной или более спонтанной химической реакции(ям), катализируемым ферментами химическим реакции (ям) и/или метаболической химической реакции(ям), или их комбинации после введения in vivo с получением соединения, описанного в настоящем документе, которое является биологически активным или является предшественником биологически активного соединения. Тем не менее, следует понимать, что в некоторых случаях пролекарство является биологически активным. Необходимо также понимать, что пролекарства могут часто служить для улучшения эффективности или безопасности лекарственного средства благодаря улучшению биодоступности при пероральном введении, фармакодинамического периода полувыведения и тому подобного. Пролекарства также относится к производным описанных в настоящем документе соединений, которые включают группы, которые просто маскируют нежелательные свойства лекарственных средств или улучшают доставку лекарственного средства. Например, одно или более соединений, описанных в настоящем документе, могут проявлять нежелательное свойство, которое предпочтительно блокируют или минимизируют, которое может стать фармакологическим, фармацевтическим или фармакокинетическим барьером при клиническом применении лекарственного средства, таким как низкая абсорбция лекарственного средства при пероральном введении, отсутствие специфичности к месту действия, химическая нестабильность, токсичность и плохое соблюдение режима лечения пациентом (плохой вкус, запах, боль в месте инъекции, и тому подобное), и другие. Следует понимать, что в настоящем документе пролекарства или другая стратегия с использованием обратимых производных, могут быть полезны для оптимизации клинического применения лекарственного средства.
В настоящем документе термин «уходящая группа» относится к реакционноспособной функциональной группе, которая генерирует электрофильный сайт на атоме, к которому он присоединен таким образом, что нуклеофилы могут быть добавлены к электрофильному сайту на указанном атоме. Иллюстративные уходящие группы, включают, но не ограничиваются ими, галогены, необязательно замещенные фенолы, ацилоксигруппы, сульфонокси группы и тому подобное. Следует понимать, что такие уходящие группы, могут быть на алкиле, ациле и т.п. Такие уходящие группы, могут также называться в настоящем документе как активирующие группы, например, когда уходящая группа присутствует на ациле. Кроме того, традиционные пептидные, амидные и сложноэфирные агенты сочетания, такие как, но не ограничиваясь ими РуВор, ВОР-Сl, ВОР, пентафторфенол, изобутилхлорформиат и т.п., образуют различные промежуточные соединения, которые включают уходящую группу, как определено в настоящем документе, на карбонильной группе.
Следует понимать, что в каждом случае, описанном в настоящем документе, обозначение диапазона целых чисел для любой переменной описывает обозначенный диапазон, каждый индивидуальный элемент в указанном диапазоне, а также все возможные поддиапазоны для этой переменной. Например, обозначение, что n представляет собой целое число от 0 до 8, описывает этот диапазон, индивидуальные и выбираемые значения 0, 1, 2, 3, 4, 5, 6, 7 и 8, такие как n равно 0, или n равно 1 или n равно 2 и т.д. Кроме того, обозначение, что n представляет собой целое число от 0 до 8, также описывает каждый поддиапазон, каждый из которых может служить основанием еще одному варианту реализации, таком как n представляет собой целое число от 1 до 8, от 1 до 7, от 1 до 6, от 2 до 8, от 2 до 7, от 1 до 3, от 2 до 4, и т.д.
В настоящем документе термины «обработка», «приведение в контакт» или «взаимодействие», когда они относятся к химической реакции, как правило, означают добавление или смешивание двух или более реагентов в соответствующих условиях, позволяющих осуществить химическое превращение или химическую реакцию, и/или получить указанный и/или требуемый продукт. Следует понимать, что реакция, которая приводит к указанному и/или требуемому продукту, необязательно может происходить непосредственно из комбинации двух реагентов, которые были первоначально добавлены. Другими словами, может быть одно или более промежуточных соединений, которые образуются в смеси, которая, в конечном счете, приводит к образованию указанного и/или требуемого продукта.
В настоящем документе термин «композиция» в целом относится к любому продукту, содержащему определенные ингредиенты в определенных количествах, а также любой продукт, который получен прямо или косвенно из комбинаций определенных ингредиентов в определенных количествах. Следует понимать, что композиции, описанные в настоящем документе, могут быть получены из выделенных соединений, описанных в настоящем документе, или из солей, растворов, гидратов, сольватов и других форм соединений, описанных в настоящем документе. Также следует понимать, что композиции могут быть получены из различных аморфных, неаморфных, частично кристаллических, кристаллических и/или других морфологических форм соединений, описанных в настоящем документе. Также следует понимать, что композиции могут быть получены из различных гидратов и/или сольватов соединений, описанных в настоящем документе. Таким образом, следует понимать, что такие фармацевтические композиции, которые перечисляют соединения, описанные в настоящем документе, включают каждую из или любую комбинацию различных морфологических форм и/или сольватных или гидратных форм соединений, описанных в настоящем документе. Кроме того, следует понимать, что композиции могут быть получены из различных сокристаллов соединений, описанных в настоящем документе.
Иллюстративно, композиции могут включать один или более носителей, разбавителей и/или вспомогательных веществ. Соединения, описанные в настоящем документе, или композиции, их содержащие, могут быть приготовлены в терапевтически эффективном количестве в любых традиционных лекарственных формах, подходящих для способов, описанных в настоящем документе. Соединения, описанные в настоящем документе, или композиции, их содержащие, включая такие составы, могут быть введены с помощью широкого спектра традиционных способов, описанных в настоящем документе, а также широкого спектра форматов дозирования с использованием хорошо известных процедур (см. в целом, Remington: The Science и Practice of Pharmacy, (21st ed., 2005)).
Термин «терапевтически эффективное количество», используемый в настоящем документе, относится к такому количеству активного соединения или фармацевтического агента, которое вызывает биологический или медицинский ответ в тканевой системе, животном или человеке, рассматриваемом исследователем, ветеринаром, врачом или другим клиницистом, которое включает ослабление симптомов заболевания или расстройства, подвергаемого лечению. В одном аспекте терапевтически эффективное количество представляет собой количество, которое может лечить или облегчить заболевание или симптомы заболевания при разумном соотношении польза/риск, применимых к любому медицинскому лечению. Тем не менее, следует понимать, что общая суточная доза соединений и композиций, описанных в настоящем документе, может быть определена лечащим врачом в рамках здравого медицинского суждения. Специфический терапевтически эффективный уровень дозы для любого конкретного пациента будет зависеть от множества факторов, включая расстройство, подвергаемое лечению, и тяжесть заболевания; активность конкретного используемого соединения; конкретную используемой композиции; возраст, массу тела, общее состояние здоровья, пол и диету пациента: время введения, способ введения и скорость выведения конкретного используемого соединения; продолжительность лечения; лекарственные средства, используемые в комбинации или случайно совместно с конкретным используемым соединением; и подобных факторов, хорошо известных исследователю, ветеринару, лечащему врачу или другому клиницисту обычной квалификации.
Необходимо также отметить, что терапевтически эффективное количество, будь то со ссылкой на монотерапию или комбинированную терапию, преимущественно выбирают принимая во внимание на какую-либо токсичность или другие нежелательные побочные эффекты, которые могут возникнуть во время введения одного или более соединений, описанных в настоящем документе. Кроме того, следует понимать, что совместные терапии, описанные в настоящем документе, могут допускать введение более низких доз соединений, которые показывают такую токсичность или другой нежелательный побочный эффект, где указанные более низкие дозы ниже порогов токсичности или ниже в терапевтическом окне, чем можно было бы в противном случае вводить в отсутствие совместной терапии.
В дополнение к иллюстративным дозировкам и протоколам дозирования, описанным в настоящем документе, следует понимать, что эффективное количество любого одного или смеси соединений, описанных в настоящем документе, может быть легко определено практикующим диагностом или врачом с использованием известных методов и/или путем наблюдения результатов, полученных в аналогичных условиях. При определении эффективного количества или дозы, ряд факторов рассматриваются диагностом или врачом, в том числе, но не ограничиваясь ими, виды млекопитающих, включая человека, его размер, возраст и общее состояние здоровья, конкретное заболевание или расстройство, степень или участие или тяжесть заболевания или расстройства, реакцию отдельного пациента, конкретное вводимое соединения, способ введения, характеристику биодоступности вводимого препарата, выбранный режим дозирования, использование сопутствующих медикаментов и другие обстоятельства, имеющие значение.
Дозировка каждого из соединений заявленных комбинаций зависит от нескольких факторов, в том числе: от способа введения, состояния, подлежащего лечению, тяжести состояния, от того следует ли лечить или предотвращать состояние, а также возраста, веса и здоровья лица, подлежащего лечению. Кроме того, фармакогеномическая (влияние генотипа на фармакокинетические, фармакодинамические профили или профиль эффективности терапевтического средства) информация о конкретном пациенте может повлиять на дозировку.
Следует понимать, что в способах, описанных в настоящем документе, отдельные компоненты совместного введения или комбинации могут быть введены с помощью любого подходящего средства, одновременно, одновременно, последовательно, раздельно или в одном фармацевтическом составе. Там, где совместно вводимые соединения или композиции вводят в виде отдельных лекарственных форм, количество доз, вводимых в сутки для каждого соединения, может быть одинаковым или различным. Соединения или композиции могут быть введены с помощью одних и тех же или различных способов введения. Соединения или композиции могут быть введены в соответствии с одновременными или чередующимися режимами, в одно и тоже или разное время в течение курса терапии, одновременно разделенных или единичных формах.
Термин «введение», используемый в настоящем документе, включает все средства введения соединений и композиций, описанных в настоящем документе, животному-хозяину, в том числе, но не ограничиваясь ими, пероральное (по), внутривенное (вв), внутримышечное (вм), подкожное (пк), трансдермальное (тд), ингаляционные, буккальное, глазное, сублингвальное, вагинальное, ректальное и тому подобное. Соединения и композиции, описанные в настоящем документе, могут быть введены в виде единичных дозированных форм и/или составов, содержащих традиционные нетоксичные фармацевтически приемлемые носители, адъюванты и/или носители.
При получении фармацевтических композиций из соединений, описанных в данном описании, терапевтически эффективное количество одного или более соединений в любой из различных форм, описанных в настоящем документе, может быть смешано с одним или более вспомогательными веществами, разбавлено одним или более вспомогательными веществами или заключено в таком носителе, который может быть в форме капсулы, саше, бумаги или другого контейнера. Вспомогательные вещества могут служить в качестве разбавителя, и могут быть твердыми, полутвердыми или жидкими материалами, которые действуют как переносящая среда, носитель или среда для активного ингредиента. Таким образом, состав композиций может быть в форме таблеток, пилюль, порошков, таблеток для рассасывания, саше, крахмальных капсул, эликсиров, суспензий, эмульсий, растворов, сиропов, аэрозолей (в твердой или в жидкой среде), мазей, мягких и твердых желатиновых капсул, суппозиториев, стерильных растворов для инъекций и стерильных упакованных порошков. Композиции могут содержать от примерно 0,1% до примерно 99,9% активных ингредиентов, в зависимости от выбранной дозы и лекарственной формы.
Термин «антагонист», используемый в настоящем документе, относится к полному или частичному антагонисту. В то время как частичный антагонист любой внутренней активности может быть полезным, частичные антагонисты иллюстративно демонстрируют по меньшей мере примерно 50% антагонистическое действие или по меньшей мере примерно 80% антагонистического действие. Термин также включает соединения, которые являются полными антагонистами одного или более рецепторов вазопрессина. Следует понимать, что иллюстративные методы, описанные в настоящем документе, требуют терапевтически эффективные количества антагонистов рецепторов вазопрессина; следовательно соединения, проявляющие частичный антагонизм в отношении одного или более рецепторов вазопрессина могут быть введены в более высоких дозах, чтобы обеспечить достаточную активность антагониста по ингибированию эффектов вазопрессина или агониста вазопрессина.
Эффективное применение соединений, композиций и способов, описанных в настоящем документе, для лечения или облегчения одного или более эффектов нейродегенеративного заболевания с использованием одного или более соединений, описанных в настоящем документе, может быть основано на животных моделях, таких как мышиные, собачьи, свиные модели заболевания и животных моделях приматов, не представляющих собой человека. Например, следует понимать, что нейродегенеративные заболевания у человека могут характеризоваться потерей функции и/или развитием симптомов, каждый из которых может быть выявлен у животных, таких как мыши и другие суррогатные подопытные животные. В частности, мышиные модели, описанные в настоящем документе, могут быть использованы для оценки способов лечения и фармацевтических композиций, описанных в настоящем документе, чтобы определить терапевтически эффективные количества, описанные в настоящем документе.
Каждая публикация, цитируемая в настоящем документе, включена в данное описание посредством ссылки.
Следующие примеры дополнительно иллюстрируют конкретные варианты реализации настоящего изобретения; однако следующие иллюстративные примеры не должны быть истолкованы как ограничивающие изобретение.
ПРИМЕРЫ
ПРИМЕРЫ СПОСОБОВ
ПРИМЕР. Анализ связывания рецептора вазопрессина V1a человека. Клеточную линию, экспрессирующую рецептор V1a человека в клетках СНО (далее также называемые как клеточная линия hV1a) получали от Dr. Michael Brownstein, NIMH, Bethesda, MD, USA. Последовательность кДНК hV1a описана Thibonnier et al., Journal of Biological Chemistry, 269, 3304-3310 (1994), и способ экспрессии был таким же, как описано у Morel et al. (1992). Клеточную линию hV1a выращивали в альфа-MEM с 10% фетальной бычьей сывороткой и 250 мкг/мл G418 (Gibco, Grand Island, NY, USA). Для конкурентного анализа связывания клетки hV1a размещали в 6-луночный культуральный планшет при 1:10 разведении из достигшей конфлуэнтности колбы, и сохраняли в культуре в течение по меньшей мере двух дней. Затем культуральную среду удаляли, клетки промывали 2 мл связывающего буфера (25 мМ Hepes, 0,25% BSA, 1x DMEM, РН=7,0). В каждую лунку добавляли 990 мкл связывающего буфера, содержащего 1 нМ 3Н-AVP, и впоследствии добавляли 10 мкл серийных разведений примеров соединений, растворенных в ДМСО. Все инкубации проводили в трех экземплярах, и кривые зависимости ингибирования от дозировки состояли из точек, соответствующих общему связыванию (ДМСО) и 5 концентрациям (0,1, 1,0, 10, 1000 и 1000 нМ) тестируемых агентов, охватывающих IC50. 100 нМ не меченого AVP (Sigma) использовали для оценки неспецифического связывания. Клетки инкубировали в течение 45 минут при 37°С, смесь для анализа удаляли и каждую лунку промывали три раза PBS (рН=7,4). 1 мл 2% SDS добавляли в каждую лунку и содержимому планшетов давали осесть в течение в течение 30 минут. Все содержимое из лунки переносили во флакон для подсчета сцинтилляции. Каждую лунку промывали 0,5 мл PBS, который затем добавляли в соответствующие флаконы. Затем добавляли сцинтилляционную жидкость (Ecoscint, National Diagnostics, Atlanta, Georgia) в количестве 3 мл на сосуд. Проводили подсчет образцов на счетчике сцинтилляции жидкостей (Beckman LS3801). Значения IC50 подсчитывали с помощью программного обеспечения Prism Curve для построения кривых по точкам.
Все алкандиоловые сложные эфиры и амиды, примеры которых приведены в предыдущих примерах, растворенные в ДМСО, тестировали в данном анализе. Кривые связывания были получены в соответствии с методами, описанными Thibonnier et al. (1994). [3H]-AVP добавляли к клеточным культурам hV1a, с последующим добавлением 10-кратных разбавлений каждого исследуемого соединения. Все активные соединения показали дозозависимую кривую конкурентного связывания, со значениями IC50 и Ki, характерными для высокой аффинности связывания с рецепторами V1a в клетках СНО, экспрессирующих V1a человека (клеточная линия hV1a). Например, Пример 225 показал дозозависимую кривую конкурентного связывания со значениями IC50 (1,86-2,13 нМ) и Ki (1,14-1,30 нМ).
Аффинность связывания (IC50) и константы ингибирования (Ki) для иллюстративных соединений приведены в следующей таблице.
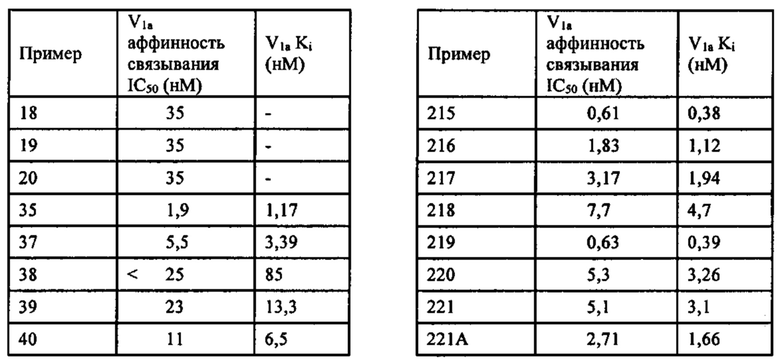
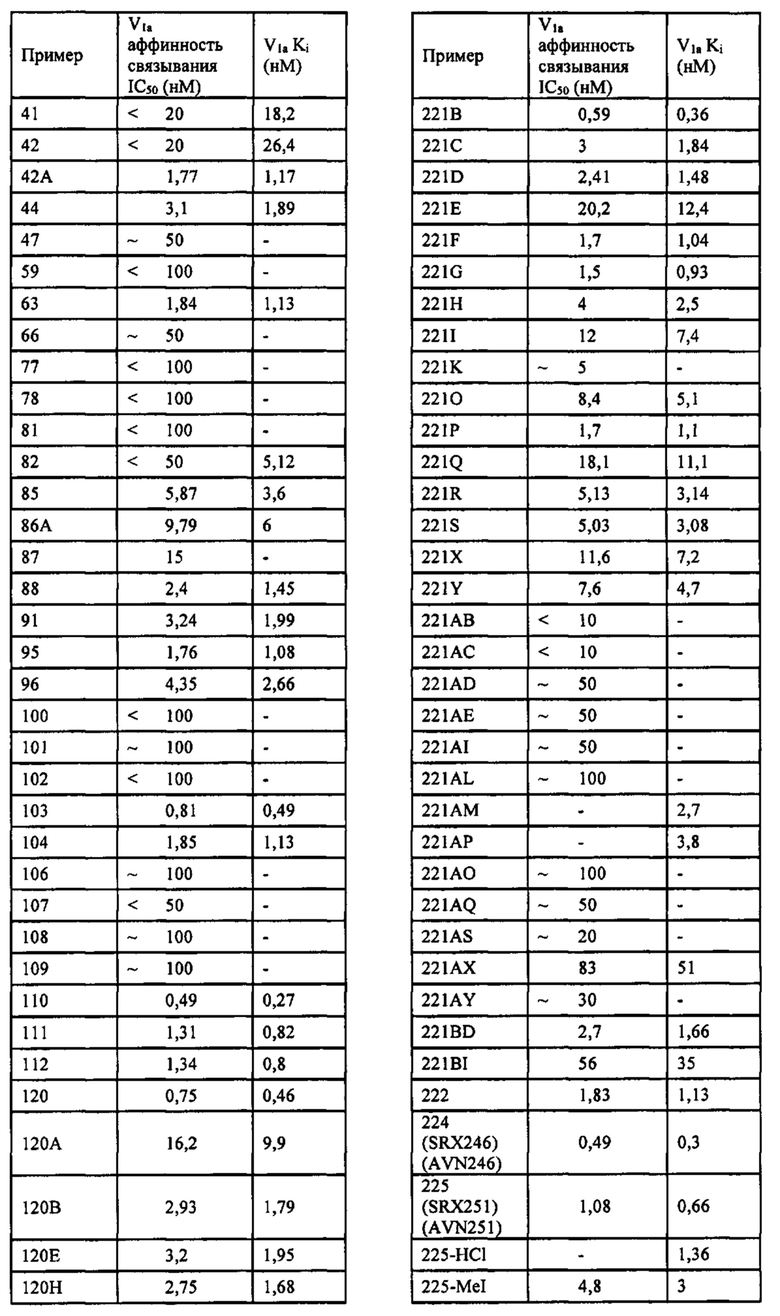
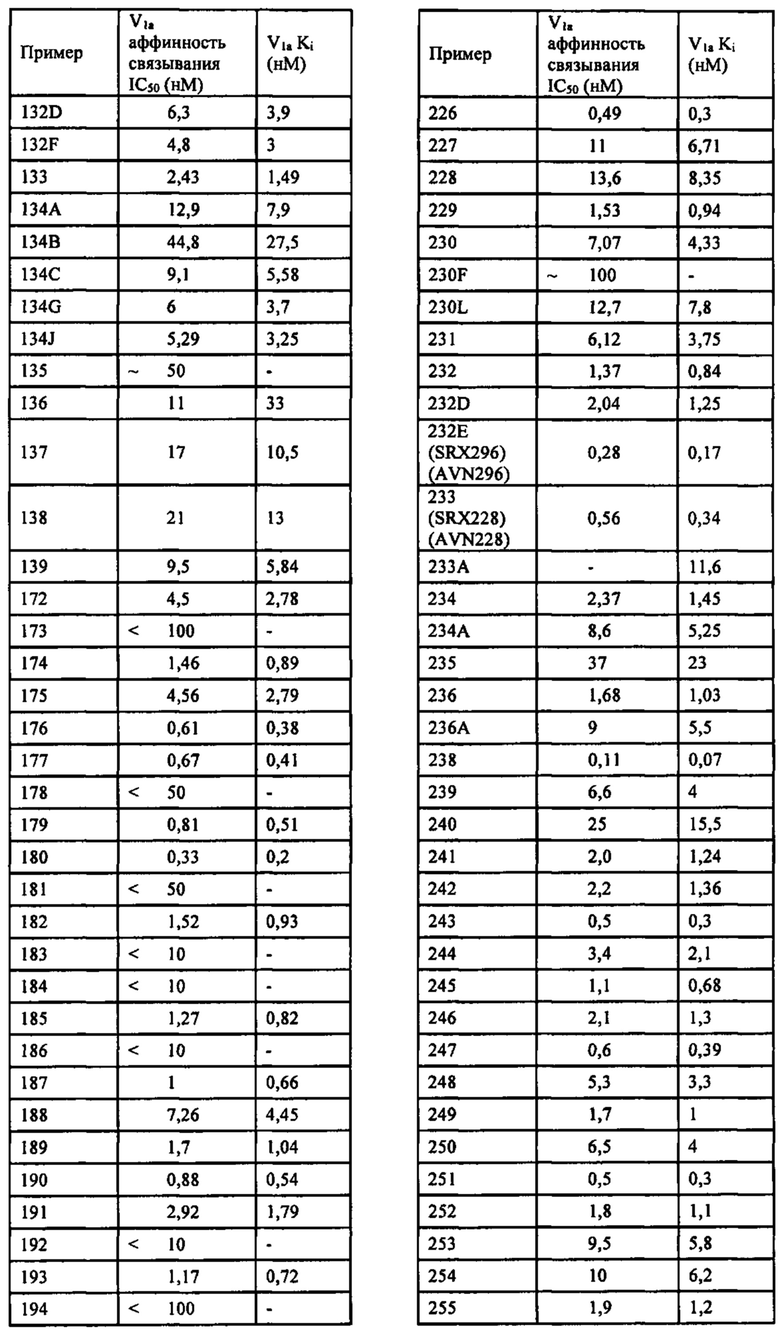
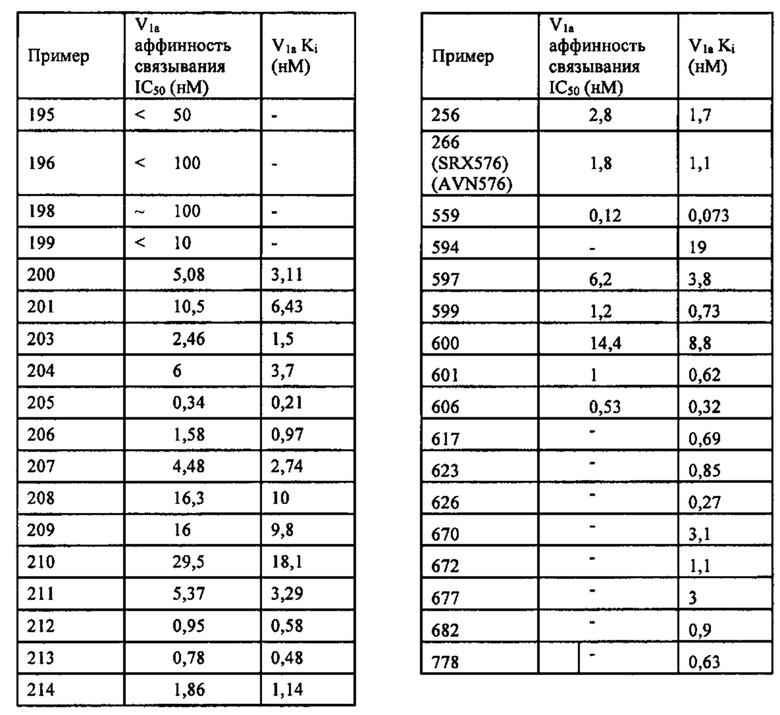
ПРИМЕР. Клетки, экспрессирующие человеческий рецептор вазопрессина V1b. кДНК рецептора вазопрессина 1b (hV1b) человека (см. Lolait et al., "Extrapituitary expression of the rat V1b vasopressin receptor gene" Proc. Natl. Acad. Sci. USA. 92:6783-7 (1995); de Keyzer et al., "Cloning and characterization of the human V3(V1b) pituitary vasopressin receptor" FEBS Lett. 356:215-20 (1994); Sugimoto et al., "Molecular cloning and functional expression of a cDNA encoding the human V1b vasopressin receptor" J. Biol. Chem. 269:27088-92 (1994)) встраивали в вектор экспрессии клеток млекопитающих PCI-neo (Promega) по сайту EcoR1. Рекомбинантную плазмиду, несущую кДНК HV1B, выделяли из трансформированных клонов E.Coli и использовали для трансфекции клеток яичника китайского хомячка (СНО-К1, АТСС). Два микрограмма ДНК рецептора hV1b вводили в 105 клеток СНО, культивированных в 6-луночном планшете, используя методику трансфекции, опосредованную Fugene-6 (Boehringer Mannheim). Через двадцать четыре часа после трансфекции клетки культивировали в условиях отбора по G-418 (0,25 мг/мл), добавленного в культуральную среду. Спустя три дня проводили ограниченное разбавление для получения изолированных клонов клеток в 96-луночных планшетах. После 2-недельного периода роста моноклоны распределяли по двум группам 12-луночных планшетов. По достижении конфлюентности одну группу лунок исследовали на способность связывать меченный тритием аргинин-вазопрессин (NEN). Вначале были выявлены девять положительных клонов из числа 60 исследованных, и клоны, показавшие наиболее высокое связывание AVP, сохраняли в качестве перманентных линий клеток для скрининга по аффинности к hV1b.
ПРИМЕР. Клеточный анализ связывания человеческого или крысиного рецептора V1b. Клеточные линии V1b (клетки, экспрессирующие человеческий или крысиный рецептор V1b) выращивали в среде альфа-MEM с добавлением 10% фетальной бычьей сыворотки и 250 мкг/мл G418 (Gibco, Grand Island, NY) в колбе объемом 75 см3. Для конкурентного анализа связывания клетки hV1b отделяли друг от друга с помощью не содержащего ферментов раствора для разделения клеток на основе PSB (Specialty Media, Phillipursburg, NJ), следуя инструкции производителя. Клетки помещали в 12-луночные культуральные планшеты в количестве одна колба на 18 планшетов, (количество следует регулировать в зависимости от степени конфлюентности клеток) и сохраняли в культуре в течение 2-3 дней. Затем культуральную среду удаляли, клетки один раз промывали 2 мл связывающего буфера (25 мМ Hepes, 0,25% BSA, 1×DMEM, рН=7,0) при комнатной температуре. В каждую лунку добавляли 990 мкл связывающего буфера, содержащего 1 нМ 3H-AVP и затем 10 мкл последовательно разбавленных исследуемых соединений или не меченый AVP (все растворы в ДМСО). Все инкубации проводили в трех экземплярах и получали кривые зависимости ингибирования от дозировки, состоящие из точек, соответствующих общему связыванию (только ДМСО) и 5 концентрациям (0,1, 1,0, 10, 1000 и 1000 нм) тестируемого агента или не меченого AVP, охватывающие IC50. Клетки инкубировали в течение 30 минут при 37°С в увлажненном инкубаторе. Затем смесь для анализа удаляли и каждую лунку три раза промывали PBS (рН=7,4). После промывания добавляли 1 мл 2% SDS в каждую лунку и содержимому планшетов давали осесть в течение 15 мин при комнатной температуре. Осторожно постукивали по планшетам, чтобы убедиться в отслоении разрушенных клеток. Содержимое лунок полностью переносили во флакон для подсчета сцинтилляции. Затем каждую лунку промывали 0,5 мл PBS и добавляли в соответствующий флакон. Затем добавляли сцинтилляционную жидкость (Ecoscint, National Diagnostics, Atlanta, Georgia) в количестве 3 мл на сосуд. Проводили подсчет образцов на счетчике сцинтилляции жидкостей (Beckman LS801). Рассчитывали значения IC50 и Ki, используя программное обеспечение Prism Curve для построения кривых по точкам. Иллюстративные соединения, показанные в предыдущей таблице, показывают константу связывания более 100 нМ или более 1000 нМ. Иллюстративные данные по ингибированию (Ki, нМ) приведены в следующей таблице для выбранных примеров соединений.

ПРИМЕР. Ингибирование метаболизма фосфатидилинозита (V1a). Физиологические эффекты вазопрессина опосредуются конкретными рецепторами, связанными с G-белком. Рецептор вазопрессина V1a связан с семейством Gq/G11 G-белков и опосредует метаболизм фосфатидилинозита. Агонистический или антагонистический характер описанных в настоящей заявке соединений может быть определен по их способности ингибировать опосредованный вазопрессином метаболизм фосфатидилинозита с применением процедуры, описанной в следующих параграфах. Иллюстративные соединения, Примеры 35, 44, 88, 110 и 133, исследовали в данном анализе, и было установлено, что они являются антагонистами вазопрессина V1a.
ПРИМЕР. Ингибирование метаболизма фосфатидилинозита, опосредованного рецептором вазопрессина V1b - функциональный анализ активности антагонистов. Физиологические эффекты вазопрессина опосредуются конкретными рецепторами, связанными с G-белком. Рецептор вазопрессина V1b связан с G-белком, который связан с сAMP. Агонистический или антагонистический характер описанных в настоящей заявке соединений может быть определен по их способности ингибировать опосредованный вазопрессином метаболизм фосфатидилинозита с применением стандартных методик, включая методики, описанной в следующих параграфах.
Клеточная культура и маркировка клеток. За три дня до проведения анализа близкие к конфлюэнтности культуры клеток hV1a или hV1b разделяли и высевали в 6-луночные планшеты для культур тканей, причем примерно 100 лунок засеивали из каждой 75 см2 колбы (разделение в эквивалентном соотношении 12:1). Каждая лунка содержала 1 мл ростовой среды с 2 мкКюри [3Н]миоинозита (American Radiolabeled Chemicals, St. Louis, MO, USA).
Клетки, экспрессирующие человеческие или крысиные рецепторы V1b, выращивали на альфа-модифицированной минимальной поддерживающей среде, содержавшей 10% фетальной бычьей сыворотки и 0,25 мг/мл G418. За три дня до проведения анализа близкие к конфлюэнтности культуры разделяли и высевали в 6-луночные планшеты для культур тканей, причем примерно 100 лунок засевали из каждой 75 см2 колбы (разделение в эквивалентном соотношении 12:1). Каждая лунка содержала 1 мл ростовой среды с 2 мкКюри [3Н]миоинозита (American Radiolabeled Chemicals, St. Louis, MO).
Инкубирование (V1a и V1b). Все анализы проводили в трех экземплярах, за исключением исходного и 10 нМ AVP (для обоих n=6). Аргинин вазопрессин (AVP) Peninsula Labs, Belmont, СА, USA (#8103)) растворяли в 0,1N уксусной кислоте. Тестовые агенты растворяли в ДМСО в день эксперимента и разбавляли ДМСО до 200 раз, т.е. конечной тестируемой концентрации. Тестируемые агенты и AVP (или соответствующие объемы ДМСО) по отдельности добавляли в 5 мкл ДМСО в стеклянные пробирки 12×75 мм, содержавшие 1 мл аналитического буфера (сбалансированный солевой раствор Tyrode, содержавший 50 мМ глюкозы, 10 мМ LiCl, 15 мМ HEPES, рН 7,4, 10 мкМ фосфорамидона и 100 мкМ бактирацина). Инкубирование проводили в случайном порядке. Инкубирование начинали с удаления среды, содержавшей метку, один раз промывая монослой 1 мл 0,9% NaCl и перенося содержимое пробирок для анализа в соответствующие лунки. Планшеты инкубировали в течение 1 ч при 37°С. Инкубирование прерывали удалением инкубационной среды и добавлением 500 мкл ледяной 5% (масс./об.) трифторуксусной кислоты и оставлением полученной смеси на 15 минут.
Измерение [3Н]инозитофосфатов (V1a и V1b). Колонки BioRad Poly-Prep Econo-Columns наполняли 0,3 мл формиатной смолы AG 1 Х-8 100-200. Смолу смешивали с водой в соотношении 1:1 ив каждую колонку добавляли 0,6 мл. Затем колонки промывали 10 мл воды. Под каждую колонку помещали сцинтилляционный флакон (20 мл). Содержимое каждой лунки переносили в миниколонку, после чего лунку промывали 0,5 мл дистиллированной воды, которую также добавляли в миниколонку. Затем колонки дважды промывали 5 мл 5 мМ миоинозита для элюирования свободного инозита. Аликвоты (1 мл) полученной жидкости переносили в новые 20 мл сцинтилляционные флаконы, добавляли 10 мл Beckman Ready Protein Plus. После окончания промывки миоинозитом, пустые сцинтилляционные флаконы помещали под колонки и элюировали [3Н]инозитфосфаты троекратным добавлением 1 мл 0,5 М формиата аммония, содержавшего 0,1 N муравьиную кислоту. Условия элюирования оптимизировали для получения моно-, бис- и трисфосфатов инозита, без элюирования более метаболически инертных тетракис-, пентакис- и гексакис фосфатов. К каждому образцу добавляли 10 мл сцинтилляционной жидкости с высокой солевой емкостью, такой как Tru-Count High Salt Capacity или Packard Hionic-Fluor. Содержание инозит липидов измеряли путем добавления 1 мл 2% додецилсульфата натрия (SDS) в каждую лунку, после чего давали содержимому лунки осесть в течение по крайней мере 30 мин, и переносили раствор в 20 мл сцинтилляционные флаконы, в которые затем добавляли 10 мл сцинтилляционной жидкости Beckman Ready Protein Plus. Производили подсчет образцов на счетчике сцинтилляции жидкостей Beckman LS 3801. Общее включение инозита для каждой лунки рассчитывали как сумму свободного инозита, инозитфосфатов и инозитлипидов.
Данные анализа (V1a и V1b): эксперименты концентрация-ингибирование. Кривые зависимости концентрация-отклик для AVP и кривые концентрация-ингибирование для тестируемых агентов по сравнению с 10 нМ AVP исследовали нелинейным методом наименьших квадратов - подгонки кривых относительно 4-параметрической логистической функции. Варьировали параметры исходного и максимального уровней инозитфосфатов, EC50 или IC50, а также коэффициент Хилла для достижения наилучшего соответствия. В процессе подгонки кривых весовые коэффициенты выбирали в соответствии с предположением, что среднеквадратичное отклонение пропорционально числу радиоактивных распадов в минуту. В каждом эксперименте строили полные кривые концентрация-отклик для AVP. Значения IC50 преобразовывали в значения Ki, которые отражают антагонистические активности в отношении AVP в выработке сигнальной молекулы IP3, с применением уравнения Cheng-Prusoff, основываясь на значении EC50 для AVP в том же эксперименте. Содержание инозитфосфатов выражали как число распадов в минуту на 106 распадов в минуту общего количества инозита.
Данные анализа (V1a и V1b): эксперименты конкурентоспособности. Эксперименты по определению V1a конкурентоспособности тестируемых агентов заключались в построении кривых концентрация-отклик для AVP в отсутствии и в присутствии тестируемого агента в двух или более концентрациях. Эксперименты по определению V1b конкурентоспособности тестируемых агентов заключались в построении кривых концентрация-отклик для AVP в отсутствие и в присутствии по меньшей мере пяти концентраций тестируемого агента. Данные согласовывали со следующим логистическим уравнением, описывающим конкурентное связывание
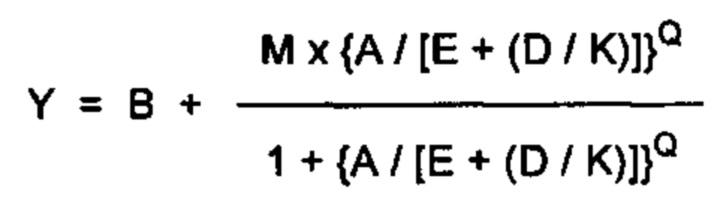
где Y означает число распадов в минуту для инозитфосфатов, В означает концентрацию исходных инозитфосфатов, М означает максимальное увеличение концентрации инозитфосфатов, А означает концентрацию агониста (AVP), Е представляет собой EC50 для агониста, D означает концентрацию антагониста (тестируемый агент), K представляет собой Ki антагониста и Q означает кооперативность (коэффициент Хилла).
Соединение Примера 225 проявило дозозависимое подавление действия AVP с IC50 (2,68 нМ) и Ki (0,05 нМ). Указанные значения соотносятся с высокой аффинностью связывания Примера 225 и его ингибированием инозитлипидного синтеза посредством рецептора вазопрессина V1a.
ПРИМЕР. Экспрессия AVPR1A в мозгу с HD. Было неожиданно обнаружено, что экспрессия AVPR1A в мозгу с HD эквивалентна нормальному мозгу. Высококачественную РНК (показатель целостности >7) получали из образцов коры головного мозга из посмертного головного мозга с HD и посмертного нормального головного мозга соответствующего возраста/пола с использованием стандартных методов. Обратную транскрипцию (RT) проводили (12 контрольных РНК, 10 HD РНК) и количественную ПЦР в реальном времени проводили в соответствии с инструкцией изготовителя. Образцы загружали в четырех экземплярах; были включены контроли без матрицы (отрицательные) и не-RT контроли. Уровни экспрессии мРНК V1a нормализовали по β-актину. Анализ полученных данных проводили с использованием программного обеспечения CFX ManagerTM, которое показало, что уровни мРНК рецептора V1a в мозге с HD и контрольных мозгах были сходными. Поэтому, несмотря на то, нейродегенерация при HD привела к потере значительного количества ткани и функциональности, передача сигналов вазопрессина все еще функционирует на уровнях, эквивалентных здоровым людям. Тем не менее из-за нейродегенерации в настоящем изобретении полагают, что такие в противном случае нормальные уровни AVP и AVPR1a представляют состояние чрезмерной сигнализации у пациента с HD.
ПРИМЕР. Модуляция передачи сигнала AVP в человеческом мозге, модель нейропсихиатрических аспектов нейродегенеративных заболеваний. Было обнаружено, что в настоящем изобретении селективные антагонисты AVPR1a являются эффективными для лечения нейропсихиатрических симптомов HD, AD и PD. Соединения, описанные в настоящем документе, в том числе SRX228, SRX246, SRX251, SRX296 и SRX576, достигают терапевтически эффективных концентраций в областях мозга, где присутствует чрезмерная передача сигнала при нейродегенеративных заболеваниях, и, следовательно, являются эффективными для коррекции дисфункции при HD, AD и PD.
ПРИМЕР. Модель нейродегенеративных заболеваний (ND). Испытуемых субъектов рандомизировали на модельную группу ND (например, n=15) и базовую контрольную группу (например, n=14). Модельной группе ND вводили интраназально аргининвазопрессин (IN-AVP), 40 ME Pitressin (JHP Pharmaceuticals) в стерильном водном растворе. Дозы IN-AVP вводили из 3 мл интраназальных распылителей (MAD300; Wolfe Tory Medical, Salt Lake City) за 45 минут до визуализации фМРТ. Базовой контрольной группе вводили интраназально только носитель. Все испытуемые субъекты оценивали с помощью визуализации фМРТ.
ПРИМЕР. Визуализация фМРТ. Данные получали с помощью 16 канального магнитно-резонансного томографа Philips Achieva Quasar dual 16 Channel в Центре визуализации мозга Университета Чикаго с использованием обработки изображений с использованием спиральной визуализирующей последовательности, чтобы минимизировать пропадание сигнала в вентральной доле мозга. Сигнал контрастности, зависящий от степени насыщения крови кислородом (BOLD), получали во время того, как каждый испытуемый субъект смотрел 4 блока незнакомых эмоциональных выражений лиц (лица Экмана), при этом каждый блок продолжался 20 секунд и состоял из 5 лиц каждой категории эмоций, отображающейся в течение 4 секунд. Категории включали: сердитые лица, нейтральные лица, счастливые лица и точки фиксации. Испытуемым субъектом давали «неявное» задание определения пола каждого изображения с помощью кнопки. Статистические параметрические карты создавали на основе предварительно обработанных 3 мм3 изображений, пространственно сглаженные с ядром 8 мм, отфильтрованные по полосе, чтобы удалить дрейф, проверенных на чрезмерное движение с коррекцией движения. Изображения от каждого индивидуума перевели в шаблон эхопланарного представления в пространстве Монреальского неврологического института. Воксельный полный анализ мозга проводился по порогами данных на >10 смежных вокселей, с небольшой коррекцией объема р <0,05, для изучения влияния тестируемого соединения по сравнению с плацебо на BOLD-активность в предварительных регионах, представляющих интерес (ROI). ROI выявленных кластеров различий BOLD извлекали в качестве оценок параметров средней интенсивности BOLD-сигнала в анатомически определенных подструктурах и экспортировали в SPSS (IBM; Armont, New York) для ANCOVA, изменяя параллельно базовые оценки параметров в соответствующих ROI. Извлеченные оценки параметров предварительных ROI также исследовали с RM-ANOVA в SPSS с факторами внутри субъектов и межсубъектными факторами для всех комбинаций тестируемого соединения по сравнению с плацебо, и IN-AVP по сравнению с интраназальным плацебо. Сравнения были сделаны между эмоциональными состояниями (сердитые лица) и различными нейтральными состояниями (нейтральные лица, счастливые лица, точки фиксации). Сравнения также были сделаны между эмоциональными состояниями (нейтральные лица) и различными нейтральными состояниями (счастливые лица, точки фиксации).
Все испытуемые субъекты, как в базовой контрольной группе, так и группе модели ND, показали увеличение BOLD-сигнала в определенных областях головного мозга, как измерено с помощью фМРТ при просмотре сердитых лица. Все испытуемые субъекты, как в базовой контрольной группе, так и группе модели ND, показали снижение BOLD-сигнала в тех же областях при просмотре счастливых лиц или точек фиксации. Увеличенный BOLD-сигнал наблюдался особенно в правой и левой височно-теменной коре (ТРС), предклинье, передней части поясной извилины и медиальной префронтальной коре головного мозга, миндалевидном теле и скорлупе. Эти области мозга участвуют в социальном распознавании и эмоциональной обработке. В частности, активация левого ТРС отражает внимательность, и активация правого ТРС связана с мышлением о мыслях и мотивах других. Нейроны в этом регионе отправляют свои аксоны к передней части поясной извилины и медиальной префронтальной коре головного мозга, где принимаются исполнительные решения о характере предполагаемого эмоционального ввода, чтобы идентифицировать угрозы, а также для принятия решений и соответствующих мер реагирования. В условиях, представляющих чрезмерную передачу сигнала, такие исполнительные функции или решения нарушаются, что приводит к неадекватному агрессивному поведению, раздражительности и/или гневу.
В соответствии с вышеупомянутой теорией разума, при просмотре сердитых лиц, испытуемые субъекты в группе модели ND, получающие IN-AVP, показывали усиленный BOLD-сигнал по сравнению с базовой контрольной группой, получающей плацебо интраназально. Кроме того, испытуемые в субъекты в группе модели ND показывали увеличенный BOLD-сигнал при просмотре нейтральных лиц по сравнению с базовой контрольной группой, где BOLD-сигнал был одинаков при просмотре нейтральных лиц, счастливых лиц и точек фиксации. Увеличенный BOLD-сигнал при просмотре нейтральных лиц согласуется с неправильной интерпретацией эмоционального состояния, представленного нейтральной лицом, в качестве предполагаемой угрозы, а также запуск агрессивного поведения, раздражительности и/или гнева. Такая неправильная интерпретация эмоционального состояния наблюдается с потерей контроля исполнительных функций при нейродегенеративных заболеваниях, в том числе HD, AD и PD. Сказанное подтверждает вывод о том, что состояние чрезмерной передачи сигнала вазопрессина присутствует при нейродегенеративных заболеваниях, таких как HD, AD и PD.
ПРИМЕР. Лечение нейропсихиатрических симптомов с применением антагонистов вазопрессина. Первую группу испытуемых субъектов в базовой контрольной группе, получавшую плацебо интраназально, рандомизировали по тестируемым соединениям или плацебо. Вторую группу испытуемых в группе модели ND, принимающую IN-AVP, рандомизировали по тестируемым соединениям или плацебо. Тестируемое соединение, например, SRX228, SRX246, SRX251, SPX296 или SRX576 или плацебо вводили в слепой форме в течение 5-10 дней (в среднем 7,3 +/- 1,3 дней, минимум 5 дней, максимум 11 дней) до фМРТ. Альтернативно, тестируемое соединение, например, SRX228, SRX246, SRX251, SRX296 или SRX576 или плацебо вводили в слепой форме в течение после интраназального введения IN-AVP или плацебо, и до фМРТ. Все субъекты, рандомизированные по тестируемым соединениям (n=15) показали наглядные уровни тестируемого соединения, и все субъекты, рандомизированные по плацебо (n=14) не показали детектируемых уровней тестируемого соединения. Например, тестируемое соединение представляло собой SRX246 (т=15; 80,120 или 160 мг перорально два раза в день) в сравнении с плацебо (n=14) в пероральных капсулах; или тестируемое соединение представляло собой SRX251 (n=15; 80, 120 или 160 мг перорально два раза в день) по сравнению с плацебо (n=14) в пероральных капсулах.
BOLD-сигнал значительно снижается у всех испытуемых субъектов, предварительно обработанных тестируемым соединением, по сравнению с плацебо при просмотре сердитых лиц. BOLD-сигнал значительно снижается у всех испытуемых субъектов, постобработанных тестируемым соединением, по сравнению с плацебо при просмотре сердитых лиц. BOLD-сигнал значительно снижается у испытуемых субъектов модели ND, получающих IN-AVP, предварительно обработанных тестируемым соединением, по сравнению с плацебо при просмотре нейтральных лиц. BOLD-сигнал значительно снижается у испытуемых субъектов модели ND, получающих IN-AVP, постобработанных тестируемым соединением, по сравнению с плацебо, при просмотре нейтральных лиц.
На Фиг. 1 показано структурное изображение высокого расширения уменьшения BOLD-сигнала в височно-теменной доле коры (поле Бродмана 39) после предварительной обработки SRX246 в группе модели ND, получающей IN-AVP. По сравнению с плацебо предварительная обработка с SRX246 значительно снизила (р<0,001, >10 смежных вокселей) активацию сигнала BOLD после IN-AVP височно-теменной доле коры (поле Бродмана 39) (белые области показывают Т-статистическую величину) и миндалине при просмотре сердитых лиц по сравнению с точкой фиксации. Столбец с градацией серого показывает Т-статистическую величину, где наблюдаемая активность изменяется в данной области после региональной коррекции для ошибки второго рода (скорректированная групповая вероятность ошибки (FEW) р=.017; Т (1,27)=4,59).
По сравнению с плацебо постобработка SRX246 значительно снижает (р<0,05, >10 смежных вокселей) активацию сигнала BOLD после IN-AVP в височно-теменной доле коры (поле Бродмана 39) и миндалине когда при просмотре сердитых лиц по сравнению со счастливыми лицами (данные не показаны).
На Фиг. 2 показано структурное изображение высокого расширения уменьшения BOLD-сигнала в передней поясной коре и медиальной префронтальной коре после предварительной обработки SRX246 в группе модели ND, получающей IN-AVP. По сравнению с плацебо предварительная обработка с SRX246 значительно снизила (р<0,005,>10 смежных вокселей) активацию сигнала BOLD после IN-AVP медиальной префронтальной коре при просмотре сердитых лиц по сравнению с точкой фиксации и значительно уменьшила кортикальную активность в отношении сердитых лиц в передней поясной коре и медиальной префронтальной коре (ые области показывают Т-статистическую величину). Столбец с градацией серого показывает Т-статистическую величину, где наблюдаемая активность изменяется в данной области после региональной коррекции для ошибки второго рода (скорректированная групповая вероятность ошибки (FEW р=.015; Т (1, 27)=4,66).
По сравнению с плацебо постобработка SRX246 значительно снижает активацию сигнала BOLD после IN-AVP в передней поясной коре и медиальной префронтальной коре при просмотре сердитых лиц по сравнению со счастливыми лицами.
ПРИМЕР. Модель стресса и агрессии «резидент-интрудер» у крыс. Нейровизуализацию использовали для оценки блокады стресса/возбуждения с тестируемым соединением по сравнению с контролем. Эффект AVN251-HCl на функциональный контур был исследован с использованием метода визуализации для бодрствующих крыс. Дополнительные подробности анализа описаны в Ferris et al. Imaging the neural circuitry and chemical control of aggressive motivation. BMC Neuroscience 9: 111 (2008). Представление эффектов ЦНС для AVN251-HCl и дифференцированные нейробиологические изменения, производимых AVN251-HCl, сравнивали с флуоксетином. AVN251-HCl оставляет сексуальную мотивацию неизменной, в то время как флуоксетин заметно уменьшает активацию указанного контура, что приводит к снижению либидо и реакции на самку.
У самцов крыс в компании сокамерника женского пола происходила пилоэрекция в присутствии самца-интрудера. Пилоэрекция является признаком стресса и агрессивных намерений и связана с активацией контура стресса/возбуждения в головном мозге. Активация контура стресса в ответ самца-интрудера оценивали путем получения снимков мозга, если смотреть с хвостовой/тыльной перспективы в виде полупрозрачной оболочки. Локализация активированных вокселей отображается в виде 3D объемов активации, которые состоят из 10 субъектов каждый. После полной регистрации и сегментации статистические ответы для каждого субъекта усредняются повоксельно. Эти усредненные вокселы превышающие 2,0% порог показаны в их соответствующем пространственном местоположении. Функциональные изображения получены на бодрствующих крысах при 4,7Т.
Самцов-резидентов крыс из шести пар самцов/самок визуализировали после полного пробуждения, и представляли им их самку или их самку + интрудер, что является высокострессовым раздражителем. В ходе одного сеанса визуализации, самцов обрабатывали путем перорального введения Примером 225 (AVN251) (5 мг/кг), Примером 224 (AVN246) (5 мг/кг) или носителем перорально через зонд. Общий объем активации мозга у самцов-резидентов, сталкивающихся с их самкой в одиночку, самкой плюс интрудер и самкой плюс интрудер в присутствии AVN251-HCl, рассматривали в виде 3D-моделей. Обработка AVN251-HCl (5 мг/кг) блокирует активацию контура стресса. Наблюдалось общее снижение BOLD-сигнала в основных областях, ответственных за некорректное поведение, посредством обработки AVN251-HCl,. Тем не менее, сексуальная мотивация, по оценке презентации новой готовой к спариванию самки, не зависит от блокады рецептора V1a. Функция мезокортиколимбической системы вознаграждения дофамином в ответ на сексуальный мотивирующий стимул (эстроген-прогестерон примитированная самка) остается неизменной в присутствии AVN251-HCl. Визуализация показывает надежную активацию различных областей мозга, когда новая самка представлена в качестве стимула. Кроме того, самцы-резиденты, обработанные AVN251-HCl, показывали нормальное сексуальное поведение по отношению к готовым к спариванию самкам (самки обработанные эстрогеном/прогестероном после овариэктомии) в своей домашней клетке. В частности, SRX251-HCl избирательно блокирует агрессивные мотивации, но не сексуальную мотивацию, о чем свидетельствуют минимальные изменения BOLD-сигнала в первичной обонятельной системе и путях получения награды в мезокортиколимбической дофаминергической системе, в том числе прелимбальной коре, центре подкрепления, вентральном паллидуме, медиальном заднем таламусе и вентральной покрышке. Напротив, обработка флуоксетином приводит к снижению активации как контура стресса, так и мезокортиколимбической системы вознаграждения допамином.
ПРИМЕР. Нейровизуализация конкретных областей головного мозга, показывающая блокаду стресса. Бодрствующих крыс визуализировали при представлении им их самки или их самки + интрудер. Предварительная обработка с AVN251 (5 мг/кг) или AVN246 (5 мг/кг) за 90 минут до начала сеанса тестирования блокировала реакцию на стресс/возбуждение, особенно в областях мозга, ответственных за эмоциональную обработку и оценку угроз, включая миндалину, кору (височно-теменную кору, переднюю поясную кору, и медиальную префронтальную кору), гиппокамп и таламус. Аналогичные результаты наблюдали с SRX228, SRX246, SRX251, SRX296 и SRX576. Сексуальная мотивация и поведение остались неизменными. Оценивали отдельные участки мозга, в том числе миндалину, кору, гиппокамп и таламус, каждый из которых показал аналогичные результаты. На Фиг. 3 показан снимок головного мозга для миндалины, коры, гиппокампа и таламуса для необработанных контролей в ходе парадигмы стресса самка + интрудер. На Фиг. 4 показан снимок головного мозга для миндалины, коры, гиппокампа и таламуса для животных, предварительно обработанных SRX251 в ходе парадигмы стресса самка + интрудер. На каждом снимке темные затененные области представляют собой активацию передачи сигнала рецептора вазопрессина. В каждом случае, обработанные животные (Фиг. 4) показали более низкую активацию передачи сигнала рецептора вазопрессина, чем необработанные контрольные (Фиг. 3), в каждой из областей мозга.
ПРИМЕР. Модель «резидент-интрудер» у хомяков. Размещение незнакомых самцов хомяков в домашнюю клетку другого самца хомяка позволяет выявить хорошо определенную последовательность агонистического поведения у резидента, которое включает агрессию нападения. Самцов сирийских золотистых хомячков (Mesocricetus auratus) (140-150 г), полученных из лаборатории Harlan Sprague-Dawley Laboratories (Indianapolis, IN) помещали по одному в клетки из плексигласа (24 см × 24 см × 20 см), содержали в режиме обратного цикла свет:темнота (14L:10D; свет включали в 19:00) и снабжали пищей и водой без ограничения. Животным давали привыкнуть к режиму обратного цикла свет:темнота в течение двух недель до тестирования. Все тесты поведения проводили во время темновой фазы суточного цикла.
Измерение поведения и анализ. Хомяки являются ночными животными и поэтому такие поведенческие тесты выполняли в течение первых четырех часов темновой фазы при слабом красном освещении. Резидента оценивали на стресс, например, задержку перед укусом интрудера, общее время контакта с интрудером, общее количество укусов и ольфакторное мечение, в течение 10-минутного периода испытания (Ferris & Potegal (1988)). Ольфакторное мечение представляет собой форму обонятельной коммуникации, в которой хомяк выгибает спину и трется среднебрюшными железами (flank gland), выделяющими феромон, об объекты в окружающей среде (Johnston, R.E. Communication, In: The Hamster Reproduction and Behavior. Ed Siegel, H.I. Plenum Press, New York, pp 121-154 (1985)). Частота ольфакторного мечения значительно усиливается во время агрессивных столкновений и особенно увеличена у доминирующих животных, инициирующих и выигрывающих бои (Ferris et al., Physiology и Behavior, 40:661-664 (1987)).
Соединения, описанные в настоящем документе, тестировали с использованием пяти групп пяти животных в каждом диапазоне доз (100 нг/кг, 10 мкг/кг, 1 мг/кг, 10 мг/кг, и физиологический раствор в качестве контроля). Через девяносто мин после перорального введения через зонд интрудер был помещен в домашнюю клетку и резидентов оценивали по наступательной агрессии. После тестирования агрессии, животных подвергали скринингу на двигательную активность в камере "открытое поле" и сексуальную мотивацию.
Параметрические данные, т.е. задержки и время контакта, анализировали с помощью однофакторного дисперсионного анализа ANOVA с последующим ретроспективным анализом Newman-Keuls. Непараметрические данные, т.е., количество укусов и ольфакторных мечений, анализировали с помощью теста Крускала-Уоллиса с последующим U-тестом Манна - Уитни для определения различий между группами.
Задержка укуса увеличилась и количество укусов снизилось после введения соединений, описанных в настоящем документе, что указывает на более низкий уровень стресса у обработанных животных. Время контакта также может быть увеличено.
ПРИМЕР. Модель депрессии на основе постоянного подчинения у мышей. Социальный стресс является фактором в этиологии нескольких психопатологий, где индивидуумы различаются по уязвимости. Взрослые самцы мышей подвергаются модели хронического психосоциального стресса, в которой пары резидент/интрудер живут в состоянии постоянного сенсорного контакта и физически взаимодействуют на ежедневной основе. Животные интрудеры, хронически подчиненные согласно данной процедуре, демонстрируют поведение, характерное для депрессии и расстройств, связанных с депрессией.
ПРИМЕР. Антидепрессивный эффект в тесте социального взаимодействия. Хроническое социальное подчинение является стандартным методом получения животных, которые демонстрируют депрессивные физиологические и поведенческие профили. Парадигма быстрого подчинения у мышей приводит к снижению поведения социального взаимодействия, где зависимые величины представляют собой пройденное расстояние и временя в зоне взаимодействия. 28-й суточный режим обработки хлордиазепоксидом (CDP), стандартным транквилизатором, не оказывает никакого влияния на отрицательные эффекты, вызванные хронической подчиненностью. Дополнительные подробности описаны в Berton et al. Essential role of BDNF in the mesolimbic dopamine pathway in social defeat stress. Science 311(5762):864-8 (Feb. 10, 2006).
Вкратце, самцы линии C57B1/6J терпели поражение ежедневно в течение 10 дней от резидентов, крайне агрессивных самцов CF-1. Через 5 минут после прямого воздействия, перфорированную пластиковую перегородку вставляли в клетку, которая позволила осуществлять обонятельный и визуальный контакт без физического поражения на оставшиеся 23 ч 55 мин каждый день. Самцов С57 подвергали взаимодействию с различными самцами резидентами в другой клетке, каждый день, чтобы увеличить стресс процедуры (следует отметить, что все самцы CF-1 атакован интрудера каждый день). В конце процедуры 10 суточного поражения, самцов С57 тестировали в устройстве открытого поля во время темной фазы. Доминирующего самца сажали в зону устройства открытого поля, называемого «зоной социального взаимодействия». Время и расстояние, пройденное в зоне, записывали. Самцов С57 затем случайным образом распределяли среди следующих групп: AVN246-HCl (2 мг/кг), физиологический раствор (0,45%) или хлордиазепоксид (10 мг/кг). Обработку проводили ежедневно (ип) в течение 28 дней и животных повторно тестировали. Изменения в поведении определяли путем вычисления разницы показателей (посттест-претест) и анализировали указанные показатели.
Как показано в таблице, обработка AVN251-HCl значительно увеличила как расстояние, так и время в зоне взаимодействия, что свидетельствует о том, что описанные в настоящем документе соединения, обращали дефицит в поведении социального взаимодействия после социального подчинения.

(а) существенно отличается от CDP и физиологического раствора (р<0,05). Наблюдалась статистически значимая разница (р<0,05) между тестируемым соединением и как необработанным контролем (физиологический раствор), так и отрицательным контролем хлордиазепоксидом (CDP). CDP, стандартный транквилизатор, не имел никакого эффекта. Результаты подтверждают, что дефицит в социальном взаимодействии, вызванный хронической подчиненностью, восприимчив к соединениям, описанным в настоящем документе, но не к транквилизаторам. Наблюдалось, что AVN246 показывало такие же результаты, как показано на Фиг. 5. Статистически значимое различие (*, р<0,05) наблюдалась между тестируемым соединением и необработанным контролем (физиологический раствор) и отрицательным контролем хлордиазепоксидом (CDP) по расстоянию, пройденному в зоне взаимодействия.
ПРИМЕР. Анксиолитический эффект в челночной камере со светом/темнотой. Челночная камера со светом/темнотой представляет собой стандартный и хорошо изученный анализ на анксиолитическое действие тестируемого соединения. Крысы естественным образом избегают светлой стороны камеры, потому что она вызывает у них стресс. Увеличение времени на светлой стороне в группе обработки по сравнению с контролем отражает анксиолитический эффект (Bourin and Hascoet, 2003). Взрослым самцам крыс линии Long Evans вводили AVN251 (0,1-2 мг/кг) перорально через зонд за 90 мин до начала испытаний челночная камера со светом/темнотой. Дозозависимое снижение тревожности наблюдалось в ответ на AVN251 по сравнению с носителем. В зависимости от дозы, тестируемые животные проводили значительно (**, р<0,01) больше времени на свету (Фиг. 6А), значительно (**, р<0,01) меньше времени в темноте (Фиг. 6В), и делали больше переходов свет-темнота (Фиг. 6С) после обработки 1 или 2 мг/кг AVN251.
ПРИМЕР. Фармакокинетика. Соединения, описанные в настоящем документе, быстро абсорбируется после перорального введения. Соединения, описанные в настоящем документе, проникают через гематоэнцефалический барьер и достигают терапевтически эффективных концентраций в ЦНС. Соединения, описанные в настоящем документе, могут быть дозированы в соответствии с широким спектром протоколов, включая, но не ограничиваясь ими, четыре раза в сутки, два раза в сутки, и тому подобное. Соединения, описанные в настоящем документе, демонстрируют дозозависимое увеличение Cmax и ППК при введении дозы в соответствии с различными протоколами, в том числе, но не ограничиваясь четыре раза в сутки, два раза в сутки. Например, дозирование два раза в сутки показывает 1,7-кратное накопление и улучшенное Т1/2 для SRX246.
ПРИМЕР. Общий способ синтеза. Проксимальный амидный подход, который допускает вариации синтеза на дистальной амидной части; проксимальный амид присоединяют первым, с последующим варьированием дистального амида посредством параллельного синтеза.
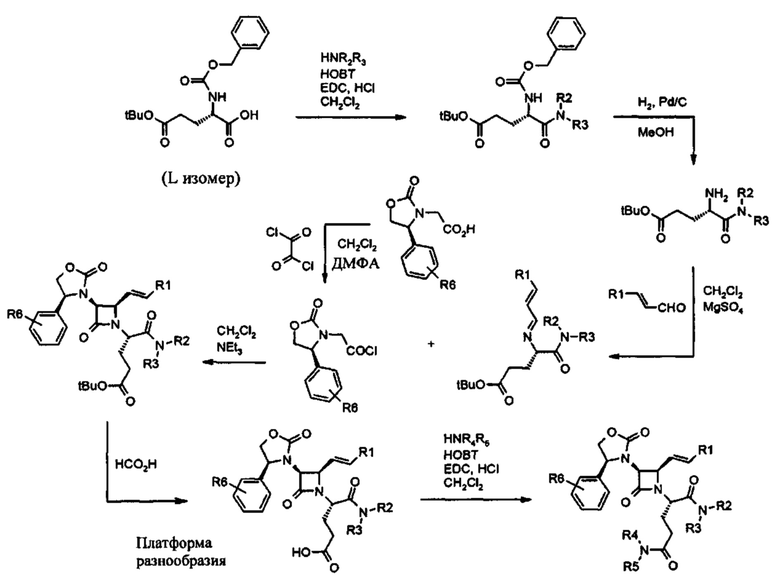
Дистальный амидный подход, который допускает вариации синтеза в проксимальной части; Дистальный амид присоединяют первым, с последующим варьированием проксимального амида посредством параллельного синтеза.
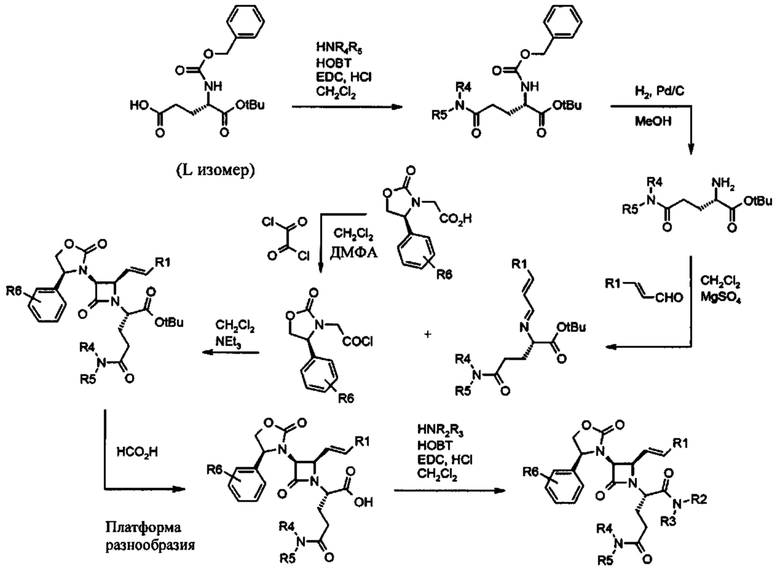
Синтез AVN251 показан ниже. Все остальные соединения получают аналогичным способом с соответствующим выбором исходных веществ.
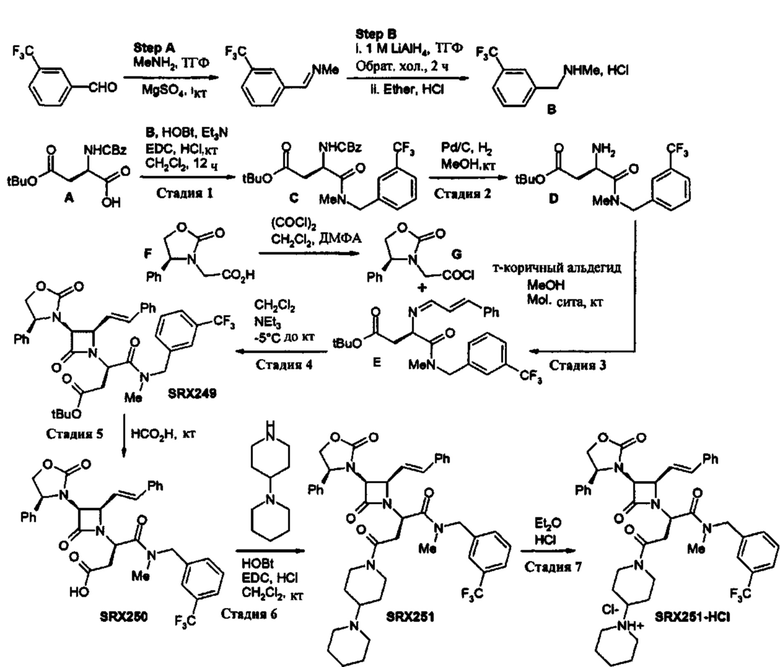
Дополнительные подробности и альтернативные способы синтеза для получения соединений, описанных в настоящем документе, описаны в патенте США №7119083, описание которого включено в настоящее описание посредством ссылки во всей их полноте. Соединения, описанные в настоящем документе, могут быть получены и введены в соответствии со способами, описанными в патенте США №7119083. Дополнительные подробности описаны в Guillon, C.D., et al., Azetidinones as vasopressin V1a antagonists. Bioorg Med Chem, 15(5):2054-80 (2007).
ПРИМЕРЫ СОЕДИНЕНИЙ
Пример 1. (4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлорид. Раствор 1,0 эквивалента (4(S)-фенилоксазолидин-2-он-3-ил)уксусной кислоты (Evans, Патент США №4665171) и 1,3 эквивалента оксалилхлорида в 200 мл дихлорметана обрабатывали каталитическим количеством безводного диметилформамида (85 мкл/миллиэквивалента производного уксусной кислоты) с получением бурного выделения газа. Через 45 минут выделение газа прекратилось и реакционную смесь концентрировали при пониженном давлении с получением указанного в заголовке соединения в виде беловатого твердого вещества после высушивания в течение 2 ч в вакууме.
Пример 1А. (4(R)-фенилоксазолидин-2-он-3-ил)ацетилхлорид. Пример 1А получали согласно процедуре Примера 1, за исключением того, что (4(R)-фенилоксазолидин-2-он-3-ил)уксусную кислоту использовали вместо (4(S)-фенилоксазолидин-2-он-3-ил)уксусной кислоты (см., Evans & Sjogren, Tetrahedron Lett. 26:3783 (1985)).
Пример 1B. Метил-(4(S)-фенилоксазолидин-2-он-3-ил)ацетат. Раствор (4(S)-фенилоксазолидин-2-он-3-ил)уксусной кислоты (1 г, 4,52 ммоль) (полученный согласно Evans в патенте США №4665171) в 20 мл безводного метанола, обрабатывали ежечасно 5 эквивалентами ацетилхлорида, в общей сложности 20 эквивалентами. Полученный раствор перемешивали в течение ночи. Остаток, полученный после выпаривания МеОН, повторно растворяли в 30 мл CH2Cl2 и обрабатывали 50 мл насыщенного водного Na2CO3. Органический слой выпаривали и сушили (MgSO4) с получением указанного в заголовке соединения в виде бесцветного масла (1,001 г, 94%); 1Н ЯМР (CDCl3) δ 3,37 (d, J=18,0 Гц, 1H), 3,69 (s, 3Н),4,13 (t, J=8,3 Гц, 1H),4,28 (d, J=18,0 Гц, 1H), 4,69 (t, J=8,8 Гц, 1H), 5,04 (t, J=8,4 Гц, 1H), 7,26-7,29 (m, 2H), 7,36-7,42 (m, 3H).
Пример 1С. Метил-2-(4(S)-фенилоксазолидин-2-он-3-ил)пропаноат. Раствор метил-(4(S)-фенилоксазолидин-2-он-3-ил)ацетата (1 г, 4,25 ммоль) в 10 мл безводного ТГФ при -78°С обрабатывали 4,68 мл (4,68 ммоль) 1 М раствора бис(триметилсилил)амида лития в ТГФ. Реакционную смесь перемешивали в течение 1 ч. при примерно -70°С до добавления MeI (1,59 мл, 25,51 ммоль). После завершения превращения азетидинона, реакцию гасили насыщенным водным NH4Cl и разделяли между EtOAc и водой. Органический слой промывали последовательно насыщенным водным бисульфитом натрия и насыщенным водным NaCl. Полученный органический слой сушили (MgSO4) и выпаривали с получением указанного в заголовке соединения (смесь диастереомеров) в виде белого твердого вещества (1,06 г, 93%); 1Н ЯМР (CDCl3) δ 1,07/1,53 (d/d, J=7,5 Гц, 3Н), 3,59/3,74 (s/s, 3Н), 3,85/4,48 (q/q, J=7,5 Гц, 1Н), 4,10-4,14 (m, 1Н), 4,60-4,64/4,65-4,69 (m/m, 1Н), 4,88-4,92/4,98-5,02 (m/m, 1Н), 7,24-7,40 (m, 5Н).
Пример 1D. 2-(4(S)-Фенилоксазолидин-2-он-3-ил)пропановая кислота. К раствору метил-2-(4(S)-фенилоксазолидин-2-он-3-ил)пропаноата (1 г, 4,01 ммоль) в 35 мл МеОН при 0°С добавляли 14,3 мл (12,04 ммоль) 0,84 М раствор LiOH в воде. Реакционную смесь затем перемешивали в течение 3 ч. при комнатной температуре. После полного гидролиза азетидинона МеОН удаляли путем выпаривания, неочищенный остаток растворяли в CH2Cl2 и обрабатывали насыщенным водным NaCl. Полученный органический слой сушили (MgSO4) и выпаривали с получением указанного в заголовке соединения (рацемическая смесь) в виде белого твердого вещества (0,906 г, 96%); 1Н ЯМР (CDCl3) δ 1,13/1,57 (d/d, J=7,5 Гц, 3H), 3,75/4,50 (q/q, J=7,5 Гц, 1H), 4,10-4,16 (m, 1H), 4,62-4,72 (m, 1H), 4,92-5,03 (m, 1H), 7,32-7,43 (m, 5H).
Пример 1E. 2-(4(S)-Фенилоксазолидин-2-он-3-ил)пропаноилхлорид. Раствор 1 эквивалента Примера 1D и 1,3 эквивалента оксалилхлорида в 200 мл CH2Cl2 (150 мл/г производного пропановой кислоты) обрабатывали каталитическим количеством безводного ДМФА (85 мкл/ммоль производного пропановой кислоты) с получением бурного выделения газа. Через 45 мин выделение газа прекратилось и реакционную смесь концентрировали при пониженном давлении с получением указанного в заголовке соединение в виде беловатого твердого вещества после высушивания в течение 2 ч в вакууме.
Пример 2. Общая процедура образования амида из активированного сложноэфирного производного. α-(3-трифторметил)бензиламид β-трет-бутилового эфира N-бензилоксикарбонил-L-аспарагиновой кислоты. Раствор β-трет-бутилового эфира α-N-гидроксисукцинимидного эфира N-бензилоксикарбонил-L-аспарагиновой кислоты (1,95 г, 4,64 ммоль, Advanced ChemTech) в 20 мл сухого тетрагидрофурана обрабатывали 0,68 мл (4,74 ммоль)3-(трифторметил)бензиламина. После завершения (ТСХ, 60:40 гексаны/этилацетат), смесь выпаривали и полученное масло разделяли между дихлорметаном и насыщенным водным раствором бикарбоната натрия. Органический слой выпаривали с получением 2,23 г (количественный выход) указанного в заголовке соединения в виде белого твердого вещества; 1Н ЯМР (CDCl3) δ 1,39 (s, 9Н), 2,61 (dd, J=6,5 Гц, J=17,2 Гц, 1H), 2,98 (dd, J=3,7 Гц, J=17,0 Гц, 1Н), 4,41 (dd, J=5,9 Гц, J=15,3 Гц, 1H), 4,50-4,57 (m, 2H), 5,15 (s, 2H), 5,96-5,99 (m, 1H), 6,95 (s, 1H), 7,29-7,34 (m, 5H), 7,39-7,43 (m, 2H), 7,48-7,52 (m, 2H).
Примеры 2A-2C и 3-5 получали в соответствии с процедурой Примера 2, за исключением того, что α-N-гидроксисукцинимидный эфир β-трет-бутилового эфира N-бензилоксикарбонил-L-аспарагиновой кислоты заменяли соответствующим производным аминокислоты, и 3-(трифторметил)бензиламин заменяли соответствующим амином.
Пример 2А. α-[4-(2-фенилэтил)]пиперазинамид β-трет-бутилового эфира N-бензилоксикарбонил-L-аспарагиновой кислоты. α-N-гидроксисукцинимидный эфир β-трет-бутилового эфира N-бензилоксикарбонил-L-аспарагиновой кислоты (5,0 г, 12 ммоль, Advanced ChemTech) и 4-(фенилэтил)пиперазин 2,27 мл (11,9 ммоль) приводили к получению 5,89 г (количественный выход) указанного в заголовке соединения в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,40 (s, 9Н), 2,45-2,80 (m, 10H), 3,50-3,80 (m, 4Н), 4,87-4,91 (m, 1Н), 5,08 (s, 2H), 5,62-5,66 (m, 1H), 7,17-7,33 (m, 10H).
Пример 2В. α-(3-трифторметил)бензиламид γ-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты. α-N-гидроксисукцинимидный эфир β-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты (4,83 г, 11,1 ммоль, Advanced ChemTech) и 3-(трифторметил)бензиламин) 1,63 мл (11,4 ммоль) приводили к получению 5,41 г (98%) указанного в заголовке соединения в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,40 (s, 9Н), 1,88-1,99 (m, 1Н), 2,03-2,13 (m, 1H), 2,23-2,33 (m, 1H), 2,38-2,47 (m, 1H), 4,19-4,25 (s, 1H), 4,46-4,48 (m, 2H), 5,05-5,08 (m, 2H), 5,67-5,72 (m, 1H), 7,27-7,34 (m, 5H), 7,39-7,43 (m, 2H), 7,48-7,52 (m, 2H).
Пример 2C. α-[4-(2-фенилэтил)]пиперазинамид γ-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты. α-N-гидроксисукцинимидный эфир γ-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты (5,0 г, 12 ммоль, Advanced ChemTech) и 4-(фенилэтил)пиперазин 2,19 мл (11,5 ммоль) приводили к получению 5,87 г (количественный выход) указанного в заголовке соединения в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,43 (s, 9Н); 1,64-1,73 (m, 1Н); 1,93-2,01 (m, 1H); 2,23-2,40 (m, 2Н); 2,42-2,68 (m, 6Н); 2,75-2,85 (m, 2Н); 3,61-3,74 (m, 4Н); 4,66-4,73 (m, 1H); 5,03-5,12 (m, 2Н); 5,69-5,72 (m, 1Н); 7,16-7,34 (m, 10Н).
Пример 3. α-[4-(2-фенилэтил)]пиперазинамид β-трет-бутилового эфира N-бензилоксикарбонил-L-аспарагиновой кислоты. α-N-гидроксисукцинимидный эфир β-трет-бутилового эфира N-бензилоксикарбонил-L-аспарагиновой кислоты (5,0 г, 12 ммоль, Advanced ChemTech) и 4-(фенилэтил)пиперазин 2,27 мл (11,9 ммоль) приводили к получению 5,89 г (количественный выход) указанного в заголовке соединения в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,40 (s, 9Н), 2,45-2,80 (m, 10H), 3,50-3,80 (m, 4Н), 4,87-4,91 (m, 1Н), 5,08 (s, 2H), 5,62-5,66 (m, 1H), 7,17-7,33 (m, 10H).
Пример 4. N-бензилоксикарбонил-L-глутаминовой кислоты γ-трет-бутилового эфира α-(3-трифторметил)бензиламид. α-N-гидроксисукцинимидный эфир β-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты (4,83 г, 11,1 ммоль, Advanced ChemTech) и 3-(трифторметил)бензиламин) 1,63 мл (11,4 ммоль) приводили к получению 5,41 г (98%) указанного в заголовке соединения в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,40 (s, 9Н), 1,88-1,99 (m, 1H), 2,03-2,13 (m, 1H), 2,23-2,33 (m, 1H), 2,38-2,47 (m, 1H), 4,19-4,25 (s, 1H), 4,46-4,48 (m, 2H), 5,05-5,08 (m, 2H), 5,67-5,72 (m, 1H), 7,27-7,34 (m, 5H), 7,39-7,43 (m, 2H), 7,48-7,52 (m, 2H).
Пример 5. α-[4-(2-фенилэтил)]пиперазинамид γ-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты. α-N-гидроксисукцинимидный эфир γ-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты (5,0 г, 12 ммоль, Advanced ChemTech) и 4-(фенилэтил)пиперазин 2,19 мл (11,5 ммоль) приводили к получению 5,87 г (количественный выход) указанного в заголовке соединения в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,43 (s, 9Н); 1,64-1,73 (m, 1Н); 1,93-2,01 (m, 1Н); 2,23-2,40 (m, 2Н); 2,42-2,68 (m, 6Н); 2,75-2,85 (m, 2Н); 3,61-3,74 (m, 4Н); 4,66-4,73 (m, 1Н); 5,03-5,12 (m, 2Н); 5,69-5,72 (m, 1Н); 7,16-7,34 (m, 10Н).
Пример 5А. N-[(9Н-Флуорен-9-ил)метоксикарбонил]-O-(бензил)-D-серин трет-бутиловый эфир. К-[(9Н-Флуорен-9-ил)метоксикарбонил]-O-(бензил)-D-серин (0,710 г, 1,70 ммоль) в дихлорметане (8 мл) обрабатывали трет-бутилацетатом (3 мл) и концентрированной серной кислотой (40 мкл) в герметично закрытой колбе при 0°С. После завершения (ТСХ) реакцию гасили дихлорметаном (10 мл) и насыщенным водным бикарбонатом калия (15 мл). Органический слой промывали дистиллированной водой и выпаривали. Полученный остаток очищали с помощью колоночной флэш-хроматографии (98:2 дихлорметан/метанол) с получением указанного в заголовке соединения в виде бесцветного масла (0,292 г, 77%); 1Н ЯМР (CDCl3) δ 1,44 (s, 9Н); 3,68 (dd, J=2,9 Гц, J=9,3 Гц, 1Н); 3,87 (dd, J=2,9 Гц, J=9,3 Гц, 1H); 4,22 (t, J=7,l Гц, 1H); 4,30-4,60 (m, 5H); 5,64-5,67 (m, 1H); 7,25-7,39 (m, 9H); 7,58-7,61 (m, 2H); 7,73-7,76 (m, 2H).
Пример 5B. O-(Бензил)-D-серин-трет-бутиловый эфир. Пример 5А (0,620 г, 1,31 ммоль) в дихлорметане (5 мл) обрабатывали трис(2-аминоэтил)амином (2,75 мл) в течение 5 ч. Полученную смесь промывали дважды фосфатным буфером (рН=5,5), один раз насыщенным водным бикарбонатом калия и выпаривали с получением 0,329 г (количественный выход) указанного в заголовке соединения в виде беловатого твердого вещества; 1Н ЯМР (CD3OD) δ 1,44 (s, 9Н); 3,48 (dd, J=J'=4,2 Гц, 1H); 3,61 (dd, J=4,0 Гц, J=9,2 Гц, 1H); 3,72 (dd, J=4,6 Гц, J=9,2 Гц, 1H); 4,47 (d, J=12,0 Гц, 1H); 4,55 (d, J=12,0 Гц, 1H); 7,26-7,33 (m, 5H).
Пример 6. Общая процедура образования амида из карбоновой кислоты, α-(3-трифторметил)бензиламид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты. Раствор 1 г (2,93 ммоль) моногидрата β-трет-бутилового эфира N-бензилоксикарбонил-В-аспарагиновой кислоты (Novabiochem) в 3-4 мл дихлорметана обрабатывали путем последовательного добавления 0,46 мл (3,21 ммоль) 3-(трифторметил)бензиламина, 0,44 г (3,23 ммоль) 1-гидрокси-7-бензотриазола, и 0,62 г (3,23 ммоль) 1-[3-(диметиламино)пропил]-3-этилкарбодиимида гидрохлорида. Через по меньшей мере 12 часов при комнатной температуре или до завершения реакции, как определено с помощью тонкослойной хроматографии (элюент 95:5 дихлорметан/метанол), реакционную смесь промывали последовательно насыщенным водным раствором бикарбоната натрия и дистиллированной водой. Органический слой выпаривали с получением 1,41 г (количественный выход) указанного в заголовке соединения в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,39 (s, 9Н); 2,61 (dd, J=6,5 Гц, J=17,2 Гц, 1H); 2,98 (dd, J=4,2 Гц, J=17,2 Гц, 1H); 4,41 (dd, J=5,9 Гц, J=15,3 Гц, 1H); 4,50-4,57 (m, 2H); 5,10 (s, 2H); 5,96-6,01 (m, 1H); 6,91-7,00 (m, 1H); 7,30-7,36 (m, 5H); 7,39-7,43 (m, 2H); 7,48-7,52 (m, 2H).
Примеры 7-7H получали в соответствии с процедурой Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли соответствующим производным аминокислоты, и 3-(трифторметил)бензиламин заменяли соответствующим амином.
Пример 7. α-(3-трифторметил)бензиламид γ-трет-бутилового эфира N-бензилоксикарбонил-D-глутаминовой кислоты. γ-трет-бутиловый эфир N-бензилоксикарбонил-D-глутаминовой кислоты (1,14 г, 3,37 ммоль) и 0,53 мл (3,70 ммоль, Novabiochem) 3-(трифторметил)бензиламина приводили к получению 1,67 г (количественный выход) Примера 7 в виде беловатого твердого вещества. Пример 7 демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 7А. γ-(4-циклогексил)пиперазинамид α-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты. α-трет-бутиловый эфир N-бензилоксикарбонил-L-глутаминовой кислоты (1,36 г, 4,03 ммоль) и 0,746 г (4,43 ммоль) 1-циклогексилпиперазин приводили к получению 1,93 г (98%) Примера 7А в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,02-1,12 (m, 5Н); 1,43 (s, 9Н), 1,60-1,64 (m, 1H); 1,80-1,93 (m, 5H); 2,18-2,52 (m, 8H); 3,38-3,60 (m, 4H); 4,20-4,24 (m, 1H); 5,03-5,13 (m, 2H); 5,53-5,57 (m, 1H); 7,28-7,34 (m, 5H).
Пример 7B. α-(2-фтор-3-трифторметил)бензиламид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты. Моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (Novabiochem) (0,25 г, 0,73 ммоль) и 0,12 мл (2-фтор-3-трифторметил)бензиламина приводили к получению 0,365 г (количественный выход) Примера 7В в виде беловатого твердого вещества; 1H ЯМР (CDCl3) δ 1,38 (s, 9Н); 2,59 (dd, J=6,5 Гц, J=17,0 Гц, 1Н); 2,95 (dd, J=4,3 Гц, J=17,0 Гц, 1H); 4,46-4,56 (m, 3H); 5,11 (s, 2H); 5,94-5,96 (m, 1H); 7,15 (t, J=8,0 Гц, 1H); 7,30-7,36 (m, 5H); 7,47-7,52 (m, 2H).
Пример 7C. α-[(S)-α-метилбензил]амид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты. Моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (Novabiochem) (0,25 г, 0,73 ммоль) и 0,094 мл (S)-α-метилбензиламина приводили к получению 0,281 г (90%) Примера 7С в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,41 (s, 9Н); 1,44 (d, J=7,0 Гц, 3Н); 2,61 (dd, J=7,0 Гц, J=17,0 Гц, 1H); 2,93 (dd, J=4,0 Гц, J=17,5 Гц, 1Н); 4,50-4,54 (m, 1Н); 5,04-5,14 (m, 3Н); 5,94-5,96 (m, 1Н); 6,76-6,80 (m, 1H); 7,21-7,37 (m, 10Н).
Пример 7D. α-[(R)-α-метилбензил]амид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты. Моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (Novabiochem) (0,25 г, 0,73 ммоль) и 0,094 мл (R)-α-метилбензиламина приводили к получению 0,281 г (90%) Примера 7D в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,38 (s, 9Н); 1,43 (d, J=6,9 Гц, 3Н); 2,54 (dd, J=7,3 Гц, J=17,2 Гц, 1H); 2,87 (dd, J=4,1 Гц, J=17,3 Гц, 1Н); 4,46-4,50 (m, 1Н); 4,99-5,15 (m, 3Н); 5,92-5,96 (m, 1Н); 6,78-6,82 (m, 1Н); 7,21-7,33 (m, 10Н).
Пример 7Е. α-[N-метил-N-(3-трифторметилбензил)]амид γ-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты, γ-трет-бутиловый эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (0,303 г, 0,89 ммоль, Novabiochem) и 0,168 г (0,89 ммоль,) N-метил-N-(3-трифторметилбензил)амина приводили к получению 0,287 г (65%) Примера 7Е в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,40 (s, 9Н); 2,55 (dd, J=5,8 Гц, J=15,8 Гц, 1Н); 2,81 (dd, J=7,8 Гц, J=15,8 Гц, 1Н); 3,10 (s, 3Н); 4,25 (d, J=15,0 Гц, 1Н); 4,80 (d, J=15,5 Гц, 1H); 5,01-5,13 (m, 3Н); 5,52-5,55 (m, 1Н); 7,25-7,52 (m, 10Н).
Пример 7F. α-[(S)-1-(3-трифторметилфенил)этил]амид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты. Моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (Novabiochem) (84 мг, 0,25 ммоль) и 47 мг (S)-1-(3-трифторметилфенил)этиламина приводили к получению 122 мг (количественный выход) Примера 7F в виде беловатого твердого вещества. Пример 7F демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 7G. α-[(R)-1-(3-трифторметилфенил)этил]амид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты. Моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (Novabiochem) (150 мг, 0,44 ммоль) и 83 мг (R)-1-(3-трифторметилфенил)этиламина приводили к получению 217 мг (количественный выход) Примера 7G в виде беловатого твердого вещества. Пример 7G демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 7Н. γ-(3-трифторметил)бензиламид α-метилового эфира N-бензилоксикарбонил-D-глутаминовой кислоты. α-метиловый эфир N-бензилоксикарбонил-D-глутаминовой кислоты (508 мг, 1,72 ммоль) и 317 мг (1,81 ммоль) 3-(трифторметил)бензиламина приводили к получению 662 мг (85%) Примера 7Н в виде беловатого твердого вещества. Пример 7Н демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 8. Общая процедура гидрирования бензилоксикарбониламина. α-(3-трифторметил)бензиламид β-трет-бутилового эфира L-аспарагиновой кислоты. Суспензию 2,23 г (4,64 ммоль) α-(3-трифторметил)бензиламид β-трет-бутилового эфира N-бензилоксикарбонил-L-аспарагиновой кислоты и палладия (5% масс. на активированном угле, 0,642 г) в 30 мл метанола оставляли в атмосфере водорода до полного превращения, как определено с помощью тонкослойной хроматографии (элюент 95:5 дихлорметан/метанол). Реакционную смесь фильтровали с удалением палладия на угле и фильтрат выпаривали с получением 1,52 г (96%) указанного в заголовке соединения в виде масла; 1Н ЯМР (CDCl3) δ 1,42 (s, 9Н); 2,26 (brs, 2Н); 2,63-2,71 (m, 1Н); 2,82-2,87 (m, 1H); 3,75-3,77 (m, 1H); 4,47-4,50 (m, 2H); 7,41-7,52 (m, 4H); 7,90 (brs, 1H).
Примеры 9-13P получали в соответствии с процедурой Примера 8, за исключением того, что α-(3-трифторметил)бензиламид β-трет-бутилового эфира N-бензилоксикарбонил-L-аспарагиновой кислоты заменяли соответствующим производным аминокислоты.
Пример 9. α-[4-(2-фенилэтил)]пиперазинамид β-трет-бутилового эфира L-аспарагиновой кислоты. α-[4-(2-фенилэтил)]пиперазинамид β-трет-бутилового эфира N-бензилоксикарбонил-L-аспарагиновой кислоты (5,89 г, 11,9 ммоль) приводил к получению 4,24 г (98%) Примера 9 в виде беловатого масла; 1Н ЯМР (CDCl3): δ 1,42 (s, 9Н); 2,61-2,95 (m, 10Н); 3,60-3,90 (m, 4Н); 4,35-4,45 (m, 1Н); 7,17-7,29 (m, 5H).
Пример 10. α-(3-трифторметил)бензиламид β-трет-бутилового эфира D-аспарагиновой кислоты. α-(3-трифторметил)бензиламид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (1,41 г, 2,93 ммоль) приводил к получению 0,973 г (96%) Примера 10 в виде беловатого масла; 1Н ЯМР (CDCl3): δ 1,42 (s, 9Н); 2,21 (brs, 2Н); 2,67 (dd, J=7,1 Гц, J=16,8 Гц, 1Н); 2,84 (dd, J=3,6 Гц, J=16,7 Гц, 1H); 3,73-3,77 (m, 1H); 4,47-4,50 (m, 2H); 7,41-7,52 (m, 4H); 7,83-7,87 (m, 1H).
Пример 11. α-(3-трифторметил)бензиламид γ-трет-бутилового эфира L-глутаминовой кислоты. α-(3-трифторметил)бензиламид γ-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты (5,41 г, 10,9 ммоль) приводил к получению 3,94 г (количественный выход) Примера 11 в виде беловатого масла; 1Н ЯМР (CDCl3): δ 1,41 (s, 9Н); 1,73-1,89 (m, 3Н); 2,05-2,16 (m, 1Н); 2,32-2,38 (m, 2H); 3,47 (dd, J=5,0 Гц, J=7,5 Гц, 1H); 4,47-4,49 (m, 2H); 7,36-7,54 (m, 4H); 7,69-7,77 (m, 1H).
Пример 12. α-[4-(2-фенилэтил)]пиперазинамид γ-трет-бутилового эфира L-глутаминовой кислоты. α-[4-(2-фенилэтил)]пиперазинамид γ-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты (5,86 г, 11,50 ммоль) приводил к получению 4,28 г (99%) Примера 12 в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,39 (s, 9Н); 2,00-2,08 (m, 1Н); 2,38-2,46 (m, 1H); 2,55-2,90 (m, 9H); 3,61-3,82 (m, 4H); 4,48-4,56 (m, 1H); 7,17-7,26 (m,5H).
Пример 13. α-(3-трифторметил)бензиламид γ-трет-бутилового эфира D-глутаминовой кислоты. α-(3-трифторметил)бензиламид γ-трет-бутилового эфира N-бензилоксикарбонил-D-глутаминовой кислоты (1,667 г, 3,37 ммоль) приводил к получению 1,15 г (94%) Примера 13 в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,41 (s, 9Н); 1,80-2,20 (m, 4Н); 2,31-2,40 (m, 2Н); 3,51-3,59 (m, 1Н); 4,47-4,49 (m, 2H); 7,39-7,52 (m, 4H); 7,71-7,79 (m, 1H).
Пример 13A. γ-(4-циклогексил)пиперазиншид α-трет-бутилового эфира L-глутаминовой кислоты. γ-(4-циклогексил)пиперазинамид α-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты (1,93 г, 3,96 ммоль) приводил к получению 1,30 г (93%) Примера 13А в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,02-1,25 (m, 5Н); 1,41 (s, 9Н); 1,45-1,50 (m, 1Н); 1,56-1,60 (m, 1H); 1,69-1,80 (m, 6H); 3,30 (dd, J=4,8 Гц, J=8,5 Гц, 1H); 3,44 (t, J=9,9 Гц, 2H); 3,56 (t, J=9,9 Гц, 2H).
Пример 13В. α-(2-фтор-3-трифторметил)бензиламид β-трет-бутилового эфира D-аспарагиновой кислоты. α-(2-фтор-3-трифторметил)бензиламид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (0,36 г, 0,72 ммоль) приводил к получению 0,256 г (92%) Примера 13В в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,39 (s, 9Н); 2,50 (brs, 2Н); 2,74 (dd, J=7,0 Гц, J=16,5 Гц, 1Н); 2,86 (dd, J=4,8 Гц, J=16,8 Гц, 1H); 3,89 (brs, 2H); 4,47-4,57 (m, 2H); 7,16 (t, J=7,8 Гц, 1H); 7,48 (t, J=7,3 Гц, 1H); 7,56 (t, J=7,3 Гц, 1H); 7,97-8,02 (m, 1H).
Пример 13C. эфира α-[(S)-α-метил]бензиламид β-трет-бутилового D-аспарагиновой кислоты. α-[(S)-α-метилбензил]амид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (0,275 г, 0,65 ммоль) приводил к получению 0,17 г (90%) Примера 13С в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,40 (s, 9Н); 1,47 (d, J=6,9 Гц, 3Н); 1,98 (brs, 2Н); 2,49 (dd, J=7,9 Гц, J=17,7 Гц, 1Н); 2,83 (dd, J=3,6 Гц, J=16,7 Гц, 1H); 3,69 (brs, 1H); 4,99-5,10 (m, 1H); 7,19-7,33 (m, 5H); 7,65-7,68 (m, 1H).
Пример 13D. α-[(R)-α-метилбензил]амид β-трет-бутилового эфира D-аспарагиновой кислоты. α-[(R)-α-метилбензил]амид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (0,273 г, 0,64 ммоль) приводил к получению 0,187 г (количественный выход) Примера 13D в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,38 (s, 9Н); 1,46 (d, J=6,9 Гц, 3Н); 1,79 (brs, 2Н); 2,51 (dd, J=7,8 Гц, J=17,5 Гц, 1H); 2,87 (dd, J=3,6 Гц, J=16,9 Гц, 1H); 4,19 (brs, 1H); 4,99-5,11 (m, 1H); 7,18-7,34 (m, 5H); 7,86-7,90 (m, 1H).
Пример 13E. α-[N-метил-N-(3-трифторметилбензил)]амид β-трет-бутилового эфира D-аспарагиновой кислоты. α-[N-метил-N-(3-трифторметилбензил)]амид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (0,282 г, 0,57 ммоль) приводил к получению 0,195 г (95%) Примера 13Е в виде беловатого масла. Пример 13Е демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 13F. α-[4-(2-фенилэтил)]пиперазинамид β-трет-бутилового эфира L-аспарагиновой кислоты. α-[4-(2-фенилэтил)]пиперазинамид β-трет-бутилового эфира N-бензилоксикарбонил-L-аспарагиновой кислоты (5,89 г, 11,9 ммоль) приводил к получению 4,24 г (98%) Примера 13F в виде беловатого масла; 1Н ЯМР (CDCl3): α 1,42 (s, 9Н); 2,61-2,95 (m, 10Н); 3,60-3,90 (m, 4Н); 4,35-4,45 (m, 1H); 7,17-7,29 (m, 5Н).
Пример 13G. α-(3-трифторметил)бензиламид β-трет-бутилового эфира D-аспарагиновой кислоты. α-(3-трифторметил)бензиламид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (1,41 г, 2,93 ммоль) приводил к получению 0,973 г (96%) Примера 13G в виде беловатого масла; 1Н ЯМР (CDCl3): δ 1,42 (s, 9Н); 2,21 (brs, 2Н); 2,67 (dd, J=7,1 Гц, J=16,8 Гц, 1Н); 2,84 (dd, J=3,6 Гц, J=16,7 Гц, 1Н); 3,73-3,77 (m, 1Н); 4,47-4,50 (m, 2Н); 7,41-7,52 (m, 4Н); 7,83-7,87 (m, 1H).
Пример 13Н. α-(3-трифторметил)бензиламид кислоты γ-трет-бутилового эфира L-глутаминовой. α-(3-трифторметил)бензиламид γ-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты (5,41 г, 10,9 ммоль) приводил к получению 3,94 г (количественный выход) Примера 13Н в виде беловатого масла; 1Н ЯМР (CDCl3): δ 1,41 (s, 9Н); 1,73-1,89 (m, 3Н); 2,05-2,16 (m, 1Н); 2,32-2,38 (m, 2Н); 3,47 (dd, J=5,0 Гц, J=7,5 Гц, 1Н); 4,47-4,49 (m, 2Н); 7,36-7,54 (m, 4Н); 7,69-7,77 (m, 1Н).
Пример 13I. α-[4-(2-фенилэтил)]пиперазинамид γ-трет-бутилового эфира L-глутаминовой кислоты. α-[4-(2-фенилэтил)]пиперазинамид γ-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты (5,86 г, 11,50 ммоль) приводил к получению 4,28 г (99%) Примера 13I в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,39 (s, 9Н); 2,00-2,08 (m, 1Н); 2,38-2,46 (m, 1H); 2,55-2,90 (m, 9H); 3,61-3,82 (m, 4H); 4,48-4,56 (m, 1H); 7,17-7,26 (m, 5H).
Пример 13J. α-(3-трифторметил)бензиламид γ-трет-бутилового эфира D-глутаминовой кислоты. α-(3-трифторметил)бензиламид γ-трет-бутилового эфира N-бензилоксикарбонил-D-глутаминовой кислоты (1,667 г, 3,37 ммоль) приводил к получению 1,15 г (94%) Примера 13J в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,41 (s, 9Н); 1,80-2,20 (m, 4Н); 2,31-2,40 (m, 2Н); 3,51-3,59 (m, 1H); 4,47-4,49 (m, 2H); 7,39-7,52 (m, 4H); 7,71-7,79 (m, 1H).
Пример 13K. γ-(4-циклогексил)пиперазинамид α-трет-бутилового эфира L-глутаминовой кислоты. γ-(4-циклогексил)пиперазинамид α-трет-бутилового эфира N-бензилоксикарбонил-L-глутаминовой кислоты (1,93 г, 3,96 ммоль) приводил к получению 1,30 г (93%) Примера 13К в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,02-1,25 (m, 5Н); 1,41 (s, 9Н); 1,45-1,50 (m, 1Н); 1,56-1,60 (m, 1H); 1,69-1,80 (m, 6H); 3,30 (dd, J=4,8 Гц, J=8,5 Гц, 1H); 3,44 (t, J=9,9 Гц, 2H); 3,56 (t, J=9,9 Гц, 2H).
Пример 13L. α-(2-фтор-3-трифторметил)бензиламид β-трет-бутилового эфира D-аспарагиновой кислоты. α-(2-фтор-3-трифторметил)бензиламид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (0,36 г, 0,72 ммоль) приводил к получению 0,256 г (92%) Примера 13L в виде беловатого масла; 1Н ЯМР (CDCl3) δ 1,39 (s, 9Н); 2,50 (brs, 2Н); 2,74 (dd, J=7,0 Гц, J=16,5 Гц, 1Н); 2,86 (dd, J=4,8 Гц, J=16,8 Гц, 1H); 3,89 (brs, 2H); 4,47-4,57 (m, 2H); 7,16 (t, J=7,8 Гц, 1H); 7,48 (t, J=7,3 Гц, 1H); 7,56 (t, J=7,3 Гц, 1H); 7,97-8,02 (m, 1H).
Пример 13M. α-[(S)-1-(3-трифторметилфенил)этил]амид β-трет-бутилового эфира D-аспарагиновой кислоты. α-[(S)-1-(3-трифторметилфенил)этил]амид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (120 мг, 0,24 ммоль) приводил к получению 91 мг (91%) Примера 13М в виде беловатого масла, и демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 13N. α-[(R)-1-(3-трифторметилфенил)этил]амид β-трет-бутилового эфира D-аспарагиновой кислоты. α-[(R)-1-(3-трифторметилфенил)этил]амид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (217 мг, 0,44 ммоль) приводил к получению 158 мг (количественный выход) Примера 13N в виде беловатого масла, и демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 13O. α-N-метил-N-(3-трифторметилбензил)]амид β-трет-бутилового эфира D-аспарагиновой кислоты. α-[N-метил-N-(3-трифторметилбензил)]амид β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты (0,282 г, 0,57 ммоль) приводил к получению 0,195 г (95%) Примера 13O в виде беловатого масла, и демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 13Р. γ-(3-трифторметил)бензиламид α-метилового эфира D-глутаминовой кислоты. γ-(3-трифторметил)бензиламид α-метилового эфира N-бензилоксикарбонил-D-глутаминовой кислоты (764 мг, 1,69 ммоль) приводил к получению г (516 мг, 96%) Примера 13Р в виде беловатого масла, и демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 14. Общая процедура образования 2-азетидинона из имина и ацетилхлорида.
Стадия 1: Общая процедура образования имина из производного аминокислоты. Раствор 1 эквивалента сложного эфира α-аминокислоты или амида в дихлорметане обрабатывали последовательно 1 эквивалентом соответствующего альдегида и высушивающим агентом, таким как сульфат магния или силикагель, с количеством примерно 2 грамм высушивающего агента на грамм исходного сложного эфира или амида α-аминокислоты. Реакционную смесь перемешивали при комнатной температуре пока все реагенты не израсходовались по показаниям тонкослойной хроматографии. Реакции обычно завершались в течение часа. Реакционную смесь затем фильтровали, фильтрационный осадок промывали дихлорметаном, и фильтрат концентрировали при пониженном давлении с получением требуемого имина, который использовали на следующей стадии.
Стадия 2: Общая процедура для 2+2 циклоприсоединения имина и ацетилхлорида. Раствор имина в дихлорметане (10 мл дихлорметана/1 грамм имина) охлаждали до 0°С. К охлажденному раствору добавляли 1,5 эквивалентов соответствующего амина, как правило триэтиламина, с последующим добавлением по каплям раствора в дихлорметане 1,1 эквивалента соответствующего ацетилхлорида, такого как описанный Примере 1 (10 мл дихлорметана/1 г соответствующего ацетилхлорида). Реакционную смесь оставляли нагреваться до комнатной температуры в течение 1 ч и затем гасили путем добавления насыщенного водного раствора хлорида аммония. Полученную смесь разделяли между водой и дихлорметаном. Слои разделяли и органический слой промывали последовательно 1N соляной кислотой, насыщенным водным бикарбонатом натрия и насыщенным водным хлоридом натрия. Органический слой сушили над сульфатом магния и концентрировали при пониженном давлении. Остаток может быть использован непосредственно для дальнейший реакций, или очищали с помощью хроматографии или с помощью кристаллизации из соответствующей системы растворителей, если необходимо. В каждом случае согласно реакции 2+2 стереохимия β-лактама может быть подтверждена спектром кругового дихроизма/оптического ротационного рассеяния (CD/ORD). Иллюстративно, примеры (αR,3S,4R) и (αS,3S,4R) β-лактамные платформы стереохимической конфигурации из предыдущих синтезов могут быть использованы в качестве стандартов CD/ORD.
Пример 15. трет-Бутил-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил] ацетат. С использованием процедуры Примера 14 имин получали из 4,53 г (34,5 ммоль) трет-бутилового эфира глицина и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 5,5 г (30%) Примера 15 в виде бесцветных кристаллов (перекристаллизованный, н-хлорбутан); т.п. 194-195°С.
Пример 16. Общая процедура ацилирования азетидин-2-он-1-илацетата. Раствор (азетидин-2-он-1-ил)ацетата в тетрагидрофуране (0,22 М в азетидиноне) охлаждали до -78°С и добавляли бис(триметилсилил)амид лития (2,2 эквивалентов). Полученный анион обрабатывали соответствующим ацилгалогенидом (1,1 эквивалентов). После завершения превращения азетидинона реакционную смесь гасили насыщенным водным хлоридом аммония и разделяли между этилацетатом и водой. Органическую фазу промывали последовательно 1N соляной кислотой, насыщенным водным бикарбонатом натрия и насыщенным водным хлоридом натрия. Полученный органический слой сушили (сульфат магния) и выпаривали. Остаток очищали с помощью хроматографии на силикагеле с соответствующим элюентом, таким как 3:2 гексан/этилацетат.
Пример 17. 2,2,2-Трихлорэтил-2(RS)-(трет-бутоксикарбонил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]ацетат.
С использованием процедуры Примера 16, 9,0 г (20 ммоль) Пример 15 ацилировали 4,2 г (20 ммоль) трихлорэтилхлорформиата с получением 7,0 г (56%) Примера 17; т.п. 176-178°С.
Пример 18. N-(3-трифторметилбензил)амид 2(RS)-(трет-Бутоксикарбонил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Раствор 0,20 г (0,32 ммоль) Примера 17 и 52 мкл (0,36 ммоль) (3-трифторметилбензил)амина в ТГФ нагревали с обратным холодильником. После завершения превращения (ТСХ) растворитель выпаривали и остаток перекристаллизовали (хлороформ/гексан) с получением 0,17 г (82%) Примера 18 в виде белого твердого вещества; т.п. 182-184°С.
Пример 18 А. N-(2-фтор-3-трифторметилбензил)амид 2(RS)-(трет-Бутоксикарбонил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 18А получали в соответствии с процедурой Примера 18, используя 2-фтор-3-(трифторметил)бензиламин вместо (3-трифторметилбензил)амина. Пример 18А получали в виде белого твердого вещества (140 мг, 41%), и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Примеры 19-25AF получали в соответствии с процедурой Примера 14, где соответствующее производное аминокислоты и альдегид использовали на Стадии 1, и соответствующий ацетилхлорид использовали на Стадии 2.
Пример 19. N-(3-трифторметилбензил)амид 2(S)-(трет-Бутоксикарбонилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 1,52 г (4,39 ммоль) α-(3-трифторметил)бензиламида β-трет-бутилового эфира L-аспарагиновой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 2,94 г оранжево-коричневого масла, которое приводило к получению, после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/этилацетат), к 2,06 г (70%) Примера 19 в виде белого твердого вещества; 1Н ЯМР (CDCl3) δ 1,39 (s, 9Н); 2,46 (dd, J=11,1 Гц, J=16,3 Гц, 1Н); 3,18 (dd, J=3,8 Гц, J=16,4 Гц, 1H); 4,12-4,17 (m, 1H); 4,26 (d, J=5,0 Гц, 1H); 4,45 (dd, J=6,0 Гц, J=14,9 Гц, 1H); 4,54 (dd, J=5,3 Гц, J=9,8 Гц, 1H); 4,58-4,66 (m, 3H); 4,69-4,75 (m, 1H); 4,81 (dd, J=3,8 Гц, J=11,1 Гц, 1H); 6,25 (dd, J=9,6 Гц, J=15,8 Гц, 1H); 6,70 (d, J=15,8 Гц, 1H); 7,14-7,17 (m, 2H); 7,28-7,46 (m, 11H); 7,62 (s, 1H); 8,27-8,32 (m, 1H).
Пример 19 А. N-(3-трифторметилбензил)амид 2(S)-(трет-Бутоксикарбонилметил)-2-[3(R)-(4(R)-фенилоксазолидин-2-он-3-ил)-4(S)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 19А получали в соответствии со способом Примера 19 за исключением того, что 2-(4(R)-фенилоксазолидин-2-он-3-ил)ацетилхлорид (Пример 1А) использовали вместо 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлорида. Пример 19А получали в виде белого твердого вещества (41 мг, 13%); 1Н ЯМР (CDCl3) δ 1,37 (s, 9Н); 3,11 (dd, J=3,7 Гц, J=17,8 Гц, 1Н); 3,20 (dd, J=10,6 Гц, J=17,8 Гц, 1H); 4,02 (dd, J=3,7 Гц, J=10,6 Гц, 1H); 4,10-4,17 (m, 1H); 4,24 (d, J=4,9 Гц, 1H); 4,4652-4,574 (dd, J=5,9 Гц, J=15,1 Гц, 1H); 4,58-4,76 (m, 4H); 6,27 (dd, J=9,6 Гц, J=15,8 Гц, 1H); 6,79 (d, J=15,8 Гц, 1H); 7,23-7,53 (m, 13H); 7,63 (s, 1H); 8,51-8,55 (m, 1H).
Пример 20. N-(3-трифторметилбензил)амид 2(S)-(трет-Бутоксикарбонилэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 3,94 г (10,93 ммоль) α-(3-трифторметил)бензиламида γ-трет-бутилового эфира L-глутаминовой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 5,53 г (75%) Примера 20 после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,36 (s, 9Н); 1,85-1,96 (m, 1Н); 2,18-2,49 (m, 3Н); 4,14-4,19 (m, 1H); 4,30 (d, J=4,9 Гц, 2H); 4,44 (dd, J=6,1 Гц, J=14,9 Гц, 1H); 4,56-4,67 (m, 4H); 4,71-4,75 (m, 1H); 6,26 (dd, J=9,6 Гц, J=15,8 Гц, 1H); 6,71 (d, J=15,8 Гц, 1H); 7,16-7,18 (m, 2H); 7,27-7,49 (m, 11H); 7,60 (s, 1H); 8,08-8,12 (m, 1H).
Пример 21. N-[4-(2-фенилэтил)]пиперазинамид 2(S)-(трет-Бутоксикарбонилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 4,20 г (11,6 ммоль) α-[4-(2-фенилэтил)]пиперазинамида β-трет-бутилового эфира L-аспарагиновой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 4,37 г (55%) Примера 21 после очистки с помощью колоночной флеш-хроматографии (50:50 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,34 (s, 9Н); 2,26-2,32 (m, 1Н); 2,46-2,63 (m, 4H); 2,75-2,89 (m, 4H); 3,24-3,32 (m, 1H); 3,49-3,76 (m, 3H); 4,07-4,13 (m, 1H); 4,30 (d, J=4,6 Гц, 1H); 4,22-4,48 (m, 1H); 4,55-4,61 (m, 1H); 4,69-4,75 (m, 1H); 5,04-5,09 (m, 1H); 6,15 (dd, J=9,3 Гц, J=15,9 Гц, 1H); 6,63 (d, J=15,8 Гц, 1H); 7,18-7,42 (m, 15H).
Пример 22. N-[4-(2-фенилэтил)]пиперазинамид 2(S)-(трет-Бутоксикарбонилэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 2,54 г (6,75 ммоль) α-[4-(2-фенилэтил)]пиперазинамида γ-трет-бутилового эфира L-глутаминовой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 3,55 г (76%) Примера 22 после очистки с помощью колоночной флеш-хроматографии (50:50 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,32 (s, 9Н); 1,96-2,07 (m, 1Н); 2,15-2,44 (m, 6H); 2,54-2,62 (m, 2H); 2,69-2,81 (m, 3Н); 3,28-3,34 (m, 1H); 3,59-3,68 (m, 1H); 4,08-4,13 (m, 1H); 4,33-4,44 (m, 2H); 4,48-4,60 (m, 2H); 4,67-4,77 (m, 1H); 6,14 (dd, J=8,9 Гц, J=16,0 Гц, 1H); 6,62 (d, J=16,0 Гц, 1H); 7,16-7,42 (m, 15 H).
Пример 23. N-(3-трифторметилбензил)амид 2(R)-(трет-Бутоксикарбонилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 0,973 г (2,81 ммоль) α-(3-трифторметил)бензиламида β-трет-бутилового эфира D-аспарагиновой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 1,53 г (82%) Примера 23 после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,37 (s, 9Н); 3,10 (dd, J=3,7 Гц, J=17,8 Гц, 1Н); 3,20 (dd, J=10,7 Гц, J=17,8 Гц, 1H); 4,02 (dd, J=3,6 Гц, J=10,6 Гц, 1H); 4,11-4,17 (m, 1H); 4,24 (d, J=4,9 Гц, 1H); 4,46 (dd, J=5,8 Гц, J=15,1 Гц, 1H); 4,58-4,67 (m, 3Н); 4,70-4,76 (m, 1H); 6,27 (dd, J=9,5 Гц, J=15,8 Гц, 1H); 6,79 (d, J=15,8 Гц, 1H); 7,25-7,50 (m, 13H); 7,63 (s, 1H); 8,50-8,54 (m, 1H).
Пример 23 А. N-(3-трифторметилбензил)амид 2(R)-(трет-Бутоксикарбонилметил)-2-[3(R)-(4(R)-фенилоксазолидин-2-он-3-ил)-4(S)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 23А получали в соответствии со способом Примера 23 за исключением того, что 2-(4(R)-фенилоксазолидин-2-он-3-ил)ацетилхлорид (Пример 1А) использовали вместо 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлорида. Пример 23А получали в виде белого твердого вещества (588 мг, 49%); 1Н ЯМР (CDCl3) δ 1,39 (s, 9Н); 2,47 (dd, J=11,2 Гц, J=16,3 Гц, 1Н); 3,18 (dd, J=3,8 Гц, J=16,3 Гц, 1H); 4,15 (t, J=8,25, Гц 1H); 4,26 (d, J=5,0 Гц, 1H); 4,45 (dd, J=6,0 Гц, J=15,0 Гц, 1H); 4,52-4,57 (m, 3H); 4,63 (t, J=9 Гц, 1H); 4,70 (t, J=8 Гц, 1H); 4,81 (dd, J=3,8 Гц, J=10,8 Гц, 1H); 6,25 (dd, J=9,8 Гц, J=15,8 Гц, 1H); 6,70 (d, J=15,8 Гц, 1H); 7,15-7,17 (m, 2H); 7,27-7,51 (m, 11H); 7,62 (s, 1H); 8,27-8,32 (m, 1H).
Пример 24. N-(3-трифторметилбензил)амид 2(R)-(трет-Бутоксикарбонилэтил)-2-[3(S)-(4(S)-фенилоксазо лидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 1,15 г (3,20 ммоль) α-(3-трифторметил)бензиламида γ-трет-бутилового эфира D-глутаминовой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 1,84 г (85%) Примера 24 после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,37 (s, 9Н); 2,23-2,39 (m, 4Н); 3,71-3,75 (m, 1Н); 4,13-4,18 (m, 1H); 4,31 (d, J=4,9 Гц, 1H); 4,44-4,51 (m, 2H); 4,56-4,68 (m, 2H); 4,71-4,76 (m, 1H); 6,26 (dd, J=9,5 Гц, J=15,8 Гц, 1H); 6,71 (d, J=15,8 Гц, 1H); 7,25-7,52 (m, 13H); 7,63 (s, 1H); 8,25-8,30 (m, 1H).
Пример 25. N-(4-циклогексил)пиперазинамид 2(S)-(трет-Бутоксикарбонилэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 2,58 г (5,94 ммоль) α-(4-циклогексил)пиперазинамида γ-трет-бутилового эфира L-глутаминовой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлорид (Пример 1) с получением 3,27 г (94%) Примера 25 после очистки с помощью колоночной флеш-хроматографии (95:5 дихлорметан/метанол); 1Н ЯМР (CDCl3) δ 1,32 (s, 9Н); 1,10-1,18 (m, 1Н); 1,20-1,31 (m, 2H); 1,38-1,45 (m, 2H); 1,61-1,66 (m, 1H); 1,84-1,89 (m, 2H); 1,95-2,01 (m, 1H); 2,04-2,14 (m, 3H); 2,20-2,24 (m, 1H); 2,29-2,35 (m, 1H); 2,85-2,92 (m, 1H); 3,24-3,32 (m, 1H); 3,36-3,45 (m, 2H); 3,80-3,86 (m, 1H); 4,08 (t, J=8,3 Гц, 1H); 4,27 (d, J=5,0 Гц, 1H); 4,31-4,55 (m, 4H); 4,71 (t, J=8,3 Гц, 1H); 4,83-4,90 (m, 1H); 6,18 (dd, J=9,1 Гц, J=15,9 Гц, 1H); 6,67 (d, J=15,9 Гц, 1H); 7,25-7,44 (m, 10H); 8,22 (brs, 1H).
Пример 25A. трет-Бутил-2(S)-(2-(4-циклогексилпиперазинилкарбонил)этил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]ацетат. Имин получали из 1,282 г (3,63 ммоль) γ-(4-циклогексил)пиперазинамида α-трет-бутилового эфира L-глутаминовой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 1,946 г (80%) Примера 25А после очистки с помощью колоночной флеш-хроматографии (50:50 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,15-1,26 (m, 6Н); 1,39 (s, 9Н); 1,55-1,64 (m, 2Н); 1,77-1,83 (m, 3Н); 2,22-2,35 (m, 2Н); 2,40-2,50 (m, 6Н); 2,75-2,79 (m, 1H); 3,43-3,48 (m, 1H); 3,56-3,60 (m, 2Н); 3,75-3,79 (m, 1Н); 4,10 (t, J=8,3 Гц, 1Н); 4,31-4,35 (m, 2Н); 4,58 (t, J=8,8 Гц, 1Н); 4,73 (t, J=8,4 Гц, 1Н); 6,17 (dd, J=8,6 Гц, J=16,0 Гц, 1Н); 6,65 (d, J=16,0 Гц, 1Н); 7,27-7,42 (m, 10Н).
Пример 25В. N-(2-фтор-3-трифторметилбензил)амид 2(R)-(трет-Бутоксикарбонилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 0,256 г (0,70 ммоль) α-(2-фтор-3-трифторметил)бензиламида β-трет-бутилового эфира D-аспарагиновой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 0,287 г (60%) Примера 25В после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,38 (s, 9Н); 3,12 (dd, J=4,0 Гц, J=17,8 Гц, 1H); 3,20 (dd, J=10,4 Гц, J=17,8 Гц, 1H); 4,05 (dd, J=3,9 Гц, J=10,4 Гц, 1H); 4,14 (dd, J=J'=8,2 Гц, 1H); 4,25 (d, J=4,9 Гц, 1H); 4,59-4,67 (m, 4H); 4,74 (t, J=8,3 Гц, 1H); 6,36 (dd, J=9,6 Гц, J=15,8 Гц, 1H); 6,83 (d, J=15,8 Гц, 1H); 7,02-7,07 (m, 1H); 7,28-7,55 (m, 12H); 8,44-8,48 (m, 1H).
Пример 25C. N-[(S)-α-метилбензил]амид 2(R)-(трет-Бутоксикарбонилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 0,167 г (0,57 ммоль) [(S)-α-метилбензил]амида β-трет-бутилового эфира D-аспарагиновой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 0,219 г (63%) Примера 25С после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,35 (s, 9Н); 1,56 (d, J=7,0 Гц, 3Н); 2,97 (dd, J=3,5 Гц, J=18,0 Гц, 1Н); 3,15 (dd, J=11,0 Гц, J=17,5 Гц, 1H); 4,01 (dd, J=3,0 Гц, J=11,0 Гц, 1H); 4,14 (t, J=8,5 Гц, 1H); 4,24 (d, J=5,0 Гц, 1H); 4,57 (dd, J=5,0 Гц, J=9,5 Гц, 1H); 4,64 (t, J=8,8 Гц, 1H); 5,07 (t, J=8,5 Гц, 1H); 5,03-5,09 (m, 1H); 6,43 (dd, J=9,5 Гц, J=16,0 Гц, 1H); 6,83 (d, J=16,0 Гц, 1H); 7,16-7,20 (m, 1H); 7,27-7,49 (m, 14H); 8,07-8,10 (m, 1H).
Пример 25D. N-[(R)-α-метилбензил]амид 2(R)-(трет-Бутоксикарбонилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 0,187 г (0,46 ммоль) [(R)-α-метилбензил]амида β-трет-бутилового эфира D-аспарагиновой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 0,25 г (64%) Примера 25D после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,36 (s, 9Н); 1,59 (d, J=7,1 Гц, 3Н); 3,10 (dd, J=3,5 Гц, J=17,8 Гц, 1H); 3,22 (dd, J=10,9 Гц, J=17,8 Гц, 1H); 3,93 (dd, J=3,5 Гц, J=10,8 Гц, 1H); 4,14 (t, J=8,1 Гц, 1H); 4,24 (d, J=5,0 Гц, 1H); 4,58 (dd, J=5,0 Гц, J=9,5 Гц, 1H); 4,65 (t, J=8,7 Гц, 1H); 4,74 (t, J=8,2 Гц, 1H); 5,06-5,14 (m, 1H); 6,32 (dd, J=9,5 Гц, J=15,8 Гц, 1H); 6,74 (d, J=15,8 Гц, 1H); 7,19-7,43 (m, 15H); 8,15-8,18 (m, 1H).
Пример 25E. N-метил-N-(3-трифторметилбензил)амид 2(R)-(трет-Бутоксикарбонилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил] уксусной кислоты. Имин получали из 0,195 г (0,41 ммоль) α-[N-метил-N-(3-трифторметилбензил)]амида β-трет-бутилового эфира D-аспарагиновой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 0,253 г (69%) Примера 25Е после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,36 (s, 9Н); 2,53 (dd, J=4,0 Гц, J=17,0 Гц, 1Н); 3,06 (dd, J=10,8 Гц, J=16,8 Гц, 1H); 3,13 (s, 3H); 4,12 (dd, J=8,0 Гц, J=9,0 Гц, 1H); 4,26 (d, J=5,0 Гц, 1H); 4,38 (d, J=15,0 Гц, 1H); 4,46 (dd, J=5,0 Гц, J=9,5 Гц, 1H); 4,56 (t, J=6,8 Гц, 1H); 4,70-4,79 (m, 2H); 5,27 (dd, J=4,0 Гц, J=11,0 Гц, 1H); 6,22 (dd, J=9,3 Гц, J=15,8 Гц, 1H); 6,73 (d, J=15,8 Гц, 1H); 7,33-7,45 (m, 14H).
Пример 25F. N-(3-трифторметилбензил)амид 2(S)-(трет-Бутоксикарбонилэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-хлорстир-2-ил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 1,62 г (4,44 ммоль) α-(3-трифторметил)бензиламида γ-трет-бутилового эфира L-глутаминовой кислоты и α-хлоркоричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 0,708 г (22%) Примера 25F после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,35 (s, 9Н); 1,68 (brs, 1H); 2,19-2,35 (m, 2H); 2,40-2,61 (m, 2H); 4,13 (dd, J=7,5 Гц, J=9,0 Гц, 1H); 4,22 (t, J=7,0 Гц, 1H); 4,34 (d, J=4,5 Гц, 1H); 4,45 (dd, J=5,5 Гц, J=15,0 Гц, 1H); 4,51-4,60 (m, 3H); 4,89 (dd, J=7,5 Гц, J=8,5 Гц, 1H); 6,89 (s, 1H); 7,28-7,54 (m, 14H).
Пример 25G. N-(3-трифторметилбензил)амид 2(R)-(трет-Бутоксикарбонилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2'-метоксистир-2-ил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 0,34 г (0,98 ммоль) α-(3-трифторметилбензил)амида β-трет-бутилового эфира D-аспарагиновой кислоты и 2'-метоксикоричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 0,402 г (59%) Примера 25G после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,35 (s, 9Н); 1,68 (brs, 1Н); 2,19-2,35 (m, 2H); 2,40-2,61 (m, 2H); 4,13 (dd, J=7,5 Гц, J=9,0 Гц, 1H); 4,22 (t, J=7,0 Гц, 1H); 4,34 (d, J=4,5 Гц, 1H); 4,45 (dd, J=5,5 Гц, J=15,0 Гц, 1H); 4,51-4,60 (m, 3H); 4,89 (dd, J=7,5 Гц, J=8,5 Гц, 1H); 6,89 (s, 1H); 7,28-7,54 (m, 14H).
Пример 25H. трет-Бутил-(2R)-(Бензилоксиметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]ацетат. Имин получали из 0,329 г (1,31 ммоль) трет-бутилового эфира O-(бензил)-D-серина (Пример 5В) и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 0,543 г (73%) Примера 25Н после очистки с помощью колоночной флеш-хроматографии (90:10 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,39 (s, 9Н); 3,56 (dd, J=2,7 Гц, J=9,5 Гц, 1Н); 3,82 (dd, J=4,8 Гц, J=9,5 Гц, 1H); 4,11 (t, J=8,3 Гц, 1H); 4,21-4,29 (m, 2H); 4,50-4,58 (m, 3H); 4,71-4,78 (m, 2H); 6,19 (dd, J=9,1 Гц, J=16,0 Гц, 1H); 6,49 (d, J=16,0 Гц, 1H); 7,07-7,11 (m, 1H); 7,19-7,40 (m, 14H).
Пример 25I. трет-Бутил-2(S)-(2-(4-циклогексилпиперазинилкарбонил)метил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]ацетат. Имин получали из 0,3 г (0,88 ммоль) γ-(4-циклогексил)пиперазинамида α-трет-бутилового эфира L-аспарагиновой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 464 мг (80%) Примера 251 в виде белого твердого вещества после очистки с помощью колоночной флеш-хроматографии (50:50 гексаны/этилацетат). Пример 25I демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 25J. трет-Бутил 3(R)-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-3-метил-4(R)-(стир-2-ил)азетидин-2-он-1-ил]-3-[(3-трифторметил)фенилметиламинокарбонил]пропаноат. Имин получали из 0,307 г (0,89 ммоль) α-(3-трифторметил)бензиламида β-трет-бутилового эфира D-аспарагиновой кислоты (Пример 20) и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)пропаноилхлорид (Пример 1Е) с получением 120 мг (20%) после очистки с помощью колоночной флеш-хроматографии (гексаны 70% / EtOAc 30%); 1H ЯМР (CDCl3) δ 1,25 (s, 3Н), 1,38 (s, 9Н); 3,09 (dd, J=3,0 Гц, J=18,0 Гц, 1H); 3,33 (dd, J=12,5 Гц, J=18,0 Гц, 1H); 4,01 (dd, J=3,0 Гц, J=11,5 Гц, 1H); 4,04 (dd, J=3,5 Гц, J=8,8 Гц, 1H); 4,42 (d, J=9,0 Гц, 1H); 4,45-4,51 (m, 3H); 4,61-4,66 (m, 1H); 4,75 (dd, J=3,5 Гц, J=8,5 Гц, 1H); 6,23 (dd, J=9,0 Гц, J=15,5 Гц, 1H); 6,78 (d, J=15,5 Гц, 1H); 7,23-7,53 (m, 13H); 7,64 (s, 1H).
Пример 25K. N-(3-трифторметилбензил)амид 2(R)-(трет-Бутоксикарбонилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(проп-1-енил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 0,289 г (0,83 ммоль) α-(3-трифторметил)бензиламида β-трет-бутилового эфира D-аспарагиновой кислоты и кротоновый альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 381 мг (76%) Примера 25К после очистки с помощью колоночной флеш-хроматографии (99:1 CH2Cl2/МеОН); 1Н ЯМР (CDCl3) δ 1,36 (s, 9Н), 1,69 (dd, J=2 Гц, J=6,5 Гц, 3Н); 3,08 (dd, J=3,3 Гц, J=17,8 Гц, 1Н); 3,18 (dd, J=11 Гц, J=17,5 Гц, 1H); 3,94 (dd, J=3,5 Гц, J=11 Гц, 1H); 4,12 (d, J=5 Гц, 1H); 4,15 (dd, J=7 Гц, J=8 Гц, 1H); 4,35 (dd, J=4,8 Гц, J=9,8Hz, 1H); 4,44 (dd, J=6 Гц, J=15 Гц, 1H); 4,61 (dd, J=6 Гц, J=15 Гц, 1H); 4,67-4,75 (m, 2H); 5,52-5,58 (m, 1H); 5,92-6,00 (m, 1H); 7,33-7,60 (m, 9H); 8,47-8,50 (m, 1H).
Пример 25O. Метил-2(S)-(трет-Бутоксикарбонилэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]ацетат. Имин получали из 433 мг (1,99 ммоль) γ-трет-бутилового эфира α-метилового эфира L-глутаминовой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 682 мг (64%) Примера 25O после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,32 (s, 9Н); 2,10-2,26 (m, 1Н); 2,30-2,41 (m, 3Н); 3,66 (s, 3Н); 3,95-3,99 (m, 1H); 4,16 (dd, J=7,5 Гц, J=9 Гц, 1H); 4,38 (dd, J=5 Гц, J=9 Гц, 1H); 4,55 (d, J=5 Гц 1H); 4,61 (t, J=9 Гц, 1H); 4,86 (dd, J=7,5 Гц, J=9 Гц, 1H); 6,00 (dd, J=9 Гц, J=16 Гц, 1H); 6,60 (d, J=16 Гц, 1H); 7,26-7,43 (m, 10H).
Пример 25M. трет-Бутил-2(S)-(метоксикарбонилэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]ацетат. Имин получали из 428 мг (1,97 ммоль) γ-трет-бутилового эфира α-метилового эфира L-глутаминовой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 864 мг (82%) Примера 25М после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/этилацетат); 1Н ЯМР (CDCl3) δ 1,40 (s, 9Н); 2,12-2,27 (m, 1H); 2,32-2,55 (m, 3Н); 3,50 (s, 3Н); 3,72 (dd, J=4,6 Гц, J=10,4 Гц, 1H); 4,12-4,17 (m, 1H); 4,34 (dd, J=5 Гц, J=9 Гц, 1H); 4,50 (d, J=5 Гц, 1H); 4,60 (t, J=8,9 Гц, 1Н); 4,81-4,86 (m, 1H); 6,06 (dd, J=9 Гц, J=16 Гц, 1H); 6,59 (d, J=16 Гц, 1H); 7,25-7,42 (m, 10H).
Пример 25P. Метил-2(S)-(трет-Бутоксикарбонилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]ацетат. Имин получали из 424 мг (2,09 ммоль) γ-трет-бутилового эфира α-метилового эфира L-аспарагиновой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 923 мг (85%) Примера 25Р после перекристаллизации из смеси CH2Cl2/гексаны; 1Н ЯМР (CDCl3) δ 1,41 (s, 9Н); 2,77 (dd, J=7,5 Гц, J=16,5 Гц, 1Н); 3,00 (dd, J=7 Гц, J=16,5 Гц, 1H); 4,16 (dd, J=7. 5Hz, J=9 Гц, 1H); 4,41-48 (m, 2H); 4,55 (d, J=5 Гц, 1H); 4,60 (t, J=8,8 Гц, 1H); 4,86 (dd, J=7,5 Гц, J=9 Гц, 1H); 5,93 (dd, J=9,5 Гц, J=15,5 Гц, 1H); 6,61 (d, J=15,5 Гц, 1H); 7,25-7,43 (m, 10H).
Пример 25L. N-[(R)-1-(3-трифторметилфенил)этил]амид 2(R)-(трет-Бутоксикарбонилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 160 мг (0,44 ммоль) α-[(R)-1-(3-трифторметилфенил)этил]амида β-трет-бутилового эфира D-аспарагиновой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 166 мг (55%) Примера 25L после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/ EtOAc). Пример 25L демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 25N. N-[(S)-1-(3-трифторметилфенил)этил]амид 2(R)-(трет-Бутоксикарбонилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 120 мг (0,22 ммоль) α-[(S)-1-(3-трифторметилфенил)этил]амида β-трет-бутилового эфира D-аспарагиновой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 75 мг (50%) Примера 25N после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/EtOAc). Пример 25N демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 25Q. Метил-2(R)-(2-(3-трифторметилбензил)аминокарбонил)этил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]ацетат. Имин получали из 517 мг (1,62 ммоль) γ-(3-трифторметил)бензиламида α-метилового эфира D-глутаминовой кислоты и коричный альдегид объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 527 мг (51%) Примера 25Q после очистки с помощью колоночной флеш-хроматографии (50:50 гексаны/ EtOAc). Пример 25Q демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Следующие соединения получали согласно способам, описанным в настоящем документе:
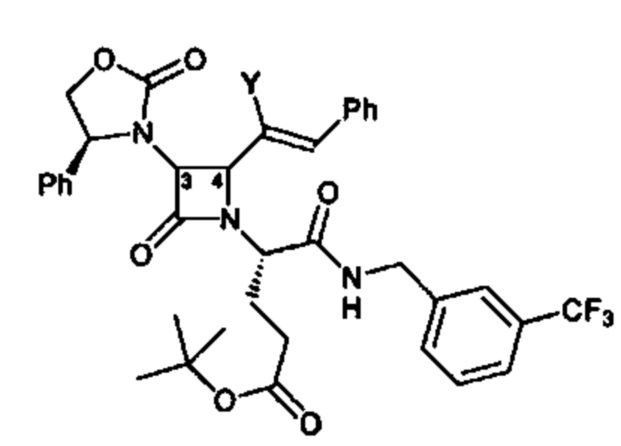

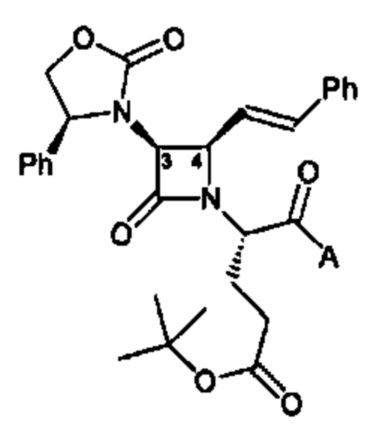

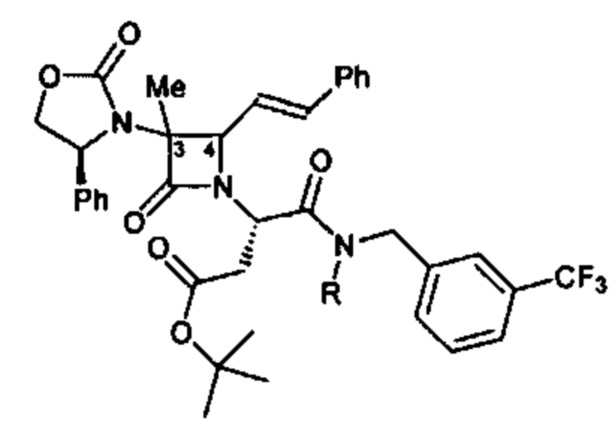
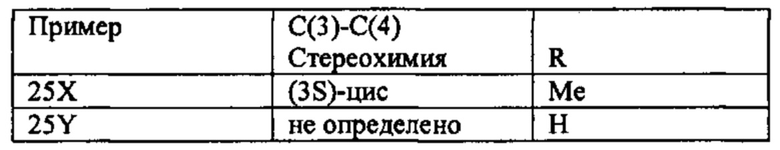
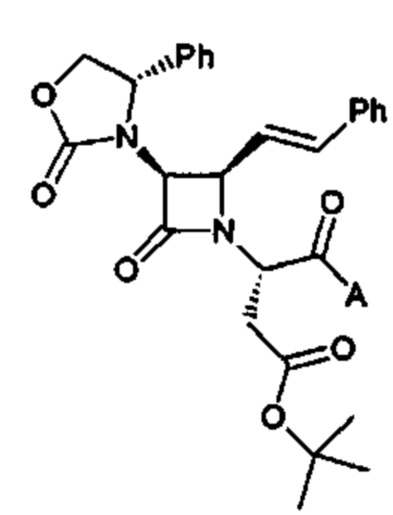
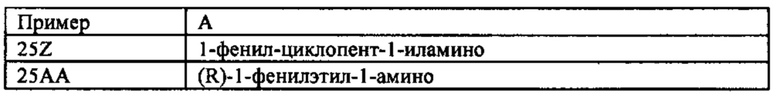
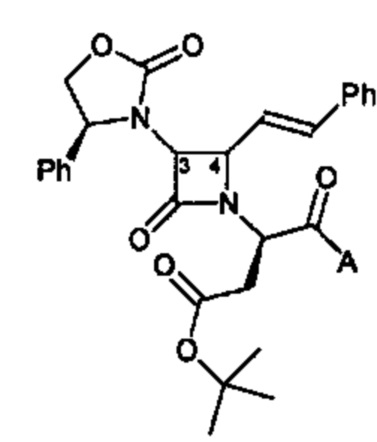

Пример 25 AF. трет-бутил-2(S)-(2-(3-трифторметилбензил)аминокарбонил)этил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]ацетат.
Пример 26. Общая процедура гидролиза трет-бутилового эфира. Раствор производного трет-бутилового эфира в муравьиной кислоте, как правило. 1 г в 10 мл, перемешивали при комнатной температуре пока не сложный эфир не перестал обнаруживаться с помощью тонкослойной хроматографии (дихлорметан 95%/метанол 5%), типичное время реакции составляло примерно 3 часа. Муравьиную кислоту выпаривали при пониженном давлении; полученный твердый остаток разделяли между дихлорметаном и насыщенным водным бикарбонатом натрия. Органический слой выпаривали с получением беловатого твердого вещества, которое можно использовать непосредственно для дальнейших реакций, или перекристаллизовали из соответствующей системы растворителей, если необходимо.
Примеры 27-34АЕ получали из соответствующего трет-бутилового эфира в соответствии с процедурой, использованной в Примере 26.
Пример 27. N-(3-трифторметилбензил)амид 2(R,S)-(карбокси)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 18 (0,30 г, 0,46 ммоль) гидролизовали с получением 0,27 г (количественный выход) Примера 27 в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 4,17-5,28 (m, 9Н); 6,21-6,29 (m, 1Н), 6,68-6,82 (m, 1H); 7,05-7,75 (m, 13H); 9,12-9,18 (m, 1H).
Пример 28. N-(3-трифторметилбензил)амид 2(S)-(Карбоксиметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 19 (1,72 г, 2,59 ммоль) гидролизовали с получением 1,57 г (количественный выход) Примера 28 в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 2,61 (dd, J=9,3 Гц, J=16,6 Гц, 1Н); 3,09-3,14 (m, 1H); 4,10-4,13 (m, 1H); 4,30 (d, J=4,5 Гц, 1H); 4,39-4,85 (m, 6H); 6,20 (dd, J=9,6 Гц, J=15,7 Гц, 1H); 6,69 (d, J=15,8 Гц, 1H); 7,12-7,15 (m, 2H); 7,26-7,50 (m, 11H); 7,61 (s, 1H); 8,41-8,45 (m, 1H).
Пример 28A. N-(3-трифторметилбензил)амид 2(S)-(карбоксиметил)-2-[3(R)-(4(R)-фенилоксазолидин-2-он-3-ил)-4(S)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 19А (41 мг, 0,06 ммоль) гидролизовали с получением 38 мг (количественный выход) Примера 28А в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 2,26 (d, J=7 Гц, 1H); 4,03 (t, J=7 Гц, 1H); 4,16 (t, J=8 Гц, 1H); 4,26 (d, J=4,3 Гц, 1H); 4,46 (dd, J=5,7 Гц, J=15,1, 1H); 4,53-4,75 (m, 5H); 6,25 (dd, J=9,5 Гц, J=15,7 Гц, 1H); 6,77 (d, J=15,7 Гц, 1H); 7,28-7,53 (m, 13H); 7,64 (s, 1H); 8,65-8,69 (m, 1H).
Пример 29. 1H-(3-трифторметилбензил)амид 2(S)-(Карбоксиэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 20 (4,97 г, 7,34 ммоль) гидролизовали с получением 4,43 г (97%) Примера 29 в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,92-2,03 (m, 1Н); 2,37-2,51 (m, 3Н); 4,13-4,19 (m, 1Н); 3,32 (d, J=4,9 Гц, 1Н); 4,35-4,39 (m, 1Н); 4,44 (dd, J=5,9 Гц, J=14,9 Гц, 1Н); 4,50-4,57 (m, 2Н); 4,61-4,67 (m, 1Н); 4,70-4,76 (m, 1Н); 6,24 (dd, J=9,6 Гц, J=15,8 Гц, 1Н); 6,70 (d, J=15,8 Гц, 1Н); 7,18-7,47 (m, 14Н).
Пример 30. N-[4-(2-фенилэтил)]пиперазинамид 2(S)-(карбоксиметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 21 (1,88 г, 2,78 ммоль) гидролизовали с получением 1,02 г (60%) Примера 30 в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 2,63 (dd, J=6,0 Гц, J=16,5 Гц, 1Н); 2,75-2,85 (m, 1H); 3,00 (dd, J=8,2 Гц, J=16,6 Гц, 1H); 3,13-3,26 (m, 4H); 3,37-3,56 (m, 4H); 3,86-4,00 (m, 1H); 4,05-4,11 (m, 1H); 4,24 (d, J-5,0 Гц, 1H); 4,46-4,66 (m, 1H); 4,65-4,70 (m, 1H); 5,10-5,15 (m, 1H); 6,14 (dd, J=9,3 Гц, J=15,9 Гц, 1H); 6,71 (d, J=15,9 Гц, 1H); 7,22-7,41 (m, 15H); 12,02 (s, 1H).
Пример 31. N-[4-(2-фенилэтил)]пиперазинамид 2(S)-(Карбоксиэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 22 (0,383 г, 0,55 ммоль) гидролизовали с получением 0,352 г (количественный выход) Примера 31 в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,93-2,01 (m, 1H); 2,07-2,36 (m, 6H); 2,82-2,90 (m, 1H); 3,00-3,20 (m, 4H); 3,36-3,54 (m, 4H); 3,74-3,82 (m, 1H); 4,06-4,11 (m, 1H); 4,29 (d, J=4,9 Гц, 1H); 4,33-4,46 (m, 2H); 4,50-4,58 (m, 2H); 4,67-4,72 (m, 1H); 4,95-5,00 (m, 1H); 6,18 (dd, J=9,2 Гц, J=16,0 Гц, 1H); 6,67 (d, J=15,9 Гц, 1H); 7,19-7,42 (m, 15H); 8,80 (brs, 1H).
Пример 32. N-(3-трифторметилбензил)амид 2(R)-(карбоксиметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 23 (1,51 г, 2,27 ммоль) гидролизовали с получением 1,38 г (количественный выход) Примера 32 в виде беловатого твердого вещества.
Пример 32А. N-(3-трифторметилбензил)амид 2(R)-(карбоксиметил)-2-[3(R)-(4(R)-фенилоксазолидин-2-он-3-ил)-4(S)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 23А (550 мг, 0,83 ммоль) гидролизовали с получением 479 мг (95%) Примера 32А в виде беловатого твердого вещества. Пример 32А демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 33. N-(3-трифторметилбензил)амид 2(R)-(Карбоксиэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 24 (0,604 г, 0,89 ммоль) гидролизовали с получением 0,554 г (количественный выход) Примера 33 в виде беловатого твердого вещества.
Пример 34. N-(4-циклогексил)пиперазинамид 2(S)-(Карбоксиэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 25 (0,537 г, 0,80 ммоль) гидролизовали с получением 0,492 г (количественный выход) Примера 34 в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,09-1,17 (m, 1H); 1,22-1,33 (m, 2Н); 1,40-1,47 (m, 2Н); 1,63-1,67 (m, 1Н); 1,85-1,90 (m, 2H); 1,95-2,00 (m, 1H); 2,05-2,15 (m, 3H); 2,20-2,24 (m, 1H); 2,30-2,36 (m, 1H); 2,85-2,93 (m, 1H); 3,25-3,33 (m, 1H); 3,36-3,46 (m, 2H); 3,81-3,87 (m, 1H); 4,08 (t, J=8,3 Гц, 1H); 4,28 (d, J=5,0 Гц, 1H); 4,33-4,56 (m, 4H); 4,70 (t, J=8,3 Гц, 1H); 4,83-4,91 (m, 1H); 6,17 (dd, J=9,1 Гц, J=15,9 Гц, 1H); 6,67 (d, J=15,9 Гц, 1H); 7,25-7,44 (m, 10H); 8,22 (brs, 1H).
Пример 34А. 2(S)-(2-(4-циклогексилпиперазинилкарбонил)этил)-2- [3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 25A (0,787 г, 1,28 ммоль) гидролизовали с получением 0,665 г (92%) Примера 34А в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,05-1,13 (m, 1Н); 1,20-1,40 (m, 5Н); 1,60-1,64 (m, 1Н); 1,79-1,83 (m, 2Н); 2,00-2,05 (m, 2Н); 2,22-2,44 (m, 3Н); 2,67-2,71 (m, 1Н); 2,93-3,01 (m, 4Н); 3,14-3,18 (m, 1Н); 3,38-3,42 (m, 1Н); 3,48-3,52 (m, 1H); 3,64-3,69 (m, 1Н); 4,06-4,14 (m, 2Н); 4,34-4,43 (m, 2Н); 4,56 (t, J=8,8 Гц, 1Н); 4,73 (t, J=8,4 Гц, 1Н); 6,15 (dd, J=9,1 Гц, J=16,0 Гц, 1Н); 6,65 (d, J=16,0 Гц, 1Н); 7,25-7,42 (m, 10Н).
Пример 34 В. N-(2-фтор-3-трифторметилбензил)карбоксамид 2(R)-(карбоксиметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 25 В (0,26 г, 0,38 ммоль) гидролизовали с получением 0,238 г (количественный выход) Примера 34В в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 3,27 (d, J=7,2 Гц, 1H); 4,06 (t, J=7,2 Гц, 1H); 4,15 (t, J=8,1 Гц, 1H); 4,27 (d, J=4,8 Гц, 1H); 4,56-4,76 (m, 5H); 6,34 (dd, J=9,5 Гц, J=15,7 Гц, 1H); 6,80 (d, J=15,7 Гц, 1H); 7,06 (t, J=7,7 Гц, 1H); 7,31-7,54 (m, 12H); 8,58 (t, J=5,9 Гц, 1H).
Пример 34C. N-[(S)-α-метилбензил]амид 2(R)-(карбоксиметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 25С (0,215 г, 0,35 ммоль) гидролизовали с получением 0,195 г (количественный выход) Примера 34С в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,56 (d, J=7,0 Гц, 1Н); 3,10 (dd, J=4,5 Гц, J=17,9 Гц, 1H); 3,18 (dd, J=9,8 Гц, J=17,9 Гц, 1H); 4,00 (dd, J=4,5 Гц, J=9,7 Гц, 1H); 4,14 (t, J=8,2 Гц, 1H); 4,26 (d, J=4,7 Гц, 1H); 5,02-5,09 (m, 1H); 6,41 (dd, J=9,4 Гц, J=15,8 Гц, 1H); 6,78 (d, J=15,8 Гц, 1H); 7,18 (t, J=7,3 Гц, 1H); 7,26-7,43 (m, 12H); 8,29 (d, J=8,2 Гц, 1H).
Пример 34D. N-[(R)-α-метилбензил]амид 2(R)-(карбоксиметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 25D (0,22 г, 0,35 ммоль) гидролизовали с получением 0,20 г (количественный выход) Примера 34D в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,59 (d, J=7,0 Гц, 1H); 3,25 (d, J=7,0 Гц, 2H); 3,92 (t, J=7,3 Гц, 1H); 4,15 (t, J=8,3 Гц, 1H); 4,26 (d, J=5,0 Гц, 1H); 4,52 (dd, J=4,8 Гц, J=9,3 Гц, 1H); 4,65 (t, J=8,8 Гц, 1H); 4,72 (t, J=8,3 Гц, 1H); 5,07-5,28 (m, 1H); 6,29 (dd, J=9,5 Гц, J=15,6 Гц, 1H); 6,71 (d, J=16,0 Гц, 1H); 7,20-7,43 (m, 13H); 8,31 (d, J=8,0 Гц, 1H).
Пример 34E. N-метил-N-(3-трифторметилбензил)амид 2(R)-(карбоксиметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 25Е (0,253 г, 0,37 ммоль) гидролизовали с получением 0,232 г (количественный выход) Примера 34Е в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 3,07-3,15 (m, 4Н); 4,13 (t, J=8,2 Гц, 1Н); 4,30 (d, J=4,9 Гц, 1H); 4,46-4,78 (m, 5H); 5,23 (dd, J=4,6 Гц, J=9,7 Гц, 1H); 6,20 (dd, J=9,4 Гц, J=15,9 Гц, 1H); 6,73 (d, J=15,9 Гц, 1H); 7,25-7,43 (m, 15H).
Пример 34F. N-(3-трифторметилбензил)амид 2(S)-(Карбоксиэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-хлорстир-2-ил)азетидин-2-он-1-ил]уксусной кислоты. Пример 25F (0,707 г, 0,99 ммоль) гидролизовали с получением 0,648 г (99%) Примера 34F в виде беловатого твердого вещества; 1H ЯМР (CDCl3) δ 2,22-2,28 (m, 2H); 2,49-2,64 (m, 2Н); 4,09 (t, J=8,0 Гц, 1H); 4,25-4,62 (m, 6H); 4,87 (t, J=8,0 Гц, 1H); 6,88 (s, 1H); 7,25-7,66 (m, 15H).
Пример 34G. N-(3-трифторметилбензил)амид 2(R)-(карбоксиметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2'-метоксистир-2-ил)азетидин-2-он-1-ил]уксусной кислоты. Пример 25G (0,268 г, 0,39 ммоль) гидролизовали с получением 0,242 г (98%) Примера 34G в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 3,26 (d, J=7,1 Гц, 1Н); 3,79 (s, 3Н); 4,14 (t, J=8,2 Гц, 1H); 4,25 (d, J=4,5 Гц, 1H); 4,51 (dd, J=5,9 Гц, J=15,5 Гц, 1H); 4,53-4,66 (m, 4H); 6,36 (dd, J=9,4 Гц, J=15,8 Гц, 1H); 8,88 (t, J=8,2 Гц, 1H); 6,70 (d, J=15,8 Гц, 1H); 7,18 (d, J=6,5 Гц, 1H); 7,25-7,48 (m, 10H); 7,48 (s, 1H); 8,66-8,69 (m, 1H).
Пример 34H. (2R)-(Бензилоксиметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусная кислота. Пример 25Н (0,16 г, 0,28 ммоль) гидролизовали с получением 0,144 г (количественный выход) Примера 34Н в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 3,65 (dd, J=4,0 Гц, J=9,5 Гц, 1H); 3,82 (dd, J=5,5 Гц, J=9,5 Гц, 1H); 4,11 (dd, J=7,8 Гц, J=8,8 Гц, 1H); 4,33 (s, 2H); 4,50 (d, J=5,0 Гц, 1H); 4,57 (t, J=9,0 Гц, 1H); 4,67 (dd, J=4,0 Гц, J=5,0 Гц, 1H); 4,69 (dd, J=5,0 Гц, J=9,5 Гц, 1H); 4,75 (t, J=8,0 Гц, 1H); 6,17 (dd, J=9,3 Гц, J=15,8 Гц, 1H); 6,55 (d, J=16,0 Гц, 1H); 7,09-7,12 (m, 2H); 7,19-7,42 (m, 13H).
Пример 34I. 2(S)-(2-(4-циклогексилпиперазинилкарбонил)метил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусная кислота. Пример 25I (737 мг, 1,12 ммоль) гидролизовали с получением 640 мг (95%) Примера 34I в виде беловатого твердого вещества. Пример 34I он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 34J. 3(R)-[3(S)-(4(S)-Фенилоксазолидин-2-он-3-ил)-3-метил-4(R)-(стир-2-ил)азетидин-2-он-1-ил]-3-[(3-трифторметил)фенилметиламинокарбонил]пропановая кислота. Используя общий способ Примера 26, 120 мг (0,18 ммоль) Примера 25J гидролизовали с получением 108 мг (98%) Примера 34J в виде беловатого твердого вещества; 1Н ЯМР (CDCl3) δ 1,22 (s, 3Н); 3,25 (dd, J=3,5 Гц, J=18,0 Гц, 1Н); 3,36 (dd, J=10,8 Гц, J=18,2 Гц, 1H); 4,01 (dd, J=4,0 Гц, J=10,5 Гц, 1H); 4,05 (dd, J=3,8 Гц, J=8,8 Гц, 1H); 4,33 (d, J=9,0 Гц, 1H); 4,44-4,51 (m, 3H); 4,61-4,66 (m, 1H); 4,73 (dd, J=3,8 Гц, J=8,8 Гц, 1H); 6,19 (dd, J=9,0 Гц, J=16,0 Гц, 1H); 6,74 (d, J=16,0 Гц, 1H); 7,22-7,54 (m, 13H); 7,65 (s, 1H).
Пример 34K. N-(3-трифторметилбензил)амид 2(R)-(карбоксиметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(пропен-1-ил)азетидин-2-он-1-ил]уксусной кислоты. Используя общий способ Примера 26, 160 мг (0,27 ммоль) Примера 25K гидролизовали с получением 131 мг (90%) Примера 34K в виде беловатого твердого вещества. 1Н ЯМР (CDCl3) δ 1,69 (dd, J=1 Гц, J=6,5 Гц, 3Н); 3,23 (d, J=7 Гц, 1H); 3,93 (t, J=7,3Hz, 1H); 4,14-4,20 (m, 3H); 4,29 (dd, J=5 Гц, J=9,5 Гц, 1H); 4,43 (dd, J=6 Гц, J=15 Гц, 1H); 4,61 (dd, J-6,5 Гц, J=15 Гц, 1H); 4,66-4,74 (m, 2H); 5,50-5,55 (m, 1H); 5,90-5,98 (m, 1H); 7,32-7,60 (m, 9H); 8,60-8,64 (m, 1H).
Пример 34L. N-[(R)-1-(3-трифторметилфенил)этил]амид 2(R)-(карбоксилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 25L (166 мг, 0,24 ммоль) гидролизовали с получением 152 мг (количественный выход) Примера 34L в виде беловатого твердого вещества; и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 34М. 2(S)-(Метоксикарбонилэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 25М (875 мг, 1,64 ммоль) гидролизовали с получением 757 мг (97%) Примера 34М в виде беловатого твердого вещества, и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 34N. N-[(S)-1-(3-трифторметилфенил)этил]амид 2(R)-(карбоксилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 25N (38,5 мг, 0,057 ммоль) гидролизовали с получением 35 мг (количественный выход) Примера 34N в виде беловатого твердого вещества, и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 34O. 2(S)-(трет-Бутоксикарбонилэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусная кислота. Пример 25O (97 мг, 0,18 ммоль) растворяли в смеси метанол/тетрагидрофуран (2,5 мл/2 мл) и подвергали взаимодействию с гидроксидом лития (0,85 мл 0,85М раствора в воде; 0,72 ммоль) в течение 6 часов при комнатной температуре. Реакционную смесь разбавляли 15 мл дихлорметана и добавляли водную соляную кислоту (1М) до достижения рН водного слоя 5 (как измерено с помощью стандартной рН индикаторной бумаги). Органический слой затем отделяли и выпаривали досуха с получением 84 мг (89%) Примера 34O в виде беловатого твердого вещества, и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 34Р. 2(S)-(трет-Бутоксикарбонилэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусная кислота. Пример 25Р (200 мг, 0,39 ммоль) гидролизовали в соответствии со способом, используемым в Примере 34O, с получением 155 мг (88%) Примера 34Р в виде беловатого твердого вещества; и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 34Q. 2(R)-(2-(3-трифторметилбензил)амино-1-илкарбонил)этил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусная кислота. Пример 25Q (150 мг, 0,24 ммоль) гидролизовали в соответствии со способом, используемым в Примере 340 с получением 143 мг (97%) Примера 34Q в виде беловатого твердого вещества, и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 34R. N-(3-трифторметилбензил)амид 2(R)-(трет-Бутоксикарбонилметил)-2-[3(RS)-2-тиенилметил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Имин получали из 290 мг (0,84 ммоль) α-(3-трифторметил)бензиламида β-трет-бутилового эфира D-аспарагиновой кислоты и коричный альдегид объединяли с 2-тиофенацетилхлоридом с получением 42 мг (8%) Примера 34R после очистки с помощью колоночной флеш-хроматографии (70:30 гексаны/этилацетат), и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Следующие соединения получали в соответствии со способами, описанными в настоящем документе:
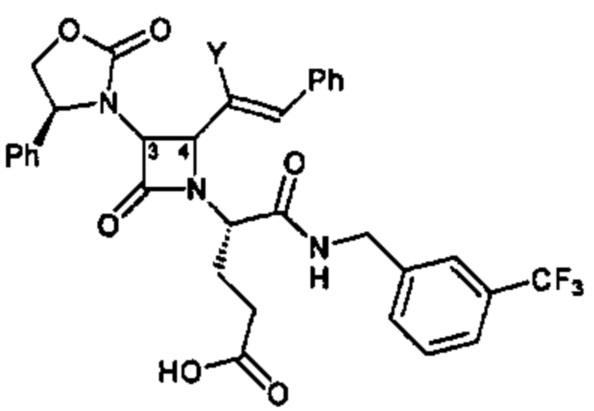

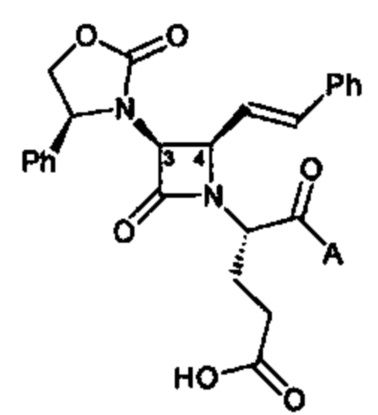

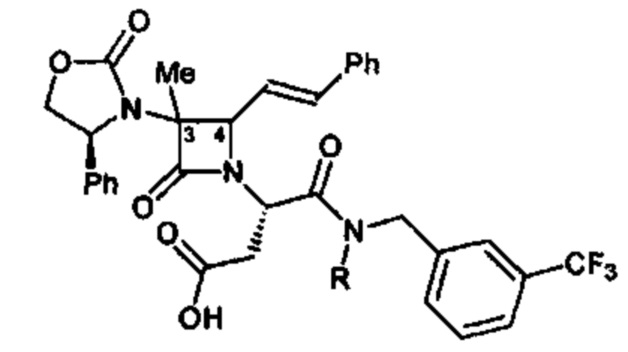

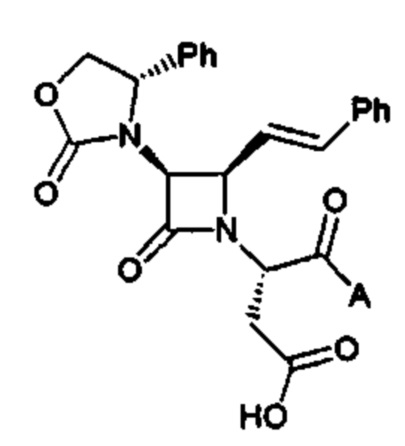

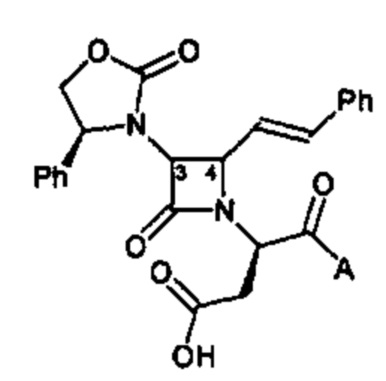

Примеры 36-42А, показанные в следующей таблице, получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 27, и 3-(трифторметил)бензиламин заменяли соответствующим амином; все перечисленные Примеры демонстрировали 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
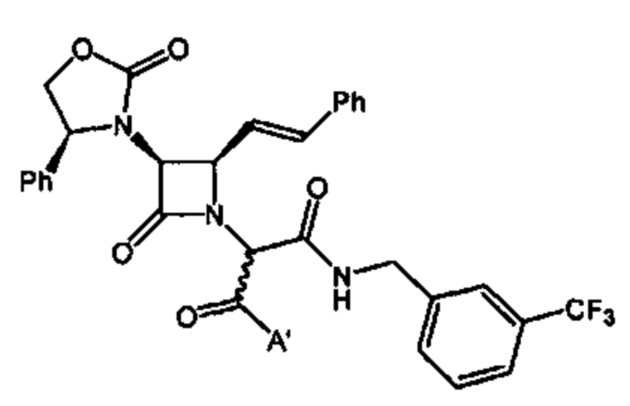

Примеры 43-86А, показанные в следующей таблице, получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 28, и 3-(трифторметил)бензиламин заменяли соответствующим амином; все перечисленные Примеры демонстрировали 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
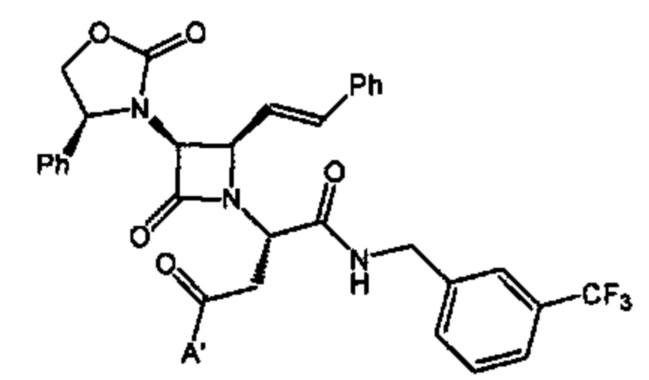

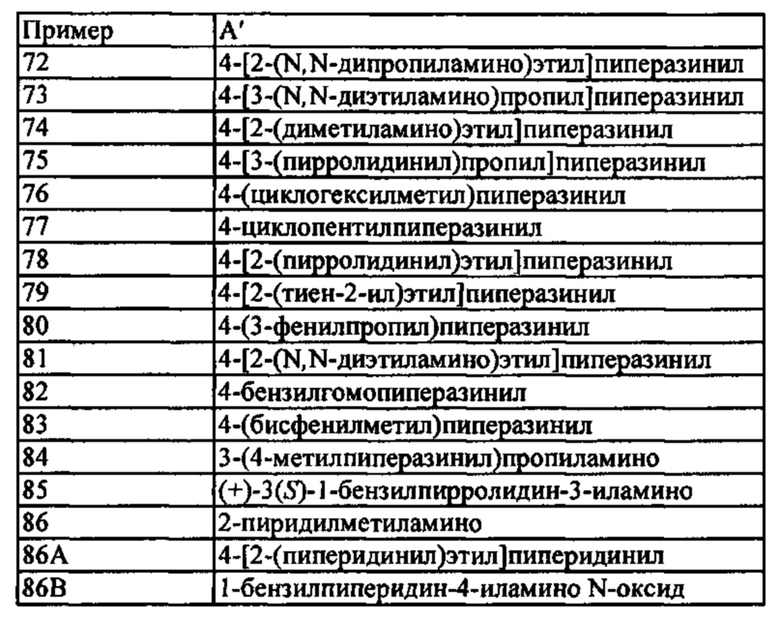
Пример 86В. Пример 63 (44 мг, 0,06 ммоль) растворяли в 4 мл дихлорметана и подвергали взаимодействию с 3- хлорпероксибензойной кислотой (12 мг, 0,07 ммоль) до завершения реакции по оценке ТСХ (дихлорметан 94%/метанол 6%, УФ-детектирование). Реакцию гасили водным раствором сульфита натрия, слой дихлорметана промывали 5% водным бикарбонатом натрия и дистиллированной водой. В результате выпаривания слоя дихлорметана получали Пример 86В в виде беловатого твердого вещества (35 мг, 78%), и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Примеры 121-132, показанные в следующей таблице, получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 30, и 3-(трифторметил)бензиламин заменяли соответствующим амином; все перечисленные Примеры демонстрировали 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
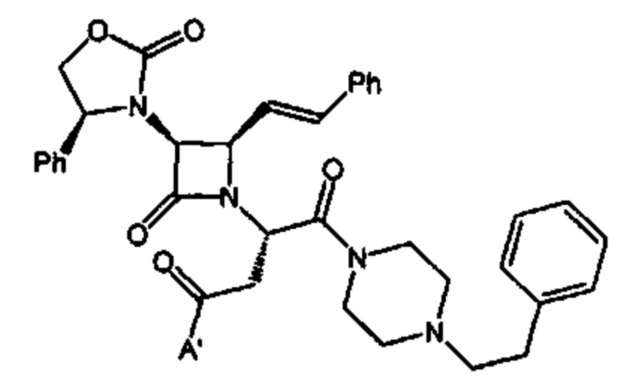


Примеры 132А-132В, показанные в следующей таблице, получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 341, и 3-(трифторметил)бензиламин заменяли соответствующим амином; все перечисленные Примеры демонстрировали 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
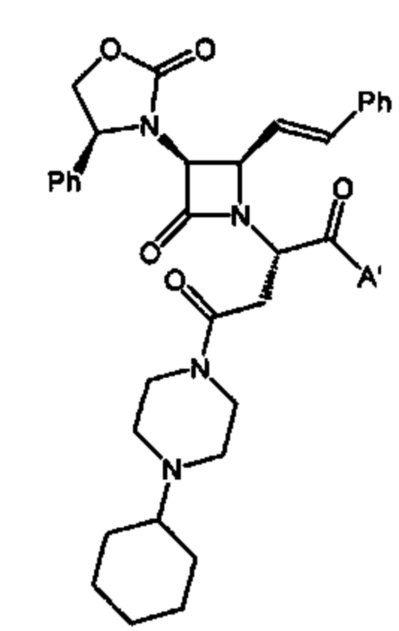

Пример 132С N-(4-циклогексил)пиперазинамид 2(S)-(трет-Бутоксикарбонилметил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил] уксусной кислоты. Пример 132С получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34Р, и 3-(трифторметил)бензиламин заменяли на 1-циклогексилпиперазин. Пример 132С демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Соединения, показанные в следующей таблице, получали в соответствии со способами, описанными в настоящем документе.
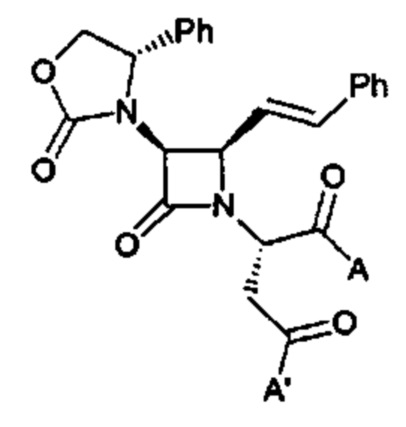
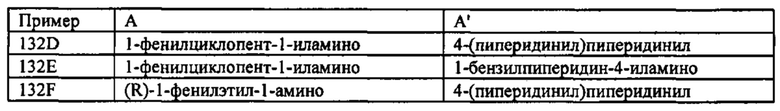
Примеры 133-134G, показанные в следующей таблице, получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 32, и 3-(трифторметил)бензиламин заменяли соответствующим амином; все перечисленные Примеры демонстрировали 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
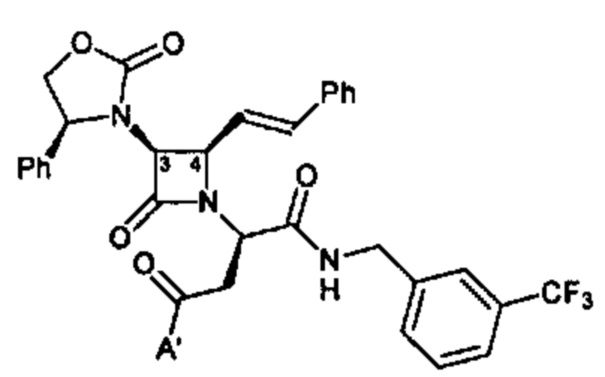

Пример 134Н. Пример 134Н получали с использованием процедуры Примера 86В, за исключением того, что Пример 133 заменяли на Пример 110. Пример 134Н получали в виде беловатого твердого вещества (48 мг, 94%), и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 134I. N-(3-трифторметилбензил)амид 2(R)-[[4-(Пиперидинил)пиперидинил]карбоксиметил]-2-[3(S)-(4(R)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 134I получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 32А, и 3-(трифторметил)бензиламин заменяли на 4-(пиперидинил)пиперидин, и он демонстрировал 1H ЯМР спектр, согласующийся с предполагаемой структурой.
Соединения, показанные в следующей таблице, получали в соответствии со способами, описанными в настоящем документе.
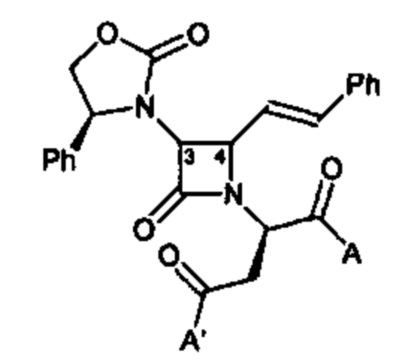

Пример 222. N-(2-фтор-3-трифторметилбензил)карбоксамид 2(R)-[[4-(Пиперидинил)пиперидинил]карбонилметил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 222 получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34В, и 3-(трифторметил)бензиламин заменяли на 4-(пиперидинил)пиперидин; Пример 222 демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 223. N-[(S)-α-метилбензил]амид 2(R)-[[4-(Пиперидинил)пиперидинил]карбонилметил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидан-2-он-1-ил]уксусной кислоты. Пример 223 получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34С, и 3-(трифторметил)бензиламин заменяли на 4-(пиперидинил)пиперидин; Пример 223 демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 224. N-[(R)-α-метилбензил]амид 2(R)-[[4-(Пиперидинил)пиперидинил]карбонилметил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 224 получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34D, и 3-(трифторметил)бензиламин заменяли на 4-(пиперидинил)пиперидин; Пример 223 демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 225. N-метил-N-(3-трифторметилбензил)амид 2(R)-[[4-(Пиперидинил)пиперидинил]карбонилметил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 225 получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34Е, и 3-(трифторметил)бензиламин заменяли на 4-(пиперидинил)пиперидин; Пример 223 демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой; Вычислено для C43H48F3N5O5: С, 66,91; Н, 6,27; N, 9,07; обнаружено. С, 66,68; Н, 6,25; N, 9,01.
Пример 225 Гидрохлоридная соль. Пример 225 (212,5 мг) растворяли в 30 мл сухого Er2O. Сухой газообразный HCl барботировали через указанный раствор, что приводтло к быстрому образованию беловатого осадка. Добавление HCl прекращали, до тех пор, пока не прекратилось видимое образование осадка (са. 5 минут). Твердое вещество выделяли путем фильтрования с отсасыванием, промывали дважды 15 мл сухого Et2O и сушили до 213,5 мг (96% выход) беловатого твердого вещества; Вычислено для C43H49CIF3N5O5: С, 63,89; Н, 6,11; N, 8,66; Сl, 4,39; обнаружено. С, 63,41; Н, 5,85; N, 8,60; Сl, 4,86.
Пример 225А. N-[(S)-α-метилбензил]амид 2(R)-[[4-[2-(пиперидинил)этил]пиперидинил]карбонилметил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 225А получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34С, и 3-(трифторметил)бензиламин заменяли на 4-[2-(пиперидинил)этил]пиперидин. Пример 225А демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 225В. N-[(R)-α-метилбензил]амид 2(R)-[[4-[2-(пиперидинил)этил]пиперидинил]карбонилметил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 225В получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34D, и 3-(трифторметил)бензиламин заменяли на 4-[2-(пиперидинил)этил]пиперидин. Пример 225 В демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 225С. N-[(R)-1-(3-трифторметилфенил)этил]амид 2(R)-[[4-(Пиперидинил)пиперидинил]карбонилметил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 225С получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34L, и 3-(трифторметил)бензиламин заменяли на 4-(пиперидинил)пиперидин. Пример 225С демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 225D. N-[(S)-1-(3-трифторметилфенил)этил]амид 2(R)-[[4-Пиперидинил)пиперидинил]карбонилметил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 225D получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-гилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34М, и 3-(трифторметил)бензиламин заменяли на 4-(пиперидинил)пиперидин. Пример 225D демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Примеры 87-120Е, показанные в следующей таблице, получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 29, и 3-(трифторметил)бензиламин заменяли соответствующим амином; все перечисленные Примеры демонстрировали 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
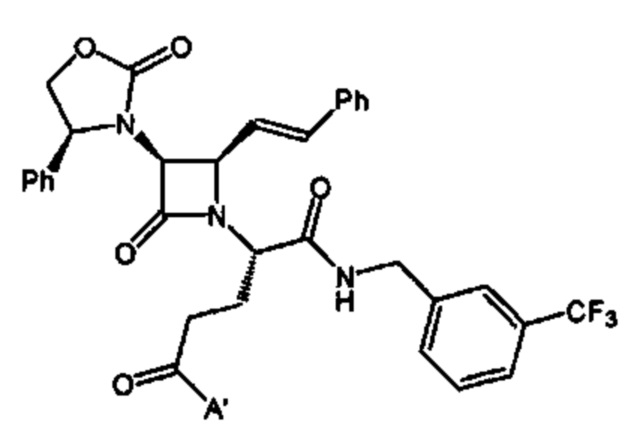


Пример 120F. Пример 120F получали с использованием процедуры Примера 86В, за исключением того, что Пример 63 заменяли на Пример 110 с получением беловатого твердого вещества (54,5 мг, 98%). Пример 120F демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 120G. N-(3-трифторметилбензил)амид 2(S)-(Метоксикарбонилэтил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 120G получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34М, и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 35. N-(3-трифторметилбензил)амид 2(S)-[4-(2-фенилэтил)пиперазинил-карбонилэтил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. С использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на карбоновую кислоту Примера 29 и 3-(трифторметил)бензиламин заменяли на 4-(2-фенилэтил)пиперазин, получали указанное в заголовке соединения; 1Н ЯМР (CDCl3) δ 2,21-2,23 (m, 1Н); 2,25-2,45 (m, 6H); 2,52-2,63 (m, 3Н); 2,72-2,82 (m, 2H); 3,42-3,48 (m, 2H); 3,52-3,58 (m, 1H); 4,13-4,18 (m, 1H); 4,26 (dd, J=5,1 Гц, J=8,3 Гц, 1H); 4,29 (d, J=5,0 Гц, 1H); 4,44 (dd, J=6,0 Гц, J=15,0 Гц, 1H); 4,54 (dd, J=6,2 Гц, J=14,9 Гц, 1H); 4,61-4,68 (m, 2H); 4,70-4,75 (m, 1H); 6,27 (dd, J=9,6 Гц, J=15,8 Гц, 1H); 6,73 (d, J=15,8 Гц, 1H); 7,16-7,60 (m, 19H); 8,07-8,12 (m, 1H); FAB+(M+H)+/z 794; Элементный анализ вычислен для C45H46F3N5O5: С, 68,08; Н, 5,84; N, 8,82; обнаружено: С, 67,94; Н, 5,90; N, 8,64.
Примеры 141-171, показанные в следующей таблице, получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34, и 3-(трифторметил)бензиламин заменяли соответствующим амином; все перечисленные Примеры демонстрировали 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
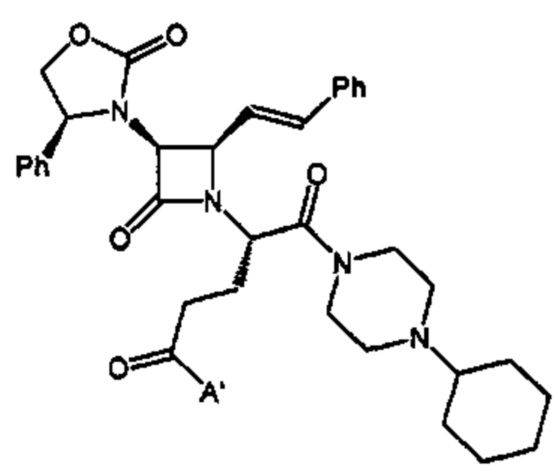

Примеры 172-221R, показанные в следующей таблице, получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34А, и 3-(трифторметил)бензиламин заменяли соответствующим амином; все перечисленные Примеры демонстрировали 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
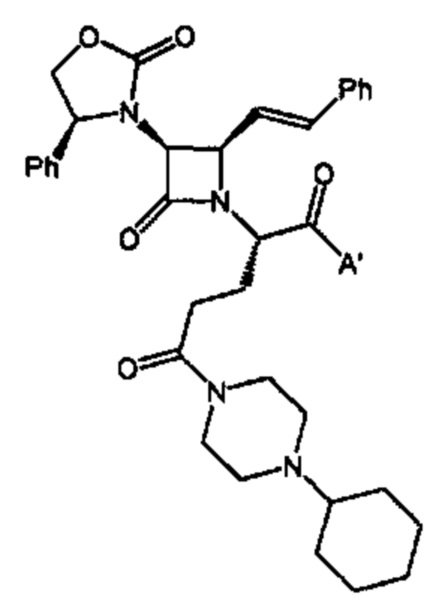


Соединения, показанные в следующей таблице, получали в соответствии со способами, описанными в настоящем документе.
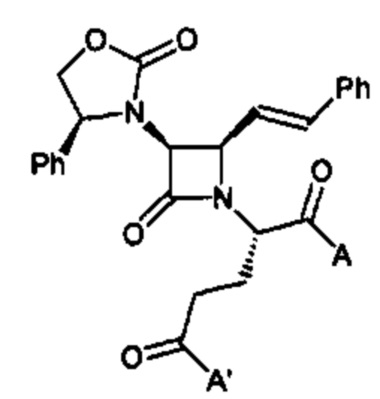

Примеры 135-140, показанные в следующей таблице, получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 33, и 3-(трифторметил)бензиламин заменяли соответствующим амином; все перечисленные Примеры демонстрировали 1H ЯМР спектр, согласующийся с предполагаемой структурой.
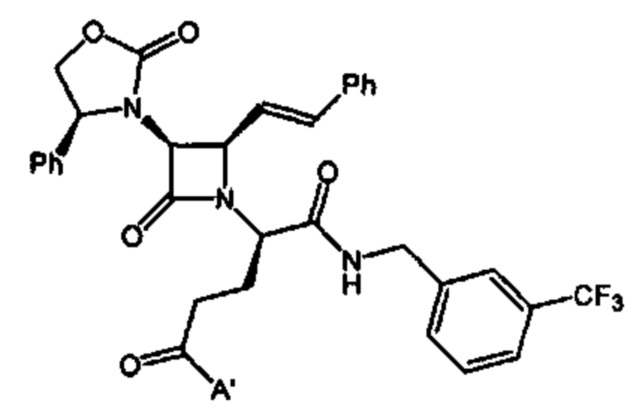

Пример 140 А. N-(4-циклогексил)пиперазинамид 2(R)-(2-(3-трифторметилбензил)амино-1-илкарбонил)этил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 140А получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34Q, и 3-(трифторметил)бензиламин заменяли на 1-циклогексил-пиперазин, и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Примеры 226-230С, показанные в следующей таблице, получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34F, и 3-(трифторметил)бензиламин заменяли соответствующим амином; все перечисленные Примеры демонстрировали 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
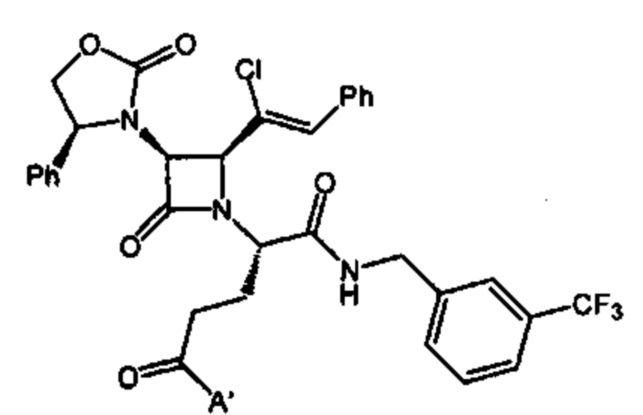

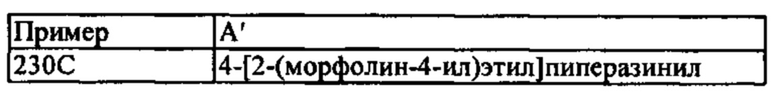
Следующие соединения получали в соответствии со способами, описанными в настоящем документе:
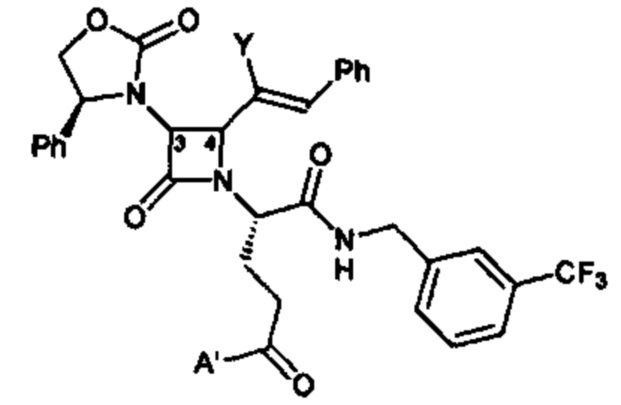
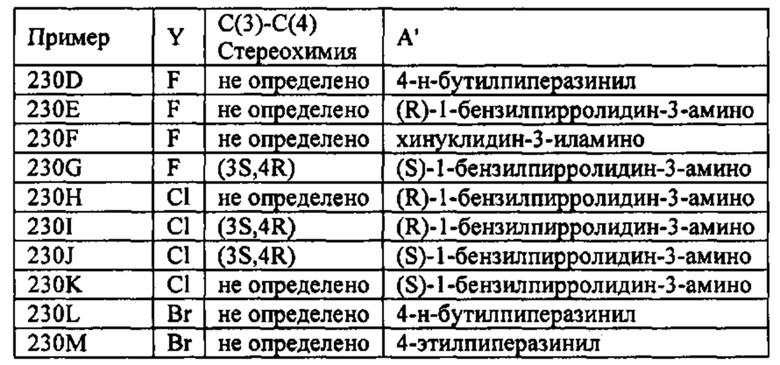
Пример 86С. N-(3-трифторметилбензил)амид 2(S)-[[4-
(Пиперидинил)пиперидинил]карбонилметил]-2-[3(S)-(4(R)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Пример 86С получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 28А, и 3-(трифторметил)бензиламин заменяли на 4-(пиперидинил)пиперидин, и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 231. N-(3-трифторметилбензил)амид 2(R)-[[4-(Пиперидинил)пиперидинил]карбонилметил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2'-метоксистир-2-ил)азетидин-2-он-1-ил]уксусной кислоты. Пример 231 получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34G, и 3-(трифторметил)бензиламин заменяли на 4-(пиперидинил)пиперидин, и он демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Примеры 232-233А, показанные в следующей таблице, получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34Н, и 3-(трифторметил)бензиламин заменяли соответствующим амином; все перечисленные Примеры демонстрировали 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
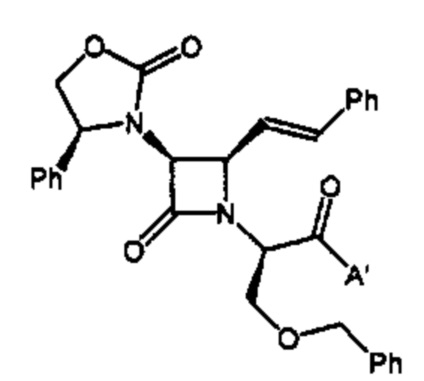

Пример 234. N-(3-трифторметилбензил)амид (2RS)-[4-(пиперидинил)пиперидинилкарбонил]-2-метил-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты.
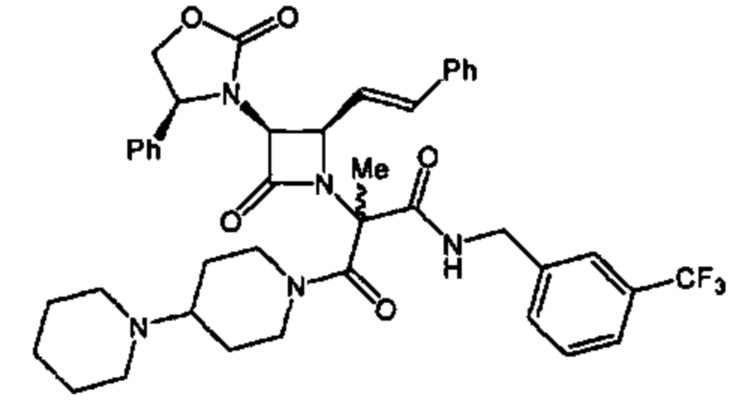
Пример 37 (50 мг, 0,067 ммоль) в тетрагидрофуране (4 мл) обрабатывали последовательно гидридом натрия (4 мг, 0,168 ммоль) и метилйодидом (6 мкл, 0,094 ммоль) при -78°С. Полученную смесь медленно нагревали до комнатной температуры и выпаривали. Полученный остаток разделяли между дихлорметаном и водой и органический слой выпаривали. Полученный остаток очищали с помощью хроматографии на силикагеле (95:5 хлороформ/метанол) с получением 28 мг (55%) указанного в заголовке соединения в виде беловатого твердого вещества; MS (ES+): m/z=757 (М+).
Пример 234А. 4-(Пиперидинил)-пиперидинил-3(R)-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-3-метил-4(R)-(стир-2-ил)азетидин-2-он-1-ил]-3-[(3-трифторметил)фенилметиламинокарбонил]пропановая кислота.
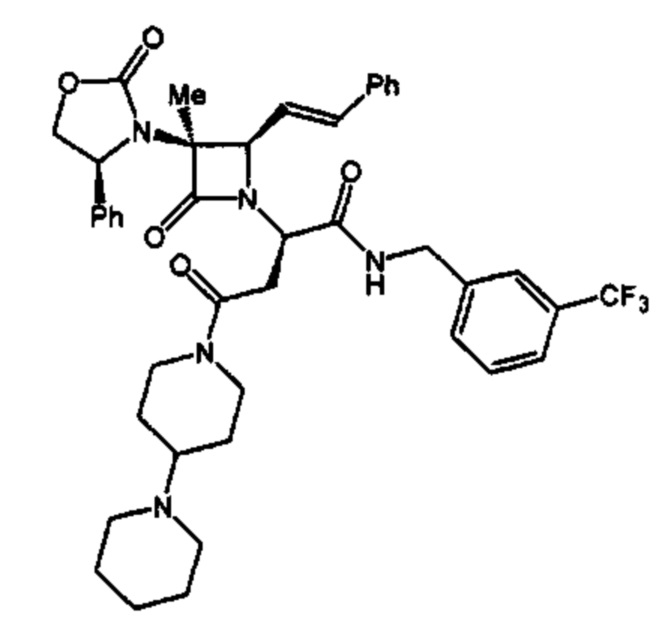
С использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на карбоновую кислоту Примера 34J и 3-(трифторметил)бензиламин заменяли на 4-(пиперидинил)пиперидин, получали указанное в заголовке соединение с количественным выходом; MS (m+H)+ 772.
Соединения, показанные в следующей таблице, получали в соответствии со способами, описанными в настоящем документе.
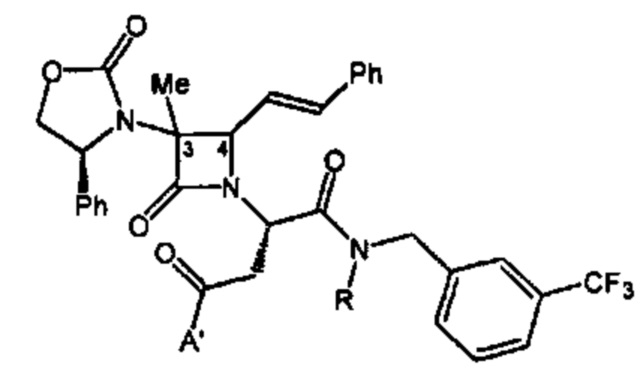

Пример 235. N-(3-трифторметилбензил)амид 2(S)-[[(1-Бензилпиперидин-4-ил)амино]карбонилметил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-фенилет-1-ил)азетидин-2-он-1-ил]уксусной кислоты. Пример 235 получали с использованием процедуры Примера 8, за исключением того, что α-(3-трифторметил)бензиламид β-трет-бутилового эфира N-бензилоксикарбонил-L-аспарагиновой кислоты заменяли на Пример 63 (50 мг, 0,064 ммоль) с получением 40 мг (80%) Примера 235 в виде беловатого твердого вещества; Пример 235 демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 236. N-(3-трифторметилбензил)амид (2S)-[(4-циклогексилпиперазинил)карбонилэтил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-фенилет-1-ил)азетидин-2-он-1-ил]уксусной кислоты. Пример 236 получали с использованием процедуры Примера 8, за исключением того, что α-(3-трифторметил)бензиламид β-трет-бутилового эфира N-бензилоксикарбонил-L-аспарагиновой кислоты заменяли на Пример 110 (50 мг, 0,065 ммоль) с получением 42 мг (84%) Примера 236 в виде беловатого твердого вещества; Пример 236 демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 236А. R-[(R)-1,2,3,4-тетрагидронафт-1-ил]амид (2S)-[(4-циклогексилпиперазинил)карбонилэтил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-фенилет-1-ил)азетидин-2-он-1-ил]уксусной кислоты. Пример 236А получали с использованием процедуры Примера 8, за исключением того, что α-(3-трифторметил)бензиламид β-трет-бутилового эфира N-бензилоксикарбонил-L-аспарагиновой кислоты заменяли на Пример 215 (76 мг, 0,10 ммоль) с получением 69 мг (90%) Примера 236А в виде беловатого твердого вещества. Пример 236А демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 237. N-(3-трифторметилбензил)амид 2(R)-[[4-(пиперидинил)пиперидинил]карбонилметил]-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(пропен-1-ил)азетидин-2-он-1-ил]уксусной кислоты. Пример 237 получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на Пример 34К, и 3-(трифторметил)бензиламин заменяли на 4-(пиперидинил)пиперидин. Пример 237 демонстрировал 1Н ЯМР спектр, согласующийся с предполагаемой структурой.
Пример 238. N-[4-[2-(пиперид-1-ил)этил]пиперидин-1-ил]амид (2S)-(Бензилтиометил)-2-[3(S)-(4(S)-фенилоксазолидин-2-он-3-ил)-4(R)-(2-стирил)азетидин-2-он-1-ил]уксусной кислоты. Указанный пример получали с использованием процедуры Примера 6, за исключением того, что моногидрат β-трет-бутилового эфира N-бензилоксикарбонил-D-аспарагиновой кислоты заменяли на соответствующий аналог с защищенным бензилом цистеином, и 3-(трифторметил)бензиламин заменяли на 4-[2-(пиперид-1-ил)этил]пиперидин.
Стадия 1. N-трет-бутилоксикарбонил-(S)-(бензил)-D-цистеин-[4-(2-(1-пиперидил)этил)]пиперидиненамид. N-трет-бутилоксикарбонил-(S)-Бензил-N-(трет-бутилоксикарбонил)-D-цистеин (0,289 г, 0,93 ммоль) и 4-[2-(1-пиперидил)этил]пиперидин (0,192 г, 0,98 ммоль) в дихлорметане (20 мл) приводили к получению 0,454 г (количественный выход) Примера X в виде беловатого твердого вещества. 1Н ЯМР (CDCl3) δ 0,89-1,15 (m, 2Н); 1,39-1,44 (m, 16Н); 1,54-1,61 (m, 4Н); 1,62-1,71 (m, 1H); 2,21-2,35 (m, 5H); 2,49-2,58 (m, 2H); 2,66-2,74 (m, 1H); 2,79-2,97 (m, 1H); 3,67-3,76 (m, 3H); 4,48-4,51 (m, 1H); 4,72-4,75 (m, 1H); 5,41-5,44 (m, 1H); 7,19-7,34 (m, 5H).
Стадия 2. (S)-(бензил)-D-цистеин-[4-(2-(1-пиперидил)этил)] пиперидиненамид, дигидрохлорид. N-трет-Бутилоксикарбонил-(S)-(бензил)-D-цистеин-[4-(2-(1-пиперидил)этил)]пиперидиненамид (0,453 г, 0,93 ммоль) подвергали взаимодействию в течение ночи с ацетилхлоридом (0,78 мл, 13,80 ммоль) в безводном метаноле (15 мл). Указанного в заголовке соединения получали в виде беловатого твердого вещества путем выпаривания реакционной смеси досуха (0,417 г, 97%). 1Н ЯМР (CD3OD) δ 0,94-1,29 (m, 2Н); 1,49-1,57 (m, 1Н); 1,62-1,95 (m, 10Н); 2,65-2,80 (m, 2H); 2,81-2,97 (m, 4H); 3,01-3,14 (m, 2H); 3,50-3,60 (m, 3Н); 3,81-3,92 (m, 2H); 4,41-4,47 (m, 2H); 7,25-7,44 (m, 5H).
Стадия 3. Используя общие процедуры, описанные в настоящем документе, имин получали из (S)-(бензил)-D-цистеин-[4-(2-(1-пиперидил)этил)]пиперидиненамида, дигидрохлорида (0,417 г, 0,90 ммоль) и коричный альдегида в присутствии триэтиламина (0,26 мл, 1,87 ммоль), объединяли с 2-(4(S)-фенилоксазолидин-2-он-3-ил)ацетилхлоридом (Пример 1) с получением 0,484 г (76%) Примера 238 в виде беловатого твердого вещества после перекристаллизации из смеси дихлорметан/гексаны. 1Н ЯМР (CDCl3) δ 0,89-1,06 (m, 2Н); 1,40-1,44 (m, 5Н); 1,57-1,67 (m, 6Н); 2,25-2,43 (m, 6Н); 2,45-2,59 (m, 2Н); 2,71-2,88 (m, 2Н); 3,55-3,70 (m, 3Н); 4,11-4,17 (m, 1Н); 4,37-4,47 (m, 2H); 4,54-4,61 (m, 1H); 4,64-4,69 (m, 1H); 4,76-4,84 (m, 2H); 6,05-6,19 (m, 1H); 6,66-6,71 (m, 1H); 7,12-7,40 (m, 15H).
Следующие соединения описаны
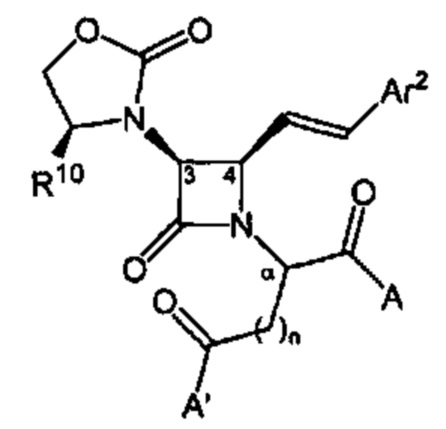
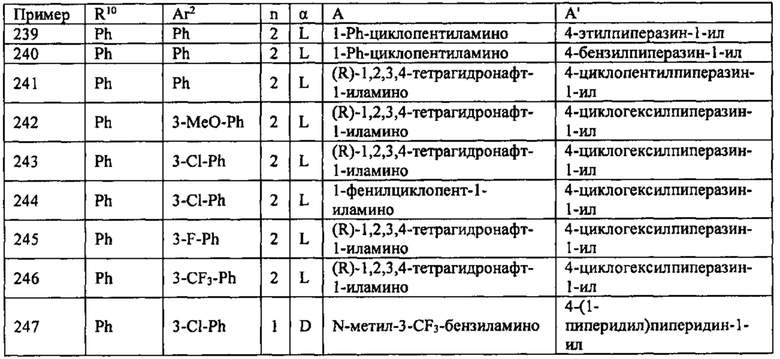
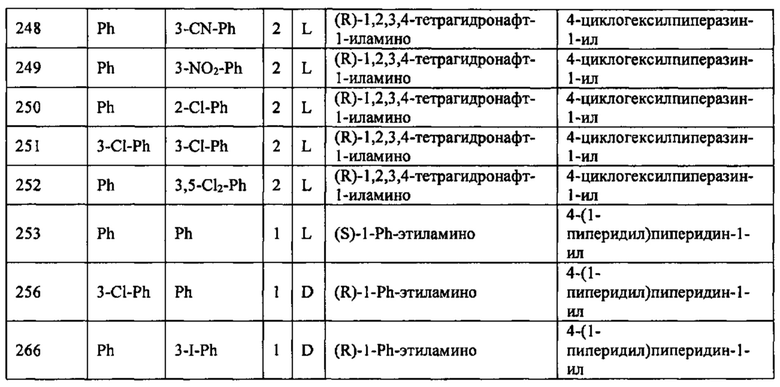
Следующие соединения описаны
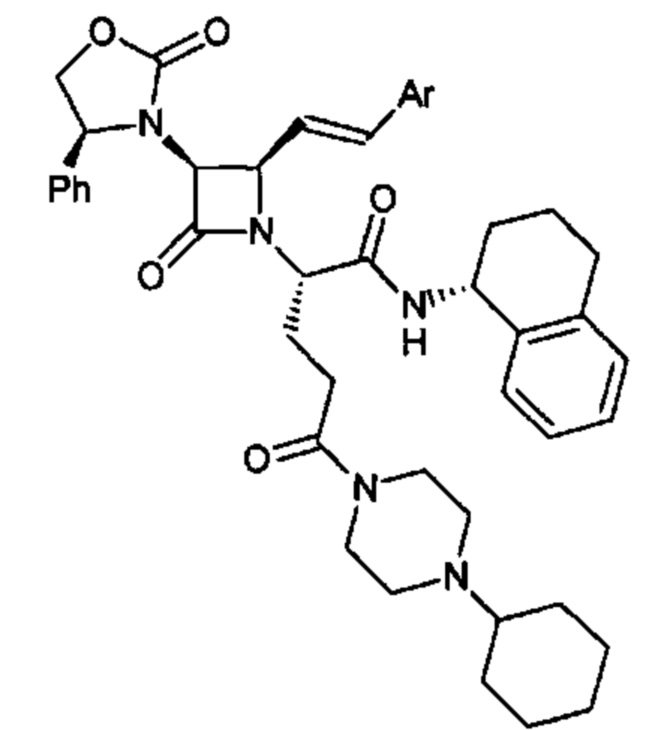

Следующие соединения описаны
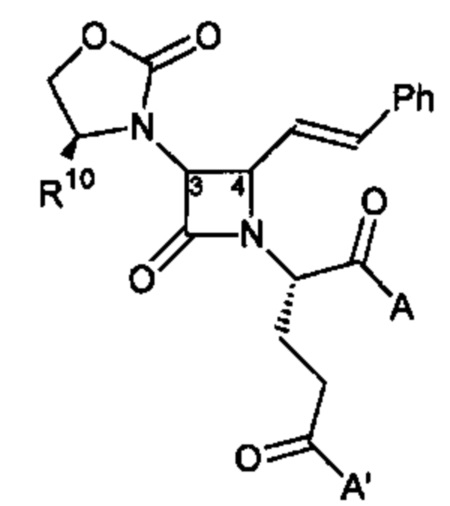


Следующие соединения описаны
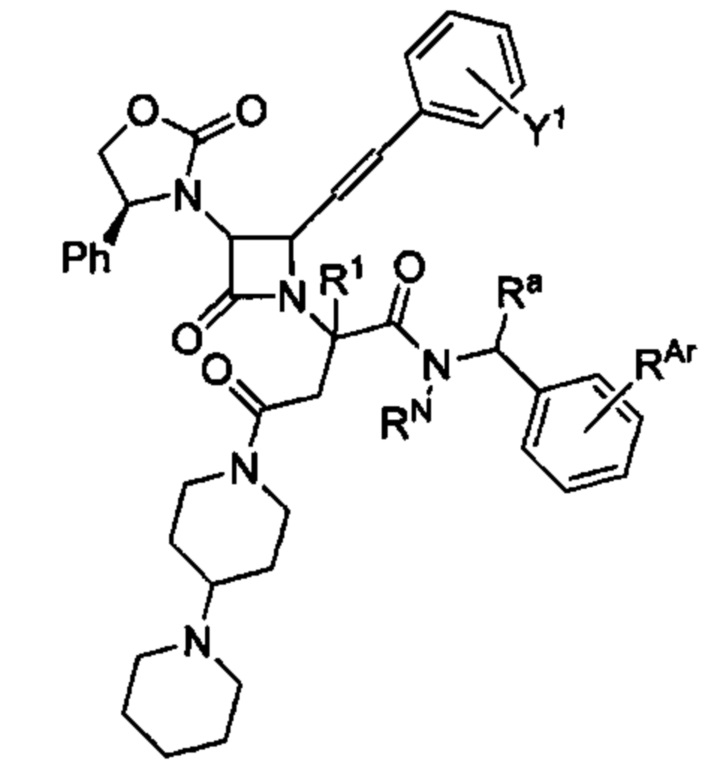
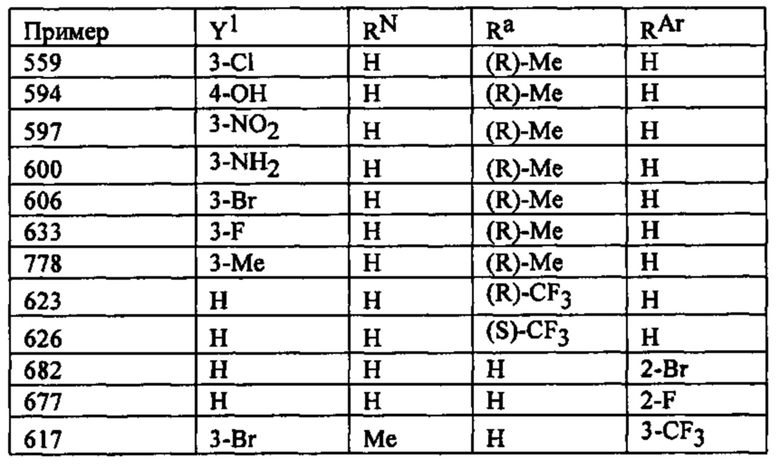
Следующие соединения описаны
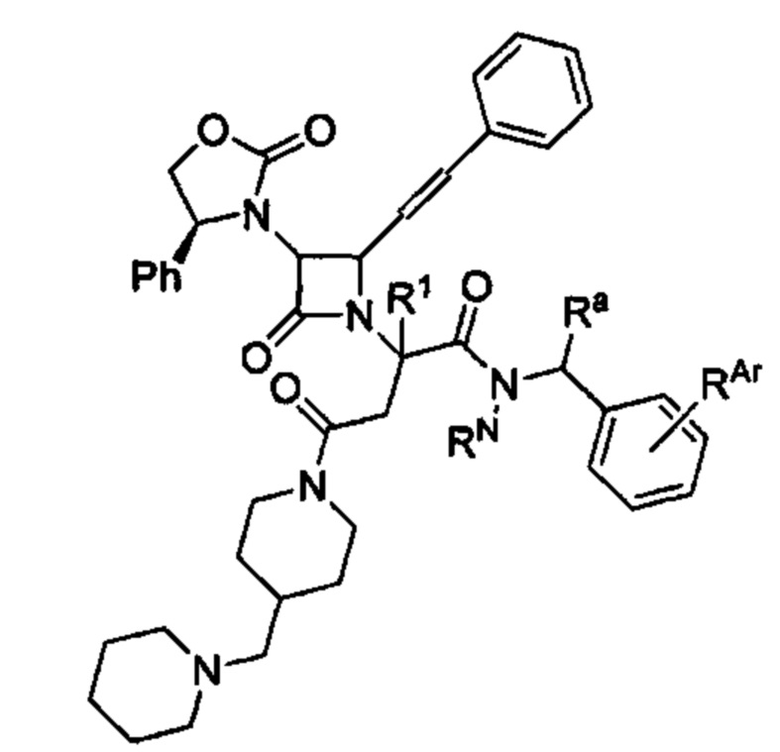
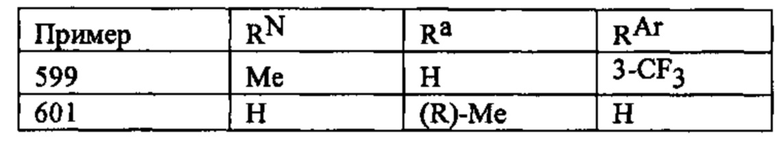
Следующие соединения описаны
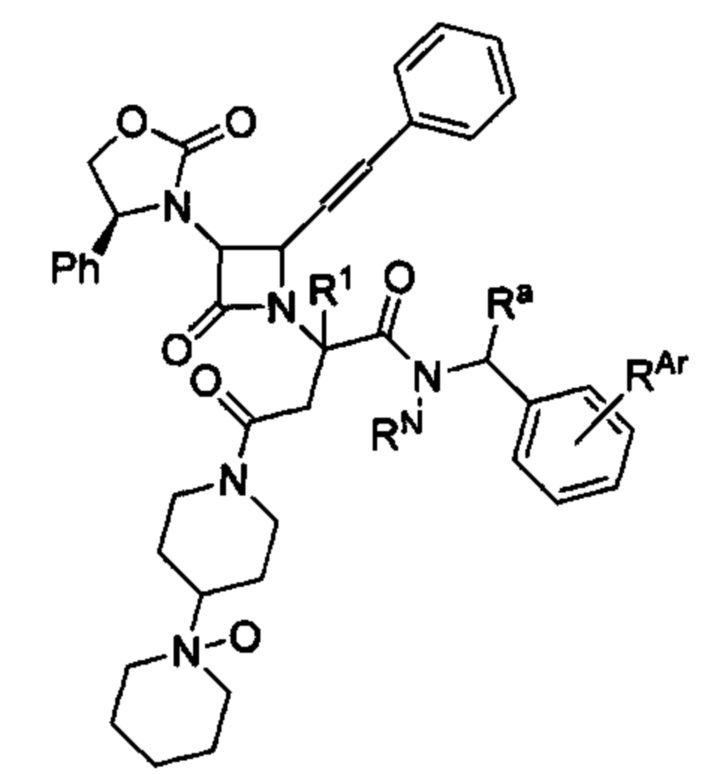
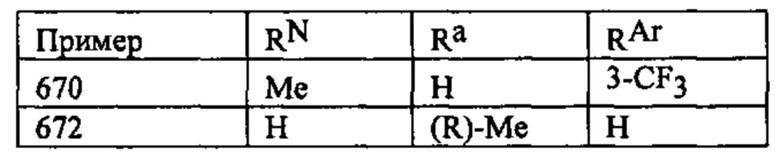
В таблице ниже показаны выбранные соединений, дополнительно охарактеризованные с помощью масс-спектрального анализа с использованием FAB+ с наблюдением соответствующего (М+Н)+ исходного иона.
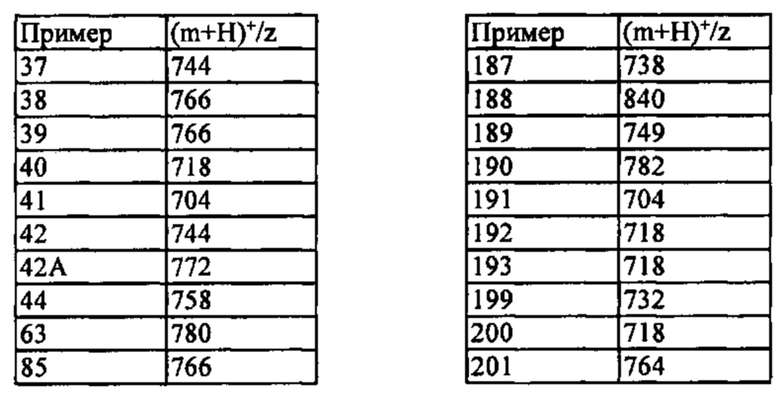

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ЛЕЧЕНИЯ ПОСТТРАВМАТИЧЕСКОГО СТРЕССОВОГО РАССТРОЙСТВА | 2011 |
|
RU2775783C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ПОСТТРАВМАТИЧЕСКОГО СТРЕССОВОГО РАССТРОЙСТВА | 2011 |
|
RU2623209C9 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ ПОВРЕЖДЕНИЯ ГОЛОВНОГО МОЗГА | 2018 |
|
RU2797548C2 |
| ПИРРОЛОПИРАЗИНОВЫЕ ИНГИБИТОРЫ КИНАЗЫ | 2012 |
|
RU2673064C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИЛИРОВАННЫХ ЦИКЛОПЕНТИЛПИРИМИДИНОВЫХ СОЕДИНЕНИЙ | 2013 |
|
RU2643811C2 |
| СОЕДИНЕНИЯ ТИЕНОПИРИМИДИНА | 2013 |
|
RU2637925C2 |
| СОЕДИНЕНИЯ ПИРИДАЗИНАМИДА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ТИРОЗИНКИНАЗЫ СЕЛЕЗЕНКИ (SYK) | 2013 |
|
RU2627661C2 |
| ПРОИЗВОДНЫЕ 5-АМИНОЦИКЛИЛМЕТИЛОКСАЗОЛИДИН-2-ОНА | 2008 |
|
RU2492169C2 |
| ЗАМЕЩЕННЫЕ 2,6-ДИОКСОПИПЕРИДИНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБЫ СНИЖЕНИЯ УРОВНЕЙ TNF-α | 1997 |
|
RU2177944C2 |
| ЗАМЕЩЕННЫЕ 2,6-ДИОКСОПИПЕРИДИНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБЫ СНИЖЕНИЯ УРОВНЕЙ TNF-АЛЬФА | 1997 |
|
RU2595250C1 |
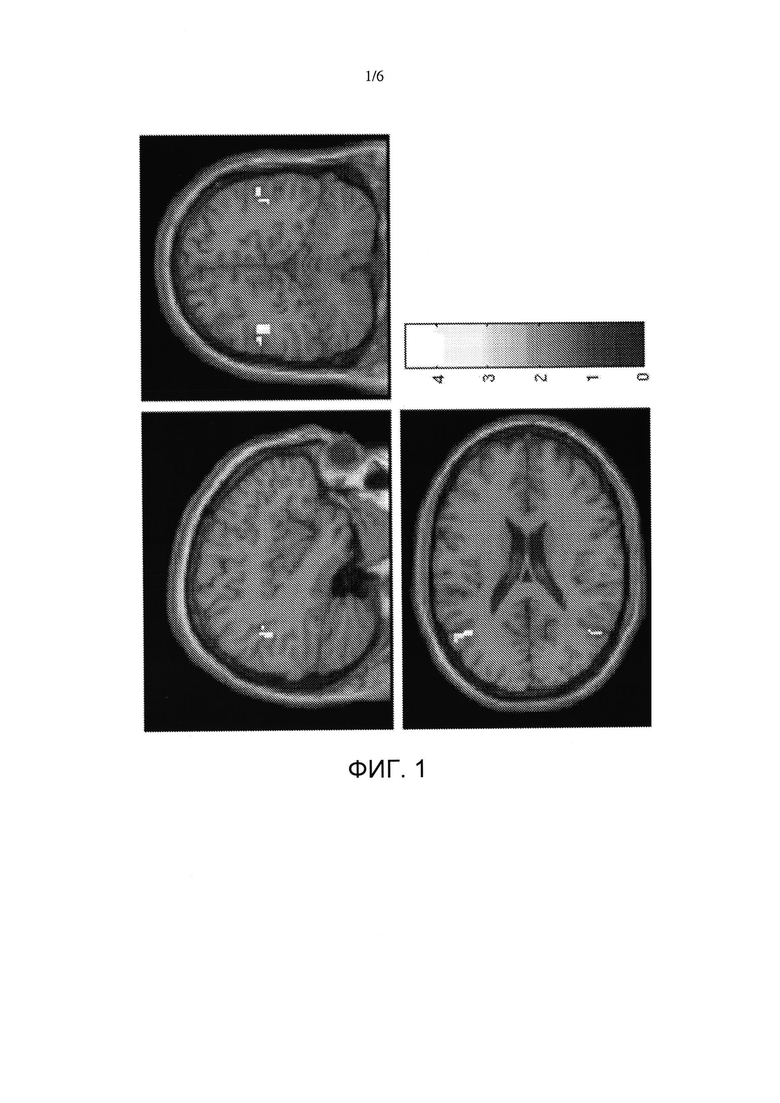
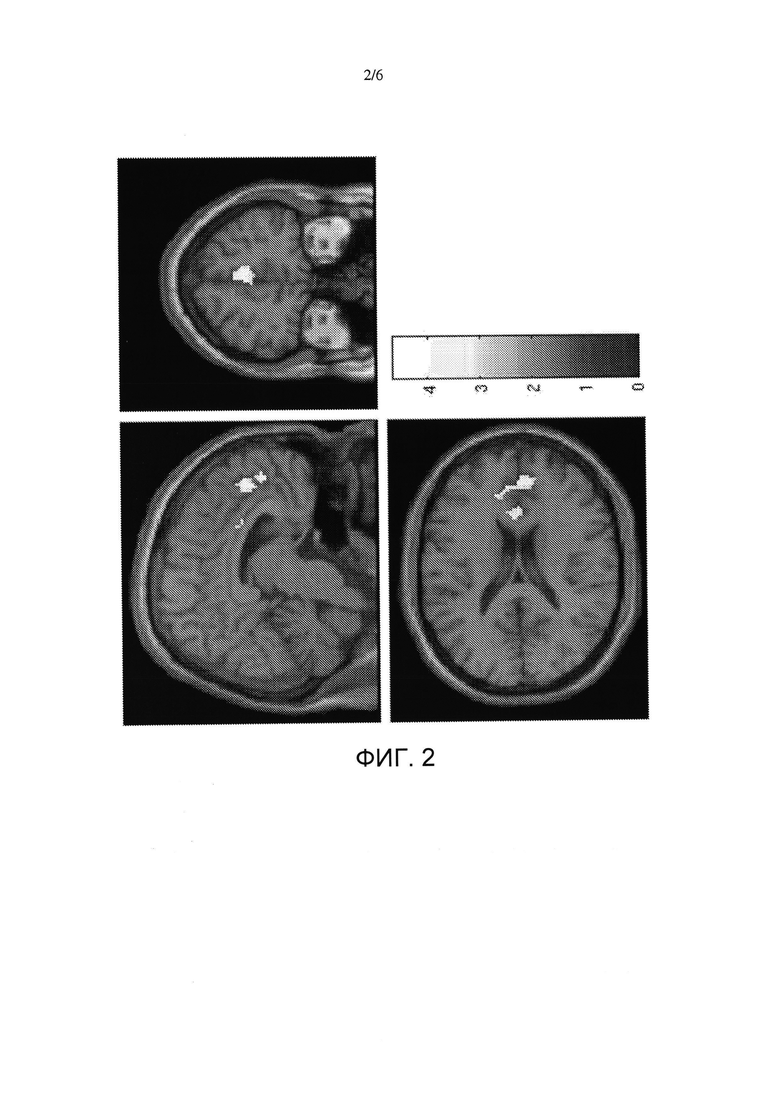
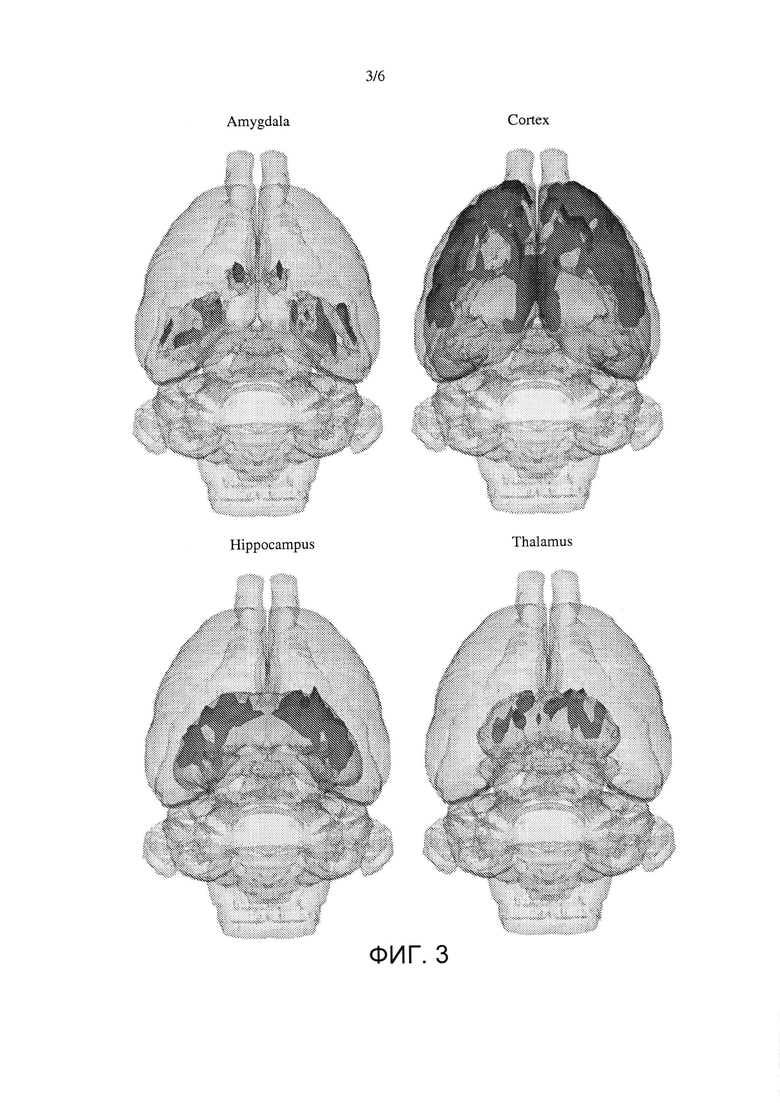
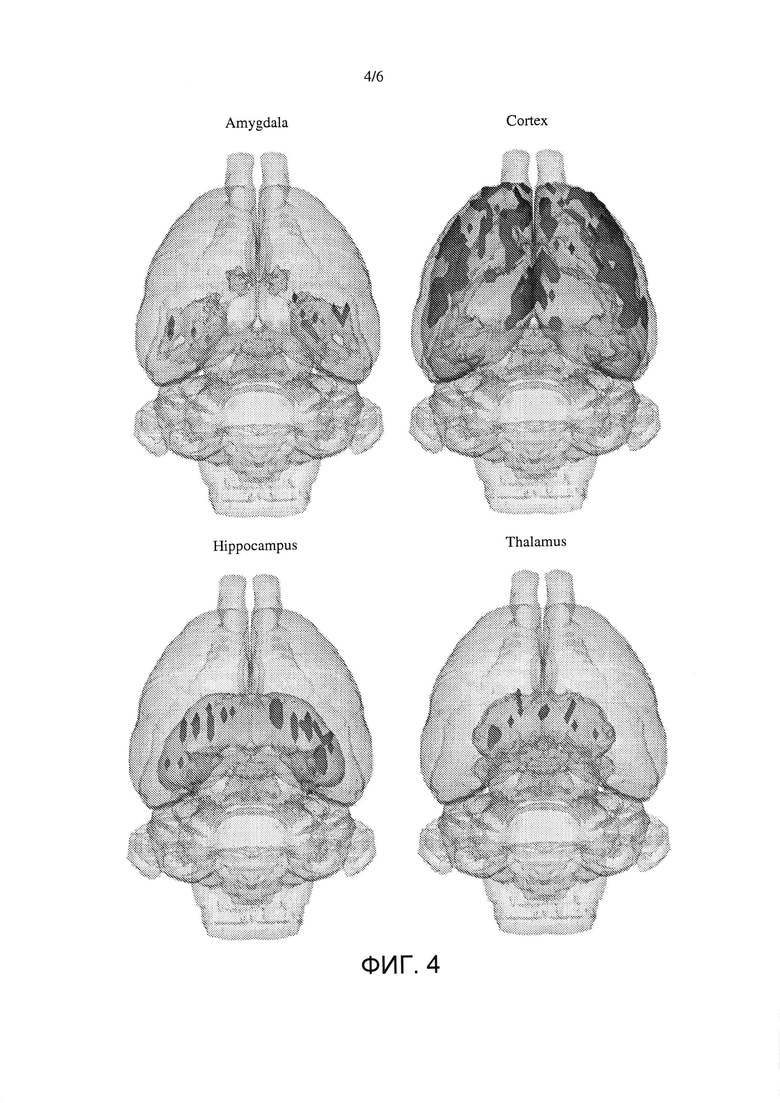
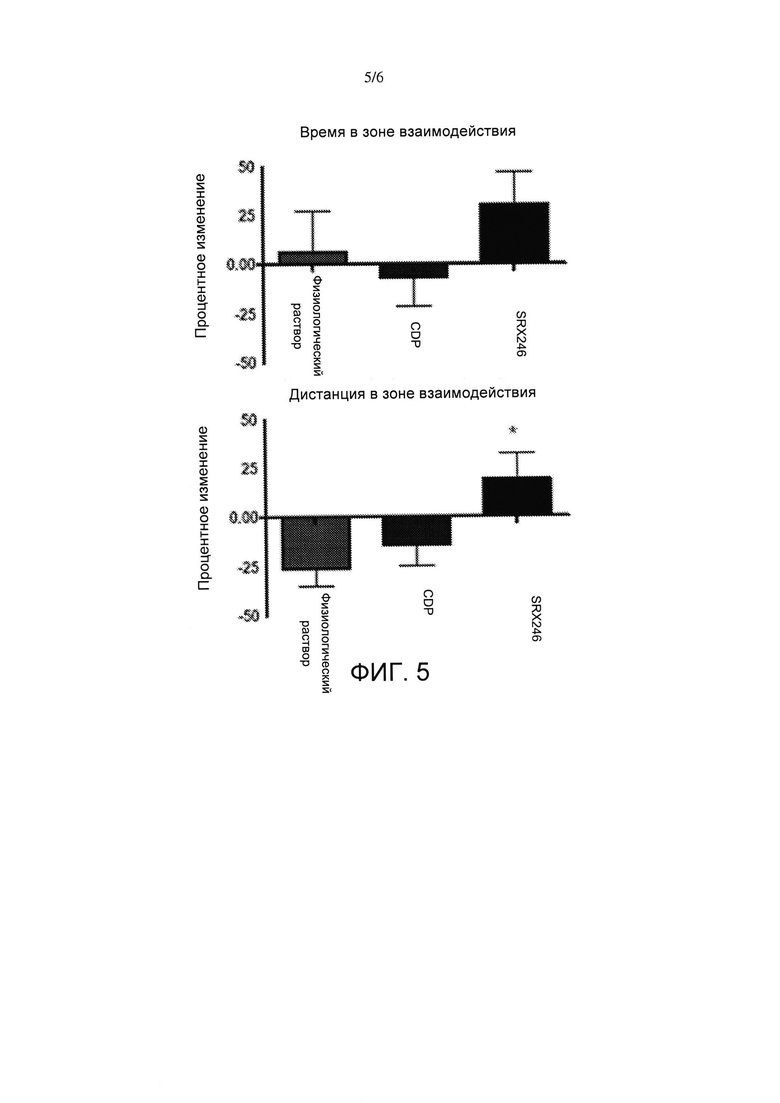
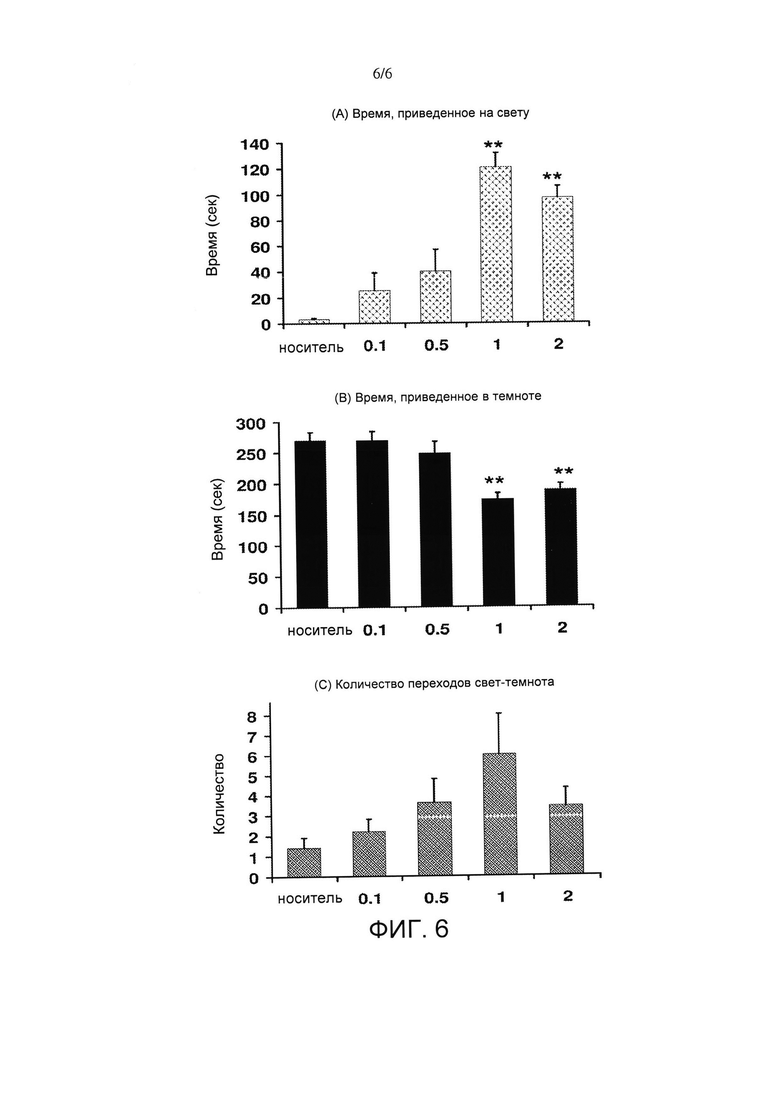
Группа изобретений относится к области медицины, а именно к неврологии, и предназначена для лечения нейродегенеративного заболевания. Способ лечения нейродегенеративного заболевания, выбранного из болезни Хантингтона, болезни Паркинсона или болезни Альцгеймера у животного-хозяина, включает стадию введения композиции, содержащей эффективное количество одного или более селективных антагонистов V1a-рецепторов вазопрессина животному-хозяину. В другом воплощении обеспечивается применение одного или более селективных антагонистов V1a-рецепторов вазопрессина или его фармацевтически приемлемых солей для лечения нейродегенеративного заболевания или расстройства, выбранного из болезни Хантингтона, болезни Паркинсона или болезни Альцгеймера у животного-хозяина. Использование группы изобретений обеспечивает эффективное лечение заболевания, выбранного из болезни Хантингтона, болезни Паркинсона или болезни Альцгеймера. 2 н. и 46 з.п. ф-лы, 18 табл., 672 пр., 6 ил.
1. Способ лечения нейродегенеративного заболевания, выбранного из болезни Хантингтона, болезни Паркинсона или болезни Альцгеймера у животного-хозяина, включающий стадию введения композиции, содержащей эффективное количество одного или более селективных антагонистов V1a-рецепторов вазопрессина животному-хозяину, где один или более селективных антагонистов V1a-рецепторов вазопрессина выбраны из соединений формулы (III):
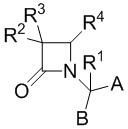 (III)
(III)
и их фармацевтически приемлемых солей, где
A представляет собой остаток карбоновой кислоты, сложного эфира или амида;
B представляет собой остаток карбоновой кислоты, сложного эфира или амида; или B представляет собой остаток спирта или тиола или их производные;
R1 представляет собой водород или C1-C6 алкил;
R2 представляет собой водород, алкил, алкенил, алкинил, алкокси, алкилтио, галоген, галогеналкил, циано, формил, алкилкарбонил или заместитель, выбранный из группы, состоящей из -CO2R8, -CONR8R8′ и -NR8(COR9); где каждый R8 и R8′ независимо выбран из водорода, алкила, циклоалкила, необязательно замещенного арила или необязательно замещенного арилалкила; или R8 и R8′ взяты вместе с присоединенным атомом азота с образованием гетероциклильной группы; и где R9 выбран из водорода, алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила, необязательно замещенного гетероарилалкила и R8R8′N-(C1-C4 алкила);
R3 представляет собой амино, амидо, ациламидо или уреидогруппу, которая необязательно замещена; или R3 представляет собой азотсодержащую гетероциклильную группу, присоединенную по атому азота; и
R4 представляет собой алкил, алкенил, алкинил, циклоалкил, циклоалкенил, алкилкарбонил, необязательно замещенный арил, необязательно замещенный арилалкил, необязательно замещенный арилгалогеналкил, необязательно замещенный арилалкоксиалкил, необязательно замещенный арилалкенил, необязательно замещенный арилгалогеналкенил или необязательно замещенный арилалкинил.
2. Способ по п. 1, отличающийся тем, что заболевание включает нейропсихиатрические симптомы, выбранные из группы, состоящей из агрессивности, раздражительности и гнева, и их комбинации.
3. Способ по п. 1, отличающийся тем, что один или более антагонистов выбраны из соединений формулы:
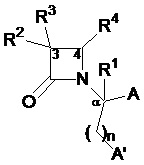 (I)
(I)
и их фармацевтически приемлемых солей, где
каждый A и A' независимо выбран из –CO2H или его сложноэфирного или амидного производного;
n представляет собой целое число, выбранное из от 0 до примерно 3;
R1 представляет собой водород или C1-C6 алкил;
R2 представляет собой водород, алкил, алкенил, алкинил, алкокси, алкилтио, галоген, галогеналкил, циано, формил, алкилкарбонил или заместитель, выбранный из группы, состоящей из -CO2R8, -CONR8R8′ и -NR8(COR9); где каждый R8 и R8′ независимо выбран из водорода, алкила, циклоалкила, необязательно замещенного арила или необязательно замещенного арилалкила; или R8 и R8′ взяты вместе с присоединенным атомом азота с образованием гетероцикла; и где R9 выбран из водорода, алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила, необязательно замещенного гетероарилалкила и R8R8′N-(C1-C4 алкила);
R3 представляет собой амино, амидо, ациламидо или уреидогруппу, которая необязательно замещена; или R3 представляет собой азотсодержащую гетероциклильную группу, присоединенную по атому азота; и
R4 представляет собой алкил, алкенил, алкинил, циклоалкил, циклоалкенил, алкилкарбонил, необязательно замещенный арил, необязательно замещенный арилалкил, необязательно замещенный арилгалогеналкил, необязательно замещенный арилалкоксиалкил, необязательно замещенный арилалкенил, необязательно замещенный арилгалогеналкенил или необязательно замещенный арилалкинил.
4. Способ по п. 1, отличающийся тем, что один или более антагонистов выбраны из соединений формулы:
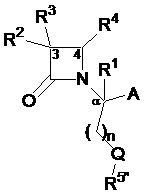 (II)
(II)
и их фармацевтически приемлемых солей, где
A представляет собой –CO2H или его сложноэфирное или амидное производное;
Q представляет собой кислород; или Q представляет собой серу или дисульфид или их окисленные производные;
n представляет собой целое число от 1 до 3;
R1, R2, R3 и R4 являются такими, как определено в формуле I; и
R5'' выбран из водорода, алкила, циклоалкила, алкоксиалкила, необязательно замещенного арилалкила, необязательно замещенного гетероциклила или необязательно замещенного гетероциклилалкила и необязательно замещенного аминоалкила.
5. Способ по п. 3, отличающийся тем, что один или оба A и A′ представляют собой независимо выбранную монозамещенную амидогруппу формулы C(O)NHX-, или дизамещенную амидогруппу формулы C(O)NR14X-, где R14 выбран из гидрокси, алкила, алкоксикарбонила и бензила; и X выбран из алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, гетероциклила, гетероциклил-(C1-C4 алкила), R6R7N- и R6R7N-(C2-C4 алкила), где каждый гетероциклил выбран независимо; и где R6 в каждом случае выбран независимо из водорода или алкила; и R7 в каждом случае выбран независимо из алкила, циклоалкила, необязательно замещенного арила, или необязательно замещенного арилалкила; или R6 и R7 взяты вместе с присоединенным атомом азота с образованием необязательно замещенного гетероцикла.
6. Способ по п. 3, отличающийся тем, что один или оба A и A′ представляют собой амид независимо выбранного необязательно замещенного азотсодержащего гетероцикла, присоединенного по азоту.
7. Способ по п. 3, отличающийся тем, что A имеет формулу
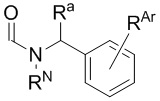
где RN представляет собой водород или необязательно замещенный алкил или группу, образующую пролекарство амида; Ra представляет собой водород или необязательно замещенный алкил; и RAr представляет собой водород или один или более арильных заместителей.
8. Способ по п. 3, отличающийся тем, что один или оба A и A′ представляют собой дизамещенную амидогруппу формулы C(O)NR14X, где R14 выбран из гидрокси, алкила, алкоксикарбонила и бензила; и X выбран из алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, гетероциклила, гетероциклил-(C1-C4 алкила), R6R7N-, и R6R7N-(C2-C4 алкила), где каждый гетероциклил выбран независимо.
9. Способ по п. 3, отличающийся тем, что один или оба A и A′ представляют собой амид необязательно замещенного азотсодержащего гетероцикла, присоединенного по азоту.
10. Способ по п. 3, отличающийся тем, что один или оба A и A′ представляют собой амид замещенного пиперидина или пиперазина.
11. Способ по п. 3, отличающийся тем, что один или оба A и A′ представляют собой амид пиперидина или пиперазина формул:
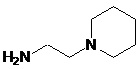
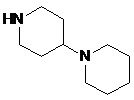
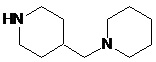
 или
или 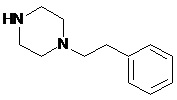 .
.
12. Способ по п. 3, отличающийся тем, что A′ представляет собой амид замещенного пиперидина или пиперазина.
13. Способ по п. 4, отличающийся тем, что Q представляет собой кислород или серу.
14. Способ по п. 13, где R” представляет собой необязательно замещенный арилалкил.
15. Способ по п. 4, где A представляет собой амид замещенного пиперидина или пиперазина.
16. Способ по п. 3 или 4, отличающийся тем, что n представляет собой 1 или 2.
17. Способ по п. 3 или 4, отличающийся тем, что R2 представляет собой водород или алкил.
18. Способ по п. 3 или 4, отличающийся тем, что R1 представляет собой водород.
19. Способ по п. 3 или 4, отличающийся тем, что R3 имеет формулу:
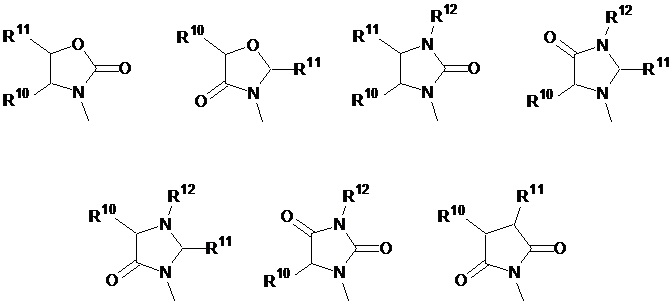
где каждый из R10 и R11 независимо выбран из водорода, необязательно замещенного алкила, необязательно замещенного циклоалкила, алкоксикарбонила, алкилкарбонилокси, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного арилалкилокси, необязательно замещенного арилалкилкарбонилокси, дифенилметокси и трифенилметокси; и R12 выбран из водорода, алкила, циклоалкила, алкоксикарбонила, необязательно замещенного арилоксикарбонила, необязательно замещенного арилалкила и необязательно замещенного арилоила.
20. Способ по п. 19, отличающийся тем, что R3 имеет формулу:
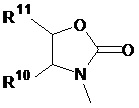 .
.
21. Способ по п. 3 или 4, отличающийся тем, что R4 имеет формулы:
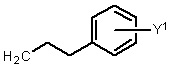
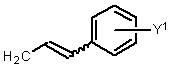
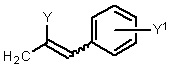
где Y представляет собой электроноакцепторную группу и Y1 представляет собой водород или один или более арильных заместителей, выбранных из группы, состоящей из галогена, гидрокси, амино, нитро, необязательно замещенного алкила и необязательно замещенного алкокси.
22. Способ по п. 4, отличающийся тем, что R5’’ представляет собой необязательно замещенный арил(C1-C4 алкил).
23. Способ по п. 22, отличающийся тем, что R5’’ представляет собой необязательно замещенный бензил.
24. Способ по п. 1, отличающийся тем, что композиция содержит один или более антагонистов, выбранных из группы, включающей
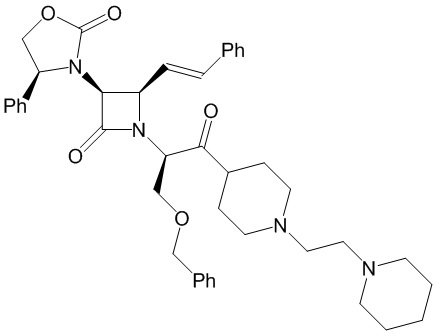 (SRX228)
(SRX228)
или его фармацевтически приемлемую соль,
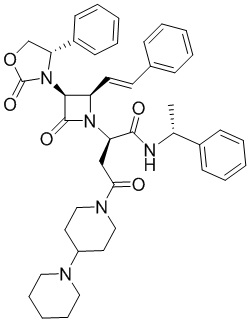 (SRX246)
(SRX246)
или его фармацевтически приемлемую соль,
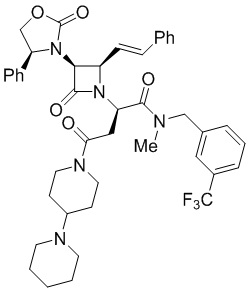 (SRX251)
(SRX251)
или его фармацевтически приемлемую соль,
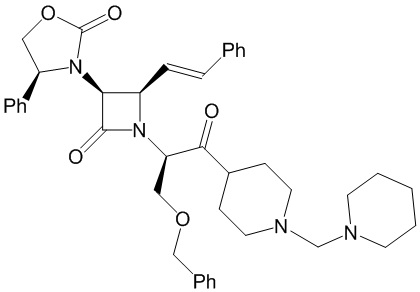 (SRX296)
(SRX296)
или его фармацевтически приемлемую соль,
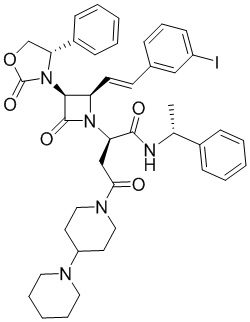 (SRX576)
(SRX576)
или его фармацевтически приемлемую соль, или их комбинации.
25. Применение одного или более селективных антагонистов V1a-рецепторов вазопрессина формулы (III) или его фармацевтически приемлемых солей для лечения нейродегенеративного заболевания или расстройства, выбранного из болезни Хантингтона, болезни Паркинсона или болезни Альцгеймера у животного-хозяина
 (III),
(III),
где
A представляет собой остаток карбоновой кислоты, сложного эфира или амида;
B представляет собой остаток карбоновой кислоты, сложного эфира или амида; или B представляет собой остаток спирта или тиола или их производные;
R1 представляет собой водород или C1-C6 алкил;
R2 представляет собой водород, алкил, алкенил, алкинил, алкокси, алкилтио, галоген, галогеналкил, циано, формил, алкилкарбонил или заместитель, выбранный из группы, состоящей из -CO2R8, -CONR8R8′ и -NR8(COR9); где каждый R8 и R8′ независимо выбран из водорода, алкила, циклоалкила, необязательно замещенного арила или необязательно замещенного арилалкила; или R8 и R8′ взяты вместе с присоединенным атомом азота с образованием гетероциклильной группы; и где R9 выбран из водорода, алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила, необязательно замещенного гетероарилалкила и R8R8′N-(C1-C4 алкила);
R3 представляет собой амино, амидо, ациламидо или уреидогруппу, которая необязательно замещена; или R3 представляет собой азотсодержащую гетероциклильную группу, присоединенную по атому азота; и
R4 представляет собой алкил, алкенил, алкинил, циклоалкил, циклоалкенил, алкилкарбонил, необязательно замещенный арил, необязательно замещенный арилалкил, необязательно замещенный арилгалогеналкил, необязательно замещенный арилалкоксиалкил, необязательно замещенный арилалкенил, необязательно замещенный арилгалогеналкенил или необязательно замещенный арилалкинил.
26. Применение по п. 25, отличающееся тем, что заболевание включает нейропсихиатрические симптомы, выбранные из группы, состоящей из агрессивности, раздражительности и гнева, и их комбинации.
27. Применение по п. 25, отличающееся тем, что один или более антагонистов выбраны из соединений формулы:
 (I)
(I)
и их фармацевтически приемлемых солей, где
каждый A и A' независимо выбран из –CO2H или его сложноэфирного или амидного производного;
n представляет собой целое число, выбранное из от 0 до примерно 3;
R1 представляет собой водород или C1-C6 алкил;
R2 представляет собой водород, алкил, алкенил, алкинил, алкокси, алкилтио, галоген, галогеналкил, циано, формил, алкилкарбонил или заместитель, выбранный из группы, состоящей из -CO2R8, -CONR8R8′ и -NR8(COR9); где каждый R8 и R8′ независимо выбран из водорода, алкила, циклоалкила, необязательно замещенного арила или необязательно замещенного арилалкила; или R8 и R8′ взяты вместе с присоединенным атомом азота с образованием гетероцикла; и где R9 выбран из водорода, алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила, необязательно замещенного гетероарилалкила и R8R8′N-(C1-C4 алкила);
R3 представляет собой амино, амидо, ациламидо или уреидогруппу, которая необязательно замещена; или R3 представляет собой азотсодержащую гетероциклильную группу, присоединенную по атому азота; и
R4 представляет собой алкил, алкенил, алкинил, циклоалкил, циклоалкенил, алкилкарбонил, необязательно замещенный арил, необязательно замещенный арилалкил, необязательно замещенный арилгалогеналкил, необязательно замещенный арилалкоксиалкил, необязательно замещенный арилалкенил, необязательно замещенный арилгалогеналкенил или необязательно замещенный арилалкинил.
28. Применение по п. 25, отличающееся тем, что один или более антагонистов выбраны из соединений формулы:
 (II)
(II)
и их фармацевтически приемлемых солей, где
A представляет собой –CO2H или его сложноэфирное или амидное производное;
Q представляет собой кислород; или Q представляет собой серу или дисульфид или его окисленное производное;
n представляет собой целое число от 1 до 3;
R1, R2, R3 и R4 являются такими, как определено в формуле I; и
R5'' выбран из водорода, алкила, циклоалкила, алкоксиалкила, необязательно замещенного арилалкила, необязательно замещенного гетероциклила или необязательно замещенного гетероциклилалкила и необязательно замещенного аминоалкила.
29. Применение по п. 27, отличающееся тем, что один или оба A и A′ представляют собой независимо выбранную монозамещенную амидогруппу формулы C(O)NHX-, или дизамещенную амидогруппу формулы C(O)NR14X-, где R14 выбран из гидрокси, алкила, алкоксикарбонила и бензила; и X выбран из алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, гетероциклила, гетероциклил-(C1-C4 алкила), R6R7N- и R6R7N-(C2-C4 алкила), где каждый гетероциклил выбран независимо; и где R6 в каждом случае выбран независимо из водорода или алкила; и R7 в каждом случае выбран независимо из алкила, циклоалкила, необязательно замещенного арила, или необязательно замещенного арилалкила; или R6 и R7 взяты вместе с присоединенным атомом азота с образованием необязательно замещенного гетероцикла.
30. Применение по п. 27, отличающееся тем, что один или оба A и A′ представляют собой амид независимо выбранного необязательно замещенного азотсодержащего гетероцикла, присоединенного по азоту.
31. Применение по п. 27, отличающееся тем, что один или оба A и A′ представляют собой дизамещенную амидогруппу формулы C(O)NR14X, где R14 выбран из гидрокси, алкила, алкоксикарбонила и бензила; и X выбран из алкила, циклоалкила, алкоксиалкила, необязательно замещенного арила, необязательно замещенного арилалкила, гетероциклила, гетероциклил-(C1-C4 алкила), R6R7N-, и R6R7N-(C2-C4 алкила), где каждый гетероциклил выбран независимо.
32. Применение по п. 27, отличающееся тем, что один или оба A и A′ представляют собой амид необязательно замещенного азотсодержащего гетероцикла, присоединенного по азоту.
33. Применение по п. 27, отличающееся тем, что один или оба A и A′ представляют собой амид замещенного пиперидина или пиперазина.
34. Применение по п. 27, отличающееся тем, что один или оба A и A′ представляют собой амид пиперидина или пиперазина формул:






 или
или  .
.
35. Применение по п. 27, отличающееся тем, что A имеет формулу

где RN представляет собой водород или необязательно замещенный алкил или группу, образующую пролекарство амида; Ra представляет собой водород или необязательно замещенный алкил; и RAr представляет собой водород или один или более арильных заместителей.
36. Применение по п. 27, отличающееся тем, что A′ представляет собой амид замещенного пиперидина или пиперазина.
37. Применение по п. 28, отличающееся тем, что Q представляет собой кислород или серу.
38. Применение по п. 37, где R” представляет собой необязательно замещенный арилалкил.
39. Применение по п. 28, где A представляет собой амид замещенного пиперидина или пиперазина.
40. Применение по п. 27 или 28, отличающееся тем, что n представляет собой 1 или 2.
41. Применение по п. 27 или 28, отличающееся тем, что R2 представляет собой водород или алкил.
42. Применение по п. 27 или 28, отличающееся тем, что R1 представляет собой водород.
43. Применение по п. 27 или 28, отличающееся тем, что R3 имеет формулу:

где каждый из R10и R11 независимо выбран из водорода, необязательно замещенного алкила, необязательно замещенного циклоалкила, алкоксикарбонила, алкилкарбонилокси, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного арилалкилокси, необязательно замещенного арилалкилкарбонилокси, дифенилметокси и трифенилметокси; и R12 выбран из водорода, алкила, циклоалкила, алкоксикарбонила, необязательно замещенного арилоксикарбонила, необязательно замещенного арилалкила и необязательно замещенного арилоила.
44. Применение по п. 43, отличающееся тем, что R3 имеет формулу:
 .
.
45. Применение по п. 27 или 28, отличающееся тем, что R4 имеет формулы:



где Y представляет собой электроноакцепторную группу и Y1 представляет собой водород или один или более арильных заместителей, выбранных из группы, состоящей из галогена, гидрокси, амино, нитро, необязательно замещенного алкила и необязательно замещенного алкокси.
46. Применение по п. 28, отличающееся тем, что R5’’ представляет собой необязательно замещенный арил(C1-C4 алкил).
47. Применение по п. 46, отличающееся тем, что R5’’ представляет собой необязательно замещенный бензил.
48. Применение по п. 25, отличающееся тем, что один или более антагонистов выбраны из группы, включающей:
 (SRX228)
(SRX228)
или его фармацевтически приемлемую соль,
 (SRX246)
(SRX246)
или его фармацевтически приемлемую соль,
 (SRX251)
(SRX251)
или его фармацевтически приемлемую соль,
 (SRX296)
(SRX296)
или его фармацевтически приемлемую соль,
 (SRX576)
(SRX576)
или его фармацевтически приемлемую соль, или их комбинации.
| US 2011059935 A1, 10.03.2011 | |||
| US 2011071160 A1, 24.03.2011 | |||
| US 2009170825 A1, 02.07.2009 | |||
| WO 2007109615 A2, 27.09.2007 | |||
| US 2008280870 A1, 13.11.2008. |
Авторы
Даты
2021-02-10—Публикация
2015-03-27—Подача