Предлагаемое изобретение относится к области создания искусственной мышцы (ИМ) медицинского назначения и может быть применено как в биомиметических, так и в биомеханических протезах, а также в робототехнике и актюаторах (приводах).
Одним из методов лечения поздней стадии сердечной недостаточности является трансплантация сердца. Однако, даже при доступности трансплантата (сердце донора, механическое сердце), операция трансплантации сердца очень сложная, инвазивная, рискованная и дорогая процедура. Она продлевает жизнь в среднем меньше чем на 10 лет.
Пересадка скелетной мышцы в область вокруг сердца, т.е. кардиомиопластика, лишь симптоматически улучшает состояние пациента. Однако процедура пересадки очень сложная и дорогая, подобно трансплантации сердца. Другие методы лечения сердца также не дают существенных улучшений состояния пациента.
В связи с этим актуальна задача создания искусственной мышцы, выполняющей механическую функцию поврежденной сердечной ткани. Подобные функции выполняют различные приводы, актюаторы и ИМ в технических системах, однако их применения в инвазивных медицинских системах очень осложнены или пока невозможны.
Действительно, известны многочисленные пневматические и гидравлические приводы и актюаторы - прототипы искусственных мышц [1-5], а также приводы на эффекте памяти формы [6, 7]. Они имеют высокие механические и мощностные показатели, например, их мощность, приведенная на единицу массы, составляет: Pm~1,0 кВт/кг. Это выше, чем у сердечной мышцы человека - Pm~0,33 кВт/кг. Во многих случаях они используются в робототехнике, а в некоторых случаях для создания протезов наружного применения, в частности, для восстановления движения коленного сустава или для усиления работы человеческих конечностей. Эти ИМ имеют большие массо-габариты и не пригодны в качестве инвазивных имплантируемых медицинских изделий.
Известна ИМ мышца из композиционного материала в составе различных полимеров (нейлон, полиэтилен, полиорганосилоксан и др.) и нитей интерметаллида (Ni-Ti - нитинол) [8]. Такая ИМ работает при нагреве и охлаждении полимера и имеет замедленное действие и гистерезисы. Возможно, такие материалы перспективны к применению в робототехнике и в неинвазивном протезировании, но в инвазивной имплантации неприемлемы, ввиду опасности перегрева окружающих тканей.
Существуют широкий класс электроактивных полимеров (ЭАП), которые активно исследуются с целью создания на их основе ИМ. Некоторые ЭАП чувствительны к сильному электрическому полю, имеют высокие коэффициенты полезного действия, но питаются высоковольтным напряжением (≥1 кВ), и их инвазивное использование в человеческом теле в качестве ИМ не является безопасным и удобным [9].
Так называемые ионные ЭАП активизируются переносом ионов. В них реализуется высокое значение нагрузочной силы при небольшом значении электрического напряжения 1-3 В [10]. ИМ на основе ионного ЭАП содержит: полимер, электролит, электроды и другие элементы. Из них основным является активный элемент (АЭ), состоящий из слоя различных материалов, чередующихся в виде «сэндвича»: металл, полимер, электролит, полимер, металл. Все составные части (материалы, конструкции) требуют оптимального подбора, чтобы данный тип ИМ на базе ионного ЭАП имел удовлетворяющие степени безопасности и биосовместимости для ее инвазивного применения.
Наиболее близким к предлагаемому изобретению относится патент «Искусственные сфинкторы и искусственные мышцы на основе электроактивных полимеров», содержащий ионные электроактивные полимеры, на поверхностях которых нанесены металлические электроды, заплату для сердечней ткани в виде многочисленных активных элементов [11]. Для повышения степени биосовместимости в предложенной ИМ в качестве электродов на поверхностях АЭ используются слои из благородных металлов (Au, Pt, Pd, Ag и т.д.). Недостатками являются сложность нанесения слоев, труднодоступность и дороговизна благородных металлов.
Задача предлагаемого изобретения состоит в улучшение биосовместимости материалов и удешевления процесса нанесения электропроводящего биосовместимого композиционного наноматериала.
Поставленная задача решается тем, что в искусственной мышце в качестве заплаты для сердечной ткани на основе электроактивных полимеров (ЭАП), в заплату толщиной ≤200 мкм капсулируются активные элементы, содержащих электропроводящие слои из композиционного наноматериала толщиной 20-30 мкм, ЭАП и - электролит, причем композиционный наноматериал состоит из 85 мас. % бычьего сывороточного альбумина, 10 мас. % углеродных нанотрубок и воды.
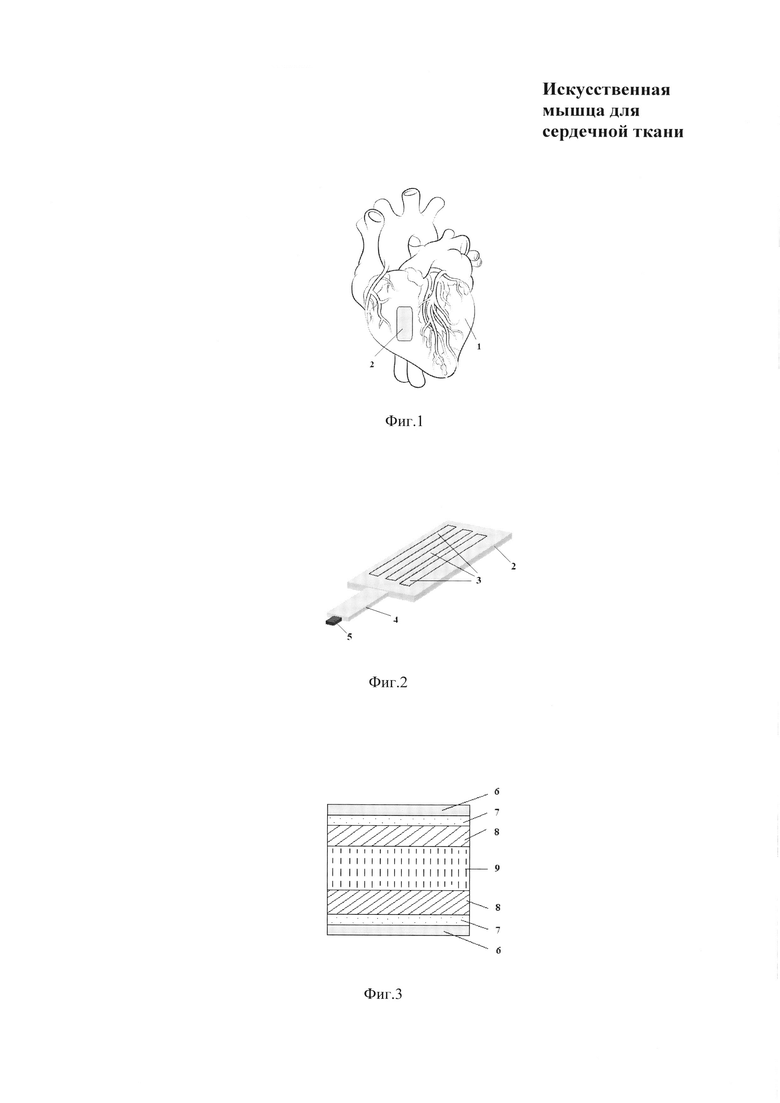
Предложенная ИМ для сердечной ткани представляет собой заплату, накладываемую на место, где повреждена сердечная ткань. На фиг. 1 показан эскиз сердца 1 и ИМ виде заплаты 2 на сердечной ткани. ИМ может деформироваться вместе с сердечной тканью и тем самым будет заменять (восстанавливать) механическое движение поврежденной сердечной ткани. На фиг. 2 приведен ориентировочный внешний вид заплаты, во внутрь которой капсулированы АЭ и другие элементы. Заплата состоит: 3 - многочисленные АЭ, 4 - шина для питания и управления АЭ, 5 - разъем для соединения источника питания и система управления. Толщина заплаты находится в области ≤200 мкм. Другие размеры и форму заплаты подбирают соответственно размерам и формы поврежденной поверхности сердечной ткани, на которой заплата накладывается. На фиг. 3 изображен разрез одного АЭ, где 6 - изолирующий слой, 7 - электропроводящие слои из композиционного наноматериала БСА/УНТ, 8 - ЭАП, 9 - электролит.
Принцип работы АЭ заключается в следующем. После подачи электрического питания на электродах 7 через 8 и 9 проходит ионный ток. Ионы на одном из электродов 7 собираются одной полярности, т.е. происходит окисление, а на другом собираются ионы другой полярности и происходит восстановление. Следовательно, производится изгиб полоски АЭ в сторону катода, т.е. деформируется АЭ и то место сердечной ткани, на котором он расположен.
Важной частью АЭ являются электроды, через которые подаются электрические сигналы на ЭАП. В прототипе используются электроды из слоев благородных металлов, которые позволяют получить высокие значения удельной проводимости. Необходимое условие - низкое поверхностное сопротивление электрода RSe=R⋅S (R - сопротивление, S - площадь поверхности) - позволяет не препятствовать прохождению высокого значения импульса тока через АЭ и получению высокой мощности деформации. Действительно, максимальная удельная проводимость большинства ионных полимеров находится на уровне σр≤10 См/м и, с учетом приблизительной толщины полимера dp~50 мкм, его поверхностное сопротивление приблизительно будет равно RSp~0,5 μОм⋅м2. С учетом тех фактов, что АЭ состоит из двух ЭАП и электролита, а также может присутствовать контактное сопротивление между различными поверхностями (металл/полимер; электролит/полимер), реальное значение поверхностного сопротивления АЭ может быть в несколько раз выше, чем оценочное RSp. Однако возможное поверхностное сопротивление электрода на уровне RSe≤0,05 μОм⋅м2 практически не ограничит импульс тока и соответственно мощность деформации АЭ, поскольку RSe<<RSp.
Приготовление дисперсии композиционного наноматериала БСА/УНТ и нанесение из него электропроводящих слоев на АЭП рассмотрен в примере 1.
Пример 1. Композиционный наноматериал БСА/УНТ имел в составе: БСА - фирма-производитель "AMFESCO" (USA) [12]; УНТ - одностенные углеродные нанотрубки (ОУНТ), фирма производитель "UglerodChg" [13], или многостенные углеродные нанотрубки (МУНТ) типа «Таунит-МД», фирма производитель «ООО НаноТехцентр», г. Тамбов [14].
В дистиллированной воде добавляется УНТ и дисперсия, тщательно перемешивается в магнитной мешалке в течение 4 ч. Водная дисперсия с УНТ диспергируется в ультразвуковом (УЗ) диспергаторе (Qsonica модель Q700) в течение 30 мин. В дальнейшем к дисперсии добавляется БСА и перемешивается в магнитной мешалке в течение 4 ч. Полученная водная дисперсия БСА/УНТ декантируется в течение 24 часов и перед нанесением на поверхность полимера она снова перемешивается в магнитной мешалке в течение 30 мин, и диспергируется в УЗ бане в течение 30 мин. Водная дисперсия содержит 15 мас. % БСА, 1,5 мас. % УНТ и остальная - вода, однако в слоях после сушки соотношение составных частей существенно меняется.
Дисперсия БСА/УНТ наносится на поверхности полимера методом шелкографии. Также дисперсии БСА/УНТ и УНТ наносятся на стеклянные пластинки, которые считаются контрольными. Образовавшиеся слои на полимерах и стеклянных пластинках сушатся при комнатной температуре. Сопротивление слоев определяется четырехзондовым методом. Из данных сопротивления и геометрических размеров слоев определяется их удельная объемная проводимость σ. Толщина слоев находится в области d ~ 5-30 мкм.
После сушения слои теряют влагу и приобретают состав: 85 мас. % БСА/10 мас. % ОУНТ или 85 мас. % БСА/10 мас. % МУНТ, остальная - вода (влага).
Пример 2. Основным АЭ использовался сухой ЭАП виде полиэтиленоксид (ПЭО). На поверхностях слоя ПЭО методом шелкографии или пульверизатором наносился дисперсия БСА/УНТ. Масса слоев контролировался методом взвешивания, что позволяло контролировать их толщину с точностью ±15%. В дальнейшем слои сушились в нормальных условиях в течение 100-120 мин. Полученные слои на поверхностях ПЭО служили проводящими электродами, и в целом такие образцы ЭАП представляли собой прототипами ИМ.
Отметить, что в композиционном наноматериале БСА/УНТ следует прилагать нанотрубки в области 2-10 мас. % УНТ. Действительно, при росте концентрации УНТ наноматериал постепенно теряет эластичность, т.е. увеличивается его модуль упругости Е и при >> 10 мас. % УНТ она может превосходить значение EH~200 кПа для человеческой кожной и мышечной тканей [15]. Следовательно, ИМ на основе такого композитного наноматериала не приемлемо так, как для его эффективной работы требуется выполнения условие Е≤EH. При концентрациях ≤2 мас. % УНТ значительно уменьшается удельная электропроводность наноматериала, поэтому эффективность ИМ на его основе резко подает.
Максимальное значение σ≈500 См/м получены для слоев d~20 мкм в составе 85 мас. % БСА/10 мас. % ОУНТ. С учетом данных σ и d для слоя БСА/УНТ следует поверхностное сопротивление RS~0,04 μОм⋅м2. Это имеет такой же порядок, как RSe≈0,05 μОм⋅м2, необходимый для электрода находящегося на поверхности полимера. Для слоев d~30 мкм составом 85 мас. % БСА/10 мас. % МУНТ получены σ≈400 См/м, что дает значение RS~0,075 μОм⋅м2.
Несколько более высокое значение RS~0,075 μОм⋅м2 в слоях содержащих МУНТ относительно RSe≈0,05 μОм⋅м2 для слоев с ОУНТ вызвано тем обстоятельством, что одностенные нанотрубки обладают более высокой удельной проводимостью, чем многостенные нанотрубки. Индивидуальные УНТ имеют σ≥107 См/м, а контрольные слои из УНТ - σ≥105 См/м. В самом деле, матрица БСА в отсутствии нанотрубок практически не проводит электричество - ее объемная удельная проводимость σ≤10-6 См/м. После добавления наполнителя виде УНТ матрица БСА приобретает высокое значение σ, и поэтому слои композитного наноматериала БСА/УНТ становятся электропроводящими.
Таким образом, предложенные слои толщинами 20-30 мкм на основе биосовместимого композиционного наноматериала БСА/УНТ имеют высокую проводимость (низкое поверхностное сопротивление) и могут выполнять функцию электродов в искусственной мышце на основе ионного ЭАП.
Предложенная ИМ с электродами из основы биосовместимого композиционного наноматериала БСА/УНТ имеет существенные преимущества относительно ИМ с электродами из благородных металлов.
В предложенной заявке для образования электропроводящих слоев водная дисперсии БСА/УНТ наносится на ЭАП практически любыми способами, которые применяются для нанесения лакокрасочных материалов. Самым простым и доступным является шелкография, что подобно нанесению дисперсии с помощью кисти. В прототипе наиболее простым способом получения металлических слоев на АЭП считается процедура «Внедрение частиц металла в полимер». Она состоит из следующих шагов:
- полимер вымачивается в растворе соли Pt(NH3)4Cl2;
- потом наносится восстановительный раствор борогидрид натрия NaBH4;
- для ускорения восстановления также добавляют гидразин H2N-NH2 и гидроксиламин NH2OH.
Несмотря на то, что в прототипе рассмотренная процедура нанесения металлических электродов является самой простой, все-таки она гораздо сложнее, дороже и медлительнее, чем способ нанесения электродов в предложенной заявке.
К важным преимуществам относится: дешевизна материалов БСА и УНТ. В частности, Цена композита БСА/УНТ в основном определяется ценой УНТ. Например, для МУНТ≤100 руб./г. Поскольку в композит БСА/УНТ входит небольшая часть УНТ, тогда для него возможная цена может быть ≤10 руб./г. Используемые в прототипе благородные металлы гораздо дороже, например, цена золота ≥1200 руб./г.
В случае разрушения заплаты электроды АЭ могут соприкасаться с тканью и физиологической жидкостью. В этом случае важным становиться степень биосовместимости. В предложенной заявке используемый композитный наноматериал БСА/УНТ имеет высокую степень биосовместимости, так как состоит из биологического материала БСА, используемого в медицине как лекарственный препарат, а также из небольшого количество УНТ, которые в композите под влиянием БСА функционализируются и практически не уходят из матрицы БСА. Применяемые благородные металлы в прототипе могут вызвать аллергические реакции и их степень биосовместимости является невысокой.
Таким образом, поставленная задача выполнена: улучшена биосовместимости материалов и удешевлена процесс нанесения электропроводящего биосовместимого композиционного наноматериала.
ИСТОЧНИКИ ИНФОРМАЦИИ:
1. G. Waycaster, S. Wu, X. Shen, "A pneumatic artificial muscle actuated above-knee prosthesis", Dynamic Systems and Control Conference, vol. 1, pp. 12-15, 2010.
2. Y. Park, B. Chen, D. Young, "Bio-inspired active soft orthotic device for ankle foot pathologies", International Conference on Intelligent Robots and Systems, 2011.
3. D. Ferris, J. Czerniecki, B. Hannaford, "An ankle-foot orthosis powered by artificial pneumatic muscles", Journal of Applied Biomechanics, vol. 21, pp. 189-197, 2005.
4. G. Andrikopoulos, G. Nikolakopoulos, S. Manesis, " A Survey on applications of Pneumatic Artificial Muscles", Mediterranean Conference on Control & Automation, 2011.
5. R. Tiwari, M. Meller, K. Wajcs, C. Moses, I. Reveles, E. Garcia, "Hydraulic artificial muscles", Journal of Intelligent Material Systems and Structures, vol. 23, no. 3, pp. 301-312, 2012.
6. S. Mirvakili, A. Ravandi, I. Hunter, C. Haines; N. Li, J. Foroughi, S. Naficy, G. Spinks; R. Baughman, J. Madden, "Simple and strong: Twisted silver painted nylon artificial muscle actuated by Joule heating", Electroactive Polymer Actuators and Devices, vol. 9056, 2014.
7. S. Mirvakili, I. Hunter, "Multidirectional Artificial Muscles from Nylon", Advanced Materials, vol. 29, no. 4, 2017.
8. Патент РФ 2563815
9. Патент РФ 2577923
10. V. Palmre, D. Pugal, K. Kim, K. Leang, K. Asaka, A. Aabloo, "Nanothorn electrodes for ionic polymer-metal composite artificial muscles ", Scientific Reports, vol. 4, 2014.
11. Патент US 7128707 (прототип)
12. http://www.amresco-inc.com/ALBUMIN-BOVINE-0332.cmsx
13. http://sk.ru/net/1120187/
14. http://www.nanotc.ru/producrions/87-cnm-taunit
15. Liang X., and Boppart S.A. / Biomechanical Properties of In Vivo Human Skin From Dynamic Optical Coherence Elastography // IEEE Transactions on Biomedical Engineering, 2010, 57(4), pp. 953-959. DOI: 10.1109/TBME.2009.2033464.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТКАНЕИНЖЕНЕРНАЯ КОНСТРУКЦИЯ ДЛЯ РЕГЕНЕРАЦИИ СЕРДЕЧНОЙ ТКАНИ | 2019 |
|
RU2725860C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОСТРУКТУРИРОВАННОГО КОМПОЗИЦИОННОГО ЭЛЕКТРОПРОВОДЯЩЕГО ПОКРЫТИЯ | 2015 |
|
RU2606842C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСОВМЕСТИМОГО НАНОСТРУКТУРИРОВАННОГО КОМПОЗИЦИОННОГО ЭЛЕКТРОПРОВОДЯЩЕГО МАТЕРИАЛА | 2011 |
|
RU2473368C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСОВМЕСТИМОГО НАНОМАТЕРИАЛА | 2016 |
|
RU2633088C1 |
| УНИПОЛЯРНЫЙ ДАТЧИК ДЕФОРМАЦИИ | 2018 |
|
RU2685570C1 |
| БИПОЛЯРНЫЙ ДАТЧИК ДЕФОРМАЦИИ НА ОСНОВЕ БИОСОВМЕСТИМОГО НАНОМАТЕРИАЛА | 2017 |
|
RU2662060C1 |
| Способ изготовления нанокомпозитного имплантата связки сустава | 2019 |
|
RU2744710C2 |
| Гибридный материал на основе поли-3-амино-7-метиламино-2-метилфеназина и одностенных углеродных нанотрубок и способ его получения | 2016 |
|
RU2635606C2 |
| ДАТЧИКИ НА ОСНОВЕ ЭЛЕКТРОАКТИВНЫХ ПОЛИМЕРОВ И СПОСОБЫ ВОСПРИЯТИЯ | 2016 |
|
RU2723887C2 |
| БИОСОВМЕСТИМЫЙ НАНОМАТЕРИАЛ ДЛЯ ЛАЗЕРНОГО ВОССТАНОВЛЕНИЯ ЦЕЛОСТНОСТИ РАССЕЧЕННЫХ БИОЛОГИЧЕСКИХ ТКАНЕЙ | 2017 |
|
RU2657611C1 |
Изобретение относится к медицинской технике, натотехнологиям, биомедицинским, биомеханическим протезам, может быть применено в робототехнике и актюаторах (приводах). Для создания искусственной мышцы (ИМ), выполняющей механическую функцию поврежденной сердечной ткани, наиболее подходящими являются ИМ на основе ионных электроактивных полимеров (ЭАП), в которых реализуется высокое значение нагрузочной силы при небольшом значении электрического напряжения (1-3 В). В предлагаемой ИМ в качестве заплаты для сердечной ткани на основе ЭАП в заплату толщиной <200 мкм капсулируют активные элементы, содержащие электропроводящие слои из композиционного наноматериала толщиной 20-30 мкм, ЭАП и электролит. Причем композиционный наноматериал состоит из 85 мас. % бычьего сывороточного альбумина (БСА), 10 мас. % углеродных нанотрубок (УНТ) и воды. Используемый композитный наноматериал позволяет упростить и удешевить процесс его нанесения на заплату, обладает высокой степенью биосовместимости, не вызывает аллергических реакций. 3 ил.
Искусственная мышца в качестве заплаты для сердечной ткани на основе электроактивных полимеров (ЭАП), отличающаяся тем, что в заплату толщиной <200 мкм капсулированы активные элементы, содержащие электропроводящие слои из композиционного наноматериала толщиной 20-30 мкм, ЭАП и электролит, причем композиционный наноматериал состоит из 85 мас. % бычьего сывороточного альбумина, 10 мас. % углеродных нанотрубок и воды.
| Учёные создали гибридную сердечную мышцу из нанотрубок и клеток сердца | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Дата размещения подтверждена на сайте: https://web.archive.org/web/20130212180123/www.vesti.ru/doc.html?id=103080 | |||
| ИСКУССТВЕННАЯ МЫШЦА | 2014 |
|
RU2563815C1 |
| УСТРОЙСТВА, СИСТЕМЫ И СПОСОБЫ ИЗГОТОВЛЕНИЯ ТКАНИ | 2011 |
|
RU2560393C2 |
| US 20090259315 A1, 15.10.2009 | |||
| JP 2010124867 A, 10.06.2010 | |||
| CN 103617761 B, 17.02.2016 | |||
| МЭНЬОН Д | |||
| и др | |||
| Использование скелетных мышц для поддержки инвалидизированного миокарда | |||
| Грудная и сердечно-сосудистая хирургия, 1990, N 8, С | |||
| Коридорная многокамерная вагонеточная углевыжигательная печь | 1921 |
|
SU36A1 |
| PALMRE V et al | |||
| Nanothorn electrodes for ionic polymer-metal composite artificial muscles, Scientific Reports, 2014, vol | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| LI Y et al | |||
| Artificial Cardiac Muscle with or without the Use of Scaffolds | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
Авторы
Даты
2018-12-14—Публикация
2017-12-26—Подача