Область техники, к которой относится изобретение
Настоящее изобретение относится к способу окисления 5-гидроксиметилфурфураля, который можно проводить в растворителе или смеси растворителей, включающей по меньшей мере один высококипящий полярный растворитель (hbS), с получением 2,5-фурандикарбоновой кислоты.
Уровень техники
2,5-Фурандикарбоновая кислота (ниже в настоящем изобретении обозначенная, как FDCA) доступна из многих возобновляемых ресурсов и является привлекательным промежуточным продуктом для получения молекул для различных вариантов применения, таких как сельскохозяйственные химикаты, лекарственные средства, пестициды, фармакологические средства или бактерицидные агенты. Наиболее важной группой превращений FDCA является полимеризация в полиамиды, сложные полиэфиры или полигидразины. (Lewkowski, 2001).
Каталитическое окисление 5-гидроксиметилфурфураля (ниже в настоящем изобретении обозначен, как HMF), полученного дегидратацией гексозы, потенциально является наиболее важным путем синтеза FDCA из возобновляемых ресурсов. В литературе описано много разных методик окисления HMF с получением FDCA в качестве основного продукта. Однако не описан способ, делающий возможным легкое сочетание образования HMF и окисления. Это в основном обусловлено использованием разных типов растворителей на этих стадиях.
Окисление HMF в FDCA на первой стадии проходит через диформилфуран (ниже в настоящем изобретении обозначен, как DFF) или гидроксиметилфуранкарбоновую кислоту (HMFCA) и на следующей стадии через формилфуранкарбоновую кислоту (FFCA). Основная схема приведена ниже:
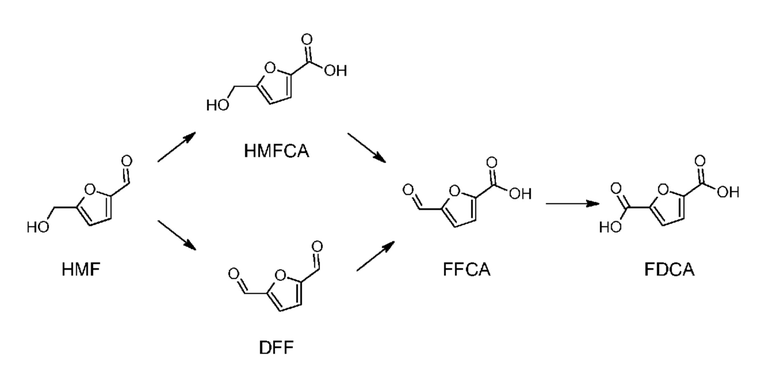
Чаще всего окисление проводят в воде, спиртах или карбоновых кислотах.
В US 3326944 описано окисление HMF в FDCA в воде с использованием гидроксида натрия и катализаторов платинового типа (ниже в настоящем изобретении обозначены, как PTC).
В EP 0356703 описано окисление HMF в водной среде с помощью PTC и при значении pH, равном не более 8. Это значение регулируют при проведении способа путем непрерывного добавления основания.
В US 8193382 описано такое же окисление в воде или уксусной кислоте. В этом случае в качестве основания используют слабые основания, такие как карбонаты или фосфаты. Катализаторами, использующимися в этом способе, также являются PTC.
В US 8865921 описана каталитическая система Co/Mn/Br, которую также используют для синтеза терефталевой кислоты, для окисления HMF, но также эфиров HMF, 5-(хлорметил)фурфураля и других родственных соединений. Эти способы также проводят в уксусной кислоте или смесях уксусной кислоты с водой. Эта же химическая система и растворители с другими методиками описаны в патенте US 8242292, в котором описано улучшение посредством непрерывного удаления воды, и в WO 2013/033058, в котором реакцию проводят в распылительном реакторе. Оба способа проводят в уксусной кислоте или смесях уксусная кислота/вода.
Окисление HMF в апротонных средах описано только для селективного окисления в диформилфуран. В US 7700788 описано окисление HMF в DFF в метиленхлориде.
Исходно вещество для стадии окисления в этом случае является предметом спора, HMF, является важным промежуточным продуктом, получаемых из реакции дегидратации гексозы (глюкоза, фруктоза). Этот синтез, в отличие от окисления, обычно не проводят в воде вследствие низких выходов. Максимальные выходы HMF, достижимые в воде, находятся в диапазоне от 50% до 60%.
Tuercke et al. (2009) описали непрерывный способ в микрореакторе в воде при катализе с помощью HCl с получением 54% HMF.
Высокие селективности для дегидратации фруктозы или глюкозы обеспечиваются только в высококипящих полярных апротонных растворителях, таких как диметилсульфоксид (DMSO), N-метил-2-пирролидон (NMP), N,N-диметилформамид (DMF) или N,N-диметилацетамид (DMA).
В настоящее время в качестве растворителя используют в основном DMSO, как указано в US 4590283 (Roquette Freres). Однако DMF, DMA или NMP характеризуются высокими селективностями и превосходными выходами, как показано в этом же документе или более ранних, таких как EP 2703395 или US 7317116 B2.
Для этих способов для перехода к стадии окисления необходимо удаление высококипящего растворителя или по меньшей мере значительной его части.
В другой методике используют воду в качестве растворителя и двухфазные системы для экстракции HMF в органическую фазу для исключения регидратации. Такие методики приводят к превосходным результатам с выходом HMF до 90%. Все же для получения таких хороших результатов необходимо добавление DMSO или NMP в водную фазу. Затем этот растворитель также экстрагируют в органическую фазу и необходимо отделять его от HMF, что делает способ экономически невыгодным. Улучшение этого подхода возможно только при использовании меньшего количества высококипящего растворителя, которое необходимо удалить. См. (Chheda et al., 2007).
Обзор научной литературы по получению HMF из гексозы с отделением в водные среды и полярные апротонные растворители приведен в публикации (Teong et al., 2014).
В заявке PCT/EP2015/063578 (предварительно не опубликована) раскрыто селективное получение окисленных производных фурана из HMF, где способ окисления проводят непрерывно в потоке, описаны средства изменения параметров реакции, растворителем для способа окисления является вода и диполярный апротонный растворитель. Предпочтительно, если в качестве сорастворителя содержится NMP.
В современном уровне техники стадию окисления HMF следует проводить не в таком растворителе, как использовавшийся при предшествующем образовании HMF, если на обеих стадиях необходимы высокие выходы. Обычно HMF выделяют после дегидратации и затем возвращают на стадию окисления, для чего необходимо трудоемкое отделение высококипящего растворителя и это приводит к снижению выхода HMF.
Удаление растворителя можно провести путем выпаривания. Однако установлено, что для этого необходимо поддерживать температуры ниже 50°C для исключения разложения HMF. Соответственно, необходимы очень низкие давления для удаления высококипящих растворителей. Это почти невозможно и очень дорого осуществить в случае крупномасштабного промышленного способа.
Альтернативной методикой является экстракция высококипящего растворителя. Однако растворимость HMF в органических растворителях, способность экстрагировать полярные высококипящие растворители является хорошей и, таким образом, большие количества HMF теряются в органической фазе.
Для преодоления очевидных затруднений с отделением HMF от высококипящих полярных растворителей использовали несколько разных методик.
Bicker (Bicker et al., 2005) описали дегидратацию в суперкритических жидкостях, таких как разные смеси ацетон/вода, что обеспечивает полное превращение и выход, равный 77%.
В EP 1427715 B2 описан однореакторный синтез DFF из углевода. На первой стадии проводят дегидратацию с получением HMF на второй проводят окисление в DFF с использованием соединений ванадия в качестве катализатора.
Кроме того, окисление HMF в DFF в DMSO описано в литературе, например, в публикации Grasset et al. (2013) с использованием интеркалированных фосфатов-оксидов ванадия в качестве катализатора, или в публикации Amarasekara et al. (2008), с использованием катализаторов Mn(III)-сален. Окисление HMF в FDCA в этих системах не описано.
Для экономичного способа было бы благоприятно перейти от стадии дегидратации к стадии окисления без дополнительной обработки.
Ribeiro et al (2003) предложили однореакторную методику в лабораторном масштабе превращения фруктозы в FDCA с использованием ацетилацетоната кобальта в золь-гелевом диоксиде кремния в качестве катализатора. Они обеспечили превосходный выход, равный 72% за обе стадии. Все же пригодность этой системы реакции для больших масштабов остается сомнительной.
Насколько известно авторам настоящего изобретения, до настоящего времени не описан технически выполнимый способ объединения синтеза HMF с последующим окислением HMF без промежуточной дорогостоящей обработки.
Эта задача решена способом по пункту 1 формулы изобретения. Предпочтительные варианты осуществления настоящего изобретения раскрыты в зависимых пунктах формулы изобретения.
Краткое описание чертежей
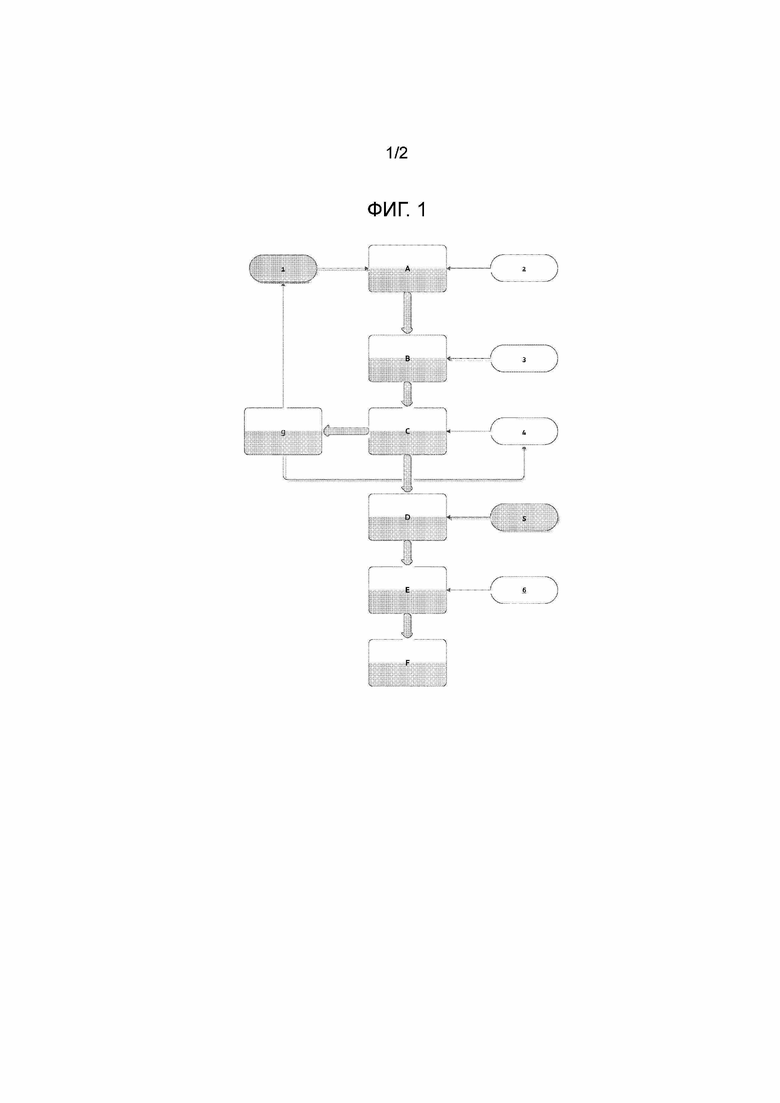
На фиг. 1 приведена схема способа, на которой представлен типичный предпочтительный вариант осуществления настоящего изобретения.
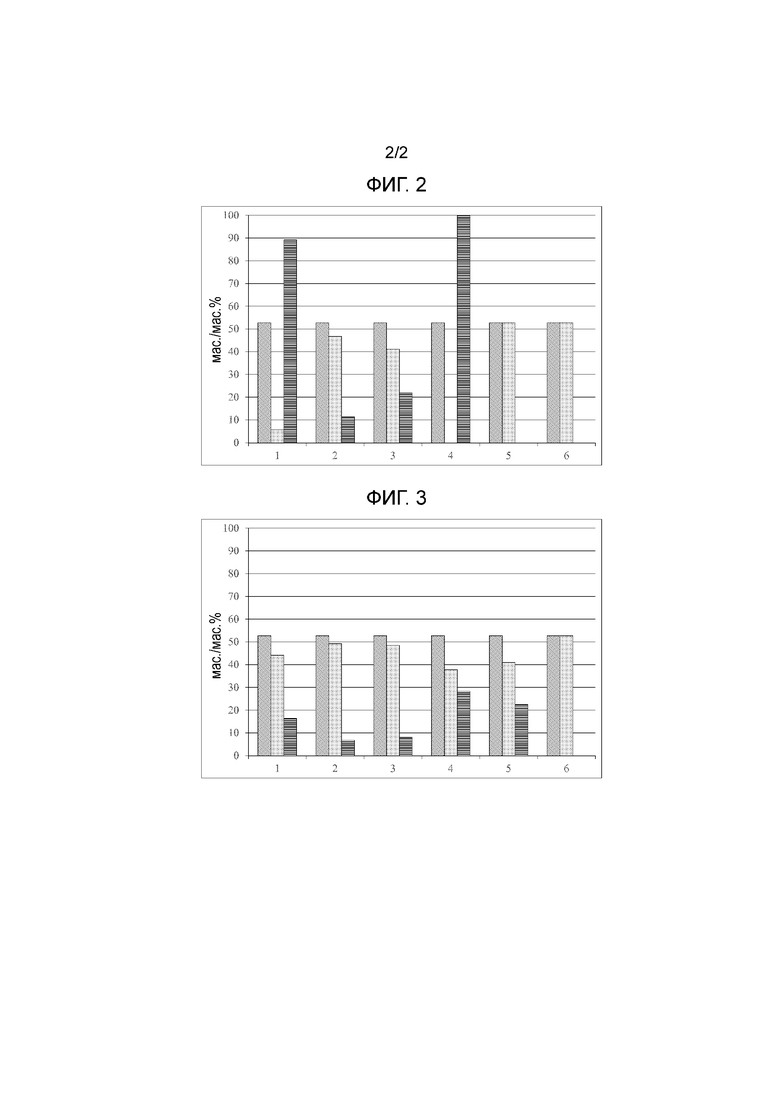
На фиг. 2 приведены результаты исследований по экстракции, относящихся к экстракции NMP.
На фиг. 3 приведены результаты исследований по экстракции, относящихся к экстракции DMSO.
Подробное описание изобретения
Авторы настоящего изобретения неожиданно обнаружили улучшенный экономичный способ, который позволяет окислить HMF в высококипящих полярных растворителях в FDCA без необходимости выделения или концентрирования HMF до стадии окисления.
Соответственно, в одном объекте настоящее изобретение относится к способу получения 2,5-фурандикарбоновой кислоты (FDCA) путем окисления 5-гидроксиметил-2-фурфураля (HMF), указанный HMF находится в растворе в высококипящем полярном растворителе и воде, где указанный способ характеризуется комбинацией
- первой стадии окисления, на которой HMF по меньшей мере частично окисляется в указанном растворе с образованием первой реакционной смеси, включающей по меньшей мере одну одноатомную кислоту, выбранную из группы, включающей 5-гидроксиметилфуран-2-карбоновую кислоту (HMFA) и 5-формилфуран-2-карбоновую кислоту (FFCA) и необязательно FDCA
- стадии экстракции после первой стадии окисления, на которой указанный высококипящий полярный растворитель экстрагируют из указанной первой реакционной смеси растворителем для экстракции, где указанная по меньшей мере одна одноатомная кислота остается в водной фазе,
- второй стадии окисления, на которой указанная по меньшей мере одна одноатомная кислота окисляется в FDCA.
Для задач настоящего изобретения "высококипящий полярный растворитель" (далее также используется аббревиатура "hbs") означает растворитель, температуре кипения которого выше, чем у воды и который смешивается с водой.
Предпочтительно, если высококипящий полярный растворитель выбран из группы, включающей полярные апротонные растворители и их смеси. Специалист в данной области техники понимает, что растворители, обладающие проницаемостью, равной 5 или более, предпочтительно 15 или более, считаются полярными и что растворители, не содержащие атомы водорода, которые могут быть донорами водородной связи, считаются апротонными. Особенно предпочтительными являются неполярные апротонные растворители, все атомы водорода которых (если они имеются) ковалентно связаны с атомом углерода.
Более предпочтительно, если высококипящий полярный растворитель выбран из группы, включающей диметилсульфоксид (DMSO), N-метил-2-пирролидон (NMP), N,N-диметилформамид (DMF) или N,N-диметилацетамид (DMA) и их смеси. Наиболее предпочтительным растворителем является NMP.
Неожиданно было установлено, что возможно проведение окисления HMF в FDCA без необходимости предварительного удаления высококипящего полярного растворителя предыдущей стадии ч получением HMF посредством трехстадийного способа:
На первой стадии HMF окисляется в смеси высококипящего полярного растворителя и воды насколько возможно полностью с получением продуктов окисления по меньшей мере одной из одноатомных кислот HMF (FFCA, HMFCA) и также в конечном счете частично FDCA. В частности, на первой стадии можно получить смесь FFCA, HMFCA и FDCA.
Второй стадией является экстракция высококипящего полярного растворителя из щелочного раствора с оставлением солей одноатомных кислот и FDCA полностью в водной фазе. Непрореагировавший HMF из первой стадии, а также DFF в качестве побочного продукта первой стадии переносят в органическую фазе этой экстракции.
На третьей стадии окисление одноатомных кислот в FDCA завершается в воде. Все три стадии можно провести в периодическом режиме, а также в непрерывном режиме.
На первой стадии окисления частичное окисление HMF проводят в мягких условиях. высокие давления, высокие температуры, сильную щелочность или высокие концентрации основания можно исключить, поскольку не требуется полное превращение в FDCA. Условия на этой стадии выбраны так, чтобы исключить образование DFF и довести до максимума образование одноатомных кислот и FDCA.
В частности, было установлено, что, хотя принципиально возможно окислить HMF в FDCA за одну стадию путем использования сильных оснований, некоторые количества HMF разлагаются во время реакции, что приводит к твердым примесям, которые могут заблокировать реактор, что делает этот режим неподходящим, особенно в случае непрерывного режима реакции.
Таким образом, установлено, что на первой стадии окисления полезно использовать слабые основания, такие как обладающие значением pKa, равным от 7,5 до 13. Основание предпочтительно выбрано из группы, включающей карбонаты и фосфаты, особенно неорганические карбонаты и фосфаты. Наиболее предпочтительно, если в качестве основания используют Na3PO4 и/или Na2HPO4
Значение pH на первой стадии окисления может, в частности, равняться от 10 до 12. Для обеспечения депротонирования кислотных групп полное количество молей использующегося основания может быть по меньшей мере вдвое больше, чем количество молей HMF.
Таким образом, условия выбирают так, чтобы кислотные группы, образовавшиеся на стадии окисления, как можно более полно переходили в форму соло, только форма соли оставалась растворенной в водном растворе.
Кроме того, установлено, что благоприятно использование некоторых количеств воды.
Если вода уже не содержится в реакционной смеси проведенного ранее получения HMF, ее также следует добавить на этой стадии окисления. Это можно просто сделать вместе с добавлением основания. Содержание воды в раствор может находиться в диапазоне от 1 до 80%. Более предпочтительно, если содержание воды равно от 40 до 60%.
Другими предпочтительными условиями для первой стадии окисления являются:
- окислителем является кислород или воздух
- молярный избыток кислорода по сравнению с HMF составляет от 0,5 до 1,5 раз, предпочтительно от 0,9 до 1,4 раз, наиболее предпочтительно 1,25 раз
- давление при реакции находится в диапазоне от 1 бар до 100 бар, предпочтительно от 5 бар до 40 бар, наиболее предпочтительно 20 бар
- температура находится в диапазоне от 50°C до 130°C, предпочтительно от 60°C до 100°C, наиболее предпочтительно 90°C
- время пребывания при реакции равно 30 мин или менее, предпочтительно 15 мин или менее.
Только часть из указанных выше параметров можно установить такими, как указано выше. Предпочтительно можно использовать комбинацию нескольких или, наиболее предпочтительно, всех указанных выше условий.
Катализатором для первой стадии окисления может быть любой подходящий катализатор окисления, такой как катализаторы платинового типа (PTC), CuO/AgO, CuO или CoO. Предпочтительно использовать смешанный катализатор оксид меди/оксид серебра.
Реакционная среда (RM1), полученная на первой стадии окисления, содержит в основном HMFCA, FFCA и FDCA.
На второй стадии высококипящий полярный растворитель экстрагируют подходящим низкокипящим органическим растворителем (экстракция). Непрореагировавшие HMF и DFF направляются в органическую фазу, а соли одноатомных кислот (HMFCA, FFCA) и искомый продукт FDCA остаются в водной фазе.
Растворителем для экстракции для стадии экстракции предпочтительно является низкокипящий растворитель и более предпочтительно, если он выбран из группы, включающей этилацетат, трихлорметан и их смеси. Эти растворители приводят к превосходным результатам с точки зрения количества необходимого растворителя и количества стадий экстракции при экстракции высококипящего полярного растворителя из реакционной смеси. Применима периодическая, а также непрерывная экстракция.
Водную фазу, полученную на стадии экстракции, направляют на вторую стадию окисления для полного окисления в FDCA. Вторую стадию окисления можно провести с использованием более жестких условий, чем на первой стадии окисления, чтобы завершить окисления одноатомных кислот. HMF и DFF, являющиеся наиболее нестабильными соединениями в способе, на этой стадии больше не содержатся в реакционной смеси. Кроме того, на этой стадии присутствие воды в качестве растворителя исключает затруднения в связи с возможным самопроизвольным окислением растворителя при высоких концентрациях окислительного реагента и исключает возможную связанную с этим опасность. Кроме того, таким образом можно исключить возможное депротонирование инициирует реакции разложения высококипящего полярного растворителя сильными основаниями, что приводит к образованию осадков и потерям дорогостоящего растворителя.
Таким образом, на второй стадии окисления можно использовать любое основание для поддержания значения pH в щелочной области от 7,0 до 14,0 и более предпочтительно от 10,0 до 12,0. Более предпочтительно использовать гидроксид натрия или калия.
Другими предпочтительными условиями для второй стадии окисления являются:
- окислителем является кислород или воздух
- молярный избыток кислорода по сравнению с HMF составляет от 0,5 до 5 раз, предпочтительно от 1,0 до 3,0 раз, наиболее предпочтительно 2,0 раз
- давление при реакции находится в диапазоне от 1 бар до 100 бар, предпочтительно от 5 бар до 40 бар, наиболее предпочтительно 20 бар
- температура находится в диапазоне от 80°C до 180°C, предпочтительно от 90°C до 130°C, наиболее предпочтительно 110°C
- используют основание со значением pKa, равным более 13, наиболее предпочтительно NaOH
- время пребывания при реакции равно 30 мин или менее, предпочтительно 15 мин или менее.
И в этом случае только часть из указанных выше параметров можно установить такими, как указано выше. Предпочтительно можно использовать комбинацию нескольких или, наиболее предпочтительно, всех указанных выше условий.
Катализатором для второй стадии окисления также может быть любой подходящий катализатор окисления. Предпочтительно использовать катализаторы на основе платины.
FDCA, полученную на второй стадии окисления, можно превратить в свободную кислоту с помощью водного раствора кислоты. Осаждение свободной кислоты из реакционной смеси можно исключить с помощью фильтрования.
Как отмечено выше, в предпочтительном варианте осуществления настоящего изобретения на указанной первой стадии окисления часть HMF остается непрореагировавшей и/или окисляется в 2,5-диформилфуран (DFF) и на указанной стадии экстракции указанный непрореагировавший HMF и/или указанный DFF экстрагируют из указанной первой реакционной смеси.
Указанный экстрагированный непрореагировавший HMF и/или указанный экстрагированный DFF предпочтительно рециркулируют в раствор до первой стадии окисления.
Другой предпочтительный вариант осуществления настоящего изобретения отличается тем, что после стадии экстракции растворитель для экстракции и высококипящий полярный растворитель отделяют друг от друга.
В частности, и растворитель для экстракции, и высококипящий растворитель можно рециркулировать. Степень рециркуляции может находиться в диапазоне от 40 до 99%.
Разделение можно провести путем отгонки низкокипящего растворителя для экстракции. Растворитель для экстракции можно рециркулировать на стадию экстракции.
Высококипящий полярный растворитель можно рециркулировать на предыдущую стадию синтеза HMF. В особенности в случае, если высококипящий полярный растворитель содержит значительные количества непрореагировавшего HMF и/или DFF после стадии экстракции, высококипящий полярный растворитель также можно рециркулировать на первую стадию окисления. И затем рециркулированный высококипящий полярный растворитель можно очистить. На этой стадии для экстракции высококипящих полярных растворителей можно использовать любой не смешивающийся с водой.
Способ, предлагаемый в настоящем изобретении, можно провести в периодическом или непрерывном режиме. Способ, предлагаемый в настоящем изобретении, является особенно благоприятным в контексте способа с непрерывным режимом. В связи с этим, способ, предлагаемый в настоящем изобретении, можно успешно объединить с предшествующим способом получения HMF, в особенности если эту предыдущую стадию проводят в непрерывном режиме.
На фиг. 1 приведена схема способа, на которой представлен типичный предпочтительный вариант осуществления настоящего изобретения.
Смесь фруктозы и высококипящего растворителя (1) и смесь HCl и воды (2) загружают на стадию дегидратации (A). На стадии дегидратации (A) получают HMF в смеси воды и высококипящего растворителя.
Эту смесь направляют на первую стадию окисления (B) с использованием водного раствора основания и воздуха или кислорода в качестве окислительного реагента (3).
Смесь, полученную в первом окислении (B), содержащую HMFCA и/или FFCA и необязательно FDCA, а также остатки HMF и DFF, направляют на стадию экстракции (C), использующую растворитель для экстракции 4.
Органическую фазу, полученную после экстракции, содержащую HMF, DFF, высококипящий растворитель, а также растворитель для экстракции можно направить на стадию дистилляции (g). Высококипящий растворитель, необязательно содержащий HMF и DFF, в значительной части рециркулируют в исходный раствор (1).
Растворитель для экстракции рециркулируют на стадию экстракции (4).
Водную фазу, содержащую HMFCA и/или FFCA и необязательно FDCA, направляют на вторую стадию окисления (D), на которой используется водный раствор сильного основания и воздух или кислород в качестве окислительного реагента (5).
После завершения окисления реакционную смесь нейтрализуют или подкисляют (E) водным раствором кислоты (6) для превращения соли FDCA в свободную кислоту, которая осаждается из водной фазы.
На стадии фильтрования (F) из реакционной смеси получают твердую FDCA.
Примеры
1.) NMP/NaOH/Pt-C/воздух/22 бар/90°C
i) Окисление 1 - в NMP, Pt-C, 17 бар и 80°C, NaOH
Исходный раствор A получают путем растворения 5-гидроксиметилфурфураля (99%) в 95 г NMP (99,5%, Sigma Aldrich) и 5 г деионизированной воды. Исходный раствор B представляет собой 15% NaOH раствор, полученный из 150,41 г NaOH и 850,18 г деионизированной воды.
В непрерывной проточной установке раствор A и раствор B вводят во взаимодействие в 1/16-дюймовом тройниковом смесителе. Скорость потока раствора A равна 0,08 мл/мин и раствора B 0,06 мл/мин. Полученную смесь прямо вводят во взаимодействие с 125 мл/мин потоком воздуха, затем смесь поступает в действующий реактор. В этом случае реактором был реактор со струйным течением жидкости с платиной на активированном угле в качестве катализатора. Реактор с двойным кожухом нагревают при 80°C и обеспечивают время пребывания, равное 30 мин для данных скоростей потока. В системе в целом создают давление, равное 22 бар, с помощью клапана, поддерживающего заданное давление.
Полученная на этой стадии реакционная смесь не содержит HMF. Смесь продуктов окисления по данным анализа с помощью HPLC (высокоэффективная жидкостная хроматография) содержит FDCA: 73,67%, HMFCA: 18,10%, FFCA: 7,67%, DFF: 0,41% и 0,15% неизвестных продуктов окисления. Кроме того, при использовании этой процедуры образуется небольшое количество темного твердого вещества, что приводит к сокращению цикла службы катализатора неподвижного слоя.
ii.) Экстракция этилацетатом
Реакционную смесь (20,4 мл), собранную на первой стадии окисления, экстрагировали 6 раз с помощью 20 мл этилацетата на цикл для удаления NMP. На хроматограмме HPLC после этой процедуры не обнаруживается переход кислот в водную фазу. DFF полностью переносился в органическую фазу.
iii.) Окисление 2 - в H2O, Pt-C, 17 бар и 80°C, NaOH
Водный раствор кислот (FCDA, HMFCA и FFCA), полученный экстракцией, перекачивают при скорости потока, равной 0,08 мл/мин, в тройниковый смеситель для смешивания с потоком 0,06 мл/мин 15% раствора щелочи в тройниковом смесителе. Эту щелочную смесь вводят во взаимодействие с воздухом в тройниковом смесителе (скорость потока воздуха равна 125 мл при нормальных условиях/мин). Эту смесь вводят в реактор со струйным течением жидкости с платиной на активированном угле в качестве катализатора. Время пребывания в реакторе равно 30 мин при 100°C. В установке в целом создают давление, равное 25 бар.
Отбор проб проводили непрерывно при комнатной температуре. Полученная реакционная смесь по данным спектров HPLC содержало 100,0% FDCA. Суммарный выход способа по данным количественного анализа с помощью HPLC равнялся 82%.
2.) DMSO/Na2HPO4/Pt-C/воздух/17 бар/80°C
i) Окисление 1 - в DMSO, Pt-C, 17 бар и 80°C, Na2HPO4
Способ проводили в лабораторной установке непрерывного действия, эквивалентной использованной в примере 1. Исходный раствор A получали путем смешивания 32,8 г HMF и 200,3 г DMSO; раствор B представлял собой 11,5% раствор динатрийгидрофосфата, полученный путем приготовления насыщенной смеси (38,15 г Na2HPO4 и 45 г деионизированной воды), дважды разбавленной деионизированной водой в объемном отношении 1:1.
Параметры обработки: время пребывания 30 мин при 80°C и 18 бар. Использующимся катализатором являлась платина на активированном угле.
Смесь продуктов окисления по данным анализа с помощью HPLC содержит FDCA: 9,33%, HMFCA: 4,11%, FFCA: 27,67%, DFF: 16,23% и 41,70% HMF. Примерно 1% составляли неидентифицированные побочные продукты.
ii.) Экстракция трихлорметаном
Экстракцию DMSO проводили трихлорметаном. 21,1 мл Реакционной смеси экстрагировали 6 раз с помощью 20 мл трихлорметана в каждом цикле.
DFF полностью экстрагировали в органическую фазу. В водной фазе полностью оставались кислоты, а также часть непрореагировавшего HMF (4,7% по данным HPLC).
iii.) Окисление 2 - в H2O, Pt-C, 17 бар и 80°C, NaOH
Водную фазу из стадии экстракции обрабатывали на второй стадии окисления. Скорости потоков на этой стадии составляли 0,08 для реакционной смеси из экстракции, 0,06 для 11,5% водного раствора Na2HPO4 и 125 мл воздуха при нормальных условиях/мин. Использующимся катализатором являлась платина на активированном угле и параметры обработки были следующими: 100°C и 22 бар.
Полученная реакционная смесь содержала 57,80% FDCA, 13,64% HMFCA и 23,14% FFCA. Суммарный выход способа по данным количественной HPLC равнялся 37%.
3.) NMP/Na2HPO4/CuO/Al2O3/воздух/17 бар/80°C
i) Окисление 1 - в NMP, Pt-C, 17 бар и 80°C, Na2HPO4
Способ проводили в масштабированной лабораторной установке непрерывного действия, эквивалентной использованной выше в примерах. Исходный раствор A получали путем смешивания 65,6 г HMF и 400,0 г NMP; раствор B представлял собой 15% раствор фосфата натрия, полученный путем смешивания 150,0 г Na2HPO4 и 850,0 г деионизированной воды.
Скорости потоков, использованные в этом исследовании, составляли 2,86 мл/мин для раствора A, 2,14 мл/мин для раствора B и 250,0 воздуха при нормальных условиях/мин. Другие параметры обработки были следующими: время пребывания 10 мин при 90°C и 18 бар. Использующимся катализатором был оксид меди на оксиде алюминия.
Смесь продуктов окисления, полученная в этом исследовании, по данным анализа с помощью HPLC содержала FDCA: 9,20%, HMFCA: 86,39%, FFCA: 0,13%, DFF: 0,36% и 2,82% HMF. Примерно 1% составляют неидентифицированные побочные продукты.
ii.) Экстракция этилацетатом
Экстракцию NMP проводили этилацетатом. 50 мл Реакционной смеси экстрагировали 6 раз с помощью 40 мл этилацетата в каждом цикле.
FDCA, HMFCA и FFCA полностью оставались в водной фазе. В водной фазе также обнаружены небольшие количества HMF (0,5% по данным HPLC). DFF полностью переходил в органическую фазу и его отбрасывали.
iii.) Окисление 2 - в H2O, Pt-C, 17 бар и 90°C, NaOH
Водную фазу из стадии экстракции обрабатывали на второй стадии окисления в небольшой лабораторной установке, также использованной в примере 1 и 2. Скорости потоков на этой стадии также равнялись 0,08 мл/мин для реакционной смеси, использованной для экстракции, 0,06 мл/мин для 15% водного раствора NaOH и 125 мл воздуха при нормальных условиях/мин. Использующимся катализатором являлась платина на активированном угле и параметры обработки были следующими: 100°C и 22 бар.
По данным анализа с помощью HPLC полученные реакционные смеси содержали 99,51% FDCA, 0,34% HMFCA и примерно 0,1% неизвестных побочных продуктов. Суммарный выход способа по данным количественной HPLC равнялся 85%.
4.) NMP/NaOH/CuO-AgO/воздух/22 бар/90°C
i) Окисление 1 - в NMP, CuO-AgO, 17 бар и 90°C, NaOH
Для этого эксперимента использовали такую же лабораторную установку непрерывного действия, как в примере 1 и 2. Раствор A получали из 16,4 г HMF и 100 г NMP. Раствор B представлял собой 15% раствор гидроксида натрия в воде.
Скорости потоков для раствора A равнялась 0,08 мл/мин и 0,06 мл/мин для раствора B; для потока воздуха она равнялась 125 мл/мин. Смешивание проводили в тройниковых смесителях и реакцию проводили в реакторе со струйным течением жидкости. В реакторе устанавливали значения 90°C и 22 бар и время пребывания равнялось 15 мин.
Использующимся в этом эксперименте катализатором был катализатор CuO/AgO на оксиде алюминия. Этот катализатор получали в соответствии с литературой (Tian et al., 2008).
Во время эксперимента наблюдалось медленное повышение давления в системе вследствие забивания нерастворимым гумусом, что также приводило к сниженной степени превращения после 6 ч работы установки.
Смесь продуктов окисления по данным анализа с помощью HPLC содержит FDCA: 27,65%, HMFCA: 71,37%. Не найдены обнаруживаемые с помощью HPLC количества FFCA, DFF или HMF.
ii.) Экстракция этилацетатом
20,9 мл Реакционной смеси вводили 6 раз во взаимодействие с 20 мл этилацетата для экстракции NMP из водной фазы.
Анализ с помощью HPLC показал, что FDCA и HMFCA полностью оставались в водной фазе.
iii.) Окисление 2 - в H2O, Pt-C, 17 бар и 80°C, NaOH
Вторую стадию окисления проводили в установке, аналогичной использованной на первой стадии окисления, и при таких же параметрах. Только катализатор в реакторе заменяли на использованную ранее платину на активированном угле.
Полученная реакционная смесь содержала 93,65% FDCA, 5,26% HMFCA и примерно 1% неидентифицированных побочных продуктов или промежуточных продуктов. Суммарный выход способа окисления по данным HPLC равнялся 88%. Однако этот выход не сохранялся в течение более продолжительного проведения способа вследствие забивания, наблюдающегося на первой стадии окисления вследствие образования черной смолы.
5.) Исследования экстракции
i) Экстракция NMP из водной фазы разными растворителями
Смесь 24,12 г NMP (53%(мас./мас.), затененная полоса на фиг. 2) и 21,2 г деионизированной воды готовили в качестве исходного раствора для отделения NMP от воды.
Этот раствор переносили в делительную воронку. 21,2 г Этилацетата добавляли к раствору NMP, обе фазы сразу энергично вводили во взаимодействие и затем разделяли. Регистрировали массы отдельных фаз и отбирали небольшой образец водной фазы для определения содержания NMP с помощью количественной HPLC хроматографии.
Эту процедуру повторяли 5 раз для водной фазы с таким же количеством свежего растворителя на каждой стадии для обеспечения всего шести отдельных стадий экстракции. Содержание оставшегося NMP в водной фазе определяли с помощью количественной HPLC хроматографии.
Экстракцию NMP, описанную выше для этилацетата, проводили при одинаковых соотношениях также с дибутиловым эфиром, толуолом, тетрагидрофураном, трихлорметаном и н-бутанолом.
С помощью этилацетата (набор данных 1 на фиг. 2) обеспечена остаточная концентрация NMP, равная 5,7% (пунктирная полоса на фиг. 2). Это соответствует удалению 89,8% NMP из водной фазы за 6 стадий экстракции (полоса с горизонтальными линиями на фиг. 2). Этот результат превзойден при использовании трихлорметана (набор данных 4), с помощью которого NMP удален из водной фазы в такой степени, что он больше не обнаруживается. Дибутиловый эфир (набор данных 2, 11,5%) и толуол (набор данных 3, 21,9%) приводили к значительно более плохим результатам. Тетрагидрофуран (набор данных 5) и н-бутанол (набор данных 6) приводили к однофазной системе.
Результаты приведены на фиг. 2. Затененная полоса на фиг. 2 соответствует исходной концентрации NMP, пунктирная полоса соответствует концентрации NMP после 6 стадий экстракции и полоса с горизонтальными линиями относительному количеству NMP, удаленного за 6 стадий.
ii) Экстракция DMSO из водной фазы разными растворителями
17,28 г DMSO и 15,13 г деионизированной воды смешивали и переносили в делительную воронку. 15,20 г Этилацетата добавляли к этому раствору. Двухфазную систему энергично перемешивали в течение 10 мин и затем фазы разделяли.
Регистрировали массы обеих фаз и отбирали образец водной фазы для анализа с помощью количественной HPLC.
Экстракцию NMP из водной фазы повторяли 5 раз с помощью 15,2 г этилацетата на каждой стадии. После каждой стадии регистрировали массы и проводили количественное исследование с помощью HPLC.
Такую же процедуру экстракции, как описанная для этилацетата, также проводили с дибутиловым эфиром, толуолом, трихлорметаном, тетрагидрофураном и н-бутанолом.
Результаты приведены на фиг. 3. Полосы обладают такими же значениями, как на фиг. 2, описанном выше.
16,4% DMSO удаляли из водной фазы этилацетатом (набор данных 1 на фиг. 3). Лучшие результаты получены с трихлорметаном (набор данных 4, 28,3%) и тетрагидрофураном (набор данных 5, 22,5%). Толуол (набор данных 3, 8,1%) и дибутиловый эфир (набор данных 2, 6,7%) обнаружили даже меньшую способность удалять DMSO. н-Бутанол (набор данных 6) не приводил к разделению фаз.
Непатентная литература:
Amarasekara, A.S., Green, D., McMillan, E., 2008. Efficient oxidation of 5-hydroxymethylfurfural to 2, 5-diformylfuran using Mn (III)- salen catalysts. Catalysis Communications 9, 286-288.
Bicker, M., Kaiser, D., Ott, L., Vogel, H., 2005. Dehydration of D-fructose to hydroxymethylfurfural in sub-and supercritical fluids. The journal of supercritical fluids 36, 118-126.
Chheda, J.N., Roman-Leshkov, Y., Dumesic, J.A., 2007. Production of 5-hydroxymethylfurfural and furfural by dehydration of biomass-derived mono-and poly-saccharides. Green Chemistry 9, 342-350.
Grasset, F.L., Katryniok, B., Paul, S., Nardello-Rataj, V., Pera-Titus, M., Clacens, J.-M., De Campo, F., Dumeignil, F., 2013. Selective oxidation of 5-hydroxymethylfurfural to 2, 5-diformylfuran over intercalated vanadium phosphate oxides. RSC Advances 3, 9942-9948.
Lewkowski, J., 2001. Synthesis, chemistry and applications of 5-hydroxymethyl-furfural and its derivatives. Arkivoc I, 17-54.
Teong, S.P., Yi, G., Zhang, Y., 2014. Hydroxymethylfurfural production from bioresources: past, present and future. Green Chemistry 16, 2015-2026.
Tian, Q., Shi, D., Sha, Y., 2008. CuO and Ag2O/CuO catalyzed oxidation of aldehydes to the corresponding carboxylic acids by molecular oxygen. Molecules 13, 948-957.
Tuercke, T., Panic, S., Loebbecke, S., 2009. Microreactor Process for the Optimized Synthesis of 5-Hydroxymethylfurfural: A Promising Building Block Obtained by Catalytic Dehydration of Fructose. Chemical engineering & technology 32, 1815-1822.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ФУРАН-2,5-ДИКАРБОНОВОЙ КИСЛОТЫ | 2016 |
|
RU2732326C2 |
| Способ получения 2,5-фурандикарбоновой кислоты | 2014 |
|
RU2640203C2 |
| Совместное получение мономеров, в том числе по меньшей мере одного мономера на биологической основе | 2021 |
|
RU2799202C1 |
| Совместное получение мономеров, в том числе по меньшей мере одного мономера на биологической основе | 2021 |
|
RU2799207C2 |
| СПОСОБ СИНТЕЗА 5-ГИДРОКСИМЕТИЛФУРФУРАЛЯ (5-HMF) ИЗ УГЛЕВОДОВ | 2019 |
|
RU2797180C2 |
| КОМПОЗИЦИЯ ТЕРЕФТАЛЕВОЙ КИСЛОТЫ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2008 |
|
RU2519254C2 |
| Очистка диметилового эфира 2,5-фурандикарбоновой кислоты и других этерифицированных продуктов | 2021 |
|
RU2837146C1 |
| СПОСОБ СЕЛЕКТИВНОГО ОКИСЛЕНИЯ 5-ГИДРОКСИМЕТИЛФУРФУРОЛА | 2015 |
|
RU2703511C2 |
| СПОСОБ ЭПОКСИДИРОВАНИЯ ОЛЕФИНОВ | 2003 |
|
RU2327694C2 |
| СПОСОБ КАТАЛИТИЧЕСКОГО ГИДРОФОРМИЛИРОВАНИЯ ВЫСШИХ ОЛЕФИНОВ В ПРИСУТСТВИИ ЦИКЛИЧЕСКИХ ЭФИРОВ УГОЛЬНОЙ КИСЛОТЫ | 2003 |
|
RU2336261C2 |
Изобретение относится к способу получения 2,5-фурандикарбоновой кислоты (FDCA) путем окисления 5-гидроксиметил-2-фурфураля (HMF), где указанный HMF находится в растворе в апротонном высококипящем полярном растворителе и воде, характеризующемуся комбинацией: первой стадии окисления, на которой HMF по меньшей мере частично окисляется в указанном растворе с образованием первой реакционной смеси, включающей по меньшей мере одну одноатомную кислоту, выбранную из группы, включающей 5-гидроксиметилфуран-2-карбоновую кислоту (HMFA) и 5-формилфуран-2-карбоновую кислоту (FFCA) и необязательно FDCA; стадии экстракции после первой стадии окисления, на которой указанный высококипящий полярный растворитель экстрагируют из указанной первой реакционной смеси растворителем для экстракции, где указанная по меньшей мере одна одноатомная кислота остается в водной фазе, второй стадии окисления, на которой указанная по меньшей мере одна одноатомная кислота окисляется в FDCA. Технический результат – разработан новый способ получения 2,5-фурандикарбоновой кислоты с высоким выходом, который позволяет окислить HMF в высококипящих полярных растворителях без выделения или концентрирования HMF до стадии окисления. 8 з.п. ф-лы, 3 ил.
1. Способ получения 2,5-фурандикарбоновой кислоты (FDCA) путем окисления 5-гидроксиметил-2-фурфураля (HMF), указанный HMF находится в растворе в апротонном высококипящем полярном растворителе и воде, характеризующийся комбинацией
- первой стадии окисления, на которой HMF по меньшей мере частично окисляется в указанном растворе с образованием первой реакционной смеси, включающей по меньшей мере одну одноатомную кислоту, выбранную из группы, включающей 5-гидроксиметилфуран-2-карбоновую кислоту (HMFA) и 5-формилфуран-2-карбоновую кислоту (FFCA) и необязательно FDCA,
- стадии экстракции после первой стадии окисления, на которой указанный высококипящий полярный растворитель экстрагируют из указанной первой реакционной смеси растворителем для экстракции, где указанная по меньшей мере одна одноатомная кислота остается в водной фазе,
- второй стадии окисления, на которой указанная по меньшей мере одна одноатомная кислота окисляется в FDCA.
2. Способ по п. 1, отличающийся тем, что высококипящий полярный растворитель выбран из группы, включающей диметилсульфоксид (DMSO), N-метил-2-пирролидон (NMP), N,N-диметилформамид (DMF) или N,N-диметилацетамид (DMA) и их смеси.
3. Способ по любому из предыдущих пунктов, отличающийся тем, что на первой стадии окисления используют основание со значением pKa, равным от 7,5 до 13,0, предпочтительно выбранное из группы, включающей фосфаты, карбонаты и их смеси, наиболее предпочтительно выбранное из группы, включающей Na3PO4, Na2HPO4 и их смеси.
4. Способ по любому из предыдущих пунктов, отличающийся тем, что содержание воды в указанном растворе до первой стадии окисления равно от 1% до 80%, предпочтительно от 30% до 50%.
5. Способ по любому из предыдущих пунктов, отличающийся тем, что растворитель для экстракции для стадии экстракции выбран из группы, включающей этилацетат, трихлорметан и их смеси.
6. Способ по любому из предыдущих пунктов, отличающийся тем, что окислительный реагент для указанной первой стадии окисления, или указанной второй стадии окисления, или для обеих стадий окисления выбран из группы, включающей кислород или воздух.
7. Способ по любому из предыдущих пунктов, отличающийся тем, что на указанной первой стадии окисления часть HMF остается непрореагировавшей и/или окисляется в 2,5-диформилфуран (DFF) и что на указанной стадии экстракции указанный непрореагировавший HMF и/или указанный DFF экстрагируют из указанной первой реакционной смеси.
8. Способ по п. 7, отличающийся тем, что указанный экстрагированный непрореагировавший HMF и/или указанный экстрагированный DFF рециркулируют в раствор до первой стадии окисления.
9. Способ по любому из предыдущих пунктов, отличающийся тем, что после стадии экстракции растворитель для экстракции и высококипящий полярный растворитель отделяют друг от друга.
| WO 2014122319 A1, 14.08.2014 | |||
| WO 2012161967 A1, 31.01.2013 | |||
| СПОСОБ СЕЛЕКТИВНОГО ОКИСЛЕНИЯ 5-ГИДРОКСИМЕТИЛФУРФУРОЛА | 2015 |
|
RU2703511C2 |
| Способ получения 2,5-фурандикарбоновой кислоты | 2014 |
|
RU2640203C2 |
Авторы
Даты
2021-03-22—Публикация
2016-12-07—Подача