Изобретение относится к экспериментальной медицине, а именно к токсикологии и экологии, и может быть использовано для моделирования хронической токсической коагулопатии у экспериментальных животных.
Ртуть - один из наиболее распространенных тяжелых металлов (Raj D., Maiti S. Sources, Toxicity, and Remediation of Mercury: An Essence Review. Environ. Monit. Assess. 2019; 191 doi: 10.1007/s10661-019-7743-2.), обладающих высокой биологической активностью по отношению к живым организмам. Влияние соединений ртути на клетки и организм человека в настоящее время активно изучается (Авцин А.П. и соавт.1991). Показано, что длительное поступление в организм соединений ртути может приводить к ее накоплению в органах и тканях человека оказывать генотоксическое, цитотоксическое и органотоксическое действие способствуя полиорганным структурно-функциональным повреждениям.
Анализ современной литературы показывает, что процессы внутрисосудистого свертывания крови могут быть составляющим компонентом многих патологических процессов в организме: патологии сердечно-сосудистой системы, гипертонической болезни, нарушения мозгового кровообращения, патологии печени и почек (Byshevskiĭ A.Sh., Galian S.L. 2006; Момот A.П. и др. 2011; Мельник А.А. 2016). Актуальным является изучение процессов системы гемостаза и их роль в развитии соматической патологии при хронической интоксикации (Власов А.П., Григорьева Т.И., Лещанкина Н.Ю., 2009).
Современные схемы лечения хронической интоксикации включают антикоагулянтную терапию и длительный, иногда пожизненный прием пероральных антикоагулянтов (Shafi S.T., et al. 2014; Oliveira М., et al. 2017; Monahan R.C., et al. 2017). Вместе с тем недавние исследования установили, что это может привести к развитию антикоагулянт-ассоциированной нефропатии как у пациентов с хронической болезнью почек, так и пациентов без патологии почек (Kalaitzidis R.G., DuniA., Liapis G., Balafa О., et al. Anticoagulant-related nephropathy: a case report and review of the literature of an increasingly recognized entity. Int Urol Nephrol. 2017; 49: 1401-7.). При этом до конца не известны механизмы развития почечной патологии под влиянием антикоагулянтов.
Таким образом проблема коррекции системы гемостаза при хронической интоксикации остается открытой. Актуальным является разработка способов моделирования токсической коагулопатии, для последующего изучения методов профилактики данной патологии.
Существуют лишь единичные работы, описывающие разнонаправленные и противоречивые изменения в системе гемостаза под влиянием различных соединений ртути. У рабочих, профессионально подвергающихся воздействию паров ртути, описано статистически значимое увеличение времени свертывания крови с повышением образования тромбина (Nowakowska, В et al. "Wpfyw zawodowego narazenia nа rteć metaliczna na wybrane parametry hemostazy " [The effect of occupational exposure to metallic mercury on selected parameters of hemostasis]. Medycyna pracy vol. 48,5 (1997): 529-38.; Wierzbicki, R., Prazanowski, M., Michalska, M., Krajewska, U. and Mielicki, W.P. Disorders in blood coagulation in humans occupationally exposed to mercuric vapors. J. Trace Elem. Exp.Med., 2002, 15, 21-29. https://doi.org/10.1002/jtra. 1055; Song YG. Effects of chronic mercury poisoning on blood coagulation and fibrinolysis systems.// Zhonghua laodong weisheng zhiyebing zazhi (Chinese journal of industrial hygiene and occupational diseases) vol. 2005, 23,6: 405-7.).
В опытах ex vivo, было показано повышение протромботической активности эритроцитов вследствие увеличения экспрессии фосфатидилсерина на внешней поверхности мембран эритроцитов (Maseko Р.В, van Rooy М., Taute Н. Whole blood ultrastructural alterations by mercury, nickel and manganese alone and in combination: An ex vivo investigation // Toxicology and industrial health, 2021, 37(2), 98-111. https://doi.or2/10.1177/0748233720983114; Notariale, R., Infantino, R., Palazzo, E., & Manna, C. (2021). Erythrocytes as a Model for Heavy Metal-Related Vascular Dysfunction: The Protective Effect of Dietary Components. International journal of molecular sciences, 22(12), 6604. https://doi.org/10.3390/ijms22126604). Недостатком является сложность экстраполяции данных экспериментов ex vivo на процессы, происходящие в живом организме.
Следует отметить, что ряд современных авторов утверждает, что воздействие высоких доз ртути не оказывает влияния на свертывающую систему крови (Nielsen, V.G. Lethal concentrations of mercury or lead do not affect coagulation kinetics in human plasma // J Thromb Thrombolysis 2019, 48, 697-698. doi.org/10.1007/s11239-019-01921-x.). Так в эксперименте не отмечено существенной разницы в значениях кинетических параметров свертывания по сравнению со значениями, полученными для плазмы без добавления ртути.
Такая противоречивость и разрозненность сведений определили цель предлагаемого изобретения - создание модели хронической токсической коагулопатии.
Известен способ (Arbi S, Oberholzer НМ, Van Rooy MJ, Venter С, Bester MJ. Effects of chronic exposure to mercury and cadmium alone and in combination on the coagulation system of Sprague-Dawley rats // Ultrastruct Pathol. 2017 Jun 15:1-9. doi: 10.1080/01913123.2017.1327909), включающий введение в организм крыс Sprague-Dawley солей кадмия и ртути, растворенных в питьевой воде, в дозе, превышающей ПДК в 1000 раз в течение 28 дней. Было выявлено, что соли кадмия и ртути способны активировать прокоагулянтные свойства тромбоцитов.
Недостатком данного способа является сложность определения количества ртути, поступающей в организм с питьевой водой на единицу массы тела животного и отсутствие сведений о состоянии плазменного звена системы гемостаза при воздействии тяжелого металла на организм экспериментального животного.
Наиболее близким к заявляемому является способ моделирования коагулопатии на крысах с введением органического соединения ртути (Kostka В, Michalska М, Krajewska U, WierzbickiR. Blood coagulation changes in rats poisoned with methylmercuric chloride (MeHg) // Pol J Pharmacol Pharm. 1989 Mar-Apr; 41 (2): 183-9., PMID: 2594581). Введение однократной дозы метилртути (17,9 мг Hg / кг) и повторной дозы (5 × 8 мг Hg/кг/день) приводило к гиперкоагуляции. Наблюдалось уменьшение времени свертывания, повышение уровня фибриногена в плазме и характерные для гиперкоагуляции изменения тромбоэластографических показателей. Одновременно отмечались признаки нарушения активности тромбоцитов: снижение скорости агрегации и ретракции сгустка, а также увеличение времени кровотечения.
Недостатком способа является выбор соединения ртути, доза, и длительность введения. Известно, что разные соединения ртути имеют разные физико-химические свойства, и соответственно разную токсичность, и разные органы мишени повреждающего воздействия (Eto К, Takizawa Y, Akagi H, et al. Differential diagnosis between organic and inorganic mercury poisoning in human cases-the pathologic point of view. Toxicol Pathol. 1999; 27(6):664-671. doi:10.1177/019262339902700608.). Так, токсичность органических соединений ртути (метил ртуть в том числе), а также паров металлической ртути обусловлена их высокой липофильностью а, следовательно, биодоступностью и распределением по всем органам и системам, с преимущественным поражением нервной системы. Неорганические соединения ртути преимущественно оказывают нефротоксическое действие, могут накапливаться в эпителии почечных канальцев и вызывать его повреждение. Ранее некоторые соединения ртути использовались в клинике в качестве противопаразитарных средств, а также ртутные диуретики - промеран, меркузал и новурит.В настоящее время ртуть содержащие препараты запрещены к использованию вследствие высокой токсичности.
Недостатком данного способа также является то, что воздействие ртути на организм в течение короткого времени (5 дней) и высоких дозах, близких к полулетальным, не позволяет получить способ моделирования хронической коагулопатии. Эксперимент проводимый в течение двух месяцев с введение низких дозировок является более приближенным к натуральным условиям, моделирует поступление ртути в организм с пищей и водой из окружающей среды в условиях антропогенного загрязнения. Более информативно в разные сроки (две недели, один и два месяца) в динамике, изучение механизмов развития коагулопатии.
Заявляемое изобретение направлено на решение задачи, заключающейся в разработке способа моделирования хронической токсической коагулопатии у крыс в эксперименте.
Решение этой задачи позволяет более полно изучить в динамике патофизиологические механизмы развития коагулопатии при хронической ртутной интоксикации, создать способ моделирования хронической токсической коагулопатии, повышающий воспроизводимость, удобный для проведения эксперимента на животных и экономически выгодный.
Для достижения этого технического результата заявляемый способ моделирования хронической токсической коагулопатии у крыс в эксперименте, включающий введение экспериментальным животным соединения ртути, отличается тем, что белым крысам линии Wistar каждый день в течение 60 дней вводят раствор хлорида ртути через атравматичный зонд в желудок в дозе 0,5 мг/кг веса животного, где на единицу раствора, равную 0,3 мл, приходится 0,05 мг ртути по металлу.
Данный способ отличается от прототипа использованием в качестве токсического вещества -хлорида ртути (неорганического соединения ртути), длительностью и дозировкой введения металла.
Между отличительными признаками заявляемого изобретения и техническим результатом существует следующая причинно-следственная связь: длительное введение хлорида ртути в дозе 0,5 мг/кг приводит к развитию хронической токсической коагулопатии у экспериментальных животных. Это является удобной и приближенной к натуральным условиям моделью.
По имеющимся у авторов сведениям совокупность существенных признаков, характеризующих сущность заявляемого изобретения, не известна, что позволяет сделать вывод о соответствии изобретения критерию «новизна».
По мнению авторов, сущность заявляемого изобретения не следует для специалистов явным образом из известного уровня медицины, так как из него не выявляется вышеуказанная возможность получения способа моделирования хронической токсической коагулопатии у крыс в эксперименте. В научно-медицинской литературе нами не выявлено описание использования хлорида ртути для моделирования хронической токсической коагулопатии у экспериментальных животных, что позволяет сделать вывод о соответствии изобретения условию патентоспособности «изобретательский уровень».
Совокупность существенных признаков, характеризующих сущность изобретения, в принципе может быть многократно использована в медицине с получением результата, заключающегося в более точном и легко воспроизводимом способе развития хронической токсической коагулопатии, что позволяет сделать вывод о соответствии изобретения критерию «промышленная применимость».
Данный способ осуществляется следующим образом. Для получения токсического вещества хлорид ртути растворяют в дистиллированной воде таким образом, что в единице раствора, равной 0,3 мл, содержится 0,05 мг ртути (в пересчете на металл). На каждые 100 г веса крысы вводят 0,3 мл токсического раствора, что не является чрезмерной водной нагрузкой на организм экспериментального животного.
Раствор хлорида ртути вводят через атравматичный зонд в желудок в дозе 0,5 мг/кг, ежедневно 1 раз в сутки в течение 60 дней группе животных из 10 крыс. Материалом для исследования является цельная кровь, а также богатая и бедная тромбоцитами плазма крови. Забор крови, стабилизация и получение образцов плазмы осуществляются с учетом международных стандартов по клинической лабораторной диагностике для исследований в области гемостаза (Момот А.П. Патология гемостаза. Принципы и алгоритмы клинико-лабораторной диагностики, СПб.: Формат, 2006, 208 с.).
В пробах плазмы крови определяются следующие показатели:
• агрегационную активность тромбоцитов (индуктор АДФ - 10,0 мкг/мл) (Баркаган, З.С., Момот А.П. Диагностика и контролируемая терапия нарушений гемостаза, М.: Нъюдиамед-АО, 2008, 292 с. ).
• АЧТВ-активированное частичное тромбопластиновое время по Caen et al. (1968);
• ПВ - протромбиновое время по Quick (1935);
• ВПФМ - относительное время полимеризации фибрин-мономеров,
• Ф-ген - содержание фибриногена в плазме по Clauss (1961);
• Активность протеина С;
• АТ(III) - активность антитромбина III в плазме крови по В.А. Макарову и соавт.(2002);
• СЭЛ - время спонтанного эуглобулинового лизиса;
• РФМК - количество растворимых фибрин-мономерных комплексов (Елыкомов В.А., Момот А.П. Способ определения количества растворимого комплекса фибрин-мономера в плазме крови/Авторское свидетельство 1371219, 1987, СССР);
Коагулологические исследования были выполнены с применением наборов реагентов НПО «Ренам» и ООО фирмы «Технология-Стандарт», Россия на турбидиметрическом агрегометре АР-2110, коагулометре CGL-2110 спектрофотометре PV-1251C, «Solar» (Беларусь).
При проведении опытов на животных руководствовались правилами лабораторной практики в РФ (приказ МЗ РФ от 01.04.2016 г. №199).
Статистическую обработку полученных результатов проводили с использованием пакета программ "STATISTICA 10.0" (StatSoft) и Microsoft Excel 2016.
Данные представлены в виде медианы (Me) и интерквартильного размаха (Q25÷Q75). Достоверность различий оценивали при помощи непараметрического U-критерия Манна-Уитни. Различия считались достоверными при р<0,05.
Пример. Крысам-самцам линии Вистар в течение одного месяца (10 крыс) и двух месяцев (10 крыс) ежедневно один раз в сутки через зонд в желудок вводили раствор хлорида ртути в дозе 0,5 мг/кг веса животного. Контролем служили интактные животные (10 крыс) содержащиеся в стандартных условиях вивария. Состояние системы гемостаза оценивали через один и два месяца. В крови определяли показатели, характеризующие состояние сосудисто-тромбоцитарного звена гемостаза (количество тромбоцитов и их агрегационную активность), коагуляционного звена (АЧТВ, ПВ, ВПФМ, активность протеина С, активность AT (III), время СЭЛ), содержание фибриногена и уровня тромбинемии (РФМК).
Исследование состояния системы гемостаза у животных через один месяц экспериментов выявило развитие прокоагулянтных тенденций с одновременной активацией противосвертывающего и фибринолитического звеньев системы гемостаза (Таблица 1.). У крыс увеличивалась степень АДФ-индуцированной агрегации тромбоцитов и их количество. Количество фибриногена возрастало. Происходила активация свертывания крови как по внешнему пути, так и по внутреннему пути (по укорочению АЧТВ и ПВ). Выявлялось увеличение активности протеина С и антитромбина III, происходило укорочение времени спонтанного эуглобулинового лизиса. Через два месяца выявлялось увеличение степени АДФ агрегации тромбоцитов, но их количество снижалось по сравнению с данными через один месяц и не отличалось достоверно от контроля. Удлинялось протромбиновое время. Время полимеризации фибринмономеров укорачивалось. Концентрация фибриногена уменьшалась достоверно относительно опыта через один месяц, достигая контрольных значений. Вместе с тем происходила депрессия противосвертывающих и фибринолитических механизмов. Активность антитромбина уменьшалась, время спонтанного эуглобулинового лизиса удлинялось. Развивалась тромбинемия, содержание растворимых фибринмономерных комплексов достоверно возрастало (Полученные результаты отражены в таблице 1.).
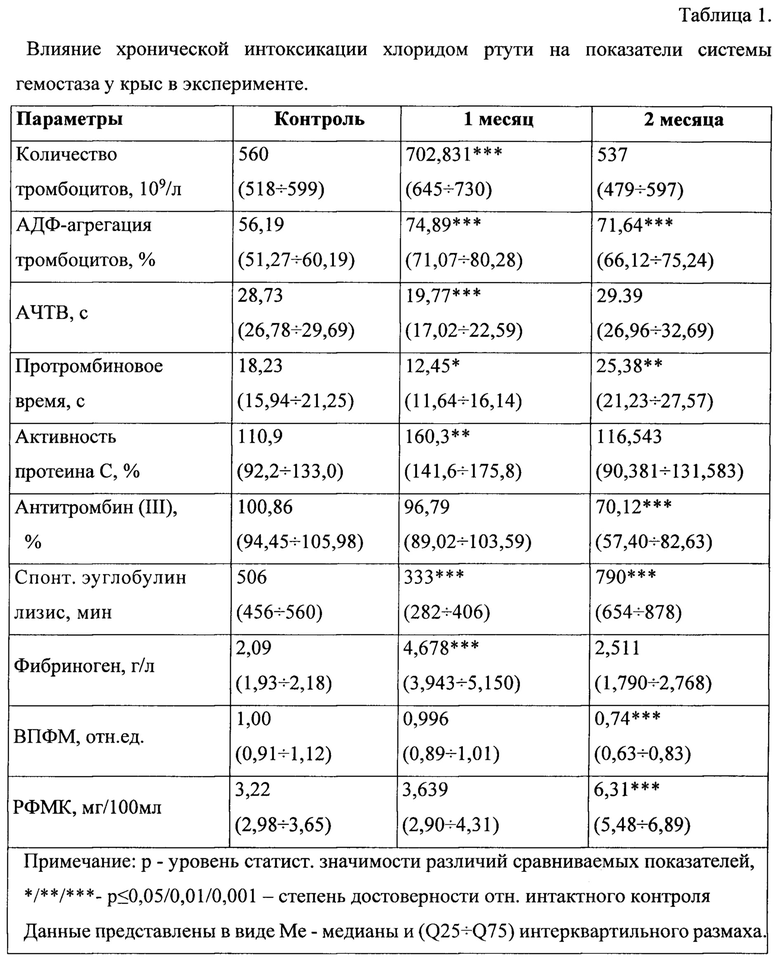
Данные проведенных экспериментов демонстрируют развитие гиперкоагуляционного синдрома, характеризующегося повышенной готовностью циркулирующей крови к свертыванию, с возрастанием в крови содержания маркеров активации гемостаза, подавлением антикоагулянтной и фибринолитической активности (А.П. Момот, Л.П. Цывкина, И.А. Тараненко Современные методы распознавания тромботической готовности, Барнаул, Изд-во Алт.ун-та, 2011, С.138.), что может приводить к нарушению процессов микроциркуляции, увеличению вязкости крови, замедлению венозного кровотока - развитию преходящих и начальных признаков органной дисфункции.
Предлагаемый способ моделирования хронической токсической коагулопатии у экспериментальных животных является эффективным, позволяет подробно изучить патофизиологические механизмы формирования токсической коагулопатии при длительной ртутной интоксикации и может способствовать разработке и поиску средств для лечения и профилактики нарушений свертывающей системы крови.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ моделирования хронической токсической коагулопатии у экспериментальных животных | 2017 |
|
RU2661722C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОНИЧЕСКОЙ ТОКСИЧЕСКОЙ КОАГУЛОПАТИИ У КРЫС | 2023 |
|
RU2800860C1 |
| СПОСОБ ПРОФИЛАКТИКИ ХРОНИЧЕСКОЙ СУЛЕМОВОЙ КОАГУЛОПАТИИ У КРЫС В ЭКСПЕРИМЕНТЕ | 2022 |
|
RU2788609C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОМ-ИНДУЦИРОВАННОЙ КОАГУЛОПАТИИ У КРЫС В ЭКСПЕРИМЕНТЕ | 2020 |
|
RU2743812C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОНИЧЕСКОЙ КОАГУЛОПАТИИ У ЖИВОТНЫХ В ЭКСПЕРИМЕНТЕ | 2020 |
|
RU2746831C1 |
| СПОСОБ ПРОФИЛАКТИКИ ТОКСИЧЕСКОЙ КОАГУЛОПАТИИ У КРЫС | 2022 |
|
RU2794030C1 |
| СПОСОБ ПРОФИЛАКТИКИ ТОКСИЧЕСКОЙ КОАГУЛОПАТИИ У КРЫС | 2023 |
|
RU2829177C2 |
| Способ профилактики хронической токсической коагулопатии у экспериментальных животных | 2018 |
|
RU2683723C1 |
| СПОСОБ ПРОФИЛАКТИКИ ХРОНИЧЕСКОЙ МОЛИБДЕНОВОЙ КОАГУЛОПАТИИ | 2020 |
|
RU2739690C1 |
| Способ профилактики хронической свинцовой коагулопатии у экспериментальных животных | 2019 |
|
RU2706386C1 |
Изобретение относится к экспериментальной медицине, а именно к токсикологии и экологии, и может быть использовано для моделирования хронической токсической коагулопатии у экспериментальных животных. Для этого ежедневно один раз в сутки в течение 60 дней вводят через зонд в желудок крысы раствор хлорида ртути в дозе 0,5 мг/кг в пересчете на металл. При этом в единице раствора, равной 0,3 мл, содержится 0,05 мг ртути. Способ обеспечивает развитие токсической коагулопатии у животного за счет оптимальной дозы и срока воздействия металла, что может быть использовано при поиске средств для профилактики и лечения токсической коагулопатии. 1 табл., 1 пр.
Способ моделирования хронической токсической коагулопатии у крыс в эксперименте, включающий внутрижелудочное введение экспериментальным животным соединения ртути, отличающийся тем, что животным каждый день в течение 60 дней вводят раствор хлорида ртути через зонд в желудок в дозе 0,5 мг/кг веса животного, где на единицу раствора, равную 0,3 мл, приходится 0,05 мг ртути по металлу.
| Способ моделирования хронической токсической коагулопатии у экспериментальных животных | 2017 |
|
RU2661722C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОНИЧЕСКОЙ КОАГУЛОПАТИИ У ЖИВОТНЫХ В ЭКСПЕРИМЕНТЕ | 2020 |
|
RU2746831C1 |
| ARBI S | |||
| et al | |||
| Effects of chronic exposure to mercury and cadmium alone and in combination on the coagulation system of Sprague-Dawley rats /Ultrastructural Pathology, 2017, DOI: 10.1080/01913123.2017.1327909, 10 pages | |||
| FALNOGA I | |||
| et al | |||
| Mercury toxicokinetics in Wistar rats exposed to | |||
Авторы
Даты
2022-12-14—Публикация
2022-05-04—Подача