Настоящее изобретение касается фармацевтической композиции, содержащей твердую дисперсию аморфного кладрибина и фармацевтически приемлемый водорастворимый носитель. В качестве фармацевтически приемлемого водорастворимого носителя может выступать высушенный распылением мальтодекстрин из высокоамилозного гороха. Фармацевтическая композиция может использоваться как лекарственный препарат, особенно для лечения рассеянного склероза.
Предпосылки настоящего изобретения
Кладрибин (2-CdA), 2-хлоро-2'-дезоксиаденозин, формула 1,
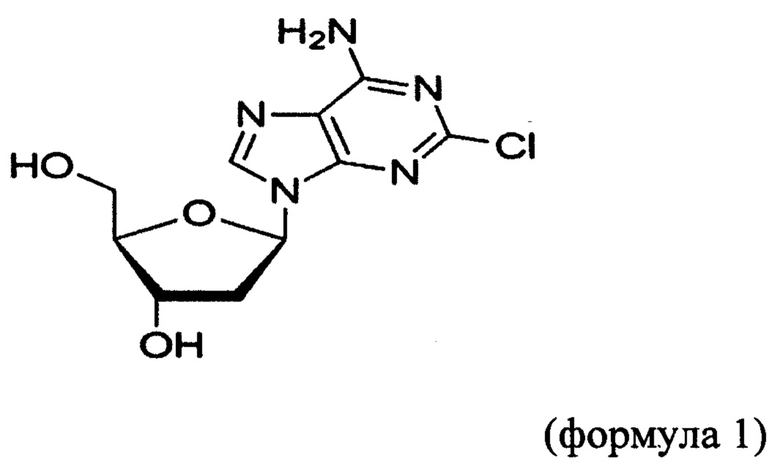
является противоопухолевым средством, которое используется в лечении лимфопролиферативных заболеваний, включая лейкоз ворсистых клеток (ЛВК), острый миелобластный лейкоз (ОМЛ), хронический лимфоцитарный лейкоз (ХЛЛ), лангергансоклеточный гистиоцитоз, неходжкинские лимфомы, макроглобулинемию Вальденстрема и рецидивирующе-ремиттирующий рассеянный склероз. 2-CdA - это пропрепарат, который преобразуется в соответствующий нуклеотид (неотъемлемое требование для обеспечения цитотоксичности). Трифосфатный аналог ингибирует различные процессы, задействованные в синтезе ДНК иРНК. Более того, воздействие нуклеозидного аналога на лейкозные клетки может подразумевать модуляцию путей апоптоза, контроля клеточного цикла или путей сигнальной трансдукции.
Кладрибин может вводится инъекциями или приниматься внутрь. Однако физико-химические свойства кладрибина в значительной степени затрудняют получение готовой лекарственной формы для перорального применения. Во-первых, при комнатной температуре наблюдается лишь незначительная растворимость в воде. Следовательно, абсорбция при приеме внутрь ограничивается скоростью растворения, и требуется помощь в растворении и скорости растворимости для повышения биодоступности при пероральном приеме. Во-вторых, кладрибин чувствителен к средам с низким значением рН. При кислотном значении рН распад заметно увеличивается со временем, даже при физиологических температурах. При рН 2 и температуре 37° через 6 ч в растворе остается только 13% 2-CdA; при рН 1 через 2 ч при температуре 37°С содержание 2-CdA составляет всего 2%; расчетный период полураспада Т1/2 равен 1,6 ч (рН 2, 37°С) и 0,37 ч (рН 1, 37°С) (Tarasiuk A, Skierski J, Kazimierczuk Z, Stability of 2-chloro-2'-deoxyadenosine at various pH and temperature. Arch Immunol Ther Exp (Warsz). 1994;42(1):13-5).
Соответственно, и низкая растворимость, и низкое значение рН кладрибина существенно затрудняют разработку готовой лекарственной формы для перорального приема.
Основные препятствия к успешной разработке готовой лекарственной формы кладрибина для приема внутрь заключаются в сочетании следующего: а) узкое окно абсорбции в верхнем отделе тонкого кишечника, где кладрибин проникает в ткани через нуклеозидные транспортные белки, разбросанные по эпителиальной выстилке кишечника, и подвергается внутриклеточному фосфорилированию до активной формы, 2-CdA трифосфата, при участии дезоксицитидин киназы в мишеневидных клетках; и b) разрушение под воздействием низкого рН и при участии определенных ферментов, например, пурин-нуклеозидфосфорилазы, вырабатываемых микробной микрофлорой.
Таким образом, если лекарственное вещество не будет быстро высвобождаться в верхнем отделе тонкого кишечника, оно будет характеризоваться низкой биодоступностью и подвергнется быстрому разрушению; именно эти опасения придают такую важность профилю высвобождения.
Растворимость и скорость растворения - два важных параметра, которые следует учитывать для достижения терапевтической эффективности препарата при пероральном приеме. Плохая растворимость в воде и профиль растворения нерастворимых лекарств остаются серьезной проблемой формулирования и разработки готовых лекарственных форм для приема внутрь.
В попытке улучшить растворимость и увеличить скорость растворения плохо растворяющихся лекарственных препаратов применялись различные методики, включая твердую дисперсию (ТД), микронизацию, формы на основе липидов, микронизированные формы и комплексирование. ТД и комплексирование с применением гидрофильных носителей показали перспективность в улучшении растворимости и растворения плохо растворяющихся лекарств. Улучшенные профили растворимости и растворения форм на основе ТД и комплексирования можно объяснить уменьшением размера частиц, изменением кристаллической формы лекарства на аморфную форму, солюбилизирующим действием гидрофильных носителей и лучшей смачиваемостью лекарственного вещества, окруженного носителями.
Комплекс гипофильного лекарственного вещества и гидрофильного носителя (комплексы включения) можно получить путем простого смешивания лекарственного вещества и наполнителей, что обеспечит улучшенную солюбилизацию вещества. Комплексы включения получают введением неполярной молекулы (гостевая молекулы) в полость другой молекулы (молекула-хозяин). Чаще всего в качестве молекулы-хозяина используются циклодекстрины.
Комплексирование циклодекстрина имеет преимущества вследствие низкой гигроскопичности, низкой токсичности, высокой текучести, прекрасной совместимости и сжимаемости, что увеличивает стабильность лекарственного вещества и увеличивает срок хранения.
Циклодекстрины - это циклические олигосахариды с гидрофильной внешней поверхностью и гидрофобной центральной полостью. Такая молекулярная структура наделяет циклодекстрины некоторыми уникальными свойствами. Гидрофильная внешняя поверхность молекулы делает ее растворимой в воде, а гидрофобная полость создает микросреду для неполярных молекул соответствующего размера. В водных растворах циклодекстрины способны образовать комплексы включения со многими лекарственными веществами, поглощая всю молекулу вещества или, точнее, некоторую неполярную часть молекулы в полость.
Понятие «твердая дисперсия» относится к группе твердых препаратов, в состав которых входит не менее двух разных компонентов, как правило, гидрофильная матрица и гидрофобное лекарственное вещество.
В литературе описывается несколько методов твердой дисперсии: выпаривание растворителя, пластицирование, плавление или сращение, экструзия расплава, совместное осаждение, совместное выпаривание, высушивание распылением, заключение в гель, технология сверхкритической жидкости, лиофилизация.
Говоря о дисперсии компонентов, когда система химически и физически однородна или гомогенна либо состоит из одной фазы (в терминах термодинамики), твердая дисперсия называется «твердый раствор» или «гладкий раствор». Такие системы не содержат сколько-нибудь значимого количества активных ингредиентов в кристаллической или микрокристаллической форме, о чем свидетельствуют результаты термоанализа (дифференциальная сканирующая калориметрия) или рентгеновский структурный анализ (широкоугольное рассеяние рентгеновских лучей).
Один из основополагающих принципов получения твердых дисперсий состоит в получении аморфного состояния, которое считается более растворимым по сравнению с кристаллическим состоянием, поскольку в аморфном состоянии для разрушения кристаллической решетки, в отличие от кристаллической формы, энергия не требуется.
В патенте US 6194395 (приоритет от 25.02.1999 г.), использовали 2-гидроксипропил-β-циклодекстрин (HPBCD) для улучшения растворимости кладрибина в воде и чувствительности на низкий рН.
Позже в патенте US 8785415 (приоритет от 28.03.2003) описали образование комплекса из аморфного кладрибина и циклодекстрина как смесь аморфного комплекса включения кладрибина с аморфным циклодекстрином, смесь аморфного свободного кладрибина, связанного с аморфным циклодекстрином, как комплекс невключения и аморфный свободный кладрибина, а также их влияние на абсорбцию кладрибина при приеме внутрь.
Авторы вышеуказанного патента описали только один способ получения комплекса кладрибин-циклодекстрин (сублимационная сушка). Согласно патенту US 8785415, для получения формы необходимы манипуляции с большим количеством воды и длительное комплексирование из-за ограниченной растворимости кладрибина. Для получения готовой лекарственной формы потребуются дорогостоящие процессы, оборудование, большое количество энергии и времени.
Фактически, готовая лекарственная форма, приготовленная по упомянутому выше патенту, представляет собой смесь комплексного и абсорбированного АФИ в соотношении соответственно от 30-40% до 70-60%, что существенно затрудняет управление и предсказуемость процесса и может повлиять на растворимость и разложение АФИ в желудке с низкой абсорбцией 2-CdA. Кроме того, нет прямых доказательств положительного влияния 30-40% 2-CdA в комплексе включения на остальные абсорбированные молекулы на поверхности носителя.
Таким образом, принимая во внимание описанное выше, все еще есть потребность в альтернативных, улучшенных фармацевтических составах, содержащих аморфный кладрибин - стабильный, простой и недорогой в получении, но в то же время приемлемый для коммерческой продажи. Исходя из этого, желательно получить стабильный аморфный кладрибин и найти надежный процесс получения такого стабильного аморфного кладрибина.
Краткое изложение изобретения
Настоящее изобретение касается фармацевтической композиции, содержащей твердую дисперсию аморфного кладрибина и фармацевтически приемлемый водорастворимый носитель.
Было обнаружено, что твердая дисперсия аморфного кладрибина и водорастворимого носителя обеспечивает высокую стабильность при низком значении рН и высокую биодоступность.
В качестве фармацевтически приемлемого водорастворимого носителя может выступать высушенный распылением мальтодекстрин из высокоамилозного гороха. Высушенный распылением мальтодекстрин из высокоамилозного гороха можно получить путем частичного гидролиза горохового крахмала в качестве носителя. Такой носитель предлагает новый технический подход в получении стабильной твердой дисперсии с аморфным кладрибином, которая подошла бы для получения готовых лекарственных форм для перорального приема. Твердая дисперсия улучшает общие показатели высвобождения лекарственного вещества, характерные для плохо растворяющегося кладрибина.
Весовое отношение кладрибина и фармацевтически приемлемого водорастворимого носителя в твердой дисперсии может быть не ниже 1:3, предпочтительнее 1:4.
Весовое отношение кладрибина и фармацевтически приемлемого водорастворимого носителя может составлять от 1:3 до 1:20, лучше от 1:4 до 1:15, оптимальнее от 1:5 до 1:15 и лучше всего от 1:5 до 1:10.
Твердая дисперсия может содержать остаточный растворитель в количестве не более 10% от веса твердой дисперсии, предпочтительнее не более 9%, лучше не более 7%, еще лучше не более 5%, но оптимальнее всего не более 2%.
Фармацевтическая композиция может также содержать один или несколько фармацевтически приемлемых наполнителей.
Фармацевтическая композиция может принимать форму таблетки или капсулы.
Фармацевтическая композиция может использоваться как лекарственный препарат, особенно для лечения рассеянного склероза.
Ниже описано применение фармацевтической композиции для перорального приема и/или парентерального введения.
Настоящее изобретение также касается способа получения твердой дисперсии аморфного кладрибина и фармацевтически приемлемого водорастворимого носителя, протекающего в два этапа:
- приготовление раствора, содержащего кладрибин и фармацевтически приемлемый водорастворимый носитель в растворителе или смеси растворителей, и
- удаление растворителя из раствора, предпочтительно вакуумным выпариванием, высушиванием распылением или сублимационной сушкой.
Кладрибин может иметь кристаллическую, полиморфную или аморфную форму и растворяться в растворителе или смеси растворителей для получения раствора.
В качестве фармацевтически приемлемого водорастворимого носителя может выступать высушенный распылением мальтодекстрин из высокоамилозного гороха. Весовое отношение кладрибина и фармацевтически приемлемого водорастворимого носителя в растворе может быть не ниже 1:3, предпочтительнее 1:4.
Весовое отношение кладрибина и фармацевтически приемлемого водорастворимого носителя может составлять от 1:3 до 1:20, лучше от 1:4 до 1:15, оптимальнее от 1:5 до 1:15 и лучше всего от 1:5 до 1:10.
Раствор готовится с использованием не менее одного растворителя: вода и спирт С1-С4, предпочтительно вода, этанол, метанол и изопропанол и их смеси, предпочтительнее, чтобы растворитель представлял собой смесь воды и этанола или воды и изопропанола.
Содержание воды возможно на уровне не менее 70% (вес/вес) готового растворителя. Растворителем может быть водно-спиртовой раствор.
После удаления из раствора растворителя или смеси растворителей полученное твердое вещество можно высушить. Высушенное твердое вещество может содержать остаточный растворитель в количестве не более 10% от веса твердой дисперсии, предпочтительнее не более 9%, лучше не более 7%, еще лучше не более 5%, но оптимальнее всего не более 2%.
Краткое описание чертежей
Далее изобретение описывается с упоминанием фигур:
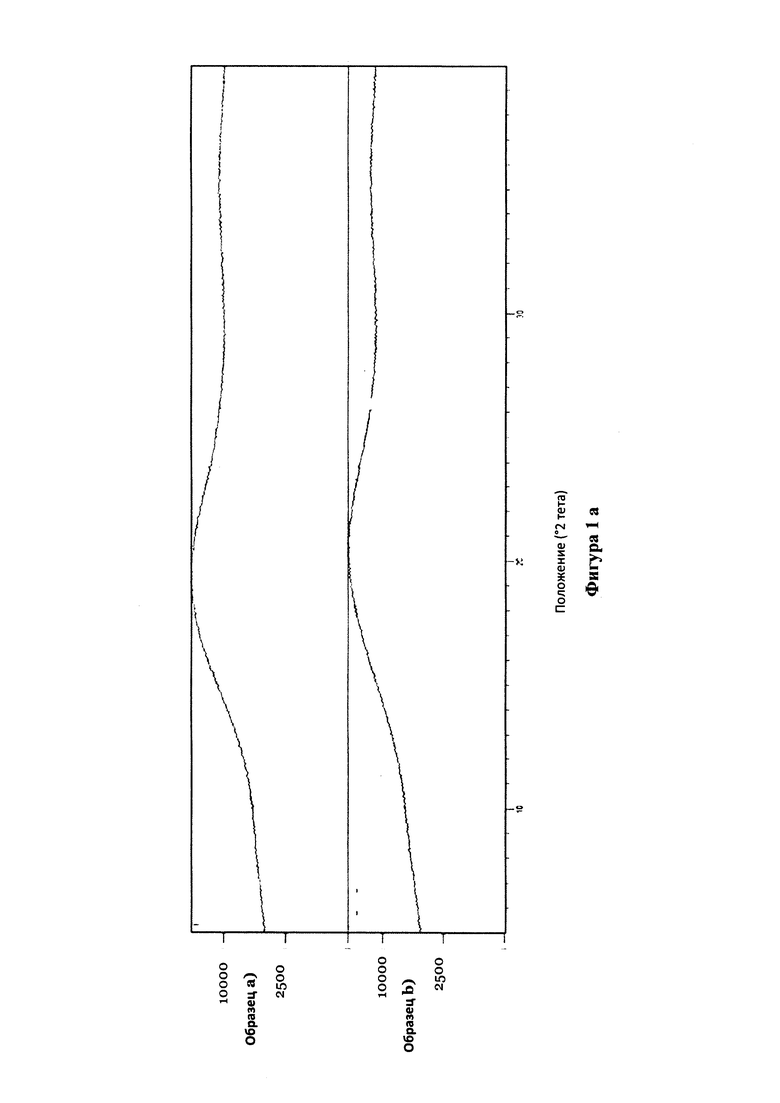
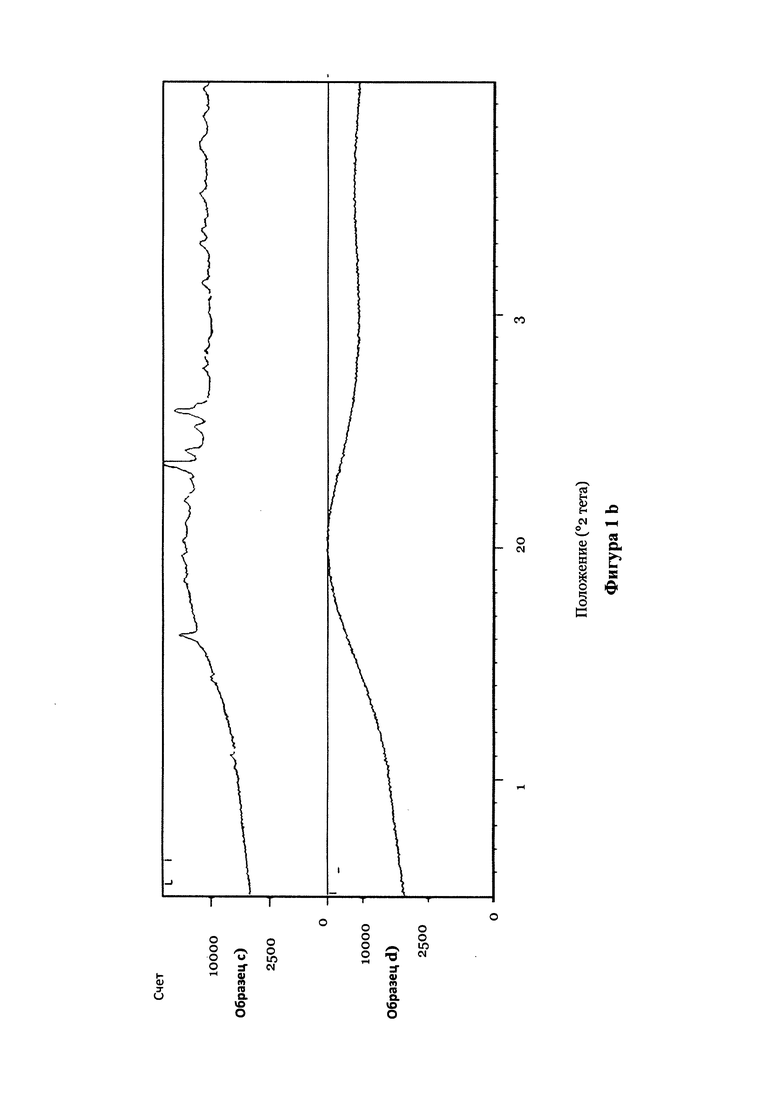
Фиг. 1 а, b снимки рентгеновской дифракции комплексов кладрибина при реализации настоящего изобретения и эталонов;
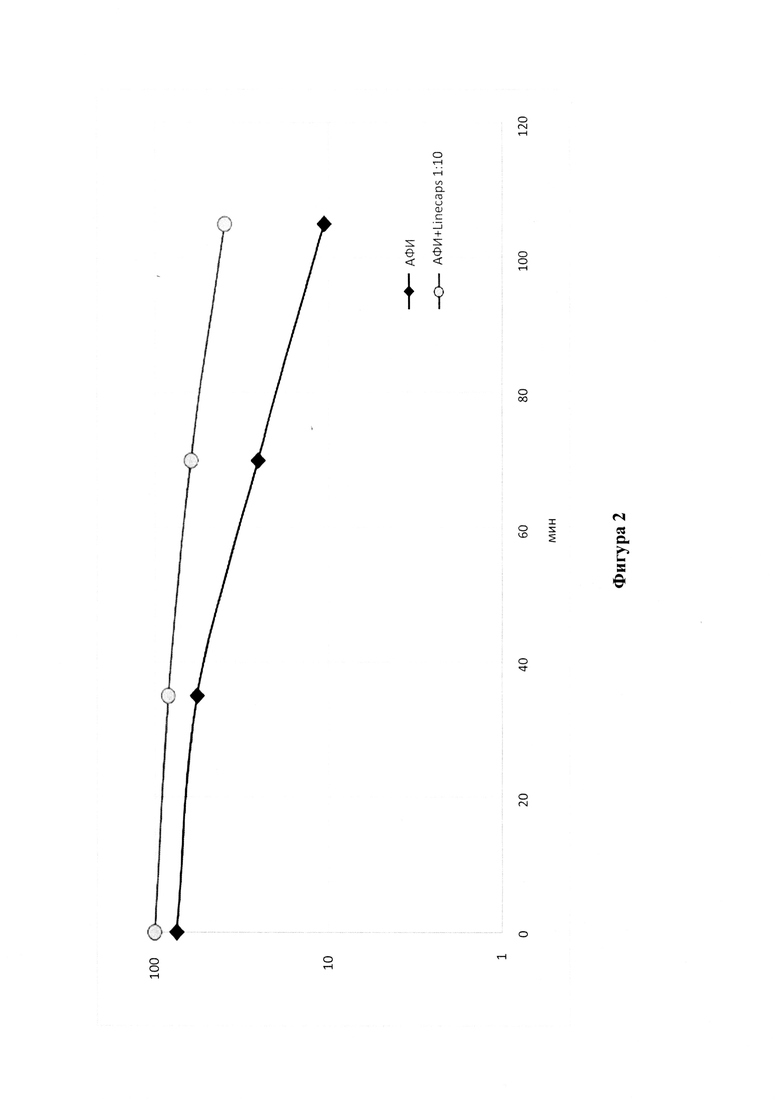
Фиг.2 Поведение АФИ кладрибина и твердой дисперсии в буферном растворе НС1 при рН 1,4.
Подробное изложение изобретения
Ниже реализация и вариации настоящего изобретения описаны более подробно. Тем не менее, следует подчеркнуть, что настоящее изобретение не ограничивается такой реализацией и вариациями. Также упоминается, что возможным представляется описание лишь отдельных сценариев реализации изобретения. Тем не менее, опытный человек поймет, что свойства, описываемые в отношении такой реализации, можно объединять по-разному и что отдельные характеристики могут быть опущены, если это будет приемлемым в определенном случае.
Настоящее изобретение касается фармацевтической композиции, содержащей твердую дисперсию аморфного кладрибина и фармацевтически приемлемый носитель.
Тем не менее, приводится описание способа получения твердой дисперсии аморфного кладрибина, в соответствии с одним сценарием реализации, с использованием, по меньшей мере, следующего:
a. получение раствора, содержащего кладрибин и фармацевтически приемлемый носитель в растворителе или смеси растворителей;
b. удаление растворителя из раствора а);
c. Необязательное высушивание твердого вещества, полученного в п. b), для получения необходимой твердой дисперсии кладрибина.
Кладрибин в форме аморфного премикса для описываемого применения достаточно стабильный и подходит для использования в фармацевтических композициях, предназначенных для лечения заболеваний, включая среди прочего рассеянный склероз.
Далее описывается способ получения аморфного кладрибина: удаление растворителя из раствора кладрибина и фармацевтически приемлемого носителя. Также описывается способ получения твердой дисперсии, состоящей из аморфного кладрибина: удаление растворителя из раствора кладрибина с добавлением фармацевтически приемлемого носителя.
Раствор кладрибина можно получить растворением кладрибина в растворителе или смеси растворителей. Любую полиморфную форму можно использовать для приготовления раствора, например, кристаллические формы, включая сольваты и гидраты.
В попытках найти потенциально новые солюбилизаторы кладрибина, которые можно было бы использовать в коммерческом производстве аморфного кладрибина, был апробирован высушенный распылением мальтодекстрин из высокоамилозного гороха Kleptose® Linecaps.
Kleptose® Linecaps (мальтодекстрин из горохового крахмала) богат неразветвленной и растворимой амилозой. Такая амилозная фракция позволяет получить соединения включения, необходимые для маскировки вкуса и других применений. Амилоза существует в форме спиральных структур, и, подобно циклодекстрину, у них есть гидрофильная внешняя поверхность и гидрофобная внутренняя полость, созданная за счет гликозидных эфирных связей, образующих полость, которая позволяет амилозе инкапсулировать определенные лекарственные вещества.
Инкапсулирующая способность амилозы может также улучшить растворимость молекул определенных лекарственных веществ в холодной воде. Тем не менее, для соответствия способности циклодекстринов к солюбилизации требуется большее количество Kleptose® Linecaps по весу (примерно в 10 раз больше) вследствие большой молекулярной массы. Что касается молярных характеристик, Kleptose® Linecaps и циклодекстрины обладают схожим действием.
В соответствии с приведенной информацией Kleptose Linecaps должны растворяться путем образования комплекса включения CLD только при высоких соотношениях Linecaps: АФИ. Для кладрибина соотношение должно быть близко к 1:100.
Удивительно, что когда Linecaps развели в водно-спиртовом растворе, его воздействие на растворимость неожиданно улучшилось. Было обнаружено, что использование водно-спиртового раствора приводит к значительному сокращению количества горохового мальтодекстрина, необходимого для растворения и стабилизации кладрибина в растворе, и после выпаривания получается стабильная аморфная твердая дисперсия, пригодная для готовых лекарственных форм для перорального применения с приемлемой стабильностью и профилем растворения.
Настоящее изобретение основано на выводе о том, что комбинация высушенного распылением мальтодекстрина из высокоамилозного гороха, полученного путем частичного гидролиза горохового крахмала, в качестве носителя и водно-спиртового раствора предлагает новый технический подход к получению стабильной твердой дисперсии с аморфной АФИ кладрибина, приемлемой для производства готовых лекарственных форм для приема внутрь.
Кладрибин и Kleptose Linecaps можно растворять одним растворителем или разными растворителями и затем смешивать. При реализации изобретения описанная твердая дисперсия включает кладрибин и носитель в весовых соотношениях в диапазоне от примерно 1:3 до примерно 1:15, предпочтительно от 1:5 до 1:10.
В качестве растворителей для растворения кладрибина и носителя можно использовать среди прочего смесь воды и органических растворителей, например, спиртов С1-С4. Примерами органических растворителей, которые можно использовать в настоящем изобретении, могут служить этанол, метанол, изопропанол и их смесь. Количество растворителя, используемого для растворения, зависит от типа растворителя и температуры растворения.
Linecaps плохо растворяются в растворе воды: EtOH. При растворении Linecaps в воде с последующим добавлением EtOH в соотношении до 1:1 (объем/ объем) он сохраняет растворимость, а растворенный кладрибин остается стабильным в течение нескольких дней.
Температура растворения может колебаться от примерно 35°С до примерно 60°С, в зависимости от типа растворителя, используемого для солюбилизации. Допускается и любая другая температура при условии получения прозрачного раствора.
При желании полученный раствор можно профильтровать для удаления нерастворившихся частиц до последующей обработки. Нерастворившиеся частицы можно удалить фильтрацией, центрифугованием, отстаиванием и другими способами. Фильтрация раствора осуществляется через бумагу, стекловолокно или другой мембранный материал.
Растворитель может удаляться подходящими способами, например, атмосферным выпариванием или выпариванием под вакуумом. Такие способы включают вакуумное выпаривание, высушивание распылением и сублимационную сушку (лиофилизацию).
Растворитель может выпариваться под вакуумом, например, ниже 100 мм рт.ст. либо ниже 600 мм рт.ст. при температуре от около -20°С до 70°С. Могут использоваться различные температуры и значения вакуума при условии, что количество примесей в препарате не будет увеличиваться.
Например, высушивание распылением или выпаривание в роторном испарителе Буки больше подходит для промышленных масштабов при производстве партий около 100 г, 1 кг или больше. В соответствии с настоящим изобретением аморфная форма, полученная высушиванием распылением или в испарителе Буки, быстро растворяется из фармацевтической композиции.
Полученный аморфный материал можно собрать из оборудования, например, соскребанием либо другими способами, подходящими для того или иного устройства, можно в атмосфере азота.
По желанию высушивание твердого препарата можно проводить при приемлемых условиях для получения необходимой твердой дисперсии кладрибина в аморфной форме, практически не содержащей растворители. При вариантах реализации настоящего изобретения твердая дисперсия кладрибина содержит остаточные растворители в количестве не мнее1%, но не более 10% от веса твердой дисперсии. В одном определенном применении твердая дисперсия содержит остаточный растворитель в количестве не более 2% по весу. В другом применении твердая дисперсия содержит остаточный растворитель в количестве от 4% до 7% по весу.
Высушивание может продолжаться о тех пор, пока количество остаточного растворителя не достигнет нужного значения, например, диапазона, определенного Международной конференцией по гармонизации технических требований к регистрации лекарственных средств для человека. Рекомендованный показатель растворителя зависит от типа растворителя, но не должен превышать 5000 промилле, или около 4000 промилле, или около 3000 промилле.
Высушивание может протекать при пониженном давлении, например, ниже 650 мм рт.ст. или ниже 50 мм рт.ст., при температуре от 35°С до 70°С. Высушивание может длиться в течение необходимого периода времени, достаточного для получения желаемого результата, например, от 1 часа до 20 часов, и дольше. Длительность высушивания может быть большей или меньшей, в зависимости от спецификации препарата.
Для высушивания может использоваться подходящее оборудование, например, полочная сушилка, вакуумная печь, сушильный шкаф, сушилка с псевдоожиженным слоем или тому подобное.
Кладрибин и его примеси могут анализироваться методом ВЭЖХ.
В настоящем изобретении также описывается способ приготовления фармацевтических композиций, содержащих аморфный кладрибин и один или несколько фармацевтически приемлемых наполнителей. Способ может подразумевать смешивание или гранулирование аморфной твердой дисперсии кладрибина с одним или несколькими фармацевтически приемлемыми наполнителями, после чего следует изготовление таблеток или инкапсулирование с использованием хорошо известного оборудования и способов.
Фармацевтические композиции в рамках настоящего изобретения имеют профиль растворения, типичный для составов с немедленным высвобождением. При приготовлении и хранении фармацевтические композиции по настоящему изобретению остаются в аморфной форме.
Фармацевтические композиции по настоящему изобретению могут упаковываться в блистерный материал. Блистерный материал, используемый по настоящему изобретению, может быть любым блистерным материалом, известным специалисту среднего звена. Блистерный материал по настоящему изобретению выбирается из следующих материалов: политетрафторэтилен, ПВХ/ алюминий, дюплекс/ алюминий, триплекс/ алюминий и алюминий/ алюминий. Для обеспечения защиты композиций по настоящему изобретению, например, от влажности, предотвращая тем самым переход в полиморфную форму, предпочтительнее выбирать политетрафторэтилен, триплекс/ алюминий и алюминий/ алюминий.
Фармацевтическая композиция по настоящему изобретению может использоваться в качестве лекарственного препарата. Как правило, фармацевтическая композиция предназначена для лечения рассеянного склероза.
Настоящее изобретение иллюстрируется следующими примерами.
Пример 1: Кладрибин : Linecaps в соотношении 1:10 по весу
5,0 г Linecaps растворили в 25 мл дистиллированной воды при помешивании при комнатной температуре, после чего добавили 10 мл этанола. 0,5 г кладрибина суспендировали в растворе Linecaps : вода : этанол и нагрели до температуры 50°С. После того, как раствор стал прозрачным, а распылительную сушилку нагрели, раствор перекачали в распылительную сушилку, где растворитель выпаривали и собирали твердое вещество.
Аналогичный процесс выполнялся с использованием изопропанола вместо этанола.
Записывали результаты порошкового рентгеноструктурного анализа образцов (фиг. 1). Контрольный образец а) - это порошок linecaps, использовавшийся для получения описанной выше композиции кладрибин : linecaps. Образец b) - это твердая дисперсия кладрибин : linecaps в весомом соотношении 1:10 в воде/ этаноле, как описано выше. Контрольный образец с) - это физическая смесь кладрибина и linecaps в весомом соотношении 1:10, т.е. не в форме твердой дисперсии аморфного кладрибина. Образец d) - это твердая дисперсия кладрибин-linecaps в весомом соотношении 1:10 в воде/ изопропаноле, как описано выше.
Результаты рентгеновской дифракции образца b) и образца d) показывают, что изолированная твердая дисперсия полностью аморфна. Тех же результатов удалось добиться при применении вакуумного выпаривания или высушивания распылением для высушивания/ удаления растворителя (не показано).
Для сравнения, раствор с) (физическая смесь кладрибина и linecaps) показывает, что соединение кладрибин, по меньшей мере, частично в кристаллической форме.
Пример 2: Поведение АФИ клодрибина и твердой дисперсии в буферном растворе HCl при рН 1,4
Влияние твердой дисперсии на стабильность кладрибина проверяли при рН 1,4 и температуре 37°С.
10 мг АФИ кладрибина (контрольный образец) или 10 мг твердой дисперсии кладрибина по настоящему изобретению, например, полученной, как описано в примере 1 выше, растворяли в буферном растворе HCl при рН 1,4. Время, когда твердая дисперсия полностью растворялась, принимали за точку отсчета. Оба образца помещали в автоматический пробозаборник и определяли концентрации кладрибина за период, равный 105 минутам. Как видно из рис. 2, твердая дисперсия кладрибина была значительно более стабильной при рН
1,4 по сравнению с чистым АФИ кладрибином. При выражении через относительное сравнение площадей концентрация твердой дисперсии кладрибина составила примерно на 75% больше, чем концентрация кладрибина через 105 минут. Кривая площади рассчитывалась по формуле трапеций.
Пример 3: Таблетки кладрибина
Таблетки кладрибина получали прямым прессованием. 110,0 г твердой дисперсии кладрибина-linecaps в соотношении 1:10 (55% общего веса) по настоящему изобретению, например, полученной, как описано в примере 1 выше, просеивали и затем смешивали с 78,0 г микрокристаллической целлюлозы (39% общего веса) и 10 г кроскармелезы натрия (5% общего веса), затем добавляли 2 г стеарата магния (1% общего веса).
Полученную порошковую смесь таблетировали в таблетки по 200 мг, содержащие 10 мг кладрибина. Измеренные профили растворения в буферном растворе с рН 4,5 представлены в таблице ниже:
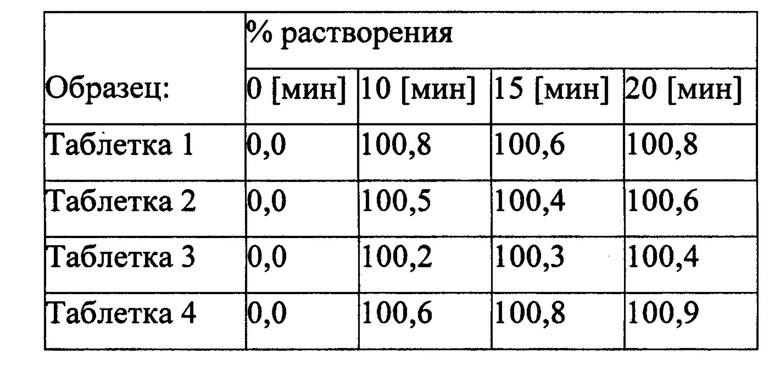
Результаты показывают, что исследованные таблетки растворялись быстро, полное растворение достигнуто через 10 минут, требования к растворению быстро растворяющихся препаратов соблюдены.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ | 2018 |
|
RU2809144C2 |
| ПОРОШКООБРАЗНЫЕ ТВЕРДЫЕ ДИСПЕРСИИ, ВКЛЮЧАЮЩИЕ КВЕРЦЕТИН, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ КОМПОЗИЦИИ | 2018 |
|
RU2772020C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2011 |
|
RU2589842C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1996 |
|
RU2159107C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2005 |
|
RU2373923C2 |
| ЭЛЕКТРОПРЯДЕНЫЕ АМОРФНЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2003 |
|
RU2331411C2 |
| СПОСОБ ПОЛУЧЕНИЯ АМОРФНЫХ КО-ЭВАПОРАТОВ КЛАДРИБИНА С ЦИКЛОДЕКСТРИНАМИ | 2021 |
|
RU2758436C1 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, МАСКИРУЮЩИЕ ВКУС | 2005 |
|
RU2399370C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, ВКЛЮЧАЮЩИЕ КОЛЛОИДНУЮ ДВУОКИСЬ КРЕМНИЯ | 2002 |
|
RU2322970C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ИНГИБИТОРЫ PARP | 2019 |
|
RU2785677C1 |
Группа изобретений относится к фармацевтической композиции кладрибина. Фармацевтическая композиция кладрибина содержит твердую дисперсию аморфного кладрибина и фармацевтического приемлемого водорастворимого носителя, где в качестве фармацевтически приемлемого водорастворимого носителя используется высушенный распылением мальтодекстрин из высокоамилозного гороха и где весовое отношение кладрибина и фармацевтически приемлемого водорастворимого носителя в твердой дисперсии составляет не ниже 1:3. Также раскрыты способ получения композиции и твердая дисперсия аморфного кладрибина и фармацевтически приемлемого водорастворимого носителя. Группа изобретений обеспечивает высокую стабильность при низком значении рН и высокую биодоступность кладрибина. 3 н. и 10 з.п. ф-лы, 2 ил., 1 табл., 3 пр.
1. Фармацевтическая композиция кладрибина, содержащая твердую дисперсию аморфного кладрибина и фармацевтически приемлемого водорастворимого носителя, где в качестве фармацевтически приемлемого водорастворимого носителя используется высушенный распылением мальтодекстрин из высокоамилозного гороха и где весовое отношение кладрибина и фармацевтически приемлемого водорастворимого носителя в твердой дисперсии составляет не ниже 1:3.
2. Фармацевтическая композиция кладрибина по п. 1, где весовое отношение кладрибина и фармацевтически приемлемого водорастворимого носителя в твердой дисперсии составляет не более 1:4.
3. Фармацевтическая композиция кладрибина по п. 1, где весовое отношение кладрибина и фармацевтически приемлемого водорастворимого носителя составляет от 1:3 до 1:20, лучше от 1:4 до 1:15, оптимальнее от 1:5 до 1:15 и лучше всего от 1:5 до 1:10.
4. Фармацевтическая композиция кладрибина по любому из пп. 1-3, где твердая дисперсия содержит остаточный растворитель в количестве не более 10% от веса твердой дисперсии, предпочтительнее не более 9%, лучше не более 7%, еще лучше не более 5%, но оптимальнее всего не более 2%.
5. Фармацевтическая композиция кладрибина по любому из пп. 1-4, содержащая также один или несколько фармацевтически приемлемых наполнителей.
6. Фармацевтическая композиция кладрибина по любому из пп. 1-5, выполненная в форме таблетки или капсулы.
7. Фармацевтическая композиция кладрибина по любому из пп. 1-6 для перорального и/или парентерального введения.
8. Способ получения композиции по п. 1, протекающий в два этапа:
- приготовление водно-спиртового раствора, содержащего кладрибин и фармацевтически приемлемый водорастворимый носитель в растворителе или смеси растворителей, и
- удаление растворителя из раствора вакуумным выпариванием, высушиванием распылением или сублимационной сушкой,
где в качестве фармацевтически приемлемого водорастворимого носителя используется высушенный распылением мальтодекстрин из высокоамилозного гороха и где весовое отношение кладрибина и фармацевтически приемлемого водорастворимого носителя в твердой дисперсии составляет не ниже 1:3.
9. Способ по п. 8, где кладрибин имеет кристаллическую, полиморфную или аморфную форму и растворяется в растворителе или смеси растворителей для получения раствора.
10. Способ по пп. 8, 9, где раствор готовится с использованием не менее одного растворителя: вода и спирт С1-С4, предпочтительно вода, этанол, метанол и изопропанол и их смеси, предпочтительнее, чтобы растворитель представлял собой смесь воды и этанола или воды и изопропанола.
11. Способ по пп. 8-10, где содержание воды не менее 50%, предпочтительнее не менее 60%, еще лучше не менее 70% (вес./ вес.) от общего количества растворителя.
12. Способ по пп. 8-11, где после удаления растворителя или смеси растворителей из полученного раствора твердое вещество высушивается.
13. Твердая дисперсия аморфного кладрибина и фармацевтически приемлемого водорастворимого носителя, полученная по пп. 8-12.
| US 20110097306 A1, 28.04.2011 | |||
| ФАРМАЦЕВТИЧЕСКАЯ ДОЗИРОВАННАЯ ФОРМА, СОДЕРЖАЩАЯ ПОЛИМЕРНУЮ КОМПОЗИЦИЮ-НОСИТЕЛЬ | 2009 |
|
RU2519679C9 |
| СУПРАМОЛЕКУЛЯРНЫЙ КОМПЛЕКС, ОБЛАДАЮЩИЙ ПРОТИВОВОСПАЛИТЕЛЬНОЙ И АНГИОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2533231C1 |
| СПОСОБ ВОСПРОИЗВЕДЕНИЯ И УСТРОЙСТВО ДЛЯ ИНТЕРАКТИВНОГО РЕЖИМА С ИСПОЛЬЗОВАНИЕМ РАЗМЕЧЕННЫХ ДОКУМЕНТОВ | 2003 |
|
RU2340018C2 |
| US 20030073649 A1, 17.04.2003. | |||
Авторы
Даты
2021-05-21—Публикация
2020-01-29—Подача