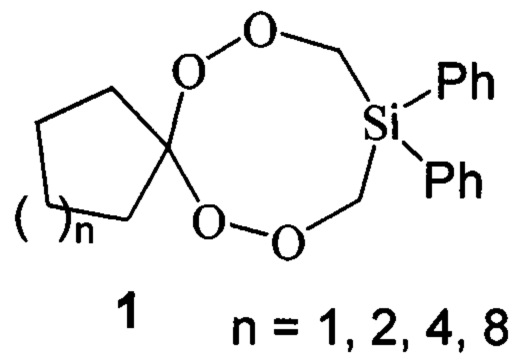
Предлагаемое изобретение относится к области органической химии, конкретно, к дифенилтетраоксасиласпироалканам общей формулы (1) и способу их получения
Кремнийсодержащие органические пероксиды широко применяются при получении полимеров (W. von Hahn, Metzinger L. Makromol. Chem. 1956, 21, 113-119. Semchikov Yu.D., Kopylova N.A., Yablokova N.Y., Nistratova L.N. Eur. Polym. J. 1986, 22, 569. Терман Л.М., Бревнова Т.Н., Сутина О.Д., Семенов В.В., Ганюшкин А.В. Изв. АН СССР. Сер. хим. 1980, 629. Сапожников Д.А., Сахарова А.А., Волкова Т.В., Никулина A.M., Терентьев А.О., Борисов Д.А., Афоничева О.В., Коростылев Е.В., Выгодский Я.С.. Изв. АН. Сер. Физ., 2010, 1081. Копылова Н.А., Кабанова Е.Г., Яблокова Н.В., Семчиков Ю.Д., Пузанкова В.А. Высокомол. соединения. Сер. А, 1981, 31, 301. Фомин В.А., Петрухин И.В. Журн. общ. химии, 1997, 67, 6321), в качестве реагентов гидроксилирования (Taddei М., Ricci A. Synthesis, 1986, 633. Camici L., Dembech P., Ricci A., Seconi G., Taddei M. Tetrahedron, 1988, 44, 4197. Davis F.A., Lai G.S., Wei J. Tetrahedron Lett., 1988, 29, 4269), пероксидирования (Dussault P.H., Lee I.Q., Lee H.-J., Lee R.J., Niu Q.J., Schultz J.A., Zope U.R.. J. Org. Chem., 2000, 65, 8407. Ahmed A., Dussault P.H. Tetrahedron, 2005, 61, 4657. Dai P., Dussault P.H. Org. Lett., 2005, 7, 4333. Dai P., Trullinger Т.К., Liu X., Dussault P.H. J. Org. Chem., 2006, 71, 2283.) и окисления (Camporeale M., Fiorani Т., Troisi L., Adam W., Curci R., Edwards J.O. J. Org. Chem., 1990, 55, 93. Ahmed A., Dussault P.H. Tetrahedron, 2005, 61, 4657).
Известен способ получения 1,2,4,5,7,8-гексаоксасилонанов формулы 4, основанный на реакции диалкилдихлорсиланов 3 с 1,1'-бис(гидроперокси)пероксидами 2 в присутствии оснований (Terent'ev А.О., Platonov М.М., Tursina A.I., Chemyshev V.V., Nikishin G.I. J. Org. Chem., 2008, 73, 3169) по схеме:
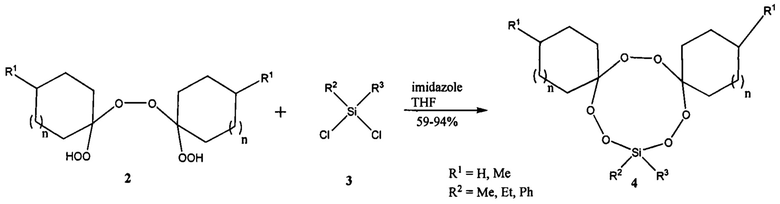
Известным способом не могут быть получены дифенил-тетраоксасиласпироалканы общей формулы (1).
Известен способ получения 9-членных 1,2,7,8-тетраокса-3,6-дисилонанов 7 с выходом до 95% конденсацией 1,2-бис(диметилхлорсилил)этана 6 с гем-бисгидропероксидами 5 в присутствии 2.1 эквивалентов имидазола (Arzumanyan A.V., Novikov R.A., Terent'ev А.О., Platonov M.M., Lakhtin V.G., Arkhipov D.E., Korlyukov A.A., Chernyshev V.V., Fitch A.N., Zdvizhkov A.T., Krylov I.B., Tomilov Y.V., Nikishin G.I. Organometallics 2014, 33, 2230).
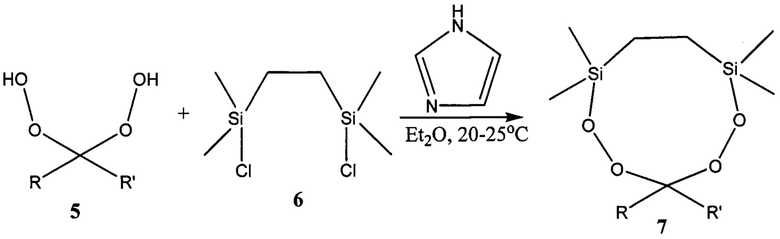
R=R'=циклоалканы
Известным способом не могут быть получены дифенил-тетраоксасиласпироалканы общей формулы (1).
Известен способ получения 12-членных циклических пероксидов 10а-с с выходом 77-90% взаимодействием 1,1'-дигидропероксипероксидов 8а-с с дихлордисиланом 9 в присутствии имидазола (Arzumanyan A.V., Novikov R.A., Terent'ev А.О., Platonov M.M., Lakhtin V.G., Arkhipov D.E., Korlyukov A.A., Chernyshev V.V., Fitch A.N., Zdvizhkov A.T., Krylov LB., Tomilov Y.V., Nikishin G.I. Organometallics 2014, 33, 2230).
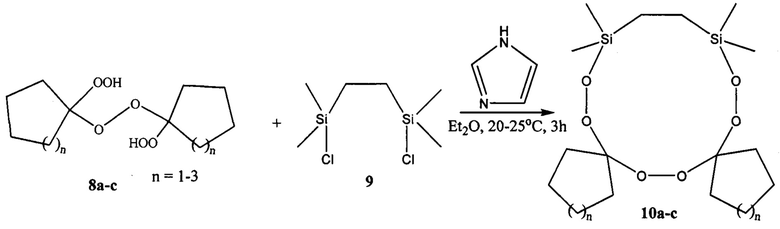
Известным способом не могут быть получены дифенил-тетраоксасиласпироалканы общей формулы (1).
Известен способ получения 18-членных Si-содержащих тетрапероксидов 12 из 1,2-бис(диметилхлорсилил)этена 11 и 1,1-бис(гидроперокси)-4-трет-бутилциклогексана 5с в присутствии имидазола (Arzumanyan A.V., Novikov R.A., Terent'ev А.О., Platonov M.M., Lakhtin V.G., Arkhipov D.E., Korlyukov A.A., Chernyshev V.V., Fitch A.N., Zdvizhkov A.T., Krylov LB., Tomilov Y.V., Nikishin G.I. Organometallics 2014, 33, 2230).
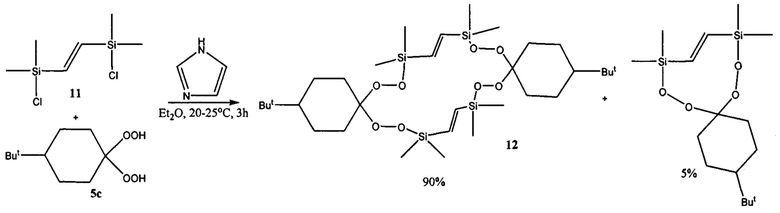
Известным способом не могут быть получены дифенил-тетраоксасиласпироалканы общей формулы (1).
Известен способ получения гексасиланонапероксида 14 (30%) в смеси с тетрасилагексапероксидом 15 (50%) реакцией бис(диметилхлорсилил)-этина 13 с 1,1'-дигидропероксиди(циклогептил)пероксидом 8b в присутствии имидазола (Arzumanyan A.V., Novikov R.A., Terent'ev A.O., Platonov M.M., Lakhtin V.G., Arkhipov D.E., Korlyukov A.A., Chernyshev V.V., Fitch A.N., Zdvizhkov A.T., Krylov I.B., Tomilov Y.V., Nikishin G.L Organometallics 2014, 33, 2230). Пероксиды 14 и 15 малостабильные соединения, самопроизвольно разлагаются за 1-2 суток при хранении в реакционной массе в ЯМР-ампуле даже при температурах ниже 0°С.
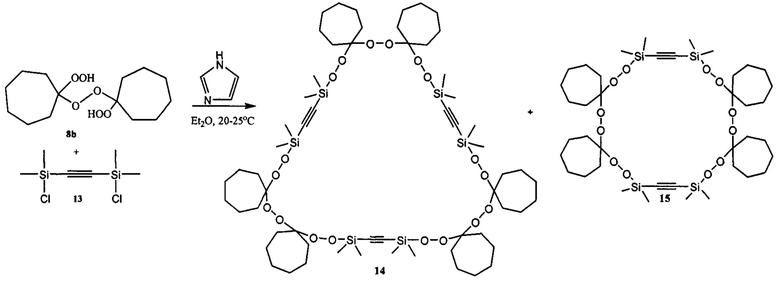
Известным способом не могут быть получены дифенил-тетраоксасиласпироалканы общей формулы (1).
Известен способ получения силамакропероксидов, содержащих два 9-членных циклов, соединенных -СН2-СН2-, -СН=СН- и -С=С-мостиком 20а,b, 21-23 взаимодействием тетрахлордисиланов 16а, 17b, 18, 19 с дигидропероксипероксидами 8а-с в диэтиловом эфире при 20-25°С с использованием имидазола в качестве основания (Arzumanyan A.V., Terent'ev А.О., Novikov R.A., Lakhtin V.G., Chernyshev V.V., Fitch A.N., Nikishin G.L. Eur. J. Org. Chem. 2014, 6877). 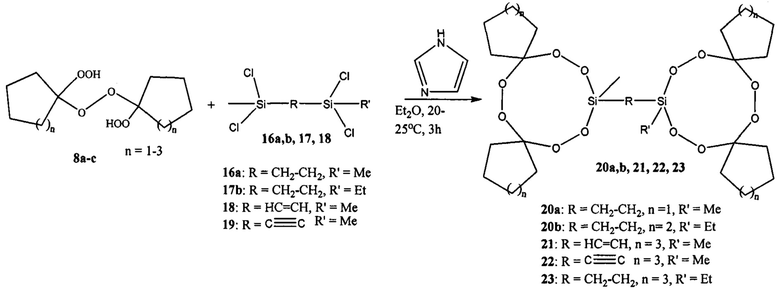
Известным способом не могут быть получены дифенил-тетраоксасиласпироалканы общей формулы (1).
Таким образом, в литературе отсутствуют сведения о способах получения дифенилтетраоксасиласпироалканов формулы (1).
Предлагается новый способ селективного получения дифенил-тетраоксасиласпироалканов общей формулы (1).
Сущность способа заключается во взаимодействии гем-дигидропероксидов (1,1-дигидропероксициклопентан, или 1,1-дигидропероксициклогексан, или 1,1-дигидропероксициклооктан, или 1,1-дигидропероксициклододекан) с бис(метоксиметил)дифенилсиланом в присутствии катализатора La(NО3)3⋅6Н2O, взятых в мольном соотношении гем-дигидропероксид: бис(метоксиметил)дифенилсилан: La(NО3)3⋅6Н2O =10:10:(0.03-0.07), предпочтительно 10:10:0.05, при комнатной температуре (~20°С) и атмосферном давлении в тетрагидрофуране в качестве растворителя в течение 4-6 ч, предпочтительно 5 ч. Выход дифенил-тетраоксасиласпироалканов (1) составляет 76-88%. Реакция проходит по схеме:
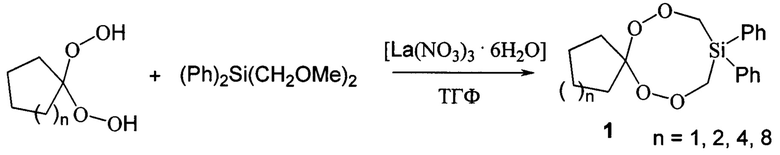
Дифенилтетраоксасиласпироалканы (1) образуются только лишь с участием гам-дигидропероксидов и бис(метоксиметил)дифенилсиланом. В присутствии других Si-содержащих соединений (например, дифенилсилан) целевые продукты (1) не образуются. Без катализатора реакция не идет.
Проведение указанной реакции в присутствии катализатора La(NО3)3⋅6Н2O больше 7 мол. % не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора La(NО3)3⋅6Н2O менее 3 мол. % снижает выход продукта (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при 20°С.При температуре выше 20°С (например, 60°С) снижается селективность реакции и увеличиваются энергозатраты, а при температуре ниже 20°С (например, -10°С) снижается скорость реакции. Опыты проводили в тетрагидрофуране, т.к. в нем хорошо растворяются исходные реагенты.
Существенные отличия предлагаемого способа:
В известном способе реакция конденсации идет с участием в качестве исходных соединений 1,1'-дигидропероксипероксидов с дихлордисиланом в присутсвии 2.1 эквивалента имидазола. Способ не позволяет получать дифенилтетраоксасиласпироалканы общей формулы (1).
В предлагаемом способе в качестве исходных реагентов применяются гем-дигидропероксиды, бис(метоксиметил)дифенилсилан и La(NО3)3⋅6Н2O в каталитических количествах. В отличие от известных предлагаемый способ позволяет получать индивидуальные дифенилтетраоксасиласпироалканы общей формулы (1).
Способ поясняется следующими примерами:
ПРИМЕР 1. Синтез исходного бис(метоксиметил)дифенилсилана (получен по методике: Tacke, Reinhold; Link, Matthias; Bentlage-Felten, Anke; Zilch, Harald. Zeitschrift fuer Naturforschung, Teil B: Anorganische Chemie, Organische Chemie, 1985, 40B(7), 942). В круглодонную колбу, снабженной обратным холодильником помещают 0.7 г (4 ммоль) дифенилсилана, 0.24 г (8 ммоль) параформа и 20 мл СН3ОН кипятят в течение 3 часов до полного растворения параформа. Из реакционной массы выделяют бис(метоксиметил)дифенилсилана с выходом 95%.
ПРИМЕР 2. Синтез исходного 1,1-дигидропероксициклопентана (получен по методике: Terent'ev, А.О.; Platonov, Y.N. Ogobin, G.L Nikishin. Synthetic comm. 2007, 37, 1281-1287). Круглодонную колбу, установленную на магнитной мешалке, помещают 0.35 г (3.57 ммоль) конц. H2SO4 и 9.2 г (95.2 ммоль) 35% р-ра H2O2, добавляют в течение 15 минут 1 г (11.9 ммоль) циклопентанон, перемешивают в течение 2 часов при 20°С.Из реакционной массы выделяют 1,1-дигидропероксициклопентан с выходом 80%. ПРИМЕР 3. В сосуд Шленка, установленный на магнитной мешалке, помещают 5 мл тетрагидрофурана, 1.34 г (10 ммоль) 1,1-дигидропероксициклопентана (Terent'ev, А.О.; Platonov, Y.N. Ogobin, G.I. Nikishin. Synthetic comm. 2007, 37, 1281-1287), 0.02 г (0.05 ммоль) La(NО3)3⋅6Н2O и 2.72 г (10 ммоль) бис(метоксиметил)дифенилсилана (Таске, Reinhold; Link, Matthias; Bentlage-Felten, Anke; Zilch, Harald. Zeitschrift fuer Naturforschung, Teil B: Anorganische Chemie, Organische Chemie, 1985, 40B(7), 942) перемешивают в течение 5 часов при 20°С.Из реакционной массы выделяют 9,9-дифенил-6,7,11,12-тетраокса-9-силаспиро[4.7]додекан с выходом 76%о.
Другие примеры, подтверждающие способ, приведены в табл.1.
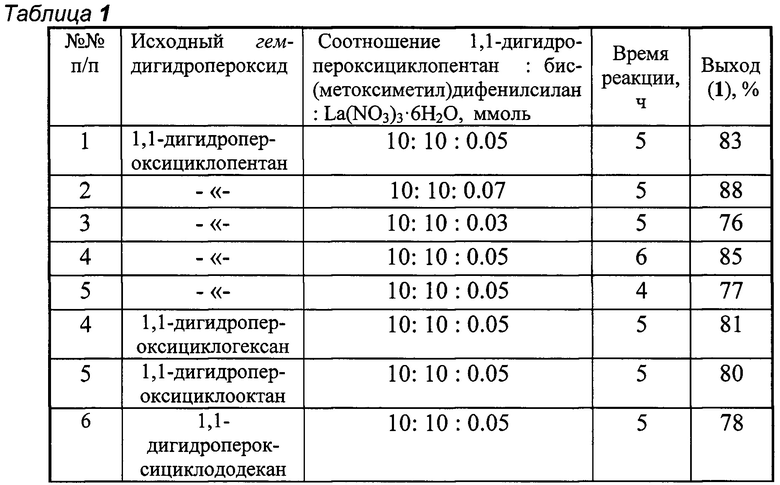
Все опыты проводили в тетрагидрофуране при комнатной температуре (~20°С).
9,9-Дифенил-6,7,11,12-тетраокса-9-силаспиро[4.7]додекан. Б/ц масло; 0.26 г (76%), Rf 0.74 (PE/Et2O=10/1). Спектр ЯМР 1H (CDCl3), δ, м.д.: 1.72-1.79 м (8Н, СН2), 1.98-2.09 м (8Н, СН2), 4.03-4.15 м (4Н, СН2), 7.32-7.47 м (4Н, СН), 7.66-7.75 м (6Н, СН). Спектр ЯМР 13С (CDCl3), δ, м.д.: 24.6, 33.3, 67.7, 106.3, 122.2, 122.5, 127.8, 134.3. MALDI TOF/TOF, m/z: 341 [M-H]+. Найдено, %, С, 66.62; H, 6.46. C19H22O4Si Вычислено, %, С, 66.64; Н, 6.48.
10,10-Дифенил-7,8,12,13-тетраокса-10-силаспиро[5.7]тридекан. Б/ц масло; 0.27 г (77%), Rf 0.76 (PE/Et2O=10/1). Спектр ЯМР 1Н (CDCl3), δ, м.д.: 1.26-1.33 м (6Н, СН2), 1.48-1.70 м (4Н, СН2), 4.00-4.20 м (4Н, СН2), 7.41-7.47 м (4Н, СН), 7.66-7.67 м (6Н, СН). Спектр ЯМР 13С (CDCl3), δ, м.д.: 21.5, 25.6, 30.1, 68.0, 109.9, 128.2, 129.3, 131.5, 135.7. MALDI TOF/TOF, m/z: 355 [М-Н]+. Найдено, %, С, 67.36; Н, 6.77. C20H24O4Si. Вычислено, %, С, 67.38; Н, 6.79.
4,4-Дифенил-1,2,6,7-тетраокса-4-силаспиро[7.7]пентадекан. Б/ц масло; 0.28 г (77%), Rf 0.76 (PE/Et2O=10/1). Спектр ЯМР 1Н (CDCl3), δ, м.д.: 1.40-1.43 м (2Н, СН2), 1.56-1.60 м (4Н, СН2), 1.89-1.94 м (4Н, СН2), 2.44-2.46 м (4Н, СН2), 4.01-4.22 м (4Н, СН2), 7.38-7.47 м (4Н, СН), 7.63-7.65 м (6Н, СН). Спектр ЯМР 13С (CDCl3), δ, м.д.: 24.7, 25.7, 27.2, 61.9, 107.3, 127.9, 129.9, 131.5, 135.7. MALDI TOF/TOF, m/z: 383 [М-Н]+. Найдено, %, С, 68.70; Н, 7.32. C22H28O4Si Вычислено, %, С, 68.72; Н, 7.34.
4,4-Дифенил-1,2,6,7-тетраокса-4-силаспиро[7.11]нонадекан. Б/ц масло; 0.38 г (88%), Rf 0.78 (PE/Et2O=10/1). Спектр ЯМР 1Н (CDCl3), δ, м.д.: 1.28-1.24 м (8Н, СН2), 1.71-1.76 м (8Н, СН2), 2.47-2.49 м (6Н, СН2), 4.04-4.20 м (4Н, СН2), 7.35-7.47 м (4Н, СН), 7.61-7.75 м (6Н, СН). Спектр ЯМР 13С (CDCl3), δ, м.д.: 22.3, 22.6, 24.6, 40.4, 62.0, 106.9, 127.8, 127.9, 130.3, 134.3. MALDI TOF/TOF, m/z: 339 [М-Н]+. Найдено, %, С, 70.85; Н, 8.22. C26H36O4Si. Вычислено, %, С, 70.87; Н, 8.24%.
| название | год | авторы | номер документа |
|---|---|---|---|
| 3,3-ДИАЛКИЛ-7,7-ДИФЕНИЛ-1,2,4,5,7-ТЕТРАОКСАСИЛОКАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2020 |
|
RU2770047C1 |
| ДИФЕНИЛГЕКСАОКСАСИЛАДИСПИРОАЛКАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2020 |
|
RU2750321C1 |
| ДИФЕНИЛТЕТРАОКСАСИЛАДИСПИРОАЛКАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2020 |
|
RU2750288C1 |
| Замещенные трициклические органические монопероксиды и способ их получения | 2020 |
|
RU2752760C1 |
| Способ получения трициклических органических дипероксидов | 2020 |
|
RU2752957C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЦИКЛОАЛКИЛЗАМЕЩЕННЫХ 1, 5, 3-ДИТИАЗЕПАНОВ | 2015 |
|
RU2601313C1 |
| Pt-СОДЕРЖАЩАЯ РЕГЕНЕРИРУЕМАЯ КАТАЛИТИЧЕСКАЯ СИСТЕМА И СПОСОБ ГИДРОСИЛИЛИРОВАНИЯ НЕПРЕДЕЛЬНЫХ СОЕДИНЕНИЙ С ЕЁ ИСПОЛЬЗОВАНИЕМ | 2023 |
|
RU2806031C1 |
| ТРИЦИКЛИЧЕСКИЕ ОРГАНИЧЕСКИЕ МОНОПЕРОКСИДЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2466133C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,7-ДИАЛКИЛ-2,3а,5а,7,8а,10а-ГЕКСААЗАПЕРГИДРОПИРЕНОВ | 2014 |
|
RU2561506C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 2,7-ДИАЛКИЛ-4,9(10)-ДИМЕТИЛ-2,3а,5а,7,8а,10а-ГЕКСААЗАПЕРГИДРОПИРЕНОВ | 2017 |
|
RU2688220C2 |
Изобретение относится к области органической химии. Предложены дифенилтетраоксасиласпироалканы формулы (1) и способ их получения взаимодействием гем-дигидропероксидов с бис(метоксиметил)дифенилсиланом в присутствии катализатора La(NO3)3⋅6Н2О. Технический результат - предложенные дифенилтетраоксасиласпироалканы расширяют ассортимент реагентов гидроксилирования, пероксидирования и окисления при получении полимеров, а предложенный способ получения позволяет получать дифенилтетраоксасиласпироалканы селективно и с хорошим выходом. 2 н.п. ф-лы, 1 табл., 2 пр.
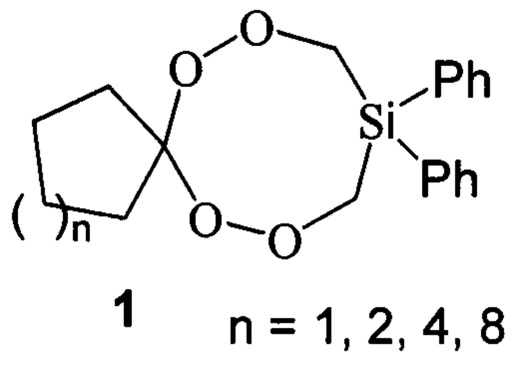
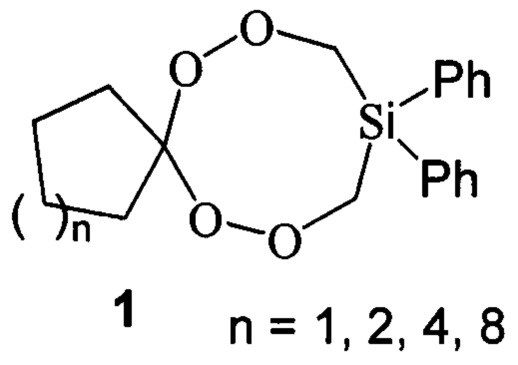
1. Дифенилтетраоксасиласпироалканы общей формулы (1):
2. Способ получения дифенилтетраоксасиласпироалканов (1), отличающийся тем, что гем-дигидропероксиды (1,1-дигидропероксициклопентан, или 1,1-дигидропероксициклогексан, или 1,1-дигидропероксициклооктан, или 1,1-дигидропероксициклодо декан) подвергают взаимодействию с бис(метоксиметил)дифенилсиланом в присутствии катализатора La(NO3)3⋅6Н2О при мольном соотношении гем-дигидропероксид: бис(метоксиметил)дифенилсилан:La(NO3)3⋅6Н2О=10:10:(0.03-0.07) при комнатной температуре (~20°С) и атмосферном давлении в тетрагидрофуране в качестве растворителя в течение 4-6 ч.
| Arzumanyan A.V | |||
| et al | |||
| Six peroxide groups in one molecule - synthesis of nine-membered bicyclic silyl peroxides | |||
| Eur | |||
| J | |||
| Org | |||
| Chem., 2014, vol.31, p.6877 | |||
| Arzumanyan A.V | |||
| et al | |||
| Synthesis of silicon-containing macrocyclic peroxides | |||
| Organometallics, 2014, vol.33, No.9, pp.2230-2246 | |||
| Арзуманян А.В | |||
| Новые классы циклических кремнийорганических |
Авторы
Даты
2021-07-07—Публикация
2020-11-02—Подача