Изобретение относится к медицине, а именно к неонатологии и может быть использовано для прогнозирования развития в раннем неонатальном периоде тяжелой дыхательной недостаточности у новорожденных, родившихся у матерей с преэклампсией.
Актуальность способа обусловлена тем, что по данным ВОЗ непосредственной причиной смерти детей в первые дни жизни в 70-80% случаев являются респираторные нарушения различной этиологии [Геппе Н.А., Волков И.К. Перспективы развития и проблемы детской пульмонологии в России // Пульмонология. - 2007. - №4. - С. 6]. Дыхательная недостаточность (ДН) - клинический синдром ряда заболеваний, в патогенезе которых главная роль принадлежит нарушениям легочного газообмена, при этом возникает неспособность дыхательной системы обеспечивать нормальный газовый состав крови, или поддержание его достигается за счет крайнего напряжения компенсаторных механизмов.
Для оценки тяжести дыхательных расстройств у недоношенных новорожденных используется шкала Сильвермана, для доношенных новорожденных - шкала Даунса. Результат оценивают по сумме баллов: 2-3 балла - легкое расстройство дыхания; 4-6 баллов - расстройство дыхания средней тяжести; более 6 баллов - тяжелое расстройство дыхания [Неонатология: национальное руководство / под ред. Н.Н. Володина. - М.: ГЭОТАР Медиа, 2007. - 848 с.].
Наиболее частыми причинами дыхательной недостаточности у новорожденных в первые дни жизни являются респираторный дистресс-синдром (РДС) и врожденная пневмония. Частота встречаемости РДС зависит от гестационного возраста. У детей, родившихся в сроке гестации до 30 недель частота РДС составляет 60-66%, от 30 до 34 недель - от 10% до 25%, более 34 недель - менее 5%. [Принципы ведения новорожденных с респираторным дистресс-синдромом: методические рекомендации / под ред. Н.Н. Володина. - М.: Российская ассоциация специалистов перинатальной медицины, 2016. - 24 с.]. Среди доношенных новорожденных частота врожденной пневмонии составляет около 1%, среди недоношенных - 10% [Неонатология: национальное руководство. Краткое издание [Электронный ресурс] / под ред. Н.Н. Володина. - М.: ГЭОТАР-Медиа, 2013. - 896 с. https://www.rosmedlib.ru/book/ISBN9785970424438.html].
Наибольший научный интерес к этим нозологическим формам у новорожденных, как РДС, так и врожденной пневмонии, обусловлен их преобладанием в структуре респираторных нарушений, тяжелым клиническим течением, высоким риском развития осложнений, а также значительными экономическими затратами на лечение данных заболеваний.
Известно, что преэклампсия является фактором риска преждевременных родов и развития дыхательных нарушений у новорожденных. Частота респираторных нарушений у новорожденных от женщин с умеренной преэклампсией составляет 40,6%, а у новорожденных от женщин с тяжелой преэклампсией - 71,1% [Состояние здоровья новорожденных, родившихся от матерей с гипертензивными расстройствами при беременности / Н.В. Харламова, Т.В. Чаша, И.А. Панова и др. // Вестник ИвГМА. - 2017. - Т. 22, №3. - С. 19-23].
Разработка способа прогнозирования тяжелой дыхательной недостаточности у новорожденных детей, родившихся у матерей с преэклампсией, обеспечит персонифицированный подход к ведению данной категории пациентов, а также своевременность начала проведения профилактических и лечебных мероприятий с целью предотвращения формирования данной патологии, что улучшит показатели здоровья и качества жизни детей.
Известен способ прогнозирования посленаркозной дыхательной недостаточности у хирургических больных, заключающийся в том, что на предоперационном осмотре по клинико-неврологическим симптомам выделяют больных с шейным остеохондрозом и дополнительно назначают рентгенологическое исследование шейного отдела позвоночника для определения группы риска с возможными циркуляторными расстройствами в вертебробазилярном бассейне и последующим развитием посленаркозной дыхательной недостаточности, далее проводят лечебно-профилактические мероприятия, включающие дополнительную медикаментозную предоперационную подготовку препаратами, улучшающими мозговой кровоток и ограничение подвижности головы при проведении интубации трахеи во время анестезии [Пат. №2187806 Российская Федерация. Способ прогнозирования посленаркозной дыхательной недостаточности у хирургических больных / Костылев А.Н. // Изобретения. Полезные модели. - 2002. - №23].
Существенным недостатком способа является то, что он разработан для прогноза посленаркозной дыхательной недостаточности у хирургических больных с наличием шейного остеохондроза и не применим у новорожденных, родившихся от матерей с преэклампсией.
Известен способ прогнозирования дыхательной недостаточности у больных бронхиальной астмой, включающий выделение ДНК из лимфоцитов периферической венозной крови, генотипирование методом ПЦР полиморфного локуса rs1837253 гена тимусного стромального лимфопоэтина (TSLP), и при выявлении генотипа СС прогнозируют риск развития дыхательной недостаточности у больных бронхиальной астмой [Пат. №2639122 Российская Федерация. Способ прогнозирования дыхательной недостаточности у больных бронхиальной астмой / Мухаммадиева Г.Ф., Каримов Д.О., Кутлина Т.Г., Валова Я.В., Бакиров А.Б., Шагалина А.У., Идиятуллина Э.Ф. // Изобретения. Полезные модели. - 2017. - №35].
Существенным недостатком способа является то, что он разработан для прогноза дыхательной недостаточности у больных с бронхиальной астмой и не применим у новорожденных, родившихся от матерей с преэклампсией.
Известен способ прогнозирования риска дыхательной недостаточности, почечной недостаточности или тромбопении у пациента, страдающего сепсисом, заключающийся в том, что измеряют концентрацию эндокана в образце крови, полученной от упомянутого септического пациента, и сравнивают с концентрацией эндокана с заданными пороговыми значениями, представляющими концентрации, измеренные в среднем у пациентов, у которых не развилась дыхательная недостаточность. При концентрации более низкой, чем предварительно определенное значение, прогнозируют дыхательную недостаточность через 48-72 часа после поступления больных с сепсисом в отделение интенсивной терапии [Пат. 2589903 Российская Федерация. Способы и наборы для прогнозирования риска дыхательной недостаточности, почечной недостаточности или тромбопении у пациента, страдающего сепсисом, путем измерения уровней эндокана в крови / Лассаль Ф. // Изобретения. Полезные модели. - 2016. - №19].
Существенным недостатком способа является то, что данный способ разработан для прогноза дыхательной недостаточности у больных страдающих сепсисом и не применим у новорожденных, родившихся от матерей с преэклампсией.
Техническим результатом заявляемого способа является прогнозирование тяжелой дыхательной недостаточности у новорожденных, родившихся у матерей с преэклампсией.
Технический результат достигается путем определения в пуповинной крови новорожденного содержания тромбомодулина и при его значении равном 63,2 нг/мл или более прогнозируют развитие тяжелой дыхательной недостаточности в раннем неонатальном периоде.
Способ осуществляется следующим образом.
При рождении ребенка производят забор 1,5 мл пуповинной крови в пробирки с наполнителем цитрат натрия. Кровь центрифугируют в течение 15 минут при скорости 3000 об/мин для получения плазмы крови. Определение содержания тромбомодулина осуществляется иммуноферментным методом на анализаторе «EL-808» (США) реагентами фирмы «Cloud-Clone Corp» (США) согласно методике к набору. Результат выражается в нг/мл. При значении тромбомодулина равном или более 63,2 нг/мл прогнозируют развитие тяжелой дыхательной недостаточности в раннем неонатальном периоде.
Новизна заявляемого способа заключается в том, что впервые предлагается прогнозировать развитие тяжелой дыхательной недостаточности в раннем неонатальном периоде у новорожденных, родившихся у матерей с преэклампсией, по определению в пуповинной крови содержания тромбомодулина.
Тромбомодулин (ТМ) это специфический мембранный белок, он является регулятором гемостатических функций в организме. ТМ связывает тромбин, при этом комплекс тромбин-тромбомодулин активирует антикоагулянтную систему протеина С и тромбин-активируемого ингибитора фибринолиза (TAFI), который замедляет фибринолиз. ТМ в норме практически отсутствует в циркуляции, повышение его уровней в крови свидетельствует о снижении фибринолитической активности и риске развития тромбообразования в организме [Кузник Б.И. Клеточные и молекулярные механизмы регуляции системы гемостаза в норме и при патологии. - Чита, 2010. - 832 с.].
Ранее тромбомодулин использовался в качестве маркера для оценки активности гемостаза и мониторинга антитромботической терапии у пациентов, получающих антикоагулянтные препараты. [Алгоритм диагностики гемостаза и мониторинг антитромботической терапии: методические рекомендации / Л.П. Папаян, О.Г. Головина, А.В. Чечеткин и др. - СПб.: Агентство «ВиТ-принт», 2016. - 20 с.]. Определение тромбомодулина используется для диагностики эндотелиальной дисфункции у новорожденных из группы перинатального риска по развитию гипоксически-ишемических и геморрагических нарушений центральной нервной системы [Роль тромбомодулина в диагностике эндотелиальной дисфункции у новорожденных из группы перинатального риска / А.С. Тородова, Е.А. Лукьянова, С.Б. Бережанская, А.Я. Бабиянц // Журнал фундаментальной медицины и биологии. - 2013. - №4. - С. 48-52], для оценки степени тяжести сепсиса у новорожденных [Нао L., Wang N. Changes in plasma thrombomodulin and D-dimer levels and their clinical significance in neonates with sepsis // Zhongguo Dang Dai Er Ke Za Zhi. - 2013. - Vol. 15, №10. - P. 841-844].
Известно, что при преэклампсии во время беременности у женщины происходит нарушение маточно-плацентарного кровообращения, что приводит к развитию эндотелиальной дисфункции у плода. [Клинико-лабораторная оценка эндотелиальной дисфункции в сосудах пупочного канатика при гестозе / Е.В. Филькина, Л.В. Посисеева, С.Б. Назаров и др. // Регионарное кровообращение и микроциркуляция. - 2009. - Т. 8, №3(31). - С. 73-75].
Мы предполагаем, что при преэклампсии у женщины на фоне развития эндотелиальной дисфункции в сосудах пуповины происходит повышение тромбомодулина, что сопровождается нарушением регуляции гемостатических функций и снижением фибринолиза не только в пуповинной крови, но и в крови плода. Известно, что при снижении фибринолиза у новорожденных происходит отложение фибрин-мономеров в легочной ткани, что приводит к развитию дыхательной недостаточности [Кузьменко Г.Н., Чемоданов В.В., Назаров С.Б. Клиническое значение нарушений регуляции функции эндотелия в развитии респираторного дистресс-синдрома у недоношенных новорожденных // Педиатрия. - 2008. - Т. 87, №1. - С. 22-27].
Отличительные признаки способа: у новорожденных, родившихся у матерей с преэклампсией, определяют содержание тромбомодулина в пуповинной крови, и при его значении равном или более 63,2 нг/мл прогнозируют развитие тяжелой дыхательной недостаточности в раннем неонатальном периоде.
Сущность заявляемого способа поясняется следующими примерами.
Пример 1.
Ребенок П. мужского пола, от 2 беременности, протекавшей на фоне мочекаменной болезни, хронического пиелонефрита, анемии, кольпита, центрального предлежания плаценты, преэклампсии, фетоплацентарной недостаточности, хронической внутриутробной гипоксии плода. В связи с развитием тяжелой преэклампсии проведено досрочное оперативное родоразрешение - кесарево сечение в сроке 30 недель. Антенатальная профилактика респираторного дистресс-синдрома кортикостероидами проведена частично. Масса тела ребенка при рождении 1180 грамм, длина 38 см. Оценка по шкале Апгар 4/6 баллов.
По заявляемому способу в пуповинной крови определено содержание тромбомодулина, которое составило 19,0 нг/мл, что указывает на вероятное отсутствие тяжелой дыхательной недостаточности в раннем неонатальном периоде.
Оценка тяжести дыхательных нарушений по шкале Сильвермана составила 4 балла, что соответствует о средней степени тяжести дыхательной недостаточности. В родильном зале проводились первичные реанимационные мероприятия, вводился препарат сурфактанта, начата неинвазивная искусственная вентиляция легких методом CPAP. Ребенок из родовой переведен в отделение реанимации новорожденных с диагнозом «Умеренная асфиксия, врожденная пневмония, дыхательная недостаточность средней степени тяжести».
При наблюдении за ребенком дыхательная недостаточность в раннем неонатальном периоде не нарастала. Длительность СРАР составила 1 сутки 23 часа, после чего ребенок был переведен на респираторную поддержку в условиях кислородной маски, которая продолжалась в течение 3 суток 10 часов. Признаки тяжелой дыхательной недостаточности отсутствовали на протяжении всего раннего неонатального периода.
Прогноз по заявляемому способу подтвердился.
Пример 2.
Ребенок Г. женского пола, от 3 беременности (в анамнезе 2 медицинских аборта) 1 преждевременных родов в 33 недели. Беременность протекала на фоне анемии, ожирения, кольпита, угрозы прерывания в 1 триместре, преэклампсии, фетоплацентарной недостаточности, хронической внутриутробной гипоксии плода. В связи с развитием тяжелой преэклампсии в 33 недели было проведено экстренное досрочное оперативное родоразрешение - кесарево сечение. Антенатальная профилактика респираторного дистресс-синдрома кортикостероидами не проводилась. Масса тела ребенка при рождении 1370 г, длина 36 см. Оценка по шкале Апгар 4/6 баллов.ъ
По заявляемому способу в пуповинной крови определено содержание тромбомодулина, которое составило 64,9 нг/мл, что указывает на вероятное развитие тяжелой дыхательной недостаточности в раннем неонатальном периоде.
Оценка по шкале Сильвермана при рождении составила - 4 балла, что соответствует средней степени тяжести дыхательной недостаточности. В родильном зале проводились первичные реанимационные мероприятия, эндотрахеально введен препарат сурфактанта, начата неинвазивная искусственная вентиляция легких методом CPAP. Ребенок из родовой переведен в отделение реанимации новорожденных с диагнозом «умеренная асфиксия, респираторный дистресс-синдром, дыхательная недостаточность средней степени тяжести».
При наблюдении за ребенком через 18 часов после рождения отмечалось нарастание дыхательной недостаточности: оценка по шкале Сильвермана составила 6 баллов, что соответствует тяжелой степени дыхательной недостаточности. Ребенку проведена интубация трахеи, начата искусственная вентиляция легких. Длительность искусственной вентиляции легких составила 10 суток 13 часов 55 минут.
Прогноз по заявляемому способу подтвердился.
Пример 3.
Ребенок А. мужского пола от 2 беременности (в анамнезе самопроизвольный выкидыш в 16 недель), 1 преждевременных родов в 33 недели. Беременность протекала на фоне ожирения, хронического пиелонефрита в стадии ремиссии, угрозы прерывания в 1 триместре, фетоплацентарной недостаточности. С 32 недели беременности у женщины развилась умеренная преэклампсия. Роды путем экстренного кесарева сечения в связи с преждевременной отслойкой нормально расположенной плаценты. Антенатальная профилактика респираторного дистресс-синдрома проведена частично. Ребенок родился с массой тела 1920 грамм, длиной тела 45 см. Оценка по шкале Апгар составила 4/6 баллов.
По заявляемому способу в пуповинной крови определено содержание тромбомодулина, которое составило 68,9 нг/мл, что указывает на вероятное развитие тяжелой дыхательной недостаточности в раннем неонатальном периоде.
Оценка тяжести дыхательных нарушений по шкале Сильвермана составила 5 баллов, что соответствует средней степени тяжести дыхательной недостаточности. В родильном зале проводились первичные реанимационные мероприятия, вводился препарат сурфактанта малоинвазивным методом, начата неинвазивная искусственная вентиляция легких методом СРАР. Ребенок из родовой переведен в отделение реанимации новорожденных с диагнозом «Умеренная асфиксия, респираторный дистресс-синдром новорожденного, дыхательная недостаточность средней степени тяжести».
При наблюдении за новорожденным на 5 сутки жизни отмечено нарастание дыхательной недостаточности: оценка по шкале Сильвермана составила 7 баллов, что соответствует тяжелой степени дыхательной недостаточности. Ребенок переведен на искусственную вентиляцию легких через интубационную трубку. Продолжительность искусственной вентиляции легких составила 5 суток.
Прогноз по заявляемому способу подтвердился.
Пример 4.
Ребенок Д., женского пола от I беременности, I своевременных родов в 38 недель, возраст матери 26 лет. Беременность протекала на фоне угрозы прерывания в 1 триместре, острой респираторной инфекции без подъема температуры во 2 триместре, анемии, миопии средней степени, гестационного пиелонефрита, дрожжевого кольпита. В 35 недель у женщины была диагностирована умеренная преэклампсия, в сроке 38 недель было выполнено плановое кесарево сечение. Ребенок родился с массой тела - 2990 грамм, длиной тела - 49 см. Оценка по шкале Апгар 7/8 баллов.
По заявляемому способу в пуповинной крови определено содержание тромбомодулина, которое составило 63,2 нг/мл, что указывает на вероятное развитие тяжелой дыхательной недостаточности в раннем неонатальном периоде.
Оценка тяжести дыхательных нарушений по шкале Даунса составила 0 баллов, что свидетельствует об отсутствии дыхательной недостаточности. Состояние с рождения было расценено как удовлетворительное. Ребенок из родовой переведен в палату новорожденных послеродового отделения с диагнозом «Доношенный новорожденный».
При наблюдении за новорожденным на 2 сутки жизни появились клинические признаки дыхательной недостаточности, которая быстро нарастала: оценка по шкале Даунса составила 6 баллов, что соответствует тяжелой степени дыхательной недостаточности. Ребенок переведен в отделение реанимации и интенсивной терапии с диагнозом «Врожденная пневмония, тяжелая дыхательная недостаточность», где произведена интубация трахеи, начата искусственная вентиляция легких. Продолжительность искусственной вентиляции легких составила 3 суток 22 часа.
Прогноз по заявляемому способу подтвердился.
Пример 5.
Ребенок Д., мужского пола, от I беременности, I преждевременных родов в 36 недель, возраст матери 32 года. Беременность протекала на фоне угрозы прерывания в 1 триместре, анемии, умеренной преэклампсии с 30 недель. В 36 недель в связи с развитием тяжелой преэклампсии было проведено досрочное родоразрешение, выполнена операция кесарево сечение. Масса тела ребенка при рождении 2340 грамм, длина - 43 см. Оценка по шкале Апгар составила 6/7 баллов.
По заявляемому способу в пуповинной крови определено содержание тромбомодулина, которое составило 15,6 нг/мл, что указывает на вероятное отсутствие тяжелой дыхательной недостаточности в раннем неонатальном периоде.
Оценка по шкале Сильвермана составила 2 балла, что соответствует легким дыхательным нарушениям. Ребенок из родовой переведен в отделение новорожденных с диагнозом: «Состояние после умеренной асфиксии. Недоношенность 36 недель».
Через 8 часов после рождения отмечено прогрессирование дыхательных нарушений, оценка по шкале Сильвермана составила 4 балла, что соответствует средней степени дыхательной недостаточности. Ребенок переведен в отделение реанимации и интенсивной терапии с диагнозом «Наблюдение по врожденной пневмонии, дыхательная недостаточность средней степени тяжести», где начата неинвазивная респираторная терапия методом CPAP, которая продолжалась 3 суток. Признаки тяжелой дыхательной недостаточности отсутствовали на протяжении всего раннего неонатального периода.
Прогноз по заявляемому способу подтвердился.
Пример 6.
Ребенок Д., от 3 беременности, 3 своевременных родов в 38 недель, возраст матери 35 лет. Беременность протекала на фоне обострения генитального герпеса в 20 недель, фетоплацентарной недостаточности, задержки роста плода. В 34 недели у женщины была диагностирована умеренная преэклампсия. В сроке 38 недель было выполнено плановое кесарево сечение. Масса тела ребенка при рождении - 2640 грамм, длина тела - 48 см. Оценка по шкале Апгар 8/9 баллов.
По заявляемому способу в пуповинной крови определено содержание тромбомодулина, которое составило 22,2 нг/мл, что указывает на вероятное отсутствие тяжелой дыхательной недостаточности в раннем неонатальном периоде.
Оценка тяжести дыхательных нарушений по шкале Даунса составила 0 баллов, что свидетельствует об отсутствии дыхательной недостаточности. Ребенок из родовой переведен в отделение новорожденных с диагнозом «Доношенный новорожденный».
Признаки тяжелой дыхательной недостаточности отсутствовали на протяжении всего раннего неонатального периода.
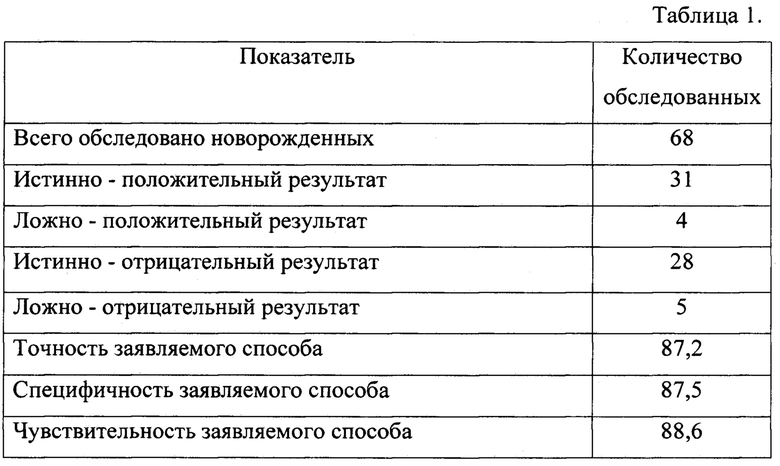
Прогноз по заявляемому способу подтвердился. Результаты исследования представлены в таблице 1.
Преимущества заявляемого способа:
1. Неинвазивность для ребенка.
2. Заявляемый способ прост в выполнении: основывается на определении одного показателя и не требует сложных математических расчетов.
3. Способ быстр в исполнении: продолжительность 2 часа.
4. Способ может использоваться как скрининговый.
5. Способ позволяет прогнозировать развитие тяжелой дыхательной недостаточности как у доношенных, так и у недоношенных новорожденных.
6. Способ обеспечивает персонифицированный подход к ведению пациентов, а также своевременность начала проведения профилактических и лечебных мероприятий.
7. Предлагаемый способ имеет высокую точность - 87,2%, чувствительность 88,6%, специфичность 87,5%.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования дыхательных нарушений у новорожденных, родившихся у матерей с преэклампсией | 2019 |
|
RU2693830C1 |
| Способ прогнозирования внутрижелудочковых кровоизлияний у недоношенных новорожденных, родившихся у матерей с преэклампсией | 2022 |
|
RU2792565C1 |
| Способ прогнозирования развития внутрижелудочковых кровоизлияний у недоношенных новорожденных | 2020 |
|
RU2741727C1 |
| Способ прогнозирования внутрижелудочковых кровоизлияний у недоношенных новорожденных гестационного возраста 28-36,6 недель в раннем неонатальном периоде | 2024 |
|
RU2836096C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ БРОНХОЛЕГОЧНОЙ ДИСПЛАЗИИ У ДЕТЕЙ С ВРОЖДЕННОЙ ПНЕВМОНИЕЙ | 2010 |
|
RU2439569C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ БРОНХОЛЕГОЧНОЙ ДИСПЛАЗИИ ТЯЖЕЛОЙ СТЕПЕНИ У НЕДОНОШЕННЫХ ДЕТЕЙ С ЭКСТРЕМАЛЬНО НИЗКОЙ МАССОЙ ТЕЛА В НЕОНАТАЛЬНОМ ПЕРИОДЕ | 2017 |
|
RU2649830C1 |
| Способ прогнозирования течения респираторного дистресса у новорождённых старше 35 недель гестации | 2023 |
|
RU2830183C1 |
| Способ прогнозирования исходов инфекционно-воспалительной патологии у глубоконедоношенных новорожденных | 2016 |
|
RU2619343C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ БРОНХОЛЕГОЧНОЙ ДИСПЛАЗИИ У НЕДОНОШЕННЫХ ДЕТЕЙ С ЭКСТРЕМАЛЬНО НИЗКОЙ МАССОЙ ТЕЛА ПРИ РОЖДЕНИИ | 2012 |
|
RU2514013C2 |
| Способ прогнозирования течения транзитного тахипноэ новорождённых у доношенных детей | 2021 |
|
RU2766813C1 |
Изобретение относится к медицине, а именно к неонатологии, и может быть использовано для прогнозирования тяжелой дыхательной недостаточности у новорожденных, родившихся у матерей с преэклампсией, путем определения содержания тромбомодулина в пуповинной крови. При его значении, равном или более 63,2 нг/мл, прогнозируют развитие тяжелой дыхательной недостаточности в раннем неонатальном периоде. Способ обеспечивает возможность прогнозирования тяжелой дыхательной недостаточности у новорожденных, родившихся у матерей с преэклампсией, за счет использования неинвазивного метода определения содержания тромбомодулина в пуповинной крови, что обеспечивает персонифицированный подход к ведению новорожденных от матерей с преэклампсией, а также своевременность начала проведения профилактических и лечебных мероприятий с целью предотвращения развития тяжелой дыхательной недостаточности. 1 табл., 6 пр.
Способ прогнозирования тяжелой дыхательной недостаточности у новорожденных, родившихся у матерей с преэклампсией, путем определения содержания тромбомодулина в пуповинной крови, и при его значении, равном или более 63,2 нг/мл, прогнозируют развитие тяжелой дыхательной недостаточности в раннем неонатальном периоде.
| Способ прогнозирования дыхательных нарушений у новорожденных, родившихся у матерей с преэклампсией | 2019 |
|
RU2693830C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НЕОНАТАЛЬНЫХ ПНЕВМОНИЙ | 2017 |
|
RU2663912C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ДЫХАТЕЛЬНЫХ НАРУШЕНИЙ У НОВОРОЖДЕННЫХ ДЕТЕЙ | 1997 |
|
RU2128469C1 |
| Способ прогнозирования пневмонии у новорожденных | 1987 |
|
SU1630790A1 |
| ПОПОВА И.Г | |||
| и др | |||
| Способ прогнозирования тяжелой дыхательной недостаточности у новорожденных, родившихся у матерей с преэклампсией | |||
| Материалы конгресса "XV Международный конгресс по репродуктивной медицине" | |||
| Способ регенерирования сульфо-кислот, употребленных при гидролизе жиров | 1924 |
|
SU2021A1 |
| NAKO | |||
Авторы
Даты
2021-07-12—Публикация
2020-11-09—Подача