Изобретение относится к медицине, в частности к неонатологии, и может быть использовано для прогнозирования течения респираторного дистресса у новорожденных старше 35 недель гестации на этапе родового зала в процессе проведения респираторной терапии методом постоянного положительного давления в дыхательных путях и решения вопроса о госпитализации пациента в отделение реанимации и интенсивной терапии новорожденных (ОРИТН).
Становление адекватного самостоятельного дыхания после рождения является ключевым процессом адаптации ребенка к внеутробной жизни. Этому способствуют ряд механизмов, происходящих в кардиореспираторной системе, а именно: созревание альвеол и сосудов системы легких, выработка достаточного количество сурфактанта, своевременная реадсорбция фетальной жидкости [1,2]. Однако существуют факторы, отрицательно влияющие на послеродовую респираторную адаптацию ребенка. Важнейшими из них являются недоношенность, врожденные инфекции, врожденные пороки развития, а также соматические и акушерские заболевания матери [3,4,5]. Первичная оценка дыхательных нарушений у новорожденных основывается на физикальном осмотре и данных сатурации крови. Дальнейшая дифференциальная диагностика включает в себя комплекс клинических, лабораторных и инструментальных обследований. В родильном зале в момент развития первичных дыхательных нарушении (ДН) или респираторного дистресса, расширенная диагностика состояния ребенка зачастую недоступна, а ограничивается оценкой общего состояния ребенка и уровня ДН с помощью клинических шкал. Симптомы ДН у ребенка с различными патологиями неспецифичны и проявляются тахипноэ с частотой дыхания (ЧД) более 60 в мин, стонущим дыханием, раздуванием крыльев носа, дрожаниемподбородка, втяжением надключичных и подключичных ямок, яремной вырезки, межреберий, грудины и гаррисоновой борозды, асинхронным участием в акте дыхания грудной клетки и живота, гипоксемией с развитием цианоза, а также патологической аускультативной картиной в легких [2,6]. На основании этих данных клиницистами разработаны шкалы оценки ДН, такие как модифицированная шкала Доунс (англ. Dowries, далее шкала Доунс), Сильверман-Андерсон (англ. Silverman-Andersen scale, далее шкала Сильверман), RDOS-Infant (англ. Respiratory Distress Observation Scale-Infant) и др. В свою очередь отечественные клинические рекомендации [7], а также приказ Минздрава России №203н 2017 г. [8] указывают на необходимость оценки ДН при синдроме дыхательных расстройств у новорожденных по шкале Сильверман (для недоношенных) или шкале Доунс для доношенных. Использование перечисленных методов диагностики могут помочь добиться большей стандартизации клинических стратегии в определении степени ДН, необходимой респираторной терапии и выбора отделения госпитализации ребенка.
Актуальность определяется тем, что ДН после рождения являются главной причиной необходимости оказания реанимационных мероприятий и перевода в ОРИТН [9].
Известен способ прогнозирования риска возникновения дыхательных расстройств и их осложнений у новорожденных [10]. Основные положения диссертации касаются непосредственно респираторного дистресс-синдрома новорожденных РДСН:
Прогнозировать развитие РДСН с точностью 100% можно при одновременном наличии у пациента не менее 6 любых из 12 возможных признаков: потребности в респираторной терапии с первых минут рождения; острых воспалительных заболеваний беременной; первой или второй беременности; первых родов от первой беременности; оценки по шкале Апгар на 5-й минуте от 2 до 4 баллов; массы при рождении 1015-1387 г; генотипа СТ полиморфного локуса 3953С>Т гена 1Ь-1В\возраста матери до 23 лет илиболее 31 года; генотипа А1А2 или А1А1 УШИ интрона 2 гена 1Ь-1 оценки по шкале Апгар на первой минуте 2-7 баллов, длины тела новорожденного 39.4-42.7 см, наличия мертворождений и смерти новорожденного в анамнезе матери.
Факторами риска респираторного дистресс-синдрома новорожденных являются аллель С полиморфного локуса 1580ОТ гена 8ЕТРВ, аллель О полиморфного локуса 252А>С гена ЬТА. Недостатки способа:
- способ не специфичен и является методом прогноза дыхательных нарушений любого генеза,
- для осуществления прогноза требуется большое количество показателей - 6,
- требуется забор крови для проведения трудоемких и дорогостоящих исследований: определение генотипа,
- большие трудо- и времязатраты на выполнение способа.
Известен способ прогнозирования развития респираторного дистресс -синдрома у недоношенных новорожденных (патент RU 2291445, 2005) путем исследования крови беременной с угрозой преждевременных родов и реализацией риска родов в течение 7 суток, определения концентрации нитритов, малонового диальдегида, с учетом наличия или отсутствия угрозы невынашивания беременности на более ранних сроках и расчетах дискриминантой функции.
Недостатки способа:
- ограниченный контингент пациентов - недоношенные новорожденные,
- требуется забор биологического материала для проведения трудоемких и дорогостоящих исследований,
- большие трудо- и времязатраты на проведение способа.
Известен способ диагностики тяжести респираторного дистресс-синдрома у недоношенных новорожденных (патент RU 2159937, 2000). При исследовании белков плазмы крови определяют содержание протеина С и по значению диагностируют степень тяжести (легкую, среднюю, тяжелую) респираторного дистресс-синдрома.
Недостатки способа: Ограниченный контингент пациентов-недоношенные новорожденные, не позволяет прогнозировать исход заболевания при тяжелом течении респираторного дистресс-синдрома и принять решение о лечении в ОРИТН.
Известен способ прогнозирования дыхательных расстройств у доношенных и недоношенных новорожденных путем определения уровня поверхностно активных фосфолипидов (ПАФХ) в амниотической жидкости [11].
Недостатки способа: точность метода варьирует от 68 до 85%; метод определения ПАФХ трудоемкий и дорогостоящий; в случае преждевременного излития околоплодных вод за пределами родильного дома, забор амниотической жидкости невозможен.
Известен способ прогнозирования течения транзитного тахипноэ новорожденных у доношенных детей (патент RU 2766813, 2021). Для его выполнения при развитии ранних проявлений дыхательной недостаточности проводят оценку тяжести дистресс-синдрома по шкале Доунса в баллах, учитывают оценку по шкале Апгар на 1 и 5 минуте в баллах. Затем по разработанной формуле рассчитывают дискриминантную функцию d. При d<0 прогноз неблагоприятный - велика вероятность госпитализации в ОРИТН, при d>0 прогноз благоприятный. Изобретение позволяет на этапе родового зала прогнозировать течение ТТН и определять отделение для госпитализации новорожденного, что обеспечивает своевременное проведение необходимых лечебных мероприятий, снизив тяжесть течения ТТН и избежать возможные осложнения.
Недостатки способа: необходимость использования дополнительных устройств для расчета формулы - компьютера, планшета, смартфона, а также ограниченный контингент пациентов - только доношенные с диагнозом транзиторное тахипное у новорожденных.
Поставленная задача - разработка способа прогнозирования течения респираторного дистресса у новорожденных старше 35 недель гестации на этапе родового зала с целью своевременной госпитализации в ОРИТН.
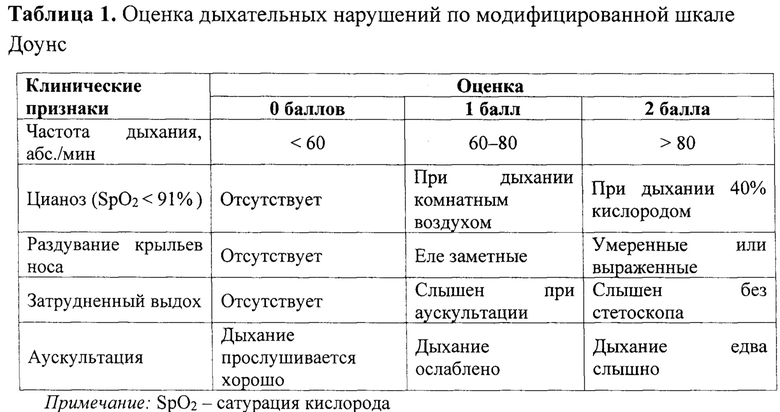
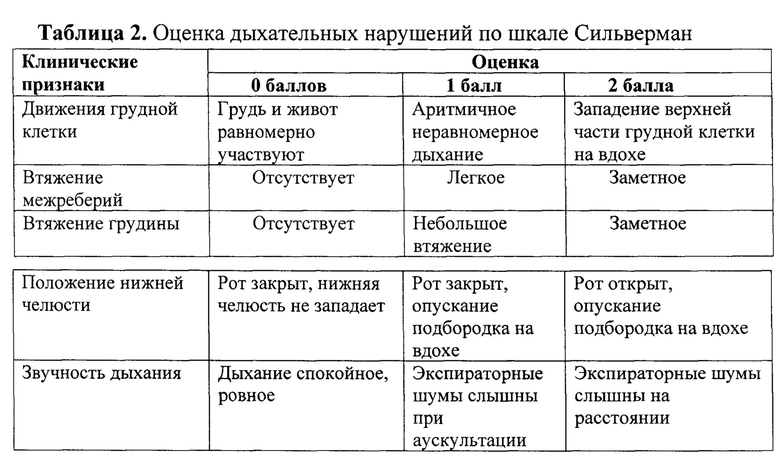
Прогнозирование течения респираторного дистресса у новорожденных старше 35 недель гестации осуществляется в родовом зале, через 20 мин проведения СРАР-терапии. Для этого врач проводит оценку ДН по шкалам Доунс (табл. 1) и Сильверман (табл. 2). Если оценка по шкале Сильверман оказалась 3-4 балла, а оценка по шкале Доунс на 1 балл выше, при этом по шкале Доунс 1 балл установлен за наличие кислородной зависимости, то относительный риск госпитализации в ОРИТН составляет 8,519, 95% ДИ 2,014-36,024, с чувствительностью 0.833 и специфичностью 0.721.
Авторами поведено проспективное одноцентровое когортное исследование. В исследование были включены новорожденные 350 недель гестации и старше с развитием ДН на этапе родового зала. Исследование проводилось на базе Екатеринбургского клинического перинатального центра (ЕКПЦ) с 01.03 по 15.08.2023 г. Критерии включения:
- новорожденные с гестационным возрастом (ГВ)≥35 недель;
- развитие ДН на этапе родового зала в течение 1 часа после рождения с оценкой по шкале Доунс >3 баллов.
Критерии исключения:
- перевод на искусственную вентиляцию легких (ИВЛ) в родовом зале;
- клинически значимые врожденные пороки развития или хромосомные аномалии;
- любое условие, которое, по мнению исследователя, может подвергать ребенка неоправданному риску.
В итоге общую выборку составили 73 ребенка.
СРАР-терапия в клиническом исследовании начиналась с помощью стандартного оборудования родильного зала - Т-образного реанимационного дыхательного контура и лицевой маски с переходом на мононазальный CP АР с помощью эндотрахеальной трубки, введенной в носовой ход до уровня носоглотки.
СРАР-терапию инициировали в родовом зале в первые 60 мин после рождения при оценке ДН по шкале Доунс ≥3 баллов (табл. 1). Стартовые параметры СРАР: Среднее давление в дыхательных путях (англ. MAP - MeanAirway Pressure) устанавливали на уровне 8 см H2O, FiO2 (фракция O2 во вдыхаемой смеси) - 21%. Далее была возможна корректировка FiO2 ступенчато на 10-20% в сторону как увеличения, так и снижения концентрации кислорода для поддержания сатурации крови, измеренной на правой руке, до значений 91-95%. В течение 5 мин после инициации СРАР устанавливали орогастральный зонд, который оставляли открытым.
На 20 мин СРАР проводилась оценка ДН по шкале Доунс:
• при оценке<3 баллов эндотрахеальная трубка извлекалась из носа, и в течение 5 мин исследователь проводил наблюдение за ребенком:
если в течение этого срока оценка ДН оставалась<3 баллов и вместе с тем не было отмечено нарушения функций других органов и систем, ребенок переводился в НО;
если оценка ДН увеличивалась до 3 баллов и выше, исследователь возобновлял проведение СРАР с применением описанных выше параметров MAP и FiO2;
• при сохранении оценки ДН на исходном уровне 3-5 баллов СРАР продолжалась без изменения стартовых параметров;
• при увеличении оценки ДН с 3-4 до 5 и более баллов или с 5 до 6 и более баллов ребенка переводили в ОРИТН на соответствующем состоянию типе респираторной поддержки (СРАР или ИВЛ);
• при сохранении оценки ДН на исходном уровне 6 баллов или ее увеличении ребенок переводился в ОРИТН на соответствующем состоянию типе респираторной поддержке (СРАР или ИВЛ).
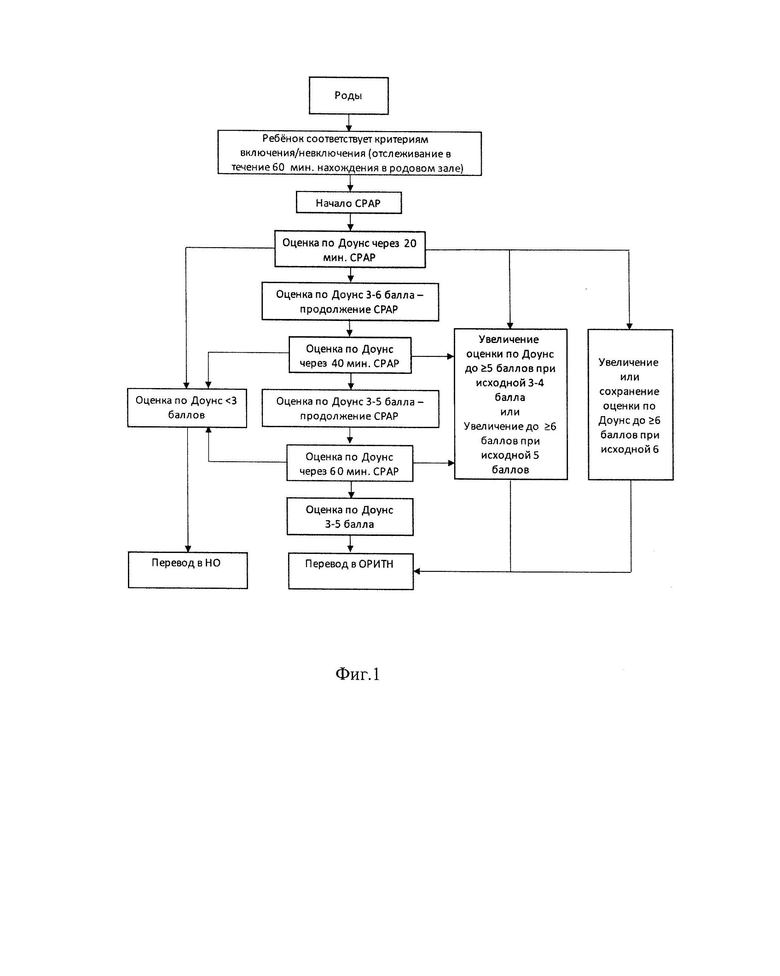
Аналогичные вышеописанным действия проводили также через 40 и 60 мин после начала мононазальной СРАР. На Фиг. 1 показана - Маршрутизация новорожденных в процессе СРАР-терапии в родовом зале по протоколу). Из НО и ОРИТН пациенты могли быть переведены в отделение патологии новорожденных, если они нуждались в дополнительном лечении и наблюдении в связи с неврологической симптоматикой, энтеральной недостаточностью, при сохраняющихся дыхательных нарушениях (нетребующих СРАР) или гипербилирубинемии с необходимостью проведения фототерапии.
Критерии перевода на ИВЛ: изначальная оценка ДН>6 баллов по шкале Доунс; нарастание ДН с 3-5 до>6 баллов на фоне СРАР-терапии; угнетение сознания; судорожный синдром; апноэ без эффекта на тактильную стимуляцию, а также любые другие условия, которые, по мнению специалиста, являются причиной перевода ребенка на ИВЛ.
Одновременно с оценкой ДН у пациента по шкале Доунс на всех этапах, проводилась оценка по шкале Сильверман (табл. 2). Фиксировались в индивидуальной регистрационной карте (ИРК) следующие показатели: фамилия пациента, дата проведения исследования, время начала СРАР с точностью до мин, оценки в баллах по шкале Доунс и Сильверман в процессе проведения СРАР - на 0 мин, 20 мин, и, если СРАР продолжался, то на 40 и 60 мин.
Накопление, корректировка, систематизация исходной информации и визуализация полученных результатов осуществлялись в электронных таблицах Microsoft Office Excel 2016. Статистический анализ проводился с использованием программы BioStat (разработчик - AnalystSoft Inc. США). Количественные показатели оценивались на предмет соответствия нормальному распределению, для этого использовался критерий Шапиро-Уилка (при числе исследуемых менее 50) и критерий Колмогорова-Смирнова (при числе исследуемых более 50). Учитывая, что большинство полученных данных не соответствовало закону нормального распределения, результаты представлены при помощи значений медианы (Me), нижнего и верхнего квартилей (QL; QH). Номинальные данные описывались с указанием абсолютных значений и процентных долей. Для сравнения количественных показателей использовался U-критерий Манна-Уитни для двух независимых выборок. Сравнение номинальных данных проводилось при помощи критерия χ2 Пирсона. За критический уровень значимости принято 2-х стороннее значение р<0,05. С помощью таблиц сопряженности, был рассчитанотносительный риск (OP), 95% доверительный интервал (ДИ), стандартная ошибка ОР, чувствительность и специфичность, а также число больных, которых необходимо лечить (NNT).
Результаты исследования
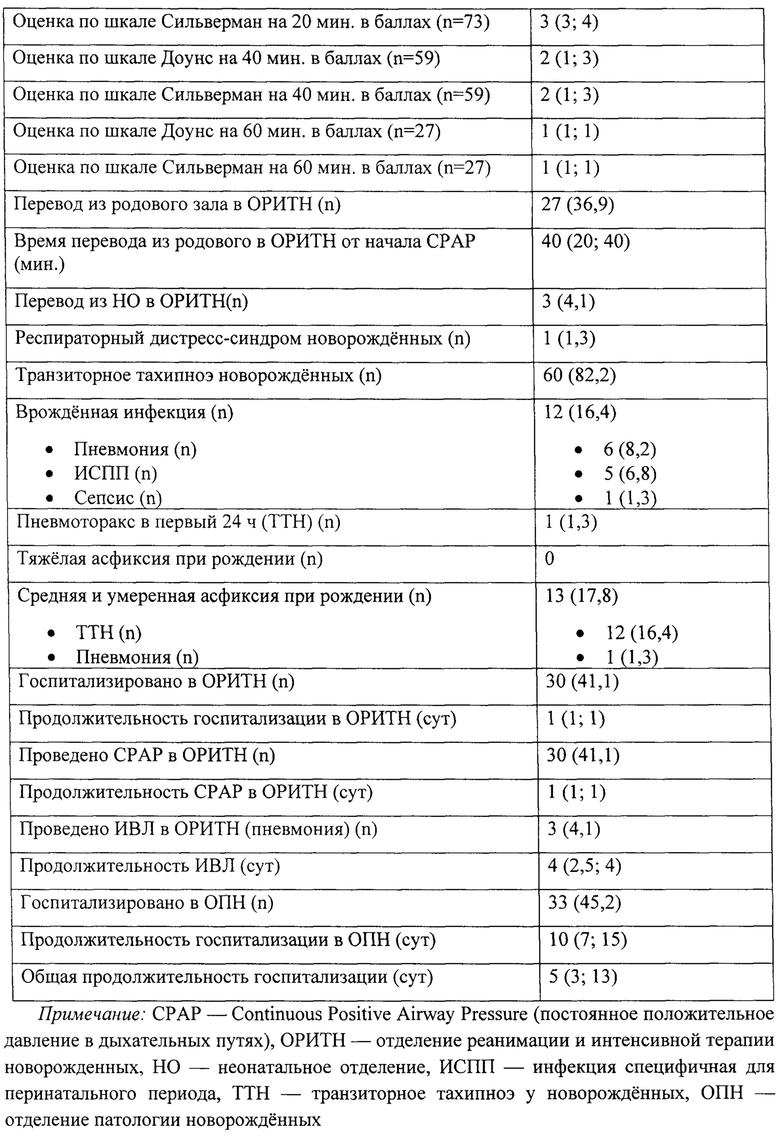
В табл. 3 приведены характеристики общей выборки исследования, которые описывают пол, росто-весовые показатели, ГВ, оценки по шкале Апгар, особенности беременности и родов, время начала СРАР-терапии в родовом зале, оценки ДН по исследуемым шкалам, распределение по нозологиям, а также характеристики респираторной терапии и продолжительность лечения пациентов в отделениях ЕКПЦ. Стоит отметить, что медиана времени перевода в ОРИТН от начала СРАР составила 40 (20; 40 мин).

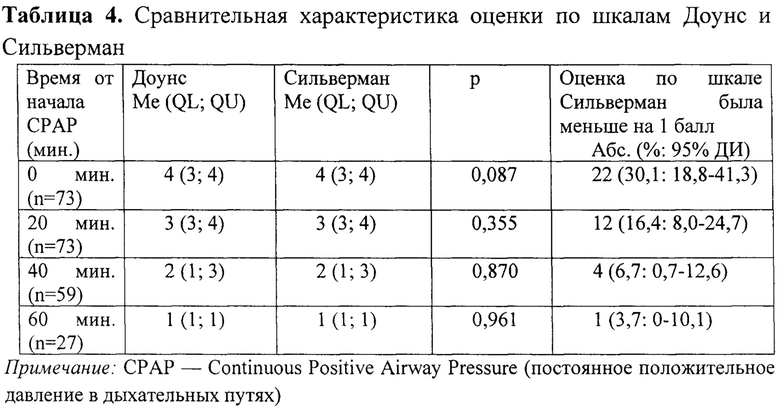
В табл. 4 приведены сравнительные характеристики оценки ДН у пациентов общей выборки по исследуемым шкалам с уровнем значимости. Также в результате анализа полученных данных обнаружено, что оценка по шкале Сильверман отличалась в меньшую сторону на 1 балл у 22 из 73 детей на 0 мин СРАР, 12 детей из 73 на 20 мин СРАР, 4 из 59 на 40 мин СРАР и у 1 ребенка из 27 на 60 мин СРАР. В каждом таком случае по шкале Доунс (табл. 1) наблюдалась кислородная зависимость у ребенка на 1 балл. Статистически значимых различий при сравнении групп не обнаружено.
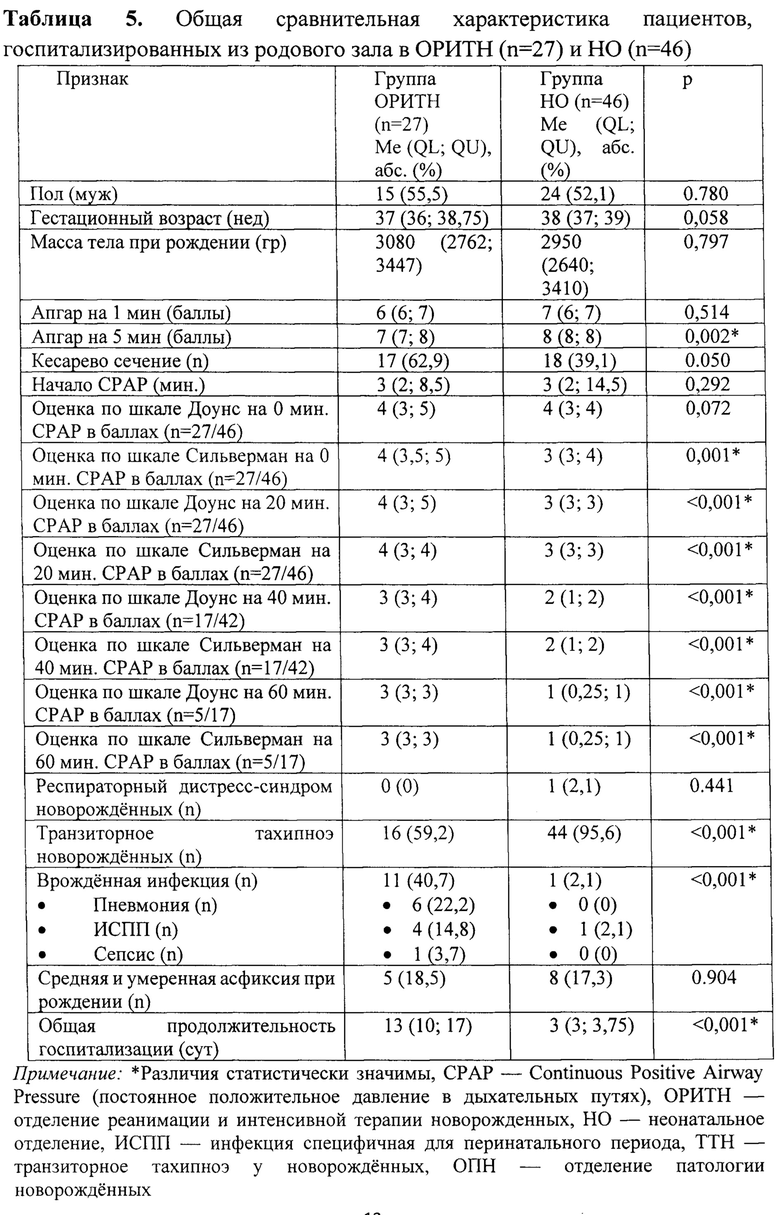
В ходе исследования, общая выборка новорожденных, разделена на 2 группы по принципу перевода в ОРИТН или НО из родового зала. Группу ОРИТН составили 27 детей, а группу НО 46 детей. Между группами проведен сравнительный анализ исходных характеристик, анамнеза родов и нозологий (табл. 5). В группе ОРИТН статистически значимо ниже оказалась оценка по шкале Апгар на 5 мин, а также выше оценки ДН по всем шкалам во всех временных точках измерения кроме 0 мин по шкале Доунс. В группе ОРИТН статистически значимо чаще установлен диагноз врожденной инфекции и реже ТТН в сравнении с группой НО. Продолжительность госпитализации оказалась закономерно статистически значимо выше в группе ОРИТН.
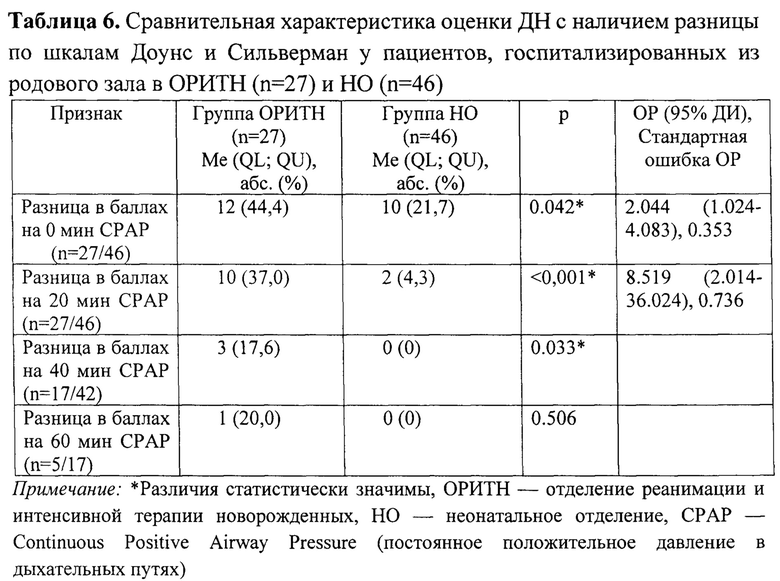
В группах ОРИТН и НО выделены пациенты с наличием разницы в оценке ДН по исследуемым шкалам. Между выделенными показателями проведен сравнительный анализ (табл. 6). Так в группе ОРИТН выявлено статистически значимо большее число пациентов с разницей в оценке по шкалам Доунс и Сильверман на 0 ми. СРАР с чувствительностью 0.545 и специфичностью 0.706 и NNT - 4.404. На 20 мин СРАР также большее число пациентов имело отличие в группе ОРИТН в сравнении с группой НО, с чувствительностью 0.833 и специфичностью 0.721 и NNT - 3.059.
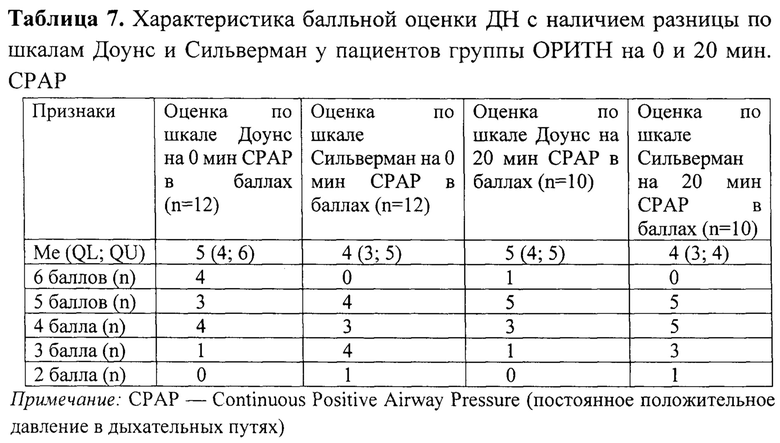
В табл. 7 представлена характеристика балльной оценки ДН с наличием разницы по шкалам Доунс и Сильверман у пациентов группы ОРИТН на 0 и 20 мин.
В ходе исследования выявлено, что при медианной оценке по шкале Сильверман на 20 мин 4 (3;4) балла и при одновременной оценке по шкале Доунс на 1 балл выше и наличие О2 зависимости до 40% относительный риск госпитализации в ОРИТН составляет 8,519, 95% ДИ 2,014-36,024, с чувствительностью 0.833 и специфичностью 0.721.
Сущность заявляемого способа прогноза поясняется следующими примерами.
Пример 1. Пациент А., родился мальчик в сроке гестации 365 недель с весом 2450 г, с оценкой по шкале Апгар на 1 и 5 минуте 6/7 баллов. Адаптировался на груди у матери. Через 4 мин после рождения появилось тахипноэ, стонущее дыхание, втяжение межреберий. Неонатолог поместил ребенка на открытое реанимационное место и провел оценку по шкалам Сильверман (3 балла) и Доунс (3 балла) и инициировал проведение СРАР-терапии. Через 20 мин неонатолог провел повторную оценку по шкалам Сильверман (3 балла) и Доунс (4 балла). Для поддержания сатурации на правой руке ребенку потребовалась увеличение фракции О2 (FiO2) до 30%. При этих показателях относительный риск госпитализации в ОРИТН составляет 8,519. Несмотря на то, что степень дыхательных нарушений умеренная, неонатолог принялрешение о переводе ребенка в ОРИТН с диагнозом ТТН. Своевременное обеспечение оптимальной респираторной терапии методом BinCPAP (биназальный СРАР) в ОРИТН позволило быстро купировать ДН, через 4 часа отлучить ребенка от респираторной терапии, не проводя установку венозного доступа и инфузионной терапии и в возрасте 18 часов жизни перевод в НО для совместного пребывания с матерью. Ребенок выписан домой в удовлетворительном состоянии на 4 сутки жизни. Прогноз по заявляемому способу подтвердился.
Пример 2. Ребенок Б., девочка, родилась в сроке гестации 380 недель, с весом 3410 г и оценкой по шкале Апгар на 1 и 5 минуте 7/8 баллов. Адаптировалась на груди у матери. На 30 мин жизни неонатолог обратил внимание на стонущее дыхание, раздувание крыльев носа и втяжение надключичных ямок. Ребенок перемещен на открытое реанимационное место и проведена оценка ДН по шкалам Сильверман (4 балла) и Доунс (4 балла). Начато проведение СРАР терапии. Через 20 мин неонатолог провел повторную оценку по шкалам Сильверман (4 балла) и Доунс (4 балла) - оценка не изменилась, О2 зависимости не наблюдалось, в таком случае риск перевода в ОРИТН низкий, СРАР-терапия продолжена. На 40 мин терапии проведена повторная оценка ДН по шкалам Сильверман (3 балла) и Доунс (2 балла), СРАР продолжен. На 60 мин терапии оценка ДН по шкалам Доунс и Сильверман оказалась 1 балл. Ребенок отлучен от СРАР-терапии. Учитывая отсутствие нарушения витальных функций, девочка вместе с мамой переведена в НО с диагнозом ТТН и выписана домой на 3 сутки жизни в удовлетворительном состоянии. Прогноз по заявляемому способу подтвердился.
Пример 3. Ребенок В, мальчик в сроке гестации 393 недель с весом 3820 г и оценкой по шкале Апгар на 1 и 5 минуте 6/8 баллов. Сразу после рождения появились ДН оцененные неонатологом по шкалам Сильверман (5 баллов) и Доунс (5 баллов). Начато проведение СРАР терапии. На 20 мин СРАР, степень ДН снизилась с оценкой по шкалам Сильверман (3 баллов) и Доунс (4 баллов), где 1 балл по шкале Доунс установлен за наличие О2 зависимости до 35%. Втаком случае риск госпитализации в ОРИТН крайне велик. Однако неонатолог продолжил проведение СРАР терапии, до 60 мин. Оценка ДН по шкалам Доунс и Сильверман на 20, 40 и 60 мин проведения СРАР не изменилась, ребенок переведен в ОРИТН, где в течение 1 часа наросла О2 зависимость до 60%. Проведена интубация и перевод пациента на ИВЛ с жесткими параметрами. Клинически и по данным ЭХО КГ диагностирована персистирующая легочная гипертензия на фоне течения врожденной пневмонии. Длительность ИВЛ составила 6 суток, а пребывание в ОРИТН - 9 суток. После ОРИТН ребенок переведен в отделение патологии новорожденных и выписан на 17 сутки с установленным диагнозом ишемия головного мозга средней степени тяжести. Прогноз по заявляемому способу подтвердился.
Новизна способа
Прогностическая значимость совместной оценки ДН у новорожденных старше 35 недель гестации по шкалам Доунс и Сильверман выявлена впервые.
Преимущества способа
1. Прогноз осуществляется в кратчайшие сроки при развитии ДН на этапе родового зала - 20 мин.
2. Способ не травматичен для новорожденного.
3. Применяются рекомендованные национальными согласительными документами, валидизирванные и повсеместно используемые шкалы.
4. Предлагаемый способ имеет высокую чувствительность 0.833, и специфичность 0.721.
5. Способ не требует специальной подготовки и может быть выполнен средним медицинским персоналом (например, медицинской сестрой или акушеркой).
6. Прогноз можно осуществить в течение короткого времени - не более 1 мин.
7. Для выполнения прогноза не требуется специальных приспособлений, забора биологического материала и дорогостоящих реактивов.
Таким образом, предлагаемый способ уже через 20 мин проведения СРАР-терапии на этапе родового зала позволяет прогнозировать течения респираторного дистресса при различных патологиях, своевременно принимать решение об эффективности проводимой терапии и переводе ребенка в ОРИТН или продолжении СРАР, избрать тем самым адекватную тактику лечения и снизить тяжесть течения респираторного дистресса.
Предлагаемый способ может быть использован в практике родильных домов и перинатальных центров, с целью прогнозирования течения респираторного дистресса у новорожденных при различных патологиях (респираторный дистресс-синдром, транзиторное тахипное у новорожденного, врожденная инфекция и др.) со сроком гестации 350 и более и решения вопроса о необходимости госпитализации в ОРИТН.
Использованная литература
1. Hooper S.B., Те Pas А.В., Kitchen M.J. Respiratory transition in the newborn: a three-phase process. Arch Dis Child Fetal Neonatal Ed. 2016; 101(3): F266-F271. doi: 10.1136/archdischild-2013-305704.
2. Шестак E.B., Ковтун О.П. Транзиторное тахипноэ новорожденного: патогенез, диагностика и лечение. Вопросы современной педиатрии. 2022; 21(1): 11-18. https://doi.org/10.15690/vsp.v21 i 1.2381.
3. Berazategui J.P., Aguilar A., Escobedo M., et al. Risk factors for advanced resuscitation in tenn and near-term infants: a case-control study. Arch Dis Child Fetal Neonatal Ed. 2017; 102(1): F44-F50. doi: 10.1136/archdischild-2015-309525.
4. Santomartino G.A., Blank D.A., Heng A., et al. Perinatal predictors of clinical instability at birth in late-preterm and terra infants. Eur J Pediatr. 2023; 182(3): 987-995. doi: 10.1007/s00431 -022-04684-5.
5. Ковтун О.П., Шестак E.B., Ксенофонтова О.Л. Анализ факторов риска, определяющих тяжесть течения транзиторного тахипноэ новорожденных и позволяющих прогнозировать тактику лечения. Российский вестник перинатологии и педиатрии. 2022; 67(2): 71-75. https://doi.org/10.21508/1027-4065-2022-67-2-71-75.
6. Д.Ю. Овсянников, Н.Н. Володин. Заболевания легких у новорожденных: трудности диагностики, диагностические критерии и последствия. Педиатрияим.Г.Н. Сперанского. 2022; 101 (3): 170-177. - DOI: 10.24110/0031-403Х-2022-101-3-170-177.
7. Ведение новорожденных с респираторным дистресс-синдромом. Клинические рекомендации под редакцией Володина Н.Н. 2016. https://raspm.ru/files/0236-rds-br2.pdf.
8. Приказ Министерства здравоохранения Российской Федерации от 10 мая 2017 г. №203н «Об утверждении критериев оценки качества медицинской помощи». [Order of the Ministry of Health of the Russian Federation dated May 10, 2017 No. 203н “Ob utverzhdenii kriteriev otsenki kachestva meditsinskoi pomoshchi”. (In Russ).] Доступно no: http://www.consultant.ru/document/cons doc LAW 216975. Ссылка активна на 28.10.2023.
9. Методическое письмо министерства здравоохранения Российмкой Федерации. Реанимация и стабилизация состояния новорожденных детей в родильном зале. 2020 под редакцией проф. Байбариной Е.Н. [Metodicheskoe pis'mo ministerstva zdravoohranenija Rossijmkoj Federacii. Reanimacija i stabilizacija sostojanija novorozhdjonnyh detej v rodil'nom zale. 2020 pod redakciej prof. Bajbarinoj E.N. (in Russ)].
10. Богданова P.3., Прогнозирование риска возникновения дыхательных расстройств и их осложнений у новорожденных автореф. дис.на соиск. учен, степ, к.м.н., 2011.
11. Ларюшкина P.M. Диагностика и прогнозирование дыхательных расстройств у новорожденных детей: автореф. дис.на соиск. учен. степ, к.м.н.,- Иваново, 1980. 23 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования течения транзитного тахипноэ новорождённых у доношенных детей | 2021 |
|
RU2766813C1 |
| Способ определения тактики ведения пациентов с транзиторным тахипноэ у новорожденных на этапе родового зала | 2022 |
|
RU2791125C1 |
| Способ прогнозирования тяжелой дыхательной недостаточности у новорожденных, родившихся у матерей с преэклампсией | 2020 |
|
RU2751287C1 |
| Способ профилактики и лечения повреждений тканей носа у недоношенных новорождённых при проведении неинвазивной респираторной терапии у пациентов в сроке гестации 22-29 | 2024 |
|
RU2835996C1 |
| Способ прогнозирования дыхательных нарушений у новорожденных, родившихся у матерей с преэклампсией | 2019 |
|
RU2693830C1 |
| Способ прогнозирования кровотечений у недоношенных новорожденных с очень низкой и экстремально низкой массой тела | 2016 |
|
RU2623868C1 |
| Способ оценки тяжести состояния новорожденных | 2024 |
|
RU2841005C1 |
| Способ оценки тяжести состояния новорожденного с органной дисфункцией | 2024 |
|
RU2841466C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДОВ ВРОЖДЕННОЙ ПНЕВМОНИИ У ГЛУБОКОНЕДОНОШЕННЫХ НОВОРОЖДЕННЫХ | 2013 |
|
RU2543343C1 |
| Способ прогнозирования развития внутрижелудочковых кровоизлияний у недоношенных новорожденных | 2020 |
|
RU2741727C1 |
Изобретение относится к медицине, а именно к неонатологии, и может быть использовано для прогнозирования течения респираторного дистресса у новорожденных старше 35 недель гестации. При проведении в родовом зале СРАР-терапии в течение 20 мин проводится совместная оценка дыхательной недостаточности по модифицированным шкалам Доунс и Сильверман. При наличии оценки по Сильверман 3-4 балла и оценке по Доунс на 1 балл выше, а также наличии кислородной зависимости с потребностью в кислороде с FiO2 до 40%, прогнозируют тяжелое течение респираторного дистресса и высокий риск госпитализации в отделение реанимации и интенсивной терапии новорожденных. Способ позволяет прогнозировать течение респираторного дистресса при различных патологиях, своевременно принимать решение об эффективности проводимой терапии и переводе ребенка в отделение реанимации и интенсивной терапии или продолжении СРАР, избрать тем самым адекватную тактику лечения и снизить тяжесть течения респираторного дистресса за счет оценки совокупности наиболее значимых показателей. 1 ил., 7 табл., 3 пр.
Способ прогнозирования течения респираторного дистресса у новорожденных старше 35 недель гестации, отличающийся тем, что на 20 минуте проведения CPAP-терапии проводят совместную оценку дыхательных нарушений по модифицированным шкалам Доунс и Сильверман в соответствии с таблицами 1 и 2, представленными в описании, и если оценка по шкале Сильверман составляет 3-4 балла, а по шкале Доунс на 1 балл выше, а также при наличии кислородной зависимости с потребностью в кислороде с FiO2 до 40%, прогнозируют тяжелое течение респираторного дистресса и высокий риск госпитализации в отделение реанимации и интенсивной терапии новорожденных.
| Способ прогнозирования течения транзитного тахипноэ новорождённых у доношенных детей | 2021 |
|
RU2766813C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДА РЕСПИРАТОРНОГО ДИСТРЕСС-СИНДРОМА У НОВОРОЖДЕННЫХ С ПЕРИНАТАЛЬНЫМ ПОРАЖЕНИЕМ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ | 2006 |
|
RU2308724C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДА РЕСПИРАТОРНОГО ДИСТРЕСС-СИНДРОМА У НОВОРОЖДЕННЫХ, НАХОДЯЩИХСЯ НА ИСКУССТВЕННОЙ ВЕНТИЛЯЦИИ ЛЕГКИХ | 2006 |
|
RU2311645C1 |
| Пружина для батана к ткацкому станку | 1925 |
|
SU2080A1 |
| ПОПОВА И.Г | |||
| и др | |||
| Роль тромбомодулина при развитии дыхательных нарушений у новорожденных, родившихся у матерей с преэклампсией | |||
| Современные проблемы науки и образования | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
| Шкив для канатной передачи | 1920 |
|
SU109A1 |
| PILLAI M.S | |||
| et al | |||
| Clinical Prediction Score for | |||
Авторы
Даты
2024-11-14—Публикация
2023-12-18—Подача