Изобретение относится к области медицины и может быть использовано для профилактики и лечения кожных Т-клеточных лимфом, реакции «трансплантат против хозяина», отторжения при трансплантации аллогенных органов, а также ряда аутоиммунных заболеваний.
Одним из применяемых в настоящее время способов борьбы с вышеперечисленными заболеваниями является экстракорпоральный фотоферез (фотоферез, ЭКФ) - введение в организм реципиента особым образом обработанных мононуклеарных клеток.
Экстракорпоральный фотоферез - многоступенчатая циклическая процедура, в которой мононуклеары, полученные методом афереза периферической крови пациента, после применения фотосенсибилизатора 8-метоксипсоралена (8-МОП) в концентрации 60-400 нг/мкл подвергаются облучению ультрафиолетом А (1-2 Дж/см2) и затем возвращаются пациенту.
Механизм этого воздействия еще до конца не изучен, однако установлено, что ЭКФ инициирует апоптоз мононуклеаров в кровеносной системе реципиента.
Апоптоз - процесс программируемой, индуцируемой самими клетками гибели, который в отличие от некроза является физиологическим процессом утилизации дефектных клеток. Он подразделяется на ранний и поздний. При раннем апоптозе целостность поверхностной мембраны не нарушена, а при позднем - начинается фрагментация поверхностной мембраны. Именно клетки, находящиеся в поздней стадии апоптоза, индуцируют созревание дендритных клеток, превращая их в активные антигенпрезентирующие клетки, взаимодействие Т-клеток с которыми приводит к активации Т-регуляторных лимфоцитов, т.е. вызывают антигенассоциированный иммунный ответ.
Таким образом, для успешного проведения профилактики и лечения, мононуклеарные клетки должны попадать в кровеносную систему реципиента еще живыми и начинать апоптоз уже в ней.
Известен способ профилактики и лечения отторжения почечного трансплантата, включающий проведение экстракорпорального фотофереза путем введения после операции фотосенсибилизатора, выделение концентрата мононуклеарных клеток, разведение его физраствором с последующим ультрафиолетовым облучением полученной суспензии, возвращение ее в кровеносное русло, отличающийся тем, что первый сеанс фотофереза проводят на 3-4 сутки после трансплантации почки, при этом дополнительно сразу после ультрафиолетового облучения проводят замещение физраствора плазмой крови в том же объеме, а затем осуществляют введение в смесь цитокина - гранулоцит-макрофагального колониестимулирующего фактора в дозе 80-120 нг/мл, затем осуществляют инкубацию полученного состава в течение 90-120 минут, замещают плазму с цитокином физраствором в том же объеме с последующим возвращением полученной суспензии в кровеносное русло, на курс 15 сеансов, причем в первые две недели проводят два сеанса в неделю, последующие шесть недель по одному сеансу в неделю, в течение третьего месяца два сеанса, четвертый, пятый и шестой месяц - по одному сеансу в месяц (патент РФ №2508924, опубл. 10.03.2014 г.).
Недостатком известного решения является ограниченная доступность экстракорпорального фотофереза из-за высокой стоимости процедуры, необходимости обучения персонала и наличия специального оборудования, помещений, невозможности длительного хранения и транспортировки полученных мононуклеарных клеток, высокий риск развития осложнений, таких как аллергические реакции и фотосенсибилизация (https://pubmed.ncbi.nlm.nih.gov/33054950/; https://www.mskcc.org/ru/cancer-care/patient-education/frequently-asked-questions-about-photopheresis).
Задачей, на решение которой направлено заявляемое изобретение, является разработка способа индукции антигенассоциированного иммунного ответа, который бы обеспечивал эффект, аналогичный наблюдаемому при проведении ЭКФ, т.е. возможность применения для профилактики и лечения кожных Т-клеточных лимфом, реакции «трансплантат против хозяина», отторжения при трансплантации аллогенных органов, а также ряда аутоиммунных заболеваний, а так же, при необходимости, их длительное хранение и транспортировку.
Поставленная задача решается путем разработки способа индукции антигенассоциированного иммунного ответа в виде введения мононуклеаров, подвергшихся предварительному криоконсервированию, который включает:
1. получение концентрата мононуклеарных клеток, при необходимости, разделение их на дозы в количестве достаточном для проведения полного или части курса профилактики или лечения указанных выше заболеваний;
2. криоконсервирование мононуклеарных клеток в растворе охлажденного полиглюкина, предпочтительно до температуры +2…+6°С, с добавлением криопротектора (10% диметилсульфоксида) и помещение мононуклеарных клеток в холодильное оборудование, обеспечивающее замораживание до минус 70°С, при необходимости длительного хранения и/или транспортировки - дальнейшее помещение замороженных мононуклеаров в жидкий азот;
3. размораживание и согревание до температуры 37°С с применением устройств контроля температуры;
4. введение реципиенту.
Основной технический результат разработки заключается в получении и введении мононуклеарных клеток, которые обеспечивают эффект, аналогичный наблюдаемому при проведении ЭКФ.
Дополнительным техническим результатом представленного изобретения является повышение доступности процедуры за счет длительного хранения и транспортировки клеток с возможностью их дальнейшего клинического использования в любой медицинской организации, что крайне важно в связи с ограниченностью медицинских организаций (в соответствии с приказом Минздрава России №73н, РАН №2 от 20.02.2019 г. «Об утверждении перечня учреждений здравоохранения, осуществляющих забор, заготовку и трансплантацию органов и (или) тканей человека» число организаций, в которых осуществляется забор и заготовку тканей человека, ограничено и обозначенные учреждения распределены на территории РФ неравномерно, в ряде субъектов РФ не представлены).
Также дополнительным техническим результатом представленного изобретения является снижение затрат за счет исключения этапа экстракорпорального фотофереза и возможности разделения полученного продукта на терапевтические дозы, и снижение риска развития осложнений, связанных с процедурами афереза и экстракорпорального фотофереза.
Сущность изобретения пояснена на графических материалах:
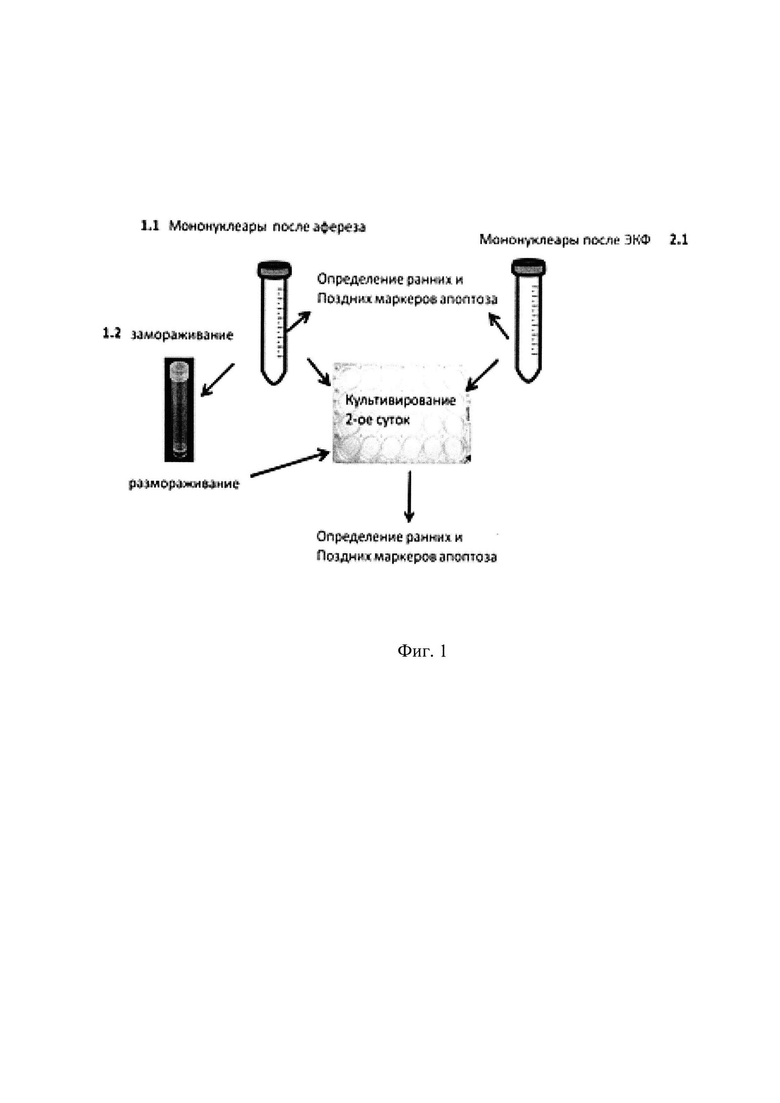
Фиг. 1 - Схема проведения способа;
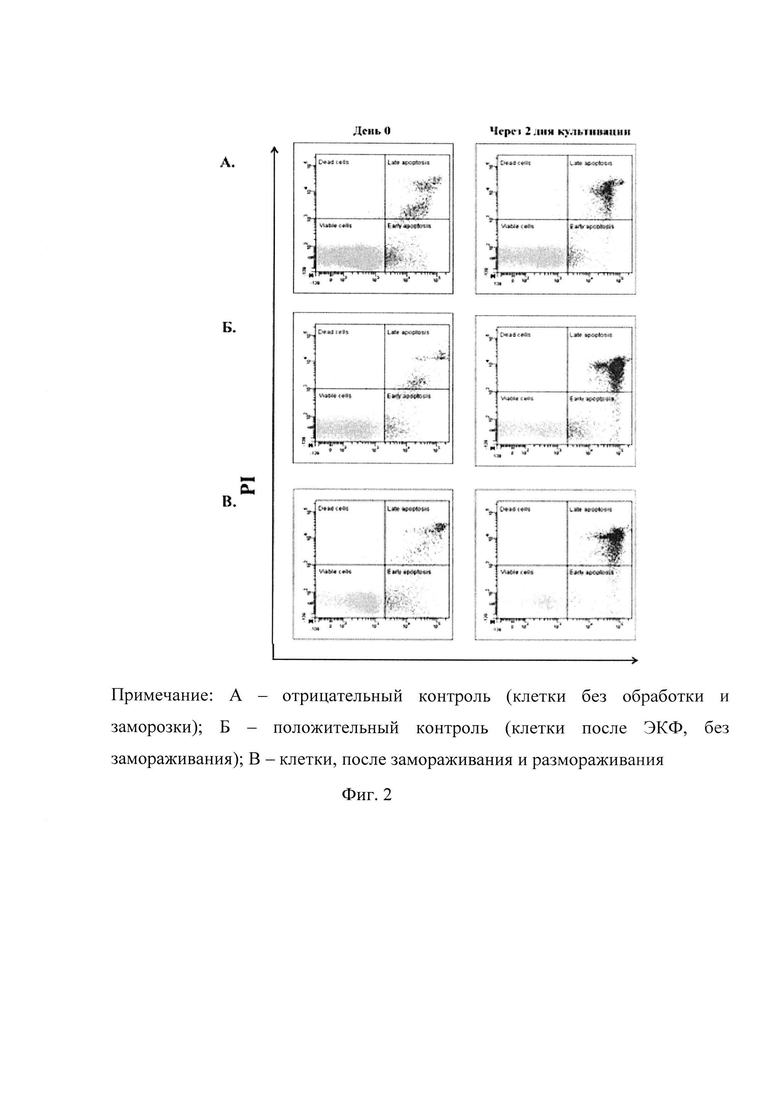
Фиг. 2 - Данные цитометрического анализа апоптоза в лимфоцитах;
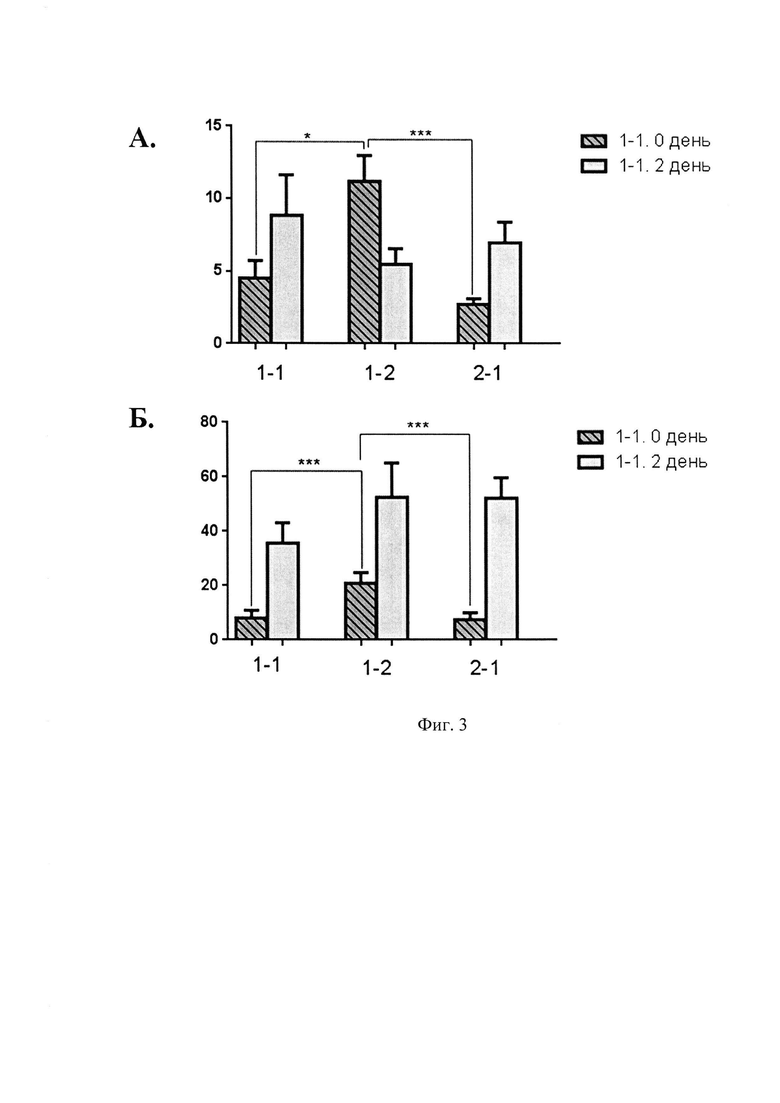
Фиг. 3 - Количество лимфоцитов в ранней (А) и поздней (Б) стадиях апоптоза в исследованных лейкоконцентратах.
Сущность изобретения пояснена экспериментами по разработке способа (схемы представлены на Фиг. 1) и его осуществления, которые не ограничивают объем изобретения.
Было отобрано 20 образцов мононуклеаров, полученных от 12 пациентов (пяти больным аферез мононуклеаров проводили от 2 до 4 раз в разные дни с интервалом более 1 недели). В исследование было включено 5 женщин и 7 мужчин. Возраст от 19 до 68 лет (медиана 35 лет). В качестве основного заболевания у 10 пациентов был острый лейкоз, 2 пациента с лимфомой. 11 больным была выполнена трансплантация аллогенных гемопоэтических клеток (алло-ТГСК) от полностью совместимого донора: 5 больным от родственных доноров и 6 больным - от неродственных доноров; 1 пациентке от гаплоидентичного донора.
Аферез мононуклеаров проводили на клеточном сепараторе SpectraOptia (Terumo ВСТ, Япония/США) в режиме сбора мононуклеаров со следующими параметрами процедуры: соотношение кровь/антикоагулянт - 12:1; настройка сбора (collection preferred) - 40. В результате было обработано от 0,8 до 1,7 от объема циркулирующей крови (ОЦК) (медиана 1,19), медиана времени процедуры - 180 мин (120-250 мин), медиана объема полученного продукта афереза составила 85 мл (60-120 мл).
Образцы для исследования отбирались непосредственно после афереза мононуклеаров (группы 1.1, 1.2), и после ЭКФ (группа 2.1). Образцы 1.1 и 1.2 отбирали из контейнера системы для сбора мононуклеаров (Spectra Optia Collection Set 10110, TerumoBCT, Япония/США) во встроенный в систему контейнер для отбора проб. Затем осуществляли облучение образцов 2.1 на аппарате Macogenic G2 (Macopharma, Франция) согласно рекомендациям производителя: продолжительность облучения составила от 546 до 682 сек (медиана 606 сек) в дозе 2 Дж/см2. После облучения производили отбор образцов из группы 2.1. Часть образцов анализировались сразу (группы 1.1 и 2.1), а часть (группа 1.2) замораживали до температуры минус 70°С в охлажденном до +4…+6°С растворе полиглюкина с добавлением 10% диметилсульфоксида. Размораживание осуществляли при 37°С с применением устройств контроля температуры и отмывали средой RPMI1640 с 10% человеческой инактивированной сывороткой IV группы. После разморозки анализировали образцы группы 1.2.
Часть образцов из каждой группы проанализировали до и после 48-часового культивирования, чтобы проверить изменение уровня апоптоза в динамике.
Поскольку у разных популяций лейкоцитов апоптоз происходит с различной скоростью на протяжении нескольких суток, 5 образцов были прокультивированы для определения динамики изменения уровня раннего и позднего апоптоза с течением времени. Культивирование проводили в среде RPMI1640 с добавлением 10% человеческой инактивированной сыворотки IV группы, 2 мМ глютамина, 100 ед/мл пенициллина и 50 мкг/мл стрептомицина. Клетки рассаживали по 106 на мл в 24-ячеечные планшеты. Мононуклеары культивировали в течение 2-х суток при температуре 37°С и 5% СО2. Счет клеток производился в камере Горяева после окраски генцианвиолетом на 3% уксусной кислоте или 0,5% трипановым синим.
Для оценки апоптоза клеток использовали набор FITC Annexin V Apoptosis Detection Kit I ("BD Biosciences", США), включающий аннексии V FITC и пропидия йодид (PI). Для отделения лейкоцитов использовали анти-CD45 АРС-Су7 моноклональные антитела (клон 2D1). Для окрашивания брали около 0,2×106 клеток, отмывали 1 мл среды RPMI1640 с 10% человеческой инактивированной сывороткой IV группы. Осадок ресуспензировали в 100 мкл аннексин-связывающего буфера и вносили антитела согласно инструкции к набору. Инкубировали 20 минут при комнатной температуре. После этого добавляли к образцу еще 400 мкл аннексин-связывающего буфера и проводили цитометрический анализ с помощью проточного цитофлюориметра BD FACSCanto II ("BD Biosciences", США).
Цитометрический анализ включал в себя выделение лимфоцитов, основываясь на высоком показателе экспрессии антигена CD45 и низких показателях прямого и бокового светорассеяния этих клеток, с последующим определением количества клеток на ранней и поздней стадиях апоптоза. Клетками на ранних стадиях апоптоза считались те, что связывались только с аннексином V, а на поздних стадиях - и с аннексином V, и с PL
Данные определения количества клеток на стадиях раннего и позднего апоптоза представлены на Фиг. 2.
Статистический анализ данных проводили с помощью GraphPad Prism 6. Проверку нормальности распределения выполняли с использованием критерия Шапиро-Уилка. Сравнение полученных данных осуществляли с помощью парного критерия Уилкоксона с поправками на множественное сравнение. Значимыми признавались отличия при р<0,05.
Сравнение доли лимфоцитов в поздней стадии апоптоза между различными группами показало, что до культивирования в лейкоконцентратах подвергшихся замораживанию и размораживанию (группа 1.2) количество клеток было достоверно больше, чем в контрольной группе (образец 1.1) и в группе образцов сразу после ЭКФ (2.1). Доля клеток в ранней стадии апоптоза также была больше в образцах после размораживания (группа 1.2) по сравнению с образцами контрольной группы (1.1) и группы, после ЭКФ (группа 2.1).
После культивирования количество клеток в ранней стадии апоптоза во всех группах достоверно не изменялось, количество же клеток на поздней стадии апоптоза достоверно повышалось во всех группах, кроме контрольной (1.1) (р<0,001), в ней оно не изменялось.
Учитывая данные проведенной работы, можно сказать, что процент лимфоцитов в поздней стадии апоптоза через 2-е суток культивирования сопоставим как при проведении ЭКФ, так и при криоконсервировании лейкоконцентрата без каких-либо иных воздействий.
Таким образом, учитывая отсутствие значимой разницы, обоснованным является проведение сбора мононуклеаров, при необходимости, разделение мононуклеаров на несколько доз и их криоконсервирование с последующим размораживанием и возвратом продукта пациенту.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КРИОКОНСЕРВИРОВАННЫХ МОНОНУКЛЕАРНЫХ КЛЕТОК | 2020 |
|
RU2743816C1 |
| Малообъемный метод экстракорпоральной фотохимиотерапии | 2021 |
|
RU2791659C1 |
| Контейнер для деления на дозы, хранения и клинического использования компонентов крови, клеточных суспензий и жидкостей (варианты) | 2023 |
|
RU2801095C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ОТТОРЖЕНИЯ ПОЧЕЧНОГО ТРАНСПЛАНТАТА | 2013 |
|
RU2508924C1 |
| Способ отмывания криоконсервированных мезенхимальных стромальных клеток | 2024 |
|
RU2829884C1 |
| Т-КЛЕТКИ ЦЕНТРАЛЬНОЙ ПАМЯТИ ПРОТИВ ТРЕТЬЕЙ СТОРОНЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В ТРАНСПЛАНТАЦИИ И ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ | 2009 |
|
RU2506311C2 |
| СПОСОБ КРИОКОНСЕРВИРОВАНИЯ ПУПОВИННОЙ КРОВИ | 2004 |
|
RU2263448C1 |
| МИК-ТЕРАПИЯ ДЛЯ СПЕЦИФИЧЕСКОЙ ИММУНОСУПРЕССИИ ПРИ ТРАНСПЛАНТАЦИИ | 2019 |
|
RU2806545C2 |
| УСТРОЙСТВА И СПОСОБЫ ДЛЯ ОТБОРА КЛЕТОК, УСТОЙЧИВЫХ К АПОПТОТИЧЕСКИМ СИГНАЛАМ, И ОБЛАСТИ ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2630301C2 |
| Способ трансплантации аутологичных гемопоэтических стволовых клеток периферической крови | 2019 |
|
RU2734121C1 |
Изобретение относится к области медицины, может быть использовано для профилактики и лечения кожных Т-клеточных лимфом, реакции «трансплантат против хозяина», отторжения при трансплантации аллогенных органов, а также ряда аутоиммунных заболеваний и касается способа индукции антигенассоциированного иммунного ответа для профилактики или лечения кожных Т-клеточных лимфом, реакции «трансплантат против хозяина», отторжения при трансплантации аллогенных органов. Способ заключается во введении пациенту концентрата мононуклеарных клеток, подвергнутых замораживанию до температуры минус 70°С в растворе охлажденного до температуры 2-6°С полиглюкина с добавлением криопротектора, с последующим размораживанием и согреванием до 37°С с применением устройств контроля температуры. При этом перед замораживанием концентрат мононуклеарных клеток, при необходимости, делят на дозы в количестве, достаточном для проведения полного или части курса профилактики или лечения, с возможностью хранения и транспортировки продукта при температуре минус 196° в сосуде Дьюара. В качестве криопротектора целесообразно использовать 10% диметилсульфоксида. Разработанная методика получения мононуклеарных клеток обеспечивает эффект, аналогичный наблюдаемому при проведении экстракорпорального фотофереза, а также, при необходимости, их длительное хранение и транспортировку. 2 з.п. ф-лы, 3 ил.
1. Способ индукции антигенассоциированного иммунного ответа для профилактики или лечения кожных Т-клеточных лимфом, реакции «трансплантат против хозяина», отторжения при трансплантации аллогенных органов, заключающийся во введении пациенту концентрата мононуклеарных клеток, подвергнутых замораживанию до температуры минус 70°С в растворе охлажденного до температуры 2…6°С полиглюкина с добавлением криопротектора, с последующим размораживанием и согреванием до 37°С с применением устройств контроля температуры.
2. Способ по п. 1, отличающийся тем, что перед замораживанием концентрат мононуклеарных клеток, при необходимости, делят на дозы в количестве, достаточном для проведения полного или части курса профилактики или лечения, с возможностью хранения и транспортировки продукта при температуре минус 196° в сосуде Дьюара.
3. Способ по п. 1, отличающийся тем, что в качестве криопротектора используют 10% диметилсульфоксида.
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ОТТОРЖЕНИЯ ПОЧЕЧНОГО ТРАНСПЛАНТАТА | 2013 |
|
RU2508924C1 |
| МЕТОД ИНДУКЦИИ ИММУННОГО ОТВЕТА ОРГАНИЗМА МЛЕКОПИТАЮЩИХ-2 | 2004 |
|
RU2278704C2 |
| СПОСОБ КОМПЕНСАЦИИ ГЛОБУЛЯРНОГО ОБЪЕМА КРОВИ И ИММУНОМОДУЛИРУЮЩЕГО ВОЗДЕЙСТВИЯ ПРИ ТРАНСПЛАНТАЦИИ | 2011 |
|
RU2452519C1 |
| СПОСОБ ГЕНЕРАЦИИ АНТИГЕН-СПЕЦИФИЧЕСКИХ ЦИТОТОКСИЧЕСКИХ КЛЕТОК С ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2458985C1 |
| СПОСОБ ГЕНЕРАЦИИ АНТИГЕН-СПЕЦИФИЧЕСКИХ ЦИТОТОКСИЧЕСКИХ КЛЕТОК С АКТИВНОСТЬЮ ПРОТИВ КЛЕТОК РАКА ЯИЧНИКА | 2012 |
|
RU2508298C2 |
| WO 2008107370 A1, 12.09.2008 | |||
| WO 2008083174 A2, 10.07.2008 | |||
| WO 2006081576 A2, 03.08.2006 | |||
| КУЛИКОВА Е | |||
| В | |||
| ИНДУКЦИЯ ПРОТИВООПУХОЛЕВОГО ИММУННОГО ОТВЕТА IN VITRO ДЕНДРИТНЫМИ КЛЕТКАМИ, ТРАНСФИЦИРОВАННЫМИ | |||
Авторы
Даты
2021-08-11—Публикация
2021-02-10—Подача