Изобретение относится к медицине и предназначено для оценки эффективности лечения и его оптимизации ингибитором тирозинкиназ первого поколения - иматинибом, больных с локализованными и генерализованными формами ГИСО.
Гастроинтестинальные стромальные опухоли (ГИСО; gastrointestinal stromal tumor- GIST) - наиболее распространенные опухоли желудочно-кишечного тракта (ЖКТ) мезенхимального происхождения, на долю которых приходится 80% от сарком и 0,1-3% от всех злокачественных новообразований этой локализации.
Открытие основного патогенетического механизма, ответственного за развитие ГИСО, - гиперактивация-KIT рецептора, а также результаты предклинических исследований послужили основанием для оценки эффективности препарата STI-571 (иматиниба мезилат, Гливек) при данном заболевании. Иматиниб является низкомолекулярным ингибитором ряда рецепторных (с- KIT, PDGFRA) и нерецепторных тирозинкиназ (Abl, Bcr- Abl).
Несмотря на то, что первичная резистентность к иматинибу или его непереносимость встречаются лишь у 15% больных ГИСО, поддержание эффективности продолжительной терапии иматинибом остается сложной задачей.
Известны способы определения эффективности терапии иматинибом, на основании данных исследования крови пациента с выявлением абсолютного числа нейтрофилов и тромбоцитов; или определения значения билирубина и печеночных трансминаз (АЛТ, ACT), по которым осуществляют корректировку назначаемой суточной дозы иматиниба и определяют эффективность проводимого лечения и его корректировку (Клинические рекомендации. Гастроинтестинальные стромальные опухоли. 2018. С. 19. http://www.oncology.ru/association/clinical-guidelines/2018/giso_pr2018.pdf).
Недостатками вышепредставленных методик является то, что определение трансаминаз и печеночных проб выступает в этой ситуации как показатель определения побочных явлений при использование иматиниба и не обладают точностью в определении эффективности лечения препаратом. Рассматривая значимость показателей абсолютного числа тромбоцитов и нейтрофилов также свидетельствуют о степени токсичности, но не об определении истинной эффективности препарата, что не позволяет выбрать его адекватную коррекцию для эффективного лечения.
Известен способ лечения стромальных опухолей желудочно-кишечного тракта, который представлен в патенте РФ 2537223 (МПК А61К 31/506, публ. 2014), включающий введение заранее установленного фиксированного количества иматиниба мезилата в суточной дозе от 400 до 800 мг, отбор образца крови после проведения первых 30 суток лечения, определение минимального уровня иматиниба в плазме крови
Недостатком этого способа является то, что в связи с очень высоким заданным диапазоном концентраций иматиниба невозможна точная оценка эффективности терапии, что не позволяет корректно индивидуализировать лечение.
Наиболее близким является способ оптимизации лечения стромальных опухолей желудочно-кишечного тракта, включающий введение заранее установленного фиксированного количества иматиниба мезилата в суточной дозе 400 мг, отбор образца крови после проведения первых 30 суток лечения, определение минимального уровня иматиниба в плазме крови методом высокоэффективной жидкостной хроматографии и тандемной масс- спектрометрии, выявление значений при которых нужна корректировка дозы иматиниба мезилата, повторное контрольное определение концентрации препарата в сыворотке крови через 30 дней после корректировки (С.Т. Адлейба и др. «Клинический опыт эффективного использования таргетной терапии у пациентов с диссеминированной формой гастроинтестинальной стромальной опухоли». Сибирский онкологический ж-л, 2019, т. 18, №3, с. 109-113).
Недостатком этого способ является то, что его применение рассматривается только при определенных значениях концентрации иматиниба, не выявлены те значения концентрации в сыворотке крови, которые требуют корректировки дозы препарата, что не позволяет расширить возможность применения данного способа у большой группы пациентов с данным заболеванием.
Задача предлагаемого изобретения - устранение указанных недостатков, повышение эффективности терапии иматинибом, индивидуализация лечения за счет определения концентрации препарата в плазме крови больных.
Для решения поставленной задачи, при оптимизации лечения стромальных опухолей желудочно-кишечного тракта, включающего введение заранее установленного фиксированного количества иматиниба мезилата в суточной дозе 400 мг, отбор образца крови после проведения первых 30 суток лечения, определение минимального уровня иматиниба в плазме крови методом высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии, выявление значений при которых нужна корректировка дозы иматиниба мезилата, повторное контрольное определение концентрации препарата в сыворотке крови через 30 дней после корректировки, предложено при выявлении уровня иматиниба в пределах 500-899 нг/мл суточную дозу увеличивать на 200 мг. При выявлении уровня иматиниба в значении ниже 500 нг/ мл суточную дозу увеличивают на 400 мг, а при выявлении уровня иматиниба выше 1500 нг/мл суточную дозу уменьшают на 200 мг. При выявлении уровня иматиниба в пределах 900-1500 нг/мл лечение предлагается продолжать в прежней суточной дозе.
Благодаря данному методу возможно своевременно выявить снижение концентрации иматиниба в плазме крови больных и провести коррекцию суточной дозы препарата для улучшения результатов лечения.
Способ осуществляется следующим образом.
Стандартной дозировкой иматиниба для лечения больных ГИСО считается 400 мг сутки перорально. Все пациенты первоначально получали стандартную суточную дозу иматиниба, далее через 30 дней от начала приема данного препарата осуществлялся забор венозной крови пациентов в объеме не менее 5 мл для определения концентрации препарата методом высокоэффективной жидкостной хроматографии с детекцией метода тандемной масс- спектрометрии.
(https://e.mail.ru/attach/15946315100713169937/0%3В1/?folder-id=0&x-email=bruvs%40mail.ru)
После получения данных о концентрации препарата проводилась коррекция суточной дозы иматиниба.
При выявлении уровня иматиниба в пределах 900-1500 нг/мл лечение продолжалось в прежней суточной дозе - 400 мг с последующим динамическим контролем, в соответствии со стандартными клиническими рекомендациями, каждые 3 месяца, повторные определения концентрации препарата производились в случае подтвержденного прогрессирования по данным объективного обследования.
При выявлении уровня иматиниба в значении ниже 500 нг/ мл суточную дозу увеличивают на 400 мг с контролем уровня иматиниба через 30 суток. Если не достигался уровень иматиниба 900-1500 нг/мл, то повторно изменялась предлагаемая дозировка в соответствии с данным способом. При достижении уровня иматиниба 900-1500 нг/мл лечение продолжалось в измененной суточной дозе с последующим динамическим контролем каждые 3 месяца.
При выявлении уровня иматиниба в пределах 500-899 нг/мл суточную дозу увеличивали на 200 мг с контролем уровня иматиниба через 30 суток. При достижении уровня иматиниба 900-1500 нг/мл лечение продолжалось в прежней суточной дозе - 600 мг с последующим динамическим контролем каждые 3 месяца.
При выявлении уровня иматиниба выше 1500 нг/мл суточную дозу уменьшали на 200 мг, также с контролем уровня иматиниба через 30 суток.
Корректировка суточной дозы обеспечивало адекватную эффективную терапию.
Пример.
Пациентке В., 1941 г.р., с диагнозом гастроинтестинальная стромальная опухоль тонкой кишки, 27.07.2016 была назначена терапия иматинибом в стандартной дозе 400 мг/сутки. Через 30 дней от начала приема препарата была определена первичная концентрация иматиниба по предлагаемому способу и она составила 458 нг/мл (от 25. 08. 2016). В связи с выявлением сниженной концентрации препарата была проведена коррекция лечения и с 07.09.2016 г. доза иматиниба была увеличена до 800 мг/сутки. Через 30 дней было выполнено повторное определение концентрации препарата и она составила 1434 нг/мл, что коррелировало с положительной динамикой опухолевого процесса по данным объективного обследования и может свидетельствовать об эффективности индивидуализации терапии у данной пациентки.
Через 6 месяцев от начала терапии при контрольном КТ-исследовании ОБП от 22.02.2017 г. была выявлена положительная динамика. При следующем контрольном КТ - исследовании от 16.05.2017 г. (через 10 месяцев от начала приема препарата) отмечалась стабилизация и удержание достигнутого в феврале эффекта в печени и костях.
Осуществление данного способа представлено на клинических примерах, которые представлены в Таблице 1.
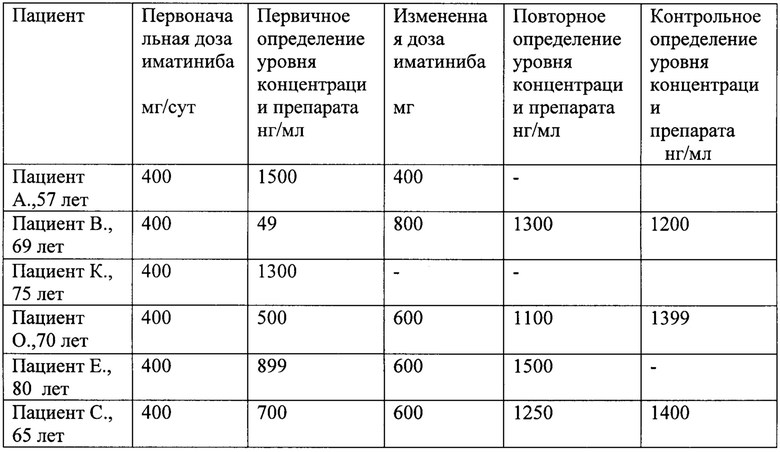
Все пациенты, данные корректировки лечения которых представлены в таблице, после определения эффективности предложенной дозировки иматиниба, длительное время удерживали достигнутый эффект.
По предлагаемому способу был определен уровень иматиниба в плазме крови у 57 больных с морфологически верифицированным диагнозом ГИСО. При определении концентрации иматиниба с помощью данного метода, была подобрана адекватная суточная доза в 92,3% случаев (у 48 пациентов), прогрессирование на подобранной дозе иматиниба с помощью данного метода наблюдалось у 7,7% пациентов (4 пациента).
Применение предлагаемого способа позволяет своевременно изменить суточную дозу иматиниба на основе данных о концентрации препарата в плазме пациентов и повысить эффективность лечения и качество жизни за счет индивидуального подхода к лечению данной группы пациентов. Объективное улучшение коррелировалось с субъективным улучшением качества жизни пациентов: исчезала слабость, уменьшились боли, улучшилось общее состояние пациентов, улучшился аппетит, стали более активные. Благодаря индивидуальной коррекции дозы препарата удается вовремя предупредить развитие нежелательных побочных явлений, что также улучшает качество жизни данных пациентов.
В связи с недоступностью во всех субъектах РФ генно-мутационного анализа, данный способ может использоваться как один из альтернативных путей для оптимизации назначения иматиниба.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПТИМИЗАЦИИ ЛЕЧЕНИЯ ИМАТИНИБОМ ПРОЛИФЕРАТИВНЫХ ЗАБОЛЕВАНИЙ, ОПОСРЕДОВАННЫХ РЕЦЕПТОРОМ ТИРОЗИНКИНАЗЫ KIT | 2009 |
|
RU2537223C2 |
| Способ лечения первичного метастатического рака предстательной железы | 2022 |
|
RU2796395C1 |
| СПОСОБ ОПТИМИЗАЦИИ ЛЕЧЕНИЯ ЛЕЙКОЗА, ПОЛОЖИТЕЛЬНОГО ПО ФИЛАДЕЛЬФИЙСКОЙ ХРОМОСОМЕ, ИНГИБИТОРАМИ Ab1-ТИРОЗИНКИНАЗЫ | 2007 |
|
RU2483732C2 |
| СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ ГОЛОВНОГО МОЗГА | 2015 |
|
RU2578472C1 |
| СПОСОБ ВЫБОРА ТАКТИКИ ЛЕЧЕНИЯ МЕСТНО-РАСПРОСТРАНЕННОГО РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2013 |
|
RU2524309C1 |
| Способ лечения рака предстательной железы | 2019 |
|
RU2731002C1 |
| ПРИМЕНЕНИЕ МИДОСТАУРИНА ДЛЯ ЛЕЧЕНИЯ ЖЕЛУДОЧНО-КИШЕЧНЫХ СТРОМАЛЬНЫХ ОПУХОЛЕЙ | 2005 |
|
RU2410098C2 |
| Способ выбора тактики лечения местно-распространенного рака предстательной железы N0 | 2018 |
|
RU2680015C1 |
| СПОСОБ ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2015 |
|
RU2604409C1 |
| Способ лечения рака прямой кишки | 2018 |
|
RU2691345C1 |
Изобретение относится к медицине и предназначено для оптимизации лечения иматинибом стромальных опухолей желудочно-кишечного тракта. Способ включает введение заранее установленного фиксированного количества иматиниба мезилата в суточной дозе 400 мг. Отбор образца крови после проведения первых 30 суток лечения. Определение минимального уровня иматиниба в плазме крови методом высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии. Выявление значений, при которых нужна корректировка дозы иматиниба мезилата, повторное контрольное определение концентрации препарата в сыворотке крови через 30 дней после корректировки. При выявлении уровня иматиниба в пределах 500-899 нг/мл суточную дозу увеличивают на 200 мг, при выявлении уровня иматиниба в значении ниже 500 нг/ мл суточную дозу увеличивают на 400 мг, при выявлении уровня иматиниба выше 1500 нг/мл суточную дозу уменьшают на 200 мг, а при выявлении уровня иматиниба в пределах 900-1500 нг/мл лечение продолжают в прежней суточной дозе. Изобретение позволяет своевременно изменить суточную дозу иматиниба на основе данных о концентрации препарата в плазме пациентов и повысить эффективность лечения и качество жизни за счет индивидуального подхода к лечению данной группы пациентов. 1 пр., 1 табл.
Способ оптимизации лечения стромальных опухолей желудочно-кишечного тракта, включающий введение заранее установленного фиксированного количества иматиниба мезилата в суточной дозе 400 мг, отбор образца крови после проведения первых 30 суток лечения, определение минимального уровня иматиниба в плазме крови методом высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии, выявление значений, при которых нужна корректировка дозы иматиниба мезилата, повторное контрольное определение концентрации препарата в сыворотке крови через 30 дней после корректировки, отличающийся тем, что при выявлении уровня иматиниба в пределах 500-899 нг/мл суточную дозу увеличивают на 200 мг, при выявлении уровня иматиниба в значении ниже 500 нг/ мл суточную дозу увеличивают на 400 мг, при выявлении уровня иматиниба выше 1500 нг/мл суточную дозу уменьшают на 200 мг, а при выявлении уровня иматиниба в пределах 900-1500 нг/мл лечение продолжают в прежней суточной дозе.
| СПОСОБ ОПТИМИЗАЦИИ ЛЕЧЕНИЯ ИМАТИНИБОМ ПРОЛИФЕРАТИВНЫХ ЗАБОЛЕВАНИЙ, ОПОСРЕДОВАННЫХ РЕЦЕПТОРОМ ТИРОЗИНКИНАЗЫ KIT | 2009 |
|
RU2537223C2 |
| АДЛЕЙБА С.Т | |||
| и др | |||
| КЛИНИЧЕСКИЙ ОПЫТ ЭФФЕКТИВНОГО ИСПОЛЬЗОВАНИЯ ТАРГЕТНОЙ ТЕРАПИИ У ПАЦИЕНТКИ C ДИССЕМИНИРОВАННОЙ ФОРМОЙ ГАСТРОИНТЕСТИНАЛЬНОЙ СТРОМАЛЬНОЙ ОПУХОЛИ / СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ, 2019; 18(3), стр | |||
| Шкив для канатной передачи | 1920 |
|
SU109A1 |
| КОГОНИЯ Л.М | |||
| и др | |||
| Клинический опыт индивидуализации таргетной терапии пациентки с | |||
Авторы
Даты
2021-08-13—Публикация
2020-09-29—Подача