Изобретение относится к медицинской и прикладной микробиологии, при работах с вирусами в целях обеспечения безопасных условий труда и, может быть использовано при гигиенической оценке тканей и нетканых материалов, предназначенных для изготовления средств индивидуальной защиты, а также иной текстильной промышленности.
Предлагаемый способ позволяет в лабораторных условиях оценить в процентном соотношении проницаемость тканей и нетканых материалов вирусными частицами.
При изготовлении средств индивидуальной защиты, предназначенных для работы с вирусами, относящимися к I-IV группам патогенности, важно учитывать высокую степень защиты от проникновения вирусных частиц через используемый материал. Особо важно это при работе в очагах особо опасных инфекций вирусной природы, а также при ликвидации чрезвычайных ситуаций санитарно-эпидемиологического характера, когда риск обсеменения средств индивидуальной защиты и заражения человека очень высок.
Однако, несмотря на большие достижения санитарной вирусологии и профилактической медицины, способов оценки проницаемости тканей и нетканых материалов вирусными частицами в отечественной нормативно-правовой базе отсутствует.
Анализ известных технических решений из уровня техники показал, что на данный момент методик по определению проницаемости тканей и нетканых материалов вирусными частицами не известен.
Известен способ определения проницаемости микроорганизмами тканей и нетканых материалов (ГОСТ 12.4.136-84 «Система стандартов безопасности труда. Средства индивидуальной защиты. Метод определения проницаемости микроорганизмами»), но он пригоден исключительно для определения проницаемости тканей и нетканых материалов бактериями, так как основывается на использовании питательных сред, рассчитанных на выращивание прокариотических клеток тест-культур Staphylococcus aureus или Escherichia coli. Сущность способа заключается в сравнении количества выросших колоний микроорганизмов, проникших через испытываемую пробу, с количеством колоний микроорганизмов, выросших на контрольных пластинках. Применение метода предусматривается при проектировании специальной одежды, средств защиты головы и рук, разработке новых тканей и материалов В связи с этим использование вышеописанного метода не представляется возможным для определения проницаемости вирусными частицами тканей и нетканых материалов.
Наиболее близких аналогов из области техники не выявлено.
Задачей изобретения является разработка способа, позволяющего с высокой достоверностью оценить проницаемость вирусными частицами тканей и нетканых материалов.
Достигаемым при использовании предлагаемого изобретения техническим результатом является определение проницаемости тканей и нетканых материалов вирусными частицами, совершенствование показателей защищенности средств индивидуальной защиты и повышение точности оценки защитных свойств при проектировании специальной одежды, средств индивидуальной защиты, различных фильтров и других изделий, где используются ткани и нетканые материалы, а так же разработке новых тканей и материалов за счет определения проницаемости вирусных частиц.
Технический результат достигается тем, что в способе определения проницаемости вирусными частицами ткани и нетканых материалов, первоначально осуществляют визуальный осмотр и выбраковку исследуемых образцов с механическими повреждениями, влияющими на проницаемость, отобранные пробы исследуемых образцов нарезают на лоскуты в форме круга диаметром 47 мм из расчета по 3 лоскута на исследование с каждого образца ткани, которые подвергают стерилизации в стеклянных чашках Петри в паровом стерилизаторе в течение 20 мин при температуре 121±1,0°С и давлении 1 Па, полученные стерильные лоскуты последовательно размещают в приборе для напорного фильтрования с емкостью для жидкости и диаметром фритты 47 мм в качестве фильтрующего элемента, через который под давлением 1-6 атмосфер пропускают 10 мл разведенной в физиологическом растворе суспензии вакцинного штамма вируса полиомиелита Sabin 1 в концентрации 105 вирусных частиц в 1 мл (в.ч./мл) исходной суспензии, обрабатывают полученный элюат с использованием хлороформа или стерилизующих фильтрующих, насадок, затем обработанный элюат исследуют на количество профильтрованных вирусных частиц, вычисляют проницаемость ткани и нетканых материалов вирусными частицами как произведение отношения среднего арифметического количества вирусных частиц, обнаруженных в элюатах с трех лоскутов отобранной пробы, к количеству вирусных частиц, обнаруженных в разведенной вирусной суспензии, использованной в исследовании, на 100.
Пробы исследуемых образцов нарезают на лоскуты в форме круга диаметром 47 мм из расчета по 3 лоскута на исследование с каждого образца ткани - размер нарезанных лоскутов позволяет использовать их в качестве фильтрующего элемента в приборе для напорного фильтрования с фриттой диаметром 47 мм и использовать малые объемы разведенной в физиологическом растворе вирусной суспензии; трехкратная повторность проведения исследований с использованием лоскутов с одной пробы ткани позволяет получить статистически достоверные и репрезентативные данные. Для уменьшения стандартной ошибки количество повторности с использованием заранее подготовленных лоскутов можно увеличить.
Подготовленные к исследованию лоскуты подвергают стерилизации в стеклянных чашках Петри в паровом стерилизаторе в течение 20 мин при температуре 120±1,0°С и давлении 1 Па - выбранные параметры обеспечивают стерилизацию исследуемых образцов.
Величина давления при фильтровании 1-6 атмосфер выбрана из условия высокой плотности исследуемых образцов ткани и нетканых материалов и служит для форсированного фильтрования растворенной в физиологическом растворе вирусной суспензии сквозь отобранные образцы ткани и нетканых материалов.
Использование прибора для фильтрования, обеспечивающего давление 1-6 атмосфер, позволяет быстрому и беспрепятственному прохождению суспензии, содержащей вирусные частицы, через плотность ткани и нетканых материалов.
Предлагаемый способ определения проницаемости вирусными частицами тканей и нетканых материалов осуществляют следующим образом.
Через образцы ткани без физических повреждений или иных дефектов, влияющих на проницаемость вирусными частицами, под давлением профильтровывают разведенную в физиологическом растворе суспензию вакцинального штамма полиовируса Sabin 1, затем полученный элюат исследуют на количество проникших сквозь образец вирусных частиц количественными культуральными методами или методом количественного ОТ-ПЦР с детекцией в режиме реального времени.
Перед началом исследования необходимо уточнить у изготовителя ткани или нетканого материала информацию о возможности автоклавирования образца без потери его первоначальных свойств. Если ткань или нетканый материал не выдерживает температуру 120±2,0°С и давления 0,11±0,02 Мпа, то исследовать данную ткань или нетканый материал на проницаемость вирусными частицами не представляется возможным.
Полученные образцы ткани или нетканого материала инспектируют на отсутствие механических повреждений или прочих дефектов, влияющих на их проницаемость, а затем нарезают на лоскуты в форме круга диаметром 47 мм из расчета по 3 лоскута с каждого образца ткани, а затем, предварительно уложив в стеклянные чашки Петри, стерилизуют в автоклаве в течение 20 мин при температуре 120±1,0°С, давлении 1 Па.
Для одного образца ткани или нетканого материала проводят исследование проницаемости вирусными частицами минимум трех лоскутов.
Прибор для напорного фильтрования с емкостью для жидкости тщательно промывается под проточной водой, устанавливается в ламинарном шкафу II класса биологической безопасности а затем, после высыхания, протирается 70% спиртом.
Рядом последовательных разведений в физиологическом растворе готовят суспензию вакцинного штамма вируса полиомиелита Sabin 1 в концентрации 1×105 (в.ч./мл) из расчета 40 мл на 3 лоскута одного отобранного образца ткани или нетканого материала. Для исследований, предполагающих увеличение количество лоскутов с одного образца ткани или нетканого материала, объем используемой разведенной в физиологическом растворе вирусной суспензии увеличивают из расчета по 10 мл на 1 дополнительный лоскут. При этом вирусная суспензия - это суспензия из вирусных частиц, полученная из исходного вируса. Исходный вирус - это вирус, полученный из референс-центров, размноженный в объемах, достаточных для длительной работы с данным пассажем, при минимальных количествах пассажей.
Стерильный лоскут в форме круга образца ткани с помощью пинцета аккуратно помещают в прибор для фильтрования под напором на место, предназначенное для сменного фильтра, так, чтобы не образовывалось складок. Под выходное отверстие прибора ставится градуированная стерильная емкость для сбора элюата.
В прибор для фильтрования под напором через специализированное отверстие заливают вирусную суспензию в количестве 10 мл, а затем тщательно закручивают защитную крышку отверстия для герметизации прибора.
В емкости прибора для фильтрования с помощью компрессора создают давление в 1-2 атмосфер для форсированния проницаемости жидкости сквозь лоскут. Если количество профильтрованной сквозь лоскут жидкости не соответствует 10 мл, то давление увеличивают до 4-6 атмосфер.
После прохождения всего объема жидкости сквозь лоскут, компрессор выключают, а затем спускают давление из прибора. Отобранную жидкость переливают в стерильный флакон, подвергают обработке с использованием хлороформа или с использованием стерилизующих фильтрующих насадок и отдают на вирусологическое исследование количественными культуральными методами или методом количественного ОТ-ПЦР с детекцией в режиме реального времени.
Собранный и обработанный элюат допускается хранить в холодильнике при 4°С в течение суток.
После стравливания воздуха из прибора извлекают использованный лоскут ткани или нетканого материала и инспектируют на механические повреждения. В случае, если лоскут не выдержал давления и приобрел физические дефекты, влияющие на его проницаемость, данная проба элюата считается недействительной.
После каждого проведенного исследования лоскута прибор подвергают дезинфекции.
Проницаемость вирусными частицами (Пв) в процентах определяют по формуле
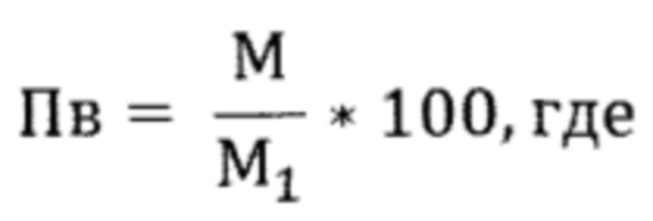
М - среднее арифметическое количества вирусных частиц, обнаруженных в элюатах с трех лоскутов отобранной пробы ткани.
M1 - количество вирусных частиц, обнаруженных в разведенной вирусной суспензии, использованной в исследовании.
Предлагаемый способ поясняется примерами.
Пример 1
Полученные образцы ткани №1 инспектируют на отсутствие механических повреждений или прочих дефектов, влияющих на ее проницаемость, а затем вырезают 3 лоскута в форме круга диаметром 47 мм, а затем, предварительно уложив в стеклянные чашки Петри, стерилизуют в автоклаве в течение 20 мин при температуре 120±1,0°С, давлении 1 Па.
Прибор для напорного фильтрования с емкостью для жидкости тщательно промывают под проточной водой, устанавливают в ламинарном шкафу II класса биологической опасности а затем, после высыхания, протирают 70% спиртом.
Рядом последовательных разведений готовят 40 мл суспензии вакцинного штамма полиовируса Sabin 1 в концентрации 1×105 (в.ч./мл).
Проводят последовательное исследование проницаемости ткани на трех лоскутах с обязательной дезинфекцией прибора для фильтрования под напором после каждого лоскута.
Стерильный круглый лоскут образца ткани с помощью пинцета аккуратно помещают в прибор для фильтрования под напором вместо фильтра так, чтобы не образовывалось складок. Под выходное отверстие прибора ставят градуированную стерильную емкость для сбора элюата.
В прибор для фильтрования под напором через специализированное отверстие заливают вирусную суспензию в количестве 10 мл, а затем тщательно закручивают защитную крышку отверстия для герметизации прибора.
В емкости прибора для фильтрования с помощью компрессора создают давление в 1-2 атмосфер для форсирования проницаемости жидкости сквозь ткань.
После прохождения всего объема жидкости сквозь ткань, компрессор выключают, а затем спускают давление из прибора. Отобранную жидкость переливают в стерильный флакон, подвергают обработке с применением стерилизующих фильтрующих насадок и отдают на вирусологическое исследование методом расчета титра вируса в тканевых цитопатогенных дозах.
После стравливания воздуха из прибора извлекают использованный лоскут ткани и инспектируют на механические повреждения. Все три лоскута ткани №1 выдержали испытание.
Для определения проницаемости вирусами (Пв) методом расчета титра вируса в тканевых цитопатогенных дозах исследованию на культуре клеток НЕР-2 подвергают используемую в испытании разведенную вирусную суспензию и все элюаты, полученные с использованием этой суспензии.
Для проведения анализа готовят серию последовательных десятикратных разведений вируссодержащего материала. Каждое разведение вируссодержащей жидкости в объеме 0,2 мл вносят в 4 пробирки с культурой клеток. Состояние культур периодически проверяют под микроскопом, отмечая на 4 и 7 сутки пробирки с дегенерацией клеток
Полученные результаты:
Лоскут №1: 4,6*104 (в.ч./мл)
Лоскут №2: 7,0*104 (в.ч./мл)
Лоскут №3: 4,6*104 (в.ч./мл)
Вирусная суспензия: 8,7*104 (в.ч./мл)
Проницаемость вирусными частицами (Пв) в процентах определяют по формуле
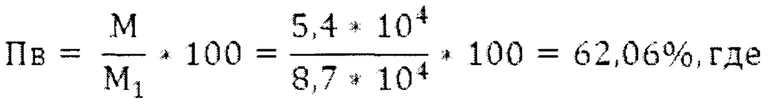
М - средняя арифметическое количества вирусных частиц, обнаруженных в элюатах с трех лоскутов отобранной пробы ткани.
M1 - количество вирусных частиц, обнаруженных в разведенной вирусной суспензии, использованной в исследовании.
Вывод: проницаемость вирусными частицами ткани №1 составляет 62,06%.
Пример 2
Полученные образцы ткани №2 инспектируют на отсутствие механических повреждений или прочих дефектов, влияющих на ее проницаемость, а затем вырезают 3 лоскута в форме круга диаметром 47 мм, а затем, предварительно уложив в стеклянные чашки Петри, стерилизуют в автоклаве в течение 20 мин при температуре 120±1,0°С, давлении 1 Па.
Прибор для напорного фильтрования с емкостью для жидкости тщательно промывают под проточной водой, устанавливают в ламинарном шкафу II класса биологической опасности а затем, после высыхания, протирают 70% спиртом.
Рядом последовательных разведений готовят 40 мл суспензии вакцинного штамма полиовируса Sabin 1 в концентрации 1×105 (в.ч./мл).
Проводят последовательное исследование проницаемости ткани на трех лоскутах с обязательной дезинфекцией прибора для фильтрования под напором после каждого лоскута.
Стерильный круглый лоскут образца ткани с помощью пинцета аккуратно помещают в прибор для фильтрования под напором вместо фильтра так, чтобы не образовывалось складок. Под выходное отверстие прибора ставят градуированную стерильную емкость для сбора элюата.
В прибор для фильтрования под напором через специализированное отверстие заливают вирусную суспензию в количестве 10 мл, а затем тщательно закручивают защитную крышку отверстия для герметизации прибора.
В емкости прибора для фильтрования с помощью компрессора создают давление в 1-2 атмосфер для форсирования проницаемости жидкости сквозь ткань.
После прохождения всего объема жидкости сквозь ткань, компрессор выключают, а затем спускают давление из прибора. Отобранную жидкость переливают в стерильный флакон, подвергают обработке с применением стерилизующих фильтрующих насадок и отдают на вирусологическое исследование методом количественного ОТ-ПЦР с детекцией в режиме реального времени.
После стравливания воздуха из прибора извлекают использованный лоскут ткани и инспектируют на механические повреждения. Все три лоскута ткани №2 выдержали испытание.
Определяют содержание нуклеиновых кислот полиовируса Sabin 1 методом ОТ-ПЦР с детекцией в режиме реального времени следующим образом:
1) Проводят выделение нуклеиновых кислот вируса полиомиелита из полученных элюатов в соответствии с используемым набором для выделения вирусной РНК;
2) Подготавливают компоненты и реагенты, необходимые для проведения ОТ-ПЦР в режиме реального времени, согласно инструкции к набору реагентов для выявления вируса полиомиелита Sabin 1;
3) Проводят количественную ОТ-ПЦР в режиме реального времени согласно инструкции к набору реагентов для выявления вируса полиомиелита Sabin 1. В соответствии с инструкцией к набору реагентов для количественного выявления вируса полиомиелита Sabin 1 с помощью компьютерной программы, проводится расчет концентрации РНК исследуемых вирусов.
Полученные результаты:
Лоскут №1: 5,6*104 (в.ч./мл)
Лоскут №2: 6,1*104 (в.ч./мл)
Лоскут №3: 6,6*104 (в.ч./мл)
Вирусная суспензия: 8,9*104 (в.ч./мл)
Проницаемость вирусными частицами (Пв) в процентах определяют по формуле:
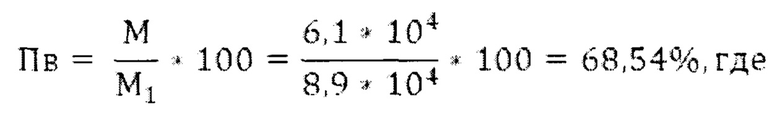
М - средняя арифметическое количества вирусных частиц, обнаруженных в элюатах с трех лоскутов отобранной пробы ткани.
М1 - количество вирусных частиц, обнаруженных в разведенной вирусной суспензии, использованной в исследовании.
Вывод: проницаемость вирусными частицами ткани №2 составляет 68,54%.
Пример 3
Полученные образцы ткани №3 инспектируют на отсутствие механических повреждений или прочих дефектов, влияющих на ее проницаемость, а затем вырезают 3 лоскута в форме круга диаметром 47 мм, а затем, предварительно уложив в стеклянные чашки Петри, стерилизуют в автоклаве в течение 20 мин при температуре 120±1,0°С, давлении 1 Па.
Прибор для напорного фильтрования с емкостью для жидкости тщательно промывают под проточной водой, устанавливают в ламинарном шкафу II класса биологической опасности а затем, после высыхания, протирают 70% спиртом.
Рядом последовательных разведений готовят 40 мл суспензии вакцинного штамма полиовируса Sabin 1 в концентрации 1×105 (в.ч./мл).
Проводят последовательное исследование проницаемости ткани на трех лоскутах с обязательной дезинфекцией прибора для фильтрования под напором после каждого лоскута.
Стерильный круглый лоскут образца ткани с помощью пинцета аккуратно помещают в прибор для фильтрования под напором вместо фильтра так, чтобы не образовывалось складок. Под выходное отверстие прибора ставят градуированную стерильную емкость для сбора элюата.
В прибор для фильтрования под напором через специализированное отверстие заливают вирусную суспензию в количестве 10 мл, а затем тщательно закручивают защитную крышку отверстия для герметизации прибора.
В емкости прибора для фильтрования с помощью компрессора создают давление в 1-2 атмосфер для форсирования проницаемости жидкости сквозь ткань.
После прохождения всего объема жидкости сквозь ткань, компрессор выключают, а затем спускают давление из прибора. Отобранную жидкость переливают в стерильный флакон, подвергают обработке с применением стерилизующих фильтрующих насадок и отдают на вирусологическое исследование методом бляшек.
После стравливания воздуха из прибора извлекают использованный лоскут ткани и инспектируют на механические повреждения. Все три лоскута ткани №3 выдержали испытание.
Готовят серию последовательных десятикратных разведений вируссодержащей жидкости. Каждое разведение вируссодержащей жидкости в объеме 0,2 мл вносят в 2-4 плоскостенных флакона с культурой клеток НЕР-2, выпуская жидкость из пипетки легкой стрункой, чтобы не повредить монослой. Флаконы слегка покачивают, чтобы равномерно распределить вируссодержащую жидкость по монослою. Зараженные флаконы инкубируют при +37±0,1°С в течение 60 минут, а затем заливают агаровым покрытием.
Количество бляшек подсчитывают на 3, 4, 5, 6, 7 сутки.
Подсчитывают результаты.
Полученные результаты:
Лоскут №1: 3,3*104 (в.ч./мл)
Лоскут №2: 4,5*104 (в.ч./мл)
Лоскут №3:2,1*104 (в.ч./мл)
Вирусная суспензия: 9,6*104 (в.ч./мл)
Проницаемость вирусными частицами (Пв) в процентах определяют по формуле:
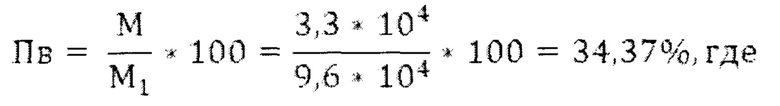
М - средняя арифметическое количества вирусных частиц, обнаруженных в элюатах с трех лоскутов отобранной пробы ткани.
М1 - количество вирусных частиц, обнаруженных в разведенной вирусной суспензии, использованной в исследовании.
Вывод: проницаемость вирусными частицами ткани №3 составляет 34,37%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРОНИЦАЕМОСТИ ТКАНЫХ И НЕТКАНЫХ МАТЕРИАЛОВ ДЛЯ ИСПОЛЬЗОВАНИЯ В КАЧЕСТВЕ СРЕДСТВ ИНДИВИДУАЛЬНОЙ ЗАЩИТЫ ОТ БАКТЕРИАЛЬНОГО С РАЗНЫМ СТРОЕНИЕМ КЛЕТОЧНОЙ СТЕНКИ И ГРИБКОВОГО ЗАРАЖЕНИЯ ВОЗДУШНО-КАПЕЛЬНЫМ И КОНТАКТНО-БЫТОВЫМ ПУТЕМ | 2021 |
|
RU2770008C1 |
| ВАКЦИНА IPV-DPT | 2007 |
|
RU2447898C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К ВИРУСАМ ПОЛИОМИЕЛИТА 1, 3 ТИПОВ В СЫВОРОТКЕ КРОВИ | 2017 |
|
RU2642657C1 |
| Способ выявления РНК модифицированного вакцинного полиовируса типа 2 (nOPV2) методом ОТ-ПЦР в реальном времени | 2022 |
|
RU2795703C1 |
| ИНАКТИВИРОВАННАЯ ПОЛИОВАКЦИНА | 2011 |
|
RU2599453C2 |
| ИММУНОАДЪЮВАНТНАЯ КОМПОЗИЦИЯ ДЛЯ ВАКЦИН ПРОТИВ ИНФЕКЦИОННЫХ АГЕНТОВ ВИРУСНОЙ И БАКТЕРИАЛЬНОЙ ПРИРОДЫ | 2018 |
|
RU2697527C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ D-АНТИГЕНА ПОЛИОВИРУСОВ 1-3 ТИПОВ | 2012 |
|
RU2535058C2 |
| Способ спектрометрического определения концентрации рибонуклеопротеина вируса бешенства по оценке количества молекул вирусной РНК в сырье для антирабических вакцин | 2020 |
|
RU2748475C1 |
| КОМБИНИРОВАННАЯ ВАКЦИНА, ВКЛЮЧАЮЩАЯ АНТИГЕНЫ ДИФТЕРИИ, СТОЛБНЯКА, АЦЕЛЛЮЛЯРНОГО КОКЛЮША, HAEMOPHILUS INFLUENZAE И ПОЛИОВИРУСА, ЕЕ ПРИМЕНЕНИЕ И СПОСОБ ПРОИЗВОДСТВА | 2009 |
|
RU2526214C2 |
| Способ спектрометрического определения концентрации 146S частиц вируса ящура в неинактивированном сырье для вакцины по оценке количества молекул вирусной РНК, выделенной после иммунного захвата вирионов | 2019 |
|
RU2712769C1 |
Изобретение относится к медицине и прикладной микробиологии, а именно к способу определения проницаемости вирусными частицами вакцинного штамма вируса полиомиелита Sabin 1 ткани и нетканых материалов. Способ определения проницаемости вирусными частицами вакцинного штамма вируса полиомиелита Sabin 1 ткани и нетканых материалов, в котором первоначально осуществляют визуальный осмотр и выбраковку исследуемых образцов с механическими повреждениями, влияющими на проницаемость, отобранные пробы исследуемых образцов нарезают на лоскуты в форме круга диаметром 47 мм из расчета по 3 лоскута на исследование с каждого образца ткани, которые подвергают стерилизации в стеклянных чашках Петри в паровом стерилизаторе в течение 20 мин при температуре 120±1,0°С и давлении 1 Па, полученные стерильные лоскуты последовательно размещают в приборе для напорного фильтрования с емкостью для жидкости и диаметром фритт 47 мм в качестве фильтрующего элемента, через который под давлением 1-6 атмосфер пропускают 10 мл разведенной в физиологическом растворе суспензии вакцинного штамма вируса полиомиелита Sabin 1, в концентрации 105 вирусных частиц/мл, обрабатывают полученный элюат с использованием хлороформа или стерилизующих фильтрующих насадок, затем обработанный элюат исследуют на количество профильтрованных вирусных частиц, вычисляют проницаемость ткани и нетканых материалов вирусными частицами вируса полиомиелита как произведение отношения среднего арифметического количества вирусных частиц, обнаруженных в элюатах с трех лоскутов отобранной пробы, к количеству вирусных частиц, обнаруженных в разведенной вирусной суспензии, использованной в исследовании, на 100. Вышеописанный способ позволяет с высокой достоверностью оценить проницаемость вирусными частицами вакцинного штамма вируса полиомиелита Sabin 1 тканей и нетканых материалов. 3 пр.
Способ определения проницаемости вирусными частицами вакцинного штамма вируса полиомиелита Sabin 1 ткани и нетканых материалов, в котором первоначально осуществляют визуальный осмотр и выбраковку исследуемых образцов с механическими повреждениями, влияющими на проницаемость, отобранные пробы исследуемых образцов нарезают на лоскуты в форме круга диаметром 47 мм из расчета по 3 лоскута на исследование с каждого образца ткани, которые подвергают стерилизации в стеклянных чашках Петри в паровом стерилизаторе в течение 20 мин при температуре 120±1,0°С и давлении 1 Па, полученные стерильные лоскуты последовательно размещают в приборе для напорного фильтрования с емкостью для жидкости и диаметром фритт 47 мм в качестве фильтрующего элемента, через который под давлением 1-6 атмосфер пропускают 10 мл разведенной в физиологическом растворе суспензии вакцинного штамма вируса полиомиелита Sabin 1, в концентрации 105 вирусных частиц/мл, обрабатывают полученный элюат с использованием хлороформа или стерилизующих фильтрующих насадок, затем обработанный элюат исследуют на количество профильтрованных вирусных частиц, вычисляют проницаемость ткани и нетканых материалов вирусными частицами вируса полиомиелита как произведение отношения среднего арифметического количества вирусных частиц, обнаруженных в элюатах с трех лоскутов отобранной пробы, к количеству вирусных частиц, обнаруженных в разведенной вирусной суспензии, использованной в исследовании, на 100.
| Средства индивидуальной защиты | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРОНИЦАЕМОСТИ АЭРОЗОЛЬНЫХ ФИЛЬТРОВ В ОТНОШЕНИИ МИКРООРГАНИЗМОВ | 2006 |
|
RU2327142C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ОБРАЗЦА ДЛЯ ОПРЕДЕЛЕНИЯ МИКРООРГАНИЗМОВ (ВАРИАНТЫ) И НАБОР ДЛЯ ОБРАБОТКИ ОБРАЗЦА ДЛЯ ОПРЕДЕЛЕНИЯ МИКРООРГАНИЗМОВ | 1995 |
|
RU2145977C1 |
| C | |||
| DAVID LYTLE et al | |||
| A Simple Method To Test Condoms for Penetration by Viruses // Applied and environmental microbiology, 1992, v | |||
| Способ окисления боковых цепей ароматических углеводородов и их производных в кислоты и альдегиды | 1921 |
|
SU58A1 |
| Счетный прибор | 1925 |
|
SU3180A1 |
Авторы
Даты
2021-08-18—Публикация
2020-12-22—Подача