ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
По данной заявке испрашивается приоритет на основании предварительной патентной заявки США № 61/940339, поданной 14 февраля 2014 г., полное содержание которой включено в настоящий документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится, главным образом, к области молекулярной биологии и медицины. Более конкретно, оно относится к способам получения химерных антигенных рецепторов (CAR).
ОПИСАНИЕ ПРЕДШЕСТВУЮЩЕГО УРОВНЯ ТЕХНИКИ
Адоптивный перенос T-клеток является перспективным терапевтическим подходом, который может быть использован для лечения рака. Адоптивный перенос T-клеток включает выделение и наращивание антигенспецифических T-клеток, которые способны избирательно уничтожать клетки опухолей. Как правило, T-клетки выделяют из организма субъекта и культивируют in vitro. Химерный антигенный рецептор (CAR) можно вводить в T-клетку in vitro для направления T-клетки, после повторного введения ее в организм субъекта, на избирательное уничтожение клеток опухолей, основанное на экспрессии антигена (например, Wieczorek et al. 2013; Berry et al., 2013).
Одна из проблем, связанных с адоптивным переносом T-клеток, заключается в том, что существует значительная вариабельность в том, какой CAR может работать более эффективно у конкретных популяций пациентов, например, при лечении конкретной формы рака. Вследствие очень большого числа различных возможных CAR, способных проявлять терапевтическую активность против рака, которые потенциально могут быть получены, в настоящее время клиницистам очень трудно предвидеть, какой CAR может проявлять терапевтическую активность против конкретного вида рака или подвида рака. Ввиду значительного терапевтического потенциала адоптивного переноса T-клеток, существует явная потребность в усовершенствованных способах идентификации и получения новых CAR.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В некоторых аспектах настоящее изобретение относится к способам получения CAR, и по изобретению предложены конкретные CAR. В некоторых аспектах предложены способы получения большого числа CAR, которые можно подвергать скринингу на активность против конкретного вида рака или подвида рака; таким образом, можно получать и идентифицировать CAR, проявляющий улучшенный терапевтический потенциал против конкретного вида рака или подвида рака. Предложенные в настоящем документе CAR можно вводить в качестве терапии субъекту или пациенту-человеку, например, для лечения рака.
Клинические данные свидетельствуют о том, что конкретная конструкция химерного антигенного рецептора (CAR), направляющего T-клетки к определенному ассоциированному с опухолью антигену (TAA), может иметь разный терапевтический потенциал у разных пациентов. Например, CD19-специфические CAR второго поколения, активируемые через химерные CD28/CD3-дзета или CD137/CD3-дзета, могут приводить к превосходным клиническим результатам, когда аутологичные генетически модифицированные T-клетки вводят пациентам с острым, но не хроническим, лейкозом B-клеточной линии. Для решения этой проблемы в настоящем документе предложены способы получения видов CAR, которые могут проявлять улучшенный противоопухолевый эффект для конкретной опухоли.
Например, в настоящем документе предложены способы, которые можно использовать для получения и скрининга большого числа CAR на их способность лечить рак у конкретного пациента; таким образом, способы можно использовать для персонализации терапии для пациента и выбора конкретного CAR, обладающего улучшенным терапевтическим потенциалом для конкретного пациента или подгруппы пациентов с конкретной формой рака. В клиническом подходе к генной терапии можно использовать электроперенос ДНК плазмид из системы транспозонов «спящая красавица» (Sleeping Beauty (SB)), например, для уменьшения стоимости и сложности при производстве индивидуальных конструкций CAR для небольших подгрупп пациентов. В таких способах персонализации CAR+ T-клеток можно использовать получение большого числа молекул CAR, которые можно подвергать скринингу и оценивать их способность приносить пользу конкретному пациенту.
В некоторых аспектах предложены способы для высокопроизводительной сборки молекул CAR с использованием системы тройной сайт-специфической рекомбинации (также называемой платформой «EZ-CAR»). В некоторых вариантах осуществления эти способы могут позволять осуществлять быстрое комбинирование 3 компонентов прототипа CAR из (i) одноцепочечного вариабельного фрагмента (scFv), определяющего специфичность, (ii) каркаса/шарнира, который присоединяет scFv, выступающий над поверхностью клетки, и (iii) одного или более внутриклеточных сигнальных доменов. Например, как показано в приведенных ниже примерах, CD19-специфический CAR, который активируется через химерный CD28/CD3-дзета, был получен с использованием платформы EZ CAR параллельно с CD19RCD28mζ CAR+ T-клетками клинической категории (CG CAR).
В некоторых вариантах осуществления CAR, предложенный в настоящем документе или полученный способами по настоящему изобретению, может быть совместно экспрессирован в T-клетке с мембраносвязанным IL-15. Таким образом, T-клетка может выживать или существовать в состоянии покоя без существенной пролиферации in vitro или in vivo. Напротив, как описано ранее, T-клетки, экспрессирующие CAR, как правило, погибают, когда цитокины выводят из системы in vitro, и эта гибель клеток может служить в качестве меры обеспечения безопасности в определенных случаях, когда T-клетки вводят в клинической практике. Пролиферацию T-клеток, как правило, измеряют с использованием теста с автономными клетками. Таким образом, в отличие от некоторых ранее идентифицированных CAR, в случае которых T-клетки не способны сохраняться in vitro без антигенной стимуляции, в настоящем документе предложены CAR, которые могут индуцировать цитотоксичность без автономного роста in vitro. В зависимости от конкретного нужного варианта осуществления CAR, полученный способами по настоящему изобретению или предложенный в настоящем документе, может быть экспрессирован в T-клетке либо с совместной экспрессией в T-клетке мембраносвязанного IL-15, либо без нее.
Один из аспектов настоящего изобретения относится к композиции, содержащей: (a) множество первых векторов, кодирующих один или более отличающихся антигенсвязывающих доменов; (b) множество вторых векторов, кодирующих один или более отличающихся шарнирных доменов; и (c) множество третьих векторов, кодирующих один или более отличающихся эндодоменов; при этом по меньшей мере два из первых, вторых и третьих векторов включают множество из двух или более векторов, кодирующих отличающиеся антигенсвязывающие домены, шарнирные домены и/или эндодомены, соответственно, и кроме того, при этом векторы содержат сайты для гомологичной рекомбинации, позволяющие получать четвертый вектор, кодирующий химерный антигенный рецептор (CAR).
В настоящем изобретении применительно к белковым доменам и полипептидам, таким как антигенсвязывающие домены, шарнирные домены, трансмембранные домены и эндодомены, термин «отличающиеся» означает домены, имеющие, содержащие или состоящие из разных полипептидных (аминокислотных) последовательностей. Например, два «отличающихся» антигенсвязывающих домена могут связывать один и тот же антиген (фактически, даже один и тот же эпитоп на этом антигене), однако антигенсвязывающие домены являются «отличающимися», если составляющие их аминокислотные последовательности отличаются друг от друга. Аналогично, два «отличающихся» антигенсвязывающих домена, различающиеся по составляющим их аминокислотным последовательностям, также могут специфически связывать разные антигены и эпитопы. И наоборот, описанные в настоящем документе две молекулы (полипептиды) с идентичными аминокислотными последовательностями не являются «отличающимися» полипептидами.
В некоторых вариантах осуществления множество первых векторов кодируют множество отличающихся антигенсвязывающих доменов, множество вторых векторов кодируют один шарнирный домен, и множество третьих векторов кодируют множество отличающихся эндодоменов. В некоторых вариантах осуществления множество первых векторов кодируют множество отличающихся антигенсвязывающих доменов, множество вторых векторов кодируют множество отличающихся шарнирных доменов, и множество третьих векторов кодируют множество отличающихся эндодоменов. В некоторых вариантах осуществления множество первых векторов кодируют множество отличающихся антигенсвязывающих доменов, множество вторых векторов кодируют множество отличающихся шарнирных доменов, и множество третьих векторов кодируют один эндодомен. В некоторых вариантах осуществления множество первых векторов кодируют один антигенсвязывающий домен, множество вторых векторов кодируют множество отличающихся шарнирных доменов, и множество третьих векторов кодируют множество отличающихся эндодоменов. В некоторых вариантах осуществления антигенсвязывающие домены содержат или состоят из scFv. Третьи векторы могут кодировать трансмембранный домен. Вторые векторы могут кодировать трансмембранный домен. В некоторых вариантах осуществления композиция дополнительно содержит множество пятых векторов, кодирующих один или более трансмембранных доменов; при этом первые векторы, вторые векторы, третьи векторы и пятые векторы содержат сайты гомологичной рекомбинации для получения четвертого вектора, кодирующего химерный антигенный рецептор (CAR). Первый вектор может содержать первую последовательность и второй сайт гомологичной рекомбинации. Второй вектор может содержать вторую последовательность гомологичной рекомбинации и третью последовательность гомологичной рекомбинации. Третий вектор может содержать третью последовательность гомологичной рекомбинации и четвертую последовательность гомологичной рекомбинации. Третий вектор может содержать третью последовательность гомологичной рекомбинации и четвертую последовательность гомологичной рекомбинации. Четвертый вектор содержит первую последовательность гомологичной рекомбинации и четвертую последовательность гомологичной рекомбинации. Первый вектор, второй вектор и/или третий вектор могут кодировать транспозазу. Транспозаза может представлять собой Tc1-подобную транспозазу лососевых (SB). В некоторых вариантах осуществления 1, 2, 3, 4 или все из первого вектора, второго вектора, третьего вектора, четвертого вектора и/или пятого вектора представляют собой транспозонный вектор «спящая красавица» (SB) или piggyBac. Альтернативно, в некоторых вариантах осуществления первый вектор, второй вектор, третий вектор, четвертый вектор и/или пятый вектор не является транспозонным вектором «спящая красавица» (SB) или piggyBac; например, в некоторых вариантах осуществления CAR можно получать без использования вектора «спящая красавица» (SB) или piggyBac, и тогда CAR впоследствии может быть вставлен в вектор, подходящий для трансфицирования T-клеток (например, вставлен в вектор «спящая красавица» (SB), как описано, например, в публикации Singh et al., 2015). Тем не менее, в некоторых вариантах осуществления создание CAR, уже присутствующего в векторе, который подходит для трансфицирования T-клеток, может упрощать процесс или уменьшать количество этапов, необходимых как для создания CAR, так и для трансфицирования T-клетки. Отличающися антигенсвязывающие домены могут избирательно связывать разные антигены. В некоторых вариантах осуществления отличающиеся антигенсвязывающие домены избирательно связывают один и тот же антиген. Антигенсвязывающий домен может избирательно связывать CD19, универсальный антиген (мыши), HER-3, GD2, Gp75, белок CS1, мезотелин, фосфатидилсерин, cMyc, CD22, CD4, CD44v6, CD45, CD28, CD3, CD3e, CD123, CD138, CD52, CD56, CD74, CD30, Gp75, CD38, CD33, CD20, слитый продукт Her1/HER3, GD2, углевод, Aspergillus, ROR1, c-MET, EGFR, дектин, эбола, грибок, GP, HERV-K (HERVK), NY-ESO-1, VEGF-R2, TGF-b2R, IgG4, биотин или O-AcGD2. Отличающиеся антигенсвязывающие домены могут состоять из, или содержать scFv. Шарнирная область может состоять из, или содержать 12 ак пептид (GAGAGCAAGTACGGCCCTCCCTGCCCCCCTTGCCCT; SEQ ID NO: 1), t-20 ак пептид, IgG4 Fc ΔEQ, IgG4 Fc ΔQ, (t-12 ак+t-20 ак), mKate, phiLov, dsRed, Venus, eGFP, CH3 HA, (CD8α+t-20 ак), двойной t-20 ак, (t-20 ак+CD8α), (CD8α+лейциновая застежка Basep1), (CD8α+лейциновая застежка Acid1), 2D3, CD8α или IgG4 Fc. По меньшей мере один из эндодоменов может содержать CD3ζ. По меньшей мере один из эндодоменов может содержать один или более доменов ITAM. В некоторых вариантах осуществления по меньшей мере один из эндодоменов содержит (CD28+CD3ζ), (CD28+CD27+CD3ζ), (CD28+OX40+CD3ζ), (CD28+4-1BB+CD3ζ), (CD28+CD27+OX40+CD3ζ), (CD28+4-1BB+CD27+CD3ζ), (CD28+4-1BB+OX40+CD3ζ), (4-1BB+CD3ζ), (4-1BB+OX40+CD3ζ), (4-1BB+CD27+CD3ζ), (CD27+CD3ζ), (CD27+OX40+CD3ζ), (CD28Δ+CD3ζ), (CD28Δ+CD27+CD3ζ), (CD28Δ+OX40+CD3ζ), (CD28Δ+4-1BB+CD3ζ), (CD28Δ+4-1BB+OX40+CD3ζ), (CD28Δ+CD27+OX40+CD3ζ), (CD28Δ+4-1BB+CD27+CD3ζ), (4-1BB+ICOS+CD3ζ), (CD28+ICOS+CD3ζ), (ICOS+CD3ζ), CD3ζ или только CD28. В некоторых вариантах осуществления CAR можно тестировать на активность, например, с использованием платформы iQueTM Screener (IntelliCyt, Albuquerque, NM). В некоторых вариантах осуществления CAR можно оценивать на наличие одной или более характеристик (например, жизнеспособности, повышающей регуляции сигналов активации, повышающей регуляции CD25, высвобождения цитокинов и/или уничтожения клеток) при экспрессии в клетках, таких как T-клетки, с использованием такого метода, как, например, проточная цитометрия.
Другой аспект настоящего изобретения относится к композиции, содержащей коллекцию векторов, кодирующих химерные антигенные рецепторы, которые кодируют множество отличающихся антигенсвязывающих доменов, шарнирных доменов и эндодоменов, при этом векторы в указанной коллекции рандомизированы в отношении указанных доменов.
Другой аспект настоящего изобретения относится к способу получения множества векторов, каждый из которых кодирует химерный антигенный рецептор (CAR), включающему: (i) получение композиции, содержащей множество векторов по настоящему изобретению (например, описанных выше); и (ii) создание для композиции условий, достаточных для того, чтобы отличающиеся антигенсвязывающие домены, шарнирные домены и/или эндодомены, содержащиеся в, или кодируемые указанными векторами, могли рекомбинировать за счет гомологичной рекомбинации, с получением множества четвертых векторов, при этом каждый из указанных четвертых векторов кодирует CAR. Способ может дополнительно включать осуществление экспрессии CAR в клетке. Способ может дополнительно включать тестирование CAR на активность. В некоторых вариантах осуществления один или более из первых векторов кодируют область scFv. В некоторых вариантах осуществления один или более из третьих векторов кодируют трансмембранный домен. В некоторых вариантах осуществления один или более из вторых векторов кодируют трансмембранный домен. Способ может дополнительно включать произвольное включение за счет рекомбинации пятого вектора, кодирующего трансмембранный домен, для образования совместно с указанными первыми векторами, вторыми векторами и третьими векторами указанного четвертого вектора. В некоторых вариантах осуществления указанные первые векторы и указанные вторые векторы произвольно соединяются из множества векторов, кодирующих множество отличающихся областей scFv и множество отличающихся шарнирных областей. В некоторых вариантах осуществления указанные первые векторы и указанные третьи векторы произвольно соединяются из множества векторов, кодирующих множество отличающихся областей scFv и множество отличающихся эндодоменов. В некоторых вариантах осуществления указанные вторые векторы и указанные третьи векторы произвольно соединяются из множества векторов, кодирующих множество отличающихся шарнирных областей и множество отличающихся эндодоменов. В некоторых вариантах осуществления указанные первые векторы, указанные вторые векторы и указанные третьи векторы произвольно соединяются из множества векторов, кодирующих множество отличающихся областей scFv, множество отличающихся шарнирных областей и множество отличающихся эндодоменов. Способ может дополнительно включать получение указанных четвертых векторов за счет произвольного соединения указанных первых векторов из первой библиотеки векторов, кодирующих множество областей scFv, произвольного соединения указанных вторых векторов из второй библиотеки векторов, кодирующих множество областей scFv, и произвольного соединения указанных третьих векторов из третьей библиотеки векторов, кодирующих множество эндодоменов, с образованием указанного четвертого вектора, кодирующего CAR. Первые векторы могут содержать первую последовательность и второй сайт гомологичной рекомбинации. Вторые векторы могут содержать вторую последовательность гомологичной рекомбинации и третью последовательность гомологичной рекомбинации. Третьи векторы могут содержать третью последовательность гомологичной рекомбинации и четвертую последовательность гомологичной рекомбинации. Третьи векторы могут содержать третью последовательность гомологичной рекомбинации и четвертую последовательность гомологичной рекомбинации. Четвертые векторы могут содержать первую последовательность гомологичной рекомбинации и четвертую последовательность гомологичной рекомбинации. Первые векторы, вторые векторы и/или третьи векторы могут кодировать транспозазу. В некоторых вариантах осуществления шестой вектор кодирует транспозазу, и при этом способ включает внедрение, введение электропорацией или трансфицирование одного или более из указанных четвертых векторов и указанного шестого вектора в клетку. Транспозаза может представлять собой Tc1-подобную транспозазу лососевых (SB). Способ может дополнительно включать культивирование или содержание клеток, трансфицированных CAR, в присутствии искусственных антигенпредставляющих клеток (иАПК), которые могут стимулировать размножение CAR-экспрессирующих T-клеток. В некоторых вариантах осуществления все из области scFv, шарнирной области и эндодомена закодированы в транспозонном векторе «спящая красавица» (SB) или piggyBac. В некоторых вариантах осуществления все из первого вектора, второго вектора и/или третьего вектора произвольно соединены за счет указанной рекомбинации из множества векторов, кодирующих множество отличающихся областей scFv, шарнирных областей и эндодоменов. В некоторых вариантах осуществления все из указанных первых векторов, вторых векторов и третьих векторов содержат транспозон; и при этом указанное соединение за счет гомологичной рекомбинации представляет собой сайт-специфическую рекомбинацию. В некоторых вариантах осуществления все из первых векторов и вторых векторов имеют первый сайт гомологичной рекомбинации; и при этом все из вторых векторов и третьих векторов имеют второй сайт гомологичной рекомбинации. В некоторых вариантах осуществления первые векторы имеют третий сайт рекомбинации, и при этом четвертые векторы имеют четвертый сайт рекомбинации, причем третий сайт рекомбинации и четвертый сайт рекомбинации могут создавать возможность гомологичной рекомбинации в клетке. Клетка может представлять собой T-клетку, такую как, например, альфа-бета T-клетка, гамма-дельта T-клетка или NK-клетка, или NKT-клетка. В некоторых вариантах осуществления клетка представляет собой плюрипотентную клетку, такую как, например, стволовая клетка или индуцированная плюрипотентная стволовая клетка. В некоторых вариантах осуществления клетка получена из стволовой клетки, индуцированной плюрипотентной стволовой клетки или стволовой клетки. Клетка может представлять собой T-клетку или NK-клетку, полученную из индуцированной плюрипотентной стволовой клетки. В некоторых вариантах осуществления указанные отличающиеся антигенсвязывающие домены включают по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9 или более scFv, которые избирательно узнают разные антигены. В некоторых вариантах осуществления указанные отличающиеся антигенсвязывающие домены включают по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9 или более scFv, которые избирательно узнают (то есть, специфически связывают) один и тот же антиген. В некоторых вариантах осуществления антигенсвязывающие домены избирательно (специфически) связывают CD19, универсальный антиген (мыши), HER-3, GD2, Gp75, белок CS1, мезотелин, фосфатидилсерин, cMyc, CD22, CD4, CD44v6, CD45, CD28, CD3, CD3e, CD123, CD138, CD52, CD56, CD74, CD30, Gp75, CD38, CD33, CD20, слитый продукт Her1/HER3, GD2, углевод, Aspergillus, ROR1, c-MET, EGFR, дектин, эбола, грибок, GP, HERV-K, NY-ESO-1, VEGF-R2, TGF-b2R, IgG4, биотин или O-AcGD2. В некоторых вариантах осуществления указанные антигенсвязывающие домены содержат или состоят из scFv. Шарнирная область может кодировать 12 ак пептид (GAGAGCAAGTACGGCCCTCCCTGCCCCCCTTGCCCT; SEQ ID NO: 1), t-20 ак пептид, IgG4 Fc ΔEQ, IgG4 Fc ΔQ, (t-12 ак+t-20 ак), mKate, phiLov, dsRed, Venus, eGFP, CH3 HA, (CD8α+t-20 ак), двойной t-20 ак, (t-20 ак+CD8α), (CD8α+лейциновая застежка Basep1), (CD8α+лейциновая застежка Acid1), 2D3, CD8α или IgG4 Fc. Эндодомен может кодировать CD3ζ. Эндодомен может кодировать один или более доменов ITAM. В некоторых вариантах осуществления эндодомен кодирует (CD28+CD3ζ), (CD28+CD27+CD3ζ), (CD28+OX40+CD3ζ), (CD28+4-1BB+CD3ζ), (CD28+CD27+OX40+CD3ζ), (CD28+4-1BB+CD27+CD3ζ), (CD28+4-1BB+OX40+CD3ζ), (4-1BB+CD3ζ), (4-1BB+OX40+CD3ζ), (4-1BB+CD27+CD3ζ), (CD27+CD3ζ), (CD27+OX40+CD3ζ), (CD28Δ+CD3ζ), (CD28Δ+CD27+CD3ζ), (CD28Δ+OX40+CD3ζ), (CD28Δ+4-1BB+CD3ζ), (CD28Δ+4-1BB+OX40+CD3ζ), (CD28Δ+CD27+OX40+CD3ζ), (CD28Δ+4-1BB+CD27+CD3ζ), (4-1BB+ICOS+CD3ζ), (CD28+ICOS+CD3ζ), (ICOS+CD3ζ), CD3ζ или только CD28. В некоторых вариантах осуществления CAR можно тестировать на активность, например, с использованием платформы iQueTM Screener (IntelliCyt, Albuquerque, NM). В некоторых вариантах осуществления CAR можно оценивать на наличие одной или более характеристик (например, жизнеспособности, повышающей регуляции сигналов активации, повышающей регуляции CD25, высвобождения цитокинов и/или уничтожения клеток) при экспрессии в клетках, таких как T-клетки, с использованием такого метода, как, например, проточная цитометрия. В некоторых вариантах осуществления указанная активность включает способность CAR избирательно связывать раковую клетку, избирательно связывать патоген, избирательно связывать клетку, вовлеченную в аутоиммунное заболевание, или стимулировать активацию T-клетки, разрушение T-клетки, дифференциацию T-клетки, пролиферацию T-клетки, дедифференциацию T-клетки, движение T-клетки, продукцию цитокинов T-клеткой или уничтожение T-клеткой.
В некоторых вариантах осуществления раковая клетка представляет собой рак яичника, лимфому, почечноклеточный рак, В-клеточное злокачественное новообразование, CLL, B-ALL, ALL, лейкоз, В-клеточное злокачественное новообразование или лимфому, лимфому из клеток мантийной зоны, вялотекущую B-клеточную лимфому, лимфому Ходжкина, AML, рак шейки матки, рак молочной железы, колоректальный рак, рак яичника, нейробластому, рак кожи, меланому, рак легкого, остеосаркому, глиому, опухоль из эпителиальных клеток, рак предстательной железы или педиатрический рак. Патоген может представлять собой вирус, грибок или бактерию. В некоторых вариантах осуществления указанное тестирование включает визуализацию отдельной клетки, генетический анализ отдельной клетки, оценку отдельной T-клетки или популяций T-клеток; количественную оценку специфического уничтожения или серийного уничтожения, экспрессии гена, экспрессии белка, движения к или от мишени, пролиферации, индуцированной активацией гибели клеток, секреции цитокинов или секреции хемокинов. Способ может дополнительно включать выбор отдельного CAR из указанного множества векторов на основании свойства отдельного CAR. Способ может дополнительно включать терапевтическое введение отдельного CAR субъекту. Субъект может быть млекопитающим, таким как, например, человек.
Другой аспект настоящего изобретения относится к полипептиду, содержащему или состоящему из CAR 217 (SEQ ID NO: 2), CAR 194 (SEQ ID NO: 3), CAR 212 (SEQ ID NO: 4), CAR 213 (SEQ ID NO: 5), CAR 265 (SEQ ID NO: 6), CAR 214 (SEQ ID NO: 56), CAR 215 (SEQ ID NO: 57), CAR 216 (SEQ ID NO: 58), CAR 218 (SEQ ID NO: 59), CAR 193 (SEQ ID NO: 55) или CAR 268 (SEQ ID NO: 7).
Другой аспект настоящего изобретения относится к трансформированной T-клетке, экспрессирующей полипептид, содержащий или состоящий из CAR 217 (SEQ ID NO: 2), CAR 194 (SEQ ID NO: 3), CAR 212 (SEQ ID NO: 4), CAR 213 (SEQ ID NO: 5), CAR 265 (SEQ ID NO: 6), CAR 214 (SEQ ID NO: 56), CAR 215 (SEQ ID NO: 57), CAR 216 (SEQ ID NO: 58), CAR 218 (SEQ ID NO: 59), CAR 193 (SEQ ID NO: 55) или CAR 268 (SEQ ID NO: 7). Клетка может представлять собой иммортализованную клетку. T-клетка может представлять собой альфа-бета T-клетку, гамма-дельта T-клетку, NK-клетку, NKT-клетку, стволовую клетку, клетки, полученные из стволовых клеток, включая клетки иммунной системы.
Другой аспект настоящего изобретения относится к фармацевтическому препарату, содержащему трансформированную T-клетку по настоящему изобретению.
Еще один аспект настоящего изобретения относится к нуклеиновой кислоте, кодирующей химерный антигенный рецептор, содержащий или состоящий из CAR 217 (SEQ ID NO: 2), CAR 194 (SEQ ID NO: 3), CAR 212 (SEQ ID NO: 4), CAR 213 (SEQ ID NO: 5), CAR 265 (SEQ ID NO: 6), CAR 214 (SEQ ID NO: 56), CAR 215 (SEQ ID NO: 57), CAR 216 (SEQ ID NO: 58), CAR 218 (SEQ ID NO: 59), CAR 193 (SEQ ID NO: 55) или CAR 268 (SEQ ID NO: 7). Нуклеиновая кислота может содержаться в T-клетке, такой как, например, альфа-бета T-клетка, гамма-дельта T-клетка, NK-клетка, NKT-клетка, стволовая клетка или T-клетка, полученная из плюрипотентной клетки. T-клетка может содержаться в фармацевтически приемлемом носителе или эксципиенте.
Другой аспект настоящего изобретения относится к композиции, содержащей библиотеку разных кодирующих CAR векторов, при этом векторы в указанной библиотеке рандомизированы в отношении отличающихся антигенсвязывающих доменов, шарнирных доменов и/или эндодоменов. В некоторых вариантах осуществления библиотека рандомизирована в отношении отличающихся антигенсвязывающих доменов, шарнирных доменов и эндодоменов. В некоторых вариантах осуществления библиотека рандомизирована в отношении отличающихся антигенсвязывающих доменов и эндодоменов. В некоторых вариантах осуществления библиотека рандомизирована в отношении отличающихся антигенсвязывающих доменов и шарнирных доменов. В некоторых вариантах осуществления библиотека рандомизирована в отношении отличающихся шарнирных доменов и эндодоменов.
Примеры антигенсвязывающих доменов, шарнирных областей, трансмембранных доменов и эндодоменов, которые могут быть использованы в способах по настоящему изобретению для получения CAR, приведены ниже в таблице 1. Антигенсвязывающие домены, шарнирные области, трансмембранные домены и эндодомены приведены в таблице 1 лишь в качестве неограничивающих примеров, и предполагается, что можно выбирать практически любой антигенсвязывающий домен (например, нацеленный на злокачественную клетку, бактерию, грибок, вирус, или инфицированную вирусом клетку), нужный для конкретного клинического применения. В таблице 1 приведена мишень антигенсвязывающего домена (например, «CD19» может означать область scFv, которая избирательно связывает CD19). В некоторых вариантах осуществления антигенсвязывающий домен содержит или состоит из scFv, которая избирательно связывает антиген. Если нужно, можно рандомизировать часть scFv (например, часть вариабельной области scFv). В некоторых вариантах осуществления антигенсвязывающий домен избирательно связывает белок. Альтернативно, антигенсвязывающий домен может избирательно связывать углевод, экспрессированный на мишени, такой как, например, грибок, вирус, бактерия или злокачественная клетка. Например, в некоторых вариантах осуществления антигенсвязывающий домен содержит или состоит из дектина-1, который может избирательно связывать β-глюканы и углевод, присутствующий в клеточных стенках грибков. В некоторых вариантах осуществления CAR может избирательно связывать вирус, например, CAR может связывать вирусный белок, такой как белок оболочки вируса гепатита (например, Krebs et al., 2013). В некоторых вариантах осуществления антигенсвязывающий домен представляет собой цитокин. Антигенсвязывающий домен может избирательно связывать белок, углевод или сахар. В некоторых вариантах осуществления CAR получают из множества антигенсвязывающих доменов, которые избирательно связывают одну мишень, антиген, или антигенсвязывающие домены могут иметь перекрывающиеся антигены. В некоторых вариантах осуществления CAR получают из множества антигенсвязывающих доменов, которые избирательно связывают разные мишени или антигены. Эндодомен в CAR может приводить к возникновению ингибирующего сигнала (например, PD-1, CTLA-4, TIM-3, LAG-3, BTLA, ITIM, SHP-1, LAIR-1, TIGIT, Siglecs) или стимулирующего сигнала (например, CD27, CD28, ICOS, CD134, CD137, LCK, DAP10, ITAM, ZAP-70, LAT, SLP-76, цитокины, а также рецепторы цитокинов; а также комбинации и мутации) в клетке, экспрессирующей CAR, такой как, например, T-клетка или клетка - естественный киллер (NK). Когда антигенсвязывающая область избирательно узнает антиген, эндодомен может заставлять или стимулировать клетку (например, T-клетку или NK-клетку), содержащую CAR, активировать уничтожение, миграцию, дифференциацию, дедифференциацию клетки, или приводить к индукции апоптозного сигнала в клетке. Апоптозный сигнал может включать или представлять собой апоптозный сигнал CTLA4 и/или апоптозный сигнал PD1 (белок программируемой гибели 1). В некоторых вариантах осуществления более одного отдельного CAR может быть экспрессировано в клетке, такой как, например, T-клетка или NK-клетка. Например, первый CAR и второй CAR могут экспрессироваться в клетке, при этом первый CAR избирательно связывает антиген на здоровой клетке и индуцирует ингибирующий сигнал через первый эндодомен (например, снижая вероятность того, что T-клетка или NK-клетка повредит здоровую клетку), а второй CAR избирательно связывает антиген на клетке-мишени (например, злокачественной клетке, грибке, инфицированной вирусом клетке, бактерии) и индуцирует стимулирующий сигнал через второй эндодомен (например, стимулируя или вызывая уничтожение клетки-мишени T-клеткой или NK-клеткой). CAR, полученный способами по настоящему изобретению, можно встраивать в целевую клетку, такую как, например, T-клетка или NK-клетка, в виде интегрирующей ДНК (например, путем электропорации и гомологичной рекомбинации с помощью вектора или системы транспозазы/транспозона) или в виде не интегрирующей ДНК или РНК (например, вирусная доставка мРНК с использованием такого вирусного вектора, как, например, лентивирус или ретровирус). В некоторых вариантах осуществления T-клетка, кодирующая CAR по настоящему изобретению, представляет собой иммортализованную клетку; такие иммортализованные клетки можно использовать для оценки или измерения терапевтического потенциала или токсичности CAR. Таким образом, множество CAR можно подвергать скринингу на желательный фармакологический профиль, токсичность в отношении болезнетворных клеток или патогенов, отсутствие токсичности для здоровых клеток и/или терапевтическую эффективность.
Таблица 1. Молекулы ДНК, которые можно комбинировать в качестве антигенсвязывающего домена-шарнирного-сигнального доменов для создания CAR
ζ - дзета; Δ - мутант; примечание=4-1BB также называют CD137; «+» означает слияние разных областей.
Например, в некоторых вариантах осуществления можно использовать следующие антигенсвязывающие домены, шарниры/каркасы, трансмембранные домены и эндодомены, которые приведены в таблице 2. Примеры последовательностей, входящих в сигнальные домены, например, в таблице 1 или таблице 2, включают CD27 (SEQ ID NO: 41), CD28 (SEQ ID NO: 42), CD28Δ (SEQ ID NO: 43), CD134 (OX40) (SEQ ID NO: 44), CD137 (41BB) (SEQ ID NO: 45), ICOS (SEQ ID NO: 46) и CD3-дзета (SEQ ID NO: 47). Примеры анти-EGFR доменов scFv, приведенных в таблице 2, включают нимотуксимаб (SEQ ID NO: 48) и цетуксимаб (SEQ ID NO: 49). В качестве примера scFv против фосфатидилсерина, приведенных в таблице 2, можно назвать бавитуксимаб (SEQ ID NO: 50).
Таблица 2: Пример библиотек, используемых для создания CAR
Используемый в настоящем документе термин «химерные антигенные рецепторы (CAR)» или «CAR» включает искусственные T-клеточные рецепторы, химерные T-клеточные рецепторы или химерные иммунорецепторы. CAR, как правило, представляют собой сконструированные рецепторы, которые могут придавать искусственную специфичность конкретной иммунной эффекторной клетке. CAR можно использовать для придания специфичности моноклонального антитела T-клетке, за счет этого создается возможность получения большого количества специфических T-клеток, например, для использования в адоптивной клеточной терапии. В некоторых вариантах осуществления CAR придают клетке специфичность в отношении ассоциированного с опухолью антигена. В предпочтительных вариантах осуществления CAR содержат эндодомен (содержащий внутриклеточный домен активации), трансмембранный домен, шарнирную или каркасную область и внеклеточный домен, содержащий направляющий домен (например, scFv из моноклонального антитела). В некоторых вариантах осуществления внеклеточный направляющий домен может представлять собой лиганд рецептора (например, пептид, который избирательно связывает белковый рецептор). В некоторых вариантах осуществления можно делать мишенью злокачественные клетки путем перенаправления специфичности T-клеток за счет использования CAR, специфического для злокачественных клеток (например, путем использования анти-CD19 scFv для нацеливания на раковые клетки B-линии дифференцировки).
Примеры областей scFv, шарнирных/каркасных областей, трансмембранных доменов и эндодоменов приведены в таблице 1, и примеры соответствующих последовательностей также приведены в настоящем документе. Обратите внимание, что в таблице 1 области scFv могут означать множество областей scFv для конкретной мишени (например, «CD19» в таблице 1 может означать одну последовательность моноклонального антитела или в некоторых предпочтительных вариантах осуществления это может означать множество областей scFv, полученных из моноклональных антител, которые избирательно направлены на CD19). Предполагается, что способы по настоящему изобретению можно использовать для получения CAR, представляющего собой, например, продукт слияния любого сочетания области scFv, шарнира/каркаса, трансмембранного домена и эндодомена из таблицы 1. Например, в некоторых вариантах осуществления CAR может содержать область scFv, избирательно направленную на CD19 (например, происходящую из мышиного, человеческого или гуманизированного моноклонального антитела), которая слита с шарнирной/каркасной областью IgG4 Fc, трансмембранным доменом CD28 и эндодоменом, содержащим CD28 и CD3ζ. В некоторых вариантах осуществления CAR может содержать область scFv, избирательно направленную на ROR1, которая слита с шарнирной/каркасной областью IgG4 Fc, трансмембранным доменом CD28 и эндодоменом, содержащим CD28 и CD3ζ. В некоторых вариантах осуществления CAR может содержать область scFv, избирательно направленную на ROR1, которая слита с шарнирной/каркасной областью IgG4 Fc, трансмембранным доменом CD28 и эндодоменом, содержащим 4-1BB и CD3ζ. В некоторых вариантах осуществления CAR может содержать область scFv, избирательно направленную на CD19 (например, происходящую из мышиного, человеческого или гуманизированного моноклонального антитела), которая слита с шарнирной/каркасной областью IgG4 Fc, трансмембранным доменом CD28 и эндодоменом, содержащим CD28 и CD3ζ.
Используемый здесь термин «антиген» означает молекулу, которая может быть связана антителом или T-клеточным рецептором. Антиген, как правило, можно использовать для вызывания гуморального иммунного ответа и/или клеточного иммунного ответа, приводящего к продуцированию B и/или T-лимфоцитов.
При использовании в настоящем описании форма единственного числа существительных может означать «один или более». При использовании в формуле изобретения настоящего документа в сочетании со словом «содержащий» форма единственного числа существительных может означать «один или более чем один».
Слово «или» в формуле изобретения используют в значении «и/или», если специально не указано, что это слово означает исключительно альтернативные варианты, или что альтернативные варианты являются взаимоисключающими, хотя в описании изобретения имеет силу определение, означающее только альтернативные варианты и «и/или». При использовании здесь «другой» может означать по меньшей мере второй или более.
В тексте данной заявки слово «примерно» используют для указания на то, что значение включает присущую погрешность устройства, способа, используемого для определения значения, или вариацию, которая существует среди субъектов исследования.
Другие цели, признаки и преимущества настоящего изобретения станут очевидными из следующего далее подробного описания. Следует понимать, однако, что подробное описание и конкретные примеры, демонстрирующие предпочтительные варианты осуществления изобретения, приведены исключительно с иллюстративной целью, поскольку различные изменения и модификации в пределах сущности и объема изобретения станут очевидными для специалистов в данной области из этого подробного описания.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Следующие чертежи составляют часть настоящего описания и включены для дополнительной демонстрации некоторых аспектов настоящего изобретения. Изобретение может быть лучше понято при ссылке на один или более из этих чертежей в сочетании с подробным описанием конкретных вариантов осуществления, приведенным в настоящем документе.
Фиг. 1. Клонирующие векторы, используемые для сборки CAR с использованием трех донорских плазмид, экспрессирующих (i) конкретные scFv, (ii) внеклеточные шарниры и (iii) эндодомены. Данный подход будет адаптирован для создания панелей CAR, различающихся по шарнирной, трансмембранной и внутриклеточной областям. Выполняют конструирование молекул CAR из компонентов scFv, IgG4 Fc (длинный шарнир) или CD8a (средний шарнир), или только пептида (короткий шарнир) и CD3ζ в сочетаниях с разными сигнальными доменами с использованием системы тройных сайтов рекомбинации. Происходит рекомбинация библиотеки scFv, отдельных каркасов и сигнальных доменов, закодированных в трех донорских плазмидах (исходные клоны), для экспрессии ДНК вектора. Этот подход позволяет получать множество видов CAR в формате scFv-B-каркас-C-сигнальный домен(ы).
Фиг. 2A-B: (фиг. 2A). Экспрессия CAR (Fc) и CD8+ в T-клетках через 66 дней после электропорации, определенная методом проточной цитометрии. Клетки были размножены в присутствии иАПК, нагруженных антигеном CD19 (клон 4); (фиг. 2B). Лизис CD19+ EL-4 сравнивали с фоновым лизисом CD19neg EL-4 в 4-ч анализе с высвобождением хрома при использовании CD19CAR+ T-клеток клинической категории (CG), CD19CAR+ T-клеток, полученных методом тройных сайтов рекомбинации (EZ CAR), и CARneg T-клеток. CARneg T-клетки были размножены в присутствии облученных и нагруженных анти-CD3 (OKT3) иАПК клона №4, полученных из клеток K562.
Фиг. 3: Конструкции CAR. CAR 212=SEQ ID NO: 4; CAR 213=SEQ ID NO: 5; CAR 214=SEQ ID NO: 56; CAR 215=SEQ ID NO: 57; CAR 216=SEQ ID NO: 58; CAR 217=SEQ ID NO: 2; CAR 218=SEQ ID NO: 59; CAR 193=SEQ ID NO: 55.
Фиг. 4: Отслеживаемые плазмиды «спящая красавица».
Фиг. 5: Экспрессия CAR.
Фиг. 6: Кинетика экспрессии CAR.
Фиг. 7: Фенотип.
Фиг. 8A-B: Расширенный фенотип представлен на фиг. 8A и фиг. 8B.
Фиг. 9: Вестерн-блот анализ.
Фиг. 10: Кинетика размножения.
Фиг. 11: Кратность размножения: Общее количество клеток.
Фиг. 12: Кратность размножения: CAR+ T-клетки.
Фиг. 13: Цитотоксичность.
Фиг. 14: 4-1BB CAR: Цитотоксичность.
Фиг. 15: ТМ домен: Цитотоксичность.
Фиг. 16: Спейсер (IgG4 против CD8): Цитотоксичность.
Фиг. 17: Продуцирование IFN-γ.
Фиг. 18: 4-1BB CAR: продуцирование IFN-γ.
Фиг. 19: ТМ домен: продуцирование IFN-γ.
Фиг. 20: Спейсер (IgG4 против CD8): продуцирование IFN-γ.
Фиг. 21: Безопасность: ПЦР для транспозазы SB11.
Фиг. 22: Безопасность: число копий CAR (кПЦР).
Фиг. 23: Безопасность: Автономный рост. Как показано на фигуре, наблюдается отсутствие автономного роста.
Фиг. 24: Конструкция CAR. Пример CAR приведен на правой стороне фигуры.
Фиг. 25: CD3-дзета. Искомая=SEQ ID NO: 51; исследуемая - верх=SEQ ID NO: 52; исследуемая - центр=SEQ ID NO: 53; исследуемая - низ=SEQ ID NO: 54.
Фиг. 26: Конструкции CAR.
Фиг. 27: CAR.
Фиг. 28: Экспрессия CAR.
Фиг. 29: Кинетика размножения.
Фиг. 30: Кинетика размножения.
Фиг. 31: Цитотоксичность.
Фиг. 32: Цитотоксичность.
Фиг. 33: Маркеры памяти. Показан процент экспрессии CD27, CD62L, CD28 и CCR7 на CAR+ T-клетках (экспрессионные конструкты показаны на фиг. 26).
Фиг. 34: Продуцирование IFN-γ.
Фиг. 35: Продуцирование IFN-γ (PMA-иономицин)
Фиг. 36: Автономный рост.
Фиг. 37: Число копий CAR.
Фиг. 38: Число копий CAR.
Фиг. 39: Число копий CAR.
Фиг. 40A-E: Была проведена трансфекция клеток 293-HEK плазмидами, несущими ДНК CAR (pSBSO EZ CAR) методом с липофектамином. Трансфицированные клетки анализировали методом проточной цитометрии после окрашивания анти-Fc или анти-идиотипическими (анти-CD19 svFv) антителами.
Фиг. 41A-B: фиг. 41A. Nalm-6; EL-4 CD19+ клетки; опухолевые клетки пациента с MCL и CLL (мишени), и ранее были модифицированы для экспрессии GFP. 5×103 клеток-мишеней инкубировали с CD19RIgG4CD28CAR T-клетками, CD19RCD8αCD28 CAR T-клетками и CARneg T-клетками (используемыми в качестве контроля) в возрастающих концентрациях в течение 4 часов. Через 4 часа клетки были перенесены в устройство iQue компании IntelliCyt и анализ данных был проведен с использованием его запатентованного программного обеспечения. Фиг. 42B. Графики представляют процент уничтожения CAR T-клетками клеток опухолей. Соотношение между эффекторными клетками и клетками-мишенями находилось в диапазоне от 0 до 40 клеток.
Фиг. 42: 5×103 клеток-мишеней (EL-4 CD19+ гранзим B клеточный репортер) инкубировали с CD19RIgG4CD28CAR T-клетками клинической категории, EZ CD19RCD8αCD28 CAR T-клетками и CARneg T-клетками (используемыми в качестве контроля) в возрастающих концентрациях в течение 4 и 10 часов. После завершения инкубации клетки были перенесены в устройство iQue компании IntelliCyt и анализ данных был проведен с использованием его запатентованного программного обеспечения. Графики представляют процент уничтожения CAR T-клетками клеток опухолей. Соотношение между эффекторными клетками и клетками-мишенями находилось в диапазоне от 0 до 20 клеток.
ОПИСАНИЕ ИЛЛЮСТРАТИВНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
В настоящем документе предложены способы получения химерных антигенных рецепторов (CAR). В способе используют множество векторов, каждый из которых кодирует антигенсвязывающий домен (например, область scFv), шарнирную область, трансмембранную область и/или эндодомен. Например, в некоторых вариантах осуществления первый вектор кодирует антигенсвязывающий домен, второй вектор кодирует шарнирную область, и третий вектор кодирует эндодомен. В некоторых вариантах осуществления трансмембранная область закодирована либо во втором векторе, в третьем векторе, либо в четвертом векторе. В некоторых предпочтительных вариантах осуществления векторы способны к гомологичной рекомбинации, с образованием нуклеиновой кислоты, кодирующей CAR, содержащий антигенсвязывающий домен, шарнирную область, трансмембранную область и эндодомен. Таким образом, можно создавать множество CAR и проводить скрининг на желаемую активность, такую как, например, избирательное узнавание и уничтожение раковой клетки, экспрессирующей антиген, который избирательно связывается CAR. Затем CAR может экспрессироваться в клетке, такой как T-клетка или клетка-естественный киллер (NK), в виде интегрирующей нуклеиновой кислоты (например, ДНК, интегрированной в геном хозяина с использованием транспозазы/транспозона) или в виде не интегрирующей нуклеиновой кислоты (например, мРНК, доставляемой с помощью вирусного вектора, такого как лентивирус или ретровирус). T-клетку или NK-клетку, экспрессирующую CAR, затем можно вводить в фармацевтическом препарате или эксципиенте субъекту, такому как пациент-человек, для лечения или предотвращения заболевания (например, рака, грибковой инфекции, бактериальной инфекции или вирусной инфекции).
I. Получение библиотеки
Библиотеки, кодирующие множество областей scFv, шарнирных/каркасных областей, трансмембранных доменов и эндодоменов (сигнальных доменов), можно получать методами, известными специалисту в данной области. В некоторых вариантах осуществления множество возможностей существует для двух или трех из областей scFv, шарнирных/каркасных областей и эндодоменов (сигнальных доменов). В некоторых вариантах осуществления множество возможностей существует для двух, трех или всех из областей scFv, шарнирных/каркасных областей, трансмембранных доменов и эндодоменов (сигнальных доменов). Примеры областей scFv, шарнирных/каркасных областей, трансмембранных доменов и эндодоменов (сигнальных доменов) приведены, например, в таблице 1. В некоторых вариантах осуществления библиотека может кодировать множество scFv, которые направлены на разные антигены, такие как несколько противораковых или направляющих на опухоль антигенов; в других вариантах осуществления библиотека может кодировать множество разных scFv, которые избирательно связывают одну мишень (например, один противораковый антиген, такой как CD19, и так далее). Таким образом, способы можно использовать либо для определения, какой направляющий на опухоль конструкт может действовать более эффективно для конкретного клеточного образца (например, для использования в персонализированной медицине), либо способы можно использовать для идентификации нового CAR, который действует более эффективно при направлении на конкретный антиген. Область scFv, как правило, содержит вариабельную легкую (VL) и вариабельную тяжелую (VH) цепь, полученные из антитела. В некоторых вариантах осуществления части областей VL и VH можно рандомизировать, если необходимо. Общие способы получения библиотек включают, например, создание дрожжевых библиотек, бактериальных, фаговых библиотек, инфильтрирующих B-клеток, гибридом (в том числе из клеток человека и грызунов) или библиотек из клеток лам, верблюдов, библиотек из клеток лошадей, а также in silico методы (смотри, например, Lennard, 2002).
В некоторых вариантах осуществления проводят слияние разных векторов, кодирующих scFv, шарнирную/каркасную область, трансмембранный домен и эндодомен, с образованием одного вектора, кодирующего CAR. Слияние может осуществляться за счет опосредованной транспозоном гомологичной рекомбинации.
Например, в некоторых вариантах осуществления векторы, кодирующие scFv, шарнирную/каркасную область, трансмембранный домен и/или эндодомен, могут представлять собой ДНК плазмиды «спящая красавица» (SB) или piggyBac. ДНК плазмиды «спящая красавица» (SB) и piggyBac описаны, например, в публикациях Maiti et al. (2013), Singh et al. (2008) и Huls et al. (2013). В некоторых вариантах осуществления транспозон опосредован Tc1-подобной транспозазой лососевых (SB). В некоторых предпочтительных вариантах осуществления вектор, кодирующий CAR, трансфицирован или включен в T-клетки субъекта, такого как пациент-человек с раком, методами, описанными в публикациях Singh et al., 2014 или Huls et al. Например, ДНК векторы, полученные с помощью системы «спящая красавица» (SB), можно использовать, чтобы избежать расходов и производственных сложностей, связанных с трансдуцированием T-клеток рекомбинантными вирусными векторами. После электропорации транспозон/транспозаза может повышать эффективность интеграции плазмид, используемых для экспрессии CAR и других трансгенов, в T-клетки. Система SB, скомбинированная с искусственными антигенпредставляющими клетками (иАПК), позволяет избирательно наращивать и производить CAR(+) T-клетки, подходящие для использования в организме человека. В некоторых вариантах осуществления за синхронным электропереносом двух ДНК плазмид, транспозона SB (кодирующего интересующий CAR) и транспозазы SB (например, SB11), может следовать отбор стабильных интегрантов путем добавления каждые 7 дней (цикл стимуляции) γ-облученных иАПК в присутствии растворимых рекомбинантных человеческих IL-2 и IL-21. Например, можно проводить 4 цикла (28 дней непрерывного культивирования) для достижения подходящих для клинического применения количеств T-клеток, стабильно экспрессирующих интересующий CAR. Систему транспозон/транспозаза можно использовать для доставки T-клеток, экспрессирующих CAR, как описано, например, в публикации Hackett et al.
II. Химерные антигенные рецепторы
Варианты осуществления настоящего изобретения включают получение и идентификацию нуклеиновых кислот, кодирующих полипептид антигенспецифического химерного антигенного рецептора (CAR). В некоторых вариантах осуществления CAR является гуманизированным для уменьшения иммуногенности (hCAR).
В некоторых вариантах осуществления CAR может узнавать эпитоп, состоящий из области, общей между одним или более антигенами. Распознающие структуру рецепторы, такие как дектин-1, можно использовать для создания специфичности в отношении углеводного антигена. В конкретных вариантах осуществления связывающая область может содержать определяющие комплементарность области моноклонального антитела, вариабельные области моноклонального антитела и/или его антигенсвязывающие фрагменты. В некоторых вариантах осуществления связывающая область представляет собой scFv. В другом варианте осуществления пептид (например, цитокин), который связывается с рецептором или клеточной мишенью, может быть включен в качестве возможной или заменяющей scFv области в связывающую область CAR. Таким образом, в некоторых вариантах осуществления CAR можно создавать из множества векторов, кодирующих множество областей scFv и/или других направляющих белков. Определяющая комплементарность область (CDR) представляет собой короткую аминокислотную последовательность, присутствующую в вариабельных доменах белков - рецепторов антигена (например, иммуноглобулина и T-клеточного рецептора), которая соответствует антигену и, таким образом, обеспечивает рецептору специфичность для конкретного антигена. Каждая полипептидная цепь рецептора антигена содержит три области CDR (CDR1, CDR2, и CDR3). Поскольку рецепторы антигена, как правило, состоят из двух полипептидных цепей, у каждого антигенного рецептора имеется шесть CDR, которые вступают в контакт с антигеном - каждая тяжелая и легкая цепь содержит три CDR. Поскольку большинство вариаций в последовательности, связанных с избирательностью иммуноглобулинов и T-клеточного рецептора, как правило, имеют место в областях CDR, эти области иногда называют гипервариабельными доменами. Среди них, область CDR3 обладает наибольшей вариабельностью, поскольку она закодирована за счет рекомбинации областей VJ (VDJ в случае тяжелой цепи и αβ цепи TCR).
Кодирующая CAR нуклеиновая кислота, полученная по настоящему изобретению, может содержать один или более генов, либо генных фрагментов человека для усиления клеточной иммунотерапии для пациентов-людей. В некоторых вариантах осуществления полноразмерная кДНК CAR или кодирующая область может быть получена способами, описанными в настоящем документе. Антигенсвязывающие области или домен могут содержать фрагмент цепей VH и VL одноцепочечного вариабельного фрагмента (scFv), происходящего из конкретного человеческого моноклонального антитела, таких как те, которые описаны в патенте США 7109304, содержание которого включено в настоящий документ посредством ссылки. В некоторых вариантах осуществления scFv содержит антигенсвязывающие домены человеческого антигенспецифического антитела. В некоторых вариантах осуществления область scFv представляет собой антигенспецифическую scFv, закодированную последовательностью, которая оптимизирована в соответствии с частотой использования кодонов, свойственной человеку, для экспрессии в человеческих клетках.
Конструкция антигенсвязывающего домена CAR может быть мультимерной, такой как диатело или мультимеры. Мультимеры могут быть образованы за счет перекрестного спаривания вариабельных частей легкой и тяжелой цепей в структуру, которая может быть названа диателом. В некоторых вариантах осуществления шарнирная часть CAR может быть укорочена или исключена (то есть, с образованием CAR, который содержит только антигенсвязывающий домен, трансмембранную область и внутриклеточный сигнальный домен). Множество шарнирных областей можно использовать по настоящему изобретению, например, приведенных в таблице 1. В некоторых вариантах осуществления шарнирная область может иметь первый остаток цистеина, сохраненный или мутированный за счет замены на остаток пролина или серина, или быть укорочена вплоть до первого остатка цистеина. Fc-часть может быть делетирована из scFv, используемой в качестве антигенсвязывающей области для получения CAR в соответствии с настоящим изобретением. В некоторых вариантах осуществления антигенсвязывающая область может кодировать только один из Fc-доменов, например, или CH2, или CH3 домен из человеческого иммуноглобулина. Также можно включать шарнир, CH2 и CH3 область человеческого иммуноглобулина, которые были модифицированы для улучшения димеризации и олигомеризации. В некоторых вариантах осуществления шарнирная часть может содержать или состоять из пептида длиной 8-14 аминокислот (например, пептид 12 ак), части CD8α или IgG4 Fc. В некоторых вариантах осуществления антигенсвязывающий домен может быть подвешен к клеточной поверхности с использованием домена, который способствует олигомеризации, такого как CD8-альфа. В некоторых вариантах осуществления антигенсвязывающий домен может быть подвешен к клеточной поверхности с использованием домена, который узнается моноклональным антителом (мАт) клона 2D3 (мАт клона 2D3 описано, например, в публикации Singh et al., 2008).
Эндодомен или внутриклеточный сигнальный домен CAR, как правило, может вызывать или стимулировать активацию по меньшей мере одной из нормальных эффекторных функций иммунной клетки, содержащей CAR. Например, эндодомен может стимулировать такую эффекторную функцию T-клетки, как, например, цитолитическая активность или хелперная активность, включая секрецию цитокинов. Эффекторная функция у «необученной» T-клетки, T-клетки памяти или T-клетки типа клетки памяти, может включать антиген-зависимую пролиферацию. Термин «внутриклеточный сигнальный домен» или «эндодомен» относится к части CAR, которая может передавать сигнал эффекторной функции и/или направлять клетку на выполнение специализированной функции. Хотя, как правило, целый внутриклеточный сигнальный домен может быть включен в CAR, в некоторых случаях можно включать укороченную часть эндодомена. Как правило, эндодомены включают укороченные эндодомены, при этом укороченный эндодомен сохраняет способность к передаче сигнала эффекторной функции в клетке.
В некоторых вариантах осуществления эндодомен содержит дзета-цепь T-клеточного рецептора или любую из ее гомологов (например, эта, дельта, гамма или эпсилон), MB1 цепь, B29, Fc RIII, Fc RI, а также сочетание сигнальных молекул, например, CD3ζ и CD28, CD27, 4-1BB, DAP-10, OX40, а также их сочетания, а также другие аналогичные молекулы и фрагменты. Можно использовать внутриклеточные сигнальные фрагменты других членов семейств активирующих белков, таких как FcγRIII и FcεRI. Примеры этих альтернативных трансмембранных и внутриклеточных доменов можно найти, например, в публикациях Gross et al. (1992), Stancovski et al. (1993), Moritz et al. (1994), Hwu et al. (1995), Weijtens et al. (1996) и Hekele et al. (1996), полное содержание которых включено в настоящий документ посредством ссылки. В некоторых вариантах осуществления эндодомен может содержать человеческий внутриклеточный домен CD3ζ.
Антигенспецифический внеклеточный домен и внутриклеточный сигнальный домен предпочтительно связаны с помощью трансмембранного домена. Трансмембранные домены, которые можно включать в CAR, включают, например, человеческие IgG4 Fc шарнирную и Fc-области, человеческий трансмембранный домен CD4, человеческий трансмембранный домен CD28, трансмембранный человеческий домен CD3ζ, или мутантный по цистеину человеческий домен CD3ζ, или трансмембранные домены из человеческого трансмембранного сигнального белка, такого как, например, CD16 и CD8, и рецептор эритропоэтина. Примеры трансмембранных доменов приведены, например, в таблице 1.
В некоторых вариантах осуществления эндодомен содержит последовательность, кодирующую костимулирующие рецепторы, такие как, например, модифицированный внутриклеточный сигнальный домен CD28 или костимулирующий рецептор CD28, CD27, OX-40 (CD134), DAP10 или 4-1BB (CD137). В некоторых вариантах осуществления как первичный сигнал, инициируемый CD3 ζ, так и дополнительный сигнал, обеспечиваемый человеческим костимулирующим рецептором, можно включать в CAR для более эффективной активации трансформированных T-клеток, что может способствовать улучшению персистенции in vivo и терапевтическому успеху адоптивной иммунотерапии. Как указано в таблице 1, эндодомен или внутриклеточный рецепторный сигнальный домен может содержать дзета-цепь CD3, одну или в сочетании с костимулирующими сигнальными доменами Fcγ RIII, такими как, например, CD28, CD27, DAP10, CD137, OX40, CD2, 4-1BB. В некоторых вариантах осуществления эндодомен содержит часть или все из одного или более из дзета-цепи TCR, CD28, CD27, OX40/CD134, 4-1BB/CD137, FcεRIγ, ICOS/CD278, IL-2Rбета/CD122, IL-2Rальфа/CD132, DAP10, DAP12 и CD40. В некоторых вариантах осуществления 1, 2, 3, 4 или более цитоплазматических доменов можно включать в эндодомен. Например, установлено, что в некоторых CAR по меньшей мере два или три сигнальных домена, слитые вместе, могут приводить к аддитивному или синергетическому эффекту.
В некоторых аспектах можно получать выделенный сегмент нуклеиновой кислоты и экспрессионную кассету, содержащую последовательности ДНК, кодирующие CAR. Можно использовать различные векторы. В некоторых предпочтительных вариантах осуществления с помощью вектора можно доставлять ДНК, кодирующую CAR, в иммунные клетки, такие как T-клетки. Экспрессия CAR может происходить под контролем регулируемого эукариотического промотора, такого как, например, промотор MNDU3, промотор CMV, промотор EF1-альфа или промотор убиквитина. Кроме того, вектор может содержать селективный маркер, если не по другой причине, то для облегчения манипуляций in vitro. В некоторых вариантах осуществления CAR может быть экспрессирован in vitro с мРНК, транскрибированной с ДНК-матрицы.
Молекулы химерного антигенного рецептора являются рекомбинантными и характеризуются их способностью как связывать антиген, так и передавать сигналы активации за счет фрагментов активации иммунорецепторов (ITAM), имеющихся в их цитоплазматической части. Рецепторные конструкты, в которых используют антигенсвязывающий фрагмент (например, полученный из одноцепочечных антител (scFv)), имеют дополнительное преимущество, являясь «универсальными», поскольку они могут связывать нативный антиген на поверхности клетки-мишени независимым от HLA образом. Например, можно осуществлять слияние конструктов scFv с последовательностями, кодирующими внутриклеточную часть дзета-цепи (ζ) комплекса CD3, гамма-цепи Fc-рецептора и sky тирозинкиназы (Eshhar et al., 1993; Fitzer-Attas et al., 1998). Эффекторные механизмы перенаправленных T-клеток, включая узнавание опухоли и лизис за счет CTL, были отмечены для нескольких мышиных и человеческих систем антиген-scFv: ζ (Eshhar et al., 1997; Altenschmidt et al., 1997; Brocker et al., 1998).
Антигенсвязывающая область может, например, быть из человеческих или не принадлежащих человеку scFv. Одной из возможных проблем при использовании антигенсвязывающих областей, не принадлежащих человеку, например, из мышиных моноклональных антител, является сниженная эффекторная функция в организме человека и сниженная способность проникать в опухолевые массы. Кроме того, моноклональные антитела, отличные от человеческих, могут узнаваться в организме хозяина-человека как чужеродный белок и, таким образом, повторяющиеся инъекции таких чужеродных антител могут являться причиной индукции иммунных ответов, приводящих к причиняющим вред реакциям гиперчувствительности. В случае мышиных моноклональных антител этот эффект был назван ответом «антитела человека против антител мыши» (HAMA). В некоторых вариантах осуществления при включении последовательностей человеческого антитела или scFv в CAR может иметь место небольшой, или вовсе отсутствовать, HAMA ответ по сравнению с использованием некоторых мышиных антител. Аналогично, включение человеческих последовательностей в CAR можно использовать для уменьшения или избегания риска опосредованного иммунной системой узнавания или элиминации эндогенными T-клетками, которые имеются у реципиента и могут узнавать процессированный антиген в контексте HLA.
В некоторых вариантах осуществления CAR содержит: a) внутриклеточный сигнальный домен, b) трансмембранный домен, c) шарнирную область и d) внеклеточный домен, содержащий антигенсвязывающую область. В некоторых вариантах осуществления внутриклеточный сигнальный домен и трансмембранный домен закодированы с эндодоменом в одном векторе, который может быть слит (например, посредством транспозон-направленной гомологичной рекомбинации) с вектором, кодирующим шарнирную область, и вектором, кодирующим антигенсвязывающую область. В других вариантах осуществления внутриклеточная сигнальная область и трансмембранная область могут быть закодированы двумя отдельными векторами, которые являются слитыми (например, посредством транспозон-направленной гомологичной рекомбинации).
В некоторых вариантах осуществления антигенспецифическая часть CAR, также называемая внеклеточным доменом, содержащая антигенсвязывающую область, избирательно направлена на ассоциированный с опухолью антиген. Ассоциированный с опухолью антиген может быть любого типа при условии, что он экспрессирован на клеточной поверхности клеток опухолей. Примеры ассоциированных с опухолью антигенов, на которые могут быть направлены CAR, полученные в соответствии с настоящим изобретением, включают, например, CD19, CD20, канцероэмбриональный антиген, альфафетопротеин, CA-125, MUC-1, CD56, EGFR, c-Met, AKT, Her2, Her3, эпителиальный опухолевый антиген, ассоциированный с меланомой антиген, мутантный p53, мутантный ras, дектин-1 и так далее. В некоторых вариантах осуществления эта антигенспецифическая часть CAR представляет собой scFv. Примеры направленных на опухоли scFv приведены в таблице 1. В некоторых вариантах осуществления CAR может быть совместно экспрессирован с мембраносвязанным цитокином, например, для улучшения персистенции в случае низкого количества ассоциированного с опухолью антигена. Например, CAR может быть совместно экспрессирован с мембраносвязанным IL-15.
В некоторых вариантах осуществления внутриклеточный ассоциированный с опухолью антиген, такой как, например, HA-1, сурвивин, WT1 и p53, может являться мишенью для CAR. Это может быть достигнуто при использовании CAR, экспрессированного на универсальной T-клетке, которая узнает процессированный пептид, происходящий из внутриклеточного ассоциированного с опухолью антигена, в контексте HLA. Кроме того, универсальную T-клетку можно генетически модифицировать для экспрессии спаренного T-клеточного рецептора, который узнает процессированный внутриклеточный ассоциированный с опухолью антиген в контексте HLA.
Патоген, узнаваемый CAR, может быть патогеном практически любого типа, однако в некоторых вариантах осуществления патоген представляет собой грибок, бактерию или вирус. Иллюстративные вирусные патогены включают патогены из семейств Adenoviridae, вирус Эпштейна-Барр (EBV), цитомегаловирус (CMV), респираторно-синцитиальный вирус (RSV), JC вирус, BK вирус, HSV, семейство вирусов HHV, Picornaviridae, Herpesviridae, Hepadnaviridae, Flaviviridae, Retroviridae, Orthomyxoviridae, Paramyxoviridae, Papovaviridae, полиомавирус, Rhabdoviridae и Togaviridae. Иллюстративные патогенные вирусы являются возбудителями оспы, гриппа, эпидемического паротита, кори, ветряной оспы, лихорадки эбола и краснухи. Иллюстративные патогенные грибки включают Candida, Aspergillus, Cryptococcus, Histoplasma, Pneumocystis и Stachybotrys. Иллюстративные патогенные бактерии включают Streptococcus, Pseudomonas, Shigella, Campylobacter, Staphylococcus, Helicobacter, E. coli, Rickettsia, Bacillus, Bordetella, Chlamydia, Spirochetes и Salmonella. В некоторых вариантах осуществления рецептор дектин-1 для патогенов можно использовать для создания CAR, который узнает углеводную структуру на клеточной стенке такого грибка, как Aspergillus. В другом варианте осуществления можно создавать CAR на основе антитела, узнающего вирусные детерминанты (например, гликопротеины из CMV и вируса эбола), для остановки вирусной инфекции и патологии.
В некоторых вариантах осуществления «голую» ДНК или подходящий вектор, кодирующий CAR, можно вводить в T-клетки субъекта (например, T-клетки, полученные от пациента-человека с раком или другим заболеванием). Способы стабильного трансфицирования T-клеток методами электропорации с использованием «голой» ДНК известны в данной области. Смотри, например, патент США № 6410319. «Голая» ДНК, как правило, означает ДНК, кодирующую химерный рецептор по настоящему изобретению, содержащуюся в плазмидном экспрессионном векторе в правильной ориентации для экспрессии. В некоторых вариантах осуществления использование «голой» ДНК может сокращать время, необходимое для получения T-клеток, экспрессирующих CAR, полученный способами по настоящему изобретению.
Альтернативно, можно использовать вирусный вектор (например, ретровирусный вектор, аденовирусный вектор, аденоассоциированный вирусный вектор или лентивирусный вектор) для введения химерного конструкта в T-клетки. Как правило, вектор, кодирующий CAR, который используют для трансфицирования T-клетки от субъекта, не должен реплицироваться в T-клетках субъекта. Известно большое число векторов на основе вирусов, в случае которых число копий вируса, поддерживаемое в клетке, является достаточно низким, чтобы сохранялась жизнеспособность клетки. Иллюстративные векторы включают векторы pFB-neo (STRATAGENE®), а также векторы на основе HIV, SV40, EBV, HSV или BPV.
После того, как установлено, что трансфицированная или трансдуцированная T-клетка способна экспрессировать CAR в виде поверхностного мембранного белка с нужной регуляцией и на нужном уровне, можно определять, является ли химерный рецептор функциональным в клетке-хозяине для обеспечения индукции нужного сигнала. Впоследствии трансдуцированные T-клетки можно возвращать или вводить субъекту для активации противоопухолевых ответов у субъекта. Для облегчения введения трансдуцированные T-клетки можно включать в фармацевтическую композицию или включать в имплантат, подходящий для введения in vivo, с соответствующими носителями или разбавителями, которые предпочтительно являются фармацевтически приемлемыми. Способы получения такой композиции или имплантата описаны в данной области (смотри, например, Remington's Pharmaceutical Sciences, 16е издание, Mack, ed. (1980)). Когда это целесообразно, трансдуцированные T-клетки, экспрессирующие CAR, можно формулировать в препарат в полутвердой или жидкой форме, такой как капсула, раствор, инъекция, ингаляционное средство или аэрозоль, обычным образом для соответствующего им пути введения. Можно использовать способы, известные в данной области, для предотвращения или сведения к минимуму высвобождения и абсорбции композиции до того, как она достигнет целевой ткани или органа, либо для гарантии своевременного высвобождения композиции. Как правило, предпочтительно использовать фармацевтически приемлемую форму, которая не лишает эффективности клетки, экспрессирующие химерный рецептор. Таким образом, желательно, чтобы T-клетки были включены в фармацевтическую композицию, содержащую сбалансированный солевой раствор, такой как сбалансированный солевой раствор Хэнкса или обычный солевой раствор.
III. Искусственные антигенпредставляющие клетки
В некоторых случаях иАПК полезны для получения основанных на CAR терапевтических композиций и препаратов клеточной терапии. Для общего руководства по получению и использованию антигенпредставляющих систем смотри, например, патенты США №№ 6225042, 6355479, 6362001 и 6790662; публикации патентных заявок США №№ 2009/0017000 и 2009/0004142, а также международную публикацию № WO 2007/103009).
иАПК можно использовать для наращивания T-клеток, экспрессирующих CAR. При встрече с опухолевым антигеном сигналы, доставляемые T-клеткам антигенпредставляющими клетками, могут влиять на программирование T-клеток и их последующую терапевтическую эффективность. Это обстоятельство стимулировало усилия по разработке искусственных антигенпредставляющих клеток, позволяющих осуществлять контроль над сигналами, поступающими к T-клеткам (Turtle et al., 2010). Помимо интересующих антитела или антигена, системы иАПК также могут содержать по меньшей мере одну экзогенную вспомогательную молекулу. Можно использовать любое подходящее число и сочетание вспомогательных молекул. Вспомогательную молекулу можно выбирать из таких вспомогательных молекул, как костимулирующие молекулы и молекулы адгезии. Иллюстративные костимулирующие молекулы включают CD70 и B7.1 (также называемую B7 или CD80), которые могут связываться с молекулами CD28 и/или CTLA-4 на поверхности T-клеток, тем самым оказывая влияние, например, на размножение T-клеток, Th1 дифференциацию, кратковременное выживание T-клеток и секрецию цитокинов, таких как интерлейкин (IL)-2 (смотри Kim et al., 2004). Молекулы адгезии могут включать углевод-связывающие гликопротеины, такие как селектины, трансмембранные связывающие гликопротеины, такие как интегрины, кальций-зависимые белки, такие как кадгерины, а также однопроходные трансмембранные белки суперсемейства иммуноглобулинов (Ig), такие как молекулы межклеточной адгезии (ICAM), которые стимулируют, например, контакт клетки с клеткой или клетки с матриксом. Иллюстративные молекулы адгезии включают LFA-3 и ICAM, такие как ICAM-1. Устройства, методы и реагенты, полезные для отбора, клонирования, получения и экспрессии иллюстративных вспомогательных молекул, включая костимулирующие молекулы и молекулы адгезии, описаны, например, в патентах США №№ 6225042, 6355479 и 6362001.
Клетки, выбранные для получения из них иАПК, предпочтительно дефектны по внутриклеточному процессингу антигена, внутриклеточной направленной миграции пептидов и/или внутриклеточному нагружению пептидами молекул MHC класса I или класса II, или являются пойкилотермными (то есть, менее чувствительными к колебаниям температуры, чем линии клеток млекопитающих), либо обладают как дефектами, так и пойкилотермными свойствами. Предпочтительно, клетки, выбранные для получения из них иАПК, также лишены способности экспрессировать по меньшей мере один эндогенный аналог (например, эндогенную молекулу MHC класса I или класса II, и/или эндогенные вспомогательные молекулы, описанные выше) для экзогенных молекул MHC класса I или класса II и вспомогательных молекул, которые вводят в клетки. Кроме того, иАПК предпочтительно сохраняют дефекты и пойкилотермные свойства, которые имеются у клеток до того, как их модифицируют для получения иАПК. Иллюстративные иАПК либо представляют собой, либо происходят из линии клеток, дефицитной по транспортеру, ассоциированному с процессингом антигенов (TAP), такой как линия клеток насекомых. Иллюстративной пойкилотермной линией клеток насекомых является линия клеток дрозофилы, такая как линия клеток Schneider 2 (например, Schneider, J.m 1972). Иллюстративные способы получения, наращивания и культивирования клеток Schneider 2 описаны в патентах США №№ 6225042, 6355479 и 6362001.
иАПК можно подвергать циклу замораживания-размораживания. Например, иАПК можно замораживать, создавая контакт соответствующего сосуда, содержащего иАПК, с подходящим количеством жидкого азота, твердого диоксида углерода (сухого льда) или аналогичного низкотемпературного материала так, чтобы замораживание происходило быстро. Затем замороженные иАПК размораживают, либо извлекая иАПК из низкотемпературного материала и перенося в условия обычной комнатной температуры, либо применяя метод ускоренного размораживания, в котором для сокращения времени размораживания используют умеренно теплую водяную баню или теплую руку. Кроме того, иАПК можно замораживать и хранить в течение длительного периода времени до размораживания. Замороженные иАПК также можно размораживать и затем лиофилизировать до дальнейшего использования. Консерванты, которые могут неблагоприятно влиять на процедуру замораживания-размораживания, такие как диметилсульфоксид (ДМСО), полиэтиленгликоли (ПЭГ) и другие консерванты, предпочтительно не должны содержаться в среде, содержащей иАПК, которые подвергают циклу замораживания-размораживания, или должны быть в значительной степени удалены, например, путем переноса иАПК в среду, практически лишенную таких консервантов.
В других предпочтительных вариантах осуществления ксеногенная нуклеиновая кислота и нуклеиновая кислота, эндогенная для иАПК, могут быть инактивированы путем сшивки, так что практически никакого клеточного роста, репликации или экспрессии нуклеиновой кислоты не происходит после инактивации. Например, иАПК можно инактивировать после экспрессии экзогенных молекул MHC и вспомогательных молекул, представления таких молекул на поверхности иАПК и нагружения представленных MHC молекул выбранным пептидом или пептидами. Соответственно, такие инактивированные и нагруженные выбранным пептидом иАПК, хотя и практически неспособные к пролиферации или репликации, могут сохранять функцию представления выбранного пептида. Сшивка также может приводить к получению иАПК, которые практически свободны от загрязняющих микроорганизмов, таких как бактерии и вирусы, без существенного снижения антигенпредставляющей функции иАПК. Таким образом, сшивку можно использовать для сохранения важных АПК функций у иАПК, при этом устраняя беспокойство по поводу безопасности препарата клеточной терапии, разработанного с использованием иАПК. Для получения информации о методах, имеющих отношение к сшивке и иАПК, смотри, например, публикацию патентной заявки США № 20090017000, содержание которой включено в настоящий документ посредством ссылки.
IV. Примеры
Следующие примеры включены для демонстрации предпочтительных вариантов осуществления изобретения. Специалистам в данной области должно быть понятно, что методы, раскрытые в следующих далее примерах, представляют собой методы, которые, как установлено авторами изобретения, хорошо подходят для осуществления на практике изобретения и, таким образом, могут считаться предпочтительными методами для этого. Однако специалисты в данной области, в свете настоящего раскрытия, должны признать, что множество изменений можно вносить в раскрытые конкретные варианты осуществления и все еще получать подобный или аналогичный результат без отклонения от сущности и объема изобретения.
Пример 1
Материалы и методы
Получение ДНК плазмид клинической категории
Транспозон SB, CoOpCD19RCD28 ζ/pSBSO, экспрессирует оптимизированный по кодонам для человека (CoOp) CoOpCD19RCD28ζ CAR 2го поколения под контролем гибридного композитного промотора EF-1/HTLV (InvivoGen), состоящего из фактора элонгации 1a (EF-1a [Kim et al., 1990] и 5’-нетранслируемой области вируса T-клеточного лейкоза человека (HTLV) [Singh et al., 2011; Davies et al., 2010]. Получение этой ДНК плазмиды описано на фигуре 1. Транспозаза SB, SB11, под промотором цитомегаловируса (CMV) экспрессируется в цис-форме с ДНК плазмиды pCMV-SB11 (Singh et al., 2011; Singh et al., 2008). Обе плазмиды были полностью секвенированы и изготовлены в Waisman Clinical Biomanufacturing Facility (Madison, WI) с использованием канамицина для отбора бактериального штамма DH5a E. coli.
Получение ДНК плазмид с тройной сайт-специфической рекомбинацией - EZ-собранных-CAR
С использованием последовательности ДНК из CAR, описанного выше (CoOpCD19RCD28z/pSBSO), части: CD19 ScFv, шарнир IgG4 Fc и трансмембранную и цитозольную части домена CD28, конъюгированные с сигнальным доменом CD3ζ, фланкировали сайтами рекомбинации лямбда, синтезировали с помощью Geneart (Life Technologies) в виде ПЦР-продуктов. Эти три части индивидуально вставляли в плазмиды pDonors221 (с помощью фермента BP клоназы (оба реагента от компании Invitrogen)). Проводили рекомбинацию трех плазмид с использованием тройной сайт-специфической рекомбинации плазмиды «спящая красавица» при помощи фермента LR PLUS клоназы (Invitrogen), с получением EZ-собранного CD19CD28ζ CAR в формате scFv-B-каркас-C-сигнальный домен(ы) (фиг. 1).
Подсчет клеток
Анализ с исключением трипанового синего использовали для различения живых и мертвых клеток и подсчета на приборе Cellometer (Nexecelom Bioscience) (Singh et al., 2011).
Выделение МКПК
Продукты лейкафереза от двух здоровых доноров-добровольцев мужского пола приобретали у компании Key Biologics LLC (Memphis, TN). Мононуклеарные клетки периферической крови (МКПК) выделяли в системе Biosafe Sepax (Eysins, Switzerland), адаптированной авторами изобретения для работы в соответствии с требованиями cGMP. Вкратце, после закрытия всех зажимов в устройстве CS-900, 100 мл фиколла (GE Healthcare) асептически переносили с помощью 60-мл шприцев в мешок с градиентом плотности среды («мешок с фиколлом») через соединитель с люэровской насадкой, и трубку термически запаивали с помощью ручного устройства для запаивания (Sebra, модель № 2380). Устройство было подключено с помощью иглы к 1000-мл мешку, содержащему буфер CliniMACS (PBS/ЭДТА, Miltenyi, каталожный № 70026) с 20 мл 25% человеческого сывороточного альбумина (ЧСА) (Baxter) (2% по объему, промывочный буфер), для промываний, мешку для конечного продукта [300-мл переносной пакет с переходником (Baxter/Fenwal 4R2014)] и мешку с реагентом/кровью. Используя протокол разделения в градиенте плотности (v126), поршень шприца помещали в центрифужную камеру и покрывали Sepax иАПК (клон № 4) для избирательного размножения CAR+ T-клеток. Использовали c-облученные иАПК для увеличения количества генетически модифицированных T-клеток. Размороженные иАПК от WCB наращивали в CM вплоть до 60 дней в мешках для культивирования клеток VueLife и собирали, используя процедуру сбора Biosafe Sepax II. Вкратце, устройство CS-490.1 соединяли с 300-мл мешком для конечного продукта (переносным пакетом) через соединитель с люэровской насадкой. Разделительную камеру устанавливали в углубление, трубку вставляли в оптический датчик и запорные краны устанавливали в T-положении. После подключения линии датчика давления мешок с продуктом и мешки с супернатантом/плазмой подвешивали на держателе. В меню Sepax выбирали модифицированный протокол PBSCv302 и входной объем обрабатываемого продукта (начальный объем) устанавливали на #840 мл. После валидации и тестирования устройства начинали процедуру. После завершения мешки удаляли, зажимы закрывали и устройство удаляли. Клетки из мешка с конечным продуктом асептически извлекали, дважды промывали промывочной средой (10% ЧСА в Plasmalyte) и подсчитывали. иАПК облучали (100 Гр) с использованием облучающего устройства CIS BIO International (IBL-437 каталожный № 09433) и замораживали для более позднего использования в среде для криоконсервации, используя морозильную камеру с контролируемой скоростью замораживания (Planer Kryo 750). Нагруженные анти-CD3 (OKT3) иАПК клона № 4, полученные из клеток K562, использовали для наращивания контрольных (CARneg) аутологичных T-клеток, не подвергнутых генетической модификации. Полученные из культуры иАПК инкубировали в течение ночи в бессывороточной среде X-Vivo 15 (каталожный № 04-744Q, Lonza), содержащей 0,2% ацетилцистеина (Acetadote, Cumberland Pharmaceuticals), называемой средой для нагружения (LM). На следующий день клетки промывали, облучали (100 Гр) с использованием облучающего устройства Gamma Cell 1000 Elite Cs-137 (MDS Nordion), ресуспендировали в LM в концентрации 106 клеток/мл вместе с очищенными антителами против CD3 человека (клон-OKT3, 16-0037-85, eBioscience) функциональной категории в количестве 1 мг/106 клеток и инкубировали при осторожном перемешивании на 3-D вращающем устройстве (Lab-Line) при температуре 4°C в течение 30 минут. После трех промываний LM клетки использовали в экспериментах или замораживали аликвотами в парах жидкого азота для последующего использования.
Изготовление CAR+ T-клеток
Размороженные МКПК ресуспендировали в (i) наборе человеческих T-клеток (каталожный № VPA-1002, Lonza; 100 мкл для 2×107 клеток в одной кювете) с (ii) ДНК плазмидой (CoOpCD19RCD28/pSBSO), кодирующей транспозон CD19RCD28 CAR (15 мкг сверхспиральной ДНК на 2×107 МКПК на кювету), и (iii) ДНК плазмидой (pCMVSB11), кодирующей транспозазу SB11 (5 мкг сверхспиральной ДНК на 2×107 МКПК на кювету). Эту смесь немедленно переносили в кювету (Lonza), подвергали электропорации (определяя день 0 культивирования) с использованием устройства Nucleofector II (программа U-14, Amaxa/Lonza), оставляли в 10% полной среде RPMI на 2-3 часа и, после замены половины среды, инкубировали в течение ночи при температуре 37°C в атмосфере 5% CO2. На следующий день клетки собирали, подсчитывали, определяли фенотип методом проточной цитометрии и совместно культивировали с c-облученными иАПК в соотношении 1:2 (CAR+ T-клетка:иАПК), что соответствовало дню 1 культивирования и началу 7-дневного цикла стимуляции. IL-21 (каталожный № AF-200-21, PeproTech) и IL-2 (каталожный № NDC 65483-116-07, Novartis) добавляли по схеме понедельник-среда-пятница, начиная со дня 1 и дня 7, соответственно. NK-клетки могут предотвращать увеличение количества CAR+ T-клеток, особенно если их избыточный рост происходит на ранних этапах процесса культивирования. Вследствие этого, проводили истощение по CD56, если количество CD3negCD56+ клеток возрастало на 10%, с использованием гранул для CD56 (каталожный № 70206, Miltenyi Biotech, 20 мл гранул/107 клеток) на колонках LS (каталожный № 130-042-401, Miltenyi Biotech) в буфере CliniMACS, содержащем 25% ЧСА (80 мл/107 клеток).
Получение контрольных CARneg T-клеток
В качестве контроля, 5×106 суррогатно трансфицированных МКПК совместно культивировали с облученными и нагруженными анти-CD3 (OKT3) иАПК клона #4, полученными из клеток K562, в соотношении 1:1 в 7-дневном цикле стимуляции. Во все культуры добавляли IL-21 (30 нг/мл), начиная со дня 1 культивирования, и IL-2 (50 Ед/мл), начиная через 7 дней после начала культивирования. Впоследствии все цитокины добавляли через день.
Иммунологический фенотип клеток
Клетки окрашивали с помощью антител в 100 мл буфера для FACS (2% ЭБС, 0,1% азида натрия) в течение 30 минут при температуре 4°C. Сбор данных производили с использованием прибора FACSCalibur (BD Bioscience) и анализировали с помощью программы FCS Express 3.00.0612.
Анализ с высвобождением хрома
T-клетки оценивали на их цитотоксичность в стандартном 4-часовом анализе с высвобождением хрома, используя 51Cr-меченые клетки-мишени. T-клетки высевали в тройном повторе при плотности 1×105, 0,5×105, 0,25×105, 0,125×105 в планшет (Costar). После инкубации 50 мкл супернатанта собирали в LumaPlate (Perkin Elmer), просчитывали на приборе TopCount NXT (Perkin Elmer), и процент специфического лизиса рассчитывали по формуле:

Спонтанное и максимальное высвобождение определяли путем количественного определения хрома в кондиционированном супернатанте от клеток-мишеней, инкубированных с CM или 0,1% Triton X-100 (Sigma), соответственно, и 0,0625×105 клеток/лунку с 5×103 клеток-мишеней в 96-луночном V-донном планшете (Manufacturee Novo Software, Thornhill, Ontario, Canada).
Пример 2
Получение CD19+ CAR
CD19+ CAR получали с использованием способа, описанного выше в примере 1 (называемого способом «EZ»). Эти CD19+ CAR (CD19CAR) сравнивали с CD19CAR клинической категории («CG»), полученными описанным ранее способом.
Данные показали, что система тройной сайт-специфической рекомбинации позволяла получать CD19CAR (EZ), аналогичные CD19CAR клинической категории (CG). Следы, оставленные сайтами рекомбинации в плазмидах, не мешали экспрессии и функционированию CAR (фиг. 2A-B).
Пример 3
Получение CAR, содержащих трансмембранные домены (CD8, CD28) и сигнальные домены (CD28, 4-1BB)
Различные протестированные CAR продемонстрировали сходные показатели размножения, цитотоксичности и Th1 цитотоксичности. CD19-BB-z продемонстрировал продуцирование Th2 цитокинов на более низком уровне; in vivo он был эффективным в контроле заболевания у мышей (Molecular Therapy 17 (8): 1453-1464, 2009). Тем не менее, существует опасение, связанное с тем, что клетки-мишени сохранялись in vitro без антигенной стимуляции.
CAR, используемые в клинике, приведены ниже в таблице 2. В некоторых вариантах осуществления CAR по настоящему изобретению не имеет конкретную конструкцию, показанную ниже в таблице 2. Альтернативно, в некоторых вариантах осуществления способы по настоящему изобретению можно использовать для получения другого вида CAR, имеющего характеристики CAR, указанного ниже в таблице 2, который, тем не менее, отличается от CAR, в настоящее время используемых в клинике.
Таблица 2: CAR в клинике
Дизайн конкретных конструктов CAR показан на фиг. 3. На фиг. 3 приведены схематические изображения различных CAR, полученных с использованием сочетания CD19 scfv, шарнира CD8α или стебля IgG4 Fc, трансмембранного (ТМ) домена CD8 или ТМ CD28, или TM CD137 и с сигнализацией через эндодомен CD28 или CD137 наряду с эндодоменом CD3-дзета.
Конструкты CAR, показанные на фиг. 3, затем клонировали в плазмиды «спящая красавица», содержащие маркеры SIM и FRA для отслеживания в исследованиях конкурентной репопуляции при амплификации с использованием обычного праймера CVseq7. Отслеживаемые плазмиды «спящая красавица» приведены на фиг. 4.
Конструкты CAR, показанные на фиг. 3, вводили электропорацией в T-клетки с использованием Amaxa Nucleofector II и совместно культивировали с иАПК в течение 28 дней в присутствии цитокинов (IL2, IL-21). Показана экспрессия CAR в день после электропорации (день 1) и через 28 дней совместного культивирования с иАПК (день 28). Приведены точечные диаграммы для CD3 и CAR, при этом CD3 и анти-CD19 scfv специфические Ат были использованы для распознавания T-клеток и CAR. Результаты экспрессии CAR показаны на фиг. 5.
Конструкты CAR, показанные на фиг. 3, оценивали на экспрессию CAR в течение 28 дней, и результаты приведены. Через 21 день большинство культур демонстрировали экспрессию CAR >80%. Кинетика экспрессии CAR показана на фиг. 6.
Процент экспрессии для CD4 и CD8 T-клеток в культурах после нуклеофекции CAR с фиг. 3 показан после 28 дней совместного культивирования с иАПК. Результаты для этих фенотипов показаны на фиг. 7.
Через 28 дней совместного культивирования CAR+ T-клетки (экспрессирующие CAR, показанные на фиг. 3) оценивали на экспрессию маркеров, связанных с памятью (CD45RA, CCR7, CD27), активацией (CD69, HLA-DR), цитотоксическими свойствами (перфорин, гранзим B), истощением/старением (CD57, KLRG1, PD1) и адгезией (CD39, CD150). Результаты для этого расширенного фенотипа приведены на фиг. 8A-B.
CAR+ T-клетки (экспрессирующие CAR, показанные на фиг. 3) оценивали на экспрессию CD3ζ методом вестерн-блоттинга. Клеточные лизаты разделяли электрофорезом в денатурирующих условиях, выполняли перенос, и экспрессию химерного CD3ζ измеряли с использованием первичных мышиных мАт против CD3ζ человека и HRP-конъюгированных антител козы против IgG мыши, используя субстрат SuperSignal West Femto Maximum Sensitivity. Наблюдали полосы химерного CD3ζ на уровне 52, 71 и 78 кДа в зависимости от размера конструктов CAR. Эти результаты вестерн-блоттинга приведены на фиг. 9.
T-клетки, в которые электропорацией были введены конструкты CAR (показанные на фиг. 3), стимулировали при помощи иАПК K562 в день 1 и затем каждые 7 дней в течение 28 дней. В конце каждого цикла стимуляции клетки подсчитывали, используя метод с исключением трипанового синего, и фенотипировали на экспрессию CD3 и CAR. Графики, приведенные на фиг. 10, показывают полученное количество клеток для всех, CD3 и CAR+ T-клеток с течением времени.
Было измерено размножение клеток. Кратность размножения для всех клеток (фиг. 11) и CAR+ (фиг. 12) T-клеток рассчитывали в день 14, 21 и 28 совместного культивирования путем сравнения количеств с результатами для дня 1 (после электропорации). Результаты приведены на фиг. 11 и фиг. 12.
Была измерена цитотоксичность для CAR-экспрессирующих T-клеток (CAR+ T-клеток). CAR+ T-клетки (экспрессирующие CAR, показанные на фиг. 3) оценивали на их цитотоксичность против CD19+ опухолевых клеток-мишеней (Daudiβ2m, NALM-6 и CD19+ EL-4) по сравнению с CD19neg EL-4 в стандартном 4-часовом анализе с высвобождением хрома. Результаты приведены на фиг. 13, фиг. 14, фиг. 15 и фиг. 16.
Определяли внутриклеточное продуцирование IFN-γ. CAR+ T-клетки (экспрессирующие конструкты, показанные на фиг. 3) инкубировали с (CD19+ и CD19neg) стимулирующими клетками в присутствии ингибитора белкового транспорта в течение 4-6 часов, фиксировали, пермеабилизировали и окрашивали специфическими для IFN-γ мАт. PMA-иономицин использовали в качестве положительного контроля. Результаты для внутриклеточного продуцирования IFN-γ показаны на фиг. 17, фиг. 18, фиг. 19 и фиг. 20.
Выполняли ПЦР для транспозазы SB11. ДНК, выделенную из CAR+ T-клеток (фиг. 3), амплифицировали с использованием специфических для SB11 праймеров в термоциклере. Ген GAPDH использовали в качестве гена «домашнего хозяйства», и линеаризованную плазмиду pCMV-SB11, геномную ДНК из клеток Jurkat, экспрессирующих SB11, использовали в качестве положительных контролей. CARneg клетки (без ДНК) использовали в качестве отрицательных контролей. Эти результаты ПЦР приведены на фиг. 21.
Число копий CAR определяли с использованием количественной ПЦР (кПЦР). Количество интегрированного трансгена CAR в клетках (с конструктами CAR, показанными на фиг. 3) оценивали путем амплификации геномной ДНК с использованием праймеров и зондов, специфичных для стебля IgG4 Fc и инвертированных/прямых повторов (IR/DR). Ген РНКазы P использовали в качестве внутреннего контроля, и клетки линии Jurkat, экспрессирующие одну копию CAR, использовали для построения стандартной кривой. Результаты приведены на фиг. 22.
Затем CAR+ T-клетки изучали на наличие или отсутствие автономного роста. Аномальный рост CAR+ T-клеток (экспрессирующих конструкты CAR, показанные на фиг. 3) отслеживали и измеряли путем культивирования T-клеток в отсутствие цитокинов и иАПК. Клетки подсчитывали каждые 7 дней, и процентную долю живых/мертвых клеток (со дня 1) рассчитывали и строили график. Как показано на фиг. 23, более 80% T-клеток погибали ко дню 14, что свидетельствовало об отсутствии автономного роста.
Различные CAR могли быть экспрессированы (>80%), размножены (~1010) и являлись цитотоксическими (~60%, Daudi) в сходной степени. Каркасные домены (IgG4 или CD8α) были использованы для создания CAR и не влияли на экспрессию или активность. Трансмембранные домены (CD8, CD28) не влияли на активность. Трансмембранный домен 4-1BB (216) влиял на экспрессию (анти-scFv Ат), но не на цитотоксичность и продуцирование цитокинов. Сочетание сигнальных доменов, CD28 и 4-1BB, не имело аддитивного эффекта. CAR+ T-клетки проявляли фенотип клеток памяти/эффекторных клеток. CAR, содержащие только 4-1BB домен (212, 214, 217), отличались более высокой экспрессией CCR7 по сравнению с другими. Клетки экспрессировали маркеры, характерные для памяти (CD27-hi, CD45RA-hi, CCR7-lo), активации (CD69-med, HLA-DR-hi), цитолиза (гранзим-hi, перфорин-lo) и адгезии (CD39-hi, CD150-lo), однако наблюдались незначительные количества ингибиторных маркеров (CD57, PD1, KLRG1). Все CAR, включая те, что содержали домен 4-1BB, были лишены транспозазы SB11 и не были способны к автономной пролиферации.
Пример 4
Получение CAR, содержащих CD3-дзета
В данном примере описаны CAR, содержащие CD3ζ. Общая схема дизайна CAR приведена на фиг. 24. На фиг. 24 показано сравнение дизайна CAR (фиг. 24, справа) с молекулой антитела (фиг. 24, слева).
Последовательности CD3ζ приведены на фиг. 25. Последовательность CD3-дзета и ее изоформы приведены на фиг. 25. Конструкции CAR содержали CD3-дзета (изоформу 1), которая образует один из сигнальных фрагментов эндодомена и имеет три ITAM.
Конкретные конструкты CAR показаны на фиг. 26 и фиг. 27. На фиг. 26 приведено схематическое изображение CD19-специфических CAR, имеющих длинный (IgG4), средний (шарнир CD8α) и короткий (IgG 12 ак) стебли, которые сигнализируют через эндодомены CD28 или CD137. Номенклатура молекул CAR с разными стеблями и сигнальными фрагментами приведена на фиг. 27.
Была измерена экспрессия CAR. Экспрессию CAR (показанных на фиг. 26) измеряли в день после электропорации (день 1) и через 28 дней совместного культивирования с иАПК (день 28). Точечные диаграммы для CD3 и CAR (при измерении с помощью CD19 scfv-специфического мАт) представлены на фиг. 28.
Была измерена кинетика размножения для CAR. T-клетки, в которые электропорацией были введены конструкты CAR (показанные на фиг. 26), совместно культивировали с иАПК в 7-дневном цикле стимуляции. Клетки подсчитывали и оценивали на экспрессию CD3 и CAR. Результаты приведены на фиг. 29 и фиг. 30.
Была измерена цитотоксичность CAR+ T-клеток. После 28 дней совместного культивирования CAR+ T-клетки (экспрессирующие конструкты, показанные на фиг. 26) оценивали на цитотоксичность против опухолевых клеток-мишеней в анализе с высвобождением хрома. Как показано на фиг. 31, процент цитотоксичности измеряли при разных соотношениях эффектора и мишени для CD19RCD28 (CAR 194) и CD19RCD137 (CAR 217) CAR в отношении CD19+ и CD19neg опухолевых клеток-мишеней. Как показано на фиг. 32, были получены данные для процента лизиса CD19+ EL-4 CAR+ T-клетками (экспрессирующими конструкты CAR, показанные на фиг. 26) при соотношении Э:М, составляющем 20:1. Измеряли процент экспрессии CD27, CD62L, CD28 и CCR7 на CAR+ T-клетках (экспрессирующих конструкты, показанные на фиг. 26), и результаты приведены на фиг. 33.
Для CAR+ T-клеток измеряли внутриклеточное продуцирование цитокинов. Стимулирующие клетки (CD19+ и CD19neg) инкубировали с CAR+ T-клетками (экспрессирующими CAR, показанные на фиг. 26) в течение 4 часов в присутствии ингибитора белкового транспорта и окрашивали с помощью мАт к IFN-γ и IL-2. PMA-иономицин служил в качестве положительного контроля, и T-клетки в отдельности служили в качестве отрицательного контроля. На фиг. 34 показана процентная доля продуцирующих IFN-γ клеток после стимуляции. На фиг. 35 показано разрушение продуцирующих IFN-γ и/или IL-2 клеток после инкубации со стимулирующим клетки коктейлем (PMA-иономицин).
CAR+ T-клетки изучали на наличие или отсутствие автономного роста. CAR+ T-клетки (экспрессирующие CAR, показанные на фиг. 26), оценивали на отсутствие у них способности к аномальному росту без внешней стимуляции (цитокины и иАПК) в течение 18 дней. Через 18 дней более 80% клеток были мертвыми, что свидетельствовало об отсутствии нежелательного роста. Как показано на фиг. 36, наблюдалось отсутствие автономного роста.
В CAR+ T-клетках определяли число копий CAR. Число копий интегрированных молекул CAR оценивали с использованием праймеров/зондов, специфичных для областей IgG4-Fc и IR/DR, методом кПЦР. Как показано на фиг. 37, число копий интегрированных CAR (CAR, показанных на фиг. 26) определяли с использованием зонда для IR/DR. На фиг. 38 и фиг. 39 сводные данные по числу копий CAR приведены в таблице и в графической форме для конструктов CAR (как для конструктов CAR, показанных на фиг. 3, так и конструктов CAR, показанных на фиг. 26), протестированных в двух отдельных экспериментах (P491; C714 и GCR357861).
Эти данные демонстрируют, что CAR с разными спейсерами могут быть экспрессированы, и клетки могут расти in vitro в системе культивирования, описанной в настоящем документе. Установлено, что все CAR отличаются сходной экспрессией. Максимальную цитотоксичность в отношении CD19+ EL-4 наблюдали в случае CAR с шарнирной областью CD8. Сходную экспрессию CD62L и CD28 наблюдали в случае всех протестированных CAR. Высокую частоту интеграции, определенную по числу копий CAR, наблюдали для всех CAR, за исключением CAR, содержащих стебель IgG4 Fc. Отсутствие автономного роста и SB11 определяли методом ПЦР. В отличие от предыдущих сообщений, включение спейсера 12aa в CAR не придавало улучшенные функциональные свойства в данных исследованиях.
Пример 5
Быстрая сборка CAR из основных компонентов
Авторы изобретения создали CD19-специфический CAR, который активируется через химерный CD28/CD3-дзета, с использованием платформы EZ CAR параллельно с CD19RCD28mζ CAR+ T-клетками клинической категории (CG CAR). Последовательности CAR, как CD28/CD3-ζ клинической категории, так и EZ CAR CD19RCD28mζ, включали в транспозонные векторы «спящая красавица» и вводили электропорацией в T-клетки. После электропорации T-клетки культивировали в присутствии CD19+ искусственных антигенпредставляющих клеток (также называемых активирующими и способствующими размножению клетками, или АиРК) для антиген-специфического размножения T-клеток. Экспрессию CAR на поверхности T-клеток измеряли каждую неделю методом проточной цитометрии (экспрессия Fc+), результаты свидетельствовали о сходной экспрессии CAR в CD19 CAR T-клетках клинической категории и EZ CD19 CAR T-клетках. Также проводили анализ с высвобождением хрома (CRA) для оценки киллерной функции CD19 CAR+ T-клеток, полученных с использованием платформы EZ CAR, в отношении клеток опухолей. Через 4 часа инкубации процент специфического лизиса клеток, как установлено, составлял 52% в случае EZ CAR T-клеток и 49% в случае CG CAR T-клеток.
Данные результаты свидетельствуют о том, что с использованием описанных способов были получены функциональные CAR+ T-клетки. Затем авторы изобретения осуществили быструю сборку CAR с использованием способов, описанных выше, в сочетании с библиотекой плазмид, содержащих следующие три компонента молекулы CAR: (i) анти-CD19 scFv (ii) 5 шарниров различных размеров (длинный - IgG4a и IgG4 ΔEQ, средний - CD8α, короткий - t-20 ак и t-12 ак) и (iii) разные сочетания 7 сигнальных доменов (CD27, CD28, CD28ΔY173→F173, CD134, CD137, CD278) с доменом CD3ζ. Трансфицирование клеток HEK 293 плазмидой, содержащей трансген CAR, использовали для скрининга 27 разных конструктов CAR с целью подтверждения экспрессии белка CAR на клеточной поверхности. Было проведено высокопроизводительное тестирование отдельных молекул CAR с использованием iQueTM Screener (Intellicyt, Albuquerque, NM), высокопроизводительного проточного цитометра, при этом анализы на цитотоксичность проводили с использованием сконструированных клеток-мишеней, экспрессирующих флуоресцентный репортер гранзим B или GFP. Результаты представлены на фиг. 40A-E.
Проводили дополнительные эксперименты для скрининга молекул CAR с использованием iQueTM от компании IntelliCyt. Прибор iQueTM выполняет высокопроизводительную проточную цитометрию, комплементарную технологию, которая позволяет получать информацию путем изучения больших популяций клеток с использованием возможностей мультиплексирования и анализа каждой клетки. Авторы изобретения адаптировали данную технологию для получения информации о терапевтическом потенциале T-клеток, модифицированных панелями CAR. T-клетки из лунок можно окрашивать на жизнеспособность, а также на сигналы активации (например, повышающую регуляцию CD25), высвобождение цитокинов и уничтожение клеток. Таким образом, авторы изобретения адаптировали iQue Screener и использовали его возможности для выполнения мультиплексного определения цитокинов с помощью гранул и для клеточных анализов. Полученные результаты свидетельствуют о том, что эту технологию можно использовать для тестирования большого количества разных CAR T-клеток, полученных с использованием платформы EZ CAR. С помощью прибора iQueTM от компании IntelliCyt были получены данные эксперимента, в котором 2 популяции CAR T-клеток оценивали на их способность к уничтожению клеток-мишеней. Результаты представлены на фиг. 41A-B и фиг. 42. Эти результаты показывают, что молекулы CAR были активны и что метод с прибором iQue™ можно эффективно использовать для оценки активности CAR.
Все способы, раскрытые и заявленные в настоящем документе, можно применять и осуществлять без излишнего экспериментирования в свете настоящего описания. Хотя композиции и способы по данному изобретению описаны применительно к предпочтительным вариантам осуществления, специалистам в данной области будет понятно, что можно использовать вариации в способах и в этапах или в последовательности этапов способов, описанных в настоящем документе, без отклонения от концепции, сущности и объема изобретения. Более конкретно, будет понятно, что реагенты, описанные в настоящем документе, могут быть заменены определенными реагентами, которые являются как химически, так и физиологически родственными, и при этом будут получены такие же или аналогичные результаты. Все такие заменители - аналоги и модификации, очевидные для специалистов в данной области, считаются находящимися в пределах сущности, объема и концепции изобретения, которые определены в прилагаемой формуле изобретения.
СПИСОК ЛИТЕРАТУРЫ
Все приведенные далее литературные источники, в той степени, в которой они предоставляют иллюстративные, методические или другие детали, дополняющие те, которые изложены в настоящем документе, специально включены в настоящий документ посредством ссылки.
Патентная публикация США № 2009/0017000
Патентная публикация США № 2009/0004142
Патент США № 6225042
Патент США № 6355479
Патент США № 6362001
Патент США № 6410319
Патент США № 6790662
Патент США № 7109304
WO 2007/103009
Ahmed and Cheung, FEBS Lett. 2014 Jan 21; 588(2): 288-97.
Altenschmidt et al., Adoptive transfer of in vitro-targeted, activated T lymphocytes results in total tumor regression, J Immunol. 1997 Dec 1; 159(11): 5509-15.
Audet et al., Sci Rep. 2014 Nov 6; 4: 6881.
Berry et al. Adoptive immunotherapy for cancer: the next generation of gene-engineered immune cells. Tissue Antigens. 2009 Oct; 74(4): 277-89.
Brocker et al., Adv. Immunol., 68: 257, 1998.
Curtin et al., MAbs. 2015 Jan 2; 7(1): 265-75.
Czerwiński et al., Drug Metab Dispos. 2015 Jan; 43(1): 42-52.
Davies J.K., Singh H., Huls H., Yuk D., Lee D.A., et al. (2010) Combining CD19 redirection and alloanergization to generate tumor-specific human T cells for allogeneic cell therapy of B-cell malignancies. Cancer Res 70: 3915-3924.
de Weers et al., J Immunol. 2011 Feb 1; 186(3): 1840-8.
Duong et al., (2013) Engineering T Cell Function Using Chimeric Antigen Receptors Identified Using a DNA Library Approach. PLOS ONE 8(5): e63037.
Eshhar et al., Specific activation and targeting of cytotoxic lymphocytes through chimeric single chains consisting of antibody-binding domains and the gamma or zeta subunits of the immunoglobulin and T-cell receptors. Proc Natl Acad Sci US A.; 90(2): 720-4, 1993.
Eshhar, Tumor-specific T-bodies: towards clinical application. Cancer Immunol Immunother. 1997 Nov-Dec; 45(3-4): 131-6, 1997.
Fitzer-Attas et al., Harnessing Syk family tyrosine kinases as signaling domains for chimeric single chain of the variable domain receptors: optimal design for T cell activation. J Immunol. 1998 Jan 1; 160(1): 145-54, 1998.
Funakoshi et al., Cancer Treat Rev. 2014 Dec; 40(10): 1221-9.
Gerber et al., Clin Cancer Res. 2011 Nov 1; 17(21): 6888-96.
Goldberg et al., J Clin Oncol. 2014 May 10; 32(14): 1445-52.
Gross et al., Expression of immunoglobulin-T-cell receptor chimeric molecules as functional receptors with antibody-type specificity. Proc. Natl. Acad. Sci. USA, 86: 10024-10028, 1989.
Gross et al. (1992) Endowing T cells with antibody specificity using chimeric T cell receptors. FASEB J. 1992 Dec; 6(15): 3370-8.
Hackett et al., A transposon and transposase system for human application, Mol Ther. 2010 Apr; 18(4): 674-83).
Hekele et al. Growth retardation of tumors by adoptive transfer of cytotoxic T lymphocytes reprogrammed by CD44v6-specific scFv:zeta-chimera. Int J Cancer. 1996 Oct 9; 68(2): 232-8, 1996.
Huls et al., Clinical Application of Sleeping Beauty and Artificial Antigen Presenting Cells to Genetically Modify T Cells from Peripheral and Umbilical Cord Blood. J. Vis. Exp., doi: 10.3791/50070, 2013.
Huls et al. «Clinical application of Sleeping Beauty and artificial antigen presenting cells to genetically modify T cells from peripheral and umbilical cord blood» J Vis Exp. 2013 Feb 1; (72): e50070.
Humblet-Baron and Baron, Immunol Cell Biol. 2015 Feb 10. doi: 10.1038/icb.2014.120.
Hwu et al. (1995) In vivo antitumor activity of T cells redirected with chimeric antibody/T-cell receptor genes. Cancer Res. 1995 Aug 1; 55(15): 3369-73.
Ikeda et al., Clin Cancer Res. 2009 Jun 15; 15(12): 4028-37.
Jabbour et al., Am J Hematol, 2014 Nov 18.
Kaufmann et al., Hum Pathol. 1997 Dec; 28(12): 1373-8.
Kaufman et al., Br J Haematol. 2013 Nov; 163(4): 478-86.
Kim D.W., Uetsuki T., Kaziro Y., Yamaguchi N., Sugano S. (1990) Use of the human elongation factor 1 alpha promoter as a versatile and efficient expression system. Gene 91: 217-223.
Kim et al., 2004, Nature, Vol. 22(4), pp. 403-410.
Kim et al., Immunology. 2010 Aug; 130(4): 545-55.
Kong et al., Leuk Res. 2014 Nov; 38(11): 1320-6.
Krebs et al., T cells expressing a chimeric antigen receptor that binds hepatitis B virus envelope proteins control virus replication in mice. Gastroenterology. 2013 Aug; 145(2): 456-65.
Le Garff-Tavernier et al., Haematologica. 2014 Dec 31.
Lennard S., Standard protocols for the construction of scFv libraries. Methods Mol Biol. 2002; 178: 59-71.
Leung, Molecular Imaging and Contrast Agent Database (MICAD), Bethesda (MD): National Center for Biotechnology Information (US); 2004-2013, 2010 Mar 25.
Leung 2011, IRDye800CW-anti-CD105 TRC105 chimeric monoclonal antibody. Molecular Imaging and Contrast Agent Database (MICAD). Bethesda (MD): National Center for Biotechnology Information (US); 2004-2013, 2011 Dec 01.
Maiti et al., Sleeping beauty system to redirect T-cell specificity for human applications. J Immunother. 36(2): 112-23, 2013.
Manero et al., Haematologica. 2013 Feb; 98(2): 217-21.
Molecular Therapy 17 (8): 1453-1464, 2009.
Moritz et al. (1994) Cytotoxic T lymphocytes with a grafted recognition specificity for ERBB2-expressing tumor cells. Proc Natl Acad Sci USA. 1994 May 10; 91(10): 4318-22.
Patel et al., Anticancer Res. 2008 Sep-Oct; 28(5A): 2679-86.
Qiu et al., PLoS Negl Trop Dis. 2012; 6(3): e1575.
Remington's Pharmaceutical Sciences, 16е издание, Mack, ed. (1980).
Rushworth et al., (2014) «Universal Artificial Antigen Presenting Cells to Selectively Propagate T Cells Expressing Chimeric Antigen Receptor Independent of Specificity» J Immunother. May; 37(4): 204-13.
Sarup et al., Mol Cancer Ther. 2008 Oct; 7(10): 3223-36.
Schneider, J. Embryol. Exp. Morph. 1972 Vol 27, pp. 353-365.
Schultz-Thater et al., Br J Cancer. 2000 Jul; 83(2): 204-8.
Shin et al., Immune Netw. 2011 Apr; 11(2): 114-22.
Singh et al., Redirecting specificity of T-cell populations for CD19 using the Sleeping Beauty system. Cancer Res., 68: 2961-2971, 2008.
Singh H., Figliola M.J., Dawson M.J., Huls H., Olivares S., et al. (2011) Reprogramming CD19-specific T cells with IL-21 signaling can improve adoptive immunotherapy of B-lineage malignancies. Cancer Res 71: 3516-3527.
Singh et al. «A new approach to gene therapy using Sleeping Beauty to genetically modify clinical-grade T cells to target CD19». Immunol Rev. 2014 Jan; 257(1): 181-90.
Singh et al., «Manufacture of T cells using the Sleeping Beauty system to enforce expression of a CD19-specific chimeric antigen receptor». Cancer Gene Ther. 2015 Jan 16.
Stancovski et al. (1993).
Stynen et al., Fungal Cell Wall and Immune Response, NATO ASI Series Volume 53, 1991, pp 181-193.
Sun et al., Cell Mol Immunol. 2007 Jun; 4(3): 209-14.
Turtle et al., «Artificial antigen-presenting cells for use in adoptive immunotherapy», Cancer J. 2010 Jul-Aug; 16(4): 374-81.
Verel, Int J Cancer. 2002 May 20; 99(3): 396-402.
Vincent and Samuel, Journal of Immunological Methods, Volume 165, Issue 2, 15 October 1993, Pages 177-182.
Wang et al., Immunology. 2015 Feb; 144(2): 254-62.
Weijtens et al. (1996) Single chain Ig/gamma gene-redirected human T lymphocytes produce cytokines, specifically lyse tumor cells, and recycle lytic capacity. J Immunol. 1996 Jul 15; 157(2): 836-43.
Wieczorek et al., Genetically Modified T Cells for the Treatment of Malignant Disease. Transfus Med Hemother. 2013 Dec; 40(6): 388-402.
Winiarska et al., MAbs. 2014; 6(5): 1300-13.
Zhuang et al., Cancer Cell Int. 2014 Nov 30; 14(1): 109.
Zhang et al., Angiogenesis. 2002; 5(1-2): 35-44.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> BOARD OF REGENTS, THE UNIVERSITY OF TEXAS SYSTEM
<120> ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ
<130> UTFC.P1231WO
<140> НЕИЗВЕСТНО
<141> 2015-02-16
<150> 61/940,339
<151> 2014-02-14
<160> 59
<170> PatentIn version 3.5
<210> 1
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 1
gagagcaagt acggccctcc ctgcccccct tgccct 36
<210> 2
<211> 2037
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 2
atgctgctgc tggtgaccag cctgctgctg tgtgagctgc cccaccccgc ctttctgctg 60
atccccgaca tccagatgac ccagaccacc tccagcctga gcgccagcct gggcgaccgg 120
gtgaccatca gctgccgggc cagccaggac atcagcaagt acctgaactg gtatcagcag 180
aagcccgacg gcaccgtcaa gctgctgatc taccacacca gccggctgca cagcggcgtg 240
cccagccggt ttagcggcag cggctccggc accgactaca gcctgaccat ctccaacctg 300
gagcaggagg acatcgccac ctacttttgc cagcagggca acacactgcc ctacaccttt 360
ggcggcggaa caaagctgga gatcaccggc agcacctccg gcagcggcaa gcctggcagc 420
ggcgagggca gcaccaaggg cgaggtgaag ctgcaggaga gcggccctgg cctggtggcc 480
cccagccaga gcctgagcgt gacctgtacc gtgtccggcg tgtccctgcc cgactacggc 540
gtgtcctgga tccggcagcc ccctaggaag ggcctggagt ggctgggcgt gatctggggc 600
agcgagacca cctactacaa cagcgccctg aagagccggc tgaccatcat caaggacaac 660
agcaagagcc aggtgttcct gaagatgaac agcctgcaga ccgacgacac cgccatctac 720
tactgtgcca agcactacta ctacggcggc agctacgcca tggactactg gggccagggc 780
accagcgtga ccgtgtccag cgagagcaag tacggccctc cctgcccccc ttgccctgcc 840
cccgagttcc tgggcggacc cagcgtgttc ctgttccccc ccaagcccaa ggacaccctg 900
atgatcagcc ggacccccga ggtgacctgt gtggtggtgg acgtgtccca ggaggacccc 960
gaggtccagt tcaactggta cgtggacggc gtggaggtgc acaacgccaa gaccaagccc 1020
cgggaggagc agttcaatag cacctaccgg gtggtgtccg tgctgaccgt gctgcaccag 1080
gactggctga acggcaagga atacaagtgt aaggtgtcca acaagggcct gcccagcagc 1140
atcgagaaaa ccatcagcaa ggccaagggc cagcctcggg agccccaggt gtacaccctg 1200
ccccctagcc aagaggagat gaccaagaat caggtgtccc tgacctgcct ggtgaagggc 1260
ttctacccca gcgacatcgc cgtggagtgg gagagcaacg gccagcccga gaacaactac 1320
aagaccaccc cccctgtgct ggacagcgac ggcagcttct tcctgtacag caggctgacc 1380
gtggacaaga gccggtggca ggagggcaac gtctttagct gctccgtgat gcacgaggcc 1440
ctgcacaacc actacaccca gaagagcctg tccctgagcc tgggcaagat gttctgggtg 1500
ctggtcgtgg tgggtggcgt gctggcctgc tacagcctgc tggtgacagt ggccttcatc 1560
atcttttggg tgaagagagg ccggaagaaa ctgctgtaca tcttcaagca gcccttcatg 1620
cggcccgtgc agaccaccca ggaagaggac ggctgcagct gccggttccc cgaggaagag 1680
gaaggcggct gcgaactgcg ggtgaagttc agccggagcg ccgacgcccc tgcctaccag 1740
cagggccaga accagctgta caacgagctg aacctgggcc ggagggagga gtacgacgtg 1800
ctggacaagc ggagaggccg ggaccctgag atgggcggca agccccggag aaagaaccct 1860
caggagggcc tgtataacga actgcagaaa gacaagatgg ccgaggccta cagcgagatc 1920
ggcatgaagg gcgagcggcg gaggggcaag ggccacgacg gcctgtacca gggcctgagc 1980
accgccacca aggataccta cgacgccctg cacatgcagg ccctgccccc cagatga 2037
<210> 3
<211> 2034
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 3
atgctgctgc tggtgaccag cctgctgctg tgtgagctgc cccaccccgc ctttctgctg 60
atccccgaca tccagatgac ccagaccacc tccagcctga gcgccagcct gggcgaccgg 120
gtgaccatca gctgccgggc cagccaggac atcagcaagt acctgaactg gtatcagcag 180
aagcccgacg gcaccgtcaa gctgctgatc taccacacca gccggctgca cagcggcgtg 240
cccagccggt ttagcggcag cggctccggc accgactaca gcctgaccat ctccaacctg 300
gagcaggagg acatcgccac ctacttttgc cagcagggca acacactgcc ctacaccttt 360
ggcggcggaa caaagctgga gatcaccggc agcacctccg gcagcggcaa gcctggcagc 420
ggcgagggca gcaccaaggg cgaggtgaag ctgcaggaga gcggccctgg cctggtggcc 480
cccagccaga gcctgagcgt gacctgtacc gtgtccggcg tgtccctgcc cgactacggc 540
gtgtcctgga tccggcagcc ccctaggaag ggcctggagt ggctgggcgt gatctggggc 600
agcgagacca cctactacaa cagcgccctg aagagccggc tgaccatcat caaggacaac 660
agcaagagcc aggtgttcct gaagatgaac agcctgcaga ccgacgacac cgccatctac 720
tactgtgcca agcactacta ctacggcggc agctacgcca tggactactg gggccagggc 780
accagcgtga ccgtgtccag cgagagcaag tacggccctc cctgcccccc ttgccctgcc 840
cccgagttcc tgggcggacc cagcgtgttc ctgttccccc ccaagcccaa ggacaccctg 900
atgatcagcc ggacccccga ggtgacctgt gtggtggtgg acgtgtccca ggaggacccc 960
gaggtccagt tcaactggta cgtggacggc gtggaggtgc acaacgccaa gaccaagccc 1020
cgggaggagc agttcaatag cacctaccgg gtggtgtccg tgctgaccgt gctgcaccag 1080
gactggctga acggcaagga atacaagtgt aaggtgtcca acaagggcct gcccagcagc 1140
atcgagaaaa ccatcagcaa ggccaagggc cagcctcggg agccccaggt gtacaccctg 1200
ccccctagcc aagaggagat gaccaagaat caggtgtccc tgacctgcct ggtgaagggc 1260
ttctacccca gcgacatcgc cgtggagtgg gagagcaacg gccagcccga gaacaactac 1320
aagaccaccc cccctgtgct ggacagcgac ggcagcttct tcctgtacag caggctgacc 1380
gtggacaaga gccggtggca ggagggcaac gtctttagct gctccgtgat gcacgaggcc 1440
ctgcacaacc actacaccca gaagagcctg tccctgagcc tgggcaagat gttctgggtg 1500
ctggtcgtgg tgggtggcgt gctggcctgc tacagcctgc tggtgacagt ggccttcatc 1560
atcttttggg tgaggagcaa gcggagcaga ggcggccaca gcgactacat gaacatgacc 1620
ccccggaggc ctggccccac ccggaagcac taccagccct acgcccctcc cagggacttc 1680
gccgcctacc ggagccgggt gaagttcagc cggagcgccg acgcccctgc ctaccagcag 1740
ggccagaacc agctgtacaa cgagctgaac ctgggccgga gggaggagta cgacgtgctg 1800
gacaagcgga gaggccggga ccctgagatg ggcggcaagc cccggagaaa gaaccctcag 1860
gagggcctgt ataacgaact gcagaaagac aagatggccg aggcctacag cgagatcggc 1920
atgaagggcg agcggcggag gggcaagggc cacgacggcc tgtaccaggg cctgagcacc 1980
gccaccaagg atacctacga cgccctgcac atgcaggccc tgccccccag atga 2034
<210> 4
<211> 1491
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 4
atgctgctgc tggtgaccag cctgctgctg tgtgagctgc cccaccccgc ctttctgctg 60
atccccgaca tccagatgac ccagaccacc tccagcctga gcgccagcct gggcgaccgg 120
gtgaccatca gctgccgggc cagccaggac atcagcaagt acctgaactg gtatcagcag 180
aagcccgacg gcaccgtcaa gctgctgatc taccacacca gccggctgca cagcggcgtg 240
cccagccggt ttagcggcag cggctccggc accgactaca gcctgaccat ctccaacctg 300
gagcaggagg acatcgccac ctacttttgc cagcagggca acacactgcc ctacaccttt 360
ggcggcggaa caaagctgga gatcaccggc agcacctccg gcagcggcaa gcctggcagc 420
ggcgagggca gcaccaaggg cgaggtgaag ctgcaggaga gcggccctgg cctggtggcc 480
cccagccaga gcctgagcgt gacctgtacc gtgtccggcg tgtccctgcc cgactacggc 540
gtgtcctgga tccggcagcc ccctaggaag ggcctggagt ggctgggcgt gatctggggc 600
agcgagacca cctactacaa cagcgccctg aagagccggc tgaccatcat caaggacaac 660
agcaagagcc aggtgttcct gaagatgaac agcctgcaga ccgacgacac cgccatctac 720
tactgtgcca agcactacta ctacggcggc agctacgcca tggactactg gggccagggc 780
accagcgtga ccgtgtccag caagcccacc accacccctg cccccagacc tccaacccca 840
gcccctacaa tcgccagcca gcccctgagc ctgaggcccg aagcctgtag acctgccgct 900
ggcggagccg tgcacaccag aggcctggat ttcgcctgcg acatctacat ctgggcccct 960
ctggccggca cctgtggcgt gctgctgctg agcctggtca tcaccctgta ctgcaaccac 1020
cggaacaaga gaggccggaa gaaactgctg tacatcttca agcagccctt catgcggccc 1080
gtgcagacca cccaggaaga ggacggctgc agctgccggt tccccgagga agaggaaggc 1140
ggctgcgaac tgcgggtgaa gttcagccgg agcgccgacg cccctgccta ccagcagggc 1200
cagaaccagc tgtacaacga gctgaacctg ggccggaggg aggagtacga cgtgctggac 1260
aagcggagag gccgggaccc tgagatgggc ggcaagcccc ggagaaagaa ccctcaggag 1320
ggcctgtata acgaactgca gaaagacaag atggccgagg cctacagcga gatcggcatg 1380
aagggcgagc ggcggagggg caagggccac gacggcctgt accagggcct gagcaccgcc 1440
accaaggata cctacgacgc cctgcacatg caggccctgc cccccagatg a 1491
<210> 5
<211> 1488
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 5
atgctgctgc tggtgaccag cctgctgctg tgtgagctgc cccaccccgc ctttctgctg 60
atccccgaca tccagatgac ccagaccacc tccagcctga gcgccagcct gggcgaccgg 120
gtgaccatca gctgccgggc cagccaggac atcagcaagt acctgaactg gtatcagcag 180
aagcccgacg gcaccgtcaa gctgctgatc taccacacca gccggctgca cagcggcgtg 240
cccagccggt ttagcggcag cggctccggc accgactaca gcctgaccat ctccaacctg 300
gagcaggagg acatcgccac ctacttttgc cagcagggca acacactgcc ctacaccttt 360
ggcggcggaa caaagctgga gatcaccggc agcacctccg gcagcggcaa gcctggcagc 420
ggcgagggca gcaccaaggg cgaggtgaag ctgcaggaga gcggccctgg cctggtggcc 480
cccagccaga gcctgagcgt gacctgtacc gtgtccggcg tgtccctgcc cgactacggc 540
gtgtcctgga tccggcagcc ccctaggaag ggcctggagt ggctgggcgt gatctggggc 600
agcgagacca cctactacaa cagcgccctg aagagccggc tgaccatcat caaggacaac 660
agcaagagcc aggtgttcct gaagatgaac agcctgcaga ccgacgacac cgccatctac 720
tactgtgcca agcactacta ctacggcggc agctacgcca tggactactg gggccagggc 780
accagcgtga ccgtgtccag caagcccacc accacccctg cccctagacc tccaacccca 840
gcccctacaa tcgccagcca gcccctgagc ctgaggcccg aagcctgtag acctgccgct 900
ggcggagccg tgcacaccag aggcctggat ttcgcctgcg acatctacat ctgggcccct 960
ctggccggca cctgtggcgt gctgctgctg agcctggtca tcaccctgta ctgcaaccac 1020
cggaatagga gcaagcggag cagaggcggc cacagcgact acatgaacat gaccccccgg 1080
aggcctggcc ccacccggaa gcactaccag ccctacgccc ctcccaggga cttcgccgcc 1140
taccggagcc gggtgaagtt cagccggagc gccgacgccc ctgcctacca gcagggccag 1200
aaccagctgt acaacgagct gaacctgggc cggagggagg agtacgacgt gctggacaag 1260
cggagaggcc gggaccctga gatgggcggc aagccccgga gaaagaaccc tcaggagggc 1320
ctgtataacg aactgcagaa agacaagatg gccgaggcct acagcgagat cggcatgaag 1380
ggcgagcggc ggaggggcaa gggccacgac ggcctgtacc agggcctgag caccgccacc 1440
aaggatacct acgacgccct gcacatgcag gccctgcccc ccagatga 1488
<210> 6
<211> 1380
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 6
atgctgctgc tggtgaccag cctgctgctg tgtgagctgc cccaccccgc ctttctgctg 60
atccccgaca tccagatgac ccagaccacc tccagcctga gcgccagcct gggcgaccgg 120
gtgaccatca gctgccgggc cagccaggac atcagcaagt acctgaactg gtatcagcag 180
aagcccgacg gcaccgtcaa gctgctgatc taccacacca gccggctgca cagcggcgtg 240
cccagccggt ttagcggcag cggctccggc accgactaca gcctgaccat ctccaacctg 300
gagcaggagg acatcgccac ctacttttgc cagcagggca acacactgcc ctacaccttt 360
ggcggcggaa caaagctgga gatcaccggc agcacctccg gcagcggcaa gcctggcagc 420
ggcgagggca gcaccaaggg cgaggtgaag ctgcaggaga gcggccctgg cctggtggcc 480
cccagccaga gcctgagcgt gacctgtacc gtgtccggcg tgtccctgcc cgactacggc 540
gtgtcctgga tccggcagcc ccctaggaag ggcctggagt ggctgggcgt gatctggggc 600
agcgagacca cctactacaa cagcgccctg aagagccggc tgaccatcat caaggacaac 660
agcaagagcc aggtgttcct gaagatgaac agcctgcaga ccgacgacac cgccatctac 720
tactgtgcca agcactacta ctacggcggc agctacgcca tggactactg gggccagggc 780
accagcgtga ccgtgtccag cgagagcaag tacggccctc cctgcccccc ttgccctttc 840
tgggtgctgg tcgtggtggg tggcgtgctg gcctgctaca gcctgctggt gacagtggcc 900
ttcatcatct tttgggtgag gagcaagcgg agcagaggcg gccacagcga ctacatgaac 960
atgacccccc ggaggcctgg ccccacccgg aagcactacc agccctacgc ccctcccagg 1020
gacttcgccg cctaccggag ccgggtgaag ttcagccgga gcgccgacgc ccctgcctac 1080
cagcagggcc agaaccagct gtacaacgag ctgaacctgg gccggaggga ggagtacgac 1140
gtgctggaca agcggagagg ccgggaccct gagatgggcg gcaagccccg gagaaagaac 1200
cctcaggagg gcctgtataa cgaactgcag aaagacaaga tggccgaggc ctacagcgag 1260
atcggcatga agggcgagcg gcggaggggc aagggccacg acggcctgta ccagggcctg 1320
agcaccgcca ccaaggatac ctacgacgcc ctgcacatgc aggccctgcc ccccagatga 1380
<210> 7
<211> 1383
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 7
atgctgctgc tggtgaccag cctgctgctg tgtgagctgc cccaccccgc ctttctgctg 60
atccccgaca tccagatgac ccagaccacc tccagcctga gcgccagcct gggcgaccgg 120
gtgaccatca gctgccgggc cagccaggac atcagcaagt acctgaactg gtatcagcag 180
aagcccgacg gcaccgtcaa gctgctgatc taccacacca gccggctgca cagcggcgtg 240
cccagccggt ttagcggcag cggctccggc accgactaca gcctgaccat ctccaacctg 300
gagcaggagg acatcgccac ctacttttgc cagcagggca acacactgcc ctacaccttt 360
ggcggcggaa caaagctgga gatcaccggc agcacctccg gcagcggcaa gcctggcagc 420
ggcgagggca gcaccaaggg cgaggtgaag ctgcaggaga gcggccctgg cctggtggcc 480
cccagccaga gcctgagcgt gacctgtacc gtgtccggcg tgtccctgcc cgactacggc 540
gtgtcctgga tccggcagcc ccctaggaag ggcctggagt ggctgggcgt gatctggggc 600
agcgagacca cctactacaa cagcgccctg aagagccggc tgaccatcat caaggacaac 660
agcaagagcc aggtgttcct gaagatgaac agcctgcaga ccgacgacac cgccatctac 720
tactgtgcca agcactacta ctacggcggc agctacgcca tggactactg gggccagggc 780
accagcgtga ccgtgtccag cgagagcaag tacggccctc cctgcccccc ttgccctttc 840
tgggtgctgg tcgtggtggg tggcgtgctg gcctgctaca gcctgctggt gacagtggcc 900
ttcatcatct tttgggtgaa gagaggccgg aagaaactgc tgtacatctt caagcagccc 960
ttcatgcggc ccgtgcagac cacccaggaa gaggacggct gcagctgccg gttccccgag 1020
gaagaggaag gcggctgcga actgcgggtg aagttcagcc ggagcgccga cgcccctgcc 1080
taccagcagg gccagaacca gctgtacaac gagctgaacc tgggccggag ggaggagtac 1140
gacgtgctgg acaagcggag aggccgggac cctgagatgg gcggcaagcc ccggagaaag 1200
aaccctcagg agggcctgta taacgaactg cagaaagaca agatggccga ggcctacagc 1260
gagatcggca tgaagggcga gcggcggagg ggcaagggcc acgacggcct gtaccagggc 1320
ctgagcaccg ccaccaagga tacctacgac gccctgcaca tgcaggccct gccccccaga 1380
tga 1383
<210> 8
<211> 720
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 8
atctgcgaca tccagatgac ccagagccct gccagcctgt ctaccagcct gggcgagaca 60
gtgaccatcc agtgtcaggc cagcgaggac atctactctg gcctggcttg gtatcagcag 120
aagcccggca agagccctca gctgctgatc tacggcgcca gcgacctgca ggacggcgtg 180
ccaagcagat tcagcggcag cggctccgga acccagtaca gcctgaagat caccagcatg 240
cagaccgagg acgagggcgt gtacttctgc cagcaaggcc tgacctaccc tagaaccttc 300
ggaggaggca ccaagctgga actgaagggc ggaggcggaa gtggaggcgg aggatctggc 360
ggcggaggct ctgaagtgca gctgcagcag tctggcgctg aactggtccg gcctggcact 420
agcgtgaagc tgtcctgcaa ggtgtccggc gacaccatca ccttctacta catgcacttc 480
gtgaagcaga ggccaggaca gggcctggaa tggatcggca gaatcgaccc tgaggacgag 540
agcaccaagt acagcgagaa gttcaagaac aaggccaccc tgaccgccga caccagcagc 600
aacaccgcct acctgaagct gtctagcctg acctccgagg acaccgccac ctacttttgc 660
atctacggcg gctactactt cgactactgg ggccagggcg tgatggtcac cgtgtccagc 720
<210> 9
<211> 741
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 9
ctgatccccg acatccagat gacccagacc acctccagcc tgagcgccag cctgggcgac 60
cgggtgacca tcagctgccg ggccagccag gacatcagca agtacctgaa ctggtatcag 120
cagaagcccg acggcaccgt caagctgctg atctaccaca ccagccggct gcacagcggc 180
gtgcccagcc ggtttagcgg cagcggctcc ggcaccgact acagcctgac catctccaac 240
ctggagcagg aggacatcgc cacctacttt tgccagcagg gcaacacact gccctacacc 300
tttggcggcg gaacaaagct ggagatcacc ggcagcacct ccggcagcgg caagcctggc 360
agcggcgagg gcagcaccaa gggcgaggtg aagctgcagg agagcggccc tggcctggtg 420
gcccccagcc agagcctgag cgtgacctgt accgtgtccg gcgtgtccct gcccgactac 480
ggcgtgtcct ggatccggca gccccctagg aagggcctgg agtggctggg cgtgatctgg 540
ggcagcgaga ccacctacta caacagcgcc ctgaagagcc ggctgaccat catcaaggac 600
aacagcaaga gccaggtgtt cctgaagatg aacagcctgc agaccgacga caccgccatc 660
tactactgtg ccaagcacta ctactacggc ggcagctacg ccatggacta ctggggccag 720
ggcaccagcg tgaccgtgtc c 741
<210> 10
<211> 723
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 10
cagatcgtgc tgacccagag ccccgccatc atgagcgcca gccctggcga gaaggtgacc 60
atgacctgca gcgccagcag cagcgtgagc tacatgaact ggtatcagca gaagagcggc 120
accagcccca agcggtggat ctacgacacc agcaagctgg ccagcggcgt gcccgcccac 180
ttcaggggca gcggatctgg gacttcctac tctctgacca tcagcggcat ggaagccgag 240
gatgccgcta cttactactg ccagcagtgg agcagcaacc ccttcacctt cggctccggc 300
accaagctgg aaatcaaccg gggaggcggc ggttccggcg gaggtggctc tggcggtggc 360
ggaagtcagg tgcagctgca gcagagcgga gccgagctgg ccagacctgg cgcctccgtg 420
aagatgagct gcaaggccag cggctacacc ttcacccggt acaccatgca ctgggtgaag 480
cagagacccg gccagggcct ggaatggatc ggctacatca accccagccg gggctacacc 540
aactacaacc agaagttcaa ggacaaggcc accctgacca ccgacaagag cagcagcacc 600
gcctacatgc agctgtccag cctgacctcc gaggacagcg ccgtgtacta ctgcgcccgg 660
tactacgacg accactactg cctggactac tggggccagg gcaccacact gaccgtgagc 720
agc 723
<210> 11
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 11
ctgatccccg acgtgcagat cacccagagc cccagctacc tggccgccag ccctggcgag 60
acaatcacca tcaactgccg ggccagcaag agcatcagca aggacctggc ctggtatcag 120
gaaaagcccg gcaagaccaa caagctgctg atctacagcg gcagcaccct gcagagcggc 180
atccccagca gattcagcgg cagcggctcc ggaaccgact tcaccctgac catcagcagc 240
ctggaacccg aggacttcgc catgtactac tgccagcagc acaacaagta cccctacacc 300
ttcggcggag gcaccaagct ggaaatcaag ggcagcacct ccggcagcgg caagcctggc 360
agcggcgagg gcagcaccaa gggccaggtg cagctgcagc agccaggcgc cgagctggtg 420
aaacctggcg cccctgtgaa gctgagctgc aaggccagcg gctacacctt caccaactac 480
tggatgaact ggatcaagca gaggcccggc agaggcctgg aatggatcgg cagaatcgac 540
cccagcgaca gcgagagcca ctacaaccag aagttcaagg acaaggccac actgaccgtg 600
gacaagagca gcaacaccgc ctacatccag ctgtcttctc tgaccagcga ggacagcgcc 660
gtgtactatt gcgccagata cgactacgac gacaccatgg actactgggg ccagggcacc 720
agcgtgaccg tgtct 735
<210> 12
<211> 810
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 12
atggattttc aggtgcagat tttcagcttc ctgctaatca gtgcctcagt cataatgtct 60
agaatggccc aggtgcaact gcagcagtca ggggctgagc tggctagacc tggggcttca 120
gtgaagatgt cctgcaaggc ttctggctac acctttacta cctacacaat acactgggta 180
agacggaggc ctggacacga tctggaatgg attggataca ttaatcctag cagtggatgt 240
tctgactaca atcaaaactt caagggcaag accacattga ctgcagacaa gtcctccaac 300
acagcctaca tgcaactgaa cagcctgaca tctgaggact ctgcggtcta ttactgtgca 360
agaagagcgg actatggtaa ctacgaatat acctggtttg cttactgggg ccaagggacc 420
acggtcaccg tctcctcaag tggaggcggt tcaggtggag gtggctctgg cggtggcgga 480
tcggtcatcg agctcactca gtctccaaaa ttcatgtcca catcagtagg agacagggtc 540
aacgtcacct acaaggccag tcagaatgtg ggtactaatg tagcctggtt tcaacaaaaa 600
ccagggcaat ctcctaaagt tctgatttac tcggcatctt accgatacag tggagtccct 660
gatcgcttca caggcagtgg atctggaaca gatttcactc tcaccatcag caatgtgcag 720
tctgaagact tggcagagta tttctgtcag caatatcaca cctatcctct cacgttcgga 780
gggggcacca agctggaaat caaacggtcg 810
<210> 13
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 13
caggtgcagc tggtgcagag cggcggcggc ctggtgcagc atggcggcag cctgcgcctg 60
agctgcgcgg cgagcggctt tacctttagc agctatgaaa tgaactgggt gcgccaggcg 120
ccgggcaaag gcctggaatg ggtgagcggc attagcggca gcggcggcag cacctattat 180
gcggatagcg tgaaaggccg ctttaccccc attagccgcg ataacagcaa aaacaccctg 240
tatctgcaga tgaaccgcct gcgcgcggaa gataccgcgg tgtattattg cgcgcgcgat 300
aacggctggg aactgaccga ttggtatttt gatctgtggg gccgcggcac catggtgacc 360
gtgagcagcg gcggcggcgg cagcggcggc ggcggcagcg gcggcggcgg cagcgatatt 420
cagatgaccc agagcccgag caccctgagc gcgagcattg gcgatcgcgt gaccattacc 480
tgccgcgcga gcgaaggcat ttatcattgg ctggcgtggt atcagcagaa accgggcaaa 540
gcgccgaaac tgctgattta taaagcgagc agcctggcga gcggcgcgcc gagccgcttt 600
agcggcagcg gcagcggcac cgattttacc ctgaccatta gcagcctgca gccggatgat 660
tttgcgacct attattgcca gcagtatagc aactatccgc tgacctttgg cggcggcacc 720
aaactggaaa ttaaa 735
<210> 14
<211> 747
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 14
gacgttgtga tgacccagac ccctctgagc ctgcctgtgt ccctgggaga tcaggccagc 60
atcagctgca gaagcagcca gagcctgctg aagaacaacg gcaacacctt cctgcactgg 120
tatctgcaga agtccggcca gtcccccaag ctgctgatct acaaggtgtc caaccggctg 180
agcggcgtgc ccgatagatt ttctggctct ggcagcggca cctacttcac cctgaagatc 240
agccgggtgg aagccgagga cctgggcgtg tacttctgta gccagagcac ccacatccct 300
tacaccttcg gcggaggcac caagctggaa ctgaagcggg gcagcacctc cggcagcggc 360
aagcctggca gcggcgaggg cagcaccaag ggcgaagtga agctggtgga aagcggcgga 420
ggcctggtgc tgcctggcga ttctctgaga ctgagctgcg ccaccagcga gttcaccttc 480
accgactact acatgacctg ggtgcgccag ccccccagaa aggctctgga atggctgggc 540
ttcatccgga accgggccaa cggctacacc accgagtaca accctagcgt gaagggccgg 600
ttcaccatca gccgggacaa cagccagagc atcctgtacc tgcagatgaa caccctgcgg 660
accgaggaca gcgccaccta ctactgtgct cgggtgtcca actgggcctt cgactattgg 720
ggccagggca ccaccctgac cgtgtct 747
<210> 15
<211> 759
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 15
gacatcaaga tgacccagag ccccagctct atgtacgcca gcctgggcga gcgcgtgacc 60
atcacctgta aagccagccc cgacatcaac agctacctga gctggttcca gcagaagccc 120
ggcaagagcc ccaagaccct gatctaccgg gccaacagac tggtggatgg cgtgcccagc 180
agattcagcg gcggaggctc tggccaggac tacagcctga ccatcaactc cctggaatac 240
gaggacatgg gcatctacta ctgcctgcag tacgacgagt tcccctacac cttcggaggc 300
ggcaccaagc tggaaatgaa gggcagcaca agcggcagcg gcaagcctgg atctggcgag 360
ggaagcacca agggcgaagt gaagctggtg gaatctggcg gcggactcgt gaagcctggc 420
ggctctctga agctgtcttg tgccgccagc ggcttcacct tcagcagcta cgccatgagc 480
tgggtgcggc agatccccga gaagcggctg gaatgggtgg ccagcatcag cagaggcgga 540
accacctact accccgactc tgtgaagggc cggttcacca tcagccggga caacgtgcgg 600
aacatcctgt acctgcagat gagcagcctg cggagcgagg acaccgccat gtactactgt 660
ggcagatacg actacgacgg ctactatgcc atggattact ggggccaggg caccagcgtg 720
accgtgtcta gccagggaac ctccgtgaca gtgtccagc 759
<210> 16
<211> 759
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 16
gaagtacatc tggttgagtc tggtggagac ttagtgaagc ctggagggtc cctgaaactc 60
tcctgtgcag cctctggatt cactttcagt cactatggca tgtcttgggt tcgccagact 120
ccagacaaga ggctggagtg ggtcgcaacc attggtagtc gtggtactta cacccactat 180
ccagacagtg tgaagggacg attcaccatc tccagagaca atgacaagaa cgccctgtac 240
ctgcaaatga acagtctgaa gtctgaagac acagccatgt attactgtgc aagaagaagt 300
gaattttatt actacggtaa tacctactat tactctgcta tggactactg gggccaaggc 360
accacggtca ccgtctcctc aggtggcggt ggcagcggcg gtggtgggtc cggtggcggc 420
ggatctgaca tcgtactcac acagtctcca gctagcctgg ctgtatctct aggacagagg 480
gccaccatct cctgcagagc cagcgaaagt gttgataatt atggctttag ttttatgaac 540
tggttccaac agaaaccagg acagccaccc aaactcctca tctatgctat atccaaccga 600
ggatccgggg tccctgccag gtttagtggc agtgggtctg ggacagactt cagcctcaac 660
atccatcctg tagaggagga tgatcctgca atgtatttct gtcagcaaac taaggaggtt 720
ccgtggacgt tcggagctgg caccaagctc gagatcaaa 759
<210> 17
<211> 543
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 17
atggccatct ggcggagcaa cagcggcagc aacaccctgg aaaacggcta cttcctgagc 60
cggaacaaag agaaccacag ccagcccacc cagagcagcc tggaagatag cgtgaccccc 120
accaaggccg tgaaaaccac cggcgtgctg tccagcccct gccctcccaa ctggatcatc 180
tacgagaaga gctgctacct gttcagcatg agcctgaaca gctgggacgg cagcaagcgg 240
cagtgctggc agctgggcag caacctgctg aagatcgaca gcagcaacga gctgggcttc 300
atcgtgaagc aggtgtccag ccagcccgac aactccttct ggatcggcct gagcaggccc 360
cagaccgagg tgccctggct gtgggaggac ggctccacct tcagctccaa cctgttccag 420
atccggacca ccgccacaca ggaaaacccc agccccaact gcgtgtggat ccacgtgagc 480
gtgatctacg accagctgtg cagcgtgccc agctacagca tctgcgagaa gaaattcagc 540
atg 543
<210> 18
<211> 987
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 18
atggattttc aggtgcagat tttcagcttc ctgctaatca gtgcctcagt cataatgtct 60
agacaattcc aagtgaagct ggaggagtct ggggctgagc ttgtgaggcc aggggccttg 120
gtcaagttgt cctgcaaaac ttctggcttc aacattaaag actacttttt acactgggtg 180
agacagaggc ctgaccaggg cctggagtgg attggatgga ttaatcctga taatggtaat 240
actgtttatg acccgaagct tcagggcacg gccagtttaa cagcagacac atcctccaac 300
acagtctact tgcagctcag cggcctgaca tctgaggaca ctgccgtcta tttctgtact 360
cggagggact atacttatga aaaggctgct ctggactact ggggtcaggg agcctcagtc 420
atcgtctcct cagccaaaac aacagcccca tcggtctatc cactggcccc tgtgtgtgga 480
gatacaactg gctcctcggt gactctagga tgcctggtca agagatctgg cggtggcggt 540
tctggtggcg gtggctccgg cggtggcggt tctggagctc gacattgtgc tcacacagac 600
tccaaatcca tgtccatgtc agtaggagag agggtcacct tgacctgcaa ggccagtgag 660
aatgtggtta cttatgtttc ctggtatcaa cagaaaccag agcagtctcc taaactgctg 720
atatacgggg catccaaccg gtacactggg gtccccgatc gcttcacagg cagtggatct 780
gcaacagatt tcactctgac catcagcagt gtgcaggctg aagaccttgc agattatcac 840
tgtggacagg gttacagcta tccgtacacg ttcggagggg ggaccaagct ggaaataaaa 900
cgggctgatg ctgcaccaac ttatccgcat caccatcatc atcatcatct gcagatatcc 960
agcacagtgg cggccgctcg agtctag 987
<210> 19
<211> 753
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 19
ctgatcccca tggcccaggt gaagctgcag cagagcggcc ctgatctggt gaagcctggc 60
gccagcgtga agatcagctg caaggccagc ggctacagct tcaccggcta ctacatgcac 120
tgggtgaaac agagccacgg caagagcctg gaatggatcg gcagagtgaa ccccaatagc 180
ggcggcacca gctacaacca gaagttcaag gacaaggcca tcctgaccgt ggacaagagc 240
agcagcaccg cctacatgga actgcggagc ctgaccagcg aggacagcgc cgtgtactac 300
tgcgcccggt ccaagggcaa ctacttctac gccatggact actggggcca gggcaccacc 360
gtgaccgtgt ctagcagcgg cggaggaagc ggagggggag gatctggcgg aggcggcagc 420
gatatcgagc tgacccagag ccctagcagc ctggccgtgt cactgggcca gagagccacc 480
atcagctgca gagcctccga gagcgtggat agccacggca ccagcctgat gcactggtat 540
cagcagaagc ccggccagcc ccccaagttc ctgatctacc gggccagcaa cctggaaagc 600
ggcatccccg ccagattttc cggcagcggc agcagaaccg acttcaccct gaccatcaac 660
cccgtggaga cagacgacgt ggccatctac tactgccagc agagcaacga ggaccctccc 720
acctttggcg gaggcaccaa gctggaactg aag 753
<210> 20
<211> 732
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 20
gaagtgcagc tggtggaatc tggcggcgga ctggtgcagc ctggcggatc tctgagactg 60
agctgtgccg ccagcggctt cgacttcagc cggtactgga tgagctgggt gcgccaggcc 120
cctggcaaag gcctggaatg gatcggcgag atcaaccccg acagcagcac catcaactac 180
gcccccagcc tgaaggacaa gttcatcatc agccgggaca acgccaagaa cagcctgtac 240
ctgcagatga actccctgcg ggccgaggac accgccgtgt actattgcgc cagacccgac 300
ggcaactact ggtacttcga cgtgtggggc cagggcaccc tcgtgacagt gtctggcagc 360
acaagcggct ctggcaagcc tggatctggc gagggctcta ccaagggcga catccagatg 420
acccagagcc ccagcagcct gtctgccagc gtgggcgaca gagtgaccat cacatgcaag 480
gccagccagg acgtgggaat cgccgtggcc tggtatcagc agaaacccgg caaggtgccc 540
aagctgctga tctactgggc cagcaccaga cacaccggcg tgcccgatag attttccggc 600
agcggctccg gcaccgactt caccctgaca atcagctccc tgcagcctga ggacgtggcc 660
acctactact gccagcagta cagcagctac ccctacacct tcggacaggg caccaaggtg 720
gaaatcaagc gg 732
<210> 21
<211> 720
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 21
caggtgcagc tgcagcagtc tggccccgag ctggaaaaac ctggcgcctc cgtgaagatc 60
agctgcaagg ccagcggcta cagcttcacc ggctacacca tgaactgggt caagcagagc 120
cacggcaaga gcctggaatg gatcggcctg atcaccccct acaacggcgc cagcagctac 180
aaccagaagt tccggggcaa ggccaccctg accgtggaca agtctagcag caccgcctac 240
atggacctgc tgagcctgac cagcgaggac agcgccgtgt acttctgtgc cagaggcggc 300
tacgacggca gaggcttcga ttattggggc cagggcacca ccgtgacagt gtctagcgga 360
gtgggaggat ctggcggagg cggaagtggc ggagggggat ctgatatcga gctgacccag 420
agccccgcca tcatgtctgc tagccctggc gagaaagtga ccatgacctg cagcgccagc 480
tccagcgtgt cctacatgca ctggtatcag cagaagtccg gcaccagccc caagcggtgg 540
atctacgaca caagcaagct ggcctctggc gtgcccggca gattttctgg cagcggctcc 600
ggcaacagct actccctgac aatcagcagc gtggaagccg aggacgacgc cacctactac 660
tgccagcagt ggagcggcta ccccctgact tttggagccg gcaccaagct ggaaatcaag 720
<210> 22
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 22
agccaggaag agatgaccaa gaaccaggtg tccctgacct gcctcgtgaa gggcttctac 60
<210> 23
<211> 141
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 23
aagcctacca caacccctgc ccccagacct cctacacccg cccctacaat tgccagccag 60
cctctgtctc tgaggcccga ggcttgtaga cctgctgctg gcggagccgt gcacaccaga 120
ggactggatt tcgcctgcga c 141
<210> 24
<211> 696
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 24
agcgagagca agtacggccc tccctgcccc ccttgccctg cccccgagtt cctgggcgga 60
cccagcgtgt tcctgttccc ccccaagccc aaggacaccc tgatgatcag ccggaccccc 120
gaggtgacct gtgtggtggt ggacgtgtcc caggaggacc ccgaggtcca gttcaactgg 180
tacgtggacg gcgtggaggt gcacaacgcc aagaccaagc cccgggagga gcagttcaat 240
agcacctacc gggtggtgtc cgtgctgacc gtgctgcacc aggactggct gaacggcaag 300
gaatacaagt gtaaggtgtc caacaagggc ctgcccagca gcatcgagaa aaccatcagc 360
aaggccaagg gccagcctcg ggagccccag gtgtacaccc tgccccctag ccaagaggag 420
atgaccaaga atcaggtgtc cctgacctgc ctggtgaagg gcttctaccc cagcgacatc 480
gccgtggagt gggagagcaa cggccagccc gagaacaact acaagaccac cccccctgtg 540
ctggacagcg acggcagctt cttcctgtac agcaggctga ccgtggacaa gagccggtgg 600
caggagggca acgtctttag ctgctccgtg atgcacgagg ccctgcacaa ccactacacc 660
cagaagagcc tgtccctgag cctgggcaag atgttc 696
<210> 25
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 25
agccaggaag agatgaccaa gaaccaggtg tccctgacct gcctcgtgaa gggcttctac 60
<210> 26
<211> 696
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 26
agcgagagca agtacggccc tccctgcccc ccttgccctg cccccgagtt cctgggcgga 60
cccagcgtgt tcctgttccc ccccaagccc aaggacaccc tgatgatcag ccggaccccc 120
gaggtgacct gtgtggtggt ggacgtgtcc caggaggacc ccgaggtcca gttcaactgg 180
tacgtggacg gcgtggaggt gcacaacgcc aagaccaagc cccgggagga gcagttccag 240
agcacctacc gggtggtgtc cgtgctgacc gtgctgcacc aggactggct gaacggcaag 300
gaatacaagt gtaaggtgtc caacaagggc ctgcccagca gcatcgagaa aaccatcagc 360
aaggccaagg gccagcctcg ggagccccag gtgtacaccc tgccccctag ccaagaggag 420
atgaccaaga atcaggtgtc cctgacctgc ctggtgaagg gcttctaccc cagcgacatc 480
gccgtggagt gggagagcaa cggccagccc gagaacaact acaagaccac cccccctgtg 540
ctggacagcg acggcagctt cttcctgtac agcaggctga ccgtggacaa gagccggtgg 600
caggagggca acgtctttag ctgctccgtg atgcacgagg ccctgcacaa ccactacacc 660
cagaagagcc tgtccctgag cctgggcaag atgttc 696
<210> 27
<211> 696
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 27
agcgagagca agtacggccc tccctgcccc ccttgccctg cccccgagtt cgaaggcgga 60
cccagcgtgt tcctgttccc ccccaagccc aaggacaccc tgatgatcag ccggaccccc 120
gaggtgacct gtgtggtggt ggacgtgtcc caggaggacc ccgaggtcca gttcaactgg 180
tacgtggacg gcgtggaggt gcacaacgcc aagaccaagc cccgggagga gcagttccag 240
agcacctacc gggtggtgtc cgtgctgacc gtgctgcacc aggactggct gaacggcaag 300
gaatacaagt gtaaggtgtc caacaagggc ctgcccagca gcatcgagaa aaccatcagc 360
aaggccaagg gccagcctcg ggagccccag gtgtacaccc tgccccctag ccaagaggag 420
atgaccaaga atcaggtgtc cctgacctgc ctggtgaagg gcttctaccc cagcgacatc 480
gccgtggagt gggagagcaa cggccagccc gagaacaact acaagaccac cccccctgtg 540
ctggacagcg acggcagctt cttcctgtac agcaggctga ccgtggacaa gagccggtgg 600
caggagggca acgtctttag ctgctccgtg atgcacgagg ccctgcacaa ccactacacc 660
cagaagagcc tgtccctgag cctgggcaag atgttc 696
<210> 28
<211> 711
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 28
atggtgtcca agggcgagga actgatcaaa gaaaacatgc acatgaagct gtacatggaa 60
ggcaccgtga acaaccacca cttcaagtgc accagcgagg gagagggcaa gccctacgag 120
ggcacccaga ccatgcggat caaggtggtc gagggcggac ctctgccctt cgccttcgac 180
atcctggcca caagcttcat gtacggcagc aagaccttca tcaaccacac ccagggcatc 240
cccgatttct tcaagcagag cttccccgag ggcttcacct gggagagagt gaccacctac 300
gaggacggcg gcgtgctgac cgccacccag gacaccagcc tgcaggacgg ctgcctgatc 360
tacaacgtga agatccgggg cgtgaacttc cccagcaacg gccccgtgat gcagaagaaa 420
accctgggct gggaggccag caccgagatg ctgtaccctg ccgatggcgg cctggaaggc 480
agagccgaca tggccctgaa actggtcggc ggagggcacc tgatctgcaa cctgaaaacc 540
acctacagaa gcaagaagcc cgccaagaac ctgaagatgc ccggcgtgta ctacgtggac 600
cggcggctgg aaaggatcaa agaggccgac aaagaaacct acgtggagca gcacgaggtg 660
gccgtggccc ggtactgcga cctgccctcc aagctgggcc acaaactgaa c 711
<210> 29
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 29
atgatcgaga agtccttcgt gatcaccgac ccccggctgc ccgactaccc tatcatcttt 60
gccagcgacg gcttcctgga actgaccgag tacagccggg aagagatcat gggccggaac 120
gccagattcc tgcagggccc cgaaaccgat caggccaccg tgcagaagat ccgggacgcc 180
atcagggacc agcgggaaac cacagtgcag ctgatcaact acaccaagag cggcaagaag 240
ttctggaacc tgctgcatct gcagcccgtg cgggatagaa agggcggcct gcagtacttc 300
atcggcgtgc agctcgtggg cagcgaccac gtg 333
<210> 30
<211> 675
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 30
atggccagca gcgaggacgt gatcaaagaa ttcatgcggt tcaaagtgcg gatggaaggc 60
agcgtgaacg gccacgagtt cgagattgag ggcgagggcg aaggcagacc ctacgaggga 120
acacagaccg ccaagctgaa agtgaccaag ggcggacccc tgcccttcgc ctgggatatc 180
ctgagccccc agttccagta cggcagcaag gtgtacgtga agcaccccgc cgacatcccc 240
gactacaaga agctgagctt ccccgagggc ttcaagtggg agagagtgat gaacttcgag 300
gacggcggcg tcgtgaccgt gacccaggat agctctctgc aggacggcag cttcatctac 360
aaagtgaagt ttatcggcgt gaacttcccc agcgacggcc ccgtgatgca gaaaaagacc 420
atgggctggg aggccagcac cgagagactg taccctagag atggcgtgct gaagggcgag 480
atccacaagg ccctgaagct gaaggatggc ggccactacc tggtggaatt caagagcatc 540
tacatggcca agaaacccgt gcagctgccc ggctactact acgtggacag caagctggac 600
atcaccagcc acaacgagga ctacaccatc gtggaacagt acgagcgggc cgagggccgg 660
caccatctgt ttctg 675
<210> 31
<211> 717
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 31
atggtgtcca agggcgagga actgttcacc ggcgtggtgc ccatcctggt ggaactggat 60
ggcgacgtga acggccacaa gttcagcgtg tccggcgagg gcgaaggcga cgccacatat 120
ggcaagctga ccctgaagct gatctgcacc accggcaagc tgcccgtgcc ttggcctacc 180
ctcgtgacca cactgggcta cggcctgcag tgcttcgcca gataccccga ccatatgaag 240
cagcacgact tcttcaagag cgccatgccc gagggctacg tgcaggaacg gaccatcttc 300
tttaaggacg acggcaacta caagaccagg gccgaagtga agttcgaggg cgacaccctc 360
gtgaaccgga tcgagctgaa gggcatcgac ttcaaagagg acggcaacat cctgggccac 420
aagctggagt acaactacaa cagccacaac gtgtacatca ccgccgacaa gcagaagaac 480
ggcatcaagg ccaacttcaa gatccggcac aacatcgagg acggcggcgt gcagctggcc 540
gatcactacc agcagaacac ccctatcggc gacggccctg tgctgctgcc cgacaatcac 600
tacctgagct accagagcgc cctgagcaag gaccccaacg agaagcggga ccacatggtg 660
ctgctggaat tcgtgaccgc cgctggcatc accctgggca tggacgagct gtacaag 717
<210> 32
<211> 717
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 32
atggtgagca agggcgagga gctgttcacc ggggtggtgc ccatcctggt cgagctggac 60
ggcgacgtaa acggccacaa gttcagcgtg tccggcgagg gcgagggcga tgccacctac 120
ggcaagctga ccctgaagtt catctgcacc accggcaagc tgcccgtgcc ctggcccacc 180
ctcgtgacca ccctgaccta cggcgtgcag tgcttcagcc gctaccccga ccacatgaag 240
cagcacgact tcttcaagtc cgccatgccc gaaggctacg tccaggagcg caccatcttc 300
ttcaaggacg acggcaacta caagacccgc gccgaggtga agttcgaggg cgacaccctg 360
gtgaaccgca tcgagctgaa gggcatcgac ttcaaggagg acggcaacat cctggggcac 420
aagctggagt acaactacaa cagccacaac gtctatatca tggccgacaa gcagaagaac 480
ggcatcaagg tgaacttcaa gatccgccac aacatcgagg acggcagcgt gcagctcgcc 540
gaccactacc agcagaacac ccccatcggc gacggccccg tgctgctgcc cgacaaccac 600
tacctgagca cccagtccgc cctgagcaaa gaccccaacg agaagcgcga tcacatggtc 660
ctgctggagt tcgtgaccgc cgccgggatc actctcggca tggacgagct gtacaag 717
<210> 33
<211> 363
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 33
gccaagggcc agcctcggga gccccaggtg tacaccctgc cccctagcca agaggagatg 60
accaagaatc aggtgtccct gacctgcctg gtgaagggct tctaccccag cgacatcgcc 120
gtggagtggg agagcaacgg ccagcccgag aacaactaca agaccacccc ccctgtgctg 180
gacagcgacg gcagcttctt cctgtacagc aggctgaccg tggacaagag ccggtggcag 240
gagggcaacg tctttagctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 300
aagagcctgt ccctgagcct gggcaagatg ttctacccat acgatgttcc agattacgct 360
tac 363
<210> 34
<211> 708
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 34
atggtgagca agggcgagga gaccacaatg ggcgtaatca agcccgacat gaagatcaag 60
ctgaagatgg agggcaacgt gaatggccac gccttcgtga tcgagggcga gggcgagggc 120
aagccctacg acggcaccaa caccatcaac ctggaggtga aggagggagc ccccctgccc 180
ttctcctacg acattctgac caccgcgttc gcctacggca acagggcctt caccaagtac 240
cccgacgaca tccccaacta cttcaagcag tccttccccg agggctactc ttgggagcgc 300
accatgacct tcgaggacaa gggcatcgtg aaggtgaagt ccgacatctc catggaggag 360
gactccttca tctacgagat acacctcaag ggcgagaact tcccccccaa cggccccgtg 420
atgcagaaga agaccaccgg ctgggacgcc tccaccgaga ggatgtacgt gcgcgacggc 480
gtgctgaagg gcgacgtcaa gcacaagctg ctgctggagg gcggcggcca ccaccgcgtt 540
gacttcaaga ccatctacag ggccaagaag gcggtgaagc tgcccgacta tcactttgtg 600
gaccaccgca tcgagatcct gaaccacgac aaggactaca acaaggtgac cgtttacgag 660
agcgccgtgg cccgcaactc caccgacggc atggacgagc tgtacaag 708
<210> 35
<211> 423
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 35
aagcctacca caacccctgc ccccagacct cctacacccg cccctacaat tgccagccag 60
cctctgtctc tgaggcccga ggcttgtaga cctgctgctg gcggagccgt gcacaccaga 120
ggactggatt tcgcctgcga caagcctacc acaacccctg cccccagacc tcctacaccc 180
gcccctacaa ttgccagcca gcctctgtct ctgaggcccg aggcttgtag acctgctgct 240
ggcggagccg tgcacaccag aggactggat ttcgcctgcg acagcagcgg cggcggcggc 300
agcggcggcg gcggcagcgg cggcggcggc agcgcgcagc tgaaaaaaaa actgcaggcg 360
ctgaaaaaaa aaaacgcgca gctgaaatgg aaactgcagg cgctgaaaaa aaaactggcg 420
cag 423
<210> 36
<211> 423
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 36
aagcctacca caacccctgc ccccagacct cctacacccg cccctacaat tgccagccag 60
cctctgtctc tgaggcccga ggcttgtaga cctgctgctg gcggagccgt gcacaccaga 120
ggactggatt tcgcctgcga caagcctacc acaacccctg cccccagacc tcctacaccc 180
gcccctacaa ttgccagcca gcctctgtct ctgaggcccg aggcttgtag acctgctgct 240
ggcggagccg tgcacaccag aggactggat ttcgcctgcg acagcagcgg cggcggcggc 300
agcggcggcg gcggcagcgg cggcggcggc agcgcccagc tggaaaaaga gctgcaggcc 360
ctggaaaaag aaaacgctca gctggaatgg gaactgcagg ctctggaaaa agagctggcc 420
cag 423
<210> 37
<211> 69
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 37
tgggtgctgg tcgtggtggg tggcgtgctg gcctgctaca gcctgctggt gacagtggcc 60
ttcatcatc 69
<210> 38
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 38
attatctcat tcttcctggc cctgacctct accgccctgc tgtttctgct gttctttctg 60
accctgcggt tcagcgtggt g 81
<210> 39
<211> 84
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 39
atctacatct gggcgccctt ggccgggact tgtggggtcc ttctcctgtc actggttatc 60
accctttact gcaaccacag gaac 84
<210> 40
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 40
ctctgctacc tgctggatgg aatcctcttc atctatggtg tcattctcac tgccttgttc 60
ctg 63
<210> 41
<211> 144
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 41
cagcggcgga agtacagaag caacaagggc gagagccccg tggaacctgc cgagccttgc 60
agatacagct gccccagaga ggaagagggc agcaccatcc caatccagga agattaccgg 120
aagcccgagc ccgcctgtag ccct 144
<210> 42
<211> 132
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 42
ttttgggtga ggagcaagcg gagcagaggc ggccacagcg actacatgaa catgaccccc 60
cggaggcctg gccccacccg gaagcactac cagccctacg cccctcccag ggacttcgcc 120
gcctaccgga gc 132
<210> 43
<211> 132
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 43
ttttgggtga ggagcaagcg gagcagaggc ggccacagcg acttcatgaa catgaccccc 60
cggaggcctg gccccacccg gaagcactac cagccctacg cccctcccag ggacttcgcc 120
gcctaccgga gc 132
<210> 44
<211> 108
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 44
agggaccaga gactgcctcc cgatgcccac aaacctccag gcggcggaag cttcagaacc 60
cccatccagg aagaacaggc cgacgcccac agcaccctgg ccaagatt 108
<210> 45
<211> 126
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 45
aagcggggca gaaagaagct gctgtacatc ttcaagcagc ccttcatgcg gcccgtgcag 60
accacccagg aagaggacgg ctgctcctgc agattccccg aggaagaaga aggcggctgc 120
gagctg 126
<210> 46
<211> 102
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 46
aagaaaaagt acagcagcag cgtgcacgac cccaacggcg agtacatgtt catgcgggcc 60
gtgaacaccg ccaagaagtc cagactgacc gacgtgaccc tg 102
<210> 47
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 47
cgggtgaagt tcagccggag cgccgacgcc cctgcctacc agcagggcca gaaccagctg 60
tacaacgagc tgaacctggg ccggagggag gagtacgacg tgctggacaa gcggagaggc 120
cgggaccctg agatgggcgg caagccccgg agaaagaacc ctcaggaggg cctgtataac 180
gaactgcaga aagacaagat ggccgaggcc tacagcgaga tcggcatgaa gggcgagcgg 240
cggaggggca agggccacga cggcctgtac cagggcctga gcaccgccac caaggatacc 300
tacgacgccc tgcacatgca ggccctgccc cccaga 336
<210> 48
<211> 759
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 48
gatattcaga tgacccagag cccgagcagc ctgagcgcga gcgtgggcga tcgcgtgacc 60
attacctgcc gcagcagcca gaacattgtg catagcaacg gcaacaccta tctggattgg 120
tatcagcaga ccccgggcaa agcgccgaaa ctgctgattt ataaagtgag caaccgcttt 180
agcggcgtgc cgagccgctt tagcggcagc ggcagcggca ccgattttac ctttaccatt 240
agcagcctgc agccggaaga tattgcgacc tattattgct ttcagtatag ccatgtgccg 300
tggacctttg gccagggcac caaactgcag attaccggca gcacctccgg cagcggcaag 360
cctggcagcg gcgagggcag caccaagggc agccaggtgc agctgcagca gagcggcgcg 420
gaagtgaaaa aaccgggcag cagcgtgaaa gtgagctgca aagcgagcgg ctataccttt 480
accaactatt atatttattg ggtgcgccag gcgccgggcc agggcctgga atggattggc 540
ggcattaacc cgaccagcgg cggcagcaac tttaacgaaa aatttaaaac ccgcgtgacc 600
attaccgcgg atgaaagcag caccaccgcg tatatggaac tgagcagcct gcgcagcgaa 660
gataccgcgt tttatttttg cacccgccag ggcctgtggt ttgatagcga tggccgcggc 720
tttgattttt ggggccaggg caccaccgtg accgtgagc 759
<210> 49
<211> 732
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 49
gatattctgc tgacccagag cccggtgatt ctgagcgtga gcccgggcga acgcgtgagc 60
tttagctgcc gcgcgagcca gagcattggc accaacattc attggtatca gcagcgcacc 120
aacggcagcc cgcgcctgct gattaaatat gcgagcgaaa gcattagcgg cattccgagc 180
cgctttagcg gcagcggcag cggcaccgat tttaccctga gcattaacag cgtggaaagc 240
gaagatattg cggattatta ttgccagcag aacaacaact ggccgaccac ctttggcgcg 300
ggcaccaaac tggaactgaa aggcagcacc tccggcagcg gcaagcctgg cagcggcgag 360
ggcagcacca agggcagcca ggtgcagctg aaacagagcg gcccgggcct ggtgcagccg 420
agccagagcc tgagcattac ctgcaccgtg agcggcttta gcctgaccaa ctatggcgtg 480
cattgggtgc gccagagccc gggcaaaggc ctggaatggc tgggcgtgat ttggagcggc 540
ggcaacaccg attataacac cccgtttacc agccgcctga gcattaacaa agataacagc 600
aaaagccagg tgttttttaa aatgaacagc ctgcagagca acgataccgc gatttattat 660
tgcgcgcgcg cgctgaccta ttatgattat gaatttgcgt attggggcca gggcaccctg 720
gtgaccgtga gc 732
<210> 50
<211> 726
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 50
gaagtgcagc tgcagcagag cggcccggaa ctggaaaaac cgggcgcgag cgtgaaactg 60
agctgcaaag cgagcggcta tagctttacc ggctataaca tgaactgggt gaaacagagc 120
catggcaaaa gcctggaatg gattggccat attgatccgt attatggcga taccagctat 180
aaccagaaat ttcgcggcaa agcgaccctg accgtggata aaagcagcag caccgcgtat 240
atgcagctga aaagcctgac cagcgaagat agcgcggtgt attattgcgt gaaaggcggc 300
tattatggcc attggtattt tgatgtgtgg ggcgcgggca ccaccgtgac cgtgagcagc 360
ggcggaggcg gctctggcgg cggaggatca ggtggcggag gatccgatat tcagatgacc 420
cagagcccga gcagcctgag cgcgagcctg ggcgaacgcg tgagcctgac ctgccgcgcg 480
agccaggata ttggcagcag cctgaactgg ctgcagcagg gcccggatgg caccattaaa 540
cgcctgattt atgcgaccag cagcctggat agcggcgtgc cgaaacgctt tagcggcagc 600
cgcagcggca gcgattatag cctgaccatt agcagcctgg aaagcgaaga ttttgtggat 660
tattattgcc tgcagtatgt gagcagcccg ccgacctttg gcgcgggcac caaactggaa 720
ctgaaa 726
<210> 51
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 51
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
85 90 95
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 52
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 52
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Gln Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
50 55 60
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
100 105
<210> 53
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 53
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Gln Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
50 55 60
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 54
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 54
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
85 90 95
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 55
<211> 2034
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 55
atgctgctgc tggtgaccag cctgctgctg tgtgagctgc cccaccccgc ctttctgctg 60
atccccgaca tccagatgac ccagaccacc tccagcctga gcgccagcct gggcgaccgg 120
gtgaccatca gctgccgggc cagccaggac atcagcaagt acctgaactg gtatcagcag 180
aagcccgacg gcaccgtcaa gctgctgatc taccacacca gccggctgca cagcggcgtg 240
cccagccggt ttagcggcag cggctccggc accgactaca gcctgaccat ctccaacctg 300
gagcaggagg acatcgccac ctacttttgc cagcagggca acacactgcc ctacaccttt 360
ggcggcggaa caaagctgga gatcaccggc agcacctccg gcagcggcaa gcctggcagc 420
ggcgagggca gcaccaaggg cgaggtgaag ctgcaggaga gcggccctgg cctggtggcc 480
cccagccaga gcctgagcgt gacctgtacc gtgtccggcg tgtccctgcc cgactacggc 540
gtgtcctgga tccggcagcc ccctaggaag ggcctggagt ggctgggcgt gatctggggc 600
agcgagacca cctactacaa cagcgccctg aagagccggc tgaccatcat caaggacaac 660
agcaagagcc aggtgttcct gaagatgaac agcctgcaga ccgacgacac cgccatctac 720
tactgtgcca agcactacta ctacggcggc agctacgcca tggactactg gggccagggc 780
accagcgtga ccgtgtccag cgagagcaag tacggccctc cctgcccccc ttgccctgcc 840
cccgagttcc tgggcggacc cagcgtgttc ctgttccccc ccaagcccaa ggacaccctg 900
atgatcagcc ggacccccga ggtgacctgt gtggtggtgg acgtgtccca ggaggacccc 960
gaggtccagt tcaactggta cgtggacggc gtggaggtgc acaacgccaa gaccaagccc 1020
cgggaggagc agttcaatag cacctaccgg gtggtgtccg tgctgaccgt gctgcaccag 1080
gactggctga acggcaagga atacaagtgt aaggtgtcca acaagggcct gcccagcagc 1140
atcgagaaaa ccatcagcaa ggccaagggc cagcctcggg agccccaggt gtacaccctg 1200
ccccctagcc aagaggagat gaccaagaat caggtgtccc tgacctgcct ggtgaagggc 1260
ttctacccca gcgacatcgc cgtggagtgg gagagcaacg gccagcccga gaacaactac 1320
aagaccaccc cccctgtgct ggacagcgac ggcagcttct tcctgtacag caggctgacc 1380
gtggacaaga gccggtggca ggagggcaac gtctttagct gctccgtgat gcacgaggcc 1440
ctgcacaacc actacaccca gaagagcctg tccctgagcc tgggcaagat gttctgggtg 1500
ctggtcgtgg tgggtggcgt gctggcctgc tacagcctgc tggtgacagt ggccttcatc 1560
atcttttggg tgaggagcaa gcggagcaga ggcggccaca gcgactacat gaacatgacc 1620
ccccggaggc ctggccccac ccggaagcac taccagccct acgcccctcc cagggacttc 1680
gccgcctacc ggagccgggt gaagttcagc cggagcgccg acgcccctgc ctaccagcag 1740
ggccagaacc agctgtacaa cgagctgaac ctgggccgga gggaggagta cgacgtgctg 1800
gacaagcgga gaggccggga ccctgagatg ggcggcaagc cccggagaaa gaaccctcag 1860
gagggcctgt ataacgaact gcagaaagac aagatggccg aggcctacag cgagatcggc 1920
atgaagggcg agcggcggag gggcaagggc cacgacggcc tgtaccaggg cctgagcacc 1980
gccaccaagg atacctacga cgccctgcac atgcaggccc tgccccccag atga 2034
<210> 56
<211> 2040
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 56
atgctgctgc tggtgaccag cctgctgctg tgtgagctgc cccaccccgc ctttctgctg 60
atccccgaca tccagatgac ccagaccacc tccagcctga gcgccagcct gggcgaccgg 120
gtgaccatca gctgccgggc cagccaggac atcagcaagt acctgaactg gtatcagcag 180
aagcccgacg gcaccgtcaa gctgctgatc taccacacca gccggctgca cagcggcgtg 240
cccagccggt ttagcggcag cggctccggc accgactaca gcctgaccat ctccaacctg 300
gagcaggagg acatcgccac ctacttttgc cagcagggca acacactgcc ctacaccttt 360
ggcggcggaa caaagctgga gatcaccggc agcacctccg gcagcggcaa gcctggcagc 420
ggcgagggca gcaccaaggg cgaggtgaag ctgcaggaga gcggccctgg cctggtggcc 480
cccagccaga gcctgagcgt gacctgtacc gtgtccggcg tgtccctgcc cgactacggc 540
gtgtcctgga tccggcagcc ccctaggaag ggcctggagt ggctgggcgt gatctggggc 600
agcgagacca cctactacaa cagcgccctg aagagccggc tgaccatcat caaggacaac 660
agcaagagcc aggtgttcct gaagatgaac agcctgcaga ccgacgacac cgccatctac 720
tactgtgcca agcactacta ctacggcggc agctacgcca tggactactg gggccagggc 780
accagcgtga ccgtgtccag cgagagcaag tacggccctc cctgcccccc ttgccctgcc 840
cccgagttcc tgggcggacc cagcgtgttc ctgttccccc ccaagcccaa ggacaccctg 900
atgatcagcc ggacccccga ggtgacctgt gtggtggtgg acgtgtccca ggaggacccc 960
gaggtccagt tcaactggta cgtggacggc gtggaggtgc acaacgccaa gaccaagccc 1020
cgggaggagc agttcaatag cacctaccgg gtggtgtccg tgctgaccgt gctgcaccag 1080
gactggctga acggcaagga atacaagtgt aaggtgtcca acaagggcct gcccagcagc 1140
atcgagaaaa ccatcagcaa ggccaagggc cagcctcggg agccccaggt gtacaccctg 1200
ccccctagcc aagaggagat gaccaagaat caggtgtccc tgacctgcct ggtgaagggc 1260
ttctacccca gcgacatcgc cgtggagtgg gagagcaacg gccagcccga gaacaactac 1320
aagaccaccc cccctgtgct ggacagcgac ggcagcttct tcctgtacag caggctgacc 1380
gtggacaaga gccggtggca ggagggcaac gtctttagct gctccgtgat gcacgaggcc 1440
ctgcacaacc actacaccca gaagagcctg tccctgagcc tgggcaagat gatctacatc 1500
tgggcccctc tggccggcac ctgtggcgtg ctgctgctga gcctggtcat caccctgtac 1560
tgcaaccacc ggaacaagag aggccggaag aaactgctgt acatcttcaa gcagcccttc 1620
atgcggcccg tgcagaccac ccaggaagag gacggctgca gctgccggtt ccccgaggaa 1680
gaggaaggcg gctgcgaact gcgggtgaag ttcagccgga gcgccgacgc ccctgcctac 1740
cagcagggcc agaaccagct gtacaacgag ctgaacctgg gccggaggga ggagtacgac 1800
gtgctggaca agcggagagg ccgggaccct gagatgggcg gcaagccccg gagaaagaac 1860
cctcaggagg gcctgtataa cgaactgcag aaagacaaga tggccgaggc ctacagcgag 1920
atcggcatga agggcgagcg gcggaggggc aagggccacg acggcctgta ccagggcctg 1980
agcaccgcca ccaaggatac ctacgacgcc ctgcacatgc aggccctgcc ccccagatga 2040
<210> 57
<211> 2037
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 57
atgctgctgc tggtgaccag cctgctgctg tgtgagctgc cccaccccgc ctttctgctg 60
atccccgaca tccagatgac ccagaccacc tccagcctga gcgccagcct gggcgaccgg 120
gtgaccatca gctgccgggc cagccaggac atcagcaagt acctgaactg gtatcagcag 180
aagcccgacg gcaccgtcaa gctgctgatc taccacacca gccggctgca cagcggcgtg 240
cccagccggt ttagcggcag cggctccggc accgactaca gcctgaccat ctccaacctg 300
gagcaggagg acatcgccac ctacttttgc cagcagggca acacactgcc ctacaccttt 360
ggcggcggaa caaagctgga gatcaccggc agcacctccg gcagcggcaa gcctggcagc 420
ggcgagggca gcaccaaggg cgaggtgaag ctgcaggaga gcggccctgg cctggtggcc 480
cccagccaga gcctgagcgt gacctgtacc gtgtccggcg tgtccctgcc cgactacggc 540
gtgtcctgga tccggcagcc ccctaggaag ggcctggagt ggctgggcgt gatctggggc 600
agcgagacca cctactacaa cagcgccctg aagagccggc tgaccatcat caaggacaac 660
agcaagagcc aggtgttcct gaagatgaac agcctgcaga ccgacgacac cgccatctac 720
tactgtgcca agcactacta ctacggcggc agctacgcca tggactactg gggccagggc 780
accagcgtga ccgtgtccag cgagagcaag tacggccctc cctgcccccc ttgccctgcc 840
cccgagttcc tgggcggacc cagcgtgttc ctgttccccc ccaagcccaa ggacaccctg 900
atgatcagcc ggacccccga ggtgacctgt gtggtggtgg acgtgtccca ggaggacccc 960
gaggtccagt tcaactggta cgtggacggc gtggaggtgc acaacgccaa gaccaagccc 1020
cgggaggagc agttcaatag cacctaccgg gtggtgtccg tgctgaccgt gctgcaccag 1080
gactggctga acggcaagga atacaagtgt aaggtgtcca acaagggcct gcccagcagc 1140
atcgagaaaa ccatcagcaa ggccaagggc cagcctcggg agccccaggt gtacaccctg 1200
ccccctagcc aagaggagat gaccaagaat caggtgtccc tgacctgcct ggtgaagggc 1260
ttctacccca gcgacatcgc cgtggagtgg gagagcaacg gccagcccga gaacaactac 1320
aagaccaccc cccctgtgct ggacagcgac ggcagcttct tcctgtacag caggctgacc 1380
gtggacaaga gccggtggca ggagggcaac gtctttagct gctccgtgat gcacgaggcc 1440
ctgcacaacc actacaccca gaagagcctg tccctgagcc tgggcaagat gatctacatc 1500
tgggcccctc tggccggcac ctgtggcgtg ctgctgctga gcctggtcat caccctgtac 1560
tgcaaccacc ggaataggag caagcggagc agaggcggcc acagcgacta catgaacatg 1620
accccccgga ggcctggccc cacccggaag cactaccagc cctacgcccc tcccagggac 1680
ttcgccgcct accggagccg ggtgaagttc agccggagcg ccgacgcccc tgcctaccag 1740
cagggccaga accagctgta caacgagctg aacctgggcc ggagggagga gtacgacgtg 1800
ctggacaagc ggagaggccg ggaccctgag atgggcggca agccccggag aaagaaccct 1860
caggagggcc tgtataacga actgcagaaa gacaagatgg ccgaggccta cagcgagatc 1920
ggcatgaagg gcgagcggcg gaggggcaag ggccacgacg gcctgtacca gggcctgagc 1980
accgccacca aggataccta cgacgccctg cacatgcagg ccctgccccc cagatga 2037
<210> 58
<211> 2037
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 58
atgctgctgc tggtgaccag cctgctgctg tgtgagctgc cccaccccgc ctttctgctg 60
atccccgaca tccagatgac ccagaccacc tccagcctga gcgccagcct gggcgaccgg 120
gtgaccatca gctgccgggc cagccaggac atcagcaagt acctgaactg gtatcagcag 180
aagcccgacg gcaccgtcaa gctgctgatc taccacacca gccggctgca cagcggcgtg 240
cccagccggt ttagcggcag cggctccggc accgactaca gcctgaccat ctccaacctg 300
gagcaggagg acatcgccac ctacttttgc cagcagggca acacactgcc ctacaccttt 360
ggcggcggaa caaagctgga gatcaccggc agcacctccg gcagcggcaa gcctggcagc 420
ggcgagggca gcaccaaggg cgaggtgaag ctgcaggaga gcggccctgg cctggtggcc 480
cccagccaga gcctgagcgt gacctgtacc gtgtccggcg tgtccctgcc cgactacggc 540
gtgtcctgga tccggcagcc ccctaggaag ggcctggagt ggctgggcgt gatctggggc 600
agcgagacca cctactacaa cagcgccctg aagagccggc tgaccatcat caaggacaac 660
agcaagagcc aggtgttcct gaagatgaac agcctgcaga ccgacgacac cgccatctac 720
tactgtgcca agcactacta ctacggcggc agctacgcca tggactactg gggccagggc 780
accagcgtga ccgtgtccag cgagagcaag tacggccctc cctgcccccc ttgccctgcc 840
cccgagttcc tgggcggacc cagcgtgttc ctgttccccc ccaagcccaa ggacaccctg 900
atgatcagcc ggacccccga ggtgacctgt gtggtggtgg acgtgtccca ggaggacccc 960
gaggtccagt tcaactggta cgtggacggc gtggaggtgc acaacgccaa gaccaagccc 1020
cgggaggagc agttcaatag cacctaccgg gtggtgtccg tgctgaccgt gctgcaccag 1080
gactggctga acggcaagga atacaagtgt aaggtgtcca acaagggcct gcccagcagc 1140
atcgagaaaa ccatcagcaa ggccaagggc cagcctcggg agccccaggt gtacaccctg 1200
ccccctagcc aagaggagat gaccaagaat caggtgtccc tgacctgcct ggtgaagggc 1260
ttctacccca gcgacatcgc cgtggagtgg gagagcaacg gccagcccga gaacaactac 1320
aagaccaccc cccctgtgct ggacagcgac ggcagcttct tcctgtacag caggctgacc 1380
gtggacaaga gccggtggca ggagggcaac gtctttagct gctccgtgat gcacgaggcc 1440
ctgcacaacc actacaccca gaagagcctg tccctgagcc tgggcaagat gattatctca 1500
ttcttcctgg ccctgacctc taccgccctg ctgtttctgc tgttctttct gaccctgcgg 1560
ttcagcgtgg tcaagagagg ccggaagaaa ctgctgtaca tcttcaagca gcccttcatg 1620
cggcccgtgc agaccaccca ggaagaggac ggctgcagct gccggttccc cgaggaagag 1680
gaaggcggct gcgaactgcg ggtgaagttc agccggagcg ccgacgcccc tgcctaccag 1740
cagggccaga accagctgta caacgagctg aacctgggcc ggagggagga gtacgacgtg 1800
ctggacaagc ggagaggccg ggaccctgag atgggcggca agccccggag aaagaaccct 1860
caggagggcc tgtataacga actgcagaaa gacaagatgg ccgaggccta cagcgagatc 1920
ggcatgaagg gcgagcggcg gaggggcaag ggccacgacg gcctgtacca gggcctgagc 1980
accgccacca aggataccta cgacgccctg cacatgcagg ccctgccccc cagatga 2037
<210> 59
<211> 2160
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический олигонуклеотид
<400> 59
atgctgctgc tggtgaccag cctgctgctg tgtgagctgc cccaccccgc ctttctgctg 60
atccccgaca tccagatgac ccagaccacc tccagcctga gcgccagcct gggcgaccgg 120
gtgaccatca gctgccgggc cagccaggac atcagcaagt acctgaactg gtatcagcag 180
aagcccgacg gcaccgtcaa gctgctgatc taccacacca gccggctgca cagcggcgtg 240
cccagccggt ttagcggcag cggctccggc accgactaca gcctgaccat ctccaacctg 300
gagcaggagg acatcgccac ctacttttgc cagcagggca acacactgcc ctacaccttt 360
ggcggcggaa caaagctgga gatcaccggc agcacctccg gcagcggcaa gcctggcagc 420
ggcgagggca gcaccaaggg cgaggtgaag ctgcaggaga gcggccctgg cctggtggcc 480
cccagccaga gcctgagcgt gacctgtacc gtgtccggcg tgtccctgcc cgactacggc 540
gtgtcctgga tccggcagcc ccctaggaag ggcctggagt ggctgggcgt gatctggggc 600
agcgagacca cctactacaa cagcgccctg aagagccggc tgaccatcat caaggacaac 660
agcaagagcc aggtgttcct gaagatgaac agcctgcaga ccgacgacac cgccatctac 720
tactgtgcca agcactacta ctacggcggc agctacgcca tggactactg gggccagggc 780
accagcgtga ccgtgtccag cgagagcaag tacggccctc cctgcccccc ttgccctgcc 840
cccgagttcc tgggcggacc cagcgtgttc ctgttccccc ccaagcccaa ggacaccctg 900
atgatcagcc ggacccccga ggtgacctgt gtggtggtgg acgtgtccca ggaggacccc 960
gaggtccagt tcaactggta cgtggacggc gtggaggtgc acaacgccaa gaccaagccc 1020
cgggaggagc agttcaatag cacctaccgg gtggtgtccg tgctgaccgt gctgcaccag 1080
gactggctga acggcaagga atacaagtgt aaggtgtcca acaagggcct gcccagcagc 1140
atcgagaaaa ccatcagcaa ggccaagggc cagcctcggg agccccaggt gtacaccctg 1200
ccccctagcc aagaggagat gaccaagaat caggtgtccc tgacctgcct ggtgaagggc 1260
ttctacccca gcgacatcgc cgtggagtgg gagagcaacg gccagcccga gaacaactac 1320
aagaccaccc cccctgtgct ggacagcgac ggcagcttct tcctgtacag caggctgacc 1380
gtggacaaga gccggtggca ggagggcaac gtctttagct gctccgtgat gcacgaggcc 1440
ctgcacaacc actacaccca gaagagcctg tccctgagcc tgggcaagat gttctgggtg 1500
ctggtcgtgg tgggtggcgt gctggcctgc tacagcctgc tggtgacagt ggccttcatc 1560
atcttttggg tgaggagcaa gcggagcaga ggcggccaca gcgactacat gaacatgacc 1620
ccccggaggc ctggccccac ccggaagcac taccagccct acgcccctcc cagggacttc 1680
gccgcctacc ggagcaagag aggccggaag aaactgctgt acatcttcaa gcagcccttc 1740
atgcggcccg tgcagaccac ccaggaagag gacggctgca gctgccggtt ccccgaggaa 1800
gaggaaggcg gctgcgaact gcgggtgaag ttcagccgga gcgccgacgc ccctgcctac 1860
cagcagggcc agaaccagct gtacaacgag ctgaacctgg gccggaggga ggagtacgac 1920
gtgctggaca agcggagagg ccgggaccct gagatgggcg gcaagccccg gagaaagaac 1980
cctcaggagg gcctgtataa cgaactgcag aaagacaaga tggccgaggc ctacagcgag 2040
atcggcatga agggcgagcg gcggaggggc aagggccacg acggcctgta ccagggcctg 2100
agcaccgcca ccaaggatac ctacgacgcc ctgcacatgc aggccctgcc ccccagatga 2160
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР С КОСТИМУЛИРУЮЩИМ ДОМЕНОМ 4-1BB | 2020 |
|
RU2830540C2 |
| КЛЕТКА | 2015 |
|
RU2768019C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ К КАППА-АНТИГЕНУ МИЕЛОМЫ И ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2743188C2 |
| ЛЕЧЕНИЕ РАКА С ПОМОЩЬЮ ГУМАНИЗИРОВАННОГО АНТИ-CD19 ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА | 2014 |
|
RU2711975C2 |
| CAR-T-КЛЕТКИ, СПЕЦИФИЧЕСКИ НАЦЕЛЕННЫЕ НА АНТИГЕН CD19 | 2020 |
|
RU2826298C2 |
| СПОСОБЫ ТЕРАПИИ НА ОСНОВЕ CAR Т-КЛЕТОК С ПОВЫШЕННОЙ ЭФФЕКТИВНОСТЬЮ | 2016 |
|
RU2788131C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ЭКСПРЕССИРУЮЩИХ ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР КЛЕТОК | 2015 |
|
RU2751362C2 |
| ЛЕЧЕНИЕ РАКА С ИСПОЛЬЗОВАНИЕМ ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА CLL-1 | 2015 |
|
RU2741120C2 |
| ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ С ИСПОЛЬЗОВАНИЕМ ГУМАНИЗИРОВАННОГО ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА ПРОТИВ ВСМА | 2015 |
|
RU2751660C2 |
| ЛЕЧЕНИЕ РАКА С ИСПОЛЬЗОВАНИЕМ ХИМЕРНОГО АНТИГЕНСПЕЦИФИЧЕСКОГО РЕЦЕПТОРА НА ОСНОВЕ ГУМАНИЗИРОВАННОГО АНТИТЕЛА ПРОТИВ EGFRvIII | 2014 |
|
RU2831418C2 |
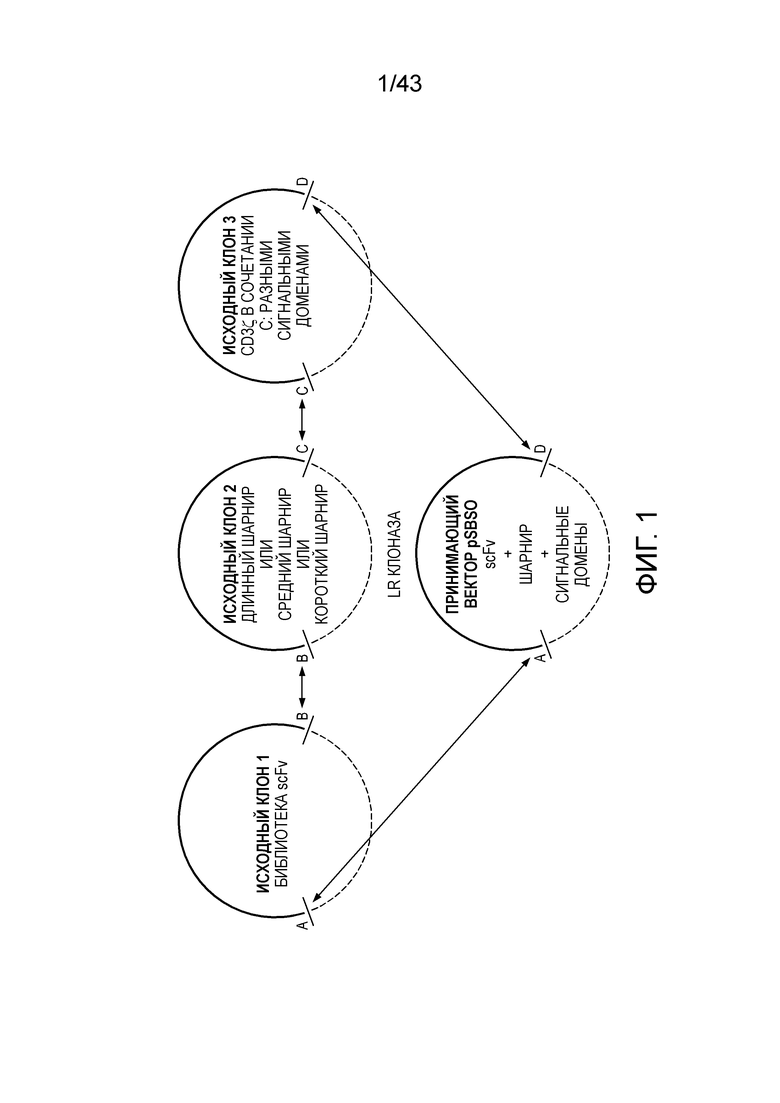




























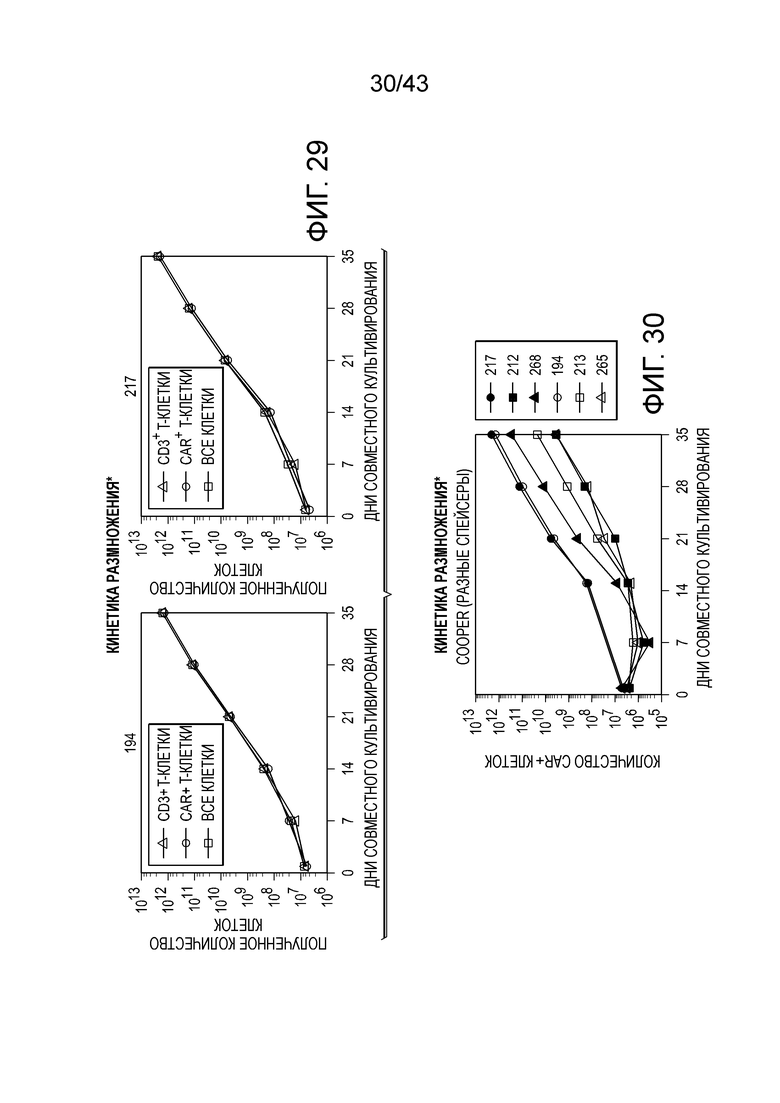













Изобретение относится к области биотехнологии, конкретно к CD19-специфическому полипептиду химерного антигенного рецептора (CAR), кодируемому последовательностью ДНК с SEQ ID NO:5, нуклеотидами 1-1485 SEQ ID NO:5 или нуклеотидами 67-1485 SEQ ID NO:5, и может быть использовано в медицине. Изобретение позволяет получить Т-клетки, нацеленные на CD19, которые можно использовать для эффективной терапии CD19+ злокачественных новообразований. 11 н. и 6 з.п. ф-лы, 42 ил., 2 табл., 5 пр.
1. CD19-специфический полипептид химерного антигенного рецептора, кодируемый последовательностью ДНК с последовательностью SEQ ID NO:5, нуклеотидами 1-1485 SEQ ID NO:5 или нуклеотидами 67-1485 SEQ ID NO:5.
2. Нуклеиновая кислота, кодирующая CD19-специфический полипептид химерного антигенного рецептора, кодируемый последовательностью SEQ ID NO:5, нуклеотидами 1-1485 SEQ ID NO:5 или нуклеотидами 67-1485 SEQ ID NO:5.
3. Транспозонный вектор «спящая красавица», содержащий нуклеиновую кислоту по п. 2, где введение транспозонного вектора «спящая красавица» в клетку приводит к экспрессии CD19-специфического полипептида химерного антигенного рецептора.
4. T-клетка для применения в лечении CD19+-рака, содержащая CD19-специфический полипептид химерного антигенного рецептора, кодируемый последовательностью SEQ ID NO:5, нуклеотидами 1-1485 SEQ ID NO:5 или нуклеотидами 67-1485 SEQ ID NO:5, где Т-клетка экспрессирует CD19-специфический полипептид химерного антигенного рецептора на поверхности клетки.
5. Т-клетка для применения в лечении CD19+-рака, содержащая: а) CD19-специфический полипептид химерного антигенного рецептора, кодируемый последовательностью SEQ ID NO:5, нуклеотидами 1-1485 SEQ ID NO:5 или нуклеотидами 67-1485 SEQ ID NO:5, и b) мембраносвязанный цитокин, где Т-клетка экспрессирует CD19-специфический полипептид химерного антигенного рецептора на поверхности клетки.
6. Т-клетка по п. 5, где мембраносвязанный цитокин представляет собой мембраносвязанный IL-5.
7. Т-клетка, содержащая нуклеиновую кислоту по п. 2, где Т-клетка экспрессирует CD19-специфический полипептид химерного антигенного рецептора на клеточной поверхности.
8. Т-клетка, содержащая нуклеиновую кислоту по п. 2 и мебраносвязанный цитокин, где Т-клетка экспрессирует CD19-специфический полипептид химерного антигенного рецептора на клеточной поверхности.
9. Т-клетка по п. 8, где мембраносвязанный цитокин представляет собой мембраносвязанный IL-5.
10. Т-клетка, содержащая транспозонный вектор «спящая красавица» по п. 3, где Т-клетка экспрессирует CD19-специфический полипептид химерного антигенного рецептора на клеточной поверхности.
11. Т-клетка, содержащая транспозонный вектор «спящая красавица» по п. 3 и мембраносвязанный цитокин, где Т-клетка экспрессирует CD19-специфический полипептид химерного антигенного рецептора на клеточной поверхности.
12. Т-клетка по п. 11, где мембраносвязанный цитокин представляет собой мембраносвязанный IL-5.
13. Т-клетка по любому из пп. 4-12, представляющая собой иммортализованную клетку.
14. T-клетка по любому из пп. 4-13, представляющая собой альфа-бета T-клетку, гамма-дельта T-клетку или NKT-клетку.
15. Фармацевтическая композиция для лечения CD19+ злокачественного новообразования, содержащая эффективное количество T-клетки по любому из пп. 4-14 и фармацевтически приемлемый носитель.
16. Применение Т-клетки по любому из пп. 4-14 для лечения CD19+ злокачественного новообразования.
17. Применение Т-клетки по п. 16, где рак представляет собой В-клеточное злокачественное новообразование или лимфому.
| US 2013280220 A1, 24.10.2013 | |||
| WO 2013063419 A2, 02.05.2013 | |||
| WO 2013176915 A1, 28.11.2013 | |||
| US 2013266551 A1, 10.10.2013 | |||
| ЛИКАРЬ Ю | |||
| Н | |||
| и др., Использование мутированного варианта человеческой деоксицитидинкиназы в качестве репортерного гена для оценки адоптивной Т-клеточной терапии, Вопросы гематологии, онкологии и иммунопатологии в педиатрии, |
Авторы
Даты
2021-08-24—Публикация
2015-02-16—Подача