Изобретение относится к косметической или дерматологической композиции, предназначенной для местного нанесения, содержащей по меньшей мере один 1,3-диглицерид, охарактеризованный ниже, а также к ее применению для улучшения резистентности рогового слоя эпидермиса, в частности, к внешним факторам, таким как холод или тепло, тем самым защищая его свойства кожного барьера.
Одной из основных функций кожи является формирование физического барьера, который помимо защиты от окружающей среды, путем предотвращения проникновения агрессивных микроорганизмов или химических элементов, должен поддерживать физиологическую среду организма, ограничивая потерю воды, благодаря относительной гидрофобности. Несмотря на существование разногласий относительно различных путей прохождения через кожу, в большинстве случаев считается, что проникновение через межкорнеоцитное пространство также служит элементом регуляции проницаемости кожи [1]. Эффективность кожного барьера определяется значительным числом последовательных событий адсорбции-десорбции, связанных с диффузией молекул через ламеллярные слои рогового слоя. Дифракция рентгеновских лучей, используемая для характеризации кожного барьера, обнаруживает наличие двух ламеллярных фаз с периодом повторяемости 6 и 13 нм, преимущественно расположенных в латеральных фазах кристалла (орторомбическая латеральная организация) [2, 3, 4]. Действительно, при физиологических значениях температуры длинные алифатические цепи церамидов и жирных кислот образуют с холестерином и его эфирами матрикс, имеющий гелеобразное состояние, который является непроницаемым для трансэпидермального тока влаги.
У субъектов с интактным кожным барьером трансэпидермальный ток влаги (также обозначаемый трансэпидермальной потерей влаги) составляет приблизительно 5 мг/см2 [5], однако может достигать более высоких значений в случае агрессивных внешних воздействий, обусловленных различными факторами окружающей среды, такими как холод или тепло. В этой связи, было показано, что обычное нахождение в среднем в течение 3 часов в условиях солнечного освещения под открытым небом (температура окружающей среды 26,6°С) достаточно для того, чтобы вызвать повышение температуры кожи на 4,7°С (изначально имеющей температуру 31,7°С) [6] и что температура кожи может превысить 40°С всего через 20 минут нахождения на солнце в астрономический полдень летом [7]. Такое повышение температуры кожи затем вызывает разжижение липидов межкорнеоцитного пространства, переходящих в жидкокристаллическое состояние, что способствует существенному увеличению трансэпидермальной потери влаги [4].
Таким образом, изменение / ослабление кожного барьера создает благоприятные условия для усиленного проникновения экзогенных соединений (загрязняющих агентов, раздражающих агентов или аллергизирующих веществ (также называемых аллергенами)), предпочтительно липофильных экзогенных соединений, которые в ряде случаев могут вызывать раздражение или аллергические реакции, или окислительный стресс.
Некоторые органические загрязняющие агенты, такие как бензо[а]пирен, поступающий из выхлопных газов, являются не только аллергенными, но и считаются канцерогенными (канцерогены 1 группы).
Диглицериды описаны в литературе и обладают биологический, косметической и/или терапевтической активностями. В документе KR 2013058299 описано применение композиции, содержащей 1,3-диолеин или 1,3-дилинолеил-рац-глицерол, для предупреждения или лечения гиперпигментации. Аналогично, препараты на основе производных жирных кислот, в том числе диглицеридов, заявлены как агенты, препятствующие старению кожи (WO 03/014073 А1), как эмоленты (JP02115117 А), или применялись в составе гигиенической губной помады (JP52061240A). Некоторые диглицериды применяют в настоящее время в косметических композициях в низкой концентрации (<1% по массе) в качестве агентов, придающих текстуру. Однако, в настоящее время ни один из документов не описывает и не позволяет предположить, что 1,3-диглицериды могут обладать свойствами, которые могут представлять интерес для противодействия ослаблению функции кожного барьера, в частности, под воздействием внешних факторов (холод, тепло).
Данное изобретение нацелено на преодоление недостатков существующего уровня техники благодаря предложению активных агентов, стабилизирующих межкорнеоцитное пространство, и их применению в косметических или дерматологических композициях для противодействия ослаблению кожного барьера, в частности, под воздействием внешних факторов. Достижение большей стабильности межкорнеоцитного пространства само по себе открывает новые перспективы в области косметических и дерматологических продуктов для ухода за кожей, в том числе за кожей лица, кожей тела и кожей головы, и/или для макияжа. Такие активные агенты могут применяться в косметических или дерматологических композициях для местного нанесения для защиты кожи, в том числе кожи лица, кожи тела и кожи головы, в частности, против некоторых вредных эффектов (таких как аллергия, раздражение и т.д.), обусловленных проникновением в кожу экзогенных соединений, указанное проникновение в кожу усиливается под воздействием внешних факторов, таких как тепло.
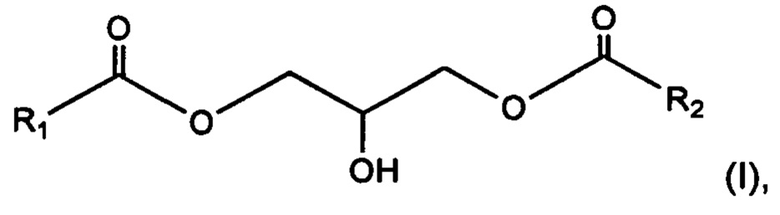
Неожиданно обнаружили, что применение 1,3-диглицерида, имеющего общую формулу (I):
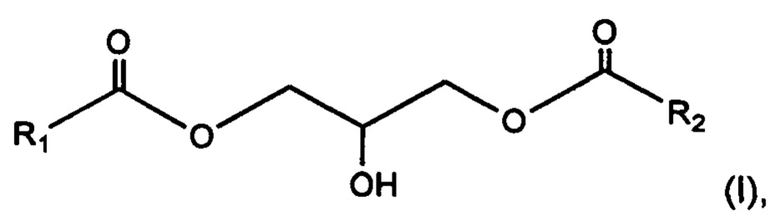
где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал, в косметической или дерматологической композиции позволяет после местного нанесения ограничить ослабление кожного барьера, которое может быть обусловлено внешними факторами. Авторы изобретения, в частности, обнаружили, что указанные 1,3-диглицериды при нанесении на кожу стабилизируют изменение состояния липидов, присутствующих в межкорнеоцитном пространстве; это изменение состояния наблюдается, в частности, под влиянием температуры.
Для оценки изменения в организации липидных фаз рогового слоя эпидермиса авторы изобретения использовали инфракрасную спектроскопию (ATR-FTIR: от англ. Attenuated total reflectance - Fourier transform infrared Spectroscopy, ИК-спектроскопия нарушенного полного внутреннего отражения с Фурье-преобразованием) для анализа изменения колебаний на основной частоте νCH2 алифатических цепей указанных липидов под влиянием температуры. Более конкретно, положение полосы поглощения, соответствующей валентным колебаниям СН2, выражается волновым числом приблизительно 2848 см-1. Например, повышение температуры поверхности кожи вызывает смещение волновых чисел указанных полос к большим значениям. Такое смещение указывает на тот факт, что липиды в роговом слое эпидермиса под воздействием тепла принимают менее упорядоченную конформацию, что сопровождается увеличением текучести углеводородных цепей, заполняющих межкорнеоцитное пространство (см. Пример 1).
В рамках данного изобретения также было показано, что, с одной стороны, стабилизирующая способность 1,3-диглицеридов в отношении нагретой липидной фазы увеличивает длину эстерифицированных цепей (см. Пример 2) и с другой стороны, что 1,3-диглицериды оказывают на нагретую липидную фазу стабилизирующее влияние, существенно превосходящее таковое 1,2-диглицеридов (см. Пример 3). При этом в рамках данного изобретения не исключается применение 1,3-диглицерида, который будет находиться в смеси с небольшими количествами 1,2-диглицеридов, часто присутствующих вследствие условий промышленного производства.
Кроме того, исследование in vivo на здоровых добровольцах позволило продемонстрировать, что применение глицерила 1,3-дистеарата позволяет стабилизировать организацию межкорнеоцитных липидов кожи при нагреве от 30 до 45°С. Данный благоприятный эффект сохраняется по меньшей мере на протяжении 4 часов после нанесения глицерила 1,3-дистеарата (см. Пример 4).
Исследование ex vivo также позволяет продемонстрировать, что нанесение глицерила 1,3-дистеарата на кожу позволяет ограничить повышенную вследствие нагревания проницаемость кожи для такого загрязняющего агента, как бензо[а]пирен.
Таким образом, объект данного изобретения относится к местной косметической или дерматологической композиции, содержащей по меньшей мере один 1,3-диглицерид, имеющий общую формулу (I):
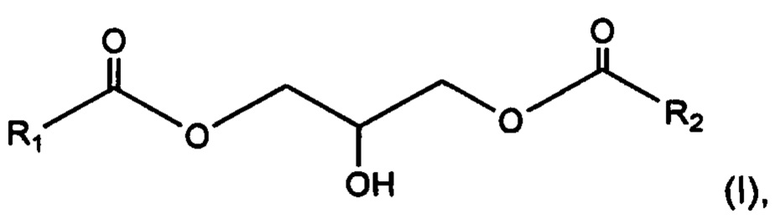
где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал;
и дополнительно содержащей и по меньшей мере один косметический или дерматологический эксципиент для местного нанесения на кожу.
1,3-диглицериды, имеющие общую формулу (I), указанную выше, могут быть получены, в частности, как описано в публикации Liu et al. [9]. Они могут найти применение в композициях по изобретению в качестве действующего вещества и, более конкретно, в качестве стабилизирующего агента межкорнеоцитного пространства.
Термин «межкорнеоцитное пространство» означает пространство, содержащее липидную фазу, которая расположена между корнеоцитами рогового слоя (также обозначаемого stratum corneum - см. реферат), образующего кожный барьер.
В рамках данной патентной заявки термин «стабилизирующий агент межкорнеоцитного пространства» используется, в частности, для обозначения агента, ограничивающего дестабилизацию межкорнеоцитного пространства, в частности, под воздействием внешних факторов, и который, таким образом, выполняет барьерную функцию, препятствуя проникновению экзогенных веществ, таких как химические агенты или микроорганизмы, которые могут вызывать раздражение и/или быть аллергенами, или загрязняющих агентов, которые могут вызывать окислительный стресс, в коже, особенно подвергаемой воздействию внешних факторов.
Указанный эффект стабилизации/дестабилизации межкорнеоцитного пространства можно оценивать, помимо прочего, согласно протоколу, приведенному в Примере 2.
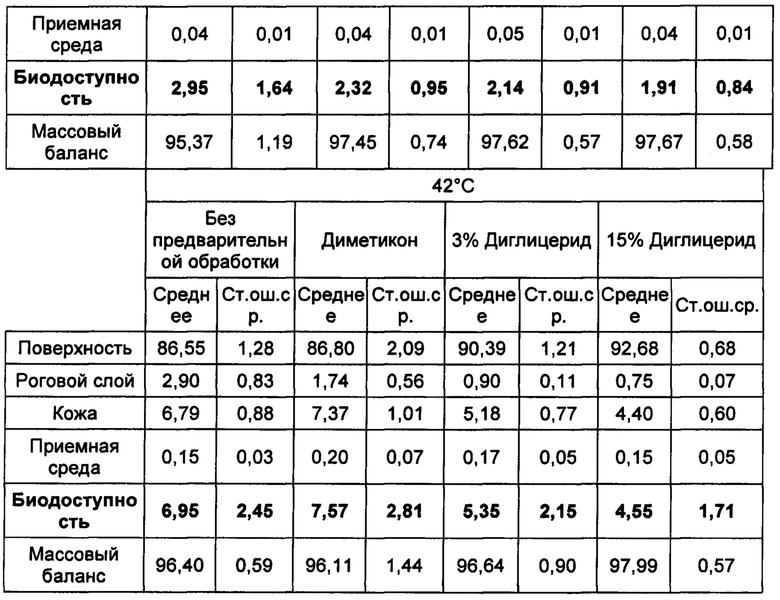
Что касается проникновения экзогенных веществ, исследование ex vivo (см. Пример 6) подтверждает тот факт, что на биодоступность бензо[а]пирена оказывает большое влияние температура кожи: она увеличивается в два раза, когда температура кожи изменяется от 32°С до 42°С (повышается от 2,95 до 6,95% дозы, нанесенной на кожу).
Это иллюстрирует необходимость усиления кожного барьера путем стабилизации межкорнеоцитного пространства для ограничения проникновения экзогенных веществ, в частности, когда внешние условия приводят к увеличению внешней температуры, особенно до приблизительно 42°С или выше.
Исследование биодоступности бензо[а]пирена после нанесения 1,3-диглицерида формулы I на исследуемую кожу также подтверждает, что соединения 1,3-диглицерида, охарактеризованные выше, обеспечивают указанную стабилизацию и, следовательно, защиту кожи.
Действительно, после нанесения 1,3-диглицерида формулы I и, в частности, глицерила 1,3-дистеарата в дозе 3% или 15% на кожу, находящуюся при температуре 42°С, наблюдалось существенное снижение проникновения бензо[а]пирена по сравнению с исходным состоянием и с носителем.
Термин «внешние факторы» означает в терминах данного изобретения внешние условия, такие как тепло или холод, предпочтительно тепло, приводящее к изменению температуры кожи, которое может дестабилизировать межкорнеоцитное пространство. В предпочтительном воплощении тепло, такое как в летний период, или при нахождении на солнце, может вызывать повышение температуры кожи, в частности, выше чем приблизительно 35°С, в частности, выше чем приблизительно 40°С, и может вызывать то, что в данном изобретении называют разжижением липидов межкорнеоцитного пространства.
Влияние внешней температуры на организацию межкорнеоцитного пространства рогового слоя эпидермиса можно, помимо прочего, оценивать согласно модели, приведенной в Примере 1 (анализ изменения волнового числа колебаний νCH2 при помощи инфракрасной спектроскопии).
В этой связи, как уже упоминалось, было показано, что обычное нахождение в среднем в течение 3 часов в условиях солнечного освещения под открытым небом (внешняя температура 26,6°С) достаточно для того, чтобы вызвать повышение температуры кожи на 4,7°С (исходно равной 31,7°С) [6], и что температура кожи может превысить 40°С всего через 20 минут нахождения на солнце в астрономический полдень летом [7].
Такое повышение температуры кожи затем вызывает разжижение липидов межкорнеоцитного пространства, переходящих в жидкокристаллическое состояние, что способствует существенному увеличению трансэпидермальной потери влаги [4].
В конкретном воплощении изобретения радикалы R1 и R2 являются идентичными и представляют С13-С40 насыщенный и неразветвленный алкильный радикал.
Согласно другому воплощению изобретения радикалы R1 и R2 представляют, независимо друг от друга, С15-С23, в частности, С15-С19 насыщенный и неразветвленный алкильный радикал. Радикалы R1 и R2 также могут быть идентичными и представлять С15-С23, в частности, С15-С19 насыщенный и неразветвленный алкильный радикал.
Радикалы R1 и R2, как идентичные, так и различные, предпочтительно идентичные, представляют, в частности, углеводородную цепь пальмитиновой, стеариновой или арахиновой кислоты, а именно пентадецильный, гептадецильный или нонадецильный радикал.
1,3-диглицерид по изобретению, в частности, будет представлять собой глицерила 1,3-дипальмитат, глицерила 1,3-дистеарат или их смесь.
1,3-диглицериды, имеющие формулу (I) по изобретению предпочтительно составляют от 0,5 до 10%, более конкретно, от 1 до 5% и еще более конкретно, от 3 до 5% по массе от общей массы композиции.
Согласно другому воплощению 1,3-диглицериды, имеющие формулу (I) по изобретению, составляют от 5 до 10% по массе от общей массы композиции.
Композиции по данному изобретению также содержат 1,2-диглицерид. Действительно, используемые 1,3-диглицериды обычно содержат небольшие остаточные количества 1,2-диглицерида. Однако количество 1,2-диглицерида в композициях по изобретению предпочтительно не будет превышать 10% по массе, в частности 5% по массе от общей массы 1,3- и 1,2-диглицеридов.
Композиции для местного нанесения по изобретению предназначены для нанесения на кожу. Указанные композиции могут быть более или менее жидкими и быть в виде крема, лосьона, молочка, сыворотки, мази, геля или пенки. Они также могут быть в твердой форме, такой как карандаш, или наноситься на кожу в форме аэрозоля. Указанные композиции в частности могут быть в форме маслянистого раствора, эмульсии масло-в-воде, вода-в-масле или множественной эмульсии.
1,3-диглицериды, имеющие формулу (I) по изобретению, предпочтительно вводят в композиции в диспергированной форме.
Под «диспергированной формой» в данном изобретении понимают, что 1,3-диглицерид, имеющий формулу (I) по изобретению, находится в форме твердых частиц, которые диспергированы в дисперсионной фазе.
Так, композиции по изобретению будут предпочтительно содержать по меньшей мере один 1,3-диглицерид, имеющий формулу (I) по изобретению, в диспергированной форме, т.е. присутствующий в композиции в форме диспергированных твердых частиц.
Согласно предпочтительному воплощению средний диаметр твердых частиц 1,3-диглицерида формулы (I) по изобретению составляет более 100 нм и менее 50 мкм. Такое значение получают путем определения гранулометрического состава частиц при помощи лазерной дифракции.
В конкретном воплощении 1,3-диглицериды формулы (I) по изобретению будут диспергированы в жировой фазе, например, в силиконе, и предпочтительно, в нелетучем силиконе, эфире, минеральном масле или растительном масле, или их смеси. Среди силиконов можно упомянуть диметикон (нелетучий).
Композиция по изобретению обеспечивает защиту кожного барьера, которая остается комфортной на протяжении всего дня. В частности, ее можно наносить на чувствительную, склонную к повреждению и/или реагирующую на раздражение кожу, в частности, на кожу младенца.
Объектом данного изобретения также является композиция по изобретению, описанная выше, для применения в защите кожи, в том числе кожи лица, кожи тела и кожи головы.
Данное изобретение также относится к применению композиции, описанной выше, для защиты кожи, в том числе кожи лица, кожи тела и кожи головы.
Данное изобретение также относится к способу защиты кожи, в том числе кожи лица, кожи тела и кожи головы, включающему введение индивидууму, которому это необходимо, эффективного количества композиции, описанной выше.
Объектом данного изобретения также является композиция по изобретению, описанная выше, для применения в противодействии ослаблению кожного барьера.
Данное изобретение также относится к применению композиции, описанной выше, для противодействия ослаблению кожного барьера.
Данное изобретение также относится к способу противодействия ослаблению кожного барьера, включающему введение индивидууму, которому это необходимо, эффективного количества композиции, описанной выше.
Объектом данного изобретения также является композиция по изобретению, описанная выше, для применения в предупреждении или уменьшении проникновения экзогенных молекул в кожу после ослабления кожного барьера.
Данное изобретение также относится к применению композиции, описанной выше, для предупреждения или уменьшения проникновения экзогенных молекул в кожу после ослабления кожного барьера.
Данное изобретение также относится к способу предупреждения или уменьшения проникновения экзогенных молекул после ослабления кожного барьера, включающему введение индивидууму, которому это необходимо, эффективного количества композиции, описанной выше.
Ослабление кожного барьера может быть вызвано, в частности, воздействием внешних факторов, таких как холод или тепло, более конкретно, тепло, в частности, в случае пребывания на солнце.
Указанное ослабление, в частности, приводит к дестабилизации межкорнеоцитного пространства, которую можно оценивать, помимо прочего, согласно протоколу, приведенному в Примере 1.
Экзогенные молекулы могут, в частности, представлять собой раздражающие вещества (продукты гигиены, растворители и т.д.) или аллергенные вещества (парфюмерия, домашняя пыль, микробные агенты и т.д.). В частности, экзогенные молекулы являются липофильными.
Объектом данного изобретения также является 1,3-диглицерид, имеющий общую формулу (I):
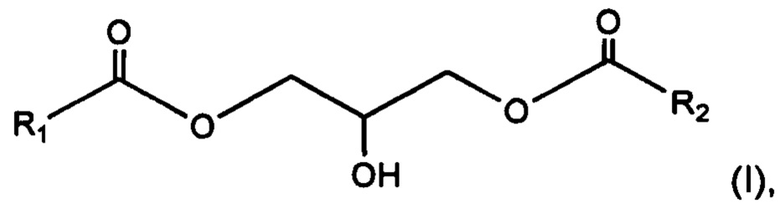
где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал,
для применения в защите кожи, в том числе кожи лица, кожи тела и кожи головы.
Объектом данного изобретения также является применение 1,3-диглицерида, имеющего общую формулу (I):
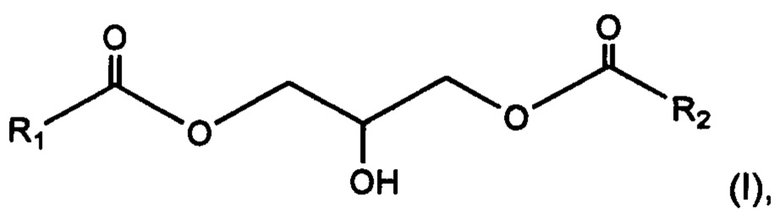
где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал,
для изготовления косметической или дерматологической композиции для местного нанесения, предназначенной для защиты кожи, в том числе кожи лица, кожи тела и кожи головы.
Данное изобретение также относится к применению 1,3-диглицерида, имеющего общую формулу (I):

где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал,
для защиты кожи, в том числе кожи лица, кожи тела и кожи головы.
Данное изобретение также относится к способу защиты кожи, в том числе кожи лица, кожи тела и кожи головы, включающему введение индивидууму, которому это необходимо, эффективного количества 1,3-диглицерида, имеющего общую формулу (I):
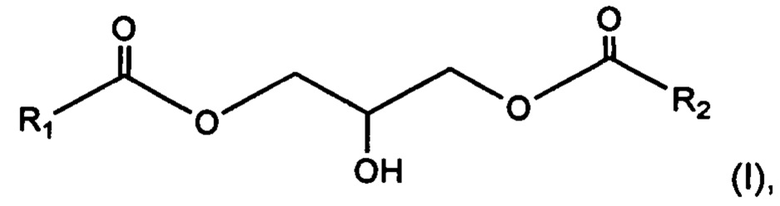
где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал.
Объектом данного изобретения также является 1,3-диглицерид, имеющий общую формулу (I):
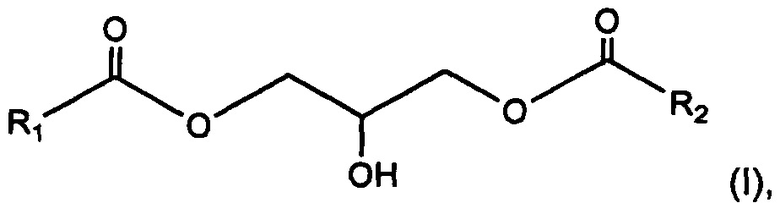
где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал,
для применения в противодействии ослаблению кожного барьера.
Данное изобретение также относится к применению 1,3-диглицерида, имеющего общую формулу (I):
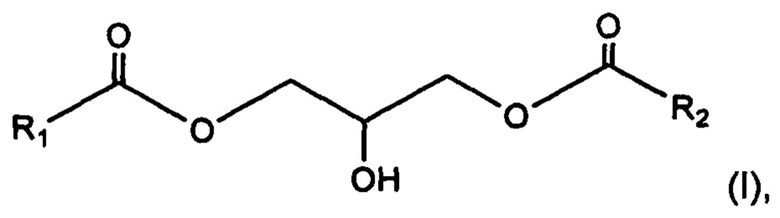
где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал,
для изготовления косметической или дерматологической композиции для местного нанесения, предназначенной для противодействия ослаблению кожного барьера.
Данное изобретение также относится к применению 1,3-диглицерида, имеющего общую формулу (I):
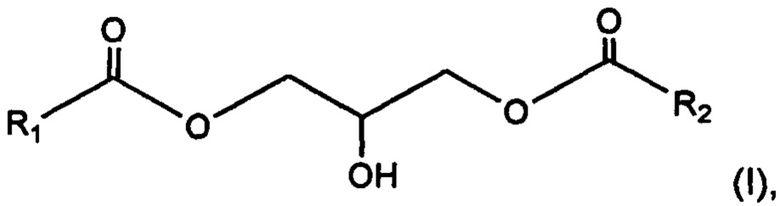
где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал,
для противодействия ослаблению кожного барьера.
Данное изобретение также относится к способу противодействия ослаблению кожного барьера, включающему введение индивидууму, которому это необходимо, эффективного количества 1,3-диглицерида, имеющего общую формулу (I):
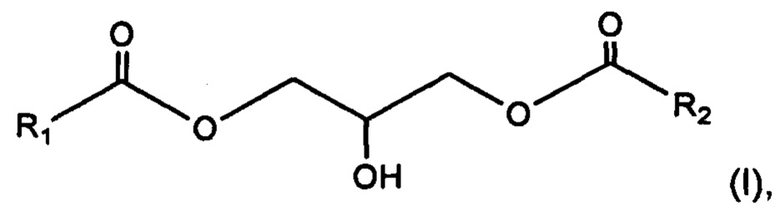
где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал.
Объектом данного изобретения также является 1,3-диглицерид, имеющий общую формулу (I):
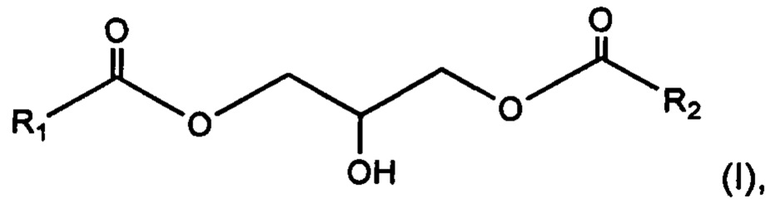
где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал,
для местного применения в предупреждении или уменьшении проникновения экзогенных молекул после ослабления кожного барьера.
Данное изобретение также относится к применению 1,3-диглицерида, имеющего общую формулу (I):
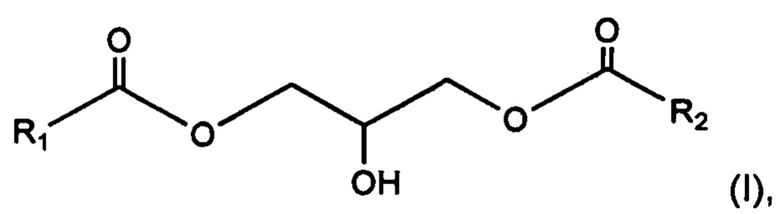
где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал,
для изготовления косметической или дерматологической композиции для местного нанесения, предназначенной для предупреждения или уменьшения проникновения экзогенных молекул после ослабления кожного барьера.
Данное изобретение также относится к применению 1,3-диглицерида, имеющего общую формулу (I):
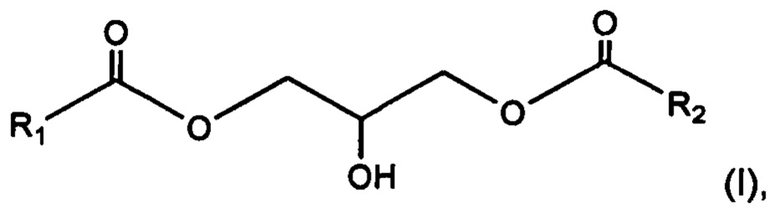
где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал,
для предупреждения или уменьшения проникновения экзогенных молекул после ослабления кожного барьера. В частности, экзогенные молекулы являются липофильными.
Данное изобретение также относится к способу предупреждения или уменьшения проникновения экзогенных молекул после ослабления кожного барьера, включающему введение индивидууму, которому это необходимо, эффективного количества 1,3-диглицерида, имеющего общую формулу (I):
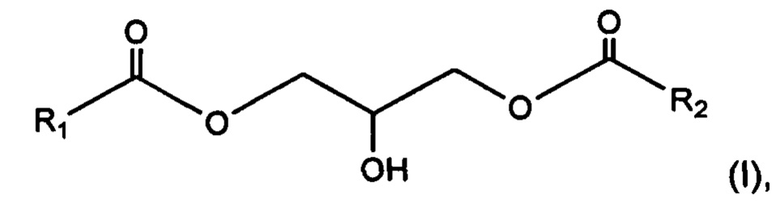
где радикалы R1 и R2 представляют, независимо друг от друга, С13-С40 насыщенный и неразветвленный алкильный радикал.
Ослабление кожного барьера может быть вызвано, в частности, воздействием внешних факторов, таких как холод или тепло, более конкретно, тепло, в частности, в случае пребывания на солнце.
Указанное ослабление, в частности, приводит к дестабилизации межкорнеоцитного пространства, которую можно оценивать, помимо прочего, согласно протоколу, приведенному в Примере 1.
Экзогенные молекулы могут, в частности, представлять собой раздражающие вещества (продукты гигиены, растворители и т.д.) или аллергенные вещества (парфюмерия, домашняя пыль, микробные агенты и т.д.).
В конкретном воплощении изобретения радикалы R1 и R2 являются идентичными и представляют С13-С40 насыщенный и неразветвленный алкильный радикал.
Согласно другому воплощению изобретения радикалы R1 и R2 представляют, независимо друг от друга, С15-С23, в частности, С15-С19 насыщенный и неразветвленный алкильный радикал. Радикалы R1 и R2 также могут быть идентичными и представлять С15-С23, в частности, С15-С19 насыщенный и неразветвленный алкильный радикал.
Радикалы R1 и R2, идентичные или различные, более предпочтительно идентичные, представляют, в частности, углеводородную цепь пальмитиновой, стеариновой или арахиновой кислоты, а именно пентадецильный, гептадецильный или нонадецильный радикал.
1,3-диглицерид по изобретению, в частности, будет представлять собой глицерила 1,3-дипальмитат, глицерила 1,3-дистеарат или их смесь.
Данное изобретение проиллюстрировано следующими примерами и графическими материалами.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
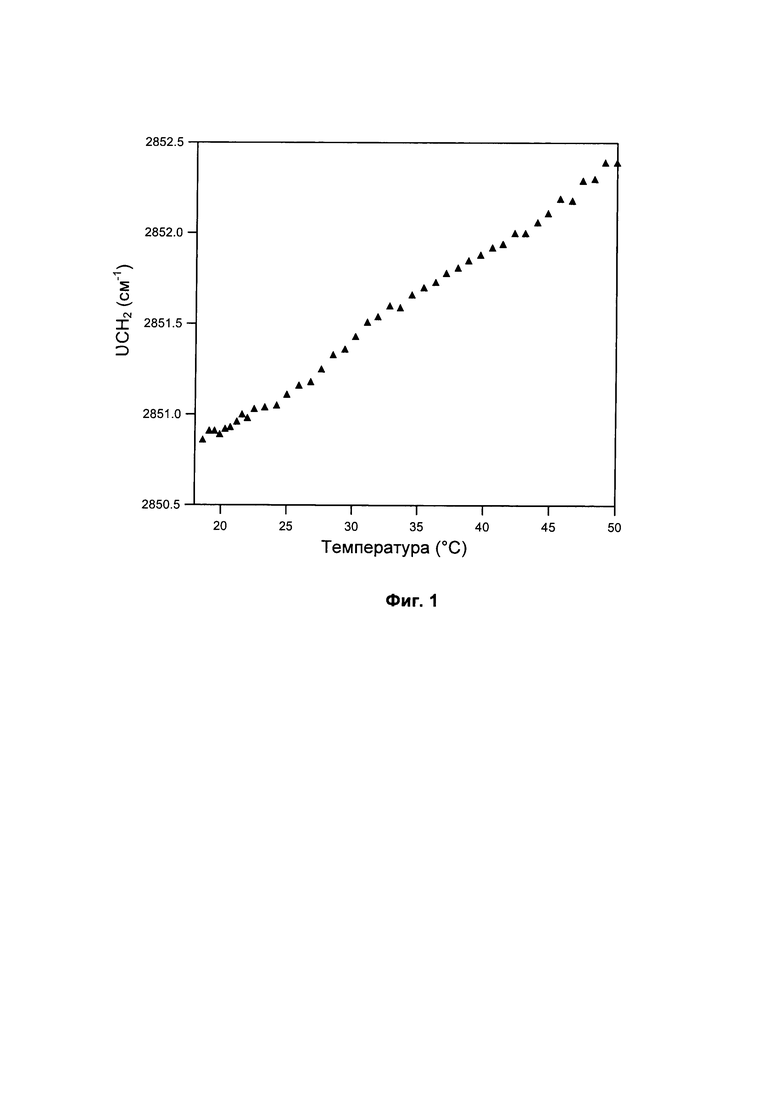
На Фиг. 1 показано волновое число колебаний νCH2 алифатических цепей межкорнеоцитных липидов в зависимости от температуры.
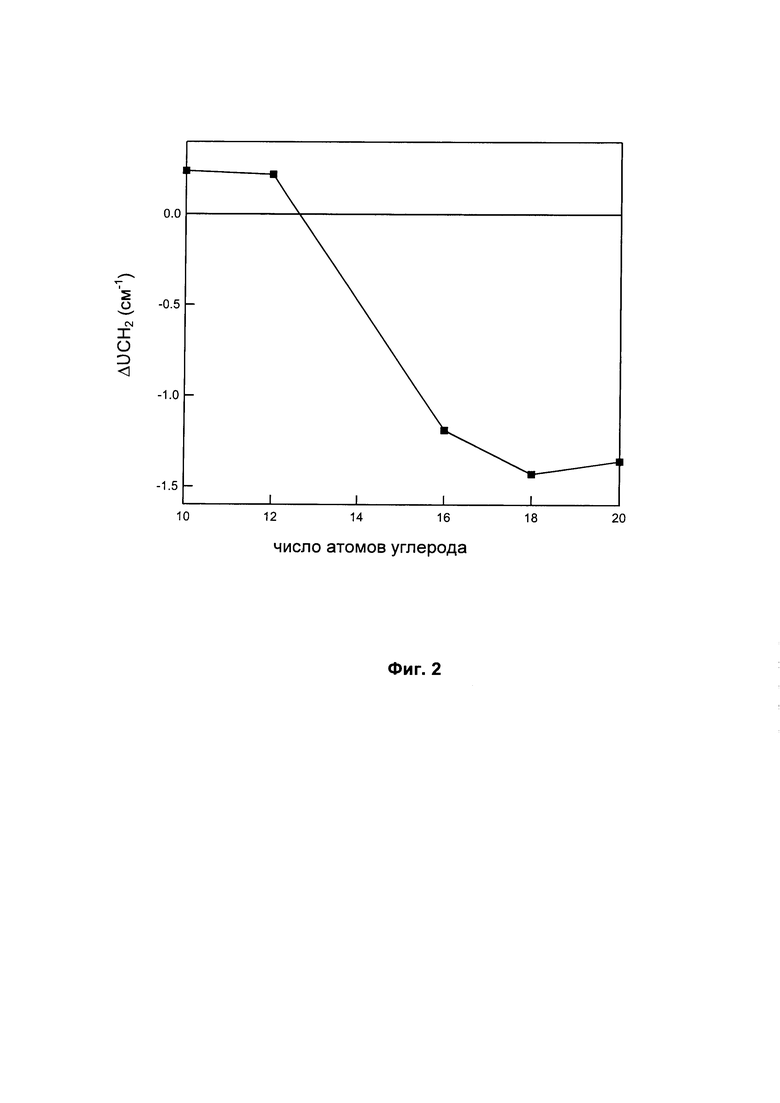
На Фиг. 2 показано изменение волнового числа колебаний νCH2 алифатических цепей межкорнеоцитных липидов в присутствии и отсутствии 1,3-диглицерида, в зависимости от длины цепи 1,3-диглицерида.
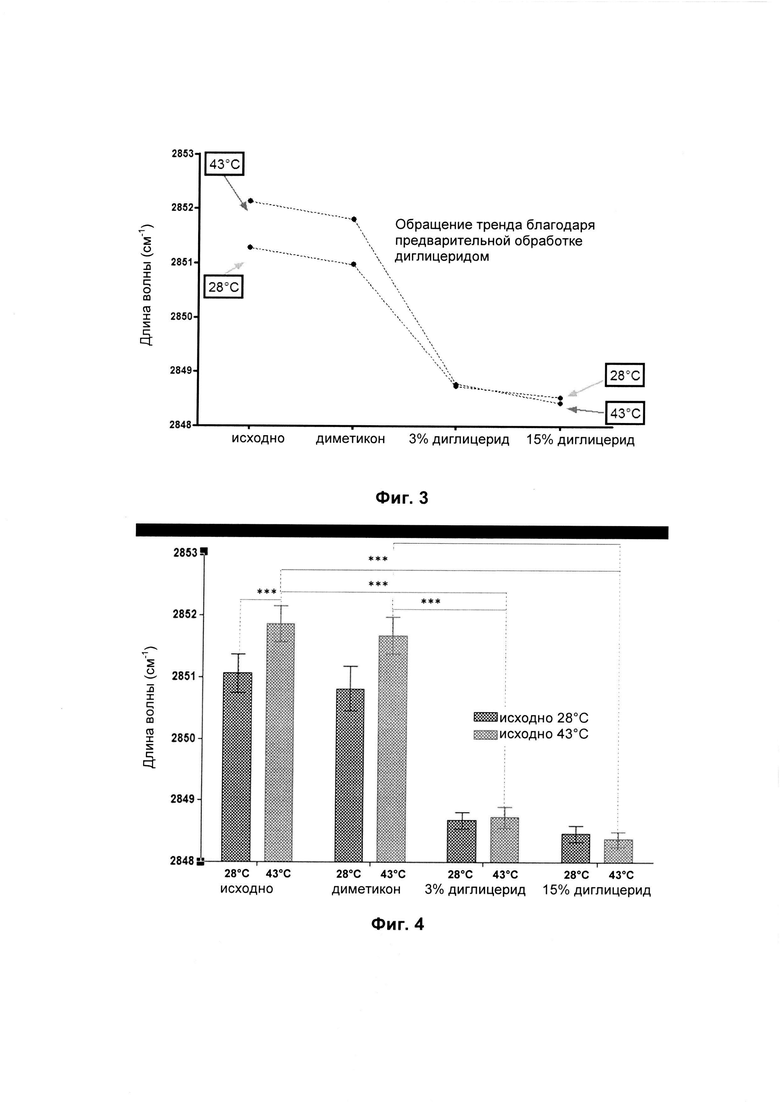
На Фиг. 3 и 4 показано смещение полосы симметричных валентных колебаний СН2 при 28°С и 43°С с предварительной обработкой кожи или без.
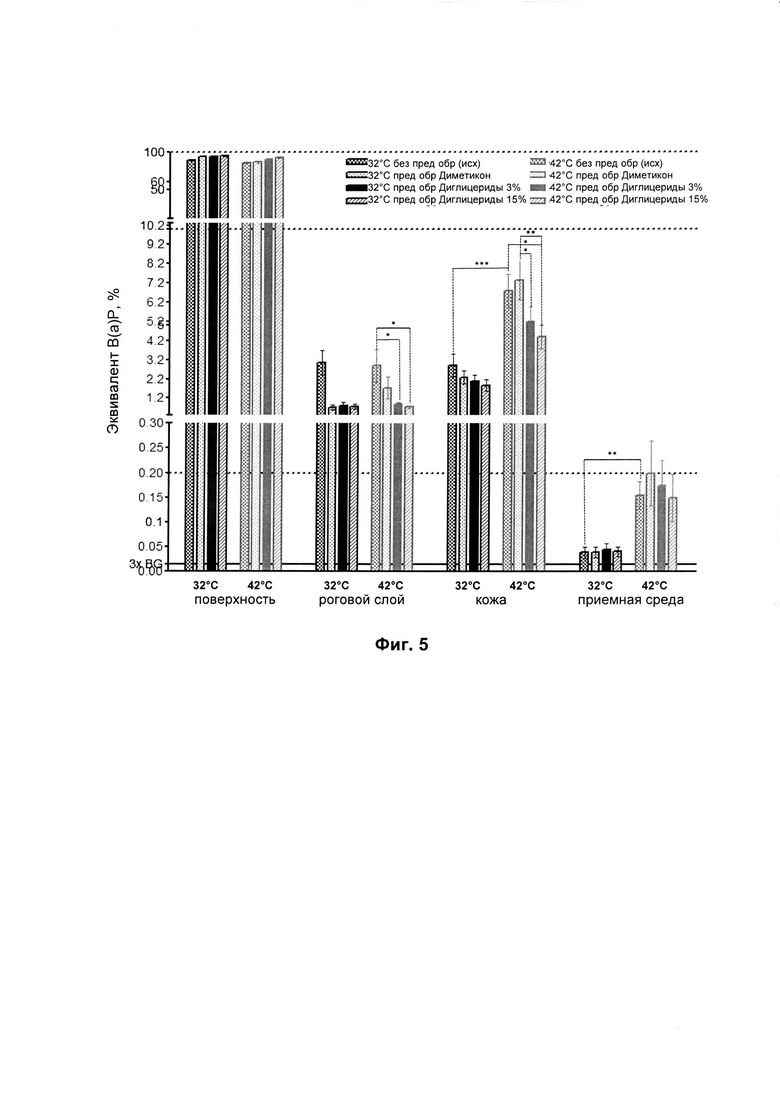
На Фиг. 5 представлено выраженное в процентах количество В(а)Р, обнаруженного в различных отсеках диффузионной ячейки Франца через 24 ч (среднее ± стандартная ошибка среднего; n=8).
ОПИСАНИЕ ПРИМЕРОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Пример 1. Модификация организации межкорнеоцитного пространства под влиянием тепла
Исследование проводили на липидах, выделенных из рогового слоя эпидермиса предплечья для создания модели, наиболее приближенной к реальности. Для изучения изменения колебаний на основной частоте νCH2 алифатических цепей в зависимости от температуры применяли инфракрасную спектроскопию (ATR-FTIR).
Изменение волнового числа колебаний νCH2 в зависимости от температуры в диапазоне от 18 до 50°С показано на Фиг. 1.
Заметили, что при низких температурах значение валентных колебаний νCH2 смеси липидов составляет 2850,7 см-1, что является характеристическим для орторомбической/гексагональной фазы, а при более высоких температурах волновое число увеличивается, достигая значения 2852,4 см-1, характерного для жидкой фазы.
Наблюдавшееся увеличение волнового числа отражает изменение состояния и разжижение межкорнеоцитных липидов под воздействием температуры.
Пример 2. Обнаружение стабилизирующего эффекта 1,3-диглицеридов и влияния длины их цепи на организацию межкорнеоцитных липидов
Исследования проводили в аналогичных условиях, используя экстракты липидов предплечья, куда наносили стандартное количество диглицерида (3 мкг диглицерида на 30 мкг образца). На Фиг. 2 показано влияние длины цепи 1,3-диглицерида на параметр νCH2 при проведении измерений при 40°С.
Эти результаты позволяют обнаружить влияние длины алифатических цепей глицеридов. При температурах, близких к живым организмам, 1,3-дикаприн (C10), а также 1,3-дилауроилглицерол (С12) не влияют на организацию межкорнеоцитных липидов. При анализе Фиг. 2 обнаруживается существенное стабилизирующее влияние, начиная с длины цепи С14, а начиная с длины цепи С16 можно заметить, что частота валентных колебаний СН2 сохраняется на относительно низких значениях по сравнению с экстрактом, лишенным диглицерида. Кроме того, данные результаты обнаруживают, что по мере увеличения длины алкильной цепи диглицеридов увеличивается стабилизирующая способность в отношении разжижения липидов кожи под воздействием тепла.
Пример 3. Сравнение 1,3-диглицерида/1,2-диглицерида
Исследование, описанное в Примере 2, повторили с 1,2-дистеароил-рац-глицеролом (1,2-диглицеридом) и сравнили с исследованием, проведенным с глицерила 1,3-дистеаратом (1,3-диглицеридом). Полученные результаты приведены в Таблице 1 ниже.

Приведенные результаты явно демонстрируют превосходящий эффект 1,3-диглицеридов на стабилизацию межкорнеоцитного пространства.
Пример 4. Выявление стабилизирующего влияния на организацию межкорнеоцитного пространства после нанесения глицерила 1,3-дистеарата в клинических условиях in vivo
Исследование проводили на здоровых добровольцах. Данные в ИК области спектра получали при помощи вспомогательного датчика ATR-FTIR на внутренней поверхности предплечья в зоне площадью 10 см2.
Исследовали обработанную зону (с нанесением глицерила 1,3-дистеарата in vivo) и контрольную зону (без нанесения глицерила 1,3-дистеарата).
Изучали две концентрации глицерила 1,3-дистеарата (Таблица 2: 0,5 мг/см2 и Таблица 3: 0,15 мг/см2).
Момент времени Т0: вначале кожу нагревали до температуры от 30 до 45°С.
Затем после нанесения глицерила 1,3-дистеарата in vivo на обрабатываемую зону оценивали изменения волнового числа, связанные с валентными колебаниями νCH2 по сравнению с референтным измерением без нанесения продукта (контрольная зона) спустя различное время с момента времени Т0: Т 30 минут, Т 1 ч 30 минут и Т 4 часа.
Полученные данные объединены в Таблицах 2 и 3 и позволяют сделать несколько заключений.


В Таблицах 2 и 3 показаны изменения волнового числа, связанные с валентными колебаниями νCH2 алифатических цепей межкорнеоцитных липидов при 40°С в присутствии глицерила 1,3-дистеарата по сравнению с референтным измерением без глицерила 1,3-дистеарата.
Во-первых, четко показано, что глицерила 1,3-дистеарат, применяемый в нормальных условиях, позволяет стабилизировать организацию межкорнеоцитного пространства кожи при нагревании от 30 до 45°С.
Во-вторых, показано, что данный стабилизирующий эффект, проявляющийся непосредственно при нанесении диглицерида, сохраняется по меньшей мере в течение 4 часов.
Пример 5. Примеры композиций по изобретению
Композиция 1: Форма масло/вода

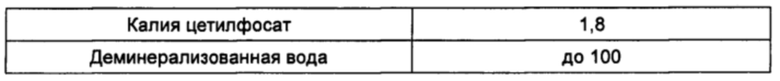
Композиция 2: Форма вода/масло

Композиция 3: Кремообоазный гель
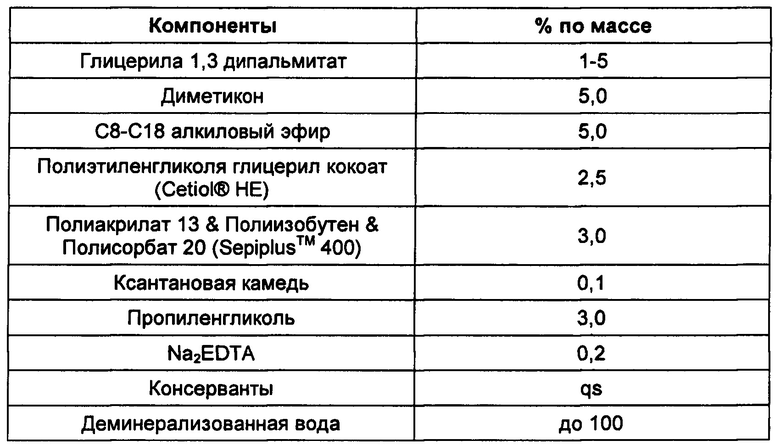
Композиция 4: Крем
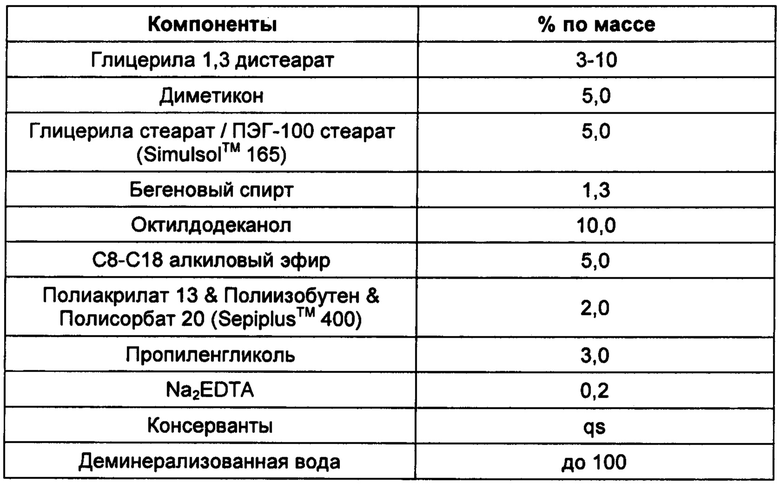
Пример 6. Оценка влияния 1.3-диглицеридов на проникновение в кожу бензо[а]пирена
Для оценки влияния 1,3-диглицеридов на организацию липидов и барьерную функцию рогового слоя in vitro разработали и провели исследования кожной проницаемости для известного загрязняющего вещества (бензо[а]пирена (В(а)Р). У тех же доноров проводили измерения при помощи ИК-спектроскопии с Фурье-преобразованием (FTIR) и исследовали проникновение В(а)Р в кожу, чтобы связать организацию липидов и изменение барьерной функции кожи «снаружи внутрь» при нагревании кожи до 42°С.
Во-первых, продемонстрировали, что повышение температуры поверхности кожи от 32°С до 42°С изменяет организацию липидов и нарушает барьерную функцию кожи «снаружи внутрь», о чем свидетельствует увеличение проникновения В(а)Р в кожу.
Во-вторых, оценивали влияние предварительной обработки 3% и 15% глицерила 1,3-дистеаратом, смешанным с диметиконом, на изменение организации липидов рогового слоя и проникновение В(а)Р в кожу, вызванные повышением температуры.
Материалы и методы
СОЕДИНЕНИЯ
Исследуемые вещества:
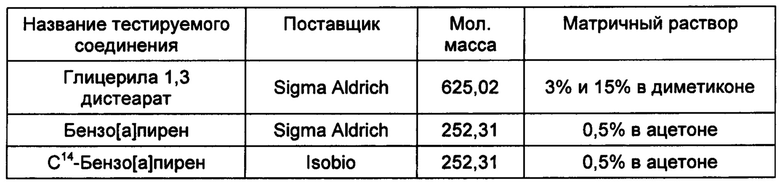
Растворимость
Растворимость В(а)Р хорошо описана в литературе. Благодаря своим физико-химическим свойствам В(а)Р обладает очень низкой растворимостью в воде. Программное обеспечение Episuite предсказывает растворимость 13,3 мкг/л, и данные эксперимента подтвердили указанный результат при 25°С [11].
В данном исследовании количество В(а)Р в процентах, обнаруженного в приемной среде, в худшем случае достигало 0,13% от нанесенной дозы, соответствуя 12,51 мкг/л. Основываясь на этих данных, авторы изобретения добавляли 4% бычий сывороточный альбумин (БСА) для увеличения растворимости В(а)Р и во избежание повреждения кожи. Поверхностно-активные вещества и этанол запрещались во избежание модификации функции кожного барьера.
ОСНОВНЫЕ ПОЛОЖЕНИЯ
Исследование проводили в соответствии с
- Рекомендациями Организации экономического сотрудничества и развития (ОЭСР) о тестировании химических соединений: рекомендация 428, абсорбция через кожу: способ in vitro (13 апреля 2004);
- Рекомендациями Научного комитета по обеспечению безопасности потребителей (НКБП), основными критериями оценки кожной абсорбции косметических ингредиентов in-vitro, в редакции от марта 2006.
СХЕМА ЭКСПЕРИМЕНТА
Заданные температуры:
измерения при помощи ИК-спектроскопии с Фурье-преобразованием:
Образцы кожи нагревали со скоростью 1°С/мин и регистрировали спектр при температуре от 28°С до 43°С.

Эксперимент с поступлением в кожу
Для исследования поступления в кожу задавали две температуры. Традиционно в исследованиях поступления в кожу температура поверхности кожи составляет 32°С. Данная температура соответствует температуре поверхности кожи in vivo.
Предыдущие исследования, проводившиеся in vitro отделением биофизики и визуализации на липидах при помощи FTIR, показали, что при 40°С дезорганизация липидов начинает становиться видимой. На основании этих результатов температуру 42°С выбрали для возможности наблюдать за дезорганизацией липидов в ходе эксперимента с поступлением в кожу.
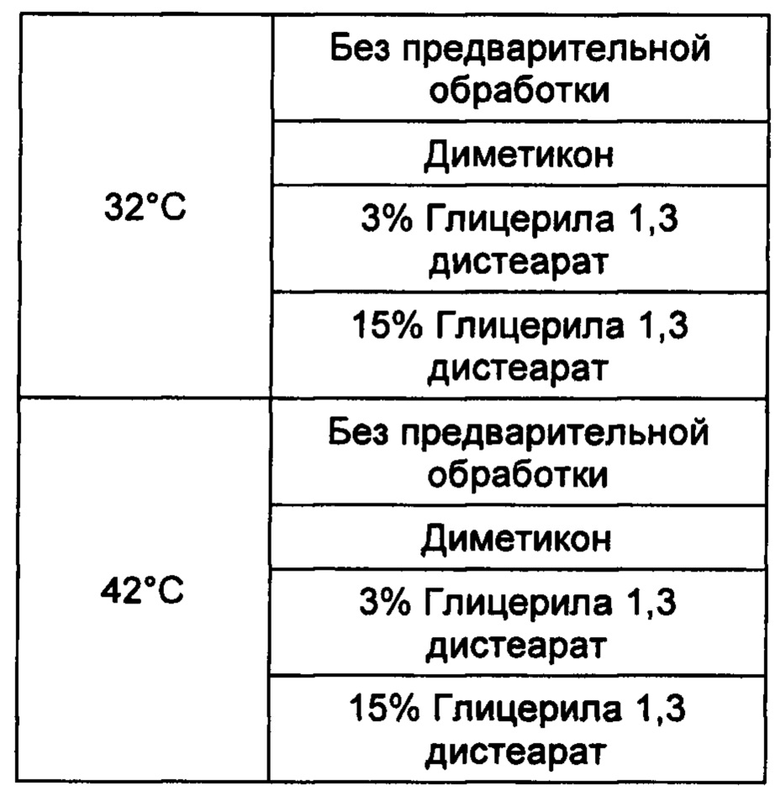
Эксперимент с поступлением в кожу:

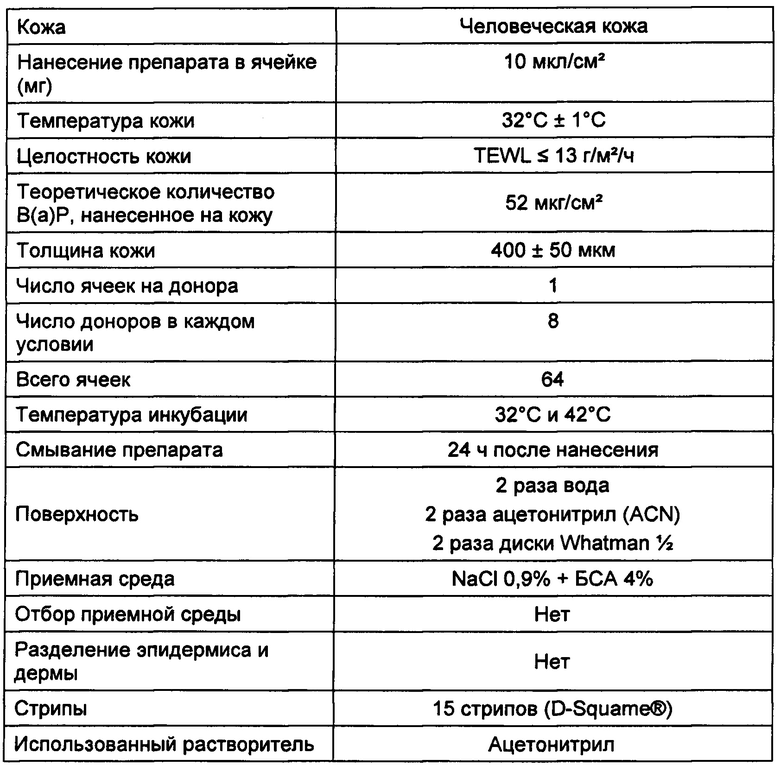
Исследование проникновения в кожу проводили на 8 донорах, один и тот же донор был задействован в каждом из условий эксперимента:

Организация липидов - измерения при помощи FTIR
Через 30 минут после предварительной обработки проводили измерения при помощи FTIR для оценки молекулярной организации липидного матрикса рогового слоя. За основу взяли исследование положения полосы симметричных валентных колебаний СН2 около 2850 см-1, в зависимости от температуры: образцы кожи нагревали со скоростью 1°С/мин и регистрировали спектр при температуре от 28°С до 43°С с предварительной обработкой и без. Положение полосы симметричных валентных колебаний СН2 является характеристическим для организации липидов и может быть связано с барьерной функцией.
СЧИТЫВАЕМЫЕ ПАРАМЕТРЫ
- Исследование кожного экспланта при помощи FTIR (положение полосы симметричных валентных колебаний СН2) в зависимости от температуры;
- Исследование проникновения в кожу
• Общее количество обнаруженного В(а)Р;
• Распределение по отсекам в процентах от нанесенного В(а)Р;
• Распределение по отсекам в мкг/см2.
ОБРАБОТКА ДАННЫХ
Исследование проводили на 8 донорах, один тот же донор был задействован в каждом из условий эксперимента.
В соответствии с рекомендациями ОЭСР 428 и НКБП, количество обнаруженного В(а)Р должно составлять от 85% до 115% от нанесенной дозы.
Результаты, полученные для В(а)Р, представлены в Таблицах и на графиках, где они выражены следующим образом:
- % от нанесенной дозы на поверхности, в роговом слое, коже и в приемной среде;
- мкг/см2 В(а)Р на поверхности, в роговом слое, коже и в приемной среде.
Результаты представлены с точностью до 2 знаков после запятой в процентах и по количеству в мкг/см2.
В данном протоколе использовали следующую формулу:
- Стандартная ошибка среднего:

- Биодоступность
Сумма количеств, обнаруженных в коже и в приемной среде.
Межгрупповое сравнение проводили при помощи парного t-критерия Стьюдента в программе Graph Pad Prism. Статистический анализ подлежал интерпретации при n>5.
Результаты
ОРГАНИЗАЦИЯ ЛИПИДОВ - ИЗМЕРЕНИЯ ПРИ ПОМОЩИ FTIR
Исследования при помощи FTIR проводили на эксплантах кожи человека (8 доноров) с предварительной обработкой или без. Образцы кожи нагревали со скоростью 1°С/мин и регистрировали спектр при температуре от 28°С до 43°С.
На Фиг. 3 и 4 показано влияние температуры на полосы симметричных валентных колебаний СН2. При нагревании кожи без предварительной обработки наблюдались существенные различия в организации липидов, со смещением полосы симметричных валентных колебаний СН2 от 2851,2 см-1 при 28°С до 2852,12 см-1 при 43°С (Т критерий, значение р<0,05). Предварительная обработка 3% или 15% глицерила 1,3-дистеаратом позволяет существенно снизить влияние нагревания на организацию липидов (Т критерий, значение р<0,05). При предварительной обработке 3% глицерила 1,3-дистеаратом при 43°С наблюдалось смещение полосы симметричных валентных колебаний СН2 от 2852,12 см-1 (исходное значение при 43°С) до 2848,7 см-1. Предварительная обработка глицерила 1,3-дистеаратом уменьшает смещение полосы симметричных валентных колебаний СН2, вызванное нагреванием кожи: смещение составляет только 0,05 см-1 после предварительной обработки 3% глицерила 1,3-дистеаратом и 0,81 см-1 без предварительной обработки.
ИССЛЕДОВАНИЕ ПРОНИКНОВЕНИЯ В КОЖУ
Всего обнаружено:
Общее количество обнаруженного соединения во всех диффузионных ячейках соответствовала допустимым нормам, варьируя от 94,9% до 97,6% от нанесенной дозы, что позволяло валидировать исследование.
Распределение по отсекам в процентах от нанесенной дозы.
Полученные результаты приведены в Таблице 4 ниже и на Фиг. 5.
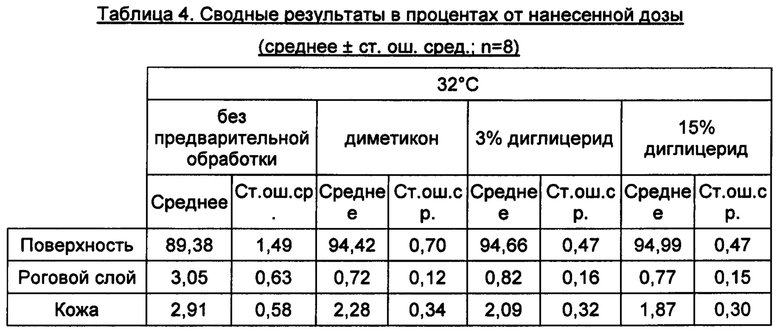
Большую часть нанесенной дозы В(а)Р обнаруживали на поверхности (до 94,5% от нанесенной дозы).
Биодоступность В(а)Р (кожа + приемная среда) при 32°С была низкой, т.е. до 2,95% от нанесенной дозы. Биодоступность В(а)Р существенно повышалась и достигала 6,95% от нанесенной дозы при нагреве кожи до 42°С (Т критерий, значение р<0,05).
Предварительная обработка только несущей средой (диметиконом) существенно не изменяла биодоступность В(а)Р, какой бы ни была температура кожи (Т критерий, значение р<0,05).
После предварительной обработки 3% или 15% глицерида 1,3-дистеаратом в качестве диглицерида наблюдалось существенное снижение биодоступности В(а)Р при 43°С. Действительно, биодоступность при использовании несущей среды (диметикона) составляла 7,57% от наносимой дозы и снижалась до 5,35% и 4,35% от наносимой дозы после предварительной обработки 3% и 15% глицерида 1,3-дистеаратом, соответственно.
При 42°С выраженное в процентах количество В(а)Р, обнаруженного в роговом слое, снижалось после нанесения глицерида 1,3-дистеарата. Для соединений с такими физико-химическими свойствами, как у В(а)Р (липофильные соединения), роговой слой, который представляет собой липофильный компартмент, выполняет функцию резервуара. Таким образом, снижение выраженного в процентах количества В(а)Р, обнаруженного в роговом слое, предотвращает диффузию этого соединения в более глубокие слои кожи даже если кожа не нагревается.
Результаты, полученные для проникновения В(а)Р в кожу, коррелируют с результатами, полученными в исследованиях при помощи FTIR.
Заключение:
Результаты, полученные для проникновения В(а)Р в кожу через 24 ч после нанесения на кожу, коррелируют с результатами, полученными в исследованиях при помощи FTIR. Эти данные показывают, что изменение организации липидов при температуре около 42°С вызывает ослабление барьерной функции и увеличивает биодоступность таких внешних загрязняющих агентов, как В(а)Р. Это свидетельствует о том, что применение 1,3-диглицеридов существенно улучшает барьерную функцию; оценивали предварительную обработку 3% и 15% диглицерида 1,3-дистеаратом в диметиконе. Предварительная обработка глицерида 1,3-дистеаратом позволяет стабилизировать организацию липидов (исследования при помощи FTIR) и улучшают барьерную функцию «извне-внутрь», о чем свидетельствует исследование проникновения В(а)Р в кожу. Существенное улучшение барьерной функции и стабилизация липидов наблюдались даже при предварительной обработке 3% глицерида 1,3-дистеаратом.
Источники информации
[1] Fabienne Berthaud, Mila Boncheva. Correlation between the properties of the lipid matrix and the degrees of integrity and cohesion in healthy human stratum corneum. Exp Dermatol, 20(3):255-262, Mar 2011.
[2] Mila Boncheva, Fabienne Damien,  Normand. Molecular organization of the lipid matrix in intact stratum corneum using atr-ftir spectroscopy. Biochim Biophys Acta, 1778(5): 1344-1355, May 2008.
Normand. Molecular organization of the lipid matrix in intact stratum corneum using atr-ftir spectroscopy. Biochim Biophys Acta, 1778(5): 1344-1355, May 2008.
[3] Fabienne Damien, Mila Boncheva. The extent of orthorhombic lipid phases in the stratum corneum determines the barrier efficiency of human skin in vivo. J Invest Dermatol, 130(2):611-614, Feb 2010.
[4]  Groen, Dana S. Poole, Gert S. Gooris, Joke A. Bouwstra. Is an orthorhombic lateral packing and a proper lamellar organization important for the skin barrier function? Biochimica and Biophysica Acta (BBA) - Biomembranes, 1808(6): 1529-1537, 2011.
Groen, Dana S. Poole, Gert S. Gooris, Joke A. Bouwstra. Is an orthorhombic lateral packing and a proper lamellar organization important for the skin barrier function? Biochimica and Biophysica Acta (BBA) - Biomembranes, 1808(6): 1529-1537, 2011.
[5] Coderch L,  O, de la Maza A, Parra JL. Ceramides and skin function. Am J Clin Dermatol. 2003, 4(2): 107-29.
O, de la Maza A, Parra JL. Ceramides and skin function. Am J Clin Dermatol. 2003, 4(2): 107-29.
[6] Cho S, Lee MJ, Kim MS, Lee S, Kim YK, Lee DH, Lee CW, Cho KH, Chung JH. Infrared plus visible light and heat from natural sunlight participate in the expression of MMPs and type Iprocollagen as well as infiltration of inflammatory cell in human skin in vivo. Journal of Dermatological Science (2008) 50, 123-133.
[7] Jin Young Seo, Jin Ho Chung. Thermal aging: A new concept of skin aging. Journal of Dermatological Science Supplement, 2(1):S13-S22, 2006. Proceedings of the 5th Annual Meeting of the Japanese Photoaging Research Society.
[8] Scalia S, Mezzena M, Ramaccini D. Encapsulation of the UV filters ethylhexyl methoxycinnamate and butyl methoxydibenzoylmethane in lipid microparticles: effect on in vivo human skin permeation. Skin Pharmacol Physiol. 2011, 24(4): 182-9.
[9] Ning Liu, Yong Wang, Qiangzhong Zhao, Qingli Zhang, Mourning Zhao. Fast synthesis of 1,3-DAG by Lecitase® Ultra-catalyzed esterification in solvent-free system. Eur. J. Lipid Sci. Technol. 2011, 113, 973-979.
[10] KR 2013058299, WO 03/014073 A1, JP 02115117 A, JP 52061240 A.
[11] May WE et al., J. Chem. Ref. Data 1983, 28: 197-200.
Изобретение относится к местной косметической или дерматологической композиции, содержащей 1,3-диглицерид, имеющий общую формулу (I):
где радикалы R1 и R2 представляют, независимо друг от друга, С15-С19 насыщенный и неразветвленный алкильный радикал и по меньшей мере один косметический или дерматологический эксципиент для местного нанесения на кожу. Изобретение также относится к указанной композиции или 1,3-диглицериду, имеющему формулу (I) для его применения в защите кожи, в противодействии ослаблению кожного барьера и в предупреждении или уменьшении проникновения экзогенных молекул в кожу после ослабления кожного барьера. Технический результат – создание косметических или дерматологических композиций для противодействия ослаблению кожного барьера, в частности, под воздействием внешних факторов, достижение большей стабильности межкорнеоцитного пространства позволяет открывать новые перспективы в области косметических и дерматологических продуктов для ухода за кожей, в том числе за кожей лица, кожей тела и кожей головы, и/или для макияжа. 8 н. и 16 з.п. ф-лы, 4 табл., 5 ил., 6 пр.
1. Местная косметическая композиция, содержащая 1,3-диглицерид, имеющий общую формулу (I):
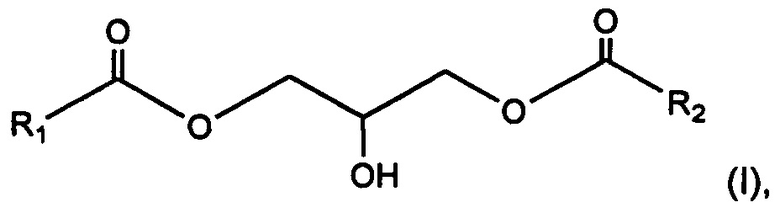
где радикалы R1 и R2 представляют, независимо друг от друга, С15-С19 насыщенный и неразветвленный алкильный радикал и косметические эксципиенты для местного нанесения на кожу, где указанный 1,3-диглицерид присутствует в местной косметической композиции в количестве от 0,5 % до 10 % по массе относительно общей массы указанной композиции, где в местной косметической композиции может присутствовать 1,2-диглицерид в количестве, которое не превышает 10 % по массе от общей массы 1,3- и 1,2-диглицеридов.
2. Композиция по п. 1, отличающаяся тем, что R1 и R2 являются идентичными.
3. Композиция по п. 1, отличающаяся тем, что 1,3-диглицерид представляет собой глицерила 1,3-дипальмитат, глицерила 1,3-дистеарат или их смесь.
4. Композиция по любому из пп. 1-3, отличающаяся тем, что количество 1,3-диглицерида составляет от 1% до 5% по массе относительно общей массы указанной композиции.
5. Композиция по любому из пп. 1-4, отличающаяся тем, что количество 1,2-диглицерида не превышает 5% по массе от общей массы 1,3-1,2-диглицеридов.
6. Композиция по любому из пп. 1-5, отличающаяся тем, что 1,3-диглицерид присутствует в композиции в форме диспергированных твердых частиц.
7. Местная дерматологическая композиция, содержащая 1,3-диглицерид, имеющий общую формулу (I):

где радикалы R1 и R2 представляют, независимо друг от друга, С15-С19 насыщенный и неразветвленный алкильный радикал и дерматологические эксципиенты для местного нанесения на кожу, где указанный 1,3-диглицерид присутствует в местной дерматологической композиции в количестве от 0,5 % до 10 % по массе относительно общей массы указанной композиции, где в местной дерматологической композиции может присутствовать 1,2-диглицерид в количестве, которое не превышает 10 % по массе от общей массы 1,3- и 1,2-диглицеридов.
8. Композиция по п. 7, отличающаяся тем, что R1 и R2 являются идентичными.
9. Композиция по п. 7, отличающаяся тем, что 1,3-диглицерид представляет собой глицерила 1,3-дипальмитат, глицерила 1,3-дистеарат или их смесь.
10. Композиция по любому из пп. 7-9, отличающаяся тем, что количество 1,3-диглицерида составляет от 1% до 5% по массе относительно общей массы указанной композиции.
11. Композиция по любому из пп. 7-10, отличающаяся тем, что количество 1,2-диглицерида не превышает 5% по массе от общей массы 1,3-1,2-диглицеридов.
12. Композиция по любому из пп. 7-11, отличающаяся тем, что 1,3-диглицерид присутствует в композиции в форме диспергированных твердых частиц.
13. Способ защиты кожи, в том числе кожи лица, кожи тела и кожи головы, включающий введение композиции по любому из пп. 1-12.
14. Способ противодействия ослаблению кожного барьера, включающий введение композиции по любому из пп. 1-12.
15. Способ предупреждения или уменьшения проникновения экзогенных молекул в кожу после ослабления кожного барьера, включающий введение композиции по любому из пп. 1-12.
16. Способ по п. 14 или 15 для лечения и профилактики раздражения, аллергической реакции или окислительного стресса.
17. Способ по любому из пп. 14-16, отличающийся тем, что кожный барьер ослабевает под влиянием внешних факторов, таких как холод или тепло, предпочтительно тепло.
18. Применение 1,3-диглицерида, имеющего общую формулу
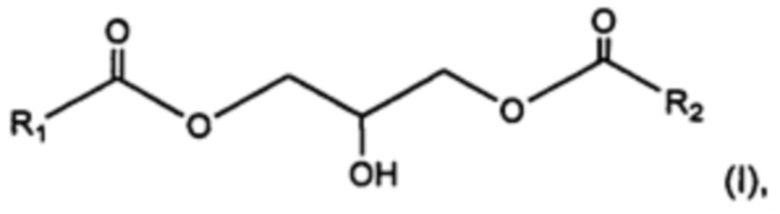
где радикалы R1 и R2 представляют, независимо друг от друга, С15-С19 насыщенный и неразветвленный алкильный радикал для защиты кожи, в том числе кожи лица, кожи тела и кожи головы.
19. Применение 1,3-диглицерида, имеющего общую формулу

где радикалы R1 и R2 представляют, независимо друг от друга, С15-С19 насыщенный и неразветвленный алкильный радикал для противодействия ослаблению кожного барьера.
20. Местное применение 1,3-диглицерида, имеющего общую формулу

где радикалы R1 и R2 представляют, независимо друг от друга, С15-С19 насыщенный и неразветвленный алкильный радикал для предупреждения или уменьшения проникновения экзогенных молекул после ослабления кожного барьера.
21. Применение по п. 19 или 20 для лечения или профилактики раздражения, аллергической реакции или окислительного стресса.
22. Применение по любому из пп. 19-21, отличающееся тем, что кожный барьер ослабевает под влиянием внешних факторов, таких как холод или тепло, предпочтительно тепло.
23. Применение по любому из пп. 18-22, отличающееся тем, что R1 и R2 являются идентичными.
24. Применение по любому из пп. 18-22, отличающееся тем, что 1,3-диглицерид представляет собой глицерила 1,3-дипальмитат, глицерила 1,3-дистеарат или их смесь.
| WO 2004084646 A2, 07.10.2004 | |||
| Устройство для балансировки роторов | 1983 |
|
SU1216690A1 |
| СПОСОБ ПОДГОТОВКИ К ХРАНЕНИЮ ЯБЛОК СВЕЖИХ СПЕЦИАЛЬНОГО НАЗНАЧЕНИЯ | 2006 |
|
RU2318364C1 |
| DE 4430851 C1, 07.09.1995 | |||
| US 4957740 A, 18.09.1990 | |||
| КОМПОЗИЦИЯ ДЛЯ ПОЛУЧЕНИЯ КОСМЕТИЧЕСКИХ И ЛЕКАРСТВЕННЫХ ЭМУЛЬСИЙ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2011 |
|
RU2460511C1 |
Авторы
Даты
2021-10-12—Публикация
2016-12-08—Подача