Изобретение относится к медицине, а именно к биотехнологии, иммунологии, имплантологии, и может быть использовано при выборе синтетических материалов для медицинских целей по способности предотвращать развитие воспалительного ответа.
В настоящее время результаты исследований в области химии обеспечивают медицину и, в частности имплантологию, широким набором синтетических полимерных материалов, которые по многим своим характеристикам занимают лидирующие позиции при создании эндопротезов и других имплантируемых в организм человека изделий. Однако все эти материалы являются чужеродными для его внутренней среды. Характерной и типичной реакцией иммунной системы на вживление таких имплантатов становится развитие воспаления, когда иммунокомпетентные клетки, наращивая свой защитный потенциал, обусловливают развитие осложнений, вплоть до отторжения имплантируемого объекта. Основное внимание исследователей на современном этапе сконцентрировано на поиске путей предотвращения развития таких реакций, однако методические подходы для оценки синтетических полимеров, разрабатываемых и предлагаемых для использования с различными медицинскими целями, с этих позиций оставляют желать лучшего.
Известен способ сравнительной оценки реакции иммунокомпетентных клеток в ответ на действие различных вживляемых материалов в стоматологии на основе цитоморфологического исследования с учетом индекса сдвига нейтрофилов [Рыжова И.Л., Денисова В.Ю. Изучение биосовместимости современных конструкционных полимерных материалов // Уральский медицинский журнал. - 2010. - № 08(73). - С. 36-39].
Недостатки прототипа: низкая эффективность способа при высокой стоимости, связанная с трудоемкостью, продолжительностью во времени, преимущественном выявлении воспалительной реакции, развивающейся в ответ на микробные агенты, а также отсутствием учета активности иммунокомпетентных клеток.
Технический результат: повышение эффективности способа за счет снижения временных и трудозатрат, возможность одномоментной проверки значительного количества образцов, комплексной оценки пролиферативной и цитокин-продуцирующей активности мононуклеарных клеток при их непосредственном контакте с образцами, позволяющей определять направленность иммунного ответа, обосновывая выбор перспективного для медицины материала.
Результат достигается с помощью контактного способа воздействия образцов синтетических полимеров на клетки иммунной системы (мононуклеарные лейкоциты), содержащиеся в периферической венозной крови человека, с оценкой продукции ими противовоспалительных цитокинов in vitro по показателю индекса стимуляции, что в сравнительном анализе результатов тестирования позволит выбрать наиболее перспективные образцы.
Способ осуществляют следующим образом.
У добровольца получают пробу периферической венозной крови и с помощью градиентного (фиколл-верографин; ρ=1,077 г/см3) центрифугирования выделяют популяцию мононуклеарных лейкоцитов. Клетки трижды отмывают свежим охлажденным раствором Хенкса (ООО «Биолот», Россия) и доводят до 2×106 клеток/мл. После этого клеточную суспензию вносят в лунки круглодонного планшета с предварительно размещенными там образцами разных синтетических полимеров в форме цилиндра длиною 3 мм и диаметром 1 мм. В качестве контроля используют лунки с образцами из стекла и лунки, не содержащие синтетических материалов. Планшеты инкубируют в термостате ТС-80 (Анкар, Россия) при 37°С в условиях 5% СО2 в течение 72 ч. По окончании инкубации в лунках подсчитывают общее число клеток и в том числе количество жизнеспособных в тесте с трипановым синим [Мельникова Н.А., Шубина О.С., Дуденкова Н.А., Лапшина М.В., Лиференко О.В., Тимошкина О.И. Исследование жизнеспособности клеток при воздействии ацетата свинца на организм крысы // Современные проблемы науки и образования. - 2013. - № 5. - С. 495]. Содержимое лунок после инкубации центрифугируют и надосадочную жидкость используют для определения концентрации противовоспалительных цитокинов ИЛ-4 и ИЛ-10 с помощью иммуноферментного метода [Симбирцев А.С., Тотолян А.А. Цитокины в лабораторной диагностике // Инфекционные болезни: новости, мнения, обучение. - 2015. - № 2 (11). - С. 82-98.]. Для вычисления удельной продукции каждого цитокина в присутствии синтетического полимера (УП, пг/кл.) или в присутствии стекла (УС, пг/кл.) производят пересчет количества цитокинов на 1 жизнеспособную клетку по формулам:
УП=Ц/КЛЦ или УС=С/КЛС, где
Ц - концентрация цитокина в пробе с синтетическим полимером, пг/мл;
КЛЦ - количество мононуклеарных лейкоцитов в пробе с синтетическим полимером, в 1 мл;
С - концентрация цитокина в пробе со стеклянным образцом, пг/мл;
КЛС - количество мононуклеарных лейкоцитов в пробе со стеклом, в 1 мл.
Далее для оценки направленности иммунного ответа для каждого противовоспалительного цитокина вычисляют индекс стимуляции (ИС), как отношение удельной продукции цитокина в пробе с полимерным образцом к продукции того же цитокина в пробе со стеклом по формуле:
ИС=УП/УС, где
УП - удельная продукция цитокина в присутствии синтетического полимерного образца, пг/клетка;
УС - удельная продукция цитокина в присутствии стекла, пг/клетка;
Индекс стимуляции равный и более 1 указывает на пригодность использования в медицинских целях синтетического полимера, т.е. образец стимулирует продукцию противовоспалительного цитокина, предупреждая развитие воспаления.
Примеры конкретного выполнения
Пример 1. У добровольца У. получили пробу периферической венозной крови из кубитальной вены. С помощью градиентного (фиколл-верографин; ρ=1,077 г/см3) центрифугирования выделили популяцию мононуклеарных лейкоцитов. Клетки трижды отмыли свежим охлажденным раствором Хенкса и довели до 2×106 клеток/мл. После этого клеточную суспензию внесли в лунки круглодонного планшета с предварительно размещенными там образцами разных синтетических полимеров, условно обозначенные как «№ 1», «№ 2», «№ 3» и «№ 4». Каждый образец был в форме цилиндра длиною 3 мм и диаметром 1 мм. В качестве контролей использовали лунки с образцами из стекла и лунки, не содержащие синтетических полимеров. Планшеты инкубировали при 37°С в условиях 5% СО2 в течение 72 ч. По окончании инкубации в лунках подсчитывали общее число клеток, в том числе количество жизнеспособных в тесте с трипановым синим. Надосадочную жидкость после центрифугирования содержимого лунок использовали для определения концентрации ИЛ-4 и ИЛ-10 с помощью иммуноферментного метода. Уровень каждого из цитокинов пересчитали на 1 жизнеспособную клетку. После этого проводили расчет индекса стимуляции.
Полученные результаты представлены в таблице 1.
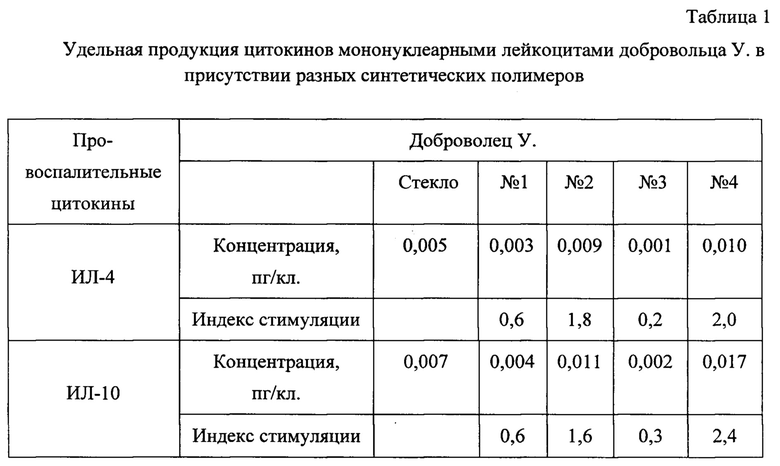
По показателям индекса стимуляции видно, что для добровольца У. будут пригодными для применения синтетические полимеры из которых изготовлены образцы № 2 и № 4. Иммунокомпетентные клетки в присутствии этих образцов не будут стимулировать воспалительный ответ, что обусловлено активной продукцией противовоспалительных цитокинов в их присутствии. Напротив, присутствие образцов № 1 и № 3 совместно с клетками добровольца У. не будут стимулировать лейкоциты на продукцию противовоспалительных цитокинов.
Пример 2. У добровольца С. получили пробу периферической венозной крови из кубитальной вены. С помощью градиентного (фиколл-верографин; ρ=1,077 г/см3) центрифугирования выделили популяцию мононуклеарных лейкоцитов. Клетки трижды отмыли свежим охлажденным раствором Хенкса и довели до 2×106 клеток/мл. После этого клеточную суспензию внесли в лунки круглодонного планшета с предварительно размещенными там образцами разных синтетических полимеров, условно обозначенные как «№ 1», «№ 2», «№ 3» и «№ 4». Каждый образец был в форме цилиндра длиною 3 мм и диаметром 1 мм. В качестве контролей использовали лунки с образцами из стекла и лунки, не содержащие синтетических полимеров. Планшеты инкубировали при 37°С в условиях 5% СО2 в течение 72 ч. По окончании инкубации в лунках подсчитывали общее число клеток, в том числе количество жизнеспособных в тесте с трипановым синим. Надосадочную жидкость после центрифугирования содержимого лунок использовали для определения концентрации ИЛ-4 и ИЛ-10 с помощью иммуноферментного метода.
Уровень цитокинов пересчитали на 1 жизнеспособную клетку. После этого проводили расчет индекса стимуляции.
Полученные результаты представлены в таблице 2.
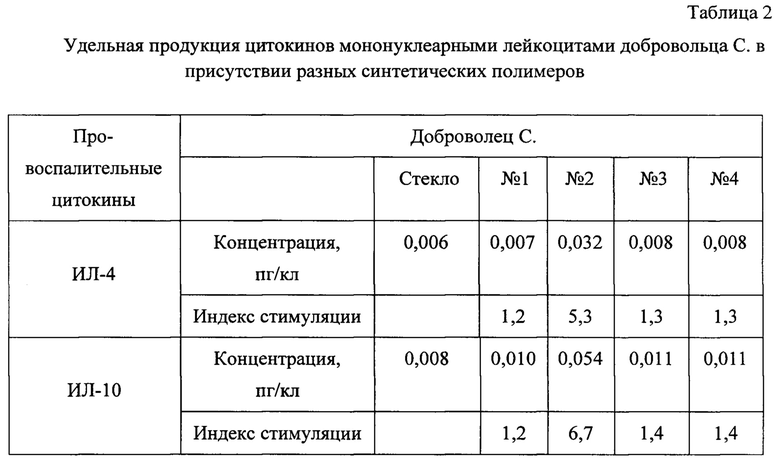
По показателям индекса стимуляции видно, что в присутствии всех четырех образцов клетки повышают продукцию противовоспалительных цитокинов. Однако в присутствии образца № 2 наблюдается максимальная продукция цитокинов. В целом, все четыре образца синтетического полимерного материала будут пригодны для использования в медицинских целях, но более перспективным представляется материал образца № 2.
Пример 3. У добровольца Ж. получили пробу периферической венозной крови из кубитальной вены. С помощью градиентного (фиколл-верографин; ρ=1,077 г/см3) центрифугирования выделили популяцию мононуклеарных лейкоцитов. Клетки трижды отмыли свежим охлажденным раствором Хенкса и довели до 2×106 клеток/мл. После этого клеточную суспензию внесли в лунки круглодонного планшета с предварительно размещенными там образцами разных синтетических полимеров, условно обозначенные как «№ 1», «№ 2», «№ 3» и «№ 4». Каждый образец был в форме цилиндра длиною 3 мм и диаметром 1 мм. В качестве контролей использовали лунки с образцами из стекла и лунки, не содержащие синтетических полимеров. Планшеты инкубировали при 37°С в условиях 5% СО2 в течение 72 ч. По окончании инкубации в лунках подсчитывали общее число клеток, в том числе количество жизнеспособных в тесте с трипановым синим.
Надосадочную жидкость после центрифугирования содержимого лунок использовали для определения концентрации ИЛ-4 и ИЛ-10 с помощью иммуноферментного метода. Уровень каждого из цитокинов пересчитали на 1 жизнеспособную клетку. После этого проводили расчет индекса стимуляции.
Полученные результаты представлены в таблице 3.
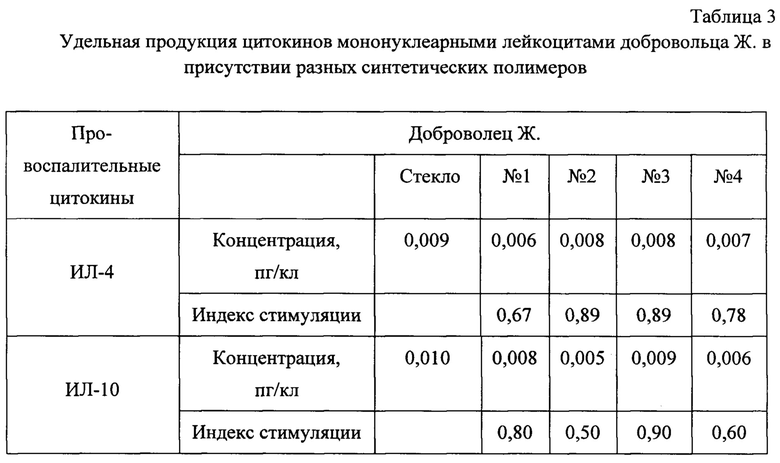
По показателям индекса стимуляции видно, что в присутствии всех четырех образцов клетки не повышают продукцию противовоспалительных цитокинов, что указывает на непригодность этих образцов для использования в медицинских целях.
Таким образом, использование предложенного способа позволяет снизить временные и трудозатраты при оценке пригодности использования синтетических полимеров с медицинскими целями, дает возможность одномоментной проверки значительного количества образцов, комплексной оценки пролиферативной и цитокин-продуцирующей активности мононуклеарных клеток при их непосредственном контакте с образцами, а также показывает направленность иммунного ответа, что должно быть в основе выбора перспективного для медицинского применения материала.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ индивидуальной оценки биосовместимости с организмом имплантируемых полимерных материалов | 2020 |
|
RU2743220C1 |
| СПОСОБ СТИМУЛЯЦИИ ЭНДОГЕННОЙ ПРОДУКЦИИ ЦИТОКИНОВ И ГЕМОПОЭТИЧЕСКИХ ФАКТОРОВ | 2012 |
|
RU2498821C1 |
| Способ применения композиции, включающей действующее вещество энисамия йодид | 2023 |
|
RU2827810C1 |
| СПОСОБ МОДИФИКАЦИИ МОНОЦИТОВ ПЕРИФЕРИЧЕСКОЙ КРОВИ ДЛЯ ПОВЫШЕНИЯ ИХ ПАРАКРИННОЙ АКТИВНОСТИ ПРИ АУТОЛОГИЧЕСКОЙ ТРАНСПЛАНТАЦИИ | 2012 |
|
RU2497947C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОСПАЛИТЕЛЬНЫХ ОСЛОЖНЕНИЙ ПРИ ЭНДОПРОТЕЗИРОВАНИИ КРУПНЫХ СУСТАВОВ | 2006 |
|
RU2321865C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ ЦИТОКИНОВ, ПОДАВЛЯЮЩИХ Т-ЛИМФОЦИТЫ НОВОРОЖДЕННЫХ | 2003 |
|
RU2246732C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2528337C1 |
| СПОСОБ ДИАГНОСТИКИ ВТОРИЧНОЙ ИММУНОЛОГИЧЕСКОЙ НЕДОСТАТОЧНОСТИ ПРИ ТУБЕРКУЛЕЗЕ ЛЕГКИХ | 2012 |
|
RU2504784C1 |
| СПОСОБ ОЦЕНКИ СОВМЕСТНОГО ДЕЙСТВИЯ ГЛЮКОКОРТИКОИДОВ И ИНТЕРЛЕЙКИНА-7 НА ФУНКЦИОНАЛЬНОЕ СОЗРЕВАНИЕ Т-ЛИМФОЦИТОВ НОВОРОЖДЕННЫХ | 2007 |
|
RU2363954C2 |
| МОДУЛЯЦИЯ ШАПЕРОНИНОМ 10 СЕКРЕЦИИ ЦИТОКИНОВ И ХЕМОКИНОВ, ИНДУЦИРУЕМОЙ TOLL-ПОДОБНЫМ РЕЦЕПТОРОМ | 2005 |
|
RU2446817C2 |
Изобретение относится к медицине, а именно к биотехнологии, иммунологии, имплантологии, и может быть использовано для оценки пригодности использования в медицинских целях синтетических полимеров. У добровольца получают образец периферической венозной крови, затем ее центрифугируют для получения популяции мононуклеарных лейкоцитов. Полученную клеточную суспензию вносят в лунки круглодонного планшета с размещенными в них образцами синтетических полимеров в форме цилиндра длиною 3 мм и диаметром 1 мм в количестве 1 штуки на лунку. Планшет инкубируют при 5% СО2 в течение 72 ч при температуре 37°С. Определяют количество мононуклеарных лейкоцитов и концентрацию противовоспалительных цитокинов ИЛ-4 и ИЛ-10, выражая полученные показатели в виде индекса стимуляции (ИС), который рассчитывают по формуле: ИС=УП/УС, предварительно определив удельную продукцию каждого из цитокинов в присутствии синтетического полимера (УП, пг/кл.) и удельную продукцию каждого из цитокинов в присутствии стекла (УС, пг/кл.) по формулам:
УП=Ц/КЛЦ; УС=С/КЛС, где
Ц - концентрация цитокина в пробе с синтетическим полимером, пг/мл;
КЛЦ - количество мононуклеарных лейкоцитов в пробе с синтетическим полимером, в 1 мл;
С - концентрация цитокина в пробе со стеклянным образцом, пг/мл;
КЛС - количество мононуклеарных лейкоцитов в пробе со стеклом, в 1 мл. Проводят оценку пригодности использования в медицинских целях синтетических полимеров. Величина ИС, равная и более 1, указывает на пригодность их использования в медицинских целях. Способ обеспечивает повышение эффективности, снижение временных и трудозатрат, возможность одномоментной проверки значительного количества образцов, комплексной оценки пролиферативной и цитокин-продуцирующей активности мононуклеарных клеток при их непосредственном контакте с образцами, позволяющей определять направленность иммунного ответа, обосновывая выбор перспективного для медицины материала, за счет осуществления контактного способа воздействия образцов синтетических полимеров на клетки иммунной системы - мононуклеарные лейкоциты, содержащиеся в периферической венозной крови человека, с оценкой продукции ими противовоспалительных цитокинов in vitro по показателю индекса стимуляции, что в сравнительном анализе результатов тестирования позволяет выбрать наиболее перспективные образцы. 3 табл., 3 пр.
Способ оценки пригодности использования в медицинских целях синтетических полимеров, отличающийся тем, что получают у добровольца образец периферической венозной крови, затем ее центрифугируют для получения популяции мононуклеарных лейкоцитов, полученную клеточную суспензию вносят в лунки круглодонного планшета с размещенными в них образцами синтетических полимеров в форме цилиндра длиною 3 мм и диаметром 1 мм в количестве 1 штуки на лунку, далее планшет инкубируют при 5% СО2 в течение 72 ч при температуре 37°С, далее определяют количество мононуклеарных лейкоцитов и концентрацию противовоспалительных цитокинов ИЛ-4 и ИЛ-10, выражая полученные показатели в виде индекса стимуляции (ИС), который рассчитывают по формуле: ИС=УП/УС, предварительно определив удельную продукцию каждого из цитокинов в присутствии синтетического полимера (УП, пг/кл.) и удельную продукцию каждого из цитокинов в присутствии стекла (УС, пг/кл.) по формулам:
УП=Ц/КЛЦ; УС=С/КЛС, где
Ц – концентрация цитокина в пробе с синтетическим полимером, пг/мл;
КЛЦ – количество мононуклеарных лейкоцитов в пробе с синтетическим полимером, в 1 мл;
С – концентрация цитокина в пробе со стеклянным образцом, пг/мл;
КЛС – количество мононуклеарных лейкоцитов в пробе со стеклом, в 1 мл; далее оценивают пригодность использования в медицинских целях синтетических полимеров – величина ИС, равная и более 1, указывает на пригодность их использования в медицинских целях.
| Способ индивидуальной оценки биосовместимости с организмом имплантируемых полимерных материалов | 2020 |
|
RU2743220C1 |
| Способ оценки биосовместимости скаффолдов | 2019 |
|
RU2714461C1 |
| СПОСОБ ОЦЕНКИ БИОСОВМЕСТИМОСТИ СТОМАТОЛОГИЧЕСКИХ ПОЛИМЕРНЫХ ПЛОМБИРОВОЧНЫХ МАТЕРИАЛОВ | 2011 |
|
RU2477487C2 |
| СПОСОБ ОЦЕНКИ БИОСОВМЕСТИМОСТИ ИМПЛАНТИРУЕМЫХ ИЗДЕЛИЙ | 2015 |
|
RU2605821C1 |
| US 20040241690 A1, 02.12.2004 | |||
| LOCK A | |||
| et al., The role of in vitro immune response assessment for biomaterials | |||
| J Funct Biomater | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| BERNARD M | |||
| et al., Biocompatibility of polymer-based biomaterials | |||
Авторы
Даты
2021-12-06—Публикация
2021-01-21—Подача