ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение в целом предусматривает способы выделения материала, например белка, например, из жидких смесей на основе культур клеток, с использованием аффинного связывания нанокристаллической целлюлозы (CNC) с химерами с доменом, связывающим белок и целлюлозу.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
СВМ представляют собой углеводсвязывающие модули, которые встречаются в разных организмах [1]. Целлюлозосвязывающий домен (CBD) является одним из примеров СВМ. CBDclos [2] представляет собой домен белка, который выделяют из бактерии Clostridium cellulovorans. Он прочно связывается с целлюлозой и образует стабильную, но обратимую связь, которая может выдерживать усилие сдвига и умеренные изменения рН в сторону кислых и основных значений (рН 4-10) и солености (раствор NaCl от 10 мМ до насыщенного). CBD ранее использовали для очистки белков на целлюлозных колонках [6]. Однако отсутствие целлюлозных гранул, пригодных для хроматографии, с большой площадью поверхности, способностью выдерживать высокие скорости потока и высокое давление, ограничивает его применение.
Частицы нанокристаллической целлюлозы (CNC или NCC) представляют собой небольшие (~300 нм) кристаллиты с высоким значением относительного удлинения, которые получают из целлюлозы различными способами. [3-5]. Каждая частица может связывать свыше 10 доменов CBDclos. Материал нетоксичен и абсолютно безопасен. Он также довольно устойчив к изменениям рН (от 1 до 13) и высоким значениям усилия сдвига. Это дешевый и широко доступный материал.
В патенте США №5856201 [7] раскрыто высокое сродство белка с целлюлозосвязывающим доменом (CBD) к кристаллической целлюлозе и слитым белкам на основе CBD и второго белка, а также способы аффинного разделения с применением такого слитого продукта.
Способы тангенциальной фильтрации являются усовершенствованием способов простой ("тупиковой") мембранной фильтрации. Создавая турбулентный поток с высоким усилием сдвига, перпендикулярный поверхности мембраны, они могут удалять слой геля, который образуется на поверхности мембраны, и таким образом увеличивать проницаемость и продолжительность эксплуатации. [8]. Способы мембранной тангенциальной фильтрации используют для очень больших масштабов (100 м3/день) в пищевой промышленности, для осветления и концентрирования молочных продуктов, фруктовых и овощных соков, напитков, пива, вина и многого другого. Дополнительными видами применения для больших масштабов являются операции обработки препаратов крови и отходов. [8]. В зависимости от значения отсечения мембраны, мембраны для тангенциальной фильтрации могут обеспечивать очищение от частиц широкого диапазона размеров, начиная от ионов соли (обратный осмос) и вплоть до частиц песка. Они также могут функционировать при очень высоком содержании сухих твердых веществ (60 г/100 г-1) и вязкости [9]. Мембранные способы, однако, в основном используются для относительно грубых, предварительных стадий очистки для разделения частиц или белков, которые значительно различаются по размеру. Для эффективного отделения требуется разность размеров на 1 порядок (10 раз) между отделяемыми частицами [10]. Это ограничивает использование способа для последующей очистки и доочистки, где требуется отделение конкретной частицы от популяции белков или частиц одинакового размера.
Хроматографические способы разделения (колоночная хроматография) используются там, где требуются высокая степень чистоты и, следовательно, высокая степень селективности, и по сути они являются интенсивно используемым средством разделения белков в биофармацевтической промышленности. В то же время, хроматографические способы являются дорогостоящими (на их долю приходится >70% от общих последующих затрат [11]), длительными и требуют сложных предварительных приготовлений. Ввиду их стоимости и сложности масштабирования они являются менее подходящими для способов обработки больших объемов. Поскольку потребность в больших количествах белков высокой степени очистки увеличивается, возрастает потребность в альтернативных способах очистки [12].
ССЫЛКИ
[1] Shoseyov, О.; Shani, Z.; Levy, I., Carbohydrate binding modules: biochemical properties and novel applications. Microbiology and Molecular Biology Reviews 2006, 70 (2), 283-295.
[2] Goldstein, M.A.; Takagi, M.; Hashida, S.; Shoseyov, O.; Doi, R.; Segel, I., Characterization of the cellulose-binding domain of the Clostridium cellulovorans cellulose-binding protein A. Journal of bacteriology 1993, 175 (18), 5762-5768.
[3] Charreau, H.; L Foresti, M.;  A., Nanocellulose patents trends: a comprehensive review on patents on cellulose nanocrystals, microfibrillated and bacterial cellulose. Recent patents on nanotechnology 2013, 7(1), 56-80.
A., Nanocellulose patents trends: a comprehensive review on patents on cellulose nanocrystals, microfibrillated and bacterial cellulose. Recent patents on nanotechnology 2013, 7(1), 56-80.
[4] Rebouillat, S.; Pla, F., State of the art manufacturing and engineering of nanocellulose: a review of available data and industrial applications. 2013.
[5] Peng, В.; Dhar, N.; Liu, H.; Tarn, K., Chemistry and applications of nanocrystalline cellulose and its derivatives: a nanotechnology perspective. The Canadian Journal of Chemical Engineering 2011, 89 (5), 1191-1206.
[6] Shpigel, E.; Goldlust, A.; Eshel, A; Ber, I. K.; Efroni, G.; Singer, Y.; Levy, I.; Dekel, M.; Shoseyov, O., Expression, purification and applications of staphylococcal Protein A fused to cellulose-binding domain. Biotechnology and applied biochemistry 2000, 31 (3), 197-203.
[7] US Patent No. 5,856,201.
[8] Marinaccio, P.J.; Repetti, R.V., Cross-flow filtration. Google Patents: 1989.
[9] Daufin, G.; Escudier, J.-P.; Carrere, H.; Berot, S.; Fillaudeau, L.; Decloux, M., Recent and emerging applications of membrane processes in the food and dairy industry. Food and Byproducts Processing 2001, 79 (2), 89-102.
[10] Cheryan, M., Ultrafiltration and Microfiltration Handbook. Taylor & Francis: 1998.
[11] Azevedo, A.M.; Rosa, P.A.; Ferreira, I.F.; Aires-Barros, M.R., Chromatography-free recovery of biopharmaceuticals through aqueous two-phase processing. Trends in biotechnology 2009, 27(4), 240-247.
[12]  J.; Etzel, M., Alternatives to chromatographic separations. Biotechnology progress 2007, 23 (1), 42-45.
J.; Etzel, M., Alternatives to chromatographic separations. Biotechnology progress 2007, 23 (1), 42-45.
[13] Forsgren, A.;  J., "Protein A" from S. aureus I. Pseudo-immune reaction with human γ-globulin. The Journal of Immunology 1966, 97 (6), 822-827.
J., "Protein A" from S. aureus I. Pseudo-immune reaction with human γ-globulin. The Journal of Immunology 1966, 97 (6), 822-827.
[14] Updyke, Т.V.; Nicolson, G.L., Immunoaffinity isolation of membrane antigens with biotinylated monoclonal antibodies and immobilized streptavidin matrices. Journal of immunological methods 1984, 73 (1), 83-95.
[15] Stols, L.; Gu, M.; Dieckman, L.; Raffen, R.; Collart, F.R.; Donnelly, M.I., A new vector for high-throughput, ligation-independent cloning encoding a tobacco etch virus protease cleavage site. Protein expression and purification 2002, 25 (1), 8-15.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения разработали способ, в котором используются объединенные признаки углеводсвязывающих модулей (СВМ) и нанокристаллической целлюлозы (CNC) для "вылавливания" специфических веществ, представляющих интерес (AOI), например белков (POI - белок, представляющий интерес), которые необязательно находятся или продуцируются в культуре. Способ основан на экспрессировании в клеточной культуре химеры СВМ-белок, содержащей СВМ, присоединенный к гетерологичному белку (HP) или домену, обеспечивающему аффинность, с сильной аффинностью к HP, с последующим осуществлением ряда этапов фильтрации, при этом присоединение CNC к части химеры СВМ-НР, представляющей собой СВМ, обеспечивает окончательное выделение требуемого белка. Как отмечено в данном документе, белок можно выделять в чистом виде или практически чистом виде и можно выделять в виде продукта слияния.
Способы по настоящему изобретению обеспечивают быстрый, экономичный и эффективный трехстадийный способ очистки/выделения с применением устройств и технологий для фильтрации, как, например, для половолоконной, тангенциальной фильтрации и т.д. Способы основаны на обратимом связывании химеры, состоящей из СВМ и AOI, такого как белок, например гетерологичный белок (HP), с CNC посредством СВМ-части химеры путем создания больших аддуктов белок/CNC, которые отделяют от загрязняющих веществ посредством фильтрации и могут впоследствии использовать в исходном виде. CBM-AOI, например химеру СВМ-белок или химеру СВМ-НР можно высвобождать от частиц CNC различными способами, например путем изменения рН или путем протеолиза, и белок, например HP, можно дополнительно отделять от СВМ с помощью различных методов расщепления или разделения, как описано ниже.
Преимущество настоящего изобретения заключается в том, что оно сочетает в себе преимущества как способов разделение на полых волокнах, так и способов хроматографического разделения, что позволяет обрабатывать очень большие объемы растворов с широким спектром белков и твердых частиц, обеспечивая при этом очень высокую степень селективности, обычно встречающуюся только в аффинной хроматографии. Описанные в данном документе способы исключают необходимость заполнения колонки и связанные с этим ограничения, такие как высокие значения давления, низкие скорости потока и забивание. В то время как в аффинной хроматографии связывающая способность смолы с целевым белком не превышает десятков миллиграммов на 1 грамм смолы, в настоящем изобретении емкость на 1 г CNC достигает сотен миллиграммов. Кроме того, способность избирательно задерживать целевой белок в концентрате при использовании микрофильтрации является огромным преимуществом по сравнению с ультрафильтрацией, которая обычно связана с высоким давлением, относительно низкой скоростью фильтрации и проблемами засорения.
Таким образом, в одном из своих аспектов настоящее изобретение предусматривает способ выделения белка, такого как гетерологичный белок (HP), из жидкой смеси, при этом способ включает:
- пропускание неочищенной смеси, содержащей химеру СВМ-белок, например химеру СВМ-НР, через первую фильтрационную мембрану с получением фильтрата, содержащего СВМ-белок, например СВМ-НР (при этом оставляя в концентрате примеси с высокой молекулярной массой или большим размером, которые можно удалить в отходы);
- приведение химеры, например СВМ-НР, в контакт с CNC с обеспечением взаимодействия с, например, химерой СВМ-НР с получением смеси, содержащей комплекс химера-CNC, например комплекс CBM-HP-CNC;
- фильтрование смеси, содержащей комплекс химера-CNC, например комплекс CBM-HP-CNC, через вторую фильтрационную мембрану с получением концентрата, содержащего комплекс; и
- необязательно отделение СВМ-НР и/или HP от комплекса CBM-HP-CNC для выделения белка или HP;
при этом каждая из первой и второй фильтрационных мембран являющихся одинаковыми или разными, имеют размер пор, выбранный для обеспечения проникновения через них (или фильтрации или пересечения) химеры СВМ-белок и для предотвращения (или остановки) проникновения комплекса.
В некоторых вариантах осуществления настоящее изобретение предусматривает способ выделения гетерологичного белка (HP) из жидкой смеси, при этом способ включает:
- пропускание, фильтрование неочищенной смеси, содержащей химеру СВМ-НР, через первую фильтрационную мембрану с получением фильтрата, содержащего СВМ-НР (при этом оставляя в концентрате примеси с высокой молекулярной массой или с большим размером, которые можно удалить в отходы);
- приведение химеры СВМ-НР в контакт с CNC с обеспечением взаимодействия с химерой СВМ-НР и с получением смеси, содержащей комплекс CBM-HP-CNC;
- пропускание, фильтрование смеси, содержащей комплекс CBM-HP-CNC, через вторую фильтрационную мембрану с получением концентрата, содержащего комплекс CBM-HP-HP-CNC; и
- необязательно отделение СВМ-НР и/или HP от комплекса CBM-HP-CNC; при этом каждая из первой и второй фильтрационных мембран, являющихся одинаковыми или разными, имеет размер пор, выбранный для обеспечения проникновения через них (или фильтрации или пересечения) химеры СВМ-НР и для предотвращения (или остановки) проникновения комплекса CBM-HP-CNC.
В некоторых вариантах осуществления первая и вторая фильтрационные мембраны являются одинаковыми, а в некоторых вариантах осуществления в способе используется одна мембрана.
В некоторых вариантах осуществления первая и вторая фильтрационные мембраны выбраны из половолоконных мембран.
В некоторых вариантах осуществления первая и вторая фильтрационные мембраны представляют собой микрофильтрационные мембраны.
В некоторых вариантах осуществления фильтрационная мембрана имеет размер пор от 0,2 до 60 кДа.
В некоторых вариантах осуществления способ включает получение химеры СВМ-НР в неочищенной смеси. В некоторых вариантах осуществления СВМ-НР продуцируется/экспрессируется в клетке-хозяине, например в растительных клетках. В некоторых вариантах осуществления СВМ-НР имеет растительное происхождение.
В некоторых вариантах осуществления способ включает добавление CNC к фильтрату, содержащему химеру СВМ-НР, в условиях, обеспечивающих взаимодействие между химерой CBD-HP и CNC, с получением тем самым смеси, содержащей комплекс CBM-HP-CNC.
Термин "гетерологичный белок " обычно относится к белку, который получен из того же или другого организма по сравнению с организмом в котором он производится (например, бактериальная линия клеток, трансформированная или трансдуцированная вектором, кодирующим белок млекопитающего в гетерологичной системе экспрессии). Гетерологичные белки обычно получают путем вставки ДНК, кодирующей белок, с помощью технологии рекомбинантной ДНК в экспрессионный вектор, который используют для трансформации организма-хозяина (например, дрожжевой клетки-хозяина). Некоторыми неограничивающими примерами гетерологичных белков являются ферменты (например, ферменты модификации нуклеиновых кислот) и их субстратсвязывающие домены, протеазы, лимфокины, интерфероны, гормоны и предшественники гормонов, полипептиды, пептиды, антитела и фрагменты антител, антигены, антигенные эпитопы и их варианты, ДНК-связывающие белки, их рецепторы и фрагменты, вирусные антигены или иммуногены и любой полипептид и гликопротеин, которые можно экспрессировать в организме-хозяине, который отличается от организма, являющегося источником указанного белка. Таким образом, химера может образовываться между СВМ и любым одним или несколькими ферментами (например, ферментами модификации нуклеиновых кислот) и их субстратсвязывающими доменами, протеазами, лимфокинами, интерферонами, гормонами и предшественниками гормонов, полипептидами, пептидами, антителами и фрагментами антител, антигенами, антигенными эпитопами и их вариантами, ДНК-связывающими белками, рецепторами и их фрагментами, вирусными антигенами или иммуногенами и любым полипептидом и гликопротеином, которые можно экспрессировать в организме-хозяине, который отличается от организма, являющегося источником указанного белка, и т.д.
HP может находиться в неочищенной смеси или среде, обычно в форме "жидкой смеси", которая также содержит вещества-примеси, продукты конкурирующих реакций, продукты распада клеток и/или множество других материалов. Примеси, из которых HP (или вещество, представляющее интерес, как указано ниже) необходимо селективно выделить, могут включать любое одно или несколько из следующих органических соединений (например, белков, нуклеиновых кислот), клеток, клеточных компонентов (макромолекул, продуктов распада клеток), малых молекул, таких как полифенолы; алкалоидов; нерастворимых веществ, таких как компоненты клеточной стенки (например, целлюлоза, лигнин); вирусов; бактерий; частиц пыли; солей; пестицидов; и полимеров, таких как крахмал и гликоген.
Как используется в данном документе, термин "химера СВМ-НР" (используемый взаимозаменяемо с термином слитый белок) обычно относится к белку, полученному путем объединения друг с другом по меньшей мере двух белков, один из которых представляет собой СВМ, а другой - HP. СВМ представляет собой углеводсвязывающий модуль, содержащий непрерывную аминокислотную последовательность в ферменте, активном в отношении углеводов, при этом углеводсвязывающей активностью обладает отдельная складка. Некоторыми неограничивающими примерами СВМ являются представители семейства углеводсвязывающих модулей от 1 до 83, известные в данной области техники и доступные в базе данных CAZy для семейств структурно связанных каталитических и углеводсвязывающих модулей или функциональных доменов ферментов. СВМ могут проявлять существенные различия в отношении субстратной специфичности, потому связывают молекулы, такие как моносахарид (например, галактоза, лактоза, арабиноза), соединение с гликозидной связью и полисахариды (например, целлюлозу, глюкоманнан, ксилан, крахмал, хитин) с различными степенями аффинности.
В некоторых вариантах осуществления СВМ представляет собой целлюлозосвязывающий домен (CBD).
CBD представляет собой модуль из непрерывной аминокислотной последовательности, находящийся в белке, который может связывать целлюлозу/кристаллическую целлюлозу. При получении химеры CBD-HP согласно настоящему изобретению CBD может быть присоединен к С-концу или N-концу белка. Химера СВМ-НР по настоящему изобретению, в некоторых вариантах осуществления представляющая собой химеру CBD-HP, характеризуется аффинностью связывания целлюлозы (при измерении с помощью константы диссоциации [Kd]), составляющей от 0,5 мкМ до 5 мкМ. Аффинность связывания можно поддерживать в определенном диапазоне значений рН и в условиях применения разных буферов и ее можно устранить, например, для высвобождения CBD от присоединенной к нему CNC, например, путем повышения рН до значения выше чем приблизительно 11.
HP может содержать более одной единицы CBD (например, одну единицу CBD на С-конце HP и другую единицу CBD на N-конце HP). В соответствии с настоящим изобретением белок с CBD может представлять собой вариант, производное, фрагмент или химическую модификацию любого из белков или белковых доменов, описанных, например, в базе данных CAZy, доступной по адресу http://www.cazy.org/carbohydrate-binding-modules.html, при условии, что фрагмент, производное, вариант или модификация сохраняют свойства связывания CNC. В некоторых вариантах осуществления каждая единица CBD может быть связана с одним или несколькими HP, которые могут быть одинаковыми или разными.
В некоторых вариантах осуществления белок с CBD представляет собой функциональный гомолог CBD, характеризующийся по меньшей мере 70%, 80%, 90% или 95% гомологией с аминокислотной последовательностью, имеющей номера доступа в базе данных GeneBank, представленные в http://www.cazy.org/carbohydrate-binding-modules.html. Термин "гомология" обычно относится к степени комплементарности с последовательностью сравнения (например, с SEQ ID NO в GeneBank), где последовательность может характеризоваться частичной гомологией (например, 70% гомологией) или полной гомологией (т.е. 100% идентичностью) в отношении эталонной последовательности. Термин "Х% гомология" (например, 70% гомология) не ограничивается последовательностями, характеризующимися Х% гомологией по всей длине белка. Таким образом, выражение "70% гомология" также включает гомологию, наблюдающуюся в определенных функциональных областях.
В некоторых вариантах осуществления CBD выбирают из СВМ2-СВМ13, СВМ16-СВМ17, СВМ20-СВМ28, СВМ40-СВМ46 и СВМ61-СВМ67, как известно в данной области техники. В целях окончательного оформления база данных CAZY, предоставленная по адресу http://www.cazy.org/carbohydrate-binding-modules.html. включена в данный документ посредством ссылки во всей своей полноте.
В некоторых вариантах осуществления функциональная область представляет собой определенный набор аминокислот, обладающих способностью связывать целлюлозу с высокой аффинностью и обратимым образом. В некоторых вариантах осуществления функциональные области состоят из приблизительно 200 аминокислот. В некоторых других вариантах осуществления функциональные области состоят из приблизительно 185 аминокислот. В некоторых других вариантах осуществления функциональные области состоят из приблизительно 50 аминокислот.
В некоторых вариантах осуществления белок с CBD имеет аминокислотную последовательность из Ruminiclostridium thermocellum, имеющую номер в GeneBank EEU00265.1. В некоторых вариантах осуществления последовательность CBD представляет собой
NLKVEFYNSNPSDTTNSINPQFKVTNTGSSAIDLSKLTLRYYYTVDGQKDQTFWCDHAAIIGSNGSYNGITSNVKGTFVKMSSSTNNADTYLEISFTGGTLEPGAHVQIQGRFAKNDWSNYTQSNDYSFKSASQFVEWDQVTAYLNGVLVWGKEPGGSVVPSTQPVTTPPATTKPPATTIPP.
В некоторых вариантах осуществления CBD представляет собой функциональное производное CBD.
Как используется в данном документе, термин "функциональное производное CBD" относится к любому "фрагменту", "варианту", "аналогу" или "химическому производному" аминокислотной последовательности белка с CBD, показанной в последовательностях GENEBANK выше, которые сохраняют способность связываться с целлюлозой с высокой аффинностью и обратимым образом.
В некоторых вариантах осуществления длина функционального производного CBD составляет от приблизительно 2 до приблизительно 160 аминокислот. В некоторых других вариантах осуществления длина функционального производного CBD составляет от 25 до 125 аминокислот. В других вариантах осуществления длина функционального производного CBD составляет от 50 до 100 аминокислот.
Используемый в данном документе термин "фрагмент" обычно относится к белку с CBD, полученному из белка с CBD, как определено в данном документе, имеющему встречающуюся в природе последовательность. В некоторых вариантах осуществления фрагмент, представляющий собой CBD, получают путем протеолитического расщепления полноразмерного белка с CBD. В других вариантах осуществления фрагмент, представляющий собой CBD, получают с помощью рекомбинации, путем соответствующей модификации последовательности ДНК, кодирующей белок с CBD, путем удаления одной или нескольких аминокислот в одном или нескольких положениях С-конца, N-конца и/или внутри встречающейся в природе последовательности. В соответствии с настоящим изобретением фрагменты CBD, используемые для получения описанной в данном документе, например, химеры CDB-HP, можно подвергать скринингу в отношении способности связывать целлюлозу с высокой аффинностью и обратимым образом, чтобы установить идентичность или полезность функциональной производной.
"Вариант" представляет собой молекулу, в которой аминокислотная последовательность, характер гликозилирования или другое свойство встречающейся в природе молекулы были модифицированы ковалентным или нековалентным образом, и включает мутанты. Некоторые неограничивающие примеры вариантов включают аминокислотные замены, делеции и/или вставки, при условии, что конечная конструкция обладает требуемой способностью связывать целлюлозу с высокой аффинностью и обратимым образом.
Аминокислотные замены в белке с CBD можно осуществлять на основе сходства по полярности, заряду, растворимости, гидрофобности, гидрофильно ста и/или амфипатической природы вовлеченных остатков. Например, отрицательно заряженные аминокислоты включают аспарагиновую кислоту и глутаминовую кислоту; положительно заряженные аминокислоты включают лизин и аргинин; аминокислоты с незаряженными полярными концевыми группами или неполярными концевыми группами, характеризующиеся сходными значениями гидрофильности, включают следующие: лейцин, изолейцин, валин; глицин, аланин; аспарагин, глутамин; серии, треонин; фенилаланин и тирозин. Вариант также может содержать дополнительные аминокислоты в одном или нескольких положениях С-конца, N-конца и во встречающейся в природе последовательности CBD, при условии, что вариант сохраняет способность связывать целлюлозу с высокой аффинностью и обратимым образом.
Термин "химическое производное" обычно относится к белку с CBD, полученному путем химической модификации встречающегося в природе белка с CBD или его варианта. Некоторыми неограничивающими примерами химической модификации являются замены атома Н на, например, алкильную, ацильную или аминогруппу.
Для получения описанной в данном документе химеры CBD-HP можно использовать нуклеиновую кислоту, кодирующую CBD, для конструирования рекомбинантных экспрессионных векторов, способных экспрессировать белок с CBD или химеру CBD-HP. Экспрессионные векторы (т.е. конструкция на основе нуклеиновой кислоты), используемые для экспрессирования указанной химеры, обычно содержат нуклеотидные последовательности, содержащие транскрипционную и трансляционную регуляторную информацию, являющиеся функционально связанными (т.е. связаны таким образом, что регуляторные последовательности ДНК и экспрессируемая последовательность ДНК связаны таким образом, чтобы обеспечить транскрипцию и, в конечном счете, трансляцию РНК в химерный полипептид CBD-HP). В соответствии с настоящим изобретением при конструировании экспрессионного вектора для химеры CBD-HP нуклеиновую кислоту, кодирующую белок с CBD, связывают или присоединяют к нуклеиновой кислоте, кодирующей HP, так чтобы открытая рамка считывания белка с CBD и второго белка оставались в неизменном виде, обеспечивая осуществление трансляции слитого белка с CBD. Нуклеиновую кислоту, кодирующую CBD, можно получить из различных источников, представляющих собой клетки, которые продуцируют целлюлозосвязывающие домены, которые связываются с высокой аффинностью и обратимым образом, или которые продуцируют мРНК, кодирующую CBD.
В некоторых вариантах осуществления нуклеиновую кислоту, кодирующую белок с CBD, получают из Clostridium cellulovorans.
В других вариантах осуществления нуклеиновую кислоту, кодирующую CBD, получают, как описано в патенте США №5856201, включенном в данный документ посредством ссылки.
В соответствии с настоящим изобретением нуклеиновую кислоту, кодирующую белок с CBD, можно получить из выделенной и очищенной ДНК из источников, представляющих собой клетки, или путем геномного клонирования. Если источником белка с CBD является генетическое клонирование, можно получать либо кДНК-, либо геномные библиотеки клонов с использованием методик, общеизвестных в данной области техники. Библиотеки можно подвергать скринингу в отношении конкретной нуклеиновой кислоты, кодирующей CBD, с помощью нуклеотидных зондов, которые по существу комплементарны определенной части гена. Если требуется обнаружение белка с CBD, кодируемого консервативными нуклеотидными областями, нуклеотидные зонды основаны на нуклеотидных последовательностях CBD, которые сохраняются от вида к виду. Если требуется обнаружение белка с CBD, кодируемого уникальными нуклеотидными областями, нуклеотидные зонды основаны на уникальных нуклеотидных последовательностях CBD. Альтернативно, кДНК или геномную ДНК можно использовать в качестве матриц для ПЦР-клонирования с подходящими олигонуклеотидными праймерами. Для конструирования экспрессионных векторов можно выбрать полноразмерные клоны, т.е. клоны, содержащие всю кодирующую область требуемого белка с CBD, или можно лигировать перекрывающиеся кДНК друг с другом с образованием полной кодирующей последовательности. Альтернативно, ДНК, кодирующие CBD, можно синтезировать полностью или частично путем химического синтеза с использованием методов, считающихся стандартными в данной области техники.
Как легко понять специалисту в данной области техники, выбор подходящего экспрессионного вектора зависит от различных параметров, например:
- будет ли он использоваться для амплификации нуклеиновых кислот или для экспрессии нуклеиновых кислот;
- размер нуклеиновой кислоты, которая должна быть вставлена в вектор;
- клетка-хозяин, подлежащая трансформации вектором.
В соответствии с настоящим изобретением каждый вектор может содержать различные компоненты в зависимости от его функции (амплификация нуклеиновой кислоты или экспрессия нуклеиновой кислоты) и клетки-хозяина с которой он совместим.
Слитый белок CBD-HP можно получить путем субклонирования ДНК CBD-HP в экспрессионный вектор (например, экспрессионный вектор на основе Escherichia coli), который продуцирует химерный слитый белок CBD-HP под управлением/контролем рекомбинантного плазмидного вектора в клетке-хозяине (т.е. система культивирования на основе клеток). "Клетка-хозяин" (в данном документе взаимозаменяемо с 'системой культивирования на основе клеток') представляет собой тип клеток, способных к росту в культуре и способных экспрессировать белок с CBD или химеру CBD-HP. Клетка-хозяин может представлять собой клетки, выращенные в культуре in vitro, в том числе клетки прокариот, эукариот и насекомых. Клетку-хозяина можно выбирать из штамма, в котором обеспечивается модулирование экспрессии вставленных последовательностей или модификация и процессинг продукта гена определенным требуемым образом. Например, экспрессия с определенных промоторов может повышаться в присутствии определенных индукторов (например, ионов цинка и кадмия в случае промоторов металлотионеина). Можно выбирать такую клетку-хозяина, чтобы она секретировала минимальные количества протеолитических ферментов.
В некоторых вариантах осуществления система культивирования на основе клеток представляет собой бактериальную систему, выбранную из системы на основе Escherichia coli, Corynebacterium и Pseudomonas fluorescens. В других вариантах осуществления система культивирования на основе клеток представляет собой эукариотическую систему, выбранную из системы на основе Saccharomyces cerevisiae, Pichia Pastoris, мицелиальных грибов, клеток, инфицированных бакуловирусом, системы нелитической экспрессии на основе клеток насекомых и на основе лейшманий. В других вариантах осуществления система культивирования на основе клеток представляет собой систему на основе клеток млекопитающих, выбранную из системы на основе клеток яичника китайского хомячка(СНО), клеток эмбриональной почки человека (HEK), клеток яичника китайского хомячка, лимфобластных клеток миеломы мыши, клеток эмбриональной почки человека (HEK-293), эмбриональных клеток сетчатки человека и клеток амниоцитов человека (например, Glycotope и CEVEC). В других вариантах осуществления система культивирования на основе клеток представляет собой бесклеточную систему, которая содержит все клеточные компоненты, необходимые для синтеза белка, и в которой белки получают in vitro с использованием очищенной РНК-полимеразы, рибосом, тРНК и рибонуклеотидов.
Химеру на основе CBD или CBD-HP можно получить как описано в патенте США №5856201, включенном в настоящий документ посредством ссылки.
Соответственно, экспрессию белка с CBD или слитого белка CBD-HP можно контролировать. Способность контролировать экспрессию важна, если белок с CBD или слитый белок CBD-HP является летальным для клетки-хозяина. В некоторых вариантах осуществления, HP представляет собой рекомбинантный белок, полученный в виде химеры с белком CBD, где CBD слит с N- или С-концом HP. В некоторых вариантах осуществления часть химеры, представляющую собой HP, можно слить с третьим белком или присоединить к нему.
В некоторых вариантах осуществления HP получают в виде химеры с другим элементом (например, стрептавидином, Fc-фрагментом, антигеном и т.д.), который впоследствии может связываться с СВМ (или связываться с СВМ, присоединенным к аналогу элемента). Таким образом, в соответствии с настоящем изобретением HP можно присоединить к СВМ либо непосредственно, например, если он продуцируется в виде непрерывной аминокислотной цепи с помощью рекомбинации, либо его можно связать с СВМ посредством другого домена или взаимодействия, например, белка A/Fc-фрагмента, стрептавидина/биотина и т.д. В некоторых вариантах осуществления HP соединен с СВМ посредством сайта расщепления (например, домена TEV) или образует химеру CBD-HP.
В некоторых вариантах осуществления химера CBD-HP содержит по меньшей мере один линкер (например, расщепляемый линкер). Линкер может иметь длину от 1 до 100 аминокислот или от 2 до 20 аминокислот, может быть вставлен между СВМ и HP и может усиливать протеолитическую стабильность химеры CBD-HP во время ее воспроизведения в культуре клеток (например, во время повторных пассажей).
"Неочищенная смесь", из которой AOI, например HP, должен быть выделен в виде химеры с CBD, обычно представляет собой жидкую смесь для культивирования клеток (т.е. культуру клеток-хозяев, такую как культура клеток дрожжей или Е. coli), которая содержит смесь интактных и фракционированных клеток, которые обогащены определенной в данном документе химерой CBD-HP-белок. Неочищенная смесь может также содержать другие компоненты (например, макромолекулы), такие как нуклеиновые кислоты, белки, углеводы, полифенолы и большие неполимерные молекулы, такие как липиды. В некоторых вариантах осуществления сырая смесь представляет собой гомогенат, образованный путем разрушения клеточной мембраны клеток, содержащихся в культуре клеток.
"Фильтрационная мембрана", используемая в соответствии с настоящим изобретением, обычно представляет собой микромембрану, которая обеспечивает пропускание жидкости (например, загрязненной или неочищенной) с отделением микроорганизмов и взвешенных частиц, содержащихся в жидкости. Первая и вторая фильтрационные мембраны могут быть одинаковыми или разными и могут иметь размер пор, обеспечивающий проникновение через них химеры СВМ-НР, в то же время предотвращающий проникновение комплекса CBM-HP-CNC, как определено. В некоторых вариантах осуществления фильтрационная мембрана, используемая в способе, является одинаковой для обеих этапов фильтрации. В некоторых вариантах фильтрационная мембрана имеет размер пор от 0,2 мкм до соответствующего границе отсечения по молекулярной массе 60 кДа.
Мембрана может представлять собой любую подходящую фильтрационную мембрану, известную в данной области техники, которая может действовать в качестве физического барьера, который пропускает определенные компоненты (например, белки) в зависимости от их физических и/или химических свойств. Фильтрационная мембрана подходит для отфильтровывания требуемой молекулы (например, химеры CDB-HP) из описанной в данном документе неочищенной смеси. Фильтрационная мембрана обладает достаточной прочностью (например, чтобы противостоять разрыву и растягиванию во время фильтрации) и достаточной гидрофильностью (чтобы обеспечить достаточное смачивание). В соответствии с настоящим изобретением первое значение отсечения по молекулярной массе фильтрационной мембраны (т.е. растворенный компонент с наименьшей молекулярной массой, в дальтонах, в котором 90% растворенного компонента задерживается мембраной) составляет приблизительно 50 кДа.
В некоторых вариантах осуществления, фильтрационные мембраны, используемые для любого из этапов фильтрации, могут быть одинаковыми и могут быть изготовлены, сконфигурированы, сконструированы или использованы аналогичным образом. Поскольку считается, что размер пор мембраны необходимо выбирать в диапазоне от 0,2 мкм до соответствующего границе отсечения по молекулярной массе 60 кДа, такой выбор размера пор предназначен для охвата как микрофильтрационных мембран с размерами пор в диапазоне от 0,1 до 10 мкм, так и ультрафильтрационных мембран с размерами пор в диапазоне от 0,1 до 0,01 мкм. Альтернативно, фильтрационные мембраны можно выбирать на основании их отсечения по молекулярной массе, при этом это значение составляет не более 60 кДа.
Таким образом, можно выбирать мембраны, имеющие размер пор от 0,2 до 10 мкм или от 0,01 до 0,1 мкм или отсечение по молекулярной массе, составляющее не более 60 кДа.
В некоторых вариантах осуществления наименьший размер мембраны выбирают на основании размера пор, при этом он составляет 0,2 мкм, а наибольший размер выбирают на основании границы отсечения молекулярной массы, при этом он не превышает 60 кДа.
В некоторых вариантах осуществления одна или обе фильтрационные мембраны имеют размер пор от 0,45 мкм до 60 кДа (граница отсечения по молекулярной массе). В некоторых вариантах осуществления фильтрационная мембрана имеет размер пор от 1 мкм до 50 кДа (граница отсечения по молекулярной массе). В некоторых вариантах осуществления фильтрационная мембрана имеет размер пор приблизительно 0,2 мкм.
Фильтрационную мембрану используют в соответствии с настоящим изобретением для отфильтровывания описанной в данном документе химеры CBD-HP (например, полученной с помощью способов на основе рекомбинации) из неочищенной смеси, содержащей клетки-хозяева, которые продуцировали химеру. Неочищенная смесь обычно содержит химеру CBD-HP, а также различные растворимые и нерастворимые загрязняющие вещества, описанные в данном документе. Так, например, при границе отсечения по молекулярной массе приблизительно 300 кДа фильтрационная мембрана задерживает крупные частицы и бактерии, при этом большинство глобулярных белков и малых молекул легко проникают через нее вместе с химерой СВМ-НР. После того, как большая часть СВМ-НР была отфильтрована через мембрану, концентрат (содержащий в основном загрязнители) удаляют в отходы.
Фильтрационные мембраны можно выбирать из половолоконных мембран, которые могут быть из любого материала, доступного в данной области техники, такого как керамические половолоконные мембраны, производимые Pall membralox, GEA, Novasep Kerasep, и полимерные половолоконные мембраны, производимые GE, Sartorius, и т.д.
После отделения химеры добавляют CNC (например, частицы CNC) и обеспечивают ее взаимодействие с химерой с получением комплекса CBM-HP-CNC, формирующегося после связывания CNC с СВМ-частью химеры СВМ-НР. В соответствии с настоящим изобретением CNC можно добавлять в форме суспензии частиц CNC в воде или фосфатном буфере с низкой проводимостью, при этом концентрация частиц CNC в суспензии составляет от приблизительно 0,01% до 10 вес.% или от 0,5% до 2%.
В некоторых вариантах осуществления связывание CNC с химерой СВМ-НР осуществляют в 10 мМ фосфатном буфере при рН 7,4.
В некоторых вариантах осуществления CNC инкубируют с фильтратом, содержащим химеру, в течение периода времени, составляющего от 10 минут до 240 минут, при нейтральном рН (например, в 1-100 мМ фосфатном буфере при рН 7,4), при температуре, составляющей от 4 до 20°С или приблизительно 4°С, до пропускания смеси, содержащей комплекс CBM-HP-CNC, через фильтрационную мембрану.
"Кристаллическая наноцеллюлоза" (CNC) представляет собой материал, полученный из целлюлозы, в форме кристаллов целлюлозы с нанометровым диапазоном размеров (для всех размеров - высоты, длины и ширины). CNC может быть получена из целлюлозы любого типа, в том числе бактериальной целлюлозы, растительной целлюлозы и т.д. В соответствии с настоящим изобретением CNC, применяемая в описанных здесь способах, может быть из коммерчески доступного источника или получена в соответствии с известными методиками, такими как способ, описанный в WO 2012/014213 или эквивалентной ей заявке на патент США, включенных в настоящий документ посредством ссылки.
В некоторых вариантах осуществления CNC отличается тем, что характеризуется степенью кристалличности по меньшей мере 50%. В некоторых других вариантах осуществления CNC является монокристаллической. В некоторых вариантах осуществления CNC получают из целлюлозы различного происхождения в виде частиц (например, фибрилл или в других случаях в виде кристаллического материала) и выбирают так, чтобы их длина составляла по меньшей мере приблизительно 100 нм. В некоторых вариантах осуществления длина CNC составляет не более 1000 мкм. В других вариантах осуществления длина частиц CNC составляет от приблизительно 100 нм до 1000 мкм, от приблизительно 100 нм до 900 мкм, от приблизительно 100 нм до 600 мкм или от приблизительно 100 нм до 500 мкм. В других вариантах осуществления длина частиц CNC составляет от приблизительно 100 нм до 1000 нм, от приблизительно 100 нм до 900 нм, от приблизительно 100 нм до 800 нм, от приблизительно 100 нм до 600 нм, от приблизительно 100 до 500 нм, от приблизительно от 100 до 400 нм, от приблизительно 100 до 300 нм или от приблизительно 100 до 200 нм.
В соответствии с настоящим изобретением толщина CNC может составлять приблизительно от 5 нм до 100 нм, и может быть выбрана такая CNC, значение относительного удлинения (отношение длины к диаметру) которой составляет 10 и более. В некоторых вариантах осуществления значение относительного удлинения составляет от 67 до 100. В некоторых вариантах осуществления выбирают такую CNC, длина которой составляет от приблизительно 100 нм до 400 нм, а толщина - от приблизительно 5 нм до 30 нм.
В соответствии со способом по настоящему изобретению смесь, содержащую комплекс CBM-HP-CNC (например, CBD-HP-CNC), пропускают через другую или такую же фильтрационную мембрану, которая из-за увеличения размера не позволяет комплексу CBD-HP-CNC проникать через нее. Фильтрат (например, содержащий различные растительные белки) удаляют в отходы, а концентрат, содержащий (очищенный) комплекс CBM-HP-CNC, затем обрабатывают с выделением или отделением HP. Отделение HP от комплекса CBM-HP-CNC можно осуществлять с применением различных химических процедур (например, элюирования с применением повышения рН, протеолиза), которые являются общеизвестными в данной области техники. Например, отделения химеры СВМ-НР от частиц CNC можно достичь путем повышения рН с получением тем самым химеры СВМ-НР, из которой после протеолиза с помощью подходящего протеолитического фермента высвобождается HP из химеры СВМ-НР. В некоторых вариантах осуществления выделение HP можно осуществлять путем повышения рН приблизительно до уровня рН от 11 до 12 с высвобождением химеры СВМ-НР от NCC с последующим добавлением по меньшей мере одного протеолитического фермента с высвобождением СВМ от HP. Некоторыми неограничивающими примерами протеолитического фермента являются эндопептидаза ядерных включений а вируса гравировки табака (TEV), фактор X, энтерокиназа, тромбин HRV-3C, фицин и папаин.
HP, полученный способом по настоящему изобретению, можно использовать для "вылавливания" вещества, представляющего интерес (AOI), которое может представлять собой вещество на основе аминокислоты или на основе отличного от аминокислоты соединения. Таким образом, способ может дополнительно включать этап, на котором обеспечивают взаимодействие между выделенным HP или химерой на основе HP, например химерой СВМ-НР, и по меньшей мере одним AOI. AOI может представлять собой любое вещество или материал, способные к аффинному связыванию с HP. Такие вещества могут быть выбраны из веществ на основе аминокислоты, где HP представляет собой антитело, рецептор, фермент, субстрат и тому подобное или их фрагмент; вещества на основе нуклеиновой кислоты, где HP представляет собой белок, связывающий нуклеиновую кислоту, или его фрагмент; сахара, жирной кислоты или малой органической молекулы, содержащей пептидный фрагмент, способный аффинно связываться с ним.
Таким образом, в другом аспекте настоящее изобретение предусматривает способ выделения вещества, представляющего интерес (AOI), из жидкой смеси, при этом способ включает:
- обработку среды, содержащей по меньшей мере один AOI, с помощью химеры СВМ-НР (которую необязательно получают и выделяют в соответствии со способом по настоящему изобретению, как определено выше; или которую получают и выделяют любым другим способом) в условиях, обеспечивающих связывание между AOI и химерой СВМ-НР, с получением смеси, содержащей комплекс CBM-HP-AOI;
- добавление CNC к смеси, содержащей комплекс CBM-HP-AOI, с образованием комплекса CNC-CBM-HP-AOI;
- пропускание смеси, содержащей комплекс CNC-CBM-HP-AOI, через фильтрационную мембрану, не допускающую проникновения комплекса CNC-CBM-HP-AOI, с получением концентрата, содержащего комплекс CNC-CBM-HP-AOI; и
- выделение AOI из комплекса.
Фильтрационная мембрана может быть определена, как указано выше.
В некоторых вариантах осуществления способ дополнительно включает этап получения среды, содержащей AOI, подлежащее выделению. В некоторых вариантах осуществления среда представляет собой неочищенную смесь, определенную в данном документе, содержащую AOI, и таким образом ее можно пропускать через фильтрационную мембрану, характеризующуюся размером пор приблизительно 0,2 микрона, с частичным удалением примесей из среды.
Чтобы выделить/отделить AOI от комплекса CNC-CBD-HP-AOI, можно выполнять различные химические процедуры, общеизвестные в данной области техники. Например, AOI можно высвобождать путем снижения рН до значения рН от 1,5 до 3, добавления конкретной соли, такой как NaCl, хлорид гуанидиния, или ацетата металла, такого как ацетат лития, или растворителя, такого как этанол и н-бутанол. AOI должен проходить через мембрану после высвобождения и таким образом очищаться от раствора. В некоторых вариантах осуществления смесь, содержащая комплекс CNC-CBM-HP-AOI, дополнительно очищают посредством дополнительного диализа (разделения молекул в растворе по разнице в скорости их диффузии через полупроницаемую мембрану) или фильтрации перед выделением AOI из комплекса CNC-CBD-HP-AOI.
В некоторых вариантах осуществления концентрат (смесь), содержащий комплекс CNC-CBM-HP-AOI, собирают и хранят для дальнейшей обработки при необходимости.
В других вариантах осуществления, чтобы высвободить CNC из комплекса CNC-CBM-HP-AOI или комплекса CNC-CBM-HP, полученного способами по настоящему изобретению, рН смеси, содержащей комплекс, повышают до уровня от приблизительно 10 до приблизительно 13. В соответствии с такими вариантами осуществления CNC можно удалять в отходы или перерабатывать и комплекс CBM-HP-AOI можно собирать (например, с помощью фильтрации).
В других вариантах осуществления для выделения чистого HP можно применять подходящую протеазу, описанную в данном документе. В соответствии с такими вариантами осуществления линкерный белок, находящийся между белком СВМ и белком HP, подвергают гидролизу, и как следствие HP обретает способность проникать через мембрану и собирается в фильтрате. Комплекс CNC-CBM удаляют в отходы вместе с концентратом.
В еще других вариантах осуществления, если AOI должен быть выделен из комплекса CNC-CBM-HP-AOI, где HP аффинно связан с AOI (например, представляющим собой другой белок, малую молекулу, последовательность нуклеиновой кислоты и т.д.), связь между HP и AOI расщепляют с применением подходящей химической процедуры (например, изменения рН или концентрации соли). Таким образом, например, если антитело (представляющее собой AOI) связано с белком А (представляющим собой HP), который связан с СВМ -CNC, низкое значение рН обеспечит только высвобождение антитела от белка А, но не CBD от CNC.
В некоторых вариантах осуществления СВМ представляет собой CBD, как определено в данном документе.
В соответствии с настоящим изобретением любой из этапов фильтрации в способах, описанных в данном документе, можно повторять по меньшей мере один раз (например, с использованием нескольких объемов буфера) до достижения требуемой степени чистоты.
Схематическое изображение способа согласно настоящему изобретению представлено на фиг. 1А-1Е, где, как показано на фиг. 1А неочищенную смесь, содержащую как химеру, так и загрязнители всех размеров, фильтруют, например, через мембрану с размером пор 0,2 мкм. Задерживаются только большие нерастворимые частицы, и их модно удалить в отходы после проникновения всего количества химеры. Затем фильтрат, содержащий химеру, приводят в контакт, как показано на фиг. 1В, с CNC, которую добавляют к смеси, и после короткого периода инкубации фильтруют через другую, похожую или идентичную фильтрационную мембрану, например мембрану с размером пор 0,2 мкм. Проникают только малые растворимые молекулы и загрязняющие белки, и их удаляют в отходы. Как показано на фиг. 1С, как только достигается желаемая степень чистоты, рН повышают, и CBD высвобождается от частиц NCC. Химера (например, на основе белка, представляющего интерес, POI) свободно проникает через мембрану, и ее собирают. Концентрат (теперь содержащий только NCC) удаляют в отходы.
Если требуется только чистая химера, без фрагмента, представляющего собой CBD, как показано на фиг. 1D, можно добавить подходящий протеолитический фермент. После разрыва связи между CBD и AOI/HP (например, POI) CBD остается связанным с NCC, и AOI/HP (например, POI) свободно проникает через мембрану, и его собирают. Однако, если, как показано на Фиг. 1Е, требуется комплекс NCC-CBD-HP/AOI (например, NCC-IL-2-TEV-CBD), его можно собирать непосредственно после стадии В. Таким образом, настоящее изобретение дополнительно предусматривает способ выделения HP из жидкой смеси, при этом способ включает:
- пропускание неочищенной смеси, содержащей химеру из по меньшей мере одного углеводсвязывающего модуля и по меньшей мере одного HP (химера СВМ-НР), через первую фильтрационную мембрану с получением фильтрата, содержащего химеру СВМ-НР;
- приведение химеры СВМ-НР в контакт с нанокристаллами целлюлозы (CNC) с обеспечением взаимодействия с химерой СВМ-НР с получением смеси, содержащей комплекс CBM-HP-CNC;
- пропускание смеси, содержащей комплекс CBM-HP-CNC, через вторую фильтрационную мембрану с получением концентрата, содержащего комплекс CBM-HP-CNC; и
- отделение HP и/или химеры СВМ-НР от комплекса CBM-HP-CNC;
при этом первая и вторая фильтрационные мембраны, являющиеся одинаковыми или разными, имеют размер пор, выбранный для обеспечения проникновения через них химеры СВМ-НР и предотвращения проникновения через них комплекса CBM-HP-CNC.
В некоторых вариантах осуществления способ дополнительно включает получение химеры СВМ-НР в неочищенной смеси таким образом, чтобы ее можно было выделить из нее. В некоторых вариантах осуществления неочищенная смесь дополнительно содержит по меньшей мере один другой материал, выбранный из нуклеиновых кислот, белков, углеводов, полифенолов и больших неполимерных молекул. В некоторых вариантах осуществления неочищенная смесь представляет собой гомогенат, образованный путем разрушения клеточной мембраны клеток, содержащихся в культуре клеток.
В некоторых вариантах осуществления химеру СВМ-НР продуцируют или экспрессируют в клетке-хозяине.
В некоторых вариантах осуществления химеру СВМ-НР продуцируют в растительных клетках.
В некоторых вариантах осуществления способ дополнительно включает выделение химеры СВМ-НР и/или HP. В некоторых вариантах осуществления сначала выделяют химеру СВМ-НР и впоследствии и нее выделяют HP.
В некоторых вариантах осуществления способ дополнительно включает обработку жидкой среды, содержащей по меньшей мере одно вещество, представляющее интерес (AOI), с помощью химеры СВМ-НР в условиях, обеспечивающих связывание между по меньшей мере одним AOI и химерой СВМ-НР, с получением смеси, содержащей комплекс CBM-HP-AOI.
В некоторых вариантах осуществления этот способ включает выделение AOI из комплекса CBM-HP-AOI.
В некоторых вариантах осуществления СВМ представляет собой целлюлозосвязывающий домен (CBD).
В некоторых вариантах осуществления первая и вторая фильтрационные мембраны являются одинаковыми.
В некоторых вариантах осуществления химера СВМ-НР представляет собой химеру CBD-HP.
В некоторых вариантах осуществления HP выделяют в форме, подходящей для использования в способе выделения вещества, представляющего интерес.
Настоящее изобретение, кроме того, предусматривает способ выделения вещества, представляющего интерес (AOI), из жидкой смеси, при этом способ включает:
- получение химеры СВМ-НР в соответствии со способом по настоящему изобретению;
- обработку жидкой среды, содержащей по меньшей мере одно AOI, с помощью химеры СВМ-НР в условиях, обеспечивающих связывание между по меньшей мере одним AOI и химерой СВМ-НР, с получением смеси, содержащей комплекс CBM-HP-AOI;
- добавление CNC к смеси, содержащей комплекс CBM-HP-AOI, с образованием комплекса CNC-CBM-HP-AOI;
- пропускание смеси, содержащей комплекс CNC-CBM-HP-AOI, через фильтрационную мембрану, имеющую размер пор, не допускающий проникновение комплекса CNC-CBM-HP-AOI, с получением концентрата, содержащего комплекс CNC-CBM-HP-AOI; и
- выделение AOI из комплекса.
Настоящее изобретение, кроме того, предусматривает способ выделения вещества, представляющего интерес (AOI), из жидкой смеси, при этом способ включает:
- обработку жидкой среды, содержащей по меньшей мере одно AOI, с помощью химеры СВМ-НР в условиях, обеспечивающих связывание между по меньшей мере одним AOI и химерой СВМ-НР, с получением смеси, содержащей комплекс CBM-HP-AOI;
- добавление CNC к смеси, содержащей комплекс CBM-HP-AOI, с образованием комплекса CNC-CBM-HP-AOI;
- пропускание смеси, содержащей комплекс CNC-CBM-HP-AOI, через фильтрационную мембрану, имеющую размер пор, не допускающий проникновение комплекса CNC-CBM-HP-AOI, с получением концентрата, содержащего комплекс CNC-CBM-HP-AOI; и включая
- выделение AOI из комплекса.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На следующих фигурах продемонстрированы некоторые полезные признаки настоящего изобретения. Следует подчеркнуть, что показанные данные приведены в качестве примера и в целях иллюстративного рассмотрения варианта осуществления настоящего изобретения.
На фиг. 1А-1Е представлено схематическое изображение способа выделения в соответствии с настоящим изобретением.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Если не указано иное, все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понимается специалистом обычной квалификации в области техники, к которой относится настоящее изобретение. Хотя при практическом применении или испытании настоящего изобретения можно применять любые способы и материалы, подобные или эквивалентные тем, которые описаны в данном документе, предпочтительные способы и материалы описаны ниже.
В одном из своих основных аспектов настоящее изобретение предусматривает способ получения гетерогенного белка, присутствующего в жидкой смеси, при этом способ включает:
- получение гетерогенного белка (HP), присоединенного к целлюлозосвязывающему домену (CBD), в первой неочищенной смеси;
- пропускание первой неочищенной смеси через первую фильтрационную мембрану, имеющую первое значение отсечения, составляющее от 60 кДа (UF-диапазон) до 0,45 микрон (MF-диапазон), и удаление в отходы концентрата, состоящего из крупных загрязняющих частиц, с получением фильтрата;
- добавление к фильтрату (2) частиц CNC с получением второй смеси;
- пропускание второй смеси (3) через вторую фильтрационную мембрану, характеризующуюся значением отсечения, составляющим не более 0,45 мкм, с получением тем самым очищенного гетерогенного белка, присоединенного к частицам CNC.
Гетерогенный белок (HP) может представлять собой белок, представляющий интерес, который необходимо получить в качестве конечного продукта, например рекомбинантный белок, полученный в виде химеры с белком CBD, или полученный в виде химеры с другим элементом (стрептавидином, Fc-фрагментом, антигеном и т.д.), которые могут впоследствии связываться с CBD (или связываться с CBD, присоединенным к аналогу элемента).
HP может использоваться для "вылавливания" вещества, представляющего интерес (которое может представлять собой вещество на основе аминокислоты или на основе отличного от аминокислоты соединения) из неочищенной смеси.
В соответствии с этим вторым аспектом настоящее изобретение относится к получению вещества, представляющего интерес, присутствующего в жидкой смеси, которое способно к аффинному связыванию с гетерогенным белком, при этом способ включает:
- добавление к жидкой смеси гетерогенного белка (HP), присоединенного к целлюлозосвязывающему домену (CBD), в первой неочищенной смеси;
- либо до, либо после добавления химеры CBD-HP, пропускание первой неочищенной смеси через первую фильтрационную мембрану, характеризующуюся первым значением отсечения, составляющим от 10 кДа (UF) до 0,45 микрона (MF-диапазон), и удаление в отходы концентрата, состоящего из крупных загрязняющих частиц, с получением фильтрата;
- добавление к фильтрату (2) частиц CNC с получением второй смеси;
- пропускание второй смеси (3) через вторую фильтрационную мембрану, характеризующуюся значением отсечения, составляющим не более 0,45 микрона, и получение концентрата с получением тем самым вещества, представляющего интерес.
Следует отметить, что на этапе 2 предпочтительно добавлять химеру CBD-HP после первой фильтрации, таким образом делая возможным применение мембраны с более низким значением отсечения и, следовательно, улучшая очистку.
Способ может дополнительно включать дополнительные этапы, которые известны в данной области техники, для разделения аффинно связанного вещества, представляющего интерес, и гетерогенного белка, в том числе без ограничения регулирование рН, регулирование ионной силы, добавление хаотропных или космотропных средств, мочевины, органических растворителей или детергентов, Сахаров, нуклеотидов (например, АТФ), регулирование температуры или вырезание доменов, обеспечивающих аффинное связывание. Любые добавленные материалы можно впоследствии удалять в отходы с помощью дополнительного диализа или фильтрации.
Вещество, представляющее интерес (AOI), способное к аффинному связыванию с гетерогенным белком, может представлять собой вещество на основе аминокислоты (при этом HP представляет собой антитело, рецептор, фермент, субстрат и т.п. или их фрагмент), вещество на основе нуклеиновой кислоты (и при этом HP представляет собой белок, связывающий нуклеиновую кислоту, или его фрагмент), сахар, малую органическую молекулу, представляющую собой жирную кислоту, которые содержат молекулу на основе аминокислоты (представляющую собой HP), способную к аффинному связыванию с ними.
Следующие части актуальны как в отношении первого, так и второго вариантов. Как правило, первая мембрана и вторая мембрана являются одинаковыми, при этом они характеризуются значением отсечения, составляющим 0,2 микрона.
Мембраны могут представлять собой половолоконные мембраны или мембраны для тангенциальной фильтрации.
HP либо непосредственно присоединен к CBD, например получен в виде непрерывного аминокислотной цепи рекомбинантным способом, либо связан с ним посредством другого домена или взаимодействия, например, белок A/Fc-фрагмент, стрептавидин/биотин и т.д. Также возможно связать HP с CBD посредством сайта расщепления, такого как домен TEV. В результате этого образуется химера CBD-HP.
Концентрат, полученный на этапе (4) способа по настоящему изобретению, можно дополнительно обрабатывать следующим образом.
- Если требуется весь комплекс CNC-CBD-HP, его можно просто собрать.
- Если требуемым продуктом является химера CBD-HP и CNC подлежит удалению в отходы, рН повышают приблизительно до значения 10,5-13, при этом белки быстро высвобождаются и проникают через мембрану, где собираются. Частицы CNC удаляют в отходы (поскольку их стоимость незначительна) или перерабатывают.
- Если требуется только чистый HP, в раствор добавляют подходящую протеазу, которая подвергает линкерный белок гидролизу в положении между белком CBD и белком HP, таким образом высвобождая HP от CBD, который остается связанным с NCC. Высвобожденный HP теперь способен проникать через мембрану и собирается в фильтрате, а комплекс CNC-CBD удаляют в отходы вместе с концентратом.
Отделение HP от вырезанного CBD необходимо только в очень специфическом случае, где химеру CBD-HP вырезают, и CBD высвобождается от CNC; в противном случае CBD остается связанным с CNC и его удаляют в отходы вместе с ним.
Если же химеру сначала высвобождают от CNC, а затем подвергают расщеплению, разделение можно выполнять с помощью хроматографии или других способов разделения, которые зависят от конкретных биохимических свойств белка.
Преимущество настоящего изобретения заключается в том, что оно сочетает в себе преимущества как способов мембранного разделения, так и способов хроматографического разделения: с его помощью можно обрабатывать очень большие объемы растворов с широким спектром белков и твердых частиц, обеспечивая при этом очень высокую селективность, встречающуюся только в аффинной хроматографии. Это исключает необходимость заполнения колонки и связанные с этим ограничения, такие как высокие значения давления, низкие скорости потока и забивание.
Обычно в аффинной хроматографии связывающая способность смолы для аффинной хроматографии с целевым белком составляет не более 10 миллиграммов на 1 грамм смолы. В настоящем изобретении емкость 1 г CNC достигает сотен миллиграммов на 1 грамм CNC. Кроме того, способность избирательно задерживать целевой белок в концентрате при использовании микрофильтрации является огромным преимуществом по сравнению с ультрафильтрацией, которая обычно связана с высоким давлением, относительно низкой скоростью фильтрации и проблемами засорения.
Описанный способ очистки обеспечивает быструю, экономичную и эффективную трехстадийную очистку белка с применением существующих устройств и технологий для фильтрации, как, например, для половолоконной и тангенциальной фильтрации и т.д. Способ по настоящему изобретению основан на обратимом связывании химеры, состоящей из целлюлозосвязывающего домена (CBD) и гетерогенного белка (HP), с кристаллической наноцеллюлозой (CNC) посредством части химеры, представляющей собой CBD, и с образованием таким образом больших аддуктов белок/CNC. Аддукты отделяют от загрязняющих веществ посредством фильтрации и впоследствии используются в исходном виде или химеру (CBD-HP) высвобождают от частиц CNC путем изменения рН или протеолиза, или HP отделяют от CBD с помощью различных методов расщепления или разделения, как будет объяснено ниже.
HP должны быть либо непосредственно присоединены к CBD, либо связаны с ним посредством другого домена или взаимодействия, например белок A/Fc-фрагмент, стрептавидин/биотин и т.д. Также возможно связать HP с CBD посредством сайта расщепления, такого как домен TEV. В результате этого образуется химера CBD-HP.
Гетерогенный белок (HP) может представлять собой белок, представляющий интерес, который должен быть получен в качестве конечного продукта, например рекомбинантный белок, полученный в виде химеры с белком CBD, или полученный в виде химеры с другим элементом (стрептавидин, Fc-фрагмент, антиген), которые могут впоследствии связываться с CBD (или связываться с CBD, прикрепленным к аналогу элемента).
Альтернативно, HP представляет собой белок (антитело или фрагмент, рецептор или фрагмент, субстратсвязывающий домен фермента, субстрат, ДНК-связывающий белок и т.д.), который способен к аффинному связыванию с белком, представляющим интерес, присутствующим в образце, который необходимо отделить.
Химеру CBD-HP можно получать, например, с помощью способов на основе рекомбинации и ее необходимо очищать от неочищенной смеси, в которой она была получена. В таком случае неочищенную смесь, которая содержит химеру CBD-HP и загрязняющие вещества различных типов и размеров (как растворимые, так и нерастворимые), сначала фильтруют через микрофильтрационную мембрану с размером пор 0,1-0,45 мкм, предпочтительно 0,2 мкм, предпочтительно половолоконную мембрану или мембрану для тангенциальной фильтрации. При этом значении отсечения мембрана задерживает крупные частицы и бактерии, но большинство глобулярных белков и малых молекул легко проникают через нее вместе с химерой CBD-HP. После отделения большей части CBD-HP концентрат (теперь содержащий в основном загрязнители) удаляют в отходы.
Если CBD-HP предназначен для "вылавливания" из неочищенной смеси белка, представляющего интерес (который аффинно связывается с частью химеры, представляющей собой HP), можно осуществлять те же этапы, что и выше, или альтернативно сначала неочищенную смесь фильтруют через микрофильтрационную мембрану с размером пор 0,1-0,45 мкм, предпочтительно 0,2 мкм, предпочтительно половолоконную мембрану или устройство для тангенциальной фильтрации. При этом значении отсечения мембрана задерживает крупные частицы и бактерии, кроме большинства глобулярных белков, и только после этого этапа добавляют CBD-HP.
На второй стадии добавляют CNC, CBD-HP связывает частицы CNC и образует большие аддукты, которые теперь больше, чем значение отсечения мембраны, составляющее 0,1-0,45 мкм, предпочтительно значение отсечения мембраны, составляющее 0,2 мкм, и не могут проникать через мембрану. Поэтому они задерживаются в концентрате, в то время как все другие загрязняющие малые молекулы и белки удаляются. Можно осуществлять любое количество замен объема буфера до достижения требуемой степени чистоты.
На последней стадии продукт собирают. Это можно выполнить одним из четырех способов.
В тех случаях, если HP является белком, представляющим интерес (например, продуцируется рекомбинантными методами):
5. Если требуется весь комплекс CNC-CBD-HP, его можно просто собрать.
6. Если требуемым продуктом является химера CBD-HP и CNC подлежит удалению в отходы, рН повышают до значения рН приблизительно 10,5-11, при этом белки быстро высвобождаются и проникают через мембрану, где собираются, частицы CNC удаляют в отходы (поскольку их стоимость незначительна) или перерабатывают.
7. Если требуется только чистый HP, в раствор добавляют подходящую протеазу, которая подвергает линкерный белок гидролизу в положении между белком CBD и белком HP, таким образом высвобождая HP от CBD, который остается связанным с NCC. Высвобожденный HP теперь способен проникать через мембрану и собирается в фильтрате, а комплекс CNC-CBD удаляют в отходы вместе с концентратом.
8. В случаях, если HP является аффинно связанным с другим веществом (другим белком, малой молекулой, последовательностью нуклеиновой кислоты и т.д.), которое представляет собой вещество, представляющее интерес, аффинную связь между HP и веществом, представляющим интерес, нарушают либо, в случае если HP все еще является таким, как указано в пункте (1) выше, либо отделенным, как в пунктах 2 или 3 выше, например, путем изменения рН или концентрации соли. Необходимо определить подходящие условия, при которых нарушается только аффинное связывание, без высвобождения CBD от CNC.
Кристаллическая наноцеллюлоза (CNC, как используется в настоящем документе) относится к кристаллам целлюлозы с нанометровым диапазоном размеров во всех измерениях (длина и ширина) из любого типа целлюлозы, в том числе бактериальной целлюлозы, растительной целлюлозы и т.д. В некоторых вариантах осуществления наноцеллюлозный материал отличается тем, что характеризуется степенью кристалличности по меньшей мере 50%. В других вариантах осуществления нано целлюлозный материал является монокристаллическим.
В некоторых вариантах осуществления нано целлюлозный материал, полученный из целлюлозы различного происхождения в виде частиц (например, фибрилл или в других случаях в виде кристаллического материала), выбирают так, чтобы их длина составляла по меньшей мере приблизительно 100 нм. В других вариантах осуществления их длина составляет не более чем приблизительно 1000 мкм. В других вариантах осуществления длина частиц наноцеллюлозного материала составляет от приблизительно 100 нм до 1000 мкм, от приблизительно 100 нм до 900 мкм, от приблизительно 100 нм до 600 мкм или от приблизительно 100 нм до 500 мкм.
В некоторых вариантах осуществления длина частиц CNC составляет от приблизительно 100 нм до 1000 нм, от приблизительно 100 нм до 900 нм, от приблизительно 100 нм до 800 нм, от приблизительно 100 нм до 600 нм, от приблизительно 100 нм до 500 нм, от приблизительно 100 нм до 400 нм, от приблизительно 100 нм до 300 нм или от приблизительно 100 нм до 200 нм. Толщина CNC может варьировать от приблизительно 5 нм до 100 нм.
Фибриллы CNC можно выбирать так, чтобы их значение относительного удлинения (отношение длины к диаметру) составляло 10 и более. В некоторых вариантах осуществления значение относительного удлинения составляет 67-100.
NCNC выбирают так, чтобы ее длина составляла от приблизительно 100 нм до 400 нм, а толщина от приблизительно 5 нм до 30 нм.
NCC можно применять в том виде, в котором она коммерчески доступна, или ее можно получать в соответствии с известными методами, такими как способ, описанный в WO 2012/014213 или эквивалентной ей заявке на патент США, включенных в настоящий документ посредством ссылки.
Белок с CBD
Белок с CBD может представлять собой вариант, производное, фрагмент или химическую модификацию любого из белков или белковых доменов, указанных в http://www.cazy.org/carbohydrate-binding-modules.html. при условии, что фрагмент, производное, вариант или модификация сохраняют свойства связывания CNC.
Белок с CBD по настоящему изобретению представляет собой белок, характеризующийся по меньшей мере 70% гомологией с аминокислотной последовательностью, такой как аминокислотные последовательности под вышеприведенными номерами доступа в GenBank, предпочтительно по меньшей мере 80% гомологией, более предпочтительно по меньшей мере 90% гомологией и наиболее предпочтительно по меньшей мере 95% гомологией. Термин "Х% гомология" не ограничивается последовательностями, характеризующимися Х% гомологией по всей длине белка. Выражение 70% гомология также включает Х% гомологию, наблюдающуюся в определенных функциональных областях белка с CBD под вышеуказанными номерами доступа в Genebank. Примером функциональной области может быть определенный набор аминокислот, обладающих способностью связывать целлюлозу с высокой аффинностью и обратимым образом. Такие белковые гомологи могут также упоминаться здесь как "функциональные гомологи CBD". В одном варианте осуществления настоящего изобретения такая функциональная область может содержать приблизительно 100 аминокислот. В другом варианте осуществления настоящего изобретения такая функциональная область может содержать приблизительно 50 аминокислот. Наиболее желательным белком с CBD по настоящему изобретению является белок, содержащий аминокислотную последовательность, указанную выше.
Используемый в данном документе термин "функциональное производное CBD" относится к любому "фрагменту", "варианту", "аналогу" или "химическому производному" аминокислотной последовательности белка с CBD, показанной в последовательностях Genebank, указанных выше, которые сохраняют способность связываться с целлюлозой с высокой аффинностью и обратимым образом, и его длина предпочтительно составляет от приблизительно 2 до приблизительно 160 аминокислот, более предпочтительно от приблизительно 25 до приблизительно 125 аминокислот и наиболее предпочтительно от приблизительно 50 до приблизительно 100 аминокислот.
Термин "фрагмент" используется для обозначения белка с CBD, который получен из показанного белка с CBD и имеет встречающуюся в природе последовательность. Такой фрагмент может быть получен путем протеолитического расщепления полноразмерного белка. Альтернативно, фрагмент получают с помощью рекомбинации - путем соответствующей модификации последовательности ДНК, кодирующей белок с CBD, с удалением одной или нескольких аминокислот в одном или нескольких положениях С-конца, N-конца и внутри встречающейся в природе последовательности. Фрагменты белка с CBD могут быть подвергнуты скринингу на способность связывать целлюлозу с высокой аффинностью и обратимым образом для определения идентичности или полезности функционального производного.
Используемый в данном документе термин "вариант" определяется как молекула, в которой аминокислотная последовательность, характер гликозилирования или другой признак встречающейся в природе молекулы были модифицированы ковалентным или нековалентным образом, и включает мутанты. Некоторые из вариантов, подпадающих под данное изобретение, содержат аминокислотные делеции, замены и/или вставки, при условии, что конечная конструкция обладает требуемой способностью связывать целлюлозу с высокой аффинностью и обратимым образом. Аминокислотные замены в белке с CBD можно осуществлять на основе сходства по полярности, заряду, растворимости, гидрофобности, гидрофильности и/или амфипатической природы вовлеченных остатков. Например, отрицательно заряженные аминокислоты включают аспарагиновую и глутаминовую кислоты; положительно заряженные аминокислоты включают лизин и аргинин; аминокислоты с незаряженными полярными концевыми группами или неполярными концевыми группами, характеризующиеся сходными значениями гидрофильности, включают следующие: лейцин, изолейцин, валин; глицин, аланин; аспарагин, глутамин; серии, треонин; фенилаланин, тирозин. В определение варианта также включены белки, которые содержат дополнительные аминокислоты в одном или нескольких положениях С-конца, N-конца и во встречающейся в природе последовательности CBD, при условии, что вариант сохраняет способность связывать целлюлозу с высокой аффинностью и обратимым образом.
Используемый в данном документе термин "химическое производное" относится к белку с CBD, полученному путем химической модификации встречающегося в природе белка с CBD или его варианта. Иллюстративным примером химической модификации может быть замена атома Н на алкильную, ацильную или аминогруппу.
Химера CBD-HP
Используемый в данном документе термин "химера CBD-HP" относится к объединению по меньшей мере двух белков, белка с CBD и второго белка, представляющего собой HP. В некоторых вариантах осуществления настоящего изобретения HP может быть слит с третьим белком или присоединен к нему. В настоящем изобретении примеры HP включают ферменты, такие как ферменты модификации нуклеиновых кислот, протеазы, гормоны или предшественники гормонов, полипептиды, пептиды, антитела, антигены, антигенные эпитопы и их варианты.
Для конструирования рекомбинантных экспрессионных векторов, способных экспрессировать белок с CBD или химеру CBD-HP по настоящему изобретению, можно применять нуклеиновую кислоту, кодирующую CBD. Конструкция на основе нуклеиновой кислоты способна экспрессировать белок, если она содержит нуклеотидные последовательности, содержащие транскрипционную и трансляционную регуляторную информацию, и такие последовательности являются "функционально связанными" с кодирующими нуклеотидными последовательностями. "Функционально связанный" относится к связи, в которой регуляторные последовательности ДНК и подлежащая экспрессии последовательность ДНК связаны таким образом, чтобы обеспечить транскрипцию и, в конечном итоге, трансляцию.
При конструировании экспрессионного вектора для химеры CBD-HP нуклеиновую кислоту, кодирующую белок с CBD, связывают или присоединяют к нуклеиновой кислоте, кодирующей HP, так чтобы открытая рамка считывания белка с CBD и второго белка оставались в неизменном виде, обеспечивая осуществление трансляции слитого белка с CBD. Нуклеиновую кислоту, кодирующую CBD, можно получить из различных источников, представляющих собой клетки, которые продуцируют целлюлозосвязывающие домены, которые связываются с высокой аффинностью и обратимым образом, или которые продуцируют мРНК, кодирующую CBD. Предпочтительным источником нуклеиновой кислоты, кодирующей CBD, является Clostridium cellulovorans. Нуклеиновую кислоту, кодирующую CBD, можно получить, как описано в патенте США №5856201, включенном в данный документ посредством ссылки.
Нуклеиновую кислоту, кодирующую белок с CBD по настоящему изобретению, можно получить из выделенной и очищенной ДНК из источников, представляющих собой клетки, или путем геномного клонирования. С применением методик, общеизвестных в данной области техники можно получать либо кДНК-, либо геномные библиотеки клонов, и их можно подвергать скринингу в отношении конкретной нуклеотидной кислоты, кодирующей CBD, с помощью нуклеотидных зондов, которые по существу комплементарны определенной части гена. Если требуется обнаружение белка с CBD, кодируемого консервативными нуклеотидными областями, нуклеотидные зонды должны основываться на нуклеотидных последовательностях CBD, которые сохраняются от вида к виду. Если требуется обнаружение белка с CBD, кодируемого уникальными нуклеотидными областями, нуклеотидные зонды должны основываться на уникальных нуклеотидных последовательностях CBD. Альтернативно, кДНК или геномную ДНК можно использовать в качестве матриц для ПЦР-клонирования с подходящими олигонуклеотидными праймерами. Для конструирования экспрессионных векторов можно выбрать полноразмерные клоны, т.е. клоны, содержащие всю кодирующую область требуемого белка с CBD, или можно лигировать перекрывающиеся кДНК друг с другом с образованием полной кодирующей последовательности. Альтернативно, ДНК, кодирующие CBD, можно синтезировать полностью или частично путем химического синтеза с использованием методов, считающихся стандартными в данной области техники.
Доступно много векторов, и выбор соответствующего вектора будет зависеть от различных факторов, таких как без ограничения факторы, представленные ниже: 1) будет ли он использоваться для амплификации нуклеиновых кислот или для экспрессии нуклеиновых кислот, 2) размер нуклеиновой кислоты, которая должна быть вставлена в вектор, и 3) клетка-хозяин, подлежащая трансформации вектором. Каждый вектор содержит различные компоненты в зависимости от его функции (амплификация нуклеиновой кислоты или экспрессия нуклеиновой кислоты) и клетки-хозяина с которой он совместим.
Термин "клетка-хозяин" относится к тем клеткам, которые способны расти в культуре и способны экспрессировать белок с CBD или химеру CBD-HP. Клетки-хозяева по настоящему изобретению охватывают клетки в культуре in vitro и включают клетки прокариот, эукариот и насекомых. Можно выбрать штамм клетки-хозяина, в котором обеспечивается модулирование экспрессии вставленных последовательностей или модификация и процессинг продукта гена определенным требуемым образом. Экспрессия определенных промоторов может повышаться в присутствии определенных индукторов (например, ионов цинка и кадмия в случае промоторов металлотионеина). Следовательно, экспрессия белка с CBD или слитого белка с CBD может контролироваться. Способность контролировать экспрессию будет важна, если белок с CBD или слитый белок с CBD является летальным для клетки-хозяина. Модификации (например, фосфорилирование) и процессинг (например, расщепление) белковых продуктов важны для функции белка. У различных клеток-хозяев имеются характерные и специфические механизмы для посттрансляционного процессинга и модификации белка. Для обеспечения правильной модификации и процессинга экспрессируемого белка с CBD или слитого белка с CBD можно выбирать соответствующие линии клеток или системы-хозяева. Предпочтительно клетка-хозяин должна секретировать минимальные количества протеолитических ферментов.
Другие подробности получения CBD или химеры CBD-HP можно найти в публикации заявки на патент США №5856201, включенной в настоящий документ посредством ссылки.
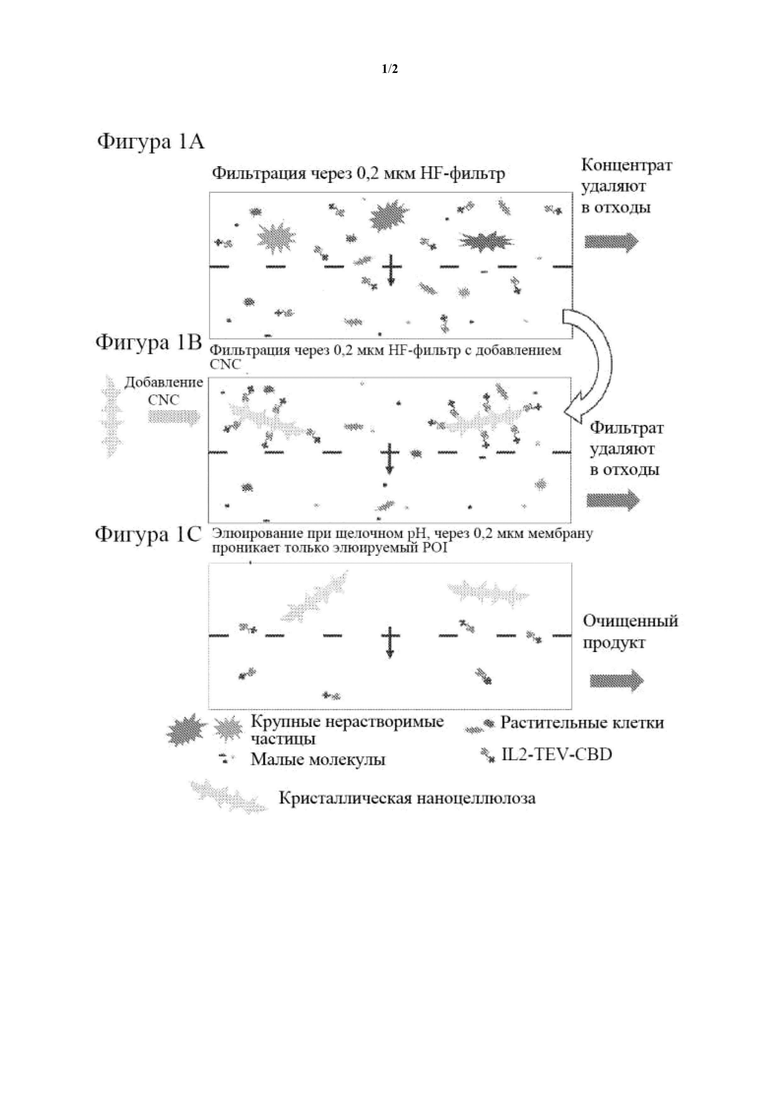

Группа изобретений относится к способам для выделения специфических веществ, представляющих интерес (AOI), таких как белки, которые необязательно присутствуют или продуцируются в культуре. Способы основаны на обратимом связывании химеры, состоящей из целлюлозосвязывающего домена (CBD) и вещества, представляющего интерес (AOI), такого как белок, например гетерологичный белок (HP), с нанокристаллами целлюлозы (CNC) для создания больших аддуктов белок/CNC, которые отделяют от загрязняющих веществ посредством фильтрации через керамическую половолоконную мембрану или полимерную половолоконную мембрану. Затем выделение AOI, например белка, может быть выделен из комплекса. Изобретения обеспечивают быстрый и эффективный трехстадийный способ очистки/выделения AOI с применением устройств и технологий для фильтрации, позволяют обрабатывать очень большие объемы растворов с широким спектром белков и твердых частиц, обеспечивая при этом очень высокую степень селективности, исключают необходимость проведения аффинной хроматографии. 3 н. и 9 з.п. ф-лы, 1 ил.
1. Способ выделения гетерологичного белка (HP) из жидкой смеси, при этом способ включает:
- пропускание неочищенной смеси, содержащей химеру из целлюлозосвязывающего домена (CBD) и по меньшей мере одного HP (химера CBD-HP), через первую фильтрационную мембрану с получением фильтрата, содержащего химеру CBD-HP, где фильтрационная мембрана представляет собой керамическую половолоконную мембрану или полимерную половолоконную мембрану;
- приведение химеры CBD-HP в контакт с нанокристаллами целлюлозы (CNC) с обеспечением взаимодействия с химерой CBD-HP с получением смеси, содержащей комплекс CBD-HP-CNC;
- пропускание смеси, содержащей комплекс CBD-HP-CNC, через вторую фильтрационную мембрану, представляющую собой керамическую половолоконную мембрану или полимерную половолоконную мембрану, с получением концентрата, содержащего комплекс CBD-HP-CNC; и
- отделение химеры CBD-HP от комплекса CBD-HP-CNC с последующим выделением из нее HP;
при этом первая и вторая фильтрационные мембраны, являющиеся одинаковыми или разными, имеют размер пор, выбранный для обеспечения проникновения через них химеры CBD-HP и предотвращения проникновения через них комплекса CBD-HP-CNC.
2. Способ по п. 1, включающий получение химеры CBD-HP в неочищенной смеси, где неочищенная смесь необязательно дополнительно содержит по меньшей мере один другой материал, выбранный из нуклеиновых кислот, белков, углеводов, полифенолов и больших неполимерных молекул.
3. Способ по п. 2, где химера CBD-HP продуцируется или экспрессируется в клетке-хозяине.
4. Способ по п. 1, дополнительно включающий обработку жидкой среды, содержащей по меньшей мере одно вещество, представляющее интерес (AOI), с помощью химеры CBD-HP в условиях, обеспечивающих связывание между по меньшей мере одним AOI и химерой CBD-HP, с получением смеси, содержащей комплекс CBD-HP-AOI.
5. Способ по п. 4, включающий выделение AOI из комплекса CBD-HP-AOI.
6. Способ выделения вещества, представляющего интерес (AOI), из жидкой смеси, при этом способ включает:
- получение химеры CBD-HP путем пропускания неочищенной смеси, содержащей химеру из CBD и по меньшей мере одного HP (химера CBD-HP), через первую фильтрационную мембрану с получением фильтрата, содержащего химеру CBD-HP, где фильтрационная мембрана представляет собой керамическую половолоконную мембрану или полимерную половолоконную мембрану;
- обработку жидкой среды, содержащей по меньшей мере одно AOI, с помощью химеры CBD-HP в условиях, обеспечивающих связывание между по меньшей мере одним AOI и химерой CBD-HP, с получением смеси, содержащей комплекс CBD-HP-AOI;
- добавление CNC к смеси, содержащей комплекс CBD-HP-AOI, с образованием комплекса CNC-CBD-HP-AOI;
- пропускание смеси, содержащей комплекс CNC-CBD-HP-AOI, через фильтрационную мембрану, представляющую собой керамическую половолоконную мембрану или полимерную половолоконную мембрану, имеющую размер пор, не допускающий проникновения комплекса CNC-CBD-HP-AOI, с получением концентрата, содержащего комплекс CNC-CBD-HP-AOI; и
- выделение AOI из комплекса.
7. Способ выделения вещества, представляющего интерес (AOI), из жидкой смеси, при этом способ включает:
- обработку жидкой среды, содержащей по меньшей мере одно AOI, с помощью химеры CBD-HP в условиях, обеспечивающих связывание между по меньшей мере одним AOI и химерой CBD-HP, с получением смеси, содержащей комплекс CBD-HP-AOI;
- добавление CNC к смеси, содержащей комплекс CBD-HP-AOI, с образованием комплекса CNC-CBD-HP-AOI;
- пропускание смеси, содержащей комплекс CNC-CBD-HP-AOI, через фильтрационную мембрану, представляющую собой керамическую половолоконную мембрану или полимерную половолоконную мембрану, имеющую размер пор, не допускающий проникновения комплекса CNC-CBD-HP-AOI, с получением концентрата, содержащего комплекс CNC-CBD-HP-AOI; и включительно
- выделение AOI из комплекса.
8. Способ по п. 6 или 7, дополнительно включающий получение среды, содержащей AOI, из которой должен быть выделен AOI.
9. Способ по п. 7, дополнительно включающий получение среды, содержащей химеру CBD-HP.
10. Способ по любому из предыдущих пунктов, где часть химеры CBD-HP, представляющую собой НР, получают в виде химеры с другим элементом, который впоследствии связывается с CBD.
11. Способ по любому из предыдущих пунктов, где в химере CBD-НР HP необязательно присоединен к CBD непосредственно.
12. Способ по п. 8, где AOI выбрано из вещества на основе аминокислоты, при этом НР представляет собой антитело, рецептор, фермент, субстрат или их фрагмент; вещества на основе нуклеиновой кислоты, при этом HP представляет собой белок, связывающий нуклеиновую кислоту, или его фрагмент; сахара, жирной кислоты или органической молекулы, содержащих пептидный фрагмент, способный к аффинному связыванию с HP.
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| US 5856201 A, 05.01.1999 | |||
| NAHALKA J., NIDETZKY B., Fusion to a pull-down domain: a novel approach of producingTrigonopsis variabilis D-amino acid oxidase as insoluble enzyme aggregates | |||
| BIOTECHNOLOGY AND BIOENGINEERING, 2007, v.97, no.3, p.454-461, DOI: 10.1002/bit.21244 | |||
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА, ШТАММ Escherichia coli, ХИМЕРНЫЙ БЕЛОК И ИХ ПРИМЕНЕНИЕ | 2010 |
|
RU2422524C1 |
Авторы
Даты
2021-12-17—Публикация
2018-03-29—Подача