Настоящее изобретение относится к конструированию и сверхсинтезу полученных методами генной инженерии полифункциональных ферментов, разрушающих клеточную оболочку растений, и к их применениям в качестве усовершенствованного ферментативного инструмента для увеличения ценности сельскохозяйственных побочных продуктов.
Сельскохозяйственные остатки являются большим возобновляемым ресурсом для биоконверсии лигноцеллюлозы. Ежедневно выработка пищевой промышленности создает большое количество таких побочных продуктов, которые считаются загрязняющими отходами и подлежат уничтожению. Проводится множество научных исследований, направленных на увеличение ценности этих побочных продуктов в биотехнологическом секторе. Среди представляющих ценность соединений феруловая кислота (4-гидрокси-3-метокси-коричная кислота) является очень привлекательным фенольным соединением, о котором известно, что это самая распространенная гидроксикоричная кислота в растительном мире. Феруловая кислота, к примеру, может быть использована как антиоксидант (23) или преобразована с помощью бактерий в «натуральный» ванилин, который является дорогостоящей добавкой в пищевой, косметической и фармацевтической промышленностях (4, 26). Среди сельскохозяйственных побочных продуктов кукурузные и пшеничные отруби являются потенциальными субстратами благодаря присутствию большого количества феруловой кислоты в их клеточной стенке - 3% и 1% (вес/вес) соответственно (43). В физиологии растений феруловая кислота является основным структурным компонентом, обладающим важными физическими и химическими свойствами клеточной оболочки растений. В частности, она может выступать в качестве сшивающего агента между лигнином и углеводородами или между самими углеводородами (16), оказывая влияние на целостность клеточной оболочки и тем самым снижая степень биологического разрушения, вызываемого микробными ферментами (6).
Микроорганизмы выработали ферменты, такие как ферулоилэстеразы (EC 3.1.1.73), способные к гидролизу эфирных связей между феруловой кислотой и полисахаридами клеточной оболочки растений. Эти ферменты улучшают доступность для других лигноцеллюлозных ферментов к полисахаридному остову (в качестве обзора см. 12). Предыдущие исследования показывают, что ферулоилэстеразы действуют синергически с разрушающими основную полисахаридную цепь ферментами, такими как β-(1,4)-эндоксиланазы, увеличивая выход феруловой кислоты из клеточных оболочек растений и образуя ее в количестве, достаточном для ряда приложений (2, 15, 50). Мицелиальные грибы, такие как Aspergillus niger, являются хорошо известными продуцентами ферментов, разрушающих клеточную оболочку растений. Два разных гена, кодирующих ферулоилэстеразы из A. niger, уже были клонированы (10, 11), а соответствующие им рекомбинантные белки сверхсинтезированы в Pichia pastoris и A. niger (24, 30, 41). Несколько ферулоилэстераз из грибов были очищены и охарактеризованы (18, 47), но других генов не было клонировано. В предыдущей работе описано получение из Penicillium funiculosum первой коричной эстеразы грибов (тип B) с С-концевым доменом, наиболее сходным с группой 1 углеводородосвязывающих модулей (Carbohydraye-Binding-Module, CBM) (27). Большое количество гликозильных гидролаз из анаэробных и аэробных микроорганизмов имеют модульную структуру. В дополнение к каталитическому домену один или более некаталитических CBM могут быть расположены либо в N-концевой области, либо в C-концевой области, либо в обеих областях. CBM были классифицированы по семействам, исходя из их аминокислотной последовательности и трехмерной структуры (http://afmb.cnrs-mrs.fr/CAZY/index.html). Основная функция CBM заключается в разрушении нерастворимого субстрата (45). Например, они ответственны за поддержание расположения каталитического домена в близости к субстрату, увеличивая продолжительность и близость их контакта. Более того, в некоторых случаях CBM может также изменять микрофибриллярую целлюлозную структуру, ослабляя водородные связи собранных вместе целлюлозных цепей (13, 14, 33).
В настоящем изобретении содержатся соображения о синергическом эффекте между отдельными и слитыми ферментами грибов (таких как A. niger), разрушающими клеточную оболочку растений. В недавнем исследовании, основанном на генно-инженерной бактериальной целлюлозоме, физическая близость двух каталитических компонентов позволяла наблюдать увеличенный синергизм в отношении эволюционно-консервативных субстратов (17). На основании этого авторы сконструировали химерный белок, связывающий грибную ферулоилэстеразу с клостридиальным докериновым доменом, который вместе с другим ферментом пересаживался на бактериальный CBM-содержащий опорный белок (31). Однако выход рекомбинантного белка был недостаточно высок для тестов приложений в промышленном масштабе, и в связи с этим была выработана новая стратегия. В этой работе авторы сделали гибрид (слитый белок) из двух грибных ферментов: ферулоилэстеразы А (FAEA) и ксиланазы B (XYNB) из A. niger, разделенных гипергликозилированным линкерным пептидом, с образованием бифункционального фермента (FLX), который обладает повышенной эффективностью выделения феруловой кислоты. Кроме того, авторы изобретения добавили также вторую конструкцию, содержащую CBM грибов из A. niger целлобиогидролазы B (CBHB) на C-концевом участке указанного бифункционального фермента (FLXLC). Оба гибридных фермента были успешно синтезированы в A. niger и полностью охарактеризованы в отношении биохимических и кинетических аспектов, а также использованы для получения феруловой кислоты из природных субстратов: кукурузных и пшеничных отрубей. Целью этой работы являлось сравнение эффективности выделения феруловой кислоты при использовании отдельных или слитых ферментов для исследования ферментативной синергии, происходящей благодаря физической близости ферментов грибов. Более того, в конструкции FLXLC был исследован эффект присоединения CBM к C-концевой части бифункционального фермента.
Настоящее изобретение основывается на демонстрации синергического эффекта от слияния в один химерный белок ферментов, разрушающих клеточную оболочку растений, в случае когда указанные ферменты не содержат СВМ, при сравнении с использованием одиночных ферментов, разрушающих клеточную оболочку растений.
Таким образом, основной целью настоящего изобретения является создание новых слитых белков, включающих не содержащие СВМ-домен ферменты, разрушающие клеточную оболочку растений.
Другая цель настоящего изобретения заключается в разработке нового способа получения представляющих интерес соединений, связанных с оболочками растительных клеток путем использования указанных слитых белков на растениях и преимущественно на сельскохозяйственных побочных продуктах, в качестве субстратов.
Настоящее изобретение относится к применению слитых белков, включающих по меньшей мере два фермента, разрушающих оболочки растительных клеток, причем указанные ферменты не содержат углеводородосвязывающей молекулы (Carbohydraye-Binding-Molecule, СВМ) в С-концевой области, и дополнительно СВМ; указанные ферменты и СВМ являются рекомбинантными белками, соответствующими нативным белкам в грибах или их мутированным формам. Слитые белки используются в процессах разрушения растительных клеточных оболочек в рамках приготовления из растений или растительных побочных продуктов, целевых соединений, содержащихся в оболочке растительной клетки, или в рамках отбеливания бумажной массы и бумаги.
Выражение «ферменты, разрушающие растительную клеточную оболочку» относится к ферментам, которые способны осуществлять расщепление компонентов клеточной оболочки, таких как целлюлоза, гемицеллюлоза и лигнин. Разрушающие оболочки растительных клеток ферменты в указанных слитых белках являются одинаковыми или отличными один от другого.
Выражение «C-концевая углеводородосвязывающая молекула» относится к молекуле, обладающей афинностью к целлюлозе, которая направляет связанный с ней фермент к целлюлозе.
Более детально, изобретение относится к определенному выше применению, в котором ферменты, разрушающие растительные клеточные оболочки и не содержащие CBM, являются гидролазами, выбираемыми из:
- целлюлаз, таких как целлобиогидролазы, эндоглюканазы и экзоглюканазы или β-глюкозидазы,
- гемицеллюлаз, таких как ксиланазы,
- лигниназ, способных разрушать лигнины, таких как лакказы, пероксидаза марганца, пероксидаза лигнина, многосторонняя пероксидаза, или вспомогательных ферментов, таких как целлобиоз дезгидрогеназы и спиртовые арил оксидазы,
- гидролаз коричных эфиров, способных выделять коричные кислоты, такие как феруловая кислота, и гидролизовать связи диферуловой кислоты между цепями гемицеллюлозы, таких как ферулоилэстеразы, коричные эстеразы и гидролазы хлорогеновой кислоты.
Более детально, изобретение касается определенного выше применения, в котором ферменты, разрушающие растительные клеточные оболочки и не содержащие CBM, выбирают из ферулоилэстераз и ксиланаз.
Более детально, изобретение относится к определенному выше применению, в котором ферменты, разрушающие растительные клеточные оболочки и не содержащие CBM, соответствуют нативным ферментам, или их мутированным формам, грибов, выбранных из:
* аскомицетов, таких как штаммы как Aspergillus, и более конкретно Aspergillus niger,
* базидиомицетов, таких как штаммы как Pycnoporus или Halociphina, и более конкретно Pycnoporus cinnabarinus, Pycnoporus sanguineus или Halociphina villosa.
Более конкретно, изобретение касается определенного выше применения, в котором ферменты, разрушающие растительные клеточные оболочки и не содержащие CBM, соответствуют нативным ферментам, или их мутированным формам, из штаммов Asperagillus, например такого, как Asperagillus niger.
Более конкретно, изобретение относится к определенному выше применению, в котором, по меньшей мере, один из ферментов, разрушающих растительные клеточные оболочки, является ферулоилэстеразой, выбранной из:
- ферулоилэстеразы А из A. niger, представленной SEQ ID NO: 2, кодируемой нуклеиновой кислотой, представленной SEQ ID NO: 1,
- ферулоилэстеразы В из A. niger, представленной SEQ ID NO: 4, кодируемой нуклеиновой кислотой, представленной SEQ ID NO: 3.
Более конкретно, изобретение относится к определенному выше применению, в котором, по меньшей мере, один из ферментов, разрушающих растительные клеточные оболочки, является ксиланазой, определенной выше, такой как ксиланаза В из A. niger, представленной SEQ ID NO: 6, кодируемой нуклеиновой кислотой, представленной SEQ ID NO: 5.
Более конкретно, изобретение касается определенного выше применения, в котором ферменты, разрушающие растительные клеточные оболочки и не содержащие СВМ, соответствуют нативным ферментам, или их мутированным формам, грибов, выбранных из аскомицетов, таких штаммов как Asperagillus, и более конкретно, Asperagillus niger.
СВМ, которые могут быть использованы в соответствии с настоящим изобретением, принадлежат к группе 1.
Более конкретно, изобретение касается определенного выше применения, в котором СВМ представляет собой СВМ, присутствующую в целлобиогидролазе В из A. niger, и представленную SEQ ID NO: 8, кодируемую нуклеиновой кислотой, представленной SEQ ID NO: 7.
Изобретение также относится к определенному выше применению слитых белков, содержащих линкеры между по меньшей мере двумя белками, содержащими указанные слитые белки, причем указанными линкерами являются полипептиды длиной от 10 до 100 аминокислот, преимущественно около 50 аминокислот.
Более конкретно, изобретение касается определенного выше применения слитых белков, в котором линкер встроен между каждым из белков, входящих в состав указанных слитых белков.
Более конкретно, изобретение касается определенного выше применения, в котором линкером является гипергликозилированный полипептид, такой как имеющий последовательность, представленную SEQ ID NO: 10, содержащуюся в целлобиогидролазе В из А. niger и кодируемый нуклеиновой кислотой, представленной SEQ ID NO: 9.
Более конкретно, изобретение также относится к определенному выше применению слитых белков между ферулоилэстеразой и ксиланазой и дополнительно СВМ.
Более конкретно, изобретение касается определенного выше применения слитых белков, включающих ферулоилэстеразу А из А. niger, представленную SEQ ID NO: 4, или ферулоилэстеразу В из А. niger, представленную SEQ ID NO: 4, и ксиланазу В из А. niger, представленную SEQ ID NO: 6.
Более конкретно, изобретение относится к определенному выше применению слитого белка, включающего ферулоилэстеразу А из А. niger, представленную SEQ ID NO: 2, и ксиланазу В из A. niger, представленную SEQ ID NO: 6, причем указанный слитый белок содержит последовательность, представленную SEQ ID NO: 10 в качестве гипергликозилированного линкера между двумя начальными белками, и представлен SEQ ID NO: 12.
Изобретение относится также к определенному выше применению слитых белков, включающих ферулоилэстеразу А из А. niger, представленную SEQ ID NO: 2, ксиланазу В из A. niger, представленную SEQ ID NO: 6, и СВМ, представленную SEQ ID NO: 8, содержащуюся в целлобиогидролазе В из А. niger.
Более конкретно, изобретение касается определенного выше применения слитого белка, включающего ферулоилэстеразу А из А. niger, представленную SEQ ID NO: 2, ксиланазу В из А. niger, представленную SEQ ID NO: 6, и СВМ, представленную SEQ ID NO: 8, причем указанный слитый белок содержит последовательность, представленную SEQ ID NO: 10 в качестве гипергликозилированного линкера между каждым из трех начальных белков, и представлен SEQ ID NO: 14.
Более конкретно, изобретение относится к определенному выше применению слитого белка, включающего ферулоилэстеразу В из А. niger, представленную SEQ ID NO: 4, и ксиланазу В из A. niger, представленную SEQ ID NO: 6, причем указанный слитый белок содержит последовательность, представленную SEQ ID NO: 10 в качестве гипергликозилированного линкера между двумя начальными белками, и представлен SEQ ID NO: 16.
Более конкретно, изобретение касается определенного выше применения слитых белков, включающих ферулоилэстеразу В из А. niger, представленную SEQ ID NO: 4, ксиланазу В из A. niger, представленную SEQ ID NO: 6, и СВМ, представленную SEQ ID NO: 8, содержащуюся в целлобиогидролазе В из А. niger.
Более конкретно, изобретение относится к определенному выше применению слитого белка, включающего ферулоилэстеразу В из А. niger, представленную SEQ ID NO: 4, ксиланазу В из А. niger, представленную SEQ ID NO: 6, и СВМ, представленную SEQ ID NO: 8, причем указанный слитый белок содержит последовательность, представленную SEQ ID NO: 10 в качестве гипергликозилированного линкера между каждым из трех начальных белков и представлен SEQ ID NO: 18.
Изобретение также относится к определенному выше применению для осуществления способов разрушения растительных клеточных оболочек в рамках получения следующих представляющих интерес соединений:
- биоэтанола,
- антиоксидантов, таких как феруловая кислота или кофейная кислота, которые относятся к коричным кислотам, и гидрокситирозол, или галлиевая кислота,
- вкусоароматических добавок, таких как ванилин или п-гидроксибензалдегид, получаемых биотрансформацией феруловой кислоты или п-кумариновой кислоты соответственно,
- или в рамках отбеливания бумажной массы и бумаги.
Изобретение также относится к определенному выше применению, в котором указанные слитые белки напрямую добавляются к растениям или растительным побочным продуктам в качестве субстрата или секретируются клетками грибов, трансформированными нуклеиновыми кислотами, кодирующими указанные слитые белки, такие как грибы, указанные выше, и в частности A. niger и Pycnoporus cinnabarinus; при этом указанные грибы находятся в прямом контакте с указанными растениями или растительными побочными продуктами в качестве субстратов.
Изобретение также касается способа разрушения растительных клеточных оболочек для получения из растений и растительных побочных продуктов целевых соединений, находящихся в оболочках растительных клеток, отличающегося тем, что он включает следующие стадии:
- ферментативную обработку растений или растительных побочных продуктов и промышленных отходов слитыми белками, определенными выше, или трансформированными клетками грибов, определенными выше,
- дополнительно физическую обработку паром растений или растительных побочных продуктов в сочетании с действием слитых белков,
- дополнительно биотрансформацию соединений, выделяющихся из клеточных оболочек в процессе вышеуказанной ферментативной обработки, с использованием соответствующих микроорганизмов или ферментов,
- выделение и, если необходимо, очистку интересующих соединений, высвобождающихся из клеточных оболочек во время указанной ферментативной обработки или полученных на указанной стадии биотрансформации.
Предпочтительно растения, обработанные слитыми белками в способе по изобретению, выбирают из сахарной свеклы, пшеницы, кукурузы, риса или из любых деревьев, используемых в бумажной промышленности.
Предпочтительно растительные побочные продукты или промышленные отходы, обработанные слитыми белками в способе по изобретению, выбирают из пшеничной соломы, кукурузных отрубей, пшеничных отрубей, рисовых отрубей, яблочных выжимок, кофейных выжимок, кофейных побочных продуктов, отработанной воды оливкового прессования.
Более конкретно, изобретение касается определенного выше способа получения антиоксидантов в качестве целевых соединений, включающего
- обработку растений или растительных побочных продуктов слитыми белками, содержащими, по меньшей мере, два из следующих разрушающих клеточную оболочку ферментов, которые не содержат CBM: ферулоилэстеразы А, ферулоилэстеразы В, гидролазы хлорогеновой кислоты, ксилоназы, в которой слитый белок предпочтительно выбирается из ферулоилэстеразы А-ксиланазы, ферулоилэстеразы В-ксиланазы, ферулоилэстеразы А-ферулоилэстеразы А-ксиланазы, гидролазы хлорогеновой кислоты - ксиланазы.
- выделение и, если необходимо, очистку антиоксидантов, высвобождающихся из клеточных оболочек указанных растений или растительных побочных продуктов.
Более конкретно, изобретение относится к способу, определенному выше, получения коричных кислот, таких как феруловая кислота в качестве интересующего антиоксиданта, в котором используемый слитый белок содержит ферулоилэстеразу и ксиланазу и может содержать CBM, как определено выше, и, в частности, выбирается из SEQ ID NO: 12, SEQ ID NO: 14, SEQ ID NO: 16 и SEQ ID NO: 18.
Преимущественно в рамках получения антиоксидантов, таких как феруловая кислота, растения, обрабатываемые вышеописанными слитыми белками, выбирают из следующей группы: сахарная свекла, пшеница, кукуруза, рис; или растительные побочные продукты или промышленные отходы, обрабатываемые вышеописанными слитыми белками, выбирают из следующей группы: пшеничная солома, кукурузные отруби, пшеничные отруби, рисовые отруби, яблочные выжимки, кофейные выжимки, кофейные побочные продукты, отработанная вода оливкового прессования.
Изобретение также относится к способу, определенному выше, получения вкусоароматических добавок в качестве целевых соединений, включающему в себя:
- обработку растений или растительных побочных продуктов слитыми белками, используемыми в рамках получения антиоксидантов, как определено выше,
- биотрансформацию соединений, выделяемых из клеточных оболочек на предшествующей стадии с помощью контакта указанных соединений с неопределенными ферментами, продуцируемыми микроорганизмами, выбранными из аскомицетов или базидиомицетов, таких как A. niger или P. Cinnabarinus соответственно,
- выделение и, если необходимо, очистку вкусоароматических добавок, полученных на предшествующей стадии биотрансформации.
Более конкретно, изобретение относится к способу, определенному выше, получения ванилина в качестве целевой вкусоароматической добавки, в котором используемый слитый белок выбирают из белков, используемых для получения феруловой кислоты как определено выше, и стадию биотрансформации осуществляют приведением в контакт ферулой кислоты, выделяемой из клеточных оболочек, с неопределенными ферментами, продуцируемыми аскомицетами или базидиомицетами, такими как A. niger или P. Cinnabarinus соответственно.
Предпочтительно растения и растительные побочные продукты или промышленные отходы, используемые в рамках получения вкусовых добавок, таких как ванилин, выбирают из тех, которые упоминались выше для получения антиоксидантов.
Изобретение также относится к способу, определенному выше, получения биоэтанола в качестве целевого соединения, включающему:
- обработку растений или растительных побочных продуктов слитыми белками, содержащими, по меньшей мере, два разрушающих растительные клеточные оболочки фермента, которые не имеют CBM, из следующей группы: целлюлазы, гемицеллюлазы, эстеразы, лакказы, пероксидазы, арилалкул оксидазы, причем слитый белок предпочтительно выбирают из эндоглюканазы-экзоглюканазы, лакказы-ксиланазы, ксиланазы-целлюлазы (эндо- или экзоглюканазы), предпочтительно, чтобы указанная обработка сочеталась с физической обработкой указанных растений или растительных побочных продуктов,
- биотрансформацию обработанных растений или растительных побочных продуктов, полученных на предыдущей стадии, в ферментируемые сахара с использованием слитых белков, описанных выше, или трансформированных грибов, секретирующих слитые белки, в сочетании с ферментами, выбираемыми из целлюлаз, гемицеллюлаз, или эстераз, или микроорганизмов, выбираемых из аскомицетов, таких как A. niger или Trichoderma reesei.
- биотрансформацию ферментируемых сахаров в биоэтанол с помощью дрожжей.
Более конкретно, изобретение относится к определенному выше способу получения ферментируемых сахаров для последующего получения биоэтанола, в котором слитый белок выбирается из эндоглюканазы-экзоглюканазы, лакказы-ксиланазы, ксиланазы-целлюлазы (эндо-или экзоглюканазы).
Преимущественно растения и растительные побочные продукты или промышленные отходы, используемые в рамках получения биоэтанола, выбирают из следующих: древесины, однолетние растения или сельскохозяйственные побочные продукты.
Изобретение также относится к способу отбеливания бумажной массы и бумаги, включающему:
- химическую и физическую обработку растений или растительных побочных продуктов в комбинации со слитыми белками, содержащими, по меньшей мере, два разрушающих растительные клеточные оболочки фермента, которые не имеют CBM, из следующей группы: ферулоилэстераза А, ферулоилэстераза В, ксиланаза, лакказа, арилалкул оксидаза, пероксидаза марганца, пероксидаза лигнина, версатиловая пероксидаза или целлобиозная дегидрогеназа.
- дополнительно размягчение обработанных растений или растительных побочных продуктов, полученных на предыдущей стадии, трансформированными грибами, секретирующими слитые белки, содержащие, по меньшей мере, два разрушающих растительные клеточные оболочки фермента, которые не имеют CBM, из следующей группы: ферулоилэстераза А, ферулоилэстераза В, ксиланаза, лакказа, арилалкул оксидаза, пероксидаза марганца, пероксидаза лигнина, версатиловая пероксидаза или целлобиозная дегидрогеназа;
- биоотбеливание обработанных растений или растительных побочных продуктов, полученных на предыдущей стадии, трансформированными грибами, секретирующими слитые белки, содержащие, по меньшей мере, два разрушающих растительные клеточные оболочки фермента, которые не имеют CBM, из следующей группы: ферулоилэстераза А, ферулоилэстераза В, ксиланаза, лакказа, арилалкул оксидаза, пероксидаза марганца, пероксидаза лигнина, версатиловая пероксидаза или целлобиозная дегидрогеназа.
Изобретение более конкретно относится к способу, описанному выше, отбеливания бумажной массы и бумаги, в котором слитый белок, используемый на первой стадии обработки растений и растительных побочных продуктов, выбирают из ферулоилэстеразы А-ксиланазы, ферулоилэстеразы В-ксиланазы, ферулоилэстеразы А-ферулоилэстеразы А-ксиланазы, ферулоилэстеразы А-ферулоилэстеразы В-ксиланазы, лакказы-ксиланазы, арилалкул ксиланазы-пероксидазы марганца; слитый белок, секретируемый трансформированными грибами и используемый на стадии биоразмягчения, выбирают из: ферулоилэстеразы А-ксиланазы, ферулоилэстеразы В-ксиланазы, ферулоилэстеразы А-ферулоилэстеразы А-ксиланазы, ферулоилэстеразы А-ферулоилэстеразы В-ксиланазы, лакказы-ксиланазы, арилалкул ксиланазы-пероксидазы марганца, сверхпродуцируемых Р. Cinnabarinus или A. niger, и слитый белок, используемый на стадии биоотбеливания, выбирают из: ферулоилэстеразы А-ксиланазы, ферулоилэстеразы В-ксиланазы, ферулоилэстеразы А-ферулоилэстеразы А-ксиланазы, ферулоилэстеразы А-ферулоилэстеразы В-ксиланазы, лакказы-ксиланазы, арилалкул ксиланазы-пероксидазы марганца.
Изобретение также относится к слитым белкам, включающим по меньшей мере два разрушающих растительные клеточные оболочки фермента, которые не содержат С-концевую углеводородосвязывающую молекулу (СВМ) и дополнительно СВМ, при этом указанные ферменты и СВМ являются рекомбинантными белками, соответствующими нативным белкам в грибах или их мутированными формами, как определено выше.
Более конкретно, изобретение относится к слитым белкам, определенным выше, включающим в себя линкеры между не менее двумя из белков, входящих в указанные слитые белки, причем эти линкеры определены выше.
Более конкретно, изобретение относится к слитым белкам, определенным выше, включающим ферулоилэстеразу и ксиланазу и дополнительно СВМ.
Изобретение более конкретно касается слитых белков, определенных выше, включающих ферулоилэстеразу А из A. niger, представленную SEQ ID NO: 2, или ферулоилэстеразу В из A. niger, представленную SEQ ID NO: 4, и ксиланазу В из A. niger, представленную SEQ ID NO: 6.
Изобретение более конкретно касается слитых белков, как определено выше, включающих ферулоилэстеразу А из А. niger, представленную SEQ ID NO: 2 и ксиланазу В из А. niger, представленную SEQ ID NO: 6, причем указанные слитые белки содержат последовательность, представленную SEQ ID NO: 10 в качестве гипергликозилированного линкера между двумя начальными белками, и представлены SEQ ID NO: 12.
Изобретение также относится к слитым белкам, как определено выше, включающим ферулоилэстеразу А из А. niger, представленную SEQ ID NO: 2, ксиланазу В из А. niger, представленную SEQ ID NO: 6, и СВМ, представленную SEQ ID NO: 8, содержащимся в целлобиогидролазе В из А. niger.
Изобретение более конкретно относится к слитым белкам, как определено выше, включающим ферулоилэстеразу А из А. niger представленную SEQ ID NO: 2 и ксиланазу В из A. niger, представленную SEQ ID NO: 6, и СВМ, представленную SEQ ID NO: 8, причем указанные составные белки содержат последовательность, представленную SEQ ID NO: 10 в качестве гипергликозилированного линкера между каждым из трех начальных белков, и представлены SEQ ID NO: 14.
Изобретение более конкретно касается слитых белков, как определено выше, включающих ферулоилэстеразу В из A. niger, представленную SEQ ID NO: 4, и ксиланазу В из А. niger, представленную SEQ ID NO: 6, причем указанные слитые белки содержат последовательность, представленную SEQ ID NO: 10 в качестве гипергликозилированного линкера между двумя начальными белками, и представлены SEQ ID NO: 16.
Изобретение также относится к слитым белкам, как определено выше, включающим ферулоилэстеразу В из А. niger, представленную SEQ ID NO: 4, ксиланазу В из А. niger, представленную SEQ ID NO: 6, и СВМ, представленную SEQ ID NO: 8, содержащуюся в целлобиогидролазе В из А. niger.
Изобретение более конкретно относится к слитому белку, как определено выше, включающему ферулоилэстеразу В из А. niger, представленную SEQ ID NO: 4 и ксиланазу В из А. niger, представленную SEQ ID NO: 6, и СВМ, представленную SEQ ID NO: 8, причем указанные слитые белки содержат последовательность, представленную SEQ ID NO: 10 в качестве гипергликозилированного линкера между каждым из трех начальных белков, и представлены SEQ ID NO: 18.
Изобретение также относится к нуклеиновым кислотам, кодирующим слитый белок, определенный выше.
Изобретение более конкретно относится к нуклеиновым кислотам, представленным SEQ ID NO: 11, 13, 15 и 17, кодирующим слитые белки, представленные SEQ ID NO: 12, 14, 16 и 18 соответственно.
Изобретение также относится к нуклеиновым кислотам, представленным SEQ ID NO: 19 и 21, соответствующим SEQ ID NO: 11 и 13, где последовательность SEQ ID NO: 1 заменена на последовательность SEQ ID NO: 23, кодирующую пре-ферулоилэстеразу А, соответствующую SEQ ID NO: 24, причем указанные нуклеиновые кислоты SEQ ID NO: 19 и 21 кодируют пре-белки слитых белков, соответствующих последовательностям SEQ ID NO: 20 и 22.
Изобретение также относится к нуклеиновым кислотам, представленным SEQ ID NO: 25 и 27, соответствующим SEQ ID NO: 15 и 17, где последовательность SEQ ID NO: 3 заменена на последовательность SEQ ID NO: 29, кодирующую пре-ферулоилэстеразу В, соответствующую SEQ ID NO: 30, причем указанные нуклеиновые кислоты SEQ ID NO: 25 и 27 кодируют пре-белки слитых белков, соответствующих последовательностям SEQ ID NO: 20 и 22.
Изобретение также относится к векторам, таким как pAN 52.3, трансформированным нуклеиновой кислотой, определенной выше.
Изобретение также относится к клеткам-хозяевам, таким как аскомицеты или базодиомицеты, и более конкретно A. niger и P. Cinnabarinus, трансформированным нуклеиновыми кислотами, определенными выше, с использованием вышеуказанных векторов.
Изобретение также относится к способу получения слитых белков, определенных выше, включая культивирование in vitro клеток хозяина, как определено выше, выделение и, если необходимо, очистку слитых белков, продуцируемых указанными клетками-хозяевами в культуре.
Изобретение также иллюстрируется следующим подробным описанием получения и свойств химерных ферментов FLX (SEQ ID NO: 12) и FLXLC (SEQ ID NO: 14).
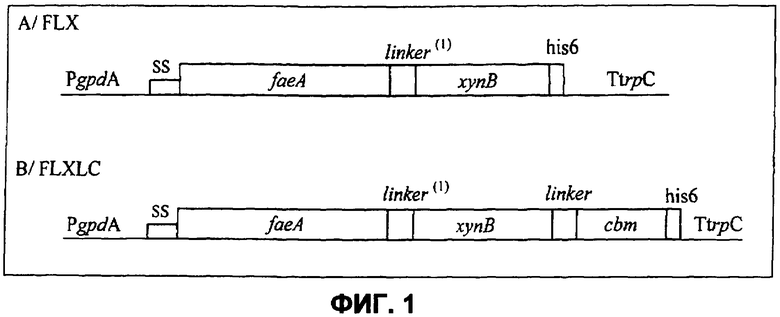
Два химерных фермента были сконструированы и успешно сверхсинтезированы в Aspergillus niger. Конструкция FLX состоит из последовательностей, кодирующих ферулоилэстеразу А (FAEA), соединенную с эндонуклеазой В (XYNB) из A. niger. С-концевой углеводород-связывающий модуль (CBM семейство 1) был присоединен к FLX, образуя второй гибридный фермент: FLXLC. Между каждым из белков был вставлен линкер для стабилизации конструкции. Гибридные белки очищались до состояния гомогенности, и была произведена оценка их молекулярных масс: 72 кДа и 97 кДа для FLX и FLXLC соответственно. Целостность гибридных ферментов проверялась иммунодетекцией, которая показала единственную форму при использовании антител к FAEA и полигистидиновой метке. Физико-химические свойства каждого каталитического модуля этих бифункциональных ферментов соответствовали свойствам отдельных ферментов. Кроме того, авторами было проверено, что FLXLC демонстрировал высокую афинность к микрокристаллической целлюлозе (Avicel) с параметрами связывания, соответствующими Kd 9,9×10-8M для константы диссоциации и 0,98 мкмоль/г целлюлозы для емкости связывания. Оба бифункциональных фермента были исследованы для определения их способности к выделению феруловой кислоты из природных субстратов: кукурузных и пшеничных отрубей. По сравнению с отдельными ферментами FAEA и XYNB был получен более высокий синергический эффект при использовании FLX и FLXLC для обоих субстратов. Более того, синергизм выделения феруловой кислоты увеличивался для FLXLC по сравнению с FLX при использовании кукурузных отрубей в качестве субстрата, подтверждая положительную роль CBM. В заключение эти результаты показывают, что образование составных бифункциональных ферментов из природных отдельных гидролаз клеточной оболочки и CBM из A. niger позволяет увеличить синергический эффект разрушения сложных субстратов.
Материалы и методы
Штаммы и культуральные среды
Штамм Escherichia coli JM109 (Promega) использовали для конструирования и культивирования векторов, в то время как A. niger штамм D15#26 (pyrg-) (22) - для продукции рекомбинантных белков. После ко-трансформации векторов, содержащих ген pyrG и экспрессионную кассету FLX или FLXLC соответственно (фиг.1), A. niger выращивался для селекции на твердой минимальной среде (без уридина), содержащей 70 мМ NaNO3, 7 мМ KCl, 11 мМ KH2HPO4, 2 мМ MgSO4, 1% глюкозы (вес/объем), и следовые элементы [1000x смесь: 76 мМ ZnSO4, 25 мМ MnCl2, 18 мМ FeSO4, 7,1 мМ CoCl2, 6,4 мМ CuSO4, 6,2 мМ Na2MoO4, 174 мМ этилендиаминтетрауксусной кислоты (ЭДТА)]. Для скрининга трансформантов на предмет продукции рекомбинантных белков в жидкой среде споры в концентрации 1×106/мл были посеяны в 100 мл культуральной среды, содержащей 70 мМ NaNO3, 7 мМ KCl, 200 мМ Na2HPO4, 2 мМ MgSO4, 6% глюкозы (вес/объем) и следовые элементы, в 500 мл колбе с перегородками. Для выделения геномной ДНК использовался штамм BRFM131 (Banque de Ressources Fongiques de Marseille), а полученная ДНК использовалась в качестве матрицы для стратегии ПЦР амплификации линкер-CBM последовательности.
Конструирование экспрессионных векторов и трансформация грибов
Слияние последовательностей, кодирующих FAEA (SEQ ID NO: 19; Y09330), XYNB (SEQ ID NO: 5; AYl 26481), и CBM (SEQ ID NO: 7; AFl 56269) из A. Niger производилось по методу ПЦР с перекрывающейся элонгацией (41), используя 5'-GGACTCATGAAGCAATTCTCTGCAAAATAC-3' (BspHl) в качестве прямого праймера и 5'-ACTGGAGTAAGTCGAGCCCCAAGTACAAGCTCCGCT-3' в качестве обратного праймера. Геномная ДНК, кодирующая линкерную область CBHB (SEQ ID NO: 9; AF156269), была получена амплификацией штамма BRFM131 A. niger с использованием прямого праймера 5'-AGCGGAGCTTGTACTTGGGGCTCGACTTACTCCAGT-3' и обратного праймера 5'-GGTCGAGCTCGGGGTCGACGCCGCCGATGTCGAACT-3'. Наконец, ген xynB был амплифицирован из кДНК (29) с использованием прямого праймера 5'-AGTTCGACATCGGCGGCGTCGACCCCGAGCTCGACC-3' и обратного праймера GGCTAAGCTTTTAGTGGTGGTGGTGGTGGTGCTGAACAGTGATGGACGAAG-S' (Hind III) (His-tag подчеркнут штриховой линией во всех последовательностях). Полученные перекрывающиеся фрагменты смешивались, и составная последовательность синтезировалась в одностадийной реакции с использованием двух внешних праймеров. Конструкция была клонирована в вектор pGEM-T (Promega), а клонированный ПЦР фрагмент проверялся секвенированием. Составной фрагмент был клонирован в NcoI-HindIII линеаризованный и дефосфорилированный pAN52.3 вектор для получения pELX плазмиды (фиг.1А). Плазмида FLXLC была сконструирована с использованием pFLX в качестве матрицы для амплификации фрагмента, кодирующего рекомбинантную последовательность FAEA-линкер-XYNB, с использованием прямого праймера 5'-GGACTCATGAAGCAATTCTCTGCAAAATAC-3' (BspHI) и обратного праймера 5'-ACTGGAGTAAGTCGAGCCCTGAACAGTGATGGACGA-3'. Геномная ДНК из штамма A. niger BRFM131 использовалась в качестве субстрата для ПЦР амплификации последовательности линкер-CBM с помощью двух специфических праймеров, сконструированных на основе имеющейся последовательности cbhB (AF156269): прямой праймер 5'-TCGTCCATCACTGTTCAGGGCTCGACTTACTCCAGT-3' и обратный праймер 5'-ATGCAAGCTTTTAGTGGTGGTGGTGGTGGTGCAAACACTGCGAGTAGTAC-3' (HindIII). Составной фрагмент был синтезирован методом ПЦР с перекрывающейся элонгацией с использованием двух внешних праймеров, проверен сиквенированием и клонирован в вектор pAN52.3 для получения вектора pFLXLC (фиг.1В). В обоих экспрессионных векторах для экспрессии рекомбинантных последовательностей использовались промотор гена глицеральдегид-3-фосфат дегидрогеназы (gpdA) A. nidulans, 5' нетранслируемая область мРНК гена gpdA и терминатор trpC A. nidulans. Кроме того, для таргетирования секреции обоих рекомбинантных белков использовался сигнальный пептид (21 аминокислота) из FAEA.
Обе ко-трансформации грибов производились, как описано авторами Punt и van den Hondel (39), с использованием экспрессионных векторов pFLX и pFLXLC соответственно и pAB4-1 (48), содержащим маркер селекции pyrG, в отношении 10:1. Кроме того, штамм D15#26 A. niger был трансформирован геном pyrG без экспрессионного вектора для контрольного эксперимента. Селекция ко-трансформантов на уридиновую прототрофийность проводилась на чашках с селективной минимальной средой (без уридина), которые инкубировались 8 дней при температуре 30°С. Для скрининга трансформантов культивировались и ежедневно проверялись 40 индивидуальных клонов из каждой трансформации.
Скрининг активностей ферулоилэстеразы и ксиланазы
Наблюдения за культурами производились в течение 14 дней при 30°С в инкубаторе со встряхиванием (130 об/мин). pH ежедневно подводился до 5,5 с помощью 1М раствора лимонной кислоты. Каждые культуральные условия повторялись дважды. Ежедневно из жидкой культуральной среды отбирались аликвоты (1 мл), из которых мицелий убирался фильтрацией. Активность эстеразы измерялась так, как описано выше с использованием метилферулата (МФА) в качестве субстрата (40), в то время как активность ксиланазы определялась по количеству ксилозы, выделяемой из 1% (вес/объем) ксилана березовой древесины, по методу, предложенному Bailey et al (1). Ферменты инкубировались с раствором ксилана [1% (вес/объем) раствор ксилана березовой древесины, 50 мМ буфер цитрата натрия pH 5,5] при 45°С в течение 5 мин. Выделенные восстанавливающие сахара определялись по методу DNS, используя ксилозу в качестве стандарта (35). Все анализы проводились с использованием контрольных образцов для учета поправок на фон в образцах фермента и субстрата.
Активность выражалась в нкатал (nkat) единицах; 1 nkat определялся как количество фермента, которое катализирует выделение 1 нмол феруловых кислот или 1 нмол восстанавливающих сахаров в секунду при установленных условиях. Каждый эксперимент повторялся дважды, а измерения - трижды, причем стандартная девиация составляла менее 2% от среднего значения активности эстеразы и менее 5% от активности ксиланазы.
Очистка рекомбинантных белков
Наилучшее выделение для каждого из конструктов засевалось, используя те же условия, что и в процедуре скрининга. Культура собиралась после 8 дней роста, фильтровалась (0,7 микрон) и концентрировалась ультрацентрифугированием через полиэтерсульфоновую мембрану (граница по молекулярной массе составляла 30 кДа) (Millipore). Сконцентрированные фракции подвергались диализу против 30 мМ Tris-HCl, pH 7,0 (буфер связывания) и выделение белков с His-тагом производилось на Хелирующей Сефарозной колонке быстрового потока (13×15 см) (Amersham Biosciences) (38). Что касается одиночных белков, рекомбинантная ксиланаза В, которая содержит фрагмент His-тага, также очищалась на Хелирующей Сефарозной колонке быстрого потока, как было описано (29). Наконец, рекомбинантный белок FAEA очищался по одностадийной процедуре, с использованием фенил-сефарозной колонки, как было описано (41).
Характеристика рекомбинантных белков
Белковый анализ и определение N-концевого аминокислотного сиквенса. Концентрация белка определялась по методу Лоури (34) с использованием бычьего сывороточного альбумина в качестве стандарта. Наработка и очистка белка контролировались с помощью окраски Кумасси SDS-PAGE полиакриламидных (11% полиакриламида) гелей. Определение N-концевого сиквенса производилось по методу деградации Эдмана после электроблоттинга образцов FLX и FLXLC (100 мкг) на мембрану из поливинилидин дифторида (Millipore). Анализы производились на установке Applied Biosystem 470A.
Анализ вестерн блоттинга. После электрофореза суммарного и очищенного белков в 11% SDS-PAGE полиакриламидном геле по методу Лаеммли (28) производился электроблоттинг белков на BA85 нитроцеллюлозные мембраны (Schleicher and Schuell) при комнатной температуре в течение 45 мин. Мембраны инкубировались в блокирующем растворе (50 мМ Tris, 150 мМ NaCl и 2% (об/об) молока pH 7,5) в течение ночи при 4°С. После этого мембраны отмывались в растворе TBS-0,2% tween и обрабатывались блокирующим раствором, содержащим анти-FAEA сыворотку в разбавлении 1/8000 или сыворотку антиполигистидин-пероксидазы (Sigma). В случае анти-FAEA антител мембраны затем инкубировались с анти-кроличьим иммуноглобулином G козы, конъюгированным с пероксидазой хрена (Promega). Детектирование сигналов производилось с использованием хемилюменисцентного набора для Вестерн блоттинга (Roche) в соответствии с рекомендованной производителем процедурой.
Температурная и pH стабильности рекомбинантных белков. Термостабильность очищенных рекомбинантных белков тестировалась в интервале от 30° до 70°С. Аликвоты пре-инкубировались при указанной температуре, а также после охлаждения до 0°С, активности эстеразы и ксиланазы тестировались так, как указано выше при стандартных условиях. После инкубации производился анализ образцов на SDS-PAGE полиакриламидном геле с целью проверки целостности бифункциональных белков. Влияние pH на стабильность белков исследовалось инкубацией очищенных рекомбинантных белков в цитрат-фосфатном буфере (pH 2,5-7,0) и фосфате натрия (pH 7,0-8,0). Все инкубации производились в течение 90 мин, после которых аликвоты переносились в стандартную реакционную смесь для определения величины остаточной активности. Активность, определенная до пре-инкубации, считалась 100% активностью.
Влияние температуры и pH на активности эстеразы и ксиланазы. Для определения оптимальной температуры при используемых условиях аликвоты рекомбинантных белков инкубировались при различных температурах (от 30° до 70°С) и определялись активности эстеразы и ксиланазы. Оптимальный pH определялся с использованием цитрат-фосфатного буфера (pH 2,5-7,0) и натрий-фосфатного буфера (pH 7,0-8,0) при стандартных условиях.
Определение целлюлозо-связывающей емкости и констант диссоциации. Образцы очищенных FLX и FLXLC добавлялись в 2-мл центрифужные пробирки, содержащие целлюлозу в 25 мМ калий фосфатном буфере (pH 7), до общего объема 2 мл. Способность FLX (контроля) и FLXLC к связыванию Avicel PH101 целлюлозы (Fluka) определялась с использованием различных количеств рекомбинантных белков (от 30 до 170 мкг) и постоянного количества целлюлозы (2 мг). Оба рекомбинантных белка инкубировались с целлюлозой 1 час при 4°С при слабом покачивании. После центрифугирования (4000g, 10 мин) определялось количество оставшихся белков в супернатанте (несвязавшийся фермент). Количество фермента, связанного с целлюлозой, рассчитывалось вычитанием величины несвязавшегося FLX или FLXLC из общего количества добавленного фермента. Анализ результатов производился с помощью построения двойной-обратной зависимости (1/(связанный фермент) от 1/(несвязавшийся фермент)). Константа диссоциации определяется как 1/B=(Kd/Bmax × 1/F)+1/Bmax, где B - концентрация связавшегося фермента и F - концентрация свободного фермента (21, 37).
Тесты приложения
Ферментативный гидролиз. Пшеничные отруби (ПО) и кукурузные отруби (КО) обескрахмаливали. Эти субстраты затем подвергали термической обработке при 130°С в течение 10 мин. Ферментативный гидролиз производили в 0,1M буфере 3-N-морфолинопропансульфокислоты (MOPS), содержащем 0,01% азида натрия при pH 6,0 в термостатически контролируемом инкубаторе со всряхиванием при 40°С. ПО или КО (200 мг) инкубировались с очищенными FAEA (SEQ E) NO: 2), XYNB (SEQ ID NO: 6), FAEA+XYNB, FLX и FLXLC независимо, в конечном объеме 5 мл. Концентрации очищенного фермента для отдельных и бифункциональных ферментов были следующими: 11 нкатал активности эстеразы и 6496 нкатал активности ксиланазы на 200 мг сухих отрубей для каждого анализа. Это отношение соответствует моляр-молярному отношению, определенному для очищенного бифункционального фермента. Каждый анализ производили дважды, а стандартное отклонение составляло менее 5% от среднего значения для ПО и КО.
Получение щелочь-экстрагируемой гидроксикоричной кислоты. Общее содержание щелочь-экстрагируемой гидроксикоричной кислоты определяли путем добавления 20 мг ПО или КО к 2н NaOH и инкубацией в течение 30 мин при 35°С в темноте. pH доводили до 2 с помощью 2н HCl. Фенольные кислоты экстрагировали три раза с помощью 3 мл эфира. Органическую фазу переносили в пробирку для анализа и высушивали при 40°С. Затем к сухому экстракту добавляли один миллилитр раствора метанола с водой (50:50) (об/об) и образцы вносили в ВЭЖХ систему так, как описано в следующем разделе. Общее содержание щелочь-экстрагируемой феруловой кислоты принимали за 100% для ферментативного анализа.
Определение феруловой кислоты. Ферментативные гидролизаты разбавляли наполовину 100% метанолом, центрифугировали при 12000g 5 мин и супернатанты фильтровали через 0,2 мкм нейлоновый фильтр (Gelman Sciences, Acrodisc 13, Ann Arbor, MI). Затем фильтраты анализировали на ВЭЖХ (25 мкл на нанесение). ВЭЖХ анализ производили при 280 нм и 30°С на установке модели HP1100 (Hewlett-Packard Rockville, MD), снабженной изменяемым UV/VIS детектором и автоматическим образец-инжектором на 100 образцов. Разделения осуществляли на колонке обратной фазы Merck RP-18 (Chromolith 3,5 мкм 4,6×100 мм, Merck). Скорость потока составляла 1,4 мл/мин. В качестве подвижной фазы использовали 1% уксусную кислоту и 10% ацетонитрил в воде (А) против ацетонитрила 100% (В) при общем времени работы 20 мин, при этом градиент изменялся следующим образом: сольвент В начинался от 0% в течение 2 мин, затем увеличивался до 50% за 10 мин, до 100% за 3 мин до окончания процесса. Результаты обрабатывали на HP 3365 ChemStation и количественный анализ производили при помощи внешней стандартной калибровки.
РЕЗУЛЬТАТЫ
Дизайн и исследование наработки бифункциональных ферментов
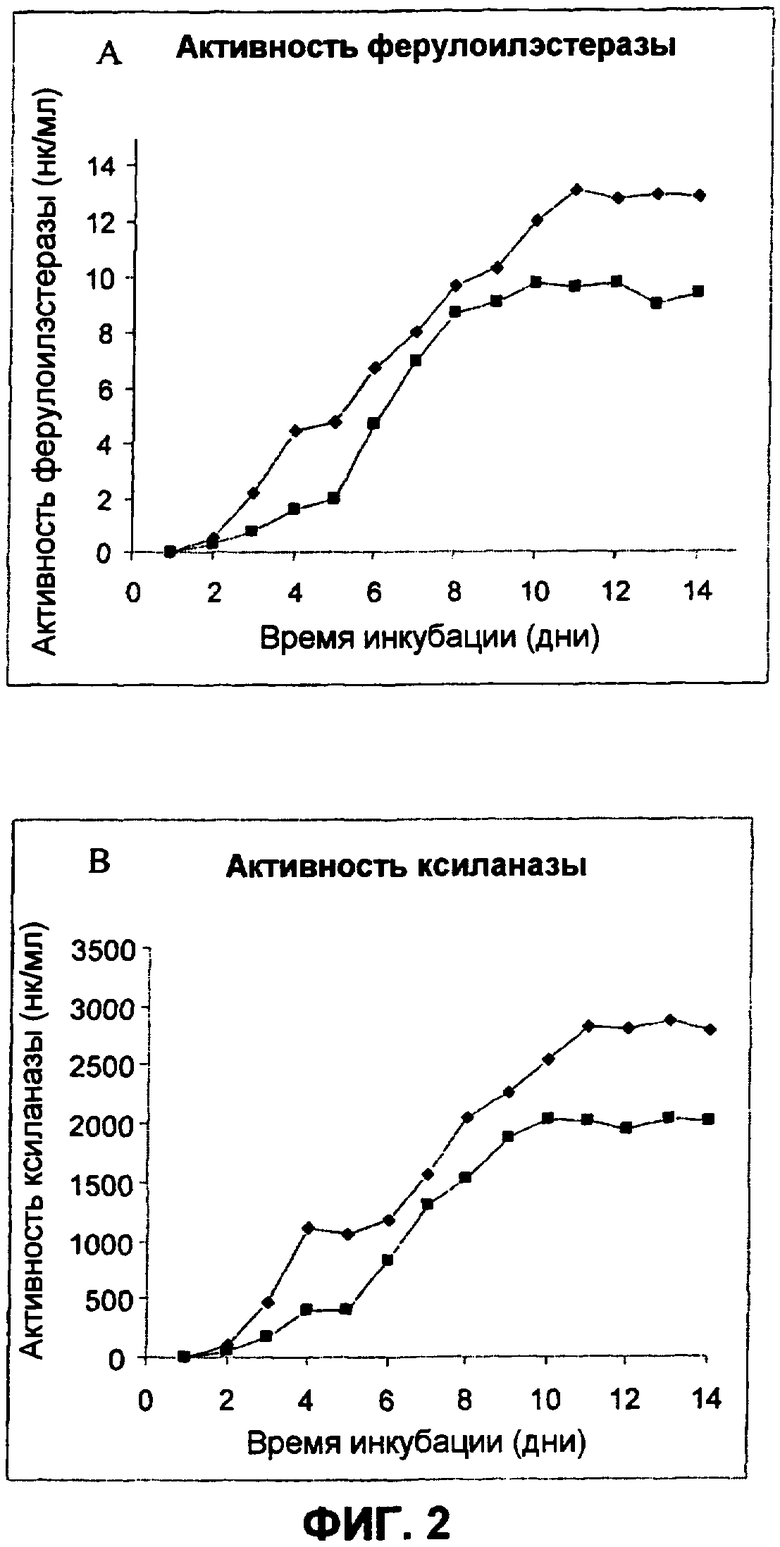
Последовательности из A. niger, кодирующие ферулоилэстеразу А (FAEA) и ксиланазу В (XYNB), были генетически слиты добавлением между двумя белками последовательности из гена целлобиогидролазы В (cbhB), кодирующей гипергликозилированный линкер (фиг.1А). Для получения второй конструкции FLXLC соответствующий слитый FLX был дополнительно слит с частичной последовательностью гена cbhB из A. niger, кодирующей линкер-CBM (фиг.1В). Оба транслируемых составных белка были помещены под контроль сильного конститутивного промотора gpdA и trpC терминатора с эндогенной сигнальной последовательностью faeA для таргетирования секреции. Протопласты A. niger D15#26 были ко-трансформированы смесью экспрессионного вектора pFLX или pFLXLC и плазмиды pAB4-1, содержащей ген pyrG. Селекция трансформантов производилась по их росту на чашке с минимальной средой без уридина. 40 трансформантов для каждой конструкции засевались в среду с минимальной глюкозой, подавляющей эндогенную экспрессию генов faeA и xynB. Для контрольных клеток-хозяев, трансформированных pAB4-1, активность эстеразы или ксиланазы не была обнаружена. Для обеих конструкций активности эстеразы и ксиланазы детектировались во внеклеточной среде трансформантов после 2 дней роста (фиг.2). Активности ферулоилэстеразы и ксиланазы определялись как синхронные во время роста в культуре. Активности увеличивались вплоть до 10 дня и до 11 дня для лучших трансформантов FLXLC и FLX соответственно и достигали уровня, который оставался более-менее стабильным до 14 дня. Максимальная активность эстеразы составляла 13,0 нкат/мл для FLX и 9,8 нкат/мл для FLXLC трансформантов. Максимальные полученные значения для активности ксиланазы составляли 2870 нкат/мл для FLX и 2038 нкат/мл для FLXLC трансформаций. Принимая во внимание соответствующую удельную активность партнера FAEA в бифункциональных ферментах, выход продукта оценивался как 1,4 г/л и 1,5 г/л для FLX и FLXLC трансформантов, соответственно.
Биохимические и кинетические характеристики бифункциональных ферментов
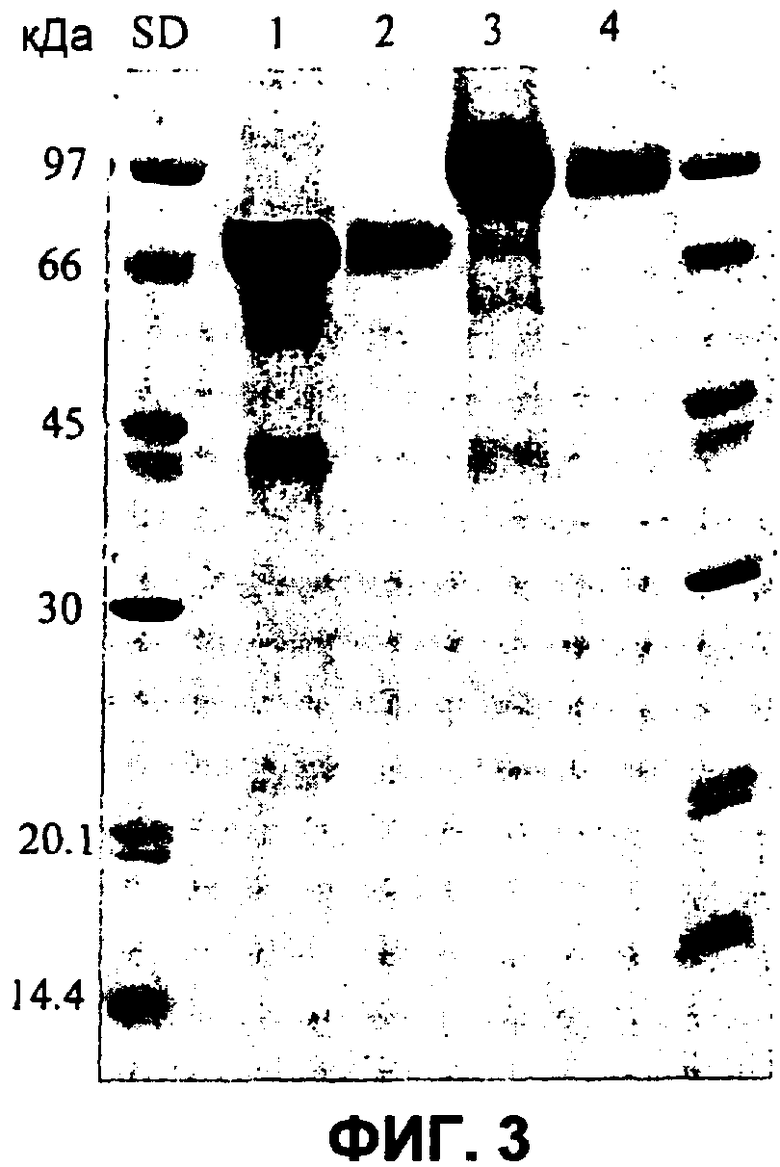
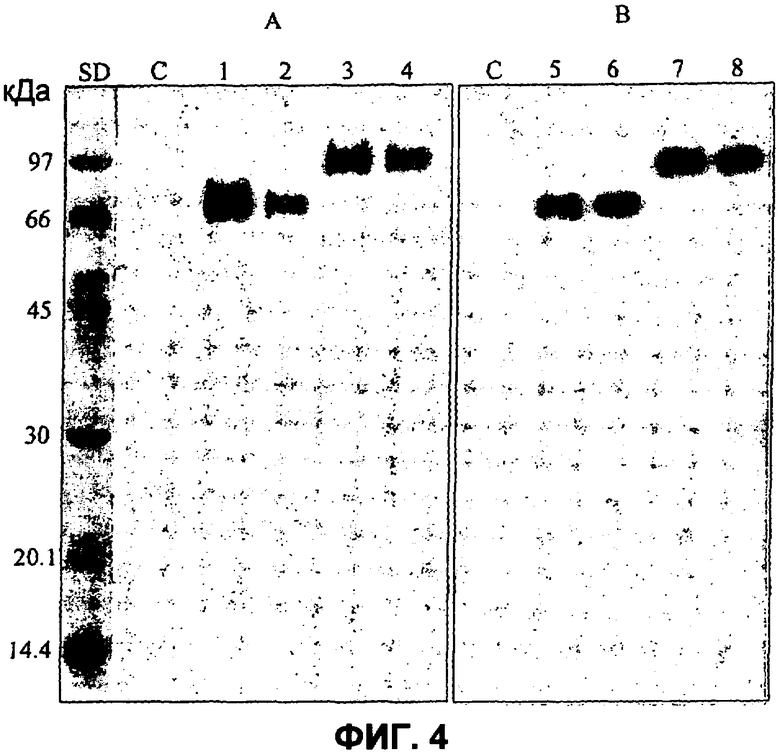
SDS-PAGE электрофорез и анализ Вестерн блоттинга. В обоих случаях полученные белки контролировались с помощью электрофореза на SDS-PAGE полиакриламидном геле (фиг.3, дорожки 1 и 3). Наиболее интенсивные полосы около 72 кДа и 97 кДа, наблюдаемые среди суммарных внеклеточных белков, соответствовали FLX и FLXLC трансформантам соответственно. Разница между наблюдаемыми и теоретическими молекулярными массами FLX и FLXLC предположительно говорит о гликозилировании около 12% (вес/вес) и 26% (вес/вес) соответственно. Рекомбинантные ферменты очищались на колонке Хелирующей Сефарозы Быстрого Потока (Chelating Sepharose Fast Flow), а гомогенность фракций контролировалась с помощью SDS-PAGE электрофореза (дорожки 2 и 4).
Оба химерных фермента из супернатантов суммарных белков и очищенных фракций иммунодетектировались с использованием антител к FAEA (фиг.4А). Единственная полоса проявлялась из суммарного белкового экстракта (дорожки 1, 3) и из очищенных образцов (дорожки 2, 4) для FLX и FLXLC трансформантов соответственно. Для иммунодетекции использовались также антитела к C-концевой гистидиновой метке для контроля целостности рекомбинантных белков, поскольку антитела к ксиланазе или CBM были недоступны (фиг.4В). В этом случае также для FLX и FLXLC детектировалась единственная полоса, подтверждая, что бифункциональные ферменты были получены как интактные белки без каких-нибудь форм деградации (дорожки 5 и 8). Отрицательный контроль (С) подтверждал, что оба антитела являлись специфичными к эпитопу и что эндогенный FAEA не образовывался при данных условиях культивирования.
N-концевое сиквенирование. Первые пять аминокислот FLX и FLXLC были сиквенированы (ASTQG) и сравнены с аминокислотами из нативного FAEA. Сравнение показало 100% идентичность между рекомбинантными белками и нативным FAEA. Эти результаты подтвердили, что FLX и FLXLC были процессированы корректно.
Анализ афинности бифункциональных белков к целлюлозе и способности к связыванию. В противоположность FLX, FLXLC содержит в C-концевой области CBM из гена целлобиогидролазы В (cellobiohydrolase B) A. niger. Осуществляли анализ взаимодействия FLXLC с целлюлозой для определения параметров связывания CBM. Афинность связывания с целлюлозой и емкость связывания FLXLC были определены в отношении микрокристаллической целлюлозы Avicel PH101. Полученные значения для константы диссоциации и емкости связывания составляли 9,9×10-8М и 0,98 мкмол/г Avicel соответственно. Как и предполагалось, взаимодействия для химерного фермента FLX (без CBM) не наблюдалось.
Биохимические и кинетические параметры. Для контроля того, не изменились ли характеристики каждого фермента в результате соединения двух ферментативных партнеров в присутствии или в отсутствие CBM, биохимические и кинетические параметры FLX FLXLC сравнивались с таковыми для свободных рекомбинантных FLX и FLXLC в соответствии с активностями эстеразы и ксиланазы (таблица 1). В отношении оптимального pH и стабильности не было обнаружено существенных различий между обоими бифункциональными ферментами и отдельными FLX и FLXLC. В отношении оптимальной температуры и стабильности единственное различие касалось небольшого сдвига для активности ксиланазы. Кроме того, целостность FLX и FLXLC контролировалась с помощью SDS-PAGE электрофореза после их инкубации при различных температурах. Оба бифункционльных фермента были полностью стабильными вплоть до 45°С и частично расщеплялись при 50°С. Начальные аминокислоты расщепленной формы были сиквенированы и оказались следующими: GSGSS. Сравнение сиквенса FLX и FLXLC показавает 100% идентичность с сиквенсом в линкере. Эти результаты показали, что гипергликозилированный линкер является стабильным до 45°С и что расщепление происходит при 50°С в области после GSGSS сиквенса. Химерный белок FLXLC, содержащий две линкерные последовательности, расщеплялся только в C-концевом линкере (между FLX и FLXLC). Был произведен поиск возможного места протеазного расщепления в аминокислотных последовательностях обоих гибридных белков с помощью программы пептидного разрезания (19), однако такого места расщепления в области сиквенса GSGSS обнаружено не было.
В отношении кинетических характеристик измерялись константы Михаэлиса для FLX и FLXLC по графику Лайнуивера-Берка с использованием метилферулата и ксилана березовой древесины в качестве субстратов. Значения, найденные для FLX и FLXLC, находились в соответствии со значениями, найденными для рекомбинантных FAEA и XYNB в отдельности (таблица 1). Удельные активности бифункциональных ферментов были определены, исходя из активностей ферулоилэстеразы и ксиланазы, и сравнены со значениями для FAEA и XYNB в отдельности (таблица 1). Значения, найденные для бифункциональных ферментов, были близки к значениям для FAE и XYNB в отдельности.
В заключение эти результаты подтвердили, что биохимические и кинетические параметры для составных ферментативных модулей (FAEA и XYNB) в основном сохранялись в бифункциональных комплексах FLX и FLXLC.
Ферментативное выделение феруловой кислоты из пшеничных и кукурузных отрубей
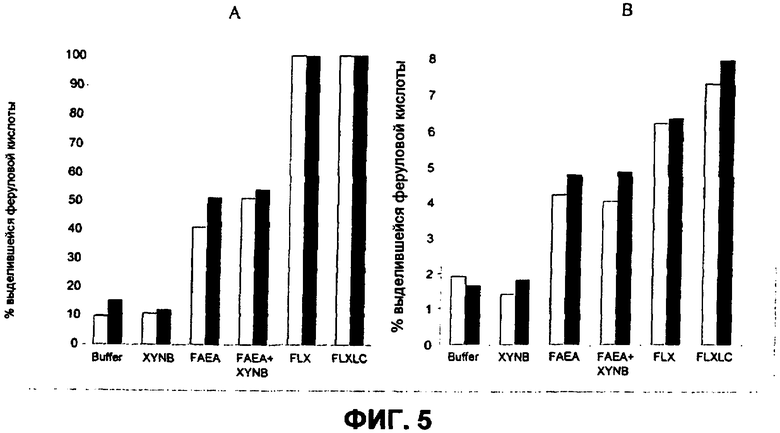
Для изучения синергического эффекта, вызванного физической близостью двух ферментов в бифункциональных белках, и влияния добавления CBM белки FLX и FLXLC сравнивались с одиночными ферментами FAEA и XYNB в отношении эффективности выделения феруловой кислоты. Все ферменты очищались до состояния гомогенности и инкубировались с ПО и КО, так как последние содержат большое количество феруловой кислоты в свих клеточных оболочках. В случае отдельного FAEA 41% и 51% суммарной щелочь-экстрагируемой феруловой кислоты выделялось из ПО за 4 и 16 часов соответственно (фиг.5А). Эти величины немного увеличивались до 51% (4 ч) и 54% (16 ч) при добавлении XYNB в отдельности. Что касается эффекта FLX и FLXLC наблюдалось полное выделение феруловой кислоты всего за 4 ч инкубации. С использованием КО в качестве субстрата (фиг.5В) свободный FAEA высвобождал 4,2% и 4,8% феруловой кислоты за 4 ч и 16 ч соответственно, и добавление XYNB не увеличивало эту величину. В то же время FLX и FLXLC были в состоянии высвобождать 6,2% и 7,2% за 4 ч гидролиза соответственно. Если ферментативная обработка производилась в течение 16 ч, выход увеличивался до 6,3% и 7,9% для FLX и FLXLC соответственно. Были также определены и сравнены факторы синергизма между одиночными (FAEA + XYNB) и составными ферментами (FLX и FLXLC). Как рассчитано в таблице 2, расчетное отношение было больше 1, показывая, что для обоих субстратов синергический эффект является более высоким для бифункциональных ферментов, чем для соответствующих одиночных ферментов. Относительно выделения феруловой кислоты из КО более высокая синергия наблюдалась для FLXLC (1,80 и 1,62), чем для FLX (1,53 и 1,30) за 4 ч и 16 ч соответственно. В заключение данные результаты показали, что для обоих субстратов бифункциональные ферменты FLX и FLXLC являлись более эффективными для выделения феруловой кислоты по сравнению с соответствующими ферментами в отдельности (FAEA + XYNB). Кроме того, из этих результатов можно заключить, что FLXLC является более подходящим для выделения феруловой кислоты при использовании КО в качестве субстрата, что говорит о возможном положительном эффекте, производимом CBM.
Заключение
Для биоразрушения клеточной оболочки растений из-за их гетерогенности по составу и структуре требуется большое количество различных ферментов. Определенные сочетания различных гидролитических ферментов основной цепи со вспомогательными ферментами показали важный синергический эффект, приводящий к эффективному разрушению клеточной оболочки (9, 12). В этом исследовании два фермента, разрушающие клеточную оболочку растений, и углеводородо-связывающий модуль из A. niger были слиты в гибридную молекулу для исследования синергического эффекта в процессе разрушения природных субстратов. Конструирование подобных гибридных белков является одним из основных аспектов белкового инжиниринга, дающим возможность большому количеству приложений. В данном случае концепция заключается в использовании двух функциональных единиц для образования усовершенствованных бифункциональных белков (3, 36). Подобные многомодульные структуры можно часто наблюдать в природе, которые образуют ферменты с более чем одной ферментативной активностью или белковой функцией. В области биотехнологии некоторые белки уже были исследованы, включая, например такие, как гибрид между α-амилазой и глюкоамилазой (44). Результаты данного исследования показывают увеличение ферментативной эффективности по сравнению с отдельными ферментами в процессе разрушения необработанного крахмала. В другой работе была сконструирована химерная ксиланаза/эндоглюканаза (XynCenA) c внутренним CBM, но дальнейшие результаты показали, что эффект гидролиза гибридного фермента в отношении гомогенных ксиланов или целлюлозных субстратов был незначительным по сравнению с одиночным ферментом, однако тесты приложения на природных субстратах проведены не были (46).
Для оценки эффекта, возникающего благодаря физической близости двух гидролаз клеточных оболочек, FAEA и XYNB были слиты вместе (конструкция FLX). Во второй конструкции (FLXLC) для таргетирования бифункционального фермента к целлюлозе в C-концевой области был присоединен CBM грибов из A. niger CBHB. Для обеих конструкций гипергликозилированный линкерный пептид был вставлен между каждой молекулой (FAEA, XYNB или CBM) по трем основным причинам. Во-первых, известно, что линкер оставляет возможность для модулей независимо образовывать третичную структуру и сохранять конформационную свободу относительно друг друга (36). В данном случае как ферулоилэстераза, так и ксиланаза были способны принимать эту конформацию, и сконструированные бифункциональные белки являлись активными с биохимическими и кинетическими свойствами, соответствующими отдельным ферментам. Во-вторых, высокая степень гликозилирования линкера позволяет увеличивать стабильность последовательности белков, предохраняя линкер от протеазной активности и, наконец, избегая частой проблемы, связанной с расщеплением между составными модулями (8, 36). Такой эффект действительно наблюдался, так как оба бифункциональных белка были стабильными, как показано на SDS-PAGE электрофорезе и Вестерн блоттинг анализе. В то же время было показано, что стабильность гибридных ферментов имеет определенные границы при термической обработке. В самом деле, влияние термической обработки на целостность FLX и FLXLC показало, что они оставались стабильными до 45°С, а затем расщеплялись в области линкера при 50°С. Наконец, гликозилированный линкер может играть положительную роль в секреции, увеличивая выход продукта, как показано для гипергликозилированного линкера из A. niger гликоамилазы (32). В самом деле, сайты гликозилирования благодаря присутствию одного или двух линкеров для FLX и FLXLC соответственно могли увеличивать время нахождения рекомбинантных белков в эндоплазматическом ретикулуме, добавляя время для образования правильной третичной структуры и приводя к увеличению продукции (42). Эта последняя гипотеза могла бы объяснить, почему выход продукта для обоих бифункциональных ферментов был выше, чем выход, полученный для соответствующих отдельных рекомбинантных ферментов (29, 41).
С целью изучения синергического эффекта, возникающего из-за близости обоих ферментативных модулей, а не простого увеличения из-за модификации ферментативных свойств как результата изменения белковой конформации во время образования третичной структуры, биохимические и кинетические характеристики каждого модуля были тщательно исследованы. Все основные биохимические и кинетические свойства обоих бифункиональных белков FLX и FLXLC, т.е. температурная и pH стабильности, оптимальная температура и pH, Km и удельная активность находились в тех же пределах, как и для отдельных ферментов. Относительно CBM, взятого из A. niger CBHB, анализы связывания производились на целлюлозе, так как она не была охарактеризована в прошлом (20). Avicel целлюлоза обладает важной степенью полимеризации, характеризуемой 100-250 гликопиранозными единицами и 50-60% кристаллической формы с кристаллической фазой, составленной главным образом из типа Iβ, характерной для высших растений (49). Результаты показали, что FLXLC обладает афинностью к Avicel, подтверждая, что структура CBM не изменена и что CBM сохранил свои функции в гибридном ферменте.
Наконец, оба бифункциональных белка были проанализированы для изучения эффекта физической близости двух комплементарных ферментов грибов на ферментативную синергию и влияние добавления CBM. Тест приложения был основан на выделении феруловой кислоты из двух природных и модельных субстратов, ПО и КО, известных своим высоким содержанием феруловой кислоты в своих растительных клеточных оболочках - около 1% и 3% (вес/вес) соответственно (43). Оба субстрата были получены из сельского хозяйства и могут иметь ценность в сельскохозяйственной промышленности, косметическом и фармацевтическом секторах (4, 26). Отдельные ферменты были способны высвобождать 54% и 4,8% феруловой кислоты из ПО и КО соответственно. В отличие от этого бифукциональные ферменты эффективно высвобождали всю феруловую кислоту из ПО и до 6,3% или 7,9% из КО в зависимости от присутствия или отсутствия CBM. До настоящего времени предыдущие результаты по выделению феруловой кислоты из ПО были получены с использованием ксиланазы из Trichoderma viride и FAEA из A. niger, в которых высвобождалось максимум 95% (вес/вес) суммарной феруловой кислоты (15). В случае ПО значительное количество феруловой кислоты (до 13,6%) высвобождалось из Humicola insolens при использовании коммерческого препарата Novozym 342 (5). В то же время следует принять во внимание тот факт, что этот коммерческий препарат содержал различные виды ферментативной активности. В данном анализе с помощью обработки бифункциональными ферментами феруловая кислота высвобождалась полностью из ПО, в то время как менее 8% образовывалось из КО. Несмотря на то что содержание феруловой кислоты в кукурузных отрубях выше, чем в пшеничных отрубях, ксилан в кукурузных отрубях является более замещенным на следы ксилозы, арабинозы и галактозы (7, 15). Таким образом, наблюдаемое различие может быть объяснено числом замещений в гетероксилановой основе кукурузы присутствием высоко разветвленной ксилозы в боковых цепях и наличием связей между арабинозой и ксилозой вблизи от групп феруловой кислоты, что в значительной степени ограничивает доступность фермента. Наконец, при рассмотрении гидролиза КО с использованием FLXLC положительный эффект от CBM на высвобождение феруловой кислоты, вероятно, возникает благодаря (i) таргетированию к целлюлозе, которое увеличивает концентрацию фермента вблизи субстрата, и/или (ii) дестабилизации целлюлозной структуры, делая субстрат более доступным. В качестве заключения к тестам применения с использованием FLX и FLXLC можно отметить, что для обоих субстратов был получен лучший синергический эффект для выделения феруловой кислоты по сравнению с отдельными ферментами FAEA и XYNB. Было сделано предположение, что общее повышение синергии происходило из-за физической близости каждого ферментативного партнера в бифункциональных ферментах, так как все основные биохимические и кинетические свойства для каждого партнера в гибридных белках не изменялись. В случае FLXLC положительный эффект на синергию производило C-концевое добавление CBM. Более того, также можно предположить, что пространственная ориентация активных сайтов не изменялась между составными модулями.
В качестве общего заключения было показано, что конструирование новых ферментативных инструментов для разрушения клеточных оболочек растений с использованием комплементарных гидролаз клеточных оболочек, таких как вспомогательный фермент FAEA и фермент, расщепляющий основную цепь (XYNB), является заслуживающей внимание стратегией увеличения синергического эффекта ферментативных партнеров. Для биотехнологических приложений использование подобных гибридных белков является альтернативой к дорогостоящим и загрязняющим химическим обработкам или служит для усовершенствования уже существующих ферментативных процессов для повышения ценности растительных побочных продуктов в производстве бумажной массы и бумаги, агро-промышленности и секторах производства биотоплива.
ФИГУРЫ
Фиг.1 Экспрессионные кассеты, используемые в данном исследовании. Для конструирования FLX вставки (А) последовательности из A. niger, кодирующие FAEA, линкерную область из CBHB и XYNB, были слиты вместе. Во второй конструкции (В) матрица FLX была слита с последовательностью cbhb, кодирующей последовательность линкера и CBM, образуя FLXLC вставку. Экспрессионные кассеты находились под контролем gpdA промотора и trpC терминатора. Обе конструкции содержали последовательность, кодирующую шесть гистидинов на 3' конце.
(1) Последовательность, кодирующая линкер: GSTYSSGSSSGSGSSSSSSSTTTKATSTTLKTTSTTSSGSSSTSAA.
Фиг.2 Временная зависимость активностей внеклеточных ферулоилэстеразы и ксиланазы из A. niger. Измерения активностей ферулоилэстеразы (А) и ксиланазы (В) производились для лучших FLX (♦) и FLXLC (■) трансформантов. Активности определялись с использованием метилферулата и ксилана из березовой древесины в качестве субстратов для эстеразы и ксиланазы соответственно.
Фиг.3 Анализ в SDS-PAGE полиакриламидном геле внеклеточных белков, продуцируемых FLX и FLXLC трансформантами. На SDS-PAGE 11% полиакриламидный гель наносились суммарный и очищенный белки из FLX (дорожки 1 и 2 соответственно) и FLXLC (дорожки 3 и 4 соответственно). Гель окрашивался Кумасси синим (Coomassie blue). SD: стандарты молекулярной массы.
Фиг.4. Вестерн-блоттинг гибридизация суммарного и очищенного белков, продуцируемых FLX и FLXLC трансформантами. В иммунодетекции суммарных внеклеточных и очищенных белков из FLX и FLXLC трансформантов использовались антитела к FAEA (A) или His-Tag (B). Дорожки 1,5: суммарные внеклеточные белки из FLX трансформанта. Дорожки 2,6: очищенный FLX. Дорожки 3,7: суммарные внеклеточные белки из FLXLC трансформанта. Дорожки 4,8: очищенный FLXLC. С: контрольный штамм D15#26, трансформированный pAB4-1. Детектирование производилась с помощью хемолюминесценции.
Фиг.5. Сравнение эффективности высвобождения феруловой кислоты под действием отдельных или бифункциональных ферментов. Для гидролиза феруловой кислоты отдельными или бифункциональными ферментами использовались отруби пшеницы (А) или отруби кукурузы (В). Выход феруловой кислоты определялся с помощью ВЭЖХ за 4 ч (белый столбик) и 16 ч (черный столбик). Активности выражались в процентах от суммарного количества феруловой кислоты, содержащейся в субстрате. Стандартное отклонение составляла менее 5% от среднего значения для отрубей пшеницы и отрубей кукурузы.
(3) Km выражались в моль для активности ферулоилэстеразы и в миллилитрах для активности ксиланазы.
(4) Удельные активности выражались в нкатал на нмол белка с целью облегчения сравнения между отдельными и бифункциональными белками.
Для pH и температуры стабильности инкубация производилась в течение 90 минут.
Фактор синергизма определялся следующим образом:
(феруловая кислота, выделенная с помощью бифункциональных ферментов FLX или FLXLC)/(феруловая кислота, выделенная с помощью отдельных ферментов FAEA+XYNB).
Источники информации

































































Изобретение относится к биотехнологии. Представлен разрушающий клеточные оболочки слитый белок, включающий ферулоилэстеразу и ксиланазу, которые не содержат С-концевую углеводород-связывающую молекулу (СВМ). Указанный слитый белок в случае необходимости включает СВМ из третьего фермента, при этом ферменты и СВМ являются рекомбинантными белками, соответствующими нативным белкам грибов. Кроме того, предложено применение данного слитого белка для осуществления способов разрушения клеточных оболочек растений в рамках получения из растений или растительных побочных продуктов соединений, представляющих интерес. Также представлены нуклеиновая кислота, кодирующая указанный слитый белок, экспрессирующий вектор, трансформированный указанной нуклеиновой кислотой, и клетка-хозяин, содержащая указанный вектор. Описан способ получения указанных слитых белков, включающий культивирование клеток-хозяев, выделение и, если необходимо, очистку слитых белков, продуцируемых указанными клетками-хозяевами в культуре. Предложен способ получения из растительных продуктов целевых соединений, который включает следующие стадии: 1) ферментативную обработку растительных продуктов слитыми белками, или трансформированными клетками грибов, 2) в случае необходимости обработку растительных продуктов паром в сочетании с действием слитых белков, 3) в случае необходимости биотрансформацию соединений, выделяемых из клеточных оболочек в процессе вышеуказанной ферментативной обработки, 4) извлечение и если необходимо, очистку целевых соединений. Изобретение позволяет увеличить эффект разрушения клеточных оболочек растений. 9 н. и 15 з.п. ф-лы, 5 ил., 2 табл.
1. Применение слитого белка, включающего ферулоилэстеразу и ксиланазу, при этом указанные ферменты таковы, что они не содержат С-концевую углеводородосвязывающую молекулу (carbohydrate-binding-molecule, СВМ), и, в случае необходимости, СВМ из третьего фермента, причем указанные ферменты и СВМ являются рекомбинантными белками, соответствующими нативным белкам в грибах, для осуществления способов разрушения клеточных оболочек растений в рамках получения из растений или растительных побочных продуктов, соединений, представляющих интерес и содержащихся в клеточных оболочках растений.
2. Применение слитого белка, включающего ферулоилэстеразу и ксиланазу, при этом указанные ферменты таковы, что они не содержат С-концевую углеводородосвязывающую молекулу (carbohydrate-binding-molecule, СВМ), и, в случае необходимости, СВМ из третьего фермента, причем указанные ферменты и СВМ являются рекомбинантными белками, соответствующими нативным белкам в грибах, для осуществления способов разрушения клеточных оболочек растений в рамках отбеливания бумажной массы и бумаги.
3. Применение слитого белка по п.1 или 2, в котором ферменты, разрушающие клеточную оболочку растений и не содержащие СВМ, соответствуют нативным ферментам грибов, выбранных из:
аскомицетов, таких, как:
- штаммы Aspergillus, и более конкретно, Aspergillus niger,
- штаммы Trichoderma, и более конкретно, Trichoderma reesei,
базидиомицетов, таких, как штаммы Pycnoporus или Halocyphina, и более конкретно, Pycnoporus cinnabarinus, Pycnoporus sanguineus или Halocyphina villosa.
4. Применение слитого белка по п.1 или 2, в котором ферменты, разрушающие клеточную оболочку растений и не содержащие СВМ, соответствуют нативным ферментам из штаммов Aspergillus, таких, как Aspergillus niger.
5. Применение слитого белка по п.1, в котором по меньшей мере один фермент, разрушающий клеточную оболочку растений, является ферулоилэстеразой и выбирается из:
- ферулоилэстеразы А из А. niger, представленной SEQ ID NO:2,
- или ферулоилэстеразы В из А. niger, представленной SEQ ID NO:4.
6. Применение слитого белка по п.1 или 2, в котором по меньшей мере один фермент, разрушающий клеточную оболочку растений, является ксиланазой, такой, как ксиланаза В из А. niger, представленная SEQ ID NO:6.
7. Применение слитого белка по п.1 или 2, в котором белок, являющийся СВМ, выбирают из СВМ, присутствующих в нативных ферментах грибов, выбранных из аскомицетов, таких, как штаммы Aspergillus, и более конкретно, Aspergillus niger.
8. Применение слитого белка по п.1 или 2, в котором СВМ является СВМ, присутствующей в целлобиогидролазе В из А. niger и представленной SEQ ID NO:8.
9. Применение слитого белка по п.1 или 2, содержащего линкеры между по меньшей мере двумя белками, входящими в указанный слитый белок, при этом линкеры являются полипептидами длиной от 10 до 100 аминокислот преимущественно около 50 аминокислот.
10. Применение слитого белка по п.1 или 2, в котором линкер включен между каждым белком, входящим в указанный слитый белок.
11. Применение слитого белка по п.1 или 2, в котором линкером является гипергликозилированный полипептид, такой, как имеющий последовательность, представленную SEQ ID NO:10, содержащуюся в целлобиогидролазе В из A. niger.
12. Применение слитого белка по п.1 или 2, включающего ферулоилэстеразу и ксиланазу и, в случае необходимости, СВМ, такого, как:
- слитый белок, включающий ферулоилэстеразу А из А. niger, представленную SEQ ID NO:2, и ксиланазу В из А. niger, представленную SEQ ID NO:6, при этом указанный слитый белок содержит последовательность, представленную SEQ ID NO:10, в качестве гипергликозилированного линкера между двумя предшествующими белками, и представленный SEQ ID NO:12,
- слитый белок, включающий ферулоилэстеразу А из А. niger, представленную SEQ ID NO:2, и ксиланазу В из А. niger, представленную SEQ ID NO:6, и СВМ, представленную SEQ ID NO:8 и присутствующую в целлобиогидролазе В из А. niger,
- слитый белок, включающий ферулоилэстеразу А из А. niger, представленную SEQ ID NO:2, и ксиланазу В из А. niger, представленную SEQ ID NO:6, и СВМ, представленную SEQ ID NO:8, при этом указанный слитый белок содержит последовательность, представленную SEQ ID NO:10, в качестве гипергликозилированного линкера между каждым из трех предшествующих белков, и представленный SEQ ID NO:14,
- слитый белок, включающий ферулоилэстеразу В из А. niger, представленную SEQ ID NO:4, и ксиланазу В из А. niger, представленную SEQ ID NO:6, при этом указанный слитый белок содержит последовательность, представленную SEQ ID NO:10, в качестве гипергликозилированного линкера между двумя предшествующими белками, и представленный SEQ ID NO:16,
- слитый белок, включающий ферулоилэстеразу В из A. niger, представленную SEQ ID NO:4, и ксиланазу В из А. niger, представленную SEQ ID NO:6, и СВМ, представленную SEQ ID NO:8 и присутствующую в целлобиогидролазе В из А. niger,
- слитый белок, включающий ферулоилэстеразу В из А. niger, представленную SEQ ID NO:4, и ксиланазу В из А. niger, представленную SEQ ID NO:6, и СВМ, представленную SEQ ID NO:8, при этом указанный слитый белок содержит последовательность, представленную SEQ ID NO:10, в качестве гипергликозилированного линкера между каждым из трех предшествующих белков, и представленный SEQ ID NO:18.
13. Применение по любому из пп.1 или 2 для осуществления способов разрушения клеточных оболочек растений в рамках получения следующих целевых соединений:
- биоэтанола,
- антиоксидантов, таких, как феруловая килота или кофейная кислота, которые являются коричными кислотами, и гидрокситирозол, или галлиевая кислота,
- вкусоароматических добавок, таких, как ванилин или п-гидроксибензальдегид, получаемых путем биотрансформации феруловой кислоты или п-кумариновой кислоты соответственно.
14. Применение по любому из пп.1 или 2 для осуществления способов разрушения клеточных оболочек растений в рамках отбеливания бумажной массы и бумаги с сопутствующим получением биоэтанола или без него.
15. Разрушающий клеточные оболочки слитый белок, включающий ферулоилэстеразу и ксиланазу, которые не содержат С-концевую углеводородосвязывающую молекулу (СВМ), причем указанный слитый белок в случае необходимости включает СВМ из третьего фермента, при этом ферменты и СВМ являются рекомбинантными белками, соответствующими нативным белкам грибов.
16. Разрушающий клеточные оболочки слитый белок по п.15, в котором:
- ферменты, разрушающие клеточную оболочку растений, которые не содержат СВМ, определены в любом из пп.3-5,
- СВМ определен в п.7 или 8.
17. Разрушающий клеточные оболочки слитый белок по п.15, включающий линкеры между по меньшей мере двумя белками, содержащимися в указанных слитых белках, при этом указанные линкеры определены в любом из пп.9-11.
18. Разрушающий клеточные оболочки слитый белок по п.15 или 16, включающий ферулоилэстеразу и ксиланазу, и в случае необходимости СВМ, такой, как:
- слитый белок, включающий ферулоилэстеразу А из A. niger, представленную SEQ ID NO:2, и ксиланазу В из А. niger, представленную SEQ ID NO:6, при этом указанный слитый белок содержит последовательность, представленную SEQ ID NO:10, в качестве гипергликозилированного линкера между двумя предшествующими белками, и представленный SEQ ID NO:12,
- слитый белок, включающий ферулоилэстеразу А из А. niger, представленную SEQ ID NO:2, и ксиланазу В из А. niger, представленную SEQ ID NO:6, и СВМ, представленную SEQ ID NO:8 и присутствующую в целлобиогидролазе В из А. niger,
- слитый белок, включающий ферулоилэстеразу А из А. niger, представленную SEQ ID NO:2, и ксиланазу В из А. niger, представленную SEQ ID NO:6, и СВМ, представленную SEQ ID NO:8, при этом указанный слитый белок содержит последовательность, представленную SEQ ID NO:10, в качестве гипергликозилированного линкера между каждым из трех предшествующих белков, и представленный SEQ ID NO:14,
- слитый белок, включающий ферулоилэстеразу В из A. niger, представленную SEQ ID NO:4, и ксиланазу В из А. niger, представленную SEQ ID NO:6, при этом указанный слитый белок содержит последовательность, представленную SEQ ID NO:10, в качестве гипергликозилированного линкера между двумя предшествующими белками, и представленный SEQ ID NO:16,
- слитый белок, включающий ферулоилэстеразу В из А. niger, представленную SEQ ID NO:4, и ксиланазу В из А. niger, представленную SEQ ID NO:6, и СВМ, представленную SEQ ID NO:8 и присутствующую в целлобиогидролазе В из А. niger,
- слитый белок, включающий ферулоилэстеразу В из А. niger, представленную SEQ ID NO:4, и ксиланазу В из А. niger, представленную SEQ ID NO:6, и СВМ, представленную SEQ ID NO:8, при этом указанный слитый белок содержит последовательность, представленную SEQ ID NO:10, в качестве гипергликозилированного линкера между каждым из трех предшествующих белков, и представленный SEQ ID NO:18.
19. Нуклеиновая кислота, кодирующая слитый белок, представленный аминокислотной последовательностью SEQ ID NO:12, SEQ ID NO:14, SEQ ID NO:16 или SEQ ID NO:18.
20. Вектор экспрессии, трансформированный нуклеиновой кислотой, определенной в п.19.
21. Клетка-хозяин, продуцирующая слитый белок по п.18, трансформированная с использованием вектора, определенного в п.20.
22. Способ получения из растений или растительных побочных продуктов целевых соединений, содержащихся в растительных клеточных оболочках, путем разрушения клеточных оболочек, который характеризуется тем, что включает следующие стадии:
- ферментативную обработку растений или растительных побочных продуктов слитыми белками, определенными в любом из пп.15-18, или трансформированными клетками грибов, определенными в п.21,
- в случае необходимости, физическую обработку растений или растительных побочных продуктов паром в сочетании с действием слитых белков,
- в случае необходимости, биотрансформацию соединений, выделяемых из клеточных оболочек в процессе вышеуказанной ферментативной обработки, с помощью соответствующих микроорганизмов или ферментов,
- извлечение и, если необходимо, очистку целевых соединений, выделяемых из клеточных оболочек в процессе вышеуказанной ферментативной обработки или полученных на вышеуказанной стадии биотрансформации.
23. Способ по п.22 для получения антиоксидантов, таких, как феруловая кислота, или кофейная кислота, которые являются коричными кислотами, и гидрокситирозол, или галлиевая кислота; вкусоароматических добавок, таких, как ванилин или п-гидроксибензалдегид, получаемых путем биотрансформации феруловой кислоты или п-кумариновой кислоты, соответственно, биоэтанола,
или для отбеливания бумажной массы и бумаги.
24. Способ получения слитых белков, определенных в пп.15-18, включающий культивирование in vitro клеток-хозяев по п.21, выделение и, если необходимо, очистку слитых белков, продуцируемых указанными клетками-хозяевами в культуре.
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| FAULDS C.B., et | |||
| al., «Release of ferulic acid from wheat bran by a ferulic acid esterase (FEA-III) from Aspergillus niger" // Appl MicrobiolBiotechnol | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| DE VRIES R.P., et al.: "The feaA genes from Aspergillus niger and Aspergillus tubingensis encode ferulic acid | |||
Авторы
Даты
2011-11-10—Публикация
2006-07-26—Подача