Изобретение относится к медицине, а именно к фармакологии, клинической фармакологии и онкологии. Предложено применение бис(3,5-ди-трет-бутил-4-гидроксифенилтиолат)диметилолова (Ме3) в качестве средства для ингибирования метастазирования.
Интенсивное метастазирование является одной из главных причин смерти пациентов, имеющих злокачественные новообразования. Меланома - чрезвычайно злокачественная и достаточно распространенная опухоль [1]. Неблагоприятный прогноз при лечении больных меланомой [2] в основном обусловлен агрессивным метастазированием опухоли различными путями: гематогенным, лимфогенным и лимфогематогенным. Метастатические клетки меланомы относительно устойчивы к применяемым в терапии лекарственным препаратам. В настоящее время применяется широкий спектр противоопухолевых и антиметастатических препаратов, но они недостаточно эффективны как в отношении первичного очага, так и метастатических поражений, и обладают высокой токсичностью и низкой избирательностью действия по отношению к клеткам злокачественной опухоли.
Несмотря на некоторые успехи в лечении меланомы, поиск новых антиметастатических веществ остается актуальной задачей экспериментальной фармакологии и онкологии.
Анализ современной литературы указывает на перспективность такого поиска среди металлоорганических соединений, содержащих антиоксидантные группы. Сочетание двух активных фрагментов: комплекса металла и протектора (антиоксиданта), обеспечивают рациональное соотношение «активность-токсичность», снижение побочных реакций при сохранении антиметастатического эффекта.
Особый научно-практический интерес вызывают соединения олова (Sn), относящиеся к классу металлоорганических соединений и содержащие связи «олово-углерод» [3]. Органические соединения олова обладают особой устойчивостью в физиологической среде и высокой цитотоксичностью. Механизм цитотоксического действия оловоорганических соединений обусловлен несколькими факторами: ингибированием ряда ферментов и полимеризации белка тубулина за счет связывания атома Sn с SH-группами; образованием реакционноспособных радикальных частиц при гомолитическом разрыве связи Sn-С; генерированием активных метаболитов кислорода (АМК), индукцией окислительного стресса, приводящего к нарушению проницаемости мембран [4, 5].
Наиболее известными и используемыми синтетическими антиоксидантами являются соединения фенольного ряда. Будучи акцепторами свободных радикалов, антиоксиданты нашли широкое применение в качестве ингибиторов свободно-радикальных процессов с возможностью модулирования развития метастазирования [6]. Среди большого многообразия различных производных особое место занимают пространственно-затрудненные фенолы, в частности, производные 2,6-ди-трет-бутилфенола [7]. Из литературных источников известен синтез новых оловоорганических соединений (ООС) общей формулы MenSn(SR)4-n (n=2, 3), содержащих фрагмент 2,6-ди-трет-бутилфенола (R = 3,5-ди-трет-бутил-4-гидроксифенил) с целью изучения их влияния на процессы неферментативного и ферментативного пероксидного окисления ненасыщенных жирных кислот липидов, а также на связывание с SH-группами белка тубулина. В этой работе получены соединения олова MenSn(SR)4-n взаимодействием соответствующих хлоридов олова и 2,6-ди-трет-бутил-4-меркаптофенола (RSH) в метаноле в присутствии гидроксида калия [8].
Широко распространенным в клинической практике антиоксидантом является мексидол (3-окси-6-метил-2-этилпиридина сукцинат), который в силу его способности влиять на основные звенья патогенеза различных заболеваний, сопровождающихся окислительным стрессом и процессами свободнорадикального окисления, обладает широким спектром фармакологического действия. Для мексидола на примере модели перевиваемой меланомы мышей В16 установлена способность ингибировать спонтанное метастазирование [9]. У животных оценивали объем первичного опухолевого узла, частоту метастазирования опухоли, количество метастазов на поверхности легких, подсчитывали индекс ингибирования метастазирования (ИИМ). Мексидол вводили ежедневно в/м с 1 суток после перевивки опухоли, в дозах 10 и 50 мг/кг.
Техническим результатом изобретения является антиметастатическое средство, пригодное для внутрибрюшинного введения.
Технический результат достигается действием бис(3,5-ди-трет-бутил-4-гидроксифенилтиолат)диметилолова (Ме3).
По своей структуре Ме3 гибридная молекула, содержащая и оловоорганический и протекторный антиоксидантный фрагмент 2,6-ди-трет-бутилфенола.
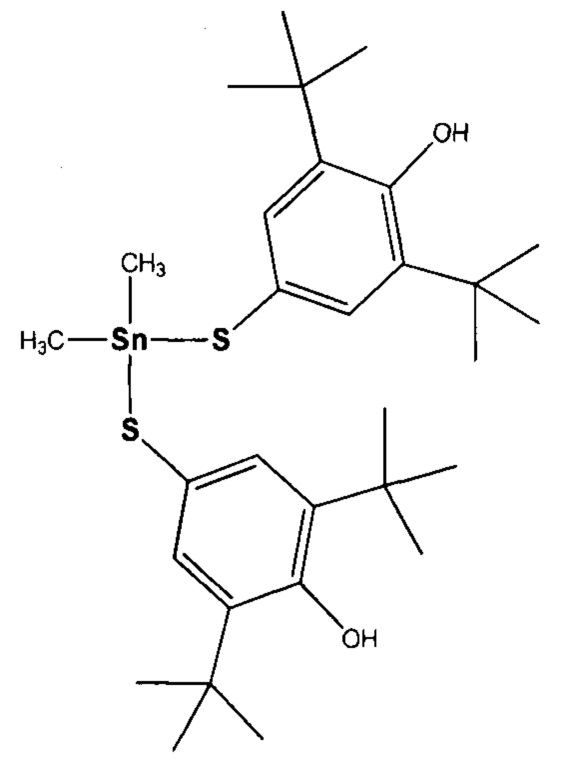
Ниже приведен пример синтеза бис(3,5-ди-трет-бутил-4-гидроксифенилтиолат)диметилолова (Ме3) [8].
Пример. К раствору 200 мг (0,9 ммоль) Me2SnCl2 и 428 мг (1,8 ммоль) 2,6-ди-трет-бутил-4-меркаптофенола в 4 мл этанола добавляли по каплям при перемешивании 1.8 мл (1.8 ммоль) 1М раствора КОН в течение 30 мин. Выпавший белый осадок отфильтровывали, промывали водой, петролейным эфиром. Осадок высушивали на воздухе в течение 24 ч. Выход 313 мг (55%). Тпл 115-118°С.
Спектр ЯМР 1Н (δ, м.д.): 0.43 (s, 6 Н, 2СН3), 1.42 (s, 36 Н, 8 С(СН3)3), 5.13 (s, 2 Н, 2 ОН), 7.36 (s, 4 Н, 2 Ar).
13С (δ, м.д. CDCl3): 1.94 (2 CH3Sn), 30.27 (12 СН3, 4 But) 34.34 (С(СН3)3), 120.88, 131.49, 136.58, 153.20 (2 Carom).
ИК-спектр (см-1): 3633,2 (νOH); 2998-2871,5 (νC-H); 1423; 1309,43; 1230,4; 1155,1; 875,5; 765,6; 715,5.
Найдено (%): С 57.62; Н 7.61. Вычислено (%): С 57.79; Н 7.76. C30H48O2S2Sn.
Исследование ингибирующей активности.
Все манипуляции с животными, в том числе выведение из эксперимента, осуществляли в соответствии с правилами, принятыми «Европейской конвенцией по защите позвоночных животных, используемых для экспериментов или в иных научных целях».
Исследование антиметастатической активности Ме3 проведено на мышах-самках линии С57В 1/6 (36 животных) с подкожно перевитой меланомой В16, для которой характерно 100%-ное спонтанное метастазирование в легкие, с использованием внутрибрюшинного введения препарата.
Поддержание и перевивку опухолевого штамма осуществляли в соответствии с общепринятыми методами для линии С57В 1/6. Инокуляцию опухолевых клеток проводили подкожно в правую подмышечную область каждой мыши по 50 мг опухолевой взвеси в физиологическом растворе при разведении 1:10.
Через 48 часов после перевивки меланомы В16 мышам-самкам линии С57В 1/6 вводили:
1 группа животных - 1%-ный водный желатиновый раствор Ме3 в разовой дозе 75 мг/кг 1 раз в сутки в течение 5 дней, внутрибрюшинно (суммарная доза 375 мг/кг);
2 группа животных (группа сравнения) - мексидол (ФАРМАСОФТ, Россия), который применяли внутрибрюшинно в дозе 10 мг/кг 1 раз в сутки в течение 5 дней;
3 группа (контроль) - 1%-ный водный желатиновый раствор в эквивалентных объемах, внутрибрюшинно.
Через 18 суток после перевивки опухоли всех животных подвергали эвтаназии в СО2 камере и проводили некропсию.
При анализе было установлено, что в группе животных, получивших Ме3 (группа 1) индекс ингибирования метастазирования составил 54%. У животных, получивших мексидол (группа 2), индекс ингибирования метастазирования составил 31%, что в 1,7 раз ниже, чем у животных группы 1 (см. таблица №1).
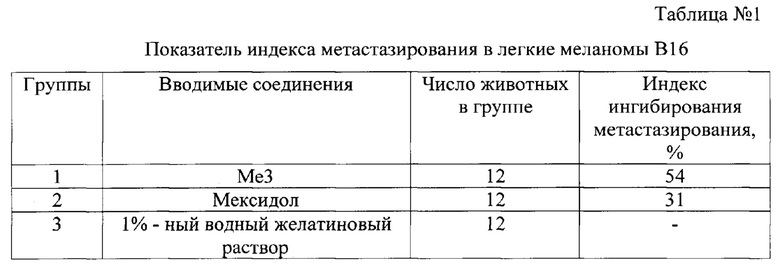
Можно заключить, что фармакологическая субстанция Ме3 при внутрибрюшинном применении значительно снижает количество и частоту метастазов меланомы В16 в легкие у мышей, проявляя более выраженные антиметастатические свойства, чем мексидол.
Литература:
1. Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. Состояние онкологической помощи населению России в 2019 году. - М.: МНИОИ им. П.А. Герцена - филиал ФГБУ «НМИЦ радиологии» Минздрава России, 2020. - илл. - 239 с. ISBN 978-5-85502-255-1/.
2. Современные методы диагностики и лечения меланомы. Лазарев Ю.Д. Фундаментальные аспекты психического здоровья. 2018. №3. С. 6-10.
3. Wang R.S., Chen L.C., Yang Н., Fu М.А., Cheng J., Wu X.L., Gao Y., Huang Z.B, Chen X.J. Superconductivity in an organometallic compound. Phys Chem Chem Phys. 2019; 21:25976-25981. DOI:10.1039/C9CP04227J.
4. Banti C.N., Hadjikakou S.K., Sismanoglu Т., Hadjiliadis N. Antiproliferative and antitumor activity of organotin(IV) compounds. An overview of the last decade and future perspectives. J. Inorg. Biochem. 2019; 194:114-152. DOI: 10.1016/j.jinorgbio.2019.02.003.
5. Gasser G., Metzler-Nolte N. The potential of organometallic complexes in medicinal chemistry. Curr. Op. Chem. Biol. 2012; 16:84-91. DOI: 10.1016/j.cbpa.2012.01.013.
6. Prasad S., Gupta S.C., Tyagi A.K. Reactive oxygen species (ROS) and cancer: Role of antioxidative nutraceuticals // Cancer Lett. 2016 Mar 29. pii: S0304-3835(16)30202-6. doi: 10.1016/j.canlet.2016.03.042.
7. Antonenko T.A., Shpakovsky D.B., Vorobyov M.A., Gracheva Yu A., Kharitonashvili E.V., Dubova L.G., Shevtsova E.F., Tafeenko V.A., Aslanov L.A., Iksanova AG., Shtyrlin Yu G., Milaeva E.R. Antioxidative vs cytotoxic activities of organotin complexes bearing 2,6-di-tert-butylphenol moieties. Appl. Organomet. Chem. 2018; 32(7):e4381. DOI: 10.1002/aoc.4381.
8. Мухатова E.M., Осипова В.П., Коляда M.H., Мовчан Н.О., Шпаковский Д.Б., Грачева Ю.А., Орлова СИ., Милаева Е.Р. Синтез и антиоксидантная активность новых оловоорганических соединений, содержащих фрагмент 2,6-ди-трет-бутилфенола // Доклады Академии наук, Москва, 2013, т. 451, №1, с. 46-49.
9. Скопин П.И. Влияние мексидола на антиметастатическую активность противоопухолевых препаратов // Аспирантский вестник Поволжья. - №3-4. 2009. - с. 104-107.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО ДЛЯ ИНГИБИРОВАНИЯ МЕТАСТАЗИРОВАНИЯ В ЛЕГКИХ | 2021 |
|
RU2765955C1 |
| СПОСОБ КОМБИНИРОВАННОЙ ТЕРАПИИ МЕЛАНОМЫ В16 В МЕТРОНОМНОМ РЕЖИМЕ В ЭКСПЕРИМЕНТЕ | 2022 |
|
RU2792561C1 |
| Средство для ингибирования метастазирования в легких | 2016 |
|
RU2632703C1 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО | 2016 |
|
RU2623034C1 |
| СПОСОБ ДОСТИЖЕНИЯ АНТИМЕТАСТАТИЧЕСКОГО ЭФФЕКТА В ЭКСПЕРИМЕНТЕ | 2017 |
|
RU2661704C1 |
| Способ усиления противометастатического действия цисплатина и снижения его побочного действия на систему гемостаза | 2023 |
|
RU2825825C1 |
| Способ подавления роста меланомы В16 у лабораторных животных | 2022 |
|
RU2784443C2 |
| Средство, обладающее антипролиферативной и антиметастатической активностью по отношению к карциноме легкого Льюиса при внутрибрюшинном введении | 2022 |
|
RU2792144C1 |
| Фармацевтическая композиция на основе соединения палладия | 2015 |
|
RU2613305C2 |
| АНТИМЕТАСТАТИЧЕСКАЯ КОМПОЗИЦИЯ | 2006 |
|
RU2308966C1 |
Изобретение относится к применению бис(3,5-ди-трет-бутил-4-гидроксифенилтиолат)диметилолова в качестве средства для ингибирования метастазирования меланомы в легких. Технический результат заключается в снижении частоты развития и количества метастазов меланомы в легких. 1 табл., 1 пр.
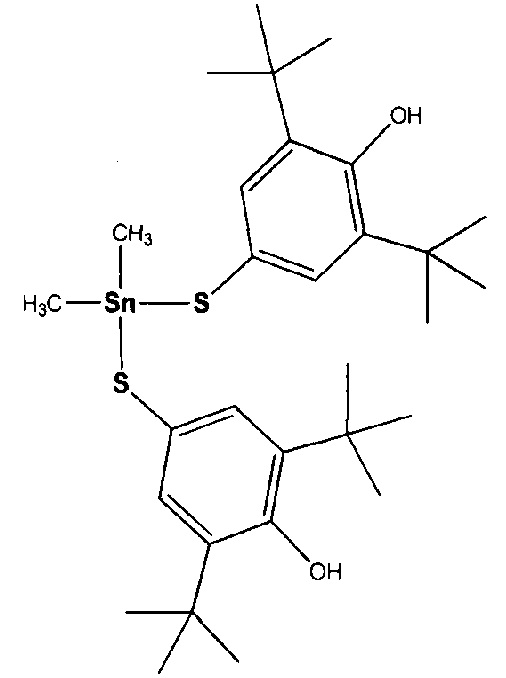
Применение бис(3,5-ди-трет-бутил-4-гидроксифенилтиолат)диметилолова в качестве средства для ингибирования метастазирования меланомы в легких.
| Средство для ингибирования метастазирования в легких | 2016 |
|
RU2632703C1 |
| Е | |||
| М | |||
| Мухатова и др | |||
| "СИНТЕЗ И АНТИОКСИДАНТНАЯ АКТИВНОСТЬ НОВЫХ ОЛОВООРГАНИЧЕСКИХ СОЕДИНЕНИЙ, СОДЕРЖАЩИХ ФРАГМЕНТ 2,6-ДИ-трет-БУТИЛФЕНОЛА", ДОКЛАДЫ АКАДЕМИИ НАУК, 2013, том 451, N1, с | |||
| Способ изготовления звездочек для французской бороны-катка | 1922 |
|
SU46A1 |
| D | |||
| B | |||
| Shpakovsky et al "Synthesis, antiradical activity and in vitro cytotoxicity of novel organotin complexes based on | |||
Авторы
Даты
2021-12-22—Публикация
2021-03-30—Подача