Изобретение относится к медицине, а именно к экспериментальным исследованиям в онкологии, и может быть использовано для ингибирования метастазирования меланомы В16 у мышей-опухоленосителей.
Проблема метастазирования является одной из важнейших в онкологии, поскольку именно метастазы являются основной причиной смерти онкологических больных, даже после успешного воздействия на первичный опухолевый очаг. Поэтому разработка и применение схем лечения, направленных на индукцию антиметастатического эффекта, является актуальной для современной онкологии.
Методы противоопухолевого лечения нередко являются иммунодепрессивными, что после временного эффекта способствует развитию из химиорезистентных клеток опухоли и ее метастазированию в иммуноскомпротетированном организме. Такая проблема диктует необходимость экспериментальной разработки новых вариантов биотерапии опухолей, включая иммунокоррекцию в качестве терапии сопровождения.
В последнее время активно изучается антиметастатический эффект биологически активных соединений растительного происхождения. Известны работы, в которых показано противоопухолевое и антиметастатическое действие растительных средств из алкалоидоносных растений (см. Поветьева Т.Н., Пашинский В.Г., Семенов А.А., Жапова Ц., Погодаева Н.Н., Хоружая Т.Г. «Исследование противоопухолевых и антиметаститических свойств растительных средств из аконита байкальского» // Сибирский онкологический журнал. 2002. №3-4. С. 138-141; см. Алефиров А.Н., Беспалов В.Г., Стуков А.Н., Семенов А.Л., Лесиовская Е.Е. «Антиметастатическая активность настойки подземной части ACONITUMSOONGARICUM (RANUNCULACEAE) на моделях перевиваемых опухолей» // Растительные ресурсы. 2014. Т. 50. Вып. 2. С. 254-270) и полисахаридов растительного происхождения (см. Лопатина К.А. и соавт. Доклиническое исследование лекарственной формы α(1;2)-L-рамно-α(1;4)-D-галактопиранозилуронана из корневищ аира болотного ACORUSCALAMUSL. в онкологическом эксперименте // Сибирский онкологический журнал. 2015. №1. С. 59-63). В данных исследованиях отмечен антиметастатический эффект разной степени выраженности (от 31,8% до 100%) под воздействием вытяжек аконита байкальского разной концентрации, настойки аконита джунгарского или раствора полисахарида аира болотного на моделях перевиваемых опухолей меланомы В16 и карциномы легкого Льюиса.
Известен способ применения и других веществ с последующей оценкой их действия на рост и метастазирование опухоли: антибиотика ряда макролидов (см. Козлов A.M., Киселев С.М., Перетолчина Н.М., Аклеев А.В. «Противоопухолевая и антиметастатическая активность рулида в режиме монотерапии и при сочетанном применении с цисплатином»//Российский биотерапевтический журнал. 2006. Т. 5. №3. С. 134-141). В своем эксперименте авторы получили значимое противоопухолевое (ТРО=51%) и антиметастатическое (ТРМ=55%) действие антибиотика на карциному легкого Льюиса. Действие препарата на меланому В16 показано только in vitro, отмечена антиинвазивная активность рулида при высокой концентрации (0,2-0,4 мМ). Однако не описано действие препарата на меланому В16 in vivo.
В качестве протиотипа нами взята работа Е.В. Фадеевой, Е.А. Лебединской, Е.В. Лебединской (см. «Влияние иммуномодулятора стимфорте на рост и метастазирование меланомы В16 у мышей» // Успехи современного естествознания. 2010. №7. С. 53-54), в которой авторы описывают влияние иммуномодулятора стимфорте в режиме монотерапии и в сочетании с мелатонином на стандартную модель перевиваемой опухоли - меланому В16. В своей работе авторы использовали водную вытяжку из тканей и органов ужа, которая обнаруживает иммуностимулирующее действие, активируя различные звенья иммунитета. Эффект достигался при воздействии препарата в монорежиме и выражался в увеличении продолжительности жизни животных, значительной регрессии опухоли (>50%) на 14 сутки после имплантации и достоверное антиметастатическое действие. Стимфорте в сочетании с мелатонином не влиял ни на продолжительность жизни, ни на динамику роста опухоли, ни на метастазирование меланомы. Несмотря на заявленное антиметастатическое действие, авторы не приводят числовых значений индекса ингибирования метастазирования, что не позволяет оценить эффект.
Учитывая все вышесказанное, можно отметить, что в литературе нет данных об изучении комплексного воздействия иммуномодуляторов на основе цитокинов на рост и метастазирование меланомы В16.
Техническим результатом изобретения является экспериментальное достижение антиметастатического эффекта путем применения цитокиновых иммуномодуляторов.
Технический результат достигается тем, что мышам-опухоленосителям с меланомой В16 через 10 дней после перевивки поочередно через день вводят по 0,3 мл 150 МЕ «Ронколейкина» и 0,3 мл 150 ME «Ингарона» в течение 8 дней.
Изобретение «Способ достижения антиметастатического эффекта в эксперименте» является новым, так как оно не известно из уровня медицины при исследовании действия цитокиновых иммуномодуляторов на рост и метастатическую активность перевивной меланомы В16.
Новизна изобретения заключается в том, что впервые было получено 100% ингибирование метастазирования в результате применения сочетания цитокиновых иммуномодуляторов.
Изобретение является промышленно применимым, так как может быть использовано в здравоохранении при проведении экспериментальных исследований в НИИ онкологии. Поскольку эти препараты имеют необходимые документы на клиническое применение, используются при различных заболеваниях, они могут быть использованы в комплексном лечении злокачественных опухолей не только для иммунокоррекции, но и с целью индукции антиметастатического эффекта.
«Способ достижения антиметастатического эффекта в эксперименте» выполняется следующим образом.
Мышам линии С57В1/6 массой 18-20 г осуществляют перевивку опухоли меланомы В16 под кожу спины над правой лопаткой. Мыши содержатся в стандартных условиях вивария. По достижении опухолью замеряемого размера начинают ежедневное паратуморальное введение препарата. Поочередно через день вводят по 0,3 мл 150 ME «Ронколейкина» и 0,3 мл 150 ME «Ингарона». Всего выполняется 8 инъекций на каждое животное по 1 инъекции в день. Суммарная концентрация препаратов на одно животное составила по 600 ME Ронколейкина и Ингарона. В динамике введения и после его окончания оценивают изменение объема опухоли, а после эвтаназии степень поражения легких метастазами, в результате чего устанавливают полное ингибирование метастазирования по сравнению с контрольной группой.
По результатам эксперимента рассчитывают торможение роста опухоли (ТРО) и индекс ингибирования метастазирования (ИИМ):
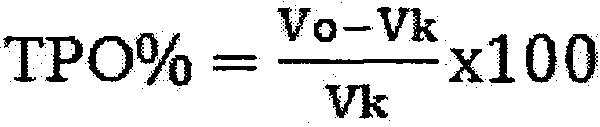 ,
,
где Vo и Vk - величина Vcp в опыте и в контроле (см. Трещалина Е.М., Жукова О.С., Герасимова Г.К. и др. Методические указания по изучению противоопухолевой активности фармакологических веществ. В кн. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. / Под ред. Р.У. Хабриева. Изд. 2. М., Медицина. 2005. С. 637-651)
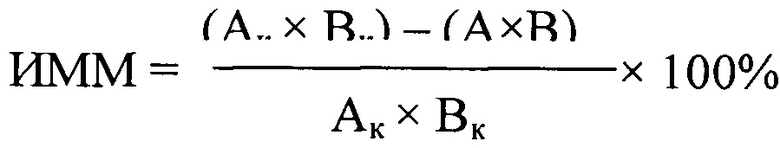 ,
,
где Ак и А - частота метастазирования в легкие у мышей контрольной и опытной групп; Вк и В - среднее число метастазов в легких контрольной и опытной групп (см. Архипов С.А., Юнкер В.М. Изменение интенсивности метастазирования в легкие перевиваемых опухолей мышей в зависимости от величины перевивочной дозы опухолевых клеток // Исследование по индукции и метастазированию опухолей у экспериментальных животных. Новосибирск. 1984. С. 14-32).
В ходе исследования мышам-опухоленосителям с перевиваемой меланомой В16 вводили различные комбинации препаратов по схеме:
1. 4 дня «Ронколейкин» паратуморально, затем 4 дня «Доксорубицин».
2. «Ронколейкин» и «Ингарон» через день паратуморально.
3. Чередование «Ронколейкин», «Ингарон» и «Рефнот» паратуморально.
4. «Доксорубицин» ежедневно.
5. Контрольная группа - вводили физиологический раствор.
Введение препаратов осуществляется в дозе и концентрации, соответствующих каждому препарату: «Ронколейкин» - 0,3 мл (150 ME), «Рефнот» - 0,5 мл (50 ME), «Ингарон» - 0,3 мл (150 ME), «Доксорубицин» - 0,2 мл (4 мкг). Всего выполняется 8 инъекций на каждое животное по 1 инъекции в день. Суммарная концентрация препаратов на одно животное составила: в первой группе 600 ME Ронколейкина и 16 мкг Доксорубицина, во второй группе по 600 ME Ронколейкина и Ингарона, в третьей группе по 450 ME Ронколейкина (3 инъекции) и Ингарона (3 инъекции) и 100 ME Рефнота (2 инъекции), в четвертой группе 32 мкг Доксорубицина. В динамике введения и после его окончания оценивают изменение объема опухоли, а после эвтаназии степень поражения легких метастазами, в результате чего устанавливают, что все сочетания препаратов тормозят рост опухоли в процессе введения, а также проявляют антиметастатический эффект разной степени выраженности.
Результаты исследования предствлены в таблице 1.
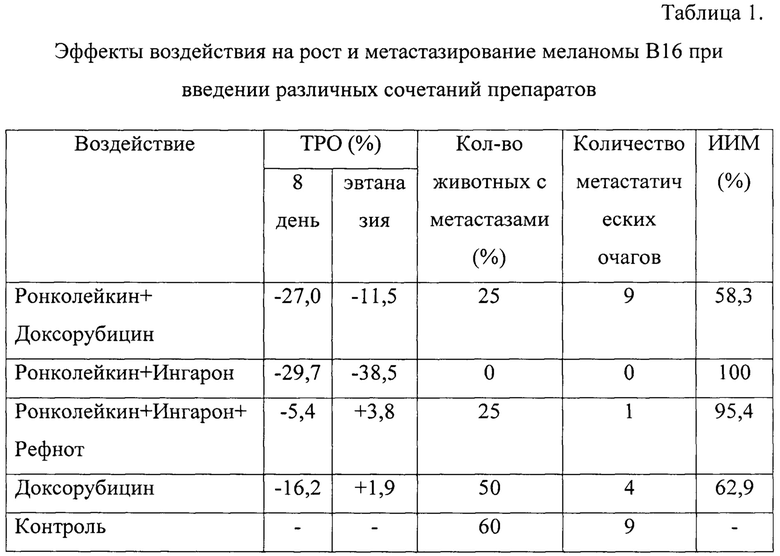
Из данных, представленных в таблице 1, видно, что максимальный эффект был достигнут при введении комбинации Ронколейкин + Ингарон: высокий процент ТРО как в процессе введения (29,7%), так и после окончания воздействия (38,5%), отсутствие животных с метастазами (ИИМ=100%). Подобный, но менее выраженный эффект обнаруживает и комбинация Ронколейкин + Доксорубицин: тормозит рост опухоли как в процессе введения (27%), так и после окончания воздействия (11,5%), и обнаруживает средний антиметастатический эффект (ИИМ=58,3%). Интересный эффект получен от воздействия 3-х иммуномодуляторов (Ронко + Инг + Реф): ярко выраженный антиметастатический эффект (ИИМ=95,4%) сопровождается лишь незначительным торможением роста первичного опухолевого очага (5,4% пока происходит воздействие). Под воздействием Доксорубицина получено хотя и более значительное торможение роста опухоли (16,2%) относительно воздействия трех иммуномодуляторов, однако антиметастатический эффект менее выражен (62,9%).
Технико-экономическая эффективность способа достижения антиметастатического эффекта в эксперименте заключается в возможности полного ингибирования метастазирования перевиваемой меланомы В16 цитокиновыми иммуномодуляторами путем их паратуморального введения мышам-опухоленосителям.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство для ингибирования метастазирования в легких | 2016 |
|
RU2632703C1 |
| Способ подавления роста меланомы В16 у лабораторных животных | 2022 |
|
RU2784443C2 |
| ИНГИБИТОР АНГИОГЕНЕЗА, АНТИАНГИОГЕННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2005 |
|
RU2287341C1 |
| АНТИМЕТАСТАТИЧЕСКАЯ КОМПОЗИЦИЯ | 2006 |
|
RU2308966C1 |
| Фармацевтическая композиция на основе соединения палладия | 2015 |
|
RU2613305C2 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО | 2016 |
|
RU2623034C1 |
| КОРРЕКТОР ПАРАНЕОПЛАСТИЧЕСКИХ ПОВРЕЖДЕНИЙ И ТОКСИЧЕСКИХ ЭФФЕКТОВ ЦИТОСТАТИЧЕСКОЙ ПОЛИХИМИОТЕРАПИИ | 2008 |
|
RU2385324C1 |
| Способ усиления противометастатического действия цисплатина и снижения его побочного действия на систему гемостаза | 2023 |
|
RU2825825C1 |
| СРЕДСТВО ДЛЯ ИНГИБИРОВАНИЯ МЕТАСТАЗИРОВАНИЯ В ЛЕГКИХ | 2021 |
|
RU2762730C1 |
| СПОСОБ КОМБИНИРОВАННОЙ ТЕРАПИИ МЕЛАНОМЫ В16 В МЕТРОНОМНОМ РЕЖИМЕ В ЭКСПЕРИМЕНТЕ | 2022 |
|
RU2792561C1 |
Изобретение относится к медицине, а именно к экспериментальным исследованиям в онкологии, и может быть использовано в разработке способов достижения антиметастатического эффекта. Способ включает паратуморальное введение иммуномодуляторов мышам-опухоленосителям с меланомой В16 через 10 дней после перевивки. Для этого поочередно через день вводят по 0,3 мл 150 МЕ «Ронколейкина» и 0,3 мл 150 МЕ «Ингарона» в течение 8 дней. Способ обеспечивает полное ингибирование метастазирования по сравнению с контрольной группой, а также тормозит рост опухоли. 1 табл.
Способ достижения антиметастатического эффекта в эксперименте, включающий паратуморальное введение иммуномодуляторов, отличающийся тем, что мышам-опухоленосителям с меланомой В16 через 10 дней после перевивки поочередно через день вводят по 0,3 мл 150 МЕ «Ронколейкина» и 0,3 мл 150 МЕ «Ингарона» в течение 8 дней.
| СПОСОБ ПРОФИЛАКТИКИ МЕТАСТАТИЧЕСКОГО ПОРАЖЕНИЯ ЛЕГКИХ В ЭКСПЕРИМЕНТЕ | 2013 |
|
RU2546034C1 |
| АНТИМЕТАСТАТИЧЕСКАЯ КОМПОЗИЦИЯ | 2006 |
|
RU2308966C1 |
| СПОСОБ ПОВЫШЕНИЯ ПРОТЕКТИВНОСТИ МЕЛИОИДОЗНЫХ АНТИГЕНОВ ЦИТОКИНАМИ | 2008 |
|
RU2376031C1 |
| CN 103933048 A, 23.07.2014 | |||
| KR 2016102829 A, 31.08.2016 | |||
| АРТАМОНОВА Е.В | |||
| Модификаторы биологических реакций (иммуномодуляторы, интерфероны, интерлейкины) в терапии злокачественных опухолей | |||
| Эффективная фармакотерапия., 2014, 14, с.8-21 | |||
| SIVEEN KS et al | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| Can J Physiol Pharmacol | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| ZHANG L et al | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| IUBMB Life | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
Авторы
Даты
2018-07-19—Публикация
2017-04-17—Подача