Изобретение относится к медицине, а именно к фармакологии, клинической фармакологии и онкологии, и может быть использовано в качестве средства для ингибирования метастазирования.
Интенсивное метастазирование является одной из главных причин смерти пациентов, имеющих злокачественные новообразования. Метастазирование в легкие одна из самых частых моделей метастазирования. Несмотря на некоторые успехи в лечении злокачественных новообразований, поиск новых антиметастатических веществ остается актуальной задачей экспериментальной фармакологии и онкологии.
Анализ современной литературы указывает на перспективность такого поиска среди оловоорганических соединений (ООС), содержащих, по крайней мере, одну связь «олово-углерод» [1, 2, 3].
Комбинация ООС с антиоксидантным фрагментом может привести к появлению кандидата с высокой противоопухолевой активностью против широкого спектра опухолей и, одновременно, к уменьшению их общей токсичности. Введение в молекулу ООС антиоксидантного фрагмента 2,6-ди-трет-бутилфенола является достоверным способом снижения токсичности исходного соединения [4].
Наиболее известными и используемыми синтетическими антиоксидантами являются соединения фенольного ряда. Будучи акцепторами свободных радикалов, антиоксиданты нашли широкое применение в качестве ингибиторов свободно-радикальных процессов с возможностью модулирования развития метастазирования [5].
Среди большого многообразия различных производных особое место занимают пространственно-затрудненные фенолы, в частности, производные 2,6-ди-трет-бутилфенола [6]. Из литературных данных известно, что синтезирован ряд ООС комплексов со связями Sn-S формул Me2Sn(SR)2; Et2Sn(SR)2; (n-Bu)2Sn(SR)2; Ph2Sn(SR)2; R2Sn(SR)2; Me3SnSR; Ph3SnSR (R=3,5-ди-трет-бутил-4-гидроксифенил), и охарактеризован элементным анализом, 1Н, 13С ЯМР и ИК спектроскопии [7]. Кристаллические структуры соединений были определены методом рентгеноструктурного анализа. Тетраэдрическая геометрия вокруг центра Sn в монокристаллах была подтверждена рентгеновской кристаллографией. Высокая антирадикальная активность комплексов была подтверждена спектрофотометрически в ДФПГ-тесте (ДФГТГ=дифенилпикрилгидразин). Было изучено сродство связывания ООС с тубулином за счет взаимодействия атома олова с SH-группами белка. Обнаружено, что ООС могут взаимодействовать с колхициновым сайтом тубулина, что делает их перспективными антимитотическими препаратами. Соединения были протестированы на их цитотоксичность in vitro в отношении клеток аденокарциномы молочной железы человека (MCF-7) и шейки матки человека (HeLa). Комплексы были также протестированы против нормальных клеток фибробластов легких плода человека (MRC-5). Комплексы проявляют значительно более низкую цитостатическую активность в отношении нормальной клеточной линии MRC-5 по сравнению с используемыми опухолевыми клеточными линиями MCF-7 и HeLa. Для комплекса трифенилолова определена высокая активность в отношении клеточных линий со значениями ИК50 250 нм (MCF-7) и 160 нм (HeLa) сооответственно, в то время как введение пространственно-затрудненных фенольных групп снижает цитотоксичность комплексов в отношении нормальных клеток.
Широко распространенным в клинической практике антиоксидантом является мексидол (3-окси-6-метил-2-этилпиридина сукцинат), который в силу его способности влиять на основные звенья патогенеза различных заболеваний, сопровождающихся окислительным стрессом и процессами свободнорадикального окисления, обладает широким спектром фармакологического действия. Для мексидола установлена способность ингибировать спонтанное метастазирование [8].
Техническим результатом изобретения является антиметастатическое средство, пригодное для внутрибрюшинного введения.
Технический результат достигается действием (3,5-ди-трет-бутил-4-гидроксифенилтиолат)трифенилолова (Ме5).
По своей структуре Ме5 гибридная молекула, содержащая и оловоорганический и протекторный антиоксидантный фрагмент 2,6-ди-трет-бутилфенола.
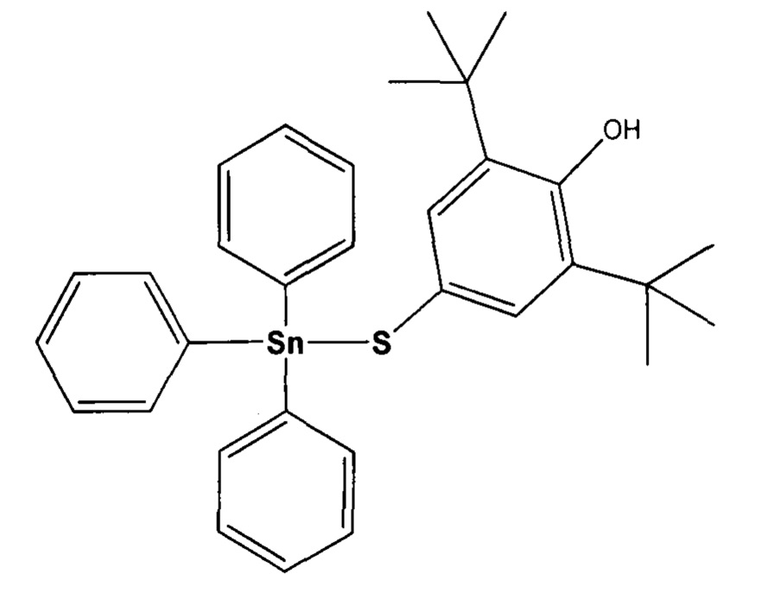
Ниже приведен пример синтеза (3,5-ди-трет-бутил-4-гидроксифенилтиолат)трифенилолова [7].
К раствору 193 мг (0,5 ммоль) Ph3SnCl и 119 мг (0,5 ммоль) 2,6-ди-трет-бутил-4-меркаптофенола в 4 мл метанола добавляли 0,5 мл (0,5 ммоль) 1М КОН, реакционную смесь перемешивали в течение 30 мин. Выпавший белый осадок отфильтровывали, промывали водой, петролейным эфиром. Осадок высушивали на воздухе в течение 24 ч. Выход 293 мг (74%). Тпл 158 -160°С.
ЯМР 1Н (δ, м.д., CDCl3): 1,22 (с, 18 Н, 4 С(СН3)3), 5,04 (с, 1 Н, 1 ОН), 7.11 (с, 2 Н, С6Н2), 7,34-7,54 (м, 15 Н, 3 С6Н5). 13С (δ, м.д.): 29,95 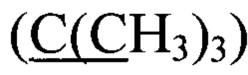 , 34,09
, 34,09 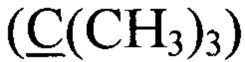 , 120.12 (С1), 128.73
, 120.12 (С1), 128.73 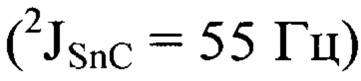 , 129.58 (С2), 132.07, 136.33, 136.75 (С2,
, 129.58 (С2), 132.07, 136.33, 136.75 (С2, 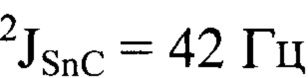 ), 137.97 (СЗ), 152.93 (С4).
), 137.97 (СЗ), 152.93 (С4).
ИК-спектр (см-1): 3619,7 (νOH): 2998,8-2871,5 (νCH): 1427,1; 1232,3; 727,0; 696,2; 449,3.
Найдено (%): С 65,53; Н 6,14. S, 5.26. Вычислено (%): С 65,43; Н 6,18. S, 5.46.C32H36OSSn.
Исследование ингибирующей активности.
Исследование антиметастатической активности Ме5 проведено на мышах-самках линии С57В1/6 с подкожно перевитой эпидермоидной карциномой легкого Lewis (36 животных), для которой характерно 100%-ное спонтанное метастазирование в легкие, с использованием внутрибрюшинного введения препарата.
Все манипуляции с животными, в том числе выведение из эксперимента, осуществляли в соответствии с правилами, принятыми «Европейской конвенцией по защите позвоночных животных, используемых для экспериментов или в иных научных целях».
Поддержание и перевивку опухолевого штамма осуществляли в соответствии с общепринятыми методами для линии С57В1/6.
Инокуляцию опухолевых клеток проводили подкожно в правую подмышечную область каждой мыши по 50 мг опухолевой взвеси в физиологическом растворе при разведении 1:10.
Через 48 часов после перевивки эпидермоидной карциномы легкого Lewis мышам-самкам линии С57В1/6 вводили:
1 группа животных - 1% - ный водный желатиновый раствор Ме5 в разовой дозе 50 мг/кг 1 раз в сутки в течение 5 дней (суммарная доза 250 мг/кг), внутрибрюшинно;
2 группа животных (группа сравнения) - мексидол (ФАРМАСОФТ, Россия), который применяли внутрибрюшинно в дозе 10 мг/кг 1 раз в сутки в течение 5 дней;
3 группа (контроль) - 1% - ный водный желатиновый раствор в эквивалентных объемах, внутрибрюшинно.
Через 21 день после перевивки опухоли всех животных подвергали эвтаназии в CO2 камере и проводили некропсию.
Полученные результаты показали, что показатель ингибирования метастазирования в группе животных, получивших Ме5 составил 68% (группа 1). У животных, получивших мексидол, показатель ингибирования метастазирования составил 42% (группа 2). Полученные результаты представлены в таблице № 1.
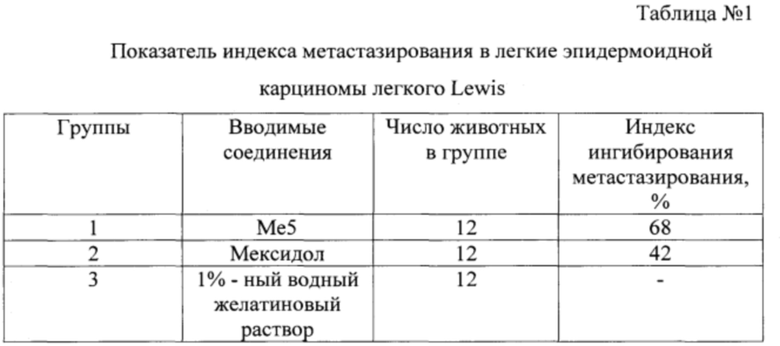
Таким образом, фармакологическая субстанция (3,5-ди-трет-бутил-4-гидроксифенилтиолат)трифенилолова (Ме5) при внутрибрюшинном применении значительно снижает количество и частоту метастазов эпидермоидной карциномы легкого Lewis в легкие у мышей, проявляя более выраженные антиметастатические свойства, чем мексидол.
Источники информации
1. In vitro cytotoxic activity of tri-n-butyltin(IV)lupinylsulfide hydrogen fumarate (IST-FS 35) and preliminary antitumor activity in vivo. Alama A, Viale M, Cilli M, Bruzzo C, Novelli F, Tasso B, Sparatore F. Invest New Drugs. 2009 Apr;27(2): 124-30. doi: 10.1007/sl0637-008-9148-x. Epub 2008 Jun 19. PMID: 18563295 [PubMed - indexed for MEDLINE].
2. Anticancer and cytotoxic effects of a triorganotin compound with 2-mercapto-nicotinic acid in malignant cell lines and tumor bearing Wistar rats. Verginadis II, Karkabounas S, Simos Y, Kontargiris E, Hadjikakou SK, Batistatou A, Evangelou A, Charalabopoulos K. Eur J Pharm Sci. 2011 Feb 14;42(3):253-61. doi: 10.1016/j.ejps.2010.11.015. Epub 2010 Dec 3. PMID: 21130873 [PubMed -indexed for MEDLINE].
3. Cytotoxicity in vitro and preliminary antitumor activity in vivo of a novel organotin compound. Barbieri F, Viale M, Sparatore F, Favre A, Cagnoli M, Bruzzo С, Novelli F, Alama A. Anticancer Res. 2000 Mar-Apr; 20(2A):977-80. PMID: 10810384 [PubMed - indexed for MEDLINE].
4. Снижение прооксидантной активности бутильных и фенильных производных олова в присутствии мезо-тетракис(3,5-ди-трет-бутил-4-гидроксифенил) порфирина. Коляда М.Н., Осипова В.П., Берберова Н.Т., Пименов Ю.Т., МилаеваЕ.Р. Макрогетероциклы. 2017. Т. 10. №1. С. 57-61.
5. Prasad S., Gupta S.C., Tyagi А.К. Reactive oxygen species (ROS) and cancer: Role of antioxidative nutraceuticals. Cancer Lett. 2016 Mar 29. pii: S0304-3835(16)30202-6. doi: 10.1016/j.canlet.2016.03.042.
6. Antonenko T.A., Shpakovsky D.B., Vorobyov M.A., Gracheva Yu A., Kharitonashvili E.V., Dubova L.G., Shevtsova E.F., Tafeenko V.A., Aslanov L.A., Iksanova A.G., Shtyrlin Yu G., Milaeva E.R. Antioxidative vs cytotoxic activities of organotin complexes bearing 2,6-di-tert-butylphenol moieties. Appl. Organomet. Chem. 2018; 32(7):e4381. DOI: 10.1002/aoc.4381.
7. D.B. Shpakovsky, C.N. Banti, E.M. Mukhatova, Yu.A. Gracheva, V.P. Osipova, N.T. Berberova, D.V. Albov, T.A. Antonenko, L.A. Aslanov, E.R. Milaeva, S.K. Hadjikakou, Synthesis, antiradical activity and in vitro cytotoxicity of novel organotin complexes based on 2,6-di-tert-butyl-4-mercaptophenol, Dalton Trans., 2014, 43, 6880-6890.
8. Скопин П.И. Влияние мексидола на антиметастатическую активность противоопухолевых препаратов. Аспирантский вестник Поволжья. - № 3-4. 2009. - с. 104-107.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО ДЛЯ ИНГИБИРОВАНИЯ МЕТАСТАЗИРОВАНИЯ В ЛЕГКИХ | 2021 |
|
RU2762730C1 |
| СПОСОБ КОМБИНИРОВАННОЙ ТЕРАПИИ МЕЛАНОМЫ В16 В МЕТРОНОМНОМ РЕЖИМЕ В ЭКСПЕРИМЕНТЕ | 2022 |
|
RU2792561C1 |
| Средство для ингибирования метастазирования в легких | 2016 |
|
RU2632703C1 |
| СРЕДСТВО ДЛЯ КОРРЕКЦИИ ЦИТОТОКСИЧЕСКИХ ЭФФЕКТОВ ПАРАНЕОПЛАСТИЧЕСКИХ ПРОЦЕССОВ И ХИМИОТЕРАПИИ, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2447888C1 |
| Средство, обладающее антипролиферативной и антиметастатической активностью по отношению к карциноме легкого Льюиса при внутрибрюшинном введении | 2022 |
|
RU2792144C1 |
| Средство на основе енаминогидразонотиазольного производного усниновой кислоты, обладающее способностью усиливать цитотоксическое, противоопухолевое и антиметастатическое действие топотекана | 2024 |
|
RU2833910C1 |
| Новые пространственно-затрудненные фенолы, содержащие бензофуроксановые фрагменты, обладающие противоопухолевой активностью | 2022 |
|
RU2796810C1 |
| СПОСОБ ДОСТИЖЕНИЯ АНТИМЕТАСТАТИЧЕСКОГО ЭФФЕКТА В ЭКСПЕРИМЕНТЕ | 2017 |
|
RU2661704C1 |
| ПРОТИВОВОСПАЛИТЕЛЬНОЕ СРЕДСТВО С АНТИКОАГУЛЯНТНОЙ, ПРОТИВООПУХОЛЕВОЙ И АНТИМЕТАСТАТИЧЕСКОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2412712C1 |
| Производные 2-аминохроменов проявляющие противоопухолевую активность. Фармацевтические композиции | 2018 |
|
RU2704262C1 |
Изобретение относится к применению (3,5-ди-трет-бутил-4-гидроксифенилтиолат)трифенилолова в качестве средства для ингибирования метастазирования эпидермоидной карциномы Lewis в легких. Технический результат: антиметастатическое средство, пригодное для внутрибрюшинного введения. 1 табл.
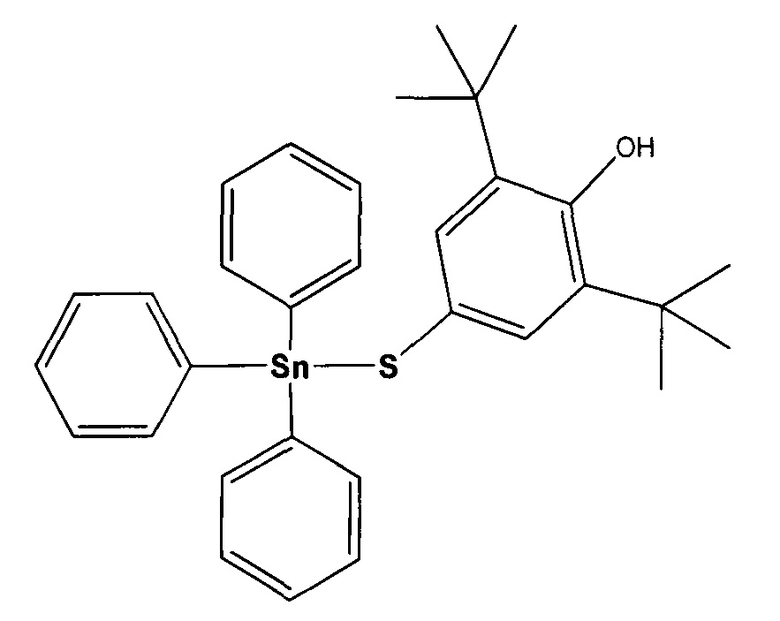
Применение (3,5-ди-трет-бутил-4-гидроксифенилтиолат)трифенилолова в качестве средства для ингибирования метастазирования эпидермоидной карциномы Lewis в легких.
| Средство для ингибирования метастазирования в легких | 2016 |
|
RU2632703C1 |
| D.B | |||
| Shpakovsky et al., "Synthesis, antiradical activity and in vitro cytotoxicity of novel organotin complexes based on 2,6-di-tert-butyl-4-mercaptophenol", Dalton Transactions, 2014, vol | |||
| Зубчатое колесо со сменным зубчатым ободом | 1922 |
|
SU43A1 |
| ГАЛЬВАНИЧЕСКАЯ БАТАРЕЯ | 1927 |
|
SU6880A1 |
| RU 2058165 C1, 20.04.1996 | |||
| Закром для пневматической подачи смески на чесальные аппараты | 1931 |
|
SU26946A1 |
| Прибор для разметки поперечного профиля шпалы перед ее вычесыванием | 1925 |
|
SU9873A1 |
Авторы
Даты
2022-02-07—Публикация
2021-03-30—Подача