УРОВЕНЬ ТЕХНИКИ
Рутин, О-гликозилсодержащий флавоноид, демонстрирует широкий спектр видов биологической активности.
Например, было показано, что он предупреждает образование кровяных сгустков. Предупреждение образования кровяных сгустков может помочь снизить вероятность развития угрожающих жизни состояний, таких как инфаркт миокарда, инсульт, легочная эмболия и тромбоз глубоких вен. См. Punithavathi et al., Cardiovasc. Toxicol., 2010, 10(3):181-189, Ortolani et al., Transplant Proc., 1995, 27 (5):2877-2888), Morling et al. 2013, Cochrane Database Syst. Rev. 4:Apr 30, и Morling et al., 2018, Cochrane Database Syst Rev. 11:Nov 8.
В другом примере рутин был протестирован для лечения хронической венозной недостаточности (CVI). CVI является распространенным состоянием, вызываемым дисфункцией клапанов с ассоциированной с ней обструкцией или без нее, обычно в нижних конечностях.
Однако рутин имеет низкую биодоступность вследствие плохого всасывания, которое ограничивает его потенциал в качестве терапевтического средства. Для повышения биодоступности рутина был разработан ферментативно модифицированный рутин (EMR) с более высокой растворимостью в воде. См. Toyo Sugar Refining Co., Ltd HP (альфа G-рутин). Тем не менее, EMR представляет собой смесь по меньшей мере трех биологически активных производных рутина. См. Akiyama et al., J. Food Hyg. Soc. Japan, 1999, 41:54-60. Является непрактичным использование такой смеси активных ингредиентов в качестве лекарственного средства у человека в соответствии с рекомендациями Федерального управления по лекарственным средствам США.
Существует необходимость в разработке композиций, демонстрирующих высокое пероральное всасывание рутина с улучшенной растворимостью в воде без описанных выше недостатков.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Для удовлетворения описанной выше потребности предусматривается растворимая в воде композиция, которая содержит рутин, L-аргинин и щелочную соль аскорбиновой кислоты. В композиции молярное соотношение между рутином, L-аргинином и щелочной солью аскорбиновой кислоты составляет 1: 1,6-3,0: 0,1-2,0.
Детали изобретения указаны в описании ниже. Другие признаки, задачи и преимущества изобретения станут очевидными из подробного описания, чертежей, и из прилагаемой формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Приведенное ниже описание относится к прилагаемым чертежам, среди которых:
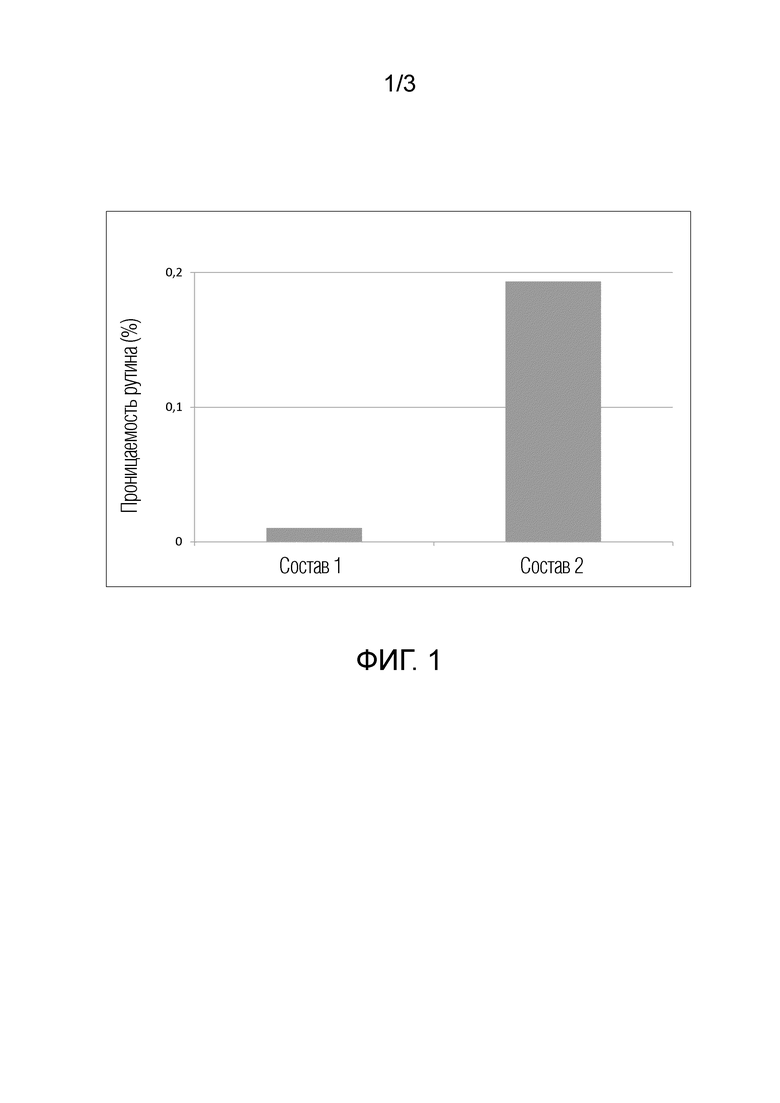
На фиг. 1 представлена столбиковая диаграмма, демонстрирующая проницаемость (%) состава 1 (рутин) и состава 2 (рутин/Arg) в клетки Сасо-2;
На фиг. 2 представлен график концентрации рутина в плазме против времени; и
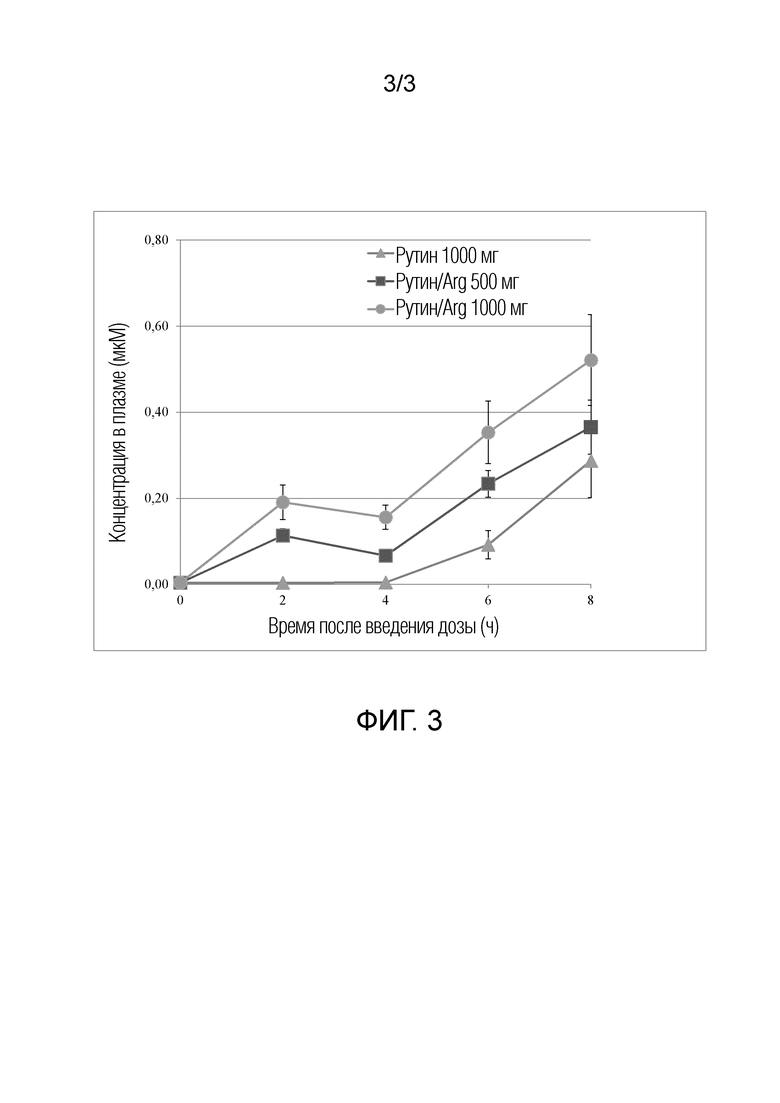
На фиг. 3 представлен график концентрации рутина в плазме против времени.
ПОДРОБНОЕ ОПИСАНИЕ
Как упоминалось выше, описана растворимая в воде композиция, которая содержит L-аргинин, рутин и щелочную соль аскорбиновой кислоты. Молярное соотношение между этими тремя компонентами составляет 1: 1,6-3,0: 0,1-2,0. В другой композиции по изобретению соотношение составляет 1: 1,8-2,8: 0,2-1,5. Иллюстративная растворимая в воде композиция содержит рутин, L-аргинин и щелочную соль аскорбиновой кислоты в молярном соотношении 1: 2,3: 0,42.
Примечательно, что щелочная соль аскорбиновой кислоты может представлять собой натриевую соль или калиевую соль. В конкретной композиции щелочная соль может представлять собой соль натрия.
Растворимая в воде фармацевтическая композиция также может включать витамин В1, витамин В3, витамин В6, витамин В9 или витамин В12, в дополнение к рутину, L-аргинину и щелочной соли аскорбиновой кислоты. Молярное соотношение рутина и каждого растворимого в воде витамина в композиции может составлять 1: 0,01-0,1.
Растворимые в воде композиции рутина, L-аргинина и щелочной соли аскорбиновой кислоты, описанные выше, можно получать способами, указанными в патентных заявках США №62/661255 и 62/720651 и международной заявке № РСТ/JP2019/017262, содержание которых включено в настоящее описание в качестве ссылок в полном объеме.
В растворимой в воде композиции рутина может присутствовать в количестве 10 масс. % или выше (например, 20 масс. % или выше, 30 масс. % или выше, и 50 масс. % или выше). L-аргинин также присутствует в количестве 10 масс. % или выше (например, 20 масс. % или выше, 30 масс. % или выше, и 50 масс. % или выше). Щелочная соль аскорбиновой кислоты присутствует в количестве 2 масс. % или выше (например, 4 масс. % или выше, 6 масс. % или выше, и 10 масс. % или выше).
Растворимая в воде композиция, либо в твердой форме, либо в жидкой форме, может быть включена в составы для фармацевтического, медицинского применения, для консервирования пищи или косметического применения.
Например, растворимая в воде композиция может быть составлена для перорального введения в качестве жидкости, капсулы, таблетки, пилюли или геля. Композиция в форме капсулы или таблетки может иметь кишечно-растворимое покрытие.
Составы для перорального введения также могут содержать фармацевтически активное вещество, фармацевтически приемлемый эксципиент или их комбинацию. Эти составы могут представлять собой фармацевтический препарат, пищевую добавку, натуральный медицинский продукт, косметический продукт, продукт питания или напиток.
При составлении для местного введения композиция может представлять собой раствор, линимент, лосьон, крем, мазь, пасту, гель или эмульгель. Составы для местного применения также могут содержать фармацевтически активное вещество, приемлемый для местного применения эксципиент или их комбинацию. Такие составы могут представлять собой косметический продукт, продукт для ухода за кожей или фармацевтический продукт.
Без дальнейших деталей полагают, что специалист в данной области может на основе приведенного выше описании использовать настоящее изобретение в его наиболее полной степени. Таким образом, приведенные ниже конкретные примеры следует истолковывать как только иллюстративные, но не ограничивающие оставшуюся часть изобретения никоим образом. Публикации, цитированные в настоящем описании, включены в настоящее описание в качестве ссылок в полном объеме.
ПРИМЕР 1: Получение водной композиции рутина/L-аргинина/аскорбиновой кислоты
Композицию, содержавшую рутин, L-аргинина и аскорбат, приготавливали в воде путем смешения 0,0071 моль рутина с водным раствором, содержавшим 0,020 моль L-аргинина, нагревания смеси до 80°С до полного растворения рутина и добавления 0,0010 моль аскорбата натрия.
После охлаждения описанного выше раствора проводили тестирование стабильности рутина посредством нагревания смеси до 50°С и количественного определения посредством ВЭЖХ интактного рутина, оставшегося через 0 ч, 5 ч и 24 ч. Результаты показали, что количество интактного рутина через 5 ч и 24 ч при 50°С составляло 100% и 97,2%, соответственно, от первоначального количества рутина в растворе.
Сходное испытание проводили для оценки стабильности флавоноида, родственного рутину, т.е. катехина, после растворения его L-аргинином и аскорбатом натрия. Количество интактного катехина, оставшееся в растворе через 5 ч и 24 ч при 50°С, составляло 30,8% и 2,3%, соответственно. Было совершенно неожиданным, что происходила деградация только 2,8% рутина через 24 ч, по сравнению с 97,7% катехина в идентичных условиях.
ПРИМЕР 2: Получение твердой композиции рутина/L-аргинина/аскорбиновой кислоты
Вторую композицию рутинна/L-аргинина/аскорбата получали, растворяя 125,0 г L-аргинина (0,72 моль) в 650 мл воды, нагретой до 45°С, добавляя 22,9 г натриевой соли L-аскорбиновой кислоты (0,12 моль) и 29,9 г гидрогенизированного декстрина и перемешивая до полного растворения.
К описанному раствору добавляли 170,3 г рутина тригидрата (0,26 моль) и полученную смесь нагревали при 80°С в течение 30 мин. После завершения растворения рутина раствор сушили распылением и просеивали через сито размера 8 0 с получением желто-оранжевой твердой композиции (326,9 г).
ПРИМЕР 3: Получение фармацевтических составов рутина
Составы рутин/аскорбат и рутин/L-аргинин/аскорбат получали с компонентами, представленными в таблице 1 ниже. Для исследований растворения составы использовали как есть. Для клинических испытаний составы инкапсулировали в устойчивые к кислотам капсулы гипромеллозы отсроченного высвобождения размера #1 (DRcaps™), производимые Capsugel.


ПРИМЕР 4: Испытание растворимости
Способность рутина растворяться в воде из состава 1 и состава 2 тестировали как указано ниже.
Каждое из количества состава 1, содержавшего 250 мг рутина, и количества состава 2, содержавшего 250 мг рутина, добавляли для отделения 25 мл дистиллированной H2O и встряхивали в течение 30 с. Аликвоту удаляли (0 мин.), после чего каждую смесь нагревали при 37°С при медленном перемешивании. Аликвоты собирали из каждой смеси через 5 мин и 30 мин после начала тепловой обработки. Каждую аликвоту пропускали через 0,4 5-мкм фильтр и измеряли концентрацию рутина в фильтрате посредством ВЭЖХ. Результаты представлены ниже в таблице 2.
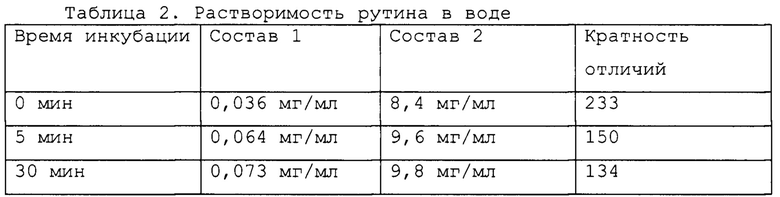
Результаты показали, что количество рутина, растворившегося из состава 2, т.е. рутин/L-аргинин/аскорбат, было в от 134 до 233 раз более высоким, чем количество рутина, растворившегося из состава 1, который свободен от L-аргинина. Очевидно, состав 2 содержит значительно более растворимый рутин, чем состав 1.
ПРИМЕР 5 Испытание проницаемости в клетках Сасо-2
Проникновение лекарственного средства в культивируемые клетки кишечника Сасо-2 определяют для прогнозирования относительной скорости всасывания лекарственного средства при пероральном введении.
Составы, описанные выше в примере 3, растворяли по отдельности в растворе. 500-мкл аликвоту каждого раствора добавляли на апикальную сторону клеток Сасо-2, которые культивировали в течение 19 суток, и 2000 мкл буфера HBSS помещали на базолатеральную сторону клеток. Клетки культивировали в инкубаторе в течение 2 часов при 37°С, после чего среду извлекали как с апикальной, так и с базолатеральной стороны клеток. Концентрацию рутина в среде определяли посредством ВЭЖХ, и степень всасывания с апикальной стороны на базолатеральную сторону определяли по следующему уравнению:

Результаты представлены на фиг. 1. Состав 2, который содержал рутин, L-аргинин и аскорбат, демонстрировал выраженное повышение проницаемости (всасывания) в 18 раз по сравнению с составом 1, который содержал рутин и аскорбат, но был лишен L-аргинина.
ПРИМЕР 6: Клиническое испытание фармакокинетики
Проводили рандомизированное клиническое фармакокинетическое испытание для сравнения двух различных составов рутина, описанных выше в примере 2, введенных в однократной дозе 8 добровольцам в условиях натощак. В испытании участвовали здоровые мужчины в возрасте от 25 до 39 лет включительно, имеющие величины индекса массы тела в диапазоне 18,6-24,7.
Капсулы, содержавшие составы 1 и 2, показанные в таблице 1, получали, как описано выше. Каждый доброволец принимал (i) четыре капсулы, содержавшие состав 1 (рутин/аскорбат; всего 1000 мг рутина), (ii) две капсулы, содержавшие состав 2 (рутин/L-аргинин/аскорбат; всего 500 мг рутина), или (iii) четыре капсулы состава 2 (рутин/L-аргинин/аскорбат; 1000 мг рутин) в течение трех суток тестирования, вводимых в соответствии с заранее рандомизированной последовательностью.
Уровни рутина измеряли в образцах крови, полученных от участников до дозирования (0 ч) и через 0,5 ч, 1 ч, 2 ч, 4 ч и 8 ч после дозирования в соответствии с общеизвестными методиками с удалением определенных образцов через 4 8 ч после дозирования. Более конкретно, для измерения уровней рутина плазму, полученную из каждого образца крови, сначала обрабатывали для расщепления рутина и его метаболитов на агликоны кверцетин и изорамнетин, которые затем количественно определяли посредством ВЭЖХ.
В кратком изложении, 200 мкл образцов плазмы смешивали с 10 мкл 10% дитиотреитола и 50 мкл уксусной кислоты в концентрации 0,58 моль/л. Смесь обрабатывали 100 Е бета-глкжуронидазы типа Н-5 (которая обладает активностью бета-глюкуронидазы и сульфатазы, т.е. активностью расщепления) в 0,1 М натрий-ацетатном буфере (рН5,0) в течение 120 мин при 37°С.
После расщепления к каждому образцу добавляли 500 мкл 10 мМ щавелевой кислоты и смесь центрифугировали при 10000 * g в течение 5 мин. Все обработанные образцы подвергали твердофазной экстракции с использованием предварительно кондиционированных кассет Oasis HLB в соответствии с инструкциями изготовителя (Waters, Milford MA USA). Экстрагированные элюаты упаривали в атмосфере азота и подвергали анализу посредством ВЭЖХ путем нанесения каждого элюита на колонку С18 (Waters ACQUITY UPLC ВЕН; 1,7 мкм, 2,1×100 мм), применения градиентной системы растворителей для ВЭЖХ из 0,1% муравьиной кислоты в H2O/ 0,1% муравьиной кислоты в ацетонитриле, и детекции присутствия кверцетина и изорамнетина с использованием ACQUITY UPLC I-class Plus⋅ Xevo TQ-S micro (Waters). Концентрацию каждого агликона вычисляли с использованием стандартной кривой, полученной с аутентичными внутренними стандартами кверцетина и изорамнетина. Предел анализа для кверцетина и изорамнетина в описанных выше условиях составлял 3,3 нМ.
Результаты представлены на фиг. 2 и 3.
На фиг. 2 представлена динамика концентраций в плазме конъюгированных метаболитов рутина в ходе периода 4 8 ч после израходования 500 мг рутина в качестве рутина/L-аргинина/аскорбата и после израсходования 1000 мг рутина также в качестве рутина/L-аргинина/аскорбата. Концентрация метаболитов в плазме стабильно возрастала, достигая максимального уровня через 8,5 ч (500 мг) и 9,3 ч (1000 мг) после приема. Уровни снизились до фонового уровня после этого через 24 ч.
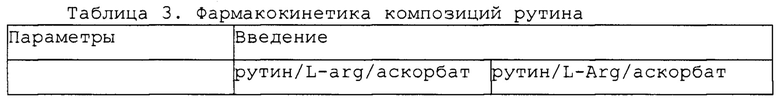
Фармакокинетические параметры, вычисленные из профилей, сходных с профилями, представленными на фиг. 2, представлены в таблице 3 ниже.

На фиг. 3 представлена динамика концентраций в плазме конъюгированных метаболитов рутина в ходе периода 8 ч после дозирования 500 мг рутина в качестве рутина/аскорбата, 500 мг рутина в качестве рутина/L-аргинина/аскорбата, и 1000 мг рутина также в качестве рутина/L-аргинина/аскорбата. Профиль фармакокинетики через 8 ч рутина/L-аргинина/аскорбата как в случае 500 мг, так и в случае 1000 мг, продемонстрировал появление метаболитов рутина в плазме значительно быстрее, чем появление метаболитов рутина без L-аргинина.
Фармакокинетические параметры, вычисленные из профилей, сходных с профилями, представленными на фиг. 3, представлены в таблице 4 ниже.
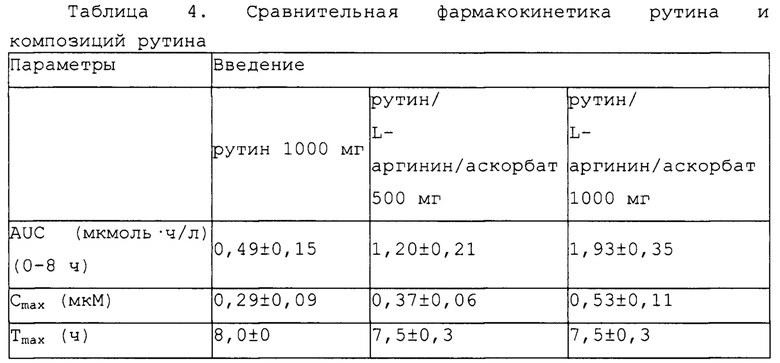
Вычисленная площадь под кривой (AUC) рутина/L-аргинина/аскорбата в количестве 500 мг и 1000 мг продемонстрировала зависимую от дозы взаимосвязь. Кроме того, AUC рутина/L-аргинина/аскорбата в количестве 500 мг и 1000 мг в моменты времени 0-8 ч была приблизительно в 2,5 и 4,0 раз более высокой, чем AUC рутина без L-аргинина, соответственно. Очевидно, всасывание рутина значительно повышалось посредством комбинирования его с L-аргинином и аскорбатом.
ДРУГИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
Все из признаков, описанных в описании, можно комбинировать в любой комбинации. Каждый признак, описанный в настоящем описании, может быть заменен альтернативным признаком, имеющим такое же, эквивалентное или сходное назначение. Таким образом, если нет иных явных указаний, каждый описанный признак является только примером общей серии эквивалентных или сходных признаков.
Кроме того, из приведенного выше описания специалист в данной области может без труда установить существенные характеристики настоящего изобретения и без отклонения от его сущности и объема и может внести различные изменения и модификации изобретения для адаптации его к различным применениям и условиям. Таким образом, также в объем формулы изобретения входят другие варианты осуществления.

Изобретение относится к фармацевтической промышленности, а именно к растворимой в воде фармацевтической композиции рутина. Растворимая в воде композиция рутина, содержащая рутин, L-аргинин и щелочную соль аскорбиновой кислоты, в которой молярное соотношение между рутином, L-аргинином и щелочной солью аскорбиновой кислоты составляет 1:1,6-3,0:0,1-2,0. Вышеописанная растворимая композиция рутина является стабильной. 17 з.п. ф-лы, 3 ил., 4 табл., 6 пр.
1. Растворимая в воде композиция рутина, содержащая рутин, L-аргинин и щелочную соль аскорбиновой кислоты, где молярное соотношение между рутином, L-аргинином и щелочной солью аскорбиновой кислоты составляет 1:1,6-3,0:0,1-2,0.
2. Растворимая в воде композиция рутина по п.1, где щелочная соль аскорбиновой кислоты представляет собой соль натрия или соль калия.
3. Растворимая в воде композиция рутина по п.2, где композиция представляет собой пероральный состав, выбранный из группы, состоящей из жидкости, капсулы, таблетки, пилюли и геля.
4. Растворимая в воде композиция рутина по п.2, где композиция представляет собой состав для местного применения, выбранный из группы, состоящей из раствора, линимента, лосьона, крема, мази, пасты, геля и эмульгеля.
5. Растворимая в воде композиция рутина по п.2, где композиция представляет собой пригодный для длительного хранения продукт питания.
6. Растворимая в воде композиция рутина по п.1, дополнительно содержащая витамин B1, витамин B3, витамин B6, витамин B9 или витамин B12.
7. Растворимая в воде композиция рутина по п.6, где композиция представляет собой пероральный состав, выбранный из группы, состоящей из жидкости, капсулы, таблетки, пилюли и геля.
8. Растворимая в воде композиция рутина по п.6, где композиция представляет собой состав для местного применения, выбранный из группы, состоящей из раствора, линимента, лосьона, крема, мази, пасты, геля и эмульгеля.
9. Растворимая в воде композиция рутина по п.2, дополнительно содержащая витамин B1, витамин B3, витамин B6, витамин B9 или витамин B12.
10. Растворимая в воде композиция рутина по п.1, где молярное соотношение между рутином, L-аргинином и щелочной солью аскорбиновой кислоты составляет 1:1,8-2,8:0,2-1,5.
11. Растворимая в воде композиция рутина по п.10, где молярное соотношение между рутином, L-аргинином и щелочной солью аскорбиновой кислоты составляет 1:2,3:0,42.
12. Растворимая в воде композиция рутина по п.10, где щелочная соль аскорбиновой кислоты представляет собой соль натрия или соль калия.
13. Растворимая в воде композиция рутина по п.10, где композиция представляет собой пероральный состав, выбранный из группы, состоящей из жидкости, капсулы, таблетки, пилюли и геля.
14. Растворимая в воде композиция рутина по п.10, где композиция представляет собой состав для местного применения, выбранный из группы, состоящей из раствора, линимента, лосьона, крема, мази, пасты, геля и эмульгеля.
15. Растворимая в воде композиция рутина по п.10, где композиция представляет собой средство, повышающее срок хранения, для продукта питания.
16. Растворимая в воде композиция рутина по п.10, дополнительно содержащая витамин B1, витамин B3, витамин B6, витамин B9 или витамин B12.
17. Растворимая в воде композиция рутина по п.16, где композиция представляет собой пероральный состав, выбранный из группы, состоящей из жидкости, капсулы, таблетки, пилюли и геля.
18. Растворимая в воде композиция рутина по п.16, где композиция представляет собой состав для местного применения, выбранный из группы, состоящей из раствора, линимента, лосьона, крема, мази, пасты, геля и эмульгеля.
| УСТАНОВКА И СПОСОБ НЕПРЕРЫВНОГО ТРАВЛЕНИЯ СТАЛЬНЫХ ПОЛОС | 2008 |
|
RU2451772C2 |
| Складной контейнер | 1982 |
|
SU1018896A1 |
| DE 202008006741 U1, 05.11.2009 | |||
| Устройство управления литьевой машиной | 1983 |
|
SU1164056A1 |
| СМОЛА ДЛЯ ПАСТЫ | 2014 |
|
RU2646428C2 |
| JPS 6176552 A, 19.04.1986 | |||
| Лекарственный препарат для профилактики и лечения токсического гепатита | 2016 |
|
RU2633590C1 |
Авторы
Даты
2021-12-30—Публикация
2020-09-15—Подача