ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет по временной патентной заявке США №62/610149, поданной 23 декабря 2017 года, временной патентной заявке США №62/650250, поданной 29 марта 2018 года, временной патентной заявке США №62/665445, поданной 1 мая 2018 года, временной патентной заявке США №62/680544, поданной 4 июня 2018 года, временной патентной заявке США №62/686656, поданной 18 июня 2018 года, временной патентной заявке США №62/688324, поданной 21 июня 2018 года, временной патентной заявке США №62/692623, поданной 29 июня 2018 года, временной патентной заявке США №62/745253, поданной 12 октября 2018 года, и временной патентной заявке США №62/757741, поданной 8 ноября 2018 года, полное содержание каждой из которых включено в настоящее описание в качестве ссылки для всех целей.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка включает список последовательностей, поданный в электронном виде в формате ASCII и включенный, таким образом, в настоящую заявку в качестве ссылки в полном объеме. Указанная копия ASCII, созданная 21 декабря 2018 года, названа 129267-00120_SL.txt и имеет размер 588687 байт.
УРОВЕНЬ ТЕХНИКИ
Активные иммунные ответы зависят от эффективного презентирования антигенов и костимуляторных сигналов антигенпрезентирующих клеток (APC). После интернализации антигена APC могут экспонировать антиген-главный комплекс гистосовместимости (MHC) класса I и II на мембране вместе с костимуляторными сигналами для активации антигенспецифических T-клеток, играющих роль в адаптивном иммунном ответе. In vivo индуцирование T-клеточных ответов в значительной степени зависит от взаимодействий с профессиональными антигенпрезентирующими клетками (APC), в частности, дендритными клетками (DC), презентирующими, например, опухолеспецифические антигены. Как правило, антигенспецифические T-клетки можно примировать и амплифицировать ex vivo перед их переносом обратно пациенту. Например, при адоптивном переносе клеток (ACT) опухолеспецифические T-клетки выделяют, а затем выращивают ex vivo для получения большого количества клеток для трансфузии. В качестве одного из типов APC, дендритные клетки (DC), как правило, используют для максимизации стимуляции T-клеток ex vivo. Однако, при использовании природных APC, таких как DC, возникают некоторые проблемы, включая отсутствие знаний об оптимальных нагруженных антигеном DC и получение неоднозначных результатов в клинических испытаниях (Steenblock E.R. et al., Expert Opin. Biol. Ther. 2009; 9: 451-464; Melief CMJ Immunity. 2008; 29: 372-383; Palucka K. and Banchereau J. Immunity. 2013; 39: 38-48). Кроме того, выделение и стимуляция ex vivo аутологичных DC требует большого количества времени и является дорогостоящей, кроме того, качество полученных ex vivo DC может быть непостоянным (Steenblock E.R. et al. 2009; Kim J.V. et al. Nat. Biotechnol. 2004; 22: 403-410). Таким образом, использование полученных из пациента аутологичных DC ограничивает стандартизацию протоколов лечения на основе DC (Steenblock E.R. et al. 2009; Kim J.V. et al. 2004).
Искусственные APC (aAPC) представляют собой инженерные платформы для активации и экспансии T-клеток, предназначенные для преодоления указанных выше проблем, при этом имитирующие взаимодействие между DC и T-клетками. Они включают множество систем, включая синтетические биоматериалы, сконструированные для активации и/или экспансии желаемых популяций иммунных клеток (например, T-клеток). Эти системы могут действовать, имитируя взаимодействие между DC и T-клетками. Например, разработано несколько жестких частиц размером с клетку, таких как латексные микрочастицы, покрытые полистиролом магнитные микрочастицы и биодеградируемые микрочастицы из сополимера молочной и гликолевой кислот. Эффективность этих частиц в индуцировании активации и/или экспансии иммунных клеток, по-видимому, в значительной степени зависит от свойств используемых материалов. Например, частицы размером более 200 нм, как правило, удерживаются в месте инокуляции, в то время как меньшие частицы могут захватываться DC (см., например, Reddy et al. (2006) J. Control. Release 112: 26-34). В отличие от этого, мембрана природных APC является гораздо более динамичной, чем внешняя поверхность этих частиц.
В этой области сохраняется потребность в создании улучшенных способов стимуляции T-клеток и введения в действие достаточных количеств терапевтических T-клеток для адоптивной иммунотерапии. Настоящее изобретение относится к новым и обладающим признаками изобретения терапевтическим средствам на основе эритроцитов (RCT), в частности, aAPC для имитации функции APC, таких как дендритные клетки (DC), для стимуляции T-клеток и индуцирования, например, иммунных ответов против опухоли или инфекционного заболевания или для супрессии активности T-клеток для профилактики, например, аутоиммунных нарушений.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к искусственным антигенпрезентирующим клеткам (aAPC), в частности, эритроидным клеткам и безъядерным клеткам (например, безъядерным эритроидным клеткам и тромбоцитам), сконструированным для активации или супрессии T-клеток. Сконструированные эритроидные клетки могут являться ядросодержащими, например, эритроцитарными клетками-предшественниками. Сконструированные эритроидные клетки могут являться безъядерными эритроидными клетками, например, ретикулоцитами или эритроцитами.
aAPC, представленные в настоящем описании, обладают многочисленными преимуществами относительно использования сферических наночастиц, таких как жесткие aAPC на основе частиц. Исключительно в качестве примера, внешняя поверхность наночастицы является жесткой и неподвижной и, таким образом, ограничивает движение полипептидов на ее поверхности, в то время как внешняя мембрана aAPC, как представлено в настоящем описании (т.е. эритроидной клетки или безъядерной клетки), является динамичной и текучей. Таким образом, aAPC по настоящему изобретению делает возможной более значительную молекулярную подвижность и более эффективную молекулярную реорганизацию по сравнению с наночастицами, что очень благоприятно для образования иммунологического синапса и стимуляции T-клеток.
Таким образом, в одном из аспектов настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает безъядерную клетку, где безъядерная клетка содержит на своей поверхности по меньшей мере один экзогенный антигенный полипептид, приведенный в таблице 1 или таблицах 14, 15 и 20-24. В некоторых вариантах осуществления по меньшей мере один экзогенный антигенный полипептид является опухолевым антигеном, антигеном аутоиммунного заболевания, вирусным антигеном, бактериальным антигеном или паразитарным антигеном. В некоторых вариантах осуществления по меньшей мере один экзогенный антигенный полипептид выбран из группы, состоящей из: меланома-ассоциированного антигена-A (MAGE-A), антигена протеазы гранул нейтрофилов, антигена NY-ESO-1/LAGE-2, антигена теломеразы, антигена гликопротеина 100 (gp100), антигена вируса Эпштейна-Барр (EBV), антигена вируса папилломы человека (HPV) и антигена вируса гепатита B (HBV).
В одном из аспектов настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает безъядерную клетку, где безъядерная клетка содержит на своей поверхности первый экзогенный антигенный полипептид и второй экзогенный антигенный полипептид, и где первый экзогенный антигенный полипептид и второй экзогенный антигенный полипептид имеют аминокислотные последовательности, перекрывающиеся по меньшей мере на 2 аминокислоты. В некоторых вариантах осуществления перекрывание составляет от 2 аминокислот до 23 аминокислот.
В некоторых вариантах осуществления первый экзогенный антигенный полипептид, второй экзогенный полипептид или первый и второй экзогенные антигенные полипептиды являются опухолевым антигеном, антигеном аутоиммунного заболевания, вирусным антигеном, бактериальным антигеном или паразитарным антигеном. В некоторых вариантах осуществления первый экзогенный антигенный полипептид, второй экзогенный полипептид или первый и второй экзогенные антигенные полипептиды представляют собой полипептид, приведенный в таблице 1 или таблицах 14, 15 и 20-24. В некоторых вариантах осуществления первый экзогенный антигенный полипептид, второй экзогенный полипептид или первый и второй экзогенные антигенные полипептиды выбраны из группы, состоящей из: меланома-ассоциированного антигена-A (MAGE-A), антигенов протеаз гранул нейтрофилов, антигенов NY-ESO-1/LAGE-2, антигенов теломеразы, антигенов гликопротеина 100 (gp100), антигенов вируса Эпштейна-Барр (EBV), антигенов вируса папилломы человека (HPV) и антигенов вируса гепатита B (HBV).
В некоторых вариантах осуществления aAPC дополнительно содержит на своей поверхности экзогенный антигенпрезентирующий полипептид. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом MHC класса I, одноцепочечным слитым белком MHC класса I, полипептидом MHC класса II или одноцепочечным слитым белком MHC класса II. В некоторых вариантах осуществления полипептид MHC класса I выбран из группы, состоящей из: HLA A, HLA B и HLA C. В некоторых вариантах осуществления полипептид MHC класса II выбран из группы, состоящей из: HLA-DPα, HLA-DPβ, HLA-DM, HLA DOA, HLA DOB, HLA DQα, HLA DQβ, HLA DRα и HLA DRβ.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает безъядерную клетку, где безъядерная клетка содержит на своей поверхности экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I или одноцепочечным слитым белком MHC класса II.
В некоторых вариантах осуществления одноцепочечный слитый белок MHC класса I содержит α-цепь и β2m-цепь. В некоторых вариантах осуществления одноцепочечный слитый белок MHC класса I дополнительно содержит мембранный якорь. В некоторых вариантах осуществления экзогенный антигенный полипептид соединяют с одноцепочечным слитым белком MHC класса I с помощью линкера. В некоторых вариантах осуществления линкер является расщепляемым линкером. В некоторых вариантах осуществления одноцепочечный слитый белок MHC класса II содержит α-цепь и β-цепь. В некоторых вариантах осуществления одноцепочечный слитый белок MHC класса II дополнительно содержит мембранный якорь. В некоторых вариантах осуществления экзогенный антигенный полипептид соединяют с одноцепочечным слитым белком MHC класса II с помощью линкера. В некоторых вариантах осуществления линкер является расщепляемым линкером. В некоторых вариантах осуществления якорь содержит белок гликофорин A (GPA) или трансмембранный домен небольшого интегрального мембранного белка 1 (SMIM1). В некоторых вариантах осуществления экзогенный антигенный полипептид связан с экзогенным антигенпрезентирующим полипептидом ковалентно. В некоторых вариантах осуществления экзогенный антигенный полипептид связан с экзогенным антигенпрезентирующим полипептидом нековалентно.
В некоторых вариантах осуществления aAPC дополнительно содержит на своей поверхности по меньшей мере один экзогенный костимуляторный полипептид. В некоторых вариантах осуществления по меньшей мере один экзогенный костимуляторный полипептид выбран из группы, состоящей из 4-1BBL, LIGHT, антитела против CD28, CD80, CD86, CD70, OX40L, GITRL, TIM4, SLAM, CD48, CD58, CD83, CD155, CD112, ИЛ-15Rα, слитого с ИЛ-15, ИЛ-21, ICAM-1, лиганда LFA-1, антитела против CD3 и их комбинации. В некоторых вариантах осуществления aAPC содержит на своей поверхности по меньшей мере два, по меньшей мере 3, по меньшей мере 4 или по меньшей мере 5 экзогенных костимуляторных полипептидов.
В некоторых вариантах осуществления aAPC дополнительно содержит на своей поверхности экзогенный цитокиновый полипептид. В некоторых вариантах осуществления экзогенный цитокиновый полипептид выбран из группы, состоящей из: ИЛ-2, ИЛ-15, ИЛ-Rα, слитого с ИЛ-15, ИЛ-7, ИЛ-12, ИЛ-18, ИЛ-21, ИЛ-4, ИЛ-6, ИЛ-23, ИЛ-27, ИЛ-17, ИЛ-10, TGF-бета, ИФН-гамма, ИЛ-1 бета, ГМ-КСФ и ИЛ-25.
В некоторых вариантах осуществления aAPC может активировать T-клетку, взаимодействующую с aAPC. В некоторых вариантах осуществления активация включает активацию CD8+ T-клеток, активацию CD4+ T-клеток, стимуляцию цитотоксической активности T-клеток, стимуляцию секреции цитокинов T-клетками и/или любую их комбинацию.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для супрессии активности T-клетки, где aAPC включает безъядерную клетку, где безъядерная клетка содержит на своей поверхности экзогенный антигенпрезентирующий полипептид, экзогенный антигенный полипептид и по меньшей мере один экзогенный коингибиторный полипептид, приведенный в таблице 7.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для супрессии активности T-клетки, где aAPC включает безъядерную клетку, где безъядерная клетка содержит на своей поверхности экзогенный антигенпрезентирующий полипептид, экзогенный антигенный полипептид, приведенный в таблице 1 или таблицах 16-19, и по меньшей мере один экзогенный коингибиторный полипептид.
В некоторых вариантах осуществления aAPC дополнительно содержит метаболит-изменяющий полипептид.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для супрессии активности T-клетки, где aAPC включает безъядерную клетку, где безъядерная клетка содержит на своей поверхности экзогенный антигенпрезентирующий полипептид, экзогенный антигенный полипептид и по меньшей мере один метаболит-изменяющий полипептид.
В некоторых вариантах осуществления aAPC дополнительно содержит экзогенный коингибиторный полипептид. В некоторых вариантах осуществления экзогенный коингибиторный полипептид является ИЛ-35, ИЛ-10, VSIG-3 или агонистом LAG3. В некоторых вариантах осуществления метаболит-изменяющий полипептид является IDO, Arg1, CD39, CD73, TDO, TPH, iNOS, COX2 или PGE-синтазой.
В некоторых вариантах осуществления aAPC может супрессировать T-клетку, взаимодействующую с aAPC. В некоторых вариантах осуществления супрессия включает ингибирование пролиферации T-клетки, анергию T-клетки или индуцирование апоптоза T-клетки. В некоторых вариантах осуществления T-клетка является CD4+ T-клеткой или CD8+ T-клеткой.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации регуляторной T-клетки (Treg-клетки), где aAPC включает безъядерную клетку, где безъядерная клетка содержит на своей поверхности экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид.
В некоторых вариантах осуществления aAPC дополнительно содержит на своей поверхности экзогенный полипептид для экспансии Treg. В некоторых вариантах осуществления экзогенный полипептид для экспансии Treg является CD25-специфическим ИЛ-2, TNFR2-специфическим ФНО, агонистом против DR3 (VEGI/TL1A-специфическим), 41BBL, TGFβ.
В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом MHC класса II или одноцепочечным слитым белком MHC класса II. В некоторых вариантах осуществления полипептид MHC класса II выбран из группы, состоящей из: HLA-DPα, HLA-DPβ, HLA-DM, HLA DOA, HLA DOB, HLA DQα, HLA DQβ, HLA DRα и HLA DRβ. В некоторых вариантах осуществления одноцепочечный слитый белок MHC класса II содержит α-цепь и β-цепь. В некоторых вариантах осуществления одноцепочечный слитый белок MHC класса II дополнительно содержит мембранный якорь. В некоторых вариантах осуществления экзогенный антигенный полипептид соединяют с одноцепочечным слитым белком MHC класса II с помощью линкера. В некоторых вариантах осуществления линкер является расщепляемым линкером. В некоторых вариантах осуществления якорь содержит белок гликофорин A (GPA) или трансмембранный домен небольшого интегрального мембранного белка 1 (SMIM1). В некоторых вариантах осуществления экзогенный антигенный полипептид связан с экзогенным антигенпрезентирующим полипептидом ковалентно. В некоторых вариантах осуществления экзогенный антигенный полипептид связан с экзогенным антигенпрезентирующим полипептидом нековалентно.
В некоторых вариантах осуществления экзогенный антигенный полипептид имеет длину от 8 аминокислот до 24 аминокислот.
В некоторых вариантах осуществления безъядерная клетка является безъядерной эритроидной клеткой или тромбоцитом.
В другом аспекте настоящее изобретение относится к способу активации антигенспецифической T-клетки, включающему приведение T-клетки в контакт с aAPC по любому из указанных выше аспектов и, таким образом, активацию антигенспецифической T-клетки.
В другом аспекте настоящее изобретение относится к способу индуцирования пролиферации T-клетки, экспрессирующей рецепторную молекулу, включающему приведение T-клетки в контакт с aAPC по любому из указанных выше аспектов, где костимуляторный полипептид специфически связывается с рецепторной молекулой, и, таким образом, индуцирование пролиферации указанной T-клетки.
В другом аспекте настоящее изобретение относится к способу экспансии субпопуляции из популяции T-клеток, включающему приведение популяции T-клеток, содержащей по меньшей мере одну T-клетку из субпопуляции, в контакт с aAPC по любому из указанных выше аспектов, где экзогенный костимуляторный полипептид, содержащийся на поверхности aAPC, специфически связывается с рецепторной молекулой по меньшей мере на одной T-клетке из субпопуляции, и где связывание экзогенного костимуляторного полипептида с рецепторной молекулой индуцирует пролиферацию по меньшей мере одной T-клетки из субпопуляции, и, таким образом, экспансию субпопуляции из популяции T-клеток.
В другом аспекте настоящее изобретение относится к способу супрессии активности T-клетки, включающему приведение T-клетки в контакт с aAPC по любому из указанных выше аспектов и, таким образом, супрессию активности T-клетки.
В другом аспекте настоящее изобретение относится к способу активации Treg-клетки, включающему приведение Treg-клетки в контакт с aAPC по любому из указанных выше аспектов и, таким образом, активацию Treg-клетки.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, нуждающегося в измененном иммунном ответе, включающему приведение T-клетки индивидуума в контакт с aAPC по любому из указанных выше аспектов и, таким образом, лечение индивидуума, нуждающегося в измененном иммунном ответе.
В некоторых вариантах осуществления приведение в контакт осуществляют in vitro. В некоторых вариантах осуществления приведение в контакт осуществляют in vivo.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, нуждающегося в измененном иммунном ответе, включающему: a) определение профиля экспрессии антигена на клетке индивидуума, b) селекцию искусственной антигенпрезентирующей клетки (aAPC), где aAPC является сконструированной безъядерной клеткой, содержащей на своей поверхности антигенпрезентирующий полипептид и по меньшей мере один первый экзогенный антигенный полипептид, и c) введение aAPC индивидууму и, таким образом, лечение индивидуума, нуждающегося в измененном иммунном ответе.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, нуждающегося в измененном иммунном ответе, включающему: a) определение статуса HLA индивидуума, b) селекцию искусственной антигенпрезентирующей клетки (aAPC), иммунологически совместимой с индивидуумом, где aAPC является сконструированной безъядерной клеткой, содержащей на своей поверхности по меньшей мере один первый экзогенный антигенный полипептид и по меньшей мере один антигенпрезентирующий полипептид, и c) введение aAPC индивидууму и, таким образом, лечение индивидуума, нуждающегося в измененном иммунном ответе.
В некоторых вариантах осуществления индивидуум нуждается в повышенном иммунном ответе. В некоторых вариантах осуществления индивидуум имеет злокачественное новообразование или инфекционное заболевание. В некоторых вариантах осуществления индивидуум нуждается в сниженном иммунном ответе. В некоторых вариантах осуществления индивидуум имеет аутоиммунное заболевание или аллергическое заболевание.
В другом аспекте настоящее изобретение относится к способу индуцирования T-клеточного ответа на антиген у нуждающегося в этом индивидуума, включающему: получение популяции клеток из индивидуума, где популяция включает T-клетку, приведение популяции клеток в контакт с aAPC по любому из указанных выше аспектов, где приведение популяции клеток в контакт с aAPC индуцирует пролиферацию антигенспецифической T-клетки, являющейся специфической по меньшей мере к одному экзогенному антигенному полипептиду, и введение антигенспецифической T-клетки индивидууму и, таким образом, индуцирование T-клеточного ответа на антиген у нуждающегося в этом индивидуума. В некоторых вариантах осуществления способ дополнительно включает выделение антигенспецифической T-клетки из популяции клеток.
В другом аспекте настоящее изобретение относится к способу экспансии популяции регуляторных T-клеток (Treg), включающему: получение популяции клеток из индивидуума, где популяция включает Treg-клетку, приведение популяции в контакт с aAPC по любому из указанных выше аспектов, где приведение популяции в контакт с aAPC индуцирует пролиферацию Treg-клетки, и, таким образом, экспансию популяции Treg-клеток. В некоторых вариантах осуществления способ дополнительно включает выделение Treg-клетки из популяции клеток. В некоторых вариантах осуществления способ дополнительно включает введение Treg-клетки индивидууму.
В другом аспекте настоящее изобретение относится к способу получения aAPC по любому из указанных выше аспектов, включающему: встраивание экзогенной нуклеиновой кислоты, кодирующей экзогенный антигенный полипептид в ядросодержащую клетку; и культивирование ядросодержащей клетки в условиях, подходящих для энуклеации и продукции экзогенного антигенного полипептида, и, таким образом, получение безъядерной клетки и, таким образом, получение aAPC.
В одном из вариантов осуществления ядросодержащая клетка является ядросодержащей эритроидной клеткой-предшественником. В одном из вариантов осуществления безъядерная клетка (например, сконструированная безъядерная клетка) является безъядерной эритроидной клеткой, например, эритроцитом или ретикулоцитом. В одном из вариантов осуществления безъядерная клетка (например, сконструированная безъядерная клетка) является тромбоцитом.
В другом аспекте настоящее изобретение относится к способу получения aAPC по любому из указанных выше аспектов, включающему: встраивание экзогенной нуклеиновой кислоты, кодирующей экзогенный антигенпрезентирующий полипептид, в ядросодержащую клетку; культивирование ядросодержащей клетки в условиях, подходящих для энуклеации и продукции экзогенного антигенпрезентирующего полипептида, и, таким образом, получение безъядерной клетки; и приведение безъядерной клетки в контакт с по меньшей мере одним экзогенным антигенным полипептидом, где по меньшей мере один экзогенный антигенный полипептид связывается с экзогенным антигенпрезентирующим полипептидом, презентируемым на поверхности безъядерной клетки, и, таким образом, получение aAPC.
В одном из вариантов осуществления по меньшей мере один экзогенный антигенный полипептид специфически связывается с экзогенным антигенпрезентирующим полипептидом, презентируемым на поверхности безъядерной клетки.
В одном из вариантов осуществления ядросодержащая клетка является ядросодержащей эритроидной клеткой-предшественником. В одном из вариантов осуществления безъядерная клетка (например, сконструированная безъядерная клетка) является безъядерной эритроидной клеткой, например, эритроцитом или ретикулоцитом. В одном из вариантов осуществления безъядерная клетка (например, сконструированная безъядерная клетка) является тромбоцитом.
В другом аспекте настоящее изобретение относится к способу получения aAPC по любому из указанных выше аспектов, включающему: встраивание экзогенной нуклеиновой кислоты, кодирующей экзогенный антигенный полипептид, в ядросодержащую клетку; встраивание экзогенной нуклеиновой кислоты, кодирующей экзогенный антигенпрезентирующий полипептид, в ядросодержащую клетку; и культивирование ядросодержащей клетки в условиях, подходящих для энуклеации и продукции экзогенного антигенного полипептида и экзогенного антигенпрезентирующего полипептида, и, таким образом, получение безъядерной клетки, и, таким образом, получение aAPC.
В одном из вариантов осуществления ядросодержащая клетка является ядросодержащей эритроидной клеткой-предшественником. В одном из вариантов осуществления безъядерная клетка (например, сконструированная безъядерная клетка) является безъядерной эритроидной клеткой, например, эритроцитом или ретикулоцитом. В одном из вариантов осуществления безъядерная клетка (например, сконструированная безъядерная клетка) является тромбоцитом.
В некоторых вариантах осуществления экзогенная нуклеиновая кислота содержит ДНК. В некоторых вариантах осуществления экзогенная нуклеиновая кислота содержит РНК.
В некоторых вариантах осуществления стадия встраивания включает вирусную трансдукцию. В некоторых вариантах осуществления стадия встраивания включает электропорацию. В некоторых вариантах осуществления стадия встраивания включает использование одного или более из: опосредованного липосомами переноса, аденовируса, аденоассоциированного вируса, вируса герпеса, вектора на основе ретровируса, липофекции и лентивирусных векторов.
В другом аспекте настоящее изобретение относится к способу получения иммунологически совместимой искусственной антигенпрезентирующей клетки (aAPC), где aAPC включает безъядерную клетку, содержащую на поверхности клетки экзогенный антигенный полипептид, включающему: приведение ядросодержащей клетки в контакт с нуклеазой и по меньшей мере одной гРНК, расщепляющими эндогенную нуклеиновую кислоту, что приводит к продукции эндогенного антигенпрезентирующего полипептида, эндогенного якорного полипептида или эндогенного костимуляторного полипептида или что приводит к ингибированию экспрессии эндогенной микроРНК; встраивание экзогенной нуклеиновой кислоты, кодирующей экзогенный антигенный полипептид, в ядросодержащую клетку; и культивирование ядросодержащей клетки в условиях, подходящих для энуклеации и продукции и презентирования экзогенного антигенного полипептида с помощью эндогенного антигенпрезентирующего полипептида, и, таким образом, получение безъядерной клетки, и, таким образом, получение иммунологически совместимой aAPC.
В некоторых вариантах осуществления экзогенную нуклеиновую кислоту приводят в контакт с нуклеазой и по меньшей мере одной гРНК.
В еще одном аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку или безъядерную клетку, где эритроидная клетка или безъядерная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, приведенный в таблице 1.
В некоторых вариантах осуществления по меньшей мере один экзогенный антигенный полипептид является опухолевым антигеном, антигеном аутоиммунного заболевания, вирусным антигеном, бактериальным антигеном или паразитарным антигеном.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку или безъядерную клетку, где эритроидная клетка или безъядерная клетка презентирует, например, содержит на своей поверхности, первый экзогенный антигенный полипептид и второй экзогенный антигенный полипептид, и где первый экзогенный антигенный полипептид и второй экзогенный антигенный полипептид имеют аминокислотные последовательности, перекрывающиеся по меньшей мере на 2 аминокислоты.
В некоторых вариантах осуществления перекрывание составляет от 2 аминокислот до 23 аминокислот.
В некоторых вариантах осуществления aAPC дополнительно презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид.
В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом MHC класса I, одноцепочечным слитым белком MHC класса I, полипептидом MHC класса II или одноцепочечным слитым белком MHC класса II.
В некоторых вариантах осуществления полипептид MHC класса I выбран из группы, состоящей из: HLA A, HLA B и HLA C.
В некоторых вариантах осуществления полипептид MHC класса II выбран из группы, состоящей из: HLA-DPα, HLA-DPβ, HLA-DM, HLA DOA, HLA DOB, HLA DQα, HLA DQβ, HLA DRα и HLA DRβ.
В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления эритроидная клетка является безъядерной эритроидной клеткой.
В еще одном аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку или безъядерную клетку, где эритроидная клетка или безъядерная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I или одноцепочечным слитым белком MHC класса II, где, например, экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом.
В некоторых вариантах осуществления одноцепочечный слитый белок MHC класса I содержит якорь, α-цепь и β2m-цепь. В некоторых вариантах осуществления экзогенный антигенный полипептид соединяют с одноцепочечным слитым белком MHC I с помощью линкера. В некоторых вариантах осуществления линкер является расщепляемым линкером.
В некоторых вариантах осуществления одноцепочечный слитый белок MHC класса II содержит якорь, α-цепь и β-цепь. В некоторых вариантах осуществления экзогенный антигенный полипептид соединяют с одноцепочечным слитым белком MHC класса II с помощью линкера. В некоторых вариантах осуществления линкер является расщепляемым линкером. В некоторых вариантах осуществления якорь является мембранным белком типа 1. В некоторых вариантах осуществления якорь является мембранным белком типа 2. В некоторых вариантах осуществления якорь является GPI-связанным белком. В некоторых вариантах осуществления якорь является GPA или SMIM1.
В некоторых вариантах осуществления экзогенный антигенный полипептид связан с экзогенным антигенпрезентирующим полипептидом. В некоторых вариантах осуществления экзогенный антигенный полипептид связан с экзогенным антигенпрезентирующим полипептидом ковалентно или нековалентно.
В некоторых вариантах осуществления aAPC по любому из указанных выше аспектов дополнительно презентирует, например, содержит на своей поверхности по меньшей мере один экзогенный костимуляторный полипептид.
В некоторых вариантах осуществления по меньшей мере один экзогенный костимуляторный полипептид выбран из группы, состоящей из 4-1BBL, LIGHT, антитела против CD28, CD80, CD86, CD70, OX40L, GITRL, TIM4, SLAM, CD48, CD58, CD83, CD155, CD112, ИЛ-7, ИЛ-12, ИЛ-15Rα, слитого с ИЛ-15, ИЛ-21, ICAM-1, лиганда LFA-1, антитела против CD3 и их комбинации.
В некоторых вариантах осуществления aAPC презентирует, например, содержит на своей поверхности, по меньшей мере два, по меньшей мере 3, по меньшей мере 4 или по меньшей мере 5 экзогенных костимуляторных полипептидов.
В некоторых вариантах осуществления aAPC может активировать T-клетку, взаимодействующую с aAPC. В некоторых вариантах осуществления активация включает активацию CD8+ T-клеток, активацию CD4+ T-клеток, стимуляцию цитотоксической активности T-клеток, стимуляцию секреции цитокинов T-клетками и/или любую их комбинацию.
В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления, эритроидная клетка является безъядерной эритроидной клеткой.
В другом аспекте, настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для супрессии активности T-клетки, где aAPC включает эритроидную клетку или безъядерную клетку, где эритроидная клетка или безъядерная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, экзогенный антигенный полипептид и по меньшей мере один экзогенный коингибиторный полипептид, приведенный в таблице 7, где, например, экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом. В некоторых вариантах осуществления эритроидная клетка является безъядерной эритроидной клеткой.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для супрессии активности T-клетки, где aAPC включает эритроидную клетку или безъядерную клетку, где эритроидная клетка или безъядерная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, экзогенный антигенный полипептид, приведенный в таблице 1, и по меньшей мере один экзогенный коингибиторный полипептид, где, например, экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом. В некоторых вариантах осуществления эритроидная клетка является безъядерной эритроидной клеткой.
В некоторых вариантах осуществления aAPC дополнительно содержит метаболит-изменяющий полипептид.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для супрессии активности T-клетки, где aAPC включает эритроидную клетку или безъядерную клетку, где эритроидная клетка или безъядерная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, экзогенный антигенный полипептид и по меньшей мере один метаболит-изменяющий полипептид, где, например, экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом.
В некоторых вариантах осуществления aAPC дополнительно содержит экзогенный коингибиторный полипептид. В некоторых вариантах осуществления экзогенный коингибиторный полипептид является ИЛ-35, ИЛ-10, VSIG-3, PD-L1 или агонистом LAG3.
В некоторых вариантах осуществления метаболит-изменяющий полипептид является IDO, Arg1, CD39, CD73, TDO, TPH, iNOS, COX2 или PGE-синтазой.
В некоторых вариантах осуществления aAPC может супрессировать T-клетку, взаимодействующую с aAPC.
В некоторых вариантах осуществления супрессия включает ингибирование пролиферации T-клетки, анергию T-клетки или индуцирование апоптоза T-клетки. В некоторых вариантах осуществления T-клетка является CD4+ T-клеткой или CD8+ T-клеткой.
В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления эритроидная клетка является безъядерной эритроидной клеткой.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации регуляторной T-клетки (Treg-клетки), где aAPC включает эритроидную клетку или безъядерную клетку, где эритроидная клетка или безъядерная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где, например, экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом.
В некоторых вариантах осуществления aAPC дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид для экспансии Treg.
В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом MHC класса II или одноцепочечным слитым белком MHC класса II. В некоторых вариантах осуществления полипептид MHC класса II выбран из группы, состоящей из: HLA-DPα, HLA-DPβ, HLA-DM, HLA DOA, HLA DOB, HLA DQα, HLA DQβ, HLA DRα и HLA DRβ. В некоторых вариантах осуществления одноцепочечный слитый белок MHC класса II содержит якорь, α-цепь и β-цепь.
В некоторых вариантах осуществления экзогенный антигенный полипептид соединяют с одноцепочечным слитым белком MHC класса II с помощью линкера. В некоторых вариантах осуществления линкер является расщепляемым линкером.
В некоторых вариантах осуществления якорь является GPA или SMIM1.
В некоторых вариантах осуществления экзогенный антигенный полипептид связан с экзогенным антигенпрезентирующим полипептидом. В некоторых вариантах осуществления экзогенный антигенный полипептид связан с экзогенным антигенпрезентирующим полипептидом ковалентно или нековалентно.
В некоторых вариантах осуществления экзогенный полипептид для экспансии Treg является ИЛ-2, CD25-специфическим ИЛ-2, TNFR2-специфическим ФНО, агонистом против DR3 (VEGI/TL1A-специфическим), 4-1BBL, TGFβ.
В некоторых вариантах осуществления экзогенный антигенный полипептид имеет длину от 8 аминокислот до 24 аминокислот.
В некоторых вариантах осуществления безъядерная клетка является эритроидной клеткой или тромбоцитом.
В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления эритроидная клетка является безъядерной эритроидной клеткой.
В другом аспекте настоящее изобретение относится к способу активации антигенспецифической T-клетки, включающему приведение T-клетки в контакт с aAPC, представленной в настоящем описании, и, таким образом, активацию антигенспецифической T-клетки.
В другом аспекте настоящее изобретение относится к способу индуцирования пролиферации T-клетки, экспрессирующей рецепторную молекулу, включающему приведение T-клетки в контакт с aAPC, представленной в настоящем описании, где костимуляторный полипептид специфически связывается с рецепторной молекулой, таким образом, индуцируя пролиферацию указанной T-клетки.
В другом аспекте настоящее изобретение относится к способу экспансии субпопуляции популяции T-клеток, включающему приведение популяции T-клеток, содержащих по меньшей мере одну T-клетку из субпопуляции, в контакт с aAPC, представленной в настоящем описании, где экзогенный костимуляторный полипептид, презентируемый на aAPC, специфически связывается с рецепторной молекулой по меньшей мере на одной T-клетке из субпопуляции, и где связывание экзогенного костимуляторного полипептида с рецепторной молекулой индуцирует пролиферацию по меньшей мере одной T-клетки из субпопуляции, и, таким образом, экспансию субпопуляции популяции T-клеток.
В другом аспекте настоящее изобретение относится к способу супрессии активности T-клеток, включающему приведение T-клетки в контакт с aAPC, представленной в настоящем описании и, таким образом, супрессию активности T-клетки.
В другом аспекте настоящее изобретение относится к способу активации Treg-клетки, включающему приведение Treg-клетки в контакт с aAPC, представленной в настоящем описании, и, таким образом, активацию Treg-клетки.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, нуждающегося в измененном иммунном ответе, включающему приведение T-клетки индивидуума в контакт с aAPC, представленной в настоящем описании, и, таким образом, лечение индивидуума, нуждающегося в измененном иммунном ответе.
В некоторых вариантах осуществления приведение в контакт осуществляют in vitro или in vivo.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, нуждающегося в измененном иммунном ответе, включающему: a) определение профиля экспрессии антигена на клетке индивидуума; b) селекцию искусственной антигенпрезентирующей клетки (aAPC), где aAPC является сконструированной эритроидной клеткой, экспрессирующей антигенпрезентирующий полипептид и по меньшей мере один первый экзогенный антигенный полипептид; и c) введение aAPC индивидууму и, таким образом, лечение индивидуума, нуждающегося в измененном иммунном ответе.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, нуждающегося в измененном иммунном ответе, включающему: a) определение статуса HLA индивидуума; b) селекцию искусственной антигенпрезентирующей клетки (aAPC), иммунологически совместимой с индивидуумом, где aAPC является сконструированной эритроидной клеткой, экспрессирующей по меньшей мере один первый экзогенный антигенный полипептид и по меньшей мере один антигенпрезентирующий полипептид; и c) введение aAPC индивидууму и, таким образом, лечение индивидуума, нуждающегося в измененном иммунном ответе.
В некоторых вариантах осуществления индивидуум нуждается в повышенном иммунном ответе. В некоторых вариантах осуществления индивидуум имеет злокачественное новообразование или инфекционное заболевание. В некоторых вариантах осуществления индивидуум нуждается в сниженном иммунном ответе. В некоторых вариантах осуществления индивидуум имеет аутоиммунное заболевание или аллергическое заболевание.
В другом аспекте настоящее изобретение относится к способу индуцирования T-клеточного ответа на антиген у нуждающегося в этом индивидуума, включающему: получение популяции клеток из индивидуума, где популяция включает T-клетку; приведение популяции клеток в контакт с aAPC, представленной в настоящем описании, где приведение популяции клеток в контакт с aAPC индуцирует пролиферацию антигенспецифической T-клетки, специфической в отношении по меньшей мере одного экзогенного антигенного полипептида, и введение антигенспецифической T-клетки индивидууму и, таким образом, индуцирование T-клеточного ответа на антиген у нуждающегося в этом индивидуума.
В некоторых вариантах осуществления способ дополнительно включает выделение антигенспецифической T-клетки из популяции клеток.
В другом аспекте настоящее изобретение относится к способу экспансии популяции регуляторных T-клеток (Treg), включающему: получение популяции клеток из индивидуума, где популяция включает Treg-клетку; приведение популяции в контакт с aAPC, представленной в настоящем описании, где приведение популяции в контакт с aAPC индуцирует пролиферацию Treg-клетки, и, таким образом, экспансию популяции Treg-клеток.
В некоторых вариантах осуществления способ дополнительно включает выделение Treg-клетки из популяции клеток.
В некоторых вариантах осуществления способ дополнительно включает введение Treg-клетки индивидууму.
В некоторых вариантах осуществления каждого из указанных выше способов эритроидная клетка является безъядерной эритроидной клеткой.
В другом аспекте настоящее изобретение относится к способу получения aAPC по настоящему изобретению, включающему: встраивание экзогенной нуклеиновой кислоты, кодирующей экзогенный антигенный полипептид, в ядросодержащую клетку; и культивирование ядросодержащей клетки в условиях, подходящих для экспрессии и презентирования экзогенного антигенного полипептида и энуклеации, и, таким образом, получение безъядерной клетки, и, таким образом, получение aAPC.
В другом аспекте настоящее изобретение относится к способу получения aAPC по настоящему изобретению, включающему: встраивание экзогенной нуклеиновой кислоты, кодирующей экзогенный антигенпрезентирующий полипептид, в ядросодержащую клетку; культивирование ядросодержащей клетки в условиях, подходящих для экспрессии и презентирования экзогенного антигенпрезентирующего полипептида и энуклеации, и, таким образом, получение безъядерной клетки; и приведение безъядерной клетки в контакт с по меньшей мере одним экзогенным антигенным полипептидом, где по меньшей мере один экзогенный антигенный полипептид связывается с экзогенным антигенпрезентирующим полипептидом, презентируемым на безъядерной клетке, и, таким образом, получение aAPC.
В некоторых вариантах осуществления экзогенная нуклеиновая кислота содержит ДНК или РНК.
В некоторых вариантах осуществления стадия встраивания включает вирусную трансдукцию. В некоторых вариантах осуществления стадия встраивания включает электропорацию. В некоторых вариантах осуществления стадия встраивания включает использование одного или более из: опосредованного липосомами переноса, аденовируса, аденоассоциированного вируса, вируса герпеса, вектора на основе ретровируса, липофекции и лентивирусного вектора.
В другом аспекте настоящее изобретение относится к способу получения иммунологически совместимой искусственной антигенпрезентирующей клетки (aAPC), где aAPC включает безъядерную клетку, презентирующую, например, содержащую на своей поверхности, экзогенный антигенный полипептид, включающему: приведение ядросодержащей клетки в контакт с нуклеазой и по меньшей мере одной гРНК, расщепляющими эндогенную нуклеиновую кислоту, что приводит к экспрессии эндогенного антигенпрезентирующего полипептида, эндогенного якорного полипептида или эндогенного костимуляторного полипептида или что приводит к ингибированию экспрессии эндогенной микроРНК; встраивание экзогенной нуклеиновой кислоты, кодирующей экзогенный антигенный полипептид, в ядросодержащую клетку; и культивирование ядросодержащей клетки в условиях, подходящих для экспрессии и презентирования экзогенного антигенного полипептида с помощью эндогенного антигенпрезентирующего полипептида и энуклеации, и, таким образом, получение безъядерной клетки, и, таким образом, получение иммунологически совместимой aAPC.
В некоторых вариантах осуществления экзогенную нуклеиновую кислоту приводят в контакт с нуклеазой и по меньшей мере одной гРНК.
В некоторых вариантах осуществления по любому из указанных выше аспектов и вариантов осуществления эритроидная клетка является безъядерной эритроидной клеткой.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигуры предназначены для иллюстрирования одного или более признаков, аспектов или вариантов осуществления изобретения, а не для ограничения.
Фиг. 1A и фиг. 1B являются схемами, на которых показан различный дизайн для экспрессии молекул MHC класса I и MHC класса II на эритроидных клетках. На фиг. 1A показана схема дизайна для экспрессии конструкций одноцепочечный пептид-MHC класса II. Как показано на фиг. 1A, экзогенный пептид связывают с β-цепью MHC класса II, связанной с α-цепью MHC класса II, связанной с мембранным якорем, таким как GPA или SMIM. На фиг. 1B показана схема дизайна для экспрессии конструкций одноцепочечный пептид-MHC класса I. Как показано на фиг. 1B, экзогенный пептид связывают с субъединицей β-2m MHC класса I, связанной с α-субъединицей MHC класса I, связанной с мембранным якорем, таким как GPA или SMIM.
Фиг. 2 является графиком, на котором показано, что сконструированные эритроциты мыши, презентирующие MHC класса I (овальбумин) и 4-1BBL, активируют овальбумин-специфические T-клетки.
Фиг. 3 является графиком, на котором показано, что овальбумин-специфические T-клетки, подвергнутые экспансии с использованием эритроцитов мыши, презентирующих MHC класса I (овальбумин) и 4-1BBL, являются очень активными и специфическими при цитолизе опухолевых клеток.
Фиг. 4A является схемой, на которой показан дизайн эксперимента для исследования пролиферации T-клеток OT1 в лимфоузлах и селезенке.
Фиг. 4B является схемой репрезентативных данных, где показано, что mRCT-4-1BBL OVA специфически приводят к экспансии и активируют T-клетки OT1, в то время как mRCT-4-1BBL без MHC класса I, презентирующего пептид овальбумина на поверхности клетки, не приводят к экспансии и не активируют T-клетки OT1. В рамках изобретения термин "терапевтическое средство на основе эритроцитов мыши" (или mRCT) относится к сконструированным эритроидным клеткам мыши (например, сконструированной безъядерной клетке), представленным в настоящем описании. В рамках изобретения термин "RCT" (терапевтическое средство на основе эритроцитов) относится к сконструированным эритроидным клеткам человека (например, сконструированной безъядерной клетке), представленным в настоящем описании.
Фиг. 4C является графиком, на котором показаны наблюдения in vivo пролиферации и активации T-клеток OT1 с помощью mRCT-4-1BBL OVA в кровотоке, селезенке и лимфоузле.
Фиг. 5A-D являются графиками, на которых показано, что эритроидные клетки, сконструированные для презентирования MHC класса I (овальбумина) и 4-1BBL, демонстрируют эффект дозы овальбумин-специфических T-клеток in vivo.
Фиг. 6 является графиком, на котором показано, что вторая доза эритроидных клеток, сконструированных для презентирования MHC класса I (овальбумина) и 4-1BBL, значительно повышает CD8+ OT1 T-клетки и в лимфоузле, и в селезенке.
Фиг. 7 является графиком, на котором показано, что эритроидные клетки, сконструированные для презентирования MHC класса I (gp100) и 4-1BBL, активируют gp100-специфические T-клетки in vitro.
Фиг. 8A является схемой, на которой показаны разные версии HLA-A2 (HPV E7), экспрессируемого на RCT. На фиг. 8A "YMLDLQPETGGGGS(G4S)2" показана как SEQ ID NO: 895 и "(G4S)4" показана как SEQ ID NO: 733.
Фиг. 8B и 8C являются графиками, на которых показана активность HLA-A2 (HPV E7), экспрессируемого на RCT, при стимуляции HPV-специфических T-клеток in vitro.
Фиг. 9 является графиком, на котором показано изменение среднего объема опухоли (мм3) с течением времени после рандомизации опухоли, где мышам вводят mRCT (контроль) и mRCT-OVA-4-1BBL в дни 1, 4 и 8 после инъекции CD8+ T-клеток OT1.
Фиг. 10 является графиком, на котором показано изменение объема отдельной опухоли (мм3) с течением времени после рандомизации опухоли, где мышам вводят mRCT (контроль) и mRCT-OVA-4-1BBL в дни 1, 4 и 8 после инъекции CD8+ T-клеток OT1.
Фиг. 11 является графиком, на котором показан процент выживания мышей с течением времени после рандомизации опухоли, где мышам вводят mRCT (контроль) и mRCT-OVA-4-1BBL в дни 1, 4 и 8 после инъекции CD8+ T-клеток OT1.
На фиг. 12 показаны результаты экспериментов по проточной цитометрии с гейтированием по экспрессии CD44+ для определения пролиферации CD8+ T-клеток OT1.
Фиг. 13 является графиком, на котором показано количество CD8+ T-клеток OT1 в день 4 после совместной инкубации mRCT (контрольных и подвергнутых клик-реакции) с CD8+ T-клетками OT1. Фиг. 14A является графиком, на котором показано, что трижды подвергнутые клик-реакции mRCT (mRCT-OVA-4-1BBL-IL7, mRCT-OVA-4-1BBL-IL12 или mRCT-OVA-4-1BBL-IL15) демонстрируют повышенную пролиферацию CD8+ T-клеток OT1 по сравнению с дважды подвергнутыми клик-реакции mRCT (mRCT-OVA-4-1BBL).
Фиг. 14B представляет собой панель графиков, на которых показаны процентные доли стволовых T-клеток памяти (Tscm), T-клеток центральной памяти (Tcm) и эффекторных T-клеток памяти (Tem), активированных дважды подвергнутых клик-реакции mRCT (mRCT-OVA-4-1BBL),или трижды подвергнутых клик-реакции mRCT (mRCT-OVA-4-1BBL-IL7, mRCT-OVA-4-1BBL-IL12 или mRCT-OVA-4-1BBL-IL15).
Фиг. 15A и 15B являются графиками, на которых показано, что у мышей, которым вводили mRCT-OVA-4-1BBL, наблюдают контроль опухоли EG7.OVA даже после повторной стимуляции опухолевыми клетками EG7.OVA.
Фиг. 16A является схемой, на которой показана временная шкала для мышей, повторно стимулируемых пептидом OVA (SIINFEKL (SEQ ID NO: 721)) и неполным адъювантом Фрейнда (IFA).
Фиг. 16B является графиком, на котором показано, что мыши, которым вводили mRCT-OVA, имели более низкое количество клеток OT1 после повторной стимуляции пептидом OVA по сравнению с мышами, которым вводили только mRCT, и в селезенке, и в лимфоузле.
Фиг. 16C является графиком, на котором показано, что на количество эндогенных CD8+ T-клеток не влияла повторная стимуляция пептидом OVA по сравнению с мышами, которым вводили только mRCT, и в селезенке, и в лимфоузле.
Фиг. 17A является схемой, на которой показаны разные варианты конфигураций для презентирования сигналов 1 и 2 на поверхности RCT.
Фиг. 17B является схемой, на которой показаны разные варианты конфигураций для презентирования сигналов 1, 2 и 3 на поверхности RCT.
ПОДРОБНОЕ ОПИСАНИЕ
Настоящее изобретение основано на разработке искусственных антигенпрезентирующих клеток (aAPC) с эффективным презентированием сигнала, которые можно использовать, например, для иммунотерапии aAPC in vivo и экспансии T-клеток ex vivo. В частности, настоящее изобретение основано по меньшей мере частично на неожиданном открытии того, что эритроидные клетки, и в частности сконструированные эритроидные клетки, можно конструировать, помимо прочего, для активации, экспансии или дифференцировки/дедифференцировки T-клеток, супрессии активности T-клеток, супрессии эффекторных T-клеток и/или стимуляции и экспансии регуляторных T-клеток.
Многие модификации и другие варианты осуществления изобретения, представленные в настоящем описании, будут очевидны специалисту в области, к которой относится настоящее изобретение, при использовании идей, представленных в описании и на сопутствующих чертежах. Таким образом, следует понимать, что изобретение не ограничено конкретными описанными вариантами осуществления, и что модификации и другие варианты осуществления предназначены для включения в объем формулы изобретения. Хотя в настоящем описании используют конкретные термины, их используют исключительно в общем и описательном смысле, а не для ограничения изобретения.
Определения
В рамках изобретения термины в единственном числе включают ссылку на множественное число, если контекст четко не указывает на иное.
Использование альтернатив (например, термина "или") следует понимать как обозначение одной, обеих или любой комбинации альтернатив.
В рамках изобретения термин "приблизительно" по отношению к измеримому значению, такому как количество, длительность периода времени и т.п., предназначен для включения колебаний на ±20% или ±10%, более предпочтительно - ±5%, даже более предпочтительно - ±1%, и еще более предпочтительно - ±0,1% от указанного значения, т.к. такие колебания подходят для осуществления описываемых способов.
В рамках изобретения любой диапазон концентраций, диапазон процентных долей, диапазон соотношений или диапазон целых значений следует понимать как включающий значение любого целого числа в указанном диапазоне и, при необходимости, его долей (таких как одна десятая и одна сотая от целого числа), если не указано иначе.
В рамках изобретения термины "содержат", "содержащий", "содержит" и "состоящий из" должны быть синонимами для терминов "включают", "включающий" и "включает" и являются инклюзивными или неограничивающими терминами, определяющими наличие следующего за ним термина, например, компонента, и не исключают наличие дополнительных неуказанных компонентов, признаков, элементов, членов, стадий, известных в этой области или представленных в настоящем описании.
В рамках изобретения термины "такой как", "например" и т.п. должны означать примеры вариантов осуществления и не ограничивают объем настоящего изобретения.
Если не указано иначе, все технические и научные термины, используемые в настоящем описании, имеют значение, общепринято понятное специалисту в области, к которой относится настоящее изобретение. Хотя в практическом осуществлении для тестирования настоящего изобретения можно использовать любые способы и материалы, схожие или эквивалентные способам и материалам, представленным в настоящем описании, предпочтительные материалы и способы представлены в настоящем описании.
В рамках изобретения термин "введение" и его варианты относятся к введению композиции или средства индивидууму и включают одновременное и последовательное введение композиции или средства. Термин "введение" может относиться, например, к терапевтическим, фармакокинетическим, диагностическим, исследовательским способам, способам с использованием плацебо и экспериментальным способам. Термин "введение" также включает лечение in vitro и ex vivo. Введение композиции или средства индивидууму осуществляют любым подходящим путем, включая пероральное, легочное, интраназальное, парентеральное (внутривенное, внутримышечное, интраперитонеальное или подкожное), ректальное, внутрилимфатическое или местное введение. Введение включает самостоятельное введение и введение другим человеком. Введение можно осуществлять любым подходящим путем. Подходящий путь введения позволяет композиции или средству выполнять свою предполагаемую функцию. Например, если подходящим путем является внутривенный путь, композицию вводят посредством введения композиции или средства в вену индивидуума.
В рамках изобретения термин "антигенпрезентирующая клетка (APC)" относится к клетке, процессирующей и экспонирующей чужеродные антигены вместе с молекулами главного комплекса гистосовместимости (MHC) на своей поверхности.
В рамках изобретения термин "искусственная антигенпрезентирующая клетка" относится к клеткам, сконструированным для встраивания одной или более молекул (например, экзогенных полипептидов), обеспечивающих необходимые T-клеточно-рецепторые (TCR), костимуляторные явления и/или явления адгезии, необходимые для образования иммунного синапса.
В рамках изобретения термин "аутоиммунные нарушения", как правило, относится к состояниям, при которых иммунная система индивидуума атакует собственные клетки организма, вызывая деструкцию ткани. Аутоиммунные нарушения можно диагностировать с использованием анализов крови, анализа цереброспинальной жидкости, электромиограммы (измерения функции мышц) и магнитно-резонансной томографии головного мозга, но особенно подходящим является анализ крови на аутоантитела. Как правило, антитела класса IgG ассоциированы с аутоиммунными заболеваниями.
В рамках изобретения термин "биологический образец" относится к любому типу материала биологического происхождения, выделенному из индивидуума, включая, например, ДНК, РНК, липиды, углеводы и белок. Термин "биологический образец" включает ткани, клетки и биологические жидкости, выделенные из индивидуума. Биологические образцы включают, в качестве неограничивающих примеров, цельную кровь, плазму, сыворотку, сперму, слюну, слезы, мочу, фекалии, пот, буккальный соскоб, кожу, цереброспинальную жидкость, костный мозг, желчь, волосы, биоптат мышцы, ткань органа или другой материал биологического происхождения, известный специалистам в этой области. Биологические образцы можно получать из индивидуумов для диагностики или исследования, или их можно получать из здоровых индивидуумов в качестве контролей или для фундаментальных исследований.
В рамках изобретения термин "злокачественное новообразование" относится к заболеваниям, при которым аномальные клетки делятся без контроля и могут инвазировать другие ткани. Существует более 100 разных типов злокачественных новообразований. Большинство злокачественных новообразований называют по органу или типу клеток, в которых они образуются, например, злокачественное новообразование, возникающее в толстом кишечнике, называют раком толстого кишечника; злокачественное новообразование, возникающее в меланоцитах кожи, называют меланомой. Типы злокачественных новообразований можно группировать по более обширным категориям. Основные категории злокачественных новообразований включают: карциному (означает злокачественное новообразование, образующееся в коже или тканях, выстилающих или покрывающих внутренние органы, и его подтипы, включая аденокарциному, базальноклеточную карциному, плоскоклеточную карциному и переходноклеточную карциному); саркому (означает злокачественное новообразование, образующееся в костной ткани, хрящах, жире, мышцах, кровеносных сосудах или других соединительных или поддерживающих тканях); лейкоз (означает злокачественное новообразование, образующееся в кроветворной ткани (например, костном мозге) и вызывает продукцию больших количеств аномальных клеток крови и их поступление в кровоток; лимфому и миелому (означает злокачественное новообразование, образующееся в клетках иммунной системы); и злокачественные новообразования центральной нервной системы (ЦНС) (означает злокачественные новообразования, образующиеся в тканях головного мозга и спинного мозга). Термин "миелодиспластический синдром" относится к типу злокачественного новообразования, при котором костный мозг не производит достаточное количество здоровых клеток крови (лейкоцитов, эритроцитов и тромбоцитов) и обнаруживают аномальные клетки крови и/или костного мозга. Миелодиспластический синдром может переходить в острый миелолейкоз (AML). В некоторых вариантах осуществления злокачественное новообразование выбрано из злокачественных новообразований, включающих, в качестве неограничивающих примеров, острый лимфобластный лейкоз (ALL), острый миелолейкоз (AML), рак анального канала, рак желчных протоков, рак мочевого пузыря, злокачественное новообразование костной ткани, колоректальный рак, опухоль головного мозга, рак молочной железы, рак с неизвестной первичной локализацией, метастазы в кости, метастазы в головном мозге, метастазы в печени, метастазы в легких, карциноидную опухоль, рак шейки матки, хориокарциному, хронический лимфоцитарный лейкоз (CLL), хронический миелолейкоз (CML), рак толстого кишечника, колоректальный рак, рак эндометрия, злокачественное новообразование глаза, рак желчного пузыря, рак желудка, гестационную трофобластическую болезнь (GTT), волосатоклеточный лейкоз, рак головы и шеи, лимфому Ходжкина, рак почки, рак гортани, лейкоз, рак печени, рак легких, лимфому, меланомный рак кожи, мезотелиому, злокачественные новообразования мужской половой системы, пузырный занос, рак ротовой полости и ротоглотки, миелому, назальные и синусовые злокачественные новообразования, рак носоглотки, неходжкинскую лимфому (NHL), рак пищевода, рак яичников, рак поджелудочной железы, рак полового члена, рак предстательной железы, редкие злокачественные новообразования, рак прямой кишки, рак слюнных желез, вторичные злокачественные новообразования, рак кожи (немеланомный), саркому мягких тканей, рак желудка, рак яичка, рак щитовидной железы, рак с неизвестной первичной локализацией, рак матки, рак влагалища и рак женских наружных половых органов.
В рамках изобретения термин "клик-реакция" относится к диапазону реакций, используемых для ковалентного связывания первого и второго остатка для удобного получения связанных продуктов. Как правило, они имеют одну или более из следующих характеристик: они являются быстрыми, являются специфическими, имеют высокий выход, являются эффективными, являются спонтанными, не изменяют значительно биосовместимость связываемых веществ, имеют высокую скорость реакции, приводят к образованию стабильного продукта, способствуют образованию одного продукта реакции, имеют высокую атомную эффективность, являются хемоселективными, являются модульными, являются стереоселективными, являются нечувствительными к кислороду, являются нечувствительными к воде, приводят к высокой чистоте, приводит к образованию только безвредных или относительно нетоксичных побочных продуктов, которые можно удалять нехроматографическими способами (например, посредством кристаллизации или дистилляции), не требуют растворителя, или их можно проводить в растворителе, являющемся безвредным или физиологически совместимым, например, воде, являются стабильными в физиологических условиях. Примеры включают азид-алкиновую реакцию, диен-диенофильную реакцию или тиол-алкеновую реакцию. Можно использовать другие реакции. В некоторых вариантах осуществления клик-реакция является быстрой, специфической и приводит к высокому выходу.
В рамках изобретения термин "модуль клик-реакции" относится к химическому остатку, способному реагировать со вторым модулем в клик-реакции с образованием сигнатуры клик-реакции. В некоторых вариантах осуществления модуль клик-реакции содержится в связывающем реагенте, и связывающий реагент может дополнительно содержат реакционноспособный в отношении субстрата остаток.
В рамках изобретения термин "цитокин" относится к небольшим растворимым белковым веществам, секретируемым клетками, имеющим различные эффекты в отношении других клеток. Цитокины опосредуют множество важных физиологических функций, включая рост, развитие, заживление ран и иммунный ответ. Они действуют, связываясь с их клеточно-специфическими рецепторами, локализованными на клеточной мембране, позволяющими отдельному каскаду передачи сигнала начинаться в клетке, что в конечном итоге будет приводить к биохимическим и фенотипическим изменениям в клетках-мишенях. Цитокины могут действовать локально и на расстоянии от места высвобождения. Они включают цитокины I типа, включающие многие из интерлейкинов, а также несколько гемопоэтических факторов роста; цитокины II типа, включая интерфероны и интерлейкин-10; молекулы, родственные фактору некроза опухоли ("ФНО"), включая ФНОα и лимфотоксин; члены суперсемейства иммуноглобулинов, включая интерлейкин 1 ("ИЛ-1"); и хемокины, семейство молекул, играющих критическую роль в широком спектре иммунных и воспалительных функций. Один и тот же цитокин может иметь разные эффекты в отношении клетки в зависимости от состояния клетки. Зачастую цитокины регулируют экспрессию других цитокинов и запускают их каскады. Неограничивающие примеры цитокинов включают ИЛ-1α, ИЛ-1β, ИЛ-2, ИЛ-3, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-7, ИЛ-8, ИЛ-9, ИЛ-10, ИЛ-11, ИЛ-12/ИЛ-23 P40, ИЛ-13, ИЛ-15, ИЛ-17, ИЛ-18, ИЛ-21, ИЛ-23, TGF-β, ИФНγ, ГМ-КСФ, Groα, MCP-1 и ФНОα.
В рамках изобретения термин "эндогенный" предназначен для обозначения нативной формы соединения (например, низкомолекулярного соединения) или процесса. Например, в некоторых вариантах осуществления термин "эндогенный" относится к нативной форме нуклеиновой кислоты или полипептида в их природной локализации в организме или геноме организма.
В рамках изобретения термин "сконструированная клетка" означает генетически модифицированную клетку или ее потомство. В некоторых вариантах осуществления сконструированную клетку (например, сконструированную безъядерную клетку) можно получать с использованием связывающих реагентов для связывания экзогенного полипептида с поверхностью клетки (например, с использованием клик-химии).
В рамках изобретения термин "безъядерная" относится к клетке, например, ретикулоциту или зрелому эритроциту, в которой отсутствует ядро. В варианте осуществления безъядерная клетка является клеткой, потерявшей свое ядро при дифференцировке из клетки-предшественника, например, гемопоэтической стволовой клетки (например, CD34+ клетки), общего миелоидного предшественника (CMP), мегакариоцитарной эритроцитарной клетки-предшественника (MEP), эритроцитарной бурст-образующей единицы (BFU-E), эритроцитарной колониеобразующей единицы (CFU-E), проэритробласта, раннего базофильного эритробласта, позднего базофильного эритробласта, полихромного эритробласта или ортохромного эритробласта, или индуцированной плюрипотентной клетки, в ретикулоцит или зрелый эритроцит. В варианте осуществления безъядерная клетка является клеткой, потерявшей свое ядро при дифференцировке in vitro из клетки-предшественника, например, гемопоэтической стволовой клетки (например, CD34+ клетки), общего миелоидного предшественника (CMP), мегакариоцитарной эритроцитарной клетки-предшественника (MEP), эритроцитарной бурст-образующей единицы (BFU-E), эритроцитарной колониеобразующей единицы (CFU-E), проэритробласта, раннего базофильного эритробласта, позднего базофильного эритробласта, полихромного эритробласта или ортохромного эритробласта, или индуцированной плюрипотентной клетки в ретикулоцит или зрелый эритроцит. В варианте осуществления в безъядерное клетке отсутствует ДНК. В варианте осуществления безъядерная клетка неспособна экспрессировать полипептид, например, неспособна транскрибировать и/или транслировать ДНК в белок, например, в ней отсутствует клеточный аппарат, необходимый для транскрипции и/или транслировать ДНК в белок. В некоторых вариантах осуществления безъядерная клетка является эритроцитом, ретикулоцитом или тромбоцитом.
В некоторых вариантах осуществления безъядерные клетки не являются тромбоцитами и, таким образом, являются "несодержащими тромбоциты безъядерными" клетками (клетками "PFE"). Следует понимать, что тромбоциты не имеют ядер, и в этом конкретном варианте осуществления тромбоциты не предназначены для включения.
В рамках изобретения термин "эритроидная клетка" включает ядросодержащий эритроцит, эритроцитарный предшественник, безъядерный зрелый эритроцит и ретикулоцит. В рамках изобретения эритроидная клетка включает эритроидную клетку-предшественника, клетку, способную дифференцироваться в ретикулоцит или эритроцит. Например, эритроидные клетки-предшественники включают любую из стволовых клеток пуповинной крови, CD34+ клетку, гемопоэтическую стволовую клетку (HSC), колониеобразующую клетку селезенки (CFU-S), общий миелоидный предшественник (CMP), бластоцитарную колониеобразующую клетку, эритроидную бурст-образующую единицу (BFU-E), магакариоцитарно-эритроидную клетку-предшественника (MEP), эритроидную колониеобразующую единицу (CFU-E), ретикулоцит, эритроцит, индуцированную плюрипотентную стволовую клетку (iPSC), мезенхимальную стволовую клетку (MSC), полихромный нормобласт, ортохромный нормобласт. Препарат эритроидных клеток может включать любые из этих клеток или их комбинацию. В некоторых вариантах осуществления эритроидные клетки-предшественники являются "бессмертными" или иммортализованными клетками. Например, иммортализованные эритробластные клетки можно получать посредством ретровирусной трансдукции CD34+ гемопоэтических клеток-предшественников для экспрессии Oct4, Sox2, Klf4, cMyc и супрессии TP53 (например, как описано в Huang et al., Mol Ther (2014) Mol. Ther. 22(2): 451-63, полное содержание которой включено в настоящее описание в качестве ссылки). Кроме того, клетки могут быть предназначены для аутологичного использования или представляют собой источник для аллогенной трансфузии. В некоторых вариантах осуществления эритроидные клетки культивируют. В варианте осуществления эритроидная клетка является безъядерным эритроцитом.
В рамках изобретения термин "экзогенный" при использовании в отношении нуклеиновой кислоты включает трансген и рекомбинантные нуклеиновые кислоты.
В рамках изобретения термин "экзогенная нуклеиновая кислота" относится к нуклеиновой кислоте (например, гену), не являющейся нативной для клетки, но встраиваемой в клетку или предшественника клетки. Экзогенная нуклеиновая кислота может включать область или открытую рамку считывания (например, ген), являющуюся гомологичной или идентичной эндогенной нуклеиновой кислоте, нативной для клетки. В некоторых вариантах осуществления экзогенная нуклеиновая кислота содержит РНК. В некоторых вариантах осуществления экзогенная нуклеиновая кислота содержит ДНК. В некоторых вариантах осуществления экзогенную нуклеиновую кислоту встраивают в геном клетки. В некоторых вариантах осуществления экзогенная нуклеиновая кислота процессируется клеточным аппаратом с образованием экзогенного полипептида. В некоторых вариантах осуществления экзогенная нуклеиновая кислота не удерживается клеткой или клеткой, являющейся потомством клетки, в которую встраивали экзогенную нуклеиновую кислоту.
В рамках изобретения термин "экзогенный полипептид" относится к полипептиду, непродуцируемому клеткой дикого типа этого типа или присутствующему на более низких уровнях в клетке дикого типа, чем в клетке, содержащей экзогенный полипептид. В некоторых вариантах осуществления термин "экзогенный полипептид" относится к полипептиду, встраиваемому в клетку или на клетку, или экспрессия которого клеткой вызвана посредством встраивания экзогенной нуклеиновой кислоты, кодирующей экзогенный полипептид, в клетку или в предшественника клетки. В некоторых вариантах осуществления экзогенный полипептид является полипептидом, кодируемым экзогенной нуклеиновой кислотой, встраиваемой в клетку или предшественника клетки, где нуклеиновая кислота, необязательно, не удерживается клеткой. В некоторых вариантах осуществления экзогенный полипептид является полипептидом, конъюгированным с поверхностью клетки химическими или ферментативными способами.
В рамках изобретения термин "экспрессировать" или "экспрессия" относится к процессу продукции полипептида, включая транскрипцию и трансляцию. Экспрессию, например, можно повышать с помощью ряда подходов, включая: повышение количества генов, кодирующих полипептид, повышения транскрипции гена (например, посредством помещения гена под контроль конститутивного промотора), повышения трансляции гена, нокаута конкурентного гена или комбинации этих и/или других подходов.
В рамках изобретения термины "первый", "второй", "третий" и т.д. в отношении экзогенных полипептидов или нуклеиновых кислот используют для удобства различения при наличии нескольких типов экзогенного полипептида или нуклеиновой кислоты. Использование этих терминов не предназначено для придания конкретного порядка или ориентации экзогенных полипептидов или нуклеиновой кислоты, если не указано иначе.
В рамках изобретения термин "проточная цитометрия" относится к способу исследования фенотипа и характеристик клеток. С помощью нее определяют клетки или частицы при их движении в потоке жидкости через лазер (усиления света с помощью индуцированного излучения)/луч света мимо области считывания. Измеряют относительное светорассеяние и флуоресценцию с цветовым разделением микроскопических частиц. Проточный анализ и дифференциация клеток основаны на размере, гранулярности и того, несут ли клетки флуоресцентные молекулы в форме антител или красителей. Когда клетка проходит через пучок лазера, свет рассеивается во всех направлениях, и свет, рассеиваемый в прямом направлении под небольшими углами (0,5-10°) от оси, пропорционален квадрату радиуса сферы и размеру клетки или частицы. Свет может проходить в клетку; таким образом, светорассеяние 90° (прямоугольное, боковое) можно определять с помощью мечения связанными с флуорохромом антителами или окрашивания флуоресцентными мембранными, цитоплазматическими или ядерными красителями. Таким образом, можно облегчать дифференцирование типов клеток, определение наличия мембранных рецепторов и антигенов, мембранного потенциала, pH, ферментативной активности и содержания ДНК. Проточные цитометры являются многопараметрическими, регистрирующими несколько измерений на каждой клетке; таким образом, можно идентифицировать гомогенную субпопуляцию в гетерогенной популяции (Marion G. Macey, Flow cytometry: principles and applications, Humana Press, 2007). В активируемой флуоресценцией сортировке клеток (FACS), позволяющей выделять отдельные популяции клеток, слишком схожие по физическим характеристикам для разделения по размеру или плотности, используют флуоресцентные метки для детекции поверхностных белков, экспрессирующихся дифференциально, что делает возможным тщательное разделение физически гомогенных популяций клеток.
В рамках изобретения термин "ген" используют в широком смысле для обозначения любого сегмента нуклеиновой кислоты, ассоциированного с экспрессией указанной РНК или белка. Таким образом, гены включают области, кодирующие экспрессируемую РНК (как правило, включающую кодирующие полипептид последовательности) и, зачастую, регуляторные последовательности, необходимые для их экспрессии. Гены можно получать из различных источников, включая клонирование из интересующего источника или синтез с использованием информации об известной или прогнозируемой последовательности, и они могут включать последовательности, сконструированные так, что они имеют конкретные желательные параметры.
В рамках изобретения термины "активировать", "стимулировать", "усиливать", "повышать" и/или "индуцировать" (и подобные термины) используют взаимозаменяемо, как правило, для обозначения их улучшающего или повышающего действия, прямо или косвенно, концентрации, уровня, функции, активности или свойств относительно природного, ожидаемого или среднего или относительно контрольных условий. Термин "активировать" относится к первичному ответу, индуцируемому посредством лигирования остатка на поверхности клетки. Например, в отношении рецепторов такая стимуляция приводит к лигированию рецептора и последующему явлению передачи сигнала. Что касается стимуляция T-клетки, такая стимуляция относится к лигированию остатка на поверхности T-клетки, которое в некоторых вариантах осуществления затем индуцирует явление передачи сигнала, такое как связывание комплекса TCR/CD3. Кроме того, явление стимуляции может активировать клетку и положительно или отрицательно регулировать экспрессию или секрецию молекулы. Таким образом, лигирование остатков на поверхности клетки, даже в отсутствие явления прямой передачи сигнала, может приводить к реорганизации структур цитоскелета или коалесцированию остатков на поверхности клетки, каждое из которых может служить для повышения, модификации или изменения последующих клеточных ответов. "Активация" включает активацию CD8+ T-клеток, активацию CD4+ T-клеток, стимуляцию цитотоксической активности T-клеток, стимуляцию секреции цитокинов T-клетками, детектируемые эффекторные функции, модификацию состояния дифференцировки T-клетки (например, стимуляцию экспансии и дифференцировки из эффекторной T-клетки в T-клетку памяти) и/или любую их комбинацию. Термин "активированные T-клетки" относится, в частности, к T-клеткам, проходящим через деление клеток.
В рамках изобретения термин "измененный иммунный ответ" относится к изменению формы или характера иммунного ответа, например, стимуляции или ингибированию иммунного ответа, например, измеряемого с помощью анализа ELISPOT (клеточного иммунного ответа), ICS (анализа окрашивания внутриклеточных цитокинов) и анализа тетрамеров главного комплекса гистосовместимости (MHC) для детекции и количественного анализа антигенспецифических T-клеток, количественного анализа популяции антигенспецифических CD4+ T-клеток крови или количественного анализа популяции антигенспецифических CD8+ T-клеток крови, на измеримое количество, или где повышение составляет по меньшей мере 10%, по меньшей мере 20%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99%, по меньшей мере 100% по сравнению с подходящим контролем (например, контрольной композицией, в которой дендритные клетки не нагружены опухолеспецифическими клетками или не нагружены пептидом, происходящим из опухолеспецифических клеток).
В рамках изобретения полипептиды, обозначаемые в настоящем описании как "рекомбинантные", являются полипептидами, полученными способами рекомбинантной ДНК, включая полипептиды, получаемые способами, основанными на способе искусственной рекомбинации, такой как полимеразная цепная реакция (ПЦР) и/или клонирование в вектор с использованием ферментов рестрикции.
В рамках изобретения термин "одноцепочечное антитело (scFv)" относится к антителу, в котором область VL и VH соединяют с помощью линкера (например, синтетической последовательности аминокислотных остатков) для получения непрерывной белковой цепи. Линкер является достаточно длинным, чтобы позволить белковой цепи сворачиваться на саму себя и образовывать моновалентный антигенсвязывающий участок (см., например, Bird et al., 1988, Science 242:423-26 и Huston et al., 1988, Proc. Natl. Acad. Sci. USA 85:5879-83).
В рамках изобретения термин "специфически связывается" относится к способности полипептида или полипептидного комплекса распознавать и связываться с лигандом in vitro или in vivo, при этом, по существу, не распознавая или не связывая другие молекулы в микроокружении. В некоторых вариантах осуществления специфическое связывание можно охарактеризовывать по равновесной константе диссоциации по меньшей мере приблизительно 1×106 M или менее (например, меньшая равновесная константа диссоциации означает более сильное связывание). Способы определения специфического связывания двух молекул хорошо известны в этой области и включают, например, равновесный диализ, поверхностный плазмонный резонанс и т.п.
В рамках изобретения термины "индивидуум", "организм-хозяин" и "пациент" используют в настоящем описании взаимозаменяемо, и они относятся к любому млекопитающему, диагностика, лечение или терапия которого является желательной, в частности, к людям. Способы, представленные в настоящем описании, можно использовать для терапии людей и в ветеринарии. В некоторых вариантах осуществления индивидуум представляет собой млекопитающего, и в конкретных вариантах осуществления индивидуум является человеком.
В рамках изобретения фраза "нуждающийся в этом индивидуум" относится к индивидууму, (i) которому будут вводить aAPC (или фармацевтическую композицию, содержащую aAPC) по настоящему изобретению, (ii) вводят aAPC (или фармацевтическую композицию, содержащую aAPC) по настоящему изобретению; или (iii) вводили aAPC (или фармацевтическую композицию, содержащую aAPC) по настоящему изобретению, если контекст или использование фразы не указывает на иное.
В рамках изобретения термины "супрессировать", "снижать", "препятствовать" и/или "ингибировать" (и подобные термины), как правило, относятся к снижению, прямо или косвенно, концентрации, уровня, функции, активности или свойств относительно природного, ожидаемого или среднего или относительно контрольных условий.
В рамках изобретения термины "супрессия иммунных клеток" или "ингибирование иммунных клеток" относится к процессу (например, явлению передачи сигнала), вызывающему или приводящему к ингибированию или супрессии одного или более клеточных ответов или активностей иммунной клетки, выбранных из: пролиферации, дифференцировки, секреции цитокинов, высвобождения цитотоксических эффекторных молекул, цитотоксической активности и экспрессии маркеров активации, или приводящему к анергии иммунной клетки или индуцированию апоптоза иммунной клетки. Подходящие анализы для измерения ингибирования или супрессии иммунных клеток известны в этой области и представлены в настоящем описании.
В рамках изобретения термин "фармацевтически приемлемый носитель" включает любой из стандартных фармацевтических носителей, такой как фосфатно-солевой буферный раствор, вода, эмульсии, такие как "масло-в-воде" или "вода-в-масле", и различные типы увлажнителей. Термин также включает любые из средств, одобренных регулирующим органом федерального правительства США или указанных в Фармакопее США для использования на животных, включая людей, а также любой носитель или дилюент, не вызывающий значительное раздражение у индивидуума и не подавляющий биологическую активность и свойства вводимого соединения.
В рамках изобретения термины "терапевтическое количество", "терапевтически эффективное количество", "эффективное количество, или "фармацевтически эффективное количество" активного средства (например, aAPC, как представлено в настоящем описании) используют взаимозаменяемо для обозначения количества, достаточного для достижения планируемого благоприятного эффекта лечения. Однако, уровни доз основаны на различных факторах, включая тип повреждения, возраст, массу тела, пол, состояние здоровья пациента, тяжесть состояния, путь введения и конкретное используемое активное средство. Таким образом, режим дозирования можно варьировать в широких пределах, но их может определять лечащий врач общепринятым образом с использованием стандартных способов. Кроме того, термины "терапевтическое количество", "терапевтически эффективные количества" и "фармацевтически эффективные количества" включают профилактические количества композиций по настоящему изобретению. При профилактическом использовании по настоящему изобретению фармацевтические композиции или лекарственные средства вводят пациенту, имеющему предрасположенность или иной риск развития заболевания, нарушения или состояния в количестве, достаточном для устранения или снижения риска, уменьшения тяжести или задержки дебюта заболевания, нарушения или состояния, включая биохимические, гистологические и/или поведенческие симптомы заболевания, нарушения или состояния, их осложнений и промежуточных патологических фенотипов, появляющихся при развитии заболевания, нарушения или состояния. Как правило, предпочтительно использовать максимальную дозу, т.е. наиболее высокую безопасную дозу согласно некоторому медицинскому заключению. Термины "дозы" и "дозировка" используют в настоящем описании взаимозаменяемо.
В рамках изобретения термин "терапевтический эффект" относится к следствию лечения, результатам, которые, как считают, являются желательными и благоприятными. Терапевтический эффект может включать, прямо или косвенно, прекращение, снижение или устранение манифестации заболевания. Терапевтический эффект также может включать, прямо или косвенно, прекращение, снижение или устранение прогрессирования манифестации заболевания.
В случае любого терапевтического средства, представленного в настоящем описании, терапевтически эффективное количество исходно можно определять с помощью предварительных исследований in vitro и/или моделей на животных. Терапевтически эффективную дозу также можно определять с помощью данных о людях. Используемую дозу можно корректировать с учетом относительной биодоступности и активности вводимого соединения. Коррекция дозы для достижения максимальной эффективности с учетом описанных выше способов и других хорошо известных способов входит в объем навыков специалистов в этой области. Ниже приведены общие принципы определения терапевтической эффективности, которые можно найти в главе 1 Goodman and Gilman's Pharmacological Basis of Therapeutics, 10th Edition, McGraw-Hill (New York) (2001), включенной в настоящее описание в качестве ссылки.
Фармакокинетические принципы представляют собой основу для модификации режима дозирования для достижения желаемой степени терапевтической эффективности с минимальными неприемлемыми нежелательными явлениями. В случаях, когда концентрацию лекарственного средства в плазме можно измерять и сопоставлять с терапевтическим окном, можно получать дополнительное руководство по модификации дозы.
В рамках изобретения, термины "лечить" и/или "лечение" включают устранение, по существу, ингибирование, замедление или реверсирование прогрессирования состояния, по существу, улучшение клинических симптомов состояния или, по существу, профилактику появления клинических симптомов состояния, достижение благоприятных или желательных клинических результатов. Термин "лечение" дополнительно относится к осуществлению одного или более из следующего: (a) снижения тяжести нарушения; (b) ограничения развития симптомов, характерных для нарушений, подвергаемых лечению; (c) ограничения ухудшения симптомов, характерных для нарушений, подвергаемых лечению; (d) ограничения рецидивирования нарушений у пациентов, ранее имевших нарушения; и (e) ограничения рецидивирования симптомов у пациентов, ранее бывших бессимптомными в отношении нарушений.
Благоприятные или желательные клинические результаты, такие как фармакологические и/или физиологические эффекты, включают, в качестве неограничивающих примеров, профилактику возникновения заболевания, нарушения или состояния у индивидуума, который может быть предрасположен к заболеванию, нарушению или состоянию, но у которого еще не развились или проявились симптомы заболевания (профилактическое лечение), облегчение симптомов заболевания, нарушения или состояния, снижение степени заболевания, нарушения или состояния, стабилизацию (т.е. отсутствие ухудшения) заболевания, нарушения или состояния, профилактику распространения заболевания, нарушения или состояния, задержку или замедление прогрессирования заболевания, нарушения или состояния, улучшение или временное облегчение заболевания, нарушения или состояния и их комбинации, а также пролонгирование выживаемости по сравнению с выживаемостью, ожидаемой при отсутствии лечения.
В рамках изобретения термин "экзогенный антигенный полипептид" относится к экзогенному полипептиду, способному индуцировать иммунный ответ. Экзогенный антигенный полипептид может связываться с экзогенным антигенпрезентирующим полипептидом.
В рамках изобретения термин "экзогенный антигенпрезентирующий полипептид" относится к набору белков поверхности клетки, связывающихся с антигенами и экспонирующих их на поверхности клетки для распознавания соответствующими T-клетками. Семейство генов MHC разделяют на три подгруппы: класса I, класса II и класса III. Молекулы MHC класса I являются гетеродимерами, состоящими из двух полипептидных цепей, α-цепи и цепи β2-микроглобулина (b2m). Молекулы MHC класса I содержат субъединицы β2 таким образом, что они могут распознаваться только корецепторами CD8. Молекулы MHC класса II также являются гетеродимерами, состоящими из α- и β-полипептидных цепей. Обозначение цепей, например, α1, α2 и т.д., относится к отдельным доменам в гене HLA. Молекулы MHC класса II содержат субъединицы β1 и β2 и могут распознаваться корецепторами CD4. MHC человека также называет комплексом HLA (лейкоцитарного антигена человека). В некоторых вариантах осуществления термин "экзогенный антигенпрезентирующий полипептид" относится к белкам поверхности клетки HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQA1, HLA-DQB1, HLA-DPA1, HLA-DPB1, способных связываться с антигенами и экспонировать их на поверхности клетки. Экзогенные антигенпрезентирующие полипептиды более подробно описаны ниже.
В рамках изобретения термин "экзогенный T-клеточный костимуляторный полипептид" включает полипептид на антигенпрезентирующей клетке (например, aAPC), специфически связывающийся с когнатной костимуляторной молекулой на T-клетке (например, молекулой MHC, B- и T-лимфоцитарным аттенюатором (CD272) и Toll-подобным рецептором), таким образом, обеспечивающий сигнал, который, в дополнение к первичному сигналу, обеспечиваемому, например, связыванием комплекса TCR/CD3 с молекулой MHC, нагруженной пептидом, опосредует T-клеточный ответ, включая, в качестве неограничивающих примеров, пролиферацию, активацию, дифференцировку и т.п. Костимуляторный полипептид также включает, помимо прочего, антитело, специфически связывающееся с костимуляторной молекулой, присутствующей на T-клетке. Примеры экзогенных костимуляторных полипептидов более подробно описаны ниже.
В рамках изобретения термин "экзогенный T-клеточный коингибиторный полипептид" относится к любому полипептиду, вызывающему супрессию T-клетку, включая ингибирование активности T-клетки, ингибирование пролиферации T-клеток, анергию T-клеток или индуцирование апоптоза T-клеток. Примеры экзогенных коингибиторных полипептидов более подробно описаны ниже.
В рамках изобретения термин "экзогенный метаболит-изменяющий полипептид" относится к любому полипептиду, участвующему в катаболизме или анаболизме метаболита в клетке, где метаболит-изменяющий полипептид может влиять на метаболизм T-клетки. Примеры метаболит-изменяющих полипептидов более подробно описаны ниже.
В рамках изобретения термин "Treg-костимуляторный полипептид" относится к экзогенному полипептиду, вызывающему экспансию регуляторных T-клеток (Treg). В некоторых вариантах осуществления Treg-костимуляторный полипептид стимулирует Treg-клетки посредством стимуляции по меньшей мере одного из трех сигналов, участвующих в развитии Treg-клеток. Примеры экзогенных Treg-костимуляторных полипептидов более подробно описаны ниже.
В рамках изобретения термины "полипептид", "пептид" и "белок" используют в настоящем описании взаимозаменяемо для обозначения полимера аминокислотных остатков. Термины относятся к аминокислотным полимерам, в которых один или более аминокислотных остатков являются искусственным химическим аналогом соответствующей природной аминокислоты, а также полимерам природных аминокислот. Природа таких аналогов природных аминокислот является такой, что при встраивании в белок этот белок является особенно реакционноспособным в отношении антител, индуцированных против того же белка, но состоящего полностью из природных аминокислот. Термины "полипептид", "пептид" и "белок" также включают модификации, включающие, в качестве неограничивающих примеров, гликозилирование, присоединение липидов, сульфатирование, гамма-карбоксилирование остатков глутаминовой кислоты, гидроксилирование и АДФ-рибозилирование. Следует понимать, что, как хорошо известно и как указано выше, полипептиды могут не быть полностью линейными. Например, полипептиды могут являться разветвленными в результате убиквитинилирования, и они могут являться кольцевыми, с разветвлением или без него, как правило в результате посттрансляционных событий, включая природный процессинг и явления, обусловленные манипуляциями человеком и не возникающие в природе. Кольцевые, разветвленные и разветвленные кольцевые полипептиды можно синтезировать посредством нетрансляционного природного процесса и полностью синтетическими способами. В некоторых вариантах осуществления пептид имеет любую длину или размер.
В рамках изобретения термин "молекула нуклеиновой кислоты" относится к одноцепочечному или двухцепочечному полимеру дезоксирибонуклеотидных или рибонуклеотидных оснований. Он включает хромосомную ДНК и самореплицирующиеся плазмиды, векторы, мРНК, тРНК, миРНК и т.д., которые могут быть рекомбинантными, и с которых могут экспрессироваться экзогенные полипептиды при встраивании нуклеиновой кислоты в клетку.
Следующие термины используют в настоящем описании для описания взаимосвязи между двумя или более нуклеиновыми кислотами или полинуклеотидами: (a) "референсная последовательность", (b) "окно сравнения", (c) "идентичность последовательности", (d) "процент идентичности последовательности" и (e) "значительная идентичность". (a) Термин "референсная последовательность" относится к последовательности, используемой в качестве основы для сравнения последовательностей. Референсная последовательность может представлять собой субпопуляцию или всю совокупность определенной последовательности; например, в качестве сегмента полноразмерной последовательности кДНК или гена или полной последовательности кДНК или гена. (b) Термин "окно сравнения" относится к смежному и определенному сегменту полинуклеотидной последовательности, где полинуклеотидную последовательность можно сравнивать с референсной последовательностью, и где часть полинуклеотидной последовательности в окне сравнения может содержать добавления или делеции (т.е. пропуски) по сравнению с референсной последовательностью (несодержащей добавления или делеции) для оптимального выравнивания двух последовательностей. Как правило, длина окна сравнения составляет по меньшей мере 20 смежных нуклеотидов и, необязательно, может составлять по меньшей мере 30 смежных нуклеотидов, по меньшей мере 40 смежных нуклеотидов, по меньшей мере 50 смежных нуклеотидов, по меньшей мере 100 смежных нуклеотидов или более. Специалистам в этой области понятно, что во избежание высокого сходства с референсной последовательностью из-за исключения пропусков в полинуклеотидной последовательности, как правило, включают штраф за пропуск и вычитают его из количества совпадений. Способы выравнивания последовательностей для сравнения хорошо известны в этой области. Оптимальное выравнивание последовательностей в целях сравнения можно осуществлять с помощью алгоритма локальной гомологии Smith and Waterman, Adv. Appl. Math. 2:482 (1981); алгоритма гомологичного выравнивания Needleman and Wunsch, J. Mol. Biol. 48:443 (1970); способом поиска сходства Pearson and Lipman, Proc. Natl. Acad. Sci. 85:2444 (1988); с помощью компьютеризованных воплощений этих алгоритмов, включая, в качестве неограничивающих примеров: CLUSTAL в программе PC/Gene от Intelligenetics, Mountain View, Calif.; GAP, BESTFIT, BLAST, FASTA и TFASTA в пакете программ Wisconsin Genetics, Genetics Computer Group (GCG), 575 Science Dr., Madison, Wis., USA; программа CLUSTAL хорошо описана в Higgins and Sharp, Gene 73:237-244 (1988); Higgins and Sharp, CABIOS 5:151-153 (1989); Corpet, et al., Nucleic Acids Research 16:10881-90 (1988); Huang, et al., Computer Applications in the Biosciences, 8:155-65 (1992), и Pearson, et al., Methods in Molecular biology, 24:307-331 (1994). Семейство программ BLAST, которые можно использовать для поиска сходства в базах данных, включает: BLASTN для поисковых нуклеотидных последовательностей в базах данных о нуклеотидных последовательностях; BLASTX для поисковых нуклеотидных последовательностей в базах данных о белковых последовательностях; BLASTP для поисковых белковых последовательностей в базах данных о белковых последовательностях; TBLASTN для поисковых белковых последовательностей в базах данных о нуклеотидных последовательностях; и TBLASTX для поисковых нуклеотидных последовательностей в базах данных о белковых последовательностях. См., Current Protocols in Molecular biology, глава 19, Ausubel, et al., Eds., Greene Publishing and Wiley-Interscience, New York (1995). Если не указано иначе, значения идентичности/сходства последовательностей, приведенные в настоящем описании, относятся к значениям, полученным с помощью пакета программа BLAST 2.0 с использованием параметров по умолчанию. Altschul et al., Nucleic Acids Res. 25:3389-3402 (1997). Программное обеспечение для осуществления анализов BLAST является общедоступным, например, в National Center for Biotechnology Information. Этот алгоритм включает первичную идентификацию пар последовательностей с высокими баллами (HSP) посредством идентификации коротких слов длины W в поисковой последовательности, совпадающих или соответствующих некоторому пороговому значению баллов с положительным значением T при выравнивании со словом той же длины с последовательностью из базы данных. T обозначают как порог показателя сходства соседних слов (Altschul et al., выше). Эти исходные совпадения соседних слов выступают в качестве затравки для инициации поиска для обнаружения более длинных HSP, содержащих их. Затем совпадения слов удлиняют в обоих направлениях вдоль каждой последовательности настолько, насколько совокупные баллы выравнивания могут быть увеличены. Совокупные баллы вычисляют с использованием, в случае нуклеотидных последовательностей, параметров M (поощрительные баллы для пары совпадающих остатков; всегда >0) и N (баллы штрафов для несовпадающих остатков; всегда <0). В случае аминокислотных последовательностей для вычисления совокупных баллов используют матрицу замен. Удлинение совпадений слов в каждом направлении прекращают, если: совокупные баллы выравнивания снижаются на количество X относительно их максимального достигнутого значения; совокупные баллы падают до нуля или ниже из-за накопления одного или более выравнивания остатков с отрицательными баллами; или достигнут конец любой последовательности. Параметры алгоритма BLAST W, T и X определяют чувствительность и скорость выравнивания. В программе BLASTN (в случае нуклеотидных последовательностей) по умолчанию используют длину слова (W) 11, ожидание (E) 10, пороговое значение 100, M=5, N=-4 и сравнение обеих цепей. В случае аминокислотных последовательностей в программе BLASTP по умолчанию используют длину слова (W) 3, ожидание (E) 10 и матрицу замен BLOSUM62 (см. Henikoff & Henikoff (1989) Proc. Natl. Acad. Sci. USA 89:10915). В дополнение к вычислению процента идентичности последовательности, с помощью алгоритма BLAST также осуществляют статистический анализ сходства между двумя последовательностями (см., например, Karlin & Altschul, Proc. Natl. Acad. Sci. USA 90:5873-5787 (1993)). Одной из мер сходства, обеспечиваемой алгоритмом BLAST, является наименьшая суммарная вероятность (P(N)), являющаяся показателем вероятности, с которой совпадение между двумя нуклеотидными или аминокислотными последовательностями произойдет случайно. При поиске BLAST полагают, что белки можно моделировать в виде случайных последовательностей. Однако многие реальные белки содержат области неслучайных последовательностей, которые могут представлять собой гомополимерные тяжи, короткие повторы или области, обогащенные одной или более аминокислотами. Такие области низкой сложности можно выравнивать между неродственными белками, даже притом, что другие области белка являются полностью непохожими. Для снижения таких выравниваний низкой сложности можно использовать ряд программ-фильтров низкой сложности. Например, можно использовать фильтры низкой сложности SEG (Wooten and Federhen, Comput. Chem., 17:149-163 (1993)) и XNU (Claverie and States, Comput. Chem., 17:191-201 (1993)) в отдельности или в комбинации. (c) Термин "идентичность последовательности" или "идентичность" в отношении двух последовательностей нуклеиновой кислоты или полипептидных последовательностей используют в настоящем описании для обозначения остатков в двух последовательностях, являющихся одинаковыми при выравнивании для максимального соответствия в определенном окне сравнения. Если процент идентичности последовательности используют по отношению к белкам, необходимо отметить, что положения остатков, не являющихся идентичными, зачастую отличаются консервативными аминокислотными заменами, т.е. аминокислотные остатки заменяют другими аминокислотными остатками со схожими химическими свойствами (например, зарядом или гидрофобностью) и, таким образом, не изменяют функциональные свойства молекулы. Если последовательности отличаются консервативными заменами, процент идентичности последовательности можно корректировать в сторону повышения для поправки на консервативную природу замены. Указывают, что последовательности, отличающиеся такими консервативными заменами, имеют "сходство последовательности" или "сходство". Способы внесения этих поправок хорошо известны специалистам в этой области. Как правило, они включают подсчет баллов консервативной замены в качестве частичного, а не полного несовпадения, таким образом, повышая процент идентичности последовательности. Таким образом, например, если идентичной аминокислоте присваивают баллы 1, а неконсервативной замене присваивают нулевой балл, консервативной замене присваивают баллы между нулем и 1. Баллы консервативных замен вычисляют, например, с помощью алгоритма Meyers and Miller, Computer Applic. Biol. Sci., 4:11-17 (1988), например, воплощенного в программе PC/GENE (Intelligenetics, Mountain View, Calif., USA). (d) Термин "процент идентичности последовательности" используют в настоящем описании для обозначения значения, определяемого посредством сравнения двух оптимально выровненных последовательностей в окне сравнения, где часть полинуклеотидной последовательности в окне сравнения может содержать добавления или делеции (т.е. пропуски) по сравнению с референсной последовательностью (несодержащей добавления или делеции) для оптимального выравнивания двух последовательностей. Процент вычисляют посредством определения количества положений, в которых идентичное основание нуклеиновой кислоты или аминокислотный остаток встречается в обеих последовательностях, для получения количества совпадающих положений, разделяя количество совпадающих положений на общее количество положений в окне сравнения и умножая результат на 100 для получения процента идентичности последовательности. (e) Термин "значительная идентичность" полинуклеотидных последовательностей означает, что полинуклеотид содержит последовательность, имеющую по меньшей мере 70% идентичности последовательности, по меньшей мере 80% идентичности последовательности, по меньшей мере 90% идентичности последовательности и по меньшей мере 95% идентичности последовательности по сравнению с референсной последовательностью с использованием одной из описанных программ для выравнивания с использованием стандартных параметров. Специалисту в этой области будет понятно, что эти значения можно корректировать соответствующим образом для определения соответствующей идентичности белков, кодируемых двумя нуклеотидными последовательностями, с учетом вырожденности кодонов, сходства аминокислот, расположения рамки считывания и т.п. Термин "значительная идентичность" аминокислотных последовательностей для этих целей, как правило, означает идентичность последовательности по меньшей мере 60% или по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95%. Другим показателем того, что нуклеотидные последовательности являются, по существу, идентичными, является то, гибридизуются ли две молекулы друг с другом в строгих условиях. Однако, нуклеиновые кислоты, не гибридизующиеся друг с другом в строгих условиях, все равно являются, по существу, идентичными, если полипептиды, которые они кодируют, являются, по существу, идентичными. Это может возникать, например, если копию нуклеиновой кислоты получают с использованием максимальной вырожденности кодонов, допускаемой генетическим кодом. Одним из показателей того, что две последовательности нуклеиновой кислоты являются, по существу, идентичными, является то, что полипептид, который кодирует первая нуклеиновая кислота, иммунологически перекрестно реагирует с полипептидом, кодируемым второй нуклеиновой кислотой. Также можно получать мутации в нуклеотидных последовательностях белков по настоящему изобретению с учетом генетического кода, включая вырожденность кодонов.
В рамках изобретения термин "вариант" относится к полипептиду, отличающемуся от исходного белка одной или более заменами, делециями, инсерциями или другими модификациями аминокислот. Эти модификации не изменяют значительно биологическую активность исходного белка. Во многих случаях вариант сохраняет по меньшей мере 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или 100% биологической активности исходного белка. Биологическая активность варианта также может являться более высокой, чем биологическая активность исходного белка. Вариант может являться природным, таким как аллельный вариант или полиморфизм, или умышленно сконструированным.
Аминокислотная последовательность варианта является, по существу, идентичной последовательности исходного белка. Во многих вариантах осуществления вариант имеет по меньшей мере 50%, 60%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% или более глобальной идентичности или сходства последовательности по отношению к исходному белку. Идентичность или сходство последовательности можно определять различными известными в этой области способами, такими как Basic Local Alignment Tool (BLAST), анализ матрицы точек или способ динамического программирования. В одном из примеров идентичность или сходство последовательности определяют с использованием программ GAP Genetics Computer Group (GCG) (алгоритм Needleman-Wunsch). Аминокислотные последовательности варианта и исходного белка могут являться, по существу, идентичными в одной или более областях, но отличаться в других областях. Вариант может включать фрагмент (например, биологически активный фрагмент полипептида). В некоторых вариантах осуществления во фрагменте может отсутствовать до приблизительно 1, 2, 3, 4, 5, 10, 20, 30, 40, 50 или 100 аминокислотных остатков на N-конце, C-конце или обоих концах (независимо) полипептида по сравнению с полноразмерным полипептидом.
I. КЛЕТКИ ИММУННОЙ СИСТЕМЫ
Существует большое количество клеточных взаимодействий, составляющих иммунную систему. Эти взаимодействия происходят в специфических парах рецептор-лиганд, передающих сигнал в обоих направлениях таким образом, что каждая клетка получает инструкции на основе временного и пространственного распределения этих сигналов.
Модели на мышах очень полезны в обнаружении иммуномодуляторных путей, но клиническая польза этих путей не всегда переносима от инбредных линий мышей к аутбредной популяции людей, т.к. аутбредная популяция людей может включать индивидуумов, которые в разной степени зависят от индивидуальных путей иммуномодуляции.
Клетки иммунной системы включают лимфоциты, моноциты/макрофаги, дендритные клетки, близкородственные клетки Лангерганса, естественные киллеры (NK), тучные клетки, базофилы и других членов миелоидной линии клеток. Кроме того, группа специализированных эпителиальных и стромальных клеток создает анатомическое окружение, в котором развивается иммунная система, зачастую посредством секреции критических факторов, регулирующих рост и/или активацию генов клеток иммунной системы, которые также играют ключевую роль в фазу индуцирования и эффекторную фазу ответа (Paul, W. E., "Chapter 1: The Immune system: an introduction," Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999), p. 102).
Клетки иммунной системы обнаруживают в периферических организованных тканях, таких как селезенка, лимфоузлы, пейеровы бляшки кишечника и миндалины. Лимфоциты также обнаруживают в центральных лимфоидных органах, тимусе и костном мозге, где они проходят стадии развития, в ходе которых они приобретают способность опосредовать огромное количество ответов зрелой иммунной системы. Значительная часть лимфоцитов и макрофагов содержит рециркулирующую совокупность клеток, обнаруживаемых в крови и лимфе, обеспечивающих доставку иммунокомпетентных клеток в места, где они необходимы, и позволяющих иммунитету, образующемуся локально, становиться генерализованным (Paul, W. E., "Chapter 1: The Immune system: an introduction," Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999), p. 102).
Термин "лимфоцит" относится к небольшому лейкоциту, образующемуся в лимфатической ткани по всему организму, и у здоровых взрослых лимфоциты составляют до приблизительно 22-28% общего количества лейкоцитов в циркулирующей крови, играющих значительную роль в защите организма от заболеваний. Отдельные лимфоциты специализируются на том, что они готовы ответить на ограниченный набор структурно родственных антигенов посредством рекомбинации их генетического материала (например, для образования T-клеточного рецептора и B-клеточного рецептора). Эта готовность, существующая перед первым контактом иммунной системы с указанным антигеном, выражается в наличии рецепторов, специфических в отношении детерминант (эпитопов) на антигене на поверхностной мембране лимфоцита. Каждый лимфоцит обладает уникальной популяцией рецепторов, все из которых имеют идентичные антигенсвязывающие участки. Один набор или клон лимфоцитов отличается от другого клона структурой антигенсвязывающей областью рецепторов и, таким образом, отличается эпитопами, которые он может распознавать. Лимфоциты отличаются друг от друга не только специфичностью своих рецепторов, но также и своими функциями (Paul, W. E., "Chapter 1: The Immune system: an introduction," Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999), p. 102).
Различают два обширных класса лимфоцитов: B-лимфоциты (B-клетки), являющиеся предшественниками антитело-секретирующих клеток, и T-лимфоциты (T-клетки).
B-лимфоциты
B-лимфоциты образуются из гемопоэтических клеток костного мозга. Зрелая B-клетка может активироваться антигеном, содержащим эпитопы, распознаваемые поверхностью клетки. Активация может являться прямой, зависящей от перекрестного связывания мембранных молекул Ig антигеном (активация B-клеток, зависящей от перекрестного связывания), или непрямой, посредством взаимодействия с хелперной T-клеткой в процессе, обозначаемом как когнатная помощь. Во многих физиологических ситуациях стимулы перекрестного связывания рецептора и когнатной помощи действуют синергически для достижения более интенсивных B-клеточных ответов (Paul, W. E., "Chapter 1: The Immune system: an introduction," Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999)).
Для активации B-клеток, зависящей от перекрестного связывания, необходимо, чтобы антиген содержал множество копий эпитопа, комплементарного участку связывания рецепторов поверхности клетки, т.к. каждая B-клетка экспрессирует молекулы Ig с идентичными вариабельными областями. Такое требование удовлетворяется другими антигенами с повторяющимися эпитопами, такими как капсульные полисахариды микроорганизмов или белки вирусной оболочки. Активация B-клеток, зависящая от перекрестного связывания, представляет собой основной протективный иммунный ответ, развивающийся против этих микроорганизмов (Paul, W. E., "Chapter 1: The Immune system: an introduction", Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999)).
Когнатная помощь позволяет B-клеткам формировать ответы на антигены, которые не могут перекрестно связывать рецепторы и, в то же время, обеспечивает костимуляторные сигналы, и позволяет восстанавливать B-клетки из состояния инактивации, когда они подвергаются стимуляции явлениями слабого перекрестного связывания. Когнатная помощь зависит от связывания антигена иммуноглобулином (Ig) мембраны B-клетки, эндоцитоза антигена и его фрагментации на пептиды в эндосомальном/лизосомальном компартменте клетки. Некоторые из образующихся пептидов попадают в бороздку специализированного набора белков поверхности клетки, известных как молекулы главного комплекса гистосовместимости (MHC) класса II. Образующиеся комплексы MHC класса II/пептид экспрессируются на поверхности клетки и действуют как лиганды для антигенспецифических рецепторов набора T-клеток, обозначаемых как CD4+ T-клетки. CD4+ T-клетки на своей поверхности несут рецепторы, специфические в отношении комплекса MHC класса II B-клетки/пептид. Активация B-клеток зависит не только от связывания T-клетки через его T-клеточный рецептор (TCR), но это взаимодействие также позволяет активационному лиганду на T-клетке (лиганду CD40) связываться с его рецептором на B-клетке (CD40), осуществляя передачу сигнала активации B-клеток. Кроме того, хелперные T-клетки секретируют несколько цитокинов, регулирующих рост и дифференцировку стимулированной B-клетки посредством связывания с рецепторами цитокинов на B-клетке (Paul, W. E., "Chapter 1: The Immune system: an introduction, "Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999)).
Во время когнатной помощи для продукции антител лиганд CD40 транзиторно экспрессируется на активированных CD4+ хелперных T- клетках и связывается с CD40 на антигенспецифических B-клетках, таким образом, передавая второй костимуляторный сигнал. Последний сигнал необходим для роста и дифференцировки B-клеток и для образования B-клеток памяти посредством предотвращения апоптоза B-клеток герминативного центра, контактировавших с антигеном. Гиперэкспрессия лиганда CD40 в B- и T-клетках вовлечена в патогенную продукцию аутоантител у людей-пациентов с SLE (Desai-Mehta, A. et al., "Hyperexpression of CD40 ligand by B and T cells in human lupus and its role in pathogenic autoantibody production," J. Clin. Invest. Vol. 97(9), 2063-2073, (1996)).
T-лимфоциты
T-лимфоциты, образующиеся из предшественников в гемопоэтической ткани, подвергаются дифференцировке в тимусе, а затем заселяют периферическую лимфоидную ткань и становятся рециркулирующей совокупностью лимфоцитов. T-лимфоциты или T-клетки опосредуют широкий спектр иммунологических функций. Они включают способность помогать B-клеткам развиваться в антитело-продуцирующие клетки, способность повышать микробицидное действие моноцитов/макрофагов, ингибирование некоторых типов иммунных ответов, прямой цитолиз клеток-мишеней и мобилизацию воспалительного ответа. Эти эффекты зависят от экспрессии T-клетками специфических молекул поверхности клетки и секреции цитокинов (Paul, W. E., "Chapter 1: The Immune system: an introduction", Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999)).
T-клетки отличаются от B-клеток своим механизмом распознавания антигенов. Иммуноглобулин, B-клеточный рецептор, связывается с отдельными эпитопами на растворимых молекулах или твердых поверхностях. B-клеточные рецепторы распознают эпитопы, экспрессирующиеся на поверхности нативных молекул. В то время как антитело и B-клеточные рецепторы развиваются так, чтобы связывать и защищать от микроорганизмов во внеклеточных жидкостях, T-клетки распознают антигены на поверхности других клеток и опосредуют их функции посредством взаимодействия с этими антигенпрезентирующих клеток (APC) и изменения их свойств. Существует три основных типа APC в периферических лимфоидных органах, которые могут активировать T-клетки: дендритные клетки, макрофаги и B-клетки. Наиболее активными из них являются дендритные клетки, единственной функцией которых является презентирование чужеродных антигенов T-клеткам. Незрелые дендритные клетки локализуются в тканях по всему организму, включая кожу, кишечник и дыхательные пути. Когда они контактируют с проникающими микроорганизмами в этих местах, они осуществляют эндоцитоз патогенов и их продуктов и переносят их с лимфой в локальные лимфоузлы или лимфоидную ткань кишечника. Контакт с патогеном индуцирует созревание дендритных клеток из захватывающей антиген клетки в APC, которые могут активировать T-клетки. APC экспонируют три типа белковых молекул на своей поверхности, играющих роль в активации T-клетки для ее превращения в эффекторную клетку: (1) белки MHC, презентирующие чужеродный антиген T-клеточному рецептору; (2) костимуляторные белки, связывающиеся с комплементарными рецепторами на поверхности T-клеток; и (3) молекулы межклеточной адгезии, позволяющие T-клетке связываться с APC в течение периода времени, достаточно большого, чтобы они активировались ("Chapter 24: The adaptive immune system", Molecular biology of Cell, Alberts, B. et al., Garland Science, NY, (2002)).
T-клетки подразделяют на два разных класса с учетом экспрессии ими рецепторов поверхности клетки. Большая часть T-клеток экспрессирует T-клеточные рецепторы (TCR), состоящие из α- и β-цепей. Небольшая группа T-клеток экспрессирует рецепторы, состоящие из γ- и δ-цепей. Среди α/β T-клеток есть две субпопуляции: клетки, экспрессирующие корецепторную молекулу CD4 (CD4+ T-клетки); и клетки, экспрессирующие CD8 (CD8+ T-клетки). Эти клетки отличаются тем, как они распознают антиген и своими эффекторными и регуляторными функциями.
CD4+ T-клетки являются основными регуляторными клетками иммунной системы. Их регуляторная функция зависит от экспрессии молекул на их поверхности, таких как лиганд CD40, экспрессия которого индуцируется, когда T-клетки активируются, и широкого спектра цитокинов, которые они секретируют при активации.
T-клетки также опосредуют важные эффекторные функции, некоторые из которых определяют по профилю секретируемых ими цитокинов. Цитокины могут являться токсичными непосредственно для клеток-мишеней и могут мобилизовать мощные воспалительные механизмы.
Кроме того, T-клетки, в частности CD8+ T-клетки, могут развиваться в цитотоксические T-лимфоциты (CTL), способные эффективно лизировать клетки-мишени, экспрессирующие антигены, распознаваемые CTL (Paul, W. E., "Chapter 1: The Immune system: an introduction," Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999)).
T-клеточные рецепторы (TCR) распознают комплекс, состоящий из пептида, образовавшегося при протеолизе антигена и связанного со специальной бороздкой белка MHC класса II или класса I. CD4+ T-клетки распознают только комплексы пептид/MHC класса II, в то время как CD8+ T-клетки распознают комплексы пептид/MHC класса I (Paul, W. E., "Chapter 1: The Immune system: an introduction," Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999)).
Лиганд TCR (т.е. комплекс пептид/белок MHC) образуется в APC. В основном, молекулы MHC класса II связываются с пептидами, образовавшимися из белков, захваченных APC посредством эндоцитоза. Эти нагруженные пептидом молекулы MHC класса II затем экспрессируются на поверхности клетки, где они доступны для связывания CD4+ T-клетками с помощью TCR, способных распознавать экспрессируемый на поверхности клетки комплекс. Таким образом, CD4+ T-клетки специализируются на реакции с антигенами, происходящими из внеклеточных источников (Paul, W. E., "Chapter 1: The Immune system: an introduction," Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999)).
В отличие от этого, молекулы MHC класса I, в основном, нагружены пептидами, образовавшимися из внутренне синтезируемых белков, таких как вирусные белки. Эти пептиды продуцируются из цитозольных белков посредством протеолиза в протеасоме и транслоцируются в шероховатый эндоплазматический ретикулум. Такие пептиды, как правило, состоят из девяти аминокислот, связаны с молекулами MHC класса I и перемещены к поверхности клетки, где они могут распознаваться CD8+ T-клетками, экспрессирующими соответствующие рецепторы. Это придает T-клеточной системе, в частности, CD8+ T-клеткам, способность определять клетки, экспрессирующие белки, отличающиеся или продуцирующиеся в гораздо больших количествах, чем в остальных клетках организма (например, вирусные антигены) или мутантные антигены (такие как активные продукты онкогенов), даже если эти белки в своей интактной форме ни экспрессируются на поверхности клетки, ни секретируются (Paul, W. E., "Chapter 1: The Immune system: an introduction," Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999)).
T-клетки также можно классифицировать с учетом их функции в качестве хелперных T-клеток, T-клеток, участвующих в индуцировании клеточного иммунитета, супрессорных T-клеток и цитотоксических T-клеток.
Хелперные T-клетки
Хелперные T-клетки являются T-клетками, стимулирующими B-клетки с развитием гуморальных ответов на белки и другие T-клеточно-зависимые антигены. T-клеточно-зависимые антигены являются иммуногенами, в которых отдельные эпитопы встречаются лишь однократно или ограниченное количество раз таким образом, что они неспособны перекрестно связываться с мембранным иммуноглобулином (Ig) B-клеток или делают это неэффективно. B-клетки связываются с антигеном посредством своего мембранного Ig, и комплекс подвергаются эндоцитозу. В эндосомальном и лизосомальном компартментах, антиген фрагментируется на пептиды под действием протеолитических ферментов, и один или более образовавшихся пептидов нагружается на молекулы MHC класса II, транспортируемые через этот везикулярный компартмент. Затем образующийся комплекс пептид/MHC класса II экспортируется на мембрану поверхности B-клетки. T-клетки с рецепторами, специфическими в отношении молекулярного комплекса пептид/MHC класса II, распознают этот комплекс на поверхности B-клетки. (Paul, W. E., "Chapter 1: The Immune system: an introduction," Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia (1999)).
Активация B-клеток зависит от связывания T-клетки через ее TCR и взаимодействия лиганда CD40 T-клетки (CD40L) с CD40 на B-клетке. T-клетки не экспрессируют CD40L конститутивно. Вместо этого, экспрессия CD40L индуцируется в результате взаимодействия с APC, экспрессирующими когнатный антиген, распознаваемый TCR T-клетки, и CD80 или CD86. CD80/CD86, как правило, экспрессируется активированными, а не покоящимися B-клетками таким образом, что хелперное взаимодействие, включающее активированную B-клетку и T-клетку, может приводить к эффективной продукции антител. Однако во многих случаях исходное индуцирование CD40L на T-клетках зависит от распознавания ими антигена на поверхности APC, конститутивно экспрессирующих CD80/86, таких как дендритные клетки. Такие активированные хелперные T-клетки затем могут эффективно взаимодействовать с B-клетками и помогать им. Перекрестное связывание мембранного Ig на B-клетке, даже если и является неэффективным, может действовать синергически с взаимодействием CD40L/CD40, приводя к интенсивной активации B-клеток. Последующие события в рамках B-клеточного ответа, включая пролиферацию, секрецию Ig и переключение классов экспрессируемых Ig, зависит или усиливается под действием T-клеточных цитокинов (Paul, W. E., "Chapter 1: The Immune system: an introduction," Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999)).
CD4+ T-клетки имеют склонность к дифференцировке в клетки, главным образом, секретирующие цитокины ИЛ-4, ИЛ-5, ИЛ-6 и ИЛ-10 (TH2-клетки), или клетки, в основном, продуцирующие ИЛ-2, ИФНγ и лимфотоксин (TH1-клетки). TH2-клетки очень эффективны в помощи B-клеткам в развитии в антитело-продуцирующие клетки, в то время как TH1-клетки являются эффективными индукторами клеточных иммунных ответов, включающих усиление микробицидной активности моноцитов и макрофагов и последующее повышение эффективности лизиса микроорганизмов во внутриклеточных везикулярных компартментах. Хотя CD4+ T-клетки с фенотипом TH2-клеток (т.е. ИЛ-4, ИЛ-5, ИЛ-6 и ИЛ-10) являются эффективными хелперными клетками, TH1-клетки также могут являться хелперами (Paul, W. E., "Chapter 1: The Immune system: an introduction, "Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999)).
Вовлечение T-клеток в индуцирование клеточного иммунитета
T-клетки также могут повышать способность моноцитов и макрофагов разрушать внутриклеточные микроорганизмы. В частности, интерферон-гамма (ИФНγ), продуцируемый хелперными T-клетками, усиливает несколько механизмов, посредством которых мононуклеарные фагоциты разрушают внутриклеточные бактерии и паразитов, включая образование оксида азота и индуцирование продукции фактора некроза опухоли (ФНО). TH1-клетки эффективны в усилении микробицидного действия, т.к. они продуцируют ИФНγ. В отличие от этого, два из основных цитокинов, продуцируемых TH2-клетками, ИЛ-4 и ИЛ-10, блокируют эти активности (Paul, W. E., "Chapter 1: The Immune system: an introduction," Fundamental Immunology, 4th Edition, Ed. Paul, W. E., Lippicott-Raven Publishers, Philadelphia, (1999)).
Регуляторные T-клетки (Treg)
Иммунный гомеостаз поддерживается с помощью контролируемого баланса между инициированием и отрицательной регуляцией иммунного ответа. Механизмы апоптоза и анергии T-клеток (механизм толерантности, при котором T-клетки, по существу, функционально инактивируются после контакта с антигеном (Scwartz, R. H., "T Cell anergy", Annu. Rev. Immunol., Vol. 21: 305-334 (2003)) вносят вклад в отрицательную регуляцию иммунного ответа. Третий механизм представлен активной супрессией активированных T-клеток супрессорными или регуляторными CD4+ T-клетками (Treg) (обзор в Kronenberg, M. et al., "Regulation of immunity by self-reactive T cells", Nature, Vol. 435: 598-604 (2005)). CD4+ Treg, конститутивно экспрессирующие альфа-цепь рецептора ИЛ-2 (ИЛ-2Rα) (CD4+ CD25+), являются природной субпопуляцией T-клеток, являющейся анергичной и супрессорной (Taams, L. S. et al., "Human anergic/suppressive CD4+CD25+ T cells: a highly differentiated и apoptosis-prone population", Eur. J. Immunol. Vol. 31: 1122-1131 (2001)). Истощение CD4+CD25+ Treg приводит к системному аутоиммунному заболеванию у мышей. Кроме того, перенос этих Treg предотвращает развитие аутоиммунного заболевания. CD4+CD25+ Treg человека, схожие с аналогичными клетками мыши, образуются в тимусе и отличаются способностью супрессировать пролиферацию T-клеток-респондеров с помощью механизма, зависящего от межклеточных контактов, неспособностью продуцировать ИЛ-2 и анергическим фенотипом in vitro. CD4+CD25+ T-клетки человека можно разделять на супрессорные (CD25high) и несупрессорные (CD25low) клетки в зависимости от уровня экспрессии CD25. Показано, что член семейства факторов транскрипции Forkhead, FOXP3, экспрессируется в CD4+CD25+ Treg мыши и человека и, по-видимому, является основным геном, контролирующим развитие CD4+CD25+ Treg (Battaglia, M. et al., "Rapamycin promotes expansion of functional CD4+CD25+Foxp3+ regulator T cells of both healthy subjects and type 1 diabetic patients", J. Immunol., Vol. 177: 8338-8347, (2006)).
Цитотоксические T-лимфоциты
CD8+ T-клетки, распознающие пептиды из белков, продуцируемых в клетке-мишени, имеют цитотоксические свойства в том смысле, что они приводят к лизису клеток-мишеней. Механизм CTL-индуцируемого лизиса включает продукцию CTL перфорина, молекулы, которая может встраиваться в мембрану клеток-мишеней и способствовать лизису этой клетки. Опосредованный перфорином лизис усиливается гранзимами, группой ферментов, продуцируемых активируемыми CTL. Многие активные CTL также экспрессируют большие количества лиганда Fas на своей поверхности. Взаимодействие лиганда Fas на поверхности CTL с Fas на поверхности клетки-мишени инициирует апоптоз в клетке-мишени, что приводит к гибели этих клеток. Опосредованный CTL лизис, по-видимому, является основным механизмом деструкции инфицированных вирусом клеток.
Активация лимфоцитов
Термины "активация" или "активация лимфоцитов" относятся к стимуляции лимфоцитов специфическими антигенами, неспецифическими митогенами или аллогенными клетками, что приводит к синтезу РНК, белка и ДНК и продукции лимфокинов; после этого следует пролиферация и дифференцировка различных эффекторных клеток и клеток памяти. Активация T-клеток зависит от взаимодействия комплекса TCR/CD3 с его когнатным лигандом, пептидом, связанным с бороздкой молекулы MHC класса I или класса II. Молекулярные события, запускаемые активацией рецептора, являются комплексными. Одной из наиболее ранних стадий, по-видимому, является активация тирозинкиназы, приводящая к фосфорилированию тирозина ряда субстратов, контролирующему несколько путей передачи сигнала. Они включают набор адаптерных белков, связывающих TCR с путем Ras, фосфолипазу Cγ1, фосфорилирование тирозина которой повышает ее каталитическую активность и активирует метаболический путь инозитолфосфолипидов, что приводит к повышению концентрации свободного внутриклеточного кальция и активации протеинкиназы C, и группу других ферментов, контролирующих рост и дифференцировку клеток. В дополнение к активации рецептора, для полной отвечаемости T-клетки необходима осуществляемая вспомогательными клетками костимуляторная активность, например, активация CD28 на T-клетке и CD80 и/или CD86 на APC.
T-клетки памяти
После распознавания и эрадикации патогенов посредством адаптивных иммунных ответов подавляющее большинство (90-95%) T-клеток подвергается апоптозу, при этом остальные клетки образуют совокупность T-клеток памяти, обозначаемых как T-клетки центральной памяти (TCM), эффекторные T-клетки памяти (TEM) и резидентные T-клетки памяти (TRM) (Clark, R.A., "Resident memory T cells in human health and disease", Sci. Transl. Med., 7, 269rv1, (2015)). CD45RA экспрессируется на наивных T-клетках, а также CD4+ и CD8+ эффекторных клетках. После контакта с антигеном T-клетки центральной памяти и эффекторные T-клетки памяти начинают экспрессировать CD45RO и утрачивают экспрессию CD45RA. Таким образом, CD45RA или CD45RO используют для общего дифференцирования наивных популяций и популяций памяти. CCR7 и CD62L являются двумя другими маркерами, которые можно использовать для различения T-клеток центральной памяти и эффекторных T-клеток памяти. Наивные клетки и клетки центральной памяти экспрессируют CCR7 и CD62L для миграции во вторичные лимфоидные органы. Таким образом, наивные T-клетки представляют собой CD45RA+CD45RO-CCR7+CD62L+, T-клетки центральной памяти представляют собой CD45RA-CD45RO+CCR7+CD62L+, и эффекторные T-клетки памяти представляют собой CD45RA-CD45RO+CCR7-CD62L-.
По сравнению со стандартными T-клетками, эти T-клетки памяти являются долгоживущими клетками с разными фенотипами, такими как экспрессия специфических поверхностных маркеров, быстрая продукция различных профилей цитокинов, способность направлять функцию эффекторных клеток и уникальные профили распределения хоминга. T-клетки памяти демонстрируют быстрые реакции после повторного воздействия соответствующих антигенов для устранения повторной инфекции возбудителя и, таким образом, быстрого восстановления баланса иммунной системы. Растущие доказательства подтверждают, что аутоиммунные T-клетки памяти препятствуют большинству попыток лечения или излечения аутоиммунных заболеваний (Clark, R.A., "Resident memory T cells in human health and disease", Sci. Transl. Med., Vol. 7, 269rv1, (2015)).
II. ИСКУССТВЕННЫЕ АНТИГЕНПРЕЗЕНТИРУЮЩИЕ КЛЕТКИ (aAPC)
Настоящее изобретение относится к эритроидным клеткам (например, безъядерным эритроидным клеткам) и безъядерным клеткам, сконструированным для активации или супрессии T-клеток. В некоторых вариантах осуществления безъядерная клетка является эритроидной клеткой, например, утратившей свое ядро при дифференцировке из эритроцитарной клетки-предшественника. Однако следует понимать, что не все безъядерные клетки являются эритроидными клетками, и, таким образом, безъядерные клетки, представленные в настоящем описании, также могут включать, например, тромбоциты. В некоторых вариантах осуществления безъядерные клетки не являются тромбоцитами и, таким образом, являются несодержащими тромбоциты безъядерными клетками. В некоторых аспектах настоящего изобретения безъядерная клетка является ретикулоцитом или эритроцитом (полностью зрелым эритроцитом (RBC)). Эритроциты имеют ряд преимуществ по сравнению с другими клетками, включая то, что они являются неаутологичными (например, по существу, у них отсутствует главный комплекс гистосовместимости (MHC)), имеют большее время циркуляции в организме индивидуума (например, более 30 дней) и пригодны для получения в больших количествах.
Специалистам в этой области с учетом настоящего описания будет понятно, что многочисленные иммунорегуляторные молекулы можно использовать для получения практически неограниченного диапазона aAPC, используя способы, представленные в настоящем описании. Т.е. в этой области существует представление о явлениях и молекулах, вовлеченных в активацию и индуцирование T-клеток.
В некоторых аспектах настоящее изобретение относится к сконструированной эритроидной клетке или безъядерной клетке, содержащей экзогенный полипептид, например, содержащей или презентирующей экзогенный полипептид на поверхности клетки. Экзогенные полипептиды по настоящему изобретению включают, в качестве неограничивающих примеров, экзогенные антигенные полипептиды, экзогенные антигенпрезентирующие полипептиды, экзогенные костимуляторные полипептиды, экзогенные коингибиторные полипептиды, экзогенные модулирующие метаболизм полипептиды и экзогенные Treg-костимуляторные полипептиды.
Экзогенные антигенные полипептиды
Экзогенный антигенный полипептид является полипептидом, способным индуцировать иммунный ответ. В некоторых вариантах осуществления экзогенный антигенный полипептид является полипептидом, который посредством индуцирования иммунного ответа ингибирует злокачественное новообразование, например, уменьшает или облегчает причину или симптом злокачественного новообразования, или улучшает значение параметра, ассоциированного со злокачественным новообразованием. В некоторых вариантах осуществления экзогенный антигенный полипептид является полипептидом, который посредством индуцирования иммунного ответа ингибирует инфекционное заболевание, например, уменьшает или облегчает причину или симптом инфекционного заболевания, или улучшает значение параметра, ассоциированного с инфекционным заболеванием. В некоторых вариантах осуществления экзогенный антигенный полипептид является полипептидом, который посредством индуцирования иммунного ответа ингибирует аутоиммунное заболевание, например, уменьшает или облегчает причину или симптом аутоиммунного заболевания, или улучшает значение параметра, ассоциированного с аутоиммунным заболеванием.
В некоторых вариантах осуществления экзогенный антигенный полипептид содержит или состоит из антигенного полипептида, выбранного из таблицы 1, или его фрагмента или варианта, или молекулы антитела против него.
Таблица 1
 , 2011
, 2011
PVTWRRAPA
37
312-320
Cw6
18
FRSGLDSYV
50
126-134
AD
PVAS
PVAS
KSRWSGSHQFEQLS
HQY
IETQSSSSEEIV
VIA
( 46-54)
PRAAEVPR
(14-33)
LQQL
GSCPGMPHL
(81-102)
GSCPGMPHL
(81-102)
GA
FPRFFMVAKQ
INSSVF
Pascolo, 2001 , 2004
, 2004
EY
TKAE
KAE
LEY
YR
LEY
ETS
KYR
HL
IV
SG
RA
AE
AE
IR
AR
HGVTSA
Chen, 2000
Valmori, 2000
(1-11)
(18-27)
GL , 2002
, 2002
VF
MEAELARRSLAQ
MEAELARRSLAQ
ILTIRLTAADHR
VPRAAEVPR
(14-33)
ILTIRLT
CLQQL
MEAELARRSLAQ
NILTIRLTAADHR
MEAELARRSLAQ
PM
GA
FSK
VYMKRK
AMT
AM
WTHRLRE
EKIVYVY
FKVTLPPF
QLVVYEEI
KRAADFH
NYEVMTK
QLVVYEEI
GE
GE
GE
RSQ
QTPG
NRS
LVNEEATGQFRV
QV
NNS
TVY
QRLD
PEPE
VTVYH
TVY
VILGVLLLIGCWY
CRR
Qf
HVGTQCALTRR
KGHGHS
YEKLSAE
DSLEDYD
DT
Wang, 1998
SGP
Skipper, 1996b
FP
QD
QWLQRHRP
GSAV (SEQ ID NO: 13)
RFT (SEQ ID NO: 14)
KEFV (SEQ ID NO: 15)
AAV
CG
CVN
VVS
QEY
TGALQ
PA
AA
STL
VAK
VT
KQ
QR
NGLL (SEQ ID NO: 8)
FWL (SEQ ID NO: 9)
MTNL (SEQ ID NO: 10)
IPV (SEQ ID NO: 11)
NCRP (SEQ ID NO: 12)
NCRP (SEQ ID NO: 12)
INK
Schmidt, 2003
RAKN
DDI
VAHL
SRKH
SRKH
VVHLYRNGK
В других вариантах осуществления антигенный полипептид является антигенным полипептидом из любого из антигенов, представленных в настоящем описании. Например, в некоторых вариантах осуществления антигенный полипептид является антигенным полипептидом из антигена, выбранного из антигенов, приведенных в таблицах 1 и 14-24. В некоторых вариантах осуществления антигенный полипептид является антигенным полипептидом из антигена, выбранного из антигенов, приведенных в таблице 16. В некоторых вариантах осуществления антигенный полипептид является антигенным полипептидом из антигена, выбранного из антигенов, приведенных в таблице 17. В некоторых вариантах осуществления антигенный полипептид является антигенным полипептидом из антигена, выбранного из антигенов, приведенных в таблице 18. В некоторых вариантах осуществления антигенный полипептид является антигенным полипептидом из антигена, выбранного из антигенов, приведенных в таблице 19. В некоторых вариантах осуществления антигенный полипептид является антигенным полипептидом из антигена, выбранного из антигенов, приведенных в таблице 20. В некоторых вариантах осуществления антигенный полипептид является антигенным полипептидом из антигена, выбранного из антигенов, приведенных в таблице 21. В некоторых вариантах осуществления антигенный полипептид является антигенным полипептидом из антигена, выбранного из антигенов, приведенных в таблице 22. В некоторых вариантах осуществления антигенный полипептид является антигенным полипептидом из антигена, выбранного из антигенов, приведенных в таблице 23 В некоторых вариантах осуществления антигенный полипептид является антигенным полипептидом из антигена, выбранного из антигенов, приведенных в таблице 24.
Пример антигенного полипептида, например, полипептид человека, выбранный из таблицы 1 или таблиц 14-24, включает:
a) природную форму полипептида человека, например, природную форму полипептида человека, не ассоциированную с состоянием заболевания;
b) полипептид человека, имеющий последовательность, содержащуюся в базе данных, например, базе данных GenBank, на 22 декабря 2017 года, например, природную форму полипептида человека, не ассоциированную с состоянием заболевания, имеющую последовательность, содержащуюся в базе данных, например, базе данных GenBank, на 22 декабря 2017 года;
c) полипептид человека, имеющий последовательность, отличающуюся не более чем на 1, 2, 3, 4, 5 или 10 аминокислотных остатков от последовательности по п. a) или b);
d) полипептид человека, имеющий последовательность, отличающуюся не более чем на 1, 2, 3, 4, 5 или 10% своих аминокислотных остатков от последовательности по п. a) или b);
e) полипептид человека, имеющий последовательность по существу, не отличающуюся от последовательности по п. a) или b); или
f) полипептид человека, имеющий последовательность по п. c), d) или e), по существу, не отличающуюся по биологической активности, например, ферментативной активности (например, специфичности или обороту) или связывающей активности (например, специфичности связывания или аффинности) от полипептида человека, имеющего последовательность по п. a) или b). Пептиды-кандидаты по п. f) можно получать и подвергать скринингу на схожую активность, как представлено в настоящем описании, и они будут эквивалентными, если экспрессируются в сконструированных эритроидных клетках, как представлено в настоящем описании.
В вариантах осуществления экзогенный антигенный полипептид содержит полипептид человека или его фрагмент, например, весь полипептид человека по пп. a), b), c), d), e) или f) или его фрагмент по предшествующему абзацу. В варианте осуществления экзогенный полипептид содержит слитый полипептид, содержащий весь полипептид человека по пп. a), b), c), d), e) или f) или его фрагмент по предшествующему абзацу и дополнительную аминокислотную последовательность. В варианте осуществления дополнительная аминокислотная последовательность содержит весь полипептид человека по пп. a), b), c), d), e) или f) или его фрагмент по предшествующему абзацу для другого полипептида человека.
В некоторых вариантах осуществления экзогенные антигенные полипептиды презентируют на антигенпрезентирующих полипептидах, например, экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I или MHC класса II).
В некоторых вариантах осуществления экзогенный антигенный полипептид имеет длину от 8 аминокислот до 24 аминокислот, например, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23 или 24 аминокислот. В дополнительных вариантах осуществления в экзогенный антигенный полипептид встраивают расщепляемый участок.
MAGE-A
Антигены MAGE-A экспрессируются в различных злокачественных новообразованиях разного гистологического происхождения и зародышевых клетках. Антигены MAGE-A принадлежат к крупному семейству раково-тестикулярных антигенов (CTA), экспрессию которых постоянно обнаруживают в злокачественных новообразованиях разного гистологического происхождения и зародышевых клетках (Simpson et al. Nat Rev Cancer. 2005 Aug; 5(8):615-25). Семейство генов MAGE-A включает 12 членов (MAGE-A1, MAGE-A2, MAGE-A3, MAGE-A4, MAGE-A5, MAGE-A6, MAGE-A7, MAGE-A8, MAGE-A9, MAGE-A10, MAGE-A11, MAGE-A12), локализованных на хромосоме Xq28 (Chomez et al., Cancer Res. 2001 Jul 15; 61(14):5544-51; DePlaen et al., Immunogenetics. 1994; 40(5):360-9). MAGE-A1, -A2, -A3, -A4, -A6, -A10 и -A12 экспрессируются в значительной части первичных и метастатических опухолей различных гистологических типов и являются мишенями для специфических в отношении опухолевых антигенов цитотоксических T-лимфоцитов. Индивидуальная экспрессия MAGE-A варьируется в зависимости от типа опухоли, но, в целом, подавляющее большинство опухолей экспрессирует по меньшей мере один антиген MAGE-A. Конкретные продукты генов идентифицированы посредством иммуногистохимии в злокачественных новообразованиях разного гистологического происхождения, включая значительную долю случаев немелкоклеточного рака легких (NSCLC), рака мочевого пузыря, рака пищевода и рака головы и шеи, миеломы, сарком и трижды негативного рака молочной железы (Juretic et al. Lancet Oncol. 2003 Feb; 4(2):104-9; Curigliano et al., Ann Oncol. 2011 Jan; 22(1):98-103; vanBaren et al., Ann Oncol. 2011 Jan; 22(1):98-103; Antonescu et al., Hum Pathol. 2002 Feb; 33(2):225-9).
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A. В дополнительном варианте осуществления антиген MAGE-A выбран из MAGE-A1, MAGE-A2, MAGE -A3, MAGE-A4, MAGE-A5, MAGE-A6, MAGE-A7, MAGE-A8, MAGE-A9, MAGE-A10, MAGE-A11 и MAGE-A12. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A1. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A2. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A3. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A4. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A5. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A6. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A7. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A8. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A9. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A10. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A11. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A12. В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном MAGE-A. В некоторых вариантах осуществления антиген MAGE-A выбран из MAGE-A1, MAGE-A2, MAGE -A3, MAGE-A4, MAGE-A5, MAGE-A6, MAGE-A7, MAGE-A8, MAGE-A9, MAGE-A10, MAGE-A11 и MAGE-A12. В некоторых вариантах осуществления антиген MAGE-A выбран из MAGE-A1, MAGE-A2, MAGE -A3, MAGE-A4, MAGE-A6, MAGE-A10 и MAGE-A12.
В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является антигеном MAGE-A1. В некоторых вариантах осуществления антиген MAGE-A1 выбран из группы, состоящей из EADPTGHSY (SEQ ID NO: 123), KVLEYVIKV (SEQ ID NO: 126), SLFRAVITK (SEQ ID NO: 127), EVYDGREHSA (SEQ ID NO: 129), RVRFFFPSL (SEQ ID NO: 130), EADPTGHSY (SEQ ID NO: 123), REPVTKAEML (SEQ ID NO: 131), KEADPTGHSY (SEQ ID NO: 132), DPARYEFLW (SEQ ID NO: 133), ITKKVADLVGF (SEQ ID NO: 134), SAFPTTINF (SEQ ID NO: 135), SAYGEPRKL (SEQ ID NO: 136), RVRFFFPSL (SEQ ID NO: 130), SAYGEPRKL (SEQ ID NO: 136), TSCILESLFRAVITK (SEQ ID NO: 137), PRALAETSYVKVLEY (SEQ ID NO: 138), FLLLKYRAREPVTKAE (SEQ ID NO: 139) и EYVIKVSARVRF (SEQ ID NO: 140).
В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является антигеном MAGE-A2. В некоторых вариантах осуществления антиген MAGE-A2 выбран из группы, состоящей из YLQLVFGIEV (SEQ ID NO: 141), EYLQLVFGI (SEQ ID NO: 145), REPVTKAEML (SEQ ID NO: 131), EGDCAPEEK (SEQ ID NO: 146) и LLKYRAREPVTKAE (SEQ ID NO: 147).
В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является антигеном MAGE-A3. В некоторых вариантах осуществления антиген MAGE-A3 выбран из группы, состоящей из EVDPIGHLY (SEQ ID NO: 148), FLWGPRALVD (SEQ ID NO: 149), KVAELVHFL (SEQ ID NO: 150), TFPDLESEF (SEQ ID NO: 153), VAELVHFLL (SEQ ID NO: 154), MEVDPIGHLY (SEQ ID NO: 155), EVDPIGHLY (SEQ ID NO: 148), REPVTKAEML (SEQ ID NO: 131), AELVHFLLLI (SEQ ID NO: 157), EVDPIGHLY (SEQ ID NO: 148), WQYFFPVIF (SEQ ID NO: 158), EGDCAPEEK (SEQ ID NO: 146), KKLLTQHFVQENYLEY (SEQ ID NO: 159), RKVAELVHFLLLKYR (SEQ ID NO: 160), KKLLTQHFVQENYLEY (SEQ ID NO: 159), ACYEFLWGPRALVETS (SEQ ID NO: 161), RKVAELVHFLLLKYR (SEQ ID NO: 160), VIFSKASSSLQL (SEQ ID NO: 162), VIFSKASSSLQL (SEQ ID NO: 162), VFGIELMEVDPIGHL (SEQ ID NO: 163), GDNQIMPKAGLLIIV (SEQ ID NO: 164), TSYVKVLHHMVKISG (SEQ ID NO: 165), RKVAELVHFLLLKYRA (SEQ ID NO: 166) и FLLLKYRAREPVTKAE (SEQ ID NO: 139).
В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является антигеном MAGE-A4. В вариантах осуществления антиген MAGE-A4 выбран из группы, состоящей из EVDPASNTYJ (SEQ ID NO: 167) и GVYDGREHTV (SEQ ID NO: 168).
В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является антигеном MAGE-A5.
В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является антигеном MAGE-A6. В некоторых вариантах осуществления антиген MAGE-A6 выбран из группы, состоящей из SESLKMIF (SEQ ID NO: 170), MVKISGGPR (SEQ ID NO: 171), EVDPIGHVY (SEQ ID NO: 172), REPVTKAEML (SEQ ID NO: 131), EGDCAPEEK (SEQ ID NO: 146), ISGGPRISY (SEQ ID NO: 173), LLKYRAREPVTKAE (SEQ ID NO: 147).
В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном MAGE-A7.
В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном MAGE-A8.
В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном MAGE-A9 (SEQ ID NO: 176). В некоторых вариантах осуществления антиген MAGE-A9 является ALSVMGVYV.
В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном MAGE-A10. В некоторых вариантах осуществления антиген MAGE-A10 выбран из группы, состоящей из GLYDGMEHLI (SEQ ID NO: 715) и DPARYEFLW (SEQ ID NO: 133).
В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном MAGE-A11.
В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном MAGE-A12. В некоторых вариантах осуществления антиген MAGE-A12 выбран из группы, состоящей из FLWGPRALVE (SEQ ID NO: 179), VRIGHLYIL (SEQ ID NO: 180), EGDCAPEEK (SEQ ID NO: 146), REPFTKAEMLGSVIR (SEQ ID NO: 181) и AELVHFLLLKYRAR (SEQ ID NO: 182).
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере, один экзогенный антигенный полипептид, содержащий эпитоп, общий для нескольких опухолевых антигенов семейства MAGE-A. В некоторых вариантах осуществления экзогенный антигенный полипептид содержит эпитоп p248v9 (YLEYRQVPV (SEQ ID NO: 124)), иммуногенный пептид, презентируемый HLA-A*0201 и способный индуцировать цитотоксические T-лимфоциты (CTL), распознающие все антигены MAGE-A. В некоторых вариантах осуществления экзогенный антигенный полипептид содержит эпитоп p248g9 (YLEYRQVPG (SEQ ID NO: 156)), иммуногенный пептид, способный индуцировать CTL, распознающие MAGE-A2, A3, A4, A6, A10, A12. В некоторых вариантах осуществления экзогенный антигенный полипептид содержит эпитоп p248d9 (YLEYRQVPD (SEQ ID NO: 125)), иммуногенный пептид, способный индуцировать CTL, распознающие MAGE-A1.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является p248v9 (YLEYRQVPV (SEQ ID NO: 124)). В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является p248g9 (YLEYRQVPG (SEQ ID NO: 156)). В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является p248d9 (YLEYRQVPD (SEQ ID NO: 125)).
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является p248v9 (YLEYRQVPV (SEQ ID NO: 124)). В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является p248g9 (YLEYRQVPG (SEQ ID NO: 156)). В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является p248d9 (YLEYRQVPD (SEQ ID NO: 125)). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является MHC I HLA-A, например, MHC I HLA-A *201.
В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, p248v9 (YLEYRQVPV (SEQ ID NO: 124)), слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A *201, слитым с трансмембранным доменом GPA (GPA). В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, p248g9 (YLEYRQVPG (SEQ ID NO: 156)), слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A *201, слитым с трансмембранным доменом GPA (GPA). В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, p248d9 (YLEYRQVPD (SEQ ID NO: 125)), слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A *201, слитым с трансмембранным доменом GPA (GPA).
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A, приведенным в таблице 1. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A, приведенным в таблице 1, и дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A, выбранным из антигенов MAGE-A, приведенных в таблице 1, и дополнительно презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является соответствующим HLA MHC класса I или MHC класса II, приведенным в таблице 1 для конкретного антигена MAGE-A. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A, выбранным из антигенов MAGE-A, приведенных в таблице 1, и дополнительно презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является соответствующим HLA MHC класса I или MHC класса II, приведенным в таблице 1 для конкретного антигена MAGE-A, и экзогенный полипептид, содержащий 4-1BBL. В другом варианте осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MAGE-A, выбранным из антигенов MAGE-A, приведенных в таблице 1, и дополнительно презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является соответствующим HLA MHC класса I, приведенным в таблице в таблице 1 для конкретного антигена MAGE-A, и экзогенный полипептид, содержащий 4-1BBL.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид содержит или состоит из антигена MAGE-A, выбранного из EADPTGHSY (SEQ ID NO: 123), KVLEYVIKV (SEQ ID NO: 126), SLFRAVITK (SEQ ID NO: 127), EVYDGREHSA (SEQ ID NO: 129), RVRFFFPSL (SEQ ID NO: 130), EADPTGHSY (SEQ ID NO: 123), REPVTKAEML (SEQ ID NO: 131), KEADPTGHSY (SEQ ID NO: 132), DPARYEFLW (SEQ ID NO: 133), ITKKVADLVGF (SEQ ID NO: 134), SAFPTTINF (SEQ ID NO: 135), SAYGEPRKL (SEQ ID NO: 136), RVRFFFPSL (SEQ ID NO: 130), SAYGEPRKL (SEQ ID NO: 136), TSCILESLFRAVITK (SEQ ID NO: 137), PRALAETSYVKVLEY (SEQ ID NO: 138), FLLLKYRAREPVTKAE (SEQ ID NO: 139), EYVIKVSARVRF (SEQ ID NO: 140), YLQLVFGIEV (SEQ ID NO: 141), EYLQLVFGI (SEQ ID NO: 145), REPVTKAEML (SEQ ID NO: 131), EGDCAPEEK (SEQ ID NO: 146), LLKYRAREPVTKAE (SEQ ID NO: 147), EVDPIGHLY (SEQ ID NO: 148), FLWGPRALVD (SEQ ID NO: 149), KVAELVHFL (SEQ ID NO: 150), TFPDLESEF (SEQ ID NO: 153), VAELVHFLL MEVDPIGHLY (SEQ ID NO: 716), EVDPIGHLY (SEQ ID NO: 148), REPVTKAEML (SEQ ID NO: 131), AELVHFLLLI (SEQ ID NO: 157), MEVDPIGHLY (SEQ ID NO: 155), WQYFFPVIF (SEQ ID NO: 158), EGDCAPEEK (SEQ ID NO: 146), KKLLTQHFVQENYLEY (SEQ ID NO: 159), RKVAELVHFLLLKYR (SEQ ID NO: 160), KKLLTQHFVQENYLEY (SEQ ID NO: 159), ACYEFLWGPRALVETS (SEQ ID NO: 161), RKVAELVHFLLLKYR (SEQ ID NO: 160), VIFSKASSSLQL (SEQ ID NO: 162), VIFSKASSSLQL (SEQ ID NO: 162), VFGIELMEVDPIGHL (SEQ ID NO: 163), GDNQIMPKAGLLIIV (SEQ ID NO: 164), TSYVKVLHHMVKISG (SEQ ID NO: 165), RKVAELVHFLLLKYRA (SEQ ID NO: 166), FLLLKYRAREPVTKAE (SEQ ID NO: 139), EVDPASNTYj (SEQ ID NO: 167), GVYDGREHTV (SEQ ID NO: 168), NYKRCFPVI (SEQ ID NO: 169), SESLKMIF (SEQ ID NO: 170), MVKISGGPR (SEQ ID NO: 171), EVDPIGHVY (SEQ ID NO: 172), REPVTKAEML (SEQ ID NO: 131), EGDCAPEEK (SEQ ID NO: 146), ISGGPRISY (SEQ ID NO: 173), LLKYRAREPVTKAE (SEQ ID NO: 147), ALSVMGVYV (SEQ ID NO: 176), GLYDGMEHLI (SEQ ID NO: 715), DPARYEFLW (SEQ ID NO: 133), FLWGPRALVE (SEQ ID NO: 179), VRIGHLYIL (SEQ ID NO: 180), EGDCAPEEK (SEQ ID NO: 146), REPFTKAEMLGSVIR (SEQ ID NO: 181) и AELVHFLLLKYRAR (SEQ ID NO: 182).
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид содержит или состоит из антигена MAGE-A, выбранного из EADPTGHSY (SEQ ID NO: 123), KVLEYVIKV (SEQ ID NO: 126), SLFRAVITK (SEQ ID NO: 127), EVYDGREHSA (SEQ ID NO: 129), RVRFFFPSL (SEQ ID NO: 130), EADPTGHSY (SEQ ID NO: 123), REPVTKAEML (SEQ ID NO: 131), KEADPTGHSY (SEQ ID NO: 132), DPARYEFLW (SEQ ID NO: 133), ITKKVADLVGF (SEQ ID NO: 134), SAFPTTINF (SEQ ID NO: 135), SAYGEPRKL (SEQ ID NO: 136), RVRFFFPSL (SEQ ID NO: 130), SAYGEPRKL (SEQ ID NO: 136), TSCILESLFRAVITK (SEQ ID NO: 137), PRALAETSYVKVLEY (SEQ ID NO: 138), FLLLKYRAREPVTKAE (SEQ ID NO: 139), EYVIKVSARVRF (SEQ ID NO: 140), YLQLVFGIEV (SEQ ID NO: 141), EYLQLVFGI (SEQ ID NO: 145), REPVTKAEML (SEQ ID NO: 131), EGDCAPEEK (SEQ ID NO: 146), LLKYRAREPVTKAE (SEQ ID NO: 147), EVDPIGHLY (SEQ ID NO: 148), FLWGPRALVD (SEQ ID NO: 149), KVAELVHFL (SEQ ID NO: 150), TFPDLESEF (SEQ ID NO: 153), VAELVHFLL MEVDPIGHLY (SEQ ID NO: 716), EVDPIGHLY (SEQ ID NO: 148), REPVTKAEML (SEQ ID NO: 131), AELVHFLLLI (SEQ ID NO: 157), MEVDPIGHLY (SEQ ID NO: 155), WQYFFPVIF (SEQ ID NO: 158), EGDCAPEEK (SEQ ID NO: 146), KKLLTQHFVQENYLEY (SEQ ID NO: 159), RKVAELVHFLLLKYR (SEQ ID NO: 160), KKLLTQHFVQENYLEY (SEQ ID NO: 159), ACYEFLWGPRALVETS (SEQ ID NO: 161), RKVAELVHFLLLKYR (SEQ ID NO: 160), VIFSKASSSLQL (SEQ ID NO: 162), VIFSKASSSLQL (SEQ ID NO: 162), VFGIELMEVDPIGHL (SEQ ID NO: 163), GDNQIMPKAGLLIIV (SEQ ID NO: 164), TSYVKVLHHMVKISG (SEQ ID NO: 165), RKVAELVHFLLLKYRA (SEQ ID NO: 166), FLLLKYRAREPVTKAE (SEQ ID NO: 139), EVDPASNTYj (SEQ ID NO: 167), GVYDGREHTV (SEQ ID NO: 168), NYKRCFPVI (SEQ ID NO: 169), SESLKMIF (SEQ ID NO: 170), MVKISGGPR (SEQ ID NO: 171), EVDPIGHVY (SEQ ID NO: 172), REPVTKAEML (SEQ ID NO: 131), EGDCAPEEK (SEQ ID NO: 146), ISGGPRISY (SEQ ID NO: 173), LLKYRAREPVTKAE (SEQ ID NO: 147), ALSVMGVYV (SEQ ID NO: 176), GLYDGMEHLI (SEQ ID NO: 715), DPARYEFLW (SEQ ID NO: 133), FLWGPRALVE (SEQ ID NO: 179), VRIGHLYIL (SEQ ID NO: 180), EGDCAPEEK (SEQ ID NO: 146), REPFTKAEMLGSVIR (SEQ ID NO: 181) и AELVHFLLLKYRAR (SEQ ID NO: 182), и где эритроидная клетка дополнительно содержит экзогенный полипептид, содержащий 4-1BBL.
В дополнительном варианте осуществления aAPC, представленную в настоящем описании, содержащую любой из экзогенных антигенных полипептидов, содержащих антиген MAGE-A (например, антиген MAGE-A1, MAGE-A2, MAGE -A3, MAGE-A4, MAGE-A5, MAGE-A6, MAGE-A7, MAGE-A8, MAGE-A9, MAGE-A10, MAGE-A11 или MAGE-A12, как указано выше), можно конструировать так, чтобы она дополнительно содержала экзогенный полипептид, содержащий 4-1BBL. В другом дополнительном варианте осуществления aAPC, представленную в настоящем описании, содержащую по меньшей мере один экзогенный антигенный полипептид, содержащий эпитоп, общий для одного или более антигенов MAGE-A (например, p248v9, p248g9 и/или p248d9), как представлено в настоящем описании, можно конструировать так, чтобы она дополнительно содержала экзогенный полипептид, содержащий 4-1BBL.
aAPC, представленную в настоящем описании, содержащую любой из экзогенных антигенных полипептидов, содержащих антиген MAGE-A (например, антиген MAGE-A1, MAGE-A2, MAGE-A3, MAGE-A4, MAGE-A5, MAGE-A6, MAGE-A7, MAGE-A8, MAGE-A9, MAGE-A10, MAGE-A11 или MAGE-A12, как указано выше), можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, содержащую любой из экзогенных антигенных полипептидов, содержащих антиген MAGE-A (например, антиген MAGE-A1, MAGE-A2, MAGE -A3, MAGE-A4, MAGE-A5, MAGE-A6, MAGE-A7, MAGE-A8, MAGE-A9, MAGE-A10, MAGE-A11 или MAGE-A12, как указано выше), и дополнительно содержащую экзогенный полипептид, содержащий 4-1BBL, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. Кроме того, aAPC,как представлено в настоящем описании, содержащую экзогенный антигенный полипептид, содержащий эпитоп, общий для одного или более антигенов MAGE-A (например, p248v9, p248g9 и/или p248d9), можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. Кроме того, aAPC, представленную в настоящем описании, содержащую экзогенный антигенный полипептид, содержащий эпитоп, общий для одного или более антигенов MAGE-A (например, p248v9, p248g9 и/или p248d9), и дополнительно содержащую экзогенный полипептид, содержащий 4-1BBL, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже.
Протеаза гранул нейтрофилов
Эластаза нейтрофилов, протеиназа 3 и катепсин G являются тремя гомологичными протеазами, принадлежащими к химотрипсиновому суперсемейству сериновых протеаз. Они действуют в комбинации с активными формами кислорода, способствуя деградации поглощенных микроорганизмов внутри фаголизосом. Эти протеазы также экстернализуются в активной форме во время активации нейтрофилов в очагах воспаления, таким образом, внося вклад в регуляцию воспалительных и иммунных ответов. В дополнение к участию в деструкции патогенов и регуляции провоспалительных процессов, сериновые протеазы нейтрофилов (NSP) также участвуют в различных воспалительных заболеваниях человека, включая хронические заболевания легких (хроническую обструктивную болезнь легких, кистозный фиброз, острое повреждение легких и острый респираторный дистресс-синдром) и злокачественные новообразования. Например, протеиназа 3 выражено экспрессируется при остром миелогенном лейкозе и в клетках рака предстательной железы (Kolnin et al., Blood 2016 128:1025). Также показано, что протеиназа 3 и эластаза нейтрофилов аномально экспрессируются в клетках рака молочной железы (Desmedt et al. Int J Cancer, 2006 Dec 1:119).
Эластаза нейтрофилов является ферментом, который у людей кодируется геном ELANE. Эластаза нейтрофилов секретируется нейтрофилами и макрофагами во время воспаления и разрушает бактерии и ткань организма-хозяина. Протеиназа 3 является ферментом, который у людей кодируется геном PRTN3. В нейтрофилах человека протеиназа 3 участвует в протеолитическом образовании противомикробных пептидов. Она также является мишенью антинейтрофильных цитоплазматических антител (ANCA) класса c-ANCA (цитоплазматического подтипа), типа антител, часто обнаруживаемого при гранулематозе с полиангиитом. Катепсин G является белком, который у людей кодируется геном CTSG. Кодируемая протеаза имеет специфичность, схожую с таковой у химотрипсина C, и может участвовать в уничтожении и расщеплении поглощаемых патогенов и в ремоделировании соединительной ткани в очагах воспаления. Кроме того, кодируемый белок является противомикробным и имеет бактерицидную активность против S. aureus и N. gonorrhoeae.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном протеазы гранул нейтрофилов. В дополнительном варианте осуществления протеаза гранул нейтрофилов выбрана из эластазы нейтрофилов, протеиназы 3 и катепсина G. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном эластазы нейтрофилов. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном протеиназы 3. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном катепсина G.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном эластазы нейтрофилов, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном протеиназы 3, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном катепсина G, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном протеазы гранул нейтрофилов. В дополнительном варианте осуществления протеаза гранул нейтрофилов выбрана из эластазы нейтрофилов, протеиназы 3 и катепсина G.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном протеазы гранул нейтрофилов, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL. В дополнительном варианте осуществления протеаза гранул нейтрофилов выбрана из эластазы нейтрофилов, протеиназы 3 и катепсина G.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где экзогенный антигенный полипептид является антигеном протеазы гранул нейтрофилов, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL. В дополнительном варианте осуществления протеаза гранул нейтрофилов выбрана из эластазы нейтрофилов, протеиназы 3 и катепсина G.
В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является антигеном эластазы нейтрофилов. В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является антигеном протеиназы 3. В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является антигеном катепсина G.
PR1 (VLQELNVTV (SEQ ID NO: 225)) является HLA-A2-рестриктированным пептидом, образующимся из миелоидных белков протеиназы 3 и эластазы нейтрофилов. PR1 распознается на клетках миелолейкоза цитотоксическими T-лимфоцитами (CTL), преимущественно уничтожающими лейкоз и вносящими вклад в цитогенетическую ремиссию.
Таким образом, настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является PR1.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является PR1.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является PR1, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является PR1. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является PR1, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2.
В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, PR1, слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2, слитым с трансмембранным доменом GPA (GPA).
В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, PR1, слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2, слитым с трансмембранным доменом GPA (GPA), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL.
aAPC, представленную в настоящем описании, содержащую любой из экзогенных антигенных полипептидов, содержащих протеазу гранул нейтрофилов антиген (например, антиген эластазы нейтрофилов, антиген протеиназы 3 или антиген катепсина G), можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, содержащую любой из экзогенных антигенных полипептидов, содержащих антиген протеазы гранул нейтрофилов (например, антиген эластазы нейтрофилов, антиген протеиназы 3, или антиген катепсина G), и дополнительно содержащую экзогенный полипептид, содержащий 4-1BBL, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, содержащую экзогенный антигенный полипептид, содержащий PR1, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, содержащую экзогенный антигенный полипептид, содержащий PR1, и дополнительно содержащую экзогенный полипептид, содержащий 4-1BBL, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже.
NY-ESO-1/LAGE-2
Раково-тестикулярные (C/T) антигены являются категорией опухолевых антигенов с нормальной экспрессией, ограниченной мужскими половыми клетками в яичке, но не в соматических тканях взрослого организма. В некоторых случаях CT-антигены также экспрессируются в яичнике и трофобласте. В злокачественном новообразовании регуляция этого гена нарушена, что приводит к экспрессии CT-антигена в части опухолей различных типов. Раково-тестикулярный антиген 1 (также известный как аутоиммуногенный раково-тестикулярный антиген NY-ESO-1 или LAGE-2) является белком, который у людей кодируется геном CTAG1B. Раково-тестикулярный антиген NY-ESO-1, исходно клонированный посредством подхода SEREX (серологического анализа экспрессионных библиотек рекомбинантной опухолевой кДНК) при раке пищевода, вызывает гуморальный и клеточный иммунные ответы у значительной доли пациентов с NY-ESO-1-экспрессирующими злокачественными новообразованиями (Stockert et al., J. Exp. Med. 1998; 187:1349-1354; Jager et al. J. Exp. Med. 1998; 187:265-270).
В одном из аспектов искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном NY-ESO-1/LAGE-2. В некоторых вариантах осуществления эритроидная клетка является безъядерной эритроидной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В одном из аспектов искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном NY-ESO-1/LAGE-2, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL. В некоторых вариантах осуществления сконструированная эритроидная клетка является безъядерной клеткой.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном NY-ESO-1/LAGE-2. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2 или HLA-A24. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса II DP4. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном NY-ESO-1/LAGE-2, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2 или HLA-A24. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса II DP4. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В некоторых вариантах осуществления aAPC по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном NY-ESO-1/LAGE-2, приведенным в таблице 1. В некоторых вариантах осуществления aAPC по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном NY-ESO-1/LAGE-2, приведенным в таблице 1, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL. В некоторых вариантах осуществления aAPC по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном NY-ESO-1/LAGE-2, выбранным из антигенов NY-ESO-1/LAGE-2, приведенных в таблице 1, и дополнительно презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II из соответствующего HLA MHC класса I/класса II, приведенного в таблице 1 для конкретного антигена NY-ESO-1/LAGE-2. В некоторых вариантах осуществления aAPC по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном NY-ESO-1/LAGE-2, выбранным из антигенов NY-ESO-1/LAGE-2, приведенных в таблице 1, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II из соответствующего HLA MHC класса I/класса II, приведенного в таблице 1 для конкретного антигена NY-ESO-1/LAGE-2, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, содержащий полученный из NY-ESO-1/LAGE-2 пептид. В некоторых вариантах осуществления полученный из NY-ESO-1/LAGE-2 пептид является связывающим HLA класса I полипептидом, полученным из NY-ESO-1/LAGE-2. В некоторых вариантах осуществления связывающий HLA класса I полипептид, полученный из NY-ESO-1/LAGE-2, является SLLMWITQC (SEQ ID NO: 110). В некоторых вариантах осуществления эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, содержащий по меньшей мере один экзогенный связывающий HLA класса II полипептид, полученный из NY-ESO-1/LAGE-2. В некоторых вариантах осуществления связывающий HLA класса II полипептид, полученный из NY-ESO-1/LAGE-2, является SLLMWITQCFLPVF (SEQ ID NO: 114).
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является SLLMWITQC (SEQ ID NO: 110). В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является SLLMWITQCFLPVF (SEQ ID NO: 114).
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является SLLMWITQC (SEQ ID NO: 110). В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является SLLMWITQCFLPVF (SEQ ID NO: 114).
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является SLLMWITQC (SEQ ID NO: 110). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2 или HLA-A24. В некоторых вариантах осуществления настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является SLLMWITQCFLPVF (SEQ ID NO: 114). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса II DP4.
В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, SLLMWITQC (SEQ ID NO: 110), слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2 или HLA-24, слитым с трансмембранным доменом GPA (GPA).
В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, SLLMWITQCFLPVF (SEQ ID NO: 114), слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса II HLA-DP4, слитым с трансмембранным доменом GPA (GPA).
В вариантах осуществления по меньшей мере один экзогенный антигенный полипептид является антигеном NY-ESO-1/LAGE-2, выбранным из SLLMWITQC (SEQ ID NO: 110), MLMAQEALAFL (SEQ ID NO: 109), YLAMPFATPME (SEQ ID NO: 204), ASGPGGGAPR (SEQ ID NO: 205), LAAQERRVPR (SEQ ID NO: 111), TVSGNILTIR (SEQ ID NO: 206), APRGPHGGAASGL (SEQ ID NO: 207), MPFATPMEAEL (SEQ ID NO: 208), KEFTVSGNILTI (SEQ ID NO: 209), MPFATPMEA (SEQ ID NO: 210), FATPMEAEL (SEQ ID NO: 211), FATPMEAELAR (SEQ ID NO: 212), LAMPFATPM (SEQ ID NO: 213), ARGPESRLL (SEQ ID NO: 214), SLLMWITQCFLPVF (SEQ ID NO: 114), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), EFYLAMPFATPM (SEQ ID NO: 216), PGVLLKEFTVSGNILTIRLTAADHR (SEQ ID NO: 217), RLLEFYLAMPFA (SEQ ID NO: 218), QGAMLAAQERRVPRAAEVPR (SEQ ID NO: 115), PFATPMEAELARR (SEQ ID NO: 219), PGVLLKEFTVSGNILTIRLT (SEQ ID NO: 220), VLLKEFTVSG (SEQ ID NO: 221), AADHRQLQLSISSCLQQL (SEQ ID NO: 116), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), LKEFTVSGNILTIRL (SEQ ID NO: 222), PGVLLKEFTVSGNILTIRLTAADHR (SEQ ID NO: 217), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), KEFTVSGNILT (SEQ ID NO: 223), LLEFYLAMPFATPM (SEQ ID NO: 224) и AGATGGRGPRGAGA (SEQ ID NO: 119).
В некоторых вариантах осуществления aAPC по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном NY-ESO-1/LAGE-2, выбранным из SLLMWITQC (SEQ ID NO: 110), MLMAQEALAFL (SEQ ID NO: 109), YLAMPFATPME (SEQ ID NO: 204), ASGPGGGAPR (SEQ ID NO: 205), LAAQERRVPR (SEQ ID NO: 111), TVSGNILTIR (SEQ ID NO: 206), APRGPHGGAASGL (SEQ ID NO: 207), MPFATPMEAEL (SEQ ID NO: 208), KEFTVSGNILTI (SEQ ID NO: 209), MPFATPMEA (SEQ ID NO: 210), FATPMEAEL (SEQ ID NO: 211), FATPMEAELAR (SEQ ID NO: 212), LAMPFATPM (SEQ ID NO: 213), ARGPESRLL (SEQ ID NO: 214), SLLMWITQCFLPVF (SEQ ID NO: 114), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), EFYLAMPFATPM (SEQ ID NO: 216), PGVLLKEFTVSGNILTIRLTAADHR (SEQ ID NO: 217), RLLEFYLAMPFA (SEQ ID NO: 218), QGAMLAAQERRVPRAAEVPR (SEQ ID NO: 115), PFATPMEAELARR (SEQ ID NO: 219), PGVLLKEFTVSGNILTIRLT (SEQ ID NO: 220), VLLKEFTVSG (SEQ ID NO: 221), AADHRQLQLSISSCLQQL (SEQ ID NO: 116), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), LKEFTVSGNILTIRL (SEQ ID NO: 222), PGVLLKEFTVSGNILTIRLTAADHR (SEQ ID NO: 217), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), KEFTVSGNILT (SEQ ID NO: 223), LLEFYLAMPFATPM (SEQ ID NO: 224) и AGATGGRGPRGAGA (SEQ ID NO: 119), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL.
В некоторых вариантах осуществления aAPC по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном NY-ESO-1/LAGE-2, выбранным из SLLMWITQC (SEQ ID NO: 110), MLMAQEALAFL (SEQ ID NO: 109), YLAMPFATPME (SEQ ID NO: 204), ASGPGGGAPR (SEQ ID NO: 205), LAAQERRVPR (SEQ ID NO: 111), TVSGNILTIR (SEQ ID NO: 206), APRGPHGGAASGL (SEQ ID NO: 207), MPFATPMEAEL (SEQ ID NO: 208), KEFTVSGNILTI (SEQ ID NO: 209), MPFATPMEA (SEQ ID NO: 210), FATPMEAEL (SEQ ID NO: 211), FATPMEAELAR (SEQ ID NO: 212), LAMPFATPM (SEQ ID NO: 213), ARGPESRLL (SEQ ID NO: 214), SLLMWITQCFLPVF (SEQ ID NO: 114), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), EFYLAMPFATPM (SEQ ID NO: 216), PGVLLKEFTVSGNILTIRLTAADHR (SEQ ID NO: 217), RLLEFYLAMPFA (SEQ ID NO: 218), QGAMLAAQERRVPRAAEVPR (SEQ ID NO: 115), PFATPMEAELARR (SEQ ID NO: 219), PGVLLKEFTVSGNILTIRLT (SEQ ID NO: 220), VLLKEFTVSG (SEQ ID NO: 221), AADHRQLQLSISSCLQQL (SEQ ID NO: 116), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), LKEFTVSGNILTIRL (SEQ ID NO: 222), PGVLLKEFTVSGNILTIRLTAADHR (SEQ ID NO: 217), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), KEFTVSGNILT (SEQ ID NO: 223), LLEFYLAMPFATPM (SEQ ID NO: 224) и AGATGGRGPRGAGA (SEQ ID NO: 119), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II из соответствующего HLA MHC класса I/класса II, приведенного в таблице 1 для конкретного антигена NY-ESO-1/LAGE-2, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является SLLMWITQC (SEQ ID NO: 110), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является SLLMWITQCFLPVF (SEQ ID NO: 114), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL.
aAPC, представленную в настоящем описании, содержащую (например, содержащую на своей поверхности) экзогенный антигенный полипептид, содержащий антиген NY-ESO-1/LAGE-2, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, содержащую (например, содержащую на своей поверхности) экзогенный антигенный полипептид, содержащий антиген NY-ESO-1/LAGE-2, и дополнительно содержащую (например, содержащую на своей поверхности) экзогенный полипептид, содержащий 4-1BBL, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, содержащую (например, содержащую на своей поверхности) по меньшей мере один экзогенный полученный из NY-ESO-1/LAGE-2 пептид (например, SLLMWITQC (SEQ ID NO: 110) или SLLMWITQCFLPVF (SEQ ID NO: 114)), как представлено в настоящем описании, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, содержащую (например, содержащую на своей поверхности) по меньшей мере один экзогенный полученный из NY-ESO-1/LAGE-2 пептид (например, SLLMWITQC (SEQ ID NO: 110) или SLLMWITQCFLPVF (SEQ ID NO: 114)) и дополнительно содержащую экзогенный полипептид, содержащий 4-1BBL, как представлено в настоящем описании, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже.
Теломераза/hTERT
Теломеразная обратная транскриптаза (сокращенно обозначаемая как TERT или hTERT у людей) является рибонуклеопротеиновым ферментом, необходимым для репликации концов хромосом у большинства эукариот. Теломераза поддерживает теломерные концы посредством добавления теломерного повтора TTAGGG. Экспрессия теломеразы играет роль в клеточном старении, т.к. она в норме репрессируется в постнатальных соматических клетках, что приводит к прогрессирующему укорочению теломер. Теломеразная активность ассоциирована с тем, сколько раз клетка может делиться, что играет важную роль в бессмертии линий клеток, таких как злокачественные клетки.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном теломеразы. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном теломеразы, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном теломеразы человека (hTERT). В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном теломеразы человека (hTERT), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном теломеразы. В некоторых вариантах осуществления антиген теломеразы является антигеном теломеразы человека (hTERT). В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном теломеразы, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. В некоторых вариантах осуществления антиген теломеразы является антигеном теломеразы человека (hTERT). В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ILAKFLHWL (SEQ ID NO: 658). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RLVDDFLLV (SEQ ID NO: 659). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RPGLLGASVLGLDDI (SEQ ID NO: 663). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является LTDLQPYMRQFVAHL (SEQ ID NO: 664). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является ILAKFLHWL (SEQ ID NO: 658). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является RLVDDFLLV (SEQ ID NO: 659). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является RPGLLGASVLGLDDI (SEQ ID NO: 663). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является LTDLQPYMRQFVAHL (SEQ ID NO: 664). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ILAKFLHWL (SEQ ID NO: 658), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RLVDDFLLV (SEQ ID NO: 659), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RPGLLGASVLGLDDI (SEQ ID NO: 663), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является LTDLQPYMRQFVAHL (SEQ ID NO: 664), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является ILAKFLHWL (SEQ ID NO: 658), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является RLVDDFLLV (SEQ ID NO: 659), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является RPGLLGASVLGLDDI (SEQ ID NO: 663), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является LTDLQPYMRQFVAHL (SEQ ID NO: 664), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является ILAKFLHWL (SEQ ID NO: 658). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является ILAKFLHWL (SEQ ID NO: 658), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является RLVDDFLLV (SEQ ID NO: 659). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является RLVDDFLLV (SEQ ID NO: 659), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является RPGLLGASVLGLDDI (SEQ ID NO: 663). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса II HLA-DR7. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса II HLA-DR7.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является RPGLLGASVLGLDDI (SEQ ID NO: 663), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса II HLA-DR7. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса II HLA-DR7.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является LTDLQPYMRQFVAHL (SEQ ID NO: 664). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса II HLA-DR11. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса II HLA-DR11.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является LTDLQPYMRQFVAHL (SEQ ID NO: 664), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса II HLA-DR11. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса II HLA-DR11.
В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, ILAKFLHWL (SEQ ID NO: 658), слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2, слитым с трансмембранным доменом GPA (GPA).
В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, ILAKFLHWL (SEQ ID NO: 658), слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2, слитым с трансмембранным доменом GPA (GPA), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий 4-1BBL.
aAPC, представленную в настоящем описании, презентирующую (например, содержащую на своей поверхности) антиген теломеразы, в частности, антиген hTERT, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, презентирующую (например, содержащую на своей поверхности) антиген теломеразы, в частности, антиген hTERT, и дополнительно презентирующую (например, содержащую на своей поверхности) экзогенный полипептид, содержащий 4-1BBL, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, презентирующую (например, содержащую на своей поверхности) описанный выше антиген hTERT, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, презентирующую (например, содержащую на своей поверхности) описанный выше антиген hTERT и дополнительно презентирующую (например, содержащую на своей поверхности) экзогенный полипептид, содержащий 4-1BBL, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже.
Миелиновый олигодендроцитарный гликопротеин (MOG)
Миелиновый олигодендроцитарный гликопротеин (MOG) является мембранным белком, экспрессируемым на поверхности олигодендроцитов и внешней поверхности миелиновой оболочки. Из-за своей локализации MOG является основным антигеном-мишенью, вовлеченным в иммуноопосредованную демиелинизацию. Белок MOG может участвовать в завершении и поддержании миелиновой оболочки и межклеточной коммуникации.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MOG. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MOG, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий коингибиторный полипептид. В некоторых вариантах осуществления коингибиторный полипептид является PD-L1. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном MOG, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий полипептид для экспансии Treg. В некоторых вариантах осуществления полипептид для экспансии Treg является ИЛ-2. В некоторых вариантах осуществления полипептид для экспансии Treg является CD25-специфическим ИЛ-2. В некоторых вариантах осуществления антиген MOG является антигеном MOG человека. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для ингибирования T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном MOG. В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для ингибирования T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном MOG, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий коингибиторный полипептид. В некоторых вариантах осуществления коингибиторный полипептид является PD-L1. В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации регуляторных T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном MOG, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий, полипептид для экспансии Treg. В некоторых вариантах осуществления полипептид для экспансии Treg является CD25-специфическим ИЛ-2. В некоторых вариантах осуществления антиген MOG является антигеном MOG человека. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является MEVGWYRSPFSRVVHLYRNGK (SEQ ID NO: 690).
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является MEVGWYRSPFSRVVHLYRNGK (SEQ ID NO: 690), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий коингибиторный полипептид. В некоторых вариантах осуществления коингибиторный полипептид является PD-L1.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является MEVGWYRSPFSRVVHLYRNGK (SEQ ID NO: 690), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий полипептид для экспансии Treg. В некоторых вариантах осуществления полипептид для экспансии Treg является CD25-специфическим ИЛ-2.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации регуляторных T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является MEVGWYRSPFSRVVHLYRNGK (SEQ ID NO: 690).
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для ингибирования T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является MEVGWYRSPFSRVVHLYRNGK (SEQ ID NO: 690), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий коингибиторный полипептид. В некоторых вариантах осуществления коингибиторный полипептид является PD-L1.
В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является антигеном MOG, слитым с экзогенным антигенпрезентирующим полипептидом, MHC класса II, слитым с трансмембранным доменом GPA (GPA). В некоторых вариантах осуществления антиген MOG является антигеном MOG человека. В некоторых вариантах осуществления антиген MOG слит с экзогенным антигенпрезентирующим полипептидом, MHC класса II, слитым с GPA в виде одноцепочечного слитого белка.
В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является антигеном MOG, слитым с экзогенным антигенпрезентирующим полипептидом, MHC класса II, слитым с трансмембранным доменом GPA (GPA), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий коингибиторный полипептид. В некоторых вариантах осуществления коингибиторный полипептид является PD-L1. В некоторых вариантах осуществления антиген MOG является антигеном MOG человека. В некоторых вариантах осуществления антиген MOG слит с экзогенным антигенпрезентирующим полипептидом, MHC класса II, слитым с GPA в виде одноцепочечного слитого белка.
В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является антигеном MOG, слитым с экзогенным антигенпрезентирующим полипептидом, MHC класса II, слитым с трансмембранным доменом GPA (GPA), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий полипептид для экспансии Treg. В некоторых вариантах осуществления полипептид для экспансии Treg является ИЛ-2. В некоторых вариантах осуществления полипептид для экспансии Treg является CD25-специфическим ИЛ-2. В некоторых вариантах осуществления антиген MOG является антигеном MOG человека. В некоторых вариантах осуществления антиген MOG слит с экзогенным антигенпрезентирующим полипептидом, MHC класса II, слитым с GPA в виде одноцепочечного слитого белка.
aAPC, представленную в настоящем описании, презентирующую (например, содержащую на своей поверхности) антиген MOG, можно использовать в лечении рассеянного склероза, как более подробно описано ниже. aAPC, представленную в настоящем описании, презентирующую (например, содержащую на своей поверхности) антиген MOG и дополнительно презентирующую (например, содержащую на своей поверхности) экзогенный полипептид, содержащий коингибиторный полипептид, можно использовать в лечении рассеянного склероза, как более подробно описано ниже. aAPC, представленную в настоящем описании, презентирующую (например, содержащую на своей поверхности) антиген MOG и дополнительно презентирующую (например, содержащую на своей поверхности) экзогенный полипептид, содержащий коингибиторный полипептид, где коингибиторный полипептид является PD-L1, можно использовать в лечении рассеянного склероза, как более подробно описано ниже. aAPC, представленную в настоящем описании, презентирующую (например, содержащую на своей поверхности) антиген MOG и дополнительно презентирующую (например, содержащую на своей поверхности) экзогенный полипептид, содержащий полипептид для экспансии Treg, можно использовать в лечении рассеянного склероза, как более подробно описано ниже. aAPC, представленную в настоящем описании, презентирующую (например, содержащую на своей поверхности) антиген MOG и дополнительно презентирующую (например, содержащую на своей поверхности) экзогенный полипептид, содержащий полипептид для экспансии Treg, где полипептид для экспансии Treg является CD25-специфическим ИЛ-2, можно использовать в лечении рассеянного склероза, как более подробно описано ниже.
gp100
Гликопротеин 100, gp100 или меланоцитарный белок PMEL является трансмембранным гликопротеином типа I, которым богаты меланосомы.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном gp100. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном gp100, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. В некоторых вариантах осуществления антиген gp100 является антигеном gp100 человека. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном gp100. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является MHC класса I. В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном gp100, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является MHC класса I. В некоторых вариантах осуществления антиген gp100 является антигеном gp100 человека. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RLMKQDFSV (SEQ ID NO: 314). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RLPRIFCSC (SEQ ID NO: 315). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является LIYRRRLMK (SEQ ID NO: 316). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ALLAVGATK (SEQ ID NO: 317). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является IALNFPGSQK (SEQ ID NO: 318). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RSYVPLAHR (SEQ ID NO: 319). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ALNFPGSQK (SEQ ID NO: 320). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ALNFPGSQK (SEQ ID NO: 320). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является VYFFLPDHL (SEQ ID NO: 321). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RTKQLYPEW (SEQ ID NO: 322). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является HTMEVTVYHR (SEQ ID NO: 323). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является SSPGCQPPA (SEQ ID NO: 324). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является VPLDCVLYRY (SEQ ID NO: 325). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является LPHSSSHWL (SEQ ID NO: 326). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является SNDGPTLI (SEQ ID NO: 327). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является GRAMLGTHTMEVTVY (SEQ ID NO: 328). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является WNRQLYPEWTEAQRLD (SEQ ID NO: 329). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является TTEWVETTARELPIPEPE (SEQ ID NO: 330). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является TGRAMLGTHTMEVTVYH (SEQ ID NO: 331). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является GRAMLGTHTMEVTVY (SEQ ID NO: 328).
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RLMKQDFSV (SEQ ID NO: 314), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RLPRIFCSC (SEQ ID NO: 315), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является LIYRRRLMK (SEQ ID NO: 316), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ALLAVGATK (SEQ ID NO: 317), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является IALNFPGSQK (SEQ ID NO: 318), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RSYVPLAHR (SEQ ID NO: 319), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ALNFPGSQK (SEQ ID NO: 320), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ALNFPGSQK (SEQ ID NO: 320), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является VYFFLPDHL (SEQ ID NO: 321), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RTKQLYPEW (SEQ ID NO: 322), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является HTMEVTVYHR (SEQ ID NO: 323), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является SSPGCQPPA (SEQ ID NO: 324), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является VPLDCVLYRY (SEQ ID NO: 325), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является LPHSSSHWL (SEQ ID NO: 326), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является SNDGPTLI (SEQ ID NO: 327), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является GRAMLGTHTMEVTVY (SEQ ID NO: 328), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является WNRQLYPEWTEAQRLD (SEQ ID NO: 329), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является TTEWVETTARELPIPEPE (SEQ ID NO: 330), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является TGRAMLGTHTMEVTVYH (SEQ ID NO: 331), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является GRAMLGTHTMEVTVY (SEQ ID NO: 328), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RLMKQDFSV (SEQ ID NO: 314), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RLPRIFCSC (SEQ ID NO: 315), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является LIYRRRLMK (SEQ ID NO: 316), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ALLAVGATK (SEQ ID NO: 317), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является IALNFPGSQK (SEQ ID NO: 318), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RSYVPLAHR (SEQ ID NO: 319), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ALNFPGSQK (SEQ ID NO: 320), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ALNFPGSQK (SEQ ID NO: 320), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является VYFFLPDHL (SEQ ID NO: 321), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RTKQLYPEW (SEQ ID NO: 322), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является HTMEVTVYHR (SEQ ID NO: 323), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является SSPGCQPPA (SEQ ID NO: 324), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является VPLDCVLYRY (SEQ ID NO: 325), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является LPHSSSHWL (SEQ ID NO: 326), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является SNDGPTLI (SEQ ID NO: 327), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является GRAMLGTHTMEVTVY (SEQ ID NO: 328), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является WNRQLYPEWTEAQRLD (SEQ ID NO: 329), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является TTEWVETTARELPIPEPE (SEQ ID NO: 330), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является TGRAMLGTHTMEVTVYH (SEQ ID NO: 331), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является GRAMLGTHTMEVTVY (SEQ ID NO: 328), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RLMKQDFSV (SEQ ID NO: 314), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RLPRIFCSC (SEQ ID NO: 315), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является LIYRRRLMK (SEQ ID NO: 316), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ALLAVGATK (SEQ ID NO: 317), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является IALNFPGSQK (SEQ ID NO: 318), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RSYVPLAHR (SEQ ID NO: 319), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ALNFPGSQK (SEQ ID NO: 320), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является ALNFPGSQK (SEQ ID NO: 320), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является VYFFLPDHL (SEQ ID NO: 321), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RTKQLYPEW (SEQ ID NO: 322), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является HTMEVTVYHR (SEQ ID NO: 323), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является SSPGCQPPA (SEQ ID NO: 324), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является VPLDCVLYRY (SEQ ID NO: 325), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является LPHSSSHWL (SEQ ID NO: 326), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является SNDGPTLI (SEQ ID NO: 327), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является GRAMLGTHTMEVTVY (SEQ ID NO: 328), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является WNRQLYPEWTEAQRLD (SEQ ID NO: 329), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является TTEWVETTARELPIPEPE (SEQ ID NO: 330), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является TGRAMLGTHTMEVTVYH (SEQ ID NO: 331), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является GRAMLGTHTMEVTVY (SEQ ID NO: 328), и экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL.
aAPC, представленную в настоящем описании, презентирующую, например, содержащую на своей поверхности, антиген gp100, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, презентирующую, например, содержащую на своей поверхности, антиген gp100, и дополнительно презентирующую, например, содержащую на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, презентирующую, например, содержащую на своей поверхности, антиген gp100, и дополнительно презентирующую, например, содержащую на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид, где костимуляторный полипептид является 4-1BBL, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, презентирующую, например, содержащую на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является антигеном gp100, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. aAPC, представленную в настоящем описании, презентирующую, например, содержащую на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является антигеном gp100, и дополнительно презентирующую, например, содержащую на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид, где костимуляторный полипептид является 4-1BBL, можно использовать в лечении злокачественного новообразования, как более подробно описано ниже. В некоторых вариантах осуществления злокачественное новообразование является меланомой.
Вирус Эпштейна-Барр (EBV)
EBV является гаммагерпесвирусом человека с тропизмом к B-лимфоцитам (Kieff and Liebowitz, в Virology, eds. Fields, B. N., Knipe, D. M. et al., p. 1889-1919, Raven Press, Ltd.: New York, 1990). EBV является чрезвычайно широко распространенным фактором окружающей среды, инфицирующим 80-100 процентов индивидуумов по всему миру. Начальная или первичная инфекция может быть острой или субклинической. После этого следует длительный период, в течение которого инфекция EBV является латентной в B-лимфоцитах, присутствующих в циркулирующей крови, лимфоузлах и селезенке.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном EBV. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном EBV, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. В некоторых вариантах осуществления антиген EBV является антигеном EBV человека. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном EBV. В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном EBV, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. В некоторых вариантах осуществления антиген EBV является антигеном EBV человека. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является антигенным пептидом gp350. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является VLQWASLAV (SEQ ID NO: 698). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является антигенным полипептидом EBNA1. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является FMVFLQTHI (SEQ ID NO: 699). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является FLQTHIFAEV (SEQ ID NO: 700). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является SIVCYFMVFL (SEQ ID NO: 701). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является CLGGLLTMV (SEQ ID NO: 691). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является GLCTLVAML (SEQ ID NO: 692). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является FLYALALLL (SEQ ID NO: 693). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является YVLDHLIVV (SEQ ID NO: 694). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RLRAEAQVK (SEQ ID NO: 695). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является AVFDRKSDAK (SEQ ID NO: 696). Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RPPIFIRLL (SEQ ID NO: 697).
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является антигенным пептидом gp350, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является VLQWASLAV (SEQ ID NO: 698), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является антигенным полипептидом EBNA1, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является FMVFLQTHI (SEQ ID NO: 699), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является FLQTHIFAEV (SEQ ID NO: 700), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является SIVCYFMVFL (SEQ ID NO: 701), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является CLGGLLTMV (SEQ ID NO: 691), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является GLCTLVAML (SEQ ID NO: 692), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является FLYALALLL (SEQ ID NO: 693), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является YVLDHLIVV (SEQ ID NO: 694), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RLRAEAQVK (SEQ ID NO: 695), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является AVFDRKSDAK (SEQ ID NO: 696), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является RPPIFIRLL (SEQ ID NO: 697), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является антигенным пептидом gp350. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является VLQWASLAV (SEQ ID NO: 698). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является антигенным полипептидом EBNA1. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является FMVFLQTHI (SEQ ID NO: 699). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является FLQTHIFAEV (SEQ ID NO: 700). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является SIVCYFMVFL (SEQ ID NO: 701). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является CLGGLLTMV (SEQ ID NO: 691). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является GLCTLVAML (SEQ ID NO: 692). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является FLYALALLL (SEQ ID NO: 693). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является YVLDHLIVV (SEQ ID NO: 694). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является RLRAEAQVK (SEQ ID NO: 695). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A3. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A3. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является AVFDRKSDAK (SEQ ID NO: 696). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A11. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A11. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является RPPIFIRLL (SEQ ID NO: 697). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-B7. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-B7.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является антигенным пептидом gp350, например, VLQWASLAV (SEQ ID NO: 698), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является антигенным пептидом EBNA1, например, FMVFLQTHI (SEQ ID NO: 699), FLQTHIFAEV (SEQ ID NO: 700), SIVCYFMVFL (SEQ ID NO: 701) или одним из антигенных полипептидов EBV, приведенных в таблице 1, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2.
aAPC, представленную в настоящем описании, презентирующую, например, содержащую на своей поверхности, антиген EBV, можно использовать в лечении аутоиммунного заболевания, ассоциированного с возбудителем инфекции. В некоторых вариантах осуществления экзогенные антигенные полипептиды презентируются на антигенпрезентирующих полипептидах, например, экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами гистосовместимости (MHC класса I, MHC класса II). В некоторых вариантах осуществления аутоиммунное заболевание, ассоциированное с возбудителем инфекции, является рассеянным склерозом (MS), как более подробно описано ниже. aAPC, представленную в настоящем описании, презентирующую, например, содержащую на своей поверхности, антиген EBV, и дополнительно презентирующую, например, содержащую на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид, можно использовать в лечении аутоиммунного заболевания, ассоциированного с возбудителем инфекции. В некоторых вариантах осуществления аутоиммунное заболевание, ассоциированное с возбудителем инфекции, является рассеянным склерозом (MS), как более подробно описано ниже. aAPC, представленную в настоящем описании, презентирующую, например, содержащую на своей поверхности, антиген EBV, и дополнительно презентирующую, например, содержащую на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид, где костимуляторный полипептид является 4-1BBL, можно использовать в лечении аутоиммунного заболевания, ассоциированного с возбудителем инфекции. В некоторых вариантах осуществления аутоиммунное заболевание, ассоциированное с возбудителем инфекции, является рассеянным склерозом (MS), как более подробно описано ниже.
Вирус папилломы человека (HPV)
Папилломавирусы являются небольшими онкогенными ДНК-вирусами, являющимися высоко видоспецифичными. К настоящему времени описано более 70 отдельных генотипов вируса папилломы человека (HPV). HPV, как правило, являются специфическими в отношении кожи (например, HPV-1 и -2) или слизистых оболочек (например, HPV-6 и -11) и, как правило, вызывают доброкачественные опухоли (бородавки), сохраняющиеся в течение нескольких месяцев или лет. Некоторые HPV также ассоциированы со злокачественными новообразованиями, такими как HPV-положительный рак головы и шеи и рак шейки матки. Наиболее сильной положительной ассоциацией между HPV и злокачественным новообразованием человека является ассоциация между HPV-16 и HPV-18 и карциномой шейки матки.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном HPV. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном HPV-E7. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном HPV-E6. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном HPV, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является антигеном HPV-E7, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. В некоторых вариантах осуществления антиген HPV является антигеном HPV человека. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном HPV. В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном HPV-E7. В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном HPV, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном HPV-E7, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. В некоторых вариантах осуществления антиген HPV является антигеном HPV человека. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является YMLDLQPET (SEQ ID NO: 713), YMLDLQPETT (SEQ ID NO: 714) или TIHDIILECV (SEQ ID NO: 712). В некоторых вариантах осуществления экзогенный антигенный полипептид является YMLDLQPET (SEQ ID NO: 713).
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является YMLDLQPET (SEQ ID NO: 713), YMLDLQPETT (SEQ ID NO: 714) или TIHDIILECV (SEQ ID NO: 712), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления экзогенный антигенный полипептид является YMLDLQPET (SEQ ID NO: 713). В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является HPV-E7. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является YMLDLQPET (SEQ ID NO: 713), YMLDLQPETT (SEQ ID NO: 714) или TIHDIILECV (SEQ ID NO: 712). В некоторых вариантах осуществления экзогенный антигенный полипептид является YMLDLQPET (SEQ ID NO: 713). В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2.
Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является HPV-E7, где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. Настоящее изобретение также относится к искусственной антигенпрезентирующей клетке (aAPC), включающей эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, и где экзогенный антигенный полипептид является YMLDLQPET (SEQ ID NO: 713), YMLDLQPETT (SEQ ID NO: 714) или TIHDIILECV (SEQ ID NO: 712), где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления экзогенный антигенный полипептид является YMLDLQPET (SEQ ID NO: 713). В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. В вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I HLA-A2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2.
В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является антигеном HPV, слитым с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2, слитым с трансмембранным доменом GPA (GPA). В некоторых вариантах осуществления антиген HPV является антигеном HPV человека. В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является HPV-E7, слитым с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2, слитым с трансмембранным доменом GPA (GPA). В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где экзогенный антигенный полипептид является TIHDIILECV (SEQ ID NO: 712), слитым с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2, слитым с трансмембранным доменом GPA (GPA).
aAPC, представленную в настоящем описании, презентирующую антиген HPV, можно использовать в лечении злокачественного новообразования, ассоциированного с онкогенным вирусом (например, HPV). aAPC, представленную в настоящем описании, презентирующую антиген HPV и дополнительно презентирующую экзогенный полипептид, содержащий костимуляторный полипептид, можно использовать в лечении злокачественного новообразования, ассоциированного с онкогенным вирусом (например, HPV). aAPC, представленную в настоящем описании, презентирующую антиген HPV и дополнительно презентирующую экзогенный полипептид, содержащий костимуляторный полипептид, где костимуляторный полипептид является 4-1BBL, можно использовать в лечении злокачественного новообразования, ассоциированного с онкогенным вирусом (например, HPV), как более подробно описано ниже. В вариантах осуществления HPV-ассоциированным злокачественным новообразованием является HPV-положительный рак головы и шеи. В некоторых вариантах осуществления HPV-ассоциированным злокачественным новообразованием является HPV-положительный рак шейки матки.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является CD33.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является CD123.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка (aAPC) по настоящему изобретению включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где по меньшей мере один экзогенный антигенный полипептид является CD38.
В различных вариантах осуществления указанных выше аспектов aAPC презентирует, например, содержит на своей поверхности, по меньшей мере два, по меньшей мере 3, по меньшей мере 4 или по меньшей мере 5 экзогенных антигенных полипептидов.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток (например, cytotoxic CD8+ T-клетки), где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид получают из вируса Эпштейна-Барр (EBV). aAPC может дополнительно содержать экзогенный костимуляторный полипептид, как представлено в настоящем описании.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток (например, цитотоксических CD8+ T-клеток), где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является gp350 или его иммуногенным пептидом. В конкретном варианте осуществления иммуногенный пептид gp350 содержит или состоит из пептида HLA A2 (VLQWASLAV (SEQ ID NO: 698)). aAPC может дополнительно содержать экзогенный костимуляторный полипептид, как представлено в настоящем описании. В конкретном варианте осуществления экзогенный костимуляторный полипептид является 4-1BBL.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток (например, цитотоксических CD8+ T-клеток), где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является EBNA1 или его иммуногенным пептидом. В конкретном варианте осуществления иммуногенный пептид EBNA1 содержит или состоит из пептида, выбранного из FMVFLQTHI (SEQ ID NO: 699), FLQTHIFAEV (SEQ ID NO: 700) и SIVCYFMVFL (SEQ ID NO: 701). aAPC может дополнительно содержать экзогенный костимуляторный полипептид как представлено в настоящем описании. В конкретном варианте осуществления экзогенный костимуляторный полипептид является 4-1BBL.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для экспансии регуляторных T-клеток (Treg), где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид получают из вируса Эпштейна-Барр (EBV). aAPC может дополнительно содержать экзогенный костимуляторный полипептид, как представлено в настоящем описании.
В другом аспекте настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для супрессии аутореактивных T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид получают из вируса Эпштейна-Барр (EBV). aAPC может дополнительно содержать экзогенный коингибиторный полипептид, как представлено в настоящем описании.
В другом аспекте настоящее изобретение относится к aAPC, сконструированной для активации патоген-специфических T-клеток, включающей эритроидную клетку (например, безъядерную эритроидную клетку), где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид является антигенным полипептидом из патогена или возбудителя инфекции, приведенным в таблицах 21-24, или его иммуногенным пептидом. aAPC может дополнительно содержать экзогенный костимуляторный полипептид, как представлено в настоящем описании.
В другом аспекте настоящее изобретение относится к aAPC, сконструированной для активации специфических в отношении вируса гепатита B (HBV) T-клеток, включающей эритроидную клетку (например, безъядерную эритроидную клетку), где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, и где экзогенный антигенный полипептид получают из вируса гепатита B (HBV). aAPC может дополнительно содержать, например, на поверхности клетки, экзогенный костимуляторный полипептид, как представлено в настоящем описании. В вариантах осуществления по меньшей мере один костимуляторный полипептид выбран из группы, состоящей из 4-1BBL, ИЛ-2, ИЛ-12, ИЛ-15, ИЛ-18, ИЛ-21 и любой их комбинации, например, ИЛ-12 и ИЛ-15 или 4-1BBL и ИЛ-15. В некоторых вариантах осуществления aAPC дополнительно содержит дополнительный экзогенный полипептид, где дополнительный экзогенный полипептид содержит, например, на поверхности клетки, ингибитор контрольных точек. В некоторых вариантах осуществления ингибитор контрольных точек является молекулой антитела против PD1. В конкретном варианте осуществления aAPC включает эритроидную клетку, где эритроидная клетка содержит, например, на поверхности клетки, один или более экзогенных полипептидов, где один или более экзогенных полипептидов включают: экзогенный антигенный полипептид, содержащий HBV-специфический антиген или его иммуногенный пептид, экзогенный антигенпрезентирующий полипептид, например, полипептид или одноцепочечный слитый белок MHC класса I или MHC класса I, экзогенный костимуляторный полипептид, например, ИЛ-12 или 4-1BBL, и ингибитор контрольных точек, например, антитело против PD1.
Экзогенные антигенпрезентирующие полипептиды
Экзогенные антигенпрезентирующие полипептиды по настоящему изобретению включают полипептиды семейства генов MHC, разделяемые на три подгруппы: класс I, класс II и класс III.
Молекулы MHC класса I являются гетеродимерами, состоящими из двух полипептидных цепей, α-цепи и цепи β2-микроглобулина (b2m). α-цепи класса I состоят из одного полипептида, состоящего из трех внеклеточных доменов, обозначаемых как α1, α2 и α3, трансмембранной области, заякоривающей его в плазматической мембране, и короткого внутрицитоплазматического хвоста. b2m состоит из одной молекулы, нековалентно связанной с α-цепью. Только α-цепь является полиморфной и кодируется геном HLA, в то время как субъединица b2m не является полиморфной и кодируется геном микроглобулина бета-2. Молекулы MHC класса I содержат субъединицы β2, поэтому могут распознаваться только корецепторами CD8.
В некоторых вариантах осуществления по настоящему изобретению экзогенный антигенпрезентирующий полипептид, содержащийся в aAPC, является молекулой MHC класса I и включает сигнальную последовательность. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является молекулой MHC класса I и не включает сигнальную последовательность.
Молекулы MHC класса II также являются гетеродимерами, состоящими из полипептидной α- и β-цепи. Обозначение цепей, например, α1, α2, и β1 и β2, относится к отдельным доменам (или субъединицам) в гене HLA и гене β. CD4 связывается с областью β2. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является молекулой MHC класса II и включает сигнальную последовательность. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является молекулой MHC класса II и не включает сигнальную последовательность.
Экзогенные антигенпрезентирующие полипептиды по настоящему изобретению могут включать субъединицы комплекса поверхности клетки или молекулы поверхности клетки, например, MHC класса I или MHC класса II, где MHC класса I или MHC класса II функционируют, связывая экзогенный антигенный полипептид. В некоторых вариантах осуществления экзогенные антигенпрезентирующие полипептиды являются субъединицами MHC класса II, и их функцией является связывание экзогенного антигенного полипептида. В некоторых вариантах осуществления экзогенные антигенпрезентирующие полипептиды являются субъединицами MHC класса I, и их функцией является связывание экзогенного антигенного полипептида. В некоторых вариантах осуществления полипептид MHC класса I или полипептид MHC класса II содержит лидерную (сигнальную) последовательность. В некоторых вариантах осуществления полипептид MHC класса I или полипептид MHC класса II не содержит лидерную (сигнальную) последовательность. В некоторых вариантах осуществления лидерная последовательность слита с экзогенным антигенпрезентирующим полипептидом (например, MHC класса I или полипептид MHC класса II, в которых отсутствует лидерная (сигнальная) последовательность). В некоторых вариантах осуществления полипептид MHC класса I является слитым полипептидом, содержащим лидерную последовательность. В некоторых вариантах осуществления полипептид MHC класса II является слитым полипептидом, содержащим лидерную последовательность. В некоторых вариантах осуществления лидерная последовательность выбрана из последовательностей, приведенных в таблице 2.
Таблица 2. Лидерные последовательности
В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является функциональным MHC класса I, и экзогенные антигенпрезентирующие полипептиды являются MHC класса I (альфа-цепью 1-3) и бета-2 микроглобулином или их фрагментами или вариантами. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является функциональным MHC класса II, и экзогенные антигенпрезентирующие полипептиды являются альфа-цепью MHC класса II (альфа-цепью 1 и 2) и бета-цепью MHC класса II (бета-цепью 1 и 2) или их фрагментами или вариантами. В некоторых вариантах осуществления молекула MHC содержит MHC класса I или II человека, например, альфа-субъединицу MHC класса II и бета-субъединицу MHC класса II, или слитую молекулу, содержащую обе субъединицы или их антигенпрезентирующие фрагменты. В некоторых вариантах осуществления α-цепь HLA ковалентно связана (например, в слитом белке) или нековалентно связана с β-цепью.
aAPC, включающую эритроидную клетку (например, безъядерную эритроидную клетку) или безъядерную клетку, как представлено в настоящем описании, с антигенпрезентирующими полипептидами, представленными в настоящем описании (например, MHC класса I и MHC класса II) используют в некоторых вариантах осуществления для индуцирования иммунитета и/или презентирования антигена. В некоторых вариантах осуществления aAPC содержит один белок, являющийся слитым белком молекулы MHC и антигена, например, одноцепочечную конструкцию пептид-MHC, содержащую полипептид MHC класса I или MHC класса II и экзогенный антигенный полипептид. В других вариантах осуществления неприкрепленный к мембране компонент комплекса, например, пептид, или β2-микроглобулин собирается с другим средством в клетке перед транспортом к поверхности, секретируется клеткой, а затем захватывается на поверхности прикрепляющим к мембране компонентом мультимера, или его добавляют в очищенной форме к aAPC.
В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит α-цепь MHC класса I и b2m-цепь MHC класса I. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит только α-цепь MHC класса I. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит только b2m-цепь MHC класса I. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит α-цепь MHC класса I и b2m-цепь MHC класса I, и α-цепь MHC класса I и b2m-цепь MHC класса I соединены нековалентно. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит α-цепь MHC класса I и b2m-цепь MHC класса I, и α-цепь MHC класса I и b2m-цепь MHC класса I соединены ковалентно или слиты. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит одноцепочечный слитый белок MHC класса I, где экзогенный антигенный полипептид связывают с α-цепью MHC класса I. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит одноцепочечный слитый белок MHC класса I, где экзогенный антигенный полипептид связывают с b2m-цепью MHC класса I. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит одноцепочечный слитый белок MHC класса I, где экзогенный антигенный полипептид связывают с β2m-субъединицей MHC класса I, связанной с α-субъединицей MHC класса I.
В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит α-цепь MHC класса II и β-цепь MHC класса II. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит только α-цепь MHC класса II. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит только β-цепь MHC класса II. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит α-цепь MHC класса II и β-цепь MHC класса II, и α-цепь MHC класса II и β-цепь MHC класса II соединены нековалентно. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит α-цепь MHC класса II и β-цепь MHC класса II, и α-цепь MHC класса II и β-цепь MHC класса II соединены ковалентно или слиты. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит одноцепочечный слитый белок MHC класса II, где экзогенный антигенный полипептид связывают с α-цепью MHC класса II. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит одноцепочечный слитый белок MHC класса II, где экзогенный антигенный полипептид связывают с β-цепью MHC класса II. В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит одноцепочечный слитый белок MHC класса II, где экзогенный антигенный полипептид связывают с β-цепью MHC класса II, связанной с α-цепью MHC класса II.
В некоторых вариантах осуществления одноцепочечный слитый белок MHC класса I или одноцепочечный слитый белок MHC класса II содержит якорь. В некоторых вариантах осуществления якорь является мембранным белком типа 1. В некоторых вариантах осуществления якорный мембранный белок типа 1 выбран из группы, состоящей из гликофорина A (GPA); гликофорина B (GPB); басигина (также известного как CD147); CD44; CD58 (также известного как LFA3); молекулы межклеточной адгезии 4 (ICAM4); базальной молекулы клеточной адгезии (BCAM); CR1; CD99; эритробластного мембранно-ассоциированного белка (ERMAP); соединительной молекулы адгезии A (JAM-A); нейропластина (NPTN); AMIGO2; и подобного молекуле клеточной адгезии DS белка 1 (DSCAML1). В некоторых вариантах осуществления якорь является мембранным белком типа 2. В некоторых вариантах осуществления якорный мембранный белок типа 2 выбран из группы, состоящей из небольшого интегрального мембранного белка 1 (SMIM1), рецептора трансферрина (CD71), трансмембранного FasL и Kell. В некоторых вариантах осуществления якорь является GPI-связанным мембранным белком. В некоторых вариантах осуществления якорный GPI-связанный мембранный белок выбран из группы, состоящей из CD59, CD55 и семафорина 7A (SEMA7A). В некоторых вариантах осуществления якорь является небольшим интегральным мембранным белком 1 (SMIM1). В некоторых вариантах осуществления якорь является гликофориновым якорем и, в частности, гликофорином A (GPA) или его фрагментом. В некоторых вариантах осуществления якорь выбран из аминокислотной последовательности, приведенной в таблице 3.
Таблица 3. Якорные последовательности
В некоторых вариантах осуществления экзогенный антигенный полипептид соединяют с одноцепочечным слитым белком MHC класса I или MHC класса II с помощью линкера. В некоторых вариантах осуществления одноцепочечный слитый белок MHC класса I или MHC класса II соединяют с якорной последовательностью с помощью линкера. В одном из вариантов осуществления линкер является расщепляемым линкером. В некоторых вариантах осуществления линкер выбран из аминокислотной последовательности, приведенной в таблице 4.
Таблица 4. Линкерные последовательности
В некоторых вариантах осуществления экзогенный антигенный полипептид нагружают на молекулу MHC класса I, и ее функцией является презентирование экзогенного антигенного полипептида. В некоторых вариантах осуществления экзогенный антигенный полипептид нагружают на молекулу MHC класса II, и ее функцией является презентирование экзогенного антигенного полипептида. В некоторых вариантах осуществления экзогенные антигенные полипептиды презентируются на антигенпрезентирующих полипептидах, например, экзогенный антигенный полипептид специфически связан с экзогенными антигенпрезентирующими полипептидами, например, молекулами MHC класса I и/или класса II. Экзогенный антигенный полипептид можно связывать ковалентно или нековалентно с антигенпрезентирующим полипептидом. В некоторых вариантах осуществления экзогенный антигенный пептид является свободным и может специфически связываться с антигенпрезентирующим полипептидом, презентируемым на поверхности искусственной антигенпрезентирующей клетки. В некоторых вариантах осуществления связывающие реагенты можно использовать для связывания экзогенного полипептида с антигенпрезентирующим полипептидом, презентируемым на поверхности клетки. В некоторых вариантах осуществления для связывания экзогенного полипептида с антигенпрезентирующим полипептидом, презентируемым на поверхности клетки, можно использовать клик-химию, как подробно описано в настоящем описании.
В этой области известно множество анализов для анализа аффинности связывания и/или определения того, связывается ли антигенный полипептид специфически с конкретным лигандом (например, молекулой MHC). Например, в некоторых вариантах осуществления для определения константы связывания комплекса между двумя полипептидами можно использовать поверхностный плазмонный резонанс (Biacore®). В этом анализе константу диссоциации комплекса можно определять посредством мониторинга изменений показателя преломления относительно времени, когда буфер проходит по чипу. Другие подходящие анализы для измерения связывания одного полипептида с другим включают, например, иммунологические анализы, такие как твердофазный иммуноферментный анализ (ELISA) и радиоиммунологический анализ (RIA) или определение связывания посредством мониторинга изменения спектроскопических или оптических свойств белков с использованием флуоресценции, поглощения УФ, кругового дихроизма или ядерного магнитного резонанса (ЯМР). Другие неограничивающие примеры анализов включают вестерн-блоттинг, аналитическое ультрацентрифугирование и спектроскопию (см., например, Scatchard et al (1949) Ann. N.Y. Acad. Sci. 51:660; Wilson (2002) Science 295: 2103; Woffi et al. (1993) Cancer Res. 53:2560; патенты США №№5283173, 5468614 и международную патентную публикацию № WO 2018/005559. Альтернативно, связывание антигенного полипептида с конкретным лигандом (например, молекулой MHC) можно определять с использованием прогностического алгоритма. Например, способы прогнозирования эпитопов MHC класса II и класса II хорошо известны в этой области и включают TEPITOPE (см., например, Meister et al. (1995) Vaccine 13: 581-91), EpiMatrix (De Groot et al. (1997) AIDS Res Hum Retroviruses 13: 529-31), способ Predict (Yu et al. (2002) Mol. Med. 8: 137-48), алгоритм прогнозирования эпитопов SYFPEITHI (Schuler et al. (2007) Methods Mol Biol. 409: 75-93) и Rankpep (Reche et al. (2002) Hum Immunol. 63(9): 701-9). Дополнительные алгоритмы для прогнозирования эпитопов MHC класса I и класса II описаны, например, в Kessler and Melief (2007) Leukemia 21(9): 1859-74.
В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид выбран из группы, состоящей из HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQA1, HLA-DQB1, HLA-DPA1, HLA-DPB1, способных связывать антигены и экспонировать их на поверхности клетки.
В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом MHC класса I или одноцепочечным слитым белком MHC класса I. В дополнительном варианте осуществления полипептид MHC класса I является HLA-A. В некоторых вариантах осуществления полипептид HLA-A включает одноцепочечный слитый полипептид HLA-A, где полипептид HLA-A связывают с экзогенным антигенным полипептидом. В некоторых вариантах осуществления одноцепочечный слитый полипептид HLA-A включает мембранный якорь. В некоторых вариантах осуществления мембранный якорь выбран из мембранного якоря, приведенного в таблице 3. В некоторых вариантах осуществления одноцепочечный слитый полипептид HLA-A включает линкер (например, между антигенным пептидом и бета-цепью, между бета-цепью и альфа-цепью или между альфа-цепью и якорем). В некоторых вариантах осуществления линкер выбран из последовательности, приведенной в таблице 4. В некоторых вариантах осуществления одноцепочечный слитый полипептид HLA-A включает лидерную последовательность. В некоторых вариантах осуществления лидерная последовательность выбрана из последовательности, приведенной в таблице 2. В некоторых вариантах осуществления лидерная последовательность HLA-A слита с экзогенным антигенпрезентирующим полипептидом, связанным с мембранным якорем.
В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом MHC класса I или одноцепочечным слитым белком MHC класса I. В дополнительном варианте осуществления полипептид MHC класса I является HLA-B. В некоторых вариантах осуществления полипептид HLA-B содержит одноцепочечный слитый полипептид HLA-B, где полипептид HLA-B связывают с экзогенным антигенным полипептидом. В некоторых вариантах осуществления одноцепочечный слитый полипептид HLA-B включает мембранный якорь. В некоторых вариантах осуществления мембранный якорь выбран из мембранного якоря, приведенного в таблице 3. В некоторых вариантах осуществления одноцепочечный слитый полипептид HLA-B включает линкер (например, между антигенным пептидом и бета-цепью, между бета-цепью и альфа-цепью или между альфа-цепью и якорем). В некоторых вариантах осуществления линкер выбран из последовательности, приведенной в таблице 4. В некоторых вариантах осуществления одноцепочечный слитый полипептид HLA-B включает лидерную последовательность. В некоторых вариантах осуществления лидерная последовательность выбрана из последовательности, приведенной в таблице 2. В некоторых вариантах осуществления лидерная последовательность HLA-B слита с экзогенным антигенпрезентирующим полипептидом, связанным с мембранным якорем.
В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом MHC класса I или одноцепочечным слитым белком MHC класса I. В дополнительном варианте осуществления полипептид MHC класса I является HLA-C. В некоторых вариантах осуществления полипептид HLA-C содержит одноцепочечный слитый полипептид HLA-C, где полипептид HLA-C связывают с экзогенным антигенным полипептидом. В некоторых вариантах осуществления одноцепочечный слитый полипептид HLA-C включает мембранный якорь. В некоторых вариантах осуществления мембранный якорь выбран из последовательности, приведенной в таблице 3. В некоторых вариантах осуществления одноцепочечный слитый полипептид HLA-C включает линкер (например, между антигенным пептидом и бета-цепью, между бета-цепью и альфа-цепью или между альфа-цепью и якорем). В некоторых вариантах осуществления линкер выбран из последовательности, приведенной в таблице 4. В некоторых вариантах осуществления одноцепочечный слитый полипептид HLA-C включает лидерную последовательность. В некоторых вариантах осуществления лидерная последовательность выбран из последовательности, приведенной в таблице 2. В некоторых вариантах осуществления лидерная последовательность HLA-C слита с экзогенным антигенпрезентирующим полипептидом, связанным с мембранным якорем.
В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом MHC класса II или одноцепочечным слитым белком MHC класса II. В дополнительном варианте осуществления полипептид MHC класса II выбран из группы, состоящей из HLA-DPα, HLA-DPβ, HLA-DM, HLA DOA, HLA-DOB, HLA-DQα, HLA-DQβ, HLA-DRα и HLA-DRβ. В некоторых вариантах осуществления полипептид HLA-DPA содержит одноцепочечный слитый полипептид HLA-DPA, где HLA-DPA полипептид связывают с экзогенным антигенным полипептидом. В некоторых вариантах осуществления полипептид HLA-DPB содержит одноцепочечный слитый полипептид HLA-DPB, где HLA-DPB полипептид связывают с экзогенным антигенным полипептидом. В некоторых вариантах осуществления полипептид HLA-DM содержит одноцепочечный слитый полипептид HLA-DM, где полипептид HLA-DM связывают с экзогенным антигенным полипептидом. В некоторых вариантах осуществления полипептид HLA-DOA содержит одноцепочечный слитый полипептид HLA-DOA, где полипептид HLA-DOA связывают с экзогенным антигенным полипептидом. В некоторых вариантах осуществления полипептид HLA-DOB содержит одноцепочечный слитый полипептид HLA-DOB, где полипептид HLA-DOB связывают с экзогенным антигенным полипептидом. В некоторых вариантах осуществления полипептид HLA-DQA содержит одноцепочечный слитый полипептид HLA-DQA, где полипептид HLA-DQA связывают с экзогенным антигенным полипептидом. В некоторых вариантах осуществления полипептид HLA-DQB содержит одноцепочечный слитый полипептид HLA-DQB, где полипептид HLA-DQB связывают с экзогенным антигенным полипептидом. В некоторых вариантах осуществления полипептид HLA-DRA содержит одноцепочечный слитый полипептид HLA-DRA, где полипептид HLA-DRA связывают с экзогенным антигенным полипептидом. В некоторых вариантах осуществления полипептид HLA-DRB содержит одноцепочечный слитый полипептид HLA-DRB, где полипептид HLA-DRB связывают с экзогенным антигенным полипептидом. В некоторых вариантах осуществления одноцепочечные слитые полипептиды включают мембранный якорь. В некоторых вариантах осуществления мембранный якорь выбран из последовательность, приведенной в таблице 3. В некоторых вариантах осуществления одноцепочечные слитые полипептиды включают линкер (например, между антигенным пептидом и бета-цепью, между бета-цепью и альфа-цепью или между альфа-цепью и якорем). В некоторых вариантах осуществления линкер выбран из последовательности, приведенной в таблице 4. В некоторых вариантах осуществления одноцепочечные слитые полипептиды включают лидерную последовательность. В некоторых вариантах осуществления лидерная последовательность выбрана из последовательности, приведенной в таблице 2.
Известно, что белковые продукты генов MHC класса I и класса II являются высоко полиморфными, таким образом, настоящее изобретение также включает полиморфные формы MHC. Существует более 200 аллелей некоторых генов MHC класса I и класса II человека. За исключением локуса DRα, являющегося функционально мономорфным, каждый локус имеет множество аллелей (Janeway CA Jr, Travers P, Walport M, et al. Immunobiology: The Immune System in Health and Disease. 5th edition. New York: Garland Science; 2001, в полном объеме включенная в настоящее описание в качестве ссылки), каждый аллель имеет относительно высокую частоту в популяции.
В некоторых вариантах осуществления полипептид MHC класса I является HLA-A. В некоторых вариантах осуществления полипептид HLA-A содержит аллель HLA-A, выбранный из группы, состоящей из A*01:01, A*02:01, A*03:01, A*24:02, A*11:01, A*29:02, A*32:01, A*68:01, A*31:01, A*25:01, A*26:01, A*23:01, A*30:01.
В некоторых вариантах осуществления полипептид MHC класса I является HLA-B. В некоторых вариантах осуществления полипептид HLA-B содержит аллель HLA-B, выбранный из группы, состоящей из B*08:01, B*07:02, B*44:02, B*15:01, B*40:01, B*44:03, B*35:01, B*51:01, B*27:05, B*57:01, B*18:01, B*14:02, B*13:02, B*55:01, B*14:01, B*49:01, B*37:01, B*38:01, B*39:01, B*35:03, B*40:02.
В некоторых вариантах осуществления полипептид MHC класса I является HLA-C. В некоторых вариантах осуществления полипептид HLA-C содержит аллель HLA-C, выбранный из группы, состоящей из C*07:01, C*07:02, C*05:01, C*06:02, C*04:01, C*03:04, C*03:03, C*02:02, C*16:01, C*08:02, C*12:03, C*01:02, C*15:02, C*07:04, C*14:02.
В некоторых вариантах осуществления полипептид MHC класса II выбран из группы, состоящей из HLA-DPα, HLA-DPβ, HLA-DM, HLA DOA, HLA-DOB, HLA-DQα, HLA-DQβ, HLA-DRα и HLA-DRβ. В некоторых вариантах осуществления полипептид HLA-DPα содержит аллель HLA-DPα, выбранный из группы, состоящей из DPA1*01:03, DPA1*02:01, DPA1*02:07. В некоторых вариантах осуществления полипептид HLA-DPβ содержит аллель HLA-DPβ, выбранный из группы, состоящей из DPB1*04:01, DPB1*02:01, DPB1*04:02, DPB1*03:01, DPB1*01:01, DPB1*11:01, DPB1*05:01, DPB1*10:01, DPB1*06:01, DPB1*13:01, DPB1*14:01 и DPB1*17:01. В некоторых вариантах осуществления полипептид HLA-DQα содержит аллель HLA-DQα, выбранный из группы, состоящей из DQA1*05:01, DQA1*03:01, DQA1*01:02, DQA1*02:01, DQA1*01:01, DQA1*01:03 и DQA1*04:01. В некоторых вариантах осуществления полипептид HLA-DQβ содержит аллель HLA-DQβ, выбранный из группы, состоящей из DQB1*03:01, DQB1*02:01, DQB1*06:02, DQB1*05:01, DQB1*02:02, DQB1*03:02, DQB1*06:03, DQB1*03:03, DQB1*06:04, DQB1*05:03 и DQB1*04:02. В некоторых вариантах осуществления полипептид HLA-DRβ содержит аллель HLA-DRβ, выбранный из группы, состоящей из DRB1*07:01, DRB1*03:01, DRB1*15:01, DRB1*04:01, DRB1*01:01, DRB1*13:01, DRB1*11:01, DRB1*04:04, DRB1*13:02, DRB1*08:01, DRB1*12:01, DRB1*11:04, DRB1*09:01, DRB1*14:01, DRB1*04:07 и DRB1*14:04.
В некоторых вариантах осуществления антигенпрезентирующий полипептид содержит полипептид аллеля HLA, содержащий или состоящий из аминокислотной последовательности, приведенной в таблице 5. В некоторых вариантах осуществления полипептид аллеля MHC содержит сигнальный пептид. В других вариантах осуществления полипептид аллеля MHC не включает сигнальный пептид. Таким образом, в некоторых вариантах осуществления антигенпрезентирующий полипептид содержит аминокислотную последовательность по любой из SEQ ID NO: 741-838, приведенной в таблице 5, за исключением аминокислотной последовательности сигнального пептида (выделена подчеркиванием в последовательностях в таблице 5). В других вариантах осуществления антигенпрезентирующий полипептид содержит аминокислотную последовательность по любой из SEQ ID NO: 741-838, представленных в таблице 5, включая аминокислотную последовательность сигнального пептида (выделена подчеркиванием в последовательностях в таблице 5).
Таблица 5. Аллели HLA
(регистрационный номер в IMGT/HLA HLA00001)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00005)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00037)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00050)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00043)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00086)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00101)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00115)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00092)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00071)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00073)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00048)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00089)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00433)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00434)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00427)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00430)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00420)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00413)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00411)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00404)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00475)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00446)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00455)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00401)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00467)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00406)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00462)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00146)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00132)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00318)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00162)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00291)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00319)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00237)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00344)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00225)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00381)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00213)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00158)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00153)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00368)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00157)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00340)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00265)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00267)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00271)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00239)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00293)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00719)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00671)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00865)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00685)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00664)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00797)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00751)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00689)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00798)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00723)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00789)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00756)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00749)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00833)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00693)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00836)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00613)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00608)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00602)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00607)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00601)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00604)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00612)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00625)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00622)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00646)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00638)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00623)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00627)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00647)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00629)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00648)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00640)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00637)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00499)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00504)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA15619)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00521)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00517)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00522)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00520)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00514)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00528)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00523)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00527)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00524)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00530)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00531)
* Прогнозируемый сигнальный пептид подчеркнут
(регистрационный номер в IMGT/HLA HLA00534)
* Прогнозируемый сигнальный пептид подчеркнут
Дополнительные аминокислотные последовательности аллелей MHC известны в этой области и доступны, например, в базе данных IMGT/HLA (доступной в сети интернет по адресу ebi.ac.uk/ipd/imgt/hla/; см. Robinson et al. Nucl. Acids Res. 43: D423-431 (2015)).
В некоторых вариантах осуществления полипептид является экзогенным антигенпрезентирующим полипептидом, представленным в настоящем описании. Пример экзогенного антигенпрезентирующего полипептида включает:
a) природную форму полипептида человека;
b) полипептид человека, имеющий последовательность, содержащуюся в базе данных, например, базе данных GenBank, на 22 декабря 2017 года;
c) полипептид человека, имеющий последовательность, отличающуюся на не более чем 1, 2, 3, 4, 5 или 10 аминокислотных остатков от последовательности по п. a) или b);
d) полипептид человека, имеющий последовательность, отличающуюся на не более чем 1, 2, 3, 4, 5 или 10% аминокислотных остатков от последовательности по п. a) или b);
e) полипептид человека, имеющий последовательность, по существу, не отличающуюся от последовательности по п. a) или b); или
f) полипептид человека, имеющий последовательность по п. c), d) или e), по существу, не отличающуюся по биологической активности, например, ферментативной активности (например, специфичности или оборот) или связывающей активности (например, специфичности или аффинности связывания с антигенным пептидом) от полипептида человека, имеющего последовательность по п. a) или b). Пептиды-кандидаты по п. f) можно получать и подвергать скринингу на схожую активность, как представлено в настоящем описании, и они будут эквивалентны при экспрессии в сконструированных эритроидных клетках, как представлено в настоящем описании.
В вариантах осуществления экзогенный антигенпрезентирующий полипептид содержит полипептид человека или его фрагмент, например, весь полипептид человека или фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу. В варианте осуществления экзогенный антигенпрезентирующий полипептид содержит слитый полипептид, содержащий весь полипептид человека или фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу и дополнительную аминокислотную последовательность. В варианте осуществления дополнительная аминокислотная последовательность содержит весь полипептид человека или фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу для другого экзогенного антигенпрезентирующего полипептида человека.
В некоторых вариантах осуществления по настоящему изобретению искусственная антигенпрезентирующая клетка включает эритроидную клетку или безъядерную клетку, несодержашую эндогенный антигенпрезентирующий полипептид (например, молекулу MHC класса I или MHC класса II). В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку или безъядерную клетку, полученную из эритроидной клетки-предшественника, генетически модифицированной для делеции и/или изменения экспрессии эндогенного антигенпрезентирующего полипептида (например, молекулы MHC класса I или MHC класса II).
Экзогенные костимуляторные полипептиды
Экзогенный костимуляторный полипептид включает полипептид на антигенпрезентирующей клетке (например, aAPC), специфически связывающийся с когнатной костимуляторной молекулой на T-клетке (например, молекулой MHC, B- и T-лимфоцитарным аттенюатором (CD272) и Toll-подобным рецептором), таким образом, обеспечивающий сигнал, опосредующий T-клеточный ответ, включая, в качестве неограничивающих примеров, пролиферацию, активацию, дифференцировку и т.п. Костимуляторный полипептид также включает, помимо прочего, антитело, специфически связывающееся с костимуляторной молекулой, присутствующей на T-клетке. Такое антитело, предпочтительно, связывается с костимуляторной молекулой на T-клетке и действует в качестве ее агониста.
В некоторых вариантах осуществления желаемый ответ представляет собой гибель клетки, например, инфицированной клетки. В некоторых вариантах осуществления костимуляторные полипептиды запускают множество путей активации T-клеток для индуцирования иммунного ответа. В некоторых вариантах осуществления aAPC, содержащая, помимо прочего, костимуляторные полипептиды, способствует пролиферации T-клеток. В вариантах осуществления один или более (например, 2, 3, 4, 5 или более) костимуляторных полипептидов содержат активирующий полипептид из таблицы 6 ниже или его активирующий T-клетки вариант (например, фрагмент). В вариантах осуществления один или более (например, 2, 3, 4, 5 или более) костимуляторных полипептидов содержат молекулу антитела (например, агонистическое антитело), связывающегося с рецептором-мишенью из таблицы 6, или его активирующий T-клетки вариант (например, фрагмент). В некоторых вариантах осуществления костимуляторные полипептиды содержат разные лиганды активации T-клеток, например, один или более активирующих полипептидов из таблицы 6, в любой их комбинации, для стимуляции T-клеток. В некоторых вариантах осуществления aAPC включает эритроидную клетку (например, безъядерную клетку), презентирующую, например, содержащую на своей поверхности, 4-1BBL, OX40L и CD40L или их фрагменты или варианты. В вариантах осуществления эти белки передают сигнал через комплементарные пути активации. Костимуляторные полипептиды можно получать из эндогенных лигандов активации T-клеток или из молекул антител против рецепторов-мишеней.
Таблица 6. Костимуляторные полипептиды
В некоторых вариантах осуществления полипептид, содержащий 4-1BBL, является укороченным с N-конца 4-1BBL (например, SEQ ID NO: 851). В некоторых вариантах осуществления полипептид, содержащий 4-1BBL, является полноразмерным 4-1BBL.
В некоторых вариантах осуществления один или более костимуляторных полипептидов содержат активирующий цитокин, интерферон или член семейства ФНО, например, ИФНα, ИЛ-2, ИЛ-6 или любую их комбинацию. Активирующие цитокины, интерфероны и члены семейства ФНО, которые можно использовать в изобретении, дополнительно описаны ниже. В вариантах осуществления один или более костимуляторных полипептидов содержат один или более активирующих цитокинов, интерферонов или членов семейства ФНО и дополнительно содержат один или более активирующих полипептидов или лигандов (например, из таблицы 6) или их активирующих T-клетки вариантов (например, фрагментов), или одну или более молекул антител (например, агонистических антител), связывающихся с костимуляторным T-клеточным рецептором-мишенью (например, из таблицы 6) или его активирующим T-клетки вариантом (например, фрагментом).
Экспансия T-клеток
В некоторых вариантах осуществления настоящее изобретение относится к aAPC, которые можно использовать для специфического индуцирования пролиферации T-клетки, экспрессирующей известную костимуляторную молекулу. Способ включает приведение T-клетки, подлежащей экспансии, в контакт с aAPC, презентирующей (например, содержащей на своей поверхности) экзогенный полипептид, специфически связывающийся с костимуляторной молекулой, экспрессируемой T-клеткой. Таким образом, приведение T-клетки в контакт с aAPC, содержащей, в частности, костимуляторный лиганд, специфически связывающийся с когнатной костимуляторной молекулой, экспрессирующейся на поверхности T-клетки, стимулирует T-клетки и индуцирует пролиферацию T-клеток, таким образом, что легко можно получать большие количества T-клеток. aAPC приводят к экспансии T-клеток "специфически" в том смысле, что только T-клетки, экспрессирующие конкретную костимуляторную молекулу, подвергаются экспансии под действием aAPC. Таким образом, если T-клетка, подлежащая экспансии, находится в смеси клеток, некоторые или большинство из которых не экспрессируют костимуляторную молекулу, только интересующая T-клетка будет индуцироваться так, чтобы подвергаться пролиферации и экспансии. T-клетку можно дополнительно очищать с использованием широкого спектра способов разделения и очистки клеток, таких как способы, известные в этой области и/или представленные где-либо в настоящем описании.
Как будет понятно специалистам в этой области с учетом раскрытия, представленного в настоящем описании, интересующую T-клетку не обязательно идентифицировать или выделять перед экспансией с использованием aAPC. Это является результатом того, что aAPC является селективной и будет приводить только к экспансии T-клеток, экспрессирующих когнатную костимуляторную молекулу.
В некоторых вариантах осуществления полипептид является экзогенным костимуляторным полипептидом, представленным в настоящем описании. Пример костимуляторного полипептида включает:
a) природную форму полипептида человека;
b) полипептид человека, имеющий последовательность, содержащуюся в базе данных, например, базе данных GenBank , на 22 декабря 2017 года;
c) полипептид человека, имеющий последовательность, отличающуюся на не более чем 1, 2, 3, 4, 5 или 10 аминокислотных остатков от последовательности по п. a) или b);
d) полипептид человека, имеющий последовательность, отличающуюся на не более чем 1, 2, 3, 4, 5 или 10% аминокислотных остатков от последовательности по п. a) или b);
e) полипептид человека, имеющий последовательность по существу, не отличающуюся от последовательности по п. a) или b); или
f) полипептид человека, имеющий последовательность по п. c), d) или e), по существу, не отличающуюся по биологической активности, например, ферментативной активности (например, специфичности или обороту) или связывающей активности (например, специфичности или аффинности связывания), от полипептида человека, имеющего последовательность по п. a) или b). Пептиды-кандидаты по п. f) можно получать и подвергать скринингу на схожую активность, как представлено в настоящем описании, и они будут эквивалентны при экспрессии в сконструированных эритроидных клетках, как представлено в настоящем описании.
В вариантах осуществления экзогенный костимуляторный полипептид содержит полипептид человека или его фрагмент, например, весь полипептид человека или его фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу. В варианте осуществления экзогенный костимуляторный полипептид содержит слитый полипептид, содержащий весь полипептид человека или его фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу и дополнительную аминокислотную последовательность. В варианте осуществления дополнительная аминокислотная последовательность содержит весь полипептид человека или его фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу для другого костимуляторного полипептида человека.
В вариантах осуществления клетка aAPC направленно воздействует на множество путей активации T-клеток в комбинации (например, как описано в таблице 6 выше), например, с использованием лигандов, или молекул антител, или и тех, и других, коэкспрессирующихся (или копрезентируемых) на aAPC.
В некоторых вариантах осуществления по меньшей мере один экзогенный костимуляторный полипептид выбран из группы, состоящей из 4-1BBL, LIGHT, CD80, CD86, CD70, ИЛ-7, ИЛ-12, OX40L, GITRL, TIM4, SLAM, CD48, CD58, CD83, CD155, CD112, ИЛ-15Rα, слитого с ИЛ-15, ИЛ-2, ИЛ-21, лиганда для ICAM-1, лиганда LFA-1 и их комбинации. В некоторых вариантах осуществления по меньшей мере один экзогенный костимуляторный полипептид является агонистическим антителом для когнатного рецептора костимуляторного лиганда. Например, в некоторых вариантах осуществления костимуляторный полипептид является агонистическим антителом против 4-1-BB, рецептором LIGHT (HVEM), рецептором CD80, рецептором CD86, OX40, GITR, рецептором TIM4 (TIM1), рецептором SLAM, рецептором CD48 (CD2), рецептором CD58 (CD2), рецептором CD83, рецептором CD155 (CD226), рецептором CD112 (CD226), рецептором ИЛ-2 (CD25, CD122, CD132), рецептором ИЛ-21, ICAM и их комбинациями. В некоторых вариантах осуществления по меньшей мере один экзогенный костимуляторный полипептид является антителом против CD3 или антителом против CD38 и их комбинациями. В другом варианте осуществления aAPC презентирует, например, содержит на своей поверхности по меньшей мере два, по меньшей мере 3, по меньшей мере 4 или по меньшей мере 5 экзогенных костимуляторных полипептидов. В некоторых вариантах осуществления костимуляторные белки слиты друг с другом, например, ИЛ-21 слит с ИЛ-2.
В некоторых вариантах осуществления один или более костимуляторных полипептидов включают мембранный якорь или слиты с ним. В некоторых вариантах осуществления мембранный якорь выбран из последовательности, приведенной в таблице 3. В некоторых вариантах осуществления один или более костимуляторные полипептиды включают лидерную последовательность или слиты с ней. В некоторых вариантах осуществления лидерная последовательность выбрана из последовательности, приведенной в таблице 2.
Экзогенные коингибиторные полипептиды
Экзогенный коингибиторный полипептид является любым полипептидом, супрессирующим T-клетку, включая ингибирование активности T-клеток, ингибирование пролиферации T-клеток, анергию T-клеток или индуцирование апоптоза T-клетки.
В некоторых вариантах осуществления экзогенный коингибиторный полипептид является ингибиторным полипептидным лигандом на антигенпрезентирующей клетке, специфически связывающимся с когнатной коингибиторной молекулой на T-клетке. В некоторых вариантах осуществления коингибиторный полипептидный лиганд является ингибиторным полипептидом, приведенным в таблице 7.
В некоторых вариантах осуществления экзогенный коингибиторный полипептид является агонистом (например, антителом), специфически связывающимся с коингибиторным рецептором на T-клетке. В некоторых вариантах осуществления агонист является антителом, связывающимся с рецептором, выбранным из группы, состоящей из: PD1, CTLA4, TIM3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG3, VISTA, BTLA, TIGIT, LAIR1, CD160 и 2B4. В других вариантах осуществления агонист является антителом, связывающимся с рецептором-мишенью на T-клетке, приведенным в таблице 7.
Таблица 7. Коингибиторные полипептиды
В некоторых вариантах осуществления экзогенный коингибиторный полипептид является антителом, блокирующим связывание костимуляторного полипептида с его когнатным костимуляторным рецептором. В различных вариантах осуществления экзогенный коингибиторный полипептид является антителом, блокирующим связывание 4-1BBL, LIGHT, CD80, CD86, CD70, OX40L, GITRL, TIM4, SLAM, CD48, CD58, CD83, CD155, CD112, ИЛ-15Rα, слитого с ИЛ-15, ИЛ-2, ИЛ-21, ICAM, лиганда LFA-1, антитела против CD3 или антитела против CD28 с их рецептором.
В других вариантах осуществления коингибиторный полипептид выбран из ИЛ-35, ИЛ-10 или VSIG-3.
В некоторых вариантах осуществления экзогенный коингибиторный полипептид является VSIG-3.
В других вариантах осуществления клетка aAPC направленно воздействует на множество ингибиторных путей T-клеток в комбинации (например, как описано в таблице 7 выше), например, с использованием лигандов или молекул антител или и тех, и других, коэкспрессирующихся на aAPC.
В некоторых вариантах осуществления полипептид является экзогенным коингибиторным полипептидом, представленным в настоящем описании. Пример коингибиторного полипептида включает:
a) природную форму полипептида человека;
b) полипептид человека, имеющий последовательность, содержащуюся в базе данных, например, базе данных GenBank , на 22 декабря 2017 года;
c) полипептид человека, имеющий последовательность, отличающуюся на не более чем 1, 2, 3, 4, 5 или 10 аминокислотных остатков от последовательности по п. a) или b);
d) полипептид человека, имеющий последовательность, отличающуюся на не более чем 1, 2, 3, 4, 5 или 10% аминокислотных остатков от последовательности по п. a) или b);
e) полипептид человека, имеющий последовательность по существу, не отличающуюся от последовательности по п. a) или b); или
f) полипептид человека, имеющий последовательность по п. c), d) или e), по существу, не отличающуюся по биологической активности, например, ферментативной активности (например, специфичности или обороту) или связывающей активности (например, специфичности или аффинности связывания), от полипептида человека, имеющего последовательность по п. a) или b). Пептиды-кандидаты по п. f) можно получать и подвергать скринингу на схожую активность, как представлено в настоящем описании, и они будут эквивалентны при экспрессии в сконструированных эритроидных клетках, как представлено в настоящем описании.
В вариантах осуществления экзогенный коингибиторный полипептид содержит полипептид человека или его фрагмент, например, весь полипептид человека или его фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу. В варианте осуществления экзогенный коингибиторный полипептид содержит слитый полипептид, содержащий весь полипептид человека или его фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу и дополнительную аминокислотную последовательность. В варианте осуществления дополнительная аминокислотная последовательность содержит весь полипептид человека или его фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу для другого коингибиторного полипептида человека.
В некоторых вариантах осуществления aAPC презентирует, например, содержит на своей поверхности, по меньшей мере два, по меньшей мере 3, по меньшей мере 4 или по меньшей мере 5 экзогенных коингибиторных полипептидов.
В некоторых вариантах осуществления один или более коингибиторных полипептидов включают мембранный якорь или слиты с ним. В некоторых вариантах осуществления мембранный якорь выбран из последовательности, приведенной в таблице 3. В некоторых вариантах осуществления один или более коингибиторных полипептидов включают лидерную последовательность или слиты с ней. В некоторых вариантах осуществления лидерная последовательность выбрана из последовательности, приведенной в таблице 2.
Сигналы активации T-клетки
Для эффективного индуцирования пролиферации, активации и экспансии T-клеток необходима передача нескольких сигналов из aAPC к наивным T-клеткам. Эти сигналы общепринято обозначают как сигнал 1, сигнал 2 и сигнал 3, и они описаны ниже. В некоторых вариантах осуществления aAPC, представленные в настоящем описании, содержат один или более экзогенных полипептидов, содержащих сигнал 1, один или более экзогенных полипептидов, содержащих сигнал 2, и/или один или более экзогенных полипептидов, содержащих сигнал 3, в любой комбинации, как описано ниже. В некоторых вариантах осуществления в дополнение к сигналу 1, сигналу 2 и сигналу 3, aAPC, представленные в настоящем описании, дополнительно содержат один или более экзогенных полипептидов, содержащих одну или более молекул клеточной адгезии для дополнительного облегчения взаимодействий между T-клетками и aAPC. Следует понимать, что если aAPC содержит один или более экзогенных полипептидов, содержащих сигнал 1, и/или один или более экзогенных полипептидов, содержащих сигнал 2, и/или один или более экзогенных полипептидов, содержащих сигнал 3 (и, необязательно, один или более полипептидов, содержащих молекулы клеточной адгезии), все из экзогенных полипептидов, содержащих сигнал 1, и/или сигнал 2, и/или сигнал 3, и/или, молекулу клеточной адгезии, содержатся на одной и той же aAPC.
aAPC, представленные в настоящем описании, обладают множеством преимуществ по сравнению с использованием сферических наночастиц, таких как жесткие aAPC на основе частиц. Например, мембрана aAPC, представленной в настоящем описании (т.е. сконструированной эритроидной клетки или безъядерной клетки) является гораздо более динамичной и текучей, чем внешняя поверхность наночастицы, являющаяся жесткой и неподвижной, и, таким образом, ограничивает движение полипептидов на их поверхности. Текучесть мембраны aAPC делает возможной более высокую молекулярную подвижность и более эффективную молекулярную реорганизацию и предпочтительна для образования иммунологического синапса и стимуляции T-клеток. В некоторых вариантах осуществления aAPC, представленные в настоящем описании, содержащие один или более экзогенных полипептидов, содержащих сигнал 1, один или более экзогенных полипептидов, содержащих сигнал 2, и/или один или более экзогенных полипептидов, содержащих сигнал 3, в любой комбинации, как описано ниже, на поверхности клеток, обеспечивают более контролируемую стимуляцию T-клеток, что, таким образом, делает возможным размножение T-клеток со специфическим фенотипом и активностью. В некоторых вариантах осуществления при конструировании aAPC таким образом, что они содержат сигнал 1, и/или сигнал 2, и/или сигнал 3 на поверхности клетки, aAPC обеспечивают оптимальный контроль над сигналами, передаваемыми T-клетками.
Сигнал 1 - Распознавание антигена
Активация T-клеток происходит после того, как T-клеточный рецептор (TCR) распознает специфический пептидный антиген, презентируемый на комплексах MHC aAPC, представленных в настоящем описании. Как правило, экзогенные антигенные полипептиды, презентируемые на MHC класса II, распознаются TCR в комбинации с T-клеточным корецептором CD4. Экзогенные антигенные полипептиды, презентируемые на MHC класса I, распознаются TCR в комбинации с T-клеточным корецептором CD8. Лигирование TCR с комплексом пептид-MHC приводит к передаче сигналов, необходимых для активации T-клетки.
В некоторых вариантах осуществления сигнал 1 содержит еще один экзогенный полипептид, содержащий антигенпрезентирующий полипептид. В некоторых вариантах осуществления сигнал 1 содержит антигенпрезентирующий полипептид, специфически связанный (презентируемый) с антигенным пептидом (например, ковалентно или нековалентно). В некоторых вариантах осуществления антигенпрезентирующий полипептид является полипептидом MHC класса I, одноцепочечным слитым белком MHC класса I, полипептидом MHC класса II или одноцепочечным слитым белком MHC класса II. В некоторых вариантах осуществления полипептид MHC класса I выбран из группы, состоящей из HLA A, HLA B и HLA C. В некоторых вариантах осуществления полипептид MHC класса II выбран из группы, состоящей из HLA-DPα, HLA-DPβ, HLA-DM, HLA DOA, HLA DOB, HLA DQα, HLA DQβ, HLA DRα и HLA DRβ.
Сигнал 2 - Костимуляция
Для того чтобы стать полностью активированными, T-клеткам необходим второй сигнал в дополнение к TCR-опосредованному распознаванию антигена. Этот второй сигнал или костимуляция важны для правильной активации T-клеток. В некоторых вариантах осуществления сигнал 2 содержит один или более экзогенных костимуляторных полипептидов. В некоторых вариантах осуществления один или более экзогенных костимуляторных полипептидов выбраны из группы, состоящей из 4-1BBL, LIGHT, антитела против CD28, CD80, CD86, CD70, OX40L, GITRL, TIM4, SLAM, CD48, CD58, CD83, CD155, CD112, ИЛ-15, ИЛ-15Rα, слитого с ИЛ-15, ИЛ-21, ICAM-1, лиганда LFA-1, антитела против CD3 и любой их комбинации. В некоторых вариантах осуществления сигнал 2 содержит один или более экзогенных костимуляторных полипептидов, выбранных из группы, состоящей из 4-1BBL, CD80, CD86, CD83, CD70, LIGHT, HVEM, CD40L, OX40L, TL1A, GITRL и CD30L.
Сигнал 3 - Цитокины
Для индуцирования более эффективной экспансии и специфической дифференцировки T-клеток можно использовать третий сигнал (сигнал 3). В некоторых вариантах осуществления сигнал 3 содержит один или более экзогенных полипептидов, содержащих один или более цитокинов. В некоторых вариантах осуществления сигнал 3 содержит один или более экзогенных полипептидов, выбранных из группы, состоящей из ИЛ-2, ИЛ-15, ИЛ-7, ИЛ-12, ИЛ-18, ИЛ-21, ИЛ-4; ИЛ-6, ИЛ-23, ИЛ-27, ИЛ-17, ИЛ-10, TGF-бета, ИФН-гамма, ИЛ-1 бета, ГМ-КСФ, ИЛ-15, ИЛ-15Rα, слитого с ИЛ-15, и ИЛ-25
В дополнение к иммуностимуляторным цитокинам, иммуноингибиторные цитокины могут снижать иммунный ответ или приводить к толерантности. Таким образом, в некоторых вариантах осуществления сигнал 3 содержит один или более экзогенных коингибиторных полипептидов. В некоторых вариантах осуществления один или более экзогенных коингибиторных полипептидов выбраны из группы, состоящей из ИЛ-35, ИЛ-10, VSIG-3 и агониста LAG3.
В некоторых вариантах осуществления aAPC содержит на своей поверхности экзогенный полипептид, содержащий сигнал 1.
В некоторых вариантах осуществления aAPC содержит на своей поверхности экзогенный полипептид, содержащий сигнал 1, и экзогенный полипептид, содержащий сигнал 2. В некоторых вариантах осуществления aAPC содержит на своей поверхности экзогенный полипептид, содержащий сигнал 1, экзогенный полипептид, содержащий сигнал 2, и экзогенный полипептид, содержащий сигнал 3. В некоторых вариантах осуществления aAPC содержит на своей поверхности более одного экзогенного полипептида, содержащего более одного сигнала 1, и экзогенный полипептид, содержащий сигнал 2. В некоторых вариантах осуществления aAPC содержит на своей поверхности более одного экзогенного полипептида, содержащего более одного сигнала 1, экзогенный полипептид, содержащий сигнал 2, и экзогенный полипептид, содержащий сигнал 3. В некоторых вариантах осуществления aAPC содержит на своей поверхности экзогенный полипептид, содержащий сигнал 1, и более одного экзогенного полипептида, содержащего более одного сигнала 2. В некоторых вариантах осуществления aAPC содержит на своей поверхности экзогенный полипептид, содержащий сигнал 1, более одного экзогенного полипептида, содержащего более одного сигнала 2, и экзогенный полипептид, содержащий сигнал 3. В некоторых вариантах осуществления aAPC содержит на своей поверхности экзогенный полипептид, содержащий сигнал 1, экзогенный полипептид, содержащий сигнал 2, и более одного экзогенного полипептида, содержащего более одного сигнала 3. В некоторых вариантах осуществления aAPC содержит на своей поверхности более одного экзогенного полипептида, содержащего более одного сигнала 1, экзогенный полипептид, содержащий сигнал 2, и более одного экзогенного полипептида, содержащего более одного сигнала 3. В некоторых вариантах осуществления aAPC содержит на своей поверхности более одного экзогенного полипептида, содержащего более одного сигнала 1, более одного экзогенного полипептида, содержащего более одного сигнала 2, и экзогенный полипептид, содержащий сигнал 3. В некоторых вариантах осуществления aAPC содержит на своей поверхности более одного экзогенного полипептида, содержащего более одного сигнала 1, более одного экзогенного полипептида, содержащего более одного сигнала 2, и более одного экзогенного полипептида, содержащего более одного сигнала 3.
В некоторых вариантах осуществления aAPC содержит экзогенный полипептид, содержащий сигнал 1, и экзогенный полипептид, содержащий сигнал 2, где сигнал 1 и сигнал 2 выбраны из следующих комбинаций: MHC класса I и 4-1BBL; MHC класса II и 4-1BBL; MHC класса I и CD80; MHC класса II и CD80; MHC класса I и CD86; MHC класса II и CD86; MHC класса I и CD83; MHC класса II и CD83; MHC класса I и CD70; MHC класса II и CD70; MHC класса I и LIGHT; MHC класса II и LIGHT; MHC класса I и HVEM; MHC класса II и HVEM; MHC класса I и CD40L; MHC класса II и CD40L; MHC класса I и OX40L; MHC класса II и OX40L; MHC класса I и TL1A; MHC класса II и TL1A; MHC класса I и GITRL; MHC класса II и GITRL; MHC класса I и CD30L; или MHC класса II и CD30L.
В некоторых вариантах осуществления aAPC содержит экзогенный полипептид, содержащий сигнал 1, экзогенный полипептид, содержащий сигнал 2, и экзогенный полипептид, содержащий сигнал 3, где сигнал 1, сигнал 2 и сигнал 3 выбраны из следующих комбинаций:
MHC класса I, 4-1BBL и ИЛ-2; MHC класса II, 4-1BBL и ИЛ-2; MHC класса I, CD80 и ИЛ-2; MHC класса II, CD80 и ИЛ-2; MHC класса I, CD86 и ИЛ-2; MHC класса II, CD86 и ИЛ-2; MHC класса I, CD83 и ИЛ-2; MHC класса II, CD83 и ИЛ-2; MHC класса I, CD70 и ИЛ-2; MHC класса II, CD70 и ИЛ-2; MHC класса I, LIGHT и ИЛ-2; MHC класса II, LIGHT и ИЛ-2; MHC класса I, HVEM и ИЛ-2; MHC класса II, HVEM и ИЛ-2; MHC класса I, CD40L и ИЛ-2; MHC класса II, CD40L и ИЛ-2; MHC класса I, OX40L и ИЛ-2; MHC класса II, OX40L и ИЛ-2; MHC класса I, TL1A и ИЛ-2; MHC класса II, TL1A и ИЛ-2; MHC класса I, GITRL и ИЛ-2; MHC класса II, GITRL и ИЛ-2; MHC класса I, CD30L и ИЛ-2; MHC класса II, CD30L и ИЛ-2; MHC класса I, 4-1BBL и ИЛ-15; MHC класса II, 4-1BBL и ИЛ-15; MHC класса I, CD80 и ИЛ-15; MHC класса II, CD80 и ИЛ-15; MHC класса I, CD86 и ИЛ-15; MHC класса II, CD86 и ИЛ-15; MHC класса I, CD83 и ИЛ-15; MHC класса II, CD83 и ИЛ-15; MHC класса I, CD70 и ИЛ-15;MHC класса II, CD70 и ИЛ-15; MHC класса I, LIGHT и ИЛ-15; MHC класса II, LIGHT и ИЛ-15; MHC класса I, HVEM и ИЛ-15; HC класса II, HVEM и ИЛ-15; MHC класса I, CD40L и ИЛ-15; MHC класса II, CD40L и ИЛ-15; MHC класса I, OX40L и ИЛ-15; MHC класса II, OX40L и ИЛ-15; MHC класса I, TL1A и ИЛ-15; MHC класса II, TL1A и ИЛ-15; MHC класса I, GITRL и ИЛ-15; MHC класса II, GITRL и ИЛ-15; MHC класса I, CD30L и ИЛ-15; MHC класса II, CD30L и ИЛ-15; MHC класса I, 4-1BBL и ИЛ-7; MHC класса II, 4-1BBL и ИЛ-7; MHC класса I, CD80 и ИЛ-7; MHC класса II, CD80 и ИЛ-7; MHC класса I, CD86 и ИЛ-7; MHC класса II, CD86 и ИЛ-7; MHC класса I, CD83 и ИЛ-7; MHC класса II, CD83 и ИЛ-7; MHC класса I, CD70 и ИЛ-7; MHC класса II, CD70 и ИЛ-7; MHC класса I, LIGHT и ИЛ-7; MHC класса II, LIGHT и ИЛ-7; MHC класса I, HVEM и ИЛ-7; MHC класса II, HVEM и ИЛ-7; MHC класса I, CD40L и ИЛ-7; MHC класса II, CD40L и ИЛ-7; MHC класса I, OX40L и ИЛ-7; MHC класса II, OX40L и ИЛ-7; MHC класса I, TL1A и ИЛ-7; MHC класса II, TL1A и ИЛ-7; MHC класса I, GITRL и ИЛ-7; MHC класса II, GITRL и ИЛ-7; MHC класса I, CD30L и ИЛ-7; MHC класса II, CD30L и ИЛ-7; MHC класса I, 4-1BBL и ИЛ-12; MHC класса II, 4-1BBL и ИЛ-12; MHC класса I, CD80 и ИЛ-12; MHC класса II, CD80 и ИЛ-12; MHC класса I, CD86 и ИЛ-12; MHC класса II, CD86 и ИЛ-12; MHC класса I, CD83 и ИЛ-12; MHC класса II, CD83 и ИЛ-12; MHC класса I, CD70 и ИЛ-12; MHC класса II, CD70 и ИЛ-12; MHC класса I, LIGHT и ИЛ-12; MHC класса II, LIGHT и ИЛ-12; MHC класса I, HVEM и ИЛ-12; MHC класса II, HVEM и ИЛ-12; MHC класса I, CD40L и ИЛ-12; MHC класса II, CD40L и ИЛ-12; MHC класса I, OX40L и ИЛ-12; MHC класса II, OX40L и ИЛ-12; MHC класса I, TL1A и ИЛ-12; MHC класса II, TL1A и ИЛ-12; MHC класса I, GITRL и ИЛ-12; MHC класса II, GITRL и ИЛ-12; MHC класса I, CD30L и ИЛ-12; MHC класса II, CD30L и ИЛ-12; MHC класса I, 4-1BBL и ИЛ-18; MHC класса II, 4-1BBL и ИЛ-18; MHC класса I, CD80 и ИЛ-18; MHC класса II, CD80 и ИЛ-18; MHC класса I, CD86 и ИЛ-18; MHC класса II, CD86 и ИЛ-18; MHC класса I, CD83 и ИЛ-18; MHC класса II, CD83 и ИЛ-18; MHC класса I, CD70 и ИЛ-18; MHC класса II, CD70 и ИЛ-18; MHC класса I, LIGHT и ИЛ-18; MHC класса II, LIGHT и ИЛ-18; MHC класса I, HVEM и ИЛ-18; MHC класса II, HVEM и ИЛ-18; MHC класса I, CD40L и ИЛ-18; MHC класса II, CD40L и ИЛ-18; MHC класса I, OX40L и ИЛ-18; MHC класса II, OX40L и ИЛ-18; MHC класса I, TL1A и ИЛ-18; MHC класса II, TL1A и ИЛ-18; MHC класса I, GITRL и ИЛ-18; MHC класса II, GITRL и ИЛ-18; MHC класса I, CD30L и ИЛ-18; MHC класса II, CD30L и ИЛ-18; MHC класса I, 4-1BBL и ИЛ-21; MHC класса II, 4-1BBL и ИЛ-21; MHC класса I, CD80 и ИЛ-21; MHC класса II, CD80 и ИЛ-21; MHC класса I, CD86 и ИЛ-21; MHC класса II, CD86 и ИЛ-21; MHC класса I, CD83 и ИЛ-21; MHC класса II, CD83 и ИЛ-21; MHC класса I, CD70 и ИЛ-21; MHC класса II, CD70 и ИЛ-21; MHC класса I, LIGHT и ИЛ-21; MHC класса II, LIGHT и ИЛ-21; MHC класса I, HVEM и ИЛ-21; MHC класса II, HVEM и ИЛ-21; MHC класса I, CD40L и ИЛ-21; MHC класса II, CD40L и ИЛ-21; MHC класса I, OX40L и ИЛ-21; MHC класса II, OX40L и ИЛ-21; MHC класса I, TL1A и ИЛ-21; MHC класса II, TL1A и ИЛ-21; MHC класса I, GITRL и ИЛ-21; MHC класса II, GITRL и ИЛ-21; MHC класса I, CD30L и ИЛ-21; MHC класса II, CD30L и ИЛ-21; MHC класса I, 4-1BBL и ИЛ-4; MHC класса II, 4-1BBL и ИЛ-4; MHC класса I, CD80 и ИЛ-4; MHC класса II, CD80 и ИЛ-4; MHC класса I, CD86 и ИЛ-4; MHC класса II, CD86 и ИЛ-4; MHC класса I, CD83 и ИЛ-4; MHC класса II, CD83 и ИЛ-4; MHC класса I, CD70 и ИЛ-4; MHC класса II, CD70 и ИЛ-4; MHC класса I, LIGHT и ИЛ-4; MHC класса II, LIGHT и ИЛ-4; MHC класса I, HVEM и ИЛ-4; MHC класса II, HVEM и ИЛ-4; MHC класса I, CD40L и ИЛ-4; MHC класса II, CD40L и ИЛ-4; MHC класса I, OX40L и ИЛ-4; MHC класса II, OX40L и ИЛ-4; MHC класса I, TL1A и ИЛ-4; MHC класса II, TL1A и ИЛ-4; MHC класса I, GITRL и ИЛ-4; MHC класса II, GITRL и ИЛ-4; MHC класса I, CD30L и ИЛ-4; MHC класса II, CD30L и ИЛ-4; MHC класса I, 4-1BBL и ИЛ-6; MHC класса II, 4-1BBL и ИЛ-6; MHC класса I, CD80 и ИЛ-6; MHC класса II, CD80 и ИЛ-6; MHC класса I, CD86 и ИЛ-6; MHC класса II, CD86 и ИЛ-6; MHC класса I, CD83 и ИЛ-6; MHC класса II, CD83 и ИЛ-6; MHC класса I, CD70 и ИЛ-6; MHC класса II, CD70 и ИЛ-6; MHC класса I, LIGHT и ИЛ-6; MHC класса II, LIGHT и ИЛ-6; MHC класса I, HVEM и ИЛ-6; MHC класса II, HVEM и ИЛ-6; MHC класса I, CD40L и ИЛ-6; MHC класса II, CD40L и ИЛ-6; MHC класса I, OX40L и ИЛ-6; MHC класса II, OX40L и ИЛ-6; MHC класса I, TL1A и ИЛ-6; MHC класса II, TL1A и ИЛ-6; MHC класса I, GITRL и ИЛ-6; MHC класса II, GITRL и ИЛ-6; MHC класса I, CD30L и ИЛ-6; MHC класса II, CD30L и ИЛ-6; MHC класса I, 4-1BBL и ИЛ-23; MHC класса II, 4-1BBL и ИЛ-23; MHC класса I, CD80 и ИЛ-23; MHC класса II, CD80 и ИЛ-23; MHC класса I, CD86 и ИЛ-23; MHC класса II, CD86 и ИЛ-23; MHC класса I, CD83 и ИЛ-23; MHC класса II, CD83 и ИЛ-23; MHC класса I, CD70 и ИЛ-23; MHC класса II, CD70 и ИЛ-23; MHC класса I, LIGHT и ИЛ-23; MHC класса II, LIGHT и ИЛ-23; MHC класса I, HVEM и ИЛ-23; MHC класса II, HVEM и ИЛ-23; MHC класса I, CD40L и ИЛ-23; MHC класса II, CD40L и ИЛ-23; MHC класса I, OX40L и ИЛ-23; MHC класса II, OX40L и ИЛ-23; MHC класса I, TL1A и ИЛ-23; MHC класса II, TL1A и ИЛ-23; MHC класса I, GITRL и ИЛ-23; MHC класса II, GITRL и ИЛ-23; MHC класса I, CD30L и ИЛ-23; MHC класса II, CD30L и ИЛ-23; MHC класса I, 4-1BBL и ИЛ-27; MHC класса II, 4-1BBL и ИЛ-27; MHC класса I, CD80 и ИЛ-27; MHC класса II, CD80 и ИЛ-27; MHC класса I, CD86 и ИЛ-27; MHC класса II, CD86 и ИЛ-27; MHC класса I, CD83 и ИЛ-27; MHC класса II, CD83 и ИЛ-27; MHC класса I, CD70 и ИЛ-27; MHC класса II, CD70 и ИЛ-27; MHC класса I, LIGHT и ИЛ-27; MHC класса II, LIGHT и ИЛ-27; MHC класса I, HVEM и ИЛ-27; MHC класса II, HVEM и ИЛ-27; MHC класса I, CD40L и ИЛ-27; MHC класса II, CD40L и ИЛ-27; MHC класса I, OX40L и ИЛ-27; MHC класса II, OX40L и ИЛ-27; MHC класса I, TL1A и ИЛ-27; MHC класса II, TL1A и ИЛ-27; MHC класса I, GITRL и ИЛ-27; MHC класса II, GITRL и ИЛ-27; MHC класса I, CD30L и ИЛ-27; MHC класса II, CD30L и ИЛ-27; MHC класса I, 4-1BBL и ИЛ-17; MHC класса II, 4-1BBL и ИЛ-17; MHC класса I, CD80 и ИЛ-17; MHC класса II, CD80 и ИЛ-17; MHC класса I, CD86 и ИЛ-17; MHC класса II, CD86 и ИЛ-17; MHC класса I, CD83 и ИЛ-17; MHC класса II, CD83 и ИЛ-17; MHC класса I, CD70 и ИЛ-17; MHC класса II, CD70 и ИЛ-17; MHC класса I, LIGHT и ИЛ-17; MHC класса II, LIGHT и ИЛ-17; MHC класса I, HVEM и ИЛ-17; MHC класса II, HVEM и ИЛ-17; MHC класса I, CD40L и ИЛ-17; MHC класса II, CD40L и ИЛ-17; MHC класса I, OX40L и ИЛ-17; MHC класса II, OX40L и ИЛ-17; MHC класса I, TL1A и ИЛ-17; MHC класса II, TL1A и ИЛ-17; MHC класса I, GITRL и ИЛ-17; MHC класса II, GITRL и ИЛ-17; MHC класса I, CD30L и ИЛ-17; MHC класса II, CD30L и ИЛ-17; MHC класса I, 4-1BBL и ИЛ-10; MHC класса II, 4-1BBL и ИЛ-10; MHC класса I, CD80 и ИЛ-10; MHC класса II, CD80 и ИЛ-10; MHC класса I, CD86 и ИЛ-10; MHC класса II, CD86 и ИЛ-10; MHC класса I, CD83 и ИЛ-10; MHC класса II, CD83 и ИЛ-10; MHC класса I, CD70 и ИЛ-10; MHC класса II, CD70 и ИЛ-10; MHC класса I, LIGHT и ИЛ-10; MHC класса II, LIGHT и ИЛ-10; MHC класса I, HVEM и ИЛ-10; MHC класса II, HVEM и ИЛ-10; MHC класса I, CD40L и ИЛ-10; MHC класса II, CD40L и ИЛ-10; MHC класса I, OX40L и ИЛ-10; MHC класса II, OX40L и ИЛ-10; MHC класса I, TL1A и ИЛ-10; MHC класса II, TL1A и ИЛ-10; MHC класса I, GITRL и ИЛ-10; MHC класса II, GITRL и ИЛ-10; MHC класса I, CD30L и ИЛ-10; MHC класса II, CD30L и ИЛ-10; MHC класса I, 4-1BBL и TGF-бета; MHC класса II, 4-1BBL и TGF-бета; MHC класса I, CD80 и TGF-бета; MHC класса II, CD80 и TGF-бета; MHC класса I, CD86 и TGF-бета; MHC класса II, CD86 и TGF-бета; MHC класса I, CD83 и TGF-бета; MHC класса II, CD83 и TGF-бета; MHC класса I, CD70 и TGF-бета; MHC класса II, CD70 и TGF-бета; MHC класса I, LIGHT и TGF-бета; MHC класса II, LIGHT и TGF-бета; MHC класса I, HVEM и TGF-бета; MHC класса II, HVEM и TGF-бета; MHC класса I, CD40L и TGF-бета; MHC класса II, CD40L и TGF-бета; MHC класса I, OX40L и TGF-бета; MHC класса II, OX40L и TGF-бета; MHC класса I, TL1A и TGF-бета; MHC класса II, TL1A и TGF-бета; MHC класса I, GITRL и TGF-бета; MHC класса II, GITRL и TGF-бета; MHC класса I, CD30L и TGF-бета; MHC класса II, CD30L и TGF-бета; MHC класса I, 4-1BBL и ИФН-гамма; MHC класса II, 4-1BBL и ИФН-гамма; MHC класса I, CD80 и ИФН-гамма; MHC класса II, CD80 и ИФН-гамма; MHC класса I, CD86 и ИФН-гамма; MHC класса II, CD86 и ИФН-гамма; MHC класса I, CD83 и ИФН-гамма; MHC класса II, CD83 и ИФН-гамма; MHC класса I, CD70 и ИФН-гамма; MHC класса II, CD70 и ИФН-гамма; MHC класса I, LIGHT и ИФН-гамма; MHC класса II, LIGHT и ИФН-гамма; MHC класса I, HVEM и ИФН-гамма; MHC класса II, HVEM и ИФН-гамма; MHC класса I, CD40L и ИФН-гамма; MHC класса II, CD40L и ИФН-гамма; MHC класса I, OX40L и ИФН-гамма; MHC класса II, OX40L и ИФН-гамма; MHC класса I, TL1A и ИФН-гамма; MHC класса II, TL1A и ИФН-гамма; MHC класса I, GITRL и ИФН-гамма; MHC класса II, GITRL и ИФН-гамма; MHC класса I, CD30L и ИФН-гамма; MHC класса II, CD30L и ИФН-гамма; MHC класса I, 4-1BBL и ИЛ-1 бета; MHC класса II, 4-1BBL и ИЛ-1 бета; MHC класса I, CD80 и ИЛ-1 бета; MHC класса II, CD80 и ИЛ-1 бета; MHC класса I, CD86 и ИЛ-1 бета; MHC класса II, CD86 и ИЛ-1 бета; MHC класса I, CD83 и ИЛ-1 бета; MHC класса II, CD83 и ИЛ-1 бета; MHC класса I, CD70 и ИЛ-1 бета; MHC класса II, CD70 и ИЛ-1 бета; MHC класса I, LIGHT и ИЛ-1 бета; MHC класса II, LIGHT и ИЛ-1 бета; MHC класса I, HVEM и ИЛ-1 бета; MHC класса II, HVEM и ИЛ-1 бета; MHC класса I, CD40L и ИЛ-1 бета; MHC класса II, CD40L и ИЛ-1 бета; MHC класса I, OX40L и ИЛ-1 бета; MHC класса II, OX40L и ИЛ-1 бета; MHC класса I, TL1A и ИЛ-1 бета; MHC класса II, TL1A и ИЛ-1 бета; MHC класса I, GITRL и ИЛ-1 бета; MHC класса II, GITRL и ИЛ-1 бета; MHC класса I, CD30L и ИЛ-1 бета; MHC класса II, CD30L и ИЛ-1 бета; MHC класса I, 4-1BBL и ГМ-КСФ; MHC класса II, 4-1BBL и ГМ-КСФ; MHC класса I, CD80 и ГМ-КСФ; MHC класса II, CD80 и ГМ-КСФ; MHC класса I, CD86 и ГМ-КСФ; MHC класса II, CD86 и ГМ-КСФ; MHC класса I, CD83 и ГМ-КСФ; MHC класса II, CD83 и ГМ-КСФ; MHC класса I, CD70 и ГМ-КСФ; MHC класса II, CD70 и ГМ-КСФ; MHC класса I, LIGHT и ГМ-КСФ; MHC класса II, LIGHT и ГМ-КСФ; MHC класса I, HVEM и ГМ-КСФ; MHC класса II, HVEM и ГМ-КСФ; MHC класса I, CD40L и ГМ-КСФ; MHC класса II, CD40L и ГМ-КСФ; MHC класса I, OX40L и ГМ-КСФ; MHC класса II, OX40L и ГМ-КСФ; MHC класса I, TL1A и ГМ-КСФ; MHC класса II, TL1A и ГМ-КСФ; MHC класса I, GITRL и ГМ-КСФ; MHC класса II, GITRL и ГМ-КСФ; MHC класса I, CD30L и ГМ-КСФ; MHC класса II, CD30L и ГМ-КСФ; MHC класса I, 4-1BBL и ИЛ-25; MHC класса II, 4-1BBL и ИЛ-25; MHC класса I, CD80 и ИЛ-25; MHC класса II, CD80 и ИЛ-25; MHC класса I, CD86 и ИЛ-25; MHC класса II, CD86 и ИЛ-25; MHC класса I, CD83 и ИЛ-25; MHC класса II, CD83 и ИЛ-25; MHC класса I, CD70 и ИЛ-25; MHC класса II, CD70 и ИЛ-25; MHC класса I, LIGHT и ИЛ-25; MHC класса II, LIGHT и ИЛ-25; MHC класса I, HVEM и ИЛ-25; MHC класса II, HVEM и ИЛ-25; MHC класса I, CD40L и ИЛ-25; MHC класса II, CD40L и ИЛ-25; MHC класса I, OX40L и ИЛ-25; MHC класса II, OX40L и ИЛ-25; MHC класса I, TL1A и ИЛ-25; MHC класса II, TL1A и ИЛ-25; MHC класса I, GITRL и ИЛ-25; MHC класса II, GITRL и ИЛ-25; MHC класса I, CD30L и ИЛ-25; или MHC класса II, CD30L и ИЛ-25.
Следует понимать, что в случае любой из указанных выше комбинаций сигнала 1, сигнала 2 и/или сигнала 3 молекула MHC класса I может являться любым антигенпрезентирующим полипептидом MHC класса I или одноцепочечным слитым полипептидом MHC класса I, представленными в настоящем описании. Аналогично, следует понимать, что в случае любой из указанных выше комбинаций сигнала 1, сигнала 2 и/или сигнала 3 молекула MHC класса II может являться любым антигенпрезентирующим полипептидом MHC класса II или одноцепочечным слитым полипептидом MHC класса I, представленными в настоящем описании
Молекулы клеточной адгезии
В некоторых вариантах осуществления в дополнение к сигналу 1, сигналу 2 и/или сигналу 3, aAPC, представленные в настоящем описании, дополнительно содержат на поверхности клетки один или более экзогенных полипептидов, содержащих молекулы клеточной адгезии. Молекулы клеточной адгезии дополнительно облегчают взаимодействие между T-клетками и aAPC. В некоторых вариантах осуществления молекулы клеточной адгезии опосредуют или облегчают образование иммунологического синапса. В некоторых вариантах осуществления одна или более молекул клеточной адгезии выбраны из группы, состоящей из ICAM4/LW, CD36, CD58/LFA3, CD47, VLA4, BCAM/Lu, CD44, CD99/MIC2, ICAM1, JAM1 и CD147 или любой их комбинации.
В некоторых вариантах осуществления aAPC содержит на своей поверхности экзогенный полипептид, содержащий сигнал 1, экзогенный полипептид, содержащий сигнал 2, и один или более экзогенных полипептидов, содержащих молекулы клеточной адгезии. В некоторых вариантах осуществления aAPC содержит на своей поверхности экзогенный полипептид, содержащий сигнал 1, экзогенный полипептид, содержащий сигнал 2, экзогенный полипептид, содержащий сигнал 3, и один или более экзогенных полипептидов, содержащих молекулы клеточной адгезии.
В некоторых вариантах осуществления aAPC содержит на своей поверхности более одного экзогенного полипептида, содержащего более одного сигнала 1, экзогенный полипептид, содержащий сигнал 2, и один или более экзогенных полипептидов, содержащих молекулы клеточной адгезии. В некоторых вариантах осуществления aAPC содержит на своей поверхности более одного экзогенного полипептида, содержащего более одного сигнала 1, экзогенный полипептид, содержащий сигнал 2, экзогенный полипептид, содержащий сигнал 3, и один или более экзогенных полипептидов, содержащих молекулы клеточной адгезии.
В некоторых вариантах осуществления aAPC содержит на своей поверхности экзогенный полипептид, содержащий сигнал 1, более одного экзогенного полипептида, содержащего более одного сигнала 2, и один или более экзогенных полипептидов, содержащих молекулы клеточной адгезии. В некоторых вариантах осуществления aAPC содержит на своей поверхности экзогенный полипептид, содержащий сигнал 1, более одного экзогенного полипептида, содержащего более одного сигнала 2, экзогенный полипептид, содержащий сигнал 3, и один или более экзогенных полипептидов, содержащих молекулы клеточной адгезии.
В некоторых вариантах осуществления aAPC содержит на своей поверхности экзогенный полипептид, содержащий сигнал 1, экзогенный полипептид, содержащий сигнал 2, более одного экзогенного полипептида, содержащего более одного сигнала 3, и один или более экзогенных полипептидов, содержащих молекулы клеточной адгезии.
В некоторых вариантах осуществления aAPC содержит на своей поверхности более одного экзогенного полипептида, содержащего более одного сигнала 1, экзогенный полипептид, содержащий сигнал 2, более одного экзогенного полипептида, содержащего более одного сигнала 3, и один или более экзогенных полипептидов, содержащих молекулы клеточной адгезии.
В некоторых вариантах осуществления aAPC содержит на своей поверхности более одного экзогенного полипептида, содержащего более одного сигнала 1, более одного экзогенного полипептида, содержащего более одного сигнала 2, экзогенного полипептида, содержащего сигнал 3, и один или более экзогенных полипептидов, содержащих молекулы клеточной адгезии.
В некоторых вариантах осуществления aAPC содержит на своей поверхности более одного экзогенного полипептида, содержащего более одного сигнала 1, более одного экзогенного полипептида, содержащего более одного сигнала 2, более одного экзогенного полипептида, содержащего более одного сигнала 3, и один или более экзогенных полипептидов, содержащих молекулы клеточной адгезии.
В некоторых вариантах осуществления один или более экзогенных полипептидов, содержащих сигнал 1, один или более экзогенных полипептидов, содержащих сигнал 2, один или более экзогенных полипептидов, содержащих сигнал 3, и один или более экзогенных полипептидов, содержащих молекулы клеточной адгезии, выбраны из экзогенных полипептидов, приведенных в таблице 8.
Таблица 8. Молекулы клеточной адгезии
В вариантах осуществления, если aAPC содержит полипептид, содержащий сигнал 1, и полипептид, содержащий сигнал 2, полипептиды могут находиться на поверхности aAPC в разных конфигурациях, например, как показано на фиг. 17A. В некоторых вариантах осуществления полипептид, содержащий сигнал 1, и полипептид, содержащий сигнал 2, присутствуют в виде независимых, отдельных полипептидов (например, каждый полипептид содержит якорь) и, например, кодируются нуклеиновыми кислотами, находящимися на двух отдельных лентивирусных векторах, используемые для серийной трансдукции или котрансдукции эритроидной клетки-предшественника (два лентивирусных вектора).
В некоторых вариантах осуществления полипептид, содержащий сигнал 1, и полипептид, содержащий сигнал 2, присутствуют в виде слитого полипептида, например, соединенного или связанного посредством линкерной последовательности, где каждый полипептид содержит якорь (сигнал 1+2 в виде слитого пептида). В этих вариантах осуществления слитый полипептид кодируется одним лентивирусным вектором, используемым для трансдукции эритроидной клетки-предшественника.
В некоторых вариантах осуществления полипептид, содержащий сигнал 1, и полипептид, содержащий сигнал 2, присутствуют на поверхности клетки (например, каждый полипептид содержит якорь), где полипептиды разделены вирусным элементом 2A. В этой области известно множество элементов 2A, и их можно использовать, как представлено в настоящем описании, включая T2A, P2A, E2A и F2A (см., например, Liu et al. (2017) Sci. Rep. 7(1): 2193, включенную в настоящее описание в качестве ссылки в полном объеме). В некоторых вариантах осуществления полипептид, содержащий сигнал 1, и полипептид, содержащий сигнал 2, разделены T2A (меткой Skip T2A). В этих вариантах осуществления полипептиды кодируются одним лентивирусным вектором, используемым для трансдукции эритроидной клетки-предшественника.
В вариантах осуществления, если aAPC содержит полипептид, содержащий сигнал 1, полипептид, содержащий сигнал 2, и полипептид, содержащий сигнал 3, полипептиды могут присутствовать на поверхности aAPC в разных конфигурациях, например, как показано на фиг. 17. В некоторых вариантах осуществления полипептид, содержащий сигнал 1, и полипептид, содержащий сигнал 2, находится в форме слитого полипептида, например, соединенного линкера, и полипептид, содержащий сигнал 3, является отдельным полипептидом (вариант 1). В некоторых вариантах осуществления полипептид, содержащий сигнал 1, и полипептид, содержащий сигнал 3, находится в форме слитого полипептида, например, соединенного линкером, и полипептид, содержащий сигнал 2, является отдельным полипептидом (вариант 2). В некоторых вариантах осуществления полипептид, содержащий сигнал 2, и полипептид, содержащий сигнал 3, находятся в форме слитого полипептида, например, соединенного линкером, и полипептид, содержащий сигнал 1, является отдельным полипептидом (вариант 3). Следует понимать, что в этих вариантах осуществления при получении aAPC слитый полипептид (содержащий сигналы 1 и 2, сигналы 2 и 3 или сигналы 1 и 3) может кодироваться одним лентивирусным вектором, и отдельный полипептид (сигнал 1, сигнал 2 или сигнал 3) может кодироваться вторым лентивирусным вектором.
В некоторых вариантах осуществления связь или линкер между сигналом 1 и сигналом 2, между сигналом 1 и сигналом 3 или между сигналом 2 и сигналом 3 является линкером поли-GlySer. В некоторых вариантах осуществления связь или линкер между сигналом 1 и сигналом 2, между сигналом 1 и сигналом 3 или между сигналом 2 и сигналом 3 является шноркельным линкером.
Примеры слитых конструкций, содержащих сигнал 1 и сигнал 2, приведены в таблице 9 ниже.
Таблица 9. Конструкции
В другом аспекте настоящее изобретение относится к любой из полипептидных последовательностей, соответствующих слитому белку, приведенному в таблице 9. В одном из вариантов осуществления слитый полипептид содержит лидерную последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-бета-2-микроглобулин (B2M)-HLA-A*02:01, приведенный в SEQ ID NO: 843. В одном из вариантов осуществления слитый полипептид содержит B2ML-пептид E711-19 HPV16-B2M-HLA-A*02:01 Y84A, приведенный в SEQ ID NO: 844. В одном из вариантов осуществления слитый полипептид содержит B2ML - пептид E711-19 HPV16-B2M-HLA-A*02:01 Y84C, приведенный в SEQ ID NO: 845. В одном из вариантов осуществления слитый полипептид содержит B2ML-пептид E711-19 HPV16 -B2M-HLA-A*02:01-гликофорин A (GPA), приведенный в SEQ ID NO: 726. В одном из вариантов осуществления слитый полипептид содержит B2ML-пептид E711-19 HPV16-B2M-HLA-A*02:01 Y84A-GPA, приведенный в SEQ ID NO: 846. В одном из вариантов осуществления слитый полипептид содержит B2ML-пептид E711-19 HPV16-B2M-HLA-A*02:01 Y84C -GPA, приведенный в SEQ ID NO: 847. В одном из вариантов осуществления слитый полипептид содержит лидерную последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-линкер-бета-2-микроглобулин (B2M)-линкер-HLA-A*02:01 Y84A -линкер-GPA-T2A-сигнальный пептид GPA-укороченный с N-конца 4-1BBL-линкер v17-GPA, приведенный в SEQ ID NO: 848. В одном из вариантов осуществления слитый полипептид содержит лидерную последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-линкер-бета-2-микроглобулин (B2M)-линкер-HLA-A*02:01 Y84A-линкер-GPA-T2A, приведенный в SEQ ID NO:849. В одном из вариантов осуществления слитый полипептид содержит SMIM1-линкер-IL-12p40-линкер-IL-12p35, приведенный в SEQ ID NO: 873. В одном из вариантов осуществления слитый полипептид содержит сигнальный пептид GPA-4-1BBL-линкер v17-GPA, приведенный в SEQ ID NO: 850. В одном из вариантов осуществления слитый полипептид содержит сигнальный пептид GPA-укороченный с N-конца 4-1BBL-линкер-GPA-T2A-лидерная последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-линкер-бета-2-микроглобулин-линкер-HLA-A*02:01 Y84A-линкер-GPA, приведенный в SEQ ID NO: 854. В одном из вариантов осуществления слитый полипептид содержит сигнальный пептид GPA-укороченный с N-конца 4-1BBL-линкер-GPA-T2A, приведенный в SEQ ID NO: 855. В одном из вариантов осуществления слитый полипептид содержит T2A-лидерная последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-линкер-бета-2-микроглобулин-линкер-HLA-A*02:01 Y84A-линкер-GPA, приведенный в SEQ ID NO: 856. В одном из вариантов осуществления слитый полипептид содержит лидерную последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-линкер-бета-2-микроглобулин (B2M)-линкер-HLA-A*02:01 Y84A-линкер-GPA-линкер-полноразмерный 4-1BBL, приведенный в SEQ ID NO: 857. В одном из вариантов осуществления слитый полипептид содержит лидерную последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-линкер-бета-2-микроглобулин (B2M)-линкер-HLA-A*02:01 Y84A-линкер-GPA-шноркельный линкер-линкер-укороченный с N-конца 4-1BBL, приведенный в SEQ ID NO: 859. В одном из вариантов осуществления слитый полипептид содержит лидерную последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-линкер-бета-2-микроглобулин (B2M)-линкер-HLA-A*02:01 Y84A-линкер-GPA-линкер-SMIM1-линкер-IL-12p40-линкер-IL-12p35, приведенный в SEQ ID NO: 860. В одном из вариантов осуществления слитый полипептид содержит лидерную последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-линкер-бета-2-микроглобулин (B2M)-линкер-HLA-A*02:01 Y84A-линкер-GPA-шноркельный линкер-SMIM1-линкер-IL-12p40-линкер-IL-12p35, приведенный в SEQ ID NO: 863. В одном из вариантов осуществления слитый полипептид содержит лидерную последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-линкер-бета-2-микроглобулин (B2M)-линкер-HLA-A*02:01 Y84A-линкер-GPA-шноркельный линкер-линкер-IL-12p40-линкер-IL-12p35, приведенный в SEQ ID NO: 864. В одном из вариантов осуществления слитый полипептид содержит Лидерная последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-линкер-бета-2-микроглобулин (B2M)-линкер-HLA-A*02:01 Y84A-линкер-GPA-T2A-GPA сигнальный пептид-IL-7-линкер v14-GPA, приведенный в SEQ ID NO: 865. В одном из вариантов осуществления слитый полипептид содержит лидерную последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-линкер-бета-2-микроглобулин (B2M)-линкер-HLA-A*02:01 Y84A-линкер-GPA-T2A, приведенный в SEQ ID NO: 849. В одном из вариантов осуществления слитый полипептид содержит сигнальный пептид GPA-IL-7-линкер v14-GPA, приведенный в SEQ ID NO: 866. В одном из вариантов осуществления слитый полипептид содержит лидерную последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-линкер-бета-2-микроглобулин (B2M)-линкер-HLA-A*02:01 Y84A-линкер-GPA-T2A-сигнальный пептид GPA-IL-15-линкер-IL-15Ra-линкер v14-GPA, приведенный в SEQ ID NO: 868. В одном из вариантов осуществления слитый полипептид содержит сигнальный пептид GPA-IL-15-линкер-IL-15Ra-линкер v14-GPA, приведенный в SEQ ID NO: 869. В одном из вариантов осуществления слитый полипептид содержит лидерную последовательность бета-2-микроглобулина (B2ML)-пептид E711-19 HPV16-линкер-бета-2-микроглобулин (B2M)-линкер-HLA-A*02:01 Y84A-линкер-GPA-T2A-SMIM1-линкер-IL-12p40-линкер-IL-12p35, приведенный в SEQ ID NO: 872.
В некоторых вариантах осуществления настоящее изобретение относится к нуклеиновой кислоте, кодирующей слитый полипептид, содержащий аминокислотную последовательность, приведенную в таблице 9. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к аминокислотной последовательности, приведенной в таблице 9. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 843. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 844. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 845. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 726. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 846. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 847. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 848. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO:849. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 850. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 854. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 855. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 856. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 857. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 859. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 860. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 863. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 864. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 865. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 849. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 866. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 868. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 869. В некоторых вариантах осуществления нуклеиновая кислота кодирует слитый полипептид, где слитый полипептид имеет по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности по отношению к SEQ ID NO: 872.
В некоторых вариантах осуществления полипептид, содержащий 4-1BBL, является укороченным с N-конца 4-1BBL (SEQ ID NO: 851). В некоторых вариантах осуществления полипептид, содержащий 4-1BBL, является полноразмерным 4-1BBL.
Настоящее изобретение также относится к aAPC, содержащей первый экзогенный полипептид и второй экзогенный полипептид, где первый экзогенный полипептид содержит слитый белок, содержащий экзогенный антигенный пептид, экзогенный антигенпрезентирующий полипептид и мембранный якорный полипептид, где второй экзогенный полипептид содержит один или более полипептидов, выбранных из группы, состоящей из: экзогенного костимуляторного полипептида, экзогенного коингибиторного полипептида, экзогенного полипептида для экспансии Treg и экзогенного цитокинового полипептида, и где aAPC получают способом, включающим встраивание экзогенной нуклеиновой кислоты, кодирующей первый экзогенный полипептид, в ядросодержащую клетку (например, ядросодержащую эритроидную клетку-предшественника); встраивание экзогенной нуклеиновой кислоты, кодирующей второй экзогенный полипептид, в ядросодержащую клетку (например, ядросодержащую эритроидную клетку-предшественника); и культивирование ядросодержащей клетки (например, ядросодержащей эритроидной клетки-предшественника) в условиях, подходящих для энуклеации и для получения первого экзогенного полипептида и второго экзогенного полипептида. В некоторых вариантах осуществления экзогенный антигенный полипептид выбран из антигенного полипептида, приведенного в таблице 1 или таблицах 14-24. В некоторых вариантах осуществления первый экзогенный полипептид содержит слитый белок, содержащий экзогенный антигенный пептид, слитый с экзогенным антигенпрезентирующим полипептидом, слитым с мембранным якорным полипептидом. В некоторых вариантах осуществления экзогенный антигенный полипептид выбран из группы, состоящей из: меланома-ассоциированного антигена-A (MAGE-A), антигенов протеаз гранул нейтрофилов, антигенов NY-ESO-1/LAGE-2, антигенов теломеразы, антигенов миелинового олигодендроцитарного гликопротеина (MOG), антигенов гликопротеина 100 (gp100), антигенов вируса Эпштейна-Барр (EBV), антигенов вируса папилломы человека (HPV) и антигенов вируса гепатита B (HBV). В некоторых вариантах осуществления экзогенный антигенный полипептид дополнительно содержит лидерную последовательность. В некоторых вариантах осуществления лидерная последовательность является лидерной последовательностью бета-2-микроглобулин (B2M) или сигнальным пептидом GPA. В некоторых вариантах осуществления мембранный якорь является гликофорином A (GPA) или его фрагментом или небольшим интегральным мембранным белком 1 (SMIM1). В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является полипептидом MHC класса I, одноцепочечным слитым белком MHC класса I, полипептидом MHC класса II или одноцепочечным слитым белком MHC класса II. В некоторых вариантах осуществления полипептид MHC класса I выбран из группы, состоящей из: HLA-A, HLA-B и HLA-C.В некоторых вариантах осуществления полипептид MHC класса II выбран из группы, состоящей из: HLA-DPα, HLA-DPβ, HLA-DM, HLA-DOA, HLA-DOB, HLA-DQα, HLA-DQβ, HLA-DRα и HLA-DRβ. В некоторых вариантах осуществления одноцепочечный слитый белок MHC класса I содержит α-цепь и β2m-цепь и, необязательно, якорный полипептид. В некоторых вариантах осуществления экзогенный антигенный полипептид соединяют с одноцепочечным слитым белком MHC класса I с помощью линкера. В некоторых вариантах осуществления линкер является расщепляемым линкером. В некоторых вариантах осуществления одноцепочечный слитый белок MHC класса II содержит якорь, α-цепь и, необязательно, β-цепь. В некоторых вариантах осуществления экзогенный антигенный полипептид соединяют с одноцепочечным слитым белком MHC класса II с помощью линкера. В некоторых вариантах осуществления линкер является расщепляемым линкером. В некоторых вариантах осуществления экзогенный цитокиновый полипептид выбран из группы, состоящей из: ИЛ-2, ИЛ-15, ИЛ-15Rα, слитого с ИЛ-15, ИЛ-7, ИЛ-12, ИЛ-18, ИЛ-21, ИЛ-4, ИЛ-6, ИЛ-23, ИЛ-27, ИЛ-17, ИЛ-10, TGF-бета, ИФН-гамма, ИЛ-1 бета, ГМ-КСФ и ИЛ-25. В некоторых вариантах осуществления экзогенный костимуляторный полипептид выбран из группы, состоящей из 4-1BBL, LIGHT, антитела против CD28, CD80, CD86, CD70, OX40L, GITRL, TIM4, SLAM, CD48, CD58, CD83, CD155, CD112, ИЛ-15Rα, слитого с ИЛ-15, ИЛ-21, ICAM-1, лиганда LFA-1, антитела против CD3 и их комбинации. В некоторых вариантах осуществления экзогенный коингибиторный полипептид выбран из группы, состоящей из: ИЛ-35, ИЛ-10, VSIG-3 и агониста LAG3. В некоторых вариантах осуществления экзогенный полипептид для экспансии Treg выбран из группы, состоящей из: CD25-специфического ИЛ-2, TNFR2-специфического ФНОα, агониста против DR3 (VEGI/TL1A-специфического), 4-1BBL, TGFβ и их комбинации. В некоторых вариантах осуществления aAPC дополнительно содержит экзогенный полипептид, содержащий молекулу адгезии. В некоторых вариантах осуществления молекула адгезии выбрана из группы, состоящей из: ICAM4/LW, CD36, CD58/LFA3, CD47, VLA4, BCAM/Lu, CD44, CD99/MIC2, ICAM1 и CD147. В некоторых вариантах осуществления aAPC по п.90, где экзогенная нуклеиновая кислота включает ДНК или РНК. В некоторых вариантах осуществления стадия встраивания включает вирусную трансдукцию или электропорацию. В некоторых вариантах осуществления стадия встраивания включает использование одного или более из: опосредованного липосомами переноса, аденовируса, аденоассоциированного вируса, вируса герпеса, вектора на основе ретровируса, липофекции и лентивирусного вектора. В некоторых вариантах осуществления стадия встраивания включает встраивание первой экзогенной нуклеиновой кислоты, кодирующей первый экзогенный полипептид, и второй экзогенной нуклеиновой кислоты, кодирующей второй экзогенный полипептид, посредством трансдукции с использованием лентивирусного вектора, где первая экзогенная нуклеиновая кислота и вторая экзогенная нуклеиновая кислота содержатся в одном лентивирусном векторе. В некоторых вариантах осуществления стадия встраивания включает встраивание первой экзогенной нуклеиновой кислоты, кодирующей первый экзогенный полипептид, посредством трансдукции с использованием первого лентивирусного вектора и встраивание второй экзогенной нуклеиновой кислоты, кодирующей второй экзогенный полипептид, посредством трансдукции с использованием второго лентивирусного вектора. В некоторых вариантах осуществления первая и/или вторая экзогенная нуклеиновая кислота содержит промотор, выбранный из группы, состоящей из: промотора бета-глобина, промотора вируса стволовых клеток мыши (MSCV), промотора вируса лейкоза гиббонов (GALV), промотора фактора элонгации 1 альфа человека (EF1-альфа), предраннего энхансера CMV, промотора бета-актина кур (CAG) и промотора фосфоглицераткиназы 1 человека (PGK).
Иммунологический синапс
Как представлено в настоящем описании, сконструированные эритроидные клетки (т.е. aAPC) по настоящему изобретению обеспечивают множество преимуществ по сравнению с использованием сферических наночастиц, таких как жесткие aAPC на основе частиц. Молекулярная подвижность (например, движение лигандов в клеточной мембране) и молекулярная кластеризация являются важными признаками образования иммунологического синапса. Мембрана aAPC, представленных в настоящем описании, является гораздо более динамичной и текучей, чем внешняя поверхность наночастицы и, таким образом, делает возможной гораздо более эффективную молекулярную реорганизацию и кластеризацию MHC во время образования иммунологического синапса или опосредование трогоцитоза. Кроме того, в отличие от небольшого размера наночастиц, aAPC по настоящему изобретению обеспечивают большую площадь поверхности для образования функциональных кластеров микронного масштаба в иммунологическом синапсе. В некоторых вариантах осуществления aAPC, представленные в настоящем описании, сконструированы для образования иммунологического синапса, где иммунологический синапс облегчает активацию T-клеток.
Иммунологический синапс (или иммунный синапс, или IS) представляет собой область контакта между антигенпрезентирующей клеткой и лимфоцитом, таким как T/B-клетка или NK-клетка. Иммунологический синапс может состоять из молекул, участвующих в активации T-клетки, составляющих типичные паттерны, называемые кластерами активации. В соответствии с лучше всего изученной моделью, иммунный синапс также известен как супрамолекулярный кластер активации (SMAC) (Monks et al., Nature 1998, 395 (6697): 82-86, включенная в настоящее описание в качестве ссылки в полном объеме), состоящий из концентрических колец (центральных, периферических или дистальных областей), каждое из которых содержит сегрегированные кластеры белков. Молекулы в иммунологическом синапсе включают антигенпрезентирующие молекулы (например, молекулу MHC класса I или MHC класса II), молекулы адгезии, костимуляторные молекулы и коингибиторные молекулы.
Иммунологический синапс является динамической структурой, образовавшейся после кластеризации T-клеточных рецепторов в микрокластеры, которые в конечном итоге двигаются к центру иммунологического синапса. Пространственные и временные изменения этих молекул в области контакта T-лимфоцита и APC регулируют структуру иммунного синапса и T-лимфоцитарный иммунный ответ. В основном, эффективная активация CD4+ и CD8+ T-клеток ассоциирована с образованием функционального иммунологического синапса (Y. Kaizuka, et al. Proc. Natl. Acad. Sci. U.S.A., 104 (2007), pp. 20296-20301, в полном объеме включенная в настоящее описание в качестве ссылки).
В некоторых вариантах осуществления настоящее изобретение относится к aAPC, которые могут образовывать иммунологический синапс между aAPC и иммунной клеткой, такой как T-клетка, B-клетка или NK-клетка. В некоторых вариантах осуществления aAPC по настоящему изобретению имеют способность собирать более одной молекулы MHC в иммунологический синапс.
Исходное взаимодействие в иммунологическом синапсе происходит между функционально-связанным антигеном лимфоцитов 1 (LFA-1), находящимся в периферическом SMAC T-клетки, и интегриновыми молекулами адгезии (такими как ICAM-1 или ICAM-2) на APC. После связывания с APC T-клетка может удлинять псевдоподии и сканировать поверхность клетки-мишени для обнаружения специфического комплекса пептид-MHC. Процесс образования начинается с того, что T-клеточный рецептор (TCR) связывается с комплексом пептид-MHC на антигенпрезентирующей клетке и инициирует активацию передачи сигнала через образование микрокластеров/липидных рафтов (Varma et al., Immunity. 2006 Jul;25(1):117-27, включенная в настоящее описание в качестве ссылки в полном объеме).
Это является неожиданным открытием в соответствии с настоящим изобретением, что сконструированные эритроидные клетки или безъядерные клетки (т.е. aAPC) по настоящему изобретению могут инициировать и образовывать активный иммунологический синапс, несмотря на отсутствие эндогенного ICAM1 на своей поверхности. Без желания быть связанными какой-либо теорией, полагают, что другие интегрины, такие как JAM1 и/или ICAM-4, от природы находящиеся на поверхности эритроидных клеток, могут выполнять роль ICAM-1 в образовании функционального иммунологического синапса.
Таким образом, в некоторых вариантах осуществления aAPC по настоящему изобретению содержат один или более экзогенных полипептидов клеточной адгезии для опосредования или облегчения образования иммунологического синапса. В некоторых вариантах осуществления одна или более молекул клеточной адгезии выбраны из группы, состоящей из ICAM4/LW, CD36, CD58/LFA3, CD47, VLA4, BCAM/Lu, CD44, CD99/MIC2, ICAM1, JAM1 и CD147 или любой их комбинации.
Преимуществом настоящего изобретения является то, что сконструированные эритроидные клетки (т.е. aAPC), представленные в настоящем описании, имеют текучую клеточную мембрану, обеспечивающую динамическое молекулярное движение и, таким образом, делают возможной эффективную молекулярную реорганизацию и кластеризацию MHC, что необходимо для стимуляции T-клеток. Передача сигнала инициируется и поддерживается в микрокластерах TCR, образующихся непрерывно на периферии иммунологического синапса и транспортирующихся к центру для образования центрального SMAC. Во время образования центрального SMAC микрокластеры могут двигаться независимо друг от друга и могут сливаться с образованием более крупных кластеров с непрерывным движением. Пороговая плотность кластеров MHC класса I необходима для поддержания активной передачи иммунных сигналов (Anikeeva et al., PLoS One. 2012;7(8):e41466; Bullock et al., J Immunol. 2000 Mar 1;164(5):2354-61; Bullock et al., J Immunol. 2003 Feb 15;170(4):1822-9; Jiang et al., Immunity. 2011 Jan 28;34(1):13-23, каждая из которых включена в настоящее описание в качестве ссылки в полном объеме). Таким образом, в некоторых вариантах осуществления aAPC, представленные в настоящем описании, могут опосредовать кластеризацию молекул MHC с плотностью, являющейся эффективной для образования функционального иммунологического синапса и для активации передачи иммунных сигналов.
Другим следствием молекулярной реорганизации при функционировании иммунного синапса является межклеточный перенос мембранных белков APC в T-клетку. T-клетки получают гликопротеины MHC класса I и класса II от APC вместе с костимуляторными молекулами и мембранными патчами с помощью механизма, обозначаемого как трогоцитоз. Как представлено в настоящем описании, мембрана aAPC, представленных в настоящем описании, делает возможной эффективную молекулярную реорганизацию и кластеризацию MHC благодаря своей текучести. В некоторых вариантах осуществления aAPC по настоящему изобретению делает возможной или опосредует молекулярную реорганизацию при образовании иммунного синапса таким образом, что происходит трогоцитоз.
Размеры иммунологического синапса можно определять различными известными в этой области способами, включая микроскопию, такую как флуоресцентная микроскопия полного внутреннего отражения (TIRFM) (Varma et al., 2006). Исследования показали, что иммунологический синапс состоит из SMAC микронного размера (Varma et al., 2006; Dustin et al., Science. 2002, 298(5594):785-9, включенная в настоящее описание в качестве ссылки в полном объеме). В некоторых вариантах осуществления aAPC по настоящему изобретению могут образовывать иммунологический синапс со средним диаметром приблизительно от 0,5 мкм до 5,0 мкм. В некоторых вариантах осуществления aAPC по настоящему изобретению может образовывать иммунологический синапс со средним диаметром по меньшей мере приблизительно 0,5 мкм. В некоторых вариантах осуществления aAPC по настоящему изобретению может образовывать функциональный иммунологический синапс со средним диаметром приблизительно от 0,5 мкм до 4,5 мкм, приблизительно от 0,5 мкм до 4,0 мкм, приблизительно от 0,5 мкм до 3,5 мкм, приблизительно от 0,5 мкм до 3,0 мкм, приблизительно от 0,5 мкм до 2,5 мкм, приблизительно от 0,5 мкм до 2,0 мкм, приблизительно от 0,5 мкм до 1,5 мкм, приблизительно от 0,5 мкм до 1,0 мкм, приблизительно от 1,0 мкм до 5,0 мкм, приблизительно от 1,0 мкм до 4,5 мкм, приблизительно от 1,0 мкм до 4,0 мкм, приблизительно от 1,0 мкм до 3,5 мкм, приблизительно от 1,0 мкм до 3,0 мкм, приблизительно от 1,0 мкм до 2,5 мкм, приблизительно от 1,0 мкм до 2,0 мкм, приблизительно от 1,0 мкм до 1,5 мкм, приблизительно от 1,5 мкм до 5,0 мкм, приблизительно от 1,5 мкм до 4,5 мкм, приблизительно от 1,5 мкм до 4,0 мкм, приблизительно от 1,5 мкм до 3,5 мкм, приблизительно от 1,5 мкм до 3,0 мкм, приблизительно от 1,5 мкм до 2,5 мкм, приблизительно от 1,5 мкм до 2,0 мкм, приблизительно от 2,0 мкм до 5,0 мкм, приблизительно от 2,0 мкм до 4,5 мкм, приблизительно от 2,0 мкм до 4,0 мкм, приблизительно от 2,0 мкм до 3,5 мкм, приблизительно от 2,0 мкм до 3,0 мкм, приблизительно от 2,0 мкм до 2,5 мкм, приблизительно от 2,0 мкм до 5,0 мкм, приблизительно от 2,5 мкм до 4,5 мкм, приблизительно от 2,5 мкм до 4,0 мкм, приблизительно от 2,5 мкм до 3,5 мкм, приблизительно от 2,5 мкм до 3,0 мкм, приблизительно от 3,0 мкм до 5,0 мкм, приблизительно от 3,0 мкм до 4,5 мкм, приблизительно от 3,0 мкм до 4,0 мкм, приблизительно от 3,0 мкм до 3,5 мкм, приблизительно от 3,5 мкм до 5,0 мкм, приблизительно от 3,5 мкм до 4,5 мкм, приблизительно от 3,5 мкм до 4,0 мкм, приблизительно от 4,0 мкм до 5,0 мкм, приблизительно от 4,0 мкм до 4,5 мкм, приблизительно от 4,5 мкм до 5,0 мкм. В некоторых вариантах осуществления aAPC по настоящему изобретению может образовывать функциональный иммунологический синапс со средним диаметром по меньшей мере 0,5 мкм, 0,6 мкм, 0,7 мкм, 0,8 мкм, 0,9 мкм, 1,0 мкм, 1,5 мкм, 2,0 мкм, 2,5 мкм, 3 мкм, 3,5 мкм, 4,0 мкм или 5 мкм.
Как представлено в настоящем описании, преимуществом aAPC по настоящему изобретению является текучесть клеточной мембраны aAPC, делающая возможной эффективную молекулярную реорганизацию. Конкретные пути передачи сигнала приводят к поляризации T-клетки посредством ориентации ее центросом в сторону иммунологического синапса. Накопление и поляризация актина запускается взаимодействиями TCR/CD3 с интегринами и небольшими ГТФазами. Эти взаимодействия способствуют полимеризации актина, и когда актин накапливается и реорганизуется, это способствует кластеризации TCR и интегринов. Эти высокодинамические контакты отличаются непрерывными явлениями ремоделирования цитоскелета, которые не только структурируют область контакта, но также прикладывают значительные механические силы, влияющие на передачу информации в иммунную клетку и из нее (Basu et al., Trends Cell Biol. 2017 Apr; 27(4): 241-254; Hivroz et al., Front Immunol. 2016; 7: 46; включенные в настоящее описание в качестве ссылки в полном объеме). Адгезионные силы прочности при растяжении между TCR и интегринами в участке иммунологического синапса можно определять посредством, например, атомно-силовой микроскопии, биомембранной силовой микроскопии (BFP), тракционной микроскопии и т.д. (Hivroz et al., Front Immunol. 2016; 7: 46, включенная в настоящее описание в качестве ссылки в полном объеме).
В некоторых вариантах осуществления прочность при растяжении является мерой адгезионных сил между T-клеточным рецептором и молекулами иммунологического синапса, например, комплексом пептид-MHC, образованным aAPC. В некоторых вариантах осуществления aAPC может образовывать иммунологический синапс с прочностью при растяжении, достаточной для активации иммунной клетки. В некоторых вариантах осуществления aAPC по настоящему изобретению может образовывать синапс с прочностью при растяжении приблизительно от 1 пН до 30000 пН. В некоторых вариантах осуществления aAPC по настоящему изобретению может образовывать синапс с прочностью при растяжении приблизительно от 1 пН до 20000 пН, приблизительно от 1 пН до 10000 пН, приблизительно от 1 пН до 9000 пН, приблизительно от 1 пН до 8000 пН, приблизительно от 1 пН до 7000 пН, приблизительно от 1 пН до 6000 пН, приблизительно от 1 пН до 5000 пН, приблизительно от 1 пН до 4000 пН, приблизительно от 1 пН до 3000 пН, приблизительно от 1 пН до 2000 пН, приблизительно от 1 пН до 1000 пН, приблизительно от 1000 пН до 30000 пН, приблизительно от 1000 пН до 20000 пН, приблизительно от 1000 пН до 10000 пН, приблизительно от 1000 пН до 9000 пН, приблизительно от 1000 пН до 8000 пН, приблизительно от 1000 пН до 7000 пН, приблизительно от 1000 пН до 6000 пН, приблизительно от 1000 пН до 5000 пН, приблизительно от 1000 пН до 4000 пН, приблизительно от 1000 пН до 3000 пН, приблизительно от 1000 пН до 2000 пН. В некоторых вариантах осуществления оптимальные механические силы между комплексом пептид-MHC и TCR в иммунологическом синапсе составляют по меньшей мере, 1 пН, 1,5 пН, 2,0 пН, 3,0 пН, 4,0 пН, 5,0 пН, 6,0 пН, 7,0 пН, 8,0 пН, 9,0 пН, 10 пН, 20 пН, 30 пН, 40 пН, 50 пН, 60 пН, 70 пН, 80 пН, 90 пН, 100 пН, 500 пН, 1000 пН, 2000 пН, 3000 пН, 4000 пН, 5000 пН, 6000 пН, 7000 пН, 8000 пН, 9000 пН, 10000 пН, 11000 пН, 12000 пН, 13000 пН, 14000 пН, 15000 пН или 20000 пН. В некоторых вариантах осуществления aAPC, представленные в настоящем описании, могут вызывать механические силы между комплексом пептид-MHC и TCR в иммунологическом синапсе для активации иммунной клетки.
Treg-костимуляторные и коингибиторные полипептиды
Регуляторные T-клетки ("Treg") являются специализированной субпопуляцией T-клеток, супрессирующих активацию иммунной системы и, таким образом, поддерживающих толерантность к аутоантигенам. Treg-клетки составляют 5-10% CD4+ T-клеток у людей и грызунов. Treg-клетки составляют 5-10% CD4+ T-клеток у людей и грызунов и конститутивно экспрессируют CD4 и CD25, а также фактор транскрипции FoxP3 (CD4+CD25+FoxP3+), участвующий в их развитии и функции. ИЛ-2 также, по-видимому, играет важную роль в развитии Treg-клеток и гомеостазе, т.к. у животных с дефицитом ИЛ-2 или компонентов его рецептора развивается гиперпролиферация T-клеток и аутоиммунные заболевания, которые можно корректировать посредством адоптивного переноса Treg-клеток из наивных животных. Аналогично, отсутствие передачи сигналов через взаимодействие CD28/CD80 ассоциировано со сниженным количеством и функциональностью Treg-клеток, что позволяет предполагать, что эта система рецептор/лиганд играет важную роль в развитии и функционировании Treg-клеток.
В некоторых вариантах осуществления настоящее изобретение относится к Treg-костимуляторным полипептидам, являющимся экзогенными полипептидами, приводящими к экспансии регуляторных T-клеток (Treg). В некоторых вариантах осуществления Treg-костимуляторные полипептиды приводят к экспансии Treg-клеток посредством стимуляции по меньшей мере одного из трех сигналов, вовлеченных в развитии Treg-клеток. Сигнал 1 активирует TCR, и его можно стимулировать с помощью антител, таких как антитела против CD3, или антигенов, передающих сигналы через TCR. Сигнал 2 может быть опосредован несколькими разными молекулами, включая иммунные костимуляторные молекулы, такие как CD80 и 4-1BBL. Сигнал 3 передается через цитокины, такие как ИЛ-2 или TGFβ. В некоторых вариантах осуществления Treg-костимуляторные полипептиды стимулируют один из этих сигналов. В другом варианте осуществления Treg-костимуляторные полипептиды стимулируют два из этих сигналов. В еще одном варианте осуществления Treg-костимуляторные полипептиды стимулируют три из этих сигналов.
Сигнал 1
Антигены, которые можно использовать в качестве Treg-костимуляторных полипептидов для стимуляции сигнала 1, включают антигены, ассоциированные с целевым заболеванием или состоянием. Например, аутоантигены и инсулин (особенно подходящий для лечения диабета 1 типа), коллаген (особенно подходящий для лечения ревматоидного артрита), основной миелиновый белок (особенно подходящий для лечения рассеянного склероза) и MHC (для лечения и профилактики отторжения чужеродного трансплантата). Антигены можно вводить как часть конъюгата. Необязательно, антиген получают в качестве части комплекса MHC/антиген. В этом варианте осуществления MHC и антиген независимо могут являться чужеродными или сингенными. Например, можно использовать MHC донора и аллогенный или сингенный антиген.
Сигнал 2
Примеры Treg-костимуляторных полипептидов для стимуляции сигнала 2 включают членов семейств B7 и ФНО, например, членов семейств B7 и CD28, представленных ниже в таблице 10, и членов семейства ФНО, представленных в таблице 11.
Таблица 10. Treg-костимуляторные полипептиды: члены семейства B7 и CD28
Таблица 11. Treg-костимуляторные полипептиды: члены семейства ФНО
Сигнал 3
Примеры Treg-костимуляторных полипептидов для стимуляции сигнала 3, включают цитокины и факторы роста, стимулирующие сигнал 3, такие как ИЛ-2, ИЛ-4 и TGF-β (включая TGF-β1, TGF-β2 и TGF-β3). В этой области известны остатки ИЛ-2 и ИЛ-4, которые можно использовать в иммунотерапевтических способах. См., например, Earle et al., 2005, выше; Thorton et al., 2004, J. Immunol. 172: 6519-23; Thorton et al., 2004, Eur. J. Immunol. 34: 366-76. В одном из вариантов осуществления используют зрелую часть цитокина.
В некоторых вариантах осуществления Treg-костимуляторный полипептид является CD25-специфическим ИЛ-2. В некоторых вариантах осуществления Treg-костимуляторный полипептид является TNFR2-специфическим ФНО. В некоторых вариантах осуществления Treg-костимуляторный полипептид является агонистом против DR3 (VEGI/TL1A-специфическим). В некоторых вариантах осуществления Treg-костимуляторный пептид является 4-1BBL. В некоторых вариантах осуществления Treg-костимуляторный пептид является TGF-бета.
В других вариантах осуществления настоящее изобретение относится к Treg-коингибиторным полипептидам, являющимся экзогенными полипептидами, ингибирующими Treg-клетки. В некоторых вариантах осуществления ингибирование Treg можно использовать в лечении злокачественного новообразования, например, посредством таргетинга хемокинов, участвующих в миграции Treg. Другие ингибиторы Treg могут направленно воздействовать на любые из рецепторов, указанных в таблицах 10 или 11, например, антитело против OX40, антитело против GITR или антитело против CTLA4, или лиганды TLR.
В некоторых вариантах осуществления Treg-костимуляторные полипептиды или их активные фрагменты можно связывать или экспрессировать в виде слитого белка с членом связывающейся пары для использования в соответствии с настоящим изобретением. Примером связывающейся пары является биотин и стрептавидин (SA) или авидин.
В некоторых вариантах осуществления Treg-костимуляторные полипептиды или их активные фрагменты являются частью слитого белка, содержащего Treg-костимуляторный полипептид и член связывающейся пары, такой как CSA. Слитые белки можно получать любым из ряда различных известных в этой области способов. Например, один или более из полипептидов-компонентов слитых белков можно синтезировать химически или получать с использованием хорошо известной технологии рекомбинантных нуклеиновых кислот. (В рамках изобретения термин "нуклеиновая кислота" относится к РНК или ДНК.) Последовательности нуклеиновой кислоты, которые можно использовать в настоящем изобретении, можно получать с использованием, например, полимеразной цепной реакции (ПЦР). Различные способы ПЦР описаны, например, в PCR Primer: A Laboratory Manual, Dieffenbach 7 Dveksler, Eds., Cold Spring Harbor Laboratory Press, 1995. Слитые пептиды более подробно описаны в настоящем описании ниже.
Конъюгат может включать линкер, такой как пептидный линкер, между членом связывающейся пары и костимуляторной молекулой. Длину и композицию линкера можно выбирать для повышения активности любого функционального конца молекулы. Линкер может иметь длину более 20 аминокислот. В некоторых вариантах осуществления линкер имеет длину, как правило, от приблизительно 3 до приблизительно 30 аминокислот, например, от приблизительно 5 до приблизительно 20 аминокислот, от приблизительно 5 до приблизительно 15 аминокислот, от приблизительно до приблизительно 10 аминокислот. Однако можно использовать более длинные или короткие линкеры, или можно вообще обходиться без линкера. В связи с этим, можно использовать гибкие линкеры (например, (Gly4Ser)3 (SEQ ID NO: 1)), такие как используемые для соединения тяжелых и легких цепей одной цепи антитела. См., например, Huston et al., 1988, Proc. Nat. Acad. Sci. USA, 85: 5879-5883; патенты США №№5091513, 5132405, 4956778; 5258498 и 5482858, каждый из которых включен в настоящее описание в качестве ссылки в полном объеме. Другими линкерами являются FENDAQAPKS (SEQ ID NO: 717) или LQNDAQAPKS (SEQ ID NO: 718). В качестве линкера также можно использовать один или более доменов Fc-области иммуноглобулина (например, CH1, CH2 и/или CH3).
В некоторых вариантах осуществления полипептид является экзогенным Treg-костимуляторным полипептидом, представленным в настоящем описании. Пример Treg-костимуляторного полипептида включает:
a) природную форму полипептида человека;
b) полипептид человека, имеющий последовательность, содержащуюся в базе данных, например, базе данных GenBank , на 22 декабря 2017 года;
c) полипептид человека, имеющий последовательность, отличающуюся на не более чем 1, 2, 3, 4, 5 или 10 аминокислотных остатков от последовательности по п. a) или b);
d) полипептид человека, имеющий последовательность, отличающуюся на не более чем 1, 2, 3, 4, 5 или 10% аминокислотных остатков от последовательности по п. a) или b);
e) полипептид человека, имеющий последовательность, по существу, не отличающуюся от последовательности по п. a) или b); или
f) полипептид человека, имеющий последовательность по п. c), d) или e), по существу, не отличающуюся по биологической активности, например, ферментативной активности (например, специфичности или обороту) или связывающей активности (например, специфичности или аффинности связывания), от полипептида человека, имеющего последовательность по п. a) или b). Пептиды-кандидаты по п. f) можно получать и подвергать скринингу на схожую активность, как представлено в настоящем описании, и они будут эквивалентны при экспрессии в сконструированных эритроидных клетках, как представлено в настоящем описании.
В вариантах осуществления экзогенный Treg-костимуляторный полипептид содержит полипептид человека или его фрагмент, например, весь полипептид человека или его фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу. В варианте осуществления экзогенный Treg-костимуляторный полипептид содержит слитый полипептид, содержащий весь полипептид человека или его фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу и дополнительную аминокислотную последовательность. В варианте осуществления дополнительная аминокислотная последовательность содержит весь полипептид человека или его фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу для другого Treg-костимуляторного полипептида человек.
В некоторых вариантах осуществления aAPC презентирует, например, содержит на своей поверхности, по меньшей мере два, по меньшей мере 3, по меньшей мере 4 или по меньшей мере 5 экзогенных Treg-костимуляторных полипептидов.
В некоторых вариантах осуществления один или более Treg-костимуляторных или коингибиторных полипептидов включают мембранный якорь или слиты с ним. В некоторых вариантах осуществления мембранный якорь выбран из последовательности, приведенной в таблице 3. В некоторых вариантах осуществления один или более Treg-костимуляторных или коингибиторных полипептидов включают лидерную последовательность или слиты с ней. В некоторых вариантах осуществления лидерная последовательность выбрана из последовательности, приведенной в таблице 2.
Экзогенные метаболит-изменяющие полипептиды
В некоторых вариантах осуществления настоящего изобретения термин "экзогенный метаболит-изменяющий полипептид" относится к любому полипептиду, участвующему в катаболизме или анаболизме метаболита в клетке, где метаболит-изменяющий полипептид может влиять на метаболизм T-клетки. Примеры метаболит-истощающих полипептидов, как представлено в настоящем описании, изменяют уровни метаболитов в локальном окружении клетки. Например, в некоторых вариантах осуществления метаболит-истощающий полипептид способствует оксидативному катаболизму триптофана.
Примеры метаболит-изменяющих полипептидов включают CD39, CD73, аргиназу (Arg1), которую можно использовать для истощения аргинина, индоламин-2,3-диоксигеназу (IDO), которую можно использовать для истощения триптофана; ингибиторы триптофан-2,3-диоксигеназы (TDO-2), которые можно использовать для истощения триптофана; ингибиторы триптофан-5-гидроксилазы (TPH), которые снижают синтез 5-HT и которые можно использовать для истощения триптофана; циклооксигеназу-2 (COX-2) и простагландин (PGE)-синтазу (PGES), которую можно использовать для образования простагландина E2 (PGE2); и индуцибельную синтазу оксида азота (iNOS), которую можно использовать для образования NO.
В некоторых вариантах осуществления полипептид является экзогенным метаболит-изменяющим полипептидом, представленным в настоящем описании. Пример метаболит-изменяющего полипептида включает:
a) природную форму полипептида человека;
b) полипептид человека, имеющий последовательность, содержащуюся в базе данных, например, базе данных GenBank , на 22 декабря 2017 года;
c) полипептид человека, имеющий последовательность, отличающуюся на не более чем 1, 2, 3, 4, 5 или 10 аминокислотных остатков от последовательности по п. a) или b);
d) полипептид человека, имеющий последовательность, отличающуюся на не более чем 1, 2, 3, 4, 5 или 10% аминокислотных остатков от последовательности по п. a) или b);
e) полипептид человека, имеющий последовательность по существу, не отличающуюся от последовательности по п. a) или b); или
f) полипептид человека, имеющий последовательность по п. c), d) или e), по существу, не отличающуюся по биологической активности, например, ферментативной активности (например, специфичности или обороту) или связывающей активности (например, специфичности или аффинности связывания), от полипептида человека, имеющего последовательность по п. a) или b). Пептиды-кандидаты по п. f) можно получать и подвергать скринингу на схожую активность, как представлено в настоящем описании, и они будут эквивалентны при экспрессии в сконструированных эритроидных клетках, как представлено в настоящем описании.
В вариантах осуществления экзогенный метаболит-изменяющий полипептид содержит полипептид человека или его фрагмент, например, весь полипептид человека или его фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу. В варианте осуществления экзогенный метаболит-изменяющий полипептид содержит слитый полипептид, содержащий весь полипептид человека или его фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу и дополнительную аминокислотную последовательность. В варианте осуществления дополнительная аминокислотная последовательность содержит весь полипептид человека или его фрагмент по п. a), b), c), d), e) или f) по предшествующему абзацу для другого метаболит-изменяющего полипептида человека.
В некоторых вариантах осуществления один или более экзогенных метаболит-изменяющих полипептидов включают мембранный якорь или слиты с ним. В некоторых вариантах осуществления мембранный якорь выбран из последовательности, приведенной в таблице 3. В некоторых вариантах осуществления один или более экзогенных метаболит-изменяющих полипептидов включают лидерную последовательность или слиты с ней. В некоторых вариантах осуществления лидерная последовательность выбрана из последовательности, приведенной в таблице 2.
Цитокины/хемокины
Кроме того, настоящее изобретение включает aAPC, трансдуцированные с использованием нуклеиновой кислоты, кодирующей по меньшей мере один цитокин, по меньшей мере один хемокин или и тот, и другой. Таким образом, настоящее изобретение включает цитокин, включая полноразмерную форму, фрагмент, гомолог, вариант или мутант цитокина. Цитокин включает белок, который может влиять на биологическую функцию другой клетки. Биологическая функция, на которую влияет цитокин, может включать, в качестве неограничивающих примеров, рост клеток, дифференцировку клеток или гибель клеток. Предпочтительно, цитокин по настоящему изобретению может связываться со специфическим рецептором на поверхности клетки, таким образом, влияя на биологическую функцию клетки.
Предпочтительный цитокин включает, помимо прочего, гемопоэтический фактор роста, интерлейкин, интерферон, молекулу суперсемейства иммуноглобулинов, молекулу семейства фактора некроза опухоли и/или хемокин. Более предпочтительный цитокин по настоящему изобретению, помимо прочего, включает гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ), фактор некроза опухоли альфа (ФНОα), фактор некроза опухоли бета (ФНОβ), макрофагальный колониестимулирующий фактор (М-КСФ), интерлейкин-1 (ИЛ-1), интерлейкин-2 (ИЛ-2), интерлейкин-4 (ИЛ-4), интерлейкин-5 (ИЛ-5), интерлейкин-6 (ИЛ-6), интерлейкин-7 (ИЛ-7), интерлейкин-10 (ИЛ-10), интерлейкин-12 (ИЛ-12), интерлейкин-15 (ИЛ-15), интерлейкин-21 (ИЛ-21), интерлейкин-35 (ИЛ-35), интерферон альфа (ИФНα), интерферон бета (ИФНβ), интерферон гамма (ИФНγ) и IGIF.
Хемокин, включая его гомолог, вариант, мутант или фрагмент, включает альфа-хемокин или бета-хемокин, включая, в качестве неограничивающих примеров, C5a, интерлейкин-8 (ИЛ-8), моноцитарный хемотаксический фактор 1 альфа (MIP1α), моноцитарный хемотаксический фактор 1 бета (MIP1β), моноцитарный хемоаттрактантный белок 1 (MCP-1), моноцитарный хемоаттрактантный белок 3 (MCP-3), фактор активации тромбоцитов (PAFR), N-формил-метионил-лейцил-[3H]фенилаланин (FMLPR), лейкотриен B4 (LTB4R), гастрин-высвобождающий пептид (GRP), RANTES, эотаксин, лимфотактин, IP10, 1-309, ENA78, GCP-2, NAP-2 и/или MGSA/gro. Специалисту в этой области с учетом идей, представленных в настоящем описании, будет понятно, что настоящее изобретение включает хемокин и цитокин, например, хорошо известный в этой области, а также тот, который будет открыт в будущем.
В некоторых вариантах осуществления цитокин на aAPC служит в качестве полипептида для стимуляции сигнала 3. Следует понимать, что в некоторых вариантах осуществления aAPC по настоящему изобретению могут приводить к экспансии и/или активации T-клетки посредством стимуляции всех трех сигналов, участвующих в развитии T-клеток. Сигнал 1 активирует TCR, и его можно стимулировать антигенами, передающими сигнал через TCR. Сигнал 2 может быть опосредован несколькими разными молекулами, включая любые иммунные костимуляторные молекулы, представленные в настоящем описании, такие как 4-1BBL. Сигнал 3 может передаваться через цитокины, такие как ИЛ-15. Не желая быть связанными какой-либо теорией, предполагают, что наличие сигнала 3, например, от третьего экзогенного полипептида на aAPC, в дополнение к сигналам 1 и 2 от первого и второго экзогенного полипептида, соответственно, например, антигена и костимуляторного полипептида, как представлено в настоящем описании, повышает способность aAPC стимулировать популяцию T-клеток памяти и, таким образом, обеспечивать более длительную эффективность, например, эффективность против рецидива опухоли или повторного заражения возбудителем инфекции. В некоторых вариантах осуществления полипептид для стимуляции сигнала 3 является ИЛ-15. В некоторых вариантах осуществления aAPC содержит третий экзогенный полипептид, стимулирующий сигнал 3. В одном из вариантов осуществления третий экзогенный полипептид, стимулирующий сигнал 3, является ИЛ-15.
В некоторых вариантах осуществления сконструированная эритроидная клетка, например, безъядерная клетка, содержит одну или более (например, 2, 3, 4, 5 или более) субъединиц цитокинового рецептора из таблицы 12 или их цитокин-связывающие варианты или фрагменты. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит два или три (например, все) субъединицы цитокинового рецептора из одной строки таблицы 12 или их цитокин-связывающие варианты или функциональные фрагменты. Цитокиновые рецепторы могут присутствовать на поверхности эритроидной клетки. Экспрессируемые рецепторы, как правило, имеют последовательность рецептора человека дикого типа или ее вариант или фрагмент, который может связываться с лигандом-мишенью и секвестрировать его. В вариантах осуществления две или более субъединицы цитокинового рецептора связывают друг с другом, например, в виде слитого белка.
В вариантах осуществления один или более (например, 2 или все) из цитокинов слиты с трансмембранными доменами (например, трансмембранным доменом GPA или другим трансмембранным доменом, представленным в настоящем описании), например, таким образом, что цитокин находится на поверхности эритроидной клетки. В вариантах осуществления эритроидная клетка дополнительно содержит молекулу таргетинга, например, направляющую молекулу или молекулу таргетинга, описанную в WO2007030708, например, на стр. 34-45, при этом эта заявка включена в настоящее описание в качестве ссылки в полном объеме.
В некоторых вариантах осуществления один или более цитокинов включают мембранный якорь или слиты с ним. В некоторых вариантах осуществления мембранный якорь выбран из последовательности, приведенной в таблице 3. В некоторых вариантах осуществления один или более цитокинов включают лидерную последовательность или слиты с ней. В некоторых вариантах осуществления лидерная последовательность выбрана из последовательности, приведенной в таблице 2.
Таблица 12. Цитокины и рецепторы
Сконструированные эритроидные клетки
В некоторых аспектах настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку или безъядерную клетку, где эритроидная клетка или безъядерная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенный полипептид, приведенный в таблице 1. Таким образом, настоящее изобретение включает aAPC, содержащую нуклеиновую кислоту, кодирующую интересующий антиген, приведенный в таблице 1. В некоторых вариантах осуществления по меньшей мере один экзогенный антигенный полипептид является опухолевым антигеном, антигеном аутоиммунного заболевания, вирусным антигеном или бактериальным антигеном. В некоторых вариантах осуществления безъядерная клетка является эритроидной клеткой, например, утратившей свое ядро при дифференцировке из эритроцитарной клетки-предшественника. Однако следует понимать, что не все безъядерные клетки являются эритроидными клетками, и, таким образом, безъядерные клетки по настоящему изобретению также могут включать, например, тромбоциты. В некоторых вариантах осуществления безъядерные клетки не являются тромбоцитами и, таким образом, являются несодержащими тромбоциты безъядерными клетками. В некоторых аспектах настоящего изобретения эритроидная клетка является ретикулоцитом или эритроцитом. Эритроциты обладают рядом преимуществ по сравнению с другими клетками, включая то, что они являются неаутологичными (например, в них, по существу, отсутствует главный комплекс гистосовместимости (MHC)), имеют большее время циркуляции в организме индивидуума (например, более 30 дней) и подходят для получения в больших масштабах. В некоторых аспектах настоящего изобретения сконструированные эритроидные клетки являются ядросодержащими.
Эритроидная клетка, необязательно, дополнительно содержит второй, другой экзогенный полипептид. Эритроидная клетка необязательно дополнительно содержит второй и третий другие экзогенные полипептиды. Эритроидная клетка, необязательно, дополнительно содержит второй, третий и четвертый другие экзогенные полипептиды. Эритроидная клетка, необязательно, дополнительно содержит второй, третий, четвертый и пятый другие экзогенные полипептиды. В некоторых вариантах осуществления эритроидная клетка, необязательно, дополнительно содержит 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более других экзогенных полипептидов. В некоторых вариантах осуществления эритроидная клетка, необязательно, дополнительно содержит 1-100, 1-200 других экзогенных полипептидов.
В некоторых вариантах осуществления эритроидная клетка (например, сконструированная эритроидная клетка), содержащая антиген (например, экзогенный антигенный полипептид), может процессировать и презентировать антиген в контексте экзогенного антигенпрезентирующего полипептида, например, MHC (если клетку также трансдуцируют с использованием нуклеиновой кислоты, кодирующей молекулу MHC класса I или класса II), где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом (например, молекулой MHC класса I или класса II), таким образом, приводя к образованию антигенспецифических T-клеток и экспансии их популяции. Таким образом, интересующий антиген можно встраивать в aAPC по настоящему изобретению, где aAPC презентирует антиген в контексте комплекса MHC класса I или II (например, антигенный полипептид специфически связан с комплексом MHC класса I или II), т.е. молекулу MHC "нагружают" антигеном, и aAPC можно использовать для получения антигенспецифической T-клетки. Таким образом, в некоторых аспектах настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает сконструированную эритроидную клетку, где сконструированная эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом (например, молекулой MHC класса I или класса II).
В других вариантах осуществления эритроидная клетка содержит один или более антигенов, не являющихся процессированными и презентируемыми MHC, т.е. настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток без рестриктирования по MHC. В некоторых вариантах осуществления настоящее изобретение относится к aAPC, включающей антитела против CD3 (включая одноцепочечные антитела). В некоторых вариантах осуществления антитела против CD3 (включая одноцепочечные антитела) экспрессируются на поверхности aAPC. В некоторых вариантах осуществления настоящее изобретение относится к aAPC, включающей антитела против CD4 и CD8. В других вариантах осуществления антитела против CD4 и CD8 экспрессируются на поверхности aAPC для активации соответствующих популяций иммунных клеток.
В других аспектах настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает сконструированную эритроидную клетку, где сконструированная эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенный полипептид и экзогенный костимуляторный полипептид.
В некоторых аспектах настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II. В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления сконструированная эритроидная клетка является безъядерной эритроидной клеткой.
В других аспектах настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации и экспансии T-клеток, где aAPC включает сконструированную эритроидную клетку, где сконструированная эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, экзогенный антигенный полипептид, экзогенный костимуляторный полипептид и экзогенный полипептид для экспансии T-клеток, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом (например, молекулой MHC класса I или класса II).
В некоторых вариантах осуществления aAPC может активировать T-клетку, приведенную в контакт с aAPC.
В другом варианте осуществления стимуляция включает активацию CD8+ T-клеток, активацию CD4+ T-клеток, стимуляцию цитотоксической активности T-клеток, стимуляцию секреции цитокинов T-клетками и/или любую их комбинацию.
В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления сконструированная эритроидная клетка является безъядерной клеткой.
В другом примере экзогенные полипептиды содержат активирующий T-клетки лиганд и средство, ингибирующее иммунную ингибиторную молекулу (например, иммунный ингибиторный рецептор), например, CD80 и антитело против PD1, в иммуноонкологических условиях. В другом варианте осуществления одно средство является активирующим 4-1BBL или его фрагментом или вариантом, и второе средство является молекулой антитела, блокирующей передачу сигнала PD1 (например, молекулой антитела против PD1 или PD-L1). Таким образом, в вариантах осуществления T-клетку-мишень и активируют, и предотвращают ее репрессию.
В некоторых вариантах осуществления целью является активация или ингибирование T-клеток. Для обеспечения того, чтобы T-клетки подвергались преимущественному направленному воздействию по сравнению с другими иммунными клетками, которые также могут экспрессировать активирующие или ингибиторные рецепторы, как представлено в настоящем описании, один из экзогенных полипептидов на эритроидной клетке может содержать молекулу таргетинга, например, молекулу антитела, связывающуюся с T-клеточным рецептором (TCR) или другим T-клеточным маркером. Молекулы таргетинга более подробно описаны ниже. В некоторых вариантах осуществления можно увеличивать или ингибировать специфический подтип или клон T-клеток. В некоторых вариантах осуществления один или более из экзогенных полипептидов на эритроидной клетке является молекулой пептид-MHC, которая будет селективно связываться с T-клеточным рецептором антигенспецифическим образом.
В некоторых аспектах настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для супрессии активности T-клетки, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, экзогенный антигенный полипептид и по меньшей мере один экзогенный коингибиторный полипептид, приведенный в таблице 7, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом (например, молекулой MHC класса I или класса II).
В других аспектах настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для супрессии активности T-клетки, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, экзогенный антигенный полипептид, приведенный в таблице 1, и по меньшей мере один экзогенный коингибиторный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом (например, молекулой MHC класса I или класса II).
В некоторых аспектах настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для супрессии активности T-клетки, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, экзогенный антигенный полипептид и по меньшей мере один метаболит-изменяющий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом (например, молекулой MHC класса I или класса II).
В других аспектах настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для супрессии T эффекторные клетки, где aAPC включает сконструированную эритроидную клетку, где сконструированная эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид, экзогенный антиген, экзогенный ингибитор пролиферации и экзогенный истощающий аминокислоты полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом (например, молекулой MHC класса I или класса II).
В некоторых вариантах осуществления aAPC может супрессировать T-клетки, приведенные в контакт с aAPC. В других вариантах осуществления aAPC может супрессировать T-клетку, взаимодействующую с aAPC. В дополнительных вариантах осуществления супрессия включает ингибирование пролиферации T-клетки, анергию T-клетки или индуцирование апоптоза T-клетки.
В некоторых аспектах настоящее изобретение относится к искусственной антигенпрезентирующей клетке (aAPC), сконструированной для активации регуляторной T-клетки (Treg-клетка), где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом (например, молекулой MHC класса I или класса II). В некоторых вариантах осуществления aAPC дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид для экспансии Treg.
В некоторых вариантах осуществления T-клетка по любому из аспектов и вариантов осуществления, представленных в настоящем описании, является CD4+ T-клеткой или CD8+ T-клеткой.
В некоторых вариантах осуществления эритроидная клетка содержит экзогенный полипептид (например, экзогенные антигенные полипептиды, экзогенные антигенпрезентирующие полипептиды, экзогенные костимуляторные полипептиды, экзогенные коингибиторные полипептиды, экзогенные истощающие аминокислота полипептиды и экзогенные Treg-костимуляторные полипептиды), где эритроидная клетка, необязательно, дополнительно содержит второй экзогенный полипептид (например, экзогенные антигенные полипептиды, экзогенные антигенпрезентирующие полипептиды, экзогенные костимуляторные полипептиды, экзогенные коингибиторные полипептиды, экзогенные истощающие аминокислоты полипептиды и экзогенные Treg-костимуляторные полипептиды) является экзогенным полипептидом, представленным в настоящем описании.
В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления сконструированная эритроидная клетка является безъядерной клеткой.
Настоящее изобретение также следует считать включающим "мутанты", "производные" и "варианты" экзогенных полипептидов, представленных в настоящем описании (или ДНК, кодирующей их), где мутанты, производные и варианты являются костимуляторными лигандами, цитокинами, антигенами (например, антигенами опухолевых клеток, вирусные антигены и другие антигены), измененные в одной или более аминокислотах (или, в отношении нуклеотидной последовательности, кодирующей их, изменены в одной или более парах оснований), таким образом, что получаемый пептид (или ДНК) не является идентичным последовательностям, перечисленным в настоящем описании, но имеет то же биологическое свойство, что и пептиды, представленные в настоящем описании, в том, что пептид имеет биологические/биохимические свойства костимуляторного лиганда, цитокина, антигена и т.п. по настоящему изобретению (например, экспрессию aAPC, где приведение aAPC, экспрессирующей белок, в контакт с T-клеткой опосредует пролиферацию или иначе влияет на T-клетку). Для получения мутанта, производного или варианта белка по настоящему изобретению можно использовать любой из ряда способов с использованием способов рекомбинантной ДНК, хорошо известных в этой области, таких как, например, описываемые в Sambrook and Russell (2001, Molecular Cloning, A Laboratory Approach, Cold Spring Harbor Press, Cold Spring Harbor, N.Y.), и Ausubel et al. (2002, Current Protocols in Molecular biology, John Wiley & Sons, NY). Способы встраивания изменений аминокислот в белок или полипептид посредством изменения последовательности ДНК, кодирующей полипептид, хорошо известны в этой области и также описаны в этих и других источниках.
Настоящее изобретение также включает то, что функциональные фрагменты или варианты белков, приведенных в таблицах 1-24, можно получать и подвергать скринингу на схожую активность, как представлено в настоящем описании, и они будут эквивалентны при экспрессии в сконструированных эритроидных клетках, как представлено в настоящем описании.
Специалистам в этой области с учетом идей, представленных в настоящем описании, будет понятно, что aAPC по настоящему изобретению не ограничены каким-либо образом любым конкретным антигеном, цитокином, костимуляторным лигандом, антителом, специфически связывающимся с костимуляторной молекулой, и т.п. Точнее, настоящее изобретение включает aAPC, содержащую множество молекул, все из которых экспрессируются под контролем одной промоторной/регуляторной последовательности или под контролем более одной такой последовательности. Кроме того, настоящее изобретение включает введение одну или более aAPC по настоящему изобретению, где различные aAPC кодируют разные молекулы. Т.е. различные молекулы (например, костимуляторные лиганды, антигены, цитокины и т.п.) могут действовать в цис-положении (т.е. находится в одной aAPC и/или кодируется одной нуклеиновой кислотой или разными молекулами нуклеиновой кислоты в одной aAPC) или в транс-положении (т.е. различные молекулы экспрессируются разными aAPC).
Сконструированные эритроидные клетки, содержащие три или более экзогенных полипептидов
В вариантах осуществления сконструированная эритроидная клетка, представленная в настоящем описании, содержит три или более, например, по меньшей мере 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 50, 100, 200, 500 или 1000 экзогенных полипептидов. В вариантах осуществления популяция эритроидных клеток, представленная в настоящем описании, содержит три или более, например, по меньшей мере 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 50, 100, 200, 500, 1000, 2000 или 5000 экзогенных полипептидов, например, где разные эритроидные клетки в популяции содержат разные экзогенные полипептиды, или где разные эритроидные клетки в популяции содержат разные множества экзогенных полипептидов.
Тилинг
В некоторых вариантах осуществления первый экзогенный антигенный полипептид и второй экзогенный антигенный полипептид имеют перекрывающиеся аминокислотные последовательности. В некоторых вариантах осуществления aAPC конструируют для активации T-клеток, где aAPC включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, первый экзогенный антигенный полипептид и второй экзогенный антигенный полипептид, и где первый экзогенный антигенный полипептид и второй экзогенный антигенный полипептид имеют аминокислотные последовательности, перекрывающиеся по меньшей мере на 2 аминокислоты. В некоторых вариантах осуществления перекрывание составляет от 2 аминокислот до 23 аминокислот, например, перекрывание составляет 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22 или 23 аминокислоты. В некоторых вариантах осуществления экзогенный антигенный полипептид имеет длину 8-10 аминокислот, и перекрывание составляет 6-8 аминокислот. В некоторых вариантах осуществления длина экзогенного антигенного полипептида составляет 14-20 аминокислот, и перекрывание составляет 12-18 аминокислот. Таким образом, "черепичные" полипептиды обеспечивают более обширное распознавание антигена. В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления сконструированная эритроидная клетка является безъядерной клеткой.
Способы тилинга полипептидов известны в этой области и описаны, например, в Harding et al., где описывают разработку и тестирование 15-мерных полипептидов, перекрывающихся на 12 аминокислот, которые тестировали в анализе пролиферации CD4+ T-клеток человека (Molecular Cancer Therapeutics, November 2005, Volume 4, Issue 11, включенная в настоящее описание в качестве ссылки в полном объеме). В Sticker, et al. описывают способ на основе клеток человека для идентификации функциональных CD4(+) T-клеточных эпитопов в любом белке (J Immunol Methods. 2003 Oct 1;281(1-2):95-108, включенная в настоящее описание в качестве ссылки в полном объеме).
Модификации
Один или более из экзогенных белков могут иметь посттрансляционные модификации, характерные для эукариотических клеток, например, клеток млекопитающих, например, клеток человека. В некоторых вариантах осуществления один или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более) из экзогенных белков являются гликозилированными, фосфорилированными или и теми, и другими. Детекцию гликопротеинов in vitro можно осуществлять с помощью гелей ПААГ с SDS и вестерн-блоттинга с использованием модификации способов с реактивами Шиффа (PAS). Клеточную локализацию гликопротеинов можно определять с использованием флуоресцентных конъюгатов лектина, известных в этой области. Фосфорилирование можно анализировать посредством вестерн-блоттинга с использованием фосфо-специфических антител.
Посттрансляционные модификации также включают конъюгацию с гидрофобной группой (например, миристоилирование, пальмитоилирование, изопренилирование, пренилирование или глипирование), конъюгацию с кофактором (например, липоилирование, присоединение флавинового остатка (например, FMN или FAD), присоединение гема C, фосфопантетеинилирование или образование ретинилиденового шиффова основания), образование дифтамида, присоединение этаноламин фосфоглицерина, образование гипузина, ацилирование (например, O-ацилирование, N-ацилирование или S-ацилирование), формилирование, ацетилирование, алкилирование (например, метилирование или этилирование), амидирование, бутирилирование, гамма-карбоксилирование, малонилирование, гидроксилирование, йодирование, добавление нуклеотидов, такое как ADP-рибозилирование, окисление, образование фосфатного сложного эфира (O-связанного) или фосфорамидата (N-связанного), (например, фосфорилирование или аденилирование), пропионилирование, образование пироглутамата, S-глутатионилирование, S-нитрозилирование, сукцинилирование, сульфатирование, ISG-илирование, сумоилирование, убиквитинилирование, неддилирование или химическую модификацию аминокислоты (например, цитруллинирование, дезамидирование, элиминилирование или карбамилирование), образование дисульфидного мостика, рацемизацию (например, пролина, серина, аланина или метионина). В вариантах осуществления гликозилирование включает добавление гликозильной группы к аргинину, аспарагину, цистеину, гидроксилизину, серину, треонину, тирозину или триптофану, приводящее к образованию гликопротеина. В вариантах осуществления гликозилирование включает, например, O-связанное гликозилирование или N-связанное гликозилирование.
В некоторых вариантах осуществления один или более из экзогенных полипептидов является слитым белком, например, является слитым белком с эндогенным эритроцитарным белком или его фрагментом, например, трансмембранным белком, например, GPA или его трансмембранным фрагментом. В некоторых вариантах осуществления один или более из экзогенных полипептидов слит с доменом, способствующим димеризации или мультимеризации, например, со вторым слитым экзогенным полипептидом, необязательно, содержащим домен димеризации. В некоторых вариантах осуществления домен димеризации содержит часть молекулы антитела, например, Fc-домен или домен CH3. В некоторых вариантах осуществления первый и второй домены димеризации содержат мутации "выступ-во-впадину" (например, выступ T366Y и впадину Y407T), способствующие гетеродимеризации.
Число копий
В некоторых вариантах осуществления первый экзогенный полипептид и второй экзогенный полипептид имеют количественное соотношение приблизительно 1:1, приблизительно от 2:1 до 1:2, приблизительно от 5:1 до 1:5, приблизительно от 10:1 до 1:10, приблизительно от 20:1 до 1:20, приблизительно от 50:1 до 1:50, приблизительно от 100:1 до 1:100 по массе или по количеству копий.
В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере 10 копий, 100 копий, 1000 копий, 5000 копий, 10000 копий, 25000 копий, 50000 копий или 100000 копий каждого из первого экзогенного полипептида и второго экзогенного полипептида. В некоторых вариантах осуществления количество копий первого экзогенного полипептида составляет не более чем на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90% или не более чем в 2, 5, 10, 20, 50, 100, 200, 500 или 1000 раз больше, чем количество копий второго экзогенного полипептида. В некоторых вариантах осуществления количество копий второго экзогенного полипептида составляет не более чем на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90% или не более чем в 2, 5, 10, 20, 50, 100, 200, 500 или 1000 раз больше, чем количество копий первого экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления сконструированная эритроидная клетка является ядросодержащей клеткой.
В некоторых вариантах осуществления первый экзогенный полипептид включает от приблизительно 50000 до приблизительно 600000 копий первого экзогенного полипептида, например, приблизительно 50000, 60000, 60000, 80000, 90000, 100000, 110000, 120000, 130000, 140000, 150000, 155000, 160000, 165000, 170000, 175000, 180000, 185000, 190000, 195000, 200000, 205000, 210000, 215000, 220000, 225000, 230000, 235000, 240000, 245000, 250000, 255000, 260000, 265000, 270000, 275000, 280000, 285000, 290000, 295000, 300000, 305000, 310000, 315000, 320000, 325000, 330000, 335000, 340000, 345000, 350000, 355000, 360000, 365000, 370000, 375000, 380000, 385000, 390000, 395000, 400000, 450000, 500000, 550000, 600000 копий первого полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит приблизительно 50000-600000, приблизительно 100000-600000, приблизительно 100000-500000, приблизительно 100000-400000, приблизительно 100000-150000, приблизительно 150000-300000 или 150000-200000 копий первого экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 75000 копий первого экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 100000 копий первого экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 125000 копий первого экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 150000 копий первого экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 175000 копий первого экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 200000 копий первого экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 250000 копий первого экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 300000 копий первого экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 400000 копий первого экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 500000 копий первого экзогенного полипептида. В некоторых вариантах осуществления второй экзогенный полипептид содержит от приблизительно 50000 до приблизительно 600000 копий второго экзогенного полипептида, например, приблизительно 50000, 60,000, 60000, 80000, 90000, 100000, 110000, 120000, 130000, 140000, 150000, 155000, 160000, 165000, 170000, 175000, 180000, 185000, 190000, 195000, 200000, 205000, 210000, 215000, 220000, 225000, 230000, 235000, 240000, 245000, 250000, 255000, 260000, 265000, 270000, 275000, 280000, 285000, 290000, 295000, 300000, 305000, 310000, 315000, 320000, 325000, 330000, 335000, 340000, 345000, 350000, 355000, 360000, 365000, 370000, 375000, 380000, 385000, 390000, 395000, 400000, 450000, 500000, 550000, 600000 копий второго полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит приблизительно 50000-600000, приблизительно 100000-600000, приблизительно 100000-500000, приблизительно 100000-400000, приблизительно 100000-150000, приблизительно 150000-300000 или 150000-200000 копий второго экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 75000 копий второго экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 100000 копий второго экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 125000 копий второго экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 150000 копий второго экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 175000 копий второго экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 200000 копий второго экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 250000 копий второго экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 300000 копий второго экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 400000 копий второго экзогенного полипептида. В некоторых вариантах осуществления сконструированная эритроидная клетка содержит по меньшей мере приблизительно 500000 копий второго экзогенного полипептида.
В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления сконструированная эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления сконструированная эритроидная клетка является ядросодержащей клеткой.
Время полужизни in vivo
В некоторых вариантах осуществления экзогенный полипептид, представленный в настоящем описании, при включении в сконструированную эритроидную клетку или безъядерную клетку и на нее и введении индивидууму демонстрирует пролонгированное время полужизни in vivo по сравнению с соответствующим экзогенным полипептидом, который вводят отдельно (т.е. не на или в клетке, представленной в настоящем описании). В некоторых вариантах осуществления экзогенный полипептид имеет время полужизни in vivo, превышающее время полужизни in vivo соответствующего экзогенного полипептида, который вводят отдельно, или время полужизни in vivo соответствующей пегилированной версии экзогенного полипептида, который вводят отдельно. В некоторых вариантах осуществления экзогенный полипептид имеет время полужизни in vivo приблизительно от 24 часов до 240 дней (например, 24 часа, 36 часов, 48 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9 дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 31 день, 32, дня, 33 дня, 34 дня, 35 дней, 36 дней, 37 дней, 38 дней, 39 дней, 40 дней, 41 день, 42 дня, 43 дня, 44 дня, 45 дней, 46 дней, 47 дней, 48 дней, 49 дней, 50 дней, 51 день, 52 дня, 53 дня, 54 дня, 55 дней, 56 дней, 57 дней, 58 дней, 59 дней, 60 дней, 61 день, 62 дня, 63 дня, 64 дня, 65 дней, 66 дней, 67 дней, 68 дней, 69 дней, 70 дней, 71 день, 72 дня, 73 дня, 74 дня, 75 дней, 76 дней, 77 дней, 78 дней, 79 дней, 80 дней, 81 день, 82 дня, 83 дня, 84 дня, 85 дней, 86 дней, 87 дней, 88 дней, 89 дней, 90 дней, 91 день, 92 дня, 93 дня, 94 дня, 95 дней, 96 дней, 97 дней, 98 дней, 99 дней, 100 дней, 101 день, 102 дня, 103 дня, 104 дня, 105 дней, 106 дней, 107 дней, 108 дней, 109 дней, 110 дней, 111 дней, 112 дней, 113 дней, 114 дней, 115 дней, 116 дней, 117 дней, 118 дней, 119 дней, 120 дней, 121 день, 122 дня, 123 дня, 124 дня, 125 дней, 126 дней, 127 дней, 128 дней, 129 дней, 130 дней, 131 день, 132 дня, 133 дня, 134 дня, 135 дней, 136 дней, 137 дней, 138 дней, 139 дней, 140 дней, 141 день, 142 дня, 143 дня, 144 дня, 145 дней, 146 дней, 147 дней, 148 дней, 149 дней, 150 дней, 151 день, 152 дня, 153 дня, 154 дня, 155 дней, 156 дней, 157 дней, 158 дней, 159 дней, 160 дней, 161 день, 162 дня, 163 дня, 164 дня, 165 дней, 166 дней, 167 дней, 168 дней, 169 дней, 170 дней, 171 день, 172 дня, 173 дня, 174 дня, 175 дней, 176 дней, 177 дней, 178 дней, 179 дней, 180 дней, 181 день, 182 дня, 183 дня, 184 дня, 185 дней, 186 дней, 187 дней, 188 дней, 189 дней, 190 дней, 191 день, 192 дня, 193 дня, 194 дня, 195 дней, 196 дней, 197 дней, 198 дней, 919 дней, 200 дней, 201 день, 202 дня, 203 дня, 204 дня, 205 дней, 206 дней, 207 дней, 208 дней, 209 дней, 210 дней, 211 дней, 212 дней, 213 дней, 214 дней, 215 дней, 216 дней, 217 дней, 218 дней, 219 дней, 220 дней, 221 день, 222 дня, 223 дня, 224 дня, 225 дней, 226 дней, 227 дней, 228 дней, 229 дней, 230 дней, 231 день, 232 дня, 233 дня, 234 дня, 235 дней, 236 дней, 237 дней, 238 дней, 239 дней или 240 дней. В некоторых вариантах осуществления экзогенный полипептид имеет время полужизни in vivo более 1 дня, 2 дней, 3 дней, 5 дней, 10 дней, 25 дней, 50 дней, 75 дней, 100 дней, 125 дней, 150 дней, 175 дней, 200 дней, 225 дней, 235 дней или 250 дней. В некоторых вариантах осуществления экзогенный полипептид имеет время полужизни in vivo 1 неделю, 2 недели, 3 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, год или более.
В некоторых вариантах осуществления aAPC по настоящему изобретению остается в кровотоке после введения индивидууму в течение по меньшей мере от приблизительно 1 дня до приблизительно 240 дней (например, в течение по меньшей мере приблизительно 1 дня, 2 дней, 3 дней, 4 дней, 5 дней, 6 дней, 7 дней, 8 дней, 9 дней, 10 дней, 11 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 дня, 22 дней, 23 дней, 24 дней, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 31 дня, 32 дней, 33 дней, 34 дней, 35 дней, 36 дней, 37 дней, 38 дней, 39 дней, 40 дней, 41 дня, 42 дней, 43 дней, 44 дней, 45 дней, 46 дней, 47 дней, 48 дней, 49 дней, 50 дней, 51 дня, 52 дней, 53 дней, 54 дней, 55 дней, 56 дней, 57 дней, 58 дней, 59 дней, 60 дней, 61 дня, 62 дней, 63 дней, 64 дней, 65 дней, 66 дней, 67 дней, 68 дней, 69 дней, 70 дней, 71 дня, 72 дней, 73 дней, 74 дней, 75 дней, 76 дней, 77 дней, 78 дней, 79 дней, 80 дней, 81 дня, 82 дней, 83 дней, 84 дней, 85 дней, 86 дней, 87 дней, 88 дней, 89 дней, 90 дней, 91 дня, 92 дней, 93 дней, 94 дней, 95 дней, 96 дней, 97 дней, 98 дней, 99 дней, 100 дней, 101 дня, 102 дней, 103 дней, 104 дней, 105 дней, 106 дней, 107 дней, 108 дней, 109 дней, 110 дней, 111 дней, 112 дней, 113 дней, 114 дней, 115 дней, 116 дней, 117 дней, 118 дней, 119 дней, 120 дней, 121 дня, 122 дней, 123 дней, 124 дней, 125 дней, 126 дней, 127 дней, 128 дней, 129 дней, 130 дней, 131 дня, 132 дней, 133 дней, 134 дней, 135 дней, 136 дней, 137 дней, 138 дней, 139 дней, 140 дней, 141 дня, 142 дней, 143 дней, 144 дней, 145 дней, 146 дней, 147 дней, 148 дней, 149 дней, 150 дней, 151 дня, 152 дней, 153 дней, 154 дней, 155 дней, 156 дней, 157 дней, 158 дней, 159 дней, 160 дней, 161 дня, 162 дней, 163 дней, 164 дней, 165 дней, 166 дней, 167 дней, 168 дней, 169 дней, 170 дней, 171 дня, 172 дней, 173 дней, 174 дней, 175 дней, 176 дней, 177 дней, 178 дней, 179 дней, 180 дней, 181 дня, 182 дней, 183 дней, 184 дней, 185 дней, 186 дней, 187 дней, 188 дней, 189 дней, 190 дней, 191 дня, 192 дней, 193 дней, 194 дней, 195 дней, 196 дней, 197 дней, 198 дней, 199 дней, 200 дней, 201 дня, 202 дней, 203 дней, 204 дней, 205 дней, 206 дней, 207 дней, 208 дней, 209 дней, 210 дней, 211 дней, 212 дней, 213 дней, 214 дней, 215 дней, 216 дней, 217 дней, 218 дней, 219 дней, 220 дней, 221 дня, 222 дней, 223 дней, 224 дней, 225 дней, 226 дней, 227 дней, 228 дней, 229 дней, 230 дней, 231 дня, 232 дней, 233 дней, 234 дней, 235 дней, 236 дней, 237 дней, 238 дней, 239 дней или 240 дней.
В некоторых вариантах осуществления aAPC по настоящему изобретению презентирует антигенный полипептид во время циркуляции aAPC в сосудистом русле. В некоторых вариантах осуществления aAPC по настоящему изобретению презентирует антигенный полипептид в селезенке.
Редактирование генома
В некоторых аспектах настоящее изобретение относится к способу получения иммунологически совместимой искусственной антигенпрезентирующей клетки (aAPC), где aAPC включает сконструированную эритроидную клетку, экспрессирующую экзогенный антигенный полипептид, где способ включает приведение aAPC в контакт с нуклеазой и по меньшей мере одной гРНК, расщепляющими эндогенную нуклеиновую кислоту MHC, где эндогенная нуклеиновая кислота MHC подвергается репарации путем редактирования генома, что приводит к снижению уровня экспрессии эндогенной нуклеиновой кислоты MHC, и, таким образом, получение иммунологически совместимой aAPC. В некоторых вариантах осуществления сконструированная эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления сконструированная эритроидная клетка является ядросодержащей клеткой.
В некоторых вариантах осуществления клетка генетически модифицирована с использованием нуклеазы, направленно воздействующей одну или более выбранных последовательностей ДНК. Такие способы можно использовать для индуцирования точного расщепления в выбранных участках в эндогенных геномных локусах. Генную инженерию, в рамках которой ДНК встраивают, заменяют или удаляют из генома, например, в определенной интересующей области, с использованием направляемых нуклеаз, можно обозначать как "редактирование генома". Примеры таких нуклеаз включают нуклеазы с цинковыми пальцами (ZFN), эффекторную нуклеазу, подобную активаторам транскрипции (TALEN), сконструированную мегануклеазу, хоминг-эндонуклеазы и РНК-направляемые нуклеазы, такиие как CRISPR (короткие палиндромные повторы, регулярно расположенные группами)-ассоциированные (Cas) нуклеазы, например, полученные из бактериальных систем CRISPR/Cas типа II (например, Cas9).
В некоторых вариантах осуществления изменение сначала встраивают с использованием CRISPR (т.е. повышая эндогенную экспрессию MHC класса I). Затем антиген для презентирования также встраивают посредством CRISPR, и он процессируется внутри клетки.
В некоторых вариантах осуществления нуклеаза содержит домен расщепления ДНК и ДНК-связывающий домен (DBD), направляющий нуклеазу к конкретной последовательности ДНК, таким образом, позволяя использовать нуклеазу для конструирования геномных изменений в зависимости от последовательности. Домен расщепления ДНК может создавать двухцепочечный разрыв (DSB) или ник в последовательности, к которой он направлен, или вблизи нее. ZFN содержат DBD, выбранные или сконструированные на основе DBD белков с цинковыми пальцами (ZF). DBD белков с ZF связывают ДНК в соответствии с последовательностью с помощью одного или более цинковых пальцев, являющихся областями аминокислотной последовательности, структура которых стабилизирована посредством координации ионом цинка. TALEN содержат DBD, выбранные или сконструированные на основе DBD эффекторов, подобных активаторам транскрипции (TAL), (TALE) Xanthomonas spp. Димеры ZFN или TALEN индуцируют направленные DSB ДНК, стимулирующие пути ответа на повреждение ДНК. Специфичность связывания сконструированного домена с цинковыми пальцами направляет ZFN к специфическому участку генома. TALE содержат множество 33-35-аминокислотных повторяющихся доменов, каждый из которых распознает одну пару оснований. Подобно ZFN, TALEN индуцируют направленные DSB, активирующие пути ответа на повреждение ДНК и позволяющие осуществлять специальные изменения. Домен расщепления ДНК сконструированной сайт-специфической нуклеазы может содержать каталитический домен из природной эндонуклеазы, такой как эндонуклеаза Fokl или ее вариант. В некоторых вариантах осуществления варианты домена расщепления Fokl с мутациями, созданными для улучшения специфичности расщепления и/или активности расщепления, можно использовать (см., например, Guo, J., et al. (2010) Journal of Molecular biology 400 (1): 96-107; Doyon, Y., et al., (2011) Nature Methods 8: 74-79). Мегануклеазы являются специфическими в отношении последовательности эндонуклеазами, отличающимися крупным участком распознавания (двухцепочечные последовательности ДНК от 12 до приблизительно 40 пар оснований). Участок, как правило, встречается не более раза в указанном геноме. Специфичность мегануклеазы можно менять посредством встраивания изменений в последовательность нуклеазы (например, в ДНК-связывающий домен), а затем селекции функциональных ферментов, способных расщеплять варианты природного участка распознавания или посредством связывания или слияния белковых доменов из разных нуклеаз.
В некоторых вариантах осуществления для осуществления редактирования генома можно использовать РНК-направляемую нуклеазу. Например, используют системы на основе CRISPR/Cas. В некоторых вариантах осуществления нуклеазу Cas, такую как Cas9 (например, Cas9 Streptococcus pyogenes, Streptococcus thermophiles или Neisseria meningiditis или ее вариант), встраивают в клетки вместе с гидовой РНК, содержащей последовательность, комплементарную интересующей последовательности (РНК иногда обозначают как одиночную гидовую РНК). Область комплементарности может иметь длину, например, приблизительно 20 нуклеотидов. Нуклеаза Cas, например, Cas9, направляется к конкретной интересующей последовательности ДНК с помощью гидовой РНК. Гидовую РНК можно конструировать так, чтобы она имела комплементарность к целевой интересующей последовательности в геноме, например, последовательности в любом интересующем гене или межгенной области. При нуклеазной активности белка Cas, например, Cas9, расщепляется ДНК, что может повреждать ген или расщеплять его, что позволяет встраивать другую последовательность ДНК. В некоторых вариантах осуществления множество sgRNA, содержащих последовательности, комплементарные разным генам, например, 2, 3, 4, 5 или более генам, встраивают в одну и ту же клетку последовательно или совместно. Таким образом, в некоторых вариантах осуществления изменения во множество генов можно вносить на одной стадии.
В основном, использование систем на основе нуклеаз для генной инженерии, например, редактирования генома, включает встраивание нуклеазы в клетки и поддержание клеток в условиях и в течение периода времени, подходящих для расщепления нуклеазой ДНК клетки. В случае систем CRISP/Cas также встраивают гидовую РНК. Нуклеазу, как правило, встраивают в клетку посредством встраивания нуклеиновой кислоты, кодирующей нуклеазу. Нуклеиновую кислоту можно функционально связывать с промотором, способным направлять экспрессию в клетке, и ее можно встраивать в клетку в плазмиде или другом векторе. В некоторых вариантах осуществления можно встраивать мРНК, кодирующую нуклеазу. В некоторых вариантах осуществления нуклеаза может встраиваться самостоятельно. sgRNA можно встраивать напрямую (такими способами, как трансфекция) или посредством ее экспрессии с конструкции нуклеиновой кислоты, такой как экспрессирующий вектор. В некоторых вариантах осуществления sgRNA и белок Cas экспрессируются с одного экспрессирующего вектора, встроенного в клетку, или, в некоторых вариантах осуществления, с разных экспрессирующих векторов. В некоторых вариантах осуществления множество sgRNA, содержащих последовательности, комплементарную разным генам, например, 2, 3, 4, 5 или более генам, встраивают в одну и ту же клетку отдельно, или вместе с РНК, или посредством встраивания одной или более конструкций нуклеиновой кислоты, кодирующих sgRNA, в клетку для внутриклеточной транскрипции.
После расщепления нуклеазой целевой локус (например, в геноме клетки) может подвергаться воздействию одного из двух основных путей репарации ДНК, а именно негомологичного соединения концов (NHEJ) или гомологичной репарации (HDR). В отсутствие подходящей матрицы для репарации, имеющей достаточно гомологии к последовательностям, фланкирующим участок расщепления, для стимуляции HDR (см. обсуждение ниже), DSB повторно лигируются посредством NHEJ, что может приводить к инсерции или делеции. NHEJ можно использовать, например, для конструирования нокаутных генов или получения белков с измененной активностью. Например, инсерция или делеция в экзоне может приводить к мутации со сдвигом рамки считывания или образованию преждевременного стоп-кодона. Можно получать два или более DSB для получения более крупных делеций в геноме.
В некоторых вариантах осуществления, в дополнение к нуклеазе, в клетку встраивают нуклеиновую кислоту (например, плазмидную или линейную ДНК), содержащую интересующую последовательность, подлежащую встраиванию в геном в участок расщепления. В некоторых вариантах осуществления интересующую последовательность встраивают в ген. Интересующей последовательностью можно заменять ген по меньшей мере частично. В некоторых вариантах осуществления нуклеиновая кислота содержит последовательности, гомологичные для последовательностей, фланкирующих участок расщепления, таким образом, что стимулируют гомологичную репарацию. В некоторых вариантах осуществления нуклеиновая кислота содержит желаемое изменение по сравнению с последовательностью, присутствующей в геноме клетки в участке расщепления или вблизи нее. Нуклеиновую кислоту, содержащую последовательность, подлежащую по меньшей мере частичному встраиванию в геном, например, последовательность нуклеиновой кислоты, содержащую гомологичные последовательности и желаемое изменение, можно обозначать как "донорную последовательность". Донорная последовательность может по меньшей мере частично физически интегрироваться в геном в участок разрыва или можно использовать в качестве матрицы для репарации разрыва, что приводит к встраиванию всей нуклеотидной последовательности, присутствующей в доноре, или ее части в геном клетки. Таким образом, последовательность в геноме клетки можно изменять и, в некоторых вариантах осуществления, преобразовывать в последовательность, присутствующую в донорной нуклеиновой кислоте. В некоторых вариантах осуществления донорная последовательность может содержаться в кольцевой ДНК (например, плазмиде), линейной двухцепочечной ДНК (например, линеаризованной плазмиде или продукте ПЦР) или одноцепочечной ДНК, например, одноцепочечном олигонуклеотиде. В некоторых вариантах осуществления донорная последовательность имеет приблизительно от 10-25 п.н. и приблизительно 50-100 п.н. гомологии с любой стороны или каждой стороны целевого участка в геноме. В некоторых вариантах осуществления можно использовать более длинную гомологичную последовательность, например, приблизительно от 100-500 п.н. до приблизительно 1-2 т.п.н. или более. В некоторых вариантах осуществления изменение вносят в один аллель гена. В некоторых вариантах осуществления первое изменение вносят в один аллель гена, а другое изменение вносят в другой аллель. В некоторых вариантах осуществления одно и то же изменение вносят в оба аллеля. В некоторых вариантах осуществления два аллеля или целевых участка (или более) можно генетически модифицировать за одну стадию. В некоторых вариантах осуществления два аллеля или целевых участка (или более) можно генетически модифицировать на разных стадиях.
Способы конструирования, получения и использования ZFN и/или TALEN описаны, например, в WO2011097036; Urnov, FD, et al., Nature Reviews Genetics (2010), 11: 636-646; Miller JC, et al., Nat Biotechnol. (2011) 29(2): 143-8; Cermak, T., et al. Nucleic Acids Research (2011) 39 (12): e82, Sanjana, N. E. et al. A transcription activator-like effector toolbox for genome engineering. Nat Protoc 7, 171-192 (2012) и ссылках в любой из них. Обзор способов редактирования генома с использованием ZFN, TALEN и CRISPR/Cas представлен в Gaj, T., et al., Trends Biotechnol. 2013 Jul; 31(7):397-405. Epub 2013 May 9. Использование систем CRISPR/Cas в конструировании генома описано, например, в Cong L, et al. Multiplex genome engineering using CRISPR/Cas systems. Science. 2013; 339(6121):819-23; Mali P, et al., RNA-guided human genome engineering via Cas9. Science. 2013; 339(6121):823-6; Wang, H. et al. One-step generation of mice carrying mutations in multiple genes by CRISPR/Cas-mediated genome engineering. Cell 153, 910-918 (2013); Ran, F. A. et al. Double Nicking by RNA-Guided CRISPR Cas9 for Enhanced Genome Editing Specificity. 154 Cell 1380-1389 (2013); Mali, P., et al., Nat Methods. 2013; 10(10):957-63; Ran, FA, Nat Protoc. 2013;8(11):2281-308. В некоторых вариантах осуществления нуклеазу, расщепляющую только одну цепь дцДНК (никазу), можно использовать для стимуляции HDR без активации пути репарации NHEJ. Никазы можно получать посредством инактивации каталитической активности одного мономера нуклеазы в димере ZFN или TALEN, необходимом для расщепления двойной цепи, или инактивации каталитического домена белка Cas. Например, с помощью мутаций одного из каталитических остатков (D10 в домене нуклеазы RuvC и H840 в домене нуклеазы HNH), например, в аланины (D10A, H840A), превращают Cas9 в ДНК-никазы.
В некоторых вариантах осуществления систему на основе CRISP/Cas можно использовать для модуляции экспрессии генов. Например, коэкспрессия гидовой РНК с каталитически неактивной Cas9, у которой отсутствует эндонуклеазная активность, приводит к образованию комплекса распознавания ДНК, который может специфически противодействовать транскрипционной элонгации, связыванию РНК-полимеразы или связыванию факторов транскрипции. Эта система, иногда обозначаемая как CRISPR-интерференция (CRISPRi), может эффективно репрессировать экспрессию генов-мишеней в клетках млекопитающих (Qi, S., et al., Cell, 2013;152(5): 1173-83; Larson, MH, et al, Nat Protoc. 2013;8(11):2180-96). Прикрепляя любой из множества эффекторных доменов к каталитически неактивной Cas9, можно получать химерный белок Cas9, который можно использовать для достижения специфического в отношении последовательности контроля над экспрессией генов и/или модификацией ДНК. Подходящие эффекторные домены включают, например, домен активации транскрипции (такой как домены, содержащие домен трансактивации VP16, например, VP64), домен коактивации транскрипции, транскрипционный ингибиторный или коингибиторный домен, домен межбелковых взаимодействий, ферментативный домен и т.д. Гидовая РНК направляет химерный белок Cas9 к интересующему участку в геноме (например, в элементе контроле экспрессии, таком как промотор, или вблизи него), таким образом, эффекторный домен вызывает эффект, такой как активация или ингибирование транскрипционной активности (см., например, Gilbert LA, et al. Cell. 2013;154(2):442-51; Maeder МЛ, et a., Nat Methods, 2013; 10(10):977-9). Подходящими эффекторными доменами могут являться любые из доменов, присутствующих в природных белках, способных выполнять интересующую функцию (например, ингибирование или активацию транскрипции).
Клетки, подвергнутые воздействию посредством генной инженерии, можно подвергать селекции или анализировать для идентификации или выделения клеток, экспрессирующих желаемый рекомбинантный продукт гена, или клеток, в которых отсутствует экспрессия эндогенного гена, поврежденного посредством генной инженерии или имеющего какое-либо желаемое генетическое изменение. Например, в некоторых вариантах осуществления донорная последовательность или вектор, используемый для доставки донорной последовательности, может содержать селективный маркер, который можно использовать для селекции клеток, содержащих встроенную по меньшей мере часть донорной последовательности, содержащей селективный маркер, в своем геноме. В некоторых вариантах осуществления селекцию не используют. В некоторых вариантах осуществления клетки можно подвергать скринингу, например, посредством Саузерн-блоттинга, для идентификации клеток или клонов, имеющих желаемое генетическое изменение. При желании, клетки можно тестировать на уровень экспрессии или активность рекомбинантного продукта гена или эндогенного продукта гена или на одно или более функциональных свойств, ассоциированных или придаваемых рекомбинантным или эндогенным продуктом гена, или по любым другим интересующим критериям. Подходящие способы анализа известны специалистам в этой области и включают, например, вестерн-блоттинг, проточную цитометрию, FACS, иммунофлуоресцентную микроскопию, анализы ELISA, аффинные способы, в которых клетки приводят в контакт со средством, способным связываться с интересующим белком, с помощью которого метят или удерживают клетки, экспрессирующие белок, и т.д. Функциональные анализы можно выбирать с учетом идентичности рекомбинантного продукта гена, эндогенного продукта гена и/или интересующей функции или свойства. Например, функциональное свойство может являться способностью связываться с интересующим антигеном или способностью вызывать цитотоксичность против клеток-мишеней, экспрессирующих интересующий антиген. Клетки можно анализировать, например, посредством PGR, Саузерн-блоттинга или секвенирования, для определения количества встроенных последовательностей ДНК, их локализации и/или для определения того, произошли ли желаемые геномные изменения. Одну или более клеток, имеющих желаемые изменения, уровень экспрессии и/или функциональные свойства, можно идентифицировать, выращивать, подвергать экспансии. Клетки или их потомство можно использовать для получения линии клеток, подвергаемой SorTagging, и/или хранить для последующего использования.
Популяции сконструированных эритроидных клеток
В одном из аспектов настоящее изобретение относится к популяциям клеток, содержащим сконструированные эритроидные клетки по настоящему изобретению, например, множество или популяцию сконструированных эритроидных клеток. В различных вариантах осуществления популяция сконструированных эритроидных клеток содержит преимущественно безъядерные клетки, преимущественно ядросодержащие клетки или смесь безъядерных и ядросодержащих клеток. В таких популяциях клеток безъядерные клетки могут содержать ретикулоциты, эритроциты или смесь ретикулоцитов и эритроцитов. В некоторых вариантах осуществления безъядерные клетки являются ретикулоцитами. В некоторых вариантах осуществления безъядерные клетки являются эритроцитами.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток состоит, по существу, из безъядерных клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит преимущественно или по существу безъядерные клетки. Например, в некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит по меньшей мере приблизительно 80% или более безъядерных клеток. В некоторых вариантах осуществления популяция, представленная в настоящем описании, содержит по меньшей мере приблизительно 80%, приблизительно 81%, приблизительно 82%, приблизительно 83%, приблизительно 84%, приблизительно 85%, приблизительно 86%, приблизительно 87%, приблизительно 88%, приблизительно 89%, приблизительно 90%, приблизительно 91%, приблизительно 92%, приблизительно 93%, приблизительно 94%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99 или приблизительно 100% безъядерных клеток. В некоторых вариантах осуществления популяция, представленная в настоящем описании, содержит более приблизительно 80% безъядерных клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит более приблизительно 80%, приблизительно 81%, приблизительно 82%, приблизительно 83%, приблизительно 84%, приблизительно 85%, приблизительно 86%, приблизительно 87%, приблизительно 88%, приблизительно 89%, приблизительно 90%, приблизительно 91%, приблизительно 92%, приблизительно 93%, приблизительно 94%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98% или приблизительно 99% безъядерных клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит от приблизительно 80% до приблизительно 100% безъядерных клеток, например, от приблизительно 80% до приблизительно 95%, от приблизительно 80% до приблизительно 90%, от приблизительно 80% до приблизительно 85%, от приблизительно 85% до приблизительно 100%, от приблизительно 85% до приблизительно 95%, от приблизительно 85% до приблизительно 90%, от приблизительно 90% до приблизительно 100%, от приблизительно 90% до приблизительно 95% или от приблизительно 95% до приблизительно 100% безъядерных клеток.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит менее приблизительно 20% ядросодержащих клеток. Например, в вариантах осуществления популяция сконструированных эритроидных клеток содержит менее приблизительно 1%, приблизительно 2%, приблизительно 3%, приблизительно 5%, приблизительно 6%, приблизительно 7%, приблизительно 8%, приблизительно 9%, приблизительно 10%, приблизительно 11%, приблизительно 12%, приблизительно 13%, приблизительно 14%, приблизительно 15%, приблизительно 16%, приблизительно 17%, приблизительно 18%, приблизительно 19% или менее приблизительно 20% ядросодержащих клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит менее приблизительно 1% ядросодержащих клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит менее приблизительно 2% ядросодержащих клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит менее приблизительно 3% ядросодержащих клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит менее приблизительно 4% ядросодержащих клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит менее приблизительно 5% ядросодержащих клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит менее приблизительно 10% ядросодержащих клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит менее приблизительно 15% ядросодержащих клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит от 0% до 20% ядросодержащих клеток. В некоторых вариантах осуществления популяции сконструированных эритроидных клеток содержат приблизительно от 0% до 20% ядросодержащих клеток, например, приблизительно от 0% до 19%, приблизительно от 0% до 15%, приблизительно от 0% до 10%, приблизительно от 0% до 5%, приблизительно от 0% до 4%, приблизительно от 0% до 3%, приблизительно от 0% до 2% ядросодержащих клеток или приблизительно от 5% до 20%, приблизительно от 10% до 20% или приблизительно от 15% до 20% ядросодержащих клеток.
В некоторых вариантах осуществления настоящее изобретение относится к популяции сконструированных эритроидных клеток по настоящему изобретению, где популяция сконструированных эритроидных клеток содержит менее 20% ядросодержащих клеток и по меньшей мере 80% безъядерных клеток, или содержит менее 15% ядросодержащих клеток и по меньшей мере 85% ядросодержащих клеток, или содержит менее 10% ядросодержащих клеток и по меньшей мере 90% безъядерных клеток, или содержит менее 5% ядросодержащих клеток и по меньшей мере 95% безъядерных клеток. В некоторых вариантах осуществления настоящее изобретение относится к популяциям сконструированных эритроидных клеток по настоящему изобретению, где популяция сконструированных эритроидных клеток содержит приблизительно 0% ядросодержащих клеток и приблизительно 100% безъядерных клеток, приблизительно 1% ядросодержащих клеток и приблизительно 99% безъядерных клеток, приблизительно 2% ядросодержащих клеток и приблизительно 98% безъядерных клеток, приблизительно 3% ядросодержащих клеток и приблизительно 97% безъядерных клеток, приблизительно 4% ядросодержащих клеток и приблизительно 96% безъядерных клеток, приблизительно 5% ядросодержащих клеток и приблизительно 95% безъядерных клеток, приблизительно 6% ядросодержащих клеток и приблизительно 94% безъядерных клеток, приблизительно 7% ядросодержащих клеток и приблизительно 93% безъядерных клеток, приблизительно 8% ядросодержащих клеток и приблизительно 92% безъядерных клеток, приблизительно 9% ядросодержащих клеток и приблизительно 91% безъядерных клеток, приблизительно 10% ядросодержащих клеток и приблизительно 90% безъядерных клеток, приблизительно 11% ядросодержащих клеток и приблизительно 89% безъядерных клеток, приблизительно 12% ядросодержащих клеток и приблизительно 88% безъядерных клеток, приблизительно 13% ядросодержащих клеток и приблизительно 87% безъядерных клеток, приблизительно 14% ядросодержащих клеток и приблизительно 86% безъядерных клеток, приблизительно 85% ядросодержащих клеток и приблизительно 85% безъядерных клеток, приблизительно 16% ядросодержащих клеток и приблизительно 84% безъядерных клеток, приблизительно 17% ядросодержащих клеток и приблизительно 83% безъядерных клеток, приблизительно 18% ядросодержащих клеток и приблизительно 82% безъядерных клеток, приблизительно 19% ядросодержащих клеток и приблизительно 81% безъядерных клеток или приблизительно 20% ядросодержащих клеток и приблизительно 80% безъядерных клеток.
В другом варианте осуществления популяция сконструированных эритроидных клеток содержит преимущественно или по существу ядросодержащие клетки. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток состоит, по существу, из ядросодержащих клеток. В различных вариантах осуществления ядросодержащие клетки в популяции сконструированных эритроидных клеток являются эритроцитарными клетками-предшественниками (или полностью зрелыми эритроцитами). В вариантах осуществления эритроцитарные клетки-предшественники выбраны из группы, состоящей из плюрипотентных гемопоэтических стволовых клеток (HSC), мультипотентных миелоидных клеток-предшественников, клеток CFU-S, клеток BFU-E, клеток CFU-E, пронормобластов, базофильных нормобластов, полихромных нормобластов и ортохромных нормобластов.
В некоторых вариантах осуществления эритроцитарные клетки-предшественники, например, гемопоэтические стволовые клетки, получают из донора с первой отрицательной группой крови.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток содержит по меньшей мере приблизительно 10%, по меньшей мере приблизительно 20%, по меньшей мере приблизительно 30%, по меньшей мере приблизительно 40%, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или 100% ядросодержащих клеток.
Следует понимать, что во время получения сконструированных эритроидных клеток по настоящему изобретению некоторая фракция клеток может не становиться конъюгированной с экзогенным полипептидом или трансдуцированной для экспрессии экзогенного полипептида. Таким образом, в некоторых вариантах осуществления популяция сконструированных эритроидных клеток, представленная в настоящем описании, содержит смесь сконструированных эритроидных клеток и немодифицированных эритроидных клеток, т.е. некоторая фракция клеток в популяции не будет содержать, презентировать или экспрессировать экзогенный полипептид. Например, в различных вариантах осуществления популяция сконструированных эритроидных клеток может содержать по меньшей мере приблизительно 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% сконструированных эритроидных клеток, где остальные эритроидные клетки в популяции не являются сконструированными. В вариантах осуществления единичная стандартная доза сконструированных эритроидных клеток может содержать в различных вариантах осуществления по меньшей мере, приблизительно 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% сконструированных эритроидных клеток, где остальные эритроидные клетки в дозе не являются сконструированными.
III. СПОСОБЫ ПОЛУЧЕНИЯ ИСКУССТВЕННЫХ АНТИГЕНПРЕЗЕНТИРУЮЩИХ КЛЕТОК
Настоящее изобретение относится к различным способам получения aAPC.
Способы производства безъядерных эритроидных клеток, содержащих экзогенное средство (например, полипептид), описаны, например, в публикациях международных заявок № WO 2015/073587 и WO2015/153102, каждая из которых включена в настоящее описание в качестве ссылки в полном объеме.
В некоторых вариантах осуществления гемопоэтические клетки-предшественники, например, CD34+ гемопоэтические клетки-предшественники (например, клетки человека (например, взрослого человека) или мыши), приводят в контакт с нуклеиновой кислотой или нуклеиновыми кислотами, кодирующими один или более экзогенных полипептидов, и клеткам позволяют подвергаться экспансии и дифференцировке в культуре. В некоторых вариантах осуществления CD34+ клетки являются иммортализованными, например, содержат гены E6 и/или E7 вируса папилломы человека (HPV; например, HPV типа 16). В некоторых вариантах осуществления иммортализованная CD34+ гемопоэтическая клетка-предшественник является клеткой линии BEL-A (см. Trakarnasanga et al. (2017) Nat. Commun. 8: 14750). Дополнительные иммортализованные CD34+ гемопоэтические клетки-предшественники описаны в патентах США №№9951350 и 8975072. В некоторых вариантах осуществления иммортализованную CD34+ гемопоэтическую клетку-предшественника приводят в контакт с нуклеиновой кислотой или нуклеиновыми кислотами, кодирующими один или более экзогенных полипептидов, и клеткам позволяют подвергаться экспансии и дифференцировке в культуре.
В одном из аспектов настоящее изобретение относится к способу получения иммунологически совместимой искусственной антигенпрезентирующей клетки (aAPC), где aAPC включает эритроидную клетку или безъядерную клетку, презентирующую, например, содержащую на своей поверхности, экзогенный антигенный полипептид, где способ включает приведение ядросодержащей клетки в контакт с нуклеазой и по меньшей мере одной гРНК, расщепляющими эндогенную нуклеиновую кислоту, что приводит к экспрессии эндогенного антигенпрезентирующего полипептида, эндогенного якорного полипептида или эндогенного костимуляторного полипептида или что приводит к ингибированию экспрессии эндогенной микроРНК; встраивание экзогенной нуклеиновой кислоты, кодирующей экзогенный антигенный полипептид, в ядросодержащую клетку и культивирование ядросодержащей клетки в условиях, подходящих для экспрессии и презентирования экзогенного антигенного полипептида посредством эндогенного антигенпрезентирующего полипептида, энуклеацию и, таким образом, получение безъядерной клетки, и, таким образом, получение иммунологически совместимой aAPC. Способы получения aAPC представлены в настоящем описании, однако следует понимать, что эти способы являются неограничивающими.
Физические характеристики сконструированных эритроидных клеток
В некоторых вариантах осуществления эритроидные клетки, представленные в настоящем описании, имеют одну или более (например, 2, 3, 4 или более) физических характеристик, представленных в настоящем описании, например, осмотическую резистентность, размер клеток, концентрацию гемоглобина или содержание фосфатидилсерина. Не желая быть связанными какой-либо теорией, полагают, что в некоторых вариантах осуществления сконструированная эритроидная клетка, экспрессирующая экзогенный белок, имеет физические характеристики, напоминающие характеристики необработанной эритроидной клетки дикого типа. В отличие от этого, гипотонически нагруженная эритроидная клетка иногда демонстрирует аномальные физические характеристики, такие как повышенная осмотическая резистентность, измененный размер клеток, сниженная концентрация гемоглобина или повышенные уровни фосфатидилсерина на внешнем слое клеточной мембраны.
В некоторых вариантах осуществления сконструированная эритроидная клетка, например, безъядерная клетка, содержит экзогенный белок, кодируемый экзогенной нуклеиновой кислотой, неудерживаемой клеткой, неочищенной или несуществующей полностью вне эритроидной клетки. В некоторых вариантах осуществления эритроидная клетка находится в композиции, в которой отсутствует стабилизатор.
Осмотическая резистентность
В некоторых вариантах осуществления сконструированная эритроидная клетка, например, безъядерная клетка, демонстрирует, по существу, ту же осмотическую резистентность мембраны, что и выделенная, некультивированная эритроидная клетка, несодержащая экзогенный полипептид. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток имеет осмотическую резистентность менее 50% клеточного лизиса при 0,3%, 0,35%, 0,4%, 0,45% или 0,5% NaCl. Осмотическую резистентность можно анализировать способом по примеру 59 из WO2015/073587, включенного в настоящее описание в качестве ссылки в полном объеме.
Размер клеток
В некоторых вариантах осуществления сконструированная эритроидная клетка, например, безъядерная клетка, имеет приблизительно тот же диаметр или объем, что необработанная эритроидная клетка дикого типа. В некоторых вариантах осуществления популяция эритроидных клеток имеет средний диаметр приблизительно 4, 5, 6, 7 или 8 мкм, и, необязательно, стандартное отклонение в популяции составляет менее 1, 2 или 3 мкм. В некоторых вариантах осуществления один или более эритроидная клетка имеет диаметр приблизительно 4-8, 5-7 или приблизительно 6 мкм. В некоторых вариантах осуществления диаметр эритроидной клетки составляет менее приблизительно 1 мкм, более приблизительно 20 мкм, от приблизительно 1 мкм до приблизительно 20 мкм, от приблизительно 2 мкм до приблизительно 20 мкм, от приблизительно 3 мкм до приблизительно 20 мкм, от приблизительно 4 мкм до приблизительно 20 мкм, от приблизительно 5 мкм до приблизительно 20 мкм, от приблизительно 6 мкм до приблизительно 20 мкм, от приблизительно 5 мкм до приблизительно 15 мкм или от приблизительно 10 мкм до приблизительно 30 мкм. В некоторых вариантах осуществления диаметр клеток измеряют с использованием гематологической системы Advia 120.
В некоторых вариантах осуществления средний объем клетки в случае эритроидных клеток составляет более 10 фл, 20 фл, 30 фл, 40 фл, 50 фл, 60 фл, 70 фл, 80 фл, 90 фл, 100 фл, 110 фл, 120 фл, 130 фл, 140 фл, 150 фл или более 150 фл. В некоторых вариантах осуществления средний объем клетки в случае эритроидных клеток составляет менее 30 фл, 40 фл, 50 фл, 60 фл, 70 фл, 80 фл, 90 фл, 100 фл, 110 фл, 120 фл, 130 фл, 140 фл, 150 фл, 160 фл, 170 фл, 180 фл, 190 фл, 200 фл или менее 200 фл. В некоторых вариантах осуществления средний объем клетки в случае эритроидных клеток составляет 80-100, 100-200, 200-300, 300-400 или 400-500 фемтолитров (фл). В некоторых вариантах осуществления популяция эритроидных клеток имеет средний объем клетки, приведенный в этом абзаце, и стандартное отклонение в популяции составляет менее 50, 40, 30, 20, 10, 5 или 2 фл. В некоторых вариантах осуществления средний объем клетки измеряют, с использованием устройства для гематологических анализов, например, счетчик Коултера.
Концентрация гемоглобина
В некоторых вариантах осуществления сконструированная эритроидная клетка, например, безъядерная клетка, имеет содержание гемоглобина, схожее с его содержанием в необработанной эритроидной клетке дикого типа. В некоторых вариантах осуществления эритроидные клетки содержат более 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9% или более 10% фетального гемоглобина. В некоторых вариантах осуществления эритроидные клетки содержат по меньшей мере приблизительно 20, 22, 24, 26, 28 или 30 пг и, необязательно, до приблизительно 30 пг общего гемоглобина. В некоторых вариантах осуществления уровни гемоглобина определяют способом с использованием реактива Драбкина по примеру 33 из WO2015/073587, включенного в настоящее описание в качестве ссылки в полном объеме.
Содержание фосфатидилсерина
В некоторых вариантах осуществления сконструированная эритроидная клетка, например, искусственные антигенпрезентирующие клетки, представленные в настоящем описании, или безъядерная клетка, имеет приблизительно то же содержание фосфатидилсерина на внешнем слое клеточной мембраны, что и необработанная эритроидная клетка дикого типа. Фосфатидилсерин находится преимущественно на внутреннем слое клеточной мембраны необработанных эритроидных клеток дикого типа, и гипотоническая нагрузка может вызывать распределение фосфатидилсерина к внешнему слою, где он может запускать иммунный ответ. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (например, искусственные антигенпрезентирующие клетки, представленные в настоящем описании) или безъядерные клетки содержат менее приблизительно 30, 25, 20, 15, 10, 9, 8, 6, 5, 4, 3, 2 или 1% клеток, положительных при окрашивании аннексином V. В некоторых вариантах осуществления воздействие фосфатидилсерина анализируют посредством окрашивания аннексин-V-FITC, связывающегося преимущественно с PS, и измерения флуоресценции FITC посредством проточной цитометрии, например, с использованием способа по примеру 54 из WO2015/073587, включенного в настоящее описание в качестве ссылки в полном объеме.
Другие характеристики
В некоторых вариантах осуществления сконструированная эритроидная клетка (например, сконструированная безъядерная эритроидная клетка), или сконструированная безъядерная клетка, или популяция сконструированных эритроидных клеток или сконструированных безъядерных клеток содержит один или более (например, все) из эндогенного GPA (C235a), рецептора трансферрина (CD71), Band 3 (CD233) или интегрин альфа 4 (C49d). Эти белки можно измерять, например, как описано в примере 10 публикации международной заявки № WO 2018/009838, включенной в настоящее описание в качестве ссылки в полном объеме. Процентная доля GPA-положительных клеток и Band 3-положительных клеток, как правило, повышается во время созревания эритроидной клетки, и процентная доля интегрин альфа 4-положительных клеток, как правило, остается высокой на всем протяжении созревания.
В некоторых вариантах осуществления популяция эритроидных клеток содержит по меньшей мере приблизительно 50%, 60%, 70%, 80%, 90% или 95% (и, необязательно, до 90 или 100%) клеток, положительных по GPA. В некоторых вариантах осуществления наличие GPA определяют с использованием FACS.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит по меньшей мере приблизительно 50%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% GPA+ (т.е. CD235a+) клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит от приблизительно 50% до приблизительно 100% (например, от приблизительно 60% до приблизительно 100%, от приблизительно 65% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 75% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 85% до приблизительно 100%, от приблизительно 90% до приблизительно 100%, от приблизительно 95% до приблизительно 100%, от приблизительно 75% до приблизительно 99%, от приблизительно 80% до приблизительно 99%, от приблизительно 85% до приблизительно 99%, от приблизительно 90% до приблизительно 99%, от приблизительно 95% до приблизительно 99%, от приблизительно 75% до приблизительно 95%, от приблизительно 80% до приблизительно 95%, от приблизительно 85% до приблизительно 95%, от приблизительно 90% до приблизительно 95%, от приблизительно 95% до приблизительно 98%) GPA+ клеток. В некоторых вариантах осуществления наличие GPA определяют с использованием FACS.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит по меньшей мере приблизительно 50%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% CD71+ клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит от приблизительно 70% до приблизительно 100% (например, от приблизительно 75% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 85% до приблизительно 100%, от приблизительно 90% до приблизительно 100%, от приблизительно 95% до приблизительно 100%, от приблизительно 75% до приблизительно 99%, от приблизительно 80% до приблизительно 99%, от приблизительно 85% до приблизительно 99%, от приблизительно 90% до приблизительно 99%, от приблизительно 95% до приблизительно 99%, от приблизительно 75% до приблизительно 95%, от приблизительно 80% до приблизительно 95%, от приблизительно 85% до приблизительно 95%, от приблизительно 90% до приблизительно 95%, от приблизительно 95% до приблизительно 98%) CD71+ клеток. В некоторых вариантах осуществления наличие CD71 (рецептора трансферрина) определяют с использованием FACS.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит по меньшей мере приблизительно 50%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% CD233+ клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит от приблизительно 70% до приблизительно 100% (например, от приблизительно 75% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 85% до приблизительно 100%, от приблизительно 90% до приблизительно 100%, от приблизительно 95% до приблизительно 100%, от приблизительно 75% до приблизительно 99%, от приблизительно 80% до приблизительно 99%, от приблизительно 85% до приблизительно 99%, от приблизительно 90% до приблизительно 99%, от приблизительно 95% до приблизительно 99%, от приблизительно 75% до приблизительно 95%, от приблизительно 80% до приблизительно 95%, от приблизительно 85% до приблизительно 95%, от приблизительно 90% до приблизительно 95%, от приблизительно 95% до приблизительно 98%) CD233+ клетки. В некоторых вариантах осуществления наличие CD233 (Band 3) определяют с использованием FACS.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит по меньшей мере приблизительно 50%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% CD47+ клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит от приблизительно 70% до приблизительно 100% (например, от приблизительно 75% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 85% до приблизительно 100%, от приблизительно 90% до приблизительно 100%, от приблизительно 95% до приблизительно 100%, от приблизительно 75% до приблизительно 99%, от приблизительно 80% до приблизительно 99%, от приблизительно 85% до приблизительно 99%, от приблизительно 90% до приблизительно 99%, от приблизительно 95% до приблизительно 99%, от приблизительно 75% до приблизительно 95%, от приблизительно 80% до приблизительно 95%, от приблизительно 85% до приблизительно 95%, от приблизительно 90% до приблизительно 95%, от приблизительно 95% до приблизительно 98%) CD47+ клетки. В некоторых вариантах осуществления наличие CD47 (интегрин-ассоциированного белка) определяют с использованием FACS.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит по меньшей мере приблизительно 50%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% CD36- (CD36-отрицательных) клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит от приблизительно 70% до приблизительно 100% (например, от приблизительно 75% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 85% до приблизительно 100%, от приблизительно 90% до приблизительно 100%, от приблизительно 95% до приблизительно 100%, от приблизительно 75% до приблизительно 99%, от приблизительно 80% до приблизительно 99%, от приблизительно 85% до приблизительно 99%, от приблизительно 90% до приблизительно 99%, от приблизительно 95% до приблизительно 99%, от приблизительно 75% до приблизительно 95%, от приблизительно 80% до приблизительно 95%, от приблизительно 85% до приблизительно 95%, от приблизительно 90% до приблизительно 95%, от приблизительно 95% до приблизительно 98%) CD36- (CD36-отрицательных) клеток. В некоторых вариантах осуществления наличие CD36 определяют с использованием FACS.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит по меньшей мере приблизительно 50%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% CD34- (CD34-отрицательных) клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит от приблизительно 70% до приблизительно 100% (например, от приблизительно 75% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 85% до приблизительно 100%, от приблизительно 90% до приблизительно 100%, от приблизительно 95% до приблизительно 100%, от приблизительно 75% до приблизительно 99%, от приблизительно 80% до приблизительно 99%, от приблизительно 85% до приблизительно 99%, от приблизительно 90% до приблизительно 99%, от приблизительно 95% до приблизительно 99%, от приблизительно 75% до приблизительно 95%, от приблизительно 80% до приблизительно 95%, от приблизительно 85% до приблизительно 95%, от приблизительно 90% до приблизительно 95%, от приблизительно 95% до приблизительно 98%) CD34- (CD34-отрицательных) клеток. В некоторых вариантах осуществления наличие CD34 определяют с использованием FACS.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит по меньшей мере приблизительно 50%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% CD235a+/CD47+/CD233+ клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит от приблизительно 70% до приблизительно 100% (например, от приблизительно 75% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 85% до приблизительно 100%, от приблизительно 90% до приблизительно 100%, от приблизительно 95% до приблизительно 100%, от приблизительно 75% до приблизительно 99%, от приблизительно 80% до приблизительно 99%, от приблизительно 85% до приблизительно 99%, от приблизительно 90% до приблизительно 99%, от приблизительно 95% до приблизительно 99%, от приблизительно 75% до приблизительно 95%, от приблизительно 80% до приблизительно 95%, от приблизительно 85% до приблизительно 95%, от приблизительно 90% до приблизительно 95%, от приблизительно 95% до приблизительно 98%) CD235a+/CD47+/CD233+ клеток.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит по меньшей мере приблизительно 50%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% CD235a+/CD47+/CD233+/ CD34-/CD36- клеток. В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит от приблизительно 70% до приблизительно 100% (например, приблизительно от 75% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 85% до приблизительно 100%, от приблизительно 90% до приблизительно 100%, от приблизительно 95% до приблизительно 100%, от приблизительно 75% до приблизительно 99%, от приблизительно 80% до приблизительно 99%, от приблизительно 85% до приблизительно 99%, от приблизительно 90% до приблизительно 99%, от приблизительно 95% до приблизительно 99%, от приблизительно 75% до приблизительно 95%, от приблизительно 80% до приблизительно 95%, от приблизительно 85% до приблизительно 95%, от приблизительно 90% до приблизительно 95%, от приблизительно 95% до приблизительно 98%) CD235a+/CD47+/CD233+/ CD34-/CD36- клеток.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток, содержащая эритроидные клетки, содержит менее приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% эхиноцитов.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (например, искусственных антигенпрезентирующих клеток, представленных в настоящем описании), содержащая эритроидные клетки, содержит менее приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% эхиноцитов.
В некоторых вариантах осуществления популяция сконструированных эритроидных клеток (сконструированных безъядерных эритроидных клеток) или сконструированных безъядерных клеток содержит менее приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% пиреноцитов.
В некоторых вариантах осуществления эритроидная клетка является безъядерной, например, популяция клеток, содержащих эритроидные клетки, используемая в качестве терапевтического препарата, представленного в настоящем описании, является более чем на 50%, 60%, 70%, 80%, 90% безъядерной. В некоторых вариантах осуществления клетка, например, эритроидная клетка, содержит ядро, являющееся нефункциональным, например, подвергнутым инактивации. В некоторых вариантах осуществления сконструированная эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления сконструированная эритроидная клетка является ядросодержащей клеткой.
Выделение эритроцитов
Зрелые эритроциты можно выделять различными способами, такими как, например, с использованием вошера для клеток, проточного клеточного сепаратора, разделения в градиенте плотности, активируемой флуоресценцией сортировки клеток (FACS), иммуномагнитное истощение Miltenyi (MACS) или комбинации этих способов (см., например, van der Berg et al., Clin. Chem. 33:1081-1082 (1987); Bar-Zvi et al., J. Biol. Chem. 262:17719-17723 (1987); Goodman et al., Exp. Biol. Med. 232:1470-1476 (2007)).
Эритроциты можно выделять из цельной крови посредством простого центрифугирования (см., например, van der Berg et al., Clin. Chem. 33:1081-1082 (1987)). Например, цельную кровь с добавлением ЭДТА можно центрифугировать при 800×g в течение 10 мин при 4°C. Удаляют богатую тромбоцитами плазму и лейкоцитарную пленку и промывают эритроциты три раза изотоническим физиологическим раствором (NaCl, 9 г/л).
Альтернативно, эритроциты можно выделять с использованием центрифугирования в градиенте плотности с различными средами для разделения, такими как, например, фиколл, гипак, гистопак, перколл, Sigmacell или их комбинации. Например, объем гистопак-1077 наслаивают на равный объем гистопак-1119. Цельную кровь с добавлением ЭДТА, разведенную 1:1 в равном объеме изотонического физиологического раствора (NaCl, 9 г/л), наслаивают на гистопак и центрифугируют образец при 700×g в течение 30 мин при комнатной температуре. В этих условиях гранулоциты мигрируют к поверхности 1077/1119, лимфоциты, другие мононуклеарные клетки и тромбоциты остаются на поверхности раздела плазма/1077, и эритроциты осаждаются. Эритроциты дважды промывают изотоническим физиологическим раствором.
Альтернативно, эритроциты можно выделять посредством центрифугирования с использованием ступенчатого градиента перколла (См., например, Bar-Zvi et al., J. Biol. Chem. 262:17719-17723 (1987)). Например, свежую кровь смешивают с раствором антикоагулянта, содержащим 75 мМ цитрат натрия и 38 мМ лимонную кислоту, и клетки быстро промывают Hepes-забуференным физиологическим раствором. Лейкоциты и тромбоциты удаляют посредством адсорбции с использованием смеси α-целлюлозы и Sigmacell (1:1). Эритроциты далее выделяют из ретикулоцитов и остаточных лейкоцитов посредством центрифугирования в ступенчатом градиенте 45/75% перколла в течение 10 мин при 2500 об./мин. с помощью ротора Sorvall SS34. Эритроциты выделяют в осадке, в то время как ретикулоциты собираются на поверхности раздела 45/75%, и оставшиеся лейкоциты собираются на поверхности раздела 0/45%. Перколл удаляют из эритроцитов с помощью нескольких промывок в Hepes-забуференном физиологическом растворе. Другие материалы, которые можно использовать для создания градиентов плотности для выделения эритроцитов, включают OPTIPREP, 60%-ный раствор йодиксанола в воде (Axis-Shield, Dundee, Scotland).
Эритроциты можно отделять от ретикулоцитов, например, с использованием проточной цитометрии (см., например, Goodman el al., Exp. Biol. Med. 232:1470-1476 (2007)). В этом случае цельную кровь центрифугируют (550×g, 20 мин, 25°C) для отделения клеток от плазмы. Клеточный осадок ресуспендируют в фосфатно-солевом буфере, а затем фракционируют на фиколл-паке (плотность 1,077), например, посредством центрифугирования (400×g, 30 мин, 25°C), для отделения эритроцитов от лейкоцитов. Получаемый клеточный осадок ресуспендируют в RPMI, дополненной 10% эмбриональной телячьей сывороткой, и сортируют с помощью устройства для FACS, такого как, например, Becton Dickinson FACSCalibur (BD Biosciences, Franklin Lakes, N.J., USA), с учетом размера и гранулярности.
Эритроциты можно выделять посредством иммуномагнитного истощения (см., например, Goodman, el al., (2007) Exp. Biol. Med. 232:1470-1476). В этом случае магнитные частицы со специфическим в отношении типа клеток антителами используют для элиминации не-эритроцитов. Например, эритроциты выделяют из большей части других компонентов крови с использованием градиента плотности, как представлено в настоящем описании, с последующим иммуномагнитным истощением любых остаточных ретикулоцитов. Клетки предварительно обрабатывают сывороткой с антителом человека в течение 20 мин при 25°C, а затем обрабатывают антителами против ретикулоцит-специфических антигенов, таких как, например, CD71 и CD36. Антитела можно напрямую присоединять к магнитным частицам или конъюгировать с PE, например, с которым будут реагировать магнитные частицы с антителом против PE. С помощью комплекса антитело-магнитная частица можно селективно выделять остаточные ретикулоциты, например, из популяции эритроцитов.
Эритроциты также можно выделять с использованием афереза. Аферез включает получение цельной крови из пациента или донора, отделение компонентов крови посредством центрифугирования или сортировки клеток, отбора одной или более из отделенных частей и переливания остальных компонентов обратно пациенту или донору. Для этой цели в настоящее время используют ряд устройств, таких как, например, устройства Amicus и Alyx от Baxter (Deerfield, Ill., USA), устройство Trima Accel от Gambro BCT (Lakewood, Colo., USA) и устройство MCS+9000 от Haemonetics (Braintree, Mass., USA). Для достижения подходящей степени чистоты клеток могут потребоваться дополнительные способы очистки.
Ретикулоциты представляют собой незрелые эритроциты и составляют приблизительно 1% эритроцитов в организме человека. Ретикулоциты развиваются и созревают в костном мозге. После высвобождения в кровоток ретикулоциты быстро подвергаются терминальной дифференцировке в зрелые эритроциты. Подобно зрелым эритроцитам, ретикулоциты не имеют клеточного ядра. В отличие от зрелых эритроцитов, ретикулоциты сохраняют способность осуществлять синтез белка. В некоторых вариантах осуществления aAPC включает безъядерный эритроцит.
Ретикулоциты разного возраста можно выделять из периферической крови с учетом различий в плотности клетки при созревании ретикулоцитов. Ретикулоциты можно выделять из периферической крови с использованием дифференциального центрифугирования с различными градиентами плотности. Например, для выделения ретикулоцитов можно использовать градиенты перколла (см., например, Noble el al., Blood 74:475-481 (1989)). Стерильные изотонические растворы перколла с плотностью 1,096 и 1,058 г/мл получают посредством разведения перколла (Sigma-Aldrich, Saint Louis, Mo., USA) до конечной концентрации 10 мМ триэтаноламина, 117 мМ NaCl, 5 мМ глюкозы и 1,5 мг/мл бычьего сывороточного альбумина (BSA). Эти растворы имеют осмолярность от 295 до 310 мОсм. Пять миллилитров, например, из первого раствора перколла (плотность 1,096) добавляют в стерильную коническую центрифужную пробирку 15 мл. Два миллилитра, например, из второго раствора перколла (плотность 1,058) наслаивают на первый раствор перколла с более высокой плотностью. От двух до четырех миллилитров цельной крови наслаивают сверху в пробирке. Пробирку центрифугируют при 250×g в течение 30 мин в центрифуге с охлаждением с колебательными пробирочными штативами. Ретикулоциты и некоторые лейкоциты мигрируют к границе раздела между двумя слоями перколла. Клетки на поверхности раздела переносят в новую пробирку и дважды промывают фосфатно-солевым буфером (PBS) с 5 мМ глюкозой, 0,03 мМ азидом натрия и 1 мг/мл BSA. Остаточные лейкоциты удаляют посредством хроматографии в PBS на эксклюзионной колонке.
Альтернативно, ретикулоциты можно выделять посредством положительной селекции с использованием подхода иммуномагнитного разделения (см., например, Brun et al., Blood 76:2397-2403 (1990)). В этом подходе используют преимущество большого количества рецепторов трансферрина, экспрессирующихся на поверхности ретикулоцитов, относительно эритроцитов перед созреванием. Магнитные частицы, покрытые антителом против рецептора трансферрина, можно использовать для селективного выделения ретикулоцитов из смешанной популяции клеток крови. Антитела против рецептора трансферрина разных видов млекопитающего, включая человека, доступны в коммерческих источниках (например, Affinity BioReagents, Golden, Colo., USA; Sigma-Aldrich, Saint Louis, Mo., USA). Антитело против трансферрина можно напрямую связывать с магнитными частицами. Альтернативно, антитело против трансферрина можно косвенно связывать с магнитными частицами с помощью вторичного антитела. Например, моноклональное антитело мыши 10D2 (Affinity BioReagents, Golden, Colo., USA) против трансферрина человека можно смешивать с иммуномагнитными частицами, покрытыми иммуноглобулином G овцы против мыши (Dynal/Invitrogen, Carlsbad, Calif., USA). Затем иммуномагнитные частицы инкубируют с лейкоцит-истощенной фракцией эритроцитов. Частицы и эритроциты инкубируют при 22°C при осторожном перемешивании в течение 60-90 мин с последующим выделением частиц с прикрепленными ретикулоцитами с использованием магнитного поля. Выделенные ретикулоциты можно удалять из магнитных частиц с использованием, например, раствора DETACHaBEAD (Invitrogen, Carlsbad, Calif., USA). Альтернативно, ретикулоциты можно выделять при выращивании и созревании in vitro CD34+ гемопоэтических стволовых клеток способами, представленными в настоящем описании.
Терминально дифференцированные безъядерные эритроциты можно отделять от других клеток с учетом содержания в них ДНК. В неограничивающем примере клетки сначала метят витальным красителем ДНК, таким как Hoechst 33342 (Invitrogen Corp.). Hoechst 33342 является проникающим в клетки ядерным контрастным красителем, испускающим синюю флуоресценцию при связывании с двухцепочечной ДНК. Недифференцированные клетки-предшественники, макрофаги или другие ядросодержащие клетки в культуре окрашивают Hoechst 33342, в то время как безъядерные эритроциты являются Hoechst-отрицательными. Hoechst-положительные клетки можно отделять от безъядерных эритроцитов с использованием активируемой флуоресценцией сортировки клеток или других способов сортировки клеток. Краситель Hoechst можно удалять из выделенных эритроцитов посредством диализа или других подходящих способов.
Носители для полипептидов, представленных в настоящем описании
В то время как во многих вариантах осуществления в настоящем описании один или более (например, два или более) экзогенных полипептидов находятся на безъядерной эритроидной клетке или в ней, следует понимать, что любой полипептид или комбинация экзогенных полипептидов, представленных в настоящем описании, также может находиться на другом носителе или в нем. Носитель может включать, например, клетку, эритроидную клетку, частицу, наночастицу, мицеллу, липосому или экзосому. Например, в некоторых аспектах настоящее изобретение относится к носителю (например, клетке, эритроидной клетке, частице, наночастице, мицелле, липосоме или экзосоме), содержащему, например, на своей поверхности, одно или более средств, представленных в настоящем описании. В некоторых вариантах осуществления одно или более средств включают средство, выбранное из полипептида из любой из таблиц 1 или 14-24, или его фрагмента или варианта, или молекулы антитела против него. В некоторых вариантах осуществления носитель содержит два или более средств, представленных в настоящем описании, например, любую пару средств, представленных в настоящем описании.
Гетерогенные популяции клеток
В то время как во многих вариантах осуществления в настоящем описании один или более (например, два или более) экзогенных полипептидов находятся на одной клетке или в ней, следует понимать, что любой полипептид или комбинация полипептидов, представленных в настоящем описании, также может находиться на множестве клеток. Например, в некоторых аспектах настоящее изобретение относится к множеству эритроидных клеток, где первая клетка из множества содержит первый экзогенный полипептид, и вторая клетка из множества содержит второй экзогенный полипептид. В некоторых вариантах осуществления множество клеток содержит два или более полипептида, представленных в настоящем описании, например, любую пару полипептидов, представленных в настоящем описании. В некоторых вариантах осуществления менее 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20%, 10%, 5%, 2% или 1% клеток в популяции содержат и первый экзогенный полипептид, и второй экзогенный полипептид.
Клетки, инкапсулированные в мембране
В некоторых вариантах осуществления безъядерные эритроидных клетки или другие носители, представленные в настоящем описании, инкапсулируют в мембране, например, полупроницаемой мембране. В некоторых вариантах осуществления мембрана содержит полисахарид, например, анионный полисахарид альгинат. В некоторых вариантах осуществления полупроницаемая мембрана не пропускает клетки, но позволяет проходить низкомолекулярным соединениям или макромолекулам, например, метаболитам, белкам или ДНК. В некоторых вариантах осуществления мембрана является мембраной, описанной в Lienert et al., "Synthetic biology in mammalian cells: next generation research tools and therapeutics" Nature Reviews Molecular Cell Biology 15, 95-107 (2014), включенной в настоящее описание в качестве ссылки в полном объеме. Не желая быть связанными какой-либо теорией, полагают, что в некоторых вариантах осуществления мембрана защищает клетки от иммунной системы и/или удерживает множество клеток вблизи друг друга, облегчая взаимодействие друг с другом или продуктами друг друга.
Эритроцитарные клетки-предшественники
Настоящее изобретение относится к сконструированным эритроцитарным клеткам-предшественникам и способам получения сконструированных эритроцитарных клеток-предшественников, ретикулоцитов и эритроцитов.
Плюрипотентные стволовые клетки дают начало эритроцитами посредством эритропоэза. Стволовая клетка выглядит как небольшой лимфоцит и не имеет функциональных способностей эритроцита. Стволовые клетки имеют способность к неограниченному делению, отсутствующую у зрелых клеток. Некоторые из дочерних клеток, возникающих из стволовой клетки, приобретают эритроидные характеристики с накоплением поколений и с течением времени. Большинство из эритроидных клеток в костном мозге имеют другую морфологию, но ориентацию на эритроидное созревание наблюдают даже у клеток, не приобретших морфологические признаки, отличающиеся от эритроидного ростка. Эти клетки распознают по типу колоний, которые они образуют in vitro. Различают две такие клетки. Эритроидная бурст-образующая единица (BFU-E) возникает из стволовой клетки и дает начало эритроидной колониеобразующей единице (CFU-E). CFU-E дает начало пронормобласту, наиболее незрелой из эритроидных клеток с отдельной морфологией. BFU-E и CFU-E образуют очень небольшую фракцию клеток костного мозга. Морфологически определяют пять эритроидных предшественников в костном мозге, окрашиваемых по Романовскому-Гимзе. Пятью стадиями от наиболее незрелой до наиболее зрелой являются проэритробласт, базофильный нормобласт (ранний эритробласт), полихромный нормобласт (промежуточный эритробласт), ортохромный нормобласт (поздний эритробласт) и ретикулоцит. BFU-E (эритроидная бурст-образующая единица), CFU-E (эритроидная колониеобразующая единица), пронормобласт (проэритробласт), базофильный нормобласт, полихромный нормобласт и ортохромный нормобласт являются линейно-специфическими.
В таблице 13 ниже приведены морфологические признаки предшественников эритроцитов и эритроцитарных клеток.
Таблица 13. Морфологические признаки предшественников эритроцитов и эритроцитарных клеток
Нормальные эритроциты человека экспрессируют CD36, молекулу адгезии моноцитов, тромбоцитов и эндотелиальных клеток (van Schravendijk MR et al., Blood. 1992 Oct 15;80(8):2105-14). Таким образом, в некоторых вариантах осуществления для идентификации эритроцитов человека можно использовать антитело против CD36.
Любой известный в этой области тип клеток, способных дифференцироваться в эритроцит, т.е. любую эритроцитарную клетку-предшественника, можно модифицировать способами, представленными в настоящем описании, для получения сконструированных эритроцитарных клеток-предшественников. В некоторых вариантах осуществления эритроцитарные клетки-предшественники, модифицированные способами, представленными в настоящем описании, являются клетками, находящимися в процессе дифференцировки в эритроцит, т.е. клетки имеют тип, о котором известно, что он существует в ходе эритропоэза млекопитающего. Например, клетки могут являться плюрипотентными гемопоэтическими стволовыми клетками (HSC) или CD34+ клетками, мультипотентными миелоидными клетками-предшественниками, клетками CFU-S, клетками BFU-E, клетками CFU-E, пронормобластами (проэритробластами), базофильными нормобластами, полихромными нормобластами и ортохромными нормобластами. Модифицированные эритроцитарные клетки-предшественники, представленные в настоящем описании, могут дифференцироваться в сконструированные ретикулоциты или эритроциты in vitro при использовании известных в этой области способов, т.е. при использовании молекул, о которых известно, что они стимулируют эритропоэз, например, SCF, эритропоэтина, ИЛ-3 и/или ГМ-КСФ, представленных в настоящем описании ниже. Альтернативно, модифицированные эритроцитарные клетки-предшественники предоставляют в композиции по настоящему изобретению, и они могут дифференцироваться в эритроциты после введения индивидууму in vivo.
В некоторых вариантах осуществления эритроидную клетку-предшественника не модифицируют генетически для делеции и/или изменения экспрессии эндогенного антигенпрезентирующего полипептида (например, молекулы MHC класса I или MHC класса II).
В некоторых вариантах осуществления эритроцитарные клетки-предшественники, например, гемопоэтические стволовые клетки, получают от донора с первой отрицательной группой крови.
Культивирование
Источники для получения aAPC, представленных в настоящем описании, включают циркулирующие клетки, такие как эритроидные клетки. Подходящий источник клеток можно выделять из индивидуума, как представлено в настоящем описании, из полученных из пациента гемопоэтических или эритроидных клеток-предшественников, полученных из иммортализованных линий эритроидных клеток, или полученных из индуцированных плюрипотентных стволовых клеток, необязательно, культивируемых и дифференцированных. Способы получения эритроцитов способами культивирования клеток хорошо известны в этой области, например, Giarratana et al., Blood 2011, 118:5071, Huang et al., Mol Ther 2013, предварительная электронная публикация от 3 сентября, или Kurita et al., PLOS One 2013, 8:e59890, содержание каждой из которых включено в настоящее описание в качестве ссылки в полном объеме. Способы варьируются в зависимости от факторов роста, исходных линий клеток, времени культивирования и морфологических признаков, по которым охарактеризовывают получаемые клетки. Также разработаны системы культивирования для получения крови, которую можно использовать вместо переливания донорской крови (Fibach et al. 1989 Blood 73:100). Недавно показано, что CD34+ клетки дифференцировались до ретикулоцитарной стадии, а затем их успешно переливали человеку (Giarratana et al., Blood 2011, 118:5071). Следует понимать, что в некоторых вариантах осуществления полученные из пациента гемопоэтические или эритроидные клетки-предшественники, например, гемопоэтические стволовые клетки, получают из донора с первой отрицательной группой крови.
Настоящее изобретение относится к способам культивирования эритроидных клеток и aAPC, полученных из эритроидных клеток. Эритроидные клетки можно культивировать из гемопоэтических клеток-предшественников, включая, например, CD34+ гемопоэтические клетки-предшественники (Giarratana et al., Blood 2011, 118:5071), индуцированные плюрипотентные стволовые клетки (Kurita et al., PLOS One 2013, 8:e59890) и эмбриональные стволовые клетки (Hirose et al. 2013 Stem Cell Reports 1:499). В этой области известны смеси факторов роста и дифференцировки, подходящие для экспансии и дифференцировки клеток-предшественников. Неограничивающие примеры подходящих факторов экспансии и дифференцировки включают фактор стволовых клеток (SCF), интерлейкин (ИЛ), такой как ИЛ-1, ИЛ-2, ИЛ-3, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-7, ИЛ-8, ИЛ-9, ИЛ-11, ИЛ-12, КСФ, Г-КСФ, тромбопоэтин (TPO), ГМ-КСФ, эритропоэтин (EPO), Flt3, Flt2, PIXY 321 и фактор ингибирования лейкоза (LIF).
Эритроидные клетки можно культивировать из гемопоэтических предшественников, таких как CD34+ клетки, посредством приведения клеток-предшественников в контакт с определенными факторами в многостадийном способе культивирования. Например, эритроидные клетки можно культивировать из гемопоэтических предшественников в трехстадийном способе.
Первая стадия может включать приведение клеток в культуре в контакт с фактором стволовых клеток (SCF) в количестве 1-1000 нг/мл, эритропоэтином (EPO) в количестве 1-100 ед./мл и интерлейкином-3 (ИЛ-3) в количестве 0,1-100 нг/мл. Первая стадия, необязательно, включает приведение клеток в культуре в контакт с лигандом, связывающим и активирующим ядерный рецептор гормонов, таким как, например, глюкокортикоидный рецептор, эстрогеновый рецептор, прогестероновый рецептор, андрогеновый рецептор или рецептор прегнана x. Лиганды для этих рецепторов включают, например, кортикостероид, такой как, например, дексаметазон в количестве 10 нМ-100 мкМ или гидрокортизон в количестве 10 нМ-100 мкМ; эстроген, такой как, например, бета-эстрадиол в количестве 10 нМ-100 мкМ; прогестоген, такой как, например, прогестерон в количестве 10 нМ-100 мкМ, гидроксипрогестерон в количестве 10 нМ-100 мкМ, 5a-дигидропрогестерон в количестве 10 нМ-100 мкМ, 11-дезоксикортикостерон в количестве 10 нМ-100 мкМ или прогестин, такой как, например, хлормадинон ацетат в количестве 10 нМ-100 мкМ; андроген, такой как, например, тестостерон в количестве 10 нМ-100 мкМ, дигидротестостерон в количестве 10 нМ-100 мкМ или андростендион в количестве 10 нМ-100 мкМ; или лиганд рецептора прегнана x, такой как, например, рифампицин в количестве 10 нМ-100 мкМ, гиперфорин в количестве 10 нМ-100, экстракт зверобоя продырявленного (гиперицин) в количестве 10 нМ-100 мкМ, или витамин E-подобные молекулы, такие как, например, токоферол в количестве 10 нМ-100. Первая стадия, необязательно, также может включать приведение клеток в культуре в контакт с инсулин-подобной молекулой, такой как, например, инсулин в количестве 1-50 мкг/мл, инсулиноподобный фактор роста 1 (IGF-1) в количестве 1-50 мкг/мл, инсулиноподобный фактор роста 2 (IGF-2) в количестве 1-50 мкг/мл, или механозависимый фактор роста в количестве 1-50 мкг/мл. Первая стадия, необязательно, может дополнительно включать приведение клеток в культуре в контакт с трансферрином в количестве 0,1-5 мг/мл.
Первая стадия, необязательно, может включать приведение клеток в культуре в контакт с одним или более интерлейкинами (ИЛ) или факторами роста, такими как, например, ИЛ-1, ИЛ-2, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-7, ИЛ-8, ИЛ-9, ИЛ-11, ИЛ-12, гранулоцитарный колониестимулирующий фактор (Г-КСФ), макрофагальный колониестимулирующий фактор (М-КСФ), гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ), тромбопоэтин, фактор роста фибробластов (FGF), фактор роста тромбоцитов (PDGF), трансформирующий фактор роста бета (TGF-B), фактор некроза опухоли альфа (ФНОα), фактор роста и развития мегакариоцитов (MGDF), фактор ингибирования лейкоза (LIF) и лиганд Flt3. Каждый интерлейкин или фактор роста, как правило, можно добавлять в концентрации 0,1-100 нг/мл. Первая стадия, необязательно, также может включать приведение клеток в культуре в контакт с белками сыворотки или небелковыми молекулами, такими как, например, эмбриональная телячья сыворотка (1-20%), плазма человека (1-20%), плазманат (1-20%), сыворотка человека (1-20%), альбумин (0,1-100 мг/мл) или гепарин (0,1-10 ед./мл).
Вторая стадия может включать приведение клеток в культуре в контакт с фактором стволовых клеток (SCF) в количестве 1-1000 нг/мл и эритропоэтином (EPO) в количестве 1-100 ед./мл. Вторая стадия, необязательно, также может включать приведение клеток в культуре в контакт с инсулин-подобной молекулой, такой как например, инсулин в количестве 1-50 мкг/мл, инсулиноподобный фактор роста 1 (IGF-1) в количестве 1-50 мкг/мл, инсулиноподобный фактор роста 2 (IGF-2) в количестве 1-50 мкг/мл или механозависимый фактор роста в количестве 1-50 мкг/мл. Вторая стадия, необязательно, может дополнительно включать приведение клеток в культуре в контакт с трансферрином в количестве 0,1-5 мг/мл. Вторая стадия, необязательно, также может включать приведение клеток в культуре в контакт с белками сыворотки или небелковыми молекулами, такими как, например, эмбриональная телячья сыворотка (1-20%), плазма человека (1-20%), плазманат (1-20%), сыворотка человека (1-20%), альбумин (0,1-100 мг/мл) или гепарин (0,1-10 ед./мл).
Третья стадия может включать приведение клеток в культуре в контакт с эритропоэтином (EPO) в количестве 1-100 ед./мл. Третья стадия, необязательно, может включать приведение клеток в культуре в контакт с фактором стволовых клеток (SCF) в количестве 1-1000 нг/мл. Третья стадия, необязательно, может дополнительно включать приведение клеток в культуре в контакт с инсулин-подобной молекулой, такой как, например, инсулин в количестве 1-50 мкг/мл, инсулиноподобный фактор роста 1 (IGF-1) в количестве 1-50 мкг/мл, инсулиноподобный фактор роста 2 (IGF-2) в количестве 1-50 мкг/мл или механозависимый фактор роста в количестве 1-50 мкг/мл. Третья стадия, необязательно, также может включать приведение клеток в культуре в контакт с трансферрином в количестве 0,1-5 мг/мл. Третья стадия, необязательно, также может включать приведение клеток в культуре в контакт с белками сыворотки или небелковыми молекулами, такими как, например, эмбриональная телячья сыворотка (1-20%), плазма человека (1-20%), плазманат (1-20%), сыворотка человека (1-20%), альбумин (0,1-100 мг/мл) или гепарин (0,1-10 ед./мл).
В некоторых вариантах осуществления способы экспансии и дифференцировки aAPC, включающих эритроидную клетку, например, безъядерную клетку, презентирующую (например, содержащую на своей поверхности) один или более экзогенных полипептидов, не включают культивирование aAPC в среде, содержащей лиганд миелопролиферативного рецептора (mpl).
Способ культивирования, необязательно, может включать приведение клеток известным в этой области способом в контакт с молекулой, например, молекулой ДНК, молекулой РНК, мРНК, миРНК, микроРНК, lncRNA, shRNA, гормоном или низкомолекулярным соединением, активирующим или приводящим к нокдауну одного или более генов. Гены-мишени могут включать, например, гены, кодирующие фактор транскрипции, фактор роста или рецептор фактора роста, включая, в качестве неограничивающих примеров, например, GATA1, GATA2, cMyc, hTERT, p53, EPO, SCF, инсулин, EPO-R, SCF-R, трансферрин-R, инсулин-R.
В некоторых вариантах осуществления CD34+ клетки помещают в культуру, содержащую различные количества IMDM, FBS, глутамина, BSA, голотрансферрина, инсулина, дексаметазона, бета-эстрадиола, ИЛ-3, SCF и эритропоэтина, в трех различных стадиях дифференцировки в течение всего 22 дней.
В некоторых вариантах осуществления CD34+ клетки помещают в культуру, содержащую различные количества IMDM, FBS, глутамина, BSA, голотрансферрина, инсулина, дексаметазона, бета-эстрадиола, ИЛ-3, SCF и тромбопоэтина, в трех различных стадиях дифференцировки в течение всего 14 дней.
В некоторых вариантах осуществления CD34+ клетки помещают в культуру, содержащую различные количества IMDM, FBS, глутамина, BSA, голотрансферрина, инсулина, дексаметазона, бета-эстрадиола, ИЛ-3, SCF и Г-КСФ, в трех различных стадиях дифференцировки в течение всего 15 дней.
В некоторых вариантах осуществления эритроидные клетки подвергают экспансии по меньшей мере в 100, 1000, 2000, 5000, 10000, 20000, 50000 или 100000 раз (и, необязательно, до 100000, 200000 или 500000 раз). В некоторых вариантах осуществления количество клеток измеряют с использованием автоматизированного счетчика клеток.
В некоторых вариантах осуществления популяция эритроидных клеток содержит по меньшей мере 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95 или 98% (и, необязательно, до приблизительно 80, 90 или 100%) сконструированных эритроидных клеток. В некоторых вариантах осуществления энуклеацию измеряют посредством FACS с использованием ядерного окрашивания. В некоторых вариантах осуществления по меньшей мере 30, 35, 40, 45, 50, 55, 60, 65, 70, 75 или 80% (и, необязательно, до приблизительно 70, 80, 90 или 100%) эритроидных клеток в популяции содержат один или более (например, 2, 3, 4 или более) экзогенных полипептидов. В некоторых вариантах осуществления экспрессию полипептидов измеряют по эритроидным клеткам с использованием меченых антител против полипептидов. В некоторых вариантах осуществления по меньшей мере 30, 35, 40, 45, 50, 55, 60, 65, 70, 75 или 80% (и, необязательно, до приблизительно 70, 80, 90 или 100%) эритроидных клеток в популяции являются безъядерными и содержат один или более (например, 2, 3, 4 или более) экзогенных полипептидов. В некоторых вариантах осуществления популяция эритроидных клеток содержит приблизительно 1×109-2×109, 2×109-5×109, 5×109-1×1010, 1×1010-2×1010, 2×1010-5×1010, 5×1010-1×1011, 1×1011-2×1011, 2×1011-5×1011, 5×1011-1×1012, 1×1012-2×1012, 2×1012-5×1012 или 5×1012-1×1013 клеток.
В некоторых вариантах осуществления во время культивирования желательной может являться лишь частичная дифференцировка эритроидных клеток-предшественников, например, гемопоэтических стволовых клеток, in vitro, что позволяет дальнейшей дифференцировке, например, дифференцировке в ретикулоциты или полностью зрелые эритроциты, происходить после введения индивидууму in vivo (см., например, Neildez-Nguyen et al., Nature Biotech. 20:467-472 (2002)). Следует понимать, что в различных вариантах осуществления изобретения созревание и/или дифференцировку in vitro можно прекращать на любой желаемой стадии. Например, выделенные CD34+ гемопоэтические стволовые клетки можно подвергать экспансии in vitro, как описано где-либо в настоящем описании, например, в среде, содержащей различные факторы, включая, например, интерлейкин-3, лиганд Flt3, фактор стволовых клеток, тромбопоэтин, эритропоэтин, трансферрин и инсулин-подобный фактор роста, для достижения желаемой стадии дифференцировки. Получаемые сконструированные эритроидные клетки можно охарактеризовывать по поверхностной экспрессии CD36 и GPA и других характеристикам, специфическим для конкретного желаемого типа клеток, и можно переливать их индивидууму, в организме которого происходит терминальная дифференцировка для созревания эритроцитов.
В некоторых вариантах осуществления сконструированные эритроидные клетки подвергают частичной экспансии из эритроидных клеток-предшественников до любой стадии созревания перед энуклеацией, но не включая ее, и, таким образом, они остаются ядросодержащими клетками, например, эритроцитарными клетками-предшественниками. В некоторых вариантах осуществления получаемые клетки являются ядросодержащими и эритроидными линейно-специфическими. В некоторых вариантах осуществления получаемые клетки выбраны из мультипотентных миелоидных клеток-предшественников, клеток CFU-S, клеток BFU-E, клеток CFU-E, пронормобластов (проэритробластов), базофильных нормобластов, полихромных нормобластов и ортохромных нормобластов. Конечные стадии дифференцировки, включая энуклеацию, происходят после введения индивидууму сконструированной эритроидной клетки, т.е. в таких вариантах осуществления стадия энуклеации происходит in vivo. В другом варианте осуществления сконструированные эритроидные клетки подвергают экспансии и дифференцировке in vitro до стадии энуклеации для получения, например, ретикулоцитов. В таких вариантах осуществления, если сконструированные эритроидные клетки дифференцируются до стадии ретикулоцитов, конечная стадия дифференцировки в эритроциты происходит только после введения сконструированной эритроидной клетки индивидууму, т.е. стадия терминальной дифференцировки происходит in vivo. В другом варианте осуществления сконструированные эритроидные клетки подвергают экспансии и дифференцировке in vitro до стадии терминальной дифференцировки для получения эритроцитов.
Также следует понимать, что в некоторых вариантах осуществления сконструированные эритроидные клетки можно подвергать экспансии и дифференцировке из эритроидных клеток-предшественников, например, гемопоэтических стволовых клеток, так, чтобы они становились гемопоэтическими клетками другой линии, например, чтобы они становились тромбоцитами. Специалистам в этой области хорошо известны способы созревания и дифференцировки гемопоэтических клеток различных линий, таких как тромбоциты. В некоторых вариантах осуществления такие сконструированные тромбоциты, экспрессирующие экзогенные полипептиды, как представлено в настоящем описании, считают входящими в объем настоящего изобретения.
В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления сконструированная эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления сконструированная эритроидная клетка является ядросодержащей клеткой.
В некоторых вариантах осуществления безъядерная клетка, представленная в настоящем описании, является тромбоцитом. В этой области известны способы производства тромбоцитов in vitro (см., например, Wang and Zheng (2016) Springerplus 5(1): 787 и патент США №9574178). Способы производства тромбоцитов, включающих экзогенный полипептид, описаны, например, в публикациях международных патентных заявок №№ WO 2015/073587 и WO2015/153102, каждая из которых включена в настоящее описание в качестве ссылки в полном объеме. Получение тромбоцитов частично регулируется сигнальными механизмами, индуцируемыми взаимодействием между тромбопоэтином (TPO) и его клеточным рецептором TPOR/MPUc-MPL. Кроме того, показано, что многие цитокины (например, фактор стволовых клеток (SCF), ИЛ-1, ИЛ-3, ИЛ-6, ИЛ-11, фактор ингибирования лейкоза (LIF), Г-КСФ, ГМ-КСФ, М-КСФ, эритропоэтин (EPO), лиганд kit и интерферон) обладают тромбоцитопоэтической активностью.
В некоторых вариантах осуществления тромбоциты получают из гемопоэтических клеток-предшественников, таких как CD34+ гемопоэтические стволовые клетки, индуцированные плюрипотентные стволовые клетки или эмбриональные стволовые клетки. В некоторых вариантах осуществления тромбоциты получают посредством приведения клеток-предшественников в контакт с определенными факторами в многостадийном способе культивирования. В некоторых вариантах осуществления многостадийный способ культивирования включает: культивирование популяции гемопоэтических клеток-предшественников в условиях, подходящих для получения популяции клеток-предшественников мегакариоцитов, и культивирование популяции клеток-предшественников мегакариоцитов в условиях, подходящих для получения тромбоцитов. В этой области известны смеси факторов роста и дифференцировки, подходящие для экспансии и дифференцировки клеток-предшественников и получения тромбоцитов. Неограничивающие примеры подходящих факторов экспансии и дифференцировки включают фактор стволовых клеток (SCF), лиганд Flt-3/Flk-2 (FL), TPO, ИЛ-11, ИЛ-3, ИЛ-6 и ИЛ-9. Например, в некоторых вариантах осуществления тромбоциты можно получать посредством высевания CD34+ HSC в бессывороточной среде в количестве 2-4×104 клеток/мл и обновления среды в день культивирования 4 посредством добавления равного объема среды. В день культивирования 6 клетки подсчитывают и анализируют: 1,5×105 клеток промывают и высевают в 1 мл той же среды, дополненной смесью цитокинов, содержащей TPO (30 нг/мл), SCF (1 нг/мл), ИЛ-6 (7,5 нг/мл) и ИЛ-9 (13,5 нг/мл), для индуцирования дифференцировки мегакариоцитов. Ко дню культивирования 10 приблизительно от четверти до приблизительно половины суспензионной культуры заменяют свежей средой. Клетки культивируют во влажной атмосфере (10% CO2) при 39°C в течение первых 6 дней культивирования и при 37°C в течение последних 8 дней культивирования. Жизнеспособные ядросодержащие клетки подсчитывают с помощью гемоцитометра после окрашивания трипановым синим. Состояние дифференцировки тромбоцитов в культуре можно оценивать посредством проточной цитометрия или количественной ПЦР, как описано в примерах 44 и 45 публикации международной патентной заявки № WO 2015/073587, включенной в настоящее описание в качестве ссылки.
Экспрессия экзогенных полипептидов
В некоторых вариантах осуществления aAPC, включающую сконструированную эритроидную клетку или безъядерную клетку, презентирующую один или более экзогенных полипептидов, получают посредством приведения подходящей выделенной клетки, например, эритроидной клетки, ретикулоцита, эритроидной клетки-предшественника, тромбоцита или предшественника тромбоцита, в контакт с экзогенной нуклеиновой кислоты, кодирующей полипептид по настоящему изобретению (например, экзогенные антигенные полипептиды, экзогенные антигенпрезентирующие полипептиды, экзогенные костимуляторные полипептиды, экзогенные коингибиторные полипептиды, экзогенные истощающие аминокислоты полипептиды и экзогенные Treg-костимуляторные полипептиды).
В некоторых вариантах осуществления экзогенный полипептид кодируется ДНК, которую приводят в контакт с ядросодержащей эритроидной клеткой-предшественником или ядросодержащей тромбоцитарной клеткой-предшественником. В некоторых вариантах осуществления экзогенный полипептид кодируется РНК, которую приводят в контакт с тромбоцитом, ядросодержащей эритроидной клеткой, ядросодержащей тромбоцитарной клеткой-предшественником или ретикулоцитом. В некоторых вариантах осуществления экзогенный полипептид приводят в контакт с первичным тромбоцитом, ядросодержащей эритроидной клеткой, ядросодержащей тромбоцитарной клеткой-предшественником, ретикулоцитом или эритроцитом.
Экзогенный полипептид может экспрессироваться с трансгена, встроенного в эритроидную клетку посредством электропорации, химической или полимерной трансфекции, вирусной трансдукции, механического разрушения мембраны или другим способом; экзогенный полипептид, экспрессирующийся с мРНК, встроенной в клетку посредством электропорации, химической или полимерной трансфекции, вирусной трансдукции, механического разрушения мембраны или другим способом; экзогенный полипептид, гиперэкспрессирующийся с нативного локуса посредством встраивания внешнего фактора, например, активатора транскрипции, репрессора транскрипции или энхансера секреторного пути; и/или полипептид, синтезируемый, экстрагируемый или продуцируемый клеткой-продуцентом или другой внешней системой и встраиваемый в эритроидную клетку.
Экзогенные полипептиды (например, экзогенные антигенные полипептиды, экзогенные антигенпрезентирующие полипептиды, экзогенные костимуляторные полипептиды, экзогенные коингибиторные полипептиды, экзогенные истощающие аминокислоты полипептиды и экзогенные Treg-костимуляторные полипептиды) можно встраивать посредством трансфекции одной или множества копий генов, трансдукции с использованием вируса или электропорации в присутствии ДНК или РНК. Способы экспрессии экзогенных белков в клетках млекопитающих хорошо известны в этой области. Например, экспрессию экзогенного фактора IX в гемопоэтических клетках индуцируют посредством вирусной трансдукции CD34+ клеток-предшественников, см. Chang et al., Nat Biotechnol 2006, 24:1017.
В некоторых вариантах осуществления два или более полипептида кодируются одной нуклеиновой кислотой, например, одним вектором. В вариантах осуществления один вектор содержит отдельный промотор для каждого гена, содержит два белка, исходно транскрибируемых в одном полипептиде, содержащем участок расщепления протеазой в середине, таким образом, что при последующем протеолитическом процессинге образуются два белка, или имеет любую другую подходящую конфигурацию. В некоторых вариантах осуществления два или более полипептида кодируются двумя или более нуклеиновыми кислотами, например, каждый вектор кодируется одним из полипептидов.
Нуклеиновые кислоты, такие как ДНК-экспрессирующие векторы или мРНК, для получения экзогенных полипептидов можно встраивать в клетки-предшественники (например, эритроидную клетку-предшественника или тромбоцитарного предшественника и т.п.), подходящие для получения экзогенных полипептидов, представленных в настоящем описании. Клетки-предшественники можно выделять из исходного источника или получать из подвергнутой экспансии популяция клеток-предшественников с помощью общепринятой рекомбинантной технологии, как представлено в настоящем описании. В некоторых случаях экспрессирующие векторы можно конструировать известными в этой области способами таким образом, что они могут встраиваться в геном клеток посредством гомологичной или негомологичной рекомбинации.
В некоторых вариантах осуществления гемопоэтические клетки-предшественники, например, CD34+ гемопоэтические клетки-предшественники, приводят в контакт с нуклеиновой кислотой или нуклеиновыми кислотами, кодирующими один или более экзогенных полипептидов, и клеткам позволяют подвергаться экспансии и дифференцировке в культуре.
В некоторых случаях, например, в случае aAPC, являющейся эритроидной клеткой, содержащей один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных полипептидов для экспансии T-клеток, экзогенных коингибиторных полипептидов, экзогенных ингибиторов пролиферации, экзогенных истощающих аминокислоты полипептидов, экзогенных полипептидов для экспансии регуляторных T-клеток, экзогенных замещающих полипептидов), используют нуклеиновую кислоту, кодирующую полипептид, которая может селективно направлять и разрезать геном, например, CRISPR/Cas9, эффекторную нуклеазу, подобную активаторам транскрипции (TALEN) или нуклеазу с цинковыми пальцами, для направления инсерции экзогенной нуклеиновой кислоты из экспрессирующего вектора, кодирующего экзогенный полипептид, в конкретное место в геноме, например, локус CR1 (1q32.2), локус гемоглобина (11p15.4). Таким образом, в одном из аспектов настоящее изобретение относится к способу получения иммунологически совместимой искусственной антигенпрезентирующей клетки (aAPC), где aAPC включает сконструированную эритроидную клетку, экспрессирующую экзогенный антигенный полипептид, где способ включает приведение aAPC в контакт с нуклеазой и по меньшей мере одной гРНК, расщепляющими эндогенную нуклеиновую кислоту MHC, где эндогенная нуклеиновая кислота MHC подвергается репарации с помощью пути редактирования генома, что приводит к снижению уровня экспрессии эндогенной нуклеиновой кислоты MHC и, таким образом, получению иммунологически совместимой aAPC.
В некоторых вариантах осуществления один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов) можно клонировать в плазмидные конструкции для трансфекции. Способы переноса экспрессирующих векторов в клетки, подходящие для получения aAPC, представленных в настоящем описании, включают в качестве неограничивающих примеров, опосредованный вирусами перенос генов, опосредованный липосомами перенос, трансформацию, "генную пушку", трансфекцию и трансдукцию, например, опосредованный вирусами перенос генов, например, с использованием векторов на основе ДНК-вирусов, таких как аденовирус, аденоассоциированный вирус и вирус герпеса, а также векторы на основе ретровирусов. Примеры способов переноса генов включают, например, использование депротеинизированной ДНК, осаждение CaPO4, осаждение DEAE-декстраном, электропорацию, слияние протопластов, липофекцию и микроинъекцию в клетки.
В некоторых вариантах осуществления рекомбинантную ДНК, кодирующую каждый экзогенный полипептид, можно клонировать в лентивирусный вектор для встраивания в эритроидные клетки. В некоторых вариантах осуществления лентивирусный вектор содержит ДНК, кодирующую один экзогенный полипептид, для встраивания в эритроидные клетки. В других вариантах осуществления лентивирусный вектор содержит два, три, четыре или более экзогенных полипептидов, как представлено в настоящем описании, для встраивания в эритроидные клетки. В некоторых вариантах осуществления рекомбинантную ДНК, кодирующую один или более экзогенных полипептидов, можно клонировать в плазмидную конструкцию ДНК, кодирующую подвергаемый селекции признак, такой как ген резистентности к антибиотику. В некоторых вариантах осуществления рекомбинантную ДНК, кодирующую экзогенные полипептиды, можно клонировать в плазмидную конструкцию, адаптированную для стабильной экспрессии каждого рекомбинантного белка в эритроидных клетках.
В некоторых вариантах осуществления можно использовать лентивирусную систему, где с помощью вектора для переноса с последовательностями экзогенных полипептидов (например, одной, двумя, тремя, четырьмя или более последовательностями экзогенных полипептидов), оболочечного вектора и упаковочного вектора трансфицируют клетки-хозяева для продукции вируса. В некоторых вариантах осуществления с помощью лентивирусных векторов можно трансфицировать клетки-хозяева посредством любой из трансфекции с осаждением фосфатом кальция, липидной трансфекции или электропорации, и инкубировать их в течение ночи. В вариантах осуществления, в которых вместе с последовательностью экзогенного полипептида можно использовать флуоресцентный репортер, флуоресценцию клеток-хозяев можно проверять после инкубации в течение ночи. Среду для культивирования клеток-хозяев, содержащих вирусные частицы, можно собирать 2 или 3 раза каждые 8-12 часов и центрифугировать для осаждения открепленных клеток и клеточного детрита. Затем среду для культивирования можно использовать напрямую, замораживать или концентрировать, при необходимости.
Клетку-предшественника, подвергаемую переносу экзогенной нуклеиновой кислоты, кодирующей экзогенный полипептид, можно культивировать в подходящих условиях, делающих возможной дифференцировку в зрелые безъядерные эритроциты, например, в способе культивирования in vitro, представленном в настоящем описании. Получаемые безъядерные эритроциты экспонируют белки, ассоциированные со зрелыми эритроцитами, например, гемоглобин, гликофорин A, и экзогенные полипептиды, которые можно валидировать и количественно анализировать стандартными способами (например, посредством вестерн-блоттинга или анализа FACS). Выделенные зрелые безъядерные эритроциты, содержащие экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, и тромбоциты, содержащие экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, являются двумя неограничивающими примерами aAPC по настоящему изобретению.
В некоторых вариантах осуществления aAPC получают посредством приведения ретикулоцита в контакт с экзогенной нуклеиновой кислотой, кодирующей антигенный полипептид. В некоторых вариантах осуществления антигенный полипептид кодируется РНК, которую приводят в контакт с ретикулоцитом. В некоторых вариантах осуществления антигенный полипептид является полипептидом, который приводят в контакт с ретикулоцитом.
Выделенные ретикулоциты можно трансфицировать с использованием мРНК, кодирующей один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов) для получения aAPC. Матричную РНК можно получать при транскрипции in vitro плазмидной конструкции кДНК, содержащей кодирующую последовательность, соответствующую одному или более экзогенным полипептидам. Например, последовательность кДНК, соответствующую экзогенному полипептиду, можно встраивать в клонирующий вектор, содержащий последовательность промотора, совместимую с конкретными РНК-полимеразами. Например, клонирующий вектор ZAP EXPRESS pBK-CMV (Stratagene, La Jolla, Calif., USA) содержит последовательность промотора T3 и T7, совместимую с РНК-полимеразами T3 и T7, соответственно. В случае транскрипции in vitro смысловой мРНК плазмиду линеаризуют по участку рестрикции ниже стоп-кодонов, соответствующих концу кодирующей последовательности экзогенного полипептида. мРНК транскрибируют с линейной матрицы ДНК с использованием коммерчески доступного набора, такого как, например, набор RNAMAXX High Yield Transcription Kit (Stratagene, La Jolla, Calif., USA). В некоторых случаях желательным может являться получение 5'-m7GpppG-кэпированной мРНК. В связи с этим, транскрипцию линеаризованной матрицы кДНК можно осуществлять с использованием, например, набора mMESSAGE mMACHINE High Yield Capped RNA Transcription Kit от Ambion (Austin, Tex., USA). Транскрипцию можно осуществлять в объеме реакционной смеси 20-100 мкл при 37°C в течение от 30 мин до 4 ч. Транскрибируемую мРНК очищают от реакционной смеси посредством короткой обработки ДНКазой I для удаления линеаризованной матрицы ДНК с последующим осаждением в 70% этаноле в присутствии хлорида лития, ацетата натрия или ацетата аммония. Целостность транскрибируемой мРНК можно оценивать с использованием электрофореза в агароза-формальдегидном геле или коммерчески доступных, готовых гелях Novex TBE (например, Novex, Invitrogen, Carlsbad, Calif., USA).
Матричную РНК, кодирующую один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов), можно встраивать в ретикулоциты с использованием различных подходов, включая, например, липофекцию и электропорацию (van Tandeloo et al., Blood 98:49-56 (2001)). В случае липофекции, например, 5 мкг транскрибируемой in vitro мРНК в Opti-MEM (Invitrogen, Carlsbad, Calif., USA) инкубируют в течение 5-15 мин в соотношении 1:4 с катионным липидом DMRIE-C (Invitrogen). Альтернативно, для трансфекции клеток с использованием мРНК можно использовать различные катионные липиды или катионные полимеры включая, например, DOTAP, различные формы полиэтиленимина, поли-L-лизин (Sigma-Aldrich, Saint Louis, Mo., USA) и Superfect (Qiagen, Inc., Valencia, Calif., USA; см., например, Bettinger et al., Nucleic Acids Res. 29:3882-3891 (2001)). Получаемые комплексы мРНК/липид инкубируют с клетками (1-2×106 клеток/мл) в течение 2 ч. при 37°C., промывают и возвращают в культуру. В случае электропорации, например, приблизительно от 5 до 20×106 клеток в 500 мкл Opti-MEM (Invitrogen, Carlsbad, Calif., USA) смешивают с приблизительно 20 мкг транскрибируемой in vitro мРНК и подвергают электропорации в кювете 0,4 см с использованием, например, устройства Easyject Plus (EquiBio, Kent, United Kingdom). В некоторых случаях может потребоваться тестирование различного напряжения, емкости и объемов электропорации для определения подходящих условий для трансфекции ретикулоцита с использованием конкретной мРНК. В основном, параметры электропорации, необходимые для эффективной трансфекции клеток с использованием мРНК, по-видимому, являются менее вредными для клеток, чем необходимые для электропорации ДНК (van Tandeloo et al., Blood 98:49-56 (2001)).
Альтернативно, ретикулоцит можно трансфицировать с помощью мРНК с использованием стратегии пептид-опосредованной доставки РНК (см., например, Bettinger et al., Nucleic Acids Res. 29:3882-3891 (2001)). Например, катионный липид полиэтиленимин 2 кДа (Sigma-Aldrich, Saint Louis, Mo., USA) можно комбинировать с пептидом мелиттином (Alta Biosciences, Birmingham, UK) для повышения эффективности трансфекции мРНК, в частности, в постмитотических первичных клетках. Пептид мелиттин можно конъюгировать с PEI с использованием дисульфидного кросс-линкера, такого как, например, гетеробифункциональный кросс-линкер сукцинимидил-3-(2-пиридилдитио)-пропионат. Транскрибируемую in vitro мРНК предварительно инкубируют в течение от 5 до 15 мин с мелиттин-PEI для получения комплекса РНК/пептид/липид. Затем этот комплекс добавляют к клеткам в бессывороточной среде для культивирования в течение от 2 до 4 ч. при 37°C во влажной атмосфере 5% CO2, а затем удаляют и позволяют трансфицированным клеткам продолжать расти в культуре.
В некоторых вариантах осуществления aAPC получают посредством приведения подходящей выделенной эритроидной клетки-предшественника или тромбоцитарного предшественника в контакт с экзогенной нуклеиновой кислотой, кодирующей один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов). В некоторых вариантах осуществления экзогенный полипептид кодируется ДНК, которую приводят в контакт с ядросодержащей эритроидной клеткой-предшественником или ядросодержащей тромбоцитарной клеткой-предшественником. В некоторых вариантах осуществления экзогенный полипептид кодируется РНК, которую приводят в контакт с тромбоцитом, ядросодержащей эритроидной клеткой или ядросодержащей тромбоцитарной клеткой-предшественником.
Один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов) можно генетически встраивать в эритроидные клетки-предшественники, тромбоцитарные предшественники или ядросодержащие эритроидные клетки перед терминальной дифференцировкой различными способами с использованием ДНК, включая транзиторную или стабильную трансфекцию и подходы генной терапии. Экзогенные полипептиды можно экспрессировать на поверхности и/или в цитоплазме зрелого эритроцита или тромбоцита.
Для трансфекции клеток с использованием ДНК, кодирующей один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов) можно использовать вирусный перенос генов. В качестве носителей для переноса генов можно использовать ряд вирусов, включая вирус лейкоза мышей Молони (ммLV), аденовирус, аденоассоциированный вирус (AAV), вирус простого герпеса (HSV), лентивирусы, такие как вирус иммунодефицита человека 1 (ВИЧ 1), и спумавирусы, такие как пенящие вирусы, например, (См., например, Osten et al., HEP 178:177-202 (2007)). С помощью ретровирусов, например, эффективно трансдуцируют клетки млекопитающих, включая клетки человека, и они интегрируются в хромосомы, обеспечивая стабильный перенос генов.
С помощью одного или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов) можно трансфицировать эритроидную клетку-предшественника, тромбоцитарного предшественника или ядросодержащую эритроидную клетку, они могут экспрессироваться, а затем удерживаться и находиться в зрелом эритроците или тромбоците. Подходящим вектором является остов вектора на основе вируса лейкоза мышей Молони (ммLV) (Malik et al., Blood 91:2664-2671 (1998)). Векторы на основе MMLV, онкогенного ретровируса, в настоящее время используют в клинических испытаниях генной терапии (Hossle et al., News Physiol. Sci. 17:87-92 (2002)). Например, конструкцию ДНК, содержащую кДНК, кодирующую экзогенный полипептид, можно получать в остове вектора MMLV стандартными способами молекулярной биологии. С помощью конструкции трансфицируют пакующую линию клеток, такую как, например, клетки PA317, и вирусный супернатант используют для трансфекции клеток-продуцентов, таких как, например, клетки PG13. Вирусный супернатант PG13 инкубируют с эритроидной клеткой-предшественником, тромбоцитарным предшественником или ядросодержащей эритроидной клеткой, выделенной и культивируемой или свежевыделенной, как представлено в настоящем описании. Экспрессию экзогенного полипептида можно подвергать мониторингу посредством анализа FACS (активируемой флуоресценцией сортировки клеток), например, с использованием флуоресцентно меченого антитела против экзогенного полипептида, если он находится на поверхности aAPC. Схожие способы можно использовать для экспрессии экзогенного полипептида, находящегося внутри aAPC.
Необязательно, в трансфекции можно использовать флуоресцентно отслеживаемую молекулу, такую как, например, зеленый флуоресцентный белок (GFP), с использованием вирусного подхода (Tao et al., Stem cells 25:670-678 (2007)). Эктопические ретровирусные векторы, содержащие ДНК, кодирующую усиленный зеленый флуоресцентный белок (EGFP) или красный флуоресцентный белок (например, DsRed-Express), упаковывают с использованием пакующей клетки, такой как, например, линия клеток Phoenix-Eco (распространяемая Orbigen, San Diego, Calif.). Пакующие линии клеток стабильно экспрессируют вирусные белки, необходимые для упаковки вируса включая, например, gag, pol и env. Супернатанты клеток Phoenix-Eco, в которые отщепляются вирусные частицы, используют для трансдукции, например, эритроидных клеток-предшественников, тромбоцитарных предшественников или ядросодержащих эритроидных клеток. В некоторых случаях трансдукцию можно осуществлять на специально покрытой поверхности, например, фрагментами рекомбинантного фибронектина для улучшения эффективности опосредованного ретровирусами переноса генов (например, RetroNectin, Takara Bio USA, Madison, Wis.). Клетки инкубируют в покрытых RetroNectin планшетах с ретровирусными супернатантами Phoenix-Eco и подходящими кофакторами. Трансдукцию можно повторять на следующий день. В этом случае процентную долю клеток, экспрессирующих EGFP или DsRed-Express, можно анализировать посредством FACS. Другие репортерные гены, которые можно использовать для оценки эффективности трансдукции, включают, например, бета-галактозидазу, хлорамфеникол-ацетилтрансферазу и люциферазу, а также низкоаффинный рецептор фактора роста нервов (LNGFR), и антиген поверхности клеток человека CD24 (Bierhuizen et al., Leukemia 13:605-613 (1999)).
Для встраивания генетического материала в подходящие эритроидные клетки, тромбоциты или их предшественники для получения aAPC можно использовать невирусные векторы. Невирусно-опосредованный перенос генов отличается от опосредованного вирусами переноса генов тем, что плазмидные векторы не содержат белки, являются менее токсичными, их использование легче масштабировать, и они не являются преференциальными в отношении клетки-хозяина. "Депротеинизированная ДНК" из плазмидных векторов сама по себе неэффективна для доставки генетического материала, кодирующего полипептид, в клетку, и, таким образом, ее комбинируют со способом доставки генов, делающим возможным их проникновение в клетки. Для переноса невирусных векторов в подходящие эритроидные клетки, тромбоциты или их предшественников можно использовать ряд способов доставки, включая химические и физические способы.
Невирусный вектор, кодирующий один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов) можно встраивать в подходящие эритроидные клетки, тромбоциты или их предшественников с использованием синтетических макромолекул, таких как катионные липиды и полимеры (Papapetrou et al., Gene Therapy 12:S118-S130 (2005)). Катионные липосомы, например, образуют комплексы с ДНК через зарядовые взаимодействия. Положительно заряженные комплексы ДНК/липид связываются с отрицательной поверхностью клеток и захватываются клеткой посредством эндоцитоза. Этот подход можно использовать, например, для трансфекции гемопоэтических клеток (см., например, Keller et al., Gene Therapy 6:931-938 (1999)). В случае эритроидных клеток, тромбоцитов или их предшественников плазмидную ДНК (приблизительно 0,5 мкг в 25-100 мкл бессывороточной среды, такой как, например, OptiMEM (Invitrogen, Carlsbad, Calif.)) смешивают с катионной липосомой (приблизительно 4 мкг в 25 мкл бессывороточной среды), такой как коммерчески доступный реагент для трансфекции Lipofectamine™. (Invitrogen, Carlsbad, Calif.), и инкубируют в течение по меньшей мере 20 мин для получения комплексов. Комплекс ДНК/липосома добавляют в подходящие эритроидные клетки, тромбоциты или их предшественников и инкубируют в течение 5-24 ч., после чего можно анализировать экспрессию трансгена полипептида. Альтернативно, можно использовать другие коммерчески доступные липосомные средства для трансфекции (например, In vivo GeneSHUTTLE., Qbiogene, Carlsbad, Calif.).
Необязательно, катионный полимер, такой как, например, полиэтиленимин (PEI), можно использовать для эффективной трансфекции эритроидных клеток-предшественников, например, гемопоэтических и полученных из пуповинной крови CD34+ клеток (см., например, Shin et al., Biochim. Biophys. Acta 1725:377-384 (2005)). Клетки CD34+ человека выделяют из пуповинной крови человека и культивируют в модифицированной по способу Исков среде Дульбекко, дополненной 200 нг/мл фактора стволовых клеток и 20% термически инактивированной эмбриональной телячьей сыворотки. Плазмидную ДНК, кодирующую экзогенный полипептид, инкубируют с разветвленными или линейными PEI разного размера от 0,8 K до 750 K (Sigma Aldrich, Saint Louis, Mo., USA; Fermetas, Hanover, Md., USA). PEI получают в виде стокового раствора в 4,2 мг/мл дистиллированной воды и немного закисляют до pH 5,0 с использованием HCl. ДНК можно комбинировать с PEI в течение 30 мин при комнатной температуре при различных соотношениях азот/фосфат на основе следующих вычислений: 1 мкг ДНК содержит 3 нмоль фосфата, и 1 мкл стокового раствора PEI содержит 10 нмоль азота амина. Выделенные CD34+ клетки высевают с комплексом ДНК/катионный полимер, центрифугируют при 280×g в течение 5 мин и инкубируют в среде для культивирования в течение 4 или более часов до анализа экспрессии гена полипептида.
Плазмидный вектор можно встраивать в подходящие эритроидные клетки, тромбоциты или их предшественников с использованием физического способа, такого как опосредованная частицами трансфекция, "генная пушка", биолистика или технология бомбардировки частицами (Papapetrou, et al., (2005) Gene Therapy 12:S118-S130). В этом случае ДНК, кодирующую полипептид, абсорбируют на частицах золота и вводят в клетки посредством генной пушки. Этот подход можно использовать, например, для трансфекции эритроидных клеток-предшественников, например, гемопоэтических стволовых клеток, полученных из пуповинной крови (см., например, Verma et al., Gene Therapy 5:692-699 (1998)). В связи с этим, пуповинную кровь выделяют и разводят в три раза в фосфатно-солевом буфере. CD34+ клетки очищают с использованием моноклонального антитела против CD34 в комбинации с магнитными микрочастицами, покрытыми вторичным антителом, и системой магнитного выделения (например, Miltenyi MiniMac System, Auburn, Calif., USA). CD34+ обогащенные клетки можно культивировать, как представлено в настоящем описании. В случае трансфекции, плазмидную ДНК, кодирующую полипептид, осаждают на частице, например, частицах золота, посредством обработки хлоридом кальция и спермидином. После промывки покрытых ДНК частиц этанолом частицы можно вводить в культивируемые клетки с использованием, например, системы Biolistic PDS-1000/He System (Bio-Rad, Hercules, Calif., USA). Для оценки эффективности трансфекции можно использовать репортерный ген, такой как, например, бета-галактозидаза, хлорамфеникол-ацетилтрансфераза, люцифераза или зеленый флуоресцентный белок.
Необязательно, для встраивания плазмидного вектора в подходящие эритроидные клетки, тромбоциты или их предшественников можно использовать способы электропорации. При электропорации создают временные поры в клеточной мембране, позволяющие встраивать различные молекулы в клетки, включая, например, ДНК и РНК, а также антитела и лекарственные средства. В связи с этим, CD34+ клетки выделяют и культивируют, как представлено в настоящем описании. Непосредственно перед электропорацией клетки выделяют посредством центрифугирования в течение 10 мин при 250×g при комнатной температуре и ресуспендируют в количестве 0,2-10×106 жизнеспособных клеток/мл в буфере для электропорации, таком как, например, X-VIVO 10, дополненном 1,0% сывороточным альбумином человека (HSA). Плазмидную ДНК (1-50 мкг) добавляют в соответствующую кювету для электропорации вместе с 500 мкл суспензии клеток. Электропорацию можно осуществлять с использованием, например, электропоратора ECM 600 (Genetronics, San Diego, Calif., USA) с напряжением в диапазоне от 200 В до 280 В и длительностью импульсов в диапазоне от 25 до 70 миллисекунд. Коммерчески доступным является ряд альтернативных устройств для электропорации, которые можно использовать для этой цели (например, Gene Pulser XCELL, BioRad, Hercules, Calif.; Cellject Duo, Thermo Science, Milford, Mass.). Альтернативно, эффективную электропорацию выделенных CD34+ клеток можно осуществлять с использованием следующих параметров: кювета 4 мм, 1600 мкФ, 550 В/см и 10 мкг ДНК на 500 мкл клеток в количестве 1×105 клеток/мл (Oldak et al., Acta Biochimica Polonica 49:625-632 (2002)).
Для трансфекции подходящих эритроидных клеток, тромбоцитов или их предшественников также можно использовать нуклеофекцию, являющуюся формой электропорации. В этом случае, трансфекцию осуществляют с использованием электрических параметров в специфических для типа клеток растворах, позволяющих ДНК (или другим реагентам) напрямую транспортироваться в ядро, таким образом, снижая риск возможной деградации в цитоплазме. Например, для трансфекции подходящих эритроидных клеток, тромбоцитов или их предшественников можно использовать набор Human CD34 CELL NYCLEOFECTOR Kit (from Amaxa Inc.). В этом случае, 1-5×106 клеток в растворе Human CD34 CELL NUCLEOFECTOR смешивают с 1-5 мкг ДНК и трансфицируют с помощью устройства NUCLEOFECTOR с использованием предварительно запрограммированных параметров, определяемых по инструкциям производителя.
Эритроидные клетки, тромбоциты или их предшественников можно трансфицировать невирусно с использованием общепринятого экспрессирующего вектора, который не может самореплицироваться в клетках млекопитающих, пока не интегрируется в геном. Альтернативно, эритроидные клетки, тромбоциты или их предшественников можно трансфицировать с использованием эписомного вектора, который может персистировать в ядре клетки-хозяина в виде автономно реплицирующихся генетических единиц без интеграции в хромосомы (Papapetrou et al., Gene Therapy 12:S118-S130 (2005)). В этих векторах используют генетические элементы, полученные из вирусов, в норме экстрахромосомно реплицирующихся в клетках после латентной инфекции, таких как, например, EBV, полиомавирус человека BK, вирус папилломы крупного рогатого скота-1 (BPV-1), вирус простого герпеса-1 (HSV) и вирус обезьян 40 (SV40). Для невирусного переноса генов также можно использовать искусственные хромосомы человека (Vanderbyl et al., Exp. Hematol. 33:1470-1476 (2005)).
Экзогенные нуклеиновые кислоты, кодирующие один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов), можно собирать в экспрессирующие векторы стандартными способами молекулярной биологии, известными в этой области, например, посредством расщепления рестриктазами, ПЦР с удлинением перекрывающихся фрагментов и сборки Гибсона.
Экзогенные нуклеиновые кислоты могут содержать ген, кодирующий один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов), в норме экспрессирующихся на поверхности клетки, например, эритроидной клетки, слитый с геном, кодирующим эндогенный или нативный мембранный белок, таким образом, что экзогенный полипептид экспрессируется на поверхности клетки. Например, экзогенный ген, кодирующий экзогенный антигенный полипептид, можно клонировать на N-конец после лидерной последовательности мембранного белка типа 1, на C-конец мембранного белка типа 2 или выше участка присоединения GPI GPI-связанного мембранного белка.
Для встраивания гибких аминокислотных линкеров между двумя слитыми генами можно использовать стандартные способы клонирования. Например, гибкий линкер является поли-глициновым поли-сериновым линкером, таким как [Gly4Ser]3 (SEQ ID NO: 1), общеупотребительный для получения одноцепочечных фрагментов антител из полноразмерных антител (Antibody Engineering: Methods & Protocols, Lo 2004), или полипептидами ala-gly-ser-thr, такими как полипептиды, используемые для получения одноцепочечных репрессоров Arc (Robinson & Sauer, PNAS 1998). В некоторых вариантах осуществления гибкий линкер придает полипептиду больше гибкости и стерической свободы, чем эквивалентная конструкция без гибкого линкера.
Между слитыми генами можно помещать эпитопную метку, такую как, например, последовательность нуклеиновой кислоты, кодирующая эпитопную метку HA - аминокислоты YPYDVPDYA (SEQ ID NO: 2), метку CMyc - аминокислоты EQKLISEEDL (SEQ ID NO: 3) или метку Flag - аминокислоты DYKDDDDK (SEQ ID NO: 4). Эпитопную метку можно использовать для простой детекции и количественного анализа экспрессии с использованием антител против эпитопной метки посредством проточной цитометрии, вестерн-блоттинга или иммунопреципитации.
В некоторых вариантах осуществления aAPC содержит один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов) и по меньшей мере один другой гетерологичный полипептид. По меньшей мере один другой гетерологичный полипептид может являться флуоресцентным белком. Флуоресцентный белок можно использовать в качестве репортера для оценки эффективности трансдукции. В некоторых вариантах осуществления флуоресцентный белок используют в качестве репортера для оценки уровней экспрессии экзогенного полипептида, если оба из них образуются из одного транскрипта. В некоторых вариантах осуществления по меньшей мере один другой полипептид является гетерологичным и обеспечивает функцию, такой как, например, множество антигенов, множество мишеней для захвата, ферментативный каскад. В некоторых вариантах осуществления рекомбинантная нуклеиновая кислота содержит ген, кодирующий антигенный полипептид, и второй ген, где второй ген отделен от гена, кодирующего антигенный полипептид, полученной из вируса последовательностью T2A (gagggcagaggaagtcttctaacatgcggtgacgtggaggsgsstcccggccct (SEQ ID NO: 5)), посттрансляционно расщепляемый на два зрелых белка.
В некоторых вариантах осуществления экзогенная нуклеиновая кислота, кодирующая экзогенный антигенпрезентирующий полипептид, содержит последовательность гена для белка поверхности клетки MHC, слитую с 3'-концом последовательности Kell и амплифицированную с использованием ПЦР. В некоторых вариантах осуществления экзогенная нуклеиновая кислота, кодирующая экзогенный антигенпрезентирующий полипептид содержит последовательность гена для белка поверхности клетки MHC, слитую с поли-глициновым/сериновым линкером, после которой следует 3'-конец последовательности Kell, и амплифицированную с использованием ПЦР. В некоторых вариантах осуществления экзогенная нуклеиновая кислота, кодирующая экзогенный антигенпрезентирующий полипептид, содержит 3'-конец последовательность гена белка поверхности клетки MHC, слитую с последовательностью эпитопной метки, которая может представлять собой одну из метки HA, метки зеленого флуоресцентного белка, метки Myc, хитин-связывающего белка, мальтоза-связывающего белка, глютатион-S-трансферазы, полигистидиновой метки, тиоредоксина, поли(NANP), метки FLAG, метки V5, AviTag, метки кальмодулина, полиглутаматной метки, E-метки, S-метки, SBP-метки, Softag-1, Softag-3, метки Strep, TC-метки, VSV-метки, Xpress-метки, Isopeptag, SpyTag, белка-носителя биотина и карбоксила, Nus-метки, Fc-метки или Ty-метки или их комбинацию. Целая конструкция слита с 3'-концом последовательности Kell, а затем амплифицировали с использованием ПЦР. Экзогенные генные конструкции, кодирующие различные экзогенные антигенпрезентирующие полипептиды, например, затем нагружают в лентивирусный вектор и используют для трансдукции популяции клеток.
В некоторых вариантах осуществления популяцию эритроидных клетки инкубируют с лентивирусными векторами, содержащими экзогенную нуклеиновую кислоту, кодирующую один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов), конкретные плазмиды для которых могут включать pLKO.1 puro, клонирующий вектор PLKO.1--TRC, pSico, FUGW, pLVTHM, pLJM1, pLion11, pMD2.G, pCMV-VSV-G, pCI-VSVG, pCMV-dR8.2 dvpr, psPAX2, pRSV-Rev и pMDLg/pRRE для получения aAPC. Векторы можно вводить в количестве 10, 100, 1000, 10000 БОЕ и инкубировать в течение 12 ч.
В некоторых вариантах осуществления aAPC является эритроидной клеткой, презентирующей, например, содержащей на своей поверхности, экзогенный антигенпрезентирующий полипептид, конъюгированный с одним или более экзогенными антигенными полипептидами. В других вариантах осуществления aAPC является эритроидной клеткой, презентирующей, например, содержащей на своей поверхности, экзогенный антигенпрезентирующий полипептид, экзогенный антигенный полипептид и по меньшей мере один экзогенный костимуляторный полипептид, являющийся частью пары в конъюгате. В других вариантах осуществления aAPC является эритроидной клеткой, презентирующей, например, содержащей на своей поверхности, экзогенный антигенпрезентирующий полипептид, экзогенный антигенный полипептид и по меньшей мере один экзогенный коингибиторный полипептид, являющийся частью пары в конъюгате. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
Конъюгацию можно осуществлять химически или ферментативно. Химическую конъюгацию можно осуществлять посредством ковалентного связывания экзогенного антигенпрезентирующего полипептида с одним или более экзогенными антигенными полипептидами с использованием линкера или без него. Химическую конъюгацию можно осуществлять посредством ковалентного связывания костимуляторного полипептида и члена связывающейся пары с использованием линкера или без него. Химическую конъюгацию можно осуществлять посредством ковалентного связывания коингибиторного полипептида и члена связывающейся пары с использованием линкера или без него. Получение таких конъюгатов входит в объем навыков специалиста в этой области, и известны различные способы конъюгации, при этом выбор конкретного способа зависит от конъюгируемых материалов. В полипептид (на C- или N-конец) добавляют аминокислоты, содержащие ионизируемые боковые цепи, например, аспарагиновую кислоту, глутаминовую кислоту, лизин, аргинин, цистеин, гистидин или тирозин, и несодержащиеся в активной части полипептидной последовательности, служащие в своем непротонированном состоянии в качестве мощного нуклеофила для включения в различные реакции биоконъюгации с реакционноспособными группами, присоединенными к полимерам, например, гомо- или гетеробифункциональному PEG (например, Lutolf and Hubbell, Biomacromolecules 2003; 4:713-22, Hermanson, Bioconjugate Techniques, London. Academic Press Ltd; 1996).
В варианте осуществления экзогенный антигенпрезентирующий полипептид можно связывать с одним или более экзогенными антигенными полипептидами с помощью мостика биотин-стрептавидин. В других вариантах осуществления костимуляторный полипептид и член связывающейся пары связывают с помощью мостика биотин-стрептавидин. В других вариантах осуществления коингибиторный полипептид и член связывающейся пары связывают с помощью мостика биотин-стрептавидин.
Например, биотинилированный антигенный полипептид можно связывать с неспецифически биотинилированной поверхностью экзогенного антигенпрезентирующего полипептида с помощью стрептавидинового мостика. Конъюгацию с биотином можно осуществлять с помощью ряда химических способов (см., например, Hirsch et al., Methods Mol. Biol. 295: 135-154 (2004)). Экзогенный антигенпрезентирующий полипептид можно биотинилировать с использованием амин-реактивного реагента для биотинилирования, такого как, например, сульфо-NHS-SS-биотин EZ-Link (сульфосукцинимидил-2-(биотинамидо)-этил-1,3-дитиопропионат; Pierce-Thermo Scientific, Rockford, Ill., USA; см., например, Jaiswal et al., Nature Biotech. 21:47-51 (2003)). Например, выделенные эритроидные клетки можно инкубировать в течение 30 мин при 4°C в 1 мг/мл раствора сульфо-NHS-SS в фосфатно-солевом буфере. Избыток биотинового реагента удаляют посредством промывки клеток Трис-забуференным физиологическим раствором. Затем проводят реакцию биотинилированных клеток с биотинилированным экзогенным антигенным полипептидом в присутствии стрептавидина для получения aAPC, презентирующих экзогенный антигенпрезентирующий полипептид, связанный с одним или более экзогенными антигенными полипептидами с помощью биотин-стрептавидинового мостика.
Эритроидные клетки, представленные в настоящем описании, также можно получать с использованием связывающих реагентов для связывания экзогенного полипептида с клеткой. Например, можно использовать клик-химию. Связывающие реагенты можно использовать для сопряжения экзогенного полипептида с клеткой, например, если экзогенный полипептид является комплексом или трудным для экспрессии полипептидом, например, полипептидом, например, мультимерным полипептидом; крупным полипептидом; полипептидом, дериватизированным in vitro; экзогенным полипептидом, который может быть токсичным для эритроидных клеток или который не экспрессируется эффективно в эритроидных клетках. Клик-химия и другие способы конъюгации для функционализации эритроидных клеток описаны в международной заявке № PCT/US 2018/000042, по которой испрашивается приоритет по временной патентной заявке США №62/460589, поданной 17 февраля 2017 года, и временной патентной заявке США №62/542142, поданной 8 июля 2017 года.
Таким образом, в некоторых вариантах осуществления эритроидная клетка, представленная в настоящем описании, содержит по меньшей мере, более или приблизительно 5000, 10000, 50000, 100000, 200000, 300000, 400000, 500000 связывающих реагентов на клетку. В некоторых вариантах осуществления эритроидные клетки получают способом, включающим a) соединение первого связывающего реагента с эритроидной клеткой и, таким образом, получение фармацевтического препарата, продукта или промежуточного продукта. В варианте осуществления способ дополнительно включает: b) приведение клетки в контакт с экзогенным полипептидом, соединенным со вторым связывающим реагентом, например, в условиях, подходящих для реакции первого связывающего реагента со вторым связывающим реагентом. В вариантах осуществления два или более экзогенных полипептида соединяют с клеткой (например, с использованием клик-химии). В вариантах осуществления первый экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии), и второй экзогенный полипептид содержит полипептид, экспрессирующийся с экзогенной нуклеиновой кислоты.
В некоторых вариантах осуществления один или более связывающих реагентов используют для соединения одного или более экзогенных полипептидов с эритроидной клеткой, представленной в настоящем описании. В некоторых вариантах осуществления два или более связывающих реагента используют для соединения двух или более экзогенных полипептида с эритроидной клеткой, представленной в настоящем описании. В некоторых вариантах осуществления два или более экзогенных полипептида соединяют с клеткой (например, с использованием клик-химии) с использованием того же связывающего реагента. В некоторых вариантах осуществления два или более экзогенных полипептида соединяют с клеткой (например, с использованием клик-химии) с использованием разных связывающих реагентов. В некоторых вариантах осуществления первый экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием первого связывающего реагента и второй экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием второго связывающего реагента. В некоторых вариантах осуществления три или более экзогенных полипептида соединяют с клеткой (например, с использованием клик-химии) с использованием того же связывающего реагента. В некоторых вариантах осуществления три или более экзогенных полипептида соединяют с клеткой (например, с использованием клик-химии) с использованием разных связывающих реагентов. В некоторых вариантах осуществления первый экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием первого связывающего реагента, второй экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием первого связывающего реагента и третий экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием второго связывающего реагента. В некоторых вариантах осуществления первый экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием первого связывающего реагента, второй экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием второго связывающего реагента и третий экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием первого связывающего реагента. В некоторых вариантах осуществления первый экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием первого связывающего реагента, второй экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием второго связывающего реагента и третий экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием второго связывающего реагента.
В варианте осуществления один или более связывающих реагентов используют для соединения одного или более экзогенных полипептидов с эритроидной клеткой, представленной в настоящем описании, где эритроидная клетка является эритроидной клеткой человека. В некоторых вариантах осуществления эритроидная клетка является клеткой человека, и два или более связывающих реагента используют для соединения двух или более экзогенных полипептидов с эритроидной клеткой. В некоторых вариантах осуществления эритроидная клетка является клеткой человека, и два или более экзогенных полипептида соединяют с клеткой (например, с использованием клик-химии) с использованием одного и того же связывающего реагента. В некоторых вариантах осуществления эритроидная клетка является клеткой человека, и два или более экзогенных полипептида соединяют с клеткой (например, с использованием клик-химии) с использованием разных связывающих реагентов. В некоторых вариантах осуществления эритроидная клетка является клеткой человека, и первый экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием первого связывающего реагента и второй экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием второго связывающего реагента. В некоторых вариантах осуществления эритроидная клетка является клеткой человека, и три или более экзогенных полипептида соединяют с клеткой (например, с использованием клик-химии) с использованием того же связывающего реагента. В некоторых вариантах осуществления эритроидная клетка является клеткой человека, и три или более экзогенных полипептида соединяют с клеткой (например, с использованием клик-химии) с использованием разных связывающих реагентов. В некоторых вариантах осуществления эритроидная клетка является клеткой человека, и первый экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием первого связывающего реагента, второй экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием первого связывающего реагента и третий экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием второго связывающего реагента. В некоторых вариантах осуществления эритроидная клетка является клеткой человека, и первый экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием первого связывающего реагента, второй экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием второго связывающего реагента и третий экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием первого связывающего реагента. В некоторых вариантах осуществления эритроидная клетка является клеткой человека, и первый экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием первого связывающего реагента, второй экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием второго связывающего реагента и третий экзогенный полипептид соединяют с клеткой (например, с использованием клик-химии) с использованием второго связывающего реагента.
В вариантах осуществления преимуществом настоящего изобретения является использование двух разных связывающих реагентов для клик-реакции трех или более экзогенных полипептидов с эритроидной клеткой, и в частности с эритроидной клеткой человека. Не желая быть связанными какой-либо теорией, полагают, что настоящее изобретение включает то, что в эритроидных клетках, содержащих три или более экзогенных полипептида, соединенных с клеткой (например, с использованием клик-химии) с использованием разных связывающих реагентов, конкуренция между экзогенными полипептидами за связывающие реагенты снижена, и в результате максимизируют количество копий экзогенных полипептидов.
В некоторых вариантах осуществления связывающий реагент содержит азидный связывающий реагент. В некоторых вариантах осуществления азидный связывающий реагент содержит азидоалкильный остаток, азидоарильный остаток или азидогетероарильный остаток. Примеры азидных связывающих реагентов включают сульфо-NHS-сложный эфир3-азидопропионовой кислоты, NHS-сложный эфир азидоуксусной кислоты, сложный эфир азидо-PEG-NHS, азидопропиламин, азидо-PEG-амин, азидо-PEG-малеимид, бис-сульфон-PEG-азид или их производные. Связывающие реагенты также могут содержать алкеновый остаток, например, трансциклоалкеновый остаток, оксаноборнадиеновый остаток или тетразиновый остаток. Дополнительные связывающие реагенты можно найти в Click Chemistry Tools (https://clickchemistrytools.com/) или Lahann, J (ed) (2009) Click Chemistry for Biotechnology and Materials Science, каждый из которых включен в настоящее описание в качестве ссылки в полном объеме.
В другом варианте осуществления антигенный полипептид присоединяют к клетке, например, эритроидной клетке, посредством ковалентного присоединения для получения aAPC, включающей эритроидную клетку, презентирующую один или более экзогенных антигенных полипептидов (например, первого экзогенного антигенного полипептида или первого антигенного полипептида и второго экзогенного антигенного полипептида). Например, антигенный полипептид можно дериватизировать и связывать с эритроидной клеткой или тромбоцитом с использованием связывающего соединения, содержащего электрофильную группу, которая будет реагировать с нуклеофилами на эритроидной клетке или тромбоците, для образования связи. Типичные электрофильные группы представляют собой αβ-ненасыщенные карбонилы, алкилгалиды и тиоловые реагенты, такие как замещенные малеимиды. Кроме того, связывающее соединение можно соединять с антигенным полипептидом с помощью одной или более из функциональных групп в полипептиде, таких как аминогруппы, карбоксильные группы и триозиновые группы. Для этой цели связывающие соединения должны содержать свободные карбоксильные группы, свободные аминогруппы, ароматические аминогруппы и другие группы, способные реагировать с функциональными группами фермента. Сильно заряженные антигенные полипептиды также можно получать для иммобилизации, например, на эритроидных клетках или тромбоцитах посредством электростатического связывания для получения aAPC. Примеры этих производных включают полилизиловые и полиглутамиловые ферменты.
Выбор реакционноспособной группы, включенной в производное, зависит от условий реакции, используемых для связывания электрофила с нуклеофильными группами на эритроидной клетке или тромбоците для иммобилизации. Желательно, чтобы главный фактор не приводил к инактивации связывающего реагента перед связыванием экзогенного полипептида, иммобилизованного посредством присоединения к эритроидной клетке или тромбоциту. Такую иммобилизацию с помощью реакций связывания можно осуществлять рядом способов. Как правило, связывающий реагент можно использовать для получения мостика между экзогенным полипептидом и эритроидной клеткой или тромбоцитом. В этом случае связывающий реагент должен иметь функциональную группу, такую как карбоксильная группа, которую можно заставлять реагировать с экзогенным полипептидом. Один из способов подготовки экзогенного полипептида к конъюгации включает использование карбоксильных групп в связывающем реагенте для получения смешанных ангидридов, реагирующих с экзогенным полипептидом, в котором используют активатор, способный образовывать смешанные ангидриды. Типичными такими активаторами являются изобутилхлорформиат или другие хлорформиаты, образующие смешанный ангидрид со связывающими реагентами, такими как 5,5'-(дитиобис(2-нитробензойная кислота) (DTNB), p-хлорбензоат ртути (CMB) или m-малеимидобензойная кислота (MBA). Смешанный ангидрид связывающего реагента реагирует с экзогенным полипептидом, образуя реакционноспособное производное, которое в свою очередь может реагировать с нуклеофильными группами на эритроидной клетке или тромбоците для иммобилизации экзогенного полипептида.
Функциональные группы на антигенном полипептиде, такие как карбоксильные группы, можно активировать карбодиимидами и подобными активаторами. Затем функциональные группы на мостикообразующем реагенте, такие как аминогруппы, будут реагировать с активированной группой на экзогенном полипептиде с образованием реакционноспособного производного. Кроме того, связывающий реагент должен содержать вторую реакционноспособную группу, которая будет реагировать с соответствующими нуклеофильными группами на эритроидной клетке или тромбоците с образованием мостика. Типичными реакционноспособными группами являются алкилирующие средства, такие как йодуксусная кислота, αβ-ненасыщенные карбонильные соединения, такие как акриловая кислота и т.п., тиоловые реагенты, такие как соединения ртути, замещенные малеимиды и т.п.
Альтернативно, функциональные группы на антигенном полипептиде можно активировать так, чтобы они реагировали непосредственно с нуклеофилами, например, на эритроидных клетках или тромбоцитах, для устранения необходимости использования мостикообразующего соединения. Для этой цели используют активатор, такой как K-реагент Вудворда или подобный реагент, приводящий к превращению карбоксильных групп в экзогенном полипептиде в енольные сложные эфиры, отличающиеся от смешанных ангидридов. Енольные сложноэфирные производные экзогенных полипептидов затем реагируют с нуклеофильными группами, например, на эритроидной клетке или тромбоците, для иммобилизации антигенного полипептида и, таким образом, получения aAPC.
В некоторых вариантах осуществления aAPC, содержащую эритроидную клетку, презентирующую (например, содержащую на своей поверхности) один или более экзогенных антигенных полипептидов, получают посредством приведения эритроидной клетки в контакт с антигенным полипептидом и, необязательно, нагрузкой, где приведение в контакт не включает конъюгацию антигенного полипептида с эритроидной клеткой с использованием участка присоединения, содержащего Band 3 (CD233), аквапорин-1, Glut-1, антиген Kidd, RhAg/R1i50 (CD241), Rli (CD240), Rh30CE (CD240CE), Rh30D (CD240D), Kx, гликофорин B (CD235b), гликофорин C (CD235c), гликофорин D (CD235d), Kell (CD238), Duffy/DARCi (CD234), CR1 (CD35), DAF (CD55), глобозид, CD44, ICAM-4 (CD242), Lu/B-CAM (CD239), XG1/XG2 (CD99), EMMPRIN/нейротелин (CD147), JMH, гликозилтрансферазу, Cartwright, Dombrock, C4A/CAB, Scianna, MER2, стоматин, BA-1 (CD24), GPIV (CD36), CD108, CD139 или антиген H (CD173). В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В некоторых вариантах осуществления aAPC включает эритроидную клетку, презентирующую (например, содержащую на своей поверхности) один или более экзогенных антигенных полипептидов, где один или более экзогенных антигенных полипептидов ферментативно конъюгируют.
В конкретных вариантах осуществления антигенный полипептид можно конъюгировать с поверхностью, например, эритроидной клетки или тромбоцита, различными химическими и ферментативными способами, включая, в качестве неограничивающих примеров, химическую конъюгацию с бифункциональными сшивающими средствами, такими как, например, гетеробифункциональный кросс-линкер сложный эфир NHS-малеимид для соединения первичной аминогруппы с восстановленной тиольной группой. Эти способы также включают ферментативные стратегии, такие как, например, транспептидазная реакция, опосредованная ферментом сортазой, для соединения одного полипептида, содержащего акцепторную последовательность LPXTG (SEQ ID NO: 6) или LPXTA (SEQ ID NO: 7), с полипептидом, содержащим N-концевую донорную последовательность GGG, см. например, Swee et al., PNAS 2013. Способы также включают комбинированные способы, такие как например, опосредованная сортазой конъюгация модулей клик-реакции (азида и алкина) на антигене и клетке, соответственно, с последующей реакцией циклоприсоединения для химического связывания антигена с клеткой, см. например, Neves et al., Bioconjugate Chemistry, 2013. Опосредованная сортазой модификация белков описана в международной заявке № PCT/US 2014/037545 и международной заявке № PCT/US 2014/037554, обе из которых включены в настоящее описание в качестве ссылки в полном объеме.
В некоторых вариантах осуществления белок модифицируют посредством конъюгации субстрата сортазы, содержащего аминокислоту, пептид, белок, полинуклеотид, углевод, метку, атом металла, контрастное средство, катализатор, неполипептидный полимер, распознаваемый элемент, низкомолекулярное соединение, липид, линкер, метку, эпитоп, антиген, терапевтическое средство, токсин, радиоактивный изотоп, частицу или остаток, содержащий реакционноспособную химическую группу, например, модуль клик-реакции.
При желании, каталитический связеобразующий полипептидный домен можно экспрессировать на или в, например, эритроидной клетке или тромбоците, внутриклеточно или внеклеточно. Существует множество каталитических связеобразующих полипептидов, включая транспептидазы, сортазы и изопептидазы, включая полученные из Spy0128, белка, выделенного из Streptococcus pyogenes.
В некоторых вариантах осуществления любые из полипептидов, представленных в настоящем описании, не конъюгируют с клеткой с использованием сортазы.
Показано, что разделение аутокаталитической, образующей изопептидную связь субъединицы (CnaB2 домен) Spy0128 приводит к образованию двух отдельных полипептидов, сохраняющих каталитическую активность со специфичностью друг для друга. Полипептиды в этой системе обозначают как SpyTag и SpyCatcher. После смешивания SpyTag и SpyCatcher подвергаются образованию изопептидной связи между Asp117 на SpyTag и Lys31 на SpyCatcher (Zakeri and Howarth, JACS 2010, 132:4526). Реакция совместима с клеточной средой и является высокоспецифической для конъюгации белка/пептида (Zakeri, B.; Fierer, J. O.; Celik, E.; Chittock, E. C.; Schwarz-Linek, U.; Moy, V. T.; Howarth, M. Proc. Natl. Acad. Sci. U.S.A. 2012, 109, E690-E697). Показано, что SpyTag и SpyCatcher направляют посттрансляционную топологическую модификацию в эластин-подобном белке. Например, размещение SpyTag на N-конце и SpyCatcher на C-конце направляет образование кольцевых эластин-подобных белков (Zhang et al, Journal of the American Chemical Society, 2013).
Компоненты SpyTag и SpyCatcher можно менять местами таким образом, что система, в которой молекула A слита с SpyTag и молекула B слита с SpyCatcher, функционально эквивалентна системе, в которой молекула A слита с SpyCatcher и молекула B слита с SpyTag. В целях по настоящему изобретению, при использовании SpyTag и SpyCatcher следует понимать, что комплементарную молекулу можно заменять.
Каталитический связеобразующий полипептид, такой как система SpyTag/SpyCatcher, можно использовать для присоединения антигенного полипептида к поверхности, например, эритроидной клетки, такой как сконструированная эритроидная клетка, для получения aAPC. Полипептидную последовательность SpyTag можно экспрессировать на внеклеточной поверхности эритроидной клетки. Полипептид SpyTag, например, можно подвергать слиянию с N-концом трансмембранного белка типа 1 или типа 3, например, гликофорином A, подвергать слиянию с C-концом трансмембранного белка типа 2, например, Kell, встроенного в рамке считывания на внеклеточном конце или во внеклеточную петлю многопроходного трансмембранного белка, например, Band 3, слитого с GPI-акцепторным полипептидом, например, CD55 или CD59, слитым с заякоренным в липидной цепи полипептидом, или подвергать слиянию с периферическим мембранным белком. Последовательность нуклеиновой кислоты, кодирующую слитый белок SpyTag, можно экспрессировать в aAPC. Антигенный полипептид можно подвергать слиянию с SpyCatcher. Последовательность нуклеиновой кислоты, кодирующая слитый белок SpyCatcher, может экспрессироваться и секретироваться из той же эритроидной клетки, которая экспрессирует слитый белок SpyTag. Альтернативно, последовательность нуклеиновой кислоты, кодирующую слитый белок SpyCatcher, можно получать экзогенно, например, в бактериальной клетке, грибковой клетке, клетке насекомого, клетке млекопитающего или бесклеточной системе продукции. После реакции полипептидов SpyTag и SpyCatcher будет образовываться ковалентная связь, с помощью которой соединяют антигенный полипептид с поверхностью эритроидной клетки для получения aAPC. Эритроидная клетка, содержащая слитый антигенный полипептид, является примером aAPC, содержащей конъюгированный антигенный полипептид.
В некоторых вариантах осуществления полипептид SpyTag можно экспрессировать в виде слитого пептида с N-концом гликофорина A под контролем промотора Gatal в эритроидной клетке. Экзогенный полипептид (например, экзогенные антигенные полипептиды, экзогенные антигенпрезентирующие полипептиды, экзогенные костимуляторные полипептиды, экзогенные коингибиторные полипептиды, экзогенные истощающие аминокислоты полипептиды и экзогенные Treg-костимуляторные полипептиды), слитые с последовательностью полипептида SpyCatcher, можно экспрессировать под контролем промотора Gatal в той же эритроидной клетке. После экспрессии обоих слитых полипептидов будет образовываться изопептидная связь между полипептидами SpyTag и SpyCatcher, образуя ковалентную связь между поверхностью эритроидной клетки и экзогенным полипептидом.
В другом варианте осуществления полипептид SpyTag можно экспрессировать в виде слитого пептида с N-концом гликофорина A под контролем промотора Gatal в эритроидной клетке. Экзогенный полипептид (например, экзогенные антигенные полипептиды, экзогенные антигенпрезентирующие полипептиды, экзогенные костимуляторные полипептиды, экзогенные коингибиторные полипептиды, экзогенные истощающие аминокислоты полипептиды и экзогенные Treg-костимуляторные полипептиды), слитые с последовательностью полипептида SpyCatcher можно экспрессировать в подходящей экспрессионной системе на основе клеток млекопитающего, например, клетках HEK293. После экспрессии слитого полипептида SpyTag на эритроидной клетке, слитый полипептид SpyCatcher можно приводить с ней в контакт. В подходящих условиях реакции между полипептидами SpyTag и SpyCatcher будет образовываться изопептидная связь, образуя ковалентную связь между поверхностью эритроидной клетки и антигенным полипептидом. Эритроидная клетка, содержащая слитый антигенный полипептид, является примером aAPC, содержащей конъюгированный антигенный полипептид.
Между экзогенными полипептидами могут образовываться другие слитые молекулы, и это включает прямую или непрямую конъюгацию. Экзогенные полипептиды можно конъюгировать напрямую друг с другом или косвенно через линкер. Линкер может являться пептидом, полимером, аптамером или нуклеиновой кислотой. Полимер может являться, например, природным, синтетическим, линейным или разветвленным. Антигенные полипептиды могут содержать гетерологичный слитый белок, содержащий первый полипептид и второй полипептид, со слитым белком, содержащим полипептиды, соединенные напрямую друг с другом или с использованием промежуточных линкерных последовательностей и/или дополнительных последовательностей на одном или обоих концах. Конъюгацию с линкером можно осуществлять с помощью ковалентных связей или ионных связей.
В некоторых вариантах осуществления полипептид нагружают в aAPC, включающую эритроидную клетку. В некоторых вариантах осуществления полипептид нагружают в aAPC, включающую безъядерную клетку. В некоторых вариантах осуществления полипептид нагружают в aAPC, включающую ядросодержащую клетку. В некоторых вариантах осуществления aAPC, включающие эритроидные или безъядерные клетки, получают посредством нагрузки, например, эритроидных клеток или тромбоцитов одним или более экзогенными полипептидами, таким образом, что один или более экзогенных полипептидов интернализуются в эритроидные клетки или тромбоциты. Необязательно, эритроидные клетки или тромбоциты дополнительно можно нагружать полезной нагрузкой, такой как, например, терапевтическое средство.
Для нагрузки, например, эритроидных клеток или тромбоцитов экзогенным полипептидом можно использовать ряд способов. Подходящие способы включают, например, гипотонический лизис, гипотонический диализ, осмос, осмотические импульсы, осмотический шок, ионофорез, электропорацию, обработку ультразвуком, микроинъекцию, осаждение кальцием, интеркаляцию мембраны, опосредованную липидами трансфекцию, обработку детергентом, вирусную инфекцию, диффузию, рецептор-опосредованный эндоцитоз, использование доменов белковой трансдукции, бомбардировку частицами, слияние мембран, замораживание-размораживание, механическое разрушение и фильтрацию. Любой такой способ или их комбинацию можно использовать для получения aAPC, включающих сконструированную эритроидную клетку, презентирующую (например, содержащую на своей поверхности) один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов), представленных в настоящем описании.
В случае гипотонического лизиса, например, эритроидную клетку подвергают воздействию буфера с низкой ионной силой, что приводит к ее разрыву. Экзогенный полипептид распределяется внутри клетки. Эритроидную клетку, в частности эритроцит, можно гипотонически лизировать посредством добавления 30-50-кратного объемного избытка 5 мМ фосфатного буфера (pH 8) к осадку выделенных эритроцитов. Получаемые мембраны лизированных клеток выделяют посредством центрифугирования. Осадок мембран лизированных эритроцитов ресуспендируют и инкубируют в присутствии экзогенного полипептида в буфере с низкой ионной силой, например, в течение 30 мин. Альтернативно, мембраны лизированных эритроцитов можно инкубировать с экзогенным полипептидом всего в течение одной минуты или нескольких дней в зависимости от лучших условий, определяемых по эффективной нагрузке эритроидных клеток.
Альтернативно, эритроидные клетки, в частности эритроциты, можно нагружать экзогенным полипептидом с использованием контролируемого диализа против гипотонического раствора для набухания клеток и создания пор в клеточной мембране (см., например, патенты США №№4327710, 5753221 и 6495351). Например, осадок выделенных эритроцитов ресуспендируют в 10 мМ HEPES, 140 мМ NaCl, 5 мМ глюкозе, pH 7,4, и диализуют против буфера с низкой ионной силой, содержащего 10 мМ NaH2PO4, 10 мМ NaHCO3, 20 мМ глюкозы и 4 мМ MgCl2, pH 7,4. Через 30-60 мин эритроциты дополнительно диализуют против раствора 16 мМ NaH2PO4, pH 7,4, содержащего экзогенный полипептид в течение еще 30-60 мин. Все из этих действий можно осуществлять при температуре 4°C. В некоторых случаях предпочтительной может являться нагрузка большого количества эритроидных клеток, в частности эритроцитов, посредством диализа, и можно использовать специальное устройство для этой цели (см., например, патенты США №№4327710, 6139836 и 6495351 B2).
Нагруженные эритроидные клетки, в частности эритроциты, можно высвобождать посредством осторожного нагревания в присутствии физиологического раствора, такого как, например, 0,9% физиологический раствор, фосфатно-солевого буфера, раствора Рингера, среды для культивирования клеток, плазмы крови или лимфатической жидкости. Например, хорошо замкнутые мембраны можно получать посредством обработки разрушенных эритроидных клеток, в частности эритроцитов, в течение 1-2 мин в 150 мМ солевом растворе, например, 100 мМ фосфата (pH 8,0) и 150 мМ хлорида натрия, при температуре 60°C. Альтернативно, клетки можно инкубировать при температуре 25-50°C в течение от 30 мин до 4 ч. (см., например, патентную заявку США №2007/0243137 A1). Альтернативно, разрушенные эритроциты можно высвобождать посредством инкубации в 5 мМ аденине, 100 мМ инозине, 2 мМ АТФ, 100 мМ глюкозе, 100 мМ пирувате Na, 4 мМ MgCl2, 194 мМ NaCl, 1,6 M KCl, и 35 мМ NaH2PO4, pH 7,4, при температуре 37°C в течение 20-30 мин (см., например, патент США №5753221).
В случае электропорации, например, эритроидные клетки или тромбоциты подвергают воздействию электрического поля, что вызывает образование временных отверстий в клеточной мембране, что позволяет одному или более экзогенным полипептидам (например, экзогенным антигенным полипептидам, экзогенным антигенпрезентирующим полипептидам, экзогенным костимуляторным полипептидам, экзогенным полипептидам для экспансии T-клеток, экзогенным коингибиторным полипептидам, экзогенным ингибиторам пролиферации, экзогенным истощающим аминокислоты полипептидам, экзогенным полипептидам для экспансии регуляторных T-клеток, экзогенным замещающим полипептидам) диффундировать в клетку (см., например, патент США №4935223). Эритроидные клетки, в частности эритроциты, например, суспендируют в физиологических и электропроводящих средах, таких как несодержащая тромбоциты плазма, в которые добавляют один или более экзогенных полипептидов. Смесь в объеме в диапазоне от 0,2 до 1,0 мл помещают в кювету для электропорации и охлаждают на льду в течение 10 мин. Кювету помещают в кювету для электропорации, такую как, например, ECM 830 (BTX Instrument Division, Harvard Apparatus, Holliston, Mass.). Клетки подвергают электропорации с использованием одного импульса приблизительно 2,4 миллисекунд и напряженностью поля приблизительно 2,0 кВ/см. Альтернативно, электропорацию эритроидных клеток, в частности эритроцитов, можно осуществлять с использованием двойных импульсов 2,2 кВ при 0,25 мкФ с помощью устройства Bio-Rad Gene Pulsar (Bio-Rad, Hercules, Calif., USA) для достижения емкости нагрузки более 60% (Flynn et al., Cancer Lett. 82:225-229 (1994)). Кювету помещают обратно на лед на 10-60 мин, а затем на водяную баню при 37°C для индуцирования высвобождения клеточной мембраны. Для получения aAPC, представленных в настоящем описании, можно использовать любой подходящий способ электропорации.
В случае обработки ультразвуком эритроидные клетки, например, подвергают воздействию звуковых волн высокой интенсивности, что вызывает временное разрушение клеточной мембраны, что позволяет одному или более экзогенным полипептидам (например, экзогенным антигенным полипептидам, экзогенным антигенпрезентирующим полипептидам, экзогенным костимуляторным полипептидам, экзогенным коингибиторным полипептидам, экзогенным истощающим аминокислоты полипептидам и экзогенным Treg-костимуляторным полипептидам) диффундировать в клетку. Для получения aAPC, представленных в настоящем описании, можно использовать любой подходящий способ обработки ультразвуком.
В случае обработки детергентом эритроидные клетки, например, обрабатывают слабым детергентом, временно разрушающим клеточную мембрану, создавая отверстия, через которые могут диффундировать один или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов). После нагрузки клеток детергент вымывают из клеток. Например, детергент может являться сапонином. Для получения aAPC, представленных в настоящем описании, можно использовать любой подходящий способ обработки детергентом.
В случае рецептор-опосредованного эндоцитоза эритроидные клетки, например, могут иметь поверхностный рецептор, который после связывания одного или более экзогенных полипептидов (например, экзогенных антигенных полипептидов, экзогенных антигенпрезентирующих полипептидов, экзогенных костимуляторных полипептидов, экзогенных коингибиторных полипептидов, экзогенных истощающих аминокислоты полипептидов и экзогенных Treg-костимуляторных полипептидов) индуцирует интернализацию рецептора и связанных экзогенных полипептидов. Для получения aAPC, включающей эритроидную клетку, презентирующую (например, содержащую на своей поверхности) один или более экзогенных полипептидов, представленных в настоящем описании, можно использовать любой подходящий способ эндоцитоза.
В случае механической бомбардировки эритроидные клетки, например, можно бомбардировать одним или более экзогенными полипептидами (например, экзогенными антигенными полипептидами, экзогенными антигенпрезентирующими полипептидами, экзогенными костимуляторными полипептидами, экзогенными коингибиторными полипептидами, экзогенными истощающими аминокислоты полипептидами и экзогенными Treg-костимуляторными полипептидами), присоединенными к тяжелой или заряженной частице, такой как, например, микроносители золота, и механически или электрически ускоряют таким образом, что они пересекают клеточную мембрану. Бомбардировку микрочастицами можно осуществлять с использованием, например, устройства Helios Gene Gun (от, например, Bio-Rad, Hercules, Calif., USA). Для получения aAPC, представленных в настоящем описании, можно использовать любой подходящий способ бомбардировки микрочастицами.
В случае фильтрации эритроидные клетки или тромбоциты и экзогенные полипептиды можно пропускать через фильтр с размером пор меньше размера клетки, что вызывает временное разрушение клеточной мембраны и позволяет экзогенным полипептидам проникать в клетку. Для получения aAPC, включающих сконструированные эритроидные клетки, презентирующие (например, содержащие на поверхности клетки) экзогенные полипептиды, представленные в настоящем описании, можно использовать любой подходящий способ фильтрации.
В случае замораживания-размораживания эритроидные клетки подвергают нескольким циклам замораживания-размораживания, что приводит к разрушению клеточной мембраны (см., например, патентную заявку США №2007/0243137 A1). В этом случае осадок эритроцитарной массы (0,1-1,0 мл) смешивают с равным объемом (0,1-1,0 мл) изотонического раствора (например, фосфатно-солевого буфера), содержащего один или более экзогенных полипептидов. Эритроциты замораживают посредством погружения пробирки, содержащей клетки и один или более экзогенных полипептидов, в жидкий азот. Альтернативно, клетки можно замораживать, помещая пробирку в морозильную камеру при -20°C или -80°C. Затем клетки размораживают, например, на водяной бане при 23°C и, при необходимости, цикл повторяют для увеличения нагрузки. Для получения aAPC, включающих сконструированные эритроидные клетки, презентирующие (например, содержащие на поверхности клетки) экзогенные полипептиды, представленные в настоящем описании, можно использовать любой подходящий способ замораживания-размораживания.
Можно определять экзогенные полипептиды на aAPC. Наличие экзогенного полипептида можно валидировать и количественно анализировать с использованием стандартных способов молекулярной биологии, например, вестерн-блоттинга или анализа FACS. Экзогенные полипептиды, присутствующие во внутриклеточной среде, можно количественно анализировать после лизиса клеток или с использованием флуоресцентной детекции.
В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления эритроидная клетка является ядросодержащей клеткой.
Носители для полипептидов, представленных в настоящем описании
В одном из аспектов один или более полипептидов, представленных в настоящем описании, нагружают, присоединяют (например, иммобилизуют или конъюгируют) к поверхности и/или заключают в неклеточный носитель для доставки. Неклеточный носитель для доставки может являться, например, нанолипидным гелем, полимерной частицей, агарозной частицей, латексной частицей, частицей диоксида кремния, липосомой или многослойными везикулами. В некоторых вариантах осуществления неклеточный носитель для доставки содержит или состоит из наночастицы диаметром от приблизительно 1 нм до приблизительно 900 нм. В некоторых вариантах осуществления неклеточный носитель для доставки имеет средний диаметр от приблизительно 0,1 до приблизительно 20 мкм (такой как от приблизительно 0,5 мкм до приблизительно 10 мкм, например, приблизительно 5 мкм или менее (например, от приблизительно 2,5 до приблизительно 5 мкм)). В некоторых вариантах осуществления неклеточный носитель для доставки имеет средний диаметр от приблизительно 1 мкм до приблизительно 10 мкм. В некоторых вариантах осуществления неклеточный носитель для доставки содержит биодеградируемый полимер. В некоторых вариантах осуществления неклеточный носитель для доставки содержит природный полимер. В некоторых вариантах осуществления неклеточный носитель для доставки содержит синтетический полимер. Типичные полимеры включают, в качестве неограничивающих примеров, поли(гидроксикислоту), полигидроксиалканоат, поликапролактон, поликарбонат, полиамид, полиэфирамид, поли(акриламид), поли(сложный эфир), поли(алкилцианоакрилаты), поли(молочную кислоту) (PLA), поли(гликолевые кислоты) (PGA), сополимер D, L-молочной и гликолевой кислот (PLGA) и их комбинации. В некоторых вариантах осуществления неклеточный носитель для доставки содержит агарозу, латекс или полистирол. Один или более из полипептидов, представленных в настоящем описании, можно конъюгировать с неклеточным носителем для доставки стандартными, известными в этой области способами (см., например, Ulbrich et al. (2016) Chem Rev. 116(9): 5338-431). Конъюгация может являться ковалентной или нековалентной. Например, в вариантах осуществления, в которых неклеточный носитель для доставки является липосомой, полипептид, представленный в настоящем описании, можно присоединять к липосоме через цепь полиэтиленгликоля (PEG). В конъюгацию полипептида с липосомой также можно включать тиоэфирные связи, например, посредством реакции тиолов и малеимидных групп. Сшивающие средства можно использовать для получения сульфгидрильных групп для присоединения полипептидов к неклеточным носителям для доставки (см., например, Paszko and Senge (2012) Curr. Med. Chem. 19(31): 5239-77). В некоторых вариантах осуществления в любом из терапевтических способов, представленных в настоящем описании, можно использовать неклеточные носители для доставки, содержащие один или более из полипептидов, представленных в настоящем описании.
IV. СПОСОБЫ ПРИМЕНЕНИЯ ИСКУССТВЕННЫХ АНТИГЕНПРЕЗЕНТИРУЮЩИХ КЛЕТОК
Настоящее изобретение включает различные способы применения aAPC, представленных в настоящем описании. Как будет понятно специалисту в этой области с учетом раскрытия, представленного в настоящем описании, дозу и время введения aAPC можно адаптировать для каждого применения, представленного в настоящем описании. Более конкретно, если желательно обеспечивать стимуляцию T-клеток с использованием некоторых молекул, экспрессируемых aAPC, или нескольких aAPC с последующей стимуляцией с использованием другой aAPC или нескольких aAPC, экспрессирующих другой, пусть и перекрывающийся, набор молекул, то можно использовать комбинацию цис- и транс-подходов. По существу, aAPC по настоящему изобретению и способы, представленные в настоящем описании, обеспечивают почти неограниченный набор вариантов, и настоящее изобретение не ограничено каким-либо образом какой-либо комбинацией или подходом. Специалисты в этой области с учетом идей, представленных в настоящем описании, и знаний в этой области легко могут определять желаемый подход для каждой конкретной T-клетки.
В одном из аспектов настоящее изобретение относится к способу активации антигенспецифической T-клетки, включающему приведение T-клетки в контакт с aAPC, представленной в настоящем описании, и, таким образом, активацию антигенспецифической T-клетки. В некоторых вариантах осуществления активация антигенспецифической T-клетки включает активацию антигенспецифической T-клетки с фенотипом центральной памяти. В некоторых вариантах осуществления активация антигенспецифической T-клетки включает стимуляцию экспансии T-клеток памяти. В других вариантах осуществления активация антигенспецифической T-клетки включает дифференцировку или дедифференцировку T-клеток. Например, долгоживущие CD8+ T-клетки памяти получают из субпопуляции эффекторных T-клеток способом дедифференцировки.
В другом аспекте настоящее изобретение относится к способу супрессии активности T-клетки, включающему приведение T-клетки в контакт с aAPC, сконструированной для супрессии активности T-клетки, и, таким образом, супрессию активности T-клетки.
В другом аспекте настоящее изобретение относится к способу активации Treg-клетки, включающему приведение Treg-клетки в контакт с aAPC, сконструированной для активации регуляторной T-клетка (Treg), и, таким образом, активацию Treg-клетки.
В другом аспекте настоящее изобретение относится к способу индуцирования пролиферации T-клетки, экспрессирующей рецепторную молекулу, включающему приведение T-клетки в контакт с aAPC, представленной в настоящем описании, где костимуляторный полипептид специфически связывается с рецепторной молекулой, и, таким образом, индуцирование пролиферации указанной T-клетки.
Настоящее изобретение также включает способ специфического индуцирования пролиферации T-клетки, экспрессирующей известную костимуляторную молекулу. Способ включает приведение популяции T-клеток, содержащей по меньшей мере одну T-клетку, экспрессирующую известную костимуляторную молекулу в контакт с aAPC, сконструированной для презентирования лиганда костимуляторной молекулы. Как представлено где-либо в настоящем описании, если aAPC экспрессирует по меньшей мере один костимуляторный лиганд, специфически связывающийся с костимуляторной молекулой на T-клетке, связывание костимуляторной молекулы с ее когнатным костимуляторным лигандом индуцирует пролиферацию T-клетки. Таким образом, интересующую T-клетку индуцируют для пролиферации, не выделяя сначала клетку из популяции клеток. Кроме того, этот способ представляет собой быстрый анализ для определения того, экспрессируют ли какие-либо клетки в популяции конкретную интересующую костимуляторную молекулу, т.к. с помощью приведения клеток в контакт с aAPC будут индуцировать пролиферацию и осуществлять детекцию выращиваемых клеток и, таким образом, определение того, что T-клетка, экспрессирующая интересующую костимуляторную молекулу, присутствует в образце. Таким образом, если известна по меньшей мере одна костимуляторная молекула на поверхности клетки, любую интересующую T-клетку можно выращивать и выделять.
Настоящее изобретение также включает способ специфической экспансии субпопуляции из популяции T-клеток. Более конкретно, способ включает приведение популяции T-клеток, содержащей по меньшей мере одну T-клетку из интересующей субпопуляции, в контакт с aAPC, которая может приводить к экспансии этой T-клетки, или по меньшей мере aAPC, экспрессирующей по меньшей мере один костимуляторный лиганд, специфически связывающийся с когнатной костимуляторной молекулой на поверхности T-клетки. Связывание костимуляторной молекулы с ее партнером по связыванию-костимуляторным лигандом индуцирует пролиферацию T-клетки и, таким образом, специфическую экспансию субпопуляции из популяции T-клеток. Специалисту в этой области с учетом раскрытия, представленного в настоящем описании, будет понятно, что субпопуляции T-клеток включают T-хелперы (TH1 и TH2), экспрессирующие CD4, цитотоксические T-лимфоциты (CTL) (Tc1 или Tc2), регуляторные T-клетки (Treg), TC/S, наивные T-клетки, T-клетки памяти, T-клетки центральной памяти, эффекторные T-клетки памяти и γΔT-клетки. Таким образом, популяции клеток, обогащенные конкретной субпопуляцией T-клеток, легко можно получать способом по настоящему изобретению.
В некоторых вариантах осуществления T-клетки подвергают экспансии в от приблизительно 100 до приблизительно 1000000 раз или от приблизительно 1000 до приблизительно 1000000 раз, например, от 1000 до приблизительно 100000 раз.
Пригодность T-клеток после экспансии ex vivo является великолепным показателем их способности функционировать in vivo. Таким образом, в некоторых вариантах осуществления также измеряют способность aAPC индуцировать ключевой ген выживания клеток Bcl-xL. Процентную долю апоптотических клеток в культуре во время экспансии используют для определения того, обеспечивают ли какие-либо aAPC на основе клеток конкретное преимущество в плане выживания подвергаемым экспансии T-клеткам. Кроме того, можно измерять длину теломер клеток после экспансии ex vivo для определения того, является ли конкретная aAPC более эффективной в сохранении репликативного потенциала клеток, экспансию которой она вызывает.
Настоящее изобретение также включает способ идентификации костимуляторных лигандой или их комбинации, специфически индуцирующих активацию субпопуляции T-клеток. В кратком изложении, способ включает приведение популяции T-клеток в контакт с aAPC, презентирующей (например, содержащей на своей поверхности) по меньшей мере один костимуляторный лиганд, и сравнение уровня пролиферации субпопуляции T-клеток, приведенной в контакт с aAPC, с уровнем пролиферации в остальном идентичной субпопуляции T-клеток, неприведенной в контакт с aAPC. Более высокий уровень пролиферации субпопуляции T-клеток, приведенной в контакт с aAPC, по сравнению с уровнем пролиферации в остальном идентичной субпопуляции T-клеток, неприведенной в контакт с aAPC, является показателем того, то костимуляторный лиганд специфически индуцирует активацию субпопуляции T-клеток, к которой принадлежит T-клетка.
Способ позволяет идентифицировать костимуляторный лиганд, приводящий к специфической экспансии субпопуляции T-клеток, о котором ранее не было известно, что он является фактором, приводящим к экспансии этой субпопуляции T-клеток. Специалистам в этой области будет понятно, что для минимизации количества скринингов предпочтительно трансдуцировать достаточное количество нуклеиновых кислот, кодирующих костимуляторные лиганды, таким образом, что можно снижать количество анализов. Кроме того, благодаря комбинированию различных белков (например, стимуляторного лиганда, костимуляторного лиганда, антигена, цитокина и т.п.) способ делает возможным анализ того, какие комбинации факторов приведут к получению наиболее эффективной aAPC или комбинации aAPC для экспансии субпопуляции T-клеток. Таким образом, можно исследовать различные требования для выращивания и активации каждой субпопуляции T-клеток. Кроме того, для оценки экспансии T-клеток можно использовать окрашивание CFSE. aAPC смешивают с CD8+ T-клетками (например, индивидуума, страдающего заболеванием или нарушением, таким как аутоиммунное заболевание, инфекционное заболевание или злокачественное новообразование). Для сравнения исходной скорости экспансии клеток клетки подвергают окрашиванию CFSE для определения того, насколько хорошо каждая aAPC индуцирует пролиферацию всех T-клеток. Окрашивание CFSE обеспечивает гораздо более количественную конечную точку и делает возможным одновременное фенотипирование подвергнутых экспансии клеток. Каждый день после стимуляции из каждой культуры удаляют аликвоту клеток и анализируют посредством проточной цитометрии. Окрашивание CFSE делает клетки высокофлуоресцентными. После деления клеток флуоресценция уменьшается наполовину, и, таким образом, чем больше раз делятся клетки, тем менее флуоресцентными они становятся. Способность каждой aAPC индуцировать пролиферацию T-клеток количественно анализируют посредством измерения количества клеток, делящихся один раз, два раза, три раза и т.д. aAPC, индуцирующую наибольшее количество делений клеток в конкретный момент времени, считают наиболее мощным средством для экспансии.
Для определения того, насколько хорошо эти aAPC стимулируют длительный рост T-клеток, получают кривые роста клеток. Эти эксперименты проводят точно так же, как эксперименты по окрашиванию CFSE, но не используют CFSE. Каждые 2-3 дня культивирования T-клетки удаляют из соответствующих культур и подсчитывают с использованием счетчика Коултера, с помощью которого измеряют количество присутствующих клеток и средний объем клеток. Средний объем клеток является лучшим показателем того, когда необходимо повторно стимулировать клетки. В основном, если T-клетки правильно стимулированы, они увеличивают свой объем в три раза. Когда этот объем снижается до более чем приблизительно половины от исходного бласта, может потребоваться повторная стимуляция T-клеток для поддержаний логарифмической линейной экспансии (Levine et al., 1996, Science 272:1939-1943; Levine et al., 1997, J. Immunol. 159:5921-5930). Вычисляют время, которое требуется каждой aAPC для индуцирования 20 удвоений популяции. Относительные различия каждой aAPC в отношении индуцирования этого уровня экспансии T-клеток является важным критерием, используемым для включения конкретной aAPC в клинические испытания.
Фенотипы клеток, экспансию которых вызывает каждая aAPC, охарактеризовывают для определения того, будет ли конкретная субпопуляция подвергаться преференциальной экспансии. Перед каждой повторной стимуляцией осуществляют анализ фенотипа подвергаемых экспансии популяций T-клеток для определения состояния дифференцировки подвергаемых экспансии T-клеток с использованием определения CD27 и CD28, предложенного Appay et al. (2002, Nature Med. 8, 379-385), и определения CCR7, предложенного Sallusto et al. (1999, Nature 401:708-712). Внутриклеточное окрашивание перфорина и гранзима B используют для оценки цитолитического потенциала.
В одном из аспектов способ включает приведение различных aAPC в контакт с субпопуляцией T-клеток без того, чтобы сначала охарактеризовывать костимуляторные молекулы на поверхности T-клеток субпопуляции. Кроме того, настоящее изобретение включает способ, в котором костимуляторные молекулы, присутствующие на поверхности T-клеток субпопуляции, исследуют перед приведением aAPC в контакт с клеткой. Таким образом, настоящее изобретение относится к новому анализу для определения требований к росту для различных субпопуляций T-клеток.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, нуждающегося в измененном иммунном ответе, включающему приведение T-клеток индивидуума в контакт с APC, представленными в настоящем описании, и, таким образом, лечение индивидуума, нуждающегося в измененном иммунном ответе. В некоторых вариантах осуществления приведение в контакт осуществляют in vitro или in vivo. В некоторых вариантах осуществления приведение в контакт осуществляют in vitro. В некоторых вариантах осуществления приведение в контакт осуществляют in vivo.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, нуждающегося в измененном иммунном ответе, включающему a) определение статуса HLA индивидуума, b) селекцию искусственной антигенпрезентирующей клетки (aAPC), иммунологически совместимой с индивидуумом, где aAPC является сконструированной эритроидной клеткой, экспрессирующей первый экзогенный антигенный полипептид, и c) введение aAPC индивидууму и, таким образом, лечение индивидуума, нуждающегося в измененном иммунном ответе.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, нуждающегося в измененном иммунном ответе, включающему a) определение профиля экспрессии антигена у индивидуума, b) селекцию искусственной антигенпрезентирующей клетки (aAPC), где aAPC является сконструированной эритроидной клеткой, экспрессирующей первый экзогенный антигенный полипептид, и c) введение aAPC индивидууму и, таким образом, лечение индивидуума, нуждающегося в измененном иммунном ответе.
Иммунный ответ, индуцируемый у индивидуума посредством введения aAPC по настоящему изобретению, может включать клеточные иммунные ответы, опосредованные CD8+ T-клетками, способными уничтожать опухолевые и инфицированные клетки, и ответы CD4+ T-клеток. Также можно индуцировать гуморальные иммунные ответы, опосредованные, главным образом, B-клетками, продуцирующими антитела после активации CD4+ T-клетками. Для анализа типа иммунного ответа, индуцированного с помощью композиций по настоящему изобретению, можно использовать различные способы, хорошо известные в этой области, например, описанные в Coligan et al., Current Protocols in Immunology, John Wiley & Sons Inc., 1994.
Цитотоксические CD8+ T-клетки отвечают на антигены, связанные с молекулами MHC класса I. Хелперные CD4+ T-клетки отвечают на антигены, связанные с молекулами MHC класса II. Активированные CD4+ T-клетки, в свою очередь, активируют новые и существующие CD8+ T-клетки (антигенспецифические и наивные CD8+ T-клетки). Таким образом, в некоторых вариантах осуществления изобретения aAPC, приводящие к экспансии и активации антигенспецифических CD8+ T-клеток (aAPC, содержащие антиген, связанный с MHC класса I), можно вводить с aAPC, активирующими CD4+ T-клетки (aAPC, содержащими антиген, связанный с MHC класса II), таким образом, потенцируя иммунный ответ. В некоторых вариантах осуществления aAPC, приводящие к экспансии и активации антигенспецифических CD8+ T-клеток, можно вводить с aAPC, активирующими CD4+ T-клетки, таким образом, синергически повышая устойчивость иммунного ответа. В некоторых вариантах осуществления aAPC, содержащие антиген, связанный с MHC класса I, и костимуляторный полипептид, можно вводить с aAPC, содержащими антиген, связанный с MHC класса II. В других вариантах осуществления aAPC, содержащие антиген, связанный с MHC класса I, можно вводить с aAPC, содержащими антиген, связанный с MHC класса II, и костимуляторный полипептид. В некоторых вариантах осуществления aAPC, содержащие антиген, связанный с MHC класса I, и костимуляторный полипептид, можно вводить с aAPC, содержащими антиген, связанный с MHC класса II, и костимуляторный полипептид.
В некоторых вариантах осуществления индивидууму вводят aAPC, содержащие экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенпрезентирующий полипептид является полипептидом MHC класса I или одноцепочечным слитым белком MHC класса I, вместе с aAPC, содержащими экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенпрезентирующий полипептид является полипептидом MHC класса II или одноцепочечным слитым белком MHC класса II. Введение антигена, связанного с MHC класса I, в комбинации с антигеном, связанным с MHC класса II, обеспечивает выполнение комплементарной функции CD8+ и CD4+ T-клеток.
В дополнительных аспектах настоящее изобретение также относится к способам экспансии популяции T-клеток посредством лигирования молекул на поверхности клеток. Кроме того, целью является предоставление способа индуцирования популяции T-клеток из индивидуума для быстрой пролиферации с экспоненциальным ростом в течение длительного периода времени до количеств, достаточных для исследовательских целей, включающего выделение популяции T-клеток из индивидуума, активацию популяции T-клеток посредством приведения T-клеток ex vivo в контакт с по меньшей мере одним экзогенным полипептидом, обеспечивающим первичный сигнал активации для T-клеток, и стимуляцию активированных T-клеток по меньшей мере одним вторым экзогенным полипептидом, обеспечивающим костимуляторный сигнал, таким образом, что T-клетки, получившие первичный сигнал активации, стимулируют для быстрой пролиферации. В частности, целью является предоставление такого способа, если индивидуум является человеком, и способ дополнительно включает использование активированных T-клеток для идентификации антигенов у индивидуума. Кроме того, если индивидуум инфицирован и страдает заболеванием или состоянием, с которым ассоциирован по меньшей мере один антиген, способ по настоящему изобретению дополнительно включает использование активированных T-клеток для идентификации по меньшей мере одного антигена. Антиген может содержать, в качестве неограничивающих примеров, опухолевый антиген, антиген, связанный с аутоиммунным нарушением или состоянием, или инфекционным заболеванием, или патогеном. Способ дополнительно включает скрининг по меньшей мере одного антигена в качестве молекулы-мишени для исследовательских целей или для разработки вакцины на основе по меньшей мере одного антигена.
Лечение состояний, при которых можно достичь благоприятного эффекта при модуляции T-клеточного ответа
Способы введения сконструированных эритроидных клеток, содержащих (например, презентирующих) экзогенное средство (например, полипептиды), описывают, например, в WO2015/073587 и WO2015/153102, каждый из которых включен в качестве ссылки в полном объеме.
В вариантах осуществления aAPC, включающие сконструированные эритроидные клетки, представленные в настоящем описании, вводят индивидууму, например, млекопитающему, например, человеку. Неограничивающие примеры млекопитающих, которых можно лечить, включают людей, домашних животных (например, собак, кошек и т.п.), сельскохозяйственных животных (например, коров, овец, свиней, лошадей и т.п.) и лабораторных животных (например, обезьян, крыс, мышей, кроликов, морских свинок и т.п.). Способы, представленные в настоящем описании, можно использовать для терапии человека и в ветеринарии. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В некоторых вариантах осуществления эритроидные клетки вводят пациенту каждые 1, 2, 3, 4, 5 или 6 месяцев.
В некоторых вариантах осуществления дозы эритроидных клеток содержат приблизительно 1×109-2×109, 2×109-5×109, 5×109-1×1010, 1×1010-2×1010, 2×1010-5×1010, 5×1010-1×1011, 1×1011-2×1011, 2×1011-5×1011, 5×1011-1×1012, 1×1012-2×1012, 2×1012-5×1012 или 5×1012-1×1013 клеток.
В некоторых вариантах осуществления эритроидные клетки вводят пациенту по схеме введения (доза и периодичность введения), достаточной для поддержания функции вводимых эритроидных клеток в кровотоке пациента в течение периода от 2 недель до года, например, от одного месяца до одного года или более, например, по меньшей мере 2 недели, 4 недели, 6 недель, 8 недель, 3 месяца, 6 месяцев, года, 2 лет.
В некоторых вариантах осуществления эритроидные клетки (например, aAPC, представленные в настоящем описании) вводят пациенту в двух дозах или более (например, 2, 3, 4 или более дозах). В дополнительных вариантах осуществления эритроидные клетки (например, aAPC, представленные в настоящем описании) вводят пациенту в двух дозах или более, где вторую дозу вводят за один раз после первой дозы, когда пролиферацию T-клеток определяют как пиковую. В некоторых вариантах осуществления aAPC по настоящему изобретению вводят в первой дозе, где первая доза стимулирует пролиферацию и активацию T-клеток. После первой дозы aAPC по настоящему изобретению вводят во второй дозе, когда T-клетки активируются, и пролиферация находится на пике, для стимуляции экспансии T-клеток. Не желая быть связанными какой-либо теорией, полагают, что введение aAPC по настоящему изобретению в двух или более дозах повышает способность aAPC стимулировать популяцию T-клеток памяти и, таким образом, обеспечивать более длительную эффективность, например, эффективность против рецидива опухоли или повторного заражения возбудителем инфекции.
Пиковую пролиферацию T-клеток можно определять способами, известными специалистам в этой области. Например, пиковую пролиферацию T-клеток можно определять по включению 3H-тимидина пролиферирующими T-клетками или посредством мечения пролиферирующих T-клеток флуоресцентным красителем сукцинимидиловым сложным эфиром диацетата 5,6-карбоксифлуоресцеина (CFSE).
В некоторых аспектах настоящее изобретение относится к способу лечения заболевания или состояния, представленного в настоящем описании, включающему введение нуждающемуся в этом индивидууму композиции, представленной в настоящем описании, например, aAPC, представленных в настоящем описании. В некоторых вариантах осуществления заболевание или состояние является злокачественным новообразованием. В некоторых вариантах осуществления заболевание или состояние является аутоиммунным заболеванием. В некоторых вариантах осуществления заболевание или состояние является аутоиммунным заболеванием, ассоциированным или запускаемым возбудителем инфекции. В некоторых вариантах осуществления заболевание или состояние является инфекционным заболеванием.
В некоторых аспектах настоящее изобретение относится к применению aAPC, представленных в настоящем описании, для лечения заболевания или состояния, представленного в настоящем описании, например, злокачественного новообразования, аутоиммунного заболевания, такого как аутоиммунное заболевание, запускаемое возбудителем инфекции, или инфекционного заболевания. В некоторых аспектах настоящее изобретение относится к применению aAPC, представленных в настоящем описании, для производства лекарственных средств для лечения заболевания или состояния, представленного в настоящем описании, например, злокачественного новообразования, аутоиммунного заболевания, такого как аутоиммунное заболевание, запускаемое возбудителем инфекции, или инфекционного заболевания.
В некоторых вариантах осуществления aAPC содержит первый экзогенный полипептид, содержащий первое терапевтическое средство (например, противоопухолевое терапевтическое средство, терапевтическое средство против аутоиммунного заболевания, терапевтическое средство против инфекционного заболевания). В некоторых предпочтительных вариантах осуществления первое терапевтическое средство является антигеном, например, опухолевым антигеном, антигеном, ассоциированным с аутоиммунным нарушением или состоянием, таким как аутоиммунное заболевание, запускаемое возбудителем инфекции, или инфекционным заболеванием или патогеном. В вариантах осуществления aAPC дополнительно содержит второй экзогенный полипептид, где второй экзогенный полипептид содержит антигенпрезентирующий полипептид, например, MHC класса I или MHC класса II. В вариантах осуществления aAPC дополнительно содержит третий экзогенный полипептид, где третий экзогенный полипептид содержит по меньшей мере один костимуляторный полипептид, коингибиторный полипептид или полипептид для экспансии Treg, как представлено в настоящем описании.
В некоторых вариантах осуществления aAPC содержит первый экзогенный полипептид, содержащий первое терапевтическое средство (например, противоопухолевое терапевтическое средство, терапевтическое средство против аутоиммунного заболевания, терапевтическое средство против инфекционного заболевания), и второй экзогенный полипептид, содержащий второе терапевтическое средство (например, противоопухолевое терапевтическое средство, терапевтическое средство против аутоиммунного заболевания, терапевтическое средство против инфекционного заболевания). В некоторых предпочтительных вариантах осуществления терапевтическое средство является антигенным полипептидом, например, опухолевым антигеном, антигеном, ассоциированным с аутоиммунным нарушением или состоянием, таким как аутоиммунное заболевание, запускаемое возбудителем инфекции, или инфекционным заболеванием или патогеном. В вариантах осуществления aAPC дополнительно содержит третий экзогенный полипептид, где третий экзогенный полипептид содержит антигенпрезентирующий полипептид, например, MHC класса I или MHC класса II. В вариантах осуществления aAPC дополнительно содержит четвертый экзогенный полипептид, где четвертый экзогенный полипептид содержит по меньшей мере один костимуляторный полипептид, коингибиторный полипептид или полипептид для экспансии Treg, как представлено в настоящем описании.
В некоторых вариантах осуществления aAPC содержит первый экзогенный полипептид, содержащий первое терапевтическое средство (например, противоопухолевое терапевтическое средство, терапевтическое средство против аутоиммунного заболевания, терапевтическое средство против инфекционного заболевания), второй экзогенный полипептид, содержащий второе терапевтическое средство (например, противоопухолевое терапевтическое средство, терапевтическое средство против аутоиммунного заболевания, терапевтическое средство против инфекционного заболевания), и третий экзогенный полипептид, содержащий третье терапевтическое средство (например, противоопухолевое терапевтическое средство, терапевтическое средство против аутоиммунного заболевания, терапевтическое средство против инфекционного заболевания). В некоторых предпочтительных вариантах осуществления терапевтическое средство является антигенным полипептидом, например, опухолевым антигеном, антигеном, ассоциированным с аутоиммунным нарушением или состоянием, или инфекционным заболеванием или патогеном. В вариантах осуществления aAPC дополнительно содержит четвертый экзогенный полипептид, где четвертый экзогенный полипептид содержит антигенпрезентирующий полипептид, например, MHC класса I или MHC класса II. В вариантах осуществления aAPC дополнительно содержит пятый экзогенный полипептид, где третий экзогенный полипептид содержит по меньшей мере один костимуляторный полипептид, коингибиторный полипептид или полипептид для экспансии Treg, как представлено в настоящем описании.
В вариантах осуществления любые два или более из первого, второго и третьего терапевтического средства могут распознавать, связывать и/или воздействовать на одну и ту же мишень, например, рецептор поверхности клетки и/или эндогенный белок человека. Альтернативно, первое, второе и третье терапевтическое средство могут воздействовать на разные мишени.
Первая, вторая или третья мишени могут являться членами одного биологического пути, где, необязательно, мишени являются рецепторами поверхности клетки, эндогенными белками человека. В рамках изобретения термин "путь" или "биологический путь" относится к множеству биологических молекул, например, полипептидов, действующих совместно последовательным образом. Примеры путей включают каскады передачи сигнала и каскады комплемента. В некоторых вариантах осуществления путь начинается с детекции внеклеточного сигнала и заканчивается изменением транскрипции гена-мишени. В некоторых вариантах осуществления путь начинается с детекции цитоплазматического сигнала и заканчивается изменением транскрипции гена-мишени. Путь может являться линейным или разветвленным. Если он является разветвленным, он может иметь множество входных сигналов (быть сходящимся) или множество выходных сигналов (быть расходящимся).
Первая, вторая или третья мишень могут находиться на одних и тех же типах клеток или разных типах клеток. В некоторых вариантах осуществления первый экзогенный полипептид связывается с первой клеткой, например, первым типом клеток, и второй экзогенный полипептид связывается со второй клеткой, например, вторым типом клеток. В некоторых вариантах осуществления первый и второй типы клеток являются одинаковыми. В некоторых вариантах осуществления первый и второй типы клеток отличаются. В некоторых вариантах осуществления первый экзогенный полипептид локализует сконструированную эритроидную клетку в желаемом участке, например, клетке человека, и второй экзогенный полипептид имеет терапевтическую активность, например, антигенпрезентирующую активность.
В некоторых вариантах осуществления терапевтическое средство является подходящим экзогенным антигеном, выбранным для взаимодействия со специфической мишенью. Подходящие мишени включают молекулы, ассоциированные с конкретным заболеванием, нарушением или состоянием (например, злокачественным новообразованием, аутоиммунным заболеванием, инфекционным заболеванием). Однако мишени также можно выбирать независимо от конкретного заболевания, нарушения или состояния.
В некоторых вариантах осуществления эффект первого и второго или и первого, и второго, и третьего экзогенного полипептида является синергическим. Термин "синергический" или "синергия" означает более чем аддитивный эффект комбинации двух или более средств (например, полипептидов, являющихся частью сконструированной эритроидной клетки) по сравнению с их отдельными эффектами. В некоторых вариантах осуществления синергическая активность является более чем аддитивным эффектом сконструированной эритроидной клетки, содержащей первый полипептид и второй полипептид, по сравнению с эффектом сконструированной эритроидной клетки, содержащей первый полипептид, и сконструированной эритроидной клетки, содержащей второй полипептид. В некоторых вариантах осуществления синергическая активность присутствует, если первое средство приводит к детектируемому уровню выходного сигнала X, второе средство приводит к детектируемому уровню выходного сигнала X, и первое и второе средства вместе приводят к более чем аддитивному уровню выходного сигнала X.
Злокачественное новообразование
В некоторых вариантах осуществления настоящее изобретение относится к aAPC, включающей эритроидную клетку (например, безъядерную эритроидную клетку) или безъядерную клетку, содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит терапевтическое средство для лечения злокачественного средства (противоопухолевое терапевтическое средство). В некоторых вариантах осуществления aAPC содержит первый экзогенный полипептид, содержащий первое противоопухолевое терапевтическое средство, и второй экзогенный полипептид, содержащий второе противоопухолевое терапевтическое средство. В некоторых вариантах осуществления aAPC содержит первый экзогенный полипептид, содержащий первое противоопухолевое терапевтическое средство, второй экзогенный полипептид, содержащий второе противоопухолевое терапевтическое средство, и третий экзогенный полипептид, содержащий третье противоопухолевое терапевтическое средство. Любые два или более из первого, второго и третьего противоопухолевого терапевтического средства могут воздействовать на одну и ту же мишень, например, рецептор поверхности клетки и/или эндогенный белок человека. Альтернативно, первое, второе и третье противоопухолевое терапевтическое средство могут действовать на разные мишени. Любые два или более из первой, второй и третьей мишеней могут являться членами одного и того же биологического пути, где, необязательно, мишени являются рецепторами поверхности клетки, эндогенными белками человека. Первая, вторая или третья мишень могут находиться на разных типах клеток. В некоторых вариантах осуществления первый экзогенный полипептид локализует сконструированную эритроидную клетку в желаемом участке, например, клетке человека, и второй экзогенный полипептид имеет терапевтическую активность, например, антигенпрезентирующую активность.
В некоторых предпочтительных вариантах осуществления первое терапевтическое средство является антигеном, например, опухолевым антигеном. В некоторых вариантах осуществления первое терапевтическое средство и второе терапевтическое средство является антигеном, например, опухолевым антигеном. В некоторых вариантах осуществления первое, второе и третье терапевтическое средство является антигеном, например, опухолевым антигеном.
В вариантах осуществления aAPC дополнительно содержит дополнительный экзогенный полипептид, где дополнительный экзогенный полипептид содержит антигенпрезентирующий полипептид, например, молекулу MHC (например, MHC класса I или MHC класса II). В вариантах осуществления aAPC дополнительно содержит дополнительный экзогенный полипептид, где дополнительный экзогенный полипептид содержит по меньшей мере один костимуляторный полипептид. В некоторых вариантах осуществления aAPC дополнительно содержит дополнительный экзогенный полипептид, содержащий антигенпрезентирующий полипептид и дополнительный экзогенный полипептид, содержащий по меньшей мере один костимуляторный полипептид.
В некоторых вариантах осуществления aAPC содержит первый экзогенный полипептид, содержащий антигенпрезентирующий полипептид, например, молекулу MHC (например, MHC класса I или MHC класса II), и второй экзогенный полипептид содержит антиген (например, опухолеассоциированный антиген).
В некоторых вариантах осуществления изобретения aAPC, приводящие к экспансии и активации антигенспецифических CD8+ T-клеток в опухоли (aAPC, содержащие антиген, связанный с MHC класса I), можно вводить с aAPC, активирующими CD4+ T-клетки (aAPC, содержащими антиген, связанный с MHC класса II), активирующими и антигенспецифические, и наивные CD8+ T-клетки в опухоли и лимфоузлах и, таким образом, потенцирующими устойчивый противоопухолевый ответ. В некоторых вариантах осуществления aAPC, приводящие к экспансии и активации антигенспецифических CD8+ T-клеток в опухоли, можно вводить с aAPC, активирующими CD4+ T-клетки, активирующими и антигенспецифические, и наивные CD8+ T-клетки в опухоли и лимфоузлах, таким образом, синергически повышая устойчивость иммунного ответа.
В некоторых вариантах осуществления aAPC, содержащие первый экзогенный антигенпрезентирующий полипептид и второй экзогенный полипептид, содержащий антиген (например, первый опухолеассоциированный антиген), где экзогенный антигенпрезентирующий полипептид является полипептидом MHC класса I или одноцепочечным слитым белком MHC класса I, вводят индивидууму совместно с aAPC, содержащими первый экзогенный антигенпрезентирующий полипептид и второй экзогенный полипептид, содержащий антиген (например, второй опухолеассоциированный антиген), где экзогенный антигенпрезентирующий полипептид является полипептидом MHC класса II или одноцепочечным слитым белком MHC класса II. В некоторых вариантах осуществления aAPC, содержащие антиген, связанный с MHC класса I, и костимуляторный полипептид, можно вводить с aAPC, содержащими антиген, связанный с MHC класса II. В других вариантах осуществления aAPC, содержащие антиген, связанный с MHC класса I, можно вводить с aAPC, содержащими антиген, связанный с MHC класса II, и костимуляторный полипептид. В некоторых вариантах осуществления aAPC, содержащие антиген, связанный с MHC класса I, и костимуляторный полипептид, можно вводить с aAPC, содержащими антиген, связанный с MHC класса II, и костимуляторный полипептид.
Не желая быть связанными какой-либо теорией, полагают, что презентирование опухолевого антигена MHC класса I и MHC класса II в комбинации с мощной костимуляцией потенциально может приводить к устойчивому опухолеспецифическому цитолизу.
В настоящем изобретении предусмотрено, что антиген может являться любым опухолевым антигеном или его антигенной частью, известным в этой области, включая, в качестве неограничивающих примеров, любые один или более из антигенов или их антигенных частей, приведенных в таблице 1. Специалистам в этой области будет понятно, что aAPC, содержащие антиген, приведенный в таблице 1, можно использовать для лечения злокачественного новообразования, например, конкретного злокачественного новообразования, соответствующего конкретному антигену или антигенному пептиду, приведенному в таблице 1.
Таким образом, в некоторых аспектах настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, представленных в настоящем описании, и, таким образом, лечение злокачественного новообразования.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит опухолеассоциированный антиген, и, таким образом, лечение злокачественного новообразования. Настоящее изобретение включает любую комбинацию конкретного злокачественного новообразования в качестве злокачественного новообразования, подлежащего лечению с помощью способа, и опухолеассоциированного антигена в качестве антигена, подлежащего презентированию на aAPC, представленных совместно в таблице 1.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов включает антиген MAGE-A, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов включает антиген MAGE-A1, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления антиген MAGE-A1 является антигеном MAGE-A1, приведенным в таблице 1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов включает антиген MAGE-A2, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления антиген MAGE-A2 является антигеном MAGE-A2, приведенным в таблице 1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов включает антиген MAGE-A3, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления антиген MAGE-A3 является антигеном MAGE-A3, приведенным в таблице 1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов включает антиген MAGE-A4, таким образом лечение злокачественного новообразования. В некоторых вариантах осуществления антиген MAGE-A4 является антигеном MAGE-A4, приведенным в таблице 1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов включает антиген MAGE-A5, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления антиген MAGE-A5 является антигеном MAGE-A5, приведенным в таблице 1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов включает антиген MAGE-A6, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления антиген MAGE-A6 является антигеном MAGE-A6, приведенным в таблице 1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов включает антиген MAGE-A7, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления антиген MAGE-A7 является антигеном MAGE-A7, приведенным в таблице 1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов включает антиген MAGE-A8, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления антиген MAGE-A8 является антигеном MAGE-A8, приведенным в таблице 1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов включает антиген MAGE-A9, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления антиген MAGE-A9 является антигеном MAGE-A9, приведенным в таблице 1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов включает антиген MAGE-A10, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления антиген MAGE-A10 является антигеном MAGE-A10, приведенным в таблице 1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов включает антиген MAGE-A11, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления антиген MAGE-A11 является антигеном MAGE-A11, приведенным в таблице 1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов включает антиген MAGE-A12, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления антиген MAGE-A12 является антигеном MAGE-A1, приведенным в таблице 1. В некоторых вариантах осуществления антиген MAGE-A2 является антигеном MAGE-A12, приведенным в таблице 1.
В некоторых вариантах осуществления злокачественное новообразование является острым миелогенным лейкозом (AML). В некоторых вариантах осуществления злокачественное новообразование является меланомой. В некоторых вариантах осуществления злокачественное новообразование является солидной опухолью.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает иммуногенный пептид антигена MAGE-A. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает эпитоп, общий для нескольких опухолевых антигенов из семейства MAGE-A. В некоторых вариантах осуществления экзогенный антигенный полипептид является p248v9, иммуногенным пептидом, презентируемым HLA-A*0201 и способным индуцировать цитотоксические T-лимфоциты, распознающие все антигены MAGE-A. В некоторых вариантах осуществления экзогенный антигенный полипептид является иммуногенным пептидом p248g9 (YLEYRQVPG (SEQ ID NO: 156)). В некоторых вариантах осуществления экзогенный антигенный полипептид является иммуногенным пептидом p248d9 (YLEYRQVPD (SEQ ID NO: 125)).
В некоторых вариантах осуществления злокачественное новообразование является острым миелогенным лейкозом (AML). В некоторых вариантах осуществления злокачественное новообразование является меланомой. В некоторых вариантах осуществления злокачественное новообразование является солидной опухолью.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает антиген протеазы гранул нейтрофилов, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает антиген эластазы нейтрофилов, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает антиген протеиназы 3, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает антиген катепсина G, и, таким образом, лечение злокачественного новообразования.
В некоторых вариантах осуществления злокачественное новообразование является острым миелогенным лейкозом (AML). В некоторых вариантах осуществления злокачественное новообразование является хроническим миелогенным лейкозом (CML). В некоторых вариантах осуществления злокачественное новообразование является раком молочной железы. В некоторых вариантах осуществления злокачественное новообразование является раком легких. В некоторых вариантах осуществления злокачественное новообразование является меланомой. В некоторых вариантах осуществления злокачественное новообразование является солидной опухолью.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит PR1 (VLQELNVTV (SEQ ID NO: 225)).
В некоторых вариантах осуществления злокачественное новообразование является острым миелогенным лейкозом (AML). В некоторых вариантах осуществления злокачественное новообразование является хроническим миелогенным лейкозом (CML). В некоторых вариантах осуществления злокачественное новообразование является раком молочной железы. В некоторых вариантах осуществления злокачественное новообразование является раком легких. В некоторых вариантах осуществления злокачественное новообразование является меланомой. В некоторых вариантах осуществления злокачественное новообразование является солидной опухолью.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает антиген NY-ESO-1/LAGE-2, и, таким образом, лечение злокачественного новообразования.
В некоторых вариантах осуществления злокачественное новообразование является множественной миеломой. В некоторых вариантах осуществления злокачественное новообразование является немелкоклеточным раком легких. В некоторых вариантах осуществления злокачественное новообразование является раком яичников. В некоторых вариантах осуществления злокачественное новообразование является меланомой. В некоторых вариантах осуществления злокачественное новообразование является солидной опухолью.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает по меньшей мере один полученный из NY-ESO-1/LAGE-2 пептид. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает по меньшей мере один экзогенный связывающий HLA класса I полипептид, полученный из NY-ESO-1/LAGE-2. В некоторых вариантах осуществления полипептид является SLLMWITQC (SEQ ID NO: 110). В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает по меньшей мере один экзогенный связывающий HLA класса II полипептид, полученный из NY-ESO-1/LAGE-2. В некоторых вариантах осуществления полипептид является SLLMWITQCFLPVF (SEQ ID NO: 114).
В некоторых вариантах осуществления экзогенный антигенный полипептид содержит антиген NY-ESO-1/LAGE-2, выбранный из SLLMWITQC (SEQ ID NO: 110), MLMAQEALAFL (SEQ ID NO: 109), YLAMPFATPME (SEQ ID NO: 204), ASGPGGGAPR (SEQ ID NO: 205), LAAQERRVPR (SEQ ID NO: 111), TVSGNILTIR (SEQ ID NO: 206), APRGPHGGAASGL (SEQ ID NO: 207), MPFATPMEAEL (SEQ ID NO: 208), KEFTVSGNILTI (SEQ ID NO: 209), MPFATPMEA (SEQ ID NO: 210), FATPMEAEL (SEQ ID NO: 211), FATPMEAELAR (SEQ ID NO: 212), LAMPFATPM (SEQ ID NO: 213), ARGPESRLL (SEQ ID NO: 214), SLLMWITQCFLPVF (SEQ ID NO: 114), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), EFYLAMPFATPM (SEQ ID NO: 216), PGVLLKEFTVSGNILTIRLTAADHR (SEQ ID NO: 217), RLLEFYLAMPFA (SEQ ID NO: 218), QGAMLAAQERRVPRAAEVPR (SEQ ID NO: 115), PFATPMEAELARR (SEQ ID NO: 219), PGVLLKEFTVSGNILTIRLT (SEQ ID NO: 220), VLLKEFTVSG (SEQ ID NO: 221), AADHRQLQLSISSCLQQL (SEQ ID NO: 116), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), LKEFTVSGNILTIRL (SEQ ID NO: 222), PGVLLKEFTVSGNILTIRLTAADHR (SEQ ID NO: 217), LLEFYLAMPFATPMEAELARRSLAQ (SEQ ID NO: 215), KEFTVSGNILT (SEQ ID NO: 223), LLEFYLAMPFATPM (SEQ ID NO: 224) и AGATGGRGPRGAGA (SEQ ID NO: 119). В некоторых вариантах осуществления антиген NY-ESO-1/LAGE-2 является одним или более антигенами NY-ESO-1/LAGE-2, приведенными в таблице 1.
В некоторых вариантах осуществления злокачественное новообразование является множественной миеломой. В некоторых вариантах осуществления злокачественное новообразование является немелкоклеточным раком легких. В некоторых вариантах осуществления злокачественное новообразование является раком яичников. В некоторых вариантах осуществления злокачественное новообразование является меланомой. В некоторых вариантах осуществления злокачественное новообразование является солидной опухолью.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов является полипептидом gp100. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов является полипептидом gp100, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом (например, молекулой MHC класса I или класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном gp100. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом (например, молекулой MHC класса I или класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I или полипептидом или одноцепочечным слитым белком MHC класса II, где экзогенный антигенный полипептид является антигеном gp100, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом (например, молекулой MHC класса I или класса II), где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где экзогенный антигенный полипептид является антигеном gp100. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является MHC класса I-2Db. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую экзогенный антигенпрезентирующий полипептид и экзогенный антигенный полипептид, где экзогенный антигенпрезентирующий полипептид является полипептидом или одноцепочечным слитым белком MHC класса I, где экзогенный антигенный полипептид является антигеном gp100, и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, экзогенный полипептид, содержащий костимуляторный полипептид. В некоторых вариантах осуществления костимуляторный полипептид является 4-1BBL. В некоторых вариантах осуществления экзогенный антигенпрезентирующий полипептид является MHC класса I-2Db.
В некоторых вариантах осуществления экзогенный антигенный полипептид содержит антиген gp100, выбранный из KTWGQYWQV (SEQ ID NO: 306), (A)MLGTHTMEV (SEQ ID NO: 307), IMDQVPFSV (SEQ ID NO: 308), ITDQVPFSV (SEQ ID NO: 309), YLEPGPVTA (SEQ ID NO: 310), LLDGTATLRL (SEQ ID NO: 311), VLYRYGSFSV (SEQ ID NO: 312), SLADTNSLAV (SEQ ID NO: 313), RLMKQDFSV (SEQ ID NO: 314), RLPRIFCSC (SEQ ID NO: 315), LIYRRRLMK (SEQ ID NO: 316), ALLAVGATK (SEQ ID NO: 317), IALNFPGSQK (SEQ ID NO: 318), RSYVPLAHR (SEQ ID NO: 319), ALNFPGSQK (SEQ ID NO: 320), ALNFPGSQK (SEQ ID NO: 320), VYFFLPDHL (SEQ ID NO: 321), RTKQLYPEW (SEQ ID NO: 322), HTMEVTVYHR (SEQ ID NO: 323), SSPGCQPPA (SEQ ID NO: 324), VPLDCVLYRY (SEQ ID NO: 325), LPHSSSHWL (SEQ ID NO: 326), SNDGPTLI (SEQ ID NO: 327), GRAMLGTHTMEVTVY (SEQ ID NO: 328), WNRQLYPEWTEAQRLD (SEQ ID NO: 329), TTEWVETTARELPIPEPE (SEQ ID NO: 330), TGRAMLGTHTMEVTVYH (SEQ ID NO: 331), GRAMLGTHTMEVTVY (SEQ ID NO: 328). В некоторых вариантах осуществления антиген gp100 является одним или более антигенами gp100, приведенными в таблице 1.
В некоторых вариантах осуществления злокачественное новообразование является множественной миеломой. В некоторых вариантах осуществления злокачественное новообразование является немелкоклеточным раком легких. В некоторых вариантах осуществления злокачественное новообразование является раком яичников. В некоторых вариантах осуществления злокачественное новообразование является меланомой. В некоторых вариантах осуществления злокачественное новообразование является солидной опухолью.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает антиген теломеразы, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает человек теломераза, и, таким образом, лечение злокачественного новообразования. В некоторых вариантах осуществления злокачественное новообразование является острым миелогенным лейкозом (AML).
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает ILAKFLHWL (SEQ ID NO: 658).
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает RLVDDFLLV (SEQ ID NO: 659).
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает RPGLLGASVLGLDDI (SEQ ID NO: 663).
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает LTDLQPYMRQFVAHL (SEQ ID NO: 664).
В некоторых вариантах осуществления злокачественное новообразование является острым миелогенным лейкозом (AML).
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего острый миелогенный лейкоз (AML), включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает PR1 (VLQELNVTV (SEQ ID NO: 225)). В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего острый миелогенный лейкоз (AML), включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает PR1 (VLQELNVTV (SEQ ID NO: 225)), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий костимуляторный полипептид. В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего острый миелогенный лейкоз (AML), включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных антигенных полипептидов, где один из одного или более экзогенных антигенных полипептидов включает PR1 (VLQELNVTV (SEQ ID NO: 225)), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL. В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего острый миелогенный лейкоз (AML), включающему введение индивидууму эффективного количества aAPC, включающих по меньшей мере один экзогенный антигенный полипептид, PR1 (VLQELNVTV (SEQ ID NO: 225)), слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2, слитым с трансмембранным доменом GPA (GPA), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий костимуляторный полипептид. В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего острый миелогенный лейкоз (AML), включающему введение индивидууму эффективного количества aAPC, включающих по меньшей мере один экзогенный антигенный полипептид, PR1 (VLQELNVTV (SEQ ID NO: 225)), слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2, слитым с трансмембранным доменом GPA (GPA), и где эритроидная клетка дополнительно презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный полипептид, содержащий 4-1BBL.
Настоящее изобретение не ограничено конкретным типом злокачественного новообразования, скорее любое злокачественное новообразование рассматривают как подлежащее лечению с помощью aAPC, представленных в настоящем описании. В некоторых вариантах осуществления злокачественное новообразование включает, в качестве неограничивающих примеров, злокачественное новообразование, выбранное из острого лимфобластного лейкоза (ALL), острого миелолейкоза (AML), рака анального канала, рака желчных протоков, рака мочевого пузыря, злокачественного новообразования костной ткани, рака толстого кишечника, опухоли головного мозга, рака молочной железы, рака с неизвестной первичной локализацией, метастазов в кости, метастазов в головном мозге, метастазов в печени, метастазов в легких, карциноида, рака шейки матки, хориокарциномы, хронического лимфоцитарного лейкоза (CLL), хронического миелолейкоза (CML), рака толстого кишечника, колоректального рака, рака эндометрия, злокачественного новообразования глаза, рака желчного пузыря, рака желудка, гестационной трофобластической болезни (GTT), волосатоклеточного лейкоза, рака головы и шеи, лимфомы Ходжкина, рака почки, рака гортани, лейкоза, рака печени, рака легких, лимфомы, меланомного рака кожи, мезотелиомы, рака мужской половой системы, пузырного заноса, рака ротовой полости и ротоглотки, миеломы, рака носовой полости и синусов, рака носоглотки, неходжкинской лимфомы (NHL), рака пищевода, рака яичников, рака поджелудочной железы, рака полового члена, рака предстательной железы, редких злокачественных новообразований, рака прямой кишки, рака слюнных желез, вторичных злокачественных новообразований, рака кожи (немеланомного), саркомы мягких тканей, рака желудка, рака яичка, рака щитовидной железы, рака с неизвестной первичной локализацией, рака матки, рака влагалища и рака женских наружных половых органов.
В некоторых вариантах осуществления злокачественное новообразование является лейкозом, например, AML или ALL. В других вариантах осуществления злокачественное новообразование является печеночноклеточной карциномой. В других вариантах осуществления злокачественное новообразование выбрано из рака шейки матки, рака головы и шеи, лимфом и светлоклеточной карциномы почек.
Неоантиген представляет собой класс опухолевых антигенов, возникающих в результате опухолеспецифических мутаций, изменяющих аминокислотную последовательность кодируемых геномом белков. Неоантиген может включать полипептидную последовательность или нуклеотидную последовательность. Мутация может включать инсерционно-делеционную мутацию (инсерцию или делецию) со сдвигом рамки считывания или без сдвига рамки считывания, миссенс- или нонсенс-замену, изменение участка сплайсинга, геномную перестановку или слияние генов или любое геномное изменение или изменение экспрессии, приводящие к образованию neoORF. Мутация также может включать вариант сплайсинга. Посттрансляционные модификации, специфические для опухолевой клетки, могут включать аномальное фосфорилирование. Посттрансляционные модификации, специфические для опухолевой клетки, также могут включать образовавшийся в протеасоме сплайсированный антиген. См. Liepe et al., A large fraction of HLA class I ligands are proteasome-generated spliced peptides; Science. 2016 Oct. 21; 354 (6310):354-358. Опухолевый неоантиген является неоантигеном, присутствующим в опухолевой клетке или ткани индивидуума, но не в соответствующей нормальной клетке или ткани индивидуума.
С помощью недавних анализов наборов данных из Атласа ракового генома (TCGA) выявлена связь геномного ландшафта опухолей с опухолевым иммунитетом, включающая роль неоантигенной нагрузки в регуляции T-клеточных ответов (Brown et al., Genome Res. 2014 May; 24(5):743-50, 2014) и идентификацию соматических мутаций, ассоциированных с иммунными инфильтратами (Rutledge et al., Clin Cancer Res. 2013 Sep 15; 19(18):4951-60, 2013). Rooney et al. (2015 Jan 15; 160(1-2):48-61), что позволяет предполагать, что неоантигены и вирусы, вероятно, регулируют цитолитическую активность, и выявлять известные и новые мутации, позволяющие опухолям противостоять атаке иммунной системы.
В некоторых вариантах осуществления антиген является неоантигеном, определенным в злокачественной клетке индивидуума. В некоторых вариантах осуществления неоантиген является перекрестно-реагирующим неоантигеном. Способы идентификации неоантигенов известны в этой области и описаны, например, в патенте США №10055540, в полном объеме включенном в настоящее описание в качестве ссылки. Неоантигенные полипептиды и перекрестно-реагирующие неоантигенные полипептиды описаны, например, в PCT/US2016/033452, патентной публикации США №20180055922, Schumacher and Hacohen et al. (Curr Opin Immunol. 2016 Aug;41:98-103), Gubin, MM et al. (Nature. 2014 Nov 27; 515(7528):577-81), Schumacher and Schreiber, Science. 2015 Apr 3; 348(6230):69-74), Ott PA., et al., Nature. 2017 Jul 13;547(7662):217-221, все из которых включены в настоящее описание в качестве ссылки в полном объеме.
Таким образом, в некоторых вариантах осуществления экзогенный антигенный полипептид является неоантигенным полипептидом. В некоторых вариантах осуществления экзогенный антигенный полипептид является неоантигенным полипептидом, приведенным в базе данных The Comprehensive Tumor-Specific Neoantigen Database (TSNAdb v1.0); доступной по адресу biopharm.zju.edu.cn/tsnadb и описанной в Wu et al., Genomics Proteomics Bioinformatics 16 (2018) 276-282. В некоторых вариантах осуществления экзогенный антигенный полипептид является неоантигенным полипептидом, приведенным в патенте США №10055540, в полном объеме включенном в настоящее описание в качестве ссылки. В некоторых вариантах осуществления неоантигенный полипептид выбран из полипептида, приведенного в таблице 14.
Таблица 14. Неоантигенные полипептиды
В некоторых вариантах осуществления неоантигенный полипептид выбран из полипептида, приведенного в таблице 15.
Таблица 15. Неоантигенные полипептиды
В случае высокоагрессивных срединных глиом рекуррентная точечная мутация в гене гистона-3 (H3F3A) вызывает аминокислотную замену лизина метионином в положении 27 (K27M). В Ochs et al. (Oncoimmunology. 2017; 6(7):e1328340, включенной в настоящее описание в качестве ссылки в полном объеме) показано, что пептидная вакцина против K27M-мутантного гистона-3 может индуцировать эффективные, специфические в отношении мутации, опосредованные цитотоксическими T-клетками и T-хелпер-1-клетками иммунные ответы в гуманизированной модели главного комплекса гистосовместимости (MHC) на мышах. Таким образом, в некоторых вариантах осуществления неоантигенный полипептид является H3F3A (K27M) (SEQ ID NO: 890).
В некоторых вариантах осуществления злокачественное новообразование является злокачественным новообразованием, ассоциированным с онкогенным вирусом, например, вирусом Эпштейна-Барр (EBV), вирусом гепатита B и C (HBV и HCV), вирусом папилломы человека (HPV), вирусом саркомы Капоши (KSV) и полиомавирусами. В некоторых других вариантах осуществления злокачественное новообразование является злокачественным новообразованием, в котором идентифицированы ретровирусные эпитопы. Злокачественные новообразования, ассоциированные с вирусом, и которые можно лечить способами по настоящему изобретению, включают, в качестве неограничивающих примеров, рак шейки матки, рак головы и шеи, лимфомы и светлоклеточную карциному почки.
Молекулы лейкоцитарного антигена человека (HLA) необходимы для иммунного распознавания и последующего цитолиза неопластических клеток иммунной системы, т.к., чтобы распознаваться T-клеточными рецепторами, опухолевые антигены должны презентироваться в соответствии с HLA-рестриктированием. Некоторые опухолевые клетки используют аномальную экспрессию неклассических молекул HLA-I (HLA-E и HLA-G), функционирующих в качестве ингибиторных лигандов для иммунокомпетентных клеток, для избегания распознавания иммунной системой и облегчения ускользания от иммунного надзора (Moreau et al., Cell Mol Life Sci. 2002 Sep; 59(9):1460-6, включенная в настоящее описание в качестве ссылки в полном объеме). Альфа-цепь G антигена гистосовместимости HLA класса I (HLA-G) является неклассической молекулой MHC класса I, содержащей тяжелую α-цепь, содержащую один или более доменов альфа-1, альфа-2 и альфа-3.
В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка содержит на своей поверхности экзогенный антигенный полипептид, где экзогенный антигенный полипептид является полученным из HLA-G полипептидом. В некоторых вариантах осуществления полученные из HLA-G полипептиды выбраны из полипептидов, представленных ниже:
HLA-G146-154 - DYLALNEDL (SEQ ID NO: 891)
HLA-G194-202 - RYLENGKEM (SEQ ID NO: 892)
HLA-G139-148 - RYAYDGKDYL (SEQ ID NO: 893)
HLA-G141-150 - AYDGKDYLAL (SEQ ID NO: 894)
В некоторых вариантах осуществления представленные выше пептиды (SEQ ID NO: 891-894) связываются со специфическим аллелем HLA-A: HLA-A*24:02 (например, HLA-A*24:02:01:01). В некоторых вариантах осуществления представленные выше пептиды (SEQ ID NO: 891-894) связываются с другими аллелями HLA, представленными в настоящем описании.
В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, PR1, рестриктированный по лейкоцитарному антигену человека (HLA)-A2 пептид, слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2, слитым с трансмембранным доменом GPA (GPA) (PR1-HLA-A2-GPA). В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В некоторых вариантах осуществления aAPC по настоящему изобретению используют для лечения сильно васкуляризованных опухолей. Не желая быть связанными какой-либо теорией, полагают, что более высокая васкуляризация делает опухоли более доступными для aAPC, включающих безъядерные клетки (например, эритроидные клетки) по настоящему изобретению. Васкуляризацию можно измерять, например, по межкапиллярному расстоянию (как считают отражающему оксигенацию опухоли) и плотности микрососудов (обеспечивает гистологическую оценку ангиогенеза опухоли). Сильно васкуляризованная опухоль может являться любой опухолью сосудистого происхождения, например, гемангиомой, лимфангиомой, гемангиоэндотелиомой, саркомой Капоши, ангиосаркомой и гемангиобластомой.
В других вариантах осуществления aAPC по настоящему изобретению используют для лечения опухолей с сосудистой сетью с повышенной проницаемостью. Существует общее мнение, что кровеносные сосуды в опухолях являются аномальными. Одним из проявлений этой аномалии является дефективный эндотелий с повышенной проницаемостью. Проницаемость кровеносных сосудов не только влияет на внутреннюю среду опухолей и, вероятно, скорость ангиогенеза, но также регулирует доступ терапевтических средств. Не желая быть связанными какой-либо теорией, полагают, что более проницаемый кровеносный сосуд будет обеспечивать больше доступа для aAPC, включающей безъядерные клетки (например, эритроидные клетки) по настоящему изобретению.
Аутоиммунные заболевания
За последние два десятилетия был достигнут значительный прогресс в лечении диапазона аутоиммунных нарушений, при которых у многих пациентов наблюдают улучшение качества жизни в результате такого лечения. Несмотря на этот успех, существующие терапевтические подходы для аутоиммунных заболеваний являются, в общем или в частности, иммуносупрессорными и вызывают высокий риск оппортунистических инфекций и гемобластозов у пациентов, как в случае ингибиторов JAK, антител против ФНО и таргетированных антител против CD20. В до трети случаев пациенты с аутоиммунными нарушениями не отвечают на лечение, и наиболее отвечающие пациенты в конечном тоге теряют ответ с течением времени.
Хотя пусковой механизм большинства аутоиммунных заболеваний остается неизвестным, как правило, следует понимать, что клиническое заболевание является результатом утраты толерантности к собственным клеткам индивидуума. В принятой модели заболевания учитывают генетическую предрасположенность, запускаемую явлением из окружающей среды, приводящем к нарушению опосредованной T-клетками иммунной супрессии. В целом, восстановление периферической толерантности должно обеспечивать полное или частичное излечение пациента.
За годы исследовано множество конкурентных подходов для восстановления периферической толерантности. Они включают пероральное введение и прямую инъекцию белка или пептида с иммуносупрессией или без нее, получением несущих пептид наночастиц и адоптивным переносом сконструированных регуляторных T-клеток. До настоящего времени эти подходы не доказали свою успешность в клинических испытаниях поздних фаз, но эта область продолжает прогрессировать. При прямом введении пептидов и наночастиц сталкиваются с проблемами биораспределения, стабильности, презентирования и ориентации, что ограничивает эффективность межклеточной передачи сигнала. К настоящему времени все подходы адоптивного переноса являются аутологичными и имеют некоторые из тех же проблем с обработкой и масштабируемостью, которые ограничивают использование других способов клеточной терапии.
Таким образом, в некоторых вариантах осуществления aAPC по настоящему изобретению обеспечивают получение нового и улучшенного способа лечения аутоиммунных заболеваний. Способы лечения аутоиммунных заболеваний имеют множество преимуществ, включая, например, эффективное презентирование антигена на поверхности клетки (эритроидной клетки) вместе с антигенпрезентирующим полипептидом, например, MHC класса I или II, и чрезвычайно большим временем полужизни aAPC в кровотоке, таким образом, обеспечивая более длительное воздействие правильно презентированного антигена.
Таким образом, в некоторых вариантах осуществления настоящее изобретение относится к aAPC, включающим эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит терапевтическое средство против аутоиммунного заболевания. В некоторых вариантах осуществления aAPC содержит первый экзогенный полипептид, содержащий первое терапевтическое средство против аутоиммунного заболевания, и второй экзогенный полипептид, содержащий второе терапевтическое средство против аутоиммунного заболевания. В некоторых вариантах осуществления aAPC содержит первый экзогенный полипептид, содержащий первое терапевтическое средство против аутоиммунного заболевания, второй экзогенный полипептид, содержащий второе терапевтическое средство против аутоиммунного заболевания, и третий экзогенный полипептид, содержащий третье терапевтическое средство против аутоиммунного заболевания. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
Первое, второе и третье терапевтическое средство против аутоиммунного заболевания может действовать на одну и ту же мишень, например, рецептор поверхности клетки и/или эндогенный белок человека. Альтернативно, первое, второе и третье противоопухолевое терапевтическое средство может действовать на разные мишени. Первая, вторая или третья мишени могут являться членами одного биологического пути, где, необязательно, мишени являются рецепторами поверхности клетки и/или эндогенными белками человека. Первая, вторая или третья мишени могут находиться на разных типах клеток. В вариантах осуществления первое, второе и/или третье терапевтическое средство против аутоиммунного заболевания является первым, вторым и/или третьим экзогенным полипептидом, представленным в настоящем описании. Например, в некоторых вариантах осуществления первый экзогенный полипептид локализует сконструированную эритроидную клетку в желаемом участке, например, клетке человека, и второй экзогенный полипептид имеет терапевтическую активность, например, антигенпрезентирующую активность.
В некоторых вариантах осуществления первый экзогенный полипептид содержит антигенпрезентирующий полипептид, например, молекулу MHC (например, MHC класса I или MHC класса II), и второй экзогенный полипептид содержит антиген. В некоторых вариантах осуществления MHC класса I выбран из HLA A, HLA B и HLA C. В некоторых вариантах осуществления MHC класса II выбран из HLA-DPα, HLA-DPβ, HLA-DM, HLA DOA, HLA DOB, HLA DQα, HLA DQβ, HLA DRα и HLA DRβ. Специалисту в этой области будет понятно, что, в предпочтительных вариантах осуществления антиген ассоциирован или является причиной или триггером аутоиммунного нарушения. Например, антиген может являться аутоантигеном, на который направлен аутоиммунный ответ. В некоторых вариантах осуществления антиген выбран из антигенов, приведенных в таблице 16, или их антигенной части. В некоторых вариантах осуществления антиген выбран из антигенов, приведенных в таблице 17, или их антигенной части. В некоторых вариантах осуществления антиген выбран из антигенов, приведенных в таблице 18, или их антигенной части. В способах лечения аутоиммунного нарушения по настоящему изобретению, если aAPC содержит антигенпрезентирующий полипептид и антиген, приведенный в таблицах 16, 17 или 18, или его антигенную часть, aAPC можно вводить индивидууму для лечения аутоиммунного нарушения, соответствующего антигену, приведенному в таблицах 16, 17 или 18.
В одном из аспектов aAPC конструируют для супрессии нежелательной активности T-клетки, ассоциированной с аутоиммунным нарушением или регулирующей его. Таким образом, в некоторых вариантах осуществления aAPC дополнительно содержит по меньшей мере один экзогенный коингибиторный полипептид, представленный в настоящем описании. В некоторых вариантах осуществления экзогенный коингибиторный полипептид выбран из коингибиторных полипептидов, приведенных в таблице 7. В некоторых вариантах осуществления экзогенный коингибиторный полипептид выбран из ИЛ-35, ИЛ-10, VSIG-3 и агониста LAG3. В некоторых вариантах осуществления коингибиторный полипептид супрессирует аутореактивные T-клетки.
В другом аспекте aAPC конструируют для стимуляции регуляторных T-клеток, таким образом, смещая иммунную систему обратно к более толерогенному состоянию. Таким образом, в некоторых вариантах осуществления aAPC дополнительно содержит по меньшей мере один костимуляторный полипептид, представленный в настоящем описании. В этом аспекте в предпочтительных вариантах осуществления по меньшей мере один экзогенный костимуляторный полипептид приводит к экспансии регуляторных T-клеток (Treg) и является, например, экзогенным Treg-костимуляторным полипептидом, представленным в настоящем описании. В некоторых вариантах осуществления экзогенный костимуляторный полипептид выбран из костимуляторных полипептидов, приведенных в таблице 10. В некоторых вариантах осуществления костимуляторный полипептид выбран из костимуляторных полипептидов, приведенных в таблице 11.
В еще одном аспекте aAPC конструируют для экспансии и стимуляции T-клеток, например, цитотоксических CD8+ T-клеток. В этом аспекте аутоиммунное нарушение, предпочтительно, является аутоиммунным нарушением, вызванным или запускаемым возбудителем инфекции. В вариантах осуществления aAPC дополнительно содержит по меньшей мере один экзогенный костимуляторный полипептид, представленный в настоящем описании. В вариантах осуществления по меньшей мере один экзогенный костимуляторный полипептид приводит к экспансии цитотоксических CD8+ T-клеток. В некоторых вариантах осуществления экзогенный костимуляторный полипептид выбран из костимуляторных полипептидов, приведенных в таблице 6. В некоторых вариантах осуществления костимуляторные полипептиды выбраны из группы, состоящей из 4-1BBL, LIGHT, антитела против CD28, CD80, CD86, CD70, OX40L, ИЛ-7, ИЛ-12, GITRL, TIM4, SLAM, CD48, CD58, CD83, CD155, CD112, ИЛ-15Rα, слитого с ИЛ-15, ИЛ-21, ICAM-1, лиганда LFA-1, антитела против CD3 и их комбинации. Этот аспект более подробно описан ниже.
В некоторых аспектах настоящее изобретение относится к способу лечения индивидуума, имеющего аутоиммунное заболевание, включающему введение индивидууму эффективного количества эритроидных клеток, представленных в настоящем описании, и, таким образом, лечение аутоиммунного заболевания. В различных вариантах осуществления аутоиммунное заболевание может являться аутоиммунным заболеванием, приведенным в таблицах 16, 17 или 18. В таких способах aAPC, которые можно использовать для лечения аутоиммунного нарушения, содержит экзогенный антигенпрезентирующий полипептид и антигенный полипептид, где антигенный полипептид может являться антигеном, приведенным в таблицах 16, 17 или 18, или его антигенной частью, где aAPC, содержащие антиген, приведенный в таблицах 16, 17 или 18, используют для лечения соответствующего аутоиммунного нарушения, приведенного в таблицах 16, 17 или 18.
Например, в некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего аутоиммунное заболевание рассеянный склероз (MS). В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где антигенный пептид является MOG. В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где антигенный пептид является MOG, и экзогенный антигенпрезентирующий полипептид, являющийся одноцепочечным слитым белком MHC класса II, где антигенпрезентирующий полипептид слит с GPA (MOG-MHC класса II-GPA). В некоторых вариантах осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где антигенный пептид является MOG, экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, являющимся одноцепочечным слитым белком MHC класса II, и по меньшей мере один полипептид для экспансии Treg/Treg-костимуляторный полипептид. В некоторых вариантах осуществления пептид для экспансии Treg/Treg-костимуляторный пептид является CD25-специфическим ИЛ-2. В дополнительном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где антигенный пептид является MOG, экзогенный антигенпрезентирующий полипептид, где экзогенный антигенный полипептид специфически связан с экзогенным антигенпрезентирующим полипептидом, являющимся одноцепочечным слитым белком MHC класса II, и по меньшей мере один коингибиторный полипептид. В некоторых вариантах осуществления коингибиторный полипептид является PD-L1.
В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
В некоторых вариантах осуществления аутоиммунное заболевание является заболеванием с одним антигеном. Примеры заболеваний с одним антигеном и связанные с ними антигены приведены в таблице 16 ниже.
Таблица 16. Аутоиммунные заболевания и ассоциированные с ними отдельные антигены
В других вариантах осуществления аутоиммунное заболевание является заболеванием с множеством антигенов. В вариантах осуществления, где аутоиммунное заболевание является заболеванием с множеством антигенов, индивидуума можно лечить с использованием aAPC, направленных против более одного, например, двух, трех, четырех или более антигенов. Специалистам в этой области будет понятно, что множество антигенов может присутствовать на одной aAPC или на отдельных aAPC, где индивидууму для лечения нарушения вводят комбинацию двух, трех, четырех или более отдельных aAPC, содержащих один антиген. Примеры заболеваний с множеством антигенов и ассоциированных с ними антигенов приведены в таблице 17 ниже.
Таблица 17. Аутоиммунные заболевания и ассоциированные с ними множественные антигены
В некоторых вариантах осуществления аутоиммунное заболевание выбрано из группы, состоящей из обыкновенной пузырчатки, миастении, оптиконевромиелита, буллезного пемфигоида, целиакии, рассеянного склероза, диабета 1 типа, ревматоидного артрита и мембранозного гломерулонефрита. В некоторых вариантах осуществления аутоиммунное заболевание выбрано из заболеваний, приведенных в таблице 18 ниже.
Таблица 18. Антигены для MS, диабета 1 типа, RA и мембранозного нефрита
В некоторых вариантах осуществления aAPC по настоящему изобретению используют для регуляции индуцирования толерантности у индивидуума с диабетом I типа. В одном конкретном варианте осуществления искусственная антигенпрезентирующая клетка включает эритроидную клетку, где эритроидная клетка презентирует, например, содержит на своей поверхности, по меньшей мере один экзогенный антигенный полипептид, где антигенный пептид является B-цепью инсулина, и в частности частью B-цепи инсулина. В некоторых вариантах осуществления часть B-цепи инсулина представляет собой аминокислоты 9-23 B-цепи инсулина. В некоторых вариантах осуществления эритроидная клетка является безъядерной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей клеткой.
Заболевания иммунной активации также включают воспалительные заболевания, такие как, например, болезнь Крона, язвенный колит, целиакия или другое идиопатическое воспалительное заболевание кишечника. Заболевания иммунной активации также включают аллергические заболевания, такие как, например, астма, аллергия на арахис, аллергия на моллюсков, аллергия на пыльцу, аллергия на белок молока, аллергия на укусы насекомых и аллергия на латекс, аллергия на перхоть животных, аллергия на черный орех и грецкий орех, аллергия на бразильский орех, аллергия на кешью, аллергия на каштан, аллергия на клеща домашней пыли, аллергия на яйца, аллергия на рыбу, аллергия на фундук, аллергия на плесень, аллергия на пыльцу, аллергия на травы, аллергия на моллюсков, аллергия на сою, аллергия на лесной орех и аллергия на пшеницу.
Заболевания иммунной активации также включают иммунную активацию в ответ на терапевтический белок, вводимый для лечения первичного состояния, уменьшающую эффективность терапевтического белка, такого как, например, фактор свертывания VIII при гемофилии A, фактор свертывания IX при гемофилии B, антитела против фактора некроза опухоли альфа (ФНОα) при ревматоидном артрите и других воспалительных заболеваний, глюкоцереброзидаза при болезни Гоше, любой рекомбинантный белок, используемый для фермент-заместительной терапии или аспарагиназа при остром лимфобластном лейкозе (ALL).
В некоторых вариантах осуществления пациент страдает аутоиммунным заболеванием или состоянием или опосредованным аутоантителом заболеванием или состоянием, при котором иммунная система пациента активна против эндогенной (собственной) молекулы, например, белкового антигена, таким образом, что иммунная система атакует эндогенную молекулу, вызывает воспаление, повреждает ткань и иначе вызывает симптомы аутоиммунного или опосредованного аутоантителом заболевания или состояния. Иммунный ответ может регулироваться антителами, связывающимися с эндогенной молекулой, или гиперреактивными T-клетками, атакующими клетки, экспрессирующие эндогенную молекулу, или другими иммунными клетками, такими как регуляторные T-клетки, NK-клетки, NKT-клетки или B-клетки. В этих вариантах осуществления антигенный белок или его фрагмент, соответствующий эндогенной (собственной) молекуле, может экспрессироваться на aAPC, включающей эритроидную клетку, презентирующую (например, содержащую на своей поверхности) один или более экзогенных полипептидов, представленных в настоящем описании. aAPC при введении один или более раз пациенту, страдающему заболеванием или состоянием, будет достаточно для индуцирования толерантности к антигенному белку таким образом, что он больше не индуцирует активацию иммунной системы, и, таким образом, будут лечить или улучшать симптомы основного заболевания или состояния. В некоторых вариантах осуществления aAPC используют для стимуляции регуляторных T-клеток, таким образом, смещая иммунную систему обратно к более толерогенному состоянию в отношении эндогенной (собственной) молекулы.
В некоторых вариантах осуществления пациент страдает аллергическим заболеванием, например, аллергией на перхоть животных, черный орех, бразильский орех, кешью, каштан, клеща домашней пыли, яйца, грецкий орех, рыбу, фундук, яд насекомых, латекс, молоко, плесень, арахис, пыльцу, травы, моллюсков, сою, лесной орех или пшеницу. У пациента, страдающего аллергией, может развиваться иммунный ответ после контакта антигенного фрагмента аллергена, например, при питании, кожном контакте, инъекции или воздействии окружающей среды. Иммунный ответ может включать антитело IgE, сенсибилизированные тучные клетки, дегрануляцию, высвобождение гистамина и анафилаксию, а также канонические иммунные клетки, такие как T-клетки, B-клетки, дендритные клетки, регуляторные T-клетки, NK-клетки, нейтрофилы и NKT-клетки. Аллергическая реакция может вызывать дискомфорт, или она может быть достаточного тяжелой, чтобы вызвать смерть, и, таким образом, требует постоянного внимания со стороны пациента, а также его семьи и опекунов. В этих вариантах осуществления антигенный белок или его фрагмент может презентироваться на эритроидной клетке aAPC по настоящему изобретению. Популяции этих клеток при введении одного или более раз пациенту, страдающему аллергическим заболеванием или состоянием, будет достаточно для индуцирования толерантности к антигенному белку таким образом, что он больше не индуцирует активацию иммунной системы после воздействия, и, таким образом, будут лечить или улучшать симптомы основного аллергического заболевания или состояния.
Аутоиммунные заболевания, ассоциированные с возбудителем инфекции
В некоторых вариантах осуществления настоящее изобретение относится к способам лечения аутоиммунного заболевания или нарушения, ассоциированного или запускаемого возбудителем инфекции. Примеры аутоиммунных заболеваний или нарушений, ассоциированных или запускаемых возбудителем инфекции, приведены в таблице 19.
Таблица 19. Аутоиммунные заболевания и ассоциированные с ними возбудители инфекции.
Любое аутоиммунное нарушение, ассоциированное с возбудителем инфекции, вызывающим, в качестве неограничивающих примеров, нарушения, приведенные в таблице 19, считают подлежащими лечению с помощью aAPC по настоящему изобретению.
В рамках изобретения аутоиммунное заболевание, ассоциированное с возбудителем инфекции, можно лечить посредством введения индивидууму aAPC, содержащей первый экзогенный полипептид, содержащий антигенпрезентирующий полипептид (например, молекулу MHC, такую как MHC класса I или MHC класса II), и второй экзогенный полипептид, содержащий антиген или его фрагмент из возбудителя инфекции (т.е. aAPC, направленной против специфического возбудителя инфекции, запускающего заболевания).
В конкретном варианте осуществления aAPC, которая можно использовать для лечения аутоиммунного нарушения, ассоциированного с возбудителем инфекции, дополнительно содержит третий экзогенный полипептид, содержащий по меньшей мере один костимуляторный полипептид. В варианте осуществления костимуляторный полипептид активирует цитотоксические CD8+ T-клетки для таргетинга и элиминации клеток, инфицированных возбудителем инфекции. Например, цитотоксические CD8+ T-клетки могут направленно воздействовать, супрессировать и/или устранять аутореактивные B-клетки, инфицированные возбудителем инфекции. Костимуляторный полипептид может являться любым костимуляторным полипептидом, представленным в настоящем описании. В вариантах осуществления по меньшей мере один экзогенный костимуляторный полипептид приводит к экспансии цитотоксических CD8+ T-клеток. В некоторых вариантах осуществления экзогенный костимуляторный полипептид выбран из костимуляторных полипептидов, приведенных в таблице 6. В некоторых вариантах осуществления костимуляторные полипептиды выбраны из группы, состоящей из 4-1BBL, LIGHT, антитела против CD28, CD80, CD86, CD70, OX40L, ИЛ-7, ИЛ-12, GITRL, TIM4, SLAM, CD48, CD58, CD83, CD155, CD112, ИЛ-15Rα, слитого с ИЛ-15, ИЛ-21, ICAM-1, лиганда LFA-1, антитела против CD3 и их комбинации.
В некоторых вариантах осуществления аутоиммунное заболевание, ассоциированное с возбудителем инфекции, является рассеянным склерозом (MS). Несколько возбудителей инфекции ассоциированы с MS. Примеры возбудителей инфекции, ассоциированных с MS, приведены в таблице 20. В вариантах осуществления возбудитель инфекции, ассоциированный с аутоиммунным нарушением, является вирусом.
Таблица 20. Возбудители инфекции, ассоциированные с рассеянным склерозом (MS)
В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего MS, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит антиген возбудителя инфекции, приведенный в таблице 20, или его иммуногенный пептид, и, таким образом, лечение MS. В вариантах осуществления aAPC дополнительно содержат молекулу MHC и, необязательно, костимуляторный полипептид.
В конкретном варианте осуществления возбудитель инфекции, ассоциированный с MS, является вирусом Эпштейна-Барр (EBV). Не желая быть связанными какой-либо теорией, полагают, что во время первичной инфекции EBV инфицирует аутореактивные наивные B-клетки в миндалинах, заставляя их проникать в герминативные центры, где они интенсивно пролиферируют и дифференцируются в латентно инфицированные аутореактивные B-клетки памяти, которые затем выходят из миндалин и циркулируют в кровотоке. Количество инфицированных EBV B-клеток в норме контролируется EBV-специфическими цитотоксическими CD8+ T-клетками, уничтожающими пролиферирующие и литические инфицированные B-клетки, но только если нет дефекта в защитном механизме. Выжившие инфицированные EBV аутореактивные B-клетки памяти поступают в ЦНС, где они поселяются и продуцирует олигоклональные IgG и патогенные аутоантитела, атакующие миелин и другие компоненты ЦНС. Аутореактивные T-клетки, активированные в периферических лимфоидных органах под действием общей системной инфекции, циркулируют в кровотоке и поступают в ЦНС, где они реактивируются инфицированными EBV аутореактивными B-клетками, презентирующими пептиды ЦНС (Cp), связанные с молекулами главного комплекса гистосовместимости (MHC). Эти инфицированные EBV B-клетки подают костимуляторные сигналы выживания (B7) на рецептор CD28 на аутореактивных T-клетках и, таким образом, ингибируют индуцируемый активацией апоптоз T-клеток, в норме происходящий, когда аутореактивные T-клетки поступают в ЦНС и взаимодействуют с непрофессиональными антигенпрезентирующими клетками, такими как астроциты и микроглия, не экспрессирующие костимуляторные молекулы B7. После реактивации аутореактивных T-клеток инфицированными EBV аутореактивными B-клетками, они продуцируют цитокины, такие как интерлейкин-2 (ИЛ-2), интерферон-γ (ИФНγ) и фактор некроза опухоли (ФНО), и регулируют аутоиммунную атаку на ЦНС с последующим разрушением олигодендроцитов и миелина.
Таким образом, в некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего MS, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит антиген EBV. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего MS, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит антиген EBV из таблицы 1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего MS, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит антиген EBV, выбранный из антигена gp350 или EBNA1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего MS, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит антиген EBV, выбранный из: VLQWASLAV (SEQ ID NO: 698), FMVFLQTHI (SEQ ID NO: 699), FLQTHIFAEV (SEQ ID NO: 700), SIVCYFMVFL (SEQ ID NO: 701), CLGGLLTMV (SEQ ID NO: 691), GLCTLVAML (SEQ ID NO: 692), FLYALALLL (SEQ ID NO: 693), YVLDHLIVV (SEQ ID NO: 694), RLRAEAQVK (SEQ ID NO: 695), AVFDRKSDAK (SEQ ID NO: 696), RPPIFIRLL (SEQ ID NO: 697). Ожидают, что такие aAPC будут устранять инфицированные EBV аутореактивные B-клетки, чтобы, таким образом, лечить MS. В вариантах осуществления aAPC дополнительно содержат молекулу MHC и, необязательно, костимуляторный полипептид. В некоторых вариантах осуществления антиген EBV является gp350 или его иммуногенным пептидом (например, пептидом HLA A2 VLQWASLAV (SEQ ID NO: 698)). В некоторых вариантах осуществления антиген EBV является EBNA1 или его иммуногенным пептидом (например, FMVFLQTHI (SEQ ID NO: 699), FLQTHIFAEV (SEQ ID NO: 700) или SIVCYFMVFL (SEQ ID NO: 701)). В некоторых вариантах осуществления антиген EBV является FMVFLQTHI (SEQ ID NO: 699). В некоторых вариантах осуществления антиген EBV является FLQTHIFAEV (SEQ ID NO: 700). В некоторых вариантах осуществления антиген EBV является SIVCYFMVFL (SEQ ID NO: 701).
В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего MS, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит gp350 или его иммуногенный пептид, и, таким образом, лечение MS. В некоторых вариантах осуществления иммуногенный пептид gp350 содержит или состоит из пептида HLA A2 VLQWASLAV (SEQ ID NO: 698). В некоторых вариантах осуществления иммуногенный пептид gp350 способен индуцировать цитотоксические CD8+ T-клетки, распознающие антиген gp350.
В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего MS, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит EBNA1 или его иммуногенный пептид, и, таким образом, лечение MS. В некоторых вариантах осуществления иммуногенный пептид EBNA1 содержит или состоит из пептида, выбранного из FMVFLQTHI (SEQ ID NO: 699), FLQTHIFAEV (SEQ ID NO: 700) и SIVCYFMVFL (SEQ ID NO: 701). В некоторых вариантах осуществления иммуногенный пептид EBNA1 способен индуцировать цитотоксические CD8+ T-клетки, распознающие антиген EBNA1.
В рамках изобретения существует несколько альтернативных способов, посредством которых можно конструировать aAPC и использовать их для лечения аутоиммунного заболевания, ассоциированного или запускаемого возбудителем инфекции у индивидуума. Например, аутоиммунное заболевание, ассоциированное с возбудителем инфекции, альтернативно можно лечить посредством введения индивидууму aAPC, содержащей первый экзогенный полипептид, содержащий антигенпрезентирующий полипептид (например, молекулу MHC, такую как MHC класса I или MHC класса II), второй экзогенный полипептид, содержащий антиген или его фрагмент, и, необязательно, третий экзогенный полипептид, содержащий по меньшей мере один коингибиторный полипептид или по меньшей мере один Treg-костимуляторный полипептид (также обозначаемый в настоящем описании как полипептид для экспансии Treg). В некоторых вариантах осуществления антиген или его антигенный фрагмент получают из возбудителя инфекции (т.е. возбудителя инфекции, запускающего заболевание). В некоторых вариантах осуществления антиген или его антигенный фрагмент является антигеном, ассоциированным с вызванным возбудителем инфекции аутоиммунным нарушением (например, аутополипептидом).
В некоторых вариантах осуществления, как описано выше, для любого аутоиммунного нарушения более типично, если aAPC, которую можно использовать для лечения аутоиммунного нарушения, ассоциированного с возбудителем инфекции, содержит Treg-костимуляторный полипептид/полипептид для экспансии Treg. Treg-костимуляторный полипептид/полипептид для экспансии Treg может являться любым полипептидом для экспансии Treg, представленным в настоящем описании. В варианте осуществления Treg-костимуляторный полипептид/полипептид для экспансии Treg приводит к экспансии Treg, которые, в свою очередь, супрессируют T-клетки, образующиеся у индивидуума в ответ на возбудителя инфекции.
В некоторых вариантах осуществления, как описано выше, для любого аутоиммунного нарушения более типично, если aAPC, которую можно использовать для лечения аутоиммунного нарушения, ассоциированного с возбудителем инфекции, содержит коингибиторный полипептид. Коингибиторный полипептид может являться любым коингибиторным полипептидом, представленным в настоящем описании. В варианте осуществления коингибиторный полипептид супрессирует T-клетки, образующиеся у индивидуума в ответ на возбудителя инфекции.
В другом варианте осуществления аутоиммунное заболевание не ассоциировано с возбудителем инфекции. В случае аутоиммунного заболевания, неассоциированного с возбудителем инфекции, специалисту в этой области с учетом идей, представленных в настоящем описании, будет понятно, что аутоиммунное заболевание можно лечить посредством введения индивидууму aAPC, содержащей первый экзогенный полипептид, содержащий антигенпрезентирующий полипептид (например, молекулу MHC, такую как MHC класса I или MHC класса II), второй экзогенный полипептид, содержащий антиген или его фрагмент (например, антигенный полипептид из эндогенного (собственного) полипептида, на который направлена аутоиммунная активность), и третий экзогенный полипептид, содержащий по меньшей мере один коингибиторный полипептид или по меньшей мере один полипептид для экспансии Treg. В этих вариантах осуществления aAPC вводят индивидууму для индуцирования периферической толерантности к антигену, запускающему аутоиммунный ответ.
Инфекционные заболевания
В некоторых вариантах осуществления настоящее изобретение относится к aAPC, включающей эритроидную клетку (например, безъядерную эритроидную клетку) или безъядерную клетку, содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит терапевтическое средство против инфекционного заболевания. В некоторых вариантах осуществления эритроидная клетка является безъядерной эритроидной клеткой. В некоторых вариантах осуществления эритроидная клетка является ядросодержащей эритроидной клеткой.
В рамках изобретения термин "терапевтическое средство против инфекционного заболевания" относится к экзогенному полипептиду, ингибирующему инфекционное заболевание, например, уменьшающему или смягчающему причину или симптом инфекционного заболевания, или улучшающему значение параметра, ассоциированного с инфекционным заболеванием, например, вирусную нагрузку или бактериальную нагрузку. В вариантах осуществления терапевтическое средство против инфекционного заболевания является первым или вторым экзогенным полипептидом, который при презентировании или экспрессии другим экзогенным полипептидом ингибирует инфекционное заболевание. В варианте осуществления первое или второе терапевтическое средство против инфекционного заболевания имеет активность в отсутствие другого. В вариантах осуществления терапевтическое средство против инфекционного заболевания ингибирует инфекционное заболевание напрямую, например, посредством уничтожения патогенов. В вариантах осуществления терапевтическое средство против инфекционного заболевания ингибирует инфекционное заболевание посредством стимуляции иммунного ответа индивидуума, например, в качестве вакцины.
В некоторых вариантах осуществления aAPC содержит первый экзогенный полипептид, содержащий первое терапевтическое средство против инфекционного заболевания, и второй экзогенный полипептид, содержащий второе терапевтическое средство против инфекционного заболевания. В некоторых вариантах осуществления aAPC содержит первый экзогенный полипептид, содержащий первое терапевтическое средство против инфекционного заболевания, второй экзогенный полипептид, содержащий второе терапевтическое средство против инфекционного заболевания, и третий экзогенный полипептид, содержащий третье терапевтическое средство против инфекционного заболевания.
Первое, второе и третье терапевтическое средство против инфекционного заболевания могут воздействовать на одну мишень, например, рецептор поверхности клетки и/или эндогенный белок человека. Альтернативно, первое, второе и третье противоопухолевое терапевтическое средство могут воздействовать на разные мишени. Первая, вторая или третья мишени могут являться членами одного биологического пути, где, необязательно, мишени являются рецепторами поверхности клетки, эндогенными белками человека. Первая, вторая или третья мишени могут находиться на разных типах клеток. В некоторых вариантах осуществления первый экзогенный полипептид локализует сконструированную эритроидную клетку в желаемом участке, например, клетке человека, и второй экзогенный полипептид имеет терапевтическую активность, например, антигенпрезентирующую активность.
В некоторых предпочтительных вариантах осуществления терапевтическое средство против инфекционного заболевания является антигеном, например, антигеном из патогена или возбудителя инфекции (при этом термины "патоген" и "возбудитель инфекции" в настоящем описании используют взаимозаменяемо). В некоторых вариантах осуществления первое терапевтическое средство является антигеном, например, антигеном из патогена. В некоторых вариантах осуществления первое терапевтическое средство и второе терапевтическое средство является антигеном, например, антигеном из патогена. В некоторых вариантах осуществления первое, второе и третье терапевтическое средство является антигеном, например, антигеном из патогена.
В вариантах осуществления aAPC дополнительно содержит дополнительный экзогенный полипептид, где дополнительный экзогенный полипептид содержит антигенпрезентирующий полипептид, например, молекулу MHC (например, MHC класса I или MHC класса II). В вариантах осуществления aAPC дополнительно содержит дополнительный экзогенный полипептид, где дополнительный экзогенный полипептид содержит по меньшей мере один костимуляторный полипептид. В некоторых вариантах осуществления aAPC дополнительно содержит дополнительный экзогенный полипептид, содержащий антигенпрезентирующий полипептид и дополнительный экзогенный полипептид, содержащий по меньшей мере один костимуляторный полипептид.
В некоторых вариантах осуществления aAPC содержит первый экзогенный полипептид, содержащий антигенпрезентирующий полипептид, например, молекулу MHC (например, MHC класса I или MHC класса II), и второй экзогенный полипептид, содержащий антиген. В различных вариантах осуществления антиген является антигеном патогена, например, вирусного патогена, бактериального патогена, грибкового патогена или паразитарного патогена.
В рамках изобретения антиген может являться любым патогенным антигеном или его антигенной частью, известной в этой области. Примеры патогенов, в случае которых один или более антигенных пептидов могут презентироваться на эритроидной клетке по настоящему изобретению, подробно описаны ниже, но этим они не ограничены. В различных вариантах осуществления антигенный пептид получают из патогена, приведенного в любой из таблиц 21, 22, 23 и 24 ниже. В некоторых вариантах осуществления антигенный пептид получают из патогена, приведенного в таблице 21. В некоторых вариантах осуществления антигенный пептид получают из патогена, приведенного в таблице 22. В некоторых вариантах осуществления антигенный пептид получают из патогена, приведенного в таблице 23. В некоторых вариантах осуществления антигенный пептид получают из патогена, приведенного в таблице 24. Специалистам в этой области будет понятно, что aAPC, представленную в настоящем описании, содержащую антиген из конкретного патогена или возбудителя инфекции, можно вводить индивидууму для лечения инфекции у индивидуума, вызванной этим патогеном или возбудителем инфекции. Специалистам в этой области также будет понятно, что aAPC, представленную в настоящем описании, содержащую антиген из конкретного патогена или возбудителя инфекции, можно вводить индивидууму для лечения заболевания или нарушения у индивидуума, где заболевание или нарушение вызвано, прямо или косвенно, инфекцией этого патогена или возбудителя инфекции.
В некоторых аспектах настоящее изобретение относится к способу лечения индивидуума, имеющего инфекционное заболевание, включающему введение индивидууму эффективного количества эритроидных клеток, представленных в настоящем описании индивидууму, и, таким образом, лечение инфекционного заболевания.
В другом аспекте настоящее изобретение относится к способу лечения индивидуума, имеющего инфекционное заболевание, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку) или безъядерную клетку, содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит патогенный антиген, и, таким образом, лечение инфекционного заболевания.
В некоторых вариантах осуществления терапевтическое средство против инфекционного заболевания выбрано из противомикробного полипептида, указанного в общедоступной биоинформатической базе данных, такой как CAMP, CAMP выпуск 2 (Collection of sequences and structures of antimicrobial peptides), база данных противомикробных пептидов (aps.unmc.edu/AP/main.php), LAMP, BioPD и ADAM (A Database of Anti-Microbial peptides) (bioinformatics.cs.ntou.edu.tw/adam/). Базы данных противомикробных пептидов можно разделять на две категории на основе источника пептидов, которые он содержит, как специальные базы данных и общие базы данных. Эти базы данных имеют различные инструменты для анализа и прогнозирования противомикробных пептидов. Например, CAMP включает прогнозирование AMP, калькулятор признаков, поиск BLAST, clustalW, VAST, PRATT, Helical Wheel и т.д. Кроме того, ADAM позволяет пользователям осуществлять поиск по взаимосвязи последовательность AMP-структура.
В некоторых вариантах осуществления терапевтическое средство против инфекционного заболевания выбрано из вирусного полипептида. В этих вариантах осуществления aAPC включает эритроидную клетку (например, безъядерную эритроидную клетку) или безъядерную клетку, содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит антигенный вирусный полипептид, и aAPC вводят индивидууму для лечении инфекции вируса.
Вирусные инфекции включают аденовирус, вирус коксаки, вирус гепатита A, вирус полиомиелита, вирус Эпштейна-Барр, вирус простого герпеса типа 1, вирус простого герпеса типа 2, цитомегаловирус человека, вирус герпеса человека типа 8, вирус ветряной оспы, вирус гепатита B, вирусы гепатита C, вирус иммунодефицита человека (ВИЧ), вирус гриппа, вирус кори, вирус эпидемического паротита, вирус парагриппа, респираторно-синцитиальный вирус, папилломавирус, вирус бешенства и вирус краснухи. Другие вирусные мишени включают Paramyxoviridae (например, пневмовирус, морбилливирус, метапневмовирус, респировирус или рубулавирус), Adenoviridae (например, аденовирус), Arenaviridae (например, аренавирус, такой как вирус лимфоцитарного хориоменингита), Arteriviridae (например, вирус репродуктивно-респираторный синдром свиней или вирус артериита лошадей), Bunyaviridae (например, флебовирус или гантавирус), Caliciviridae (например, вирус Норуолк), Coronaviridae (например, коронавирус или торовирус), Filoviridae (например, Эбола-подобные вирусы), Flaviviridae (например, гепацивирус или флавивирус), Herpesviridae (например, вирус простого герпеса, варицелловирус, цитомегаловирус, розеоловирус или лимфокриптовирус), Orthomyxoviridae (например, вирус гриппа или тоготовирус), Parvoviridae (например, парвовирус), Picomaviridae (например, энтеровирус или гепатовирус), Poxviridae (например, ортопоксвирус, авипоксвирус или лепорипоксвирус), Retroviridae (например, лентивирус или спумавирус), Reoviridae (например, ротавирус), Rhabdoviridae (например, лиссавирус, новирабдовирус или везикуловирус) и Togaviridae (например, альфавирус или рубивирус). Конкретные примеры этих вирусов включают респираторный коронавирус человека, вирусы гриппа A-C, вирусы гепатита A-G и вирусы простого герпеса 1-9.
Примеры вирусных патогенов приведены ниже в таблице 21. В некоторых вариантах осуществления вирусный патоген выбран из вируса гепатита B, вируса гепатита C, вируса Эпштейна-Барр, цитомегаловируса (CMV).
Таблица 21. Вирусные патогены
В некоторых вариантах осуществления антигены выбраны из вирусных антигенов, ретровирусных антигенов и антигенов яичка. Например, в некоторых вариантах осуществления вирус выбран из вируса Эпштейна-Барр (EBV), вируса гепатита B (HBV), вируса гепатита C (HCV), вируса папилломы человека (HPV), вируса саркомы Капоши (KSV) и полиомавирусов. В некоторых вариантах осуществления вирус является вирусом гепатита B (HBV).
В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, ассоциированное с онкогенным вирусом (например, HPV), включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит антиген HPV из таблицы 1. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, ассоциированное с онкогенным вирусом (например, HPV), включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит антиген HPV-E7. В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего злокачественное новообразование, ассоциированное с онкогенным вирусом (например, HPV), включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую экзогенный полипептид, где экзогенный полипептид содержит YMLDLQPET (SEQ ID NO: 713), YMLDLQPETT (SEQ ID NO: 714) или TIHDIILECV (SEQ ID NO: 712). В некоторых вариантах осуществления экзогенный полипептид содержит YMLDLQPET (SEQ ID NO: 713). В некоторых вариантах осуществления экзогенный полипептид является YMLDLQPET (SEQ ID NO: 713).
В некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего вирусную инфекцию, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит антиген из возбудителя инфекции, приведенного в таблице 21, или его иммуногенный пептид, и, таким образом, лечение вирусной инфекции. В вариантах осуществления aAPC дополнительно содержат молекулу MHC и, необязательно, костимуляторный полипептид.
В некоторых вариантах осуществления настоящее изобретение относится к способам лечения инфекции гепатита B, например, хронической инфекции HBV. По оценкам до 250 миллионов людей по всему миру имеют хронический гепатит B, передающий, главным образом, in utero или во время родов. Хронический HBV вызывает цирроз и печеночноклеточную карциному. Патология HBV может являться результатом рекрутирования специфических для антигена гепатита B T-клеток из неантигенспецифических T-клеток, секретирующих цитокины, вызывающие повреждение печени. Предполагают, что истощенные T-клетки являются ключом к этиологии хронического гепатита. Показано, что HBV-специфические T-клетки реактивируются при блокировании PD1, например, с помощью антитела против PD1 и/или ИЛ-12 (Schirdewahn et al. J. Infect. Dis. 2017; Fisicaro et al Gastroenterology 2010; и Schurich PLOS Pathogens, 2013, содержание каждой из которых включено в настоящее описание в качестве ссылки в полном объеме). Таким образом, в настоящем изобретении предусмотрено, что aAPC, представленные в настоящем описании, можно использовать для лечения хронического HBV посредством реактивации HBV-специфических T-клеток, например, для цитолитической или нецитолитической противовирусной активности.
Таким образом, в некоторых вариантах осуществления настоящее изобретение относится к способу лечения индивидуума, имеющего вирусную инфекцию гепатита B (HBV), например, хронический гепатит B, включающему введение индивидууму эффективного количества aAPC, включающих эритроидную клетку (например, безъядерную эритроидную клетку), содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит HBV-специфический антиген или его иммуногенный пептид, и, таким образом, лечение инфекции HBV. В некоторых вариантах осуществления инфекция HBV является хронической инфекцией HBV. В вариантах осуществления aAPC дополнительно содержат экзогенный антигенпрезентирующий полипептид, т.е. молекулу MHC, например, одноцепочечный слитый белок MHC класса I или MHC класса I. В некоторых вариантах осуществления aAPC дополнительно содержит по меньшей мере один экзогенный костимуляторный полипептид. В вариантах осуществления по меньшей мере один костимуляторный полипептид выбран из группы, состоящей из 4-1BBL, ИЛ-2, ИЛ-12, ИЛ-15, ИЛ-18, ИЛ-21 и любой их комбинации, например, ИЛ-12 и ИЛ-15 или 4-1BBL и ИЛ-15. В некоторых вариантах осуществления aAPC дополнительно содержит дополнительный экзогенный полипептид, где дополнительный экзогенный полипептид содержит ингибитор контрольных точек. В некоторых вариантах осуществления ингибитор контрольных точек является молекулой антитела против PD1. В конкретном варианте осуществления aAPC включает эритроидную клетку, содержащую один или более экзогенных полипептидов, где один или более экзогенных полипептидов содержат: экзогенный антигенный полипептид, содержащий HBV-специфический антиген или его иммуногенный пептид, экзогенный антигенпрезентирующий полипептид, например, одноцепочечный слитый белок MHC класса I или MHC класса I, экзогенный костимуляторный полипептид, например, ИЛ-12 или 4-1BBL, и ингибитор контрольных точек, например, антитело против PD1.
В некоторых вариантах осуществления терапевтическое средство против инфекционного заболевания выбрано из бактериального полипептида. В этих вариантах осуществления aAPC включает эритроидную клетку (например, безъядерную эритроидную клетку) или безъядерную клетку, содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит антигенный бактериальный полипептид, и aAPC вводят индивидууму для лечения бактериальной инфекции.
Бактериальные инфекции включают, в качестве неограничивающих примеров, Mycobacteria, Rickettsia, Mycoplasma, Neisseria meningitides, Neisseria gonorrheoeae, Legionella, Vibrio cholerae, Streptococci, Staphylococcus aureus, Staphylococcus epidermidis, Pseudomonas aeruginosa, Corynobacteria diphtheriae, Clostridium spp., энтеротоксигенную Eschericia coli, Bacillus anthracis, Rickettsia, Bartonella henselae, Bartonella quintana, Coxiella burnetii, Chlamydia, Mycobacterium leprae, Salmonella; Shigella; Yersinia enterocolitica; Yersinia pseudotuberculosis; Legionella pneumophila; Mycobacterium tuberculosis; Listeria monocytogenes; Mycoplasma spp.; Pseudomonas fluorescens; Vibrio cholerae; Haemophilus influenzae; Bacillus anthracis; Treponema pallidum; Leptospira; Borrelia; Corynebacterium diphtheriae; Francisella; Brucella melitensis; Campylobacter jejuni; Enterobacter; Proteus mirabilis; Proteus и Klebsiella pneumoniae.
Примеры бактериальных патогенов приведены ниже в таблице 22.
Таблица 22. Бактериальные патогены
В некоторых вариантах осуществления терапевтическое средство против инфекционного заболевания выбрано из грибкового полипептида. В этих вариантах осуществления aAPC включает эритроидную клетку (например, безъядерную эритроидную клетку) или безъядерную клетку, содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит антигенный грибковый полипептид, и aAPC вводят индивидууму для лечения грибковой инфекции.
Примеры грибковых патогенов приведены ниже в таблице 23.
Таблица 23. Грибковые патогены
В некоторых вариантах осуществления терапевтическое средство против инфекционного заболевания выбрано из паразитарного полипептида. В этих вариантах осуществления aAPC включает эритроидную клетку (например, безъядерную эритроидную клетку) или безъядерную клетку, содержащую один или более экзогенных полипептидов, где один из одного или более экзогенных полипептидов содержит антигенный паразитарный полипептид, и aAPC вводят индивидууму для лечения паразитарной инфекции.
Примеры паразитарных патогенов приведены ниже в таблице 24.
Таблица 24. Паразитарные патогены
В некоторых вариантах осуществления инфекционные заболевания вызваны стафилококками с множественной лекарственной устойчивостью. В других вариантах осуществления инфекционные заболевания вызваны псевдомонадами. В другом варианте осуществления инфекционное заболевание является нозокомиальной инфекцией (т.е. любыми системными или локализованными состояниями, являющимися результатом реакции на возбудитель инфекции или токсин), которые трудно лечить, например, инфекцией, вызванной Clostridium difficile.
Другие
Другие заболевания и нарушения предусмотрены для лечения с помощью aAPC по настоящему изобретению. Неограничивающие примеры включают сердечно-сосудистые заболевания и иммунные заболевания.
Индивидуумы
Способы, представленные в настоящем описании, предназначены для использования в отношении любого индивидуума, который может получить пользу от этих способов. Таким образом, термины "индивидуумы" и "пациенты" (используемые взаимозаменяемо) включают людей, а также не являющихся человеком индивидуумов, в частности, одомашненных животных.
В некоторых вариантах осуществления индивидуум и/или животное представляет собой млекопитающего, например, человека, мышь, крысу, морскую свинку, собаку, кошку, лошадь, корову, свинью, кролика, овцу или не являющегося человеком примата, такого как мартышка, шимпанзе или павиан. В других вариантах осуществления индивидуум и/или животное не является млекопитающим. В некоторых вариантах осуществления индивидуум и/или животное является человеком. В некоторых вариантах осуществления человек является ребенком. В других вариантах осуществления человек является взрослым человеком. В других вариантах осуществления человек является человеком пожилого возраста. В других вариантах осуществления человека можно обозначать как пациента.
В некоторых вариантах осуществления человек имеет возраст в диапазоне от приблизительно 0 месяцев до приблизительно 6 месяцев, от приблизительно 6 до приблизительно 12 месяцев, от приблизительно 6 до приблизительно 18 месяцев, от приблизительно 18 до приблизительно 36 месяцев, от приблизительно 1 до приблизительно 5 лет, от приблизительно 5 до приблизительно 10 лет, от приблизительно 10 до приблизительно 15 лет, от приблизительно 15 до приблизительно 20 лет, от приблизительно 20 до приблизительно 25 лет, от приблизительно 25 до приблизительно 30 лет, от приблизительно 30 до приблизительно 35 лет, от приблизительно 35 до приблизительно 40 лет, от приблизительно 40 до приблизительно 45 лет, от приблизительно 45 до приблизительно 50 лет, от приблизительно 50 до приблизительно 55 лет, от приблизительно 55 до приблизительно 60 лет, от приблизительно 60 до приблизительно 65 лет, от приблизительно 65 до приблизительно 70 лет, от приблизительно 70 до приблизительно 75 лет, от приблизительно 75 до приблизительно 80 лет, от приблизительно 80 до приблизительно 85 лет, от приблизительно 85 до приблизительно 90 лет, от приблизительно 90 до приблизительно 95 лет или от приблизительно 95 до приблизительно 100 лет.
В других вариантах осуществления индивидуум является не являющимся человеком животным, и, таким образом, настоящее изобретение относится к ветеринарному применению. В конкретном варианте осуществления не являющееся человеком животное является домашним животным. В другом конкретном варианте осуществления не являющееся человеком животное является сельскохозяйственным животным. В некоторых вариантах осуществления индивидуум является пациентом-человеком со злокачественным новообразованием, которого нельзя подвергать химиотерапии, например, пациент не отвечает на химиотерапию или слишком болен, чтобы иметь подходящее терапевтическое окно для химиотерапии (например, имеет слишком много побочных эффектов, ограничивающих схему введения или схему лечения). В некоторых вариантах осуществления индивидуум является пациентом-человеком, имеющим заболевание на поздней стадии и/или метастазирующие заболевание.
В некоторых вариантах осуществления индивидуума выбирают для лечения с использованием aAPC, включающей эритроидную клетку, презентирующую (например, содержащую на своей поверхности) один или более экзогенных полипептидов по настоящему изобретению. В некоторых вариантах осуществления индивидуума выбирают для лечения злокачественного новообразования с использованием aAPC, включающей эритроидную клетку, презентирующую (например, содержащую на своей поверхности) один или более экзогенных полипептидов по настоящему изобретению. В некоторых вариантах осуществления индивидуума выбирают для лечения аутоиммунного заболевания с использованием aAPC, включающей эритроидную клетку, презентирующую (например, содержащую на своей поверхности) один или более экзогенных полипептидов по настоящему изобретению. В некоторых вариантах осуществления индивидуума выбирают для лечения инфекционного заболевания с использованием aAPC, включающей эритроидную клетку, презентирующую (например, содержащую на своей поверхности) один или более экзогенных полипептидов по настоящему изобретению.
В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления эритроидная клетка является безъядерной эритроидной клеткой. В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления эритроидная клетка является ядросодержащей эритроидной клеткой.
V. ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ
Настоящее изобретение включает получение и применение фармацевтических композиций, содержащих aAPC по настоящему изобретению в качестве активного ингредиента. Такая фармацевтическая композиция может состоять из активного ингредиента в отдельности, в виде комбинации по меньшей мере одного активного ингредиента (например, эффективной дозы aAPC) в форме, подходящей для введения индивидууму, или в виде фармацевтической композиции, которая может содержать активный ингредиент и один или более фармацевтически приемлемые носителей, один или более дополнительных (активных и/или неактивных) ингредиентов или некоторые их комбинации.
В некоторых вариантах осуществления настоящее изобретение относится к фармацевтической композиции, содержащей множество aAPC, представленных в настоящем описании, и фармацевтический носитель. В других вариантах осуществления настоящее изобретение относится к фармацевтической композиции, содержащей популяцию aAPC, представленных в настоящем описании, и фармацевтический носитель. Следует понимать, что в фармацевтической композиции по настоящему изобретению могут присутствовать любые отдельные aAPC, множество aAPC или популяция aAPC, представленных где-либо в настоящем описании.
В некоторых вариантах осуществления фармацевтические композиции, представленные в настоящем описании, содержат сконструированные (т.е. модифицированные) эритроидные клетки и немодифицированные эритроидные клетки. Например, в различных вариантах осуществления единичная стандартная доза aAPC может содержать приблизительно, по меньшей мере или не более 10%, 20%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95% или 99% сконструированных эритроидных клеток, где остальные эритроидные клетки в композиции не являются сконструированными.
В некоторых вариантах осуществления фармацевтические композиции, представленные в настоящем описании, содержат aAPC, содержащие сконструированные безъядерные эритроидные клетки и ядросодержащие эритроидные клетки. Например, в различных вариантах осуществления единичная стандартная доза сконструированных эритроидных клеток (например, безъядерных и ядросодержащих эритроидных клеток) может содержать приблизительно или по меньшей мере 10%, 20%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% безъядерных эритроидных клеток, где остальные эритроидные клетки в композиции являются ядросодержащими.
Фармацевтические композиции по настоящему изобретению можно вводить способом, подходящим для заболевания, подлежащего лечению (или профилактике). Количество и частоту введения будут определять по таким факторам, как состояние пациента и тип и тяжесть заболевания пациента, хотя подходящие дозы можно определять посредством клинических испытаний.
Введение фармацевтических композиций можно осуществлять любым удобным способом, включая аэрозольную ингаляцию, инъекцию, прием внутрь, переливание, имплантацию или трансплантацию. Композиции по настоящему изобретению можно вводить пациенту подкожно, внутрикожно, внутримышечно, посредством внутривенной (i.v.) инъекции или интраперитонеально. Фармацевтические композиции можно инъецировать непосредственно в опухоль или лимфоузел.
В рамках изобретения термин "фармацевтически приемлемый носитель" означает химическую композицию, с которой можно комбинировать активный ингредиент и которую после ингибирования можно использовать для введения активного ингредиента индивидууму.
Составы фармацевтических композиций, представленные в настоящем описании, можно получать любым способом, уже известным в области фармакологии или который будет разработан в будущем. В основном, такие способы получения включают стадию объединения активного ингредиента с носителем или одним или более другими дополнительными ингредиентами, а затем, при необходимости или желании, формования или упаковки продукта в желаемый однодозовый или многодозовый контейнер.
Хотя описание фармацевтических композиций, представленных в настоящем описании, в принципе, относится к фармацевтическим композициям, подходящим для этичного введения людям, специалистам в этой области следует понимать, что такие композиции, как правило, подходят для введения животным всех типов. Модификация фармацевтических композиций, подходящих для введения людям, чтобы сделать композиции подходящими для введения различным животным, хорошо понятна, и, как правило, специалист в области ветеринарной фармакологии может создавать и осуществлять такую модификацию с использованием рутинного экспериментирования или без него. Индивидуумы, для которых предусмотрено введение фармацевтических композиций по настоящему изобретению, включают, в качестве неограничивающих примеров, людей и других приматов, млекопитающих, включая коммерчески важных млекопитающих, таких как не являющиеся человеком приматы, крупный рогатый скот, свиньи, лошади, овцы, кошки и собаки, птиц, включая коммерчески важных птиц, таких как куры, утки, гуси и индейку, рыбу, включая выращенную на ферме рыбу и аквариумную рыбу, и ракообразных, такие как выращенные на ферме моллюски.
Фармацевтические композиции, которые можно использовать в способах по настоящему изобретению, можно получать, упаковывать или продавать в составах, подходящих для перорального, ректального, вагинального, парентерального, местного, легочного, интраназального, внутриочагового, буккального, офтальмологического, внутривенного, внутриорганного или другого пути введения. Другие составы по настоящему изобретению включают проектируемые наночастицы, липосомные препараты, "запечатанные" эритроциты, содержащие активный ингредиент и иммунологические составы.
Фармацевтическую композицию по настоящему изобретению можно получать, упаковывать или продавать нерасфасованными, в виде единичной стандартной дозы или множества единичных стандартных доз. В рамках изобретения термин "стандартная доза" относится к отдельному количеству фармацевтической композиции, содержащей заранее определенное количество активного ингредиента. Количество активного ингредиента, как правило, равно дозе активного ингредиента, которое будут вводить индивидууму, или подходящей доле такой дозы, такой как, например, половина или треть такой дозы.
Относительные количества активного ингредиента, фармацевтически приемлемого носителя и любых дополнительных ингредиентов в фармацевтической композиции по настоящему изобретению будет варьироваться в зависимости от типа, размера и состояния индивидуума, подвергаемого лечению, и пути, которым композицию будут вводить. В качестве примера, композиция может содержать от 0,1% до 100% (масс./масс.) активного ингредиента.
В дополнение к активному ингредиенту, фармацевтическая композиция по настоящему изобретению может дополнительно содержать один или более дополнительных фармацевтически активных средств. В частности, подходящие дополнительные средства включают антиэметики и поглотители, такие как цианидные и цианатные поглотители и AZT, ингибиторы протеаз, ингибиторы обратной транскриптазы, интерлейкин-2, интерфероны, цитокины и т.п.
Составы с контролируемым или замедленным высвобождением фармацевтической композиции по настоящему изобретению можно получать общепринятыми способами.
В рамках изобретения "парентеральное введение" фармацевтической композиции включает любой путь введения, отличающийся физическим преодолением ткани индивидуума и введением фармацевтической композиции через отверстие в ткани. Таким образом, парентеральное введение включает, в качестве неограничивающих примеров, введение фармацевтической композиции посредством инъекции композиции, введение композиции через хирургический разрез, введение композиции через пересекающую ткань нехирургическую рану и т.п. В частности, термин "парентеральное введение" предназначен для включения, в качестве неограничивающих примеров, подкожного введения, интраперитонеального введения, внутримышечного введения, интрастернальной инъекции и инфузии при почечном диализе.
Составы фармацевтической композиции, подходящие для парентерального введения, содержат активный ингредиент в комбинации с фармацевтически приемлемым носителем, таким как стерильная вода или стерильный изотонический физиологический раствор. Такие составы можно получать, упаковывать или продавать в форме, подходящей для болюсного введения или непрерывного введения. Инъецируемые составы можно получать, упаковывать, или продавать в стандартной лекарственной форме, например, в ампулах или многодозовых контейнерах, содержащих консервант. Составы для парентерального введения включают, в качестве неограничивающих примеров, суспензии, растворы, эмульсии в масляных или водных носителях, пасты и имплантируемые составы с замедленным высвобождением или биодеградируемые составы. Такие составы могут дополнительно содержать один или более дополнительных ингредиентов, включая, в качестве неограничивающих примеров, суспендирующие, стабилизирующие или диспергирующие средства.
Фармацевтические композиции можно получать, упаковывать или продавать в форме стерильной инъецируемой водной или масляной суспензии или раствора. Эту суспензию или раствор можно оставлять, как известно в этой области, и они могут содержать, в дополнение к активному ингредиенту, дополнительные ингредиенты, такие как диспергирующие средства, увлажнители или суспендирующие средства, представленные в настоящем описании. Такие стерильные инъецируемые составы можно получать с использованием нетоксичного, парентерально приемлемого дилюента или растворителя, такого как, например, вода или 1,3-бутандиол. Другие приемлемые дилюенты и растворители включают, в качестве неограничивающих примеров, раствор Рингера, изотонический раствор хлорида натрия и жирные масла, такие как синтетические моно- или диглицериды. Другие вводимые парентерально составы, которые можно использовать, включают составы, содержащие активный ингредиент в микрокристаллической форме, в липосомном препарате или в виде компонента биодеградируемых полимерных систем. Композиции для замедленного высвобождения или имплантации могут содержать фармацевтически приемлемые полимерные или гидрофобные материалы, такие как эмульсия, ионообменная смола, умеренно растворимый полимер или умеренно растворимая соль.
aAPC по настоящему изобретению и/или T-клетки, подвернутые экспансии с использованием aAPC, можно вводить животному, предпочтительно, человеку. Если вводят T-клетки, подвернутые экспансии с использованием aAPC по настоящему изобретению, количество вводимых клеток может находиться в диапазоне от приблизительно 1 миллиона до приблизительно 300 миллиардов клеток. Если вводят сами aAPC с T-клетками, подвергнутыми такой экспансии, или без них, их можно вводить в количестве в диапазоне от приблизительно 100000 до приблизительно одного миллиарда клеток, где клетки подвергают инфузии животному, предпочтительно, нуждающемуся в этом пациенту-человеку. Точная вводимая доза будет варьироваться в зависимости от любого количества факторов, включая, в качестве неограничивающих примеров, тип животного и тип заболевания, подвергаемого лечению, возраста животного и пути введения.
aAPC можно вводить животному несколько раз в день или реже, например, раз в день, раз в неделю, раз в две недели, раз в месяц или даже реже, например, раз в несколько месяцев или даже раз в год или менее. Частота введения будет очевидна специалистам в этой области и будет зависеть от любого количества факторов, в качестве неограничивающих примеров, таких как тип и тяжесть заболевания, подвергаемого лечению, типа и возраста животного и т.д.
aAPC (или клетки, подвергнутые экспансии с помощью них) можно вводить совместно с различными другими соединениями (помимо прочего, цитокинами, химиотерапевтическими и/или противовирусными лекарственными средствами). Альтернативно, соединения можно вводить за час, день, неделю, месяц или даже больше до aAPC (или клеток, подвергнутых экспансии с помощью них) или использовать любую комбинацию таких временных интервалов. Кроме того, соединения можно вводить через час, день, неделю или даже больше после введения aAPC (или клеток, подвергнутых экспансии с помощью них) или использовать любую комбинацию таких временных интервалов. Частота и схема введение будут очевидны специалистам в этой области и будут зависеть от любого количества факторов, таких как, в качестве неограничивающих примеров, тип и тяжесть заболевания, подвергаемого лечению, возраст и состояние здоровья животного, тип вводимого соединения или соединений, путь введения различных соединений и aAPC (или клеток, подвергнутых экспансии с помощью них) и т.п.
Кроме того, специалисту в этой области будет понятно с учетом раскрытия, представленного в настоящем описании, что, если aAPC предназначены для введения млекопитающим, клетки обрабатывают таким образом, что они находятся в "состоянии отсутствия роста"; т.е. клетки не могут делиться при введении млекопитающему. Как представлено где-либо в настоящем описании, клетки можно облучать, чтобы сделать их неспособными к росту или делению после введения млекопитающему. В этой области известны другие способы, включая гаптенизацию (например, с использованием динитрофенила и других соединений), чтобы сделать клетки, подлежащие введению, особенно человеку, неспособными к росту, и эти способы не описаны далее в настоящем описании. Кроме того, безопасность введения aAPC, которые делали неспособными к делению in vivo, определяют в фазе I клинических испытаний с использованием aAPC, трансфицированных с использованием плазмидных векторов, кодирующих некоторые из молекул, представленных в настоящем описании.
Способы комбинированного лечения
В некоторых вариантах осуществления настоящее изобретение относится к способам, дополнительно включающим введение индивидууму дополнительного средства. В некоторых вариантах осуществления настоящее изобретение относится к совместному введению и/или совместному составлению.
В некоторых вариантах осуществления введение aAPC действуют синергично при совместном введении с другим средством, и их вводят в дозах, являющихся более низкими, чем дозы, общепринято используемые в случаях, когда такие средства используют в качестве монотерапии.
В некоторых вариантах осуществления, включая, в качестве неограничивающих примеров, использование в случае злокачественных новообразований, настоящее изобретение относится к химиотерапевтическим средствам в качестве дополнительных средств. Неограничивающие примеры химиотерапевтических средств включают алкилирующие средства, такие как тиотепа и циклофосфамид CYTOXAN®; алкилсульфонаты такие как бусульфан, импросульфан и пипосульфан; азиридины, такие как бензодопа, карбоквон, метуредопа и уредопа; этиленимины и метилмеламины, включая алтретамин, триэтиленмеламин, триэтиленфосфамид, триэтилентиофосфамид и триметилоломеламин; ацетогенины (например, буллатацин и буллатацинон); камптотецин (включая синтетический аналог топотекан); бриостатин; каллистатин; CC-1065 (включая его синтетические аналоги адозелесин, карзелесин и бизелесин); криптофицины (например, криптофицин 1 и криптофицин 8); доластатин; дуокармицин (включая синтетические аналоги, KW-2189 и CB 1-TM1); элецтеробин; панкратистатин; саркодиктин; спонгистатин; азотистые иприты, такие как хлорамбуцил, хлорнафазин, хлорфосфамид, эстрамустин, ифосфамид, мехлоретамин, гидрохлорид оксида мехлоретамина, мелфалан, новэмбихин, фенестрин, преднимустин, трофосфамид, урамустин; нитрозомочевину, такие как кармустин, хлорозотоцин, фотемустин, ломустин, нимустин и ранимустин; антибиотики, такие как енединовые антибиотики (например, калихимицин, в частности, калихимицин гамма и калихимицин омега; динемицин, включая динемицин A; бисфосфонаты, такие как клодронат; эсперамицин; а также хромофор неокарциностатин и родственные хромопротеиновые енединовые антибиотики-хромофоры), аклациномицины, актиномицин, аутрамицин, азасерин, блеомицины, кактиномицин, карабицин, каминомицин, карцинофилин, хромомицины, дактиномицин, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлейцин, доксорубицин ADRIAMICIN® (включая морфолино-доксорубицин, цианоморфолино-доксорубицин, 2-пирролино-доксорубицин и дезоксидоксорубицин), эпирубицин, эзорубицин, идарубицин, марцелломицин, митомицины, такие как митомицин C, микофеноловую кислоту, ногаламицин, оливомицины, пепломицин, потфиромицин, пуромицин, квеламицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, зиностатин, зорубицин; антиметаболиты, такие как метотрексат и 5-фторурацил (5-FU); аналоги фолиевой кислоты, такие как деноптерин, метотрексат, птероптерин, триметрексат; аналоги пурина, такие как флударабин, 6-меркаптопурин, тиамиприн, тиогуанин; аналоги пиримидина, такие как анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидезоксиуридин, доксифлуридин, эноцитабин, флоксуридин; андрогены, такие как калустерон, дромостанолон пропионат, эпитиостанол, мепитиостан, тестолактон; средства, угнетающие функции надпочечников, такие как аминоглютетимид, митотан, трилостан; компенсатор фолиевой кислоты, такой как фролиновая кислота; ацеглатон; гликозид альдофосфамида; аминолевулиновую кислоту; энилурацил; амсакрин; бестрабуцил; бисантрен; эдатраксат; демеколцин; диазиквон; элформитин; ацетат эллиптиния; эпотилон; этоглюцид; нитрат галлия; гидроксимочевину; лентинан; лонидаинин; майтанзиноиды, такие как майтанзин и ансамитоцины; митогуазон; митоксантрон; мопиданмол; нитраэрин; пентостатин; фенамет; пирарубицин; лозоксантрон; подофиллиновую кислоту; 2-этилгидразид; прокарбазин; полисахаридный комплекс PSK; разоксан; ризоксин; сизофуран; спирогерманий; тенуазоновую кислоту; триазиквон; 2,2',2''-трихлортриэтиламин; трихотецены (например, T-2 токсин, верракурин A, роридин A и ангуидин); уретан; виндезин; дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид ("Ara-C"); циклофосфамид; тиотепа; таксоиды, например, паклитаксел TAXOL® (Bristol-Myers Squibb Oncology, Princeton, N.J.), несодержащий кремофора ABRAXANE®, состав паклитаксела на основе сконструированных связанных с альбумином наночастиц, и доксетаксел TAXOTERE®; хлорамбуцил; гемцитабин GEMZAR®; 6-тиогуанин; меркаптопурин; метотрексат; аналоги платины, такие как цисплатин, оксалиплатин и карбоплатин; винбластин; платину; этопозид (VP-16); ифосфамид; митоксантрон; винкристин; навельбин, винорелбин; новантрон; тенипозид; эдатрексат; дауномицин; аминоптерин; кселода; ибандронат; иринотекан (камптосар, CPT-11) (включая схему лечения иринотеканом м 5-FU и лейковорином); ингибитор топоизомеразы RFS 2000; дифторметилорнитин (DMFO); ретиноиды, такие как ретиноевая кислота; капецитабин; комбретастатин; лейковорин (LV); оксалиплатин, включая схему лечения оксалиплатином (FOLFOX); лапатиниб (TYKERB); ингибиторы PKC-α, Raf, H-Ras, EGFR (например, эрлотиниб (тарцева)) и VEGF-A, снижающие пролиферацию клеток, и фармацевтически приемлемые соли, кислоты или производные указанных выше соединений. Кроме того, способы лечения могут дополнительно включать применение радиации.
Некоторые опухоли человека могут элиминироваться иммунной системой пациента. Например, введение моноклонального антитела против иммунной молекулы "контрольных точек" может приводить к полному ответу и ремиссии опухоли. Механизмом действия таких антител является ингибирование иммунной регуляторной молекулы, которую опухоли используют в качестве защиты от противоопухолевого иммунного ответа. Ингибируя эти молекулы "контрольных точек" (например, с помощью антагонистического антитела), можно позволять CD8+ T-клеткам пациента пролиферировать и разрушать опухолевые клетки.
Например, введение моноклонального антитела, в качестве неограничивающего примера, против CTLA-4 или PD-1 может приводить к полному ответу и ремиссии опухоли. Механизмом действия таких антител является ингибирование CTLA-4 или PD-1, которые опухоли используют для защиты от противоопухолевого иммунного ответа. Ингибируя эти молекулы "контрольных точек" (например, с помощью антагонистического антитела), можно позволять CD8+ T-клеткам пациента пролиферировать и разрушать опухолевые клетки.
Таким образом, aAPC, включающие безъядерную клетку или эритроидную клетку, презентирующую (например, содержащую на своей поверхности) один или более экзогенных полипептидов, представленных в настоящем описании, можно использовать в комбинации с одним или более блокирующими антителами против иммунной молекулы "контрольных точек". Например, в некоторых вариантах осуществления композиции, представленные в настоящем описании, можно использовать в комбинации с одним или более блокирующими антителами против молекулы, такой как CTLA-4 или PD-1. Например, композиции, представленные в настоящем описании, можно использовать в комбинации со средством, блокирующим, снижающим и/или ингибирующим PD-1 и PD-L1 или PD-L2 и/или связывание PD-1 с PD-L1 или PD-L2 (в качестве неограничивающего примера, один или более из ниволумаба (ONO-4538/BMS-936558, MDX1106, OPDIVO, BRISTOL MYERS SQUIBB), пембролизумаба (KEYTRUDA, Merck), пидилизумаба (CT-011, CURE TECH), MK-3475 (MERCK), BMS 936559 (BRISTOL MYERS SQUIBB), MPDL328OA (ROCHE)). В варианте осуществления композиции, представленные в настоящем описании, можно использовать в комбинации со средством, блокирующим, снижающим и/или ингибирующим активность CTLA-4 и/или связывание CTLA-4 с одним или более рецепторами (например, CD80, CD86, AP2M1, SHP-2 и PPP2R5A). Например, в некоторых вариантах осуществления иммуномодулирующее средство является антителом, таким как, в качестве неограничивающих примеров, ипилимумаб (MDX-010, MDX-101, Yervoy, BMS) и/или тремелимумаб (Pfizer). Блокирующие антитела против этих молекул можно получать от, например, Bristol Myers Squibb (New York, N.Y.), Merck (Kenilworth, N.J.), Medlmmune (Gaithersburg, Md.) и Pfizer (New York, N.Y.).
Кроме того, композиции aAPC, представленные в настоящем описании, можно использовать в комбинации с одним или более блокирующими антителами против иммунной молекулы "контрольных точек", такой как, например, BTLA, HVEM, TIM3, GALS, LAG3, VISTA, KIR, 2B4, CD160 (также обозначаемый как BY55), CGEN-15049, киназы CHK 1 и CHK2, A2aR, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), GITR, GITRL, галектин-9, CD244, CD160, TIGIT, SIRPα, ICOS, CD172a и TMIGD2 и различные лиганды семейства B-7 (включая, в качестве неограничивающих примеров, B7-1, B7-2, B7-DC, B7-H1, B7-H2, B7-H3, B7-H4, B7-H5, B7-H6 и B7-H7).
В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления эритроидная клетка является безъядерной эритроидной клеткой. В некоторых вариантах осуществления по указанным выше аспектам и вариантам осуществления эритроидная клетка является ядросодержащей эритроидной клеткой
В некоторых вариантах осуществления настоящее изобретение относится к фармацевтической композиции, содержащей множество сконструированных эритроидных клеток, представленных в настоящем описании, и фармацевтический носитель. В других вариантах осуществления настоящее изобретение относится к фармацевтической композиции, содержащей популяцию сконструированных эритроидных клеток, представленных в настоящем описании, и фармацевтический носитель. Следует понимать, что в фармацевтической композиции по настоящему изобретению могут находиться любая отдельная сконструированная эритроидная клетка, множество сконструированных эритроидных клеток или популяция сконструированных эритроидных клеток, представленных где-либо в настоящем описании.
В некоторых вариантах осуществления фармацевтические композиции, представленные в настоящем описании, содержат сконструированные (т.е. модифицированные) эритроидные клетки и немодифицированные эритроидные клетки. Например, в различных вариантах осуществления единичная стандартная доза эритроидных клеток (например, модифицированных и немодифицированных эритроидных клеток) может содержать приблизительно, по меньшей мере или не более 10%, 20%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95% или 99% сконструированных эритроидных клеток, где остальные эритроидные клетки в композиции не являются сконструированными.
В некоторых вариантах осуществления фармацевтические композиции, представленные в настоящем описании, содержат сконструированные безъядерные эритроидные клетки и ядросодержащие эритроидные клетки. Например, в различных вариантах осуществления единичная стандартная доза сконструированных эритроидных клеток (например, безъядерных и ядросодержащих эритроидных клеток) может содержать приблизительно или по меньшей мере 10%, 20%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% безъядерных эритроидных клеток, где остальные эритроидные клетки в композиции являются ядросодержащим.
VI. НАБОРЫ
Настоящее изобретение включает различные наборы, содержащие aAPC по настоящему изобретению, нуклеиновую кислоту, кодирующую различные белки, антитело, специфически связывающееся с костимуляторной молекулой на поверхности T-клетки, и/или нуклеиновую кислоту, кодирующую антитело по настоящему изобретению, антиген или цитокин, аппликатор и инструкции, в которых описано использованием набора для осуществления способов по настоящему изобретению. Хотя ниже описаны примеры наборов, специалистам в этой области с учетом настоящего описания будет очевидно содержание других наборов, которые можно использовать. Каждый из этих наборов входит в объем настоящего изобретения.
Настоящее изобретение включает набор для специфического индуцирования пролиферации T-клетки, экспрессирующей известную костимуляторную молекулу. Это является результатом того, что приведение T-клетки в контакт с aAPC специфически индуцирует пролиферацию T-клетки. Набор используют в соответствии со способами, представленными в настоящем описании. В кратком изложении, набор можно использовать для введения aAPC по настоящему изобретению к T-клеткам, экспрессирующим по меньшей мере одну костимуляторную молекулу. Как более подробно описано где-либо в настоящем описании, это является результатом того, что данные, представленные в настоящем описании, свидетельствуют о том, что приведение T-клетки в контакт с aAPC, содержащей костимуляторный лиганд, специфически связывающийся с когнатной костимуляторной молекулой, присутствующей в T-клетке, опосредует стимуляцию и активацию T-клетки. Кроме того, T-клетки, полученные с использованием этого набора, можно вводить животному для достижения терапевтических результатов.
Набор дополнительно содержит аппликатор, который можно использовать для введения aAPC к T-клеткам. Конкретный аппликатор, включенный в набор, будет зависеть, например, от способа, используемого для введения aAPC, а также T-клеток, подвергаемых экспансии с помощью aAPC, и такие аппликаторы хорошо известны в этой области и могут включать, в частности, пипетку, шприц и т.п. Кроме того, набор содержит инструкции по использованию набора. Эти инструкции включают описание, представленное в настоящем описании, в простом виде.
Набор включает фармацевтически приемлемый носитель. Композицию предоставляют в подходящем количестве, как представлено где-либо в настоящем описании. Кроме того, путь введения и частота введения являются такими, как представлено где-либо выше в настоящем описании.
Набор включает aAPC, содержащие широкий спектр молекул, в качестве неограничивающих примеров, таких как молекулы, представленные в настоящем описании. Однако, специалистам в этой области с учетом идей, представленных в настоящем описании, будет понятно, что описание никоим образом не ограничивает эти или любые другие комбинации молекул. Наоборот, комбинации, представленные в настоящем описании, приведены в иллюстративных целях и никоим образом не ограничивают комбинации, представленные в настоящем описании. Кроме того, набор включает набор, в котором каждую молекулу, подлежащую трансдукции в aAPC предоставляют в виде выделенной нуклеиновой кислоты, кодирующей молекулу, вектора, содержащего нуклеиновую кислоту, кодирующую молекулу, и любую их комбинацию, включая случаи, когда по меньшей мере две молекулы кодируются смежными нуклеиновыми кислотами и/или кодируются одним и тем же вектором.
Все публикации и патентные заявки, процитированные в настоящем описании, включены в него в качестве ссылки в полном объеме для всех целей так, как если бы каждая отдельная публикация или патентная заявка была конкретно и индивидуально включена в качестве ссылки для всех целей. Публикации, обсуждаемые в настоящем описании, представлены исключительно для их раскрытия до даты подачи настоящей заявки. Ничто в настоящем описании не следует истолковывать как признание того, что авторы настоящего изобретения не могут относить такое раскрытие к более ранней дате в силу предшествующего раскрытия или по любой другой причине.
ПРИМЕРЫ
Пример 1. Получение эритроидных клеток, генетически сконструированных для экспрессии слитого белка MOG-MHC класса II-GPA
Результаты
Эритроидные клетки трансдуцируют для экспрессии слитого белка, содержащего экзогенный антигенный пептид, миелиновый олигодендроцитарный гликопротеин (MOG), слитый с экзогенным антигенпрезентирующим полипептидом, в частности, MHC класса II, слитым с трансмембранным доменом GPA (GPA), служащим в качестве мембранного якоря (MOG-MHC класса II-GPA). На фиг. 1A показана схема дизайна экспрессии пептида MOG и MHC класса II в виде одноцепочечного слитого белка, где экзогенный пептид (MOG) связывают с β-цепью MHC класса II, которую связывают с α-цепью MHC класса II, которую связывают с мембранным якорем GPA. Культивирование и трансдукцию клеток осуществляют, как описано в разделе "Способы" ниже, для получения эритроидных клеток, экспрессирующих MOG, презентируемый MHC класса II на поверхности клетки, заякоренным трансмембранным доменом GPA.
Для валидации экспрессии антигенных пептидов в сконструированных эритроидных клетках используют связывание меченого аллофикоцианином (APC) или фикоэритрином (PE) антитела против MOG. Для валидации экспрессии антигенпрезентирующего пептида MHC класса II в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса II.
Способы
Получение лентивирусного вектора
Ген, кодирующий слитый белок MOG-MHC класса II-GPA, клонируют в участок множественного клонирования лентивирусного вектора pCDH с промоторной последовательностью MSCV от System Biosciences. Лентивирус получают в клетках 293T посредством трансфекции клеток с использованием лентивирусного вектора pPACKH1 (System Biosciences) и pCDH, содержащего ген MOG-MHC класса II-GPA. Затем клетки высевают в свежую среду для культивирования. Вирусный супернатант собирают через 48 часов после замены среды посредством центрифугирования при 1500 об./мин. в течение 5 минут. Супернатант собирают и замораживают в аликвотах при -80°C.
Экспансия и дифференцировка эритроидных клеток
CD34+ клетки человека, полученные из клеток мобилизованной периферической крови нормальных людей-доноров, приобретают в замороженном виде в AllCells Inc. Способ экспансии/дифференцировки включает 3 стадии. На первой стадии размороженные CD34+ эритроидные клетки-предшественники культивируют в среде MDM Искова, содержащей рекомбинантный инсулин человека, трансферрин человека, рекомбинантный фактор стволовых клеток человека и рекомбинантный интерлейкин 3 человека. На второй стадии эритроидные клетки культивируют в среде MDM Искова, дополненной бычьим сывороточным альбумином, рекомбинантным инсулином человека, трансферрином человека, рекомбинантным фактором стволовых клеток человека, рекомбинантным эритропоэтином человека и L-глутамином. На третьей стадии эритроидные клетки культивируют в среде MDM Искова, дополненной трансферрином человека, рекомбинантным инсулином человека, рекомбинантным эритропоэтином человека и гепарином. Культуры поддерживают при 37°C в инкубаторе при 5% CO2.
Трансдукция эритроидных клеток-предшественников
Эритроидные клетки-предшественники трансдуцируют на стадии 1 описанного выше способа культивирования. Эритроидные клетки в среде для культивирования объединяют с лентивирусным супернатантом и полибреном. Инфицирования достигают посредством центрифужной инокуляции, центрифугируя планшет при 2000 об./мин. в течение 90 минут при комнатной температуре. После центрифужной инокуляции клетки инкубируют при 37°C в течение ночи.
Связывание антител
Для валидации экспрессии антигенпрезентирующего пептида MHC класса II в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса II (например, моноклональное антитело против HLA-DR человека (HLA класса II), конъюгированное с аллофикоцианином, клон Immu-357 от Beckman Coulter Life Sciences). Связывание антитела измеряют посредством проточной цитометрии по флуоресценции APC или PE. Гейт устанавливают с учетом окрашенных нетрансдуцированных клеток.
Пример 2. Получение и валидация in vitro эритроидных клеток, генетически сконструированных для коэкспрессии слитого белка MOG-MHC класса II-GPA и коингибиторного полипептида
Результаты
Эритроидные клетки трансдуцируют для экспрессии слитого белка, содержащего экзогенный антигенный пептид MOG, слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса II, слитым с трансмембранным доменом GPA (GPA) (MOG-MHC класса II-GPA), как описано в примере 1. Эритроидные клетки котрансдуцируют для дополнительной экспрессии экзогенного коингибиторного пептида PD-L1. Культивирование и трансдукцию клеток осуществляют, как описано в разделе "Способы" ниже, для получения эритроидных клеток, экспрессирующих MOG, презентируемый MHC класса II на поверхности, заякоренным с помощью трансмембранного домена GPA, и коэкспрессирующих PD-L1.
Для валидации экспрессии антигенпрезентирующего пептида MHC класса II в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса II, как описано в примере 1. Для валидации экспрессии PD-L1 в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против PD-L1.
Эффект сконструированных эритроидных клеток (MOG-MHC класса II-GPA и PD-L1) анализируют посредством определения одного или более эффектов в отношении супрессии T-клетки, включая (1) ингибирование активности T-клеток, (2) ингибирование пролиферации T-клеток и/или (3) индуцирование апоптоза T-клеток.
Способы
Получение лентивирусного вектора
Конструируют гены слитого белка MOG-MHC класса II-GPA и PD-L1. Гены, кодирующие белки, клонируют в участок множественного клонирования лентивирусного вектора pCDH с промоторной последовательностью MSCV от System Biosciences таким образом, что один вектор содержит гены для обоих экзогенных белков. Лентивирус получают в клетках 293T посредством трансфекции клеток с использованием лентивирусного вектора pPACKH1 (System Biosciences) и pCDH, содержащего гены MOG-MHC класса II-GPA и PD-L1. Клетки высевают в свежую среду для культивирования. Вирусный супернатант собирают через 48 часов после замены среды посредством центрифугирования при 1500 об./мин. в течение 5 минут. Супернатант собирают и замораживают в аликвотах при -80°C.
Трансдукция эритроидных клеток-предшественников
Экспансию и дифференцировку эритроидных клеток осуществляют по примеру 1 с использованием описанных выше лентивирусных векторов. Эритроидные клетки-предшественники трансдуцируют на стадии 1 способа культивирования. Эритроидные клетки в среде для культивирования объединяют с лентивирусным супернатантом и полибреном. Инфицирования достигают посредством центрифужной инокуляции, центрифугируя планшет при 2000 об./мин. в течение 90 минут при комнатной температуре. После центрифужной инокуляции клетки инкубируют при 37°C в течение ночи.
Связывание антител
Для валидации экспрессии антигенпрезентирующего пептида MHC класса II в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса II, как описано в примере 1. Для валидации экспрессии PD-L1 в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против PD-L1 (например, APC-меченого антитела против CD274 человека (B7-H1, PD-L1) (Biolegend)). Связывание антител измеряют посредством проточной цитометрии по флуоресценции APC или PE. Гейт устанавливают с учетом окрашенных нетрансдуцированных клеток.
Функциональные валидационные анализы
Эффекты сконструированных эритроидных клеток, коэкспрессирующих MOG-MHC класса II-GPA и PD-L1, в отношении супрессии T-клеток анализируют посредством определения одного или более из (1) ингибирования активности T-клеток, (2) ингибирования пролиферации T-клеток и (3) индуцирования апоптоза T-клеток. Ингибирование активности T-клеток определяют, например, посредством анализа цитокинов с супернатантах с использованием коммерчески доступных наборов для ELISA на ИЛ-2, ИФНγ и ИЛ-10 человека (R&D Systems). Например, после обработки сконструированными эритроидными клетками детекция ингибирования секреции ИЛ-2 активированными T-клетками будет свидетельствовать об антипролиферативном эффекте сконструированных эритроидных клеток, коэкспрессирующих MOG-MHC класса II-GPA и PD-L1. Ингибирование пролиферации T-клеток анализируют, например, посредством мечения клеток флуоресцентным красителем сукцинимидиловым сложным эфиром диацетата 5,6-карбоксифлуоресцеина (CFSE). Клетки, пролиферирующие в ответ на сконструированную эритроидную клетку, демонстрируют снижение интенсивности флуоресценции CFSE, которую измеряют напрямую посредством проточной цитометрии. Альтернативно, для оценки скорости роста T-клеток, стимулированных эритроидными клетками, сконструированными для коэкспрессии слитого белка MOG-MHC класса II-GPA и коингибиторного полипептида PD-L1, можно использовать включение радиоактивного тимидина. Индуцирование апоптоза T-клетки с помощью сконструированных эритроидных клеток, коэкспрессирующих MOG-MHC класса II-GPA и PD-L1, анализируют с использованием, например, окрашивания флуорохром-конъюгированным аннексином V. BATF является фактором транскрипции bZIP, играющим важную роль в регуляции дифференцировки и функционирования во многих линиях лимфоцитов. В линии CD8+ T-клеток повышенная экспрессия BATF в истощенных CD8+ T-клетках супрессирует их эффекторную функцию. Показано, что BAFT является центральным регулятором ранней дифференцировки эффекторных CD8+ T-клеток. Таким образом, для определения эффекта MOG-MHC класса II-GPA и PD-L1 в отношении супрессии T-клеток можно использовать анализ экспрессии факторов транскрипции, таких как основной ATF-подобный фактор транскрипции с лейциновой молнией (BATF).
Пример 3. Получение и валидация in vitro эритроидных клеток, генетически сконструированных для коэкспрессии слитого белка MOG-MHC класса II-GPA и полипептида для экспансии Treg
Результаты
Эритроидные клетки трансдуцируют для экспрессии слитого белка, содержащего экзогенный антигенный пептид MOG, слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса II, слитым с трансмембранным доменом GPA (GPA) (MOG-MHC класса II-GPA), как описано в примере 1. Эритроидные клетки также трансдуцируют для дополнительной экспрессии экзогенного полипептида для экспансии Treg, полипептида TNFR2-специфического ФНОα. Культивирование и трансдукцию клеток осуществляют, как описано в разделе "Способы" ниже, для получения эритроидных клеток, экспрессирующих MOG, презентируемый MHC класса II на поверхности, заякоренным с помощью трансмембранного домена GPA, и коэкспрессирующих полипептид TNFR2-специфического ФНОα.
Для валидации экспрессии антигенных пептидов в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против ФНОα. Для валидации экспрессии антигенпрезентирующего пептида MHC класса II в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса II. Функциональную активность эффекта сконструированных эритроидных клеток (MOG-MHC класса II-GPA и TNFR2-специфического ФНОα) анализируют с использованием анализа пролиферации на основе CD4+ T-клеток человека, как описано в примере 2.
Способы
Получение лентивирусного вектора
Конструируют гены слитого белка MOG-MHC класса II-GPA и TNFR2-специфческого ФНОα. Гены, кодирующие белки, клонируют в участок множественного клонирования лентивирусного вектора pCDH с промоторной последовательностью MSCV от System Biosciences таким образом, что один вектор содержит гены для обоих экзогенных белков. Лентивирус получают в клетках 293T посредством трансфекции клеток с использованием лентивирусного вектора pPACKH1 (System Biosciences) и pCDH, содержащего гены MOG-MHC класса II-GPA и TNFR2-специфического ФНОα. Клетки высевают в свежую среду для культивирования. Вирусный супернатант собирают через 48 часов после замены среды посредством центрифугирования при 1500 об./мин. в течение 5 минут. Супернатант собирают и замораживают в аликвотах при -80°C.
Трансдукция эритроидных клеток-предшественников
Экспансию и дифференцировку эритроидных клеток осуществляют по примеру 1 с использованием описанных выше лентивирусных векторов. Эритроидные клетки-предшественники трансдуцируют на стадии 1 способа культивирования. Эритроидные клетки в среде для культивирования объединяют с лентивирусным супернатантом и полибреном. Инфицирования достигают посредством центрифужной инокуляции, центрифугируя планшет при 2000 об./мин. в течение 90 минут при комнатной температуре. После центрифужной инокуляции клетки инкубируют при 37°C в течение ночи.
Связывание антител
Для валидации экспрессии антигенпрезентирующего пептида MHC класса II в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса II, также как описано в примере 1. Для валидации экспрессии мутанта TNFR2-специфического ФНОα в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против ФНОα. Связывание любого из антител измеряют посредством проточной цитометрии по флуоресценции APC или PE. Гейт устанавливают с учетом окрашенных нетрансдуцированных клеток.
Функциональные валидационные анализы
Функциональную активность анализируют с использованием анализа пролиферации на основе CD4+ T-клеток человека. Клетки метят флуоресцентным красителем сукцинимидиловым сложным эфиром диацетата 5,6-карбоксифлуоресцеина (CFSE). Клетки, пролиферирующие в ответ на сконструированные эритроциты демонстрируют снижение интенсивности флуоресценции CFSE, которую измеряют напрямую посредством проточной цитометрии. Альтернативно для анализа скорости роста T-клеток, стимулированных эритроидными клетками, сконструированными для коэкспрессии слитого белка MOG-MHC класса II-GPA и полипептида CD25-специфического ИЛ-2 для экспансии Treg можно использовать включение радиоактивного тимидина.
Функциональную активность также анализируют с использованием анализа супрессии Treg in vitro. Такой анализ описывают в Collinson and Vignali (Methods Mol Biol. 2011; 707: 21-37, включенной в настоящее описание в качестве ссылки в полном объеме).
Пример 4. Активность безъядерных эритроидных клеток, коэкспрессирующих слитый белок MOG-MHC класса II-GPA и коингибиторный полипептид или полипептид для экспансии Treg в модели EAE на мышах
Экспериментальный аутоиммунный энцефаломиелит (EAE) представляет модель, наиболее общеупотребительную для исследования эффективности потенциальных лекарственных средств для лечения рассеянного склероза (MS). Из-за значительного сходства с MS, EAE используют для исследования патогенеза аутоиммунности, воспаления ЦНС, демиелинизации, миграции клеток и индуцирования толерантности. EAE отличается параличом (в некоторых моделях паралич является рецидивирующе-ремиттирующим), воспалением ЦНС и демиелинизацией. Для индуцирования EAE у самок мышей C57BL/6 используют наборы Hooke Kits™ для вызывания EAE у мышей C57BL/6 (Hooke Laboratories). Используя этот способ, EAE у мышей C57BL/6 индуцируют посредством иммунизации эмульсией MOG35-55 или MOG1-125 в полном адъюванте Фрейнда (CFA) с последующим введением коклюшного токсина в PBS сначала в день иммунизации, а затем снова на следующий день. Типичный дебют EAE наступает через 9-14 дней после иммунизации, при этом пик заболевания наступает через 3-5 дней после дебюта в случае каждой мыши. Пик длится в течение 1-3 дней с последующим частичным восстановлением. У приблизительно 25% мышей будут наблюдать повышение тяжести EAE (рецидив) после начального частичного восстановления. Как правило, это происходит через 20-27 дней после иммунизации. Используют группы по 10-12 мышей с 4-6 мышей на клетку.
Сконструированные безъядерные эритроидные клетки, содержащие MOG-MHC класса II-GPA и PD-L1 или MOG-MHC класса II-GPA и CD25-специфический ИЛ-2, составляют в буфере, подходящем для безъядерных эритроидных клеток. Введение сконструированных безъядерных эритроидных клеток начинается во время дебюта EAE. Если сконструированные безъядерные эритроидные клетки тестируют на способность реверсировать течение хронического EAE, введение начинают через 7-14 дней после дебюта заболевания. Мышей приписывают к группам лечения, когда у них развивается EAE (непрерывное включение в исследование) или в фиксированное время после иммунизации, но всегда сбалансировано для получения групп со схожим временем дебюта EAE и схожими баллами дебюта EAE. Если включение в исследование осуществляют после дебюта EAE, мышей также уравновешивают по максимальным баллам перед включением.
Введение дозы осуществляют при клинических баллах=1, как указано в таблице 25 ниже.
Введение животным можно осуществлять 1-3 раза в сутки. Частота введения составляет каждые 2-14 дней, например, каждые 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 дней.
Оценку эффектов сконструированных безъядерных эритроидных клеток, экспрессирующих MOG-MHC класса II-GPA и PD-L1, или эритроидных клеток, содержащих MOG-MHC класса II-GPA и CD25-специфический ИЛ-2, осуществляют с использованием одного или более из (1) балльной оценки EAE; (2) изменения массы тела и (3) гистологического анализа, как подробно описано ниже.
Балльная оценка EAE
Как правило, EAE оценивают по шкале от 0 до 5, включая "промежуточные" баллы (т.е. 0,5, 1,5, 2,5, 3,5), когда клиническая картина находится между двумя определенными баллами. Способ балльной оценки немного отличается в зависимости от стадии заболевания (дебют/пик и восстановление) для каждой отдельной мыши. Чтобы избежать неосознанного смещения при балльной оценки, мышей маскировано оценивает специалист, которому неизвестно, каких мышей подвергали какому лечению.
Таблица 25. Балльная оценка EAE мыши - дебют и пик
При захвате за основание хвоста хвост напряжен и выпрямлен. Задние конечности, как правило, раздвинуты. Когда мышь ходит, не наблюдают изменения походки или наклона головы.
При захвате за основание хвоста хвост напряжен за исключением кончика. В хвосте чувствуется напряжение мышц, в то время когда хвост продолжает двигаться.
При захвате за основание хвоста, вместо выпрямления весь хвост свисает с пальца. Задние конечности, как правило, раздвинуты. Не наблюдают признаков движения хвоста.
При захвате за основание хвоста, весь хвост свисает с пальца. Когда мышь падает на проволочную решетку, по меньшей мере одна задняя конечность постоянно проваливается. Походка лишь слегка шаткая.
При захвате за основание хвоста, задние конечности не расходятся, а удерживаются вместе. Когда наблюдают за ходящей мышью, четко видна шаткая походка. На одной ступне могут подволакиваться пальцы, но у другой конечности не наблюдают очевидного торможения движений.
- или -
Мышь выглядит в соответствии с баллами 0,0, но наблюдают очевидные признаки наклона головы при ходьбе. Равновесие нарушено.
Обе задние конечности двигаются одинаково, но у обеих наблюдают подволакивание ступней (мышь спотыкается).
- или -
Отсутствие движений в одной конечности/полное подволакивание одной конечности, но движение в другой конечности.
- или -
Тяжесть EAE кажется слабой при захвате (как в случае баллов 0,0-1,5), но наблюдают выраженный наклон головы, что заставляет мышь иногда падать.
- или -
Снижение тонуса хвоста и почти полный паралич задних конечностей. Мышь "загребает" одной или обеими задними конечностями, но ни одна из задних конечностей не может двигаться вперед от заднего бедра.
- или -
Снижение тонуса хвоста с параличом одной передней и одной задней конечности.
- или -
ВСЕ из: Тяжелый наклон головы,
Тяжелый наклон головы, Ходьба только вдоль края клетки,
Ходьба только вдоль края клетки, Наталкивание на стенки клетки,
Наталкивание на стенки клетки,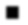 Верчение при захвате за основание хвоста.
Верчение при захвате за основание хвоста.
Мышь двигается по клетке, но при помещении ее на бок не может выпрямиться. Задние конечности расположены вместе на одной стороне тела.
- или -
Мышь двигается по клетке, но задняя часть тела плоская как блин, придавая вид горба передней половине тела мыши.
Мышь минимально двигается по клетке, но выглядит активной и питается.
После достижения мышью баллов 4,0 в течение 2 дней зачастую рекомендуют умерщвление. Однако, при ежедневном введении s.c. жидкостей большинство мышей C57BL/6 могут восстановиться до 3,5 или 3,0, в то время как мыши SJL могут полностью восстановиться, даже если они достигают баллов 4,0 на пике заболевания. Если мышь умерщвляют из-за тяжелого паралича, этой мыши приписывают баллы 5,0 на все оставшееся время эксперимента.
Мышь имеет минимальное движение в передних конечностях. Мышь с трудом отвечает на контакт.
Рекомендовано умерщвление. Если мышь умерщвляют из-за тяжелого паралича, этой мыши приписывают баллы 5,0 на все оставшееся время эксперимента.
- или -
Обнаруживают гибель мыши из-за паралича.
- OR -
Мышь умерщвляют из-за тяжелого паралича.
На стадии восстановления EAE у большинства мышей хвост больше не будет мягким, но и не будет нормальным; он жесткий на ощупь и "загибается крючком". Задние конечности могут начать двигаться (как при нажатии на педали), но мышь не может ходить. Каждое изменение затрудняет балльную оценку. Таким образом, если это происходит, для этих мышей используют следующие модификации указанных выше критериев, представленные ниже в таблице 26:
Таблица 26. Модифицированная балльная оценка EAE мышей
- или -
Мышь имеет шаткую походку (как описано для баллов 2,5 выше), и не может сделать больше двух шагов без заваливания на бок. Мышь не может выпрямиться.
- или -
У мыши плохо двигаются задние конечности (как описано для баллов 2,5 выше), и у нее наблюдают частичный паралич передних конечностей, о чем свидетельствует то, что она держит голову ниже, чем в норме, и неспособность мыши выпрямиться, когда ее кладут на бок.
Масса тела
В течение EAE изменения массы тела отражают тяжесть заболевания. Мыши часто теряют небольшое количество массы в день после иммунизации. По-видимому, это является результатом эффектов вводимого адъюванта и коклюшного токсина. Затем мыши неуклонно повышают свою массу тела до дебюта заболевания. В день дебюта EAE мыши неизменно теряют 1-2 г своей массы тела (5-10% массы тела). Потеря веса продолжается с прогрессированием тяжести EAE, при этом потеря на пике заболевания достигает приблизительно 20% их массы тела до дебюта. Наиболее вероятно, потеря веса является результатом паралича и сниженного потребления пищи, а также высокой продукции провоспалительных цитокинов, таких как ФНО, во время активной фазы воспаления. После достижения пика заболевания мыши медленно набирают вес, даже если их клинические баллы не улучшаются. Это повышение массы может являться результатом отрицательной регуляции воспаления, что приводит к более низким уровням провоспалительных цитокинов в крови. Мыши, которым не вводили средство или которым вводили носитель, как правило, имеют приблизительно 90% своей массы терла перед иммунизацией через 28 дней после иммунизации.
Гистология
Гистологический анализ осуществляют в конце исследования (как правило, через приблизительно 28 дней после иммунизации) или тогда, когда группа, которой вводят носитель, достигает пика заболевания (как правило, через 14-18 дней после иммунизации). Воспаление при EAE, как правило, начинается в поясничной области спинного мозга, распространяясь по всему спинному мозгу к пику заболевания.
При дебюте заболевания количество очагов воспаления сильно коррелирует с тяжестью заболевания. Количество очагов повышается в некоторой степени до достижения пика заболевания, когда, как правило, обнаруживают 6-15 очагов воспаления/срез на всем протяжении спинного мозга. На хронической стадии EAE (начинается через несколько дней после пика заболевания) многие очаги воспаления разрешаются, что, как правило, приводит к 3-4 очагам воспаления на каждом срезе спинного мозга через приблизительно 28 дней после иммунизации.
Т.к. наибольшее количество очагов воспаления обнаруживают на ранних стадиях заболевания, если гистологический анализ осуществляют в конце исследования, мыши, которые имеют поздний дебют EAE, зачастую имеют больше очагов воспаления в спинном мозге, чем можно было бы ожидать, исходя из их клинических баллов. Например, в день исследования 28 мышь с дебютом EAE через 27 дней после иммунизации и конечными клиническими баллами 2, вероятно, будут иметь больше очагов воспаления, чем мыши с дебютом EAE через 9 дней после иммунизации и конечными баллами 3,5. Аналогично, мышь, у которой наблюдают рецидив незадолго до конца исследования (рецидив определяют как 1 или более очков повышения клинических баллов), как правило, будет иметь больше очагов воспаления в конце исследования, чем мышь со стабильным хроническим заболеванием, даже если эти две мыши имеют одинаковые клинические баллы в конце исследования.
В течение первых двух дней после дебюта заболевания, как правило, не обнаруживают демиелинизацию, но ее обнаруживают на пике заболевания (через 4-5 дней после дебюта EAE), и она продолжается во время хронической фазы EAE. Баллы демиелинизации не изменяются значительно между пиком и 28 днями после иммунизации и, как правило, в среднем составляют от 1,2 до 2,5.
Демиелинизацию оценивают с использованием срезов, окрашенных люксолом прочным синим (LFB), и срезов, окрашенных гематоксилином и эозином. На срезах LFB белое вещество спинного мозга окрашивается темно-синим, и демиелинизированные области имеют более светлую синюю окраску и ассоциированы с крупными вакуолями. На срезах, окрашенных гематоксилином и эозином, нарушение нормальной структуры с крупными вакуолями является показателем демиелинизации.
Апоптотические клетки определяют на срезах, окрашенных гематоксилином и эозином, и, как правило, не обнаруживают их в течение первых двух дней развития заболевания. Их обнаруживают на пике и во время хронической стадии EAE. Среднее количество апоптотических клеток, как правило, составляет от 2 до 4 на срез.
В вариантах осуществления введение безъядерных эритроидных клеток, экспрессирующих MOG-MHC класса II-GPA и PD-L1, или эритроидных клеток, экспрессирующих MOG-MHC класса II-GPA и CD25-специфический ИЛ-2, будет приводить к одному или более из улучшения баллов EAE или снижения количества очагов воспаления по сравнению с контрольными мышами, которым вводили носитель.
Пример 5. Получение эритроидных клеток, генетически сконструированных для экспрессии слитого белка PR1-HLA-A2-GPA
Результаты
Эритроидные клетки трансдуцируют для экспрессии слитого белка, содержащего PR1, пептид, рестриктированный по лейкоцитарном антигену человека (HLA)-A2, слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2, слитым с трансмембранным доменом GPA (GPA) (PR1-HLA-A2-GPA). На фиг. 1B показана схема дизайна экспрессии пептида PR1 и MHC класса I в виде одноцепочечного слитого белка. Культивирование и трансдукцию клеток осуществляют, как описано в разделе "Способы" ниже, для получения эритроидных клеток, экспрессирующих PR1, презентируемый MHC класса I на поверхности, заякоренным с помощью трансмембранного домена GPA.
Для валидации экспрессии антигенного пептида в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против PR1. Для валидации экспрессии антигенпрезентирующего пептида MHC класса I в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса I.
Способы
Получение лентивирусного вектора
Ген, кодирующий слитый белок PR1-HLA-A2-GPA, клонируют в участок множественного клонирования лентивирусного вектора pCDH с промоторной последовательностью MSCV от System Biosciences. Лентивирус получают в клетках 293T посредством трансфекции клеток с использованием лентивирусного вектора pPACKH1 (System Biosciences) и pCDH, содержащего ген PR1-HLA-A2-GPA. Затем клетки высевают в свежую среду для культивирования. Вирусный супернатант собирают через 48 часов после замены среды посредством центрифугирования при 1500 об./мин. в течение 5 минут. Супернатант собирают и замораживают в аликвотах при -80°C.
Экспансия и дифференцировка эритроидных клеток
Клетки CD34+ человека, полученные из клеток мобилизованной периферической крови нормальных людей-доноров, приобретают замороженными в AllCells Inc. Способ экспансии/дифференцировки включает 3 стадии. На первой стадии размороженные CD34+ эритроидные клетки-предшественники культивируют в среде MDM Искова, содержащей рекомбинантный инсулин человека, трансферрин человека, рекомбинантный фактор стволовых клеток человека и рекомбинантный интерлейкин 3 человека. На второй стадии эритроидные клетки культивируют в среде MDM Искова, дополненной бычьим сывороточным альбумином, рекомбинантным инсулином человека, трансферрином человека, рекомбинантным фактором стволовых клеток человека, рекомбинантным эритропоэтином человека и L-глутамином. На третьей стадии эритроидные клетки культивируют в среде MDM Искова, дополненной трансферрином человека, рекомбинантным инсулином человека, рекомбинантным эритропоэтином человека и гепарином. Культуры поддерживают при 37°C в инкубаторе при 5% CO2.
Трансдукция эритроидных клеток-предшественников
Эритроидные клетки-предшественники трансдуцируют на стадии 1 описанного выше способа культивирования. Эритроидные клетки в среде для культивирования объединяют с лентивирусным супернатантом и полибреном. Инфицирования достигают посредством центрифужной инокуляции, центрифугируя планшет при 2000 об./мин. в течение 90 минут при комнатной температуре. После центрифужной инокуляции клетки инкубируют при 37°C в течение ночи.
Связывание антител
Для валидации экспрессии слитого белка PR1-HLA-A2-GPA в сконструированных эритроидных клетках используют связывание меченого аллофикоцианином (APC) или фикоэритрином (PE) антитела против PR1-HLA-A2 (например, моноклонального антитела против PR1/HLA-A2 Hu8F4). Связывание антитела измеряют посредством проточной цитометрии по флуоресценции APC или PE. Гейт устанавливают с учетом окрашенных нетрансдуцированных клеток.
Для валидации экспрессии антигенпрезентирующего пептида MHC класса I в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса I (например, антитела против HLA-A2 (MA1-80117), Invitrogen)). Связывание любого из антител измеряют посредством проточной цитометрии по флуоресценции APC или PE. Гейт устанавливают с учетом окрашенных нетрансдуцированных клеток.
Пример 6. Получение и валидация in vitro эритроидных клеток, генетически сконструированных для коэкспрессии слитого белка PR1-HLA-A2-GPA и костимуляторного полипептида
Результаты
Эритроидные клетки трансдуцируют для экспрессии слитого белка, содержащего PR1, пептид, рестриктированный по лейкоцитарному антигену человека (HLA)-A2, слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2, слитым с трансмембранным доменом GPA (PR1-HLA-A2-GPA). На фиг. 1B показана схема дизайна экспрессии пептида PR1 и MHC класса I в виде одноцепочечного слитого белка. Эритроидные клетки также трансдуцируют для дополнительной экспрессии экзогенного костимуляторного пептида 4-1BBL. Культивирование и трансдукцию клеток осуществляют, как описано в разделе "Способы" ниже, для получения эритроидных клеток, экспрессирующих PR1, презентируемый MHC класса I на поверхности, заякоренным с помощью трансмембранного домена GPA.
Для валидации экспрессии соответствующих пептидов в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против PR1 или против 4-1BBL с экзогенными пептидами PR1 и 4-1BBL. Для валидации экспрессии антигенпрезентирующего пептида MHC класса I в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса I.
Функциональную активность эффекта сконструированных эритроидных клеток (PR1-HLA-A2-GPA, 4-1BBL) анализируют по их способности стимулировать исходную активацию и пролиферацию первичных CD8+ T-клеток.
Способы
Получение лентивирусного вектора
Конструируют гены слитого белка PR1-HLA-A2-GPA и 4-1BBL. Гены, кодирующие белок, клонируют в участок множественного клонирования лентивирусного вектора pCDH с промоторной последовательностью MSCV от System Biosciences таким образом, что один вектор содержит гены обоих экзогенных белков. Лентивирус получают в клетках 293T посредством трансфекции клеток с использованием лентивирусного вектора pPACKH1 (System Biosciences) и pCDH, содержащего гены PR1-HLA-A2-GPA и 4-1BBL. Клетки высевают в свежую среду для культивирования. Вирусный супернатант собирают через 48 часов после замены среды посредством центрифугирования при 1500 об./мин. в течение 5 минут. супернатант собирают и замораживают в аликвотах при -80°C.
Трансдукция эритроидных клеток-предшественников
Экспансию и дифференцировку эритроидных клеток осуществляют по примеру 5 с использованием описанных выше лентивирусных векторов. Эритроидные клетки-предшественники трансдуцируют на стадии 1 способа культивирования. Эритроидные клетки в среде для культивирования объединяют с лентивирусным супернатантом и полибреном. Инфицирования достигают посредством центрифужной инокуляции, центрифугируя планшет при 2000 об./мин. в течение 90 минут при комнатной температуре. После центрифужной инокуляции клетки инкубируют при 37°C в течение ночи
Связывание антител
Для валидации экспрессии слитого белка PR1-HLA-A2-GPA в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против PR1, как описано в примере 5. Для валидации экспрессии антигенпрезентирующего полипептида MHC класса I в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса I, также как описано в примере 5. Для валидации экспрессии 4-1BBL в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против 4-1BBL (R&D Systems). Связывание любого из антител измеряют посредством проточной цитометрии по флуоресценции APC или PE. Гейт устанавливают с учетом окрашенных нетрансдуцированных клеток.
Функциональные валидационные анализы
Эритроидные клетки, генетически сконструированные для коэкспрессии слитого белка PR1-HLA-A2-GPA и костимуляторного полипептида 4-1BBL, тестируют на их способность стимулировать исходную активацию и пролиферацию первичных CD8+ T-клеток. T-клетки стимулируют сконструированными эритроидными клетками и оценивают следующие параметры: (1) скорость роста T-клеток, стимулированных aAPC, определяемая посредством стандартного анализа включения тимидина, с помощью чего определяют общее количество ДНК, синтезируемой в смешанной культуре; (2) индуцирование пролиферации и деления CD4+ T-клеток; (3) жизнеспособность CD8+ T-клеток, стимулированных различными aAPC во время культивирования по флуоресцентному окрашиванию аннексином V и йодидом пропидия; (4) экспрессия Bcl-xL и ИЛ-2, двух генов, участвующих в выживании и пролиферации T-клеток, соответственно, с использованием количественной RT-ПЦР в реальном времени для определения уровней кодирования мРНК Bcl-xL и ИЛ-2 в равновесном состоянии.
Продукция цитокинов
Цитокины являются важными эффекторными молекулами и дают представление о дифференцировке T-клеток. Количественно анализируют способность эритроидных клеток, сконструированных для коэкспрессии слитого белка PR1-HLA-A2-GPA и костимуляторного пептида 4-1BBL, индуцировать некоторые цитокины CD8+ T-клеток, например, ИЛ-2 (ключевой фактор роста T-клеток для экспансии ex vivo, и способность клеток индуцировать продукцию ИЛ-2 хорошо коррелирует с долговременным потенциалом к росту); ИЛ-4 (маркер дифференцировки TH2); и ИЛ-10 (иммуносупрессорный цитокин, который может являться суррогатом для разрастания регуляторных T-клеток). Другие цитокины включают, в качестве неограничивающих примеров, TGF-β (по той же причине, что и ИЛ-10); ИФНγ (маркер дифференцировки TH1 и важный эффекторный цитокин); и ФНОα (важный эффекторный цитокин). Количественный анализ можно осуществлять способом ELISPOT (анализ иммуноферментных пятен), с помощью которого определяют T-клетки, секретирующие указанный цитокин (например, интерферон-гамма [ИФНγ]) в ответ на стимуляцию антигеном. T-клетки культивируют с антигенпрезентирующими клетками в лунках, покрытых антителами против ИФНγ. Секретируемый ИФНγ захватывают с помощью антитела из покрытия, а затем определяют с помощью второго антитела, связанного с хромогенным субстратом. Таким образом, локально секретируемые молекулы цитокина образуют пятна, при этом каждое пятно соответствует одной ИФНγ-секретирующей клетке. Количество пятен позволяет определять долю ИФНγ-секретирующих клеток, специфических для указанного антигена, в анализируемом образце. Анализ ELISPOT также описан для детекции фактора некроза опухоли альфа, интерлейкина-4 (ИЛ-4), ИЛ-5, ИЛ-6, ИЛ-10, ИЛ-12, гранулоцитарно-макрофагального колониестимулирующего фактора.
Пример 7. Активность безъядерных эритроидных клеток, сконструированных для коэкспрессии слитого белка PR1-HLA-A2-GPA и костимуляторного полипептида, в модели острого миелогенного лейкоза (AML) на мышах in vivo
Показано, что пептид PR1 является антигеном лейкоза человека. Показано, что PR1-специфические цитотоксические T-лимфоциты (CTL), полученные in vitro из здоровых доноров, лизируют P3-экспрессирующие клетки AML пациентов. Кроме того, показано, что адоптивный перенос PR1-CTL, полученных in vitro, ассоциирован со снижением клеток AML у мышей NOD/SCID (Molldrem et al., Cancer Res. 1999; 59:2675-2681; Molldrem et al., Nat Med. 2000; 6:1018-1023; Rezvani et al., Blood. 2003; 102:2892-2900; содержание каждой из которых включено в настоящее описание в качестве ссылки в полном объеме).
Хорошо известных мышей NOD/SCID используют в качестве модели для определения того, содержит ли аспират костного мозга мышей, которым вводили PR1-CTL, больше бластов AML в гиперцеллюлярном костном мозге по сравнению с мышами, которым вводили PR1-CTL и безъядерные эритроидные клетки, сконструированные для коэкспрессии слитого белка PR1-HLA-A2-GPA и 4-1BBL. Модель также используют для определения того, являются ли уровни PR1-CTL более высокими у мышей, которым вводили безъядерные эритроидные клетки, сконструированные для коэкспрессии слитого белка PR1-HLA-A2-GPA и 4-1BBL, чем у мышей, которым не вводили безъядерные эритроидные клетки. Модель также используют для определения того, поддерживают ли мыши, которым вводили безъядерные эритроидные клетки, сконструированные для коэкспрессии слитого белка PR1-HLA-A2-GPA и 4-1BBL, эффекторный фенотип CD45RA- CD28+ по сравнению с мышами, которым не вводили безъядерные эритроидные клетки.
Получение PR1-CTL
PR1-CTL подвергают экспансии в смешанной культуре описанным ранее способом с некоторой модификацией (Molldrem et al., Blood. 1996; 88:2450-2457, содержание которой включено в настоящее описание в качестве ссылки в полном объеме). Аутологичные дендритные клетки (DC) получают из HLA-A2.1+ здорового донора. В кратком изложении, адгезивные моноциты нормального донора стимулируют в течение 7 дней с использованием комбинации цитокинов гранулоцитарно-макрофагального колониестимулирующего фактора (ГМ-КСФ) (500 МЕ/мл) и интерферона α (ИФНα). Собирают активированные DC и анализируют долю клеток посредством FACS по экспрессии CD80 и CD14. В присутствии ИЛ-2 (20 МЕ/мл) в DC вводят пептиды PR1, PR2 или pp65. PR2 (RLFPDFFTRV (SEQ ID NO: 720)) является другим HLA-A2-рестриктированным пептидом, полученным из протеиназы 3, но PR2-CTL не могут уничтожать лейкозные клетки (Molldrem et al., Blood. 1996). Мононуклеарные клетки периферической крови (PMBC) еженедельно стимулируют аутологичными DC, в которые вводили пептиды, в течение 3-4 недель. Собирают долю PR1-CTL и тестируют на специфический лизис с использованием анализа цитотоксичности CTL, использованного ранее (Molldrem et al., Blood. 1996, содержание которой включено в настоящее описание в качестве ссылки в полном объеме). Остальные CTL из смешанной культуры очищают с помощью сортера с использованием антител для одновременного истощения CD4+ клеток, B-клеток и естественных киллеров (NK).
Модель ксенотрансплантата AML на мышах NOD/SCID
Мышей NOD/SCID-HLA-A2.1 используют для приживления клеток AML. Получают образцы костного мозга человека с AML и клетки AML от пациентов вводят внутривенно облученным (200 сГр) мышам NOD/SCID. Образцы костного мозга с AML выбирают с учетом способности успешно приживляться в костном мозге в различных дозах через 2 недели после переноса. Небольшое количество PR1-специфических T-клеток адоптивно переносят мыши NOD-SCID с приживленным AML в отдельности или вместе с безъядерными эритроидными клетками, сконструированными для коэкспрессии слитого белка PR1-HLA-A2-GPA и 4-1BBL. Животных умерщвляют через 2 недели после переноса и ткани собирают для анализа посредством проточной цитометрии (FACS) и иммуногистохимии (IHC). Ab против CD45 человека и Ab против CD45.2 мыши используют для идентификации клеток человеческого происхождения. Дифференциальный подсчет клеток осуществляют на цитоспиновых препаратах и мазках, полученных из костного мозга. Фиксированные формалином, погруженные в парафин срезы собранных тканей органов окрашивают гематоксилином и эозином.
CD45RA- CD28+ эффекторный фенотип
Для валидации CD45RA-CD28+ эффекторного фенотипа используют APC-меченое или PE-меченое антитело против CD45RA (Biolegend) и APC-меченое или PE-меченое антитело против CD28 (Biolegend). Связывание антитела измеряют посредством проточной цитометрии по флуоресценции APC или PE. Гейт устанавливают с учетом окрашенных нетрансдуцированных клеток.
В вариантах осуществления аспират костного мозга мышей, которым вводили PR1-CTL, содержит больше бластов AML в гиперцеллюлярном костном мозге по сравнению с мышами, которым вводили PR1-CTL и безъядерные эритроидные клетки, сконструированные для коэкспрессии слитого белка PR1-HLA-A2-GPA и 4-1BBL. В других вариантах осуществления уровни PR1-CTL выше у мышей, которым вводили безъядерные эритроидные клетки, сконструированные для коэкспрессии слитого белка PR1-HLA-A2-GPA и 4-1BBL, чем у мышей, которым не вводили безъядерные эритроидные клетки. В других вариантах осуществления мыши, которым вводили безъядерные эритроидные клетки, сконструированные для коэкспрессии слитого белка PR1-HLA-A2-GPA и 4-1BBL, поддерживают CD45RA- CD28+ эффекторный фенотип по сравнению с мышами, которым не вводили безъядерные эритроидные клетки.
Пример 8. Получение и валидация in vitro эритроидных клеток, генетически сконструированных для коэкспрессии слитого белка gp100-H-2Db-GPA и костимуляторного полипептида
Результаты
Эритроидные клетки трансдуцируют для экспрессии слитого белка, содержащего gp100, меланомный антиген, слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I H-2Db, слитым с трансмембранным доменом GPA (gp100-H-2Db-GPA). Эритроидные клетки также трансдуцируют для дополнительной экспрессии экзогенного костимуляторного пептида 4-1BBL. Культивирование и трансдукцию клеток осуществляют, как описано в разделе "Способы" ниже, для получения эритроидных клеток, экспрессирующих gp100, презентируемый MHC класса I на поверхности, заякоренным с помощью трансмембранного домена GPA.
Для валидации экспрессии соответствующих пептидов в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против gp100 или против 41-BBL с экзогенными пептидами gp100 и 4-1BBL. Для валидации экспрессии антигенпрезентирующего пептида MHC класса I в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса I.
Функциональную активность эффекта сконструированных эритроидных клеток (gp100-H-2Db-GPA, 4-1BBL) анализируют по их способности стимулировать исходную активацию и пролиферацию первичных CD8+ T-клеток.
Способы
Получение лентивирусного вектора
Конструируют гены слитого белка gp100-H-2Db-GPA и 4-1BBL. Гены, кодирующие белки, клонируют в участок множественного клонирования лентивирусного вектора pCDH с промоторной последовательностью MSCV от System Biosciences таким образом, что один вектор содержит гены для обоих экзогенных белков. Лентивирус получают в клетках 293T посредством трансфекции клеток с использованием лентивирусного вектора pPACKH1 (System Biosciences) и pCDH, содержащего гены gp100-H-2Db и 4-1BBL. Клетки высевают в свежую среду для культивирования. Вирусный супернатант собирают через 48 часов после замены среды посредством центрифугирования при 1500 об./мин. в течение 5 минут. Супернатант собирают и замораживают в аликвотах при -80°C.
Трансдукция эритроидных клеток-предшественников
Экспансию и дифференцировку эритроидных клеток осуществляют по примеру 5 с использованием описанного выше лентивирусного вектора. Эритроидные клетки-предшественники трансдуцируют на стадии 1 способа культивирования. Эритроидные клетки в среде для культивирования объединяют с лентивирусным супернатантом и полибреном. Инфицирования достигают посредством центрифужной инокуляции, центрифугируя планшет при 2000 об./мин. в течение 90 минут при комнатной температуре. После центрифужной инокуляции клетки инкубируют при 37°C в течение ночи.
Связывание антител
Для валидации экспрессии слитого белка gp100-H-2Db-GPA в сконструированных эритроидных клетках используют связывание биотинилированного антитела против gp100 (например, TB-M505-M, MBL International Corp.). Связывание биотинилированного антитела определяют с помощью авидиновых конъюгатов при мечении клеточной поверхности и проточной цитометрии/активируемой флуоресценцией сортировке клеток (FACS). Для валидации экспрессии антигенпрезентирующего пептида MHC класса I в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса I (например, PE-конъюгированного моноклонального антитела против MHC класса I (H-2Db) (28-14-8), Thermofisher Scientific). Для валидации экспрессии 4-1BBL в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против 4-1BBL (R&D Systems). Связывание любого из антител измеряют посредством проточной цитометрии по флуоресценции APC или PE. Гейт устанавливают с учетом окрашенных нетрансдуцированных клеток.
Функциональные валидационные анализы
Эритроидные клетки, генетически сконструированные для коэкспрессии слитого белка gp100-H-2Db-GPA и костимуляторного полипептида 4-1BBL, тестируют на их способность стимулировать исходную активацию и пролиферацию первичных CD8+ T-клеток. T-клетки стимулируют сконструированными эритроидными клетками и оценивают следующие параметры: (1) скорость роста T-клеток, стимулированных aAPC, определяемая с помощью стандартного анализа включения тимидина, с помощью которого получают общее количество ДНК, синтезируемой в смешанной культуре; (2) индуцирование пролиферации и деления CD4+ T-клеток; (3) жизнеспособность CD8+ T-клеток, стимулированных различными aAPC во время культивирования, при флуоресцентном окрашивании аннексином V и йодидом пропидия; (4) экспрессия Bcl-xL и ИЛ-2, двух генов, участвующих в выживании и пролиферации T-клеток, соответственно, при использовании количественной RT-ПЦР в реальном времени для определения уровней кодирования мРНК Bcl-xL и ИЛ-2 в равновесном состоянии.
Продукция цитокинов
Количественно анализируют способность эритроидных клеток, сконструированных для коэкспрессии слитого белка gp100-H-2Db-GPA и костимуляторного пептида 4-1BBL, индуцировать некоторые цитокины CD8+ T-клеток, например, ИЛ-2 (ключевой фактор роста T-клеток для экспансии ex vivo, и способность клеток индуцировать ИЛ-2 хорошо коррелирует с долговременным потенциалом к росту); ИЛ-4 (маркер дифференцировки TH2); и ИЛ-10 (иммуносупрессорный цитокин, который может являться суррогатом для разрастания регуляторных T-клеток). Другие цитокины включают, в качестве неограничивающих примеров, TGF-β (по той же причине, что и ИЛ-10), ИФНγ (маркер дифференцировки TH1 и важный эффекторный цитокин) и ФНОα (важный эффекторный цитокин). Количественный анализ можно осуществлять способом ELISPOT (анализ иммуноферментных пятен), с помощью которого определяют T-клетки, секретирующие указанный цитокин (например, интерферон гамма [ИФНγ]) в ответ на стимуляцию антигеном. T-клетки культивируют с антигенпрезентирующими клетками в лунках, покрытых антителами против ИФНγ. Секретируемый ИФНγ захватывают с помощью антитела покрытия, а затем определяют с помощью второго антитела, связанного с хромогенным субстратом. Таким образом, локально секретируемые молекулы цитокинов образуют пятна, при этом каждое пятно соответствует одной ИФНγ-секретирующей клетке. Количество пятен позволяет определять долю ИФНγ-секретирующих клеток, специфических для указанного антигена, в анализируемом образце. Анализ ELISPOT также описан для детекции фактора некроза опухоли альфа, интерлейкина-4 (ИЛ-4), ИЛ-5, ИЛ-6, ИЛ-10, ИЛ-12, гранулоцитарно-макрофагального колониестимулирующего фактора.
Пример 9. Активность безъядерных эритроидных клеток, сконструированных для коэкспрессии слитого белка gp100-H-2Db-GPA и костимуляторного полипептида, в модели меланомы B-16 на мышах
Субпопуляцию пациентов с метастазирующей меланомой можно успешно лечить посредством введения рекомбинантного интерлейкина-2 (rИЛ-2), иногда вводимого вместе с аутологичными реактивными в отношении меланомы лимфоцитами, подвергнутыми экспансии ex vivo (Rosenberg, 1997; Rosenberg, 1999). В последнее время в ряде разных лабораторий использовали эти противоопухолевые лимфоциты для клонирования меланома-ассоциированных антигенов, включающих, как правило, немутантные антигены дифференцировки меланоцитов (MDA), группу, включающую gp100 (Overwijk and Restifo, Curr Protoc Immunol. 2001 may; CHAPTER: Unit-20.1, содержание которой включено в настоящее описание в качестве ссылки в полном объеме).
Подкожную модель широко используют для оценки терапии во многих моделях опухолей, включая меланому B16. После подкожной инъекции B16 за 5-10 дней будут образовывать пальпируемую опухоль, которая будет расти до 1×1×1 см за 14-21 день. Если позволить ей расти еще больше, опухоль зачастую некротизируется в центре и начинает изъязвляться или кровоточить; целесообразно умерщвлять мышей до достижения этого состояния. Типичная используемая доза составляет 1×105 клеток/мышь, что является 1,5-2-кратной минимальной туморогенной дозой для нормальных мышей C57BL/6.
Модель меланомы B16 на мышах используют в качестве модели для определения того, могут ли безъядерные эритроидные клетки, сконструированные для коэкспрессии слитого белка gp100-H-2Db-GPA и костимуляторного пептида 4-1BBL, устранять клетки меланомы B16 у мыши.
Способы получения клеток B-16 и их инокуляции мышам описаны в Overwijk and Restifo (Curr Protoc Immunol. 2001 мая; CHAPTER: Unit-20.1, включенной в качестве ссылки в настоящее описание в полном объеме). Введение сконструированных эритроидных клеток начинают, когда опухоли становятся пальпируемыми. Клетки составляют в PBS или другом буфере.
В вариантах осуществления введение сконструированных безъядерных эритроидных клеток будет приводить к одному или обоим из ингибирования приживления опухолевых клеток или уменьшения размера опухоли по сравнению с немодифицированными контрольными клетками.
Пример 10. Эритроидные клетки, сконструированные для презентирования MHC класса I (овальбумина) и 4-1BBL, активируют овальбумин-специфические T-клетки in vitro
Эритроидные клетки мыши конъюгировали с MHC класса I, презентирующим пептид овальбумина, и 4-1BBL с использованием клик-химии (клик-химия для функционализации эритроидных клеток описана в международной заявке № PCT/US 2018/000042, по которой испрашивается приоритет по временной патентной заявке США №62/460589, поданной 17 февраля 2017 года, и временной патентной заявке США №62/542142, поданной 8 июля 2017 года, включенных в настоящее описание в качестве ссылки в полном объеме). В кратком изложении, периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и метили 0,04 мМ 6'-азидо-NHS-сложным эфиром а PBS, pH 8, в течение 30 мин при комнатной температуре. Азидо-меченые mRCT инкубировали с 40 мкМ m4-1BBL-DBCO-тиолинкера при комнатной температуре в течение 1 ч. и дополнительно инкубировали при 4°C в течение ночи. mRCT-m4-1BBL подвергали клик-реакции с биотином посредством инкубации с 1 мкМ водорастворимого DBCO-биотина при комнатной температуре в течение 1 ч. с последующей инкубацией с нейтравидином при молярном соотношении 1:1 биотина и нейтравидина. Затем связанные с нейтравидином клетки инкубировали с биотинилированным мономером H-2Kb SIINFEKL (SEQ ID NO: 721) при молярном соотношении 1:1 биотина и мономера в течение 1 ч. при комнатной температуре.
CD8+ T-клетки выделяли из вторичных лимфоидных органов трансгенных мышей OT1 с использованием набора для отрицательной селекции от Miltenyi и метили 1 мкМ CFSE. 2E5 меченых CFSE CD8+ T-клеток OT1 высевали в каждую лунку 96-луночного планшета. Различные количества (3E6, 1E6, 3,3E5 или 1,1E5 клеток) mRCT, mRCT-4-1BBL, mRCT-MHC(ova) или mRCT-MHC(ova)+4-1BBL высевали в среды cRPMI в лунки, содержащие CD8+ T-клетки OT1, и инкубировали в течение двух дней при 37°C. Супернатант культуры собирали для измерения концентрации ИЛ-2 и ИФНγ посредством ELISA на цитокины. Клетки промывали и окрашивали антителом против CD8, красителем LIVE/DEAD и антителом против CD44 для количественного анализа экспансии и активации T-клеток.
Как показано на фиг. 2, эритроидные клетки мыши, презентирующие MHC класса I (овальбумин) и 4-1BBL на поверхности клетки, или эритроидные клетки мыши, презентирующие MHC класса I (овальбумин) в отдельности (RCT-aAPC (ova)), мощно активируют овальбумин-специфические T-клетки in vitro. Эти результаты свидетельствуют о способности мощно и селективно вызывать экспансию и активацию антигенспецифической T-клетки при использовании сконструированных безъядерных клеток, как представлено в настоящем описании.
В исследованиях, схожих с представленными выше, эритроидные клетки человека трансдуцировали для коэкспрессии овальбумина и 4-1BBL, а не конъюгировали с использованием клик-химии. В этих экспериментах CD34+ клетки здорового человека-донора подвергали экспансии и трансдукции с использованием концентрированного лентивируса HA-GPA, GPA-m4-1BBL или b2ML-OVAH2Kb-GPA при MOI 20. hRCT-MHC(ova)+4-1BBL получали посредством двойной (одновременной) трансдукции с использованием концентрированного лентивируса GPA-m4-1BBL и b2ML-OVAH2Kb-GPA при MOI 20, соответственно. hRCT собирали в день созревания 9 и фильтровали через лейкоцитарный фильтр PAL для обогащения безъядерных клеток. Уровень экспрессии и количество копий определяли посредством окрашивания с использованием связанного с антителом против m4-1BBL и против SIINFEKL (SEQ ID NO: 721) H2Kb и калибровали по стандартным кривым для частиц Bangs.
CD8+ T-клетки выделяли из вторичных лимфоидных органов трансгенных мышей OT1 с использованием набора для отрицательной селекции от Miltenyi и метили 1 мкМ CFSE. 3E5 меченых CFSE CD8+ T-клеток OT1 высевали в каждую лунку 96-луночного планшета. Различные количества (3E6, 6E5, 3E5 или 1,5E5 клеток) hRCT-HA-GPA, hRCT-m4-1BBL, hRCT-MHC(ova) или hRCT- MHC(ova)+4-1BBL высевали в лунки, содержащие CD8+ T-клетки OT1. Количество клеток hRCT-m4-1BBL и hRCT-MHC(ova) в каждой лунке корректировали таким образом, чтобы количество молекул m4-1BBL и MHC(ova) соответствовало общему количеству молекул в лунках, соответствующих hRCT- MHC(ova)+m4-1BBL. Клетки hRCT и OT1 инкубировали при 37°C в течение 3 дней. Супернатант культуры собирали для измерения концентрации ИЛ-2 и ИФНγ посредством ELISA на цитокины. Клетки промывали и окрашивали с помощью антитела против CD8, красителя LIVE/DEAD и антитела против CD44 для количественного анализа экспансии и активации T-клеток. Результаты этого исследования свидетельствуют о том, что эритроидные клетки человека, трансдуцированные для коэкспрессии овальбумина и m4-1BBL, мощно активируют овальбумин-специфические T-клетки in vitro, демонстрирующие высокую экспрессию CD44, что схоже с результатами, полученными с использованием mRCT, сконструированных с помощью клик-химии (описанных выше и показанными на фиг. 2).
Пример 11. Овальбумин-специфические T-клетки, подвергнутые экспансии и активации с помощью эритроидных клеток, прещентирующих MHC класса I (овальбумин) и 4-1BBL, селективно уничтожают овальбумин-экспрессирующие опухолевые клетки in vitro
Эритроидные клетки мыши конъюгировали с MHC класса I, презентирующим пептид овальбумина, и 4-1BBL с использованием клик-химии (клик-химия для функционализации эритроидных клеток описана во временной патентной заявке США №62/460589, поданной 17 февраля 2017 года, и временной патентной заявке США №62/542142, поданной 8 июля 2017 года, включенных в настоящее описание в качестве ссылки в полном объеме). В кратком изложении, периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и метили 0,04 мМ 6'-азидо-NHS-сложным эфиром в PBS, pH 8, в течение 30 мин при комнатной температуре. Азидо-меченые mRCT инкубировали с 40 мкМ m4-1BBL-DBCO-тиолинкера при комнатной температуре в течение 1 ч. и дополнительно инкубировали при 4°C в течение ночи. mRCT-m4-1BBL подвергали клик-реакции с биотином посредством инкубации с 1 мкМ водорастворимого DBCO-биотина при комнатной температуре в течение 1 ч. с последующей инкубацией с нейтравидином при молярном соотношении 1:1 биотина и нейтравидина. Затем связанные с нейтравидином клетки инкубировали с биотинилированным мономером H-2Kb SIINFEKL (SEQ ID NO: 721) при молярном соотношении 1:1 биотина и мономера в течение 1 ч. при комнатной температуре.
CD8+ T-клетки выделяли из вторичных лимфоидных органов трансгенных мышей OT1 с использованием набора для отрицательной селекции от Miltenyi и метили 1 мкМ CFSE. 1,2E6 меченых CFSE CD8+ T-клеток OT1 культивировали с 1,2E7 aAPC (mRCT-4-1BBL H2Kb OVA) в каждой лунке 24-луночного планшета. Клетки OT1 собирали после трех дней инкубации и обрабатывали буфером ACK для лизиса mRCT. Затем для тестирования активности клеток OT1 в отношении опухолевых клеток 1E4 опухолевых клеток, меченых дальним красным красителем CellTrace, а именно родительских опухолевых клеток EL4 или экспрессирующих овальбумин опухолевых клеток EG7.OVA (каждые из которых представляют собой клетки-мишени), высевали в каждую лунку 96-луночных планшетов с U-образным дном. Клетки OT1 (эффекторные клетки) добавляли в лунки при соотношении эффектора и мишени (E:T) 10:1, 5:1, 2:1, 1:1 или 0:1. После 22 часов инкубации клетки окрашивали красителем LIVE/DEAD и фиксировали 2% параформальдегидом для количественного анализа живых клеток-мишеней в каждой лунке.
Результаты этого эксперимента показаны на фиг. 3. Примечательно, что овальбумин-специфические T-клетки (T-клетки OT1), подвергнутые экспансии и активации эритроидными клетками мыши, презентирующими MHC класса I (овальбумин) и 4-1BBL, селективно уничтожали овальбумин-экспрессирующие опухолевые клетки или клетки EG7.OVA, в то время как родительские клетки, не экспрессирующие овальбумин (клетки EL4), не подвергались атаке и уничтожению. Способность приводить к значительной экспансии и активировать конкретную популяцию опухолеспецифических T-клеток для уничтожения опухолей in vivo имеет сходство с подходами CAR-T, в которых вводят популяцию опухолеспецифических T-клеток, которые могут подвергаться экспансии в организме пациента, иногда неконтролируемо. Значительным преимуществом настоящего изобретения является то, что, контролируя дозу сконструированных безъядерных клеток, представленных в настоящем описании, можно эффективнее контролировать экспансию опухолеспецифических T-клеток и, в конечном итоге, безопасность и эффективность терапии.
Пример 12. Эритроидные клетки, сконструированные для презентирования MHC класса I (овальбумина) и 4-1BBL, активируют овальбумин-специфические T-клетки, мигрирующие в лимфоузлы, in vivo
Эритроидные клетки мыши конъюгировали с MHC класса I, презентирующим пептида овальбумин, и 4-1BBL с использованием клик-химии (клик-химия для функционализации эритроидных клеток описана во временной патентной заявке США №62/460589, поданной 17 февраля 2017 года, и временной патентной заявке США №62/542142, поданной 8 июля 2017 года, включенных в настоящее описание в качестве ссылки в полном объеме). В кратком изложении, периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и метили 0,04 мМ 6'-азидо-NHS-сложного эфира в PBS, pH 8, в течение 30 мин при комнатной температуре. Азидо-меченые mRCT инкубировали с 40 мкМ m4-1BBL-DBCO-тиолинкера при комнатной температуре в течение 1 ч. и дополнительно инкубировали при 4°C в течение ночи. mRCT-m4-1BBL подвергали клик-реакции с биотином посредством инкубации с 1 мкМ водорастворимого DBCO-биотина при комнатной температуре в течение 1 ч. с последующей инкубацией с нейтравидином при молярном соотношении 1:1 биотина и нейтравидина. Затем связанные с нейтравидином клетки инкубировали с биотинилированным мономером H-2Kb SIINFEKL (SEQ ID NO: 721) при молярном соотношении 1:1 биотина и мономера в течение 1 ч. при комнатной температуре.
CD8+ T-клетки выделяли из вторичных лимфоидных органов трансгенных мышей RAG2-/-OT1 с использованием набора для отрицательной селекции от Miltenyi и метили флуоресцентным красителем (10 мкМ CFSE). 1,8E6 клеток OT1 инъецировали внутривенно мышам C57BL/6 в день -1. В день 0 мышам инъецировали внутривенно 1E8 aAPC (mRCT-4-1BBL или mRCT-4-1BBL H2Kb OVA). В день 4 мышей умерщвляли и окрашивали суспензии отдельных клеток из селезенки и лимфоузлов с помощью NIR Zombie (APC 41BB), Pacific blue (CD44), BV650 (CD8) и BV785 (CD62L) и анализировали посредством проточной цитометрии. Пролиферацию T-клеток OT1 подвергали мониторингу по последующему ослаблению сигнала флуоресцентного красителя в лимфоузлах или селезенке. На фигуре 4A показано схематическое изображение дизайна эксперимента. Результаты эксперимента показаны на фигурах 4B и 4C, где фигура 4B является схемой репрезентативных данных, где показано, что mRCT-4-1BBL OVA специфически приводят к экспансии и активации T-клеток OT1, в то время как mRCT-4-1BBL без MHC класса I, презентирующего пептид овальбумина на поверхности клетки, не приводят к экспансии и активации T-клеток OT1.
Результаты этого эксперимента in vivo на мышах, как представлено на фигуре 4C, показали, что mRCT-4-1BBL H2Kb OVA специфически приводят к экспансии и активации T-клеток OT1, о чем свидетельствует повышенная экспрессия CD44. Кроме того, обнаружено, что большинство активируемых T-клеток OT1 демонстрируют фенотип центральной памяти, которые, как обнаруживают, являются ключевой популяцией, регулирующей эффективность терапевтических средств на основе T-клеток. Результаты также свидетельствовали о том, что эти T-клетки OT1 мигрируют в лимфоузлы, где, как ожидают, они подвергнутся дальнейшей экспансии и активации, что подтверждает их потенциал в отношении эффективной мобилизации в организме, и в опухоль для поддержания устойчивого противоопухолевого ответа. В отличие от этого, mRCT-4-1BBL без MHC класса I, презентирующего пептид овальбумина на поверхности клетки, не приводят к экспансии или активации T-клеток OT1, что, таким образом, свидетельствует о том, что mRCT-aAPC имитируют функционирование антигенпрезентирующих клеток in vivo.
Пример 13. Получение и валидация in vitro эритроидных клеток, генетически сконструированных для коэкспрессии слитого белка gp350-HLA-A2-GPA и костимуляторного полипептида
Результаты
Эритроидные клетки трансдуцируют для экспрессии слитого белка, содержащего иммуногенный пептид из кодируемого вирусом Эпштейна-Барр гликопротеина 350 (gp350), являющегося рестриктированным по (HLA)-A2, слитый с экзогенным антигенпрезентирующим полипептидом, MHC класса I HLA-A2, слитым с трансмембранным доменом GPA (gp350-HLA-A2-GPA). Примером используемого иммуногенного пептида gp350 является VLQWASLAV (SEQ ID NO: 698). Эритроидные клетки также трансдуцируют для дополнительной экспрессии экзогенного костимуляторного пептида 4-1BBL. Культивирование и трансдукцию клеток осуществляют, как описано в разделе "Способы" ниже, для получения эритроидных клеток, экспрессирующих gp350, презентируемый MHC класса I на поверхности, заякоренным с помощью трансмембранного домена GPA.
Для валидации экспрессии соответствующих пептидов в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против gp350 или против 4-1BBL с экзогенными пептидами gp350 и 4-1BBL. Для валидации экспрессии антигенпрезентирующего пептида MHC класса I в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса I.
Функциональную активность эффекта сконструированных эритроидных клеток (gp350-HLA-A2-GPA, 4-1BBL) анализируют по их способности стимулировать исходную активацию и пролиферацию первичных CD8+ T-клеток.
Способы
Получение лентивирусного вектора
Конструируют гены слитого белка gp350-HLA-A2-GPA и 4-1BBL. Гены, кодирующие белки, клонируют в участок множественного клонирования лентивирусного вектора pCDH с промоторной последовательностью MSCV от System Biosciences таким образом, что один вектор содержит гены для обоих экзогенных белков. Лентивирус получают в клетках 293T посредством трансфекции клеток с использованием лентивирусного вектора pPACKH1 (System Biosciences) и pCDH, содержащего гены gp350-HLA-A2-GPA и 4-1BBL. Клетки высевают в свежую среду для культивирования. Вирусный супернатант собирают через 48 часов после замены среды посредством центрифугирования при 1500 об./мин. в течение 5 минут. Супернатант собирают и замораживают в аликвотах при -80°C.
Трансдукция эритроидных клеток-предшественников
Экспансию и дифференцировку эритроидных клеток осуществляют по примеру 5 и трансдуцируют с использованием описанных выше лентивирусных векторов. Эритроидные клетки-предшественники трансдуцируют на стадии 1 способа культивирования. Эритроидные клетки в среде для культивирования объединяют с лентивирусным супернатантом и полибреном. Инфицирования достигают посредством центрифужной инокуляции, центрифугируя планшет при 2000 об./мин. в течение 90 минут при комнатной температуре. После центрифужной инокуляции клетки инкубируют 37°C в течение ночи.
Связывание антител
Для валидации экспрессии слитого белка gp350-HLA-A2-GPA в сконструированных эритроидных клеток используют связывание APC-меченого или PE-меченого антитела против gp350. Связывание антитела измеряют посредством проточной цитометрии по флуоресценции APC или PE. Гейт устанавливают с учетом окрашенных нетрансдуцированных клеток. Для валидации экспрессии антигенпрезентирующего полипептида MHC класса I в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против MHC класса I, как описано в примере 5. Для валидации экспрессии 4-1BBL в сконструированных эритроидных клетках используют связывание APC-меченого или PE-меченого антитела против 4-1BBL (R&D Systems). Связывание любого из антител измеряют посредством проточной цитометрии по флуоресценции APC или PE. Гейт устанавливают с учетом окрашенных нетрансдуцированных клеток.
Функциональные валидационные анализы
Эритроидные клетки, генетически сконструированные для коэкспрессии слитого белка gp350-HLA-A2-GPA и костимуляторного полипептида 4-1BBL, тестируют на их способность стимулировать исходную активацию и пролиферацию первичных CD8+ T-клеток. T-клетки стимулируют с помощью сконструированных эритроидных клеток и оценивают следующие параметры: (1) скорость роста T-клеток, стимулированных aAPC, определяемая с использованием стандартного анализа включения тимидина, с помощью которого получают общее количество ДНК, синтезируемой в смешанной культуре; (2) индуцирование пролиферации и деления CD4+ T-клеток; (3) жизнеспособность CD8+ T-клеток, стимулируемых различными aAPC во время культивирования, при флуоресцентном окрашивании аннексином V и йодидом пропидия; (4) экспрессия Bcl-xL и ИЛ-2, двух генов, участвующих в выживании и пролиферации T-клеток, соответственно, с использованием количественной RT-ПЦР в реальном времени для определения уровней кодирования мРНК Bcl-xL и ИЛ-2 в равновесном состоянии.
Продукция цитокинов
Цитокины являются важными эффекторными молекулами и дают представление о дифференцировке T-клеток. Количественно анализируют способность эритроидных клеток, сконструированных для коэкспрессии слитого белка gp350-HLA-A2-GPA и костимуляторного пептида 4-1BBL, индуцировать некоторые цитокины CD8+ T-клеток, например, ИЛ-2 (ключевой фактор роста T-клеток для экспансии ex vivo, и способность клеток индуцировать ИЛ-2 хорошо коррелирует с долговременным потенциалом к росту); ИЛ-4 (маркер дифференцировки TH2); и ИЛ-10 (иммуносупрессорный цитокин, который может являться суррогатом разрастания регуляторных T-клеток). Другие цитокины включают, в качестве неограничивающих примеров, TGF-β (по той же причине, что и ИЛ-10), ИФНγ (маркер дифференцировки TH1 и важный эффекторный цитокин) и ФНОα (важный эффекторный цитокин). Количественный анализ можно осуществлять способом ELISPOT (анализ иммуноферментных пятен), с помощью которого определяют T-клетки, секретирующие указанный цитокин (например, интерферон гамма [ИФНγ]) в ответ на стимуляцию антигеном. T-клетки культивируют с антигенпрезентирующими клетками в лунках, покрытых антителами против ИФНγ. Секретируемый ИФНγ захватывают с помощью антитела покрытия, а затем определяют с помощью второго антитела, связанного с хромогенным субстратом. Таким образом, локально секретируемые молекулы цитокинов образуют пятна, при этом каждое пятно соответствует одной ИФНγ-секретирующей клетке. Количество пятен позволяет определять долю ИФНγ-секретирующих клеток, специфических для указанного антигена в анализируемом образце. Анализ ELISPOT также описан для детекции фактора некроза опухоли альфа, интерлейкина-4 (ИЛ-4), ИЛ-5, ИЛ-6, ИЛ-10, ИЛ-12, гранулоцитарно-макрофагального колониестимулирующего фактора.
Пример 14. Активность безъядерных эритроидных клеток, сконструированных для коэкспрессии слитого белка EBV-HLA-A2-GPA и костимуляторного полипептида, в модели EBV мыши in vivo
Показано, что несколько пептидов EBV являются антигенами лейкоза человека. Кроме того, несколько мышиных систем используют в качестве моделей инфекции EBV и ассоциированных заболеваний. Модель ксенотрансплантата EBV мыши NOD/NSG можно использовать для тестирования RTX-aAPC на EBV-ассоциированный MS (как исходно описано в Fujiwara et al., 2013, Pathogens, Mar 14;2(1):153-76, содержание которой включено в настоящее описание в качестве ссылки в полном объеме) для тестирования способности системы препятствовать EBV-активированным аутореактивным B-клеткам. Модель ксенотрансплантата EBV NOD/NSG получают с использованием NOD/LtSz-SCID ИЛ-2rg-/- (NSG). В день трансплантации 2-5 мышей подвергают облучению в дозе 100 сГр и внутрипеченочной трансплантации клеток CD34+ человека, выделенных из эмбриональной печени или пуповинной крови. EBV инокулируют интраперитонеально. Затем мышам вводят aAPC с молекулами MHC класса I или MHC класса II, презентирующими пептиды EBV, с костимуляторной молекулой (т.е. 4-1BBL). aAPC являются эритроцитами мыши, подвергнутыми клик-реакции с молекулами MHC, нагруженными пептидом EBV, и костимуляторной молекулой, или, альтернативно, безъядерными эритроидными клетками человека, сконструированными для экспрессии слитого белка пептида EBV-MHC класса I-GPA и костимуляторной молекулы (например, aAPC, описанными в примере 13). Ожидают, что эти aAPC будут активировать CD8+ или CD4+ T-клетки, специфические для пептидов EBV, которые, в свою очередь, уничтожат клетки, презентирующие пептиды EBV с помощью MHC класса I или II. Это может включать истощение B-клеток, становящихся лимфопролиферативными. Животных умерщвляют через 4-10 недель после переноса и анализируют ответы EBV-специфических T-клеток с использованием анализа ELISPOT на ИФНγ, как описано ранее (J Exp Med. 2009 Jun 8; 206(6):1423-34, содержание которой включено в настоящее описание в качестве ссылки). После введения aAPC T-клетки также окрашивают на маркеры активации, включая, например, CD62L, CD44 и/или 41BB, для оценки фенотипов мышей с введением aAPC или без него.
Пример 15. Эритроидные клетки, сконструированные для презентирования MHC класса I (овальбумина) и 4-1BBL, вызывают дозозависимый ответ овальбумин-специфических T-клеток in vivo
Эритроидные клетки мыши конъюгировали с презентирующим пептид овальбумина MHC класса I и 4-1BBL с использованием клик-химии (клик-химия для функционализации эритроидных клеток описана в международной заявке № PCT/US 2018/000042, по которой испрашивается приоритет по временной патентной заявке США №62/460589, поданной 17 февраля 2017 года, и временной патентной заявке США №62/542142, поданной 8 июля 2017 года, включенных в настоящее описание в качестве ссылки в полном объеме). В кратком изложении, периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и метили 0,04 мМ 6'-азидо-NHS-сложным эфиром в PBS, pH 8, в течение 30 мин при комнатной температуре. Азидо-меченые mRCT инкубировали с 40 мкМ m4-1BBL-DBCO-тиолинкера и мономера H-2Kb SIINFEKL-DBCO-тиолинкера (SEQ ID NO: 721) при комнатной температуре в течение 1 ч. и дополнительно инкубировали при 4°C в течение ночи.
CD8+ T-клетки выделяли из вторичных лимфоидных органов трансгенных мышей OT1 с использованием набора для отрицательной селекции от Miltenyi и метили флуоресцентным красителем (10 мкМ CFSE). 2E6 клеток OT1 инъецировали внутривенно мышам C57BL/6 в день 0. В день 0 через 4 часа после инъекции OT1 мышам внутривенно инъецировали 1E6, 1E7 или 1E8 aAPC (mRCT-4-1BBL H2Kb OVA). В день 4 мышей умерщвляли и суспензии отдельных клеток из селезенки и лимфоузлов окрашивали с помощью PE cy7 (CD44), APC (CD122), ad BV650 (CD27) и анализировали посредством проточной цитометрии. Активацию и пролиферацию T-клеток OT1 подвергали мониторингу по ослаблению сигнала флуоресцентного красителя в лимфоузлах или селезенке.
Как показано на фиг. 5, эритроидные клетки мыши, презентирующие MHC класса I (овальбумин) (mRCT-aAPC (ova) 4-1BBL), мощно индуцируют активацию и пролиферацию овальбумин-специфических T-клеток дозозависимым образом in vivo, о чем свидетельствует повышенная интенсивность флуоресценции CFSE (фиг. 5A) и экспрессия CD44 (фиг. 5B). Результаты также свидетельствуют о том, что активированные T-клетки OT1 демонстрируют фенотип памяти, на что указывает положительная регуляция ключевых маркеров памяти CD122 и CD27 (фиг. 5C и 5D) in vivo. Эти результаты свидетельствуют о способности мощно и селективно вызывать экспансию и активацию антигенспецифических T-клеток при использовании сконструированных безъядерных клеток, как представлено в настоящем описании.
Пример 16. Вторая доза эритроидных клеток, сконструированных для презентирования MHC класса I (овальбумина) и 4-1BBL, значительно стимулирует CD8+ T-Клетки OT1 в лимфоузле и селезенке.
Эритроидные клетки мыши получали, как описано в примере 15. CD8+ T-клетки выделяли из вторичных лимфоидных органов трансгенных мышей OT1, как описано в примере 15. В кратком изложении, мышам внутривенно инъецировали 1E9 aAPC (mRCT-4-1BBL или mRCT-4-1BBL H2Kb OVA) в день 0 и день 3. В день 6 мышей умерщвляли и окрашивали суспензии отдельных клеток из селезенки и лимфоузлов с помощью NIR Zombie, FITC (CD44), BV650 (CD8) и BV785 (CD62L) и анализировали посредством проточной цитометрии.
Пролиферацию T-клеток OT1 подвергали мониторингу по ослаблению сигнала флуоресцентного красителя в лимфоузлах или селезенке. Пептид SIINFEKL (SEQ ID NO: 721) (10 мкг) и адъювант LPS (50 нг), разведенный в PBS, вводили в качестве положительных контролей для индуцирования пролиферации T-клеток OT-1. Результаты эксперимента представлены на фиг. 6, где показано, что вторая доза mRCT-4-1BBL OVA в день 3 значительно повышает количество T-клеток OT1 относительно второй дозы LPS и пептида в день 3. Введение второй дозы aAPC в это время вызывает >200-кратную экспансию клеток OT1 с фенотипом, подобным фенотипу памяти, в периферической крови и вторичных лимфоидных органах. В отличие от этого, вторая доза mRCT-4-1BBL OVA в день 7 не повышала значительно количество T-клеток OT1 (данные не представлены). Наблюдали, что количество T-клеток находится на пике в течение 3-4 дней после исходного введения RCT. Таким образом, не желая быть связанными какой-либо теорией, полагают, что введение второй дозы во время пика исходного количества OT-1 T-клеток (в дни 3-4) будет наиболее эффективным в отношении индуцирования значительного изменения количества T-клеток.
Пример 17. Эритроидные клетки, сконструированные для презентирования MHC класса I (gp100) и 4-1BBL, активируют gp100-специфические T-клетки in vitro
Эритроидные клетки мыши конъюгировали с MHC класса I, презентирующим опухолевый пептид gp100, и 4-1BBL с использованием клик-химии (клик-химия для функционализации эритроидных клеток описана в международной заявке № PCT/US 2018/000042, по которой испрашивается приоритет по временной патентной заявке США №62/460589, поданной 17 февраля 2017 года, и временной патентной заявке США №62/542142, поданной 8 июля 2017 года, включенных в настоящее описание в качестве ссылки). В кратком изложении, периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и метили 0,04 мМ 6'-азидо-NHS-сложного эфира в PBS, pH 8, в течение 30 мин при комнатной температуре. Азидо-меченые mRCT инкубировали с 40 мкМ m4-1BBL-DBCO-тиолинкера при комнатной температуре в течение 1 ч. и дополнительно инкубировали при 4°C в течение ночи. mRCT-m4-1BBL подвергали клик-реакции с биотином посредством инкубации с 1 мкМ водорастворимого DBCO-биотина при комнатной температуре в течение 1 ч. с последующей инкубацией с нейтравидином при молярном соотношении 1:1 биотина и нейтравидина. Затем нейтраивдин-связанные клетки инкубировали с биотинилированным мономером H-2Db gp100 (KVPRNQDWL (SEQ ID NO: 722)) при молярном соотношении 1:1 биотина и мономера в течение 1 ч. при комнатной температуре.
Клетки Pmel-1, популяцию трансгенных CD8+ T-клеток против gp100, выделяли из вторичных лимфоидных органов мышей с использованием набора для отрицательной селекции от Miltenyi и метили 1 мкМ CFSE. 2E5 меченых CFSE первичных CD8+ T-клеток высевали в каждую лунку 96-луночного планшета. Различные количества (3E6, 1E6, 3,3E5 или 1,1E5 клеток) mRCT, mRCT-4-1BBL, mRCT-gp100-H2Db или mRCT-gp100-H2Db+4-1BBL высевали в среды cRPMI в лунки, содержащие CD8+ T-клетки, при соотношениях mRCT:T-клетки 10:1, 3,3:1, 1,1:1 и 0,37:1 (слева направо на фигуре 7) и инкубировали в течение двух дней при 37°C. Клетки промывали и окрашивали с помощью антитела против CD8, красителя LIVE/DEAD для количественного анализа экспансии и активации T-клеток.
Как показано на фиг. 7, эритроидные клетки мыши, презентирующие MHC класса I (gp100) и 4-1BBL на поверхности клетки, мощно активируют gp100-специфические T-клетки in vitro относительно эритроидных клеток мыши, презентирующих только MHC класса I (gp100). Эти результаты свидетельствуют о способности мощно и селективно вызывать экспансию другого типа антигенспецифических T-клеток по сравнению с овальбумин-специфическими T-клетками при использовании сконструированных безъядерных клеток, как представлено в настоящем описании.
Пример 18. Получение разных версий HLA-A2 (HPV E7), экспрессируемых на RCT
Для экспрессии HPV P1 (HPV16 E7 11-20), как показано на фигуре 8A, а также HPV P1-2 (HPV16 E7 11-19) использовали конструкции ДНК трех разных версий HLA-A2 (HLA-A2 дикого типа, HLA-A2 Y84A и HLA-A2 Y84C+L2C). Последовательности этих конструкций приведены ниже. См., например, Hansen et al., 2010, Trends Immunol. 31(10): 363-369.
HLA-A2v1 (дикого типа):
MSRSVALAVLALLSLSGLEAYMLDLQPETTGGGGSGGGGSGGGGSIQRTPKIQVYSRHPAENGKSNFLNCYVSGFHPSDIEVDLLKNGERIEKVEHSDLSFSKDWSFYLLYYTEFTPTEKDEYACRVNHVTLSQPKIVKWDRDMGGGGSGGGGSGGGGSGGGGSGSHSMRYFFTSVSRPGRGEPRFIAVGYVDDTQFVRFDSDAASQRMEPRAPWIEQEGPEYWDGETRKVKAHSQTHRVDLGTLRGYYNQSEAGSHTVQRMYGCDVGSDWRFLRGYHQYAYDGKDYIALKEDLRSWTAADMAAQTTKHKWEAAHVAEQLRAYLEGTCVEWLRRYLENGKETLQRTDAPKTHMTHHAVSDHEATLRCWALSFYPAEITLTWQRDGEDQTQDTELVETRPAGDGTFQKWAAVVVPSGQEQRYTCHVQHEGLPKPLTLRWEPSSQPTIPIGSGSGSGSEDGSGSGSGSLSTTEVAMHTSTSSSVTKSYISSQTNDTHKRDTYAATPRAHEVSEISVRTVYPPEEETGERVQLAHHFSEPEITLIIFGVMAGVIGTILLISYGIRRLIKKSPSDVKPLPSPDTDVPLSSVEIENPETSDQ* (SEQ ID NO: 723)
HLA-A2v2 (Y84A):
MSRSVALAVLALLSLSGLEAYMLDLQPETTGGGGSGGGGSGGGGSIQRTPKIQVYSRHPAENGKSNFLNCYVSGFHPSDIEVDLLKNGERIEKVEHSDLSFSKDWSFYLLYYTEFTPTEKDEYACRVNHVTLSQPKIVKWDRDMGGGGSGGGGSGGGGSGGGGSGSHSMRYFFTSVSRPGRGEPRFIAVGYVDDTQFVRFDSDAASQRMEPRAPWIEQEGPEYWDGETRKVKAHSQTHRVDLGTLRGAYNQSEAGSHTVQRMYGCDVGSDWRFLRGYHQYAYDGKDYIALKEDLRSWTAADMAAQTTKHKWEAAHVAEQLRAYLEGTCVEWLRRYLENGKETLQRTDAPKTHMTHHAVSDHEATLRCWALSFYPAEITLTWQRDGEDQTQDTELVETRPAGDGTFQKWAAVVVPSGQEQRYTCHVQHEGLPKPLTLRWEPSSQPTIPIGSGSGSGSEDGSGSGSGSLSTTEVAMHTSTSSSVTKSYISSQTNDTHKRDTYAATPRAHEVSEISVRTVYPPEEETGERVQLAHHFSEPEITLIIFGVMAGVIGTILLISYGIRRLIKKSPSDVKPLPSPDTDVPLSSVEIENPETSDQ* (SEQ ID NO: 724)
HLA-A2v3 (Y84C и L2C):
MSRSVALAVLALLSLSGLEAYMLDLQPETTGCGGSGGGGSGGGGSIQRTPKIQVYSRHPAENGKSNFLNCYVSGFHPSDIEVDLLKNGERIEKVEHSDLSFSKDWSFYLLYYTEFTPTEKDEYACRVNHVTLSQPKIVKWDRDMGGGGSGGGGSGGGGSGGGGSGSHSMRYFFTSVSRPGRGEPRFIAVGYVDDTQFVRFDSDAASQRMEPRAPWIEQEGPEYWDGETRKVKAHSQTHRVDLGTLRGCYNQSEAGSHTVQRMYGCDVGSDWRFLRGYHQYAYDGKDYIALKEDLRSWTAADMAAQTTKHKWEAAHVAEQLRAYLEGTCVEWLRRYLENGKETLQRTDAPKTHMTHHAVSDHEATLRCWALSFYPAEITLTWQRDGEDQTQDTELVETRPAGDGTFQKWAAVVVPSGQEQRYTCHVQHEGLPKPLTLRWEPSSQPTIPIGSGSGSGSEDGSGSGSGSLSTTEVAMHTSTSSSVTKSYISSQTNDTHKRDTYAATPRAHEVSEISVRTVYPPEEETGERVQLAHHFSEPEITLIIFGVMAGVIGTILLISYGIRRLIKKSPSDVKPLPSPDTDVPLSSVEIENPETSDQ*(SEQ ID NO: 725)
Эти 3 версии HLA-A2 использовали для экспрессии одноцепочечного варианта HPV P1-2-HLA-A2-GPA:
MSRSVALAVLALLSLSGLEAYMLDLQPETGGGGSGGGGSGGGGSIQRTPKIQVYSRHPAENGKSNFLNCYVSGFHPSDIEVDLLKNGERIEKVEHSDLSFSKDWSFYLLYYTEFTPTEKDEYACRVNHVTLSQPKIVKWDRDMGGGGSGGGGSGGGGSGGGGSGSHSMRYFFTSVSRPGRGEPRFIAVGYVDDTQFVRFDSDAASQRMEPRAPWIEQEGPEYWDGETRKVKAHSQTHRVDLGTLRGYYNQSEAGSHTVQRMYGCDVGSDWRFLRGYHQYAYDGKDYIALKEDLRSWTAADMAAQTTKHKWEAAHVAEQLRAYLEGTCVEWLRRYLENGKETLQRTDAPKTHMTHHAVSDHEATLRCWALSFYPAEITLTWQRDGEDQTQDTELVETRPAGDGTFQKWAAVVVPSGQEQRYTCHVQHEGLPKPLTLRWEPSSQPTIPIGSGSGSGSEDGSGSGSGSLSTTEVAMHTSTSSSVTKSYISSQTNDTHKRDTYAATPRAHEVSEISVRTVYPPEEETGERVQLAHHFSEPEITLIIFGVMAGVIGTILLISYGIRRLIKKSPSDVKPLPSPDTDVPLSSVEIENPETSDQ (SEQ ID NO: 726)
Получение лентивирусного вектора
Конструируют гены HPV слитого белка P1-HLA-A2-GPA и 4-1BBL. Гены, кодирующие белки, клонировали в участок множественного клонирования лентивирусного вектора pCDH с промоторной последовательностью MSCV от System Biosciences таким образом, что один вектор содержал гены обоих экзогенных белков. Лентивирус продуцировали в клетках 293T посредством трансфекции клеток с использованием лентивирусного вектора pPACKH1 (System Biosciences) и pCDH, содержащего гены HPV P1-HLA-A2-GPA и 4-1BBL. Альтернативно, можно использовать отдельные векторы, содержащие гены HPV P1-HLA-A2-GPA и 4-1BBL. Клетки высевали в свежую среду для культивирования. Вирусный супернатант собирали через 48 часов после замены среды посредством центрифугирования при 1500 об./мин. в течение 5 минут. Супернатант собирали и замораживали в аликвотах при -80°C.
Трансдукция эритроидных клеток-предшественников
Экспансию и дифференцировку эритроидных клеток осуществляли по примеру 5 с использованием описанных выше лентивирусных векторов. Эритроидные клетки-предшественники трансдуцировали на стадии 1 способа культивирования. Эритроидные клетки в среде для культивирования объединяли с лентивирусным супернатантом и полибреном. Инфицирования достигали посредством центрифужной инокуляции, центрифугируя планшет при 2000 об./мин. в течение 90 минут при комнатной температуре. После центрифужной инокуляции клетки инкубировали при 37°C в течение ночи
Связывание антител
Для валидации экспрессии слитого белка HPV P1-HLA-A2-GPA в сконструированных эритроидных клетках использовали связывание APC-меченого или PE-меченого антитела против бета-2-микроглобулина, как описано в примере 5. Для валидации экспрессии антигенпрезентирующего полипептида MHC класса I в сконструированных эритроидных клетках использовали связывание APC-меченого или PE-меченого антитела против MHC класса I, также как описано в примере 5. Для валидации экспрессии 4-1BBL в сконструированных эритроидных клетках использовали связывание APC-меченого или PE-меченого антитела против 4-1BBL (R&D Systems). Связывание любого из антител измеряли посредством проточной цитометрии по флуоресценции APC или PE. Гейт устанавливали с учетом окрашенных нетрансдуцированных клеток.
Пример 19: Активность HLA-A2 (HPV E7), экспрессируемого на RCT, в стимуляции HPV-специфических T-клеток in vitro
RCT человека, экспрессирующие 4-1BBL, HLA-A2 HPV P1 или и 4-1BBL, и HLA-A2 HPV P1, получали, по существу, как описано в примере 18. Эти RCT, коэкспрессирующие слитый белок HPV P1-HLA-A2-GPA и костимуляторный полипептид 4-1BBL, тестировали на способность стимулировать исходную активацию и пролиферацию первичных CD8+ T-клеток, по существу, как описано в примере 6. В качестве положительных контролей использовали клетки T2, в которые вводили пептид CMV или HPV.
Первичные CD8+ клетки человека приобретали в Astarte Biologics. Различные количества RCT человека высевали в среды cRPMI в лунки, содержащие 4E4 или 2E4 CD8+ T-клеток при соотношении RCT:T-клетки 10:1, 2:1 и 0,4:1 (слева направо для каждой RCT на фигурах 8B и 8C) и инкубировали в течение двух дней при 37°C.
Для измерения клеточных уровней Nur77 и ИФНγ использовали внутриклеточное окрашивание. В кратком изложении, клетки фиксировали 200 мкл буфера для фиксации IC и инкубировали в течение 20-60 минут в темноте при комнатной температуре. Образцы центрифугировали при 400-600×g при комнатной температуре в течение 5 минут. Выбрасывали супернатант и добавляли 200 мкл буфера для пермеабилизации. Образцы центрифугировали при 400-600×g при комнатной температуре в течение 5 минут. Выбрасывали супернатант и осадок ресуспендировали в приблизительно 100 мкл 1-кратного буфера для пермеабилизации. Без промывки добавляли напрямую конъюгированное антитело (PE-конъюгированное антитело против Nur77 и APC-конъюгированное антитело против ИФНγ) с последующей инкубацией в течение по меньшей мере 30 минут в темноте при комнатной температуре. Nur77 и ИФНγ анализировали через 2, 6 и 24 часа после инкубации RCT с первичными CD8+ T-клетками.
Проточный цитометрический анализ позволяет предполагать, что все тестируемые версии HLA-A2 (HPV E7) хорошо экспрессировались на поверхности RCT человека (данные не представлены). Кроме того, все три версии приводили к активации E7 HPV-специфических T-клеток, что определяли по экспрессии Nur77 (фиг. 8B) и секреции ИФНγ (фиг. 8C). Эти результаты свидетельствуют о способности мощно и селективно активировать антигенспецифические T-клетка, например, HPV-специфические T-клетки, при использовании сконструированных безъядерных клеток, как представлено в настоящем описании.
Пример 20. Овальбумин-специфические T-клетки, подвергнутые экспансии и активации с помощью эритроидных клеток, презентирующих MHC класса I (овальбумин) и 4-1BBL, уменьшают объем опухоли
Эритроидные клетки мыши конъюгировали с MHC класса I, презентирующим пептид овальбумина, и 4-1BBL с использованием клик-химии, как описано в примере 15. В кратком изложении, периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и метили 0,04 мМ 6'-азидо-NHS-сложным эфиром в PBS, pH 8, в течение 30 мин при комнатной температуре. Азидо-меченые mRCT инкубировали с 40 мкМ m4-1BBL-DBCO-тиолинкера и 40 мкМ мономера H-2Kb SIINFEKL-DBCO-тиолинкера (SEQ ID NO: 721) при комнатной температуре в течение 1 ч., а затем дополнительно инкубировали при 4°C в течение ночи.
CD8+ T-клетки выделяли из вторичных лимфоидных органов трансгенных мышей OT1 с использованием набора для отрицательной селекции от Miltenyi и метили 10 мкМ красителя CellTrace Violet.
2×106 опухолевых клеток, экспрессирующих овальбумин (EG7.OVA), инъецировали подкожно (s.c.) мышам B6 Cd45.1 за 7 дней до введения. Экспериментальные группы мышей (7 на группу) являлись следующими:
(1) Доза OT1: 2×106 OT1 (i.v.); доза клеток: 1×109 RCT мыши (mRCT) (i.v.);
(2) Доза OT1: 2×106 OT1 (i.v.); доза клеток: 1×109 RCT мыши, презентирующих MHC класса I (овальбумин) и 4-1BBL (mRCT-OVA-4-1BBL) (i.v.).
Первый день введения OT1 и mRCT определяли с учетом объема опухоли. В день 0 опухоли рандомизировали по объемам опухолей 60-193 мм3 при среднем объеме 141 мм3. Адоптивный перенос T-клеток OT1 в дозах, определенных для указанных выше групп (1) и (2), осуществляли посредством внутривенной инъекции мышам дикого типа (день 1). Затем мышам вводили 1×109 mRCT или mRCT-OVA-41-BBL, как указано для групп (1) и (2) выше, в дни 1, 4 и 8. Наблюдали значительную пролиферацию OT1 через 3-4 дня после введения, что определяли по ослаблению CTV. Вторую дозу вводили через 4 дня после первой дозы, что соответствует времени максимальной экспансии клеток OT1. Объем опухоли измеряли в течение дней 1-14 и умерщвляли мышей, когда объемы опухолей достигали более 2000 мм3.
Результаты этого эксперимента показаны на фиг. 9-11. На фиг. 9 показано изменение среднего объема опухоли (мм3) с течением времени после рандомизации опухоли, если введение осуществляли в дни 1, 4 и 8. На фиг. 10 показаны отдельные объемы опухоли (мм3) с течением времени после рандомизации опухоли, если введение осуществляли в дни 1, 4 и 8. Результаты на фиг. 9 и фиг. 10 свидетельствуют о том, что mRCT-OVA-4-1BBL могли активировать опухолеспецифические T-клетки (OT1) в дозе 2×106, о чем свидетельствует уменьшение объема опухоли EG7.OVA с течением времени по сравнению с mRCT. Введение aAPC mRCT-OVA-4-1BBL мышам, несущим опухоли EG7.OVA, вызывало ингибирование роста опухоли на 60% ко дню 7 после введения по сравнению с контролями, что соответствует повышенной экспансии OT1 (фиг. 9). Фиг. 11 является графиком, на котором показан процент выживания мышей с течением времени. Как показано на фиг. 11, 7 из 7 мышей, которым вводили mRCT-OVA-4-1BBL, выживали ко дню 14 после рандомизации, в то время как только 4 из 7 мышей, которым вводили mRCT, выживали ко дню 14 после рандомизации. Кроме того, в отдельном схожем эксперименте наблюдали, что все мыши, которым вводили aAPC, демонстрировали повышенную инфильтрацию OT1 опухолей EG7.OVA, при этом в некоторых опухолях дополнительно наблюдали инфильтрацию эндогенными овальбумин-специфическими T-клетками (данные не представлены).
Этот эксперимент повторяли, в целом, как описано выше, за исключением того, что адоптивный перенос T-клеток OT1 осуществляли в дозе 5×105 OT1 (i.v.), и в дополнение к группе мышей, которым вводили mRCT-OVA-4-1BBL, включали следующие дополнительные контрольные группы (12 мышей на группу): фосфатно-солевой буфер (PBS), пептид SIINFEKL (SEQ ID NO: 721) и липополисахарид (LPS), mRCT-OVA и mRCT-4-1BBL. В этом эксперименте 2×106 опухолевых клеток, экспрессирующих овальбумин (EG7.OVA), инъецировали подкожно (s.c.) мышам дикого типа в день -9, рандомизацию опухолей осуществляли в день 0, когда объем опухоли составлял 52-130 мм3 и в среднем составлял 97 мм3, введение OT1 осуществляли в день 1 и введение mRCT осуществляли в дни 1, 5 и 9.
Результаты этих экспериментов (данные не представлены) свидетельствуют о том, что, аналогично первом эксперименту, mRCT-OVA-4-1BBL активировал опухолеспецифические T-клетки (OT1), о чем свидетельствует снижение объема опухоли EG7.OVA с течением времени по сравнению с объемом опухоли в случае контрольных mRCT, PBS и пептид+LPS. Не наблюдали значимых различий среди этих контролей. Кроме того, не наблюдали снижения объема опухоли в случае mRCT-OVA и mRCT-4-1BBL по сравнению с объемом опухоли в случае контрольных mRCT. Эти результаты свидетельствуют о том, что комбинация OVA и 4-1BBL на mRCT была необходимой для наблюдаемого контроля опухоли.
Пример 21. Получение эритроидных клеток, презентирующих MHC класса I (овальбумин), 4-1BBL и ИЛ-15 (OVA-H2Kb+4-1BBL+ИЛ-15)
Эритроидные клетки мыши конъюгировали с каждым из MHC класса I, презентирующего пептид овальбумина (OVA-H2Kb), 4-1BBL и ИЛ-15 с использованием модификации клик-химии (клик-химия для функционализации эритроидных клеток описана в международной заявке № PCT/US 2018/000042, по которой испрашивается приоритет по временной патентной заявке США №62/460589, поданной 17 февраля 2017 года, и временной патентной заявке США №62/542142, поданной 8 июля 2017 года, включенных в настоящее описание в качестве ссылки). В этом случае конъюгации трех пептидов на эритроидных клетках мыши достигали с использованием двух разных модулей клик-реакции, дибензоциклооктиновой группы (DBCO) и транс-циклооктена (TCO). Трижды подвергнутые клик-реакции клетки получали с использованием следующих реагентов: Fc-hIL-15TP (меченый TCO); Fc-hIL-15TP (меченый DBCO); m4-1BBL (тиолинкер DBCO) и OVA-H2Kb (тиолинкер DBCO). В кратком изложении, реакции осуществляли следующим образом:
OVA-4-1BBL-IL-15 (MTZ-TCO)
Периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и 1×108 mRCT метили с помощью 0,04 мМ 6'-азидо-NHS-сложного эфира и 0,04 мМ метилтетразин-PEG-NHS-сложного эфира (MTZ) в PBS, pH 8, в течение 30 мин при комнатной температуре. Добавляли 5 мкл 20 мкМ Fc-hIL-15TP (меченого TCO) и 5 мкл 50 мкМ OVA-H2Kb-DBCO-тиолинкера и инкубировали в течение 1 ч. при комнатной температуре. К клеткам добавляли 5 мкл 50 мкМ m4-1BBL-DBCO-тиолинкера и смесь инкубировали в течение ночи при 4°C.
OVA-4-1BBL-IL-15 (AZ-DBCO)
Периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и 1×108 mRCT метили с помощью 0,04 мМ 6'-азидо-NHS-сложного эфира в PBS, pH 8, в течение 30 мин при комнатной температуре. Азидо-меченые mRCT инкубировали с 5 мкл 20 мкМ Fc-hIL-15TP-DBCO и 5 мкл 50 мкМ OVA-H2Kb-DBCO-тиолинкера в течение 1 ч. при комнатной температуре. К клеткам добавляли 5 мкл 50 мкМ m4-1BBL-DBCO-тиолинкера и смесь инкубировали в течение ночи при 4°C.
OVA-4-1BBL
Периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и 1×108 mRCT метили с помощью 0,04 мМ 6'-азидо-NHS-сложного эфира в PBS, pH 8, в течение 30 мин при комнатной температуре. Азидо-меченые mRCT инкубировали с 5 мкл 50 мкМ m4-1BBL-DBCO-тиолинкера и 5 мкл 50 мкМ OVA-H2Kb-DBCO-тиолинкера и смесь инкубировали в течение ночи при 4°C.
Определяли количество копий ИЛ-15, OVA и 4-1BBL в случае mRCT, трижды подвергнутых клик-реакции с OVA-4-1BBL-IL-15 (MTZ-TCO) или OVA-4-1BBL-IL-15 (AZ-DBCO), и mRCT, дважды подвергнутых клик-реакции с OVA-4-1BBL. Хотя количество копий для каждого из OVA и 4-1BBL было схожим в трех группах, mRCT, трижды подвергнутые клик-реакции с OVA-4-1BBL-IL-15 (MTZ-TCO), демонстрировали значительно более высокое количество копий ИЛ-15 по сравнению с mRCT, трижды подвергнутыми клик-реакции с OVA-4-1BBL-IL-15 (AZ-DBCO) (см. таблицу 27 ниже).
Таблица 27. Количество копий
Не желая быть связанными какой-либо теорией, полагают, что mRCT, трижды подвергнутые клик-реакции с альтернативным модулем клик-реакции (MTZ-TCO), избегали потенциальной конкуренции с DBCO с достижением более высокого количества копий ИЛ-15.
Пример 22: Эритроидные клетки, презентирующие MHC класса I (овальбумин), 4-1BBL и ИЛ-15 (OVA-H2Kb+4-1BBL+ИЛ-15), демонстрируют повышенную пролиферацию CD8+ T-клеток OT1 по сравнению с клетками, презентирующими MHC класса I (овальбумин) и 4-1BBL (OVA-H2Kb+4-1BBL)
RCT мыши получали, как описано в примере 20. CD8+ T-клетки выделяли из селезенки трансгенных мышей OT1 с использованием набора для отрицательной селекции от Miltenyi и метили 10 мкМ CFSE. 2E5 меченых CFSE CD8+ T-клеток OT1 высевали в каждую лунку 96-луночного планшета. Неподвергнутые клик-реакции mRCT, трижды подвергнутые клик-реакции mRCT (OVA-4-1BBL-IL-15 (MTZ-TCO) и OVA-4-1BBL-IL-15 (AZ-DBCO)) или дважды подвергнутые клик-реакции mRCT (OVA-4-1BBL, и OVA-4-1BBL+растворимый ИЛ-15 (20 нг/мл) и CD8+ T-клетки OT1 совместно инкубировали в соотношениях 25:1, 10:1 и 4:1 (mRCT:OT1) и инкубировали в течение 4 дней при 37°C и 5% CO2. В день 4 клетки окрашивали с помощью Pacific blue (CD44) и BV785 (CD62L) и анализировали посредством проточной цитометрии. CD44 использовали в качестве маркера пролиферации CD8+ T-клеток. Результаты этого эксперимента показаны на фиг. 12. Результаты свидетельствовали о том, что mRCT, трижды подвергнутые клик-реакции с OVA-4-1BBL-IL-15 (MTZ-TCO), запускали повышенную пролиферацию CD8+ T-клеток OT1 ко дню 4 по сравнению с mRCT-OVA-4-1BBL (дважды подвергнутыми клик-реакции), и что mRCT, трижды подвергнутые клик-реакции с OVA-4-1BBL-IL-15 (MTZ-TCO), запускали пролиферацию CD8+ T-клеток OT1 ко дню 4, схожую с mRCT OVA-4-1BBL (дважды подвергнутыми клик-реакции) в комбинации с растворимым ИЛ-15. Как показано на фиг. 12, вторая панель слева, mRCT, трижды подвергнутые клик-реакции с альтернативным модулем клик-реакции (MTZ-DBCO), также запускали пролиферацию CD8+ T-клеток OT1 ко дню 4.
Также определяли пролиферацию CD8+ T-клеток OT1 в день 4. Как показано на фиг. 13, результаты свидетельствуют о том, что mRCT, трижды подвергнутые клик-реакции с OVA-4-1BBL-IL-15 (MTZ-TCO), стимулировали значительную пролиферацию CD8+ T-клеток OT1 с уровнем, схожим с уровнем, достигаемым при использовании комбинации mRCT OVA-4-1BBL (дважды подвергнутых клик-реакции) и растворимого ИЛ-15. Кроме того, mRCT, трижды подвергнутые клик-реакции с OVA+4-1BBL+ИЛ-15 (MTZ-TCO), повышали пролиферацию CD8+ T-клеток OT1 до более высокого уровня, чем mRCT, трижды подвергнутые клик-реакции с модулем DBCO, OVA-H2Kb+4-1BBL (AZ-DBCO). Как показано выше в таблице 27, mRCT, трижды подвергнутые клик-реакции с OVA-4-1BBL-IL-15 (MTZ-TCO), демонстрировали более высокое количество копий ИЛ-15 по сравнению с mRCT, трижды подвергнутыми клик-реакции с OVA-4-1BBL-IL-15 (AZ-DBCO), что свидетельствует о том, что наблюдаемая повышенная пролиферация CD8+ T-клеток OT1 по меньшей мере частично являлась результатом большего количества копий ИЛ-15. Кроме того, определяли процентную долю эффекторных T-клеток и T-клеток памяти в популяциях CD8+ T-клеток OT1. Обнаружено, что процент CD8+ T-клеток, являвшихся эффекторными T-клетками или T-клетками памяти, не отличался значительно в группах дважды подвергнутых клик-реакции mRCT и трижды подвергнутых клик-реакции mRCT (данные не представлены).
В целом, результаты этого эксперимента свидетельствуют о том, что комбинация сигналов 1, 2 и 3 на эритроцитах, в частности, комбинация OVA, 4-1BBL и ИЛ-15, способствует более высокой пролиферации CD8+ T-клеток, чем сигналы 1 и 2, т.е. OVA и 4-1BBL, в отдельности.
Пример 23. Получение эритроидных клеток, презентирующих MHC класса I (овальбумин), 4-1BBL и ИЛ-12 (OVA-H2Kb+4-1BBL+ИЛ-12)
Эритроидные клетки мыши конъюгировали с каждым из MHC класса I, презентирующего пептид овальбумина (OVA-H2Kb), 4-1BBL и ИЛ-12 с использованием модификации клик-химии (клик-химия для функционализации эритроидных клеток описана в международной заявке № PCT/US 2018/000042, по которой испрашивается приоритет по временной патентной заявке США №62/460589, поданной 17 февраля 2017 года, и временной патентной заявке США №62/542142, поданной 8 июля 2017 года, включенных в настоящее описание в качестве ссылки в полном объеме). Трижды подвергнутые клик-реакции клетки получали с использованием следующих реагентов: Fc-mIL-12Fc (меченого сложным эфиром TCO-PEG4-NHS); m4-1BBL (тиолинкера DBCO) и OVA-H2Kb (тиолинкера DBCO). В кратком изложении, реакции осуществляли следующим образом:
OVA-4-1BBL-IL-12 (MTZ-TCO)
Периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и 1×108 mRCT метили с помощью 0,04 мМ 6'-азидо-NHS-сложного эфира и 0,02 мМ метилтетразин-PEG-NHS-сложного эфира (MTZ) в PBS, pH 9, в течение 30 мин при комнатной температуре. Добавляли 5 мкл 20 мкМ сложного эфира Fc-mIL-12Fc-TCO-PEG4-NHS и 5 мкл 50 мкМ OVA-H2Kb-DBCO-тиолинкера и инкубировали в течение 1 ч. при комнатной температуре. К клеткам добавляли 5 мкл 50 мкМ m4-1BBL-DBCO-тиолинкера и инкубировали смесь в течение ночи при 4°C.
OVA-4-1BBL
Периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и 1×108 mRCT метили с помощью 0,04 мМ 6'-азидо-NHS-сложного эфира и 0,02 мМ метилтетразин-PEG-NHS-сложного эфира (MTZ) в PBS, pH 9, в течение 30 мин при комнатной температуре. Азидо-меченые mRCT инкубировали с 5 мкл 50 мкМ m4-1BBL-DBCO-тиолинкера и 5 мкл 50 мкМ OVA-H2Kb-DBCO-тиолинкера и смесь инкубировали в течение ночи при 4°C.
Определяли количество копий ИЛ-12, OVA и 4-1BBL в случае mRCT, трижды подвергнутых клик-реакции с OVA-4-1BBL-IL-12, и mRCT, дважды подвергнутых клик-реакции с OVA-4-1BBL (см. таблицу 28 ниже).
Таблица 28. Количество копий
Пример 24. Получение эритроидных клеток, презентирующих MHC класса I (овальбумин), 4-1BBL и ИЛ-7 (OVA-H2Kb+4-1BBL+ИЛ-7)
Эритроидные клетки мыши конъюгировали с каждым из MHC класса I, презентирующего пептид овальбумина (OVA-H2Kb), 4-1BBL и ИЛ-7 с использованием модификации клик-химии (клик-химия для функционализации эритроидных клеток описана в международной заявке № PCT/US 2018/000042, по которой испрашивается приоритет по временной патентной заявке США №62/460589, поданной 17 февраля 2017 года, и временной патентной заявке США №62/542142, поданной 8 июля 2017 года, включенных в настоящее описание в качестве ссылки в полном объеме). Трижды подвергнутые клик-реакции клетки получали с использованием следующих реагентов: Fc-mIL-7 (меченого сложным эфиром DBCO-сульфо-NHS); m4-1BBL (тиолинкера DBCO) и OVA-H2Kb (тиолинкера DBCO). В кратком изложении, реакции осуществляли следующим образом:
OVA-4-1BBL-IL-7 (AZ-DBCO)
Периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и 1×108 mRCT метили с помощью 0,04 мМ 6'-азидо-NHS-сложного эфира и 0,02 мМ метилтетразин-PEG-NHS-сложого эфира (MTZ) в PBS, pH 9, в течение 30 мин при комнатной температуре. Азидо-меченые mRCT инкубировали с 5 мкл 20 мкМ сложного эфира Fc-mIL-7-DBCO-сульфо-NHS и 5 мкл 50 мкМ OVA-H2Kb-DBCO-тиолинкера в течение 1 ч. при комнатной температуре. К клеткам добавляли 5 мкл 50 мкМ m4-1BBL-DBCO-тиолинкера и смесь инкубировали в течение ночи при 4°C.
OVA-4-1BBL
Периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и 1×108 mRCT метили с помощью 0,04 мМ 6'-азидо-NHS-сложного эфира и 0,02 мМ метилтетразин-PEG-NHS-сложного эфира (MTZ) в PBS, pH 9, в течение 30 мин при комнатной температуре. Азидо-меченые mRCT инкубировали с 5 мкл 50 мкМ m4-1BBL-DBCO-тиолинкера и 5 мкл 50 мкМ OVA-H2Kb-DBCO-тиолинкера и смесь инкубировали в течение ночи при 4°C.
Определяли количество копий ИЛ-7, OVA и 4-1BBL в случае mRCT, трижды подвергнутых клик-реакции с OVA-4-1BBL-IL-7, и mRCT, дважды подвергнутых клик-реакции с OVA-4-1BBL (см. таблицу 29 ниже).
Таблица 29. Количество копий
Пример 25: Эритроидные клетки, презентирующие MHC класса I (овальбумин) и 4-1BBL с ИЛ-7 (OVA-H2Kb+4-1BBL+ИЛ-7), ИЛ-12 (OVA-H2Kb+4-1BBL+ИЛ-12) или ИЛ-15 (OVA-H2Kb+4-1BBL+ИЛ-15), демонстрируют повышенную пролиферацию CD8+ T-клеток OT1 по сравнению с клетками, презентирующими 4-1BBL (OVA-H2Kb+41-BBL)
RCT мыши получали, например, как описано, в примерах 21, 23 и 24. CD8+ T-клетки выделяли из селезенки и лимфоузлов трансгенных мышей OT1 с использованием набора для отрицательной селекции от Miltenyi и метили 1 мкМ CellTrace Violet. 2E5 меченых CellTrace Violet CD8+ T-клеток OT1 высевали в каждую лунку 96-луночного планшета. Неподвергнутые клик-реакции mRCT или трижды подвергнутые клик-реакции mRCT (OVA-4-1BBL-IL-7, OVA-4-1BBL-IL-12, или OVA-4-1BBL-IL-15) и CD8+ T-клетки OT1 совместно инкубировали в соотношениях 1:1,1, 1:3,3 и 1:10 (mRCT:OT1) и инкубировали в течение 4 дней при 37°C и 5% CO2. В день 4 анализировали маркеры пролиферации, активации и памяти T-клеток OT1 посредством проточной цитометрии. Клетки окрашивали с помощью FITC (CD44), APC (CD122) и BV785 (CD62L). Результаты этого эксперимента показаны на фиг. 14. Результаты свидетельствовали о том, что mRCT, трижды подвергнутые клик-реакции с OVA-4-1BBL-IL-7, OVA-4-1BBL-IL-12 или OVA-4-1BBL-IL-15, запускали повышенную пролиферацию CD8+ T-клеток OT1 ко дню 4, как mRCT OVA-4-1BBL (дважды подвергнутые клик-реакции) (фиг. 14A). Кроме того, определяли процентные доли фенотипов стволовых T-клеток памяти (Tscm), T-клеток центральной памяти (Tcm) и эффекторных T-клеток памяти (Tem) в популяциях CD8+ T-клеток OT1. Обнаружено, что mRCT, трижды подвергнутые клик-реакции с OVA-4-1BBL-IL-7, OVA-4-1BBL-IL-12 или OVA-4-1BBL-IL-15, запускали повышенную активацию фенотипа Tcm, в то время как mRCT, дважды подвергнутые клик-реакции с mRCT OVA-4-1BBL, запускали приблизительно равную активацию фенотипов Tem и Tcm (фиг. 14B).
В целом, результаты этого эксперимента свидетельствуют о том, что комбинация сигналов 1, 2 и 3 на эритроцитах, в частности, комбинация OVA-4-1BBL-IL-7, OVA-4-1BBL-IL-12 или OVA-4-1BBL-IL-15, стимулирует более высокую пролиферацию CD8+ T клеток, чем сигналы 1 и 2, т.е. OVA и 4-1BBL, в отдельности.
Пример 26: У мышей, которым вводили эритроидные клетки, презентирующие MHC класса I (овальбумин) и 4-1BBL, наблюдают контроль опухоли EG7.OVA даже после повторной стимуляции опухолевыми клетками EG7.OVA
Эритроидные клетки мыши конъюгировали с MHC класса I, презентирующим пептид овальбумина, и 4-1BBL с использованием клик-химии, как описано в примере 15. В кратком изложении, периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и метили 0,04 мМ 6'-азидо-NHS-сложного эфира в PBS, pH 9, в течение 30 мин при комнатной температуре. Азидо-меченые mRCT инкубировали с 40 мкМ m4-1BBL-DBCO-тиолинкера и 5 мкл 50 мкМ OVA-H2Kb-DBCO-тиолинкера при комнатной температуре в течение 1 ч., а затем дополнительно инкубировали при 4°C в течение ночи. CD8+ T-клетки выделяли из вторичных лимфоидных органов трансгенных мышей OT1 с использованием набора для отрицательной селекции от Miltenyi и метили 1 мкМ CellTrace Violet.
Мышам C57BL/6 подкожно инъецировали 2E6 опухолевых клеток EG7.OVA. Когда опухоль достигала приблизительно 140 мм3, этих мышей рандомизировали по двум группам по 7 мышей. Затем этих мышей подвергали переносу 2E6 T-клеток OT1 в день 1 после рандомизации и вводили 1E9 mRCT или mRCT-OVA-4-1BBL в дни 1, 4 и 8 после рандомизации. Мышей, излечившихся при использовании mRCT-OVA-4-1BBL (n=2), повторно стимулировали с помощью 2E5 EG7.OVA через 37 дней после первичной инъекции опухолевого материала параллельно с совпадающими по возрасту наивными мышами. Наивных мышей также подвергали переносу 5E5 CD8+ T-клеток OT1 через 7 дней после инъекции опухолевого материала. Каждые 2-3 дня измеряли опухолевую массу. Как показано на фиг. 15A, результаты этого эксперимента свидетельствуют о том, что мыши, которых ранее лечили mRCT-OVA-4-1BBL, могли отторгать опухолевые клетки EG7.OVA, которые использовали для повторной стимуляции, о чем свидетельствует уменьшение объема опухоли EG7.OVA с течением времени по сравнению с объемом опухоли у мышей, неподвергнутых лечению.
В независимом эксперименте мышам C57BL/6 подкожно инъецировали 2E6 клеток EG7.OVA. Когда опухоль достигала приблизительно 100 мм3, этих мышей рандомизировали в две группы по 12 мышей. Затем их подвергали переносу 5E5 T-клеток OT1 и вводили им 1E9 mRBC или mRBC-OVA-4-1BBL в дни 0, 4 и 8 после рандомизации. Мышь, излечившуюся при использовании mRBC-OVA-4-1BBL (n=1), повторно стимулировали с помощью 2E5 клеток EG7.OVA через 35 дней после первичной инъекции опухолевого материала параллельно с совпадающими по возрасту наивными мышами. Наивных мышей также подвергали переносу 4E5 CD8+ T-клеток OT1 через 11 дней после инъекции опухолевого материала. Каждые 2-3 дня измеряли опухолевую массу. Как показано на фиг. 15B, результаты этого эксперимента свидетельствуют о том, что даже после повторной стимуляции опухолевыми клетками EG7.OVA, mRCT-OVA-4-1BBL продолжали активировать опухолеспецифические T-клетки (OT1), о чем свидетельствует уменьшение объема опухоли EG7.OVA с течением времени по сравнению с объемом опухоли у мышей, неподвергнутых лечению.
В целом, эти результаты свидетельствуют о том, что мыши, которых ранее излечили от опухолей EG7.OVA посредством введения mRCT, поддерживают анамнестический ответ посредством предотвращения роста опухоли после повторной стимуляции опухолевыми клетками EG7.OVA.
Пример 27: Мыши, которым вводили эритроидные клетки, презентирующие только MHC класса I (овальбумин), демонстрируют анергию антигенспецифических T-клеток после повторной стимуляции антигеном и адъювантом
Эритроидные клетки мыши конъюгировали с MHC класса I, презентирующим пептид овальбумина, с использованием клик-химии, как описано в примере 15. В кратком изложении, периферическую кровь мыши фильтровали через лейкоцитарный фильтр PAL и метили с помощью 0,04 мМ 6'-азидо-NHS-сложного эфира в PBS, pH 8, в течение 30 мин при комнатной температуре. Азидо-меченые mRCT инкубировали с 50 мкМ OVA-H2Kb-DBCO-тиолинкера при комнатной температуре в течение 1 ч., а затем дополнительно инкубировали и при 4°C в течение ночи. CD8+ T-клетки выделяли из вторичных лимфоидных органов трансгенных мышей OT1 с использованием набора для отрицательной селекции от Miltenyi и метили 10 мкМ CellTrace Violet.
Мышей C57BL/6 подвергали переносу 2E6 T-клеток OT1 в день 0 и вводили 1E9 mRCT или mRCT-OVA в дни 0, 4, и 7. В день 13 мышей повторно стимулировали пептидом OVA (SIINFEKL (SEQ ID NO: 721)) и неполным адъювантом Фрейнда (IFA), как показано на фигуре 16A. Мыши, которым вводили mRCT-OVA, имели более низкие количества клеток OT1 после повторной стимуляции пептидом OVA по сравнению с мышами, которым вводили только mRCT в селезенке и лимфоузел, как показано на фигуре 16B. Как показано на фигуре 16C, на количества эндогенных CD8+ T-клеток не влияло какое-либо лечение. В целом, эти результаты свидетельствуют о том, что mRCT-OVA могли запускать анергию или делецию антигенспецифических T-клеток, о чем свидетельствует снижение количества OT1.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> RUBIUS THERAPEUTICS, INC.
<120> ИСКУССТВЕННЫЕ АНТИГЕНПРЕЗЕНТИРУЮЩИЕ КЛЕТКИ И СПОСОБЫ ИХ
ПРИМЕНЕНИЯ
<130> 129267-00120
<140>
<141>
<150> 62/757,741
<151> 2018-11-08
<150> 62/745,253
<151> 2018-10-12
<150> 62/692,623
<151> 2018-06-29
<150> 62/688,324
<151> 2018-06-21
<150> 62/686,656
<151> 2018-06-18
<150> 62/680,544
<151> 2018-06-04
<150> 62/665,445
<151> 2018-05-01
<150> 62/650,250
<151> 2018-03-29
<150> 62/610,149
<151> 2017-12-23
<160> 895
<170> PatentIn version 3.5
<210> 1
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 2
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 2
Tyr Pro Tyr Asp Val Pro Asp Tyr Ala
1 5
<210> 3
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 3
Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu
1 5 10
<210> 4
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 4
Asp Tyr Lys Asp Asp Asp Asp Lys
1 5
<210> 5
<211> 54
<212> ДНК
<213> Вирус Thosea asigna
<400> 5
gagggcagag gaagtcttct aacatgcggt gacgtggagg sgsstcccgg ccct 54
<210> 6
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<220>
<221> MOD_RES
<222> (3)..(3)
<223> Любая аминокислота
<400> 6
Leu Pro Xaa Thr Gly
1 5
<210> 7
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<220>
<221> MOD_RES
<222> (3)..(3)
<223> Любая аминокислота
<400> 7
Leu Pro Xaa Thr Ala
1 5
<210> 8
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 8
Ala Leu Asp Val Tyr Asn Gly Leu Leu
1 5
<210> 9
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 9
Phe Leu Phe Leu Leu Phe Phe Trp Leu
1 5
<210> 10
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 10
Thr Leu Met Ser Ala Met Thr Asn Leu
1 5
<210> 11
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 11
Ile Leu Leu Trp Gln Pro Ile Pro Val
1 5
<210> 12
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 12
Tyr Leu Pro Phe Arg Asn Cys Arg Pro
1 5
<210> 13
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 13
Asn Leu Val Arg Asp Asp Gly Ser Ala Val
1 5 10
<210> 14
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 14
Arg Leu Phe Ala Phe Val Arg Phe Thr
1 5
<210> 15
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 15
Val Val Gln Asn Phe Ala Lys Glu Phe Val
1 5 10
<210> 16
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 16
Phe Val Glu His Asp Asp Glu Ser Pro Gly Leu
1 5 10
<210> 17
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 17
Tyr Thr Asp Phe His Cys Gln Tyr Val
1 5
<210> 18
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 18
Phe Ile Ala Ser Asn Gly Val Lys Leu Val
1 5 10
<210> 19
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (16)..(16)
<223> D-аминокислота
<400> 19
Tyr Ser Val Tyr Phe Asn Leu Pro Ala Asp Thr Ile Tyr Thr Asn His
1 5 10 15
<210> 20
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 20
Phe Pro Ser Asp Ser Trp Cys Tyr Phe
1 5
<210> 21
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 21
Ser Tyr Leu Asp Ser Gly Ile His Phe
1 5
<210> 22
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (13)..(13)
<223> D-аминокислота
<400> 22
Phe Ser Trp Ala Met Asp Leu Asp Pro Lys Gly Ala Glu
1 5 10
<210> 23
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 23
Ala Cys Asp Pro His Ser Gly His Phe Val
1 5 10
<210> 24
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 24
Cys Ile Leu Gly Lys Leu Phe Thr Lys
1 5
<210> 25
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (10)..(10)
<223> D-аминокислота
<400> 25
Ala Val Cys Pro Trp Thr Trp Leu Arg Gly
1 5 10
<210> 26
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 26
Ile Leu Asp Lys Val Leu Val His Leu
1 5
<210> 27
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (15)..(15)
<223> D-аминокислота
<400> 27
Thr Leu Tyr Gln Asp Asp Thr Leu Thr Leu Gln Ala Ala Gly Glu
1 5 10 15
<210> 28
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 28
Gly Leu Phe Gly Asp Ile Tyr Leu Ala
1 5
<210> 29
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 29
Lys Ile Leu Asp Ala Val Val Ala Gln Lys
1 5 10
<210> 30
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 30
Glu Thr Val Ser Glu Gln Ser Asn Val
1 5
<210> 31
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 31
Met Ile Phe Glu Lys His Gly Phe Arg Arg Thr Thr Pro Pro
1 5 10
<210> 32
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 32
Ser Leu Ala Asp Glu Ala Glu Val Tyr Leu
1 5 10
<210> 33
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 33
Thr Leu Asp Trp Leu Leu Gln Thr Pro Lys
1 5 10
<210> 34
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (10)..(10)
<223> D-аминокислота
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="Leu"
<220>
<221> УЧАСТОК
<222> (1)..(10)
<223> /примечание="варианты остатков, приведенные в последовательности, не
имеют приоритета относительно остатков в аннотациях вариантов положений"
<400> 34
Ile Leu Asn Ala Met Ile Ala Lys Ile Ile
1 5 10
<210> 35
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 35
Cys Tyr Met Glu Ala Val Ala Leu
1 5
<210> 36
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 36
Trp Arg Arg Ala Pro Ala Pro Gly Ala
1 5
<210> 37
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 37
Pro Val Thr Trp Arg Arg Ala Pro Ala
1 5
<210> 38
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 38
Cys Val Glu Trp Leu Arg Ile Tyr Leu Glu Asn Gly
1 5 10
<210> 39
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 39
Ser Leu Phe Glu Gly Ile Asp Ile Tyr Thr
1 5 10
<210> 40
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 40
Ala Glu Pro Ile Asn Ile Gln Thr Trp
1 5
<210> 41
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 41
Leu Met Ile Ser Arg Thr Pro Glu Val
1 5
<210> 42
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 42
Phe Leu Glu Gly Asn Glu Val Gly Lys Thr Tyr
1 5 10
<210> 43
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 43
Lys Thr Leu Thr Ser Val Phe Gln Lys
1 5
<210> 44
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 44
Phe Leu Asp Glu Phe Met Glu Gly Val
1 5
<210> 45
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 45
Lys Leu Val Val Val Gly Ala Val Gly Val
1 5 10
<210> 46
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 46
Leu Val Val Val Gly Ala Val Gly Val
1 5
<210> 47
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 47
Val Val Val Gly Ala Val Gly Val Gly
1 5
<210> 48
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 48
Glu Glu Lys Leu Ile Val Val Leu Phe
1 5
<210> 49
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 49
Ser Glu Leu Phe Arg Ser Gly Leu Asp Ser Tyr
1 5 10
<210> 50
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 50
Phe Arg Ser Gly Leu Asp Ser Tyr Val
1 5
<210> 51
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 51
Glu Ala Phe Ile Gln Pro Ile Thr Arg
1 5
<210> 52
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (12)..(12)
<223> D-аминокислота
<400> 52
Arg Val Ile Lys Asn Ser Ile Arg Leu Thr Leu Glu
1 5 10
<210> 53
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 53
Gln Gln Ile Thr Lys Thr Glu Val
1 5
<210> 54
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 54
Lys Glu Leu Glu Gly Ile Leu Leu Leu
1 5
<210> 55
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 55
Pro Tyr Tyr Phe Ala Ala Glu Leu Pro Pro Arg Asn Leu Pro Glu Pro
1 5 10 15
<210> 56
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 56
Ile Leu Asp Thr Ala Gly Arg Glu Glu Tyr
1 5 10
<210> 57
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 57
Arg Pro His Val Pro Glu Ser Ala Phe
1 5
<210> 58
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 58
Lys Ile Phe Ser Glu Val Thr Leu Lys
1 5
<210> 59
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 59
Ser His Glu Thr Val Ile Ile Glu Leu
1 5
<210> 60
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 60
Gly Glu Leu Ile Gly Ile Leu Asn Ala Ala Lys Val Pro Ala Asp
1 5 10 15
<210> 61
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 61
Lys Ile Asn Lys Asn Pro Lys Tyr Lys
1 5
<210> 62
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 62
Lys Leu Ser Glu Gln Glu Ser Leu Leu
1 5
<210> 63
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 63
Met Leu Thr Asn Ser Cys Val Lys Leu
1 5
<210> 64
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 64
Phe Met Val Glu Leu Val Glu Gly Ala
1 5
<210> 65
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 65
Gly Val Arg Gly Arg Val Glu Glu Ile
1 5
<210> 66
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 66
Ser Ser Lys Ala Leu Gln Arg Pro Val
1 5
<210> 67
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 67
Ala Thr Gly Phe Lys Gln Ser Ser Lys
1 5
<210> 68
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 68
His Ser Ala Thr Gly Phe Lys Gln Ser Ser Lys
1 5 10
<210> 69
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 69
Lys Gln Ser Ser Lys Ala Leu Gln Arg
1 5
<210> 70
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 70
Gly Phe Lys Gln Ser Ser Lys Ala Leu
1 5
<210> 71
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 71
Ala Thr Gly Phe Lys Gln Ser Ser Lys Ala Leu Gln Arg Pro Val Ala
1 5 10 15
Ser
<210> 72
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 72
Leu Ala Thr Glu Lys Ser Arg Trp Ser
1 5
<210> 73
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 73
Leu Ala Thr Glu Lys Ser Arg Trp Ser Gly
1 5 10
<210> 74
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 74
Phe Gly Leu Ala Thr Glu Lys Ser Arg
1 5
<210> 75
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 75
Gly Asp Phe Gly Leu Ala Thr Glu Lys
1 5
<210> 76
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 76
Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu Ala Thr Glu Lys
1 5 10 15
Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu Ser
20 25
<210> 77
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 77
Phe Leu Ile Ile Trp Gln Asn Thr Met
1 5
<210> 78
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 78
Thr Met Lys Gln Ile Cys Lys Lys Glu Ile Arg Arg Leu His Gln Tyr
1 5 10 15
<210> 79
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (10)..(10)
<223> D-аминокислота
<400> 79
Arg Ile Ala Glu Cys Ile Leu Gly Met Ile
1 5 10
<210> 80
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 80
Ile Gly Arg Ile Ala Glu Cys Ile Leu Gly Met Asn Pro Ser Arg
1 5 10 15
<210> 81
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 81
Tyr Val Asp Phe Arg Glu Tyr Glu Tyr Tyr
1 5 10
<210> 82
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 82
Val Val Met Ser Trp Ala Pro Pro Val
1 5
<210> 83
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (11)..(11)
<223> D-аминокислота
<400> 83
Ser Leu Tyr Lys Phe Ser Pro Phe Pro Leu Gly
1 5 10
<210> 84
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 84
Val Val Pro Cys Glu Pro Pro Glu Val
1 5
<210> 85
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 85
Asn Ser Asn His Val Ala Ser Gly Ala Gly Glu Ala Ala Ile Glu Thr
1 5 10 15
Gln Ser Ser Ser Ser Glu Glu Ile Val
20 25
<210> 86
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 86
Ser Pro Ala Asn Ser Ile Arg His Asn Leu
1 5 10
<210> 87
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 87
Ser Pro Gln Asn Ser Ile Arg His Asn Leu
1 5 10
<210> 88
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 88
Leu Leu Leu Asp Asp Leu Leu Val Ser Ile
1 5 10
<210> 89
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 89
Ala Met Ala Pro Ile Lys Val Arg Leu
1 5
<210> 90
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 90
Gly Tyr Asp Gln Ile Met Pro Lys Lys
1 5
<210> 91
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 91
Gly Tyr Asp Gln Ile Met Pro Lys Ile
1 5
<210> 92
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 92
Gln Arg Pro Tyr Gly Tyr Asp Gln Ile Met
1 5 10
<210> 93
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 93
Leu Glu Glu Lys Lys Gly Asn Tyr Val
1 5
<210> 94
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (10)..(10)
<223> D-аминокислота
<400> 94
Arg Leu Ser Ser Cys Val Pro Val Ala Gly
1 5 10
<210> 95
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 95
Ala Ala Arg Ala Val Phe Leu Ala Leu
1 5
<210> 96
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 96
Lys Pro Leu Phe Arg Arg Met Ser Ser Leu Glu Leu Val Ile Ala
1 5 10 15
<210> 97
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 97
Phe Leu Asp Arg Phe Leu Ser Cys Met
1 5
<210> 98
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 98
Ser Leu Ile Ala Ala Ala Ala Phe Cys Leu Ala
1 5 10
<210> 99
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 99
Tyr Arg Pro Arg Pro Arg Arg Tyr
1 5
<210> 100
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 100
Tyr Tyr Trp Pro Arg Pro Arg Arg Tyr
1 5
<210> 101
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена=" "
<220>
<221> УЧАСТОК
<222> (1)..(10)
<223> /примечание="варианты остатков, приведенные в последовательности, не
имеют приоритета относительно остатков в аннотациях вариантов положений"
<400> 101
Val Leu Pro Asp Val Phe Ile Arg Cys Val
1 5 10
<210> 102
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 102
Phe Leu Ala Glu Leu Ala Tyr Asp Leu
1 5
<210> 103
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 103
Ala Thr Phe Leu Gly Ser Leu Thr Trp Lys
1 5 10
<210> 104
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 104
Met Leu Ala Val Ile Ser Cys Ala Val
1 5
<210> 105
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 105
Arg Gln Lys Arg Ile Leu Val Asn Leu
1 5
<210> 106
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 106
Asn Tyr Asn Asn Phe Tyr Arg Phe Leu
1 5
<210> 107
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 107
Glu Tyr Ser Lys Glu Cys Leu Lys Glu Phe
1 5 10
<210> 108
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 108
Glu Tyr Leu Ser Leu Ser Asp Lys Ile
1 5
<210> 109
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 109
Met Leu Met Ala Gln Glu Ala Leu Ala Phe Leu
1 5 10
<210> 110
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 110
Ser Leu Leu Met Trp Ile Thr Gln Cys
1 5
<210> 111
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 111
Leu Ala Ala Gln Glu Arg Arg Val Pro Arg
1 5 10
<210> 112
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 112
Glu Leu Val Arg Arg Ile Leu Ser Arg
1 5
<210> 113
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 113
Ala Pro Arg Gly Val Arg Met Ala Val
1 5
<210> 114
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 114
Ser Leu Leu Met Trp Ile Thr Gln Cys Phe Leu Pro Val Phe
1 5 10
<210> 115
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 115
Gln Gly Ala Met Leu Ala Ala Gln Glu Arg Arg Val Pro Arg Ala Ala
1 5 10 15
Glu Val Pro Arg
20
<210> 116
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 116
Ala Ala Asp His Arg Gln Leu Gln Leu Ser Ile Ser Ser Cys Leu Gln
1 5 10 15
Gln Leu
<210> 117
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 117
Cys Leu Ser Arg Arg Pro Trp Lys Arg Ser Trp Ser Ala Gly Ser Cys
1 5 10 15
Pro Gly Met Pro His Leu
20
<210> 118
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 118
Ile Leu Ser Arg Asp Ala Ala Pro Leu Pro Arg Pro Gly
1 5 10
<210> 119
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 119
Ala Gly Ala Thr Gly Gly Arg Gly Pro Arg Gly Ala Gly Ala
1 5 10
<210> 120
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 120
Arg Tyr Cys Asn Leu Glu Gly Pro Pro Ile
1 5 10
<210> 121
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 121
Lys Trp Thr Glu Pro Tyr Cys Val Ile Ala Ala Val Lys Ile Phe Pro
1 5 10 15
Arg Phe Phe Met Val Ala Lys Gln
20
<210> 122
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 122
Lys Cys Cys Lys Ile Arg Tyr Cys Asn Leu Glu Gly Pro Pro Ile Asn
1 5 10 15
Ser Ser Val Phe
20
<210> 123
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 123
Glu Ala Asp Pro Thr Gly His Ser Tyr
1 5
<210> 124
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 124
Tyr Leu Glu Tyr Arg Gln Val Pro Val
1 5
<210> 125
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 125
Tyr Leu Glu Tyr Arg Gln Val Pro Asp
1 5
<210> 126
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 126
Lys Val Leu Glu Tyr Val Ile Lys Val
1 5
<210> 127
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 127
Ser Leu Phe Arg Ala Val Ile Thr Lys
1 5
<210> 128
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 128
Asn Tyr Lys His Cys Phe Pro Glu Ile
1 5
<210> 129
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 129
Glu Val Tyr Asp Gly Arg Glu His Ser Ala
1 5 10
<210> 130
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 130
Arg Val Arg Phe Phe Phe Pro Ser Leu
1 5
<210> 131
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 131
Arg Glu Pro Val Thr Lys Ala Glu Met Leu
1 5 10
<210> 132
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 132
Lys Glu Ala Asp Pro Thr Gly His Ser Tyr
1 5 10
<210> 133
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 133
Asp Pro Ala Arg Tyr Glu Phe Leu Trp
1 5
<210> 134
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 134
Ile Thr Lys Lys Val Ala Asp Leu Val Gly Phe
1 5 10
<210> 135
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 135
Ser Ala Phe Pro Thr Thr Ile Asn Phe
1 5
<210> 136
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 136
Ser Ala Tyr Gly Glu Pro Arg Lys Leu
1 5
<210> 137
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 137
Thr Ser Cys Ile Leu Glu Ser Leu Phe Arg Ala Val Ile Thr Lys
1 5 10 15
<210> 138
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 138
Pro Arg Ala Leu Ala Glu Thr Ser Tyr Val Lys Val Leu Glu Tyr
1 5 10 15
<210> 139
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 139
Phe Leu Leu Leu Lys Tyr Arg Ala Arg Glu Pro Val Thr Lys Ala Glu
1 5 10 15
<210> 140
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 140
Glu Tyr Val Ile Lys Val Ser Ala Arg Val Arg Phe
1 5 10
<210> 141
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 141
Tyr Leu Gln Leu Val Phe Gly Ile Glu Val
1 5 10
<210> 142
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 142
Leu Val His Phe Leu Leu Leu Lys Tyr
1 5
<210> 143
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 143
Lys Met Val Glu Leu Val His Phe Leu
1 5
<210> 144
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 144
Leu Val Gln Glu Asn Tyr Leu Glu Tyr
1 5
<210> 145
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 145
Glu Tyr Leu Gln Leu Val Phe Gly Ile
1 5
<210> 146
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 146
Glu Gly Asp Cys Ala Pro Glu Glu Lys
1 5
<210> 147
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 147
Leu Leu Lys Tyr Arg Ala Arg Glu Pro Val Thr Lys Ala Glu
1 5 10
<210> 148
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 148
Glu Val Asp Pro Ile Gly His Leu Tyr
1 5
<210> 149
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (10)..(10)
<223> D-аминокислота
<400> 149
Phe Leu Trp Gly Pro Arg Ala Leu Val Asp
1 5 10
<210> 150
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 150
Lys Val Ala Glu Leu Val His Phe Leu
1 5
<210> 151
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 151
Leu Val Phe Gly Ile Glu Leu Met Glu Val
1 5 10
<210> 152
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 152
Ile Met Pro Lys Ala Gly Leu Leu Ile
1 5
<210> 153
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 153
Thr Phe Pro Asp Leu Glu Ser Glu Phe
1 5
<210> 154
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 154
Val Ala Glu Leu Val His Phe Leu Leu
1 5
<210> 155
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 155
Met Glu Val Asp Pro Ile Gly His Leu Tyr
1 5 10
<210> 156
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 156
Tyr Leu Glu Tyr Arg Gln Val Pro Gly
1 5
<210> 157
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (10)..(10)
<223> D-аминокислота
<400> 157
Ala Glu Leu Val His Phe Leu Leu Leu Ile
1 5 10
<210> 158
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 158
Trp Gln Tyr Phe Phe Pro Val Ile Phe
1 5
<210> 159
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 159
Lys Lys Leu Leu Thr Gln His Phe Val Gln Glu Asn Tyr Leu Glu Tyr
1 5 10 15
<210> 160
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 160
Arg Lys Val Ala Glu Leu Val His Phe Leu Leu Leu Lys Tyr Arg
1 5 10 15
<210> 161
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 161
Ala Cys Tyr Glu Phe Leu Trp Gly Pro Arg Ala Leu Val Glu Thr Ser
1 5 10 15
<210> 162
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 162
Val Ile Phe Ser Lys Ala Ser Ser Ser Leu Gln Leu
1 5 10
<210> 163
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 163
Val Phe Gly Ile Glu Leu Met Glu Val Asp Pro Ile Gly His Leu
1 5 10 15
<210> 164
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 164
Gly Asp Asn Gln Ile Met Pro Lys Ala Gly Leu Leu Ile Ile Val
1 5 10 15
<210> 165
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 165
Thr Ser Tyr Val Lys Val Leu His His Met Val Lys Ile Ser Gly
1 5 10 15
<210> 166
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 166
Arg Lys Val Ala Glu Leu Val His Phe Leu Leu Leu Lys Tyr Arg Ala
1 5 10 15
<210> 167
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="Leu"
<220>
<221> УЧАСТОК
<222> (1)..(10)
<223> /примечание="варианты остатков, приведенные в последовательности, не
имеют приоритета относительно остатков в аннотациях вариантов положений"
<400> 167
Glu Val Asp Pro Ala Ser Asn Thr Tyr Ile
1 5 10
<210> 168
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 168
Gly Val Tyr Asp Gly Arg Glu His Thr Val
1 5 10
<210> 169
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 169
Asn Tyr Lys Arg Cys Phe Pro Val Ile
1 5
<210> 170
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 170
Ser Glu Ser Leu Lys Met Ile Phe
1 5
<210> 171
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 171
Met Val Lys Ile Ser Gly Gly Pro Arg
1 5
<210> 172
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 172
Glu Val Asp Pro Ile Gly His Val Tyr
1 5
<210> 173
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 173
Ile Ser Gly Gly Pro Arg Ile Ser Tyr
1 5
<210> 174
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 174
Lys Val Ala Glu Leu Val Arg Phe Leu
1 5
<210> 175
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 175
Gly Leu Met Asp Val Gln Ile Pro Thr
1 5
<210> 176
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 176
Ala Leu Ser Val Met Gly Val Tyr Val
1 5
<210> 177
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (10)..(10)
<223> D-аминокислота
<400> 177
Gly Leu Tyr Asp Gly Met Glu His Leu Leu
1 5 10
<210> 178
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 178
Ser Leu Leu Lys Phe Leu Ala Lys Val
1 5
<210> 179
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (10)..(10)
<223> D-аминокислота
<400> 179
Phe Leu Trp Gly Pro Arg Ala Leu Val Glu
1 5 10
<210> 180
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 180
Val Arg Ile Gly His Leu Tyr Ile Leu
1 5
<210> 181
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 181
Arg Glu Pro Phe Thr Lys Ala Glu Met Leu Gly Ser Val Ile Arg
1 5 10 15
<210> 182
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 182
Ala Glu Leu Val His Phe Leu Leu Leu Lys Tyr Arg Ala Arg
1 5 10
<210> 183
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 183
Ile Leu Phe Gly Ile Ser Leu Arg Glu Val
1 5 10
<210> 184
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 184
Lys Val Val Glu Phe Leu Ala Met Leu
1 5
<210> 185
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 185
Ser Ser Ala Leu Leu Ser Ile Phe Gln Ser Ser Pro Glu
1 5 10
<210> 186
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 186
Ser Phe Ser Tyr Thr Leu Leu Ser Leu
1 5
<210> 187
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 187
Val Ser Ser Phe Phe Ser Tyr Thr Leu
1 5
<210> 188
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 188
Leu Leu Phe Gly Leu Ala Leu Ile Glu Val
1 5 10
<210> 189
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 189
Ala Leu Lys Asp Val Glu Glu Arg Val
1 5
<210> 190
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 190
Thr Leu Asp Glu Lys Val Ala Glu Leu Val
1 5 10
<210> 191
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 191
Lys Val Leu Glu Phe Leu Ala Lys Leu
1 5
<210> 192
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 192
Phe Leu Ala Lys Leu Asn Asn Thr Val
1 5
<210> 193
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 193
Val Ile Trp Glu Val Leu Asn Ala Val
1 5
<210> 194
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 194
Ser Glu Ser Ile Lys Lys Lys Val Leu
1 5
<210> 195
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 195
Ala Ser Ser Thr Leu Tyr Leu Val Phe
1 5
<210> 196
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 196
Ser Ser Thr Leu Tyr Leu Val Phe Ser Pro Ser Ser Phe Ser Thr
1 5 10 15
<210> 197
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 197
Phe Leu Trp Gly Pro Arg Ala Leu Ala
1 5
<210> 198
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 198
Gln Leu Val Phe Gly Ile Glu Val Val
1 5
<210> 199
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 199
Pro Asp Thr Arg Pro Ala Pro Gly Ser Thr Ala Pro Pro Ala His Gly
1 5 10 15
Val Thr Ser Ala
20
<210> 200
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 200
Gln Gly Gln His Phe Leu Gln Lys Val
1 5
<210> 201
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 201
Ser Leu Leu Met Trp Ile Thr Gln Cys Phe Leu
1 5 10
<210> 202
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 202
Gln Leu Ser Leu Leu Met Trp Ile Thr
1 5
<210> 203
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 203
Leu Leu Met Trp Ile Thr Gln Cys Phe
1 5
<210> 204
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 204
Tyr Leu Ala Met Pro Phe Ala Thr Pro Met Glu
1 5 10
<210> 205
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 205
Ala Ser Gly Pro Gly Gly Gly Ala Pro Arg
1 5 10
<210> 206
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 206
Thr Val Ser Gly Asn Ile Leu Thr Ile Arg
1 5 10
<210> 207
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 207
Ala Pro Arg Gly Pro His Gly Gly Ala Ala Ser Gly Leu
1 5 10
<210> 208
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 208
Met Pro Phe Ala Thr Pro Met Glu Ala Glu Leu
1 5 10
<210> 209
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 209
Lys Glu Phe Thr Val Ser Gly Asn Ile Leu Thr Ile
1 5 10
<210> 210
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 210
Met Pro Phe Ala Thr Pro Met Glu Ala
1 5
<210> 211
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 211
Phe Ala Thr Pro Met Glu Ala Glu Leu
1 5
<210> 212
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 212
Phe Ala Thr Pro Met Glu Ala Glu Leu Ala Arg
1 5 10
<210> 213
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 213
Leu Ala Met Pro Phe Ala Thr Pro Met
1 5
<210> 214
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 214
Ala Arg Gly Pro Glu Ser Arg Leu Leu
1 5
<210> 215
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 215
Leu Leu Glu Phe Tyr Leu Ala Met Pro Phe Ala Thr Pro Met Glu Ala
1 5 10 15
Glu Leu Ala Arg Arg Ser Leu Ala Gln
20 25
<210> 216
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 216
Glu Phe Tyr Leu Ala Met Pro Phe Ala Thr Pro Met
1 5 10
<210> 217
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 217
Pro Gly Val Leu Leu Lys Glu Phe Thr Val Ser Gly Asn Ile Leu Thr
1 5 10 15
Ile Arg Leu Thr Ala Ala Asp His Arg
20 25
<210> 218
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 218
Arg Leu Leu Glu Phe Tyr Leu Ala Met Pro Phe Ala
1 5 10
<210> 219
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 219
Pro Phe Ala Thr Pro Met Glu Ala Glu Leu Ala Arg Arg
1 5 10
<210> 220
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 220
Pro Gly Val Leu Leu Lys Glu Phe Thr Val Ser Gly Asn Ile Leu Thr
1 5 10 15
Ile Arg Leu Thr
20
<210> 221
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 221
Val Leu Leu Lys Glu Phe Thr Val Ser Gly
1 5 10
<210> 222
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 222
Leu Lys Glu Phe Thr Val Ser Gly Asn Ile Leu Thr Ile Arg Leu
1 5 10 15
<210> 223
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 223
Lys Glu Phe Thr Val Ser Gly Asn Ile Leu Thr
1 5 10
<210> 224
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 224
Leu Leu Glu Phe Tyr Leu Ala Met Pro Phe Ala Thr Pro Met
1 5 10
<210> 225
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 225
Val Leu Gln Glu Leu Asn Val Thr Val
1 5
<210> 226
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 226
Ala Leu Cys Asn Thr Asp Ser Pro Leu
1 5
<210> 227
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 227
Leu Leu Ala Ala Arg Ala Ile Val Ala Ile
1 5 10
<210> 228
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 228
Thr Ser Thr Thr Ser Leu Glu Leu Asp
1 5
<210> 229
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 229
Phe Leu His His Leu Ile Ala Glu Ile His
1 5 10
<210> 230
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 230
Asp Leu Trp Lys Glu Thr Val Phe Thr
1 5
<210> 231
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 231
Leu Tyr Ala Thr Val Ile His Asp Ile
1 5
<210> 232
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 232
Ile Leu Asp Ser Ser Glu Glu Asp Lys
1 5
<210> 233
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 233
Lys Ala Ser Glu Lys Ile Phe Tyr Val
1 5
<210> 234
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 234
Arg Leu Gln Gly Ile Ser Pro Lys Ile
1 5
<210> 235
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 235
Glu Lys Ile Gln Lys Ala Phe Asp Asp Ile Ala Lys Tyr Phe Ser Lys
1 5 10 15
<210> 236
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 236
Phe Gly Arg Leu Gln Gly Ile Ser Pro Lys Ile
1 5 10
<210> 237
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 237
Trp Glu Lys Met Lys Ala Ser Glu Lys Ile Phe Tyr Val Tyr Met Lys
1 5 10 15
Arg Lys
<210> 238
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 238
Lys Ile Phe Tyr Val Tyr Met Lys Arg Lys Tyr Glu Ala Met Thr
1 5 10 15
<210> 239
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 239
Lys Ile Phe Tyr Val Tyr Met Lys Arg Lys Tyr Glu Ala Met
1 5 10
<210> 240
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 240
Ile Asn Lys Thr Ser Gly Pro Lys Arg Gly Lys His Ala Trp Thr His
1 5 10 15
Arg Leu Arg Glu
20
<210> 241
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 241
Tyr Phe Ser Lys Lys Glu Trp Glu Lys Met Lys Ser Ser Glu Lys Ile
1 5 10 15
Val Tyr Val Tyr
20
<210> 242
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 242
Met Lys Leu Asn Tyr Glu Val Met Thr Lys Leu Gly Phe Lys Val Thr
1 5 10 15
Leu Pro Pro Phe
20
<210> 243
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 243
Lys His Ala Trp Thr His Arg Leu Arg Glu Arg Lys Gln Leu Val Val
1 5 10 15
Tyr Glu Glu Ile
20
<210> 244
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 244
Leu Gly Phe Lys Val Thr Leu Pro Pro Phe Met Arg Ser Lys Arg Ala
1 5 10 15
Ala Asp Phe His
20
<210> 245
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 245
Lys Ser Ser Glu Lys Ile Val Tyr Val Tyr Met Lys Leu Asn Tyr Glu
1 5 10 15
Val Met Thr Lys
20
<210> 246
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 246
Arg Leu Ser Asn Arg Leu Leu Leu Arg
1 5
<210> 247
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 247
Ser Leu Gly Trp Leu Phe Leu Leu Leu
1 5
<210> 248
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 248
Leu Ser Arg Leu Ser Asn Arg Leu Leu
1 5
<210> 249
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 249
Leu Thr Tyr Val Ser Phe Arg Asn Leu
1 5
<210> 250
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 250
Asp Leu Pro Ala Tyr Val Arg Asn Leu
1 5
<210> 251
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 251
Phe Leu Thr Gly Asn Gln Leu Ala Val
1 5
<210> 252
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 252
Gly Ala Phe Glu His Leu Pro Ser Leu
1 5
<210> 253
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 253
Arg Leu Ala Arg Leu Ala Leu Val Leu
1 5
<210> 254
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 254
Pro Leu Ala Asp Leu Ser Pro Phe Ala
1 5
<210> 255
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 255
Ile Leu Leu Arg Asp Ala Gly Leu Val
1 5
<210> 256
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 256
Cys Glu Phe His Ala Cys Trp Pro Ala Phe Thr Val Leu Gly Glu
1 5 10 15
<210> 257
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 257
Ala Thr Thr Asn Ile Leu Glu His Tyr
1 5
<210> 258
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 258
Glu Val Ile Ser Cys Lys Leu Ile Lys Arg
1 5 10
<210> 259
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 259
Ser Tyr Arg Asn Glu Ile Ala Tyr Leu
1 5
<210> 260
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 260
Arg Gln Lys Lys Ile Arg Ile Gln Leu
1 5
<210> 261
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 261
His Leu Gly Ser Arg Gln Lys Lys Ile Arg Ile Gln Leu Arg Ser Gln
1 5 10 15
<210> 262
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 262
Cys Ala Thr Trp Lys Val Ile Cys Lys Ser Cys Ile Ser Gln Thr Pro
1 5 10 15
Gly
<210> 263
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 263
Ala Phe Leu Arg His Ala Ala Leu
1 5
<210> 264
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 264
Asp Tyr Pro Ser Leu Ser Ala Thr Asp Ile
1 5 10
<210> 265
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 265
Tyr Met Met Pro Val Asn Ser Glu Val
1 5
<210> 266
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 266
Lys Leu Ala Thr Ala Gln Phe Lys Ile
1 5
<210> 267
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 267
Val Tyr Val Lys Gly Leu Leu Ala Lys Ile
1 5 10
<210> 268
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 268
Ala Leu Val Asp Ala Gly Val Pro Met
1 5
<210> 269
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 269
Phe Leu Trp Gly Pro Arg Ala Tyr Ala
1 5
<210> 270
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 270
Arg Leu Leu Val Pro Thr Gln Phe Val
1 5
<210> 271
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 271
Asn Leu Ser Ser Ala Glu Val Val Val
1 5
<210> 272
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 272
Lys Thr Val Asn Glu Leu Gln Asn Leu
1 5
<210> 273
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 273
Phe Leu Pro Asp His Ile Asn Ile Val
1 5
<210> 274
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 274
Lys Thr Pro Phe Val Ser Pro Leu Leu
1 5
<210> 275
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 275
Gln Leu Leu Asp Gly Phe Met Ile Thr Leu
1 5 10
<210> 276
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 276
Tyr Leu Val Gly Asn Val Cys Ile Leu
1 5
<210> 277
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 277
Glu Leu Ser Asp Ser Leu Gly Pro Val
1 5
<210> 278
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 278
Ile Leu Ser Leu Glu Leu Met Lys Leu
1 5
<210> 279
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 279
Ser Leu Glu Glu Asn Ile Val Ile Leu
1 5
<210> 280
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 280
Lys Gly Ser Gly Lys Met Lys Thr Glu
1 5
<210> 281
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 281
Glu Tyr Arg Gly Phe Thr Gln Asp Phe
1 5
<210> 282
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 282
Arg Leu Ala Glu Tyr Gln Ala Tyr Ile
1 5
<210> 283
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 283
Leu Leu Gln Ala Glu Ala Pro Arg Leu
1 5
<210> 284
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 284
Trp Leu Glu Tyr Tyr Asn Leu Glu Arg
1 5
<210> 285
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 285
Gln Ile Arg Pro Ile Phe Ser Asn Arg
1 5
<210> 286
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 286
Val Tyr Asp Tyr Asn Cys His Val Asp Leu
1 5 10
<210> 287
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 287
Ala Tyr Ile Asp Phe Glu Met Lys Ile
1 5
<210> 288
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (10)..(10)
<223> D-аминокислота
<400> 288
Tyr Leu Ser Gly Ala Asn Leu Asn Leu Gly
1 5 10
<210> 289
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 289
Ile Met Ile Gly Val Leu Val Gly Val
1 5
<210> 290
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 290
Gly Val Leu Val Gly Val Ala Leu Ile
1 5
<210> 291
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 291
Val Leu Tyr Gly Pro Asp Ala Pro Thr Val
1 5 10
<210> 292
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 292
Tyr Leu Ser Gly Ala Asn Leu Asn Val
1 5
<210> 293
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 293
Ala Thr Val Gly Ile Met Ile Gly Val
1 5
<210> 294
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 294
His Leu Phe Gly Tyr Ser Trp Tyr Lys
1 5
<210> 295
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 295
Gln Tyr Ser Trp Phe Val Asn Gly Thr Phe
1 5 10
<210> 296
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 296
Thr Tyr Ala Cys Phe Val Ser Asn Leu
1 5
<210> 297
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 297
His Arg Trp Cys Ile Pro Trp Gln Arg Leu
1 5 10
<210> 298
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 298
Ala Tyr Val Cys Gly Ile Gln Asn Ser Val Ser Ala Asn Arg Ser
1 5 10 15
<210> 299
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 299
Asp Thr Gly Phe Tyr Thr Leu His Val Ile Lys Ser Asp Leu Val Asn
1 5 10 15
Glu Glu Ala Thr Gly Gln Phe Arg Val
20 25
<210> 300
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 300
Tyr Ser Trp Arg Ile Asn Gly Ile Pro Gln Gln His Thr Gln Val
1 5 10 15
<210> 301
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 301
Thr Tyr Tyr Arg Pro Gly Val Asn Leu Ser Leu Ser Cys
1 5 10
<210> 302
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 302
Glu Ile Ile Tyr Pro Asn Ala Ser Leu Leu Ile Gln Asn
1 5 10
<210> 303
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 303
Tyr Ala Cys Phe Val Ser Asn Leu Ala Thr Gly Arg Asn Asn Ser
1 5 10 15
<210> 304
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 304
Leu Trp Trp Val Asn Asn Gln Ser Leu Pro Val Ser Pro
1 5 10
<210> 305
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 305
Asn Ser Ile Val Lys Ser Ile Thr Val Ser Ala Ser Gly
1 5 10
<210> 306
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 306
Lys Thr Trp Gly Gln Tyr Trp Gln Val
1 5
<210> 307
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена=" "
<220>
<221> УЧАСТОК
<222> (1)..(10)
<223> /примечание="варианты остатков, приведенные в последовательности, не
имеют приоритета относительно остатков в аннотациях вариантов положений"
<400> 307
Ala Met Leu Gly Thr His Thr Met Glu Val
1 5 10
<210> 308
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 308
Ile Met Asp Gln Val Pro Phe Ser Val
1 5
<210> 309
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 309
Ile Thr Asp Gln Val Pro Phe Ser Val
1 5
<210> 310
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 310
Tyr Leu Glu Pro Gly Pro Val Thr Ala
1 5
<210> 311
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 311
Leu Leu Asp Gly Thr Ala Thr Leu Arg Leu
1 5 10
<210> 312
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 312
Val Leu Tyr Arg Tyr Gly Ser Phe Ser Val
1 5 10
<210> 313
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 313
Ser Leu Ala Asp Thr Asn Ser Leu Ala Val
1 5 10
<210> 314
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 314
Arg Leu Met Lys Gln Asp Phe Ser Val
1 5
<210> 315
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 315
Arg Leu Pro Arg Ile Phe Cys Ser Cys
1 5
<210> 316
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 316
Leu Ile Tyr Arg Arg Arg Leu Met Lys
1 5
<210> 317
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 317
Ala Leu Leu Ala Val Gly Ala Thr Lys
1 5
<210> 318
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 318
Ile Ala Leu Asn Phe Pro Gly Ser Gln Lys
1 5 10
<210> 319
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 319
Arg Ser Tyr Val Pro Leu Ala His Arg
1 5
<210> 320
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 320
Ala Leu Asn Phe Pro Gly Ser Gln Lys
1 5
<210> 321
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 321
Val Tyr Phe Phe Leu Pro Asp His Leu
1 5
<210> 322
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 322
Arg Thr Lys Gln Leu Tyr Pro Glu Trp
1 5
<210> 323
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 323
His Thr Met Glu Val Thr Val Tyr His Arg
1 5 10
<210> 324
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 324
Ser Ser Pro Gly Cys Gln Pro Pro Ala
1 5
<210> 325
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 325
Val Pro Leu Asp Cys Val Leu Tyr Arg Tyr
1 5 10
<210> 326
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 326
Leu Pro His Ser Ser Ser His Trp Leu
1 5
<210> 327
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 327
Ser Asn Asp Gly Pro Thr Leu Ile
1 5
<210> 328
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 328
Gly Arg Ala Met Leu Gly Thr His Thr Met Glu Val Thr Val Tyr
1 5 10 15
<210> 329
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 329
Trp Asn Arg Gln Leu Tyr Pro Glu Trp Thr Glu Ala Gln Arg Leu Asp
1 5 10 15
<210> 330
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 330
Thr Thr Glu Trp Val Glu Thr Thr Ala Arg Glu Leu Pro Ile Pro Glu
1 5 10 15
Pro Glu
<210> 331
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 331
Thr Gly Arg Ala Met Leu Gly Thr His Thr Met Glu Val Thr Val Tyr
1 5 10 15
His
<210> 332
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 332
Phe Leu Asn Gln Thr Asp Glu Thr Leu
1 5
<210> 333
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 333
Met Gln Leu Ile Tyr Asp Ser Ser Leu
1 5
<210> 334
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 334
Lys Leu Leu Met Val Leu Met Leu Ala
1 5
<210> 335
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 335
Leu Ile Tyr Asp Ser Ser Leu Cys Asp Leu
1 5 10
<210> 336
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 336
Ala Ile Asp Glu Leu Lys Glu Cys Phe
1 5
<210> 337
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 337
Thr Thr Asn Ala Ile Asp Glu Leu Lys
1 5
<210> 338
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 338
Pro Leu Leu Glu Asn Val Ile Ser Lys
1 5
<210> 339
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена=" "
<220>
<221> УЧАСТОК
<222> (1)..(10)
<223> /примечание="варианты остатков, приведенные в последовательности, не
имеют приоритета относительно остатков в аннотациях вариантов положений"
<400> 339
Glu Ala Ala Gly Ile Gly Ile Leu Thr Val
1 5 10
<210> 340
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 340
Ile Leu Thr Val Ile Leu Gly Val Leu
1 5
<210> 341
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 341
Glu Ala Ala Gly Ile Gly Ile Leu Thr Val
1 5 10
<210> 342
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена=" "
<220>
<221> УЧАСТОК
<222> (1)..(10)
<223> /примечание="варианты остатков, приведенные в последовательности, не
имеют приоритета относительно остатков в аннотациях вариантов положений"
<400> 342
Ala Glu Glu Ala Ala Gly Ile Gly Ile Leu Thr
1 5 10
<210> 343
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 343
Arg Asn Gly Tyr Arg Ala Leu Met Asp Lys Ser
1 5 10
<210> 344
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 344
Tyr Thr Thr Ala Glu Glu Ala Ala Gly Ile Gly Ile Leu Thr Val Ile
1 5 10 15
Leu Gly Val Leu Leu Leu Ile Gly Cys Trp Tyr Cys Arg Arg
20 25 30
<210> 345
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 345
Glu Glu Ala Ala Gly Ile Gly Ile Leu Thr Val Ile
1 5 10
<210> 346
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 346
Ala Ala Gly Ile Gly Ile Leu Thr Val Ile Leu Gly Val Leu
1 5 10
<210> 347
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (9)..(9)
<223> D-аминокислота
<220>
<221> MOD_RES
<222> (14)..(14)
<223> D-аминокислота
<400> 347
Ala Pro Pro Ala Tyr Glu Lys Leu Pro Ser Ala Glu Gln Phe
1 5 10
<210> 348
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 348
Arg Asn Gly Tyr Arg Ala Leu Met Asp Lys Ser Leu His Val Gly Thr
1 5 10 15
Gln Cys Ala Leu Thr Arg Arg
20
<210> 349
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 349
Met Pro Arg Glu Asp Ala His Phe Ile Tyr Gly Tyr Pro Lys Lys Gly
1 5 10 15
His Gly His Ser
20
<210> 350
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 350
Lys Asn Cys Glu Pro Val Val Pro Asn Ala Pro Pro Ala Tyr Glu Lys
1 5 10 15
Leu Ser Ala Glu
20
<210> 351
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 351
Thr Ile Leu Leu Gly Ile Phe Phe Leu
1 5
<210> 352
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 352
Phe Leu Ala Leu Ile Ile Cys Asn Ala
1 5
<210> 353
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 353
Lys Leu Leu Gly Pro His Val Glu Gly Leu
1 5 10
<210> 354
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 354
Lys Leu Leu Gly Pro His Val Leu Gly Val
1 5 10
<210> 355
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 355
Gly Leu Phe Asp Glu Tyr Leu Glu Met Val
1 5 10
<210> 356
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 356
Ser Leu Ser Lys Ile Leu Asp Thr Val
1 5
<210> 357
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 357
Leu Leu Ser His Gly Ala Val Ile Glu Val
1 5 10
<210> 358
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 358
Leu Tyr Ser Ala Cys Phe Trp Trp Leu
1 5
<210> 359
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 359
Ile Met Leu Cys Leu Ile Ala Ala Val
1 5
<210> 360
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 360
Phe Leu Thr Pro Lys Lys Leu Gln Cys Val
1 5 10
<210> 361
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 361
Val Ile Ser Asn Asp Val Cys Ala Gln Val
1 5 10
<210> 362
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 362
Val Leu His Trp Asp Pro Glu Thr Val
1 5
<210> 363
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 363
Phe Leu Arg Asn Phe Ser Leu Met Val
1 5
<210> 364
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 364
Phe Val Phe Leu Arg Asn Phe Ser Leu
1 5
<210> 365
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 365
Phe Leu Arg Asn Phe Ser Leu Met Leu
1 5
<210> 366
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 366
Met Ser Leu Gln Arg Gln Phe Leu Arg
1 5
<210> 367
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 367
Ile Ser Pro Asn Ser Val Phe Ser Gln Trp Arg Val Val Cys Asp Ser
1 5 10 15
Leu Glu Asp Tyr Asp
20
<210> 368
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 368
Ser Leu Pro Tyr Trp Asn Phe Ala Thr Gly
1 5 10
<210> 369
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 369
Ser Gln Trp Arg Val Val Cys Asp Ser Leu Glu Asp Tyr Asp Thr
1 5 10 15
<210> 370
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 370
Val Tyr Asp Phe Phe Val Trp Leu His Tyr
1 5 10
<210> 371
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 371
Ser Leu Asp Asp Tyr Asn His Leu Val
1 5
<210> 372
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 372
Phe Val Trp Leu His Tyr Tyr Ser Val
1 5
<210> 373
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 373
Ser Val Tyr Asp Phe Phe Val Trp Leu
1 5
<210> 374
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 374
Thr Leu Asp Ser Gln Val Met Ser Leu
1 5
<210> 375
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 375
Leu Leu Gly Pro Gly Arg Pro Tyr Arg
1 5
<210> 376
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 376
Ala Asn Asp Pro Ile Phe Val Val Leu
1 5
<210> 377
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 377
Gln Cys Thr Glu Val Arg Ala Asp Thr Arg Pro Trp Ser Gly Pro
1 5 10 15
<210> 378
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 378
Ala Leu Pro Tyr Trp Asn Phe Ala Thr Gly
1 5 10
<210> 379
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 379
Lys Cys Asp Ile Cys Thr Asp Glu Tyr
1 5
<210> 380
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 380
Asp Ser Asp Pro Asp Ser Phe Gln Asp Tyr
1 5 10
<210> 381
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 381
Ser Ser Asp Tyr Val Ile Pro Ile Gly Thr Tyr
1 5 10
<210> 382
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 382
Met Leu Leu Ala Val Leu Tyr Cys Leu
1 5
<210> 383
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 383
Cys Leu Leu Trp Ser Phe Gln Thr Ser Ala
1 5 10
<210> 384
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 384
Tyr Met Asp Gly Thr Met Ser Gln Val
1 5
<210> 385
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 385
Ala Phe Leu Pro Trp His Arg Leu Phe
1 5
<210> 386
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 386
Ile Tyr Met Asp Gly Thr Ala Asp Phe Ser Phe
1 5 10
<210> 387
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 387
Gln Cys Ser Gly Asn Phe Met Gly Phe
1 5
<210> 388
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 388
Thr Pro Arg Leu Pro Ser Ser Ala Asp Val Glu Phe
1 5 10
<210> 389
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 389
Leu Pro Ser Ser Ala Asp Val Glu Phe
1 5
<210> 390
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 390
Leu His His Ala Phe Val Asp Ser Ile Phe
1 5 10
<210> 391
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (10)..(10)
<223> D-аминокислота
<400> 391
Ser Glu Ile Trp Arg Asp Ile Asp Phe Asp
1 5 10
<210> 392
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 392
Gln Asn Ile Leu Leu Ser Asn Ala Pro Leu Gly Pro Gln Phe Pro
1 5 10 15
<210> 393
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 393
Ser Tyr Leu Gln Asp Ser Asp Pro Asp Ser Phe Gln Asp
1 5 10
<210> 394
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 394
Phe Leu Leu His His Ala Phe Val Asp Ser Ile Phe Glu Gln Trp Leu
1 5 10 15
Gln Arg His Arg Pro
20
<210> 395
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 395
Ser Ala Cys Asp Val Ser Val Arg Val Val
1 5 10
<210> 396
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 396
Tyr Thr Asp Phe Val Gly Glu Gly Leu
1 5
<210> 397
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 397
Tyr Leu Ile Glu Leu Ile Asp Arg Val
1 5
<210> 398
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 398
Ser Val Ala Ser Thr Ile Thr Gly Val
1 5
<210> 399
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 399
Cys Ile Thr Phe Gln Val Trp Asp Val
1 5
<210> 400
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 400
Phe Leu Pro His Phe Gln Ala Leu His Val
1 5 10
<210> 401
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 401
Arg Ser Asp Ser Gly Gln Gln Ala Arg Tyr
1 5 10
<210> 402
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 402
Leu Leu Tyr Lys Leu Ala Asp Leu Ile
1 5
<210> 403
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 403
Ser Leu Ala Met Leu Asp Leu Leu His Val
1 5 10
<210> 404
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 404
Met Val Tyr Asp Leu Tyr Lys Thr Leu
1 5
<210> 405
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 405
Arg Leu Asp Phe Asn Leu Ile Arg Val
1 5
<210> 406
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 406
Gly Leu Gln His Trp Val Pro Glu Leu
1 5
<210> 407
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 407
Asn Leu Phe Glu Thr Pro Val Glu Ala
1 5
<210> 408
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 408
Lys Leu Asp Val Gly Asn Ala Glu Val
1 5
<210> 409
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 409
Tyr Leu Leu Gln Gly Met Ile Ala Ala Val
1 5 10
<210> 410
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 410
Tyr Leu Gln Gly Met Ile Ala Ala Val
1 5
<210> 411
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 411
Pro Leu Phe Asp Phe Ser Trp Leu Ser Leu
1 5 10
<210> 412
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 412
Trp Leu Ser Leu Lys Thr Leu Leu Ser Leu
1 5 10
<210> 413
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 413
Tyr Leu Asn Asp His Leu Glu Pro Trp Ile
1 5 10
<210> 414
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 414
Cys Gln Trp Gly Arg Leu Trp Gln Leu
1 5
<210> 415
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 415
Val Phe Leu Pro Cys Asp Ser Trp Asn Leu
1 5 10
<210> 416
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 416
Cys Ile Pro Pro Asp Ser Leu Leu Phe Pro Ala
1 5 10
<210> 417
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 417
Tyr Thr Leu Asp Arg Asp Ser Leu Tyr Val
1 5 10
<210> 418
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 418
Phe Ile Ile Glu Asn Leu Lys Ala Ala
1 5
<210> 419
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 419
Phe Ile Leu Pro Val Leu Gly Ala Val
1 5
<210> 420
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 420
Val Leu Leu Gln Ala Gly Ser Leu His Ala
1 5 10
<210> 421
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 421
Leu Leu Gly Asn Cys Leu Pro Thr Val
1 5
<210> 422
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 422
Ser Leu Gln Ala Leu Lys Val Thr Val
1 5
<210> 423
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 423
Lys Phe Leu Asp Ala Leu Ile Ser Leu
1 5
<210> 424
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 424
Leu Leu Asn Ala Phe Thr Val Thr Val
1 5
<210> 425
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 425
Phe Ala Trp Glu Arg Val Arg Gly Leu
1 5
<210> 426
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 426
Gly Leu Gly Leu Pro Lys Leu Tyr Leu
1 5
<210> 427
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 427
Leu Met Ala Gly Cys Ile Gln Glu Ala
1 5
<210> 428
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 428
Leu Leu Glu Glu Met Phe Leu Thr Val
1 5
<210> 429
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 429
Lys Val His Pro Val Ile Trp Ser Leu
1 5
<210> 430
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 430
Leu Met Leu Gln Asn Ala Leu Thr Thr Met
1 5 10
<210> 431
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 431
Tyr Val Asp Pro Val Ile Thr Ser Ile
1 5
<210> 432
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 432
Phe Met Thr Arg Lys Leu Trp Asp Leu
1 5
<210> 433
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 433
Arg Leu Leu Ala Ser Leu Gln Asp Leu
1 5
<210> 434
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 434
Ala Leu Tyr Gly Asp Ile Asp Ala Val
1 5
<210> 435
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 435
Leu Leu Asp Arg Phe Leu Ala Thr Val
1 5
<210> 436
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 436
Ile Leu Ile Asp Trp Leu Val Gln Val
1 5
<210> 437
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 437
Ala Lys Tyr Leu Met Glu Leu Thr Met
1 5
<210> 438
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 438
Ala Gly Tyr Leu Met Glu Leu Cys Cys
1 5
<210> 439
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 439
Leu Leu Gly Ala Thr Cys Met Phe Val
1 5
<210> 440
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 440
Asn Pro Pro Ser Met Val Ala Ala Gly Ser Val Val Ala Ala Val
1 5 10 15
<210> 441
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 441
Val Leu Glu Gly Met Glu Val Val
1 5
<210> 442
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 442
Lys Leu Lys His Tyr Gly Pro Gly Trp Val
1 5 10
<210> 443
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 443
Asp Phe Met Ile Gln Gly Gly Asp Phe
1 5
<210> 444
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 444
Lys Phe His Arg Val Ile Lys Asp Phe
1 5
<210> 445
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 445
Trp Leu Gln Tyr Phe Pro Asn Pro Val
1 5
<210> 446
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 446
Ala Leu Gly Gly His Pro Leu Leu Gly Val
1 5 10
<210> 447
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 447
Ile Thr Asp Phe Gly Leu Ala Lys Leu
1 5
<210> 448
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 448
Thr Met Asn Gly Ser Lys Ser Pro Val
1 5
<210> 449
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 449
Tyr Gln Leu Asp Pro Lys Phe Ile Val
1 5
<210> 450
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 450
Gly Leu Lys Ala Gly Val Ile Ala Val
1 5
<210> 451
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 451
Ile Leu Tyr Glu Asn Asn Val Ile Thr Val
1 5 10
<210> 452
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 452
Ile Leu Tyr Glu Asn Asn Val Ile Val
1 5
<210> 453
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 453
Arg Tyr Gln Leu Asp Pro Lys Phe Ile
1 5
<210> 454
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 454
Val Leu Leu Leu Val Leu Ala Gly Val
1 5
<210> 455
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 455
Thr Leu Ala Asp Phe Asp Pro Arg Val
1 5
<210> 456
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 456
Val Leu Ala Gly Val Gly Phe Phe Ile
1 5
<210> 457
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 457
Ile Met Asn Asp Met Pro Ile Tyr Met
1 5
<210> 458
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 458
Asp Val Thr Phe Asn Ile Ile Cys Lys Lys Cys Gly
1 5 10
<210> 459
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 459
Phe Met Val Glu Asp Glu Thr Val Leu
1 5
<210> 460
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 460
Phe Ile Asn Asp Glu Ile Phe Val Glu Leu
1 5 10
<210> 461
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 461
Lys Tyr Asp Cys Phe Leu His Pro Phe
1 5
<210> 462
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 462
Lys Tyr Val Gly Ile Glu Arg Glu Met
1 5
<210> 463
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (10)..(10)
<223> D-аминокислота
<400> 463
Asn Thr Tyr Ala Ser Pro Arg Phe Lys Phe
1 5 10
<210> 464
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 464
Phe Val Gly Glu Phe Phe Thr Asp Val
1 5
<210> 465
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 465
Glu Tyr Ile Leu Ser Leu Glu Glu Leu
1 5
<210> 466
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 466
His Leu Ser Thr Ala Phe Ala Arg Val
1 5
<210> 467
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 467
Lys Tyr Leu Lys Leu Ser Ser Ser Glu Leu
1 5 10
<210> 468
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 468
Thr Met Thr Arg Val Leu Gln Gly Val
1 5
<210> 469
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 469
Gly Val Asn Pro Val Val Ser Tyr Ala Val
1 5 10
<210> 470
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 470
Val Leu Gln Val Gly Leu Pro Ala Leu
1 5
<210> 471
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 471
Pro Ala Phe Ser Tyr Ser Phe Phe Val
1 5
<210> 472
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 472
Leu Leu Leu Gly Pro Leu Gly Pro Leu
1 5
<210> 473
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 473
Lys Met Leu Lys Ser Phe Leu Lys Ala
1 5
<210> 474
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 474
Ala Leu Pro Pro Pro Leu Met Leu Leu
1 5
<210> 475
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 475
Trp Leu Ser Leu Leu Phe Lys Lys Leu
1 5
<210> 476
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 476
Lys Ile Phe Gly Ser Leu Ala Phe Leu
1 5
<210> 477
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 477
Ile Ile Ser Ala Val Val Gly Ile Leu
1 5
<210> 478
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 478
Ala Leu Cys Arg Trp Gly Leu Leu Leu
1 5
<210> 479
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 479
Ile Leu His Asn Gly Ala Tyr Ser Leu
1 5
<210> 480
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 480
Arg Leu Leu Gln Glu Thr Glu Leu Val
1 5
<210> 481
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 481
Val Val Leu Gly Val Val Phe Gly Ile
1 5
<210> 482
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 482
Tyr Met Ile Met Val Lys Cys Trp Met Ile
1 5 10
<210> 483
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 483
His Leu Tyr Gln Gly Cys Gln Val Val
1 5
<210> 484
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 484
Tyr Leu Val Pro Gln Gln Gly Phe Phe Cys
1 5 10
<210> 485
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 485
Pro Leu Gln Pro Glu Gln Leu Gln Val
1 5
<210> 486
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 486
Thr Leu Glu Glu Ile Thr Gly Tyr Leu
1 5
<210> 487
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 487
Ala Leu Ile His His Asn Thr His Leu
1 5
<210> 488
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 488
Pro Leu Thr Ser Ile Ile Ser Ala Val
1 5
<210> 489
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 489
Lys Leu Phe Gly Ser Leu Ala Phe Val
1 5
<210> 490
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 490
Ile Thr Asp Phe Gly Leu Ala Arg Leu
1 5
<210> 491
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 491
Lys Val Phe Gly Ser Leu Ala Phe Val
1 5
<210> 492
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 492
Ala Val Val Gly Ile Leu Leu Val Val
1 5
<210> 493
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 493
Gln Leu Phe Glu Asp Asn Tyr Ala Leu
1 5
<210> 494
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 494
Gln Ile Ala Lys Gly Met Ser Tyr Leu
1 5
<210> 495
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 495
Leu Ile Ala His Asn Gln Val Arg Gln Val
1 5 10
<210> 496
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 496
Val Leu Arg Glu Asn Thr Ser Pro Lys
1 5
<210> 497
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 497
Thr Tyr Leu Pro Thr Asn Ala Ser Leu
1 5
<210> 498
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 498
Arg Tyr Ala Met Thr Val Trp Tyr Phe
1 5
<210> 499
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 499
Phe Leu Leu Gly Leu Ile Phe Leu Leu
1 5
<210> 500
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 500
Leu Leu Leu Gly Ile Gly Ile Leu Val
1 5
<210> 501
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 501
Leu Leu Gln Leu Gly Tyr Ser Gly Arg Leu
1 5 10
<210> 502
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 502
Leu Leu Gln Leu Tyr Ser Gly Arg Leu
1 5
<210> 503
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 503
Ser Leu Leu Ser Gly Asp Trp Val Leu
1 5
<210> 504
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 504
Gly Leu Gln Leu Gly Val Gln Ala Val
1 5
<210> 505
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 505
Pro Leu Thr Glu Tyr Ile Gln Pro Val
1 5
<210> 506
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 506
Ala Pro Leu Leu Arg Trp Val Leu
1 5
<210> 507
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 507
Leu Leu Leu Leu Asp Val Ala Pro Leu
1 5
<210> 508
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 508
Leu Leu Asp Val Ala Pro Leu Ser Leu
1 5
<210> 509
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 509
Tyr Ser Trp Met Asp Ile Ser Cys Trp Ile
1 5 10
<210> 510
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 510
Ser Pro Arg Trp Trp Pro Thr Cys Leu
1 5
<210> 511
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 511
Ala Leu Leu Glu Ile Ala Ser Cys Leu
1 5
<210> 512
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 512
Ala Pro Ala Gly Arg Pro Ser Ala Ser Arg
1 5 10
<210> 513
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 513
Arg Ser Arg Arg Val Leu Tyr Pro Arg
1 5
<210> 514
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 514
Ala Pro Ala Gly Arg Pro Ser Ala Ser
1 5
<210> 515
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (1)..(9)
<223> D-аминокислота
<400> 515
Val Leu Tyr Pro Arg Val Val Arg Arg
1 5
<210> 516
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 516
Trp Leu Pro Phe Gly Phe Ile Leu Ile
1 5
<210> 517
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 517
Trp Tyr Glu Gly Leu Asp His Ala Leu
1 5
<210> 518
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 518
Ala Leu Met Glu Gln Gln His Tyr Val
1 5
<210> 519
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 519
Gly Val Ala Leu Gln Thr Met Lys Gln
1 5
<210> 520
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 520
Phe Met Asn Lys Phe Ile Tyr Glu Ile
1 5
<210> 521
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 521
Gly Leu Ser Pro Asn Leu Asn Arg Phe Leu
1 5 10
<210> 522
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 522
Pro Leu Phe Gln Val Pro Glu Pro Val
1 5
<210> 523
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 523
Ile Leu Leu Trp Ala Ala Arg Tyr Asp
1 5
<210> 524
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 524
Glu Tyr Ser Arg Arg His Pro Gln Leu
1 5
<210> 525
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 525
Ala Tyr Thr Lys Lys Ala Pro Gln Leu
1 5
<210> 526
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 526
Glu Tyr Tyr Leu Gln Asn Ala Phe Leu
1 5
<210> 527
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 527
Lys Tyr Ile Gln Glu Ser Gln Ala Leu
1 5
<210> 528
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 528
Arg Ser Cys Gly Leu Phe Gln Lys Leu
1 5
<210> 529
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 529
Gln Leu Ala Val Ser Val Ile Leu Arg Val
1 5 10
<210> 530
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 530
Gln Leu Tyr Ala Leu Pro Cys Val Leu
1 5
<210> 531
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 531
Ala Leu Leu Asn Ile Lys Val Lys Leu
1 5
<210> 532
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 532
Phe Leu Gly Tyr Leu Ile Leu Gly Val
1 5
<210> 533
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 533
Ser Val Ser Glu Ser Asp Thr Ile Arg Ser Ile Ser Ile Ala Ser
1 5 10 15
<210> 534
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 534
Leu Leu Ala Asn Gly Arg Met Pro Thr Val Leu Gln Cys Val Asn
1 5 10 15
<210> 535
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 535
Arg Met Pro Thr Val Leu Gln Cys Val Asn Val Ser Val Val Ser
1 5 10 15
<210> 536
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 536
Leu Leu Ser Asp Asp Asp Val Val Val
1 5
<210> 537
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 537
Ala Gln Pro Asp Thr Ala Pro Leu Pro Val
1 5 10
<210> 538
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 538
Cys Ile Ala Glu Gln Tyr His Thr Val
1 5
<210> 539
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 539
Glu Thr Val Glu Leu Gln Ile Ser Leu
1 5
<210> 540
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 540
Thr Leu Tyr Glu Ala Val Arg Glu Val
1 5
<210> 541
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 541
Lys Leu Val Glu Arg Leu Gly Ala Ala
1 5
<210> 542
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 542
Asp Val Trp Ser Phe Gly Ile Leu Leu
1 5
<210> 543
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 543
Thr Phe Asp Tyr Leu Arg Ser Val Leu
1 5
<210> 544
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 544
His Tyr Thr Asn Ala Ser Asp Gly Leu
1 5
<210> 545
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 545
Asp Tyr Leu Arg Ser Val Leu Glu Asp Phe
1 5 10
<210> 546
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 546
Gln Leu Cys Pro Ile Cys Arg Ala Pro Val
1 5 10
<210> 547
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 547
Arg Leu Ala Ser Phe Tyr Asp Trp Leu Pro
1 5 10
<210> 548
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 548
Ser Leu Gly Ser Pro Val Leu Gly Leu
1 5
<210> 549
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 549
Gly Pro Arg Glu Ser Arg Pro Pro Ala
1 5
<210> 550
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 550
Phe Leu Pro Glu Phe Gly Ile Ser Ser Ala
1 5 10
<210> 551
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 551
Arg Ile Asp Ile Thr Leu Ser Ser Val
1 5
<210> 552
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 552
Gly Tyr Cys Ala Ser Leu Phe Ala Ile Leu
1 5 10
<210> 553
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 553
Leu Pro Ala Val Val Gly Leu Ser Pro Gly Glu Gln Glu Tyr
1 5 10
<210> 554
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 554
Val Gly Gln Asp Val Ser Val Leu Phe Arg Val Thr Gly Ala Leu Gln
1 5 10 15
<210> 555
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 555
Val Leu Phe Tyr Leu Gly Gln Tyr
1 5
<210> 556
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 556
Leu Leu Gly Asp Leu Phe Gly Val
1 5
<210> 557
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 557
Thr Leu Asn Asp Glu Cys Trp Pro Ala
1 5
<210> 558
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 558
Glu Arg Ile Ser Ser Thr Leu Asn Asp Glu Cys Trp Pro Ala
1 5 10
<210> 559
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 559
Thr Ser Arg Glu Gln Phe Leu Pro Ser Glu Gly Ala Ala
1 5 10
<210> 560
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 560
Cys Pro Pro Trp His Pro Ser Glu Arg Ile Ser Ser Thr Leu
1 5 10
<210> 561
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 561
Arg Leu Pro Pro Lys Pro Pro Leu Ala
1 5
<210> 562
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 562
Arg Cys Pro Pro Lys Pro Pro Leu Ala
1 5
<210> 563
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 563
Thr Leu Lys Cys Asp Cys Glu Ile Leu
1 5
<210> 564
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 564
Arg Leu Gly Pro Thr Leu Met Cys Leu
1 5
<210> 565
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 565
Leu Leu Leu Glu Ala Val Pro Ala Val
1 5
<210> 566
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 566
Trp Leu Pro Lys Ile Leu Gly Glu Val
1 5
<210> 567
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 567
Val Leu Ser Val Asn Val Pro Asp Val
1 5
<210> 568
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 568
Cys Met His Leu Leu Leu Glu Ala Val
1 5
<210> 569
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 569
Ala Leu Leu Ala Leu Thr Ser Ala Val
1 5
<210> 570
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 570
Ala Gln Cys Gln Glu Thr Ile Arg Val
1 5
<210> 571
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 571
Leu Thr Leu Leu Ala Leu Leu Ala Leu Thr Ser Ala Val Ala Lys
1 5 10 15
<210> 572
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (10)..(10)
<223> D-аминокислота
<400> 572
Gly Leu Pro Pro Asp Val Gln Arg Val His
1 5 10
<210> 573
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 573
Ser Leu Phe Pro Asn Ser Pro Lys Trp Thr Ser Lys
1 5 10
<210> 574
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 574
Gln Leu Leu Ile Lys Ala Val Asn Leu
1 5
<210> 575
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 575
Ser Thr Leu Cys Gln Val Glu Pro Val
1 5
<210> 576
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 576
Ala Tyr Val Pro Gln Gln Ala Trp Ile
1 5
<210> 577
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 577
Val Tyr Ser Asp Ala Asp Ile Phe Leu
1 5
<210> 578
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 578
Asn Tyr Ser Val Arg Tyr Arg Pro Gly Leu
1 5 10
<210> 579
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 579
Leu Tyr Ala Trp Glu Pro Ser Phe Leu
1 5
<210> 580
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 580
Ser Thr Ala Pro Pro Val His Asn Val
1 5
<210> 581
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 581
Leu Leu Leu Leu Thr Val Leu Thr Val
1 5
<210> 582
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 582
Ser Thr Ala Pro Pro Ala His Gly Val
1 5
<210> 583
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 583
Asp Val Thr Ser Ala Pro Asp Asn Lys
1 5
<210> 584
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 584
Val Pro Gly Trp Gly Ile Ala Leu Leu
1 5
<210> 585
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 585
Asp Pro Ser Thr Asp Tyr Tyr Gln Glu Leu
1 5 10
<210> 586
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 586
Thr Glu Ala Ala Ser Arg Tyr Asn Leu
1 5
<210> 587
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 587
Pro Gly Ser Thr Ala Pro Pro Ala His Gly Val Thr
1 5 10
<210> 588
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 588
Thr Cys Gln Pro Thr Cys Arg Ser Leu
1 5
<210> 589
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 589
Gly Cys Glu Leu Lys Ala Asp Lys Asp Tyr
1 5 10
<210> 590
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 590
Ala Tyr Gly Leu Asp Phe Tyr Ile Leu
1 5
<210> 591
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 591
Leu Leu Gly Arg Asn Ser Phe Glu Val
1 5
<210> 592
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 592
Arg Met Pro Glu Ala Ala Pro Pro Val
1 5
<210> 593
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 593
Leu Leu Pro Glu Asn Asn Val Leu Ser Pro Val
1 5 10
<210> 594
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 594
Ser Leu Pro Pro Pro Gly Thr Arg Val
1 5
<210> 595
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 595
Tyr Leu Gly Ser Tyr Gly Phe Arg Leu
1 5
<210> 596
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 596
Ser Met Pro Pro Pro Gly Thr Arg Val
1 5
<210> 597
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 597
Gly Leu Ala Pro Pro Gln His Leu Ile Arg Val
1 5 10
<210> 598
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 598
Lys Leu Cys Pro Val Gln Leu Trp Val
1 5
<210> 599
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 599
Lys Thr Cys Pro Val Gln Leu Trp Val
1 5
<210> 600
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 600
Ala Ile Tyr Lys Gln Ser Gln His Met
1 5
<210> 601
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 601
Ser Gln Lys Thr Tyr Gln Gly Ser Tyr
1 5
<210> 602
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 602
Thr Arg Val Leu Ala Met Ala Ile Tyr
1 5
<210> 603
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 603
Pro Gly Thr Arg Val Arg Ala Met Ala Ile Tyr Lys Gln
1 5 10
<210> 604
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 604
His Leu Ile Arg Val Glu Gly Asn Leu Arg Val Glu
1 5 10
<210> 605
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 605
Lys Leu Ala Lys Pro Leu Ser Ser Leu
1 5
<210> 606
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 606
Val Leu Leu Gly Met Glu Gly Ser Val
1 5
<210> 607
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 607
Ala Leu Pro Ser Phe Gln Ile Pro Val
1 5
<210> 608
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 608
Gln Leu Met Ala Phe Asn His Leu Val
1 5
<210> 609
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 609
Thr Leu Pro Gly Tyr Pro Pro His Val
1 5
<210> 610
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 610
Cys Thr Ala Cys Arg Trp Lys Lys Ala Cys Gln Arg
1 5 10
<210> 611
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 611
Ile Ile Gly Gly Gly Met Ala Phe Thr
1 5
<210> 612
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 612
Val Leu Asp Gly Leu Asp Val Leu Leu
1 5
<210> 613
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 613
Ser Leu Tyr Ser Phe Pro Glu Pro Glu Ala
1 5 10
<210> 614
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 614
Ala Leu Tyr Val Asp Ser Leu Phe Phe Leu
1 5 10
<210> 615
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 615
Ser Leu Leu Gln His Leu Ile Gly Leu
1 5
<210> 616
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (10)..(10)
<223> D-аминокислота
<400> 616
Leu Tyr Val Asp Ser Leu Phe Phe Leu Cys
1 5 10
<210> 617
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 617
Gly Gln His Leu His Leu Glu Thr Phe
1 5
<210> 618
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 618
Phe Gly Leu Phe Pro Arg Leu Cys Pro Val
1 5 10
<210> 619
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 619
His Ser Thr Asn Gly Val Thr Arg Ile Tyr
1 5 10
<210> 620
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 620
Val Leu Ala Gly Gly Phe Phe Leu Leu
1 5
<210> 621
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 621
Leu Tyr Ser Asp Pro Ala Asp Tyr Phe
1 5
<210> 622
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 622
Asn Tyr Ala Arg Thr Glu Asp Phe Phe
1 5
<210> 623
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 623
Leu Lys Leu Ser Gly Val Val Arg Leu
1 5
<210> 624
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MOD_RES
<222> (11)..(11)
<223> D-аминокислота
<400> 624
Pro Leu Pro Pro Ala Arg Asn Gly Gly Leu Gly
1 5 10
<210> 625
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 625
Ser Pro Ser Ser Asn Arg Ile Arg Asn Thr
1 5 10
<210> 626
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 626
Tyr Met Phe Asp Val Thr Ser Arg Val
1 5
<210> 627
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 627
Ile Met Phe Asp Val Thr Ser Arg Val
1 5
<210> 628
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 628
His Pro Leu Val Phe His Thr Asn Arg
1 5
<210> 629
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 629
Ile Ile Met Phe Asp Val Thr Ser Arg
1 5
<210> 630
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 630
Leu Ala Ala Leu Pro His Ser Cys Leu
1 5
<210> 631
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 631
Gly Leu Ala Ser Phe Lys Ser Phe Leu Lys
1 5 10
<210> 632
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 632
Met Ala Gln Lys Arg Ile His Ala Leu
1 5
<210> 633
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 633
Lys Asn Lys Arg Ile Leu Met Glu His
1 5
<210> 634
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 634
Arg Ala Gly Leu Gln Val Arg Lys Asn Lys
1 5 10
<210> 635
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена=" "
<220>
<221> УЧАСТОК
<222> (1)..(10)
<223> /примечание="варианты остатков, приведенные в последовательности, не
имеют приоритета относительно остатков в аннотациях вариантов положений"
<400> 635
Ala Leu Trp Pro Trp Leu Leu Met Ala Thr
1 5 10
<210> 636
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 636
Asn Ser Gln Pro Val Trp Leu Cys Leu
1 5
<210> 637
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 637
Leu Pro Arg Trp Pro Pro Pro Gln Leu
1 5
<210> 638
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 638
Asp Tyr Ser Ala Arg Trp Asn Glu Ile
1 5
<210> 639
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 639
Ala Tyr Asp Phe Leu Tyr Asn Tyr Leu
1 5
<210> 640
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 640
Ser Tyr Thr Arg Leu Phe Leu Ile Leu
1 5
<210> 641
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 641
Lys Met Asp Ala Glu His Pro Glu Leu
1 5
<210> 642
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 642
Phe Leu Thr Pro Leu Arg Asn Phe Leu
1 5
<210> 643
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 643
Ala Trp Ile Ser Lys Pro Pro Gly Val
1 5
<210> 644
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 644
Ser Ala Trp Ile Ser Lys Pro Pro Gly Val
1 5 10
<210> 645
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 645
Met Tyr Ile Phe Pro Val His Trp Gln Phe
1 5 10
<210> 646
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 646
Asp Tyr Ile Gly Pro Cys Lys Tyr Ile
1 5
<210> 647
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 647
Lys Leu Gln Glu Leu Asn Tyr Asn Leu
1 5
<210> 648
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 648
Met Ile Ala Val Phe Leu Pro Ile Val
1 5
<210> 649
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 649
Phe Leu Tyr Thr Leu Leu Arg Glu Val
1 5
<210> 650
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 650
Leu Leu Leu Gly Thr Ile His Ala Leu
1 5
<210> 651
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 651
His Gln Gln Tyr Phe Tyr Lys Ile Pro Ile Leu Val Ile Asn Lys
1 5 10 15
<210> 652
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 652
Glu Leu Thr Leu Gly Glu Phe Leu Lys Leu
1 5 10
<210> 653
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 653
Gln Met Phe Phe Cys Phe Lys Glu Leu
1 5
<210> 654
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 654
Leu Met Leu Gly Glu Phe Leu Lys Leu
1 5
<210> 655
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 655
Thr Leu Pro Pro Ala Trp Gln Pro Phe Leu
1 5 10
<210> 656
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 656
Thr Leu Gly Glu Phe Leu Lys Leu Asp Arg Glu Arg Ala Lys Asn
1 5 10 15
<210> 657
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 657
Ala Tyr Ala Cys Asn Thr Ser Thr Leu
1 5
<210> 658
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 658
Ile Leu Ala Lys Phe Leu His Trp Leu
1 5
<210> 659
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 659
Arg Leu Val Asp Asp Phe Leu Leu Val
1 5
<210> 660
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 660
Leu Leu Thr Ser Arg Leu Arg Phe Ile
1 5
<210> 661
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 661
Arg Leu Phe Phe Tyr Arg Lys Ser Val
1 5
<210> 662
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 662
Lys Leu Phe Gly Val Leu Arg Leu Lys
1 5
<210> 663
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 663
Arg Pro Gly Leu Leu Gly Ala Ser Val Leu Gly Leu Asp Asp Ile
1 5 10 15
<210> 664
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 664
Leu Thr Asp Leu Gln Pro Tyr Met Arg Gln Phe Val Ala His Leu
1 5 10 15
<210> 665
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 665
Phe Leu Pro Ala Thr Leu Thr Met Val
1 5
<210> 666
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 666
Phe Leu Tyr Asp Asp Asn Gln Arg Val
1 5
<210> 667
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 667
Tyr Gln Leu Cys Leu Thr Asn Ile Phe
1 5
<210> 668
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 668
Leu Met Ala Leu Pro Pro Cys His Ala Leu
1 5 10
<210> 669
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 669
Ser Arg Phe Gly Gly Ala Val Val Arg
1 5
<210> 670
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 670
Phe Leu Ser Thr Leu Thr Ile Asp Gly Val
1 5 10
<210> 671
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 671
Ala Ser Leu Asp Ser Asp Pro Trp Val
1 5
<210> 672
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 672
Asp Leu Leu Ser His Ala Phe Phe Ala
1 5
<210> 673
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 673
Thr Ser Glu Lys Arg Pro Phe Met Cys Ala Tyr
1 5 10
<210> 674
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 674
Arg Met Phe Pro Asn Ala Pro Tyr Leu
1 5
<210> 675
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 675
Tyr Met Phe Pro Asn Ala Pro Tyr Leu
1 5
<210> 676
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 676
Cys Met Thr Trp Asn Gln Met Asn Leu
1 5
<210> 677
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 677
Cys Tyr Thr Trp Asn Gln Met Asn Leu
1 5
<210> 678
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 678
Arg Trp Pro Ser Cys Gln Lys Lys Phe
1 5
<210> 679
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 679
Leu Ser His Leu Gln Met His Ser Arg Lys His
1 5 10
<210> 680
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 680
Lys Arg Tyr Phe Lys Leu Ser His Leu Gln Met His Ser Arg Lys His
1 5 10 15
<210> 681
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 681
Leu Leu Ser Gly Gln Pro Ala Ser Ala
1 5
<210> 682
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 682
Asn Val Leu His Phe Phe Asn Ala Pro Leu
1 5 10
<210> 683
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 683
Lys Leu Pro Asn Ser Val Leu Gly Arg
1 5
<210> 684
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 684
Arg Val Ala Ala Leu Ala Arg Asp Ala Pro
1 5 10
<210> 685
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 685
Leu Leu Val Leu Leu Tyr Ser Lys Leu
1 5
<210> 686
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 686
Tyr Leu Met Asp Thr Ser Gly Lys Val
1 5
<210> 687
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 687
Val Pro Tyr Gly Ser Phe Lys His Val
1 5
<210> 688
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 688
Arg Leu Tyr Pro Trp Gly Val Val Glu Val
1 5 10
<210> 689
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 689
Cys His Ile Leu Leu Gly Asn Tyr Cys
1 5
<210> 690
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 690
Met Glu Val Gly Trp Tyr Arg Ser Pro Phe Ser Arg Val Val His Leu
1 5 10 15
Tyr Arg Asn Gly Lys
20
<210> 691
<211> 9
<212> БЕЛОК
<213> Epstein Barr Virus
<400> 691
Cys Leu Gly Gly Leu Leu Thr Met Val
1 5
<210> 692
<211> 9
<212> БЕЛОК
<213> Epstein Barr Virus
<400> 692
Gly Leu Cys Thr Leu Val Ala Met Leu
1 5
<210> 693
<211> 9
<212> БЕЛОК
<213> Epstein Barr Virus
<400> 693
Phe Leu Tyr Ala Leu Ala Leu Leu Leu
1 5
<210> 694
<211> 9
<212> БЕЛОК
<213> Epstein Barr Virus
<400> 694
Tyr Val Leu Asp His Leu Ile Val Val
1 5
<210> 695
<211> 9
<212> БЕЛОК
<213> Epstein Barr Virus
<400> 695
Arg Leu Arg Ala Glu Ala Gln Val Lys
1 5
<210> 696
<211> 10
<212> БЕЛОК
<213> Epstein Barr Virus
<400> 696
Ala Val Phe Asp Arg Lys Ser Asp Ala Lys
1 5 10
<210> 697
<211> 9
<212> БЕЛОК
<213> Epstein Barr Virus
<400> 697
Arg Pro Pro Ile Phe Ile Arg Leu Leu
1 5
<210> 698
<211> 9
<212> БЕЛОК
<213> Epstein Barr Virus
<400> 698
Val Leu Gln Trp Ala Ser Leu Ala Val
1 5
<210> 699
<211> 9
<212> БЕЛОК
<213> Epstein Barr Virus
<400> 699
Phe Met Val Phe Leu Gln Thr His Ile
1 5
<210> 700
<211> 10
<212> БЕЛОК
<213> Epstein Barr Virus
<400> 700
Phe Leu Gln Thr His Ile Phe Ala Glu Val
1 5 10
<210> 701
<211> 10
<212> БЕЛОК
<213> Epstein Barr Virus
<400> 701
Ser Ile Val Cys Tyr Phe Met Val Phe Leu
1 5 10
<210> 702
<211> 11
<212> БЕЛОК
<213> Cytomegalovirus
<400> 702
Tyr Ser Glu His Pro Thr Phe Thr Ser Gln Tyr
1 5 10
<210> 703
<211> 9
<212> БЕЛОК
<213> Cytomegalovirus
<400> 703
Val Thr Glu His Asp Thr Leu Leu Tyr
1 5
<210> 704
<211> 9
<212> БЕЛОК
<213> Cytomegalovirus
<400> 704
Asn Leu Val Pro Met Val Ala Thr Val
1 5
<210> 705
<211> 9
<212> БЕЛОК
<213> Cytomegalovirus
<400> 705
Val Leu Glu Glu Thr Ser Val Met Leu
1 5
<210> 706
<211> 11
<212> БЕЛОК
<213> Cytomegalovirus
<400> 706
Thr Thr Val Tyr Pro Pro Ser Ser Thr Ala Lys
1 5 10
<210> 707
<211> 9
<212> БЕЛОК
<213> Cytomegalovirus
<400> 707
Gly Pro Ile Ser Gly His Val Leu Lys
1 5
<210> 708
<211> 10
<212> БЕЛОК
<213> Cytomegalovirus
<400> 708
Thr Pro Arg Val Thr Gly Gly Gly Ala Met
1 5 10
<210> 709
<211> 10
<212> БЕЛОК
<213> Cytomegalovirus
<400> 709
Arg Pro His Glu Arg Asn Gly Phe Thr Val
1 5 10
<210> 710
<211> 9
<212> БЕЛОК
<213> Influenza virus
<400> 710
Val Ser Asp Gly Gly Pro Asn Leu Tyr
1 5
<210> 711
<211> 9
<212> БЕЛОК
<213> Influenza virus
<400> 711
Gly Ile Leu Gly Phe Val Phe Thr Leu
1 5
<210> 712
<211> 10
<212> БЕЛОК
<213> Human papilloma virus
<400> 712
Thr Ile His Asp Ile Ile Leu Glu Cys Val
1 5 10
<210> 713
<211> 9
<212> БЕЛОК
<213> Human papilloma virus
<400> 713
Tyr Met Leu Asp Leu Gln Pro Glu Thr
1 5
<210> 714
<211> 10
<212> БЕЛОК
<213> Human papilloma virus
<400> 714
Tyr Met Leu Asp Leu Gln Pro Glu Thr Thr
1 5 10
<210> 715
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 715
Gly Leu Tyr Asp Gly Met Glu His Leu Ile
1 5 10
<210> 716
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 716
Val Ala Glu Leu Val His Phe Leu Leu Met Glu Val Asp Pro Ile Gly
1 5 10 15
His Leu Tyr
<210> 717
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 717
Phe Glu Asn Asp Ala Gln Ala Pro Lys Ser
1 5 10
<210> 718
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 718
Leu Gln Asn Asp Ala Gln Ala Pro Lys Ser
1 5 10
<210> 719
<211> 7
<212> БЕЛОК
<213> Human herpesvirus 6
<400> 719
Pro Arg Thr Pro Pro Pro Ser
1 5
<210> 720
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 720
Arg Leu Phe Pro Asp Phe Phe Thr Arg Val
1 5 10
<210> 721
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 721
Ser Ile Ile Asn Phe Glu Lys Leu
1 5
<210> 722
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 722
Lys Val Pro Arg Asn Gln Asp Trp Leu
1 5
<210> 723
<211> 597
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 723
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Thr Gly Gly
20 25 30
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg
35 40 45
Thr Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys
50 55 60
Ser Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile
65 70 75 80
Glu Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His
85 90 95
Ser Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr
100 105 110
Thr Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn
115 120 125
His Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val
165 170 175
Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val
180 185 190
Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg
195 200 205
Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp
210 215 220
Asp Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val
225 230 235 240
Asp Leu Gly Thr Leu Arg Gly Tyr Tyr Asn Gln Ser Glu Ala Gly Ser
245 250 255
His Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg
260 265 270
Phe Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile
275 280 285
Ala Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala
290 295 300
Gln Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu
305 310 315 320
Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu
325 330 335
Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His
340 345 350
Met Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp
355 360 365
Ala Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp
370 375 380
Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala
385 390 395 400
Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly
405 410 415
Gln Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys
420 425 430
Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile
435 440 445
Gly Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser
450 455 460
Gly Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser
465 470 475 480
Ser Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys
485 490 495
Arg Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile
500 505 510
Ser Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val
515 520 525
Gln Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe
530 535 540
Gly Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly
545 550 555 560
Ile Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro
565 570 575
Ser Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro
580 585 590
Glu Thr Ser Asp Gln
595
<210> 724
<211> 597
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 724
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Thr Gly Gly
20 25 30
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg
35 40 45
Thr Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys
50 55 60
Ser Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile
65 70 75 80
Glu Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His
85 90 95
Ser Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr
100 105 110
Thr Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn
115 120 125
His Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val
165 170 175
Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val
180 185 190
Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg
195 200 205
Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp
210 215 220
Asp Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val
225 230 235 240
Asp Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser
245 250 255
His Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg
260 265 270
Phe Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile
275 280 285
Ala Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala
290 295 300
Gln Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu
305 310 315 320
Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu
325 330 335
Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His
340 345 350
Met Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp
355 360 365
Ala Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp
370 375 380
Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala
385 390 395 400
Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly
405 410 415
Gln Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys
420 425 430
Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile
435 440 445
Gly Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser
450 455 460
Gly Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser
465 470 475 480
Ser Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys
485 490 495
Arg Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile
500 505 510
Ser Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val
515 520 525
Gln Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe
530 535 540
Gly Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly
545 550 555 560
Ile Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro
565 570 575
Ser Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro
580 585 590
Glu Thr Ser Asp Gln
595
<210> 725
<211> 597
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 725
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Thr Gly Cys
20 25 30
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg
35 40 45
Thr Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys
50 55 60
Ser Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile
65 70 75 80
Glu Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His
85 90 95
Ser Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr
100 105 110
Thr Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn
115 120 125
His Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val
165 170 175
Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val
180 185 190
Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg
195 200 205
Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp
210 215 220
Asp Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val
225 230 235 240
Asp Leu Gly Thr Leu Arg Gly Cys Tyr Asn Gln Ser Glu Ala Gly Ser
245 250 255
His Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg
260 265 270
Phe Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile
275 280 285
Ala Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala
290 295 300
Gln Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu
305 310 315 320
Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu
325 330 335
Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His
340 345 350
Met Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp
355 360 365
Ala Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp
370 375 380
Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala
385 390 395 400
Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly
405 410 415
Gln Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys
420 425 430
Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile
435 440 445
Gly Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser
450 455 460
Gly Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser
465 470 475 480
Ser Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys
485 490 495
Arg Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile
500 505 510
Ser Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val
515 520 525
Gln Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe
530 535 540
Gly Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly
545 550 555 560
Ile Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro
565 570 575
Ser Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro
580 585 590
Glu Thr Ser Asp Gln
595
<210> 726
<211> 596
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 726
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Tyr Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser
465 470 475 480
Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg
485 490 495
Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser
500 505 510
Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln
515 520 525
Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly
530 535 540
Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile
545 550 555 560
Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser
565 570 575
Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu
580 585 590
Thr Ser Asp Gln
595
<210> 727
<211> 150
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 727
Met Tyr Gly Lys Ile Ile Phe Val Leu Leu Leu Ser Ala Ile Val Ser
1 5 10 15
Ile Ser Ala Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser
20 25 30
Ser Ser Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His
35 40 45
Lys Arg Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu
50 55 60
Ile Ser Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg
65 70 75 80
Val Gln Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile
85 90 95
Phe Gly Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr
100 105 110
Gly Ile Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu
115 120 125
Pro Ser Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn
130 135 140
Pro Glu Thr Ser Asp Gln
145 150
<210> 728
<211> 131
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 728
Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser Val
1 5 10 15
Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg Asp
20 25 30
Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser Val
35 40 45
Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln Leu
50 55 60
Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly Val
65 70 75 80
Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile Arg
85 90 95
Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser Pro
100 105 110
Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu Thr
115 120 125
Ser Asp Gln
130
<210> 729
<211> 78
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 729
Met Gln Pro Gln Glu Ser His Val His Tyr Ser Arg Trp Glu Asp Gly
1 5 10 15
Ser Arg Asp Gly Val Ser Leu Gly Ala Val Ser Ser Thr Glu Glu Ala
20 25 30
Ser Arg Cys Arg Arg Ile Ser Gln Arg Leu Cys Thr Gly Lys Leu Gly
35 40 45
Ile Ala Met Lys Val Leu Gly Gly Val Ala Leu Phe Trp Ile Ile Phe
50 55 60
Ile Leu Gly Tyr Leu Thr Gly Tyr Tyr Val His Lys Cys Lys
65 70 75
<210> 730
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 730
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala
20
<210> 731
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 731
Met Tyr Gly Lys Ile Ile Phe Val Leu Leu Leu Ser Glu Ile Val Ser
1 5 10 15
Ile Ser Ala
<210> 732
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 732
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 733
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 733
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 734
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 734
Gly Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser
1 5 10 15
Gly Ser
<210> 735
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 735
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
1 5 10 15
Gly Ser
<210> 736
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 736
Gly Cys Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 737
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 737
Gly Gly Ser Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Ser
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Ser
20
<210> 738
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 738
Ser Gly Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
1 5 10 15
Gly Ser Gly Gly Gly Gly Ser Ser Pro Ala
20 25
<210> 739
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 739
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly
20
<210> 740
<211> 58
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 740
Ser Gly Arg Gly Ala Ser Ser Gly Ser Ser Gly Ser Gly Ser Gln Lys
1 5 10 15
Lys Pro Arg Tyr Glu Ile Arg Trp Lys Val Val Val Ile Ser Ala Ile
20 25 30
Leu Ala Leu Val Val Leu Thr Val Ile Ser Leu Ile Ile Leu Ile Met
35 40 45
Leu Trp Gly Ser Gly Met Gln Ser Pro Ala
50 55
<210> 741
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 741
Met Ala Val Met Ala Pro Arg Thr Leu Leu Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Gln Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Phe Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Gln Lys Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Gln Glu Thr Arg Asn Met Lys Ala His Ser Gln
85 90 95
Thr Asp Arg Ala Asn Leu Gly Thr Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Asp Gly Ser His Thr Ile Gln Ile Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Phe Leu Arg Gly Tyr Arg Gln Asp Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Met Ala Ala Gln Ile Thr Lys Arg Lys Trp Glu Ala Val His Ala
165 170 175
Ala Glu Gln Arg Arg Val Tyr Leu Glu Gly Arg Cys Val Asp Gly Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Pro
195 200 205
Pro Lys Thr His Met Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Leu Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Ile Ala Gly Leu Val Leu Leu Gly Ala
305 310 315 320
Val Ile Thr Gly Ala Val Val Ala Ala Val Met Trp Arg Arg Lys Ser
325 330 335
Ser Asp Arg Lys Gly Gly Ser Tyr Thr Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala Cys Lys Val
355 360 365
<210> 742
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 742
Met Ala Val Met Ala Pro Arg Thr Leu Val Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Gln Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Phe Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Gln Arg Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln
85 90 95
Thr His Arg Val Asp Leu Gly Thr Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly
115 120 125
Ser Asp Trp Arg Phe Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Met Ala Ala Gln Thr Thr Lys His Lys Trp Glu Ala Ala His Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala
195 200 205
Pro Lys Thr His Met Thr His His Ala Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Gln Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Ile Ala Gly Leu Val Leu Phe Gly Ala
305 310 315 320
Val Ile Thr Gly Ala Val Val Ala Ala Val Met Trp Arg Arg Lys Ser
325 330 335
Ser Asp Arg Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala Cys Lys Val
355 360 365
<210> 743
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 743
Met Ala Val Met Ala Pro Arg Thr Leu Leu Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Gln Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Phe Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Gln Arg Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Gln Glu Thr Arg Asn Val Lys Ala Gln Ser Gln
85 90 95
Thr Asp Arg Val Asp Leu Gly Thr Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Ile Gln Ile Met Tyr Gly Cys Asp Val Gly
115 120 125
Ser Asp Gly Arg Phe Leu Arg Gly Tyr Arg Gln Asp Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Met Ala Ala Gln Ile Thr Lys Arg Lys Trp Glu Ala Ala His Glu
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Asp Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Pro
195 200 205
Pro Lys Thr His Met Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Leu Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Ile Ala Gly Leu Val Leu Leu Gly Ala
305 310 315 320
Val Ile Thr Gly Ala Val Val Ala Ala Val Met Trp Arg Arg Lys Ser
325 330 335
Ser Asp Arg Lys Gly Gly Ser Tyr Thr Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala Cys Lys Val
355 360 365
<210> 744
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 744
Met Ala Val Met Ala Pro Arg Thr Leu Val Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Gln Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Ser Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Gln Arg Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Glu Glu Thr Gly Lys Val Lys Ala His Ser Gln
85 90 95
Thr Asp Arg Glu Asn Leu Arg Ile Ala Leu Arg Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Met Met Phe Gly Cys Asp Val Gly
115 120 125
Ser Asp Gly Arg Phe Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Met Ala Ala Gln Ile Thr Lys Arg Lys Trp Glu Ala Ala His Val
165 170 175
Ala Glu Gln Gln Arg Ala Tyr Leu Glu Gly Thr Cys Val Asp Gly Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Pro
195 200 205
Pro Lys Thr His Met Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Val Pro Ile Val Gly Ile Ile Ala Gly Leu Val Leu Leu Gly Ala
305 310 315 320
Val Ile Thr Gly Ala Val Val Ala Ala Val Met Trp Arg Arg Asn Ser
325 330 335
Ser Asp Arg Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala Cys Lys Val
355 360 365
<210> 745
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 745
Met Ala Val Met Ala Pro Arg Thr Leu Leu Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Gln Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Gln Arg Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Gln Glu Thr Arg Asn Val Lys Ala Gln Ser Gln
85 90 95
Thr Asp Arg Val Asp Leu Gly Thr Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Asp Gly Ser His Thr Ile Gln Ile Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Phe Leu Arg Gly Tyr Arg Gln Asp Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Met Ala Ala Gln Ile Thr Lys Arg Lys Trp Glu Ala Ala His Ala
165 170 175
Ala Glu Gln Gln Arg Ala Tyr Leu Glu Gly Arg Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Pro
195 200 205
Pro Lys Thr His Met Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Leu Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Ile Ala Gly Leu Val Leu Leu Gly Ala
305 310 315 320
Val Ile Thr Gly Ala Val Val Ala Ala Val Met Trp Arg Arg Lys Ser
325 330 335
Ser Asp Arg Lys Gly Gly Ser Tyr Thr Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala Cys Lys Val
355 360 365
<210> 746
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 746
Met Ala Val Met Ala Pro Arg Thr Leu Leu Leu Leu Leu Leu Gly Ala
1 5 10 15
Leu Ala Leu Thr Gln Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Thr Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Gln Arg Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Leu Gln Thr Arg Asn Val Lys Ala Gln Ser Gln
85 90 95
Thr Asp Arg Ala Asn Leu Gly Thr Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Ile Gln Met Met Tyr Gly Cys Asp Val Gly
115 120 125
Ser Asp Gly Arg Phe Leu Arg Gly Tyr Arg Gln Asp Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Met Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala
195 200 205
Pro Lys Thr His Met Thr His His Ala Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ser Val Val
260 265 270
Val Pro Ser Gly Gln Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Ile Ala Gly Leu Val Leu Phe Gly Ala
305 310 315 320
Val Phe Ala Gly Ala Val Val Ala Ala Val Arg Trp Arg Arg Lys Ser
325 330 335
Ser Asp Arg Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Met Ser Leu Thr Ala Cys Lys Val
355 360 365
<210> 747
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 747
Met Ala Val Met Ala Pro Arg Thr Leu Leu Leu Leu Leu Leu Gly Ala
1 5 10 15
Leu Ala Leu Thr Gln Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Phe Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Gln Arg Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Gln Glu Thr Arg Asn Val Lys Ala His Ser Gln
85 90 95
Thr Asp Arg Glu Ser Leu Arg Ile Ala Leu Arg Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Ile Gln Met Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Gln Gln Asp Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Met Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala
195 200 205
Pro Lys Thr His Met Thr His His Ala Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ser Val Val
260 265 270
Val Pro Ser Gly Gln Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Ile Ala Gly Leu Val Leu Phe Gly Ala
305 310 315 320
Met Phe Ala Gly Ala Val Val Ala Ala Val Arg Trp Arg Arg Lys Ser
325 330 335
Ser Asp Arg Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Met Ser Leu Thr Ala Cys Lys Val
355 360 365
<210> 748
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 748
Met Ala Val Met Ala Pro Arg Thr Leu Val Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Gln Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Gln Arg Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Arg Asn Val Lys Ala Gln Ser Gln
85 90 95
Thr Asp Arg Val Asp Leu Gly Thr Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Ile Gln Met Met Tyr Gly Cys Asp Val Gly
115 120 125
Ser Asp Gly Arg Phe Leu Arg Gly Tyr Arg Gln Asp Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Met Ala Ala Gln Thr Thr Lys His Lys Trp Glu Ala Ala His Val
165 170 175
Ala Glu Gln Trp Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala
195 200 205
Pro Lys Thr His Met Thr His His Ala Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Val Ala Val Val
260 265 270
Val Pro Ser Gly Gln Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Ile Ala Gly Leu Val Leu Phe Gly Ala
305 310 315 320
Val Ile Thr Gly Ala Val Val Ala Ala Val Met Trp Arg Arg Lys Ser
325 330 335
Ser Asp Arg Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala Cys Lys Val
355 360 365
<210> 749
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 749
Met Ala Val Met Ala Pro Arg Thr Leu Leu Leu Leu Leu Leu Gly Ala
1 5 10 15
Leu Ala Leu Thr Gln Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Thr Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Gln Arg Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Arg
65 70 75 80
Pro Glu Tyr Trp Asp Gln Glu Thr Arg Asn Val Lys Ala His Ser Gln
85 90 95
Ile Asp Arg Val Asp Leu Gly Thr Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Ile Gln Met Met Tyr Gly Cys Asp Val Gly
115 120 125
Ser Asp Gly Arg Phe Leu Arg Gly Tyr Gln Gln Asp Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Met Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Pro
195 200 205
Pro Lys Thr His Met Thr His His Ala Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ser Val Val
260 265 270
Val Pro Ser Gly Gln Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Ile Ala Gly Leu Val Leu Phe Gly Ala
305 310 315 320
Val Phe Ala Gly Ala Val Val Ala Ala Val Arg Trp Arg Arg Lys Ser
325 330 335
Ser Asp Arg Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Met Ser Leu Thr Ala Cys Lys Val
355 360 365
<210> 750
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 750
Met Ala Val Met Ala Pro Arg Thr Leu Val Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Gln Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Gln Arg Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Arg Asn Val Lys Ala His Ser Gln
85 90 95
Thr Asp Arg Glu Ser Leu Arg Ile Ala Leu Arg Tyr Tyr Asn Gln Ser
100 105 110
Glu Asp Gly Ser His Thr Ile Gln Arg Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Phe Leu Arg Gly Tyr Gln Gln Asp Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Met Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Thr Ala His Glu
165 170 175
Ala Glu Gln Trp Arg Ala Tyr Leu Glu Gly Arg Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala
195 200 205
Pro Lys Thr His Met Thr His His Ala Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ser Val Val
260 265 270
Val Pro Ser Gly Gln Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Ile Ala Gly Leu Val Leu Phe Gly Ala
305 310 315 320
Val Ile Ala Gly Ala Val Val Ala Ala Val Met Trp Arg Arg Lys Ser
325 330 335
Ser Asp Arg Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Met Ser Leu Thr Ala Cys Lys Val
355 360 365
<210> 751
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 751
Met Ala Val Met Ala Pro Arg Thr Leu Val Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Gln Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Gln Arg Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Arg Asn Val Lys Ala His Ser Gln
85 90 95
Thr Asp Arg Ala Asn Leu Gly Thr Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Asp Gly Ser His Thr Ile Gln Arg Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Phe Leu Arg Gly Tyr Gln Gln Asp Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Met Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Thr Ala His Glu
165 170 175
Ala Glu Gln Trp Arg Ala Tyr Leu Glu Gly Arg Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala
195 200 205
Pro Lys Thr His Met Thr His His Ala Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ser Val Val
260 265 270
Val Pro Ser Gly Gln Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Ile Ala Gly Leu Val Leu Phe Gly Ala
305 310 315 320
Val Ile Ala Gly Ala Val Val Ala Ala Val Met Trp Arg Arg Lys Ser
325 330 335
Ser Asp Arg Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Met Ser Leu Thr Ala Cys Lys Val
355 360 365
<210> 752
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 752
Met Ala Val Met Ala Pro Arg Thr Leu Val Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Gln Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Ser Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Gln Arg Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Glu Glu Thr Gly Lys Val Lys Ala His Ser Gln
85 90 95
Thr Asp Arg Glu Asn Leu Arg Ile Ala Leu Arg Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Met Met Phe Gly Cys Asp Val Gly
115 120 125
Ser Asp Gly Arg Phe Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Met Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Asp Gly Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Pro
195 200 205
Pro Lys Thr His Met Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Val His Ile Val Gly Ile Ile Ala Gly Leu Val Leu Leu Gly Ala
305 310 315 320
Val Ile Thr Gly Ala Val Val Ala Ala Val Met Trp Arg Arg Asn Ser
325 330 335
Ser Asp Arg Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala Cys Lys Val
355 360 365
<210> 753
<211> 365
<212> БЕЛОК
<213> Homo sapiens
<400> 753
Met Ala Val Met Ala Pro Arg Thr Leu Leu Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Gln Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Ser Thr Ser Val Ser Arg Pro Gly Ser Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Gln Arg Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Arg
65 70 75 80
Pro Glu Tyr Trp Asp Gln Glu Thr Arg Asn Val Lys Ala Gln Ser Gln
85 90 95
Thr Asp Arg Val Asp Leu Gly Thr Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Ile Gln Ile Met Tyr Gly Cys Asp Val Gly
115 120 125
Ser Asp Gly Arg Phe Leu Arg Gly Tyr Glu Gln His Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Met Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Trp
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Pro
195 200 205
Pro Lys Thr His Met Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Leu Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Ile Ala Gly Leu Val Leu Leu Gly Ala
305 310 315 320
Val Ile Thr Gly Ala Val Val Ala Ala Val Met Trp Arg Arg Lys Ser
325 330 335
Ser Asp Arg Lys Gly Gly Ser Tyr Thr Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala Cys Lys Val
355 360 365
<210> 754
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 754
Met Arg Val Met Ala Pro Arg Ala Leu Leu Leu Leu Leu Ser Gly Gly
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Cys Ser His Ser Met Arg Tyr Phe
20 25 30
Asp Thr Ala Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ser
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Asn Tyr Lys Arg Gln Ala Gln
85 90 95
Ala Asp Arg Val Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Asp Gly Ser His Thr Leu Gln Arg Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asp Gln Ser Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Leu Glu Ala Ala Arg Ala
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Glu Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Leu Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Gln Glu Gln Arg Tyr Thr Cys His Met Gln His Glu
275 280 285
Gly Leu Gln Glu Pro Leu Thr Leu Ser Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Met Gly Ile Val Ala Gly Leu Ala Val Leu Val Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Val Thr Ala Met Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Cys Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Thr Cys Lys Ala
355 360 365
<210> 755
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 755
Met Arg Val Met Ala Pro Arg Ala Leu Leu Leu Leu Leu Ser Gly Gly
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Cys Ser His Ser Met Arg Tyr Phe
20 25 30
Asp Thr Ala Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ser
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Lys Tyr Lys Arg Gln Ala Gln
85 90 95
Ala Asp Arg Val Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Asp Gly Ser His Thr Leu Gln Arg Met Ser Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asp Gln Ser Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Leu Glu Ala Ala Arg Ala
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Glu Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Leu Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Gln Glu Gln Arg Tyr Thr Cys His Met Gln His Glu
275 280 285
Gly Leu Gln Glu Pro Leu Thr Leu Ser Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Met Gly Ile Val Ala Gly Leu Ala Val Leu Val Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Val Thr Ala Met Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Cys Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Thr Cys Lys Ala
355 360 365
<210> 756
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 756
Met Arg Val Met Ala Pro Arg Thr Leu Ile Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Cys Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Gln Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Lys Tyr Lys Arg Gln Ala Gln
85 90 95
Thr Asp Arg Val Asn Leu Arg Lys Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Arg Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asn Gln Phe Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Lys Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Arg Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Lys Thr Leu Gln Arg Ala Glu His
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Glu Pro Leu Thr Leu Arg Trp Gly Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Met Ala Val Val Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Ser Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Ala Cys Lys Ala
355 360 365
<210> 757
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 757
Met Arg Val Met Ala Pro Arg Thr Leu Ile Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Cys Ser His Ser Met Arg Tyr Phe
20 25 30
Asp Thr Ala Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ser
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Lys Tyr Lys Arg Gln Ala Gln
85 90 95
Ala Asp Arg Val Asn Leu Arg Lys Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Asp Gly Ser His Thr Leu Gln Trp Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asp Gln Ser Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Trp Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Glu His
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Glu Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Met Ala Val Val Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Ser Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Ala Cys Lys Ala
355 360 365
<210> 758
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 758
Met Arg Val Met Ala Pro Arg Thr Leu Ile Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Ser Thr Ser Val Ser Trp Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Glu Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Lys Tyr Lys Arg Gln Ala Gln
85 90 95
Ala Asp Arg Val Asn Leu Arg Lys Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Asp Gly Ser His Thr Leu Gln Arg Met Phe Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asn Gln Phe Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Arg Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Glu His
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Trp Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Glu Pro Leu Thr Leu Arg Trp Lys Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Leu Ala Val Leu Gly Ala Met Val Ala Val Val Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Ser Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Ala Cys Lys Ala
355 360 365
<210> 759
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 759
Met Arg Val Met Ala Pro Arg Thr Leu Ile Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Val Ser Arg Pro Gly Arg Gly Glu Pro His Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Lys Tyr Lys Arg Gln Ala Gln
85 90 95
Thr Asp Arg Val Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Ile Ile Gln Arg Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asp Gln Tyr Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Leu Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Lys Asn Gly Lys Glu Thr Leu Gln Arg Ala Glu His
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Trp Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Glu Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Val Ala Val Val Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Ser Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Ala Cys Lys Ala
355 360 365
<210> 760
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 760
Met Arg Val Met Ala Pro Arg Thr Leu Ile Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Val Ser Arg Pro Gly Arg Gly Glu Pro His Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Lys Tyr Lys Arg Gln Ala Gln
85 90 95
Thr Asp Arg Val Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Arg Ser His Ile Ile Gln Arg Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asp Gln Tyr Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Leu Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Lys Asn Gly Lys Glu Thr Leu Gln Arg Ala Glu His
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Trp Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Glu Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Val Ala Val Val Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Ser Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Ala Cys Lys Ala
355 360 365
<210> 761
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 761
Met Arg Val Met Ala Pro Arg Thr Leu Leu Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Cys Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Val Ser Arg Pro Ser Arg Gly Glu Pro His Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Lys Tyr Lys Arg Gln Ala Gln
85 90 95
Thr Asp Arg Val Asn Leu Arg Lys Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Arg Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asp Gln Ser Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Trp Arg Ala Tyr Leu Glu Gly Glu Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Glu His
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Thr Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Glu Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Val Ala Val Val Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Ser Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Ala Cys Lys Ala
355 360 365
<210> 762
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 762
Met Arg Val Met Ala Pro Arg Thr Leu Ile Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Cys Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Lys Tyr Lys Arg Gln Ala Gln
85 90 95
Thr Asp Arg Val Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Trp Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asp Gln Ser Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Ala
165 170 175
Ala Glu Gln Gln Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Glu His
195 200 205
Pro Lys Thr His Val Thr His His Leu Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Glu Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Val Ala Val Val Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Ser Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Ala Cys Lys Ala
355 360 365
<210> 763
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 763
Met Arg Val Met Ala Pro Arg Thr Leu Ile Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Cys Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Gln Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Lys Tyr Lys Arg Gln Ala Gln
85 90 95
Thr Asp Arg Val Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Arg Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asn Gln Phe Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Lys Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Arg Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Lys Thr Leu Gln Arg Ala Glu His
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Glu Pro Leu Thr Leu Arg Trp Gly Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Met Ala Val Val Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Ser Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Ala Cys Lys Ala
355 360 365
<210> 764
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 764
Met Arg Val Met Ala Pro Arg Thr Leu Ile Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Cys Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Lys Tyr Lys Arg Gln Ala Gln
85 90 95
Ala Asp Arg Val Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Trp Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asp Gln Ser Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Trp Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Glu His
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Glu Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Met Ala Val Val Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Ser Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Ala Cys Lys Ala
355 360 365
<210> 765
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 765
Met Arg Val Met Ala Pro Arg Thr Leu Ile Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Cys Ser His Ser Met Lys Tyr Phe
20 25 30
Phe Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ser
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Lys Tyr Lys Arg Gln Ala Gln
85 90 95
Thr Asp Arg Val Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Trp Met Cys Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asp Gln Tyr Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Arg Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Glu His
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Trp Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Met
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Glu Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Val Ala Val Val Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Ser Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Ala Cys Lys Ala
355 360 365
<210> 766
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 766
Met Arg Val Met Ala Pro Arg Thr Leu Leu Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Cys Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Val Ser Arg Pro Gly Arg Gly Glu Pro His Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Asn Tyr Lys Arg Gln Ala Gln
85 90 95
Thr Asp Arg Val Asn Leu Arg Lys Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Ile Ile Gln Arg Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asp Gln Leu Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Glu His
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Glu Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Met Ala Val Val Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Ser Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Ala Cys Lys Ala
355 360 365
<210> 767
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 767
Met Arg Val Met Ala Pro Arg Ala Leu Leu Leu Leu Leu Ser Gly Gly
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Cys Ser His Ser Met Arg Tyr Phe
20 25 30
Asp Thr Ala Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ser
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Lys Tyr Lys Arg Gln Ala Gln
85 90 95
Ala Asp Arg Val Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Asp Gly Ser His Thr Phe Gln Arg Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asp Gln Phe Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Leu Glu Ala Ala Arg Ala
165 170 175
Ala Glu Gln Asp Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Lys Thr Leu Gln Arg Ala Glu Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Leu Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Gln Glu Gln Arg Tyr Thr Cys His Met Gln His Glu
275 280 285
Gly Leu Gln Glu Pro Leu Thr Leu Ser Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Met Gly Ile Val Ala Gly Leu Ala Val Leu Val Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Val Thr Ala Met Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Cys Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Thr Cys Lys Ala
355 360 365
<210> 768
<211> 366
<212> БЕЛОК
<213> Homo sapiens
<400> 768
Met Arg Val Met Ala Pro Arg Thr Leu Ile Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Cys Ser His Ser Met Arg Tyr Phe
20 25 30
Ser Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Gly Glu Pro Arg Ala Pro Trp Val Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Lys Tyr Lys Arg Gln Ala Gln
85 90 95
Thr Asp Arg Val Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Trp Met Phe Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asp Gln Ser Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Arg Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Glu His
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Trp Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Glu Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Leu Ala Val Leu Gly Ala Val Val Ala Val Val Met Cys Arg Arg Lys
325 330 335
Ser Ser Gly Gly Lys Gly Gly Ser Cys Ser Gln Ala Ala Ser Ser Asn
340 345 350
Ser Ala Gln Gly Ser Asp Glu Ser Leu Ile Ala Cys Lys Ala
355 360 365
<210> 769
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 769
Met Leu Val Met Ala Pro Arg Thr Val Leu Leu Leu Leu Ser Ala Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Asp Thr Ala Met Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ser
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Glu Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Gln Ile Phe Lys Thr Asn Thr Gln
85 90 95
Thr Asp Arg Glu Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Ser Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asn Gln Tyr Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Asp Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Asp Thr Leu Glu Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Val Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Ala Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Cys Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 770
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 770
Met Leu Val Met Ala Pro Arg Thr Val Leu Leu Leu Leu Ser Ala Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ser
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Glu Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Gln Ile Tyr Lys Ala Gln Ala Gln
85 90 95
Thr Asp Arg Glu Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Ser Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asp Gln Tyr Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Arg Arg Ala Tyr Leu Glu Gly Glu Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Asp Lys Leu Glu Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Val Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Ala Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Cys Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 771
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 771
Met Arg Val Thr Ala Pro Arg Thr Leu Leu Leu Leu Leu Trp Gly Ala
1 5 10 15
Val Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Met Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Thr
35 40 45
Val Gly Tyr Val Asp Asp Thr Leu Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Thr Ser Pro Arg Lys Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Ile Ser Lys Thr Asn Thr Gln
85 90 95
Thr Tyr Arg Glu Asn Leu Arg Thr Ala Leu Arg Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Ile Ile Gln Arg Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asp Gln Asp Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Asp Arg Ala Tyr Leu Glu Gly Leu Cys Val Glu Ser Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Val Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Val Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Ala Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Cys Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 772
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 772
Met Arg Val Thr Ala Pro Arg Thr Val Leu Leu Leu Leu Ser Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Met Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Met Ala Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Ile Ser Lys Thr Asn Thr Gln
85 90 95
Thr Tyr Arg Glu Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Arg Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asp Gln Ser Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Trp Arg Ala Tyr Leu Glu Gly Leu Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Thr Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 773
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 773
Met Arg Val Thr Ala Pro Arg Thr Val Leu Leu Leu Leu Ser Ala Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
His Thr Ala Met Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Thr
35 40 45
Val Gly Tyr Val Asp Asp Thr Leu Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Thr Ser Pro Arg Lys Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Ile Ser Lys Thr Asn Thr Gln
85 90 95
Thr Tyr Arg Glu Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Arg Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asn Gln Tyr Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Ser Gln Arg Lys Leu Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Glu Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Asp Lys Leu Glu Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Val Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Ala Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Cys Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 774
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 774
Met Arg Val Thr Ala Pro Arg Thr Leu Leu Leu Leu Leu Trp Gly Ala
1 5 10 15
Val Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Met Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Thr
35 40 45
Val Gly Tyr Val Asp Asp Thr Leu Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Thr Ser Pro Arg Lys Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Ile Ser Lys Thr Asn Thr Gln
85 90 95
Thr Tyr Arg Glu Asn Leu Arg Thr Ala Leu Arg Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Ile Ile Gln Arg Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asp Gln Asp Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Leu Cys Val Glu Ser Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Val Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Val Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Ala Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Cys Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 775
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 775
Met Arg Val Thr Ala Pro Arg Thr Val Leu Leu Leu Leu Trp Gly Ala
1 5 10 15
Val Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Met Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Thr Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Gln Ile Phe Lys Thr Asn Thr Gln
85 90 95
Thr Tyr Arg Glu Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Ile Ile Gln Arg Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asp Gln Ser Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Leu Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Thr Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 776
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 776
Met Arg Val Thr Ala Pro Arg Thr Val Leu Leu Leu Leu Trp Gly Ala
1 5 10 15
Val Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Met Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Thr Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Gln Ile Phe Lys Thr Asn Thr Gln
85 90 95
Thr Tyr Arg Glu Asn Leu Arg Ile Ala Leu Arg Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Trp Gln Thr Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asn Gln Tyr Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Leu Cys Val Glu Trp Leu
180 185 190
Arg Arg His Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Thr Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 777
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 777
Met Arg Val Thr Ala Pro Arg Thr Leu Leu Leu Leu Leu Trp Gly Ala
1 5 10 15
Val Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
His Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Thr
35 40 45
Val Gly Tyr Val Asp Asp Thr Leu Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Glu Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Ile Cys Lys Ala Lys Ala Gln
85 90 95
Thr Asp Arg Glu Asp Leu Arg Thr Leu Leu Arg Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Asn Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr His Gln Asp Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Glu Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Val Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Ala Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Cys Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 778
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 778
Met Arg Val Thr Ala Pro Arg Thr Val Leu Leu Leu Leu Trp Gly Ala
1 5 10 15
Val Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Met Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Met Ala Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Gly Glu Thr Arg Asn Met Lys Ala Ser Ala Gln
85 90 95
Thr Tyr Arg Glu Asn Leu Arg Ile Ala Leu Arg Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Ile Ile Gln Val Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asp Gln Ser Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Leu Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Val Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Ala Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Cys Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 779
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 779
Met Arg Val Thr Ala Pro Arg Thr Leu Leu Leu Leu Leu Trp Gly Ala
1 5 10 15
Val Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
His Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ser
35 40 45
Val Gly Tyr Val Asp Gly Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Thr Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Gln Ile Ser Lys Thr Asn Thr Gln
85 90 95
Thr Tyr Arg Glu Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Arg Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asp Gln Ser Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg His Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Thr Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 780
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 780
Met Leu Val Met Ala Pro Arg Thr Val Leu Leu Leu Leu Ser Ala Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ser
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Glu Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Gln Ile Cys Lys Thr Asn Thr Gln
85 90 95
Thr Asp Arg Glu Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Trp Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asn Gln Phe Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg His Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Val Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Ala Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 781
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 781
Met Arg Val Thr Ala Pro Arg Thr Leu Leu Leu Leu Leu Trp Gly Ala
1 5 10 15
Val Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Met Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Thr
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Thr Ser Pro Arg Met Ala Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Ile Ser Lys Thr Asn Thr Gln
85 90 95
Thr Tyr Arg Glu Asn Leu Arg Thr Ala Leu Arg Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Trp Gln Thr Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asn Gln Leu Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Leu Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Glu Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Val Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Ala Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Cys Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 782
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 782
Met Arg Val Thr Ala Pro Arg Thr Leu Leu Leu Leu Leu Trp Gly Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Met Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Glu Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Gln Ile Tyr Lys Ala Gln Ala Gln
85 90 95
Thr Asp Arg Glu Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Trp Gln Thr Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asn Gln Leu Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Thr Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 783
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 783
Met Leu Val Met Ala Pro Arg Thr Val Leu Leu Leu Leu Ser Ala Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ser
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Glu Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Gln Ile Cys Lys Thr Asn Thr Gln
85 90 95
Thr Asp Arg Glu Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Trp Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asn Gln Phe Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg His Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Val Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Ala Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 784
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 784
Met Arg Val Thr Ala Pro Arg Thr Val Leu Leu Leu Leu Ser Ala Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
His Thr Ala Met Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Thr
35 40 45
Val Gly Tyr Val Asp Asp Thr Leu Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Thr Ser Pro Arg Lys Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Ile Ser Lys Thr Asn Thr Gln
85 90 95
Thr Tyr Arg Glu Asn Leu Arg Ile Ala Leu Arg Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Trp Gln Arg Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asn Gln Leu Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Glu
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Leu Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Thr Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 785
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 785
Met Arg Val Thr Ala Pro Arg Thr Leu Leu Leu Leu Leu Trp Gly Ala
1 5 10 15
Val Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
His Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ser
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Thr Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Ile Ser Lys Thr Asn Thr Gln
85 90 95
Thr Tyr Arg Glu Asp Leu Arg Thr Leu Leu Arg Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Ile Gln Arg Met Ser Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly Tyr Asn Gln Phe Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Asp Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Thr Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 786
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 786
Met Leu Val Met Ala Pro Arg Thr Val Leu Leu Leu Leu Ser Ala Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ser
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Glu Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Gln Ile Cys Lys Thr Asn Thr Gln
85 90 95
Thr Tyr Arg Glu Asn Leu Arg Ile Ala Leu Arg Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Arg Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asn Gln Phe Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Thr Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Val Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Ala Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 787
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 787
Met Leu Val Met Ala Pro Arg Thr Val Leu Leu Leu Leu Ser Ala Ala
1 5 10 15
Leu Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ser
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Glu Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Gln Ile Cys Lys Thr Asn Thr Gln
85 90 95
Thr Asp Arg Glu Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Arg Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asn Gln Phe Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Thr Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Val Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Ala Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 788
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 788
Met Arg Val Thr Ala Pro Arg Thr Val Leu Leu Leu Leu Trp Gly Ala
1 5 10 15
Val Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
Tyr Thr Ala Met Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala
35 40 45
Val Gly Tyr Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Ala Ser Pro Arg Thr Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Asn Thr Gln Ile Phe Lys Thr Asn Thr Gln
85 90 95
Thr Tyr Arg Glu Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Ile Ile Gln Arg Met Tyr Gly Cys Asp Leu Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asp Gln Phe Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Ser Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Leu Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Val Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Ile Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Thr Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Ser Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 789
<211> 362
<212> БЕЛОК
<213> Homo sapiens
<400> 789
Met Arg Val Thr Ala Pro Arg Thr Leu Leu Leu Leu Leu Trp Gly Ala
1 5 10 15
Val Ala Leu Thr Glu Thr Trp Ala Gly Ser His Ser Met Arg Tyr Phe
20 25 30
His Thr Ser Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Thr
35 40 45
Val Gly Tyr Val Asp Asp Thr Leu Phe Val Arg Phe Asp Ser Asp Ala
50 55 60
Thr Ser Pro Arg Lys Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly
65 70 75 80
Pro Glu Tyr Trp Asp Arg Glu Thr Gln Ile Ser Lys Thr Asn Thr Gln
85 90 95
Thr Tyr Arg Glu Ser Leu Arg Asn Leu Arg Gly Tyr Tyr Asn Gln Ser
100 105 110
Glu Ala Gly Ser His Thr Leu Gln Ser Met Tyr Gly Cys Asp Val Gly
115 120 125
Pro Asp Gly Arg Leu Leu Arg Gly His Asn Gln Tyr Ala Tyr Asp Gly
130 135 140
Lys Asp Tyr Ile Ala Leu Asn Glu Asp Leu Arg Ser Trp Thr Ala Ala
145 150 155 160
Asp Thr Ala Ala Gln Ile Thr Gln Arg Lys Trp Glu Ala Ala Arg Val
165 170 175
Ala Glu Gln Leu Arg Ala Tyr Leu Glu Gly Glu Cys Val Glu Trp Leu
180 185 190
Arg Arg Tyr Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Ala Asp Pro
195 200 205
Pro Lys Thr His Val Thr His His Pro Ile Ser Asp His Glu Ala Thr
210 215 220
Leu Arg Cys Trp Ala Leu Gly Phe Tyr Pro Ala Glu Ile Thr Leu Thr
225 230 235 240
Trp Gln Arg Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu
245 250 255
Thr Arg Pro Ala Gly Asp Arg Thr Phe Gln Lys Trp Ala Ala Val Val
260 265 270
Val Pro Ser Gly Glu Glu Gln Arg Tyr Thr Cys His Val Gln His Glu
275 280 285
Gly Leu Pro Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Ser
290 295 300
Thr Val Pro Ile Val Gly Ile Val Ala Gly Leu Ala Val Leu Ala Val
305 310 315 320
Val Val Ile Gly Ala Val Val Ala Ala Val Met Cys Arg Arg Lys Ser
325 330 335
Ser Gly Gly Lys Gly Gly Ser Tyr Ser Gln Ala Ala Cys Ser Asp Ser
340 345 350
Ala Gln Gly Ser Asp Val Ser Leu Thr Ala
355 360
<210> 790
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 790
Met Val Cys Leu Lys Leu Pro Gly Gly Ser Cys Met Ala Ala Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Gln Pro Arg Phe Leu Trp Gln Gly Lys Tyr Lys Cys His Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Gln Phe Leu Glu Arg Leu Phe Tyr Asn Gln Glu
50 55 60
Glu Phe Val Arg Phe Asp Ser Asp Val Gly Glu Tyr Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Val Ala Glu Ser Trp Asn Ser Gln Lys Asp Ile
85 90 95
Leu Glu Asp Arg Arg Gly Gln Val Asp Thr Val Cys Arg His Asn Tyr
100 105 110
Gly Val Gly Glu Ser Phe Thr Val Gln Arg Arg Val His Pro Glu Val
115 120 125
Thr Val Tyr Pro Ala Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Ser Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Ala Gly Val Val Ser Thr Gly Leu
165 170 175
Ile Gln Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Val Met Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Thr Gly Phe Leu Ser
260 265
<210> 791
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 791
Met Val Cys Leu Arg Leu Pro Gly Gly Ser Cys Met Ala Val Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Glu Tyr Ser Thr Ser Glu Cys His Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Tyr Leu Asp Arg Tyr Phe His Asn Gln Glu
50 55 60
Glu Asn Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Asp Ala Glu Tyr Trp Asn Ser Gln Lys Asp Leu
85 90 95
Leu Glu Gln Lys Arg Gly Arg Val Asp Asn Tyr Cys Arg His Asn Tyr
100 105 110
Gly Val Val Glu Ser Phe Thr Val Gln Arg Arg Val His Pro Lys Val
115 120 125
Thr Val Tyr Pro Ser Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Ser Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Thr Gly Val Val Ser Thr Gly Leu
165 170 175
Ile His Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Val Thr Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Arg Gly Phe Leu Ser
260 265
<210> 792
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 792
Met Val Cys Leu Lys Leu Pro Gly Gly Ser Cys Met Thr Ala Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ser Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Trp Gln Pro Lys Arg Glu Cys His Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Phe Leu Asp Arg Tyr Phe Tyr Asn Gln Glu
50 55 60
Glu Ser Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Asp Ala Glu Tyr Trp Asn Ser Gln Lys Asp Ile
85 90 95
Leu Glu Gln Ala Arg Ala Ala Val Asp Thr Tyr Cys Arg His Asn Tyr
100 105 110
Gly Val Val Glu Ser Phe Thr Val Gln Arg Arg Val Gln Pro Lys Val
115 120 125
Thr Val Tyr Pro Ser Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Ser Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Leu Asn Gly Gln Glu Glu Lys Ala Gly Met Val Ser Thr Gly Leu
165 170 175
Ile Gln Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Val Thr Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Thr Gly Phe Leu Ser
260 265
<210> 793
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 793
Met Val Cys Leu Lys Phe Pro Gly Gly Ser Cys Met Ala Ala Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Glu Gln Val Lys His Glu Cys His Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Phe Leu Asp Arg Tyr Phe Tyr His Gln Glu
50 55 60
Glu Tyr Val Arg Phe Asp Ser Asp Val Gly Glu Tyr Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Asp Ala Glu Tyr Trp Asn Ser Gln Lys Asp Leu
85 90 95
Leu Glu Gln Lys Arg Ala Ala Val Asp Thr Tyr Cys Arg His Asn Tyr
100 105 110
Gly Val Gly Glu Ser Phe Thr Val Gln Arg Arg Val Tyr Pro Glu Val
115 120 125
Thr Val Tyr Pro Ala Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Asn Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Thr Gly Val Val Ser Thr Gly Leu
165 170 175
Ile Gln Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Leu Thr Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Thr Gly Phe Leu Ser
260 265
<210> 794
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 794
Met Val Cys Leu Lys Leu Pro Gly Gly Ser Cys Met Thr Ala Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Trp Gln Leu Lys Phe Glu Cys His Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Leu Leu Glu Arg Cys Ile Tyr Asn Gln Glu
50 55 60
Glu Ser Val Arg Phe Asp Ser Asp Val Gly Glu Tyr Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Asp Ala Glu Tyr Trp Asn Ser Gln Lys Asp Leu
85 90 95
Leu Glu Gln Arg Arg Ala Ala Val Asp Thr Tyr Cys Arg His Asn Tyr
100 105 110
Gly Val Gly Glu Ser Phe Thr Val Gln Arg Arg Val Glu Pro Lys Val
115 120 125
Thr Val Tyr Pro Ser Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Ser Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Ala Gly Val Val Ser Thr Gly Leu
165 170 175
Ile Gln Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Val Thr Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Thr Gly Phe Leu Ser
260 265
<210> 795
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 795
Met Val Cys Leu Arg Leu Pro Gly Gly Ser Cys Met Ala Val Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Glu Tyr Ser Thr Ser Glu Cys His Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Phe Leu Asp Arg Tyr Phe His Asn Gln Glu
50 55 60
Glu Asn Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Asp Ala Glu Tyr Trp Asn Ser Gln Lys Asp Ile
85 90 95
Leu Glu Asp Glu Arg Ala Ala Val Asp Thr Tyr Cys Arg His Asn Tyr
100 105 110
Gly Val Val Glu Ser Phe Thr Val Gln Arg Arg Val His Pro Lys Val
115 120 125
Thr Val Tyr Pro Ser Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Ser Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Thr Gly Val Val Ser Thr Gly Leu
165 170 175
Ile His Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Val Thr Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Arg Gly Phe Leu Ser
260 265
<210> 796
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 796
Met Val Cys Leu Arg Leu Pro Gly Gly Ser Cys Met Ala Val Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Glu Tyr Ser Thr Ser Glu Cys His Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Phe Leu Asp Arg Tyr Phe Tyr Asn Gln Glu
50 55 60
Glu Tyr Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Asp Glu Glu Tyr Trp Asn Ser Gln Lys Asp Phe
85 90 95
Leu Glu Asp Arg Arg Ala Ala Val Asp Thr Tyr Cys Arg His Asn Tyr
100 105 110
Gly Val Gly Glu Ser Phe Thr Val Gln Arg Arg Val His Pro Lys Val
115 120 125
Thr Val Tyr Pro Ser Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Ser Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Thr Gly Val Val Ser Thr Gly Leu
165 170 175
Ile His Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Val Thr Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Arg Gly Phe Leu Ser
260 265
<210> 797
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 797
Met Val Cys Leu Lys Phe Pro Gly Gly Ser Cys Met Ala Ala Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Glu Gln Val Lys His Glu Cys His Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Phe Leu Asp Arg Tyr Phe Tyr His Gln Glu
50 55 60
Glu Tyr Val Arg Phe Asp Ser Asp Val Gly Glu Tyr Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Asp Ala Glu Tyr Trp Asn Ser Gln Lys Asp Leu
85 90 95
Leu Glu Gln Arg Arg Ala Ala Val Asp Thr Tyr Cys Arg His Asn Tyr
100 105 110
Gly Val Val Glu Ser Phe Thr Val Gln Arg Arg Val Tyr Pro Glu Val
115 120 125
Thr Val Tyr Pro Ala Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Asn Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Thr Gly Val Val Ser Thr Gly Leu
165 170 175
Ile Gln Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Leu Thr Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Thr Gly Phe Leu Ser
260 265
<210> 798
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 798
Met Val Cys Leu Arg Leu Pro Gly Gly Ser Cys Met Ala Val Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Glu Tyr Ser Thr Ser Glu Cys His Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Phe Leu Asp Arg Tyr Phe His Asn Gln Glu
50 55 60
Glu Asn Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Asp Ala Glu Tyr Trp Asn Ser Gln Lys Asp Ile
85 90 95
Leu Glu Asp Glu Arg Ala Ala Val Asp Thr Tyr Cys Arg His Asn Tyr
100 105 110
Gly Val Gly Glu Ser Phe Thr Val Gln Arg Arg Val His Pro Lys Val
115 120 125
Thr Val Tyr Pro Ser Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Ser Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Thr Gly Val Val Ser Thr Gly Leu
165 170 175
Ile His Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Val Thr Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Arg Gly Phe Leu Ser
260 265
<210> 799
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 799
Met Val Cys Leu Arg Leu Pro Gly Gly Ser Cys Met Ala Val Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Glu Tyr Ser Thr Gly Glu Cys Tyr Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Phe Leu Asp Arg Tyr Phe Tyr Asn Gln Glu
50 55 60
Glu Tyr Val Arg Phe Asp Ser Asp Val Gly Glu Tyr Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Ser Ala Glu Tyr Trp Asn Ser Gln Lys Asp Phe
85 90 95
Leu Glu Asp Arg Arg Ala Leu Val Asp Thr Tyr Cys Arg His Asn Tyr
100 105 110
Gly Val Gly Glu Ser Phe Thr Val Gln Arg Arg Val His Pro Lys Val
115 120 125
Thr Val Tyr Pro Ser Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Ser Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Thr Gly Val Val Ser Thr Gly Leu
165 170 175
Ile His Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Val Thr Ser Pro Leu Thr Val Glu Trp Ser Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Thr Gly Phe Leu Ser
260 265
<210> 800
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 800
Met Val Cys Leu Arg Leu Pro Gly Gly Ser Cys Met Ala Val Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Glu Tyr Ser Thr Gly Glu Cys Tyr Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Leu Leu Glu Arg His Phe His Asn Gln Glu
50 55 60
Glu Leu Leu Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Val Ala Glu Ser Trp Asn Ser Gln Lys Asp Ile
85 90 95
Leu Glu Asp Arg Arg Ala Ala Val Asp Thr Tyr Cys Arg His Asn Tyr
100 105 110
Gly Ala Val Glu Ser Phe Thr Val Gln Arg Arg Val His Pro Lys Val
115 120 125
Thr Val Tyr Pro Ser Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Ser Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Thr Gly Val Val Ser Thr Gly Leu
165 170 175
Ile His Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Val Thr Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Arg Gly Phe Leu Ser
260 265
<210> 801
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 801
Met Val Cys Leu Arg Leu Pro Gly Gly Ser Cys Met Ala Val Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Glu Tyr Ser Thr Ser Glu Cys His Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Phe Leu Asp Arg Tyr Phe Tyr Asn Gln Glu
50 55 60
Glu Tyr Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Asp Glu Glu Tyr Trp Asn Ser Gln Lys Asp Phe
85 90 95
Leu Glu Asp Arg Arg Ala Ala Val Asp Thr Tyr Cys Arg His Asn Tyr
100 105 110
Gly Val Val Glu Ser Phe Thr Val Gln Arg Arg Val His Pro Lys Val
115 120 125
Thr Val Tyr Pro Ser Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Ser Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Thr Gly Val Val Ser Thr Gly Leu
165 170 175
Ile His Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Val Thr Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Arg Gly Phe Leu Ser
260 265
<210> 802
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 802
Met Val Cys Leu Lys Leu Pro Gly Gly Ser Cys Met Ala Ala Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Gln Pro Arg Phe Leu Lys Gln Asp Lys Phe Glu Cys His Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Tyr Leu His Arg Gly Ile Tyr Asn Gln Glu
50 55 60
Glu Asn Val Arg Phe Asp Ser Asp Val Gly Glu Tyr Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Val Ala Glu Ser Trp Asn Ser Gln Lys Asp Phe
85 90 95
Leu Glu Arg Arg Arg Ala Glu Val Asp Thr Val Cys Arg His Asn Tyr
100 105 110
Gly Val Gly Glu Ser Phe Thr Val Gln Arg Arg Val His Pro Glu Val
115 120 125
Thr Val Tyr Pro Ala Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Ser Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Ala Gly Val Val Ser Thr Gly Leu
165 170 175
Ile Gln Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Val Met Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Thr Gly Phe Leu Ser
260 265
<210> 803
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 803
Met Val Cys Leu Arg Leu Pro Gly Gly Ser Cys Met Ala Val Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Glu Tyr Ser Thr Ser Glu Cys His Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Phe Leu Asp Arg Tyr Phe His Asn Gln Glu
50 55 60
Glu Phe Val Arg Phe Asp Ser Asp Val Gly Glu Tyr Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Ala Ala Glu His Trp Asn Ser Gln Lys Asp Leu
85 90 95
Leu Glu Arg Arg Arg Ala Glu Val Asp Thr Tyr Cys Arg His Asn Tyr
100 105 110
Gly Val Val Glu Ser Phe Thr Val Gln Arg Arg Val His Pro Lys Val
115 120 125
Thr Val Tyr Pro Ser Lys Thr Gln Pro Leu Gln His Tyr Asn Leu Leu
130 135 140
Val Cys Ser Val Ser Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Thr Gly Val Val Ser Thr Gly Leu
165 170 175
Ile His Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Val Thr Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Arg Gly Phe Leu Ser
260 265
<210> 804
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 804
Met Val Cys Leu Lys Phe Pro Gly Gly Ser Cys Met Ala Ala Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Glu Gln Val Lys His Glu Cys His Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Phe Leu Asp Arg Tyr Phe Tyr His Gln Glu
50 55 60
Glu Tyr Val Arg Phe Asp Ser Asp Val Gly Glu Tyr Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Asp Ala Glu Tyr Trp Asn Ser Gln Lys Asp Leu
85 90 95
Leu Glu Gln Arg Arg Ala Glu Val Asp Thr Tyr Cys Arg His Asn Tyr
100 105 110
Gly Val Gly Glu Ser Phe Thr Val Gln Arg Arg Val Tyr Pro Glu Val
115 120 125
Thr Val Tyr Pro Ala Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Asn Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Thr Gly Val Val Ser Thr Gly Leu
165 170 175
Ile Gln Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Leu Thr Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Thr Gly Phe Leu Ser
260 265
<210> 805
<211> 266
<212> БЕЛОК
<213> Homo sapiens
<400> 805
Met Val Cys Leu Arg Leu Pro Gly Gly Ser Cys Met Ala Val Leu Thr
1 5 10 15
Val Thr Leu Met Val Leu Ser Ser Pro Leu Ala Leu Ala Gly Asp Thr
20 25 30
Arg Pro Arg Phe Leu Glu Tyr Ser Thr Gly Glu Cys Tyr Phe Phe Asn
35 40 45
Gly Thr Glu Arg Val Arg Phe Leu Asp Arg Tyr Phe His Asn Gln Glu
50 55 60
Glu Phe Val Arg Phe Asp Ser Asp Val Gly Glu Tyr Arg Ala Val Thr
65 70 75 80
Glu Leu Gly Arg Pro Ala Ala Glu His Trp Asn Ser Gln Lys Asp Leu
85 90 95
Leu Glu Arg Arg Arg Ala Glu Val Asp Thr Tyr Cys Arg His Asn Tyr
100 105 110
Gly Val Val Glu Ser Phe Thr Val Gln Arg Arg Val His Pro Lys Val
115 120 125
Thr Val Tyr Pro Ser Lys Thr Gln Pro Leu Gln His His Asn Leu Leu
130 135 140
Val Cys Ser Val Ser Gly Phe Tyr Pro Gly Ser Ile Glu Val Arg Trp
145 150 155 160
Phe Arg Asn Gly Gln Glu Glu Lys Thr Gly Val Val Ser Thr Gly Leu
165 170 175
Ile His Asn Gly Asp Trp Thr Phe Gln Thr Leu Val Met Leu Glu Thr
180 185 190
Val Pro Arg Ser Gly Glu Val Tyr Thr Cys Gln Val Glu His Pro Ser
195 200 205
Val Thr Ser Pro Leu Thr Val Glu Trp Arg Ala Arg Ser Glu Ser Ala
210 215 220
Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu Gly Leu Leu
225 230 235 240
Phe Leu Gly Ala Gly Leu Phe Ile Tyr Phe Arg Asn Gln Lys Gly His
245 250 255
Ser Gly Leu Gln Pro Arg Gly Phe Leu Ser
260 265
<210> 806
<211> 254
<212> БЕЛОК
<213> Homo sapiens
<400> 806
Met Ile Leu Asn Lys Ala Leu Met Leu Gly Ala Leu Ala Leu Thr Thr
1 5 10 15
Val Met Ser Pro Cys Gly Gly Glu Asp Ile Val Ala Asp His Val Ala
20 25 30
Ser Tyr Gly Val Asn Leu Tyr Gln Ser Tyr Gly Pro Ser Gly Gln Tyr
35 40 45
Thr His Glu Phe Asp Gly Asp Glu Gln Phe Tyr Val Asp Leu Gly Arg
50 55 60
Lys Glu Thr Val Trp Cys Leu Pro Val Leu Arg Gln Phe Arg Phe Asp
65 70 75 80
Pro Gln Phe Ala Leu Thr Asn Ile Ala Val Leu Lys His Asn Leu Asn
85 90 95
Ser Leu Ile Lys Arg Ser Asn Ser Thr Ala Ala Thr Asn Glu Val Pro
100 105 110
Glu Val Thr Val Phe Ser Lys Ser Pro Val Thr Leu Gly Gln Pro Asn
115 120 125
Ile Leu Ile Cys Leu Val Asp Asn Ile Phe Pro Pro Val Val Asn Ile
130 135 140
Thr Trp Leu Ser Asn Gly His Ser Val Thr Glu Gly Val Ser Glu Thr
145 150 155 160
Ser Phe Leu Ser Lys Ser Asp His Ser Phe Phe Lys Ile Ser Tyr Leu
165 170 175
Thr Leu Leu Pro Ser Ala Glu Glu Ser Tyr Asp Cys Lys Val Glu His
180 185 190
Trp Gly Leu Asp Lys Pro Leu Leu Lys His Trp Glu Pro Glu Ile Pro
195 200 205
Ala Pro Met Ser Glu Leu Thr Glu Thr Val Val Cys Ala Leu Gly Leu
210 215 220
Ser Val Gly Leu Val Gly Ile Val Val Gly Thr Val Phe Ile Ile Arg
225 230 235 240
Gly Leu Arg Ser Val Gly Ala Ser Arg His Gln Gly Pro Leu
245 250
<210> 807
<211> 255
<212> БЕЛОК
<213> Homo sapiens
<400> 807
Met Ile Leu Asn Lys Ala Leu Met Leu Gly Ala Leu Ala Leu Thr Thr
1 5 10 15
Val Met Ser Pro Cys Gly Gly Glu Asp Ile Val Ala Asp His Val Ala
20 25 30
Ser Tyr Gly Val Asn Leu Tyr Gln Ser Tyr Gly Pro Ser Gly Gln Tyr
35 40 45
Ser His Glu Phe Asp Gly Asp Glu Glu Phe Tyr Val Asp Leu Glu Arg
50 55 60
Lys Glu Thr Val Trp Gln Leu Pro Leu Phe Arg Arg Phe Arg Arg Phe
65 70 75 80
Asp Pro Gln Phe Ala Leu Thr Asn Ile Ala Val Leu Lys His Asn Leu
85 90 95
Asn Ile Val Ile Lys Arg Ser Asn Ser Thr Ala Ala Thr Asn Glu Val
100 105 110
Pro Glu Val Thr Val Phe Ser Lys Ser Pro Val Thr Leu Gly Gln Pro
115 120 125
Asn Thr Leu Ile Cys Leu Val Asp Asn Ile Phe Pro Pro Val Val Asn
130 135 140
Ile Thr Trp Leu Ser Asn Gly His Ser Val Thr Glu Gly Val Ser Glu
145 150 155 160
Thr Ser Phe Leu Ser Lys Ser Asp His Ser Phe Phe Lys Ile Ser Tyr
165 170 175
Leu Thr Phe Leu Pro Ser Ala Asp Glu Ile Tyr Asp Cys Lys Val Glu
180 185 190
His Trp Gly Leu Asp Glu Pro Leu Leu Lys His Trp Glu Pro Glu Ile
195 200 205
Pro Thr Pro Met Ser Glu Leu Thr Glu Thr Val Val Cys Ala Leu Gly
210 215 220
Leu Ser Val Gly Leu Val Gly Ile Val Val Gly Thr Val Leu Ile Ile
225 230 235 240
Arg Gly Leu Arg Ser Val Gly Ala Ser Arg His Gln Gly Pro Leu
245 250 255
<210> 808
<211> 255
<212> БЕЛОК
<213> Homo sapiens
<400> 808
Met Ile Leu Asn Lys Ala Leu Leu Leu Gly Ala Leu Ala Leu Thr Thr
1 5 10 15
Val Met Ser Pro Cys Gly Gly Glu Asp Ile Val Ala Asp His Val Ala
20 25 30
Ser Cys Gly Val Asn Leu Tyr Gln Phe Tyr Gly Pro Ser Gly Gln Tyr
35 40 45
Thr His Glu Phe Asp Gly Asp Glu Gln Phe Tyr Val Asp Leu Glu Arg
50 55 60
Lys Glu Thr Ala Trp Arg Trp Pro Glu Phe Ser Lys Phe Gly Gly Phe
65 70 75 80
Asp Pro Gln Gly Ala Leu Arg Asn Met Ala Val Ala Lys His Asn Leu
85 90 95
Asn Ile Met Ile Lys Arg Tyr Asn Ser Thr Ala Ala Thr Asn Glu Val
100 105 110
Pro Glu Val Thr Val Phe Ser Lys Ser Pro Val Thr Leu Gly Gln Pro
115 120 125
Asn Thr Leu Ile Cys Leu Val Asp Asn Ile Phe Pro Pro Val Val Asn
130 135 140
Ile Thr Trp Leu Ser Asn Gly Gln Ser Val Thr Glu Gly Val Ser Glu
145 150 155 160
Thr Ser Phe Leu Ser Lys Ser Asp His Ser Phe Phe Lys Ile Ser Tyr
165 170 175
Leu Thr Phe Leu Pro Ser Ala Asp Glu Ile Tyr Asp Cys Lys Val Glu
180 185 190
His Trp Gly Leu Asp Gln Pro Leu Leu Lys His Trp Glu Pro Glu Ile
195 200 205
Pro Ala Pro Met Ser Glu Leu Thr Glu Thr Val Val Cys Ala Leu Gly
210 215 220
Leu Ser Val Gly Leu Met Gly Ile Val Val Gly Thr Val Phe Ile Ile
225 230 235 240
Gln Gly Leu Arg Ser Val Gly Ala Ser Arg His Gln Gly Pro Leu
245 250 255
<210> 809
<211> 254
<212> БЕЛОК
<213> Homo sapiens
<400> 809
Met Ile Leu Asn Lys Ala Leu Met Leu Gly Ala Leu Ala Leu Thr Thr
1 5 10 15
Val Met Ser Pro Cys Gly Gly Glu Asp Ile Val Ala Asp His Val Ala
20 25 30
Ser Tyr Gly Val Asn Leu Tyr Gln Ser Tyr Gly Pro Ser Gly Gln Phe
35 40 45
Thr His Glu Phe Asp Gly Asp Glu Glu Phe Tyr Val Asp Leu Glu Arg
50 55 60
Lys Glu Thr Val Trp Lys Leu Pro Leu Phe His Arg Leu Arg Phe Asp
65 70 75 80
Pro Gln Phe Ala Leu Thr Asn Ile Ala Val Leu Lys His Asn Leu Asn
85 90 95
Ile Leu Ile Lys Arg Ser Asn Ser Thr Ala Ala Thr Asn Glu Val Pro
100 105 110
Glu Val Thr Val Phe Ser Lys Ser Pro Val Thr Leu Gly Gln Pro Asn
115 120 125
Thr Leu Ile Cys Leu Val Asp Asn Ile Phe Pro Pro Val Val Asn Ile
130 135 140
Thr Trp Leu Ser Asn Gly His Ser Val Thr Glu Gly Val Ser Glu Thr
145 150 155 160
Ser Phe Leu Ser Lys Ser Asp His Ser Phe Phe Lys Ile Ser Tyr Leu
165 170 175
Thr Phe Leu Pro Ser Ala Asp Glu Ile Tyr Asp Cys Lys Val Glu His
180 185 190
Trp Gly Leu Asp Glu Pro Leu Leu Lys His Trp Glu Pro Glu Ile Pro
195 200 205
Ala Pro Met Ser Glu Leu Thr Glu Thr Val Val Cys Ala Leu Gly Leu
210 215 220
Ser Val Gly Leu Val Gly Ile Val Val Gly Thr Val Leu Ile Ile Arg
225 230 235 240
Gly Leu Arg Ser Val Gly Ala Ser Arg His Gln Gly Pro Leu
245 250
<210> 810
<211> 255
<212> БЕЛОК
<213> Homo sapiens
<400> 810
Met Ile Leu Asn Lys Ala Leu Leu Leu Gly Ala Leu Ala Leu Thr Thr
1 5 10 15
Val Met Ser Pro Cys Gly Gly Glu Asp Ile Val Ala Asp His Val Ala
20 25 30
Ser Cys Gly Val Asn Leu Tyr Gln Phe Tyr Gly Pro Ser Gly Gln Tyr
35 40 45
Thr His Glu Phe Asp Gly Asp Glu Glu Phe Tyr Val Asp Leu Glu Arg
50 55 60
Lys Glu Thr Ala Trp Arg Trp Pro Glu Phe Ser Lys Phe Gly Gly Phe
65 70 75 80
Asp Pro Gln Gly Ala Leu Arg Asn Met Ala Val Ala Lys His Asn Leu
85 90 95
Asn Ile Met Ile Lys Arg Tyr Asn Ser Thr Ala Ala Thr Asn Glu Val
100 105 110
Pro Glu Val Thr Val Phe Ser Lys Ser Pro Val Thr Leu Gly Gln Pro
115 120 125
Asn Thr Leu Ile Cys Leu Val Asp Asn Ile Phe Pro Pro Val Val Asn
130 135 140
Ile Thr Trp Leu Ser Asn Gly Gln Ser Val Thr Glu Gly Val Ser Glu
145 150 155 160
Thr Ser Phe Leu Ser Lys Ser Asp His Ser Phe Phe Lys Ile Ser Tyr
165 170 175
Leu Thr Phe Leu Pro Ser Ala Asp Glu Ile Tyr Asp Cys Lys Val Glu
180 185 190
His Trp Gly Leu Asp Gln Pro Leu Leu Lys His Trp Glu Pro Glu Ile
195 200 205
Pro Ala Pro Met Ser Glu Leu Thr Glu Thr Val Val Cys Ala Leu Gly
210 215 220
Leu Ser Val Gly Leu Val Gly Ile Val Val Gly Thr Val Phe Ile Ile
225 230 235 240
Gln Gly Leu Arg Ser Val Gly Ala Ser Arg His Gln Gly Pro Leu
245 250 255
<210> 811
<211> 255
<212> БЕЛОК
<213> Homo sapiens
<400> 811
Met Ile Leu Asn Lys Ala Leu Leu Leu Gly Ala Leu Ala Leu Thr Thr
1 5 10 15
Val Met Ser Pro Cys Gly Gly Glu Asp Ile Val Ala Asp His Val Ala
20 25 30
Ser Cys Gly Val Asn Leu Tyr Gln Phe Tyr Gly Pro Ser Gly Gln Phe
35 40 45
Thr His Glu Phe Asp Gly Asp Glu Gln Phe Tyr Val Asp Leu Glu Lys
50 55 60
Lys Glu Thr Ala Trp Arg Trp Pro Glu Phe Ser Lys Phe Gly Gly Phe
65 70 75 80
Asp Pro Gln Gly Ala Leu Arg Asn Met Ala Val Ala Lys His Asn Leu
85 90 95
Asn Ile Met Ile Lys Arg Tyr Asn Ser Thr Ala Ala Thr Asn Glu Val
100 105 110
Pro Glu Val Thr Val Phe Ser Lys Ser Pro Val Thr Leu Gly Gln Pro
115 120 125
Asn Thr Leu Ile Cys Leu Val Asp Asn Ile Phe Pro Pro Val Val Asn
130 135 140
Ile Thr Trp Leu Ser Asn Gly His Ala Val Thr Glu Gly Val Ser Glu
145 150 155 160
Thr Ser Phe Leu Ser Lys Ser Asp His Ser Phe Phe Lys Ile Ser Tyr
165 170 175
Leu Thr Phe Leu Pro Ser Ala Asp Glu Ile Tyr Asp Cys Lys Val Glu
180 185 190
His Trp Gly Leu Asp Gln Pro Leu Leu Lys His Trp Glu Pro Glu Ile
195 200 205
Pro Ala Pro Met Ser Glu Leu Thr Glu Thr Val Val Cys Ala Leu Gly
210 215 220
Leu Ser Val Gly Leu Val Gly Ile Val Val Gly Thr Val Phe Ile Ile
225 230 235 240
Gln Gly Leu Arg Ser Val Gly Ala Ser Arg His Gln Gly Pro Leu
245 250 255
<210> 812
<211> 254
<212> БЕЛОК
<213> Homo sapiens
<400> 812
Met Ile Leu Asn Lys Ala Leu Leu Leu Gly Ala Leu Ala Leu Thr Thr
1 5 10 15
Val Met Ser Pro Cys Gly Gly Glu Asp Ile Val Ala Asp His Val Ala
20 25 30
Ser Tyr Gly Val Asn Leu Tyr Gln Ser Tyr Gly Pro Ser Gly Gln Tyr
35 40 45
Thr His Glu Phe Asp Gly Asp Glu Gln Phe Tyr Val Asp Leu Gly Arg
50 55 60
Lys Glu Thr Val Trp Cys Leu Pro Val Leu Arg Gln Phe Arg Phe Asp
65 70 75 80
Pro Gln Phe Ala Leu Thr Asn Ile Ala Val Thr Lys His Asn Leu Asn
85 90 95
Ile Leu Ile Lys Arg Ser Asn Ser Thr Ala Ala Thr Asn Glu Val Pro
100 105 110
Glu Val Thr Val Phe Ser Lys Ser Pro Val Thr Leu Gly Gln Pro Asn
115 120 125
Thr Leu Ile Cys Leu Val Asp Asn Ile Phe Pro Pro Val Val Asn Ile
130 135 140
Thr Trp Leu Ser Asn Gly His Ser Val Thr Glu Gly Val Ser Glu Thr
145 150 155 160
Ser Phe Leu Ser Lys Ser Asp His Ser Phe Phe Lys Ile Ser Tyr Leu
165 170 175
Thr Phe Leu Pro Ser Ala Asp Glu Ile Tyr Asp Cys Lys Val Glu His
180 185 190
Trp Gly Leu Asp Glu Pro Leu Leu Lys His Trp Glu Pro Glu Ile Pro
195 200 205
Ala Pro Met Ser Glu Leu Thr Glu Thr Val Val Cys Ala Leu Gly Leu
210 215 220
Ser Val Gly Leu Val Gly Ile Val Val Gly Thr Val Phe Ile Ile Arg
225 230 235 240
Gly Leu Arg Ser Val Gly Ala Ser Arg His Gln Gly Pro Leu
245 250
<210> 813
<211> 261
<212> БЕЛОК
<213> Homo sapiens
<400> 813
Met Ser Trp Lys Lys Ala Leu Arg Ile Pro Gly Gly Leu Arg Ala Ala
1 5 10 15
Thr Val Thr Leu Met Leu Ala Met Leu Ser Thr Pro Val Ala Glu Gly
20 25 30
Arg Asp Ser Pro Glu Asp Phe Val Tyr Gln Phe Lys Ala Met Cys Tyr
35 40 45
Phe Thr Asn Gly Thr Glu Arg Val Arg Tyr Val Thr Arg Tyr Ile Tyr
50 55 60
Asn Arg Glu Glu Tyr Ala Arg Phe Asp Ser Asp Val Glu Val Tyr Arg
65 70 75 80
Ala Val Thr Pro Leu Gly Pro Pro Asp Ala Glu Tyr Trp Asn Ser Gln
85 90 95
Lys Glu Val Leu Glu Arg Thr Arg Ala Glu Leu Asp Thr Val Cys Arg
100 105 110
His Asn Tyr Gln Leu Glu Leu Arg Thr Thr Leu Gln Arg Arg Val Glu
115 120 125
Pro Thr Val Thr Ile Ser Pro Ser Arg Thr Glu Ala Leu Asn His His
130 135 140
Asn Leu Leu Val Cys Ser Val Thr Asp Phe Tyr Pro Ala Gln Ile Lys
145 150 155 160
Val Arg Trp Phe Arg Asn Asp Gln Glu Glu Thr Thr Gly Val Val Ser
165 170 175
Thr Pro Leu Ile Arg Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met
180 185 190
Leu Glu Met Thr Pro Gln His Gly Asp Val Tyr Thr Cys His Val Glu
195 200 205
His Pro Ser Leu Gln Asn Pro Ile Thr Val Glu Trp Arg Ala Gln Ser
210 215 220
Glu Ser Ala Gln Ser Lys Met Leu Ser Gly Ile Gly Gly Phe Val Leu
225 230 235 240
Gly Leu Ile Phe Leu Gly Leu Gly Leu Ile Ile His His Arg Ser Gln
245 250 255
Lys Gly Leu Leu His
260
<210> 814
<211> 261
<212> БЕЛОК
<213> Homo sapiens
<400> 814
Met Ser Trp Lys Lys Ala Leu Arg Ile Pro Gly Gly Leu Arg Ala Ala
1 5 10 15
Thr Val Thr Leu Met Leu Ser Met Leu Ser Thr Pro Val Ala Glu Gly
20 25 30
Arg Asp Ser Pro Glu Asp Phe Val Tyr Gln Phe Lys Gly Met Cys Tyr
35 40 45
Phe Thr Asn Gly Thr Glu Arg Val Arg Leu Val Ser Arg Ser Ile Tyr
50 55 60
Asn Arg Glu Glu Ile Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg
65 70 75 80
Ala Val Thr Leu Leu Gly Leu Pro Ala Ala Glu Tyr Trp Asn Ser Gln
85 90 95
Lys Asp Ile Leu Glu Arg Lys Arg Ala Ala Val Asp Arg Val Cys Arg
100 105 110
His Asn Tyr Gln Leu Glu Leu Arg Thr Thr Leu Gln Arg Arg Val Glu
115 120 125
Pro Thr Val Thr Ile Ser Pro Ser Arg Thr Glu Ala Leu Asn His His
130 135 140
Asn Leu Leu Val Cys Ser Val Thr Asp Phe Tyr Pro Ala Gln Ile Lys
145 150 155 160
Val Arg Trp Phe Arg Asn Asp Gln Glu Glu Thr Ala Gly Val Val Ser
165 170 175
Thr Pro Leu Ile Arg Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met
180 185 190
Leu Glu Met Thr Pro Gln Arg Gly Asp Val Tyr Thr Cys His Val Glu
195 200 205
His Pro Ser Leu Gln Ser Pro Ile Thr Val Glu Trp Arg Ala Gln Ser
210 215 220
Glu Ser Ala Gln Ser Lys Met Leu Ser Gly Ile Gly Gly Phe Val Leu
225 230 235 240
Gly Leu Ile Phe Leu Gly Leu Gly Leu Ile Ile His His Arg Ser Gln
245 250 255
Lys Gly Leu Leu His
260
<210> 815
<211> 261
<212> БЕЛОК
<213> Homo sapiens
<400> 815
Met Ser Trp Lys Lys Ala Leu Arg Ile Pro Gly Asp Leu Arg Val Ala
1 5 10 15
Thr Val Thr Leu Met Leu Ala Met Leu Ser Ser Leu Leu Ala Glu Gly
20 25 30
Arg Asp Ser Pro Glu Asp Phe Val Phe Gln Phe Lys Gly Met Cys Tyr
35 40 45
Phe Thr Asn Gly Thr Glu Arg Val Arg Leu Val Thr Arg Tyr Ile Tyr
50 55 60
Asn Arg Glu Glu Tyr Ala Arg Phe Asp Ser Asp Val Gly Val Tyr Arg
65 70 75 80
Ala Val Thr Pro Gln Gly Arg Pro Asp Ala Glu Tyr Trp Asn Ser Gln
85 90 95
Lys Glu Val Leu Glu Gly Thr Arg Ala Glu Leu Asp Thr Val Cys Arg
100 105 110
His Asn Tyr Glu Val Ala Phe Arg Gly Ile Leu Gln Arg Arg Val Glu
115 120 125
Pro Thr Val Thr Ile Ser Pro Ser Arg Thr Glu Ala Leu Asn His His
130 135 140
Asn Leu Leu Val Cys Ser Val Thr Asp Phe Tyr Pro Gly Gln Ile Lys
145 150 155 160
Val Arg Trp Phe Arg Asn Asp Gln Glu Glu Thr Ala Gly Val Val Ser
165 170 175
Thr Pro Leu Ile Arg Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met
180 185 190
Leu Glu Met Thr Pro Gln Arg Gly Asp Val Tyr Thr Cys His Val Glu
195 200 205
His Pro Ser Leu Gln Ser Pro Ile Thr Val Glu Trp Arg Ala Gln Ser
210 215 220
Glu Ser Ala Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu
225 230 235 240
Gly Leu Ile Phe Leu Gly Leu Gly Leu Ile Ile Arg Gln Arg Ser Gln
245 250 255
Lys Gly Leu Leu His
260
<210> 816
<211> 261
<212> БЕЛОК
<213> Homo sapiens
<400> 816
Met Ser Trp Lys Lys Ser Leu Arg Ile Pro Gly Asp Leu Arg Val Ala
1 5 10 15
Thr Val Thr Leu Met Leu Ala Ile Leu Ser Ser Ser Leu Ala Glu Gly
20 25 30
Arg Asp Ser Pro Glu Asp Phe Val Tyr Gln Phe Lys Gly Leu Cys Tyr
35 40 45
Phe Thr Asn Gly Thr Glu Arg Val Arg Gly Val Thr Arg His Ile Tyr
50 55 60
Asn Arg Glu Glu Tyr Val Arg Phe Asp Ser Asp Val Gly Val Tyr Arg
65 70 75 80
Ala Val Thr Pro Gln Gly Arg Pro Val Ala Glu Tyr Trp Asn Ser Gln
85 90 95
Lys Glu Val Leu Glu Gly Ala Arg Ala Ser Val Asp Arg Val Cys Arg
100 105 110
His Asn Tyr Glu Val Ala Tyr Arg Gly Ile Leu Gln Arg Arg Val Glu
115 120 125
Pro Thr Val Thr Ile Ser Pro Ser Arg Thr Glu Ala Leu Asn His His
130 135 140
Asn Leu Leu Ile Cys Ser Val Thr Asp Phe Tyr Pro Ser Gln Ile Lys
145 150 155 160
Val Arg Trp Phe Arg Asn Asp Gln Glu Glu Thr Ala Gly Val Val Ser
165 170 175
Thr Pro Leu Ile Arg Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met
180 185 190
Leu Glu Met Thr Pro Gln Arg Gly Asp Val Tyr Thr Cys His Val Glu
195 200 205
His Pro Ser Leu Gln Ser Pro Ile Thr Val Glu Trp Arg Ala Gln Ser
210 215 220
Glu Ser Ala Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu
225 230 235 240
Gly Leu Ile Phe Leu Gly Leu Gly Leu Ile Ile Arg Gln Arg Ser Arg
245 250 255
Lys Gly Leu Leu His
260
<210> 817
<211> 261
<212> БЕЛОК
<213> Homo sapiens
<400> 817
Met Ser Trp Lys Lys Ala Leu Arg Ile Pro Gly Gly Leu Arg Ala Ala
1 5 10 15
Thr Val Thr Leu Met Leu Ser Met Leu Ser Thr Pro Val Ala Glu Gly
20 25 30
Arg Asp Ser Pro Glu Asp Phe Val Tyr Gln Phe Lys Gly Met Cys Tyr
35 40 45
Phe Thr Asn Gly Thr Glu Arg Val Arg Leu Val Ser Arg Ser Ile Tyr
50 55 60
Asn Arg Glu Glu Ile Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg
65 70 75 80
Ala Val Thr Leu Leu Gly Leu Pro Ala Ala Glu Tyr Trp Asn Ser Gln
85 90 95
Lys Asp Ile Leu Glu Arg Lys Arg Ala Ala Val Asp Arg Val Cys Arg
100 105 110
His Asn Tyr Gln Leu Glu Leu Arg Thr Thr Leu Gln Arg Arg Val Glu
115 120 125
Pro Thr Val Thr Ile Ser Pro Ser Arg Thr Glu Ala Leu Asn His His
130 135 140
Asn Leu Leu Val Cys Ser Val Thr Asp Phe Tyr Pro Ala Gln Ile Lys
145 150 155 160
Val Arg Trp Phe Arg Asn Gly Gln Glu Glu Thr Ala Gly Val Val Ser
165 170 175
Thr Pro Leu Ile Arg Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met
180 185 190
Leu Glu Met Thr Pro Gln Arg Gly Asp Val Tyr Thr Cys His Val Glu
195 200 205
His Pro Ser Leu Gln Ser Pro Ile Thr Val Glu Trp Arg Ala Gln Ser
210 215 220
Glu Ser Ala Gln Ser Lys Met Leu Ser Gly Ile Gly Gly Phe Val Leu
225 230 235 240
Gly Leu Ile Phe Leu Gly Leu Gly Leu Ile Ile His His Arg Ser Gln
245 250 255
Lys Gly Leu Leu His
260
<210> 818
<211> 261
<212> БЕЛОК
<213> Homo sapiens
<400> 818
Met Ser Trp Lys Lys Ala Leu Arg Ile Pro Gly Gly Leu Arg Val Ala
1 5 10 15
Thr Val Thr Leu Met Leu Ala Met Leu Ser Thr Pro Val Ala Glu Gly
20 25 30
Arg Asp Ser Pro Glu Asp Phe Val Tyr Gln Phe Lys Gly Met Cys Tyr
35 40 45
Phe Thr Asn Gly Thr Glu Arg Val Arg Leu Val Thr Arg Tyr Ile Tyr
50 55 60
Asn Arg Glu Glu Tyr Ala Arg Phe Asp Ser Asp Val Gly Val Tyr Arg
65 70 75 80
Ala Val Thr Pro Leu Gly Pro Pro Ala Ala Glu Tyr Trp Asn Ser Gln
85 90 95
Lys Glu Val Leu Glu Arg Thr Arg Ala Glu Leu Asp Thr Val Cys Arg
100 105 110
His Asn Tyr Gln Leu Glu Leu Arg Thr Thr Leu Gln Arg Arg Val Glu
115 120 125
Pro Thr Val Thr Ile Ser Pro Ser Arg Thr Glu Ala Leu Asn His His
130 135 140
Asn Leu Leu Val Cys Ser Val Thr Asp Phe Tyr Pro Ala Gln Ile Lys
145 150 155 160
Val Arg Trp Phe Arg Asn Asp Gln Glu Glu Thr Thr Gly Val Val Ser
165 170 175
Thr Pro Leu Ile Arg Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met
180 185 190
Leu Glu Met Thr Pro Gln Arg Gly Asp Val Tyr Thr Cys His Val Glu
195 200 205
His Pro Ser Leu Gln Asn Pro Ile Ile Val Glu Trp Arg Ala Gln Ser
210 215 220
Glu Ser Ala Gln Ser Lys Met Leu Ser Gly Ile Gly Gly Phe Val Leu
225 230 235 240
Gly Leu Ile Phe Leu Gly Leu Gly Leu Ile Ile His His Arg Ser Gln
245 250 255
Lys Gly Leu Leu His
260
<210> 819
<211> 261
<212> БЕЛОК
<213> Homo sapiens
<400> 819
Met Ser Trp Lys Lys Ala Leu Arg Ile Pro Gly Asp Leu Arg Val Ala
1 5 10 15
Thr Val Thr Leu Met Leu Ala Met Leu Ser Ser Leu Leu Ala Glu Gly
20 25 30
Arg Asp Ser Pro Glu Asp Phe Val Tyr Gln Phe Lys Gly Met Cys Tyr
35 40 45
Phe Thr Asn Gly Thr Glu Arg Val Arg Leu Val Thr Arg His Ile Tyr
50 55 60
Asn Arg Glu Glu Tyr Ala Arg Phe Asp Ser Asp Val Gly Val Tyr Arg
65 70 75 80
Ala Val Thr Pro Gln Gly Arg Pro Asp Ala Glu Tyr Trp Asn Ser Gln
85 90 95
Lys Glu Val Leu Glu Gly Thr Arg Ala Glu Leu Asp Thr Val Cys Arg
100 105 110
His Asn Tyr Glu Val Ala Phe Arg Gly Ile Leu Gln Arg Arg Val Glu
115 120 125
Pro Thr Val Thr Ile Ser Pro Ser Arg Thr Glu Ala Leu Asn His His
130 135 140
Asn Leu Leu Val Cys Ser Val Thr Asp Phe Tyr Pro Gly Gln Ile Lys
145 150 155 160
Val Arg Trp Phe Arg Asn Asp Gln Glu Glu Thr Ala Gly Val Val Ser
165 170 175
Thr Pro Leu Ile Arg Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met
180 185 190
Leu Glu Met Thr Pro Gln Arg Gly Asp Val Tyr Thr Cys His Val Glu
195 200 205
His Pro Ser Leu Gln Ser Pro Ile Thr Val Glu Trp Arg Ala Gln Ser
210 215 220
Glu Ser Ala Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu
225 230 235 240
Gly Leu Ile Phe Leu Gly Leu Gly Leu Ile Ile Arg Gln Arg Ser Gln
245 250 255
Lys Gly Leu Leu His
260
<210> 820
<211> 261
<212> БЕЛОК
<213> Homo sapiens
<400> 820
Met Ser Trp Lys Lys Ala Leu Arg Ile Pro Gly Gly Leu Arg Val Ala
1 5 10 15
Thr Val Thr Leu Met Leu Ala Met Leu Ser Thr Pro Val Ala Glu Gly
20 25 30
Arg Asp Ser Pro Glu Asp Phe Val Tyr Gln Phe Lys Gly Met Cys Tyr
35 40 45
Phe Thr Asn Gly Thr Glu Arg Val Arg Leu Val Thr Arg Tyr Ile Tyr
50 55 60
Asn Arg Glu Glu Tyr Ala Arg Phe Asp Ser Asp Val Gly Val Tyr Arg
65 70 75 80
Ala Val Thr Pro Leu Gly Pro Pro Asp Ala Glu Tyr Trp Asn Ser Gln
85 90 95
Lys Glu Val Leu Glu Arg Thr Arg Ala Glu Leu Asp Thr Val Cys Arg
100 105 110
His Asn Tyr Gln Leu Glu Leu Arg Thr Thr Leu Gln Arg Arg Val Glu
115 120 125
Pro Thr Val Thr Ile Ser Pro Ser Arg Thr Glu Ala Leu Asn His His
130 135 140
Asn Leu Leu Val Cys Ser Val Thr Asp Phe Tyr Pro Ala Gln Ile Lys
145 150 155 160
Val Arg Trp Phe Arg Asn Asp Gln Glu Glu Thr Thr Gly Val Val Ser
165 170 175
Thr Pro Leu Ile Arg Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met
180 185 190
Leu Glu Met Thr Pro Gln Arg Gly Asp Val Tyr Thr Cys His Val Glu
195 200 205
His Pro Ser Leu Gln Asn Pro Ile Ile Val Glu Trp Arg Ala Gln Ser
210 215 220
Glu Ser Ala Gln Ser Lys Met Leu Ser Gly Ile Gly Gly Phe Val Leu
225 230 235 240
Gly Leu Ile Phe Leu Gly Leu Gly Leu Ile Ile His His Arg Ser Gln
245 250 255
Lys Gly Leu Leu His
260
<210> 821
<211> 261
<212> БЕЛОК
<213> Homo sapiens
<400> 821
Met Ser Trp Lys Lys Ala Leu Arg Ile Pro Gly Asp Leu Arg Val Ala
1 5 10 15
Thr Val Thr Leu Met Leu Ala Met Leu Ser Ser Leu Leu Ala Glu Gly
20 25 30
Arg Asp Ser Pro Glu Asp Phe Val Tyr Gln Phe Lys Gly Met Cys Tyr
35 40 45
Phe Thr Asn Gly Thr Glu Arg Val Arg Leu Val Thr Arg His Ile Tyr
50 55 60
Asn Arg Glu Glu Tyr Ala Arg Phe Asp Ser Asp Val Gly Val Tyr Arg
65 70 75 80
Ala Val Thr Pro Gln Gly Arg Pro Val Ala Glu Tyr Trp Asn Ser Gln
85 90 95
Lys Glu Val Leu Glu Arg Thr Arg Ala Glu Leu Asp Thr Val Cys Arg
100 105 110
His Asn Tyr Glu Val Gly Tyr Arg Gly Ile Leu Gln Arg Arg Val Glu
115 120 125
Pro Thr Val Thr Ile Ser Pro Ser Arg Thr Glu Ala Leu Asn His His
130 135 140
Asn Leu Leu Val Cys Ser Val Thr Asp Phe Tyr Pro Gly Gln Ile Lys
145 150 155 160
Val Gln Trp Phe Arg Asn Asp Gln Glu Glu Thr Ala Gly Val Val Ser
165 170 175
Thr Pro Leu Ile Arg Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met
180 185 190
Leu Glu Met Thr Pro Gln Arg Gly Asp Val Tyr Thr Cys His Val Glu
195 200 205
His Pro Ser Leu Gln Ser Pro Ile Thr Val Glu Trp Arg Ala Gln Ser
210 215 220
Glu Ser Ala Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu
225 230 235 240
Gly Leu Ile Phe Leu Gly Leu Gly Leu Ile Ile Arg Gln Arg Ser Gln
245 250 255
Lys Gly Leu Leu His
260
<210> 822
<211> 269
<212> БЕЛОК
<213> Homo sapiens
<400> 822
Met Ser Trp Lys Lys Ser Leu Arg Ile Pro Gly Asp Leu Arg Val Ala
1 5 10 15
Thr Val Thr Leu Met Leu Ala Ile Leu Ser Ser Ser Leu Ala Glu Gly
20 25 30
Arg Asp Ser Pro Glu Asp Phe Val Tyr Gln Phe Lys Gly Leu Cys Tyr
35 40 45
Phe Thr Asn Gly Thr Glu Arg Val Arg Gly Val Thr Arg His Ile Tyr
50 55 60
Asn Arg Glu Glu Tyr Val Arg Phe Asp Ser Asp Val Gly Val Tyr Arg
65 70 75 80
Ala Val Thr Pro Gln Gly Arg Pro Asp Ala Glu Tyr Trp Asn Ser Gln
85 90 95
Lys Glu Val Leu Glu Gly Ala Arg Ala Ser Val Asp Arg Val Cys Arg
100 105 110
His Asn Tyr Glu Val Ala Tyr Arg Gly Ile Leu Gln Arg Arg Val Glu
115 120 125
Pro Thr Val Thr Ile Ser Pro Ser Arg Thr Glu Ala Leu Asn His His
130 135 140
Asn Leu Leu Ile Cys Ser Val Thr Asp Phe Tyr Pro Ser Gln Ile Lys
145 150 155 160
Val Arg Trp Phe Arg Asn Asp Gln Glu Glu Thr Ala Gly Val Val Ser
165 170 175
Thr Pro Leu Ile Arg Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met
180 185 190
Leu Glu Met Thr Pro Gln Arg Gly Asp Val Tyr Thr Cys His Val Glu
195 200 205
His Pro Ser Leu Gln Ser Pro Ile Thr Val Glu Trp Arg Ala Gln Ser
210 215 220
Glu Ser Ala Gln Ser Lys Met Leu Ser Gly Val Gly Gly Phe Val Leu
225 230 235 240
Gly Leu Ile Phe Leu Gly Leu Gly Leu Ile Ile Arg Gln Arg Ser Arg
245 250 255
Lys Gly Pro Gln Gly Pro Pro Pro Ala Gly Leu Leu His
260 265
<210> 823
<211> 261
<212> БЕЛОК
<213> Homo sapiens
<400> 823
Met Ser Trp Lys Lys Ala Leu Arg Ile Pro Gly Gly Leu Arg Val Ala
1 5 10 15
Thr Val Thr Leu Met Leu Ala Met Leu Ser Thr Pro Val Ala Glu Gly
20 25 30
Arg Asp Ser Pro Glu Asp Phe Val Phe Gln Phe Lys Gly Met Cys Tyr
35 40 45
Phe Thr Asn Gly Thr Glu Arg Val Arg Gly Val Thr Arg Tyr Ile Tyr
50 55 60
Asn Arg Glu Glu Tyr Ala Arg Phe Asp Ser Asp Val Gly Val Tyr Arg
65 70 75 80
Ala Val Thr Pro Leu Gly Arg Leu Asp Ala Glu Tyr Trp Asn Ser Gln
85 90 95
Lys Asp Ile Leu Glu Glu Asp Arg Ala Ser Val Asp Thr Val Cys Arg
100 105 110
His Asn Tyr Gln Leu Glu Leu Arg Thr Thr Leu Gln Arg Arg Val Glu
115 120 125
Pro Thr Val Thr Ile Ser Pro Ser Arg Thr Glu Ala Leu Asn His His
130 135 140
Asn Leu Leu Val Cys Ser Val Thr Asp Phe Tyr Pro Ala Gln Ile Lys
145 150 155 160
Val Arg Trp Phe Arg Asn Asp Gln Glu Glu Thr Thr Gly Val Val Ser
165 170 175
Thr Pro Leu Ile Arg Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met
180 185 190
Leu Glu Met Thr Pro Gln Arg Gly Asp Val Tyr Thr Cys His Val Glu
195 200 205
His Pro Ser Leu Gln Asn Pro Ile Ile Val Glu Trp Arg Ala Gln Ser
210 215 220
Glu Ser Ala Gln Ser Lys Met Leu Ser Gly Ile Gly Gly Phe Val Leu
225 230 235 240
Gly Leu Ile Phe Leu Gly Leu Gly Leu Ile Ile His His Arg Ser Gln
245 250 255
Lys Gly Leu Leu His
260
<210> 824
<211> 260
<212> БЕЛОК
<213> Homo sapiens
<400> 824
Met Arg Pro Glu Asp Arg Met Phe His Ile Arg Ala Val Ile Leu Arg
1 5 10 15
Ala Leu Ser Leu Ala Phe Leu Leu Ser Leu Arg Gly Ala Gly Ala Ile
20 25 30
Lys Ala Asp His Val Ser Thr Tyr Ala Ala Phe Val Gln Thr His Arg
35 40 45
Pro Thr Gly Glu Phe Met Phe Glu Phe Asp Glu Asp Glu Met Phe Tyr
50 55 60
Val Asp Leu Asp Lys Lys Glu Thr Val Trp His Leu Glu Glu Phe Gly
65 70 75 80
Gln Ala Phe Ser Phe Glu Ala Gln Gly Gly Leu Ala Asn Ile Ala Ile
85 90 95
Leu Asn Asn Asn Leu Asn Thr Leu Ile Gln Arg Ser Asn His Thr Gln
100 105 110
Ala Thr Asn Asp Pro Pro Glu Val Thr Val Phe Pro Lys Glu Pro Val
115 120 125
Glu Leu Gly Gln Pro Asn Thr Leu Ile Cys His Ile Asp Lys Phe Phe
130 135 140
Pro Pro Val Leu Asn Val Thr Trp Leu Cys Asn Gly Glu Leu Val Thr
145 150 155 160
Glu Gly Val Ala Glu Ser Leu Phe Leu Pro Arg Thr Asp Tyr Ser Phe
165 170 175
His Lys Phe His Tyr Leu Thr Phe Val Pro Ser Ala Glu Asp Phe Tyr
180 185 190
Asp Cys Arg Val Glu His Trp Gly Leu Asp Gln Pro Leu Leu Lys His
195 200 205
Trp Glu Ala Gln Glu Pro Ile Gln Met Pro Glu Thr Thr Glu Thr Val
210 215 220
Leu Cys Ala Leu Gly Leu Val Leu Gly Leu Val Gly Ile Ile Val Gly
225 230 235 240
Thr Val Leu Ile Ile Lys Ser Leu Arg Ser Gly His Asp Pro Arg Ala
245 250 255
Gln Gly Thr Leu
260
<210> 825
<211> 260
<212> БЕЛОК
<213> Homo sapiens
<400> 825
Met Arg Pro Glu Asp Arg Met Phe His Ile Arg Ala Val Ile Leu Arg
1 5 10 15
Ala Leu Ser Leu Ala Phe Leu Leu Ser Leu Arg Gly Ala Gly Ala Ile
20 25 30
Lys Ala Asp His Val Ser Thr Tyr Ala Ala Phe Val Gln Thr His Arg
35 40 45
Pro Thr Gly Glu Phe Met Phe Glu Phe Asp Glu Asp Glu Gln Phe Tyr
50 55 60
Val Asp Leu Asp Lys Lys Glu Thr Val Trp His Leu Glu Glu Phe Gly
65 70 75 80
Arg Ala Phe Ser Phe Glu Ala Gln Gly Gly Leu Ala Asn Ile Ala Ile
85 90 95
Leu Asn Asn Asn Leu Asn Thr Leu Ile Gln Arg Ser Asn His Thr Gln
100 105 110
Ala Ala Asn Asp Pro Pro Glu Val Thr Val Phe Pro Lys Glu Pro Val
115 120 125
Glu Leu Gly Gln Pro Asn Thr Leu Ile Cys His Ile Asp Arg Phe Phe
130 135 140
Pro Pro Val Leu Asn Val Thr Trp Leu Cys Asn Gly Glu Pro Val Thr
145 150 155 160
Glu Gly Val Ala Glu Ser Leu Phe Leu Pro Arg Thr Asp Tyr Ser Phe
165 170 175
His Lys Phe His Tyr Leu Thr Phe Val Pro Ser Ala Glu Asp Val Tyr
180 185 190
Asp Cys Arg Val Glu His Trp Gly Leu Asp Gln Pro Leu Leu Lys His
195 200 205
Trp Glu Ala Gln Glu Pro Ile Gln Met Pro Glu Thr Thr Glu Thr Val
210 215 220
Leu Cys Ala Leu Gly Leu Val Leu Gly Leu Val Gly Ile Ile Val Gly
225 230 235 240
Thr Val Leu Ile Ile Lys Ser Leu Arg Ser Gly His Asp Pro Arg Ala
245 250 255
Gln Gly Pro Leu
260
<210> 826
<211> 260
<212> БЕЛОК
<213> Homo sapiens
<400> 826
Met Arg Pro Glu Asp Arg Met Phe His Ile Arg Ala Val Ile Leu Arg
1 5 10 15
Ala Leu Ser Leu Ala Phe Leu Leu Ser Leu Arg Gly Ala Gly Ala Ile
20 25 30
Lys Ala Asp His Val Ser Thr Tyr Ala Met Phe Val Gln Thr His Arg
35 40 45
Pro Thr Gly Glu Phe Met Phe Glu Phe Asp Glu Asp Glu Gln Phe Tyr
50 55 60
Val Asp Leu Asp Lys Lys Glu Thr Val Trp His Leu Glu Glu Phe Gly
65 70 75 80
Arg Ala Phe Ser Phe Glu Ala Gln Gly Gly Leu Ala Asn Ile Ala Ile
85 90 95
Leu Asn Asn Asn Leu Asn Thr Leu Ile Gln Arg Ser Asn His Thr Gln
100 105 110
Ala Ala Asn Asp Pro Pro Glu Val Thr Met Phe Pro Lys Glu Pro Val
115 120 125
Glu Leu Gly Gln Pro Asn Thr Leu Ile Cys His Ile Asp Arg Phe Phe
130 135 140
Pro Pro Val Leu Asn Val Thr Trp Leu Cys Asn Gly Glu Pro Val Thr
145 150 155 160
Glu Gly Val Ala Glu Ser Leu Phe Leu Pro Arg Thr Asp Tyr Ser Phe
165 170 175
His Lys Phe His Tyr Leu Thr Phe Val Pro Ser Ala Glu Asp Val Tyr
180 185 190
Asp Cys Arg Val Glu His Trp Gly Leu Asp Gln Pro Leu Leu Lys His
195 200 205
Trp Glu Ala Gln Glu Pro Ile Gln Met Pro Glu Thr Thr Glu Thr Val
210 215 220
Leu Cys Ala Leu Gly Leu Val Leu Gly Leu Val Gly Ile Ile Val Gly
225 230 235 240
Thr Val Leu Ile Ile Lys Ser Leu Arg Ser Gly His Asp Pro Arg Ala
245 250 255
Gln Gly Pro Leu
260
<210> 827
<211> 258
<212> БЕЛОК
<213> Homo sapiens
<400> 827
Met Met Val Leu Gln Val Ser Ala Ala Pro Arg Thr Val Ala Leu Thr
1 5 10 15
Ala Leu Leu Met Val Leu Leu Thr Ser Val Val Gln Gly Arg Ala Thr
20 25 30
Pro Glu Asn Tyr Leu Phe Gln Gly Arg Gln Glu Cys Tyr Ala Phe Asn
35 40 45
Gly Thr Gln Arg Phe Leu Glu Arg Tyr Ile Tyr Asn Arg Glu Glu Phe
50 55 60
Ala Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr Glu Leu
65 70 75 80
Gly Arg Pro Ala Ala Glu Tyr Trp Asn Ser Gln Lys Asp Ile Leu Glu
85 90 95
Glu Lys Arg Ala Val Pro Asp Arg Met Cys Arg His Asn Tyr Glu Leu
100 105 110
Gly Gly Pro Met Thr Leu Gln Arg Arg Val Gln Pro Arg Val Asn Val
115 120 125
Ser Pro Ser Lys Lys Gly Pro Leu Gln His His Asn Leu Leu Val Cys
130 135 140
His Val Thr Asp Phe Tyr Pro Gly Ser Ile Gln Val Arg Trp Phe Leu
145 150 155 160
Asn Gly Gln Glu Glu Thr Ala Gly Val Val Ser Thr Asn Leu Ile Arg
165 170 175
Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met Leu Glu Met Thr Pro
180 185 190
Gln Gln Gly Asp Val Tyr Thr Cys Gln Val Glu His Thr Ser Leu Asp
195 200 205
Ser Pro Val Thr Val Glu Trp Lys Ala Gln Ser Asp Ser Ala Arg Ser
210 215 220
Lys Thr Leu Thr Gly Ala Gly Gly Phe Val Leu Gly Leu Ile Ile Cys
225 230 235 240
Gly Val Gly Ile Phe Met His Arg Arg Ser Lys Lys Val Gln Arg Gly
245 250 255
Ser Ala
<210> 828
<211> 258
<212> БЕЛОК
<213> Homo sapiens
<400> 828
Met Met Val Leu Gln Val Ser Ala Ala Pro Arg Thr Val Ala Leu Thr
1 5 10 15
Ala Leu Leu Met Val Leu Leu Thr Ser Val Val Gln Gly Arg Ala Thr
20 25 30
Pro Glu Asn Tyr Leu Phe Gln Gly Arg Gln Glu Cys Tyr Ala Phe Asn
35 40 45
Gly Thr Gln Arg Phe Leu Glu Arg Tyr Ile Tyr Asn Arg Glu Glu Phe
50 55 60
Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr Glu Leu
65 70 75 80
Gly Arg Pro Asp Glu Glu Tyr Trp Asn Ser Gln Lys Asp Ile Leu Glu
85 90 95
Glu Glu Arg Ala Val Pro Asp Arg Met Cys Arg His Asn Tyr Glu Leu
100 105 110
Gly Gly Pro Met Thr Leu Gln Arg Arg Val Gln Pro Arg Val Asn Val
115 120 125
Ser Pro Ser Lys Lys Gly Pro Leu Gln His His Asn Leu Leu Val Cys
130 135 140
His Val Thr Asp Phe Tyr Pro Gly Ser Ile Gln Val Arg Trp Phe Leu
145 150 155 160
Asn Gly Gln Glu Glu Thr Ala Gly Val Val Ser Thr Asn Leu Ile Arg
165 170 175
Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met Leu Glu Met Thr Pro
180 185 190
Gln Gln Gly Asp Val Tyr Thr Cys Gln Val Glu His Thr Ser Leu Asp
195 200 205
Ser Pro Val Thr Val Glu Trp Lys Ala Gln Ser Asp Ser Ala Arg Ser
210 215 220
Lys Thr Leu Thr Gly Ala Gly Gly Phe Val Leu Gly Leu Ile Ile Cys
225 230 235 240
Gly Val Gly Ile Phe Met His Arg Arg Ser Lys Lys Val Gln Arg Gly
245 250 255
Ser Ala
<210> 829
<211> 258
<212> БЕЛОК
<213> Homo sapiens
<400> 829
Met Met Val Leu Gln Val Ser Ala Ala Pro Arg Thr Val Ala Leu Thr
1 5 10 15
Ala Leu Leu Met Val Leu Leu Thr Ser Val Val Gln Gly Arg Ala Thr
20 25 30
Pro Glu Asn Tyr Leu Phe Gln Gly Arg Gln Glu Cys Tyr Ala Phe Asn
35 40 45
Gly Thr Gln Arg Phe Leu Glu Arg Tyr Ile Tyr Asn Arg Glu Glu Phe
50 55 60
Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr Glu Leu
65 70 75 80
Gly Arg Pro Asp Glu Glu Tyr Trp Asn Ser Gln Lys Asp Ile Leu Glu
85 90 95
Glu Lys Arg Ala Val Pro Asp Arg Met Cys Arg His Asn Tyr Glu Leu
100 105 110
Gly Gly Pro Met Thr Leu Gln Arg Arg Val Gln Pro Arg Val Asn Val
115 120 125
Ser Pro Ser Lys Lys Gly Pro Leu Gln His His Asn Leu Leu Val Cys
130 135 140
His Val Thr Asp Phe Tyr Pro Gly Ser Ile Gln Val Arg Trp Phe Leu
145 150 155 160
Asn Gly Gln Glu Glu Thr Ala Gly Val Val Ser Thr Asn Leu Ile Arg
165 170 175
Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met Leu Glu Met Thr Pro
180 185 190
Gln Gln Gly Asp Val Tyr Thr Cys Gln Val Glu His Thr Ser Met Asp
195 200 205
Ser Pro Val Thr Val Glu Trp Lys Ala Gln Ser Asp Ser Ala Arg Ser
210 215 220
Lys Thr Leu Thr Gly Ala Gly Gly Phe Val Leu Gly Leu Ile Ile Cys
225 230 235 240
Gly Val Gly Ile Phe Met His Arg Arg Ser Lys Lys Val Gln Arg Gly
245 250 255
Ser Ala
<210> 830
<211> 258
<212> БЕЛОК
<213> Homo sapiens
<400> 830
Met Met Val Leu Gln Val Ser Ala Ala Pro Arg Thr Val Ala Leu Thr
1 5 10 15
Ala Leu Leu Met Val Leu Leu Thr Ser Val Val Gln Gly Arg Ala Thr
20 25 30
Pro Glu Asn Tyr Val Tyr Gln Leu Arg Gln Glu Cys Tyr Ala Phe Asn
35 40 45
Gly Thr Gln Arg Phe Leu Glu Arg Tyr Ile Tyr Asn Arg Glu Glu Phe
50 55 60
Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr Glu Leu
65 70 75 80
Gly Arg Pro Asp Glu Asp Tyr Trp Asn Ser Gln Lys Asp Leu Leu Glu
85 90 95
Glu Lys Arg Ala Val Pro Asp Arg Val Cys Arg His Asn Tyr Glu Leu
100 105 110
Asp Glu Ala Val Thr Leu Gln Arg Arg Val Gln Pro Lys Val Asn Val
115 120 125
Ser Pro Ser Lys Lys Gly Pro Leu Gln His His Asn Leu Leu Val Cys
130 135 140
His Val Thr Asp Phe Tyr Pro Gly Ser Ile Gln Val Arg Trp Phe Leu
145 150 155 160
Asn Gly Gln Glu Glu Thr Ala Gly Val Val Ser Thr Asn Leu Ile Arg
165 170 175
Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met Leu Glu Met Thr Pro
180 185 190
Gln Gln Gly Asp Val Tyr Ile Cys Gln Val Glu His Thr Ser Leu Asp
195 200 205
Ser Pro Val Thr Val Glu Trp Lys Ala Gln Ser Asp Ser Ala Arg Ser
210 215 220
Lys Thr Leu Thr Gly Ala Gly Gly Phe Val Leu Gly Leu Ile Ile Cys
225 230 235 240
Gly Val Gly Ile Phe Met His Arg Arg Ser Lys Lys Val Gln Arg Gly
245 250 255
Ser Ala
<210> 831
<211> 258
<212> БЕЛОК
<213> Homo sapiens
<400> 831
Met Met Val Leu Gln Val Ser Ala Ala Pro Arg Thr Val Ala Leu Thr
1 5 10 15
Ala Leu Leu Met Val Leu Leu Thr Ser Val Val Gln Gly Arg Ala Thr
20 25 30
Pro Glu Asn Tyr Val Tyr Gln Gly Arg Gln Glu Cys Tyr Ala Phe Asn
35 40 45
Gly Thr Gln Arg Phe Leu Glu Arg Tyr Ile Tyr Asn Arg Glu Glu Tyr
50 55 60
Ala Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr Glu Leu
65 70 75 80
Gly Arg Pro Ala Ala Glu Tyr Trp Asn Ser Gln Lys Asp Ile Leu Glu
85 90 95
Glu Lys Arg Ala Val Pro Asp Arg Val Cys Arg His Asn Tyr Glu Leu
100 105 110
Asp Glu Ala Val Thr Leu Gln Arg Arg Val Gln Pro Lys Val Asn Val
115 120 125
Ser Pro Ser Lys Lys Gly Pro Leu Gln His His Asn Leu Leu Val Cys
130 135 140
His Val Thr Asp Phe Tyr Pro Gly Ser Ile Gln Val Arg Trp Phe Leu
145 150 155 160
Asn Gly Gln Glu Glu Thr Ala Gly Val Val Ser Thr Asn Leu Ile Arg
165 170 175
Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met Leu Glu Met Thr Pro
180 185 190
Gln Gln Gly Asp Val Tyr Ile Cys Gln Val Glu His Thr Ser Leu Asp
195 200 205
Ser Pro Val Thr Val Glu Trp Lys Ala Gln Ser Asp Ser Ala Gln Ser
210 215 220
Lys Thr Leu Thr Gly Ala Gly Gly Phe Val Leu Gly Leu Ile Ile Cys
225 230 235 240
Gly Val Gly Ile Phe Met His Arg Arg Ser Lys Lys Val Gln Arg Gly
245 250 255
Ser Ala
<210> 832
<211> 258
<212> БЕЛОК
<213> Homo sapiens
<400> 832
Met Met Val Leu Gln Val Ser Ala Ala Pro Arg Thr Val Ala Leu Thr
1 5 10 15
Ala Leu Leu Met Val Leu Leu Thr Ser Val Val Gln Gly Arg Ala Thr
20 25 30
Pro Glu Asn Tyr Val Tyr Gln Leu Arg Gln Glu Cys Tyr Ala Phe Asn
35 40 45
Gly Thr Gln Arg Phe Leu Glu Arg Tyr Ile Tyr Asn Arg Gln Glu Tyr
50 55 60
Ala Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr Glu Leu
65 70 75 80
Gly Arg Pro Ala Ala Glu Tyr Trp Asn Ser Gln Lys Asp Leu Leu Glu
85 90 95
Glu Arg Arg Ala Val Pro Asp Arg Met Cys Arg His Asn Tyr Glu Leu
100 105 110
Asp Glu Ala Val Thr Leu Gln Arg Arg Val Gln Pro Lys Val Asn Val
115 120 125
Ser Pro Ser Lys Lys Gly Pro Leu Gln His His Asn Leu Leu Val Cys
130 135 140
His Val Thr Asp Phe Tyr Pro Gly Ser Ile Gln Val Arg Trp Phe Leu
145 150 155 160
Asn Gly Gln Glu Glu Thr Ala Gly Val Val Ser Thr Asn Leu Ile Arg
165 170 175
Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met Leu Glu Met Thr Pro
180 185 190
Gln Gln Gly Asp Val Tyr Ile Cys Gln Val Glu His Thr Ser Leu Asp
195 200 205
Ser Pro Val Thr Val Glu Trp Lys Ala Gln Ser Asp Ser Ala Arg Ser
210 215 220
Lys Thr Leu Thr Gly Ala Gly Gly Phe Val Leu Gly Leu Ile Ile Cys
225 230 235 240
Gly Val Gly Ile Phe Met His Arg Arg Ser Lys Lys Val Gln Arg Gly
245 250 255
Ser Ala
<210> 833
<211> 258
<212> БЕЛОК
<213> Homo sapiens
<400> 833
Met Met Val Leu Gln Val Ser Ala Ala Pro Arg Thr Val Ala Leu Thr
1 5 10 15
Ala Leu Leu Met Val Leu Leu Thr Ser Val Val Gln Gly Arg Ala Thr
20 25 30
Pro Glu Asn Tyr Leu Phe Gln Gly Arg Gln Glu Cys Tyr Ala Phe Asn
35 40 45
Gly Thr Gln Arg Phe Leu Glu Arg Tyr Ile Tyr Asn Arg Glu Glu Leu
50 55 60
Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr Glu Leu
65 70 75 80
Gly Arg Pro Glu Ala Glu Tyr Trp Asn Ser Gln Lys Asp Ile Leu Glu
85 90 95
Glu Lys Arg Ala Val Pro Asp Arg Met Cys Arg His Asn Tyr Glu Leu
100 105 110
Asp Glu Ala Val Thr Leu Gln Arg Arg Val Gln Pro Lys Val Asn Val
115 120 125
Ser Pro Ser Lys Lys Gly Pro Leu Gln His His Asn Leu Leu Val Cys
130 135 140
His Val Thr Asp Phe Tyr Pro Gly Ser Ile Gln Val Arg Trp Phe Leu
145 150 155 160
Asn Gly Gln Glu Glu Thr Ala Gly Val Val Ser Thr Asn Leu Ile Arg
165 170 175
Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met Leu Glu Met Thr Pro
180 185 190
Gln Gln Gly Asp Val Tyr Ile Cys Gln Val Glu His Thr Ser Leu Asp
195 200 205
Ser Pro Val Thr Val Glu Trp Lys Ala Gln Ser Asp Ser Ala Arg Ser
210 215 220
Lys Thr Leu Thr Gly Ala Gly Gly Phe Met Leu Gly Leu Ile Ile Cys
225 230 235 240
Gly Val Gly Ile Phe Met His Arg Arg Ser Lys Lys Val Gln Arg Gly
245 250 255
Ser Ala
<210> 834
<211> 258
<212> БЕЛОК
<213> Homo sapiens
<400> 834
Met Met Val Leu Gln Val Ser Ala Ala Pro Arg Thr Val Ala Leu Thr
1 5 10 15
Ala Leu Leu Met Val Leu Leu Thr Ser Val Val Gln Gly Arg Ala Thr
20 25 30
Pro Glu Asn Tyr Val His Gln Leu Arg Gln Glu Cys Tyr Ala Phe Asn
35 40 45
Gly Thr Gln Arg Phe Leu Glu Arg Tyr Ile Tyr Asn Arg Glu Glu Phe
50 55 60
Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr Glu Leu
65 70 75 80
Gly Arg Pro Asp Glu Glu Tyr Trp Asn Ser Gln Lys Asp Ile Leu Glu
85 90 95
Glu Glu Arg Ala Val Pro Asp Arg Val Cys Arg His Asn Tyr Glu Leu
100 105 110
Asp Glu Ala Val Thr Leu Gln Arg Arg Val Gln Pro Lys Val Asn Val
115 120 125
Ser Pro Ser Lys Lys Gly Pro Leu Gln His His Asn Leu Leu Val Cys
130 135 140
His Val Thr Asp Phe Tyr Pro Gly Ser Ile Gln Val Arg Trp Phe Leu
145 150 155 160
Asn Gly Gln Glu Glu Thr Ala Gly Val Val Ser Thr Asn Leu Ile Arg
165 170 175
Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met Leu Glu Met Thr Pro
180 185 190
Gln Gln Gly Asp Val Tyr Ile Cys Gln Val Glu His Thr Ser Leu Asp
195 200 205
Ser Pro Val Thr Val Glu Trp Lys Ala Gln Ser Asp Ser Ala Arg Ser
210 215 220
Lys Thr Leu Thr Gly Ala Gly Gly Phe Val Leu Gly Leu Ile Ile Cys
225 230 235 240
Gly Val Gly Ile Phe Met His Arg Arg Ser Lys Lys Val Gln Arg Gly
245 250 255
Ser Ala
<210> 835
<211> 258
<212> БЕЛОК
<213> Homo sapiens
<400> 835
Met Met Val Leu Gln Val Ser Ala Ala Pro Arg Thr Val Ala Leu Thr
1 5 10 15
Ala Leu Leu Met Val Leu Leu Thr Ser Val Val Gln Gly Arg Ala Thr
20 25 30
Pro Glu Asn Tyr Val Tyr Gln Leu Arg Gln Glu Cys Tyr Ala Phe Asn
35 40 45
Gly Thr Gln Arg Phe Leu Glu Arg Tyr Ile Tyr Asn Arg Glu Glu Phe
50 55 60
Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr Glu Leu
65 70 75 80
Gly Arg Pro Asp Glu Asp Tyr Trp Asn Ser Gln Lys Asp Leu Leu Glu
85 90 95
Glu Glu Arg Ala Val Pro Asp Arg Met Cys Arg His Asn Tyr Glu Leu
100 105 110
Asp Glu Ala Val Thr Leu Gln Arg Arg Val Gln Pro Lys Val Asn Val
115 120 125
Ser Pro Ser Lys Lys Gly Pro Leu Gln His His Asn Leu Leu Val Cys
130 135 140
His Val Thr Asp Phe Tyr Pro Gly Ser Ile Gln Val Arg Trp Phe Leu
145 150 155 160
Asn Gly Gln Glu Glu Thr Ala Gly Val Val Ser Thr Asn Leu Ile Arg
165 170 175
Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met Leu Glu Met Thr Pro
180 185 190
Gln Gln Gly Asp Val Tyr Ile Cys Gln Val Glu His Thr Ser Leu Asp
195 200 205
Ser Pro Val Thr Val Glu Trp Lys Ala Gln Ser Asp Ser Ala Arg Ser
210 215 220
Lys Thr Leu Thr Gly Ala Gly Gly Phe Val Leu Gly Leu Ile Ile Cys
225 230 235 240
Gly Val Gly Ile Phe Met His Arg Arg Ser Lys Lys Val Gln Arg Gly
245 250 255
Ser Ala
<210> 836
<211> 258
<212> БЕЛОК
<213> Homo sapiens
<400> 836
Met Met Val Leu Gln Val Ser Ala Ala Pro Arg Thr Val Ala Leu Thr
1 5 10 15
Ala Leu Leu Met Val Leu Leu Thr Ser Val Val Gln Gly Arg Ala Thr
20 25 30
Pro Glu Asn Tyr Val Tyr Gln Leu Arg Gln Glu Cys Tyr Ala Phe Asn
35 40 45
Gly Thr Gln Arg Phe Leu Glu Arg Tyr Ile Tyr Asn Arg Glu Glu Tyr
50 55 60
Ala Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr Glu Leu
65 70 75 80
Gly Arg Pro Ala Ala Glu Tyr Trp Asn Ser Gln Lys Asp Ile Leu Glu
85 90 95
Glu Glu Arg Ala Val Pro Asp Arg Ile Cys Arg His Asn Tyr Glu Leu
100 105 110
Asp Glu Ala Val Thr Leu Gln Arg Arg Val Gln Pro Lys Val Asn Val
115 120 125
Ser Pro Ser Lys Lys Gly Pro Leu Gln His His Asn Leu Leu Val Cys
130 135 140
His Val Thr Asp Phe Tyr Pro Gly Ser Ile Gln Val Arg Trp Phe Leu
145 150 155 160
Asn Gly Gln Glu Glu Thr Ala Gly Val Val Ser Thr Asn Leu Ile Arg
165 170 175
Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met Leu Glu Met Thr Pro
180 185 190
Gln Gln Gly Asp Val Tyr Ile Cys Gln Val Glu His Thr Ser Leu Asp
195 200 205
Ser Pro Val Thr Val Glu Trp Lys Ala Gln Ser Asp Ser Ala Arg Ser
210 215 220
Lys Thr Leu Thr Gly Ala Gly Gly Phe Val Leu Gly Leu Ile Ile Cys
225 230 235 240
Gly Val Gly Ile Phe Met His Arg Arg Ser Lys Lys Val Gln Arg Gly
245 250 255
Ser Ala
<210> 837
<211> 258
<212> БЕЛОК
<213> Homo sapiens
<400> 837
Met Met Val Leu Gln Val Ser Ala Ala Pro Arg Thr Val Ala Leu Thr
1 5 10 15
Ala Leu Leu Met Val Leu Leu Thr Ser Val Val Gln Gly Arg Ala Thr
20 25 30
Pro Glu Asn Tyr Val His Gln Leu Arg Gln Glu Cys Tyr Ala Phe Asn
35 40 45
Gly Thr Gln Arg Phe Leu Glu Arg Tyr Ile Tyr Asn Arg Glu Glu Phe
50 55 60
Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr Glu Leu
65 70 75 80
Gly Arg Pro Asp Glu Asp Tyr Trp Asn Ser Gln Lys Asp Leu Leu Glu
85 90 95
Glu Lys Arg Ala Val Pro Asp Arg Val Cys Arg His Asn Tyr Glu Leu
100 105 110
Asp Glu Ala Val Thr Leu Gln Arg Arg Val Gln Pro Lys Val Asn Val
115 120 125
Ser Pro Ser Lys Lys Gly Pro Leu Gln His His Asn Leu Leu Val Cys
130 135 140
His Val Thr Asp Phe Tyr Pro Gly Ser Ile Gln Val Arg Trp Phe Leu
145 150 155 160
Asn Gly Gln Glu Glu Thr Ala Gly Val Val Ser Thr Asn Leu Ile Arg
165 170 175
Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met Leu Glu Met Thr Pro
180 185 190
Gln Gln Gly Asp Val Tyr Ile Cys Gln Val Glu His Thr Ser Leu Asp
195 200 205
Ser Pro Val Thr Val Glu Trp Lys Ala Gln Ser Asp Ser Ala Arg Ser
210 215 220
Lys Thr Leu Thr Gly Ala Gly Gly Phe Val Leu Gly Leu Ile Ile Cys
225 230 235 240
Gly Val Gly Ile Phe Met His Arg Arg Ser Lys Lys Val Gln Arg Gly
245 250 255
Ser Ala
<210> 838
<211> 258
<212> БЕЛОК
<213> Homo sapiens
<400> 838
Met Met Val Leu Gln Val Ser Ala Ala Pro Arg Thr Val Ala Leu Thr
1 5 10 15
Ala Leu Leu Met Val Leu Leu Thr Ser Val Val Gln Gly Arg Ala Thr
20 25 30
Pro Glu Asn Tyr Val His Gln Leu Arg Gln Glu Cys Tyr Ala Phe Asn
35 40 45
Gly Thr Gln Arg Phe Leu Glu Arg Tyr Ile Tyr Asn Arg Glu Glu Phe
50 55 60
Val Arg Phe Asp Ser Asp Val Gly Glu Phe Arg Ala Val Thr Glu Leu
65 70 75 80
Gly Arg Pro Asp Glu Asp Tyr Trp Asn Ser Gln Lys Asp Ile Leu Glu
85 90 95
Glu Glu Arg Ala Val Pro Asp Arg Met Cys Arg His Asn Tyr Glu Leu
100 105 110
Asp Glu Ala Val Thr Leu Gln Arg Arg Val Gln Pro Arg Val Asn Val
115 120 125
Ser Pro Ser Lys Lys Gly Pro Leu Gln His His Asn Leu Leu Val Cys
130 135 140
His Val Thr Asp Phe Tyr Pro Gly Ser Ile Gln Val Arg Trp Phe Leu
145 150 155 160
Asn Gly Gln Glu Glu Thr Ala Gly Val Val Ser Thr Asn Leu Ile Arg
165 170 175
Asn Gly Asp Trp Thr Phe Gln Ile Leu Val Met Leu Glu Met Thr Pro
180 185 190
Gln Gln Gly Asp Val Tyr Thr Cys Gln Val Glu His Thr Ser Leu Asp
195 200 205
Ser Pro Val Thr Val Glu Trp Lys Ala Gln Ser Asp Ser Ala Arg Ser
210 215 220
Lys Thr Leu Thr Gly Ala Gly Gly Phe Val Leu Gly Leu Ile Ile Cys
225 230 235 240
Gly Val Gly Ile Phe Met His Arg Arg Ser Lys Lys Val Gln Arg Gly
245 250 255
Ser Ala
<210> 839
<211> 99
<212> БЕЛОК
<213> Homo sapiens
<400> 839
Ile Gln Arg Thr Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu
1 5 10 15
Asn Gly Lys Ser Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro
20 25 30
Ser Asp Ile Glu Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys
35 40 45
Val Glu His Ser Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu
50 55 60
Leu Tyr Tyr Thr Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys
65 70 75 80
Arg Val Asn His Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp
85 90 95
Arg Asp Met
<210> 840
<211> 284
<212> БЕЛОК
<213> Homo sapiens
<400> 840
Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser Arg Pro Gly
1 5 10 15
Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp Asp Thr Gln
20 25 30
Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met Glu Pro Arg
35 40 45
Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp Gly Glu Thr
50 55 60
Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp Leu Gly Thr
65 70 75 80
Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser His Thr Val Gln
85 90 95
Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe Leu Arg Gly
100 105 110
Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala Leu Lys Glu
115 120 125
Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln Thr Thr Lys
130 135 140
His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg Ala Tyr Leu
145 150 155 160
Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu Asn Gly Lys
165 170 175
Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met Thr His His
180 185 190
Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala Leu Ser Phe
195 200 205
Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly Glu Asp Gln
210 215 220
Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly Asp Gly Thr
225 230 235 240
Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln Glu Gln Arg
245 250 255
Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro Leu Thr Leu
260 265 270
Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile
275 280
<210> 841
<211> 284
<212> БЕЛОК
<213> Homo sapiens
<400> 841
Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser Arg Pro Gly
1 5 10 15
Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp Asp Thr Gln
20 25 30
Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met Glu Pro Arg
35 40 45
Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp Gly Glu Thr
50 55 60
Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp Leu Gly Thr
65 70 75 80
Leu Arg Gly Tyr Tyr Asn Gln Ser Glu Ala Gly Ser His Thr Val Gln
85 90 95
Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe Leu Arg Gly
100 105 110
Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala Leu Lys Glu
115 120 125
Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln Thr Thr Lys
130 135 140
His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg Ala Tyr Leu
145 150 155 160
Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu Asn Gly Lys
165 170 175
Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met Thr His His
180 185 190
Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala Leu Ser Phe
195 200 205
Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly Glu Asp Gln
210 215 220
Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly Asp Gly Thr
225 230 235 240
Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln Glu Gln Arg
245 250 255
Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro Leu Thr Leu
260 265 270
Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile
275 280
<210> 842
<211> 284
<212> БЕЛОК
<213> Homo sapiens
<400> 842
Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser Arg Pro Gly
1 5 10 15
Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp Asp Thr Gln
20 25 30
Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met Glu Pro Arg
35 40 45
Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp Gly Glu Thr
50 55 60
Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp Leu Gly Thr
65 70 75 80
Leu Arg Gly Cys Tyr Asn Gln Ser Glu Ala Gly Ser His Thr Val Gln
85 90 95
Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe Leu Arg Gly
100 105 110
Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala Leu Lys Glu
115 120 125
Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln Thr Thr Lys
130 135 140
His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg Ala Tyr Leu
145 150 155 160
Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu Asn Gly Lys
165 170 175
Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met Thr His His
180 185 190
Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala Leu Ser Phe
195 200 205
Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly Glu Asp Gln
210 215 220
Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly Asp Gly Thr
225 230 235 240
Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln Glu Gln Arg
245 250 255
Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro Leu Thr Leu
260 265 270
Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile
275 280
<210> 843
<211> 465
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 843
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Tyr Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser
465
<210> 844
<211> 465
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 844
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser
465
<210> 845
<211> 465
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 845
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Cys Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Cys Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser
465
<210> 846
<211> 596
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 846
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser
465 470 475 480
Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg
485 490 495
Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser
500 505 510
Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln
515 520 525
Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly
530 535 540
Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile
545 550 555 560
Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser
565 570 575
Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu
580 585 590
Thr Ser Asp Gln
595
<210> 847
<211> 596
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 847
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Cys Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Cys Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser
465 470 475 480
Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg
485 490 495
Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser
500 505 510
Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln
515 520 525
Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly
530 535 540
Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile
545 550 555 560
Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser
565 570 575
Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu
580 585 590
Thr Ser Asp Gln
595
<210> 848
<211> 998
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 848
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser
465 470 475 480
Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg
485 490 495
Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser
500 505 510
Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln
515 520 525
Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly
530 535 540
Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile
545 550 555 560
Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser
565 570 575
Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu
580 585 590
Thr Ser Asp Gln Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys
595 600 605
Gly Asp Val Glu Glu Asn Pro Gly Pro Met Tyr Gly Lys Ile Ile Phe
610 615 620
Val Leu Leu Leu Ser Glu Ile Val Ser Ile Ser Ala Ala Cys Pro Trp
625 630 635 640
Ala Val Ser Gly Ala Arg Ala Ser Pro Gly Ser Ala Ala Ser Pro Arg
645 650 655
Leu Arg Glu Gly Pro Glu Leu Ser Pro Asp Asp Pro Ala Gly Leu Leu
660 665 670
Asp Leu Arg Gln Gly Met Phe Ala Gln Leu Val Ala Gln Asn Val Leu
675 680 685
Leu Ile Asp Gly Pro Leu Ser Trp Tyr Ser Asp Pro Gly Leu Ala Gly
690 695 700
Val Ser Leu Thr Gly Gly Leu Ser Tyr Lys Glu Asp Thr Lys Glu Leu
705 710 715 720
Val Val Ala Lys Ala Gly Val Tyr Tyr Val Phe Phe Gln Leu Glu Leu
725 730 735
Arg Arg Val Val Ala Gly Glu Gly Ser Gly Ser Val Ser Leu Ala Leu
740 745 750
His Leu Gln Pro Leu Arg Ser Ala Ala Gly Ala Ala Ala Leu Ala Leu
755 760 765
Thr Val Asp Leu Pro Pro Ala Ser Ser Glu Ala Arg Asn Ser Ala Phe
770 775 780
Gly Phe Gln Gly Arg Leu Leu His Leu Ser Ala Gly Gln Arg Leu Gly
785 790 795 800
Val His Leu His Thr Glu Ala Arg Ala Arg His Ala Trp Gln Leu Thr
805 810 815
Gln Gly Ala Thr Val Leu Gly Leu Phe Arg Val Thr Pro Glu Ile Pro
820 825 830
Ala Gly Leu Pro Ser Pro Arg Ser Glu Gly Gly Ser Gly Gly Ser Gly
835 840 845
Gly Gly Pro Glu Asp Glu Pro Gly Ser Gly Ser Gly Gly Gly Ser Gly
850 855 860
Gly Gly Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser
865 870 875 880
Ser Ser Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His
885 890 895
Lys Arg Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu
900 905 910
Ile Ser Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg
915 920 925
Val Gln Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile
930 935 940
Phe Gly Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr
945 950 955 960
Gly Ile Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu
965 970 975
Pro Ser Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn
980 985 990
Pro Glu Thr Ser Asp Gln
995
<210> 849
<211> 616
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 849
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser
465 470 475 480
Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg
485 490 495
Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser
500 505 510
Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln
515 520 525
Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly
530 535 540
Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile
545 550 555 560
Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser
565 570 575
Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu
580 585 590
Thr Ser Asp Gln Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys
595 600 605
Gly Asp Val Glu Glu Asn Pro Gly
610 615
<210> 850
<211> 382
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 850
Pro Met Tyr Gly Lys Ile Ile Phe Val Leu Leu Leu Ser Glu Ile Val
1 5 10 15
Ser Ile Ser Ala Ala Cys Pro Trp Ala Val Ser Gly Ala Arg Ala Ser
20 25 30
Pro Gly Ser Ala Ala Ser Pro Arg Leu Arg Glu Gly Pro Glu Leu Ser
35 40 45
Pro Asp Asp Pro Ala Gly Leu Leu Asp Leu Arg Gln Gly Met Phe Ala
50 55 60
Gln Leu Val Ala Gln Asn Val Leu Leu Ile Asp Gly Pro Leu Ser Trp
65 70 75 80
Tyr Ser Asp Pro Gly Leu Ala Gly Val Ser Leu Thr Gly Gly Leu Ser
85 90 95
Tyr Lys Glu Asp Thr Lys Glu Leu Val Val Ala Lys Ala Gly Val Tyr
100 105 110
Tyr Val Phe Phe Gln Leu Glu Leu Arg Arg Val Val Ala Gly Glu Gly
115 120 125
Ser Gly Ser Val Ser Leu Ala Leu His Leu Gln Pro Leu Arg Ser Ala
130 135 140
Ala Gly Ala Ala Ala Leu Ala Leu Thr Val Asp Leu Pro Pro Ala Ser
145 150 155 160
Ser Glu Ala Arg Asn Ser Ala Phe Gly Phe Gln Gly Arg Leu Leu His
165 170 175
Leu Ser Ala Gly Gln Arg Leu Gly Val His Leu His Thr Glu Ala Arg
180 185 190
Ala Arg His Ala Trp Gln Leu Thr Gln Gly Ala Thr Val Leu Gly Leu
195 200 205
Phe Arg Val Thr Pro Glu Ile Pro Ala Gly Leu Pro Ser Pro Arg Ser
210 215 220
Glu Gly Gly Ser Gly Gly Ser Gly Gly Gly Pro Glu Asp Glu Pro Gly
225 230 235 240
Ser Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Leu Ser Thr Thr Glu
245 250 255
Val Ala Met His Thr Ser Thr Ser Ser Ser Val Thr Lys Ser Tyr Ile
260 265 270
Ser Ser Gln Thr Asn Asp Thr His Lys Arg Asp Thr Tyr Ala Ala Thr
275 280 285
Pro Arg Ala His Glu Val Ser Glu Ile Ser Val Arg Thr Val Tyr Pro
290 295 300
Pro Glu Glu Glu Thr Gly Glu Arg Val Gln Leu Ala His His Phe Ser
305 310 315 320
Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly Val Met Ala Gly Val Ile
325 330 335
Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile Arg Arg Leu Ile Lys Lys
340 345 350
Ser Pro Ser Asp Val Lys Pro Leu Pro Ser Pro Asp Thr Asp Val Pro
355 360 365
Leu Ser Ser Val Glu Ile Glu Asn Pro Glu Thr Ser Asp Gln
370 375 380
<210> 851
<211> 205
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 851
Ala Cys Pro Trp Ala Val Ser Gly Ala Arg Ala Ser Pro Gly Ser Ala
1 5 10 15
Ala Ser Pro Arg Leu Arg Glu Gly Pro Glu Leu Ser Pro Asp Asp Pro
20 25 30
Ala Gly Leu Leu Asp Leu Arg Gln Gly Met Phe Ala Gln Leu Val Ala
35 40 45
Gln Asn Val Leu Leu Ile Asp Gly Pro Leu Ser Trp Tyr Ser Asp Pro
50 55 60
Gly Leu Ala Gly Val Ser Leu Thr Gly Gly Leu Ser Tyr Lys Glu Asp
65 70 75 80
Thr Lys Glu Leu Val Val Ala Lys Ala Gly Val Tyr Tyr Val Phe Phe
85 90 95
Gln Leu Glu Leu Arg Arg Val Val Ala Gly Glu Gly Ser Gly Ser Val
100 105 110
Ser Leu Ala Leu His Leu Gln Pro Leu Arg Ser Ala Ala Gly Ala Ala
115 120 125
Ala Leu Ala Leu Thr Val Asp Leu Pro Pro Ala Ser Ser Glu Ala Arg
130 135 140
Asn Ser Ala Phe Gly Phe Gln Gly Arg Leu Leu His Leu Ser Ala Gly
145 150 155 160
Gln Arg Leu Gly Val His Leu His Thr Glu Ala Arg Ala Arg His Ala
165 170 175
Trp Gln Leu Thr Gln Gly Ala Thr Val Leu Gly Leu Phe Arg Val Thr
180 185 190
Pro Glu Ile Pro Ala Gly Leu Pro Ser Pro Arg Ser Glu
195 200 205
<210> 852
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 852
Gly Gly Ser Gly Gly Ser Gly Gly Gly Pro Glu Asp Glu Pro Gly Ser
1 5 10 15
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
20 25
<210> 853
<211> 21
<212> БЕЛОК
<213> Вирус Thosea asigna
<400> 853
Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu
1 5 10 15
Glu Asn Pro Gly Pro
20
<210> 854
<211> 998
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 854
Met Tyr Gly Lys Ile Ile Phe Val Leu Leu Leu Ser Glu Ile Val Ser
1 5 10 15
Ile Ser Ala Ala Cys Pro Trp Ala Val Ser Gly Ala Arg Ala Ser Pro
20 25 30
Gly Ser Ala Ala Ser Pro Arg Leu Arg Glu Gly Pro Glu Leu Ser Pro
35 40 45
Asp Asp Pro Ala Gly Leu Leu Asp Leu Arg Gln Gly Met Phe Ala Gln
50 55 60
Leu Val Ala Gln Asn Val Leu Leu Ile Asp Gly Pro Leu Ser Trp Tyr
65 70 75 80
Ser Asp Pro Gly Leu Ala Gly Val Ser Leu Thr Gly Gly Leu Ser Tyr
85 90 95
Lys Glu Asp Thr Lys Glu Leu Val Val Ala Lys Ala Gly Val Tyr Tyr
100 105 110
Val Phe Phe Gln Leu Glu Leu Arg Arg Val Val Ala Gly Glu Gly Ser
115 120 125
Gly Ser Val Ser Leu Ala Leu His Leu Gln Pro Leu Arg Ser Ala Ala
130 135 140
Gly Ala Ala Ala Leu Ala Leu Thr Val Asp Leu Pro Pro Ala Ser Ser
145 150 155 160
Glu Ala Arg Asn Ser Ala Phe Gly Phe Gln Gly Arg Leu Leu His Leu
165 170 175
Ser Ala Gly Gln Arg Leu Gly Val His Leu His Thr Glu Ala Arg Ala
180 185 190
Arg His Ala Trp Gln Leu Thr Gln Gly Ala Thr Val Leu Gly Leu Phe
195 200 205
Arg Val Thr Pro Glu Ile Pro Ala Gly Leu Pro Ser Pro Arg Ser Glu
210 215 220
Gly Gly Ser Gly Gly Ser Gly Gly Gly Pro Glu Asp Glu Pro Gly Ser
225 230 235 240
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Leu Ser Thr Thr Glu Val
245 250 255
Ala Met His Thr Ser Thr Ser Ser Ser Val Thr Lys Ser Tyr Ile Ser
260 265 270
Ser Gln Thr Asn Asp Thr His Lys Arg Asp Thr Tyr Ala Ala Thr Pro
275 280 285
Arg Ala His Glu Val Ser Glu Ile Ser Val Arg Thr Val Tyr Pro Pro
290 295 300
Glu Glu Glu Thr Gly Glu Arg Val Gln Leu Ala His His Phe Ser Glu
305 310 315 320
Pro Glu Ile Thr Leu Ile Ile Phe Gly Val Met Ala Gly Val Ile Gly
325 330 335
Thr Ile Leu Leu Ile Ser Tyr Gly Ile Arg Arg Leu Ile Lys Lys Ser
340 345 350
Pro Ser Asp Val Lys Pro Leu Pro Ser Pro Asp Thr Asp Val Pro Leu
355 360 365
Ser Ser Val Glu Ile Glu Asn Pro Glu Thr Ser Asp Gln Gly Ser Gly
370 375 380
Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu Glu Asn Pro
385 390 395 400
Gly Pro Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser
405 410 415
Leu Ser Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly
420 425 430
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln
435 440 445
Arg Thr Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly
450 455 460
Lys Ser Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp
465 470 475 480
Ile Glu Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu
485 490 495
His Ser Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr
500 505 510
Tyr Thr Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val
515 520 525
Asn His Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp
530 535 540
Met Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
545 550 555 560
Gly Gly Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser
565 570 575
Val Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr
580 585 590
Val Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln
595 600 605
Arg Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr
610 615 620
Trp Asp Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg
625 630 635 640
Val Asp Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly
645 650 655
Ser His Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp
660 665 670
Arg Phe Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr
675 680 685
Ile Ala Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala
690 695 700
Ala Gln Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln
705 710 715 720
Leu Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr
725 730 735
Leu Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr
740 745 750
His Met Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys
755 760 765
Trp Ala Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg
770 775 780
Asp Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro
785 790 795 800
Ala Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser
805 810 815
Gly Gln Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro
820 825 830
Lys Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro
835 840 845
Ile Gly Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly
850 855 860
Ser Gly Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser
865 870 875 880
Ser Ser Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His
885 890 895
Lys Arg Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu
900 905 910
Ile Ser Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg
915 920 925
Val Gln Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile
930 935 940
Phe Gly Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr
945 950 955 960
Gly Ile Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu
965 970 975
Pro Ser Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn
980 985 990
Pro Glu Thr Ser Asp Gln
995
<210> 855
<211> 401
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 855
Met Tyr Gly Lys Ile Ile Phe Val Leu Leu Leu Ser Glu Ile Val Ser
1 5 10 15
Ile Ser Ala Ala Cys Pro Trp Ala Val Ser Gly Ala Arg Ala Ser Pro
20 25 30
Gly Ser Ala Ala Ser Pro Arg Leu Arg Glu Gly Pro Glu Leu Ser Pro
35 40 45
Asp Asp Pro Ala Gly Leu Leu Asp Leu Arg Gln Gly Met Phe Ala Gln
50 55 60
Leu Val Ala Gln Asn Val Leu Leu Ile Asp Gly Pro Leu Ser Trp Tyr
65 70 75 80
Ser Asp Pro Gly Leu Ala Gly Val Ser Leu Thr Gly Gly Leu Ser Tyr
85 90 95
Lys Glu Asp Thr Lys Glu Leu Val Val Ala Lys Ala Gly Val Tyr Tyr
100 105 110
Val Phe Phe Gln Leu Glu Leu Arg Arg Val Val Ala Gly Glu Gly Ser
115 120 125
Gly Ser Val Ser Leu Ala Leu His Leu Gln Pro Leu Arg Ser Ala Ala
130 135 140
Gly Ala Ala Ala Leu Ala Leu Thr Val Asp Leu Pro Pro Ala Ser Ser
145 150 155 160
Glu Ala Arg Asn Ser Ala Phe Gly Phe Gln Gly Arg Leu Leu His Leu
165 170 175
Ser Ala Gly Gln Arg Leu Gly Val His Leu His Thr Glu Ala Arg Ala
180 185 190
Arg His Ala Trp Gln Leu Thr Gln Gly Ala Thr Val Leu Gly Leu Phe
195 200 205
Arg Val Thr Pro Glu Ile Pro Ala Gly Leu Pro Ser Pro Arg Ser Glu
210 215 220
Gly Gly Ser Gly Gly Ser Gly Gly Gly Pro Glu Asp Glu Pro Gly Ser
225 230 235 240
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Leu Ser Thr Thr Glu Val
245 250 255
Ala Met His Thr Ser Thr Ser Ser Ser Val Thr Lys Ser Tyr Ile Ser
260 265 270
Ser Gln Thr Asn Asp Thr His Lys Arg Asp Thr Tyr Ala Ala Thr Pro
275 280 285
Arg Ala His Glu Val Ser Glu Ile Ser Val Arg Thr Val Tyr Pro Pro
290 295 300
Glu Glu Glu Thr Gly Glu Arg Val Gln Leu Ala His His Phe Ser Glu
305 310 315 320
Pro Glu Ile Thr Leu Ile Ile Phe Gly Val Met Ala Gly Val Ile Gly
325 330 335
Thr Ile Leu Leu Ile Ser Tyr Gly Ile Arg Arg Leu Ile Lys Lys Ser
340 345 350
Pro Ser Asp Val Lys Pro Leu Pro Ser Pro Asp Thr Asp Val Pro Leu
355 360 365
Ser Ser Val Glu Ile Glu Asn Pro Glu Thr Ser Asp Gln Gly Ser Gly
370 375 380
Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu Glu Asn Pro
385 390 395 400
Gly
<210> 856
<211> 597
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 856
Pro Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu
1 5 10 15
Ser Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly
20 25 30
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg
35 40 45
Thr Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys
50 55 60
Ser Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile
65 70 75 80
Glu Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His
85 90 95
Ser Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr
100 105 110
Thr Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn
115 120 125
His Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val
165 170 175
Ser Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val
180 185 190
Asp Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg
195 200 205
Met Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp
210 215 220
Asp Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val
225 230 235 240
Asp Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser
245 250 255
His Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg
260 265 270
Phe Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile
275 280 285
Ala Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala
290 295 300
Gln Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu
305 310 315 320
Arg Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu
325 330 335
Glu Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His
340 345 350
Met Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp
355 360 365
Ala Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp
370 375 380
Gly Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala
385 390 395 400
Gly Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly
405 410 415
Gln Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys
420 425 430
Pro Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile
435 440 445
Gly Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser
450 455 460
Gly Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser
465 470 475 480
Ser Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys
485 490 495
Arg Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile
500 505 510
Ser Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val
515 520 525
Gln Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe
530 535 540
Gly Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly
545 550 555 560
Ile Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro
565 570 575
Ser Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro
580 585 590
Glu Thr Ser Asp Gln
595
<210> 857
<211> 876
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 857
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser
465 470 475 480
Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg
485 490 495
Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser
500 505 510
Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln
515 520 525
Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly
530 535 540
Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile
545 550 555 560
Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser
565 570 575
Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu
580 585 590
Thr Ser Asp Gln Ser Gly Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly
595 600 605
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Pro Ala Met Glu
610 615 620
Tyr Ala Ser Asp Ala Ser Leu Asp Pro Glu Ala Pro Trp Pro Pro Ala
625 630 635 640
Pro Arg Ala Arg Ala Cys Arg Val Leu Pro Trp Ala Leu Val Ala Gly
645 650 655
Leu Leu Leu Leu Leu Leu Leu Ala Ala Ala Cys Ala Val Phe Leu Ala
660 665 670
Cys Pro Trp Ala Val Ser Gly Ala Arg Ala Ser Pro Gly Ser Ala Ala
675 680 685
Ser Pro Arg Leu Arg Glu Gly Pro Glu Leu Ser Pro Asp Asp Pro Ala
690 695 700
Gly Leu Leu Asp Leu Arg Gln Gly Met Phe Ala Gln Leu Val Ala Gln
705 710 715 720
Asn Val Leu Leu Ile Asp Gly Pro Leu Ser Trp Tyr Ser Asp Pro Gly
725 730 735
Leu Ala Gly Val Ser Leu Thr Gly Gly Leu Ser Tyr Lys Glu Asp Thr
740 745 750
Lys Glu Leu Val Val Ala Lys Ala Gly Val Tyr Tyr Val Phe Phe Gln
755 760 765
Leu Glu Leu Arg Arg Val Val Ala Gly Glu Gly Ser Gly Ser Val Ser
770 775 780
Leu Ala Leu His Leu Gln Pro Leu Arg Ser Ala Ala Gly Ala Ala Ala
785 790 795 800
Leu Ala Leu Thr Val Asp Leu Pro Pro Ala Ser Ser Glu Ala Arg Asn
805 810 815
Ser Ala Phe Gly Phe Gln Gly Arg Leu Leu His Leu Ser Ala Gly Gln
820 825 830
Arg Leu Gly Val His Leu His Thr Glu Ala Arg Ala Arg His Ala Trp
835 840 845
Gln Leu Thr Gln Gly Ala Thr Val Leu Gly Leu Phe Arg Val Thr Pro
850 855 860
Glu Ile Pro Ala Gly Leu Pro Ser Pro Arg Ser Glu
865 870 875
<210> 858
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 858
Met Glu Tyr Ala Ser Asp Ala Ser Leu Asp Pro Glu Ala Pro Trp Pro
1 5 10 15
Pro Ala Pro Arg Ala Arg Ala Cys Arg Val Leu Pro Trp Ala Leu Val
20 25 30
Ala Gly Leu Leu Leu Leu Leu Leu Leu Ala Ala Ala Cys Ala Val Phe
35 40 45
Leu Ala Cys Pro Trp Ala Val Ser Gly Ala Arg Ala Ser Pro Gly Ser
50 55 60
Ala Ala Ser Pro Arg Leu Arg Glu Gly Pro Glu Leu Ser Pro Asp Asp
65 70 75 80
Pro Ala Gly Leu Leu Asp Leu Arg Gln Gly Met Phe Ala Gln Leu Val
85 90 95
Ala Gln Asn Val Leu Leu Ile Asp Gly Pro Leu Ser Trp Tyr Ser Asp
100 105 110
Pro Gly Leu Ala Gly Val Ser Leu Thr Gly Gly Leu Ser Tyr Lys Glu
115 120 125
Asp Thr Lys Glu Leu Val Val Ala Lys Ala Gly Val Tyr Tyr Val Phe
130 135 140
Phe Gln Leu Glu Leu Arg Arg Val Val Ala Gly Glu Gly Ser Gly Ser
145 150 155 160
Val Ser Leu Ala Leu His Leu Gln Pro Leu Arg Ser Ala Ala Gly Ala
165 170 175
Ala Ala Leu Ala Leu Thr Val Asp Leu Pro Pro Ala Ser Ser Glu Ala
180 185 190
Arg Asn Ser Ala Phe Gly Phe Gln Gly Arg Leu Leu His Leu Ser Ala
195 200 205
Gly Gln Arg Leu Gly Val His Leu His Thr Glu Ala Arg Ala Arg His
210 215 220
Ala Trp Gln Leu Thr Gln Gly Ala Thr Val Leu Gly Leu Phe Arg Val
225 230 235 240
Thr Pro Glu Ile Pro Ala Gly Leu Pro Ser Pro Arg Ser Glu
245 250
<210> 859
<211> 883
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 859
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser
465 470 475 480
Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg
485 490 495
Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser
500 505 510
Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln
515 520 525
Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly
530 535 540
Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile
545 550 555 560
Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser
565 570 575
Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu
580 585 590
Thr Ser Asp Gln Ser Gly Arg Gly Ala Ser Ser Gly Ser Ser Gly Ser
595 600 605
Gly Ser Gln Lys Lys Pro Arg Tyr Glu Ile Arg Trp Lys Val Val Val
610 615 620
Ile Ser Ala Ile Leu Ala Leu Val Val Leu Thr Val Ile Ser Leu Ile
625 630 635 640
Ile Leu Ile Met Leu Trp Gly Ser Gly Met Gln Ser Pro Ala Gly Gly
645 650 655
Ser Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly
660 665 670
Gly Ser Gly Gly Gly Ser Ala Cys Pro Trp Ala Val Ser Gly Ala Arg
675 680 685
Ala Ser Pro Gly Ser Ala Ala Ser Pro Arg Leu Arg Glu Gly Pro Glu
690 695 700
Leu Ser Pro Asp Asp Pro Ala Gly Leu Leu Asp Leu Arg Gln Gly Met
705 710 715 720
Phe Ala Gln Leu Val Ala Gln Asn Val Leu Leu Ile Asp Gly Pro Leu
725 730 735
Ser Trp Tyr Ser Asp Pro Gly Leu Ala Gly Val Ser Leu Thr Gly Gly
740 745 750
Leu Ser Tyr Lys Glu Asp Thr Lys Glu Leu Val Val Ala Lys Ala Gly
755 760 765
Val Tyr Tyr Val Phe Phe Gln Leu Glu Leu Arg Arg Val Val Ala Gly
770 775 780
Glu Gly Ser Gly Ser Val Ser Leu Ala Leu His Leu Gln Pro Leu Arg
785 790 795 800
Ser Ala Ala Gly Ala Ala Ala Leu Ala Leu Thr Val Asp Leu Pro Pro
805 810 815
Ala Ser Ser Glu Ala Arg Asn Ser Ala Phe Gly Phe Gln Gly Arg Leu
820 825 830
Leu His Leu Ser Ala Gly Gln Arg Leu Gly Val His Leu His Thr Glu
835 840 845
Ala Arg Ala Arg His Ala Trp Gln Leu Thr Gln Gly Ala Thr Val Leu
850 855 860
Gly Leu Phe Arg Val Thr Pro Glu Ile Pro Ala Gly Leu Pro Ser Pro
865 870 875 880
Arg Ser Glu
<210> 860
<211> 1231
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 860
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser
465 470 475 480
Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg
485 490 495
Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser
500 505 510
Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln
515 520 525
Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly
530 535 540
Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile
545 550 555 560
Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser
565 570 575
Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu
580 585 590
Thr Ser Asp Gln Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
595 600 605
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Met Gln Pro Gln
610 615 620
Glu Ser His Val His Tyr Ser Arg Trp Glu Asp Gly Ser Arg Asp Gly
625 630 635 640
Val Ser Leu Gly Ala Val Ser Ser Thr Glu Glu Ala Ser Arg Cys Arg
645 650 655
Arg Ile Ser Gln Arg Leu Cys Thr Gly Lys Leu Gly Ile Ala Met Lys
660 665 670
Val Leu Gly Gly Val Ala Leu Phe Trp Ile Ile Phe Ile Leu Gly Tyr
675 680 685
Leu Thr Gly Tyr Tyr Val His Lys Cys Lys Gly Gly Gly Gly Ser Gly
690 695 700
Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Trp Glu Leu Lys Lys Asp
705 710 715 720
Val Tyr Val Val Glu Leu Asp Trp Tyr Pro Asp Ala Pro Gly Glu Met
725 730 735
Val Val Leu Thr Cys Asp Thr Pro Glu Glu Asp Gly Ile Thr Trp Thr
740 745 750
Leu Asp Gln Ser Ser Glu Val Leu Gly Ser Gly Lys Thr Leu Thr Ile
755 760 765
Gln Val Lys Glu Phe Gly Asp Ala Gly Gln Tyr Thr Cys His Lys Gly
770 775 780
Gly Glu Val Leu Ser His Ser Leu Leu Leu Leu His Lys Lys Glu Asp
785 790 795 800
Gly Ile Trp Ser Thr Asp Ile Leu Lys Asp Gln Lys Glu Pro Lys Asn
805 810 815
Lys Thr Phe Leu Arg Cys Glu Ala Lys Asn Tyr Ser Gly Arg Phe Thr
820 825 830
Cys Trp Trp Leu Thr Thr Ile Ser Thr Asp Leu Thr Phe Ser Val Lys
835 840 845
Ser Ser Arg Gly Ser Ser Asp Pro Gln Gly Val Thr Cys Gly Ala Ala
850 855 860
Thr Leu Ser Ala Glu Arg Val Arg Gly Asp Asn Lys Glu Tyr Glu Tyr
865 870 875 880
Ser Val Glu Cys Gln Glu Asp Ser Ala Cys Pro Ala Ala Glu Glu Ser
885 890 895
Leu Pro Ile Glu Val Met Val Asp Ala Val His Lys Leu Lys Tyr Glu
900 905 910
Asn Tyr Thr Ser Ser Phe Phe Ile Arg Asp Ile Ile Lys Pro Asp Pro
915 920 925
Pro Lys Asn Leu Gln Leu Lys Pro Leu Lys Asn Ser Arg Gln Val Glu
930 935 940
Val Ser Trp Glu Tyr Pro Asp Thr Trp Ser Thr Pro His Ser Tyr Phe
945 950 955 960
Ser Leu Thr Phe Cys Val Gln Val Gln Gly Lys Ser Lys Arg Glu Lys
965 970 975
Lys Asp Arg Val Phe Thr Asp Lys Thr Ser Ala Thr Val Ile Cys Arg
980 985 990
Lys Asn Ala Ser Ile Ser Val Arg Ala Gln Asp Arg Tyr Tyr Ser Ser
995 1000 1005
Ser Trp Ser Glu Trp Ala Ser Val Pro Cys Ser Gly Gly Gly Gly
1010 1015 1020
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Arg Asn Leu Pro
1025 1030 1035
Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu His His Ser
1040 1045 1050
Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys Ala Arg
1055 1060 1065
Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp His
1070 1075 1080
Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
1085 1090 1095
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu
1100 1105 1110
Thr Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr
1115 1120 1125
Ser Phe Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu
1130 1135 1140
Lys Met Tyr Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu
1145 1150 1155
Met Asp Pro Lys Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala
1160 1165 1170
Val Ile Asp Glu Leu Met Gln Ala Leu Asn Phe Asn Ser Glu Thr
1175 1180 1185
Val Pro Gln Lys Ser Ser Leu Glu Glu Pro Asp Phe Tyr Lys Thr
1190 1195 1200
Lys Ile Lys Leu Cys Ile Leu Leu His Ala Phe Arg Ile Arg Ala
1205 1210 1215
Val Thr Ile Asp Arg Val Met Ser Tyr Leu Asn Ala Ser
1220 1225 1230
<210> 861
<211> 306
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 861
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 862
<211> 197
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 862
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 863
<211> 1265
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 863
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser
465 470 475 480
Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg
485 490 495
Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser
500 505 510
Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln
515 520 525
Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly
530 535 540
Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile
545 550 555 560
Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser
565 570 575
Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu
580 585 590
Thr Ser Asp Gln Ser Gly Arg Gly Ala Ser Ser Gly Ser Ser Gly Ser
595 600 605
Gly Ser Gln Lys Lys Pro Arg Tyr Glu Ile Arg Trp Lys Val Val Val
610 615 620
Ile Ser Ala Ile Leu Ala Leu Val Val Leu Thr Val Ile Ser Leu Ile
625 630 635 640
Ile Leu Ile Met Leu Trp Gly Ser Gly Met Gln Ser Pro Ala Met Gln
645 650 655
Pro Gln Glu Ser His Val His Tyr Ser Arg Trp Glu Asp Gly Ser Arg
660 665 670
Asp Gly Val Ser Leu Gly Ala Val Ser Ser Thr Glu Glu Ala Ser Arg
675 680 685
Cys Arg Arg Ile Ser Gln Arg Leu Cys Thr Gly Lys Leu Gly Ile Ala
690 695 700
Met Lys Val Leu Gly Gly Val Ala Leu Phe Trp Ile Ile Phe Ile Leu
705 710 715 720
Gly Tyr Leu Thr Gly Tyr Tyr Val His Lys Cys Lys Gly Gly Gly Gly
725 730 735
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Trp Glu Leu Lys
740 745 750
Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr Pro Asp Ala Pro Gly
755 760 765
Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu Glu Asp Gly Ile Thr
770 775 780
Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly Ser Gly Lys Thr Leu
785 790 795 800
Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly Gln Tyr Thr Cys His
805 810 815
Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu Leu Leu His Lys Lys
820 825 830
Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys Asp Gln Lys Glu Pro
835 840 845
Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys Asn Tyr Ser Gly Arg
850 855 860
Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr Asp Leu Thr Phe Ser
865 870 875 880
Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln Gly Val Thr Cys Gly
885 890 895
Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly Asp Asn Lys Glu Tyr
900 905 910
Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala Cys Pro Ala Ala Glu
915 920 925
Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala Val His Lys Leu Lys
930 935 940
Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg Asp Ile Ile Lys Pro
945 950 955 960
Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu Lys Asn Ser Arg Gln
965 970 975
Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp Ser Thr Pro His Ser
980 985 990
Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln Gly Lys Ser Lys Arg
995 1000 1005
Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr Ser Ala Thr Val
1010 1015 1020
Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala Gln Asp Arg
1025 1030 1035
Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro Cys Ser
1040 1045 1050
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1055 1060 1065
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys
1070 1075 1080
Leu His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu
1085 1090 1095
Gln Lys Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu
1100 1105 1110
Glu Ile Asp His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val
1115 1120 1125
Glu Ala Cys Leu Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu
1130 1135 1140
Asn Ser Arg Glu Thr Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala
1145 1150 1155
Ser Arg Lys Thr Ser Phe Met Met Ala Leu Cys Leu Ser Ser Ile
1160 1165 1170
Tyr Glu Asp Leu Lys Met Tyr Gln Val Glu Phe Lys Thr Met Asn
1175 1180 1185
Ala Lys Leu Leu Met Asp Pro Lys Arg Gln Ile Phe Leu Asp Gln
1190 1195 1200
Asn Met Leu Ala Val Ile Asp Glu Leu Met Gln Ala Leu Asn Phe
1205 1210 1215
Asn Ser Glu Thr Val Pro Gln Lys Ser Ser Leu Glu Glu Pro Asp
1220 1225 1230
Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu Leu His Ala Phe
1235 1240 1245
Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser Tyr Leu Asn
1250 1255 1260
Ala Ser
1265
<210> 864
<211> 1187
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 864
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser
465 470 475 480
Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg
485 490 495
Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser
500 505 510
Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln
515 520 525
Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly
530 535 540
Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile
545 550 555 560
Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser
565 570 575
Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu
580 585 590
Thr Ser Asp Gln Ser Gly Arg Gly Ala Ser Ser Gly Ser Ser Gly Ser
595 600 605
Gly Ser Gln Lys Lys Pro Arg Tyr Glu Ile Arg Trp Lys Val Val Val
610 615 620
Ile Ser Ala Ile Leu Ala Leu Val Val Leu Thr Val Ile Ser Leu Ile
625 630 635 640
Ile Leu Ile Met Leu Trp Gly Ser Gly Met Gln Ser Pro Ala Gly Gly
645 650 655
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Trp Glu
660 665 670
Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr Pro Asp Ala
675 680 685
Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu Glu Asp Gly
690 695 700
Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly Ser Gly Lys
705 710 715 720
Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly Gln Tyr Thr
725 730 735
Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu Leu Leu His
740 745 750
Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys Asp Gln Lys
755 760 765
Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys Asn Tyr Ser
770 775 780
Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr Asp Leu Thr
785 790 795 800
Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln Gly Val Thr
805 810 815
Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly Asp Asn Lys
820 825 830
Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala Cys Pro Ala
835 840 845
Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala Val His Lys
850 855 860
Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg Asp Ile Ile
865 870 875 880
Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu Lys Asn Ser
885 890 895
Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp Ser Thr Pro
900 905 910
His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln Gly Lys Ser
915 920 925
Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr Ser Ala Thr
930 935 940
Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala Gln Asp Arg
945 950 955 960
Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro Cys Ser Gly
965 970 975
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Arg Asn
980 985 990
Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu His His
995 1000 1005
Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys Ala
1010 1015 1020
Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
1025 1030 1035
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys
1040 1045 1050
Leu Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg
1055 1060 1065
Glu Thr Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys
1070 1075 1080
Thr Ser Phe Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp
1085 1090 1095
Leu Lys Met Tyr Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu
1100 1105 1110
Leu Met Asp Pro Lys Arg Gln Ile Phe Leu Asp Gln Asn Met Leu
1115 1120 1125
Ala Val Ile Asp Glu Leu Met Gln Ala Leu Asn Phe Asn Ser Glu
1130 1135 1140
Thr Val Pro Gln Lys Ser Ser Leu Glu Glu Pro Asp Phe Tyr Lys
1145 1150 1155
Thr Lys Ile Lys Leu Cys Ile Leu Leu His Ala Phe Arg Ile Arg
1160 1165 1170
Ala Val Thr Ile Asp Arg Val Met Ser Tyr Leu Asn Ala Ser
1175 1180 1185
<210> 865
<211> 943
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 865
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser
465 470 475 480
Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg
485 490 495
Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser
500 505 510
Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln
515 520 525
Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly
530 535 540
Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile
545 550 555 560
Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser
565 570 575
Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu
580 585 590
Thr Ser Asp Gln Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys
595 600 605
Gly Asp Val Glu Glu Asn Pro Gly Pro Met Tyr Gly Lys Ile Ile Phe
610 615 620
Val Leu Leu Leu Ser Glu Ile Val Ser Ile Ser Ala Asp Cys Asp Ile
625 630 635 640
Glu Gly Lys Asp Gly Lys Gln Tyr Glu Ser Val Leu Met Val Ser Ile
645 650 655
Asp Gln Leu Leu Asp Ser Met Lys Glu Ile Gly Ser Asn Cys Leu Asn
660 665 670
Asn Glu Phe Asn Phe Phe Lys Arg His Ile Cys Asp Ala Asn Lys Glu
675 680 685
Gly Met Phe Leu Phe Arg Ala Ala Arg Lys Leu Arg Gln Phe Leu Lys
690 695 700
Met Asn Ser Thr Gly Asp Phe Asp Leu His Leu Leu Lys Val Ser Glu
705 710 715 720
Gly Thr Thr Ile Leu Leu Asn Cys Thr Gly Gln Val Lys Gly Arg Lys
725 730 735
Pro Ala Ala Leu Gly Glu Ala Gln Pro Thr Lys Ser Leu Glu Glu Asn
740 745 750
Lys Ser Leu Lys Glu Gln Lys Lys Leu Asn Asp Leu Cys Phe Leu Lys
755 760 765
Arg Leu Leu Gln Glu Ile Lys Thr Cys Trp Asn Lys Ile Leu Met Gly
770 775 780
Thr Lys Glu His Gly Gly Ser Gly Gly Ser Gly Gly Gly Gly Gly Ser
785 790 795 800
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Leu Ser Thr Thr
805 810 815
Glu Val Ala Met His Thr Ser Thr Ser Ser Ser Val Thr Lys Ser Tyr
820 825 830
Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg Asp Thr Tyr Ala Ala
835 840 845
Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser Val Arg Thr Val Tyr
850 855 860
Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln Leu Ala His His Phe
865 870 875 880
Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly Val Met Ala Gly Val
885 890 895
Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile Arg Arg Leu Ile Lys
900 905 910
Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser Pro Asp Thr Asp Val
915 920 925
Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu Thr Ser Asp Gln
930 935 940
<210> 866
<211> 327
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 866
Pro Met Tyr Gly Lys Ile Ile Phe Val Leu Leu Leu Ser Glu Ile Val
1 5 10 15
Ser Ile Ser Ala Asp Cys Asp Ile Glu Gly Lys Asp Gly Lys Gln Tyr
20 25 30
Glu Ser Val Leu Met Val Ser Ile Asp Gln Leu Leu Asp Ser Met Lys
35 40 45
Glu Ile Gly Ser Asn Cys Leu Asn Asn Glu Phe Asn Phe Phe Lys Arg
50 55 60
His Ile Cys Asp Ala Asn Lys Glu Gly Met Phe Leu Phe Arg Ala Ala
65 70 75 80
Arg Lys Leu Arg Gln Phe Leu Lys Met Asn Ser Thr Gly Asp Phe Asp
85 90 95
Leu His Leu Leu Lys Val Ser Glu Gly Thr Thr Ile Leu Leu Asn Cys
100 105 110
Thr Gly Gln Val Lys Gly Arg Lys Pro Ala Ala Leu Gly Glu Ala Gln
115 120 125
Pro Thr Lys Ser Leu Glu Glu Asn Lys Ser Leu Lys Glu Gln Lys Lys
130 135 140
Leu Asn Asp Leu Cys Phe Leu Lys Arg Leu Leu Gln Glu Ile Lys Thr
145 150 155 160
Cys Trp Asn Lys Ile Leu Met Gly Thr Lys Glu His Gly Gly Ser Gly
165 170 175
Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
180 185 190
Gly Gly Gly Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr
195 200 205
Ser Ser Ser Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr
210 215 220
His Lys Arg Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser
225 230 235 240
Glu Ile Ser Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu
245 250 255
Arg Val Gln Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile
260 265 270
Ile Phe Gly Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser
275 280 285
Tyr Gly Ile Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro
290 295 300
Leu Pro Ser Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu
305 310 315 320
Asn Pro Glu Thr Ser Asp Gln
325
<210> 867
<211> 152
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 867
Asp Cys Asp Ile Glu Gly Lys Asp Gly Lys Gln Tyr Glu Ser Val Leu
1 5 10 15
Met Val Ser Ile Asp Gln Leu Leu Asp Ser Met Lys Glu Ile Gly Ser
20 25 30
Asn Cys Leu Asn Asn Glu Phe Asn Phe Phe Lys Arg His Ile Cys Asp
35 40 45
Ala Asn Lys Glu Gly Met Phe Leu Phe Arg Ala Ala Arg Lys Leu Arg
50 55 60
Gln Phe Leu Lys Met Asn Ser Thr Gly Asp Phe Asp Leu His Leu Leu
65 70 75 80
Lys Val Ser Glu Gly Thr Thr Ile Leu Leu Asn Cys Thr Gly Gln Val
85 90 95
Lys Gly Arg Lys Pro Ala Ala Leu Gly Glu Ala Gln Pro Thr Lys Ser
100 105 110
Leu Glu Glu Asn Lys Ser Leu Lys Glu Gln Lys Lys Leu Asn Asp Leu
115 120 125
Cys Phe Leu Lys Arg Leu Leu Gln Glu Ile Lys Thr Cys Trp Asn Lys
130 135 140
Ile Leu Met Gly Thr Lys Glu His
145 150
<210> 868
<211> 1095
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 868
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser
465 470 475 480
Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg
485 490 495
Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser
500 505 510
Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln
515 520 525
Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly
530 535 540
Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile
545 550 555 560
Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser
565 570 575
Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu
580 585 590
Thr Ser Asp Gln Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys
595 600 605
Gly Asp Val Glu Glu Asn Pro Gly Pro Met Tyr Gly Lys Ile Ile Phe
610 615 620
Val Leu Leu Leu Ser Glu Ile Val Ser Ile Ser Ala Asn Trp Val Asn
625 630 635 640
Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His
645 650 655
Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His Pro Ser Cys Lys
660 665 670
Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu
675 680 685
Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu Asn Leu Ile Ile
690 695 700
Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly
705 710 715 720
Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu
725 730 735
Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Gly Gly
740 745 750
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Thr Cys
755 760 765
Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val Lys Ser Tyr
770 775 780
Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly Phe Lys Arg
785 790 795 800
Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn Lys Ala Thr
805 810 815
Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile Arg Asp Pro
820 825 830
Ala Leu Val His Gln Arg Pro Ala Pro Pro Ser Thr Val Thr Thr Ala
835 840 845
Gly Val Thr Pro Gln Pro Glu Ser Leu Ser Pro Ser Gly Lys Glu Pro
850 855 860
Ala Ala Ser Ser Pro Ser Ser Asn Asn Thr Ala Ala Thr Thr Ala Ala
865 870 875 880
Ile Val Pro Gly Ser Gln Leu Met Pro Ser Lys Ser Pro Ser Thr Gly
885 890 895
Thr Thr Glu Ile Ser Ser His Glu Ser Ser His Gly Thr Pro Ser Gln
900 905 910
Thr Thr Ala Lys Asn Trp Glu Leu Thr Ala Ser Ala Ser His Gln Pro
915 920 925
Pro Gly Val Tyr Pro Gln Gly His Ser Asp Thr Thr Gly Gly Ser Gly
930 935 940
Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
945 950 955 960
Gly Gly Gly Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr
965 970 975
Ser Ser Ser Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr
980 985 990
His Lys Arg Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser
995 1000 1005
Glu Ile Ser Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly
1010 1015 1020
Glu Arg Val Gln Leu Ala His His Phe Ser Glu Pro Glu Ile Thr
1025 1030 1035
Leu Ile Ile Phe Gly Val Met Ala Gly Val Ile Gly Thr Ile Leu
1040 1045 1050
Leu Ile Ser Tyr Gly Ile Arg Arg Leu Ile Lys Lys Ser Pro Ser
1055 1060 1065
Asp Val Lys Pro Leu Pro Ser Pro Asp Thr Asp Val Pro Leu Ser
1070 1075 1080
Ser Val Glu Ile Glu Asn Pro Glu Thr Ser Asp Gln
1085 1090 1095
<210> 869
<211> 479
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 869
Pro Met Tyr Gly Lys Ile Ile Phe Val Leu Leu Leu Ser Glu Ile Val
1 5 10 15
Ser Ile Ser Ala Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile
20 25 30
Glu Asp Leu Ile Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu
35 40 45
Ser Asp Val His Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu
50 55 60
Leu Glu Leu Gln Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His
65 70 75 80
Asp Thr Val Glu Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser
85 90 95
Asn Gly Asn Val Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu
100 105 110
Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln
115 120 125
Met Phe Ile Asn Thr Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Ile Thr Cys Pro Pro Pro Met Ser Val Glu His
145 150 155 160
Ala Asp Ile Trp Val Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr
165 170 175
Ile Cys Asn Ser Gly Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr
180 185 190
Glu Cys Val Leu Asn Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro
195 200 205
Ser Leu Lys Cys Ile Arg Asp Pro Ala Leu Val His Gln Arg Pro Ala
210 215 220
Pro Pro Ser Thr Val Thr Thr Ala Gly Val Thr Pro Gln Pro Glu Ser
225 230 235 240
Leu Ser Pro Ser Gly Lys Glu Pro Ala Ala Ser Ser Pro Ser Ser Asn
245 250 255
Asn Thr Ala Ala Thr Thr Ala Ala Ile Val Pro Gly Ser Gln Leu Met
260 265 270
Pro Ser Lys Ser Pro Ser Thr Gly Thr Thr Glu Ile Ser Ser His Glu
275 280 285
Ser Ser His Gly Thr Pro Ser Gln Thr Thr Ala Lys Asn Trp Glu Leu
290 295 300
Thr Ala Ser Ala Ser His Gln Pro Pro Gly Val Tyr Pro Gln Gly His
305 310 315 320
Ser Asp Thr Thr Gly Gly Ser Gly Gly Ser Gly Gly Gly Gly Gly Ser
325 330 335
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Leu Ser Thr Thr
340 345 350
Glu Val Ala Met His Thr Ser Thr Ser Ser Ser Val Thr Lys Ser Tyr
355 360 365
Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg Asp Thr Tyr Ala Ala
370 375 380
Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser Val Arg Thr Val Tyr
385 390 395 400
Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln Leu Ala His His Phe
405 410 415
Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly Val Met Ala Gly Val
420 425 430
Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile Arg Arg Leu Ile Lys
435 440 445
Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser Pro Asp Thr Asp Val
450 455 460
Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu Thr Ser Asp Gln
465 470 475
<210> 870
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 870
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 871
<211> 175
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 871
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Asp Pro Ala Leu Val His Gln Arg Pro Ala Pro Pro Ser Thr Val
65 70 75 80
Thr Thr Ala Gly Val Thr Pro Gln Pro Glu Ser Leu Ser Pro Ser Gly
85 90 95
Lys Glu Pro Ala Ala Ser Ser Pro Ser Ser Asn Asn Thr Ala Ala Thr
100 105 110
Thr Ala Ala Ile Val Pro Gly Ser Gln Leu Met Pro Ser Lys Ser Pro
115 120 125
Ser Thr Gly Thr Thr Glu Ile Ser Ser His Glu Ser Ser His Gly Thr
130 135 140
Pro Ser Gln Thr Thr Ala Lys Asn Trp Glu Leu Thr Ala Ser Ala Ser
145 150 155 160
His Gln Pro Pro Gly Val Tyr Pro Gln Gly His Ser Asp Thr Thr
165 170 175
<210> 872
<211> 1228
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 872
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 10 15
Gly Leu Glu Ala Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly
20 25 30
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Gln Arg Thr
35 40 45
Pro Lys Ile Gln Val Tyr Ser Arg His Pro Ala Glu Asn Gly Lys Ser
50 55 60
Asn Phe Leu Asn Cys Tyr Val Ser Gly Phe His Pro Ser Asp Ile Glu
65 70 75 80
Val Asp Leu Leu Lys Asn Gly Glu Arg Ile Glu Lys Val Glu His Ser
85 90 95
Asp Leu Ser Phe Ser Lys Asp Trp Ser Phe Tyr Leu Leu Tyr Tyr Thr
100 105 110
Glu Phe Thr Pro Thr Glu Lys Asp Glu Tyr Ala Cys Arg Val Asn His
115 120 125
Val Thr Leu Ser Gln Pro Lys Ile Val Lys Trp Asp Arg Asp Met Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Ser His Ser Met Arg Tyr Phe Phe Thr Ser Val Ser
165 170 175
Arg Pro Gly Arg Gly Glu Pro Arg Phe Ile Ala Val Gly Tyr Val Asp
180 185 190
Asp Thr Gln Phe Val Arg Phe Asp Ser Asp Ala Ala Ser Gln Arg Met
195 200 205
Glu Pro Arg Ala Pro Trp Ile Glu Gln Glu Gly Pro Glu Tyr Trp Asp
210 215 220
Gly Glu Thr Arg Lys Val Lys Ala His Ser Gln Thr His Arg Val Asp
225 230 235 240
Leu Gly Thr Leu Arg Gly Ala Tyr Asn Gln Ser Glu Ala Gly Ser His
245 250 255
Thr Val Gln Arg Met Tyr Gly Cys Asp Val Gly Ser Asp Trp Arg Phe
260 265 270
Leu Arg Gly Tyr His Gln Tyr Ala Tyr Asp Gly Lys Asp Tyr Ile Ala
275 280 285
Leu Lys Glu Asp Leu Arg Ser Trp Thr Ala Ala Asp Met Ala Ala Gln
290 295 300
Thr Thr Lys His Lys Trp Glu Ala Ala His Val Ala Glu Gln Leu Arg
305 310 315 320
Ala Tyr Leu Glu Gly Thr Cys Val Glu Trp Leu Arg Arg Tyr Leu Glu
325 330 335
Asn Gly Lys Glu Thr Leu Gln Arg Thr Asp Ala Pro Lys Thr His Met
340 345 350
Thr His His Ala Val Ser Asp His Glu Ala Thr Leu Arg Cys Trp Ala
355 360 365
Leu Ser Phe Tyr Pro Ala Glu Ile Thr Leu Thr Trp Gln Arg Asp Gly
370 375 380
Glu Asp Gln Thr Gln Asp Thr Glu Leu Val Glu Thr Arg Pro Ala Gly
385 390 395 400
Asp Gly Thr Phe Gln Lys Trp Ala Ala Val Val Val Pro Ser Gly Gln
405 410 415
Glu Gln Arg Tyr Thr Cys His Val Gln His Glu Gly Leu Pro Lys Pro
420 425 430
Leu Thr Leu Arg Trp Glu Pro Ser Ser Gln Pro Thr Ile Pro Ile Gly
435 440 445
Ser Gly Ser Gly Ser Gly Ser Glu Asp Gly Ser Gly Ser Gly Ser Gly
450 455 460
Ser Leu Ser Thr Thr Glu Val Ala Met His Thr Ser Thr Ser Ser Ser
465 470 475 480
Val Thr Lys Ser Tyr Ile Ser Ser Gln Thr Asn Asp Thr His Lys Arg
485 490 495
Asp Thr Tyr Ala Ala Thr Pro Arg Ala His Glu Val Ser Glu Ile Ser
500 505 510
Val Arg Thr Val Tyr Pro Pro Glu Glu Glu Thr Gly Glu Arg Val Gln
515 520 525
Leu Ala His His Phe Ser Glu Pro Glu Ile Thr Leu Ile Ile Phe Gly
530 535 540
Val Met Ala Gly Val Ile Gly Thr Ile Leu Leu Ile Ser Tyr Gly Ile
545 550 555 560
Arg Arg Leu Ile Lys Lys Ser Pro Ser Asp Val Lys Pro Leu Pro Ser
565 570 575
Pro Asp Thr Asp Val Pro Leu Ser Ser Val Glu Ile Glu Asn Pro Glu
580 585 590
Thr Ser Asp Gln Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys
595 600 605
Gly Asp Val Glu Glu Asn Pro Gly Pro Met Gln Pro Gln Glu Ser His
610 615 620
Val His Tyr Ser Arg Trp Glu Asp Gly Ser Arg Asp Gly Val Ser Leu
625 630 635 640
Gly Ala Val Ser Ser Thr Glu Glu Ala Ser Arg Cys Arg Arg Ile Ser
645 650 655
Gln Arg Leu Cys Thr Gly Lys Leu Gly Ile Ala Met Lys Val Leu Gly
660 665 670
Gly Val Ala Leu Phe Trp Ile Ile Phe Ile Leu Gly Tyr Leu Thr Gly
675 680 685
Tyr Tyr Val His Lys Cys Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly
690 695 700
Ser Gly Gly Gly Gly Ser Ile Trp Glu Leu Lys Lys Asp Val Tyr Val
705 710 715 720
Val Glu Leu Asp Trp Tyr Pro Asp Ala Pro Gly Glu Met Val Val Leu
725 730 735
Thr Cys Asp Thr Pro Glu Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln
740 745 750
Ser Ser Glu Val Leu Gly Ser Gly Lys Thr Leu Thr Ile Gln Val Lys
755 760 765
Glu Phe Gly Asp Ala Gly Gln Tyr Thr Cys His Lys Gly Gly Glu Val
770 775 780
Leu Ser His Ser Leu Leu Leu Leu His Lys Lys Glu Asp Gly Ile Trp
785 790 795 800
Ser Thr Asp Ile Leu Lys Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe
805 810 815
Leu Arg Cys Glu Ala Lys Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp
820 825 830
Leu Thr Thr Ile Ser Thr Asp Leu Thr Phe Ser Val Lys Ser Ser Arg
835 840 845
Gly Ser Ser Asp Pro Gln Gly Val Thr Cys Gly Ala Ala Thr Leu Ser
850 855 860
Ala Glu Arg Val Arg Gly Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu
865 870 875 880
Cys Gln Glu Asp Ser Ala Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile
885 890 895
Glu Val Met Val Asp Ala Val His Lys Leu Lys Tyr Glu Asn Tyr Thr
900 905 910
Ser Ser Phe Phe Ile Arg Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn
915 920 925
Leu Gln Leu Lys Pro Leu Lys Asn Ser Arg Gln Val Glu Val Ser Trp
930 935 940
Glu Tyr Pro Asp Thr Trp Ser Thr Pro His Ser Tyr Phe Ser Leu Thr
945 950 955 960
Phe Cys Val Gln Val Gln Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg
965 970 975
Val Phe Thr Asp Lys Thr Ser Ala Thr Val Ile Cys Arg Lys Asn Ala
980 985 990
Ser Ile Ser Val Arg Ala Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser
995 1000 1005
Glu Trp Ala Ser Val Pro Cys Ser Gly Gly Gly Gly Ser Gly Gly
1010 1015 1020
Gly Gly Ser Gly Gly Gly Gly Ser Arg Asn Leu Pro Val Ala Thr
1025 1030 1035
Pro Asp Pro Gly Met Phe Pro Cys Leu His His Ser Gln Asn Leu
1040 1045 1050
Leu Arg Ala Val Ser Asn Met Leu Gln Lys Ala Arg Gln Thr Leu
1055 1060 1065
Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp His Glu Asp Ile
1070 1075 1080
Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu Pro Leu Glu
1085 1090 1095
Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr Ser Phe
1100 1105 1110
Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe Met
1115 1120 1125
Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
1130 1135 1140
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro
1145 1150 1155
Lys Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp
1160 1165 1170
Glu Leu Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln
1175 1180 1185
Lys Ser Ser Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys
1190 1195 1200
Leu Cys Ile Leu Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile
1205 1210 1215
Asp Arg Val Met Ser Tyr Leu Asn Ala Ser
1220 1225
<210> 873
<211> 612
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 873
Pro Met Gln Pro Gln Glu Ser His Val His Tyr Ser Arg Trp Glu Asp
1 5 10 15
Gly Ser Arg Asp Gly Val Ser Leu Gly Ala Val Ser Ser Thr Glu Glu
20 25 30
Ala Ser Arg Cys Arg Arg Ile Ser Gln Arg Leu Cys Thr Gly Lys Leu
35 40 45
Gly Ile Ala Met Lys Val Leu Gly Gly Val Ala Leu Phe Trp Ile Ile
50 55 60
Phe Ile Leu Gly Tyr Leu Thr Gly Tyr Tyr Val His Lys Cys Lys Gly
65 70 75 80
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Trp
85 90 95
Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr Pro Asp
100 105 110
Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu Glu Asp
115 120 125
Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly Ser Gly
130 135 140
Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly Gln Tyr
145 150 155 160
Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu Leu Leu
165 170 175
His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys Asp Gln
180 185 190
Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys Asn Tyr
195 200 205
Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr Asp Leu
210 215 220
Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln Gly Val
225 230 235 240
Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly Asp Asn
245 250 255
Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala Cys Pro
260 265 270
Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala Val His
275 280 285
Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg Asp Ile
290 295 300
Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu Lys Asn
305 310 315 320
Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp Ser Thr
325 330 335
Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln Gly Lys
340 345 350
Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr Ser Ala
355 360 365
Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala Gln Asp
370 375 380
Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro Cys Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Arg
405 410 415
Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu His
420 425 430
His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys Ala
435 440 445
Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp His
450 455 460
Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu Pro
465 470 475 480
Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr Ser
485 490 495
Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe Met
500 505 510
Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr Gln
515 520 525
Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys Arg
530 535 540
Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu Met
545 550 555 560
Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser Leu
565 570 575
Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu Leu
580 585 590
His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser Tyr
595 600 605
Leu Asn Ala Ser
610
<210> 874
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 874
Tyr Glu Met Phe Asn Asp Lys Ser Phe
1 5
<210> 875
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<220>
<221> MOD_RES
<222> (3)..(3)
<223> Pyro-Lys
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена="Leu"
<220>
<221> УЧАСТОК
<222> (1)..(11)
<223> /примечание="варианты остатков, приведенные в последовательности, не
имеют приоритета относительно остатков в аннотациях вариантов положений"
<400> 875
His Arg Xaa Glu Ile Phe Ser His Asp Phe Ile
1 5 10
<210> 876
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Leu"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Leu"
<220>
<221> MOD_RES
<222> (7)..(7)
<223> Pyro-Lys
<220>
<221> УЧАСТОК
<222> (1)..(10)
<223> /примечание="варианты остатков, приведенные в последовательности, не
имеют приоритета относительно остатков в аннотациях вариантов положений"
<400> 876
Phe Ile Ile Glu Ile Phe Xaa Glu Ser Ser
1 5 10
<210> 877
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<220>
<221> MOD_RES
<222> (4)..(4)
<223> Pyro-Lys
<400> 877
Asn Glu Ile Xaa Arg Glu Ile Arg Glu Ile
1 5 10
<210> 878
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Leu"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена="Leu"
<220>
<221> MOD_RES
<222> (15)..(15)
<223> Селеноцистеин
<220>
<221> УЧАСТОК
<222> (1)..(15)
<223> /примечание="варианты остатков, приведенные в последовательности, не
имеют приоритета относительно остатков в аннотациях вариантов положений"
<400> 878
Ile Phe Lys Ser Ile Phe Glu Met Met Ser Ile Asp Ser Ser Xaa
1 5 10 15
<210> 879
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<220>
<221> MOD_RES
<222> (11)..(11)
<223> Pyro-Lys
<400> 879
Lys Asn Phe Leu Glu Asn Phe Ile Glu Ser Xaa Phe Ile
1 5 10
<210> 880
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 880
Lys Ile Gly Asp Phe Gly Leu Ala Thr Glu Lys
1 5 10
<210> 881
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 881
Lys Leu Val Val Val Gly Ala Asp Gly Val
1 5 10
<210> 882
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 882
Lys Leu Val Val Val Gly Ala Val Gly Val
1 5 10
<210> 883
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 883
Lys Leu Val Val Val Gly Ala Val
1 5
<210> 884
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 884
Lys Ile Gly Asp Phe Gly Leu Ala Thr Glu Lys
1 5 10
<210> 885
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 885
Ala Arg His Gly Gly Trp Thr Thr Lys Met
1 5 10
<210> 886
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 886
Ala Arg His Gly Gly Trp Thr Thr Lys Met
1 5 10
<210> 887
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 887
Ser Thr Arg Asp Pro Leu Ser Glu Ile Thr Lys
1 5 10
<210> 888
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 888
Phe Gly Leu Ala Thr Glu Lys Ser Arg Trp
1 5 10
<210> 889
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 889
Leu Ala Thr Glu Lys Ser Arg Trp
1 5
<210> 890
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 890
Arg Met Ser Ala Pro Ser Thr Gly Gly Val
1 5 10
<210> 891
<211> 9
<212> БЕЛОК
<213> Unknown
<220>
<221> источник
<223> /примечание="Описание неизвестного пептида: пептид HLA-G"
<400> 891
Asp Tyr Leu Ala Leu Asn Glu Asp Leu
1 5
<210> 892
<211> 9
<212> БЕЛОК
<213> Unknown
<220>
<221> источник
<223> /примечание="Описание неизвестного пептида: пептид HLA-G"
<400> 892
Arg Tyr Leu Glu Asn Gly Lys Glu Met
1 5
<210> 893
<211> 10
<212> БЕЛОК
<213> Unknown
<220>
<221> источник
<223> /примечание="Описание неизвестного пептида: пептид HLA-G"
<400> 893
Arg Tyr Ala Tyr Asp Gly Lys Asp Tyr Leu
1 5 10
<210> 894
<211> 10
<212> БЕЛОК
<213> Unknown
<220>
<221> источник
<223> /примечание="Описание неизвестного пептида: пептид HLA-G"
<400> 894
Ala Tyr Asp Gly Lys Asp Tyr Leu Ala Leu
1 5 10
<210> 895
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 895
Tyr Met Leu Asp Leu Gln Pro Glu Thr Gly Gly Gly Gly Ser Gly Gly
1 5 10 15
Gly Gly Ser Gly Gly Gly Gly Ser
20
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ИММУНОИНДУЦИРУЮЩЕЕ СРЕДСТВО | 2016 |
|
RU2744843C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ИММУНОТЕРАПИИ | 2014 |
|
RU2729118C2 |
| ФУНКЦИОНАЛИЗИРОВАННЫЕ ЭРИТРОИДНЫЕ КЛЕТКИ | 2018 |
|
RU2779315C2 |
| ИНДУКТОР ИММУНИТЕТА | 2016 |
|
RU2835947C2 |
| ИНДУКТОР ИММУНИТЕТА | 2016 |
|
RU2758112C2 |
| ТЕРАПЕВТИЧЕСКАЯ ПРОТИВОРАКОВАЯ НЕОЭПИТОПНАЯ ВАКЦИНА | 2017 |
|
RU2782422C2 |
| НЕОАНТИГЕНЫ И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2017 |
|
RU2773273C2 |
| РЕКОМБИНАНТНЫЕ МОЛЕКУЛЫ pMHC КЛАССА II | 2017 |
|
RU2777115C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ПОЛУЧЕНИЯ КОМПОЗИЦИЙ T-КЛЕТОК И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2835034C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ПРОМЫШЛЕННЫХ ПРОДУКТОВ ИЗ РАСТИТЕЛЬНЫХ ЛИПИДОВ | 2015 |
|
RU2743384C2 |
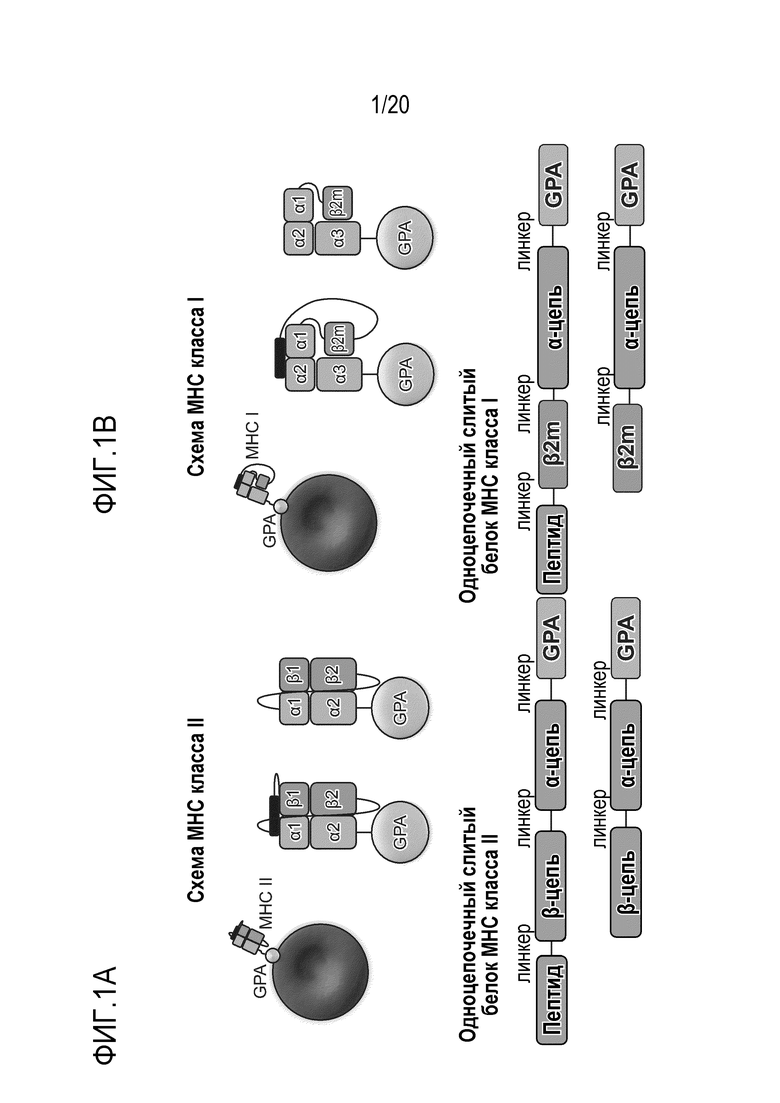

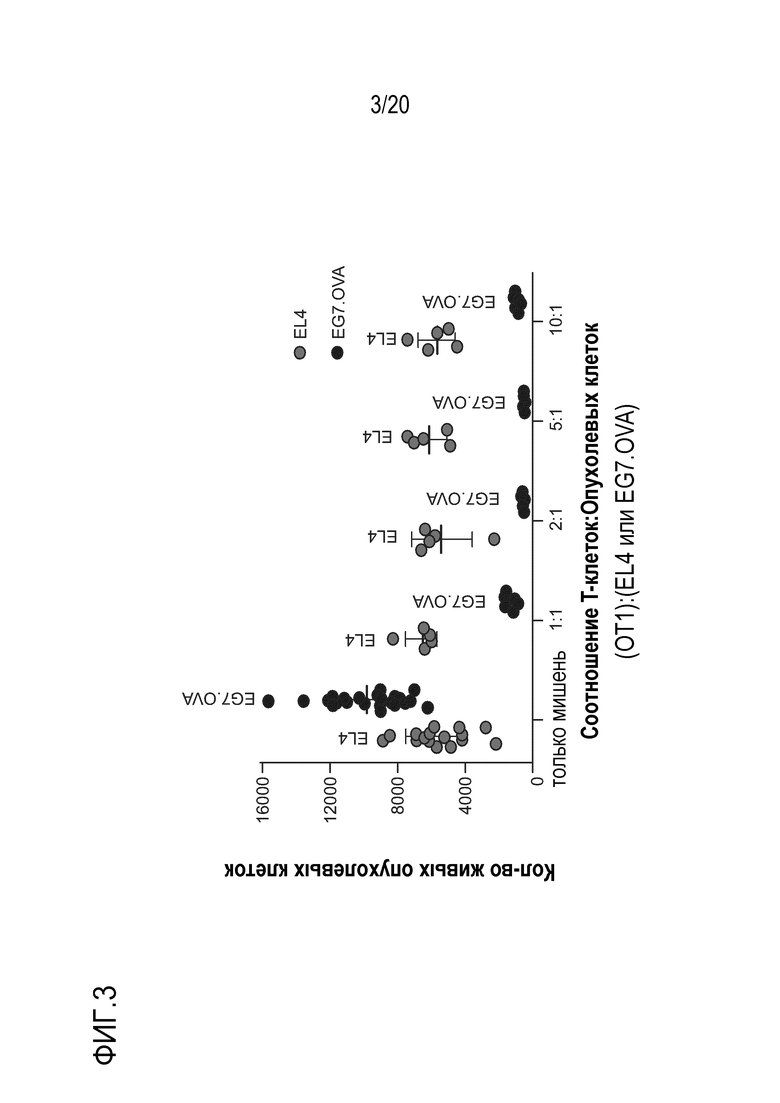
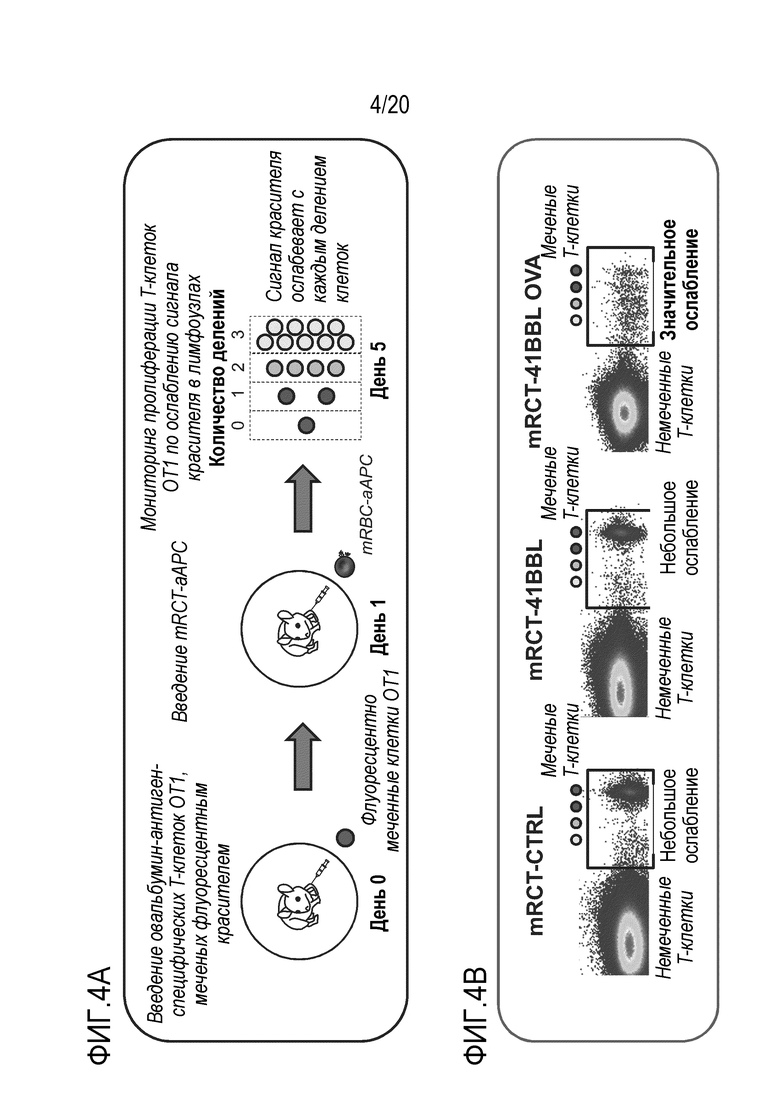

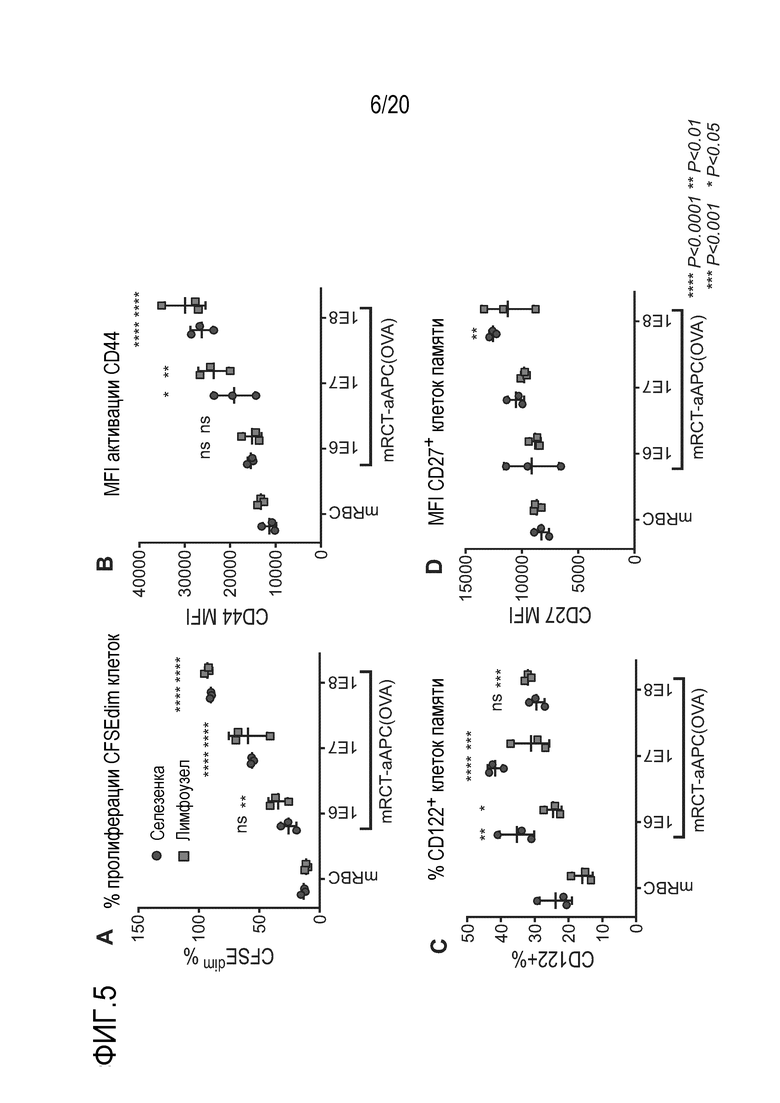
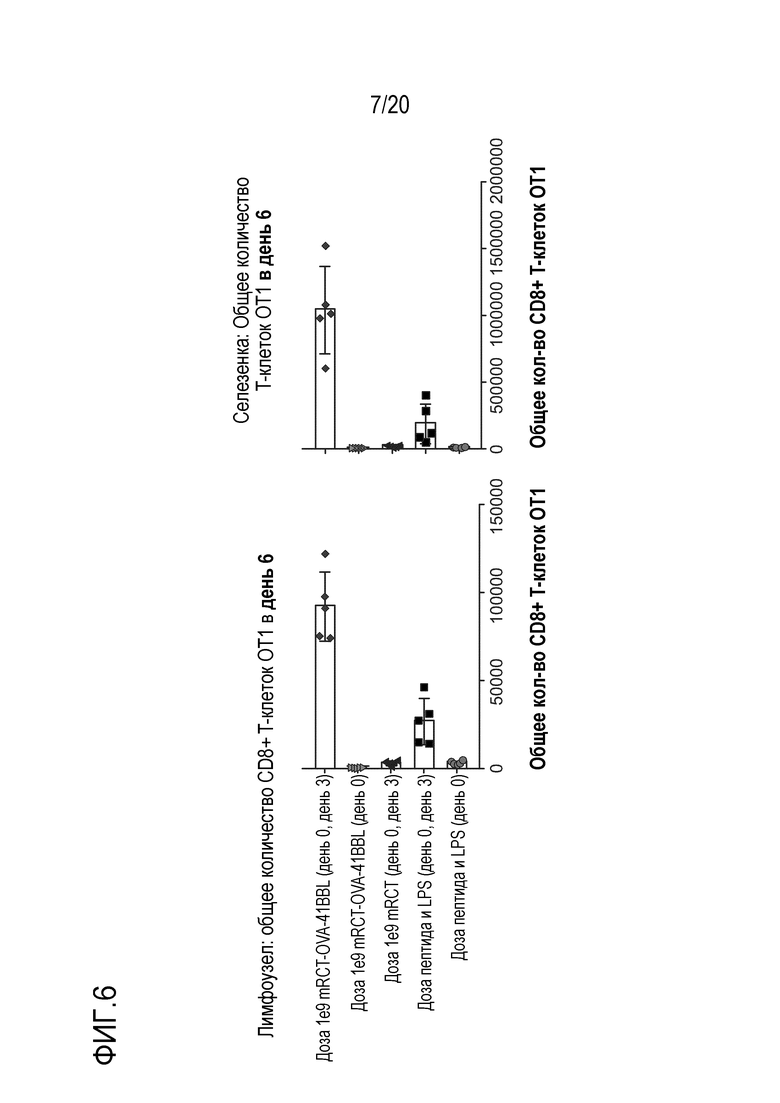
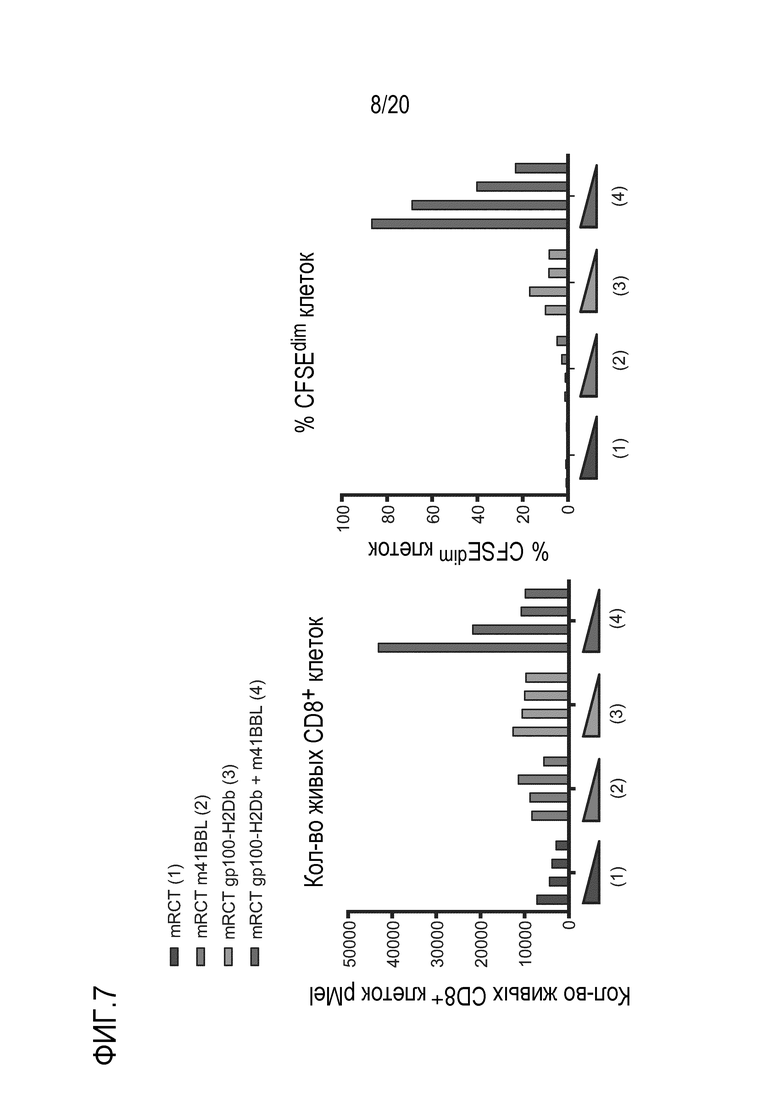
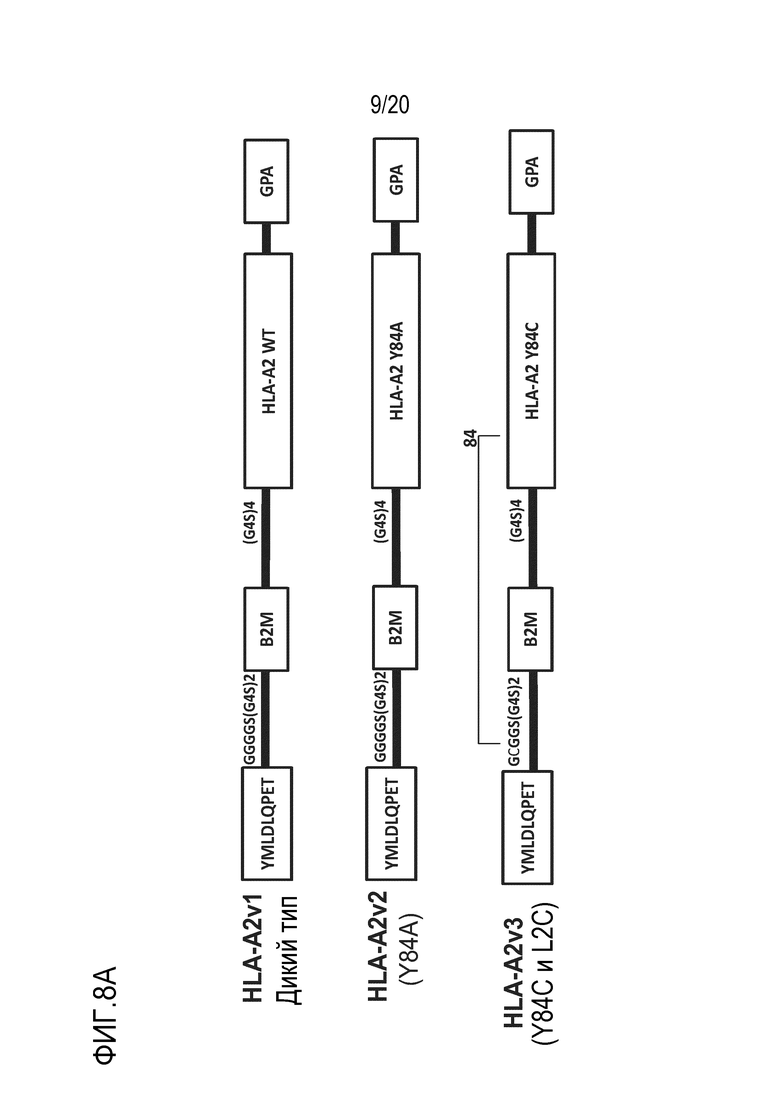



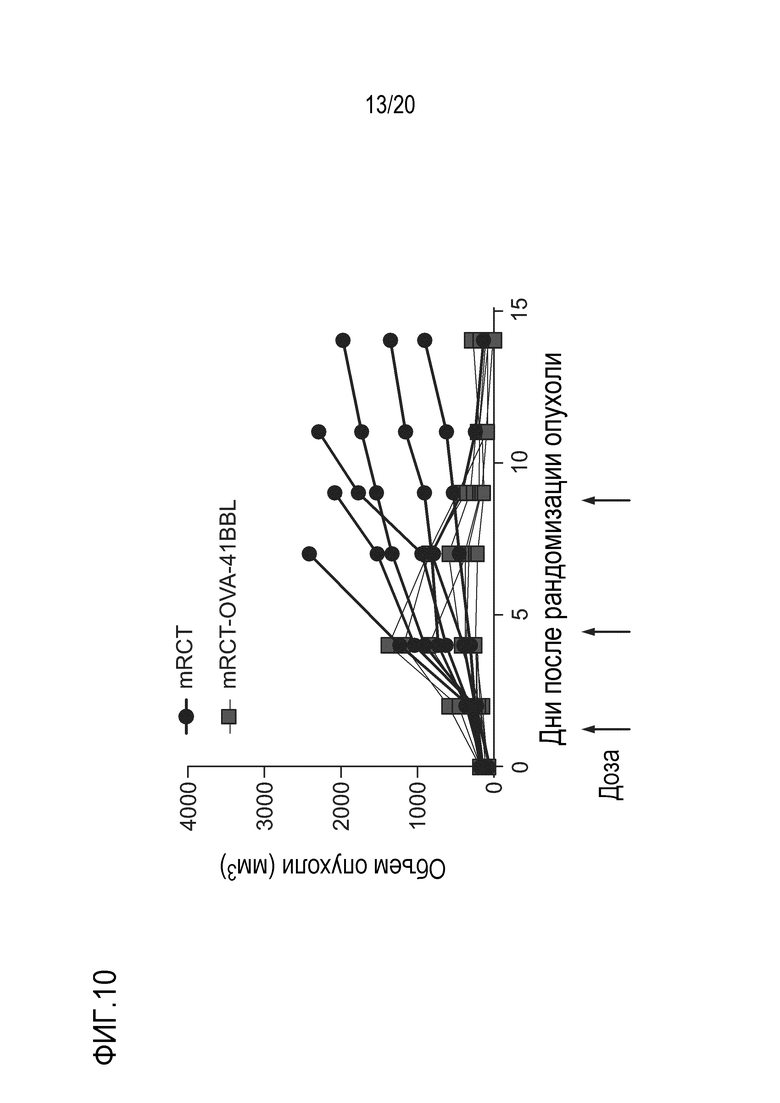

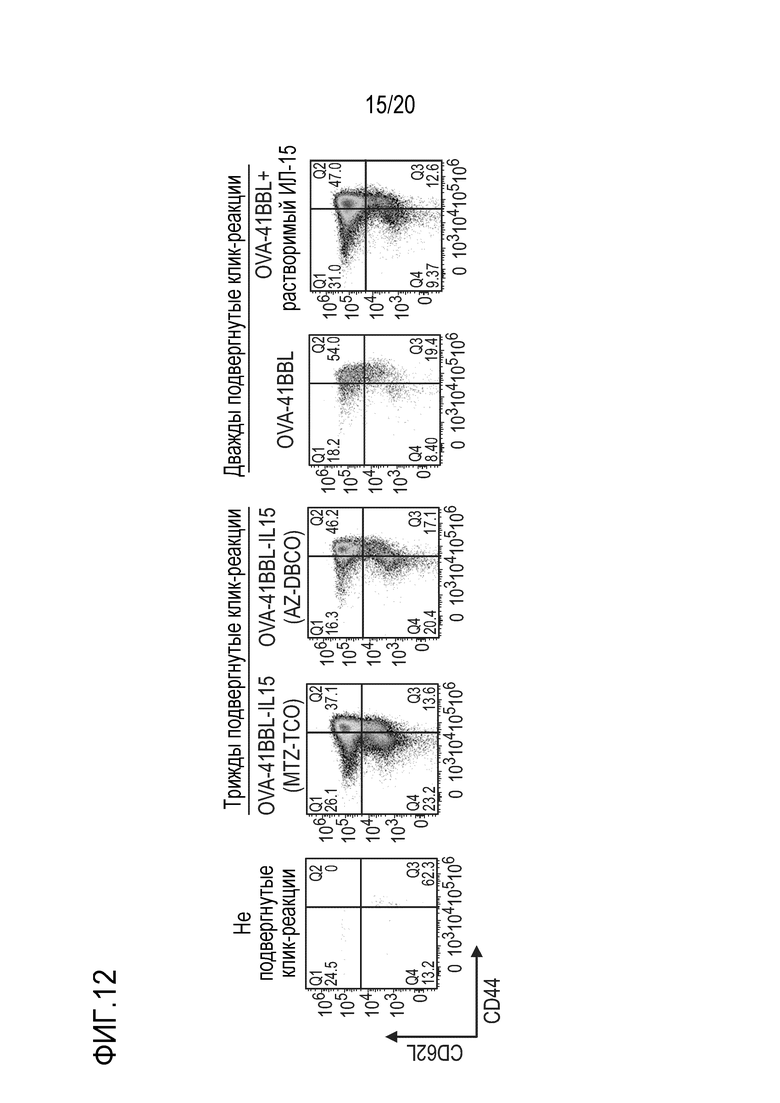

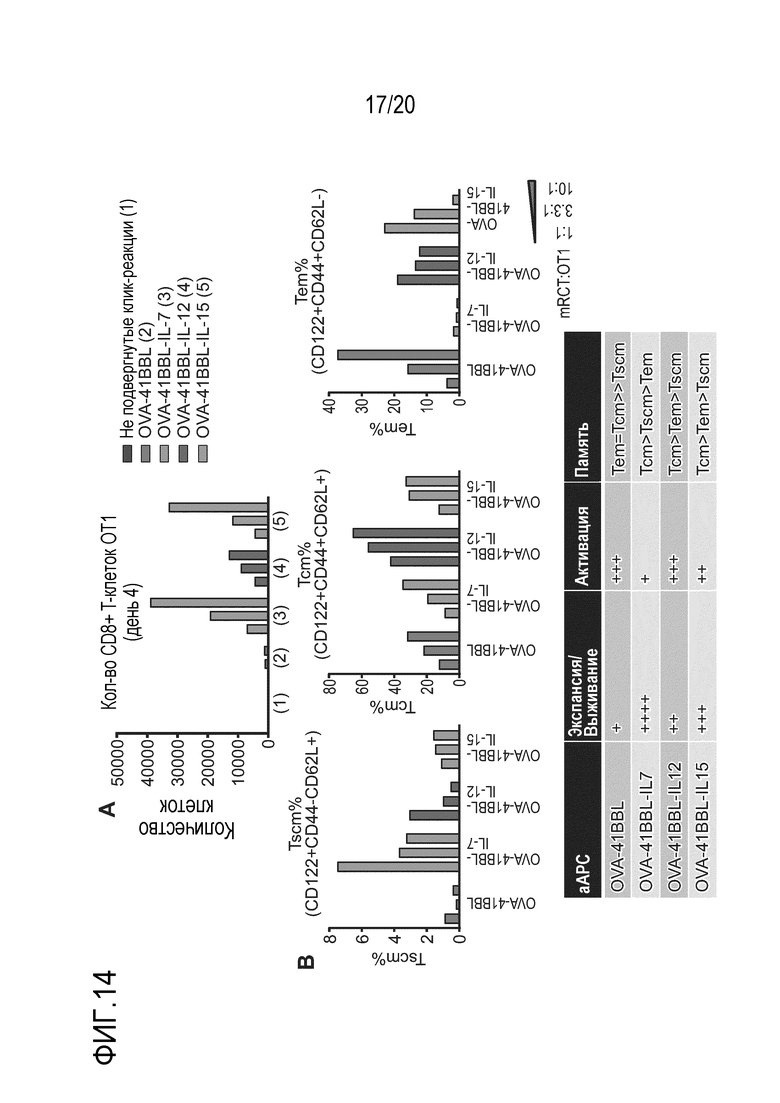
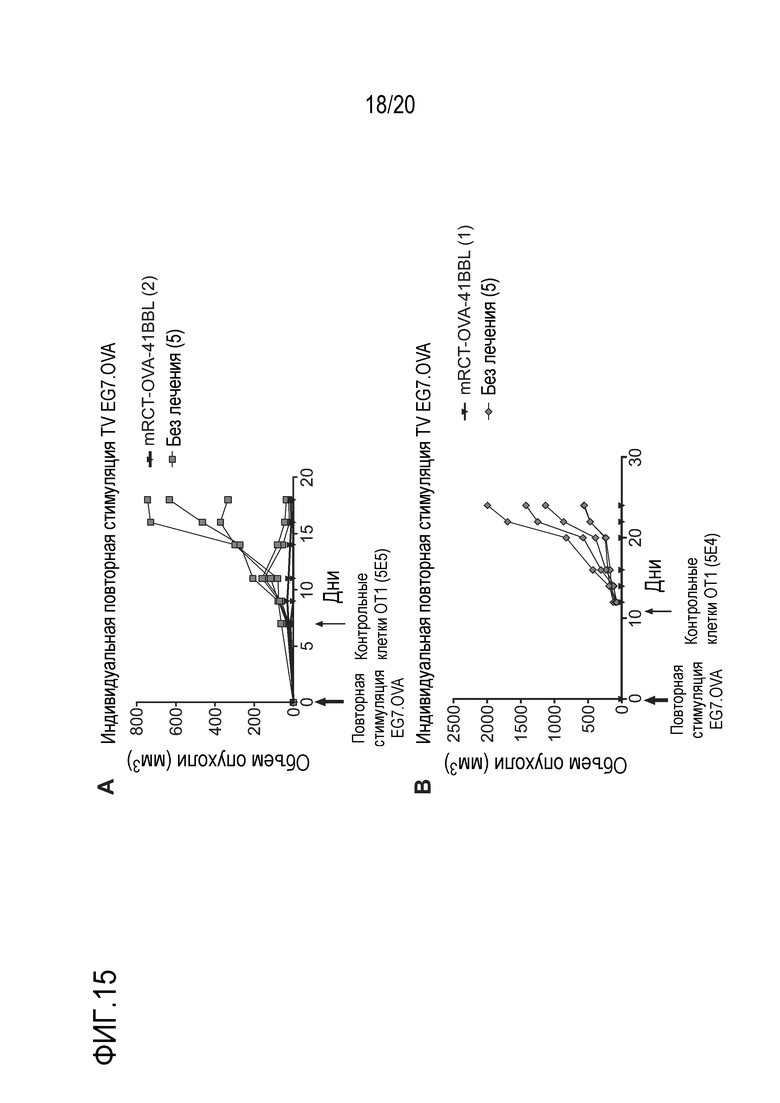

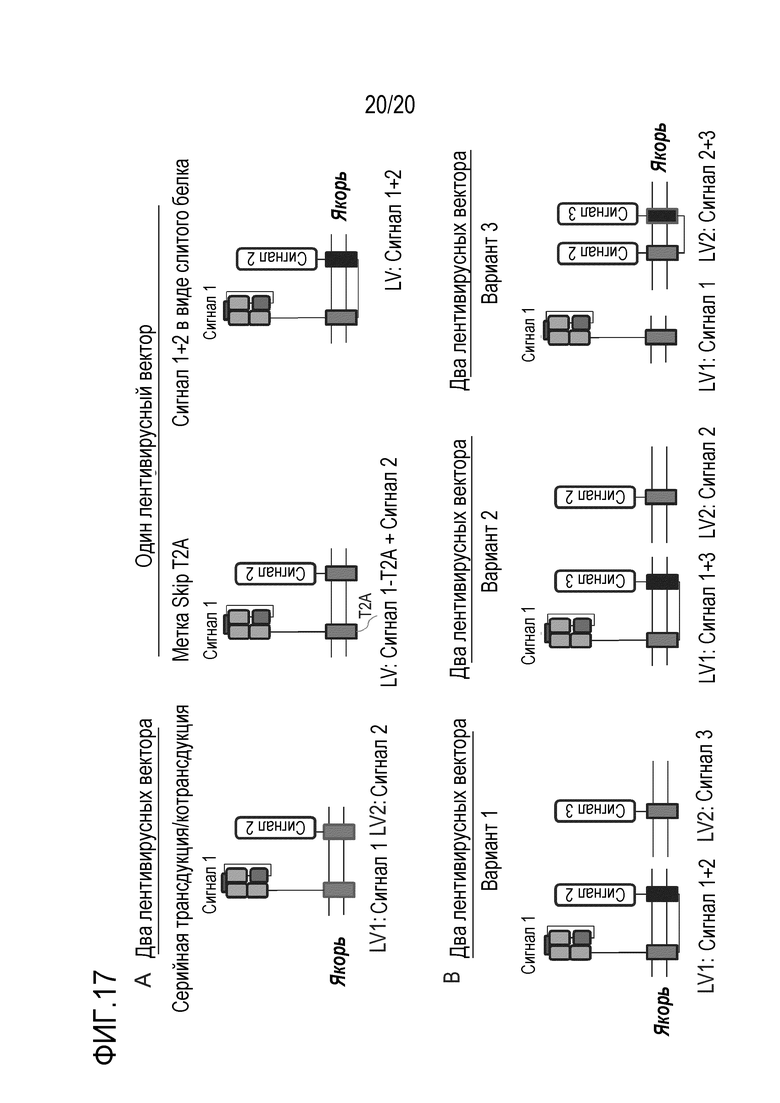
Изобретение относится к области биотехнологии, в частности к искусственной антигенпрезентирующей клетке (aAPC), а также к способу ее получения. Также раскрыто применение вышеуказанной клетки в способе активации антигенспецифической T-клетки, способе индуцирования пролиферации T-клетки, способе экспансии субпопуляции из популяции T-клеток, а также в способе индуцирования T-клеточного ответа на антиген HPV-E7. Изобретение эффективно для лечения индивидуума, имеющего HPV-положительное злокачественное новообразование. 7 н. и 27 з.п. ф-лы, 17 ил., 29 табл., 27 пр.
1. Искусственная антигенпрезентирующая клетка (aAPC) для применения в лечении индивидуума, имеющего HPV-положительное злокачественное новообразование, где aAPC включает безъядерную эритроидную клетку, где безъядерная эритроидная клетка содержит на своей поверхности слитый полипептид, содержащий экзогенный антигенпрезентирующий полипептид, соединенный с экзогенным антигенным полипептидом, где экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2, содержащим α-цепь, цепь β2-микроглобулина (β2m) и мембранный якорь, и где экзогенный антигенный полипептид содержит антиген E7 вируса папилломы человека (HPV).
2. aAPC по п. 1, где антиген Е7 HPV содержит SEQ ID NO: 713, SEQ ID NO: 714 или SEQ ID NO: 712.
3. aAPC по п. 1 или 2, где антиген E7 HPV содержит SEQ ID NO: 713.
4. aAPC по любому из пп. 1-3, где β2m-цепь содержит SEQ ID NO: 839.
5. aAPC по любому из пп. 1-4, где экзогенный антигенный полипептид соединен с β2m-цепью через линкер.
6. aAPC по п. 5, где линкер содержит SEQ ID NO: 732.
7. aAPC по любому из пп. 1-6, где экзогенный антигенпрезентирующий полипептид содержит полипептид аллеля HLA-A2*02:01.
8. aAPC по п. 7, где полипептид аллеля HLA-A2*02:01 содержит замену L2C, Y84A или Y84C.
9. aAPC по п. 7, где полипептид аллеля HLA-A2*02:01 содержит SEQ ID NO: 840, 841 или 842.
10. aAPC по любому из пп. 1-9, где α-цепь соединена с β2m-цепью через линкер.
11. aAPC по п. 10, где линкер содержит SEQ ID NO: 733.
12. aAPC по п. 10, где α-цепь соединена с мембранным якорем через линкер.
13. aAPC по п. 12, где ликер содержит SEQ ID NO: 734.
14. aAPC по любому из пп. 1-13, где мембранный якорь содержит трансмембранный домен гликофорина A (GPA) или трансмембранный домен небольшого интегрального мембранного белка 1 (SMIM1).
15. aAPC по п. 14, где мембранный якорь содержит трансмембранный домен GPA.
16. aAPC по п. 15, где мембранный якорь содержит SEQ ID NO: 728.
17. aAPC по любому из пп. 1-16, где слитый полипептид содержит последовательность, которая по меньшей мере на 90% идентична SEQ ID NO: 846.
18. aAPC по любому из пп. 1-17, где aAPC дополнительно содержит на своей поверхности по меньшей мере один экзогенный костимуляторный полипептид.
19. aAPC по п. 18, где по меньшей мере один экзогенный костимуляторный полипептид выбирают из группы, состоящей из 4-1BBL, LIGHT, антитела против CD28 или фрагмента антитела, CD80, CD86, CD70, OX40L, GITRL, TIM4, SLAM, CD48, CD58, CD83, CD155, CD112, ИЛ-15Rα, слитого с ИЛ-15, ИЛ-21, ICAM-1, лиганда LFA-1, антитела против CD3 или фрагмента антитела и их комбинации.
20. aAPC по п. 18 или 19, где по меньшей мере один экзогенный костимуляторный полипептид слит с мембранным якорем.
21. aAPC по п. 20, где мембранный якорь содержит трансмембранный домен GPA или трансмембранный домен SMIM1.
22. aAPC по любому из пп. 1-21, где aAPC дополнительно содержит на своей поверхности по меньшей мере один экзогенный цитокиновый полипептид.
23. aAPC по п. 22, где по меньшей мере один экзогенный цитокиновый полипептид выбран из группы, состоящей из: ИЛ-2, ИЛ-15, 15Rα, слитого с ИЛ-15, ИЛ-7, ИЛ-12, ИЛ-18, ИЛ-21, ИЛ-4, ИЛ-6, ИЛ-23, ИЛ-27, ИЛ-17, ИЛ-10, TGF-бета, ИФН-гамма, ИЛ-1 бета, ГМ-КСФ и ИЛ-25.
24. aAPC по п. 22 или 23, где по меньшей мере один экзогенный цитокиновый полипептид слит с мембранным якорем.
25. aAPC по п. 24, где мембранный якорь содержит трансмембранный домен GPA или трансмембранный домен SMIM1.
26. aAPC по любому из пп. 1-25, где aAPC содержит экзогенный цитокиновый полипептид 4-1BBL и экзогенный цитокиновый полипептид IL-12.
27. Способ активации антигенспецифической T-клетки, включающий приведение T-клетки в контакт с aAPC по любому из пп. 1-26 и, таким образом, активацию антигенспецифической T-клетки.
28. Способ индуцирования пролиферации T-клетки, экспрессирующей рецепторную молекулу, включающий приведение T-клетки в контакт с aAPC по любому из пп. 18-21, где по меньшей мере один костимуляторный полипептид специфически связывается с рецепторной молекулой, и, таким образом, индуцирование пролиферации T-клетки.
29. Способ экспансии субпопуляции из популяции T-клеток, включающий приведение популяции T-клеток, содержащей по меньшей мере одну T-клетку из субпопуляции, в контакт с aAPC по любому из пп. 18-21, где по меньшей мере один экзогенный костимуляторный полипептид, содержащийся на поверхности aAPC, специфически связывается с рецепторной молекулой по меньшей мере на одной T-клетке из субпопуляции, и где связывание по меньшей мере одного экзогенного костимуляторного полипептида с рецепторной молекулой индуцирует пролиферацию по меньшей мере одной T-клетки из субпопуляции, и, таким образом, экспансию субпопуляции из популяции T-клеток.
30. Способ лечения индивидуума, имеющего HPV-положительное злокачественное новообразование, включающий приведение T-клетки индивидуума в контакт с aAPC по любому из пп. 1-26 и, таким образом, лечение индивидуума.
31. Способ по любому из пп. 27-29, где приведение в контакт осуществляют in vitro или in vivo.
32. Способ по п. 30, где HPV-положительное злокачественное новообразование выбирают из группы, состоящей из рака шейки матки, рака головы и шеи и рака анального канала.
33. Способ индуцирования T-клеточного ответа на антиген HPV-E7 у нуждающегося в этом индивидуума, включающий:
получение популяции клеток из индивидуума, где популяция клеток включает T-клетку,
приведение популяции клеток в контакт с aAPC по любому из пп. 1-26, где приведение популяции клеток в контакт с aAPC индуцирует пролиферацию антигенспецифической T-клетки, являющейся специфической в отношении антигена HPV-E7, и
введение индивидууму антигенспецифической T-клетки,
таким образом, индуцирование T-клеточного ответа на антиген HPV-E7 у нуждающегося в этом индивидуума.
34. Способ получения aAPC по любому из пп. 1-26, включающий:
встраивание экзогенной нуклеиновой кислоты, кодирующей слитый полипептид, в ядросодержащую эритроидную клетку-предшественника, где слитый полипептид содержит экзогенный антигенпрезентирующий полипептид, соединенный с экзогенным антигенным полипептидом, где экзогенный антигенпрезентирующий полипептид является одноцепочечным слитым белком MHC класса I HLA-A2, содержащим α-цепь, цепь β2-микроглобулина (β2m) и мембранный якорь, и где экзогенный антигенный полипептид содержит антиген E7 вируса папилломы человека (HPV); и
культивирование ядросодержащей эритроидной клетки-предшественника в условиях, подходящих для энуклеации и продукции экзогенного антигенного полипептида, и, таким образом, получение безъядерной эритроидной клетки,
таким образом, получение aAPC.
| US 2016082046 A1, 24.03.2016 | |||
| WO 2015153102 A1, 13.03.2015 | |||
| KWONG Y | |||
| TSANG et al | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| TZU-YU LIU et al | |||
| Advances in Peptide-based Human Papillomavirus Therapeutic Vaccines, | |||
Авторы
Даты
2022-01-11—Публикация
2018-12-22—Подача