Область техники
Изобретение относится к биотехнологии, иммунологии и вирусологии. Создана фармацевтическая композиция для индукции специфического иммунитета против вируса острого респираторного синдрома SARS-CoV-2, содержащая нуклеокапсидный белок NSARS-CoV-2, имеющий аминокислотную последовательность SEQ ID NO: 1, в количестве от 20 до
100 мкг/мл и фармацевтически приемлемые вспомогательные вещества, выбранные из группы, включающей буферные агенты, поверхностно-активные вещества, адъювант, изотонический агент в фармацевтически приемлемых количествах.
Предшествующий уровень техники
В 2019 г. в Китае был обнаружен новый одноцепочечный РНК-содержащий вирус, относящимся к семейству Coronaviridae, к линии Beta-CoV B. Новый коронавирус быстро распространился по всем континентам, вызывая тяжелые состояния: вирусную пневмонию, сосудистые нарушения, усугубление хронических заболеваний. В феврале 2020 г. Всемирная Организация Здравоохранения (ВОЗ) присвоила новому вирусу официальное название SARS-CoV-2, а болезнь в случае этого вируса - название COVID-19 («Coronavirusdisease 2019»).
В настоящее время проблема профилактики инфекции коронавируса SARS-CoV-2 является большой проблемой, т.к. эффективного лекарственного средства до сих пор не разработано. Основным профилактическим средством в случае вирусных инфекцией является вакцина – средство, включающее антиген, который вызывает иммунную реакцию организма и приводит к индукции более сильного вторичного иммунного ответа. Таким образом, вакцинированный пациент либо не заражается инфекцией либо в организме происходит реакция быстрой элиминации вируса, что позволяет в этом случае переносить заболевание в более легкой форме.
Известны различные композиции вакцин для индукции иммунного ответа в случае коронавирусных инфекций нового типа.
Так, например, согласно патенту RU 2709659 известно иммунобиологическое средство на основе рекомбинантного аденовируса человека 5-го серотипа или рекомбинантного аденовируса человека 26-го серотипа, содержащее оптимизированную под экспрессию в клетках млекопитающих консенсусную последовательность полного протективного антигена S коронавируса на основании последовательностей генов белка S современных штаммов вируса 2015-2017 гг. с определенной последовательностью.
Также из патента US 10953089 известна вакцина, включающая наночастицы с гликопротеином S коронавируса SARS-CoV-2 и ядро из неионогенное ПАВ, а также буфер и адъювант на основе сапонина. Предлагаемые частицы обладают стабильностью и лучшей презентацией эпитопа антигена.
Патент CN111944064 описывает вакцину, включающую белок S-S-RBD, белок домена сборки, сигнальные белки, а также адъювант на основе сквалена. Полученная композиция представляет собой наноэмульсию «вода-в-масле».
Таким образом, техническая задача состоит в разработке и получении стабильной композиции, способной при ее введении в организм вызывать иммунный ответ и индуцировать специфический иммунитет против SARS-CoV-2. Поставленная задача решается получением композиции, содержащей нуклеокапсидный белок N SARS-CoV-2, имеющий аминокислотную последовательность SEQ ID NO: 1, в количестве от 20 до 100 мкг/мл и фармацевтически приемлемые вспомогательные вещества, выбранные из группы, включающей буферные агенты, поверхностно-активные вещества, адъювант, изотонические агенты в фармацевтически приемлемых количествах. При этом полученная композиция обладает стабильностью, способностью вызывать стойкий и длительный иммунный ответ, с высоким титром антител к инфекции коронавируса SARS-CoV-2, а также композицию можно достаточно просто получить с технологической точки зрения.
Описание фигур
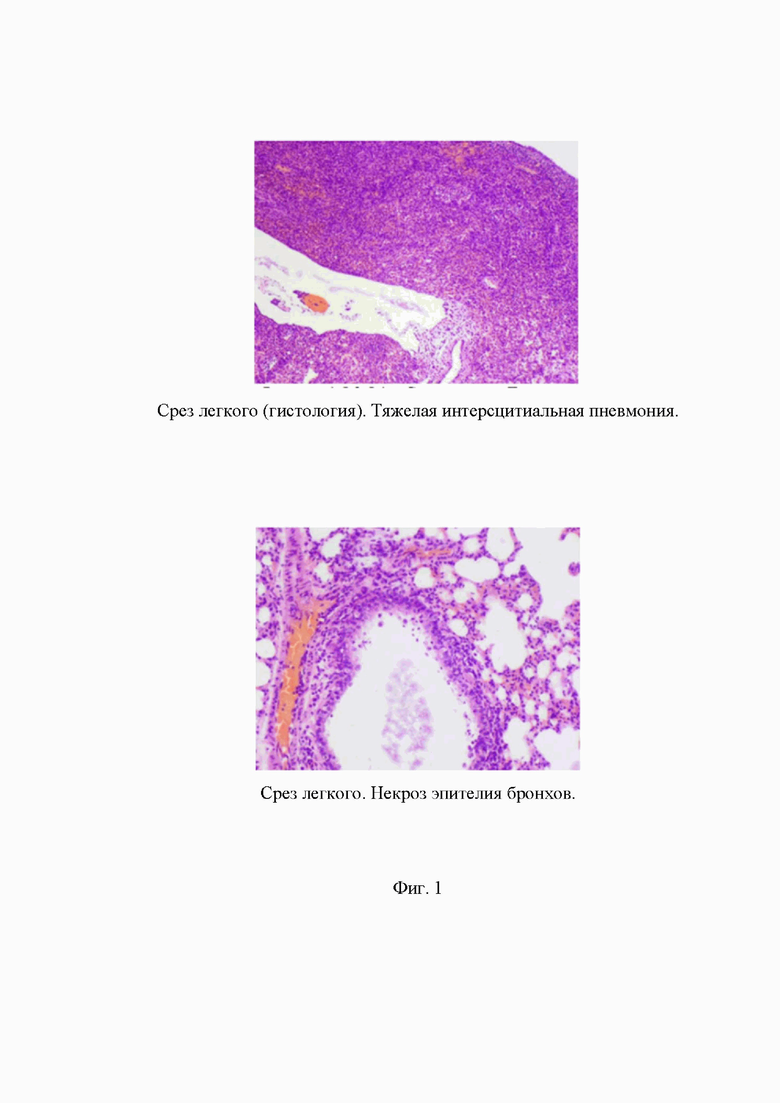
На Фиг. 1 представлены примеры выявленных изменений в легком: показано развитие тяжелой интерстициальной пневмонии и некроз эпителия, при исследовании согласно примеру 7, группа 8.
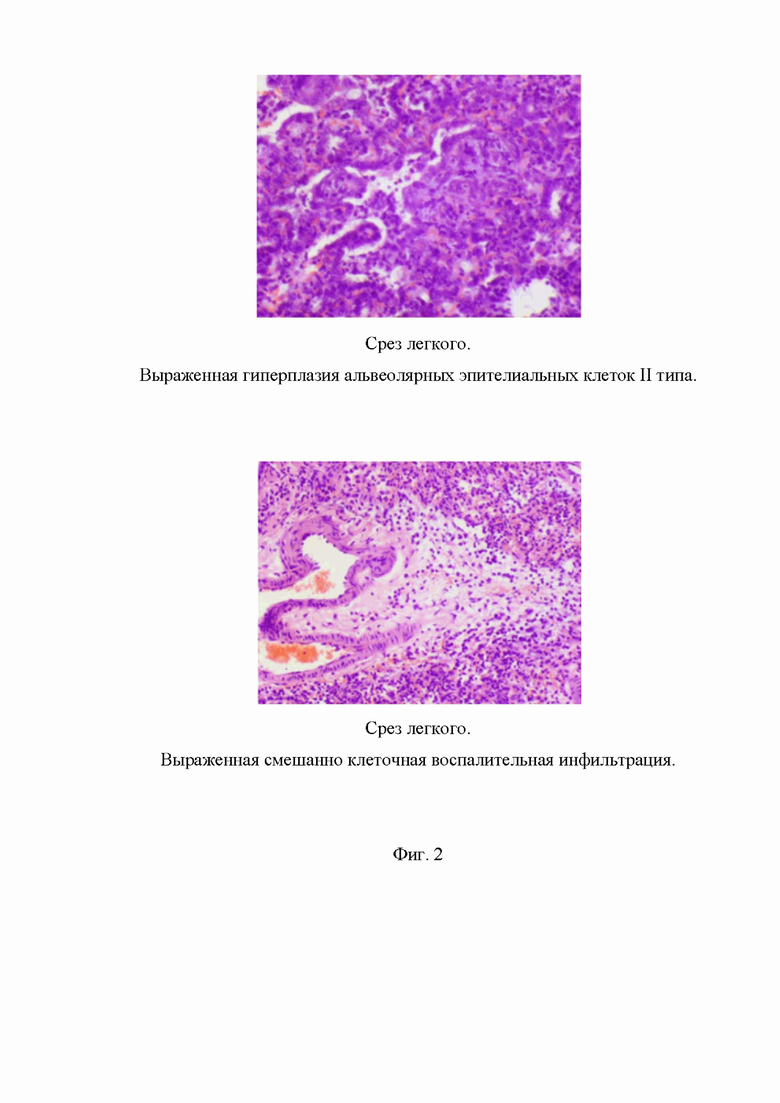
На Фиг. 2 представлены примеры выявленных изменений легких: показаны выраженные гиперплазия альвеолярных эпителиальных клеток II типа, а также смешанная выраженная смешанно клеточная воспалительная инфильтрация, при исследовании согласно примеру 7, группа 8.
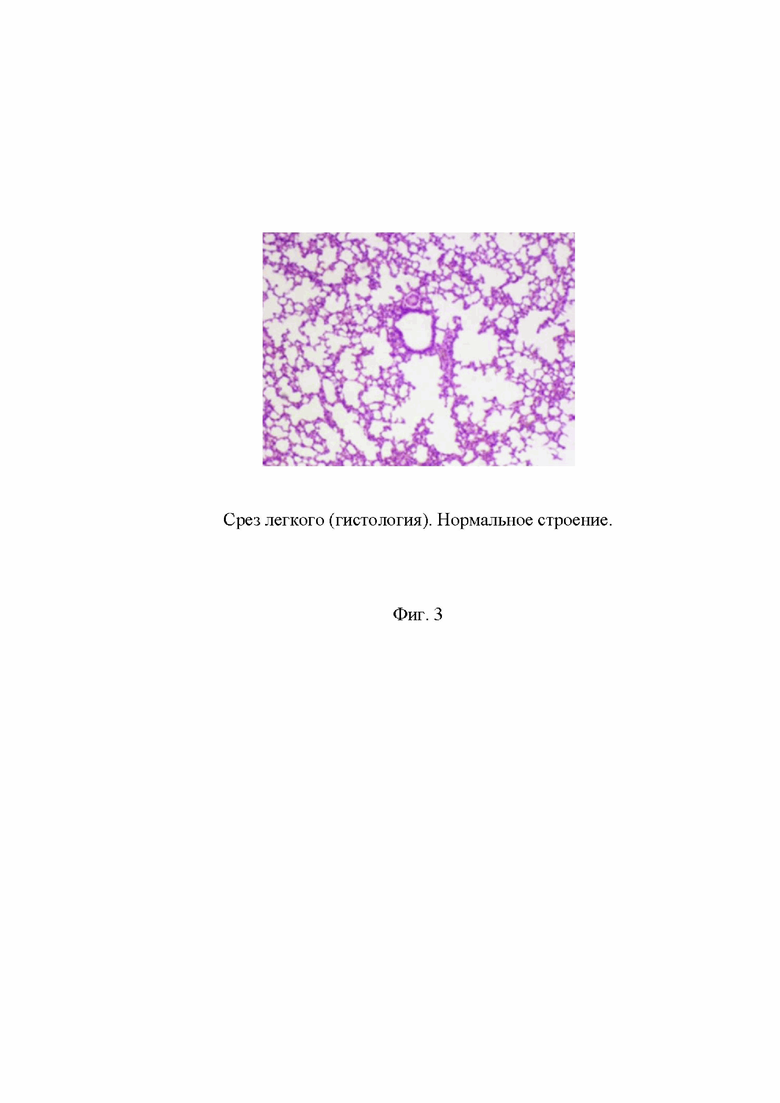
На Фиг. 3 показано нормальное строение легкого, спустя 2 недели после выздоровления животных, при исследовании согласно примеру 7, группа 7.
Подробное описание изобретения
Вакцины, как правило, представляют собой композицию, включающую антиген в виде белка или смеси белков, а также вспомогательные веществ.
Антиген является фармацевтически активной субстанцией, ответственной за развитие иммунного ответа в организме пациента. Однако, по различным причинам, вводимый антиген может быть нестабильным, например, его невозможно хранить и технологически обрабатывать без потери активности в течение определенного времени, под воздействием окружающей среды. Кроме того, при введении в организм антиген может разрушаться под действием ферментов или иных веществ организма (например, среды кровотока).
Согласно настоящему изобретению, предложена фармацевтическая композиция, предназначенная для индукции специфического иммунного ответа против вируса острого респираторного синдрома SARS-CoV-2, содержащая нуклеокапсидный белок NSARS-CoV-2, имеющий аминокислотную последовательность SEQIDNO: 1, в количестве от 20 до 100 мкг/мл и фармацевтически приемлемые вспомогательные вещества, выбранные из группы, включающей буферные агенты, поверхностно-активные вещества, адъюванты, изотонические агенты. Данные вспомогательные вещества, как правило, содержатся в композиции в фармацевтически приемлемых количествах. В одном из вариантов реализации, композиция согласно изобретению содержит нуклеокапсидный белок NSARS-CoV-2, имеющий аминокислотную последовательность SEQ ID NO: 1, в количестве от 20 до 50 мкг/мл.
В еще одном варианте реализации композиция согласно изобретению в качестве адъюванта содержит токоферол, сквалан или их комбинацию. В другом варианте реализации композиция согласно изобретению может содержать в качестве буферных агентов любой фармацевтически приемлемый буфер, который может быть использован для поддержания рН около 7, например, фосфатно-солевой буфер, малеатный буфер, тетрабутиламмония буферный раствор, боратный буфер, HEPES буфер, трис(гидроксиметил)аминометана буферный раствор, или любой другой физиологически приемлемый буфер, используемый для поддержания рН в диапазоне 7-8, предпочтительно, в диапазоне 7,2-7,6.
Также композиция согласно изобретению может содержать фармацевтические приемлемые поверхностно-активные вещества (ПАВ), например, полисорбаты, твины, сорбитаны и другие подходящие ПАВ, например, лаурилсульфата натрия, диоктилсульфосукцината натрия, диоктилсульфоната натрия, хенодезоксихолевой кислоты, натриевой соли N-лаурилсаркозина, додецилсульфата лития, натриевой соли 1-октансульфокислоты, гидрата холата натрия, дезоксихолата натрия, натриевой соли гликодезоксихолевой кислоты, бензалконийхлорида илибензетонийхлорида, моногидрата цетилпиридинийхлорида, гексадецилтриметиламмония бромида,CHAPS, CHAPSO, SB3-10, SB3-12, дигитонина, Тритона Х-100, Тритона Х-114, лауромакрогола 400,полиоксил-40-стеарата, полиоксиэтилен гидрогенизированного касторового масла 10, 40, 50 и 60, моностеаратаглицерина, полисорбата 20, 40, 60, 65 и 80, лецитина из сои, DOPC, DMPG, DMPC и DOPG; эфира сахарозы и жирных кислот, метилцеллюлозы и карбоксиметилцеллюлозы. Предпочтительная концентрация ПАВ может составлять от 0,005 до 5% масс, или, например, 1-10 мг на 1 мл. Также в композиции могут содержаться изотонические агенты, например, калия хлорид, натрия хлорид. Изотонический агент действует не только для поддержания подходящего осмотического давления, но и может выполнять функции вспомогательного стабилизатора белка в жидкой форме иди лиофилизате. Примеры изотонического агента включают растворимые в воде неорганические соли, например, хлорид натрия, сульфат натрия, цитрат натрия, хлорид кальция и их комбинация. Наиболее предпочтительным является хлорид натрия. Предпочтительно концентрация изотонического агента составляет порядка от 5 до 200 мМ, или, например, 0,1-8,5 мг на мл. В пределах данного диапазона концентрация изотонического агента может регулироваться в соответствии с видами и количествами содержащихся компонентов, с тем чтобы жидкая композиция была изотонической.
Адъюванты представляют собой компоненты, используемые в композициях вакцин, которые потенцируют иммунный ответ на антиген, и/или модулирующий его с целью получения требуемого иммунного ответа. В качестве адъювантов могут использоваться минеральные соли, например, гели алюминия гидроксида и алюминия или кальция фосфата; препараты на основе масляных эмульсий и сурфактантов, например, MF59 (микросжиженный детергент, стабилизированный в эмульсии «масло в воде»), QS21 (очищенный сапонин), AS02 [SBAS2] (эмульсия «масло в воде» + MPL + QS-21), монтанид ISA-51 и ISA-720 (стабилизированная эмульсия «вода в масле»), дисперсные адъюванты, например, виросомы (однослойные липосомальные носители, включающие гемагглютинин гриппа), AS04 ([SBAS4] соль Al с MPL), ИСКОМы (структурный комплекс сапонинов и липидов), полилактид ко-гликолид (PLG), микробные производные (естественные и синтетические), например, монофосфориллипид A (MPL), детокс (MPL + скелет клеточной стенки M. phlei), AGP [RC-529] (синтетический ацилированный моносахарид), DC_Chol (липоидные иммуностимуляторы, способные к самоорганизации в липосомы), OM-174 (производное липида A), CpG-последовательности (синтетические олигонуклеотиды, содержащие CpG-последовательности с иммуностимулирующей активностью), токоферол, сквален и сквалан и их производные, модифицированные LT и CT (генетически модифицированные бактериальные токсины для обеспечения нетоксичного действия адъювантов), эндогенные иммуномодуляторы человека, например, ГМ-КСФ человека и ИЛ-12 человека (цитокины, которые можно вводить в виде белка или кодировать плазмидами), иммудаптин (C3d тандемный повтор), инертные носители, такие как частицы золота. В предпочтительном варианте реализации композиция согласно изобретению включает в качестве адъюванта α-токоферол, сквалан и их комбинации.
В предпочтительном варианте реализации композиция согласно изобретению имеет следующий состав на 1 мл:
В более предпочтительном варианте реализации композиция согласно изобретению имеет следующий состав на 1 мл:
Композиции согласно изобретению могут представлять собой раствор, эмульсию или лиофилизат. Лиофилизат может быть получен из раствора или эмульсии стандартными для этого способами, например из раствора при лиофилизации.
Композиция согласно изобретению может применяться для профилактики или индукции специфического иммунитета против вируса острого респираторного синдрома SARS-CoV-2, т.е. использоваться в качестве вакцины. При этом содержание белка N в композиции согласно изобретению может варьироваться в зависимости от требуемой дозы для вакцинации, возраста пациента и других клинических факторов.
Применение указанной композиции для профилактики против вируса острого респираторного синдрома SARS-CoV-2 включает однократно или двукратно введение композиции. Решение об однократном или двукратном введении принимает терапевт, с учетом возраста, анамнеза пациента, наличия хронических заболеваний и иных клинических факторов. В случае двукратного введения композиция может вводиться 2 раза последовательно с интервалом не менее 2 недель, с одинаковым или различным содержанием нуклеокапсидного белка N в композиции.
Далее изобретение также предлагает способ получения композиции, содержащей белок N, который включает:
1) обеспечение нуклеокапсидного белка NSARS-CoV-2, имеющего аминокислотную последовательность SEQ ID NO: 1, в количестве от 20 до 100 мкг/мл;
2) растворение белка в водном растворителе и доведение содержания белка N в растворе до требуемой концентрации;
3) приготовление водного раствора адъюванта;
4) смешение водного раствора, содержащего белок N, и водного раствора адъюванта;
5) гомогенизация полученной смеси до получения однородного по цвету раствора;
6) регулирование полученного композиции рН до 7,2-7,6.
В одном из вариантов реализации способ получения композиции может дополнительно включать лиофилизацию полученной композиции с получением лиофилизата, используемого для восстановления растворителем перед введением пациенту. В некоторых вариантах реализация полученная композиция представляет собой эмульсию, например, типа «вода-в-масле», или «масло-в-воде».
Далее композиция согласно изобретению будет описана в примерах, которые не предназначены для ограничения объема настоящего изобретения.
Примеры
Пример 1
Получение плазмиды, содержащей ген белка
Плазмиду, содержащую ген белка N (Genbank YP_009724397.2), использовали для получения модифицированной оптимизированной по кодонам нуклеотидной последовательности с использованием CodonAdaptationIndex (http://genomes.urv.es/OPTIMIZER/). Кодоны выбраны таким образом, чтобы по возможности использовались наиболее часто встречающиеся у E. coli кодоны, а также содержание нуклеотидов гуанин и цитозин был в диапазоне 50-55%. Последовательность на 5’ и 3’ концах фланкировалась последовательностями для распознавания эндонуклеазами NcoI (CCATGG) и XhoI (CTCGAG), соответственно. Синтез гена и клонирование по указанным сайтам рестрикции в плазмиду без вставки pET-28a(+) были заказаны на коммерческой основе. Полученную плазмиду секвенировали с помощью праймеров T7_promotor (TAATACGACTCACTATAGGG), fwd_122 (GCCTTATGGTGCAAATAAGG) и fwd_300 (AAACATTGGCCGCAGATTGC) для подтверждения нуклеотидной последовательности и проверки на однонуклеотидные мутации.
Нуклеотидная последовательность соответствовала последовательности
SEQ ID NO:2.
Пример 2
Получение клеточной линии E. coli, модифицированной плазмидой
Клеточную линию E. coli трансформировали по следующему протоколу. Пробирку с компетентными клетками извлекали из морозильной камеры хранения на -80°C. Давали оттаять льду в течение 10 мин. Далее вносили
1 мкл, содержащий 1 пкг-100 нг плазмиды. Аккуратно перемешивали пробирку 4-5 раз. Полученную смесь помещали на лёд на 30 мин. Далее смесь подвергали тепловому шоку при 42°C на 30-60 c. Полученную обработанную смесь помещали на лёд на 5 мин. Вносили 950 мкл среды SOC при комнатной температуре. Инкубировали при 30°C-37°C в течение 1 - 2 ч при перемешивании 250 оборотов в минуту. Высевали 10-50 мкл на чашку с твердой селективной средой, содержащей антибиотик канамицин. Инкубировали при 30°C-37°C в течение ночи. Выросшие колонии содержат клетки E. coli, трансформированные плазмидой, несущей искусственный ген нуклеокапсидного белка N.
Таким образом получали клеточную линию E. coli с включением искусственного гена согласно изобретению.
Данная клеточная линия была депонирована во ФГБНУ «Всероссийский научно-исследовательский институт сельско-хозяйственной микробиологии (ФГБНУ ВНИИСХМ) под номером RCAM05390 (от 14.05.2021 г.).
Пример 3
Получение рекомбинантного белка N SARS-CoV-2
Биомассу E. coli, содержащую экспрессированный белок N, ресуспендировали в буфере для лизиса (Трис-HCl 50 мM, pH 9) и гомогенизировали с помощью лабораторного гомогенизатора, например, GEA Panda 1000. Все буферы, кроме буферов для хроматографии на третьей стадии очистки, содержали ингибиторы протеаз ЭДТА и ФМСФ. Затем нерастворимую фракцию биомолекул осаждали центрифугированием при 20000 x g, 4°C, 30 мин. Растворимую фракцию переносили в чистую посуду, и к ней добавляли 20% (по массе на объем) сульфата аммония для осаждения белка N. Осажденную фракцию собирали центрифугированием при 20000 x g, 4°C, 30 мин, с последующим растворением в буфере Трис-HCl 50 мM, pH 9. После фильтрации через мембрану с диаметром пор 0,22 мкм раствор использовали для хроматографической очистки. Первую стадию очистки на анион-обменной хроматографии проводили в режиме проскока (буфер Трис-HCl 50 мM, pH 9). Вторую стадию очистки на катион-обменной хроматографии проводили в режиме захвата с элюцией градиентом NaCl от 0 M до 1 M (буфер Трис-HCl 50 мM, pH 9). Третью стадию очистки на гидрофобной хроматографии проводили в режиме захвата с элюцией градиентом сульфата аммония от 1 M до 0 M (буфер NaH2PO4 50 мM, pH 7,5).
Далее проводили процесс диализа в диализных кассетах в 5 л фосфатно-солевом буфере. Процесс проходил при комнатной температуре в течение 2 ч. Затем проводили замену буфера на 5 л свежего буфера и проводили процесс при +4°С в течение 10 ч.
После окончания диализа белок извлекали из диализных кассет и фильтровали. Полученный осадок растворяли в воде для инъекций для получения лиофилизата или полученный раствор белка доводили до нужной концентрации белка путем добавления ранее полученного лиофилизата.
Полученный раствор исследовали по следующим показателям: содержание белка, рН, механические включения, прозрачность, стерильность, размер частиц. Для этого использовали стандартные методики анализа.
Пример 4
Приготовление композиции согласно изобретению
Получали водный раствор, содержащий белок N, полученный согласно примеру 3, с различными концентрациями белка: 20 мкг/мл, 30 мкг/мл, 40 мкг/мл, 50 мкг/мл, 60 мкг/мл, 70 мкг/мл, 80 мкг/мл, 90 мкг/мл, 100 мкг/мл.
В отдельную емкость помещали в зависимости от содержания белка рассчитанное количество токоферола, сквалана и полисорбата 80, частями добавляли фосфатно-солевой буфер, при постоянном перемешивании. Например, при содержании 20 мкг/мл использовали 45 г токоферола, 15 г полисорбата 80, и 15 г сквалана и 750 мл буферного раствора. После растворения полученный раствор (раствор адъюванта) разделяли на равные части и обрабатывали ультразвуком. Затем обработанные растворы объединяли в один стакан и перемешивали. Далее проводили фильтрацию раствора через мембрану 0,22 мкм. Полученный отфильтрованный раствор объединяли с растворов белка N и перемешивали до гомогенного раствора.
В некоторых случаях образовывалась эмульсия белого или желтоватого цвета.
Полученный раствор, содержащий белок N и адъювант, доводили до
рН 7,2-7,6 раствором гидроксида натрия или хлороводородной кислотой. Далее, полученный раствор разливали по стерильным флаконам и закупоривали. При необходимости, из раствора получали лиофилизат путем лиофилизации в аппарате. Для восстановления раствора для вакцинирования использовали воду для инъекций или стерильный физиологический раствор.
Пример 5
Анализ свойств композиций согласно изобретению
Для исследования свойств композиции согласно изобретению были получены следующие составы (представлены в таблице ниже).
Таблица 1
Композиции с различным содержанием белка, полученные согласно примеру 5, исследовали на стабильность перед началом исследования и по истечении 6 недель хранения в стресс-условиях (условия «ускоренного хранения»). Перед началом исследования измеряли рН, содержание белка, визуально оценивали прозрачность, гомогенность, если композиция представлял собой эмульсию. Композиции с различным содержанием нуклеокапсидного белка N разливали по стерильным флаконам, закупоривали и помещали в камеру ускоренного хранения для испытания на стабильность. В камере поддерживали температуру +20°С в течение 6 недель. По истечении времени флаконы извлекали и проводили анализ на рН и содержание белка нуклеокапсидного N. Измерение рН проводили непосредственно в растворе с помощью рН-метра. Анализ на содержание белка проводили методом спектрофотометрии, при длине волны 280 нм. Далее высчитывали снижение концентрации нуклеокапсидного белка N в исследуемом растворе после хранения в течение 6 недель по отношению к первоначальному значению.
Результаты представлены в таблице ниже.
Таблица 2
Таким образом, на основании полученных результатов можно заключить, что полученные композиции, содержащие нуклеокапсидный белок N в концентрации от 20 мкг/мл до 100 мкг/мл, являются стабильными.
Пример 6
Исследование иммуногенных свойств полученных композиций
Полученные композиции исследовали на возможность индукции специфического иммунитета (иммуногенность)
Животных вида хомячки сирийские (самки) в количестве 240 шт. случайным образом делили на следующие равные группы:
Группа № 1 – вводили композицию, содержащую 20 мкг/ мл белка.
Группа № 2 – вводили композицию, содержащую 50 мкг/ мл белка.
Группа № 3 – вводили композицию, содержащую 100 мкг/ мл белка.
Группа № 4 – вводили композицию, не содержащую белок (плацебо).
Более подробные данные по составу представлены в таблице ниже.
Таблица 3
* - все значения приведены в расчете на 1 мл композиции.
На момент начала эксперимента возраст животных составлял 6-8 недель, диапазон массы – 56,37-149,28 г. Адаптационный период составлял 5 дней, при ежедневном осмотре животных (состояние, измерение температуры). Животных содержали в стандартных условиях в соответствии с Директивой 2010/63/EU Европейского парламента и совета Европейского союза от 22.09.2010 г. по охране животных, используемых в научных целях.
Композиции вводили внутримышечно, в дозе по 0,5 мл на животное, при этом использовали дробное введение, с перерывом на 14 дней (введение в 1 день и в 15 день).
Схема эксперимента представлена в таблице ниже.
Таблица 4
Анализ ИФА на специфические антитела проводили по следующей методике.
После иммунизации композициями 1-4 мышей типа Balb/c, в возрасте 6-8 недель, дозой в объёме 500 мкл, по 250 мкл в каждое заднее бедро.
Далее, на 42 сутки после введения второй дозы мышей усыпляли в камере, наполненной CO2 газом. Далее осуществляли забор крови на содержание специфических антител и внутренних органов на гистологические анализы.
Кровь помещали в пробирки типа Eppendorf, содержащие ЭДТА в концентрации 1-2 мг/мл. Пробирки с кровью и ЭДТА центрифугировали при +4°C, в течение 20 минут. Супернатант переносили в чистые пробирки в ламинарном боксе. Полученную плазму замораживали.
Процедура: проведение иммуноферментного анализа (ИФА)
Использовали следующие реагенты:
посадочные антигены, 1 мкг/мл, 100 мкл/лунку; блокировку 0,5 % молоком в отмывочном буфере (20 мMTрис, 150 мМ NaCl, 0,05 % полисорбат 20, рН 7,4±0,1), 300 мкл/лунку.
Отмывку проводили следующим образом: сливали содержимое планшета, планшет промывали 4 раза по 300 мкл на лунку отмывочным буфером (20 мM Tрис, 150 мМ NaCl, 0,05 % полисорбат 20, рН 7,4±0,1), лунки тщательно осушали, избегая образования пузырей, путем постукивания планшета о салфетку.
При нанесении сывороток подбирали титр для каждой отдельной сыворотки, 100 мкл/лунку, термостатировали и центрифугировали.
Нанесение вторичных антител проводили при исходном разведении 1:64000, 100 мкл/лунку, с термостатированием и перемешиванием.
Отмывку проводили следующим образом: сливали содержимое планшета, планшет промывали 4 раза по 300 мкл на лунку отмывочным буфером (20 мM Трис, 150 мМ NaCl, 0,05 % полисорбат 20, рН 7,4±0,1), лунки тщательно осушали, избегая образования пузырей, путем постукивания планшета о салфетку.
Добавляли раствора хромогена, 100 мкл/лунку, 12 минут в защищенном от света месте. Далее вносили стоп-раствор, 50 мкл/лунку. Съем результатов проводили при длине волны 450 нм, референс 620 нм. Результаты считались приемлемыми, если выполнены критерии пригодности и критерии приемлемости.
Согласно IUPAC, предел обнаружения рассчитывают по стандартному отклонению холостой пробы. Для этого измеряют величину аналитического сигнала для достаточного количества холостых проб и рассчитывают стандартное отклонение их значений.
Как правило, используется формула (Kaiser H. Zurdefinitiondernachweisgrenze, dergarantiegrenzeundderdabeibenutztenbegriffe, Дёрффель К. Статистика в аналитической химии):
LOD = Average+k*SD,
где k = 3
Предел обнаружения (LOD) рассчитывают по оптической плотности блокирующего буфера по формуле:
LOD = Average+10*SD,
где average – среднее значение оптической плотности блокирующего буфера,
SD - среднеквадратичное отклонение оптической плотности блокирующего буфера,
Принимается, что в образце присутствуют специфичные антитела, если средняя оптическая плотность образца больше, чем Сut-off, при этом Сut-off = LOD + 20% (20% соответствуют критерию пригодности иммуноферментной системы для оптической плотности на уровне поглощения блокирующего буфера (бланка)):
Cut-off = 1,2* LOD = 1,2*(Average+10*SD).
Титром сыворотки считается крайнее разведение, при котором оптическая плотность превышает сигнал дискриминационного уровня (cut-off), используется усредненная оптическая плотность.
Результаты по определению титра специфических антител IgG белок представлены в таблице ниже.
Таблица 5
(1 случай титра 800)**
(1 случай титра 800)**
(1 случай титра 800)**
(1 случай титра 800)**
(1 случай титра 800)**
* - измерение до введения.
** - обнаружены титры неспецифических антител, характерных для данного вида животных.
Nd – не определено, титр отсутствует.
Выраженный иммунный ответ регистрировали при однократном и двукратном внутримышечном введении композиций в группах №№ 1-3 в дозе 0,5 мл/животное с пиком титра специфических антител на 22-й день эксперимента и с сохранением до 43-го дня в диапазоне 1:32000-1:17800. Появление специфических антител регистрировали через 15 дней после первой вакцинации животных.
Пример 7
Исследование иммуногенных свойств полученных композиций (протективность)
Полученные композиции исследовали на возможность индукции специфического иммунитета (протективность).
Оценку протективных свойств композиций оценивали после двухкратной вакцинации и заражения культурой коронавируса.
Для выработки иммунитета использовали композиций и схему вакцинации, как описано в примере 5. Для иммунизации использовали композиции, содержащие белок N в различной концентрации, а также плацебо (композицию, не содержащую белок и содержащую только растворитель и вспомогательные вещества).
Композиции для вакцинации представлены в таблице ниже.
Таблица 6
* - все значения приведены в расчете на 1 мл композиции.
Самок сирийских хомячков в количестве 50 шт. рандомно разделили на 5 групп, содержащих по 10 особей. Группы животных сначала иммунизировали на 1-й и 15-й день композициями с различным содержанием белка. Далее на 29-й день животных заражали вирусом SARS-CoV-2и регистрировали клинические проявления заболевания и выздоровления.
Обозначение группы в зависимости от введенной композиции и заражения вирусом приведены в таблице ниже.
Таблица 7
С целью формирования патологии животным под общим наркозом интраназально однократно вводили вирус SARS-CoV-2 (паспортизированный штамм ФГБНУ «ФНЦИРИП им. М.П. Чумакова РАН» №ПИК35 GISAID ID EPI_ISL_428852) в объеме 50 мкл в дозе 5 lgTCID50 на животное. На протяжении эксперимента у животных контролировали общее состояние и массу тела. Эвтаназию животных проводили на 3-й и 7-й дни после заражения. Легкие фотографировали и взвешивали для дальнейшей оценки массового коэффициента. Макроскопически проведена оценка изменений цвета и структуры легочной ткани. Правое легкое использовали для оценки микроскопических изменений. Гистологический анализ включал в себя оценку трех признаков: воспаление легких, клеточный инфильтрат и отек. Левое легкое и ткани носовых раковин использовали для оценки количества РНК вируса SARS-CoV-2 методом ОТ-ПЦР по показателю Ct.
В период иммунизации не отмечено патологических изменений в общем состоянии экспериментальных животных и снижения массы тела.
Фотографии патологий представлены на Фиг. 1-2.
Общие результаты представлены в таблице ниже.
Таблица 8
После заражения вирусом у животных отмечали: снижение массы на 10-15% входе инфекционного процесса, наличие клинической симптоматики, накопление РНКвируса в нижних и верхних дыхательных путях на 3-й день инфекции, макро- и микроскопическими изменения легких, наиболее выраженные на 7-й день развития патологии, увеличением массового коэффициента легких в 1,5 раза.
Гистологические исследования легких представлены на Фиг. 1-3.
В соответствии с полученными данными установлено, что введение композиции № 8 не привело к развитию фармакологических эффектов на течение коронавирусной инфекции у сирийских хомячков. Введение композиций, содержащих белок, №№ 5, 6, 7 оказало положительное влияние на инфекционный процесс в виде тенденции к увеличению массы тела и улучшению общего самочувствия животных на 5-й день патологии, и уменьшения выраженности гистологических изменений легочной ткани на 7-й день после заражения.
В ходе данного исследования было показано, что композиции, содержащие белок N в различных концентрациях и адъювант, обладают протективными свойствами при заражении инфекцией SARS-CoV-2. Обнаруженные свойства проявляются в виде сокращения периода болезни по полному отсутствию клинических признаков инфекции к 5-му дню после заражения, достоверного увеличения массы тела на 6-7-й дни развития инфекции с практически полным восстановлением до исходного уровня, тенденции к увеличению показателя Ct в легочной ткани на 3-й день, снижения выраженности макро- и микроскопических изменений в легочной ткани.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ФГУП СПбНИИВС ФМБА России
<120> СОСТАВ ВАКЦИНЫ ПРОТИВ COVID-19
<160> NUMBER OF SEQ ID NOS: 3
<210> SEQIDNO 1
<211> 420
<212> искусственная последовательность
<213> искусственная аминокислотная последовательность
<400> SEQUENCE1:
MGSDNGPQNQRNAPRITFGGPSDSTGSNQN 30
GERSGARSKQRRPQGLPNNTASWFTALTQH 60
GKEDLKFPRGQGVPINTNSSPDDQIGYYRR 90
ATRRIRGGDGKMKDLSPRWYFYYLGTGPEA 120
GLPYGANKDGIIWVATEGALNTPKDHIGTR 150
NPANNAAIVLQLPQGTTLPKGFYAEGSRGG 180
SQASSRSSSRSRNSSRNSTPGSSRGTSPAR 210
MAGNGGDAALALLLLDRLNQLESKMSGKGQ 240
QQQGQTVTKKSAAEASKKPRQKRTATKAYN 270
VTQAFGRRGPEQTQGNFGDQELIRQGTDYK 300
HWPQIAQFAPSASAFFGMSRIGMEVTPSGT 330
WLTYTGAIKLDDKDPNFKDQVILLNKHIDA 360
YKTFPPTEPKKDKKKKADETQALPQRQKKQ 3900
QTVTLLPAADLDDFSKQLQQSMSSADSTQA 420
<160> SEQIDNO: 2
<210> 3
<211> 6496
<212> DNA
<213> искусственная последовательность
<400> искусственная нуклеотидная последовательность
tggcgaatgggacgcgccctgtagcggcgcattaagcgcggcgggtgtggtggttacgcg 60
cagcgtgaccgctacacttgccagcgccctagcgcccgctcctttcgctttcttcccttc 120
ctttctcgccacgttcgccggctttccccgtcaagctctaaatcgggggctccctttagg 180
gttccgatttagtgctttacggcacctcgaccccaaaaaacttgattagggtgatggttc 240
acgtagtgggccatcgccctgatagacggtttttcgccctttgacgttggagtccacgtt 300
ctttaatagtggactcttgttccaaactggaacaacactcaaccctatctcggtctattc 360
ttttgatttataagggattttgccgatttcggcctattggttaaaaaatgagctgattta 420
acaaaaatttaacgcgaattttaacaaaatattaacgtttacaatttcaggtggcacttt 480
tcggggaaatgtgcgcggaacccctatttgtttatttttctaaatacattcaaatatgta 540
tccgctcatgaattaattcttagaaaaactcatcgagcatcaaatgaaactgcaatttat 600
tcatatcaggattatcaataccatatttttgaaaaagccgtttctgtaatgaaggagaaa 660
actcaccgaggcagttccataggatggcaagatcctggtatcggtctgcgattccgactc 720
gtccaacatcaatacaacctattaatttcccctcgtcaaaaataaggttatcaagtgaga 780
aatcaccatgagtgacgactgaatccggtgagaatggcaaaagtttatgcatttctttcc 840
agacttgttcaacaggccagccattacgctcgtcatcaaaatcactcgcatcaaccaaac 900
cgttattcattcgtgattgcgcctgagcgagacgaaatacgcgatcgctgttaaaaggac 960
aattacaaacaggaatcgaatgcaaccggcgcaggaacactgccagcgcatcaacaatat 1020
tttcacctgaatcaggatattcttctaatacctggaatgctgttttcccggggatcgcag 1080
tggtgagtaaccatgcatcatcaggagtacggataaaatgcttgatggtcggaagaggca 1140
taaattccgtcagccagtttagtctgaccatctcatctgtaacatcattggcaacgctac 1200
ctttgccatgtttcagaaacaactctggcgcatcgggcttcccatacaatcgatagattg 1260
tcgcacctgattgcccgacattatcgcgagcccatttatacccatataaatcagcatcca 1320
tgttggaatttaatcgcggcctagagcaagacgtttcccgttgaatatggctcataacac 1380
cccttgtattactgtttatgtaagcagacagttttattgttcatgaccaaaatcccttaa 1440
cgtgagttttcgttccactgagcgtcagaccccgtagaaaagatcaaaggatcttcttga 1500
gatcctttttttctgcgcgtaatctgctgcttgcaaacaaaaaaaccaccgctaccagcg 1560
gtggtttgtttgccggatcaagagctaccaactctttttccgaaggtaactggcttcagc 1620
agagcgcagataccaaatactgtccttctagtgtagccgtagttaggccaccacttcaag 1680
aactctgtagcaccgcctacatacctcgctctgctaatcctgttaccagtggctgctgcc 1740
agtggcgataagtcgtgtcttaccgggttggactcaagacgatagttaccggataaggcg 1800
cagcggtcgggctgaacggggggttcgtgcacacagcccagcttggagcgaacgacctac 1860
accgaactgagatacctacagcgtgagctatgagaaagcgccacgcttcccgaagggaga 1920
aaggcggacaggtatccggtaagcggcagggtcggaacaggagagcgcacgagggagctt 1980
ccagggggaaacgcctggtatctttatagtcctgtcgggtttcgccacctctgacttgag 2040
cgtcgatttttgtgatgctcgtcaggggggcggagcctatggaaaaacgccagcaacgcg 2100
gcctttttacggttcctggccttttgctggccttttgctcacatgttctttcctgcgtta 2160
tcccctgattctgtggataaccgtattaccgcctttgagtgagctgataccgctcgccgc 2220
agccgaacgaccgagcgcagcgagtcagtgagcgaggaagcggaagagcgcctgatgcgg 2280
tattttctccttacgcatctgtgcggtatttcacaccgcatatatggtgcactctcagta 2340
caatctgctctgatgccgcatagttaagccagtatacactccgctatcgctacgtgactg 2400
ggtcatggctgcgccccgacacccgccaacacccgctgacgcgccctgacgggcttgtct 2460
gctcccggcatccgcttacagacaagctgtgaccgtctccgggagctgcatgtgtcagag 2520
gttttcaccgtcatcaccgaaacgcgcgaggcagctgcggtaaagctcatcagcgtggtc 2580
gtgaagcgattcacagatgtctgcctgttcatccgcgtccagctcgttgagtttctccag 2640
aagcgttaatgtctggcttctgataaagcgggccatgttaagggcggttttttcctgttt 2700
ggtcactgatgcctccgtgtaagggggatttctgttcatgggggtaatgataccgatgaa 2760
acgagagaggatgctcacgatacgggttactgatgatgaacatgcccggttactggaacg 2820
ttgtgagggtaaacaactggcggtatggatgcggcgggaccagagaaaaatcactcaggg 2880
tcaatgccagcgcttcgttaatacagatgtaggtgttccacagggtagccagcagcatcc 2940
tgcgatgcagatccggaacataatggtgcagggcgctgacttccgcgtttccagacttta 3000
cgaaacacggaaaccgaagaccattcatgttgttgctcaggtcgcagacgttttgcagca 3060
gcagtcgcttcacgttcgctcgcgtatcggtgattcattctgctaaccagtaaggcaacc 3120
ccgccagcctagccgggtcctcaacgacaggagcacgatcatgcgcacccgtggggccgc 3180
catgccggcgataatggcctgcttctcgccgaaacgtttggtggcgggaccagtgacgaa 3240
ggcttgagcgagggcgtgcaagattccgaataccgcaagcgacaggccgatcatcgtcgc 3300
gctccagcgaaagcggtcctcgccgaaaatgacccagagcgctgccggcacctgtcctac 3360
gagttgcatgataaagaagacagtcataagtgcggcgacgatagtcatgccccgcgccca 3420
ccggaaggagctgactgggttgaaggctctcaagggcatcggtcgagatcccggtgccta 3480
atgagtgagctaacttacattaattgcgttgcgctcactgcccgctttccagtcgggaaa 3540
cctgtcgtgccagctgcattaatgaatcggccaacgcgcggggagaggcggtttgcgtat 3600
tgggcgccagggtggtttttcttttcaccagtgagacgggcaacagctgattgcccttca 3660
ccgcctggccctgagagagttgcagcaagcggtccacgctggtttgccccagcaggcgaa 3720
aatcctgtttgatggtggttaacggcgggatataacatgagctgtcttcggtatcgtcgt 3780
atcccactaccgagatatccgcaccaacgcgcagcccggactcggtaatggcgcgcattg 3840
cgcccagcgccatctgatcgttggcaaccagcatcgcagtgggaacgatgccctcattca 3900
gcatttgcatggtttgttgaaaaccggacatggcactccagtcgccttcccgttccgcta 3960
tcggctgaatttgattgcgagtgagatatttatgccagccagccagacgcagacgcgccg 4020
agacagaacttaatgggcccgctaacagcgcgatttgctggtgacccaatgcgaccagat 4080
gctccacgcccagtcgcgtaccgtcttcatgggagaaaataatactgttgatgggtgtct 4140
ggtcagagacatcaagaaataacgccggaacattagtgcaggcagcttccacagcaatgg 4200
catcctggtcatccagcggatagttaatgatcagcccactgacgcgttgcgcgagaagat 4260
tgtgcaccgccgctttacaggcttcgacgccgcttcgttctaccatcgacaccaccacgc 4320
tggcacccagttgatcggcgcgagatttaatcgccgcgacaatttgcgacggcgcgtgca 4380
gggccagactggaggtggcaacgccaatcagcaacgactgtttgcccgccagttgttgtg 4440
ccacgcggttgggaatgtaattcagctccgccatcgccgcttccactttttcccgcgttt 4500
tcgcagaaacgtggctggcctggttcaccacgcgggaaacggtctgataagagacaccgg 4560
catactctgcgacatcgtataacgttactggtttcacattcaccaccctgaattgactct 4620
cttccgggcgctatcatgccataccgcgaaaggttttgcgccattcgatggtgtccggga 4680
tctcgacgctctcccttatgcgactcctgcattaggaagcagcccagtagtaggttgagg 4740
ccgttgagcaccgccgccgcaaggaatggtgcatgcaaggagatggcgcccaacagtccc 4800
ccggccacggggcctgccaccatacccacgccgaaacaagcgctcatgagcccgaagtgg 4860
cgagcccgatcttccccatcggtgatgtcggcgatataggcgccagcaaccgcacctgtg 4920
gcgccggtgatgccggccacgatgcgtccggcgtagaggatcgagatctcgatcccgcga 4980
aattaatacgactcactataggggaattgtgagcggataacaattcccctctagaaataa 5040
ttttgtttaactttaagaaggagatataccatgggcagcgataatggcccgcagaatcag 5100
cgtaatgcaccgcgtattacctttggcggcccgagtgatagtaccggtagtaatcagaat 5160
ggtgaacgcagtggtgcacgtagcaaacagcgccgcccgcagggcctgcctaataatacc 5220
gccagttggtttaccgccctgacccagcatggcaaagaagatctgaaatttccgcgcggt 5280
cagggcgtgccgattaataccaatagcagtccggatgatcagattggctattatcgccgc 5340
gccacccgccgcattcgcggtggtgacggtaaaatgaaagatctgagcccgcgttggtat 5400
ttttattatctgggcaccggcccggaagccggtctgccttatggtgcaaataaggatggt 5460
attatttgggtggcaaccgaaggtgcactgaataccccgaaagatcatattggtacccgt 5520
aatccggcaaataatgcagcaattgttctgcagctgccgcagggtaccaccctgccgaaa 5580
ggcttttatgccgaaggcagtcgcggcggcagtcaggctagtagccgtagcagtagccgt 5640
agtcgcaatagcagtcgcaatagtaccccgggcagcagccgtggcaccagtcctgctcgt 5700
atggcaggtaatggtggtgacgccgccctggcactgctgctgctggatcgcctgaatcag 5760
ctggaaagcaaaatgagtggtaaaggccagcagcagcagggccagaccgtgaccaaaaaa 5820
tctgcagcagaagcaagcaaaaaaccgcgccagaaacgtaccgcaaccaaagcatataat 5880
gtgacccaggcctttggtcgtcgtggtccggaacagacccagggcaattttggcgatcag 5940
gaactgattcgccagggcaccgattataaacattggccgcagattgcccagtttgccccg 6000
agcgcaagcgcatttttcggcatgagtcgcattggcatggaagttaccccgagcggtacc 6060
tggctgacctataccggtgcaattaagctggatgataaagatccgaattttaaagatcag 6120
gttattctgctgaacaaacatattgatgcctataaaaccttcccgccgaccgaaccgaaa 6180
aaagataaaaagaaaaaggcagatgagacccaggcactgccgcagcgtcagaaaaaacag 6240
cagaccgtgacactgctgccggcagccgatctggatgattttagtaaacagctgcagcag 6300
agtatgagtagcgcagatagtacccaggcataactcgagcaccaccaccaccaccactga 6360
gatccggctgctaacaaagcccgaaaggaagctgagttggctgctgccaccgctgagcaa 6420
taactagcataaccccttggggcctctaaacgggtcttgaggggttttttgctgaaagga 6480
ggaactatatccggat 6496
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Искусственный ген N1new, кодирующий нуклеокапсидный белок коронавируса SARS-CoV-2, и рекомбинантная плазмида pET-28a-N1new, обеспечивающая экспрессию искусственного гена | 2021 |
|
RU2762962C1 |
| Средство и способ терапии и экстренной профилактики заболеваний, вызываемых вирусом SARS-CoV-2 на основе рекомбинантного антитела и гуманизированного моноклонального антитела | 2021 |
|
RU2769223C1 |
| Рекомбинантный белок для иммунизации против коронавируса кошек | 2023 |
|
RU2808965C1 |
| Штамм гибридных клеток животных Mus musculus 1F1 - продуцент моноклонального антитела к нуклеокапсидному белку N вируса SARS-CoV-2 | 2021 |
|
RU2769817C1 |
| Плазмидная ДНК-матрица pVAX-RBD, молекул мРНК-RBD, полученная с использованием ДНК-матрицы pVAX-RBD, обеспечивающая синтез и секрецию белка RBD SARS-CoV 2 в клетках организма млекопитающих и комплекс в виде наночастиц, содержащих молекулы мРНК-RBD, индуцирующих SARS-CoV-специфические антитела, обладающие вируснейтрализующей активностью | 2021 |
|
RU2754230C1 |
| Вакцинная композиция против коронавирусной инфекции COVID-19 | 2020 |
|
RU2743595C1 |
| Пептидные иммуногены и вакцинная композиция против коронавирусной инфекции COVID-19 с использованием пептидных иммуногенов | 2020 |
|
RU2743593C1 |
| Пептидные иммуногены и вакцинная композиция против коронавирусной инфекции COVID-19 с использованием пептидных иммуногенов | 2020 |
|
RU2738081C1 |
| Пептидные иммуногены, используемые в качестве компонентов вакцинной композиции против коронавирусной инфекции COVID-19 | 2020 |
|
RU2743594C1 |
| Рекомбинантная ДНК, обеспечивающая получение рекомбинантного белка Cov1, обладающего иммуногенными свойствами в отношении вируса SARS-CoV-2 | 2021 |
|
RU2776484C1 |
Изобретение относится к биотехнологии. Описана фармацевтическая композиция, предназначенная для индукции специфического иммунного ответа против вируса острого респираторного синдрома SARS-CoV-2, содержащая нуклеокапсидный белок SARS-CoV-2. Вакцина имеет следующий состав на 1 мл: нуклеокапсидный белок NSARS-CoV-2, имеющий аминокислотную последовательность SEQIDNO: 1 20-100 мкг; сквалан 15-40 мг; α-токоферол 5-15 мг; полисорбат 80 1-10 мг; натрий фосфорно-кислый двузамещенный 0,1-2,0 мг; калий фосфорнокислый однозамещенный 0,01-0,25 мг; калия хлорид 0,01-0,2 мг; натрия хлорид 0,1-8,5 мг; вода для инъекций до 1 мл. Также представлен способ получения указанной композиции, который включает: обеспечение нуклеокапсидного белка NSARS-CoV-2, имеющего аминокислотную последовательность SEQ ID NO: 1, в количестве от 20 до 100 мкг/мл; растворение белка в водном растворителе и доведение содержания белка N в растворе до требуемой концентрации; приготовление водного раствора адъюванта; смешение водного раствора, содержащего белок N, и водного раствора адъюванта; гомогенизация полученной смеси до получения однородного по цвету раствора; регулирование полученной композиции рН до 7,2-7,6. Изобретение позволяет получить стабильную композицию, способную при ее введении в организм вызвать иммунный ответ и индуцировать специфический иммунный ответ против SARS-CoV-2. 3 н. и 7 з.п. ф-лы, 3 ил., 8 табл., 7 пр.
1. Фармацевтическая композиция, предназначенная для индукции специфического иммунного ответа против вируса острого респираторного синдрома SARS-CoV-2, содержащая нуклеокапсидный белок SARS-CoV-2, имеющий аминокислотную последовательность SEQIDNO: 1, и имеющая следующий состав на 1 мл:
2. Композиция по п. 1, отличающаяся тем, что имеет рН от 7,2 до 7,6.
3. Композиция по пп. 1, 2, отличающаяся тем, что имеет следующий состав на 1 мл:
4. Композиция по пп. 1-3, отличающаяся тем, что представляет собой раствор, эмульсию или лиофилизат.
5. Композиция по п. 4, отличающаяся тем, что представляет собой эмульсию.
6. Применение композиции по пп. 1-5 для профилактики или индукции специфического иммунитета против вируса острого респираторного синдрома SARS-CoV-2.
7. Применение по п. 6, включающее введение композиции 2 раза последовательно с интервалом не менее 2 недель.
8. Способ получения композиции по пп. 1-5, который включает:
1) обеспечение нуклеокапсидного белка N SARS-CoV-2, имеющего аминокислотную последовательность SEQ ID NO: 1, в количестве от 20 до 100 мкг/мл;
2) растворение белка в водном растворителе и доведение содержания белка N в растворе до требуемой концентрации;
3) приготовление водного раствора адъюванта;
4) смешение водного раствора, содержащего белок N, и водного раствора адъюванта;
5) гомогенизация полученной смеси до получения однородного по цвету раствора;
6) регулирование полученной композиции рН до 7,2-7,6.
9. Способ по п. 8, дополнительно включающий лиофилизацию полученного раствора с получением лиофилизата, используемого для восстановления растворителем перед введением пациенту.
10. Способ по п. 9, отличающийся тем, что полученная композиция представляет собой эмульсию.
| US 11020475 B1, 01.06.2021 | |||
| US 10973909 B1, 13.04.2021 | |||
| Приспособление при катушечном автомате для приема готовых катушек и передачи их в сортировочный ящик | 1928 |
|
SU11419A1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ОТНОСЯЩИЕСЯ СПОСОБЫ | 2008 |
|
RU2502520C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ УЛУЧШЕННОЙ ИММУНОГЕННОСТИ СОМАТОСТАТИНА В ЛЕЧЕНИИ ДЕФИЦИТА ГОРМОНА РОСТА И ИНСУЛИНОПОДОБНОГО ФАКТОРА РОСТА | 2009 |
|
RU2519051C2 |
| RU 2016118518 A, 16.11.2017 | |||
| Капельная масленка с постоянным уровнем масла | 0 |
|
SU80A1 |
| и др., Башкирский | |||
Авторы
Даты
2022-03-14—Публикация
2021-08-05—Подача