Область техники
Группа изобретений относится к области биотехнологии и генной инженерии, в частности к рекомбинантной технологииполучения рекомбинантных белков коронавируса, которые собираются в вирусоподобные частицы, имитирующие структуру вириона SARS-CoV-2. Предложенные рекомбинантные вирусоподобные частицы могут применяться для индукции специфического иммунитета против вируса тяжелого острого респираторного синдрома SARS-CoV-2.
Уровень техники
Актуальность разработки антивирусных препаратов или вакцин для профилактики COVID-2019 не вызывает сомнений. Появление нового коронавируса SARS-CoV-2 с высоким эпидемическим потенциалом вызвало глобальную пандемию коронавирусной инфекции COVID-19, Вспышка данного заболевания впервые была зафиксирована в Ухане (Китай), в декабре 2019 года. 30 января 2020 года Всемирная организация здравоохранения объявила эту вспышку чрезвычайной ситуацией в области общественного здравоохранения, имеющей международное значение, а 11 марта — пандемией. В настоящее время COVID-19 зарегистрировано в 188 странах мира, при заболели более 36 миллионов человек, и больше миллиона умерло. В России общее количество зараженных SARS-CoV-2 достигло более миллиона человек. Вирус SARS-CoV-2 относится к семейству Coronaviridae роду Betacoronavirus.
По состоянию на 20 августа 2021 года 112 вакцин-кандидатов находились на стадии клинических исследований, и 184 — на стадии доклинических исследований. Над 2 вакцинами-кандидатами работы были прекращены [WHO. DraftlandscapeofCOVID-19 candidatevaccines].
Несмотря на то, что разработаны ряд вакцин, при создании профилактических препаратов для профилактики COVID-19, разработка нескольких платформ (технологий, используемых в производстве вакцины) для создания эффективных и безопасных вакцин просто необходима
Одной из таких технологий является создание рекомбинантных вакцин на основе вирусоподобных частиц или viruslikeparticle (ВПЧ или VLP). Вирусоподобные частицы или virus like particle (ВПЧ или VLP) представляют собой структуры размером порядка 100-150 нм, которые являются результатом самосборки вирусных белков без нуклеиновой кислоты генома внутри.
VLP содержат большое количество повторяющихся фрагментов вирусных поверхностных и/или коровых белков, представляющих собой конформационные вирусные эпитопы, которые могут вызывать Т-клеточный и В-клеточный иммунный ответы. При иммунизации VLP стимулируют дендритные клетки, которые захватывают соответствующие антигены для презентации T- и В-лимфоцитам [Roy P., Noad R. Virus-like particles as a vaccine delivery system. Myths and facts. Hum. Vaccines. 2008; 4 (1): 5–8.]. Поскольку VLP не могут реплицироваться, они обеспечивают более безопасную альтернативу живым вакцинам на основе аттенуированных вирусов. Вирусные структурные белки могут в процессе самосборки объединяться в организованные макромолекулярные структуры (капсиды), по своему строению и морфологии схожие с аутентичными вирионами и содержащие функционально активные и иммунологически соответствующие структурные белки.
VLP могут продуцироваться в различных экспрессионных системах. Наиболее перспективными считаются VLP на основе белков, полученных в бакуловирусной системе экспрессии. Эта системы дают высокие уровни экспрессии рекомбинантных белков и позволяют организовать последующее крупномасштабное производство вакцины. VLP, продуцируемые в клетках насекомых, считаются более безопасными, чем другие системы экспрессии, поскольку бакуловирусы обнаруживаются в овощах и не способны реплицироваться в клетках млекопитающих. Кроме того, клетки насекомых можно адаптировать для роста в бессывороточной (не содержащей животных продуктах среде), могут быть идентифицированы с помощью анализа кариотипа и изофермента, свободны от загрязняющих микроорганизмов, случайных агентов, ретровирусов и, как было показано, не являются онкогенными. Считается, что данная технология безопасна и используется для широкомасштабного производства VLP[Rong R, Progress in vaccine development based on baculovirus expression vector system PMID: 31001944 DOI: 10.13345/j.cjb.180301]
В данный момент на стадии доклинических и клинических исследований находятся несколько вакцинот коронавируса, основанных на бакуловирусной системе экспрессии [M. GALDIEROetal. SARS-CoV-2 vaccine development: where are we? European Review for Medical and Pharmacological Sciences 2021; 25: 2752-2784, Table VI. SARS-CoV-2 virus-like particles candidate vaccines under development.]:
1. NVX-CoV2373 (Novavax);
2. Кандидатная вакцина от Sanofi и GSK;
3. Рекомбинантная вакцина против SARS-CoV-2 (клетка Sf9) (Западно-Китайская больница Сычуаньского университета);
4. Белок RBD + адъювант FAR Сквален(Farmacológicos Veterinarios SAC (FARVET SAC)/Universidad Peruana Cayetano Heredia (UPCH)).
Представленные выше вакцины являются субъединичными вакцинами на основе рекомбинантного S белка коронавируса, полученного в бакуловирусной системе экспрессии. Недостатком рекомбинантных субъединичных вакцин, как и традиционных субъединичных вакцин, являются то, что презентация антигена может отличаться от природного вируса и будут вырабатываться антитела, не способные эффективно нейтрализовать патоген. Решением указанного недостатка может быть получение антигенов в виде вирусоподобной частицы, которая имитирует природный вирион и презентация антигена также близка к таковой у вирусной частицы.
Изпубликации [Xu R, Shi M, Li J, Song P, Li N. Construction of SARS-CoV-2 Virus-Like Particles by Mammalian Expression System [published correction appears in Front Bioeng Biotechnol. 2020 Sep09;8:1026]. FrontBioengBiotechnol. 2020;8:862. Published 2020 Jul 30. doi:10.3389/fbioe.2020.00862] известно получение рекомбинантной VLP SARS-CoV-2 с помощью плазмидной трансфекции вирусных структурных белков в клетках млекопитающих.При этомрекомбинантная вирусоподобная частица содержит рекомбинантные белки коронавируса E, M, N и S. Недостатком указанного решения является использование системы экспрессии рекомбинантных белков в клетках млекопитающих. При этом известно, что VLP, продуцируемые в клетках насекомых, считаются более безопасными, чем другие системы экспрессии, поскольку бакуловирусы обнаруживаются в овощах и не способны реплицироваться в клетках млекопитающих.
Также из документа [CN 112661819 A, опуб. 16.04.2021] известны рекомбинантные вирусоподобные частицы коронавируса SARS-CoV-2 и способ конструирования рекомбинантной вирусоподобной частицы. Согласно изобретению, вирусоподобные частицы содержат домен связывания рецептора SARS-CoV -2 (RBD) и антигена вируса гепатита В, при этом частицы получают в бакуловирусной системе экспрессии. Недостатком данного технического решения является то, что в состав вирусоподобных частиц входит, наряду с белками вируса гепатита В, только часть S белка коронавируса – RBD-домен. Несмотря на то, что на него образуются специфические антитела, они не все обладают нейтрализующими свойствами, что может повлиять на эффективность иммунобиологических препаратов, полученных с использованием данных VLP.
Данный документ может быть принят за ближайший аналог.
Таким образом, существует потребность в создании вирусоподобных частиц имеющих в своем составе полноразмерные белки SARS-CoV-2,которые формируют частицу и имитируют вирион коронавируса для получения эффективных иммунобиологических препаратов для лечения и профилактики COVID-19. При этом белки, формирующие частицу, должны быть синтезированы в бакуловирусной системе экспрессии, в которойиспользуются клетки насекомых, которые культивируют в бессывороточной, не содержащей животных продуктах среде, могут быть идентифицированы с помощью анализа кариотипа и изофермента, свободны от загрязняющих микроорганизмов, случайных агентов, ретровирусов и, как было показано, не являются онкогенными.
Раскрытие сущности изобретения
Технической задачей изобретения является разработка и оптимизация получениярекомбинантных вирусоподобных частиц, состоящих из полноразмерных белков коронавируса SARS-CoV-2с универсальным набором поверхностных антигенов, которые способны самособираться в частицу, имитирующие вирион коронавирусаи вызывать специфический иммунный ответ против вируса тяжелого острого респираторного синдрома SARS-CoV-2.
Технический результат заключается в получении устойчивых вирусоподобных частиц, содержащих актуальные антигены коронавируса SARS-CoV-2, которые способны самособираться в клетках насекомых, имитирующие вирион коронавируса и способные индуцировать специфический иммунный ответ против вируса тяжелого острого респираторного синдрома SARS-CoV-2. А также технический результат заключается в получении рекомбинантных бакуловирусов, содержащих гены, кодирующие белки коронавируса E, M, N и S (причем S белок 4-х штаммов коронавируса: подобного Уханьскому, Индийского, Южно-Африканского и Английского), которые могут самособиратся в клетках насекомых в вирусоподобную частицу.
Указанный технический результат достигается тем, что создана рекомбинантная вирусоподобная частица для индукции специфического иммунитета против вируса тяжелого острого респираторного синдрома SARS-CoV-2, содержащая рекомбинантные белки коронавируса E, M, N и один или несколько S белков различных штаммов коронавируса, содержащие нуклеотидные последовательности SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5 SEQ ID NO:6, SEQ ID NO:7, которые получены в бакуловирусной системе экспрессии насекомых, при этом вирусоподобная частица имитирует вирион SARS-CoV-2.
Существует вариант, в котором рекомбинантная вирусоподобная частица содержит рекомбинантные белки коронавируса E, M, N и S, имеющие нуклеотидные последовательности SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3 и SEQ ID NO:4.
Существует также вариант, в котором рекомбинантная вирусоподобная частица содержит рекомбинантные белки коронавируса E, M, N и S, имеющие нуклеотидные последовательности SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3 и SEQ ID NO:5.
Возможен вариант, где рекомбинантная вирусоподобная частица содержит рекомбинантные белки коронавируса E, M, N и S, имеющие нуклеотидные последовательности SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3 и SEQ ID NO:6.
Существует вариант, где рекомбинантная вирусоподобная частица содержит рекомбинантные белки коронавируса E, M, N и S, имеющие нуклеотидные последовательности SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3 и SEQ ID NO:7.
Также технический результат достигается тем, что разработан способ получения заявленной рекомбинантной вирусоподобной частицы, который включает:А) получение рекомбинантного бакуловируса, Б) коинфекцию перевиваемой линии клеток насекомых T.ni различными сочетаниями рекомбинантных бакуловирусов, В) получение вирусоподобных частиц и их очистку.
В то же время, технический результат достигается тем, что создан рекомбинантный бакуловирус для получения заявленной рекомбинантной вирусоподобной частицы, включающий ген, выбранный из группы: ген, кодирующий Е белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:1, ген, кодирующий М белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:2, ген, кодирующий N белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:3, ген, кодирующий S белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:4, ген, кодирующий S белок коронавирус, имеющий нуклеотидную последовательность SEQ ID NO:5, ген, кодирующий S белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:6, ген, кодирующий S белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:7, при этом бакуловирус обладает способностью собираться в вирусоподобные частицы, имитирующие вирион SARS-CoV-2.
Краткое описание чертежей
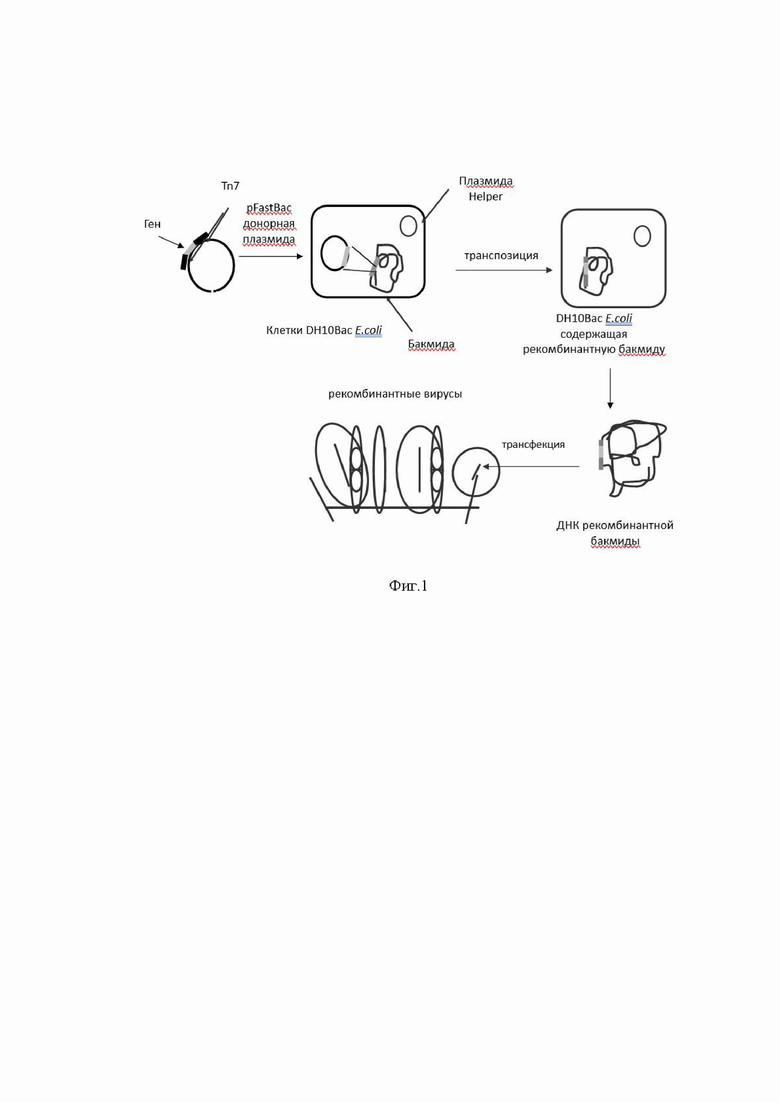
На фиг. 1 представлена схема получения бакуловирусных рекомбинантных вирусов.
На фиг.2показана проверка рекомбинантных бакмид на наличие вставки.Показан электрофорез после проведения ПЦР на наличие вставки в геноме бакуловируса.
На фиг.3А представлена культура клеток T.ni, в проходящем свете. На фиг.3Б представлен «1» пассаж бакуловируса в суспензии клеток T.ni.
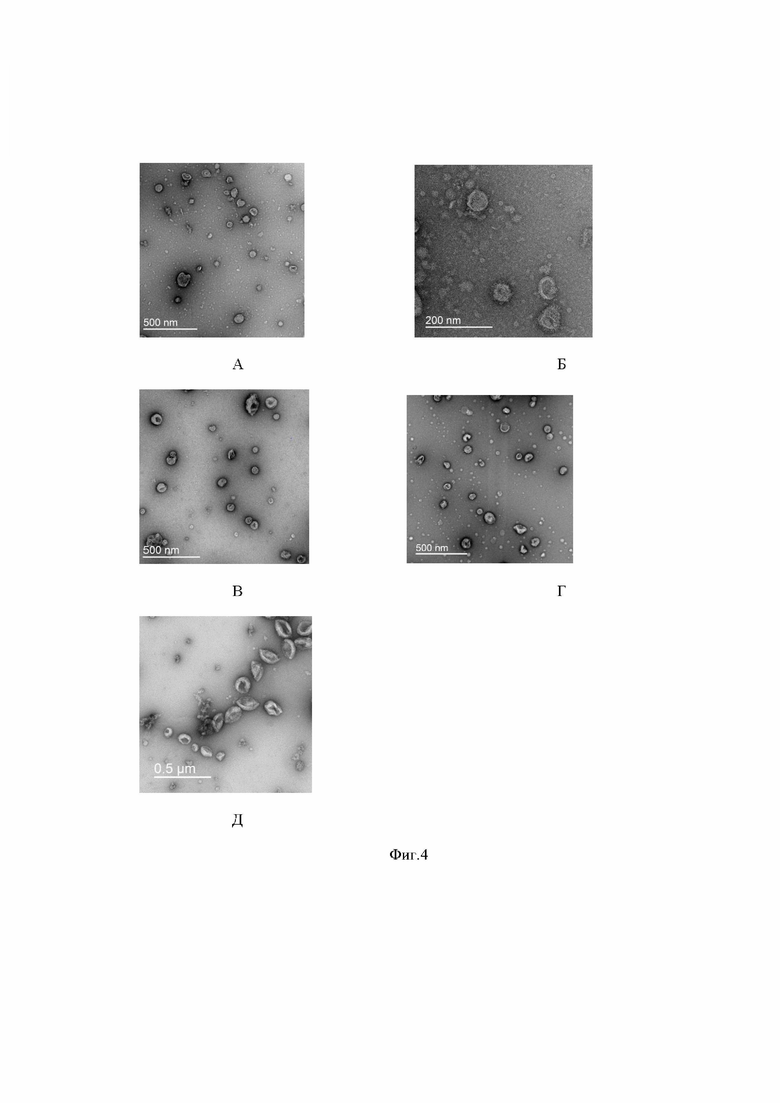
На фиг.4представлены VLPс различными поверхностными антигенами, которые визуализированы методом электронной микроскопии. На фиг.4А - VLP, содержащая белки коронавируса E, M, N и S штамма, подобного Уханьскому. На фиг.4Б - VLP, содержащая белки коронавируса E, M, N и S Английского штамма. На фиг.4В - VLP, содержащая белки коронавируса E, M, N и S Южно-Африканского штамма. На фиг.4Г - VLP, содержащая белки коронавируса E, M, N и S Индийского штамма. На фиг.4Д- VLP, содержащая белки коронавируса E, M, N и S 4- штаммов коронавируса (Уханьского, Английского, Южно-Африканского и Индийского).
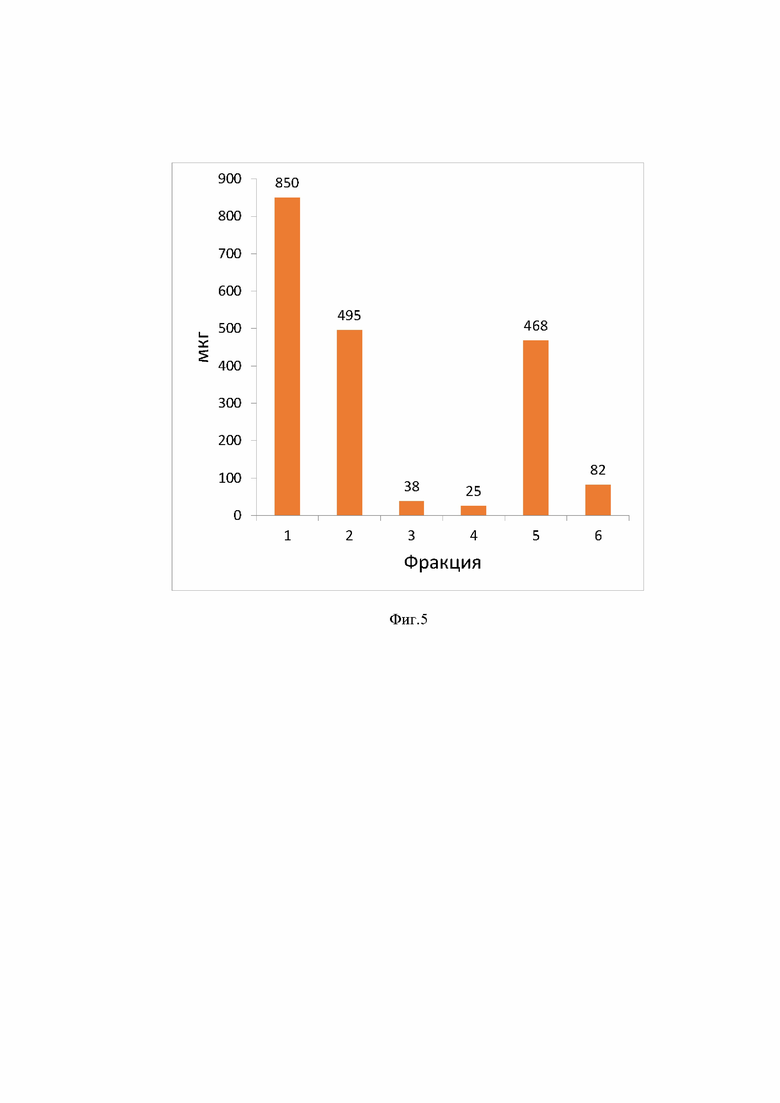
На фиг.5 показано распределение SARS-VLP в процессе предварительной очистки, где
1 – исходная культуральная жидкость SARS-VLP,
2 – супернатант после осаждения клеток центрифугированием при 1000 об/мин.,
3 – осадок клеток после центрифугирования при 1000 об/мин.,
4 – осадок после центрифугирования фракции 2 при 6000 об/мин.,
5 – супернатант после центрифугирования фракции 2 при 6000 об/мин.,
6 - супернатант после промывки и осаждения клеток фракции 3.
На фиг.6 представлена ИФА с сыворотками больных положительными и отрицательными в реакции нейтрализации (РН), где
отрРН – отрицательная в РН,
320РН – положительная в РН (титр 1:320),
20РН - положительная в РН (титр 1: 20),
отр до Covid – сыворотка, взятая более 20 лет назад.
На фиг.7 показана корреляция результатов сэндвич-ИФА с величиной титров в сыворотках больных в реакции нейтрализации (РН), где
1,4 – отрицательные сыворотки,
2 – сыворотка переболевшего, РН 1:320,
3 - сыворотка переболевшего, РН 1:160,
5 - сыворотка переболевшего, РН 1:80,
6 - сыворотка вакцинированного, РН 1:80.
Осуществление изобретения
Получение вирусоподобных частиц состоит из нескольких этапов.
На первом этапе проводились эпидемиологические исследования для определения штаммов актуальных штаммов вирусов, подбирали и оптимизировали последовательности генов вируса для клонирования в донорную плазмиду.Кодирующие последовательности были получены синтетическим путем, частота использования кодонов при этом была оптимизирована для культуры клеток насекомых.
В результате оптимизации были получены следующие последовательности:
- оптимизированная последовательность гена, кодирующего Е белок коронавируса (SEQ ID NO:1);
- оптимизированная последовательность гена, кодирующего М белок коронавируса (SEQ ID NO:2);
- оптимизированная последовательность гена, кодирующего N белок коронавируса (SEQ ID NO:3);
- оптимизированная последовательность гена, кодирующего S белок коронавируса (штамм, подобный Уханьскому, циркулирующий в конце 2020 г) (SEQ ID NO:4);
- оптимизированная последовательность гена, кодирующего S белок коронавируса (Индийский штамм) (SEQ ID NO:5);
- оптимизированная последовательность гена, кодирующего S белок коронавируса (Южно-Африканский штамм) (SEQ ID NO:6);
- оптимизированная последовательность гена, кодирующего S белок коронавируса (Английский штамм) (SEQ ID NO:7).
Следующим этапом создания вирусоподобных частиц является получение рекомбинантных белков.Для создания каждой генетической конструкции, с которой нарабатывались один или два рекомбинантных белка, использовалась система экспрессии Bac-to-Bac.
Пример 1. Получение различных рекомбинантных бакуловирусов.
Для получения бакуловируса, экспрессирующего различные белки (М, Е, N и S различных штаммов коронавируса) использовали трансферный вектор (pFastBac донорную плазмиду).Схематичное получение бакуловирусных рекомбинантных вирусов представлено на фиг.1
pFastBac донорная плазмида содержит экспрессионную кассету, в которой помимо клонированных генов находится фланкирующие последовательности транспозона Tn7. Рекомбинантная трансферная плазмида используется для трансформации клеток DH10Bac E.coli, которые содержат модифицированный бакуловирусный геном в виде большой плазмиды (бакмиды) и вектор-помощник, кодирующий фермент транспозазу.
В трансформированных клетках DH10Bac транспозаза осуществляет сайт-специфический перенос экспрессионной кассеты из трансферного вектора в модифицированный бакуловирусный геном.
Отбор рекомбинатных клонов DH10Bac осуществляется методом цветного теста, в выбранных колониях белого цвета перенос экспрессионной кассеты в бакуловирусный геном подтверждается методом ПЦР с праймерами, один из которых специфичен к клонированной последовательности, а другой – к геному бакуловируса. На фиг.2 представлен электрофорез после проведения ПЦР на наличие вставки в геноме бакуловируса.
Для дальнейшей работы отбирали клон, из которых выделили бакмиды. Выделенные рекомбинантные бакмиды смешивают с липосомным агентом Cellfectin для трансфекции клеток насекомых Sf-9 или Sf-21. Проникшая в клетку кольцевая молекула бакмидной ДНК инфекционна и запускает жизненный цикл бакуловируса в клетке. Таким образом, получаются рекомбинантные бакуловирусы.
Трансфекцию перевиваемой линии клеток Spodoptera frugiperda Sf-21 проводили очищенными препаратами бакмидной ДНК, содержащей оптимизированные гены коронавируса,с использованием катионного липосомного агента Cellfectin (Invitrogen, США), для каждой конструкции использовали по два клона (посевная концентрация клеток 5х105/мл, 10 мкл бакмиды).После трансфекции проводили еще два пассажа на клетках Sf-9 или Sf-21.
Таким образом, получили рекомбинантные бакуловирусы (фиг.3А и фиг.3Б)
Концентрацию белка в растворах определяли с использованием коммерческого набора “Micro BCA Protein Assay Kit” (Thermo, США).
Анализ структурных белков Sars-CoV-2 проводили методом электрофореза в 12% полиакриламидном геле с додецилсульфатом натрия (ПААГ-ДСН) по методу Laemmli (1970) Электрофорез проводили в пластинах полиакриламидного геля размером 70 х 100 х 0,75 на приборе Mini-PROTEAN II (Bio-Rad, США) в восстанавливающих условиях при по-стоянном напряжении 200 V. Разделяющий гель содержал 12% акриламида, 0,5% N,N-метилен-бис-акриламида, 0,375 М трис-HCl pH 8,8 и 0,1% ДСН. Фокусирующий гель содержал 4% акриламида, 10% N,N-метилен- бисакриламида в 0,125 М трис-HCl буфере pH 6,8. Для полимеризации в оба геля вносили по 0,025% персульфата аммония и 0,075% TEMED. Электродный буфер содержал 0,025 М трис-HCl, 0,192 М глицина, pH 8,3 и 0,1% ДСН. Все испытуемые пробы содержали лизирующий буфер с восстановителем (0,125 М трис-HCl, pH 6,8, 5% ДСН, 0,5% β -меркаптоэтанола, 10,8% глицерина, 0,01% бромфенолового синего) и были прогреты в течение 5 минут при 100 ℃. Заливку геля и подготовку аппарата для электрофореза к работе проводили согласно рекомендациям изготовителя. Белки в гелях окрашивали в течение 1 часа 0,1% раствором Кумасси ярко-голубого (CBB R-350) в водном растворе, содержащем 10% уксусной кислоты и 30% метанола. Избыток красителя отмывали 10% раствором уксусной кислотой такое же время с несколькими его сменами. В качестве белков-маркеров молекулярной массы использовали β-галактозидазу- 116 кД; фосфорилазу В - 94 кД, БСА- 66 кД, овальбумин- 45 кД, карбонат ангидразу-30 кД, ингибитор трипсина- 20,1 кД.
Для определения антигенной активности структурных белков SARS-CoV-2 использовали сэндвич-ИФАвестерн-блот(пример 4).
Таким образом, было определено, что были получены следующие структурные белки коронавируса M, E, N и S.
Пример 2 Получение VLP на основе рекомбинантных белков, синтезированных в бакуловирусной системе экспрессии.
VLP получали методом коинфекции, то есть одновременного заражения перевиваемой линии клеток насекомых T.ni различными сочетаниями рекомбинантных бакуловирусов. Перевиваемую культуру клеток насекомых Trichoplusia ni, культивировали в течение 4 суток после заражения. Был использован 2 пассаж рекомбинантных бакуловирусов.
VLP были очищены, как в примере 6 и визуализированы методом электронноймикроскопии, как в примере 3.
1. VLP, содержащая белки коронавируса E, M, N и S штамма, подобного Уханьскому (фиг. 4А)
2. VLP, содержащая белки коронавируса E, M, N и S Индийского штамма (фиг.4Б)
3. VLP, содержащая белки коронавируса E, M, N и S Южно-Африканского штамма (фиг.4В)
4. VLP, содержащая белки коронавируса E, M, N и S Английского штамма (фиг. 4Г)
5. VLP, содержащая белки коронавируса E, M, N и 4 S белка (штамма, подобного Уханьскому, Индийского, Южно-Африканского и Английского штамма) (фиг. 4Д).
Таким образом можно получать VLPc различными поверхностными S белками.
Пример 3 Определение эффективности синтеза VLP коронавируса, содержащих рекомбинантные белки, синтезированные в бакуловирусной системе экспрессииметодом электронной микроскопии.
3 мкл препарата, содержащего VLP, с концентрацией 12-30 мг/мл наносили на медную сетку, покрытую углеродной подложкой (Ted Pella, США) и обработанную в атмосфере тлеющего разряда, инкубировали 30 секунд при комнатной температуре. Затем на сетку наносили каплю 2% раствора ацетата урана, выдерживали 30 секунд, излишки раствора удаляли с сетки фильтровальной бумагой. Окрашенные сетки хранили в пластиковых контейнерах до использования. Исследование образцов производили в просвечивающем электронном микроскопе JEOL 2100 (JEOL, Япония), оборудованном катодом из гексаборита лантана, при ускоряющем напряжении 200 кВ. Изображения получали с увеличением х25000 с помощью ПЗС-камеры Gatan X100 с размером матрицы 2000х2000 пикселей (Gatan, США). Вирусоподобные частицы, визуализированные методом электронной микроскопии представлены на фиг. 4А.-4Д.
Таким образом, после очистки ультрацентрифугированием, VLP можно визуализировать с использованием электронной микроскопии.
Полученные частицы были проверены на специфическую активность. Для стандартизации получения активного антигена использовали метод определения S-белка в пробах SARS VLP в формате сендвич-ИФА (пример 4).
Пример 4. Определение S-белка в пробах SARS VLP в формате сендвич-ИФА.
Был синтезирован пероксидазный коньюгат и определена его иммунохимической активности полученного конъюгата методом прямого ИФА. RBD-специфические МКА1Е1 в концентрации 10 мкг/мл, 100 мкл в лунке в 0,1 М карбонатном буфере, рН=9,5 в концентрации 1 мкг/мл по 100 мкл в лунку в течение ночи при 40С. Антигенами являлись препараты VLP CoV 1, 2, 3 в концентрациях 0 – 0,23 - 0,68 – 2,05 – 6,17 – 18,5 – 55,5 – 166,6 – 500 мкг/мл. В качестве отрицательного контроля использовали препарат VLP HRV в тех же концентрациях. После 4-кратной отмывки планшета в лунки вносили по 100 мкл пероксидазного конъюгата 1Е1HRP 1/1000. Инкубировали планшет 1 час при +370С. После промывания планшета вносили по 0.1 мл субстратного раствора с тетраметилбензидином. Инкубировали 15 мин при комнатной температуре в темноте и добавляли 0.1 мл 1 М H2SO4 для остановки реакции. Оптическую плотность при 450 нм (А450) измеряли на спектрофотометре с вертикальным лучом Multiscan ЕХ (Thermo, США). Величину оптической плотности пересчитывали на мкг RBD, используя калибровочную кривую, полученную с использованием очищенного RBD, полученного в клетках млекопитающих. Таким образом было рассчитано распределение частиц по фракциям (фиг. 5).
Таким образом, был оптимизирован метод Сэндвич-ИФА для контроля специфической активности полученных частиц.
Пример 5. Специфичность VLP, определяемая методом ИФА с сыворотками больных положительными и отрицательными в реакции нейтрализации (РН).
VLP сохраняют нативную структуру белков, сравнимую с белками природного штамма коронавируса, что доказывает взаимодействие VLP с антителами пациентов, переболевших COVID-19.
В лунки планшета сорбировали VLP в разведении от 1:2 до 1:256. Затем добавляли сыворотки в разведении 1:100. Наличие взаимодействующих антител с белком S выявляли добавлением анти-IgG-человека конъюгированного с пероксидазой хрена (фиг.6).
Более того, ответ в сэндвич-ИФА коррелирует с результатами реакции нейтрализации (фиг.7).
Таким образом, полученные VLP, имитируя структуру SARS-CoV-2, при этом антигенные детерминанты презентированы таким образом, что антитела против SARS-CoV-2 связываются с ними. Следовательно, антитела, которые вырабатываются на полученные VLP, смогут вызывать специфический иммунный ответ.
Пример 6 Очистка VLP коронавируса.
Культуральную жидкость, содержащую вирус или вирусоподобные частицы, подвергали низкоскоростному центрифугированию, освобождаясь от клеток и клеточного дебриса при 1000 об/мин в течение 5 минут и при 6000 об/мин в течение 20 минут соответственно (+4°С, ротор Sorval® SS34). Распределение SARS-VLP в процессе предварительной очистки представлено на фиг. 5. Фракция 5 использовалась для выделения и очистки SARS-VLP методом ультрацентрифугирования.
Полученные осветлённые суспензии наслаивали на 6 мл 25% или 35% (w/v) сахарозы, приготовленной на буфере TNС (10 mM Tris–HCl, 140 mM NaCl, 10 mM CaCl2 рН 7.4). Центрифугировали в течение 2 часов при 28 000 об/мин (центрифуга Оptima XE-100, ротор SW 32Ti, Beckman Coulter, +4°С). Полученные осадки ресуспендировали в буфере TNС, и хранили при температуре +4°С.
Таким образом, был получен препарат, содержащий очищенные VLP.
Промышленная применимость
Все приведенные примеры подтверждают эффективность созданных рекомбинантных вирусоподобных частиц, содержащих рекомбинантные белки коронавируса E, M, N и один или несколько S белков различных штаммов коронавируса и обладающих защитными свойствами против вируса тяжелого острого респираторного синдрома SARS-CoV-2 и их промышленную применимость.
Перечень последовательностей
Оптимизированная нуклеотидная последовательность гена, кодирующего Е белок коронавируса (SEQ ID NO:1)
ATGTACTCTTTCGTGTCAGAGGAAACCGGTACTCTGATCGTGAACTCCGTCCTGCTGTTCCTGGCTTTCGTGGTCTTCCTGCTGGTGACCCTGGCTATCCTGACTGCCCTGCGCCTGTGCGCCTACTGCTGCAACATCGTGAACGTCTCCCTGGTCAAGCCTAGCTTCTACGTGTACTCCCGCGTCAAGAACCTGAACTCCAGCCGTGTGCCCGACCTGCTGGTCTAA
Оптимизированная нуклеотидная последовательность гена, кодирующего М белок коронавируса (SEQ ID NO:2)
ATGGCCGACTCTAACGGAACCATCACTGTGGAGGAACTGAAGAAGCTGCTGGAGCAGTGGAACCTGGTCATCGGTTTCCTGTTCCTGACTTGGATCTGCCTGCTGCAGTTCGCTTACGCCAACCGCAACCGTTTCCTGTACATCATCAAGCTGATCTTCCTGTGGCTGCTGTGGCCTGTGACTCTGGCTTGCTTCGTGCTGGCTGCCGTCTACCGCATCAACTGGATCACCGGTGGCATCGCTATCGCCATGGCTTGCCTGGTCGGTCTGATGTGGCTGTCCTACTTCATCGCCAGCTTCCGTCTGTTCGCTAGGACTAGATCCATGTGGAGCTTCAACCCTGAGACCAACATCCTGCTGAACGTGCCCCTGCACGGCACCATCCTGACTAGGCCACTGCTGGAGTCCGAACTGGTCATCGGTGCCGTCATCCTGAGGGGCCACCTGAGAATCGCTGGCCACCACCTGGGAAGATGCGACATCAAGGACCTGCCTAAGGAAATCACCGTGGCCACTTCTCGCACCCTGTCATACTACAAGCTCGGTGCTAGCCAGAGGGTGGCTGGAGACTCTGGTTTCGCTGCCTACTCACGCTACCGTATCGGAAACTACAAGCTGAACACCGACCACTCCAGCTCTTCAGACAACATCGCTCTGCTGGTCCAGTAA
Оптимизированная нуклеотидная последовательность гена, кодирующего N белок коронавируса (SEQ ID NO:3)
ATGTCCGACAACGGACCCCAGAACCAGCGCAACGCTCCACGTATCACCTTCGGTGGCCCTAGCGACTCTACTGGCAGCAACCAGAACGGAGAGCGTTCAGGCGCCAGATCCAAGCAGCGCCGTCCACAGGGCCTGCCTAACAACACCGCTTCTTGGTTCACCGCCCTGACTCAGCACGGAAAGGAAGACCTGAAGTTCCCTAGGGGACAGGGTGTGCCCATCAACACCAACTCCAGCCCCGACGACCAGATCGGATACTACAGGAGAGCTACTCGCCGTATCCGCGGAGGTGACGGCAAGATGAAGGACCTGTCCCCACGTTGGTACTTCTACTACCTCGGCACCGGACCTGAGGCTGGACTGCCATACGGTGCCAACAAGGACGGCATCATCTGGGTGGCTACCGAAGGAGCCCTGAACACTCCAAAGGACCACATCGGTACTCGCAACCCTGCTAACAACGCTGCCATCGTCCTGCAGCTGCCACAGGGCACCACTCTGCCTAAGGGCTTCTACGCTGAGGGAAGCAGGGGCGGATCTCAGGCCTCTTCAAGATCCAGCTCTCGCTCCCGTAACTCATCCCGCAACAGCACCCCTGGTAGCTCTAAGCGCACTTCTCCTGCTAGGATGGCTGGAAACGGTGGCGACGCTGCTCTGGCTCTGCTGCTGCTGGACCGTCTGAACCAGCTGGAGAGCAAGATGTCTGGCAAGGGCCAGCAGCAGCAGGGTCAGACCGTGACTAAGAAGTCAGCTGCCGAAGCTTCCAAGAAGCCAAGGCAGAAGAGAACCGCTACTAAGGCCTACAACGTCACCCAGGCCTTCGGAAGGAGAGGTCCTGAGCAGACTCAGGGCAACTTCGGAGACCAGGAACTGATCAGGCAGGGCACCGACTACAAGCACTGGCCCCAGATCGCTCAGTTCGCCCCATCAGCTTCCGCCTTCTTCGGAATGTCTAGAATCGGCATGGAAGTGACCCCTTCAGGAACTTGGCTGACCTACACTGGTGCTATCAAGCTGGACGACAAGGACCCCAACTTCAAGGACCAGGTCATCCTGCTGAACAAGCACATCGACGCCTACAAGACCTTCCCTCCCACTGAGCCTAAGAAGGACAAGAAGAAGAAGGCTGACGAAACCCAGGCTCTGCCACAGCGTCAGAAGAAGCAGCAGACCGTCACTCTGCTGCCAGCTGCCGACCTGGACGACTTCAGCAAGCAGCTGCAGCAGTCTATGTCATCCGCTGACTCAACTCAGGCCTAA
Оптимизированная нуклеотидная последовательность гена, кодирующего S белок коронавируса (штамм, подобный Уханьскому, циркулирующий в конце 2020 г) (SEQ ID NO:4)
ATGTTCGTTTTCCTCGTGCTCCTCCCCCTCGTTTCCTCCCAATGCGTCAACCTCACTACCCGTACCCAGCTCCCACCAGCCTACACCAACAGCTTCACTCGCGGTGTGTACTACCCCGACAAGGTCTTCCGTTCCAGCGTGCTGCACAGCACTCAGGACCTGTTCCTGCCATTCTTCTCTAACGTGACCTGGTTCCACGCCATCCACGTGAGCGGCACCAACGGCACTAAGCGCTTCGACAACCCTGTGCTGCCCTTCAACGACGGTGTCTACTTCGCTTCCACCGAGAAGTCTAACATCATCCGTGGATGGATCTTCGGCACCACTCTGGACTCAAAGACTCAGTCCCTGCTGATCGTCAACAACGCCACCAACGTGGTCATCAAGGTGTGCGAGTTCCAGTTCTGCAACGACCCTTTCCTGGGCGTCTACTACCACAAGAACAACAAGAGCTGGATGGAGTCTGAGTTCCGCGTCTACTCTTCAGCTAACAACTGCACTTTCGAGTACGTGAGCCAGCCCTTCCTGATGGACCTGGAAGGAAAGCAGGGTAACTTCAAGAACCTGAGGGAGTTCGTGTTCAAGAACATCGACGGATACTTCAAGATTTACTCAAAGCACACCCCTATCAACCTGGTGCGCGACCTGCCACAGGGTTTCTCCGCTCTGGAGCCTCTGGTGGACCTGCCCATCGGCATCAACATCACCCGCTTCCAGACTCTGCTGGCTCTGCACCGTTCCTACCTGACTCCTGGCGACTCCAGCTCTGGATGGACCGCCGGAGCTGCCGCTTACTACGTGGGTTACCTGCAACCCAGGACCTTCCTGCTGAAGTACAACGAAAACGGAACCATCACAGACGCTGTGGACTGCGCTCTGGACCCCCTGAGCGAAACCAAGTGCACTCTGAAGTCTTTCACCGTGGAGAAGGGCATCTACCAGACTAGCAACTTCAGGGTGCAGCCAACCGAATCTATCGTCAGATTCCCCAACATCACTAACCTGTGCCCATTCGGAGAGGTCTTCAACGCCACCAGATTCGCTTCCGTGTACGCCTGGAACAGGAAGAGAATCAGCAACTGCGTCGCTGACTACTCTGTGCTGTACAACAGCGCCTCTTTCTCAACCTTCAAGTGCTACGGCGTGAGCCCTACTAAGCTGAACGACCTGTGCTTCACCAACGTCTACGCCGACTCTTTCGTGATCAGGGGAGACGAGGTCAGACAGATCGCTCCCGGCCAGACTGGAAAGATCGCCGACTACAACTACAAGCTGCCAGACGACTTCACCGGCTGCGTCATCGCTTGGAACTCAAACAACCTGGACTCCAAAGTGGGTGGCAACTACAACTACCTGTACCGCCTGTTCCGTAAGAGCAACCTGAAGCCTTTCGAGAGGGACATCTCAACTGAAATCTACCAGGCTGGTTCCACCCCCTGCAACGGTGTCGAGGGCTTCAACTGCTACTTCCCACTGCAATCTTACGGTTTCCAGCCTACTAACGGTGTGGGCTACCAGCCCTACAGAGTGGTCGTGCTGTCATTCGAACTGCTGCACGCCCCAGCTACTGTGTGCGGTCCTAAGAAGTCCACCAACCTGGTCAAGAACAAGTGCGTGAACTTCAACTTCAACGGCCTGACCGGAACTGGTGTCCTGACCGAGTCAAACAAGAAGTTCCTGCCATTCCAGCAGTTCGGAAGGGACATCGCTGACACCACTGACGCTGTGCGCGACCCTCAGACCCTGGAAATCCTGGACATCACTCCTTGCAGCTTCGGAGGTGTCTCTGTGATCACCCCTGGCACCAACACTTCCAACCAGGTCGCTGTGCTGTACCAGGACGTCAACTGCACCGAGGTGCCTGTGGCTATCCACGCTGACCAGCTGACCCCAACTTGGCGCGTGTACTCCACCGGCTCCAACGTCTTCCAGACTCGTGCTGGTTGCCTGATCGGCGCCGAGCACGTGAACAACTCATACGAATGCGACATCCCAATCGGCGCTGGAATCTGCGCCTCCTACCAGACCCAGACTAACTCACCTCGCCGTGCTCGCTCCGTCGCCTCCCAGAGCATCATCGCTTACACCATGAGCCTGGGCGCTGAAAACTCTGTGGCCTACTCCAACAACAGCATCGCCATCCCAACCAACTTCACTATCTCAGTGACCACTGAGATCCTGCCTGTCTCAATGACCAAGACTTCCGTGGACTGCACTATGTACATCTGCGGAGACTCAACCGAATGCTCCAACCTGCTGCTGCAATACGGCTCCTTCTGCACCCAGCTGAACCGTGCTCTGACTGGAATCGCCGTGGAGCAGGACAAGAACACTCAGGAAGTCTTCGCTCAGGTGAAGCAAATCTACAAGACCCCTCCCATCAAGGACTTCGGCGGATTCAACTTCTCCCAGATCCTGCCCGACCCATCTAAGCCTTCAAAGCGCTCCTTCATCGAGGACCTGCTGTTCAACAAGGTCACCCTGGCCGACGCTGGATTCATCAAGCAGTACGGAGACTGCCTGGGTGACATCGCCGCTCGTGACCTGATCTGCGCTCAGAAGTTCAACGGTCTGACCGTGCTGCCACCTCTGCTGACTGACGAAATGATCGCCCAGTACACTTCAGCCCTGCTGGCTGGAACCATCACTTCCGGTTGGACCTTCGGTGCTGGTGCTGCTCTGCAAATCCCCTTCGCTATGCAGATGGCCTACAGGTTCAACGGAATCGGTGTCACCCAGAACGTGCTGTACGAGAACCAGAAGCTGATCGCTAACCAGTTCAACAGCGCCATCGGAAAGATCCAGGACTCACTGTCATCCACTGCCTCCGCTCTGGGCAAGCTGCAAGACGTCGTGAACCAGAACGCCCAGGCTCTGAACACCCTGGTCAAGCAGCTGTCCTCCAACTTCGGTGCTATCTCATCCGTGCTGAACGACATCCTGTCTCGCCTGGACAAGGTCGAGGCCGAAGTGCAGATCGACCGCCTGATCACCGGCCGCCTGCAATCCCTGCAAACCTACGTGACTCAGCAGCTGATCAGGGCCGCTGAAATCAGAGCCTCTGCTAACCTGGCCGCTACCAAGATGTCAGAGTGCGTCCTGGGTCAGTCCAAGCGTGTGGACTTCTGCGGCAAGGGATACCACCTGATGAGCTTCCCCCAGTCTGCTCCACACGGCGTCGTGTTCCTGCACGTCACCTACGTGCCTGCCCAGGAGAAGAACTTCACCACTGCCCCCGCTATCTGCCACGACGGCAAGGCTCACTTCCCAAGGGAAGGTGTCTTCGTGTCAAACGGCACCCACTGGTTCGTCACTCAGAGAAACTTCTACGAGCCTCAGATCATCACCACTGACAACACTTTCGTGTCCGGAAACTGCGACGTCGTGATCGGTATCGTCAACAACACCGTGTACGACCCACTGCAACCTGAGCTGGACAGCTTCAAGGAGGAACTGGACAAATACTTCAAGAACCACACCTCTCCCGACGTGGACCTGGGTGACATCAGCGGAATCAACGCTTCTGTCGTGAACATCCAGAAGGAGATCGACCGTCTGAACGAAGTGGCTAAGAACCTGAACGAATCCCTGATCGACCTGCAAGAGCTGGGCAAGTACGAACAGTACATCAAGTGGCCTTGGTACATCTGGCTGGGTTTCATCGCTGGCCTGATCGCCATCGTCATGGTGACCATCATGCTGTGCTGCATGACTAGCTGCTGCTCTTGCCTGAAGGGCTGCTGCTCATGCGGTTCCTGCTGCAAGTTCGATGAAGACGATTCCGAGCCCGTTCTCAAAGGAGTGAAGTTGCATTACACATAA
Оптимизированная нуклеотидная последовательность гена, кодирующего S белок коронавируса (Индийский штамм) (SEQ ID NO:5)
TCCTCCCAATGCGTCAACCTCACTACCCGTACCCAGCTCCCACCAGCCTACACCAACAGCTTCACTCGCGGTGTGTACTACCCCGACAAGGTCTTCCGTTCCAGCGTGCTGCACAGCACTCAGGACCTGTTCCTGCCATTCTTCTCTAACGTGACCTGGTTCCACGCCATCCACGTGAGCGGCACCAACGGCACTAAGCGCTTCGACAACCCTGTGCTGCCCTTCAACGACGGTGTCTACTTCGCTTCCACCGAGAAGTCTAACATCATCCGTGGATGGATCTTCGGCACCACTCTGGACTCAAAGACTCAGTCCCTGCTGATCGTCAACAACGCCACCAACGTGGTCATCAAGGTGTGCGAGTTCCAGTTCTGCAACGACCCTTTCCTGGGCGTCTACTACCACAAGAACAACAAGAGCTGGATGGAGTCTGAGTTCCGCGTCTACTCTTCAGCTAACAACTGCACTTTCGAGTACGTGAGCCAGCCCTTCCTGATGGACCTGGAAGGAAAGCAGGGTAACTTCAAGAACCTGAGGGAGTTCGTGTTCAAGAACATCGACGGATACTTCAAGATTTACTCAAAGCACACCCCTATCAACCTGGTGCGCGACCTGCCACAGGGTTTCTCCGCTCTGGAGCCTCTGGTGGACCTGCCCATCGGCATCAACATCACCCGCTTCCAGACTCTGCTGGCTCTGCACCGTTCCTACCTGACTCCTGGCGACTCCAGCTCTGGATGGACCGCCGGAGCTGCCGCTTACTACGTGGGTTACCTGCAACCCAGGACCTTCCTGCTGAAGTACAACGAAAACGGAACCATCACAGACGCTGTGGACTGCGCTCTGGACCCCCTGAGCGAAACCAAGTGCACTCTGAAGTCTTTCACCGTGGAGAAGGGCATCTACCAGACTAGCAACTTCAGGGTGCAGCCAACCGAATCTATCGTCAGATTCCCCAACATCACTAACCTGTGCCCATTCGGAGAGGTCTTCAACGCCACCAGATTCGCTTCCGTGTACGCCTGGAACAGGAAGAGAATCAGCAACTGCGTCGCTGACTACTCTGTGCTGTACAACAGCGCCTCTTTCTCAACCTTCAAGTGCTACGGCGTGAGCCCTACTAAGCTGAACGACCTGTGCTTCACCAACGTCTACGCCGACTCTTTCGTGATCAGGGGAGACGAGGTCAGACAGATCGCTCCCGGCCAGACTGGAAAGATCGCCGACTACAACTACAAGCTGCCAGACGACTTCACCGGCTGCGTCATCGCTTGGAACTCAAACAACCTGGACTCCAAAGTGGGTGGCAACTACAACTACCTGTACCGCCTGTTCCGTAAGAGCAACCTGAAGCCTTTCGAGAGGGACATCTCAACTGAAATCTACCAGGCTGGTTCCACCCCCTGCAACGGTGTCGAGGGCTTCAACTGCTACTTCCCACTGCAATCTTACGGTTTCCAGCCTACTAACGGTGTGGGCTACCAGCCCTACAGAGTGGTCGTGCTGTCATTCGAACTGCTGCACGCCCCAGCTACTGTGTGCGGTCCTAAGAAGTCCACCAACCTGGTCAAGAACAAGTGCGTGAACTTCAACTTCAACGGCCTGACCGGAACTGGTGTCCTGACCGAGTCAAACAAGAAGTTCCTGCCATTCCAGCAGTTCGGAAGGGACATCGCTGACACCACTGACGCTGTGCGCGACCCTCAGACCCTGGAAATCCTGGACATCACTCCTTGCAGCTTCGGAGGTGTCTCTGTGATCACCCCTGGCACCAACACTTCCAACCAGGTCGCTGTGCTGTACCAGGACGTCAACTGCACCGAGGTGCCTGTGGCTATCCACGCTGACCAGCTGACCCCAACTTGGCGCGTGTACTCCACCGGCTCCAACGTCTTCCAGACTCGTGCTGGTTGCCTGATCGGCGCCGAGCACGTGAACAACTCATACGAATGCGACATCCCAATCGGCGCTGGAATCTGCGCCTCCTACCAGACCCAGACTAACTCACCTCGCCGTGCTCGCTCCGTCGCCTCCCAGAGCATCATCGCTTACACCATGAGCCTGGGCGCTGAAAACTCTGTGGCCTACTCCAACAACAGCATCGCCATCCCAACCAACTTCACTATCTCAGTGACCACTGAGATCCTGCCTGTCTCAATGACCAAGACTTCCGTGGACTGCACTATGTACATCTGCGGAGACTCAACCGAATGCTCCAACCTGCTGCTGCAATACGGCTCCTTCTGCACCCAGCTGAACCGTGCTCTGACTGGAATCGCCGTGGAGCAGGACAAGAACACTCAGGAAGTCTTCGCTCAGGTGAAGCAAATCTACAAGACCCCTCCCATCAAGGACTTCGGCGGATTCAACTTCTCCCAGATCCTGCCCGACCCATCTAAGCCTTCAAAGCGCTCCTTCATCGAGGACCTGCTGTTCAACAAGGTCACCCTGGCCGACGCTGGATTCATCAAGCAGTACGGAGACTGCCTGGGTGACATCGCCGCTCGTGACCTGATCTGCGCTCAGAAGTTCAACGGTCTGACCGTGCTGCCACCTCTGCTGACTGACGAAATGATCGCCCAGTACACTTCAGCCCTGCTGGCTGGAACCATCACTTCCGGTTGGACCTTCGGTGCTGGTGCTGCTCTGCAAATCCCCTTCGCTATGCAGATGGCCTACAGGTTCAACGGAATCGGTGTCACCCAGAACGTGCTGTACGAGAACCAGAAGCTGATCGCTAACCAGTTCAACAGCGCCATCGGAAAGATCCAGGACTCACTGTCATCCACTGCCTCCGCTCTGGGCAAGCTGCAAGACGTCGTGAACCAGAACGCCCAGGCTCTGAACACCCTGGTCAAGCAGCTGTCCTCCAACTTCGGTGCTATCTCATCCGTGCTGAACGACATCCTGTCTCGCCTGGACAAGGTCGAGGCCGAAGTGCAGATCGACCGCCTGATCACCGGCCGCCTGCAATCCCTGCAAACCTACGTGACTCAGCAGCTGATCAGGGCCGCTGAAATCAGAGCCTCTGCTAACCTGGCCGCTACCAAGATGTCAGAGTGCGTCCTGGGTCAGTCCAAGCGTGTGGACTTCTGCGGCAAGGGATACCACCTGATGAGCTTCCCCCAGTCTGCTCCACACGGCGTCGTGTTCCTGCACGTCACCTACGTGCCTGCCCAGGAGAAGAACTTCACCACTGCCCCCGCTATCTGCCACGACGGCAAGGCTCACTTCCCAAGGGAAGGTGTCTTCGTGTCAAACGGCACCCACTGGTTCGTCACTCAGAGAAACTTCTACGAGCCTCAGATCATCACCACTGACAACACTTTCGTGTCCGGAAACTGCGACGTCGTGATCGGTATCGTCAACAACACCGTGTACGACCCACTGCAACCTGAGCTGGACAGCTTCAAGGAGGAACTGGACAAATACTTCAAGAACCACACCTCTCCCGACGTGGACCTGGGTGACATCAGCGGAATCAACGCTTCTGTCGTGAACATCCAGAAGGAGATCGACCGTCTGAACGAAGTGGCTAAGAACCTGAACGAATCCCTGATCGACCTGCAAGAGCTGGGCAAGTACGAACAGTACATCAAGTGGCCTTGGTACATCTGGCTGGGTTTCATCGCTGGCCTGATCGCCATCGTCATGGTGACCATCATGCTGTGCTGCATGACTAGCTGCTGCTCTTGCCTGAAGGGCTGCTGCTCATGCGGTTCCTGCTGCAAGTTCGATGAAGACGATTCCGAGCCCGTTCTCAAAGGAGTGAAGTTGCATTACACA
Оптимизированная нуклеотидная последовательность гена, кодирующего S белок коронавируса (Южно-Африканский штамм) (SEQ ID NO:6)
TCCTCCCAATGCGTCAACCTCACTACCCGTACCCAGCTCCCACCAGCCTACACCAACAGCTTCACTCGCGGTGTGTACTACCCCGACAAGGTCTTCCGTTCCAGCGTGCTGCACAGCACTCAGGACCTGTTCCTGCCATTCTTCTCTAACGTGACCTGGTTCCACGCCATCCACGTGAGCGGCACCAACGGCACTAAGCGCTTCGACAACCCTGTGCTGCCCTTCAACGACGGTGTCTACTTCGCTTCCACCGAGAAGTCTAACATCATCCGTGGATGGATCTTCGGCACCACTCTGGACTCAAAGACTCAGTCCCTGCTGATCGTCAACAACGCCACCAACGTGGTCATCAAGGTGTGCGAGTTCCAGTTCTGCAACGACCCTTTCCTGGGCGTCTACTACCACAAGAACAACAAGAGCTGGATGGAGTCTGAGTTCCGCGTCTACTCTTCAGCTAACAACTGCACTTTCGAGTACGTGAGCCAGCCCTTCCTGATGGACCTGGAAGGAAAGCAGGGTAACTTCAAGAACCTGAGGGAGTTCGTGTTCAAGAACATCGACGGATACTTCAAGATTTACTCAAAGCACACCCCTATCAACCTGGTGCGCGACCTGCCACAGGGTTTCTCCGCTCTGGAGCCTCTGGTGGACCTGCCCATCGGCATCAACATCACCCGCTTCCAGACTCTGCTGGCTCTGCACCGTTCCTACCTGACTCCTGGCGACTCCAGCTCTGGATGGACCGCCGGAGCTGCCGCTTACTACGTGGGTTACCTGCAACCCAGGACCTTCCTGCTGAAGTACAACGAAAACGGAACCATCACAGACGCTGTGGACTGCGCTCTGGACCCCCTGAGCGAAACCAAGTGCACTCTGAAGTCTTTCACCGTGGAGAAGGGCATCTACCAGACTAGCAACTTCAGGGTGCAGCCAACCGAATCTATCGTCAGATTCCCCAACATCACTAACCTGTGCCCATTCGGAGAGGTCTTCAACGCCACCAGATTCGCTTCCGTGTACGCCTGGAACAGGAAGAGAATCAGCAACTGCGTCGCTGACTACTCTGTGCTGTACAACAGCGCCTCTTTCTCAACCTTCAAGTGCTACGGCGTGAGCCCTACTAAGCTGAACGACCTGTGCTTCACCAACGTCTACGCCGACTCTTTCGTGATCAGGGGAGACGAGGTCAGACAGATCGCTCCCGGCCAGACTGGAAACATCGCCGACTACAACTACAAGCTGCCAGACGACTTCACCGGCTGCGTCATCGCTTGGAACTCAAACAACCTGGACTCCAAAGTGGGTGGCAACTACAACTACCTGTACCGCCTGTTCCGTAAGAGCAACCTGAAGCCTTTCGAGAGGGACATCTCAACTGAAATCTACCAGGCTGGTTCCACCCCCTGCAACGGTGTCAAGGGCTTCAACTGCTACTTCCCACTGCAATCTTACGGTTTCCAGCCTACTTACGGTGTGGGCTACCAGCCCTACAGAGTGGTCGTGCTGTCATTCGAACTGCTGCACGCCCCAGCTACTGTGTGCGGTCCTAAGAAGTCCACCAACCTGGTCAAGAACAAGTGCGTGAACTTCAACTTCAACGGCCTGACCGGAACTGGTGTCCTGACCGAGTCAAACAAGAAGTTCCTGCCATTCCAGCAGTTCGGAAGGGACATCGCTGACACCACTGACGCTGTGCGCGACCCTCAGACCCTGGAAATCCTGGACATCACTCCTTGCAGCTTCGGAGGTGTCTCTGTGATCACCCCTGGCACCAACACTTCCAACCAGGTCGCTGTGCTGTACCAGGACGTCAACTGCACCGAGGTGCCTGTGGCTATCCACGCTGACCAGCTGACCCCAACTTGGCGCGTGTACTCCACCGGCTCCAACGTCTTCCAGACTCGTGCTGGTTGCCTGATCGGCGCCGAGCACGTGAACAACTCATACGAATGCGACATCCCAATCGGCGCTGGAATCTGCGCCTCCTACCAGACCCAGACTAACTCACCTCGCCGTGCTCGCTCCGTCGCCTCCCAGAGCATCATCGCTTACACCATGAGCCTGGGCGCTGAAAACTCTGTGGCCTACTCCAACAACAGCATCGCCATCCCAACCAACTTCACTATCTCAGTGACCACTGAGATCCTGCCTGTCTCAATGACCAAGACTTCCGTGGACTGCACTATGTACATCTGCGGAGACTCAACCGAATGCTCCAACCTGCTGCTGCAATACGGCTCCTTCTGCACCCAGCTGAACCGTGCTCTGACTGGAATCGCCGTGGAGCAGGACAAGAACACTCAGGAAGTCTTCGCTCAGGTGAAGCAAATCTACAAGACCCCTCCCATCAAGGACTTCGGCGGATTCAACTTCTCCCAGATCCTGCCCGACCCATCTAAGCCTTCAAAGCGCTCCTTCATCGAGGACCTGCTGTTCAACAAGGTCACCCTGGCCGACGCTGGATTCATCAAGCAGTACGGAGACTGCCTGGGTGACATCGCCGCTCGTGACCTGATCTGCGCTCAGAAGTTCAACGGTCTGACCGTGCTGCCACCTCTGCTGACTGACGAAATGATCGCCCAGTACACTTCAGCCCTGCTGGCTGGAACCATCACTTCCGGTTGGACCTTCGGTGCTGGTGCTGCTCTGCAAATCCCCTTCGCTATGCAGATGGCCTACAGGTTCAACGGAATCGGTGTCACCCAGAACGTGCTGTACGAGAACCAGAAGCTGATCGCTAACCAGTTCAACAGCGCCATCGGAAAGATCCAGGACTCACTGTCATCCACTGCCTCCGCTCTGGGCAAGCTGCAAGACGTCGTGAACCAGAACGCCCAGGCTCTGAACACCCTGGTCAAGCAGCTGTCCTCCAACTTCGGTGCTATCTCATCCGTGCTGAACGACATCCTGTCTCGCCTGGACAAGGTCGAGGCCGAAGTGCAGATCGACCGCCTGATCACCGGCCGCCTGCAATCCCTGCAAACCTACGTGACTCAGCAGCTGATCAGGGCCGCTGAAATCAGAGCCTCTGCTAACCTGGCCGCTACCAAGATGTCAGAGTGCGTCCTGGGTCAGTCCAAGCGTGTGGACTTCTGCGGCAAGGGATACCACCTGATGAGCTTCCCCCAGTCTGCTCCACACGGCGTCGTGTTCCTGCACGTCACCTACGTGCCTGCCCAGGAGAAGAACTTCACCACTGCCCCCGCTATCTGCCACGACGGCAAGGCTCACTTCCCAAGGGAAGGTGTCTTCGTGTCAAACGGCACCCACTGGTTCGTCACTCAGAGAAACTTCTACGAGCCTCAGATCATCACCACTGACAACACTTTCGTGTCCGGAAACTGCGACGTCGTGATCGGTATCGTCAACAACACCGTGTACGACCCACTGCAACCTGAGCTGGACAGCTTCAAGGAGGAACTGGACAAATACTTCAAGAACCACACCTCTCCCGACGTGGACCTGGGTGACATCAGCGGAATCAACGCTTCTGTCGTGAACATCCAGAAGGAGATCGACCGTCTGAACGAAGTGGCTAAGAACCTGAACGAATCCCTGATCGACCTGCAAGAGCTGGGCAAGTACGAACAGTACATCAAGTGGCCTTGGTACATCTGGCTGGGTTTCATCGCTGGCCTGATCGCCATCGTCATGGTGACCATCATGCTGTGCTGCATGACTAGCTGCTGCTCTTGCCTGAAGGGCTGCTGCTCATGCGGTTCCTGCTGCAAGTTCGATGAAGACGATTCCGAGCCCGTTCTCAAAGGAGTGAAGTTGCATTACACA
Оптимизированная нуклеотидная последовательность гена, кодирующего S белок коронавируса (Английский штамм) (SEQ ID NO:7)
TCCTCCCAATGCGTCAACCTCACTACCCGTACCCAGCTCCCACCAGCCTACACCAACAGCTTCACTCGCGGTGTGTACTACCCCGACAAGGTCTTCCGTTCCAGCGTGCTGCACAGCACTCAGGACCTGTTCCTGCCATTCTTCTCTAACGTGACCTGGTTCCACGCCATCAGCGGCACCAACGGCACTAAGCGCTTCGACAACCCTGTGCTGCCCTTCAACGACGGTGTCTACTTCGCTTCCACCGAGAAGTCTAACATCATCCGTGGATGGATCTTCGGCACCACTCTGGACTCAAAGACTCAGTCCCTGCTGATCGTCAACAACGCCACCAACGTGGTCATCAAGGTGTGCGAGTTCCAGTTCTGCAACGACCCTTTCCTGGGCGTCTACCACAAGAACAACAAGAGCTGGATGGAGTCTGAGTTCCGCGTCTACTCTTCAGCTAACAACTGCACTTTCGAGTACGTGAGCCAGCCCTTCCTGATGGACCTGGAAGGAAAGCAGGGTAACTTCAAGAACCTGAGGGAGTTCGTGTTCAAGAACATCGACGGATACTTCAAGATTTACTCAAAGCACACCCCTATCAACCTGGTGCGCGACCTGCCACAGGGTTTCTCCGCTCTGGAGCCTCTGGTGGACCTGCCCATCGGCATCAACATCACCCGCTTCCAGACTCTGCTGGCTCTGCACCGTTCCTACCTGACTCCTGGCGACTCCAGCTCTGGATGGACCGCCGGAGCTGCCGCTTACTACGTGGGTTACCTGCAACCCAGGACCTTCCTGCTGAAGTACAACGAAAACGGAACCATCACAGACGCTGTGGACTGCGCTCTGGACCCCCTGAGCGAAACCAAGTGCACTCTGAAGTCTTTCACCGTGGAGAAGGGCATCTACCAGACTAGCAACTTCAGGGTGCAGCCAACCGAATCTATCGTCAGATTCCCCAACATCACTAACCTGTGCCCATTCGGAGAGGTCTTCAACGCCACCAGATTCGCTTCCGTGTACGCCTGGAACAGGAAGAGAATCAGCAACTGCGTCGCTGACTACTCTGTGCTGTACAACAGCGCCTCTTTCTCAACCTTCAAGTGCTACGGCGTGAGCCCTACTAAGCTGAACGACCTGTGCTTCACCAACGTCTACGCCGACTCTTTCGTGATCAGGGGAGACGAGGTCAGACAGATCGCTCCCGGCCAGACTGGAAAGATCGCCGACTACAACTACAAGCTGCCAGACGACTTCACCGGCTGCGTCATCGCTTGGAACTCAAACAACCTGGACTCCAAAGTGGGTGGCAACTACAACTACCTGTACCGCCTGTTCCGTAAGAGCAACCTGAAGCCTTTCGAGAGGGACATCTCAACTGAAATCTACCAGGCTGGTTCCACCCCCTGCAACGGTGTCGAGGGCTTCAACTGCTACTTCCCACTGCAATCTTACGGTTTCCAGCCTACTTACGGTGTGGGCTACCAGCCCTACAGAGTGGTCGTGCTGTCATTCGAACTGCTGCACGCCCCAGCTACTGTGTGCGGTCCTAAGAAGTCCACCAACCTGGTCAAGAACAAGTGCGTGAACTTCAACTTCAACGGCCTGACCGGAACTGGTGTCCTGACCGAGTCAAACAAGAAGTTCCTGCCATTCCAGCAGTTCGGAAGGGACATCGACGACACCACTGACGCTGTGCGCGACCCTCAGACCCTGGAAATCCTGGACATCACTCCTTGCAGCTTCGGAGGTGTCTCTGTGATCACCCCTGGCACCAACACTTCCAACCAGGTCGCTGTGCTGTACCAGGGCGTCAACTGCACCGAGGTGCCTGTGGCTATCCACGCTGACCAGCTGACCCCAACTTGGCGCGTGTACTCCACCGGCTCCAACGTCTTCCAGACTCGTGCTGGTTGCCTGATCGGCGCCGAGCACGTGAACAACTCATACGAATGCGACATCCCAATCGGCGCTGGAATCTGCGCCTCCTACCAGACCCAGACTAACTCACMYCGCCGTGCTCGCTCCGTCGCCTCCCAGAGCATCATCGCTTACACCATGAGCCTGGGCGCTGAAAACTCTGTGGCCTACTCCAACAACAGCATCGCCATCCCAAYCAACTTCACTATCTCAGTGACCACTGAGATCCTGCCTGTCTCAATGACCAAGACTTCCGTGACTGCACTATGTACATCTGCGGAGACTCAACCGAATGCTCCAACCTGCTGCTGCAATACGGCTCCTTCTGCACCCAGCTGAACCGTGCTCTGACTGGAATCGCCGTGGAGCAGGACAAGAACACTCAGGAAGTCTTCGCTCAGGTGAAGCAAATCTACAAGACCCCTCCCATCAAGGACTTCGGCGGATTCAACTTCTCCCAGATCCTGCCCGACCCATCTAAGCCTTCAAAGCGCTCCTTCATCGAGGACCTGCTGTTCAACAAGGTCACCCTGGCCGACGCTGGATTCATCAAGCAGTACGGAGACTGCCTGGGTGACATCCCGCTCGTGACCTGATCTGCGCTCAGAAGTTCAACGGTCTGACCGTGCTGCCACCTCTGCTGACTGACGAAATGATCGCCCAGTACACTTCAGCCCTGCTGGCTGGAACCATCACTTCCGGTTGGACCTTCGGTGCTGGTGCTGCTCTGCAAATCCCCTTCGCTATGCAGATGGCCTACAGGTTCAACGGAATCGGTGTCACCCAGAACGTGCTGTACGAGAACCAGAAGCTGATCGCTAACCAGTTCAACAGCGCCATCGGAAAGATCCAGGACTCACTGTCATCCACTGCCTCCGCTCTGGGCAAGCTGCAAGACGTCGTGAACCAGAACGCCCAGGCTCTGAACACCCTGGTCAAGCAGCTGTCCTCCAACTTCGGTGCTATCTCATCCGTGCTGAACGACATCCTGGCTCGCCTGGACAAGGTCGAGGCCGAAGTGCAGATCGACCGCCTGATCACCGGCCGCCTGCAATCCCTGCAAACCTACGTGACTCAGCAGCTGATCAGGGCCGCTGAAATCAGAGCCTCTGCTAACCTGGCCGCTACCAAGATGTCAGAGTGCGTCCTGGGTCAGTCCAAGCGTGTGGACTTCTGCGGCAAGGGATACCACCTGATGAGCTTCCCCCAGTCTGCTCCACACGGCGTCGTGTTCCTGCACGTCACCTACGTGCCTGCCCAGGAGAAGAACTTCACCACTGCCCCCGCTATCTGCCACGACGGCAAGGCTCACTTCCCAAGGGAAGGTGTCTTCGTGTCAAACGGCACCCACTGGTTCGTCACTCAGAGAAACTTCTACGAGCCTCAGATCATCACCACTCACAACACTTTCGTGTCCGGAAACTGCGACGTCGTGATCGGTATCGTCAACAACACCGTGTACGACCCACTGCAACCTGAGCTGGACAGCTTCAAGGAGGAACTGGACAAATACTTCAAGAACCACACCTCTCCCGACGTGGACCTGGGTGACATCAGCGGAATCAACGCTTCTGTCGTGAACATCCAGAAGGAGATCGACCGTCTGAACGAAGTGGCTAAGAACCTGAACGAATCCCTGATCGACCTGCAAGAGCTGGGCAAGTACGAACAGTACATCAAGTGGCCTTGGTACATCTGGCTGGGTTTCATCGCTGGCCTGATCGCCATCGTCATGGTGACCATCATGCTGTGCTGCATGACTAGCTGCTGCTCTTGCCTGAAGGGCTGCTGCTCATGCGGTTCCTGCTGCAAGTTCGATGAAGACGATTCCGAGCCCGTTCTCAAAGGAGTGAAGTTGCATTACACA
| название | год | авторы | номер документа |
|---|---|---|---|
| Вирусоподобные химерные частицы для индукции специфического иммунитета против вируса тяжелого острого респираторного синдрома SARS-CoV-2, содержащие белки коронавируса и ротавируса | 2022 |
|
RU2779810C1 |
| Вакцина на основе вирусоподобных частиц (VLP) для профилактики COVID-19 для парентерального применения | 2024 |
|
RU2834060C1 |
| Вакцина на основе вирусоподобных частиц (VLP) для профилактики COVID-19 для интраназального применения | 2024 |
|
RU2828323C1 |
| ПОЛУЧЕНИЕ ВИРУСОПОДОБНЫХ ЧАСТИЦ В РАСТЕНИЯХ | 2011 |
|
RU2655431C2 |
| Иммунобиологическое средство на основе вирусоподобных частиц для индукции специфического иммунитета против инфекции, вызываемой ротавирусом А человека | 2022 |
|
RU2795055C1 |
| Вакцина против ротавирусной инфекции человека на основе вирусоподобных частиц ротавируса | 2024 |
|
RU2829862C1 |
| Искусственный ген, кодирующий бицистронную структуру, образованную последовательностями рецептор-связующего домена гликопротеина S коронавируса SARS-CoV-2, P2A-пептида и гликопротеина G VSV, рекомбинантная плазмида pStem-rVSV-Stbl_RBD_SC2, обеспечивающая экспрессию искусственного гена и рекомбинантный штамм вируса везикулярного стоматита rVSV-Stbl_RBD_SC2, используемого для создания вакцины против коронавируса SARS-CoV-2 | 2020 |
|
RU2733831C1 |
| Рекомбинантный RBD S-белок коронавируса SARS-CoV-2 и способ его получения | 2023 |
|
RU2833839C1 |
| Искусственный ген Stbl_RBD_TrM_SC2, кодирующий бицистронную структуру, образованную последовательностями рецепторсвязывающего домена гликопротеина S коронавируса SARS-CoV-2, трансмембранного региона, P2A-пептида и гликопротеина G VSV, рекомбинантная плазмида pStem-rVSV-Stbl_RBD_TrM_SC2, обеспечивающая экспрессию искусственного гена, и рекомбинантный штамм вируса везикулярного стоматита rVSV-Stbl_RBD_TrM_SC2, используемый для создания вакцины против коронавируса SARS-CoV-2 | 2020 |
|
RU2733832C1 |
| ЭФФЕКТИВНЫЕ ВИРУСОПОДОБНЫЕ ЧАСТИЦЫ (VLPS) ГРИППА | 2004 |
|
RU2369405C2 |




Группа изобретений относится к области биотехнологии и генной инженерии. Описана рекомбинантная вирусоподобная частица для индукции специфического иммунитета против вируса тяжелого острого респираторного синдрома SARS-CoV-2, содержащая рекомбинантные белки коронавируса E, M, N и один или несколько S белков различных штаммов коронавируса, содержащие нуклеотидные последовательности SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, которые получены в бакуловирусной системе экспрессии насекомых, при этом вирусоподобная частица имитирует вирион SARS-CoV-2. Также раскрыт способ получения рекомбинантной вирусоподобной частицы. И заявлен рекомбинантный бакуловирус для получения рекомбинантной вирусоподобной частицы, включающий ген, выбранный из группы: ген, кодирующий Е белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:1, ген, кодирующий М белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:2, ген, кодирующий N белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:3, ген, кодирующий S белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:4, ген, кодирующий S белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:5, ген, кодирующий S белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:6, ген, кодирующий S белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:7. Группа изобретений обеспечивает получение устойчивых вирусоподобных частиц, содержащих актуальные антигены коронавируса SARS-CoV-2, которые способны самособираться в клетках насекомых, имитирующих вирион коронавируса и способных индуцировать специфический иммунный ответ против вируса тяжелого острого респираторного синдрома SARS-CoV-2. 3 н. и 4 з.п. ф-лы, 7 ил., 4 пр.
1. Рекомбинантная вирусоподобная частица для индукции специфического иммунитета против вируса тяжелого острого респираторного синдрома SARS-CoV-2, содержащая рекомбинантные белки коронавируса E, M, N и один или несколько S белков различных штаммов коронавируса, содержащие нуклеотидные последовательности SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, которые получены в бакуловирусной системе экспрессии насекомых, при этом вирусоподобная частица имитирует вирион SARS-CoV-2.
2. Рекомбинантная вирусоподобная частица для индукции специфического иммунитета против вируса тяжелого острого респираторного синдрома SARS-CoV-2 по п.1, отличающаяся тем, что содержит рекомбинантные белки коронавируса E, M, N и S, имеющие нуклеотидные последовательности SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3 и SEQ ID NO:4.
3. Рекомбинантная вирусоподобная частица для индукции специфического иммунитета против вируса тяжелого острого респираторного синдрома SARS-CoV-2 по. 1, отличающаяся тем, что содержит рекомбинантные белки коронавируса E, M, N и S, имеющие нуклеотидные последовательности SEQ ID NO:1, SEQ ID NO:2, Q ID NO:3 и SEQ ID NO:5.
4. Рекомбинантная вирусоподобная частица для индукции специфического иммунитета против вируса тяжелого острого респираторного синдрома SARS-CoV-2 по п.1, отличающаяся тем, что содержит рекомбинантные белки коронавируса E, M, N и S, имеющие нуклеотидные последовательности SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3 и SEQ ID NO:6.
5. Рекомбинантная вирусоподобная частица для индукции специфического иммунитета против вируса тяжелого острого респираторного синдрома SARS-CoV-2 по п.1, отличающаяся тем, что содержит рекомбинантные белки коронавируса E, M, N и S, имеющие нуклеотидные последовательности SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3 и SEQ ID NO:7.
6. Рекомбинантный бакуловирус для получения рекомбинантной вирусоподобной частицы по пп.1-5, включающий ген, кодирующий Е белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:1, ген, кодирующий М белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:2, ген, кодирующий N белок коронавируса, имеющий нуклеотидную последовательность SEQ ID NO:3, и один или несколько генов, кодирующих S белок различных штаммов коронавируса, где ген, кодирующий S белок коронавируса, имеет нуклеотидную последовательность, выбранную из группы: SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7.
7. Способ получения рекомбинантной вирусоподобной частицы для индукции специфического иммунитета против вируса тяжелого острого респираторного синдрома SARS-CoV-2 по пп.1-5, включающий:
а) получение рекомбинантного бакуловируса по п.6,
б) коинфекцию перевиваемой линии клеток насекомых T.ni различными сочетаниями рекомбинантных бакуловирусов по п.6,
в) получение вирусоподобных частиц и их очистку.
| WO 2021022008 A1, 04.02.2021 | |||
| Ю.А.БЕЛИКОВА, Ю.В.САМСОНОВ и др | |||
| СОВРЕМЕННЫЕ ВАКЦИНЫ И КОРОНАВИРУСНЫЕ ИНФЕКЦИИ, Исследования и практика в медицине 2020, т.7, 4, с | |||
| Способ подпочвенного орошения с применением труб | 1921 |
|
SU139A1 |
| WO 2021156267 A1, 12.08.2021 | |||
| WO 2021211704 A1, 21.10.2021 | |||
| US 20060216702 A1, 28.09.2006 | |||
| S.G | |||
| KAMITA, K.-D.Kang и др., Genetically Modified Baculoviruses for Pest Insect Control, | |||
Авторы
Даты
2022-03-29—Публикация
2021-12-30—Подача