Группа изобретений относится к области биотехнологии, а именно генной инженерии, касается рекомбинантного белка рецептор-связывающего домена (RBD: receptor-binding-domain) - структурного домена гликопротеина spike SARS-CoV-2 и способа его получения и может быть использовано при создании ИФА-тест-систем и для конструирования вакцин против коронавирусной инфекции - COVID-19.
SARS-CoV-2 вызывает потенциально тяжелую острую респираторную инфекцию, которая получила название COVID-19. Для данного заболевания характерно наличие таких клинических симптомов, как повышение температуры тела (более чем в 90% случаев); кашель - сухой или с небольшим количеством мокроты (более чем в 80% случаев); одышка (в 55% случаев); утомляемость (в 44% случаев); ощущение заложенности в грудной клетке (более чем в 20% случаев). Наиболее тяжелыми осложнениями COVID-19 являются пневмония, острый респираторный дистресс-синдром, острая дыхательная недостаточность, острая сердечная недостаточность, острая почечная недостаточность, септический шок, кардиомиопатии, и др. Возбудителями заболевания являются коронавирусы.
Коронавирусы (CoV), включая SARS-CoV, MERS-CoV и SARS-CoV-2, представляют собой цитоплазматические оболочечные одноцепочечные (+)РНК-вирусы с четырьмя структурными белками (S-белок, белок оболочки (Е), мембранный (M) белок и нуклеокапсидный (N) белок). S-белок является ключевым в процессе инфицирования клетки хозяина, так как именно он ответственен за распознавание и взаимодействие с рецептором - ангиотензинпревращающим ферментом 2 (АСЕ2) [Ke Z., Oton J., Qu K., Cortese M. et al. Structures and distributions of SARS-CoV-2 spike proteins on intact virions//Nature - 2020. Vol.588. - P. 1-7.]. S-белок является трансмембранным белком, его наружная область имеет S1 и S2 домены. Домен S1 содержит две субъединицы: N-концевой домен (NTD) и С-концевой домен (CTD) [Walls А.C., Park Y.J., Tortorici M.A. et al. Structure, function, and antigenicity of the SARS-CoV-2 spike glycoprotein//Cell - 2020. Vol. 181 - P. 281-292.; Su Q., Yi Y., Zou Y. The biological characteristics of SARS-CoV-2 spike protein Pro330-Leu650//Vaccine - 2020.Vol. 38 - P.5071-5075.]. Домен CTD выступает в качестве рецептор-связывающего домена (RBD). RBD гликозилирован. Три RBD образуют тример и вращаются, обеспечивая доступ к рецептору на клетке-хозяине. Критическим этапом инфекции является взаимодействие рецептор-связывающего домена (RBD) S-белка с ангиотензин-превращающим ферментом 2 (АПФ2, АСЕ2) на поверхности клеток-мишеней, которое запускает конформационные изменения в структуре шина и тем самым опосредует проникновение вируса в клетки [J. Shang, Y. Wan, С. Luo et al. Cell entry mechanisms of SARS-CoV-2//Proceedings of the Natiotal Academy of Sciences of the United States of America. - 2020. V. 117. №21 - P. 11727-11734.].
Учитывая роль RBD в инфицировании клеток, а также тот факт, что большинство нейтрализующих антител, вырабатываемых при инфекции или вакцинации, направлены на этот регион, RBD считается ключевым местом уязвимости SARS-CoV-2 [Н. Kleanthous, J.M. Silverman, K.W. Makar et al. Scientific rationale for developing potent RBD-based vaccines targeting COVID-19//Vaccines. - 2021.V.6.№1 - P. 1-10.].
Из литературных источников известно, что рекомбинантные варианты RBD SARS-CoV-2 или фрагменты S-белка, содержащие RBD, могут быть использованы для создания новых средств диагностики, терапии и профилактики коронавирусной инфекции COVID-19.
Известны плазмидные генетические конструкции, обеспечивающие экспрессию рекомбинантных RBD S-белков SARS-CoV-2 в прокариотической системе - Escherichia coli. Так, в штамме Escherichia coli BL21(DE3) были экспрессированы белки 6His-RBDshort (24,4 кД) и 6His-RBDlong (33,7 кД), после проведения дополнительных исследований которых рекомбинантный белок 6His-RBDshort может быть рассмотрен в качестве перспективного препарата для использования в терапевтических целях в качестве блокатора рецептора АСЕ2 [Громова М.С., Громов А.В., Грунина Т.М., Лящук A.M., Галушкина З.М., Субботина М.Е., Есмагамбеков И.Б., Рябова Е.И., Прокофьев В.В., Ковыршина А.В., Илюхина А.А., Шелков А.Ю., Карягина А.С., Лунин В.Г. Получение рекомбинантного RBD Spike-белка SARS-CoV-2 в клетках Escherichia coli, связывание с антителами, и противовирусная активность//Молекулярная генетика, микробиология и вирусология. - 2023 - №41. - С.28-35.]. Представлены рекомбинантные плазмидные ДНК pET/RBD, pET/N, обеспечивающие экспрессию рекомбинантных белков RBD, N коронавируса SARS-CoV-2 и содержащие плазмидный вектор рЕТ28, включающий фрагмент, кодирующий олигопептид LEHHHHHH или AAALEHHHHHH, фрагмент размером 632 п.о., кодирующий фрагмент белка S (RBD) коронавируса SARS-CoV-2 с 327 по 532 аминокислотные остатки, или фрагмент размером 1250 п.о., кодирующий белок N коронавируса SARS-CoV-2, которые обеспечивают синтез в клетках Escherichia coli рекомбинантных белков RBD [патент Республики Казахстан №35233, 2021]. Еще описана плазмидная генетическая конструкция рЕТ21_Ab_CoV-2_1.3, обеспечивающая экспрессию в прокариотической системе Escherichia coli рекомбинантного белка ABCOV-21.3, обладающего свойствами однодоменного наноантитела против SARS-CoV-2, который может служить компонентом для создания диагностикумов COVID-19 [патент РФ №2798508, 2023]. Раскрыта рекомбинантная плазмида, обеспечивающая синтез в клетках Escherichia coli указанного рекомбинантного белка, причем указанная плазмида получена путем клонирования фрагмента ДНК с нуклеотидной последовательностью SEQ ID NO: 8 или SEQ ID NO: 1 в плазмидный вектор pET39b по сайтам рестрикции NdeI/XhoI [патент РФ №2778942, 2022]. Представлены также рекомбинантные белки коронавируса SARS-CoV-2E, М, N и один или несколько S белков различных штаммов коронавируса SARS-CoV-2, содержащие нуклеотидные последовательности SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, которые получены в бакуловирусной системе экспрессии насекомых [патент РФ №2769224, 2022].
Рекомбинантные варианты RBD, полученные в различных системах экспрессии бактерий, насекомых, растений, млекопитающих, могут значительно отличаться по структуре и свойствам. Во-первых, это связано с особенностями посттрансляционных модификаций или их отсутствием в той или иной системе экспрессии. Во-вторых, несмотря на то, что домен является функционально и структурно обособленной единицей белка, при его вычленении из структуры целого белка также могут произойти структурные изменения, критически влияющие на свойства и функции молекулы.
Задача заявляемой группы изобретений - рекомбинантный RBD S-белок коронавируса SARS-CoV-2 и способ его получения.
Техническим результатом группы изобретений являются рекомбинантный RBD S-белок коронавируса SARS-CoV-2 со структурой в соответствии с последовательностью RBD Cov19:
MASNFRAQPTESIVRFPNITNLCPFGEVFNATRFASVYAWNRKRISNCVADYSVLYNSASFSTFKCYGVSPTKLNDLCFTNVYADSFVIRGDEVRQIAPGQTGKIADYNYKLPDDFTGCVIAWNSNNLDSKVGGNYNYLYRLFRKSNLKPFERDISTEIYQAGSTPCNGVEGFNCYFPLQSYGFQPTNGVGYQPYRVVVLSFELLHAPATVCGPKKSTNLVKNKCVNFNFNGLTGTGVLAESNKKFLLFQQFGRDIADTTDAVRDPQTLEILDITPCSFGGVSVITPGTNTSNQVAVLYQGVNCTEVPVAIHADQLTPTWRVYSTGSNVFQTRAGCLIGAEHVNNSYECDIPIGAGICASYQTQTNSPRRARSVASQSIIAYTMSLGAENSVAYSNNSIAIPTNFTISVTTEILPVSMTKTSVDCTMYICGHHHHHH
и способ получения RBD S-белка коронавируса SARS-CoV-2, идентичного натуральному вирусному белку по своим физико-химическим и иммунологическим свойствам.
Технический результат достигается RBD S-белком коронавируса SARS-CoV-2 размером 437 аминокислот с молекулярной массой 48,61 кДа и структурой в соответствии с последовательностью RBD Cov19, и способом его получения, включающим трансформацию клеток штамма метилотрофных дрожжей Pichia pastoris SuperMan 5-23 плазмидой, предварительно полученной в клетках Escherichia coli, несущей целевую вставку, с последующим культивированием в подходящей культуральной среде и выделением методом аффинной хроматографии.
Способ осуществляется следующим образом.
В клетках E.coli синтезируют плазмиду, содержащую последовательность, кодирующую RBD регион белка S коронавируса SARS-CoV-2 со структурой в соответствии с последовательностью RBD Cov19:
MASNFRAQPTESIVRFPNITNLCPFGEVFNATRFASVYAWNRKRISNCVADYSVLYNSASFSTFKCYGVSPTKLNDLCFTNVYADSFVIRGDEVRQIAPGQTGKIADYNYKLPDDFTGCVIAWNSNNLDSKVGGNYNYLYRLFRKSNLKPFERDISTEIYQAGSTPCNGVEGFNCYFPLQSYGFQPTNGVGYQPYRVVVLSFELLHAPATVCGPKKSTNLVKNKCVNFNFNGLTGTGVLAESNKKFLLFQQFGRDIADTTDAVRDPQTLEILDITPCSFGGVSVITPGTNTSNQVAVLYQGVNCTEVPVAIHADQLTPTWRVYSTGSNVFQTRAGCLIGAEHVNNSYECDIPIGAGICASYQTQTNSPRRARSVASQSIIAYTMSLGAENSVAYSNNSIAIPTNFTISVTTEILPVSMTKTSVDCTMYICGHHHHHH
которую используют для трансформации клеток штамма метилотрофных дрожжей Pichia pastoris SuperMan 5-23 с последующим их культивированием при температуре 30°С в течение 24 часов в среде BMGY составом 1% дрожжевой экстракт, 2% пептон, 100 мМ калий-фосфатный буфер с рН=6,0, 1,34% YNB, 4×10-5% биотин, 1% глицерин и 100 мкг/мл канамицин и выделением RBD S-белка коронавируса SARS-CoV-2 методом аффинной хроматографии.
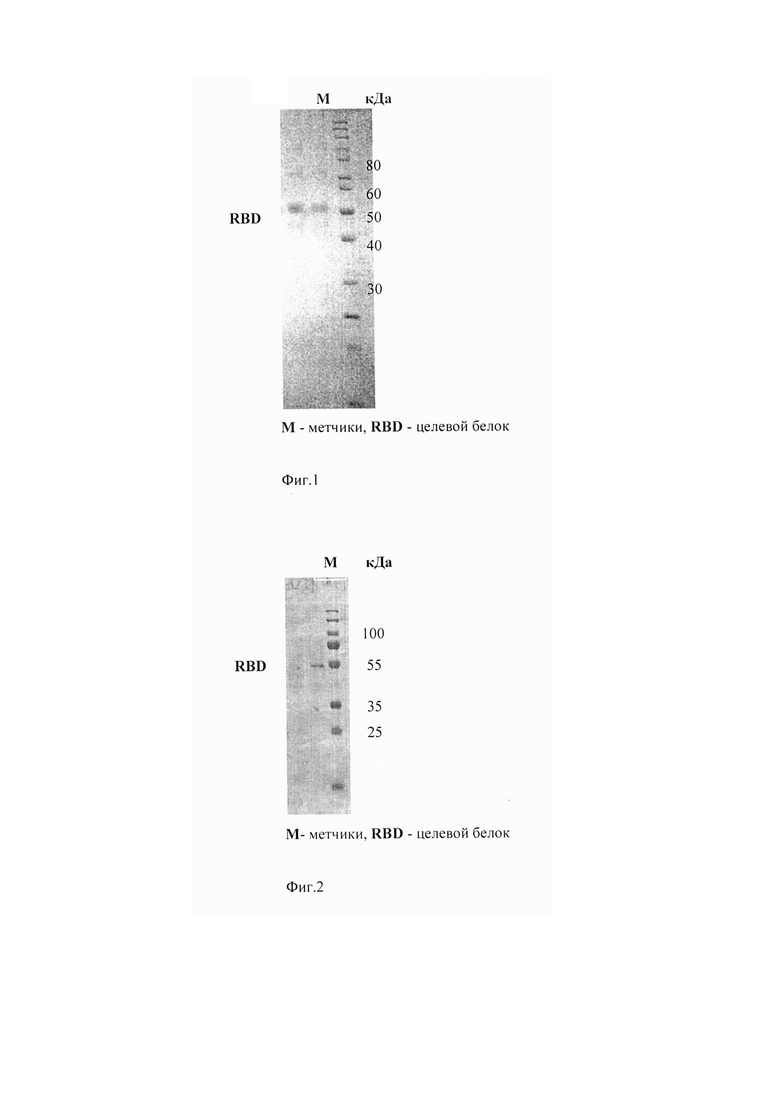
Изобретение поясняется графическими материалами, представленными на фиг. 1 и 2:
- на фиг. 1 показаны результаты очистки рекомбинантного RBD из P.pastoris
- на фиг 2 показаны результаты иммуноблоттинга, подтверждающие наличие целевого рекомбинантного белка RBD в полученных пробах.
Сущность изобретения поясняется примерами.
Пример 1. Конструирование слитого белка.
В работе использовали нуклеотидные последовательности (н.п.) генов фрагмента RBD S-белка коронавируса человека, полученных из штаммов, циркулирующих на территории России. В первичной структуре РНК коронавируса методами биоинформатики определяли участок, кодирующий RBD регион S-белка, добавляли последовательность, кодирующую 6 гистидинов, и стоп-кодон. Полученную нуклеотидную последовательность использовали для предсказания последовательности аминокислотной. Конструирование гена проводили на основе анализа нуклеотидных последовательностей с использованием пакета программ Lasergene (Dnastar, Inc). ДНК синтезировали в ООО "Люмипроб РУС" (Россия) и клонировали в составе pPicZA (Novagen, США).
Пример 2. Экспрессия и очистка рекомбинантного RBD S-белка коронавируса SARS-CoV-2.
Для экспрессии рекомбинантного белка использовали штамм метилотрофных дрожжей Pichia pastoris Super Man.5-23 (BioGrammatics, США). Клетки штамма Pichia pastoris трансформировали плазмидой, кодирующей рекомбинантный белок, с использованием мультипоратора фирмы Eppendorf (Германия). Pichia pastoris выращивали при 30°С в среде BMGY (1% дрожжевой экстракт, 2% пептон, 100 мМ калий-фосфатный буфер с рН=6,0, 1,34% YNB, 4×10-5% биотин, 1% глицерин и 100 мкг/мл канамицин) в течение 24 часов. После инкубации в данной среде клетки осаждали центрифугированием при 13 000 об/мин и +8°С в течение 15 мин на центрифуге Heraeus Megafuge 16 R (ThermoFischer Scientific, США), после чего ресуспендировали в среде BMMY (1% дрожжевой экстракт, 2% пептон, 100 мМ калий-фосфатного буфера с рН=6,0, 1,34% YNB, 4×10-5% биотин, 0,5% метанол и 100 мкг/мл канамицин) до оптической плотности 1, после чего культуру инкубировали в течение 24 часов при 30°С. Клетки повторно осаждали центрифугированием в аналогичных условиях, ресуспендировали в буфере А (50 мМ трис-HCI, 150 мМ NaCI, 8 М мочевина, 5 мМ имидазол, рН=7,5) и дезинтегрировали баллистическим методом с использованием мелких стеклянных шариков диаметром 0,5 мм (Sigma Aldrich) с добавлением свежеприготовленного 100 мМ раствора фенилметилсульфонилфторида (PMSF) в 100% изопропаноле до конечной концентрации 1 мМ. Дезинтеграцию проводили на вортексе V1-plus (Biosan, Латвия). Дезинтеграт осветляли центрифугированием при 13000 об/мин и +8°С в течение 15 мин. Затем проводили аффинную хроматографию с использованием IMAC Sepharose 6 Fast Flow (GE Healthcare, Швеция) согласно рекомендациям производителя для денатурирующих условий: супернатант наносили на предварительно уравновешенный буфером А аффинный носитель batch-методом, то есть при постоянном перемешивании на шейкере в течение 30 мин, после чего смесь переносили в колонки, промывали буфером В (50 мМ трис-HCI, 150 мМ NaCI, 8 М мочевина, 20 мМ имидазол, рН=7,5) в количестве, равном 10-15 объемам использованного аффинного носителя, и проводили элюцию целевого белка с помощью буфера С (50 мМ трис-HCI, 150 мМ NaCI, 8 М мочевина, 250 мМ имидазол, рН=7,5). Ренатурацию белка осуществляли методом диализа против 1000 объемов буфера, содержащего 10 мМ трис-HCI, рН=7,8, 5% сахарозу и 0,9% NaCI, в течение 12 часов.
Пример 3. Определение концентрации RBD S-белка коронавируса SARS-CoV-2.
Концентрацию белка в растворе определяли на спектрофотометре NanoDrop 2000 (Thermo Scientific, США) при длине волны 280 нм.
Пример 4. Электрофорез в ПААГ и иммуноблоттинг.
Все этапы экспрессии и очистки рекомбинантного белка контролировали методом электрофореза белков в 10% ПААГ в присутствии додецилсульфата натрия. Результаты визуализировали окрашиванием геля с помощью Coomassie brilliant blue R250. Использовали маркер молекулярных масс Thermo Scientific PageRuler Unstained Protein Ladder (10 to 200 kDa). Для проведения иммуноблоттинга белки переносили из геля на мембрану PVDF (Thermo Scientific, США) с использованием системы влажного переноса (Bio-Rad, США). Для контроля переноса и определения молекулярной массы использовали PageRuler Plus Prestained Protein Ladder (Thermo Scientific, США). Мембрану блокировали 1% бычьим сывороточным альбумином в фосфатно-солевом буфере и инкубировали с антителами anti-HisHRP :GG1-6F4.3.2 (Miltenyi Biotec, США). Мембрану окрашивали в растворе субстрата Super Signal West Dura Extended Duration Substrate (Thermo Scientific, США) и измеряли хемилюминесценцию с помощью сканера C-DiGit Biot Scanner (Li-Cor, США), согласно рекомендациям производителей.
Пример 5. Характеристика антигенных свойств рекомбинантного RBD S-белка коронавируса SARS-CoV-2.
Антигенные свойства исследовали методом иммуноферментного анализа. Для этого полученный RBD разводили в физиологическом растворе и сорбировали в 96-луночном планшете, инкубация продолжалась в течение 12 часов с последующей 10-кратной промывкой. Затем в лунки добавляли по 90 мкл раствора фосфатно-солевого буфера с твином (ФСБ-Т), рН=7,3, и по 10 мкл плазмы крови человека, заведомо содержащей антитела к коронавирусу согласно предварительным исследованиям. Инкубировали в термостатируемом шейкере при температуре 37°С в течение 60 минут с частотой 500 об/мин. После инкубации лунки планшета снова промывали 10 раз 1х ФСБ-Т. По окончании промывки удаляли остатки влаги и вносили во все лунки по 100 мкл раствора конъюгата (140 нг/мл), представляющего собой продуцируемые клоном 3D3cc моноклональные антитела к IgG, меченные пероксидазой хрена (МоАТ к IgG HPR) производства Hytest (Россия), и инкубировали 60 минут в шейкере при температуре 37°С. После инкубации снова повторяли отмывку 1х ФСБ-Т 10 раз. Далее вносили во все лунки по 100 мкл раствора ТМБ Hytest (Россия) и инкубировали 10 минут, избегая попадания солнечного света. Реакцию останавливали 50 мкл IN серной кислоты и измеряли величину оптической плотности на спектрофотометре Infinite М200 Pro (Tecan, Austria) в двухволновом режиме: при основной длине волны 450 нм и длине волны сравнения 680 нм. Анализ полученных данных проводили с использованием компьютерных программ Magellan 7.2 (Tecan, Austria) и Microsoft Excel (Microsoft, США).
Проведенные исследования показали, что заявляемое техническое решение позволяет получать in vitro рекомбинантный белок, представляющий собой RBD домен коронавируса SARS-CoV-2.
После индукции в Pichia pastoris нарабатывался дополнительный белок, содержащий последовательность из 6 гистидинов, что подтверждало экспрессию RBD. При сравнении набора белков Pichia pastoris в растворимой и осадочной фракциях установлено, что в растворимой фракции присутствовало некоторое количество белка с ориентировочной молекулярной массой 50-53 кДа. Расчетная масса чистого RBD составляла 48,61 кДа, дополнительно вес полученного фрагмента должен был несколько увеличиваться за счет гликозилирования, следовательно, электрофоретическая подвижность очищенного RBD совпадала с расчетной.
Сохранение антигенных свойств RBD оценивали по его взаимодействию с антителами к S-белку коронавируса, присутствующими в плазме крови лиц, контактировавших с возбудителем или вакцинированных от него. Были обследованы 123 образца сывороток крови здоровых людей, из которых 82, по предварительным данным, содержали антитела против S-белка коронавируса SARS-CoV-2, а 41 - нет. Данные были получены путем исследования образцов с помощью коммерческих тест-систем SARS-CoV-2 Ig G-ИФА-БЕСТ производства АО «Вектор-Бест». Результаты исследования полученного рекомбинантного RBD показали совпадение с предварительными данными, то есть антитела к природному S-белку распознавали рекомбинантый RBD, тогда как в сыворотках, не содержавших этих антител, реакции с рекомбинантным белком не происходило.
--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing originalFreeTextLanguageCode="en"
nonEnglishFreeTextLanguageCode="ru" dtdVersion="V1_3"
fileName="RBD.xml" softwareName="WIPO Sequence"
softwareVersion="2.3.0" productionDate="2023-09-07">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>1</ApplicationNumberText>
<FilingDate>2023-09-05</FilingDate>
</ApplicationIdentification>
<ApplicantFileReference>1</ApplicantFileReference>
<EarliestPriorityApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>1</ApplicationNumberText>
<FilingDate>2023-09-05</FilingDate>
</EarliestPriorityApplicationIdentification>
<ApplicantName languageCode="ru">Федеральное бюджетное учреждение
науки «Нижегородский научно-исследовательский институт эпидемиологии
и микробиологии им. академика И.Н. Блохиной» Федеральной службы по
надзору в сфере защиты прав потребителей и благополучия человека
(ФБУН ННИИЭМ им. академика И.Н. Блохиной
Роспотребнадзора)</ApplicantName>
<ApplicantNameLatin>Blokhina Scientific Research Institute of
Epidemiology and Microbiology of Nizhny Novgorod</ApplicantNameLatin>
<InventorName languageCode="ru">Новиков Дмитрий
Викторович</InventorName>
<InventorNameLatin>Novikov, Dmitry V.</InventorNameLatin>
<InventionTitle languageCode="ru">Рекомбинантный RBD S-белок
коронавируса SARS-CoV-2 и способ его получения</InventionTitle>
<SequenceTotalQuantity>1</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>437</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..437</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q4">
<INSDQualifier_name>note</INSDQualifier_name>
<NonEnglishQualifier_value>русский</NonEnglishQualifier_value>
</INSDQualifier>
<INSDQualifier id="q3">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>SARS-CoV-2</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>MASNFRAQPTESIVRFPNITNLCPFGEVFNATRFASVYAWNRKRISNCV
ADYSVLYNSASFSTFKCYGVSPTKLNDLCFTNVYADSFVIRGDEVRQIAPGQTGKIADYNYKLPDDFTGC
VIAWNSNNLDSKVGGNYNYLYRLFRKSNLKPFERDISTEIYQAGSTPCNGVEGFNCYFPLQSYGFQPTNG
VGYQPYRVVVLSFELLHAPATVCGPKKSTNLVKNKCVNFNFNGLTGTGVLAESNKKFLLFQQFGRDIADT
TDAVRDPQTLEILDITPCSFGGVSVITPGTNTSNQVAVLYQGVNCTEVPVAIHADQLTPTWRVYSTGSNV
FQTRAGCLIGAEHVNNSYECDIPIGAGICASYQTQTNSPRRARSVASQSIIAYTMSLGAENSVAYSNNSI
AIPTNFTISVTTEILPVSMTKTSVDCTMYICGHHHHHH</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
Группа изобретений относится к области биотехнологии, а именно генной инженерии. Описан рекомбинантный белок рецептор-связывающего домена (RBD: receptor-binding-domain) - структурного домена гликопротеина spike SARS-CoV-2. Раскрыт способ получения указанного белка. Рекомбинантный RBD S-белок коронавируса SARS-CoV-2 имеет размер 437 аминокислот с молекулярной массой 48,61 кДа. Данный белок получают трансформацией клеток штамма метилотрофных дрожжей Pichia pastoris SuperMan 5-23 синтезированной в клетках Escherichia coli плазмидой, содержащей последовательность в соответствии с последовательностью RBD Cov19: MASNFRAQPTESIVRFPNITNLCPFGEVFNATRFASVYAWNRKRISNCVADYSVLYNSASFSTFKCYGVSPTKLNDLCFTNVYADSFVIRGDEVRQIAPGQTGKIADYNYKLPDDFTGCVIAWNSNNLDSKVGGNYNYLYRLFRKSNLKPFERDISTEIYQAGSTPCNGVEGFNCYFPLQSYGFQPTNGVGYQPYRVVVLSFELLHAPATVCGPKKSTNLVKNKCVNFNFNGLTGTGVLAESNKKFLLFQQFGRDIADTTDAVRDPQTLEILDITPCSFGGVSVITPGTNTSNQVAVLYQGVNCTEVPVAIHADQLTPTWRVYSTGSNVFQTRAGCLIGAEHVNNSYECDIPIGAGICASYQTQTNSPRRARSVASQSIIAYTMSLGAENSVAYSNNSIAIPTNFTISVTTEILPVSMTKTSVDCTMYICGHHHHHH, их культивированием при температуре 30°С в течение 24 часов в среде BMGY составом: 1% дрожжевой экстракт, 2% пептон, 100 мМ калий-фосфатный буфер с рН=6,0, 1,34% YNB, 4×10-5% биотин, 1% глицерин и 100 мкг/мл канамицин и выделением методом аффинной хроматографии. Изобретение может быть использовано при создании ИФА-тест-систем и для конструирования вакцин против коронавирусной инфекции - COVID-19. 2 н.п. ф-лы, 2 ил., 5 пр.
1. Рекомбинантный RBD S-белок коронавируса SARS-CoV-2, используемый для изготовления вакцин против SARS-CoV-2 и создания иммуноферментной тест-системы для серологической диагностики SARS-CoV-2 размером 437 аминокислот с молекулярной массой 48,61 кДа и со структурой в соответствии с последовательностью SEQ ID NO: 1.
2. Способ получения белка по п. 1, включающий трансформацию клеток штамма метилотрофных дрожжей Pichia pastoris SuperMan 5-23 синтезированной в клетках Escherichia coli плазмидой, содержащей последовательность, кодирующую рекомбинантный RBD S-белок коронавируса SARS-CoV-2 по п. 1, их культивирование при температуре 30°С в течение 24 часов в среде BMGY составом: 1% дрожжевой экстракт, 2% пептон, 100 мМ калий-фосфатный буфер с pH=6,0, 1,34% YNB, 4×10-5% биотин, 1% глицерин и 100 мкг/мл канамицин и выделение методом аффинной хроматографии.
| Генная конструкция для экспрессии рекомбинантных белков на основе участка S-белка SARS-CoV-2, включающего RBD и SD1, слитого с Fc фрагментом IgG, способ получения рекомбинантных белков, антигены и антигенные композиции для индукции длительного антительного и клеточного иммунитета против вируса SARS-CoV-2 | 2021 |
|
RU2802825C2 |
| US 20230287087 A1, 14.09.2023 | |||
| WO 2021100012 A1, 27.05.2021. | |||
Авторы
Даты
2025-01-29—Публикация
2023-10-09—Подача