ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] По настоящей заявке испрашивается приоритет патентных заявок США с серийными №№ 61/708931, зарегистрированной 2 октября 2012 года, и 61/818573, зарегистрированной 2 мая 2013 года, содержание каждой из которых полностью включено в качестве ссылки для всех целей
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0002] Настоящее изобретение относится к обработанным материалам, получаемым из биомассы, включая технологические потоки биомассы (например, лигнина, сахара), при ожижении биомассы, при биопиролизе масла, черного щелока, угля, при ожижении угля, природного газа или нефти. В частности, настоящее изобретение относится к системам и способам для восстановительного расщепления связей C-O, C-N и C-S в ароматических соединениях, таких как ароматические соединения, находящиеся в таких технологических потоках.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
[0003] В последние несколько десятилетий, растущие потребности в энергии в комбинации со снижением резервов ископаемых видов топлива породили большой всплеск интереса к эффективному производству топлива и химических веществ массового производства из возобновляемых биоресурсов. Основной мишенью для экономически эффективной переработки биомассы стал природный гетеробиополимерный лигнин вследствие того, что ароматические простоэфирные структурные единицы могут обеспечивать продукты с высоким содержанием энергии и потенциальный доступ к подходящим производным для тонких химических приложений. Однако в настоящее время использование лигнина явно ограничено, так как современные технологии не обеспечивают эффективного разложения на составляющие его структурные единицы с желательной селективностью. Одной из основных трудностей, ассоциированных с таким процессом, является необходимость в восстановительном расщеплении различных типов сильных ароматических связей C-O, присутствующих в лигнине (фиг.1), что также является значимой проблемой для ожижения угля.
[0004] С дополнительными трудностями сталкиваются в обработке продуктов из угля и нефти, где усиливающееся природоохранное законодательство требует фактического устранения серы из сырьевых потоков. Окисление серы приводит к образованию оксидов сера, которые нежелательны для экологии сами по себе, а также имеют тенденцию к отравлению используемых катализаторов из драгоценных металлов, например, в каталитических конвертерах. Существует большой интерес в технологиях, где не только происходит деполимеризация биомассы, но где осуществляются действия по снижению или устранению остаточной серы из этих сырьевых материалов.
[0005] Известно, что катализаторы с Ni обеспечивают избирательные восстановительные преобразования, включающие арил-кислородные связи, но только при загрузках 5-20%, а на этих уровнях использование Ni и других переходных металлов-катализаторов является проблематичным, с точки зрения экономической и экологической перспективы. Кроме того, сведений о том, что такие катализаторы пригодны для связей C-N или C-S, нет. И хотя было бы выгодно обладать общей методологией расщепления ароматических связей C-O, в которой бы не применялся никель или другие переходные металлы-катализаторы, единственный известный альтернативный подход к расщеплению простых эфиров без использования металлов при относительно низких температурах основан на избытке щелочных металлов или на электрокаталитических процессах, которые, как правило, являются дорогостоящими, нестабильными и практически нецелесообразными.
[0006] Настоящее изобретение относится решению по меньшей мере некоторых из этих проблем.
СУЩНОСТЬ
[0007] В различных вариантах осуществления настоящего изобретения предоставлены химические системы для восстановления связей C-O, C-N и C-S, каждая система содержит смесь (a) по меньшей мере одного органосилана и (b) по меньшей мере одного сильного основания, где указанная система по существу не содержит соединений переходных металлов, и указанная система необязательно содержит по меньшей мере одно соединение-донор молекулярного водорода, молекулярный водород или оба.
[0008] В других вариантах осуществления предоставлены способы восстановления связей C-X в органическом субстрате, где X представляет собой O, N или S, где каждый способ, включает приведение определенного количества субстрата, содержащего по меньшей мере одну связь C-O, C-N или C-S в контакт с химической системой, содержащей смесь (a) по меньшей мере одного органосилана и (b) по меньшей мере одного сильного основания, в условиях, подходящих для восстановления связей C-X по меньшей мере части этого количества субстрата; где указанная химическая система по существу не содержит соединений переходных металлов, и указанная химическая система необязательно содержит по меньшей мере одно соединение-донор молекулярного водорода, молекулярный водород или оба.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0009] Настоящая заявка будет более понятна при чтении совместно с приложенными фигурами. С целью иллюстрации объекта изобретения представлены изображения иллюстративных вариантов осуществления объекта изобретения; однако описанный в настоящем документе объект изобретения не ограничен описанными конкретными способами, устройствами и системами. Кроме того, фигуры не обязательно изображены в масштабе. На фигурах:
[0010] Фиг.1A и 1B иллюстрируют примеры связей C-O, таких, которые присутствуют в лигнинах твердых пород деревьев. Фиг.1C иллюстрирует некоторые из модельных соединений, описываемых в этой заявки в отношении ключевых связей C-O.
[0011] На фиг.2 представлен спектр EPR реакционной смеси дибензофурана, Et3SiH и KOt-Bu в толуоле, как описано в примере 5.8. Такой же сигнал наблюдают без добавления дибензофурана.
ПОДРОБНОЕ ОПИСАНИЕ ИЛЛЮСТРАТИВНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0012] Настоящее изобретение основано на группе реакций, каждая из которых основана на простых смесях органосиланов и сильных оснований, которые совместно формируют восстановительные системы in situ (структура и характер которых полностью пока неизвестны), способные к активации связей C-O, C-N и C-S в жидкой фазе в жидкой фазе без обязательного присутствия переходных металлов-катализаторов, облучения УФ или электрических разрядов. Эти реакции рассматриваются как значительный прогресс в разработке практических способов разложения основанных на биомассе сырьевых потоков на ароматическое сырье и топливо. Важно, что эта реакция представляет большой интерес, так как в ней в качестве побочного продукта образуются только экологически безвредные силикаты и устранены стоки токсических металлов, как можно наблюдать почти во всех других подходах, предлагаемых в литературе в этом отношении. В случае соединений серы, протокол активации двойных связей C-S наблюдали в условиях реакции, приводящих к формальному удалению атома серы из молекулы субстрата. Это замечательное наблюдение также свойственно для десульфурирования содержащих серу примесей во фракциях неочищенной нефти, что представляет большой интерес и имеет большое значение.
[0013] Настоящее изобретение можно легче понять на основании приведенного ниже описания, взятого вместе с сопровождающими фигурами и примерами, которые все формируют часть настоящего изобретения. Следует понимать, что настоящее изобретение не ограничено конкретными продуктами, способами, условиями или параметрами, описанными или представленными в настоящем документе, и что терминология, используемая в настоящем документе, предназначена с целью описания конкретных вариантов осуществления исключительно в качестве примера и не предназначена ни для какого ограничения описываемого в заявке изобретения. Подобным образом, если конкретно не указано иначе, любое описание возможного механизма или способа действия или причины улучшения предназначено исключительно для иллюстрации, и изобретение, описанное в настоящем документе, не следует ограничивать правильностью или неправильностью любого такого предполагаемого механизма или способа действия или причины улучшения. На всем протяжении этого текста принято, что описания относятся к композициям и способам получения и использования указанных композиций. То есть, когда в описании описаны или в пункте формулы изобретения приведены характеристика или вариант осуществления, ассоциированные с композицией или способом получения или использования композиции, следует понимать, что такое описание или пункт формулы изобретения предназначены для расширения этих характеристик или варианта осуществления до вариантов осуществления в каждом из этих контекстов (т.е. композиций, способов получения и способов использования).
[0014] В настоящем описании формы единственного числа включают указание на множественное число, а указание конкретного числового значения включает по меньшей мере это конкретное значение, если по контексту явно не требуется иначе. Таким образом, например, указание на "материал" представляет собой указание по меньшей мере на один из таких материалов и их эквивалентов, известных специалистам в данной области, и т.д.
[0015] Когда значение выражено в виде приближения посредством использования ключевого слова "приблизительно", следует понимать, что конкретное значение составляет другой вариант осуществления. Как правило, использование термина "приблизительно" означает приближения, которые могут варьировать в зависимости от желаемых свойств, которые необходимо получать посредством описываемого объекта изобретения, и его необходимо истолковывать в конкретном контексте, в котором его используют на основе его функции. Специалист в данной области легко может это истолковать. В некоторых случаях одним из неограничивающих способов определения пределов слова "приблизительно" может являться количество значащих цифр, используемых для конкретного значения. В других случаях, для определения заданного диапазона, предлагаемого термином "приблизительно", для каждого значения можно использовать градации, используемые в ряде значений. Когда они приведены, все диапазоны являются включительными и комбинируемыми. То есть, указания значений, приведенных в диапазонах, включают каждое значение в этом диапазоне.
[0016] Следует понимать, что определенные признаки изобретения, которые для ясности описаны в настоящем документе в рамках отдельных вариантов осуществления, также могут быть представлены в комбинации в одном варианте осуществления. То есть, если это не является явно несовместимым или конкретно не исключено, подразумевают, что каждый отдельный вариант осуществления можно комбинировать с любым другим вариантом(ами) осуществления, и такую комбинацию следует рассматривать, как другой вариант осуществления. И наоборот, различные признаки изобретения, которые для краткости описаны в рамках одного варианта осуществления, также могут быть представлены раздельно или в любой подкомбинации. Наконец, хотя вариант осуществления может быть описан как часть ряда этапов или часть более общей структуры, каждый указанный этап сам по себе также можно рассматривать как независимый вариант осуществления, комбинируемый с другими.
[0017] Переходные термины "содержащий", "по существу состоящий из" и "состоящий" предназначены для их общего обозначения в значениях, принятых в патентной лексике; т.е. (i) "содержащий", который является синонимом "включающему", "вмещающему" или "характеризующемуся", является включительным или незамкнутым и не исключает дополнительных, неперечисленных элементов или этапов способов; (ii) "состоящий из" исключает любой элемент, этап или ингредиент, не указанный в пункте; и (iii) "по существу состоящий из" ограничивает пределы пункта указанными материалами или этапами "и тем, что существенно не влияет на основную и новую характеристику(и)" описываемого в заявке изобретения. Варианты осуществления, описываемые посредством фразы "содержащие" (или ее эквивалентов), также предоставляют, в качестве вариантов осуществления, варианты осуществления, которые независимо описаны посредством "состоящий из" и "по существу состоящий из". Для вариантов осуществления, предоставленных посредством "по существу состоящий из", основная и новая характеристика(и) реализуемы в способах (или системах, используемых в таких способах или композициях, получаемых в них) в виде не содержащего переходных металлов способа проведения восстановительного расщепления связей C-O, C-N или C-S.
[0018] Если не указано иначе, когда представлен список, следует понимать, что каждый отдельный элемент этого списка и любая комбинация из этого списка представляют собой отдельный вариант осуществления. Например, список вариантов осуществления, представленный как "A, B или C" следует понимать, как включающий варианты осуществления, "A", "B", "C", "A или B", "A или C", "B или C" или "A, B или C".
[0019] На всем протяжении этого описания, предусмотрено, что слова имеют их нормальное значение, как понимают специалисты в соответствующей области. Однако во избежание разногласий конкретно определены или уточнены значения некоторых терминов.
[0020] Как используют в настоящем документе, как правило, термин "алкил" относится к неразветвленной, разветвленной или циклической насыщенной углеводородной группе, хотя и не обязательно, содержащей от 1 до приблизительно 24 атомов углерода, предпочтительно от 1 до приблизительно 12 атомов углерода, такой как метильная, этильная, н-пропильная, изопропильная, н-бутильная, изобутильная, трет-бутильная, октильная, децильная и т.п., а также циклоалкильная группы, такие как циклопентил, циклогексил и т.п. Как правило, хотя снова не обязательно, алкильные группы в настоящем документе содержат от 1 до приблизительно 12 атомов углерода. Термин "низший алкил" означает алкильную группу с 1-6 атомами углерода, а конкретный термин "циклоалкил" означает циклическую алкильную группу, как правило, содержащую от 4 до 8, предпочтительно от 5 до 7, атомов углерода. Термин "замещенный алкил" относится к алкильным группам, замещенным одной или несколькими группами заместителей, а термины "содержащий гетероатомы алкил" и "гетероалкил" относятся к алкильным группам, в которых по меньшей мере один атом углерода замещен гетероатомом. Если не указано иначе, термины "алкил" и "низший алкил" включают неразветвленные, разветвленные, циклические, незамещенные, замещенные и/или содержащие гетероатомы алкильные и низшие алкильные группы, соответственно.
[0021] Как используют в настоящем документе, термин "алкилен" относится к дифункциональной неразветвленной, разветвленной или циклической алкильной группе, где "алкил" является таким, как определено выше.
[0022] Как используют в настоящем документе, термин "алкенил" относится к неразветвленной, разветвленной или циклической углеводородной группе с количеством атомов углерода от 2 до приблизительно 24, содержащей по меньшей мере одну двойную связь, такой как этенил, н-пропенил, изопропенил, н-бутенил, изобутенил, октенил, деценил, тетрадеценил, гексадеценил, эйкозенил, тетракозенил и т.п. Предпочтительные алкенильные группы в настоящем документе содержат от 2 до приблизительно 12 атомов углерода. Термин "низший алкенил" означает алкенильную группу из с 2-6 атомами углерода, а конкретный термин "циклоалкенил" означает циклическую алкенильную группа, предпочтительно содержащую от 5 до 8 атомов углерода. Термин "замещенный алкенил" относится к алкенильным группам, замещенным одной или несколькими группами заместителей, а термины "содержащий гетероатомы алкенил" и "гетероалкенил" относятся к алкенильным группам, в которых по меньшей мере один атом углерода замещен гетероатомом. Если не указано иначе, термины "алкенил" и "низший алкенил" включают неразветвленные, разветвленные, циклические, незамещенные, замещенные и/или содержащие гетероатомы алкенильные и низшие алкенильные группы, соответственно.
[0023] Как используют в настоящем документе, термин "алкенилен" относится к дифункциональной неразветвленной, разветвленной или циклической алкенильной группе, где "алкенил" является таким, как определено выше.
[0024] Как используют в настоящем документе, термин "алкинил" относится к неразветвленной или разветвленной углеводородной группе с количеством атомов углерода от 2 до приблизительно 24, содержащей по меньшей мере одну тройную связь, такой как этинил, н-пропинил и т.п. Предпочтительные алкинильные группы в настоящем документе содержат от 2 до приблизительно 12 атомов углерода. Термин "низший алкинил" означает алкинильную группу с 2-6 атомами углерода. Термин "замещенный алкинил" относится к алкинильной группе, замещенной одной или несколькими группами заместителей, а термины "содержащий гетероатомы алкинил" и "гетероалкинил" относятся к алкинилу, в котором по меньшей мере один атом углерода замещен гетероатомом. Если не указано иначе, термины "алкинил" и "низший алкинил" включают неразветвленную, разветвленную, незамещенную, замещенную и/или содержащую гетероатомы алкинильную и низшую алкинильную группу, соответственно.
[0025] Как используют в настоящем документе, термин "алкокси" означает алкильную группу, связанную одинарной, концевой простоэфирной связью; т.е. "алкоксигруппу" можно представить как -O-алкил, где алкил является таким, как определено выше. "Низшая алкоксигруппа" означает алкоксигруппу, содержащую от 1 до 6 атомов углерода. Аналогично, "алкенилокси" и "низшая алкенилокси" соответственно относятся к алкенильной и низшей алкенильной группе, связанной одинарной, концевой простоэфирной связью, а "алкинилокси" и "низшая алкинилокси" соответственно относятся к алкинильной и низшей алкинильной группе, связанной одинарной, концевой простоэфирной связью.
[0026] Термин "ароматическая" относится к циклическим группам, которые удовлетворяют правилу Хюккеля 4n+2 для ароматичности, и включает арильные (т.е. карбоциклические) и гетероарильные (так называемые гетероароматические) структуры, включающие арильные, аралкильные, алкарильные, гетероарильные, гетероаралкильные или алкгетероарильные группы.
[0027] Как используют в настоящем документе и если не указано иначе, термин "арил" относится к ароматическим заместителю или структуре, содержащим одно ароматическое кольцо или несколько ароматических колец, которые конденсированы, непосредственно связаны или связаны опосредованно (так, что различные ароматические кольца связаны с общей группой, такой как метиленовая или этиленовая группа). Если не модифицировано иным образом, термин "арил" относится к карбоциклическим структурам. Предпочтительные арильные группы содержат от 5 до 24 атомов углерода, а особенно предпочтительные арильные группы содержат от 5 до 14 атомов углерода. Иллюстративные арильные группы содержат одно ароматическое кольцо или два конденсированных или связанных ароматических кольца, например, фенил, нафтил, бифенил, дифениловый эфир, дифениламин, бензофенон и т.п. "Замещенный арил" относится к арильной группе, замещенной одной или несколькими группами заместителей, а термины "содержащий гетероатомы арил" и "гетероарил" относятся к арильным заместителям, в которых по меньшей мере один атом углерода замещен гетероатомом, как более подробно описано ниже.
[0028] Как используют в настоящем документе, термин "арилокси" относится к арильной группе, связанной одинарной, концевой простоэфирной связью, где "арил" является таким, как определено выше. "Арилоксигруппу" можно представить как -O-арил, где арил является таким, как определено выше. Предпочтительные арилоксигруппы содержат от 5 до 24 атомов углерода, а особенно предпочтительные арилоксигруппы содержат от 5 до 14 атомов углерода. Примеры арилоксигрупп в качестве неограничивающих примеров включают фенокси, о-галогенфенокси, м-галогенфенокси, п-галогенфенокси, о-метоксифенокси, м-метоксифенокси, п-метоксифенокси, 2,4-диметоксифенокси, 3,4,5-триметоксифенокси и т.п.
[0029] Термин "алкарил" относится к арильной группе с алкильным заместителем, а термин "аралкил" относится к алкильной группа с арильным заместителем, где "арил" и "алкил" являются такими, как определено выше. Предпочтительные алкарильные и аралкильные группы содержат от 6 до 24 атомов углерода, а особенно предпочтительные алкарильные и аралкильные группы содержат от 6 до 16 атомов углерода. Алкарильные группы включают, например, п-метилфенил, 2,4-диметилфенил, п-циклогексилфенил, 2,7-диметилнафтил, 7-циклооктилнафтил, 3-этил-циклопента-1,4-диен и т.п. Примеры аралкильных групп в качестве неограничивающих примеров включают бензил, 2-фенилэтил, 3-фенилпропил, 4-фенилбутил, 5-фенилпентил, 4-фенилциклогексил, 4-бензилциклогексил, 4-фенилциклогексилметил, 4-бензилциклогексилметил и т.п. Термины "алкарилокси" и "аралкилокси" относятся к заместителям формулы -OR, где R представляет собой алкарил или аралкил, соответственно, как только что определено.
[0030] Термин "ацил" относится к заместителям формулы -(CO)-алкил, -(CO)-арил или -(CO)-аралкил, а термин "ацилокси" относится к заместителям формулы -O(CO)-алкил, -O(CO)-арил или -O(CO)-аралкил, где "алкил", "арил и "аралкил" являются такими, как определено выше.
[0031] Термины "циклический" и "цикл" относятся к алициклическим или ароматическим группам, которые могут быть или могут не быть замещенными и/или содержащими гетероатомы, и которые могут быть моноциклическими, бициклическими или полициклическими. Термин "алициклический" используют в общепринятом смысле для обозначения алифатической циклической группы в противоположность ароматической циклической группе, и она может быть моноциклической, бициклической или полициклической. Термин "ациклический" относится к структуре, в которой в кольцевой структуре может содержаться или не содержаться двойная связь.
[0032] Термины "галогеновый", "галогенид" и "галоген" используют в общепринятом для обозначения заместителей в виде хлора, брома, фтора или иода.
[0033] "Гидрокарбил" относится к одновалентным гидрокарбильным радикалам, содержащим от 1 до приблизительно 30 атомов углерода, предпочтительно от 1 до приблизительно 24 атомов углерода, наиболее предпочтительно от 1 до приблизительно 12 атомов углерода, включающих неразветвленные, разветвленные, циклическые, насыщенные и ненасыщенные группы, такие как алкильные группы, алкенильные группы, арильные группы и т.п. Термин "низший гидрокарбил" означает гидрокарбильную группу с 1-6 атомами углерода, предпочтительно 1-4 атомами углерода, а термин "гидрокарбилен" означает двухвалентную гидрокарбильную группу, содержащую от 1 до приблизительно 30 атомов углерода, предпочтительно от 1 до приблизительно 24 атомов углерода, наиболее предпочтительно от 1 до приблизительно 12 атомов углерода, включающую неразветвленные, разветвленные, циклические, насыщенные и ненасыщенные группы. Термин "низший гидрокарбилен" означает гидрокарбиленовую группу с 1-6 атомами углерода. "Замещенный гидрокарбил" относится к гидрокарбилу, замещенному одной или несколькими группами заместителей, а термины "содержащий гетероатомы гидрокарбил" и "гетерогидрокарбил" относятся к гидрокарбилу, в котором по меньшей мере один атом углерода замещен гетероатомом. Подобным образом, "замещенный гидрокарбилен" относится к гидрокарбилену, замещенному одной или несколькими группами заместителей, а термины "содержащий гетероатомы гидрокарбилен" и гетерогидрокарбилен" относятся к гидрокарбилену, в котором по меньшей мере один атом углерода замещен гетероатомом. Если не указано иначе, термин "гидрокарбил" и "гидрокарбилен" следует понимать как включающие замещенные и/или содержащие гетероатомы гидрокарбильные и гидрокарбиленовые группы, соответственно.
[0034] Термин "содержащий гетероатомы", например, как в "содержащей гетероатомы гидрокарбильной группе" относится к молекуле углеводорода или к гидрокарбильному фрагменту молекулы, в котором один или несколько атомов углерода замещены атомом, отличным от углерода, например, азотом, кислородом, серой, фосфором или кремнием, как правило азотом, кислородом или серой. Подобным образом, термин "гетероалкил" относится к алкильному заместителю, который содержит гетероатомы, термин "гетероциклический" относится к циклическому заместителю, который содержит гетероатомы, термины "гетероарил" и "гетероароматический", соответственно, относятся к "арильному" и "ароматическому" заместителя, которые содержат гетероатомы, и т.п. Следует отметить, что "гетероциклическая" группа или соединение могут быть или могут не быть ароматическими, и дополнительно, что "гетероциклы" могут быть моноциклическими, бициклическими или полициклическими, как описано выше в отношении термина "арил". Примеры гетероалкильных групп включают алкоксиарил, замещенный алкилсульфанилом алкил, N-алкилированный аминоалкил и т.п. Примеры гетероарильных заместителей включают пирролил, пирролидинил, пиридинил, хинолинил, индолил, пиримидинил, имидазолил, 1,2,4-триазолил, тетразолил и т.д., а примеры содержащих гетероатомы алициклических групп представляют собой пирролидино, морфолино, пиперазино, пиперидино и т.д.
[0035] Под "замещенным", например, как в "замещенном гидрокарбиле", "замещенном алкиле", "замещенном ариле" и т.п., как указано в некоторых из приведенных выше определений, подразумевают то, что в гидрокарбильной, алкильной, арильной или другой группе по меньшей мере один атом водорода, связанный с атомом углерода (или другим атомом), замещен одним или несколькими неводородными заместителями. Примеры таких заместителей в качестве неограничивающих примеров включают: функциональные группы, обозначаемые в настоящем документе как "Fn", такие как галоген, гидроксил, сульфгидрил, C1-C24-алкокси, C2-C24-алкенилокси, C2-C24-алкинилокси, C5-C24-арилокси, C6-C24-аралкилокси, C6-C24-алкарилокси, ацил (включая C1-C24-алкилкарбонил (-CO-алкил) и C6-C24-арилкарбонил (-CO-арил)), ацилокси (-O-ацил, включая C2-C24-алкилкарбонилокси (-O-CO-алкил) и C6-C24-арилкарбонилокси (-O-CO-арил)), C2-C24-алкоксикарбонил ((CO)-O-алкил), C6-C24-арилоксикарбонил (-(CO)-O-арил), галогенкарбонил (-CO)-X, где X представляет собой галоген), C2-C24-алкилкарбонато (-O-(CO)-O-алкил), C6-C24-арилкарбонато (-O-(CO)-O-арил), карбокси (-COOH), карбоксилато (-COO-), карбамоил (-(CO)-NH2), моно-(C1-C24-алкил)-замещенный карбамоил (-(CO)NH(C1-C24-алкил)), ди-(C1-C24-алкил)-замещенный карбамоил (-(CO)-N(C1-C24-алкил)2), моно-(C1-C24-галогеналкил)-замещенный карбамоил (-(CO)-NH(C1-C24-алкил)), ди-(C1-C24-галогеналкил)-замещенный карбамоил (-(CO)-N(C1-C24-алкил)2), моно-(C5-C24-арил)-замещенный карбамоил (-(CO)-NH-арил), ди-(C5-C24-арил)-замещенный карбамоил (-(CO)-N(C5-C24-арил)2), ди-N-(C1-C24-алкил),N-(C5-C24-арил)-замещенный карбамоил, тиокарбамоил (-(CS)-NH2), моно-(C1-C24-алкил)-замещенный тиокарбамоил (-(CO)-NH(C1-C24-алкил)), ди-(C1-C24-алкил)-замещенный тиокарбамоил (-(CO)-N(C1-C24-алкил)2), моно-(C5-C24-арил)-замещенный тиокарбамоил (-(CO)-NH-арил), ди-(C5-C24-арил)-замещенный тиокарбамоил (-(CO)-N(C5-C24-арил)2), ди-N-(C1-C24-алкил),N-(C5-C24-арил)-замещенный тиокарбамоил, карбамидо (-NH-(CO)-NH2), циано(-C≡N), цианато (-O-C=N), тиоцианато (-S-C=N), формил (-(CO)-H), тиоформил (-(CS)-H), амино (-NH2), моно-(C1-C24-алкил)-замещенный амино, ди-( C1-C24-алкил)-замещенный амино, моно-(C5-C24-арил)-замещенный амино, ди-(C5-C24-арил)-замещенный амино, C1-C24-алкиламидо (-NH-(CO)-алкил), C6-C24-ариламидо (-NH-(CO)-арил), имино (-CR=NH, где R =водород, C1-C24-алкил, C5-C24-арил, C6-C24-алкарил, C6-C24-аралкил и т.д.), C2-C20-алкилимино (-CR=N(алкил), где R = водород, C1-C24-алкил, C5-C24-арил, C6-C24-алкарил, C6-C24-аралкил и т.д.), арилимино (-CR=N( арил), где R = водород, C1-C20-алкил, C5-C24-арил, C6-C24-алкарил, C6-C24-аралкил и т.д.), нитро (-NO2), нитрозо (-NO), сульфо (-SO2OH), сульфонат (SO2O-), C1-C24-алкилсульфанил (-S-алкил; также называемый "алкилтио"), C5-C24-арилсульфанил (-S-арил; также называемый "арилтио"), C1-C24-алкилсульфинил (-(SO)-алкил), C5-C24-арилсульфинил (-(SO)-арил), C1-C24-алкилсульфонил (-SO2-алкил), C1-C24-моноалкиламиносульфонил-SO2-N(H)-алкил), C1-C24 диалкиламиносульфонил-SO2-N(алкил)2, C5-C24-арилсульфонил (-SO2-арил), борил (-BH2), бороно (-B(OH)2), боронато (-B(OR)2, где R представляет собой алкил или другой гидрокарбил), фосфоно (-P(O)(OH)2), фосфонато (-P(O)(O)2), фосфинато (P(O)(O-)), фосфо (-PO2) и фосфин (-PH2); и гидрокарбильные группы C1-C24-алкил (предпочтительно C1-C12-алкил, более предпочтительно C1-C6-алкил), C2-C24-алкенил (предпочтительно C2-C12-алкенил, более предпочтительно C2-C6-алкенил), C2-C24-алкинил (предпочтительно C2-C12-алкинил, более предпочтительно C2-C6-алкинил), C5-C24-арил (предпочтительно C5-C24-арил), C6-C24-алкарил (предпочтительно C6-C16-алкарил) и C6-C24-аралкил (предпочтительно C6-C16-аралкил). В этих структурах заместителей, "алкильная", "алкиленовая", "алкенильная", "алкениленовая", "алкинильная", "алкиниленовая", "алкокси", "ароматическая", "арильная", "арилокси", "алкарильная" и "аралкильная" группы необязательно могут быть фторированы или перфторированы. Кроме того, указание спиртов, альдегидов, аминов, карбоновых кислот, кетонов или других подобных реакционноспособных функциональных групп также включает их защищенные аналоги. Например, указание гидрокси или спирта также включает заместители, где гидрокси защищен ацетилом (Ac), бензоилом (Bz), бензилом (Bn, Bnl), простым β-метоксиэтоксиметиловым эфиром (MEM), диметокситритилом, [бис-(4-метоксифенил)фенилметилом] (DMT), простым метоксиметиловым эфиром (MOM), метокситритил-[(4-метоксифенил)дифенилметилом, (MMT), простым п-метоксибензиловым эфиром (PMB), простым метилтиометиловым эфиром, пивалоилом (Piv), тетрагидропиранилом (THP), тетрагидрофураном (THF), тритилом (трифенилметилом, Tr), простым силиловым эфиром (наиболее широкоиспользуемые простые силиловые эфиры включают простые триметилсилиловый (TMS), трет-бутилдиметилсилиловый (TBDMS), три-изо-пропилсилилоксиметиловый (TOM) и триизопропилсилиловый (TIPS) эфиры), этоксиэтиловые эфиры (EE). Указание аминов также включает заместители, где амин защищен BOC-глициновой, карбобензилокси (Cbz), п-метоксибензилкарбониловой (Moz или MeOZ), трет-бутилоксикарбониловой (BOC), 9-флуоренилметилоксикарбониловой (FMOC), ацетиловой (Ac), бензоиловой (Bz), бензиловой (Bn), карбаматной, п-метоксибензиловой (PMB), 3,4-диметоксибензиловой (DMPM), п-метоксифениловой (PMP), тозиловой (Ts) группой или сульфонамидной (Nosyl & Nps) группой. Указание заместителя, содержащего карбонильную группу, также включает заместители, где карбонил защищен ацетальной или кетальной, ацилальной или диатановой группой. Указание заместителя, содержащего карбоксильную или карбоксилатную группу, также включает заместители, где карбоксильная или карбоксилатная группа защищена образованным ею сложным метиловым эфиром, сложным бензиловым эфиром, трет-бутиловым сложным эфиром, сложным эфиром 2,6-двузамещенного фенола (например, 2,6-диметилфенол, 2,6-диизопропилфенол, 2,6-ди-трет-бутилфенол), сложным силиловым эфиром, ортоэфиром или оксазолином.
[0036] Под "функционализированным", как в "функционализированном гидрокарбил", "функционализированным алкилом", "функционализированным олефином", "функционализированным циклическим олефином" и т.п., подразумевают, что в гидрокарбиле, алкиле, олефине, циклическом олефин или другой группе по меньшей мере один атом водорода, связанный с атомом углерода (или другим атомом) замещен одной или несколькими функциональными группами, такими как функциональные группы, описываемые в настоящем документе и выше. Термин "функциональная группа" предназначен для включения любых функциональных групп, которые подходят для применений, описываемых в настоящем документе. В частности, как используют в настоящем документе, функциональная группа обязательно должна обладать способностью реагировать или связываться с соответствующими функциональными группами на поверхности субстрата.
[0037] Кроме того, указанные выше функциональные группы, если конкретная группа допускает, могут быть дополнительно замещены одной или несколькими дополнительными функциональными группами или одной или несколькими гидрокарбильными группами, такими как группы конкретно перечисленные выше. Аналогично, указанные выше гидрокарбильные группы могут быть дополнительно замещены одной или несколькими функциональными группами или дополнительными гидрокарбильными группами, такими как конкретно перечисленные группы.
[0038] "Необязательный" или "необязательно" означает, что описанное далее условие может выполняться или нет так, что описание включает варианты, когда условие выполняется, и варианты, когда оно не выполняется. Например, фраза "необязательно замещенный" означает, что неводородный заместитель может присутствовать на данном атоме или нет, и, таким образом, описание включает структуры, где неводородный заместитель присутствует, и структуры, где неводородный заместитель не присутствует.
[0039] Настоящее изобретение включает варианты осуществления, относящиеся к химическим системам и способам восстановления связей C-O, C-N и C-S. Конкретные варианты осуществления относятся к химическим системам восстановления связей C-O, C-N и C-S, где каждая система содержит смесь (a) по меньшей мере одного органосилана и (b) по меньшей мере одного сильного основания, где указанная система предпочтительно по существу не содержит соединений переходных металлов. Хотя в определенных вариантах осуществления предусмотрено, что переходные металлы, включая переходные металлы, способные к катализу реакций силилирования, могут присутствовать в системах или способах, описываемых в настоящем документе, на уровнях, обычно ассоциируемых с такой каталитической активностью, присутствие таких металлов (даже как катализаторов или обычных соединений) не требуется и во многих случаях нежелательно. По этой причине в предпочтительных вариантах осуществления системы и способы "по существу не содержат соединений переходных металлов". Как используют в настоящем документе, термин "по существу не содержит соединений переходных металлов" предназначен для отражения того, что система эффективна в отношении своей цели восстановления связей C-O, C-N и C-S даже в отсутствие любого экзогенного (т.е. преднамеренно добавляемого или иначе) переходного металла-катализатора(ов). Если не указано иначе, в дальнейшем, термин "по существу не содержит соединений переходных металлов" определен для отражения того, что общий уровень переходных металлов в системе восстановления, независимо или в присутствии органического субстрата, составляет менее чем приблизительно 50 м.д., как измеряют посредством ICP-MS, как описано в примере 2 ниже. В дополнительных вариантах осуществления также предусмотрено, что концентрация переходных металлов составляет менее чем приблизительно 100 м.д., 50 м.д., 30 м.д., 25 м.д., 20 м.д., 15 м.д., 10 м.д. или 5 м.д. до приблизительно 1 м.д. или 0 м.д. Как используют в настоящем документе, термин "переходный металл" определен для включения Co, Rh, Ir, Fe, Ru, Os, Ni, Pd, Pt, Cu или их сочетаний. В дополнительных конкретных независимых вариантах осуществления концентрация Ni, как измеряют посредством ICP-MS, составляет менее 25 м.д., менее 10 м.д., менее 5 м.д. или менее 1 м.д.
[0040] Также, как используют в настоящем документе, термины "восстановление (как в связях C-O, C-N и C-S)" или "восстановительное расщепление" относятся к химическому преобразованию, где содержащие группы O, N или S замещаются более электроотрицательными группами, например и включая H, D или Si.
[0041] Хотя необходимости ограничивать доступ воды и кислорода к системе может и не быть, в некоторых вариантах осуществления химическая система находится и способ проводят в среде, по существу не содержащей воды, кислорода или ни воды, ни кислорода. Если не указано иначе, термин "по существу не содержит воды" относится к уровням воды менее чем приблизительно 500 м.д., а "по существу не содержит кислорода" относится к уровням кислорода, соответствующих парциальным давлениям менее 133,3 Па. Когда указано, в дополнительных независимых вариантах осуществления может быть предусмотрено, что "по существу не содержит воды" относится к уровням воды менее 1,5%, 1%, 0,5%, 1000 м.д., 500 м.д., 250 м.д., 100 м.д., 50 м.д., 10 м.д. или 1 м.д., а "по существу не содержит кислорода" относится к уровням кислорода, соответствующим парциальным давлениям менее 6,7 кПа, 1,3 кПа, 0,7 кПа, 133,3 Па, 66,7 Па, 33,3 Па, 13,3 Па, 6,7 Па или 1,3 Па.
[0042] Не намереваясь быть связанным правильностью любого предполагаемого механизма взаимодействия (особенно вследствие того, что его роль еще неизвестна), полагают, что для прохождения восстановительного расщепления важным является присутствие в процессе восстановления водорода, даже если только в тех случаях, когда водород, как полагают, образуется в процессе восстановления (см. ниже), и его присутствие, по-видимому, увеличивает (если не является необходимым) или его отсутствие уменьшает восстановительное расщепление, описываемое в настоящем документе. Представляет интерес, что на систему восстановления связей C-O, C-N и C-S положительное влияние также оказывает добавление соединений-доноров молекулярного водорода (см., например, пример 5.9, таблицу 2, пункт 18), тогда как доноры гидридов (включая, например, борогидриды, гидриды алюминия или олова) очевидно не оказывают (например, см. пример 5.12, таблицу 4, пункты 3, 5-7). Иллюстративные соединения-доноры водорода могут включать такие соединения, как 1,3-циклогексадиен, 1,4-циклогексадиен, 1,2-циклогексадиен, 1,4-циклогексадиен 1,2-дигидронафталин, 1,4-дигидронафталин, 1,2-дигидрохинолин, 3,4-дигидрохинолин, 9,10-дигидроантрацен или тетралин.
[0043] Механизм, посредством которого действуют система и способы пока не понятен, и авторы изобретения не связаны правильностью или неправильностью любой конкретной теории в качестве принципа механизма, но некоторые наблюдения указывают на возможность того, что активные кремниевые молекулы-восстановители могут представлять собой органосиликат. Кроме того, как описано в настоящем документе, восстановительное расщепление также часто сопровождается наличием силилирования органического субстрата, хотя пока неясно, являются ли такие молекулы промежуточными соединениями, побочными продуктами или обоими. Но, по-видимому, присутствие доноров водорода и самого водорода играет важную роль в определении степени преобразования и относительных величин расщепления и силилирования; см. пример 5.9, таблицу 2.
[0044] Важность водорода или доноров водорода можно наблюдать в результате ряда экспериментов, в которых специально регулировали присутствие водорода или доноров водорода. Как описано в примере 3 ниже, многие эксперименты проводили в герметичных стеклянных контейнерах. Анализ паровой фазы этих герметизированных реакционных смесей продемонстрировал формирование H2. Для выяснения его важности проводили дополнительные эксперименты, где реакционную смесь открывали в атмосфере аргона, после чего происходило значительное снижение формирования продуктов восстановительного расщепления, что компенсировалось увеличенным силилированием (пример 5.9, таблица 2, сравнить пункты 4-6). Этот результат позволяет предполагать, что молекулярный водород может быть важным для предотвращения распада активных восстанавливающихся молекул. В поисках дополнительной регуляции селективности посредством закрытия путей с радикалами, проводили эксперименты с использованием 1,4-циклогексадиена в качестве неполярного сорастворителя доноров водорода, что приводило к исключительному формированию 2 с выходом 95% (пример 5.9, таблица 2, пункт 18). Эти результаты демонстрируют возможность регулировать селективность реакции, изменяя условия реакции.
[0045] Как используют в настоящем документе, термин "органосилан" относится к соединению или реагенту, содержащему по меньшей мере одну связь кремний-водород (Si-H). Органосилан может дополнительно содержать связь кремний-углерод, кремний-кислород, кремний-азот или их сочетание, и может быть мономерным или содержаться в олигомерном или полимерном каркасе, включая связь с гетерогенной или гомогенной подложкой. В определенных вариантах осуществления эти органосилан могут включать по меньшей мере одно соединение формулы (I) или формулы (II):
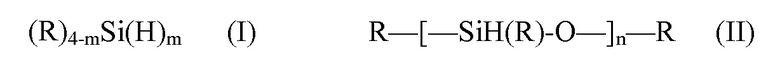
где: m представляет собой 1, 2 или 3, предпочтительно 1;
[0046] n находится в диапазоне приблизительно от 5 до приблизительно 500, приблизительно от 10 до приблизительно 100 или приблизительно от 25 до приблизительно 50; и
[0047] R независимо представляет собой необязательно замещенные C1-C12-алкил или -гетероалкил, C5-20-арил или -гетероарил, C6-30-алкарил или -гетероалкарил, C6-30-аралкил или -гетероаралкил, -O-C1-C12-алкил или -гетероалкил, -O-C5-20-арил или -гетероарил, -O-C6-30-алкарил или -гетероалкарил, -O-C6-30-аралкил или -гетероаралкил, и, если он является замещенным, заместители могут представлять собой фосфонато, фосфорил, фосфанил, фосфино, сульфонато, C1-C20-алкилсульфанил, C5-C20-арилсульфанил, C1-C20-алкилсульфонил, C5-C20-арилсульфонил, C1-C20-алкилсульфинил, C5-C20-арилсульфинил, сульфонамидо, амино, амидо, имино, нитро, нитрозо, гидроксил, C1-C20-алкокси, C5-C20-арилокси, C2-C20-алкоксикарбонил, C5-C20-арилоксикарбонил, карбоксил, карбоксилато, меркапто, формил, сложный C1-C20-тиоэфир, циано, цианато, тиоцианато, изоцианат, тиоизоцианат, карбамоил, эпокси, стиренил, силил, силилокси, силанил, силоксазанил, боронато, борил или галоген или металлсодержащую или металлоидсодержащую группу, где металлоид представляет собой Sn или Ge, где заместители необязательно могут обеспечивать связь с нерастворимым или минимально растворимым субстратом, содержащим оксид алюминия, диоксид кремния или углерод. Иллюстративные, неограничивающие органосиланы включают (R)3SiH, где R представляет собой C1-C6-алкил, в частности триэтилсилан и трибутилсилан, смешанные арилалкилсиланы, такие как PhMe2SiH, и полимерные материалы, такие как полиметилгидросилоксан (PMHS).
[0048] Как используют в настоящем документе, термин "сильное основание" относится к соединению с большой аффинностью к атомам водорода, особенно, но не только, в неводных средах. В конкретных независимых вариантах осуществления по меньшей мере одно сильное основание включает гидрид или алкоксид щелочного металла. Таким образом, следует понимать, что это определение не ограничено только классической моделью конъюгирующая кислота-основание, так как конъюгирующей кислотой гидрида может быть молекулярный водород. Одной из мер этой "сильной аффинности" может являться то, что сильное основание, если оно реагирует с водой, может реагировать до практически законченного формирования его гидроксида. Можно считать, что другие "сильные основания" включают соединения алкиллития или ионы амидов, например, бис(триметилсилил)амид калия.
[0049] По-видимому, существует иерархия активности, связанная с противоионами сильных оснований, так, что использования гидридов цезия и калия и алкоксидов является предпочтительным. Иллюстративные гидриды, пригодные по настоящему изобретению, включают гидрид кальция и гидрид калия. Подобным образом, в примере 5.9, таблице 2, пунктах 13 и 24 можно наблюдать действие температуры на эффективность реакции с гидридами, где реакция дибензофурана с KH, проводимая при 100°C, приводит к низким степеням преобразования и низким уровням образования монорасщепленного продукта, бифенил-2-ола, тогда как проведение подобного эксперимента при 165°C приводит к существенному количественному преобразованию преимущественно в этот продукт.
[0050] Пригодные алкоксиды включают алкоксиды, содержащие неразветвленные или разветвленные C1-12-алкильные группы или C5-10-ароматические или -гетероароматические группы, например, метоксид, этоксид, пропоксид, бутоксид, 2-этилгексилоксид или бензилоксид. Каждый из них по-видимому обладает сравнимой реакционноспособностью (см., например, пример 5.9, таблицу 2, сравнить с пунктами 17, 25-26 и 28). Кроме того, на уровень активности химической системы также влияет выбор противокатиона, так что предпочтительными являются алкоксиды калия или цезия. Более конкретно, показано, что в этой роли особенно эффективны метоксид, этоксид и трет-бутоксид калия и 2-этилгексилалкоксид цезия. Для сравнения, реакция Et3SiH с трет-бутоксидом лития или натрия не обеспечивает преобразования дибензофурана в бисфенил-2-ол (см., например, пример 5.9, таблицу 2, пункты 29-31), что свидетельствует о том, что противоион играет важную роль в получение активных восстановительных групп и, возможно, в активации простого эфира субстрата. Подобным образом, проведение реакции с трет-бутоксидом калия в присутствии достаточного количества 18-краун-6, действующего в качестве хелатора калия, приводит почти к полному ингибированию реакции (таблица 4, пример 5.12, пункт 2).
[0051] Хотя полагают, что относительные количества органосилана и сильного основания, при условии, что оба присутствуют в достаточных количествах, не очень важны, в определенных вариантах осуществления органосилан и по меньшей мере одно сильное основание присутствуют вместе в молярном отношении друг к другу в диапазоне приблизительно от 20:1 до приблизительно 1:2. В других вариантах осуществления эти отношения могут составлять порядка приблизительно от 5:1 до приблизительно 1:2, приблизительно от 3:1 до приблизительно 1:3 или приблизительно от 3:2 до приблизительно 2:3. В других вариантах осуществления показано, что система является эффективной, когда органосилан используют в качестве растворителя для реакций восстановления. Также в качестве растворителя для химических реакций восстановления можно использовать планируемый органический субстрат. В определенных вариантах осуществления химическую систему можно представить как содержащую органический субстрат, содержащий кислород, азот, серу или их сочетание, включая случаи, когда органический субстрат содержится в партии или технологическом потоке биомассы (например, лигнина, сахара), при ожижении биомассы, при биопиролизе масла, черного щелока, угля, при ожижении угля, природного газа или нефти.
[0052] Дополнительно восстановительная система может содержать растворитель, отличный от органосилана. Как показано на настоящий момент, предпочтительными растворителями, по-видимому, являются апротонные растворители. Также, реакциям восстановительного расщепления, по-видимому, благоприятствуют повышенные температуры, хотя они не обязательно ограничены этим ограничением (например, показано, что этилгексилалкоксид цезия восстанавливает связи C-O с триэтилсиланом при комнатной температуре). Таким образом, предпочтительными, по-видимому, являются растворители c температурами кипения (при атмосферном давлении) в диапазоне, ограниченном на нижнем конце значением приблизительно 25°C, 50°C, 75°C, 100°C, 125°C, 150°C, 175°C или 200°C и ограниченном на верхнем конце значением приблизительно 450°C, 425°C, 400°C, 375°C, 350°C, 325°C, 300°C, 275°C или 250°C. Таким образом, один из иллюстративных неограничивающих диапазонов температур кипения составляет приблизительно от 80°C до приблизительно 350°C. Иллюстративные неограничивающие растворители включают бензол, толуол, ксилол, мезитилен, нафталин, метилциклогексан и диоксан.
[0053] Как будет описано далее ниже, эти химические восстановительные системы способны к восстановительному расщеплению связей C-O, C-N или C-S. В определенных вариантах осуществления они представляют собой алкильные связи C-O, C-N или C-S или ароматические связи C-O, C-N или C-S. В отношении алкильных или ароматических связей C-O, C-N или C-S, термины "алкильный" и "ароматический" указывают на характер углерода, с которым связаны атомы кислорода, азота или серы. Как используют в настоящем документе, общий термин "ароматический" относится к циклическим группам, удовлетворяющих правилу ароматичности Хюккеля 4n+2, и включает арильные (т.е. карбоциклические) и гетероарильные структуры, включающие арильные, аралкильные, алкарильные, гетероарильные, гетероаралкильные или алкгетероарильные группы. Кроме того, ароматические связи C-O, C-N или C-S можно конфигурировать так, чтобы они были эндоциклическими в пределах циклической системы (например, пиридин, фуран, пиррол или тиофен) или экзоциклическими относительно ароматической кольцевой структуры (например, как в анизоле).
[0054] До этого момента изобретение было описано относительно химической системы, способной к восстановлению связей C-O, C-N, C-S или их сочетания, но также следует понимать, что изобретение также включает способы проведения этих преобразований. Таким образом, различные дополнительные варианты осуществления включают способы, где органический субстрат, содержащий связи C-O, C-N, C-S или их сочетание, приводят в контакт с любой из химических систем, описанных выше, в условиях, подходящих для восстановления по меньшей мере части этих связей. Таким образом, в определенных вариантах осуществления предусмотрены способы восстановления связей C-X в органическом субстрате, где X представляет собой O, N или S, где указанный способ включает приведение определенного количества субстрата, содержащего по меньшей мере одну связь C-O, C-N или C-S, в контакт с химической системой, содержащей смесь (a) по меньшей мере одного органосилана и (b) по меньшей мере одного сильного основания, в условиях, подходящих для восстановления связей C-X по меньшей мере части этого количества субстрата; где указанная химическая система предпочтительно по существу не содержит соединений переходных металлов, и указанная химическая система необязательно содержит по меньшей мере одно соединение-донор молекулярного водорода, молекулярный водород или оба. В этом контексте, термины "восстановительный" и "восстановительное расщепление" имеют то же определение как описано выше; т.е. включают химические преобразования, где по меньшей мере определенная часть групп с O, N или S заменяют менее электроотрицательными группами, например и включая H, D или Si. Конкретный характер этих химических преобразований описан в настоящем документе.
[0055] Кроме того, в отношении способов, термин "по существу не содержит соединений переходных металлов" имеет те же значения и связанные варианты осуществления, как описано выше для химической системы; т.е. отражает, что способы эффективно проводят в отсутствие любого преднамеренно добавленного переходного металла-катализатора(ов). Если не указано иначе, при описании способа или системы термин определен для отражения того, что общий уровень переходного металла, как измеряют посредством ICP-MS, как описано в примере 2 ниже, составляет менее чем приблизительно 50 м.д. В дополнительных вариантах осуществления также предусмотрено, что концентрация переходных металлов составляет менее чем приблизительно 100 м.д., 50 м.д., 30 м.д., 25 м.д., 20 м.д., 15 м.д., 10 м.д. или 5 м.д. до приблизительно 1 м.д. или 0 м.д. Как используют в настоящем документе, термин "переходный металл" определено для обозначения Co, Rh, Ir, Fe, Ru, Os, Ni, Pd, Pt, Cu или их сочетаний. В дополнительных конкретных независимых вариантах осуществления концентрация Ni, как измеряют посредством ICP-MS, составляет менее 25 м.д., менее 10 м.д., менее 5 м.д. или менее 1 м.д. Отмечая, что определенные варианты осуществления химической системы могут включать по меньшей мере один органосилан и сильное основание и необязательно дополнительно включают по меньшей мере один молекулярный донор водорода, по меньшей мере один субстрат, дополнительный растворитель или их сочетание, следует понимать, что в независимых вариантах осуществления предусмотрено, что при рассмотрении этих комбинаций смесей уровни переходных металлов поддерживают ниже уровней, только что описанных выше.
[0056] В отношении способов термин "по существу не содержит воды и/или кислорода" имеет те же значения и связанные варианты осуществления, как описано выше для самой системы. Подобным образом, те же органосиланы, сильные основания, растворители, пропорции и рабочие условия, описанные как пригодные для системы, применимы в способах использования системы. Кроме того, как показано в примерах, система пригодна когда функционирует так, что органосилан и связи C-X в субстрате присутствуют в соотношении приблизительно от 1:2 до приблизительно 10:1 и где сильное основание и связи C-X в субстрате присутствуют в диапазоне приблизительно от 1:2 до приблизительно 10:1. Обзор результатов, приведенный в примере 5.9, таблице 2, предоставляет полезный индикатор в отношении действия этих отношений в этих пределов и каждое отношение или их сочетания представляют собой отдельный вариант осуществления настоящего изобретения.
[0057] Способы описаны относительно проведения "в условиях, подходящих для восстановления связей C-X по меньшей мере части определенного количества субстрата". Такие условия включают нагревание приводимого в контакт органического субстрата и химической системы до температуры в диапазоне приблизительно от 25°C до приблизительно 450°C. В независимых вариантах осуществления это нагревание можно проводить по меньшей мере при одной из температур в диапазоне приблизительно от 25°C, приблизительно 50°C, приблизительно 75°C, приблизительно 100°C, приблизительно 150°C или приблизительно 200°C до приблизительно 450°C, приблизительно 400°C, приблизительно 350°C, приблизительно 300°C, приблизительно 250°C, приблизительно 200°C или приблизительно 150°C, включая температуры, в качестве примера приводимые в настоящем документе. Предпочтительно, но не обязательно проводить это нагревание в растворителе при температуре ниже температуры кипения растворителя, и предпочтительно, но не обязательно, в растворителе при температуре ниже температуры кипения растворителя при атмосферном давлении.
[0058] Термин "для восстановления связей C-X по меньшей мере части определенного количества субстрата" относится к условию, когда проходит расщепление отдельной связи C-X до выхода, менее чем количественный, к условию, когда проходит расщепление отдельной связи C-X с количественным выходом, к условию, когда в субстрате (отдельное соединение или их смесь) присутствуют несколько связей C-X и расщепляется только один тип связей C-X, или к их сочетанию. Для целей этого описания, если не указано иначе, условия реакции считают подходящими, если в реакции расщепляется по меньшей мере 5% по меньшей мере одной связи C-X (где X=O, N или S). Предпочтительными являются большие выходы, особенно при работе с отдельными соединениями, таким образом, предоставлены дополнительные независимые варианты осуществления, где условия реакции считают подходящими, если в реакции расщепляется по меньшей мере 10%, по меньшей мере 20%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% по меньшей мере одной связи C-X. В связанных вариантах осуществления настоящим способом могут получать продукт, в котором по меньшей мере одна из связей C-X восстановлена в степени в диапазоне от нижнего значение приблизительно 10%, приблизительно 20%, приблизительно 30%, приблизительно 40%, приблизительно 50% или приблизительно 60% до верхнего значения приблизительно 100%, приблизительно 95%, приблизительно 90%, приблизительно 80%, приблизительно 70%, приблизительно 60%, приблизительно 50% или приблизительно 40% относительно количества, исходно присутствующего в соединении-субстрате.
[0059] Такие высокие выходы для любой отдельной связи могут быть необязательны, если субстрат представляет собой протяженную группу связанных ароматических соединений, таких как представлены в лигнине (см., например, фиг.1), угле или нефтяных продуктах, в случае которых успех можно измерять по снижению молекулярной массы исходных субстратов.
[0060] Также в способах номинально во всем остальном при тех же условиях происходит расщепление различных связей C-X с различной эффективностью. Например, как можно наблюдать в примере 5.11, на схемах 1 и 2, алифатические и ароматические связи C-O при нахождении в одном и том же субстрате ведут себя различным образом. Кроме того, тогда как связи C-O и C-N, в целом приводят к продуктам с остаточными спиртовыми или аминными связями, те же условия реакции, применяемые к субстратам со связями C-S, как правило, приводят к продуктам, из которых S полностью удалена. Такое десульфурирование происходит даже в субстратах, которые исторически трудно поддаются десульфированию (например, пространственно-затрудненные дибензотиофены).
[0061] По-видимому, способы функционируют на органических ароматических субстратах, где органический субстрат содержит по меньшей мере одну связь C-O, по меньшей мере одну связь C-N, по меньшей мере одну связь C-S или комбинацию таких связей C-O, C-N или C-S. Хотя способы проверяли с использованием ряда ароматических или гетероароматических субстратов, расщеплявшиеся связи C-O, C-N или C-S не обязательно являются ароматическими связями C-O, C-N или C-S. В некоторых вариантах осуществления по меньшей мере одна из связей C-O, C-N или C-S содержит ароматический углерод. В пределах этого набора ароматические связи C-O, C-N или C-S могут быть эндоциклическими или экзоциклическими относительно ароматического кольца. Термины "эндоциклический" и "экзоциклический" относятся к положению O, N или S по отношению к ароматической циклической системе. Например, "эндоциклическая" относится к связи, в которой атом углерода и соответствующие атомы кислорода, азота или серы содержатся в ароматическом кольце; соответственно, эндоциклические связи C-O, C-N и C-S содержат фуран, пиррол и тиофен. Таким образом, органический субстрат может содержать необязательно замещенную гетероарильную группу, которая в качестве неограничивающих примеров включает фуран, пиррол, тиофен, бензофуран, бензопиррол, бензотиофен, 2,3-дигидробензофуран, ксантен, 2,3-дигидробензопиррол, 2,3-дигидробензотиофен, дибензофуран, дибензопирол, дибензотиофен или пространственно-затрудненные дибензофурановую, дибензопирроловую или дибензотиофеновую структуры. Термин "пространственно-затрудненные дибензофурановая, дибензопирроловая или дибензотиофеновая структуры" относятся к присутствие необязательно замещенных арильных, алкильных или алкоксильных заместителей в положениях 2,6 дибензофурана, дибензопиррола или дибензотиофена. Одним из важных примеров пространственно-затрудненного дибензотиофена является 2,6-диметилдибензотиофен.
[0062] В отличие от этого, термин "экзоциклический" относится к связи, в которой углерод находится в ароматическом кольце системы, а соответствующие атомы кислорода, азота или серы не находятся, и (в случае азота) наоборот. Например, фенол, фениламин (анилин), 1-метил-1H-пиррол и бензотиол содержат экзоциклические ароматические связи C-O, C-N и C-S, соответственно. Иллюстративные органические субстраты включают, но не ограничены ими, группы необязательно замещенных простых фениловых эфиров, фениламинов, фенилсульфидов, простых нафтиловых эфиров, нафтиламинов или нафтилсульфидов, N-алкил- или N-арилпирролы или их сочетания.
[0063] Как указано выше, способы также функционируют на органических ароматических субстратах, где расщепляемые связи C-O, C-N или C-S являются алифатическими (алкильными) связями C-O, C-N или C-S. Как правило, но не обязательно, алифатические (алкильные) связи C-O, C-N или C-S являются связями, в которых гетероатом также связан ароматической связью C-O, C-N или C-S, а двумя примерами являются анизол (Ph-O-CH3) и 1-метил-1H-пиррол. Интересно, и по не полностью понятным причинам, что также наблюдали, что действие ароматической группы на расщепление связей распространяется за пределы его близкодействия на гетероатом. Например, в двух примерах:
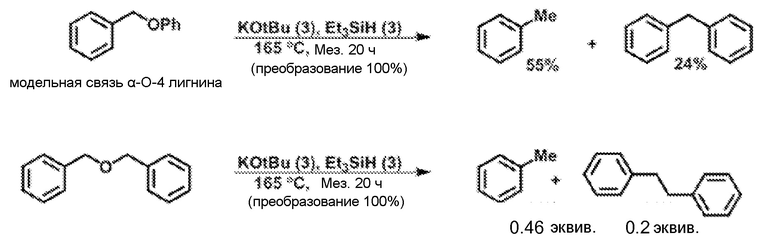
[0064] В дополнительных вариантах осуществления предусмотрено, что эти способы можно использовать для органических субстратов порционно или в потоке, отдельно или как часть смеси. Фактически, особенно привлекательно использовать эти способы, когда органический субстрат содержится в партии или технологическом потоке нефти, угля, природного газа, биомассы (например, лигнина, сахара), при биопиролизе масла, при ожижении биомассы или черного щелока, или когда такая партия или технологический поток обеспечивают растворитель для реакции.
[0065] Установлено, что системы и реакции, которые обеспечивают расщепление связей C-O, C-N, C-S, также могут обеспечивать силилирование ароматических субстратов или даже ароматических растворителей. Это указанная последней способность к силилированию является объектом совместно поданной и совместно рассматриваемой патентной заявки США, обозначенной как Attorney Docket CTEK-0133 (CIT-6650), зарегистрированной 2 октября 2013 года, озаглавленной "Transition-Metal-Free C-H Silylation of Aromatic Compounds", которая также полностью включена в качестве ссылки для всех целей. Механизм, посредством которого действуют система и способы пока еще не понят, например, является ли силилирование промежуточным этапом или побочным продуктом реакций расщепления, но, по-видимому, относительным вкладом каждого направления можно манипулировать условиями реакции. Например, при сходстве или равенстве других факторов, полагают, что повышенные температуры и более длительное время реакции благоприятствуют расщеплению связей C-O, C-N, C-S по сравнению с реакциями силилирования. Подобным образом, отсутствие водорода и молекул-доноров водорода и использование субстехиометрических количеств сильного основания (относительно органосилана), по-видимому, благоприятствует реакциям силилирования и неблагоприятно для расщепления C-X.
[0066] Приводимое ниже перечисление вариантов осуществления предназначено для дополнения, а не для замены или отмены предыдущих описаний.
[0067] Вариант осуществления 1. Химическая система для восстановления связей C-O, C-N и C-S, где указанная система содержит смесь (a) по меньшей мере одного органосилана и (b) по меньшей мере одного сильного основания, где указанная система предпочтительно по существу не содержит соединений переходных металлов, и указанная система необязательно содержит по меньшей мере одно соединение-донор молекулярного водорода, молекулярный водород или оба.
[0068] Вариант осуществления 2. Система по варианту осуществления 1, дополнительно содержащая по меньшей мере одно соединение-донор молекулярного водорода, водород или оба.
[0069] Вариант осуществления 3. Система по варианту осуществления 1 или 2, способная к восстановительному расщеплению связей C-O, C-N или C-S.
[0070] Вариант осуществления 4. Система по любому из вариантов осуществления 1-3, способная к восстановительному расщеплению ароматических связей C-O, C-N или C-S.
[0071] Вариант осуществления 5. Система по варианту осуществления 4, где связи C-O, C-N или C-S являются экзоциклическими относительно ароматической кольцевой группы.
[0072] Вариант осуществления 6. Система по варианту осуществления 4, где связи C-O, C-N или C-S являются эндоциклическими относительно ароматической кольцевой группы.
[0073] Вариант осуществления 7. Система по любому из вариантов осуществления 1-3, способная к восстановительному расщеплению алифатических связей C-O, C-N или C-S.
[0074] Вариант осуществления 8. Система по любому из вариантов осуществления 1-7, которая по существу не содержит воды, кислорода или ни воды, ни кислорода.
[0075] Вариант осуществления 9. Система по любому из вариантов осуществления 1-8, где по меньшей мере один органосилан включает органосилан формулы (I) или формулы (II):
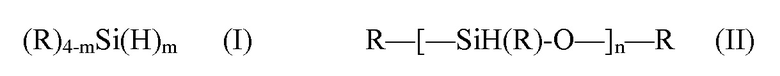
где: m представляет собой 1, 2 или 3; n представляет собой число от 10 до 100; и R независимо представляет собой необязательно замещенные C1-C12-алкил или -гетероалкил, C5-20-арил или -гетероарил, C6-30-алкарил или -гетероалкарил, C6-30-аралкил или -гетероаралкил, -O-C1-12-алкил или -гетероалкил, -O-C5-20-арил или -гетероарил, -O-C6-30-алкарил или -гетероалкарил, -O-C6-C30-аралкил или -гетероаралкил, и, если он является замещенным, заместители могут представлять собой фосфонато, фосфорил, фосфанил, фосфино, сульфонато, C1-C20-алкилсульфанил, C5-C20-арилсульфанил, C1-C20-алкилсульфонил, C5-C20-арилсульфонил, C1-C20-алкилсульфанил, C5-C20-арилсульфинил, сульфонамидо, амино, амидо, имино, нитро, нитрозо, гидроксил, C1-C20-алкокси, C5-C20-арилокси, C2-C20-алкоксикарбонил, C5-C20-арилоксикарбонил, карбоксил, карбоксилато, меркапто, формил, сложный C1-C20-тиоэфир, циано, цианато, тиоцианато, изоцианат, тиоизоцианат, карбамоил, эпокси, стиренил, силил, силилокси, силанил, силоксазанил, боронато, борил, или галоген или металлсодержащую или металлоидсодержащую группу, где металлоид представляет собой Sn или Ge, где заместители необязательно могут обеспечивать связь с нерастворимым или минимально растворимым субстратом, содержащим оксид алюминия, диоксид кремния или углерод.
[0076] Вариант осуществления 10. Система по варианту осуществления 9, где органосилан представляет собой (R)3SiH, где R представляет собой C1-6-алкил.
[0077] Вариант осуществления 11. Система по любому из вариантов осуществления 1-10, где по меньшей мере одно сильное основание включает гидрид или алкоксид щелочного металла.
[0078] Вариант осуществления 12. Система по любому из вариантов осуществления 1-11, где по меньшей мере одно сильное основание включает гидрид щелочного металла.
[0079] Вариант осуществления 13. Система по варианту осуществления 12, где по меньшей мере одно сильное основание включает гидрид кальция или гидрид калия.
[0080] Вариант осуществления 14. Система по любому из вариантов осуществления 1-11, где по меньшей мере одно сильное основание включает алкоксид щелочного металла.
[0081] Вариант осуществления 15. Система по варианту осуществления 14, где по меньшей мере один алкоксид содержит неразветвленную или разветвленную C1-12-алкильную группу или C5-10-ароматическую или -гетероароматическую группу.
[0082] Вариант осуществления 16. Система по варианту осуществления 15, где по меньшей мере один алкоксид включает метоксид, этоксид, пропоксид, бутоксид или 2-этилгексилалкоксид.
[0083] Вариант осуществления 17. Система по любому из вариантов осуществления 11-16, где основание гидрид или алкоксид щелочного металла представляет собой алкоксид калия или цезия.
[0084] Вариант осуществления 18. Система по любому из вариантов осуществления 1-17, где органосилан представляет собой триэтилсилан, а сильное основание представляет собой трет-бутоксид калия.
[0085] Вариант осуществления 19. Система по любому из вариантов осуществления 1-18, где органосилан и по меньшей мере одно сильное основание присутствуют вместе в молярном отношении друг к другу в диапазоне приблизительно от 20:1 до приблизительно 1:2.
[0086] Вариант осуществления 20. Система по любому из вариантов осуществления 1-19, дополнительно содержащая органическое соединение, где указанное соединение представляет собой растворитель, субстрат или и растворитель, и субстрат.
[0087] Вариант осуществления 21. Система по варианту осуществления 20, где органическое соединение представляет собой органический растворитель с температурой кипения при атмосферном давлении в диапазоне приблизительно от 25°C до приблизительно 450°C.
[0088] Вариант осуществления 22. Система по варианту осуществления 20 или 21, где органическое соединение представляет собой органический субстрат, содержащий кислород, азот, серу или их сочетание.
[0089] Вариант осуществления 23. Система по варианту осуществления 22, где органический субстрат содержится в технологическом потоке биомассы (например, лигнина, сахара), при ожижении биомассы, при биопиролизе масла, черного щелока, угля, при ожижении угля, природного газа или нефти.
[0090] Вариант осуществления 24. Система по любому из вариантов осуществления 1-23, где соединение переходного металла присутствует в количестве менее 10 м.д. относительно массы всей системы.
[0091] Вариант осуществления 25. Система по любому из вариантов осуществления 1-24, где соединение-донор водорода включает 1,3-циклогексадиен, 1,4-циклогексадиен, 1,2-циклогексадиен, 1,4-циклогексадиен 1,2-дигидронафталин, 1,4-дигидронафталин, 1,2-дигидрохинолин, 3,4-дигидрохинолин, 9,10-дигидроантрацен или тетралин.
[0092] Вариант осуществления 26. Способ восстановления связей C-X в органическом субстрате, где X представляет собой O, N или S, где указанный способ включает приведение определенного количества субстрата, содержащего по меньшей мере одну связь C-O, C-N или C-S в контакт с химической системой, содержащей смесь (a) по меньшей мере одного органосилана и (b) по меньшей мере одного сильного основания, в условиях, подходящих для восстановления связей C-X по меньшей мере части этого количества субстрата; где указанная химическая система предпочтительно по существу не содержит соединений переходных металлов, и указанная химическая система необязательно содержит по меньшей мере одно соединение-донор молекулярного водорода, молекулярный водород или оба.
[0093] Вариант осуществления 27. Способ по варианту осуществления 26, дополнительно включающий по меньшей мере одно соединение-донор молекулярного водорода, водород или оба.
[0094] Вариант осуществления 28. Способ по варианту осуществления 26 или 27, где органический субстрат содержит по меньшей мере одну связь C-O и, необязательно, по меньшей мере одну связь C-N, связь C-S или обе связи C-N и C-S.
[0095] Вариант осуществления 29. Способ по варианту осуществления 26 или 27, где органический субстрат содержит по меньшей мере одну связь C-N и, необязательно, по меньшей мере одну связь C-O, связь C-S или обе связи C-O и C-S.
[0096] Вариант осуществления 30. Способ по варианту осуществления 26 или 27, где органический субстрат содержит по меньшей мере одну связь C-S, и, необязательно, по меньшей мере одну связь C-O, связь C-N или обе связи C-O и C-N.
[0097] Вариант осуществления 31. Способ по любому из вариантов осуществления 26-30, дополнительно включающий по меньшей мере одно соединение-донор молекулярного водорода, сам молекулярный водород или оба.
[0098] Вариант осуществления 32. Способ по любому из вариантов осуществления 26-31, где по меньшей мере одна из связей C-O, C-N или C-S представляет собой ароматическую связь C-O, C-N или C-S.
[0099] Вариант осуществления 33. Способ по варианту осуществления 32, где по меньшей мере одна из связей C-O, C-N или C-S является экзоциклической относительно ароматической кольцевой группы.
[0100] Вариант осуществления 34. Способ по любому из вариантов осуществления 33, где по меньшей мере одна из связей C-O, C-N или C-S является эндоциклической относительно ароматической кольцевой группы.
[0101] Вариант осуществления 35. Способ по любому из вариантов осуществления 26-34, где субстрат содержит необязательно замещенные группы простого фенилового эфира, фениламина, фенилсульфида, простого нафтилового эфира, нафтиламина или нафтилсульфида или их сочетание.
[0102] Вариант осуществления 36. Способ по любому из вариантов осуществления 26-35, где субстрат содержит фурановую, пиррольную, тиофеновую, бензофурановую, бензопирроловую, бензотиофеновую, 2,3-дигидробензофурановую, 2,3-дигидробензопирроловую, 2,3-дигидробензотиофеновую, дибензофурановую, ксантеновую, дибензопироловую, дибензотиофеновую или пространственно-затрудненную дибензофурановую, дибензопирроловую или дибензотиофеновую группу.
[0103] Вариант осуществления 37. Способ по любому из вариантов осуществления 26-32, где по меньшей мере одна из связей C-O, C-N или C-S является алифатической связью C-O, C-N или C-S.
[0104] Вариант осуществления 38. Способ по любому из вариантов осуществления 26-37, который по существу не включает воды, кислорода или ни воды, ни кислорода.
[0105] Вариант осуществления 39. Способ по любому из вариантов осуществления 26-38, где по меньшей мере один органосилан включает органосилан формулы (I) или формулы (II):
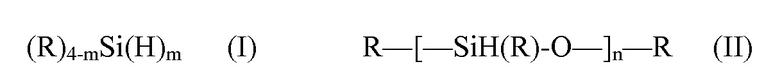
где m представляет собой 1, 2 или 3; n представляет собой число от 10 до 100; и R независимо представляет собой необязательно замещенные C1-C12-алкил или -гетероалкил, C5-20-арил или -гетероарил, C6-30-алкарил или -гетероалкарил, C6-30-аралкил или -гетероаралкил, -O-C1-C12-алкил или -гетероалкил, -O-C5-20-арил или -гетероарил, -O-C6-30-алкарил или -гетероалкарил, -O-C6-30-аралкил или -гетероаралкил, и, если он замещен, заместители могут представлять собой фосфонато, фосфорил, фосфанил, фосфино, сульфонато, C1-C20-алкилсульфанил, C5-C20-арилсульфанил, C1-C20-алкилсульфонил, C5-C20-арилсульфонил, C1-C20-алкилсульфинил, C5-C20-арилсульфинил, сульфонамидо, амино, амидо, имино, нитро, нитрозо, гидроксил, C1-C20-алкокси, C5-C20-арилокси, C2-C20-алкоксикарбонил, C5-C20-арилоксикарбонил, карбоксил, карбоксилато, меркапто, формил, сложный C1-C20-тиоэфир, циано, цианато, тиоцианато, изоцианат, тиоизоцианат, карбамоил, эпокси, стиренил, силил, силилокси, силанил, силоксазанил, боронато, борил или галоген или металлсодержащую или металлоидсодержащую группу, где металлоид представляет собой Sn или Ge, где заместители необязательно могут обеспечивать связь с нерастворимым или минимально растворимым субстратом, содержащим оксид алюминия, диоксид кремния или углерод.
[0106] Вариант осуществления 40. Способ по варианту осуществления 39, где органосилан представляет собой (R)3SiH, где R представляет собой C1-C6-алкил.
[0107] Вариант осуществления 41. Способ по любому из вариантов осуществления 26-40, где по меньшей мере одно сильное основание включает гидрид или алкоксид щелочного металла.
[0108] Вариант осуществления 42. Способ по любому из вариантов осуществления 26-41, где по меньшей мере одно сильное основание включает гидрид щелочного металла.
[0109] Вариант осуществления 43. Способ по варианту осуществления 42, где по меньшей мере одно сильное основание включает гидрид кальция или гидрид калия.
[0110] Вариант осуществления 44. Способ по любому из вариантов осуществления 26-43, где по меньшей мере одно сильное основание включает алкоксид щелочного металла.
[0111] Вариант осуществления 45. Способ по варианту осуществления 44, где по меньшей мере один алкоксид содержит неразветвленную или разветвленную C1-12-алкильную группу или C5-10-ароматическую или -гетероароматическую группу.
[0112] Вариант осуществления 46. Способ по варианту осуществления 45, где по меньшей мере один алкоксид включает метоксид, этоксид, пропоксид, бутоксид или 2-этилгексилалкоксид.
[0113] Вариант осуществления 47. Способ по любому из вариантов осуществления 39-46, где основание гидрид или алкоксид щелочного металла представляет собой алкоксид калия или цезия.
[0114] Вариант осуществления 48. Способ по любому из вариантов осуществления 26-47, где органосилан представляет собой триэтилсилан, а сильное основание представляет собой трет-бутоксид калия.
[0115] Вариант осуществления 49. Способ по любому из вариантов осуществления 26-48, где органосилан и по меньшей мере одно сильное основание присутствуют вместе в молярном отношении друг к другу в диапазоне приблизительно от 20:1 до приблизительно 1:2.
[0116] Вариант осуществления 50. Способ по любому из вариантов осуществления 26-49, где органосилан и связи C-X в субстрате присутствуют в отношении приблизительно от 1:2 до приблизительно 10:1.
[0117] Вариант осуществления 51. Способ по любому из вариантов осуществления 26-50, где сильное основание и связи C-X в субстрате присутствуют в диапазоне приблизительно от 1:2 до приблизительно 10:1.
[0118] Вариант осуществления 52. Способ по любому из вариантов осуществления 26-49, где органосилан присутствует в достаточном количестве, чтобы действовать в способе в качестве растворителя.
[0119] Вариант осуществления 53. Способ по любому из вариантов осуществления 26-51, дополнительно включающий органический растворитель.
[0120] Вариант осуществления 54. Способ по варианту осуществления 53, где указанный органический растворитель обладает температурой кипения при атмосферном давлении в диапазоне приблизительно от 25°C до приблизительно 450°C.
[0121] Вариант осуществления 55. Способ по любому из вариантов осуществления 26-54, где указанный способ включает нагревание органического субстрата и химической системы до температуры в диапазоне приблизительно от 25°C до приблизительно 450°C
[0122] Вариант осуществления 56. Способ по любому из вариантов осуществления 26-55, где соединение переходного металла присутствует в количестве менее 10 м.д. относительно массы всей системы.
[0123] Вариант осуществления 57. Способ по любому из вариантов осуществления 26-56, где соединение-донор водорода включает 1,3-циклогексадиен, 1,4-циклогексадиен, 1,2-циклогексадиен, 1,4-циклогексадиен 1,2-дигидронафталин, 1,4-дигидронафталин, 1,2-дигидрохинолин, 3,4-дигидрохинолин, 9,10-дигидроантрацен или тетралин.
[0124] Вариант осуществления 58. Способ по любому из вариантов осуществления 26-57, где органический субстрат содержится в технологическом потоке биомассы (например, лигнина, сахара), при ожижении биомассы, при биопиролизе масла, черного щелока, угля, при ожижении угля, природного газа или нефти.
[0125] Вариант осуществления 59. Способ по любому из вариантов осуществления 26-58, где указанный способ проводят в технологическом потоке биомассы (например, лигнина, сахара), при ожижении биомассы, при биопиролизе масла, черного щелока, угля, при ожижении угля, природного газа или нефти.
[0126] Вариант осуществления 60. Способ по любому из вариантов осуществления 26-59, где в способе получают продукт, в котором по меньшей мере одна из связей C-X восстановлена в количестве в диапазоне приблизительно от 40% до 100%, относительно количества, исходно присутствующего в соединении-субстрате.
ПРИМЕРЫ
[0127] Приводимые ниже примеры предоставлены для иллюстрации некоторых из принципов, описанных в настоящем описании. Хотя полагают, что каждый пример предоставляет конкретные отдельные варианты осуществления композиции, способов получения и использования, ни один из примеров не следует рассматривать как ограничивающий более общие варианты осуществления, описываемые в настоящем документе.
[0128] В приводимых ниже примерах, проведена работа для обеспечения точности в отношении используемых чисел (например, количества, температуры и т.д.), но следует учитывать определенные экспериментальные ошибки и отклонения. Если не указано иначе, температура приведена в градусах Цельсия, давление является атмосферным или близким к нему.
[0129] Пример 1: Общая информация
[0130] Если не указано иначе все реакции проводили в сухой лабораторной посуде в атмосфере аргона с использованием стандартных способов работы с линией Шленка или в перчаточной камере в разреженной среде в атмосфере азота. Мезитилен (чистота, >99,0% (GC)) перед использованием дегазировали посредством трех циклов замораживания-прокачивания-оттаивания. Все другие растворители очищали пропусканием через очистную колонку с растворителями и далее дегазировали аргоном. (1) Растворители для ЯМР для всех чувствительных к воздушной среде экспериментов сушили над CaH2 и при пониженном давлении переносили или перегоняли в сухую колбу Шленка и затем дегазировали аргоном. Триэтилсилан (99%) и дейтеротриэтилсилан (97% атомов D) приобретали в Sigma-Aldrich и перед использованием дегазировали посредством трех циклов замораживания-прокачивания-оттаивания и другие коммерчески доступные жидкие реагенты обрабатывали аналогично. Простой ди-4-(метил)фениловый эфир, 1-нафтол, 2-нафтол, 4-трет-бутиланизол, 4-метиланизол, 1,3-дифеноксибензол, 2-метоксинафталин и 1,0М раствор фторида тетрабутиламмония в THF приобретали в Sigma-Aldrich и использовали в том виде, как получено. KO-t-Bu степени возгонки (99,99%) приобретали в Sigma-Aldrich и перед использованием подвергали возгонке при пониженном давлении (4 Па, 160°C). 4-(метокси)дибензофуран, (2) простой ди-4-(трет-бутил)фениловый эфир (3), простые нафтиловые эфиры (3), простой 4-(фенил)фенилфениловый эфир (3), 2-этоксинафталин (4), 2-неопентилоксинафталин (4), 2-трет-бутилоксинафталин (5) синтезировали в соответствии со способами из литературы. Стандартные эксперименты ЯМР-спектроскопии проводили на спектрометре Varian Mercury (1H, 300 МГц), Varian Inova 400 МГц, спектрометре Varian 500 МГц, оборудованном зондом AutoX или спектрометре Varian 600 МГц, оборудованном зондом Triax. Химические сдвиги регистрировали в м.д. со сдвигом в сторону слабого поля от Me4Si с использованием пика остаточного растворителя в качестве внутреннего стандарта. Спектры анализировали и обрабатывали с использованием MestReNova версии 7. Анализы GC-FID проводили на газовом хроматографе Agilent 6890N, оборудованном капиллярной колонкой HP-5 (5%-фенил)-метилполисилоксан (Agilent). Анализ GC-MS проводили на газовом хроматографе Agilent 6850, оборудованном капиллярной колонкой HP-5 (5%-фенил)-метилполисилоксан (Agilent). Масс-спектры с высоким разрешением (EI и FAB) получали на масс-спектрометрическом оборудовании California Institute of Technology. Спектры EPR регистрировали на спектрометры Bruker EMS.
[0131] Пример 2: анализ ICP-MS
[0132] Анализ ICP-MS проводили с использованием масс-спектрометрического оборудования California Institute of Technology со 100 мг образцов дибензофурана, триэтилсилан, мезитилена и трет-бутоксида калия, которые добавляли в 50 мл пробирки для расщепления DigiTUBE (SCP Science) с последующим добавлением в каждую пробирку для расщепления 3,0 мл азотной кислоты Plasma Pure (SCP Scicncc) и нагреванием при 75°C в течение 36 часов. После расщепления каждый образец разбавляли с использованием воды Nanopure/Milli Q до 50 мл и анализ образца проводили на спектрометре ICPMS HP 4500. Полуколичественный анализ проводили с использованием для калибровки раствора лития, иттрия, церия и талия 10 м.д. Каждый образец анализировали дважды и предоставляли средние результаты измерений. (Таблица 1).
[0133] Пример 3: Общий способ
[0134] В перчаточную камеру помещали 4 мл флакон с завинчивающейся крышкой с соответствующим субстратом (0, ммоль, 1 эквив.), основанием (0,5-5 эквив.) и магнитной мешалкой с последующим добавлением растворителя (1 мл) и триэтилсилана (1-5 эквив.) шприцем. Реакционную пробирку закрывали покрытой тефлоном завинчивающейся крышкой и нагревали при данной температуре и в течение определенного времени внутри перчаточной камеры. После охлаждения до комнатной температуры, реакционную смесь цвета от черно-красного до черного разбавляли простым диэтиловым эфиром (3 мл) и осторожно гасили 1 мл 1н водной HCl. Добавляли тридекан (внутренний стандарт для GC), органический слой разделяли и водный слой экстрагировали простым эфиром (3 мл) до тех пор, пока контроль TLC не переставал выявлять присутствия активных в УФ-излучении соединений в экстрактах. Объединенные органические слои пропускали через тонкий слой целита и подвергали анализам GC/FTD, GC/MS и 1H-ЯМР. Если не указано иначе, в препаративных экспериментах выделяли и характеризовали только продукты с общим выходом, превосходящим 2%. В случае простых нафтилалкиловых эфиров использовали другой способ обработки. После охлаждения реакционную смесь разбавляли дихлорметаном (5 мл) и осторожно гасили 2 мл 1н водной HCl. Добавляли тридекан и смесь переносили в делительную воронка. Органическую фазу разделяли, и водный слой экстрагировали дихлорметаном (3 мл). Объединенные органические слои сушили над безводным MgSO4 и фильтровали. Для всех реакций продукты идентифицировали с использованием GC/MS и GC/FTD и ЯМР при сравнении с достоверными образцами. Следовые растворимые побочные продукты, наблюдаемые при восстановлении простых нафтилалкиловых эфиров, включали нафталин, 1,2,3,4-тетрагидронафталин и 5,6,7,8-тетрагидро-2-нафтол.
[0135] Пример 4: Синтез и характеристика избранных соединений
[0136] Пример 4.1: 4-(триэтилсилил)дибензофуран (3)
[0137] Указанное в заголовке соединение получали по аналогии с протоколом синтеза 4-(триметилсилил)дибензофурана Kelly и коллег; Bekele, H., et al., J. Org. Chem., 1997, 62, 2259. Данные для (3): бесцветное масло. 1H-ЯМР (500 МГц, CDCl3): δ 7,99-7,96 (м, 2Har), 7,59 (д-like, J=10 Гц, 1Har), 7,54 (дд, J=2, 5 Гц, 1Har), 7,48-7,44 (м, 1Har), 7,37-7,33 (м, 2Har), 1,03 (м, 15H, 3CH2CH3). 13C-ЯМР (126 МГц, CDCl3) δ 161,30, 156,05, 133,57, 126,92, 122,52, 122,48, 121,58,120,68, 111,75, 7,63,3,59. HRMS: [C18H22OSi] рассчитано 282,1440; измерено 282,1444.
[0138] Пример 4.2: 4,6-бис(триэтилсилил)дибензофуран (4)
[0139] К раствору дибензофурана (2,00 г, 11,9 ммоль, 1 эквив.) и тетраметилэтилендиамина (11,1 мл, 29,7 ммоль, 2,5 эквив.) в тетрагидрофуране (50 мл) медленно добавляли трет-бутиллитий (17,5 мл 1,7M раствора в пентан, 29,8 ммоль, 2,5 эквив.) при -78°C в атмосфере аргона. Смеси позволяли достигать температуры окружающей среды и перемешивание продолжали в течение 4 час с последующим добавлением хлортриэтилсилана (10,1 мл, 60 ммоль, 5 эквив.). Полученную смесь перемешивали при температуре окружающей среды в течение дополнительных 16 час. После гашения реакции раствором насыщенного хлорида аммония (40 мл) и экстракции простым диэтиловым эфиром (3×30 мл) объединенные органические слои сушили над безводным сульфатом натрия, фильтровали и фильтрат концентрировали при пониженном давлении. Неочищенную реакционную смесь очищали посредством хроматографии на диоксиде кремния (гексан) и полученный продукт перекристаллизовывали из смеси метанола и изопропанола (1:1) с получением 4,6-бис(триэтилсилил)дибензофурана (1,28 г, 2,45 ммоль, 28%) в виде бесцветных игл. Данные для (4): бесцветные иглы. Т.плавл. = 59-61°C. 1H-ЯМР (300 МГц, CDCl3) δ 7,97 (дд, J=3, 9 Гц, 2Har), 7,54 (дд, J=3, 9 Гц, 2Har), 7,33 (т, J=9 Гц, 2Har), 1,07-0,95 (м, 30 H, 6 CH2CH3). 13C-ЯМР (126 МГц, CDCl3) δ 160,90, 133,48, 122,87, 122,34, 121,57, 120,03, 7,66, 3,52. HRMS: [C24H36OSi2] рассчитано 396,2305; измерено 396,2321.
[0140] Пример 4.3: 3-(триэтилсилил)бифенил-2-ол (5)
[0141] Указанное в заголовке соединение получали посредством расщепления 3 (см. ниже). Данные для (5): белое твердое вещество. Т.плавл. = 44-46°C 1H-ЯМР (300 МГц, CDCl3) δ 7,52-7,40 (м, 5Har), 7,36 (дд, J=3, 9 Гц, 1Har), 7,23 (дд, J=3, 6 Гц, 1Har), 6,98 (т, J=9 Гц, 1Har), 5,41 (с, 1H, OH), 1,02-0,96 (м, 9H, CH3), 0,91-0,83 (м, 6H, CH2). 13C-ЯМР (75 МГц, CDCl3) δ 157,25, 137,51, 135,97, 131,30, 129,58, 129,39, 128,01, 127,17, 123,04, 120,40, 7,79, 3,69. HRMS: [C18H24OSi] рассчитано 284,1596; измерено 284,1583.
[0142] Пример 4.4: (3'-триэтилсилил)бифенил-2-ол (6)
[0143] Указанное в заголовке соединение получали посредством расщепления 3 (см. ниже). Данные для (6): бесцветное масло. 1H-ЯМР(500 МГц, CDCl3): δ 7,57-7,56 (м, 1Har), 7,54-7,52 (м, 1Har), 7,49-7,44 (м, 2Har), 7,28-7,24 (м, 2Har), 7,02-6,99 (м, 2Har), 5,24 (с, 1H, OH), 0,98 (т, J=10 Гц, 9H, CH3), 0,82 (кв, J=15 Гц, 6H, CH2). 13C ЯМР (126 МГц, CDCl3): δ 153,44, 139,07, 136,12, 134,71, 133,76, 130,23, 129,36, 129,08, 128,53, 128,44, 120,80, 115,72, 7,43, 3,31. HRMS: [C18H24OSi] рассчитано 284,1596; измерено 284,1585.
[0144] Пример 4.5: 3,3'-бис(триэтилсилил)бифенил-2-ол (7)
[0145] Указанное в заголовке соединение получали в соответствии с общим способом, нагревая дибензофуран (1, 840 мг, 5,0 ммоль, 1 эквив.) с KOt-Bu (1,12 г, 10 ммоль, 2 эквив.) и Et3SiH (4,0 мл, 25 ммоль, 5 эквив.) в 20 мл толуола в течение 20 часов при 100°C. После обработки водным кислотным раствором неочищенную реакционную смесь очищали посредством хроматографии на диоксиде кремния с использованием гексана и гексана-простого эфира (10:1) с получением среди прочих выделенных продуктов 20 мг (0,05 ммоль, 1%) 7. Данные для (7): маслянистое твердое вещество 1H-ЯМР (300 МГц, CDCl3): δ 7,53-7,44 (м, 2Har), 7,46-7,44 (м, 2Har), 7,36 (дд, J=1,5, 7,5 Гц, 1Har), 7,23 (дд, J=1,5, 7,5 Гц, 1Har), 6,98 (т, J=7 Гц, 1Har), 5,42 (с, 1H, OH), 1,01-0,96 (м, 18H, 6CH3) 0,91-0,77 (м, 15H, 6CH2). 13C ЯМР (75 МГц, CDCl3): δ 157,37, 139,45, 136,61, 135,87, 135,09, 133,86, 131,38, 129,57, 128,71, 127,55, 122,97, 120,36, 7,80, 7,57, 3,69, 3,46. HRMS: [C24H38OSi2] рассчитано 398,2461; измерено 396,2470.
[0146] Пример 5: Избранные реакции
[0147] Пример 5.1: Эксперименты по расщеплению дибензофурана и дейтерированию в препаративном масштабе
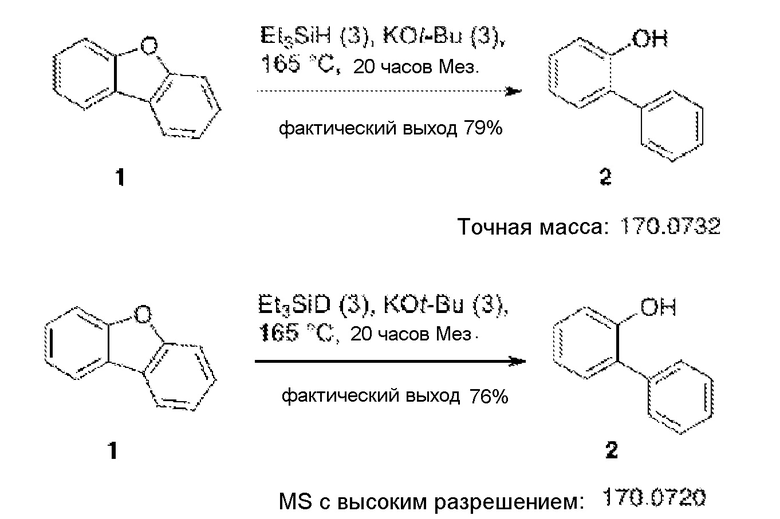
[0148] Реакцию проводили в соответствии с общим способом, нагревая дибензофуран (1, 250 мг, 1,49 ммоль, 1 эквив.), KOt-Bu (500 мг, 4,46 ммоль, 3 эквив.) и Et3SiH (713 микролитров, 4,46 ммоль, 3 эквив.) в 4,4 мл мезитилена в течение 20 часов при 165°C. После разбавления простым диэтиловым эфиром (5 мл) органическую фазу сначала промывали водой (1 мл), а затем 2,5н раствором KOH (3×20 мл). Основные водные фракции собирали и однократно промывали CH2Cl2 (25 мл) для удаления любых нежелательных органических соединений. Затем получившиеся основные водные фракции подкисляли концентрированной HCl до pH 1, а затем экстрагировали CH2Cl2 (3×25 мл). Органические фракции собирали и концентрировали при пониженном давлении с получением бледно-желтых кристаллов. После очистки посредством хроматографии на силикагеле с гексаном/этилацетатом (градиентная элюция: от 0% до 5% этилацетата) получали бифенил-2-ол (2, 198 мг, 1,16 ммоль, 79%) в виде бесцветного твердого вещества. Спектральные распределения 1H и 13C-ЯМР 1 соответствовали спектральным распределениям достоверного образца.
[0149] Идентичный способ, использованный для восстановительного расщепления дибензофурана, но с Et3SiD, приводил к получению недейтерированного бифенил-2-ола с фактическим выходом 76%. HRMS: [C12H100] рассчитано 170,0732; измерено 170,0720.
[0150] Повторяя указанный выше эксперимент с Et3SiH и Мез-d12, получали дейтерированный бифенил-2-ол с фактическим выходом 73%. HRMS: [C12H4D6O] рассчитано 176,1108; измерено 176,1115; FWHM ≈ 4 Да. В идентичном способе, применяемом для восстановительного расщепления дибензофурана, но с Et3SiD и Мез-d12, получали дейтерированный бифенил-2-ол с фактическим выходом 79%. HRMS: [C12H4D6O] рассчитано 176,1108; измерено 176,1108; FWHM~4 Да.
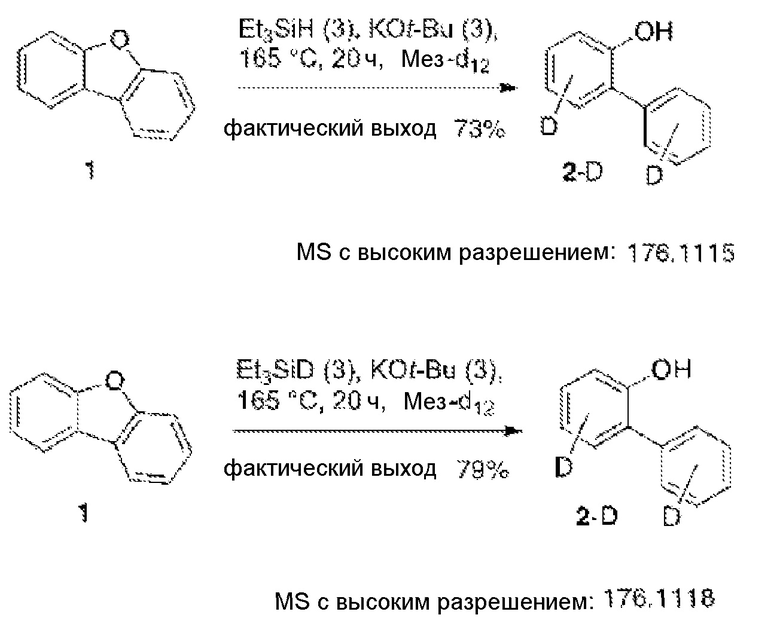
[0151] Когда проводили реакцию дибензофурана с Et3SiD в мезитилене при 165°C наблюдали очень малое включение дейтерия в 2. В соответствии с этим идентичные основные пики бифенил-2-ола, получаемого из Et3SiH или Et3SiD в Мез-d12, в спектрах MS с высоким разрешением свидетельствовали, что в условиях реакции происходил быстрый обмен H/D с растворителем. Представляет интерес, что по данным спектров протонов, углерода и HSQC дейтерированного 2, хотя частичный обмен H/D претерпевали все протоны, только для положения орто-OH этот процесс достигал завершения.
[0152] Пример 5.2: Расщепление 4-(триэтилсилил)дибензофурана
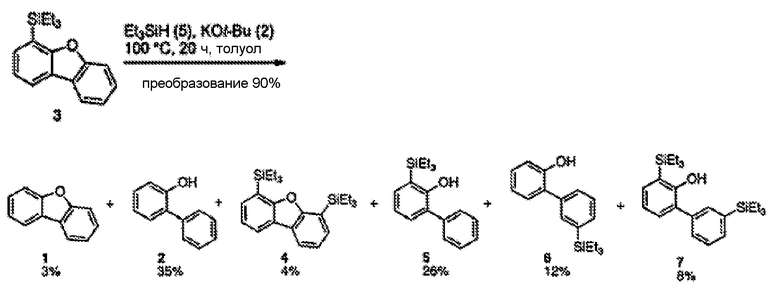
[0153] Реакцию проводили в соответствии с общим способом, нагревая 4-Et3Si-дибензофуран (3, 141 мг, 0,5 ммоль, 1 эквив.), KOt-Bu (112 мг, 1 ммоль, 2 эквив.) и Et3SiH (401 микролитров, 2,5 ммоль, 5 эквив.) в 2 мл толуола в течение 20 часов при 100°C. После обработки водным кислотным раствором неочищенную реакционную смесь очищали посредством хроматографии на диоксиде кремния с использованием гексана и гексана-простого эфира (10:1) с выделением 2-фенилфенола (2, 30 мг, 0,177 ммоль, 35%), 2-триэтилсилил-6-фенилфенола (5, 37 мг, 0,134 ммоль, 26%), 2-(3-триэтилсилилфенил)фенола (6, 17 мг, 0,063 ммоль, 12%). Количества неизрасходованного 3, а также продукты 1, 4 и 7 получали с использованием постхроматографического анализа GC-FID соответствующих смешанных фракций.
[0154] Пример 5.3: Исследование силилированных дибензофуранов в качестве промежуточных соединений в отношении расщепления связей C-O: попытки расщепления с использованием KOt-Bu
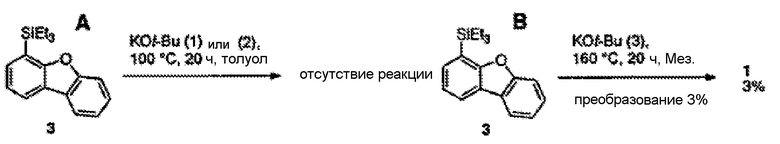
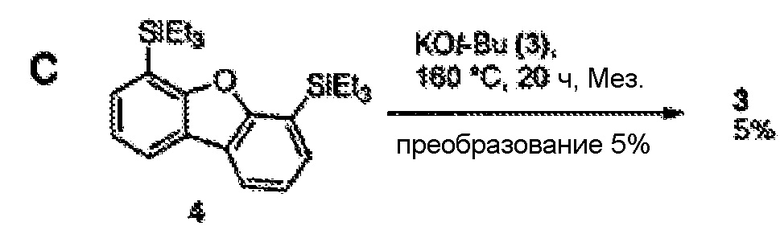
[0155] Исходное вещество 3 (14,1 мг, 0,05 ммоль, 1 эквив.) нагревали с KOt-Bu (5,6 мг или 11,2 мг, 1 или 2 эквив., соответственно) в 0,8 мл д-толуола при 100°C в течение 20 часов в пробирке J. Young в атмосфере азота. Контроль прохождения реакции посредством 1H-ЯМР продемонстрировал отсутствие преобразования 3 в обоих случаях. Подобным образом, исходные вещества 3 (28,2 мг, 0,1 ммоль, 1 эквив.) или 4 (39,6 мг 0,1 ммоль, 1 эквив.) нагревали с KOt-Bu (36,6 мг) в 0,3 мл мезитилена при 160°C в течение 20 часов. Последующий анализ неочищенных реакционных смесей посредством GC-FID или 1H-ЯМР выявил 3% преобразование до 1 в случае 3 и 5% преобразование до 3 из 4.
[0156] Пример 5.4: Расщепление 4, 6-бис(триэтилсилил)дибензофурана
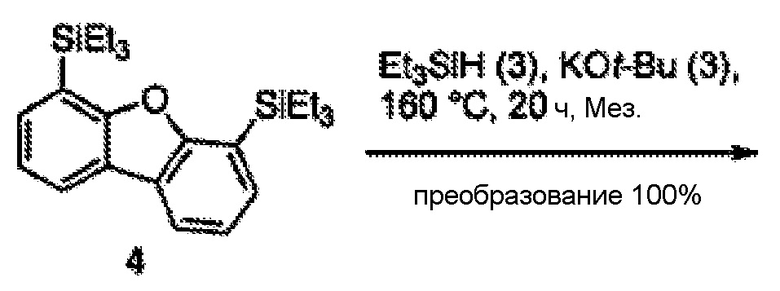
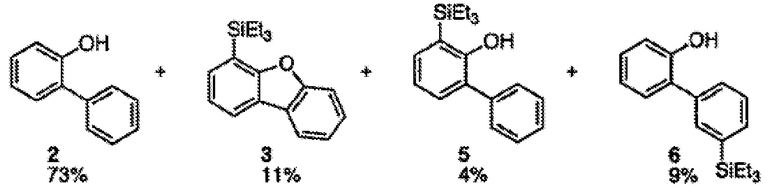
[0157] Реакцию проводили в соответствии с общим способом, нагревая 2-(3'-триэтилсилилфенил)фенола (4, 39,6 мг, 0,1 ммоль, 1 эквив.), KOt-Bu (33,6 мг, 0,3 ммоль, 3 эквив.) и Et3SiH (48 микролитров, 0,3 ммоль, 3 эквив.) в 0,2 мл мезитилена в течение 20 часов при 160°C. После обработки водным кислотным раствором, добавляли внутренний стандарт и неочищенную реакционную смесь анализировали посредством GC-FID.
[0158] Пример 5.5: Расщепление 4-(метокси)дибензофурана
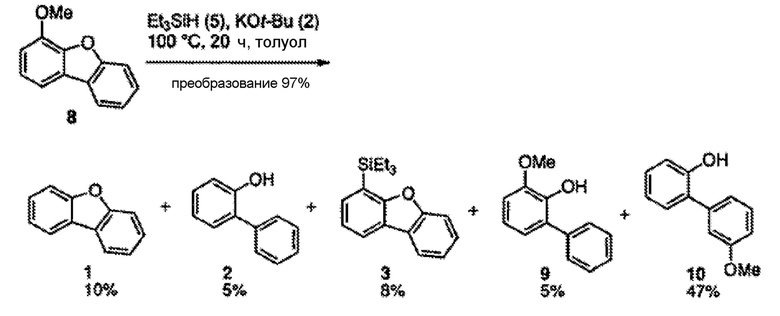
[0159] Реакцию проводили в соответствии с общим способом, нагревая 4-MeO-дибензофуран (8, 89 мг, 0,5 ммоль, 1 эквив.), KOt-Bu (112 мг, 1 ммоль, 2 эквив.) и Et3SiH (401 микролитров, 2,5 ммоль, 5 эквив.) в 2 мл толуола в течение 20 часов при 100°C. После водной обработки неочищенную реакционную смесь очищали посредством хроматографии на диоксиде кремния с использованием гексана и гексана-простого эфира с восстановлением неизрасходованного исходного вещества 8 (3 мг, 0,015 ммоль, 3%) и выделением дибензофурана (1, 8,4 мг, 0,05 ммоль, 10%; так как фракции 1 содержали небольшие количества исходного 8, количественный анализ проводили посредством 1H-ЯМР с CH2Br2 в качестве внутреннего стандарта), 1,1'-бифенил-2-ола (2, 4,3 мг, 0,025 ммоль, 5%), 4-Et3Si-дибензофурана (3, 11 мг, 0,039 ммоль, 8%), 2-метокси-6-фенил-фенола (9, мг, 0,025 ммоль, 5%), 2-(3'-метоксифенил)фенола (10, 47 мг, 0,235 ммоль, 47%). Примечание: охарактеризовывали только соединения с выходом, превосходящим 2%. Спектральные распределения 1H- и l3C-ЯМР 9 и 10 соответствовали литературным отчетам.
[0160] Пример 5.6: Синтез 4,6-ди(метил)дибензофурана
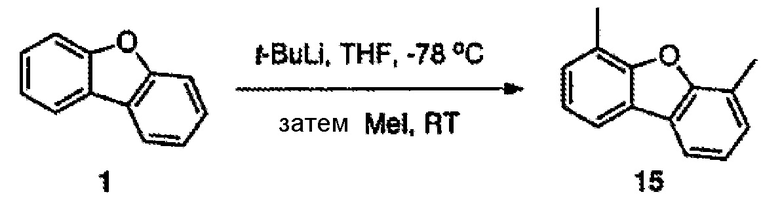
[0161] К раствору дибензофурана (2,00 г, 11,9 ммоль, 1 эквив.) и тетраметилэтилендиамина (11,1 мл, 29,7 ммоль, 2,5 эквив.) в простом диэтиловом эфире (50 мл) медленно добавляли трет-бутиллитий (17,5 мл 1,7 раствора M в пентане, 29,8 ммоль, 2,5 эквив.) при -78°C в атмосфере аргона. Смеси позволяли достигать температуры окружающей среды и перемешивание продолжали в течение 4 часов с последующим добавлением метилиодида (3,7 мл, 60 ммоль, 5 эквив.). Полученную смесь перемешивали при температуре окружающей среды в течение дополнительных 16 часов. После гашения реакции раствором насыщенного хлорида аммония (40 мл) и экстракции простым диэтиловым эфиром (3×30 мл) объединенные органические слои сушили над безводным сульфатом натрия, фильтровали и фильтрат концентрировали при пониженном давлении. Неочищенную реакционную смесь очищали посредством хроматографии на диоксиде кремния (гексан) и полученный продукт перекристаллизовывали из метанола с получением 4,6-диметилдибензофурана (480 мг, 2,45 ммоль, 21%) в виде бесцветного твердого вещества. Данные для (15): 1H-ЯМР (300 МГц, CDCl3): δ 7,75 (дд, J= 1,0, 6,0 Гц, 2Har), 7,24-7,20 (м, 4H^), 2,61 (с, 6H, 2CH3). 13C-ЯМР (75 МГц, CDCl3): δ 155,07, 128,00, 124,17, 122,60, 122,02, 118,2, 15,41. HRMS: [C14H12O] рассчитано 196,0888; измерено 196,0884.
[0162] Пример 5.7: Расщепление 4,6-ди(метил)дибензофурана
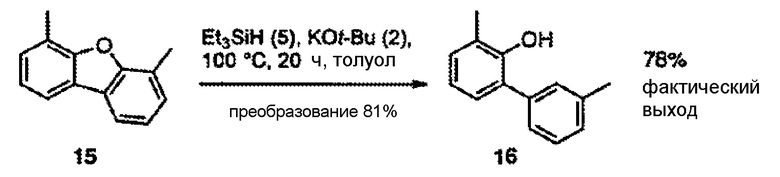
[0163] Реакцию проводили в соответствии с общим способом, нагревая 4,6-ди(метил)дибензофуран (15, 98 мг, 0,5 ммоль, 1 эквив.), KOt-Bu (112 мг, 1 ммоль, 2 эквив.) и Et3SiH (401 микролитров, 2,5 ммоль, 5 эквив.) в 2 мл толуола в течение 20 часов при 100°C. После водной обработки неочищенную реакционную смесь очищали посредством хроматографии на диоксиде кремния с использованием гексана-простого эфира в соотношении 4:1 с получением 77 мг продукта 16 в виде желтого масла. Данные для (16): 1H-ЯМР (500 МГц, CDCl3): δ 7,35 (т, J=7,5 Гц, 1Har), 7,25-7,22 (м, 2Har), 7,20-7,18 (м, 1Har), 7,11 (д-like, J=10 Гц, 1Har), 7,05 (д-like, J=7,5 Гц, 1Har), 6,87 (т, 7=7,5 Гц 1Har), 5,31 (с, 1H, OH), 2,39 (с, 3H, CH3), 2,30 (с, 3H, CH3). 13C-ЯМР (126 МГц, CDCl3): δ 150,68, 139,26, 137,36, 130,51, 129,93, 129,39, 128,73, 127,83, 127,76, 126,20, 124,70, 120,25, 21,60, 16,33. HRMS: [C14H14O] рассчитано 198,1045, измерено 198,1046.
[0164] Повторяя этот эксперимент в мезитилене при 165°C в течение 20 часов, получали 100% преобразование исходного вещества 15 с выходом 16 96%.
[0165] Хотя для надежного установления лежащих в основе путей реакции требуются всесторонние исследования механизмов реакций, отсутствие наблюдения преобразования 3 (4-(триэтилсилил)дибензофурана) в основных условиях и хорошее восстановительное расщепление 4,6-диметилдибензофурана 15 в соответствующий бифенил-2-ол 16, прохождение реакции через дегидробензолы, в виде присутствия орто-силилированных ароматических простых эфиров, которое можно предположить исходно, кажется маловероятным.
[0166] Пример 5.8: Эксперименты EPR
[0167] Дибензофуран (1, 16,8 мг, 0,1 ммоль, 1 эквив.), KOt-Bu (22,5 мг, 0,2 ммоль, 2 эквив.) и Et3SiH (80 микролитров, 0,5 ммоль, 5 эквив.) нагревали в 0,4 мл толуола в течение 1 часа при 100°C в перчаточной камере. После этого реакционную смесь разбавляли 0,8 мл толуола и фильтровали в пробирку EPR. Выясняли, что реакционная смесь является активной в EPR, и записывали спектр в пределах срока 20 мин после фильтрования (фиг.2). В контрольном эксперименте, регистрируемом без дибензофурана, наблюдали тот же сигнал, только с меньшей интенсивностью. Эти результаты соответствуют реакционноспособным радикалам, которые задокументированы для реакций гомолитического ароматического замещения. Выявлено, что добавление 1,10-фенантролина в сочетании с KOt-Bu является вредным, так как преобразования 1 не наблюдали.
[0168] Пример 5.9: Подробное изложение оптимизации для расщепления дибензофурана
[0169] Если не указано иначе эксперименты проводили с использованием общих способов, описанных в примерах 1 и 3. Выходы были воспроизводимы в пределах ±2%.
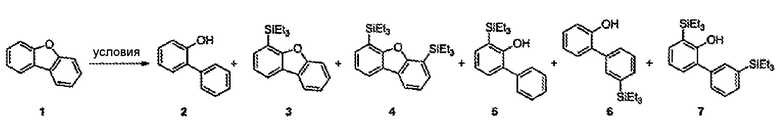
b, реакцию проводили в 0,05M растворе.
c, реакцию проводили с открытым каналом Ar
d, реакцию проводили в чистом Et3SiH.
e, с сорастворителем 1,4-циклогексадиеном (100 эквивалентов)
f, R = 2-этилгексил.
g, с использованием в качестве органосилана вместо Et3SiH полиметилгидросилоксана (PMHS)
[0170] Пример 5.10: Восстановительное расщепление простых диариловых эфиров
[0171] Для исследования расщепления связей C-O простых ариловых эфиров в необработанных субстратах и образцах, если оно проходит без нежелательного чрезмерного восстановления получаемых ароматических фрагменты, простой дифениловый эфир подвергали оптимизированным условиям реакции без добавления добавок, описанным выше. Этот субстрат приводил к получению бензола и фенола с умеренными выходами (таблица 3, пункт 1), где остаток массового баланса преимущественно составляли силилированные, а также другие неидентифицированные продукты. При наличии этого результата оценивали реакционноспособность более сложных простых диариловых эфиров. Показано, что симметричные и несимметричные простые диариловые эфиры являются подходящими субстратами и претерпевают расщепление C-O с эффективностью в диапазоне от хорошей до превосходной (пункты 2-7). Многие из оцениваемых простых диариловых эфиров продемонстрировали большую реакционноспособность по сравнению с простым дифениловым эфиром и допускают использование более мягких условий реакции. В случае простого 1-нафтилфенилового эфира (пункт 5), расщепление связей проходило региоспецифично по нафтильной связи C-O с выходом нафталина и фенола с выходом 70% и 91%, соответственно, с отсутствием детекции 1-нафтола или бензола. При использовании несимметричного простого динафтилового эфира (пункт 5) восстановление связи C-O reduction проходило региоселективно с получением 2-нафтола и 1-нафтола с хорошим объединенным выходом с соотношением двух изомеров приблизительно 4:1, соответственно. Несимметричный замещенный в пара-положении фенилом простой дифениловый эфир (пункт 7) реагирует с хорошим общим выходом и с умеренной региоселективностью в отношении восстановления немного более электронобогатой связи C-O, что свидетельствует о явном влиянии электронных эффектов на региоселективность расщепления связи C-O. Этот фактор становится определяющим для селективности расщепления моделей 4-O-5 лигнина, которые рядом с разрываемой связью C-O содержат сильные метокси-доноры (см. ниже, схема 2). Такая селективность комплементарна селективности, отмечаемой другими исследователями для гомогенного катализируемого Ni восстановления молекулярным водородом, где несимметричные простые диариловые эфиры преимущественно расщепляются со стороны более электроннодефицитного арильного кольца.
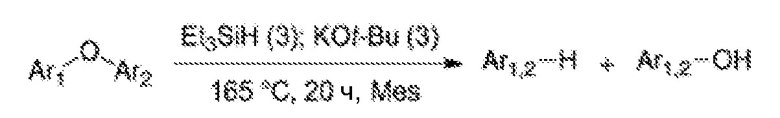
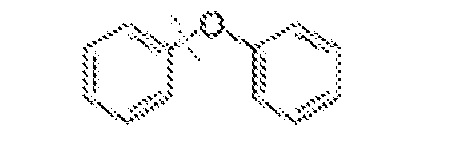
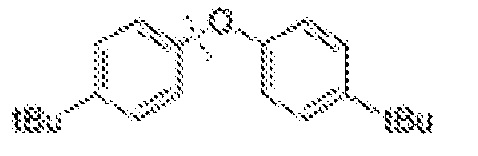
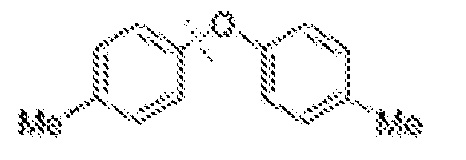

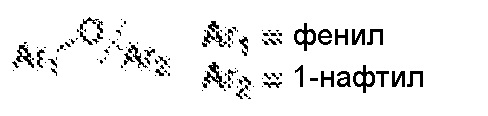
70
-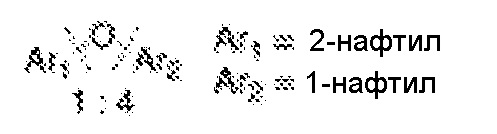
15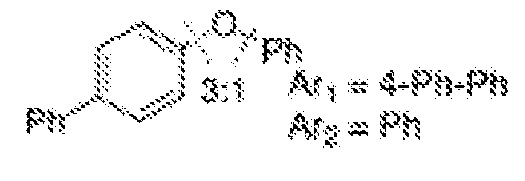
19
65
b Детектировали следовое количество 1,2,3,4-тетрагидронафталина.
c Реакцию проводили при 100°C в течение 20 часов в толуоле с 2 эквив. каждого из Et3SiH и KOt-Bu.
d Реакцию проводили при 75°C в течение 40 часов в толуоле.
[0172] Пример 5.11: Восстановительное расщепление простых арилалкиловых эфиров
[0173] Восстановление простых арилалкиловых эфиров проводили в оптимизированных условиях, используемых для простых диариловых эфиров, для исследования селективности расщепления связи C-O sp2 в сравнению со связью sp3. Реакция 2-метоксинафталина приводила к 2-нафтолу в качестве главного продукта с умеренным выходом (схема 1). Анализ GC-MS неочищенной реакционной смеси вместе с 2-метилнафталином выявил присутствие следовых количеств нафталина и дополнительных восстановленных молекул, включая продукты частичного восстановления ароматических групп. Также детектировали соединения, предположительно происходящие вследствие силилирования 2-нафтола. Подобным образом, расщепление 2-этоксинафталена в тех же условиях приводила к образованию 2-нафтола с немного большим выходом, но с теми же или аналогичными побочными продуктами. Исследовали пространственно стерически затрудненные простые эфиры для исследования приспособляемости и возможного механизма расщепления связи C-O. Несмотря на наличие большого алкильного заместителя рядом с кислородом простого эфира, реакция 2-неопентилоксинафталина приводила к образованию 2-нафтола приблизительно с тем же выходом, что и при менее объемных субстратах. Даже 2-трет-бутилоксинафтален расщеплялся с образованием ожидаемого нафтола с выходом 55% (схема 1). Контрольные эксперименты, проводимые в идентичных условиях, но без триэтилсилана приводили к получению 2-нафтола в случаях 2-этокси- и 2-трет-бутилоксинафталена, хотя и со значительно сниженными выходами. Так как 2-метокси- и 2-неопентилоксисубстраты оставались интактными при таких расщеплениях без силанов, вероятно действующим являлся механизм отщепления b. При попытке восстановления 4-трет-бутил- и 4-метиланизолов в стандартных условиях выходы соответствующих фенолов были высокими, вероятно вследствие более трудного силилирования замещенного фенильного кольца вследствие стерических затруднений (схема 2).
Схема 1
Восстановительное расщепление простых арилалкиловых эфиров
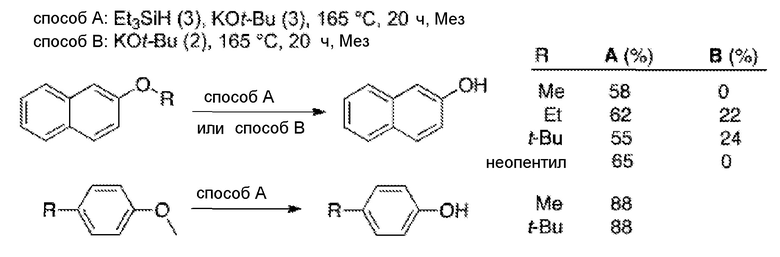
[0174] Суммарно, селективность расщепления связи C-O алкила контрастирует с селективностью, наблюдаемой в катализируемых Ni и бораном реакций расщепления C-O, где происходит восстановление C-O арила. Также характерно, что в этих условиях наблюдали только следовые количества продуктов гидрирования нафталиновых колец, что контрастирует с результатами ионного гидрирования на основе силанов, изложенного в литературе.
[0175] Информативным является сравнение с результатами, представленными выше, расщеплений метоксизамещенных простых диариловых эфиров 8 и 11 (схема 2). Хотя простые арилалкиловые эфиры демонстрируют строгое предпочтение в отношении восстановления связей кислорода с алкилами по сравнению со связями кислорода с арилами, оба метоксисубстрата на схеме 2 демонстрируют обращенную региоселективность, демонстрируя почти исключительно продукты разрыва связей кислорода с арилами. Не намереваясь быть связанным правильностью этой теории, этот эффект можно приписать присутствию донорного атома кислорода в орто-положении со связью C-O, претерпевающей разрыв. Поддержкой этого заключения является высокая селективность восстановительного открытия кольца производного дибензофурана 8, которое в основном приводит к 10. Подобным образом, наблюдают предпочтительное образование фенола и анизола со сходной селективностью в отношении фенолов 12 и 13 при расщеплении модели лигнина 11. Без связи с корректностью теории можно предполагать, что этот эффект можно объяснить резонансной стабилизацией положительного заряда атома кислорода происходящей при электрофильной активации связи C-O, которая претерпевает разрыв. Для тестирования этой гипотезы соединение 3 подвергали условиям реакции и выделяли фенолы 5 и 6 с открытым кольцом вместе с десилилированными продуктами 1 и 2 (схема 2, вставка C). В отсутствие резонансной стабилизации, селективность расщепления возвращалась в пользу изомера 5. Также следует отметить, что, таким образом, как показывает образование 1 и 2, в типичных условиях реакции реакция силилирования обратима. После иллюстрации потенциала для восстановления моделей лигнина 4-O-5 8 и 11, этот способ тестировали с использованием олигомерного простого эфира 14, содержащего шесть связей Car-O (схема 2, вставка D). Примечательно, что при 165°C достигали количественного преобразования мезитилена 14 и получали фенол, бензол, резорцинол и другие неидентифицированные продукты только с 0,5 эквивалентами силана на связь арил-кислород.
[0176] На схеме 2, соединения 1-7 относятся к соответствующим соединениям, описанным в примере 5.9.
[0177]
Схема 2
Способ A: Et3SiH (5) KOt-Bu (2), 100°C, 20 часов в толуоле
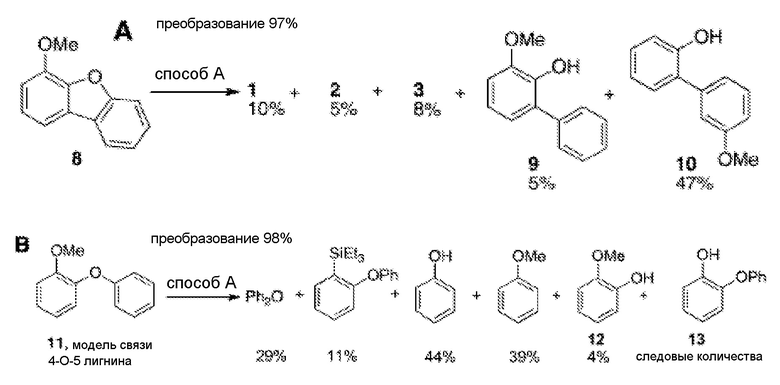
[0178]
Схема 2
Способ B: Et3SiH (3) KOt-Bu (3), 165°C, 20 часов в мезитилене
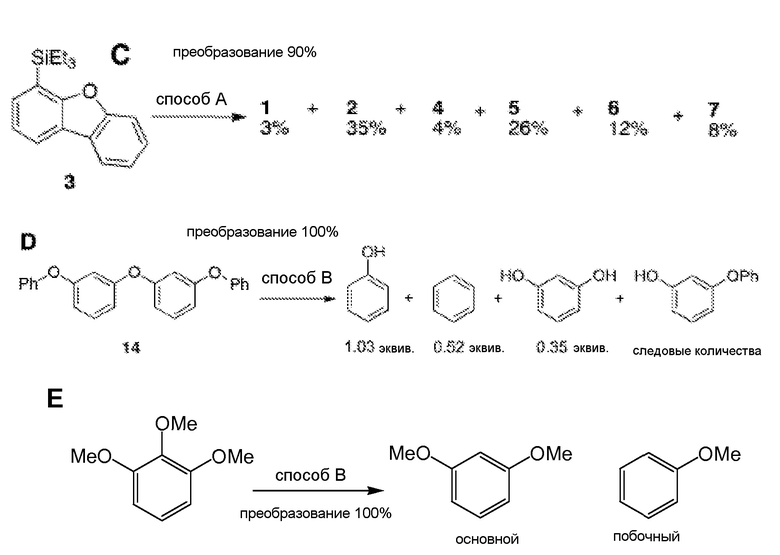
[0179] Пример 5.12: Эксперименты в отношении действия определенных добавок на расщепление дибензофурана
[0180] В дополнительных экспериментах в попытках выяснения механизма реакции тестировали реакционноспособность Et3SiH в присутствии различных добавок. Результаты представлены в приведенной ниже таблице 4. Не идентифицировали ни один из продуктов 2-7.
b, DIBAL представляет собой гидрид диизобутилалюминия
[0181] Пример 5.13: Эксперименты с простыми бензиловыми эфирами
[0182] Эксперименты проводили на простых бензиловых эфирах общими способами, описанными в примере 3. Неожиданно, способы продемонстрировали способность к индукции полного дезоксигенирования этих субстратов-моделей лигнина. По-видимому, этот тип реакционноспособности является беспрецедентным в гомогенных системах на современном уровне техники даже при повышенных температурах.
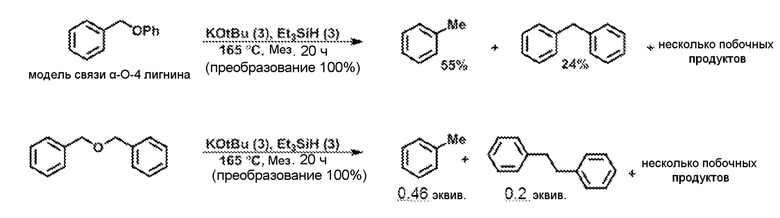
[0183] Пример 5.14: Эксперименты с гетероарильными соединениями с C-N и C-S
[0184] Эксперименты также проводили с гетероарильными соединениями с C-N и C-S. В случае соединений, содержащих связи C-N, реакционноспособность, по-видимому, является сходной с реакционноспособностью, наблюдаемой для связей C-O, и обоснованно ожидают, что широкий диапазон способов, используемых для связей C-O, может приводить к сходной реакционноспособности для связей C-N:
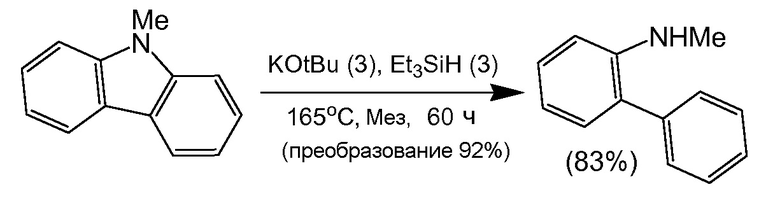
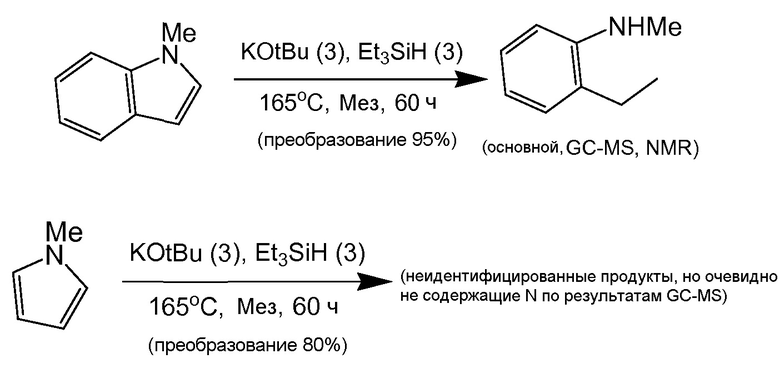
[0185] В случае соединений, включающих соединения с C-S, способы, по-видимому, как правило, приводят к полному десульфурированию молекул. Это различие в реакционноспособностях может отражать различия в энергиях связей между связями C-O, C-N и C-S (сравни энергии диссоциации связи C-X в феноле (111), анилине (104) и тиофеноле (85), все в ккал/моль). Особый интерес представляло десульфурирование даже пространственно-затрудненных дибензотиофенов в относительно мягких условиях. Ни в одном из этих преобразований не детектировали единственные продукты C-S:
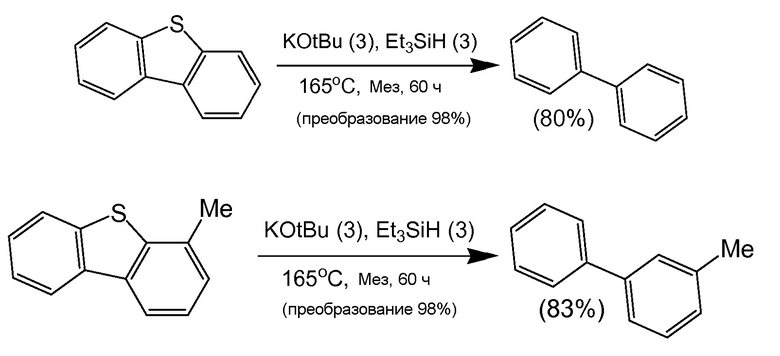
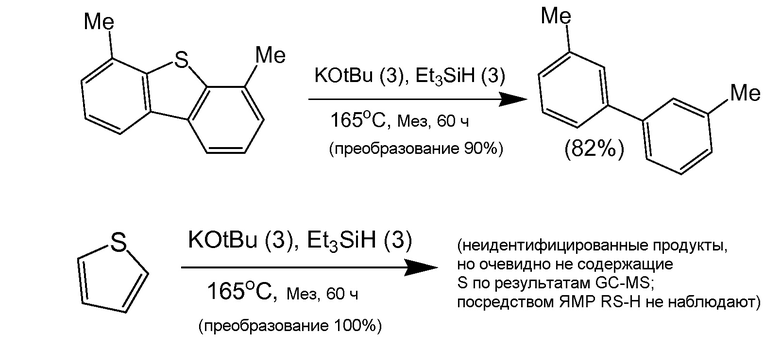
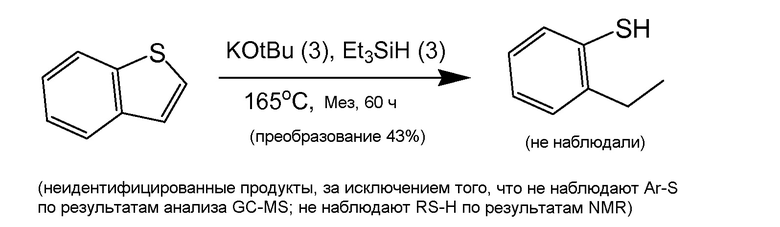
[0186] Как понятно специалистам в данной области, в соответствии с этими указаниями возможны многочисленные модификации и вариации настоящего изобретения и все они предусмотрены настоящим документом. Например, в дополнение к вариантам осуществления, описываемым в настоящем документе, в настоящем изобретении предусмотрено и заявлены варианты изобретения, являющиеся результатом комбинации признаков изобретения, перечисленных в настоящем документе и признаков цитируемых ссылок на известный уровень техники, которые дополняют признаки настоящего изобретения. Подобным образом, следует понимать, что любые описанные материал, характеристику или изделие можно использовать в комбинации с любыми другими материалом, характеристикой или изделием, и такие комбинации рассматривают, как находящиеся в объеме настоящего изобретения.
[0187] Описания каждого патента, патентной заявки и публикации, цитируемых или описанных в настоящем документе, полностью включены в настоящий документ в качестве ссылки для всех целей.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВОССТАНОВИТЕЛЬНОЕ РАСЩЕПЛЕНИЕ АРОМАТИЧЕСКИХ СВЯЗЕЙ C-O, C-N И C-S АКТИВИРОВАННЫМИ СИЛАНАМИ БЕЗ ПЕРЕХОДНЫХ МЕТАЛЛОВ | 2013 |
|
RU2650112C2 |
| СПОСОБ СНИЖЕНИЯ СОДЕРЖАНИЯ ЛИГНИНА В СЫРЬЕ ДЛЯ БИОМАССЫ | 2021 |
|
RU2783531C1 |
| СИЛИЛИРОВАНИЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ БЕЗ ПЕРЕХОДНЫХ МЕТАЛЛОВ | 2013 |
|
RU2651570C2 |
| БИОКОМПОЗИЦИОННАЯ ПЛИТА | 2011 |
|
RU2586699C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСОВ РУТЕНИЯ И ИХ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ И ИХ ПРИМЕНЕНИЕ В МЕТАТЕЗИСЕ ОЛЕФИНОВ | 2016 |
|
RU2735724C1 |
| МЕТОДЫ ПРОИЗВОДСТВА ТОПЛИВА ДЛЯ РЕАКТИВНЫХ ДВИГАТЕЛЕЙ ИЗ НАТУРАЛЬНОГО МАСЛА КАК ИСХОДНОГО СЫРЬЯ С ПОМОЩЬЮ РЕАКЦИЙ ОБМЕНА | 2009 |
|
RU2522436C2 |
| СТИЛЬБЕНОВОЕ ПРОИЗВОДНОЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2017 |
|
RU2776328C2 |
| СИНТЕЗ 1,3-БУТАДИЕНА | 2015 |
|
RU2700413C2 |
| РУТЕНИЕВЫЕ КОМПЛЕКСЫ, СОДЕРЖАЩИЕ ПАРАЦИКЛОФАНОВЫЕ И КАРБОНИЛЬНЫЕ ЛИГАНДЫ, И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ КАТАЛИЗАТОРА | 2012 |
|
RU2614415C2 |
| ПРОИЗВОДНЫЕ ЭФИРОВ ФОСФОНОВЫХ КИСЛОТ И СПОСОБЫ ИХ СИНТЕЗА | 2011 |
|
RU2581045C2 |
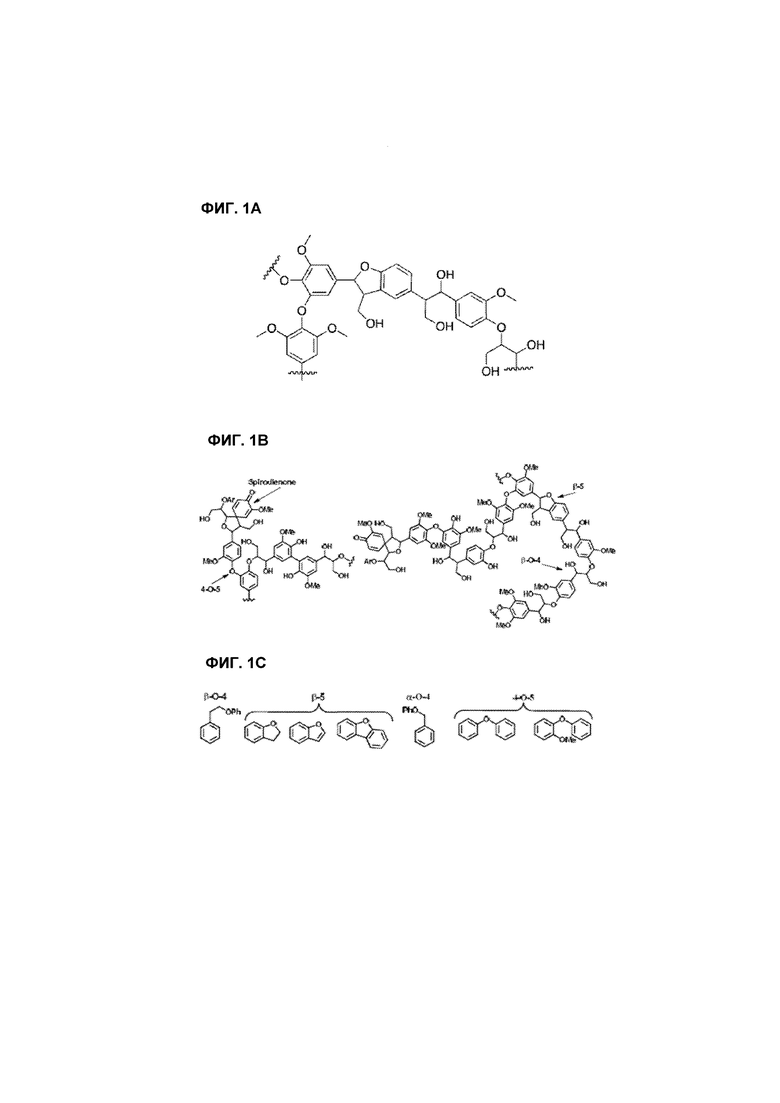
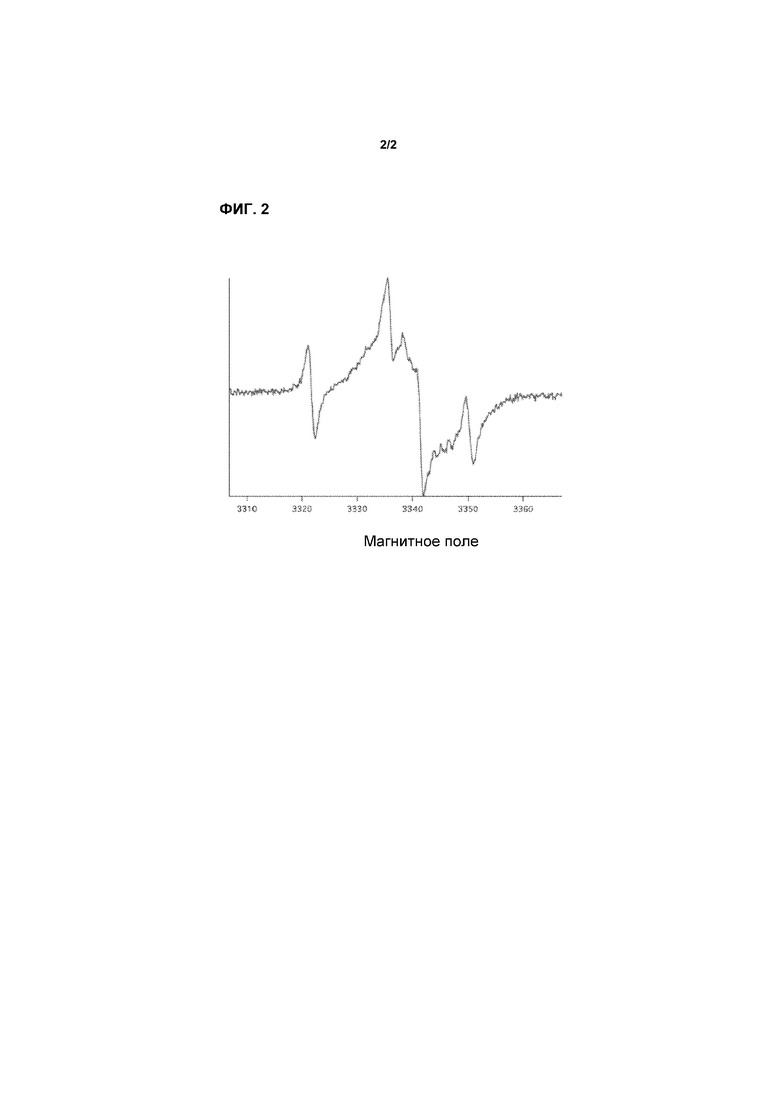
Изобретение относится к способам восстановительного расщепления связи C-S в ароматических соединениях, находящихся в технологических потоках. Предложен способ снижения серы в топливе или топливном сырье, которое содержит по меньшей мере один ароматический субстрат, содержащий сероводородную связь, где способ включает контактирование топлива или топливного сырья с химической системой, содержащей по меньшей мере один органосилан, имеющий по меньшей мере одну связь кремний-водород, по меньшей мере одно сильное основание и необязательно по меньшей мере одно соединение-донор молекулярного водорода, молекулярный водород или оба, при температуре от 75 до 450°С для уменьшения хотя бы части связей углерод-сера в органическом субстрате. Технический результат – устранение серы из сырьевых потоков для улучшения экологии и предотвращение отравления катализаторов из драгоценных металлов в каталитических конверторах. 19 з.п. ф-лы, 2 ил., 4 табл., 22 пр.
1. Способ снижения содержания серы в топливе или топливном сырье, где топливо или топливное сырье содержит по меньшей мере один ароматический субстрат, содержащий сероводородную связь, причем способ включает контактирование топлива или топливного сырья с химической системой, содержащей:
(а) по меньшей мере один органосилан, имеющий по меньшей мере одну связь кремний-водород (Si-Н) и
(b) по меньшей мере одно сильное основание, содержащее алкоксид калия, алкоксид цезия или гидрид калия, и необязательно
(c) по меньшей мере одно соединение-донор молекулярного водорода, молекулярный водород или оба;
при температуре от 75 °C до 450 °C для уменьшения хотя бы части связей углерод-сера в органическом субстрате;
где ароматический субстрат содержит необязательно замещенный тиофен, 2,3-дигидробензотиофен, бензотиофен или дибензотиофен или необязательно замещенный фенилсульфид, бензолтиол, нафтилсульфид или их комбинацию; и
где по меньшей мере один органосилан, имеющий по меньшей мере одну связь кремний-водород (Si-Н), содержит органосилан формулы (I):
(R)4-mSi(H)m (I),
где m равно 1, 2 или 3 и
R представляет собой необязательно замещенный С1-12алкил, С6-20арил, С7-30алкарил, С7-30аралкил и, если они замещены, заместители представляют собой галоген или связаны c нерастворимым или минимально растворимым субстратом, содержащим оксид алюминия, диоксид кремния или углерод.
2. Способ по п.1, в котором по меньшей мере одна углерод-серная связь экзоциклична ароматическому кольцевому фрагменту ароматического субстрата.
3. Способ по п.1, в котором по меньшей мере одна углерод-серная связь внутрициклична ароматическому кольцевому фрагменту ароматического субстрата.
4. Способ по п.1, в котором ароматический субстрат содержит по меньшей мере одну алифатическую углерод-серную связь.
5. Способ по п.1, в котором по меньшей мере один органосилан содержит алкил, арил или смешанный арилалкил-органосилан формулы (I):
(R)4-mSi(H)m (I),
где m равно 1 или 2 и
R независимо представляет собой С1-12алкил, С6-20-арил, С7-30-алкарил или С7-30-аралкил.
6. Способ по п.1, в котором по меньшей мере один органосилан представляет собой (R)3SiH, где R представляет собой C1-6алкил.
7. Способ по п.1, в котором по меньшей мере одно сильное основание содержит гидрид калия.
8. Способ по п.1, в котором по меньшей мере одно сильное основание содержит алкоксид цезия.
9. Способ по п.1, в котором алкоксид калия или алкоксид цезия содержит C1-12линейный или разветвленный алкильный фрагмент или C5-10арил или гетероарильный фрагмент.
10. Способ по п.1, в котором алкоксид калия содержит метоксид калия, этоксид калия, пропоксид калия, бутилат калия или 2-этилгексил алкоксид калия; алкоксид цезия содержит метоксид цезия, этоксид цезия, пропоксид цезия, бутоксид цезия или 2-этилгексилалкоксид цезия.
11. Способ по п.1, в котором алкоксид калия представляет собой трет-бутоксид калия.
12. Способ по п.1, в котором по меньшей мере один органосилан представляет собой триэтилсилан и по меньшей мере одно сильное основание представляет собой трет-бутоксид калия.
13. Способ по п.1, в котором топливо или топливное сырье имеют температуру кипения при давлении одной атмосферы в диапазоне от 25 до 450oC.
14. Способ по п.1, в котором топливо или топливное сырье представляет собой биопиролизное масло, черный щелок, уголь, уголь, при ожижении угля, природный газ или нефть.
15. Способ по любому из пп.1-14, в котором химическая система не содержит добавленного соединения переходного металла.
16. Способ по любому из пп.1-15, в котором присутствует по меньшей мере одно соединение-донор молекулярного водорода, молекулярный водород или оба
17. Способ по любому из пп.1-16, в котором присутствует по меньшей мере одно соединение-донор молекулярного водорода и включает 1,3-циклогексадиен, 1,4-циклогексадиен, 1,2-циклогексадиен, 1,2-дигидронафталин, 1,4-дигидронафталин, 1,2-дигидрохинолин, 3,4-дигидрохинолин, 9,10-дигидроантрацен или тетралин.
18. Способ по любому из пп.1-17, в котором контактирование осуществляют при температуре в диапазоне от 100 °C до 450 °C.
19. Способ по любому из пп.1-17, в котором контактирование осуществляют при температуре в диапазоне от 150 °C до 450 °C.
20. Способ по любому из пп.1-19, в котором каждый из органосилана и сильного основания в химической системе независимо присутствует относительно общего количества углерод-серных связей в органическом субстрате в соотношении в диапазоне от 1:2 до 10:1.
| СПОСОБ ГИДРОГЕНИЗАЦИИ УГЛЯ | 2007 |
|
RU2333930C1 |
| Байманова А.Е., Жакунова Г.Ж | |||
| Серосодержащие соединения нефти и основные методы очистки нефти и нефтяных фракций от них | |||
| Учебное пособие | |||
| Актобе, АГУ им.К.Жубенова, 2010, 36 с | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| US 6576584 B1, 10.06.2003 | |||
| СПОСОБ СЕЛЕКТИВНОЙ ОЧИСТКИ БЕНЗИНОВЫХ ФРАКЦИЙ КАТАЛИТИЧЕСКОГО КРЕКИНГА (ВАРИАНТЫ) | 2008 |
|
RU2372380C1 |
Авторы
Даты
2022-04-01—Публикация
2013-10-02—Подача