Изобретение относится к медицине, а именно - к дерматовенерологии, иммунологии и клинической лабораторной диагностике и предназначено для выявления аутореактивных антител к отдельным фрагментам экстрацеллюлярного домена десмоглеина 3-го типа (Dsg3) человека у больных пузырчаткой обыкновенной (L10.0 по МКБ-10). Изобретение может быть использовано для обнаружения аутореактивных антител к Dsg3 человека в сыворотке крови при проведении первичной диагностики пузырчатки, исследовании развития аутоимунного ответа на Dsg3 в динамике заболевания с построением соответствующего прогноза, выборе средств и методов для удаления аутореактивных антител из крови пациентов, а также для оценки эффективности проводимых терапевтических мероприятий.
Из уровня техники (Ishii K, Amagai М, Hall RP. et al.: Characterization of autoantibodies in pemphigus using antigen-specific ELISAs with baculovirus expressed recombinant desmogleins. J Immunol 1997; 159:2010-2017) известна чувствительная и специфичная экспериментальная тест-система иммуноферментного анализа (ELISA) для выявления суммарных аутоантител против Dsg3, положенная в основу коммерчески доступной тест-системы «MESACUP-2 TEST Desmoglein 3», выпускаемой фирмой MBL (Medical and Biological Laboratories Co. Ltd. Нагоя, Япония). В данной тест-системе используется полноразмерный рекомбинантный внеклеточный домен Dsg3 человека, продуцируемый клетками СНО (Chinese hamster ovary). Уровень антител в сыворотке крови оценивается индексом U/ml (Unit value/ml). Тест-система включает калибраторы 0, 20 и 100 U/ml, с использованием которых рассчитывается данный индекс. Значение индекса ≥20 свидетельствует о наличии антител к Dsg3. Существенным недостатком данной тест системы является отсутствие возможности построения калибровочного графика для количественной оценки уровня аутоантител против экстрацеллюлярного домена Dsg3, а также невозможность определения профиля аутоантител против отдельных фрагментов ЕС1-ЕС5 внеклеточного домена Dsg3 (Amagai М. Klaus-Kovtun V., Stanley J.R. Autoantibodies against a novel epithelial cadherin in pemphigus vulgaris, a disease of cell adhesion. Cell 1991; 67:869-877).
В другой известной системе ELISA (Schmidt E,  C, Rosemann A. et al. Novel ELISA systems for antibodies to desmoglein 1 and 3: correlation of disease activity with serum autoantibody levels in individual pemphigus patients. Exp Dermatol. 2010; 19: 458-463) в качестве целевых антигенов применены экстрацеллюлярные домены Dsg1 и Dsg3, экспрессированные в клеточной линии человека HEK293. Уровень активности антител в исследуемом образце оценивается в сравнительных единицах - relative units в мл (RU/ml). Для количественной характеристики активности антител в состав тест-системы входят калибраторы 2, 20 и 200 RU/ml, на основе значений оптической плотности которых строится калибровочный график. Как и в тест-системе фирмы MBL, значение активности ≥20 RU/ml свидетельствует о наличии антител к Dsg3. Разработанная Schmidt Е. et al. тест-система в настоящее время коммерциализована и выпускается фирмой Euroimmun - «Anti-Dsg3 ELISA (IgG)» (Medizinische Labordiagnostika AG,
C, Rosemann A. et al. Novel ELISA systems for antibodies to desmoglein 1 and 3: correlation of disease activity with serum autoantibody levels in individual pemphigus patients. Exp Dermatol. 2010; 19: 458-463) в качестве целевых антигенов применены экстрацеллюлярные домены Dsg1 и Dsg3, экспрессированные в клеточной линии человека HEK293. Уровень активности антител в исследуемом образце оценивается в сравнительных единицах - relative units в мл (RU/ml). Для количественной характеристики активности антител в состав тест-системы входят калибраторы 2, 20 и 200 RU/ml, на основе значений оптической плотности которых строится калибровочный график. Как и в тест-системе фирмы MBL, значение активности ≥20 RU/ml свидетельствует о наличии антител к Dsg3. Разработанная Schmidt Е. et al. тест-система в настоящее время коммерциализована и выпускается фирмой Euroimmun - «Anti-Dsg3 ELISA (IgG)» (Medizinische Labordiagnostika AG,  Germany). Недостатком данной тест системы также является отсутствие возможности охарактеризовать специфичность аутореактивных антител к отдельным фрагментам экстрацеллюлярного домена Dsg3 человека у больных вульгарной пузырчаткой.
Germany). Недостатком данной тест системы также является отсутствие возможности охарактеризовать специфичность аутореактивных антител к отдельным фрагментам экстрацеллюлярного домена Dsg3 человека у больных вульгарной пузырчаткой.
Указанный недостаток рассматриваемых тест-систем имеет принципиальное значение, поскольку имеются сообщения о возможности преобладания в разные фазы заболевания аутоантител класса IgG, специфичных к разным (проксимальным С-концевым или дистальным N-концевым) фрагментам экстрацеллюлярного домена Dsg3. При этом аутоантитела к дистальному фрагменту ЕС1, имея более низкую активность в ELISA, обладают большей патогенностью, в то время как более реакционно-активные антитела к проксимальным доменам ЕС4 и ЕС5 менее патогенны (Amagai М, Karpati S, Prussick R, Klaus-Kovtun V, Stanley J R. Autoantibodies against the amino-terminal cadherin-like binding domain of pemphigus vulgaris antigen are pathogenic. J Clin Invest 1992; 90: 919-926).
Другим аргументом в пользу необходимости анализа индивидуальных профилей иммунореактивности на способность взаимодействия с тем или иным фрагментом экстрацеллюлярного домена Dsg3 человека является т.н. «теория распространения эпитопов» (Lehmann, P.V., Forsthuber, Т., Miller, A. and Sercarz, Е.Е. Spreading of T-cell autoimmunity to cryptic determinants of an autoantigen. Nature 1992; 358: 155-157. The first description of epitope spreading in an autoimmune disease). Согласно данным представлениям, у пациентов с обыкновенной пузырчаткой клинический переход от слизистого фенотипа к слизисто-кожному происходит из-за смены мишеней для аутореактивных антител. По данным Salato V. et al. (Salato V.K., Hacker-Foegen M.K., Zelmira Lazarova Z., Fairley J.A., Lin M-S. Role of intramolecular epitope spreading in pemphigus vulgaris. Clinical Immunology 2005; 116: 54-66), у большинства пациентов со слизистой формой пузырчатки аутоантитела направлены к проксимальной (С-концевой) части экстрацеллюлярного домена Dsg3, в то время как для развития повреждений кожи характерно появление антител к дистальным (N-концевым) эпитопам. В связи с этим возникает задача персонализированного наблюдения уровня аутоантител к различным фрагментам экстрацеллюлярного домена Dsg3 человека у пациентов с различным клиническим фенотипом вульгарной пузырчатки ( R., Svoboda V., Wenzel E et al. IgG against extracellular subdomains of desmoglein 3 relates to clinical phenotype of pemphigus vulgaris Exp Dermatol 2008; 17: 35-43).
R., Svoboda V., Wenzel E et al. IgG against extracellular subdomains of desmoglein 3 relates to clinical phenotype of pemphigus vulgaris Exp Dermatol 2008; 17: 35-43).
Доступные технические решения, обеспечивающие возможность определения антигенной специфичности аутореактивных антител к отдельным фрагментам экстрацеллюлярного домена Dsg3 у больных обыкновенной пузырчаткой, из уровня техники не известны.
Техническая проблема, на решение которой направлен заявляемый способ, заключается в определении антигенной специфичности аутореактивных антител к отдельным фрагментам экстрацеллюлярного домена Dsg3 у больных обыкновенной пузырчаткой.
Техническим результатом заявляемого изобретения является возможность полуколичественной оценки аутоантител к полному экстрацеллюлярному домену десмоглеина 3-го типа и его наиболее иммуногенным отдельным фрагментам ЕС1, ЕС2, ЕС3, ЕС4, а также ЕС2-ЕС5 в сыворотке крови пациентов с вульгарной пузырчаткой.
Для решения заявленной технической проблемы и достижения технического результата предлагается применение рекомбинатного белка-антигена, содержащего рекомбинантный полноразмерный экстрацеллюлярный домен Dsg3full-His с последовательностью SEQ ID NO: 1 и его отдельные рекомбинантные фрагменты ЕС1-His, EC2-His, ЕС3-His, EC4-His, EC2-EC5-His, имеющие последовательности SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11 соответственно, для определения наличия аутореактивных антител к десмоглеину 3-го типа человека в крови больных обыкновенной пузырчаткой.
Предлагается способ определения антигенной специфичности аутореактивных антител к отдельным фрагментам экстрацеллюлярного домена десмоглеина 3-го типа человека у больных обыкновенной пузырчаткой, включающий исследование взаимодействия сыворотки крови с данным белком с использованием твердофазного иммуноферментного анализа, отличающийся тем, что в качестве антигенов для ИФА применяют белки-антигены, при этом исследование осуществляют в два этапа, на первом из которых осуществляют конкурентное истощение аутоантител к Dsg3full-His, ЕС1-His, EC2-His, ЕС3-His, EC4-His, EC2-EC5-His, имеющие последовательности SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11 соответственно, и контрольному материалу - БСА, сорбированным на твердой фазе, а на втором осуществляют определение остаточных (непрореагировавших) аутоантител по отношению к Dsg3full-His с последовательностью SEQ ID NO: 1 с последующим расчетом коэффициента конкуренции по отношению к отдельным рекомбинантным белкам по формуле:

где AR - активность сыворотки после преинкубации в контакте с иммобилизованным рекомбинантным белком - ЕС1-His, EC2-His, ЕС3-His, EC4-His, EC2-EC5-His;
APos - активность сыворотки после преинкубации с полноразмерным Dsg3full-His;
ANeg - активность сыворотки после преинкубации в контрольной лунке с иммобилизированным БСА.
Предлагается тест-система для определения эпитопной специфичности аутореактивных антител к фрагментам экстрацеллюлярного домена десмоглеина 3-го типа человека у больных обыкновенной пузырчаткой способом по п. 5, содержащая сорбент, набор реагентов, концентрат конъюгата для определения содержания IgG-антител к Dsg3, отличающаяся тем, что в качестве сорбента выбран иммуносорбент.
Набор реагентов указанной тест-системы содержит положительную (+k) сыворотку, представляющую собой индивидуальную сыворотку от пациента с обыкновенной пузырчаткой с предварительно охарактеризованной активностью в отношении Dsg3 и профилем антигенной специфичности в отношении фрагментов экстрацеллюлярного домена Dsg3 человека, и отрицательную (-k) сыворотку, сформированную из пула сывороток здоровых доноров.
Сущностью заявляемого способа, сформулированной на уровне функционального обобщения и лежащей в его основе, является следующее: двухэтапный иммуноферментный анализ, включающий конкурентное «истощение» аутоантител к рекомбинантным белкам ЕС1-His, EC2-His, ЕС3-His, EC4-His, EC2-EC5-His, сорбированным на твердой фазе, с последующим определением остаточных (непрореагировавших) аутоантител по отношению к полноразмерному экстрацеллюлярному домену десмоглеина 3-го типа человека, Dsg3full-His, позволяет охарактеризовать профиль антигенной специфичности аутореактивных антител с их выражением полуколичественной величиной (%) от общего значения аутореактивности.
Актуальность изобретения определяется ключевой патогенетической ролью в развитии обыкновенной пузырчатки, установленной для аутоантител класса IgG, направленных против основного структурного белка десмосом кожи человека - десмоглеина 3-го типа. Его экстрацеллюлярный домен, в котором выделяют 5 фрагментов (ЕС1, ЕС2, ЕС3, ЕС4, ЕС5) (англ. - extracellular domain; ЕС), вовлечен в формирование гомофильного контакта между соседствующими эпителиальными клетками. Результатом взаимодействия аутоантител с экстрацеллюлярным доменом Dsg3 является разрушение десмосом и развитие так называемого «акантолиза» - дегенеративного изменения шиповатого слоя эпидермиса, проявляющееся разрушением межклеточных мостиков и приводящего к образованию интраэпидермальных пузырей.
Изобретательский уровень заявляемого технического решения определяется применением двухэтапного иммуноферментного анализа на твердой фазе, позволяющим на первом этапе (за счет иммобилизованных в лунках полистироловых планшетов рекомбинантных белков - Dsg3full-His (имеет аминокислотную последовательность SEQ ID NO: 1 и нуклеотидную последовательность SEQ ID NO: 2), ЕС1-His (имеет аминокислотную последовательность SEQ ID NO: 3 и нуклеотидную последовательность SEQ ID NO: 4), EC2-His (имеет аминокислотную последовательность SEQ ID NO: 5 и нуклеотидную последовательность SEQ ID NO: 6), ЕС3-His (имеет аминокислотную последовательность SEQ ID NO: 7 и нуклеотидную последовательность SEQ ID NO: 8), EC4-His (имеет аминокислотную последовательность SEQ ID NO: 9 и нуклеотидную последовательность SEQ ID NO: 10), EC2-EC5-His (имеет аминокислотную последовательность SEQ ID NO: 11 и нуклеотидную последовательность SEQ ID NO: 12) осуществить специфическую сорбцию IgG, а на втором этапе определить количество остаточных (непрореагировавших) аутоантител к Dsg3-His с расчетом по оригинальной формуле полуколичественных показателей индивидуального профиля антигенной специфичности сыворотки крови больных вульгарной пузырчаткой.
Способ получения обозначенных выше рекомбинантных белков (ЕС1-His, EC2-His, ЕС3-His, EC4-His, EC2-EC5-His, Dsg3rull-His), не является предметом настоящего изобретения и является самостоятельным техническим решением.
Соответственно, при реализации заявляемого способа характеристика действий, порядок их выполнения и условия осуществления представляются следующим образом:
1) Исследуемая сыворотка крови разводится 1:100 в буфере (1% БСА в PBS), после чего аликвотами по 100 мкл вносится в лунки полистиролового планшета А, в одной из которых предварительно сорбирован рекомбинантный Dsg3full-His домен в количестве 1 мкг/лунку, в других - рекомбинантные EC1-His, EC2-His, ЕС3-His, EC4-His, EC2-EC5-His в количестве 1 мкг/лунку, а также БСА в той же концентрации для контроля неспецифической сорбции;
2) В аналогичные лунки планшета А вносятся положительная (+k) сыворотка, представляющая собой индивидуальную сыворотку от пациента с обыкновенной пузырчаткой с предварительно охарактеризованной активностью в отношении полноразмерного экстрацеллюлярного домена Dsg3 человека и профилем антигенной специфичности в отношении отдельных фрагментов экстрацеллюлярного домена Dsg3 человека, а также отрицательная (-k), сформированная из пула сывороток здоровых доноров;
3) Планшет А инкубируется в течение 18 часов при +24°С и встряхивании 200 rpm; сущностью этапа является конкурентное связывание (истощение) аутоантител определенной специфичности при взаимодействии с соответствующими рекомбинантными белками;
4) После завершения инкубации опытные и контрольные образцы исследуемых сывороток в полном объеме переносятся в лунки полистиролового планшета Б (табл. 1), сорбированного Dsg3full-His в количестве 1 мкг/лунку;
5) В дополнительные лунки планшета Б вносятся калибровочные образцы с активностями 20 и 200 RU/мл, сформированные на основе пула сывороток больных вульгарной пузырчаткой и предварительно количественно охарактеризованные по данной активности с использованием внешней (референсной) тест-системы;
6) Планшет Б заклеивается и инкубируется в том же режиме (18 час; +24°С; 200 rpm); сущностью этапа является связывание оставшихся после конкурентного «истощения» аутоантител с Dsg3full-His;
7) Планшет Б трехкратно промывается PBST;
8) В лунки планшета Б вносятся антитела к IgG человека, коньюгированные с пероксидазой хрена, после чего планшет инкубируется 60 мин при 22-24°С, затем 3-кратно промывается PBST;
9) В лунки планшета Б вносится субстратный раствор тетраметилбензидин (ТМБ) и инкубируется 30 мин;
10) Реакция останавливается внесением 4N раствора серной кислоты;
11) Оптическая плотность (ОП) результата ИФА регистрируется при 450 нм;
12) На основе ОП калибровочных образцов с активностями 20 и 200 RU/мл планшета Б строится калибровочная кривая, позволяющая определить активность каждой исследуемой сыворотки; активность выражается количественной величиной RU/мл;
13) На основе сравнения значений RU/мл каждой индивидуальной сыворотки, инкубированной в контрольной и опытных лунках планшета А и в дальнейшем анализируемой в планшете Б, рассчитывается степень ее специфического связывания (коэффициент конкуренции) по отношению к отдельным рекомбинантным белкам по формуле:
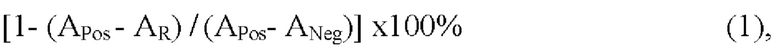
где AR - активность сыворотки после преинкубации в лунке планшета А, иммобилизованной рекомбинантным белком - ЕС1-His, EC2-His, ЕС3-His, EC4-His, EC2-EC5-His;
APos - активность сыворотки после преинкубации в лунке планшета А с Dsg3full-His;
ANeg - активность сыворотки после преинкубации в контрольной лунке планшета А с иммобилизированным БСА.
14) Качество проведенного исследования контролируется на основе значений ОП в лунках планшета Б, заполненных (-k) сывороткой (отсутствие детектируемых аутоантител) и (+k) сывороткой (наличие активности в отношении Dsg3full-His с отклонением ±10% от ранее охарактеризованного значения RU/мл; а также соответствие предварительно охарактеризованному профилю антигенной специфичности к ЕС1-His, ЕС2-His, ЕС3-His, EC4-His, EC2-EC5-His, %).
Заявляемое изобретение иллюстрируется, но никак не ограничивается следующими примерами и рисунками.
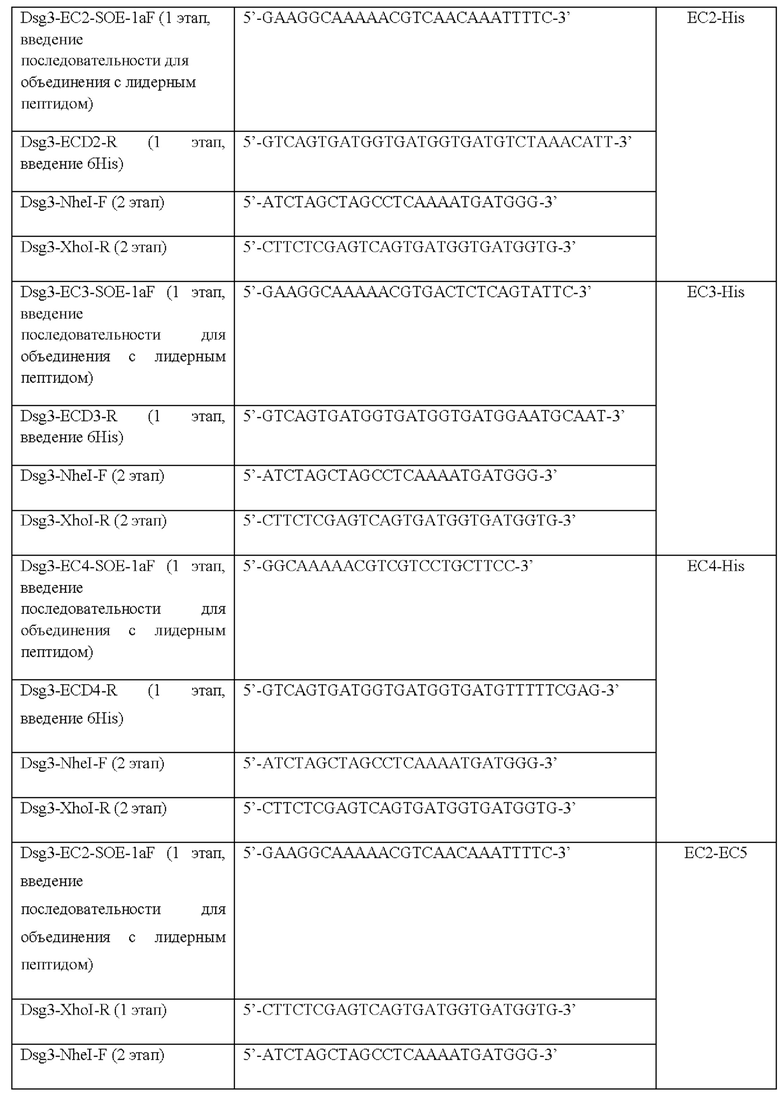
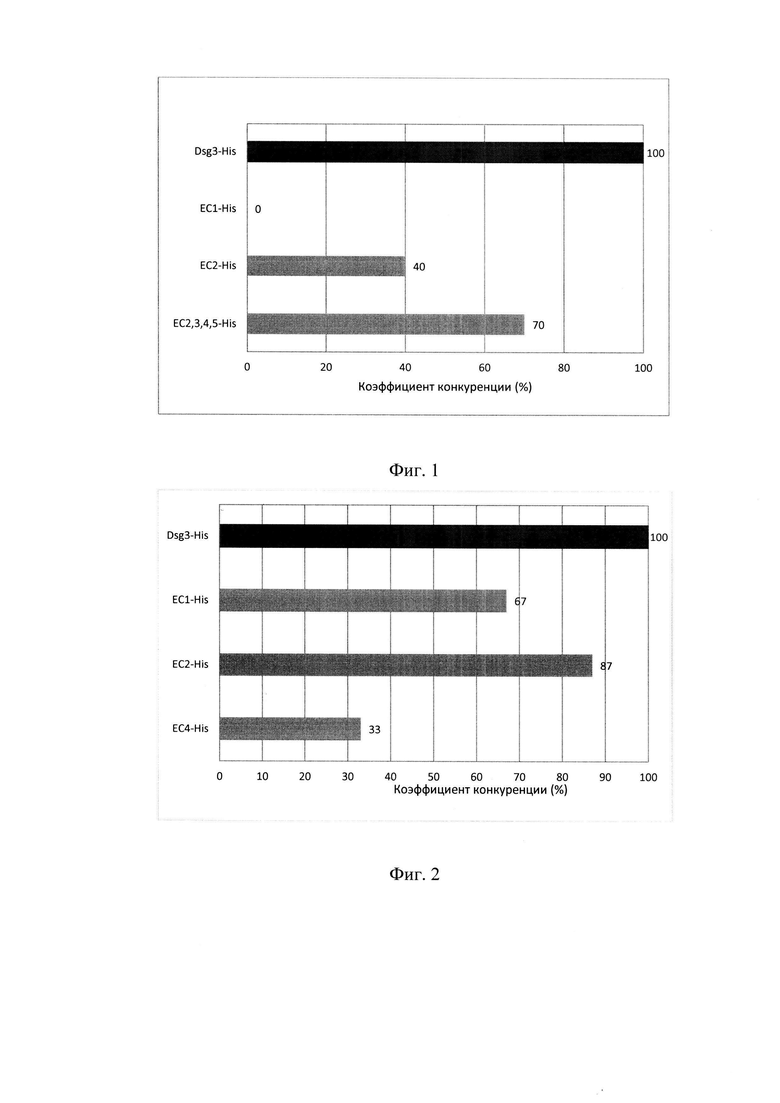
Фиг. 1 и Фиг. 2 Профиль антигенной специфичности образцов (коэффициенты конкуренции исследуемой сыворотки);
Фиг. 3. Схема экспрессионной кассеты;
Фиг. 4. Электрофореграмма (14% SDS-ПААГ для А, Б, Г, Д, Е и 10% SDS-ПААГ для В) элюированных фракций после металл-аффинной хроматографии на Ni2+-ИДА-сефарозе, нанесенных в присутствии β-меркаптоэтанола.
Пример 1.
Объектом исследования послужила сыворотка крови №0X11 из Коллекции сывороток крови от пациентов с клинически подтвержденным диагнозом «Пузырчатка обыкновенная» (L10.0 по МКБ-10), сформированной в ФГБУ «Государственный научный центр дерматовенерологии и косметологии» Минздрава России. Предварительно охарактеризованная (с использованием референсной тест-системы) суммарная активность данной сыворотки к полноразмерному внеклеточному домену Dsg3 человека характеризовалась величиной 200 RU/ml.
Конкурентное истощение аутоантител из данной сыворотки проводили на планшете А в отношении рекомбинантных белков Dsg3full-His, EC2-EC5-His, ЕС1-His, EC2-His, каждый из которых был сорбирован в дозе 1 мкг/лунку, а также БСА (контроль неспецифической сорбции) в такой же концентрации. Взаимодействие тестируемой сыворотки в объеме 100 мкл и рекомбинантных белков в планшете А проводилось при +24°С в течение 18 часов в условиях непрерывного перемешивания на шейкере при 200 rpm. После завершения инкубации образцы сыворотки в полном объеме были перенесены в лунки планшета Б, сорбированного белком Dsg3full-His в дозе 1 мкг/лунку. В дополнительные лунки планшета Б были внесены калибровочные образцы с активностями 20 и 200 RU/ml. Заполненный подобным образом планшет Б инкубировался при +24°С в течение 18 часов на шейкере при 200 rpm. Содержимое лунок было удалено и лунки трижды промыты PBS с 0,05% Tween 20 (PBST), после чего в лунки были внесены по 100 мкл антител к IgG человека, конъюгированных с пероксидазой хрена. После часовой инкубации при +24°С лунки были отмыты, как описано выше, после чего в них было внесено по 100 мкл раствора тетраметилбензидина (субстрата для пероксидазы хрена) и через 30 мин реакция была остановлена добавлением 100 мкл серной кислоты. Оптическую плотность результатов реакции регистрировали при 450 нм.
На основе ОП калибровочных образцов с активностями 20 и 200 RU/мл строили калибровочный график, по которому определяли остаточную (после преинкубации в планшете А) активность образцов исследуемой сыворотки в каждой лунке планшета Б; активность выражали количественной величиной RU/мл. На основании полученных значений активности, пользуясь формулой 1, рассчитывалась коэффициент конкуренции сыворотки с каждым представленным на планшете А рекомбинантным белком. Полученный профиль антигенной специфичности представлен на Фиг. 1.
Как следует из представленных данных, исследуемая сыворотка интенсивно взаимодействовала с Dsg3full-His (100%). При этом особенностью профиля ее антигенной специфичности являлось отсутствие детектируемого аутоиммунного ответа на наиболее «патогенный» дистальный N-концевой домен ЕС1, при выраженном реагировании с доменом ЕС2, а также проксимальными (С-концевыми) эпитопами, присутствующими в составе EC2-EC5-His конструкта.
Полученный результат позволяет оценить прогноз течения заболевания как достаточно благоприятный и ограничиться проведением традиционной консервативной терапии с использованием глюкокортикоидных гормонов.
Пример 2.
В качестве источника аутоантител к Dsg3 использована нативная сыворотка крови №0Z218, полученная от пациента с клинически подтвержденным диагнозом «Пузырчатка обыкновенная» (L10.0 по МКБ-10) в фазе обострения, находящегося на стационарном лечении в ФГБУ «Государственный научный центр дерматовенерологии и косметологии» Минздрава России. Предварительно охарактеризованная активность данной сыворотки в отношении полноразмерного внеклеточного домена Dsg3 человека характеризовалась величиной 150 RU/ml.
Конкурентное истощение аутоантител из данной сыворотки проводили на планшете А в отношении рекомбинантных белков Dsg3full-His, EC1-His, EC2-His, и EC4-His, использованных в дозе 1 мкг/лунку, а также БСА в такой же концентрации. Взаимодействие тестируемой сыворотки и рекомбинантных белков в планшете А проводилось в условиях, описанных в Примере 1. После завершения инкубации образцы сыворотки в полном объеме были перенесены в лунки планшета Б, сорбированного рекомбинантным белком Dsg3full-His. Последовательность внесения реагентов и условия проведения реакции на планшете Б соответствуют описанию в примере 1.
На основании полученных значений активности, пользуясь формулой 1, были рассчитаны коэффициенты конкуренции исследуемой сыворотки с каждым представленным на планшете А рекомбинантным белком. Полученные значения представлены на Фиг. 2.
Определенный подобным образом профиль антигенной специфичности характеризовался преимущественным аутоимунным ответом на дистальные экстрацеллюлярные фрагменты ЕС1 и ЕС2, что соответствует представлениям о них как о наиболее «патогенных» эпитопах, связанных с развитием тяжело протекающих случаев вульгарной пузырчатки.
Полученный результат свидетельствует о прогрессирующем течении заболевания, что определяет необходимость его терапии с использованием методов иммуносорбции, направленных на селективную элиминацию антител к ЕС1 и ЕС2 фрагментам.
Пример 3.
Нуклеотидные последовательности экстрацеллюлярного домена десмоглеина-3 человека (Dsg3full) и его фрагментов (ЕС1, ЕС2, ЕС3, ЕС4, ЕС2-ЕС5) были амплифицированы методом ПЦР с плазмиды pUC57, содержащей синтезированную нуклеотидную последовательность лидерного пептида (Р32926 из базы данных UniProt) - прелидерного пептида (Р32926 из базы данных UniProt) - полноразмерного экстрацеллюлярного домена (Р32926 из базы данных UniProt) - 6His с использованием специфических олигонуклеотидов (таблица 1). На первом этапе были наработаны нуклеотидные последовательности самих фрагментов экстрацеллюлярного домена Dsg3 (ЕС1, ЕС2, ЕС3, ЕС4, ЕС2-ЕС5), на втором - методом SOE-ПЦР они были объединены в одной рамке считывания с ДНК фрагментами лидерного и прелидерного пептидов на 5'-конце и 6His на 3'-конце. Нуклеотидная последовательность, кодирующая экспрессионную кассету Dsg3full-His, была наработана в один этап.

Экспрессионные кассеты были клонированы в вектор pcDNA3.4 (Invitrogen, США) по сайтам рестрикции NheI и XhoI (фиг. 3).
Правильность нуклеотидных последовательностей была подтверждена секвенированием по методу Сенгера. Полученые экспрессионные плазмиды (pcDNA 3.4_EC1-His, pcDNA 3.4_EC2-His, pcDNA 3.4_EC3-His, pcDNA 3.4_EC4-His, EC2-EC5-His и pcDNA 3.4_Dsg3 full-His) были использованы для наработки рекомбинантных белков в клетках СНО.
Трансфекцию проводили с использованием реагента Липофектамин (Invitrogen, США). Клетки СНО в количестве 4×106 клеток/мл были пересеяны в колбу Эрленмейера, содержащую 30 мл культуральной среды CD OptiCHO (Invitrogen, США). Через сутки к клеткам добавляли 18-20 мкг плазмидной ДНК, смешанной с трансфекционным агентом в пропорциях, указанных производителем. Культивирование продолжали до снижения количества живых клеток в культуре до уровня 0.3×106 клеток/мл, что составляло 10-14 суток при температуре 37°С в атмосфере, содержащей 8% CO2, при постоянном перемешивании на орбитальном шейкере со скоростью 130 об/мин.
После завершения культивирования Dsg3 full-His и отдельные его фрагменты ЕС1-His, EC2-His, ЕС3-His, EC4-His, EC2-EC5-His были выделены из культуральной жидкости с помощью металл-аффинной хроматографии на Ni2+-ИДА-сефарозе. Клетки осаждали центрифугированием при скорости вращения 1200 об/мин в течение 10 мин, затем супернатанты, содержащие целевые белки, центрифугировали в течение 15 мин при скорости вращения 4000 об/мин. До выделения супернатанты хранили при температуре 4°С.
Культуральную среду, полученную после удаления клеток, диализовали 0,02 М натрий-фосфатным буфером, рН 7.5, содержащем 0.25 М NaCl. Для подготовки носителя 1 мл ИДА-сефарозы помещали в колонку, промывали 12-15 мл mQ и наносили 200 мкл 0.2 M NiSO4. Далее промывали колонку от слабо связавшихся ионов раствором 0.02 М CH3COONa, содержащем 0.5 М NaCl, 10-12 мл mQ и уравновешивали буфером для нанесения (0.02 М натрий-фосфатным буфером, 0.25 M NaCl, рН 7.5). После чего смешивали с соответствующим диализованным супернатантом и инкубировали в течение 1 ч при 4°С и перемешивании. Полученную смесь пропускали через колонку, промывали 10 мл буфера для нанесения. Элюцию белка проводили 0.3 М имидазолом в натрий-фосфатном буфере (промывка осуществлялась последовательно 0.01 М имидазолом и 0.03 М имидазолом).
Молекулярную массу и чистоту выделенных целевых белков: EC-His, EC2-His, ЕС3-His, EC4-His, EC2-EC5-His и Dsg3 full-His, проверяли методом электрофоретического анализа в 14% или 10% SDS-ПААГ по Лэммли (фиг. 4).
--->
Перечень последовательностей
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing 1.2//EN"
"ST26SequenceListing_V1_2.dtd">
<ST26SequenceListing dtdVersion="V1_2" fileName="Тест система Dsg3"
softwareName="WIPO Sequence" softwareVersion="1.0.0-beta1" productionDate="2021-
12-10">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>2020144116/10(082584)</ApplicationNumberText>
<FilingDate>2021-05-27</FilingDate>
</ApplicationIdentification>
<ApplicantName languageCode="ru">Федеральное государственное бюджетное
учреждение науки Институт биоорганической химии им. академиков М.М. Шемякина и
Ю.А. Овчинникова Российской академии наук (ИБХ РАН), RU</ApplicantName>
<ApplicantNameLatin>Shemyakin-Ovchinnikov Institute of bioorganic
chemistry</ApplicantNameLatin>
<InventionTitle languageCode="ru">РЕКОМБИНАТНЫЕ БЕЛКИ - АНТИГЕНЫ И СПОСОБ
ОПРЕДЕЛЕНИЯ ЭПИТОПНОЙ СПЕЦИФИЧНОСТИ АУТОРЕАКТИВНЫХ АНТИТЕЛ К ОТДЕЛЬНЫМ ФРАГМЕНТАМ
ЭКСТРАЦЕЛЛЮЛЯРНОГО ДОМЕНА ДЕСМОГЛЕИНА 3-ГО ТИПА ЧЕЛОВЕКА У БОЛЬНЫХ ОБЫКНОВЕННОЙ
ПУЗЫРЧАТКОЙ, ТЕСТ-СИСТЕМА НА ИХ ОСНОВЕ</InventionTitle>
<SequenceTotalQuantity>12</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>572</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>SOURCE</INSDFeature_key>
<INSDFeature_location>1..572</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>MOL_TYPE</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>ORGANISM</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>EWVKFAKPCREGEDNSKRNPIAKITSDYQATQKITYRISGVGIDQPPFGIFVVDKNTGDI
NITAIVDREETPSFLITCRALNAQGLDVEKPLILTVKILDINDNPPVFSQQIFMGEIEENSASNSLVMILNATDADEPNHL
NSKIAFKIVSQEPAGTPMFLLSRNTGEVRTLTNSLDREQASSYRLVVSGADKDGEGLSTQCECNIKVKDVNDNFPM
FRDSQYSARIEENILSSELLRFQVTDLDEEYTDNWLAVYFFTSGNEGNWFEIQTDPRTNEGILKVVKALDYEQLQS
VKLSIAVKNKAEFHQSVISRYRVQSTPVTIQVINVREGIAFRPASKTFTVQKGISSKKLVDYILGTYQAIDEDTNKA
ASNVKYVMGRNDGGYLMIDSKTAEIKFVKNMNRDSTFIVNKTITAEVLAIDEYTGKTSTGTVYVRVPDFNDNCPT
AVLEKDAVCSSSPSVVVSARTLNNRYTGPYTFALEDQPVKLPAVWSITTLNATSALLRAQEQIPPGVYHISLVLTD
SQNNRCEMPRSLTLEVCQCDNRGICGTSYPTTSPGTRYGRPHSGRHHHHHH</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="2">
<INSDSeq>
<INSDSeq_length>1716</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..1716</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gaatgggtgaaatttgccaaaccctgcagagaaggagaagataactcaaaaagaaacccaat
tgccaagattacttcagattaccaagcaacccagaaaatcacctaccgaatctctggagtgggaatcgatcagccgccttttg
gaatctttgttgttgacaaaaacactggagatattaacataacagctatagtcgaccgggaggaaactccaagcttcctgatc
acatgtcgggctctaaatgcccaaggactagatgtagagaaaccacttatactaacggttaaaattttggatattaatgata
atcctccagtattttcacaacaaattttcatgggtgaaattgaagaaaatagtgcctcaaactcactggtgatgatactaaa
tgccacagatgcagatgaaccaaaccacttgaattctaaaattgccttcaaaattgtctctcaggaaccagcaggcacaccc
atgttcctcctaagcagaaacactggggaagtccgtactttgaccaattctcttgaccgagagcaagccagcagctatcgtc
tggttgtgagtggtgcagacaaagatggagaaggactatcaactcaatgtgaatgtaatattaaagtgaaagatgtcaacga
taacttcccaatgtttagagactctcagtattcagcacgtattgaagaaaatattttaagttctgaattacttcgatttcaa
gtaacagatttggatgaagagtacaccgataattggcttgcagtatatttctttacctctgggaatgaaggaaattggtttg
aaatacaaactgatcctagaactaatgaaggcatcctgaaagtggtgaaggctctagattatgaacaactacaaagcgtgaa
acttagtattgctgtcaaaaacaaagctgaatttcaccaatcagttatctctcgataccgagttcagtcaaccccagtcacg
attcaggtaataaatgtaagagaaggaattgcattccgtcctgcttccaagacatttactgtgcaaaaaggcataagtagca
aaaaattggtggattatatcctgggaacatatcaagccatcgatgaggacactaacaaagctgcctcaaatgtcaaatatgt
catgggacgtaacgatggtggatacctaatgattgattcaaaaactgctgaaatcaaatttgtcaaaaatatgaaccgagat
tctactttcatagttaacaaaacaatcacagctgaggttctggccatagatgaatacacgggtaaaacttctacaggcacgg
tatatgttagagtacccgatttcaatgacaattgtccaacagctgtcctcgaaaaagatgcagtttgcagttcttcaccttc
cgtggttgtctccgctagaacactgaataatagatacactggcccctatacatttgcactggaagatcaacctgtaaagttg
cctgccgtatggagtatcacaaccctcaatgctacctcggccctcctcagagcccaggaacagatacctcctggagtatacc
acatctccctggtacttacagacagtcagaacaatcggtgtgagatgccacgcagcttgacactggaagtctgtcagtgtga
caacaggggcatctgtggaacttcttacccaaccacaagccctgggaccaggtatggcaggccgcactcagggaggcatcac
catcaccatcac</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="3">
<INSDSeq>
<INSDSeq_length>115</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>SOURCE</INSDFeature_key>
<INSDFeature_location>1..115</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>MOL_TYPE</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>ORGANISM</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>EWVKFAKPCREGEDNSKRNPIAKITSDYQATQKITYRISGVGIDQPPFGIFVVDKNTGDI
NITAIVDREETPSFLITCRALNAQGLDVEKPLILTVKILDINDNPPVFSHHHHHH</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="4">
<INSDSeq>
<INSDSeq_length>345</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..345</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gaatgggtgaaatttgccaaaccctgcagagaaggagaagataactcaaaaagaaacccaa
ttgccaagattacttcagattaccaagcaacccagaaaatcacctaccgaatctctggagtgggaatcgatcagccgccttttg
gaatctttgttgttgacaaaaacactggagatattaacataacagctatagtcgaccgggaggaaactccaagcttcctgatc
acatgtcgggctctaaatgcccaaggactagatgtagagaaaccacttatactaacggttaaaattttggatattaatgata
atcctccagtattttcacatcaccatcaccatcac</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="5">
<INSDSeq>
<INSDSeq_length>116</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>SOURCE</INSDFeature_key>
<INSDFeature_location>1..116</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>MOL_TYPE</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>ORGANISM</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QQIFMGEIEENSASNSLVMILNATDADEPNHLNSKIAFKIVSQEPAGTPMFLLSRNTGEV
RTLTNSLDREQASSYRLVVSGADKDGEGLSTQCECNIKVKDVNDNFPMFRHHHHHH</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="6">
<INSDSeq>
<INSDSeq_length>348</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..348</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>caacaaattttcatgggtgaaattgaagaaaatagtgcctcaaactcactggtgatgatac
taaatgccacagatgcagatgaaccaaaccacttgaattctaaaattgccttcaaaattgtctctcaggaaccagcaggcaca
cccatgttcctcctaagcagaaacactggggaagtccgtactttgaccaattctcttgaccgagagcaagccagcagctatcg
tctggttgtgagtggtgcagacaaagatggagaaggactatcaactcaatgtgaatgtaatattaaagtgaaagatgtcaacg
ataacttcccaatgtttagacatcaccatcaccatcac</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="7">
<INSDSeq>
<INSDSeq_length>121</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>SOURCE</INSDFeature_key>
<INSDFeature_location>1..121</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>MOL_TYPE</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>ORGANISM</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>DSQYSARIEENILSSELLRFQVTDLDEEYTDNWLAVYFFTSGNEGNWFEIQTDPRTNEGI
LKVVKALDYEQLQSVKLSIAVKNKAEFHQSVISRYRVQSTPVTIQVINVREGIAFHHHHHH</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="8">
<INSDSeq>
<INSDSeq_length>363</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..363</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gactctcagtattcagcacgtattgaagaaaatattttaagttctgaattacttcgattt
caagtaacagatttggatgaagagtacaccgataattggcttgcagtatatttctttacctctgggaatgaaggaaattgg
tttgaaatacaaactgatcctagaactaatgaaggcatcctgaaagtggtgaaggctctagattatgaacaactacaaagc
gtgaaacttagtattgctgtcaaaaacaaagctgaatttcaccaatcagttatctctcgataccgagttcagtcaacccca
gtcacgattcaggtaataaatgtaagagaaggaattgcattccatcaccatcaccatcac</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="9">
<INSDSeq>
<INSDSeq_length>122</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>SOURCE</INSDFeature_key>
<INSDFeature_location>1..122</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>MOL_TYPE</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>ORGANISM</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>RPASKTFTVQKGISSKKLVDYILGTYQAIDEDTNKAASNVKYVMGRNDGGYLMIDSKTAE
IKFVKNMNRDSTFIVNKTITAEVLAIDEYTGKTSTGTVYVRVPDFNDNCPTAVLEKHHHHHH</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="10">
<INSDSeq>
<INSDSeq_length>366</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..366</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>cgtcctgcttccaagacatttactgtgcaaaaaggcataagtagcaaaaaattggtggatt
atatcctgggaacatatcaagccatcgatgaggacactaacaaagctgcctcaaatgtcaaatatgtcatgggacgtaacgat
ggtggatacctaatgattgattcaaaaactgctgaaatcaaatttgtcaaaaatatgaaccgagattctactttcatagttaa
caaaacaatcacagctgaggttctggccatagatgaatacacgggtaaaacttctacaggcacggtatatgttagagtacccg
atttcaatgacaattgtccaacagctgtcctcgaaaaacatcaccatcaccatcac</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="11">
<INSDSeq>
<INSDSeq_length>463</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>SOURCE</INSDFeature_key>
<INSDFeature_location>1..463</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>MOL_TYPE</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>ORGANISM</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QQIFMGEIEENSASNSLVMILNATDADEPNHLNSKIAFKIVSQEPAGTPMFLLSRNTGEVRT
LTNSLDREQASSYRLVVSGADKDGEGLSTQCECNIKVKDVNDNFPMFRDSQYSARIEENILSSELLRFQVTDLDEEYTDNWLA
VYFFTSGNEGNWFEIQTDPRTNEGILKVVKALDYEQLQSVKLSIAVKNKAEFHQSVISRYRVQSTPVTIQVINVREGIAFRPA
SKTFTVQKGISSKKLVDYILGTYQAIDEDTNKAASNVKYVMGRNDGGYLMIDSKTAEIKFVKNMNRDSTFIVNKTITAEVLA
IDEYTGKTSTGTVYVRVPDFNDNCPTAVLEKDAVCSSSPSVVVSARTLNNRYTGPYTFALEDQPVKLPAVWSITTLNATSAL
LRAQEQIPPGVYHISLVLTDSQNNRCEMPRSLTLEVCQCDNRGICGTSYPTTSPGTRYGRPHSGRHHHHHH</INSDSeq_
sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="12">
<INSDSeq>
<INSDSeq_length>1389</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..1389</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>caacaaattttcatgggtgaaattgaagaaaatagtgcctcaaactcactggtgatgatac
taaatgccacagatgcagatgaaccaaaccacttgaattctaaaattgccttcaaaattgtctctcaggaaccagcaggcaca
cccatgttcctcctaagcagaaacactggggaagtccgtactttgaccaattctcttgaccgagagcaagccagcagctatcg
tctggttgtgagtggtgcagacaaagatggagaaggactatcaactcaatgtgaatgtaatattaaagtgaaagatgtcaacg
ataacttcccaatgtttagagactctcagtattcagcacgtattgaagaaaatattttaagttctgaattacttcgatttca
agtaacagatttggatgaagagtacaccgataattggcttgcagtatatttctttacctctgggaatgaaggaaattggttt
gaaatacaaactgatcctagaactaatgaaggcatcctgaaagtggtgaaggctctagattatgaacaactacaaagcgtga
aacttagtattgctgtcaaaaacaaagctgaatttcaccaatcagttatctctcgataccgagttcagtcaaccccagtcac
gattcaggtaataaatgtaagagaaggaattgcattccgtcctgcttccaagacatttactgtgcaaaaaggcataagtagc
aaaaaattggtggattatatcctgggaacatatcaagccatcgatgaggacactaacaaagctgcctcaaatgtcaaatatg
tcatgggacgtaacgatggtggatacctaatgattgattcaaaaactgctgaaatcaaatttgtcaaaaatatgaaccgaga
ttctactttcatagttaacaaaacaatcacagctgaggttctggccatagatgaatacacgggtaaaacttctacaggcacg
gtatatgttagagtacccgatttcaatgacaattgtccaacagctgtcctcgaaaaagatgcagtttgcagttcttcacctt
ccgtggttgtctccgctagaacactgaataatagatacactggcccctatacatttgcactggaagatcaacctgtaaagtt
gcctgccgtatggagtatcacaaccctcaatgctacctcggccctcctcagagcccaggaacagatacctcctggagtatac
cacatctccctggtacttacagacagtcagaacaatcggtgtgagatgccacgcagcttgacactggaagtctgtcagtgtg
acaacaggggcatctgtggaacttcttacccaaccacaagccctgggaccaggtatggcaggccgcactcagggaggcatca
ccatcaccatcac</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ ПУЗЫРЧАТКИ, СОДЕРЖАЩИЕ АНТИТЕЛА ПРОТИВ ЛИГАНДА Fas | 2009 |
|
RU2556818C2 |
| ПРИМЕНЕНИЕ СЕЛЕКТИВНОГО ИММУНОСОРБЕНТА ДЛЯ УДАЛЕНИЯ АНТИТЕЛ К ДЕСМОГЛЕИНУ 3 ТИПА ИЗ СЫВОРОТКИ КРОВИ У БОЛЬНЫХ ПУЗЫРЧАТКОЙ | 2016 |
|
RU2627652C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЕЛЕКТИВНОГО ИММУНОСОРБЕНТА ДЛЯ УДАЛЕНИЯ АНТИТЕЛ-IgG К ДЕСМОГЛЕИНУ 3 ТИПА ИЗ СЫВОРОТКИ КРОВИ БОЛЬНЫХ ПУЗЫРЧАТКОЙ | 2015 |
|
RU2622005C2 |
| ЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ ПЕМФИГУСА, СОДЕРЖАЩИЕ АНТИТЕЛА К Fas-ЛИГАНДУ | 2008 |
|
RU2558260C2 |
| Антитела к CD38 и фармацевтические композиции на их основе для лечения аутоиммунного заболевания, опосредованного аутоантителами | 2020 |
|
RU2809565C2 |
| СРЕДСТВА И СПОСОБЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА | 2012 |
|
RU2601298C2 |
| ПРИМЕНЕНИЕ АНТИТЕЛА К CD151 ДЛЯ ЛЕЧЕНИЯ РАКА | 2007 |
|
RU2464041C2 |
| ПОЛИПЕПТИД ДЛЯ ЛЕЧЕНИЯ ПАТОЛОГИЧЕСКИХ ТРОМБОВ | 2019 |
|
RU2778566C1 |
| СЛИТЫЙ БЕЛОК TACI-FC И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2814988C2 |
| АНТИТЕЛО К ANGPTL3 И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2830101C1 |

Изобретение относится к области биотехнологии, конкретно к рекомбинантным антигенам десмоглеина человека, и может быть использовано в клинической лабораторной диагностике пузырчатки обыкновенной. Изобретение обеспечивает возможность определения антигенной специфичности аутореактивных антител к отдельным фрагментам экстрацеллюлярного домена десмоглеина 3-го типа человека у больных обыкновенной пузырчаткой за счет применения рекомбинатного белка-антигена, содержащего белки-антигены экстрацеллюлярного домена десмоглеина 3-го типа человека и его фрагментов, имеющих последовательности SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, соответственно. 3 н.п. ф-лы, 4 ил., 1 табл., 3 пр.
1. Применение рекомбинатного белка-антигена, содержащего белки-антигены экстрацеллюлярного домена десмоглеина 3-го типа человека и его фрагментов, имеющих последовательности SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11 соответственно, для определения антигенной специфичности аутореактивных антител к отдельным фрагментам экстрацеллюлярного домена десмоглеина 3-го типа человека у больных обыкновенной пузырчаткой.
2. Способ определения антигенной специфичности аутореактивных антител к отдельным фрагментам экстрацеллюлярного домена десмоглеина 3-го типа человека у больных обыкновенной пузырчаткой, включающий исследование взаимодействия сыворотки крови с данным белком с использованием твердофазного иммуноферментного анализа, отличающийся тем, что в качестве антигенов для ИФА применяют белки-антигены экстрацеллюлярного домена десмоглеина 3-го типа человека и его фрагменты, при этом исследование осуществляют в два этапа, на первом из которых осуществляют конкурентное истощение аутоантител к белкам-антигенам экстрацеллюлярного домена десмоглеина 3-го типа человека и его фрагментам, имеющим последовательности SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11 соответственно, и контрольному материалу - БСА, сорбированным на твердой фазе, а на втором осуществляют определение непрореагировавших аутоантител по отношению к Dsg3full-His с последовательностью SEQ ID NO 1 с последующим расчетом коэффициента конкуренции по отношению к отдельным рекомбинантным белкам по формуле:

где AR - активность сыворотки после преинкубации в контакте с иммобилизованными рекомбинантными белками - ЕС1-His, EC2-His, ЕС3-His, EC4-His, EC2-EC5-His, имеющими последовательности SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11;
APos - активность сыворотки после преинкубации с полноразмерным Dsg3full-His, имеющим последовательность SEQ ID NO: 1;
ANeg - активность сыворотки после преинкубации в контрольной лунке с иммобилизированным БСА.
3. Тест-система для определения эпитопной специфичности аутореактивных антител к фрагментам экстрацеллюлярного домена десмоглеина 3-го типа человека у больных обыкновенной пузырчаткой способом по п. 2, содержащая иммуносорбент, включающий белки-антигены экстрацеллюлярного домена десмоглеина 3-го типа человека и его фрагменты, имеющие последовательности SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11 соответственно; набор реагентов, содержащий положительную (+k) сыворотку, представляющую собой индивидуальную сыворотку от пациента с обыкновенной пузырчаткой с предварительно охарактеризованной активностью в отношении Dsg3 и профилем антигенной специфичности в отношении фрагментов экстрацеллюлярного домена Dsg3 человека, и отрицательную (-k) сыворотку, сформированную из пула сывороток здоровых доноров; и концентрат конъюгата антител к IgG человека с пероксидазой хрена для определения содержания IgG-антител к Dsg3.
| WO 2016016654 A1, 04.02.2016 | |||
| US 10301370 B2, 28.05.2019 | |||
| US 7550562 A, 23.06.2009 | |||
| СПОСОБ ИСПОЛЬЗОВАНИЯ РЕКОМБИНАНТНЫХ БЕЛКОВ SARS-COV-2 В СОСТАВЕ ТЕСТ-СИСТЕМЫ ДЛЯ ИММУНОФЕРМЕНТНОГО АНАЛИЗА С ОПРЕДЕЛЕНИЕМ УРОВНЕЙ АНТИТЕЛ КЛАССОВ IgM, IgG, IgA В СЫВОРОТКЕ/ПЛАЗМЕ КРОВИ БОЛЬНЫХ COVID-19 | 2020 |
|
RU2730897C1 |
| ПРИМЕНЕНИЕ СЕЛЕКТИВНОГО ИММУНОСОРБЕНТА ДЛЯ УДАЛЕНИЯ АНТИТЕЛ К ДЕСМОГЛЕИНУ 3 ТИПА ИЗ СЫВОРОТКИ КРОВИ У БОЛЬНЫХ ПУЗЫРЧАТКОЙ | 2016 |
|
RU2627652C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЕЛЕКТИВНОГО ИММУНОСОРБЕНТА ДЛЯ УДАЛЕНИЯ АНТИТЕЛ-IgG К ДЕСМОГЛЕИНУ 3 ТИПА ИЗ СЫВОРОТКИ КРОВИ БОЛЬНЫХ ПУЗЫРЧАТКОЙ | 2015 |
|
RU2622005C2 |
| FRANKEL A.E | |||
| et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| ARNAU J | |||
| et al | |||
| Current | |||
Авторы
Даты
2022-04-18—Публикация
2021-05-27—Подача