Область техники, к которой относится изобретение. Изобретение относится к медицине, в частности к иммунохимии, а именно к материалам для биологического связывания с помощью сорбирующих колонок. Полученный иммуносорбент может быть использован при проведении экстракорпорального воздействия при кожных заболеваниях, для лечения аутоиммунных буллезных дерматозов, а именно пузырчатки.
Уровень техники.
Иммуноглобулины (Ig) - гетеродимерные белки, которые подразделяют на классы в зависимости от структуры, свойств и антигенных особенностей их тяжелых цепей. Легкие цепи в молекулах иммуноглобулинов представлены двумя изотипами - лямбда (λ) и каппа (κ), которые различаются по химическому составу как вариабельных, так и константных участков. Тяжелые цепи иммуноглобулинов подразделены на 5 изотипов (γ, μ, α, δ, ε), которые определяют их принадлежность к одному из пяти классов иммуноглобулинов: G, M, A, D, Ε соответственно.
Иммуноглобулины класса G (IgG) составляют около 80% сывороточных иммуноглобулинов и подразделяются на четыре подкласса IgG1, IgG2, IgG3 и IgG4, каждый со своими биологическими свойствами. IgG образуются на высоте первичного иммунного ответа и при повторном введении антигена (вторичный ответ). Наиболее часто встречается IgG1 (67%), реже IgG2 и IgG3 (22 и 7% соответственно), самым редким является подкласс IgG4 (4%). При аутоимунных буллезных дерматозах вырабатываются аутоантитела, обладающие высокой тканевой специфичностью и относящиеся к IgG. [Schroeder H.W. Jr., Cavacini L. Structure and function of immunoglobulins // J Allergy Clin Immunol. - 2010. - Vol. 125(2 Suppl 2). - P. S41-52].
Пузырчатка (пемфигус) - тяжелое аутоиммунное буллезное заболевание, характеризующееся образованием пузырей и эрозий на коже и/или слизистых оболочках, [Дерматовенерология, 2010. (Клинические рекомендации / Российское общество дерматовенерологов) / [под ред. А.А. Кубановой]. - М: ДЭКС-Пресс, 2010. - 428 с.; Grando S.A. Pemphigus autoimmunity: hypotheses and realities// Autoimmunity. - 2012. - Vol.45. - №1. - P. 7-35].
Патогенетическую роль в формировании пузырей при пузырчатке играют циркулирующие аутоантитела, обладающие высокой тканевой специфичностью, относящиеся к классу иммуноглобулинов G (IgG) и вызывающие разрушение десмосом вследствие выделения протеолитических ферментов, что приводит к акантолизу [Матушевская Е.В., Кубанова А.А., Самсонов В.А. и др. Аутоантитела и аутоантигены при пузырчатке и пемфигоиде // Вестник дерматологии и венерологии. - 1995. - №5. - С. 28-33; Joly P., Bernard P., Bedane С. et al. Pemphigus. Guidelines for the diagnosis and treatment. Centres de reference des maladies huileuses auto-immunes. Societe Française de Dermatologie // Ann Dermatol Venereol. - 2011. - Vol. 138. - P. 252-258.]. У больных пузырчаткой выявлены все 4 субкласса IgG, с преобладанием в стадию обострения IgG4, а в стадию ремиссии - IgG1 [Bhol К., Mohimen Α., Ahmed A.R. Correlation of subclasses of IgG with disease activity in pemphigus vulgaris // Dermatology. - 1994. - Vol.189 Suppl 1. - P. 85-89].
Основными структурами, к которым вырабатываются аутоантитела при вульгарной пузырчатке, являются белки десмосомального аппарата - десмоглеины 3 типа (Dsg 3) [Stanley J.R., Yaar M., Hawley-Nelson P. et al. Pemphigus antibodies identify a cell surface glycoprotein synthesized by human and mouse keratinocytes // J. Clin. Invest. - 1982. - Vol. 70. - P. 281-288; Stanley J. R., Koulu L., and Thivolet C. Distinction between epidermal antigensbinding pemphigus vulgaris and pemphigus foliaceus autoantibodies // J. Clin. Invest. - 1984. - Vol. 74.- P. 313-320; Ohyama M., Ota T., Aoki M. et al. Suppression of the immune response against exogenous desmoglein 3 in desmoglein 3 knockout mice: an implication for gene therapy // J Invest Dermatol. - 2003 Apr. - Vol. 120(4). - P. 610-615]. Установлена связь между уровнем IgG к Dsg3 и тяжестью поражения при пузырчатке [Cozzani Ε, Di Zenzo G., Riva S. et al. Are clinical phenotype and autoantibody profile always concordant in pemphigus? A study in a cohort of pemphigus patients // Eur J Dermatol. - 2013 Jan-Feb. - Vol.23(l). - Р. 40-48].
Десмосомы состоят из белков клеточной адгезии, относящихся к семейству кадгеринов и соединительных (адапторных) белков, которые соединяют их с промежуточными филаментами. Белки клеточной адгезии, формирующие десмосомы - десмоглеины и десмоколлины. Эти кальцийзависимые гликозилированные протеины состоят из экстрацеллюлярного амино-терминального участка, трансмембранного домена и внутриклеточного карбокситерминального участка. Известны три формы десмоколлина (1-3 типы) и четыре десмоглеина (1-4 типы) [Махнева Н.В., Белецкая Л.В. Молекулярно-биологическая характеристика десмосом как системы межклеточного соединения // Вестник дерматологии и венерологии. - 2009. - №2. - С. 25-381.; Garrod D.R., Merritt A.J., Nie Ζ. Desmosomal cadherins // Curr. Opin. Cell Biol. - 2002. - Vol. 14. - P. 537-545].
В последние десятилетия для лечения пузырчатки используются эфферентные методы терапии: гемосорбция, плазмаферез, энтеросорбция, иммуносорбция.
Для иммуносорбции используется 3 вида сорбентов: неселективные, с низкой селективностью и с высокой степенью селективности. Неселективные сорбенты (декстрансульфат, триптофан, фенилаланинсодержащие и другие) способны сорбировать такие компоненты плазмы крови, как фибриноген, альбумин, липиды, иммуноглобулины. Сорбенты с низкой селективностью (с иммобилизованным стафилококковым протеином А, антителами к Ig человека и другими) имеют сродство к определенной фракции протеинов плазмы. Сорбенты с высокой степенью селективности извлекают только определенные протеины без изменения концентрации других компонентов плазмы пациента.
Одним из наиболее эффективных и безопасных методов лечения аутоиммунных заболеваний является экстракорпоральный метод терапии с использованием специфических иммуносорбентов [Keller F., Wagner К., Faber U. et al. Elimination kinetics of plasma exchange // Klin, Wochen schr. - 1983. - V. 61, N22. - P. 1115-1122].
Известен способ получения углеродного гемосорбента в сорбционных колонках [Грандо С.Α., Глухенький Б.Т., Романенко А.Б. и соавт. Механизмы терапевтического действия экстракорпоральной детоксикации при аутоиммунных буллезных дерматозах // Вестник дерматологии и венерологии. - 1988. - №7. - С. 6-11.; Eming R., Hertl M. Immunoadsorption in pemphigus // Autoimmunity. - 2006. - Vol. 39 (7). - P. 609-616]. Гемоперфузия проводится по вено-венозному контуру через углеродный гемосорбент в сорбционных колонках, предназначенных для очистки и фильтрации крови вне организма (СКН) со скоростью кровотока 80-120 мл/мин в объеме 1,5 объема циркулирующей плазмы. Положительный эффект иммуносорбции связывают с удалением из крови больных пузырчаткой циркулирующих аутоантител и иммунных комплексов. Однако, при использовании данных сорбентов, вследствие элиминации из сыворотки больных аутоантител и циркулирующих иммунных комплексов, без дифференциации к удалению определенных комплексов с IgG, обуславливающей более быстрое наступление клинического эффекта, наблюдался феномен рикошета (экзацербация патологического кожного процесса, сопровождающаяся резким повышением титра иммуноглобулинов в сыворотке крови больных), что является недостатком данного метода [Гребенников В.Α., Белявский А.Д., Каминский М.Ю. Изучение иммунокорригирующего и детоксицирующего воздействия гемосорбции, плазмафереза и энтеросорбции при пузырчатке // Вестник дерматологии. - 1990. - №5. - С. 33-38].
Известен способ получения триптофансодержащих сорбентов [Lüftl М., Stauber A, Mainka A, Klingel R, Schuler G, Hertl M. Successful removal of pathogenic autoantibodies in pemphigus by immunoadsorption with a tryptophan-linked polyvinylalcohol adsorber // Br J Dermatol. - 2003, Sep. - Vol.149(3). - P. 598-605]. Триптофановые столбы состояли из поливиниловых шариков, сшитых алкоголь-гелем, которые иммобилизировали гидрофобной аминокислотой и триптофаном в качестве лиганда. В исследованиях in vitro было продемонстрировано, что триптофановые столбы более эффективно удаляют все классы аутоантител при пузырчатке, чем декстрановые, преимущество которых в избирательном удалении аффинных белков. К тому же триптофановые столбцы более дешевые. Недостаток данного метода: триптофановые столбы сорбируют необходимые для жизнедеятельности компоненты плазмы крови (фибриноген, альбумин, липиды, все классы иммуноглобулинов), к тому же синтез триптофановых столбов является довольно сложным процессом.
Ближайшим аналогом-прототипом в лечении больных пузырчаткой является иммуноадсорбент с использованием стафилококкового протеина А (protein A affinity resin), представляющий собой рекомбинантный белок А Staphylococcus aureus, иммобилизованный на CNBr-активированной сефарозе FF (GEHealthcare). Преимущества данного иммуносорбента: колонки с протеином А более эффективны при элиминациии IgG, чем триптофанновые колонны; метод не требует замены компонентов плазмы [Samuelsson G. Extracorporeal immunoadsorption with protein A: technical aspects and clinical results. J Clin Apher 2001; 16: 49-52].
Однако при проведении иммуносорбции с использованием данного иммуносорбента снижается количество иммуноглобулинов всех подклассов, уменьшается концентрация антител к ДНК, человеческому лейкоцитарному антигену [Samuelsson G. Extracorporeal immunoadsorption with protein A: technical aspects and clinical results. J Clin Apher 2001; 16: 49-52].
Кроме того, после проведения иммуноадсорбции с использованием стафилококкового протеина А у больных пузырчаткой риск развития инфекционных заболеваний остается высоким, так как наряду с патогенетически значимыми аутоантителам IgG при пузырчатке во время процедуры выводятся иммуноглобулины всех подклассов (IgA, IgM, IgE), циркулирующие иммунные комплексы, иммунные комплексы другой специфичности. К тому же стоимость данного сорбента значительно выше других [Schmidt Ε., Klinker Ε., Opitz Α. et al. Protein A immunoadsorption: a novel and effective adjuvant treatment of severe pemphigus // Br J Dermatol. - 2003. - Vol. 148. - P. 1222-1229].
Заявляемый способ отличается от прототипа тем, что вместо иммунносорбентов, неспецифически связывающих белки и низкомолекулярные продукты, в качестве сорбента использована крупнозернистая агарозная матрица с ковалентно иммобилизованным рекомбинантным десмоглеином 3 типа человека, специфически связывающая антитела к десмоглеину 3 типа, в результате чего выводятся только пемфигусные, патогенетически значимые, аутоатитела к десмоглеинам 3 типа, a IgA, IgM, IgE и иммунные комплексы другой специфичности, отвечающие за иммунный ответ на вирусные и бактериальные агенты, сохраняются, уменьшая частоту развития инфекционных осложнений. В связи с этим данный вид терапии является высокоэффективным. Сорбенты с высокой степенью селективности для удаления антител - IgG, строго специфичных именно к Dsg3, из доступных источников научной и научно-технической информации не известны.
Задачей изобретения является создание способа получения иммуносорбента для селективного удаления антител - IgG к десмоглеину 3 типа из сыворотки крови больных пузырчаткой.
Целью изобретения является селективная (избирательная) степень очистки крови от антител - IgG к десмоглеину 3 типа из сыворотки крови больных пузырчаткой.
Сущность изобретения.
Технический результат, на достижение которого направлено изобретение, заключается в удалении антител - IgG к десмоглеину 3 типа из сыворотки крови больных пузырчаткой селективным иммуносорбентом. Селективный иммуносорбент может использоваться для лечения больных пузырчаткой в качестве адъювантного метода терапии.
Указанный технический результат обеспечивается способом получения иммуносорбента для селективного связывания антител - IgG к десмоглеину 3 типа, который представляет собой агарозу с N-гидроксисукцинимидными группами (NHS-активированную сефарозу) (Pierce, США), на которой иммобилизирован рекомбинантный десмоглеин 3 типа (R&D Systems, США). Высокоэффективность данного сорбента заключается в том, что используется определенный вид твердой фазы.
Осуществление изобретения.
Для получения селективного иммуносорбента для удаления антител - IgG к десмоглеину 3 типа из сыворотки крови больных пузырчаткой рекомбинантый десмоглеин 3 типа (Dsg3) (R&D Systems, США) иммобилизируется путем ковалентного связывания с твердофазным носителем, в качестве которого применяется агарозный сорбент, несущий на своей поверхности N-гидроксисукцинимидные группы: NHS-активированная агароза (Biorad, США). Выделение антител - IgG к Dsg3 из сыворотки крови человека проводится методом иммунохроматографической очистки (при прохождении растворов через сорбент путем центрифугирования с использованием центрифужных микроколонок, заполненных NHS-активированной агарозой (Pierce, США)).
Для приготовления раствора Dsg3 33 мкг рекомбинантного Dsg3 разводят в 400 мкл в охлажденном до 4°С буфере связывания/промывки - (0,1М фосфатный буфер, содержащий 0,15М NaCl, рН 7.2). Микропробирку с раствором рекомбинантного десмоглеина 3 типа осторожно встряхивают, не допуская вспенивания. В пустую центрифужную микроколонку (Pierce, США) добавляют 33 мг сухой NHS-активированной агарозы. Вносят раствор Dsg3 в микроколонку с сорбентом, закрывают верхнюю крышку и инкубируют при 4°С в течение ночи, перемешивая на лабораторном шейкере. По окончании инкубации снимают верхнюю и нижнюю крышки микроколонки, помещают микроколонку в пробирку-приемник и центрифугируют при 4°С при 1000 g в течение 1 мин в центрифуге с охлаждением Hettich Micro 24R (Hettich, Германия); фильтрат отбирают. Для отмывки от несвязавшихся белков в колонку добавляют 200 мл буфера для промывки (0,1М фосфатный буфер содержащий 0,15М NaCl, рН 7.2) и центрифугируют при 4°С при 1000 g в течение 1 мин. Повторяют процедуру отмывки, фильтраты после отмывок отбирают. В фильтратах после иммобилизации и отмывки определяют концентрацию Dsg3 по методу Бредфорд для установления эффективности иммобилизации Dsg3.
Для блокирования остаточных активных групп сорбента добавляют 100 мл раствора для блокирования (1М этаноламин) и заменяют пробирку-приемник микроколонки на нижнюю крышку, закрывают микроколонку крышкой. Инкубируют на шейкере при комнатной температуре в течение 20 мин. По окончании инкубации снимают верхнюю и нижнюю крышки микроколонки и центрифугируют при 4°С при 1000 g в течение 1 мин, фильтрат удаляют. Для отмывки от буфера для блокирования в колонку добавляют 200 мл раствора для промывки и центрифугируют при 4°С при 1000 g в течение 1 мин. Готовый сорбент используют для иммунохроматографического выделения аутоантител к Dsg3 или, если эксперимент по выделению аутоантител будет проводится позже, добавляют консервирующий раствор (0,1 M фосфатный буфер содержащий 0,05% азида натрия)) и помещают сорбент на хранение при 4°С.
Практическая применимость заявляемого селективного иммуносорбента для удаления антител - IgG к десмоглеину 3 типа из сыворотки крови больных пузырчаткой подтверждается, но не исчерпывается следующими примерами.
Пример 1. Сорбция антител - IgG к десмоглеину 3 типа из сыворотки крови больных пузырчаткой in vitro с использованием селективного иммуносорбента для удаления антител (IgG) к десмоглеину 3 типа из сыворотки крови больных пузырчаткой
Для проведения исследований по определению условий эффективного функционирования селективного иммуносорбента для удаления антител -IgG к десмоглеину 3 типа из сыворотки крови больных пузырчаткой получены сыворотки крови 15 больных пузырчаткой и 10 здоровых лиц, которые были объединены в пулы сывороток больных пузырчаткой и пул сывороток здоровых лиц соответственно. Взятие образца крови у пациента производили натощак, в утренние часы или не ранее 5-6 часов после приема пищи. Кровь для исследования брали в количестве 4,5 мл при соблюдении правил асептики. Сыворотку крови получали путем центрифугирования крови в течение 10 минут при охлаждении до 4°С в центрифуге при скорости вращения ротора 3000 оборотов в минуту.
В последующем из пулов сывороток крови больных пузырчаткой и здоровых лиц выделены циркулирующие в сыворотках крови (несвязанные) антитела - IgG и получены препараты IgG - суммарные препараты антител - IgG. Часть иммунных комплексов (связанных антител IgG) фиксируются в коже и/или слизистых оболочках, что приводит к развитию клинической картины пузырчатки.
Выделение препаратов IgG производилось стандартным способом из пула сывороток крови больных пузырчаткой, содержавшаго антитела к Dsg3 (наличие антител к Dsg3 определялось методом ИФА с помощью наборов Anti-Desmoglein 3 ELISA, Euroimmun AG, ФРГ) и здоровых добровольцев методом аффиной хроматографии на колонке с белок G - сефарозой (сефароза с иммобилизованным белком G) (Биалекса, Россия).
Колонку с G-сефарозой (сефароза с иммобилизованным белком G) уравновешивали буфером для промывки (5-10 объемов колонки). Далее вносили сыворотку крови больного пузырчаткой из расчета 2 мл сыворотки на 1 мл G-сефарозы, промывали колонку буфером для промывки, периодически измеряя оптическую плотность фракций в спектрофотометре с длиной волны 280 нм, до тех пор, пока уровень оптической плотности фракций не сравняется с оптической плотностью чистого буфера для промывки. При промывке фракции собирали в отдельную емкость, формируя т.н. «проскок».
Затем колонку промывали буфером для элюции. Элюат собирали в пробирки с трис-буфером в соотношении 1 часть трис-буфера на 4 части элюата (процедура проводилась для нейтрализации рН элюата). Длительность элюции контролировали путем измерения оптической плотности вытекающего из колонки элюата на спектрофотометре с длиной волны 280 нм. Элюцию заканчивали, когда оптическая плотность элюата снижалась до уровня оптической плотности буфера для элюции.
После хроматографии производилась проверка качества выделения антител (элюата и "проскока") методом электрофореза по Лэммли (Остерман Л.Α., 1981). При обнаружении IgG в проскоке проскок заново наносился на колонку и очистка повторялась,
Фракции элюата, содержащие атитела - IgG, для концентрирования IgG объединяли и центрифугировали в центрифужных фильтрах Amicon (Millipore, США) с пределом фильтрации 100 kDa. В процессе центрифугирования в фильтры добавляли изотонический буфер, в результате чего получали концентрированный раствор IgG в буфере.
Готовый концентрированный раствор количественно переносили в пробирки типа "эппендорф" и измеряли оптическую плотность раствора методом спектрофотометрии при длине волны 280 нм. Коэффициент экстинкции IgG был принят равным 1,4. Готовые препараты антител хранили при +4°С.
75 мг препарата IgG, полученного из пула сывороток крови 15 больных пузырчаткой, было пропущено через селективный иммуносорбент для удаления антител IgG к десмоглеину 3 типа из сыворотки крови больных пузырчаткой. После очистки от антидесмоглеиновых антител IgG на селективном иммуносорбенте препарат IgG концентрировался путем центрифугирования в течение 10 минут при 4°С в фильтрах Amicone (Millipore, Франция).
В результате иммуносорбции антител к десмоглеину 3 типа из 75 мг препарата, содержащего IgG больных пузырчаткой, было получено 65 мг очищенного от антител к десмоглеину 3 типа препарата IgG (в дальнейшем - очищенные IgG). В них еще могут быть остатки специфических антител, но большая часть специфических - удалена. 10 мг антидесмоглеиновых IgG, выделенные из пула сывороток крови больных пузырчаткой, пропущенные через колонку с селективным иммуносорбентом, связались с используемым иммуносорбентом. Из пула сывороток крови 10 здоровых лиц выделено 10 мг препарата суммарных IgG.
Из 65 мг препарата IgG, очищенного от антител к десмоглеину 3 типа, 5 мг антител в последующем были использованы для оценки эффективности иммуносорбента по степени сорбции антител к десмоглеину 3 типа из сыворотки крови больных пузырчаткой in vitro методом ИФА. Активность раствора IgG после прохождения иммуносорбента методом ИФА сравнивалась с активностью раствора суммарных IgG до прохождения иммуносорбента.
Для оценки эффективности иммуносорбента по степени сорбции антител к десмоглеину 3 типа из сыворотки крови больных пузырчаткой in vitro определяли содержание антител к Dsg3 в образцах пулов сыворотки крови больных пузырчаткой (до и после селективной иммуносорбции) и здоровых лиц методом ИФА с набором реагентов «Anti-Desmoglein 3 ELISA (IgG)» (Euroimmun AG, Германия). Активность препарата IgG после прохождения иммуносорбента сравнивалась с активностью препарата IgG до прохождения селективного иммуносорбента и активностью препарата IgG, полученного от здоровых лиц, методом ИФА. С помощью фотометра методом ИФА оценивали оптическую плотность препаратов, содержащих циркулирующие IgG к десмоглеину 3 типа.
Обследованы следующие образцы препаратов.
1. Препарат суммарных IgG, выделенный из пула сывороток крови больных пузырчаткой - Атвыд.
2. Препарат суммарных IgG, выделенный из пула сывороток крови больных пузырчаткой, пропущенный через хроматографическую колонку с используемым иммуносорбентом, твердофазным агарозным сорбентом, несущим на своей поверхности N-гидроксисукцинимидные группы: NHS-активированная агароза, частично очищенный от антител-IgG к десмоглеину 3 типа и не связавшийся с иммуносорбентом - Аточищ.
3. Препарат суммарных IgG, выделенный из пула сывороток крови здоровых лиц.
Препарат суммарных IgG, выделенный из пула сывороток крови больных пузырчаткой (Атвыд), препарат суммарных IgG, выделенный из пула сывороток крови больных пузырчаткой, пропущенный через хроматографическую колонку с используемым иммуносорбентом и очищенный от антител (не связавшихся с иммуносорбентом) (Аточищ), и препарат суммарных IgG, выделенный из пула сывороток здоровых лиц, были взяты в одинаковой концентрации - 1 мг/мл, что позволило провести сравнительный анализ оптической плотности растворов, содержащих антидесмоглеиновые антитела IgG (табл. 1).
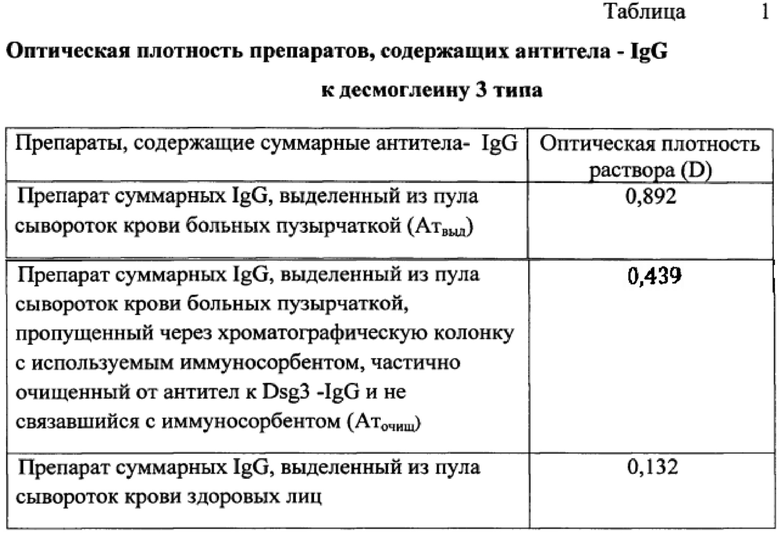
Как следует из таблицы, оптическая плотность препарата, содержащего антитела - IgG к десмоглеину 3 типа, полученного от больных пузырчаткой (0,892), в 6,8 раза больше, чем в препаратах, полученных от здоровых лиц (0,132) (минимальная оптическая плотность, при которой результат считается положительным и приводит к развитию пузырчатки, согласно инструкции к набору - 0,174). После прохождения через селективный иммуносорбент оптическая плотность препарата, содержащего антитела - IgG к десмоглеину 3 типа, полученного от больных пузырчаткой, уменьшилась до 0,439 (разница по сравнению с оптической плотностью препаратов IgG, полученных от здоровых лиц, уменьшилась до 3,3 раза).
Изменение активности антител - IgG рассчитывали по формуле
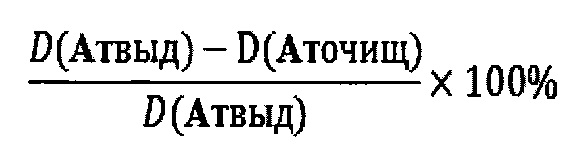
где D(Aтвыд) - оптическая плотность препарата антител - IgG, выделенного из пула сывороток крови больных пузырчаткой,
D(Aточищ) - оптическая плотность препарата антител - IgG, пропущенного через используемый твердофазный агарозный сорбент, несущий на своей поверхности N-гидроксисукцинимидные группы: NHS-активированная агароза, и очищенного от антител к десмоглеину 3 типа и не связавшихся с иммуносорбентом.
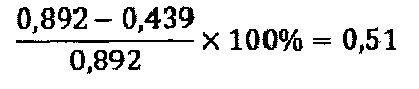
Как следует из расчетов по формуле, изменение активности антител - IgG в препаратах, выделенных из пула сывороток крови больных пузырчаткой до и после прохождения испытуемого иммуносорбента, равно 0,51, что свидетельствует о значительном снижении активности антител в препаратах антител - IgG после прохождения через испытуемый иммуносорбент.
Образец, полученный путем элюирования связавшихся антител к десмоглеину 3 типа с иммуносорбентом, был положительным, что свидетельствует о связывании антител к десмоглеину 3 типа с твердофазным агарозным сорбентом, несущим на своей поверхности N-гидроксисукцинимидные группы: NHS-активированная агароза, который ковалентно связан с рекомбинантым человеческим десмоглеином 3 типа, при прохождении через него препарата суммарных IgG.
Таким образом, из результатов, представленных выше, следует, что предложенный селективный иммуносорбент для удаления антител (IgG) к десмоглеину 3 типа из сыворотки крови больных пузырчаткой обладает хорошей способностью связывать антитела к десмоглеину 3 типа из препарата IgG, полученного от больных пузырчаткой, позволит снизить тяжесть заболевания и добиться ремиссии у больных пузырчаткой.
Пример 2. Эффективность селективного иммуносорбента для удаления антител (IgG) к десмоглеину 3 типа из сыворотки крови больных пузырчаткой in vivo на экспериментальной модели.
Проводились экспериментальные исследования по определению эффективности селективного иммуносорбента для удаления антител (IgG) к десмоглеину 3 типа из сыворотки крови больных пузырчаткой in vivo с использованием 15 лабораторных животных (новорожденных мышей линии BALB/c).
Мыши были разделены на 3 группы: 1 группе (5 мышей) - вводили по 30 мг препарата IgG, выделенного из сыворотки крови больных пузырчаткой (не очищенного на иммуносорбенте) (основная группа); 2 группе (5 мышей) - вводили по 30 мг препарата IgG, выделенного из сыворотки крови здоровых лиц (контрольная группа); 3 группе (5 мышей) - вводили по 30 мг препарата IgG, полученного из сыворотки крови больных пузырчаткой и очищенных на селективном иммуносорбенте от антител к десмоглеину 3 типа. Время экспонирования - 48 часов. По истечении времени производили забор биопсийного материала для получения биопсийного материала для гистологического исследования и метода реакции непрямой иммунофлюоресценции.
Мышам вводили 150 мкл раствора IgG в стерильном фосфатно-солевом буфере (рН 7,2) инсулиновым шприцом на 1 мл с иглой 27G и меньше (один шприц на животное).
После введений IgG от больных пузырчаткой у мышей наблюдались эрозии в абдоминальной области, по 3-бальной шкале оцениваемые как 1+ (т.е. три или менее поражений кожи) (Фиг. 1. Экспериментальная модель (препараты IgG от больного пузырчаткой). Эрозии на коже мыши), положительный симптом Никольского.
При патоморфологическом исследовании аутопсийного материала выявлены признаки акантолиза (Фиг. 2А. Гистологическая картина (субкорнеальная полость, содержащая акантолитические клетки) х50. Окр. гем. эоз.); при исследовании фиксированных IgG методом нРИФ определялась фиксация IgG в межклеточных промежутках эпидермиса (Фиг. 2Б. Реакция иммунофлюоресценции (конфокальная лазерная сканирующая микроскопия, КЛСМ х20). Фиксация IgG в межклеточных промежутках эпидермиса).
При введении препарата IgG от здоровых добровольцев не зафиксировано патологических изменений при клиническом осмотре, патоморфологическом исследовании и проведении нРИФ препаратов кожи мышей.
При введении препарата IgG, полученного от больных пузырчаткой и очищенных на предложенном иммуносорбенте от антител к десмоглеину 3 типа, не выявлены клинические, патоморфологические и иммунологические признаки пузырчатки у мышей.
Данный пример свидетельствует об эффективности удаления антител из сыворотки крови больных пузырчаткой твердофазным агарозным сорбентом, несущим на своей поверхности N-гидроксисукцинимидные группы: NHS-активированную агарозу.
Проведенные эксперименты выявили, что селективный иммуносорбент для удаления антител (IgG) к десмоглеину 3 типа из сыворотки крови больных пузырчаткой позволяет избирательно повысить степень сорбции IgG. Применение такого вида иммунсорбента у больных пузырчаткой может улучшить качество проводимой терапии, позволяет уменьшить дозы и длительность системных глюкокортикостероидных препаратов, снизить частоту развития побочных эффектов вследствие иммуносупрессивной терапии.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ СЕЛЕКТИВНОГО ИММУНОСОРБЕНТА ДЛЯ УДАЛЕНИЯ АНТИТЕЛ К ДЕСМОГЛЕИНУ 3 ТИПА ИЗ СЫВОРОТКИ КРОВИ У БОЛЬНЫХ ПУЗЫРЧАТКОЙ | 2016 |
|
RU2627652C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ПУЗЫРЧАТКИ У МЫШЕЙ МЕТОДОМ ВВЕДЕНИЯ ИММУНОГЛОБУЛИНОВ КЛАССА G | 2015 |
|
RU2613718C1 |
| РЕКОМБИНАНТНЫЕ БЕЛКИ-АНТИГЕНЫ И СПОСОБ ОПРЕДЕЛЕНИЯ ЭПИТОПНОЙ СПЕЦИФИЧНОСТИ АУТОРЕАКТИВНЫХ АНТИТЕЛ К ОТДЕЛЬНЫМ ФРАГМЕНТАМ ЭКСТРАЦЕЛЛЮЛЯРНОГО ДОМЕНА ДЕСМОГЛЕИНА 3-ГО ТИПА ЧЕЛОВЕКА У БОЛЬНЫХ ОБЫКНОВЕННОЙ ПУЗЫРЧАТКОЙ, ТЕСТ-СИСТЕМА НА ИХ ОСНОВЕ | 2021 |
|
RU2770444C1 |
| СОРБЕНТ ДЛЯ УДАЛЕНИЯ ИММУНОГЛОБУЛИНОВ | 2006 |
|
RU2325172C2 |
| СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ ПУЗЫРЧАТКИ, СОДЕРЖАЩИЕ АНТИТЕЛА ПРОТИВ ЛИГАНДА Fas | 2009 |
|
RU2556818C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОЗМОЖНОСТИ ИЗМЕНЕНИЯ КЛИНИЧЕСКОЙ ФОРМЫ ПУЗЫРЧАТКИ | 2008 |
|
RU2386400C1 |
| ИММУНОСОРБЕНТ ДЛЯ УДАЛЕНИЯ ИММУННЫХ КОМПЛЕКСОВ, ОБРАЗОВАННЫХ ИММУНОГЛОБУЛИНАМИ ЛОШАДИ ПОСЛЕ ВВЕДЕНИЯ ПРОТИВОДИФТЕРИЙНОЙ СЫВОРОТКИ, И СПОСОБ ПРОВЕДЕНИЯ ГЕМОСОРБЦИИ ПРИ ЛЕЧЕНИИ ДИФТЕРИИ | 1998 |
|
RU2161504C2 |
| СПОСОБ ОЧИСТКИ КРОВИ ОТ РЕВМАТОИДНОГО ФАКТОРА | 1991 |
|
RU2027192C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АУТОАНТИТЕЛ К ЛИПОПРОТЕИДАМ НИЗКОЙ ПЛОТНОСТИ В СЫВОРОТКЕ КРОВИ | 1997 |
|
RU2137134C1 |
| Способ получения моноспецифических антител к лактоферрицину человека | 2022 |
|
RU2795322C1 |

Изобретение относится к медицине, в частности к иммунохимии, а именно к способу получения материала для биологического связывания с помощью сорбирующих колонок. Сущность изобретения заключается в том, что разработан способ получения селективного иммуносорбента для удаления антител - IgG к десмоглеину 3 типа из сыворотки крови больных пузырчаткой с использованием твердофазного носителя, заключающийся в том, что для его получения рекомбинантый человеческий десмоглеин 3 типа (Dsg3) иммобилизируют путем ковалентного связывания с твердофазным носителем, в качестве которого применяют агарозный сорбент, несущий на своей поверхности N-гидроксисукцинимидные группы: NHS-активированную агарозу. При использовании изобретения получают иммуносорбент, обладающий высокой селективной сорбционной способностью по отношению к аутоантителам - IgG к десмоглеину 3 типа. Полученный предлагаемым способом иммуносорбент может использоваться для лечения больных пузырчаткой в качестве адъювантного метода терапии. Его применение улучшает качество терапии, позволяет уменьшить дозы и длительность системных глюкокортикостероидных препаратов, снизить частоту развития побочных эффектов вследствие иммуносупрессивной терапии. 2 ил., 1 табл., 2 пр.
Способ получения селективного иммуносорбента для удаления антител - IgG к десмоглеину 3 типа из сыворотки крови больных пузырчаткой с использованием твердофазного носителя, заключающийся в том, что для его получения рекомбинантый человеческий десмоглеин 3 типа (Dsg3) иммобилизируют путем ковалентного связывания с твердофазным носителем, в качестве которого применяют агарозный сорбент, несущий на своей поверхности N-гидроксисукцинимидные группы: NHS-активированную агарозу.
| КУБАНОВ А.А., АБРАМОВА Т.В | |||
| Современные методы терапии истинной акантолитической пузырчатки | |||
| Обзор литературы, Вестник дерматологии и венерологии | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| Найдено в Интернет, онлайн, 25.01.2017 г., найдено на http://www.vestnikdv.ru/archive/2014_4_02.pdf | |||
| ТВЕРДОФАЗНЫЙ ИММУНОФЕРМЕНТНЫЙ АНАЛИЗ (ELISA) ДЛЯ ФАКТОРА РОСТА ЭНДОТЕЛИЯ СОСУДОВ (VEGF) | 2007 |
|
RU2517301C2 |
| КУБАНОВ А.А | |||
| и др | |||
| К вопросам диагностики истинной (акантолитической) пузырчатки | |||
| В помощь практическому врачу | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Ребристый каток | 1922 |
|
SU121A1 |
| Найдено в Интернет, онлайн, 25.01.2017 г., найдено на http://www.vestnikdv.ru/archive/2014_6_14.pdf | |||
| САМОЙЛИКОВ П.В | |||
| Принципы иммуноферментного анализа, основные виды ИФА, применение в диагностике | |||
| Российский государственный медицинский университет | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| Найдено в Интернет, онлайн, 25.01.2017 г., найдено на http://www.km.ru/referats/A1FF1869BD9A43079A0AC03543FBC627 | |||
| LANGENHAN J | |||
| et al | |||
| Specific immunoadsorption of pathogenic autoantibodies in pemphigus requires the entire ectodomains of desmogleins | |||
| Exp Dermatol | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| Прибор для измерения угла наклона | 1921 |
|
SU253A1 |
Авторы
Даты
2017-06-08—Публикация
2015-11-24—Подача