Настоящее изобретение относится к молекулярной биологии и медицине, а конкретно, к ДНК-аптамерам к праймазе и ДНК-полимеразе PrimPol человека и способу применения ДНК-аптамеров для ингибирования активности PrimPol. ДНК-аптамеры настоящего изобретения могут иметь биологическое и терапевтическое применение. ДНК-аптамеры могут быть использованы в качестве ингибитора PrimPol человека, средства связывания и детекции PrimPol в научных исследованиях, а также ингибирования активности в клетках человека с целью повышения эффективности препаратов химиотерапии.
Действие большинства химиотерапевтических препаратов основано на блокировании репликации быстро делящихся опухолевых клеток с помощью повреждения ДНК. Механизмы удаления повреждений ДНК в ходе репарации и механизмы, обеспечивающие толерантность клеток к повреждениям ДНК, снижают терапевтический эффект химиотерапии. К механизмам толерантности к повреждениям ДНК относят транслезионный синтез (или «синтез через поврежденные участки») и механизм реинициации репликации после поврежденного участка с помощью праймазы и ДНК-полимеразы PrimPol.
В последние годы началась разработка ингибиторов транслезионных ДНК-полимераз человека. К настоящему моменту получены ингибиторы на основе низкомолекулярных соединений для Rev1 [Sail V. et al, ACS Chem Biol 2017, 12:1903-1912] и ДНК-полимеразы эта [Zafar MK. et al. Biochemistry 2018, 57, 1262-1273], и на основе рибозимов и РНК-аптамеров к Rev1 [Dumstorf C.A. et al, Mol. Cancer Res. 2009, 7, 247-254], ДНК-полимеразе бета [Gening L.. et al, Nucleic Acids Res 2006, 34:2579-86] и ДНК-полимеразе йота [Lakhin A.V. et al, Nucleic Acid Ther. 2012, 22: 49-57].
Праймаза и ДНК-полимераза PrimPol (“Prim” - primase, “Pol” - polymerase) относится к суперсемейству архео-эукариотических праймаз и была впервые описана в 2013 году. PrimPol участвует как в репликации геномной, так и митохондриальной ДНК. In vitro PrimPol человека осуществлять репликацию на ДНК-матрицах с некоторыми повреждениями [ . et al, Mol. Cell 2013, 52:541; Makarova A.V. et. al., DNA Repair 2018, 70:18-24]. В отличие от большинства других известных праймаз, которые синтезируют только РНК-праймеры, уникальной особенностью PrimPol является способность использовать дезоксирибонуклеотидтрифосфаты в реакции синтеза ДНК de novo [
. et al, Mol. Cell 2013, 52:541; Makarova A.V. et. al., DNA Repair 2018, 70:18-24]. В отличие от большинства других известных праймаз, которые синтезируют только РНК-праймеры, уникальной особенностью PrimPol является способность использовать дезоксирибонуклеотидтрифосфаты в реакции синтеза ДНК de novo [ . et al, Mol. Cell 2013, 52:541].
. et al, Mol. Cell 2013, 52:541].
PrimPol может запускать остановившуюся репликативную вилку, осуществляя синтез ДНК напротив поврежденного участка, или инициировать синтез ДНК после повреждения de novo. Исследования с использованием вариантов PrimPol, лишенных праймазной активности, показали, что основным механизмом репликации с участием PrimPol является репрайминг после поврежденных участков. PrimPol осуществляет репрайминг при репликации ДНК, содержащей АП-сайты, фотопродукты, G-квадруплексы и цисплатиновые сшивки [Schiavone D et al, Mol. Cell 2016, 61:161;  . et al, Struct Mol Biol 2013, 20: 1383-1389; Pilzecker B. et al, Nucleic Acids Res. 2016, 44: 4734-4744; Kobayashi K. et al, Cell Cycle 2016, 15: 1997-2008]. При репликации геномной и митохондриальной ДНК PrimPol необходима также для преодоления блоков репликации, вызванных включением нуклеотидных аналогов, терминирующих синтез ДНК, или резким падением концентрации нуклеотидов в клетке [
. et al, Struct Mol Biol 2013, 20: 1383-1389; Pilzecker B. et al, Nucleic Acids Res. 2016, 44: 4734-4744; Kobayashi K. et al, Cell Cycle 2016, 15: 1997-2008]. При репликации геномной и митохондриальной ДНК PrimPol необходима также для преодоления блоков репликации, вызванных включением нуклеотидных аналогов, терминирующих синтез ДНК, или резким падением концентрации нуклеотидов в клетке [ . et al, Struct Mol Biol 2013, 20: 1383-1389; Kobayashi K. et al, Cell Cycle 2016, 15: 1997-2008; Wan L. et al, EMBO Rep 2013, 14: 1104-1112]. Таким образом, PrimPol выполняет функцию универсального белка, возобновляющего репликацию, остановки которой вызваны широким спектром ДНК-повреждающих агентов (или другими причинами). Ожидается, что ингибирование активности PrimPol позволит сенсибилизировать опухолевые клетки к ДНК-повреждающим агентам и повысит эффективность препаратов химиотерапии.
. et al, Struct Mol Biol 2013, 20: 1383-1389; Kobayashi K. et al, Cell Cycle 2016, 15: 1997-2008; Wan L. et al, EMBO Rep 2013, 14: 1104-1112]. Таким образом, PrimPol выполняет функцию универсального белка, возобновляющего репликацию, остановки которой вызваны широким спектром ДНК-повреждающих агентов (или другими причинами). Ожидается, что ингибирование активности PrimPol позволит сенсибилизировать опухолевые клетки к ДНК-повреждающим агентам и повысит эффективность препаратов химиотерапии.
PrimPol является новой мишенью для создания лекарственных средств борьбы с химиотерапевтической резистентностью на основе ингибиторов ДНК-синтетической активности. Одним из новых подходов к разработке ингибиторов ДНК-полимераз является создание аптамеров. В предлагаемом изобретении задача ингибирования PrimPol решается путем применения ДНК-аптамеров. Проведенный патентный поиск не выявил источников информации о применении аптамеров в качестве ингибиторов PrimPol человека, а также информации о получении других ингибиторов PrimPol.
Специфичные взаимодействия между белками и нуклеиновыми кислотами лежат в основе многих клеточных биохимических процессов. Большое комбинаторное разнообразие нуклеиновых кислот и их способность формировать самые разные вторичные и третичные структуры делают возможным направленный поиск последовательностей нуклеиновых кислот, которые обладают способностью взаимодействовать с определенными белками. Такие небольшие олигонуклеотидные молекулы нуклеиновых кислот, образующие прочные комплексы с определенными молекулами-мишенями, были названы аптамерами. Аптамеры к белкам часто связываются в функционально важных участках молекулы и являются ингибиторами активности белков-мишеней. Аптамеры могут содержать одноцепочечные, двухцепочечные или трехцепочечные области.
Аптамеры получают методом систематической эволюции лигандов экспоненциальным обогащением (SELEX - «Systematic Evolution of Ligands by Exponential Enrichment») с помощью селекции из больших библиотек случайных последовательностей (комбинаторные ДНК и РНК-библиотеки), используя их способность специфически связываться с соответствующими иммобилизованными белками-лагандами. В результате нескольких раундов отбора аптамеров к иммобилизованной на аффинной смоле белка-мишени происходит постепенное обогащение библиотеки случайных последовательностей нуклеиновых кислот последовательностями, которые обладают высоким сродством. После идентификации аптамер можно получить или синтезировать по любому известному методу, включая химические методы синтеза и ферментативные методы синтеза.
По своей специфичности и высокой аффинности аптамеры, как правило, не уступают антителам, а по ряду показателей обладают преимуществом перед антителами. Аптамеры обладают низкой иммуногенностью и токсичностью, лучшей способностью проникать через биологические мембраны. Аптамеры, специфически распознающие определенные типы рецепторов, могут проникать через гематоэнцефалический барьер [Monaco I. et al, J. Med. Chem. 2017, 60: 4510-4516] и могут служить в качестве средств доставки терапевтических прапаратов. Важным преимуществом является доступность химического или ферментативного синтеза аптамеров в больших количествах и простота химической модификации нуклеиновых кислот.
На основе аптамеров разрабатывается новые препараты для лечения разных заболеваний. Некоторые лекарства на основе РНК- и ДНК-аптамеров находятся на стадии клинических испытаний или поступили на фармацевтический рынок. Аптамеры-ингибиторы были получены к некоторым РНК- и ДНК-полимеразам: РНК-полимеразе вируса гриппа [Yuan S. et. al., Antimicrob. Agents Chemother. 2015, 59:4082-4093], РНК-полимеразе энтеровируса везикулярного стоматита [Forrest S. et. al., J. Gen. Virol. 2014, 95:2649-2657], обратной транскриптазе вируса иммунодефицита человека [Shiang Nanoscale 2013, 5:2756-2764], ДНК-полимеразам бета [Gening L.. et al, Nucleic Acids Res 2006, 34:2579-86] и йота [Lakhin A.V. et al, Nucleic Acid Ther. 2012, 22: 49-57] человека. Основным механизмом ингибирования биохимической активности РНК-полимераз и ДНК-полимераз аптамерами, предположительно, является их связывание с активным центром фермента и конкуренция аптамеров за связывание с дезоксирибонуклеотидтрифосфатами. Константы диссоциации комплексов аптамеров с белками, как правило, лежат в области нано- и пикомолярных значений.
При разработке настоящего изобретения в качестве белка-мишени использовали полноразмерную рекомбинантную PrimPol человека с аффинным GST-тагом, иммобилизованную на смоле с глутатион-сефарозой. Индивидуальные аптамеры были отобраны из комбинаторной одноцепочечной ДНК-библиотеки длиной 75 нуклеотидов, содержащей центральный рандомизированный участок, окруженный участками связывания праймеров (GGGAGCTCAGAATAAACGCTCAA и TTCGACATGAGGCCCGGATC), которые необходимы для амплификации библиотеки при проведении отбора. Одноцепочечную библиотеку ДНК инкубировали с PrimPol и не связавшиеся с белком-мишенью олигонуклеотиды смывали с аффинной смолы (перед связыванием с иммобилизованным ферментом смесь аптамеров предварительно инкубировали с пустым сорбентом, чтобы исключить отбор молекул, взаимодействующих с ним). Связанные с белком-мишенью молекулы ДНК элюировали и амплифицировали в ходе ПЦР. Амплифицированная двухцепочечная ДНК была затем использована для получения обогащенной библиотеки однонитевых олигонуклеотидов. Процедура отбора была проведена 12 раз.
Настоящее изобретение обеспечивают аптамеры, обладающие способностью специфически связываться с PrimPol и ингибировать ДНК-синтетическую активность фермента. "Специфичность связывания" аптамера к его мишени означает, что аптамер связывается со своей мишенью с намного более высокой степенью аффинности, чем когда он связывается с другими, нецелевыми, компонентами в смеси или образце. Ингибирующая активность против PrimPol человека означает ингибирование любой ДНК-синтетической активности, поскольку для включения нуклеотидов при синтезе динуклеотида de novo (праймазная активность) и продолжении синтеза от 3'-ОН группы (ДНК-полимеразная активность) ферментом используется один и тот же активный центр.
ДНК-аптамеры настоящего изобретения содержат центральный район с уникальной нуклеотидной последовательностью и 5'- и 3'-концевые последовательности. Центральная уникальная часть содержит мотив G-квадруплекса, представляющий собой последовательность ДНК с четырмя повторами гуанинов и способную образовывать структуру из четырех цепей, удерживаемую G-G-парными взаимодействиями. Такие структуры отличаются высокой стабильностью в растворе. Между повторами гуанинов находится одноцепочечная область, образующая петлю и, вероятно, участвующая в прямом связывании с PrimPol.
Длина и состав аптамеров настоящего изобретения не ограничены. Уникальная центральная часть может быть использована как часть большей молекулы ДНК. ДНК-аптамеры могут содержать дополнительные вариативные районы, фланкирующие центральный район, где n представляет собой любое количество нуклеотидов приблизительно от 1 до 10, выбранных из a, c, t, g и не оказывающих неблагоприятного воздействия на свойства аптамера. 5'- и 3'-концевые последовательности могут быть модифицированы. Модификации могут быть направлены на защиту 5'- и 3'-концов от действия экзонуклеаз и включать ненуклеозидные линкеры, инвертированный dT, метиленовую групп между 4' и 2' положениями дезоксирибозы (закрытая ДНК), включать флуоресцентные вещества, радиоактивные изотопы, биотин и пептиды. Изобретение охватывает все модификации и эквиваленты, которые могут быть включены в настоящее изобретение согласно его формуле.
Настоящее изобретение и вариант его реализации иллюстрируются приведенными ниже примерами. Доказательством достижимости технического результата в примере служит ингибирование полимеризации ДНК PrimPol in vitro с помощью ДНК-аптамеров.
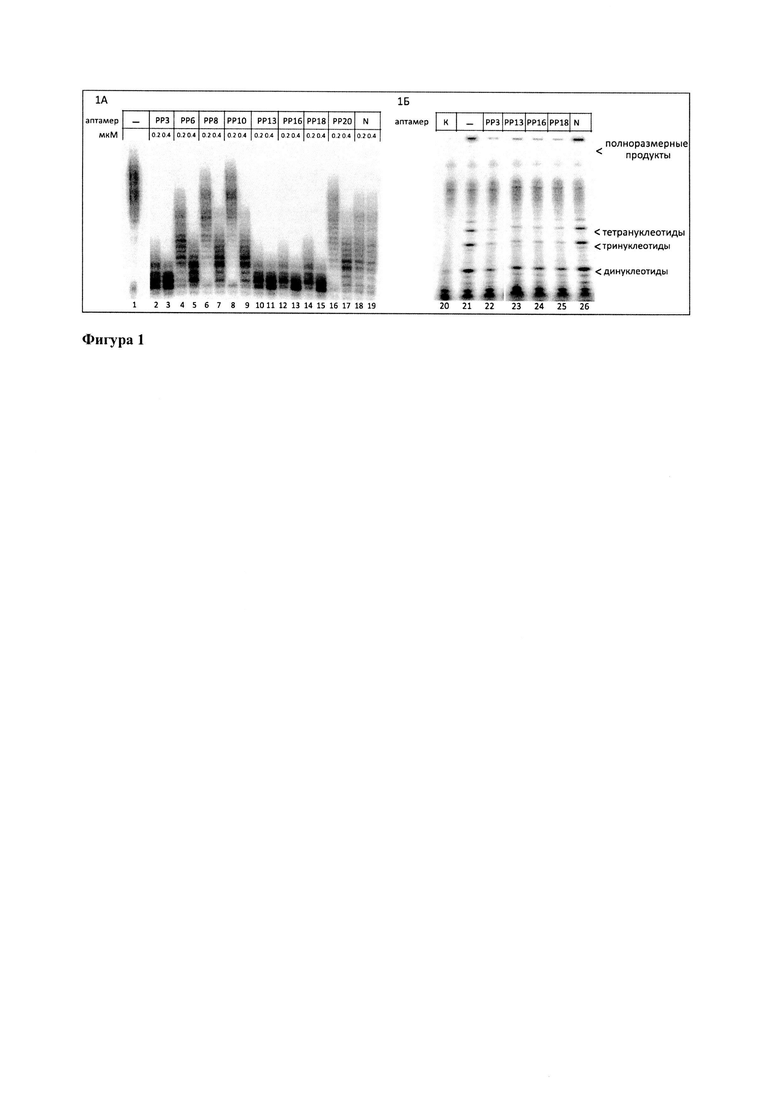
Пример 1 демонстрирует ингибирование ДНК-полимеразной активности PrimPol (фигура 1А). Одноцепочечный ДНК-аптамер или исходную библиотеку в концентрации 3 мкМ отжигали в буфере, содержащем 100 мМ NaCl, 50 мМ KCl, 30 мМ Хепес рН 7,4, 1 мМ ДТТ, нагреванием до 90°С и охлаждением до 24°С в течение 10 мин. Аптамер и контрольную библиотеку в концентрации 400 нМ или 200 нМ инкубировали с PrimPol человека в концентрации 200 нМ и олигонуклеотидным ДНК-субстратом с матричной ДНК длиной 55 нуклеотидов и 5'-32Р-меченым праймером длиной 22 нуклеотида в концентрации 30 нМ в буфере, содержащем 30 мМ Хепес рН 7,4, 8% глицерин, 10 мМ MgCl2,1 мМ ДТТ, 100 мкг/мл БСА, при 22°С в течение 5 мин. Добавляли смесь дезоксирибонуклеотидтрифосфатов в концентрации 200 мкМ и инкубировали при 37°С 30 мин. Синтез ДНК останавливали на льду добавлением равного объема смеси формамида с 40 мМ ЭДТА и красителем бромфеноловым синим. 32Р-меченые продукты синтеза ДНК разделяли в денатурирующем 23 % полиакриламидном геле и детектировали с помощью радиографии. Сокращение длины синтезируемых молекул ДНК при инкубировании PrimPol с ДНК-аптамерами PP3 (описывается формулой 1) и PP13, PP16, PP18 (описываются формулой 2), но не библиотекой свидетельствует об падении ДНК-полимеразной активности PrimPol.
Пример 2 демонстрирует ингибирование праймазной активности PrimPol (фигура 1Б). Одноцепочечный ДНК-аптамер или исходную библиотеку в концентрации 3 мкМ отжигали в буфере, содержащем 100 мМ NaCl, 50 мМ KCl, 30 мМ Хепес рН 7,4, 1 мМ ДТТ, нагреванием до 90°С и охлаждением до 24°С в течение 10 мин. Аптамер и контрольную библиотеку в концентрации 400 нМ инкубировали с PrimPol человека в концентрации 200 нМ и олигонуклеотидным ДНК-субстратом с матричной ДНК длиной 55 нуклеотидов в концентрации 30 нМ в буфере, содержащем 30 мМ Хепес рН 7,4, 8% глицерин, 10 мМ MgCl2,1 мМ ДТТ, 100 мкг/мл БСА, при 22°С в течение 5 мин. Добавляли смесь дезоксирибонуклеотидтрифосфатов в концентрации 200 мкМ, немеченый АТФ в концентрации 10 мкМ и [γ-32]Р-меченый АТФ в концентрации 20 нМ. Реакции инкубировали при 37°С 30 мин. Синтез ДНК останавливали на льду добавлением равного объема смеси формамида с 40 мМ ЭДТА и красителем бромфеноловым синим. 32Р-меченые продукты синтеза ДНК разделяли в денатурирующем 30 % полиакриламидном геле и детектировали с помощью радиографии. Падение количества синтезируемых ди-, три- и тетрануклеотидов и полноразмерных продуктов синтеза ДНК при инкубировании PrimPol с ДНК-аптамерами PP3 (описывается формулой 1) и PP13, PP16, PP18 (описываются формулой 2), но не библиотекой свидетельствует об падении праймазной активности PrimPol. Примеры 1 и 2 позволяют сделать вывод об ингибировании ДНК-синтетической способности PrimPol.
Приведенные примеры не ограничивает других возможных вариантов реализации настоящего изобретения. Аптамеры настоящего изобретения могут обладать ингибиторными активностями и против молекул PrimPol, полученных из других видов млекопитающих. ДНК-аптамеры могут служить средством для связывания и детекции PrimPol человека. ДНК-аптамер может использоваться для создания аффинного хроматографического сорбента и очистки PrimPol с помощью данного сорбента. ДНК-аптамер может служить реактивом для детекции и оценки количества PrimPol в биологических образцах. Cпособность аптамера связываться с белком-мишенью с высокой специфичностью и высокой аффинностью может облегчить детекцию белка-мишени в исследуемом образце, позволяя определить отсутствие, присутствие и концентрацию молекул PrimPol. Таким образцом может быть любой материал, полученный от организма, в том числе культуры клеток, клеточные экстракты культур клеток и тканей, срезы тканей. Мечение ДНК-атамеров флуоресцентыми красителями или радиоактивными изотопами позволит повысить чувствительность способа детекции и/или сократить время анализа.
Стабилизированные ДНК-аптамеры со сходной нуклеотидной последовательностью и структурными мотивами центрального района могут быть использованы для ингибирования активности PrimPol в клетках человека с целью повышения эффективности препаратов химиотерапии. Доставка ДНК-аптамера в клетки может быть осуществлена с помощью известных методик трансфекции и доставки нуклеиновых кислот или с помощью слияния с аптамером, который служит средством доставки (химера из двух аптамеров).
Фигура 1 показывает ингибирование ДНК-полимеразной (1А) и праймазной (1Б) активностей PrimPol человека ДНК-аптамерами in vitro. (1А). К 0,2 мкМ PrimPol добавляли 0,2 или 0,4 мкМ аптамера РР3 (описан формулой 1, дорожки 2,3), или одного из аптамеров PP13, PP16, PP18 (описываются формулой 2, дорожки 10-15), или одного из аптамеров РР6, РР8, РР10 (описываются формулами, отличными от формул 1 и 2 настоящего изобретения, дорожки 4-9). В качестве контролей добавляли исходную библиотеку (N, дорожки 18,19) или не добавляли ни ДНК-аптамеры, ни библиотеку (дорожка 1). (1Б). К 0,2 мкМ PrimPol добавляли 0,4 мкМ аптамера РР3 (описан формулой 1, дорожка 22), или одного из аптамеров PP13, PP16, PP18 (описываются формулой 2, дорожки 23-25). В качестве контролей добавляли исходную библиотеку (N, дорожка 26), не добавляли ни ДНК-аптамеры, ни библиотеку (дорожка 2) или не добавляли PrimPol (дорожка 1).
--->
Нуклеотидные последовательности
<110> Institute of Molecular Genetics of Russian Academy of Sciences
<120> DNA aptamers to human primase and DNA polymerase PrimPol
and method for inhibiting its activity
<160> 2
<210> 1
<211> 77
<212> DNA
<213> Artificial Sequence
<220>
<221> misc_feature
<222> 24
<223> Designed DNA aptamer to human PrimPol
<400> 1
gggagctcag aataaacgct caanctggtt tggtgagaga ggttgggttg agagtanttc 60
gacatgaggc ccggatc 77
<210> 2
<211> 68
<212> DNA
<213> Artificial Sequence
<220>
<221> misc_feature
<222> 24
<223> Designed DNA aptamer to human PrimPol
<400> 1
gggagctcag aataaacgct caanctggtt ggtgcacgga ggatgggntt cgacatgagg 60
cccggatc 68
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ДНК-аптамеры к ДНК-полимеразе эта человека | 2020 |
|
RU2737285C1 |
| ДНК-АПТАМЕР, ОБЛАДАЮЩИЙ ВЫСОКИМ СРОДСТВОМ К БЕЛКУ ИНТЕРЛЕЙКИН-6 | 2023 |
|
RU2814541C2 |
| ДНК-АПТАМЕРЫ, ВЗАИМОДЕЙСТВУЮЩИЕ С ПРОТРОМБИНОМ | 2018 |
|
RU2703799C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕРАПЕВТИЧЕСКОГО АГЕНТА ДЛЯ ЛЕЧЕНИЯ КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 2012 |
|
RU2501862C1 |
| СПОСОБ СОЗДАНИЯ И СЕЛЕКЦИИ БИБЛИОТЕКИ МОДИФИЦИРОВАННЫХ АПТАМЕРОВ | 2016 |
|
RU2652952C1 |
| Способ определения субстратной эффективности производных трифосфатов дезоксиуридина для ДНК-полимераз методом реакции достраивания праймера | 2019 |
|
RU2731739C1 |
| СВЯЗЫВАЮЩИЕ КОМПЛЕМЕНТ АПТАМЕРЫ И СРЕДСТВА ПРОТИВ С5, ПРИГОДНЫЕ ДЛЯ ЛЕЧЕНИЯ ГЛАЗНЫХ НАРУШЕНИЙ | 2007 |
|
RU2477137C2 |
| ДНК-аптамер, связывающий внеклеточный домен EGFR | 2018 |
|
RU2700097C1 |
| АНАЛИЗ АКТИВНОСТИ IN VITRO ДЛЯ ДНК-ПОЛИМЕРАЗЫ ВИРУСА ГЕПАТИТА В (HBV) И ЕГО ИСПОЛЬЗОВАНИЕ ДЛЯ СКРИНИНГА НА ИНГИБИТОРЫ ДНК-ПОЛИМЕРАЗЫ HBV | 1999 |
|
RU2202620C2 |
| АПТАМЕРЫ НА ОСНОВЕ ДНК ДЛЯ КАТЕПСИНА G ЧЕЛОВЕКА | 2004 |
|
RU2360000C2 |
Группа изобретений относится к молекулярной биологии. Предложены варианты ДНК-аптамера, предназначенного для специфического связывания с PrimPol человека и ингибирующего ее ДНК-полимеразную и праймазную активности. Группа изобретений обеспечивает ингибирование ДНК-синтезирующей активности PrimPol, что достигается взаимодействием ДНК-аптамеров с молекулой PrimPol. 2 н.п. ф-лы, 1 ил., 2 пр.
1. ДНК-аптамер, предназначенный для специфического связывания с PrimPol человека и ингибирующий ее ДНК-полимеразную и праймазную активности и имеющий нуклеотидную последовательность:
gggagctcag aataaacgct caanctggtt tggtgagaga ggttgggttg agagtanttc 60
gacatgaggc ccggatc 77,
где n представляет собой любое количество нуклеотидов от 1 до 10, выбранных из а, с, t, g, которые могут быть дополнительно введены в аптамер.
2. ДНК-аптамер, предназначенный для специфического связывания с PrimPol человека и ингибирующий ее ДНК-полимеразную и праймазную активности и имеющий нуклеотидную последовательность:
gggagctcag aataaacgct caanctggtt ggtgcacgga ggatgggntt cgacatgagg 60
cccggatc 68,
где n представляет собой любое количество нуклеотидов от 1 до 10, выбранных из а, с, t, g, которые могут быть дополнительно введены в аптамер.
| LAKHIN A.V | |||
| ET AL | |||
| Isolation and characterization of high affinity aptamers against DNA polymerase iota | |||
| Nucleic Acid Ther | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| GENING L.V | |||
| ET AL | |||
| RNA aptamers selected against DNA polymerase β inhibit the polymerase activities of DNA polymerases β and κ, Nucleic Acids Research, Volume 34, Issue 9, 1 May 2006, Pages 2579-2586 | |||
Авторы
Даты
2022-04-21—Публикация
2020-01-13—Подача