ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Полимеразы представляют собой ферменты фундаментальной важности для живых организмов. Они ответственны за синтез нуклеиновых кислот и их преобразование в другие нуклеиновые кислоты, необходимые для синтеза белков. Таким образом, полимеразы обнаружены во всех типах клеток, в том числе в ДНК-вирусе, вызывающем гепатит В (HBV).
HBV является причиной гепатита, одного из наиболее обычных инфекционных заболеваний человека, а возникающая в результате гепатоцеллюлярная (печеночно-клеточная) карцинома (НСС) является одним из наиболее обычных раков во всем мире. Наиболее эффективным путем в предупреждении инфекции и заболевания HBV до сих пор является иммунизация против HBV. Лицензированные в настоящее время вакцины HBV состоят из основного поверхностного антигена вируса гепатита В (HBsAg) либо в его природной форме (полученной из плазмы), либо в его рекомбинантной форме (очищенной из дрожжевых клеток). Было показано, что индуцированные этой вакциной антитела связываются с наиболее антигенным эпитопом 'а', локализованным в остатках 124-147 HBsAg, приводя к эффективной нейтрализации репликации HBV.
Хотя такая программа активной вакцинации привела к уменьшению инфекции HBV в популяции, возникало увеличивающееся число мутаций, локализованных в эпитопе 'а'. Эти индуцированные вакциной мутанты HBV вызывают беспокойство, так как они способны избежать доступной в настоящее время иммунодиагностической системы и способны независимо реплицироваться.
Тот факт, что мутации на эпитопе 'a' HBsAg приводят к возникновению аминокислотных замен в перекрывающейся ДНК-полимеразе HBV, в частности, посредством их расположения в домене обратной транскриптазы, может предполагать, что эти индуцированные вакциной мутанты имеют измененную активность обратной транскриптазы, ключевого фактора для репликации вируса.
HBV представляют собой ДНК-вирусы, которые реплицируют их геномы обратной транскрипцией промежуточной РНК. Упаковка этого РНК-прогенома в нуклеокапсиды и инициация репликации зависят первично от взаимодействия ДНК-полимеразы HBV с сигналом инкапсидации. Существуют две копии сигналов инкапсидации на прегеномной РНК. Только 5'-копия функционирует в качестве матрицы для реакции праймирования (инициации). После инициации синтеза ДНК минус-цепи олигомер ДНК (4 нуклеотида) переносится по неизвестному механизму к 3'-концу прегеномной РНК, где он гибридизуется с его комплементарными последовательностями. Затем обратная транскрипция продолжается в направлении 5'-конца РНК-матрицы. Взаимодействие между ДНК-полимеразой HBV и прегеномной РНК происходит в виде ковалентной связи между расположенным на N-конце остатком тирозина на ДНК-полимеразе и специфическим нуклеотидом в сигнале инкапсидации. Обратная транскриптаза HBV является одним из четырех доменов в большой ДНК-полимеразе. Другие домены включают в себя: i) N-концевой белок, который является ответственным за ковалентную ассоциацию этой полимеразы с прегеномной РНК; ii) спейсерный район, который является устойчивым в отношении мутаций; и iii) домен РНКазы Н, участвующий в деградации промежуточного мРНК-продукта.
Подобно другим полимеразам детектирование активности ДНК-полимеразы HBV in vitro может быть использовано в следующих трех ситуациях:
- Характеристика нового выделенного вируса в качестве репликативного вируса и оценка различий относительно других известных вирусов. Это, в частности, важно для вариантов HBV с мутациями на их поверхностных антигенах;
- Определение успеха выделения вируса из тест-материала субъекта, о котором известно, что он инфицирован;
- Оценка in vitro эффективности ингибиторов полимераз, которые могут быть антивирусными агентами.
Различные системы были установлены для измерения активности ДНК-полимеразы HBV in vitro в отсутствие вирусной репликации и других вирусных белков. Одним из представляющих интерес открытий был факт, что детектируемая праймирующая (инициаторная) активность ДНК-полимеразы HBV требует не только N-концевого белка, но также функционального домена обратной транскриптазы. Таким образом, одним из общих признаков этих систем является детектирование праймирующей (инициаторной) активности ДНК-полимеразы HBV, являющейся указанием на активность ДНК-полимеразы HBV. Две подобные системы используют ДНК-полимеразу HBV утки (DHBV), и обе продемонстрировали активность обратной транскриптазы, которая является зависимой от матрицы и праймируемой (инициируемой) белком. Одна из этих DHBV-систем использует трансляцию in vitro ДНК-полимеразы DHBV для получения лизатов, которые содержат функциональную ДНК-полимеразу, тогда как другая система упаковывает активный слитый белок ДНК-полимеразы DHBV в вирус-подобную частицу из дрожжевого ретротранспозона Туl. Активная ДНК-полимераза была измерена по ее праймирующей (инициаторной) активности, показанной радиоактивно меченым белком в присутствии праймирующего нуклеотида (т.е. [α-32P]-dGTP для ДНК-полимеразы DHBV). Сходный анализ (тест) активности был сообщен недавно для ДНК-полимеразы HBV человека. 3'-некодирующий район 350 п.н. этой полимеразы, содержащий сигнал инкапсидации, был включен во все сообщенные конструкции, что свидетельствует о его важности для анализа активности in vitro.
Одним из прямых приложений анализа активности in vitro на ДНК-полимеразу HBV человека может быть скрининг новых антивирусных агентов. Антивирусная терапия хронической инфекции HBV все еще остается проблемой, так как несколько клинических испытаний показали, что стойкий ответ на интерферон или аналоги нуклеозидов наблюдается только в 30-40% обследованных пациентов. Этот индекс реагирования является даже еще более низким в долгосрочных носителях HBV и в пациентах с ослабленным иммунитетом. Требуется создание новых протоколов для химиотерапии для ликвидации HBV, так как большинство пациентов не будут устранять вирусную инфекцию и, следовательно, будут иметь большой риск развития прогрессирующего заболевания печени и гепатоцеллюлярного (печеночно-клеточного) рака (НСС). Особый интерес представляет также оценка антивирусных действий таких агентов на мутанты поверхностных антигенов HBV человека.
Однако существуют ограничивающие факторы для антивирусного тестирования с использованием установленных анализов активности (тестов) in vitro на ДНК-полимеразу HBV человека. Одним из них было то, что во всех установленных системах требуется стадия клонирования, которая помещает кодирующий район ДНК-полимеразы HBV под контроль промотора вирусной полимеразы (например, SP6 или Т7) на плазмиде (т.е. pGEM-T). Кроме того, ДНК-полимераза HBV, экспрессируемая в некоторых системах, требует дополнительной очистки (т.е. иммунопреципитации) перед анализом ее активности. Эти утомительные манипуляции не являются практичными в связи с большим числом мутантов HBV.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Согласно первому аспекту данного изобретения обеспечен анализ активности in vitro на ДНК-полимеразу вируса гепатита В (HBV) человека, который предусматривает использование в качестве 5'-олигонуклеотида в ПЦР-амплификации ДНК-полимеразы HBV из пробы, олигонуклеотида, в который был встроен промотор SР6-вирусной полимеразы, прямую транскрипцию и трансляцию ПЦР-продуктов в эукариотических бесклеточных лизатах и измерение праймирования ДНК-полимеразы HBV в присутствии радиоактивно меченого агента.
Согласно второму аспекту данного изобретения обеспечено применение анализа в соответствии с первым аспектом данного изобретения для анализа активности различных проб сыворотки и/или для скрининга на ингибиторы ДНК-полимеразы HBV.
Согласно третьему аспекту данного изобретения обеспечено применение анализа в соответствии с первым аспектом данного изобретения для анализа и/или скрининга потенциальных анти-НВV-лекарственных средств на их способность ингибировать ДНК-праймирующую активность ДНК-полимеразы HBV человека. Такое применение предпочтительно предусматривает стадии:
a) получения по меньшей мере одной пробы в определенном объеме буфера для анализа, причем каждая проба содержит транслируемый in vitro белок ДНК-полимеразы HBV человека в эукариотическом бесклеточном лизате с использованием линейного ПЦР-продукта в качестве матрицы, РНК-матрицу для синтеза минус-цепи HBV, которая включает в себя последовательность, способную образовывать структуру типа "стебель-петля",
b) получения контрольной пробы в эквивалентном объеме тест-буфера, причем эта контрольная проба содержит транслируемый in vitro белок ДНК-полимеразы HBV человека в эукариотическом бесклеточном лизате с использованием линейного ПЦР-продукта в качестве матрицы и РНК-матрицу для синтеза минус-цепи HBV, которая включает в себя последовательность, способную образовывать структуру типа "стебель-петля", существенную для связывания и праймирования ДНК-полимеразы HBV человека,
c) инкубирования этих проб для получения комплекса, содержащего ДНК-полимеразу и радиоактивно меченый агент,
d) выделения этих комплексов из буфера для анализа и
e) измерения количества радиоактивно меченого агента в каждом выделенном комплексе, причем это количество показывает ДНК-праймирующую активность ДНК-полимеразы HBV человека.
Указанные выше стадии с), d) и е) могут быть заменены следующими стадиями:
с) инкубирования каждой указанной тест-пробирки и указанной контрольной пробирки с эквивалентными количествами радиоактивно меченого нуклеотидтрифосфата, содержащего первый нуклеотид, включенный в указанную ДНК минус-цепь HBV, при определенных условиях, благоприятных для ДНК-праймирующей активности указанной ДНК-полимеразы HBV человека, с образованием комплекса, содержащего указанную ДНК-полимеразу и указанный радиоактивно меченый нуклеотидтрифосфат;
d) выделения указанного комплекса из указанного тест-буфера в каждой указанной тест-пробирке и указанной контрольной пробирке фильтрованием через нитроцеллюлозную мембрану;
e) измерения количества указанного радиоактивно меченого нуклеотидтрифосфата в каждом указанном выделенном комплексе, причем указанное количество показывает ДНК-праймирующую активность ДНК-полимеразы HBV человека;
f) сравнения соответствующих количеств указанного радиоактивно меченого нуклеотидтрифосфата в указанных выделенных комплексах, которые остались связанными с нитроцеллюлозной мембраной, каждой указанной тест-пробирки и указанной контрольной пробирки, причем уменьшение количества указанного радиоактивно меченого нуклеотидтрифосфата в указанных выделенных комплексах указанной тест-пробирки в сравнении с указанной контрольной пробиркой свидетельствует об ингибировании указанной ДНК-праймирующей активности указанной ДНК-полимеразы HBV указанными потенциальными лекарственными средствами против HBV.
Данное изобретение относится к упрощенному анализу (тесту) активности на ДНК-полимеразу вируса гепатита В (HBV), причем данный анализ является потенциально более быстрым, чем предыдущие анализы. Способ предусматривает встраивание промотора SР6-вирусной полимеразы в олигонуклеотид, который затем используют в качестве 5'-олигонуклеотида в ПЦР-амплификации ДНК-полимеразы HBV из проб сыворотки. ПЦР-продукты, содержащие весь кодирующий район и 3'-некодирующий район 300 п.н. с сигналом инкапсидации, непосредственно транскрибируются и транслируются в бесклеточном экстракте зародышей пшеницы. Праймирование ДНК-полимеразы HBV в отношении промежуточной РНК-матрицы, ключевой индикатор ее ферментативной активности, измеряют в присутствии радиоактивно меченого [α-32P]-dTTP. Применения данного изобретения охватывают анализ активности из различных проб сыворотки (в том числе проб HBV с мутациями на основном поверхностном антигене) и скрининг на ингибиторы ДНК-полимеразы HBV.
Данное изобретение обеспечивает упрощенный способ анализа in vitro активности ДНК-полимеразы HBV человека непосредственно из линейной ДНК-матрицы, амплифицированной из проб сыворотки. Белок, включенный в анализ активности, обычно продуцируется в бесклеточной системе зародышей пшеницы путем сопряжения транскрипции и трансляции из этой линейной ДНК-матрицы, которая содержит промотор SР6-вирусной полимеразы на ее 5'-конце.
Для достижения этой и других задач данное изобретение обеспечивает способ получения ДНК-полимеразы HBV непосредственно из линейного ДНК-фрагмента, амплифицированного из пробы сыворотки. В присутствии радиоактивно меченого агента, такого как [α-32P]-dTTP, полученный белок анализируют на его праймирующую (инициирующую или затравочную) активность, ключевую стадию в репликации вируса гепатита В.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Данное изобретение обеспечивает простой, чувствительный и быстрый анализ (тест), который является специфическим для активности ДНК-полимеразы HBV. Данное изобретение включает в себя способ детектирования ДНК-полимеразной активности HBV из проб сыворотки, предусматривающий:
- Одностадийную экстракцию вирусной ДНК HBV из сыворотки с использованием смеси фенол/хлороформ;
- ПЦР-амплификацию кодирующего района ДНК-полимеразы HBV (2400 п.н.) и ее 3'-некодирующего района (310 п.н.). 5'-олигонуклеотид включает в себя 5'-проксимальный промотор SР6-вирусной полимеразы;
- In vitro трансляцию ДНК-полимеразы HBV с продуктами ПЦР-амплификации в качестве матрицы;
- Анализ (тест) активности на экстрактах, содержащих транслированную ДНК-полимеразу HBV, в присутствии радиоактивно меченого праймирующего нуклеотида.
Дополнительные объекты данного изобретения включают в себя реагенты для осуществления данного способа, способ определения ингибирующего действия веществ на полимеразную активность и применение к полимеразной активности вариантов HBV с мутациями на поверхностном антигене.
В соответствии с данным изобретением проба сыворотки может содержать вариант HBV с неспецифической ДНК-полимеразной активностью. Данное изобретение делает возможным его количественное определение. Для случаев, в которых требуются количественные измерения ДНК-полимеразной активности, анализ активности в данном изобретении может быть развит далее (т.е. измерение праймированной ДНК-полимеразы на нитроцеллюлозных мембранах). Для случаев, в которых должны быть определены ингибирующие действия молекулы на ДНК-полимеразу, количество праймированной ДНК-полимеразы может сравниваться с количеством ДНК-полимеразы, полученной из контрольной пробы, где не присутствует ингибирующая молекула.
Для лучшего понимания данного изобретения теперь будет сделана ссылка, в качестве примера, на сопутствующие графические материалы, в которых:
Фиг. 1 показывает линеаризованную геномную структуру HBV человека. Кодирующий район ДНК-полимеразы HBV человека (блок) и его 3'-некодирующий район (линия красного цвета) включали в ПЦР-амплификацию в данном изобретении. Цифры ниже обозначают положение в геноме HBV дикого типа человека подтипа adw, как определено в банке генов: стрелки указывают положения и направления олигонуклеотидов, использованных в ПЦР-амплификации, а их последовательности изображены либо выше символа стрелки (5'), либо ниже (3'). Кроме последовательности, соответствующей начальной части ДНК-полимеразы HBV (первые 27 оснований кодирующего района), вирусный промотор SP6  включен в 5'-олигонуклеотид. Локализация 5'-олигонуклеотида имеет место от положения 2309 до положения 2335 (стрелка), тогда как 3'-антисмысловой олигонуклеотид охватывает район 1917-1940 (стрелка).
включен в 5'-олигонуклеотид. Локализация 5'-олигонуклеотида имеет место от положения 2309 до положения 2335 (стрелка), тогда как 3'-антисмысловой олигонуклеотид охватывает район 1917-1940 (стрелка).
Фиг.2 представляет собой фотографию, которая показывает картину электрофореза ПЦР-продукта, амплифицированного с использованием вирусной ДНК, выделенной из сыворотки, несущей HBV дикого типа. Фрагмент с ожидаемым размером 2800 п. н. показан стрелкой. На дорожке "М" показаны также положения миграции маркеров молекулярных размеров (1 т.п.н.-ДНК-лэддер (лестница), MBI Ferments).
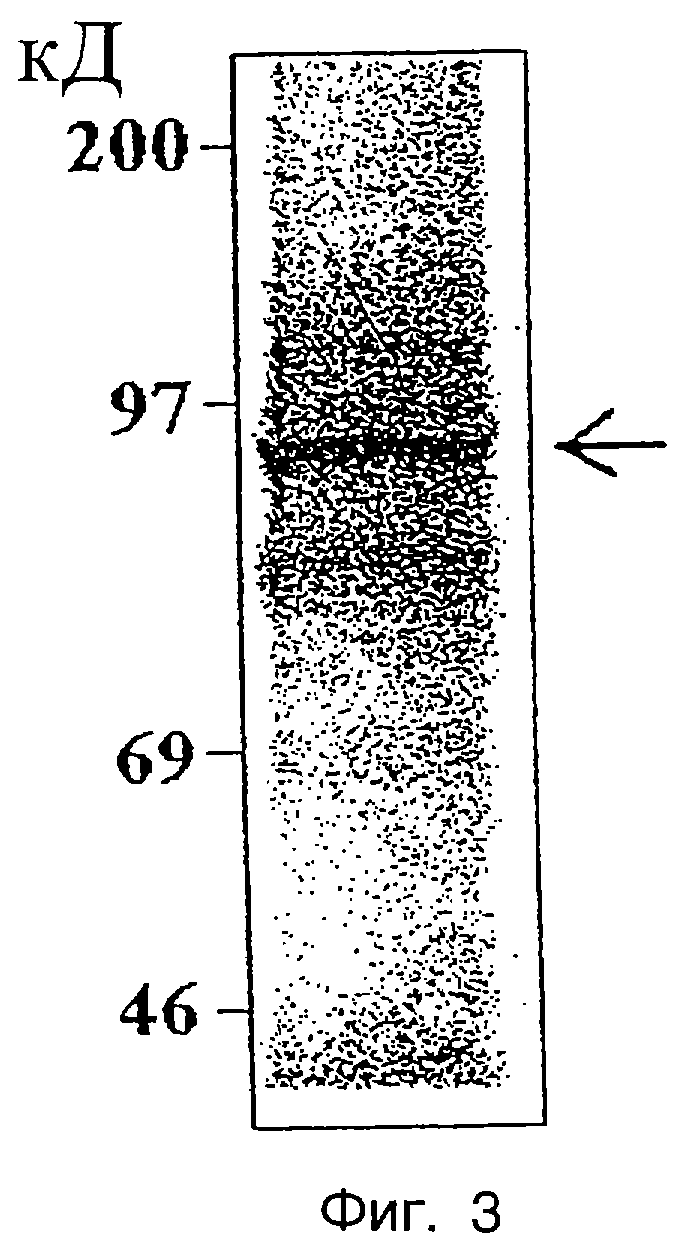
Фиг. 3 представляет собой радиоавтограф, который показывает транслированную in vitro ДНК-полимеразу HBV в лизате зародышей пшеницы, непосредственно из продукта ПЦР-амплификации в присутствии [35S]-метионина. [35S]-меченая ДНК-полимераза HBV человека 90 килодальтон (кД), как ожидалось, показана стрелкой. Слева показаны положения маркеров молекулярных размеров (Rainbow protein migration markers, Amersham).
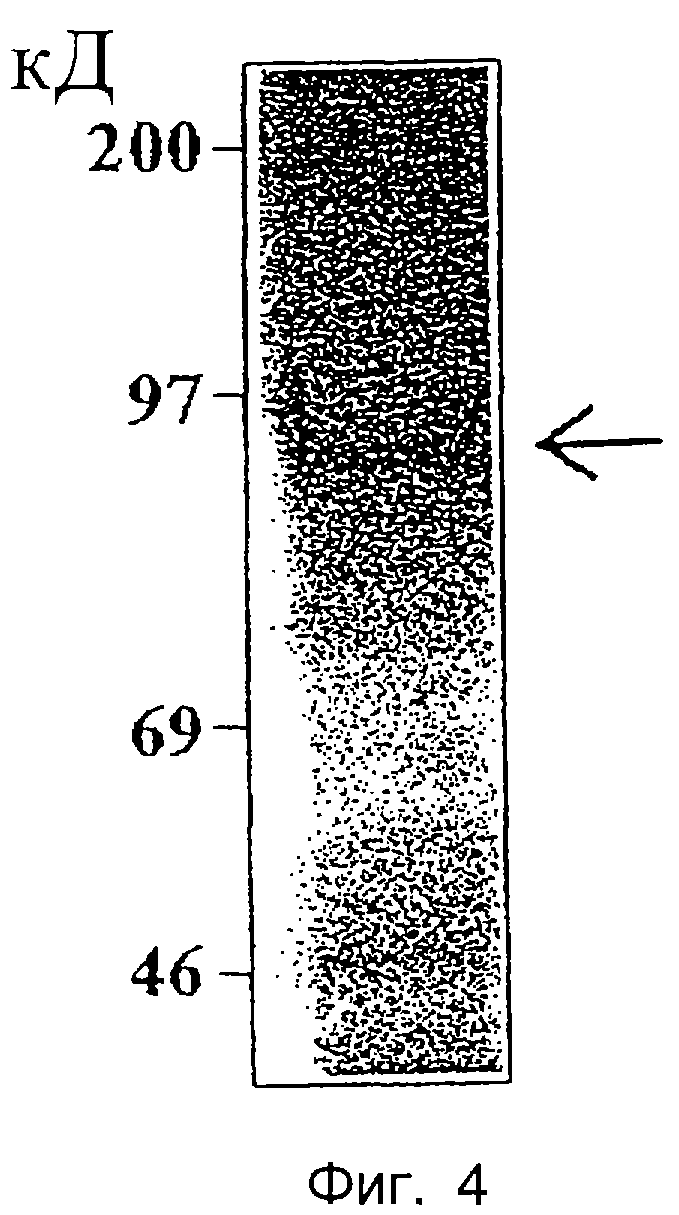
Фиг. 4 представляет собой радиоавтограф, который показывает in vitro праймирующую активность ДНК-полимеразы HBV дикого типа (синтезированной в лизате зародышей пшеницы) в присутствии [α-32P]-dTTP. [α-32P]-dТТР-меченая ДНК-полимераза HBV человека 90 килодальтон (кД), как ожидалось, показана стрелкой. Слева показаны положения маркеров молекулярных размеров (Rainbow protein migration markers, Amersham).
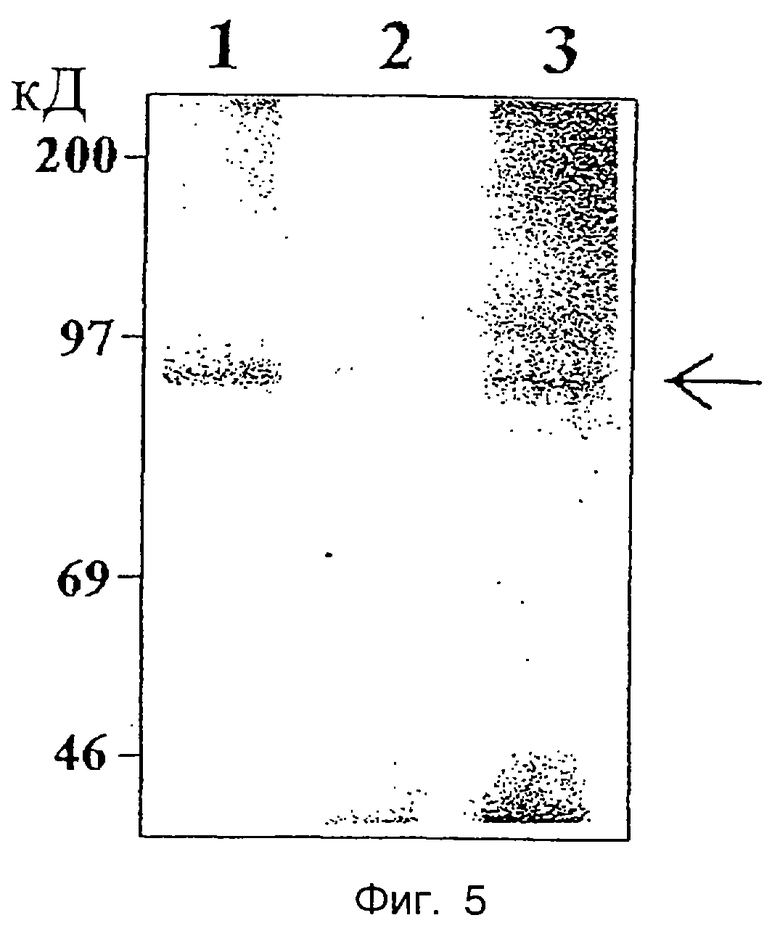
Фиг. 5 представляет собой радиоавтограф, который показывает in vitro праймирующую активность ДНК-полимеразы HBV дикого типа (дорожка 1) и мутанты поверхностного антигена 's' 145 (дорожка 2) и 's' 126 (дорожка 3) в присутствии [α-32P] -dTTP. [α-32P]-dТТР-меченая ДНК-полимераза HBV человека 90 килодальтон (кД), как ожидалось, для всех трех вирусных штаммов показана стрелкой. Слева показаны положения маркеров молекулярных размеров (Rainbow protein migration markers, Amersham).
Фиг.6 является суммированием антипраймирующих действий нуклеотидных аналогов на ДНК-полимеразу HBV дикого типа человека. Столбцы представляют радиоактивно меченую ДНК-полимеразу HBV человека, оставшуюся на нитроцеллюлозной мембране, как измерено по имп/мин. Контроль указывает in vitro праймирующую активность полимеразы HBV человека в отсутствие нуклеотидных аналогов. Результаты анализов активности в присутствии конкретного нуклеотидного аналога показаны соответственно (т. е. +ddTTP для анализа активности в присутствии ddTTP). Нет очевидного антипраймирующего эффекта, когда инкубирование проводят в присутствии либо ddTTP, либо ddATP, в сравнении с контролем. В противоположность этому ингибирующий эффект наблюдается с ddGTP, ddCTP. В соответствии с нашими результатами такой же антипраймирующий эффект наблюдается при добавлении ламивудина, который представляет собой (-)-энантиомер 3'-тиацитидина, дидезоксинуклеотидного аналога цитозина, широко используемый клинически для лечения носителей HBV с активной репликацией HBV.
ОБЩЕЕ ОПИСАНИЕ
Вирусную ДНК HBV дикого типа экстрагируют из пробы сыворотки смесью фенол/хлороформ. ПЦР-амплификацию проводят в первой стадии данного изобретения с использованием специфических олигонуклеотидов (фиг.1). 5'-смысловой олигонуклеотид образует пары с первыми 27 нуклеотидами кодирующего района ДНК-полимеразы HBV и включает в себя промотор SP6 на его проксимальном конце. 3'-антисмысловой олигонуклеотид имеет его район спаривания 300 п.н. справа (по ходу транскрипции) от стоп-кодона ДНК-полимеразы HBV. Полученные линейные продукты ДНК-амплификации 2800 п.н. (фиг.2) непосредственно подвергают in vitro транскрипции/трансляции в бесклеточной системе зародышей пшеницы в соответствии с инструкциями, обеспеченными изготовителями (Promega, U.S.A.).
При синтезе в присутствии [35S]-метионина in vitro трансляция дает белковый продукт с молекулярным размером приблизительно 90 кД, как ожидалось, для содержащего 843 аминокислоты полипептида полимеразы, показанный на фиг. 3. Этот результат согласуется с прежними сообщениями по анализу активности ДНК-полимераз DHBV и, что более важно, показывает, что ДНК-полимераза HBV человека была правильным образом транслирована с использованием линейных продуктов ПЦР-амплификации в качестве матрицы.
Для определения активности ДНК-полимеразы HBV человека реакционную смесь для трансляции in vitro, содержащую de novo синтезированую полимеразу, в отсутствие какой-либо радиоактивно меченой аминокислоты (т.е. [35S]-метионина) инкубируют в растворе, который содержит dATP, dCTP, dGTP и радиоактивно меченый [α-32P]-dTTP. Хотя любой тип метки, который обычно используют в областях анализа нуклеотидов, может быть использован для мечения нуклеотидов, которые будут включены в праймированную полимеразу, такой как флуоресцентная или абсорбционная метки, предпочтительно использовать радиоактивную метку. [α-32P]-dTTP выбран в данном изобретении вследствие его более высокой специфичности праймирования в сравнении с тремя другими нуклеотидами.
В зависимости от типа используемой метки детектирование радиоактивно меченого праймированного полимеразного продукта может быть достигнуто любым подходящим способом. Обычно оно может включать в себя стадию отделения меченых мононуклеотидов (т.е. [α-32P]-dTTP) от радиоактивно меченого праймированного полимеразного продукта. В данном изобретении продукт реакции праймирования предпочтительно анализируют при помощи электрофореза в ДСН-полиакриламидном геле. Фиг.4 показывает результаты анализа праймирующей активности ДНК-полимеразы HBV дикого типа человека в присутствии [α-32P]-dTTP, специфического праймирующего нуклеотида для фермента человека. Детектирование белковой полосы ожидаемого размера при экспонировании для радиоавтографии показывает праймирующую активность ДНК-полимеразы HBV.
Анализ полимеразной активности может быть также подвергнут мониторингу фильтрованием через нитроцеллюлозную мембрану. При подходящих условиях количественное связывание радиоактивно праймированной полимеразы может наблюдаться лишь с незначительным количеством невключенного [α-32P]-dTTP, удерживаемого на нитроцеллюлозной мембране.
Данное изобретение иллюстрируется далее нижеследующими примерами; однако, данное изобретение никоим образом не ограничивается этими примерами.
ПРИМЕРЫ
Общие экспериментальные способы
Вирусную ДНК из сыворотки, несущей HBV дикого типа, выделяли следующим образом. 200 мкл пробы сыворотки добавляли к 400 мкл лизисного буфера (Трис-хлорид 10 мМ, рН 7,4, ЭДТА 1 мМ и додецилсульфат натрия 2%) и 25 мкл протеиназы К (20 мг/мл) и инкубировали при 65oС в течение 3 часов. Затем вирусную ДНК экстрагировали смесью фенол/хлороформ и осаждали этанолом. ПЦР-амплификацию проводили с использованием следующих олигонуклеотидов. 5'-олигонуклеотид был смысловым олигонуклеотидом  и содержал промотор SP6 в его проксимальном конце (подчеркнутая последовательность) и имел его район спаривания при стартовом районе кодирующего района ДНК-полимеразы HBV (положения 2309-2340 в геноме HBV дикого типа). 3'-олигонуклеотид был антисмысловым олигонуклеотидом (ACAGTAGCTCCAAATTCТТТATAAGGGTCA), который имел его район спаривания при 300 п.н. по ходу транскрипции от стоп-кодона ДНК-полимеразы HBV (от положения 1940 до положения 1911 в геноме HBV дикого типа). Таким образом, полученный ПЦР-продукт был короче, чем продукт, установленный в опубликованных сообщениях (на 50 п.н.). [α-32P]-dTTP (3000 Ки/ммоль) и [35S]-метионин (1000 Ки/ммоль) получали из Amersham. Немеченые dATP, dCTP и dGTP получали из Promega.
и содержал промотор SP6 в его проксимальном конце (подчеркнутая последовательность) и имел его район спаривания при стартовом районе кодирующего района ДНК-полимеразы HBV (положения 2309-2340 в геноме HBV дикого типа). 3'-олигонуклеотид был антисмысловым олигонуклеотидом (ACAGTAGCTCCAAATTCТТТATAAGGGTCA), который имел его район спаривания при 300 п.н. по ходу транскрипции от стоп-кодона ДНК-полимеразы HBV (от положения 1940 до положения 1911 в геноме HBV дикого типа). Таким образом, полученный ПЦР-продукт был короче, чем продукт, установленный в опубликованных сообщениях (на 50 п.н.). [α-32P]-dTTP (3000 Ки/ммоль) и [35S]-метионин (1000 Ки/ммоль) получали из Amersham. Немеченые dATP, dCTP и dGTP получали из Promega.
Если нет других указаний, анализ полимеразной активности проводили в растворе, содержащем 100 мМ Трис-НСl (рН 7,5), 10 мМ МgСl2, 30 мМ NaCl, 10% глицерин, 4 мМ дитиотреитол, 100 мкМ каждого из немеченых дезоксирибонуклеотидтрифосфатов (dATP, dCTP и dGTP) и 5 мкКи [α-32P]-dTTP. Реакции инкубировали при 30oС в течение 30 минут, после чего аликвоту 5 мкл добавляли к 85 мкл содержащего трицин буфера для проб для электрофореза в содержащем додецилсульфат натрия полиакриламидном геле (ДСН-ПААГ) (Novex, U.S.A.), и 10 мкл анализировали на 10% ДСН-ПААГ. После электрофореза гели фиксировали вымачиванием в 10% метаноле с 10% уксусной кислотой и сушили под вакуумом. Высушенные гели экспонировали на рентгеновской пленке и сигналы определяли количественно лазерной денситометрией.
ПРИМЕР 1
Анализ полимеразной активности на мутантах поверхностного антигена HBV
Одним из прямых применений упрощенного анализа (теста) активности на ДНК-полимеразе HBV человека, сообщенных в данном изобретении, является оценка соответствующей активности вариантных HBV с мутацией на основном поверхностном антигене, в частности мутантов, индуцированных после вакцинации (т.е. 's' 145). Вирусную ДНК экстрагировали, как описано выше, из проб сыворотки, содержащих такие варианты HBV. Мутанты, включенные в данное изобретение, включали в себя 's' 145 (мутация глицин --> аргинин) и 's' 126 (треонин --> аланин), которые способны избегать доступных в настоящее время систем иммунодетектирования и способны к независимой репликации. С использованием той же самой пары олигонуклеотидов ПЦР-амплификацию проводили с вирусной ДНК в качестве матрицы на термоциклере ДНК (Perkin-Elmer, Cetus) в течение 35 циклов с использованием полимеразы Taq (Promega, U.S.A.), причем каждый цикл состоял из 1,5 мин при температуре денатурации (94oС), 2 мин при температуре отжига (53oС) и 4 мин при температуре удлинения (72oС).
ПЦР-продукт, содержащий промотор SP6 и амплифицированный из каждого мутантного HBV, добавляли в бесклеточную систему зародышей пшеницы.
Сопряженную транскрипцию/трансляцию in vitro проводили в соответствии с инструкциями, обеспеченными изготовителем (Promega, U.S.A.). Вкратце, 10 мкл ПЦР-продукта добавляли к 25 мкл экстракта зародышей пшеницы, дополненного РНК-полимеразой SP6, смесью аминокислот (в отсутствие [35S]-метионина), ингибитором РНКаз и реакционным буфером. Реакционную смесь инкубировали при 30oС в течение 60 мин. Полученные экстракты, содержащие транслированную ДНК-полимеразу HBV, добавляли к раствору, описанному в разделе "Общие экспериментальные способы", и активность полимеразы определяли, как описано выше. Результаты такого анализа, показанные на фиг.5, указывают на то, что ДНК-полимераза HBV либо мутанта 's' 145 (дорожка 2), либо мутанта 's' 126 (дорожка 3) проявляет одинаковую праймирующую активность в сравнении с активностью фермента дикого типа (дорожка 1). Альтернативно, количественные измерения могут проводиться лазерной денситометрией, которая позволяет сравнить интенсивность радиоактивно меченых праймированных полимераз.
ПРИМЕР 2
Тестирование на ингибиторы ДНК-полимеразы HBV человека
Скрининг на ингибиторы ДНК-полимеразы HBV человека обеспечил бы новые терапевтические агенты для инфекции HBV, так как эффективное ингибирование полимеразной активности будет приводить к ингибированию репликации вируса HBV. Упрощенный анализ активности, сообщенный в данном изобретении, позволил бы проводить более быстрый анализ ингибирующих действий новых обнаруженных молекул на ДНК-полимеразу вариантного HBV, несущего мутации на основном поверхностном антигене. Вкратце, ингибитор-кандидат сначала инкубировали с ДНК-полимеразой HBV дикого типа человека, которая ПЦР-была амплифицирована и транслирована in vitro, как сообщено в данном изобретении. Инкубирование проводили в присутствии [α-32P]-dTTP и с использованием остальных условий, идентичных вышеописанным условиям. Его ингибиторное действие может быть определено либо лазерной денситометрией после анализа при помощи электрофореза в ДСН-ПААГ, либо измерением количества радиоактивно меченой ДНК-полимеразы, связанной с нитроцеллюлозной мембраной после фильтрования. Важно, что анализ ингибиторных эффектов таких антивирусных агентов может быть легко применен к вариантам HBV, в том числе к индуцированному вакциной мутанту 's' 145, что также включено в данное изобретение (фиг.5). Дополнительный анализ на потенциальное ингибиторное действие, полученное из вышеуказанного анализа, может быть затем распространен на другие системы, такие как продуцирующие HBV клеточные линии и модель трансгенного животного.
В зависимости от типа используемой метки детектирование меченого гибридного ДНК-полимеразного продукта HBV может быть достигнуто любым из подходящих способов. Обычно оно может включать в себя стадию отделения меченого мононуклеотида от меченой ДНК-полимеразы HBV человека. В предпочтительном варианте детектирование достигается фильтрованием смеси пробы (которая в этой временной точке в способе анализа содержит меченую ДНК-полимеразу HBV человека и избыток меченого мононуклеотида) через нитроцеллюлозную мембрану. Не включенный избыток меченого мононуклеотида протекает через эту мембрану, тогда как меченый гибридный продукт полимеразной реакции улавливается на нитроцеллюлозной мембране. Когда метка является радиоактивной меткой, как это имеет место в упрощенном анализе, сообщенном в данном изобретении, количество радиоактивности, связанное с фильтром, может быть определено количественно при помощи считывающего показания с планшета сцинтилляционного счетчика. Такое измерение имеет явные преимущества в сравнении с предыдущим измерением, описанным в данном изобретении, заключающееся в том, что оно не предусматривает стадию электрофореза.
В данном изобретении следующие нуклеотидные аналоги, способные ингибировать ДНК-полимеразную активность HBV, могут быть анализированы на их антипраймирующую активность. Они включают в себя ddTTP, ddGTP, ddCTP, ddATP и ламивудин. Условия анализа являются идентичными условиям, описанным в разделе "Общие экспериментальные способы". Вкратце, нуклеотид в смеси для анализа заменяют соответствующим нуклеотидным аналогом в тестировании антипраймирования этого конкретного нуклеотидного аналога (т.е. dGTP должен быть заменен ddGTP для тестирования антипраймирующей активности ddGTP). Наоборот, нуклеотид не заменяют при тестировании антипраймирующей активности ddTTP (так как в данном изобретении радиоактивно меченым нуклеотидом является dTTP), а также ламивудина. В конце инкубирования реакционную смесь переносят на нитроцеллюлозную мембрану (2 х 2 см) осторожным нанесением пятен. Затем невключенный радиоактивно меченый dTTP отделяют промыванием нитроцеллюлозной мембраны в 400 мл Трис-НСl (рН 7,5), 100 мМ NaCl, 20 мМ МgСl2 и 0,5% бычьем сывороточном альбумине. Затем оставшуюся радиоактивно меченую ДНК-полимеразу HBV человека, связанную с нитроцеллюлозной мембраной, измеряют количественно с использованием считывающего показания планшета сцинтилляционного счетчика. Результаты, представленные на фиг.6, показывают значительно более низкое количество [32Р] -меченой ДНК-полимеразы HBV человека в присутствии ddCTP и ddGTP в сравнении с контрольным анализом (в отсутствие какого-либо нуклеотидного аналога), свидетельствуя, следовательно, об их антипраймирующей активности. В противоположность этому ни для ddTTP, ни для ddATP не наблюдали антипраймирующей активности.
Данное изобретение основано на упрощенном анализе активности ДНК-полимеразы HBV человека. Данное изобретение делает возможным быстрое определение ДНК-полимеразной активности HBV непосредственно из пробы сыворотки без требующегося в настоящее время клонирования. Таким образом, оно позволяет проводить быструю оценку и мониторинг увеличивающегося числа вариантных HBV с мутациями на их основном поверхностном антигене. Данное изобретение делает также возможным легко доступный тест на ингибиторные эффекты антивирусных агентов на этих вариантах HBV с особым подчеркиванием тех вариантов HBV, которые индуцируются после вакцинации (т.е. 's' 145), связанной с заболеваниями печени, и тех, которые обнаружены в бессимптомных индивидуумах, которые могли бы в конце концов приводить к заболеванию печени.


Изобретение относится к области медицины и биотехнологии и касается способа анализа активности in vitro для ДНК-полимеразы вируса гепатита В (НВV) человека, который предусматривает использование в качестве 5'-олигонуклеотида в ПЦР-амплификации ДНК-полимеразы НВV из пробы олигонуклеотида, в который был встроен промотор SP6-вирусной полимеразы, прямую транскрипцию и трансляцию ПЦР-продуктов в присутствии радиоактивно меченого агента и измерение праймирования ДНК-полимеразы НВV. Данное изобретение также обеспечивает использование такого анализа для анализа активности различных проб сыворотки, для скрининга на ингибиторы ДНК-полимеразы HBV и для тестирования и/или скрининга потенциальных лекарственных средств против HBV на их способность ингибировать ДНК-праймирующую активность ДНК-полимеразы НВV человека. Преимущество изобретения заключается в разработке более чувствительного и быстрого способа анализа. 6 с. и 8 з.п.ф-лы, 6 ил.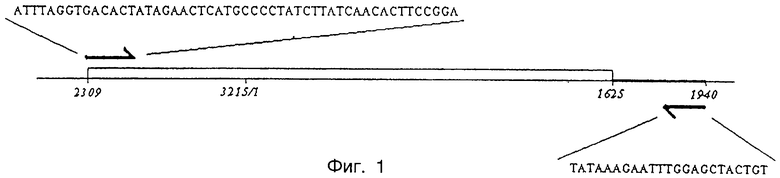
| ШТАММ ДРОЖЖЕЙ SACCHAROMYCES CEREVISIAL, СОДЕРЖАЩИЙ РЕКОМБИНАНТНУЮ ПЛАЗМИДУ YEP 63/AB, - ПРОДУЦЕНТ ПРОИЗВОДНОГО М-БЕЛКА ВИРУСА ГЕПАТИТА В ЧЕЛОВЕКА | 1994 |
|
RU2082759C1 |
| Экономайзер | 0 |
|
SU94A1 |
| US 5492817 А, 20.02.1996 | |||
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
Авторы
Даты
2003-04-20—Публикация
1999-03-13—Подача