Изобретение относится к экспериментальной биологии, медицине и фармакологии и может быть использовано при изучении механизмов развития патологии соединительной ткани и разработке способов лечения и профилактики заболеваний.
Согласно результатам, опубликованным в докладе «Global Burden of Disease» (The Lancet, 2020, Volume 396, Number 10258, p. 1129-1306), только в США расходы на медицинское обеспечение больных с нарушением опорно-двигательного аппарата в 2016 г. составили 380 млрд. американских долларов, что превосходит по объему затраты, выделяемые на сердечнососудистые заболевания и рак. Анализ показателей, основанных на статистических исследованиях причин потерянных лет жизни в связи с инвалидностью (DALY), ежегодно публикуемых ВОЗ, свидетельствует, что патологии костно-мышечной системы являются определяющими в рейтинге заболеваний и имеют устойчивую тенденцию к росту. В этой связи изучение механизмов развития нарушений опорно-двигательной системы и поиск средств профилактики заболеваний соединительной ткани является актуальным в современной биологии, медицине и фармакологии. Для получения новых знаний о патогенезе указанных болезней широкое применение находит лабораторный эксперимент, позволяющий отслеживать в динамике изменения, затрагивающие костно-мышечный аппарат, и связанные с ним системы (иммунную, эндокринную и др.), что сложно или невозможно организовать в клинике. Ключевым аспектом в изучении формирования и развития заболеваний костно-суставной системы, мониторинге эффективности проводимого лечения или профилактики, является разработка неинвазивных и информативных способов интегральной оценки локомоторного аппарата подопытных животных.
Известен способ неинвазивной диагностики суставов, основанный на оптической визуализации изображения межфаланговых суставов после предварительной обработки пальцев биосовместимым иммерсионным агентом (характеризуемым гиперосмолярным эффектом и имеющим показатель преломления равный или превышающий показатель преломления кожи), просвечиванием суставов излучением при различных длинах волн в оптической части спектра и регистрацией соответствующих изображений с помощью цифровой камеры (см. патент RU №2697594, МПК А61В 5/00 (2006.01), G01N 21/35 (2014.01), G02B 21/33 (2006.01), опубл. 15.08.2019 г.).
Известен способ диагностики ревматоидного артрита коленного сустава, заключающийся в проведении ультразвуковой эхолокации анатомических структур и количественной оценке объема синовиальной жидкости, оптической плотности тканей суставов и амплитуды осцилляций в сумке латерального заворота коленного сустава (см. патент RU №2633631, МПК2006.01 А61В 8/00, опубл. 16.10.2017 г.). При объемах синовиальной жидкости и амплитудах пульсовых осцилляций, превышающих показатели нормы, диагностируют ревматоидный артрит.
Недостатками указанных аналогов являются необходимость седации животных во время диагностических процедур, для чего им вводят анестетики или миорелаксанты, которые могут оказать модифицирующее действие на механизм развития модельной патологии или изменить лечебный эффект потенциального фармакологического вещества (или средства для профилактики), тестируемого в условиях лабораторного эксперимента. Указанное обстоятельство снижает достоверность получаемой научной информации, увеличивает объем необходимых манипуляций с животными и требует больших трудозатрат высококвалифицированных специалистов.
Наиболее близким к данному техническому решению является способ тестирования препаратов с предполагаемым психотропным или актопротекторным действием, включающий формирование контрольной и опытной групп животных, введение препарата, регистрацию локомоторной активности и измерение единиц поведения в модели «открытое поле» у лабораторных животных (см. патент RU №2601376, МПК2006.01 G09B 23/28, опубл. 10.11.2016 г.).
Тестирование осуществляется на основе измерения актометрических единиц поведения животных в модели «открытого поля» или аналогичных ему по информативности моделях (приподнятый крестообразный лабиринт, черно-белая камера). После предварительной стратификации формируют три группы экспериментальных животных, из которых для непосредственных исследований актометрического действия потенциального лекарственного препарата отбирают только одну группу с максимально высоким когнитивным показателем и средним индексом исследовательской активности. В процессе тестирования (эксперимента) регистрируют качественные и количественные показатели как врожденного, так и приобретенного поведения.
Недостатком прототипа является необходимость изначального разделения животных на три группы по типу нервной системы, которая в свою очередь напрямую связана с эндокринной системой. Последнее обстоятельство может значительным образом модифицировать патогенез заболеваний опорно-двигательной системы и, соответственно, влиять на механизм лечебного или профилактического действия тестируемых фармакологических препаратов с предполагаемым остеопротекторным (хондропротекторным) действием, что исключает возможность экстраполяции получаемых результатов на средне популяционные показатели, и, тем самым, значительно снижает информативность метода Необходимость предварительной стратификации животных в прототипе приводит к увеличению материальных затрат за счет увеличения количества экспериментальных животных и трудозатрат высококвалифицированного персонала.
Технический результат предлагаемого технического решения заключается в высокой информативности, достоверности и точности способа тестирования, снижении материальных затрат за счет сокращения количества экспериментальных животных и трудозатрат высококвалифицированных специалистов, а также в доступности инструментального обеспечения способа, его неинвазивности, экспрессности и в возможности изучения процесса в динамике.
Технический результат достигается тем, что в способе неинвазивного тестирования развития модельной патологии опорно-двигательного аппарата у лабораторных животных, включающем формирование контрольной и опытной групп животных, введение препарата, регистрацию локомоторной активности и измерение единиц поведения у животных контрольной и опытной групп в модели «открытое поле», согласно изобретению, введение препарата осуществляют опытной группе лабораторных животных, а видео регистрацию горизонтальной двигательной активности животных осуществляют в течение 3-5 минут в модели «открытое поле», которую предварительно очерчивают на равные по площади центральный круг и два концентрических ряда с секторами, а по периметру размещают стенку, затем животных сажают у стенки модели и определяют количество пересеченных секторов животными, количество стоек, количество актов груминга и количество актов дефекации и болюсов, и по ним судят о развитии патологии опорно-двигательного аппарата у лабораторных животных.
В качестве препарата лабораторным животным опытной группы вводят, например, полный адъювант Фрейнда, подкожно, в правую заднюю конечность в объеме 0,1 мл на 200 г массы тела.
Данный способ тестирования позволит повысить информативность, достоверность и точность развития модельной патологии нарушений опорно-двигательного аппарата у лабораторных животных, а также снизить материальные затраты за счет сокращения количества экспериментальных животных и трудозатрат высококвалифицированных специалистов.
При временном интервале видео регистрации поведения животных менее 3-х минут возрастает ошибка определения: первые 1-2 мин идет привыкание и знакомство животных с новыми условиями, их эмоциональный уровень дестабилизирован. При временном интервале более 5 минут нецелесообразно, поскольку знакомство животных с моделью может приводить к привыканию и замиранию, что также может оказать негативное влияние на диагностическую точность исследований. По итогам видео наблюдения
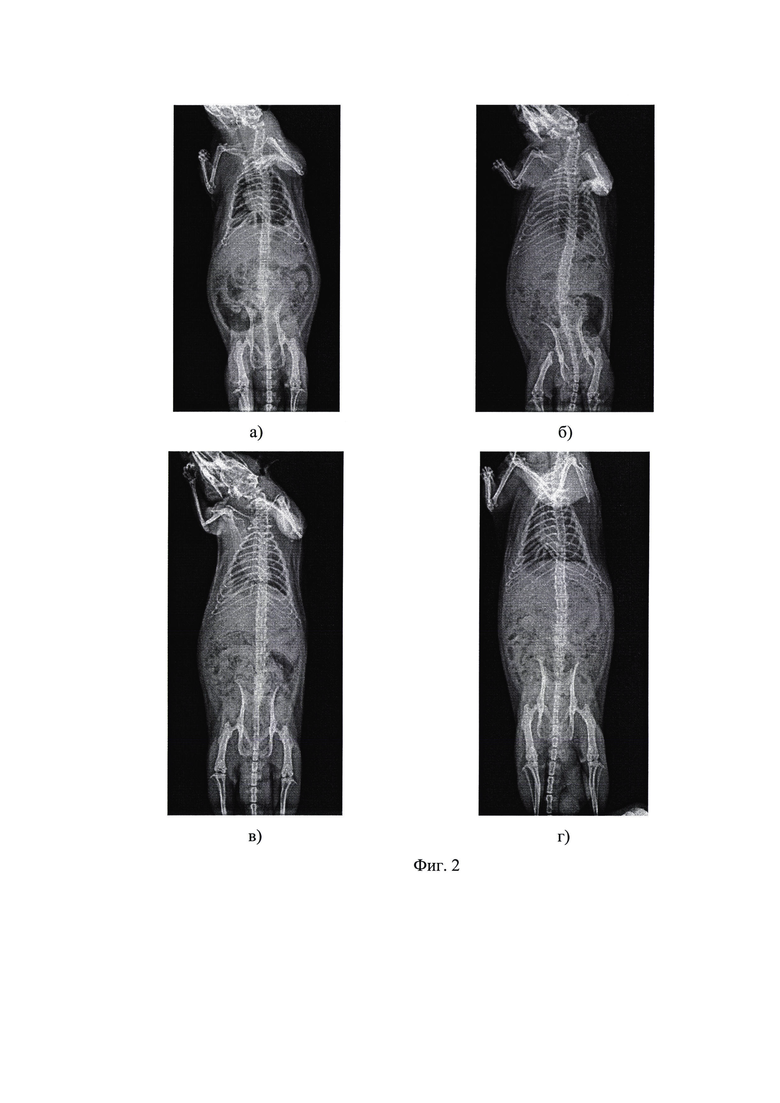
Сущность способа неинвазивного тестирования развития модельной патологии опорно-двигательного аппарата у лабораторных животных поясняется таблицей, на которой отражены показатели поведенческих реакций животных (крыс) в динамике эксперимента, и фотографиями, где на фиг. 1 - изображена модель «открытого поля» для лабораторных животных (а - пересечение секторов; б - стойка с опорой; в - стойка без опоры; г - груминг), а на фиг. 2 - результаты радиографических исследований лабораторных животных на терминальной стадии эксперимента (а, б - опытные животные; в, г - контрольные).
Развитие индуцированного ревматоидного артрита у лабораторных животных (на примере белых крыс Wistar) сопровождается неуклонным снижением количественных показателей, характеризующих горизонтальную и вертикальную активность в модели «открытого поля», на фоне стабильно сохраняющихся эмоционально-стрессовых реакций. Животные контрольной группы характеризуются незначительным относительным приростом количественных показателей, выявляющих поведение здорового организма на фоне снижения общего уровня тревожности в повторяющихся условиях экспериментальной установки «открытого поля».
Так, по мере прогрессирования адъювант-индуцированного ревматоидного артрита у крыс опытной группы значительным образом снижаются показатели горизонтальной двигательной активности. К окончанию третьей недели с момента интоксикации полным адъювантом Фрейнда, количество пересеченных секторов животными опытной группы (см. таблицу, Опыт 1) снижается на 43% (р<0,01), количество стоек с упором на стенку достоверно снижается на 70%, без упора на 49% - относительно крыс контрольной группы (Контроль 1). Все это свидетельствует о развитии дегенеративно-дистрофического суставного синдрома, приводящего к скованности в движениях пораженных суставов, что также может сопровождаться болевыми ощущениями при перемещении крыс по арене «открытого поля». При этом различия в эмоциональной реактивности сравниваемых групп животных достоверно не различаются и у животных опытной группы отмечается лишь тенденция к снижению относительного уровня тревожности (груминг на 18%, число болюсов дефекации на 22%, а самих актов дефекации - на 28%). Отмеченные наблюдения могут отражать сосредоточенность животных на болевом синдроме, который, как известно, сопровождает пациентов, начиная со второй стадии заболевания (согласно результатам физикального обследования, а также расчетам, проводимым в пересчете на временную шкалу животных, начиная от момента индуцированной патологии, у животных (крыс) к моменту первого тестирования сформированы нарушения, соответствующие 2-3-ей стадиям ревматоидного артрита), в результате чего у животных снижается двигательная и исследовательская активность, и тем самым снижается степень конфликта двух противоположных мотиваций - инстинктивной программы по исследованию нового пространства и побуждению минимизировать потенциальную опасность со стороны такового.
Из таблицы также следует, что к окончанию эксперимента (7 недель с момента введения адъюванта Фрейнда, соответственно Опыт 2, Контроль 2) у животных опытной группы отмечается достоверное 2,3-кратное снижение горизонтальной подвижности и 3-х кратное снижение общей вертикальной активности (на опору и без опоры) на фоне недостоверных изменений эмоционально-тревожного состояния (акты груминга и дефекации). Результаты рентгенографии, выполненной по завершении эксперимента, подтверждают выводы физиологических исследований и свидетельствуют о развитии глубоких структурно-дегенеративных изменений в суставном аппарате опытных животных. Для животных опытной группы оказалось характерным неравномерное сужение суставных щелей, перестройка костной структуры в межвертельной области, где обнаруживаются участки кистовидных просветлений и остеосклероза (см. фиг. 2, а). Суставные поверхности в коленных суставах уплощены. В ряде случаев контуры для вертлужной впадины не определяются. У животного (см. фиг. 2, б) отсутствует головка и шейка бедренной кости (справа).
У животных контрольной группы грубых изменений в костно-мышечной структуре не выявлено (фиг. 2, в, г).
Способ неинвазивного тестирования развития модельной патологии опорно-двигательного аппарата у лабораторных животных (крыс) осуществляется следующим образом.
Крыс разделяют на две группы: контрольную и опытную. Крысам контрольной группы вводят растворители по той же схеме и в тех же объемах, что и в опытной группе. Крысам опытной группы вводят препарат, инициирующий развитие патологии опорно-двигательного аппарата, например, полный адъювант Фрейнда, подкожно в правую заднюю конечность в объеме 0,1 мл на 200 г массы тела. Развитие патологического процесса отслежено в динамике - по истечении 3-й недели и на конечной стадии эксперимента (7-я неделя) с помощью стандартной модели «открытое поле», представляющей собой круглую арену, которую предварительно очерчивают на равные по площади центральный круг 1 и два концентрических ряда 2,3 с секторами, и по периметру размещают стенку 4 (см. фиг. 1). Стандартный диаметр установки для крыс 97 см, высота стенок 4-42 см (для мышей и морских свинок размеры подбираются меньшими или большими указанных). Животных сажают у стенки 4 и ведут видео регистрацию поведения в течение 3-5 минут. Рассчитывают количество пересеченных секторов концентрических рядов 2,3 крысами (см. фиг. 1, а), количество стоек животного с опорой на стенку (см. фиг. 1, б), без опоры (см. фиг. 1 в), количество актов груминга (см. фиг. 1, г) и подсчитывают количество актов дефекации и болюсов и по ним судят о развитии патологии опорно-двигательного аппарата у лабораторных животных.
Перед помещением в установку нового животного арену тщательно протирают 50% раствором этанола или другим растворителем для удаления следов пребывания другого животного.
Статистическую обработку полученных результатов осуществляют по критерию Манна-Уитни или аналогичного ему по информативности в соответствующих программах (например, SPSS).
Способ обеспечивает возможность неинвазивного тестирования развития модельной патологии опорно-двигательной системы у лабораторных животных в динамике или на конечной стадии эксперимента и обладает высокой информативностью, точностью и экспрессностью.
Использование предлагаемого способа неинвазивного тестирования развития модельной патологии опорно-двигательного аппарата у лабораторных животных позволит по сравнению с прототипом повысить информативность, достоверность и точность диагностирования модельной патологии у лабораторных животных, а также снизить материальные затраты, т.к. требует гораздо меньшего количества лабораторных животных, поскольку исключает предварительный отбор особей с требуемыми показателями исследовательской активности и когнитивных способностей, а также позволяет существенно сократить трудозатраты высококвалифицированных специалистов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ профилактики аутоиммунного ревматоидного артрита у крыс в эксперименте | 2021 |
|
RU2774358C1 |
| АНТИДЕПРЕССАНТНОЕ СРЕДСТВО ДЛЯ КОРРЕКЦИИ НЕЖЕЛАТЕЛЬНЫХ ПОБОЧНЫХ ЭФФЕКТОВ НЕЙРОЛЕПТИКОВ | 2019 |
|
RU2746012C2 |
| СПОСОБ ДИАГНОСТИКИ ТОКСИЧЕСКОЙ ЭНЦЕФАЛОПАТИИ У МЕЛКИХ ЛАБОРАТОРНЫХ ЖИВОТНЫХ ПРИ ХРОНИЧЕСКОМ ВОЗДЕЙСТВИИ ПАРОВ МЕТАЛЛИЧЕСКОЙ РТУТИ | 2010 |
|
RU2461893C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ МЕДИКАМЕНТОЗНОЙ НЕЙРОТОКСИЧНОСТИ С ПОМОЩЬЮ КОМПЛЕКСА ПРОТИВОТУБЕРКУЛЕЗНЫХ И АНТИМИКРОБНЫХ ПРЕПАРАТОВ | 2022 |
|
RU2795524C1 |
| Способ допплерографической оценки антиангиогенного действия в модели куриного эмбриона | 2023 |
|
RU2823747C1 |
| 9-[2-(4-ИЗОПРОПИЛФЕНОКСИ)ЭТИЛ]АДЕНИН, ОБЛАДАЮЩИЙ АНТИДЕПРЕССАНТНЫМ И ПРОТИВОСТРЕССОРНЫМ ДЕЙСТВИЕМ | 2013 |
|
RU2529817C1 |
| СПОСОБ ДИАГНОСТИКИ ОТДАЛЕННОЙ ТОКСИЧЕСКОЙ ЭНЦЕФАЛОПАТИИ У ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ | 2007 |
|
RU2383060C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ОТДАЛЕННОЙ ТОКСИЧЕСКОЙ ЭНЦЕФАЛОПАТИИ | 2007 |
|
RU2341828C1 |
| Способ коррекции нарушений микроциркуляции при экспериментальном воспалении в тканях пародонта | 2019 |
|
RU2700571C1 |
| Средство, обладающее детоксикационной активностью при алкогольной интоксикации | 2021 |
|
RU2787997C1 |

Изобретение относится к экспериментальной биологии, медицине и фармакологии и может быть использовано при изучении механизмов развития патологии соединительной ткани и разработке способов лечения и профилактики заболеваний. Способ включает формирование контрольной и опытной групп животных, введение препарата, регистрацию локомоторной активности и измерение единиц поведения у животных контрольной и опытной групп в модели «открытое поле», причем введение препарата осуществляют опытной группе лабораторных животных, а видео регистрацию горизонтальной двигательной активности животных осуществляют в течение 3-5 минут в модели «открытое поле», которую предварительно очерчивают на равные по площади центральный круг и два концентрических ряда с секторами, а по периметру размещают стенку. Затем животных сажают у стенки модели и определяют количество пересеченных секторов животными, количество стоек, количество актов груминга и количество актов дефекации и болюсов, и по ним судят о развитии патологии опорно-двигательного аппарата у лабораторных животных. В качестве препарата лабораторным животным опытной группы вводят, например, полный адъювант Фрейнда, подкожно, в правую заднюю конечность в объеме 0,1 мл на 200 г массы тела. Способ обеспечивает повышение информативности, достоверности и точности способа тестирования, снижении материальных затрат за счет сокращения количества экспериментальных животных и трудозатрат высококвалифицированных специалистов, а также в доступность инструментального обеспечения способа, его неинвазивности, экспрессности и в возможности изучения процесса в динамике. 1 з.п. ф-лы, 1 табл., 2 ил.
1. Способ неинвазивного тестирования развития модельной патологии опорно-двигательного аппарата у лабораторных животных, включающем формирование контрольной и опытной групп животных, введение препарата, регистрацию локомоторной активности контрольной и опытной групп в модели открытое поле, отличающийся тем, что введение препарата осуществляют опытной группе лабораторных животных, а видеорегистрацию горизонтальной двигательной активности животных осуществляют в течение 3 - 5 минут в модели открытое поле, которую предварительно очерчивают на равные по площади центральный круг и два концентрических ряда с секторами, а по периметру размещают стенку, затем животных сажают у стенки модели и определяют количество пересеченных секторов животными, количество стоек, количество актов груминга и количество актов дефекации и болюсов, и по ним судят о развитии патологии опорно-двигательного аппарата у лабораторных животных.
2. Способ по п. 1, отличающийся тем, что в качестве препарата лабораторным животным опытной группы вводят, например, полный адъювант Фрейнда, подкожно, в правую заднюю конечность в объеме 0,1 мл на 200 г массы тела.
| СПОСОБ ТЕСТИРОВАНИЯ ПРЕПАРАТОВ С ПРЕДПОЛАГАЕМЫМ ПСИХОТРОПНЫМ ИЛИ АКТОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 2015 |
|
RU2601376C1 |
| Способ моделирования посттравматического стрессового расстройства у лабораторных крыс | 2020 |
|
RU2746901C1 |
| Способ моделирования нарушений в организме лабораторных животных, вызванных воздействием шума в постконтактном периоде | 2017 |
|
RU2655545C1 |
| Искандерова Р.Э | |||
| и др | |||
| ВЛИЯНИЕ МЕТИОНИНА НА ПОВЕДЕНИЕ КРЫС В ТЕСТЕ "ОТКРЫТОЕ ПОЛЕ" //Синергия Наук | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| N | |||
| Способ очистки нефти и нефтяных продуктов и уничтожения их флюоресценции | 1921 |
|
SU31A1 |
| С | |||
| Хлебопекарная печь | 1924 |
|
SU1391A1 |
Авторы
Даты
2022-04-29—Публикация
2021-06-30—Подача