Изобретение относится к медицине и может быть использовано для прогнозирования риска развития послеоперационной мозговой дисфункции при плановых хирургических операциях по поводу злокачественных новообразований груди и живота.
Известен способ прогнозирования риска развития послеоперационных сердечно-сосудистых осложнений лапароскопических операций при метастатическом раке толстой кишки, включающий оценку параметров состояния сердечно-сосудистой системы у каждого больного на дооперационном этапе в качестве параметров состояния сердечнососудистой системы определяют: ударный объем левого желудочка (УО ЛЖ, мл), миокардиальный стресс в систолу (MCs, г/см2), индекс нагрузки объемом левого желудочка (ИНО ЛЖ мл/г), систолический резерв при пробе Вальсальвы (систолический резерв ΔУОВальс, %), диастолический резерв при пробе Вальсальвы (диастолический резерв ΔЕ/АВальс, %), баллы оценки риска сердечно-сосудистых осложнений по Гольдману, затем для каждого параметра определяют диагностические коэффициенты в соответствии с таблицей 1, представленной в описании, далее полученные диагностические коэффициенты суммируют и при сумме 45 и более прогнозируют высокий риск, а при сумме меньше 45 - низкий риск развития послеоперационных сердечно-сосудистых осложнений после лапароскопических операций при раке толстой кишки (патент РФ №2663078, А61В 5/00, опубл. 01.08.2018). Но данный способ применен к ограниченному кругу хирургических вмешательств и не может быть использован для оценки риска развития послеоперационной мозговой дисфункции.
В основу изобретения положена задача стратификации пациентов по группам «низкого» и «высокого» рисков путем создания более точного способа определения риска развития послеоперационной мозговой дисфункции за счет учета всех возможных комбинации факторов риска.
Решение поставленной задачи обеспечивается тем, что в способе определения риска развития послеоперационной мозговой дисфункции вероятность риска рассчитывают по формуле пробит-функции:
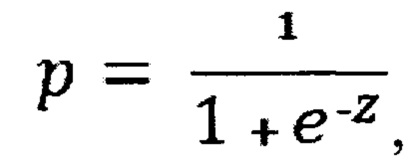 где
где
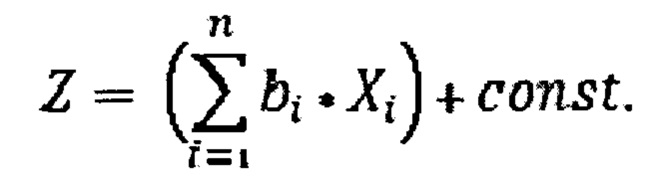
где bi - весовой коэффициент i-го фактора риска,
Xi - значение i-го фактора риска,
Const. - константа регрессионного уравнения Z,
затем определяют по этой формуле прогностически ценные факторы, для прогнозирования риска развития послеоперационной мозговой дисфункции:
- возраст старше 75 лет (А) - для которого вероятность риска развития послеоперационной мозговой дисфункции равна 69,03%;
- максимальное систолическое артериальное давление интраоперационно более 150 мм рт.ст. (В) - для которого вероятность риска развития послеоперационной мозговой дисфункции равна 70,76%;
- соблюдение антигиперхолестеринемической диеты (С) - для которого вероятность риска развития послеоперационной мозговой дисфункции равна 1,11% - протективный фактор.
При отсутствии всех этих факторов риск послеоперационной мозговой
дисфункции составил 12,16%;
при сочетании фактора А+С - 15,33%;
при сочетании фактора В+С - 16,43%;
при сочетании факторов А+В+С - 75,98%;
при сочетании фактора А+В - 97,5%. На заключительном этапе проводят стратификацию пациентов по группам «низкого» и «высокого» рисков с учетом выбранного порога классификации в 20%.
Повышение точности предлагаемого способа связано с обработкой большого массива данных и точностью самого метода обработки данных.
Риск события есть вероятность его наступления при определенных условиях. Условиями для возникновения исхода в данном случае является наличие факторов риска. Предложенный калькулятор позволяет прогнозировать вероятность (в %) развития послеоперационной мозговой дисфункции на основании сочетания наиболее прогностически ценных факторов риска для каждого из типов.
Вероятность рассчитывали по формуле пробит-функции:
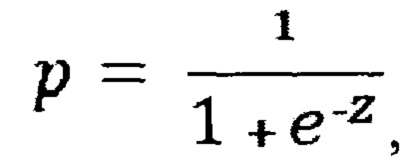 где
где
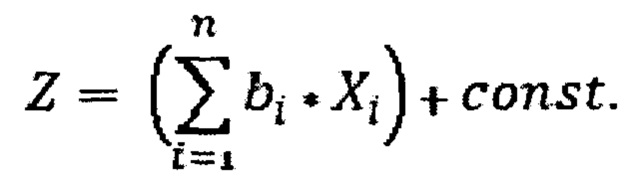
bi - весовой коэффициент i-го фактора риска
Xi - значение i-го фактора риска
Const. - константа регрессионного уравнения Z
При добавлении в модели численных факторов риска выяснено, что данные модели не обладают достаточной валидностью и/или предсказательной способностью. Поэтому в рамках данного исследования были рассчитаны дихотомические факторы риска (0 - нет фактора риска, 1 - есть) в три этапа:
1. На первом этапе отобранные независимые переменные были разделены по шкалам изменения на дихотомические, порядковые (до 5 рангов) и количественные.
2. На втором этапе выполнены следующие действия:
a. Для дихотомических факторов (пол, острое нарушение мозгового кровообращения или инфаркт миокарда в анамнезе, сахарный диабет 2 типа, курение, злоупотребление алкоголем, наличие паранеопластического синдрома, кахексия, гистологический тип опухоли, наличие зона- и/или гипокинезии по данным трансторакальной эхокардиографии, факт приема статинов, антиагрегантов, антикоагулянтов, вид хирургического доступа, факт проведения химиотерапии и др.) были рассчитаны коэффициенты корреляции ϕ (фи) с исходами (наличие или отсутствие послеоперационной мозговой дисфункции) в режиме четырехпольных таблиц сопряженности. На этап формирования моделей были отобраны факторы, имеющие значимые коэффициенты корреляции выше 0,3 по модулю.
b. Для порядковых факторов (давность завершения работы по специальности, стадия онкологического заболевания, балл по шкале ASA (Американского общества анестезиологов), уровень образования) использованы многопольные таблицы сопряженности (2*n, где n - число рангов) с выделением ранга, по достижении которого растет частота исходов. Данный ранг обозначался уровнем отсечения (cut-off), переменная из ранговой превращалась дихотомическую со значением «0», если ранг не был достигнут, и «1», если ранг был достигнут. Далее путем расчета коэффициента ϕ, как для подпункта «а», на этап формирования моделей отобраны валидные факторы риска, с. Для количественных факторов (возраст, давность установления диагноза злокачественного новообразования, индекс массы тела, индекс коморбидности Чарлсон, количество ранее выполненных хирургических операций, уровень венозной гликемии, MHO, уровень креатинина, уровень общего белка, СОЭ, количество эритроцитов, количество тромбоцитов, количество эозинофилов, гематокрит, уровень гемоглобина, фракция сердечного выброса, балл по шкале МоСА, балл по FAB, длительность хирургической операции, максимальная частота сердечных сокращений в интраоперационном периоде, минимальная частота сердечных сокращений в интраоперационном периоде, интраоперационная кровопотеря, балл при оценке болевого синдрома по ВАШ в дооперационном периоде и др.) рассчитаны cut-off уровни при помощи ROC-анализа с исходом (наличие или отсутствие послеоперационной мозговой дисфункции) в качестве прогнозируемой переменной. Значение уровня отсечения получено по максимальной сумме чувствительности и специфичности (метод Юдена). Допуск переменных на этап построения моделей осуществлялся по величине значения AUC (площадь под кривой) и значимости ее отличия от 0,5. Таким образом, для создания моделей были отобраны только дихотомические факторы риска, которые имели связь с исходами.
Построение математических моделей проведено при помощи биноминальной регрессии. Обучение моделей проведено в режиме прямого пошагового отбора с отношением правдоподобия в качестве критерия отбора: факторы добавлялись в модель, пока ее валидность не переставала улучшаться. Для улучшения качества использованы все возможные комбинации факторов риска. Порог классификации выбран 0,5. В модель включалась константа.
Проверка валидности моделей проводилась с использованием -2 Log-правдоподобия, R-квадрата Найджелкерка (аналог коэффициента детерминации для линейной регрессии). Также использовался критерий согласия Хосмера-Лемешова.
Проверка качества классификации моделей проведена при помощи расчета процента правильно предсказанных исходов, показателей чувствительности и специфичности, а также ROC-анализа.
«Высоким риском» была выбрана вероятность более 20% (порог классификации выбирали, исходя из цены ошибки классификации).
Показатели валидности и качества предсказания полученных моделей представлено в таблице.
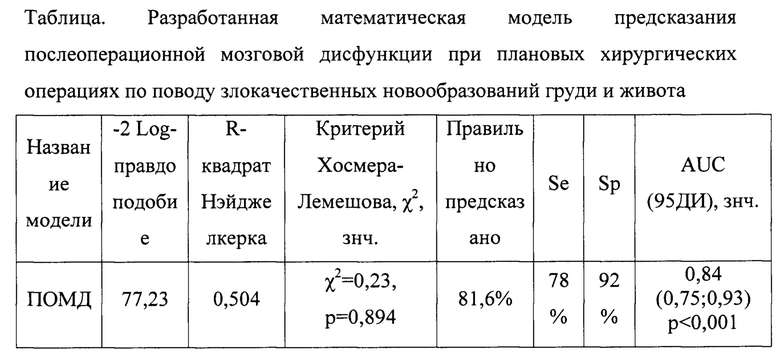
Результаты использования данной функции
Для прогнозирования риска развития послеоперационной мозговой дисфункции наиболее прогностически ценной оказалась комбинация следующих факторов:
- возраст старше 75 лет (А) - 69,03%;
- максимальное систолическое артериальное давление интраоперационно более 150 мм рт. ст.(В) - 70,76%;
- соблюдение антигиперхолестеринемической диеты (С) - 1,11% -протективный фактор.
Группа «низкого» риска (вероятность менее 20%) развития симптоматического делирия раннего послеоперационного периода:
при отсутствии всех этих факторов риск послеоперационной мозговой дисфункции составил 12,16%;
при сочетании фактора А+С - 15,33%;
при сочетании фактора В+С - 16,43%;
Группа «высокого» риска (вероятность более 20%) развития симптоматического делирия раннего послеоперационного периода:
наличие каждого из факторов А или В по отдельности;
при сочетании факторов А+В+С - 75,98%;
при сочетании фактора А+В - 97,5%.
Клинический пример №1.
Пациент Г., мужчина, 79 лет, после операции эндоскопическая резекция пищевода с пластикой узким желудочным стеблем по поводу плоскоклеточного умеренно дифференцированного рака с тенденцией к ороговению T2N1M0 ПВ стадии, по поводу которого 3 года назад получал лучевую терапию с СОД 70 Гр. Основные отрицательные моменты анамнеза у данного пациента: гипертоническая болезнь III стадии, артериальная гипертензия 3 степени, риск сердечно-сосудистых осложнений «очень высокий», хроническая сердечная недостаточность 1 ст.2 ф.кл., дислипидемия, сахарный диабет 2 типа. Пациент не получал антигиперлипидемическую терапию и не придерживался антигиперхолестеринемической диеты. Согласно результатам предоперационного нейропсихологического тестирования балл по шкале МоСА составил 16 баллов, по шкале FAB 9 баллов. Индекс коморбидности Чарлсон составил 6 баллов (возраст 70-79 лет - 3 балла; сахарный диабет без повреждения органов-мишеней, контролируемый диетой - 0 балла; наличие солидной опухоли без признаков метастазирования - 2 балла; когнитивные нарушения, соответствующие степени деменции - 1 балл). Максимальное систолическое артериальное давление в интраоперационном периоде составило 130 мм рт. ст.
Индивидуальный расчет риска послеоперационной мозговой дисфункции:
А - 69,03%.
На вторые сутки после хирургического лечения у пациента появились признаки симптоматического делирия раннего послеоперационного периода, сохранявшиеся в течение 1 суток, а при динамическом тестировании в послеоперационном периоде отмечалось снижения до 12 баллов по шкале МоСА и 8 баллов по шкале FAB. Таким образом, у пациента развились два клинических типа послеоперационной мозговой дисфункции - симптоматический делирий раннего послеоперационного периода и отсроченные когнитивные нарушения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения риска развития отсроченных когнитивных нарушений после хирургических операций по поводу злокачественных новообразований груди и живота | 2021 |
|
RU2776232C1 |
| Способ прогнозирования послеоперационного делирия у детей при оперативной коррекции септальных врождённых пороков сердца в условиях искусственного кровообращения | 2023 |
|
RU2815626C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПОСЛЕОПЕРАЦИОННОГО ДЕЛИРИЯ У ПАЦИЕНТОВ ПОЖИЛОГО ВОЗРАСТА ПОСЛЕ ТОРАКАЛЬНЫХ ОПЕРАЦИЙ | 2019 |
|
RU2727745C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОСЛОЖНЕНИЙ ПОСЛЕ ОПЕРАЦИЙ ШУНТИРОВАНИЯ КОРОНАРНЫХ АРТЕРИЙ В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ | 2013 |
|
RU2536279C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ОСТРОГО ПОЧЕЧНОГО ПОВРЕЖДЕНИЯ ПОСЛЕ ОТКРЫТОЙ РЕКОНСТРУКЦИИ БРЮШНОГО ОТДЕЛА АОРТЫ ПО ПОВОДУ АНЕВРИЗМЫ | 2024 |
|
RU2833779C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОСЛОЖНЕНИЙ В РАННЕМ ПЕРИОДЕ ПОСЛЕ ОПЕРАЦИЙ ШУНТИРОВАНИЯ КОРОНАРНЫХ АРТЕРИЙ В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ | 2013 |
|
RU2536278C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПОЛИОРГАННОЙ НЕДОСТАТОЧНОСТИ У КАРДИОХИРУРГИЧЕСКИХ БОЛЬНЫХ | 2010 |
|
RU2422092C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПОСЛЕОПЕРАЦИОННЫХ СЕРДЕЧНО-СОСУДИСТЫХ ОСЛОЖНЕНИЙ ЛАПАРОСКОПИЧЕСКИХ ОПЕРАЦИЙ ПРИ МЕТАСТАТИЧЕСКОМ РАКЕ ТОЛСТОЙ КИШКИ | 2017 |
|
RU2663078C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ СИНДРОМА ПОЛИОРГАННОЙ НЕДОСТАТОЧНОСТИ У ПАЦИЕНТОВ ПОСЛЕ КОРОНАРНОГО ШУНТИРОВАНИЯ | 2017 |
|
RU2641033C1 |
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ ПЕРИОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ У БОЛЬНЫХ ПОЖИЛОГО ВОЗРАСТА, ИМЕЮЩИХ РАК ЛЕГКИХ | 2023 |
|
RU2814747C1 |
Изобретение относится к медицине, а именно к оперативной онкологиии. Определяют прогностически ценные факторы, а именно - возраст старше 75 лет (А) - для которого вероятность развития послеоперационной мозговой дисфункции равна 69,03%; - максимальное систолическое артериальное давление интраоперационно более 150 мм рт.ст. (В) - для которого вероятность развития послеоперационной мозговой дисфункции равна 70,76%; - соблюдение антигиперхолестеринемической диеты (С) - для которого вероятность развития послеоперационной мозговой дисфункции равна 1,11% - протективный фактор. Затем определяют вероятность риска развития послеоперационной мозговой дисфункции при сочетании вышеуказанных факторов, а именно: при сочетании фактора А+С - 15,33%; при сочетании фактора В+С - 16,43%; при сочетании факторов А+В+С - 75,98%; при сочетании фактора А+В - 97,5%. На заключительном этапе проводят стратификацию пациентов по группам «низкого» и «высокого» рисков. При этом к группе «низкого» риска относят пациентов с вероятностью риска развития послеоперационной мозговой дисфункции менее 20%, а к группе «высокого» риска относят пациентов с вероятностью риска развития послеоперационной мозговой дисфункции более 20%. Способ позволяет более точно определить риск развития послеоперационной мозговой дисфункции за счет учета всех возможных комбинаций факторов риска. 1 табл., 1 пр.
Способ определения риска развития послеоперационной мозговой дисфункции, отличающийся тем, что определяют прогностически ценные факторы, а именно
- возраст старше 75 лет (А) - для которого вероятность развития послеоперационной мозговой дисфункции равна 69,03%;
- максимальное систолическое артериальное давление интраоперационно более 150 мм рт.ст. (В) - для которого вероятность развития послеоперационной мозговой дисфункции равна 70,76%;
- соблюдение антигиперхолестеринемической диеты (С) - для которого вероятность развития послеоперационной мозговой дисфункции равна 1,11% - протективный фактор,
затем по формуле определяют вероятность риска развития послеоперационной мозговой дисфункции при сочетании вышеуказанных факторов, а именно
при сочетании фактора А+С - 15,33%;
при сочетании фактора В+С - 16,43%;
при сочетании факторов А+В+С - 75,98%;
при сочетании фактора А+В - 97,5%;
на заключительном этапе проводят стратификацию пациентов по группам «низкого» и «высокого» рисков, при этом к группе «низкого» риска относят пациентов с вероятностью риска развития послеоперационной мозговой дисфункции менее 20%, а к группе «высокого» риска относят пациентов с вероятностью риска развития послеоперационной мозговой дисфункции более 20%.
| G | |||
| WINTERER et al | |||
| Personalized risk prediction of postoperative cognitive impairment - ationale for the EU-funded Bio Cog project | |||
| European Psychiatry | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВАРИАНТА ТЕЧЕНИЯ МИНИМАЛЬНОЙ МОЗГОВОЙ ДИСФУНКЦИИ | 2012 |
|
RU2489965C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПОСЛЕОПЕРАЦИОННЫХ СЕРДЕЧНО-СОСУДИСТЫХ ОСЛОЖНЕНИЙ ЛАПАРОСКОПИЧЕСКИХ ОПЕРАЦИЙ ПРИ МЕТАСТАТИЧЕСКОМ РАКЕ ТОЛСТОЙ КИШКИ | 2017 |
|
RU2663078C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ У ОНКОЛОГИЧЕСКИХ БОЛЬНЫХ | 2008 |
|
RU2384297C1 |
| АНДРЕЕВ Р.В | |||
| Особенности послеоперационной мозговой дисфункции при операциях на клапанах | |||
Авторы
Даты
2022-05-23—Публикация
2021-07-30—Подача