[0001] Данная заявка испрашивает приоритет на основании предварительной патентной заявки США №62/191990 под названием «Композиции плинабулина», поданной 13 июля 2015 г., содержание которой полностью включено в настоящий документ посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
Область техники
[0002] Настоящее изобретение относится к областям химии и медицины. Более конкретно, настоящее изобретение относится к формам и композициям плинабулина и их получению. Описание предшествующего уровня техники
[0003] Плинабулин представляет собой синтетический аналог дикетопиперазин фенилахистин (халимид), обнаруженный в морских и наземных представителях рода Aspergillus. Плинабулин структурно отличается от колхицина и его комбретастатин-подобных аналогов (например, фосбретабулина) и связывается в сайте связывания колхицина на мономерах тубулина или рядом с ним. Ранее проведенные исследования показали, что плинабулин вызывал деполимеризацию тубулина в сосудистых эндотелиальных клетках и проницаемость монослоя при низких концентрациях по сравнению с колхицином, и что он вызывал апоптоз клеток лейкоза линии Jurkat. Исследования плинабулина в монотерапии пациентов с распространенными злокачественными опухолями (раком легкого, предстательной железы и толстой кишки) показали благоприятный фармакокинетический, фармакодинамический профили и профиль безопасности.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0004] Некоторые варианты осуществления относятся к моногидрату плинабулина.
[0005] Другие варианты осуществления относятся к моногидрату плинабулина в кристаллической форме.
[0006] Некоторые варианты осуществления относятся к композиции плинабулина, содержащей более 90 масс. % плинабулина относительно общей массы композиции.
[0007] Другие варианты осуществления относятся к композиции плинабулина, содержащей более 99 масс. % плинабулина относительно общей массы молекул в композиции, отличных от молекул воды, диметилформамида, этанола, этилацетата, метанола, толуола и уксусной кислоты.
[0008] Некоторые варианты осуществления относятся к композиции плинабулина, содержащей плинабулин и не более приблизительно 1,9 масс. % примесей, относительно общей массы композиции за исключением воды.
[0009] Другие варианты осуществления относятся к композиции плинабулина, содержащей плинабулин и не более приблизительно 1 масс. % примесей, отличных от молекул растворителя, относительно общей массы молекул в композиции, отличных от молекул растворителя.
[0010] Некоторые варианты осуществления относятся к композиции плинабулина, содержащей плинабулин и не более приблизительно 1 масс. % примесей, определенных анализом методом ВЭЖХ.
[0011] Некоторые варианты осуществления относятся к способу получения моногидрата плинабулина или композиции плинабулина.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
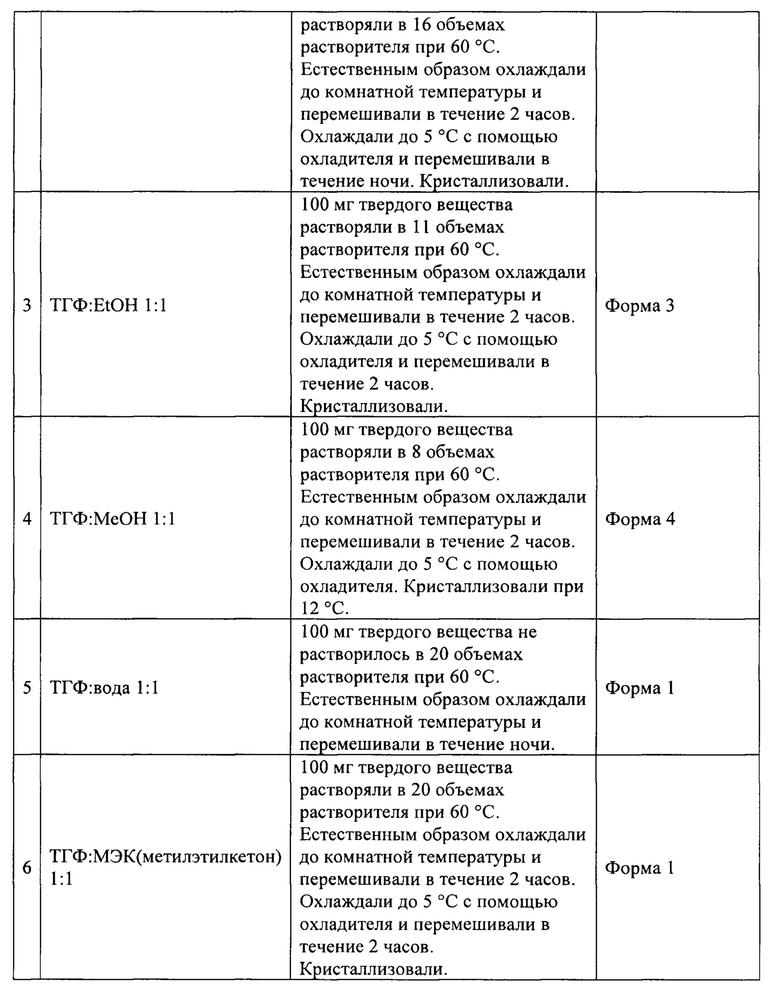
[0012] ФИГ. 1 представляет собой спектр рентгеновской порошковой дифракции (XRPD) кристаллической формы моногидрата плинабулина.
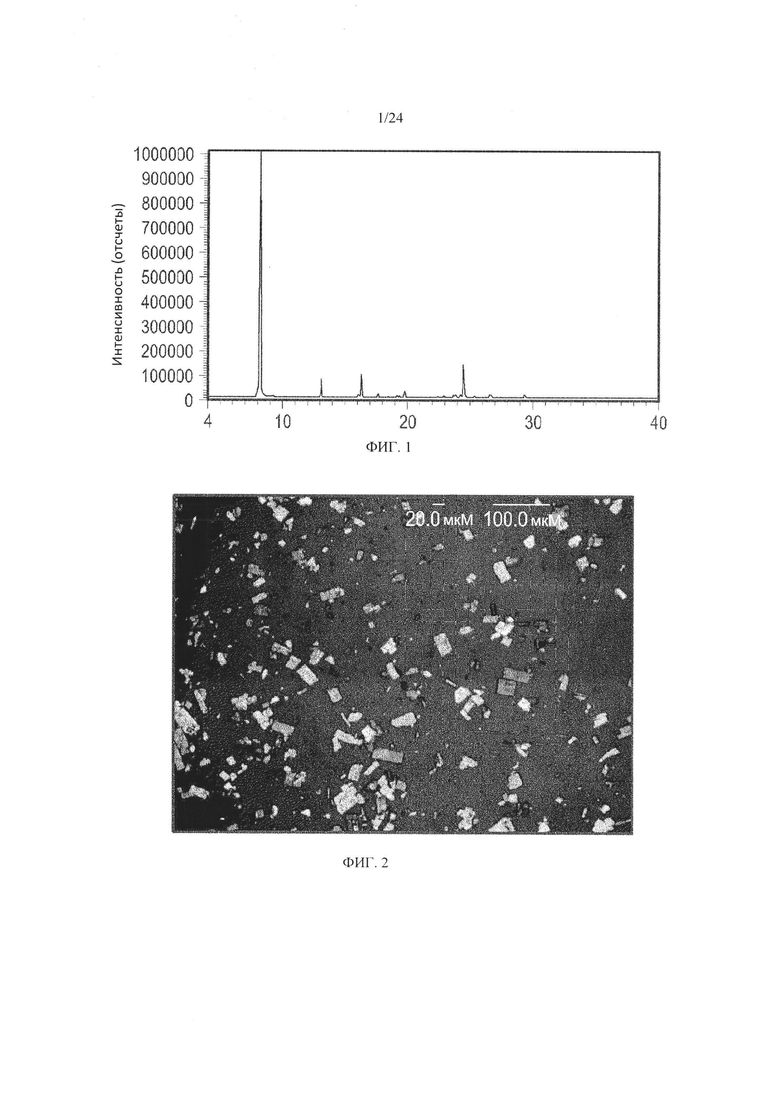
[0013] ФИГ. 2 демонстрирует снимок образца, содержащего кристаллическую форму моногидрата плинабулина, полученный с помощью поляризационной микроскопии (PLM).
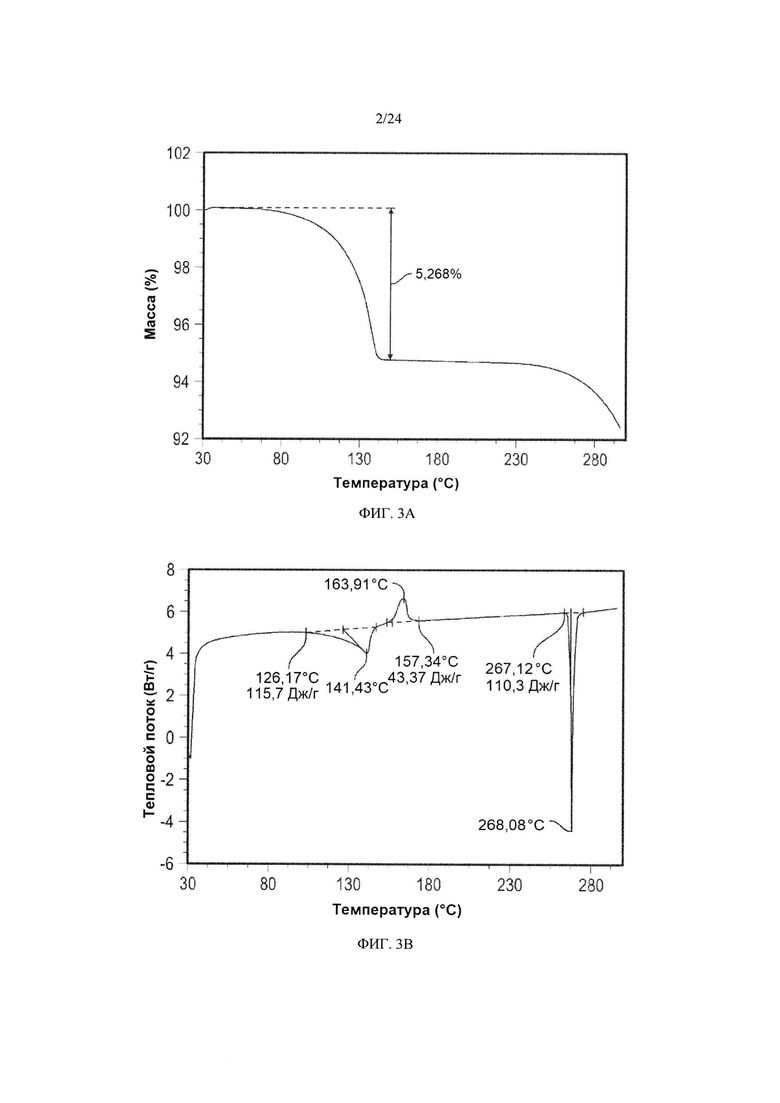
[0014] ФИГ. 3А демонстрирует термогравиметрический анализ (ТГА) кристаллической формы моногидрата плинабулина (форма 1); ФИГ. 3В демонстрирует
результаты анализа кристаллической формы моногидрата плинабулина (форма 1) методом цифровой сканирующей калориметрии (DSC); и ФИГ. 3С демонстрирует график изотермы динамической сорбции паров (DVS).
[0015] ФИГ. 4 представляет собой спектр XRPD кристаллической формы 2.
[0016] ФИГ. 5 демонстрирует снимок образца, содержащего кристаллическую форму 2, полученный с помощью PLM.
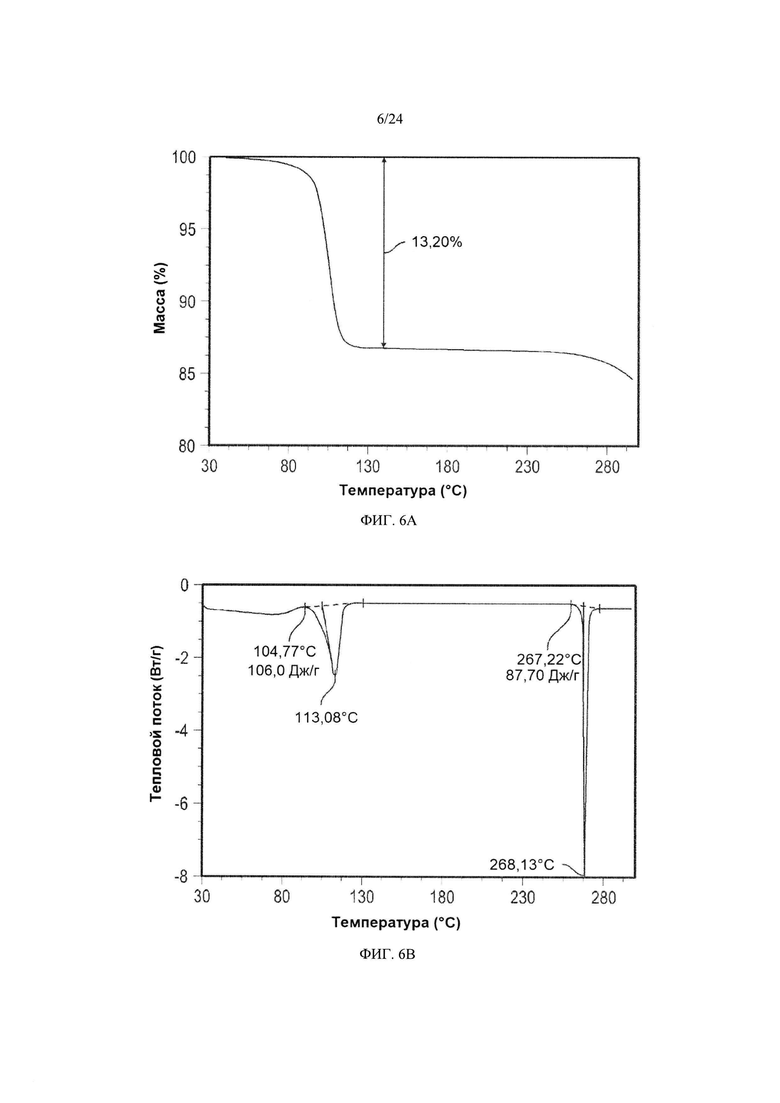
[0017] ФИГ. 6А демонстрирует результаты ТГА кристаллической формы 2, и ФИГ. 6В демонстрирует результаты анализа кристаллической формы 2 методом DSC.
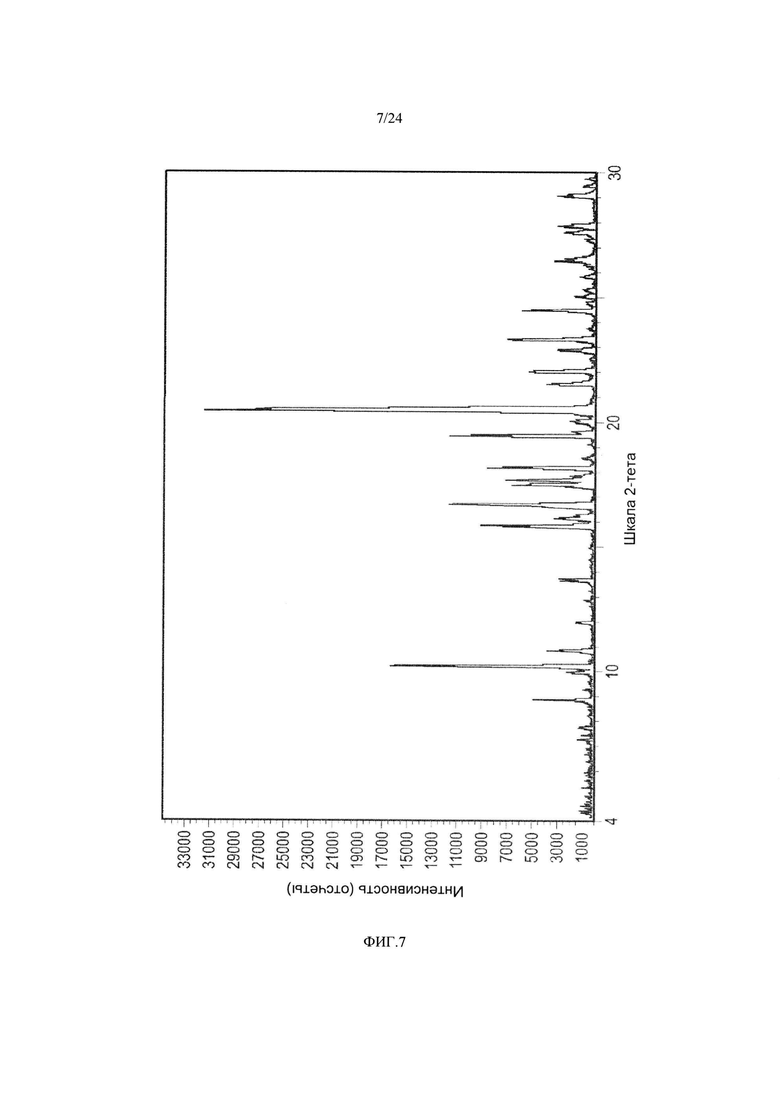
[0018] ФИГ. 7 представляет собой спектр XRPD кристаллической формы 3.
[0019] ФИГ. 8 демонстрирует снимок образца, содержащего кристаллическую форму 3, полученный с помощью PLM.
[0020] ФИГ. 9A демонстрирует результаты ТГА кристаллической формы 3; и ФИГ. 9В демонстрирует результаты анализа кристаллической формы 3 методом DSC.
[0021] ФИГ. 10 представляет собой спектр XRPD кристаллической формы 4.
[0022] ФИГ. 11 демонстрирует снимок образца, содержащего кристаллическую форму 4, полученный с помощью PLM.
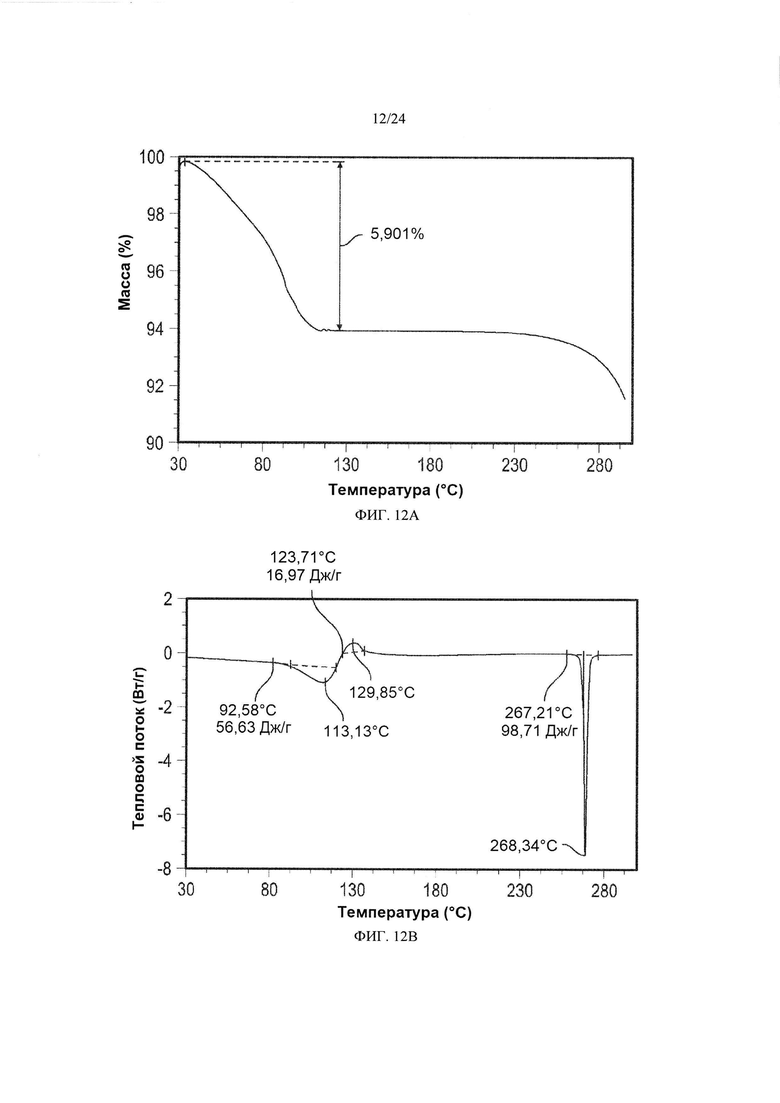
[0023] ФИГ. 12А демонстрирует результаты ТГА кристаллической формы 4; и ФИГ. 12В демонстрирует результаты анализа кристаллической формы 4 методом цифровой сканирующей калориметрии (DSC).
[0024] ФИГ. 13 представляет собой спектр XRPD кристаллической формы 5.
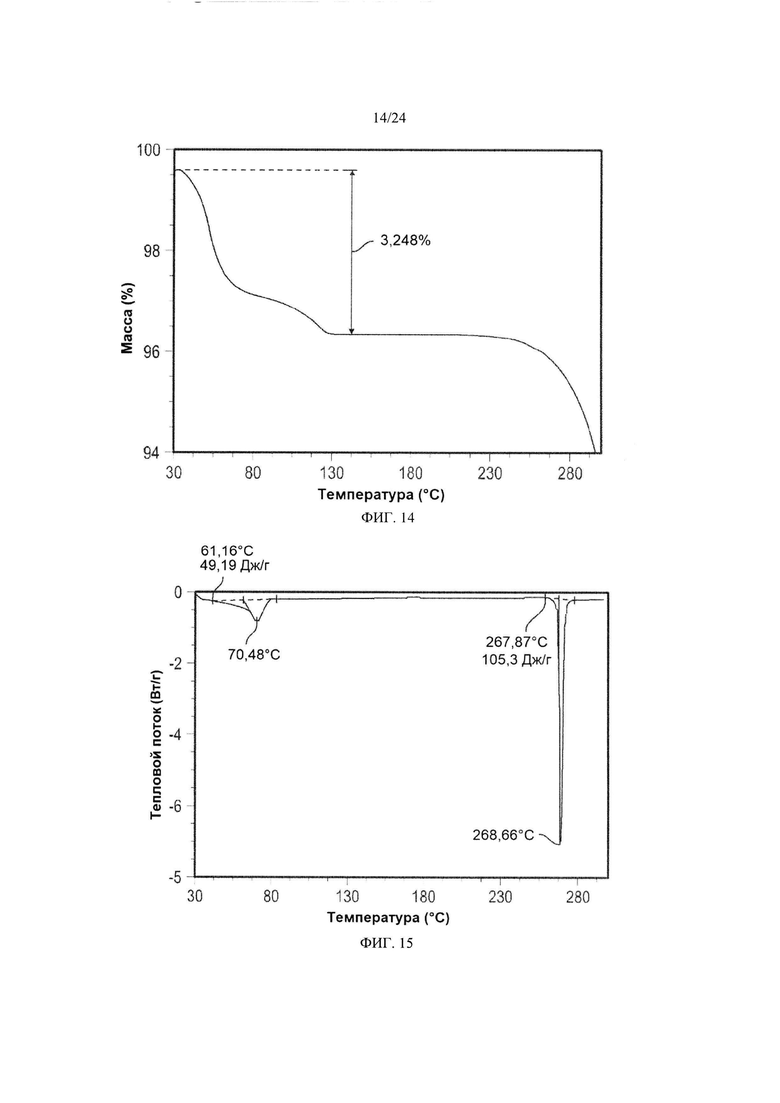
[0025] ФИГ. 14 демонстрирует результаты ТГА кристаллической формы 5
[0026] ФИГ. 15 демонстрирует результаты анализа кристаллической формы 5 методом DSC.
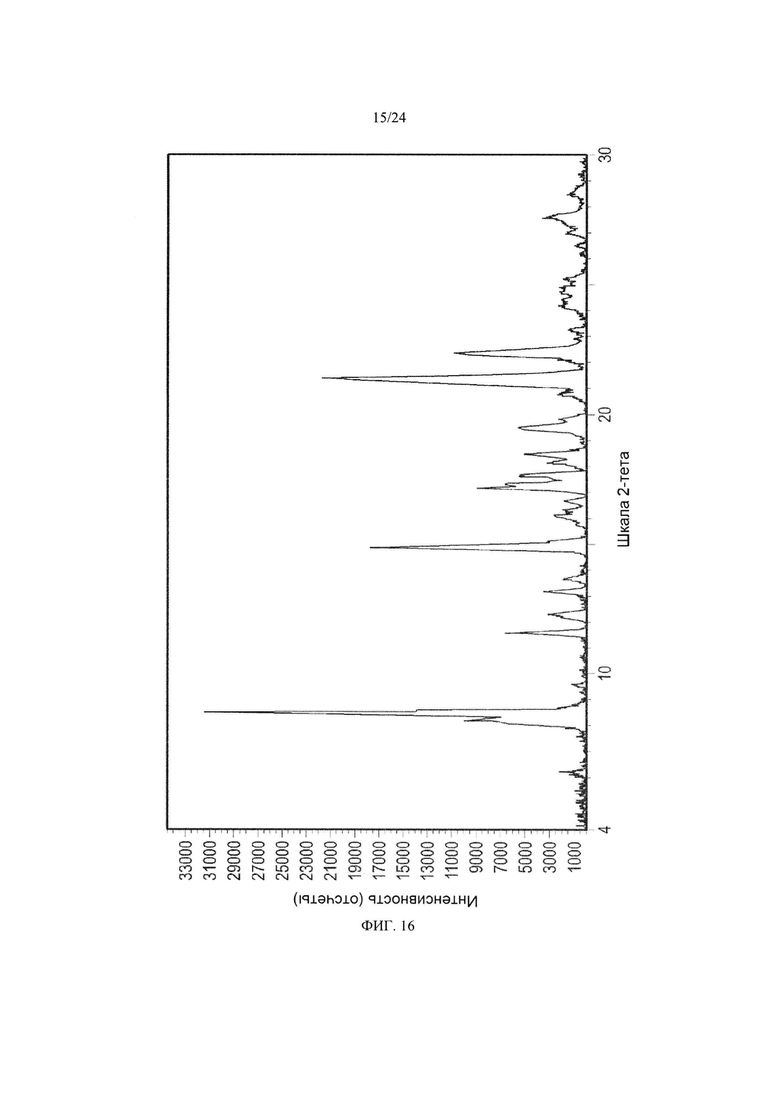
[0027] ФИГ. 16 представляет собой спектр XRPD кристаллической формы 6.
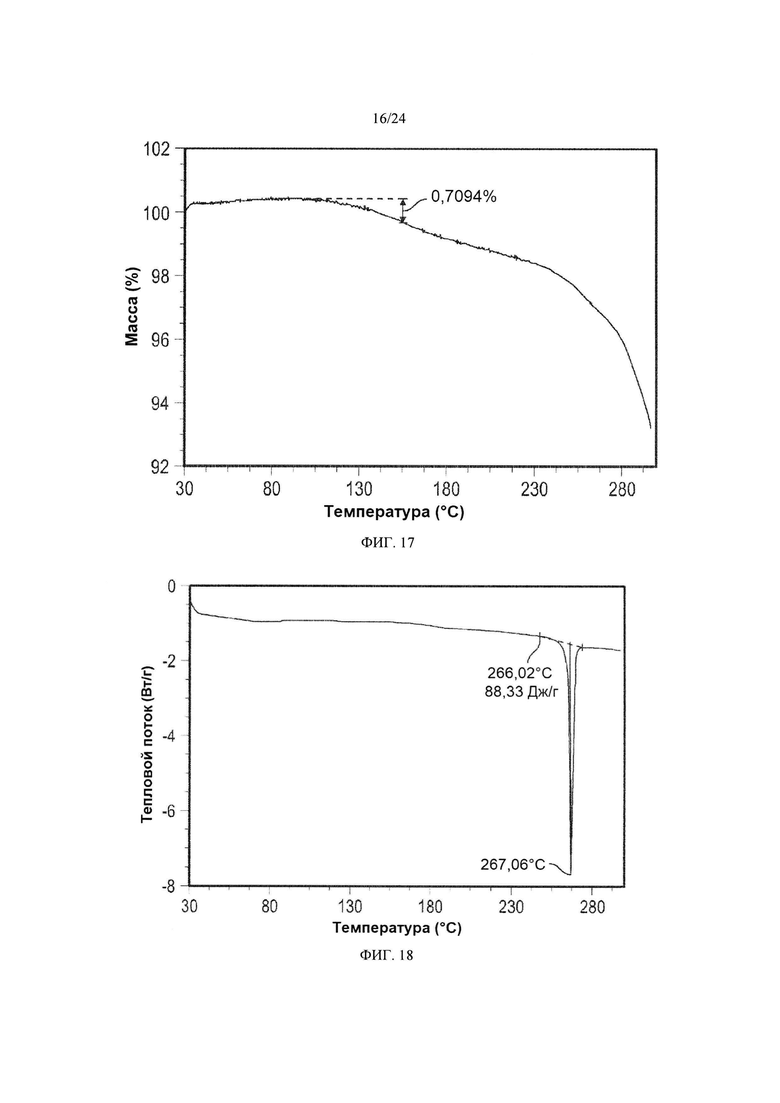
[0028] ФИГ. 17 демонстрирует результаты ТГА кристаллической формы 6
[0029] ФИГ. 18 демонстрирует результаты анализа кристаллической формы 6 методом DSC.
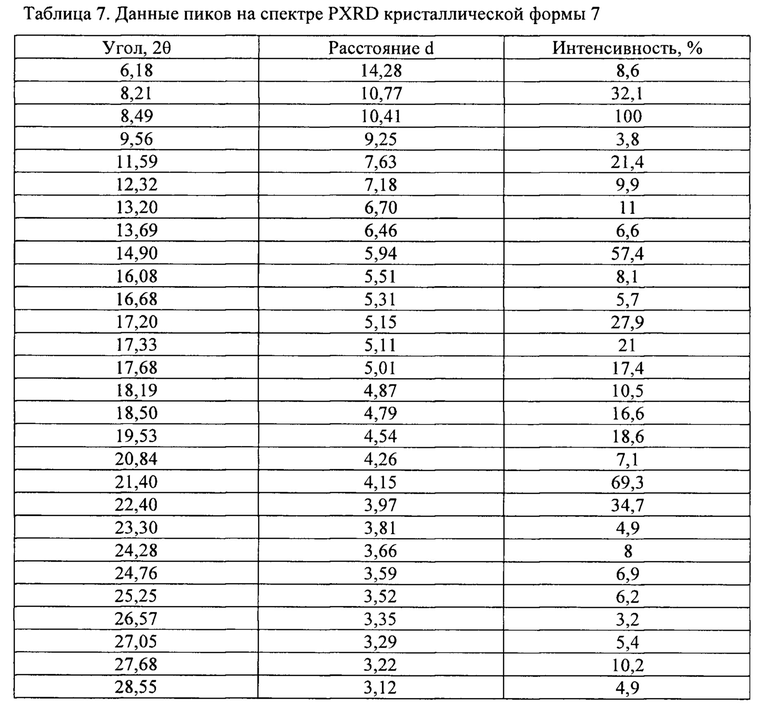
[0030] ФИГ. 19 представляет собой спектр XRPD кристаллической формы 7.
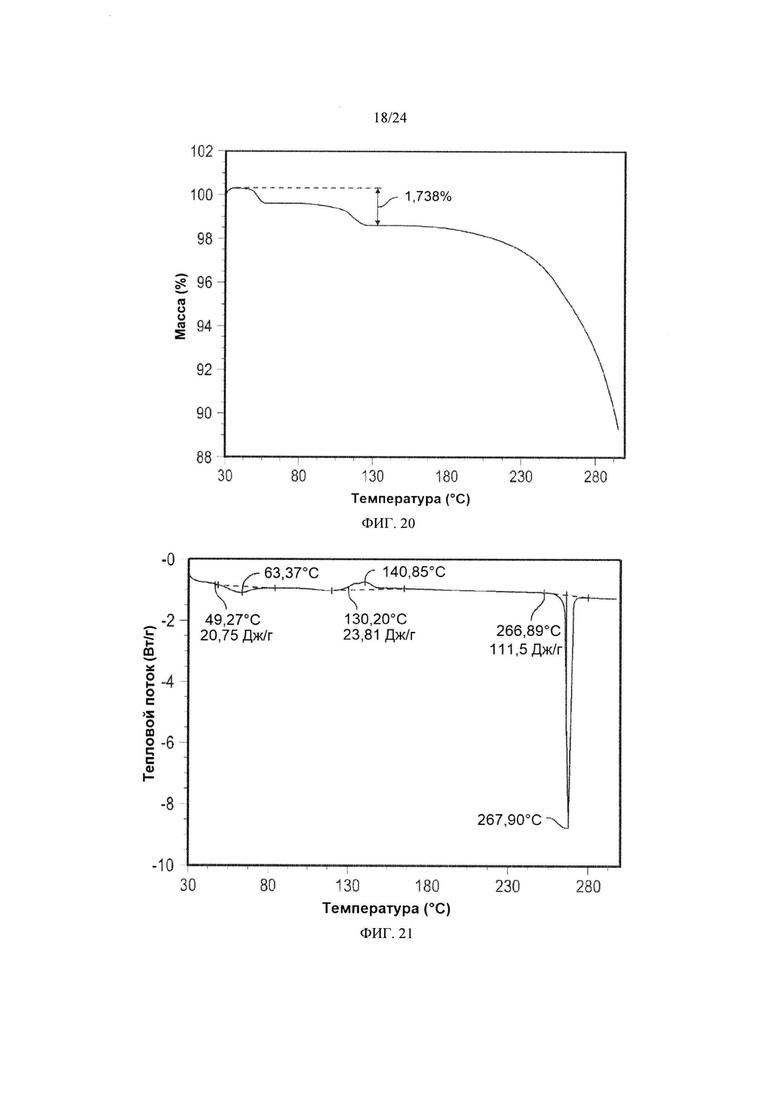
[0031] ФИГ. 20 демонстрирует результаты ТГА кристаллической формы 7
[0032] ФИГ. 21 демонстрирует результаты анализа кристаллической формы 7 методом DSC.
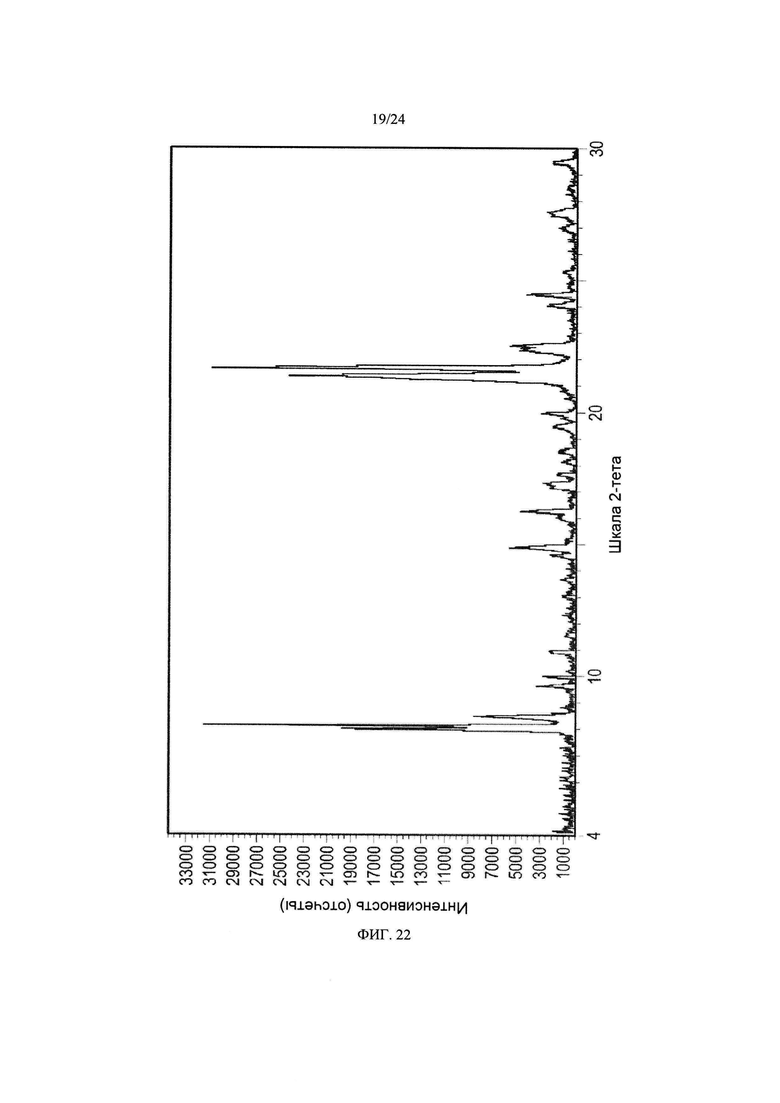
[0033] ФИГ. 22 представляет собой спектр XRPD кристаллической формы 8.
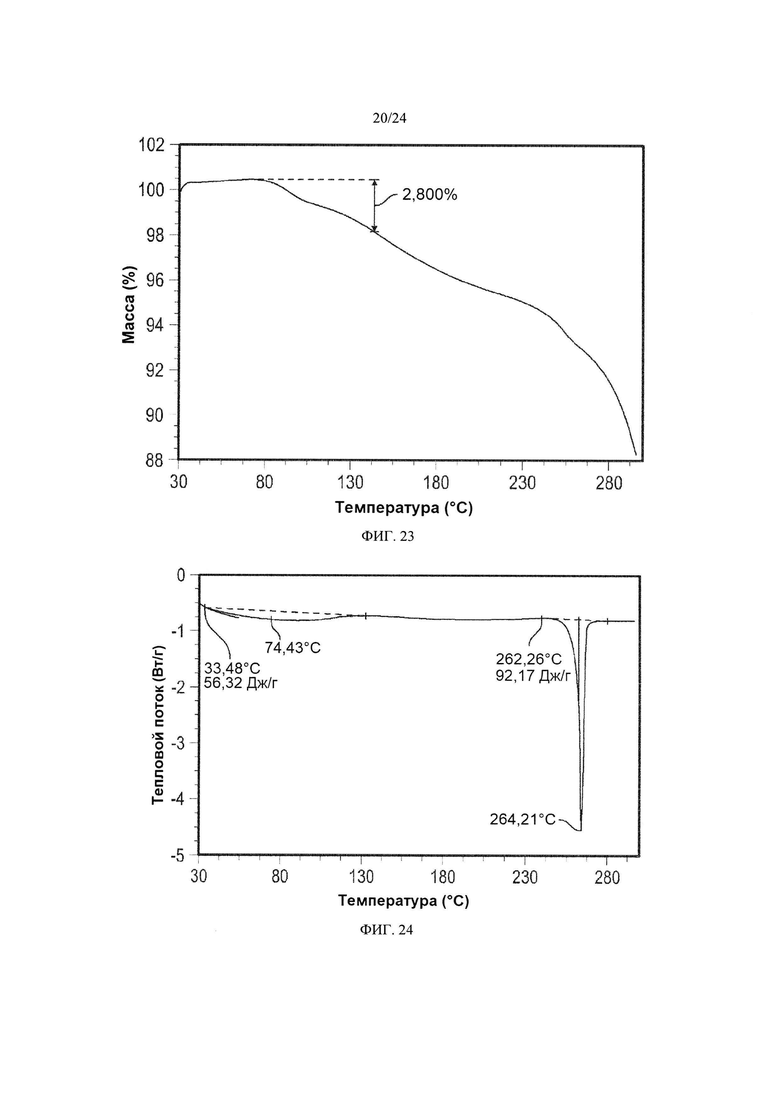
[0034] ФИГ. 23 демонстрирует результаты ТГА кристаллической формы 8.
[0035] ФИГ. 24 демонстрирует результаты анализа кристаллической формы 8 методом DSC.
[0036] ФИГ. 25 представляет собой спектр XRPD кристаллической формы 9.
[0037] ФИГ. 26 демонстрирует результаты ТГА кристаллической формы 9
[0038] ФИГ. 27 демонстрирует результаты анализа кристаллической формы 9 методом DSC.
[0039] ФИГ. 28 демонстрирует взаимное превращение полиморфных форм плинабулина.
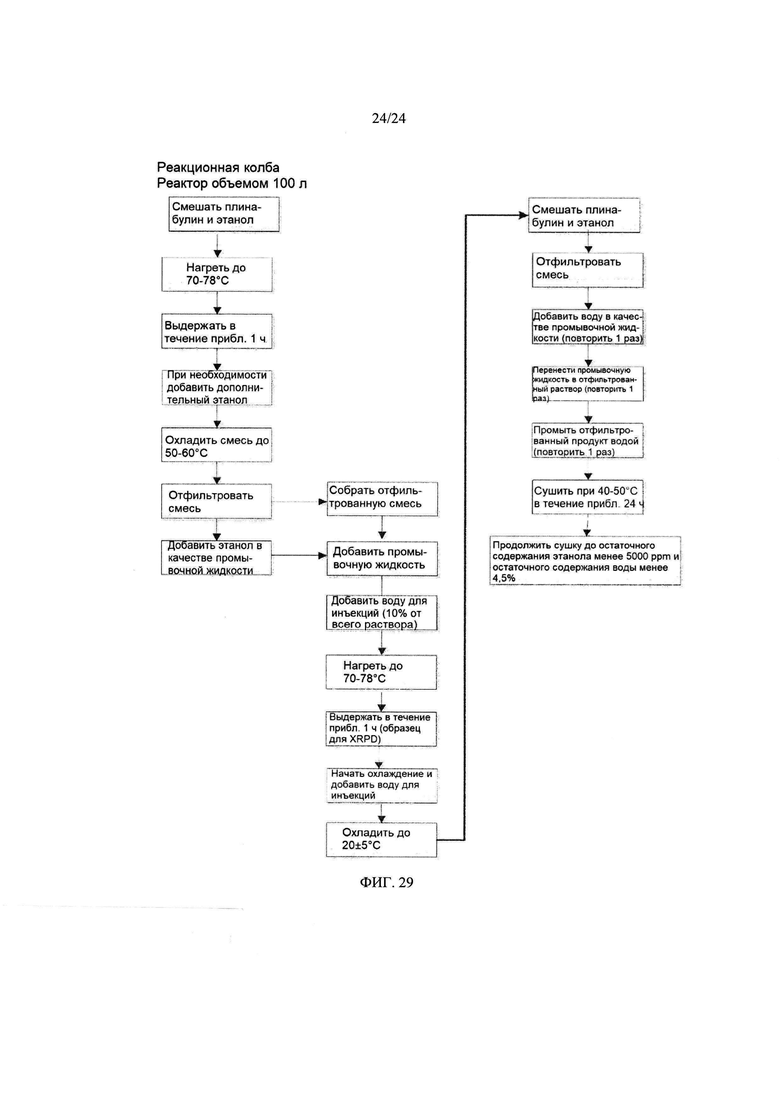
[0040] ФИГ. 29 представляет собой блок-схему получения композиции моногидрата плинабулина.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНОГО ВАРИАНТА ОСУЩЕСТВЛЕНИЯ
[0041] Плинабулин, (3Z,6Z)-3-бензилиден-6-{[5-(2-метил-2-пропанил)-1Н-имидазол-4-ил]метилен}-2,5-пиперазиндион, представляет собой синтетический аналог природного соединения фенилахистина. Плинабулин может без труда быть получен способами и методиками, раскрытыми в патентах США №№7064201 и 7919497, полностью включенных в настоящий документ посредством ссылки. Некоторые варианты осуществления относятся к полиморфам и сольватам (например, гидратам) плинабулина и содержащим их фармацевтическим композициям. Некоторые варианты осуществления включают способы получения и способы лечения. В частности, некоторые варианты осуществления относятся к моногидрату плинабулина.
Моногидрат плинабулина
[0042] Моногидрат плинабулина (форма 1) является стабильной кристаллической формой плинабулина. Спектр рентгеновской порошковой дифракции (PXRD) моногидрата плинабулина (форма 1) является по существу таким же, как показано на ФИГ. 1, соответствующие данные пиков которого представлены в табулированной форме в таблице 1.
[0043] Таблица 1. Данные пиков на спектре рентгеновской порошковой дифракции (PXRD) моногидрата плинабулина (форма 1)


[0044] В некоторых вариантах осуществления моногидрат пинабулина (форма 1), описанный в настоящем документе, включает кристаллическую форму, характеризующуюся рентгеновской порошковой дифрактограммой, содержащей по меньшей мере три характеристических пика, выбранных из группы, состоящей из пиков при приблизительно 8,1°, 13,1°, 16,3°, 23,9°, 24,2°, 24,5° и 26,6° 2θ. В некоторых вариантах осуществления моногидрат пинабулина (форма 1), описанный в настоящем документе, включает кристаллическую форму, характеризующуюся рентгеновской порошковой дифрактограммой, содержащей по меньшей мере пики при приблизительно 8,1°, 13,1°, 16,3°, 23,9°, 24,2°, 24,5° и 26,6° 2θ. В некоторых вариантах осуществления моногидрат пинабулина (форма 1), описанный в настоящем документе, включает кристаллическую форму, характеризующуюся рентгеновской порошковой дифрактограммой, содержащей по меньшей мере пики при приблизительно 8,1°, 13,1°, 16,1°, 16,3°, 19,8°, 22,9°, 23,9°, 24,2°, 24,5°, 26,6° и 29,3° 2θ.
[0045] Как хорошо известно в данной области техники, ввиду вариаций экспериментальных данных при измерении спектров рентгеновской порошковой дифракции на различных приборах положения пиков считаются равными, если величины два тета (2θ) совпадают с точностью до 0,2° (т.е., ± 0,2°). Например, в Фармакопее США указано, что если значения углов 10 наиболее сильных дифракционных пиков совпадают с точностью до ± 0,2° со значениями образца сравнения, и относительные интенсивности пиков не различаются более чем на 20%, то идентичность подтверждена. Соответственно, положения пиков, отличающиеся не более чем на 0,2° от положений, приведенных в настоящем документе, считаются идентичными. Если не указано иное, все углы дифракции рентгеновских лучей, приведенные в настоящем документе, основаны на медном источнике K-альфа.
[0046] ФИГ. 3В демонстрирует результаты анализа кристаллической формы моногидрата плинабулина (форма 1) методом цифровой сканирующей калориметрии (DSC). Как показано на ФИГ. 3В, кристаллическая форма моногидрата плинабулина (Форма 1) имеет температуру плавления, составляющую приблизительно 267°C; кристаллическая форма моногидрата плинабулина (форма 1) имеет термограмму дифференциальной сканирующей калориметрии с эндотермическими пиками при приблизительно 141°С и приблизительно 267°C.
[0047] Кристаллическая форма моногидрата плинабулина (форма 1) более стабильна, чем другие полиморфные формы. Моногидрат плинабулина (форма 1) может оставаться стабильным в ходе тестов DVS и сушки по сравнению с другими полиморфными формами, которые в ходе тестов могут демонстрировать изменение массы и разложение. Композиция плинабулина
[0048] Некоторые варианты осуществления относятся к композиции плинабулина, включающей более чем приблизительно 50 масс. % моногидрата плинабулина (форма 1), описанного в настоящем документе, относительно общей массы композиции. В некоторых вариантах осуществления композиция плинабулина включает более чем приблизительно 75 масс. % моногидрата плинабулина (форма 1), описанного в настоящем документе. В некоторых вариантах осуществления композиция плинабулина включает более чем приблизительно 90 масс. % моногидрата плинабулина, описанного в настоящем документе. В некоторых вариантах осуществления композиция плинабулина включает более чем приблизительно 95 масс. %) моногидрата плинабулина, описанного в настоящем документе. В некоторых вариантах осуществления осуществления композиция плинабулина включает более чем приблизительно 98 масс. % моногидрата плинабулина, описанного в настоящем документе. В некоторых вариантах осуществления композиция плинабулина включает более чем приблизительно 99 масс. % моногидрата плинабулина, описанного в настоящем документе. В некоторых вариантах осуществления композиция плинабулина включает моногидрат плинабулина, описанный в настоящем документе, в количестве от приблизительно 50% до приблизительно 99%, от приблизительно 60% до приблизительно 99%, от приблизительно 70% до приблизительно 99%, от приблизительно 80% до приблизительно 99%, от приблизительно 90% до приблизительно 99%, от приблизительно 95% до приблизительно 99%, or от приблизительно 97,5% до приблизительно 99% относительно общей массы композиции. Остальная часть композиции плинабулина может представлять собой другие формы плинабулина и/или другие химические соединения.
[0049] Некоторые варианты осуществления относятся к композиции плинабулина, имеющей высокую чистоту. В частности, некоторые варианты осуществления относятся к композиции плинабулина, содержащей более чем приблизительно 90 масс. % плинабулина относительно общей массы композиции. В некоторых вариантах осуществления композиция плинабулина включает более чем приблизительно 92% соединения плинабулина. В некоторых вариантах осуществления композиция плинабулина включает более чем 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91,%, 92%, 93%, 94%, 95%, 96%, 96.5%, 96%, 98%, 99% или 99,6% соединения плинабулина. В некоторых вариантах осуществления композиция плинабулина включает более чем приблизительно 99 масс. % плинабулина относительно общей массы молекул в композиции, отличных от молекул растворителя. В некоторых вариантах осуществления композиция плинабулина включает более чем приблизительно 96 масс. %, 97 масс. %, 98 масс. %, 99 масс. % или 99,6 масс. % плинабулина относительно общей массы молекул в композиции, отличных от молекул растворителя. В некоторых вариантах осуществления растворитель может представлять собой воду, диметилформамид, этанол, этилацетат, метанол, толуол и уксусную кислоту. В некоторых вариантах осуществления плинабулин в композиции высокой чистоты присутствует, по меньшей мере частично, в форме моногидрата плинабулина, как описано выше.
[0050] В некоторых вариантах осуществления композиция плинабулина включает более чем приблизительно 99 масс. % плинабулина относительно общей массы молекул в композиции, отличных от молекул воды, диметилформамида, этанола, этилацетата, метанола, толуола и уксусной кислоты. В некоторых вариантах осуществления композиция плинабулина включает более чем приблизительно 80 масс. %, 85 масс. %), 86 масс. %, 87 масс. %, 88 масс. %, 89 масс. %, 90 масс. %, 91, масс. %, 92 масс. %, 93 масс. %, 94 масс. %, 95 масс. %, 96 масс. %, 96.5 масс. %, 96 масс. %, 98 масс. %, 99 масс. % или 99,6 масс. % плинабулина относительно общей массы молекул в композиции, отличных от молекул воды, диметилформамида, этанола, этилацетата, метанола, толуола и уксусной кислоты. В некоторых вариантах осуществления плинабулин в композиции присутствует, по меньшей мере частично, в форме моногидрата плинабулина, как описано выше.
[0051] В некоторых вариантах осуществления композиция плинабулина включает более чем приблизительно 99 масс. % плинабулина, при определении анализом методом ВЭЖХ. В некоторых вариантах осуществления композиция плинабулина включает более чем приблизительно 80 масс. %, 85 масс. %, 86 масс. %, 87 масс. %, 88 масс. %, 89 масс. %, 90 масс. %, 91, масс. %, 92 масс. %, 93 масс. %, 94 масс. %, 95 масс. %), 96 масс. %, 96.5 масс. %, 96 масс. %, 98 масс. %, 99 масс. % или 99,6 масс. % плинабулина, при определении анализом методом ВЭЖХ. В некоторых вариантах осуществления плинабулин в композиции присутствует, по меньшей мере частично, в форме моногидрата плинабулина, как описано выше.
[0052] Некоторые варианты осуществления относятся к композиции плинабулина с низким содержанием примесей. Термин «примесь» при использовании в настоящем документе относится к одному или более компонентам композиции, отличным от плинабулина и воды. В некоторых вариантах осуществления примесь может включать одно или более химических соединений, вводимых в процессе синтеза плинабулина. В некоторых вариантах осуществления примесь может включать диметилформамид, этанол, этилацетат, метанол, толуол, уксусную кислоту и другой остаточный растворитель.
[0053] В некоторых вариантах осуществления композиция плинабулина включает не более приблизительно 1 масс. % примесей относительно общей массы композиции. В некоторых вариантах осуществления композиция плинабулина включает не более приблизительно 15 масс. %, 14 масс. %, 13 масс. %, 12 масс. %, 11 масс. %, 10 масс. %, 9 масс. %, 8 масс. %, 7 масс. %, 6 масс. %, 5 масс. %, 4 масс. %, 3 масс. %, 2 масс. %, 1 масс. %, 0,97 масс. %, 0,9 масс. %, 0,8 масс. %, 0,6 масс. %, 0,4 масс. % или 0,2 масс. % примесей относительно общей массы композиции. В некоторых вариантах осуществления композиция плинабулина включает не более приблизительно 1 масс. % примесей относительно общей массы молекул в композиции, отличных от молекул растворителя. В некоторых вариантах осуществления композиция плинабулина включает не более приблизительно 15 масс. %, 14 масс. %, 13 масс. %, 12 масс. %, 11 масс. %, 10 масс. %, 9 масс. %, 8 масс. %, 7 масс. %, 6 масс. %, 5 масс. %, 4 масс. %, 3 масс. %, 2 масс. %, 1 масс. %, 0,97 масс. %, 0,9 масс. %, 0,8 масс. %, 0,6 масс. %, 0,4 масс. % или 0,2 масс. % примесей относительно общей массы молекул в композиции, отличных от молекул растворителя.
[0054] В некоторых вариантах осуществления композиция плинабулина включает не более приблизительно 1,9 масс. % примесей относительно общей массы композиции за исключением воды. В некоторых вариантах осуществления композиция плинабулина включает не более приблизительно 15 масс. %, 14 масс. %, 13 масс. %, 12 масс. %, 11 масс. %, 10 масс. %, 9 масс. %, 8 масс. %, 7 масс. %, 6 масс. %, 5 масс. %, 4 масс. %, 3 масс. %, 2 масс. %, 1 масс. %, 0,97 масс. %, 0,9 масс. %, 0,8 масс. %, 0,6 масс. %, 0,4 масс. % или 0,2 масс. % примесей относительно общей массы композиции за исключением воды. В некоторых вариантах осуществления композиция плинабулина включает не более приблизительно 1 масс. % примесей относительно общей массы молекул в композиции, отличных от молекул растворителя, за исключением воды. В некоторых вариантах осуществления композиция плинабулина включает не более приблизительно 15 масс. %, 14 масс. %, 13 масс. %, 12 масс. %, 11 масс. %, 10 масс. %, 9 масс. %, 8 масс. %, 7 масс. %, 6 масс. %, 5 масс. %, 4 масс. %, 3 масс. %, 2 масс. %, 1 масс. %, 0,97 масс. %, 0,9 масс. %, 0,8 масс. %, 0,6 масс. %, 0,4 масс. % или 0,2 масс. % примесей, относительно общей массы молекул в композиции, отличных от молекул растворителя, за исключением воды.
[0055] В некоторых вариантах осуществления композиция плинабулина включает не более приблизительно 0,9 масс. % примесей, отличных от диметилформамида, этанола, этилацетата, метанола, толуола и уксусной кислоты, относительно общей массы молекул в композиции, отличных от молекул воды, диметилформамида, этанола, этилацетата, метанола, толуола и уксусной кислоты. В некоторых вариантах осуществления композиция плинабулина включает не более приблизительно 5 масс. %, 4 масс. %, 3 масс. %, 2 масс. %, 1 масс. %, 0,97 масс. %, 0,9 масс. %, 0,8 масс. %, 0,6 масс. %, 0,4 масс. % или 0,2 масс. % примесей, отличных от диметилформамида, этанола, этилацетата, метанола, толуола и уксусной кислоты, относительно общей массы молекул в композиции, отличных от молекул воды, диметилформамида, этанола, этилацетата, метанола, толуола и уксусной кислоты.
[0056] В некоторых вариантах осуществления композиция плинабулина включает не более приблизительно 1 масс. % примесей при определении анализом методом ВЭЖХ. В некоторых вариантах осуществления композиция плинабулина включает не более приблизительно 5 масс. %, 4 масс. %, 3 масс. %, 2 масс. %, 1 масс. %, 0,97 масс. %, 0,9 масс. %, 0,8 масс. %, 0,6 масс. %, 0,4 масс. % или 0,2 масс. % примесей при определении анализом методом ВЭЖХ.
Способ получения
[0057] Некоторые варианты осуществления относятся к способу получения моногидрата плинабулина или композиции плинабулина, описанных в настоящем документе, включающему: смешивание плинабулина и первой системы растворителей с образованием первой смеси, нагрев первой смеси до температуры приблизительно от 50°C до 90°C и охлаждение первой смеси с образованием первого осадка.
[0058] В некоторых вариантах осуществления способ дополнительно включает фильтрацию перед охлаждением первой смеси. В некоторых вариантах осуществления способ дополнительно включает добавление воды к первой смеси перед нагревом.
[0059] В некоторых вариантах осуществления способ, описанный в настоящем документе, дополнительно включает отфильтровывание первого осадка. В некоторых вариантах осуществления способ, описанный в настоящем документе, дополнительно включает промывку первого осадка.
В некоторых вариантах осуществления первая система растворителей может представлять собой воду, спирт или смесь воды и спирта.
[0060] В некоторых вариантах осуществления спирт выбран из метанола, этанола, изопропилового спирта, трет-бутилового спирта и н-бутилового спирта; или их смеси.
[0061] В некоторых вариантах осуществления спирт представляет собой этанол.
В некоторых вариантах осуществления нагрев первой смеси включает кипячение первой смеси с обратным холодильником.
[0062] В некоторых вариантах осуществления первую смесь нагревают до температуры приблизительно от 70°C до 78°C. В некоторых вариантах осуществления первую смесь нагревают до температуры приблизительно от 60°C до 90°C. В некоторых вариантах осуществления первую смесь нагревают до температуры приблизительно от 60°C до 80°C. В некоторых вариантах осуществления первую смесь нагревают до температуры кипения этанола.
[0063] В некоторых вариантах осуществления способ, описанный в настоящем документе, дополнительно включает поддержание первой смеси при температуре кипения с обратным холодильником в течение приблизительно 1 часа перед охлаждением первой смеси.
В некоторых вариантах осуществления нагрев первой смеси включает нагрев первой смеси до по меньшей мере 65°C, и где охлаждение первой смеси включает охлаждение первой смеси до температуры приблизительно от 50°C до 60°C.
[0064] В некоторых вариантах осуществления охлаждение первой смеси включает добавление воды к первой смеси для образования первого осадка.
[0065] В некоторых вариантах осуществления охлаждение первой смеси включает перемешивание первой смеси в течение по меньшей мере 4 часов.
В некоторых вариантах осуществления способ, описанный в настоящем документе, дополнительно включает анализ первого осадка для определения композиции плинабулина в первом осадке.
[0066] В некоторых вариантах осуществления способ, описанный в настоящем документе, дополнительно включает смешивание первого осадка и второго растворителя с образованием второй смеси и нагрев второй смеси до температуры приблизительно от 50°C до 90°C; охлаждение второй смеси с образованием второго осадка; и отфильтровывание второго осадка и промывку второго осадка.
[0067] В некоторых вариантах осуществления второй растворитель представляет собой воду, спирт или смесь воды и спирта.
[0068] В некоторых вариантах осуществления спирт выбран из метанола, этанола, изопропилового спирта, трет-бутилового спирта и н-бутилового спирта; или их смеси. В некоторых вариантах осуществления спирт представляет собой этанол.
[0069] В некоторых вариантах осуществления нагрев второй смеси включает кипячение второй смеси с обратным холодильником.
[0070] В некоторых вариантах осуществления вторую смесь нагревают до температуры приблизительно от 70°C до 78°C.
[0071] В некоторых вариантах осуществления способ, описанный в настоящем документе, включает поддержание второй смеси при температуре кипения с обратным холодильником в течение приблизительно 1 часа перед охлаждением второй смеси.
[0072] В некоторых вариантах осуществления охлаждение второй смеси включает охлаждение первой смеси до температуры приблизительно от 15°C до 30°C.
[0073] В некоторых вариантах осуществления охлаждение второй смеси включает добавление воды ко второй смеси с образованием второго осадка.
[0074] В некоторых вариантах осуществления охлаждение второй смеси включает перемешивание второй смеси в течение по меньшей мере 4 часов.
[0075] В некоторых вариантах осуществления первый осадок промывают спиртом, и промывочный спирт собирают и добавляют ко второй смеси перед нагревом.
[0076] В некоторых вариантах осуществления способ, описанный в настоящем документе, включает сушку второго осадка.
[0077] В некоторых вариантах осуществления способ, описанный в настоящем документе, включает анализ второго осадка для определения композиции плинабулина во втором осадке.
[0078] В некоторых вариантах осуществления стадии смешивания, охлаждения и фильтрации повторяют один или более раз в зависимости от композиции плинабулина во втором осадке.
[0079] Некоторые варианты осуществления относятся к способу получения моногидрата плинабулина или композиции плинабулина, где способ включает смешивание плинабулина, этанола и воды с образованием смеси. В некоторых вариантах осуществления способ включает смесь.
[0080] В некоторых вариантах осуществления объемное отношение этанола к воде составляет приблизительно 95:5. В некоторых вариантах осуществления объемное отношение этанола к воде составляет приблизительно 85:15, 90:10, 95:5, 97,5:2,5 или 99:1. В некоторых вариантах осуществления объемное отношение этанола к воде составляет приблизительно 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25.
[0081] В некоторых вариантах осуществления смесь плинабулина и системы растворителей перемешивают в течение по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15 или 20 часов. В некоторых вариантах осуществления смесь перемешивают в течение по меньшей мере 2 часов.
[0082] В некоторых вариантах осуществления смешивание или перемешивание проводят при температуре от приблизительно 10°C до приблизительно 50°C; от приблизительно 20°C до приблизительно 40°C; от приблизительно 25°C до приблизительно 35°C или от приблизительно 28°С до приблизительно 32°C. В некоторых вариантах осуществления смешивание плинабулина, этанола и воды с образованием смеси или перемешивание смеси проводят при приблизительно 20°C, 25°C, 30°C, 35°C или 40°C.
[0083] ФИГ. 29 демонстрирует блок-схему одного из способов получения композиции, содержащей форму моногидрата плинабулина. Как показано на ФИГ. 29, соединение плинабулина и этанол добавляют в реакционную колбу, и затем нагревают смесь до 70-78°C и смешивают при этой температуре в течение приблизительно 1 часа. При необходимости может быть добавлено дополнительное количество этанола. Затем колбу охлаждают до приблизительно 50-60°C, смесь фильтруют и используют этанол в качестве промывочного растворителя. Отфильтрованный раствор и промывочный раствор объединяют и добавляют воду в количестве до приблизительно 10% от объединенного раствора. Затем раствор нагревают до 70-78°C и смешивают при этой температуре в течение приблизительно 1 часа. Берут образец для анализа методом XRPD, и затем раствор охлаждают до 20±5°C и добавляют к нему воду. Смесь фильтруют, используя воду в качестве промывочной жидкости. Отфильтрованный продукт промывают водой и затем переносят на сушильные лотки для сушки при 40-50°C в течение приблизительно 24 часов или дольше, до достижения продуктом требуемых уровней содержания этанола и воды.
Кристаллическая форма 2 плинабулина
[0084] Некоторые варианты осуществления относятся к кристаллической форме 2 плинабулина и способу ее получения. Без привязки к какой-либо конкретной теории полагают, что форма 2 представляет собой сольват плинабулина с изопропиловым спиртом (ИПС).
[0085] В некоторых вариантах осуществления кристаллическая форма 2 плинабулина имеет по существу такой же спектр XRPD, как изображенный на ФИГ. 4, соответствующие данные пиков которого представлены в табулированной форме в таблице 2.
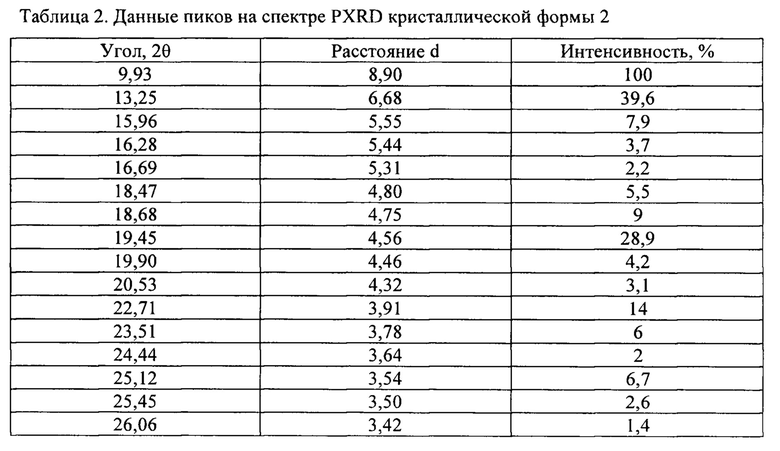

[0086] Кристаллическая форма 2 может дополнительно быть охарактеризована по существу такой же термограммой ДСК, как изображенная на ФИГ. 6В. Как показано на ФИГ. 6 В, кристаллическая форма 2 имеет температуру плавления, составляющую приблизительно 267°C; кристаллическая форма 2 плинабулина имеет термограмму дифференциальной сканирующей калориметрии с эндотермическими пиками при приблизительно 113°C и приблизительно 267°C.
Кристаллическая форма 3 плинабулина
[0087] Некоторые варианты осуществления относятся к кристаллической форме 3 плинабулина и способу ее получения. Без привязки к какой-либо конкретной теории полагают, что форма 3 представляет собой безводную форму плинабулина.
[0088] В некоторых вариантах осуществления кристаллическая форма 3 плинабулина имеет по существу такой же спектр XRPD, как изображенный на ФИГ. 7,
соответствующие данные пиков которого представлены в табулированной форме в таблице 3.

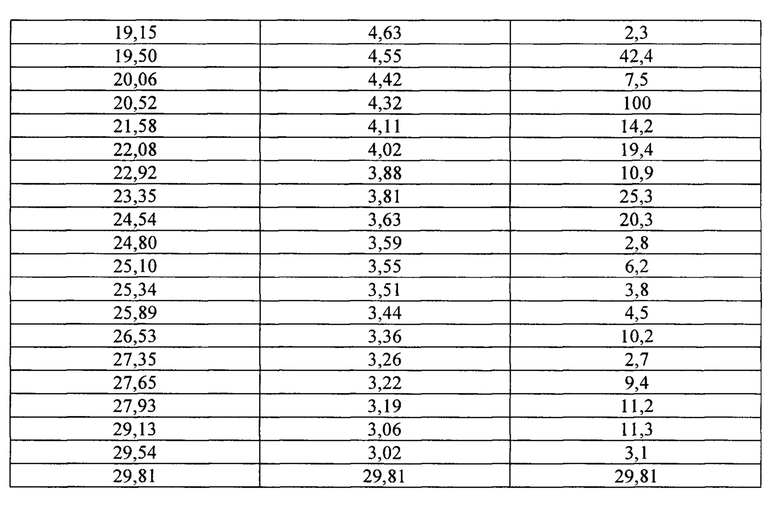
[0089] Кристаллическая форма 3 может дополнительно быть охарактеризована по существу такой же термограммой ДСК, как изображенная на ФИГ. 9В. Как показано на ФИГ. 9 В, кристаллическая форма 3 имеет температуру плавления, составляющую приблизительно 264°С; кристаллическая форма 3 имеет термограмму дифференциальной сканирующей калориметрии с эндотермическим пиком при приблизительно 264°C.
Кристаллическая форма 4 плинабулина
[0090] Некоторые варианты осуществления относятся к кристаллической форме 4 плинабулина и способу ее получения. Без привязки к какой-либо конкретной теории полагают, что форма 4 представляет собой метанольный сольват плинабулина.
[0091] В некоторых вариантах осуществления кристаллическая форма 4 плинабулина имеет по существу такой же спектр XRPD, как изображенный на ФИГ. 10, соответствующие данные пиков которого представлены в табулированной форме в таблице 4.

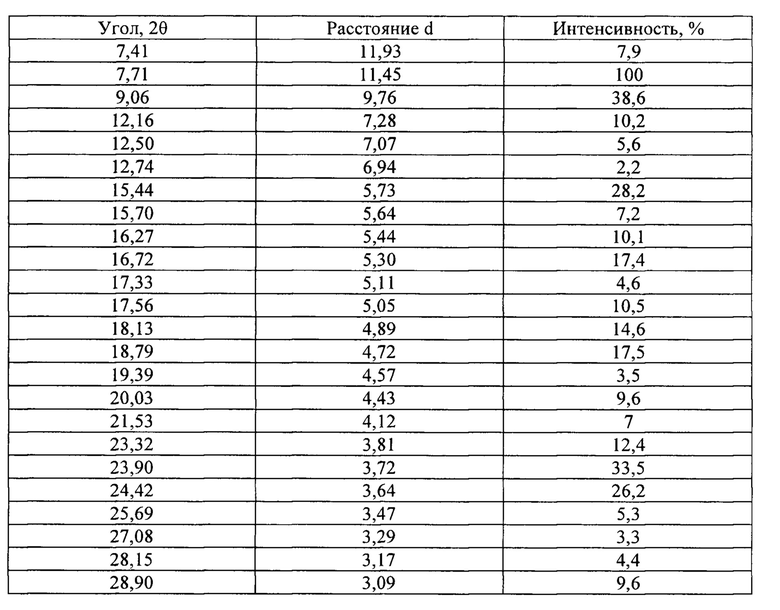
[0092] Кристаллическая форма 4 может дополнительно быть охарактеризована по существу такой же термограммой ДСК, как изображенная на ФИГ. 12 В. Как показано на ФИГ. 12 В, кристаллическая форма 4 имеет температуру плавления, составляющую приблизительно 267°C; кристаллическая форма 4 имеет термограмму дифференциальной сканирующей калориметрии с эндотермическими пиками при приблизительно 113°C и при приблизительно 264°C.
Кристаллическая форма 5 плинабулина
[0093] Некоторые варианты осуществления относятся к кристаллической форме 5 плинабулина и способу ее получения.
[0094] В некоторых вариантах осуществления кристаллическая форма 5 плинабулина имеет по существу такой же спектр XRPD, как изображенный на ФИГ. 13, соответствующие данные пиков которого представлены в табулированной форме в таблице 5.

[0095] Кристаллическая форма 5 может дополнительно быть охарактеризована по существу такой же термограммой ДСК, как изображенная на ФИГ. 15. Как показано на ФИГ. 15, кристаллическая форма 5 имеет температуру плавления, составляющую приблизительно 267°C; кристаллическая форма 5 имеет термограмму дифференциальной сканирующей калориметрии с эндотермическими пиками при приблизительно 70°C и при приблизительно 267°C.
Кристаллическая форма 6 плинабулина
[0096] Некоторые варианты осуществления относятся к кристаллической форме 6 плинабулина и способу ее получения.
[0097] В некоторых вариантах осуществления кристаллическая форма 6 плинабулина имеет по существу такой же спектр XRPD, как изображенный на ФИГ. 16, соответствующие данные пиков которого представлены в табулированной форме в таблице 6.
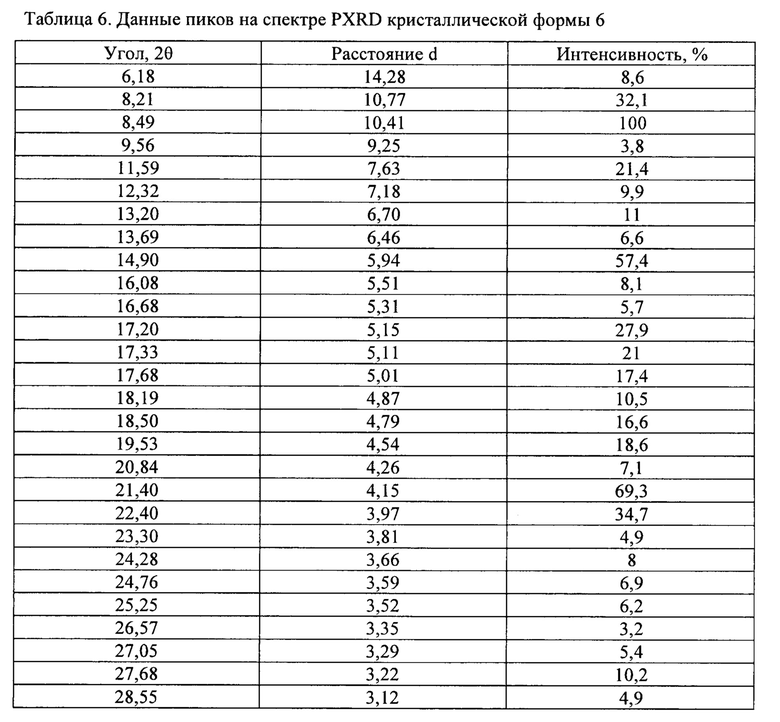
[0098] Кристаллическая форма 6 может дополнительно быть охарактеризована по существу такой же термограммой ДСК, как изображенная на ФИГ. 18. Как показано на ФИГ. 18, кристаллическая форма 6 имеет температуру плавления, составляющую приблизительно 267°C; кристаллическая форма 6 имеет термограмму дифференциальной сканирующей калориметрии с эндотермическим пиком при приблизительно 267°C.
Кристаллическая форма 7 плинабулина
[0099] Некоторые варианты осуществления относятся к кристаллической форме 7 плинабулина и способу ее получения.
[0100] В некоторых вариантах осуществления кристаллическая форма 7 плинабулина имеет по существу такой же спектр XRPD, как изображенный на ФИГ. 19, соответствующие данные пиков которого представлены в табулированной форме в таблице 7.
[0101] Кристаллическая форма 7 может дополнительно быть охарактеризована по существу такой же термограммой ДСК, как изображенная на ФИГ. 21. Как показано на ФИГ. 21, кристаллическая форма 7 имеет температуру плавления, составляющую приблизительно 267°C; кристаллическая форма 7 имеет термограмму дифференциальной сканирующей калориметрии с эндотермическими пиками при приблизительно 63°C и при приблизительно 267°C.
Кристаллическая форма 8 плинабулина
[0102] Некоторые варианты осуществления относятся к кристаллической форме 8 плинабулина и способу ее получения.
[0103] В некоторых вариантах осуществления кристаллическая форма 8 плинабулина имеет по существу такой же спектр XRPD, как изображенный на ФИГ.
22, соответствующие данные пиков которого представлены в табулированной форме в таблице 8.


[0104] Кристаллическая форма 8 может дополнительно быть охарактеризована по существу такой же термограммой ДСК, как изображенная на ФИГ. 24. Как показано на ФИГ. 24, кристаллическая форма 8 имеет температуру плавления, составляющую приблизительно 262°C; кристаллическая форма 8 имеет термограмму дифференциальной сканирующей калориметрии с эндотермическими пиками при приблизительно 74°C и при приблизительно 264°C.
Кристаллическая форма 9 плинабулина
[0105] Некоторые варианты осуществления относятся к кристаллической форме 9 плинабулина и способу ее получения.
[0106] В некоторых вариантах осуществления кристаллическая форма 9 плинабулина имеет по существу такой же спектр XRPD, как изображенный на ФИГ. 25, соответствующие данные пиков которого представлены в табулированной форме в таблице 9.


[0107] Кристаллическая форма 9 может дополнительно быть охарактеризована по существу такой же термограммой ДСК, как изображенная на ФИГ. 27. Как показано на ФИГ. 27, кристаллическая форма 9 имеет температуру плавления, составляющую приблизительно 267°C; кристаллическая форма 9 имеет термограмму дифференциальной сканирующей калориметрии с эндотермическими пиками при приблизительно 63°C, приблизительно 119°C, приблизительно 267°C и приблизительно 289°C.
Превращение полиморфных форма плинабулина
[0108] Моногидрат плинабулина (форма 1) является наиболее стабильным полиморфом из девяти обнаруженных полиморфных форм. Моногидрат плинабулина (форма 1) сохраняет стабильность в ходе процесса сушки и в ходе исследований стабильности, основанных на применении влажности (стабилен при сушке до 50°C в вакууме в течение субботы и воскресенья, никаких изменений твердой формы при воздействии влажности, превышающей 95% ОВ, в течение 13 дней).
[0109] ФИГ. 28 демонстрирует то, как форма 1 может быть превращена в остальные восемь полиморфных форм плинабулина. Например, моногидрат плинабулина (форма 1) может быть превращен в форму 2 суспендированием формы 1 в изопропиловом спирте (в объеме, приблизительно в 10 раз превышающем объем формы 1) при 30°С в течение 3 часов; форма 1 может быть превращена в форму 3 суспендированием формы 1 в этаноле (в объеме, приблизительно в 10 раз превышающем объем формы 1) при комнатной температуре в течение ночи; форма 1 может быть превращена в форму 4 суспендированием формы 1 в метаноле (в объеме, приблизительно в 10 раз превышающем объем формы 1) при 30°C в течение ночи; форма 1 может быть превращена в форму 5 суспендированием формы 1 в ацетонитриле (ACN) при 30°C и перемешивании в течение 3 дней; форма 1 может быть превращена в форму 6 получением насыщенного раствора формы 1 в изопропиловом спирте при 15°С и затем испарением в вакууме при 45°C; форма 1 может быть превращена в форму 7 получением насыщенного раствора формы 1 в метаноле при 45°С и затем испарением в вакууме при 45°C; форма 1 может быть превращена в форму 8 получением насыщенного раствора формы 1 в этилацетате (EtOAC) при 45°С и затем испарением в вакууме при 45°C; и форма 1 может быть превращена в форму 9 сначала путем превращения формы 1 в форму 4, и затем подвергания формы 4 воздействию влаги.
[0110] ФИГ. 28 также демонстрирует то, как другие формы могут быть превращены в форму 1. Например, формы 2, 3 и 4 могут быть превращены в форму 1 суспендированием этих форм в смеси этанола и воды (95:5 об/об) (объем смеси воды и этанола приблизительно в 10 раз превышает объем исходных полиморфных форм) при 30°C в течение 2 часов; форма 2 может быть превращена в форму 6 сушкой в вакуумном сушильном шкафу при 45°С в течение 5 дней; форма 4 может быть превращена в форму 7 сушкой в вакуумном сушильном шкафу при 45°C в течение ночи; и форма 4 может быть превращена в форму 9 под воздействием высокой влажности.
Введение и фармацевтические композиции
[0111] Некоторые варианты осуществления включают фармацевтические композиции, содержащие полиморф плинабулина, описанный в настоящем документе, и фармацевтически приемлемый носитель. Такая композиция может вводиться субъекту в качестве части терапевтического лечения.
[0112] В некоторых вариантах осуществления композиция может дополнительно включать один или более фармацевтически приемлемых разбавителей. В некоторых вариантах осуществления фармацевтически приемлемый разбавитель может включать Kolliphor® (полиоксил-15-гидроксистеарат). В некоторых вариантах осуществления фармацевтически приемлемый разбавитель может включать пропиленгликоль. В некоторых вариантах осуществления фармацевтически приемлемые разбавители могут включать коллифор и пропиленгликоль. В некоторых вариантах осуществления фармацевтически приемлемые разбавители могут включать коллифор и пропиленгликоль, где коллифор составляет приблизительно 40 масс. %, и пропиленгликоль составляет приблизительно 60 масс. % относительно общей массы разбавителей. В некоторых вариантах осуществления композиция может дополнительно включать один или более других фармацевтически приемлемых вспомогательных веществ.
[0113] Для получения композиций, описанных в настоящем документе, могут использоваться стандартные технологии приготовления лекарственных средств, такие как раскрытые в книге Remington: The Science and Practice of Pharmacy, 21st Ed., Lippincott Williams & Wilkins (2005), полностью включенной в настоящий документ посредством ссылки. Соответственно, некоторые варианты осуществления включают фармацевтические композиции, содержащие: (а) безопасное и терапевтически эффективное количество полиморфа плинабулина или его фармацевтически приемлемых солей; и (b) фармацевтически приемлемый носитель, разбавитель, вспомогательное вещество или их комбинацию.
[0114] Другие варианты осуществления включают совместное введение полиморфа плинабулина и дополнительного терапевтического агента в составе отдельных композиций или одной и той же композиции. Следовательно, некоторые варианты осуществления включают первую фармацевтическую композицию, содержащую: (а) безопасное и терапевтически эффективное количество полиморфа плинабулина или его фармацевтически приемлемых солей и (b) фармацевтически приемлемый носитель, разбавитель, вспомогательное вещество или их комбинацию; и вторую фармацевтическую композицию, содержащую: (а) безопасное и терапевтически эффективное количество дополнительного терапевтического агента и (b) фармацевтически приемлемый носитель, разбавитель, вспомогательное вещество или их комбинацию. Некоторые варианты осуществления включают фармацевтическую композицию, содержащую: (а) безопасное и терапевтически эффективное количество полиморфа плинабулина или его фармацевтически приемлемых солей; (b) безопасное и терапевтически эффективное количество дополнительного терапевтического агента; и (с) фармацевтически приемлемый носитель, разбавитель, вспомогательное вещество или их комбинацию.
[0115] Введение описанных в настоящем документе фармацевтических композиций может осуществляться посредством любого из обычно применяемых способов введения для агентов, обладающих схожими назначениями, включая, но не ограничиваясь перечисленным, перорально, сублингвально, буккально, подкожно, внутривенно, интраназально, местно, чрескожно, внутрикожно, внутрибрюшинно, внутримышечно, внутрилегочно, вагинально, ректально или внутриглазным способом. Пероральное и парентеральное введение являются общепринятыми для лечения показаний, являющихся предметом предпочтительных вариантов осуществления.
[0116] Термин «фармацевтически приемлемый носитель» или «фармацевтически приемлемое вспомогательное вещество» включает любые возможные растворители, диспергирующие среды, покрытия, антибактериальные и противогрибковые агенты, изотонические и задерживающие абсорбцию агенты, и тому подобное. Применение таких сред и агентов для фармацевтически активных веществ хорошо известно в данной области техники. Кроме случаев, когда любая общепринятая среда или агент несовместимы с активным ингредиентом, их применение предусмотрено в терапевтических композициях. Кроме того, могут быть включены различные адъюванты, такие как широко используемые в данной области техники. Аспекты включения различных компонентов в фармацевтические композиции описаны, например, в источниках Gilman et al. (Eds.) (1990); Goodman and Gilman: The Pharmacological Basis of Therapeutics, 8 th Ed., Pergamon Press, полностью включенных в настоящий документ посредством ссылки.
[0117] Некоторыми примерами веществ, которые могут служить в качестве фармацевтически приемлемых носителей или их компонентов, являются сахара, такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлоза и ее производные, такие как натрий карбоксиметилцеллюлоза, этилцеллюлоза и метилцеллюлоза; порошковый трагакант; солод; желатин; тальк; твердые смазывающие вещества, такие как стеариновая кислота и стеарат магния; сульфат кальция; растительные масла, такие как арахисовое масло, хлопковое масло, кунжутное масло, оливковое масло, кукурузное масло и масло какао; многоатомные спирты, такие как пропиленгликоль, глицерин, сорбит, маннит и полиэтиленгликоль; альгиновая кислота; эмульгаторы, такие как эмульгаторы твины (TWEENS); смачивающие агенты, такие как лаурилсульфат натрия; красители; вкусовые агенты; агенты для облегчения процесса таблетирования, стабилизаторы; антиоксиданты; консерванты; апирогенная вода; изотонический раствор; и фосфатные буферные растворы.
[0118] Композиции, описанные в настоящем документе, предпочтительно представлены в виде единичной лекарственной формы. При использовании в настоящем документе термин "единичная лекарственная форма" представляет собой композицию, содержащую количество соединения или композиции, подходящую для введения животному, предпочтительно субъекту-млекопитающему, в разовой дозе, согласно надлежащей медицинской практике. Тем не менее, лекарственное средство в виде разовой или единичной лекарственной формы не подразумевает, что лекарственная форма вводится раз в сутки или один раз за курс лечения. Такие лекарственные формы предусмотрены для введения один раз, два раза, три раза или большее число раз в сутки, и могут вводиться в виде инфузии в течение определенного периода времени (например, от приблизительно 30 минут до приблизительно 2-6 часов), или вводиться в виде непрерывной инфузии, и могут быть введены более одного раза за курс лечения, хотя однократное введение специально не исключено. Специалисту в данной области техники ясно, что препарат не обязательно предназначен для применения на протяжении всего курса лечения, и такие решения должны приниматься специалистами в области лечения, а не приготовления лекарственных средств.
[0119] Подходящие композиции, как описано выше, могут находиться в различных формах, подходящих для различных путей введения, например, для перорального, сублингвального, буккального, назального, ректального, местного (включая чрескожный и внутрикожный), внутриглазного, внутрицеребрального, внутричерепного, интратекального, внутриартериального, внутривенного, внутримышечного или других родственных путей введения. Специалисту в данной области техники ясно, что пероральные и назальные композиции включают композиции, вводимые путем ингаляции, и приготавливаются с помощью доступных методик. В зависимости от конкретного требуемого пути введения могут быть использованы различные фармацевтически приемлемые носители, хорошо известные в данной области техники. Фармацевтически приемлемые носители включают, например, твердые или жидкие наполнители, разбавители, гидротропные вещества, поверхностно-активные вещества и вещества для инкапсулирования. Могут быть включены необязательные фармацевтически активные вещества, по существу не препятствующие проявлению активности соединения или композиции. Количество носителя, использующегося в сочетании с соединением или композицией, является достаточным для обеспечения рационального количества вещества для введения на одну дозу соединения. Технологии и композиции для приготовления лекарственных форм, полезные для применения в способах, описанных в настоящем документе, описаны в следующих источниках, все из которых включены в настоящий документ посредством ссылки: Modern Pharmaceutics, 4 th Ed., главы 9 и 10 (Banker & Rhodes, editors, 2002); Lieberman et al., Pharmaceutical Dosage Forms: Tablets (1989); и Ansel, Introduction to Pharmaceutical Dosage Forms 8th Edition (2004).
[0120] Могут использоваться различные пероральные лекарственные формы, включая такие твердые формы, как таблетки, капсулы (например, жидкие гелевые капсулы и твердые гелевые капсулы), гранулы и нерасфасованные порошки. Таблетки могут быть получены прессованием, представлять собой тритурационные таблетки, иметь кишечнорастворимую оболочку, иметь сахарную оболочку, иметь пленочную оболочку или быть получены многократным прессованием, могут содержать подходящие связывающие вещества, смазывающие вещества, разбавители, разрыхляющие агенты, красители, вкусовые агенты, антислеживающие агенты и вещества, понижающие температуру замерзания. Жидкие пероральные лекарственные формы включают водные растворы, эмульсии, суспензии, растворы и/или суспензии, разведенные из нешипучих гранул, и шипучие препараты, разведенные из шипучих гранул, содержащие подходящие растворители, консерванты, эмульгирующие агенты, суспендирующие агенты, разбавители, подсластители, вещества, понижающие температуру замерзания, красители и вкусовые агенты.
[0121] Фармацевтически приемлемые носители, подходящие для получения единичных лекарственных форм для перорального введения, хорошо известны в данной области техники. Таблетки, как правило, содержат традиционные фармацевтически совместимые адъюванты, такие как инертные разбавители, такие как карбонат кальция, карбонат натрия, маннит, лактоза и целлюлоза; связывающие вещества, такие как крахмал, желатин и сахароза; разрыхлители, такие как крахмал, альгиновая кислота и кроскармеллоза; смазывающие вещества, такие как стеарат магния, стеариновая кислота и тальк. Для улучшения характеристик сыпучести порошковой смеси могут быть использованы скользящие вещества, такие как диоксид кремния. Для придания внешнего вида могут быть добавлены красители, такие как красители для химической и пищевой промышленности. Подходящими адъювантами для жевательных таблеток являются подсластители и вкусовые агенты, такие как аспартам, сахарин, ментол, перечная мята, сахароза и фруктовые вкусоароматические добавки. Капсулы обычно содержат один или более из раскрытых выше твердых разбавителей. Выбор соединений носителей зависит от аспектов второстепенного значения, таких как вкус, стоимость и стабильность при хранении, которые не являются существенно важными, и может легко быть сделан специалистом в данной области техники.
[0122] Пероральные композиции также включают жидкие растворы, эмульсии, суспензии и тому подобное. Фармацевтически приемлемые носители, подходящие для получения таких композиций, хорошо известны в данной области техники. Типичные компоненты носителей для сиропов, эликсиров, эмульсий и суспензий включают этанол, глицерин, пропиленгликоль, полиэтиленгликоль, жидкую сахарозу, сорбит и воду. Для суспензии типичные суспендирующие агенты включают метилцеллюлозу, натрий карбоксиметилцеллюлозу, AVICEL RC-591, трагакант и альгинат натрия; типичные смачивающие агенты включают лецитин и полисорбат 80; и типичные консерванты включают метилпарабен и бензоат натрия. Пероральные жидкие композиции могут также содержат один или более таких раскрытых выше компонентов, как подсластители, вкусовые агенты и красители.
[0123] На такие композиции может также быть нанесено покрытие традиционными способами, обычно покрытия, зависящие от pH или времени, так что описываемая композиция высвобождается в желудочно-кишечном тракте вблизи требуемого местного применения или в различные моменты времени для увеличения продолжительности требуемого эффекта. Такие лекарственные формы обычно включают, но не ограничены перечисленным, один или более из ацетатфталата целлюлозы, фталата поливинил ацетата, фталата гидроксипропилметилцеллюлозы, этилцеллюлозы, покрытий на основе Эудрагита (Eudragit), восков и шеллака.
[0124] Композиции, описанные в настоящем документе, могут необязательно включать другие активные лекарственные вещества.
[0125] Другие композиции, подходящие для достижения системной доставки описываемых соединений, включают сублингвальные, буккальные и назальные лекарственные формы. Такие композиции обычно содержат один или более растворимых наполнителей, таких как сахароза, сорбит и маннит; и связывающих веществ, таких как аравийская камедь, микрокристаллическая целлюлоза, карбоксиметилцеллюлоза и гидроксипропилметилцеллюлоза. Могут также быть включены раскрытые выше скользящие вещества, смазывающие вещества, подсластители, красители, антиоксиданты и вкусовые агенты.
[0126] Состав жидкой композиции, предназначенной для местного офтальмологического применения, разрабатывают таким образом, чтобы лекарственная форма подходила для местного введения в глаз. Комфортность должна быть увеличена насколько это возможно, тем не менее, иногда аспекты разработки состава (например, стабильность лекарственного средства) могут обусловить не полностью оптимальный уровень комфорта. В случае, когда не может быть достигнута максимальная комфортность, состав жидкости может быть разработан таким образом, чтобы жидкость была приемлема для пациента при местном офтальмологическом применении. Кроме того, офтальмологически приемлемая жидкость может быть упакована или для однократного применения, или содержать консервант для предупреждения загрязнения при многократных применениях.
[0127] Для офтальмологического применения растворы или лекарственные средства часто изготавливают, используя физиологический солевой раствор в качестве основного носителя. Офтальмологические растворы предпочтительно могут поддерживаться при комфортном уровне pH с помощью подходящей буферной системы. Препараты могут также содержать общепринятые фармацевтически приемлемые консерванты, стабилизаторы и поверхностно-активные вещества.
[0128] Консерванты, которые могут быть использованы в раскрытых в настоящем документе фармацевтических композициях, включают, но не ограничены перечисленным, хлорид бензалкония, ПГМБ (полигексаметиленбигуанид), хлорбутанол, тиомеросал, ацетат и нитрат фенилртути. Подходящим поверхностно-активным веществом является, например, Tween 80. Аналогичным образом, в раскрытых в настоящем документе фармацевтических композициях могут быть использованы различные полезные носители. Эти носители включают, но не ограничены перечисленным, поливиниловый спирт, повидон, гидроксипропилметилцеллюлозу, полоксамеры, карбоксиметилцеллюлозу, гидроксиэтилцеллюлозу и очищенную воду.
[0129] При необходимости или в случае целесообразности могут быть добавлены регуляторы тоничности. Они включают, но не ограничены перечисленным, соли, в частности, хлорид натрия, хлорид калия, маннит и глицерин, или любые другие офтальмологически приемлемые регуляторы тоничности.
[0130] При условии, что получаемый препарат является офтальмологически стабильным, могут быть использованы различные буферы и средства регулировки pH. Для многих композиций pH составляет от 4 до 9. Соответственно, буферы включают ацетатные буферы, цитратные буферы, фосфатные буферы и боратные буферы. При необходимости для регулирования pH этих препаратов могут быть использованы кислоты или основания.
[0131] Офтальмологически приемлемые антиоксиданты включают, но не ограничены перечисленным, метабисульфит натрия, тиосульфат натрия, ацетилцистеин, бутилированный гидроксианизол и бутилированный гидрокситолуол.
[0132] Другими вспомогательными компонентами, которые могут быть включены в офтальмологические препараты, являются хелатирующие агенты. Полезным комплексообразующим агентом является динатрия эдетат (ЭДТА), однако вместо него или в сочетании с ним могут быть использованы другие хелатирующие агенты.
[0133] Для местного применения могут быть использованы кремы, мази, гели, растворы или суспензии, и т.д., содержащие раскрытую в настоящем документе композицию. Лекарственные формы для местного применения могут, как правило, состоять из фармацевтически приемлемого носителя, сорастворителя, эмульгатора, усилителя проникновения, системы консерванта и смягчителя.
[0134] Для внутривенного введения композиции, описанные в настоящем документе, могут быть растворены или диспергированы в фармацевтически приемлемом разбавителе, таком как солевой раствор или раствор декстрозы. Для достижения требуемого значения pH могут быть включены подходящие вспомогательные вещества, включая, но не ограничиваясь перечисленным, NaOH, карбонат натрия, ацетат натрия, HCl и лимонную кислоту. В различных вариантах осуществления значение pH готовой композиции варьирует от 2 до 8 или предпочтительно от 4 до 7. Антиоксидантные вспомогательные вещества могут включать бисульфит натрия, ацетон бисульфит натрия, формальдегид натрия, сульфоксилат, тиомочевину и ЭДТА. Другие неограничивающие примеры подходящих вспомогательных веществ в готовых внутривенных композициях могут включать фосфаты натрия или калия, лимонную кислоту, винную кислоту, желатин и углеводы, такие как декстроза, маннит и декстран. Дополнительные приемлемые эксципиенты описаны в источниках Powell, et al., Compendium of Excipients for Parenteral Formulations, PDA J Pharm Sci and Tech 1998, 52 238-311 и Nema et al., Excipients and Their Role in Approved Injectable Products: Current Usage and Future Directions, PDA J Pharm Sci and Tech 2011, 65 287-332, оба из которых полностью включены в настоящий документ посредством ссылки. Также могут быть включены противомикробные агенты для получения бактериостатического или фунгистатического раствора, включая, но не ограничиваясь перечисленным, нитрат фенилртути, тиомеросал, хлорид бензетония, хлорид бензалкония, фенол, крезол и хлорбутанол.
[0135] Композиции для внутривенного введения могут быть предоставлены лицам, осуществляющим уход за больными, в виде одной или более твердых лекарственных форм, которые разводятся незадолго до введения с помощью подходящего разбавителя, такого как стерильная вода, физиологический раствор или водный раствор декстрозы. В других вариантах осуществления композиции представлены в растворе, готовом для парентерального введения. В других вариантах осуществления композиции представлены в растворе, который перед введением необходимо дополнительно разбавлять. В вариантах осуществления, включающих введение комбинации соединения, описанного в настоящем документе, и другого агента, такая комбинация может быть предоставлена лицам, осуществляющим уход за больными, в виде смеси, или лицам, осуществляющие уход за больными, могут смешивать два агента перед введением, или два агента могут вводиться по отдельности.
[0136] В некоторых вариантах осуществления разовая доза полиморфа плинабулина или другого терапевтического агента может составлять от приблизительно 5 мг/м2 до приблизительно 150 мг/м2 площади поверхности тела, от приблизительно 5 мг/м2 до приблизительно 100 мг/м2 площади поверхности тела, от приблизительно 10 мг/м2 до приблизительно 100 мг/м2 площади поверхности тела, от приблизительно 10 мг/м2 до приблизительно 80 мг/м2 площади поверхности тела, от приблизительно 10 мг/м2 до приблизительно 50 мг/м2 площади поверхности тела, от приблизительно 10 мг/м2 до приблизительно 40 мг/м2 площади поверхности тела, от приблизительно 10 мг/м2 до приблизительно 30 мг/м2 площади поверхности тела, от приблизительно 13,5 мг/м2 до приблизительно 100 мг/м2 площади поверхности тела, от приблизительно 13,5 мг/м2 до приблизительно 80 мг/м2 площади поверхности тела, от приблизительно 13,5 мг/м2 до приблизительно 50 мг/м2 площади поверхности тела, от приблизительно 13,5 мг/м2 до приблизительно 40 мг/м2 площади поверхности тела, от приблизительно 13,5 мг/м2 до приблизительно 30 мг/м2 площади поверхности тела, от приблизительно 15 мг/м2 до приблизительно 80 мг/м2 площади поверхности тела, от приблизительно 15 мг/м2 до приблизительно 50 мг/м2 площади поверхности тела или от приблизительно 15 мг/м2 до приблизительно 30 мг/м2 площади поверхности тела. В некоторых вариантах осуществления разовая доза полиморфа плинабулина или другого терапевтического агента может составлять от приблизительно 13,5 мг/м2 до приблизительно 30 мг/м2 площади поверхности тела. В некоторых вариантах осуществления разовая доза полиморфа плинабулина или другого терапевтического агента может составлять приблизительно 5 мг/м2, приблизительно 10 мг/м2, приблизительно 12,5 мг/м2, приблизительно 13,5 мг/м2, приблизительно 15 мг/м2, приблизительно 17,5 мг/м2, приблизительно 20 мг/м2, приблизительно 22,5 мг/м2, приблизительно 25 мг/м2, приблизительно 27,5 мг/м2, приблизительно 30 мг/м2, приблизительно 40 мг/м2, приблизительно 50 мг/м2, приблизительно 60 мг/м2, приблизительно 70 мг/м2, приблизительно 80 мг/м2, приблизительно 90 мг/м2 или приблизительно 100 мг/м2 площади поверхности тела.
[0137] В некоторых вариантах осуществления разовая доза полиморфа плинабулина или другого терапевтического агента может составлять от приблизительно 5 мг до приблизительно 300 мг, от приблизительно 5 мг до приблизительно 200 мг, от приблизительно 7.5 мг до приблизительно 200 мг, от приблизительно 10 мг до приблизительно 100 мг, от приблизительно 15 мг до приблизительно 100 мг, от приблизительно 20 мг до приблизительно 100 мг, от приблизительно 30 мг до приблизительно 100 мг, от приблизительно 40 мг до приблизительно 100 мг, от приблизительно 10 мг до приблизительно 80 мг, от приблизительно 15 мг до приблизительно 80 мг, от приблизительно 20 мг до приблизительно 80 мг, от приблизительно 30 мг до приблизительно 80 мг, от приблизительно 40 мг до приблизительно 80 мг, от приблизительно 10 мг до приблизительно 60 мг, от приблизительно 15 мг до приблизительно 60 мг, от приблизительно 20 мг до приблизительно 60 мг, от приблизительно 30 мг до приблизительно 60 мг или от приблизительно 40 мг до приблизительно 60 мг. В некоторых вариантах осуществления разовая доза полиморфа плинабулина или другого терапевтического агента может составлять от приблизительно 20 мг до приблизительно 60 мг, от приблизительно 27 мг до приблизительно 60 мг, от приблизительно 20 мг до приблизительно 45 мг или от приблизительно 27 мг до приблизительно 45 мг. В некоторых вариантах осуществления разовая доза полиморфа плинабулина или другого терапевтического агента может составлять приблизительно 5 мг, приблизительно 10 мг, приблизительно 12,5 мг, приблизительно 13,5 мг, приблизительно 15 мг, приблизительно 17,5 мг, приблизительно 20 мг, приблизительно 22,5 мг, приблизительно 25 мг, приблизительно 27 мг, приблизительно 30 мг, приблизительно 40 мг, приблизительно 50 мг, приблизительно 60 мг, приблизительно 70 мг, приблизительно 80 мг, приблизительно 90 мг, приблизительно 100 мг, приблизительно 125 мг, приблизительно 150 мг или приблизительно 200 мг.
[0138] Период введения может представлять собой курс лечения продолжительностью несколько недель, при условии что опухоль находится под контролем и что схема приема клинически переносится. В некоторых вариантах осуществления разовая доза полиморфа плинабулина или другого терапевтического агента может вводиться раз в неделю, и предпочтительно раз в каждый из 1-го и 8-го дня трехнедельного (21-дневного) курса лечения. В некоторых вариантах осуществления разовая доза полиморфа плинабулина или другого терапевтического агента может вводиться раз в неделю, два раза в неделю, три раза в неделю, четыре раза в неделю, пять раз в неделю, шесть раз в неделю или ежедневно в течение курса лечения длительностью одну неделю, две недели, три недели, четыре недели или пять недель. Введение может осуществляться в один и тот же или разные дни каждой недели курса лечения.
[0139] Курс лечения может быть повторен при условии, что схема приема клинически переносится. В некоторых вариантах осуществления курс лечения повторяют n раз, где n представляет собой целое число в диапазоне от 2 до 30. В некоторых вариантах осуществления n составляет 2, 3, 4, 5, 6, 7, 8, 9 или 10. В некоторых вариантах осуществления новый курс лечения может быть начат сразу после завершения предшествующего курса лечения. В некоторых вариантах осуществления новый курс лечения может быть начат по прошествии периода времени после завершения предшествующего курса лечения.
[0140] В некоторых вариантах осуществления композиции, описанные в настоящем документе, могут применяться в комбинации с другими терапевтическими агентами. В некоторых вариантах осуществления композиции, описанные в настоящем документе, могут вводиться или применяться в комбинации с такими видами лечения, как химиотерапия, радиационая и биологическая терапии.
ПРИМЕРЫ
Пример 1.
[0141] Образец соединения плинабулина перемешивали в этаноле и нагревали до кипения с обратным холодильником. Добавляли этанол по частям для поддержания кипения с обратным холодильником до тех пор, пока весь образец не растворился, с получением прозрачного желтого раствора. В общей сложности 124,7 г этанола потребовалось для полного растворения образца при кипячении с обратным холодильником. Затем раствору давали остыть и наблюдали за образованием осадка. Осадок наблюдали, когда температура раствора составила 49°C. Смесь повторно нагревали до кипения с обратным холодильником, получая прозрачный желтый раствор. Горячий раствор переносили в колбу Эрленмейера большего объема, промывая 9,45 г этанола (для имитации горячего фильтрования). К этому раствору, кипящему с обратным холодильником, добавляли 6,6 г воды (приблизительно 5% воды в этаноле). Раствору давали медленно остыть при перемешивании. Осадок наблюдали, когда раствор охладился до 70°C. В этот момент медленно добавляли дополнительное количество воды (128,6 г), вызывая осаждение большого количества твердого вещества. Раствору давали остыть до комнатной температуры при перемешивании. Твердые вещества отфильтровывали при 17°C и трижды промывали 20 г воды. К фильтрату добавляли в общей сложности 134 г воды, приводя к образованию мутного раствора с незначительным количеством твердого вещества, подлежащего фильтрации. В попытках вызвать осаждение дополнительного количества продукта добавляли еще 137 г воды, однако никакого дополнительного количества твердого вещества не удалось выделить. Твердое вещество сушили при 40-45°C в течение 3 дней с получением выхода 4,73 г, 97,5%. Анализ методом XRPD показал, что продукт является моногидратом плинабулина (форма 1). Анализ методом Карла Фишера показал, что содержание воды составляло 4,9%.
[0142] Анализ методом Карла Фишера после сушки при 45°C в вакууме в течение еще 70 часов показал, что содержание воды снизилось до 4,1%. XRPD этого образца показала, что он представлял собой моногидрат плинабулина (форма 1). Этот образец помещали в перчаточную камеру в открытом контейнере рядом с открытым контейнером с водой и следили за содержанием воды. Измеренное через 4 часа содержание воды составило 5,0%. Измеренное через 18,5 часов содержание воды составило 4,8%, и результат анализа методом Карла Фишера через 51 час составил 4,9%.
Пример 2.
[0143] Образец соединения плинабулина (4,92 г) перемешивали в этаноле (147,6 г) и нагревали до кипения с обратным холодильником (полностью растворимо при 75°C). Затем раствору давали остыть и следили за образованием осадка. Осадок наблюдался, когда температура раствора составила 48°C. Смесь повторно нагревали до кипения с обратным холодильником, получая прозрачный желтый раствор. К горячему раствору добавляли 295 г воды (приблизительно в два раза больше массы этанола), позволяя смеси охлаждаться в ходе добавления. Осадок наблюдали после добавления приблизительно 150 мл воды при температуре 48°C. Этому раствору давали остыть до комнатной температуры. Твердые вещества отфильтровывали и трижды промывали 20 г воды. Твердое вещество сушили при 40-45°C в течение 2,5 дней с получением выхода 4,82 г, 98,0%. Анализ методом XRPD показал, что продукт является смесью моногидрата плинабулина (форма 1) (основной компонент) и безводного плинабулина (форма 3) (второстепенный компонент). Анализ методом Карла Фишера показал, что содержание воды составляло 5,0%. Анализ методом Карла Фишера после сушки при 45°C в вакууме в течение еще 70 часов показал, что содержание воды снизилось до 4,4%. XRPD этого образца показала, что он был по существу неизменным и представлял собой смесь форм 1 и 3 с дополнительными пиками (при приблизительно 12,26°, 15,19° и 28,79° градусов 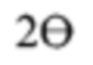 ). Этот образец помещали в перчаточную камеру в открытом контейнере рядом с открытым контейнером с водой и следили за содержанием воды. Измеренное через 4 часа содержание воды составило 5,0%. Измеренное через 18,5 часов содержание воды составило 4,9%, и результат анализа методом Карла Фишера через 51 час составил 5,1%.
). Этот образец помещали в перчаточную камеру в открытом контейнере рядом с открытым контейнером с водой и следили за содержанием воды. Измеренное через 4 часа содержание воды составило 5,0%. Измеренное через 18,5 часов содержание воды составило 4,9%, и результат анализа методом Карла Фишера через 51 час составил 5,1%.
Пример 3
[0144] Образец соединения плинабулина растворяли в 1,2-пропандиоле при интенсивном перемешивании или умеренном нагреве (50°C). Через 4 часа образец продемонстрировал пики, характерные для формы 3. После перемешивания в течение субботы и воскресенья образец суспендировали в воде и полностью превращали в моногидрат плинабулина (форма 1), на сканах XRPD которого не присутствовало каких-либо пиков, характерных для кристаллической формы 3. Аналогичный результат наблюдали в эксперименте с использованием этанола/воды, где по прошествии 1 часа и 4 часов наблюдали очень небольшие пики, характерные для формы 3, а через 66 часов наблюдали только форму 1.
Пример 4
[0145] В ходе повторной обработки соединение плинабулина (форма 3) растворяли в этаноле с соотношением 1:25 (по массе) при кипячении с обратным холодильником. Этот раствор фильтровали при температуре, превышавшей 50°C, и объединяли фильтрат с равной массой воды с получением продукта. Может быть желательным повторно нагреть пропущенный через тонкопористый фильтр этанольный раствор перед добавлением всего количества воды, и добавить приблизительно 5% воды (относительно этанола) и перемешать раствор при приблизительно 70°C для обеспечения превращения в форму 1. Затем может быть добавлено дополнительное количество воды, и смесь может быть охлаждена для выделения продукта фильтрацией. Образец может быть высушен в течение длительного периода времени для снижения содержания воды, полученного анализом по методу Карла Фишера. Один из образцов сушили в течение трех дней, что привело к результату анализа методом Карла Фишера, составившему 4,9% воды. Сушка в течение еще трех дней снизила результат анализа методом Карла Фишера до 4,1%.
[0146] Подвергание сухого продукта условиям влажной среды повысило содержание воды до приблизительно 5%, при котором оно, по-видимому, оставалось постоянным. Один из образцов с 4,1% влаги подвергали воздействию открытого контейнера с водой в перчаточной камере в течение 4 часов, в результате чего содержание воды в нем поднялось до 5,0%. По прошествии еще 14,5 часов в этих условиях измеренное содержание воды в образце составило 4,8%. По прошествии в общей сложности 51 часов результат анализа методом Карла Фишера составил 4,9%.
Пример 5
[0147] Навеску плинабулина с содержанием воды, определенным анализом по методу Карла Фишера, составлявшим приблизительно 3,1%, добавляли к смеси коллифора (40 масс. %)) и пропиленгликоля (60 масс. %). В растворе образовались нерастворимые частицы, и было установлено, что нерастворимые частицы представляли собой безводный плинабулин (форма 3). Навеску повторно обрабатывали согласно стадиям, описанным на ФИГ. 29, с образованием моногидрата плинабулина (форма 1). Анализ методом Карла Фишера показал, что содержание воды в повторно обработанном плинабулине составляло приблизительно 5,1%, что согласуется с расчетным содержанием воды в моногидрате. Моногидрат плинабулина (форма 1) полностью растворился в смеси коллифора (40 масс. %) и пропиленгликоля (60 масс. %), и в растворе не образовалось нерастворимых частиц. Следовательно, моногидрат плинабулина (форма 1) показал лучшую растворимость, чем композиции плинабулина, содержащие безводный плинабулин (форма 3).
Пример 6
[0148] Моногидрат плинабулина (кристаллическая форма 1) охарактеризовывали с помощью XRPD (кристаллическая, фиг. 1), оптической микроскопии (фиг. 2), ДСК (фиг. 3А), ТГА (фиг. 3В) и методом Карла Фишера.
[0149] Данные ДСК получали с помощью дифференциального сканирующего калориметра Q10 от ТА Instruments. Как правило, образцы (~ 2 мг) помещали в герметичные алюминиевые тигли для образцов с алодиновым покрытием и сканировали от 30 до 300°C со скоростью подачи 10°C/мин при продувке азотом со скоростью подачи 50 мл/мин. Данные ТГА получали с помощью термогравиметрического анализатора Q500 от ТА Instruments. Как правило, образцы (~ 10 мг) помещали в открытые предварительно тарированные алюминиевые тигли для образцов и сканировали от 30 до 300°C со скоростью 10°C/мин при продувке азотом со скоростью подачи 60 мл/мин. Рентгеновские порошковые дифрактограммы получали с помощью прибора D8 Advance от Bruker, оборудованного источником излучения Cu Kα (1,54°А), держателем образца с 9 возможными положениями и сверхскоростным детектором LYNXEYE. Как правило, продолжительность каждого скана составляла 180 секунд, и диапазон 29 составлял от 4 до 40°. Образцы помещали на кремниевые пластиночные держатели с нулевым фоном. Образцы анализировали с помощью гравиметрического анализатора сорбции паров воды Aquadyne DVS-2. Относительную влажность регулировали в диапазоне 2-95%, и за массой образца непрерывно наблюдали и регистрировали.
[0150] XRPD показала, что вещество является кристаллическим. Данные ДСК показали широкую эндотерму (максимум пика при 141°C, вероятнее всего потеря воды), небольшой экзотермический процесс (максимум пика при 164°C) и эндотермический процесс с острым пиком (максимум пика при 268°С). ТГА указал на потерю 5,26% массы при приблизительно 130°C (вероятнее всего потеря воды). Анализ методом Карла Фишера также показал, что вещество содержит воду в количестве 5,25 масс. %.
[0151] Образец моногидрата плинабулина (форма 1) помещали в вакуумный сушильный шкаф при 50°C в течение ночи и в течение субботы и воскресенья. Образец оставался стабильным в ходе исследований сушки, и в ходе сушки не произошло какого-либо изменения массы.
[0152] Исследование DVS проводили на моногидрате плинабулина (форма 1). Образец прибавил ~ 0,1% массы при 95% ОВ, потерянной при сушке до 0% ОВ без гистерезиса. Образец, прошедший DVS, анализировали методом XRPD, который подтвердил отсутствие какого-либо превращения. Фиг. 3С демонстрирует график изотермы DVS. XRPD образца до DVS (форма 1 моногидрата плинабулина) накладывается на XRPD образца, прошедшего DVS (форма 1 моногидрата плинабулина).
[0153] Образец моногидрата плинабулина (форма 1) помещали в среду с высокой влажностью на 13 дней, и он оставался стабильным, не меняя свою массу. Образцы до DVS и прошедшие DVS не показали каких-либо изменений на XRPD.
[0154] Тест DVS твердого вещества формы 2 показал, что образец формы 2 потерял приблизительно 7% массы при приблизительно 80% ОВ, как показано на ФИГ. 6С, и образец, прошедший DVS, отличался от образца до DVS на основе результатов анализа XRPD.
[0155] Тест DVS твердого вещества формы 3 показал, что образец формы 3 потерял приблизительно 0,2% массы при 90% ОВ, как показано на ФИГ. 9С, и образец, прошедший DVS, отличался от образца до DVS на основе результатов анализа XRPD.
[0156] Тест DVS твердого вещества формы 4 показал, что образец формы 3 потерял в массе в ходе теста, и график изотермы DVS формы 4 показан на ФИГ 12С. Образец, прошедший DVS, отличался от образца до DVS на основе результатов анализа XRPD.
[0157] Моногидрат плинабулина (форма 1) оставался стабильным в ходе тестов DVS и сушки. Для сравнения, другие полиморфные формы были нестабильными и демонстрировали изменение массы в ходе тестов DVS. Результаты тестов показали, что форма 1 более стабильна, чем другие полиморфные формы.
Пример 7
[0158] Соединение плинабулина суспендировали в 15 различных растворителях/смесях растворителей, как показано в таблице 9, при 15°C и 45°C в течение 3 дней для гравиметрического измерения растворимости. В каждом эксперименте приблизительно 70 мг твердого вещества добавляли в пробирку с последующим добавлением 0,7 мл соответствующих растворителей. Затем суспензию центрифугировали, к предварительно взвешенным пробиркам добавляли центрифутат и испаряли до сухости в вакууме. Пробирки с оставшимся твердым веществом вновь взвешивали для расчета растворимости. Соединение высоко растворимо в ТГФ (тетрагидрофуране) и обладает растворимостью от умеренной до малой в других исследованных растворителях. Данные по растворимости представлены в таблице 10.

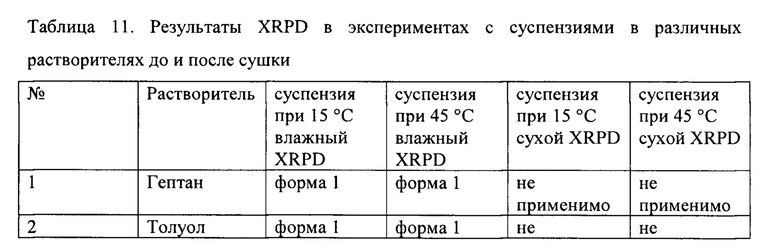
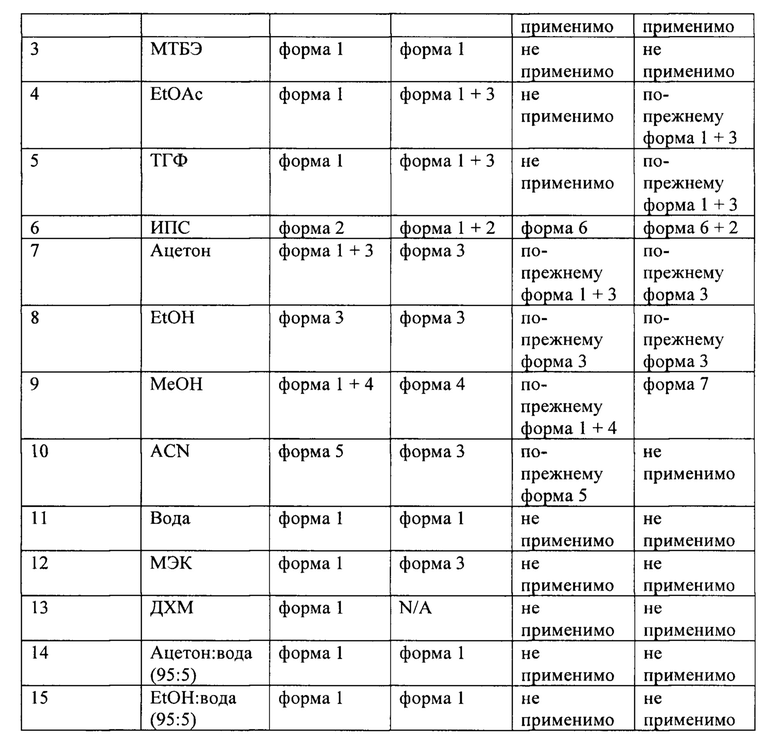
[0159] В ходе гравиметрических анализов растворимости моногидрат плинабулина (форма 1) суспендировали в различных растворителях при 15°C и при 45°C. После центрифугирования полученные твердые вещества в виде влажного осадка анализировали методом XRPD. Образцы, не представлявшие собой форму 1, сушили в вакуумном сушильном шкафу и повторно анализировали методом XRPD. Наблюдали формы 2, 3, 4, 5, 6 и 7. Эти результаты показаны в таблице 11.
[0160] Эксперименты по кристаллизации при испарении проводили путем испарения (при комнатной температуре) растворов моногидрата плинабулина в различных растворителях. Эти растворы были получены в ходе гравиметрического анализа растворимости при 15°C и при 45°C и имели различные концентрации. Полученные твердые вещества анализировали методом XRPD. Наблюдали форму 8. Эти результаты показаны в таблице 12.


[0161] Было проведено шесть экспериментов по кристаллизации при охлаждении и один эксперимент по суспендированию. Результаты этих экспериментов показаны в таблице 13.

Пример 8
[0162] Исследовали превращение различных кристаллических форм в другие формы в масштабе 200 мг.
[0163] Эксперимент в увеличенном масштабе с формой 3 проводили в масштабе 200 мг путем суспендирования твердой формы 1 в 2 мл этанола при комнатной температуре в течение ночи с получением формы 3
[0164] Эксперимент в увеличенном масштабе с формой 2 проводили в масштабе 200 мг путем суспендирования твердой формы 1 в 2 мл изопропилового спирта при 30°C в течение ночи.
[0165] Эксперимент в увеличенном масштабе с формой 4 проводили в масштабе 200 мг путем суспендирования твердой формы 1 в 2 мл МеОН при 30°C в течение ночи.
[0166] Твердую форму 3 суспендировали в смеси EtOH : воды в соотношении 95:5 при 30°C в течение 2 часов и анализировали методом XRPD, чтобы продемонстрировать превращение в форму 1.
[0167] Твердую форму 2 суспедировали (2071-16-1) в смеси EtOH:воды в соотношении 95:5 при 30°C течение 2 часов и анализировали методом XRPD, чтобы продемонстрировать превращение в форму.
[0168] Твердую форму 4 суспендировали в смеси EtOH : воды в соотношении 95:5 при 30°C в течение 2 часов и анализировали методом XRPD, чтобы продемонстрировать превращение в форму 1.
[0169] Моногидрат плинабулина (форма 1) оставался стабильным после сушки при 50°C в вакууме в течение субботы и воскресенья. Не наблюдалось изменений твердой формы при подвергании формы 1 воздействию высокой влажности (> 95% ОВ) в течение 13 дней. Было продемонстрировано, что форма 1 стабильна в ходе процесса производства, включая процесс сушки. Форма 1 также была стабильна под воздействием различных условий влажности. С другой стороны, кристаллические формы претерпевали превращение в моногидрат формы I под воздействием влаги. Следовательно, форма 1 является наиболее стабильной кристаллической формой и наиболее перспективной формой для процесса производства.
| название | год | авторы | номер документа |
|---|---|---|---|
| Твёрдые формы цефтолозана | 2014 |
|
RU2703457C2 |
| НОВЫЕ ФУМАРАТНЫЕ СОЛИ АНТАГОНИСТА ГИСТАМИНОВОГО РЕЦЕПТОРА Н3 | 2010 |
|
RU2537847C2 |
| КРИСТАЛЛИЧЕСКИЕ СОЛИ И ПОЛИМОРФЫ АНТАГОНИСТА P2X3 | 2017 |
|
RU2782068C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ИНГИБИТОРА MAGL | 2017 |
|
RU2799564C2 |
| ТВЕРДЫЕ ФОРМЫ 2-(5-(4-(2-МОРФОЛИНОЭТОКСИ)ФЕНИЛ)ПИРИДИН-2-ИЛ)-N-БЕНЗИЛАЦЕТАМИДА | 2018 |
|
RU2802964C2 |
| КРИСТАЛЛИЧЕСКАЯ ИЛИ АМОРФНАЯ ФОРМА АГОНИСТОВ FXR, ПРЕДСТАВЛЯЮЩИХ СОБОЙ ПРОИЗВОДНЫЕ СТЕРОИДОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2800751C2 |
| СОЛИ И ПОЛИМОРФЫ ЗАМЕЩЕННОГО ИМИДАЗОПИРИДИНИЛ-АМИНОПИРИДИНА | 2015 |
|
RU2732125C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ИНГИБИТОРА BTK | 2020 |
|
RU2828460C2 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА (S)-N-(5-((R)-2-(2,5-ДИФТОРФЕНИЛ)-ПИРРОЛИДИН-1-ИЛ)-ПИРАЗОЛО[1,5-A]ПИРИМИДИН-3-ИЛ)-3-ГИДРОКСИПИРРОЛИДИН-1-КАРБОКСАМИДА ГИДРОСУЛЬФАТА | 2015 |
|
RU2723990C2 |
| КРИСТАЛЛЫ АЛКИНИЛСОДЕРЖАЩЕГО СОЕДИНЕНИЯ, ЕГО СОЛИ И СОЛЬВАТА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПУТИ ПРИМЕНЕНИЯ | 2021 |
|
RU2829609C1 |












Изобретение относится к способу получения моногидрата плинабулина, включающему объединение плинабулина и первой системы растворителей с образованием первой смеси, где указанная первая система растворителей содержит этанол, нагрев первой смеси до температуры от 50 °C до 90 °C до полного растворения плинабулина, добавление воды к первой смеси с получением второй смеси и охлаждение второй смеси с образованием осадка. Технический результат: разработан новый способ получения, который позволяет получить моногидрат плинабулина. 22 з.п. ф-лы, 34 ил., 13 табл., 8 пр.
1. Способ получения моногидрата плинабулина, включающий:
объединение плинабулина и первой системы растворителей с образованием первой смеси, где указанная первая система растворителей содержит этанол;
нагрев первой смеси до температуры от 50 °C до 90 °C до полного растворения плинабулина;
добавление воды к первой смеси с получением второй смеси; и
охлаждение второй смеси с образованием осадка.
2. Способ по п. 1, дополнительно включающий фильтрацию первой смеси перед добавлением воды.
3. Способ по любому из пп. 1, 2, дополнительно включающий отфильтровывание осадка.
4. Способ по любому из пп. 1-3, дополнительно включающий промывку осадка.
5. Способ по любому из пп. 1-4, где первую смесь нагревают до температуры от 70 °C до 78 °C.
6. Способ по любому из пп. 1-5, дополнительно включающий поддержание первой смеси при температуре от 70 °C до 78 °C в течение 1 часа перед добавлением воды.
7. Способ по любому из пп. 1-6, где нагрев первой смеси включает нагрев первой смеси до по меньшей мере 65 °C.
8. Способ по любому из пп. 1-7, где охлаждение второй смеси включает перемешивание первой смеси в течение по меньшей мере 4 часов.
9. Способ по любому из пп. 1-7, дополнительно включающий анализ осадка с помощью рентгеновского порошкового дифракционного анализа.
10. Способ по любому из пп. 1-9, дополнительно включающий нагрев второй смеси до температуры от 50 °C до 90 °C.
11. Способ по п. 10, где нагрев второй смеси включает кипячение второй смеси с обратным холодильником.
12. Способ по любому из пп. 10, 11, где вторую смесь нагревают до температуры от 70 °C до 78 °C.
13. Способ по любому из пп. 10, 11, дополнительно включающий поддержание второй смеси при температуре кипения с обратным холодильником в течение 1 часа перед охлаждением второй смеси.
14. Способ по любому из пп. 10-13, где охлаждение второй смеси включает охлаждение до температуры от 15 °C до 30 °C.
15. Способ по любому из пп. 10-14, где охлаждение второй смеси включает перемешивание второй смеси в течение по меньшей мере 4 часов.
16. Способ по любому из пп. 10-15, где осадок промывают спиртом и промывочный спирт собирают и добавляют ко второй смеси перед нагревом.
17. Способ по любому из пп. 10-16, дополнительно включающий сушку осадка.
18. Способ по любому из пп. 10-17, дополнительно включающий анализ осадка для определения композиции плинабулина в осадке.
19. Способ по любому из пп. 1-18, в котором моногидрат плинабулина характеризуется рентгеновской порошковой дифрактограммой, содержащей по меньшей мере три характеристических пика, выбранных из группы, состоящей из пиков при 8,1°, 13,1°, 16,3°, 23,9°, 24,2°, 24,5° и 26,6° ± 0,2° 2θ.
20. Способ по любому из пп. 1-18, в котором моногидрат плинабулина характеризуется рентгеновской порошковой дифрактограммой, содержащей по меньшей мере пики при 8,1°, 13,1°, 16,3°, 23,9°, 24,2°, 24,5° и 26,6° ± 0,2° 2θ.
21. Способ по любому из пп. 1-18, в котором моногидрат плинабулина характеризуется рентгеновской порошковой дифрактограммой, содержащей по меньшей мере пики при 8,1°, 13,1°, 16,1°, 16,3°, 19,8°, 22,9°, 23,9°, 24,2°, 24,5°, 26,6° и 29,3° ± 0,2° 2θ.
22. Способ по любому из пп. 1-18, в котором моногидрат плинабулина имеет температуру плавления, составляющую 267 °C.
23. Способ по любому из пп. 1-18, в котором моногидрат плинабулина имеет термограмму дифференциальной сканирующей калориметрии с эндотермическими пиками при 141 °C и 267 °C.
| WO2005077940 A1, 25.08.2005 | |||
| Yuri Yamazaki, Et al, Synthesis and Structure-Activity Relationship Study of Antimicrotubule Agents Phenylahistin Derivatives with a Didehydropiperazine-2,5-dione Structure, JOURNAL OF MEDICINAL CHEMISTRY, стр.1056-1071, 09.02.2012 | |||
| WO2012035436 A1, 22.03.2012 | |||
| WO2015051543 A1, 16.04.2015 | |||
| ПРОИЗВОДНЫЕ АРОИЛПИПЕРАЗИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ | 1998 |
|
RU2258702C2 |
Авторы
Даты
2022-06-14—Публикация
2016-07-11—Подача